Область техники, в которой относится изобретение
Настоящее изобретение относится к медицине, более точно, к применению композиции на основе используемых в китайской медицине веществ для приготовления лекарственных средств в целях вторичной профилактики инфаркта миокарда.
Предпосылки создания изобретения
Сердечно-сосудистое заболевание является распространенным и частым заболеванием, представляющим собой серьезную угрозу для жизни и здоровья людей. Ежегодно в результате острых сердечно-сосудистых заболеваний в мире умирают около 20 миллионов человек, более половины из которых умирают от острого инфаркта миокарда (AMI). По мере старения населения Китая наблюдается явная тенденция роста заболеваемости AMI, которая уже приблизилась к среднему международному уровню. За счет усиленных мер контроля и лечения за последние годы смертность от инфаркта миокарда снизилась. Но пережившие его по-прежнему подвержены высокой степени риска повторных сердечно-сосудистых заболеваний, например, инфаркта миокарда, застойной сердечной недостаточности, скоропостижной смерти и т.д. Соответственно, помимо активного лечения в острой фазе следует усилить вторичную профилактику инфаркта миокарда.
Вторичная профилактика инфаркта миокарда означает профилактику сердечно-сосудистых событий и повышение качества жизни пациентов после инфаркта миокарда. Как показано во многих исследованиях, существует множество лекарств, которые по имеющимся данным обладают активным положительным эффектом в том, что касается вторичной профилактики инфаркта миокарда, например, ингибиторы образования тромбоцитов (аспирин), блокаторы β-рецепторов, статины, ингибиторы ангиотензин-превращающего фермента (ACEI) и т.д. Кроме того, на эффективность этих лекарств не влияют другие состояния пациентов, такие как возраст, пол и т.д.
Как доказано результатами крупномасштабных медицинских клинических исследований, хотя упомянутые лекарства, например ингибиторы образования тромбоцитов (аспирин), блокаторы β-рецепторов, статины, ингибиторы ангиотензин-превращающего фермента (ACEI) и т.д. способны значительно снижать показатель смертности в результате AMI, огромное число переживших AMI обычно теряют трудоспособность или умирают в результате сердечно-сосудистых событий, таких как повторный инфаркт, тяжелая аритмия, сердечная недостаточность и т.д. Кроме того, эти лекарства до известной степени вызывают неблагоприятные реакции, некоторые из которых даже являются очень серьезными. Помимо этого, на западе постепенно поняли, что воздействие одного лекарства на вторичную профилактику может не являться таким же эффективным, как воздействие сочетания лекарств, и разработали ряд составных препаратов на основе используемых в западной медицине веществ для вторичной профилактики инфаркта миокарда. В традиционной китайской медицине (ТСМ) в течение тысяч лет для лечения применяются преимущественно лекарственные средства из растительного сырья. Даже одно лекарственное средство из растительного сырья может рассматриваться как небольшой составной препарат, поскольку оно состоит из нескольких ингредиентов. Кроме того, преимуществами средств ТСМ являются повышенная эффективность, сниженная токсичность и усиленное действие за счет совместимости и сниженных побочных эффектов, что делает их приемлемыми для длительного применения в качестве средства вторичной профилактики.
Краткое изложение сущности изобретения
В основу настоящего изобретения положена задача обеспечения применения композиции на основе используемых в китайской медицине веществ для приготовления лекарственных средств в целях вторичной профилактики инфаркта миокарда. Композицию на основе используемых в китайской медицине веществ приготавливают из состава, содержащего лекарственное сырье со следующим содержанием в процентах по весу:
Radix Astragali (Huangqi в ТСМ)
22,2%-66,8%,
Radix Salviae Miltiorrhizae (Danshen)
11,6%-33,4%,
Radix Notoginseng (Sanqi)
2,5%-13,5% и
Lignum Dalbergiae Odoriferae (Jiangxiang)
14,5%-44,3%.
В соответствии с настоящим изобретением композиция на основе используемых в китайской медицине веществ снижает частоту наступления сердечно-сосудистых событий у пациентов после острого инфаркта миокарда. Сердечно-сосудистые события включают следующие заболевания: а) повторный инфаркт; б) тяжелую аритмию; в) сердечную недостаточность; г) кардиогенный шок; д) реваскуляризацию (хирургическую терапию и аортокоронарное обходное шунтирование).
В соответствии с настоящим изобретением композиция на основе используемых в китайской медицине веществ снижает частоту наступления несердечно-сосудистых событий среди пациентов после острого инфаркта миокарда. Несердечно-сосудистые события включают следующие заболевания: а) инсульт; б) эмболию легких; в) нарушения периферических сосудов; г) опухоль.
В соответствии с настоящим изобретением композиция на основе используемых в китайской медицине веществ снижает частоту наступления событий смерти среди пациентов после острого инфаркта миокарда. События смерти включают: а) смерть от ишемической болезни сердца (ИБС); б) смерть от другого сердечно-сосудистого заболевания; в) смерть от несердечно-сосудистого заболевания.
В соответствии с настоящим изобретением композиция на основе используемых в китайской медицине веществ способна ослаблять приступы стенокардии у пациентов после острого инфаркта миокарда, например, снижать частоту приступов, сокращать длительность, снижать степень боли, снижать дозу нитроглицерина и ослаблять симптомы боли в грудной клетке, стеснения в грудной клетке, одышки, усталости, учащенного сердцебиения, спонтанного потоотделения, а также бледности.
В соответствии с настоящим изобретением композиция на основе используемых в китайской медицине веществ способна повышать качество жизни пациентов после острого инфаркта миокарда. После применения композиции на основе используемых в китайской медицине веществ значительно уменьшается степень ограничения физической активности, стабилизируется состояние стенокардии и снижается частота приступов стенокардии.
В соответствии с настоящим изобретением композицию на основе используемых в китайской медицине веществ предпочтительно приготавливают из состава, содержащего лекарственное сырье со следующим содержанием в процентах по весу:
Radix Astragali (Huangqi)
30,8%-57,2%,
Radix Salviae Miltiorrhizae (Danshen)
15,4%-28,6%,
Radix Notoginseng (Sanqi) 3,5%-6,5%, и
Lignum Dalbergiae Odoriferae (Jiangxiang)
20,6%-38,2%,
наиболее предпочтительно:
Radix Astragali (Huangqi)
44,7%,
Radix Salviae Miltiorrhizae (Danshen)
26,7%,
Radix Notoginseng (Sanqi)
6,3%, и
Lignum Dalbergiae Odoriferae (Jiangxiang)
22,3%, или
Radix Astragali (Huangqi)
41,2%,
Radix Salviae Miltiorrhizae (Danshen)
23,8%,
Radix Notoginseng (Sanqi)
4,5% и
Lignum Dalbergiae Odoriferae (Jiangxiang)
30,5%.
В соответствии с настоящим изобретением композиция на основе используемых в китайской медицине веществ может быть приготовлена путем экстрагирования отдельного лекарственного сырья традиционными способами экстрагирования или известными из техники способами и смешивания. Композицию на основе используемых в китайской медицине веществ предпочтительно приготавливают способом, включающим: экстрагирование размельченных Sanqi и Danshen с водой, фильтрацию, соответствующее концентрирование фильтрата, осаждение спиртом, восстановление полученного супернатанта и непрерывное концентрирование с получением экстракта, а именно, экстракта Danshen и Sanqi; экстрагирование размельченного Huangqi с водой, фильтрацию, соответствующее концентрирование фильтрата, осаждение спиртом, восстановление полученного супернатанта и непрерывное концентрирование с получением экстракта, а именно, экстракта Huangqi; дефлегмационное экстрагирование Jiangxiang с водой и сбор эфирного масла; тщательное перемешивание упомянутых выше двух экстрактов, эфирного масла и инертных наполнителей с получением любой из фармацевтически приемлемых лекарственных форм, предпочтительно микропилюлей. Кроме того, микропилюли изготавливают на следующих стадиях, на которых используют упомянутый экстракт Danshen и Sanqi, экстракт Huangqi и ПЭГ-6000 в количестве, в 2-5 превышающем общий вес экстрактов, растворяют на водяной бане с тщательным перемешиванием, добавляют эфирное масло Jiangxiang и гармонизируют, в результате чего получают микропилюли традиционным способом. Точно так же традиционным способом может быть получена таблетка.
Для обеспечения лучшего понимания настоящего изобретения было проведено многоцентровое рандомизированное исследование двойным слепым методом с двойной имитацией и позитивным контролем. Исследование проводилось с участием 3508 пациентов с AMI, диагностированным за предшествующий период от 28 дней до 2 лет, которые согласно ТСМ были разделены на группу с дефицитом Qi и группу с синдромом застоя кровообращения. Участники исследования три раза в день через полчаса после приема пищи получали 0,5 г композиции на основе используемых в китайской медицине веществ, полученной способом по Примеру 1 (под кодовым наименованием QSYQ). В качестве лекарства для позитивного контроля использовали аспирин. Пациенты получали лечение в течение 1 года и наблюдались в течение 6 месяцев. Как показали результаты, между группой, получавшей микропилюли Qi Shen Yi Qi (изготовленные согласно настоящему изобретению), и группой, получавшей аспирин (логарифмический ранговый критерий для межгруппового сравнения), отсутствовало статистическое расхождение среди пациентов после острого инфаркта миокарда в том, что касается повторного инфаркта, несмертельного инсульта, смерти от сердечно-сосудистых заболеваний. Кроме того, не было обнаружено статистического расхождения с аспирином в том, что касается снижения частоты смертей, снижения степени тяжести, частоты и длительности приступов стенокардии, снижения дозы нитроглицерина, ослабления ряда симптомов ТСМ, например, стеснения в грудной клетке, учащенного сердцебиения, спонтанного потоотделения, бледности, а также повышения качества жизни (использовался Сиэтловский опросник качества жизни при стенокардии (SAQ)). Из этого следует, что композиция на основе используемых в китайской медицине веществ обладает сходным с аспирином действием на пациентов в том, что касается вторичной профилактики после острого инфаркта миокарда.
Используемые в изобретении сокращения
АЕ
неблагоприятное событие
FAS
полный набор данных для анализа
SS
набор данных для оценки безопасности
РР
соблюдавшие протокол испытуемые
LOCF
перенос последнего наблюдения
Mean
среднее число
SD
стандартное отклонение
Md
срединное значение
Min
минимальное значение
Max
максимальное значение
CI
доверительный интервал
HR
степень риска
Цель исследования
Исследование имело целью, в первую очередь, определить, оказывает ли длительное применение QSYQ воздействие на снижение степени риска (HR) несмертельного повторного инфаркта, смерти от сердечно-сосудистых заболеваний и несмертельного инсульта, и не уступает ли оно воздействию аспирина. Второй целью являлось понимание воздействия QS YQ на другие клинические события и качество жизни пациентов.
Общий план исследования
Было проведено многоцентровое рандомизированное клиническое исследование двойным слепым методом с двойной имитацией и позитивным контролем.
Использовался метод крупномасштабных рандомизированных контролируемых испытаний (RCT). Испытание проводилось одновременно в 16 вспомогательных центрах (стационарных лечебных учреждениях категории III) в 5 регионах на востоке, западе, юге, севере и в центральном Китае и в 84 стационарных лечебных учреждениях.
Рандомизированный метод: централизованная рандомизация В соответствии с готовой таблицей случайных последовательностей (генерированной компьютером) испытуемые были случайным методом отнесены к одной из двух лечебных групп в соотношении 1:1 посредством интерактивной системы речевой связи (IVRS).
Когда испытуемые отвечали критериям включения/исключения, исследователи использовали IVRS, которая присваивала испытуемому конкретный идентификационный код и случайный номер. Присваиваемые IVRS конкретный идентификационный код и случайный номер являлись уникальными. Они использовались для идентификации испытуемых и отображения того, какое лекарство они получали.
С целью обеспечения двойного слепого метода испытания было создано плацебо QSYQ. Требовалось, чтобы оно имело такую же упаковку и преимущественно такой же внешний вид, форму и цвет, как у QSYQ. Кроме того, плацебо таблетки аспирина имело такую же упаковку и преимущественно такой же внешний вид, форму и цвет, как у аспирина. Для каждого испытуемого рассчитанная на один месяц доза была упакована в небольшую коробку, содержащую QSYQ и плацебо аспирина или аспирин и плацебо QSYQ. Рассчитанная на три месяца доза была упакована в большую коробку, при этом каждое лекарство имело одинаковый номер.
Уникальные номера были предварительно напечатаны на этикетках исследовавшихся лекарств. С помощью IVRS лекарства случайным методом назначались испытуемым, отвечавшим требованиям. Этикетки были разделены на две части: часть была приклеена к коробкам и содержала указания по применению лекарства и другую информацию; отделяемую часть отрывали и вклеивали в таблицу распределения лекарств. Кроме того, отвечающие за назначение лекарств исследователи должны были вносить в дневник распределения лекарств номер лекарства, соответствующий каждому наблюдению.
Лекарство для позитивного контроля
В качестве стандартного лекарства для вторичной профилактики инфаркта миокарда использовался аспирин (AS).
Способ применения
1. Получавшая QSYQ лечебная группа: 0,5 г QSYQ 3 раза в день через полчаса после приема пищи и одновременно 100 мг плацебо таблетки аспирина с энтеросолюбильным покрытием (4 таблетки) один раз в день.
2. Получавшая аспирин контрольная группа: 100 мг плацебо таблетки аспирина с энтеросолюбильным покрытием (4 таблетки) один раз в день через полчаса после приема пищи и одновременно 0,5 г плацебо QSYQ 3 раза в день.
Расчет объема выборки
Объем выборки вычислялся на основании следующих предположений. Согласно опыту предыдущих клинических исследований наступление Ml (инфаркта миокарда) в течение 1 года составляла около 5%. Если допустить снижение риска смерти в результате лечения до 50% (или до HR 0,5), т.е. темп снижения 20%, необходимо в общей сложности по меньшей мере 3000 испытуемых (группа испытуемых: 1800 случаев, степень=90%, двустороннее альфа-распределение=0,05). Длительность исследования составляла 18 месяцев, первые 12 месяцев из которых длился период лечения, а последние 6 месяцев - период наблюдения.
Критерий оценки
1.1 Определения критерия
1.1.1 Конечные точки
(1) Сердечно-сосудистые события включают а) повторный инфаркт, б) тяжелую аритмию, в) сердечную недостаточность, г) кардиогенный шок, д) реваскуляризацю (хирургическую терапию и аортокоронарное обходное шунтирование).
(2) Несердечно-сосудистые события включают а) инсульт, б) эмболию легких, в) нарушения периферических сосудов, г) опухоль.
(3) События смерти включают а) смерть от ишемической болезни сердца, б) смерть от другого сердечно-сосудистого заболевания; в) смерть от несердечно-сосудистого заболевания.
1.1.2 Оценка стенокардии и симптомов ТСМ
Стенокардия
Шкала оценок симптомов
Частота
Оценка 0: отсутствие; оценка 2: 2-6 раз в неделю; оценка 4: 1-3 раза в сутки; оценка 6:4 раза или более в сутки.
Длительность
Оценка 0: отсутствие; оценка 2: длительность боли каждый раз ≤5 мин; оценка 4: 5-10 мин; оценка 6:≥10 мин.
Степень боли
Оценка 0: отсутствие; оценка 2: ослабление приступа после отдыха без оказания влияния на повседневную жизнь; оценка 4: купирование приступа с помощью лекарства и возобновление нормальной активности после ремиссии; оценка 6: влияние частых приступов на повседневную жизнь (симптомы могут возникать, например, вследствие одевания, приема пищи, ходьбы, стула).
Доза нитроглицерина
Оценка 0: отсутствие; оценка 2: 1-4 таблетки в неделю; оценка 4: 5-9 таблеток в неделю; оценка 6: 10 таблеток или более в неделю.
Симптомы ТСМ
Шкала оценок симптомов
Боль в грудной клетке
Оценка 0: отсутствие; оценка 3: ослабление приступа после отдыха, без оказания влияния на повседневную жизнь; оценка 6: купирование приступа с помощью лекарства и возобновление нормальной активности после ремиссии; оценка 9: влияние частых приступов на повседневную жизнь (симптомы могут возникать, например, вследствие одевания, приема пищи, ходьбы, стула).
Стеснение в грудной клетке
Оценка 0: отсутствие; оценка 3: периодически ощущаемое стеснение в грудной клетке, которое может ослабляться само по себе; оценка 6: частые приступы стеснения в грудной клетке, но без оказания влияния на нормальную жизнь и работу; оценка 9: стеснение в грудной клетке, которое невозможно ослабить, влияющее на нормальную жизнь и работу.
Одышка
Оценка 0: отсутствие; оценка 2: одышка после активности; оценка 4: одышка после незначительной активности; оценка 6: обычно ощущаемая одышка.
Усталость
Оценка 0: отсутствие; оценка 2: усталость, ощущаемая после значительной активности; оценка 4: усталость, ощущаемая после умеренной активности; оценка 6: усталость, ощущаемая после незначительной активности.
Учащенное сердцебиение
Оценка 0: отсутствие; оценка 1: спорадическое учащенное сердцебиение, которое может ослабляться само по себе; оценка 2: частые приступы учащенного сердцебиения, но с возможностью продолжать работу; оценка 3: постоянное учащенное сердцебиение, которое невозможно ослабить, влияющее на жизнь и работу.
Спонтанное потоотделение
Оценка 0: отсутствие; оценка 1: периодическое потоотделение после активности; оценка 2: видимое потоотделение после активности; оценка 3: частое потоотделение во время отдыха.
Бледность
Оценка 0: отсутствие; оценка 1: бледность.
1.1.3 Качество жизни
В Сиэтловском опроснике качества жизни при стенокардии (SAQ) содержится 19 вопросов в 5 разделах: ограничения физических нагрузок (PL), стабильность приступов (AS), частота приступов (AF), удовлетворенность лечением (TS) и отношение к болезни (DP). После необходимых разъяснений, данных врачами, пациенты самостоятельно ответили на вопросы.
1.2 Режим лечения
Режим лечения был поделен на 4 категории. Основная конечная точка-событие относилась к режиму первой категории, а второстепенна конечная точка-событие - к режимам второй, третьей и четвертой категорий.
К 1-й категории были отнесены несмертельный повторный инфаркт, несмертельный инсульт и смерть от сердечно-сосудистых заболеваний.
Ко 2-й категории были отнесены тяжелая аритмия, сердечная недостаточность, кардиогенный шок и реваскуляризация.
К 3-й категории были отнесены нарушения периферических сосудов, эмболия легких и смерть от несердечно-сосудистых заболеваний.
К 4-й категории были отнесены стенокардия, симптомы ТСМ и SAQ.
Основной конечной точкой исследования являлась частота наступления конечных точек-событий в течение 1 года после первого приема лекарства. При последней оценке не учитывались выбывшие испытуемые (например, аннулировавшие сознательное согласие или прекратившие наблюдаться). Конечной точкой исследования являлся 1 год после того, как последний испытуемый был методом случайного выбора включен в какую-либо группу (12 месяцев).
1.2.1 Основные показатели терапевтического действия
Частота наступления основных конечных точек-событий
В качестве конечных точек-событий первой категории были определены основные конечные точки-события, включающие несмертельный повторный инфаркт, несмертельный инсульт и смерть от сердечно-сосудистых заболеваний. Если имело место какое-либо из этих событий, оно считалось наступившей основной конечной точкой-событием. Другие случаи могли не учитываться.
Было рассчитано время наступления основных конечных точек-событий следующим способом. Время наступления конечных точек определялось как период от момента первого приема лекарства до момента наступления любого из упомянутых событий (например, если у одного заболевания имелось множество конечных точек, временем наступления основных конечных точек-событий считалось время последнего наступившего события). Если до завершения исследования испытуемые по какой-либо причине выбывали или прекращали наблюдаться, время рассчитывалось с учетом момента выбытия или прекращения наблюдения. Если испытуемые доживали до последнего наблюдения, время рассчитывалось с учетом момента последнего наблюдения.
1.2.2 Второстепенные показатели терапевтического действия
Второстепенные показатели включали полное время дожития, оценку стенокардии, оценку симптомов ТСМ и SAQ.
Полное время дожития
Конечной точкой являлась смерть по любой причине в период исследования. Другие случаи рассматривались как цензурирование.
Время наступления конечной точки-события смерти было рассчитано следующим способом. Определили период от момента первого приема лекарства до момента наступления конечных точек, и определили время наступления неконечных точек на основании способа определения основной конечной точки-события.
1.3 Показатели безопасности в основном включают:
Неблагоприятное событие, которым являются любые неблагоприятные медицинские события, произошедшие с момента подписания пациентами формы сознательного согласия (ICF) и их включения в исследование до окончания лечения независимо от того, получали ли они испытываемое лекарство.
Серьезные неблагоприятное событие включали смерть и другие случаи, угрожавшие жизни, события, приводившие к помещению в стационар для лечения, длительному к помещению в стационар для лечения, постоянной или серьезной нетрудоспособности или порокам развития.
Статистическая совокупность
1. Совокупность испытуемых, обеспечивающая полный набор данных для анализа (FAS)
В максимальном соответствии с принципом назначенного лечения был создан набор идеальных случаев, сформированный на основе случаев рандомизированных испытуемых за исключением худших или необоснованных случаев.
Обработка недостающих данных
(1). Конечные точки были обработаны в соответствии с анализом данных дожития. Смотри основные показатели терапевтического действия в разделе статистического анализа.
(2). Другие показатели лечения включали оценку стенокардии, оценку симптомов ТСМ и данные различных оценок, которые вносились в SAQ. Недостающие значения упомянутых показателей оценивались методом наиболее точной оценки переноса данных последнего наблюдения (LOCF).
2. Совокупность соблюдавших протокол (РР) испытуемых Совокупность РР также именуется достоверными случаями, достоверными
выборками или поддающимися оценке случаями. Полное соблюдение программы испытания гарантировало, что набор данных был сформирован на основании подмножества достоверных случаев согласно научной модели.
3. Совокупность испытуемых, обеспечивающая набор данных для оценки безопасности (SS)
Совокупность SS состояла из испытуемых, получивших по меньшей мере одну дозу лекарства после рандомизации.
Разделение на совокупности для статистического анализа было совместно осуществлено испытателями, администраторами данных и специалистами по статистическому анализу путем анализа данных слепого метода.
Метод статистического анализа
1.4 Общий принцип
Во всех статистических испытаниях использовался двусторонний критерий. Он предположительно имел статистическую значимость (p≤0,05, если не указано иное).
Количественные показатели представлены как среднее значение, стандартное отклонение, срединное значение, минимальное значение и максимальное значение.
Классификационные показатели представлены как число выборок и их процент.
1.5 Оценка терапевтического действия
1.5.1 Исходные данные
Исходными данными являлись данные наблюдения №1 пациентов, включенных в группу до начала лечения. Оценка исходных данных осуществлялась применительно к совокупности FAS.
Для межгруппового сравнения исходных данных суммарных и отдельных оценок стенокардии, суммарных и отдельных оценок симптомов ТСМ и оценки каждого вопроса из SAQ могла использоваться проверка по критерию Стьюдента или критерию суммы рангов Уилкоксона.
1.5.2 Оценка основного терапевтического действия
Основным терапевтическим действием являлся коэффициент выживаемости применительно к основным конечным точкам-событиям.
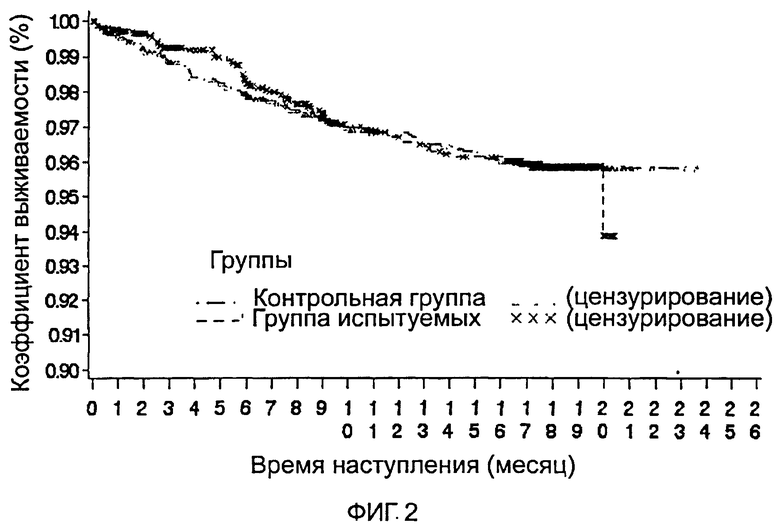
Для оценки коэффициента выживаемости применительно к основным конечным точкам-событиям как в группе испытуемых, так и в контрольной группе использовался метод Каплана-Майера. После расчета момента наступления события при квантиле 25%, 50% и 75% была построена кривая выживаемости. Для межгруппового сравнения использовался логарифмический ранговый критерий.
Для сравнительной оценки риска конечных точек в группах испытуемых и в контрольной группе и вычисления его 95% доверительного интервала использовалась модель пропорциональных рисков Кокса.
Определение и метода вычисления основных конечных точек-событий смотри в соответствующем разделе показателей терапевтического действия.
1.5.3 Оценка побочного терапевтического действия
Включает полное время дожития, оценку стенокардии, оценку симптомов ТСМ и оценку качества жизни, при этом оценку стенокардии, оценку симптомов ТСМ и оценку качества жизни определяли случайным образом через 1, 3, 6, 9,12 месяцев лечения и 18 месяцев наблюдения.
1.5.3.1 Полное время дожития
В качестве метода анализа использовался коэффициент выживаемости применительно к основным конечным точкам-событиям. Определение и метод вычисления полного времени дожития смотри в соответствующем разделе показателей терапевтического действия.
1.5.3.2 Оценка стенокардии
Общая оценка стенокардии давалась для каждого периода наблюдений и изменения результатов наблюдений по сравнению с исходными данными. Для межгруппового сравнения использовалась проверка по критерию Стьюдента или критерию суммы рангов Уилкоксона. Для каждого наблюдения определялась категория общей оценки, а для межгруппового сравнения использовалась проверка по критерию суммы рангов Уилкоксона. Для анализа изменения общей оценки данных каждого наблюдения в группах по сравнению с исходными данными использовалась проверка по критерию Стьюдента и парная проверка по критерию суммы рангов Уилкоксона.
Для каждого момента времени наблюдений и изменения данных наблюдений по сравнению с исходными данными отображалась отдельная оценка стенокардии. Для межгруппового сравнения использовалась проверка по критерию суммы рангов Уилкоксона. Для анализа изменения общей оценки данных каждого наблюдения в группах по сравнению с исходными данными использовалась парная проверка по критерию суммы рангов Уилкоксона.
1.5.3.3 Оценка симптомов ТСМ
Методом анализа являлась оценка стенокардии.
1.5.3.4 SAQ
Были описаны все результаты оценки данных SAQ в период наблюдения, а для межгруппового сравнения использовалась проверка по критерию суммы рангов Уилкоксона.
1.6 Оценка безопасности
1.6.1 Длительность участия пациентов в исследовании длительность наблюдения (дни)=(дата окончания - дата начала)+1 длительность лечения (дни)=(дата окончания - дата начала)+1
1.6.2 Показатели оценки безопасности
Неблагоприятные события оценивались в любой момент после включения в число испытуемых. Показатели оценки безопасности определялись на основании совокупность испытуемых, на которых оценивалась безопасность. 1.6.3 Метод оценки безопасности
В каждой получавшей лекарство группе по отдельности определялась наступление, доля и число неблагоприятных событий. Перечислялись испытуемые, выбывшие из исследования вследствие неблагоприятных событий, и испытуемые, пережившие сопутствующие неблагоприятные события и серьезные неблагоприятные события.
Результаты статистического анализа
Данные исследования анализировались вслепую, а затем блокировались.
Сразу после идентификации полученных слепым методом данных результаты впервые разделили на две группы А и В, и оценили основные показатели терапевтического действия. После повторной идентификации полученных слепым методом данных группа А стала группой испытуемых, а группа В - контрольной группой.
В исследовании участвовали в общей сложности 3508 человек, из которых 1748 в группе испытуемых и 1760 в контрольной группе. Совокупность FAS состояла из 3505 человек, 1746 из группы испытуемых и 1759 из контрольной группы. Совокупность РР состояла из 2956 человек, 1456 из группы испытуемых и 1500 из контрольной группы. Совокупность SS состояла из 3507 человек, 1747 из группы испытуемых и 1760 из контрольной группы.
Показатели терапевтического действия
Исходные данные
За исключением статистически значимого различия между группами в показателях усталости (Р<0,05) не было обнаружено статистически значимого
различия в других показателях (Р>0,05) из числа симптомов ТСМ.
Основные показатели терапевтического действия:
наступление основных конечных точек-событий
Таблица 1
Определение частоты наступления основных конечных точек-событий в двух группах в различные моменты времени (FAS)
Метод испытаний
Статистическое значение
Р-значение
Время
Логарифмический ранговый критерий
0,00
0,9523
Таблица 2
(FAS)-рандомизированный метод определения времени дожития согласно модели Кокса (показатель риска и 95% CI)
Итого
Данные (группа испытуемых=1746, контрольная группа=1759, N=3505
Время дожития (модель Кокса)
Группа испытуемых в сравнении с контрольной группой
1,01 (0,72, 1,42)
Отношение правдоподобия (Р)
00,(0,952)
Кривую Каплана-Майера времени до наступления основной конечной точки-события (FAS) смотри на фиг.1 и 2.
Таблица 3
Определение частоты наступления основных конечных точек-событий в двух группах в различные моменты времени (РР)
Метод испытаний
Статистическое значение
Р-значение
Время Логарифмический ранговый критерий
0,00
0,9788
Таблица 4
Рандомизированный метод определения времени дожития согласно модели Кокса (показатель риска и 95% CI)
Данные
Итого
(группа испытуемых=1456 контрольная группа=1500 N=2956)
Время дожития (модель Кокса)
Группа испытуемых в сравнении с контрольной группой
(1,00 (0,71, 1,42)
Отношение правдоподобия (Р)
0,00 (0,979)
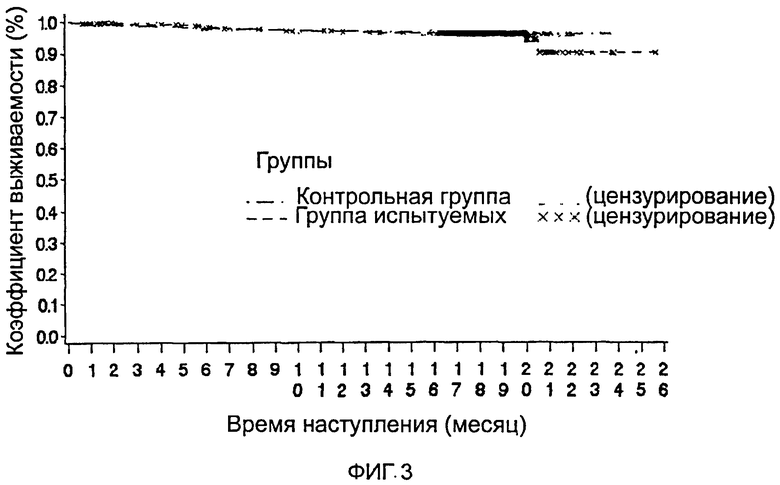
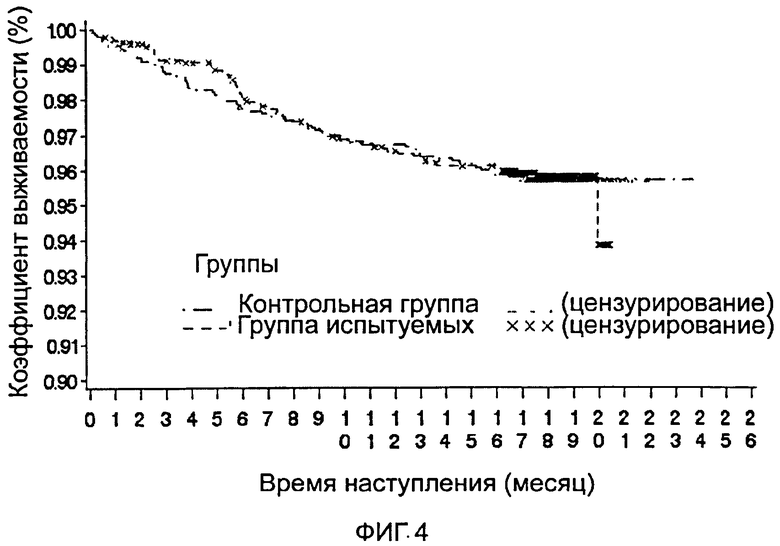
Кривую Каплана-Майера времени до наступления основной конечной точки-события (FAS) смотри на фиг.3 и 4.
1.6.4 Побочное терапевтическое действие
1.6.4.1 Полное время дожития
Таблица 5
Определение частоты наступления конечной точки-события смерти в двух группах в различные моменты времени (РР)
Метод испытаний
Статистическое значение
Р-значение
Время Логарифмический ранговый критерий
1,27
0,2592
Таблица 6
(FAS)-рандомизированный метод определения времени дожития согласно модели Кокса (показатель риска и 95% CI)
Итого
Данные (группа испытуемых=1746 контрольная=1759 итого=3505)
Время дожития (модель Кокса)
Группа испытуемых в сравнении с контрольной группой
1,29 (0,83, 2,01)
Отношение правдоподобия (Р)
1,28 (0,259)
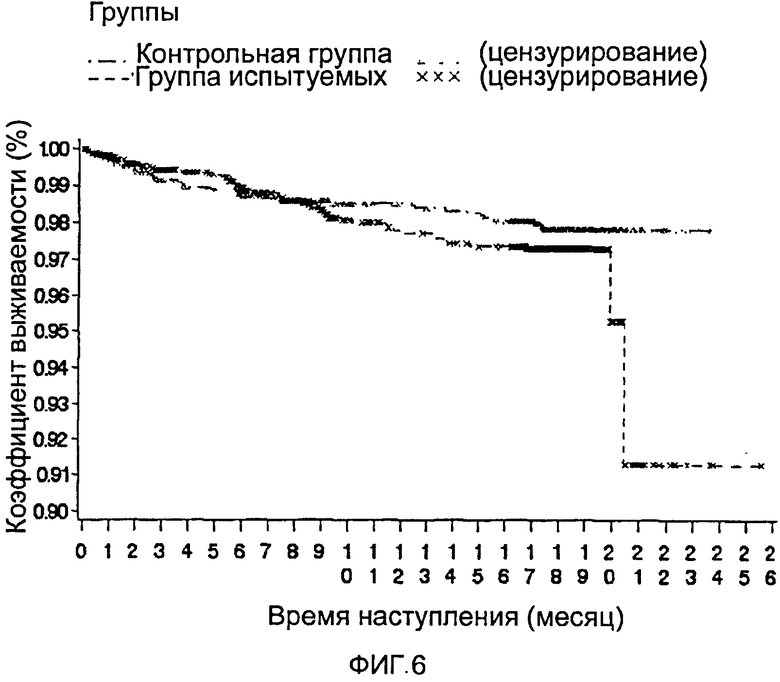
Кривую Каплана-Майера времени до наступления конечной точки-события смерти (FAS) смотри на фиг.5 и 6.
Таблица 7
Определение частоты наступления конечной точки-события смерти в двух группах в различные моменты времени (РР)
Метод испытаний
Статистическое значение
Р-значение
Время
Логарифмический ранговый критерий
1,19
0,2752
Таблица 8
(FAS)-рандомизированный метод определения времени дожития согласно модели Кокса (показатель риска и 95% CI)
Итого
Данные (группа испытуемых =1456 контрольная группа=1500 N=2956)
Время дожития (модель Кокса)
Группа A в сравнении с группой В
1,29(0,82,2,04)
Отношение правдоподобия (Р)
1,19(0,275)
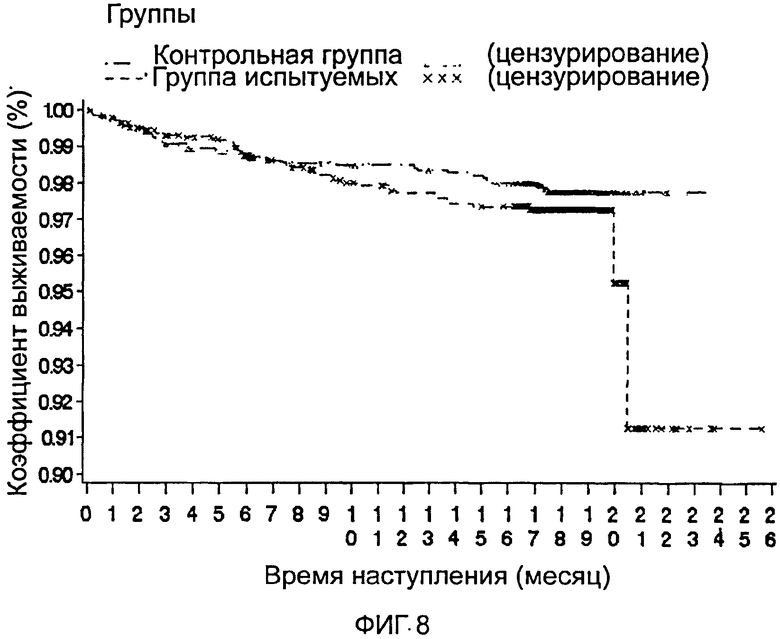
Кривую Каплана-Майера времени до наступления конечной точки-события смерти (РР) смотри на фиг.7 и 8. 1.6.4.2 Оценка стенокардии
Общая оценка стенокардии давалась для каждого периода наблюдений и изменения данных наблюдений по сравнению с исходными данными. Для межгруппового сравнения использовалась проверка по критерию Стьюдента или критерию суммы рангов Уилкоксона. Для каждого наблюдения определялась категория общей оценки, а для межгруппового сравнения использовалась проверка по критерию суммы рангов Уилкоксона. Для анализа изменения общей оценки данных каждого наблюдения в группах по сравнению с исходными данными использовалась проверка по критерию Стьюдента и парная проверка по критерию суммы рангов Уилкоксона.
Для каждого момента времени наблюдений и изменения данных наблюдений по сравнению с исходными данными отображалась отдельная оценка стенокардии. Для межгруппового сравнения использовалась проверка по критерию суммы рангов Уилкоксона. Для анализа изменения общей оценки данных каждого наблюдения в группах по сравнению с исходными данными использовалась парная проверка по критерию суммы рангов Уилкоксона.
Таблица 9
Изменение общей оценки стенокардии при каждом наблюдении
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
N (отсутствуют)
1743(16)
1721(25)
1497(3)
1447(9)
Mean (SD)
7,12(5,31)
7,21(5,20)
7,20(5,31)
7,43(5,25)
Min, Max
0,00,24,00
0,00,24,00
0,00,24,00
0,00,24,00
Md (Q3-Q1)
8,00(12,00)
8,00(9,00)
8,00(12,00)
8,00(7,00)
1 месяц после лечения
N (отсутствуют)
1744(15)
1725(21)
1489(11)
1447(9)
Mean (SD)
5,92(5,23)
5,96(5,11)
5,95(5,21)
6,06(5,17)
Min, Max
0,00,22,00
0,00,24,00
0,00,22,00
0,00,24,00
Md (Q3-Q1)
6,00(10,00)
6,00(10,00)
6,00(10,00)
6,00(10,00)
1 месяц после лечения - исходные данные
N (отсутствуют)
1743(16)
1721(25)
1488(12)
1443(13)
Mean (SD)
-1,19(3,66)
-1,24(3,86)
-1,22(3,64)
-1,36(3,82)
Min, Max
-20,00,16,00
-22,00, 16,00
-20,00,16,00
-22,00,16,00
Md (Q3-Q1)
0,00(2,00)
0,00(2,00)
0,00(2,00)
0,00(2,00)
Парная проверка по критерию
Стьюдента (Р)
-13,59(0,0000)
-13,33(0,0000)
-12,92(0,0000)
-13,57(0,0000)
3 месяца после лечения
N (отсутствуют)
1744(15)
1725(21)
1473(27)
1433(23)
Mean (SD)
5,38(5,04)
5,47(4,92)
5,32(4,99)
5,49(4,91)
Min, Max
0,00,22,00
0,00,24,00
0,00,22,00
0,00,24,00
Md(Q3-Ql)
6,00(9,00)
6,00(8,00)
6,00(9,00)
6,00(9,00)
3 месяца после лечения - исходные данные
N (отсутствуют)
1743(16)
1721(25)
1472(28)
1429(27)
Mean (SD)
-1,73(4,15)
-1,75(4,26)
-1,85(4,08)
-1,92(4,15)
Min, Max
-22,00,16,00
-22,00,15,00
-20,00,14,00
-22,00,14,00
Md (Q3-Q1)
0,00(4,00)
0,00(3,00)
0,00(4,00)
0,00(4,00)
Парная проверка по критерию
Стьюдента (Р)
-17,43(0,0000)
-17,04(0,0000)
-17,38(0,0000)
17,50(0,0000)
6 месяцев после лечения
N (отсутствуют)
1744(15)
1725(21)
1457(43)
1413(43)
Mean (SD)
4,78(4,84)
4,96(4,79)
4,54(4,68)
4,85(4,66)
Min, Max
0,00,24,00
0,00,22,00
0,00,24,00
0,00,22,00
Md (Q3-Q1)
5,00(8,00)
6,00(8,00)
5,00(8,00)
5,00(8,00)
6 месяцев после лечения - исходные данные
N (отсутствуют)
1743(16)
1721(25)
1456(44)
1409(47)
Mean (SD)
-2,34(4,40)
-2,26(4,63)
-2,58(4,34)
-2,56(4,45)
Min, Max
-24,00,14,00
-22,00,18,00
-24,00, 14,00
-22,00,18,00
Md(Q3-Ql)
0,00(5,00)
0,00(5,00)
-1,00(5,00)
-1,00(5,00)
Парная проверка по критерию
Стьюдента (Р)
-22,15(0,0000)
-20,29(0,0000)
22,67(0,0000)
21,57(0,0000)
9 месяцев после лечения
N (отсутствуют)
1744(15)
1725(21)
1443(57)
1383(73)
Mean (SD)
4,39(4,65)
4,52(4,61)
4,10(4,40)
4,24(4,36)
Min, Max
0,00,22,00
0,00,22,00
0,00,22,00
0,00,18,00
Md (Q3-Q1)
5,00(8,00)
5,00(8,00)
5,00(8,00)
5,00(8,00)
9 месяцев после лечения - исходные данные
N (отсутствуют)
1743(16)
1721(25)
1442(58)
1379(77)
Mean (SD)
-2,72(4,66)
-2,70(4,92)
-3,02(4,61)
-3,16(4,69)
Min, Max
-24,00,14,00
-24,00,18,00
-24,00,14,00
-24,00,18,00
Md(Q3-Ql)
-1,00(6,00)
-1,00(6,00)
-2,00(6,00)
-2,00(6,00)
Парная проверка по критерию
Стьюдента (Р)
-24,42(0,0000)
-22,76(0,0000)
-24,86(0,0000)
-25,04(0,0000)
12 месяцев после лечения
N (отсутствуют)
1744(15)
1725(21)
1432(68)
1373(83)
Mean (SD)
3,83(4,47)
4,03(4,42)
3,38(4,05)
3,63(4,04)
Min, Max
0,00,22,00
0,00, 22,00
0,00,18,00
0,00,20,00
Md (Q3-Q1)
0,00(7,00)
5,00(8,00)
0,00(6,00)
0,00(7,00)
12 месяцев после лечения - исходные данные
N (отсутствуют)
1743(16)
1721(25)
1431(69)
1369(87)
Mean (SD)
-3,28(4,82)
-3,19(5,05)
-3,71(4,72)
-3,79(4,71)
Min, Max
-24,00,16,00
-24,00,18,00
-24,00,16,00
-24,00,11,00
Md (Q3-Q1)
-2,00(6,00)
-2,00(6,00)
-3,00(6,00)
-3,00(6,00)
Парная проверка по критерию
Стьюдента (Р)
-28,43(0,0000)
-26,17(0,0000)
-29,75(0,0000)
-29,75(0,0000)
Последующее наблюдение
N (отсутствуют)
1443(316)
1385(361)
1408(92)
1349(107)
Mean (SD)
3,59(4,24)
3,67(4,11)
3,60(4,23)
3,68(4,10)
Min, Max
0,00,18,00
0,00,18,00
0,00,18,00
0,00,18,00
Md (Q3-Q1)
0,00(7,00)
0,00(7,00)
0,00(7,00)
0,00(7,00)
Последующее наблюдение - исходные данные
N (отсутствуют)
1443(316)
1381(365)
1408(92)
1345(111)
Mean (SD)
-3,49(4,97)
-3,74(4,93)
-3,51(4,98)
-3,73(4,90)
Min, Max
-24,00,14,00
-24,00,10,00
-24,00,14,00
-24,00,10,00
Md(Q3-Ql)
-2,00(6,00)
-2,00(7,00)
-2,00(6,00)
-2,00(7,00)
Парная проверка по критерию
Стьюдента (Р)
-26,63(0,0000)
-28,17(0,0000)
-26,42(0,0000)
-27,95(0,0000)
Таблица 10
Распределение общих оценок стенокардии при каждом наблюдении
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Легкая
1086 (62,34%)
1092 (63,45%)
917(61,26%)
880 (60,82%)
Средняя
608 (34,90%)
574 (33,35%)
539(36,01%)
516(35,66%)
Тяжелая
48 (2,76%)
55 (3,20%)
41 (2,74%)
51 (3,52%)
Итого
1742
1721
1497
1447
1 месяц после лечения
Легкая
1203 (70,19%)
1210(71,09%)
1030 (69,31%)
1013 (70,06%)
Средняя
484 (28,24%)
464 (27,26%)
434 (29,21%)
407(28,15%)
Тяжелая
27(1,58%)
28 (1,65%)
22 (1,48%)
26 (1,80%)
Итого
1714
1702
1486
1446
3 месяца после лечения
Легкая
1241 (74,94%)
1247 (75,81%)
1098 (74,54%)
1075 (75,02%)
Средняя
397 (23,97%)
386 (23,47%)
363 (24,64%)
348 (24,28%)
Тяжелая
18(1,09%)
12 (0,73%)
12(0,81%)
10(0,70%)
Итого
1656
1645
1473
1433
6 месяцев после лечения
Легкая
1273 (80,06%)
1252 (79,90%)
1172 (80,44%)
1125 (79,62%)
Средняя
309 (19,43%)
305 (19,46%)
278 (19,08%)
280 (19,82%)
Тяжелая
8 (0,50%)
10(0,64%)
7 (0,48%)
8 (0,57%)
Итого
1590
1567
1457
1413
9 месяцев после лечения
Легкая
1280 (83,77%)
1220 (83,05%)
1207 (83,65%)
1147 (82,94%)
Средняя
244(15,97%)
241(16,41%)
233(16,15%)
229(16,56%)
Тяжелая
4(0,26%)
8(0,54%)
3(0,21%)
7(0,51%)
Итого
1528
1469
1443
1383
12 месяцев после лечения
Легкая
1294(87,91%)
1217(86,31%)
1259(87,92%)
1184(86,23%)
Средняя
176(11,96%)
189(13,40%)
171(11,94%)
185(13,47%)
Тяжелая
2(0,14%)
4(0,28%)
2(0,14%)
4(0,29%)
Итого
1472
1410
1432
1373
Последующее наблюдение
Легкая
1243(86,14%)
1185(85,56%)
1215(86,29%)
1155(85,62%)
Средняя
199(13,79%)
199(14,37%)
192(13,64%)
193(14,31%)
Тяжелая
1(0,07%)
1(0,07%)
1(0,07%)
1(0,07%)
Итого
1443
1385
1408
1349
Таблица 11
Определение распределение общих оценок стенокардии при каждом наблюдении
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,55
0,5813
0,40
0,6864
I месяц после лечения
Проверка по критерию суммы рангов
-0,56
0,5775
-0,37
0,7102
3 месяца после лечения
Проверка по критерию суммы рангов
-0,63
0,5289
-0,31
0,7560
6 месяцев после лечения
Проверка по критерию суммы рангов
0,13
0,8934
0,56
0,5765
9 месяцев после лечения
Проверка по критерию суммы рангов
0,56
0,5743
0,54
0,5900
12 месяцев после лечения
Проверка по критерию суммы рангов
1,29
0,1968
1,34
0,1795
Последующее наблюдение
Проверка по критерию суммы рангов
0,44
0,6580
0,51
0,6109
Таблица 12
Изменение периодов приступов при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
480(27,54%)
444(25,80%)
404(26,99%)
358(24,74%)
1
158(9,06%)
166(9,65%)
134(8,95%)
133(9,19%)
2
928(53,24%)
958(55,67%)
801(53,51%)
819(56,60%)
4
159(9,12%)
133(7,73%)
143(9,55%)
119(8,22%)
6
18(1,03%)
20(1,16%)
15(1,00%)
18(1,24%)
Итого
1743
1721
1497
1447
1 месяц после лечения
0
638(36,58%)
606(35,13%)
541(36,33%)
501(34,62%)
1
187(10,72%)
205(11,88%)
165(11,08%)
170(11,75%)
2
812(46,56%)
835(48,41%)
698(46,88%)
704(48,65%)
4
105(6,02%)
71(4,12%)
83(5,57%)
65(4,49%)
6
2(0,11%)
8(0,46%)
2(0,13%)
7(0,48%)
Итого
1744
1725
1489
1447
1 месяц после лечения - исходные данные
-6
2(0,11%)
2(0,12%)
1(0,07%)
2(0,14%)
-5
0(0,00%)
1(0,06%)
0(0,00%)
1(0,07%)
-4
18(1,03%)
24(1,39%)
16(1,08%)
21(1,46%)
-3
6(0,34%)
6(0,35%)
6(0,40%)
4(0,28%)
-2
209(11,99%)
185(10,75%)
188(12,63%)
157(10,88%)
-1
124(7,11%)
150(8,72%)
105(7,06%)
128(8,87%)
0
1304(74,81%)
1277(74,20%)
1109(74,53%)
1076(74,57%)
1
36(2,07%)
31(1,80%)
29(1,95%)
25(1,73%)
2
41(2,35%)
43(2,50%)
31(2,08%)
28(1,94%)
3
2(0,11%)
2(0,12%)
2(0,13%)
1(0,07%)
4
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
Итого
1743
1721
1488
1443
Проверка по критерию
Уилкоксона (Р)
32430(0,0000)
-33041(0,0000)
-25398,5(0,0000)
24610,0(0,0000)
3 месяца после лечения
0
698(40,02%)
658(38,14%)
596(40,46%)
544(37,96%)
1
246(14,11%)
247(14,32%)
205(13,92%)
199(13,89%)
2
723(41,46%)
755(43,77%)
617(41,89%)
636(44,38%)
4
75(4,30%)
60(3,48%)
53(3,60%)
50(3,49%)
6
2(0,11%)
5(0,29%)
2(0,14%)
4(0,28%)
Итого
1744
1725
1473
1433
3 месяца после лечения - исходные данные
-6
4(0,23%)
2(0,12%)
2(0,14%)
2(0,14%)
-5
2(0,11%)
2(0,12%)
2(0,14%)
2(0,14%)
-4
25(1,43%)
26(1,51%)
23(1,56%)
20(1,40%)
-3
8(0,46%)
9(0,52%)
8(0,54%)
8(0,56%)
-2
275(15,78%)
245(14,24%)
243(16,51%)
210(14,70%)
-1
191(10,96%)
208(12,09%)
165(11,21%)
171(11,97%)
0
1142(65,52%)
1143(66,41%)
959(65,15%)
959(67,11%)
1
54(3,10%)
41(2,38%)
41(2,79%)
28(1,96%)
2
39(2,24%)
41(2,38%)
27(1,83%)
26(1,82%)
3
0(0,00%)
1(0,06%)
4
3(0,17%)
3(0,17%)
2(0,14%)
3(0,21%)
Итого
1743
1721
1472
1429
Проверка по критерию
Уилкоксона (Р)
-66367(0,0000)
-60228(0,0000)
-51462,5(0,0000)
-42922,5(0,0000)
6 месяцев после лечения
0
777(44,55%)
726(42,09%)
670(45,98%)
596(42,18%)
1
271(15,54%)
314(18,20%)
232(15,92%)
267(18,90%)
2
642(36,81%)
643(37,28%)
527(36,17%)
523(37,01%)
4
53(3,04%)
40(2,32%)
27(1,85%)
27(1,91%)
6
1(0,06%)
2(0,12%)
1(0,07%)
0(0,00%)
Итого
1744
1725
1457
1413
6 месяцев после лечения - исходные данные
-6
6(0,34%)
4(0,23%)
4(0,27%)
3(0,21%)
-5
0(0,00%)
3(0,17%)
0(0,00%)
3(0,21%)
-4
31(1,78%)
33(1,92%)
28(1,92%)
26(1,85%)
-3
16(0,92%)
13(0,76%)
16(1,10%)
11(0,78%)
-2
326(18,70%)
293(17,02%)
290(19,92%)
250(17,74%)
-1
265(15,20%)
301(17,49%)
234(16,07%)
261(18,52%)
0
1010(57,95%)
992(57,64%)
827(56,80%)
803(56,99%)
1
43(2,47%)
39(2,27%)
28(1,92%)
27(1,92%)
2
43(2,47%)
40(2,32%)
27(1,85%)
25(1,77%)
3
1(0,06%)
1(0,06%)
4
2(0,11%)
2(0,12%)
2(0,14%)
0(0,00%)
Итого
1743
1721
1456
1409
Проверка по критерию
Уилкоксона (Р)
-105ЕЗ(0,0000)
-104ЕЗ(0,0000)
-82797,5(0,0000)
7409,0(0,0000)
9 месяцев после лечения
0
825(47,31%)
777(45,04%)
708(49,06%)
641(46,35%)
1
354(20,30%)
392(22,72%)
312(21,62%)
345(24,95%)
2
527(30,22%)
529(30,67%)
409(28,34%)
384(27,77%)
4
36(2,06%)
25(1,45%)
12(0,83%)
13(0,94%)
6
2(0,11%)
2(0,12%)
2(0,14%)
0(0,00%)
Итого
1744
1725
1443
1383
9 месяцев после лечения - исходные данные
-6
7(0,40%)
7(0,41%)
5(0,35%)
5(0,36%)
-5
0(0,00%)
2(0,12%)
0(0,00%)
2(0,15%)
-4
43(2,47%)
40(2,32%)
39(2,70%)
33(2,39%)
-3
15(0,86%)
15(0,87%)
15(1,04%)
13(0,94%)
-2
359(20,60%)
331(19,23%)
321(22,26%)
281(20,38%)
-1
352(20,20%)
390(22,66%)
316(21,91%)
348(25,24%)
0
877(50,32%)
853(49,56%)
687(47,64%)
650(47,14%)
1
52(2,98%)
38(2,21%)
35(2,43%)
26(1,89%)
2
35(2,01%)
42(2,44%)
22(1,53%)
21(1,52%)
3
1(0,06%)
1(0,06%)
4
1(0,06%)
2(0,12%)
1(0,07%)
0(0,00%)
6
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
Итого
1743
1721
1442
1379
Проверка по критерию
Уилкоксона (Р)
-154ЕЗ(0,0000)
-152ЕЗ(0,0000)
-123547(0,0000)
-117132(0,0000)
12 месяцев после лечения
0
909 (52,12%)
850 (49,28%)
788 (55,03%)
706 (51,42%)
1
384 (22,02%)
425 (24,64%)
342 (23,88%)
378 (27,53%)
2
417(23,91%)
426 (24,70%)
294 (20,53%)
279 (20,32%)
4
33 (1,89%)
22 (1,28%)
8 (0,56%)
10(0,73%)
6
1 (0,06%)
2 (0,12%)
Итого
1744
1725
1432
1373
12 месяцев после лечения - исходные данные
-6
7 (0,40%)
8(0,46%)
5 (0,35%)
6 (0,44%)
-5
1 (0,06%)
3(0,17%)
1 (0,07%)
3 (0,22%)
-4
55 (3,16%)
45(2,61%)
51(3,56%)
36 (2,63%)
-3
15 (0,86%)
20(1,16%)
15(1,05%)
18(1,31%)
-2
401(23,01%)
364(21,15%)
358(25,02%)
312(22,79%)
-1
399(22,89%)
445(25,86%)
364(25,44%)
401(29,29%)
0
795 (45,61%)
765(44,45%)
599(41,86%)
561(40,98%)
1
36 (2,07%)
30(1,74%)
19 (1,33%)
17 (1,24%)
2
30 (1,72%)
38 (2,21%)
17 (1,19%)
15(1,10%)
3
1 (0,06%)
1 (0,06%)
4
3 (0,17%)
2(0,12%)
2(0,14%)
0 (0,00%)
Итого
1743
1721
1431
1369
Проверка по критерию
Уилкоксона (Р)
-194ЕЗ(0,0000)
-193ЕЗ(0,0000)
-158309(0,0000)
-151127(0,0000)
Последующее наблюдение
0
774(53,64%)
716(51,70%)
753(53,48%)
693(51,37%)
1
329(22,80%)
385(27,80%)
322(22,87%)
378(28,02%)
2
331(22,94%)
281(20,29%)
324(23,01%)
275(20,39%)
4
9(0,62%)
3(0,22%)
9(0,64%)
3(0,22%)
Итого
1443
1385
1408
1349
Последующее наблюдение исходные данные
-6
6(0,42%)
4(0,29%)
6(0,43%)
4(0,30%)
-5
3(0,21%)
5(0,36%)
3(0,21%)
5(0,37%)
-4
52(3,60%)
44(3,19%)
52(3,69%)
42(3,12%)
-3
29(2,01%)
30(2,17%)
29(2,06%)
29(2,16%)
-2
328(22,73%)
312(22,59%)
322(22,87%)
304(22,60%)
-1
325(22,52%)
372(26,94%)
316(22,44%)
365(27,14%)
0
645(44,70%)
572(41,42%)
626(44,46%)
557(41,41%)
1
28(1,94%)
25(1,81%)
28(1,99%)
23(1,71%)
2
25(1,73%)
17(1,23%)
24(1,70%)
16(1,19%)
4
2(0,14%)
0(0,00%)
2(0,14%)
0(0,00%)
Итого
1443
1381
1408
1345
Проверка по критерию
Уилкоксона (Р)
-14Е4(0,0000)
-149ЕЗ(0,0000)
-134334(0,0000)
-142184(0,0000)
Таблица 13
Определение изменения периодов приступов при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,33
0,7424
0,73
0,4660
1 месяц после лечения
Проверка по критерию суммы рангов
0,03
0,9749
0,54
0,5918
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
-0,45
0,6511
-0,34
0,7340
3 месяца после лечения
Проверка по критерию суммы рангов
0,91
0,3633
1,41
0,1592
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
0,22
0,8279
0,53
0,5932
6 месяцев после лечения
Проверка по критерию суммы рангов
0,61
0,5400
1,39
0,1638
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,08
0,9345
0,39
0,6981
9 месяцев после лечения
Проверка по критерию суммы рангов
0,68
0,4935
0,80
0,4246
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,20
0,8389
-0,09
0,9306
12 месяцев после лечения
Проверка по критерию суммы рангов
1,15
0,2498
1,45
0,1478
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,14
0,8926
0,25
0,7996
Последующее наблюдение
Проверка по критерию суммы рангов
-0,00
0,9960
0,06
0,9541
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
-1,39
0,1632
-1,28
0,2008
Таблица 14
Изменение длительности при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
480(27,54%)
446(25,92%)
404(26,99%)
359(24,81%)
2
798(45,78%)
834(48,46%)
687(45,89%)
681(47,06%)
4
382(21,92%)
371(21,56%)
343(22,91%)
343(23,70%)
6
83(4,76%)
70(4,07%)
63(4,21%)
64(4,42%)
Итого
1743
1721
1497
1447
1 месяц после лечения
0
638(36,58%)
605(35,07%)
541(36,33%)
500(34,55%)
2
735(42,14%)
779(45,16%)
624(41,91%)
639(44,16%)
4 '
339(19,44%)
312(18,09%)
297(19,95%)
283(19,56%)
6
32(1,83%)
29(1,68%)
27(1,81%)
25(1,73%)
Итого
1744
1725
1489
1447
1 месяц после лечения - исходные данные
-6
19(1,09%)
28(1,63%)
13(0,87%)
27(1,87%)
-4
39(2,24%)
44(2,56%)
34(2,28%)
42(2,91%)
-2
269(15,43%)
230(13,36%)
227(15,26%)
186(12,89%)
0
1329(76,25%)
1332(77,40%)
1141(76,68%)
1124(77,89%)
2
75(4,30%)
72(4,18%)
64(4,30%)
55(3,81%)
4
10(0,57%)
13(0,76%)
8(0,54%)
8(0,55%)
6
2(0,11%)
2(0,12%)
1(0,07%)
1(0,07%)
Итого
1743
1721
1488
1443
Проверка по критерию
Уилкоксона (Р)
-25517(0,0000)
-21968(0,0000)
-18004,5(0,0000)
-16427,5(0,0000)
3 месяца после лечения
0
697(39,97%)
657(38,09%)
595(40,39%)
543(37,89%)
2
729(41,80%)
774(44,87%)
606(41,14%)
636(44,38%)
4
297(17,03%)
274(15,88%)
257(17,45%)
243(16,96%)
6
21(1,20%)
20(1,16%)
15(1,02%)
11(0,77%)
Итого
1744
1725
1473
1433
3 месяца после лечения - исходные данные
-6
26(1,49%)
31(1,80%)
18(1,22%)
28(1,96%)
-4
53(3,04%)
65(3,78%)
43(2,92%)
59(4,13%)
-2
357(20,48%)
303(17,61%)
315(21,40%)
254(17,77%)
0
1207(69,25%)
1223(71,06%)
1018(69,16%)
1021(71,45%)
2
87(4,99%)
84(4,88%)
69(4,69%)
62(4,34%)
4
11(0,63%)
11(0,64%)
8(0,54%)
4(0,28%)
6
2(0,11%)
4(0,23%)
1(0,07%)
1(0,07%)
Итого
1743
1721
1472
1429
Проверка по критерию
Уилкоксона (Р)
-46314(0,0000)
-39225(0,0000)
-34635,0(0,0000)
-30105,0(0,0000)
6 месяцев после лечения
0
777(44,55%)
726(42,09%)
670(45,98%)
596(42,18%)
2
710(40,71%)
741(42,96%)
588(40,36%)
609(43,10%)
4
245(14,05%)
245(14,20%)
193(13,25%)
202(14,30%)
6
12(0,69%)
13(0,75%)
6(0,41%)
6(0,42%)
Итого
1744
1725
1457
1413
6 месяцев после лечения - исходные данные
-6
27(1,55%)
32(1,86%)
21(1,44%)
29(2,06%)
-4
77(4,42%)
73(4,24%)
66(4,53%)
63(4,47%)
-2
427(24,50%)
396(23,01%)
378(25,96%)
343(24,34%)
0
1129(64,77%)
1125(65,37%)
936(64,29%)
914(64,87%)
2
79(4,53%)
75(4,36%)
53(3,64%)
52(3,69%)
4
4(0,23%)
17(0,99%)
2(0,14%)
7(0,50%)
6
0(0,00%)
3(0,17%)
0(0,00%)
1(0,07%)
Итого
1743
1721
1456
1409
Проверка по критерию
Уилкоксона (Р)
-72188(0,0000)
-60736(0,0000)
-55351,0(0,0000)
-47590,0(0,0000)
9 месяцев после лечения
0
825(47,31%)
778(45,10%)
708(49,06%)
642(46,42%)
2
701(40,19%)
762(44,17%)
574(39,78%)
613(44,32%)
4
205(11,75%)
168(9,74%)
155(10,74%)
120(8,68%)
6
13(0,75%)
17(0,99%)
6(0,42%)
8(0,58%)
Итого
1744
1725
1443
1383
9 месяцев после лечения - исходные данные
-6
34(1,95%)
32(1,86%)
27(1,87%)
28(2,03%)
-4
86(4,93%)
100(5,81%)
73(5,06%)
88(6,38%)
-2
485(27,83%)
464(26,96%)
430(29,82%)
408(29,59%)
0
1050(60,24%)
1031(59,91%)
852(59,08%)
803(58,23%)
2
79(4,53%)
73(4,24%)
53(3,68%)
46(3,34%)
4
8(0,46%)
16(0,93%)
6(0,42%)
5(0,36%)
6
1(0,06%)
5(0,29%)
1(0,07%)
1(0,07%)
Итого
1743
1721
1442
1379
Проверка по критерию
Уилкоксона (Р)
-92350(0,0000)
-86673(0,0000)
-70632,0(0,0000)
-69556,0(0,0000)
12 месяцев после лечения
0
909 (52,12%)
851(49,33%)
788(55,03%)
707(51,49%)
2
683 (39,16%)
764(44,29%)
553(38,62%)
615(44,79%)
4
140 (8,03%)
95(5,51%)
87(6,08%)
47(3,42%)
6
12 (0,69%)
15(0,87%)
4(0,28%)
4(0,29%)
Итого
1744
1725
1432
1373
12 месяцев после лечения - исходные данные
-6
38(2,18%)
37(2,15%)
31(2,17%)
33 (2,41%)
-4
111 (6,37%)
118(6,86%)
98 (6,85%)
106 (7,74%)
-2
552(31,67%)
552(32,07%)
492(34,38%)
489(35,72%)
0
975(55,94%)
930(54,04%)
774(54,09%)
703(51,35%)
2
61(3,50%)
63(3,66%)
33(2,31%)
35(2,56%)
4
3(0,17%)
16(0,93%)
0(0,00%)
3(0,22%)
6
3(0,17%)
5(0,29%)
3(0,21%)
0(0,00%)
Итого
1743
1721
1431
1369
Проверка по критерию
Уилкоксона (Р)
-125ЕЗ(0,0000)
-122ЕЗ(0,0000)
-97476,0(0,0000)
-100131(0,0000)
Последующее наблюдение
0
774(53,64%)
716(51,70%)
753(53,48%)
693(51,37%)
2
522(36,17%)
544(39,28%)
512(36,36%)
533(39,51%)
4
144(9,98%)
122(8,81%)
141(10,01%)
120(8,90%)
6
3(0,21%)
3(0,22%)
2(0,14%)
3(0,22%)
Итого
1443
1385
1408
1349
Последующее наблюдение - исходные данные
-6
27(1,87%)
34(2,46%)
27(1,92%)
32(2,38%)
-4
106(7,35%)
112(8,11%)
103(7,32%)
110(8,18%)
-2
441(30,56%)
417(30,20%)
428(30,40%)
404(30,04%)
0
812(56,27%)
773(55,97%)
795(56,46%)
757(56,28%)
2
50(3,47%)
41(2,97%)
49(3,48%)
38(2,83%)
4
5(0,35%)
4(0,29%)
4(0,28%)
4(0,30%)
6
2(0,14%)
0(0,00%)
2(0,14%)
0(0,00%)
Итого
1443
1381
1408
1345
Проверка по критерию
Уилкоксона (Р)
-83429(0,0000)
-81093(0,0000)
-79062,5(0,0000)
-76168,0(0,0000)
Таблица 15
Определение длительности при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,16
0,8730
1,18
0,2390
1 месяц после лечения
Проверка по критерию суммы рангов
0,13
0,8998
0,54
0,5866
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
0,69
0,4881
-0,01
0,9929
3 месяца после лечения
Проверка по критерию суммы рангов
0,46
0,6480
0,79
0,4318
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
0,89
0,3749
0,32
0,747
6 месяцев после лечения
Проверка по критерию суммы рангов
1,24
0,2148
1,95
0,0508
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
1,04
0,2981
0,60
0,5475
9 месяцев после лечения
Проверка по критерию суммы рангов
0,58
0,5609
0,72
0,4739
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,07
0,9429
-0,98
0,3254
12 месяцев после лечения
Проверка по критерию суммы рангов
0,83
0,4050
1,11
0,2675
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,16
0,8740
-1,29
0,1967
Последующее наблюдение
Проверка по критерию суммы рангов
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
0,62
0,5338
0,72
0,4703
-0,95
0,3401
-0,95
0,3441
Таблица 16
Изменение боли при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
480(27,54%)
446(25,92%)
404(26,99%)
359(24,81%)
2
672(38,55%)
693(40,27%)
566(37,81%)
561(38,77%)
4
561(32,19%)
544(31,61%)
501(33,47%)
495(34,21%)
6
30(1,72%)
38(2,21%)
26(1,74%)
32(2,21%)
Итого
1743
1721
1497
1447
1 месяц после лечения
0
637(36,53%)
604(35,01%)
540(36,29%)
499(34,51%)
2
640(36,70%)
652(37,80%)
536(36,02%)
533(36,86%)
4
451(25,86%)
458(26,55%)
400(26,88%)
405(28,01%)
6
16(0,92%)
11(0,64%)
12(0,81%)
9(0,62%)
Итого
1744
1725
1488
1446
1 месяц после лечения - исходные данные
-6
7 (0,40%)
12 (0,70%)
6 (0,40%)
10(0,69%)
-4
70 (4,02%)
63 (3,66%)
61 (4,10%)
56 (3,88%)
-2
231(13,25%)
252(14,64%)
198(13,32%)
213(14,77%)
0
1353(77,62%)
1295(75,25%)
1155(77,67%)
1092(75,73%)
2
67(3,84%)
80(4,65%)
55(3,70%)
60(4,16%)
4
15(0,86%)
19(1,10%)
12(0,81%)
11(0,76%)
Итого
1743
1721
1487
1442
Проверка по критерию
Уилкоксона(Р)
-22991(0,0000)
-25059(0,0000)
-17174,0(0,0000)
-19115,5(0,0000)
3 месяца после лечения
0
697(39,97%)
657(38,09%)
595(40,39%)
543(37,89%)
2
635(36,41%)
665(38,55%)
522(35,44%)
548(38,24%)
4
402(23,05%)
392(22,72%)
349(23,69%)
335(23,38%)
6
10(0,57%)
11(0,64%)
7(0,48%)
7(0,49%)
Итого
1744
1725
1473
1433
3 месяца после лечения - исходные данные
-6
8(0,46%)
9(0,52%)
7(0,48%)
7(0,49%)
-4
89(5,11%)
102(5,93%)
77(5,23%)
89(6,23%)
-2
333(19,10%)
312(18,13%)
287(19,50%)
268(18,75%)
0
1213(69,59%)
1197(69,55%)
1026(69,70%)
999(69,91%)
2
81(4,65%)
77(4,47%)
63(4,28%)
53(3,71%)
4
19(1,09%)
23(1,34%)
12(0,82%)
13(0,91%)
6
0(0,00%)
1(0,06%)
Итого
1743
1721
1472
1429
Проверка по критерию
Уилкоксона (Р)
-44649(0,0000)
-42845(0,0000)
-34044,0(0,0000)
-32957,0(0,0000)
6 месяцев после лечения
0
780(44,72%)
726(42,09%)
671(46,09%)
596(42,18%)
2
616(35,32%)
655(37,97%)
506(34,75%)
543(38,43%)
4
340(19,50%)
333(19,30%)
274(18,82%)
269(19,04%)
6
8(0,46%)
11(0,64%)
5(0,34%)
5(0,35%)
Итого
1744
1725
1456
1413
6 месяцев после лечения - исходные данные
-6
10(0,57%)
14(0,81%)
9(0,62%)
11(0,78%)
-4
120(6,88%)
115(6,68%)
107(7,35%)
101(7,17%)
-2
403(23,12%)
405(23,53%)
352(24,19%)
348(24,70%)
0
1114(63,91%)
1081(62,81%)
923(63,44%)
887(62,95%)
2
83(4,76%)
82(4,76%)
58(3,99%)
53(3,76%)
4
13(0,75%)
23(1,34%)
6(0,41%)
8(0,57%)
6
0(0,00%)
1(0,06%)
0(0,00%)
1(0,07%)
Итого
1743
1721
1455
1409
Проверка по критерию
Уилкоксона (Р)
-71668(0,0000)
-69120(0,0000)
-56168,0(0,0000)
-53434,0(0,0000)
9 месяцев после лечения
0
825(47,31%)
777(45,04%)
707(49,03%)
640(46,34%)
2
617(35,38%)
641(37,16%)
501(34,74%)
514(37,22%)
4
293(16,80%)
293(16,99%)
230(15,95%)
223(16,15%)
6
9(0,52%)
14(0,81%)
4(0,28%)
4(0,29%)
Итого
1744
1725
1442
1381
9 месяцев после лечения - исходные данные
-6
11(0,63%)
15(0,87%)
10(0,69%)
12(0,87%)
-4
143(8,20%)
145(8,43%)
127(8,81%)
129(9,37%)
-2
450(25,82%)
430(24,99%)
396(27,48%)
365(26,51%)
0
1039(59,61%)
1026(59,62%)
840(58,29%)
815(59,19%)
2
85(4,88%)
78(4,53%)
59(4,09%)
49(3,56%)
4
15(0,86%)
23(1,34%)
9(0,62%)
6(0,44%)
6
0(0,00%)
4(0,23%)
0(0,00%)
1(0,07%)
Итого
1743
1721
1441
1377
Проверка по критерию
Уилкоксона (Р)
-92083(0,0000)
-84708(0,0000)
-72287,0(0,0000)
-65486,0(0,0000)
12 месяцев после лечения
0
910(52,18%)
850(49,28%)
788(55,07%)
706(51,42%)
2
589(33,77%)
606(35,13%)
469(32,77%)
481(35,03%)
4
237(13,59%)
254(14,72%)
173(12,09%)
183(13,33%)
6
8(0,46%)
15(0,87%)
1(0,07%)
3(0,22%)
Итого
1744
1725
1431
1373
12 месяцев после лечения - исходные данные
-6
12(0,69%)
16(0,93%)
10(0,70%)
13(0,95%)
-4
182(10,44%)
170(9,88%)
165(11,54%)
153(11,18%)
-2
489(28,06%)
471(27,37%)
433(30,28%)
403(29,44%)
0
976(56,00%)
972(56,48%)
774(54,13%)
761(55,59%)
2
76(4,36%)
68(3,95%)
46(3,22%)
37(2,70%)
4
8(0,46%)
19(1,10%)
2(0,14%)
1(0,07%)
6
0(0,00%)
5(0,29%)
0(0,00%)
1(0,07%)
Итого
1743
1721
1430
1369
Проверка по критерию
Уилкоксона (Р)
-12Е4(0,0000)
-106ЕЗ(0,0000)
-95582,0(0,0000)
-83290,5(0,0000)
Последующее наблюдение
0
774(53,64%)
716(51,70%)
753(53,48%)
693(51,37%)
2
477(33,06%)
472(34,08%)
469(33,31%)
465(34,47%)
4
190(13,17%)
196(14,15%)
185(13,14%)
190(14,08%)
6
2(0,14%)
1(0,07%)
1(0,07%)
1(0,07%)
Итого
1443
1385
1408
1349
Последующее наблюдение - исходные данные
-6
12(0,83%)
13(0,94%)
12(0,85%)
12(0,89%)
-4
165(11,43%)
162(11,73%)
162(11,51%)
158(11,75%)
-2
418(28,97%)
405(29,33%)
409(29,05%)
394(29,29%)
0
783(54,26%)
748(54,16%)
762(54,12%)
732(54,42%)
2
53(3,67%)
40(2,90%)
53(3,76%)
37(2,75%)
4
11(0,76%)
13(0,94%)
9(0,64%)
12(0,89%)
6
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
Итого
1443
1381
1408
1345
Проверка по критерию
Уилкоксона (Р)
-89749(0,0000)
-84482(0,0000)
-86649,0(0,0000)
-79905,5(0,0000)
Таблица 17
Определение изменения боли при различных наблюдениях
Данные
Метод испытаний
EAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,64
0,5250
1,22
0,2229
1 месяц после лечения
Проверка по критерию суммы рангов
0,70
0,4848
0,91
0,3621
1 месяц после лечения - Исходные данные
Проверка по критерию суммы рангов
-0,24
0,8121
-0,68
0,4946
3 месяца после лечения
Проверка по критерию суммы рангов
0,71
0,4806
0,86
0,3910
3 месяца после лечения - Исходные данные
Проверка по критерию суммы рангов
-0,01
0,9895
-0,48
0,6285
6 месяцев после лечения
Проверка по критерию суммы рангов
1,18
0,2396
1,64
0,1004
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,04
0,9698
-0,23
0,8215
9 месяцев после лечения
Проверка по критерию суммы рангов
1,20
0,2293
1,18
0,2368
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,24
0,8095
-0,25
0,7995
12 месяцев после лечения
Проверка по критерию суммы рангов
1,84
0,0652
1,96
0,0500
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,75
0,4553
0,27
0,7867
Последующее наблюдение
Проверка по критерию суммы рангов
1,07
0,2840
1,14
0,2527
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
-0,61
0,5420
-0,52
0,6037
Таблица 18
Изменение дозы нитроглицерина при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
927(53,40%)
881(51,25%)
792(53,05%)
733(50,73%)
1
1(0,06%)
1(0,06%)
1(0,07%)
1(0,07%)
2
562(32,37%)
590(34,32%)
482(32,28%)
495(34,26%)
4
172(9,91%)
175(10,18%)
155(10,38%)
153(10,59%)
6
74(4,26%)
72(4,19%)
63(4,22%)
63(4,36%)
Итого
1736
1719
1493
1445
1 месяц после лечения
0
1039(59,78%)
1000(58,00%)
884(59,61%)
840(58,17%)
1
5(0,29%)
2(0,12%)
4(0,27%)
1(0,07%)
2
503(28,94%)
548(31,79%)
436(29,40%)
456(31,58%)
4
133(7,65%)
122(7,08%)
111(7,48%)
103(7,13%)
6
58(3,34%)
52(3,02%)
48(3,24%)
44(3,05%)
Итого
1738
1724
1483
1444
1 месяц после лечения - исходные данные
-6
9(0,52%)
17(0,99%)
8(0,54%)
16(1,11%)
-4
37(2,13%)
42(2,44%)
34(2,29%)
35(2,43%)
-2
198(11,41%)
198(11,52%)
171(11,54%)
164(11,40%)
-3
1(0,06%)
0(0,00%)
0
1398(80,53%)
1361(79,17%)
1191(80,36%)
1155(80,26%)
-1
0(0,00%)
1(0,06%)
1
3(0,17%)
0(0,00%)
3(0,20%)
0(0,00%)
2
68(3,92%)
82(4,77%)
56(3,78%)
55(3,82%)
4
18(1,04%)
13(0,76%)
15(1,01%)
11(0,76%)
6
4(0,23%)
5(0,29%)
4(0,27%)
3(0,21%)
Итого
1736
1719
1482
1439
Проверка по критерию
Уилкоксона (Р)
-12666(0,0000)
-14773(0,0000)
-9718,00(0,0000)
-10692,5(0,0000)
3 месяца после лечения
0
1079(61,98%)
1044(60,52%)
926(62,95%)
863(60,43%)
1
11(0,63%)
10(0,58%)
11(0,75%)
10(0,70%)
2
515(29,58%)
550(31,88%)
428(29,10%)
457(32,00%)
4
91(5,23%)
81(4,70%)
73(4,96%)
67(4,69%)
6
45(2,58%)
40(2,32%)
33(2,24%)
31(2,17%)
Итого
1741
1725
1471
1428
3 месяца после лечения - исходные данные
-6
12(0,69%)
17(0,99%)
10(0,68%)
16(1,13%)
-5
2(0,12%)
0(0,00%)
2(0,14%)
0(0,00%)
-4
51(2,94%)
61(3,55%)
46(3,14%)
50(3,52%)
-2
263(15,15%)
268(15,59%)
232(15,81%)
223(15,68%)
-1
5(0,29%)
8(0,47%)
5(0,34%)
8(0,56%)
0
1306(75,23%)
1268(73,76%)
1101(75,05%)
1057(74,33%)
1
3(0,17%)
1(0,06%)
3(0,20%)
1(0,07%)
2
77(4,44%)
80(4,65%)
55(3,75%)
54(3,80%)
4
12(0,69%)
11(0,64%)
8(0,55%)
9(0,63%)
6
5(0,29%)
5(0,29%)
5(0,34%)
4(0,28%)
Итого
1736
1719
1467
1422
Проверка по критерию
Уилкоксона (Р)
-25905(0,0000)
-29747(0,0000)
-20832,0(0,0000)
-21134,5(0,0000)
6 месяцев после лечения
0
1139(65,38%)
1091(63,25%)
976(67,13%)
901(64,04%)
1
15(0,86%)
32(1,86%)
15(1,03%)
32(2,27%)
2
492(28,24%)
499(28,93%)
405(27,85%)
406(28,86%)
4
63(3,62%)
60(3,48%)
40(2,75%)
37(2,63%)
6
33(1,89%)
43(2,49%)
18(1,24%)
31(2,20%)
Итого
1742
1725
1454
1407
6 месяцев после лечения - исходные данные
-6
18(1,04%)
22(1,28%)
15(1,03%)
20(1,43%)
-5
3(0,17%)
1(0,06%)
3(0,21%)
1(0,07%)
-4
70(4,03%)
77(4,48%)
64(4,41%)
66(4,71%)
-3
0(0,00%)
2(0,12%)
0(0,00%)
2(0,14%)
-2
321(18,49%)
311(18,09%)
282(19,43%)
260(18,54%)
-1
4(0,23%)
17(0,99%)
4(0,28%)
17(1,21%)
0
1216(70,05%)
1176(68,41%)
1008(69,47%)
963(68,69%)
1
7(0,40%)
11(0,64%)
7(0,48%)
11(0,78%)
2
84(4,84%)
73(4,25%)
60(4,14%)
43(3,07%)
4
7(0,40%)
21(1,22%)
4(0,28%)
15(1,07%)
6
6(0,35%)
8(0,47%)
4(0,28%)
4(0,29%)
Итого
1736
1719
1451
1402
Проверка по критерию
Уилкоксона (Р)
-43476(0,0000)
-43631(0,0000)
-34895,0(0,0000)
-33070,5(0,0000)
9 месяцев после лечения
0
1169(67,11%)
1143(66,26%)
993(68,96%)
940(68,31%)
1
18(1,03%)
26(1,51%)
18(1,25%)
24(1,74%)
2
483(27,73%)
467(27,07%)
395(27,43%)
362(26,31%)
4
42(2,41%)
50(2,90%)
20(1,39%)
26(1,89%)
6
30(1,72%)
39(2,26%)
14(0,97%)
24(1,74%)
Итого
1742
1725
1440
1376
9 месяцев после лечения - исходные данные
-6
24(1,38%)
26(1,51%)
20(1,39%)
24(1,75%)
-5
3(0,17%)
1(0,06%)
3(0,21%)
1(0,07%)
-4
74(4,26%)
90(5,24%)
67(4,67%)
78(5,69%)
-3
2(0,12%)
2(0,12%)
2(0,14%)
2(0,15%)
-2
350(20,16%)
340(19,78%)
307(21,38%)
284(20,71%)
-1
8(0,46%)
16(0,93%)
8(0,56%)
15(1,09%)
0
1171(67,45%)
1127(65,56%)
955(66,50%)
898(65,50%)
1
6(0,35%)
8(0,47%)
6(0,42%)
7(0,51%)
2
84(4,84%)
87(5,06%)
60(4,18%)
52(3,79%)
4
8(0,46%)
13(0,76%)
4(0,28%)
5(0,36%)
6
6(0,35%)
9(0,52%)
4(0,28%)
5(0,36%)
Итого
1736
1719
1436
1371
Проверка по критерию
Уилкоксона (Р)
-53222(0,0000)
-55218(0,0000)
-42481,5(0,0000)
-41759,0(0,0000)
12 месяцев после лечения
0
1247(71,58%)
1200(69,57%)
1069(74,81%)
989(72,30%)
1
19(1,09%)
19(1,10%)
19(1,33%)
19(1,39%)
2
411(23,59%)
427(24,75%)
317(22,18%)
321(23,46%)
4
36(2,07%)
47(2,72%)
13(0,91%)
21(1,54%)
6
29(1,66%)
32(1,86%)
11(0,77%)
18(1,32%)
Итого
1742
1725
1429
1368
12 месяцев после лечения - исходные данные
-6
32(1,84%)
31(1,80%)
27(1,89%)
28(2,05%)
-5
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
-4
86(4,95%)
97(5,64%)
78(5,47%)
83(6,09%)
-3
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
-2
378(21,77%)
382(22,22%)
333(23,37%)
323(23,70%)
-1
9(0,52%)
13(0,76%)
9(0,63%)
13(0,95%)
0
1138(65,55%)
1084(63,06%)
921(64,63%)
855(62,73%)
1
9(0,52%)
5(0,29%)
9(0,63%)
5(0,37%)
2
69(3,97%)
85(4,94%)
41(2,88%)
49(3,60%)
4
7(0,40%)
16(0,93%)
1(0,07%)
5(0,37%)
6
6(0,35%)
6(0,35%)
4(0,28%)
2(0,15%)
Итого
1736
1719
1425
1363
Проверка по критерию
Уилкоксона (Р)
-65699(0,0000)
-67124(0,0000)
-52730,0(0,0000)
-51415,5(0,0000)
Последующее наблюдение
0
1069(74,24%)
1017(73,80%)
1044(74,31%)
989(73,70%)
1
13(0,90%)
16(1,16%)
13(0,93%)
16(1,19%)
2
334(23,19%)
316(22,93%)
325(23,13%)
309(23,03%)
4
15(1,04%)
16(1,16%)
14(1,00%)
16(1,19%)
6
9(0,63%)
13(0,94%)
9(0,64%)
12(0,89%)
Итого
1440
1378
1405
1342
Последующее наблюдение - исходные данные
-6
27(1,88%)
31(2,26%)
26(1,86%)
30(2,24%)
-5
2(0,14%)
3(0,22%)
2(0,14%)
3(0,22%)
-4
92(6,41%)
95(6,92%)
90(6,42%)
91(6,81%)
-3
2(0,14%)
1(0,07%)
2(0,14%)
1(0,07%)
-2
313(21,81%)
334(24,33%)
309(22,06%)
322(24,08%)
-1
6 (0,42%)
6(0,44%)
6(0,43%)
6(0,45%)
0
924(64,39%)
832(60,60%)
899(64,17%)
815(60,96%)
1
4(0,28%)
5(0,36%)
4(0,29%)
5(0,37%)
2
58(4,04%)
61(4,44%)
56(4,00%)
60(4,49%)
4
4(0,28%)
3(0,22%)
4(0,29%)
2(0,15%)
6
3(0,21%)
2(0,15%)
3(0,21%)
2(0,15%)
Итого
1435
1373
1401
1337
Проверка по критерию
Уилкоксона (Р)
-50803(0,0000)
-58107(0,0000)
-49134,5(0,0000)
-54176,5(0,0000)
Таблица 19
Определение изменения дозы нитроглицерина при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
1,08
0,2806
1,11
0,2656
1 месяц после лечения
Проверка по критерию суммы рангов
0,74
0,4590
0,60
0,5469
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
-0,39
0,6930
-0,70
0,4825
3 месяца после лечения
Проверка по критерию суммы рангов
0,63
0,5274
1,22
0,2225
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
-0,91
0,3643
-0,53
0,5993
6 месяцев после лечения
Проверка по критерию суммы рангов
1,17
0,2433
1,63
0,1030
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,30
0,7667
-0,34
0,7302
9 месяцев после лечения
Проверка по критерию суммы рангов
0,63
0,5312
0,50
0,6178
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,30
0,7663
-0,72
0,4731
12 месяцев после лечения
Проверка по критерию суммы рангов
1,40
0,1613
1,65
0,0988
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,14
0,8891
-0,44
0,6567
Последующее наблюдение
Проверка по критерию суммы рангов
0,29
0,7728
0,39
0,6974
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
-1,62
0,1059
-1,31
0,1917
1.6.4,3 Оценка симптомов ТСМ
Метод анализа описан в разделе стенокардии.
Таблица 20
Изменение общей оценки симптомов ТСМ при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
N (отсутствуют)
1710(49)
1689(57)
1471(29)
1419(37)
Mean (SD)
13,83(7,27)
13,98(7,06)
13,96(7,25)
14,36(7,08)
Min, Max
0,00,37,00
0,00,36,00
0,00,37,00
0,00,36,00
Md (Q3-Q1)
13,00(10,00)
13,00(10,00)
13,00(11,00)
14,00(9,00)
1 месяц после лечения
N (отсутствуют)
1717(42)
1699(47)
1467(33)
1423(33)
Mean (SD)
11,84(7,16)
11,96(7,05)
11,93(7,18)
12,20(7,15)
Min, Max
0,00,34,00
0,00,37,00
0,00,34,00
0,00,37,00
Md (Q3-Q1)
11,00(9,00)
11,00(9,00)
11,00(10,00)
12,00(10,00)
1 месяц после лечения - исходные данные
N (отсутствуют)
1710(49)
1689(57)
1462(38)
1414(42)
Mean (SD)
-1,96(4,63)
-1,99(4,58)
-2,00(4,58)
-2,14(4,52)
Min, Max
-33,00,24,00
-25,00,20,00
-28,00,24,00
-25,00,19,00
Md(Q3-Ql)
0,00(3,00)
0,00(3,00)
-1,00(3,00)
0,00(4,00)
Парная проверка по критерию
Стьюдента (Р)
-17,50(0,0000)
-17,85(0,0000)
-16,65(0,0000)
-17,82(0,0000)
3 месяца после лечения
N (отсутствуют)
1717(42)
1700(46)
1447(53)
1408(48)
Mean (SD)
10,90(6,88)
11,05(6,84)
10,88(6,85)
11,17(6,84)
Min, Max
0,00,33,00
0,00,36,00
0,00,33,00
0,00,34,00
Md (Q3-Q1)
10,00(9,00)
11,00(9,00)
10,00(9,00)
11,00(9,00)
3 месяц после лечения - исходные данные
N (отсутствуют)
1710(49)
1689(57)
1444(56)
1400(56)
Mean (SD)
-2,91(5,22)
-2,91(5,16)
-3,05(5,19)
-3,18(5,03)
Min, Max
-33,00,19,00
-27,00,19,00
-28,00,19,00
-27,00,17,00
Md (Q3-Q1)
-2,00(5,00)
-2,00(5,00)
-2,00(5,00)
-2,00(6,00)
Парная проверка по критерию
Стьюдента (Р)
-23,05(0,0000)
-23,16(0,0000)
-22,32(0,0000)
-23,65(0,0000)
6 месяцев после лечения
N (отсутствуют)
1718(41)
1700(46)
1430(70)
1388(68)
Mean (SD)
10,04(6,65)
10,15(6,49)
9,79(6,47)
10,10(6,33)
Min, Max
0,00,34,00
0,00,36,00
0,00,34,00
0,00,36,00
Md (Q3-Q1)
9,00(9,00)
10,00(7,00)
9,00(8,00)
10,00(7,00)
6 месяцев после лечения - исходные данные
N (отсутствуют)
1710(49)
1689(57)
1427(73)
1381(75)
Mean (SD)
-3,76(5,57)
-3,81(5,69)
-4,11(5,49)
-4,26(5,48)
Min, Max
-33,00,19,00
-26,00,27,00
-28,00,19,00
-26,00,27,00
Md (Q3-Q1)
-3,00(6,00)
-3,00(6,00)
-3,00(6,00)
-3,00(6,00)
Парная проверка по критерию
Стьюдента (Р)
-27,95(0,0000)
-27,52(0,0000)
-28,25(0,0000)
-28,88(0,0000)
9 месяцев после лечения
N (отсутствуют)
1718(41)
1700(46)
1416(84)
1360(96)
Mean (SD)
9,29(6,35)
9,31(6,27)
8,88(6,04)
8,98(5,93)
Min, Max
0,00,37,00
0,00,36,00
0,00,37,00
0,00,36,00
Md (Q3-Q1)
8,00(8,00)
9,00(8,00)
8,00(7,00)
9,00(7,00)
9 месяцев после лечения - исходные данные
N (отсутствуют)
1710(49)
1689(57)
1412(88)
1354(102)
Mean (SD)
-4,52(5,90)
-4,65(6,15)
-5,04(5,80)
-5,36(5,70)
Min, Max
-33,00,15,00
-28,00,27,00
-28,00,15,00
-28,00,26,00
Md(Q3-Ql)
-4,00(8,00)
-4,00(7,00)
-4,00(7,00)
-5,00(7,00)
Парная проверка по критерию
Стьюдента (Р)
-31,68(0,0000)
-31,09(0,0000)
-32,62(0,0000)
-34,56(0,0000)
12 месяцев после лечения
N (отсутствуют)
1718(41)
1700(46)
1403(97)
1350(106)
Mean (SD)
8,41(6,11)
8,42(5,97)
7,81(5,56)
7,84(5,34)
Min, Max
0,00,37,00
0,00,36,00
0,00,28,00
0,00,28,00
Md (Q3-Q1)
8,00(8,00)
8,00(8,00)
7,00(7,00)
8,00(8,00)
12 месяцев после лечения - исходные данные
N (отсутствуют)
1710(49)
1689(57)
1399(101)
1344(112)
Mean (SD)
-5,39(6,23)
-5,54(6,49)
-6,09(6,07)
-6,54(5,84)
Min, Max
-33,00,18,00
-28,00,27,00
-28,00,18,00
-28,00,15,00
Md (Q3-Q1)
-5,00(8,00)
-5,00(8,00)
-5,00(8,00)
-6,00(8,00)
Парная проверка по критерию
Стьюдента (Р)
-35,76(0,0000)
-35,06(0,0000)
-37,53(0,0000)
-41,04(0,0000)
Последующее наблюдение
N (отсутствуют)
1429(330)
1379(367)
1395(105)
1343(113)
Mean (SD)
7,71(6,03)
7,85(5,94)
7,73(6,04)
7,88(5,92)
Min, Max
0,00,32,00
0,00,33,00
0,00,32,00
0,00,33,00
Md (Q3-Q1)
7,00(7,00)
7,00(8,00)
7,00(7,00)
7,00(8,00)
Последующее наблюдение - исходные данные
N (отсутствуют)
1425(334)
1373(373)
1391(109)
1337(119)
Mean (SD)
-6,18(6,52)
-6,48(6,17)
-6,16(6,52)
-6,45(6,15)
Min, Max
-29,00,27,00
-28,00,24,00
-29,00,27,00
-28,00,24,00
Md(Q3-Ql)
-5,00(8,00)
-6,00(8,00)
-5,00(8,00)
-6,00(8,00)
Парная проверка по критерию
Стьюдента (Р)
-35,76(0,0000)
-38,90(0,0000)
-35,23(0,0000)
-38,34(0,0000)
Таблица 21
Распределение
общей оценки симптомов ТСМ
при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Легкая
828(48,48%)
772(45,82%)
701(47,69%)
617(43,57%)
Средняя
817(47,83%)
855(50,74%)
717(48,78%)
750(52,97%)
Тяжелая
63(3,69%)
58(3,44%)
52(3,54%)
49(3,46%)
Итого
1708
1685
1470
1416
1 месяц после лечения
Легкая
989(58,76%)
975(58,24%)
847(57,93%)
814(57,24%)
Средняя
675(40,11%)
673(40,20%)
600(41,04%)
586(41,21%)
Тяжелая
19(1,13%)
26(1,55%)
15(1,03%)
22(1,55%)
Итого
1683
1674
1462
1422
3 месяца после лечения
Легкая
1066(65,56%)
1064(65,80%)
946(65,38%)
911(64,84%)
Средняя
546(33,58%)
538(33,27%)
489(33,79%)
481(34,23%)
Тяжелая
14(0,86%)
15(0,93%)
12(0,83%)
13(0,93%)
Итого
1626
1617
1447
1405
6 месяцев после лечения
Легкая
1133(72,63%)
1110(72,08%)
1044(73,11%)
996(71,76%)
Средняя
418(26,79%)
420(27,27%)
377(26,40%)
384(27,67%)
Тяжелая
9(0,58%)
10(0,65%)
7(0,49%)
8(0,58%)
Итого
1560
1540
1428
1388
9 месяцев после лечения
Легкая
1149(76,70%)
1113(77,24%)
1088(76,94%)
1045(77,06%)
Средняя
345(23,03%)
323(22,41%)
323(22,84%)
307(22,64%)
Тяжелая
4 (0,27%)
5(0,35%)
3(0,21%)
4(0,29%)
Итого
1498
1441
1414
1356
12 месяцев после лечения
Легкая
1205(83,62%)
1141(82,38%)
1172(83,59%)
1108(82,20%)
Средняя
235(16,31%)
241(17,40%)
229(16,33%)
237(17,58%)
Тяжелая
1(0,07%)
3(0,22%)
1(0,07%)
3(0,22%)
Итого
1441
1385
1402
1348
Последующее наблюдение
Легкая
1205(84,50%)
1148(83,37%)
1177(84,55%)
1116(83,22%)
Средняя
218(15,29%)
226(16,41%)
212(15,23%)
222(16,55%)
Тяжелая
3(0,21%)
3(0,22%)
3(0,22%)
3(0,22%)
Итого
1426
1377
1392
1341
Таблица 22
Распределение общей оценки симптомов ТСМ при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Критерий суммы рангов
1,40
0,1628
2,08
0,0378
1 месяц после лечения
Критерий суммы рангов
0,40
0,6866
0,49
0,6253
3 месяца после лечения
Критерий суммы рангов
-0,13
0,8971
0,32
0,7520
6 месяцев после лечения
Критерий суммы рангов
0,35
0,7245
0,81
0,4172
9 месяцев после лечения
Критерий суммы рангов
-0,33
0,7401
0,06
0,9498
12 месяцев после лечения
Критерий суммы рангов
0,89
0,3716
0,99
0,3219
Последующее наблюдение
Критерий суммы рангов
0,82
0,4149
0,95
0,3439
Таблица 23
Изменение боли в грудной клетке при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
473(27,68%)
443(26,26%)
398(27,07%)
352(24,82%)
3
641(37,51%)
679(40,25%)
546(37,14%)
562(39,63%)
6
568(33,24%)
534(31,65%)
505(34,35%)
476(33,57%)
9
27(1,58%)
31(1,84%)
21(1,43%)
28(1,97%)
Итого
1709
1687
1470
1418
1 месяц после лечения
0
608(35,41%)
579(34,08%)
515(35,13%)
471(33,15%)
3
635(36,98%)
663(39,02%)
537(36,63%)
551(38,78%)
6
461(26,85%)
445(26,19%)
406(27,69%)
390(27,45%)
9
13(0,76%)
12(0,71%)
8(0,55%)
9(0,63%)
Итого
1717
1699
1466
1421
1 месяц после лечения - исходные данные
-9
0(0,00%)
1(0,06%)
0(0,00%)
1(0,07%)
-6
16(0,94%)
19(1,13%)
12(0,82%)
11(0,78%)
-3
59(3,45%)
64(3,79%)
50(3,42%)
46(3,26%)
0
1344(78,64%)
1302(77,18%)
1146(78,49%)
1097(77,75%)
3
226(13,22%)
243(14,40%)
197(13,49%)
204(14,46%)
6
60(3,51%)
54(3,20%)
52(3,56%)
48(3,40%)
9
4(0,23%)
4(0,24%)
3(0,21%)
4(0,28%)
Итого
1709
1687
1460
1411
Проверка по критерию
Уилкоксона (Р)
19785(0,0000)
20378(0,0000)
15173,50(0,0000)
15562,50(0,0000)
3 месяца после лечения
0
656(38,21%)
627(36,88%)
550(38,01%)
502(35,68%)
3
643(37,45%)
669(39,35%)
535(36,97%)
562(39,94%)
6
410(23,88%)
391(23,00%)
356(24,60%)
337(23,95%)
9
8(0,47%)
13(0,76%)
6(0,41%)
6(0,43%)
Итого
1717
1700
1447
1407
3 месяца после лечения - исходные данные
-6
20(1,17%)
22(1,30%)
14(0,97%)
12(0,86%)
-9
0(0,00%)
1(0,06%)
-3
79(4,62%)
75(4,45%)
64(4,44%)
52(3,72%)
0
1203(70,39%)
1186(70,30%)
1019(70,62%)
993(71,03%)
3
325(19,02%)
329(19,50%)
279(19,33%>)
278(19,89%)
6
76(4,45%)
71(4,21%)
63(4,37%)
61(4,36%)
9
6(0,35%)
3(0,18%)
4(0,28%)
2(0,14%)
Итого
1709
1687
1443
1398
Проверка по критерию
Уилкоксона (Р)
39088(0,0000)
37267(0,0000)
28694,00(0,0000)
28097,50(0,0000)
6 месяцев после лечения
0
729(42,43%)
692(40,71%)
613(42,93%)
549(39,61%)
3
638(37,14%)
664(39,06%)
539(37,75%)
561(40,48%)
6
345(20,08%)
334(19,65%)
272(19,05%)
272(19,62%)
9
6(0,35%)
10(0,59%)
4(0,28%)
4(0,29%)
Итого
1718
1700
1428
1386
6 месяцев после лечения - исходные данные
-9
0(0,00%)
1(0,06%)
0(0,00%)
1(0,07%)
-6
13(0,76%)
22(1,30%)
5(0,35%)
9(0,65%)
-3
80(4,68%)
87(5,16%)
57(4,00%)
61(4,43%)
0
1104(64,60%)
1060(62,83%)
919(64,54%)
869(63,06%)
3
405(23,70%)
420(24,90%)
352(24,72%)
355(25,76%)
6
101(5,91%)
92(5,45%)
86(6,04%)
79(5,73%)
9
6(0,35%)
5(0,30%)
5(0,35%)
4(0,29%)
Итого
1709
1687
1424
1378
Проверка по критерию
Уилкоксона (Р)
65165(0,0000)
63298(0,0000)
49922,50(0,0000)
47527,50(0,0000)
9 месяцев после лечения
0
791(46,04%)
741(43,59%)
661(46,71%)
594(43,68%)
3
618(35,97%)
653(38,41%)
519(36,68%)
536(39,41%)
6
305(17,75%)
291(17,12%)
233(16,47%)
225(16,54%)
9
4(0,23%)
15(0,88%)
2(0,14%)
5(0,37%)
Итого
1718
1700
1415
1360
9 месяцев после лечения - исходные данные
-9
0(0,00%)
6(0,36%)
0(0,00%)
3(0,22%)
-6
13(0,76%)
22(1,30%)
7(0,50%)
6(0,44%)
-3
81(4,74%)
73(4,33%)
58(4,11%)
49(3,62%)
0
1022(59,80%)
1005(59,57%)
826(58,58%)
803(59,35%)
3
463(27,09%)
465(27,56%)
409(29,01%)
392(28,97%)
6
124(7,26%)
111(6,58%)
106(7,52%)
96(7,10%)
9
6(0,35%)
5(0,30%)
4(0,28%)
4(0,30%)
Итого
1709
1687
1410
1353
Проверка по критерию
Уилкоксона (Р)
88123(0,0000)
79406(0,0000)
68170,00(0,0000)
60337,50(0,0000)
12 месяцев после лечения
0
858(49,94%)
820(48,24%)
725(51,67%)
666(49,33%)
3
607(35,33%)
613(36,06%)
501(35,71%)
496(36,74%)
6
248(14,44%)
252(14,82%)
176(12,54%)
186(13,78%)
9
5(0,29%)
15(0,88%)
1(0,07%)
2(0,15%)
Итого
1718
1700
1403
1350
12 месяцев после лечения - исходные данные
-6
9(0,53%)
20(1,19%)
2(0,14%)
4(0,30%)
-9
0(0,00%)
6(0,36%)
-3
70(4,10%)
64(3,79%)
45(3,22%)
36(2,68%)
0
962(56,29%)
948(56,19%)
760(54,36%)
750(55,85%)
3
511(29,90%)
501(29,70%)
455(32,55%)
422(31,42%)
6
150(8,78%)
141(8,36%)
131(9,37%)
125(9,31%)
9
7(0,41%)
7(0,41%)
5(0,36%)
6(0,45%)
Итого
1709
1687
1398
1343
Проверка по критерию
Уилкоксона (Р)
113370(0,0000)
101285(0,0000)
89514,00(0,0000)
77706,50(0,0000)
Последующее наблюдение
0
754(52,84%)
698(50,73%)
733(52,62%)
675(50,37%)
2
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
3
479(33,57%)
488(35,47%)
472(33,88%)
479(35,75%)
6
192(13,45%)
188(13,66%)
186(13,35%)
184(13,73%)
9
1(0,07%)
2(0,15%)
1(0,07%)
2(0,15%)
Итого
1427
1376
1393
1340
Последующее наблюдение - исходные данные
-9
1(0,07%)
1(0,07%)
1(0,07%)
1(0,08%)
-6
11(0,77%)
11(0,80%)
9(0,65%)
10(0,75%)
-3
47(3,31%)
44(3,21%)
47(3,39%)
41(3,08%)
-2
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
0
769(54,08%)
737(53,83%)
750(54,03%)
723(54,24%)
3
426(29,96%)
424(30,97%)
417(30,04%)
411(30,83%)
6
158(11,11%)
142(10,37%)
155(11,17%)
137(10,28%)
9
9(0,63%)
10(0,73%)
8(0,58%)
10(0,75%)
Итого
1422
1369
1388
1333
Проверка по критерию
Уилкоксона (Р)
88781(0,0000)
83074(0,0000)
85383,50(0,0000)
78026,00(0,0000)
Таблица 24
Определение изменения боли в грудной клетке при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,04
0,9672
0,73
0,4677
1 месяц после лечения
Проверка по критерию суммы рангов
0,27
0,7887
0,66
0,5063
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
0,18
0,8592
0,59
0,5581
3 месяца после лечения
Проверка по критерию суммы рангов
0,39
0,6979
0,67
0,5031
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
-0,04
0,9683
0,56
0,5785
6 месяцев после лечения
Проверка по критерию суммы рангов
0,71
0,4754
1,49
0,1367
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,19
0,8458
-0,04
0,9667
9 месяцев после лечения
Проверка по критерию суммы рангов
1,17
0,2416
1,35
0,1761
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,49
0,6257
-0,18
0,8581
12 месяцев после лечения
Проверка по критерию суммы рангов
1,13
0,2603
1,35
0,1779
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,66
0,5079
-0,36
0,7154
Последующее наблюдение
Проверка по критерию суммы рангов
1,01
0,3120
1,10
0,2717
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
0,07
0,9467
-0,03
0,9763
Таблица 25
Изменение стеснения в грудной клетке при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
473 (27,68%)
443 (26,26%)
398 (27,07%)
352 (24,82%)
3
641 (37,51%)
679 (40,25%)
546 (37,14%)
562 (39,63%)
6
568 (33,24%)
534 (31,65%)
505 (34,35%)
476 (33,57%)
9
27 (1,58%)
31 (1,84%)
21 (1,43%)
28 (1,97%)
Итого
1709
1687
1470
1418
1 месяц после лечения
0
608 (35,41%)
579 (34,08%)
515 (35,13%)
471 (33,15%)
3
635(36,98%)
663(39,02%)
537(36,63%)
551(38,78%)
6
461(26,85%)
445(26,19%)
406(27,69%)
390(27,45%)
9
13(0,76%)
12(0,71%)
8(0,55%)
9(0,63%)
Итого
1717
1699
1466
1421
1 месяц после лечения - исходные данные
-6
7(0,41%)
6(0,36%)
6(0,41%)
3(0,21%)
-3
76(4,45%)
79(4,69%)
62(4,25%)
58(4,11%)
0
1302(76,18%)
1273(75,50%)
1110(76,03%)
1067(75,57%)
3
298(17,44%)
298(17,67%)
259(17,74%)
259(18,34%)
6
21(1,23%)
26(1,54%)
19(1,30%)
21(1,49%)
9
5(0,29%)
4(0,24%)
4(0,27%)
4(0,28%)
Итого
1709
1686
1460
1412
Проверка по критерию
Уилкоксона (Р)
24545(0,0000)
25454(0,0000)
18726,50(0,0000)
19632,00(0,0000)
3 месяца после лечения
0
656(38,21%)
627(36,88%)
550(38,01%)
502(35,68%)
3
643(37,45%)
669(39,35%)
535(36,97%)
562(39,94%)
6
410(23,88%)
391(23,00%)
356(24,60%)
337(23,95%)
9
8(0,47%)
13(0,76%)
6(0,41%)
6(0,43%)
Итого
1717
1700
1447
1407
3 месяца после лечения - исходные данные
-9
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
-6
8(0,47%)
8(0,47%)
6(0,42%)
4(0,29%)
-3
85(4,97%)
92(5,46%)
70(4,85%)
62(4,43%)
0
1190(69,63%)
1141(67,67%)
994(68,88%)
944(67,53%)
3
383(22,41%)
407(24,14%)
334(23,15%)
356(25,46%)
6
37(2,17%)
34(2,02%)
34(2,36%)
28(2,00%)
9
5(0,29%)
4(0,24%)
4(0,28%)
4(0,29%)
Итого
1709
1686
1443
1398
Проверка по критерию
Уилкоксона (Р)
43093(0,0000)
47229(0,0000)
33343,50(0,0000)
36915,50(0,0000)
6 месяцев после лечения
0
729(42,43%)
692(40,71%)
613(42,93%)
549(39,61%)
3
638(37,14%)
664(39,06%)
539(37,75%)
561(40,48%)
6
345(20,08%)
334(19,65%)
272(19,05%)
272(19,62%)
9
6(0,35%)
10(0,59%)
4(0,28%)
4(0,29%)
Итого
1718
1700
1428
1386
6 месяцев после лечения - исходные данные
-9
1(0,06%)
1(0,06%)
1(0,07%)
0(0,00%)
-6
3(0,18%)
14(0,83%)
3(0,21%)
7(0,51%)
-3
88(5,15%)
88(5,22%)
64(4,49%)
56(4,06%)
0
1105(64,66%)
1046(62,04%)
904(63,44%)
846(61,30%)
1
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
3
459(26,86%) 48(2,81%)
482(28,59%)
407(28,56%)
427(30,94%)
6
51(3,02%)
42(2,95%)
41(2,97%)
9
4(0,23%)
4(0,24%)
3(0,21%)
3(0,22%)
Итого
1709
1686
1425
1380
Проверка по критерию
Уилкоксона (Р)
64831(0,0000)
68356(0,0000)
50818,00(0,0000)
54318,00(0,0000)
9 месяцев после лечения
0
791(46,04%)
741(43,59%)
661(46,71%)
594(43,68%)
3
618(35,97%)
653(38,41%)
519(36,68%)
536(39,41%)
6
305(17,75%)
291(17,12%)
233(16,47%)
225(16,54%)
9
4(0,23%)
15(0,88%)
2(0,14%)
5(0,37%)
Итого
1718
1700
1415
1360
9 месяцев после лечения - исходные данные
-9
0(0,00%)
4(0,24%)
0(0,00%)
1(0,07%)
-6
3(0,18%)
14(0,83%)
3(0,21%)
3(0,22%)
-3
93(5,44%)
80(4,74%)
65(4,61%)
49(3,62%)
0
1007(58,92%)
946(56,11%)
801(56,81%)
735(54,32%)
3
534(31,25%)
566(33,57%)
476(33,76%)
502(37,10%)
6
68(3,98%)
71(4,21%)
62(4,40%)
59(4,36%)
9
4(0,23%)
5(0,30%)
3(0,21%)
4(0,30%)
Итого
1709
1686
1410
1353
Проверка по критерию
Уилкоксона (Р)
92186(0,0000)
98615(0,0000)
73535,50(0,0000)
79748,00(0,0000)
12 месяцев после лечения
0
858(49,94%)
820(48,24%)
725(51,67%)
666(49,33%)
3
607(35,33%)
613(36,06%)
501(35,71%)
496(36,74%)
6
248(14,44%)
252(14,82%)
176(12,54%)
186(13,78%)
9
5(0,29%)
15(0,88%)
1(0,07%)
2(0,15%)
Итого
1718
1700
1403
1350
12 месяцев после лечения - исходные данные
-9
0(0,00%)
5(0,30%)
0(0,00%)
1(0,07%)
-6
3(0,18%)
12(0,71%)
2(0,14%)
0(0,00%)
-3
83(4,86%)
63(3,74%)
54(3,86%)
29(2,16%)
0
933(54,59%)
837(49,64%)
721(51,54%)
623(46,39%)
3
598(34,99%)
673(39,92%)
539(38,53%)
605(45,05%)
6
87(5,09%)
89(5,28%)
79(5,65%)
79(5,88%)
9
5(0,29%)
7(0,42%)
4(0,29%)
6(0,45%)
Итого
1709
1686
1399
1343
Проверка по критерию
Уилкоксона (Р)
120256(0,0000)
143536(0,0000)
97784,50(0,0000)
119855,5(0,0000)
Последующее наблюдение
0
754(52,84%)
698(50,73%)
733(52,62%)
675(50,37%)
2
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
3
479(33,57%)
488(35,47%)
472(33,88%)
479(35,75%)
6
192(13,45%)
188(13,66%)
186(13,35%)
184(13,73%)
9
1(0,07%)
2(0,15%)
1(0,07%)
2(0,15%)
Итого
1427
1376
1393
1340
Последующее наблюдение - исходные данные
-9
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
-6
4(0,28%)
4(0,29%)
4(0,29%)
4(0,30%)
-3
55(3,86%)
37(2,70%)
54(3,88%)
35(2,62%)
0
728(51,09%)
698(50,91%)
712(51,19%)
684(51,20%)
1
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
3
544(38,18%)
535(39,02%)
528(37,96%)
520(38,92%)
6
87(6,11%)
91(6,64%)
86(6,18%)
88(6,59%)
9
5(0,35%)
6(0,44%)
5(0,36%)
5(0,37%)
Итого
1425
1371
1391
1336
Проверка по критерию
Уилкоксона (Р)
101793(0,0000)
100320(0,0000)
96444,50(0,0000)
94303,00(0,0000)
Таблица 26
Определение изменения стеснения в грудной клетке при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,04
0,9672
0,73
0,4677
1 месяц после лечения
Проверка по критерию суммы рангов
0,27
0,7887
0,66
0,5063
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
0,25
0,8053
0,66
0,5082
3 месяца после лечения
Проверка по критерию суммы рангов
0,39
0,6979
0,67
0,5031
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
0,64
0,5218
1,24
0,2156
6 месяцев после лечения
Проверка по критерию суммы рангов
0,71
0,4754
1,49
0,1367
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,75
0,4506
1,24
0,2140
9 месяцев после лечения
Проверка по критерию суммы рангов
1,17
0,2416
1,35
0,1761
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
1,31
0,1892
1,87
0,0611
12 месяцев после лечения
Проверка по критерию суммы рангов
1,13
0,2603
1,35
0,1779
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
2,78
0,0054
3,73
0,0002
Последующее наблюдение
Проверка по критерию суммы рангов
1,01
0,3120
1,10
0,2717
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
1,13
0,2571
1,06
0,2878
Таблица 27
Изменение одышки при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемы)
Исходные данные
0
257(15,04%)
217(12,87%)
213(14,48%)
162(11,42%)
3
886(51,84%)
917(54,39%)
752(51,12%)
761(53,67%)
6
533(31,19%)
519(30,78%)
479(32,56%)
467(32,93%)
9
33(1,93%)
33(1,96%)
27(1,84%)
28(1,97%)
Итого
1709
1686
1471
1418
1 месяц после лечения
0
363(21,14%)
318(18,72%)
303(20,68%)
258(18,14%)
3
931(54,22%)
982(57,80%)
787(53,72%)
807(56,75%)
6
410(23,88%)
386(22,72%)
365(24,91%)
346(24,33%)
9
13(0,76%)
13(0,77%)
10(0,68%)
11(0,77%)
Итого
1717
1699
1465
1422
1 месяц после лечения - исходные данные
-6
0(0,00%)
1(0,06%)
0(0,00%)
1(0,07%)
-4
8(0,47%)
6(0,36%)
7(0,48%)
3(0,21%)
-2
90(5,26%)
85(5,03%)
77(5,27%)
69(4,88%)
0
1323(77,37%)
1310(77,56%)
1132(77,53%)
1099(77,72%)
2
252(14,74%)
255(15,10%)
213(14,59%)
214(15,13%)
4
30(1,75%)
25(1,48%)
25(1,71%)
21(1,49%)
6
7(0,41%)
7(0,41%)
6(0,41%)
7(0,50%)
Итого
1710
1689
1460
1414
Проверка по критерию
Уилкоксона (Р)
19212(0,0000)
19001(0,0000)
13629,00(0,0000)
13889,00(0,0000)
3 месяца после лечения
0
374(21,78%)
354(20,82%)
310(21,44%)
288(20,47%)
3
1012(58,94%)
1018(59,88%)
855(59,13%)
834(59,28%)
6
318(18,52%)
318(18,71%)
271(18,74%)
279(19,83%)
9
13(0,76%)
10(0,59%)
10(0,69%)
6(0,43%)
Итого
1717
1700
1446
1407
3 месяца после лечения - исходные данные
-6
0(0,00%)
1(0,06%)
0(0,00%)
1(0,07%)
-4
2(0,12%)
5(0,30%)
2(0,14%)
4(0,29%)
-2
93(5,44%)
108(6,39%)
76(5,27%)
84(6,00%)
0
1219(71,29%)
1181(69,92%)
1014(70,27%)
975(69,69%)
2
350(20,47%)
342(20,25%)
309(21,41%)
288(20,59%)
4
37(2,16%)
45(2,66%)
34(2,36%)
40(2,86%)
6
9(0,53%)
7(0,41%)
8(0,55%)
7(0,50%)
Итого
1710
1689
1443
1399
Проверка по критерию
Уилкоксона (Р)
38821(0,0000)
37407(0,0000)
30642,50(0,0000)
27385,50(0,0000)
6 месяцев после лечения
0
430(25,03%)
400(23,53%)
360(25,21%)
320(23,05%)
2
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
3
998(58,09%)
1024(60,24%)
838(58,68%)
849(61,17%)
6
280(16,30%)
266(15,65%)
222(15,55%)
215(15,49%)
9
9(0,52%)
10(0,59%)
7(0,49%)
4(0,29%)
Итого
1718
1700
1428
.1388
6 месяцев после лечения - исходные данные
-6
2(0,12%)
0(0,00%)
2(0,14%)
0(0,00%)
-4
2(0,12%)
7(0,41%)
2(0,14%)
4(0,29%)
-2
102(5,96%)
112(6,63%)
76(5,33%)
85(6,15%)
0
1109(64,85%)
1077(63,77%)
906(63,53%)
859(62,20%)
2
435(25,44%)
426(25,22%)
387(27,14%)
374(27,08%)
4
51(2,98%)
57(3,37%)
45(3,16%)
50(3,62%)
6
9(0,53%)
10(0,59%)
8(0,56%)
9(0,65%)
Итого
1710
1689
1426
1381
Проверка по критерию
Уилкоксона (Р)
60693(0,0000)
59612(0,0000)
48093,00(0,0000)
46755,50(0,0000)
9 месяцев после лечения
0
489(28,46%)
473(27,82%)
416(29,42%)
387(28,46%)
3
994(57,86%)
1007(59,24%)
824(58,27%)
820(60,29%)
6
227(13,21%)
207(12,18%)
169(11,95%)
150(11,03%)
9
8(0,47%)
13(0,76%)
5(0,35%)
3(0,22%)
Итого
1718
1700
1414
1360
9 месяцев после лечения - исходные данные
-6
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
-4
4(0,23%)
8(0,47%)
2(0,14%)
4(0,30%)
-2
107(6,26%)
109(6,45%)
78(5,53%)
76(5,61%)
0
1010(59,06%)
976(57,79%)
798(56,60%)
746(55,10%)
2
519(30,35%)
519(30,73%)
470(33,33%)
464(34,27%)
4
61(3,57%)
69(4,09%)
54(3,83%)
57(4,21%)
6
8(0,47%)
8(0,47%)
7(0,50%)
7(0,52%)
Итого
1710
1689
1410
1354
Проверка по критерию
Уилкоксона (Р)
85799(0,0000)
87654(0,0000)
70616,50(0,0000)
69726,00(0,0000)
12 месяцев после лечения
0
545(31,72%)
549(32,29%)
468(33,36%)
462(34,22%)
3
995(57,92%)
1024(60,24%)
820(58,45%)
831(61,56%)
6
173(10,07%)
114(6,71%)
115(8,20%)
56(4,15%)
9
5(0,29%)
13(0,76%)
0(0,00%)
1(0,07%)
Итого
1718
1700
1403
1350
12 месяцев после лечения - исходные данные
-4
2(0,12%)
6(0,36%)
1(0,07%)
1(0,07%)
-2
108(6,32%)
101(5,98%)
75(5,36%)
67(4,99%)
0
955(55,85%)
932(55,18%)
743(53,11%)
699(52,01%)
2
563(32,92%)
551(32,62%)
506(36,17%)
491(36,53%)
4
70(4,09%)
87(5,15%)
63(4,50%)
75(5,58%)
6
12(0,70%)
12(0,71%)
11(0,79%)
11(0,82%)
Итого
1710
1689
1399
1344
Проверка по критерию
Уилкоксона (Р)
104992(0,0000)
106281(0,0000)
85309,50(0,0000)
84844,50(0,0000)
Последующее наблюдение
0
509(35,62%)
470(34,08%)
493(35,34%)
455(33,88%)
2
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
3
779(54,51%)
781(56,64%)
763(54,70%)
763(56,81%)
6
137(9,59%)
124(8,99%)
135(9,68%)
122(9,08%)
9
3(0,21%)
4(0,29%)
3(0,22%)
3(0,22%)
Итого
1429
1379
1395
1343
Последующее наблюдение - исходные данные
-6
2(0,14%)
0(0,00%)
2(0,14%)
0(0,00%)
-4
0(0,00%)
2(0,15%)
0(0,00%)
2(0,15%)
-2
71(4,98%)
62(4,52%)
71(5,10%)
60(4,49%)
0
744(52,21%)
708(51,60%)
725(52,12%)
692(51,80%)
2
519(36,42%)
504(36,73%)
507(36,45%)
492(36,83%)
4
78(5,47%)
82(5,98%)
76(5,46%)
77(5,76%)
6
11(0,77%)
14(1,02%)
10(0,72%)
13(0,97%)
Итого
1425
1372
1391
1336
Проверка по критерию
Уилкоксона (Р)
93780(0,0000)
91596(0,0000)
89180,00(0,0000)
86071,00(0,0000)
Таблица 28
Определение изменения одышки при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,64
0,5233
1,27
0,2025
1 месяц после лечения
Проверка по критерию суммы рангов
0,52
0,5997
0,79
0,4302
I месяц после лечения - исходные данные
Проверка по критерию суммы рангов
0,19
0,8476
0,54
0,5878
3 месяца после лечения
Проверка по критерию суммы рангов
0,43
0,6645
0,72
0,4720
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
-0,43
0,6636
-0,56
0,5756
6 месяцев после лечения
Проверка по критерию суммы рангов
0,49
0,6222
0,85
0,3931
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,15
0,8770
0,03
0,9791
9 месяцев после лечения
Проверка по критерию суммы рангов
0,04
0,9684
0,05
0,9635
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,42
0,6767
0,64
0,5230
12 месяцев после лечения
Проверка по критерию суммы рангов
-1,41
0,1587
-1,81
0,0706
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,63
0,5258
1,00
0,3160
Последующее наблюдение
Проверка по критерию суммы рангов
0,57
0,5680
0,50
0,6158
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
0,78
0,4347
0,71
0,4756
Таблица 29
Изменение усталости при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
315(18,42%)
323(19,12%)
268(18,22%)
254(17,90%)
2
1042(60,94%)
1010(59,80%)
890(60,50%)
848(59,76%)
4
289(16,90%)
296(17,53%)
261(17,74%)
265(18,68%)
6
64(3,74%)
60(3,55%)
52(3,54%)
52(3,66%)
Итого
1710
1689
1471
1419
1 месяц после лечения
0
413(24,05%)
426(25,07%)
346(23,62%)
343(24,10%)
2
1043(60,75%)
1011(59,51%)
890(60,75%)
847(59,52%)
4
238(13,86%)
234(13,77%)
211(14,40%)
210(14,76%)
6
23(1,34%)
28(1,65%)
18(1,23%)
23(1,62%)
Итого
1717
1699
1465
1423
1 месяц после лечения - исходные данные
-6
1(0,06%)
2(0,12%)
1(0,07%)
2(0,14%)
-4
11(0,64%)
16(0,95%)
9(0,62%)
8(0,57%)
-2
98(5,73%)
107(6,34%)
87(5,96%)
89(6,30%)
0
1238(72,40%)
1162(68,88%)
1054(72,24%)
972(68,84%)
1
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
2
303(17,72%)
320(18,97%)
260(17,82%)
274(19,41%)
4
45(2,63%)
70(4,15%)
35(2,40%)
59(4,18%)
6
13(0,76%)
10(0,59%)
12(0,82%)
8(0,57%)
Итого
1710
1687
1459
1412
Проверка по критерию
Уилкоксона (Р)
30817(0,0000)
37573(0,0000)
22149,00(0,0000)
28265,00(0,0000)
3 месяца после лечения
0
480(27,96%)
471(27,71%)
409(28,28%)
378(26,87%)
2
1026(59,76%)
1018(59,88%)
864(59,75%)
849(60,34%)
4
197(11,47%)
195(11,47%)
165(11,41%)
168(11,94%)
6
14(0,82%)
16(0,94%)
8(0,55%)
12(0,85%)
Итого
1717
1700
1446
1407
3 месяца после лечения - исходные данные
-6
2(0,12%)
2(0,12%)
2(0,14%)
1(0,07%)
-4
9(0,53%)
14(0,83%)
6(0,42%)
8(0,57%)
-2
86(5,03%)
105(6,22%)
70(4,85%)
86(6,16%)
0
1107(64,74%)
1054(62,48%)
923(63,96%)
864(61,85%)
2
420(24,56%)
408(24,18%)
368(25,50%)
349(24,98%)
4
70(4,09%)
92(5,45%)
60(4,16%)
80(5,73%)
6
16(0,94%)
12(0,71%)
14(0,97%)
9(0,64%)
Итого
1710
1687
1443
1397
Проверка по критерию
Уилкоксона (Р)
63149(0,0000)
64162(0,0000)
48511,00(0,0000)
48043,00(0,0000)
6 месяцев после лечения
0
520(30,27%)
508(29,88%)
443(31,00%)
410(29,54%)
2
1048(61,00%)
1053(61,94%)
881(61,65%)
874(62,97%)
4
135(7,86%)
126(7,41%)
97(6,79%)
95(6,84%)
6
15(0,87%)
13(0,76%)
8(0,56%)
9(0,65%)
Итого
1718
1700
1429
1388
6 месяцев после лечения - исходные данные
-6
0(0,00%)
4(0,24%)
0(0,00%)
3(0,22%)
-4
12(0,70%)
9(0,53%)
8(0,56%)
3(0,22%)
-2
108(6,32%)
108(6,40%)
86(6,03%)
84(6,09%)
0
974(56,96%)
929(55,07%)
791(55,47%)
738(53,52%)
2
488(28,54%)
499(29,58%)
428(30,01%)
430(31,18%)
4
110(6,43%)
123(7,29%)
97(6,80%)
108(7,83%)
6
18(1,05%)
15(0,89%)
16(1,12%)
13(0,94%)
Итого
1710
1687
1426
1379
Проверка по критерию
Уилкоксона (Р)
95480(0,0000)
101941(0,0000)
74284,00(0,0000)
77640,00(0,0000)
9 месяцев после лечения
0
576(33,53%)
581(34,18%)
498(35,22%)
473(34,78%)
2
1035(60,24%)
1017(59,82%)
857(60,61%)
828(60,88%)
4
88(5,12%)
92(5,41%)
49(3,47%)
53(3,90%)
6
19(1,11%)
10(0,59%)
10(0,71%)
6(0,44%)
Итого
1718
1700
1414
1360
9 месяцев после лечения - исходные данные
-6
1(0,06%)
3(0,18%)
0 (0,00%)
2(0,15%)
-4
13(0,76%)
8(0,47%)
7 (0,50%)
3 (0,22%)
-2
115(6,73%)
104(6,16%)
92 (6,52%)
76 (5,63%)
0
864(50,53%)
828(49,08%)
679(48,12%)
623 (46,11%)
2
572(33,45%)
577(34,20%)
503 (35,65%)
505 (37,38%)
4
125(7,31%)
142 (8,42%)
112(7,94%)
121 (8,96%)
6
20(1,17%)
25 (1,48%)
18 (1,28%)
21 (1,55%)
Итого
1710
1687
1411
1351
Проверка по критерию
Уилкоксона (Р)
128910(0,0000)
140633(0,0000)
102138,0(0,0000)
107197,5(0,0000)
12 месяцев после лечения
0
630(36,67%)
650(38,24%)
548(39,06%)
537(39,78%)
2
1000(58,21%)
968(56,94%)
816(58,16%)
775(57,41%)
4
76(4,42%)
76(4,47%)
37(2,64%)
36(2,67%)
6
12(0,70%)
6(0,35%)
2(0,14%)
2(0,15%)
Итого
1718
1700
1403
1350
12 месяцев после лечения - исходные данные
-4
11(0,64%)
12(0,71%)
4(0,29%)
5(0,37%)
-6
0(0,00%)
1(0,06%)
-2
100(5,85%)
101(5,99%)
76(5,43%)
70(5,22%)
0
805(47,08%)
747(44,28%)
617(44,10%)
540(40,24%)
2
605(35,38%)
630(37,34%)
532(38,03%)
558(41,58%)
4
164(9,59%)
168(9,96%)
147(10,51%)
144(10,73%)
6
25(1,46%)
28(1,66%)
23(1,64%)
25(1,86%)
Итого
1710
1687
1399
1342
Проверка по критерию
Уилкоксона (Р)
160960(0,0000)
173385(0,0000)
127198,5(0,0000)
135471,5(0,0000)
Последующее наблюдение
0
611(42,76%)
590(42,82%)
597(42,80%)
570(42,47%)
2
759(53,11%)
733(53,19%)
739(52,97%)
721(53,73%)
4
56(3,92%)
53(3,85%)
56(4,01%)
50(3,73%)
6
3(0,21%)
2(0,15%)
3(0,22%)
1(0,07%)
Итого
1429
1378
1395
1342
Последующее наблюдение - исходные данные
-4
5 (0,35%)
6(0,44%)
3 (0,22%)
4 (0,30%)
-2
87(6,11%)
72(5,25%)
86 (6,18%)
71 (5,32%)
0
608 (42,67%)
533(38,88%)
598 (42,99%)
525 (39,33%)
2
537 (37,68%)
558(40,70%)
523 (37,60%)
542 (40,60%)
4
158(11,09%)
175(12,76%)
153 (11,00%)
168(12,58%)
6
30(2,11%)
27 (1,97%)
28 (2,01%)
25 (1,87%)
Итого
1425
1371
1391
1335
Проверка по критерию
Уилкоксона (Р)
136359(0,0000)
148729(0,0000)
129118,0(0,0000)
139632,5(0,0000)
Таблица 30
Определение изменения усталости при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,15
0,8815
0,59
0,5564
1 месяц после лечения
Проверка по критерию суммы рангов
-0,38
0,7052
0,11
0,9118
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
1,13
0,2603
1,60
0,1090
3 месяца после лечения
Проверка по критерию суммы рангов
0,19
0,8519
0,99
0,3202
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
-0,04
0,9663
0,02
0,9855
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,02
0,9814
0,79
0,4323
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,91
0,3633
1,06
0,2910
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,46
0,6430
0,28
0,7833
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
1,58
0,1150
1,83
0,0676
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,98
0,3255
-0,36
0,7217
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
1,21
0,2273
1,75
0,0802
Последующее наблюдение
Проверка по критерию суммы рангов
-0,07
0,9429
0,03
0,9763
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
2,34
0,0194
2,25
0,0243
Таблица 31
Изменение учащенного сердцебиения при различных наблюдениях
данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
315(18,42%)
281(16,66%)
263(17,88%)
224(15,81%)
2
803(46,96%)
780(46,24%)
690(46,91%)
644(45,45%)
4
470(27,49%)
508(30,11%)
416(28,28%)
445(31,40%)
6
122(7,13%)
118(6,99%)
102(6,93%)
104(7,34%)
Итого
1710
1687
1471
1417
1 месяц после лечения
0
427(24,87%)
393(23,13%)
353(24,11%)
319(22,42%)
1
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
2
834(48,57%)
859(50,56%)
713(48,70%)
714(50,18%)
4
398(23,18%)
386(22,72%)
351(23,98%)
338(23,75%)
6
57(3,32%)
61(3,59%)
46(3,14%)
52(3,65%)
Итого
1717
1699
1464
1423
1 месяц после лечения - исходные данные
-3
0(0,00%)
2(0,12%)
0(0,00%)
1(0,07%)
-2
1(0,06%)
2(0,12%)
1(0,07%)
1(0,07%)
-1
103(6,02%)
98(5,80%)
87(5,96%)
75(5,30%)
0
1242(72,63%)
1278(75,67%)
1051(71,99%)
1075(76,03%)
1
334(19,53%)
277(16,40%)
295(20,21%)
234(16,55%)
2
25(1,46%)
29(1,72%)
22(1,51%)
26(1,84%)
3
5(0,29%)
3(0,18%)
4(0,27%)
2(0,14%)
Итого
1710
1689
1460
1414
Проверка по критерию
Уилкоксона (Р)
31866(0,0000)
22309(0,0000)
24868,00(0,0000) 16529,00(0,0000)
3 месяца после лечения
0
480(27,96%)
438(25,76%)
403(27,87%)
350(24,88%)
2
894(52,07%)
898(52,82%)
759(52,49%)
748(53,16%)
4
310(18,05%)
320(18,82%)
261(18,05%)
275(19,55%)
6
33(1,92%)
44(2,59%)
23(1,59%)
34(2,42%)
Итого
1717
1700
1446
1407
3 месяца после лечения - исходные данные
-3
0(0,00%)
3(0,18%)
0(0,00%)
1(0,07%)
-2
2(0,12%)
4(0,24%)
1(0,07%)
2(0,14%)
-1
119(6,96%)
94(5,57%)
99(6,86%)
72(5,15%)
0
1125(65,79%)
1125(66,61%)
943(65,35%)
923(65,98%)
1
415(24,27%)
412(24,39%)
356(24,67%)
358(25,59%)
2
43(2,51%)
45(2,66%)
39(2,70%)
38(2,72%)
3
6(0,35%)
6(0,36%)
5(0,35%)
5(0,36%)
Итого
1710
1689
1443
1399
Проверка по критерию
Уилкоксона (Р)
52756(0,0000)
52032(0,0000)
39577,50(0,0000)
39872,50(0,0000)
6 месяцев после лечения
0
538(31,32%)
492(28,94%)
456(31,91%)
396(28,53%)
2
906(52,74%)
945(55,59%)
764(53,46%)
786(56,63%)
4
246(14,32%)
229(13,47%)
192(13,44%)
185(13,33%)
6
28(1,63%)
34(2,00%)
17(1,19%)
21(1,51%)
Итого
1718
1700
1429
1388
6 месяцев после лечения - исходные данные
-2
5(0,29%)
8(0,47%)
4(0,28%)
3(0,22%)
-3
0(0,00%)
2(0,12%)
-1
116(6,78%)
102(6,04%)
88(6,18%)
74(5,36%)
0
1034(60,47%)
1022(60,51%)
842(59,09%)
827(59,88%)
1
490(28,65%)
495(29,31%)
431(30,25%)
425(30,77%)
2
56(3,27%)
52(3,08%)
53(3,72%)
45(3,26%)
3
9(0,53%)
8(0,47%)
7(0,49%)
7(0,51%)
Итого
1710
1689
1425
1381
Проверка по критерию
Уилкоксона (Р)
76022(0,0000)
74546(0,0000)
60046,00(0,0000)
56797,00(0,0000)
9 месяцев после лечения
0
581(33,82%)
570(33,53%)
496(35,05%)
464(34,14%)
2
929(54,07%)
939(55,24%)
782(55,27%)
768(56,51%)
4
179(10,42%)
164(9,65%)
122(8,62%)
113(8,31%)
6
29(1,69%)
27(1,59%)
15(1,06%)
14(1,03%)
Итого
1718
1700
1415
1359
9 месяцев после лечения - исходные данные
-2
5(0,29%)
12(0,71%)
4(0,28%)
4(0,30%)
-3
0(0,00%)
2(0,12%)
-1
117(6,84%)
105(6,22%)
87(6,17%)
74(5,47%)
0
948(55,44%)
906(53,64%)
749(53,12%)
699(51,62%)
1
557(32,57%)
601(35,58%)
493(34,96%)
524(38,70%)
2
76(4,44%)
53(3,14%)
71(5,04%)
46(3,40%)
3
7(0,41%)
10(0,59%)
6(0,43%)
7(0,52%)
Итого
1710
1689
1410
1354
Проверка по критерию
Уилкоксона(Р)
102289(0,0000)
105928(0,0000)
81650,00(0,0000)
82763,00(0,0000)
12 месяцев после лечения
0
669(38,94%)
638(37,53%)
576(41,05%)
529(39,19%)
2
892(51,92%)
911(53,59%)
745(53,10%)
738(54,67%)
4
138(8,03%)
131(7,71%)
78(5,56%)
76(5,63%)
6
19(1,11%)
20(1,18%)
4(0,29%)
7(0,52%)
Итого
1718
1700
1403
1350
12 месяцев после лечения - исходные данные
-2
4(0,23%)
10(0,59%)
3(0,21%)
1(0,07%)
-3
0(0,00%)
2(0,12%)
-1
112(6,55%)
106(6,28%)
78(5,58%)
74(5,51%)
0
882(51,58%)
861(50,98%)
679(48,53%)
655(48,81%)
1
602(35,20%)
620(36,71%)
536(38,31%)
533(39,72%)
2
102(5,96%)
84(4,97%)
97(6,93%)
75(5,59%)
3
8(0,47%)
6(0,36%)
6(0,43%)
4(0,30%)
Итого
1710
1689
1399
1342
Проверка по критерию
Уилкоксона (Р)
128493(0,0000)
123688(0,0000)
103801,5(0,0000)
95022,50(0,0000)
Последующее наблюдение
0
631(44,16%)
591(42,86%)
613(43,94%)
570(42,44%о)
2
697(48,78%)
704(51,05%)
683(48,96%)
692(51,53%)
4
95(6,65%)
76(5,51%)
94(6,74%)
74(5,51%)
6
6(0,42%)
8(0,58%)
5(0,36%)
7(0,52%)
Итого
1429
1379
1395
1343
Последующее наблюдение - исходные данные
-3
1(0,07%)
0(0,00%)
1(0,07%)
0(0,00%)
-2
3(0,21%)
1(0,07%)
3(0,22%)
1(0,07%)
-1
90(6,32%)
96(7,00%)
86(6,19%)
93(6,96%)
0
690(48,46%)
651(47,45%)
677(48,71%)
634(47,46%)
1
528(37,08%)
539(39,29%)
516(37,12%)
523(39,15%)
2
97(6,81%)
73(5,32%)
93(6,69%)
73(5,46%)
3
15(1,05%)
12(0,87%)
14(1,01%)
12(0,90%)
Итого
1424
1372
1390
1336
Проверка по критерию
Уилкоксона (Р)
104286(0,0000)
98940(0,0000)
98684,00(0,0000)
94032,50(0,0000)
Таблица 32
Определение изменения учащенного сердцебиения при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
1,60
0,1095
2,06
0,0390
1 месяц после лечения
Проверка по критерию суммы рангов
0,68
0,4960
0,82
0,4149
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
-1,78
0,0743
-1,63
0,1028
3 месяца после лечения
Проверка по критерию суммы рангов
1,61
0,1080
2,14
0,0325
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
0,65
0,5179
1,09
0,2752
6 месяцев после лечения
Проверка по критерию суммы рангов
0,97
0,3297
1,58
0,1146
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,32
0,7466
0,26
0,7913
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,18
0,8559
0,31
0,7557
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,72
0,4730
0,87
0,3820
12 месяцев после лечения
Проверка по критерию суммы рангов
0,64
0,5198
1,00
0,3150
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
-0,15
0,8821
-0,31
0,7560
Последующее наблюдение
Проверка по критерию суммы рангов
0,35
0,7270
0,41
0,6795
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
-0,27
0,7903
-0,15
0,8833
Таблица 33
Изменение спонтанного потоотделения при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
430(25,15%)
409(24,22%)
367(24,95%)
333(23,47%)
1
941(55,03%)
962(56,96%)
803(54,59%)
808(56,94%)
2
298(17,43%)
284(16,81%)
265(18,01%)
246(17,34%)
3
41 (2,40%)
34 (2,01%)
36(2,45%)
32(2,26%)
Итого
1710
1689
1471
1419
1 месяц после лечения
0
603(35,12%)
541(31,84%)
518(35,36%)
449(31,55%)
1
879(51,19%)
933(54,91%)
738(50,38%)
777(54,60%)
2
215(12,52%)
206(12,12%)
195(13,31%)
182(12,79%)
3
20(1,16%)
19(1,12%)
14(0,96%)
15(1,05%)
Итого
1717
1699
1465
1423
1 месяц после лечения - исходные данные
-3
3(0,18%)
5(0,30%)
3(0,21%)
5(0,35%)
-2
17(0,99%)
8 (0,47%)
14(0,96%)
7(0,50%)
-1
94(5,50%)
108(6,39%)
77(5,27%)
82(5,80%)
0
1249(73,08%)
1227(72,65%)
1068(73,15%)
1041(73,62%)
1
279(16,33%)
276(16,34%)
238(16,30%)
228(16,12%)
2
51(2,98%)
59(3,49%)
48(3,29%)
47(3,32%)
3
16(0,94%)
6(0,36%)
12(0,82%)
4(0,28%)
Итого
1709
1689
1460
1414
Проверка по критерию
Уилкоксона (Р)
27157(0,0000)
27058(0,0000)
20342,00(0,0000)
17917,00(0,0000)
3 месяца после лечения
0
667(38,85%)
664(39,06%)
563(38,93%)
550(39,09%)
1
846(49,27%)
853(50,18%)
709(49,03%)
710(50,46%)
2
190(11,07%)
172(10,12%)
167(11,55%)
140(9,95%)
3
14(0,82%)
11(0,65%)
7(0,48%)
7(0,50%)
Итого
1717
1700
1446
1407
3 месяца после лечения - исходные данные
-3
2 (0,12%)
2(0,12%)
2(0,14%)
2(0,14%)
-2
15 (0,88%)
9(0,53%)
13(0,90%)
6(0,43%)
-1
121 (7,08%)
124(7,34%)
101(7,00%)
100(7,15%)
0
1083 (63,37%)
1068(63,23%)
898(62,23%)
877(62,73%)
1
392 (22,94%)
393(23,27%)
342(23,70%)
334(23,89%)
2
76 (4,45%)
86(5,09%)
71(4,92%)
74(5,29%)
3
20(1,17%)
7(0,41%)
16(1,11%)
5(0,36%)
Итого
1709
1689
1443
1398
Проверка по критерию
Уилкоксона (Р)
57413(0,0000)
58131(0,0000)
44586,00(0,0000)
42357,50(0,0000)
6 месяцев после лечения
0
728(42,37%)
714(42,00%)
628(43,98%)
593(42,72%)
1
833(48,49%)
842(49,53%)
676(47,34%)
688(49,57%)
2
144(8,38%)
136(8,00%)
117(8,19%)
103(7,42%)
3
13(0,76%)
8(0,47%)
7(0,49%)
4(0,29%)
Итого
1718
1700
1428
1388
6 месяцев после лечения - исходные данные
-3
0(0,00%)
3(0,18%)
0(0,00%)
3(0,22%)
-2
23(1,35%)
14(0,83%)
20(1,40%)
9(0,65%)
-1
137(8,02%)
120(7,10%)
105(7,37%)
89(6,45%)
0
959(56,11%)
973(57,61%)
774(54,32%)
785(56,88%)
1
468(27,38%)
455(26,94%)
414(29,05%)
387(28,04%)
2
93(5,44%)
112(6,63%)
88(6,18%)
96(6,96%)
3
29(1,70%)
12(0,71%)
24(1,68%)
11(0,80%)
Итого
1709
1689
1425
1380
Проверка по критерию
Уилкоксона (Р)
84041(0,0000)
82717(0,0000)
67343,00(0,0000)
60902,00(0,0000)
9 месяцев после лечения
0
788(45,87%)
776(45,65%)
678(47,95%)
647(47,57%)
1
813(47,32%)
818(48,12%)
652(46,11%)
650(47,79%)
2
105(6,11%)
100(5,88%)
79(5,59%)
61(4,49%)
3
12(0,70%)
6(0,35%)
5(0,35%)
2(0,15%)
Итого
1718
1700
1414
1360
9 месяцев после лечения - исходные данные
-3
0(0,00%)
3(0,18%)
0(0,00%)
3(0,22%)
-2
10(0,59%)
15(0,89%)
6(0,43%)
8(0,59%)
-1
154(9,01%)
110(6,51%)
122(8,65%)
80(5,92%)
0
910(53,25%)
910(53,88%)
717(50,85%)
711(52,63%)
1
491(28,73%)
508(30,08%)
434(30,78%)
426(31,53%)
2
113(6,61%)
130(7,70%)
105(7,45%)
112(8,29%)
3
31(1,81%)
13(0,77%)
26(1,84%)
11(0,81%)
Итого
1709
1689
1410
1351
Проверка по критерию
Уилкоксона (Р)
102988(0,0000)
105181(0,0000)
82586,50(0,0000)
75847,50(0,0000)
12 месяцев после лечения
0
845 (49,19%)
814(47,88%)
730 (52,03%)
673 (49,93%)
1
804 (46,80%)
813 (47,82%)
640 (45,62%)
646 (47,92%)
2
58 (3,38%)
68 (4,00%)
31 (2,21%)
28 (2,08%)
3
11 (0,64%)
5 (0,29%)
2(0,14%)
1 (0,07%)
Итого
1718
1700
1403
1348
12 месяцев после лечения - исходные данные
-2
12(0,70%)
9(0,53%)
8(0,57%)
2(0,15%)
-3
0(0,00%)
2(0,12%)
-1
137(8,02%)
116(6,87%)
103(7,37%)
81(6,03%)
0
837(48,98%)
844(49,97%)
647(46,28%)
646(48,10%)
1
550(32,18%)
546(32,33%)
483(34,55%)
463(34,48%)
2
139(8,13%)
153(9,06%)
128(9,16%)
136(10,13%)
3
34(1,99%)
19(1,12%)
29(2,07%)
15(1,12%)
Итого
1709
1689
1398
1343
Проверка по критерию
Уилкоксона (Р)
134030(0,0000)
131902(0,0000)
105721,5(0,0000)
98327,00(0,0000)
Последующее наблюдение
0
767(53,71%)
719(52,18%)
750(53,80%)
699(52,09%)
1
595(41,67%)
601(43,61%)
578(41,46%)
587(43,74%)
2
62(4,34%)
58(4,21%)
62(4,45%)
56(4,17%)
3
4(0,28%)
0(0,00%)
4(0,29%)
0(0,00%)
Итого
1428
1378
1394
1342
Последующее наблюдение - исходные данные
-3
2(0,14%)
1(0,07%)
2(0,14%)
1(0,07%)
-2
8(0,56%)
5(0,36%)
8(0,58%)
5(0,37%)
-1
119(8,36%)
92(6,71%)
116(8,35%)
91(6,81%)
0
656(46,07%)
649(47,30%)
644(46,33%)
631(47,23%)
1
466(32,72%)
464(33,82%)
451(32,45%)
452(33,83%)
2
141 (9,90%)
143(10,42%)
138(9,93%)
140(10,48%)
3
32 (2,25%)
18(1,31%)
31(2,23%)
16(1,20%)
Итого
1424
1372
1390
1336
Проверка по критерию
Уилкоксона (Р)
105998(0,0000)
101375(0,0000)
99787,50(0,0000)
95903,50(0,0001
Таблица 34
Определение изменения спонтанного потоотделения при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,03
0,9765
0,26
0,7929
1 месяц после лечения
Проверка по критерию суммы рангов
1,43
0,1536
1,55
0,1213
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
-0,29
0,7709
-0,52
0,6002
3 месяца после лечения
Проверка по критерию суммы рангов
-0,49
0,6219
-0,56
0,5750
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
0,12
0,9053
-0,03
0,9741
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,04
0,9706
0,30
0,7638
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,35
0,7234
-0,05
0,9606
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,07
0,9432
-0,17
0,8632
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
1,27
0,2053
0,82
0,4096
12 месяцев после лечения
Проверка по критерию суммы рангов
0,79
0,4302
1,02
0,3094
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
0,43
0,6642
0,41
0,6850
Последующее наблюдение
Проверка по критерию суммы рангов
0,66
0,5111
0,70
0,4831
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
0,65
0,5170
0,68
0,4968
Таблица 35
Изменение бледности при различных наблюдениях
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
0
572(33,47%)
552(32,68%)
494(33,61%)
450(31,71%)
1
741(43,36%)
731(43,28%)
626(42,59%)
623(43,90%)
2
325(19,02%)
345(20,43%)
293(19,93%)
300(21,14%)
3
71(4,15%)
61(3,61%)
57(3,88%)
46(3,24%)
Итого
1709
1689
1470
1419
1 месяц после лечения
0
713(41,53%)
695(40,91%)
613(41,81%)
569(39,99%)
1
726(42,28%)
705(41,49%)
615(41,95%)
597(41,95%)
2
245(14,27%)
269(15,83%)
211(14,39%)
231(16,23%)
3
33(1,92%)
30(1,77%)
27(1,84%)
26(1,83%)
Итого
1717
1699
1466
1423
1 месяц после лечения - исходные данные
-1
65(3,81%)
50(2,97%)
52(3,57%)
43(3,05%)
0
1477(86,48%)
1444(85,70%)
1275(87,45%)
1199(85,16%)
1
166(9,72%)
191(11,34%)
131(8,98%)
166(11,79%)
Итого
1708
1685
1458
1408
Проверка по критерию
Уилкоксона (Р)
5858,0(0,0000)
8530,5(0,0000)
3634,00(0,0000)
6457,50(0,0000)
3 месяца после лечения
0
809(47,12%)
776(45,65%)
693(47,89%)
637(45,31%)
1
677(39,43%)
697(41,00%)
566(39,12%)
586(41,68%)
2
210(12,23%)
206(12,12%)
172(11,89%)
168(11,95%)
3
21(1,22%)
21(1,24%)
16(1,11%)
15(1,07%)
Итого
1717
1700
1447
1406
3 месяца после лечения - исходные данные
-1
62(3,63%)
60(3,56%)
47(3,26%)
46(3,30%)
0
1387(81,21%)
1340(79,53%)
1177(81,68%)
1099(78,84%)
1
259(15,16%)
285(16,91%)
217(15,06%)
249(17,86%)
Итого
1708
1685
1441
1394
Проверка по критерию
Уилкоксона (Р)
15859(0,0000)
19463(0,0000)
11262,50(0,0000)
15022,00(0,0000)
6 месяцев после лечения 1 месяц после лечения
0
871(50,70%)
863(50,76%)
750(52,48%)
708(51,05%)
1
657(38,24%)
645(37,94%)
540(37,79%)
536(38,64%)
2
179(10,42%)
170(10,00%)
133(9,31%)
130(9,37%)
3
11(0,64%)
22(1,29%)
6(0,42%)
13(0,94%)
Итого
1718
1700
1429
1387
6 месяцев после лечения - исходные данные
-1
67(3,92%)
57(3,38%)
49(3,44%)
37(2,69%)
0
1322(77,40%)
1268(75,25%)
1104(77,47%)
1024(74,42%)
1
319(18,68%)
360(21,36%)
272(19,09%)
315(22,89%)
Итого
1708
1685
1425
1376
Проверка по критерию
Уилкоксона (Р)
24381(0,0000)
31664(0,0000)
17951,50(0,0000)
24533,50(0,0000)
9 месяцев после лечения
0
912(53,08%)
913(53,71%)
788(55,69%)
743(54,75%)
1
653(38,01%)
639(37,59%)
520(36,75%)
515(37,95%)
2
142(8,27%)
133(7,82%)
101(7,14%)
93(6,85%)
3
11(0,64%)
15(0,88%)
6(0,42%)
6(0,44%)
Итого
1718
1700
1415
1357
9 месяцев после лечения - исходные данные
-1
59(3,45%)
54(3,20%)
40(2,85%)
29(2,15%)
0
1284(75,18%)
1210(71,81%)
1049(74,66%)
949(70,35%)
1
365(21,37%)
421(24,99%)
316(22,49%)
371(27,50%)
Итого
1708
1685
1405
1349
Проверка по критерию
Уилкоксона (Р)
32513(0,0000)
43673(0,0000)
24633,00(0,0000)
34285,50(0,0000)
12 месяцев после лечения
0
1011(58,85%)
978(57,53%)
870(62,01%)
806(59,75%)
1
590(34,34%)
617(36,29%)
463(33,00%)
489(36,25%)
2
104(6,05%)
94(5,53%)
63(4,49%о)
53(3,93%)
3
13(0,76%)
11(0,65%)
7(0,50%)
1(0,07%)
Итого
1718
1700
1403
1349
12 месяцев после лечения - исходные данные
-1
56(3,28%)
55(3,26%)
37(2,65%)
27(2,02%)
0
1202(70,37%)
1155(68,55%)
967(69,22%)
891(66,54%)
1
450(26,35%)
475(28,19%)
393(28,13%)
421(31,44%)
Итого
1708
1685
1397
1339
Проверка по критерию
Уилкоксона (Р)
49940(0,0000)
55755(0,0000)
38359,00(0,0000)
44226,50(0,0000)
Последующее наблюдение
0
882(61,72%)
826(59,94%)
862(61,79%)
802(59,76%)
1
465(32,54%)
487(35,34%)
452(32,40%)
475(35,39%)
2
76(5,32%)
61(4,43%)
75(5,38%)
61(4,55%)
3
6(0,42%)
4(0,29%)
6(0,43%)
4(0,30%)
Итого
1429
1378
1395
1342
Последующее наблюдение - исходные данные
-1
39(2,75%)
30(2,19%)
39(2,82%)
30(2,25%)
0
950(66,95%)
914(66,76%)
932(67,29%)
892(66,92%)
1
430(30,30%)
425(31,04%)
414(29,89%)
411(30,83%)
Итого
1419
1369
1385
1333
Проверка по критерию
Уилкоксона (Р)
45943(0,0000)
45030(0,0000)
42562,50(0,0000)
42100,50(0,0000)
Таблица 36
Определение изменения бледности при различных наблюдениях
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,55
0,5821
0,82
0,4120
1 месяц после лечения
Проверка по критерию суммы рангов
0,71
0,4797
1,29
0,1977
1 месяц после лечения - исходные данные
Проверка по критерию суммы рангов
1,94
0,0522
2,46
0,0137
3 месяца после лечения
Проверка по критерию суммы рангов
0,68
0,4981
1,14
0,2523
3 месяца после лечения - исходные данные
Проверка по критерию суммы рангов
1,27
0,2024
1,79
0,0741
6 месяцев после лечения
Проверка по критерию суммы рангов
0,07
0,9429
0,83
0,4056
6 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
2,06
0,0394
2,64
0,0083
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,36
0,7175
0,39
0,6987
9 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
2,42
0,0155
3,17
0,0015
12 месяцев после лечения
Проверка по критерию суммы рангов
0,56
0,5750
0,93
0,3509
12 месяцев после лечения - исходные данные
Проверка по критерию суммы рангов
1,13
0,2598
2,05
0,0405
Последующее наблюдение
Проверка по критерию суммы рангов
0,69
0,4925
0,81
0,4160
Последующее наблюдение - исходные данные
Проверка по критерию суммы рангов
0,62
0,5363
0,72
0,4698
1.6.4.4 Сиэтловский опросник качества жизни при стенокардии (SAQ) В SAQ были представлены результаты оценок при различных наблюдениях, а для межгруппового сравнения использовался критерий суммы рангов Уилкоксона.
Таблица 37
Различные наблюдения (Вопрос 1-1)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
1(0,06%)
3(0,17%)
1(0,07%)
3(0,21%)
Умеренное ограничение
16(0,92%)
18(1,05%)
13(0,87%)
14(0,97%)
Легкое ограничение
34(1,95%)
41(2,39%)
30(2,01%)
32(2,21%)
Незначительное ограничение
102(5,86%)
104(6,05%)
87(5,82%)
88(6,09%)
Без ограничений
1582(90,92%)
1547(90,05%)
1359(90,96%)
1305(90,31%)
Другие причины ограничения
5(0,29%)
5(0,29%)
4(0,27%)
3(0,21%)
Итого
1740
1718
1494
1445
1 месяц после лечения
Значительное ограничение
2(0,11%)
0(0,00%)
1(0,07%)
0(0,00%)
Умеренное ограничение
11(0,63%)
11(0,64%)
9(0,60%)
8(0,55%)
Легкое ограничение
24(1,38%)
36(2,09%)
21(1,41%)
26(1,80%)
Незначительное ограничение
95(5,45%)
89(5,16%)
80(5,38%)
73(5,06%)
Без ограничений
1607(92,20%)
1584(91,83%)
1375(92,41%)
1333(92,31%)
Другие причины ограничения
4(0,23%)
5(0,29%)
2(0,13%)
4(0,28%)
Итого
1743
1725
1488
1444
3 месяца после лечения
Значительное ограничение
1(0,06%)
0(0,00%)
0 (0,00%)
0 (0,00%)
Умеренное ограничение
7(0,40%)
8(0,46%)
6(0,41%)
4 (0,28%)
Легкое ограничение
26(1,49%)
36(2,09%)
22(1,50%)
26(1,82%)
Незначительное ограничение
72(4,13%)
70(4,06%)
58 (3,95%)
56 (3,92%)
Без ограничений
1634(93,69%)
1609(93,28%)
1381(93,95%)
1343(93,92%)
Другие причины ограничения
4(0,23%)
2(0,12%)
3(0,20%)
1(0,07%)
Итого
1744
1725
1470
1430
6 месяцев после лечения
Значительное ограничение
1(0,06%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
4(0,23%)
7(0,41%)
4(0,28%)
3(0,21%)
Легкое ограничение
29(1,66%)
23(1,33%)
22(1,52%)
14(1,00%)
Незначительное ограничение
69(3,96%)
77(4,46%)
53(3,66%)
58(4,13%)
Без ограничений
1638(93,92%)
1613(93,51%)
1368(94,34%)
1325(94,37%)
Другие причины ограничения
3(0,17%)
5(0,29%)
3(0,21%)
4(0,28%)
Итого
1744
1725
1450
1404
9 месяцев после лечения
Значительное ограничение
1(0,06%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
5(0,29%)
9(0,52%)
3(0,21%)
5(0,36%)
Легкое ограничение
25(1,43%)
21(1,22%)
18(1,25%)
11(0,80%)
Незначительное ограничение
67(3,84%)
71(4,12%)
47(3,27%)
49(3,55%)
Без ограничений
1643(94,21%)
1618(93,80%)
1366(95,06%)
1309(94,92%)
Другие причины ограничения
3(0,17%)
6(0,35%)
3(0,21%)
5(0,36%)
Итого
1744
1725
1437
1379
12 месяцев после лечения
Значительное ограничение
1(0,06%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
4(0,23%)
7(0,41%)
1(0,07%)
1(0,07%)
Легкое ограничение
15(0,86%)
16(0,93%)
7(0,49%)
6(0,44%)
Незначительное ограничение
61(3,50%)
68(3,94%)
41(2,88%)
44(3,22%)
Без ограничений
1659(95,13%)
1630(94,49%)
1371(96,28%)
1312(96,12%)
Другие причины ограничения
4(0,23%)
4(0,23%)
4(0,28%)
2(0,15%)
Итого
1744
1725
1424
1365
Последующее наблюдение
Значительное ограничение
1(0,07%)
3(0,22%)
1(0,07%)
3(0,22%)
Умеренное ограничение
1(0,07%)
2(0,14%)
1(0,07%)
2(0,15%)
Легкое ограничение
6(0,42%)
6(0,43%)
6(0,43%)
6(0,44%)
Незначительное ограничение
45(3,12%)
45(3,23%)
44(3,12%)
45(3,32%)
Без ограничений
1386(95,98%)
1334(95,83%)
1352(95,95%)
1298(95,72%)
Другие причины ограничения
5(0,35%)
2(0,14%)
5(0,35%)
2(0,15%)
Итого
1444
1392
1409
1356
Таблица 38
Проверка различных наблюдений (Вопрос 1-1)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое знaчeние
P-значение
Исходные данные
Проверка по критерию суммы рангов
-0,90
0,3683
-0,73
0,4642
1 месяц после лечения
Проверка по критерию суммы рангов
-0,31
0,7564
0,17
0,8666
3 месяца после лечения
Проверка по критерию суммы рангов
-0,79
0,4318
-0,33
0,7400
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,21
0,8367
0,24
0,8087
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,08
0,9347
0,21
0,8305
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,83
0,4038
-0,58
0,5613
Последующее наблюдение
Проверка по критерию суммы рангов
-0,74
0,4565
-0,85
0,3960
Таблица 39
Различные наблюдения (Вопрос 1-2)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
2(0,11%)
3(0,17%)
2(0,13%)
3(0,21%)
Умеренное ограничение
18(1,03%)
17(0,99%)
13(0,87%)
14(0,97%)
Легкое ограничение
46(2,64%)
54(3,14%)
42(2,81%)
41(2,84%)
Незначительное ограничение
129(7,41%)
136(7,92%)
113(7,56%)
114(7,89%)
Без ограничений
1539(88,45%)
1505(87,60%)
1319(88,29%)
1271(87,96%)
Другие причины ограничения
6(0,34%)
3(0,17%)
5(0,33%)
2(0,14%)
Итого
1740
1718
1494
1445
1 месяц после лечения
Значительное ограничение
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
14(0,80%)
11(0,64%)
10(0,67%)
9(0,62%)
Легкое ограничение
32(1,84%)
42(2,44%)
30(2,02%)
31(2,15%)
Незначительное ограничение
116(6,66%)
124(7,19%)
99(6,65%)
103(7,13%)
Без ограничений
1575(90,36%)
1544(89,56%)
1345(90,39%)
1299(89,96%)
Другие причины ограничения
6(0,34%)
3(0,17%)
4(0,27%)
2(0,14%)
Итого
1743
1724
1488
1444
3 месяца после лечения
Значительное ограничение
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
10(0,57%)
8(0,46%)
8(0,54%)
4(0,28%)
Легкое ограничение
23(1,32%)
43(2,49%)
19(1,29%)
31(2,17%)
Незначительное ограничение
101(5,79%)
95(5,51%)
84(5,71%)
78(5,45%)
Без ограничений
1603(91,92%)
1575(91,30%)
1353(92,04%)
1315(91,96%)
Другие причины ограничения
7(0,40%)
4(0,23%)
6(0,41%)
2(0,14%)
Итого
1744
1725
1470
1430
6 месяцев после лечения
Значительное ограничение
1(0,06%)
0(0,00%)
1(0,07%)
0(0,00%)
Умеренное ограничение
8(0,46%)
8(0,46%)
6(0,41%)
4(0,28%)
Легкое ограничение
27(1,55%)
32(1,86%)
19(1,31%)
19(1,35%)
Незначительное ограничение
87(4,99%)
93(5,39%)
66(4,55%)
73(5,20%)
Без ограничений
1615(92,60%)
1586(91,94%)
1352(93,24%)
1304(92,88%)
Другие причины ограничения
6(0,34%)
6(0,35%)
6(0,41%)
4(0,28%)
Итого
1744
1725
1450
1404
9 месяцев после лечения
Значительное ограничение
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
7(0,40%)
10(0,58%)
4(0,28%)
5(0,36%)
Легкое ограничение
29(1,66%)
27(1,57%)
20(1,39%)
13(0,94%)
Незначительное ограничение
72(4,13%)
79(4,58%)
50(3,48%)
54(3,92%)
Без ограничений
1631(93,52%)
1602(92,87%)
1358(94,50%)
1301(94,34%)
Другие причины ограничения
5(0,29%)
7(0,41%)
5(0,35%)
6(0,44%)
Итого
1744
1725
1437
1379
12 месяцев после лечения
Значительное ограничение
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Умеренное ограничение
6(0,34%)
8(0,46%)
1(0,07%)
1(0,07%)
Легкое ограничение
18(1,03%)
23(1,33%)
8(0,56%)
9(0,66%)
Незначительное ограничение
67(3,84%)
79(4,58%)
45(3,16%)
52(3,81%)
Без ограничений
1647(94,44%)
1610(93,33%)
1365(95,79%)
1300(95,24%)
Другие причины ограничения
6(0,34%)
5(0,29%)
6(0,42%)
3(0,22%)
Итого
1744
1725
1425
1365
Последующее наблюдение
Значительное ограничение
2(0,14%)
3(0,22%)
2(0,14%)
3(0,22%)
Умеренное ограничение
0(0,00%)
3(0,22%)
0(0,00%)
3(0,22%)
Легкое ограничение
8(0,55%)
4(0,29%)
8(0,57%)
4(0,29%)
Незначительное ограничение
57(3,95%)
52(3,74%)
56(3,97%)
51(3,76%)
Без ограничений
1370(94,88%)
1326(95,26%)
1336(94,82%)
1291(95,21%)
Без ограничений
7(0,48%)
4(0,29%)
7(0,50%)
4(0,29%)
Итого
1444
1392
1409
1356
Таблица 40
Проверка различных наблюдений (Вопрос 1-2)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-1,07
0,2868
-0,59
0,5561
1 месяц после лечения
Проверка по критерию суммы рангов
-1,11
0,2687
-0,61
0,5434
3 месяца после лечения
Проверка по критерию суммы рангов
-1,05
0,2923
-0,62
0,5328
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,72
0,4716
-0,62
0,5356
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,49
0,6268
0,03
0,9734
12 месяцев после лечения
Проверка по критерию суммы рангов
-1,49
0,1363
-1,20
0,2294
Последующее наблюдение
Проверка по критерию суммы рангов
-0,01
0,9927
-0,01
0,9885
Таблица 41
Различные наблюдения (Вопрос 1-3)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
15(0,86%)
13(0,76%)
12(0,80%)
11(0,76%)
Умеренное ограничение
53(3,05%)
45(2,63%)
44(2,95%)
36(2,49%)
Легкое ограничение
149(8,57%)
163(9,52%)
135(9,04%)
144(9,98%)
Незначительное ограничение
340(19,56%)
348(20,32%)
307(20,56%)
305(21,14%)
Без ограничений
1170(67,32%)
1135(66,26%)
985(65,97%)
941(65,21%)
Другие причины ограничения
11(0,63%)
9(0,53%)
10(0,67%)
6(0,42%)
Итого
1738
1713
1493
1443
1 месяц после лечения
Значительное ограничение
5(0,29%)
5(0,29%)
5(0,34%)
4(0,28%)
Умеренное ограничение
34(1,95%)
34(1,97%)
25(1,68%)
27(1,87%)
Легкое ограничение
126(7,23%)
139(8,06%)
114(7,67%)
123(8,52%)
Незначительное ограничение
307(17,62%)
306(17,75%)
271(18,24%)
265(18,36%)
Без ограничений
1261(72,39%)
1233(71,52%)
1064(71,60%)
1018(70,55%)
Другие причины ограничения
9(0,52%)
7(0,41%)
7(0,47%)
6(0,42%)
Итого
1742
1724
1486
1443
3 месяца после лечения
Значительное ограничение
5(0,29%)
4(0,23%)
5(0,34%)
2(0,14%)
Умеренное ограничение
23(1,32%)
28(1,62%)
16(1,09%)
19(1,33%)
Легкое ограничение
93(5,33%)
111(6,44%)
81(5,51%)
91(6,36%)
Незначительное ограничение
296(16,97%)
305(17,69%)
257(17,48%)
265(18,53%)
Без ограничений
1318(75,57%)
1268(73,55%)
1103(75,03%)
1048(73,29%)
Другие причины ограничения
9(0,52%)
8(0,46%)
8(0,54%)
5(0,35%)
Итого
1744
1724
1470
1430
6 месяцев после лечения
Значительное ограничение
4(0,23%)
3(0,17%)
4(0,28%)
2(0,14%)
Умеренное ограничение
20(1,15%)
25(1,45%)
14(0,97%)
12(0,85%)
Легкое ограничение
86(4,93%)
92(5,34%)
65(4,48%)
75(5,34%)
Незначительное ограничение
265(15,19%)
289(16,76%)
227(15,66%)
242(17,24%)
Без ограничений
1358(77,87%)
1307(75,81%)
1131(78,00%)
1067(76,00%)
Другие причины ограничения
11(0,63%)
8(0,46%)
9(0,62%)
6(0,43%)
Итого
1744
1724
1450
1404
9 месяцев после лечения
Значительное ограничение
2(0,11%)
2(0,12%)
1(0,07%)
1(0,07%)
Умеренное ограничение
17(0,97%)
21(1,22%)
10(0,70%)
8(0,58%)
Легкое ограничение
58(3,33%)
70(4,06%)
37(2,57%)
51(3,70%)
Незначительное ограничение
238(13,65%)
272(15,78%)
196(13,64%)
218(15,83%)
Без ограничений
1421(81,48%)
1350(78,31%)
1187(82,60%)
1092(79,30%)
Другие причины ограничения
8(0,46%)
9(0,52%)
6(0,42%)
7(0,51%)
Итого
1744
1724
1437
1377
12 месяцев после лечения
Значительное ограничение
2(0,11%)
1(0,06%)
1(0,07%)
0(0,00%)
Умеренное ограничение
11(0,63%)
20(1,16%)
3(0,21%)
5(0,37%)
Легкое ограничение
54(3,10%)
46(2,67%)
30(2,11%)
26(1,90%)
Незначительное ограничение
196(11,24%)
222(12,88%)
157(11,03%)
169(12,38%)
Без ограничений
1471(84,35%)
1428(82,83%)
1225(86,03%)
1161(85,05%)
Другие причины ограничения
10(0,57%)
7(0,41%)
8(0,56%)
4(0,29%)
Итого
1744
1724
1424
1365
Последующее наблюдение
Значительное ограничение
2(0,14%)
3(0,22%)
2(0,14%)
3(0,22%)
Умеренное ограничение
6(0,42%)
6(0,43%)
6(0,43%)
6(0,44%)
Легкое ограничение
30(2,08%)
16(1,15%)
30(2,13%)
16(1,18%)
Незначительное ограничение
190(13,17%)
205(14,73%)
182(12,93%)
198(14,60%)
Без ограничений
1206(83,58%)
1157(83,12%)
1179(83,74%)
1128(83,19%)
Другие причины ограничения
9(0,62%)
5(0,36%)
9(0,64%)
5(0,37%)
Итого
1443
1392
1408
1356
Таблица 42
Проверка различных наблюдений (Вопрос 1-3)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,70
0,4863
-0,62
0,5323
1 месяц после лечения
Проверка по критерию суммы рангов
-0,76
0,4470
-0,77
0,4437
3 месяца после лечения
Проверка по критерию суммы рангов
-1,53
0,1271
-1,31
0,1906
6 месяцев после лечения
Проверка по критерию суммы рангов
-1,62
0,1045
-1,46
0,1441
9 месяцев после лечения
Проверка по критерию суммы рангов
2,25
0,0242
-2,14
0,0327
12 месяцев после лечения
Проверка по критерию суммы рангов
-1,41
0,1597
-1,07
0,2868
Последующее наблюдение
Проверка по критерию суммы рангов
-0,57
0,5701
-0,63
0,5275
Таблица 43
Различные наблюдения (Вопрос 1-4)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
59(3,41%)
64(3,73%)
51(3,43%)
56(3,88%)
Умеренное ограничение
208(12,01%)
206(12,02%)
185(12,42%)
180(12,48%)
Легкое ограничение
402(23,21%)
384(22,40%)
347(23,30%)
338(23,44%)
Незначительное ограничение
554(31,99%)
559(32,61%)
478(32,10%)
470(32,59%)
Без ограничений
495(28,58%)
485(28,30%)
414(27,80%)
384(26,63%)
Другие причины ограничения
14(0,81%)
16(0,93%)
14(0,94%)
14(0,97%)
Итого
1732
1714
1489
1442
1 месяц после лечения
Значительное ограничение
35(2,01%)
34(1,97%)
27(1,82%)
30(2,08%)
Умеренное ограничение
159(9,13%)
150(8,71%)
138(9,31%)
129(8,95%)
Легкое ограничение
349(20,05%)
332(19,27%)
303(20,43%)
281(19,50%)
Незначительное ограничение
568(32,62%)
608(35,29%)
483(32,57%)
514(35,67%)
Без ограничений
618(35,50%)
587(34,07%)
521(35,13%)
476(33,03%)
Другие причины ограничения
12(0,69%)
12(0,70%)
11(0,74%)
11(0,76%)
Итого
1741
1723
1483
1441
3 месяца после лечения
Значительное ограничение
29(1,66%)
29(1,68%)
22(1,50%)
23(1,61%)
Умеренное ограничение
120(6,88%)
120(6,96%)
105(7,16%)
97(6,79%)
Легкое ограничение
325(18,65%)
309(17,91%)
278(18,95%)
264(18,47%)
Незначительное ограничение
589(33,79%)
604(35,01%)
492(33,54%)
513(35,90%)
Без ограничений
668(38,32%)
652(37,80%)
559(38,10%)
523(36,60%)
Другие причины ограничения
12(0,69%)
11(0,64%)
11(0,75%)
9(0,63%)
Итого
1743
1725
1467
1429
6 месяцев после лечения
Значительное ограничение
29(1,66%)
26(1,51%)
20(1,38%)
18(1,28%)
Умеренное ограничение
97(5,56%)
104(6,03%)
74(5,11%)
75(5,34%)
Легкое ограничение
314(18,00%)
278(16,12%)
266(18,37%)
223(15,88%)
Незначительное ограничение
560(32,11%)
598(34,67%)
463(31,98%)
513(36,54%)
Без ограничений
731(41,92%)
713(41,33%)
613(42,33%)
570(40,60%)
Другие причины ограничения
13(0,75%)
6(0,35%)
12(0,83%)
5(0,36%)
Итого
1744
1725
1448
1404
9 месяцев после лечения
Значительное ограничение
19(1,09%)
22(1,28%)
9(0,63%)
12(0,87%)
Умеренное ограничение
85(4,87%)
80(4,64%)
63(4,39%)
50(3,63%)
Легкое ограничение
264(15,14%)
255(14,78%)
208(14,49%)
194(14,08%)
Незначительное ограничение
569(32,63%)
581(33,68%)
472(32,89%)
489(35,49%)
Без ограничений
797(45,70%)
774(44,87%)
673(46,90%)
622(45,14%)
Другие причины ограничения
10(0,57%)
13(0,75%)
10(0,70%)
11(0,80%)
Итого
1744
1725
1435
1378
12 месяцев после лечения
Значительное ограничение
13(0,75%)
17(0,99%)
2(0,14%)
7(0,51%)
Умеренное ограничение
66(3,78%)
73(4,23%)
41(2,88%)
41(3,01%)
Легкое ограничение
236(13,53%)
224(12,99%)
177(12,43%)
164(12,02%)
Незначительное ограничение
565(32,40%)
570(33,04%)
469(32,94%)
476(34,90%)
Без ограничений
853(48,91%)
831(48,17%)
724(50,84%)
669(49,05%)
Другие причины ограничения
11(0,63%)
10(0,58%)
11(0,77%)
7(0,51%)
Итого
1744
1725
1424
1364
Последующее наблюдение
Значительное ограничение
5(0,35%)
6(0,43%)
5(0,36%)
6(0,44%)
Умеренное ограничение
38(2,64%)
30(2,16%)
37(2,63%)
30(2,22%)
Легкое ограничение
177(12,28%)
176(12,67%)
172(12,23%)
173(12,79%)
Незначительное ограничение
436(30,26%)
448(32,25%)
428(30,44%)
439(32,45%)
Без ограничений
775(53,78%)
720(51,84%)
754(53,63%)
696(51,44%)
Другие причины ограничения
10(0,69%)
9(0,65%)
10(0,71%)
9(0,67%)
Итого
1441
1389
1406
1353
Таблица 44
Проверка различных наблюдений (Вопрос 1-4)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,02
0,9870
-0,63
0,5294
1 месяц после лечения
Проверка по критерию суммы рангов
-0,09
0,9267
-0,42
0,6741
3 месяца после лечения
Проверка по критерию суммы рангов
-0,07
0,9470
-0,38
0,7062
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,09
0,9282
-0,34
0,7364
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,13
0,8985
-0,37
0,7113
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,48
0,6338
-0,99
0,3205
Последующее наблюдение
Проверка по критерию суммы рангов
-0,83
0,4039
-0,98
0,3274
Таблица 45
Различные наблюдения (Вопрос 1-5)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуем
Исходные данные
Значительное ограничение
53(3,05%)
54(3,16%)
46(3,09%)
46(3,19%)
Умеренное ограничение
238(13,72%)
238(13,91%)
210(14,08%)
213(14,78%)
Легкое ограничение
357(20,58%)
369(21,57%)
309(20,72%)
315(21,86%)
Незначительное ограничение
507(29,22%)
489(28,58%)
441(29,58%)
421(29,22%)
Без ограничений
567(32,68%)
543(31,74%)
473(31,72%)
431(29,91%)
Другие причины ограничения
13(0,75%)
18(1,05%)
12(0,80%)
15(1,04%)
Итого
1735
1711
1491
1441
1 месяц после лечения
Значительное ограничение
32(1,84%)
30(1,74%)
24(1,62%)
26(1,80%)
Умеренное ограничение
196(11,26%)
182(10,57%)
166(11,20%)
161(11,17%)
Легкое ограничение
315(18,09%)
324(18,82%)
278(18,76%)
273(18,93%)
Незначительное ограничение
540(31,02%)
530(30,78%)
459(30,97%)
449(31,14%)
Без ограничений
648(37,22%)
644(37,40%)
546(36,84%)
524(36,34%)
Другие причины ограничения
10(0,57%)
12(0,70%)
9(0,61%)
9(0,62%)
Итого
1741
1722
1482
1442
3 месяца после лечения
Значительное ограничение
21(1,20%)
27(1,57%)
16(1,09%)
19(1,33%)
Умеренное ограничение
162(9,29%)
159(9,22%)
137(9,34%)
136(9,52%)
Легкое ограничение
311(17,84%)
288(16,71%)
268(18,27%)
241(16,86%)
Незначительное ограничение
528(30,29%)
556(32,25%)
441(30,06%)
473(33,10%)
Без ограничений
709(40,68%)
683(39,62%)
594(40,49%)
553(38,70%)
Другие причины ограничения
12(0,69%)
11(0,64%)
11(0,75%)
7(0,49%)
Итого
1743
1724
1467
1429
6 месяцев после лечения
Значительное ограничение
20(1,15%)
21(1,22%)
12(0,83%)
11(0,78%)
Умеренное ограничение
137(7,86%)
131(7,59%)
109(7,53%)
104(7,42%)
Легкое ограничение
292(16,75%)
286(16,58%)
244(16,86%)
231(16,48%)
Незначительное ограничение
526(30,18%)
539(31,25%)
433(29,92%)
453(32,31%)
Без ограничений
755(43,32%)
740(42,90%)
637(44,02%)
598(42,65%)
Другие причины ограничения
13(0,75%)
8(0,46%)
12(0,83%)
5(0,36%)
Итого
1743
1725
1447
1402
9 месяцев после лечения
Значительное ограничение
17(0,98%)
17(0,99%)
9(0,63%)
6(0,44%)
Умеренное ограничение
103(5,91%)
105(6,09%)
77(5,37%)
73(5,30%)
Легкое ограничение
284(16,29%)
293(16,99%)
226(15,75%)
235(17,05%)
Незначительное ограничение
503(28,86%)
493(28,58%)
408(28,43%)
400(29,03%)
Без ограничений
825(47,33%)
805(46,67%)
705(49,13%)
656(47,61%)
Другие причины ограничения
11(0,63%)
12(0,70%)
10(0,70%)
8(0,58%)
Итого
1743
1725
1435
1378
12 месяцев после лечения
Значительное ограничение
13(0,75%)
17(0,99%)
3(0,21%)
6(0,44%)
Умеренное ограничение
79(4,53%)
82(4,75%)
52(3,66%)
49(3,60%)
Легкое ограничение
260(14,92%)
260(15,07%)
198(13,93%)
205(15,04%)
Незначительное ограничение
517(29,66%)
511(29,62%)
422(29,70%)
411(30,15%)
Без ограничений
863(49,51%)
843(48,87%)
736(51,79%)
685(50,26%)
Другие причины ограничения
11(0,63%)
12(0,70%)
10(0,70%)
7(0,51%)
Итого
1743
1725
1421
1363
Последующее наблюдение
Значительное ограничение
9(0,62%)
6(0,43%)
9(0,64%)
6(0,44%)
Умеренное ограничение
57(3,96%)
62(4,47%)
57(4,05%)
61(4,51%)
Легкое ограничение
189(13,12%)
199(14,34%)
181(12,87%)
195(14,42%)
Незначительное ограничение
395(27,41%)
397(28,60%)
386(27,45%)
389(28,77%)
Без ограничений
783(54,34%)
717(51,66%)
765(54,41%)
694(51,33%)
Другие причины ограничения
8(0,56%)
7(0,50%)
8(0,57%)
7(0,52%)
Итого
1441
1388
1406
1352
Таблица 46
Проверка различных наблюдений (Вопрос 1-5)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,55
0,5790
-1,05
0,2935
1 месяц после лечения
Проверка по критерию суммы рангов
0,28
0,7792
-0,27
0,7871
3 месяца после лечения
Проверка по критерию суммы рангов
-0,28
0,7809
-0,60
0,5495
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,23
0,8186
-0,63
0,5305
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,47
0,6353
-0,85
0,3927
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,44
0,6574
-1,05
0,2944
Последующее наблюдение
Проверка по критерию суммы рангов
-1,48
0,1377
-1,68
0,0935
Таблица 47
Различные наблюдения (Вопрос 1-6)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
117(6,75%)
105(6,14%)
104(6,99%)
95(6,61%)
Умеренное ограничение
311(17,95%)
334(19,53%)
274(18,43%)
298(20,72%)
Легкое ограничение
362(20,89%)
347(20,29%)
306(20,58%)
284(19,75%)
Незначительное ограничение
479(27,64%)
493(28,83%)
416(27,98%)
424(29,49%)
Без ограничений
448(25,85%)
414(24,21%)
372(25,02%)
323(22,46%)
Другие причины ограничения
16(0,92%)
17(0,99%)
15(1,01%)
14(0,97%)
Итого
1733
1710
1487
1438
1 месяц после лечения
Значительное ограничение
90(5,18%)
82(4,77%)
70(4,75%)
73(5,08%)
Умеренное ограничение
258(14,85%)
257(14,94%)
229(15,53%)
228(15,87%)
Легкое ограничение
322(18,54%)
335(19,48%)
269(18,24%)
269(18,72%)
Незначительное ограничение
539(31,03%)
550(31,98%)
465(31,53%)
473(32,92%)
Без ограничений
514(29,59%)
481(27,97%)
429(29,08%)
383(26,65%)
Другие причины ограничения
14(0,81%)
15(0,87%)
13(0,88%)
11(0,77%)
Итого
1737
1720
1475
1437
3 месяца после лечения
Значительное ограничение
72(4,14%)
61(3,54%)
56(3,83%)
50(3,52%)
Умеренное ограничение
227(13,05%)
249(14,47%)
203(13,89%)
220(15,48%)
Легкое ограничение
317(18,23%)
298(17,32%)
262(17,92%)
229(16,12%)
Незначительное ограничение
560(32,20%)
593(34,46%)
475(32,49%)
506(35,61%)
Без ограничений
547(31,45%)
504(29,29%)
452(30,92%)
405(28,50%)
Другие причины ограничения
16(0,92%)
16(0,93%)
14(0,96%)
11(0,77%)
Итого
1739
1721
1462
1421
6 месяцев после лечения
Значительное ограничение
67(3,85%)
56(3,25%)
46(3,19%)
43(3,08%)
Умеренное ограничение
205(11,78%)
213(12,36%)
174(12,07%)
175(12,52%)
Легкое ограничение
287(16,49%)
293(17,01%)
234(16,24%)
224(16,02%)
Незначительное ограничение
569(32,70%)
584(33,89%)
476(33,03%)
492(35,19%)
Без ограничений
595(34,20%)
566(32,85%)
495(34,35%)
457(32,69%)
Другие причины ограничения
17(0,98%)
11(0,64%)
16(1,11%)
7(0,50%)
Итого
1740
1723
1441
1398
9 месяцев после лечения
Значительное ограничение
51(2,93%)
49(2,84%)
33(2,30%)
34(2,47%)
Умеренное ограничение
193(11,08%)
184(10,67%)
162(11,31%)
143(10,41%)
Легкое ограничение
275(15,79%)
289(16,76%)
209(14,59%)
218(15,87%)
Незначительное ограничение
558(32,03%)
559(32,42%)
464(32,40%)
457(33,26%)
Без ограничений
650(37,31%)
631(36,60%)
551(38,48%)
515(37,48%)
Другие причины ограничения
15(0,86%)
12(0,70%)
13(0,91%)
7(0,51%)
Итого
1742
1724
1432
1374
12 месяцев после лечения
Значительное ограничение
45(2,58%)
38(2,20%)
25(1,76%)
21(1,55%)
Умеренное ограничение
169(9,70%)
147(8,53%)
136(9,58%)
105(7,73%)
Легкое ограничение
260(14,93%)
306(17,75%)
191(13,45%)
236(17,37%)
Незначительное ограничение
548(31,46%)
532(30,86%)
453(31,90%)
423(31,13%)
Без ограничений
705(40,47%)
689(39,97%)
602(42,39%)
568(41,80%)
Другие причины ограничения
15(0,86%)
12(0,70%)
13(0,92%)
6(0,44%)
Итого
1742
1724
1420
1359
Последующее наблюдение
Значительное ограничение
32(2,22%)
21(1,52%)
32(2,28%)
21(1,55%)
Умеренное ограничение
133(9,24%)
129(9,31%)
129(9,19%)
127(9,40%)
Легкое ограничение
165(11,47%)
186(13,42%)
159(11,32%)
179(13,25%)
Незначительное ограничение
491(34,12%)
455(32,83%)
483(34,40%)
450(33,31%)
Без ограничений
606(42,11%)
588(42,42%)
589(41,95%)
567(41,97%)
Другие причины ограничения
12(0,83%)
7(0,51%)
12(0,85%)
7(0,52%)
Итого
1439
1386
1404
1351
Таблица 48
Проверка различных наблюдений (Вопрос 1-6)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,64
0,5197
-1,23
0,2193
1 месяц после лечения
Проверка по критерию суммы рангов
-0,55
0,5845
-1,18
0,2363
3 месяца после лечения
Проверка по критерию суммы рангов
-0,78
0,4342
-0,87
0,3852
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,74
0,4607
-0,90
0,3661
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,41
0,6850
-0,59
0,5534
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,38
0,7026
-0,65
0,5167
Последующее наблюдение
Проверка по критерию суммы рангов
-0,26
0,7928
-0,41
0,6830
Таблица 49
Различные наблюдения (Вопрос 1-7)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
358(20,94%)
340(20,02%)
315(21,49%)
298(20,84%)
Умеренное ограничение
332(19,42%)
355(20,91%)
285(19,44%)
315(22,03%)
Легкое ограничение
423(24,74%)
416(24,50%)
367(25,03%)
343(23,99%)
Незначительное ограничение
367(21,46%)
381(22,44%)
312(21,28%)
319(22,31%)
Без ограничений
182(10,64%)
158(9,31%)
141(9,62%)
114(7,97%)
Другие причины ограничения
48(2,81%)
48(2,83%)
46(3,14%)
41(2,87%)
Итого
1710
1698
1466
1430
1 месяц после лечения
Значительное ограничение
304(17,68%)
303(17,74%)
259(17,75%)
268(18,75%)
Умеренное ограничение
300(17,45%)
285(16,69%)
256(17,55%)
241(16,86%)
Легкое ограничение
408(23,73%)
425(24,88%)
348(23,85%)
348(24,35%)
Незначительное ограничение
437(25,42%)
447(26,17%)
371(25,43%)
374(26,17%)
Без ограничений
221(12,86%)
198(11,59%)
180(12,34%)
155(10,85%)
Другие причины ограничения
49(2,85%)
50(2,93%)
45(3,08%)
43(3,01%)
Итого
1719
1708
1459
1429
3 месяца после лечения
Значительное ограничение
274(15,88%)
281(16,42%)
232(16,01%)
245(17,31%)
Умеренное ограничение
260(15,07%)
244(14,26%)
216(14,91%)
195(13,78%)
Легкое ограничение
410(23,77%)
435(25,42%)
345(23,81%)
359(25,37%)
Незначительное ограничение
489(28,35%)
484(28,29%)
416(28,71%)
406(28,69%)
Без ограничений
240(13,91%)
217(12,68%)
195(13,46%)
172(12,16%)
Другие причины ограничения
52(3,01%)
50(2,92%)
45(3,11%)
38(2,69%)
Итого
1725
1711
1449
1415
6 месяцев после лечения
Значительное ограничение
265(15,33%)
258(15,08%)
213(14,88%)
210(15,20%)
Умеренное ограничение
233(13,48%)
233(13,62%)
180(12,58%)
173(12,52%)
Легкое ограничение
367(21,23%)
380(22,21%)
307(21,45%)
312(22,58%)
Незначительное ограничение
552(31,93%)
538(31,44%)
471(32,91%)
449(32,49%)
Без ограничений
251(14,52%)
242(14,14%)
207(14,47%)
191(13,82%)
Другие причины ограничения
61(3,53%)
60(3,51%)
53(3,70%)
47(3,40%)
Итого
1729
1711
1431
1382
9 месяцев после лечения
Значительное ограничение
247(14,29%)
239(13,97%)
194(13,71%)
190(14,00%)
Умеренное ограничение
205(11,86%)
230(13,44%)
154(10,88%)
158(11,64%)
Легкое ограничение
375(21,69%)
353(20,63%)
306(21,63%)
281(20,71%)
Незначительное ограничение
540(31,23%)
554(32,38%)
456(32,23%)
463(34,12%)
Без ограничений
309(17,87%)
278(16,25%)
259(18,30%)
222(16,36%)
Другие причины ограничения
53(3,07%)
57(3,33%)
46(3,25%)
43(3,17%)
Итого
1729
1711
1415
1357
12 месяцев после лечения
Значительное ограничение
224(12,95%)
220(12,86%)
169(12,05%)
169(12,56%)
Умеренное ограничение
192(11,10%)
209(12,22%)
138(9,84%)
137(10,18%)
Легкое ограничение
354(20,46%)
353(20,63%)
284(20,24%)
280(20,80%)
Незначительное ограничение
549(31,73%)
552(32,26%)
456(32,50%)
456(33,88%)
Без ограничений
354(20,46%)
315(18,41%)
306(21,81%)
258(19,17%)
Другие причины ограничения
57(3,29%)
62(3,62%)
50(3,56%)
46(3,42%)
Итого
1730
1711
1403
1346
Последующее наблюдение
Значительное ограничение
166(11,67%)
172(12,55%)
162(11,68%)
167(12,51%)
Умеренное ограничение
96(6,75%)
102(7,45%)
92(6,63%)
101(7,57%)
Легкое ограничение
313(22,01%)
285(20,80%)
304(21,92%)
278(20,82%)
Незначительное ограничение
497(34,95%)
489(35,69%)
483(34,82%)
478(35,81%)
Без ограничений
314(22,08%)
295(21,53%)
310(22,35%)
284(21,27%)
Другие причины ограничения
36(2,53%)
27(1,97%)
36(2,60%)
27(2,02%)
Итого
1422
1370
1387
1335
Таблица 50
Проверка различных наблюдений (Вопрос 1-7)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,24
0,8095
-0,78
0,4353
1 месяц после лечения
Проверка по критерию суммы рангов
-0,20
0,8421
-0,71
0,4769
3 месяца после лечения
Проверка по критерию суммы рангов
-0,71
0,4807
-1,04
0,3003
6 месяцев после лечения
Проверка по критерию суммы рангов
0,28
0,7763
-0,67
0,5024
9 месяцев после лечения
Проверка по критерию суммы рангов
0,56
0,5786
-0,72
0,4741
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,91
0,3617
-1,25
0,2130
Последующее наблюдение
Проверка по критерию суммы рангов
-0,76
0,4501
-0,99
0,3216
Таблица 51
Различные наблюдения (Вопрос 1-8)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
444(25,96%)
429(25,34%)
388(26,45%)
376(26,37%)
Умеренное ограничение
386(22,57%)
408(24,10%)
329(22,43%)
348(24,40%)
Легкое ограничение
404(23,63%)
399(23,57%)
358(24,40%)
335(23,49%)
Незначительное ограничение
297(17,37%)
278(16,42%)
246(16,77%)
229(16,06%)
Без ограничений
138(8,07%)
140(8,27%)
109(7,43%)
106(7,43%)
Другие причины ограничения
41(2,40%)
39(2,30%)
37(2,52%)
32(2,24%)
Итого
1710
1693
1467
1426
1 месяц после лечения
Значительное ограничение
383(22,27%)
367(21,51%)
327(22,37%)
323(22,60%)
Умеренное ограничение
353(20,52%)
353(20,69%)
304(20,79%)
291(20,36%)
Легкое ограничение
415(24,13%)
443(25,97%)
363(24,83%)
378(26,45%)
Незначительное ограничение
366(21,28%)
340(19,93%)
305(20,86%)
274(19,17%)
Без ограничений
155(9,01%)
164(9,61%)
121(8,28%)
130(9,10%)
Другие причины ограничения
48(2,79%)
39(2,29%)
42(2,87%)
33(2,31%)
Итого
1720
1706
1462
1429
3 месяца после лечения
Значительное ограничение
362(21,02%)
360(21,08%)
307(21,30%)
305(21,62%)
Умеренное ограничение
308(17,89%)
305(17,86%)
258(17,90%)
248(17,58%)
Легкое ограничение
440(25,55%)
456(26,70%)
372(25,82%)
385(27,29%)
Незначительное ограничение
376(21,84%)
357(20,90%)
311(21,58%)
292(20,69%)
Без ограничений
184(10,69%)
189(11,07%)
151(10,48%)
149(10,56%)
Другие причины ограничения
52(3,02%)
41(2,40%)
42(2,91%)
32(2,27%)
Итого
1722
1708
1441
1411
6 месяцев после лечения
Значительное ограничение
334(19,38%)
331(19,37%)
270(18,96%)
269(19,51%)
Умеренное ограничение
283(16,42%)
292(17,09%)
228(16,01%)
222(16,10%)
Легкое ограничение
436(25,30%)
447(26,16%)
369(25,91%)
374(27,12%)
Незначительное ограничение
422(24,49%)
386(22,59%)
349(24,51%)
312(22,63%)
Без ограничений
183(10,62%)
205(12,00%)
154(10,81%)
165(11,97%)
Другие причины ограничения
65(3,77%)
48(2,81%)
54(3,79%)
37(2,68%)
Итого
1723
1709
1424
1379
9 месяцев после лечения
Значительное ограничение
309(17,93%)
311(18,20%)
243(17,23%)
241(17,76%)
Умеренное ограничение
259(15,03%)
264(15,45%)
199(14,11%)
189(13,93%)
Легкое ограничение
423(24,55%)
428(25,04%)
354(25,11%)
355(26,16%)
Незначительное ограничение
464(26,93%)
433(25,34%)
387(27,45%)
353(26,01%)
Без ограничений
206(11,96%)
217(12,70%)
174(12,34%)
175(12,90%)
Другие причины ограничения
62(3,60%)
56(3,28%)
53(3,76%)
44(3,24%)
Итого
1723
1709
1410
1357
12 месяцев после лечения
Значительное ограничение
291(16,89%)
299(17,50%)
219(15,68%)
222(16,55%)
Умеренное ограничение
230(13,35%)
247(14,45%)
170(12,17%)
177(13,20%)
Легкое ограничение
426(24,72%)
411(24,05%)
349(24,98%)
333(24,83%)
Незначительное ограничение
473(27,45%)
448(26,21%)
397(28,42%)
361(26,92%)
Без ограничений
235(13,64%)
241(14,10%)
203(14,53%)
198(14,77%)
Другие причины ограничения
68(3,95%)
63(3,69%)
59(4,22%)
50(3,73%)
Итого
1723
1709
1397
1341
Последующее наблюдение
Значительное ограничение
208(14,74%)
210(15,37%)
203(14,75%)
205(15,40%)
Умеренное ограничение
168(11,91%)
182(13,32%)
163(11,85%)
178(13,37%)
Легкое ограничение
353(25,02%)
335(24,52%)
343(24,93%)
329(24,72%)
Незначительное ограничение
425(30,12%)
388(28,40%)
414(30,09%)
375(28,17%)
Без ограничений
212(15,02%)
215(15,74%)
208(15,12%)
208(15,63%)
Другие причины ограничения
45(3,19%)
36(2,64%)
45(3,27%)
36(2,70%)
Итого
1411
1366
1376
1331
Таблица 52
Проверка различных наблюдений (Вопрос 1-8)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значе
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,23
0,8193
-0,64
0,5196
1 месяц после лечения
Проверка по критерию суммы рангов
-0,01
0,9943
-0,31
0,7548
3 месяца после лечения
Проверка по критерию суммы рангов
-0,39
0,6969
-0,51
0,6122
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,52
0,6032
-0,72
0,4724
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,44
0,6604
-0,51
0,6086
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,69
0,4877
-0,97
0,3307
Последующее наблюдение
Проверка по критерию суммы рангов
-0,85
0,3968
-1,01
0,3130
Таблица 53
Различные наблюдения (Вопрос 1-9)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Значительное ограничение
802(47,34%)
818(48,69%)
705(48,55%)
711(50,25%)
Умеренное ограничение
359(21,19%)
341(20,30%)
301(20,73%)
277(19,58%)
Легкое ограничение
249(14,70%)
244(14,52%)
213(14,67%)
200(14,13%)
Незначительное ограничение
145(8,56%)
142(8,45%)
108(7,44%)
111(7,84%)
Без ограничений
40(2,36%)
36(2,14%)
33(2,27%)
28(1,98%)
Другие причины ограничения
99(5,84%)
99(5,89%)
92(6,34%)
88(6,22%)
Итого
1694
1680
1452
1415
1 месяц после лечения
Значительное ограничение
714(41,93%)
716(42,24%)
617(42,70%)
613(43,35%)
Умеренное ограничение
358(21,02%)
341(20,12%)
310(21,45%)
285(20,16%)
Легкое ограничение
284(16,68%)
314(18,53%)
239(16,54%)
262(18,53%)
Незначительное ограничение
193(11,33%)
172(10,15%)
143(9,90%)
131(9,26%)
Без ограничений
49(2,88%)
54(3,19%)
43(2,98%)
38(2,69%)
Другие причины ограничения
105(6,17%)
98(5,78%)
93(6,44%)
85(6,01%)
Итого
1703
1695
1445
1414
3 месяца после лечения
Значительное ограничение
664(38,90%)
677(39,85%)
564(39,41%)
565(40,41%)
Умеренное ограничение
342(20,04%)
338(19,89%)
293(20,48%)
281(20,10%)
Легкое ограничение
318(18,63%)
312(18,36%)
264(18,45%)
266(19,03%)
Незначительное ограничение
220(12,89%)
205(12,07%)
170(11,88%)
153(10,94%)
Без ограничений
61(3,57%)
70(4,12%)
53(3,70%)
56(4,01%)
Другие причины ограничения
102(5,98%)
97(5,71%)
87(6,08%)
77(5,51%)
Итого
1707
1699
1431
1398
6 месяцев после лечения
Значительное ограничение
606(35,42%)
625(36,76%)
490(34,70%)
498(36,32%)
Умеренное ограничение
357(20,86%)
339(19,94%)
305(21,60%)
276(20,13%)
Легкое ограничение
341(19,93%)
332(19,53%)
289(20,47%)
283(20,64%)
Незначительное ограничение
243(14,20%)
230(13,53%)
188(13,31%)
179(13,06%)
Без ограничений
58(3,39%)
72(4,24%)
50(3,54%)
54(3,94%)
Другие причины ограничения
106(6,20%)
102(6,00%)
90(6,37%)
81(5,91%)
Итого
1711
1700
1412
1371
9 месяцев после лечения
Значительное ограничение
572(33,39%)
585(34,41%)
452(32,38%)
443(32,96%)
Умеренное ограничение
353(20,61%)
348(20,47%)
292(20,92%)
282(20,98%)
Легкое ограничение
332(19,38%)
340(20,00%)
258(15,18%)
275(19,70%)
288(21,43%)
Незначительное ограничение
293(17,10%)
237(16,98%)
207(1-5,40%)
Без ограничений
67(3,91%)
70(4,12%)
59(4,23%)
47(3,50%)
Другие причины ограничения
96(5,60%)
99(5,82%)
81(5,80%)
77(5,73%)
Итого
1713
1700
1396
1344
12 месяцев после лечения
Значительное ограничение
542(31,62%)
552(32,47%)
412(29,75%)
406(30,55%)
Умеренное ограничение
350(20,42%)
345(20,29%)
289(20,87%)
276(20,77%)
Легкое ограничение
336(19,60%)
322(18,94%)
290(17,06%)
278(20,07%)
271(20,39%)
Незначительное ограничение
307(17,91%)
249(17,98%)
234(17,61%)
Без ограничений
78(4,55%)
92(5,41%)
70(5,05%)
67(5,04%)
Другие причины ограничения
101(5,89%)
99(5,82%)
87(6,28%)
75(5,64%)
Итого
1714
1700
1385
1329
Последующее наблюдение
Значительное ограничение
379(27,13%)
380(28,23%)
372(27,29%)
374(28,53%)
Умеренное ограничение
296(21,19%)
294(21,84%)
264(19,61%)
288(21,13%)
283(21,59%)
Легкое ограничение
285(20,40%)
276(20,25%)
259(19,76%)
Незначительное ограничение
287(20,54%)
276(20,51%)
279(20,47%)
268(20,44%)
Без ограничений
85(6,08%)
73(5,42%)
83(6,09%)
68(5,19%)
Другие причины ограничения
65(4,65%)
59(4,38%)
1346
65(4,77%)
59(4,50%)
Итого
1397
1363
1311
Таблица 54
Проверка различных наблюдений (Вопрос 1-9)
Данные
Метод испытаний
FAS
PP
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-0,63
0,5316
-0,70
0,4812
1 месяц после лечения
Проверка по критерию суммы рангов
-0,20
0,8424
-0,32
0,7475
3 месяца после лечения
Проверка по критерию суммы рангов
-0,54
0,5911
-0,63
0,5301
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,44
0,6593
-0,54
0,5887
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,70
0,4839
-0,76
0,4486
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,30
0,7617
-0,60
0,5458
Последующее наблюдение
Проверка по критерию суммы рангов
-0,90
0,3681
-0,98
0,3292
Таблица 55
Различные наблюдения (2-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Гораздо чаще
55(3,17%)
59(3,45%)
46(3,09%)
46(3,19%)
Несколько чаще
120(6,92%)
122(7,13%)
100(6,72%)
104(7,22%)
С той же частотой
1076(62,09%)
1091(63,73%)
938(63,00%)
938(65,14%)
Несколько реже
266(15,35%)
260(15,19%)
224(15,04%)
209(14,51%)
Гораздо реже
216(12,46%)
180(10,51%)
181(12,16%)
143(9,93%)
Итого
1733
1712
1489
1440
1 месяц после лечения
Гораздо чаще
16(0,92%)
14(0,81%)
8(0,54%)
9(0,62%)
Несколько чаще
53(3,05%)
51(2,96%)
43(2,90%)
43(2,98%)
С той же частотой
853(49,05%)
831(48,29%)
735(49,63%)
698(48,44%)
Несколько реже
530(30,48%)
544(31,61%)
447(30,18%)
451(31,30%)
Гораздо реже
287(16,50%)
281(16,33%)
248(16,75%)
240(16,66%)
Итого
1739
1721
1481
1441
3 месяца после лечения
Гораздо чаще
16(0,92%)
15(0,87%)
6(0,41%)
7(0,49%)
Несколько чаще
66(3,79%)
59(3,42%)
50(3,42%)
42(2,94%)
С той же частотой
733(42,13%)
698(40,51%)
614(41,97%)
574(40,20%)
Несколько реже
557(32,01%)
592(34,36%)
471(32,19%)
499(34,94%)
Гораздо реже
368(21,15%)
359(20,84%)
322(22,01%)
306(21,43%)
Итого
1740
1723
1463
1428
6 месяцев после лечения
Гораздо чаще
17(0,98%)
25(1,45%)
3(0,21%)
10(0,71%)
Несколько чаще
64(3,68%)
69(4,00%)
40(2,76%)
48(3,42%)
С той же частотой
650(37,33%)
584(33,89%)
528(36,46%)
460(32,79%)
Несколько реже
610(35,04%)
658(38,19%)
522(36,05%)
554(39,49%)
Гораздо реже
400(22,98%)
386(22,40%)
355(24,52%)
331(23,59%)
6
0(0,00%)
1(0,06%)
Итого
1741
1723
1448
1403
9 месяцев после лечения
Гораздо чаще
25(1,44%)
29(1,68%)
9(0,63%)
7(0,51%)
Несколько чаще
69(3,96%)
58(3,37%)
46(3,21%)
31(2,24%)
С той же частотой
626(35,94%)
583(33,84%)
501(34,94%)
450(32,59%)
Несколько реже
601(34,50%)
620(35,98%)
505(35,22%)
515(37,29%)
Гораздо реже
421(24,17%)
432(25,07%)
373(26,01%)
378(27,37%)
6
0(0,00%)
1(0,06%)
Итого
1742
1723
1434
1381
12 месяцев после лечения
Гораздо чаще
23(1,32%)
30(1,74%)
2(0,14%)
4(0,29%)
Несколько чаще
55(3,16%)
62(3,60%)
28(1,96%)
34(2,49%))
С той же частотой
659(37,83%)
638(37,03%)
528(37,05%)
500(36,63%)
Несколько реже
525(30,14%)
510(29,60%)
439(30,81%)
404(29,60%)
Гораздо реже
480(27,55%)
482(27,97%)
428(30,04%)
423(30,99%)
6
0(0,00%)
1(0,06%)
Итого
1742
1723
1425
1365
Последующее наблюдение
Гораздо чаще
3(0,21%)
6(0,43%)
3(0,21%)
6(0,44%)
Несколько чаще
107(7,40%)
130(9,36%)
104(7,38%)
127(9,39%)
С той же частотой
567(39,24%)
552(39,74%)
552(39,15%)
539(39,84%)
Несколько реже
366(25,33%)
315(22,68%)
361(25,60%)
305(22,54%)
Гораздо реже
402(27,82%)
386(27,79%)
390(27,66%)
376(27,79%)
Итого
1445
1389
1410
1353
Таблица 56
Проверка различных наблюдений (2-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-1,49
0,1361
-1,75
0,0805
1 месяц после лечения
Проверка по критерию суммы рангов
0,43
0,6660
0,35
0,7274
3 месяца после лечения
Проверка по критерию суммы рангов
0,83
0,4054
0,73
0,4662
6 месяцев после лечения
Проверка по критерию суммы рангов
0,69
0,4929
0,39
0,6986
9 месяцев после лечения
Проверка по критерию суммы рангов
1,30
0,1920
1,78
0,0754
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,07
0,9480
0,07
0,9466
Последующее наблюдение
Проверка по критерию суммы рангов
-1,35
0,1774
-1,38
0,1666
Таблица 57
Различные наблюдения (3-й вопрос)
FAS
РР
Данные
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
4 и более раза в день
55 (3,17%)
59(3,45%)
46(3,09%)
46(3,19%)
1-3 раза в день
120 (6,92%)
122(7,13%)
100(6,72%)
104(7,22%)
3 раза в неделю и чаще
1076 (62,09%)
1091(63,73%)
938(63,00%)
938(65,14%)
1-2 раза в неделю
266(15,35%)
260(15,19%)
224(15,04%)
209(14,51%)
Реже чем раз в неделю
216(12,46%)
180(10,51%)
181(12,16%)
143(9,93%)
Ни разу
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Итого
1733
1712
1489
1440
1 месяц после лечения
4 и более раза в день
16 (0,92%)
14(0,81%)
8(0,54%)
9(0,62%)
1-3 раза в день
53 (3,05%)
51(2,96%)
43(2,90%)
43(2,98%)
3 раза в неделю и чаще
853(49,05%)
831(48,29%)
735(49,63%)
698(48,44%)
1-2 раза в неделю
530(30,48%)
544(31,61%)
447(30,18%)
451(31,30%)
Реже чем раз в неделю
287(16,50%)
281(16,33%)
248(16,75%)
240(16,66%)
Ни разу
0 (0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Итого
1739
1721
1481
1441
3 месяца после лечения
4 и более раза в день
16(0,92%)
15(0,87%)
6(0,41%)
7(0,49%)
1-3 раза в день
66 (3,79%)
59(3,42%)
50(3,42%)
42(2,94%)
3 раза в неделю и чаще
733 (42,13%)
698(40,51%)
614(41,97%)
574(40,20%)
1-2 раза в неделю
557(32,01%)
592(34,36%)
471(32,19%)
499(34,94%)
Реже чем раз в неделю
368(21,15%)
359(20,84%)
322(22,01%)
306(21,43%)
Ни разу
0 (0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Итого
1740
1723
1463
1428
6 месяцев после лечения
4 и более раза в день
17(0,98%)
25(1,45%)
3(0,21%)
10(0,71%)
1-3 раза в день
64 (3,68%)
69(4,00%)
40(2,76%)
48(3,42%)
3 раза в неделю и чаще
650(37,33%)
584(33,89%)
528(36,46%)
460(32,79%)
1-2 раза в неделю
610(35,04%)
658(38,19%)
522(36,05%)
554(39,49%)
Реже чем раз в неделю
400(22,98%)
386(22,40%)
355(24,52%)
331(23,59%)
Ни разу
0 (0,00%)
1(0,06%)
0(0,00%)
0(0,00%)
Итого
1741
1723
1448
1403
9 месяцев после лечения
4 и более раза в день
25 (1,44%)
29(1,68%)
9(0,63%)
7(0,51%)
1-3 раза в день
69 (3,96%)
58(3,37%)
46(3,21%)
31(2,24%)
3 раза в неделю и чаще
626(35,94%)
583(33,84%)
501(34,94%)
450(32,59%)
1-2 раза в неделю
601(34,50%)
620(35,98%)
505(35,22%)
515(37,29%)
Реже чем раз в неделю
421(24,17%)
432(25,07%)
373(26,01%)
378(27,37%)
Ни разу
0(0,00%)
1(0,06%)
0(0,00%)
0(0,00%)
Итого
1742
1723
1434
1381
12 месяцев после лечения
4 и более раза в день
23 (1,32%)
30(1,74%)
2(0,14%)
4(0,29%)
1-3 раза в день
55 (3,16%)
62(3,60%)
28(1,96%)
34(2,49%)
3 раза в неделю и чаще
659 (37,83%)
638(37,03%)
528(37,05%)
500(36,63%)
1-2 раза в неделю
525 (30,14%)
510(29,60%)
439(30,81%)
404(29,60%)
Реже чем раз в неделю
480 (27,55%)
482(27,97%)
428(30,04%)
423(30,99%)
Ни разу
0(0,00%)
1(0,06%)
0(0,00%)
0(0,00%)
Итого
1742
1723
1425
1365
Последующее наблюдение
4 и более раза в день
3 (0,21%)
6(0,43%)
3(0,21%)
6(0,44%)
1-3 раза в день
107(7,40%)
130(9,36%)
104(7,38%)
127(9,39%)
3 раза в неделю и чаще
567(39,24%)
552(39,74%)
552(39,15%)
539(39,84%)
1-2 раза в неделю
366 (25,33%)
315(22,68%)
361(25,60%)
305(22,54%)
Реже чем раз в неделю
402 (27,82%)
386(27,79%)
390(27,66%)
376(27,79%)
Ни разу
0 (0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
Итого
1445
1389
1410
1353
Таблица 58
Проверка различных наблюдений (3-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
-1,49
0,1361
-1,75
0,0805
1 месяц после лечения
Проверка по критерию суммы рангов
0,43
0,6660
0,35
0,7274
3 месяца после лечения
Проверка по критерию суммы рангов
0,83
0,4054
0,73
0,4662
6 месяцев после лечения
Проверка по критерию суммы рангов
0,69
0,4929
0,39
0,6986
9 месяцев после лечения
Проверка по критерию суммы рангов
1,30
0,1920
1,78
0,0754
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,07
0,9480
0,07
0,9466
Последующее наблюдение
Проверка по критерию суммы рангов
-1,35
0,1774
-1,38
0,1666
Таблица 59
Различные наблюдения (4-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
4 и более раза в день
16(0,92%)
20(1,17%)
14(0,94%)
18(1,25%)
1-3 раза в день
150(8,64%)
133(7,75%)
131(8,78%)
120(8,31%)
3 раза в неделю и чаще
293(16,87%)
291(16,96%)
260(17,43%)
247(17,11%)
1-2 раза в неделю
344(19,80%)
367(21,39%)
301(20,17%)
310(21,47%)
Реже чем раз в неделю
176(10,13%)
195(11,36%)
142(9,52%)
163(11,29%)
Ни разу
758(43,64%)
710(41,38%)
644(43,16%)
586(40,58%)
Итого
1737
1716
1492
1444
1 месяц после лечения
4 и более раза в день
1(0,06%)
8(0,46%)
1(0,07%)
8(0,55%)
1-3 раза в день
114(6,54%)
111(6,44%)
97(6,52%)
106(7,33%)
3 раза в неделю и чаще
230(13,19%)
195(11,31%)
204(13,71%)
160(11,06%)
1-2 раза в неделю
306(17,55%)
363(21,06%)
259(17,41%)
301(20,80%)
Реже чем раз в неделю
167(9,58%)
196(11,37%)
135(9,07%)
159(10,99%)
Ни разу
926(53,10%)
851(49,36%)
792(53,23%)
713(49,27%)
Итого
1744
1724
1488
1447
3 месяца после лечения
4 и более раза в день
1(0,06%)
4(0,23%)
0(0,00%)
3(0,21%)
1-3 раза в день
97(5,56%)
93(5,39%)
78(5,31%)
87(6,08%)
3 раза в неделю и чаще
187(10,72%)
172(9,98%)
155(10,55%)
141(9,85%)
1-2 раза в неделю
291(16,69%)
336(19,49%)
251(17,09%)
280(19,55%)
Реже чем раз в неделю
200(11,47%)
209(12,12%)
152(10,35%)
160(11,17%)
Ни разу
968(55,50%)
910(52,78%)
833(56,71%)
761(53,14%)
Итого
1744
1724
1469
1432
6 месяцев после лечения
4 и более раза в день
2(0,11%)
2(0,12%)
1(0,07%)
0(0,00%)
1-3 раза в день
82(4,70%)
83(4,81%)
56(3,85%)
74(5,25%)
3 раза в неделю и чаще
127(7,28%)
119(6,90%)
95(6,53%)
85(6,03%)
1-2 раза в неделю
306(17,55%)
324(18,78%)
263(18,08%)
261(18,52%)
Реже чем раз в неделю
209(11,98%)
239(13,86%)
165(11,34%)
200(14,19%)
Ни разу
1018(58,37%)
958(55,54%)
875(60,14%)
789(56,00%)
Итого
1744
1725
1455
1409
9 месяцев после лечения
4 и более раза в день
2(0,11%)
3(0,17%)
1(0,07%)
0(0,00%)
1-3 раза в день
75(4,30%)
79(4,58%)
49(3,41%)
69(4,99%)
3 раза в неделю и чаще
90(5,16%)
93(5,39%)
58(4,03%)
51(3,68%)
1-2 раза в неделю
272(15,60%)
255(14,78%)
230(15,99%)
191(13,80%)
Реже чем раз в неделю
264(15,14%)
291(16,87%)
215(14,95%)
246(17,77%)
Ни разу
1041(59,69%)
1004(58,20%)
885(61,54%)
827(59,75%)
Итого
1744
1725
1438
1384
12 месяцев после лечения
4 и более раза в день
2(0,11%)
4(0,23%)
0(0,00%)
1(0,07%)
1-3 раза в день
74(4,24%)
78(4,52%)
48(3,36%)
66(4,82%)
3 раза в неделю и чаще
69(3,96%)
77(4,46%)
32(2,24%)
29(2,12%)
1-2 раза в неделю
185(10,61%)
198(11,48%)
147(10,29%)
134(9,80%)
Реже чем раз в неделю
288(16,51%)
234(13,57%)
234(16,38%)
194(14,18%)
Ни разу
1126(64,56%)
1134(65,74%)
968(67,74%)
944(69,01%)
Итого
1744
1725
1429
1368
Последующее наблюдение
4 и более раза в день
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
1-3 раза в день
41(2,84%)
57(4,10%)
40(2,83%)
56(4,14%)
3 раза в неделю и чаще
26(1,80%)
25(1,80%)
26(1,84%)
25(1,85%)
1-2 раза в неделю
192(13,28%)
173(12,45%)
186(13,17%)
168(12,41%)
Реже чем раз в неделю
232(16,04%)
234(16,83%)
227(16,08%)
233(17,21%)
Ни разу
955(66,04%)
901(64,82%)
933(66,08%)
872(64,40%)
Итого
1446
1390
1412
1354
Таблица 60
Проверка различных наблюдений (4-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
P-значение
Исходные данные
Проверка по критерию суммы рангов
-0,63
0,5273
-0,69
0,489
1 месяц после лечения
Проверка по критерию суммы рангов
-1,36
0,1727
-1,46
0,145
3 месяца после лечения
Проверка по критерию суммы рангов
-1,24
0,2164
-1,73
0,082
6 месяцев после лечения
Проверка по критерию суммы рангов
-1,26
0,2064
-1,91
0,055
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,68
0,4937
-0,73
0,465
12 месяцев после лечения
Проверка по критерию суммы рангов
0,18
0,8556
0,31
0,758
Последующее наблюдение
Проверка по критерию суммы рангов
-0,75
0,4507
-0,96
0,334
Таблица 61
Различные наблюдения (5-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Очень сильно
60(3,45%)
46(2,68%)
48(3,21%)
40(2,77%)
Умеренно
356(20,50%)
391(22,75%))
318(21,29%)
349(24,14%)
Незначительно
534(30,74%)
518(30,13%)
467(31,26%)
432(29,88%)
Слегка
328(18,88%)
328(19,08%)
287(19,21%)
269(18,60%)
Совсем не обременительно
407(23,43%)
387(22,51%)
329(22,02%)
315(21,78%)
Лекарства не принимаю
52(2,99%)
49(2,85%)
45(3,01%)
41(2,84%)
Итого
1737
1719
1494
1446
1 месяц после лечения
Очень сильно
42(2,41%)
36(2,09%)
32(2,15%)
31(2,14%)
Умеренно
304(17,43%)
288(16,70%)
271(18,24%)
245(16,92%)
Незначительно
504(28,90%)
490(28,41%)
430(28,94%)
400(27,62%)
Слегка
376(21,56%)
409(23,71%)
322(21,67%)
357(24,65%)
Совсем не обременительно
459(26,32%)
454(26,32%)
378(25,44%)
374(25,83%)
Лекарства не принимаю
59(3,38%)
48(2,78%)
53(3,57%)
41(2,83%)
Итого
1744
1725
1486
1448
3 месяца после лечения
Очень сильно
30(1,72%)
22(1,28%)
21(1,43%)
16(1,12%)
Умеренно
273(15,65%)
266(15,42%)
237(16,13%)
221(15,43%)
Незначительно
458(26,26%)
443(25,68%)
384(26,14%)
364(25,42%)
Слегка
429(24,60%)
464(26,90%)
361(24,57%)
392(27,37%)
Совсем не обременительно
478(27,41%)
467(27,07%)
399(27,16%)
383(26,75%)
Лекарства не принимаю
76(4,36%)
63(3,65%)
67(4,56%)
56(3,91%)
Итого
1744
1725
1469
1432
6 месяцев после лечения
4 и более раза в день
15(0,86%)
15(0,87%)
6(0,41%)
8(0,57%)
1-3 раза в день
201(11,53%)
200(11,59%)
160(11,00%)
146(10,36%)
3 раза в неделю и чаще
503(28,84%)
464(26,90%)
421(28,93%)
382(27,11%)
1-2 раза в неделю
460(26,38%)
495(28,70%)
393(27,01%)
418(29,67%)
Реже чем раз в неделю
490(28,10%)
476(27,59%)
410(28,18%)
391(27,75%)
Ни разу
75(4,30%)
75(4,35%)
65(4,47%)
64(4,54%)
Итого
1744
1725
1455
1409
9 месяцев после лечения
4 и более раза в день
16(0,92%)
22(1,28%)
7(0,49%)
12(0,87%)
1-3 раза в день
139(7,97%)
139(8,06%)
96(6,68%)
85(6,13%)
3 раза в неделю и чаще
513(29,42%)
468(27,13%)
424(29,49%)
376(27,13%)
1-2 раза в неделю
500(28,67%)
527(30,55%)
432(30,04%)
444(32,03%)
Реже чем раз в неделю
498(28,56%)
490(28,41%)
412(28,65%)
401(28,93%)
Ни разу
78(4,47%)
79(4,58%)
67(4,66%)
68(4,91%)
Итого
1744
1725
1438
1386
12 месяцев после лечения
4 и более раза в день
14(0,80%)
21(1,22%)
4(0,28%)
8(0,58%)
1-3 раза в день
107(6,14%)
127(7,36%)
59(4,13%)
71(5,19%)
3 раза в неделю и чаще
451(25,86%)
397(23,01%)
362(25,33%)
300(21,91%)
1-2 раза в неделю
558(32,00%)
573(33,22%)
486(34,01%)
486(35,50%)
Реже чем раз в неделю
522(29,93%)
525(30,43%)
437(30,58%)
432(31,56%)
Ни разу
92(5,28%)
82(4,75%)
81(5,67%)
72(5,26%)
Итого
1744
1725
1429
1369
Последующее наблюдение
4 и более раза в день
2(0,14%)
4(0,29%)
2(0,14%)
3(0,22%)
1-3 раза в день
46(3,17%)
48(3,45%)
45(3,18%)
48(3,54%)
3 раза в неделю и чаще
363(25,03%)
331(23,78%)
355(25,09%)
323(23,82%))
1-2 раза в неделю
478(32,97%)
469(33,69%)
465(32,86%)
456(33,63%)
Реже чем раз в неделю
452(31,17%)
445(31,97%)
442(31,24%)
431(31,78%)
Ни разу
109(7,52%)
95(6,82%)
106(7,49%)
95(7,01%)
Итого
1450
1392
1415
1356
Таблица 62
Проверка различных наблюдений (5-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию хи-квадрат
4,23
0,5166
3,82
0,5754
1 месяц после лечения
Проверка по критерию хи-квадрат
3,53
0,6184
5,28
0,3831
3 месяца после лечения
Проверка по критерию хи-квадрат
4,18
0,5234
3,89
0,5660
6 месяцев после лечения
Проверка по критерию суммы рангов
0,40
0,6867
0,62
0,5356
9 месяцев после лечения
Проверка по критерию суммы рангов
0,47
0,6408
0,92
0,3566
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,03
0,9779
0,49
0,6242
Последующее наблюдение
Проверка по критерию суммы рангов
0,07
0,9404
0,10
0,9221
Таблица 63
Различные наблюдения (6-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Не удовлетворен
20(1,15%)
12(0,70%)
17(1,14%)
12(0,83%)
В основном не удовлетворен
114(6,54%)
104(6,07%)
97(6,48%)
93(6,45%)
Частично удовлетворен
548(31,46%)
546(31,86%)
497(33,20%)
480(33,29%)
В основном удовлетворен
793(45,52%)
789(46,03%)
663(44,29%)
647(44,87%)
Полностью удовлетворен
267(15,33%)
263(15,34%)
223(14,90%)
210(14,56%)
Итого
1742
1714
1497
1442
1 месяц после лечения
Не удовлетворен
8(0,46%)
4(0,23%)
3(0,20%)
3(0,21%)
В основном не удовлетворен
70(4,01%)
69(4,00%)
65(4,37%)
57(3,94%)
Частично удовлетворен
495(28,38%)
469(27,20%)
442(29,68%)
405(27,97%)
В основном удовлетворен
857(49,14%)
860(49,88%)
713(47,88%)
718(49,59%)
Highly consent
314(18,00%)
322(18,68%)
266(17,86%)
265(18,30%)
Итого
1744
1724
1489
1448
3 месяца после лечения
Не удовлетворен
4(0,23%)
3(0,17%)
1(0,07%)
2(0,14%)
В основном не удовлетворен
46(2,64%)
51(2,96%)
37(2,51%)
41(2,86%)
Частично удовлетворен
448(25,69%)
410(23,78%)
387(26,29%)
342(23,87%)
В основном удовлетворен
904(51,83%)
905(52,49%)
752(51,09%)
759(52,97%)
Полностью удовлетворен
342(19,61%)
355(20,59%)
295(20,04%)
289(20,17%)
Итого
1744
1724
1472
1433
6 месяцев после лечения
Не удовлетворен
3 (0,17%)
2(0,12%)
0 (0,00%)
1 (0,07%)
В основном не удовлетворен
34 (1,95%)
37(2,15%)
24 (1,65%)
21 (1,49%)
Частично удовлетворен
358 (20,53%)
360 (20,88%)
293(20,14%),
285 (20,23%)
В основном удовлетворен
972 (55,73%)
941 (54,58%)
814(55,95%)
782 (55,50%)
Полностью удовлетворен
377 (21,62%)
384 (22,27%)
324 (22,27%)
320(22,71%)
Итого
1744
1724
1455
1409
9 месяцев после лечения
Не удовлетворен
4(0,23%)
3(0,17%)
1(0,07%)
2(0,14%)
В основном не удовлетворен
34(1,95%)
31(1,80%)
22(1,53%)
13(0,94%)
Частично удовлетворен
269(15,42%)
284(16,47%)
203(14,10%)
197(14,22%)
В основном удовлетворен
1025(58,77%)
996(57,77%)
855(59,38%)
825(59,57%)
Полностью удовлетворен
412(23,62%)
410(23,78%)
359(24,93%)
348(25,13%)
Итого
1744
1724
1440
1385
12 месяцев после лечения
Не удовлетворен
5(0,29%)
3(0,17%)
1(0,07%)
0(0,00%)
В основном не удовлетворен
27(1,55%)
27(1,57%)
12(0,84%)
8(0,58%)
Частично удовлетворен
204(11,70%)
236(13,69%)
137(9,59%)
144(10,53%)
В основном удовлетворен
1057(60,61%)
1017(58,99%)
882(61,72%)
842(61,55%)
Полностью удовлетворен
451(25,86%)
441(25,58%)
397(27,78%)
374(27,34%)
Итого
1744
1724
1429
1368
Последующее наблюдение
Не удовлетворен
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
В основном не удовлетворен
9(0,62%)
5(0,36%)
9(0,63%)
5(0,37%)
Частично удовлетворен
123(8,45%)
136(9,74%)
122(8,59%)
131(9,63%)
В основном удовлетворен
913(62,75%)
845(60,53%)
884(62,25%)
821(60,37%)
Полностью удовлетворен
410(28,18%)
410(29,37%)
405(28,52%)
403(29,63%)
Итого
1455
1396
1420
1360
Таблица 64
Проверка различных наблюдений (6-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,44
0,6613
0,07
0,9403
1 месяц после лечения
Проверка по критерию суммы рангов
0,91
0,3654
1,06
0,2889
3 месяца после лечения
Проверка по критерию суммы рангов
1,06
0,2890
0,78
0,4379
6 месяцев после лечения
Проверка по критерию суммы рангов
0,06
0,9548
0,19
0,8514
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,26
0,7923
0,28
0,7817
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,93
0,3518
-0,42
0,6713
Последующее наблюдение
Проверка по критерию суммы рангов
0,20
0,8407
0,26
0,7977
Таблица 65
Различные наблюдения (7-й вопрос)
Данные
FAS
РР
Контрогльная группа
Группа испытуемых
Контрольная группа }
Группа испытуемых
Исходные данные
Не удовлетворен
7(0,40%)
2(0,12%)
5(0,33%)
2(0,14%)
В основном не удовлетворен
80(4,60%)
78(4,55%)
73(4,88%)
72(5,00%)
Частично удовлетворен
463(26,61%)
447(26,09%)
418(27,94%)
396(27,48%)
В основном удовлетворен
835(47,99%)
840(49,04%)
696(46,52%)
696(48,30%)
Полностью удовлетворен
355(20,40%)
346(20,20%)
304(20,32%)
275(19,08%)
Итого
1740
1713
1496
1441
1 месяц после лечения
Не удовлетворен
3(0,17%)
1(0,06%)
2(0,13%)
1(0,07%)
В основном не удовлетворен
54(3,10%)
55(3,20%)
50(3,36%)
49(3,39%)
Частично удовлетворен
409(23,48%)
389(22,60%)
363(24,41%)
336(23,25%)
В основном удовлетворен
870(49,94%)
878(51,02%)
724(48,69%)
738(51,07%)
Полностью удовлетворен
406(23,31%)
398(23,13%)
348(23,40%)
321(22,21%)
Итого
1742
1721
1487
1445
3 месяца после лечения
Не удовлетворен
2(0,11%)
2(0,12%)
1(0,07%)
2(0,14%)
В основном не удовлетворен
34(1,95%)
38(2,21%)
27(1,84%)
33(2,31%)
Частично удовлетворен
369(21,18%)
344(19,99%)
317(21,56%)
286(20,00%)
В основном удовлетворен
942(54,08%)
919(53,40%)
786(53,47%)
765(53,50%)
Полностью удовлетворен
395(22,68%)
418(24,29%)
339(23,06%)
344(24,06%)
Итого
1742
1721
1470
1430
6 месяцев после лечения
Не удовлетворен
2(0,11%)
0(0,00%)
1(0,07%)
0(0,00%)
В основном не удовлетворен
23(1,32%)
21(1,22%)
16(1,10%)
15(1,07%)
Частично удовлетворен
267(15,33%)
269(15,63%)
217(14,93%)
206(14,66%)
В основном удовлетворен
1014(58,21%)
1005(58,40%)
846(58,22%)
833(59,29%)
Полностью удовлетворен
436(25,03%)
426(24,75%)
373(25,67%)
351(24,98%)
Итого
1742
1721
1453
1405
9 месяцев после лечения
Не удовлетворен
2(0,11%)
0(0,00%)
1(0,07%)
0(0,00%)
В основном не удовлетворен
19(1,09%)
15(0,87%)
12(0,83%)
8(0,58%)
Частично удовлетворен
210(12,06%)
210(12,20%)
157(10,92%)
139(10,06%)
В основном удовлетворен
1037(59,53%)
1043(60,60%)
859(59,74%)
855(61,87%)
Полностью удовлетворен
474(27,21%)
453(26,32%)
409(28,44%)
380(27,50%)
Итого
1742
1721
1438
1382
12 месяцев после лечения Не удовлетворен
2(0,11%)
0(0,00%)
1(0,07%)
0(0,00%)
В основном не удовлетворен
13(0,75%)
15(0,87%)
4(0,28%)
7(0,51%)
Частично удовлетворен
170(9,76%)
171(9,94%)
115(8,06%)
98(7,17%)
В основном удовлетворен
1042(59,82%))
1041(60,49%)
861(60,34%)
845(61,86%)
Полностью удовлетворен
515(29,56%)
494(28,70%)
446(31,25%)
416(30,45%)
Итого
1742
1721
1427
1366
Последующее наблюдение
Не удовлетворен
0(0,00%)
0(0,00%)
0(0,00%)
0(0,00%)
В основном не удовлетворен
4(0,28%)
4(0,29%)
4(0,28%)
4(0,29%)
Частично удовлетворен
97(6,68%)
109(7,82%)
97(6,84%)
104(7,66%)
В основном удовлетворен
908(62,49%)
823(59,08%)
881(62,13%)
800(58,95%)
Полностью удовлетворен
444(30,56%)
457(32,81%)
436(30,75%)
449(33,09%)
Итого
1453
1393
1418
1357
Таблица 66
Проверка различных наблюдений (7-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значенин
Исходные данные
Проверка по критерию суммы рангов
0,33
0,7387
-0,20
0,8442
1 месяц после лечения
Проверка по критерию суммы рангов
0,29
0,7680
0,02
0,9879
3 месяца после лечения
Проверка по критерию суммы рангов
1,06
0,2902
0,72
0,4725
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,15
0,8824
-0,15
0,8806
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,35
0,7300
0,02
0,9822
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,53
0,5985
-0,13
0,8935
Последующее наблюдение
Проверка по критерию суммы рангов
0,69
0,4897
0,84
0,3991
Таблица 67
Различные наблюдения (8-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Не удовлетворен
16(0,92%)
9(0,53%)
13(0,87%)
8(0,56%)
В основном не удовлетворен
114(6,55%)
101(5,90%)
99(6,61%)
94(6,52%)
Частично удовлетворен
538(30,90%)
542(31,64%)
487(32,53%)
466(32,34%)
В основном удовлетворен
801(46,01%)
809(47,23%)
676(45,16%)
673(46,70%)
Полностью удовлетворен
272(15,62%)
252(14,71%)
222(14,83%)
200(13,88%)
Итого
1741
1713
1497
1441
1 месяц после лечения
Не удовлетворен
6(0,34%)
5(0,29%)
2(0,13%)
4(0,28%)
В основном не удовлетворен
71(4,07%)
65(3,77%)
63(4,23%)
54(3,73%))
Частично удовлетворен
487(27,92%)
472(27,39%)
435(29,23%)
402(27,78%)
В основном удовлетворен
877(50,29%)
876(50,84%)
729(48,99%)
738(51,00%)
Полностью удовлетворен
303(17,37%)
305(17,70%)
259(17,41%)
249(17,21%)
Итого
1744
1723
1488
1447
3 месяца после лечения
Не удовлетворен
3(0,17%)
4(0,23%)
1(0,07%)
3(0,21%)
В основном не удовлетворен
54(3,10%)
57(3,31%)
42(2,85%)
43(3,01%)
Частично удовлетворен
433(24,83%)
409(23,72%)
373(25,34%)
338(23,64%)
В основном удовлетворен
921(52,81%)
910(52,78%)
770(52,31%)
764(53,43%)
Полностью удовлетворен
333(19,09%)
344(19,95%)
286(19,43%)
282(19,72%)
Итого
1744
1724
1472
1430
6 месяцев после лечения
Не удовлетворен
3(0,17%)
6(0,35%)
1(0,07%)
3(0,21%)
В основном удовлетворен
39(2,24%)
38(2,20%)
23(1,58%)
21(1,49%)
Частично удовлетворен
361(20,70%)
365(21,17%)
305(20,96%)
286(20,34%)
В основном удовлетворен
987(56,59%)
950(55,10%)
825(56,70%)
792(56,33%)
Полностью удовлетворен
354(20,30%)
365(21,17%)
301(20,69%)
304(21,62%)
Итого
1744
1724
1455
1406
9 месяцев после лечения
Не удовлетворен
6(0,34%)
6(0,35%)
4(0,28%)
2(0,14%)
В основном не удовлетворен 33(1,89%)
36(2,09%)
17(1,18%)
19(1,37%)
Частично удовлетворен
298(17,09%)
274(15,89%)
239(16,59%)
183(13,23%)
В основном удовлетворен
1017(58,31%)
1027(59,57%)
847(58,78%)
858(62,04%)
Полностью удовлетворен
390(22,36%)
381(22,10%)
334(23,18%)
321(23,21%)
Итого
1744
1724
1441
1383
12 месяцев после лечения
Не удовлетворен
5(0,29%)
5(0,29%)
0(0,00%)
0(0,00%)
В основном не удовлетворен
35(2,01%)
40(2,32%)
18(1,26%)
22(1,61%)
Частично удовлетворен
215(12,33%)
235(13,63%)
154(10,78%)
141(10,31%)
В основном удовлетворен
1048(60,09%)
1014(58,82%)
874(61,16%)
838(61,26%)
Полностью удовлетворен
441(25,29%)
430(24,94%)
383(26,80%)
367(26,83%)
Итого
1744
1724
1429
1368
Последующее наблюдение
Не удовлетворен
1(0,07%)
1(0,07%)
1(0,07%)
1(0,07%)
В основном не удовлетворен
9(0,62%)
9(0,65%)
9(0,64%)
9(0,66%)
Частично удовлетворен
155(10,67%)
137(9,82%)
154(10,87%)
133(9,79%)
В основном удовлетворен
880(60,61%)
842(60,36%)
854(60,27%)
819(60,26%)
Полностью удовлетворен
407(28,03%)
406(29,10%)
399(28,16%)
397(29,21%)
Итого
1452
1395
1417
1359
Таблица 68
Проверка различных наблюдений (8-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значени
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,05
0,9587
0,04
0,9701
1 месяц после лечения
Проверка по критерию суммы рангов
0,57
0,5686
0,71
0,4753
3 месяца после лечения
Проверка по критерию суммы рангов
0,66
0,5063
0,62
0,5342
6 месяцев после лечения
Проверка по критерию суммы рангов
0,09
0,9285
0,59
0,5535
9 месяцев после лечения
Проверка по критерию суммы рангов
0,29
0,7730
1,32
0,1885
12 месяцев после лечения
Проверка по критерию суммы рангов
0,88
0,3799
0,04
0,9715
Последующее наблюдение
Проверка по критерию суммы рангов
0,82
0,4136
0,88
0,3792
Таблица 69
Различные наблюдения (9-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Очень сильно
63(3,62%)
60(3,50%)
50(3,34%)
52(3,60%)
Умеренно
468(26,88%)
427(24,90%)
404(26,99%)
371(25,71%)
Незначительно
639(36,70%)
624(36,38%)
554(37,01%)
516(35,76%)
Слегка
366(21,02%)
409(23,85%)
313(20,91%)
335(23,22%)
Совсем не мешали
205(11,77%)
195(11,37%)
176(11,76%)
169(11,71%)
Итого
1741
1715
1497
1443
1 месяц после лечения
Очень сильно
39(2,24%)
30(1,74%)
30(2,01%)
24(1,66%)
Умеренно
328(18,81%)
309(17,93%)
282(18,94%)
267(18,45%)
Незначительно
629(36,07%)
613(35,58%)
535(35,93%)
513(35,45%)
Слегка
467(26,78%)
517(30,01%)
385(25,86%)
429(29,65%)
Совсем не мешали
281(16,11%)
254(14,74%)
257(17,26%)
214(14,79%)
Итого
1744
1723
1489
1447
3 месяца после лечения
Очень сильно
26(1,49%)
20(1,16%)
14(0,95%)
14(0,98%)
Умеренно
272(15,60%)
264(15,32%)
228(15,51%)
220(15,36%)
Незначительно
585(33,54%)
586(34,01%)
485(32,99%)
475(33,17%)
Слегка
556(31,88%)
573(33,26%)
464(31,56%)
480(33,52%)
Совсем не мешали
305(17,49%)
280(16,25%)
279(18,98%)
243(16,97%)
Итого
1744
1723
1470
1432
6 месяцев после лечения
Очень сильно
15(0,86%)
18(1,04%)
3(0,21%)
9(0,64%)
Умеренно
203(11,64%)
213(12,35%)
153(10,54%)
161(11,43%)
Незначительно
604(34,63%)
583(33,82%)
500(34,44%)
480(34,09%)
Слегка
606(34,75%)
604(35,03%)
508(34,99%)
497(35,30%)
Совсем не мешали
316(18,12%)
306(17,75%)
288(19,83%)
261(18,54%)
Итого
1744
1724
1452
1408
9 месяцев после лечения
Очень сильно
17(0,97%)
17(0,99%)
5(0,35%)
4(0,29%)
Умеренно
153(8,77%)
161(9,34%)
101(7,01%)
109(7,88%)
Незначительно
577(33,08%)
573(33,24%)
472(32,78%)
454(32,83%)
Слегка
659(37,79%)
652(37,82%)
556(38,61%)
535(38,68%)
Совсем не мешали
338(19,38%)
321(18,62%)
306(21,25%)
281(20,32%)
Итого
1744
1724
1440
1383
12 месяцев после лечения
Очень сильно
17(0,97%)
18(1,04%)
3(0,21%)
3(0,22%)
Умеренно
119(6,82%)
145(8,41%)
64(4,48%)
89(6,51%)
Незначительно
533(30,56%)
487(28,25%)
423(29,64%)
367(26,83%)
Слегка
693(39,74%)
706(40,95%)
591(41,42%)
588(42,98%)
Совсем не мешали
382(21,90%)
368(21,35%)
346(24,25%)
321(23,46%)
Итого
1744
1724
1427
1368
Последующее наблюдение
Очень сильно
2(0,14%)
2(0,14%)
2(0,14%)
2(0,15%)
Умеренно
55(3,78%)
66(4,73%)
55(3,87%)
65(4,78%)
Незначительно
397(27,29%)
361(25,86%)
388(27,32%)
353(25,97%)
Слегка
644(44,26%)
599(42,91%)
628(44,23%)
588(43,27%)
Совсем не мешали
357(24,54%)
368(26,36%)
347(24,44%)
351(25,83%)
Итого
1455
1396
1420
1359
Таблица 70
Проверка различных наблюдений (9-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значен
Р-значение
Исходные данные
Проверка по критерию суммы рангов
1,40
0,1616
0,91
0,3620
1 месяц после лечения
Проверка по критерию суммы рангов
0,76
0,4460
0,14
0,8882
3 месяца после лечения
Проверка по критерию суммы рангов
-0,09
0,9289
-0,48
0,6278
6 месяцев после лечения
Проверка по критерию суммы рангов
-0,37
0,7115
-0,99
0,3215
9 месяцев после лечения
Проверка по критерию суммы рангов
-0,64
0,5213
-0,72
0,4698
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,27
0,7852
-0,31
0,7529
Последующее наблюдение
Проверка по критерию суммы рангов
0,64
0,5233
0,48
0,6342
Таблица 71
Различные наблюдения (10-й вопрос)
Данные
FAS
РР
Контрольная группа
Группа испытуемых
Контрольная группа
Группа испытуемых
Исходные данные
Не удовлетворен
451(25,90%)
416(s24,21%)
378(25,25%)
343(23,74%)
В основном не удовлетворен
413(23,72%)
454(26,43%)
361(24,11%)
398(27,54%)
Частично удовлетворен
543(31,19%)
509 (29,63%)
483(32,26%)
434(30,03%)
В основном удовлетворен
294(16,89%)
304(17,69%)
244(16,30%)
242(16,75%)
Полностью удовлетворен
40(2,30%)
35(2,04%)
31(2,07%)
28(1,94%)
Итого
1741
1718
1497
1445
1 месяц после лечения
Не удовлетворен
396(22,71%)
390(22,62%)
331(22,24%)
326(22,58%)
В основном не удовлетворен
400(22,94%)
384(22,27%)
344(23,12%)
327(22,65%)
Частично удовлетворен
516(29,59%)
498(28,89%)
455(30,58%))
415(28,74%)
В основном удовлетворен
361(20,70%)
376(21,81%)
295(19,83%)
312(21,61%)
Полностью удовлетворен
71 (4,07%)
76(4,41%)
63(4,23%)
64(4,43%)
Итого
1744
1724
1488
1444
3 месяца после лечения
Не удовлетворен
372(21,33%)
373(21,64%)
307(20,88%)
306(21,37%)
В основном не удовлетворен
387(22,19%)
375(21,75%)
329(22,38%)
313(21,86%)
Частично удовлетворен
481(27,58%)
464(26,91%)
417(28,37%)
387(27,03%)
В основном удовлетворен
422 (24,20%)
425(24,65%)
345(23,47%)
350(24,44%)
Полностью удовлетворен
82 (4,70%)
87(5,05%)
72(4,90%)
76(5,31%)
Итого
1744
1724
1470
1432
6 месяцев после лечения
Не удовлетворен
364 (20,87%)
353(20,48%)
296(20,36%)
279(19,82%)
В основном не удовлетворен
376 (21,56%)
379(21,98%)
310(21,32%)
313(22,23%)
Частично удовлетворен
459 (26,32%)
450(26,10%)
394(27,10%)
369(26,21%)
В основном удовлетворен
464 (26,61%)
458(26,57%)
383(26,34%)
375(26,63%)
Полностью удовлетворен
81 (4,64%)
84 (4,87%)
71 (4,88%)
72(5,11%)
Итого
1744
1724
1454
1408
9 месяцев после лечения
Не удовлетворен
341 (19,55%)
342(19,84%)
271(18,81%)
263(18,99%)
В основном не удовлетворен
357 (20,47%)
341(19,78%)
288(19,99%)
271(19,57%)
Частично удовлетворен
443 (25,40%)
442(25,64%)
372(25,82%)
353(25,49%)
В основном удовлетворен
503 (28,84%)
499(28,94%)
421(29,22%)
407(29,39%)
Полностью удовлетворен
100 (5,73%)
100(5,80%)
89(6,18%)
91(6,57%)
Итого
1744
1724
1441
1385
12 месяцев после лечения
Не удовлетворен
340(19,50%)
354(20,53%)
267(18,68%)
274(20,01%)
В основном не удовлетворен
335(19,21%)
328(19,03%)
266(18,61%)
253(18,48%)
Частично не удовлетворен
399(22,88%)
372(21,58%)
323(22,60%)
277(20,23%)
В основном удовлетворен
538(30,85%)
549(31,84%)
455(31,84%)
457(33,38%)
Полностью удовлетворен
132(7,57%)
121(7,02%)
118(8,26%)
108(7,89%)
Итого
1744
1724
1429
1369
Последующее наблюдение
Не удовлетворен
269(18,50%)
268(19,20%)
257(18,11%)
257(18,90%)
В основном не удовлетворен
277(19,05%)
236(16,91%)
275(19,38%)
231(16,99%)
Частично удовлетворен
302(20,77%)
288(20,63%)
295(20,79%)
284(20,88%)
В основном удовлетворен
467(32,12%)
472(33,81%)
457(32,21%)
460(33,82%)
Полностью удовлетворен
139(9,56%)
132(9,46%)
135(9,51%)
128(9,41%)
Итого
1454
1396
1419
1360
Таблица 72
Проверка различных наблюдений (10-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,26
0,7940
-0,10
0,9211
1 месяц после лечения
Проверка по критерию суммы рангов
0,65
0,5140
0,47
0,6390
3 месяца после лечения
Проверка по критерию суммы рангов
0,23
0,8147
0,31
0,7579
6 месяцев после лечения
Проверка по критерию суммы рангов
0,17
0,8644
0,19
0,8489
9 месяцев после лечения
Проверка по критерию суммы рангов
0,10
0,9219
0,23
0,8173
12 месяцев после лечения
Проверка по критерию суммы рангов
-0,39
0,7000
-0,24
0,8140
Последующее наблюдение
Проверка по критерию суммы рангов
0,53
0,5966
0,52
0,6009
Таблица 73
Различные наблюдения (11-й вопрос)
Данные
FAS
РР
Контрольная группа Группа испытуемых
Контрольная группа Группа испытуемых
Исходные данные
Постоянно беспокоит
167(9,59%)
144(8,38%)
138(9,21%)
120(8,30%)
Часто беспокоит
416(23,88%)
421(24,51%)
376(25,10%)
364(25,19%)
Иногда беспокоит
713(40,93%)
720(41,91%)
619(41,32%)
604(41,80%)
Изредка беспокоит
374(21,47%)
377(21,94%)
306 (20,43%)
309(21,38%)
Не беспокоит
72 (4,13%)
56 (3,26%)
59 (3,94%)
48 (3,32%)
Итого
1742
1718
1498
1445
1 месяц после лечения
Постоянно беспокоит
117(6,71%)
115(6,67%)
90 (6,04%)
94 (6,50%)
Часто беспокоит
365 (20,93%)
339 (19,66%)
324(21,76%)
290(20,04%)
Иногда беспокоит
714(40,94%)
694(40,26%)
614(41,24%)
576(39,81%)
Изредка беспокоит
466 (26,72%)
488(28,31%)
389(26,12%)
412(28,47%)
Не беспокоит
82 (4,70%)
88(5,10%)
72(4,84%)
75(5,18%)
Итого
1744
1724
1489
1447
3 месяца после лечения
Постоянно беспокоит
94(5,39%)
86(4,99%)
68(4,62%)
66(4,61%)
Часто беспокоит
319(18,29%)
306(17,75%)
280(19,03%)
251(17,53%)
Иногда беспокоит
714(40,94%)
696(40,37%)
610(41,47%)
572(39,94%)
Изредка беспокоит
532(30,50%)
544(31,55%)
443(30,12%)
465(32,47%)
Не беспокоит
85(4,87%)
92(5,34%)
70(4,76%)
78(5,45%)
Итого
1744
1724
1471
1432
6 месяцев после лечения
Постоянно беспокоит
77(4,42%)
60(3,48%)
50(3,44%)
41(2,91%)
Часто беспокоит
259(14,85%)
274(15,89%)
212(14,57%)
216(15,33%)
Иногда беспокоит
727(41,69%)
686(39,79%)
621(42,68%)
555(39,39%)
Изредка беспокоит
595(34,12%)
601(34,86%)
502(34,50%)
513(36,41%)
Не беспокоит
86(4,93%)
103(5,97%)
70(4,81%)
84(5,96%)
Итого
1744
1724
1455
1409
9 месяцев после лечения
Постоянно беспокоит
60(3,44%)
50(2,90%)
35(2,43%)
29(2,09%)
Часто беспокоит
215(12,33%)
209(12,12%)
169(11,73%)
151(10,90%)
Иногда беспокоит
729(41,80%)
722(41,88%)
611(42,40%)
575(41,52%)
Изредка беспокоит
635(36,41%)
634(36,77%)
538(37,34%)
534(38,56%)
Не беспокоит
105(6,02%)
109(6,32%)
88(6,11%)
96(6,93%)
Итого
1744
1724
1441
1385
12 месяцев после лечения
Постоянно беспокоит
55(3,15%)
48(2,78%)
28(1,96%)
27(1,97%)
Часто беспокоит
161(9,23%)
182(10,56%)
114(7,98%)
122(8,91%)
Иногда беспокоит
708(40,60%)
668(38,75%)
580(40,59%)
512(37,40%)
Изредка беспокоит
696(39,91%)
712(41,30%)
601(42,06%)
610(44,56%)
Не беспокоит
124(7,11%)
114(6,61%)
106(7,42%)
98(7,16%)
Итого
1744
1724
1429
1369
Последующее наблюдение
Постоянно беспокоит
20(1,38%)
24(1,72%)
19(1,34%)
23(1,69%)
Часто беспокоит
98 (6,74%)
104(7,45%)
97(6,84%)
103(7,58%)
Иногда беспокоит
566 (38,93%).
527(37,75%)
551(38,83%)
513(37,75%)
Изредка беспокоит
642 (44,15%)
622(44,56%)
628(44,26%)
605(44,52%)
Не беспокоит
128 (8,80%)
119(8,52%)
124(8,74%)
115(8,46%)
Итого
1454
1396
1419
1359
Таблица 74
Проверка различных наблюдений (11-й вопрос)
Данные
Метод испытаний
FAS
РР
Статистическое значение
Р-значение
Статистическое значение
Р-значение
Исходные данные
Проверка по критерию суммы рангов
0,16
0,8695
0,45
0,6513
1 месяц после лечения
Проверка по критерию суммы рангов
1,23
0,2195
1,28
0,2003
3 месяца после лечения
Проверка по критерию суммы рангов
1,02
0,3068
1,65
0,0994
6 месяцев после лечения
Проверка по критерию суммы рангов
1,02
0,3085
1,37
0,1714
9 месяцев после лечения
Проверка по критерию суммы рангов
0,62
0,5353
1,31
0,1886
12 месяцев после лечения
Проверка по критерию суммы рангов
0,03
0,9761
0,62
0,5325
Последующее наблюдение
Проверка по критерию суммы рангов
-0,28
0,7817
-0,34
0,7341
1.7 Оценка безопасности
Не наблюдалось выраженных неблагоприятных событий. Описание чертежей
На фиг.1 показана кривая Каплана-Майера времени до наступления основной конечной точки-события (FAS),
на фиг.2 показана кривая Каплана-Майера времени до наступления основной конечной точки-события (FAS),
на фиг.3 показана кривая Каплана-Майера времени до наступления основной конечной точки-события (РР),
на фиг.4 показана кривая Каплана-Майера времени до наступления основной конечной точки-события (РР),
на фиг.5 показана кривая Каплана-Майера времени до наступления конечной точки-события смерти (FAS),
на фиг.6 показана кривая Каплана-Майера времени до наступления конечной точки-события смерти (FAS).
на фиг.7 показана кривая Каплана-Майера времени до наступления конечной точки-события смерти (РР).
на фиг.8 показана кривая Каплана-Майера времени до наступления конечной точки-события смерти (РР).
Варианты осуществления
Лекарственные средства согласно настоящему изобретению будут дополнительно описаны на следующих примерах, имеющих целью исключительно проиллюстрировать изобретение, а не ограничить его.
Пример 1
(1) Состав
Radix Astragali
86,5 г
Radix Salviae Miltiorrhizae
21,3 г
Radix Notoginseng
3,5 г
Lignum Dalbergiae Odoriferae
20,6 г
адъювант ПЭГ-6000
30 г
Экстрагирование Radix salvia Miltiorrhizae и Radix Notoginseng
Грубоизмельченное лекарственное сырье из Radix salvia Miltiorrhizae и Radix Notoginseng поместили в экстрактор, в который дважды добавили воду, вес которой в 7 раз превышал вес Radix salvia Miltiorrhizae и Radix Notoginseng с целью приготовления отвара в течение 2 часов каждый раз. После смешивания отваров раствор профильтровали и концентрировали, в результате чего получили 900 мл экстракта. Затем в полученный раствор экстракта медленно добавили 95% (по объему) этанола, чтобы довести окончательное содержание этанола до 70% (по объему), и дали отстояться в течение 12-24 часов, чтобы получить супернатант, который был профильтрован. Фильтрат концентрировали путем удаления этанола, в результате чего получили экстракт с относительно плотностью 1,32-1,38 (50-60°C).
Экстрагирование Radix Astragali
Измельченный round Radix Astragali поместили в экстрактор, в который дважды добавили воду, вес которой в 6 раз превышал вес Radix salvia Miltiorrhizae и Radix Notoginseng с целью приготовления отвара в течение 2 часов первый раз и 1 часа во второй раз. После смешивания отваров раствор профильтровали и концентрировали, в результате чего получили 1500 экстракта. Затем в полученный раствор экстракта медленно добавили 95% (по объему) этанола, чтобы довести окончательное содержание этанола до 60% (по объему), и дали отстояться в течение 12-24 часов, чтобы получить супернатант, который концентрировали путем удаления этанола до получения 400 мл экстракта. В полученный раствор экстракта второй раз медленно добавили 95% (по объему) этанола, чтобы довести окончательное содержание этанола до 80% (по объему), и дали отстояться в течение 12-24 часов, чтобы получить супернатант, который концентрировали путем удаления этанола, до получения 400 экстракта с относительной плотностью 1,32-1,38 (50-60°C). Экстрагирование Lignum Dalbergiae Odoriferae
Экстрагировали лекарственное сырье Lignum Dalbergiae Odoriferae путем дефлегмации в течение 5 часов с добавлением воды, вес которой в 5 раз превышал вес Lignum Dalbergiae Odoriferae, в результате чего получили эфирное масло.
Смешали упомянутый экстракт Radix salvia Miltiorrhizae и Radix Notoginseng, экстракт Radix Astragali и ПЭГ-6000 и растопили на водяной бане. Прежде, чем полностью смесь растопилась, добавили эфирное масло Lignum Dalbergiae Odoriferae. После перемешивания с целью гомогенизации смесь перенесли в машину для изготовления микропилюль и изготовили 1000 микропилюль.
Пример 2
Таким же способом, как в Примере 1, изготовили 1000 микропилюль со следующим составом:
Radix Astragali
40,6 г
Radix salvia Miltiorrhizae
44,8 г
Radix Notoginseng
11,2 г
Lignum Dalbergiae Odoriferae 38,6 г
адъювант ПЭГ-6000
30 г.
Пример 3
Таким же способом, как в Примере 1, изготовили 1000 микропилюль со следующим составом:
Radix Astragali
77,3 г
Radix salvia Miltiorrhizae
22,8 г
Radix Notoginseng
4,8 г
Lignum Dalbergiae Odoriferae
30,5 г
адъювант ПЭГ-6000
28 г.
Пример 4
Таким же способом, как в Примере 1, изготовили 1000 микропилюль со следующим составом:
Radix Astragali
40,3 г
Radix salvia Miltiorrhizae
39,2 г
Radix Notoginseng
8,2 г
Lignum Dalbergiae Odoriferae
46,8 г
адъювант ПЭГ-6000
25 г.
Пример 5
Таким же способом, как в Примере 1, изготовили 1000 микропилюль со следующим составом:
Radix Astragali
36,5 г
Radix salvia Miltiorrhizae
32,4 г
Radix Notoginseng
6,2 г
Lignum Dalbergiae Odoriferae
41,7 г
адъювант ПЭГ-6000
22 г.
Пример 6
Таким же способом, как в Примере 1, изготовили 1000 микропилюль со следующим составом:
Radix Astragali
65,2 г
Radix salvia Miltiorrhizae
38,9 г
Radix Notoginseng
9,3 г
Lignum Dalbergiae Odoriferae
32,5 г
адъювант ПЭГ-6000
40 г.
Пример 7
Таким же способом, как в Примере 1, изготовили 1000 микропилюль со следующим составом:
Radix Astragali
56,2 г
Radix salvia Miltiorrhizae
32,5 г
Radix Notoginseng
6,2 г
Lignum Dalbergiae Odoriferae
41,6 г
адъювант ПЭГ-6000
22 г.
Пример 8
Состав
Radix Astragali
86,5 г
Radix salvia Miltiorrhizae
21,3 г
Radix Notoginseng
3,5 г
Lignum Dalbergiae Odoriferae
20,6 г.
Экстрагировали лекарственное сырье таким же способом, как в Примере 1, использовали экстракт, сахарозу и декстрин в соотношении 1:3:1 по весу, и традиционным способом изготовили капсулу.
Пример 9
Состав
Radix Astragali
65,5 г
Radix salvia Miltiorrhizae
25,8 г
Radix Notoginseng
9,5 г
Lignum Dalbergiae Odoriferae
46,4 г.
Экстрагировали лекарственное сырье таким же способом, как в Примере 1, использовали экстракт, сахарозу и декстрин в соотношении 1:3:1 по весу, и традиционным способом изготовили 200 таблеток.
Пример 10
Состав
Radix Astragali
35,5 г
Radix salvia Miltiorrhizae
50,8 г
Radix Notoginseng
16,3 г
Lignum Dalbergiae Odoriferae
52,3 г.
Экстрагировали лекарственное сырье таким же способом, как в Примере 1, использовали экстракт, сахарозу и декстрин в соотношении 1:3:1 по весу, и традиционным способом изготовили 125 пакетиков с гранулами.