Способ относится к медицине, а именно к сердечно-сосудистой хирургии, и может быть использован для лечения ишемической болезни сердца.
Одним из самых опасных морфологических субстратов ишемической болезни сердца (ИБС) является атеросклеротическое поражение ствола левой коронарной артерии (ЛКА). Среди всех больных ИБС гемодинамически значимое поражение СЛКА встречается в 6-11% случаев. Однако изолированный стеноз СЛКА по данным литературы наблюдается менее чем у 1% пациентов и сопровождается крайне неблагоприятным прогнозом для жизни. Летальность при консервативном лечении достигает 35% в течение четырех лет и 56% за шесть лет наблюдения [Борисов А.И., 2001; Botman C.J. et al., 2006; Maureira P., 2010].
Известен способ эндоваскулярного лечения атеросклеротического поражения коронарных артерий [Стентирование коронарных артерий. Медицинская технология. А.Г. Осиев, Д.С. Гранкин, А.В. Бирюков, Д.А. Редькин. - Новосибирск, - 2008]. Он включает в себя следующие этапы.
Под местной анестезией по Сельдингеру пунктируют бедренную артерию, устанавливают последовательно интрадьюсер, проводниковый катетер. Через катетер в пораженную артерию проводят коронарный проводник. К месту поражения доставляют баллон-катетер и выполняют предварительную дилатацию зоны стеноза. Далее подготовленный стент на системе доставки под контролем рентгеноскопии проводят к области стеноза. Стент имплантируют давлением 16 атм, время раздутия баллона <20 с. Далее баллон, не заходя в проводниковый катетер, на половину выводят в аорту. Давлением выполняют постдилатацию проксимального отдела стентированного сегмента для плотного прилегания выступающей части стента к аорте. После имплантации стента проводят контрольную коронароангиография, систему доставки и интрадьюсер извлекают. На бедренную артерию накладывают давящую повязку на 12 часов, больным назначают строгий постельный режим, обильное питье.
К недостаткам способа относятся следующие:
1) высокие риски развития: инфаркта миокарда, жизнеугрожающих аритмий, спазма, диссекции, перфорации, острой окклюзии коронарных сосудов, развития кровотечения, тампонады перикарда;
2) необходимость постоянного приема комбинации антиагрегантов (клопидогрель и ацетилсалициловая кислота);
3) развитие рестенозов в области имплантации стента;
4) техническая невозможность стентирования из-за анатомических особенностей строения и характера поражения ствола ЛКА.
За ближайший аналог принят способ прямой реваскуляризации миокарда при локальном изолированном поражении СЛКА [Борисов А.И. «Особенности хирургического лечения больных ишемической болезнью сердца при сужении ствола левой коронарной артерии», Автореферат, СПб, 2011, 8-15]. Операцию осуществляют в несколько этапов: 1) доступ к сердцу, осуществляемый обычно путем срединной стернотомии; 2) выделение левой внутренней грудной артерии, забор аутовенозных трансплантантов; 3) канюляция восходящей части аорты и полых вен и подключение искусственного кровообращения; 4) пережатие восходящей части аорты с кардиоплегической остановкой сердца; 5) наложение дистального анастомоза между аутовеной и одной из артерий бассейна огибающей артерии; наложение анастомоза между ЛВГА и передней нисходящей артерией; 6) снятие зажима с восходящей части аорты; 7) восстановление сердечной деятельности; 8) наложение проксимального анастомоза между аутовеной и аортой; 9) профилактика воздушной эмболии; 10) окончание искусственного кровообращения; 11) деканюляция; 12) ушивание стернотомического разреза с дренированием полости перикарда.
Данный способ имеет следующие недостатки:
1) постепенное «закрытие» венозного шунта (графта) - в отдаленном периоде в течение 10 лет окклюзируется 40-50% венозных шунтов [Fitzgibbon et al. Coronary bypass graft fate and patient outcome // JACC. 1996. Vol. 28(3), P.616-26; Grondin CM et al. Comparison of late changes in internal mammary artery and saphenous vein grafts in two consecutive series of patients 10 years after operation // Circulation. 1984. Vol. 70(3 Pt 2). P.208-12];
2) нефизиологический ретроградный кровоток в шунтируемых артериях или его отсутствие;
3) высокий риск повреждения шунтов во время рестернотомии при выполнении повторных операций на сердце.
Задачи:
1) увеличить продолжительность и качество жизни больных за счет использования только аутоартериального графта;
2) снизить риск развития кровотечений, связанных с приемом антиагрегантов;
3) обезопасить выполнение рестернотомии при повторных операциях на сердце.
Сущность изобретения
При изолированном устьевом атеросклеротическом поражении ствола левой коронарной артерии непосредственно после кардиоплегии производят поперечную аортотомию на уровне сино-тубулярного гребня, циркулярно обходят ствол легочной артерии, отводят его на держалке, обеспечивая визуализацию, при помощи держалок выводят в рану ствол левой коронарной артерии, выполняют его продольную артериотомию и формируют анастомоз конец в бок между правой внутренней грудной артерией (ПВГА) и стволом левой коронарной артерии.
Техническим результатом является: 1) прогнозируемое увеличение продолжительности и качества жизни больных за счет использования в качестве кондуита аутоартериального шунта по сравнению с применением аутовен, что обусловлено его более высокой проходимостью в отдаленном периоде за счет устойчивости к развитию и прогрессированию атеросклеротического поражения (в течение 10 лет продолжает функционировать 96-98% шунтов, что, безусловно, выше, чем проходимость аутовен (40-50% за тот же период); 2) снижение риска развития гастропатий и геморрагических осложнений благодаря отсутствию необходимости в комбинированном приеме клопидогреля и ацетилсалициловой кислоты. Это связано с тем, что не производится реконструкция на коронарной артерии, атеросклеротическую бляшку не рассекают, как в случае с вшиванием заплаты в стенозированный участок. Поэтому применение в послеоперационном периоде только лишь ацетилсалициловой кислоты значительно уменьшает риск развития геморрагических осложнений и гастропатий, что особенно актуально у возрастных пациентов; 3) сохраненный антеградный физиологический кровоток по коронарным сосудам, в то время как при рутинном коронарном шунтировании кровоток по коронарным артериям антеретроградный; 4) более безопасная возможность проведения повторных операций на сердце, что связано с расположением кондуита под аортой, а не на передней поверхности сердца, как в случае применения левой внутренней грудной артерии или аутовен. Изобретение может быть использовано в системе здравоохранения при лечении ишемической болезни сердца с изолированным поражением устья ствола левой коронарной артерии на базе специализированных центров и отделений кардиохирургического профиля.
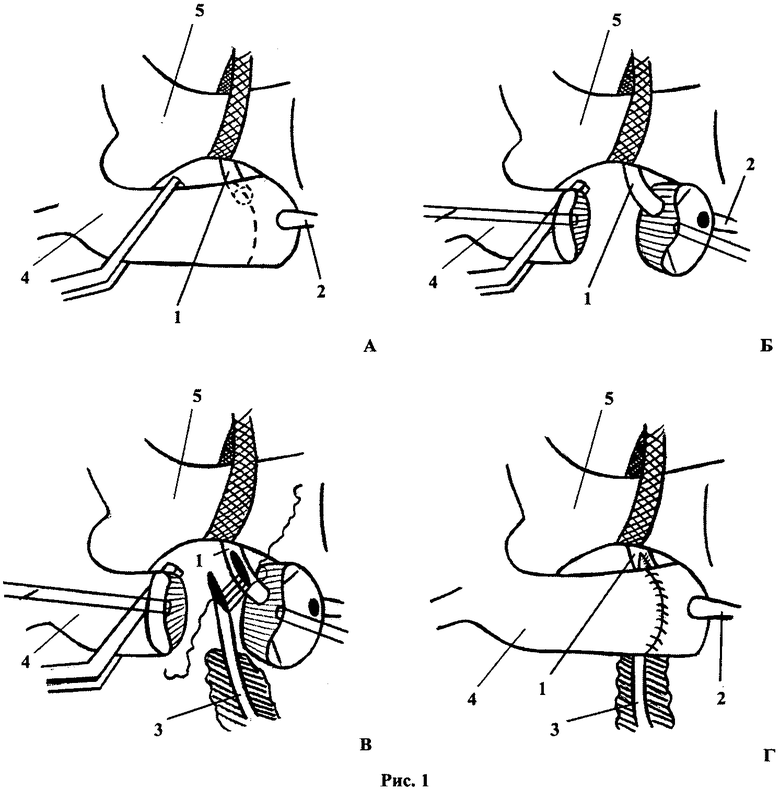
Для лучшего понимания способа на рис. 1 приведено схематическое изображение хода операции: А - общий вид операционного поля со стороны хирурга; Б - выполнена аортотомия, визуализирован ствол ЛКА; В - формирование анастомоза между стволом ЛКА и ПВГА; Г - конечный вид после восстановления целостности аорты; где 1 - ЛКА, 2 - правая коронарная артерия, 3 - ПВГА, 4 - аорта, 5 - легочная артерия.
Способ осуществляют следующим образом:
После обработки кожи антисептиком выполняют срединную стернотомию. Далее выделяют ПВГА. Вводят расчетную дозу гепарина. Затем после Т-образной перикардиотомии производят канюляцию аорты и правого предсердия и начинают искусственное кровообращение. Мобилизуют и берут на держалку ствол легочной артерии. После этого в коронарный синус устанавливают катетер для ретроградной кардиоплегии, накладывают зажим на восходящую аорту, начинают ретроградную фармако-холодовую кардиоплегию раствором «Кустодиол» (рис. 1А). Левый желудочек дренируют через правую верхнюю легочную вену. Восходящую аорту полностью поперечно пересекают на уровне сино-тубулярного гребня, нижнюю полуокружность корня аорты берут на держалки и выводят в рану, тем самым хорошо визуализируя ствол ЛКА (рис. 1Б). Далее производят его продольную артериотомию и формируют анастомоз с ПВГА по типу конец в бок нитью пролен 8/0 (рис. 1В). Целостность аорты восстанавливают непрерывным обвивным швом нитью пролен 4/0 (рис. 1Г). Снимают зажим с аорты. После восстановления ритма сердца завершают искусственное кровообращение, вводят протамин, выполняют деканюляцию, гемостаз. Рану послойно ушивают наглухо с оставлением перикардиального и правого плеврального дренажей.
Способ апробирован на 12 больных в течение 3 лет, рецидива стенокардии не было.
Пример
Выполнение способа поясняется рис. 1.
Пациент X., 55 лет, поступил в клинику с жалобами на одышку и боли давящего характера за грудиной без иррадиации, возникающие при небольшой физической нагрузке (подъем на 1 этаж), повышение АД до 200/90 мм рт. ст., учащенное сердцебиение. Коронарный анамнез - 4 года. Обследован: ЭКГ - синусовый ритм, ЧСС 70 ударов в минуту, признаки гипертрофии левого желудочка; ЭХО-КГ - фракция выброса левого желудочка - 53-55%, локальная сократимость - без четких зон гипокинеза. Коронароангиография: правый тип кровоснабжения, устьевой критический стеноз ствола левой коронарной артерии, стеноз 40% правой коронарной артерии в среднем отделе, остальные венечные артерии без гемодинамически значимых сужений. Учитывая критическое поражение ствола левой коронарной артерии, высокий класс стенокардии на фоне медикаментозной терапии, по жизненным показаниям больному выполнена прямая реваскуляризация миокарда. Учитывая изолированное локальное (только устье) поражение и достаточную его длину принято решение о выполнении шунтирования непосредственно самого ствола ЛКА.
Выполнена операция: маммарокоронарное шунтирование ствола левой коронарной артерии правой внутренней грудной артерией в условиях искусственного кровообращения и фармако-холодовой кардиоплегии.
На операции - срединная стернотомия. Выделена ПВГА. Гепарин. Начато искусственное кровообращение по схеме «аорта - правое предсердие». Легочная артерия обойдена и взята на держалку. Пережата восходящая аорта. Ретроградная фармако-холодовая кардиоплегия раствором «Кустодиол». Установлен дренаж левого желудочка через правую верхнюю легочную вену.
Восходящая аорта полностью поперечно пересечена по уровню сино-тубулярного гребня. Стенка аорты изнутри кальцинирована с переходом атеросклеротических бляшек на устье левой коронарной артерии, что и создает морфологическую картину устьевого поражения ствола ЛКА. Нижняя полуокружность корня аорты взята на держалки и выведена в рану, визуализирован ствол ЛКА. Продольная артериотомия ствола ЛКА на расстоянии 5 мм от устья: артерия дистальнее разреза практически не изменена, просвет проходим для бужа 2,5 мм. Сформирован анастомоз по типу конец в бок с ПВГА нитью пролен 8-0. Целостность аорты восстановлена обвивным швом нитью пролен 4-0. Снят зажим с аорты. Ритм сердца восстановился спонтанно. Окончание искусственного кровообращения, введение протамина, деканюляция, гемостаз. Рана послойно ушита наглухо с оставлением перикардиального и правого плеврального дренажей. Продолжительность искусственного кровообращения составила 109 минут, пережатия аорты - 65 минут. Послеоперационный период протекал гладко, приступы стенокардии не рецидивировали.
Перед выпиской выполнена контрольная коронарошунтография: анастомоз правой внутренней грудной артерии со стволом левой коронарной артерии проходим, гемодинамически значимых препятствий кровотоку не выявлено. Срок госпитализации - 6 суток. Пациент был осмотрен через 25 месяцев после операции - стенокардии нет.
Другие 10 пациентов также обследованы: 4 из них выполнена коронарошунтография, 6 - мультиспиральная компьютерная томография с контрастным усилением. Во всех случаях шунты к стволу ЛКА проходимы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ открытой эндартерэктомии при диффузном атеросклеротическом поражении передней межжелудочковой артерии | 2018 |
|
RU2717372C2 |
| СПОСОБ РЕКОНСТРУКЦИИ ПУТИ ОТТОКА ЛЕВОГО ЖЕЛУДОЧКА ПРИ ЭКСТРАВАЛЬВУЛЯРНОМ РАЗРУШЕНИИ УСТЬЯ АОРТЫ | 2004 |
|
RU2300320C2 |
| Способ хирургического лечения гигантской ложной аневризмы дуги аорты | 2016 |
|
RU2610796C1 |
| Способ хирургического лечения ишемической болезни сердца | 2022 |
|
RU2802555C1 |
| СПОСОБ ПОЛНОЙ МАЛОИНВАЗИВНОЙ ЭНДОСКОПИЧЕСКИ АССИСТИРОВАННОЙ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА ПРИ МНОГОСОСУДИСТОМ АТЕРОСКЛЕРОТИЧЕСКОМ ПОРАЖЕНИИ КОРОНАРНОГО РУСЛА | 2019 |
|
RU2723751C1 |
| СПОСОБ ПОЛУЛОСКУТНОГО ВЫДЕЛЕНИЯ ВНУТРЕННЕЙ ГРУДНОЙ АРТЕРИИ С ИСПОЛЬЗОВАНИЕМ УЛЬТРАЗВУКОВОГО ГАРМОНИЧЕСКОГО СКАЛЬПЕЛЯ | 2019 |
|
RU2731003C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С СОЧЕТАННЫМ АТЕРОСКЛЕРОТИЧЕСКИМ ПОРАЖЕНИЕМ СОННЫХ И КОРОНАРНЫХ АРТЕРИЙ | 2010 |
|
RU2476165C2 |
| Способ мобилизации сердца | 2016 |
|
RU2624815C1 |
| Способ органопротекции при протезировании проксимальной части дуги аорты | 2022 |
|
RU2789385C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ТРАХЕАЛЬНО-ЛЕГОЧНОГО КОМПЛЕКСА В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2541827C1 |
Способ относится к медицине, а именно к сердечно-сосудистой хирургии. Выполняют стернотомию. Выделяют правую внутреннюю грудную артерию. Подключают аппарат искусственного кровообращения и проводят кардиоплегию. Непосредственно после кардиоплегии производят поперечную аортотомию на уровне сино-тубулярного гребня. Циркулярно обходят ствол легочной артерии, отводят его на держалке. После чего при помощи держалок выводят в рану ствол левой коронарной артерии. Выполняют его продольную артериотомию. Затем формируют анастомоз конец в бок между правой внутренней грудной артерией и стволом левой коронарной артерии. Способ позволяет увеличить продолжительность жизни больных за счет использования только аутоартериального графта, снизить риск развития кровотечений, связанных с приемом антиагрегантов. 1 ил., 1 пр.
Способ прямой реваскуляризации миокарда при изолированном устьевом поражении ствола левой коронарной артерии, включающий выполнение стернотомии, выделение правой внутренней грудной артерии, подключение искусственного кровообращения и проведение кардиоплегии, отличающийся тем, что непосредственно после кардиоплегии производят поперечную аортотомию на уровне сино-тубулярного гребня, циркулярно обходят ствол легочной артерии, отводят его на держалке, обеспечивая визуализацию, при помощи держалок выводят в рану ствол левой коронарной артерии, выполняют его продольную артериотомию и формируют анастомоз конец в бок между правой внутренней грудной артерией и стволом левой коронарной артерии.
| БОРИСОВ А | |||
| И., Особенности хирургического лечения больных ишемической болезнью сердца при сужении ствола левой коронарной артерии, Автореферат, СПб, 2011, 8-15 | |||
| СПОСОБ РЕВАСКУЛЯРИЗАЦИИ МИОКАРДА ПОСЛЕ ИССЕЧЕНИЯ АНЕВРИЗМЫ ЛЕВОГО ЖЕЛУДОЧКА | 1994 |
|
RU2110959C1 |
| Ишенин Ю.М | |||
| Моделирование и хирургическое лечение ишемических состояний миокарда | |||
| Автореф.дис.докт., - М., 1989 | |||
| Сердечно-сосудистая хирургия / Под ред | |||
| В.И. | |||
Авторы
Даты
2015-05-20—Публикация
2014-03-25—Подача