Изобретение относится к медицине, конкретно к кардиологии, рентгеноваскулярной хирургии и клинической лабораторной диагностике.
Известно использование катетеров в ангиопластике и стентировании. Катетер, имеющий на дистальном конце баллон, продвигают вперед по проводящей струне до стенозированного участка артерии. Как только баллон поступает в стенозированный участок артерии, его подвергают раздуванию и сдуванию (инфляции и дефляции). Инфляция баллона и его последующая дефляция уменьшает выраженность стеноза артерии и способствует восстановлению адекватного кровотока в дистальном участке артерии.
Химические/физические и механические характеристики полимерного материала, из которого состоит баллон, определяют его пластичность, то есть адаптируемость баллона к артериальной системе и его сопротивляемость к растяжению, являющиеся основными характеристиками оптимального режима баллона. Требования к пластичности и прочности и размерам баллона могут меняться в зависимости от вида использования и размера сосуда, в который вводят катетер. Преимущества, которые дают различные полимеры, согласуются с конкретными механическими применениями баллонов.
Известен баллон для медицинских устройств, в частности для катетеров, используемых в ангиопластике, содержащий полиамидный сополимерный материал, отличающийся тем, что указанный сополимерный полиамидный материал представлен общей формулой H-(O-PF-OOC-PA-COO-PF-COO-PA-CO)n-OH, в которой PA является полиамидным сегментом, PF является диольным сегментом, содержащим сложные полиэфиры димерных диолов с концевыми OH-группами, и n составляет число от 5 до 20, см. патент РФ №2327489. Данный баллонный катетер способен улучшить характеристики пластичности по сравнению с баллонами предшествующего уровня техники.
Кроме того, актуальной является проблема сохранения и транспортировки образца клеточного материала, изъятого у пациента, к месту проведения сложного цитологического и/или иммуноцитохимического анализа, требующего наличия соответствующего лабораторного оборудования и квалифицированного персонала исследователей.
В настоящее время наиболее эффективным способом подготовки образца ткани для проведения сложного цитологического и/или иммуноцитохимического анализа является цитоцентрифугирование, то есть разделение на фракции клеточных элементов по размеру с целью получения препаратов. В то же время при осуществлении стадии центрифугирования живые клетки испытывают интенсивную механическую нагрузку, которая может привести к искажению их морфологии. В связи с этим большое значение имеет состав среды, в которую помещен образец живой ткани. С одной стороны, исследуемые клетки должны сохранить свои морфологические, биологические и биохимические характеристики, в частности их иммунную специфичность, а с другой стороны, среда для накопления клеток не должна препятствовать осуществлению процесса центрифугирования.
Известен раствор для консервации клеток, представляющий собой водный спиртово-буферный раствор, предназначенный для сохранения в пробе in vitro морфологии ядер клеток млекопитающих, включающий смешивающийся с водой спирт, ионы кальция и магния и буферный агент (патент EP 0772972). Известному раствору присущи недостатки, свойственные как буферным, так и спиртовым средам:
- частичное обезвоживание исследуемых клеток за счет присутствия в составе спиртов. Обезвоживание цитоплазмы приводит к нарушению внутриклеточных биохимических процессов, в частности к сморщиванию цитоплазматической мембраны и, следовательно, к изменению морфологии многих клеток, особенно злокачественных, ускорению их гибели и, в конечном результате, к искажению результатов последующего анализа;
- буферные системы являются хорошими консервантами, но не пригодны для сохранения клеточного материала в течение более десяти - двенадцати часов вследствие отсутствия в их составе источника питания клеток: белков и углеводов.
Известна также физиологическая среда для промывания, консервации и хранения клеток тканей и органов, содержащая солевые компоненты, буферные компоненты, компоненты субстрата, аминокислоты, компоненты куэнзимов, витаминные компоненты, компоненты протеинов (патент EP 1164841). Недостатком известной среды, препятствующим достижению указанных ниже технических результатов, является наличие большого количества чужеродных белков, в частности белковых компонентов сывороток, присутствие которых в исследуемой пробе может привести к искажению тонких иммунных реакций при проведении последующего иммунногистохимического анализа.
Известна питательная среда накопления образца клеток для последующего цитологического и/или иммуноцитохимического анализа так же, как известный раствор Хенкса, содержит соли NaCl, KCl, CaCl2, безводный, MgSO4·6H2O, MgCl2·6H2O, Na2HPO4·2H2O, KH2PO4, NaHCO3 и глюкозу. Особенность заявляемой среды состоит в том, что она дополнительно включает 10% раствор альбумина и полиглюкин (декстран 60000) при следующем соотношении: 10% раствор альбумина: раствор Хенкса: полиглюкин = 1: 1: 1, см. патент РФ №2246110. Изобретение позволяет создать среду для накопления, сохранения и промывания образца клеток, изъятых у пациента, для последующего цитологического и/или иммуноцитохимического анализа, максимально приближенную к естественным физиологическим условиям их существования.
Известны средства для обнаружения атеросклеротических бляшек с измененной метаболической активностью.
Известен способ обнаружения и определения состояния атеросклеротических бляшек (АСБ) посредством внутрисосудистого ультразвукового исследования. Способ позволяет исследовать элементы сосудистой стенки и состав АСБ, дает возможность проводить в реальном масштабе времени тонкий элементный анализ атеросклеротически измененного участка артерии, выявить осложненные и элементно нестабильные бляшки (Савченко А.П., Атьков О.Ю., Черкавская О.В. Внутрисосудистое ультразвуковое исследование коронарных артерий. // Методические рекомендации. http://www.angiography.su/new/doctors/metod.html). Недостатком данного способа является то, что он дает информацию только о элементных особенностях АСБ, не позволяет судить об изменениях метаболизма АСБ и не предусматривает возможность проведения терапевтических процедур.
Известен способ обнаружения воспаленных АСБ, описанный в патенте США №7977058, который предполагает введение конъюгата лиганда к макрофагам и флюорофора и регистрацию флюоресценции. Недостатком данного способа является то, что он дает информацию только о наличии воспаленной АСБ, не позволяет судить об изменениях метаболизма АСБ и не предусматривает возможность проведения терапевтических процедур.
Известен способ обнаружения АСБ с измененной метаболической активностью за счет введения 5-АЛК, измерения спектров флюоресценции при возбуждении в диапазоне длин волн 390-650 нм, определения участков с повышенным накоплением 5-АЛК-индуцированного протопорфирина IX и выявления среди этих участков областей с пиком флюоресценции в диапазоне 670-680 нм.
Известен способ обнаружения АСБ с измененной метаболической активностью, заключающийся во введении 5-аминолевулиновой кислоты, измерении спектров флюоресценции при возбуждении в диапазоне длин волн 390-650 нм, определении участков с повышенным накоплением 5-АЛК-индуцированного протопорфирина IX и выявлении среди этих участков областей с пиком флюоресценции в диапазоне 670-680 нм, см. патент РФ 2480143.
Баллонная ангиопластика артерий и метод жидкостной цитологии являются аналогами указанных изобретений. Применение метода жидкостной цитологии в сочетании с баллонной ангиопластикой артерий позволяет рассматривать баллоную ангиопластику артерий не только как лечебную, но и как диагностическую процедуру. Сочетание указанных методов в качестве диагностической процедуры до настоящего момента не использовалось в клинической практике.
Недостатком известных технических решений является возможность утратить часть клеток и неклеточных элементов АСБ при извлечении баллона. Данный недостаток обусловлен тем, что элементы АСБ могут быть смыты с баллона потоком крови в артерии, а также тем, что различные баллоны, применяемые при баллонной ангиопластике, обладают различными адгезивными свойствами.
Задачей изобретения является получение клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерии у пациентов при проведении им баллонной ангиопластики и (или) стентирования артерий. После получения клеток и неклеточных элементов АСБ указанный материал может быть подвергнут различным цитологическим, иммуноцитохимическим исследованиям, исследованиям, направленным на выявление инфекционных агентов в клетках и неклеточных элементов АСБ.
Согласно изобретению способ получения клеток и неклеточных элементов атеросклеротической бляшки, включающий процедуру баллонной ангиопластики, характеризуется тем, что после выполнения баллонной ангиопластики с поверхности баллонного катетера производят смыв клеток и неклеточных элементов, затем полученную суспензию клеток и неклеточных элементов подвергают центрифугированию, удаляют надосадочную жидкость, осуществляют ресуспензирование клеток и неклеточных элементов, затем суспензии клеток и неклеточных элементов помещают в заряженные цитобакеты, которые центрифугируют, после чего полученные препараты используют для дальнейших исследований.
Кроме того, заявленное техническое решение характеризуется рядом дополнительных факультативных признаков, раскрывающих частные случаи его практического использования, а именно:
- смыв клеток и неклеточных элементов атеросклеротической бляшки с поверхности баллонного катетера осуществляют путем помещения баллонного катетера в контейнер, содержащий стерильный фосфатно-солевой буфер, расправляют баллонный катетер за счет поддачи в него воздуха и неоднократно встряхивают;
- суспензию полученных при промывании баллонного катетера клеток и неклеточных элементов центрифугируют со скоростью 1000 об/мин в течение 10-15 минут в роторной центрифуге;
- надосадочную жидкость сливают или удаляют пипеткой;
- цитобакеты центрифугируют со скоростью 1000 об/мин в течение 5 минут.
Проявляющийся при реализации совокупности существенных признаков заявленного решения технический результат заключается в применение метода жидкостной цитологии в сочетании с баллонной ангиопластикой артерии, что является новым подходом к баллонной ангиопластике артерий как к диагностической процедуре. Это обеспечивает возможность получения клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий у пациентов при выполнении им по показаниям баллонной ангиопластики артерий.
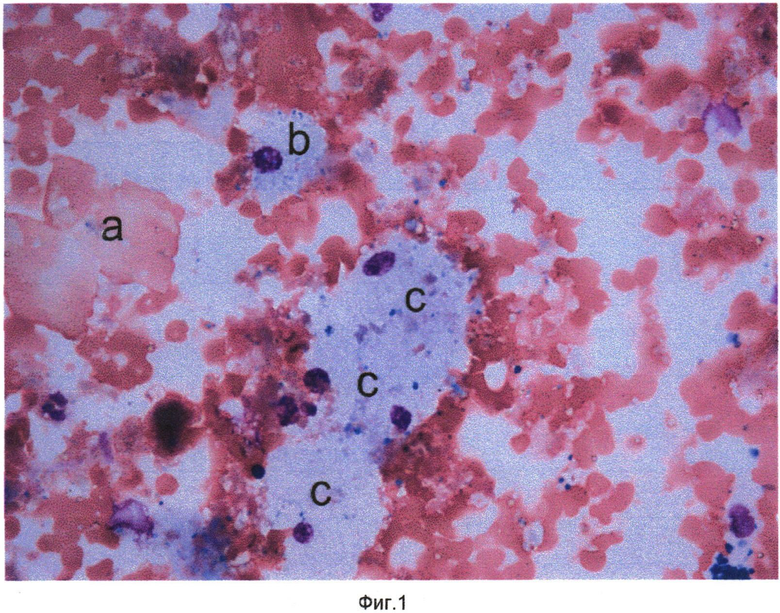
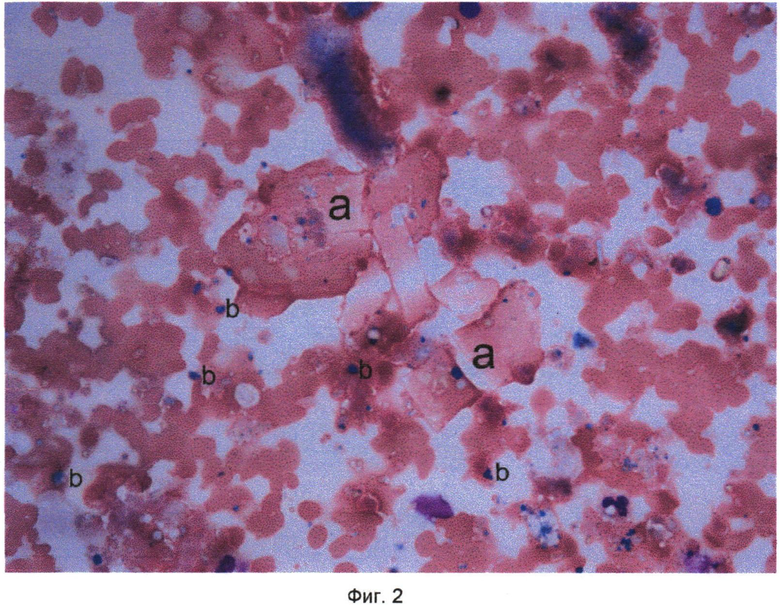
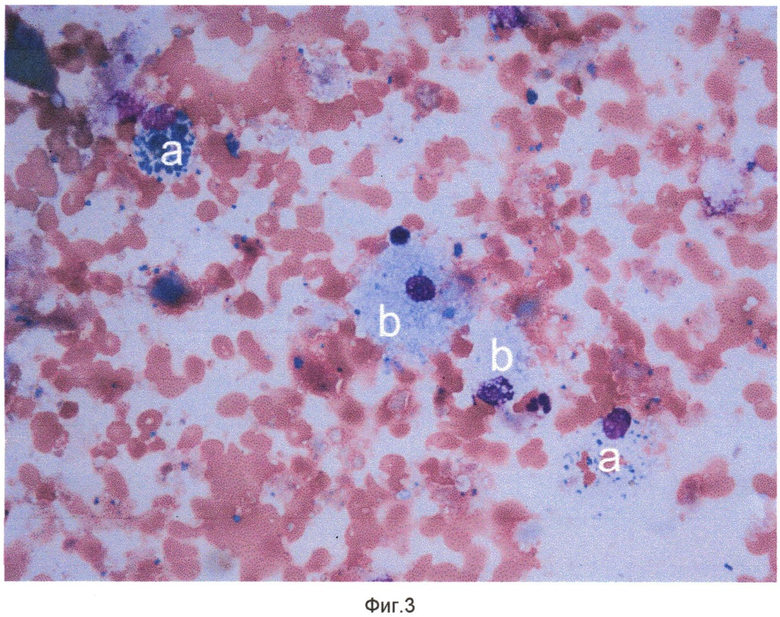
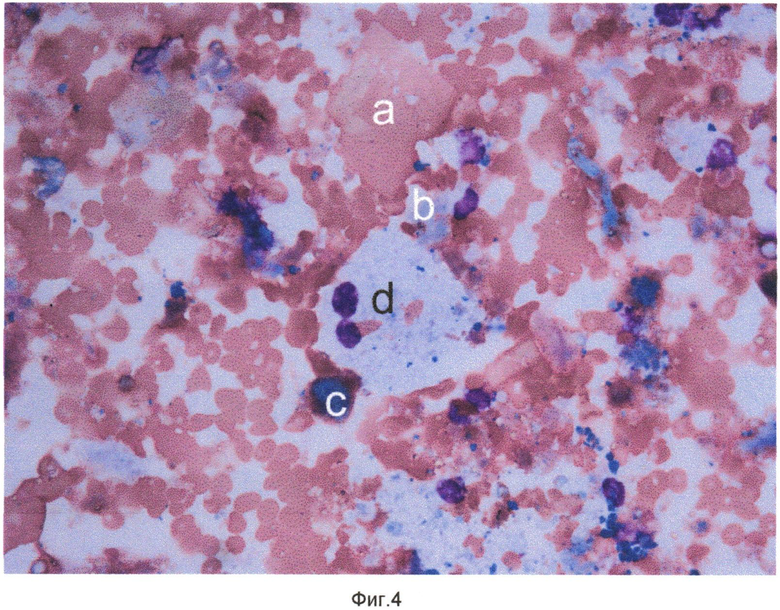
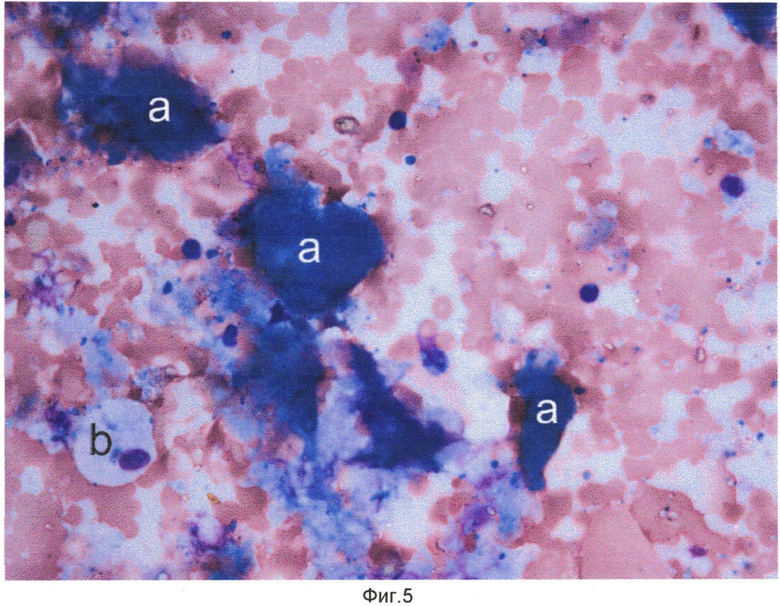
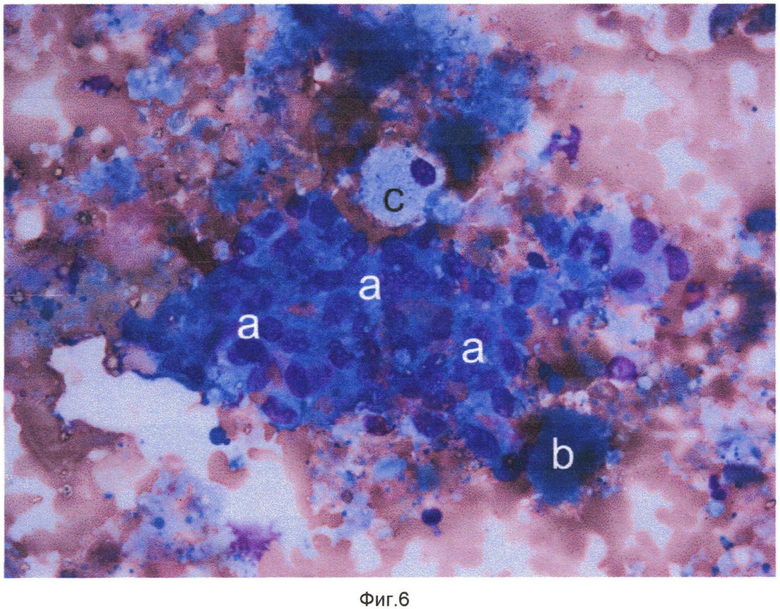
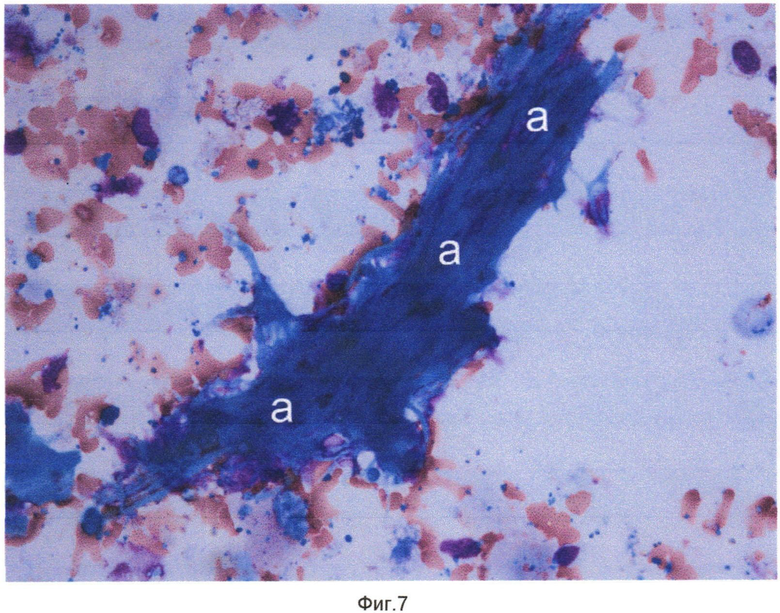
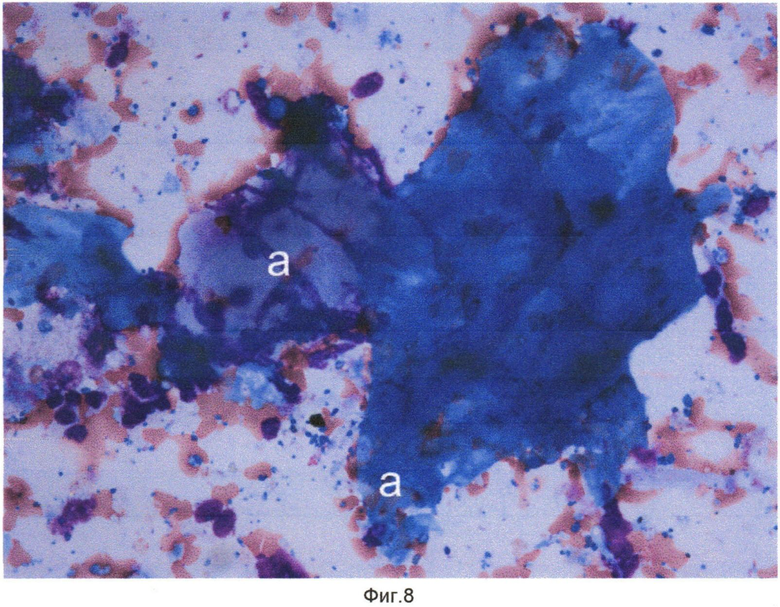
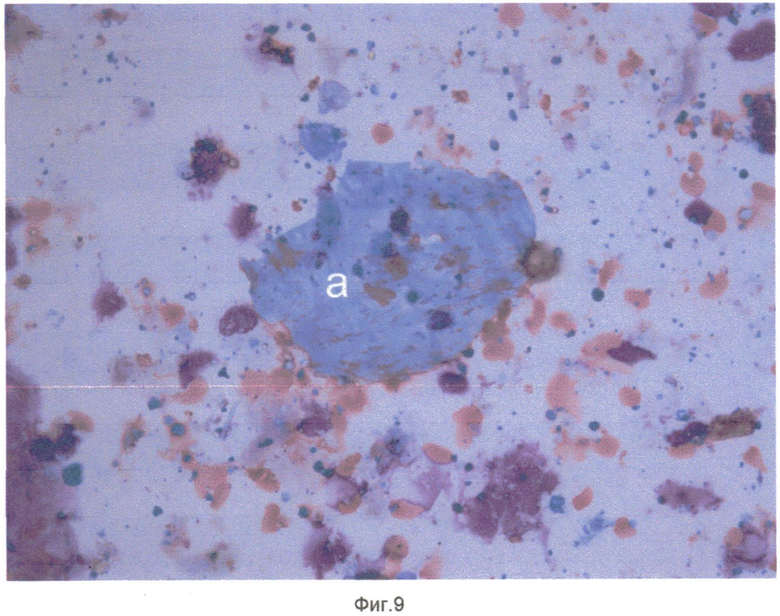
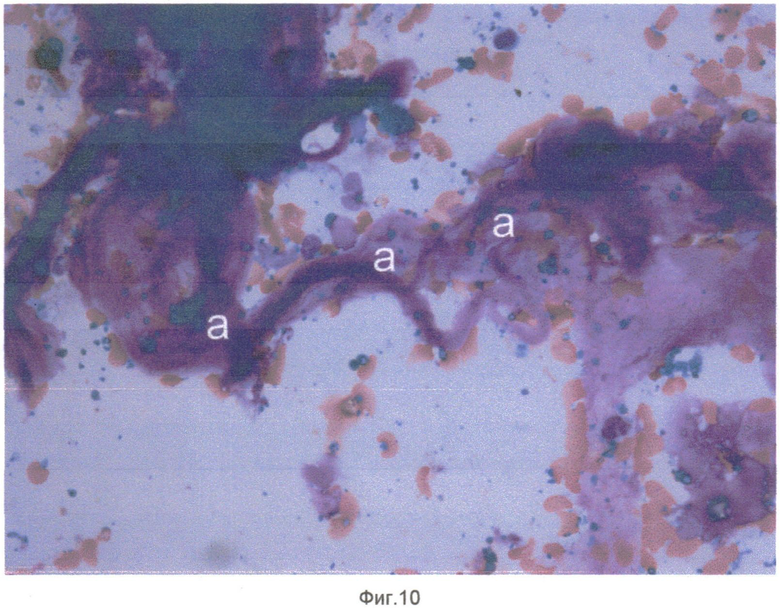
Сущность изобретения поясняется чертежами, где на фиг. 1 показаны кристаллы холестерина (a), одноядерный макрофаг - пенистая клетка (b), конгломерат пенистых клеток (c) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 2 - кристаллы холестерина (a), элементы атероматозной массы (b) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 3 - одноядерные макрофаги (a) и макрофаги - пенистые клетки (b) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 4 - кристалл холестерина (a), ядросодержащий эндотелиоцит (b), цитоплазма безъядерного эндотелиоцита (c), двухъядерный макрофаг - пенистая клетка (d) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 5 - цитоплазма безъядерных эндотелиоцитов (a), пенистая клетка (b) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 6 - конгломерат ядросодержащих эндотелиоцитов (a), цитоплазма безъядерного эндотелиоцита (b), пенистая клетка (c) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 7 - соединительнотканные волокна фиброзной капсулы (a) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 8 - часть цитоплазмы фибробласта с соединительнотканными волокнами (a) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 9 - часть цитоплазмы миофибробласта (a) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий, на фиг. 10 - соединительнотканные волокна фиброзной капсулы (a) в препарате цитоцентрифугата клеток и неклеточных элементов внутренней поверхности атеросклеротически измененного участка артерий. На всех фигурах окрашивание по Май-Грюнвельд, увеличение 400х.
Способ осуществляется следующим образом
Материалами для исследования служат смывы клеток и неклеточных элементов атеросклеротической бляшки, полученные у пациентов с различными формами ишемической болезни сердца при выполнении им по показаниям баллонной ангиопластики артерий, в частности, коронарных.
Сразу после выполнения баллонной ангиопластики катетер помещается в контейнер, содержащий 20 мл стерильного фосфатно-солевого буфера. При помощи шприца, соединенного с воздуховодом баллонного катетера, непосредственно в контейнере с фосфатно-солевым буфером баллонный катетер расправляется воздухом и несколько раз встряхивается. После промывания клеток и неклеточных элементов в фосфатно-солевом буфере указанным способом баллонный катетер подлежит утилизации, а суспензия клеток и неклеточных элементов с поверхности баллонного катетера в растворе буфера доставляется в лабораторию. 20 мл суспензии, полученной при промывании баллонного катетера, разливаются в 2 пробирки. Пробирки центрифугируются со скоростью 1000 об/мин в течение 10мин в роторной центрифуге. По окончании центрифугирования надосадочная жидкость, которая не содержит клеток и неклеточных элементов, аккуратно удаляется пипеткой либо сливается. После этого в каждую пробирку добавляется фосфатно-солевой буфер до 0.5-1 мл для ресуспензирования клеток и неклеточных элементов. Предметные стекла накрываются фильтровальной бумагой, помещаются в цитобакеты и фиксируются зажимами. Заряженные предметными стеклами цитобакеты помещаются в цитоцентрифугу. Из каждой пробирки пипеткой забирается по 0,125-0,25 мл суспензии и помещается в заряженные цитобакеты. Цитобакеты центрифугируются со скоростью 1000 об/мин в течение 5 минут. После цитоцентрифугирования и высыхания в течение 30мин либо фиксации препараты годны для дальнейших цитологических, иммуноцитохимических и прочих методов исследования.
Пример 1: Больной Г., 63 года. Диагноз: ИБС. Стенокардия напряжения II функционального класса. Атеросклероз коронарных артерий: стеноз ствола левой коронарной артерии - 30%, передней межжелудочковой артерии - 80%, 1-ой диагональной артерии - 50%, огибающей артерии - 60%, правой коронарной артерии - 50%, стеноз ретровентрикулярной ветви - 60-70%. Выполнена операция: Коронарография и коронаропластика со стентированием передней межжелудочковой артерии. Протокол операции: под контролем артериального давления в устье левой коронарной артерии установлен гайд-катетер EBU4 5F. Через область стеноза в переднюю межжелудочковую артерию на периферию проведен коронарный проводник "ATW". В область стеноза в проксимальной трети передней межжелудочковой артерии имплантирован стент с лекарственным покрытием "Xience V" 3,5×15 мм (p=12 атм). Постдилатация стента баллонным катетером "NC Trek" 3,5×8 мм (p=24 атм). Контрольная коронарография: оптимальный результат. Область ангиопластики без признаков диссекции или тромбоза. Кровоток удовлетворительный (TIMI III).
Пример 2: Больной Д., 77 лет. Диагноз: ИБС. Стенокардия напряжения и покоя IV ФК. Атеросклероз коронарных артерий: стеноз передней межжелудочковой артерии 80%, диагональной артерии 50%, огибающей артерии 95%. Выполнена операция: Коронарография и коронаропластика со стентированием передней межжелудочковой артерии, огибающей артерии. Протокол операции: Под контролем артериального давления в устье огибающей артерии установлен гайд-катетер XB4. Через область стеноза в огибающей артерии на периферию проведен коронарный проводник "Asahi Soft". Предилатация стеноза баллонным катетером "Sprinter Legend" 2,0×15 мм (p=10 атм). В область стеноза в проксимальной трети огибающей артерии имплантирован стент "Coroflex Blue" 3,5×24 мм (p=14 атм). Через область стеноза в переднюю межжелудочковую артерию на периферию проведен коронарный проводник "Asahi Soft". Предилатация стеноза баллонным катетером "Sprinter Legend" 1,5×10 мм. В область стеноза в проксимальной трети передней межжелудочковой артерии имплантирован стент с лекарственным покрытием "Xience V" 3,0×28 мм (p=14 атм). Контрольная коронарография: оптимальный результат. Область ангиопластики без признаков диссекции или тромбоза. Кровоток удовлетворительный (TIMI III).
После выполнения пациентам описанных оперативных вмешательств с поверхности баллонных катетеров произвели смыв клеточных и неклеточных элементов внутренних поверхностей атеросклеротически измененных участков артерий и указанным выше способом приготовили препараты. Окрашенные по методу Май-Грюнвельда препараты изучали с использованием световой микроскопии. В ходе световой микроскопии были обнаружены элементы атеросклеротической бляшки, отмеченные на фиг. 1-10.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения эндотелиальных клеток человека | 2022 |
|
RU2806050C2 |
| Способ прогнозирования состава эмболического материала в системе дистальной противоэмболической защиты мозга после транслюминальной баллонной ангиопластики со стентированием внутренней сонной артерии | 2022 |
|
RU2786477C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА | 2004 |
|
RU2267323C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА | 2005 |
|
RU2299730C1 |
| Способ гибридной реваскуляризации при многоуровневом поражении брахиоцефальных артерий | 2021 |
|
RU2786008C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА | 2008 |
|
RU2365380C1 |
| Способ открытой эндартерэктомии при диффузном атеросклеротическом поражении передней межжелудочковой артерии | 2018 |
|
RU2717372C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО ИНФАРКТА МИОКАРДА | 2018 |
|
RU2702146C1 |
| ЛЕЧЕНИЕ СТЕНОЗА | 2018 |
|
RU2829274C2 |
| СПОСОБ ЦИТОЛОГИЧЕСКОЙ ДИАГНОСТИКИ РАКА МОЧЕВОГО ПУЗЫРЯ | 2014 |
|
RU2547567C1 |
Изобретение относится к области медицины, а именно к способу получения клеток и неклеточных элементов атеросклеротической бляшки. Сущность способа состоит в том, что после выполнения баллонной ангиопластики с поверхности баллонного катетера производят смыв клеток и неклеточных элементов, затем полученную суспензию клеток и неклеточных элементов подвергают центрифугированию, удаляют надосадочную жидкость, осуществляют ресуспензирование клеток и неклеточных элементов, затем суспензии клеток и неклеточных элементов помещают в заряженные цитобакеты, которые центрифугируют, после чего полученные препараты используют для дальнейших исследований. Использование заявленного способа обеспечивает возможность получения клеток и неклеточных элементов атеросклеротической бляшки у пациентов при выполнении им по показаниям баллонной ангиопластики артерий. 4 з.п. ф-лы, 10 ил., 2 пр.
1. Способ получения клеток и неклеточных элементов атеросклеротической бляшки, включающий процедуру баллонной ангиопластики артерий, отличающийся тем, что после выполнения баллонной ангиопластики с поверхности баллонного катетера производят смыв клеток и неклеточных элементов, затем полученную суспензию клеток и неклеточных элементов подвергают центрифугированию, удаляют надосадочную жидкость, осуществляют ресуспензирование клеток и неклеточных элементов, затем суспензии клеток и неклеточных элементов помещают в заряженные цитобакеты, которые центрифугируют, после чего полученные препараты используют для дальнейших исследований.
2. Способ по п. 1, отличающийся тем, что смыв клеток и неклеточных элементов атеросклеротической бляшки с поверхности баллонного катетера осуществляют путем помещения баллонного катетера в контейнер, содержащий стерильный фосфатно-солевой буфер, расправляют баллонный катетер за счет поддачи в него воздуха и неоднократно встряхивают.
3. Способ по п. 1, отличающийся тем, что суспензию клеток и неклеточных элементов, полученных при промывании баллонного катетера, центрифугируют со скоростью 1000 об/мин в течение 10-15 минут в роторной центрифуге.
4. Способ по п. 1, отличающийся тем, что надосадочную жидкость удаляют пипеткой либо аккуратно сливают.
5. Способ по п. 1, отличающийся тем, что цитобакеты центрифугируют со скоростью 1000 об/мин в течение 5 минут.
| ЛЕБЕДЕВА А.М | |||
| Атеросклеротические бляшки в системе ex vivo// Креативная кардиология, 1, 2012 | |||
| Зубчатое колесо со сменным зубчатым ободом | 1922 |
|
SU43A1 |
| ОВЧИННИКОВА О.А | |||
| Механизмы нарушения структуры коллагена при дистабилизации атеросклеротической бляшки в клинике и эксперименте | |||
| Автореферат | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| ШЛЫЧКОВА Т.П | |||
| Структурные особенности и распространенность нестабильных атеросклеротических бляшек | |||
Авторы
Даты
2015-06-10—Публикация
2013-10-02—Подача