ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к химической энзимологии, в частности к созданию наночастиц антиоксидантного фермента супероксиддисмутазы в виде полиэлектролитного комплекса типа фермент/поликатион/полианион, которые предназначены для медицинского применения.
УРОВЕНЬ ТЕХНИКИ
Активные формы кислорода (АФК) являются естественными продуктами метаболизма клеток. Избыток АФК и их производных образуется в результате ряда заболеваний: болезнь Альцгеймера, Паркинсона, инфаркт, инсульт, ревматоидный артрит, воспалительное заболевание кишечника и т.д. Отдельно стоит упомянуть про процессы воспаления вообще и роль, которую играют в них АФК. Источниками свободных радикалов в зоне воспаления служат: дыхательный взрыв фагоцитов при их стимуляции, каскад арахидоновой кислоты, ферментные процессы в эндоплазматическом ретикулуме и пероксисомах, митохондриях, цитозоле, а также самоокисление катехоламинов, лейкофлавинов, гидрохинонов [Петрович Ю.А., Гуткин Д.В. Свободнорадикальное окисление и его роль в патогенезе воспаления, ишемии и стресса // Патол. физиолог. и эксперимент. терапия, 1986, Т.5, С.85-92]. В очаге воспаления процессы, связанные со свободными радикалами, значительно активируются. Например, в случае контузионной травмы спинного мозга (КТСМ), известно, что свободнорадикальное окисление является одним из основополагающих факторов в патогенезе постравматической нейродегенерации и клеточной смерти [Hall E.D., Yonkers P.A., Andrus P.K., Сох J.W., Anderson D.K. Biochemistry and pharmacology of lipid antioxidants in acute brain and spinal cord injury // J Neurotrauma, 1992, V.9., P.425-442]. Взрывообразное высвобождение свободных радикалов в области травмы спинного и/или головного мозга приводит к истощению эндогенных антиокисдантов, что способствует постравматической клеточной смерти путем неконтролируемого перекисного окисления. Это является важным фактором воспаления и сопутствующего отека, который оказывает давление на нервные волокна и приводит к дегенерации и демиелинизации нервных проводников, гибелью части аксонов и глии. Предполагается, что введение антиоксидантных препаратов непосредственно после травмы, в остром периоде, способно привести к уменьшению перекисного окисления и таким образом уменьшить объем повреждения. К числу факторов антиоксидантной защиты тканей относятся ферменты: каталаза, супероксиддисмутаза, глутатионпероксидаза, а также витамин К, α-токоферол, метионин и др.
Ферменты обладают высокой специфичностью и, как следствие, их антиоксидантная эффективность на порядок выше по сравнению с витаминами. Поэтому введение именно антиоксидантных ферментов (супероксиддисмутаза, каталаза) позволит нейтрализовать АФК в зоне травмы, способствуя уменьшению отека и нейродегенерации. Так как супероксид радикал лежит в основе цепочки превращений, приводящей к появлению самых различных АФК, в первую очередь использование супероксиддисмутазы (СОД) является приоритетным направлением.
Однако введение в организм нативных ферментов крайне нерационально, так как они подвергаются протеолизу и быстро выводятся из организма. Для увеличения времени жизни фермента и эффективности его транспорта в организме были разработаны самые разные подходы: конъюгация с полимерными цепями, включение в наноконтейнеры и др. Время циркуляции и стабильность ферментов в чужеродной среде может быть увеличена до нескольких часов путем их ПЭГилирования - модификации белка ПЭГ цепями [J.S. Beckman, R.L. Minor Jr., C.W. White, J.E. Repine, G.M. Rosen, B.A. Freeman. Superoxide dismutase and catalase conjugated to polyethylene glycol increases endothelial enzyme activity and oxidant resistance // J. Biol. Chem. 1988. V.263. P.6884-6892; F.M. Veronese, P. Caliceti, O. Schiavon, M. Sergi. Polyethylene glycol-superoxide dismutase, a conjugate in search of exploitation // Adv. Drug Deliv. Rev. 2002. V.54. P.587-606]. Однако такая модификация значительно понижает проницаемость ферментов через микрососуды в область повреждения [Francis JW, Ren J, Warren J, Brown RH Jr, Finklestein SP. Postischemic infusion of Cu/Zn superoxide dismutase or SOD: Tet451 reduces cerebral infarction following focal ischemia/reperfusion in rats. Exp Neurol. 1997; 146:435-443]. Кроме того, ПЭГилирование СОД ведет к образованию гетерогенных продуктов из-за большого количества доступных аминогрупп на поверхности фермента (20 лизинов для димера). Длина ПЭГ чрезвычайным образом влияет на биораспределение и времена циркуляции СОД-ПЭГ в организме, а также на антигенные и иммуногенные свойства конструкции [K. Knop, R. Hoogenboom, D. Fischer, U.S. Schubert. Poly(ethylene glycol) in Drug Delivery: Pros and Cons as Well as Potential Alternatives // Angew. Chem. Int. Ed. 2010, 49, 6288-6308].
Другой подход заключается во включении СОД в биоразлагаемые и биосовместимые полилактогликолевые (ПЛГ) наночастицы на основе сополимера D,L-лактид-гликоля [М.К. Reddy, V. Labhasetwar. Nanoparticle-mediated delivery of superoxide dismutase to the brain: an effective strategy to reduce ischemia-reperfusion injury // FASEB J. 2009. V.23. P.1384-1395]. Однако ПЛГ матрица затрудняет доступ субстрата к активному центру фермента и имеет достаточно большие размеры (гидродинамический диаметр 290 нм, таблица 1). Кроме того, гидролиз полилактогликоля может быстро дезактивировать ферменты в матрице [W. Jiang, S.P. Schwendeman. Stabilization of tetanus toxoid encapsulated in PLGA microspheres. Mol. Pharm. 2008. V.5. P.808-817].
Для увеличения времени жизни ферментов в крови была разработана технология их включения в липосомы [M.L. Corvo, О.С. Boerman, W.J. Oyen, L. Van Bloois, M.E. Cruz, D.J. Crommelin, G. Storm. Intravenous administration of superoxide dismutase entrapped in long circulating liposomes: in vivo fate in a rat model of adjuvant arthritis // Biochim. Biophys. Acta. 1999. V. 1419. P. 325-334; B.A. Freeman, S.L. Young, J.D. Crapo. Liposome-mediated augmentation of superoxide dismutase in endothelial cells prevents oxygen injury // J. Biol. Chem. 1983. V.258. P.12534-12542]. Внутривенное введение катионных липосом, содержащих СОД, привело к частичному уменьшению объема повреждения при ишемии головного мозга у крыс, однако липосомы оказались нестабильными (период полураспада 4,2 ч) и потенциально токсичными [Imaizumi, S., Woolworth, V., Fishman, R.A., and Chan, P.H. Liposome-entrapped superoxide dismutase reduces cerebral infarction in cerebral ischemia in rats. Stroke, 1990, V.21, P. 1312-1317; Sinha J, Das N, Basu MK. Liposomal antioxidants in combating ischemia-reperfusion injury in rat brain. Biomed Pharmacother. 2001, V.55, P.264-271]. Кроме того, СОД может постепенно высвобождаться из липосом, в зависимости от их размеров, и быстро выводиться из организма (период полувыведения свободной СОД - 6 мин).
С помощью генной инженерии были разработаны конъюгаты PEP-1-СОД 1 и РЕР-1-каталаза для лечения последствий инсульта [W.S. Eum, D.W. Kim, I.K. Hwang, K.Y. Yoo, T.C. Kang, S.H. Jang, H.S. Choi, S.H. Choi, Y.H., Kim, S.Y. Kim, H.Y. Kwon, J.H. Kang, O.S. Kwon, S.W. Cho, K.S. Lee, J. Park, M.H. Won, S.Y. Choi. In vivo protein transduction: biologically active intact pep-1-superoxide dismutase fusion protein efficiently protects against ischemic insult // Free Radic. Biol. Med. 2004, V.37, P. 1656-1669]. Однако эти конъюгаты относительно нестабильны в кровотоке и могут вызывать иммунный ответ у пациентов.
Также была разработана методика получения наночастиц (нанозимов) на основе комплексов ферментов и блок-сополимеров, основанная на самопроизвольной сборке противоположно заряженных полиионов [Klyachko N.L., Manickam D.S., Brynskikh A.M., Uglanova S.V., Li S., Higginbotham S.M., Bronich Т.K., Batrakova E.V., Kabanov A.V. Cross-linked antioxidant nanozymes for improved delivery to CNS // Nanomed. Nanotechnol. Biol. Med. 2012. V.8. P.119-129]. Это простой в техническом плане подход позволяет получить стехиометрические комплексы со 100% эффективностью загрузки ферментом (по сравнению с 32% для СОД и 21% для каталазы в случае липосом [Т. Yusa, J.D. Crapo, B.A. Freeman. Liposome-mediated augmentation of brain SOD and catalase inhibits CNS O2 toxicity // J. Appl. Physiol. 1984. V.57. P.1674-1681]). Авторами была показана биологическая активность полученных препаратов в модели гипертензии, вызванной ангиотензином-II [E.G. Rosenbaugh, J.W. Roat, L. Gao, R.F. Yang, D.S. Manickam, J.X. Yin, H.D. Schultz, Т.K. Bronich, E.V. Batrakova, A.V. Kabanov, I.H. Zucker, M.C. Zimmerman. The attenuation of central angiotensin II-dependent pressor response and intra-neuronal signaling by intracarotid injection of nanoformulated copper/zinc superoxide dismutase // Biomaterials. 2010. V.31. P.5218-5226]. Для увеличения стабильности при разведении блок-иономерного комплекса в его структуру вводили ковалентные сшивки, что приводило к существенной потери активности фермента: например, для комплекса СОД/полилизин-ПЭГ выход по активности СОД составил 45% [заявка WO 2012162490 А1, опубл. 29.11.2012; заявка US 2013/0052154 А1, опубл. 28.02.2013; Devika S. Manickam, Anna M. Brynskikh, Jennifer L. Kopanic, Paul L. Sorgen, Natalia L. Klyachko, Elena V. Batrakova, Tatiana K. Bronich, Alexander V. Kabanov. Well-defined cross-linked antioxidant nanozymes for treatment of ischemic brain injury // Journal of Controlled Release. 2012. V.162. P.636-645]. Чтобы как можно меньше затрагивать активность СОД при конъюгации, авторы вводили небольшое количество ковалентных сшивок, что в итоге привело к низкому выходу по белку (около 10%). В итоге выход по суммарной активности СОД (произведение активности на выход по белку отражает эффективность всего синтеза) составил только 5%. Поэтому актуальной является проблема получения нанозимов без существенной потери активности ферментов и с высоким выходом по белку.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Задачей, решаемой авторами настоящего изобретения, является получение наночастиц антиоксидантного фермента супероксиддисмутазы в виде полиэлектролитного комплекса состава фермент/поликатион/полианион и, в частности, разработка способа создания дисперсии, содержащей такие наночастицы.
Предлагаемая наночастица антиоксидантного фермента супероксиддисмутазы в виде полиэлектролитного комплекса типа фермент/поликатион/полианион характеризуется тем, что фермент покрыт внутренней оболочкой из поликатиона и внешней оболочкой из полианиона, при этом наночастица имеет гидродинамический диаметр в диапазоне 40-70 нм.
Такие наночастицы могут быть получены, в частности, способом, согласно которому к раствору супероксиддисмутазы (СОД) добавляют по каплям при перемешивании раствор поликатиона, затем смесь перемешивают при комнатной температуре в течение 30 минут, после чего по каплям при перемешивании добавляют раствор полианиона и выдерживают смесь при температуре 4°C в течение 8-12 часов, после чего непрореагировавшие реагенты удаляют многократным центрифугированием, используя фильтрующие системы с пределом пропускания ультрафильтрационной мембраны 50000 Да, с получением дисперсии, содержащей наночастицы фермента супероксиддисмутазы в виде полиэлектролитного комплекса типа фермент/поликатион/полианион. При этом фермент покрыт внутренней оболочкой из поликатиона и внешней оболочкой из полианиона. Наночастицы имеют гидродинамический диаметр в диапазоне 40-70 нм.
Предлагается также новый продукт - дисперсия, содержащая вышеописанные наночастицы антиоксидантного фермента супероксиддисмутазы в виде полиэлектролитных комплексов типа фермент/поликатион/полианион и полученная вышеуказанным способом.
Технический результат, достигаемый при осуществлении заявленной группы изобретений, заключается в повышении стабильности фермента в чужеродной среде, сохранении активности фермента и, как следствие, общей активности системы.
Поставленная задача решается тем, что фермент покрывается послойно положительными и отрицательно заряженными полимерами, образуя систему фермент/поликатион/полианион. Первый слой - поликатион - образует полиэлектролитный комплекс с ферментом и защищает его активный центр. Так как положительные полимеры более токсичные по сравнению с отрицательно заряженными, то вводится второй слой полимера - полианион. В результате, образуется водная дисперсия, содержащая наночастицы типа фермент/поликатион/полианион. При этом в качестве полианиона может быть использован конъюгат отрицательно заряженного полимера (полианиона) с полиэтиленгликолем или другим водорастворимым незаряженным полимерным блоком (введение в систему блок-сополимера полианион-полиэтиленгликоль) для уменьшения скорости опсонизации и увеличения времени циркуляции в крови наночастиц фермента. При таком подходе достигается большее сохранение активности фермента по сравнению с запатентованной системой фермент/поликатион (сохранение суммарной активности 5%, заявка US 2013/0052154 A1).
В качестве первого (поликатионного) слоя могут быть использованы полиаминокислоты (например, полилизин, полиаргинин, полигистидин), спермин, протамин, хитозан и другие положительно заряженные полимеры, которые основаны на мономерных звеньях, включающие: аминокислоты (например, лизин, аргинин, гистидин), виниловые мономеры (винилкапролактам, винилпиридин и др.), алкиленимины (например, этиленимин, пропиленимин, бутеленимин и др), первичные, вторичные или третичные амины, которые могут быть полностью или частично в виде аммониевой соли, и другие.
Частными вариантами настоящей группы изобретений являются упомянутые выше наночастицы и способ, согласно которым в качестве поликатиона используется протамин.
Частными вариантами настоящей группы изобретений являются упомянутые выше наночастицы и способ, согласно которым в качестве поликатиона используется полиаргинин.
В качестве второго (полианионного) слоя могут быть использованы отрицательно заряженные полимеры или блок-сополимеры состава А-В или В-А-В, где А - полярный отрицательно заряженный блок и В - полярный незаряженный блок (например, где В - это полиэтиленгликоль, полипропиленгликоль, полиоксазолин, полисахариды и др). В качестве отрицательно заряженного блока могут выступать следующие полимеры и их производные: полиаминокислоты (например, полиглутаминовая кислота, полиаспарагиновая кислота), полиметакриловая кислота, полиакриловая кислота, полилактид, карбоксилированные декстраны и другие.
Частными вариантами настоящей группы изобретений являются упомянутые выше наночастицы и способ, согласно которым в качестве полианиона используется поли(глутаминовая кислота)-полиэтиленгликоль (ПГ-ПЭГ).
КРАТКОЕ ОПИСАНИЕ чертежа
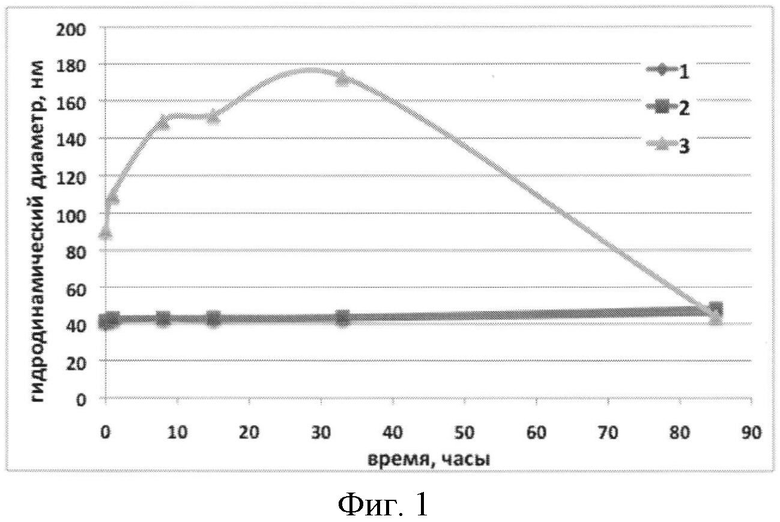
На фигуре 1 представлены результаты стабильности дисперсий полиэлектролитных наночастиц фермент/поликатион/полианион при различных значениях ионной силы среды. Образцы: 1 - СОД/протамин/ПГ-ПЭГ в фосфатном буфере (рН 7,4); 2 - СОД/протамин/ПГ-ПЭГ в физиологическом растворе (10 мМ фосфатный буфер, рН 7,4, 0,15 М NaCl); 3 - СОД/протамин/ПГ-ПЭГ в присутствии избытка низкомолекулярного электролита (10 мМ фосфатный буфер, рН 7,4, 0,6 М NaCl).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Синтез полиэлектролитных наночастиц фермент/поликатион/полианион на примере получения нанодисперсии наночастиц, содержащих фермент супероксиддисмутазу, поликатион - протамин или полиаргинин, полианион - блок-сополимер полиглутаминовой кислоты и полиэтиленгликоля.
Фермент СОД растворяли в ХЕПЕС-NaCl-буфере для получения раствора концентрацией 5 мг/мл. Затем по каплям при перемешивании добавляли раствор поликатиона (протамин или полиаргинин) концентрацией 5 мг/мл. Количество поликатиона считали как кратный избыток аминогрупп по отношению к карбоксильным группам в молекуле СОД (частным вариантом является соотношение 2:1). Смесь перемешивали в течение 30 минут при комнатной температуре. Затем по каплям при перемешивании добавляли раствор полианиона (ПГ-ПЭГ) концентрацией 5 мг/мл. Количество полианиона считали как кратный избыток карбоксильных групп по отношению к карбоксильным группам в молекуле СОД (частным вариантом является соотношение 2:1). Смесь оставляли на 8-12 часов (например, на ночь) при 4°С. Далее свободные полимеры удаляли многократным центрифугированием (2-3 раза), используя фильтрующие системы с пределом пропускания ультрафильтрационной мембраны 50000 Да (800 g, 4°С, ХЕПЕС-NaCl). Полученную дисперсию полиэлектролитных наночастиц в водном растворе собирали в эппендорф, анализировали и хранили при 4°C.
Характеризация полученной дисперсии, содержащей наночастицы антиоксидантного фермента супероксиддисмутазы в виде полиэлектролитного комплекса состава фермент/поликатион/полианион
Таблица 1. Физико-химические характеристики полученных наночастиц СОД в виде полиэлектролитного комплекса СОД/поликатион/ПГ-ПЭГ в сравнении с известными препаратами.
В Таблице 1 представлены выход по белку и выход по активности для исследованных полиэлектролитных комплексов фермент/поликатион/полианион, а также суммарная активность конечного продукта. Видно, что полученная дисперсия наночастиц имеет более высокую суммарную активность (в 4-5 раз) по сравнению с похожей системой СОД/полилизин. Размер и полидисперсность наночастиц СОД/поликатион/ПГ-ПЭГ близки к соответствующим характеристикам препарата СОД/полилизин, и значительно меньше по сравнению с ПЛГ наночастицами или липосомами, что благоприятно сказывается на биораспределении в организме. Считается, что оптимальные размеры наночастиц варьируются от 20 до 100 нм [F. Alexis, E. Pridgen, L.K. Molnar, О.С. Farokhzad, Factors affecting the clearance and biodistribution of polymeric nanoparticles, Molecular Pharmaceutics., 2008. V.5, P.505-515; S.V. Vinogradov, Т.K. Bronich, A.V. Kabanov, Nanosized cationic hydrogels for drug delivery: preparation, properties and interactions with cells. Adv. Drug Deliv. Rev., 2002. V.54, P.135-147].
Определение белка проводилось с помощью набора Micro BCA™ Protein Assay Kit в соответствии с инструкцией производителя. Метод основан на колориметрическом определении комплекса бицинхониновой кислоты с ионами Cu+, образующимися путем восстановления Cu2+ белками. Предел обнаружения белка - 0,5 мкг/мл.
Анализ активности СОД в образцах проводили с использованием двух методов, в основе которых лежат реакции ингибирования автоокисления кверцетина (а) и пирогаллола (б) по известным методикам.
а) Определение активности СОД по кверцетину [Костюк В.А., Потапович А.И., Ковалева Ж.В. Простой и чувствительный метод определения активности супероксиддисмутазы, основанный на реакции окисления кверцетина // Вопр. мед. химии. 1990. Т.36. С.88-91]. В одноразовую спектрофотометрическую кювету объемом 1 мл вносили 0-40 мкл образца и 930-970 мкл рабочего буферного раствора (0,02 M фосфатный буфер, рН 7,4 с добавлением 0,08 мМ ЭДТА и 0,125% ТМЭДА). Реакцию инициировали добавлением 30 мкл раствора кверцетина в ДМСО (0,15 мг/мл) и сразу же измеряли оптическую плотность при длине волны 406 нм (D0), образец инкубировали в течение 20 мин и вновь измеряли оптическую плотность при длине волны 406 нм (D20). В контрольной кювете (без добавления анализируемого раствора) проводили аналогичные измерения - (кD0) и (кD20).
Процент ингибирования реакции автоокисления кверцетина в анализируемых пробах рассчитывали по формуле:
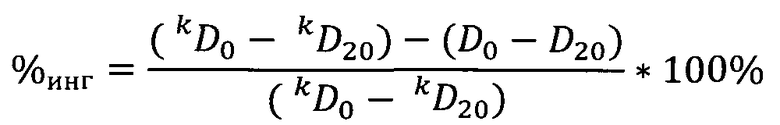
Варьировали объем анализируемого образца в кювете или разбавляли анализируемый раствор фосфатным буфером так, чтобы процент ингибирования реакции автоокисления кверцетина находился в диапазоне 30-55%. Концентрацию СОД, при которой наблюдалось 50% ингибирование реакции автоокисления кверцетина в реакционной среде, принимали за 1 Ед/мл. Для результатов в пределах 30-55% ингибирования проводили расчет активности. Учитывали разведение образца, если оно производилось.
б) Определение активности по пирогаллолу [X. Yi, M.C. Zimmerman, R. Yang, J. Tong, S. Vinogradov, A.V. Kabanov, Pluronic-modified superoxide dismutase 1 (SOD1) attenuates angiotensin II-induced increase in intracellular superoxide in neurons // Free Radic. Biol. Med. 2010. V.49. P.548-58]. Измерения проводили в 96-луночном планшете. Для одного образца использовали 12 лунок (один ряд). Последовательным разбавлением получали 12 точек объемом 20 мкл с концентрациями от 400 до 0,2 мкг/мл. Добавляли 160 мкл Трис-буфера и 20 мкл раствора пирогаллола (раствор пирогаллола в ацетоне 5 мг/мл, затем разбавляли в 10 раз водой). Строили график зависимости скорости окисления пирогаллола от концентрации СОД в логарифмическом масштабе. С помощью программного обеспечения Origin 8.1 полученную зависимость аппроксимировали кривой «доза-ответ» и находили концентрацию, соответствующую 50% ингибированию (EC50, мкг/мл). Далее рассчитывали активность по формуле:
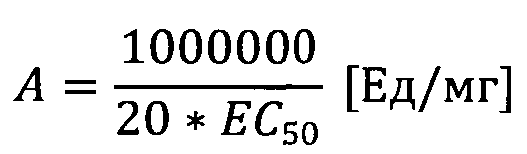
Определение размеров и поверхностного заряда образцов проводили на установке динамического лазерного светорассеяния - Zetasizer Nano ZS «Malvern Instrument», Великобритания. Аликвоту раствора исследуемого образца разбавляли до концентрации 10 мкг/мл и фильтровали через 0,2 мкм фильтр (Coming, Германия). Затем проводили измерения при комнатной температуре. Программное обеспечение, предоставленное производителем, использовали для расчета значений гидродинамического диаметра, ζ-потенциала и относительной ширины распределения частиц по размерам, равной среднеквадратичному отношению ширины распределения к среднему значению размера частиц. Средние значения гидродинамического диаметра и ζ-потенциала для всех образцов рассчитывали как минимум из трех измерений, данные представлены как среднее значение ± среднеквадратичное отклонение.
Стабильность полученных наночастиц СОД в виде полиэлектролитного комплекса СОД/поликатион/ПГ-ПЭГ оценивали во времени, используя метод динамического светорассеяния (фигура 1). Найдено, что частицы стабильны как минимум 90 часов в фосфатном буфере и в физиологическом растворе (рН 7,4, 0,15 М NaCl). При повышении ионной силы раствора (образец 3) частицы распадаются, что подтверждает стабильность системы за счет электростатических взаимодействий между полиэлектролитными блоками (в частности протамин и ПГ-ПЭГ).
Полученные данные позволяют сделать вывод о том, что наночастицы антиоксидантного фермента супероксиддисмутазы в виде полиэлектролитного комплекса типа фермент/поликатион/полианион и продукт, представляющий собой дисперсию таких наночастиц, являются перспективными для использования в медицине, в частности для лечения заболеваний, связанных с неконтролируемым выбросом реактивных свободных радикалов. Такое взрывообразное высвобождение активных форм кислорода характерно для таких заболеваний, как болезнь Альцгеймера, Паркинсона, инфаркт, инсульт, ревматоидный артрит, онкологические и аутоиммунные заболевания, различные травмы спинного и головного мозга.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМЕРНЫЕ НАНОЧАСТИЦЫ СОСТАВА ФЕРМЕНТ-ПОЛИКАТИОН-ПОЛИАНИОН, СОДЕРЖАЩИЕ АНТИОКСИДАНТНЫЙ ФЕРМЕНТ, ДЛЯ ПРИМЕНЕНИЯ В МЕДИЦИНЕ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2575836C2 |
| Способ получения водосодержащей суспензии частиц, состоящих из антиоксидантного фермента супероксиддисмутазы, поликатиона и полианиона | 2019 |
|
RU2709536C1 |
| Способ получения частиц для лечения гинекологических и проктологических заболеваний, сопровождающихся окислительным стрессом | 2019 |
|
RU2694225C1 |
| Композиция, снижающая окислительный стресс в глазу | 2019 |
|
RU2733928C2 |
| Композиция для лечения гинекологических и проктологических заболеваний, сопровождающихся окислительным стрессом | 2019 |
|
RU2733948C2 |
| Фармацевтическая композиция для лечения заболеваний глаз, сопровождающихся окислительным стрессом, и способ ее применения | 2018 |
|
RU2694226C1 |
| Ферментный биокатализатор с антиоксидантной активностью для детоксификации фосфорорганических соединений | 2017 |
|
RU2648169C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИКРОКАПСУЛИРОВАННОЙ ФОРМЫ ТЕРАПЕВТИЧЕСКОГО БЕЛКА СУПЕРОКСИДДИСМУТАЗЫ ДЛЯ ПЕРОРАЛЬНОГО ПРИМЕНЕНИЯ | 2015 |
|
RU2583923C1 |
| АСПАРТИЛЬНЫЕ ПРОИЗВОДНЫЕ ГИСТАМИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ ФЕРМЕНТОВ АНТИОКСИДАНТНОЙ ЗАЩИТЫ | 2005 |
|
RU2287524C1 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ МЕТАБОЛИЗМА В ОРГАНИЗМЕ В УСЛОВИЯХ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2010 |
|
RU2436101C1 |
Изобретение относится к химической энзимологии, в частности к созданию наночастиц антиоксидантного фермента супероксиддисмутазы для медицинского применения в виде полиэлектролитного комплекса типа фермент/поликатион/полианион, характеризующихся тем, что фермент покрыт внутренней оболочкой из поликатиона и внешней оболочкой из полианиона, где в качестве поликатиона использован протамин или полиаргинин, в качестве полианиона использован блок-сополимер поли(глутаминовой кислоты) и полиэтиленгликоля (ПГ-ПЭГ), при этом наночастица имеет гидродинамический диаметр в диапазоне 40-70 нм. Также изобретение относится к дисперсии, содержащей наночастицы антиоксидантного фермента супероксиддисмутазы для медицинского применения в виде полиэлектролитных комплексов типа фермент/поликатион/полианион, и способу получения такой дисперсии. Изобретение обеспечивает повышение стабильности фермента в чужеродной среде при сохранении его активности. 3 н. и 6 з.п. ф-лы, 1 ил., 1 табл.
1. Наночастица антиоксидантного фермента супероксиддисмутазы для медицинского применения в виде полиэлектролитного комплекса типа фермент/поликатион/полианион, характеризующаяся тем, что фермент покрыт внутренней оболочкой из поликатиона и внешней оболочкой из полианиона, где в качестве поликатиона использован протамин или полиаргинин, в качестве полианиона использован блок-сополимер поли(глутаминовой кислоты) и полиэтиленгликоля (ПГ-ПЭГ), при этом наночастица имеет гидродинамический диаметр в диапазоне 40-70 нм.
2. Способ получения дисперсии, содержащей наночастицы антиоксидантного фермента супероксиддисмутазы для медицинского применения в виде полиэлектролитных комплексов типа фермент/поликатион/полианион по п. 1, характеризующийся тем, что к раствору супероксиддисмутазы (СОД) добавляют по каплям при перемешивании раствор поликатиона - протамина или полиаргинина, затем смесь перемешивают при комнатной температуре в течение 30 минут, после чего по каплям при перемешивании добавляют раствор полианиона - блок-сополимера поли(глутаминовой кислоты) и полиэтиленгликоля, и выдерживают смесь при температуре 4°С в течение 8-12 часов, после чего непрореагировавшие реагенты удаляют многократным центрифугированием, используя фильтрующие системы с пределом пропускания ультрафильтрационной мембраны 50000 Да, с получением дисперсии, содержащей наночастицы фермента супероксиддисмутазы в виде полиэлектролитного комплекса типа фермент/поликатион/полианион.
3. Способ по п. 2, характеризующийся тем, что используют раствор супероксиддисмутазы с концентрацией 5 мг/мл в ХЕПЕС-NaCl-буфере.
4. Способ по п. 2, характеризующийся тем, что в качестве поликатиона используют протамин или полиаргинин в виде раствора с концентрацией 5 мг/мл.
5. Способ по п. 4, характеризующийся тем, что поликатион используют в количестве, рассчитанном как двухкратный избыток аминогрупп по отношению к количеству карбоксильных групп в молекуле СОД.
6. Способ по п. 2, характеризующийся тем, что в качестве полианиона используют блок-сополимер поли(глутаминовой кислоты) и полиэтиленгликоля в виде раствора с концентрацией 5 мг/мл.
7. Способ по п. 6, характеризующийся тем, что полианион используют в количестве, рассчитанном как двухкратный избыток карбоксильных групп по отношению к карбоксильным группам в молекуле СОД.
8. Способ по п. 2, характеризующийся тем, что полученную дисперсию, содержащую наночастицы фермента супероксиддисмутазы в виде полиэлектролитного комплекса типа фермент/поликатион/полианион, хранят при 4°С.
9. Дисперсия, содержащая наночастицы антиоксидантного фермента супероксиддисмутазы для медицинского применения в виде полиэлектролитных комплексов типа фермент/поликатион/полианион по п. 1, полученная способом по п. 2.
| Multilayer Thin Films / Edited by Gero Decher and Joseph B | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| KGaA | |||
| Balabushevich N.G | |||
| et al / Polyelectrolyte assembling for protein microencapsulation / J | |||
| DRUG | |||
| SCI | |||
| TECH | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| WO 2012162490 A1, 29.11.2012 | |||
| Natalia L | |||
| Klyachko et al / Cross-linked antioxidant nanozymes | |||
Авторы
Даты
2015-06-10—Публикация
2013-11-29—Подача