Изобретение относится к аналитической химии, в частности к способам извлечения солей металлов из водных растворов без органического растворителя с помощью расслаивающейся системы антипирин (АП) - сульфосалициловая кислота (ССК) - вода, которая может быть использована в производстве и анализе особо чистых металлов, например, для селективной экстракции ионов индия (III).
Известен способ экстракционного выделения индия фосфорорганическими кислотами. Экстракцию проводят смесью моноалкил-и/или диалкил- и триалкилфосфорных кислот в объемном соотношении 1:2-5; при pH водной фазы 0,25-4,5. Для реэкстракции органическую фазу обрабатывают раствором серной кислоты (100-500 г/дм3) в отношении 1:1 (Solvent extraction recovery process for indium, МПК C01G 15/00, №4, 292, 284, Sep. 29, 1981, USA).
Недостатком данного метода является применение токсичных, легко воспламеняемых растворителей, низкая избирательность экстрагента и сложность пробоподготовки.
Наиболее близким по технической сущности является способ экстракционного выделения индия, основанный на образовании иодидного комплекса индия, экстракции его в органическую фазу и последующее его определение комплексонометрическим способом. В качестве экстрагента выступает раствор диантипирилметана в хлороформе или дихлорэтане (В.Х. Аитова, В.П. Живописцев. Галлий, индий // Ученые записки ИГУ №342. 1974. С. 86).
Однако известный способ обладает рядом недостатков, а именно: применение производного антипирина - ДАМ и, как следствие, использование органических растворителей, что приводит к увеличению стоимости выделения индия, снижает безопасность работы и ухудшает состояние окружающей среды. Определяющим фактором является также недостаточная прочность иодидного комплекса индия, что сказывается на его последующем определении.
Цель изобретения заключается в применении расслаивающейся системы АП-ССК-H2O для повышения селективности извлечения индия (III) без применения органических растворителей, которые, как правило, являются легколетучими, пожароопасными, нередко токсичными.
Поставленная задача решается с помощью признаков, указанных в 1 пункте формулы изобретения, общих с прототипом, таких как способ извлечения ионов индия (III) экстракцией из водных растворов производным из группы пиразолонов с последующим комплексонометрическим определением индия (III), и отличительных существенных признаков, таких как в качестве органического реагента используют антипирин и сульфосалициловую кислоту, а в качестве высаливателя - сульфат натрия или сульфат аммония при pH 2,0-3,0.
Согласно п. 2 формулы изобретения в качестве индикатора при комплексонометрическом определении индия (III) используют ксиленоловый оранжевый.
Технический результат от вышеперечисленной совокупности существенных признаков - повышение селективности извлечения индия (III) без применения органических растворителей, которые, как правило, являются легколетучими, пожароопасными, нередко токсичными.
Антипирин и сульфосалициловая кислота представляют собой соединения структурных формул:
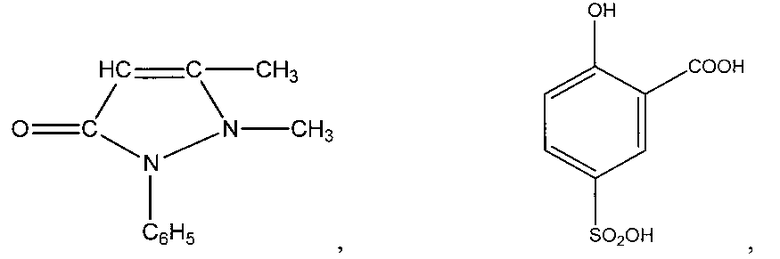
которые выпускаются отечественной промышленностью и широко применяются в фармокопии, сельском хозяйстве, медицине и др.
Применяя расслаивающуюся систему АП-ССК-H2O, были определены оптимальные условия извлечения индия (III) из водных растворов. Для этого при постоянной концентрации 0,6 моль/л раствора АП приливали разные количества ССК (2 моль/л) при общем объеме водной фазы 10-15 мл.
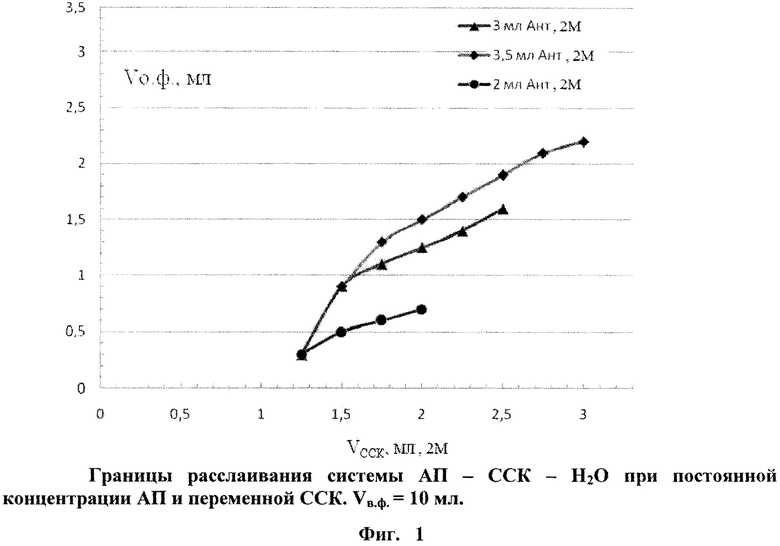
Оказалось, что при соотношении компонентов АП: ССК в молярном отношении, моль/л: 0,54-0,6: 0,3-0,32 наблюдается максимальное расслаивание системы АП-ССК-H2O. При этом объем органической фазы (ОФ), содержащий АП и ССК, составляет 2-2,2 мл (рис. 1). Именно этот объем и является достаточным для экстракции ионов индия (III).
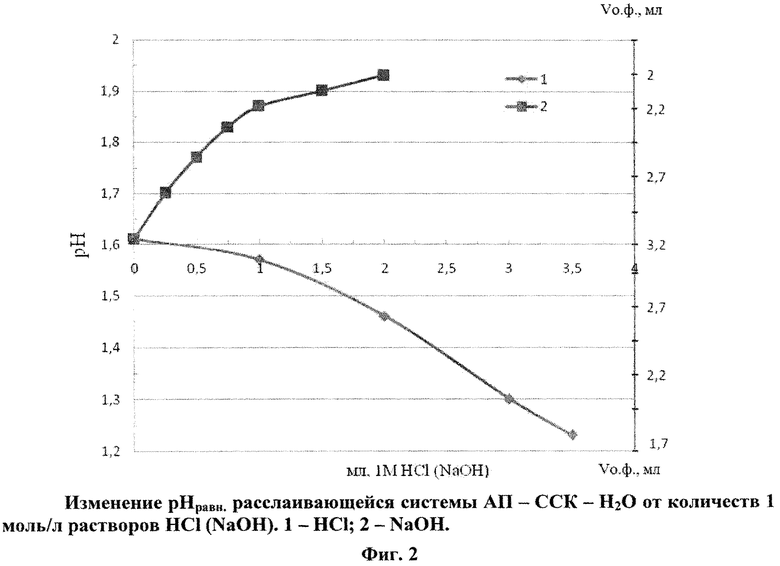
В дальнейшем было показано, что ОФ обладает большой буферной емкостью (рис. 2). Так, при добавлении 3,5 мл 1 моль/л HCl или 2 мл 1 моль/л NaOH pHравн. изменяется на 0,32-0,38 ед. pH. Объем ОФ при этом уменьшается соответственно до 1,8 и 2 мл.
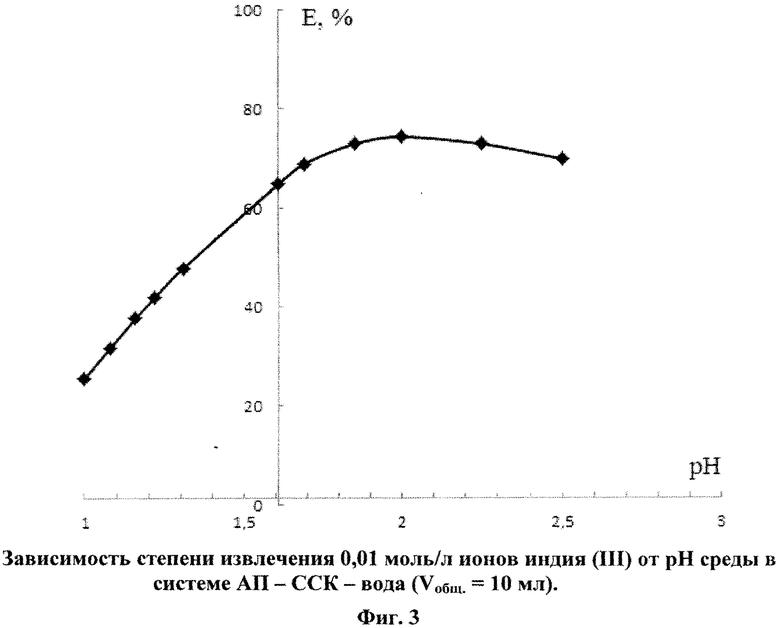
В оптимальных условиях расслаивания 0,6 моль/л АП и 0,32 моль/л ССК при объеме водной фазы 10 мл 0,01 моль/л раствор In2(SO4)3 извлекается не более чем на 74,4%. Предварительно перед экстракцией необходимо добавлять в систему 1,0 моль/л NaOH для создания pH 2, с учетом нейтрализации 0,5М H2SO4, на которой приготовлен раствор соли металла (рис. 3). Дальнейшее увеличение концентрации щелочи или серной кислоты уменьшает степень извлечения индия. Для количественного извлечения индия вводят высаливатель, например, Na2SO4 или (NH4)2SO4 в концентрации 1,0 и 1,5 моль/л соответственно.
Полученные результаты (таблица) показали, что максимальную степень извлечения (Е, %) обеспечивают Na2SO4 (99,6%) и (NH4)2SO4 (98,6%).
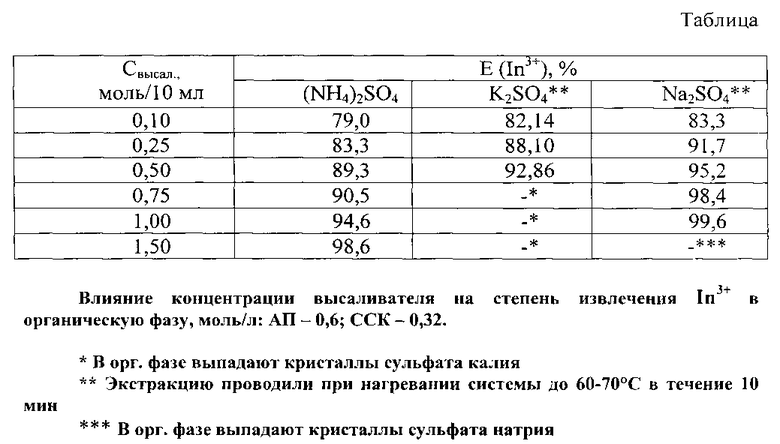
Сульфат калия малоэффективен вследствие невысокой его растворимости и неполного извлечения In(III). В случае Na2SO4 необходимо нагревать водную фазу до 60-70°C (7-10 мин) до полного растворения высаливателя. Необходимо отметить, что введение высаливателя увеличивает объем ОФ вдвое. По высаливающей способности, увеличивающей степень извлечения индия, сульфаты щелочных элементов и катиона аммония расположены в последовательности: Na2SO4>(NH4)2SO4>K2SO4.
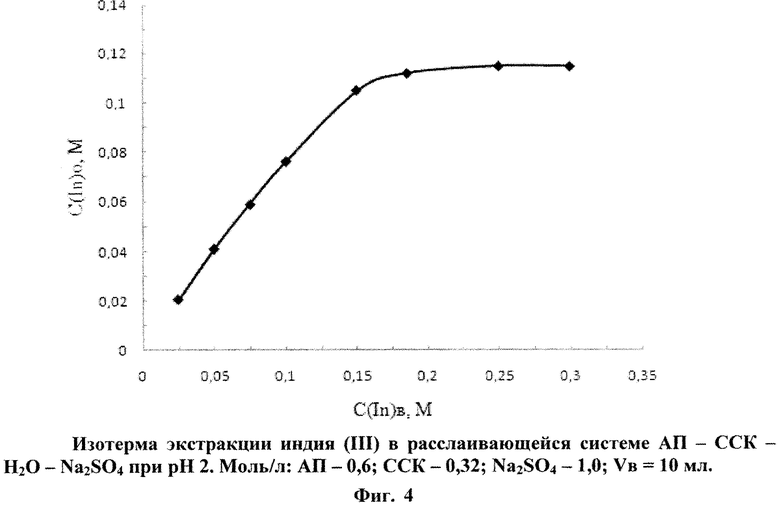
В оптимальных условиях извлечения In3+(моль/л: АП - 0,6; ССК - 0,32; Na2SO4 - 1,0) построена изотерма экстракции, согласно которой насыщение ОФ происходит при концентрации индия (III) в водной фазе, равной 0,3 моль/л (рис. 4). При этом концентрация элемента в ОФ составляет 0,118 моль/л. Логарифмическая зависимость lgD(In)-lgC(In)B показала, что в интервале концентрации In(III) в водной фазе от 0,01 до 0,1 моль/л тангенс угла наклона кривой близок к 1, что свидетельствует о мономерной форме элемента в составе комплекса.
Из приведенных данных изотермы экстракции, а также логарифмической зависимости lgD(In)-lgC(АП) и анализа насыщенных ионами индия экстрактов можно предположить соотношение компонентов в комплексе, равное ΑΠ: In(III): ССК=2:1:2. Полученное соотношение позволяет выразить комплекс в виде сольвата следующего состава
[(ССК-)2·In3+·2АП]+(АП)2·Н·ССК-.
Поскольку полученный сольват [(ССК-)2·In3+·2АП]+·(АП)2·Н·ССК- отличается высокой прочностью, то его необходимо разрушить для последующего комплексонометрического определения индия (III), разбавляя экстракт дистиллированной водой до 150 мл.
Пример 1. Селективный способ извлечения индия (III) из расслаивающейся системы АП-ССК-H2O-Na2SO4 для его последующего комплексонометрического определения.
К анализируемому раствору, содержащему 11,15 мг In3+, вводили 3 мл 2М раствора антипирина, 1,6 мл 2M раствора ССК в объеме водной фазы Vф=10 мл. Для создания необходимого значения pHравн=2,0 добавляли 1,0 моль/л NaOH и в качестве высаливателя вводили сульфат натрия до концентрации 1М в объеме 10 мл. Экстракцию ионов In3+ осуществляли в делительных воронках на 50 мл в течение 5 мин, после отстаивания органическую фазу сливали, а к водной приливали еще 1,5 мл АП, 0,8 мл ССК и проводили повторную экстракцию. В объединенных экстрактах определяли индий комплексонометрически, предварительно разбавив экстракт дистиллированной водой до 150 мл. Необходимое значение pH при титровании создавали введением 1 моль/л раствора CH3COONa (2 мл) и 5 мл ацетатного буферного раствора с pH=3,3. Контроль за содержанием ионов In3+ в экстракте осуществляли по его остатку в водной фазе по указанному выше методу. В качестве индикатора применяли 0,05%-ный раствор ксиленолового оранжевого (2-3 капли) и при энергичном перемешивании титровали раствором ЭДТА (0,020 М) до перехода окраски от малиновой до желтой.
Полученные результаты показали, что в данных условиях ионы Zn2+, Cd2+, Со2+, Ni2+, Cr3+, Μn2+(в соотношении 1:100) не мешают определению ионов индия, так как не извлекаются в ОФ.
Пример 2. Селективный способ извлечения ионов индия (III) из расслаивающейся системы АП-ССК-H2O-(NH4)2SO4 для его последующего комплексонометрического определения.
К анализируемому раствору, содержащему 11,15 мг In3+, вводили 3 мл 2М раствора АП, 1,5 мл 2М раствора ССК в объеме водной фазы Vф=10 мл. Добавляли 1,0 моль/л NaOH, создавая pH=2,0, сульфат аммония до 1,0 моль/л в объеме водной фазы 10 мл. Экстракцию ионов In3+осуществляли в делительных воронках на 50 мл при комнатной температуре в течение 5 мин, после отстаивания органическую фазу сливали, а к водной фазе приливали еще 1,5 мл АП, 0,75 мл ССК и проводили повторную экстракцию. В объединенных экстрактах определяли индий комплексонометрически по вышеописанному методу.
Сведения по экстракции показали, что в данных условиях ионы Со2+, Ni2+, Zn2+, Cd2+, Cr3+, Mn2+(в соотношении 1:100) не мешают определению ионов индия, так как не извлекаются в ОФ.
Пример 3. Селективный способ экстракционно-комплексонометрического определения макроколичеств ионов индия (III) в различных основах.
К анализируемому раствору, содержащему 22,30 мг In3+, приливали 3 мл АП, 1,5 мл ССК, 1,0 моль/л раствор NaOH до pH 2, вводили 2,97 г сульфата аммония в качестве высаливателя при объеме Vф=15 мл. Экстракцию ионов In3+ осуществляли в делительных воронках на 50 мл и комнатной температуре 20°C в течение 5 мин. После отстаивания органическую фазу сливали, а к водной приливали еще 1,5 мл АП, 0,75 мл ССК и проводили повторную экстракцию. В объединенных экстрактах определяли индий комплексонометрически по вышеописанной схеме.
Выделению и определению ионов индия не мешают щелочные элементы в соотношении к определяемому иону 1:1000, Со2+, Νi2+, Ζn2+, Cd2+, Cr3+, Mn2+ (в соотношении 1:100).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ извлечения скандия(III) для его последующего определения в системе, содержащей антипирин и сульфосалициловую кислоту | 2015 |
|
RU2645068C2 |
| Новый вариант расслаивания в системе антипирин (АП) - вода - сульфат натрия | 2015 |
|
RU2631806C2 |
| СПОСОБ ОЧИСТКИ ВОДНЫХ РАСТВОРОВ ОТ ЖЕЛЕЗА (III) | 2014 |
|
RU2565214C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ИОНОВ ОЛОВА (II) И (IV) В ВОДНЫХ РАСТВОРАХ | 2011 |
|
RU2475548C1 |
| ЭКСТРАГЕНТ ДЛЯ ВЫДЕЛЕНИЯ ИОНОВ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ | 2007 |
|
RU2333028C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАРГАНЦА (II) | 2009 |
|
RU2415415C1 |
| СПОСОБ ВЫДЕЛЕНИЯ СКАНДИЯ | 1993 |
|
RU2049728C1 |
| Состав для экстракции в водных расслаивающихся системах без органического растворителя | 2015 |
|
RU2640340C2 |
| ЭКСТРАКЦИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ ЦИНКА, КАДМИЯ, СВИНЦА И МЕДИ | 2011 |
|
RU2476853C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ РТУТИ МОДИФИКАЦИЕЙ ГРАФИТОВОГО ЭЛЕКТРОДА ИОННОЙ ЖИДКОСТЬЮ | 2006 |
|
RU2324169C9 |
Изобретение относится к аналитической химии. Способ извлечения ионов индия (III) включает его экстракцию из водных растворов производным из группы пиразолонов с последующим комплексонометрическим определением индия (III). В качестве производного из группы пиразолонов используют антипирин. Экстракцию проводят органическим реагентом, содержащим антипирин и сульфосалициловую кислоту, с добавлением высаливателя, при рН среды 2,0. В качестве высаливателя берут сульфат натрия или сульфат аммония. В качестве индикатора при комплексонометрическом определении индия (III) используют ксиленоловый оранжевый. Изобретение позволяет повысить селективность извлечения индия (III) без применения легколетучих, пожароопасных, токсичных органических растворителей. 1 з.п. ф-лы, 4 ил., 3 пр., 1 табл.
1. Способ извлечения ионов индия (III) экстракцией из водных растворов производным из группы пиразолонов с последующим комплексонометрическим определением индия (III), отличающийся тем, что в качестве производного из группы пиразолонов используют антипирин, причем экстракцию проводят органическим реагентом, содержащим антипирин и сульфосалициловую кислоту, с добавлением высаливателя, в качестве которого берут сульфат натрия или сульфат аммония, при pH среды 2,0.
2. Способ по п. 1, отличающийся тем, что в качестве индикатора при комплексонометрическом определении индия (III) используют ксиленоловый оранжевый.
| Способ концентрирования индия | 1974 |
|
SU566163A1 |
| Способ выделения индия из кислых иодидных растворов | 1986 |
|
SU1428701A1 |
| Способ извлечения индия из растворов свинцово-цинкового производства | 1984 |
|
SU1308559A1 |
| US 4292284 A, 29.09.1981 | |||
Авторы
Даты
2015-07-10—Публикация
2013-07-23—Подача