Изобретение относится к микроэкологии и иммунологии и может использоваться для оптимизации диагностики, прогнозирования и лечения инфекционно-воспалительных процессов.
Микрофлора человека является основой его микроэкологии и оказывает непосредственное влияние на жизнедеятельность и состояние макроорганизма. Микробиоценоз открытых полостей макроорганизма - динамическая микроэкологическая система, компонентами которой является макроорганизм, его микрофлора (совокупность типичных для определенного биологического вида и конкретного биотопа ассоциаций микроорганизмов) и окружающая среда, характеризующаяся способностью к саморегуляции, которая является интегральной частью организма («дополнительным органом») хозяина и местного иммунитета, в частности, и выполняет или регулирует многочисленные функции макроорганизма. Показатели состояния микробиоценозов отражают состояние реактивности макроорганизма - способность организма отвечать на воздействия внешней среды изменением своей жизнедеятельности, что обеспечивает его адаптацию к различным условиям обитания. Слизистые открытых полостей макроорганизма представляют собой единую систему. Состояние микробиоценоза и барьерной функции слизистых можно оценивать по выраженности колонизационной резистентности (КР) открытых полостей организма - физиологический феномен - способности микрофлоры и макроорганизма в кооперации защищать экосистему слизистых от патогенных микроорганизмов. КР включает комплекс местных факторов, к которым принадлежат ингибиторы микробной адгезии, биоцидные и биостатические продукты секретов, нормальную микрофлору, механические факторы (мерцательный эпителий, целостность кожи и слизистых), местные факторы врожденного и адаптивного иммунитета. К механизмам феномена КР относятся кожа и слизистые оболочки (формируют физический и экологический барьер для проникновения патологических агентов внутрь организма), движение мукоцилиарного эпителия, перистальтику кишечника, десквамацию мукозных клеток, антимикробный эффект секретов слюны, желчи, желудочного и кишечного содержимого, состав и количество муцина, напряженность кислорода по толщине биопленки, рН среды, скорость обновления мукозного эпителия [1, 2, 3, 4, 5].
В настоящее время накоплено достаточно большое количество информации о роли качественных и количественных изменений микрофлоры открытых полостей организма человека в развитии инфекционно-воспалительных процессов.
Так, начало большинства бронхолегочных заболеваний связано с развитием патологических процессов в слизистой оболочке верхних дыхательных путей и ротоглотке, которая в норме задерживает и элиминирует около 70% поступающего извне инертного и агрессивного антигенного материала. Инициация любого инфекционно-воспалительного процесса зависит от соотношения уровней индигенных и условно-патогенных микроорганизмов, формирующих данный биотоп. (6, 7). Количественные и качественные нарушения в составе микробных симбионтов десневой жидкости, нарушения их взаимодействия с макроорганизмом обуславливают развитие пародонтита (8).
Возбудители урогенитального хламидиоза и уреаплазмоза - облигатные внутриклеточные паразиты, не являющиеся патогенами, но на фоне растущей урбанизации, ухудшения социально-демографической и экологической ситуации, способны вызывать различные осложнения, оказывающие неблагоприятное воздействие как на общее состояние здоровья, так и на репродуктивную функцию. Их патогенный потенциал зависит от концентрации в организме, наличия или отсутствия определенных генов патогенности, состояния микробиоценоза биотопа, ассоциации с другими патогенными бактериями и вирусами, изменения физиологического и иммунного статуса. (9, 10).
К сожалению, до настоящего времени большинство микроэкологических исследований проводились без учета факторов местной и организменной резистентности. Вместе с тем, формирование КР слизистых, течение инфекционно-воспалительных реакций репираторного, урогенитального и желудочно-кишечного трактов определяется как индигенной микрофлорой, так и факторами местной иммунной защиты.
Известен способ оценки биоценоза полового тракта у пациенток, заключающийся в определении лизоцимной активности влагалища, pH влагалища, флоры с подсчетом общего микробного числа (методом посева на кровяной агар) (патент RU №2179849, 2002.02.27, A61K 31/19, 35/74).
Недостатками способа являются:
- невозможность проведения комплексной оценки состояния микробиоценоза влагалища с учетом количественных показателей содержания факультативно-анаэробной и облигатно-анаэробной микрофлоры в отделяемом и в соскобе из влагалища в сочетании с определением компонентов гуморальной резистентности и барьерной функции слизистой оболочки влагалища;
- недостаточная информативность лабораторного обследования для прогнозирования, оценки эффективности и стабильности коррекции состояния микробиоценоза влагалища.
Известен способ оценки микроэкологии влагалища при диагностике вагинальных инфекций, заключающийся в исключении инфекций, передаваемых половым путем, микроскопии вагинального мазка, окрашенного по Граму, и посеве вагинального отделяемого на факультативно анаэробную группу микроорганизмов и микроаэрофилы. На основании микробиологических критериев оценки состояния микроэкологии влагалища диагностируют нормоценоз, бактериальный вагиноз, вагинальный кандидоз, неспецифический вагинит, цитолитический вагиноз, атрофический кольпит или промежуточный вариант микроценоза (11).
Недостатками способа являются:
- невозможность проведения комплексной оценки состояния микробиоценоза влагалища при одновременном исследовании количественных показателей содержания факультативно-анаэробной и облигатно-анаэробной микрофлоры в отделяемом и в соскобе из влагалища в сочетании с определением компонентов гуморальной резистентности и барьерной функции слизистой оболочки влагалища;
- недостаточная информативность лабораторного обследования для прогнозирования, оценки эффективности и стабильности коррекции состояния микробиоценоза влагалища.
Известен способ оценки микробиоценоза полости матки у женщин с полипами эндометрия в постменопаузальном периоде путем определения количественного и качественного состава микрофлоры и количественной оценки показателей локального гуморального иммунитета, включающий взятие соскобного материала из полости матки, проведение посева соскобного материала для выявления видов микроорганизмов условно-патогенной факультативно-анаэробной и облигатно-анаэробной микрофлоры и их чувствительности к антибиотикам, введение в полость матки раствора реополиглюкина, определение в аспирате концентрации иммуноглобулинов IgG, IgM, IgA, свободного, секреторного компонента (sc) и секреторного иммуноглобулина А (sIgA) методом радиальной иммунодиффузии по Манчини и оценку микробиоценоза: нормоценоз полости матки на фоне атрофии эндометрия при отсутствии условно-патогенной факультативно-анаэробной и условно-патогенной облигатно-анаэробной микрофлоры и определенной концентрации иммуноглобулинов; нарушение микробиоценоза при определенном содержании условно-патогенной факультативно-анаэробной и условно-патогенной облигатно-анаэробной микрофлоры и при определенной концентрации иммуноглобулинов. Вышеописанный способ позволяет повысить эффективность диагностики (патент РФ №2430365).
Известен способ диагностики хронического урогенитального хламидиоза (патент РФ №2327995), при котором определяют в соскобном материале из уретры с использованием полимеразной цепной реакции в реальном времени уровни экспрессии толл-подобных рецепторов: TL-рецептора-2 и TL-рецептора-4 и диагностируют хронический урогенитальный хламидиоз при уровнях экспрессии в соскобном материале из уретры TL-рецептора-2 не более 5 единиц и TL-рецептора-4 не более 5 единиц. Уровни экспрессии TL-рецептора-2 и TL-рецептора-4 определяли с использованием рекомендаций по проведению полимеразной цепной реакции в реальном времени (Абрамов Д.Д., Трофимов Д.Ю., Ребриков Д.В. Точность методов полимеразной цепной реакции «в реальном времени» при определении содержания генетически модифицированных источников в пищевых продуктах // Прикладная биохимия и микробиология. - 2006. - Т. 42, №4. - С. 485-488; RU патент 2294532 C1, G01N 21/64).
Данный способ оценивает один из факторов мукозального иммунитета - врожденный иммунитет.
Задачей изобретения является разработка способа оценки состояния мукозального иммунитета слизистых открытых полостей различной локализации при прогнозировании течения инфекционно-воспалительных процессов.
Задача решается таким образом, что при установленном патогенетическом факторе проводят регистрацию степеней нарушения микробиоценоза конкретного биотопа слизистых открытых полостей различной локализации с использованием комплекса методов оценки уровней факторов колонизационной резистентности как интегрирующей составляющей мукозального иммунитета в мазках и соскобном материале со слизистых (нормальной микрофлоры, условно-патогенной микрофлоры, нейтрофилов, цитокинов, иммуноглобулинов IgG, IgM, IgA, sIgA и sc компонента и TLR-рецепторов) и в зависимости от степени нарушения микробиоценоза оценивают:
- хорошее состояние мукозального иммунитета при второй и третьей степенях нарушения микробиоценозов и прогнозируют благоприятный исход заболевания с эрадикацией возбудителя;
- нарушение мукозального иммунитета при нормоценозе и первой степени нарушения микробиоценозов и прогнозируют хроническое течение инфекционно-воспалительного процесса с персистированием возбудителя.
Под местным (мукозальным) иммунитетом подразумевается комплекс клеточных и секреторных неспецифических и специфических реакций, включающий барьерные функции клеток кожи и слизистых оболочек, фагоцитарную активность нейтрофилов и макрофагов, Т-клеточный иммунитет, антитела, антимикробные белки внешних секретов, ингибиторы ферментов, цитокины. Местный иммунитет не отождествляется с секреторным иммунитетом, но в качестве его центрального звена рассматривается В-клеточный ответ лимфоидной ткани слизистых оболочек с участием железистого эпителия, поставляющего секреторный компонент. Понятие местного иммунитета в настоящее время включает совокупность реагирования всех клеток лимфоидного ряда, заселяющих слизистые оболочки, в кооперации с макрофагами, нейтрофильными и эозинофильными гранулоцитами, тучными клетками и другими клетками соединительной ткани и эпителия [3, 12, 13, 14, 15, 16, 17]. Следовательно, микробиоценозы слизистых открытых полостей и мукозальный иммунитет можно рассматривать как интегральную структурно-функциональную систему организма.
В связи с вышесказанным и на основании проведенных комплексных исследований представляется актуальным выявление взаимосвязи характеристик микробиоценозов и факторов мукозального иммунитета слизистых открытых полостей различной локализации в норме и при инфекционной патологии.
Любой инфекционный процесс в слизистой оболочке, независимо от этиологии, развивается по одному и тому же сценарию. Первый этап - это адгезия микробов в пристеночном муцине или на эпителиальных клетках, которая обеспечивается специальными структурами возбудителя. Закрепившись, микроорганизмы начинают размножаться, что приводит к патологической колонизации слизистой - это второй этап инфекционного процесса (дисбактериоз). Следующий, третий этап инфекционного процесса - это инвазия микроорганизмов, когда они преодолевают защитный барьер слизистой оболочки и проникают в эпителиальные клетки или подлежащую ткань, вызывая при этом местную иммунную реакцию (колит, вагинит, фарингит и др.). При преодолении местного защитного барьера возможна генерализация инфекции. Патогенность отдельных видов бактерий зависит от наличия или отсутствия представителей других видов. Поэтому при оценке микробиоценозов слизистых необходимо учитывать количество и видовой состав как микроорганизмов, свободно располагающихся в просвете, так и адгезированных к эпителиальным поверхностям (пристеночная область).
Известно, что система антиинфекционной резистентности организма определяется качественным и количественным составом биопленки, формируемой индигенной микрофлорой, а также патогенными микроорганизмами на эпителиальных поверхностях, местной и организменной антиинфекционной резистеностью хозяина. Ключевым звеном в распознании макроорганизмом патогенов являются TL-рецепторы (TLR), составляющие основу мембранных комплексов и экспрессирующихся на всех клеточных элементах, участвующих в формировании резистентности (включая КР макроорганизма), в том числе и на поверхности слизистых.
TLR способны распознавать консервативные молекулярные структуры, распространенные среди определенного класса микроорганизмов и отсутствующие у человека. Антиинфекционная защита на местном уровне развивается путем формирования типичной воспалительной реакции после взаимодействия патогенов с TLR, что сопровождается активацией генов цитокинового каскада, ответственного за активацию фагоцитов и других иммунокомпетентных клеток, Ig, что, в свою очередь, определяет уровень мукозальной КР и, в дальнейшем, блокирование жизнедеятельности, дезинтеграцию и удаление инфекционного агента из организма.
Так, при изучении нами урогенитальных хламидиоза и уреаплазмоза, острых инфекционных заболеваний верхних дыхательных путей, в том числе острых и хронических бронхитов, была установлена взаимосвязь толл-подобных рецепторов - TLR (контролируют запуск цитокинового каскада местной антиинфекционной резистентности, через который запускаются иммуноглобулиновое звено и воспалительная реакция) с микрофлорой биотопа, определяющей колонизационную резистентность слизистых, характеризующей течение инфекционного процесса, выраженность клинических и лабораторных проявлений и исход заболевания (излечение, хронизация). Колонизационная резистетность выступает как неотъемлемая часть мукозального иммунитета.
Функцию TLR оценивали оригинальным запатентованным методом определения уровня экспрессии генов (TLR) полимеразной цепной реакцией (ПЦР) в реальном времени с обратной транскрипцией, с использованием специфических праймеров (RU патент 2294532). Установлено, что патогены и условно-патогенные микроорганизмы (УПМ), попадая на слизистые открытых полостей, взаимодействуют с TLR эпителиальных клеток и запускают через активизацию цитокиновой системы воспалительную реакцию. TLR-2 и TLR-4 реагируют на бактериальные патогены, a TLR-3 и TLR-8 - на вирусные. При взаимодействии возбудителя с чувствительными для него клеточными элементами слизистых TLR клеток отвечают экспрессией генов на патоген и УПМ, а при взаимодействии возбудителя с нечувствительными для него клетками эпителия слизистых - только на УПМ. При остром и хроническом инфекционных процессах ведущими этиологическими факторами инфекционного процесса являются ассоциации из бактериальных и вирусных патогенов, а также УПМ. Различные уровни активации экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8 зависят от качественного состава микробных сообществ (в частности от превалирования грамположительных или грамотрицательных возбудителей или вирусных патогенов), присутствующих на слизистых оболочках открытых полостей организма. Активация экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8 происходит более выражение в ответ на патогены и УПМ и менее выражение - на нормофлору. Показатели уровней обсемененности УПМ прямо коррелируют с показателями уровней экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8. Уровни экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8 служат критериями оценки выраженности воспалительного процессса. Повышение экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8 коррелирует с тяжестью клинических проявлений, а при выздоровлении их снижение свидетельствует об эрадикации возбудителя. Естественная или приобретенная супрессия генов TLR-2, TLR-4, TLR-3, TLR-8 обусловливает хроническое течение инфекции. При остром инфекционном процессе выявление низких уровней TLR-2, TLR-4, TLR-3, TLR-8 указывает на начало хронизации инфекционного процесса. Предложенный метод оценки TLR можно рассматривать как дополнительный лабораторный тест, уточняющий клинические формы и прогнозирующий исход заболевания.
При инфекционных поражениях открытых полостей организма родовой и видовой состав микроорганизмов патогенов и УПМ, выделенных от больных, может служить дополнительным объективным критерием тяжести течения инфекционного процесса, а также позволяет дифференцирование судить об эффективности проводимой антибактериальной терапии и вносить в нее необходимые коррективы. Острое течение инфекционного процесса сопровождается достоверным снижением уровней индигенной микрофлоры в пристеночном и просветном биотопах слизистых, повышенной колонизацией их УПМ, многократным повышением уровней экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8, цитокинов IL-1β, IL-8, INF-γ, TNF-α, иммуноглобулинов IgG, IgA, sIgA, IgM и SC и выраженностью местной воспалительной реакции (выявлена достоверная корреляционная зависимость между изменениями уровней перечисленных факторов), что свидетельствует о хорошей местной антиинфекционной резистентности. Хроническое течение инфекционного процесса, по сравнению с острым течением, сопровождается при обострении менее выраженным достоверным снижением уровней индигенной микрофлоры в пристеночном и просветном биотопах слизистых, повышением УПМ, повышением уровней экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8, цитокинов IL-1β, IL-8, INF-γ, TNF-α, иммуноглобулинов IgG, IgA, sIgA, IgM и SC и слабо выраженной местной воспалительной реакцией, что свидетельствует о нарушении и снижении мукозальной антиинфекционной резистентности.
С учетом приведенных выше сведений и положений для оценки колонизационной резистетности слизистых открытых полостей организма была предложена оригинальная методология оценки нарушений их микробиоценозов.
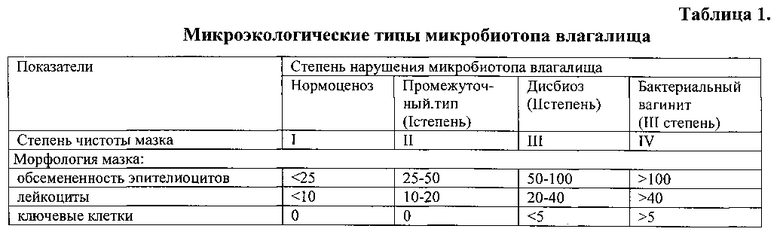
Оценка выраженности нарушений микробиоценоза влагалища (табл.1):
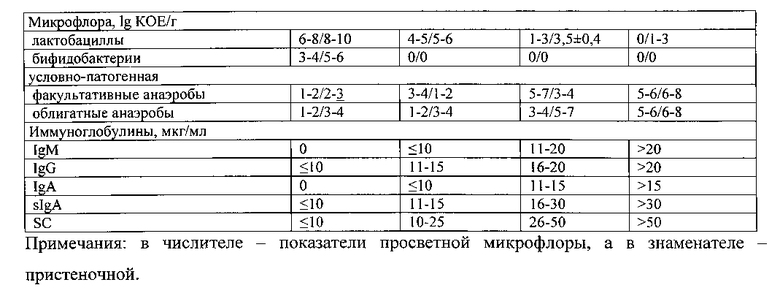
- нормоценоз влагалища (Вл) определяется при наличии на поверхности эпителиоцитов менее 25 бактериальных клеток, представленных грамположительными палочками, при количестве лейкоцитов менее 10 в поле зрения, при отсутствии ключевых клеток (I степень чистоты мазка), при содержании в отделяемом 6-8 lg КОЕ/г лактобацилл, при содержании в соскобном материале 7-10 lg КОЕ/г лактобацилл, при отсутствии в отделяемом и в соскобном материале условно-патогенной факультативно-анаэробной и облигатно-анаэробной микрофлоры и при концентрации в смыве IgA 0 мкг/мл, sIgA ≤10 мкг/мл, IgM 0 мкг/мл, SC ≤10 мкг/мл;
- промежуточный тип микробиоценоза Вл при наличии на поверхности эпителиоцитов 25-50 бактериальных клеток, представленных грамположительными палочками, единичными грамположительными кокками и грамотрицательными палочками, при количестве лейкоцитов 10-20 в поле зрения, при отсутствии ключевых клеток (II степень чистоты мазка), при содержании в отделяемом 4-5 lg КОЕ/г лактобацилл, 3-4 lg КОЕ/г условно-патогенной факультативно-анаэробной или облигатно-анаэробной микрофлоры и/или при содержании в соскобном материале 5-6 lg КОЕ/г лактобацилл, 1-2 lg КОЕ/г условно-патогенной факультативно-анаэробной или облигатно-анаэробной микрофлоры и при концентрации в смыве IgA≤10 мкг/мл, sIgA 11-15 мкг/мл, IgM≤10 мкг/мл, SC 10-25 мкг/мл;
- дисбиоз Вл при наличии на поверхности эпителиоцитов 50-100 бактериальных клеток, представленных грамположительными палочками, грамположительными кокками и грамотрицательными палочками, при количестве лейкоцитов 20-40 в поле зрения, при наличии ключевых клеток менее 5 в поле зрения (III степень чистоты мазка), при содержании в отделяемом 1-3 lg КОЕ/г лактобацилл, 5-7 lg КОЕ/г условно-патогенной факультативно-анаэробной микрофлоры и 3-4 lg КОЕ/г условно-патогенной облигатно-анаэробной микрофлоры и/или при содержании в соскобном материале 3-4 lg КОЕ/г лактобацилл, 3-4 lg КОЕ/г условно-патогенной факультативно-анаэробной микрофлоры и 5-7 lg КОЕ/г условно-патогенной облигатно-анаэробной микрофлоры и при концентрации в смыве IgA 11-15 мкг/мл, sIgA 16-30 мкг/мл, IgM 11-20 мкг/мл, SC 26-50 мкг/мл;
- бактериальный вагинит при наличии на поверхности эпителиоцитов не менее 100 бактериальных клеток, представленных единичными грамположительными палочками и обильной грамотрицательной и грамположительной палочковой и кокковой флорой, при количестве лейкоцитов не менее 40 в поле зрения, при количестве ключевых клеток не менее 5 в поле зрения (IV степень чистоты мазка), при отсутствии в отделяемом лактобацилл, при содержании в отделяемом 5-6 lg КОЕ/г монокультуры условно-патогенной факультативно-анаэробной или облигатно-анаэробной микрофлоры и/или при содержании в соскобном материале 1-3 lg КОЕ/г лактобацилл, 6-8 lg КОЕ/г монокультуры условно-патогенной факультативно-анаэробной или облигатно-анаэробной микрофлоры и при концентрации в смыве IgA>15 мкг/мл, sIgA>30 мкг/мл, IgM>20 мкг/мл, SC>50 мкг/мл.
Оценка выраженности нарушений микробиоценоза цервикального канала (табл. 2):
- нормоценоз микробиоценоза цервикального канала (Цк) определяется при количестве лейкоцитов<4 в поле зрения, при содержании в соскобном материале 1-2 lg КОЕ/г УПМ и при концентрации в смыве IgG≤8 мкг/г белка, sIgA≤7 мкг/г белка, SC≤8 мкг/г белка;
- промежуточный тип микробиоценоза Цк определяется при количестве лейкоцитов 8-10 в поле зрения, при содержании в соскобном материале 2-3 lg КОЕ/г УПМ и при концентрации в смыве IgG 10-13 мкг/г белка, sIgA 11-14 мкг/г белка, SC 13-19 мкг/г белка;
- дисбиоз микробиоценоза Цк определяется при количестве лейкоцитов 14-40 в поле зрения, при содержании в соскобном материале 3-4 lg КОЕ/г УПМ и при концентрации в смыве IgG 30-40 мкг/г белка, sIgA 20-30 мкг/г белка, SC 30-40 мкг/г белка;
- бактериальный вагинит микробиоценоза Цк определяется при количестве лейкоцитов >40 в поле зрения, при содержании в соскобном материале >4 lg КОЕ/г УПМ и при концентрации в смыве IgG>40 мкг/г белка, sIgA>30 мкг/г белка, SC>40 мкг/г белка.

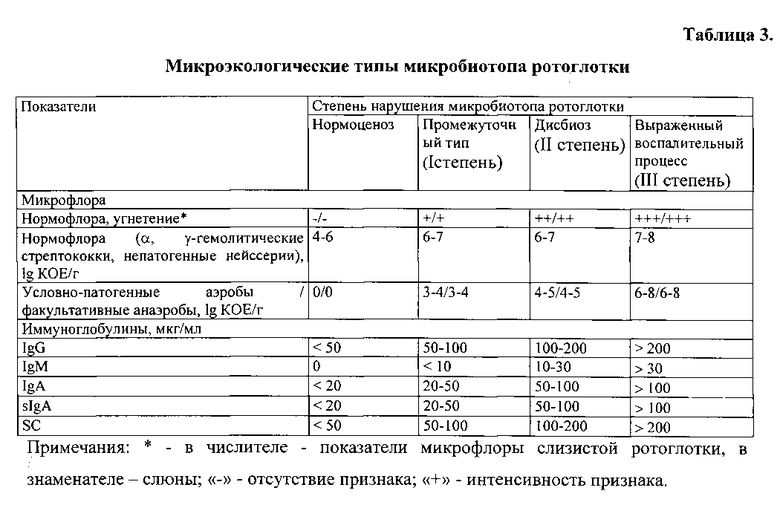
Оценка выраженности нарушений микробиоценоза ротоглотки (табл. 3):
- нормоценоз, характеризующийся отсутствием микроэкологических нарушений, присутствием индигенной микрофлоры: Streptococcus spp. в количестве 5-6 lg КОЕ/г, Neisseria spp.- 4-6 lg КОЕ/г при концентрации в слюне IgA<20 мкг/мл, sIgA<20 мкг/мл, IgM 0 мкг/мл, IgG<50 мкг/мл, SC<50 мкг/мл;
- промежуточный тип (I степень дисбиотических нарушений), характеризующийся нарастанием нормофлоры {Streptococcus spp.- до 6-7 lg КОЕ/г, Neisseria spp.- 6-7 lg КОЕ/г) и появлением УПМ в количестве до 3-4 lg КОЕ/г при концентрации в слюне IgA 20-50 мкг/мл, sIgA 20-50 мкг/мл, IgM<10 мкг/мл, IgG 50-100 мкг/мл, SC 50-100 мкг/мл;
- дисбиоз (II степень дисбиотических нарушений) ротоглотки, при котором наблюдается повышение количества нормофлоры {Streptococcus spp.- 6-7 lg КОЕ/г, Neisseria spp.- 6-7 lg КОЕ/г), повышение уровня факультативно-анаэробной УПМ до 4-5 lg КОЕ/мл, появление вирулентных вариантов УПМ, характеризующихся выраженными факторами патогенности, при концентрации в слюне IgA 50-100 мкг/мл, sIgA 50-100 мкг/мл, IgM 10-30 мкг/мл, IgG 100-200 мкг/мл, SC 100-200 мкг/мл;
- выраженный воспалительный процесс (III степень дисбиотических нарушений), характеризующийся значительным повышением содержания Streptococcus spp.- 7-8 lg КОЕ/г, Neisseria spp.- 7-8 lg КОЕ/г, УПМ и количества вирулентных микроорганизмов до 6-8 lg КОЕ/мл при концентрации в слюне IgA>100 мкг/мл, sIgA>100 мкг/мл, IgM>30 мкг/мл, IgG>200 мкг/мл, SC>200 мкг/мл.
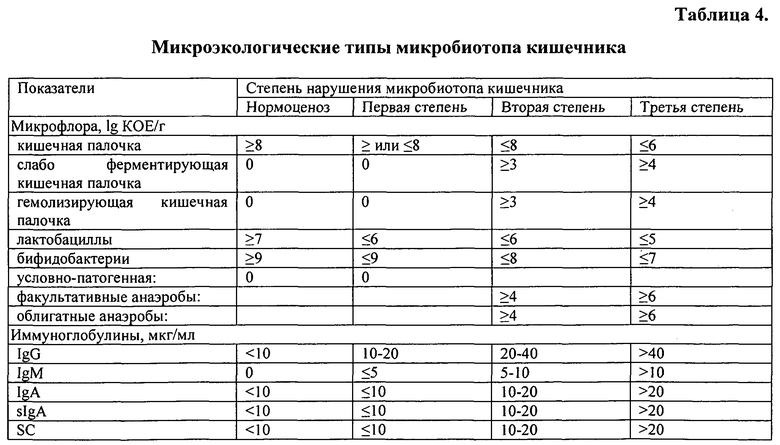
Оценка выраженности нарушений микробиоценоза кишечника (табл.4):
- нормоценоз: содержание кишечной палочки ≥8 lg КОЕ/г, лактобацилл ≥7 lg КОЕ/г, бифидобактерий ≥9 lg КОЕ/г, отсутствие УПМ при содержании в копрофильтратах IgA <10 мкг/мл, sIgA <10 мкг/мл, IgM 0 мкг/мл, IgG <10 мкг/мл, SC <10 мкг/мл;
- I степень дисбактериоза кишечника характеризуется повышенным или пониженным содержанием кишечной палочки (≥ или ≤8 lg КОЕ/г), снижением содержания лактобацилл (≤6 lg КОЕ/г) и бифидобактерий (≤9 lg КОЕ/г) при содержании в копрофильтратах IgA ≤10 мкг/мл, sIgA ≤10 мкг/мл, IgM ≤5 мкг/мл, IgG 10-20 мкг/мл, SC≤10 мкг/мл;
- II степень дисбактериоза кишечника характеризуется сниженным содержанием кишечной палочки (≤8 lg КОЕ/г), лактобацилл (≤6 lg КОЕ/г) и бифидобактерий (≤8 lg КОЕ/г), появлением УПМ в количестве ≥4 lg КОЕ/г, при содержании в копрофильтратах IgA 10-20 мкг/мл, sIgA 10-20 мкг/мл, IgM 5-10 мкг/мл, IgG 20-40 мкг/мл, SC 10-20 мкг/мл;
- Ill степень дисбактериоза кишечника характеризуется значительным снижением содержания кишечной палочки с неизмененными ферментативными свойствами (≤6 lg КОЕ/г), появлением слабоферментирующей и/или гемолизирующей кишечной палочки (≥4 lg КОЕ/г), значительным содержанием лактозонегативных энтеробактерий, грамотрицательных, глюкозу неферментирующих бактерий, кокковой флоры (≥6 lg КОЕ/г), резким снижением содержания лактобацилл и бифидобактерий ≤5 lg КОЕ/г и ≤7 lg КОЕ/г, соответственно, при содержании в копрофильтратах IgA >20 мкг/мл, sIgA >20 мкг/мл, IgM >10 мкг/мл, IgG >40 мкг/мл, SC >20 мкг/мл.
Следующие примеры подтверждают использование заявляемого способа оценки состояния музального иммунитета слизистых открытых полостей различной локализации при прогнозировании течения инфекционно-воспалительных процессов.
Пример 1.
Обследовано 30 клинически здоровых детей и 77 детей с острыми и рецидивирующими заболеваниями респираторного тракта в возрасте 3-14 лет. Дети были поделены на 3 группы: 1 группа - контрольная (30 клинически здоровых детей), 2 группа - больные с острым бронхитом (51 ребенок), 3 группа - больные с хроническим бронхитом (15 человек). Частота инфицирования аденовирусами была достоверно выше при остром бронхите по сравнению с хроническим бронхитом и клинически здоровыми пациентами. Различия в обсемененности слизистой задней стенки глотки индигенными микроорганизмами в контрольной группе и больных бронхитами детей не достоверны как по количественному содержанию, так и по частоте встречаемости, однако, у больных детей они превышали показатели нормоценоза (табл.5). Это свидетельствует о компенсированной форме дисбиотических нарушений в верхних дыхательных путях. Выявлены достоверные различия по частоте инфицирования S. aureus и грибами рода Candida при остром бронхите по сравнению с хроническим бронхитом и клинически здоровыми пациентами. Интенсивность колонизации задней стенки глотки условно-патогенными микроорганизмами (УПМ) достоверно выше при остром бронхите, а при хроническом бронхите изменения не достоверны по сравнению с клинически здоровыми пациентами. Выявление в слюне повышенных уровней общего IgE при остром и хроническом бронхитах указывает на активизацию и количественное повышение инфекционного компонента. У клинически здоровых детей нормоценоз регистрировался у 48,1% пациентов, промежуточный тип - у 44,4%, дисбиоз - у 7,4% пациентов, что достоверно отличалось от показателей при остром бронхите: нормоценоз - у 21,6% пациентов при p<0,05, промежуточный тип - у 11,8% пациентов при p<0,01, дисбиоз - у 35,3% пациентов при p<0,05, выраженный воспалительный процесс - у 31,4% пациентов при p<0,01; при хроническом бронхите нормоценоз - у 20,0% пациентов при p<0,05, промежуточный тип - у 20,0% пациентов при p<0,01, диебиоз - у 33,3% пациентов при p<0,05, выраженный воспалительный процесс - у 26,7% пациентов при p<0,01; достоверных различий между острым и хроническим бронхитом не выявлено. Следовательно, при остром бронхите нарушения микробиоценоза слизистых сдвигаются в сторону дисбиоза и выраженного воспалительного процесса. Однако высокие уровни нормофлоры в сочетании с высокими уровнями Ig обеспечивают выраженную КР, что подтверждается и высокими показателями индекса естественной колонизации назофаригеального эпителия (ИЕКНЭ). Высеваемость УПМ в титре 6 Ig КОЕ/г и выше может свидетельствовать о приобретении ею фенотипических маркеров вирулентности.
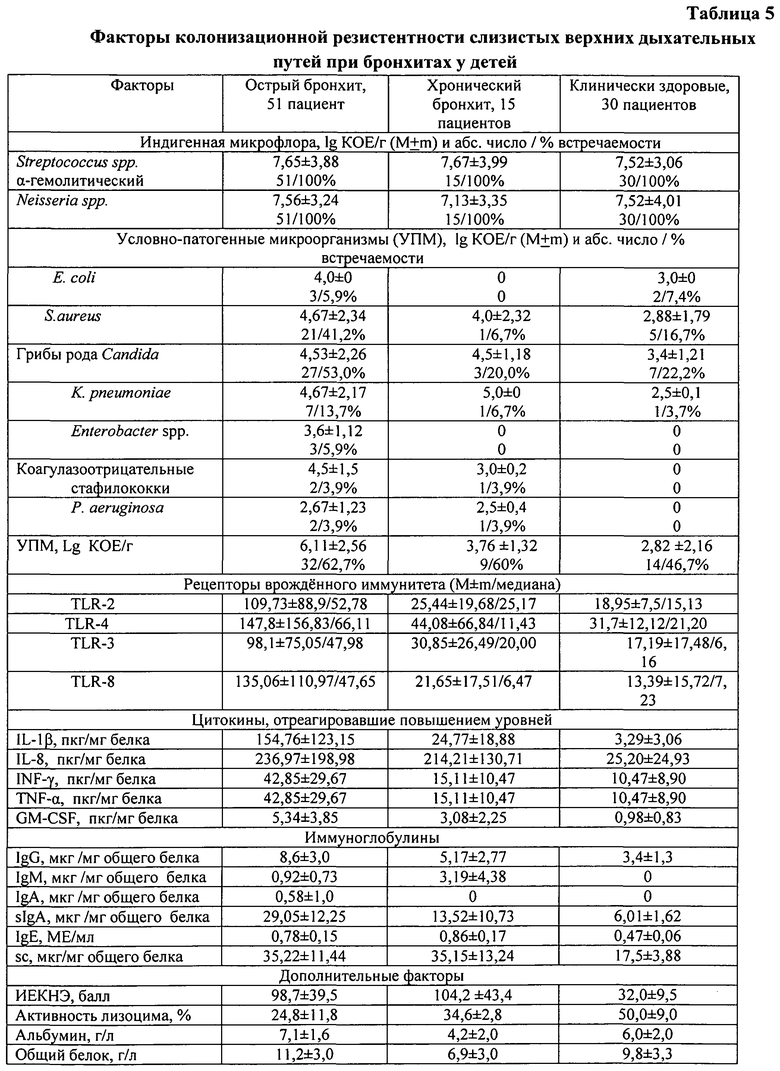
Примечания: ИЕКНЕ - индекс естественной колонизации назофарингеального эпителия.
При остром бронхите в ответ на выраженное бактериально-вирусное воздействие исследованные TLR отреагировали достоверным пятикратным повышением экспрессии генов по сравнению с хроническим бронхитом и контрольной группой. Причем, проявилась специализация TLR: TLR-2 и TLR-4 реагировали, в основном на бактериальные патогенны, а TLR-3 и TLR-8 - на вирусные патогенны. Наиболее высокие значения экспрессии генов имели место при микст инфекции, что объясняется, в определенной степени, перекрестным действием лигандов. При хроническом бронхите уровни экспрессии генов TLR в основном не отличались от контрольной группы.
При остром бронхите в ответ на достоверно высокую инфекционную нагрузку (в виде микстинфекции вирусными патогенами и УПМ) повышаются уровни экспрессии генов TLR-2, TLR-4, TLR-3 и TLR-8, запускающие в верхних дыхательных путях продукцию провоспалительных цитокинов IL-8, TNF-α и IL-1β, приводящих, в свою очередь, к увеличению содержания иммуноглобулинов, что можно расценивать как выраженную местную воспалительную иммунологическую реакцию макроорганизма, отражающую остроту инфекционного процесса и способствующую локализации инфекционного процесса, а также к стимуляции продукции дополнительных цитокинов соседними неинфицированными клетками. В ротоглотке нарастание уровней иммуноглобулинов, sIgA и sc обусловлено их синтезом in situ. Уровни экспрессии TLR прямо коррелируют с показателями уровней sIgA и лизоцима, что свидетельствует об их взаимосвязи как компонентов колонизационной резистентности, отражающих состояние врожденного иммунитета, и не коррелируют с повышенными показателями индекса ИЕКНЕ что свидетельствует о низкой адгезивной способности эпителия ротоглотки в отношениии УПМ. Все вместе указывает на высокий уровень колонизационной резистентности как показателя мукозального иммунитета. Отсутствует связь между TLR и IgE. При хроническом бронхите в ответ на слабую инфекционную нагрузку (в виде микстинфекции вирусными патогенами и УПМ) уровни экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8 не повышаются; не выявляется прямая корреляционная связь со сниженными, по сравнению с таковыми при остром бронхите, показателями уровней цитокинов, IgM, sIgA; регистрируется хронический, вялотекущий воспалительный процесс. Уровни экспрессии TLR практически прямо не коррелируют с показателями уровней sIgA и лизоцима; коррелируют с повышенными показателями индекса ИЕКНЕ, что может способствовать повышению адгезии УПМ на клетках эпителия. Все вместе обусловливает нарушение колонизационной резистентности как показателя мукозального иммунитета, способствует прогрессирующему характеру течения инфекционного процесса и дисбалансу в процессах деструкции и репарации, сопутствующих воспалению. Отсутствует связь между TLR и IgE.
При остром и хроническом бронхитах взаимосвязь рецепторов врожденного иммунитета TLR-2, TLR-4, TLR-3, TLR-8 (контролируют запуск цитокинового каскада местной антиинфекционной резистентности, через который запускаются иммуноглобулиновое звено и воспалительная реакция) с микрофлорой биотопа определяет КР слизистых, характеризует течение инфекционного процесса, выраженность клинических и лабораторных проявлений и исход заболевания (излечение, хронизация). Установлена достоверная взаимосвязь TLR с другими факторами врожденного иммунитета лизоцимом, ИЕКНЕ, sIgA и sc. Уровни IgE независимы от TLR. Пятикратное повышение уровней экспрессии генов TLR-2, TLR-4, TLR-3, TLR-8 и цитокинов IL-1β, IL-8, INF-γ, TNF-α свидетельствует о хорошей местной антиинфекционной резистентности, а отсутствие повышения указывает на ее нарушение и хроническое течение заболевания (носит диагностический и прогностический характер).
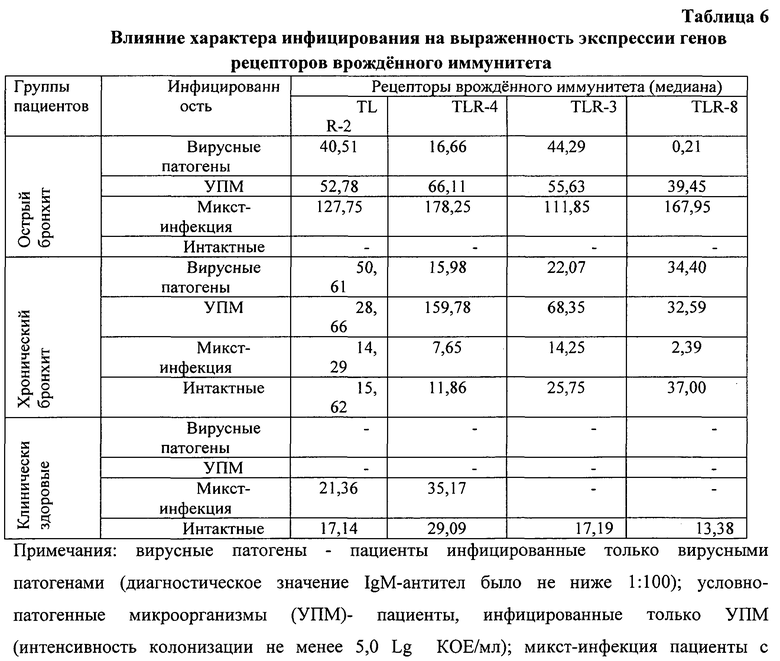

Достоверное повышение медианы экспрессии гена TLR-2 регистрировалось только при остром бронхите и при микст-инфекции по сравнению с хроническим бронхитом и контрольной группой при p<0,0001. Медиана экспрессии гена TLR-4 при остром бронхите достоверно ниже при инфицировании УПМ при сопоставлении с хроническим бронхитом (p<0,0001), достоверно выше при микст инфекции при сопоставлении с хроническим бронхитом и контрольной группой (p<0,0001), а без инфицирования достоверно выше в контрольной группе по сравнению с хроническим бронхитом (p=0,007).
Медиана экспрессии гена TLR-3 при остром бронхите достоверно выше при сопоставлении с хроническим бронхитом (p<0,006) при инфицировании вирусными патогенами и при микст инфекции (p<0,0001). Медиана экспрессии гена TLR-8 при остром бронхите достоверно выше при сопоставлении с хроническим бронхитом (p<0,006) при микст инфекции (p<0,0001); при хроническом бронхите она выше таковой при остром бронхите при инфицировании вирусными патогенами (p<0,0001), а без инфицирования достоверно выше по сравнению с контрольной группой (p=0,001). Следовательно, при остром бронхите в ответ на выраженное бактериально-вирусное воздействие исследованные TLR отреагировали достоверным повышением экспрессии генов по сравнению с хроническим бронхитом и контрольной группой. Причем, проявилась специализация TLR:
TLR-2 и TLR-4 реагировали, в основном на бактериальные патогенны, а TLR-3 и TLR-8- на вирусные патогенны. Наиболее высокие значения экспрессии генов имели место при микст-инфекции, что объясняется, в определенной степени, перекрестным действием лигандов. При хроническом бронхите уровни экспрессии генов TLR в основном не отличались от контрольной группы (Табл.6.)
Таким образом, при верифицированном патогенитеческом агенте третья степень нарушения микробиоценоза ротоглотки - выраженный воспалительный процесс отражает выраженную воспалительную реакцию при бронхитах и свидетельствует о полноценности мукозального иммунитета; вторая степень нарушения микробиоценоза ротоглотки - биоценоз является промежуточной между первой и третьей степенями и указывает на нормально протекающую реакцию мукозального иммунитета; первая степень нарушения микробиоценоза ротоглотки - промежуточный тип свидетельствует о нарушении мукозального иммунитета.
Пример 2.
Клинико-анамнестические и лабораторные данные 228 больных с урогенитальным хламидиозом (УГХ) позволили отобрать 100 пациенток, которые были разбиты на 3 группы. Группу I составила 41 пациентка - первично инфицированные больные в острой стадии инфекционного процесса. Группу II составляли 29 пациенток с хроническим течением хламидийной инфекции. В III (группа сравнения) вошли 30 пациенток - ранее переболевшие (с давно перенесенной хламидийной инфекцией). Контролем служили 32 клинически здоровые женщины (группа IV, контрольная, группа сравнения).
УПМ во влагалище (Вл) при остром урогенитальном хламидиозе (УГХ) определялись в количестве 8,1±0,4 lg КОЕ/мл, при обострении хронического УГХ - 4,6±1,0 lg КОЕ/мл, у переболевших - 2,5±1,2 lg КОЕ/мл, у клинически здоровых пациентов - 2,74±0,94 lg КОЕ/мл. Уровни выявления УПМ при остром УГХ отличались (при p<0,05) от таковых других сравниваемых групп пациентов. По частоте выявляемое™ УПМ во Вл достоверные различия выявлены между I и II (p<0,01), I и III (p<0,001), I и IV (p<0,001), II и III (p<0,01), II и IV (p<0,001), III и IV группами (p<0,01), а между группами I и II различия не достоверны. Чем выраженное патологический процесс, тем шире набор микроорганизмов и в более высоких титрах они высеваются. Косвенным свидетельством приобретения патогенных свойств УПМ может быть выделение из Вл штаммов облигатных анаэробов при остром УГХ в титре 7 lg КОЕ/г, а при обострении хронического УГХ в титре 5 lg КОЕ/г. В I группе у 43,9% пациенток выявлен бактериальный вагинит и у 56,1% - дисбиоз, во II группе у 27,5% пациенток - бактериальный вагинит и у 72,4% - дисбиоз, в III и IV группе у всех пациенток -нормоценоз. УПМ в цервикальном канале (Цк) в группе I определялись в количестве 3,70±1,56 lg КОЕ/мл, в группе II - 3,80±0,27 lg КОЕ/мл, в группе III - 1,36±0,37 lg КОЕ/мл, в группе IV - 1,94±0,73 lg КОЕ/мл. По частоте выявляемости УПМ в Цк различия выявлены между I и III (p<0,01), I и IV (p<0.001), II и IV (p<0,001), III и IV (p<0,01) группами, а между I и II, II и III группами различия не достоверны. В I группе у 19,51% пациенток регистрировался бактериальный цервицит и у 80,48% - дисбиоз, во II группе у 13,79% пациенток - бактериальный цервицит, у 51,7% - дисбиоз и у 34,48% - промежуточный тип, в III и IV группа у всех пациенток - нормоценоз. Косвенным свидетельством приобретения патогенных свойств УПМ может быть выделение из Цк штаммов облигатных анаэробов в титре 4 lg КОЕ/г. УПМ в уретре (Ур) в группе I определялись в количестве 4,20±0,51 lg КОЕ/мл, в группе II - 2,3±0,5 lg КОЕ/мл, в группе III - 2,50±0,83 lg КОЕ/мл, в группе IV - 1,32±0,37 lg КОЕ/мл. По частоте выявляемости УПМ в Ур достоверные различия выявлены между I и IV (p<0,001), II и III (p<0,01), II и IV группами (p<0,001), а между группами I и II, I и III, III и IV различия не достоверны. Косвенным свидетельством приобретения патогенных свойств УПМ может быть выделение из Ур штаммов факультативных анаэробов или облигатных анаэробов в титре 4 lg КОЕ/г.
При УГХ показатели уровней обсемененности УПМ Цк, Ур и Вл прямо коррелируют с показателями уровней экспрессии генов TLR-2 и TLR-4. Повышение экспрессии генов TLR-2 и TLR-4, как в Цк, так и в Ур, коррелирует с тяжестью клинических проявлений, зависящей как от хламидий, так и от ассоциантов (возбудителей инфекций передаваемых половым путем - ИППП и УПМ). Во Вл имеет место экспрессия генов TLR-2 и TLR-4 в ответ на УПМ, а в Цк и Ур - на УПМ и возбудителей ИППП. Активация экспрессии генов TLR-2 и TLR-4 происходит более выражение в ответ на УПМ и менее выражение при контакте с нормофлорой. Впервые установлена определяющая роль TLR-2 и TLR-4 слизистых УГТ в ответе макроорганизма на инфицирование хламидиями и УПМ при УГХ. Уровни экспрессии генов TLR-2 и TLR-4 служат критериями оценки выраженности УГХ и наличия воспалительного процесса у больных, а при выздоровлении их снижение может свидетельствовать об эрадикации возбудителя. При УГХ выявление в соскобном материале из Ур уровней экспрессии генов TLR-2 более 14 ОЕ и TLR-4 более 10 ОЕ, а в соскобном материале из Цк TLR-2 более 19 ОЕ и TLR-4 более 14 ОЕ указывает на острый УГХ;
выявление в соскобном материале из Ур уровней экспрессии генов TLR-2 не более 5 ОЕ и TLR-4 не более 5 ОЕ, а в соскобном материале из Цк TLR-2 не более 6 ОЕ и TLR-4 не более 9 ОЕ указывает на хронический УГХ или начало хронизации инфекционного процесса. Однотипные изменения показателей уровня экспрессии TLR-2 и TLR-4 в Цк и Ур пациенток с хронической формой хламидиоза указывают на развитие "феномена рецепторной депрессии", сопровождающегося дисбалансом между развитием инфекционного процесса и воспалительной реакцией. Повышение уровня экспрессии mRNA TLR-2 и TLR-4 и активности локального синтеза цитокинов в ответ на хламидийную инфекцию способствует благоприятному исходу заболевания, а низкие уровни являются плохим прогностическим признаком.
При остром хламидиозе в ответ на высокую инфекционную нагрузку (хламидий в виде моно- или микстинфекции с возбудителями ИППП и/или с УПМ) повышаются уровни экспрессии генов TLR-2, TLR-4, запускающие в Цк выраженную продукцию IL-8, TNF-α и IL-1β, приводящих, в свою очередь, к увеличению содержания лейкоцитов, белка и Ig у пациенток, что можно расценивать как выраженную местную (преимущественно по клеточному типу) иммунологическую реакцию макроорганизма, отражающую остроту инфекционного процесса и способствующую развитию воспалительной реакции и локализации распространения инфекции за пределы шейки матки, а также стимуляции продукции дополнительных цитокинов соседними неинфицированными клетками. При хроническом хламидиозе сочетание сниженной экспрессии генов TLR-2 и TLR-4 с подавлением активности локального синтеза IL-8, IL-6, TNF-α, относительно слабо выраженной лейкоцитарной реакцией, пониженными уровнями sIgA и sc, повышенным содержанием общего белка и IgG, обусловливает хронический, вялотекущий воспалительный процесс, способствует прогрессирующему характеру течения инфекционного процесса и свидетельствуют о дисфункции механизмов мукозального иммунитета Цк, дисбалансе в процессах деструкции и репарации, сопутствующих воспалению.
Таким образом, при верифицированном патогенитеческом агенте третья степень нарушения микробиоценоза слизистых урогенитального тракта - выраженный бактериальный вагинит (бактериальный цервицит) отражает выраженную воспалительную реакцию при урогенитальном хламидиозе и свидетельствует о полноценности мукозального иммунитета; вторая степень нарушения микробиоценоза ротоглотки - биоценоз является промежуточной между первой и третьей степенями и указывает на нормально протекающую реакцию мукозального иммунитета; первая степень нарушения микробиоценоза ротоглотки - промежуточный тип или нормоценоз свидетельствует о нарушении мукозального иммунитета.
Следующей задачей изобретения является разработка способа коррекции инфекционно-воспалительного процесса с учетом состояния мукозального иммунитета и прогноза течения инфекционно-воспалительного процесса.
Известен способ лечения инфекционных заболеваний (патент РФ №2146531), включающий применение антибиотиков и иммуномодуляторов, отличающийся тем, что при низком титре специфических антител в крови и с учетом принадлежности антител к классам иммуноглобулинов при подостром, стертом, инапарантном, медленном или хроническом течении инфекции ежедневно или через день применяют иммуномодулирующие средства в сочетании с пероральным и/или ректальным введением препаратов бифидумбактерина и/или ацилакта, затем при повышении титра антител в крови и с учетом принадлежности антител к классам иммуноглобулинов назначают в течение 5-14 дней антибиотикотерапию и в конце лечения повторно применяют иммуномодулирующие средства в сочетании с пероральным и/или ректальным введением препаратов бифидумбактерина и/или ацилакта.
Недостатки способа заключаются в том, что при назначении данной терапии учитывались только титры специфических антител в крови с учетом принадлежности антител к классам иммуноглобулинов при подостром, стертом, инапарантном, медленном или хроническом течении инфекции.
Задача решается таким образом, что больным с хорошим состоянием мукозального иммунитета, определенного в соответствии с заявленным способом оценки состояния мукозального иммунитета и с учетом прогноза течения инфекционно-воспалительного процесса в слизистых различной локализации назначают коррегирующую терапию с использованием общепринятых антибактериальных препаратов с подключением иммуномодулятора до момента излечения и исчезновения воспалительной реакции, а больным с нарушением мукозального иммунитета после первого курса упомянутой терапии повторно через месяц назначают второй аналогичный курс терапии до момента излечения и исчезновения воспалительной реакции.
Следующие примеры подтверждают эффективность использования заявляемого способа коррекции инфекционно-воспалительного процесса с учетом состояния мукозального иммунитета и прогноза течения инфекционно-воспалительного процесса.
Пример 1. У детей с острым и хроническим бронхитами верифицирована патогенетическая ассоциация из аденовирусов, S. aureus и грибов рода Candida. При этом при остром и хроническом бронхитах (стадия обострения), по сравнению с клинически здоровыми пациентами, достоверно чаще и с одинаковой частотой встречались вторая (дисбиоз - в 35,3% и 33,3% случаев, соответственно) и третья (выраженный воспалительный процесс - в 31,4% и 26,7% случаев, соответственно) степени дисбактериоза ротоглотки; при этом, при остром бронхите в сопоставлении с хроническим бронхитом выявлены более высокие уровни показателей экспрессии генов рецепторов врожденного иммунитета TLR и воспалительной реакции, что в совокупности свидетельствовало о высоком уровне мукозального иммунитета, наиболее выраженном при остром бронхите. Это подтвердилось эффективностью курса проведенного лечения с использованием общепринятой антибактериальной терапии с подключением иммунобиологического препарата Кипферон®: снижение показателей обсемененности вирусными патогенами, S. aureus и грибми рода Candida и отсутствие рецидива в течение полугода (срок наблюдения) у пациентов с острым бронхитом, а пациентам с хроническим бронхитом через месяц после первого курса терапии потребовалось проведение повторного курса для достижения указанного эффекта. В то же время при остром и хроническом бронхите у пациентов с нормоценозом - в 21,6% и 20,0% случаев, соответственно) и первой (промежуточный тип- в 11,8% и 20,0% случаев, соответственно) степенями дисбактериоза ротоглотки, сопровождающиеся достоверно более низкими уровнями показателей экспрессии генов рецепторов врожденного иммунитета TLR и воспалительной реакции и указывающими на нарушение мукозального иммунитета, потребовалось повторное применение курса терапии через месяц после первого для достижения лечебного эффекта - снижение показателей обсемененности вирусными патогенами, S. aureus и грибами рода Candida и отсутствие рецидива через полгода; у 11,8% пациентов с острым бронхитом и 66,7% пациентов с хроническим бронхитом через полгода выявлен рецидив заболевания. Во всех случаях выздоровление сопровождалось снижением уровней экспрессии генов TLR и выраженности воспалительной реакции на слизистых; сохранение выраженных экспрессии генов TLR и воспалительной реакции после первого курса терапии требовало его повторения.
Пример 2. При остром и хроническом (в стадии обострения) урогенитальном хламидиозе (УГХ) у пациентов в цервикальном канале верифицирована патогенетическая ассоциация из хламидий, возбудителей инфекций, передаваемых половым путем (ИППП) и условно-патогенной микрофлоры (УПМ). При этом при остром и хроническом УГХ, по сравнению с клинически здоровыми пациентами, достоверно чаще и с одинаковой частотой встречались вторая (дисбиоз - в 80,5% и 51,7% случаев, соответственно) и третья (цервицит - в 19,5% и 13,8% случаев, соответственно) степени дисбактериоза урогенитального тракта (УГТ); при этом, при остром УГХ в сопоставлении с хроническим УГХ выявлены более высокие уровни показателей рецепторов врожденного иммунитета TLR и воспалительной реакции, что в совокупности свидетельствовало о высоком уровне мукозального иммунитета, наиболее выраженном при остром УГХ. Это подтвердилось эффективностью курса проведенного лечения с использованием общепринятой антибактериальной терапии с подключением иммунобиологического препарата Кипферон®: регистрировалась эррадикация хламидий и рецидив не регистрировался в течение полугода (срок наблюдения) у пациентов с острым УГХ, а пациентам с хроническим УГХ через месяц после первого курса терапии потребовалось проведение второго курса для достижения указанного эффекта. В тоже время у пациентов с нормоценозом - (в 0% и 0% случаев,соответственно) и первой (промежуточный тип - в 80,5% и 51,7% случаев, соответственно) степенями дисбактериоза УГТ, сопровождающиеся достоверно более низкими уровнями показателей экспрессии генов рецепторов врожденного иммунитета TLR и воспалительной реакции и указывающими на нарушение мукозального иммунитета, потребовалось повторное применение курса терапии через месяц после первого для достижения лечебного эффекта - эррадикация хламидий и отсутствие рецидива заболевания через полгода; у 0% пациентов с острым УГХ и 60% пациентов с хроническим УГХ через полгода выявлено обострение заболевания. Во всех случаях выздоровление сопровождалось снижением уровней экспрессии генов TLR и выраженности воспалительной реакции на слизистых; сохранение выраженных экспрессии генов TLR и воспалительной реакции после первого курса терапии требовало его повторения.
Пример 3. При остром уреаплазмозе у пациентов во влагалище верифицирована патогенетическая ассоциация из уреаплазм, возбудителей инфекций, передаваемых половым путем (ИППП) и условно-патогенной микрофлоры (УПМ). При этом при остром уреплазмозе, по сравнению с клинически здоровыми пациентами, достоверно чаще встречались вторая (дисбиоз - в 44,0% случаев) и третья (вагинит - в 46,0% случаев) степени дисбактериоза влагалища; при этом, при остром уреаплазмозе выявлен высокий уровень показателей воспалительной реакции, что подтверждало высокий уровень мукозального иммунитета. Это также подтвердилось эффективностью курса проведенного лечения с использованием общепринятой антибактериальной терапии с подключением иммунобиологического препарата Кипферон®: у 68,0% пациентов с дисбиозом и у 88,0%
пациентов с вагинитом наступило клиническое выздоровление с эррадикацией уреаплазм после первого курса лечения, рецидив не регистрировался в течение полугода (срок наблюдения); у 32,0% пациентов с дисбиозом и у 12,0% с вагинитом через месяц после первого курса терапии потребовалось проведение второго курса для достижения указанного эффекта. В тоже время у пациентов с нормоценозом - в 0% случаев) и первой (промежуточный тип - в 10,5% случаев) степенями дисбактериоза влагалища, сопровождающиеся достоверно, по сравнению с дисбиозом и вагинитом, более низкими уровнями показателей воспалительной реакции и указывающими на нарушение мукозального иммунитета, потребовалось повторное применение курса терапии через месяц после первого для достижения лечебного эффекта - эррадикации уреаплазм и отсутствие рецидива через полгода; у 68,0% пациентов с нормоценозом и 76,0% пациентов с вагинитом через полгода выявлено обострение заболевания. Во всех случаях выздоровление сопровождалось снижением воспалительной реакции слизистых; сохранение выраженной воспалительной реакции после первого курса терапии требовало его повторения.
Таким образом, научно обоснована и подтверждена концепция о том, что взаимодействие микробиоценозов слизистых открытых полостей макроорганизма носит динамический характер, обеспечивает жизненно необходимый оптимальный уровень реактивности макроорганизма и его антиинфекционную резистентность. Тем самым, достоверно подтверждена роль микроорганизмов в обучении защитных систем макроорганизма в онтогенезе. Изменение антиинфекционной резистентности к гетерологичным патогенам на организменном и местном уровнях определяется набором факторов патогенности микроорганизмов, являющихся неотъемлемой патогенетической характеристикой возбудителей инфекций, обусловливающей, в конечном счете, прогноз и исход заболевания.
Расширены представления о механизме формирования запуска инфекционного процесса, который является следствием взаимодействия микроорганизмов биотопов слизистых и возбудителей инфекционных заболеваний с TL-рецепторами, уровень экспрессии которых взаимосвязан с выраженностью показателей местного иммунитета (секреторных иммуноглобулинов и цитокинов). Таким образом, TLR являются первым звеном в ответе организма на патоген, определяющим дальнейшее развитие инфекционного патологического процесса. Создание быстрой и неспецифической защиты против инфекций определяется способностью TLR распознавать практически все патогенассоциированные молекулярные структуры на патогенах, запускающих инфекционный процесс. Нарушение механизмов функционирования TLR приводит к развитию иммунопатологических процессов и сказываются как на развитии, так и на исходе инфекционных заболеваний.
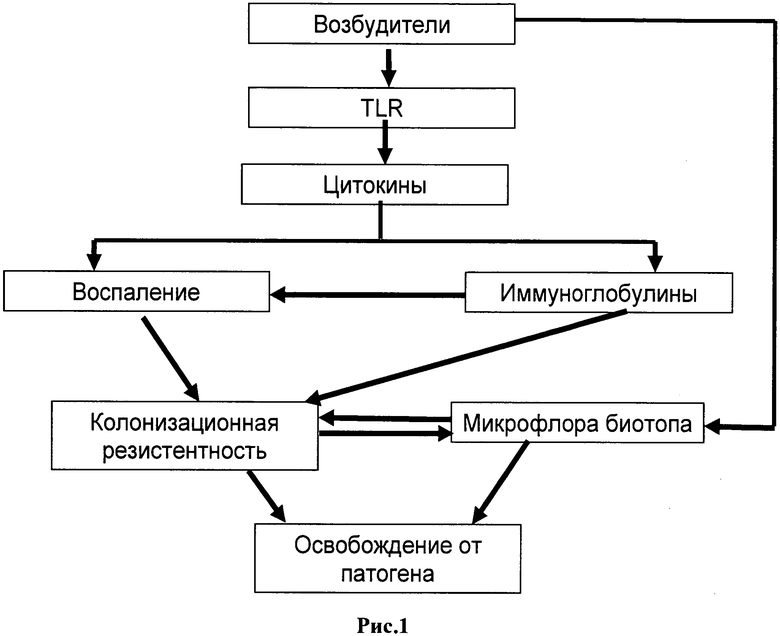
Впервые представлен алгоритм функционирования КР слизистых открытых полостей как интегральной составляющей местной антиинфекционной резистентности и мукозального иммунитета в целом. (Рис.1.)
Техническим результатом настоящего изобретения является разработка способа комплексной оценки КР слизистых как метода оценки их мукозального иммунитета. Регистрация показателей уровней TLR, цитокинов и Ig слизистых имеет диагностическое и прогностическое значение и как результат позволяет использовать определенную схему коррекции при нарушении мукозального иммунитета.
Список литературы
1. Бондаренко В.М., Мацулевич Т.В. Дисбактериоз кишечника как клинико-лабораторный синдром: современное состояние проблемы. - М., Издательская группа «ГЭОТАР-Медиа», 2007. - 300 с.
2. Воропаева Е.А., Байракова А.Л., Бичучер A.M. и др. Протеазная активность микрофлоры ротовой полости больных пародонтитом // Биомедицинская химия. - 2008. - Т.54, Вып.6. - С.706-712.
3. Иммунобиологические препараты, перспективы применения в инфектологии. Г.Г. Онищенко, В.А. Алешкин, С.С. Афанасьев, В.В. Поспелова (ред.). - М., ГОУ ВУНМЦ МЗ РФ, 2002. - 608 с.
4. Кочеровец В.И., Бунятян Н.Д. Нормальная микрофлора женских мочеполовых органов и препараты для ее коррекции. - М., Издательский дом «АКТЕОН», 2011. - 72 с.
5. Лахтин М.В., Алешкин В.А., Лахтин В.М. и др. Поведение Candida tropicalis и Candida krusei в присутствии пробиотических пектинов. // Астраханский медицинский журнал. - 2011. - Т.6, №3. - С.97-101.
6. Самсыгина Г.А. Острый бронхит у детей и его лечение // Педиатрия. - 2008. - №2. - С.25-32.
7. El Feghaly R.E., McGann L., Bonville C.A. et al. Local production of inflammatory mediators during childhood parainfluenza virus infection // Pediatr. Infect. Dis. - 2010, V.29. - P.26-31.
8. Козлов Л.В., Бичучер A.M., Мишин А.А. и др. Определение активности протеиназ крови и микроорганизмов // Биомед. химия. - 2008. - Т.54, №3. - С.314-321.
9. Фидров А.А., Скрипкин Ю.К., Кулагин В.И. и др. Некоторые актуальные вопросы урогенитальной хламидийной инфекции // Журн. "Успехи современного естествознания". - 2006 - №2. - С.24-26.
10. Donatella Pellati, loannis Mylonakis, Giulio Bertoloni et al. Genital tract infections and infertility // European J. of Obstetrics & Gynecology and Reproductive Biology. - 2008. - Vol.140. - P.3-11.
11. Иммунобиологические препараты и перспективы их применения в инфектологии /Под ред. Г.Г. Онищенко, С.С. Афанасьева, В.В. Поспеловой. М.: ГОУ ВУНМЦ МЗ РФ, 2002. С.162-169,
12. Афанасьев С.С., Алешкин В.А., Воробьев А.А. и др. Влияние препаратов цитокинов на устойчивость бактерий к антибиотикам in vitro. // Журн. микробиол. - 2005. - №3. - С.95-97.
13. Интерфероновый статус, препараты интерферона в лечении и профилактике инфекционных заболеваний и реабилитация больных. С.С. Афанасьев, Г.Г. Онищенко, В.А. Алешкин и др. (ред.). - М., Триада-Х, 2005. - 767 с.
14. Караулов А.В., Афанасьев С.С., Алешкин В.А., Лапин Б.А. (ред.) Хламидийная инфекция. Новые аспекты патогенеза, иммунологии, верификации и лечения инфекции у человека и приматов. - М., изд-во Первого МГМУ им. И.М. Сеченова, 2012. - 256 с.
15. Серебрянский Ю.Е., Афанасьев С.С., Алешкин В.А. и др. Проблемы цитокинотерапии инфекционных заболеваний. - М., 2000. - 106 с.
16. Хаитов P.M. Физиология иммунной системы. - М., ВИНИТИ РАН, 2001. - 224 с.
17. Шварцман Я.С., Хазенсон Л.Б. Местный иммунитет. - Л., Медицина, 1978. - 224 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ ЗДОРОВЬЯ ЧЕЛОВЕКА ПРИ ПРОГНОЗИРОВАНИИ ТЕЧЕНИЯ ИНФЕКЦИОННОГО ЗАБОЛЕВАНИЯ | 2014 |
|
RU2595863C2 |
| СПОСОБ ОЦЕНКИ МИКРОБИОЦЕНОЗА ПОЛОСТИ МАТКИ У ЖЕНЩИН С ПОЛИПАМИ ЭНДОМЕТРИЯ В ПОСТМЕНОПАУЗАЛЬНОМ ПЕРИОДЕ | 2010 |
|
RU2430365C1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ ЗДОРОВЬЯ ЖЕНЩИН ПРИ ПРОГНОЗИРОВАНИИ ФИЗИОЛОГИЧЕСКОГО И ОСЛОЖНЕННОГО ТЕЧЕНИЯ БЕРЕМЕННОСТИ НА РАННИХ СРОКАХ ГЕСТАЦИИ | 2014 |
|
RU2578028C1 |
| Способ персонализированного ведения беременных с инфекционной патологией урогенитального тракта на ранних сроках гестации | 2016 |
|
RU2632435C1 |
| СПОСОБ ОЦЕНКИ МИКРОБИОЦЕНОЗА ВЛАГАЛИЩА | 2004 |
|
RU2249821C1 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ТЕРАПИИ ИНФЕКЦИОННОГО ЗАБОЛЕВАНИЯ | 2015 |
|
RU2615417C1 |
| СПОСОБ ДИАГНОСТИКИ УГРОЗЫ ПРЕРЫВАНИЯ БЕРЕМЕННОСТИ | 2007 |
|
RU2390022C2 |
| Способ оценки выраженности инфекционного процесса при урогенитальной инфекции у беременных | 2019 |
|
RU2715626C1 |
| СПОСОБ КОМПЛЕКСНОЙ ДИАГНОСТИКИ ВОСПАЛИТЕЛЬНОГО ПРОЦЕССА ВУЛЬВЫ И ВЛАГАЛИЩА БАКТЕРИАЛЬНОЙ ЭТИОЛОГИИ У ДЕВОЧЕК В ВОЗРАСТЕ ОТ 0 ДО 8 ЛЕТ | 2014 |
|
RU2563182C1 |
| СПОСОБ ВЕДЕНИЯ БЕРЕМЕННЫХ С ИНФЕКЦИОННОЙ ПАТОЛОГИЕЙ УРОГЕНИТАЛЬНОГО ТРАКТА | 2017 |
|
RU2649127C1 |
Изобретение относится к иммунологии и представляет собой способ оценки состояния мукозального иммунитета слизистых открытых полостей при прогнозировании течения инфекционно-воспалительных процессов, отличающееся тем, что при установленном патогенетическом факторе проводят регистрацию степеней нарушения микробиоценоза конкретного биотопа с использованием комплекса методов оценки уровней факторов колонизационной резистентности, а именно нормальной микрофлоры, условно-патогенной микрофлоры, иммуноглобулинов - G, М, А, секреторного иммуноглобулина А и sc компонента; и в зависимости от степени нарушения микробиоценоза оценивают состояние мукозального иммунитета и прогнозируют благоприятный исход с эрадикацией возбудителя или хронизацию с персистированием возбудителя. Также изобретение относится к способу коррекции инфекционно-воспалительных процессов с подключением иммуномодулятора - Кипферон®. Изобретение обеспечивает повышение точности прогнозирования течения заболевания, а также расширение арсенала способов коррекции инфекционно-воспалительных процессов. 2 н.п. ф-лы, 3 пр., 6 табл., 1 ил.
1. Способ оценки состояния мукозального иммунитета слизистых открытых полостей различной локализации при прогнозировании течения инфекционно-воспалительных процессов, отличающийся тем, что при установленном патогенетическом факторе проводят регистрацию степеней нарушения микробиоценоза конкретного биотопа слизистых открытых полостей различной локализации с использованием комплекса методов оценки уровней факторов колонизационной резистентности как интегрирующей составляющей мукозального иммунитета в мазках и соскобном материале со слизистых, а именно нормальной микрофлоры, условно-патогенной микрофлоры, иммуноглобулинов - G, М, А, секреторного иммуноглобулина А и sc компонента; и в зависимости от степени нарушения микробиоценоза оценивают:
- хорошее состояние мукозального иммунитета при второй и третьей степенях нарушения микробиоценозов и прогнозируют благоприятный исход заболевания с эрадикацией возбудителя;
- нарушение мукозального иммунитета при нормоценозе и первой степени нарушения микробиоценозов и прогнозируют хроническое течение инфекционно-воспалительного процесса с персистированием возбудителя.
2. Способ коррекции инфекционно-воспалительных процессов, отличающийся тем, что проводят оценку состояния мукозального иммунитета слизистых открытых полостей способом по п. 1 и назначают:
- больным с хорошим состоянием мукозального иммунитета курс лечения с использованием общепринятой антибактериальной терапии с подключением иммуномодулятора - Кипферон® до момента излечения и исчезновения воспалительной реакции
- больным с нарушением мукозального иммунитета курс лечения с использованием общепринятой антибактериальной терапии с подключением иммуномодулятора - Кипферон® и повторно через месяц второй аналогичный курс терапии до момента излечения и исчезновения воспалительной реакции.
| Афанасьев С.С | |||
| и др | |||
| / Микробиоценозы открытых полостей и мукозальный иммунитет / Эффективная фармакотерапия | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Тюрин Ю.А | |||
| и др | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Задержка для челнока круглых вязальных машин | 1924 |
|
SU766A1 |
Авторы
Даты
2015-07-20—Публикация
2014-03-28—Подача