Изобретение относится к способу подготовки и анализа множества клеточных суспензий, содержащему, по меньшей мере, следующие последовательные этапы, на которых:
(a) на приемную площадку загружают множество флаконов, при этом каждый флакон содержит предназначенную для анализа клеточную суспензию;
(b) на приемную площадку загружают множество аналитических емкостей; и
(c) из флакона отбирают пробу клеточной суспензии и эту пробу вводят в аналитическую емкость; этап (с) повторяют для каждого анализируемого флакона.
Изобретение относится также к автомату для подготовки и анализа, в котором применяют этот способ.
Анализ клеточной суспензии и, например, фиксированного тонкого слоя цитологической пробы является исключительно деликатной операцией. Цитологическая диагностика охватывает диагностические технологии, основанные на морфологическом исследовании клеток. Она очень хорошо подходит для обнаружения рака и предраковых поражений, в частности, шейки матки.
Действительно, целью такого анализа является обнаружение патологических клеток, поэтому необходимо, чтобы клеточная проба была хорошо читаемой во избежание диагностических ошибок и хорошо характеризовала исследуемую зону.
Для обеспечения анализа большого количества проб и высокой скорости обработки стараются автоматизировать процесс подготовки проб с целью их анализа, а также сам их анализ. Для этого используют известные автоматы, позволяющие готовить аналитические пластинки с пробами, такими как мазки, и другими.
Автомат вышеуказанного типа описан, например, в документе US 2009/0233331.
Однако такие автоматы не всегда позволяют готовить клеточные пробы, обеспечивающие удовлетворительный анализ, и получать надежный диагноз. В таких автоматах используют устройства, включающие в себя определенное число артефактов, что создает проблемы управления давлением фильтра, приводит к изменениям клеточной морфологии и к закупориванию ячеек фильтра фрагментами. Кроме того, манипуляции различаются в зависимости от типа пробы: например, перед сбором клеток на фильтре иногда необходимо удалить эритроциты или слизь.
Таким образом, невозможно применять стандартный способ, общий для всех типов гинекологических или не гинекологических цитологических проб и ограничивающий до минимума вмешательство операторов.
Одной из задач изобретения является устранение этих недостатков за счет полной автоматизации подготовки и анализа цитологических суспензий при помощи надежного, репродуктивного и скоростного стандартного способа. Независимо от типа цитологических проб способ приготовления является одинаковым.
Поставленная задача решена в способе отбора и анализа множества клеточных суспензий, в котором этап (с) отбора пробы клеточной суспензии из флакона и введения этой пробы в аналитическую емкость содержит, по меньшей мере, этап разрушения клеточных скоплений при помощи пипеточных дозировочных средств.
Согласно другим отличительным признакам способа:
- этап (с) отбора пробы клеточной суспензии из флакона и введения этой пробы в аналитическую емкость содержит, по меньшей мере, этап перемешивания и фильтрования клеточной суспензии во флаконе,
- этап (с) отбора пробы клеточной суспензии из флакона и введения этой пробы в аналитическую емкость дополнительно содержит, по меньшей мере, следующие этапы:
(d) повторный перевод пробы в суспензию;
(e) выбор релевантных клеток посредством дифференциальной декантации;
(f) всасывание объема, полученного в результате дифференциальной декантации, при помощи пипеточных средств, при этом объем содержит предназначенную для анализа пробу;
(g) повторный перевод объема, содержащего предназначенную для анализа пробу, в однородную суспензию в пипеточных средствах;
(h) перемещение пипеточных средств для их размещения над аналитической емкостью;
(i) выливание предназначенной для анализа пробы в аналитическую емкость.
- каждая аналитическая емкость содержит декантационную чашку и аналитическую пластинку, расположенную напротив декантационной чашки, и способ содержит, по меньшей мере, следующие последовательные этапы:
(j) размещение абсорбционного листа на загрузочной площадке таким образом, чтобы каждая аналитическая пластинка располагалась между загрузочной площадкой и абсорбционным листом;
(k) загрузка множества декантационных чашек в пресс и установка пресса над площадкой таким образом, чтобы каждая декантационная чашка располагалась сверху и напротив аналитической пластинки; и
(l) нанесение тонкого слоя клеточной пробы на аналитическую пластинку, при этом нанесение тонкого слоя клеточной пробы происходит в результате введения пробы в декантационную чашку;
при этом этапы (j) и (k) осуществляют после этапа (b) загрузки множества аналитических емкостей и перед этапом (с) отбора пробы клеточной суспензии, и этап (l) осуществляют после этапа (с) отбора пробы клеточной суспензии;
- он содержит этап анализа клеточного отложения на дне декантационных чашек посредством измерения клеточной плотности на аналитических пластинках;
- он содержит автоматизированный этап окрашивания или маркировки клеток;
- он предварительно содержит этап окончательного закрывания флакона, содержащего предназначенную для анализа клеточную суспензию, при этом способ осуществляют без последующего открывания флакона; и
- каждая аналитическая емкость содержит трубку для отбора или для аликвотирования.
Объектом изобретения является также автомат для отбора проб и анализа, по меньшей мере, одной клеточной суспензии, содержащий:
- по меньшей мере, один флакон, содержащий предназначенную для анализа клеточную суспензию;
- по меньшей мере, одну приемную площадку, на которой устанавливают и точно и неподвижно крепят флакон;
- по меньшей мере, одну чашку для декантации клеточной суспензии, при этом декантационную чашку располагают и крепят точно и неподвижно на площадке;
- систему анализа, содержащую, по меньшей мере, одну аналитическую пластинку, предназначенную для размещения на ней пробы клеточной суспензии, при этом проба является объемной частью клеточной суспензии, содержащей соответствующие предназначенные для анализа элементы, и аналитическую пластинку располагают и крепят точно и неподвижно на площадке снизу и напротив декантационной чашки;
автомат содержит пипеточные средства, выполненные с возможностью отбора пробы клеточной суспензии из флакона и выливания этой пробы в декантационную чашку на аналитическую пластинку системы анализа, причем этим средства выполнены с возможностью разрушения клеточных скоплений.
Согласно другим отличительным признакам автомата:
- он содержит первый подвижный кронштейн, на котором закреплены пипеточные средства, при этом указанный кронштейн перемещается, по меньшей мере, над приемной площадкой, на которой находятся флаконы, декантационные чашки и аналитические пластинки;
- он содержит растворы для маркировки или окрашивания, которые можно смешать с цитологическим раствором при помощи пипеточных средств;
- каждый флакон и каждая аналитическая пластинка содержит визуальную маркировку, и автомат содержит средства считывания визуальных маркировок;
- средства считывания содержат съемочную камеру и установлены на втором подвижном кронштейне, при этом указанный второй кронштейн перемещается, по меньшей мере, над приемной площадкой, на которой находятся флаконы, декантационные чашки и аналитические пластинки;
- флакон содержит средства фильтрования, расположенные над декантационным конусом, при этом пипеточные средства выполнены с возможностью отбора части клеточной суспензии под средствами фильтрования и повторного направления указанной части на декантационный конус для перемешивания указанной клеточной суспензии и, по меньшей мере, одноразового пропускания части указанной суспензии через средства фильтрования для разрушения клеточных скоплений, размер которых превышает размер ячеек фильтра;
- система анализа пробы содержит средства анализа клеточной плотности клеточных отложений на дне декантационной чашки на аналитической пластинке;
- средства анализа клеточной плотности клеточных отложений на дне декантационной чашки на аналитической пластинке содержат съемочную камеру;
- система анализа пробы содержит устройство для получения виртуальной пластинки пробы;
- устройство для получения виртуальной пластинки пробы содержит съемочную камеру;
- он содержит единственную съемочную камеру, образующую средства считывания, средства анализа клеточной плотности и устройство получения виртуальной пластинки;
- он содержит опору, содержащую средства позиционирования, по меньшей мере, площадки, выполненные с возможностью неподвижного и точного крепления площадки, и кнопку, выполненную с возможностью подтверждения положения, по меньшей мере, площадки;
- он выполнен с возможностью применения описанного выше способа;
- клеточная суспензия является цитологической суспензией; и
- цитологическая суспензия содержит фиксирующий раствор, содержащий от 80% до 95% по объему:
- 590 мл физиологического раствора,
- 10 мл ПЭГ,
- 203 мл изопропилового спирта,
- 193 мл чистого этилового спирта,
- 0,01% по объему азида натрия,
и от 20% до 5% по объему 4%-го буферного формалина.
Изобретение будет более очевидно из нижеследующего описания, представленного исключительно в качестве примера, со ссылками на прилагаемые чертежи.
На фиг.1 схематично показан автомат для отбора проб и анализа в соответствии с изобретением, вид в разрезе;
на фиг.2 схематично показан автомат, изображенный на фиг.1, вид в перспективе;
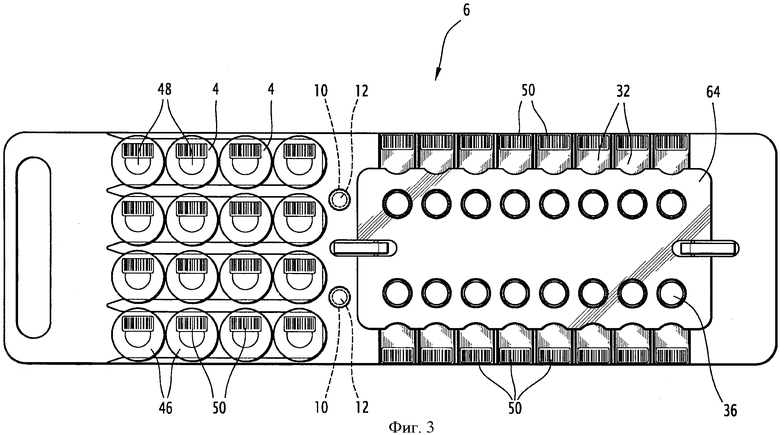
на фиг.3 схематично показана приемная площадка автомата для подготовки и анализа, на которой размещают флаконы, каждый из которых содержит клеточную суспензию, вид сверху;
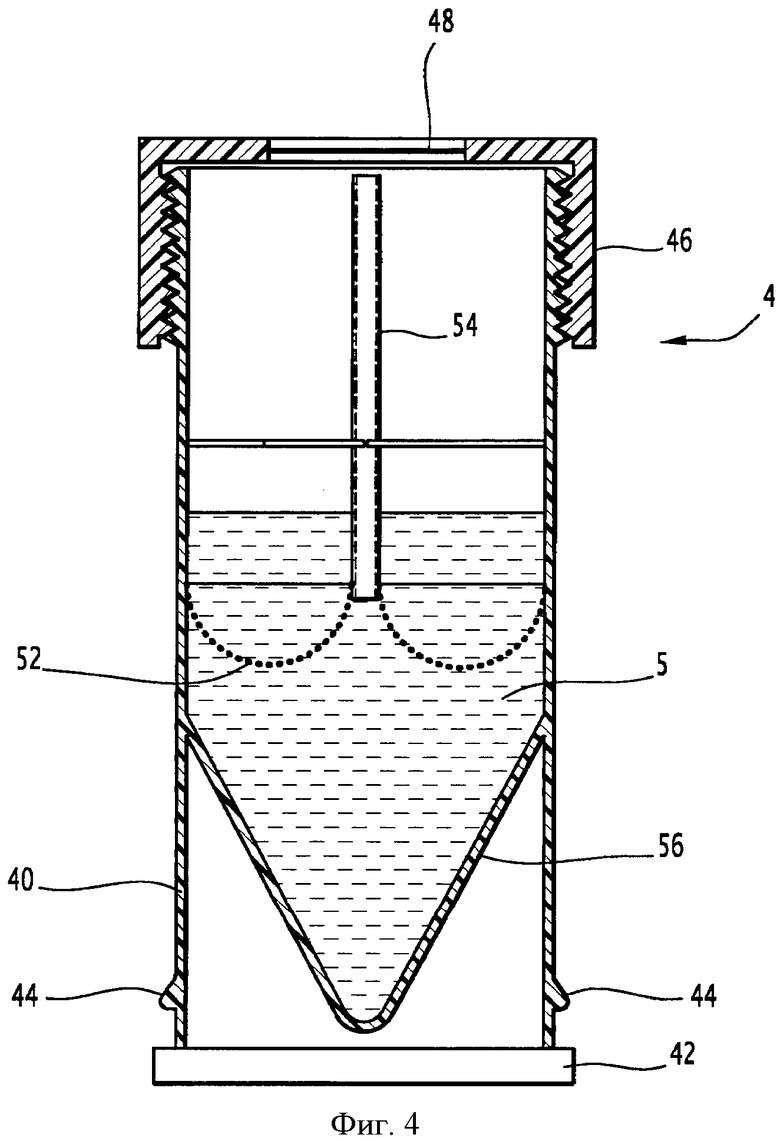
на фиг.4 показан флакон, предназначенный для установки в автомате, вид в разрезе;
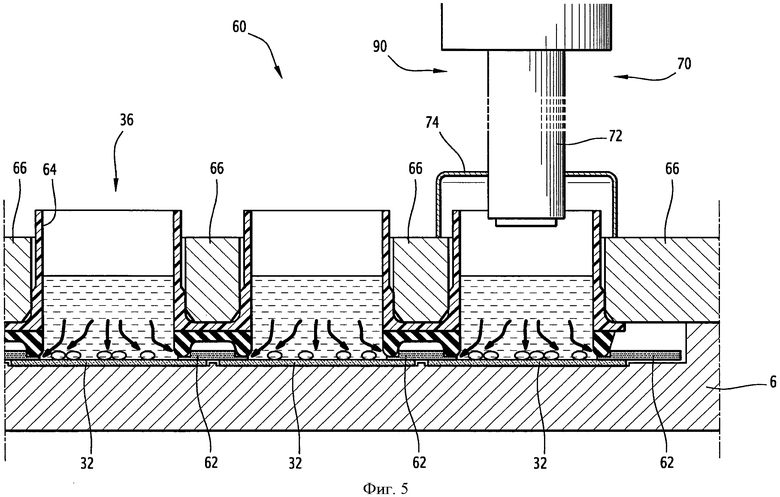
на фиг.5 показана декантационная чашка, предназначенная для установки в автомате, вид в разрезе;
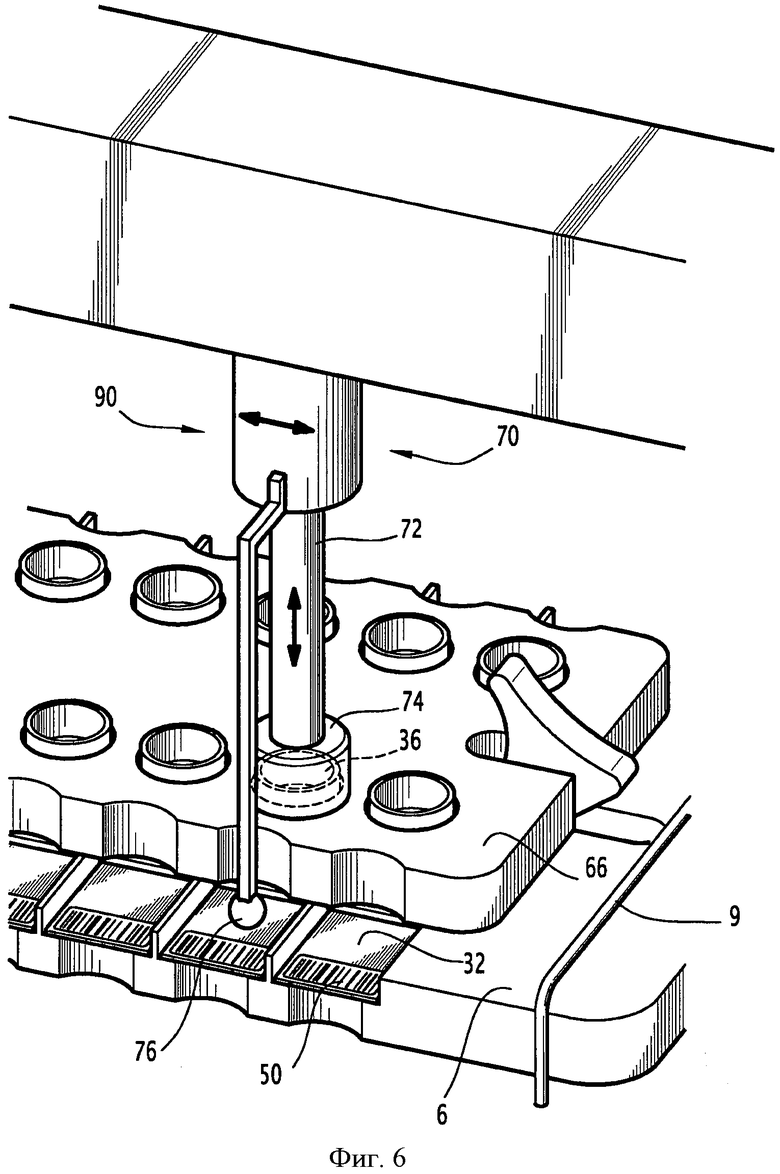
на фиг.6 схематично показаны средства анализа автомата, изображенного на фиг.1 и 2, вид в перспективе;
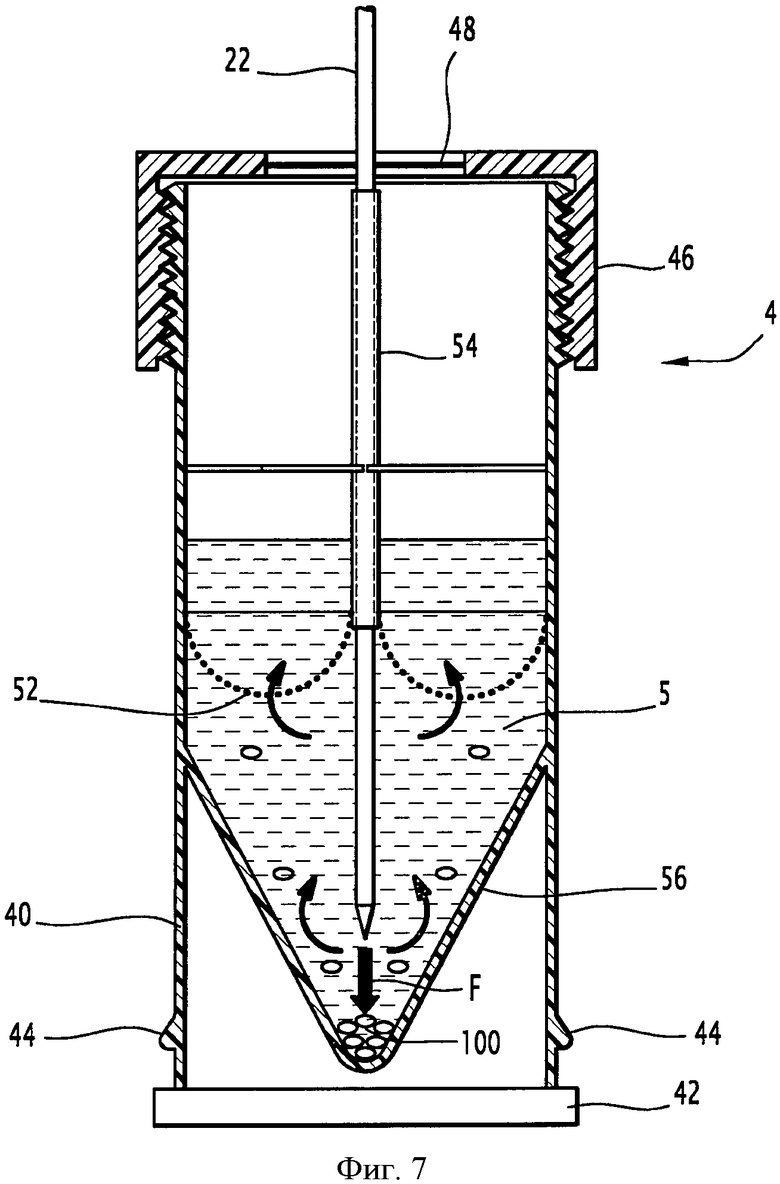
на фиг.7 показан флакон во время этапа перемешивания при осуществлении способа подготовки и анализа клеточной суспензии, вид в разрезе.
На фигурах показан автомат 2 для подготовки и анализа клеточной суспензии, позволяющий автоматизировать эту подготовку и этот анализ.
Действительно, на фиг.1 и 2 показан автомат 2 для подготовки и анализа, по меньшей мере, одного флакона 4, содержащего предназначенную для анализа клеточную суспензию 5, например, фиксированную цитологическую суспензию.
Такая цитологическая суспензия 5 может быть получена, например, в результате операции исследования шейки матки посредством взятия мазка, например, при помощи щетки для взятия мазков (не показана). Эта цитологическая суспензия содержит, в частности, клетки.
После этого щетку погружают во флакон 4, содержащий фиксатор, и очищают на фильтре для извлечения и сбора клеток и получения, таким образом, клеточной суспензии 5.
Фиксатор или фиксирующий раствор предназначен для предохранения и сохранения цитологических проб, содержащих клетки, с целью их дальнейшего анализа специалистом-цитологом. Следовательно, фиксатор должен полностью сохранять все содержащие ядра клетки и эритроциты, в частности, их морфологию в том состоянии, в котором они находились до взятия пробы.
Фиксирующий раствор предназначен для предохранения in vitro цитологической пробы, содержащей биологические клетки, предназначенные для анализа цитологом.
Как известно и было опубликовано Саккоманно и коллегами, спиртовой фиксирующий раствор может также содержать Carbowax® или полиэтиленгликоль (ПЭГ). Как известно из публикаций, формалин можно объединить с декальцинаторами или антиагрегантами, такими как этилендиаминтетрауксусная кислота (EDTA) и ее соли. Как известно и было опубликовано, к пробам, содержащим слизь, можно добавлять муколитическое средство, такое как дитиотреитол (DTT) или ацетилцистеин.
Формалин позволяет сохранять эритроциты и содержащие ядра клетки, не допуская их распада и обеспечивая исходную основу с точки зрения размера, что позволяет цитологу делать более точный диагноз.
Нижеследующий неограничивающий пример иллюстрирует фиксирующий раствор:
Пример:
раствор, содержащий в количестве 80% по объему:
- 590 мл физиологического раствора,
- 10 мл ПЭГ,
- 203 мл изопропилового спирта,
- 193 мл чистого этилового спирта,
- 0,01% по объему азида натрия,
и 20% по объему 4%-го буферного формалина.
Фиксирующий раствор в соответствии с изобретением не содержит ацетона или соединений из семейства кетонов, а также уксусной кислоты, так как эти вещества разрушают эритроциты, которые, распадаясь, высвобождают гемоглобин, закрепляющийся на клетках. Некоторые типы окрашивания, такие как окрашивание по Папаниколау, учитывая комплексный характер красителей, объединяющих несколько ядерных красителей и гемоглобин, делают цитологический и, в частности, ядерный анализ очень сложным и даже невозможным. Точно так же, отложения гемоглобина часто мешают иммуно-цитохимическим исследованиям.
Согласно изобретению, повышается качество последующих анализов пробы посредством окрашивания по Папаниколау или иммуно-цитохимических исследований пробы, зафиксированной в фиксирующем растворе, описанном в данном случае и не содержащем ацетона или соединений из семейства кетонов, а также уксусной кислоты.
Описанный выше фиксирующий раствор обеспечивает, таким образом, отличное сохранение целостности содержащих ядра клеток и эритроцитов с целью их анализа.
Кроме того, описанный выше фиксирующий раствор, содержащий ПЭГ и/или формальдегид, имеет, таким образом, плотность, отличную от классических фиксаторов, применяемых в цитологии и в основном являющихся спиртовыми. Заявитель установил, что фиксирующий раствор позволяет производить выбор нужных клеток через градиент плотности более эффективно, чем классические фиксаторы, применяемые в цитологии.
Кроме того, автомат 2 содержит, по меньшей мере, одну приемную площадку 6, на которой находится, по меньшей мере, флакон 4, содержащий предназначенную для анализа клеточную суспензию 5, и опору 8, на которой расположена приемная площадка 6.
Приемная площадка 6 предназначена для размещения множества флаконов 4, каждый из которых содержит клеточную суспензию 5, с целью быстрой и автоматической подготовки множества предназначенных для анализа клеточных суспензий 5, причем одновременно или последовательно, всех или части суспензий. Такая приемная площадка 4 уже была описана в патентной заявке ЕР-2111300, поданной на имя заявителя, и позволяет позиционировать и точно и неподвижно удерживать, по меньшей мере, флакон 4 на площадке 6. Для более полной информации специалист может обратиться к этому документу, и подробное описание этой площадки опускается. Площадка схематично показана на фиг.3.
Опора 8 содержит средства позиционирования площадки 6, выполненные с возможностью неподвижного удержания площадки в автомате 2. Эти средства позиционирования содержат средства 9 для размещения крайней части площадки 6, при этом площадку располагают напротив или внутри средств 9, когда ее устанавливают в автомат 2.
Кроме того, площадка 6 содержит средства позиционирования на опоре 8. Эти средства позиционирования содержат, по меньшей мере, одно отверстие 10, выполненное в толще площадки, но не являющееся сквозным, и предназначенное для точной установки площадки на опоре 8 автомата 2. Предпочтительно площадка 6 содержит два идентичных отверстия, расположенных ортогонально по отношению к самой длинной стороне площадки 4.
Опора 8 автомата 2 содержит средства позиционирования, дополняющие средства позиционирования площадки 6. Эти средства содержат, по меньшей мере, один шип 12 и предпочтительно столько же шипов, сколько отверстий 10 выполнено в площадке 6. Форма шипа 12 соответствует форме отверстия площадки, а его размер немного меньше, чтобы во время установки площадки 6 на опору 8 шип 12 находился внутри соответствующего отверстия 10. Таким образом, площадка 6 удерживается на опоре 8 неподвижно и точно.
Кроме того, опора 8 автомата 2 содержит кнопку или нажимную кнопку 14, предназначенную для подтверждения нормальной горизонтальной установки площадки 6 на опоре 8. Действительно, если площадка 6 установлена нормально, то есть нижняя сторона площадки полностью входит в контакт с опорой 8, так как шипы 12 зашли в отверстия 10, кнопка 14 заглубляется в опору 8 в предусмотренную для этого выемку 16, обеспечивая, таким образом, нормальную установку площадки 6 и позволяя автомату 2 работать. Если кнопка 14 не заглублена, автомат работать не может.
Кроме того, автомат 2 содержит пипеточные и дозировочные средства 20, называемые в дальнейшем пипеточными средствами или средствами отбора, то есть позволяющими отбирать и/или выливать/заливать пробу клеточной суспензии 5. Эти пипеточные средства 20 расположены над приемной площадкой 6. Проба является точной по объему дозой клеточной суспензии 5, содержащей предназначенные для анализа элементы, например, клетки.
Эти пипеточные средства 20 выполнены подвижными таким образом, чтобы проходить над каждым флаконом 4 для осуществления отбора и/или заполнения, как показано стрелками на фиг.1. Пипеточные средства 20 представляют собой, по меньшей мере, одну пипетку 22 или иглу и предпочтительно образованы множеством пипеток, например, четырьмя или восемью пипетками, расположенными параллельно для обеспечения одновременного отбора проб из множества флаконов 4 и для их одновременной подготовки с целью анализа.
Пипеточные средства 20 закреплены на первом подвижном роботизированном кронштейне на автомате 2 над площадками 6.
Устройство (отверстия 10/шипы 12 и кнопка 14), обеспечивающее точное позиционирование на опоре, позволяет избежать поломки иголок или пипеток 22, не давая им сталкиваться с краями флаконов 4, что могло бы произойти, если бы площадка была плохо позиционирована по отношению к пипеточным средствам 20. Таким образом, это позволяет избежать дополнительных расходов по техническому вмешательству для замены сломанного или деформированного оборудования.
Кроме того, автомат 2 содержит систему 30 подготовки и анализа, содержащую аналитическое устройство, предназначенную для размещения пробы клеточной суспензии 5, отбираемой и выливаемой в или на аналитическое устройство при помощи пипеточных средств 20.
Например, аналитические устройства этой системы 30 подготовки и анализа могут содержать пластинки 32 для нанесения слоя пробы, трубки 34 для отбора или аликвотирования, аналитические или декантационные чашки 36 в зависимости от способа анализа, выбранного специалистом.
Аналитические устройства 32, 34, 36 точно и неподвижно закреплены на площадке 6.
Подробное описание этой системы 30 подготовки и анализа представлено ниже.
Далее со ссылками на фиг.4 следует описание флакона 4, содержащего предназначенную для анализа клеточную суспензию 5.
Предпочтительно этот флакон 4 имеет такие же характеристики, как и описанные в документе ЕР-2111300, чтобы обеспечивать возможность крепления флакона 4 на приемной площадке 6, и некоторые характеристики, описанные в документе WO-2006/058989, для обеспечения возможности подготовки и анализа клеточной суспензии.
Как показано на фиг.4, флакон 4, содержащий цитологическую суспензию 5, содержит корпус 40, например, по существу цилиндрической формы. Начиная от этого корпуса 40, выполнены нижний борт 42 и средства 44 блокировки, расположенные с двух сторон корпуса и выступающие из него, обеспечивая блокировку флакона 4 на приемной площадке 6, как описано в документе ЕР-2111300, в продольном направлении и в направлении высоты. Средства 44 блокировки предназначены для захождения в пазы направляющих площадки 6 таким образом, чтобы заблокировать флакон 4 в приоритетном направлении. Специалист может обратиться к этому документу для ознакомления с работой этого флакона 4 во взаимодействии с приемной площадкой 6.
Кроме того, флакон 4 содержит крышку 46, например, оснащенную прокалываемой или самозатягивающейся мембраной 48, обеспечивающей прохождение пипеточных средств 10 автомата, например, пипетки. Этот прокалываемый и самозатягивающийся участок 48 позволяет, в частности, не снимать крышку 46 с флакона, чтобы произвести отбор клеточного раствора и, следовательно, обеспечить полную защиту и сохранить целостность раствора, который после отбора, произведенного врачом или лаборантом, остается в закрытом флаконе в течение всего процесса подготовки и анализа. Кроме того, это позволяет полностью устранить риск заражения или вдыхания фиксатора лаборантом.
Крышка 46 каждого флакона 4 дополнительно содержит визуальную маркировку 50 или идентификатор, предназначенный для идентификации клеточной суспензии 5, содержащейся во флаконе 4. Например, эта визуальная маркировка 50 представляет собой штрихкод. Этот идентификатор 50 обеспечивает полное отслеживание во время подготовки и анализа посредством компьютерной обработки номеров проб.
Согласно другим вариантам осуществления, средства идентификации являются другими, например, этикеткой с нанесенной на нее информацией или электронной микросхемой, типа микросхемы RFID, содержание которой можно считать дистанционно при помощи средств считывания.
Согласно варианту осуществления, предназначенному для подготовки цитологических проб, требующих применения щетки для взятия мазков, флакон 4 оборудован средствами 52 фильтрования, по меньшей мере, частично погруженными в суспензию, описанными в документе WO-2006/058989. Эти средства 52 фильтрования выполнены в виде сетки фильтрующего материала, например, образующей корзинку, периферия которой закреплена на корпусе 40 флакона, и центр которой соединен с трубкой 54, проходящей в направлении отверстия флакона, связанной со средствами удержания в положении во флаконе и выполненной с возможностью прохождения через нее средств 20 отбора клеточного раствора автомата под средствами фильтрования, в частности, пипетки 22 для всасывания суспензии.
Предпочтительно сетка фильтрующего материала представляет собой плетеный нейлон, обеспечивающий механическое действие отделения клеток во время трения щетки по материалу без повреждения пробы.
Кроме того, нижняя часть флакона 4 содержит декантационный конус 56.
Кроме того, как известно, флакон 4 содержит отверстие, предназначенное для введения съемной щетки для взятия цитологической пробы, закрепленной на рукоятке-манипуляторе. Отверстие флакона содержит упорные средства для щетки, позволяющие блокировать ее во флаконе и отделить ее от рукоятки.
Специалист может обратиться к этому документу для ознакомления с особенностями этого флакона, и поэтому его дальнейшее описание опускается. Такой флакон позволяет предохранять щетку, избегая помех или поломки иглы для отбора.
Согласно варианту осуществления, предназначенному для подготовки цитологических проб и не требующему применения щетки для взятия проб, например, для проб типа биопсии или сбора жидкостей, флакон 4 не оборудован ни центральной трубкой, ни средствами фильтрования.
Далее следует подробное описание системы 30 подготовки и анализа.
Как показано на фиг.5, система 30 подготовки и анализа предпочтительно содержит устройство 60 декантационного отложения клеток на аналитической пластинке. Такое устройство 60 декантационного отложения клеток на аналитической пластинке уже описано в документе FR-2917165, и специалист может обратиться к этому документу.
Это устройство 60 содержит, по меньшей мере, одну декантационную чашку 36, установленную над аналитической пластинкой 32, и абсорбирующий материал 62.
Аналитическая пластинка 32 содержит на конечной части средства 50 идентификации, например, визуальную маркировку типа штрихкода.
При помощи пипеточных средств 20 суспензию заливают в приемную камеру 64 декантационной чашки 36, которая расположена над аналитической пластинкой 32, и дно которой открыто и расположено напротив зоны отложения клеток аналитической пластинки 32. Дно камеры гидравлически сообщается с материалом 62, абсорбирующим жидкость-консервант или фиксатор для его постепенной абсорбции и для обеспечения равномерного декантационного отложения клеток на зону отложения клеток аналитической пластинки 32. Таким образом, получают равномерное клеточное отложение в течение короткого времени декантации.
Абсорбирующий материал 62 частично сжат декантационным прессом 66 между дном приемной камеры и аналитической пластинкой вокруг зоны клеточного отложения.
Как показано на фиг.5 и 6, система 30 подготовки и анализа содержит средства 70 измерения клеточной плотности в декантационной камере, чтобы получить аналитическую пластинку 32. Такие средства 70 измерения клеточной плотности описаны в документе FR 2922019, к которому специалист может обратиться для более полной информации.
Так, средства 70 измерения клеточной плотности содержат съемочную камеру 72, выполненную с возможностью получения изображений площадки 6, то есть содержимого декантационной камеры 64 и аналитической пластинки 32.
Кроме того, средства 70 измерения клеточной плотности содержат манжету 74, закрепленную вокруг камеры таким образом, чтобы при опускании съемочной камеры и ее размещения над декантационной камерой 64 для съемок изображений содержимого этой камеры манжета входила в контакт 74 с декантационным прессом 66 для получения темной камеры с обеспечением светонепроницаемости, чтобы оптимизировать качество съемки изображений.
Кроме того, средства 70 измерения клеточной плотности содержат средства освещения декантационной камеры, чтобы камера 72 могла производить измерение плотности. Эти средства освещения содержат, например, источник 76 света, закрепленный на камере 72. Когда камеру 72 опускают, источник 76 света максимально приближается к краю аналитической пластинки 32 для обеспечения оптимального пропускания света. При этом источник 76 света рассеивает свет в аналитической пластинке 32.
Средства 70 измерения клеточной плотности закреплены на втором подвижном роботизированном кронштейне над флаконами 4 площадок 6.
Согласно варианту, аналитические устройства этой системы 30 содержат, по меньшей мере, одну трубку 34 для отбора или аликвотирования и держатель 80, в который могут заходить трубки 34 для закрепления в неподвижном положении. Этот держатель 80 трубок 34 аликвотирования точно крепят на площадке 6, чтобы пипеточные средства 20 могли отбирать пробы цитологических растворов 5, содержащихся во флаконах 4, и выливать их в трубки 34 аликвотирования, при этом флаконы закреплены на той же площадке, что и трубки аликвотирования.
Две возможности, одна из которых соответствует декантационной чашке 36, установленной над аналитической пластинкой 32, и абсорбирующему материалу 62, а другая - трубке 34 отбора или аликвотирования, можно объединить на одном держателе для одновременного или смещенного во времени осуществления дополнительных действий систематически или во взаимосвязи с результатами анализа плотности на не окрашенной пластинке, что обеспечивает лучший контроль предшествующего анализу этапа.
Автомат 2 дополнительно содержит средства 90 дистанционного считывания, предназначенные для идентификации визуальной маркировки 32 флаконов 4. Эти средства 90 считывания содержат широкоугольную съемочную камеру и расположены над приемной площадкой 6. Эти средства 90 дистанционного считывания установлены на втором подвижном роботизированном кронштейне автомата, при этом указанный второй кронштейн перемещается над каждым флаконом 4, закрепленным на площадке 6, для считывания визуальной маркировки 50 или идентификатора, находящегося на крышке 46.
Съемочную камеру располагают таим образом, чтобы она могла считывать идентификационные данные 50 аналитической пластинки 32. Эти данные передаются, например, в компьютерную систему обработки, обеспечивающую качественный мониторинг множества аналитических пластинок и объединяющую информацию о слое клеточной пробы, находящемся на этой пластинке. Эти данные содержат, в частности, происхождение клеточной пробы, при этом маркировка аналитической пластинки связана с маркировкой флаконов 4.
Согласно предпочтительному варианту осуществления, камера 72 средств 70 анализа клеточной плотности позволяет считывать визуальные маркировки 50. Таким образом, средства 70 анализа клеточной плотности и средства 90 дистанционного считывания объединены, что дает выигрыш в пространстве.
Предпочтительно маркировки 50 ориентированы в точном и неизменном направлении после закрепления крышки на корпусе, что позволяет легко использовать средства 90 дистанционного считывания маркировок. Неизменную ориентацию можно обеспечить при помощи средств 44 блокировки флакона 4, описанных в документе EP-2111300.
За счет специальной направленности флаконов 4 эти средства 90 дистанционного считывания обеспечивают унитарное или множественное визуальное наблюдение этих флаконов с целью их унитарного или множественного соответствия с предусмотренной системой анализа (аналитические пластинки 32, трубки 34 для отбора или аликвотирования, аналитические чашки 36…), которая позиционирована неподвижно. Это значит, что средства 90 считывания позволяют считывать маркировку 50 только одного флакона или несколько маркировок одновременно. Это неподвижное позиционирование, которое соответствует, например, аналитическим пластинкам 32, расположенным в декантационном прессе 66, происходит в продолжении направляющих, описанных в документе EP-2111300 и служащих опорой для флаконов 4, таким образом, что площадка обеспечивает нормальное позиционирование флаконов 4 и пластинок 32 для средств дистанционного считывания, обеспечивающих унитарное или множественное считывание. Таким образом, можно осуществлять совместную обработку флаконов, что обеспечивает высокую скорость анализа.
Автомат дополнительно содержит не показанный процессор для сбора параметров, выбранных пользователем в зависимости от характера цитологической пробы, а также для управления роботизированными кронштейнами, пипеточными средствами 20, средствами 90 считывания, средствами 70 анализа клеточной плотности, кнопкой 14 (перемещениями, объемами проб, съемками при помощи камеры, источником света…).
Согласно варианту осуществления, автомат содержит также не показанный держатель, точно закрепленный на опоре 8 автомата 2 и содержащий флаконы с растворами, обычно используемыми для окрашивания или маркировки специфических элементов клеток, таких как ядра, цитоплазмы или другие элементы клетки. Этот держатель окрашивающих или «маркировочных» растворов позволяет осуществлять этапы окрашивания или маркировки на аналитических пластинках, часто применяемые специалистом. Этот этап окрашивания или маркировки осуществляют при помощи пипеточных средств 20, которые после размещения над флаконами с окрашивающими или маркировочными растворами отбирают необходимый объем, затем перемещаются над аналитическими пластинками, на которые пипеточные средства выливают свое содержимое.
Согласно варианту осуществления, система 30 анализа автомата 2 дополнительно содержит устройство реализации виртуальной пластинки пробы, описанное в документе FR-2931966 и содержащее съемочную камеру. Согласно варианту осуществления, используют ту же камеру, которую применяют для средств анализа и/или для средств считывания.
Таким образом, автомат содержит в данном случае единственную съемочную камеру, образующую средства 90 считывания, средства 70 анализа клеточной плотности и устройство реализации виртуальной пластинки, что позволяет получить выигрыш в месте.
Далее следует подробное описание способа подготовки и анализа этих суспензий при помощи описанного выше автомата 2 для случая подготовки аналитических пластинок 32.
Предварительно, отобрав предназначенные для подготовки и анализа клеточные пробы 5 и поместив их во флаконы 4, специалист окончательно закрывает флаконы 4 при помощи крышек 46. Действительно, способ подготовки и анализа этих суспензий в дальнейшем осуществляют без открывания флаконов 4.
В другом варианте осуществления в случае отбора цитологической пробы в виде пункции при помощи тонкой иглы (Fine Needle Aspiration) специалист может ввести клеточную пробу, проколов иглой самозатягивающуюся мембрану флакона, ни в один из моментов не открывая крышки.
Затем, после достаточного времени фиксирования клеток, например, не менее двух часов, специалист или пользователь загружает флаконы 4 с клеточными суспензиями 5 на загрузочную площадку 6, а также такое же количество емкостей системы 30 анализа, предпочтительно аналитических пластинок 32.
После этого он располагает абсорбирующий лист 62 на площадке 6 таким образом, чтобы каждая аналитическая пластинка 32 оказалась между загрузочной площадкой 6 и абсорбционным листом 62. В пресс 66 загружают множество декантационных чашек 36. Декантационный пресс 66 располагают над площадкой 6 таким образом, чтобы каждая декантационная чашка 36 находилась над аналитической пластинкой 32, как описано в документе FR-2917165.
Затем площадки 6 загружают в автомат 2 на его опору 8 и точно закрепляют при помощи взаимодополняющих средств 10, 12 позиционирования площадок 6 и опоры 8 автомата 2 и кнопки 14, которая фиксирует это положение, если оно является правильным.
Специалист или пользователь запускает программу, выбирает очень простые параметры в зависимости от числа и типа проб, размещенных на автомате и запускает процесс подготовки.
Средства 90 считывания идентифицируют визуальные маркировки 50 флаконов 4 и аналитических пластинок 32, что позволяет установить соответствие между флаконами 4, содержащими предназначенный для анализа клеточный раствор, и подготавливаемыми аналитическими пластинками 32.
Средства 20 отбора перемещают над флаконом 4, содержащим предназначенный для анализа клеточный раствор 5. Игла или пипетка 22 средств 20 отбора проходит через самозатягивающуюся мембрану 48 крышки 46 флакона 4 и погружается в клеточную суспензию.
После этого при помощи пипетки 22 средств 20 отбора осуществляют отбор пробы клеточной суспензии из флакона 4.
Для этого клеточную суспензию 5 перемешивают в аналитическом флаконе 4 при помощи пипетки 22 пипеточных средств 20 посредством всасывания/отбора первого объема клеточного раствора, затем посредством нагнетания/введения первого объема в клеточный раствор, как показано стрелкой F на фиг.7. Предпочтительно первый объем по существу составляет от 50 мкл до 2000 мкл клеточного раствора. Целью этого этапа является дробление/разрушение клеточных скоплений предназначенной для анализа цитологической пробы 5 на стенке декантационного конуса 56 флакона 4. Кроме того, клетки, повторно вводимые во флакон, проходят над средствами фильтрования для разрушения клеточных скоплений, размер которых превышает размер ячеек фильтра, что позволяет осуществить второе фильтрование пробы и повторный перевод пробы во взвешенное состояние.
После этого производят первую декантацию клеточного раствора в течение первого интервала времени. Предпочтительно первый интервал времени по существу составляет от 5 минут до 12 часов в зависимости от выбранного способа анализа, например, равен 15 минутам для подготовки аналитической пластинки. Этот этап позволяет установить градиент между предназначенными для анализа клетками и воспалительными или геморрагическими клетками, что является дифференциальной декантацией.
Затем осуществляют этап всасывания растворов, которые в дальнейшем заливают в аналитическую емкость. Этот этап содержит i) всасывание объема клея пипеточными средствами для обеспечения сцепления клеток с аналитической пластинкой 32 независимо от ее типа или объема буферного раствора, ii) в случае необходимости, объема воздуха, как описано в документе FR 2919054, затем iii) объема клеточного раствора на дне декантационного конуса 56, содержащего необходимые так называемые релевантные клетки, то есть клетки, находящиеся в нижней части раствора в результате первой дифференциальной декантации.
Предпочтительно объемы клея и клеточного раствора являются эквивалентными и по существу составляют от 50 мкл до 1000 мкл, например, 250 мкл.
В варианте осуществления с трубками для аликвотирования объем клея является нулевым.
Предпочтительно этот последний этап отбора объема клеточного раствора осуществляют в два подэтапа: первый подэтап, называемый «микросмешиванием», затем второй подэтап всасывания необходимого объема клеточного раствора.
«Микросмешивание» состоит во всасывании объема цитологического раствора непосредственно над дном декантационного конуса флакона, например, на высоте 2 мм, при этом объем составляет от 20 мкл до 200 мкл, например, 100 мкл, после чего пипеточные средства опять нагнетают часть отобранного объема, например, 50 мкл, по существу в то же место, чтобы избежать образования «мертвого объема или дна» 100, то есть для отделения клеток от дна декантационного конуса 56 за счет силы нагнетания пипеточных средств 20 и для исключительно локального повторного перевода во взвешенное состояние.
Этот этап «микросмешивания» является факультативным, и его можно заменить простым этапом отбора объема цитологического раствора.
Использование клея, предназначенного для сцепления клеток с аналитическими пластинками 32, позволяет использовать пластинки, не прошедшие специальной обработки для сцепления клеток, и сократить, таким образом, расходы на подготовку и анализ цитологических растворов.
Например, отбирают 250 мкл клея и 100 мкл цитологического раствора, содержащего нужные клетки, затем повторно нагнетают 50 мкл пробы цитологического раствора, содержащейся в пипетке, и отбирают 200 мкл цитологического раствора, чтобы получить одинаковое количество клея или буфера и необходимых клеток.
После этого пипетка 22 автоматически приводится в движение для однородного перемешивания ее содержимого, то есть клея или буфера и пробы цитологического раствора, как описано в документе FR 2919054. Этот этап позволяет также разбавить и перевести в однородную суспензию пробу в клее или буфере при помощи способа разбавления, описанного в документе FR-2919054.
В другом варианте осуществления в буферный раствор можно добавить маркеры или красители.
Затем пипеточные средства 20 помещают над декантационной чашкой 36, чтобы залить/ввести пробу в декантационную камеру 64 и реализовать аналитическую пластинку 32, содержащую предназначенный для анализа тонкий клеточный слой. Клеточный слой получают в результате введения пробы в декантационную чашку, как описано в документе FR-2917165, к которому специалист может обратиться для более полной информации.
На пластинке в течение второго интервала времени происходит вторая декантация. Предпочтительно второй интервал времени по существу составляет от 5 до 60 минут и предпочтительно равен 15 минутам для подготовки аналитической пластинки.
Этапы отбора и реализации пластинки 32 повторяют для каждого анализируемого флакона, дифференцированно отбирая патологические и релевантные клетки, необходимые специалисту-цитологу для диагноза.
Затем осуществляют описанный, например, в документе FR-2 922 019 этап анализа клеточного отложения на дне декантационных чашек 36 путем измерения клеточной плотности на аналитических пластинках 32, чтобы предложить предшествующий анализу контроль для всех проб, предназначенных для цитологического анализа или для дополнительных биологических исследований. Этот этап позволяет определить, достаточно ли клеток содержит клеточный раствор, чтобы получить удовлетворительное клеточное отложение с целью надежного диагноза и чтобы автоматически скорректировать пробу для получения клеточной плотности, необходимой для анализа пластинки 32. Этот этап обеспечивает качественный мониторинг аналитической пластинки 32, приготовленной на основе клеточного раствора 5.
Согласно варианту осуществления, за этим этапом анализа отложения клеток следует этап автоматического окрашивания или маркировки.
Согласно варианту осуществления, пипеточные средства 20 содержат множество иголок, предпочтительно четыре или восемь, позволяющих готовить и анализировать множество клеточных суспензий параллельно и повысить, таким образом, скорость подготовки аналитических пластинок.
Автомат в соответствии с изобретением позволяет автоматически обрабатывать мазки и другие цитологические пробы в тонком слое.
Одним из преимуществ автомата 2 в соответствии с изобретением является то, что он является полностью замкнутым, начиная с флакона 4 и до аналитической пластинки 32, что обеспечивает целостность всех цитологических растворов и проб и позволяет избежать рисков заражения и обеспечить безопасность для специалиста (он не вдыхает фиксатор). Это преимущество связано также с использованием флакона, объединяющего одновременно средства фильтрования и средства декантации для получения тонкого слоя цитологической пробы.
Кроме того, в отличие от автоматов, описанных в документе US 2009/0233331, флаконы 4 являются неподвижными на опоре автомата 2, и над флаконами 4 перемещаются другие системы, такие как пипеточные средства 20, средства 70 считывания и средства 90 анализа плотности, что обеспечивает полную безопасность манипулирования в лаборатории.
Кроме того, он позволяет добиться большей стандартизации. Действительно, отбор всех проб происходит:
- в одном месте с допуском в десятую миллиметра в декантационных конусах флаконов, благодаря точному и неподвижному позиционированию площадок, содержащих флаконы и другие емкости (аналитические пластинки, трубки аликвотирования, декантационные чашки);
- в одинаковом количестве с допуском в один микролитр, благодаря пипеточным средствам; и
- в одно время, так как отбор всех проб осуществляют в ходе одного процесса. Кроме того, обеспечивается полный контроль во время анализа за счет компьютерной обработки номеров проб, благодаря визуальным маркировкам 50, нанесенным на крышки флаконов, которые приводят в соответствие с маркировками емкостей для подготовки, таких как аналитические пластинки, при помощи средств дистанционного считывания этих визуальных маркировок.
Способ коррекции клеточной плотности, применяемый автоматом для реализации аналитических пластинок, позволяет, в случае необходимости, увеличить относительную плотность патологических клеток, сохраняя при этом чистый, но информативный контекст анализа и повышая качество тонкого слоя и улучшая консервацию выбранных элементов. Это обеспечивает более надежную интерпретацию по сравнению с традиционной технологией и полуавтоматическими способами цитологического анализа в тонком слое.
Кроме того, автоматическая подготовка флакона или одновременно группы флаконов позволяет существенно, на 90%, сократить время технической подготовки по сравнению с традиционной технологией и полуавтоматическими способами цитологического анализа в тонком слое.
Наконец, автоматизация позволяет получить реальную систему, обеспечивающую качество и стандартизацию отложения пробы в виде тонкого слоя, воспроизводимость тонкого слоя пробы, сохранение клеточной целостности и облегченное считывание. Она позволяет также существенно сократить технологические расходы и стоимость считывания.

Изобретение относится к способу подготовки и анализа множества клеточных суспензий, содержащий, по меньшей мере, следующие последовательные этапы, на которых: (a) загружают множество флаконов на приемную площадку, при этом каждый флакон содержит предназначенную для анализа клеточную суспензию; (b) загружают множество аналитических емкостей на приемную площадку; и (c) отбирают из флакона пробу клеточной суспензии и вводят ее в аналитическую емкость; этап (с) повторяют для каждого анализируемого флакона; (d) повторно переводят пробу в суспензию; (e) выбирают релевантные клетки посредством дифференциальной декантации; (f) производят всасывание объема, полученного в результате дифференциальной декантации, при помощи пипеточных средств, при этом объем содержит предназначенную для анализа пробу. При этом способ характеризуется тем, что этап (с) отбора пробы клеточной суспензии из флакона и введения этой пробы в аналитическую емкость содержит, по меньшей мере, этап разрушения клеточных скоплений при помощи пипеточных дозировочных средств, причем этап (f) всасывания объема включает в себя этап «микросмешивания», который состоит во всасывании объема клеточной суспензии непосредственно над дном декантационного конуса флакона с последующим повторным нагнетанием части отобранного объема по существу в то же место. Также изобретение относится к устройству. Предлагаемый способ является надежным, репродуктивным и быстрым и позволяет полностью автоматизировать подготовку и анализ цитологических суспензий. 2 н., 21 з.п. ф-лы, 7 ил.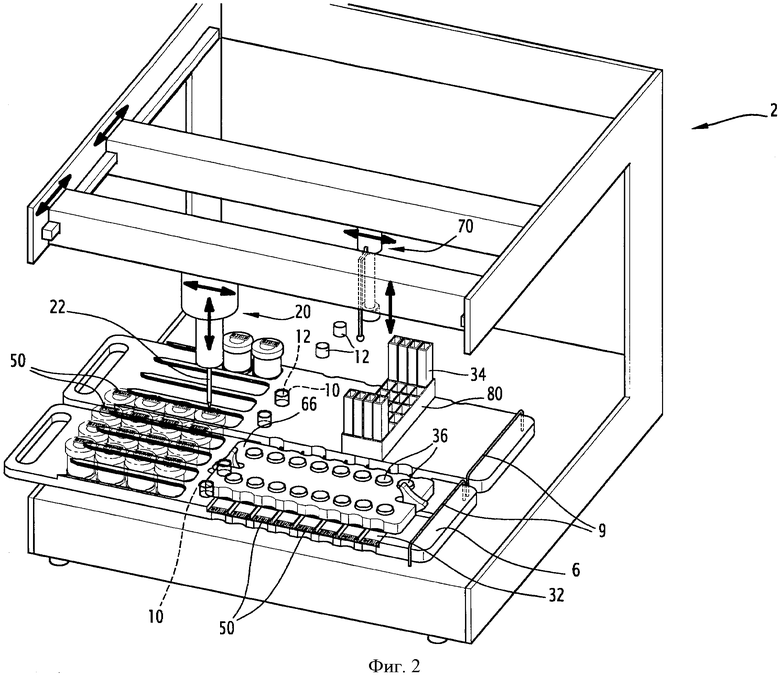
1. Способ подготовки и анализа множества клеточных суспензий (5), содержащий, по меньшей мере, следующие последовательные этапы, на которых:
(a) загружают множество флаконов (4) на приемную площадку (6), при этом каждый флакон (4) содержит предназначенную для анализа клеточную суспензию (5);
(b) загружают множество аналитических емкостей (32, 34, 36) на приемную площадку (6); и
(c) отбирают из флакона (4) пробу клеточной суспензии (5) и вводят ее в аналитическую емкость (34, 36);
этап (с) повторяют для каждого анализируемого флакона (4);
(d) повторно переводят пробу в суспензию;
(e) выбирают релевантные клетки посредством дифференциальной декантации;
(f) производят всасывание объема (100), полученного в результате дифференциальной декантации, при помощи пипеточных средств (20), при этом объем (100) содержит предназначенную для анализа пробу;
при этом указанный способ отличается тем, что этап (с) отбора пробы клеточной суспензии из флакона (4) и введения этой пробы в аналитическую емкость (34, 36) содержит, по меньшей мере, этап разрушения клеточных скоплений при помощи пипеточных дозировочных средств (20), причем этап (f) всасывания объема включает в себя этап «микросмешивания», который состоит во всасывании объема клеточной суспензии непосредственно над дном (56) декантационного конуса флакона (4) с последующим повторным нагнетанием части отобранного объема по существу в то же место.
2. Способ по п. 1, отличающийся тем, что этап (с) отбора пробы клеточной суспензии из флакона (4) и введения этой пробы в аналитическую емкость (34, 36) содержит, по меньшей мере, этап перемешивания и фильтрования клеточной суспензии во флаконе (4).
3. Способ по п. 1 или п. 2, отличающийся тем, что этап (с) отбора пробы клеточной суспензии (5) из флакона (4) и введения этой пробы в аналитическую емкость (34, 36) дополнительно содержит, по меньшей мере, следующие этапы, на которых:
(g) повторно переводят объем (100), содержащий предназначенную для анализа пробу, в однородную суспензию в пипеточных средствах (20);
(h) перемещают пипеточные средства (20) для их размещения над аналитической емкостью (34, 36);
(i) выливают предназначенную для анализа пробу в аналитическую емкость (34, 36).
4. Способ по п. 1, отличающийся тем, что каждая аналитическая емкость содержит декантационную чашку (36) и аналитическую пластинку (32), расположенную напротив декантационной чашки (36), при этом способ содержит, по меньшей мере, следующие последовательные этапы, на которых:
(j) размещают абсорбционный лист (62) на загрузочной площадке (6) таким образом, чтобы каждая аналитическая пластинка (32) располагалась между загрузочной площадкой (6) и абсорбционным листом (62);
(k) загружают множество декантационных чашек (36) в пресс (66) и устанавливают пресс (66) над площадкой (6) таким образом, чтобы каждая декантационная чашка (36) располагалась сверху и напротив аналитической пластинки (32); и
(l) наносят тонкий слой клеточной пробы на аналитическую пластинку (32), причем нанесение тонкого слоя клеточной пробы происходит в результате введения пробы в декантационную чашку (36);
при этом этапы (j) и (k) осуществляют после этапа (b) загрузки множества аналитических емкостей и перед этапом (с) отбора пробы клеточной суспензии (5), а этап (l) осуществляют после этапа (с) отбора пробы клеточной суспензии (5).
5. Способ по п. 4, отличающийся тем, что содержит этап анализа клеточного отложения на дне декантационных чашек (36) посредством измерения клеточной плотности на аналитических пластинках (32).
6. Способ по п. 1, отличающийся тем, что содержит автоматизированный этап окрашивания или маркировки клеток.
7. Способ по п. 1, отличающийся тем, что предварительно содержит этап окончательного закрывания флакона (4), содержащего предназначенную для анализа клеточную суспензию (5), при этом способ осуществляют без последующего открывания флакона (4).
8. Способ по п. 1, отличающийся тем, что каждая аналитическая емкость содержит трубку (34) для отбора или для аликвотирования.
9. Автомат (2) для подготовки и анализа, по меньшей мере, одной клеточной суспензии (5), содержащий:
- по меньшей мере, один флакон (4), содержащий предназначенную для анализа клеточную суспензию (5);
- по меньшей мере, одну приемную площадку (6), на которой установлен и точно и неподвижно закреплен флакон (4);
- по меньшей мере, одну чашку (36) для декантации клеточной суспензии (5), при этом декантационная чашка (36) расположена и закреплена точно и неподвижно на площадке (6);
- систему (30) анализа, содержащую, по меньшей мере, одну аналитическую пластинку (32), выполненную с возможностью размещения/удержания на ней пробы клеточной суспензии (5), при этом проба является объемной частью клеточной суспензии (5), содержащей соответствующие предназначенные для анализа элементы, и аналитическую пластинку (32), расположенную и закрепленную точно и неподвижно на площадке (6) снизу и напротив декантационной чашки (36);
при этом автомат (2) отличается тем, что содержит пипеточные средства (20), выполненные с возможностью отбора пробы клеточной суспензии (5) из флакона (4) и выливания этой пробы в декантационную чашку (36) на аналитическую пластинку (32) системы (30) анализа, причем эти средства (20) выполнены с возможностью разрушения клеточных скоплений и с возможностью отбора объема клеточной суспензии (5) из одного места и его повторного нагнетания по существу в то же место.
10. Автомат по п. 9, отличающийся тем, что содержит первый подвижный кронштейн, на котором закреплены пипеточные средства (20), при этом указанный кронштейн перемещается, по меньшей мере, над приемной площадкой (6), на которой расположены флаконы (4), декантационные чашки (36) и аналитические пластинки (32).
11. Автомат по п. 9 или 10, отличающийся тем, что содержит растворы для маркировки или окрашивания, которые можно смешать с цитологическим раствором при помощи пипеточных средств (20).
12. Автомат по п. 9, отличающийся тем, что каждый флакон (4) и каждая аналитическая пластинка (32) содержит визуальную маркировку (50), причем автомат содержит средства (90) считывания визуальных маркировок (50).
13. Автомат по п. 12, отличающийся тем, что средства (90) считывания содержат съемочную камеру и установлены на втором подвижном кронштейне, выполненном с возможностью перемещения, по меньшей мере, над приемной площадкой (6), на которой расположены флаконы (4), декантационные чашки (36) и аналитические пластинки (32).
14. Автомат по п. 9, отличающийся тем, что флакон (4) содержит средства (52) фильтрования, расположенные над декантационным конусом (56), при этом пипеточные средства (20) выполнены с возможностью отбора части клеточной суспензии (5) под средствами (52) фильтрования и повторного направления указанной части на декантационный конус (56)для перемешивания указанной клеточной суспензии (5) и, по меньшей мере, одноразового пропускания части указанной клеточной суспензии (5) через средства (52) фильтрования для разрушения клеточных скоплений, размер которых превышает размер ячеек фильтра.
15. Автомат по п. 9, отличающийся тем, что система (30) анализа пробы содержит средства (70) анализа клеточной плотности клеточных отложений на дне декантационной чашки (36) на аналитической пластинке (32).
16. Автомат по п. 15, отличающийся тем, что средства (70) анализа клеточной плотности клеточных отложений на дне декантационной чашки (36) на аналитической пластинке (32) содержат съемочную камеру (72).
17. Автомат по п. 9, отличающийся тем, что система (30) анализа пробы содержит устройство для получения виртуальной пластинки пробы.
18. Автомат по п. 17, отличающийся тем, что устройство для получения виртуальной пластинки пробы содержит съемочную камеру.
19. Автомат по п. 9, отличающийся тем, что содержит единственную съемочную камеру, образующую средства (90) считывания, средства (70) анализа клеточной плотности и устройство получения виртуальной пластинки.
20. Автомат по п. 9, отличающийся тем, что содержит опору, содержащую средства (9, 12) позиционирования, по меньшей мере, площадки (6), выполненные с возможностью неподвижного и точного крепления площадки, и кнопку (14), выполненную с возможностью подтверждения положения, по меньшей мере, площадки (6).
21. Автомат по п. 9, отличающийся тем, что выполнен с возможностью применения способа по любому из пп. 1-7.
22. Автомат по п. 9, отличающийся тем, что клеточная суспензия (5) является цитологической суспензией.
23. Автомат по п. 22, отличающийся тем, что цитологическая суспензия содержит фиксирующий раствор, содержащий от 80% до 95% по объему:
- 590 мл физиологического раствора,
- 10 мл ПЭГ,
- 203 мл изопропилового спирта,
- 193 мл чистого этилового спирта,
- 0,01% по объему азида натрия,
и от 20% до 5% по объему 4%-го буферного формалина.
| WO 2008104710 A2, 04.09.2008 | |||
| EP 0527059 A1, 10.02.1993 | |||
| HUMAN CELL CULTURE, VOLUME VII: HUMAN ADULT STEM CELLS, EDITED BY, JOHN R | |||
| MASTERS, P | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| УСТРОЙСТВА ДЛЯ АВТОМАТИЧЕСКОГО ПРОВЕДЕНИЯ ИММУНОАНАЛИЗА ЗА НЕСКОЛЬКО ПОСЛЕДОВАТЕЛЬНЫХ ЭТАПОВ ПО МЕНЬШЕЙ МЕРЕ ОДНОГО БИОЛОГИЧЕСКОГО ВЕЩЕСТВА ИЗ МНОЖЕСТВА БИОЛОГИЧЕСКИХ ОБРАЗЦОВ, СПОСОБ И РЕАКТИВ ДЛЯ ПРИМЕНЕНИЯ УКАЗАННЫХ УСТРОЙСТВ | 1990 |
|
RU2102758C1 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОЙ ЗАГРУЗКИ ПРОБ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2004 |
|
RU2365920C2 |
Авторы
Даты
2015-07-20—Публикация
2011-03-21—Подача