Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии, и может быть использовано для консервации, стерилизации и модификации биологического материала при изготовлении биопротезов сосудов и клапанов сердца.
При разработке кардиоваскулярных протезов особое значение придают физико-механическим характеристикам биоматериала, таким как прочность и эластичность, которые оценивают по значениям разрушающего напряжения и относительного удлинения при растяжении. Помимо механических характеристик биопротезы клапанов сердца и артерий должны обладать тромборезистентными свойствами, поскольку находятся в постоянном контакте с кровью. Мономерные эпоксисоединения, в частности диглициловый эфир этиленгликоля (ДЭЭ), на сегодняшний день успешно применяют для консервации кардиоваскулярных биологических протезов. Однако поиск более перспективных консервантов не теряет своей актуальности.
Известен способ консервации биоткани для сердечно-сосудистой хирургии, основанный на использовании консервирующего раствора диглицидилового эфира этиленгликоля (ДЭЭ) (Пат. 2008767, Рос. Федерация: МПК A01N 1/00. Способ консервирования биоткани для протезирования клапанов сердца и сосудов [Текст] / Л.С. Барбараш, С.П. Новикова, И.Ю. Журавлева и др.; патентообладатель Барбараш Л.С. (RU). - №5024513/14; заявл. 23.01.92; опубл. 15.03.94). Способ позволяет добиться высокой плотности поперечной сшивки и достаточного стерилизующего эффекта. Однако концентрация ДЭЭ на стандартном фосфатном буферном растворе снижается к 21 суткам с 5 до 0,7%. При этом pH раствора ДЭЭ к 9-м суткам достигает 11,5-12 (по сравнению с исходной 7,4-7,5), что может оказать неблагоприятное воздействие на структуру коллагена. Осмотическое давление раствора, приготовленного в соответствии с данным способом, составляет 140-145 мОсм/л, что в 2 раза ниже осмолярности плазмы крови. Низкое осмотическое давление и щелочная среда (pH 11,5-12) консервирующего и стерилизующего раствора на фосфатном буфере вызывают отек створчатой и мышечной части аортального комплекса.
Известен способ консервации и стерилизации биологических протезов, включающий обработку биоматериала раствором диглицидилового эфира этиленгликоля при температуре 5-25°C в течение 2-21 суток, при этом в качестве основы консервирующего раствора используют 0,05-0,1 M фосфат-тетраборатный буфер pH 7,4, а стерилизующий эффект обеспечивают за счет добавления 1-15%-го этилового спирта (Пат. 2350075, Рос. Федерация: МПК A01N 1/02, A61L 27/00. Способ консервации и стерилизации биологических протезов для сердечно-сосудистой хирургии [Текст] / И.Ю. Журавлева, Л.С. Барбараш, Ю.А. Кудрявцева, И.Л. Гантимурова; патентообладатель Журавлева И.Ю. (RU). - №2007125733/15; заявл. 06.07.07; опубл. 27.03.09, Бюл. 9. - 5 с.). Данная технология оказывает стерилизующий эффект за счет воздействия на биоматериал малыми концентрациями этилового спирта. Однако консервация мономерным ДЭЭ ограничивает возможность дополнительной модификации биопротезов, а прочностные свойства ДЭЭ-обработанного биоматериала значительно уступают прочности нативной ткани.
Известен способ стерилизации и консервации биологических протезов для сердечно-сосудистой хирургии (заявка WO 9209309: МПК A01N 43/20, A61L 2/00, A61L 2/18 Method of liquid sterilization [Текст] / TU Roger (US); Thyagarajan Kalathi (US); Myers Harriet Chan (US); заявитель и правообладатель Baxter int (US). - PCT/US91/08900; заявл. 25.11.91; опубл. 11.06.92). Сущность способа заключается в том, что для стерилизации биологических протезов используют 2-4%-ный раствор полиэпоксидных соединений, приготовленный на 0,1 М карбонатном буфере при pH 9,5-10,0. Для усиления стерилизующего эффекта в раствор полиэпоксидных соединений добавляют до 20 частей этанола, при этом наибольший стерилизующий эффект достигают при температуре раствора от 37°C до 45°C и добавлении 20% этанола. К основным недостаткам известного способа можно отнести: применение высоких температур раствора; использование буферного раствора со щелочным значением pH, превышающим физиологическое; добавление 20% этанола, что в конечном итоге оказывает дубящее воздействие на биологическую ткань, придавая ей ригидные свойства. Все это может неблагоприятно сказаться на структурной стабильности биоматериала и привести к дисфункции протеза после имплантации.
Наиболее близким к заявляемому является способ обработки биологических протезов, при котором нативную ткань от свежезабитых животных обрабатывают смесью эпоксисоединений при температуре 4-45°C в течение 2-21 суток с последующей обработкой раствором гепарина с концентрацией не менее 75 ед/мл при температуре 20-45° в течение 2-16 ч и этилированием 70%-ным водным раствором этанола (Пат. 2122321 Рос. Федерация: МПК A01N 1/02, Способ обработки биологических протезов для сердечно-сосудистой хирургии [Текст] / И.Ю. Журавлева, Л.С. Барбараш, С.П. Новикова, И.Л. Гантимурова; заявитель Кемеровский кардиологический центр (RU); патентообладатель Журавлева И.Ю. (RU). - №96104575/14; заявл. 06.03.96; опубл. 27.11.98). К недостаткам известного способа можно отнести использование продуктов перегонки ДЭЭ, которые обладая токсическим действием, повреждают клетки биологической ткани. К тому же обработка ксенобиопротезов, предварительно модифицированных гепарином, в растворе 70%-го этилового спирта приводит к вымыванию антикоагулянта и ригидности биоматериала, что ухудшает его биомеханические характеристики.
Техническим результатом предлагаемого изобретения является улучшение упругоэластичных и тромборезистентных характеристик биологического протеза, а также увеличение стерилизующего эффекта и устойчивости биоматериала к кальцификации.
Технический результат достигается за счет дополнительного введения в раствор консерванта диглицилового эфира этиленгликоля олигоэпоксисоединений с разветвленной структурой углеводородной цепи и увеличенным количеством реакционно-способных эпоксигрупп, что позволяет дополнительно модифицировать биологическую ткань, придавая ей заданные свойства. Кроме того, технический результат достигается за счет использования в растворе консерванта буферного раствора с осмолярностью соответствующей таковой плазмы крови.
Известно, что при консервации биологических тканей раствором мономерных эпоксисоединений основная часть реакционно-способных эпоксигрупп вступает в реакцию с аминокислотами коллагеновой матрицы, что существенно снижает возможность дальнейшей иммобилизации биологически-активных веществ на поверхности биоматериала. Включение же в состав консерванта олигоэпоксисоединений позволит не только увеличить прочность и эластичность биоматериала за счет усиления химической сшивки коллагеновых волокон, но и улучшить антитромботические характеристики раствора за счет вовлечения дополнительных реакционных эпоксигрупп в процесс модификации биотканей и увеличения количества иммобилизированного гепарина на поверхности биопротеза.
На основании проведенных исследований, включающих анализ влияния эпоксидных консервантов на структуру поверхности ксеногенного биоматериала, из синтезированных оригинальных композиций была выбрана 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопираноза (ПЭ), при оптимальном соотношении эпоксида в смеси от 5 до 30 частей.
В качестве растворителя консервантов использовали раствор 0,05-0,2 M фосфатного буфера, приготовленного на 0,9% растворе натрия хлорида (NaCl). Значение pH полученного буферного раствора составляло 7,3-7,4, а осмолярность 280-300 мОсм/л, что аналогично осмолярности плазмы крови. Данные показатели позволяют обеспечить сохранность коллагеновых волокон, избежать отека биологической ткани и, как следствие, предупредить дисфункцию биопротезов после имплантации пациентам.
Приготовление фосфатного буфера осуществляли из концентрата №1 (натрий фосфорнокислый двузамещенный - 12 водный марки «хч - химически чистый») и концентрата №2 (натрий фосфорнокислый однозамещенный одноводный марки - «хч - химически чистый») предварительно растворенных в 0,9%-ном растворе натрия хлорида. При этом для приготовления 1 л буфера использовали 120 мл концентрата №1 и 880 мл концентрата №2.
Консервирующий раствор изготавливали следующим образом: каждый из консервантов предварительно растворяли в 250 мл буферного раствора, затем размешивали и доводили объем консерванта до 1 литра буферным раствором, при этом соотношение частей ДЭЭ:ПЭ в консерванте составляло 95-70:5-30 соответственно.
Консервацию и стерилизацию биологического материала предложенным раствором осуществляли при температуре 5-25°C в течение 5-21 суток. После чего биопротезы подвергали модификации в растворе нефракционированных и низкомолекулярных гепаринов в концентрации 75-150 Едмл, таких как Эноксапарин натрия (Клексан), Надропарин (Фраксипарин), Дальтепарин (Фрагмин), Ревипарин (Кливарин), Бемипарин натрий (Цибор). Гепаринизацию выполняли при температуре от 20 до 40°C в течение 2-14 часов. Проведение модификации при температуре ниже 20°C не целесообразно, т.к. значительно увеличивается время гепаринизации, а при температуре выше 40°C возникает возможность термического поражения тканей.
Для изучения влияния предлагаемого способа предимплантационной обработки биопротезов на структуру биоматериала было проведено гистологическое исследование створок аортального клапана свиньи, перикарда и артерий крупного рогатого скота, консервированных в опытных растворах. При визуализации гистологических образцов тканей с помощью электронной микроскопии доказано, что хранение биоматериала, обработанного предложенным консервантом, не оказывает негативного воздействия на биоматериал - коллагеновые волокна извиты, расположены более компактно по сравнению с использованием раствора ДЭЭ. А плотность расположения коллагеновых волокон увеличивается в ряду ДЭЭ < ДЭЭ + 5% ПЭ < ДЭЭ + 15% ПЭ < ДЭЭ + 30% ПЭ.
Оценка прочности и эластичности биоматериала показала, что применение консервирующих растворов, содержащих смесь ДЭЭ от 95-70% и олигоэпоксисоединения 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозы от 5% до 30%, повышает прочность на 10-62% и не оказывает негативного влияния на эластичность биоматериала (табл. 1).

Использование олигоэпоксисоединений в консервирующем растворе позволяет связывать биологически активные вещества, имеющие амино-, кабокси- или гидроксигруппы, при этом сохраняется высокий антикальцинозный эффект. Количество кальция в экспериментальных исследованиях в течение трех месяцев остается на метаболическом уровне (табл. 2).

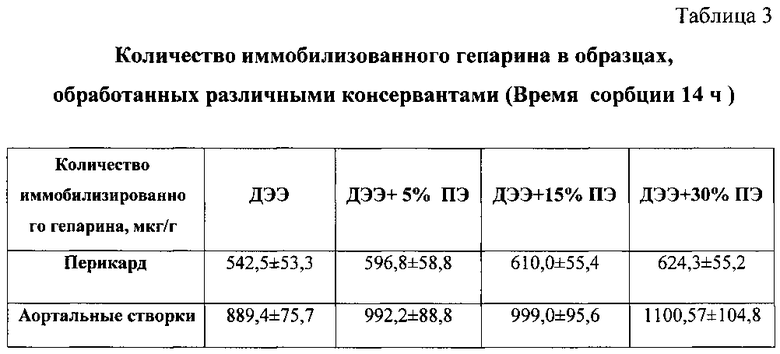
Кроме того, применение 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозы и выполнение гепаринизации образцов после этапа консервации позволяет увеличить количество иммобилизованного гепарина на поверхности биоматериала (табл. 3).
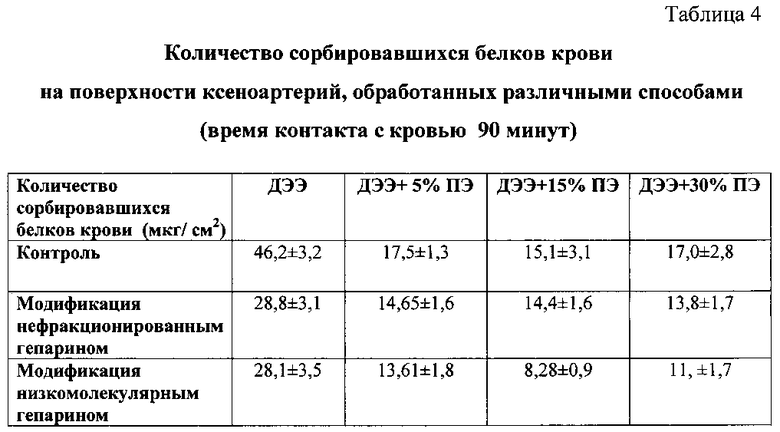
Исследование тромборезистентности биоматериала выполняли после контакта образцов с нативной кровью в течение 90 минут. Полученные результаты свидетельствуют, что добавление в состав консервирующего раствора от 5% до 30% 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозы значительно снижет количество адсорбированных на поверхности биоматериала белков крови, особенно после модификации образцов в растворе низкомолекулярного гепарина (табл. 4).
Увеличение тромборезистентных свойств биоматериала обусловлено не только увеличением сорбции гепарина, но и сглаживанием рельефа поверхности биоткани за счет более плотной сшивки коллагеновых волокон в процессе консервации биоматериала.
Предложенный способ оказывает хороший стерилизующий эффект - через сутки хранения биоматериала, контаминированного St. aureus, E. coli Ent. faecalis и грибковой флорой в растворе, приготовленном по предложенному способу, рост всех микрооганизмов полностью подавляется.
Сущность изобретения поясняется чертежами, где изображены результаты сканирующей электронной микроскопии внутренней поверхности ксеноартерий, при увеличении ×1000. При этом на фиг. 1 представлен образец, обработанный 5%-ным раствором ДЭЭ; на фиг. 2 - образец, обработанный раствором эпоксисоединений, содержащим 70% ДЭЭ + 30% ПЭ; на фиг. 3 - образец, обработанный раствором эпоксисоединений, содержащим 70% ДЭЭ + 30% ПЭ с дополнительной модификацией в растворе Эноксапарина натрия.
При изучении биоматериала наблюдали изменение рельефа поверхности биоматериала, его сглаживание. Добавление в раствор консерванта олигоэпоксисоединения усиливает химическую сшивку коллагеновых волокон в процессе консервации биоматериала за счет разветвленной структуры углеводородной цепи, что оказывает влияние и на рельеф поверхности биоткани - она становится более сглаженной фиг. 2. Последующая модификация в растворе низкомолекулярного гепарина фиг. 3 позволяет усилить сглаживающий эффект на рельеф поверхности биоткани, что в совокупности с антикоагулянтными свойствами гепарина значительно увеличивает тромборезистентность биопротезов.
Ниже приведены примеры осуществления предлагаемого способа.
Пример 1. Подготовленную по существующим методикам отбора нативные артерии ткань промывают 0,9%-ным раствором натрия хлорида, затем помещают в 2-5%-ный раствор, содержащий 95% ДЭЭ и 5% 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозы, приготовленный на 0,05-0,2 М фосфатном буфере на 0,9%-ном NaCl. По истечении 5-21 суток консервации биопротезы отмывают от консервирующего раствора трижды по 20 минут в избытке физ. раствора и погружают в раствор низкомолекулярного гепарина Эноксапарина натрия с концентрацией 75 ЕД/мл и температурой 20-40°C на 2-14 часов. Использование концентрации раствора гепарина менее 75 Ед/мл увеличит время модификации, а использование концентрации более 150 Ед/мл также нецелесообразно, т.к. количество присоединяемого препарата не увеличивается, а лишь повышается расход низкомолекулярного гепарина.
Пример 2. Подготовленную по существующим методикам отбора нативные створки клапана сердца промывают 0,9%-ным раствором натрия хлорида, затем помещают в 2-5%-ный раствор, содержащий 85% ДЭЭ и 15% 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозы, приготовленный на 0,05-0,2 М фосфатном буфере на 0,9%-ном NaCl. По истечении 5-21 суток консервации биопротезы отмывают от консервирующего раствора трижды по 20 минут в избытке физ. раствора и погружают в раствор низкомолекулярного гепарина Бемипарин натрий с концентрацией 100 ЕД/мл и температурой 20-40°C на 2-14 часов.
Пример 3. Подготовленную по существующим методикам отбора нативный ксеноперикард промывают 0,9%-ным раствором натрия хлорида, затем помещают в 2-5%-ный раствор, содержащий 70% ДЭЭ и 30% 1,2,3,4,6-пента-O-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозы, приготовленный на 0,05-0,2 М фосфатном буфере на 0,9%-ном NaCl. По истечении 5-21 суток консервации биопротезы отмывают от консервирующего раствора трижды по 20 минут в избытке физ. раствора и погружают в раствор низкомолекулярного гепарина Дальтепарин с концентрацией 150 ЕД/мл и температурой 20-40°C на 2-14 часов.
Таким образом, предложенный способ предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии позволяет увеличить прочность биоматериала, обеспечивает устойчивость к кальцификации биоткани и стерилизующий эффект, а использование низкомолекулярных гепаринов позволяет сглаживать рельеф поверхности и увеличивает тромборезистентность биопротезов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНСЕРВИРОВАНИЯ БИОТКАНИ ДЛЯ ПРОТЕЗИРОВАНИЯ КЛАПАНОВ СЕРДЦА И СОСУДОВ | 1992 |
|
RU2008767C1 |
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОГО ХРАНЕНИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2016 |
|
RU2633062C1 |
| СПОСОБ СТЕРИЛИЗАЦИИ И ПРЕДИМПЛАНТАЦИОННОГО ХРАНЕНИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2007 |
|
RU2357766C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАГЛИЦИДИЛОВОГО ЭФИРА ГЛЮКОЗЫ И КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ ДЛЯ ХИМИЧЕСКОЙ СШИВКИ КОЛЛАГЕНСОДЕРЖАЩИХ ЭНДОПРОТЕЗОВ БИОЛОГИЧЕСКОГО ПРОИСХОЖДЕНИЯ | 2014 |
|
RU2563251C1 |
| Способ предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии | 2023 |
|
RU2827028C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БИОЛОГИЧЕСКОГО ПРОТЕЗА ВЕНОЗНОГО КЛАПАНА | 2010 |
|
RU2429023C1 |
| СПОСОБ КОНСЕРВАЦИИ И СТЕРИЛИЗАЦИИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2007 |
|
RU2350075C1 |
| СПОСОБ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 1996 |
|
RU2122321C1 |
| БИОЦИДНАЯ КОМПОЗИЦИЯ ДЛЯ АСЕПТИЧЕСКОГО ХРАНЕНИЯ КОНСЕРВИРОВАННОГО ПРОТЕЗНОГО МАТЕРИАЛА ИЗ ТКАНЕЙ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ | 2014 |
|
RU2580621C1 |
| СПОСОБ ОБРАБОТКИ БИОМАТЕРИАЛОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2001 |
|
RU2196424C1 |



Изобретение относится к медицине, а именно к сердечно-сосудистой хирургии, и может быть использовано для консервации, стерилизации и модификации биологического материала при изготовлении биопротезов сосудов и клапанов сердца. Способ включает забор и отмывку нативных тканей с последующей консервацией в течение 2-21 суток в растворе смеси диглицилового эфира этиленгликоля и олигоэпоксисоединения с разветвленной структурой углеводородной цепи, приготовленного на 0,05-0,2 М фосфатном буфере и последующей гепаринизацией биологической поверхности ткани при температуре 20-40°C в течение 2-14 часов. Способ позволяет улучшить упругоэластичные и тромборезистентные характеристики биологического протеза, а также увеличить стерилизующий эффект и устойчивость биоматериала к кальцификации. 2 з.п. ф-лы, 3 ил., 4 табл., 3 пр.
1. Способ предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии, включающий забор и отмывку нативных тканей с последующей консервацией в течение 2-21 суток в растворе смеси диглицилового эфира этиленгликоля и олигоэпоксисоединения с разветвленной структурой углеводородной цепи, приготовленного на 0,05-0,2 M фосфатном буфере и последующей гепаринизацией биологической поверхности ткани при температуре 20-40°C в течение 2-14 часов, отличающийся тем, что в консервирующий раствор добавляют от 5 до 30 частей олигоэпоксисоединения от массы диэпоксида, а фосфатный буфер готовят на 0,9%-ном растворе натрия хлорида с осмолярностью 280-300 мОсм/л.
2. Способ предимплантационной обработки биологических протезов по п. 1, отличающийся тем, что в качестве олигоэпоксисоединения в смеси используют 1,2,3,4,6-пента-О-{1-[(глицидилокси)этокси]этил}-α-D-глюкопиранозу.
3. Способ предимплантационной обработки биологических протезов по п. 1, отличающийся тем, что модификацию биологической ткани осуществляют в растворе нефракционированных и низкомолекулярных гепаринов в концентрации 75-150 Ед/мл.
| СПОСОБ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 1996 |
|
RU2122321C1 |
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОЙ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ СОСУДОВ И КЛАПАНОВ СЕРДЦА | 1996 |
|
RU2120212C1 |
| US5080670 A, 14.01.1992 | |||
| WO03099346 A2, 04.12.2003 | |||
Авторы
Даты
2015-07-27—Публикация
2014-06-27—Подача