Изобретение относится к медицине, а именно к предимплантационной обработке биологических протезов для сердечно-сосудистой хирургии, и может быть использовано при хранении биологических протезов клапанов сердца, сосудов и т.п. до момента имплантации.
Известен способ стерилизации и хранения ксенопротезов в 0,5% растворе глутарового альдегида (Методические указания по стерилизации ксенобиопротезов раствором глутарового альдегида. Минздрав СССР. N 28-6/26 от 19.09.1986 г.). Недостатком данного способа является длительная отмывка биопротеза от стерилизующего раствора непосредственно перед имплантацией в течение 90 минут при интенсивном помешивании в 500 мл 0,9% стерильного раствора хлорида натрия со сменой раствора каждые 15 минут. Помимо этого, консервация и хранение биопротезов для сердечнососудистой хирургии в растворе глутарового альдегида провоцирует образование фосфата кальция в биоткани, что может приводить к дисфункции биопротеза после имплантации.
Известен способ стерилизации и предимплантационного хранения биопротезов клапана сердца или сосудов, изготовленных из химически стабилизированной ксеногенной ткани, при котором изделия помещают для стерилизации и хранения до момента имплантации в раствор 2-3-бис(гидроксиметил)-хиноксалин-1,4-диоксида при температуре от 16 до 40°С (пат. 2457867 Рос. Федерация: МПК A61L2/16, A61L27/00, A61L 31/498. Способ стерилизации и предимплантационного хранения биологических протезов из ксеногенной и аллогенной ткани для сердечно-сосудистой хирургии; правообладатель Учреждение РАМН НЦЦСХ им. А.Н. Бакулева РАМН. (RU). - №2011117782/15; заявл. 05.05.2011, опубл. 10.08.2012). Препарат 2-3-бис(гидроксиметил)-хиноксалин-1,4-диоксид обладает мощным антибактериальным и бактериостатическим действием, действует на штаммы бактерий, устойчивых к другим химиопрепаратам, включая антибиотики. Перед имплантацией необходима отмывка биопротеза, для чего его помещают в 500 мл стерильного 0,9% раствора хлорида натрия не менее чем на 30 секунд.
К недостаткам данного способа можно отнести высокую токсичность 2-3-бис (гидроксиметил)-хиноксалин-1,4-диоксида, также данный препарат обладает тератогенным, эмбриотоксическим и мутагенным действием, категорически противопоказан к применению у детей. Помимо этого, осмолярность раствора ниже, чем у плазмы крови, в которой он будет эксплуатироваться после имплантации. Низкая осмолярность раствора для хранения биопротезов может приводить к отеку биокани, которая может стать причиной дисфункции протеза после имплантации.
Таким образом, предимплантационное хранение протезов (на основе консервированных биологических тканей) в водных растворах различных препаратов, обеспечивающих их стерильность и сохранность, имеют существенные недостатки, такие как: токсичность препаратов, низкая осмолярность готовых растворов, необходимость длительной отмывки биопротезов перед имплантацией, а также узкий диапазон температур для хранения и транспортировки готовых биопротезов. Температура окружающего воздуха менее +5°С может приводить к замерзанию жидкой фазы раствора для хранения, что приводит к риску повреждения коллагеновой матрицы биоткани образующимися кристаллами льда, что в свою очередь может привести к ранней дисфункции имплантированного протеза и необходимости повторной операции для пациента.
Альтернативой водным растворам может стать глицерин, который широко применяется в фармацевтической и медицинской промышленности для улучшения эластичности различных препаратов и растворов. Глицерин также нашел свое применение и при разработке биопротезов. Он применяется как для консервации тканей, так и для длительного хранения предварительно обработанного биоматериала.
Известно применение глицерина для консервации кожи и заключается в двухэтапном погружении кожных лоскутов в растворы глицерина: 1 этап - лоскуты погружают в 70% раствор глицерина инкубируют 3 часа при 33°С при постоянном перемешивании с целью обеспечения максимального контакта между тканью раствором; 2 этап - лоскуты перекладывают в 85% раствор глицерина и инкубируют при аналогичных режимах. Дальнейшее хранение образцов происходит в 85% растворе глицерина при температуре 5°С [Morphology of glycerol-preserved human cadaver skin / C. Richter., M. Hoekstra, J. van Baare et al // Bums. 1996. - Vol.22, No. 2, pp.113-116]. Помимо сохранности структуры тканей, хранение кожных лоскутов в 85% глицерине снижает риск бактериальной контаминации и поддерживает стерильность биоматериала. Доказана сохранность свойств кожных лоскутов на протяжении пяти лет.
Также глицерин применяли для обработки фрагментов костной ткани для пластики костных дефектов [Preservation of allograft bone using a glycerol solution: a compilation of original preclinical research / B. Samsell, D. Softie, X. Q. Samsell et al. // Biomaterials Research (2019) 23:5]. Фрагменты костной ткани помещали в 77% раствор глицерина при соотношении 1:5. Далее, образцы извлекали из раствора и подвергали стерилизации гамма-облучением и хранили при комнатной температуре. Перед использованием, образцы подвергали 30 - секундной отмывке физраствором. Доклинические исследования показали, что консервация костной ткани глицерином позволяет получить материал, который сохраняет биомеханическую прочность, не оказывает негативного влияния на биосовместимость ткани, а также не требует длительной отмывки перед имплантацией.
Протезы клапана сердца, изготовленные из твердой мозговой оболочки и консервированные в растворе глицерина, применялись с 1971 года с удовлетворительными результатами. Протезы консервировали и хранили в 98% растворе глицерина при комнатной температуре в срок на 7 недель [Mechanical suitability of glycerol preserved human dura mater for construction of prosthetic cardiac valves. / K.A. McGarvey, J.M. Lee, D.R. Boughner// Biomaterials. 1984. Vol.5, Is. 2, P. 109-117]. Перед применением материал отмывали в дистиллированной воде и регидратировали в растворе Хэнкса. Результаты имплантации биопротезов клапана сердца крупным лабораторным животным показали, что технология хранения на основе применения глицерина значительно улучшает гемодинамические и антикальциевые свойства биопротеза клапана сердца.
Недостатком данного способа является высокая концентрация глицерина (98%), т.к. доказано, что высокие концентрации раствора глицерина (более 78%) оказывают цитотоксическое воздействие, при этом, генотоксический эффект отсутствует при любых концентрациях глицерина (Cytotoxicity and Genotoxicity of Bovine Pericardium Preserved in Glycerol /A.C.D. Rodas, M.J.S. Maizato, A.A. Leirner, et al. // Artificial Organs. 2008. 32(4):272-276).
Известен способ обработки биологических тканей, предварительно консервированных глутаровым альдегидом, раствором глицерина и этилового спирта в различных соотношениях (Patent USA US 8,007,992 В2 Aug. 30, 2011 «Method of treating glutaraldehyde-fixed percardial tissue with a non-aqueous mixture of glyceroland a c1-c3 alcohob). При этом, концентрация глицерина в готовой смеси для хранения биоткани составляет от 60% и выше. Данный способ обработки позволяет высушивать биопротезы, стерилизовать этиленоксидом и длительно хранить до момента имплантации пациенту. Перед имплантацией необходима регидратация в стерильном физиологическом растворе в течение 5 минут. Недостатком данного метода является использование этилового спирта, поскольку это может приводить к излишней дегидратации и иссушению биологических тканей, и как следствие, ломкости в процессе хранения и транспортировки, а также необходимость обязательной регидратации перед имплантацией. Помимо этого, высокие концентрации и/или объемы спирта могут приводить к денатурации белков и дублению биологической ткани, что негативно отразится на свойствах протезах и результатах их клинического применения.
Наиболее близким решением проблемы является метод сухого хранения протезов клапана сердца (Processing of implantable animal tissues for dry storage / Chen et al.// Patent USA 65340004 В 2. Date: 18/03/2003/). Технология заключается в том, что биоматериал, предварительно консервированный глутаровым альдегидом, погружают в водный раствор, содержащий 57 об. % глицерина. Объем водного раствора для обработки в 50 раз должен превышать объем материала. После 2 часов обработки при комнатной температуре материал извлекают из раствора и сушат на воздухе в ламинарном боксе при комнатной температуре и относительной влажности от 10% до 30% в течение 24 часов, после чего помещают в отдельные пакеты для газовой стерилизации и стерилизуют воздействием этиленоксида.
К недостаткам данного метода можно отнести недостаточное время нахождения в растворе глицерина - происходит не полная пропитка биоматериала глицерином и замещение консервирующего раствора в объеме коллагеновой матрицы биоткани, что может привести к появлению кристаллов солей буферного раствора, на котором готовится консервирующая смесь. Кристаллы фосфатов могут стать центрами накопления ионов кальция после имплантации и привести к кальцификации биопротеза и его последующей несостоятельности. Также учитывая постоянный контакт протезов с ровью пациента, обработки только раствором глицерина будет недостаточно для снижения риска тромбообразования. Также, сушка биоткани на воздухе в неконтролируемых режимах не гарантируют удаление всей влаги из биопротеза, что при хранении может привести к деградации коллагеновых волокон и ухудшению свойств изделия. Сушка на воздухе в течение 24 часов несет в себе риск контаминации биопротеза.
Техническим решением является погружение предварительно отмытого от консервирующего раствора биопротеза в водный раствор глицерина, содержание которого составляет 50-60%.
Для повышения био- и гемосовместимости в раствор глицерина добавляется антикоагулянт - нефракционированный либо низкомолекулярный гепарин в конечной концентрации 10-100 ED/мл.
Время инкубации в приготовленном растворе составляет 16-24 часа, далее биопротез высушивают.
Сушка биопротеза происходит в вакуумной камере в течение 6 часов при избыточном давлении (- 0,07) МПа. После высыхания биопротез помещается в индивидуальную упаковку и подвергается стерилизации этиленоксидом. Перед имплантацией биопротезы не требуют отмывки.
Пример изготовления
Ксеноперикардиальный лоскут (либо биопротез клапана сердца или сосуда), консервированный диглициловым эфиром этиленгликоля, отмывается от консерванта трех-кратно в избытке стерильной дистиллированной воды, после чего изделие помещается в 57% водный раствор глицерина, содержащий нефракционированный гепарин в концентрации 100 Ед/мл) на 16 часов при комнатной температуре. Затем лоскут/биопротез извлекается и помещается в вакуумную сушку при отрицательном давлении на 6 часов. После полного высыхания изделие (лоскут/биопротез) помещается в блистерную упаковку, запечатывается и подвергается стерилизации этиленоксидом 2 часа при 37°С.
При обработке биологической ткани, консервированной диглицидиловым эфиром этиленгликоля, дополнительно обработанной глицерином и высушенной в вакууме, улучшаются физико-механические свойства: прочность до обработки составила 8,77 Мпа и после 9,28 Мпа. Эластичность изменилась с 48,1% до глицеризации и 61,38% после.
Гистологический анализ подтвердил сохранность коллагеновых волокон после обработки глицерином и последующей сушки, что косвенно оказывает протективное влияние глицеризации на физико-механические свойства.
Изучение некоторых показателей гемосовместимости свидетельствует об отсутствии негативного влияния остаточного глицерина в коллагеновой матрице биоткани на компоненты крови. Показано отсутствие активации тромбоцитов после контакта с обработанным глицерином материалом (табл. 1, см. в графич. части). Добавление гепарина в раствор глицерина способствует усилению эффекта.
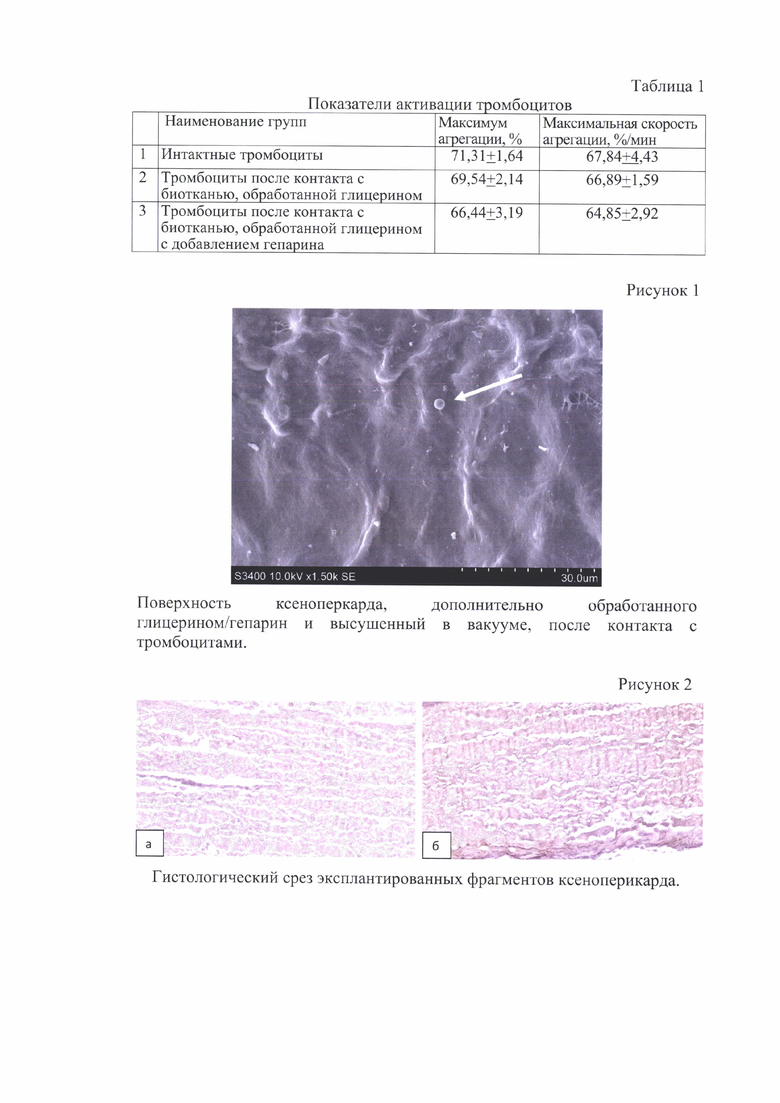
Дополнительная глицеризация (с добавлением гепарина) также не провоцирует адгезию тромбоцитов (рис. 1).
Примечание к рисунку 1: Сканирующая электронная микроскопия. Увеличение 1500. Стрелкой указан тромбоцит неизменной формы.
Величина гемолиза после контакта с глицеризованными и высушенными образцами была в среднем 0,2+0,06%, при допустимом показателе - 2%. Вывод - процесс глицеризации и последующей сушки не оказывает негативного влияния на эритроциты и тромбоциты.
Консервация биоматериала диглицидиловым эфиром этиленгликоля минимизирует риск кальцификации по сравнению с широко применяемым глутаровым альдегидом. Тем не менее любая дополнительная модификация биоматериала не должна увеличивать риск кальцификации биопротезов. С этой целью, все разработки по изменению технологии изготовления биопротезов подвергаются тестированию на кальций связывающий потенциал на модели ускоренной кальцификации на лабораторных животных, которая подразумевает имплантацию образцов биоматериалов подкожно молодым крысам - самцам на срок не менее 60 дней. После удаления во всех имплантированных фрагментах ксеноперикарда наблюдали полное отсутствие отложений кальция и сохранность коллагеновых волокон (рис. 2).
Примечание к рисунку 2: а) контроль; б) после обработки глицерином/гепарин и высушивания в вакууме. Окраска ализариновым красным. Ув. х 400.
Таким образом, результаты проведенных исследований подтверждают, что дополнительная обработка ксеноперикарда, предварительно консервированного диглицидиловым эфиром этиленгликоля и дополнительно обработанного в растворе глицерина, содержащий гепарин и высушенный в вакууме, обладает удовлетворительными физико-механическими, био- и гемосовместимыми свойствами и не увеличивает риск кальцификации биопротеза.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОЙ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2014 |
|
RU2558089C1 |
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОГО ХРАНЕНИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2016 |
|
RU2633062C1 |
| СПОСОБ ОБРАБОТКИ БИОМАТЕРИАЛОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2001 |
|
RU2196424C1 |
| СПОСОБ СТЕРИЛИЗАЦИИ И ПРЕДИМПЛАНТАЦИОННОГО ХРАНЕНИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2007 |
|
RU2357766C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ БИОЛОГИЧЕСКОГО ПРОТЕЗА ВЕНОЗНОГО КЛАПАНА | 2010 |
|
RU2429023C1 |
| СПОСОБ КОНСЕРВИРОВАНИЯ БИОТКАНИ ДЛЯ ПРОТЕЗИРОВАНИЯ КЛАПАНОВ СЕРДЦА И СОСУДОВ | 1992 |
|
RU2008767C1 |
| БИОЦИДНАЯ КОМПОЗИЦИЯ ДЛЯ АСЕПТИЧЕСКОГО ХРАНЕНИЯ КОНСЕРВИРОВАННОГО ПРОТЕЗНОГО МАТЕРИАЛА ИЗ ТКАНЕЙ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ | 2014 |
|
RU2580621C1 |
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОЙ ОБРАБОТКИ БИОПРОТЕЗОВ | 2007 |
|
RU2384309C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КЛАПАНСОДЕРЖАЩЕГО КОНДУИТА ИЗ ЯРЕМНОЙ ВЕНЫ КРУПНОГО РОГАТОГО СКОТА | 2016 |
|
RU2633544C1 |
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОЙ ОБРАБОТКИ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ СОСУДОВ И КЛАПАНОВ СЕРДЦА | 1996 |
|
RU2120212C1 |
Изобретение относится к области медицины, а именно к способу предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии. Способ предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии включает погружение в водный раствор глицерина, содержание которого составляет 50-60%, предварительно отмытых от консервирующего раствора биологических протезов, сушку биопротезов и их стерилизацию этиленоксидом, отличающийся тем, что время инкубации в растворе глицерина составляет 16-24 часа, для повышения био- и гемосовместимости в раствор глицерина добавляется антикоагулянт - нефракционированный либо низкомолекулярный гепарин в конечной концентрации 10-100 ED/мл, сушка биопротеза происходит в вакуумной камере в течение 6 часов при избыточном давлении (-0,07) МПа. Вышеописанный способ позволяет проводить предимплантационную обработку протезов для сердечно-сосудистой хирургии с повышением их био- и гемосовместимости. 2 ил., 1 табл., 1 пр.
Способ предимплантационной обработки биологических протезов для сердечно-сосудистой хирургии, включающий погружение в водный раствор глицерина, содержание которого составляет 50-60%, предварительно отмытых от консервирующего раствора биологических протезов, сушку биопротезов и их стерилизацию этиленоксидом, отличающийся тем, что время инкубации в растворе глицерина составляет 16-24 часа, для повышения био- и гемосовместимости в раствор глицерина добавляется антикоагулянт - нефракционированный либо низкомолекулярный гепарин в конечной концентрации 10-100 ED/мл, сушка биопротеза происходит в вакуумной камере в течение 6 часов при избыточном давлении (-0,07) МПа.
| US 6534004 B2, 18.03.2003 | |||
| СПОСОБ ПРЕДИМПЛАНТАЦИОННОГО ХРАНЕНИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ ДЛЯ СЕРДЕЧНО-СОСУДИСТОЙ ХИРУРГИИ | 2016 |
|
RU2633062C1 |
| ЖУРАВЛЕВА И.Ю., КУДРЯВЦЕВА Ю.А., БОРИСОВ В.В., БАРБАРАШ Л.С | |||
| Сравнительный анализ применения различных гепаринов для антитромботической модификации биоматериала // Медицина в Кузбассе | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
Авторы
Даты
2024-09-20—Публикация
2023-10-09—Подача