Перекрестная ссылка на родственные заявки
По данной заявке испрашивается приоритет находящейся в процессе одновременного рассмотрения предварительной заявки на патент США с порядковым номером 61/246215, поданной 28 сентября 2009 года, находящейся в процессе одновременного рассмотрения предварительной заявки на патент США № 61/246208, поданной 28 сентября 2009 года, и находящейся в процессе одновременного рассмотрения предварительной заявки на патент США № 61/157944, поданной 6 марта 2009 года, полное содержание каждой из которых включено в описание посредством ссылки.
Область, к которой относится изобретение
Настоящее изобретение относится к белоксодержащим пеноматериалам, их получению и их применению.
Уровень техники
Пеноматериалы используются в большом разнообразии промышленных и потребительских областей применения, включающих, например, теплоизоляцию пеноматериалами, упаковочные пеноматериалы, ударопрочные прокладки, обратные стороны покрытий, декоративные пеноматериалы для имитации деревянных украшений (мебели) и т.д. Использование таких пеноматериалов продолжает расти во всем мире. Этот рост может быть приписан, среди прочего, их легкой массе, хорошему соотношению прочности и массы, их теплоизоляционным и звукоизоляционным свойствам и энергопоглощающим свойствам пеноматериалов. Полиуретановые пеноматериалы являются очень популярными и могут быть изготовлены в разнообразных отличающихся формах. Например, полиуретановый пенопласт может быть изготовлен в гибкой, полужесткой или жесткой форме, причем гибкие пенопласты обычно являются более мягкими, менее плотными, более эластичными и более подверженными структурному восстановлению после нагрузки, чем жесткие пенопласты.
Получение полиуретановых пенопластов экстенсивно обсуждалось в области пеноматериалов. Тем не менее, общим подходом получения полиуретановых пенопластов является получение по реакции полиола и изоцианата, в результате которой образуется уретановая группа скелета молекулы. Обычно вспенивающий агент, например, инертный газ или соединение, которое образует газ, используют для создания пор внутри пеноматериала. Дополнительные модулирующие агенты, например, катализаторы и поверхностно-активные вещества, могут быть добавлены в процессе получения для модуляции свойств полученного вспененного продукта.
Недавно были предприняты попытки замены или сокращения применения сложного или простого полиэфирполиолов при получении полиуретановых пенопластов с более многосторонними, возобновляемыми, менее дорогостоящими и более благоприятными в отношении окружающей среды компонентами. Например, были получены пеноматериалы с использованием триглицеридов жирных кислот, полученных из растений. Поскольку такие материалы являются возобновляемыми, относительно недорогими, многосторонними и благоприятными в отношении окружающей среды, они являются желаемыми в качестве ингредиентов для получения пеноматериалов.
Однако все еще существует потребность в разработке возобновляемых, менее дорогостоящих и более благоприятных в отношении окружающей среды агентов, которые могут модулировать свойства пеноматериала. Например, могли бы быть выгодными возобновляемые материалы, которые можно использовать для улучшения свойств пеноматериала, таких как более высокий подъем пены, однородная пористая структура и/или пеноматериал более низкой плотности. Особенно ценным мог бы быть материал, присутствующий в побочных продуктах отходов, который может быть получен экономично и в больших количествах.
Сущность изобретения
Настоящее изобретение основывается, отчасти, на открытии того, что некоторые белковые композиции, получаемые из различных исходных материалов, например, биомассы растительных отходов, могут быть использованы для модуляции свойств пеноматериала и могут, например, давать пеноматериалы более низкой плотности, содержащие большее количество меньших по размеру, более однородных пор.
В одном аспекте изобретение обеспечивает выделенную, водорастворимую полипептидную композицию, способную стабилизировать пеноматериал на основе полиуретана. Выделенная, водорастворимая полипептидная фракция имеет один или несколько из следующих признаков: (a) полоса поглощения амида-I между приблизительно 1633 см-1 и 1680 см-1, как определено ИК-Фурье-спектроскопией твердого состояния (FTIR); (b) полоса амида-II между приблизительно 1522 см-1 и 1560 см-1, как определено FTIR твердого состояния; (c) две выраженные полосы поглощения валентных колебаний N-H 1° амида с центрами в области около 3200 см-1 и около 3300 см-1, как определено FTIR твердого состояния; (d) выраженный кластер протонированных ядер азота, определяемый в границах химического сдвига 15N в области около 94 м.д. и около 100 м.д., и в границах химического сдвига 1H в области около 7,6 м.д. и около 8,1 м.д., как определено с помощью жидкофазного двумерного ЯМР протон-азотного взаимодействия; (e) средняя молекулярная масса между приблизительно 600 и приблизительно 2500 Дальтон; (f) неспособность стабилизировать эмульсию типа масло-в-воде, в которой, когда водный раствор, содержащий 14 массовых частей белка, растворенных или диспергированных в 86 массовых частях воды, смешивают с 14 массовыми частями полимерного дифенилметандиизоцианата (PMDI), водный раствор и PMDI образуют нестабильную суспензию, которая макроскопически разделяется на фазы при статических условиях в течение пяти минут после смешивания; (g) водорастворимая полипептидная композиция способна стабилизировать пеноматериал на основе полиуретана относительно пеноматериала на основе полиуретана, образованного из той же самой исходной композиции, но лишенной водорастворимой белковой композиции; и (h) водорастворимая полипептидная композиция способна уменьшать плотность пеноматериала на основе полиуретана по меньшей мере на 5% (например, по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%) относительно пеноматериала на основе полиуретана, полученного из той же самой исходной композиции, но лишенной водорастворимой белковой композиции.
В другом аспекте изобретение обеспечивает способ получения выделенной, водорастворимой полипептидной композиции для использования при получении пеноматериала. Данный способ включает: (a) диспергирование белоксодержащего исходного материала в водном растворе при рН больше, чем приблизительно 6,5, в течение по меньшей мере 5 минут с получением суспензии, содержащей частицы вещества; (b) после стадии (a), необязательно уменьшение рН до приблизительно 4,0-5,0; и затем отделение водного раствора от содержащего частицы вещества с получением тем самым раствора, обогащенного в отношении водорастворимой полипептидной композиции, описанной в данном документе.
В некоторых вариантах осуществления способ дополнительно включает одну или несколько следующих стадий: (i) перед стадией (a), расщепление исходного материала ферментом; (ii) после стадии (a), расщепление суспензии ферментом; (iii) после стадии (b), расщепление суспензии ферментом; или (iv) после стадии (c), расщепление раствора, обогащенного водорастворимой полипептидной композицией, ферментом. Пригодные ферменты включают, например, серин-, лейцин-, лизин- или аргинин-специфическую протеазу. Способ необязательно дополнительно включает сушку водорастворимой полипептидной композиции, полученной на стадии (c).
В каждом из аспектов водорастворимая белковая композиция может быть получена из материала животного происхождения (например, молока и молочной сыворотки, рыбной кормовой муки, ткани животных) или из материала растительного происхождения (например, кукурузы, пшеницы, подсолнечника, хлопка, семян рапса, канолы (брюквы) (Brassica napus L. var. rapifera), клещевины, сои, рыжика посевного, льна, ятрофы, мальвы, земляного ореха, водорослей, бобовых, пальмы, табака, жома (выжимок) сахарного тростника и их комбинаций). В некоторых других вариантах осуществления исходным материалом (биомассой) в способе получения водорастворимой белковой композиции могут быть мука канолы, белковый изолят канолы, мука клещевины, белковый изолят клещевины или их комбинация.
В другом аспекте изобретение обеспечивает пеноматериал, полученный с использованием водорастворимой белковой композиции, описанной в данном документе. Пеноматериал может представлять собой пенополиуретан, который содержит продукт реакции смеси, содержащей: (a) описанную здесь водорастворимую полипептидную композицию; (b) реагент на основе изоцианата и (c) необязательное реагирующее с изоцианатом соединение. В некоторых вариантах осуществления смесь необязательно содержит дополнительно, среди других компонентов, поверхностно-активное вещество и/или катализатор и/или вспенивающий агент.
В другом аспекте изобретение обеспечивает пенополиуретан, содержащий продукт реакции смеси, содержащей (a) белоксодержащую композицию, (b) реагент на основе изоцианата и (c) необязательный реагирующий с изоцианатом компонент, где белоксодержащая композиция способна уменьшать плотность пенополиуретана по меньшей мере на 5% (например, по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90%) относительно пенополиуретана, полученного из той же самой смеси, но лишенной белоксодержащей композиции. В некоторых вариантах осуществления смесь необязательно может дополнительно содержать, среди других компонентов, поверхностно-активное вещество и/или катализатор и/или вспенивающий агент.
В другом аспекте изобретение обеспечивает пенополиуретан, содержащий продукт реакции смеси, содержащей (a) выделенную белоксодержащую композицию, причем белоксодержащая композиция способна диспергировать PMDI в водной среде, (b) реагент на основе изоцианата и (c) необязательный реагирующий с изоцианатом компонент. Белоксодержащая композиция содержит водонерастворимую/вододиспергируемую белковую фракцию либо отдельно, либо в комбинации с водорастворимой белковой фракцией. В некоторых вариантах осуществления смесь необязательно может дополнительно содержать, среди других компонентов, поверхностно-активное вещество и/или катализатор, или вспенивающий агент.
В каждом из предыдущих аспектов реагентом на основе изоцианата может быть органический полиизоцианат, например, полимерный дифенилметандиизоцианат, 2,4-толуолдиизоцианат, 2,6-толуолдиизоцианат, бензолдиизоцианат, м-ксилилендиизоцианат, 1,4-фенилендиизоцианат, 1,3-фенилендиизоцианат, 4,4'-дифенилдиизоцианат, 4,4'-дифенилдиметилметандиизоцианат, гексаметилендиизоцианат, толидиндиизоцианат, дианизидиндиизоцианат, 1,5-нафталиндиизоцианат, 1,4-циклогександиизоцианат или их комбинация. Альтернативно или дополнительно, реагент на основе изоцианата содержит уретан, аллофанат, мочевину, биурет, карбодиимид, уретонимин, изоцианурат или их комбинацию. В некоторых вариантах осуществления реагентом на основе изоцианата может быть полимерный дифенилметандиизоцианат.
Реагирующим с изоцианатом соединением может быть соединение, способное нуклеофильно реагировать с изоцианатом. Например, реагирующим с изоцианатом соединением может быть соединение, имеющее, например, гидроксильную группу или аминогруппу, способную реагировать с изоцианатом. В некоторых вариантах осуществления реагирующим с изоцианатом соединением является полиол, например, полиол, полученный из касторового масла, льняного масла или соевого масла. В некоторых других вариантах реагирующим с изоцианатом соединением является полиол, инициируемый соединением, выбранным из группы, состоящей из глицерина, триметилолпропана, триэтаноламина, пентаэритрита, сорбита, сахарозы, диамина, толуолдиамина, диаминодифенилметана, полиметиленполифениленполиамина, этаноламина, диэтаноламина или их смеси. Кроме того, реагирующее с изоцианатом соединение может включать водонерастворимую/вододиспергируемую полипептидную композицию, используемую отдельно или в комбинации с любым из вышеупомянутых реагирующих с изоцианатом соединений. Водонерастворимая/вододиспергируемая полипептидная композиция способна образовывать дисперсию с реагентом на основе изоцианата и становиться интегральным структурным компонентом полученного отвержденного пеноматериала. Однако, в отличие от водорастворимых полипептидных белков, водонерастворимые полипептидные композиции обычно не уменьшают плотность полученного пеноматериала.
Альтернативно или дополнительно, реагирующим с изоцианатом соединением может быть простой политиоэфир с концевой гидроксильной группой, полиамид, сложный полиэфирамид, поликарбонат, полиацеталь, полиолефин или полисилоксан, или сложный полиэфир, полученный конденсацией гликоля или полиола с более высокой функциональностью с дикарбоновой кислотой. В некоторых вариантах осуществления реагирующим с изоцианатом соединением является полиоксипропиленгликоль, полипропиленоксид-этиленоксид, пропиленгликоль, пропандиол, глицерин, аминалкоксилат или их смесь. В некоторых других вариантах осуществления реагирующим с изоцианатом соединением является полиоксипропиленгликоль.
В некоторых вариантах осуществления пеноматериал имеет плотность в диапазоне от приблизительно 0,01 г/см3 до приблизительно 0,5 г/см3, как определено при помощи ASTM D-7487. В некоторых вариантах осуществления пеноматериал может иметь плотность, которая является на 5%-80% меньше, чем плотность пеноматериала, созданного из той же самой исходной композиции, но которая лишена водорастворимой полипептидной композиции, описанной здесь, или белоксодержащей композиции, которая содержит количество водорастворимого белка, достаточное для уменьшения плотности полученного пеноматериала. В некоторых других вариантах осуществления время “сливок” пеноматериала (период между смешиванием компонентов для изготовления пенополиуретана и переходом в сметанообразную массу), определяемое при помощи ASTM D-7487, составляет менее одной минуты. В некоторых других вариантах осуществления свободная высота подъема пеноматериала, определяемая при помощи ASTM D7487, больше, чем свободная высота подъема пеноматериала из той же самой исходной композиции, но лишенной водорастворимой полипептидной композиции, описанной здесь, или белоксодержащей композиции, которая содержит количество водорастворимого белка, достаточное для уменьшения плотности полученного пеноматериала. Например, свободная высота подъема пеноматериала может быть по меньшей мере на 5% больше, чем высота подъема пеноматериала, созданного из той же самой исходной композиции, но лишенной таких белков. В некоторых других вариантах осуществления пеноматериал имеет большее количество меньших по размеру, более однородных пор по сравнению с пеноматериалом, созданным из той же самой исходной композиции, но лишенной водорастворимой полипептидной композиции, описанной здесь, или белоксодержащей композиции, которая содержит количество водорастворимого белка, достаточное для уменьшения плотности полученного пеноматериала.
В другом аспекте изобретение обеспечивает способ получения пенополиуретана, который включает стадии: (a) смешивания белоксодержащей композиции (например, водорастворимой полипептидной композиции, описанной здесь) и реагента на основе изоцианата с получением смеси; и (b) выдерживания смеси для образования пенополиуретана. Хотя водорастворимая фракция не требует обязательного выделения, чтобы быть эффективной в уменьшении плотности полученного пеноматериала, при определенных условиях желательным является разделение водорастворимой и водонерастворимой белковых фракций и добавление их в регулируемых соотношениях для модуляции свойств полученных пеноматериалов. В некоторых вариантах осуществления смесь на стадии (a) дополнительно содержит реагирующее с изоцианатом соединение. Реагент на основе изоцианата и реагирующее с изоцианатом соединение могут быть теми же самыми, которые описаны выше, для других аспектов изобретения.
Смесь на стадии (a) необязательно содержит дополнительно вспенивающий агент или соединение, которое образует вспенивающий агент. Понятно, что при определенных обстоятельствах вода способна образовывать вспенивающий агент. Водорастворимый белок может быть растворен, диспергирован или суспендирован в воде, в растворе, содержащем реагент на основе изоцианата, или в растворе, содержащем реагирующее с изоцианатом соединение.
В некоторых вариантах осуществления смесь на стадии (a) может дополнительно содержать катализатор, который способствует образованию пеноматериала. Примеры катализаторов включают, например, дилаурат дибутилолова, диацетат дибутилолова, триэтилендиамин, 2,2'-диметиламинодиэтиловый эфир, 2-диметиламиноэтанол, октоат двухвалентного олова, октоат калия, соль щелочного металла карбоновой кислоты или их комбинацию. Альтернативно или дополнительно, смесь на стадии (a) дополнительно содержит поверхностно-активное вещество, например, простой полиэфир силикона. Альтернативно или дополнительно, смесь на стадии (a) может дополнительно содержать добавку, выбранную из группы, состоящей из антипирена, наполнителя, армирующего материала, подавителя дыма, биоцида, инертного пластификатора, антистатического агента и их комбинаций.
В некоторых вариантах осуществления реагент на основе изоцианата составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) исходных материалов, используемых для получения пеноматериала. В некоторых других вариантах осуществления реагирующее с изоцианатом соединение составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) исходных материалов, используемых для получения пеноматериала. В некоторых других вариантах осуществления белоксодержащая композиция (например, водорастворимая полипептидная композиция) составляет приблизительно от 0,01% (мас./мас.) до приблизительно 50% (мас./мас.) исходных материалов, используемых для получения пеноматериала. В некоторых других вариантах осуществления пеноматериал получают при Индексе в диапазоне приблизительно от 250% до приблизительно 800%.
В другом аспекте изобретение обеспечивает премикс для получения пенополиуретана, включающий: белоксодержащую композицию (например, водорастворимую полипептидную композицию, описанную здесь, водонерастворимую/вододиспергируемую полипептидную композицию или их смесь) и реагент на основе изоцианата. Белоксодержащая композиция характеризуется как способная уменьшать плотность пенополиуретана по меньшей мере на 5% (например, по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90%) относительно пенополиуретана, образованного из той же самой смеси, но лишенной белоксодержащей композиции. Премикс включает также, среди других компонентов, реагирующее с изоцианатом соединение, вспенивающий агент или соединение, которое образует вспенивающий агент, поверхностно-активное вещество и катализатор, который способствует образованию пеноматериала.
Реагент на основе изоцианата, реагирующее с изоцианатом соединение, вспенивающий агент или соединение, которое образует вспенивающий агент, поверхностно-активное вещество и катализатор могут быть такими же, какие обсуждались в описании выше. В некоторых вариантах осуществления реагент на основе изоцианата составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) премикса. В некоторых вариантах осуществления реагирующее с изоцианатом соединение составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) премикса. В некоторых других вариантах осуществления белоксодержащая композиция (например, водорастворимая полипептидная композиция) составляет приблизительно от 0,01% (мас./мас.) до приблизительно 99% (мас./мас.) исходных материалов, используемых для получения пеноматериала.
В другом аспекте настоящее изобретение обеспечивает изделие, содержащее пеноматериал, описанный в данном документе.
Краткое описание фигур
Предшествующие и другие цели, признаки и преимущества настоящего изобретения станут очевидными из следующего описания предпочтительных вариантов осуществления, иллюстрируемых в сопутствующих фигурах. Фигуры не должны обязательно сводиться к какому-либо масштабу, причем подчеркивается вместо этого иллюстрация принципов данного изобретения, в которой:
ФИГУРА 1 является блок-схемой, показывающей стадии приблизительного способа получения выделенных полипептидных композиций, используемых в практике настоящего изобретения;
ФИГУРА 2 показывает совмещенные FTIR-спектры твердого состояния для водорастворимой и водонерастворимой белковых фракций, выделенных из партии 5-90 расщепленной клещевины;
ФИГУРА 3 показывает FTIR-спектры твердого состояния выделенных водорастворимой и водонерастворимой фракций из расщепленной клещевины, где карбониламидная область является расширенной;
ФИГУРА 4 показывает FTIR-спектры твердого состояния выделенных водорастворимой и водонерастворимой фракций из расщепленной клещевины, где область валентных колебаний N-H является расширенной;
ФИГУРА 5 показывает совмещенные FTIR-спектры твердого состояния выделенных фракций из белка клещевины (партии 5-94), показывающие расширение карбониламидной области (водорастворимой фракции и водонерастворимой/вододиспергируемой фракции);
ФИГУРА 6 показывает FTIR-спектры твердого состояния выделенных водорастворимой и водонерастворимой фракций из белка клещевины (партии 5-94), где области валентных колебаний N-H и O-H являются расширенными;
ФИГУРА 7 показывает совмещенные FTIR-спектры твердого состояния выделенных водонерастворимой/вододиспергируемой фракций из белка клещевины (партии 5-94) и из расщепленной ферментом клещевины (партии 5-90);
ФИГУРА 8 показывает совмещенные FTIR-спектры твердого состояния выделенных водорастворимой и водонерастворимой фракций из расщепленной сои, где карбониламидная область является расширенной, где спектры были вертикально масштабированы для достижения эквивалентных значений интенсивности поглощения для валентных колебаний карбонильной группы амида-I;
ФИГУРА 9 показывает совмещенные FTIR-спектры твердого состояния выделенных водорастворимой и водонерастворимой фракций из расщепленной сои, где область валентных колебаний N-H является расширенной;
ФИГУРА 10 показывает совмещенные FTIR-спектры твердого состояния выделенных водорастворимых полипептидных фракций из расщепленной сои и расщепленной клещевины;
ФИГУРА 11 показывает совмещенные FTIR-спектры твердого состояния выделенных водонерастворимых фракций из расщепленной сои и соевой муки;
ФИГУРА 12 показывает совмещенные FTIR-спектры твердого состояния ATR поверхности выделенных водонерастворимых/диспергируемых фракций из множественных белковых проб (партии 5-81 расщепленной сои, соевой муки, партии 5-94 белкового изолята клещевины, партии 5-90 расщепленной клещевины), где карбониламидная область является расширенной;
ФИГУРА 13 является двумерным HSQC1H-15N ЯМР-спектром для расщепленной клещевины (партии 5-83) в d6-ДМСО, показывающим две представляющие интерес области, обозначенные как Область A и Область B;
ФИГУРА 14 является двумерным HSQC1H-15N ЯМР-спектром для водонерастворимой/диспергируемой полипептидной фракции, полученной из расщепленной клещевины (партии 5-83), в d6-ДМСО, вновь показывающим Область A и Область B;
ФИГУРА 15 показывает пенополиуретановые материалы, полученные в соответствии с процедурами в примере 5.
ФИГУРА 16 показывает пенополиуретановые материалы, полученные в соответствии с процедурами в примере 9.
ФИГУРА 17 показывает пенополиуретановые материалы, полученные в соответствии с процедурами в примере 10, где фигура 17(A) показывает соотношение 9:10 полиизоцианат:PMDI и фигура 17(B) показывает соотношение 10:10 полиизоцианат:PMDI.
ФИГУРА 18 показывает пенополиуретаны, полученные в соответствии с процедурами в примере 11.
ФИГУРА 19 показывает пенополиуретаны, полученные в соответствии с процедурами в примере 13.
Подробное описание изобретения
Настоящее изобретение основывается, отчасти, на открытии того, что некоторые белковые фракции, полученные из различных исходных материалов (например, биомассы растительных отходов), могут быть использованы для модуляции свойств пеноматериала и могут, например, давать пеноматериалы более низкой плотности, содержащие большее количество меньших по размеру, более однородных пор. Настоящее изобретение обеспечивает выделенную, водорастворимую полипептидную композицию, способную стабилизировать пеноматериал на основе полиуретана, белоксодержащие пенополиуретаны, способы и композиции для получения белоксодержащих пенополиуретанов и изделия, содержащие указанные пенополиуретаны. Выделенная водорастворимая полипептидная композиция может быть выделена из различных источников, например, растительного материала (такого как биомасса, полученная в виде побочного продукта отходов сельскохозяйственной промышленности) или материала животного происхождения (например, молока или молочной сыворотки, рыбной кормовой муки или ткани животных).
Было обнаружено, что определенные белковые фракции (которые могут включать выделенные водорастворимые белковые композиции и содержащие неочищенный белок композиции, которые содержат определенное количество водорастворимых белков) могут быть добавлены к полиуретановым пенообразующим композициям для изменения свойств полученного пенополиуретана. Например, полученный пеноматериал может иметь, например, более низкую плотность и/или меньший, более однородный размер пор относительно пеноматериалов, получаемых из тех же самых исходных материалов, но которые лишены белковой фракции. В результате, можно получать пеноматериалы, которые требуют меньше исходного материала (например, реагентов на основе изоцианата и/или реагирующих с изоцианатом соединений) для заполнения конкретного объема. В результате, можно получать пеноматериалы с желаемыми физическими характеристиками, более дешевые, чем пеноматериалы, которые лишены белков, а также можно получать пеноматериалы без применения в композиции известных поверхностно-активных веществ для пенополиуретана. Такие белоксодержащие пенополиуретаны могут быть получены путем смешивания определенных белковых композиций, описанных здесь, реагента на основе изоцианата и необязательного реагирующего с изоцианатом соединения с получением премикса, который образует пеноматериал. Дополнительное описание белковых композиций, способных стабилизировать пеноматериал на основе полиуретана, белоксодержащих пенополиуретанов, способов и композиций для получения таких белоксодержащих пенополиуретанов и изделий, содержащих указанные пенополиуретаны, представлено ниже.
I. Полипептидные композиции
Различные белковые фракции, получаемые из биомассы животного и растительного происхождения, имеют различные физические и химические свойства. В результате, белки могут быть использованы для модуляции желаемых характеристик полученных пеноматериалов. Водорастворимые белковые фракции, описанные здесь, обеспечивают пенополиуретаны, имеющие более низкую плотность и/или меньший, более однородный размер пор, по сравнению с пеноматериалами, полученными без водорастворимой белковой фракции. В некоторых вариантах осуществления водонерастворимая/вододиспергируемая белковая фракция может быть также дополнительно добавлена к премиксу, который образует пеноматериал. Добавление водонерастворимой/вододиспергируемой белковой фракции дополнительно модифицирует свойства пеноматериала, получаемого из премикса. Добавление водонерастворимых/вододиспергируемых белков может обеспечивать структурную жесткость полученного пеноматериала и/или модулировать плотность полученного пеноматериала. Кроме того, как водонерастворимая/вододиспергируемая белковая фракция, так и водорастворимая белковая фракция могут быть использованы отдельно или в комбинации для получения адгезивов, которые описаны подробно в заявке на патент США с порядковым номером 12/719521, поданной 8 марта 2010 года, описание которой включено в описание посредством ссылки.
Термины «белок» и «полипептид» используются как синонимы и относятся к полимерам, содержащим аминокислоты, которые соединены вместе, например, посредством пептидных связей или других связей, и могут содержать природные аминокислоты или модифицированные аминокислоты. Полипептиды могут быть выделены из природных источников или синтезированы с использованием стандартных химических способов. Кроме того, полипептиды могут быть модифицированы или дериватизованы либо природными процессами, такими как посттрансляционный процессинг, либо способами химической модификации, хорошо известными в данной области. Модификации или дериватизации могут происходить в любом месте полипептида, включая, например, пептидный скелет молекулы, боковые цепи аминокислот и концевые амино- или карбоксильные группы. Модификации включают, например, циклизацию, образование дисульфидной связи, деметилирование, деаминирование, образование ковалентных поперечных связей (сшивок), образование пироглутамата, формилирование, гамма-карбоксилирование, гликозилирование, образование GPI-якоря, гидроксилирование, йодирование, метилирование, миристоилирование, окисление, пегилирование, протеолитическое расщепление, фосфорилирование и т.д. Используемый в описании термин «выделенный» относится к материалу, который удален из своей первоначальной среды (например, природной среды, если он имеет природное происхождение).
Исходный материал для получения выделенных полипептидных композиций, который может представлять собой муку или белковый изолят, может быть получен из растительного материала (например, одного или нескольких компонентов из кукурузы, пшеницы, подсолнечника, хлопка, семян рапса, канолы, клещевины, сои, рыжика посевного, льна, ятрофы, мальвы, земляного ореха, пальмы, табака, жома (выжимок) сахарного тростника и водорослей) и/или материала животного происхождения (например, молока, молочной сыворотки, рыбной кормовой муки, ткани животного). Понятно, что водорастворимая белковая фракция может быть получена различными путями, например, как описано в примерах.
Например, водорастворимые белки могут быть выделены промыванием растительного или животного материала водой и простым сбором белков, которые растворяются в водных промывках. Однако понятно, что полученные промывки могут содержать соединения, отличные от водорастворимых белков, например, водорастворимые углеводы, такие как крахмалы и сахара, и т.д. Однако учитывая, что отношение водорастворимой белковой фракции к водонерастворимой/вододиспергируемой белковой фракции может варьироваться в зависимости от ряда факторов, таких как источник исходного материала, а также любых стадий обработки, которые могли уже быть проведены на исходном материале, и учитывая, что водонерастворимый/вододиспергируемый полипептид не способствует уменьшению плотности и может даже уменьшать такое действие, предпочтительно разделять две различные полипептидные фракции и затем добавлять их вместе контролируемым образом для регулирования физических и химических свойств полученного пеноматериала и для улучшения воспроизводимости полученного пеноматериала. Если уменьшения плотности не требуется в представляющем интерес пеноматериале, тогда, как должно быть понятно, можно уменьшать или полностью элиминировать водорастворимый полипептид из композиции и использовать водонерастворимый/вододиспергируемый полипептид в качестве единственного компонента на основе белка в данной композиции. Это может быть желательным, когда целесообразно получить пеноматериал с эквивалентной или более высокой плотностью (которая влияет на модуль упругости, прочность, проницаемость и т.д.), чем сравниваемый пеноматериал, который не содержит белок, или сравниваемый пеноматериал, который содержит любое количество водорастворимой полипептидной фракции.
Аналогично, следует понимать, что водонерастворимая/вододиспергируемая белковая фракция может быть получена с использованием ряда подходов, которые подробно описаны в примерах и в ожидающей одновременного рассмотрения заявке на патент США с порядковым номером 12/719521, поданной 8 марта 2010 года, описание которой включено здесь посредством ссылки. Например, неочищенная водонерастворимая/вододиспергируемая белковая фракция может быть выделена из белкового изолята сои путем промывания водой для удаления водорастворимых белков и водорастворимых компонентов из белкового изолята сои. Хотя неочищенная водонерастворимая/вододиспергируемая белковая фракция может диспергировать ряд масел, в зависимости от конкретного применения она может быть предпочтительной для выделения более чистой формы водонерастворимой/вододиспергируемой белковой фракции. Один подход для получения как водорастворимых белковых фракций, так и водонерастворимых/вододиспергируемых белковых фракций показан схематично на фигуре 1.
Как показано на фигуре 1, исходный материал (например, размолотую муку) диспергируют в водной среде (например, воде) при рН 6,5-13 в течение по меньшей мере 5 минут, по меньшей мере 20 минут, по меньшей мере 40 минут или по меньшей мере 1 часа с образованием смеси. Исходные материалы включают, без ограничения, белок молочной сыворотки, муку канолы, белковый изолят канолы, муку клещевины, белковый изолят клещевины, соевую муку или белковый изолят сои, или их комбинацию. Затем, необязательно, рН смеси может быть понижен добавлением кислоты (для обеспечения смеси с рН в диапазоне, например, 4,0-5,0) для осаждения как части водорастворимых белков, так и водонерастворимых белков. В этот момент водорастворимые белки могут быть отделены от осадка сбором супернатанта. Следует понимать, что, в некоторых вариантах осуществления, водорастворимая белковая фракция может быть собрана перед стадией снижения рН (см. фигуру 1). Другими словами, исходный материал диспергируют в водной среде (например, воде) и водорастворимый материал (содержащий водорастворимую белковую фракцию) отделяют от водонерастворимого материала с использованием общепринятых способов разделения. Альтернативно, водорастворимый белок может быть собран после снижения рН или может быть собран из промывок, например, водных промывок, водонерастворимого материала (см. фигуру 1). Понятно, что водорастворимый белок может быть получен объединением двух или более водных фракций, собранных на различных стадиях, которые содержат водорастворимый белок.
Остаточный водонерастворимый материал (например, осадок) может быть собран. Затем собранный материал может быть промыт (при определенных обстоятельствах промыт экстенсивно) водой и оставшийся водонерастворимый/вододиспергируемый материал собирают.
Вышеописанные процедуры выделения белка могут быть модифицированы для использования водно-спиртовой смеси вместо простой воды. Например, водорастворимые белки могут быть выделены промыванием растительного или животного материала водно-спиртовой смесью и просто сбором белков, которые растворяются в водно-спиртовой смеси. Пригодными для условий выделения считаются различные спирты. В некоторых вариантах осуществления спиртом является алифатический спирт, ароматический спирт или полиол, такой как PPG-2000. В некоторых вариантах осуществления отношение воды к спирту в водно-спиртовой смеси находится в диапазоне от 10:1 до 5:1, от 5:1 до 2:1, от 2:1 до 1:2, от 1:2 до 1:5 или от 1:5 до 1:10.
Понятно, что водорастворимую белковую фракцию и/или водонерастворимую/вододиспергируемую белковую фракцию можно использовать как таковую или можно высушить и хранить до использования. Сушка может быть выполнена способами, известными в данной области, включая сушку распылением, сушку замораживанием, сушку в сушильном шкафу, сушку в вакууме или воздействие обезвоживающих солей (таких как пентоксид фосфора или хлорид лития).
Понятно, что способ может также включать одну или несколько стадий расщепления ферментами и/или химического гидролиза. Расщепление можно облегчить использованием одного или нескольких ферментов, а гидролиз можно облегчить использованием одного или нескольких химикатов, например, кислотный или щелочной гидролиз. Например, исходный материал (например, размолотая мука) может быть подвергнут ферментативному расщеплению до или после, или как до, так и после инкубирования исходного материала в щелочной водной среде. Альтернативно или дополнительно, стадия ферментативного расщепления может быть выполнена на материале после добавления кислоты для обеспечения смеси с рН в диапазоне 4,0-5,0. Альтернативно или дополнительно, собранная водорастворимая белковая фракция и/или водонерастворимый/вододиспергируемый материал после сбора могут быть подвергнуты ферментативному расщеплению. Химический гидролиз, однако, можно выполнять с использованием стадий ферментативного расщепления или заменять стадии ферментативного расщепления, указанные выше.
При некоторых обстоятельствах остаточные щелочные частицы и щелочные металлы, присутствующие в химически расщепленных белках, являются несовместимыми с полиизоцианатами и могут вызывать тримеризацию изоцианатных групп, приводя к проблемам стабильности в конечных полиизоцианатных композициях. Ферментативное расщепление, однако, может быть использовано во избежание или для уменьшения проблем стабильности изоцианата, связанных с некоторыми стадиями химического гидролиза.
Понятно, что ферменты, применимые для расщепления белковых фракций, включают эндо- или экзопротеазу бактериального, грибного, животного или растительного происхождения или их смесь. Применимые ферменты включают, например, серин-, лейцин-, лизин- или аргинин-специфическую протеазу. Примеры ферментов включают трипсин, химотрипсины A, B и C, пепсин, реннин, микробные щелочные протеазы, папаин, фицин, бромелаин, катепсин B, коллагеназу, микробные нейтральные протеазы, карбоксипептидазы A, B и C, камозиназу, анзериназу, V8-протеазу из Staphylococcus aureus и многие другие, известные в данной области. Могут быть также использованы комбинации указанных протеаз.
Также коммерчески доступны ферментные препараты, такие как, например, Alcalase®, Chymotrypsine 800s, Savinase®, Kannase®, Everlase®, Neutrase®, Flavourzyme® (все доступные от Novo Nordisk, Denmark), Protex 6.0L, Peptidase FP, Purafect®, Purastar OxAm®, Properase® (доступные от Genencor, USA), Corolase L10 (Rohm, Germany), пепсин (Merck, Germany), папаин, панкреатин, proleather N и Протеаза N (Amano, Japan), BLAP и BLAP-варианты, доступные от Henkel, K-16-подобные протеазы, доступные от KAO, или их комбинации. В таблице 1 ниже описывается аминокислотная специфичность некоторых применимых эндонуклеаз.
В зависимости от выбранного фермента (выбранных ферментов) ферментативное расщепление обычно проводят в водных условиях при подходящих условиях рН (например, в зависимости от фермента или смеси ферментов при нейтральном или низком рН). В некоторых системах расщепления расщепление оптимально имеет место при рН менее 9 или менее 8. Для некоторых случаев применения, рН водной системы расщепления белков находится в диапазоне 3-9, 4-8 или 5-7,5. Как только расщепления произошло до желаемой степени, ферментативную реакцию можно остановить и полученный продукт можно, необязательно, промыть и затем использовать как таковой или высушить с образованием порошка.
Физические и химические свойства полученной водорастворимой белковой фракции и водонерастворимой/вододиспергируемой белковой фракции описаны подробно ниже.
В некоторых вариантах осуществления белки в выделенных белковых фракциях являются модифицированными. Подходящие способы модификации или дериватизации полипептидных фракций представлены в литературе. Природа и степень модификации будут зависеть в значительной части от состава исходного материала. Производное может быть получено, например, заменой по меньшей мере части первичных аминогрупп указанного выделенного белка гидроксильными группами, деаминированием белка или заменой части амидных групп белка карбоксильными группами и т.д. В других вариантах осуществления описанные здесь выделенные полипептидные композиции могут быть получены путем взаимодействия белка с модифицирующими белок агентами, например, оксидом азота (I), азотистой кислотой, солями азотистой кислоты или их комбинацией.
A. Водорастворимая полипептидная композиция, способная стабилизировать пеноматериал на основе полиуретана
Водорастворимые белковые фракции, например, водорастворимые белковые фракции, выделенные согласно протоколу, представленному на фигуре 1, являются по существу или полностью растворимыми в воде.
Водорастворимые белковые фракции имеют один или несколько из следующих признаков: (a) полоса поглощения амида-I между приблизительно 1633 см-1 и 1680 см-1, как определено FTIR твердого состояния; (b) полоса амида-II между приблизительно 1522 см-1 и 1560 см-1, как определено FTIR твердого состояния; (c) две выраженные полосы поглощения валентных колебаний N-H 1° амида с центрами в области около 3200 см-1 и около 3300 см-1, как определено FTIR твердого состояния; (d) выраженный кластер протонированных ядер азота, определяемый в границах химического сдвига 15N в области около 94 м.д. и около 100 м.д., и в границах химического сдвига 1H в области около 7,6 м.д. и 8,1 м.д., как определено с помощью жидкофазного двумерного ЯМР протон-азотного взаимодействия; (e) средняя молекулярная масса между приблизительно 600 и приблизительно 2500 Дальтон, например, как определено MALDI масс-спектроскопией; и (f) неспособность стабилизировать эмульсию типа масло-в-воде, в которой, когда водный раствор, содержащий 14 массовых частей белка, растворенных или диспергированных в 86 массовых частях воды, смешивают с 14 массовыми частями полимерного дифенилметандиизоцианата (PMDI), водный раствор и PMDI образуют нестабильную суспензию, которая макроскопически разделяется на фазы при статических условиях в течение пяти минут после смешивания; (g) водорастворимая полипептидная композиция способна стабилизировать пеноматериал на основе полиуретана относительно пеноматериала на основе полиуретана, образованного из той же самой исходной композиции, но лишенной водорастворимой белковой композиции; и (h) водорастворимая полипептидная композиция способна уменьшать плотность пеноматериала на основе полиуретана по меньшей мере на 5% (например, по меньшей мере на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%) относительно пеноматериала на основе полиуретана, образованного из той же самой исходной композиции, но которая лишена водорастворимой полипептидной композиции.
В некоторых вариантах осуществления водорастворимые полипептидные композиции содержат значительное количество первичных аминов, карбоновых кислот, солей аминов и карбоксилатных солей относительно водонерастворимой/вододиспергируемой белковой фракции. Водорастворимая белковая фракция содержит относительно высокую концентрацию первичных аминов (в области около 3300 и 3200 см-1) относительно вторичного амина (в области около 3275 см-1), как видно на фигурах 4, 6 и 9.
B. Водонерастворимая/вододиспергируемая полипептидная композиция
Водонерастворимая/вододиспергируемая полипептидная композиция характеризуется несколькими физическими и химическими свойствами.
Одним важным свойством водонерастворимой/вододиспергируемой белковой фракции является то, что она способна диспергировать или эмульгировать масло в воде или воду в масле (см. пример 3). Белковая фракция, которая имеет такие свойства, обычно включает один или несколько из следующих признаков: (a) полоса поглощения амида-I между приблизительно 1620 см-1 и 1632 см-1 и (b) полоса амида-II между 1514 см-1 и 1521 см-1, как определено FTIR твердого состояния; (b) выраженная полоса поглощения валентных колебаний N-H 2° амида с центром в области около 3272 см-1, как определено FTIR твердого состояния; (c) средняя молекулярная масса между приблизительно 600 и приблизительно 2500 Дальтон и (d) два кластера протонированного азота, определяемые в границах химического сдвига 15N в области около 86,2 м.д. и около 87,3 м.д., и в границах химического сдвига 1H в области около 7,14 м.д. и около 7,29 м.д. для первого кластера и в границах химического сдвига 1H в области около 6,66 м.д. и 6,81 м.д. для второго кластера, как определено с помощью жидкофазного двумерного ЯМР протон-азотного взаимодействия.
В противоположность водорастворимой белковой композиции, водонерастворимая/вододиспергируемая фракция способна диспергировать или эмульгировать масло в воде или воду в масле сообразованием гомогенной эмульсии, стабильной, согласно визуальному обследованию в течение по меньшей мере 5 минут. В некоторых вариантах осуществления эта дисперсия или эмульсия по существу не проявляет разделения фаз, согласно визуальному обследованию, в течение по меньшей мере 10, 15, 20, 25 или 30 минут, или даже 1, 2, 3, 4, 5, 6, 9, 12, 18 или 24 часов после смешивания полипептидной композиции с маслом. Как показано на фигуре 3, водонерастворимая/вододиспергируемая фракция способна эмульгировать или диспергировать широкое разнообразие масел, включающих, например, органический полиизоцианат (например, PMDI), минеральное масло, соевое масло, дериватизованное соевое масло, касторовое масло, дериватизованное касторовое масло, дибутилфталат, эпоксидированное соевое масло, кукурузное масло, растительное масло, триглицерид каприловой кислоты, эвкалиптовое масло и трибутил-о-ацетилцитарт. В типичном анализе 14 массовых частей пробы представляющего интерес белка смешивают с 86 массовыми частями воды и полученный раствор или дисперсию смешивают с 14 массовыми частями масла, например, PMDI. При этих условиях, водонерастворимая/вододиспергируемая белковая фракция образует дисперсию или эмульсию, которая по существу не обнаруживает разделения фаз при визуальном обследовании в течение по меньшей мере 5 минут после смешивания полипептидной композиции с маслом.
В некоторых вариантах осуществления водонерастворимая/вододиспергируемая фракция по существу не содержит первичных аминов, карбоновых кислот, солей аминов и карбоксилатных солей. Водонерастворимая белковая/вододиспергируемая белковая фракция имеет более высокую долю вторичных аминов относительно водорастворимой белковой фракции (см. пример 1).
Водонерастворимая/вододиспергируемая белковая фракция может действовать в качестве поверхностно-активного вещества в отношении органического полиизоцианата (например, PMDI), снижая межфазное натяжение до точки, где водонерастворимый органический полиизоцианат легко эмульгируется с минимальным подводом энергии, образуя эмульсию типа масло-в-воде. Когда исходным материалом является соевый белок, может быть получена стабильная эмульсия с использованием нерасщепленного, по существу нерастворимого (фракционированного) белка. В некоторых вариантах осуществления стабильной эмульсии полиизоцианата (например, PMDI) в воде можно добиться, когда выделенный фракционированный полипептид содержит водонерастворимую/вододиспергируемую фракцию, либо отдельно, либо в комбинации с водорастворимым компонентом. В своей сухой порошкообразной форме водонерастворимый/вододиспергируемый полипептид также способен к диспергированию в масле, например, PMDI. Таким образом, в некоторых вариантах осуществления водонерастворимый полипептид может быть предварительно диспергирован в реагенте на основе изоцианата в отсутствие воды.
В некоторых вариантах осуществления описанные здесь водорастворимые и/или водонерастворимые полипептидные фракции могут иметь средневесовую молекулярную массу между приблизительно 500 и 25000 Дальтон. Применимые полипептидные фракции могут иметь средневесовую молекулярную массу между приблизительно 600 и 2500 Да, между приблизительно 700 и 2300 Да, между приблизительно 900 и 2100 Да, между приблизительно 1100 и 1900 Да, между приблизительно 1300 и 1700 Да, между приблизительно 1000 и 1300 Да, между приблизительно 2000 и 2500 Да или между приблизительно 1000 и 2500 Да.
Выделенная полипептидная композиция может быть использована для получения пеноматериалов, как описано в данном документе, путем объединения их с реакционноспособным форполимером. Реакционноспособные форполимеры могут быть выбраны из группы, состоящей из органического полиизоцианата; продукта реакции между органическим полиизоцианатом и полипептидом, полиола, полиола на основе амина, аминсодержащего соединения, гидроксисодержащего соединения, водонерастворимой/вододиспергируемой полипептидной композиции, водорастворимого полипептида или их комбинации. Понятно, однако, что пеноматериалы необязательно должны быть на основе изоцианата. Необязательные пеноматериалы могут включать любую жидкость, жидкий раствор или смесь жидкостей, которые способны полимеризоваться или желатинироваться с образованием жесткой структуры в присутствии вспенивающего агента. Жидкие смеси могут включать, например, поливинилхлоридные (PVC) пластизоли; жидкости могут включать полимеризируемые мономеры, такие как стирол и метилметакрилат; жидкие растворы могут включать полимеры, растворенные в растворителях, такие как полистирол, растворенный в сверхкритическом CO2 или толуоле. Альтернативно или дополнительно, жидкости могут также содержать форполимеры, такие как эпоксисодержащие соединения; продукт реакции между эпоксисодержащим соединением и полипептидом, полиол, полиол на основе амина, аминсодержащее соединение, гидроксисодержащее соединение или их комбинацию; органосилан; полимерный латекс; полиуретан; и их смесь.
При получении пеноматериалов выделенная полипептидная композиция, в некоторых вариантах осуществления, способна диспергировать реакционноспособный форполимер в водной среде с получением стабильной дисперсии или стабильной эмульсии. Дисперсия или эмульсия по существу не проявляет разделения фаз при визуальном обследовании в течение по меньшей мере 5 минут после смешивания полипептидной композиции с реакционноспособным форполимером. В некоторых вариантах осуществления дисперсия или эмульсия по существу не проявляет разделения фаз при визуальном обследовании в течение по меньшей мере 10, 15, 20, 25 или 30 минут, или даже 1, 2, 3, 4, 5, 6, 9, 12, 18 или 24 часов после смешивания полипептидной композиции с реакционноспособным форполимером. В некоторых вариантах осуществления дисперсия или эмульсия по существу не проявляет разделения фаз при визуальном обследовании в течение по меньшей мере 10, 15, 20, 25 или 30 минут или даже 1, 2, 3, 4, 5, 6, 9, 12, 18 или 24 часов после смешивания полипептидной композиции с маслом. Как показано в примере 3, водонерастворимая/вододиспергируемая фракция способна эмульгировать или диспергировать большой набор масел, включая, например, органический полиизоцианат (например, PMDI), минеральное масло, соевое масло, дериватизованное соевое масло, моторное масло, касторовое масло, дериватизованное касторовое масло, дибутилфталат, эпоксидированное соевое масло, кукурузное масло, растительное масло, триглицерид каприловой кислоты, эвкалиптовое масло и трибутил-о-ацетилцитрат. В типичном анализе 14 массовых частей пробы представляющего интерес белка смешивают с 86 массовыми частями воды и полученный раствор или дисперсию смешивают с 14 массовыми частями масла, например, PMDI. При данных условиях водонерастворимая/вододиспергируемая белковая фракция образует дисперсию или эмульсию, которая по существу не проявляет разделения фаз при визуальном обследовании в течение по меньшей мере 5 минут после смешивания полипептидной композиции с маслом.
В некоторых вариантах осуществления водонерастворимая/вододиспергируемая белковая фракция обеспечивает стабильную эмульсию или дисперсию, например, водную эмульсию или дисперсию, содержащую приблизительно от 1% до приблизительно 90% (мас./мас.) масла и приблизительно от 1% до приблизительно 99% (мас./мас.) выделенной полипептидной композиции, причем выделенная полипептидная композиция образует стабильную эмульсию или дисперсию масла в водной среде. Водная эмульсия или дисперсия необязательно содержит приблизительно от 1% до приблизительно 50% (мас./мас.) масла и приблизительно от 1% до приблизительно 99% (мас./мас.) выделенной полипептидной композиции. Термин «стабильные» при использовании со ссылкой на дисперсии и эмульсии относится к способности описанной здесь полипептидной фракции создавать кинетически стабильную эмульсию в течение всего срока предполагаемого применения данной дисперсии или эмульсии. Термины «эмульсия», «дисперсия» и «суспензия» используются в описании взаимозаменяемо.
II. Реагент на основе изоцианата
Используемый в описании термин «реагент на основе изоцианата» предназначен для обозначения соединения, которое содержит изоцианатную группу. Большое разнообразие содержащих изоцианат соединений известно в области, относящейся к получению пенополиуретанов, и такие соединения применимы в практике осуществления настоящего изобретения.
В некоторых вариантах осуществления реагент на основе изоцианата содержит уретан, аллофанат, мочевину, биурет, карбодиимид, уретонимин, изоцианурат или их комбинацию. Когда реагент на основе изоцианата содержит уретан, он может быть получен путем взаимодействия органического изоцианата с полиолом или другим гидроксильным соединением.
В некоторых вариантах осуществления, реагентом на основе изоцианата является органический полиизоцианат. Используемый в описании термин «полиизоцианат» относится к дифункциональным изоцианатным соединениям, изоцианатным соединениям с более высоким количеством функциональных групп и их смесям. В зависимости от обстоятельств, реакционноспособный полиизоцианат объединяют с описанным здесь выделенным и фракционированным полипептидом для образования представленных в описании композиций. Альтернативно, реагент на основе изоцианата может быть продуктом, образованным реакцией органического полиизоцианата и соединения, содержащего нуклеофильную функциональную группу, способную реагировать с изоцианатной группой. Типичные соединения, содержащие нуклеофильную функциональную группу, способную реагировать с изоцианатной группой, включают полипептид, полиол, полиол на основе амина, аминсодержащее соединение, гидроксисодержащее соединение или их комбинацию. В некоторых других вариантах осуществления используют аллофанатные форполимеры. Аллофанатные форполимеры требуют более высоких температур (или аллофанатных катализаторов) для облегчения реакции полиола с полиизоцианатом с образованием аллофанатного форполимера.
Как отмечалось выше, органический полиизоцианат может быть получен из «базового полиизоцианата». Используемый в описании термин «базовый изоцианат» относится к мономерному или полимерному соединению, содержащему по меньшей мере две изоцианатные группы. Конкретное соединение, используемое в качестве базового полиизоцианата, может быть выбрано таким образом, чтобы обеспечивать пеноматериал, имеющий определенные желаемые свойства. Например, базовый полиизоцианат может быть выбран на основе среднечисленного количества изоцианатных функциональных групп соединения. Например, в некоторых вариантах осуществления, базовый полиизоцианат может иметь среднечисленное количество изоцианатных функциональных групп 2,0 или более, или более чем 2,1, 2,3 или 2,4. В некоторых вариантах осуществления количество реакционноспособных функциональных групп полиизоцианатного компонента находится в диапазоне от более чем 1 до нескольких сотен, 2-20 или 2-10. В некоторых других вариантах осуществления количество реакционноспособных функциональных групп полиизоцианатного компонента составляет по меньшей мере 1,9. В некоторых других вариантах осуществления количество реакционноспособных функциональных групп полиизоцианатного компонента равно приблизительно 2. Типичные коммерческие полиизоцианаты (имеющие количество изоцианатных функциональных групп в диапазоне 2-3) могут быть чистыми соединениями, смесями чистых соединений, олигомерными смесями (важным примером является полимерный MDI) и их смесями.
Применимые базовые полиизоцианаты имеют, в одном варианте, среднечисленную молекулярную массу приблизительно от 100 до приблизительно 5000 г/моль, приблизительно от 120 до приблизительно 1800 г/моль, приблизительно от 150 до приблизительно 1000 г/моль, приблизительно от 170 до приблизительно 700 г/моль, приблизительно от 180 до приблизительно 500 г/моль или приблизительно от 200 до приблизительно 400 г/моль. В некоторых других вариантах осуществления по меньшей мере 80 мол.% или более чем 95 мол.% изоцианатных групп базовой полиизоцианатной композиции связаны с ароматической группой. В некоторых вариантах осуществления описанные здесь пеноматериалы имеют концентрацию свободных органически связанных изоцианатных (-NCO) групп в диапазоне приблизительно от 5% до 35% (мас./мас.), приблизительно 7%-31% (мас./мас.), 10%-25% (мас./мас.), 10%-20% (мас./мас.), 15%-27% (мас./мас.).
В некоторых вариантах осуществления базовым полиизоцианатом является ароматический полиизоцианат, такой как п-фенилендиизоцианат; м-фенилендиизоцианат; 2,4-толуолдиизоцианат; 2,6-толуолдиизоцианат; нафталиндиизоцианаты; дианизидиндиизоцианат; полиметиленполифенилполиизоцианаты; 2,4'-дифенилметандиизоцианат (2,4'-MDI); 4,4'-дифенилметандиизоцианат (4,4'-MDI); 2,2'-дифенилметандиизоцианат (2,2'-MDI); 3,3'-диметил-4,4'-бифенилендиизоцианат; их смеси; и т.п. В некоторых вариантах осуществления в качестве базового полиизоцианата используют полиметиленполифенилполиизоцианаты (полиизоцианаты ряда MDI), имеющие среднечисленное количество функциональных групп более 2.
В некоторых вариантах осуществления базовый полиизоцианат MDI имеет объединенное содержание 2,4'-MDI и 2,2'-MDI менее 18,0%, менее 15,0%, менее 10,0% или менее 5,0%.
В некоторых других вариантах осуществления в качестве полиизоцианатов для применения в качестве базового полиизоцианата используют изомеры MDI-диизоцианатов, смеси этих изомеров с полиметиленполифенилполиизоцианатами с тремя или более функциональными группами, сами полиметиленполифенилполиизоцианаты с тремя или более функциональными группами и не представляющие форполимер производные полиизоцианатов ряда MDI (такие как производные, модифицированные карбодиимидом, уретонимином и/или изоциануратом). В некоторых других вариантах осуществления базовая полиизоцианатная композиция содержит алифатический полиизоцианат (например, в небольшом количестве), например, алифатический полиизоцианат, включающий изофорондиизоцианат, 1,6-гексаметилендиизоцианат, 1,4-циклогексилдиизоцианат, или насыщенные аналоги вышеупомянутых ароматических полиизоцианатов, или их смеси.
В некоторых других вариантах осуществления базовый полиизоцианат включает полимерный полиизоцианат, например, полимерные продукты дифенилметандиизоцианата (полиметиленполифенилполиизоцианат) с количеством функциональных групп 3, 4, 5 или более. В некоторых вариантах осуществления полимерные полиизоцианаты ряда MDI включают полиизоцианат RUBINATE-M® или смесь изомеров MDI-диизоцианата и олигомеров ряда MDI с более высоким количеством функциональных групп. В некоторых вариантах осуществления базовый полиизоцианатный продукт имеет содержание свободной группы -NCO приблизительно 31,5 мас.% и среднечисленное количество функциональных групп приблизительно 2,7.
В некоторых вариантах осуществления форполимеры с концевой изоцианатной группой представляют собой уретановые форполимеры. Они могут быть получены реакцией соединения с гидроксильной функциональной группой и соединения с изоцианатной функциональной группой. В некоторых других вариантах осуществления используют аллофанатные форполимеры. Аллофанатные форполимеры обычно требуют более высоких температур (или аллофанатных катализаторов) для облегчения реакции полиола с полиизоцианатом с образованием аллофанатного форполимера.
Полиизоцианаты, используемые в описанных композициях, могут иметь формулу R(NCO)n, где n равно 2 и R может быть ароматическим, циклоалифатическим, алифатическим, каждый из которых имеет от 2 до приблизительно 20 атомов углерода. Примеры полиизоцианатов включают, но не ограничиваются ими, дифенилметан-4,4'-диизоцианат (MDI), толуол-2,4-диизоцианат (TDI), толуол-2,6-диизоцианат (TDI), метилен-бис(4-циклогексилизоцианат (Hi2MDI), 3-изоцианатометил-3,5,5-триметилциклогексилизоцианат (ÏPDI), 1,6-гександиизоцианат (HDI), нафталин-1,5-диизоцианат (NDI), 1,3- и 1,4-фенилендиизоцианат, трифенилметан-4,4',4”-триизоцианат, полимерный дифенилметандиизоцианат (PMDI), м-ксилолдиизоцианат (XDI), 1,4-циклогексилдиизоцианат (CHDI), изофорондиизоцианат, изомеры, димеры, тримеры и смеси или комбинации двух или более из них. Термин “PMDI” включает смеси PMDI, в которых присутствует мономерный MDI, например, 4,4'-, 2,2'- и/или 2,4'-MDI. В одном варианте осуществления PMDI получают фосгенированием соответствующих PMDA в присутствии инертного органического растворителя. В свою очередь, PMDA получают с помощью кислотной анилин-формальдегидной конденсации, которая может быть проведена в промышленных условиях либо непрерывно, либо периодически. Пропорции дифенилметандиаминов и гомологичных полифенилполиметиленполиаминов и их позиционная изомерия в PMDA регулируются выбором соотношений анилина, формальдегида и кислотного катализатора, а также посредством подходящей температуры и подходящего временного профиля пребывания в реакторе. Высокие значения содержания 4,4'-дифенилметандиамина вместе с одновременно низкой долей 2,4'-изомера дифенилметандиамина получают в промышленном масштабе за счет использования сильных минеральных кислот, таких как хлористоводородная кислота, в качестве катализатора при анилин-формальдегидной конденсации.
На уровень ковалентного сшивания, который оказывает влияние на жесткость пеноматериала, может влиять количество реакционноспособных функциональных групп мономеров. Количества реакционноспособных функциональных групп, обсуждаемые здесь, должны пониматься как среднечисленные количества для полимерных или олигомерных материалов (таких как полимерные полиолы, полиизоцианатные форполимеры, модифицированные уретонимин-карбодиимидом полиизоцианаты и полимерные изоцианаты ряда MDI) и абсолютные количества для чистых соединений. Количество реакционноспособных функциональных групп полиизоцианатного компонента находится в диапазоне от более 1 до нескольких сотен, 2-20 или 2-10. В некоторых вариантах осуществления количество полиизоцианатных функциональных групп равно по меньшей мере 1,9 или по меньшей мере 2,0.
Полиизоцианаты, которые являются коммерчески доступными, могут быть чистыми соединениями, смесями чистых соединений, олигомерными смесями (важным примером является полимерный MDI) и смесями вышеуказанных соединений. Диапазон количеств изоцианатных функциональных групп для коммерческих полиизоцианатов понимается в данной области как диапазон от 2 до 3. Чем выше количества реакционноспособных функциональных групп мономеров, используемых для получения пеноматериалов, тем выше должна быть плотность полимерной сетки. Сшитые в очень высокой степени пенополиуретаны склонны проявлять жесткость (твердость).
Степень сшивания не является единственным фактором, который определяет жесткость (или эластичность) пенополиуретана. Жесткость главной цепи матричного полимера, которая определяется жесткостью исходных мономеров, может также влиять на жесткость пеноматериала. Мономеры, имеющие в высокой степени жесткую главную цепь, могут образовывать жесткие пеноматериалы, которые не сшиваются или только слегка сшиваются. Примеры относительно жестких мономеров включают мономеры, имеющие высокую концентрацию ароматических колец. Комбинирование ароматического полиизоцианата и ароматического полиола приводит к образованию полимера с жесткой главной цепью, следовательно, полимер имеет склонность к жесткости и пеноматериалы, изготовленные из него, являются жесткими.
На эластичность полимера влияют также вторичные межцепочечные силы, такие как образование водородной связи и кристалличность. Поскольку полиуретаны и полимочевины, образуемые в результате реакции полиизоцианатов и полифункциональных мономеров с активным водородом, как правило, имеют высокие концентрации групп “-NH” вдоль главной цепи полимера, они часто связаны водородными связями. Эквивалентные массы мономеров определяются количеством групп “-NH” вдоль главной цепи полимера. В результате, применение мономеров с более низкой эквивалентной массой функциональных групп дает полимер, имеющий больше групп “-NH” в его структуре. Они, следовательно, имеют больше водородных связей между цепями и, таким образом, часто являются более жесткими. При всех прочих равных факторах, применение мономеров с более высокими эквивалентными массами ведет к уменьшению количества водородных связей между цепями полимера, приводя к получению более эластичного полимера. Группы мочевины склонны образовывать больше водородных связей, чем уретановые группы, так что высокая концентрация мочевины в структуре полимера приводит к более жесткому материалу, чем материал только с уретановыми группами.
Способность главной цепи полимера образовывать кристаллические, или микрокристаллические, домены во всем материале может также оказывать существенное влияние на жесткость материала. Такая способность иногда реализуется в полиуретанах, имеющих очень регулярно повторяющиеся структуры, и такие материалы могут быть очень жесткими. Вместе с тем, кристалличность может быть легко разрушена ковалентными поперечными связями (сшивками) и другими неправильностями в структуре главной цепи. Имеется пример случая, когда один фактор (например, кристалличность) может сталкиваться с другим фактором (например, сшиванием). Понятно, что действия различных факторов, регулирующих степень жесткости пеноматериала, не всегда являются аддитивными, но могут быть скорректированы для получения пеноматериалов с желаемыми свойствами, используя способы, известные специалистам с квалификацией в данной области.
III. Реагирующее с изоцианатом соединение
Используемый в описании термин «реагирующее с изоцианатом соединение» относится к соединению, содержащему химическую функциональную группу, реакционноспособную в отношении изоцианатной группы. Различные реагирующие с изоцианатом соединения известны в данной области, и предполагается, что они применимы в практике настоящего изобретения. Выбор конкретных реагирующих с изоцианатом соединений и относительных количеств таких соединений, используемых в пенообразующей композиции, может быть выполнен для обеспечения пеноматериалов, имеющих желаемые химические и физические характеристики.
A. Типы реагирующих с изоцианатом соединений
Реагирующие с изоцианатом соединения обычно нуклеофильно реагируют с реагентом на основе изоцианата. Реагирующие с изоцианатом соединения, пригодные для получения пенополиуретанов, могут быть органическими соединениями, содержащими множество групп с активным водородом, способных образовывать полимер в результате реакции с изоцианатом. Реакционноспособные функциональные группы, которые рассматриваются в качестве групп, подходящих для настоящего изобретения, включают, например, первичные спирты, вторичные спирты, полиолы, первичные амины, вторичные амины и карбоновые кислоты. Примеры первичных спиртов и вторичных спиртов включают алифатические спирты, тогда как первичные амины и вторичные амины включают ароматические амины и алифатические амины. Кроме того, реагирующее с изоцианатом соединение может включать водонерастворимую/вододиспергируемую белковую композицию и/или водорастворимую белковую композицию, используемые либо отдельно, либо в комбинации с любым из вышеуказанных реагирующих с изоцианатом соединений.
Выбор конкретного реагирующего с изоцианатом соединения может влиять на свойства полученного пеноматериала. Например, отличительным признаком эластичных пенополиуретанов является применение высокой концентрации по массе (относительно общей массы композиции) по меньшей мере одного эластичного полиола. Эластичные полиолы могут составлять, например, приблизительно от 25% до приблизительно 90% (мас./мас.) или приблизительно от 50% до приблизительно 70% (мас./мас.) состава пеноматериала и способствовать эластичной природе этих пеноматериалов. Эластичные полиолы сами являются полимерными материалами, обычно жидкостями или низкоплавящимися твердыми веществами, содержащими гидроксильные группы на концах цепи. Примерные эластичные полиолы имеют молекулярные массы в диапазоне 1500-12000 г/моль или 2000-8000 г/моль и имеют номинальные количества функциональных групп -OH 2-4, обычно 2-3. Эластичные полиолы, как подразумевает их название, имеют эластичные главные цепи и являются преимущественно алифатическими. Эластичная главная цепь является полимером с низкой температурой стеклования (например, менее 0°C или менее -10°C). Кроме того, желательно, чтобы соединение было жидким при температуре окружающей среды. Такие эластичные полиолы могут быть классифицированы по типу главной цепи полимера на три категории: простые полиэфиры, сложные полиэфиры и углеводороды. Хотя в полиоле может быть использован один из трех основных типов главной цепи, предполагается, что некоторые полиолы содержат два или три из этих основных типов главной цепи. Кроме того, для получения пеноматериала могут быть использованы смеси различных типов эластичных полиолов. Не ограничивающие изобретение примеры типов углеводородных главных цепей включают полибутадиены и полиизопрены, а также их гидрированные производные. Могут быть также использованы сополимеры бутадиена и изопрена и продукты гидрирования таких сополимеров. Не ограничивающие изобретение примеры типов главных цепей простого полиэфира включают полиоксипропилен, полиоксиэтилен, политетраметилен, полиоксибутилен и любые из их возможных сополимеров. Предпочтительные типы главных цепей простого полиэфира включают полиоксипропилены, полиоксиэтилены, сополимеры полиоксипропилена и полиоксиэтилена и политетраметилены.
В некоторых вариантах осуществления реагирующим с изоцианатом соединением является кэппированный полиоксиэтиленом полиоксипропиленполиол, который преимущественно имеет концевую первичную группу -ОН.
Простые полиэфирполиолы наиболее часто получают полимеризацией одного или нескольких алкиленоксидов (таких как этиленоксид, пропиленоксид, бутиленоксид или тетраметиленоксид) с молекулой-инициатором низкой молекулярной массы (такой как вода, аммиак, гликоль, триол или амин; с молекулярной массой менее 150) в присутствии катализатора. В этом синтезе могут быть использованы смеси инициаторов.
Широко используемым классом простых полиэфирполиолов являются кэппированные полиоксиэтиленом полиоксипропилендиолы и триолы, содержащие преимущественно пропиленоксид по массе. Другими широко используемыми классами простых полиэфирполиолов являются полиоксипропилендиолы и триолы. Полиоксипропиленполиолы играют важную роль в непрерывно производимом эластичном пеноматериале блоков пенопластов. Кэппированные полиоксиэтиленом полиоксипропиленполиолы играют важную роль в областях применения формованного эластичного пеноматериала. Такие кэппированные полиоксиэтиленом полиолы особенно хорошо подходят для отверждения в естественных условиях (холодной вулканизации) благодаря присутствию первичных -OH-групп в качестве преимущественных реагирующих с изоцианатом функциональных групп. Не ограничивающие изобретение примеры эластичных полиолов типа сложных полиэфирполиолов включают полиолы, образованные в результате конденсации низкомолекулярных алифатических диолов, имеющих молекулярную массу менее 150, с алифатическими дикарбоновыми кислотами с молекулярной массой менее 300, при условиях, которые стимулируют образование концевых гидроксильных групп. Предпочтительными алифатическими диолами для получения таких сложных полиэфиров являются двупервичные диолы. Некоторыми конкретными примерами сложных полиэфирдиолов являются поли(этиленадипаты), поли(бутиленадипаты), поли(диэтиленгликольадипаты) и их сополимеры. Данные алифатические сложные полиэфиры иногда дополнительно содержат очень малые количества триолов, таких как триметилолпропан, для увеличения количества гидроксильных функциональных групп. Эластичные полиолы простого полиэфирного типа, полученные из пропиленоксида и/или этиленоксида, являются особенно предпочтительными вследствие их низкой стоимости.
Полиолы, применимые для получения пеноматериалов, описанных здесь, включают все известные полиолы, например, полиолы, используемые в области полиуретанов. В некоторых вариантах осуществления полиол содержит первичные и/или вторичные гидроксильные (т.е. -OH) группы. В некоторых других вариантах осуществления полиол содержит по меньшей мере две первичные и/или вторичные гидроксильные группы на молекулу. Монофункциональные спирты (такие как алифатические спирты, ароматические спирты или гидроксил-функциональные мономеры, такие как гидроксил-функциональные акрилаты (для получения отверждаемых УФ или температурой материалов) могут быть использованы для кэппирования изоцианатной группы. В некоторых других вариантах осуществления полиол имеет функциональность по гидроксильной группе от 1,6 до 10, от 1,7 до 6, между 2-4 или от 2 до 3. В некоторых других вариантах осуществления диапазоном среднечисленной молекулярной массы для необязательных полиолов является 100-10000 г/моль, 400-6000 г/моль или 800-6000 г/моль.
В некоторых других вариантах осуществления применимыми полиолами являются сложные полиэфирполиолы или простые полиэфирполиолы, такие как алифатический простой полиэфирполиол. Одним типичным алифатическим простым полиэфирполиолом является полиоксипропиленгликоль со среднечисленной молекулярной массой в диапазоне от 1500 до 2500 г/моль.
В некоторых вариантах осуществления общее количество всего полиола или всех полиолов в реагирующем с изоцианатом компоненте составляет от 1% до 80%, или от 3% до 70%, или от 5% до 60% по массе в расчете на общую массу.
В некоторых других вариантах осуществления могут быть использованы алканоламины, содержащие первичные, вторичные и/или третичные аминные группы.
B. Количество реагирующего с изоцианатом соединения, используемое для образования пеноматериала
Относительные количества ингредиентов, используемых для образования пеноматериала, могут влиять на химические и физические свойства данного пеноматериала. Например, отношение количества изоцианатных групп в реагентах на основе изоцианата к общему количеству реагирующих с изоцианатом групп (т.е. общему количеству реагирующих с изоцианатом функциональных групп, которые, как можно ожидать, могли бы реагировать в условиях обработки, включая группы, вводимые вспенивающим агентом) является важным параметром. Отношение реактивных эквивалентов (изоцианат:реагирующие с изоцианатом группы) названо Индексом и может быть выражено в виде процента.
Получение пеноматериала из материала, имеющего Индекс менее 100%, может предполагать уменьшенное сшивание вследствие присутствия непрореагировавших концов цепи с уменьшением, тем самым, плотности сшивания. Однако одним исключением является случай, когда вода (вспенивающий агент) включена в большом избытке. В данной ситуации некоторая часть молекул воды ведет себя как физический вспенивающий агент (если тепло образующей пену реакции является достаточным для улетучивания его во время процесса пенообразования). С другой стороны, большой избыток воды просто остается в пеноматериале (высыхая со временем) и по существу не требует увеличения количества нереакционноспособных концов цепи полимера.
Получение пеноматериала из материала, имеющего Индекс выше 100%, может предполагать дополнительное сшивание. Дополнительное сшивание происходит в результате различных самореакций изоцианатных групп (-NCO-групп), а также в виде образования аллофанатных и биуретных групп. Типичные самореакции изоцианатных групп при обработке пеноматериала включают образование карбодиимида, образование уретонимина и образование изоцианурата (тримеризацию). Некоторые из продуктов таких самореакций могут также, необязательно, присутствовать в потоке жидкого предшественника полиизоцианата (базового полиизоцианата) но при расчете Индекса пеноуретановой композиции в расчет принимаются только свободные изоцианатные группы, которые остаются. Например, если в композиции присутствует большой избыток изоцианатных (-NCO) групп (соответствующих Индексу более чем 150%) и присутствует катализатор для тримеризации изоцианатных групп (катализатор тримеризации), то пеноматериал будет содержать значительные количества изоциануратных связей. Изоциануратные связи увеличивают существенно плотность поперечных связей (сшивок). Такие связи являются термостойкими и часто включаются в жесткие пеноматериалы для увеличения стойкости к воспламенению.
Индекс композиции пеноматериала является важным показателем того, насколько эластичным или жестким будет пеноматериал. Более ковалентное сшивание (более высокий Индекс) обычно означает более высокую жесткость. Диапазоны Индекса от 10% или менее (в чрезвычайных случаях, при использовании воды в очень большом избытке) до 150%, или от 70% до 125% могут быть использованы для получения эластичных уретановых пеноматериалов. Желаемым диапазоном Индекса для наиболее эластичных термоотверждающихся уретановых пеноматериалов является диапазон от 80% до 110%. Такой диапазон Индекса является также наиболее предпочтительным для полужестких и полуэластичных пеноматериалов. Термины полужесткий и полуэластичный используются взаимозаменяемо.
Диапазоны Индекса от 200% до 2500%, от 250% до 1500% или от 250% до 800% могут быть использованы для получения полиуретан-полиизоциануратных пеноматериалов. Такие пеноматериалы являются важным подклассом жестких уретановых пеноматериалов, используемых в качестве теплоизоляционных пеноматериалов в строительной промышленности. Вместе с тем, если полиизоциануратные связи не являются желаемыми, то диапазон Индекса может быть диапазоном от 90% до 1560% или от 100% до 125%.
Количества реакционноспособных функциональных групп для органических реагирующих с изоцианатом (активный водород) мономеров, подходящие для применения в реагирующих с изоцианатом компонентах композиции пеноматериала, находятся в диапазоне от более чем 1 до нескольких сотен, но гораздо чаще от 1,5 до 20, более обычно от 1,6 до 10. Наличие количества функциональных групп более 1,0 важно для удлинения цепи (роста/полимеризации), поскольку имеется более одной группы, с которой возможна реакция. Если количество функциональных групп равно 1,0, как в одноатомном спирте, то изоцианат станет кэппированным на конце, и реакция остановится, поскольку данная молекула не имеет больше реакционноспособных групп.
В некоторых вариантах осуществления количество реакционноспособных функциональных групп для всех образующих полимер, реагирующих с изоцианатом соединений, используемых в данной композиции, должно быть по меньшей мере 1,5 и в идеале по меньшей мере 2. Однако важный для промышленности класс применимых реагирующих с изоцианатом мономеров имеет количества функциональных групп в диапазоне от 1,5 до 2. Они представляют собой полиоксиалкилендиолы (которые номинально являются диолами), но фактически имеют количество гидроксильных функциональных групп менее чем 2.
IV. Вспенивающие агенты
При определенных обстоятельствах, дополнительный вспенивающий агент может быть включен в премикс для облегчения образования пеноматериала. Вспенивающий агент образует пузырьки (ячейки) в полимере, способствующие подъему пены в продукте. Большое количество вспенивающих агентов являются известными в данной области и рассматриваются как применимые в практике настоящего изобретения. Например, вспенивающий агент может быть физическим вспенивающим агентом, представляющим собой летучую композицию, которая является газом или превращается в газ в условиях, используемых для получения пеноматериала. Альтернативно, вспенивающий агент (например, CO2) может быть образован in situ во время получения пеноматериала добавлением к премиксу соединения (например, воды), которое реагирует с одним из компонентов премикса с образованием вспенивающего агента. Вспенивающие агенты такого типа являются химическими вспенивающими агентами. Следующим классом вспенивающих агентов являются агенты, которые разрушаются во время процесса образования пеноматериала с высвобождением газа (например, азо-функциональные соединения, такие как азобисдикарбонамид).
Обычно используемые физические вспенивающие агенты включают воздух, азот и диоксид углерода, которые вводят в жидкие химические предшественники пенополиуретана. Данный способ может быть использован для получения пеноматериалов высокой плотности. Вместе с тем, данная процедура может быть субоптимальной для получения пеноматериалов низкой плотности. Другие обычно используемые физические вспенивающие агенты включают летучие инертные органические соединения, имеющие точки кипения (при давлении в 1 атмосферу) от 0 до 50°C, от 10 до 40°C или от 20 до 35°C. В некоторых случаях таким органическим физическим вспенивающим агентом являются C1-C5 углеводород, С1-5 фторуглероды, C1-C5 гидрофторуглерод, C1-C5 хлоруглерод или их комбинация. Неограничивающие примеры таких физических вспенивающих агентов включают тетрафторэтаны, пентафторпропаны, метиленхлорид, н-пентан, изопентан и циклопентан.
Обычным химическим вспенивающим агентом является вода, где вода взаимодействует с двумя эквивалентами органических изоцианатных групп с высвобождением моля диоксида углерода (на молекулу воды) и образует мочевинную связь. Менее часто используемые химические вспенивающие агенты включают соединения карбоновых кислот, которые могут реагировать с изоцианатами с высвобождением диоксида углерода и образованием амидной связи.
Количество вспенивающего агента (вспенивающих агентов), используемое в пенообразующей композиции, может быть скорректировано для получения пеноматериала, имеющего желаемую плотность. Диапазон плотности для пористых полиуретанов изменяется уже от 0,1 фунта на кубический фут до любого количества, не достигая полной плотности (полная плотность является природной плотностью данного полимера, без какого-либо расширения (т.е. без пузырьков)). Количество вспенивающего агента(ов), необходимое для получения пеноматериала конкретной плотности из конкретной композиции пеноматериала, понятно специалистам с квалификацией в данной области. В случае применения, используют воду в количествах от 0,1 до 100% по массе или более реакционноспособных, образующих полимер мономеров, но более характерно от 0,2% до 20%. В случае применения, физические вспенивающие агенты используют в количествах от 1% до 50% по массе реакционноспособных (образующих полимер) мономеров, но более характерно от 0,2% до 30%.
V. Добавки
Кроме того, пенообразующий премикс может дополнительно содержать добавки для оптимизации свойств пеноматериала. Добавки включают катализаторы, удлинители (цепи), наполнители, поверхностно-активные вещества, регулирующие вязкость агенты, антиоксиданты, антибактериальные агенты, фунгициды, пигменты, неорганические микрочастицы и сшивающие агенты.
В некоторых вариантах осуществления катализатор (катализаторы) могут содержать приблизительно до 5 мас.% пенообразующей композиции. Обычно используемые катализаторы включают третичные амины и некоторые металлорганические соединения. Например, катализатором может быть триэтилендиамин, 2,2'-диметиламинодиэтиловый эфир, 2-диметиламиноэтанол, октоат двухвалентного олова, диацетат дибутилолова, дилаурат дибутилолова или их комбинация. Данные катализаторы запускают реакцию изоцианатов со спиртами и с водой. Другие катализаторы запускают тримеризацию изоцианатных групп с образованием изоциануратных групп. Их примеры включают октоат калия (2-этилгексаноат калия), ацетат калия и другие соли щелочных металлов растворимых карбоновых кислот. Ниже описаны дополнительные катализаторы, рассматриваемые в отношении их пригодности для получения описанных здесь пеноматериалов.
Дополнительные примерные катализаторы включают первичный амин, вторичный амин, третичный амин, металлорганическое соединение или их комбинацию. Примерные первичные амины включают, например, метиламин, этиламин, пропиламин, циклогексиламин и бензиламин. Примерные вторичные амины включают, например, диметиламин, диэтиламин и диизопропиламин. Примерные третичные амины включают, например, диазобициклооктан (Dabco), триэтиламин, диметилбензиламин, бисдиметиламиноэтиловый эфир, тетраметилгуанидин, бисдиметиламинометилфенол, 2,2'-диморфолинодиэтиловый эфир, 2-(2-диметиламиноэтокси)этанол, 2-диметиламиноэтил-3-диметиламинопропиловый эфир, бис(2-диаминоэтиловый)эфир, N,N-диметилпиперазин, N-(2-гидроксиэтоксиэтил)-2-азанорборнан, Tacat DP-914 (Texaco Chemical), Jeffcat®, N,N,N,N-тетраметилбутан-1,3-диамин, N,N,N,N-тетраметилпропан-1,3-диамин, N,N,N,N-тетраметилгексан-1,6-диамин, 2,2'-диморфолинодиэтиловый эфир (DMDEE) или их смесь. Примерные металлорганические соединения включают, например, меркаптид ди-н-октилолова, малеат, диацетат, дилаурат, дихлорид, бисдодецилмеркаптид дибутилолова, ацетат, этилгексоат и диэтилгексоат олова (II), Fe+3 2,4-пентандионат (FeAcAc) или фенилэтилдитиокарбамат свинца.
Примерные наполнители включают, например, инертные наполнители или активные наполнители. В некоторых вариантах осуществления инертным наполнителем является растительный, состоящий из микрочастиц материал, растительное масло, минеральное масло, двухосновные сложные эфиры, пропиленкарбонат, нереакционноспособные модифицированные ароматические углеводороды нефти и, в общем, любая содержащая неактивный водород жидкость, которая может быть включена в пеноматериал. Активным наполнителем могут быть мономер или полимеры пирролидона, мономер или полимеры оксизолидона, эпоксидированное масло или ненасыщенное масло, такое как льняное масло.
Кроме того, к пенообразующей композиции могут быть добавлены один или несколько поверхностно-активных веществ для изменения химических и физических свойств пеноматериала. В некоторых вариантах осуществления поверхностно-активное вещество (поверхностно-активные вещества) могут составлять до приблизительно 5 мас.% пенообразующей композиции. Примерные поверхностно-активные вещества включают, например, мономерные типы, полимерные типы или их смеси. Одним из обычно используемых поверхностно-активных веществ является органофункциональное соединение кремния, такое как простой полиэфир силикона. Комбинации различных силиконов могут быть выбраны, чтобы сбалансировать стабильность пеноматериала во время подъема с необходимостью открывания пор (в пенопластах с открытыми порами).
Другие добавки включают, например, антиоксиданты, противовспенивающие агенты, антибактериальные агенты, фунгициды, пигменты, регулирующие вязкость агенты, гелеобразующие агенты, аэрозолирующие агенты, неорганические микрочастицы (например, диоксид титана, желтый железоокисный пигмент, красный железоокисный пигмент, черный железоокисный пигмент, оксид цинка, оксид алюминия, тригидрат алюминия, карбонат кальция), глины, такие как монтмориллонит, увлажняющие агенты и т.п.
В некоторых вариантах осуществления, добавкой является вододиспергируемая добавка или водорастворимая добавка. Водорастворимые добавки включают соединения с гидроксильными функциональными группами и соединения с аминными функциональными группами (такие как глицерин, мочевина, пропиленгликоль, полипропиленгликоль, полиэтиленгликоль, триметилолпропан и их аддукты и т.д.), способные реагировать с полимерным изоцианатом, например, PMDI.
В других вариантах осуществления добавкой может быть сшивающий агент, например, сшивающий агент, который может быть использован для связывания лигноцеллюлозного материала со стеклом. Примерные сшивающие агенты включают органосилан, такой как диметилдихлорсилан (DMDCS), алкилтрихлорсилан, метилтрихлорсилан (MTCS), N-(2-аминоэтил)-3-аминопропилтриметоксисилан (AAPS) или их комбинацию. В других вариантах осуществления полипептидные фракции объединены с органосиланом. Термин «органосилан» относится к любой группе молекул, включающей мономеры, гидролизованные мономеры, гидролизованные димеры, олигомеры и продукты конденсации триалкоксисилана, имеющие общую формулу:
(RO)3Si-R'
где R означает предпочтительно группу пропил, этил, метил, изопропил, бутил, изобутил, втор-бутил, трет-бутил или ацетил, и R' означает органофункциональную группу, где функциональная группа может включать аминопропильную группу, аминоэтиламинопропильную группу, алкильную группу, винильную группу, фенильную группу, меркаптогруппу, стириламиногруппу, метакрилоксипропильную группу, глицидоксигруппу, изоцианатную группу или другие группы.
Аналогично, бистриалкоксисилан, имеющий общую формулу (RO)3Si-R'-Si(OR)3, может быть также использован в качестве «органосилана» либо отдельно, либо в комбинации с триалкоксисиланом, где R означает предпочтительно группу пропил, этил, метил, изопропил, бутил, изобутил, втор-бутил, трет-бутил или ацетил, и R' означает мостиковый органофункциональный остаток, который может содержать функциональную группу, выбранную из группы, состоящей из аминогрупп, алкильных групп, винильных групп, фенильных групп, меркаптогрупп и других групп. Аналогично, тетраалкоксисилан, имеющий общую формулу (RO)4Si, может быть также использован в качестве «органосилана» либо отдельно, либо в комбинации с триалкоксисиланом или бистриалкоксисиланом, где R означает предпочтительно группу пропил, этил, метил, изопропил, бутил, изобутил, втор-бутил, трет-бутил или ацетил.
Другие типы добавок, которые являются добавками более необязательного и специфического для конкретного применения характера, включают антипирены, наполнители, армирующие агенты (такие как стекловолокно, минеральные пластинки, такие как волластонит, и волокнистые предварительно отформованные заготовки (брикеты)), подавители дыма, биоциды, инертные пластификаторы, антистатические агенты, их комбинации и множество других. Квалифицированный специалист может выбрать подходящее количество таких добавок на основе свойств, желаемых для пеноматериала. Например, в некоторых ситуациях наполнители могут быть использованы при очень высоких уровнях и могут превышать массу образующих весь полимер мономеров в композиции. Наполнители могут включать дешевые микрочастицы, такие как карбонат кальция, глинистые минералы, опилки и древесные волокна. Волокнистые армирующие агенты могут быть также использованы при уровнях, превышающих массу образующих весь полимер мономеров в композиции. Другие типы необязательных добавок, когда они вообще используются, обычно используют при уровнях менее 15% или 10% в расчете на массу всей полимерной композиции. Большинство типов необязательных добавок используют отдельно при уровнях менее 5% в расчете на массу всей композиции.
Примеры антипиренов включают фосфорорганические соединения, галогенированные фосфорорганические соединения, галогенированные ароматические соединения, меламин (в качестве наполнителя), графит (наполнитель), тригидрат оксида алюминия (наполнитель), оксид сурьмы и комбинации вышеуказанных соединений. Данный перечень не должен рассматриваться как ограничивающий. Растворимые антипирены, как правило, являются предпочтительными и могут быть эффективными при более низких уровнях, чем антипирены типа наполнителей.
Подходящее использование добавок при составлении реакционных систем для пористых полиуретанов будет понятным для квалифицированных в данной области специалистов. Некоторые добавки содержат реагирующие с изоцианатом функциональные группы и, следовательно, должны учитываться при расчете Индекса композиций пеноматериалов, которые содержат такие добавки.
VI. Изготовление и характеристики полученных пеноматериалов
Настоящее изобретение обеспечивает получение разнообразных пеноматериалов, характеризующихся различными физическими и химическими свойствами. Например, пеноматериал может быть термоотверждающимся пеноматериалом или термопластичным пеноматериалом.
Термоотверждающийся пеноматериал получают взаимодействием жидких предшественников. Смешивание предшественников (реагента на основе изоцианата, реагирующего с изоцианатом агента, вспенивающего агента и полипептидной композиции) инициирует реакцию полимеризации и генерирует тепло. Тепло реакции способствует расширению пеноматериала. Формование конечного изделия пеноматериала имеет место во время процесса вспенивания и полимеризации, пока реакционная смесь является все еще текучей. В термоотверждающихся уретановых пеноматериалах матричный полимер часто является сшитым. Степень сшивания зависит от стехиометрии образующей полимер реакции и реакционноспособных функциональных групп используемых мономеров. Степень сшивания может значимо варьироваться, и степень сшивания можно корректировать для оптимизации свойств данного пеноматериала. Например, жесткие уретановые пеноматериалы обычно являются в большей степени сшитыми, чем эластичный уретановый пеноматериал.
При изготовлении термоотверждающихся пеноматериалов реагирующие с изоцианатом ингредиенты обычно объединяют со вспенивающим агентом (особенно, если вспенивающий агент содержит реагирующие с изоцианатом функциональные группы, как в случае воды) и необязательными добавками с получением жидкой смеси. Затем жидкую смесь смешивают с реагентом на основе изоцианата для инициирования полимеризации и вспенивания. В некоторых вариациях относительно общего процесса, часть реагирующих с изоцианатом ингредиентов может быть необязательно подвергнута предварительному взаимодействию со стехиометрическим избытком полиизоцианата для образования жидкого форполимера с концевыми изоцианатными группами. Форполимер позднее взаимодействует с остальными реагирующими с изоцианатом ингредиентами на конечной стадии (для завершения полимеризации и инициации вспенивания). В наиболее обычной вариации в отношении процесса с форполимером, форполимер содержит также оставшиеся мономерные полиизоцианатные компоненты (базовые полиизоцианаты). Их иногда называют полуфорполимерами, псевдофорполимерами или квазифорполимерами. Данные термины используются взаимозаменяемо. Если форполимер с концевыми изоцианатными группами не содержит мономерных полиизоцианатных компонентов, то его называют полным форполимером. Независимо от того, используется ли форполимер или не используется, наиболее распространенным режимом обработки для термоотверждающихся уретановых пеноматериалов является применение двух жидких компонентов (т.е. полиизоцианатный компонент и смесь реагирующих с изоцианатом мономеров плюс вспенивающие агенты плюс необязательные добавки). Существуют, однако, некоторые важные исключения из этого правила. Во время непрерывного изготовления блоков пенопластов из эластичного пеноматериала и слоистых листов жесткого пеноматериала часто используют три или более компонентов. Дополнительные компоненты могут содержать образующие реакционноспособный полимер ингредиенты композиции (такие как полиизоцианаты или полиолы).
Термопластичные пеноматериалы часто получают с использованием двухстадийной процедуры. Например, в некоторых вариантах осуществления, образующие полимер ингредиенты перерабатывают в твердые гранулы, которые компаундируют с любыми желаемыми добавками и вспенивающими агентами. Конечную операцию вспенивания и расширения выполняют с применением подведенного извне тела, обычно в экструдере. Подведенное извне тепло запускает процесс расширения посредством испарения летучего вспенивающего агента, разрушения химического вспенивающего агента для высвобождения газа или некоторой комбинацией этих процессов. Термопластичный пеноматериал формуют в устройствах для формования, и форма заперта, когда матричный полимер охлаждают и отверждают. Термопластичные уретановые пеноматериалы обычно являются линейными, хотя во время процесса формования может иметь место ограниченное сшивание.
Описанные здесь пенообразующие материалы могут быть использованы для получения эластичных пеноматериалов, жестких пеноматериалов или полужестких пеноматериалов. Эластичные пеноматериалы, изготовленные, например, из полиуретанов, часто имеют полимерные матрицы, которые являются эластомерами с разделяемыми фазами. Эластичная фаза полимера является частью, полученной из эластичного полиола. Поскольку эластичная фаза часто является преобладающей частью полимера по массе, она представляет собой непрерывную фазу. Неэластичная часть полимера является частью, полученной в результате взаимодействия полиизоцианатов с водой и (необязательно) низкомолекулярными гликолями с молекулярной массой менее 200. Такая «жесткая» фаза полимера обычно отделяется от мягкой фазы во время полимеризации. Хотя «фазы» ковалентно связаны друг с другом, они ведут себя так, как если бы они были раздельными. Таким образом, матричный полимер является эластомерным, но его жесткость определяется по относительным долям жесткой и мягкой фаз. Указанные относительные доли являются корректируемыми посредством выбора того, сколько эластичного полиола используется в виде процента от общей композиции.
Эластичные композиции пеноматериала раздуваются в основном или исключительно водой (иногда с добавлением воздуха или диоксида углерода, инжектируемого в потоки жидких химических предшественников). Получение пеноматериала более низкой плотности обычно требует больше воды (чтобы генерировать CO2 для расширения), которая продуцирует больше мочевинных групп в жесткой фазе и, следовательно, более высокую жесткость пеноматериала. Незначительные количества низкомолекулярных гликолей (с молекулярной массой менее 200, предпочтительно менее 150) иногда включают в композицию, если желаемым является упругий эластичный пеноматериал. Указанные гликоли обычно составляют менее 10% общей композиции, желательно менее 5%, и иногда их называют удлинителями цепи. Предпочтительными гликолями являются линейные двупервичные диолы, такие как этиленгликоль, 1,4-бутандиол, 1,6-гександиол и их комбинации. Пеноматериалы такого типа называют «высоко упругими» (или HR) пеноматериалами. Эластичные пеноматериалы обычно имеют значения плотности менее 5 фунтов на кубический фут, более характерно менее 3 фунтов на кубический фут, и являются преимущественно пеноматериалами с открытыми порами.
Эластичные пеноматериалы очень низкой плотности (менее 1 фунта на кубический фут) могут быть получены дроблением жестких пеноматериалов, которые содержат незначительные количества эластичных полиолов в фазе их матричного полимера. Дробление приводит к разрыванию жестких стержнеподобных сегментов, которые образуют границы между порами пеноматериала (называемых «распорками»). Такие эластичные пеноматериалы могут быть использованы в качестве амортизирующих материалов для автомобильных сидений, мебели и постельных принадлежностей. Значения плотности пеноматериалов для данных областей применения находятся в диапазоне от приблизительно 1,5 до 4 фунтов на кубический фут, более типично 1,8-3 фунта на кубический фут.
Эластичные пеноматериалы обычно являются пеноматериалами с открытыми порами, за исключением пеноматериалов с очень высокими значениями плотности (свыше 4 фунтов на кубический фут). Вследствие их открытой структуры пор раздувание водой является предпочтительным способом расширения пеноматериала. Эластичные пеноматериалы обычно получают с эластичной полимерной матрицей. Плотность сшивания в полимерной матрице является низкой и Индекс редко бывает выше 105% (часто бывает ниже 100%). Среднечисленное количество функциональных групп полиизоцианатов, используемых в эластичных пеноматериалах, является низким, обычно от 2 до 2,4, более характерно от 3 до 2,3.
Жесткие пеноматериалы обычно имеют жесткую пластиковую матрицу. Матричным полимером обычно является либо полиуретан, либо полиуретан-полиизоцианурат. В любом случае, используемые полиолы совершенно отличаются от типов, используемых в эластичных пеноматериалах. Жесткие полиолы совпадают до некоторой степени с эластичными полиолами в молекулярной массе, обычно находящейся в диапазоне от 400 до 2000, более часто от 500 до 1500. Жесткие полиолы могут быть сгруппированы в две широкие категории. Первой категорией являются ароматические сложные полиэфиры с низкой функциональностью, с жесткой главной цепью. Обычно их используют при получении полиуретан-полиизоциануратных пеноматериалов, и обычно они являются дифункциональными. Вторая категория включает простые полиэфиры с высокой функциональностью, имеющие количество функциональных групп от 3 до 10.
Ароматические сложные полиэфирполиолы, используемые в жестких пеноматериалах, обычно получают из кислот типа фталата (любого из трех коммерческих изомеров), сложных эфиров типа фталата, фталевого ангидрида или фталатных полимеров, таких как PET, путем их взаимодействия с низкомолекулярными гликолями (обычно с молекулярной массой менее 200). Предпочтительным гликолем для данной цели является диэтиленгликоль (DEG). Данный гликоль склонен к образованию полиэфирных смол (сложных полиэфиров), которые являются жидкими и имеют достаточно низкую вязкость для переработки в смешивающейся активированной системе. DEG обычно используется в большом избытке относительно ароматического предшественника и, тем самым, действует как реакционноспособный растворитель для полиэфирной смолы с концевой гидроксильной группой.
Простые полиэфирполиолы с высоким количеством функциональных групп получают взаимодействием пропиленоксида с инициатором с высоким количеством функциональных групп. Указанные жесткие полиолы характеризуются наличием более низких эквивалентных масс (на -ОН-группу), чем эквивалентные массы эластичных полиолов. Это является следствием более высокого количества функциональных групп при более низкой молекулярной массе. Эквивалентные массы таких полиолов обычно составляют менее чем 300, более характерно между 50 и 200. Это сравнимо с эластичными полиолами, которые обычно имеют гидроксильные эквивалентные массы более 500. Инициаторы, обычно используемые при получении жестких простых полиэфирполиолов, включают сахара, такие как сахароза, и ароматические полиамины, такие как толуолдиамины и олигомерные конденсаты формальдегида с анилином. Каждая из групп первичного амина у таких ароматических полиаминов взаимодействует с двумя или более молями пропиленоксида. Жесткие простые полиэфирполиолы, подобно ароматическим сложноэфирным полиолам, обычно разбавляют низкомолекулярными гликолями, такими как DEG, для достижения значений вязкости, которые являются достаточно низкими для активируемой смешиванием обработки.
Жесткие полиолы (любого типа) обычно дополнительно компаундируют с низкомолекулярными алифатическими гликолями, триолами, тетролами и алканоламинами. Примерами таких низкомолекулярных полиолов (которые обычно имеют молекулярные массы ниже 200) включают этиленгликоль, диэтиленгликоль, триэтиленгликоль, пропиленгликоль, дипропиленгликоль, трипропиленгликоль, бутандиолы, глицерин, триметилолпропан, диэтаноламин, триэтаноламин, дипропаноламин, трипропаноламин, их смеси и т.п.
Полимерные матрицы, используемые в жестких пеноматериалах, почти всегда являются сшитыми в более высокой степени, чем полимерные матрицы, используемые в эластичных пеноматериалах. Большая степень сшивания в указанных полимерах происходит от полиизоцианата. Среднечисленное количество функциональных групп полиизоцианатов, используемых в жестких пеноматериалах, находится обычно в диапазоне от 2,5 до 3. Жесткий полиизоцианурат-полиуретан является сшитым в очень высокой степени благодаря изоцианатным (тримерным) связям в полимере.
Существует непрерывность типов пеноматериалов между «эластичными» и «жесткими». Они могут называться полужесткими или полуэластичными. Указанные пеноматериалы могут быть получены с использованием комбинаций жестких и эластичных полиолов и полиизоцианатных функциональных групп где-нибудь от 2 до 3, но наиболее характерно от 2,5 до 2,8. Данные пеноматериалы используют в широком диапазоне структурных, энергопоглощающих и декоративных областях применения. Особенно важным применением полужестких/полуэластичных пеноматериалов является автомобильные, отлитые на месте перегородки между двигателем и кабиной водителя и защищающие колени подушки. Указанные пеноматериалы обычно отливают на месте позади декоративного, эластичного материала фрикционных накладок, такого как ткань или PVC. Значения плотности обычно находятся в диапазоне от 2 до 10 фунтов на кубический фут (иногда больше), в зависимости от применения. Поскольку такие пеноматериалы не являются теплоизоляционными, их наиболее часто раздувают водой.
Пористые полиуретаны более высокой плотности, со значениями плотности в диапазоне от более 10 фунтов на кубический фут до чуть меньше полной плотности, называют иногда «микропористыми» полиуретанами. Их используют в большом диапазоне областей применения, которые включают диапазон от эластичных подметок для обуви до жестких синтетических заместителей дерева и спектр полужестких/полуэластичных видов применения между этими крайностями. Микропористые эластичные полиуретановые подметки для обуви могут быть изготовлены с интегральными пленками. Пленки образуются самопроизвольно вследствие коллапса (сплющивания) пор пеноматериала вблизи поверхности пресс-формы. Центральная часть пеноматериала остается пористой. Такой механизм образования интегральной пенки стимулируется путем использования летучего физического вспенивающего агента, такого как гидрофторуглерод, который является жидким при температуре окружающей среды. Самопроизвольное образование пленки происходит, если температура поверхности пресс-формы ниже, чем тоска кипения физического вспенивающего агента. Пеноматериалы с интегральной пленкой используют также в других областях применения, например, для автомобильных подлокотников сидений и различного инвентаря. Подметки для обуви обычно изготавливают из композиций, которые состоят целиком (или почти целиком) из дифункциональных мономеров. Обычно Индекс равен 100% или иногда немного ниже (99%). Указанные полимеры могут быть получены из эластичных диолов (особенно сложных полиэфиров), низкомолекулярных диоловых удлинителей цепи, таких как 1,4-бутандиол или этиленгликоль, и диизоцианатов, таких как 4,4'-дифенилметандиизоцианат и его полуфорполимеры. Таким образом, полимеры, используемые в пеноматериалах для подметок обуви, являются по существу линейными. Вспенивающий агент обычно содержит небольшие количества воды. В отличие от этого, жесткие и полужесткие/полуэластичные микропористые пеноматериалы имеют более высокую степень сшивания. Выбор мономеров аналогичен выбору аналогов более низкой плотности. Вместе с тем, пеноматериалы более высокой плотности обычно являются пеноматериалами с закрытыми порами. На самом высоком конце спектра плотности полиуретановых пеноматериалов находятся инжекционно сформованные реакционные эластомеры (RIM). Они могут раздуваться целиком захватом малых количеств воздуха (или азота) в потоки жидкого предшественника. Данный процесс захвата, называемый иногда образованием активных центров, добивается изгнания газа в жидкие химикаты перед смешиванием встречных потоков и обработкой. Эластомеры RIM обычно образуются из полиизоцианат-реактивного потока, который содержит как эластичный полиол, так и наполнитель. Количество удлинителя цепи корректируют для контроля жесткости (или эластичности) эластомера. Примеры типичных наполнителей, используемых для получения указанных эластомеров, включают низкомолекулярные гликоли и ароматические диамины.
Понятно, что квалифицированный в данной области специалист, используя способы и композиции (например, водорастворимые белковые фракции и/или водонерастворимые/вододиспергируемые белковые фракции, определенных реагентов на основе изоцианата, определенные реагирующие с изоцианатом соединения и определенные добавки), описанные в данном документе, сможет создавать пеноматериалы, имеющие желаемые физические и химические свойства, например, плотность, жесткость, сжимаемость, упругость и т.д.. Например, если желаемым является пеноматериал с низкой плотностью, в премикс может быть включена водорастворимая белковая композиция. Напротив, включение водонерастворимой/вододиспергируемой белковой фракции можно использовать для создания пеноматериалов с более высокой плотностью и/или более высокой структурной целостностью, чем структурная целостность, которая может быть достигнута без белковой добавки (например, водорастворимого белка). Альтернативно, смесь водонерастворимого/вододиспергируемого белка может быть использована для создания пеноматериалов с требуемыми характеристиками.
В некоторых вариантах осуществления реагент на основе изоцианата составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) исходных материалов, используемых для получения пеноматериала. В некоторых других вариантах осуществления, реагирующее с изоцианатом соединение составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) исходных материалов, используемых для получения пеноматериала. В некоторых других вариантах осуществления, белоксодержащая композиция (например, водорастворимая полипептидная композиция) составляет приблизительно от 0,01% (мас./мас.) до приблизительно 50% (мас./мас.), или приблизительно от 0,01% (мас./мас.) до приблизительно 30% (мас./мас.), или приблизительно от 0,01% (мас./мас.) до приблизительно 10% (мас./мас.) исходных материалов, используемых для получения пеноматериала. В некоторых других вариантах осуществления пеноматериал получают при Индексе в диапазоне приблизительно от 250% до приблизительно 800%.
Понятно также, например, как показано в примере 11, что малые количества добавленных белковых композиций (например, неочищенного материала, белковых изолятов или выделенных водорастворимых и/или водонерастворимых белков) в премиксе пеноматериала может оказывать большое влияние на физические свойства полученных пеноматериалов. В некоторых вариантах осуществления премикс содержит менее 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, 0,5%, 0,1%, 0,05% или 0,01% (мас.) белковой композиции. В качестве примера, в примере 11 полиольная смесь (Часть B), составляющая приблизительно 0,09% в расчете на водорастворимую белковую фракцию, была способна модулировать плотность полученного пеноматериала.
Кроме того, полипептидная композиция может быть создана таким образом, чтобы она имела конкретный индекс полидисперсности. Кроме того, полипептидная композиция и адгезивная композиция могут быть созданы таким образом, чтобы они имели определенный индекс полидисперности. Термин «индекс полидисперсности» (PDI) относится к соотношению между средневесовой молекулярной массой  и среднечисленной молекулярной массой
и среднечисленной молекулярной массой

Термины «среднечисленная молекулярная масса», обозначаемая символом Mn и «средневесовая молекулярная масса», обозначаемая символом Mw, используются в соответствии с их общепринятыми значениями, которые могут быть найдены в общедоступной литературе. Средневесовая молекулярная масса и среднечисленная молекулярная масса могут быть определены с использованием аналитических процедур, описанных в данной области, например, хроматографических методов, седиментационных методов, методов рассеивания света, методов измерения вязкости растворов, методов анализа функциональных групп и методов масс-спектроскопии (например, масс-спектроскопии MALDI). Например, как проиллюстрировано в примере 2, средневесовую молекулярную массу и среднечисленную молекулярную массу полипептидной композиции определяли при помощи масс-спектрометрии MALDI. Кроме того, предполагается, что полипептидные композиции, имеющие различные молекулярные массы, могут обеспечивать композиции пеноматериалов, имеющие различные свойства. Как таковые, средневесовая молекулярная масса, среднечисленная молекулярная масса и индекс полидисперсности могут быть важным индикатором при оптимизации характеристик композиции пеноматериала. Кроме того, как описано в данном документе, молекулярную массу полипептидной композиции можно изменить, подвергая белки ферментативному расщеплению или фракционированию полипептидной композиции.
Далее, предполагается, что полипептидные композиции, имеющие различные молекулярные массы, могут обеспечивать адгезивные композиции, имеющие различные свойства. Как таковые, средневесовая молекулярная масса, среднечисленная молекулярная масса и индекс полидисперсности могут быть важными индикаторами при оптимизации характеристик адгезивной композиции. В частности, предполагается, что способность оптимизировать характеристики молекулярной массы полипептидных композиций обеспечивает преимущества при получении адгезивных композиций для конкретного применения. Дополнительные преимущества включают получение адгезивной композиции со сходными свойствами, даже хотя полипептидная композиция может быть получена из другого источника (например, сои в сравнении с клещевиной), или когда сходные источники белка собирают во время разных сезонов, на протяжении варьирующих периодов времени или из различных частей света. Например, белки, выделенные из сои и клещевины (каждая из которых имеет различные распределения молекулярной массы), могут быть получены так, что они имеют сходные распределения молекулярных масс, посредством описанных здесь способов расщепления и фракционирования. Соответственно, предполагается, что возможность измерять и регулировать соответствие распределений молекулярных масс является выгодной при оптимизации различных характеристик адгезивной композиции, например, долгосрочной воспроизводимости физических свойств и технологических свойств образованных адгезивов. Характеристики молекулярной массы полипептидной композиции можно изменить, подвергая белки ферментативному расщеплению или фракционированию в соответствии с описанными здесь процедурами.
В некоторых вариантах осуществления значение PDI премиксов, используемых для получения композиций пеноматериалов, описанных здесь, составляет приблизительно от 1 до приблизительно 3, от 1 до 1,5, от 1,5 до 2, от 2 до 2,5, от 2,5 до 3, от 1 до 2, от 1,5 до 2,5 или от 2 до 3.
VII. Области применения пеноматериала
Многочисленные сферы применения для пеноматериалов были описаны в данной области, и предполагалось, что пеноматериалы пригодны для большого разнообразия областей применения. Например, эластичные пеноматериалы, изготовленные с использованием описанных здесь способов, могут быть сформованы (отлиты в форме) (как в случае автомобильных сидений) или отлиты в виде блока и затем разрезаны по форме (как в случае фурнитуры и постельных принадлежностей). Другие важные виды применения эластичных полиуретановых пеноматериалов включают нижний слой (подложку) ковров.
Пеноматериалы могут быть также использованы в качестве теплоизоляции. Понятно, что одним из важных физических свойств теплоизоляционных пеноматериалов является теплопроводность. Для достижения самой низкой возможной теплопроводности жесткие пеноматериалы могут быть раздуты летучими гидрофторуглеродами (такими как пентафторпропаны). Указанные физические вспенивающие агенты имеют более низкие значения теплопроводности, чем воздух или диоксид углерода. В качестве вторичного вспенивающего агента можно использовать воду. Диапазоном плотности для жестких теплоизоляционных пеноматериалов является обычно диапазон от 1,5 до 4 или от 2 до 2,5 фунтов на кубический фут. Жесткие пеноматериалы могут быть залиты или инжектированы на месте, но чаще их получают в виде блока ламинированных досок. Затем ламинированные доски нарезают для придания формы и используют в конструировании. Жесткие теплоизоляционные пеноматериалы обычно являются пеноматериалами с закрытыми порами для удерживания вспенивающего агента с низкой теплопроводностью (гидрофторуглеводорода).
Жесткие пеноматериалы могут быть также использованы для чисто структурных видов применения, где теплопроводность не является важным фактором. Важным чисто структурным видом применения жестких пеноматериалов являются внутренние панели дверей автомобиля. Указанные материалы формуют и раздувают с использованием воды. Часто их армируют стекловолокнами для повышения структурной прочности. Короткие стекловолокна можно добавлять к потокам жидкого предшественника, обычно реагирующего с изоцианатом компонента. Чаще структурный армирующий агент представлен в форме стекломатов или предварительно отформованных заготовок, которые предварительно помещают в форму. Затем на мат наливают реагирующую пенообразующую смесь (перед закрыванием пресс-формы) или инжектируют ее через мат. Затем пена поднимается и протекает через мат в пресс-форму.
Пеноматериалы можно также использовать в качестве упаковки. Пеноматериалы для упаковки обычно раздуваются водой, имеют открытые поры и очень низкую плотность. Значения плотности пеноматериалов составляют обычно менее 2 фунтов на кубический фут и могут составлять менее чем 1 фунт на кубический фут. Такие пеноматериалы могут быть налиты или инжектированы вокруг подлежащих упаковке объектов.
ПРИМЕРЫ
Настоящее изобретение, которое описывается в данном документе в общем виде, будет легче пониматься со ссылкой на следующие примеры, которые включены только для целей иллюстрации определенных аспектов и вариантов осуществления настоящего изобретения и не предназначены для ограничения изобретения.
ПРИМЕР 1: Выделение полипептидных композиций
Процедуры для выделения и характеристики водорастворимой полипептидной композиции, водонерастворимой полипептидной композиции или их смеси описаны ниже.
Процедура А: Получение водорастворимой полипептидной композиции и получение водонерастворимой полипептидной композиции.
Расщепленный эверлазой белок из клещевины (партия 5-90 экспериментальных проб) получали от Prof. S. Braun в Laboratory of the Department of Applied Biology at the Hebrew University of Jerusalem, Israel. Расщепленную клещевину можно получить следующим образом: белок муки клещевины суспендируют в воде в соотношении приблизительно 1:10 мас./мас. Добавляют хлорид кальция до эффективной концентрации приблизительно 10 мМ и рН суспензии доводят до рН 9 добавлением 10 н. NaOH. Затем реакционную смесь нагревают до 55°C при перемешивании. Затем добавляют Everlase 16L Type EX® (NOVOZYMES') в соотношении 20 г на кг белка муки клещевины и смесь перемешивают при той же самой температуре в течение приблизительно 4 часов. Наконец, полученную смесь доводят до рН 3,5 лимонной кислотой и сушат распылением с получением порошка.
Расщепленный эверлазой белок из клещевины (партию 5-90) фракционировали с получением водорастворимой фракции и водонерастворимой, диспергируемой фракции. На первой стадии 300 г расщепленной клещевины суспендировали в 1 литре дистиллированной воды. Смесь встряхивали вручную и затем помещали в ванну ультразвукового дезинтегратора на 30 минут. Затем суспензию извлекали и давали ей отстояться в течение периода до двух дней для осаждения нерастворимой части (в отдельных экспериментах было обнаружено, что центрифугирование было в равной степени подходящим). В этот момент прозрачный желтый/янтарный супернатант извлекали пипеткой и оставляли для будущего использования. Затем к осадку добавляли свежую дистиллированную воду, чтобы довести общий объем снова до отметки 1 литр на контейнере. Затем процесс встряхивания, обработки ультразвуком, осаждения, извлечения супернатанта и повторного добавления свежей дистиллированной воды (промывания) повторяли (в целом 6 раз). На конечной стадии воду пипетировали из верхней части серовато-черного осадка и затем осадок сушили в вакуумной печи при 45°C. На основе сухой массы осадка было определено, что водонерастворимая/вододиспергируемая полипептидная фракция содержала приблизительно 50 мас.% расщепленной клещевины. Отдельно, 1-ый и 2-ой супернатанты объединяли и затем сушили с получением прозрачной, окрашенной в желтый цвет водорастворимой полипептидной фракции.
После сушки фракций подтверждали, что серовато-черный осадок (водонерастворимая и диспергируемая фракция) невозможно повторно растворить в воде. С другой стороны, высушенная фракция супернатанта (прозрачное/янтарное, стекловидное вещество) была полностью растворимой в воде.
Две фракции по отдельности анализировали с помощью FTIR твердого состояния (см. фигуры 2-4). Спектры на фигуре 2 показывают, что части карбоксилатных и аминных солей первично ассоциированы с водорастворимой фракцией. Фигура 3 показывает, что полоса валентных колебаний карбонильной группы амида и полосы изгиба N-H амида смещены к более высоким волновым числам в водорастворимой полипептидной фракции. Данные компоненты присутствуют, по-видимому, в водонерастворимой диспергируемой полипептидной фракции, но преобладающие полосы амида-I и амида-II смещены к более низким волновым числам. Помимо эффектов образования водородных связей, указанные различия, по-видимому, относятся к присутствию большей фракции групп первичного амида в водорастворимой полипептидной фракции и к большей фракции групп вторичного амида в вододиспергируемой полипептидной фракции (из полипептидных цепей главной цепи). Это подкрепляется областью валентных колебаний N-H, изображенной на фигуре 4.
Фигура 4 показывает FTIR-спектры твердого состояния выделенной фракции из расщепленной клещевины, где область валентных колебаний N-H из фигуры 2 является расширенной. Спектры масштабированы вертикально для достижения эквивалентных значений интенсивности поглощения для полосы валентных колебаний N-H вторичного амида с центром при 3275 см-1. Фигура 4 показывает, что преобладающим типом амида в вододиспергируемой фракции является вторичный амид главной цепи, как доказывается единственной, высокосимметричной полосой с центром при 3275 см-1. Хотя водорастворимая фракция также содержит данный тип амида, она содержит также существенно более высокие фракции первичных амидов, что доказывается присутствием двух полос валентных колебаний первичного N-H приблизительно при 3200 см-1 (симметричной) и приблизительно при 3300 см-1 (асимметричной), соответственно.
Данные спектры показывают, что водорастворимая полипептидная фракция объединяла относительно высокую концентрацию первичных аминов, свободных карбоновых кислот, солей кислот и солей аминов. Напротив, водонерастворимая/вододиспергируемая полипептидная фракция имела более высокую фракцию вторичных амидов. Кроме того, наблюдали, что полоса поглощения карбонильной группы амида-I для водонерастворимой/диспергируемой фракции появляется при волновом числе приблизительно 1625 см-1, тогда как полосу водорастворимой фракции наблюдали приблизительно при 1640 см-1. Как будет обсуждаться в других примерах, этот признак является одним из характерных различий между водорастворимой и водонерастворимой полипептидными фракциями; не только для белков клещевины, но также и для белков сои.
Процедура В: Дополнительная процедура для получения водорастворимой полипептидной композиции и получения водонерастворимой полипептидной композиции.
Расщепленный белок сои (партия 5-81) получали от Prof. S. Braun в Laboratory of Applied Biology at the Hebrew University of Jerusalem, Israel. Расщепленный белок сои был получен следующим образом: Изолят белка сои (изолят белка сои SOLPRO 958® Solbar Industries Ltd, POB 2230, Ashdod 77121, Israel) суспендировали в воде в соотношении 1:10 (мас./мас.). Значение рН суспензии доводили до рН 7 с помощью 10 н. NaOH и затем нагревали до 55°C при перемешивании. Затем добавляли Нейтразу 0,8 L® (NOVOZYMES') в соотношении 20 г на кг белка сои и смесь перемешивали при той же самой температуре в течение 4 часов. Полученную смесь (рН 6,5) сушили сушкой распылением с получением порошка светлого желтовато-коричневого цвета
Расщепленную сою (партия 5-90) фракционировали с получением водорастворимой полипептидной фракции и водонерастворимой/вододиспергируемой полипептидной фракции. На первой стадии 300 г расщепленной сои суспендировали в 1 литре дистиллированной воды. Смесь встряхивали вручную и затем помещали в ванну ультразвукового дезинтегратора на 30 минут. Аликвоты помещали в центрифужные пробирки и затем пробирки центрифугировали при 3400 об/мин в течение периода приблизительно 35 минут. Центрифугированный супернатант, который содержал водорастворимую фракцию, декантировали из оставшегося водонерастворимого осадка и выливали в отдельный контейнер для более позднего использования (этот прозрачный желтый супернатант помещали в открытый кристаллизатор и давали упариваться досуха при температуре 37°C). Затем, после первой стадии промывания, в пробирки добавляли свежую дистиллированную воду и оставшийся осадок диспергировали в воде с помощью ручного перемешивания шпателем. Объединенные процедуры центрифугирования, декантирования и повторного диспергирования выполняли в течение 5 циклов. После конечного цикла свободную жидкость, содержащую остаточный водорастворимый белок, декантировали из оставшейся пастообразной дисперсии (желтовато-персикового цвета). Полученная дисперсия (гравиметрически определенная как дисперсия с 16,24% сухого остатка по массе) содержала водонерастворимые/вододиспергируемые белки.
Наблюдали, что пастообразная дисперсия была стабильной в течение периода нескольких недель. Было также обнаружено, что дисперсию можно было легко объединить с водорастворимыми полимерами и с вододиспергируемыми полимерными латексами. Кроме того, дисперсия была легко совместима с PMDI (при добавлении к суспензии PMDI образовывалась стабильная дисперсия, и не было доказательства разделения фаз PMDI, даже после 24 часов). В отличие от этого, ни водорастворимый экстракт из расщепленной сои, ни сама расщепленная соя не были способны стабилизировать дисперсию PMDI в воде.
После высушивания аликвот обеих фракций подтверждали, что желтый осадок (водонерастворимый/диспергируемый экстракт) невозможно повторно растворить в воде. С другой стороны, высушенная фракция супернатанта (прозрачное/желтое твердое вещество) была полностью растворимой в воде. Два высушенных экстракта по отдельности анализировали с использованием FTIR твердого состояния (см. фигуры 8-10). Фигура 9 показывает совмещенные FTIR-спектры твердого состояния выделенных фракций из расщепленной сои, где область N-H является расширенной. Спектры вертикально масштабированы для получения эквивалентных значений интенсивности поглощения для полосы валентных колебаний N-H вторичного амида с центром при 3275 см-1. Фигура 9 показывает, что преобладающим типом амида в вододиспергируемой фракции является вторичный амид главной цепи, как доказывается единственной, высокосимметричной полосой с центром при 3275 см-1. Хотя водорастворимая полипептидная фракция также содержит данный тип амида, она также содержит значимо более высокие фракции первичных амидов, что доказывается присутствием двух полос валентных колебаний первичного N-H приблизительно при 3200 см-1 (симметричной) и приблизительно при 3300 см-1 (асимметричной), соответственно. Вместе эти спектры выявили, что водорастворимая полипептидная фракция состояла из относительно высокой концентрации первичных аминов. Напротив, водонерастворимая, диспергируемая полипептидная фракция состояла из более высокой фракции вторичных аминов.
Как показано на фигуре 8, полоса валентных колебаний карбонильной группы амида и полоса изгиба N-H амида смещены к более высоким волновым числам в водорастворимой фракции. Данные компоненты, по-видимому, присутствуют также в водонерастворимой диспергируемой фракции, но преобладающие полосы амида-I и амида-II смещены к более низким волновым числам. Помимо эффектов образования водородных связей, эти различия, по-видимому, относятся к присутствию более высокой фракции групп первичного амида (и/или первичных аминов) в водорастворимой полипептидной фракции (из аминокислотных фрагментов более низкой молекулярной массы) и к более высокой фракции групп вторичного амида в вододиспергируемой полипептидной фракции (из полипептидных цепей главной цепи). Это подкрепляется областью валентных колебаний N-H, изображенной на фигуре 9.
Фигура 9 показывает, что преобладающим типом амида в вододиспергируемой фракции является вторичный амид главной цепи, что доказывается единственной, высокосимметричной полосой с центром при 3275 см-1. Хотя водорастворимая фракция также содержит данный тип амида, она содержит также существенно более высокие фракции первичных аминов, что доказывается присутствием двух полос валентных колебаний первичного N-H при 3200 см-1 (симметричной) и приблизительно при 3300 см-1 (асимметричной), соответственно.
Несмотря на происхождение из двух разных растительных источников, водонерастворимые диспергируемые фракции из расщепленной сои и расщепленной клещевины являются спектрально сходными друг с другом. Напротив, водорастворимые полипептидные фракции, по-видимому, имеют разные FTIR-спектральные характеристики (см. фигуру 10). Кроме того, масс-спектрометрия MALDI показывает, что водорастворимые полипептидные фракции из расщепленной сои и расщепленной клещевины имеют различные характеристики молекулярной массы. Общность между этими типами водорастворимых фракций заключается в том, что они обе, по-видимому, содержат первичные амины/амиды.
Процедура С: Дополнительная процедура для получения водорастворимой полипептидной композиции и получения водонерастворимой полипептидной композиции
Муку клещевины (4,0 кг, содержание белка 24,8%) суспендировали в 0,1 M NaOH при отношении 10:1 мас./мас. муки к щелочи. Суспензию перемешивали в течение 18 часов при температуре окружающей среды и затем твердые вещества удаляли центрифугированием. Супернатант (приблизительно 32 литра) подкисляли до рН 4,5 с помощью 10 н. HCl. Белку давали осаждаться приблизительно при 10°C в течение 12 часов, прозрачный раствор супернатанта декантировали и тяжелый осадок (приблизительно 2 кг) собирали центрифугированием. Мокрый осадок лиофилизировали с получением 670 г белкового изолята.
Водонерастворимую и водорастворимую фракции получали путем экстракции водой. На первой стадии 10 г белкового изолята клещевины (партия 5-94) суспендировали в 50 г дистиллированной воды. Смесь диспергировали посредством механического перемешивания в течение 2 часов. Аликвоты помещали в центрифужные пробирки и затем пробирки откручивали при 3400 об/мин в течение периода приблизительно 35 минут. Центрифугированный супернатант, который содержал водорастворимую фракцию, декантировали из оставшегося водонерастворимого осадка и выливали в отдельный контейнер (этот прозрачный желтый супернатант сохраняли и сушили при 37°C для последующих экспериментов с дисперсиями и FTIR-анализов твердого состояния). Затем, после первой стадии промывания, в пробирки добавляли свежую дистиллированную воду и оставшийся осадок диспергировали в воде с помощью ручного перемешивания шпателем. Объединенные процедуры центрифугирования, декантирования и повторного диспергирования выполняли в общей сложности в виде 13 циклов. После конечного цикла свободную жидкость декантировали из оставшейся пастообразной дисперсии (водонерастворимой полипептидной фракции из исходного белка клещевины). После высушивания было определено, что паста содержала 28,58% сухого остатка, и общий выход водонерастворимой фракции составлял 62,87%. Таким образом, сам исходный белок клещевины содержал 62,87% водонерастворимого полипептидного материала и 37,12% водорастворимого полипептидного материала.
Процедура D: Получение белка расщепленной молочной сыворотки
Белок расщепленной молочной сыворотки (партия 5-72, названный в описании белком расщепленной молочной сыворотки рН 6,5) получали в виде экспериментальной пробы от Prof. S. Braun, the Laboratory of Applied Biology at the Hebrew University of Jerusalem, Israel, и готовили следующим образом: белок молочной сыворотки (WPI-95® белковый изолят молочной сыворотки; Nutritteck, 24 Seguin Street, Rigaud, QC, Canada JOP IOP) суспендировали в воде в соотношении 1:6 (мас./мас.). Значение pH суспензии доводили до рН 7 с помощью 5 н. NaOH и нагревали до 55°C при перемешивании. Затем добавляли FLAVOURZYME 500MG® (от NOVOZYMES') в соотношении 20 г на кг белка молочной сыворотки и смесь перемешивали при той же самой температуре в течение 4 часов. Значение рН полученной водной смеси было равно 6,5. Затем полученную смесь сушили распылением с получением белка расщепленной молочной сыворотки в виде бледно-желтого порошка, содержащего смесь водорастворимого и водонерастворимого полипептида.
Процедура Е: Получение белка расщепленной клещевины, подвергнутого взаимодействию с нитритом натрия
Белок муки клещевины суспендировали в воде в соотношении 1:10 (мас./мас.). Добавляли хлорид кальция при эффективной концентрации 10 мМ и рН суспензии доводили до рН 9 добавлением 10 н. NaOH. Реакционную смесь нагревали до 55°C при перемешивании. Затем добавляли Everlase 16L Type EX® (NOVOZYMES') в соотношении 10 г на кг белка муки клещевины и смесь перемешивали при той же самой температуре в течение 4 часов. Затем добавляли L-молочную кислоту (90%, 120 г на кг белка клещевины) для доведения смеси до рН 4,4, с последующим постепенным добавлением (на протяжении 20-часового периода) раствора нитрита натрия в воде (0,4 кг/л, 0,4 литра на кг белка клещевины) при перемешивании. Затем реакционной смеси давали отстояться при температуре окружающей среды в течение 40 часов. Затем добавляли Na2S2O5 (0,2 кг на кг белка клещевины) и реакционную смесь нагревали до 60°C и перемешивали в течение 15 минут. После охлаждения до температуры окружающей среды реакционную смесь доводили до рН 2,0 концентрированной HCl. Затем ее оставляли при 10°C на 18 часов и полученный осадок отделяли центрифугированием в течение 15 минут при 24000×g. Осадок ресуспендировали в 10 мМ лимонной кислоте (3 объема на 1 объем осадка), а затем собирали и после этого лиофилизировали с получением желтовато-коричневого порошка, содержащего смесь водорастворимого и водонерастворимого полипептида.
ПРИМЕР 2: Характеристика полипептидных композиций масс-спектрометрией
Данный пример описывает характеристики различных проб белков посредством MALDI-масс-спектрометрии с использованием прибора Ultraflex III от Bruker.
Прибор устанавливали в положительном режиме для детектирования положительных ионов, образуемых во время процесса ионизации. Приложенное напряжение для ускорения ионов в анализатор TOF устанавливали при 25 кВ. Анализ проводили с использованием этого прибора в режиме отраженной волны, который улучшает разрешение. Твердые пробы растворяли в ДМСО при концентрации 10 мг/мл. Водорастворимые фракции супернатанта сольватировали в воде.
Раствор каждой пробы смешивали с раствором матрикса (для аналитических целей). Матрикс представлял собой инертное соединение низкой молекулярной массы, которое поглощает при той же самой длине волны лазера, Nd:YAG 355 нм. Используемыми матриксами были: α-CHCA, альфа-циано-4-гидроксикоричная кислота, растворенная в растворе ACN/H2O (70:30) с 0,1% ТФУК в концентрации 10 мг/мл; и DCTB, T-2-[3-(4-трет-бутилфенил)-2-метил-2-пропенилиден]малононитрил, растворенный в ТГФ при концентрации 10 мг/мл. Первый матрикс использовали в основном для анализа пептидов и белков, тогда как второй матрикс, DCTB, был пригоден для анализа полимеров.
Растворы матриксов и растворы проб смешивали в соотношении объемов 10:1, соответственно. Для анализа, где в качестве матрикса использовали DCTB, добавляли Na-TФУК (10 мг/мл в ТГФ) к раствору матрикс/проба в качестве катионизирующего агента в соотношении 10:2:1 по объему (матрикс:проба:соль, соответственно). Полученные растворы в объеме 0,8 мкл наносили в виде пятен на пластинку-мишень, выполненную из полированной стали, и только после полного высушивания растворителей мишень загружали в прибор. Спектры собирали и манипуляции с ними выполняли с использованием программного обеспечения FlexAnalysis, выпускаемого Bruker Daltonics.
Значения относительной интенсивности фрагментов нормализовали и использовали для расчета параметров среднечисленной (Mn), средневесовой (Mw) и z-средней (Mz) молекулярной массы для различных проб. Результаты суммированы в таблице 2.
2 см. пример 6
3 см. пример 3
4 см. пример 1, Процедуру В
Результаты показывают, что характеристики молекулярной массы (определенные MALDI-масс-спектрометрией) конкретной полипептидной композиции могут зависеть от способа, используемого для получения полипептидной композиции. Например, наблюдали, что изолят белка клещевины имеет более высокую среднечисленную молекулярную массу, чем его расщепленная копия. Далее, после расщепления наблюдали, что среднечисленная молекулярная масса уменьшается, тогда как полидисперсность увеличивается. Такую же тенденцию наблюдали для изолята соевого белка и его расщепленной копии.
Другие экспериментальные результаты показывают, что белки в водорастворимой полипептидной композиции из расщепленной клещевины имеют более высокую среднечисленную молекулярную массу, чем их исходный белковый изолят. Однако, белки в водорастворимой полипептидной композиции из расщепленной сои имели более низкую среднечисленную молекулярную массу, чем их исходный белковый изолят сои.
Тем не менее, каждая из этих водорастворимых полипептидных композиций была способна уменьшать плотность полиуретанового пеноматериала в сравнении с пеноматериалами, полученными без полипептидной композиции. Кроме того, водорастворимые полипептидные композиции, имеющие сходные молекулярные массы и распределения молекулярных масс, могут быть получены ферментативным расщеплением белковых изолятов сои и клещевины (даже хотя изолят соевого белка имеет более высокомолекулярные белки, чем изолят белка клещевины перед ферментативным расщеплением). Вместе эти результаты указывают на то, что возможно получение пеноматериалов уменьшенной плотности из различных полипептидных композиций.
ПРИМЕР 3: Характеристики масляной дисперсии водорастворимой и водонерастворимой белковых фракций
Водонерастворимую/вододиспергируемую полипептидную фракцию и водорастворимую полипептидную фракцию выделяли из расщепленной клещевины (партия 5-108) на основе процедур, описанных в примере 1 (Процедура А). Расщепленная клещевина может быть получена следующим образом: белок муки клещевины суспендируют в воде в соотношении приблизительно 1:10 мас./мас. Добавляют хлорид кальция до эффективной концентрации приблизительно 10 мМ и рН этой суспензии доводят до рН 9 добавлением 10 н. NaOH. Затем реакционную смесь нагревают до 55°C при перемешивании. Затем добавляют Everlase 16L Type EX® (NOVOZYMES') в соотношении 10 г на кг белка муки клещевины и смесь перемешивают при той же самой температуре в течение приблизительно 4 часов. Наконец, полученную смесь доводят до рН 3,5 лимонной кислотой и сушат распылением с получением порошка.
Характеристики MALDI фрагментации молекулярных масс выделенных фракций представлены в примере 2 (таблица 2). Характеристики FTIR-спектроскопического поглощения для твердого состояния для выделенной водонерастворимой/диспергируемой полипептидной фракции согласуются с характеристиками, описанными на фигурах 2, 3, 4, 7, 9, 10, 11 и 12 (диапазон поглощения амида-I: 1620-1632 см-1; диапазон поглощения амида-II: 1514-1521 см-1). Жидкофазный двумерный ЯМР протон-азотного взаимодействия на выделенной водонерастворимой/диспергируемой полипептидной фракции обнаруживает два кластера протонированного азота, окруженных границами химического сдвига 15N приблизительно при 86,2 м.д. и 87,3 м.д.; и границами химического сдвига 1H приблизительно при 7,14 и 7,29 м.д. для первого кластера и приблизительно при 6,66 и 6,81 м.д. для второго кластера. Жидкофазный двумерный ЯМР протон-азотного взаимодействия на выделенной водорастворимой полипептидной фракции обнаруживает кластер протонированных ядер азота, определяемый в границах химического сдвига 15N в области около 94 м.д. и около 100 м.д., и в границах химического сдвига 1H в области около 7,6 м.д. и около 8,1 м.д.
Неожиданно, водонерастворимые/вододиспергируемые полипептидные фракции с этими спектральными характеристиками (в отличие от их водорастворимых копий) проявляют уникальную способность эмульгировать и стабилизировать дисперсии масла в воде и воды в масле. Такая уникальная способность диспергировать масло наблюдается с водонерастворимыми/вододиспергируемыми полипептидными композициями, которые экстрагированы и выделены из многочисленных источников, включая, но ими не ограничиваясь, (1) цельную муку или белковые изоляты из сои, канолы или клещевины, которые экстрагируются из их водорастворимых полипептидных компонентов при нейтральных или почти нейтральных условиях рН; (2) цельную муку или белковые изоляты из сои, канолы или клещевины, которые подвергают катализируемому щелочью гидролизу с последующим добавлением кислоты и последующей экстракцией водорастворимых полипептидных компонентов; (3) цельную муку или белковые изоляты из сои, канолы или клещевины, которые подвергают катализируемому кислотой гидролизу с последующим добавлением щелочи и последующей экстракцией их водорастворимых полипептидных компонентов; (4) цельную муку или белковые изоляты из сои, канолы или клещевины, которые подвергают комбинациям катализируемого щелочью гидролиза с ферментативным расщеплением, с последующим добавлением кислоты и последующей экстракцией водорастворимых полипептидных компонентов.
Понятно, что стабилизация эмульсии/дисперсии типа масло-в-воде или вода-в-масле зависит от нескольких факторов, включающих, но не ограничивающихся ими, присутствие или отсутствие стабилизирующей молекулярной частицы, такой как поверхностно-активное вещество или диспергирующий агент; природу масла (т.е. его полярность, гидрофильность, гидрофобность, параметр растворимости и т.д.); природу поверхностно-активного вещества или диспергирующего агента (т.е. величину HLB, характеристики заряда, молекулярную массу, растворимость в воде, растворимость в масле и т.д.); ионную силу водной фазы; присутствие или отсутствие добавок и примесей в масляной или водной фазах; концентрацию масла (т.е. его процент в воде); и концентрацию стабилизирующей молекулярной частицы. Кроме того, понятно, что эффективность стабилизирующей молекулярной частицы (причем «стабилизирующей молекулярной частицей» является диспергирующий агент, эмульгирующий агент или водонерастворимая/диспергируемая полипептидная композиция по настоящему изобретению) часто оценивают в соответствии с ее способностью стабилизировать эмульсию в течение некоторого определенного периода времени (т.е. для предотвращения макроскопического разделения фаз несмешивающихся масляных и водных компонентов при условиях сдвигающего усилия или при статических условиях).
Для дополнительной демонстрации общности данного вывода несколько дисперсий типа масло-в-воде готовили с водонерастворимой/вододиспергируемой полипептидной композицией, которую выделяли из белка расщепленной клещевины. Водонерастворимую/вододиспергируемую полипептидную композицию выделяли в виде пастообразной дисперсии в воде. Пасту разводили водой до 16% сухого остатка и отдельно до 14% сухого остатка. На следующей стадии аликвоты из 3 граммов каждой пасты по отдельности взвешивали в пластиковые химические стаканы на 15 мл. Затем аликвоты масел, показанных в таблице 3, по отдельности добавляли в отдельные аликвоты пасты в соотношении 1 часть масла на 1 часть твердой водонерастворимой/вододиспергируемой полипептидной композиции в расчете на массу (всего 20 смесей). Смеси перемешивали вручную шпателем и наблюдали образование гомогенных «сливок». «Сливки» оставались гомогенными без видимых признаков макроскопического разделения фаз в течение длительных периодов времени после смешивания, включающих периоды от 1 минуты после смешивания, 5 минут после смешивания, 10 минут после смешивания, 15 минут после смешивания, 30 минут после смешивания, 1 час после смешивания и 2 часа после смешивания.
В отличие от этого, аналогичный водорастворимый экстракт из расщепленной клещевины был неспособен стабилизировать дисперсии масел в воде.
Белковые композиции, не обогащенные водонерастворимыми/вододиспергируемыми фракциями, неспособны диспергировать масла. Например, 16% дисперсию сухого остатка изолята соевого белка, партия 5-81 (изолят соевого белка SOLPRO 958® Solbar Industries Ltd, POB 2230, Ashdod 77121, Israel; содержание белка приблизительно 90%) готовили добавлением 32 граммов изолята соевого белка к 168 граммам воды при рН приблизительно 4-6 (JM-570-1). Семь аликвот по 10 граммов JM-570-1 взвешивали в одноразовые химические стаканы на 20 мл. Аликвота в 10 граммов содержала 1,6 граммов изолята соевого белка и 8,4 граммов воды. Семь различных масел (а именно, PMDI, минеральное масло, соевое масло, моторное масло, касторовое масло, дибутилфталат и эпоксидированное соевое масло, см. таблицу 3) добавляли по отдельности при соотношении мас./мас. 1 часть масла на 1 часть сухого остатка белка (1,6 граммов масла добавляли к каждой 10-граммовой аликвоте). Смеси перемешивали вручную шпателем. Наблюдали, что ни одно из масел не диспергируется в содержащей 16% сухого остатка дисперсии изолята соевого белка.
ПРИМЕР 4: Характеристика полипептидных композиций с использованием корреляционных спектров двумерного ЯМР протон-азотного взаимодействия и характеристика водонерастворимой/вододиспергируемой полипептидной фракции
Водонерастворимую и водорастворимую белковые фракции получали следующим образом. Расщепленную клещевину (партия 5-83) суспендировали в воде в соотношении 1:10 мас./мас. Добавляли хлорид кальция до эффективной концентрации 10 мМ и рН суспензии доводили до рН 9 добавлением 10 н. NaOH. Реакционную смесь нагревали до 55°C при перемешивании. Затем добавляли Everlase 16L Type EX® (NOVOZYMES') в соотношении 10 г на кг белка муки клещевины и смесь перемешивали при той же самой температуре в течение 4 часов. Затем полученную смесь доводили до рН 3,5 лимонной кислотой и сушили распылением с получением желтовато-коричневого порошка. Затем водорастворимую и водонерастворимую белковые фракции собирали, как описано в примере 1 (Процедура А) и давали им сушиться на воздухе при 23°C.
Высушенный порошок, содержащий водонерастворимую белковую фракцию, растворяли в d6-ДМСО (6,8 мас.%) с получением гомогенного раствора красного цвета (Проба A). Аликвоту полученной высушенной расщепленной клещевины также растворяли в d6-ДМСО (6,8 мас.% сухого остатка) с получением сравнительного гомогенного раствора красного цвета (Проба B). FTIR-анализы твердого состояния тех же самых сухих порошков выявили явные различия в областях как валентных колебаний N-H, так и валентных колебаний карбонильной группы FTIR-спектров твердого состояния. Эти спектральные различия были отнесены к различиям в окружающих связях для образования полипептидных N-H-частей, возможно, полученным из различий во вторичной и третичной структуре. Одно из конкретных различий включало смещение в направлении более низких волновых чисел для полосы карбонильной группы амида-I в водонерастворимой/вододиспергируемой фракции. Для дополнительной характеристики указанных типов различий использовали способ двумерного ЯМР с целью характеристики очень конкретного подмножества связанных атомных ядер; а именно, протонов, связанных с азотом.
Пробы растворяли в ДМСО-d6 и помещали пробирки для ЯМР на 5 мм. Все 1H-ЯМР-спектры регистрировали на спектрометре Varian INOVA 750 МГц, снабженном Cryo Probe тройного резонанса HCN-PFG (градиента импульсного поля), при 30°C. Для одномерных (1D) 1H-NMR-спектров использовали спектральное окно 10000 Гц со временем обработки данных 3 секунды и задержкой релаксации 5 секунд. Спектры усредняли по сигналу для 16 непериодических сигналов с использованием длительности импульса протона 90° 8,6 микросекунд. Спектральные данные заполняли нулями (обнуляли) до точек 132 k и обрабатывали расширением линии 1 Гц, затем корректировали относительно фона и в качестве эталона использовали пик внутреннего остаточного растворителя ДМСО-d6 при 2,50 м.д. перед интегрированием и построением графиков.
Данные чувствительной к изменению фаз двумерной (2D) 1H-15N-градиентной-HSQC (гетероядерной одноквантовой когерентности) собирали с 2048 точками обработки данных в измерении F2 и 768 точками в измерении F1 (длительности 90° импульсов 6,3 микросекунд, и 33,5 микросекунд использовали для протона и азота, соответственно). 48 непериодических сигналов собирали для каждого приращения, с повторяющейся задержкой 1,2 секунды и временем обработки данных 0,124 секунды с разъединением GARP во время обработки данных. Полученные данные обрабатывали с взвешиванием синусного сигнала (“звонка”) и обнулением до точек 8196×8196 в измерениях F2 и Fl перед конечным преобразованием для получения 2D-корреляционных данных.
Результаты представлены на фигурах 13 и 14. Фигура 13 представляет спектр двумерного HSQC 1H-15N-ЯМР для партии 5-83 расщепленной клещевины в d6-ДМСО. Ось «y» представляет шкалу химического сдвига 15N (м.д.), а ось «x» представляет шкалу химического сдвига 1H (м.д.). Пики в спектре представляют протонированные атомы азота из всех фракций, которые присутствуют в расщепленной клещевине, как таковой (т.е. водонерастворимые/вододиспергируемые полипептидные фракции плюс водорастворимые полипептидные фракции). Наблюдали, что множественные пики в области B исчезали после удаления водорастворимых фракций (см. фигуру 14). Это указывает на то, что данные протонированные атомы азота являются специфическими для водорастворимых полипептидных фракций, тогда как по меньшей мере часть пиков в области A являются специфическими для водонерастворимой/вододиспергируемой фракции.
Фигура 14 представляет спектр двумерного HSQC 1H-15N-ЯМР для водонерастворимого/диспергируемого полипептидного экстракта из партии 5-83 расщепленной клещевины в d6-ДМСО. Ось «y» представляет шкалу химического сдвига 15N (м.д.), а ось «x» представляет шкалу химического сдвига 1H (м.д.). Пики в спектре представляют протонированные атомы азота из водонерастворимой/вододиспергируемой полипептидной фракции. Наблюдали, что пики в области B были очень слабыми в сравнении с аналогичными пиками в расщепленной клещевине перед экстракцией (см. фигуру 13). Напротив, остальные пики происходили преимущественно из протонированных атомов азота в области A. Это указывает на то, что эти протонированные атомы азота являются специфическими для водонерастворимых полипептидных фракций.
Как показано на фигуре 14, пики в спектре представляют протонированные атомы азота, которые являются специфическими для водонерастворимой/вододиспергируемой полипептидной фракции. После расширения два «пика» кажутся узкими кластерами, которые могут быть легко определены в границах химического сдвига 15N и 1H, которые их определяют: границы 15N для обоих кластеров находятся в области приблизительно 86,2 м.д. и 87,3 м.д.; и границы 1H находятся в области приблизительно 7,14 и 7,29 м.д. для первого кластера и в области приблизительно 6,66 и 6,81 м.д. для второго кластера.
Результаты проведенных исследований выявили, что, в то время как водорастворимая полипептидная фракция состояла из множественных типов протонированных атомов азота (см. фигуру 3), водонерастворимая/вододиспергируемая фракция содержала значимо меньше типов протонированных атомов азота и преимущественно характеризовалась наличием двух основных кластеров пиков протон-азот (см. фигуру 14). Указанные различия, подобно различиям, наблюдаемым с помощью FTIR твердого состояния, иллюстрируют, что окружающие химические связи в водорастворимой полипептидной фракции являются явно отличающимися от окружающих химических связей, которые существуют в водонерастворимой/диспергируемой фракции.
Вместе данные FTIR твердого состояния и ЯМР характеризуют также водонерастворимую/диспергируемую полипептидную фракцию, где имеется инфракрасная полоса поглощения амида-I твердого состояния между 1620-1632 см-1; инфракрасная полоса поглощения амида-II твердого состояния между 1514-1521 см-1; и жидкофазная пара кластеров протонированных атомов азота, определяемых корреляционным способом 1H-15N-ядерного магнитного резонанса. Более конкретно, при наблюдении пары кластеров протонированного азота посредством ЯМР с дейтерированным d6-ДМСО в качестве растворителя, с использованием способа двумерного HSQC 1H-15N-ЯМР, кластеры определяются границами химического сдвига 15N и 1H, которые определяют их: границы 15N для обоих кластеров встречаются в области приблизительно 86,2 м.д. и 87,3 м.д.; и границы 1H встречаются в области приблизительно 7,14 и 7,29 м.д. для первого кластера и в области приблизительно 6,66 и 6,81 для второго кластера.
Вместе данные FTIR твердого состояния и ЯМР характеризуют водорастворимую полипептидную фракцию, где имеется инфракрасная полоса поглощения амида-I твердого состояния в области около 1633-1680 см-1; инфракрасная полоса поглощения амида-II твердого состояния в области 1522-1560 см-1; две выраженные полосы поглощения валентных колебаний N-H 1° амида с центрами в области около 3200 см-1 и в области около 3300 см-1, как определено FTIR твердого состояния; и выраженный кластер протонированных ядер азота, определяемый в границах химического сдвига 15N в области около 94 м.д. и около 100 м.д., и в границах химического сдвига 1H в области около 7,6 м.д. и около 8,1 м.д., как определено с помощью жидкофазного двумерного ЯМР протон-азотного взаимодействия.
ПРИМЕР 5: Получение белоксодержащего полиуретанового материала
В данном примере получали и характеризовали полиуретановые пеноматериалы, содержащие водорастворимый белок расщепленной клещевины.
А - Экстракция белков полиольными смесями
Пробу JM-69-1 готовили добавлением 45 частей полиола (т.е. JEFFOL PPG-2000 от Huntsman Corporation) в стеклянный реакционный сосуд. Затем к полиолу добавляли 5 граммов белка расщепленной клещевины (партия 5-83) при перемешивании с использованием высокоскоростного ротационного (барабанного) смесителя, при нагревании, и выдерживали при температуре 95°C в течение всего времени реакции 1 час.
Пробу JM-69-2 готовили добавлением 43 частей полиола (т.е. JEFFOL PPG-2000 от Huntsman Corporation) и 2 частей дистиллированной воды в стеклянный реакционный сосуд. Смесь полиол/вода перемешивали с использованием высокоскоростного ротационного (барабанного) смесителя до тех пор, пока она не становилась гомогенной и прозрачной. Затем добавляли 5 граммов белка расщепленной клещевины (партия 5-83), при перемешивании смеси. Пробу перемешивали с использованием высокоскоростного ротационного (барабанного) смесителя при нагревании и выдерживали при температуре 95°C в течение всего времени реакции 1 час.
Как во время, так и после реакции, проба JM-69-1 была гомогенным, прозрачным материалом коричневого цвета. В противоположность этому, проба JM-69-2 вела себя совсем по-другому во время реакции. В начале реакции проба было похожа на JM-69-1. При температуре приблизительно 85°C наблюдали разделение фаз, и белок клещевины образовывал агломерат и осаждался, оставляя прозрачный, слегка желтый материал супернатанта. После перемешивания на лабораторном столе в течение 24 часов и осаждения проба JM-69-1 имела мутный супернатант над осадком и проба выглядела так же, как она выглядела непосредственно после реакции.
Ту же самую тенденцию супернатанта наблюдали с пробами JM-69-3 и JM-69-4, которые готовили при комнатной температуре (не нагревали и не подвергали реакции, как это было в случае JM-69-1 и JM-69-2). Единственным визуальным отличием, по-видимому, было то, что белок расщепленной клещевины в пробе, содержащей воду, не образовывал агломерат таким же путем, как и нагретая и участвующая в реакции проба (JM-69-2).
В одной серии экспериментов белок расщепленной сои (партия 5-81) и белок расщепленной молочной сыворотки (партия 5-80) готовили с использованием способа, описанного для пробы JM-69-2. В данных экспериментах белок не образовывал агломерат и не осаждался в процессе реакции. Однако после отстаивания на лабораторном столе белки сои и молочной сыворотки оседали на дно реакционного сосуда, приводя к слою супернатанта на верхней части осажденных белков.
В - Получение полиуретановых пеноматериалов
Для подтверждения того, что химические молекулярные частицы, экстрагированные из белковой композиции, были совместимы с раздуванием пеноматериала, несколько проб пеноматериала готовили из супернатантов проб JM-69-2, JM-71-1 и JM-71-2. Супернатант использовали, поскольку, без связи с конкретной теорией, авторы изобретения уверены в том, что данный супернатант содержит водорастворимый полипептид, который был экстрагирован полиолом (см. пример 14). Кроме того, готовили контрольную пробу таким же образом, как и пробы JM-69-2, JM-71-1 и JM-71-2, за исключением того, что не добавляли водорастворимый белок к смеси полиол/вода. Контрольную смесь полиол/вода нагревали с использованием вышеописанного профиля нагревания. Контрольной смесью была меченая проба JM-74-1.
Пеноматериал 75-3 получали смешиванием следующих компонентов: 7,1 г контрольной смеси JM-74-1, 1,6 г Jeffol A-630 от Huntsman Corporation, 0,06 г JEFFCAT DMDLC от Huntsman Corporation и 0,06 частей дилаурата дибутилолова от Air Products & Chemicals, Inc. в одноразовом химическом стакане на 150 мл. Полиольную смесь тщательно смешивали шпателем и вортексным (вихревым) смесителем. Затем в химический стакан добавляли 9 г PMDI (RUBINATE-M от Huntsman Corporation) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане.
Пеноматериал JM-75-4 получали таким же образом, за исключением того, что использовали 7,1 г супернатанта из пробы JM-69-2 вместо JM-74-1. Для пеноматериала JM-75-5 использовали 7,1 г супернатанта из пробы JM-71-1 вместо JM-74-1 и для пеноматериала JM-75-6 использовали 7,1 г супернатанта из пробы JM-71-2 вместо JM-74-1.
Другую контрольную пробу пеноматериала (JM-75-2) получали со следующим составом: 7,1 г JEFFOL PPG-2000 от Huntsman Corporation, 1,6 г JEFFOL A-630 от Huntsman Corporation, 0,06 г JEFFCAT DMDLC от Huntsman Corporation и 0,06 частей дилаурата дибутилолова от Air Products & Chemicals, Inc. и 0,39 г дистиллированной воды. Полиольную смесь готовили в одноразовом химическом стакане на 150 мл и тщательно перемешивали шпателем и вортексным (вихревым) смесителем. Затем в химический стакан добавляли 9 г PMDI (RUBINATE-M от Huntsman Corporation) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане. В данной контрольной композиции использовали то же самое отношение воды к полиолу, какое использовали в случае приготовления контрольной полиольной смеси JM-74-1, за исключением того, эту пробу не «варили».
Пеноматериалы, полученные с использованием супернатанта белка, в каждом случае имели высокий подъем и плотную структуру пор. Картины пеноматериалов представлены на фигуре 15, а дополнительные наблюдения из эксперимента представлены в таблице 4 ниже.
Приведенные данные показывают, что водорастворимые белки, собранные из супернатанта, полученного из расщепленной клещевины, увеличивают подъем полиуретановых пеноматериалов и способствуют очень однородной, мелкой структуре пор в пеноматериале. Без связи с какой-либо теорией, авторы изобретения считают, что белок действует в качестве поверхностно-активного вещества, которое делает возможными эффективное смешивание взаимодействующих компонентов и образование выделяющегося углекислого газа, обеспечивая высокий подъем пеноматериала, однородную структуру пор и более низкую плотность пеноматериала (авторы считают, что, кроме указанного полипептида, ни один из материалов, используемых для приготовления пеноматериала, не действует в качестве поверхностно-активного вещества).
ПРИМЕР 6: Получение полиуретановых пеноматериалов, содержащих расщепленный белок
В данном примере готовили ряд полиуретановых пеноматериалов путем комбинирования изоцианата, полиольной смеси и диспергированных белков сельскохозяйственных культур. Присутствие диспергированных белков приводило к пенополиуретановых пеноматериалам, которые поднимались до большей высоты и имели более мелкую пористую структуру и более низкую плотность.
Изоцианатом, используемым для компонента “A”, был RUBINATE-M, полимерный дифенилметандиизоцианат (PMDI) от Huntsman Corporation. Композиция полиольной смеси, или компонент “B”, содержала 71,4 частей JEFFOL PPG-2000 от Huntsman Corporation, 15,6 частей Jeffol A-630 от Huntsman Corporation, 3,0 части дистиллированной воды, 0,6 частей JEFFCAT DMDLC от Huntsman Corporation и 0,6 частей дилаурата дибутилолова от Air Products & Chemicals, Inc. Компонент “B” обозначали как проба JM-37-1. Изолят белка расщепленной сои (партия 5-81), белок молочной сыворотки, подвергнутый протеолизу с использованием Flavourzyme (партия 5-80), и белок муки клещевины, расщепленный с использованием Everlast (партия 5-83), получали от профессора Сергея Брауна из Hebrew University of Jerusalem.
Готовили ряд сравнительных проб пеноматериалов в стаканах добавлением 9 граммов вышеописанной полиольной смеси (проба JM-37-1) в одноразовый химический стакан на 250 мл и затем добавляли 1 грамм конкретного белка из перечня, приведенного выше. Смеси белок/полиол смешивали с использованием шпателя и вортексного (вихревого) смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. К компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и смесь тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане. Белоксодержащие пеноматериалы сравнивали с контрольным пеноматериалом, состоящим из 10 граммов полиольной смеси, описанной выше (JM-37-1), подвергнутой взаимодействию с 10 граммами PMDI. Все компоненты для экспериментов находились при температуре окружающей среды (23°C). Все реакции с пеноматериалами проводили при температуре окружающей среды.
Пеноматериалы, содержащие диспергированные белки сои, молочной сыворотки и клещевины поднимались выше, чем контрольный пеноматериал. Полученные значения плотности этих пеноматериалов представлены в таблице 5.
Кроме изменений плотности, имелись различия в пористой структуре полученных пеноматериалов. Пеноматериалы, приготовленные с белками сои и молочной сыворотки (JM-67-1 и JM67-3, соответственно), имели меньшие и более плотные поры в сравнении с пеноматериалом, изготовленным с белком клещевины (JM-67-5) и контролем (JM-67-7), оба из которых имели более крупную, более грубую структуру.
ПРИМЕР 7: Пеноматериал, полученный с использованием либо расщепленного белка клещевины, либо дериватизованного, расщепленного белка клещевины
В данном примере полиуретановый пеноматериал получали с использованием расщепленного белка клещевины и с использованием дериватизованного, расщепленного белка клещевины.
Готовили ряд сравнительных проб пеноматериалов в стаканах добавлением 9 граммов полиольной смеси, описанной в примере-6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 1 грамма расщепленного белка клещевины (партия 5-83) или дериватизованного, расщепленного белка клещевины (партия 5-82). Белок и полиольную смесь перемешивали с использованием шпателя и вортексного (вихревого) смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане. Белоксодержащие пеноматериалы сравнивали с двумя контрольными пеноматериалами: Контролем-1, состоящим из 9 граммов полиольной смеси, описанной выше (JM-37-1), подвергнутой взаимодействию с 10 граммами PMDI, и Контролем-2, состоящим из 10 граммов полиольной смеси, описанной выше (JM-37-1), подвергнутой взаимодействию с 10 граммами PMDI. Все компоненты для экспериментов находились при температуре окружающей среды (23°C). Все реакции с пеноматериалами проводили при температуре окружающей среды.
Пеноматериалы, содержащие диспергированные белки клещевины, поднимались выше, чем контрольный пеноматериал. Полученные значения плотности этих пеноматериалов представлены в таблице 6.
ПРИМЕР 8: Сравнение различных нагрузок расщепленного белка молочной сыворотки на полученном пеноматериале
В данном примере полиуретановый пеноматериал получали с использованием либо 10% (мас./мас.), либо 20% (мас./мас.) расщепленного белка молочной сыворотки.
Готовили 2 сравнительные пробы пеноматериалов в стаканах. Первую пробу, JM-43-1, готовили добавлением 9 граммов полиольной смеси, описанной в примере-6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 1 грамма расщепленного Flavourzyme белка молочной сыворотки (партия 5-80) в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане.
Вторую пробу, JM-43-2, готовили добавлением 8 граммов полиольной смеси, описанной в примере-2 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 2 граммов расщепленного Flavourzyme белка молочной сыворотки (партия 5-80) в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане. Все компоненты для экспериментов находились при температуре окружающей среды (23°C). Все реакции с пеноматериалами проводили при температуре окружающей среды.
Смесь полиол/белок для пробы JM-43-2 имела более высокую вязкость в сравнении со смесью полиол/белок JM-43-1. Тем не менее, полученные пеноматериалы поднимались приблизительно до одной и той же высоты. Структура пор каждого пеноматериала была сходной. Относительные объемные веса для среднего сечения каждой пробы представлены в таблице 7, где М1 обозначает однодюймовый поперечный разрез ниже центра поднявшегося пеноматериала, а М2 обозначает однодюймовый поперечный разрез выше центра поднявшегося пеноматериала.
В полученном пеноматериале нижнее сечение пеноматериала в стакане имело толщину приблизительно 1 дюйм, М-1 был первым средним сечением пеноматериала выше нижнего сечения и имел толщину 1 дюйм, а М-2 был вторым средним сечением пеноматериала выше М-1 и имел толщину приблизительно 1 дюйм. Авторы считают, что полиольные смеси экстрагируют водорастворимые белки из расщепленного белка молочной сыворотки и способствуют эффективному подъему пеноматериала и мелкопористой структуре. При сравнении этих пеноматериалов с контрольными пеноматериалами (JM-59-3 и JM-59-4) в примере 7 наблюдали, что плотность всех пеноматериалов в таблице 7 была ниже плотности контрольных пеноматериалов.
ПРИМЕР 9: Полиуретановый пеноматериал, изготовленный с использованием расщепленных Flavourzyme белков молочной сыворотки с различными pH
Данный пример описывает получение и характеристику полиуретановых пеноматериалов с использованием расщепленных Flavourzyme белков молочной сыворотки с различным рН.
Готовили ряд сравнительных проб пеноматериалов в стаканах для сравнения расщепленного Flavourzyme белка молочной сыворотки, полученного двумя путями. Первую пробу, JM-40-1, готовили добавлением 9 граммов полиольной смеси, описанной в примере 6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 1 грамма расщепленного Flavourzyme белка молочной сыворотки (партия 5-72) в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане.
Вторую пробу, JM-40-2, готовили добавлением 9 граммов полиольной смеси, описанной в примере 6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 1 грамма расщепленного Flavourzyme белка молочной сыворотки (партия 5-80) в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане. Все компоненты для экспериментов находились при температуре окружающей среды (23°C). Все реакции с пеноматериалами проводили при температуре окружающей среды.
Третью пробу, JM-40-5, готовили добавлением 8 граммов полиольной смеси, описанной в примере-6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 2 граммов расщепленного Flavourzyme белка молочной сыворотки (партия 5-80) в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане. Все компоненты для экспериментов находились при температуре окружающей среды (23°C). Все реакции с пеноматериалами проводили при температуре окружающей среды.
Белоксодержащие пеноматериалы сравнивали с двумя контрольными пеноматериалами: Контролем-1 (JM-40-3), содержащим 9 граммов полиольной смеси, описанной выше (JM-37-1), подвергнутой взаимодействию с 10 граммами PMDI, и Контролем-2 (JM-40-4), содержащим 10 граммов полиольной смеси, описанной выше (JM-37-1), подвергнутой взаимодействию с 10 граммами PMDI. Все компоненты для экспериментов находились при температуре окружающей среды (23°C). Все реакции с пеноматериалами проводили при температуре окружающей среды.
Изображения пеноматериалов, полученных в результате вышеуказанных процедур, показаны на фигуре 16. Пеноматериалы, полученные с расщепленным Flavourzyme белком молочной сыворотки партии № 5-80 (пробы JM-40-2 и JM-40-5), который имеет рН приблизительно 3,5, поднимались выше, чем проба пеноматериала JM-40-1, полученная с расщепленным Flavourzyme белком молочной сыворотки партии № 5-72, имеющим рН приблизительно 6,0. Кроме того, пеноматериал, полученный с расщепленным Flavourzyme белком молочной сыворотки партии № 5-80, (пробы JM-40-2 и JM-40-5), который имел рН приблизительно 3,5, поднимался выше, чем контрольные пробы пеноматериалов (т.е. JM-40-3 и JM-40-4). Плотность каждой из этих проб пеноматериалов представлена в таблице 8.
ПРИМЕР 10: Пеноматериал, полученный с использованием водорастворимой полипептидной композиции, полученной из белка расщепленной клещевины
Данный пример описывает получение полиуретанового пеноматериала, полученного с использованием водорастворимой полипептидной композиции, полученной из белка расщепленной клещевины.
А - Получение полипептидной композиции
Белок расщепленной клещевины (партия № 5-108) получали в качестве экспериментальной пробы («расщепленная клещевина») от профессора С. Брауна, из Laboratory of Applied Biology at the Hebrew University of Jerusalem, Israel. Расщепленную клещевину получали следующим образом: Белок муки клещевины суспендировали в воде в соотношении 1:10 мас./мас. Добавляли хлорид кальция до эффективной концентрации 10 мМ и рН суспензии доводили до рН 9 добавлением 10 н. NaOH. Реакционную смесь нагревали до 55°C при перемешивании. Затем добавляли Everlase 16L Type EX® (NOVOZYMES') в соотношении 10 г на кг белка муки клещевины и смесь перемешивали при той же самой температуре в течение 4 часов. Затем снижали рН полученной смеси до 3,5 лимонной кислотой и сушили распылением с получением желтовато-коричневого порошка.
Расщепленную клещевину фракционировали с получением водорастворимой полипептидной фракции и водонерастворимой/вододиспергируемой полипептидной фракции. На первой стадии 100 г расщепленной клещевины суспендировали в 0,5 литрах дистиллированной воды. Смесь перемешивали в течение периода 30 минут механическим смесителем. Затем аликвоты суспензии центрифугировали при 3400 об/мин в течение периода приблизительно 15 минут. Полученный супернатант, который содержал водорастворимую полипептидную фракцию, декантировали и использовали для экспериментов с пеноматериалами в данном примере. Оставшийся водонерастворимый осадок промывали нейтральной водой и вновь центрифугировали. Эту стадию повторяли 5 раз для водонерастворимого осадка. Водонерастворимый осадок собирали.
Процент сухого остатка измеряли для промытой, водонерастворимой/вододиспергируемой фракции с последующим высушиванием пробы в сушильном шкафу. Было обнаружено, что процент сухого остатка составлял 16,36%. Водорастворимую фракцию, которая была также выделена в первом центрифужном цикле (описанном выше), сушили в сушильном шкафу. Высушенный, водорастворимый остаток собирали и использовали для получения 16,36% раствора сухого остатка для сравнения с водонерастворимой, диспергируемой фракцией. Третью 16,36% пробу сухого остатка получали смешиванием 3,272 граммов расщепленной клещевины, партии 5-108, с 16,728 граммами воды с получением 16,36% смеси сухого остатка, которая содержит в результате как водорастворимую, так и водонерастворимую, диспергируемую фракции.
В - Получение полиуретановых пеноматериалов
Затем готовили ряд полиуретановых пеноматериалов путем комбинирования изоцианата, полиольной смеси и различных полипептидных фракций расщепленной клещевины. Полиольная смесь, используемая в этих экспериментах, была сходной со смесью, описанной в примере 6, за исключением того, что используемая вода содержала выделенные фракции расщепленного белка клещевины. Контрольные пробы готовили при подходящей концентрации воды, чтобы обеспечить одинаковое содержание воды во всех полиольных смесях. Различные композиции показаны в таблице 9.
Изоцианатом, используемым для компонента “A” был RUBINATE-M, полимерный дифенилметандиизоцианат (PMDI) от Huntsman Corporation. Композиция полиольной смеси, или компонент “B”, содержала 71,4 частей JEFFOL PPG-2000 от Huntsman Corporation, 15,6 частей Jeffol A-630 от Huntsman Corporation, 0,6 частей JEFFCAT DMDLC от Huntsman Corporation и 0,6 частей дилаурата дибутилолова от Air Products & Chemicals, Inc, и 2,51 частей дистиллированной воды для контроля или 3,0 части содержащей 16,36% сухого остатка фракции.
Изоцианат (Компонент “A”) и полиольные смеси (Компонент “B”) смешивали в двух соотношениях, 9 частей “B” к 10 частям “A” и 10 частей “B” к 10 частям “A”, которые могли представлять два разных индекса изоцианата. Из смесей получались пеноматериалы, имеющие различные характеристики. Изображения указанных пеноматериалов показаны на фигуре 17, где фигура 17А представляет пробы, содержащие 10 частей “B”:10 частей “A”, обозначаемые как 9/10полиI/PMDI, а фигура 17B представляет пробы, содержащие 10 частей “B”:10 частей “A”, обозначаемые как 10/10полиI/PMDI. При обоих соотношениях полиол/изоцианат присутствие водорастворимого полипептида приводило к полиуретановым пеноматериалам, которые имели значительный подъем и структуру меньших пор по сравнению с контролями. Проба, содержащая водонерастворимую диспергируемую фракцию (JM-582-4), не поднималась так высоко, как пробы, содержащие водорастворимые полипептидные фракции. Без связи с какой-либо теорией, авторы считают, что, возможно, увеличение высоты пеноматериала для водонерастворимой полипептидной фракции может быть приписано малому количеству водорастворимого белка в водонерастворимой белковой композиции.
ПРИМЕР 11: Пеноматериал, полученный из водорастворимых полипептидных композиций, полученных из муки клещевины или муки канолы
В данном примере полиуретановый пеноматериал получали с использованием водорастворимой полипептидной композиции, полученной из муки клещевины или муки канолы (брюквы).
А - Получение полипептидной композиции
Готовили две пробы при идентичных условиях, одну с использованием цельной муки канолы и другую, приготовленную с цельной мукой клещевины. Препарат канолы готовили следующим образом: цельную муку канолы (Canola Meal MA Viterra 00200, которая, как сообщалось, содержит приблизительно 37% белка по массе, получена от Viterra Canola Processing, Ste Agatha, MB) диспергировали в 1,0% растворе гидроксида натрия и затем смешивали с 1 М раствором HCl до конечной величины рН приблизительно 4-5. Аналогично, цельную муку клещевины (от Kopco Oil Products, Rajkot, India) диспергировали в 1,0% растворе гидроксида натрия и затем смешивали с 1 М раствором HCl до конечной величины рН приблизительно 4-5.
Пробам клещевины и канолы давали отстояться на лабораторном столе. Компонент, содержащий водонерастворимый/вододиспергируемый полипептид, осаждался, тогда как водорастворимый полипептидный компонент наблюдали в виде супернатанта. Содержание сухого остатка супернатанта определяли по высушенным в сушильном шкафу пробам. Супернатант муки клещевины имел содержание сухого остатка 2,85%, а супернатант муки канолы имел содержание сухого остатка 3,25%. Для экспериментов с пеноматериалами супернатант канолы разводили дистиллированной водой до достижения содержания сухого остатка 2,85% с тем, чтобы он был эквивалентным супернатанту пробы клещевины.
В - Получение полиуретанового пеноматериала
Ряд полиуретановых пеноматериалов получали путем комбинирования изоцианата, полиольной смеси и различных фракций супернатантов. Полиольная смесь, используемая в данных экспериментах, была сходной со смесью, описанной в примере 10. Контрольные пробы готовили при подходящей концентрации воды так, чтобы обеспечить одинаковое содержание воды во всех полиольных смесях. Сравнительные композиции показаны в таблице 10.
Изоцианатом, используемым для компонента “A”, был RUBINATE-M, полимерный дифенилметандиизоцианат (PMDI) от Huntsman Corporation. Композиция полиольной смеси, или компонент “B”, содержала 71,4 частей JEFFOL PPG-2000 от Huntsman Corporation, 15,6 частей Jeffol A-630 от Huntsman Corporation, 0,6 частей JEFFCAT DMDLC от Huntsman Corporation и 0,6 частей дилаурата дибутилолова от Air Products & Chemicals, Inc, и 2,91 частей дистиллированной воды или 3,0 части содержащей 2,85% сухого остатка растворимой фракции.
Изоцианат (Компонент “A”) и полиольные смеси (Компонент “B”) смешивали в соотношении 7 частей “B” к 10 частям “A”.
Изображения пеноматериала, полученного посредством описанных выше процедур, показаны на фигуре 18. Присутствие водорастворимых полипептидных фракций приводило к полиуретановым пеноматериалам, которые поднимались до большей высоты и имели структуру меньших пор по сравнению с контролями, лишенными водорастворимых белковых фракций.
ПРИМЕР 12: Пеноматериал, полученный с использованием водорастворимых полипептидных композиций, полученных из муки расщепленной клещевины
В данном примере полиуретановый пеноматериал получали с использованием водорастворимой полипептидной композиции, полученной из муки расщепленной клещевины.
Расщепленную клещевину (партия 5-108) фракционировали с получением водорастворимой фракции и водонерастворимой/вододиспергируемой фракции, используя процедуры выделения, как сообщалось в примере 10. Супернатант, который содержал водорастворимую полипептидную фракцию, собирали декантированием для экспериментов с пеноматериалами и оставшийся водонерастворимый осадок собирали в отдельный контейнер. В примере 10 фракции супернатанта собирали и сушили с целью получения 16,36% раствора водорастворимой полипептидной фракции. В отличие от этого, в данном примере супернатант из первого центрифужного цикла собирали и использовали как таковой, без высушивания. Содержание сухого остатка супернатанта расщепленной клещевины определяли по высушенной в сушильном шкафу аликвоте. Было обнаружено, что супернатант расщепленной клещевины с первой стадии центрифугирования имел содержание сухого остатка 8,93%.
Ряд полиуретановых пеноматериалов готовили путем комбинирования изоцианата, полиольной смеси и фракции супернатанта. Полиольная смесь, используемая в данных экспериментах, была сходной со смесью, описанной в примере 10. Контрольную пробу готовили при подходящей концентрации воды так, чтобы обеспечить одинаковое содержание воды в обеих полиольных смесях. Различные композиции показаны в таблице 11.
Изоцианат (Компонент “A”) и полиольные смеси (Компонент “B”) смешивали в двух соотношениях, 9 частей “B” к 10 частям “A” и 8 частей “B” к 10 частям “A”, которые могли представлять два разных индекса изоцианата.
Присутствие водорастворимых полипептидных фракций приводило к полиуретановым пеноматериалам, которые поднимались до большей высоты и имели структуру меньших пор по сравнению с контролями. Обе смеси: 9 частей “B” к 10 частям “A” и 8 частей “B” к 10 частям “A” вели себя сходным образом.
ПРИМЕР 13: Пеноматериал, полученный с использованием цельной муки, размолотой муки клещевины или муки расщепленной клещевины
В данном примере полиуретановый пеноматериал получали с использованием цельной муки, размолотой муки клещевины или муки расщепленной клещевины.
Расщепленную клещевину (партия 5-108) получали, как описано в примере 10. В данном примере проба цельной муки, размолотой муки и расщепленной клещевины были сухими твердыми порошками, содержащими как водорастворимую полипептидную композицию, так и водонерастворимую/вододиспергируемую полипептидную композицию.
Полиуретановые пеноматериалы получали путем комбинирования изоцианата, полиольной смеси и добавления сухих частиц клещевины к полиольной смеси. Полиольная смесь, используемая в данных экспериментах, была сходной со смесью, описанной в примере 6.
Конкретно, готовили 2 сравнительные пробы пеноматериалов в стаканах. Первую пробу, JM-560-1, готовили добавлением 9 граммов полиольной смеси, описанной в примере-6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 1 грамма размолотой до 80 микрон цельной муки клещевины в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане.
Вторую пробу, JM-555-3, готовили добавлением 9 граммов полиольной смеси, описанной в примере 6 (проба JM-37-1), в одноразовый химический стакан на 250 мл и затем добавлением 2 граммов расщепленной клещевины (партия № 5-108) в полиольную смесь. После добавления белка к полиольной смеси композицию перемешивали с использованием шпателя и вортексного смесителя для диспергирования белка. Общая масса пробы для компонентов “B” полиола/белка составляла 10 граммов. Затем к компоненту “B” в химическом стакане добавляли 10 граммов компонента “A” (PMDI) и тщательно перемешивали вручную шпателем, а затем давали свободно подниматься в химическом стакане.
Две пробы сравнивали с контрольным пеноматериалом (JM-37-1), который не содержал добавленных содержащих сухой белок порошков.
Присутствие белоксодержащих порошков приводило к полиуретановым пеноматериалам, которые поднимались до большей высоты и имели структуру меньших пор по сравнению с контролями.
ПРИМЕР 14: Характеристика смеси, образованной добавлением белковой композиции к полиольной композиции
Представляющее полиол соединение PPG 200 и белковую композицию (например, расщепленную клещевину, расщепленную сою и расщепленную молочную сыворотку) смешивали вместе в присутствии и в отсутствие воды для целей исследования, могут ли или не могут иметь место определенные химические реакции между этими компонентами. В частности, поскольку FTIR-анализы показали присутствие свободных групп карбоновых кислот в расщепленных белках, проводили исследования для испытания и идентификации существования реакций этерификации между гидроксильными концевыми группами полиола и свободными кислотными группами расщепленных белков. Данное испытание проводили в отсутствие изоцианатного компонента, так что можно было выделить потенциальную реакцию. Процедуры, используемые для смешивания полиольной и белковой композиции, сообщаются в примере 5, вместе с физическими наблюдениями смеси полиол/белок.
После завершения процедуры смешивания контейнерам с пробами давали стоять в условиях окружающей среды в течение нескольких дней. После того как осажденные компоненты из различных смесей оседали на дно контейнеров, аликвоты супернатантов доставали вместе с некоторыми пробами осажденных продуктов. Полученные аликвоты анализировали с использованием FTIR состояния раствора и создавали субтрактивные спектры с целью тестирования на присутствие или отсутствие экстрагированных и/или прореагировавших компонентов.
Субтрактивные спектры создавали вычитанием спектра чистого PPG2000 из спектров супернатантов (мультипликативные факторы = 1). Затем полученные субтрактивные спектры совмещали и сравнивали с исходными ингредиентами (PPG2000 и расщепленными белками) с целью тестирования на возможность химически превращенного продукта реакции.
Субтрактивный спектр супернатанта из смеси, которая была получена с расщепленной клещевиной в полиоле с водой, выявили присутствие соединения в супернатанте. Сравнением субтрактивного спектра со спектром для чистой расщепленной клещевины было обнаружено, что соединение супернатанта имело полосы поглощения приблизительно при 3540 см-1 и 3423 см-1. Группа 3423 см-1 появлялась только в виде плеча в исходном соединении расщепленной клещевины (преобладающее валентное колебание N-H в расщепленной клещевине появлялось приблизительно при 3270 см-1). Кроме того, преобладающая полоса N-H в чистой расщепленной клещевине отсутствовала в соединении супернатанта. Кроме того, хотя соединение супернатанта содержало доминирующую полосу расщепленной клещевины с центром вблизи 1638 см-1, не было доказательства карбонильной группы при 1717 см-1 (поглощение при 1717 см-1 в расщепленной клещевине согласуется с присутствием свободной карбоновой кислоты). Вместо этого, соединение супернатанта показало присутствие значимо отличающегося валентного колебания карбонильной группы при 1739 см-1, которое согласуется с присутствием сложного эфира.
Важно, что было определено отношение интенсивности поглощения для пика вблизи 1639 см-1 к интенсивности поглощения пика сложного эфира вблизи 1739 см-1, составляющее приблизительно 2/1, которое было почти таким же, как и сравнительное отношение пика 1639 см-1 в расщепленной клещевине к карбонильному пику вблизи 1717 см-1. Кроме того, пик 1531 см-1, который появляется в спектре расщепленной клещевины, отсутствовал в соединении супернатанта. Супернатант обнаруживает присутствие воды, что доказывается широким пиком вблизи 3550 см-1, и группой пиков между 2300 см-1 и 1900 см-1.
Совмещение спектра соединения супернатанта со спектром полиола PPG 2000 показывает, что гидроксильный пик полиола с центром вблизи 3474 см-1 явно отсутствует в соединении супернатанта. В целом, приведенные спектральные сравнения показывают, что соединение супернатанта является либо солюбилизированным частичным компонентом самого исходного белка расщепленной клещевины, либо солюбилизированным продуктом реакции между компонентом расщепленной клещевины и содержащим полиол соединением.
Чтобы определить потенциальное действие воды по этим выводам, супернатант аналогичной смеси с расщепленной клещевиной и PPG2000 готовили в отсутствие воды. В супернатанте не выявили никакого соединения. Материал, который осаждался из пробы JM-69-2 (см. пример 5), собирали отдельно и анализировали посредством FTIR, его спектр совмещали со спектром исходного материала расщепленной клещевины и спектром полиола PPG 2000. Анализ этих спектров выявил, что осадок был вполне сходным по составу с исходным белком расщепленной клещевины. Осадок не промывали, и он содержал спектральный компонент при 1092 см-1, что согласуется с присутствием примеси полиола.
В аналогичных экспериментах с белками расщепленной молочной сыворотки и расщепленной сои супернатанты собирали аналогичным образом и анализировали с помощью FTIR. Полученные субтрактивные спектры, при совмещении со спектром соединения супернатанта, который был получен с расщепленной клещевиной, показывает, что соединения супернатанта, по-видимому, имеют поразительно сходные структурные характерные признаки. Данные сходства дополнительно иллюстрируются совмещениями гидроксильной области и карбонильной области.
Как обсуждается в примере 5, добавление массы расщепленных белков к композициям полиуретановых пеноматериалов (приблизительно 5% в расчете на массу пеноматериала) приводило к удивительному уменьшению плотности пеноматериала. В свете данного наблюдения и в свете поразительного сходства между соединениями супернатанта, наблюдаемыми с помощью FTIR, проводили исследования с целью получения вспененных полиуретановых композиций путем использования соединений супернатантов вместо массы самих белков. Пеноматериалы, которые были изготовлены с соединениями супернатанта, все имели удивительно низкую плотность. Таким образом, хотя добавление массы предпочтительных расщепленных белков может приводить к благоприятным результатам, подобные результаты могут быть неожиданно достигнуты за счет добавления низкой концентрации соединения со структурными свойствами, подобными свойствам, обнаруживаемым в супернатантах данного примера. Таким образом, тенденция, наблюдаемая в результате добавления массы расщепленных белков, воспроизводилась посредством просто добавления сольватированных соединений супернатантов в отсутствие водонерастворимых белковых фракций (т.е. водорастворимых фракций, экстрагированных из расщепленного белка с использованием смеси полиола и воды), с получением желаемого эффекта уменьшения плотности в отсутствие водонерастворимой фракции, которая осаждалась из смеси полиол/вода.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
Полное описание каждого из патентных документов и научных статей, на которые делаются ссылки, включены в описание посредством ссылки для всех целей.
ЭКВИВАЛЕНТЫ
Настоящее изобретение может быть осуществлено в других конкретных формах без отклонения от его сущности или существенных характеристик. Таким образом, предыдущие варианты осуществления должны рассматриваться во всех отношениях иллюстративными, а не ограничивающими описанное здесь изобретение. Таким образом, объем настоящего изобретения указывается прилагаемой формулой изобретения, а не предыдущим описанием, и предполагается, что все изменения, которые находятся в пределах значения и диапазона эквивалентности формулы изобретения, включены в данное изобретение.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭМУЛЬСИИ И КЛЕИ, СОДЕРЖАЩИЕ БЕЛОК, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2010 |
|
RU2558365C2 |
| БЕЛОКСОДЕРЖАЩИЕ АДГЕЗИВЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2011 |
|
RU2617360C2 |
| БЕЛОКСОДЕРЖАЩИЕ АДГЕЗИВЫ И ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2012 |
|
RU2621798C2 |
| АРОМАТИЧЕСКИЕ СЛОЖНЫЕ ПОЛИЭФИРЫ, ПОЛИОЛЬНЫЕ СМЕСИ, СОДЕРЖАЩИЕ ИХ, И ПОЛУЧАЮЩИЕСЯ ИЗ НИХ ПРОДУКТЫ | 2009 |
|
RU2503690C2 |
| ПОЛИОЛЬНЫЕ КОМПОЗИЦИИ | 2017 |
|
RU2765788C2 |
| ФОРПОЛИМЕР, ПОЛИОЛЬНАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ ЭЛАСТИЧНОГО ПЕНОМАТЕРИАЛА | 2003 |
|
RU2320676C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВЯЗКОЭЛАСТИЧНЫХ ПЕНОМАТЕРИАЛОВ | 2007 |
|
RU2437898C2 |
| ПАНЕЛЬ С ПРОТИВОПОЖАРНЫМИ СВОЙСТВАМИ | 2012 |
|
RU2609044C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНОПОЛИУРЕТАНА | 2012 |
|
RU2601412C2 |
| ПОЛИИЗОЦИАНАТНЫЙ КОМПОНЕНТ, ПЕНОПОЛИУРЕТАНОВАЯ СИСТЕМА И ИЗДЕЛИЕ, ИЗГОТОВЛЕННОЕ ИЗ НИХ | 2018 |
|
RU2768646C1 |
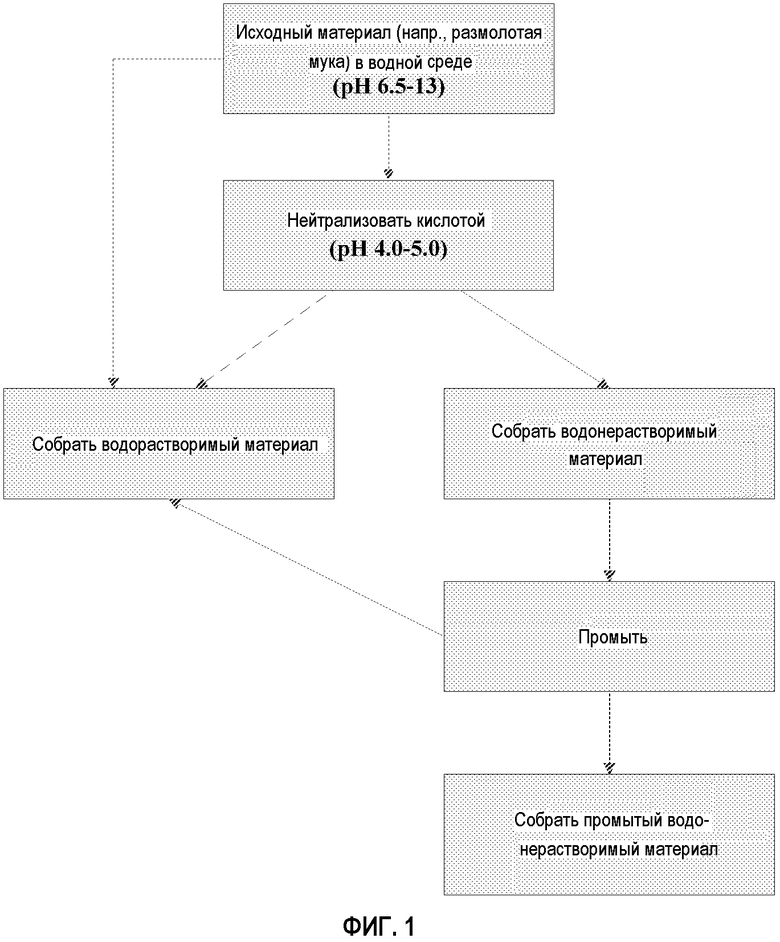

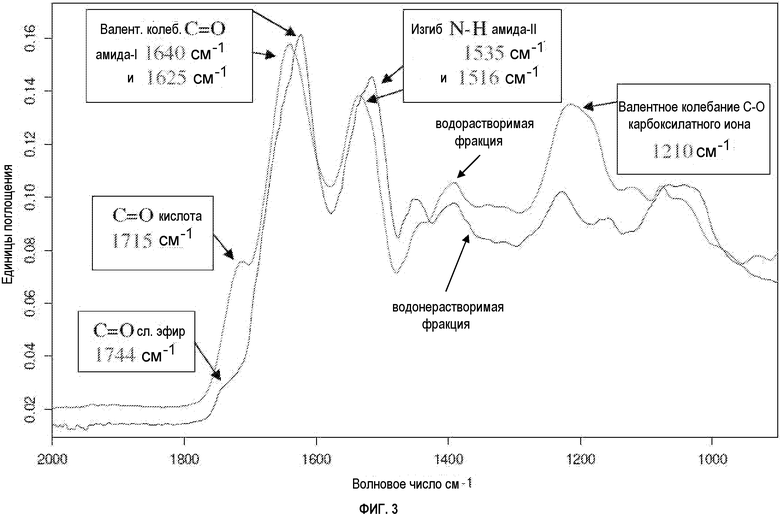

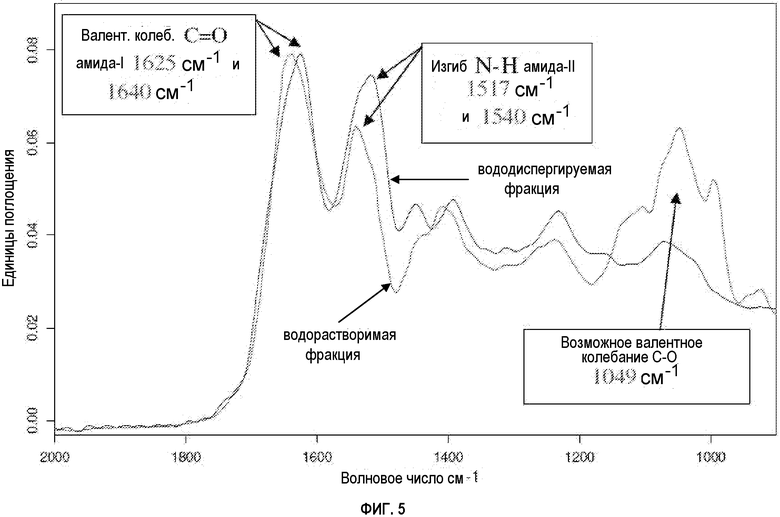
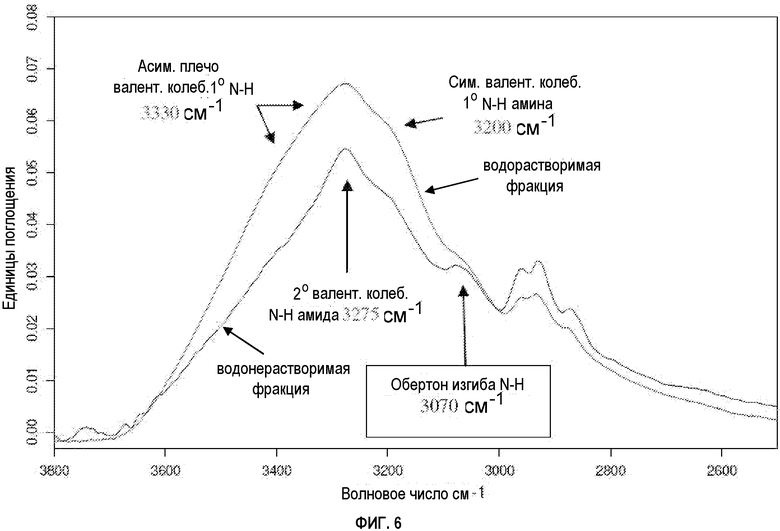

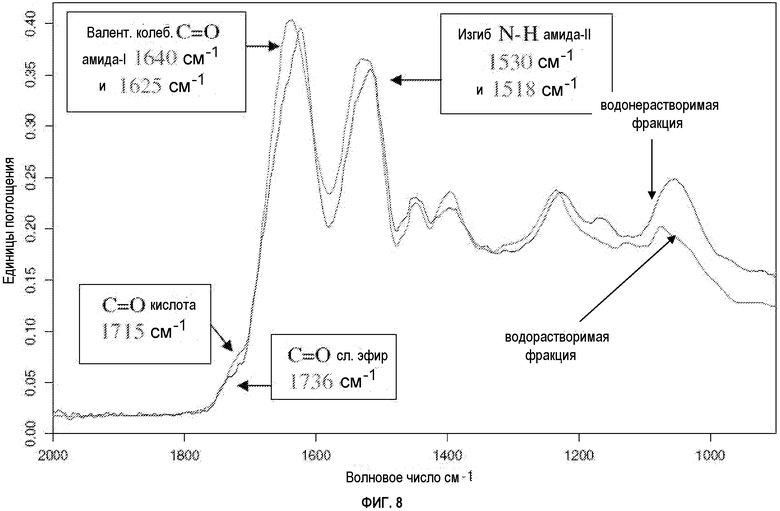
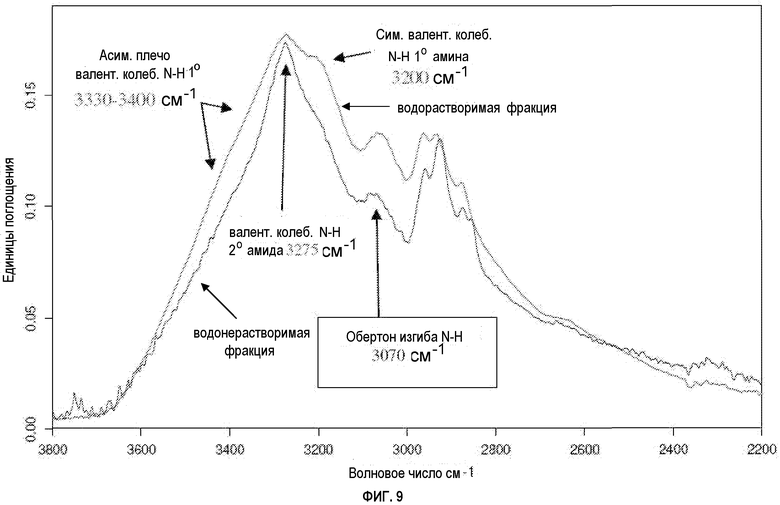
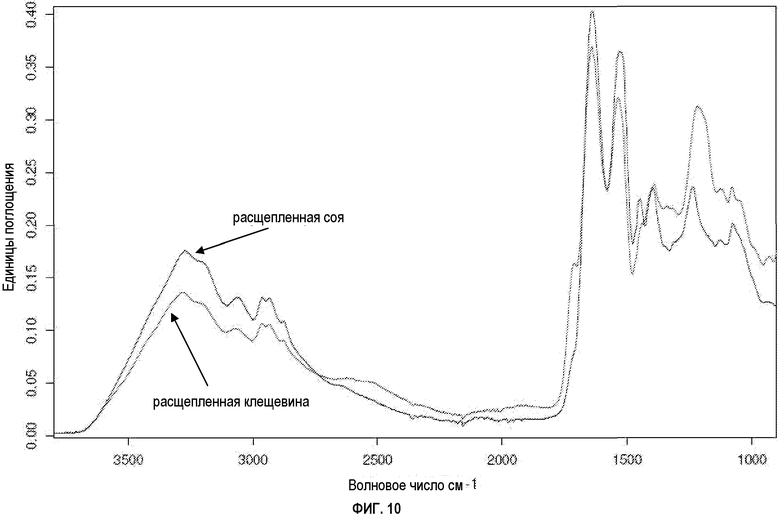

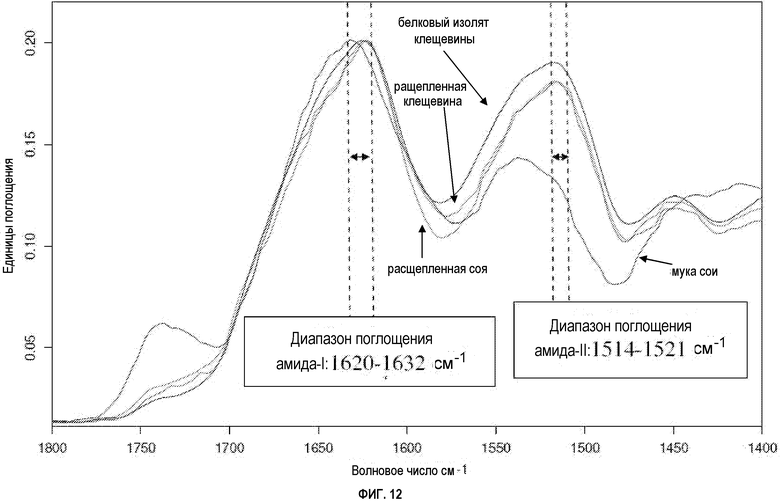







Изобретение относится к полиуретановому пеноматериалу, способу получения полиуретанового пеноматериала, премиксу для получения полиуретанового материала и изделию, содержащему пеноматериал. Полиуретановый пеноматериал представляет собой продукт реакции смеси: (а) реагент на основе изоцианата; (b) необязательное реагирующее с изоцианатом соединение и белоксодержащую композицию, способную уменьшать плотность полиуретанового пеноматериала по меньшей мере на 5% относительно полиуретанового материала, полученного из той же самой смеси, но лишенного белоксодержащей композиции. Технический результат - получение возобновляемых, менее дорогостоящих и более благоприятных в отношении окружающей среды агентов, которые могут модулировать свойства пеноматериалов. 4 н. и 76 з.п. ф-лы, 11 табл., 19 ил., 14 пр.
1. Полиуретановый пеноматериал, содержащий продукт реакции смеси, содержащей:
(a) реагент на основе изоцианата;
(b) необязательное реагирующее с изоцианатом соединение; и
(c) белоксодержащую композицию, способную уменьшать плотность полиуретанового пеноматериала по меньшей мере на 5% относительно полиуретанового пеноматериала, полученного из той же самой смеси, но лишенного белоксодержащей композиции.
2. Полиуретановый пеноматериал по п. 1, где реагентом на основе изоцианата является органический полиизоцианат.
3. Полиуретановый пеноматериал по п. 2, где органическим полиизоцианатом является полимерный дифенилметандиизоцианат, 2,4-толуолдиизоцианат, 2,6-толуолдиизоцианат, бензолдиизоцианат, м-ксилилендиизоцианат, 1,4-фенилендиизоцианат, 1,3-фенилендиизоцианат, 4,4′-дифенилдиизоцианат, 4,4′-дифенилдиметилметандиизоцианат, гексаметилендиизоцианат, толидиндиизоцианат, дианизидиндиизоцианат, 1,5-нафталиндиизоцианат, 1,4-циклогександиизоцианат или их комбинация.
4. Полиуретановый пеноматериал по п. 1, где реагент на основе изоцианата содержит уретан, аллофанат, мочевину, биурет, карбодиимид, уретонимин, изоцианурат или их комбинацию.
5. Полиуретановый пеноматериал по п. 1, где реагентом на основе изоцианата является полимерный дифенилметандиизоцианат.
6. Полиуретановый пеноматериал по п. 1, где реагирующее с изоцианатом соединение присутствует и способно нуклеофильно реагировать с изоцианатом.
7. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является соединение, имеющее гидроксильную группу или аминогруппу, способную реагировать с изоцианатом.
8. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является полиол.
9. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является полиол, полученный из касторового масла, льняного масла или соевого масла.
10. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является полиол, инициируемый соединением, выбранным из группы, состоящей из глицерина, триметилолпропана, триэтаноламина, пентаэритрита, сорбита, сахарозы, диамина, толуолдиамина, диаминодифенилметана, полиметиленполифениленполиамина, этаноламина, диэтаноламина или их смеси.
11. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является простой политиоэфир с концевой гидроксильной группой, полиамид, сложный полиэфирамид, поликарбонат, полиацеталь, полиолефин или полисилоксан, или соединением является сложный полиэфир, полученный конденсацией гликоля или полиола с более высоким количеством функциональных групп с дикарбоновой кислотой.
12. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является полиоксипропиленгликоль, полипропиленоксид-этиленоксид, пропиленгликоль, пропандиол, глицерин, аминалкоксилат или их смесь.
13. Полиуретановый пеноматериал по п. 6, где реагирующим с изоцианатом соединением является полиоксипропиленгликоль.
14. Полиуретановый пеноматериал по п. 1, где смесь дополнительно содержит поверхностно-активное вещество.
15. Полиуретановый пеноматериал по п. 1, где пеноматериал имеет плотность в диапазоне от приблизительно 0,01 г/см3 до приблизительно 0,5 г/см3, как определено при помощи ASTM D-7487.
16. Полиуретановый пеноматериал по п. 1, где пеноматериал имеет плотность, которая является на 5-80% меньше, чем плотность пеноматериала, созданного из той же самой исходной композиции, лишенной белоксодержащей композиции.
17. Полиуретановый пеноматериал по п. 1, где время образования "сливок", определяемое при помощи ASTM D-7487, составляет менее одной минуты.
18. Полиуретановый пеноматериал по п. 1, где свободная высота подъема пеноматериала, определяемая при помощи ASTM D-7487, является больше, чем свободная высота подъема пеноматериала, созданного из той же самой исходной композиции, лишенной белоксодержащей композиции.
19. Полиуретановый пеноматериал по п. 8, где свободная высота подъема пеноматериала является по меньшей мере на 5% больше, чем свободная высота подъема пеноматериала, созданного из той же самой исходной композиции, лишенной белоксодержащей композиции.
20. Полиуретановый пеноматериал по п. 1, где пеноматериал имеет большее количество малых, однородных пор в сравнении с пеноматериалом, созданным из той же самой исходной композиции, лишенной белоксодержащей композиции.
21. Полиуретановый пеноматериал по любому из пп. 1-20, где белоксодержащая композиция включает выделенную водорастворимую полипептидную композицию.
22. Полиуретановый пеноматериал по любому из пп. 1-20, где белоксодержащая композиция представляет собой выделенную водорастворимую полипептидную композицию.
23. Полиуретановый пеноматериал по п. 21, где выделенная водорастворимая полипептидная композиция включает один или несколько из следующих признаков:
(a) полоса поглощения амида-I между приблизительно 1633 см-1 и 1680 см-1, как определено ИК-Фурье-спектроскопией твердого состояния FTIR;
(b) полоса амида-II между приблизительно 1522 см-1 и 1560 см-1, как определено FTIR твердого состояния;
(c) две выраженные полосы поглощения валентных колебаний N-H 1° амида с центрами в области около 3200 см-1 и в области около 3300 см-1, как определено FTIR твердого состояния;
(d) выраженный кластер протонированных ядер азота, определяемый в границах химического сдвига 15N в области около 94 м.д. и около 100 м.д., и в границах химического сдвига 1Н в области около 7,6 м.д. и около 8,1 м.д., как определено с помощью жидкофазного двумерного ЯМР протон-азотного взаимодействия;
(e) средняя молекулярная масса между приблизительно 600 и приблизительно 2500 Дальтон;
(f) неспособность стабилизировать эмульсию типа масло-в-воде, в которой, когда водный раствор, содержащий 14 массовых частей белка, растворенных или диспергированных в 86 массовых частях воды, смешивают с 14 массовыми частями PMDI, этот водный раствор и PMDI образуют нестабильную суспензию, которая макроскопически разделяется на фазы при статических условиях в течение пяти минут после смешивания;
(g) водорастворимая полипептидная композиция способна стабилизировать пеноматериал на основе полиуретана относительно пеноматериала на основе полиуретана, образованного из той же самой исходной композиции, лишенной водорастворимой белковой композиции; или
(h) водорастворимая полипептидная композиция способна уменьшать плотность пеноматериала на основе полиуретана по меньшей мере на 5% относительно пеноматериала на основе полиуретана, образованного из той же самой исходной композиции, лишенной водорастворимой полипептидной композиции.
24. Полиуретановый пеноматериал по любому из пп. 1-20, где полипептидная композиция получена из биомассы, выбранной из группы, состоящей из молочной сыворотки, кукурузы, пшеницы, подсолнечника, хлопка, семян рапса, канолы, клещевины, сои, рыжика посевного, льна, ятрофы, мальвы, земляного ореха, табака, водорослей, выжимок (жома) сахарного тростника и их комбинаций.
25. Полиуретановый пеноматериал по п. 21, где полипептидная композиция получена из биомассы, выбранной из группы, состоящей из молочной сыворотки, кукурузы, пшеницы, подсолнечника, хлопка, семян рапса, канолы, клещевины, сои, рыжика посевного, льна, ятрофы, мальвы, земляного ореха, табака, водорослей, выжимок (жома) сахарного тростника и их комбинаций.
26. Полиуретановый пеноматериал по п. 23, где полипептидная композиция получена из биомассы, выбранной из группы, состоящей из молочной сыворотки, кукурузы, пшеницы, подсолнечника, хлопка, семян рапса, канолы, клещевины, сои, рыжика посевного, льна, ятрофы, мальвы, земляного ореха, табака, водорослей, выжимок (жома) сахарного тростника и их комбинаций.
27. Полиуретановый пеноматериал по п. 21, где полипептидная композиция получена из молочной сыворотки, семян рапса, канолы, клещевины или сои.
28. Полиуретановый пеноматериал по п. 23, где полипептидная композиция получена из молочной сыворотки, семян рапса, канолы, клещевины или сои.
29. Полиуретановый пеноматериал по п. 21, где полипептидная композиция получена из семян рапса, канолы или клещевины.
30. Полиуретановый пеноматериал по п. 23, где полипептидная композиция получена из семян рапса, канолы или клещевины.
31. Способ получения полиуретанового пеноматериала, включающий стадии:
(a) смешивания белоксодержащей композиции и реагента на основе изоцианата с получением смеси; и
(b) выдерживания смеси для образования полиуретанового пеноматериала, где белоксодержащая композиция способна уменьшать плотность полиуретанового пеноматериала по меньшей мере на 5% относительно полиуретанового пеноматериала, полученного из той же самой смеси, но лишенной белоксодержащего компонента.
32. Способ по п. 31, где белоксодержащая композиция содержит выделенную водорастворимую полипептидную композицию.
33. Способ по п. 31 или 32, где смесь на стадии (а) дополнительно содержит реагирующее с изоцианатом соединение.
34. Способ по п. 31 или 32, где реагентом на основе изоцианата является органический полиизоцианат.
35. Способ по п. 34, где органическим полиизоцианатом является полимерный дифенилметандиизоцианат, 2,4-толуолдиизоцианат, 2,6-толуолдиизоцианат, бензолдиизоцианат, м-ксилилендиизоцианат, 1,4-фенилендиизоцианат, 1,3-фенилендиизоцианат, 4,4′-дифенилдиизоцианат, 4,4′-дифенилдиметилметандиизоцианат, гексаметилендиизоцианат, толидиндиизоцианат, дианизидиндиизоцианат, 1,5-нафталиндиизоцианат, 1,4-циклогександиизоцианат или их комбинация.
36. Способ по п. 31 или 32, где реагент на основе изоцианата содержит уретан, аллофанат, мочевину, биурет, карбодиимид, уретонимин, изоцианурат или их комбинацию.
37. Способ по п. 31 или 32, где реагентом на основе изоцианата является полимерный дифенилметандиизоцианат.
38. Способ по п. 33, где реагирующим с изоцианатом соединением является соединение, способное нуклеофильно реагировать с изоцианатом.
39. Способ по п. 38, где реагирующим с изоцианатом соединением является соединение, имеющее гидроксильную группу или аминогруппу, способную реагировать с изоцианатом.
40. Способ по п. 33, где реагирующим с изоцианатом соединением является полиол.
41. Способ по п. 33, где реагирующим с изоцианатом соединением является полиол, полученный из касторового масла, льняного масла или соевого масла.
42. Способ по п. 33, где реагирующим с изоцианатом соединением является полиол, инициируемый соединением, выбранным из группы, состоящей из глицерина, триметилолпропана, триэтаноламина, пентаэритрита, сорбита, сахарозы, диамина, толуолдиамина, диаминодифенилметана, полиметиленполифениленполиамина, этаноламина, диэтаноламина или их смеси.
43. Способ по п. 33, где реагирующее с изоцианатом соединение является сложным полиэфиром, полученным конденсацией гликоля или полиола с более высоким количеством функциональных групп с дикарбоновой кислотой; или простым политиоэфиром с концевой гидроксильной группой, полиамидом, сложным полиэфирамидом, поликарбонатом, полиацеталем, полиолефином или полисилоксаном.
44. Способ по п. 33, где реагирующим с изоцианатом соединением является полиоксипропиленгликоль, полипропиленоксид-этиленоксид, пропиленгликоль, пропандиол, глицерин, аминалкоксилат или их смесь.
45. Способ по п. 33, где реагирующим с изоцианатом соединением является полиоксипропиленгликоль.
46. Способ по п. 31 или 32, где смесь на стадии (а) дополнительно содержит вспенивающий агент или соединение, которое образует вспенивающий агент.
47. Способ по п. 46, где соединением, которое образует вспенивающий агент, является вода.
48. Способ по п. 32, где водорастворимый белок растворен, диспергирован или суспендирован в воде, в растворе, содержащем реагент на основе изоцианата, или в растворе, содержащем реагирующий с изоцианатом материал.
49. Способ по п. 31 или 32, где смесь на стадии (а) дополнительно содержит катализатор, который способствует образованию пеноматериала.
50. Способ по п. 49, где катализатором является дилаурат дибутилолова, диацетат дибутилолова, триэтилендиамин, 2,2′-диметиламинодиэтиловый эфир, 2-диметиламиноэтанол, октоат двухвалентного олова, октоат калия, соль щелочного металла карбоновой кислоты или их комбинация.
51. Способ по п. 31 или 32, где смесь на стадии (а) дополнительно содержит поверхностно-активное вещество.
52. Способ по п. 51, где поверхностно-активным веществом является простой эфир силикона.
53. Способ по п. 31 или 32, где смесь на стадии (а) дополнительно содержит добавку, выбранную из группы, состоящей из антипирена, наполнителя, армирующего материала, подавителя дыма, биоцида, инертного пластификатора, антистатического агента и их комбинаций.
54. Способ по п. 31 или 32, где реагент на основе изоцианата составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) исходных материалов, используемых для получения пеноматериала.
55. Способ по п. 33, где реагирующее с изоцианатом соединение составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) исходных материалов, используемых для получения пеноматериала.
56. Способ по п. 31 или 32, где пеноматериал получают при Индексе в диапазоне от приблизительно 250% до приблизительно 800%.
57. Способ по п. 31 или 32, где белоксодержащая композиция составляет от приблизительно 0,1% (мас./мас.) до приблизительно 50% (мас./мас.) исходных материалов, используемых для получения пеноматериала.
58. Премикс для получения полиуретанового пеноматериала, содержащий:
(a) белоксодержащую композицию; и
(b) реагент на основе изоцианата,
где белоксодержащая композиция способна уменьшать плотность полиуретанового пеноматериала по меньшей мере на 5% относительно полиуретанового пеноматериала, полученного из той же самой смеси, но лишенной белоксодержащего компонента.
59. Премикс по п. 58, где белоксодержащая композиция содержит выделенную водорастворимую полипептидную композицию.
60. Премикс по п. 59, где реагентом на основе изоцианата является органический полиизоцианат.
61. Премикс по п. 60, где органическим полиизоцианатом является полимерный дифенилметандиизоцианат, 2,4-толуолдиизоцианат, 2,6-толуолдиизоцианат, бензолдиизоцианат, м-ксилилендиизоцианат, 1,4-фенилендиизоцианат, 1,3-фенилендиизоцианат, 4,4′-дифенилдиизоцианат, 4,4′-дифенилдиметилметандиизоцианат, гексаметилендиизоцианат, толидиндиизоцианат, дианизидиндиизоцианат, 1,5-нафталиндиизоцианат, 1,4-циклогександиизоцианат или их комбинация.
62. Премикс по п. 58 или 59, где реагент на основе изоцианата содержит уретан, аллофанат, мочевину, биурет, карбодиимид, уретонимин, изоцианурат или их комбинацию.
63. Премикс по п. 58 или 59, где реагентом на основе изоцианата является полимерный дифенилметандиизоцианат.
64. Премикс по п. 58 или 59, дополнительно содержащий реагирующее с изоцианатом соединение.
65. Премикс по п. 64, где реагирующим с изоцианатом соединением является соединение, способное нуклеофильно реагировать с изоцианатом.
66. Премикс по п. 65, где реагирующим с изоцианатом соединением является соединение, имеющее гидроксильную группу или аминогруппу, способную реагировать с изоцианатом.
67. Премикс по п. 64, где реагирующим с изоцианатом соединением является полиол.
68. Премикс по п. 64, где реагирующим с изоцианатом соединением является полиол, полученный из касторового масла, льняного масла или соевого масла.
69. Премикс по п. 64, где реагирующим с изоцианатом соединением является полиол, инициируемый соединением, выбранным из группы, состоящей из глицерина, триметилолпропана, триэтаноламина, пентаэритрита, сорбита, сахарозы, диамина, толуолдиамина, диаминодифенилметана, полиметиленполифениленполиамина, этаноламина, диэтаноламина или их смеси.
70. Премикс по п. 64, где реагирующее с изоцианатом соединение является сложным полиэфиром, полученным конденсацией гликоля или полиола с более высоким количеством функциональных групп с дикарбоновой кислотой; или простым политиоэфиром с концевой гидроксильной группой, полиамидом, сложным полиэфирамидом, поликарбонатом, полиацеталем, полиолефином или полисилоксаном.
71. Премикс по п. 64, где реагирующим с изоцианатом соединением является полиоксипропиленгликоль, полипропиленоксид-этиленоксид, пропиленгликоль, пропандиол, глицерин, аминалкоксилат или их смесь.
72. Премикс по п. 64, где реагирующим с изоцианатом соединением является полиоксипропиленгликоль.
73. Премикс по п. 58 или 59, дополнительно содержащий вспенивающий агент или соединение, которое образует вспенивающий агент.
74. Премикс по п. 58 или 59, дополнительно содержащий катализатор, который способствует образованию пеноматериала.
75. Премикс по п. 58 или 59, где реагент на основе изоцианата составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) премикса.
76. Премикс по п. 64, где реагирующее с изоцианатом соединение составляет приблизительно от 10% (мас./мас.) до приблизительно 90% (мас./мас.) премикса.
77. Премикс по п. 58 или 59, где белоксодержащая композиция составляет приблизительно от 0,01% (мас./мас.) до приблизительно 99% (мас./мас.) исходных материалов, используемых для получения пеноматериала.
78. Изделие, содержащее пеноматериал по любому из пп. 1-30.
79. Полиуретановый пеноматериал по п. 1, где белоксодержащая композиция дополнительно содержит белок, способный диспергировать полимерный дифенилметандиизоцианат (PMDI) в водной среде.
80. Способ по пп. 31 или 32 или премикс по любому из пп. 58-60, где полипептидная композиция получена из биомассы, выбранной из группы, состоящей из молочной сыворотки, кукурузы, пшеницы, подсолнечника, хлопка, семян рапса, канолы, клещевины, сои, рыжика посевного, льна, ятрофы, мальвы, земляного ореха, табака, водорослей, выжимок (жома) сахарного тростника и их комбинаций.
| LIN Y ET AL: "WATER-BLOWN FLEXIBLE POLYURETHANE FOAM EXTENDED WITH BIOMASS MATERIALS", JOURNAL OF APPLIED POLYMER SCIENCE, JOHN WILEY AND SONS INC | |||
| NEW YORK, vol.65, n.4, 25.07.1997 | |||
| US 3075930 A 29.01.1963 | |||
| US 4327195 A 27.04.1982 | |||
| US 7345136 B2 18.03.2008 | |||
| GB 2001331 A 31.01.1979 | |||
| ПЕНООБРАЗУЮЩИЙ СОСТАВ ДЛЯ ПЕРФОРАЦИИ ПРОДУКТИВНЫХ ПЛАСТОВ | 2003 |
|
RU2252238C1 |
Авторы
Даты
2015-08-10—Публикация
2010-03-08—Подача