Изобретение относится к области получения антимикробных композиций, относящихся к классу катионных антисептиков [1], приготовленных в процессе образования раствора, содержащего как супрамолекулярные структуры L-цистеин-серебряного раствора [2], так и молекулы хитозана. Полученные композиции могут быть использованы при производстве лекарственных средств, обладающих антимикробными свойствами в виде раствора или пленок, при разработке консервантов для объектов растительного и животного происхождения.
Супрамолекулярные системы - это полимолекулярные структуры, сформированные в результате ассоциации частиц малых размеров, таких как молекулы, олигомеры, кластеры, удерживаемых вместе межмолекулярными силами [3]. Поэтому супрамолекулярную структуру можно разделить на фрагменты, не разрывая при этом химических связей. Применение супрамолекулярных структур для разработки лекарственных композиций открывает новые перспективы для получения разнообразных медицинских препаратов широкого спектра действия. В настоящее время открыт новый класс супрамолекулярных объектов, синтезированных на основе L-цистеина и нитрата серебра [2]. Эти объекты построены из пересекающихся цепочек наноразмерных, положительно заряженных фрактальных кластеров [4] и представляют собой совокупность фрагментов трехмерной сетки, распределенных в водной или водно-органической среде [2]. Эту совокупность молекулярных структур будем именовать L-цистеин-серебряным раствором. Эти структуры способны эффективно взаимодействовать с отрицательно заряженными группами, присутствующими на клеточной поверхности микроорганизма, что придает L-цистеин-серебряному раствору свойства катионного антисептика.
К катионным антисептикам относятся химические соединения разной природы, имеющие в своей структуре сильно основные функциональные группы, среди которых важное значение имеют свободные или замещенные аминогруппы, иминогруппа, гуанидиновая группировка [1]. Основные группы этих антисептиков в слабокислой среде приобретают положительный заряд и поэтому они взаимодействуют с отрицательно заряженными цитоплазматическими мембранами бактерий, нарушая их функционирование. Хорошо известен катионный антисептик - хлоргексидин, имеющий в своем составе две сильно основные дигуанидиновые группировки [1].
Хитозан (ХЗ) - частично деацетилированное производное природного полисахарида хитина (поли[1→4)-N-ацетил-2-амино-2-дезокси-β-D-глюкопиранозы] - привлекает в последнее время внимание как биологически активное вещество, имеющее такие свойства, как биосовместимость, антимикробное действие, способность активировать макрофаги, усиливать пролиферацию фибробластов [5]. Свободные аминогруппы ХЗ протонированы, поэтому его молекулы заряжены положительно, что во многом определяет их сродство к клеткам микроорганизмов. Антибактериальные свойства ХЗ зависят от его молекулярной массы, степени деацетилирования (СД), степени протонирования свободных аминогрупп ХЗ. Растворимость ХЗ в водной среде сильно зависит от молекулярной массы, СД и кислотности раствора. По мере уменьшения степени деацетилирования кулоновское отталкивание протонированных аминогрупп ХЗ уменьшается, а вклад водородных связей, образующихся с участием ацетамидных групп ХЗ, в межмолекулярные взаимодействия возрастает. С учетом гидрофобных эффектов это приводит к усилению самоагрегации молекул ХЗ в растворах и уменьшению его растворимости. Как поликатион ХЗ может образовывать полиэлектролитные комплексы (ПЭК) с полианионами как синтетическими, например полиакриловой кислотой, так и природными, такими как, глюкозаминогликанами, полисахаридами, с полианионом ДНК, а при определенных условиях и с белками.
Исследованием уровня техники установлено, что в доступных информационных источниках описаны композиции ХЗ с разнообразными соединениями, именно низкомолекулярными веществами, кластерами металлов, неионогенными полимерами, отрицательно заряженными полиэлектролитами. При разработке композиций лежат биоактивные и комплексообразующие свойства ХЗ. Так, известна композиция, содержащая ХЗ (0,1%), аскорбиновую кислоту (0,165%) и аскорбанат натрия, применяемых в хирургической стоматологии для заживления дефектов парадонтальной ткани [6]. Разработаны антимикробные композиции на основе низкомолекулярного ХЗ, включающие в свой состав загустители, такие как поливиниловый спирт, глицерин, полиэтиленгликоль, поливинилпирролидон [7]. На свойстве ХЗ образовывать полиэлектролитные комплексы основано его применение в медицине и биотехнологии для разработки биоконструкционных материалов, пленок мембран, сорбентов [5], а также антимикробных композиций, например, с антибиотиком полипептидного типа, продуцируемого бактерией рода Streptococcus, низином [8], который содержит 34 остатка аминокислот и сам обладает бактерицидным действием на грамположительные микроорганизмы. Известны также антимикробные композиции на основе микрогранул геля хитозана и кластерных частиц серебра малых размеров [9].
В качестве прототипа авторы предлагают композицию хитозана с ионами благородных металлов, таких как золото и серебро, которая проявляет способность обеззараживающего действия на кожу. Ионы серебра и золота подавляют патогенную микрофлору. В состав композиции входит хитозан в виде геля и серебро (или золото) в количестве 0,1% по массе [10].
Таким образом, в приведенных выше примерах использование ХЗ в композициях основывается на способности хитозана 1) взаимодействовать с полианионами, 2) совмещаться с неразряженными низкомолекулярными или высокомолекулярными соединениями, 3) совмещаться с ионами или кластерами серебра.
Задачей, на решение которой направлено заявляемое изобретение, является получение нового класса антимикробных композиций, включающих наряду с молекулами ХЗ как представителя природного катионного полиэлектролита, также супрамолекулярные структуры нового катионного полиэлектролита, полученного на основе L-цистеина и нитрата серебра и также обладающего антимикробными свойствами.
Технический результат настоящего изобретения заключается в том, что получена композиция L-цистеин-серебряного раствора и хитозана, сочетающая очень разветвленные и разреженные сеточные молекулярные структуры L-цистеин-серебряного раствора и палочковидных молекул хитозана. Благодаря заряду и большой поверхности эти структуры способны эффективно взаимодействовать с отрицательно заряженными группами, присутствующим на клеточной поверхности микроорганизма, что придает композициям свойства катионного антисептика. При этом спектр антимикробного действия и эффективность ряда композиций сохраняется при меньшем суммарном содержании компонентов, чем в отдельно взятом ХЗ.
Технический результат достигается тем, что смешивают рассчитанное количество L-цистеин-серебряный раствора с массовой концентрацией 0,4% (по массовому содержанию серебра 0,16%), с рассчитанным количеством водного раствора хитозана с концентрацией 1,26%), содержащим однопроцентную уксусную или янтарную кислоту, и затем добавляют к смеси дистиллированную воду до такого объема, чтобы концентрации компонентов в композиции находились в следующих значениях:
При этом образуется слегка опалесцирующий раствор, который хранят в защищенном от света месте при температуре от 10 до 30°C.
Сущность заявляемого изобретения заключается в том, что возможно получение стабильных растворов, содержащих как молекулы хитозана, так и фрактальные структуры L-цистеин-серебряного раствора. При этом антимикробные свойства таких композиций сохраняются, а в ряде случаев превосходят антимикробные свойства составляющих компонентов. Композиции легко приготавливаются путем смешивания растворов отдельных компонентов. Возможность получения стабильных композиций таких сложных молекулярных систем, как ХЗ и ЦСР, и проявление ими антимикробных свойств не является тривиальным явлением и не вытекает с очевидностью из структуры и свойств отдельных компонентов этих композиций. Так, устойчивость раствора смеси компонентов могла бы не наблюдаться в результате протекания следующих процессов: 1) образование малорастворимых ассоциатов хитозана с фрактальной структурой ЦСР посредством их агрегации через анионы, 2) взаимное высаливание компонентов смеси, 3) коллапс фрактальной структуры ЦСР под действием кулоновского поля поликатиона хитозана. Антимикробные свойства композиции могли бы сильно ухудшаться не только в результате действия вышеуказанных факторов, но и вследствие конкуренции компонентов композиции за места связывания на поверхности микроорганизма. Таким образом, существенными обстоятельствами, влияющими на получение стабильных антимикробных композиций ХЗ с ЦСР, являются отсутствие негативного влияния компонентов композиции друг на друга, мешающее проявлять присущие каждому компоненту физико-химические и антимикробные свойства. Этот вывод является обобщением опытных фактов.
Отличие заявляемых композиций от прототипа состоит в том, что молекулы хитозана комбинируются не с ионами серебра, а с супрамолекулярной структурой L-цистеин-серебряного раствора, полученной при взаимодействии ионов серебра с природной аминокислотой L-цистеином. В L-цистеин-серебряном растворе отсутствуют свободные ионы серебра, так как они образуют с L-цистеином прочную молекулу меркаптида серебра, из которой строится супрамолекулярная структура [2]. В то время как в композиции хитозана с ионами серебра эти ионы присутствуют, так как и молекула хитозана, и ион серебра заряжены положительно, что препятствует образованию прочных комплексов. Недостаток композиций, содержащих свободные ионы серебра состоит в том, что ионы серебра обладают прижигающим и иссушающем действием на кожу и слизистые оболочки, а также, связываясь с анионами жидких сред организма, такими как хлорид-ион, фосфат-ион, карбонат-ион, образуют малорастворимые соединения.
В заявляемом изобретении представлены композиции ХЗ и ЦСР (№3÷№10) следующих составов (концентрация по массовому содержанию растворенных компонентов):
1. ЦСР C=0,1%
2. Хитозан (C=0,9%),
3. ЦСР (C=0,1%) + Хитозан (C=0,75%),
4. ЦСР (C=0,1%) + Хитозан (C=0,9%),
5. ЦСР (C=0,15%) + Хитозан (C=0,5%),
6. ЦСР (C=0,2%) + Хитозан (C=0,5%),
7. ЦСР (C=0,2%) + Хитозан (C=0,6%),
8. ЦСР (C=0,288%) + Хитозан (C=0,28%),
9. ЦСР (C=0,32%) + Хитозан (C=0,2%),
10. ЦСР (C=0,266%) + Хитозан (C=0,42%)
11. Хитозан (С=1,26%)
Система №1 представляет раствор ЦСР, а системы №2, 11 - растворы ХЗ и приготовлены для сравнения с антимикробной активностью композиций. Концентрации уксусной или янтарной кислот в композициях не приводится, так как эти компоненты носят вспомогательный характер при приготовлении исходного раствора хитозана и, как проверено опытным путем, не влияют на антимикробную активность.
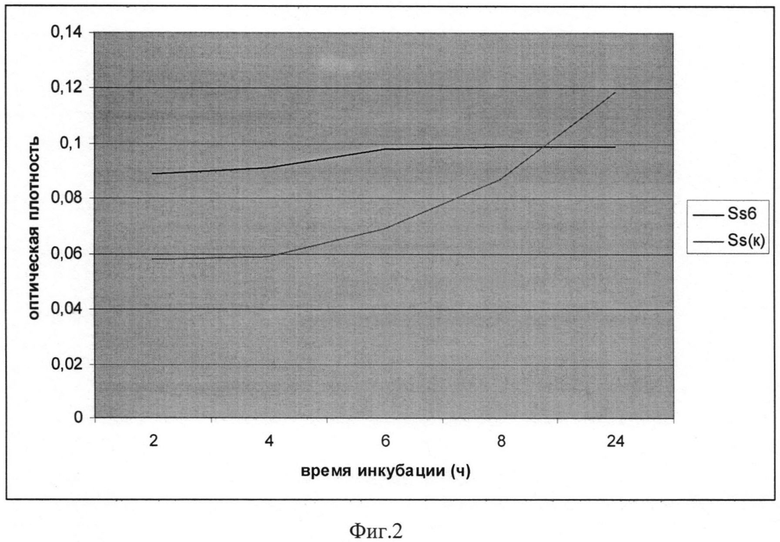
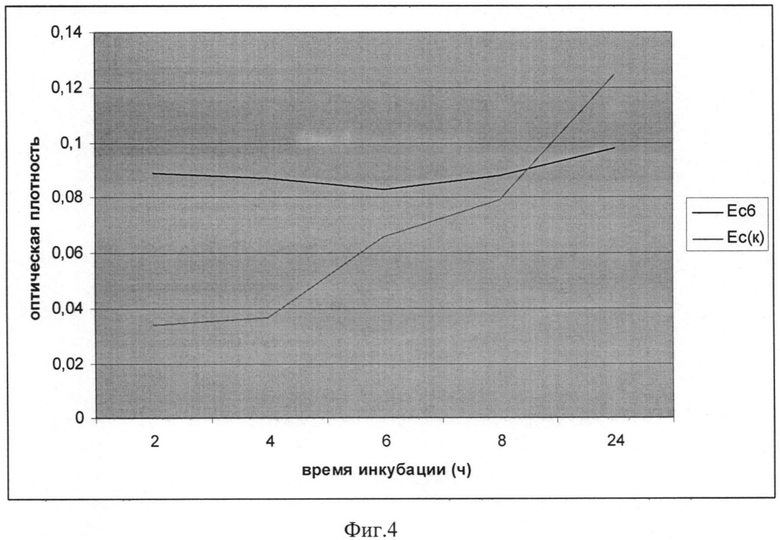
При анализе влияния испытуемых образцов на рост тестовых культур можно констатировать, что все испытанные композиции достаточно эффективно подавляют их рост (табл. 1) и (Фиг. 2, 4). Присутствие в композиции ЦСР позволяет заметно снизить содержание ХЗ, так что суммарное содержание компонентов уменьшается, а антимикробная активность практически (в пределах погрешности определения) не ухудшается или даже возрастает. Например, это видно из сравнения образцов №2 и №6 табл. 1. Этот же вывод можно сделать, сравнив антимикробную активность ХЗ (1,26%) и композиции №10 (фиг. 1-4).
Антимикробные свойства заявляемых композиций поясняются табл. 1 и графическими материалами (Фиг. 1-4).
Таблица 1. Антагонистическая активность исследуемых образцов по отношению к тест-культурам патогенных и условно-патогенных микроорганизмов, определенная методом диффузии в агар.
Фиг. 1 Динамика роста Staphylococcus aureus в присутствии 1,26% хитозана
Фиг. 2 Динамика роста Staphylococcus aureus в присутствии 0,42% ХЗ и 0,266% ЦСР
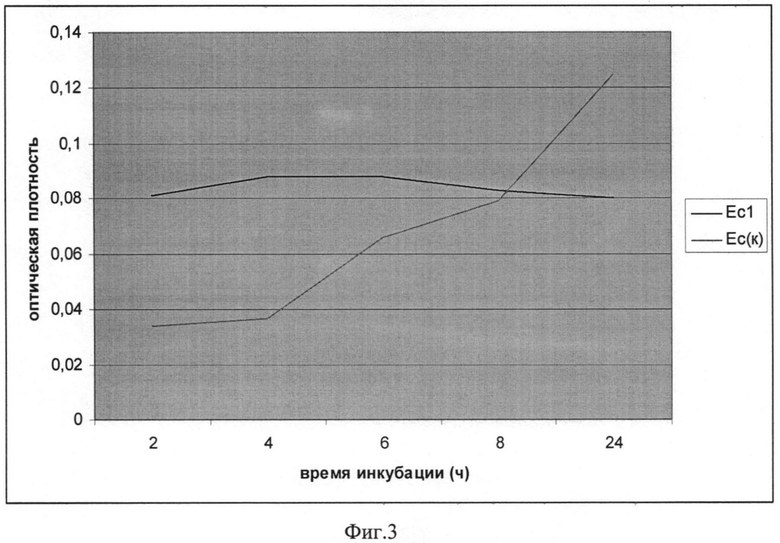
Фиг. 3 Динамика роста E.coli в присутствии 1,26% хитозана
Фиг. 4 Динамика роста E.coli в присутствии 0,42% хитозана и 0,266% ЦСР
Способ осуществления изобретения
1. Приготовление исходного раствора хитозана.
Для приготовления раствора использовался хитозан пищевой с степенью деацетилирования 95,7% (ТУ 9289-046-04689375-96, ЗАО Сонат, Россия). К 1,26 грамма ХЗ в колбе на 100 мл приливают 90 мл воды, в которой растворен 1 грамм уксусной или янтарной кислоты, и ставят в термостат при 60°C, постоянно перемешивая ее содержимое до растворения хитозана, затем раствор переносят в мерную колбу на 100 мл и доводят водой до метки.
2. Приготовление исходного раствора ЦСР концентрацией 0,4%(по массе): в колбе на 100 мл растворяют 255 мг нитрата серебра в 70 мл воды, в стаканчике на 100 мл растворяют 145,2 мг L-цистеина в 30 мл воды и этот раствор быстро приливают к раствору нитрата серебра, энергично перемешивают, закрывают притертой пробкой и ставят смесь в термостат при 60°C на 1 час.
3. Приготовление композиций ХЗ и ЦСР.
Пример 1 - приготовления композиции №10.
В стеклянный пузырек объемом 25 мл приливают 6 мл ЦСР (0.4%), затем добавляют 3 мл ХЗ (1,26%). Пузырек закрывают полиэтиленовой пробкой, энергично перемешивают встряхиванием в течение 1 минуты.
4. Испытание антимикробных свойств композиций осуществлялась двумя способами:
4.1 Антибактериальная активность композиций №1-9 проводилась методом диффузии в агар на газоне тест культур: Bacillus subtilis 6633, Staphylococcus aureus P209 АТСС 25923, E.coli АТСС 25922, Shigella sonnei III №1908, Salmonella typhimurium 5715, Pseudomonas aeruginosa ATCC 27853, Candida albicans ATCC 885-653.
Исследуемые образцы помещали микропипеткой объемом 20 мкл на засеянную тестовой культурой микроорганизмов поверхность оптимальной питательной среды и культивировали при 37°C в течение суток. Антибактериальную активность материала выражали в мм диаметра задержки роста. Результаты определения представлены в таблице 1.
4.2. Испытание антимикробных свойств композиций №10, 11.
Характер роста исследуемых микроорганизмов в мясо-пептонном бульоне в присутствии различных концентраций и комбинаций хитозана и цистеин серебряного раствора изучалась в динамике на протяжении 24 часов путем измерения оптической плотности в КФК при длине волны 560 нм.
В эксперименте участвовали 2 тест культуры микроорганизмов: грамположительные Staphylococcus aureus, грамотрицательные E.coli.
Методика определения оптической плотности исследуемого раствора Приготовление исследуемого раствора: 2 мл исследуемого образца добавляли в 8 мл мясо-пептонного бульона (МПБ) и тщательно перемешивали. Затем сюда же добавляли 0,1 мл суточной тестовой культуры, перемешивали и ставили для инкубирования в термостат. В качестве тестовых культур для данной методики были использованы следующие штаммы: патогенные и условно-патогенные микроорганизмы Staphylococcus aureus 209, Escherichia coli АТСС 25922. Для контроля роста тестовых культур по 0,1 мл каждой из них добавляли в 10 мл мясо-пептонного бульона и также инкубировали в термостате. Таким образом, для каждого образца использовалось 3 пробирки МПБ по 8 мл для приготовления исследуемых растворов и 3 пробирки МПБ по 10 мл для контроля тестовых культур.
Для измерения оптической плотности в кюветное отделение спектрофотометра устанавливали кюветы с контрольным раствором (стерильный МПБ), по отношению к которому производится измерение, и исследуемым раствором и измеряли его оптическую плотность при длине волны 540 нм.
Оптическая плотность всех исследуемых растворов измерялась в течение суток: через 2 часа, 4 часа, 6 часов, 8 часов и 24 часа. На основании полученных данных строились графики изменения оптической плотности в зависимости от времени измерения.
Список используемой литературы
1. Т. Франклин, Дж. Сноу, Биохимия антимикробного действия, М.: Мир, 1984.
2. Патент №2423384 от 8.10.2009.
3. Ж. - М. Лен. Супрамолекулярная химия. Концепции и перспективы. Наука, Новосибирск, 1998.
4. В.Смирнов. Физика фрактальных кластеров. М.: Наука, 1991).
5. М.А. Краюхина, Н.А. Самойлова, И.Я. Ямсков, Успехи химии, 77, 854 (2008).
6. Muzzarell R., Biagini G., Pugnaloni A., Reconstruction of parodontal tissue with chitosan // Biomaterials, 1989, v. 10, №9, p. 598-603.
7. Патент RU 2494776.
8. Козлов A.B. Разработка антимикробной композиции на основе низина и хитозана для применения в технологии натуральных мясных полуфабрикатов, копченостей и ветчины. Диссертация М., 2010.
9. Василенко С.К., Бурмистров В.А., Симонова О.Г., Беляев М.Д. Сила моря и серебра. НПЦ «Вектор-Инвест», Новосибирск, 2003 г.
10. Патент РФ №2197971 от 29.11.2001, дата публикации 10.02.2003.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОЙ СИСТЕМЫ РАЗВЕТВЛЕННЫХ ФРАКТАЛЬНЫХ КЛАСТЕРОВ НА ОСНОВЕ L-ЦИСТЕИНА | 2009 |
|
RU2423384C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛЕНОК С НАНОСТРУКТУРИРОВАННЫМ СЕРЕБРОМ | 2013 |
|
RU2542280C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ СЕРЕБРА | 2013 |
|
RU2526390C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОКОНЦЕНТРИРОВАННЫХ ГЕЛЕЙ НА ОСНОВЕ N-АЦЕТИЛ-L-ЦИСТЕИНА И НИТРАТА СЕРЕБРА | 2013 |
|
RU2530572C1 |
| Способ получения гелей для медицинских целей на основе L-цистеина, нитрата серебра и поливинилового спирта | 2019 |
|
RU2709181C1 |
| СПОСОБ ИЗМЕНЕНИЯ ЭФФЕКТИВНОЙ ВЯЗКОСТИ НИЗКОКОНЦЕНТРИРОВАННЫХ ГЕЛЕЙ НА ОСНОВЕ L-ЦИСТЕИНА И НИТРАТА СЕРЕБРА | 2009 |
|
RU2432937C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУПРАМОЛЕКУЛЯРНОГО ГИДРОГЕЛЯ | 2016 |
|
RU2641111C1 |
| Способ получения тиксотропных супрамолекулярных гидрогелей заданной прочности | 2017 |
|
RU2676473C1 |
| Композиция с супрамолекулярной структурой коллоидной смеси комплексных соединений наноструктурных частиц серебра или гидрозоля катионов серебра в водном или в водно-органическом растворе, обладающая антимикробным и антитоксическим действием (варианты), и способ ее получения | 2018 |
|
RU2693410C1 |
| Способ получения макропористой пленки для регенеративной медицины на основе L-цистеина, нитрата серебра и поливинилового спирта | 2020 |
|
RU2746882C1 |

Изобретение относится к микробиологии. Описана стабильная антимикробная композиция, относящаяся к классу катионных антисептиков. Композицию получают путем соединения раствора хитозана, содержащего 1% уксусную или янтарную кислоту, с раствором, содержащим супрамолекулярные фрактальные структуры, полученные в результате взаимодействия природной аминокислоты L-цистеина с ионами серебра (L-цистеин-серебряный раствор). Описанная композиция содержит 0,2-0,9% (по массе) хитозана, 0,1-0,32% L-цистеин-серебряного раствора. Полученная композиция активно подавляет развитие патогенных микроорганизмов и может быть использована при производстве лекарственных средств, обладающих антимикробными свойствами в виде раствора или пленок, при разработке консервантов для объектов растительного и животного происхождения. 4 ил., 1 табл., 1 пр.
Катионный антисептик на основе композиции L-цистеин-серебряного раствора и пищевого хитозана, обладающий антимикробной активностью по отношению к грамположительным и грамотрицательным патогенным микроорганизмам и содержащий следующие компоненты при следующем их содержании (масс. %):
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОЙ СИСТЕМЫ РАЗВЕТВЛЕННЫХ ФРАКТАЛЬНЫХ КЛАСТЕРОВ НА ОСНОВЕ L-ЦИСТЕИНА | 2009 |
|
RU2423384C1 |
| ГЕЛЬ ДЛЯ УХОДА ЗА КОЖЕЙ И ЛЕЧЕНИЯ ЕЕ ЗАБОЛЕВАНИЙ И КОМПОЗИЦИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 1995 |
|
RU2085187C1 |
| КОМПОЗИЦИЯ ДЛЯ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ РАСТЕНИЙ К БОЛЕЗНЯМ (ВАРИАНТЫ) | 1997 |
|
RU2158510C2 |
| Muzzarell R | |||
| et al, Reconstruction of parodontal tissue with chitosan, Biomaterials, 1989, v | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Способ получения раствора нитродиазобензола и применения его в крашении | 1921 |
|
SU598A1 |
Авторы
Даты
2015-09-10—Публикация
2014-04-22—Подача