Изобретение относится к области супрамолекулярной химии, изучающей способы получения супрамолекулярных структур, с определенным пространственным расположением атомов и обладающих заданными свойствами.
Супрамолекулярная структура - это пространственно организованная совокупность атомов и молекул, полученная спонтанной ассоциацией большого числа малых молекул, которая может быть расчленена на небольшие подсистемы таким способом, что при этом не разрываются химические связи. Супрамолекулярная структура, заполняющая весь объем, занятый растворителем, называется перколяционной. Если перколяционная структура обладает определенной механической прочностью, она проявляет себя как гель. Наиболее сложной задачей является получение гелей из сильно разбавленных водных растворов низкомолекулярных веществ, т.е. низкоконцентрированных гелей.
Таким образом, низкоконцентрированные гели - это супрамолекулярные структуры, полученные в результате ассоциации молекул растворенных компонентов в трехмерную сетку, заполняющую все пространство, занимаемое растворителем, причем массовая доля растворенных веществ, участвующих в построении каркаса сетки, много меньше массовой доли растворителя. Структура геля обусловлена характером межмолекулярного взаимодействия между строительными элементами трехмерной сетки, энергия которого гораздо слабее энергии ковалснтных химических связей. Низкоконцентрированные гели перспективны для применения в области нанотехнологий, биомедицины, фармакологии, моделирования живых систем.
Образование гелей в сильно разбавленных растворах низкомолекулярных соединений является редко наблюдаемым физико-химическим феноменом. Ранее было известно, что германат кальция способен образовывать гель при концентрации 0,067% [1].
Совершенно другого типа гели были получены на основе восьми производных L-цистина. Оказалось, что раствор в диметилсульфоксиде, такого производного, как, например, N,N′-дибензоил-L-цистин диамида, при разбавлении его водой желируется. При этом концентрация растворенного вещества в геле составляет всего 0,5 мМ [2].
Исследованием уровня техники установлено, что аналогом получения низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра являются низкоконцентрированные гели, полученные на основе L-цистеина и нитрата серебра посредством двухстадийного процесса. Согласно этому способу на первом этапе из L-цистеина и нитрата серебра, взятого в избытке, получают раствор, содержащий совокупность очень разветвленных и разреженных сеточных молекулярных структур, построенных из наноразмерных, положительно заряженных фрактальных кластеров. Эту совокупность молекулярных структур названа L-цистеин-серебряным раствором [3]. На втором этапе L-цистеин-серебряный раствор с концентрацией по серебру 0,25÷0,8 мМ смешивают с водным раствором сульфата щелочного или щелочноземельного металла при молярном соотношении L-цистеина и сульфата щелочного или щелочноземельного металла, изменяющемся в диапазоне от 1:0,015 до 1:0,030 [4]. Через определенное время, зависящее от концентрации компонентов, жидкая система превращается в гель. Однако способ получения гелей на основе L-цистеин-серебряного раствора и сульфатов щелочных или щелочноземельных металлов не дает алгоритма для синтеза гелей на основе N-ацетил-L-цистеина и нитрата серебра.
Технический результат настоящего изобретения заключается в том, что разработан способ получения низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра.
Технический результат достигается тем, что водный раствор N-ацетил-L-цистеина смешивают с водным раствором нитрата серебра таким образом, чтобы молярные концентрации компонентов в смеси были одинаковы и находились в диапазоне от 1 мМ до 1,8 мМ. Смесь перемешивают энергичным встряхиванием и оставляют в защищенном от света месте при комнатной температуре на 18 часов. В течение этого времени в системе формируется гель.
Ранее способов получения низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра описано не было.
Задача синтеза низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра решается путем приготовления смесей заданного состава, проведения реакции и контроля реологических свойств конечной системы с помощью предложенной шкалы прочности. Структура гелей фиксируется с помощью методов просвечивающей электронной микроскопии (ПЭМ), динамического светорассеяния (ДСР), УФ-спектроскопии.
Прочность геля на основе N-ацетил-L-цистеина и нитрата серебра оценивается по предложенной нами пятибалльной шкале, фиксирующей характер деформации столбика геля высотой 20 мм при переворачивании пробирки на угол, равный 180°. Под действием собственного веса происходит деформация материала, и определенному уровню деформации присваивается соответствующий балл. В Таблице 1 приведено описание деформации и присвоенный этой деформации балл. С помощью таблицы можно быстро оценить прочность геля, что позволит находить наиболее эффективные композиции за сравнительно короткое время.
Изобретение поясняется графическими материалами (Фиг.1-4) и Таблицей 1.
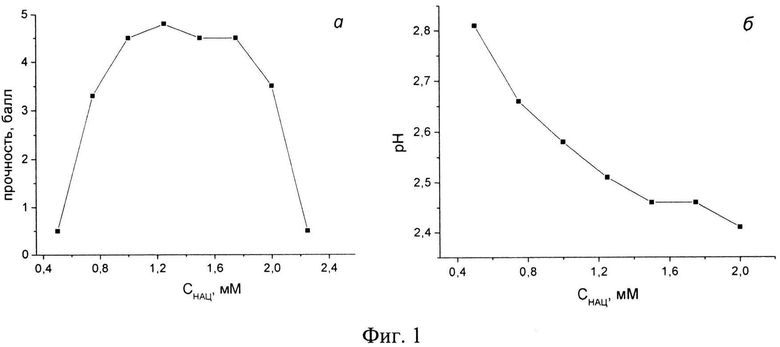
Фиг.1. Зависимость прочности гелей (а) и pH гель-образцов (б) на основе N-ацетил-L-цистеина и нитрата серебра от концентрации N-ацетил-L-цистеина; соотношение молярных концентраций компонентов 1:1.
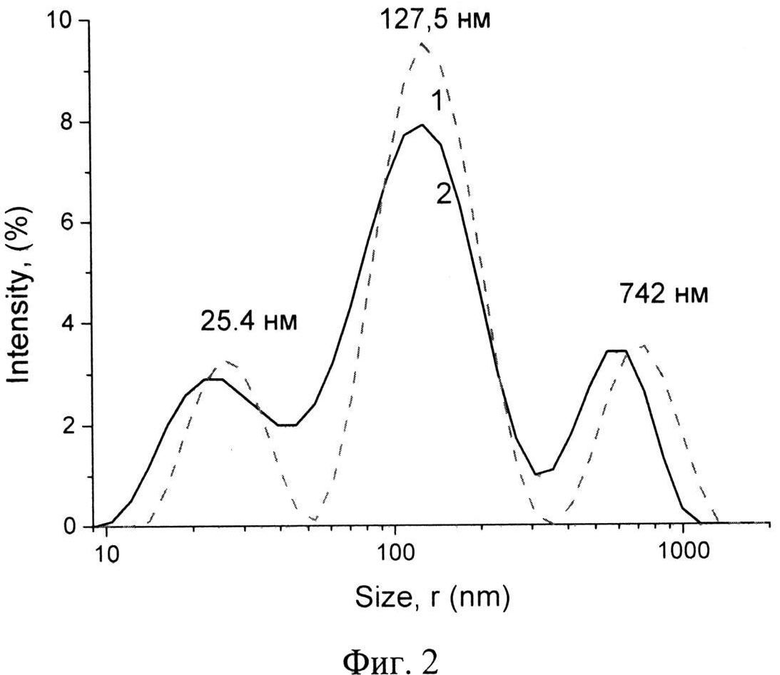
Фиг.2. Распределение гидродинамических радиусов структурных элементов пространственной сетки по данным динамического светорассеяния (в единицах интенсивности) для образцов гелей на основе N-ацетил-L-цистеина и AgNO3 в зависимости от времени стояния после момента смешивания исходных растворов: 11 (1) и 22 мин (2), (Сац.-цист.=1.25 мМ, CAgNO3=1.25 мМ).
Фиг.3. Электронно-микроскопический снимок высушенного геля на основе N-ацетил-L-цистеина и AgNO3.
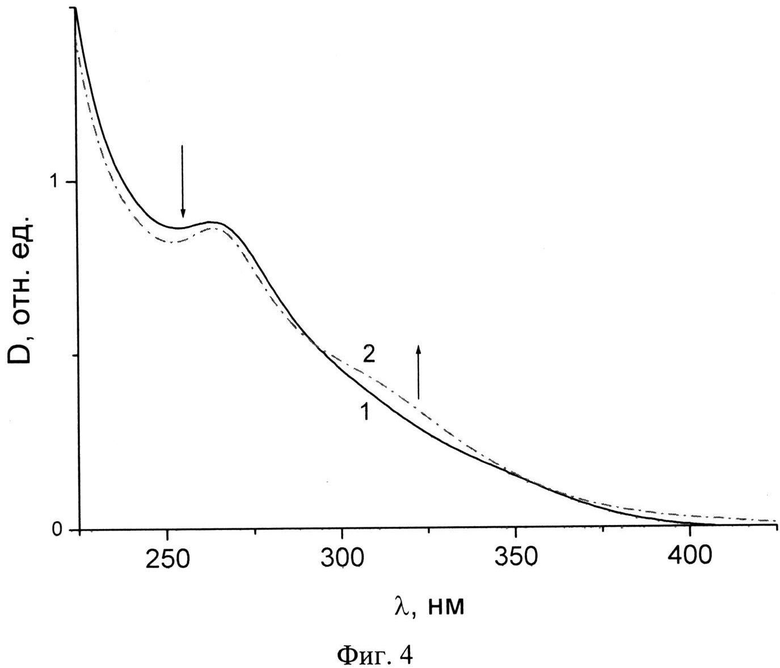
Фиг.4. УФ спектры поглощения образцов геля на основе N-ацетил-L-цистеина и AgNO3 в зависимости от времени стояния после момента смешивания исходных растворов: 1-5 мин, 2-5 часов, (Сац-цист.=1.25 мМ, CAgNO3=1.25 мМ).
Таблица 1. Описание характера деформации и оценка ее в баллах.
Выбор условий образования наиболее прочных гелей осуществлен на основании следующих фактов и экспериментов.
N-ацетил-L-цистеин является производным от L-цистеина, в котором один из атомов водорода аминогруппы замещен на ацетильную группу. N-ацетил-L-цистеин имеет другие, чем L-цистеин, кислотно-основные свойства. Так, константы ионизации L-цистеина имеют значения pKa1=1,96, pKa2=8,36, pKa3=10,28 [5], а соответствующие константы для N-ацетил-L-цистеина равны pKa1=1,7, pKa2=3,2, pKa3=9,75 [6]. Из этих данных следует, что растворы N-ацетил-L-цистеина имеют более низкие значения рН, вследствие меньшего сродства замещенной аминогруппы к протону и большей способности карбоксильной группы к ионизации. По этой причине зарядовые состояния функциональных групп этих молекул в водной среде различаются. Поэтому реакционные свойства L-цистеина и N-ацетил-L-цистеина при их взаимодействии с катионами серебра также различаются.
При сливании водных растворов N-ацетил-L-цистеина и нитрата серебра определенных концентраций образуется прозрачная смесь, которая структурируется в гель. Наиболее прочные гели формируются, когда концентрации исходных компонентов одинаковы. При избытке нитрата серебра прочность гелей уменьшается, и уже при отношении молярных концентраций 1,14 гели не образуются.
По мере увеличения концентрации компонентов прочность гелей возрастает, а затем, после достижения определенной концентрации, монотонно уменьшается (Фиг.1а). Это происходит потому, что формирование гелей происходит лишь в определенном диапазоне значений pH растворов (Фиг.1б), близких к pH изоэлектрической точки, вычисление которой по формулам [5], дает значение 2,45. В изоэлектрической точке отталкивание элементов сеточных структур минимально, а способность к ассоциации наиболее выражено.
Методом ДСР установлено образование в гелеобразующем растворе рассеивающих центров нескольких типов, которые можно идентифицировать как фрагменты сеточных структур. (Фиг.2). Измерение интенсивности динамического светорассеяния осуществляют с помощью спектрометра, включающего AL-SP-81 гониометр и цифровой фотонный коррелятор-структуратор ALV-5000 с углом рассеяния 90°. В качестве источника света используют He-Ne-лазер (длина волны - 632,8 нм) мощностью 36 МВт. Средний гидродинамический радиус частиц рассчитывают из уравнения Эйнштейн-Стокса на основании графика зависимости распределения коэффициента диффузии W(D) от коэффициента диффузии.
На Фиг.3 представлены электронно-микроскопические снимки высушенного на подложке геля, полученные при просвечивании на электронном микроскопе "LEO 912 АВ ОМПСА" (Carl Zeiss, Германия). Видно, что сеточный каркас образован кластерами размерами от 1,6 до 10 нм, которые объединены в пересекающиеся цепочки.
В силу того факта, что на основе N-ацетил-L-цистеина и нитрата серебра можно получить супрамолекулярный гель при малых концентрациях компонентов, кластеры должны иметь фрактальный характер [6, 7].
Спектроскопически гель характеризуется наличием в УФ-спектре двух полос поглощения, одна из которых имеет максимум при λ=265 им, а другая, менее выраженная, при λ=320 им (фиг.4).
Предположительно, сценарий формирования нерколяционной пространственной сечки в водном растворе N-ацетил-L-цистеина и нитрата серебра включает 6 стадий:
1 стадия - взаимодействие N-ацетил-L-цистеина с ионом серебра с образованием меркаптида серебра,
2 стадия - соединение молекул меркантида серебра в олигомерные цепочки, построенные из чередующихся атомов серебра и серы, -Ag-S(R)-Ag-S(R)-Ag-S(R)-, где R обозначает остаток молекулы N-ацетил-L-цистеина, связанный с атомом серы,
3 стадия - ассоциация олигомерных цепочек во фрактальный кластер,
4 стадия - ассоциация фрактальных кластеров в цепочки,
5 стадия - формирование из цепочек кластеров фрагментов трехмерной сетки,
6 стадия - образование из фрагментов трехмерной сетки перколяционной структуры.
Имеются существенные отличия в методе получения геля и его свойствах в заявляемом изобретении от условий получения геля, описанного в аналоге, именно:
1) в заявляемом изобретении гель получают с применением N-ацетил-L-цистеина, в то время как в аналоге с применением L-цистеина,
2) в заявляемом изобретении гель получают в одну стадию при непосредственном взаимодействии компонентов, а в аналоге - в двухстадийном процессе, требующем предварительного синтеза цистеин-серебряного раствора,
3) в заявляемом изобретении для формирования геля не требуется добавления в раствор сульфатов щелочных или щелочноземельных металлов,
4) в заявляемом изобретении наиболее прочный гель получают при эквимолярном соотношении концентраций замещенной аминокислоты и ионов серебра, а в аналоге - при отношении молярной концентрации серебра к концентрации L-цистеина равном 1,25,
5) гели на основе N-ацетил-L-цистеин и нитрата серебра не обладают тиксотропными свойствами, а гели на основе L-цистеина и нитрата серебра, представленные в аналоге, тиксотропны,
6) согласно данным ПЭМ в образцах геля на основе N-ацетил-L-цистеина формируются более крупные кластеры, чем в случае систем на основе L-цистеина,
7) электронный спектр гелей в заявляемом изобретении сильно отличается от спектра гелей на основе цистеин-серебряного раствора, представленных в аналоге. Именно, в гелях на основе N-ацетил-L-цистеина отсутствует полоса поглощения на длине волны 390 нм, характерная для гелей на основе L-цистеина,
8) в заявляемом изобретении наиболее прочные гели формируются в области рН, близкой к изоэлектрической точке N-ацетил-L-цистеина, и имеют, таким образом, сеточные структуры, несущие скомпенсированные положительные и отрицательные заряды, в то время как сеточные структуры гелей на основе L-цистеина, представленные в аналоге, несут положительный заряд.
Пример получения низкоконцентрированного геля на основе N-ацетил-L-цистеина и нитрат серебра:
1) приготавливают водный раствор N-ацетил-L-цистеина с концентрацией 10-3 мМ,
2) приготавливают водный раствор нитрата серебра с концентрацией 10-3 мМ,
3) к 14 мл дистиллированной воды приливают 3 мл раствора N-ацетил-L-цистеина, затем прибавляют 3 мл раствора нитрата серебра. Смесь перемешивают встряхиванием в течение 5 секунд, выдерживают при комнатной температуре (20°С) в защищенном от света месте в течение 18 часов.
Установлено, что гель на основе N-ацетил-L-цистеина и нитрата серебра подавляет размножение стафиллококов, поэтому перспективно его применение в медицинской практике по следующим направлениям.
В хирургии - подавление деятельности патогенной микрофлоры при лечении язв, заживлении ран, лечении пролежней и для регенерации тканей.
В ожоговой практике - как средство комплексного лечения в процессе реабилитации.
В фармакологии - для составления гелевых композиций с биологически активными компонентами.
Литература
1. Болдырев А.И. Демонстрационные опыты по физической и коллоидной химии. - М.: Высшая школа, 1976.
2. Menger P.M., Caran K.L. // J. Am. Chem. Sos. - 2000, 722, P.11679-11691.
3. Овчинников М.М., Хижняк С.Д., Пахомов П.М. Патент №2423384 от 10.07.11.
4. Овчинников М.М., Хижняк С.Д., Пахомов П.М. Патент №2432937 от 10.11.11.
5. Батлер Дж.Н. Ионные равновесия. - Л.: Химия, 1973.
6. Инцеди Я. Применение комплексов в аналитической химии. М.: Мир, 1979.
7. Смирнов Б.М. Физика фрактальных кластеров. - М.: Наука, 1991.
8. Смирнов Б.М. // УФН. - 1992. Т.162. №8. С.43.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения тиксотропных супрамолекулярных гидрогелей заданной прочности | 2017 |
|
RU2676473C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОЙ СИСТЕМЫ РАЗВЕТВЛЕННЫХ ФРАКТАЛЬНЫХ КЛАСТЕРОВ НА ОСНОВЕ L-ЦИСТЕИНА | 2009 |
|
RU2423384C1 |
| КАТИОННЫЙ АНТИСЕПТИК НА ОСНОВЕ КОМПОЗИЦИЙ L-ЦИСТЕИН-СЕРЕБРЯНОГО РАСТВОРА И ПИЩЕВОГО ХИТОЗАНА | 2014 |
|
RU2562113C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОЧАСТИЦ СЕРЕБРА | 2013 |
|
RU2526390C1 |
| СПОСОБ ИЗМЕНЕНИЯ ЭФФЕКТИВНОЙ ВЯЗКОСТИ НИЗКОКОНЦЕНТРИРОВАННЫХ ГЕЛЕЙ НА ОСНОВЕ L-ЦИСТЕИНА И НИТРАТА СЕРЕБРА | 2009 |
|
RU2432937C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУПРАМОЛЕКУЛЯРНОГО ГИДРОГЕЛЯ | 2016 |
|
RU2641111C1 |
| Способ получения гелей для медицинских целей на основе L-цистеина, нитрата серебра и поливинилового спирта | 2019 |
|
RU2709181C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛЕНОК С НАНОСТРУКТУРИРОВАННЫМ СЕРЕБРОМ | 2013 |
|
RU2542280C1 |
| Способ получения стандартов сравнения для измерения электрокинетического (дзета) потенциала | 2020 |
|
RU2746992C1 |
| Способ получения супрамолекулярного геля, содержащего наночастицы серебра | 2021 |
|
RU2761210C1 |

Изобретение относится к области супрамолекулярной химии, в частности получению низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра. Способ получения низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра включает приготовление водного раствора N-ацетил-L-цистеина и водного раствора нитрата серебра, смешивание растворов таким образом, чтобы концентрации компонентов в смеси были равны и находились в диапазоне от 1 мМ до 1,8 мМ. Затем смесь оставляют вызревать в защищенном от света месте на 18 ч при комнатной температуре. 1 табл., 4 ил.
Способ получения низкоконцентрированных гелей на основе N-ацетил-L-цистеина и нитрата серебра, характеризующийся тем, что смешивают водный раствор N-ацетил-L-цистеина с водным раствором нитрата серебра, так чтобы концентрации компонентов в исходной смеси были равны и находились в диапазоне 1÷1,8 мМ, далее смесь перемешивают энергичным встряхиванием и оставляют в защищенном от света месте при комнатной температуре на 18 часов.
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОЙ СИСТЕМЫ РАЗВЕТВЛЕННЫХ ФРАКТАЛЬНЫХ КЛАСТЕРОВ НА ОСНОВЕ L-ЦИСТЕИНА | 2009 |
|
RU2423384C1 |
| СПОСОБ ИЗМЕНЕНИЯ ЭФФЕКТИВНОЙ ВЯЗКОСТИ НИЗКОКОНЦЕНТРИРОВАННЫХ ГЕЛЕЙ НА ОСНОВЕ L-ЦИСТЕИНА И НИТРАТА СЕРЕБРА | 2009 |
|
RU2432937C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУПРАМОЛЕКУЛЯРНОГО ГЕЛЯ | 2006 |
|
RU2317305C2 |
Авторы
Даты
2014-10-10—Публикация
2013-06-13—Подача