Область техники, к которой относится изобретение
Настоящее изобретение относится к терапевтическому агенту против корнеальной эндотелиальной дисфункции. В частности, терапевтический агент против корнеальной эндотелиальной дисфункции по настоящему изобретению используют для заживления повреждения корнеального эндотелия или адгезии, поддерживания или консервирования корнеальных эндотелиальных клеток.
Уровень техники
Визуальная информация распознается, когда свет, который поступает из роговицы (прозрачной ткани в передней части глазного яблока), достигает сетчатки, возбуждая нейронные клетки сетчатки, и возникающие электрические сигналы передаются в церебральный визуальный кортекс через зрительный нерв. Чтобы иметь хорошую остроту зрения, роговица должна быть прозрачной. Прозрачность роговицы поддерживается посредством поддерживания гомеостаза 3-слойной структуры из корнеального эпителия, стромы и эндотелия. Среди них корнеальные эндотелиальные клетки поддерживают содержание воды роговицы на постоянном уровне и представляют собой важные клетки, которые поддерживают прозрачность роговицы.
Однако корнеальные эндотелиальные клетки человека имеют плохую пролиферативную способность in vivo и страдают от необратимых функциональных расстройств корнеального эндотелия из-за заболеваний, травм и повреждений при офтальмологических хирургических операциях.
Сообщалось, что в культивируемых корнеальных эндотелиальных клетках Y-27632, который представляет собой селективный ингибитор Rho-киназы (ROCK), оказывает стимулирующее воздействие на адгезию клеток (непатентный документ 1). В дополнение к этому сообщается, что инстилляция 10 мМ Y-27632 способствует заживлению повреждений корнеального эндотелия на модели кролика заживления повреждений корнеального эндотелия (непатентный документ 2).
Относительно для Y-27632 и Fasudil, которые представляют собой ингибиторы Rho-киназы, сообщается о воздействиях in vitro, таких как
1) культивирование корнеальных эндотелиальных клеток (кролик, обезьяна и тому подобное),
2) стимулирование адгезии клеток для культивируемых корнеальных эндотелиальных клеток обезьяны,
3) стимулирование клеточного цикла в культивируемых корнеальных эндотелиальных клетках обезьяны,
4) подавление апоптоза в культивируемых корнеальных эндотелиальных клетках обезьяны и
5) возможное применение культивируемых корнеальных эндотелиальных клеток при лечении заболеваний, требующих корнеальной эндотелиальной кератопластики (патентный документ 1).
Патентный документ 1 не описывает действия in vivo Y-27632 и Fasudil. В дополнение к этому, не рассматривается влияние ингибиторов Rho-киназы, иных, чем Y-27632 и Fasudil, на корнеальные эндотелиальные клетки.
Патент документ 1: WO 2009/028631
Непатентный документ 1: Okumura N, et al., Invest Ophthalmol Vis Sci. 2009, 50(8) p.3680-7
Непатентный документ 2: Invest Ophthalmol Vis Sci. 2009, 50: E-Abstract 1817.
Сущность изобретения
Целью настоящего изобретения является создание средств для эффективного и удобного лечения заболеваний, при которых повреждаются корнеальные эндотелиальные клетки с плохой пролиферативной способностью in vivo.
Решение проблемы
Авторы настоящего изобретения провели интенсивные исследования с точки зрения упомянутых выше проблем и обнаружили, что конкретное соединение в ингибиторах Rho-киназы может лечить корнеальное эндотелиальное повреждение при малой дозе или низкой концентрации. В дополнение к этому, авторы настоящего изобретения обнаружили, что соединение может показывать значительное воздействие заживления повреждений, даже когда вводится при заметно более низкой концентрации, чем обычные ингибиторы Rho-киназы, в организм с помощью местной инстилляции через корнеальный эпителий, и успешно использовали соединение для импланта для корнеальной эндотелиальной кератопластики, корнеального эндотелиального препарата и тому подобное, что привело к завершению настоящего изобретения. Соответственно, настоящее изобретение представляет собой следующее.
[1] Терапевтический агент против корнеальной эндотелиальной дисфункции, содержащий соединение, представленное следующей формулой (1):
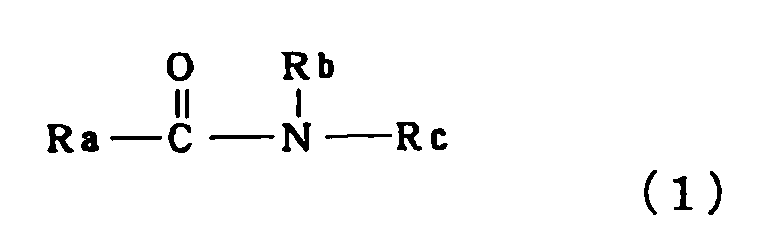 ,
,
где Ra имеет формулу (2):
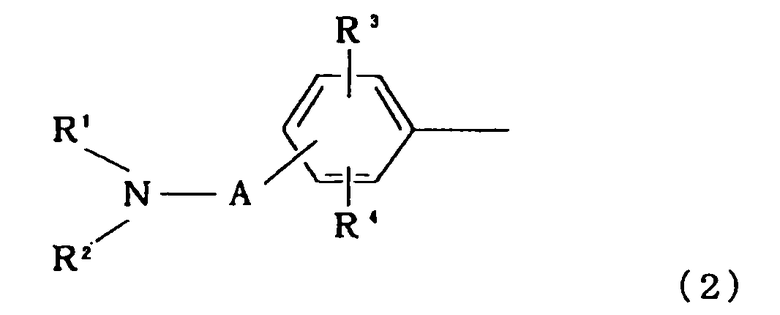 ,
,
где R1 представляет собой атом водорода, алкил или циклоалкил, циклоалкилалкил, фенил или аралкил, который необязательно имеет заместитель на кольце, или группу формулы (3):
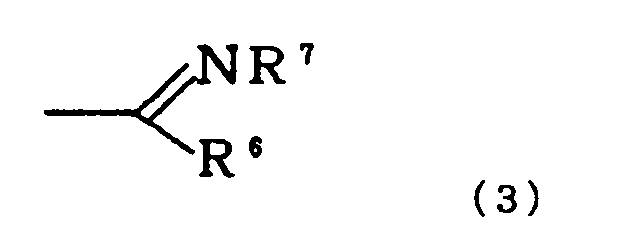 ,
,
где R6 представляет собой атом водорода, алкил или группу формулы: -NR8R9, где R8 и R9 являются одинаковыми или различными и каждый из них представляет собой атом водорода, алкил, аралкил или фенил, и R7 представляет собой атом водорода, алкил, аралкил, фенил, нитро или циано, или R6 и R7 в сочетании образуют гетероцикл, необязательно имеющий атом кислорода, атом серы или необязательно замещенный атом азота в кольце, дополнительно;
R2 представляет собой атом водорода, алкил или циклоалкил, циклоалкилалкил, фенил или аралкил, который необязательно имеет заместитель на кольце; или
R1 и R2 в сочетании образуют, вместе с соседним атомом азота, гетероцикл, необязательно имеющий атом кислорода, атом серы или необязательно замещенный атом азота в кольце, дополнительно;
R3 и R4 являются одинаковыми или различными и каждый из них представляет собой атом водорода, алкил, аралкил, атом галогена, нитро, амино, алкиламино, ациламино, гидрокси, алкокси, аралкилокси, циано, ацил, меркапто, алкилтио, аралкилтио, карбокси, алкоксикарбонил, карбамоил, алкилкарбамоил или азид;
A представляет собой группу формулы (4):
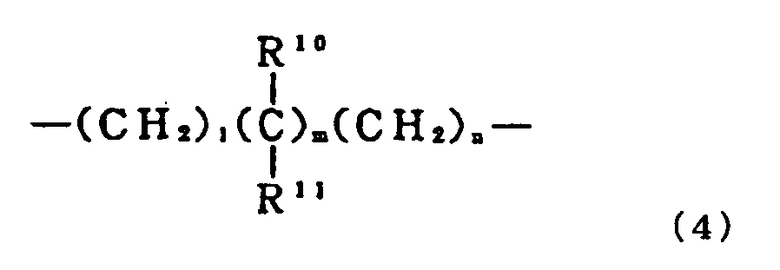 ,
,
где R10 и R11 являются одинаковыми или различными и каждый из них представляет собой атом водорода, алкил, галогеналкил, аралкил, гидроксиалкил, карбокси или алкоксикарбонил, или
R10 и R11 в сочетании образуют циклоалкил, и l, m и n, каждый, представляют собой 0 или целое число 1-3;
Rb представляет собой атом водорода или алкил; и
Rc представляет собой необязательно замещенный гетероцикл, содержащий атом азота,
или их фармакологически приемлемую соль (далее упоминается как соединение (1)) в качестве активного ингредиента.
[2] Терапевтический агент из указанного выше пункта [1], где указанная выше корнеальная эндотелиальная дисфункция представляет собой буллезную кератопатию или корнеальный эндотелиит.
[3] Терапевтический агент из указанного выше пункта [1] или [2], который представляет собой глазные капли.
[4] Терапевтический агент из любого из указанных выше пунктов [1]-[3], где указанное выше соединение (1) представляет собой (R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид (далее упоминается как соединение (Ia)).
[5] Агент для стимулирования адгезии корнеальных эндотелиальных клеток, содержащий соединение (1).
[6] Агент из указанного выше пункта [5], где указанное выше соединение (1) представляет собой соединение (Ia).
[7] Среда для культивирования корнеальных эндотелиальных клеток, содержащая соединение (1).
[8] Среда для культивирования из указанного выше пункта [7], где указанное выше соединение (1) представляет собой соединение (Ia).
[9] Раствор для хранения роговицы, содержащий соединение (1).
[10] Раствор для хранения роговицы из указанного выше пункта [9], где указанное выше соединение (1) представляет собой соединение (Ia).
[11] Имплант для корнеальной эндотелиальной кератопластики, содержащий
A) корнеальные эндотелиальные клетки,
B) каркас и
C) соединение (1).
[12] Имплант из указанного выше пункта [11], где указанные выше корнеальные эндотелиальные клетки получают от людей.
[13] Имплант из указанного выше пункта [11] или [12], где указанное выше соединение (1) представляет собой соединение (Ia).
[14] Способ получения корнеального эндотелиального препарата, включающий стадию культивирования корнеальных эндотелиальных клеток с использованием среды для культивирования, содержащей соединение (1).
[15] Способ получения из указанного выше пункта [14], где указанные выше корнеальные эндотелиальные клетки получают от людей.
[16] Способ получения из указанного выше пункта [14] или [15], где указанное выше соединение (1) представляет собой соединение (Ia).
[17] Способ лечения корнеальной эндотелиальной дисфункции, включающий стадию получения корнеального эндотелиального препарата и/или импланта для корнеальной эндотелиальной кератопластики, каждый из них содержит соединение (1), и стадию трансплантации препарата и/или импланта субъекту, нуждающемуся в кератопластике.
[18] Способ лечения из указанного выше пункта [17], где указанные выше корнеальные эндотелиальные клетки получают от людей.
[19] Способ лечения из указанного выше пункта [17] или [18], где указанная выше корнеальная эндотелиальная дисфункция представляет собой буллезную кератопатию, отёк роговой оболочки глаза или бельмо роговицы.
[20] Способ лечения из любого указанного выше [17]-[19], где указанное выше соединение (1) представляет собой соединение (Ia).
[21] Способ лечения корнеальной эндотелиальной дисфункции, включающий стадию введения эффективного количества соединения (1) и корнеальных эндотелиальных клеток субъекту, нуждающемуся в заживлении корнеальных эндотелиальных повреждений.
[22] Способ лечения из указанного выше пункта [21], где указанная выше корнеальная эндотелиальная дисфункция представляет собой буллезную кератопатию или корнеальный эндотелиит.
[23] Способ лечения из указанного выше пункта [21] или [22], где указанная выше стадия введения представляет собой местную инстилляцию.
[24] Способ лечения из любого указанного выше [21]-[23], где указанное выше соединение (1) представляет собой соединение (Ia).
[25] Применение соединения (1) для получения терапевтического агента против корнеальной эндотелиальной дисфункции.
[26] Применение из указанного выше пункта [25], где указанный выше терапевтический агент представляет собой глазные капли.
[27] Применение соединения (1) для получения агента для стимулирования адгезии корнеальных эндотелиальных клеток.
[28] Применение соединения (1) для получения среды для культивирования для корнеальных эндотелиальных клеток.
[29] Применение
A) корнеальных эндотелиальных клеток,
B) каркаса и
C) соединения (1)
для получения импланта для корнеальной эндотелиальной кератопластики.
[30] Применение из указанного выше пункта [29], где указанные выше корнеальные эндотелиальные клетки получают от людей.
[31] Применение из любого из указанных выше пунктов [25]-[30], где указанное выше соединение (1) представляет собой соединение (Ia).
[32] Корнеальный эндотелиальный препарат, который получают с помощью способа получения из любого указанного выше [14]-[16].
[33] Раствор для интраокулярной ирригации, содержащий соединение (1).
[34] Раствор для интраокулярной ирригации из указанного выше пункта [33], где указанное выше соединение (1) представляет собой соединение (Ia).
[35] Супрессор апоптоза, содержащий соединение (1).
[36] Супрессор апоптоза из указанного выше пункта [35], где указанное выше соединение (1) представляет собой соединение (Ia).
[37] Набор для лечения корнеальной эндотелиальной дисфункции, содержащий соединение (1), корнеальные эндотелиальные клетки и инструкции.
[38] Набор из указанного выше пункта [37], где указанные выше корнеальные эндотелиальные клетки являются замороженными.
[39] Набор из указанных выше пунктов [37] или [38], где указанное выше соединение (1) содержат в промывочном растворе, среде для культивирования или в растворе для суспендирования клеток.
[40] Набор из любого из указанных выше пунктов [37]-[39], где соединение (1) представляет собой соединение (Ia).
[41] Корнеальный эндотелиальный препарат, содержащий соединение (1) и корнеальные эндотелиальные клетки.
[42] Корнеальный эндотелиальный препарат из указанного выше пункта [41], где указанное выше соединение (1) представляет собой соединение (Ia).
[43] Соединение (1) для лечения корнеальной эндотелиальной дисфункции.
[44] Соединение (Ia) для лечения корнеальной эндотелиальной дисфункции.
Преимущественные воздействия изобретения
Терапевтический агент против корнеальной эндотелиальной дисфункции по настоящему изобретению содержит соединение (1), предпочтительно соединение (Ia), в качестве активного ингредиента. В результате может быть получен эффективный и удобный способ лечения или профилактики заболевания с расстройством корнеальных эндотелиальных клеток, то есть заболевания, связанного с корнеальной эндотелиальной дисфункцией (например, буллезной кератопатии, корнеального эндотелиита и тому подобное). Соединение (Ia), которое должно содержаться в терапевтическом агенте против корнеальной эндотелиальной дисфункции по настоящему изобретению, может демонстрировать эффективность даже при низкой концентрации примерно 1/30 - 1/10 Y-27632 в случае местной инстилляции. Таким образом, даже дозированная форма типа местной инстилляции, как ожидается, должна достигать корнеального эндотелия через корнеальный эпителий и сохранять свое действие. Использование терапевтического агента против корнеальной эндотелиальной дисфункции по настоящему изобретению может обеспечить расширение возможностей способов введения и превосходное лечение в виде вещества длительного действия.
Агент для стимулирования адгезии корнеальных эндотелиальных клеток по настоящему изобретению является пригодным в качестве агента для защиты корнеального эндотелия при профилактике или лечении заболевания, сопровождаемого корнеальной эндотелиальной дисфункцией. Кроме того, агент для стимулирования адгезии корнеальных эндотелиальных клеток по настоящему изобретению может быть использован в качестве агента для защиты корнеального эндотелия при профилактике или лечении корнеальной эндотелиальной дисфункции, связанной с интраокулярной хирургической операцией, такой как операция при катаракте, операция на стекловидном теле и тому подобное, при корнеальной эндотелиальной дисфункции, вызываемой повышением внутриглазного давления (в частности, при обострении глаукомы), или при корнеальной эндотелиальной дисфункции, вызываемой недостатком кислорода из-за ношения контактных линз. Поскольку среда для культивирования по настоящему изобретению содержит соединение (1), предпочтительно соединение (Ia), корнеальные эндотелиальные клетки могут хорошо культивироваться, поддерживаться или консервироваться, и становится возможным стабильное получение, поддержание или консервирование корнеального эндотелиального препарата.
Имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению может, например, иметь форму листа корнеального эндотелия in vitro и может доставляться для корнеальной эндотелиальной кератопластики вместе с корнеальными эндотелиальными клетками и их каркасом для них, в виде импланта для корнеальной эндотелиальной кератопластики. Имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению имеет характеристику интравитального слоя корнеальных эндотелиальных клеток и, как ожидается, должен улучшить долю приживаемости импланта.
Краткое описание чертежей
Фиг.1 показывает изображения, окрашенные в красный цвет ализарином, показывающие воздействие различных соединений на корнеальные эндотелиальные повреждения для модели кролика корнеального эндотелиального повреждения. Местная инстилляция отрицательного контроля (PBS): Фиг.1a, 10 мМ Y-27632: Фиг.1B, 10 мМ Fasudil: Фиг.1C, 0,32 мМ соединение (I): Фиг.1D и 0,95 мМ соединение (I): Фиг.1E.
Фиг.2 представляет собой график, показывающий воздействие местной инстилляции соединения (I) на модели кролика корнеального эндотелиального повреждения, где вертикальная ось показывает площадь дефективного корнеального эндотелия.
Фиг.3 показывает влияние соединения (I) на морфологию культивируемых корнеальных эндотелиальных клеток (один день после высеивания).
Фиг.4 показывает влияние соединения (I) на морфологию культивируемых корнеальных эндотелиальных клеток (3 дня после высеивания).
Фиг.5 показывает влияние соединения (I) на морфологию культивируемых корнеальных эндотелиальных клеток (5 дней после высеивания).
Фиг.6 показывает влияние соединения (I) на морфологию культивируемых корнеальных эндотелиальных клеток (7 дней после высеивания).
Фиг.7 показывает влияние соединения (I) на морфологию культивируемых корнеальных эндотелиальных клеток (14 дней после высеивания).
Фиг.8 показывает изменения ширины повреждения корнеальных эндотелиальных клеток после добавления медицинского препарата, где вертикальная ось показывает отношение (%) ширины повреждения после добавления медицинского препарата к ширине до его добавления, а горизонтальная ось показывает добавленный медицинский препарат. В каждой группе отношения ширины повреждения при 0 час (до добавления), 6 час (6 часов после добавления), 12 час (12 часов после добавления) и 24 час (24 часа после добавления) показаны слева.
Фиг.9 показывает количества корнеальных эндотелиальных клеток, прилипших к лунке в течение 3 часов после высеивания, где вертикальная ось показывает долю (%) отсчетов клеток по отношению к отсчетам клеток в контрольной группе как 100, а горизонтальная ось показывает добавленный медицинский препарат.
Фиг.10 показывает окрашенные с использованием иммунной метки изображения ZO-1 и Na+/K+ ATPазы в листе культивируемых корнеальных эндотелиальных клеток для трансплантации, приготовленном через 48 часов посредством добавления соединения (I), Y-27632 и ДМСО, где Фиг.10-(A) показывает окрашивание ZO-1 при добавлении различных медицинских препаратов, а Фиг.10-(B) показывает окрашивание с помощью Na+/K+ ATPазы.
Фиг.11 показывает окрашивание с использованием иммунной метки изображения ZO-1 и Na+/K+ ATPазы в листе культивируемых корнеальных эндотелиальных клеток для трансплантации, приготовленном через 14 дней посредством добавления соединения (I) и ДМСО.
Фиг.12 показывает окрашивание с использованием иммунной метки изображения корнеального эндотелия через 14 дней после инъекции корнеальных эндотелиальных клеток на модели кролика буллезной кератопатии, где Фиг.12-(A) показывает окрашивание с помощью фаллоидина, а Фиг.12-(B) показывает окрашивание с помощью Na+/K+ ATPазы.
Фиг.13 показывает отсчеты корнеальных эндотелиальных клеток через 14 дней после инъекции корнеальных эндотелиальных клеток на модели кролика буллезной кератопатии, где вертикальная ось показывает отсчеты клеток (клетки/мм2), а столбики на графике показывают контрольную группу, группу, леченную 100 мкМ Y-27632, и группу, леченную 10 мкМ соединения (I), слева.
Фиг.14 показывает изменения ширины повреждения корнеальных эндотелиальных клеток после добавления медицинского препарата, где вертикальная ось показывает отношение (%) ширины повреждения после добавления медицинского препарата к ширине до его добавления, а горизонтальная ось показывает добавленный медицинский препарат. В каждой группе отношения ширины повреждения при 0 час (до добавления), 6 час (6 часов после добавления), 12 час (12 часов после добавления) и 24 час (24 часа после добавления) показаны слева.
Фиг.15 показывает изображения, окрашенные с помощью Hoechst, PI и Annexin V, для роговицы, консервируемой в течение 3 недель в растворе для хранения, в который добавляют соединение (I) или Y-27632.
Фиг.16 показывает количества живых клеток, погибших клеток и апоптотических клеток в роговице, консервируемой в течение 2 недель в растворе для хранения, в который добавляют соединение (I) или Y-27632. Левый график показывает результаты, полученные с использованием раствора для хранения, в который добавляют соединение (I), а правый график показывает результаты, полученные с использованием раствора для хранения, в который добавляют Y-27632. В каждом графике вертикальная ось показывает отсчет клеток, а горизонтальная ось показывает окрашивающие агенты, используемые для идентификации клеток.
Фиг.17 показывает количества живых клеток, погибших клеток и апоптотических клеток в роговице, консервируемой в течение 3 недель в растворе для хранения, в который добавляют соединение (I) или Y-27632. Левый график показывает результаты, полученные с использованием раствора для хранения, в который добавляют соединение (I), а правый график показывает результаты, полученные с использованием раствора для хранения, в который добавляют Y-27632. В каждом графике вертикальная ось показывает отсчет клеток, а горизонтальная ось показывает окрашивающие агенты, используемые для идентификации клеток.
Описание вариантов осуществления
Настоящее изобретение описывается ниже. Необходимо понять, что, в настоящем описании, упоминание единственного числа включает концепцию их множественности. По этой причине, обозначения единственного числа включают концепцию их множественности, если не утверждается иного. Необходимо также понять, что термины, как используется в настоящем документе, имеют определения, обычно используемые в данной области, если не указано иного. По этой причине все технические и научные термины, используемые в настоящем документе, имеют такие же значения, как обычно понимается специалистами в данной области. В ином случае, настоящее описание (включая ссылки) имеет преимущества.
В одном из аспектов, настоящее изобретение предусматривает терапевтический агент против корнеальной эндотелиальной дисфункции. Терапевтический агент против корнеальной эндотелиальной дисфункции по настоящему изобретению (иногда упоминаемый далее как "терапевтический агент по настоящему изобретению") содержит соединение (1) в качестве активного ингредиента.
Соединение (1), используемое в настоящем изобретении, представляет собой соединение формулы (1):
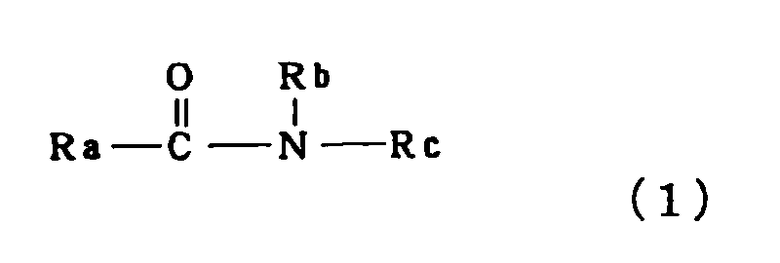 ,
,
где Ra имеет формулу (2):
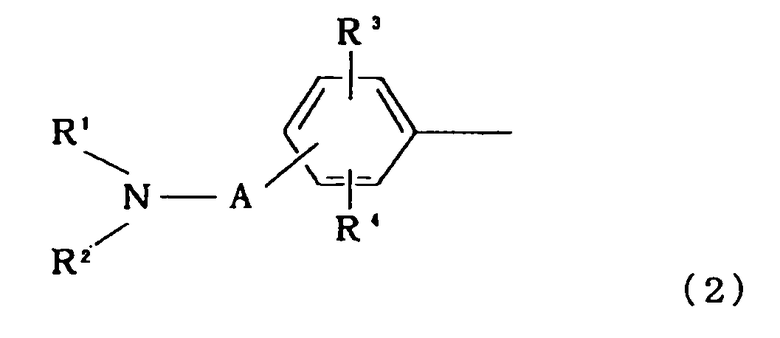 ,
,
где R1 представляет собой атом водорода, алкил или циклоалкил, циклоалкилалкил, фенил или аралкил, который необязательно имеет заместитель на кольце, или группу формулы (3):
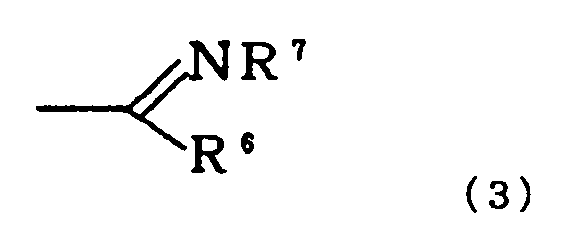 ,
,
где R6 представляет собой атом водорода, алкил или группу формулы: -NR8R9, где R8 и R9 являются одинаковыми или различными, и каждый из них представляет собой атом водорода, алкил, аралкил или фенил, и R7 представляет собой атом водорода, алкил, аралкил, фенил, нитро или циано, или R6 и R7 в сочетании образуют гетероцикл, необязательно имеющий атом кислорода, атом серы или необязательно замещенный атом азота в кольце, дополнительно;
R2 представляет собой атом водорода, алкил или циклоалкил, циклоалкилалкил, фенил или аралкил, который необязательно имеет заместитель на кольце; или
R1 и R2 в сочетании образуют, вместе с соседним атомом азота, гетероцикл, необязательно имеющий атом кислорода, атом серы или необязательно замещенный атом азота в кольце, дополнительно;
R3 и R4 являются одинаковыми или различными и каждый из них представляет собой атом водорода, алкил, аралкил, атом галогена, нитро, амино, алкиламино, ациламино, гидрокси, алкокси, аралкилокси, циано, ацил, меркапто, алкилтио, аралкилтио, карбокси, алкоксикарбонил, карбамоил, алкилкарбамоил или азид;
A представляет собой группу формулы (4):
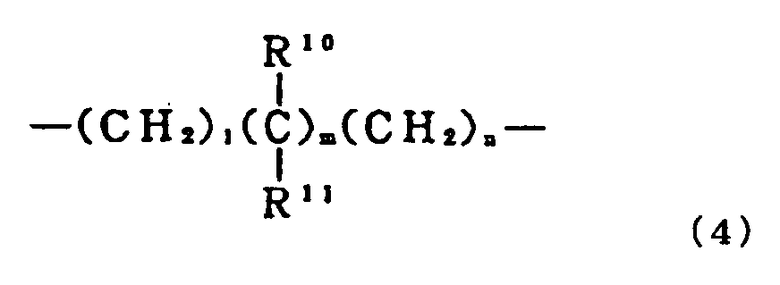 ,
,
где R10 и R11 являются одинаковыми или различными и каждый из них представляет собой атом водорода, алкил, галогеналкил, аралкил, гидроксиалкил, карбокси или алкоксикарбонил, или
R10 и R11 в сочетании образуют циклоалкил, и l, m и n, каждый, представляют собой 0 или целое число 1-3;
Rb представляет собой атом водорода или алкил и
Rc представляет собой необязательно замещенный гетероцикл, содержащий азот,
или их фармацевтически приемлемую соль.
Каждый символ в настоящем описании означает следующее.
Алкил как R1 и R2 представляет собой алкил с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, и он иллюстрируется как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил и тому подобное, при этом предпочтение отдается алкилу, имеющему 1-4 атома углерода.
Циклоалкил как R1 и R2 представляет собой циклоалкил, имеющий 3-7 атомов углерода, такой как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил.
Циклоалкилалкил как R1 и R2 представляет собой остаток, имеющий, как циклоалкильный остаток, упоминаемый выше циклоалкил, имеющий 3-7 атомов углерода, и алкил с прямой или разветвленной цепью, имеющий 1-6 атомов углерода (например, метил, этил, пропил, изопропил, бутил, пентил и гексил), как алкильный остаток, и иллюстрируется как циклопропилметил, циклобутилметил, циклопентилметил, циклогексилметил, циклогептилметил, циклопропилэтил, циклопентилэтил, циклогексилэтил, циклогептилэтил, циклопропилпропил, циклопентилпропил, циклогексилпропил, циклогептилпропил, циклопропилбутил, циклопентилбутил, циклогексилбутил, циклогептилбутил, циклопропилгексил, циклопентилгексил, циклогексилгексил, циклогептилгексил и тому подобное.
Аралкил, представленный как R1 и R2, представляет собой остаток, имеющий, как алкильный остаток, алкил, имеющий 1-4 атома углерода, и он иллюстрируется как фенилалкил, такой как бензил, 1-фенилэтил, 2-фенилэтил, 3-фенилпропил и 4-фенилбутил.
Заместитель циклоалкила, циклоалкилалкила, фенила и аралкила, который может иметь заместитель на кольце как R1 и R2, представляет собой атом галогена (например, хлор, бром, фтор и йод), алкил (такой же, как алкил, представленный как R1 и R2), алкокси (алкокси с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, такой как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси и гексилокси), аралкил (такой же, как аралкил, представленный как R1 и R2), галогеналкил (алкил как R1 и R2 замещенный 1-5 атомами галогена, такой как фторметил, дифторметил, трифторметил, 2,2,2-трифторэтил и 2,2,3,3,3-пентафторпропил), нитро, амино, циано, азид и тому подобное.
Гетероцикл, образованный с помощью R1 и R2, в сочетании вместе с соседним атомом азота, который необязательно имеет атом кислорода, атом серы или необязательно замещенный атом азота в кольце, дополнительно, предпочтительно представляет собой 5- или 6-членное кольцо или кольцо, связанное с ним. Конкретные примеры включают 1-пирролидинил, пиперидино, 1-пиперазинил, морфолино, тиоморфолино, 1-имидазолили, 2,3-дигидротиазол-3-ил и тому подобное. Заместитель на необязательно замещенном атоме азота иллюстрируется как алкил, аралкил, галогеналкил и тому подобное, где алкил, аралкил и галогеналкил являются такими же, как группы, определенные для R1 и R2.
Атом галогена, алкил, алкокси и аралкил, представленный как R3 и R4, являются такими же, как группы, иллюстрируемые для R1 и R2,
Ацил как R3 и R4 представляет собой, например, алканоил, имеющий 2-6 атомов углерода (например, ацетил, пропионил, бутирил, валерил и пивалоил), бензоил или фенилалканоил, у которого алканоильный остаток имеет 2-4 атома углерода (например, фенилацетил, фенилпропионил и фенилбутирил).
Алкиламино как R3 и R4 представляет собой остаток, имеющий, как алкильный остаток, алкил с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, и иллюстрируется как метиламино, этиламино, пропиламино, изопропиламино, бутиламино, изобутиламино, втор-бутиламино, трет-бутиламино, пентиламино, гексиламино и тому подобное.
Ациламино как R3 и R4 представляет собой остаток, имеющий, как ацильный остаток, алканоил, имеющий 2-6 атомов углерода, бензил или фенилалканоил, у которого алканоильный остаток имеет 2-4 атома углерода, и она иллюстрируется как ацетиламино, пропиониламино, бутириламино, валериламино, пивалоиламино, бензоиламино, фенилацетиламино, фенилпропиониламино, фенилбутириламино и тому подобное.
Алкилтио как R3 и R4 представляет собой остаток, имеющий, как алкильный остаток, алкил с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, и она иллюстрируется как метилтио, этилтио, пропилтио, изопропилтио, бутилтио, изобутилтио, втор-бутилтио, трет-бутилтио, пентилтио, гексилтио и тому подобное.
Аралкилокси как R3 и R4 представляет собой остаток, содержащий аралкил, имеющий как алкильный остаток, алкил, имеющий 1-4 атома углерода, и она иллюстрируется как бензилокси, 1-фенилэтилокси, 2-фенилэтилокси, 3-фенилпропилокси, 4-фенилбутилокси и тому подобное.
Аралкилтио как R3 и R4 представляет собой остаток, содержащий аралкил, имеющий, как алкильный остаток, алкил, имеющий 1-4 атома углерода, и она иллюстрируется как бензилтио, 1-фенилэтилтио, 2-фенилэтилтио, 3-фенилпропилтио, 4-фенилбутилтио и тому подобное.
Алкоксикарбонил как R3 и R4 представляет собой остаток, имеющий, как алкокси остаток, алкокси с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, и она иллюстрируется как метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, втор-бутоксикарбонил, трет-бутоксикарбонил, пентилоксикарбонил, гексилоксикарбонил и тому подобное.
Алкилкарбамоил как R3 и R4 представляет собой карбамоил с моно- или дизамещенный алкилом, имеющим 1-4 атома углерода, и он иллюстрируется как метилкарбамоил, диметилкарбамоил, этилкарбамоил, диэтилкарбамоил, пропилкарбамоил, дипропилкарбамоил, бутилкарбамоил, дибутилкарбамоил и тому подобное.
Алкил как Rb является таким же, как алкил, представленный как R1 и R2,
Гетероцикл, содержащий азот как Rc, когда он является моноциклическим, представляет собой, например, пиридин, пиримидин, пиридазин, триазин, пиразол или триазол, а когда он представляет собой конденсированное кольцо, он иллюстрируется как пирролопиридин (например, 1H-пирроло[2,3-b]пиридин, 1H-пирроло[3,2-b]пиридин и 1H-пирроло[3,4-b]пиридин), пиразолопиридин (например, 1H-пиразоло[3,4-b]пиридин и 1H-пиразоло[4,3-b]пиридин), имидазопиридин (например, 1H-имидазо[4,5-b]пиридин), пирролопиримидин (например, 1H-пирроло[2,3-d]пиримидин, 1H-пирроло[3,2-d]пиримидин и 1H-пирроло[3,4-d]пиримидин), пиразолопиримидин (например, 1H-пиразоло[3,4-d]пиримидин, пиразоло [1,5-a] пиримидин и 1H-пиразоло [4,3-d] пиримидин), имидазопиримидин (например, имидазо[1,2-a]пиримидин и 1H-имидазо[4,5-d]пиримидин), пирролотриазин (например, пирроло[1,2-a]-1,3,5-триазин и пирроло[2,1-f]-1,2,4-триазин), пиразолотриазин (например, пиразоло[1,5-a]-1,3,5-триазин), триазолопиридин (например, 1H-1,2,3-триазоло[4,5-b]пиридин), триазолопиримидин (например, 1,2,4-триазоло [1,5-a]пиримидин, 1,2,4-триазоло[4,3-a]пиримидин и 1H-1,2,3-триазоло[4,5-d]пиримидин), циннолин, хиназолин, хинолин, пиридопиридазин (например, пиридо[2,3-c]пиридазин), пиридопиразин (например, пиридо[2,3-b]пиразин), пиридопиримидин (например, пиридо[2,3-d]пиримидин и пиридо[3,2-d]пиримидин), пиримидопиримидин (например, пиримидо[4,5-d]пиримидин и пиримидо[5,4-d]пиримидин), пиразинопиримидин (например, пиразино[2,3-d]пиримидин), нафтилидин (например, 1,8-нафтилидин), тетразолопиримидин (например, тетразоло[1,5-a]пиримидин), тиенопиридин (например, тиено[2,3-b]пиридин), тиенопиримидин (например, тиено[2,3-d]пиримидин), тиазолопиридин (например, тиазоло[4,5-b]пиридин и тиазоло[5,4-b]пиридин), тиазолопиримидин (например, тиазоло[4,5-d]пиримидин и тиазоло[5,4-d]пиримидин), оксазолопиридин (например, оксазоло[4,5-b]пиридин и оксазоло[5,4-b]пиридин), оксазолопиримидин (например, оксазоло[4,5-d]пиримидин и оксазоло[5,4-d]пиримидин), фуропиридин (например, фуро[2,3-b]пиридин и фуро[3,2-b]пиридин), фуропиримидин (например, фуро[2,3-d]пиримидин и фуро[3,2-d]пиримидин), 2,3-дигидропирролопиридин (например, 2,3-дигидро-1H-пирроло[2,3-b]пиридин и 2,3-дигидро-1H-пирроло[3,2-b]пиридин), 2,3-дигидропирролопиримидин (например, 2,3-дигидро-1H-пирроло[2,3-d]пиримидин и 2,3-дигидро-1H-пирроло[3,2-d]пиримидин), 5,6,7,8-тетрагидропиридо[2,3-d]пиримидин, 5,6,7,8-тетрагидро-1,8-нафтилидин, 5,6,7,8-тетрагидрохинолин и тому подобное. Когда эти кольца образуют гидрированные ароматические кольца, атом углерода в кольце может представлять собой карбонил. Примеры их включают 2,3-дигидро-2-оксопирролопиридин, 2,3-дигидро-2,3-диоксопирролопиридин, 7,8-дигидро-7-оксо-1,8-нафтилидин, 5,6,7,8-тетрагидро-7-оксо-1,8-нафтилидин и тому подобное.
Эти кольца могут быть замещенными заместителем, таким как атом галогена, алкил, алкокси, аралкил, галогеналкил, нитро, амино, алкиламино, циано, формил, ацил, аминоалкил, моно- или диалкиламиноалкил, азид, карбокси, алкоксикарбонил, карбамоил, алкилкарбамоил, необязательно замещенная гидразино и тому подобное.
Заместитель необязательно замещенной гидразино включает, например, алкил, аралкил, нитро и циано, где алкил и аралкил являются такими же, как алкил и аралкил, представленный как R1 и R2, и необязательно замещенная гидразино иллюстрируется как метилгидразино, этилгидразино, бензилгидразино и тому подобное.
Алкил как R6 является таким же, как алкил, представленный как R1 и R2; алкил как R8 и R9 является таким же, как алкил, представленный как R1 и R2; и аралкил, представленный как R8 и R9, является таким же, как аралкил, представленный как R1 и R2.
Алкил как R7 является таким же, как алкил, представленный как R1 и R2, и аралкил, представленный как R7, является таким же, как алкил, представленный как R1 и R2.
Группа, сформированная в сочетании с помощью R6 и R7, которая образует гетероцикл, необязательно имеющий атом кислорода, атом серы или необязательно замещенный атом азота в кольце, дополнительно, может представлять собой, например, имидазол-2-ил, тиазол-2-ил, оксазол-2-ил, имидазолин-2-ил, 3,4,5,6-тетрагидропиридин-2-ил, 3,4,5,6-тетрагидропиримидин-2-ил, 1,3-оксазолин-2-ил, 1,3-тиазолин-2-ил или бензимидазол-2-ил, бензотиазол-2-ил или бензоксазол-2-ил, который может иметь заместитель, такой как атом галогена, алкил, алкокси, галогеналкил, нитро, амино, фенил, аралкил и тому подобное. Под атомом галогена, алкилом, алкокси, галогеналкилом и аралкилом подразумеваются группы, иллюстрируемые для R1 и R2.
Заместитель указанного выше необязательно замещенного атома азота может представлять собой, например, алкил, аралкил или галогеналкил, где алкил, аралкил и галогеналкил представляют собой группы, иллюстрируемые как R1 и R2.
Гидроксиалкил как R10 и R11 представляет собой алкил с прямой или разветвленной цепью, имеющий 1-6 атомов углерода, который является замещенным 1-3 гидрокси, такой как гидроксиметил, 2-гидроксиэтил, 1-гидроксиэтил, 3-гидроксипропил и 4-гидроксибутил. Алкил как R10 и R11 является таким же, как R1 и R2; галогеналкил и алкоксикарбонил как R10 и R11 являются такими же, как R1 и R2; и аралкил, представленный как R10 и R11, является таким же, как R1 и R2. Циклоалкил в сочетании, образованный с помощью R10 и R11, является таким же, как циклоалкил как R1 и R2.
Соединение (1) предпочтительно представляет собой (R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль. В дальнейшем, для удобства, (R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемая соль иногда упоминается как соединение (Ia). В качестве соли соединения, предпочтительной является фармацевтически приемлемая кислотно-аддитивная соль. Примеры кислоты включают неорганические кислоты, такие как хлористоводородная кислота, бромистоводородная кислота, серная кислота и тому подобное, органические кислоты, такие как метансульфоновая кислота, фумаровая кислота, малеиновая кислота, миндальная кислота, лимонная кислота, винная кислота, салициловая кислота и тому подобное. Среди них, (R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид моногидрохлорид (далее иногда упоминается как соединение (I)) является предпочтительным.
Соединение (Ia) может представлять собой гидрат и 1 гидрат, 2 гидрат, 1/2 гидрат, 1/3 гидрат, 1/4 гидрат, 2/3 гидрат, 3/2 гидрат, 6/5 гидрат и тому подобное, соединения (Ia) также являются охваченными настоящим изобретением.
Соединение (1), конкретно соединение (I), может конкретно синтезироваться, например, с помощью способов, описанных в WO 95/28387 и WO 2002/083175.
Соединение (1), предпочтительно соединение (Ia), особенно предпочтительно соединение (I), и их фармакологически приемлемые соли и их гидраты, которые должны быть использованы в настоящем изобретении, также упоминаются как соединение по настоящему изобретению.
В настоящем описании, "корнеальная эндотелиальная дисфункция" относится к состоянию, когда корнеальные эндотелиальные клетки являются поврежденными или ослабленными по какой-либо причине. Примеры причины включают интраокулярную хирургическую операцию, повышение внутриглазного давления, ношение контактных линз и тому подобное.
В настоящем описании, "лечение корнеальной эндотелиальной дисфункции" представляет собой концепцию, включающую не только лечение корнеальной эндотелиальной дисфункции, но также и профилактику дисфункции. В дополнение к этому "корнеальная эндотелиальная дисфункция" также включает "заболевание, связанное с корнеальной эндотелиальной дисфункцией". Примеры заболевания включают буллезную кератопатию, корнеальный эндотелиит, отёк роговой оболочки глаза, бельмо роговицы и тому подобное, и настоящее изобретение может соответствующим образом применяться к ним в качестве целевых заболеваний в соответствии с вариантом осуществления настоящего изобретения.
Корнеальные эндотелиальные клетки играют роль поддержания прозрачности роговицы. Когда плотность корнеальных эндотелиальных клеток уменьшается ниже определенного предела, роговица набухает и становится не способной поддерживать прозрачность, при этом развивается корнеальная эндотелиальная дисфункция. Терапевтический агент по настоящему изобретению стимулирует адгезию корнеальных эндотелиальных клеток и может формировать слой корнеальных эндотелиальных клеток, имеющих хорошую морфологию клеток, нормальное функционирование и высокую плотность клеток. Кроме того, терапевтический агент по настоящему изобретению подавляет апоптоз корнеальных эндотелиальных клеток и может лечить или предотвращать корнеальную эндотелиальную дисфункцию. Терапевтический агент по настоящему изобретению может лечить или предотвращать заболевание, связанное с корнеальной эндотелиальной дисфункцией, например буллезную кератопатию и корнеальный эндотелиит. В дополнение к этому терапевтический агент по настоящему изобретению может лечить или предотвращать корнеальную эндотелиальную дисфункцию, вызываемую интраокулярной хирургической операцией, такой как операция при катаракте, операция на стекловидном теле и тому подобное, корнеальную эндотелиальную дисфункцию, вызываемую повышением внутриглазного давления (в частности, обострения глаукомы), или корнеальную эндотелиальную дисфункцию, вызываемую недостатком кислорода из-за ношения контактных линз.
Терапевтический агент по настоящему изобретению не является как-либо ограниченным постольку, поскольку он имеет дозированную форму, пригодную для местного введения в глаз, и могут быть рассмотрены, например, формы интракамеральной инъекции, раствора для интраокулярной ирригации, глазных капель и тому подобное. В настоящем изобретении, предпочтительным являются раствор для интраокулярной ирригации или глазные капли, а более предпочтительными являются глазные капли в аспекте простоты введения. Они могут быть получены с использованием обычных технологий, широко используемых в данной области. Когда оно вводится местным образом в глаз в форме интракамеральной инъекции или раствора для интраокулярной ирригации, соединение по настоящему изобретению вступает в контакт с корнеальными эндотелиальными клетками in vivo, и стимулируется заживление корнеального эндотелиального повреждения. В случае глазных капель, соединение по настоящему изобретению достигает корнеальных эндотелиальных клеток эпителия роговицы через корнеальную строму. Часть его переносится во внутриглазную жидкость, вступает в контакт с корнеальными эндотелиальными клетками со стороны внутриглазной жидкости и стимулирует заживление корнеального эндотелиального повреждения.
В терапевтический агент по настоящему изобретению, в качестве добавок, могут быть добавлены стабилизатор (например, бисульфит натрия, тиосульфат натрия, эдетат натрия, цитрат натрия, аскорбиновая кислота, дибутилгидрокситолуол и тому подобное), солюбилизатор (например, глицерол, пропиленгликоль, макроголь, полиоксиэтилен - гидрированное касторовое масло, полисорбат 80 и тому подобное), суспендирующий агент (например, поливинилпирролидон, гидроксипропилметилцеллюлоза, гидроксиметилцеллюлоза, натрий карбоксиметилцеллюлоза и тому подобное), эмульгатор (например, поливинилпирролидон, лецитин соевых бобов, лецитин яичного желтка, полиоксиэтилен - гидрированное касторовое масло, полисорбат 80 и тому подобное), буферный агент (например, фосфатный буфер, ацетатный буфер, боратный буфер, карбонатный буфер, цитратный буфер, Трис буфер, глютаминовая кислота, эпсилон-аминокапроновая кислота и тому подобное), загущающий агент (например, водорастворимое производное целлюлозы, такое как метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза и тому подобное, натрий хондроитин сульфат, гиалуронат натрия, карбоксивиниловый полимер, поливиниловый спирт, поливинилпирролидон, макроголь и тому подобное), консервант (например, бензалконий хлорид, бензетоний хлорид, хлоргексидин глюконат, хлорбутанол, бензиловый спирт, натрий дегидроацетат, сложные p-гидроксибензойные эфиры, эдетат натрия, борная кислота и тому подобное), агент для придания изотоничности (например, хлорид натрия, хлорид калия, глицерол, маннитол, сорбитол, борная кислота, глюкоза, пропиленгликоль и тому подобное), регулятор pH (например, хлористоводородная кислота, гидроксид натрия, фосфорная кислота, уксусная кислота и тому подобное), освежающий агент (например, 1-ментол, d-камфара, d-борнеол, масло мяты перечной и тому подобное) и тому подобное. Количество этих добавок, которые должны быть добавлены, изменяется в зависимости от вида и применения добавки и тому подобное, и они могут быть добавлены при концентрации, при которой может быть достигнута цель добавления добавки.
Хотя количество активного ингредиента в терапевтическом агенте по настоящему изобретению изменяется в зависимости от вида соединения по настоящему изобретению, которое должно быть использовано, количество соединения (Ia) или соединения (I), как правило, составляет примерно 0,00001-1% масс/объем, предпочтительно примерно 0,00001-0,1% масс/объем, более предпочтительно примерно 0,0001-0,05% масс/объем, примерно 0,001-0,05% масс/объем, примерно 0,002-0,05% масс/объем, примерно 0,003-0,05% масс/объем, примерно 0,004-0,05% масс/объем, примерно 0,005-0,05% масс/объем, примерно 0,006-0,05% масс/объем, примерно 0,007-0,05% масс/объем, примерно 0,008-0,05% масс/объем, примерно 0,009 -0,05% масс/объем, примерно 0,01-0,05% масс/объем, примерно 0,02-0,05% масс/объем, примерно 0,03-0,05% масс/объем, примерно 0,04-0,05% масс/объем, примерно 0,003-0,04% масс/объем, примерно 0,004-0,04% масс/объем, примерно 0,005-0,04% масс/объем, примерно 0,006-0,04% масс/объем, примерно 0,007-0,04% масс/объем, примерно 0,008-0,04% масс/объем, примерно 0,009-0,04% масс/объем, примерно 0,01-0,04% масс/объем, примерно 0,02-0,04% масс/объем, примерно 0,03-0,04% масс/объем, примерно 0,003-0,03% масс/объем, примерно 0,004-0,03% масс/объем, примерно 0,005-0,03% масс/объем, примерно 0,006-0,03% масс/объем, примерно 0,007-0,03% масс/объем, примерно 0,008-0,03% масс/объем, примерно 0,009-0,03% масс/объем, примерно 0,01-0,03% масс/объем, примерно 0,02-0,03% масс/объем, примерно 0,003-0,02% масс/объем, примерно 0,004-0,02% масс/объем, примерно 0,005-0,02% масс/объем, примерно 0,006-0,02% масс/объем, примерно 0,007-0,02% масс/объем, примерно 0,008-0,02% масс/объем, примерно 0,009-0,02% масс/объем, примерно 0,01-0,02% масс/объем, примерно 0,003-0,01% масс/объем, примерно 0,004-0,01% масс/объем, примерно 0,005-0,01% масс/объем, примерно 0,006-0,01% масс/объем, примерно 0,007-0,01% масс/объем, примерно 0,008-0,01% масс/объем или примерно 0,009-0,01% масс/объем. Хотя доза и частота введения изменяются в зависимости от симптомов, возраста, массы тела и формы введения, когда он используется как глазные капли для взрослых, например препарат, содержащий примерно 0,0001-0,1% масс/объем, предпочтительно примерно 0,003-0,03% масс/объем активного ингредиента может, как правило, вводиться 1-10 раз, предпочтительно 1-6 раз, более предпочтительно 1-3 раз в день, примерно по 0,01-0,1 мл на одно введение. Когда терапевтический агент по настоящему изобретению вводится как инъекция в переднюю камеру глаза, может быть использована концентрация от 1/10 до 1/1000 от указанной выше концентрации. В терапевтическом агенте по настоящему изобретению специалисты в данной области могут соответствующим образом определять концентрацию соединения по настоящему изобретению в зависимости от болезненного состояния.
Примеры субъектов введения терапевтического агента по настоящему изобретению включают млекопитающих (например, человека, мышь, крысу, хомяка, кролика, кошку, собаку, жвачное животное, лошадь, овцу, обезьяну и тому подобное).
В настоящем описании, "стимулирование адгезии корнеальной эндотелиальной клетки" относится к стимулированию адгезии корнеальных эндотелиальных клеток. Примеры стимулирования адгезии корнеальных эндотелиальных клеток включают стимулирование адгезии между корнеальными эндотелиальными клетками, стимулирование адгезии корнеальных эндотелиальных клеток на Десцеметовой оболочке и стимулирование адгезии корнеальных эндотелиальных клеток на подложке или каркасе для культивирования.
В настоящем описании, "агент для стимулирования адгезии" представляет собой медицинский препарат, имеющий действие стимулирования адгезии. Агент для стимулирования адгезии корнеальных эндотелиальных клеток по настоящему изобретению (далее иногда будет сокращенно именоваться "агент для стимулирования адгезии по настоящему изобретению") имеет действие стимулирования адгезии корнеальных эндотелиальных клеток, выделенных из корнеальной ткани, полученной от млекопитающего, адгезии между корнеальными эндотелиальными клетками, выделенными из нее и пересеянными, адгезии корнеальных эндотелиальных клеток на Десцеметовой оболочке и адгезии корнеальных эндотелиальных клеток на подложке или каркасе для культивирования, где млекопитающее включает, например, человека, мышь, крысу, хомяка, кролика, кошку, собаку, жвачное животное, лошадь, овцу, обезьяну и тому подобное. Поскольку агент для стимулирования адгезии по настоящему изобретению является превосходным по действию стимулирования адгезии корнеальных эндотелиальных клеток, полученных от человека, которые считаются особенно сложными для культивирования и пассажа, полученные от человека корнеальные эндотелиальные клетки являются предпочтительной мишенью.
Агент для стимулирования адгезии по настоящему изобретению может быть использован в качестве агента для защиты корнеального эндотелия при лечении или профилактике заболеваний, связанных с корнеальной эндотелиальной дисфункцией. Примеры заболевания, связанного с корнеальной эндотелиальной дисфункцией, включают буллезную кератопатию, корнеальный эндотелиит и тому подобное. В дополнение к этому агент для стимулирования адгезии по настоящему изобретению также может быть использован в качестве агента для защиты корнеального эндотелия при лечении или профилактике корнеальной эндотелиальной дисфункции, вызываемой интраокулярной хирургической операцией, такой как операция при катаракте, операция на стекловидном теле и тому подобное, корнеальной эндотелиальной дисфункции, вызываемой повышенным внутриглазным давлением (в частности, обострением глаукомы), или корнеальной эндотелиальной дисфункцией, вызываемой недостатком кислорода из-за ношения контактных линз. Без какого-либо ограничения, агент для стимулирования адгезии по настоящему изобретению может содержать добавки (стабилизатор, солюбилизатор, суспендирующий агент и тому подобное), сходные с теми, которые используют для указанного выше терапевтического агента. Содержание, доза, субъект введения и тому подобное, для соединения по настоящему изобретению в качестве активного ингредиента могут также быть сходными с указанным выше терапевтическим агентом.
Агент для стимулирования адгезии по настоящему изобретению может также быть добавлен в среду для культивирования, когда корнеальные эндотелиальные клетки культивируются in vitro. Когда соединение по настоящему изобретению добавляют в среду для культивирования и окультуривание продолжают, соединение по настоящему изобретению вступает в контакт с корнеальными эндотелиальными клетками и стимулируется адгезия между корнеальными эндотелиальными клетками, адгезия корнеальных эндотелиальных клеток на Десцеметовой оболочке и адгезия корнеальных эндотелиальных клеток на подложке или каркасе для культивирования. В случае добавления агента для стимулирования адгезии по настоящему изобретению в среду для культивирования, хотя концентрация соединения по настоящему изобретению, которое содержится в среде для культивирования, и тому подобное, могут быть сходными с параметрами настоящего изобретения, рассмотренными ниже, но они необязательно ограничиваются ими.
В другом аспекте, настоящее изобретение предусматривает среду для культивирования корнеальных эндотелиальных клеток, содержащую соединение по настоящему изобретению. Соединение по настоящему изобретению, которое содержится в среде для культивирования по настоящему изобретению, является таким, как описано выше.
Без какого-либо ограничения, среда для культивирования по настоящему изобретению может содержать среду, как правило, используемую для культивирования корнеальных эндотелиальных клеток (например, среда Игла, модифицированная Дюльбекко (DMEM, Invitrogen), сыворотку (например, фетальную сыворотку теленка (FBS)), факторы роста (например, основной фактор роста фибробластов (b-FGF)), антибиотики (например, пенициллин, стрептомицин) и тому подобное.
В среде для культивирования по настоящему изобретению, хотя концентрация соединения по настоящему изобретению изменяется в зависимости от вида соединения, которое должно быть использовано, содержание соединения (Ia) или соединения (I), как правило, составляет примерно 0,001-100 мкМ, предпочтительно примерно 0,01-75 мкМ, примерно 0,05-50 мкМ, примерно 1-10 мкМ, примерно 0,01-10 мкМ, примерно 0,05-10 мкМ, примерно 0,075-10 мкМ, примерно 0,1-10 мкМ, примерно 0,5-10 мкМ, примерно 0,75-10 мкМ, примерно 1,0-10 мкМ, примерно 1,25-10 мкМ, примерно 1,5-10 мкМ, примерно 1,75-10 мкМ, примерно 2,0-10 μ, примерно 2,5-10 мкМ, примерно 3,0-10 мкМ, примерно 4,0-10 мкМ, примерно 5,0-10 мкМ, примерно 6,0-10 мкМ, примерно 7,0-10 мкМ, примерно 8,0-10 мкМ, примерно 9,0-10 мкМ, примерно 0,01-5,0 мкМ, примерно 0,05-5,0 мкМ, примерно 0,075-5,0 мкМ, примерно 0,1-5,0 мкМ, примерно 0,5-5,0 мкМ, примерно 0,75-5,0 мкМ, примерно 1,0-5,0 мкМ, примерно 1,25-5,0 мкМ, примерно 1,5-5,0 мкМ, примерно 1,75-5,0 мкМ, примерно 2,0-5,0 мкМ, примерно 2,5-5,0 мкМ, примерно 3,0-5,0 мкМ, примерно 4,0-5,0 мкМ, примерно 0,01-3,0 мкМ, примерно 0,05-3,0 мкМ, примерно 0,075-3,0 мкМ, примерно 0,1-3,0 мкМ, примерно 0,5-3,0 мкМ, примерно 0,75-3,0 мкМ, примерно 1,0-3,0 мкМ, примерно 1,25-3,0 мкМ, примерно 1,5-3,0 мкМ, примерно 1,75-3,0 мкМ, примерно 2,0-3,0 мкМ, примерно 0,01-1,0 мкМ, примерно 0,05-1,0 мкМ, примерно 0,075-1,0 мкМ, примерно 0,1-1,0 мкМ, примерно 0,5-1,0 мкМ, примерно 0,75-1,0 мкМ, примерно 0,09-3,5 мкМ, примерно 0,09-3,2 мкМ, более предпочтительно примерно 0,05-1,0 мкМ, примерно 0,075-1,0 мкМ, примерно 0,1-1,0 мкМ, примерно 0,5-1,0 мкМ, примерно 0,75-1,0 мкМ.
Среда для культивирования по настоящему изобретению предотвращает диссоциацию клеток посредством стимулирования адгезии корнеальных эндотелиальных клеток и делает возможным образование слоя корнеальных эндотелиальных клеток, имеющего хорошую морфологию клеток, нормальное функционирование и высокую плотность клеток. По этой причине ее предпочтительно используют для способа получения корнеального эндотелиального препарата по настоящему изобретению, упоминаемого ниже. В дополнение к этому, среду для культивирования по настоящему изобретению также используют для поддержания корнеальных эндотелиальных клеток.
В другом аспекте, настоящее изобретение предусматривает раствор для хранения роговицы, содержащий соединение по настоящему изобретению. Соединение по настоящему изобретению, содержащееся в растворе для хранения роговицы по настоящему изобретению, является таким, как описано выше. В настоящем описании, раствор для хранения роговицы представляет собой жидкость, используемую для консервирования трансплантата роговицы, выделенного у донора, до его трансплантации реципиенту.
Примеры раствора для хранения роговицы по настоящему изобретению включают растворы для хранения, как правило, используемые для корнеальной эндотелиальной кератопластики (среды для хранения роговицы (Optisol GS: зарегистрированное торговое наименование), среду для хранения глаз (EPII: зарегистрированное торговое наименование)), солевой раствор, фосфатный буферный солевой раствор (PBS) и тому подобное, каждый из которых содержит соединение по настоящему изобретению.
В растворе для хранения роговицы по настоящему изобретению, концентрация соединения по настоящему изобретению изменяется в зависимости от вида соединения, которое должно быть использовано. Концентрация соединения (Ia) или соединения (I), как правило, составляет примерно 0,001-100 мкМ, предпочтительно примерно 0,01-75 мкМ, примерно 0,05-50 мкМ, примерно 1-10 мкМ, примерно 0,01-10 мкМ, примерно 0,05-10 мкМ, примерно 0,075-10 мкМ, примерно 0,1-10 мкМ, примерно 0,5-10 мкМ, примерно 0,75-10 мкМ, примерно 1,0-10 мкМ, примерно 1,25-10 мкМ, примерно 1,5-10 мкМ, примерно 1,75-10 мкМ, примерно 2,0-10 мкМ, примерно 2,5-10 мкМ, примерно 3,0-10 мкМ, примерно 4,0-10 мкМ, примерно 5,0-10 мкМ, примерно 6,0-10 мкМ, примерно 7,0-10 мкМ, примерно 8,0-10 мкМ, примерно 9,0-10 мкМ, примерно 0,01-5,0 мкМ, примерно 0,05-5,0 мкМ, примерно 0,075-5,0 мкМ, примерно 0,1-5,0 мкМ, примерно 0,5-5,0 мкМ, примерно 0,75-5,0 мкМ, примерно 1,0-5,0 мкМ, примерно 1,25-5,0 мкМ, примерно 1,5-5,0 мкМ, примерно 1,75-5,0 мкМ, примерно 2,0-5,0 мкМ, примерно 2,5-5,0 мкМ, примерно 3,0-5,0 мкМ, примерно 4,0-5,0 мкМ, примерно 0,01-3,0 мкМ, примерно 0,05-3,0 мкМ, примерно 0,075-3,0 мкМ, примерно 0,1-3,0 мкМ, примерно 0,5-3,0 мкМ, примерно 0,75-3,0 мкМ, примерно 1,0-3,0 мкМ, примерно 1,25-3,0 мкМ, примерно 1,5-3,0 мкМ, примерно 1,75-3,0 мкМ, примерно 2,0-3,0 мкМ, примерно 0,01-1,0 мкМ, примерно 0,05-1,0 мкМ, примерно 0,075-1,0 мкМ, примерно 0,1-1,0 мкМ, примерно 0,5-1,0 мкМ, примерно 0,75-1,0 мкМ, примерно 0,09-3,5 мкМ или примерно 0,09-3,2 мкМ, более предпочтительно примерно 0,05-1,0 мкМ, примерно 0,075-1,0 мкМ, примерно 0,1-1,0 мкМ, примерно 0,5-1,0 мкМ или примерно 0,75-1,0 мкМ.
Раствор для хранения роговицы по настоящему изобретению предотвращает диссоциацию клеток посредством стимулирования адгезии корнеальных эндотелиальных клеток и делает возможным образование слоя корнеальных эндотелиальных клеток, имеющих хорошую морфологию клеток, нормальное функционирование и высокую плотность клеток. По этой причине его предпочтительно используют в качестве раствора для консервирования роговицы, которая должна быть использована для трансплантации органов и тому подобное. Раствор для хранения по настоящему изобретению обеспечивает воздействие подавления гибели и апоптоза клеток для корнеальных эндотелиальных клеток при консервировании. В дополнение к этому, раствор для хранения роговицы по настоящему изобретению также используют в качестве раствора для хранения при криоконсервировании корнеальных эндотелиальных клеток.
Для криоконсервирования, глицерол, диметилсульфоксид, пропиленгликоль, ацетамид и тому подобное могут быть дополнительно добавлены к раствору для хранения роговицы по настоящему изобретению.
В одном из аспектов, настоящее изобретение предусматривает корнеальный эндотелиальный препарат, содержащий соединение по настоящему изобретению и корнеальные эндотелиальные клетки. В настоящем описании, "корнеальный эндотелиальный препарат" относится к препарату, который предотвращает, уменьшает или устраняет состояние корнеальной эндотелиальной дисфункции.
Корнеальный эндотелиальный препарат по настоящему изобретению может лечить заболевание, имеющее расстройства в корнеальном эндотелии, постольку, поскольку он содержит корнеальные эндотелиальные клетки и соединение по настоящему изобретению. Если не ограничиваться теорией, это связано с тем, что, когда соединение по настоящему изобретению вступает в контакт с корнеальными эндотелиальными клетками in vivo, стимулируется адгезия корнеальных эндотелиальных клеток на Десцеметовой оболочке. В дополнение к этому, считается, что поскольку соединение по настоящему изобретению стимулирует повторную адгезию клеток, диссоциирующих во время трансплантации на Десцеметовой оболочке, и подавляет апоптоз клеток, может стимулироваться заживление корнеального эндотелиального повреждения. Какие-либо препараты, которые демонстрируют удобное и быстрое воздействие лечения, подобно корнеальному эндотелиальному препарату по настоящему изобретению, не существовали ранее, и настоящее изобретение предусматривает их впервые.
В одном из вариантов осуществления, корнеальные эндотелиальные клетки, которые должны содержаться в корнеальном эндотелиальном препарате по настоящему изобретению, могут представлять собой клетки, культивируемые в среде для культивирования, содержащей соединение по настоящему изобретению, или в среде для культивирования, не содержащей соединения по настоящему изобретению. В другом варианте осуществления, корнеальный эндотелиальный препарат по настоящему изобретению, соединение по настоящему изобретению и корнеальные эндотелиальные клетки могут смешиваться непосредственно перед введением или консервироваться как смесь. В другом варианте осуществления, корнеальный эндотелиальный препарат по настоящему изобретению может содержать среду для культивирования или раствор для хранения роговицы по настоящему изобретению, или как то, так и другое, с тем, чтобы поддерживать корнеальные эндотелиальные клетки. В другом варианте осуществления, корнеальный эндотелиальный препарат по настоящему изобретению может содержать раствор для суспендирования корнеальных эндотелиальных клеток. Как упоминается выше, когда соединение по настоящему изобретению и корнеальные эндотелиальные клетки присутствуют в области, которая должна лечиться, и вступают в контакт друг с другом, стимулируется заживление корнеального эндотелиального повреждения.
В предпочтительном варианте осуществления, корнеальный эндотелиальный препарат по настоящему изобретению может содержать соединение (Ia) ((R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамидо или его фармакологически приемлемую соль) в качестве соединения по настоящему изобретению.
Корнеальный эндотелиальный препарат по настоящему изобретению может быть использован для лечения заболеваний, связанных с корнеальной эндотелиальной дисфункцией, например буллезной кератопатии, корнеального эндотелиита, отёка роговой оболочки глаза и бельма роговицы, в частности буллезной кератопатии, вызываемой корнеальной эндотелиальной дисфункцией, связанной с дистрофией роговицы, травмой или интраокулярной хирургической операцией. В дополнение к этому корнеальный эндотелиальный препарат по настоящему изобретению может непосредственно вводиться в переднюю камеру глаза пациента, имеющего заболевание с расстройством в корнеального эндотелия, например, посредством инъекции и тому подобное.
Соединение по настоящему изобретению, корнеальные эндотелиальные клетки и тому подобное, которые должны быть использованы для корнеального эндотелиального препарата по настоящему изобретению, могут находиться в любой форме в указанном выше терапевтическом агенте по настоящему изобретению. В дополнение к этому, количество соединения по настоящему изобретению, которое должно содержаться в корнеальном эндотелиальном препарате по настоящему изобретению, может также быть сходным, но, не ограничиваясь этим, например, с содержанием в указанного выше терапевтического агента. Количество может быть определено соответствующим образом в соответствии с вариантом осуществления корнеального эндотелиального препарата.
В другом аспекте, настоящее изобретение предусматривает способ получения корнеального эндотелиального препарата, включающий стадию культивирования корнеальных эндотелиальных клеток с использованием среды для культивирования, содержащей соединение по настоящему изобретению, и корнеальный эндотелиальный препарат, полученный с помощью способа получения. Соединение по настоящему изобретению, корнеальные эндотелиальные клетки и тому подобное, которые должны быть использованы для способа получения и корнеального эндотелиального препарата по настоящему изобретению, могут находиться в любой форме, рассмотренной выше.
В одном из вариантов осуществления, способ получения по настоящему изобретению включает стадию культивирования корнеальных эндотелиальных клеток с использованием среды для культивирования по настоящему изобретению и может быть осуществлен, например, с помощью следующего далее способа.
<1> Сбор корнеальных эндотелиальных клеток и окультуривание in vitro
Корнеальные эндотелиальные клетки собирают с роговицы самого реципиента или соответствующего донора с помощью обычного способа. При рассмотрении условий трансплантации по настоящему изобретению могут быть получены аллогенные корнеальные эндотелиальные клетки. Например, Десцеметову оболочку снимают вместе с интактными корнеальными эндотелиальными клетками и обрабатывают коллагеназой и тому подобное. После изоляции корнеальных эндотелиальных клеток, корнеальные эндотелиальные клетки культивируют в среде для культивирования по настоящему изобретению. Может быть использована среда для культивирования, например, посредством соответствующего добавления FBS (фетальной сыворотки теленка), фактора роста основных фибробластов (b-FGF) и антибиотиков, таких как пенициллин, стрептомицин и тому подобное, к коммерчески доступной среде Игла, модифицированной Дюльбекко (DMEM), и дополнительного добавления к ней соединения по настоящему изобретению, предпочтительно соединения (Ia). Предпочтительно используют флакон для культивирования (чашку для культивирования) с покрытием из коллагена типа I, коллагена типа IV, фибронектина, ламинина или внеклеточного матрикса бычьих корнеальных эндотелиальных клеток и тому подобное, на поверхности. Альтернативно, может быть использован флакон для культивирования, обработанный коммерчески доступным агентом для покрытия, таким как смесь для покрытия FNC (зарегистрированное торговое наименование), и тому подобное. Посредством сочетанного использования такого покрытия и среды для культивирования по настоящему изобретению стимулируется адгезия корнеальных эндотелиальных клеток на поверхности флакона для культивирования и осуществляется хороший рост.
Хотя условия температуры для культивирования корнеальных эндотелиальных клеток не являются как-либо ограниченными постольку, поскольку корнеальные эндотелиальные клетки растут, температура составляет, например, примерно 25-примерно 45°C, предпочтительно примерно 30 - примерно 40°C из соображений эффективности роста, а еще более предпочтительно она составляет примерно 37°C. Способ культивирования осуществляют в обычном инкубаторе для культуры клеток с увлажненной атмосферой при концентрации CO2 примерно 5-10%.
<2> Пересеваемая культура
Пересеваемая культура может быть получена после роста корнеальных эндотелиальных клеток, на которые воздействуют культивированием. Пересеваемую культуру предпочтительно получают, когда клетки достигают субконфлюэнтности или конфлюэнтности. Пересеваемая культура может быть получена следующим образом. Клетки обрабатывают трипсином-EDTA и тому подобное и собирают. Среду для культивирования по настоящему изобретению добавляют к собранным клеткам с получением суспензии клеток. Обработку в центрифуге предпочтительно осуществляют во время сбора клеток или после сбора. Такая обработка в центрифуге дает суспензию клеток, имеющую высокую плотность клеток. Например, плотность клеток суспензии клеток составляет примерно 1-2×106 клеток/мл. В качестве условий для обработки в центрифуге здесь могут быть рассмотрены, например, 500 об/мин (×30 г)-1000 об/мин (×70 г), 1-10 мин.
Суспензию клеток высевают во флакон для культивирования таким же образом, как и указанную выше первичную культуру, и культивируют. Хотя отношение разбавления во время пассажа изменяется в зависимости от состояния клеток, оно составляет примерно 1:2-1:4, предпочтительно примерно 1:3. Пересеваемая культура может быть получена при условиях культивирования, сходных с условиями для указанной выше первичной культуры. Хотя время культивирования изменяется в зависимости от состояния клеток, которые должны быть использованы, оно составляет, например, 7-30 дней. Указанная выше пересеваемая культура может быть получена множество раз, при необходимости. При использовании среды для культивирования по настоящему изобретению, увеличивается адгезия клеток на ранних стадиях культивирования, при этом время культивирования может быть уменьшено.
Посредством культивирования, как упоминается выше, может быть получен корнеальный эндотелиальный препарат, содержащий корнеальные эндотелиальные клетки и соединение (предпочтительно, соединение (Ia)) по настоящему изобретению.
В другом аспекте, настоящее изобретение предусматривает набор для лечения корнеальной эндотелиальной дисфункции. Набор включает соединение по настоящему изобретению, корнеальные эндотелиальные клетки и инструкцию.
В одном из вариантов осуществления, соединение по настоящему изобретению, которое должно содержаться в наборе по настоящему изобретению, может содержаться, например, в промывочном растворе, используемом для промывки корнеальных эндотелиальных клеток, в среде для культивирования, в которой должны культивировать корнеальные эндотелиальные клетки, в растворе для суспензии клеток для суспендирования корнеальных эндотелиальных клеток и тому подобное или может находиться в форме твердого продукта (например, порошка). Это связано с тем, что когда соединение по настоящему изобретению и корнеальные эндотелиальные клетки присутствуют в области, которая должна лечиться, и вступают в контакт друг с другом, стимулируется заживление корнеального эндотелиального повреждения. В предпочтительном варианте осуществления, соединение по настоящему изобретению может представлять собой соединение (Ia) ((R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль). В другом варианте осуществления, кроме того, корнеальные эндотелиальные клетки, содержащиеся в наборе по настоящему изобретению, могут быть заморожены. Соединение по настоящему изобретению, корнеальные эндотелиальные клетки и тому подобное, которые должны быть использованы для набора по настоящему изобретению, могут находиться в любой форме, например, в указанном выше терапевтическом агенте по настоящему изобретению, в корнеальном эндотелиальном препарате и тому подобное.
В другом аспекте, настоящее изобретение предусматривает имплант для корнеальной эндотелиальной кератопластики, содержащий A) корнеальные эндотелиальные клетки, B) каркас и C) соединение по настоящему изобретению, предпочтительно соединение (Ia) ((R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль).
В настоящем описании, "имплант для корнеальной эндотелиальной кератопластики" означает кусок ткани, клетки, композицию, медицинский препарат и тому подобное, по настоящему изобретению, которые должны трансплантироваться в роговицу.
В настоящем описании, "каркас" означает материал для поддержки клеток. Каркас имеет заданную прочность и биологическую совместимость. Когда его используют в настоящем описании, каркас изготавливают из биологического вещества или из вещества, поставляемого природой, или из вещества, встречающегося в природе, или из синтетически получаемого вещества. В частности, каркас может быть сформирован из вещества (неклеточного материала), иного, чем органические формы (например, ткань, клетка). Каркас, который должен быть использован в импланте по настоящему изобретению, не является как-либо ограниченным постольку, поскольку он несет слой культивируемых корнеальных эндотелиальных клеток и может сохранять форму in vivo в течение, по меньшей мере, 3 дней после трансплантации. В дополнение к этому, каркас может играть роль каркаса для культивирования корнеальных эндотелиальных клеток in vitro или может играть только роль опоры для слоя корнеальных эндотелиальных клеток после культивирования. Предпочтительно, каркас используют для культивирования корнеальных эндотелиальных клеток, и он играет роль каркаса, непосредственно пригодного для трансплантации после завершения культивирования. В настоящем изобретении, каркас и подложка могут быть использованы взаимозаменяемо.
Примеры рассмотренного выше каркаса или подложки включают, но не ограничиваясь этим, полимерные материалы, полученные из вещества, встречающегося в природе, такие как коллаген, желатин, целлюлоза и тому подобное, синтетические полимерные материалы, такие как полистирол, полиэстр, поликарбонат, поли(N-изопропилакриламид) и тому подобное, биодеградируемые полимерные материалы, такие как полимолочная кислота, полигликолевая кислота и тому подобное, гидроксиапатит, амниотическую мембрану и тому подобное.
Хотя форма рассмотренного выше каркаса или подложки не является как-либо ограниченной постольку, поскольку она несет слой корнеальных эндотелиальных клеток и является пригодной для трансплантации, форма листа является предпочтительной. Когда имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению представляет собой лист, он может быть вырезан с размером, совпадающим с областью применения во время трансплантации. В дополнение к этому, является также возможным скатывание листа в небольшой рулон и вставка его из края повреждения. Особенно предпочтительный пример представляет собой круглая форма, перекрывающая примерно 80% площади аномального корнеального эндотелия. В дополнение к этому также является предпочтительным проделывание щели вокруг указанной выше круглой формы с тем, чтобы лист мог плотно прилегать к области применения.
В предпочтительном варианте осуществления, рассмотренный выше каркас или подложка представляет собой коллаген. В качестве коллагена, предпочтительно может быть использован лист коллагена, описанный в JP-A-2004-24852. Такой лист коллагена может быть получен, например, из амниотической мембраны в соответствии со способом, описанным в JP-A-2004-24852.
Указанный выше слой корнеальных эндотелиальных клеток предпочтительно имеет, по меньшей мере, одну из следующих далее характеристик. Более предпочтительно, он имеет две или более, а еще более предпочтительно все следующие далее характеристики.
(1) Слой клеток имеет структуру монослоя. Это является одной из физиологических характеристик корнеальных эндотелиальных клеток in vivo.
(2) Слой клеток имеет плотность клеток примерно 1000 - примерно 4000 клеток/мм2. В частности, она предпочтительно составляет примерно 2000 - примерно 3000 клеток/мм2, когда реципиент является взрослым.
(3) Клетки, составляющие слой клеток, образуют структуру гексагональной решетки. Это является одной из физиологических характеристик клеток, составляющих слой корнеальных эндотелиальных клеток in vivo. С клетками гексагональной формы, препарат по настоящему изобретению может демонстрировать функцию, сходную с физиологической функцией природного слоя корнеальных эндотелиальных клеток in vivo.
(4) Клетки в слое клеток образуют монослой клеток округлой формы. Физиологически, корнеальные эндотелиальные клетки располагаются таким же образом. Это делает возможным поддержание корнеальной нормальной функции и высокой прозрачности, и регулирования гидратирования роговицы соответствующим образом. По этой причине, при таких морфологических характеристиках, имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению, как ожидается, должен проявлять функцию, сходную с функцией слоя корнеальных эндотелиальных клеток in vivo. Поскольку имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению содержит соединение (Ia), он может хорошо удерживать корнеальные эндотелиальные клетки после трансплантации.
Приготовление слоя корнеальных эндотелиальных клеток
Суспензия клеток из корнеальных эндотелиальных клеток может быть получена в соответствии с разделами <1> Сбор и культивирование корнеальных эндотелиальных клеток in vitro и <2> Пересеваемая культура из указанного выше корнеального эндотелиального препарата. Суспензию клеток высевают на подложку, такую как коллагеновый лист и тому подобное, и культивируют. Здесь, количество высеянных клеток контролируют так, что конечный получаемый корнеальный эндотелиальный препарат имеет слой клеток, имеющий желаемую плотность клеток. Чтобы быть точным, клетки высевают так, чтобы получить слой клеток, имеющий плотность клеток примерно 1000 - примерно 4000 клеток/мм2. Культура может быть получена при условиях, сходных с условиями для указанной выше первичной культуры и тому подобное. Хотя время культивирования изменяется в зависимости от состояния клеток, которые должны быть использованы, оно составляет, например, 3-30 дней. Слой корнеальных эндотелиальных клеток может быть получен за более короткий период, в то же время сохраняя хорошую морфологию и функционирование посредством добавления соединения по настоящему изобретению, предпочтительно соединения (Ia) ((R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли) к среде для культивирования или суспензии клеток и тому подобное.
Посредством культивирования, как рассмотрено выше, имплант для корнеальной эндотелиальной кератопластики может быть получен как слой корнеальных эндотелиальных клеток, который культивируют на подложке.
В настоящем изобретении, имплант для корнеальной эндотелиальной кератопластики может содержать среду для культивирования по настоящему изобретению для поддержания корнеальных эндотелиальных клеток. В дополнение к этому, имплант для корнеальной эндотелиальной кератопластики может содержать раствор для хранения роговицы по настоящему изобретению до трансплантации. Имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению может содержать как среду для культивирования, так и раствор для хранения по настоящему изобретению. В одном из вариантов осуществления, имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению может дополнительно содержать, по меньшей мере, одну жидкую среду, выбираемую из промывочного раствора, используемого для промывки корнеальных эндотелиальных клеток, среды для культивирования, для культивирования корнеальных эндотелиальных клеток и раствора для суспендирования корнеальных эндотелиальных клеток. Как рассмотрено выше, когда соединение по настоящему изобретению и корнеальные эндотелиальные клетки присутствуют в области, которая должна лечиться, и вступают в контакт друг с другом, стимулируется заживление корнеальных эндотелиальных повреждений.
Имплант для корнеальной эндотелиальной кератопластики по настоящему изобретению может быть использован в качестве трасплантата для лечения заболевания, требующего корнеальной эндотелиальной кератопластики, например буллезной кератопатии, отёка роговой оболочки глаза, бельма роговицы, в частности буллезной кератопатии, вызываемой корнеальной эндотелиальной дисфункцией, связанной с дистрофией роговицы, травмой или интраокулярной хирургической операцией.
Соединение по настоящему изобретению и корнеальные эндотелиальные клетки и тому подобное, которые должны использоваться в импланте для корнеальной эндотелиальной кератопластики по настоящему изобретению, могут находиться в любой форме, сходной с формой указанного выше терапевтического агента, корнеального эндотелиального препарата и тому подобное, по настоящему изобретению.
В другом аспекте, настоящее изобретение предусматривает способ лечения корнеальной эндотелиальной дисфункции, включающий стадию получения корнеального эндотелиального препарата и/или импланта для корнеальной эндотелиальной кератопластики, каждый из них содержит соединение по настоящему изобретению, и стадию трансплантации корнеального эндотелиального препарата и/или импланта для корнеальной эндотелиальной кератопластики субъекту, нуждающемуся в корнеальной эндотелиальной кератопластике. В предпочтительном варианте осуществления, соединение по настоящему изобретению может представлять собой соединение (Ia) ((R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль). Корнеальный эндотелиальный препарат и имплант для корнеальной эндотелиальной кератопластики, которые должны быть использованы в способе лечения по настоящему изобретению, могут находиться в любой форме, сходной с формами указанного выше корнеального эндотелиального препарата и импланта для корнеальной эндотелиальной кератопластики. Способ лечения по настоящему изобретению является пригодным для лечения корнеальной эндотелиальной дисфункции, например буллезной кератопатии, отёка роговой оболочки глаза, бельма роговицы и тому подобное.
Субъект введения (трансплантации) корнеального эндотелиального препарата по настоящему изобретению представляет собой, например, млекопитающее (например, человека, мышь, крысу, хомяка, кролика, кошку, собаку, жвачное животное, лошадь, овцу, обезьяну и тому подобное), и человек является предпочтительным.
На стадии трансплантации, аллогенная трансплантация является предпочтительной, и корнеальный эндотелиальный препарат, полученный из корнеальных эндотелиальных клеток, аллогенных с животным, которое должно представлять собой субъект трансплантации, приготавливают предпочтительно. Когда субъект представляет собой человека, корнеальный эндотелиальный препарат, полученный от донора, имеющего такой же тип крови или тип HLA, является предпочтительным, а аутологичная трансплантация является более предпочтительной.
В другом аспекте, настоящее изобретение предусматривает супрессор апоптоза, содержащий соединение по настоящему изобретению. Здесь, соединение по настоящему изобретению может предпочтительно представлять собой соединение (Ia) ((R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль). Соединение по настоящему изобретению, которое должно использоваться для супрессора апоптоза по настоящему изобретению, может находиться в любой форме, сходной с формами указанного выше терапевтического агента по настоящему изобретению.
Супрессор апоптоза по настоящему изобретению имеет воздействие подавления развития или эволюции апоптоза и является пригодным для лечения или профилактики заболевания или патологии, вызываемой гипераномалией апоптоза, или заболевания или патологии, последовательно показывающей такое состояние.
Примеры заболевания, связанного с гипераномалией апоптоза включают вирусные инфекции, эндокринные заболевания, гематологические заболевания, гипоплазию органов, отторжение трансплантированных органов, заболевание несовместимости трансплантата и хозяина, иммунодефицит, нейродегенеративное заболевание, ишемические болезни, радиационное расстройство, ультрафиолетовое повреждение, заболевания, связанные с отравлением, недостаточность питания, воспалительное заболевание, ишемическую невропатию, сосудистое заболевание, респираторные заболевания, артикулярный синдром и тому подобное. Поскольку супрессор апоптоза по настоящему изобретению может, в частности, стимулировать заживление повреждений корнеальных эндотелиальных клеток посредством подавления апоптоза клеток, он является полезным для лечения или профилактики корнеальной эндотелиальной дисфункции. Без какого-либо ограничения, супрессор апоптоза по настоящему изобретению может содержать добавку (стабилизатор, солюбилизатор, суспендирующий агент и тому подобное), сходную с добавками для указанного выше терапевтического агента. Содержание, доза, субъект введения и тому подобное, для соединения, по настоящему изобретению в качестве активного ингредиента, могут также быть сходными с параметрами указанного выше терапевтического агента.
Примеры
Настоящее изобретение объясняется более подробно в дальнейшем с помощью ссылок на Примеры, которые, как предполагается, не являются ограничивающими. Экспериментальных животных используют в соответствии с International Guiding Principles for Biomedical Research Involving Animals, а также Act on welfare and management of animals, и со стандартом, относящимся к кормлению, содержанию и тому подобное экспериментальных животных. Этот эксперимент осуществляют в соответствии с Guidelines of Association for Research in Vision and Ophthalmology on the Use of Animals in Ophthalmic and Vision Research.
Пример приготовления: Пример приготовления исследуемого вещества
Композиция исследуемого вещества при каждой концентрации показана ниже.
0,05 или 0,1 г
Пример 1: Воздействие соединения (I) на модель кролика корнеального эндотелиального повреждения
1. Исследуемое вещество и контрольное вещество
В качестве исследуемого вещества используют (R)-(+)-N-(1H-пирроло [2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид моногидрохлорид (соединение (I)). Соединение (I) получают в соответствии со способами, описанными в WO 95/28387 и WO 2002/083175.
В этом Примере используют инстилляцию 0,95 мМ (0,03% масс/объем) соединения (I) и инстилляцию 0,32 мМ (0,01% масс/объем) соединения (I), полученного посредством разбавления указанной выше инстилляции с помощью указанного выше носителя.
В качестве веществ для положительного контроля, покупают дигидрохлорид Y-27632 (Vako Pure Chemical Industries, Co., Ltd., Cat. #253-00513) и фазудил гидрохлорид гидрат для инъекций (Eril (зарегистрированное торговое наименование), для инъекции через капельницу, Asahi Kasei Pharma), и Y-27632 и Fasudil, каждый, доводят до 10 мМ с помощью фосфатного буферного солевого раствора (PBS, Invitrogen, Cat. #14190). В дополнение к этому PBS используют в качестве вещества для отрицательного контроля.
2. Животные
Самцов японских белых кроликов (масса тела 2,5-3,0 кг, 21 кролик) покупают от Biotek Co., Ltd. и используют. Их содержат в индивидуальных клетках при температуре 23±3°C, при влажности 55±10% и при 12-часовом искусственном световом цикле (свет включают в 8 часов утра, свет выключают в 8 часов вечера). Сто граммов твердого корма (Labo R stock; Nosan Corp.) дают ежедневно каждому животному. Воду подают с помощью устройства для автоматической подачи воды.
3. Иссечение мигательной перепонки у животного
Перед началом исследования иссекают мигательную перепонку на обоих глазах животного. Конкретно, каждое животное устанавливают в позиционирующее устройство, и поверхность глаз анестезируют местным образом посредством инстилляции местной анестезии (инстилляция 0,4% Benoxil, Santen Pharmaceutical Co., Ltd.). Затем корневое положение мигательной перепонки прижимают, с помощью зажима, на 30 с, и складку, образующуюся при сжатии, отрезают с помощью ножниц. После иссечения мигательной перепонки инстиллируют антибиотиотическую мазь (глазная мазь таривид, Santen Pharmaceutical Co., Ltd.) для предотвращения инфекции. Через 4 дня после иссечения мигательной перепонки подтверждают, что используют животных, которые не имеют аномалий на внешней стороне глаза, включая область иссечения.
4. Разделение животных на группы
Толщину роговицы правого глаза каждого животного измеряют с помощью ультразвукового пахиметра (производится DGH Technologies Inc., DGH-500), и животных разделяют на 4 группы так, что толщина роговицы для каждой группы является одинаковой. Животные, используемые для каждой группы, являются следующими.
5. Создание корнеального эндотелиального повреждения
Животных подвергают общей анестезии посредством внутримышечного введения препарата для мышечных инъекций Ketalar (500 мг на 1 кг массы тела, DAIICHI SA KYO COMPANY, LIMITED, 0,6 мл) и Celactal 2% Injection (Bayer, Ltd., 0,25 мл). Затем инстиллируют Benoxil instillation 0,4% (Santen Pharmaceutical Co., Ltd., одну каплю), и глаз открывают с использованием расширителя для век.
Стержень из нержавеющей стали диаметром 7 мм, который охлаждают в жидком азоте, помещают на центральную роговицу обоих глаз 21 животного, на 15 с, для получения шарика льда в передней камере глаза и для диссоциации корнеальных эндотелиальных клеток, при этом получают корнеальное эндотелиальное повреждение.
6. Местная инстилляция
Для местной инстилляции, после создания повреждения, инстилляцию соединения (I), инстилляцию Y-27632 или инстилляцию Fasudil инстиллируют в правый глаз, а PBS инстиллируют в левый глаз 6 раз в день (в день создания повреждения, 4 раза) при 50 мкл на инстилляцию. Интервал времени между введениями в один день составляет 2 часа.
7. Сбор роговицы и измерение площади повреждения
Через 46 часов после создания повреждения кроликов подвергают эвтаназии посредством инъекции сверхдозы 5% раствора пентобарбитала натрия (пентобарбитала (Nacalai Tesque, Cat. #26427-14), растворенного в солевом растворе) в заднюю ушную вену кроликов и иссекают ткань роговицы. Корнеальные эндотелиальные клетки иссеченной роговицы окрашивают 0,5% раствором ализарина красного S (Nacalai Tesque, Cat. #01303-52), а затем исследуют под микроскопом, и окрашенные изображения области повреждения регистрируют с помощью оптического микроскопа (Olympus, BX51). Область повреждения измеряют с использованием программного обеспечения для анализа изображений Image J (NIH, ver.1.41o), наружную границу области повреждения, окрашенную ализарином красным, изображают на графике вручную, и область, окруженную с помощью этого графика, вычисляют как область повреждения. Область повреждения используют для статистического анализа (Ekuseru-Toukei 2008 for Windows, Social Survey Research Information Co., Ltd., ver. 1.10) в соответствии с (двухсторонним) тестом Даннета с множеством сравнений, и значения P <0,05 считаются статистически значимыми.
Результаты и обсуждение
Окрашенные ализарином изображения областей корнеального эндотелиального повреждения через 46 часов после создания повреждения показаны на Фиг.1, а площади повреждения корнеального эндотелия показаны на Фиг.2. Площадь области не восстановившегося повреждения составляет 2,3 мм2 для группы с инстилляцией PBS, а самое маленькое значение, 0,4 мм2, наблюдается в группе с инстилляцией 0,95 мМ соединения (I). По сравнению с группой с инстилляцией PBS, наблюдают статистически значимое уменьшение площади повреждения. В дополнение к этому, площадь повреждения составляет всего лишь 1,1 мм2 в группе с инстилляцией 0,32 мМ соединения (I), по сравнению с группой с инстилляцией PBS, и находится на таком же уровне, 1,1 мм2, для в группы с инстилляцией 10 мМ Y-27632. С другой стороны, группа с инстилляцией 10 мМ Fasudil показывает более широкую площадь невосстанавливаемого повреждения, 1,7 мм2, чем для группы с инстилляцией Y-27632.
Рассмотренные выше результаты показывают, что соединение (I) уменьшает площадь повреждения в корнеальном эндотелии при концентрации боле низкой, чем для Y-27632, доказывая возможность стимулирования заживления повреждений.
Пример 2: Воздействие введения высокой концентрации соединения (I) для модели кролика корнеального эндотелиального повреждения
Воздействие может быть подтверждено на модели кролика потери корнеального эндотелия посредством инстилляции 0,05% масс/объем (1,58 мМ) соединения (I) (местная инстилляция; 6 раз день, 2 дня).
Пример 3: Приготовление корнеальных эндотелиальных клеток кролика
Ткани глазного яблока самцов японского белого кролика (мишень для сбора: примерно 2,5 кг массы тела) покупают от Fukusaki Rabbit Warren и используют. Используют 20 глазных яблок. Ткань роговицы иссекают из полученных тканей глазных яблок кролика и отделяют Десцеметову оболочку вместе с интактными корнеальными эндотелиальными клетками. Отделенную Десцеметову оболочку инкубируют вместе с коллагеназой A (2,5 мг/мл, Roche, Cat. #1088793) при условиях 37°C, 5% CO2 в течение 2 часов. После этого клетки собирают с помощью центрифугирования (1000 об/мин (×70 г), 3 мин). Собранные клетки разбавляют средой для культивирования (DMEM (Invitrogen, Cat. #12320-032), 10% FBS и 2 нг/мл bFGF (Invitrogen, Cat. #13256-029) и 1% пенициллина/стрептомицина (Invitrogen, Cat. #15070-063)), засевают при плотности 2 глаза на лунку в 6-луночный планшет (Corning Incorporated, Cat. #3516), покрытый смесью FNC для покрытия (Athena ES, Cat. #0407), и клетки культивируют до получения конфлюентности при 37°C.
Пример 4: Воздействие на морфологию культивируемых корнеальных эндотелиальных клеток
В этом Примере соединение (I), Y-27632 дигидрохлорид (Wako Pure Chemical Industries, Co., Ltd., Cat. # 253-00513) и Fasudil (SIGMA-ALDRICH, Cat. #H139) растворяют в ДМСО (Nacalai Tesque, Cat. #13406-55) и дополнительно разбавляют средой для культивирования с получением исследуемых веществ и контрольных веществ, которые должны быть использованы.
Корнеальные эндотелиальные клетки кролика, приготовленные в Примере 3, промывают дважды фосфатным буферным солевым раствором (PBS, Invitrogen, Cat. #14190), добавляют PBS (4 мл) и клетки инкубируют при 37°C в течение 10 мин. PBS удаляют, добавляют 0,05% трипсин/EDTA (Invitrogen, Cat. #25300-054) и клетки инкубируют при 37°C в течение примерно 5 мин. К ним добавляют среду для культивирования (10 мл, DMEM (Invitrogen, Cat. #12320-032), 10% FBS, 2 нг/мл bFGF (Invitrogen, Cat. #13256-029) и 1% пенициллина/стрептомицина (Invitrogen, Cat. #15070-063)) и клетки собирают в пробирки и центрифугируют (1000 об/мин (×70 г), 3 мин). Собранные клетки разбавляют средой для культивирования (примерно 3-4 мл).
К разбавленным корнеальным эндотелиальным клеткам кролика добавляют каждый медицинский препарат до конечных концентраций 0,09, 0,32, 0,95, 3,16 и 9,47 мкМ, соединение (I), 10 мкМ Y-27632 и 10 мкМ Fasudil. Эти клетки высевают при отношении разбавления 1:8 на 1 мл на лунку в 24-луночный планшет (Corning Incorporated, Cat. #3526). В качестве контроля добавляют 0,04% ДМСО/среды для культивирования. Через 1, 3, 5, 7 и 14 дней после добавления, регистрируют изображения с помощью микроскопа. Результаты показаны на Фиг.3-7.
Согласно наблюдению, вплоть до 14 дней после высевания, клетки имеют полимегетизм, и образование связей между клетками в контрольной группе является недостаточным. В группах с добавлением 0,32, 0,95 и 3,16 мкМ соединения (I) морфология корнеальных эндотелиальных клеток поддерживается даже после пассажа, связи между клетками образуются через 14 дней после высевания, и образуется монослой клеток.
Результаты для 10 мкМ Y-27632 и Fasudil являются сходными с результатами для 0,32, 0,95 и 3,16 мкМ соединения (I).
Соединение (I), как считается, сохраняет морфологию корнеальных эндотелиальных клеток при концентрации более низкой, чем Y-27632 и Fasudil.
Пример 5: Рассмотрение модели заживления повреждений культивируемых корнеальных эндотелиальных клеток
В этом Примере используют корнеальные эндотелиальные клетки кролика, приготовленные таким же образом, как в Примере 4.
В этом Примере, кроме того, используют исследуемые вещества и контрольное вещество, приготовленное таким же образом, как в Примере 4.
Собранные корнеальные эндотелиальные клетки кролика разбавляют средой для культивирования (примерно 4 мл, DE (Invitrogen, Cat. #12320-032), 10% FBS, 2 нг/мл bFGF (Invitrogen, Cat. #13256-029) и 1% пенициллина/стрептомицина (Invitrogen, Cat. #15070-063)) и высевают при отношении разбавления 1:4 по 2 мл на лунку в 6-луночный планшет (Corning Incorporated, Cat. #3516). Клетки инкубируют до получения конфлюэнтности при условиях 37°C и 5% CO2. Повреждения создают в конфлюэнтных клетках, используя 1000-микролитровый чип (Molecular BioProducts, 2279). Затем каждый медицинский препарат добавляют в среду для культивирования до конечной концентрации 0,09, 0,32, 0,95, 3,16 и 9,47 мкМ соединения (I), 10 мкМ Y-27632 и 10 мкМ Fasudil. В качестве контроля добавляют ДМСО до конечной концентрации 0,04%.
Через 6 часов, 12 часов и 24 часа после добавления каждого медицинского препарата ширину повреждения фотографируют в разные моменты времени, и ширину повреждения оценивают с помощью анализа изображений. Результаты показаны на Фиг.8.
В группе с добавлением соединения (I) ширина повреждения значительно уменьшается через 24 часа после добавления при низкой концентрации (0,09-3,16 мкМ), в соответствии с тестом Даннета (Фиг.8). При 9,47 мкМ, не наблюдают статистически значимого отличия от контрольной группы. В соответствии с t-критерием Стьюдента, 0,95 мкМ соединения (I) показывают воздействие заживления повреждения, начиная от ранних стадий добавления.
Соединение (I), как считается, показывает воздействие заживления повреждения при концентрации (0,09-3,16 мкМ), более низкой, чем для Y-27632 и Fasudil. Согласно приведенным выше результатам, соединение (I) также стимулирует заживление повреждений для модели in vitro заживления повреждения корнеального эндотелия.
Пример 6: Воздействия на активность адгезии культивируемых корнеальных эндотелиальных клеток на планшете для культивирования.
В этом Примере используют корнеальные эндотелиальные клетки кролика, приготовленные таким же образом, как в Примере 4.
В этом Примере, кроме того, используют исследуемые вещества и контрольное вещество, приготовленное таким же образом, как в Примере 4.
Собранные корнеальные эндотелиальные клетки кролика разбавляют, и к клеткам добавляют среду для культивирования (примерно 4 мл, DMEM (Invitrogen, Cat. #12320-032), 10% FBS, 2 нг/мл bFGF (Invitrogen, Cat. #13256-029) и 1% пенициллина/стрептомицина (Invitrogen, Cat. #15070-063)). Затем в среду для культивирования добавляют каждый из медицинских препаратов до конечных концентраций 0,09, 0,32, 0,95, 3,16 и 9,47 мкМ, соединение (I), 10 мкМ Y-27632 и 10 мкМ Fasudil. В качестве контроля добавляют ДМСО до конечной концентрации 0,04%.
Эти клетки засевают в 96-луночный планшет (Corning Incorporated, Cat. #3595) при 1000 клеток/лунка. Через 3 часа после высеивания суспендированные клетки удаляют, а прилипшие клетки считают с помощью Cell Titer-Glow (зарегистрированное торговое наименование) Luminescent Cell Viability Assay (protégé Cat. #G7572).
Результаты показаны на Фиг.9. Все группы с добавлением соединения (I) увеличивают количество прилипших клеток in vitro. 0,32 мкМ соединения (I) показывают количество прилипших клеток почти на таком же уровне, как для 10 мкМ Y-27632. Количество прилипших клеток для соединения (I) достигает плато при концентрации не меньше чем 0,32 мкМ.
Резюме Примеров 4-6
Соединение (I) показывает воздействие на адгезию, морфологию клеток и заживление повреждений корнеальных эндотелиальных клеток при условиях культивирования, в частности при 0,32, 0,95 и 3,16 мкМ. Среди прочего, модель заживления повреждений показывает воздействие заживления повреждений, начиная от ранних стадий после добавления 0,95 мкМ соединения (I).
Из этих результатов ясно, что соединение (I) оказывает воздействие поддержания морфологии корнеальных эндотелиальных клеток, стимулирует их адгезию и залечивает повреждения при более низкой концентрации, по сравнению с Y-27632 и Fasudil.
Пример 7: Получение листа культивируемых корнеальных эндотелиальных клеток для трансплантации
В этом Примере используют корнеальные эндотелиальные клетки кролика, приготовленные таким же образом, как в Примере 4.
В этом Примере, кроме того, используют исследуемые вещества и контрольное вещество, приготовленное таким же образом, как в Примере 4.
Корнеальные эндотелиальные клетки кролика высевают в Vitrigel™ (Asahi Glass) при отношении разбавления 1:1, и получают лист культивируемых корнеальных эндотелиальных клеток для трансплантации. При получении листа корнеальных эндотелиальных клеток добавляют 0,95 мкМ соединения (I), 10 мкМ Y-27632 или 0,04% ДМСО. Получаемый лист корнеальных эндотелиальных клеток подвергают иммуннологическому флуоресцентному окрашиванию с помощью ZO-1 и Na+/K+ ATPазы, которые являются функциональными белками корнеальных эндотелиальных клеток, и экспрессирование подтверждается.
Лист корнеальных эндотелиальных клеток фиксируют с помощью 95% этанола (-30°C) в течение 10 мин, промывают PBS и обрабатывают 0,5% Triton X-100/PBS в течение 5 мин. Затем его обрабатывают с помощью 1% BSA/PBS в течение 1 часа и обрабатывают в течение ночи антителом анти-ZO-1 (Invitrogen, Cat. #339100) или антителом анти-Na+/K+ ATPаза (Millipore, Cat. #C464,6). После промывки PBS его обрабатывают метящим вторичным антителом Alexa-488 в течение 1 часа. После промывки PBS закрепляющую среду (Vectashield (зарегистрированное торговое наименование)), содержащую DAPI, добавляют по каплям к листу, и лист закрывают покровным стеклом. Получают изображение с помощью флуоресцентного микроскопа с целью подтверждения экспрессирования ZO-1 и Na+/K+ ATPазы. Иммунологическое окрашивание осуществляют как через 48 часов, так и через 14 дней после высевания (Фиг.10 и Фиг.11).
Пример препарата 1
Среда для культивирования приготовления листа корнеального эндотелия, содержащего соединение (I)
В этом Примере, среду для культивирования, показанную ниже, приготавливают в соответствии с обычным способом и используют.
Используют FBS, производимый Invitrogen, раствор пенициллина/стрептомицина, производимый Invitrogen (содержит 5000 ед./мл пенициллина, 5000 мкг/мл стрептомицина), основной FGF производимый Invitrogen, соединение (I), производимое Mitsubishi Tanabe Pharma Corporation, и DMEM, производимую Invitrogen.
Результаты через 48 часов после высевания показывают, что ZO-1, который представляет собой показатель барьерной функции корнеального эндотелия, экспрессируется между клетками. Экспрессирование ZO-1 между клетками, как обнаружено, является однородным в группах с добавлением соединения (I) и Y-27632. Однако, в группе с добавлением ДМСО (контрольная группа), экспрессирование может быть подтверждено только в обломках клеток (Фиг.10-(A)). В дополнение к этому Na+/K+ ATPаза, которая представляет собой показатель функционирования насоса корнеального эндотелия, обнаруживается между клетками. Экспрессирование Na+/K+ ATPазы также обнаруживается между клетками во всех группах с добавлением соединения (I) и Y-27632. Однако в контрольной группе, экспрессирование может быть подтверждено только на обломках клеток (Фиг.10-(B)).
Рассмотренные выше результаты показывают, что адгезия между клетками в контрольной группе через 48 часов после высевания является недостаточной. С другой стороны, адгезия между клетками формируется в группе с лечением Y-27632 и подтверждается экспрессирование ZO-1 и Na+/K+ ATPазы, которые являются функциональными белками, в области адгезии. Однако в группе с лечением Y-27632 лист является частично не покрытым клетками и является недостаточным в качестве листа культивируемых корнеальных эндотелиальных клеток для трансплантации.
В противоположность этому, в группе с лечением соединения (I), экспрессирование ZO-1 и Na+/K+ ATPазы подтверждается в области адгезии, формируемой между клетками, и клетки прилипают ко всей поверхности листа. Таким образом, лист считается достаточно пригодным для использования в качестве листа культивируемых корнеальных эндотелиальных клеток для трансплантации. Следовательно, обнаружено, что, посредством добавления соединения (I) в среду для культивирования, лист культивируемых корнеальных эндотелиальных клеток для трансплантации может быть получен через 48 часов после добавления. Все написанное выше демонстрирует, что при использовании соединения (I) лист культивируемых корнеальных эндотелиальных клеток, пригодный для трансплантации, может быть получен на ранней стадии.
Пример 8: Воздействие терапии с инъекцией корнеальных эндотелиальных клеток кролика с использованием соединения (I) на модель кролика буллезной кератопатии
(1) Получение модели кролика буллезной кератопатии
Самцов японских белых кроликов (Biotek Co., Ltd., 8 кроликов) подвергают следующему иссечению мигательной перепонки. Каждое животное устанавливают в позиционирующее устройство, и поверхность глаза анестезируют местным образом посредством инстилляции местной анестезии (инстилляция 0,4% Benoxil, Santen Pharmaceutical Co., Ltd.). Затем корневое положение мигательной перепонки прижимают, с помощью зажима, на 30 с, и складку, образующуюся при сжатии, вырезают с помощью ножниц. После иссечения мигательной перепонки инстиллируют антибиотическую мазь (глазную мазь, таривид, Santen Pharmaceutical Co., Ltd.) для предотвращения инфекции.
Через три дня после иссечения мигательной перепонки, осуществляют хирургическую операцию на факоэмульсификационной системе и хирургическую операцию на аспирационном канале (PEA) левого глаза. Под общей анестезией, формируют 3-миллиметровый надрез в роговичном лимбе, хрусталик иссекают с помощью инструмента для хирургической операции катаракты (NIDEK Co., Ltd.), и надрез зашивают с помощью нейлоновой нити (Mani Inc.). После хирургической операции на факоэмульсификационной системе и на аспирационном канале (PEA) инстиллируют антибиотическую мазь (глазная мазь, таривид Santen Pharmaceutical Co., Ltd.) для предотвращения инфекции. Через 5 дней после PEA животных подвергают общей анестезии посредством внутримышечного введения препарата для мышечных инъекций, Ketalar (500 мг на 1 кг массы тела, DAIICHI SANKYO COMPANY, LIMITED, 0,6 мл) и Celactal 2% Injection (Bayer, Ltd., 0,25 мл). Затем инстиллируют инстилляцию 0,4% Benoxil (Santen Pharmaceutical Co., Ltd., одна капля), и глаз открывают с использованием расширителя для век. Затем формируют 1-миллиметровый надрез в роговичном лимбе, и корнеальные эндотелиальные клетки соскребывают с помощью кремниевого хирургического инструмента для механического отделения клеток. Площадь отделения подтверждают с помощью окрашивания трипаном голубым.
(2) Инъекция корнеальных эндотелиальных клеток для модели кролика буллезной кератопатии
Корнеальные эндотелиальные клетки механически соскребают, культивируемые корнеальные эндотелиальные клетки собирают с помощью 0,05% трипсин-EDTA (Invitrogen, Cat. #25300-054) из флакона для культивирования с получением суспензии клеток. Используя среду Игла, модифицированную Дюльбекко (DMEM) (Invitrogen, 12320-032), культивируемые корнеальные эндотелиальные клетки кролика суспендируют в виде 3 групп, в 10 мкМ соединения (I)/DMEM, 100 мкМ Y-27632/DMEM и DMEM, каждую - при 1,0×106 клеток/мл. Суспензию клеток каждой группы (200 мкМ (2,0×105 клеток на один глаз)) вводят как инъекцию с помощью иглы №22 в переднюю камеру глаза из роговичного лимба приготовленной модели кролика буллезной кератопатии, и кролика фиксируют с взглядом, направленным вниз, так что лицевая сторона корнеального эндотелия находится на верхней стороне, а лицевая сторона корнеального эпителия находится на нижней стороне, в течение 3 часов. Фиксирование с взглядом, направленным вниз, осуществляют при соответствующем добавлении анестетиков, уделяя достаточное внимание защите животного.
Через 14 дней после инъекции клеток леченый глаз изолируют, и ткань роговичного лимба иссекают из изолированного глазного яблока. Полученную ткань роговичного лимба фиксируют с помощью 4% параформальдегида/PBS в течение 10 мин и блокируют в течение ночи с помощью PBS (Invitrogen, Cat. #14190-144), содержащего 1% BSA (SIGMA, Cat. #A7906-50G). После этого ткань роговичного лимба разделяют на две половины и обрабатывают с помощью метящего фаллоидина Alexa-488, окрашивающего актин (Invitrogen, Cat. #A12379), или антитела анти-Na+/K+ ATPаза, которое представляет собой маркер корнеального эндотелия (UP State, Cat. #05-369), в течение 2 часов. Группу с обработкой антителом анти-Na+/K+ ATPаза дополнительно обрабатывают вторичным антителом, меченным Alexa-488 (Invitrogen, Cat. #A-21202), в течение 1 часа. После этого клетки погружают в раствор Vectashield (зарегистрированное торговое наименование)-DAPI (Vector Laboratories, Cat. #H-1200) и закрепляют с использованием покровного стекла. Образец наблюдают под конфокальным лазерным микроскопом. Окрашенные изображения показаны на Фиг.12.
Принимая количество ядер, окрашенных DAPI, в качестве отсчета корнеальных эндотелиальных клеток, изображения, окрашенные DAPI, анализируют с помощью Image-Pro plus (Media Cybernetics, Inc.) и считают корнеальные эндотелиальные клетки. Результаты показаны на Фиг.13.
По результатам окрашивания фаллоидином, обнаружено, что культивируемые корнеальные эндотелиальные клетки из инъекции развивают фиброз в контрольной группе, обработанной только лишь DMEM; однако группа с обработкой 10 мкМ соединения (I) показывает подавление фиброза в клетках таким же образом, как в группе с обработкой 100 мкМ Y-27632 (Фиг.12-(A)). В дополнение к этому, по сравнению с контрольной группой, экспрессия Na+/K+ ATPазы обнаружена в группе с обработкой 10 мкМ соединения (I) и в группе с обработкой 100 мкМ Y-27632 (Фиг.12-(B)). Корнеальные эндотелиальные клетки считают. В результате группа с обработкой 10 мкМ соединения (I) и группа с обработкой 100 мкМ Y-27632, как тенденция, показывает более высокие отсчеты клеток, чем контрольная группа, и отсчет клеток группы с обработкой 10 мкМ соединения (I) выше, чем для группы с обработкой 100 мкМ Y-27632 (Фиг.13).
Из приведенных выше результатов, соединение (I) при дозе 10 мкМ, как считается, показывает самое высокое воздействие на культивирование корнеальных эндотелиальных клеток и является наиболее пригодным для терапии с инъекций корнеальных эндотелиальных клеток.
Пример 9: Воздействие заживления повреждений соединения (I) на корнеальные эндотелиальные клетки кролика in vitro
В этом Примере используют исследуемые вещества и контрольное вещество, приготовленные таким же образом, как в Примере 4.
(1) Приготовление корнеальных эндотелиальных клеток кролика
Ткань роговичного лимба собирают из 10 глазных яблок кролика, купленных у Funakoshi Corporation. Ткань роговичного лимба погружают в DMEM (Invitrogen, Cat. #12320-032), содержащую 1% пенициллина/стрептомицина (Invitrogen, Cat. #15140-122), и инкубируют при 37°C в течение 1 ч. Десцеметову оболочку отделяют вместе с интактными корнеальными эндотелиальными клетками, погружают в среду для культивирования (DMEM, 10% FBS, 2 нг/мл bFGF (Invitrogen, Cat. #13256-029), 1% пенициллина/стрептомицина), содержащую 2 мг/мл коллагеназы A (Roche, Cat. #1088793), и инкубируют при 37°C в течение 2 часов. Клетки собирают с помощью центрифугирования, промывают средой для культивирования и высевают во флакон T25 (Corning Incorporated, Cat. #430639), покрытый смесью FNC для покрытия (Athena ES, Cat. #0407). Флакон оставляют стоять в инкубаторе при 5% CO2 при 37°C, среду заменяют каждые 2-3 дней и клетки культивируют до получения конфлюэнтности. Клетки, которые достигают конфлюэнтности, собирают, высевают в два 6-луночных планшета (Falcon, Cat. #3046), покрытых смесью FNC для покрытия, и культивируют до получения конфлюэнтности.
(2) Получение модели заживления повреждений in vitro
Приготовленные корнеальные эндотелиальные клетки кролика собирают, высевают в 6-луночный планшет при отношении разбавления 1:4 и культивируют до получения конфлюэнтности в такой же среде для культивирования, как в указанном выше пункте (1). В конфлюэнтных клетках создают линейные повреждения, используя 1000 мкл чип (6 повреждений на лунку).
(3) Добавление медицинского препарата и оценка воздействия заживления повреждений
После создания линейных повреждений среду для культивирования заменяют, и добавляют 0,95 мкМ, 1,58 мкМ и 3,16 мкМ соединения (I), 10 мкМ Y-27632 и 0,04% ДМСО. Соединение (I) и Y-27632 растворяют в ДМСО заранее, при этом концентрацию ДМСО доводят до 0,04% для них обоих.
Ширину повреждения фотографируют в разные моменты времени, через 0, 6, 12 и 24 часа после добавления. Ширину повреждения измеряют с помощью Image-Pro plus (Media Cybernetics, Inc.). Отношение ширины повреждения каждый час вычисляют, принимая ширину в 0 час после добавления медицинского препарата за 100%, и оценивают изменения отношения ширины повреждения со временем. Отношение ширины повреждения применяют для статистического анализа в соответствии с тестом Даннета в каждый момент времени. Результаты показаны на Фиг.14.
Как результат, соединение (I) при низкой концентрации (0,95 мкМ) показывает статистически значимое отличие от контроля через 6 часов после добавления медицинского препарата, доказывая высокое воздействие заживления повреждений. В дополнение к этому соединение (I) показывает статистически значимое отличие даже через 24 часа, и в это же время Y-27632 также в первый раз показывает отличие от контроля.
По этой причине, соединение (I), как считается, показывает воздействие стимулирования заживления повреждений при концентрации (0,95-1,58 мкМ) более низкое, чем у Y-27632. Хотя 1,58 мкМ соединения (I) также показывают значимое воздействие, это воздействие слабее, чем для 0,95 мкМ соединения (I). Следовательно, концентрация соединения (I), показывающая самое высокое воздействие в модели заживления повреждения in vitro, как считается, составляет примерно 0,95 мкМ.
Пример 10: Воздействие подавления гибели клеток соединения (I), добавляемого к раствору для хранения роговицы
В этом Примере используют исследуемые вещества и контрольные вещества, приготовленные таким же образом, как в Примере 4.
Как правые, так и левые глазные яблоки 5 самцов японского белого кролика (Biotek Co., Ltd.) удаляют, и приготавливают ткани роговичного лимба. Одну ткань роговичного лимба помещают в раствор для хранения Optisol-GS (зарегистрированное торговое наименование) (Bausch & Lomb, Inc) (контроль), а другую ткань роговичного лимба помещают в Optisol-GS, содержащий 0,95 мкМ соединения (I).
Подобным же образом, ткани роговичного лимба приготавливают из других 5 самцов японского белого кроликов, одну ткань роговичного лимба помещают в Optisol-GS (контроль), а другую ткань роговичного лимба помещают в Optisol-GS, содержащий 10 мкМ Y-27632.
Образцы, содержащие каждую ткань роговичного лимба, консервируют при 4°C. Через две или три недели, ткани роговичного лимба окрашивают Hoechst (Hoechst 33342, Sigma, Cat. #B2261), PI (пропидий йодид, Sigma, Cat. #P4170) и Annexin V (Annexin V-FITC, MBL, Cat. #4700-100), и клетки в них идентифицируют как живые клетки, погибшие клетки и апоптотические клетки. Окрашенные изображения тканей роговичного лимба в образцах через 3 недели показаны на Фиг.15. В дополнение к этому, различные клетки в окрашенной роговице считают с использованием Image J (ver.1.44i, NIH, http://imagej.nih.gov/ij) и определяют среднее значение и стандартное отклонение для 5 полей зрения. Различные отсчеты клеток статистически анализируют с помощью t-теста Стьюдента. Результаты через 2 недели показаны на Фиг.16, а результаты через 3 недели показаны на Фиг.17.
Как результат, количество погибших клеток в растворе для хранения, содержащем соединение (I), значительно понижается через 2 недели по сравнению с контролем. Результаты через 3 недели показывают, что количества, как погибших клеток, так и апоптотических клеток, значительно понижаются по сравнению с контролем, когда используют раствор для хранения, содержащий соединение (I). В противоположность этому, когда используют раствор для хранения, содержащий Y-27632, значительно уменьшается только количество погибших клеток.
Приведенные выше результаты показывают, что посредством добавления соединения (I) к раствору для хранения, гибель клеток и апоптоз может подавляться более значительно, чем с помощью обычных растворов для хранения. Кроме того, продемонстрировано, что соединение (I) показывает воздействие при концентрации более низкой, чем для Y-27632.
Настоящая заявка основана на заявке на патент № 2009-299180 (дата подачи: 29 декабря 2009 года), поданной в Японии, и на Международной заявке № PCT/JP2010/071424 (дата подачи: 24 ноября 2010 года), содержание которых включается полностью в настоящий документ в качестве ссылок.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ СОДЕЙСТВИЯ АДГЕЗИИ РОГОВИЧНЫХ ЭНДОТЕЛИАЛЬНЫХ КЛЕТОК | 2008 |
|
RU2474434C2 |
| НОВОЕ ЛЕЧЕНИЕ РОГОВИЦЫ С ПРИМЕНЕНИЕМ ЛАМИНИНА | 2015 |
|
RU2718062C2 |
| СТИМУЛЯТОР ОБРАЗОВАНИЯ НЕЙРИТОВ | 2008 |
|
RU2442582C2 |
| ГЛАЗНЫЕ КАПЛИ "ИНТЕРТОНИК" | 1997 |
|
RU2121825C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ КЕРАТОКОНЪЮНКТИВАЛЬНЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2659203C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ, СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ОТЕКА РОГОВИЦЫ И ДРУГИХ ПРОЯВЛЕНИЙ РАННЕЙ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2008 |
|
RU2357743C1 |
| РАСТВОР ДЛЯ ХРАНЕНИЯ РОГОВИЦЫ, ВКЛЮЧАЮЩИЙ ГИАЛУРОНОВУЮ КИСЛОТУ, СПОСОБ ХРАНЕНИЯ ТКАНИ РОГОВИЦЫ | 1997 |
|
RU2184448C2 |
| ЛЕЧЕНИЕ АТЕРОСКЛЕРОЗА И ДРУГИХ СЕРДЕЧНО-СОСУДИСТЫХ И ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 1995 |
|
RU2235541C2 |
| ПРИМЕНЕНИЕ ЛАМИНИНА В КУЛЬТУРЕ КЛЕТОК ЭНДОТЕЛИЯ РОГОВИЦЫ | 2014 |
|
RU2704984C1 |
| Способ получения донорского трансплантата Десцеметовой мембраны с эндотелиальным слоем | 2022 |
|
RU2786330C1 |

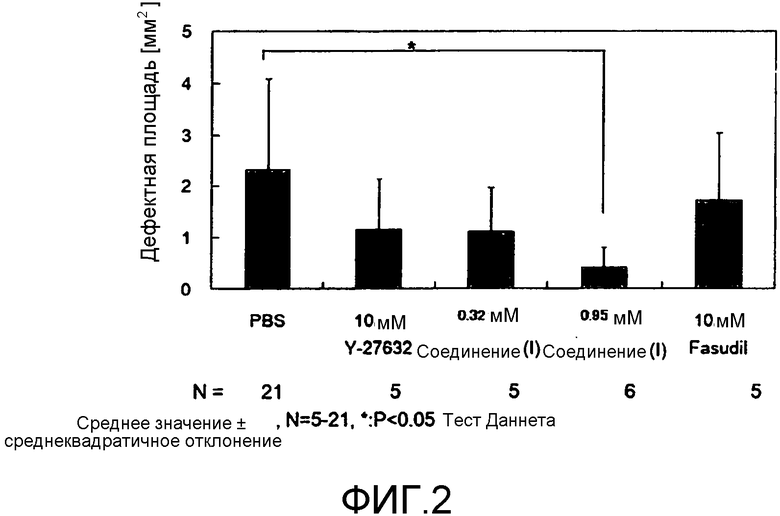
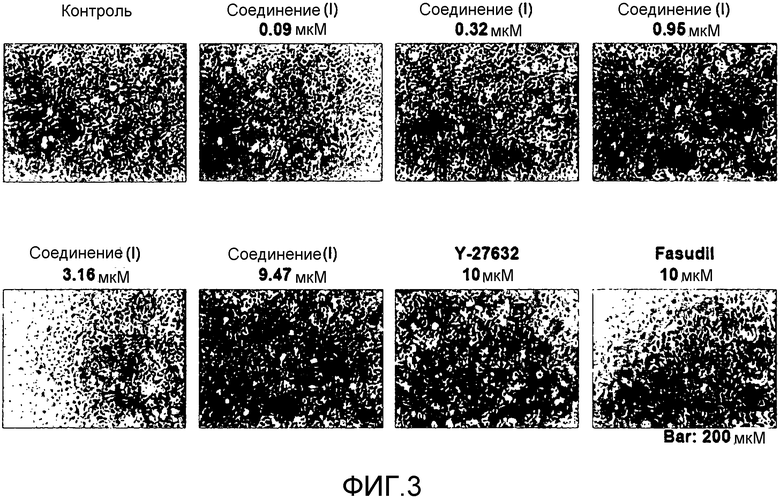
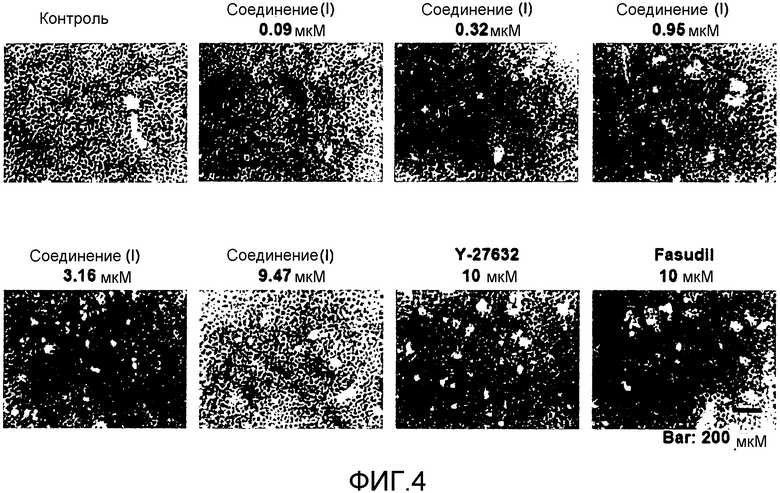
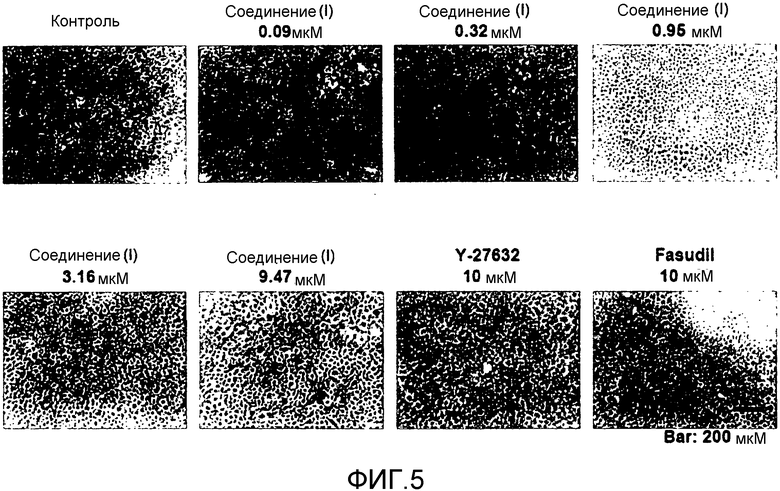
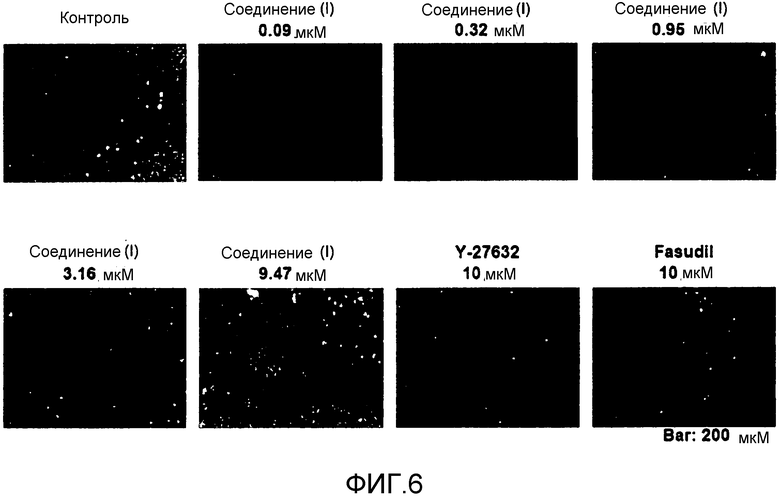
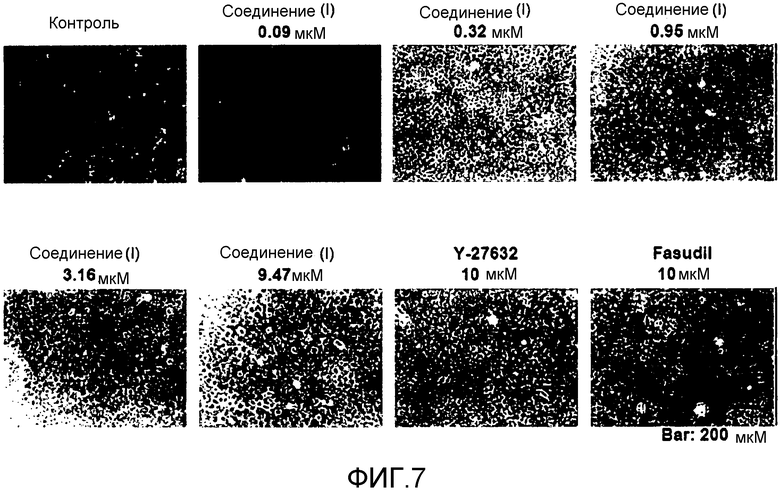
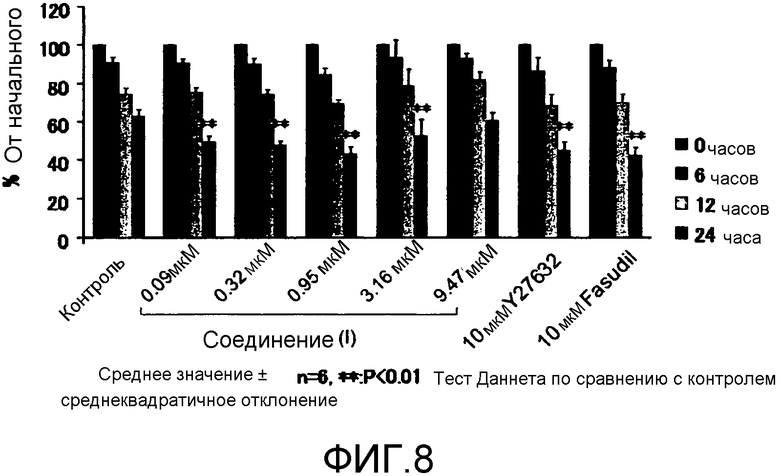
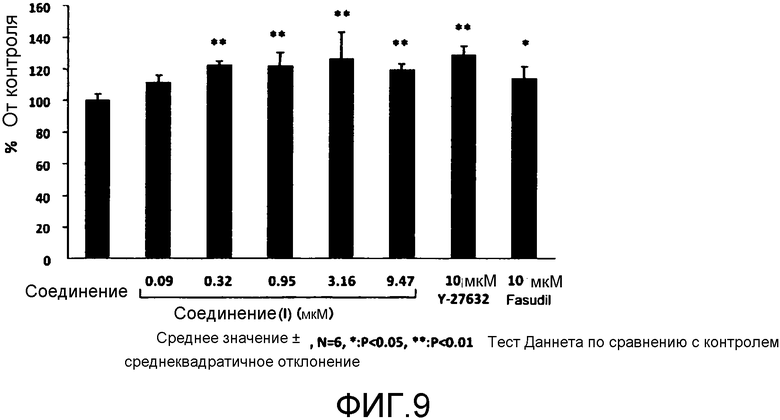




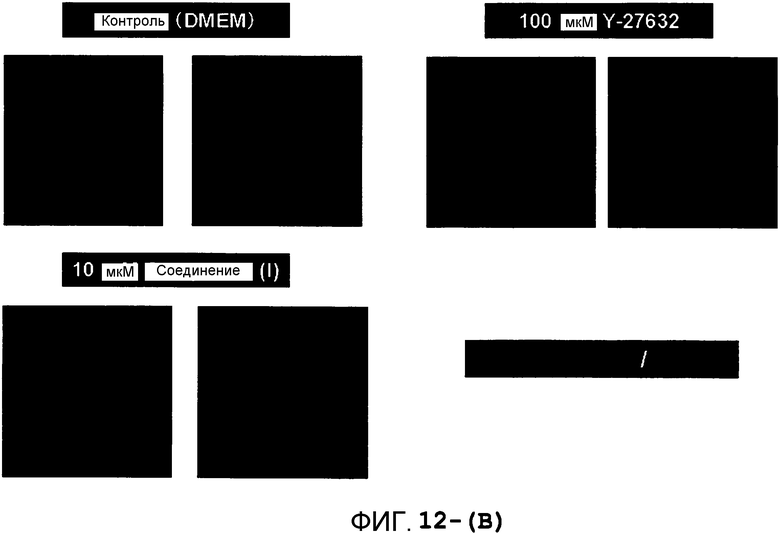
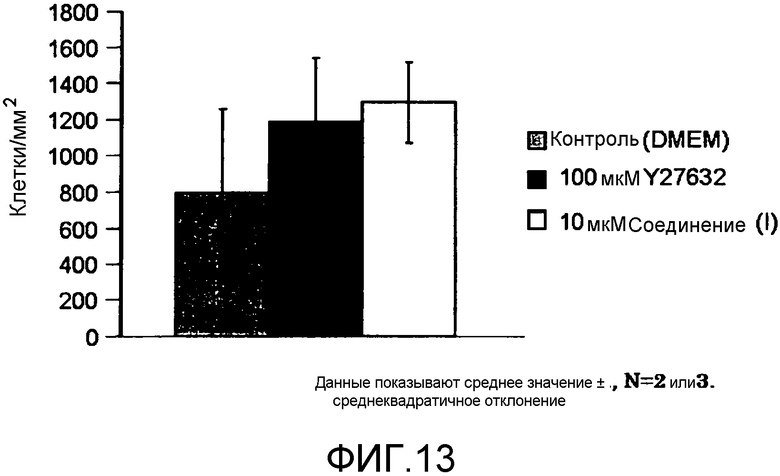
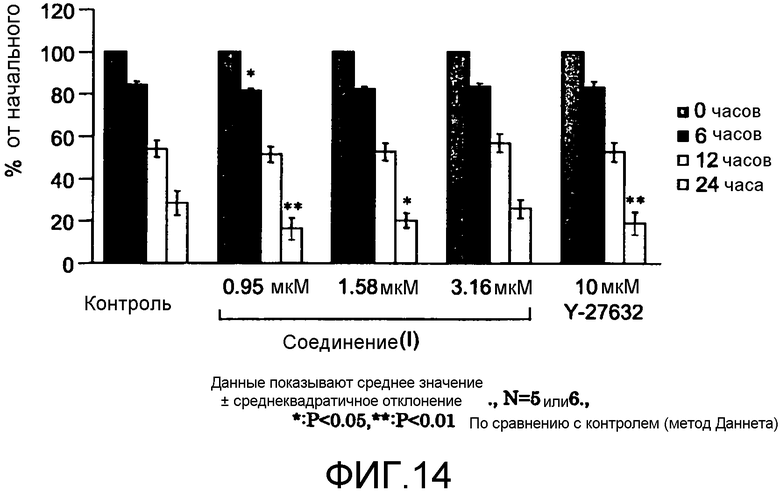

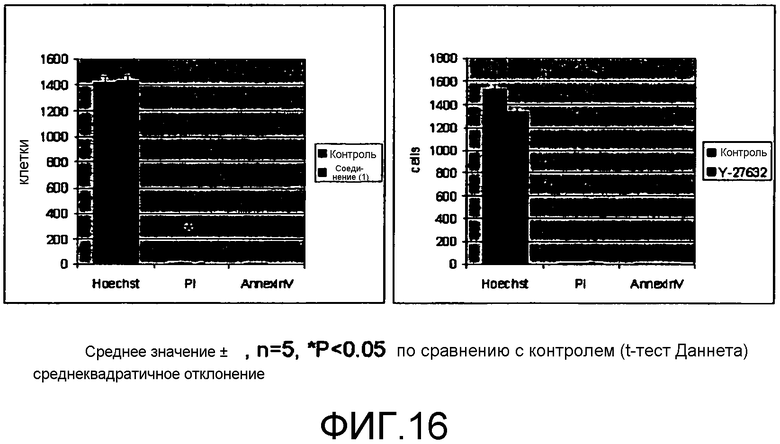
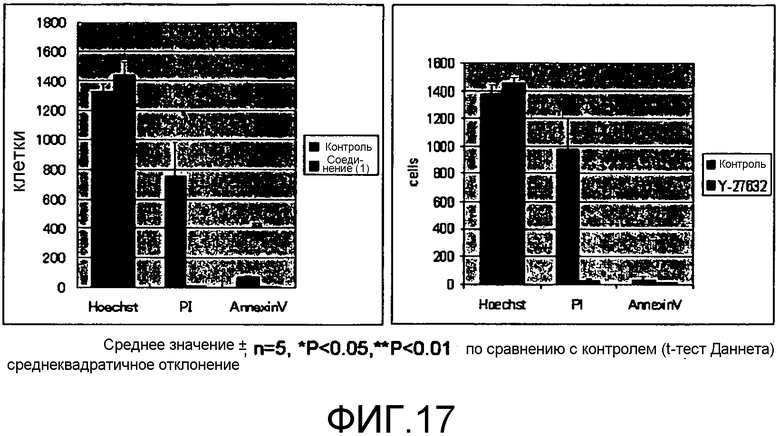
Группа изобретений относится к медицине. Терапевтический агент против корнеальной эндотелиальной дисфункции, содержащий (R)-(+)-N-(1H-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид <Y-39983> или его фармакологически приемлемую соль (соединение (Ia)) в качестве активного ингредиента, агент для стимулирования адгезии корнеальных эндотелиальных клеток, содержащий соединение (Ia), среду для культивирования корнеальных эндотелиальных клеток, содержащую агент для стимулирования адгезии, имплант для корнеальной эндотелиальной кератопластики, содержащий корнеальные эндотелиальные клетки, каркас и соединение (Ia), и способ получения корнеального эндотелиального препарата, включающий стадию культивирования корнеальных эндотелиальных клеток с использованием среды для культивирования. Средство используется для эффективного и удобного лечения заболеваний, когда повреждаются корнеальные эндотелиальные клетки с ухудшением пролиферативной способности in vivo. 13 н. и 8 з.п. ф-лы, 17 ил., 10 пр.
1. Терапевтический препарат против корнеальной эндотелиальной дисфункции, содержащий (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль в качестве активного ингредиента.
2. Терапевтический препарат по п. 1, который представляет собой глазные капли.
3. Агент для стимулирования адгезии корнеальных эндотелиальных клеток, содержащий (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль.
4. Среда для культивирования корнеальных эндотелиальных клеток, содержащая агент по п. 3.
5. Имплант для корнеальной эндотелиальной кератопластики, содержащий
A) корнеальные эндотелиальные клетки,
B) каркас и
C) (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль.
6. Имплант по п. 5, где получают корнеальные эндотелиальные клетки людей.
7. Способ получения корнеального эндотелиального препарата, включающий стадию культивирования корнеальных эндотелиальных клеток с использованием среды для культивирования, содержащей (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль.
8. Способ получения по п. 7, где получают корнеальные эндотелиальные клетки людей.
9. Способ лечения корнеальной эндотелиальной дисфункции, включающий стадию получения корнеального эндотелиального препарата и/или импланта для корнеальной эндотелиальной кератопластики, каждый из которых содержит (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамид или его фармакологически приемлемую соль, и стадию трансплантации корнеального эндотелиального препарата и/или импланта для корнеальной эндотелиальной кератопластики субъекту, нуждающемуся в корнеальной эндотелиальной кератопластике.
10. Способ по п. 9, где получают корнеальные эндотелиальные клетки людей.
11. Способ лечения корнеальной эндотелиальной дисфункции, включающий стадию введения эффективного количества (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли субъекту, нуждающемуся в заживлении корнеального эндотелиального повреждения.
12. Способ по п. 11, где стадия введения представляет собой местную инстилляцию.
13. Применение (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли для получения терапевтического агента против корнеальной эндотелиальной дисфункции.
14. Применение по п. 13, где терапевтический агент представляет собой глазные капли.
15. Применение (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли для получения агента для стимулирования адгезии корнеальных эндотелиальных клеток.
16. Применение (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли для получения среды для культивирования корнеальных эндотелиальных клеток.
17. Применение
A) корнеальных эндотелиальных клеток,
B) каркаса и
C) (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли для получения импланта для корнеальной эндотелиальной кератопластики.
18. Применение по п. 17, где получают корнеальные эндотелиальные клетки человека.
19. Корнеальный эндотелиальный препарат, полученный с помощью способа получения по п. 7 или 8.
20. Способ защиты эндотелия роговицы глаза, включающий стадию введения эффективного количества (R)-(+)-N-(1Н-пирроло[2,3-b]пиридин-4-ил)-4-(1-аминоэтил)бензамида или его фармакологически приемлемой соли субъекту, нуждающемуся в защите эндотелия роговицы глаза.
21. Способ по п. 20, где глаз является глазом человека.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2015-09-20—Публикация
2010-12-28—Подача