Область техники, к которой относится изобретение
Настоящее изобретение имеет отношение к усовершенствованным иммуноглобулинам и конъюгатам иммуноглобулинов.
Уровень техники
Моноклональные антитела имеют широкое лабораторное и терапевтическое применение. Разработаны и в течение многих лет применяются производные антител с искусственными свойствами сайт-специфической флуоресценции или связывания. Совсем недавно стали разрабатывать антитела в качестве терапевтических агентов, представляющих сейчас наиболее быстро растущий класс фармацевтических препаратов [1]. Антитела являются мультидоменными белками из двух легких и двух тяжелых цепей, соединенных дисульфидными связями. Вариабельные участки определяют связывание с определенным антигеном, а часть константных участков ответственна за эффекторные функции через связывание с Fc-рецепторами на поверхности иммунных клеток. Вследствие своего потенциала при лечении различных заболеваний, в настоящее время антитела составляют наиболее быстро растущий класс лекарственных препаратов для человека (Carter. Nature Reviews Immunology. 2006, 6(5), 343). С 2001 г. их рынок рос со средней скоростью 35% в год, что составляет самую высокую скорость среди всех категорий биотехнологических препаратов (S. Aggarwal. Nature. BioTech. 2007, 25(10), 1097).
Конструирование конъюгатов антител еще больше увеличило многосторонность применения антител. Во многих лабораторных методах ферменты или флуоресцентные зонды конъюгируют с антителами для выполнения измерительной функции, к примеру, количественного определения антигена. В случае прицельной терапии к антителам прикрепляют небольшие токсические молекулы, которые специфически связываются с биомаркерами на пораженных клетках [2-4]. Предпринимались различные подходы к конъюгации антител, прикрепление к поверхностным лизинам [5], к углеводам Fc [6] или к частично восстановленным межцепочечным дисульфидам [7].
Конъюгация антител по встроенным на поверхности цистеинам остается наиболее привлекательным вариантом, так как большинство антител не имеют других цистеинов, кроме тех, что задействованы во внутри- и межцепочечных дисульфидных связях. По специфическим сайтам замещения цистеинов могут прикрепляться небольшие молекулы через реакционноспособные тиолы типа малеимидов [8-14]. Предпочтительным было конструирование в доменах CH1 и CH3, чтобы избежать интерференции со связыванием антигена в вариабельных участках и эффекторной функцией CH2. Рассматривались различные критерии для успешной конъюгации антител через встроенные цистеины. Следует учитывать такие параметры, как домен антитела, в который вводится мутация, доступность мутированного сайта, подлежащие замене аминокислоты. Был разработан подход с высокопроизводительным скринингом для идентификации сайтов, пригодных для встраивания цистенов и конъюгации [15]. Две наиболее общие проблемы, связанные с цистеновыми вариантами антител, это олигомеризация и слабое включение метки. Однако не существует универсального инструмента для предсказания того, будет ли цистеиновый вариант антитела стабильным и эффективно конъюгироваться. Более того, в настоящее время цистеиновые варианты существуют только для доменов CL, CH1 и CH3 [8, 9, 11, 12, 15].
Таким образом, имеется потребность в дополнительных цистеиновых вариантах иммуноглобулинов, которые можно использовать для создания стабильных конъюгатов иммуноглобулинов.
Сущность изобретения
В настоящем изобретении описаны усовершенствованные иммуноглобулины и конъюгаты иммуноглобулинов с пониженным перекрестным сшиванием, которые удовлетворяют эту потребность.
Итак, один аспект охватывает конъюгаты иммуноглобулинов, содержащие по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL), 25(VH), 125(CH1), 248(CH2), 254(CH2), 286(CH2), 298(CH2) и 326(CH2), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина, и атом или молекулу, которые конъюгированы с остатком цистеина. В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 248(CH2) и 326(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 25(VH) и 286(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 254(CH2) и 298(VH). В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин выбирается из группы, содержащей IgG1, IgG2, IgG3 и IgG4. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает IgG1. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CH1 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CH2 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CH3 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен VH человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен VL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина дополнительно включает молекулу линкера, имеющую по меньшей мере два реакционноспособных сайта, причем первый реакционноспособный сайт связан с остатком цистеина иммуноглобулина, а второй реакционноспособный сайт связан с атомом или молекулой. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, содержащими молекулу линкера, молекула линкера выбирается из группы, состоящей из гидразона, дисульфида, пептида, хелатирующего агента и малеимида. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула выбираются из группы, состоящей из радионуклида, химиотерапевтического агента, микробного токсина, растительного токсина, полимера, углевода, цитокина, флуоресцентной метки, люминесцентной метки, фермент-субстратной метки, фермента, пептида, пептидомиметика, нуклеотида, siPHK, микроРНК, РНК-миметика и аптамера. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула выбираются из группы, состоящей из 90Y, 131I, 67Cu, 177Lu, 213Bi, 211At, калихеамицина, дуокармицина, майтансиноида, ауристатина, антрациклина, экзотоксина A Pseudomonas, дифтерийного токсина, рицина, полиэтиленгликоля, гидроксиэтил-крахмала и остатка маннозила. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула снижает иммуногенность немутированного иммуноглобулина. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула повышает иммуногенность немутированного иммуноглобулина. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина дополнительно обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
Другой аспект охватывает модифицированные или выделенные иммуноглобулины, содержащие по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL), 25(VH), 125(CH1), 248(CH2), 254(CH2), 286(CH2) и 326(CH2), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина. В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 248(CH2) и 326(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 25(VH) и 286(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток 254(CH2). В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин выбирается из группы, содержащей IgG1, IgG2, IgG3 и IgG4. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает IgG1. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CH1 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CH2 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CH3 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен VH человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен VL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина дополнительно обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
Следующий аспект охватывает выделенные или рекомбинантные полинуклеотиды, кодирующие иммуноглобулины из предыдущего аспекта по модифицированным иммуноглобулинам и всевозможных комбинаций предыдущих воплощений. В некоторых воплощениях полинуклеотид находится в векторе. В некоторых воплощениях вектор является экспрессионным вектором. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, с полинуклеотидом функционально связан индуцибельный промотор. Следующий аспект охватывает клетки хозяина с вектором из любого из предыдущих воплощений. В некоторых воплощениях клетки хозяина способны экспрессировать иммуноглобулин, кодируемый полинуклеотидом.
Следующий аспект охватывает способы получения иммуноглобулинов, включающие обеспечение культуральной среды, содержащей клетки хозяина из предыдущего аспекта, и помещение культуральной среды в условия, при которых экспрессируется иммуноглобулин. В некоторых воплощениях способы включают дополнительную стадию выделения экспрессированного иммуноглобулина.
Следующий аспект охватывает способы получения конъюгатов иммуноглобулинов, включающие обеспечение иммуноглобулина из предыдущего аспекта по модифицированным иммуноглобулинам и всевозможных комбинаций предыдущих воплощений, восстановление одного или нескольких замененных остатков цистеина с помощью восстановителя с образованием восстановленных остатков цистеина, и инкубирование иммуноглобулина с атомом или молекулой, причем атом или молекула реагирует с восстановленными остатками цистеина с образованием конъюгата иммуноглобулина.
Следующий аспект охватывает способы снижения перекрестного сшивания между выходящими на поверхность цистеинами иммуноглобулина в сильно концентрированной композиции конъюгатов иммуноглобулина, включающие обеспечение иммуноглобулина, замену остатка, выбранного из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), на остаток цистеина, восстановление одного или нескольких замененных остатков цистеина с помощью восстановителя с образованием восстановленных остатков цистеина, инкубирование иммуноглобулина с атомом или молекулой, причем атом или молекула реагирует с восстановленными остатками цистеина с образованием конъюгата иммуноглобулина, и формирование сильно концентрированной, жидкой композиции конъюгата иммуноглобулина, в которой концентрация конъюгата иммуноглобулина составляет по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях иммуноглобулин выбирается из группы, содержащей IgG1, IgG2, IgG3 и IgG4. В некоторых воплощениях иммуноглобулин включает IgG1. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CH1 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CH2 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CH3 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен VH человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен VL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
Следующий аспект охватывает применение конъюгата иммуноглобулина из предыдущего аспекта и всевозможных комбинаций предыдущих воплощений при получении медикамента, включающего сильно концентрированную жидкую лекарственную форму, в которой концентрация конъюгата иммуноглобулина составляет по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях медикамент предназначается для лечения аутоиммунных заболеваний, иммунологических заболеваний, инфекционных заболеваний, воспалительных заболеваний, неврологических заболеваний и онкологических и неопластических заболеваний, включая рак. В некоторых воплощениях медикамент предназначается для лечения застойной сердечной недостаточности (CHF), васкулита, красных угрей, угрей, экземы, миокардита и других заболеваний миокарда, системной красной волчанки, диабета, спондилопатии, потери синовиальных фибробластов и стромы костного мозга, потери костной массы, болезни Паже, остеокластомы; рака молочной железы; остеопении от бездействия; истощения, перидонтальных заболеваний, болезни Гоше, гистиоцитоза клеток Лангерганса, повреждения спинного мозга, острого септического артрита, размягчения костей, синдрома Кушинга, монооссальной фиброзной дисплазии, полиоссальной фиброзной дисплазии, периодонтальной реконструкция и перелома костей; саркоидоза, остеолитического рака костей, рака молочной железы, рака легких, рака почек и рака прямой кишки; костных метастазов, лечения боли в костях и гуморальной злокачественной гиперкальцемии, анкилозного спондилита и других спондилоартропатий; отторжения трансплантата, вирусных инфекций, гематологических неоплазий и неопластических заболеваний, лимфомы Ходжкина; неходжкинских лимфом (лимфомы Буркитта, мелкоклеточной лимфоцитарной лимфомы/хронического лимфолейкоза, фунгоидной гранулемы, мантиеклеточной лимфомы, фолликулярной лимфомы, диффузной крупно-В-клеточной лимфомы, лимфомы маргинальной зоны, волосковоклеточной лейкемии и лимфоплазмацитарной лейкемии), опухолей клеток-предшественников лимфоцитов, включая В-клеточную острую лимфобластическую лейкемию/лимфому и Т-клеточную острую лимфобластическую лейкемию/лимфому, тимомы, опухолей зрелых Т- и NK- (натуральных киллеров) клеток, включая лейкемию периферических Т-клеток, лейкемию/лимфому взрослых Т-клеток и лейкемию больших гранулярных лимфоцитов, гистиоцитоза клеток Ларгенганса, миелоидных неоплазий типа острой миелогенной лейкемии, включая AML с созреванием, AML без дифференцировки, острую промиелоцитную лейкемию, острую миеломоноцитарную лейкемию и острую моноцитарную лейкемию, миелодиспластических синдромов и хронических миелопролиферативных заболеваний, включая хроническую миелогенную лейкемию, опухолей центральной нервной системы, например, опухолей мозга (глиомы, нейробластомы, астроцитомы, медуллобластомы, эпендимомы и ретинобластомы), солидных опухолей (назофарингеального рака, базальноклеточной карциномы, рака поджелудочной железы, рака желчных протоков, саркомы Капоши, рака яичек, рака матки, влагалища или шейки матки, рака яичников, первичного рака печени или рака эндометрия и опухолей сосудистой системы (ангиосаркомы и гемангиоперицитомы), остеопороза, гепатита, ВИЧ, СПИД, спондилоартрита, ревматоидного артрита, воспалительных заболеваний кишечника (IBD), сепсиса и септического шока, болезни Крона, псориаза, склеродермы, реакции "трансплантат против хозяина" (GVHD), отторжения аллогенных трансплантатов островков, гематологических раковых заболеваний, как-то множестенной миеломы (ММ), миелодиспластическего синдрома (MDS) и острой миелогенной лейкемии (AML), воспаления, связанного с опухолями, повреждения периферических нервов или демиелинизирующих заболеваний. В некоторых воплощениях медикамент предназначается для лечения чешуйчатого псориаза, язвенного колита, неходжкиновской лимфомы, рака молочной железы, рака толстой и прямой кишки, ювенильного идиопатического артрита, дистрофии желтого пятна, респираторно-синцитиального вируса, болезни Крона, ревматоидного артрита, псориазного артрита, анкилозного спондилита, остеопороза, потери костной ткани в результате лечения, костных метастазов, множественной миеломы, болезни Альцгеймера, глаукомы и рассеянного склероза. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, медикамент дополнительно содержит фармацевтически приемлемый эксципиент. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, композиция содержит по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина в виде неолигомеризованного мономера. В некоторых воплощениях содержание мономера измеряется методом SDS-PAGE в невосстанавливающих условиях.
Следующий аспект охватывает применение конъюгатов иммуноглобулинов из предыдущего аспекта и всевозможных комбинаций предыдущих воплощений в качестве не подверженного олигомеризации фармацевтически активного ингредиента.
Следующий аспект охватывает применение конъюгатов иммуноглобулинов из предыдущего аспекта и всевозможных комбинаций предыдущих воплощений в качестве диагностического инструмента.
Следующий аспект охватывает применение конъюгатов иммуноглобулинов из предыдущего аспекта и всевозможных комбинаций предыдущих воплощений в качестве стандарта для высокомолекулярных белков. Другой аспект охватывает применение конъюгатов иммуноглобулинов в качестве стандарта для высокомолекулярных белков, при этом конъюгат иммуноглобулина содержит иммуноглобулин, содержащий по меньшей мере одну мутацию по остатку 440(CH3), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина, и атом или молекулу, причем атом или молекула конъюгирована с остатком цистеина.
Следующий аспект охватывает фармацевтические композиции, которые содержат конъюгат иммуноглобулина из предыдущего аспекта и всевозможных комбинаций предыдущих воплощений и фармацевтически приемлемый эксципиент. В некоторых воплощениях конъюгат иммуноглобулина содержится в концентрации по меньшей мере 10 мг/мл, по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, композиция содержит по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина в виде неолигомеризованного мономера.
Следующий аспект охватывает способы отбора остатков иммуноглобулина для мутации на цистеин, включающие вычисление склонности к пространственной агрегации первого аминокислотного остатка на поверхности иммуноглобулина, вычисление склонности к пространственной агрегации нескольких (множества) остатков иммуноглобулина в непосредственной близости от первого остатка и выбор первого аминокислотного остатка для мутации на цистеин, если склонность к пространственной агрегации первого аминокислотного остатка равна или находится между значениями 0 и -0,11 и если множество остатков имеют значения склонности к пространственной агрегации меньше 0. В некоторых воплощениях множество остатков находится в пределах 15Å от первого остатка. В некоторых воплощениях множество остатков находится в пределах 10Å от первого остатка. В некоторых воплощениях множество остатков находится в пределах 7,5Å от первого остатка. В некоторых воплощениях множество остатков находится в пределах 5Å от первого остатка. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, вычисление склонности к пространственной агрегации остатка включает вычисление склонности к пространственной агрегации для сферического участка с радиусом из центра одного атома в этом остатке. В некоторых воплощениях радиус сферического участка составляет по меньшей мере 5Å.
Следующий аспект охватывает модифицированные или выделенные иммуноглобулины, содержащие по меньшей мере одну мутацию выходящего на поверхность остатка на цистеин, при этом склонность к пространственной агрегации первого аминокислотного остатка равна или находится между значениями 0 и -0,11, а множество остатков иммуноглобулина в непосредственной близости от первого остатка имеют значения склонности к пространственной агрегации меньше 0. В некоторых воплощениях множество остатков находится в пределах 15Å от первого остатка. В некоторых воплощениях множество остатков находится в пределах 10Å от первого остатка. В некоторых воплощениях множество остатков находится в пределах 7,5Å от первого остатка. В некоторых воплощениях множество остатков находится в пределах 5Å от первого остатка. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, склонность к пространственной агрегации рассчитывают для сферического участка с радиусом из центра одного атома в этом остатке. В некоторых воплощениях радиус составляет по меньшей мере 5Å.
Следующий аспект охватывает способы отбора остатков иммуноглобулина для мутации на цистеин, включающие выбор нескольких (множества) аминокислотных остатков иммуноглобулина, причем это множество остатков выходит на поверхность иммуноглобулина, мутирование одного остатка из множества остатков на остаток цистеина, конъюгирование остатка цистеина с атомом или молекулой с образованием конъюгата иммуноглобулина, тестирование конъюгата иммуноглобулина на склонность к перекрестному сшиванию и присвоение конъюгату иммуноглобулина значения склонности к перекрестному сшиванию и отбор остатка для мутации на цистеин, если значение склонности к перекрестному сшиванию составляет I или II. В некоторых воплощениях способ дополнительно включает присвоение конъюгату иммуноглобулина значения склонности к перекрестному сшиванию II, если менее 5% конъюгатов иммуноглобулина образуют димеры и конъюгаты иммуноглобулина совсем не образуют тримеров, при этом образование димеров и тримеров измеряется сравненительным SDS-PAGE в восстанавливающих и невосстанавливающих условиях. В некоторых воплощениях способ дополнительно включает присвоение конъюгату иммуноглобулина значения склонности к перекрестному сшиванию I, если менее 1% конъюгатов иммуноглобулина образуют димеры, при этом образование димеров измеряется сравненительным SDS-PAGE в восстанавливающих и невосстанавливающих условиях.
Другие аспекты и воплощения изобретения встречаются по всему описанию.
Осуществление изобретения
Настоящее описание касается усовершенствованных иммуноглобулинов и конъюгатов иммуноглобулинов, проявляющих пониженное перекрестное сшивание. В некоторых воплощениях иммуноглобулины изобретения подвергаются модификации по определенным остаткам путем замены на цистеин. Изобретение обеспечивает модифицированные иммуноглобулины и конъюгаты иммуноглобулинов, способы получения таких иммуноглобулинов и конъюгатов иммуноглобулинов, мультивалентные или мультиспецифичные молекулы, содержащие такие иммуноглобулины, и фармацевтические композиции, содержащие иммуноглобулины, конъюгаты иммуноглобулинов или биспецифичные молекулы изобретения.
Определения
Термин "антитело" или "иммуноглобулин" в настоящем изобретении включают целые антитела и любые их антигенсвязывающие фрагменты (т.е. "антигенсвязывающие части") или отдельные цепи. "Антитело" естественного происхождения представляет собой гликопротеин, содержащий по меньшей мере две тяжелые (Н) и две легкие (L) цепи, соединенные между собой дисульфидными связями. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращенно VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов, CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращенно VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена, CL. Области VH и VL можно еще подразделить на участки гипервариабельности, именуемые участками, определяющими комплементарность (CDR), которые перемежаются с более консервативными участками, именуемыми каркасными участками (FR). Каждый VH и VL состоит из трех CDR и четырех FR, расположенных с N-конца до С-конца в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепей содержат домен связывания, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, включая различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (C1q) классической системы комплемента.
Термины "конъюгат антитела" или "конъюгат иммуноглобулина" в настоящем изобретении включают любые иммуноглобулины, их антигенсвязывающие фрагменты или отдельные цепи, химически или биологически соединенные с атомом или молекулой. Атомы или молекулы могут включать, к примеру, цитотоксины, радиоактивные агенты, противоопухолевые препараты или терапевтические агенты. Конъюгат антитела сохраняет иммунореактивность иммуноглобулина или антигенсвязывающего фрагмента, т.е. иммуноглобулин или антигенсвязывающий фрагмент конъюгата антител обладает по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности иммуноглобулина до его конъюгации с атомом или молекулой.
Термин "антигенсвязывающая часть" антитела (или просто "антигенная часть") в настоящем изобретении относится к полному антителу либо к одному или нескольким фрагментам антитела, сохраняющим способность к специфическому связыванию с антигеном, и по меньшей мере части константной области тяжелой или легкой цепи. Было показано, что антигенсвязывающая функция антитела может выполняться фрагментами полноразмерного антитела. Примеры связывающих фрагментов, охваченных термином "антигенсвязывающая часть" антитела, включают Fab-фрагмент - одновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; F(ab)2-фрагмент - двухвалентный фрагмент, содержащий два Fab-фрагмента, соединенные дисульфидным мостиком в шарнирном участке; Fd-фрагмент, состоящий из доменов VH и CH1; и Fv-фрагмент, состоящий из доменов VL и VH одного плеча антитела.
Более того, хотя два домена Fv-фрагмента, VL и VH, кодируются отдельными генами, их можно соединить с применением рекомбинантных методов, с помощью синтетического линкера, что дает возможность получать их в виде единой белковой цепи, в которой области VL и VH сочетаются с образованием одновалентной молекулы (известной как одноцепочечный Fv (scFv); например, см. Bird et al., 1988 Science 242:423-426; и Huston et al., 1988 Proc. Natl. Acad. Sci. 85:5879-5883). Такие одноцепочечные антитела также охватываются термином "антигенсвязывающий участок" антитела. Эти фрагменты антител получают с применением стандартных методик, известных специалистам в данной области, и фрагменты подвергают скринингу на пригодность таким же образом, как и интактные антитела.
"Выделенное" антитело или иммуноглобулин в настоящем изобретении означает антитело или иммуноглобулин, которые практически свободны от других компонентов, в которых эти антитела или иммуноглобулины встречаются в природе. Более того, выделенные антитела или иммуноглобулины могут быть практически свободны от других клеточных материалов и/или химикатов.
Термины "моноклональное антитело" или "композиция моноклонального антитела" в настоящем изобретении относятся к препаратам молекул антител, состоящим из одного вида молекул. Композиция моноклонального антитела обычно проявляет единственную специфичность связывания и сродство к определенному эпитопу,
Термин "антитело человека" в настоящем изобретении охватывает антитела, содержащие вариабельные области, у которых и каркасные, и CDR-участки происходят из последовательностей человека. Кроме того, если антитело содержит константную область, то оно тоже происходит из таких последовательностей человека, напр., последовательностей зародышевой линии человека или мутированных версий последовательностей зародышевой линии человека либо антител, содержащих консенсусные каркасные последовательности, выведенные при анализе каркасных последовательностей человека, как описано в Knappik et al. (2000. J Mol Biol 296, 57-86).
Антитела человека по изобретению могут включать аминокислотные остатки, не кодируемые последовательностями человека (например, мутации, введенные при случайном или сайт-специфическом мутагенезе in vitro или при соматической мутации in vivo). Однако термин "антитело человека" в настоящем изобретении не предусматривает включение антител, у которых в каркасные последовательности человека вставлены последовательности CDR, полученные из последовательностей зародышевой линии других видов млекопитающих типа мыши.
Термин «домен человека» в настоящем изобретении охватывает иммуноглобулиновые домены константной области, произошедшие от человека например, из зародышевой линии человека, иммуноглобулинов человека, например, последовательностей зародышевой линии человека или мутированных версий последовательностей зародышевой линии человека либо антител, содержащих консенсусные каркасные последовательности, выведенные при анализе каркасных последовательностей человека, как описано в Knappik et al. (2000. J Mol Biol 296, 57-86).
Термин "рекомбинантное антитело человека" в настоящем изобретении включает все антитела человека, полученные, экспрессированные, созданные или выделенные рекомбинантными методами, как-то антитела, выделенные из животных (например, мыши), трансгенных или трансхромосомных по генам иммуноглобулинов человека, или из полученной из них гибридомы, антитела, выделенные из клеток хозяина, трансформированных для экспрессии антител человека, например, из трансфектомы, антитела, выделенные из рекомбинантной, комбинаторной библиотеки антител человека, и антитела, полученные, экспрессированные, созданные или выделенные любым другим способом, включающим сплайсинг всех или части последовательностей генов иммуноглобулинов человека на другие последовательности ДНК. Такие рекомбинантные антитела человека содержат вариабельные области, в которых каркасные и CDR-участки происходят из последовательностей иммуноглобулинов зародышевой линии человека. Однако в некоторых воплощениях такие рекомбинантные антитела человека могут подвергаться мутагенезу in vitro (а при использовании животных, трансгенных по последовательностям Ig человека, - соматическому мутагенезу in vivo), при этом аминокислотные последовательности областей VH и VL рекомбинантных антител имеют последовательности, которые, хотя они и происходят из и относятся к последовательностям VH и VL зародышевой линии человека, в природе могут и не встречаться в репертуаре антител зародышевой линии человека in vivo.
"Химерное антитело" есть такая молекула антитела, в которой (а) константная область или ее часть изменена, заменена или замещена таким образом, что антиген-связывающий сайт (вариабельная область) соединяется с константной областью другого или измененного класса, эффекторной функции и/или вида либо с совершенно другой молекулой, придающей новые свойства химерному антителу, например, ферментом, токсином, гормоном, фактором роста, лекарством и т.д.; или (b) вариабельная область или ее часть изменена, заменена или замещена на вариабельную область, обладающую другой или измененной антигенной специфичностью, мышиное антитело может быть модифицировано путем замены его константной области на константную область из иммуноглобулина человека, содержащего модификацию, как изложено здесь. Вследствие замены на константную область человека химерное антитело может сохранять свою специфичность, но обладать пониженной иммуногенностью для человека и пониженной агрегацией вообще по сравнению с исходным антителом мыши или химерным антителом без приведенной здесь модификации.
"Гуманизированное" антитело есть такое антитело, которое сохраняет реактивность антитела не человека, но становится менее иммуногенным для человека. Это может достигаться, к примеру, сохранением участков CDR не человека и заменой остальных частей антитела на соответствующие части от человека (т.е. константной области, а также каркасных участков вариабельной области). Например, см. Morrison et al., Proc. Natl. Acad. Sci. USA, 81:6851-6855, 1984; Morrison and Oi, Adv. Immunol., 44:65-92, 1988; Verhoeyen et al., Science, 239:1534-1536, 1988; Padlan, Molec. Immun., 28:489-498, 1991; и Padlan, Molec. Immun., 31:169-217, 1994. Другие примеры инженерной технологии на человеке включают, без ограничения, технологию Хота, раскрытую в US 5766886.
Термины "линкер", "звено линкера" или "соединение" в настоящем изобретении относятся к химической молекуле, содержащей ковалентную связь или цепь атомов, ковалентно присоединяющих антитело к лекарственной молекуле или иной молекуле. Линкеры включают двухвалентные радикалы типа алкилдиила, арилена, гетероарилена, такие группировки, как -(CR2)nO(CR2)n-, повторяющиеся звенья алкилокси (например, полиэтиленокси, ПЭГ, полиметиленокси) и алкиламино (например, полиэтиленамино, Jeffamine™); и двухкислотные эфиры и амиды, включая сукцинат, сукцинамид, дигликолат, малонат и капроамид.
Термин "метка" в настоящем изобретении относится к любым молекулам, которые могут ковалентно присоединяться к антителам и которые функционируют для: (i) обеспечения детектируемого сигнала; (ii) взаимодействия со второй меткой для модификации детектируемого сигнала, издаваемого первой или второй меткой, например, методом FRET (резонансного переноса энергии флуоресценции); (iii) стабилизации взаимодействий или повышения сродства связывания с антигеном или лигандом; (iv) воздействия на подвижность, например, электрофоретическую подвижность или клеточную проницаемость, через заряд, гидрофобность, форму или другие физические параметры; или (v) обеспечения захватывающей группы для модулирования сродства лиганда, связывания антитела/антигена или комплексирования ионов.
Термин "гуманизирование" в настоящем изобретении относится к способу преобразования нечеловеческих антител в искусственные (инженерные) антитела человека (например, см. технологию Humaneering™ фирмы KaloBios).
В настоящем изобретении термин "изотип" обозначает любой класс антител (например, IgM, IgE, IgG, как-то IgG1 или IgG2), который обеспечивается генами константной области тяжелой цепи и обладает приведенным здесь мотивом, склонным к агрегации (и поэтому подвержен приведенным здесь модификациям, уменьшающим агрегацию).
В настоящем изобретении термин "сродство" обозначает прочность взаимодействия между антителом и антигеном на отдельном антигенном сайте. Внутри каждого антигенного сайта вариабельная область "плеча" антитела взаимодействует через слабые нековалентные силы с антигеном по многочисленным сайтам; чем больше взаимодействий, тем сильнее сродство. Приведенные здесь модификации предпочтительно не снижают сродство иммуноглобулина или приведенных здесь антител или же сродство снижается меньше, чем на 30%, на 20%, на 10% или на 5%. В настоящем изобретении при определении того, снижает ли сродство приведенная здесь модификация, сравнение проводится между иммуноглобулином или антителом с модификацией и тем же самым иммуноглобулином без модификации, но включая любые не связанные с ней мутации.
В настоящем изобретении термин "субъект" включает человека или любое другое животное.
В настоящем изобретении термин "животное, кроме человека" включает всех позвоночных, например, млекопитающих и не млекопитающих, как-то других приматов, овец, собак, кошек, лошадей, коров, цыплят, амфибий, рептилий и т.п.
Термин "химиотерапевтическое средство" в настоящем изобретении обозначает химические соединения, применимые при лечении рака. Примеры химиотерапевтических средств включают эрлотиниб (TARCEVA™, Genentech/OSI Pharm.), бортезомиб (VELCADE™, Millenium Pharm.), фулвестрант (FASLODEX™, Astrazeneca), сутент (SU11248, Pfizer), летрозол (FEMARA™, Novartis), иматиниба месилат (GLEEVEC™, Novartis), PTK787/ZK 222584 (Novartis), оксалиплатин (Eloxatin™, Sanofi), 5-FU (5-фторурацил), леуковорин, рапамицин (Sirolimus, RAPAMUNE™, Wyeth), лапатиниб (GSK572016, GlaxoSmithKline), лонафарниб (SCH 66336), сорафениб (BAY43-9006, Bayer Labs), гефитиниб (IRESSA™, Astrazeneca), AG1478, AG1571 (SU 5271; Sugen), алкилирующие реагенты, такие как тиотепа и циклофосфамид CYTOXAN™; алкил-сульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодофа, карбоквон, метуредофа и уредофа; этиленимины и метилмеламины, включая альтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметиломеламин; ацетогенины (особенно буллатацин и буллатацинон); кампотецин (включая синтетический аналог топотекан); бриостатин; каллистатин; СС-1065 (включая его синтетические аналоги адозелесин, карзелесин и бизелесин); криптофицины (в особенности криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая его синтетические аналоги KW-2189 и СВ 1-ТМ1); элеутеробин; панкратистатин; саркодиктиин; спонгистатин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, холофосфамид, эстрамустин, ифосфамид, мехлоретамин, мехлоретамина оксид гидрохлорид, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урамустин; нитромочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимустин, антибиотики, такие как энедииновые антибиотики (например, калихеамицин, особенно калихеамицин гамма1I и калихеамицин омегаI1 (Angew Chem Intl. Ed. Engl. (1994) 33:183-186); динемицин, включая динемицин А; бифосфонаты, такие как клодронат; эсперамицин, а также хромофор неокарциностатин и родственные хромофоры хромопротеидов энедииновых антбиотиков), аклациномизины, актиномицин, антрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карцинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, доксорубицин ADRIAMYCIN™ (включая морфолинодоксорубицин, цианоморфолинодоксорубицин, 2-пирролинодоксорубицин и дезоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марселломицин, такие митомицины, как митомицин С, микофеноловая кислота, ногаламицин, оливомицины, пепломицин, порфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; аналоги пуринов, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; аналоги пиримидинов, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидезоксиуридин, доксифлуридин, еноцитабин, флоксуридин; андрогены, такие как калустерон, дромостанолон пропионат, эпитиостанол, мепитиостан, тестолактон; антиадреналовые, такие как аминоглутетимид, митотан, трилостан; восполнители фолиевой кислоты, такие как фролиновая кислота; ацеглатон; альдофосфамид гликозид; аминолевулиновая кислота; енилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демекольцин; диазиквон; элформитин; эллиптиний ацетат; эпотилон; этоглуцид; нитрат галлия; гидроксимочевина; лентинан; лонидаинин; майтансиноиды, такие как майтансин и ансамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лосоксантрон; подофиллиновая кислота; 2-этилгидразид, прокарбазин; полисахаридный комплекс PSK™ (JHS Natural Products, Eugene, Oreg.); разоксан; ризоксин; сизофуран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2',2"-трихлортриэтиламин; трихотецены (в особенности Т-2 токсин, верракурин А, роридин А и ангуидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид ("Ara-С"); цклофосфамид; тиотепа; таксоиды, например, паклитаксель TAXOL™ (Bristol-Myers Squibb Oncology, Princeton, N.J.), свободный от кремофора ABRAXANE™; лекарственная форма наночастиц паклитаксела на основе альбумина (American Pharmaceutical Partners, Schaumberg, I11.), и доксетаксель TAXOTERE™ (Rhone-Poulenc Rorer, Antony, France); хлоранбуцил; гемцитабин GEMZAR™; 6-тиогуанин; меркаптопурин; метотрексат; аналоги платины, такие как цисплатин и карбоплатин; винбластин; платина; этопосид (VP-16); ифосфамид; митоксантрон; винкристин; винорелбин NAVELBINE™; новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; кселода; ибандронат; СРТ-11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноидная кислота; капецитабин; и фармацевтически приемлемые соли, кислоты или производные любых из вышеприведенных.
Под это определение "химиотерапевтического средства" также попадают: (i) антигормональные средства, которые регулируют или ингибируют действие гормонов на опухоли, как-то антиэстрогены и селективные модуляторы эстрогеновых рецепторов (SERM), в том числе тамоксифен (включая тамоксифен NOLVADEX™), ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и торемифен FARESTON™; (ii) ингибиторы ароматазы, которые ингибируют фермент ароматазу, которая регулирует образование эстрогенов в надпочечниках, в том числе 4(5)-имидазолы, аминоглутетимид, мегестрол ацетат MEGASE™, экземестан AROMASIN™, форместан, фадрозол, ворозол RIVISOR™, летрозол FEMARA™ и анастрозол ARIMIDEX™; (iii) антиандрогены, такие как флутамид, нилутамид, бикалутамид, лейпролид и госерелин; а также троксацитабин (аналог цитозина - 1,3-диоксолан-нуклеозид); (iv) ингибиторы ароматазы; (v) ингибиторы протеинкиназ; (vi) ингибиторы липидкиназ; (vii) антисмысловые олигонуклеотиды, в частности те, которые ингибируют экспрессию генов в сигнальных путях, вовлеченных в аномальную пролиферацию клеток, в том числе PKC-альфа, Ralf и H-Ras; (viii) рибозимы, такие как ингибитор экспрессии VEGF (например, рибозим ANGIOZYME™) и ингибитор экспрессии HER2; (ix) вакцины типа вакцин для генной терапии, к примеру, вакцина ALLOVECTIN™, вакцина LEUVECTIN™ и вакцина VAXID™; rIL-2PROLEUKIN™; ингибитор топоизомеразы 1 LURTOTECAN™; rmRH ABARELIX™; (х) антиангиогенные средства, такие как бевацизумаб (AVASTIN™, Genentech); и (xi) фармацевтически приемлемые соли, кислоты или производные любых из вышеприведенных.
В настоящем изобретении термин "цитокин" является общим термином для белков, высвобождаемых одной популяцией клеток, которые действуют на другие клетки в качестве межклеточных медиаторов. Примерами таких цитокинов являются лимфокины, монокины и обычные полипептидные гормоны. В число цитокинов включают и гормоны роста, такие как гормон роста человека, N-метиониловый гормон роста человека и бычий гормон роста; паратиреоидный гормон; тироксин; инсулин; проинсулин; релаксин; прорелаксин; гликопротеидные гормоны, как-то фолликуло-стимулирующий гормон (FSH), тиреод-стимулирующий гормон (TSH) и лютеинизирующий гормон (LH); печеночный фактор роста; фактор роста фибробластов; пролактин; плацентарный лактоген; α- и β-фактор некроза опухолей; субстанция, ингибирующая мюллеровы тельца; мышиный гонадотропин-связанный пептид; ингибин; активин; фактор роста сосудистого эндотелия; интегрин; тромбопоэтин (ТРО); факторы роста нервов, такие как NGF-β; фактор роста тромбоцитов; трансформирующие факторы роста (TGFs), такие как TGF-α и TGF-β; инсулиноподобный фактор роста I и II; эритропоэтин (ЕРО); остеоиндуктивные факторы; интерфероны, такие как интерферон α, β и γ; колониестимулирующие факторы (CSFs), такие как CSF макрофагов (M-CSF) CSF гранулоцитов-макрофагов (GM-CSF) и CSF гранулоцитов (G-CSF); интерлейкины (ILs), такие как IL-1, IL-1α, IL-2, IL-3, IL-4, EL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12; факторы некроза опухолей, такие как TNF-α или TNF-β; и другие полипептидные факторы, включая LIF и лиганд kit (KL). В настоящем изобретении цитокины включают белки из природных источников или из рекомбинантных клеточных культур и биологически активные эквиваленты природных последовательностей цитокинов.
В настоящем изобретении термин "оптимизированный" означает, что нуклеотидная последовательность подверглась изменению с тем, чтобы кодировать аминокислотную последовательность с использованием кодонов, являющихся предпочтительными в продуцирующих клетках или организме, обычно эукариотических клетках, клетках Pichia, клетках яичников китайского хомячка (СНО) или клетках человека. Оптимизированная нуклеотидная последовательность конструируется так, чтобы она полностью или насколько возможно сохраняла аминокислотную последовательность, кодируемую первоначальной нуклеотидной последовательностью, также известной как "исходная" последовательность. Настоящим изобретением также предусмотрена оптимизированная экспрессия таких последовательностей в других эукариотических клетках. Аминокислотные последовательности, кодируемые оптимизированными нуклеотидными последовательностями, также именуются оптимизированными.
В настоящем изобретении термин "антигенсвязывающая активность" относится к специфичности связывания иммуноглобулина или конъюгата иммуноглобулина со своим антигеном-мишенью, антигенсвязывающую активность можно измерить биологическим методом на клетках (например, определением гена-репортера), методом ELISA, поверхностного плазменного резонанса (Biacore) или любым другим методом, известным специалистам.
В настоящем изобретении термин "склонность к перекрестному сшиванию" (CLP) обозначает склонность модифицированного иммуноглобулина или конъюгата иммуно-глобулина, содержащего мутацию замены на цистеин, к перекрестному сшиванию между различными иммуноглобулинами по замененному остатку цистеина. CLP можно определить по уровню олигомеризации при измерении методом SDS-PAGE в невосстанавливающих условиях, эксклюзионной хроматографии, статического или динамического лазерного светорассеяния с эксклюзионной хроматографией или любым другим способом, известным специалистам. Класс I включает варианты, которые являются мономерными и остаются стабильными после мечения. Варианты класса II содержат небольшой процент димеров до и после мечения. Варианты класса III имеют более выраженную склонность к олигомеризации, включая образование некоторого количества тримеров. Варианты класса IV имеют еще большую склонность к олигомеризации, о чем свидетельствует присутствие агрегатов, больших, чем тримеры, особенно после мечения. Класс V включает варианты с высокой склонностью к олигомеризации подобно вариантам класса IV с дополнительными структурными отклонениями, такими как фрагментация или окраска очищенного концентрированного образца.
Термин "эпитоп" обозначает белковую детерминанту, способную специфически связываться с антителом. Эпитопы обычно состоят из химически активных поверхностных группировок молекул, как-то аминокислот или боковых цепей Сахаров, и обычно имеют специфические характеристики трехмерной структуры, а также специфические характеристики зарядов. Конформационные и неконформационные эпитопы различаются тем, что связывание с первыми, но не с последними, утрачивается в присутствии денатурирующих растворителей.
Термин "консервативно модифицированный вариант" применяется и к аминокислотным последовательностям, и к последовательностям нуклеиновых кислот. В отношении определенных последовательностей нуклеиновых кислот, консервативно модифицированные варианты означают такие нуклеиновые кислоты, которые кодируют идентичные или практически идентичные аминокислотные последовательности, а если нуклеиновая кислота не кодирует аминокислотную последовательность, то практически идентичные последовательности. Вследствие вырожденности генетического кода любой данный белок кодируется большим числом функционально идентичных нуклеиновых кислот, кодоны GCA, GCC, GCG и GCU все кодируют аминокислоту аланин. Таким образом, в каждом положении, где аланин определяется кодоном, этот кодон можно заменить на любой из соответствующих приведенных кодонов без изменения кодируемого полипептида. Такие варианты нуклеиновых кислот являются "молчащими вариантами", которые представляют собой одну разновидность консервативно модифицированных вариантов. При этом каждая последовательность нуклеиновой кислоты, кодирующая полипептид, также определяет всевозможные молчащие варианты этой нуклеиновой кислоты. Специалистам должно быть известно, что каждый кодон в нуклеиновой кислоте (за исключением AUG, который обычно является единственным кодоном для метионина, и TGG который обычно является единственным кодоном для триптофана) можно модифицировать так, чтобы получить функционально идентичную молекулу. Соответственно, в каждой описанной последовательности в неявном виде содержатся все молчащие варианты нуклеиновой кислоты, кодирующей полипептид.
Для полипептидных последовательностей "консервативно модифицированные варианты" включают индивидуальные замены, делеции или вставки в последовательности полипептида, которые приводят к замене одной аминокислоты на химически подобную аминокислоту. Таблицы консервативных замен, в которых представлены функционально сходные аминокислоты, хорошо известны в данной области. Такие консервативно модифицированные варианты являются дополнением, но не исключают полиморфные варианты, межвидовые гомологи и аллели по изобретению. Следующие восемь групп содержат аминокислоты, представляющие консервативные замены друг для друга: 1) аланин (А), глицин (G); 2) аспарагиновая кислота (D), глутаминовая кислота (Е); 3) аспарагин (N), глутамин (Q); 4) аргинин (R), лизин (K); 5) изолейцин (I), лейцин (L), метионин (М), валин (V); 6) фенилаланин (F), тирозин (Y), триптофан (W); 7) серии (S), треонин (Т); и 8) цистеин (С), метионин (М) (например, см. Creighton, Proteins (1984)).
Термины "идентичный" или степень "идентичности" в контексте двух или более последовательностей нуклеиновых кислот или полипептидов означает то, что две или несколько последовательностей или подпоследовательностей являются одинаковыми. Две последовательности "существенно идентичны", если две последовательности содержат определенный процент аминокислотных остатков или нуклеотидов, являющихся одинаковыми (например, 60% идентичности, необязательно 65%, 70%, 75%, 80%, 85%, 90%, 95%, или 99% идентичности на заданном участке или, если он не задан, то по всей последовательности), когда проводится сравнение и выравнивание на максимальное соответствие в пределах окна сравнения или на заданном участке, при измерении с помощью одного из следующих алгоритмов сравнения последовательностей или при выравнивании вручную и визуальном осмотре. Необязательно идентичность существует на участке длиной по меньшей мере в 50 нуклеотидов (или 10 аминокислот), более предпочтительно на участке длиной от 100 до 500 или 1000 и больше нуклеотидов (или 20, 50, 200 и больше аминокислот).
При сравнении последовательностей обычно одна последовательность служит референсной последовательностью, с которой сравниваются тестируемые последовательности. При использовании алгоритма сравнения последовательностей тестируемые и референсные последовательности вводятся в компьютер, при необходимости задаются координаты подпоследовательностей и задаются параметры программы для алгоритма сравнения последовательностей. Можно использовать параметры программы по умолчанию или задавать альтернативные параметры. Затем алгоритм сравнения последовательностей рассчитывает процент идентичности последовательностей для тестируемых последовательностей относительно референсной последовательности на основе параметров программы. При сравнении двух последовательностей на идентичность вовсе не обязательно, чтобы последовательности были непрерывными, но любой пробел повлечет штраф, который уменьшит общий процент идентичности. Параметры по умолчанию для Blastn: штраф за открытие пробела = 5 и штраф за расширение пробела = 2. Параметры по умолчанию для Blastp: штраф за открытие пробела = 11 и штраф за расширение пробела = 1.
"Окно сравнения" в настоящем изобретении означает отрезок из любого числа смежных положений, включая, без ограничения, от 20 до 600, обычно от 50 до 200, более предпочтительно от 100 до 150, на котором может проводиться сравнение последовательности с референсной последовательностью из того же числа смежных положений после оптимального выравнивания двух последовательностей. Способы выравнивания последовательностей для сравнения хорошо известны. Оптимальное выравнивание последовательностей для сравнения может проводиться, например, при помощи алгоритма локальной гомологии Smith and Waterman (1970) Adv. Appl. Math. 2:482c, алгоритма выравнивания по гомологии Needleman and Wunsch, J. Mol. Biol. 48:443, 1970, методом поиска сходства Pearson and Lipman, Proc. Natl. Acad. Sci. USA 85:2444, 1988, при компьютерном выполнении этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в пакете программ Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Dr., Madison, WI) или при выравнивании вручную и визуальном осмотре (например, см. Brent et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc. (Ringbou ed., 2003)).
Два примера алгоритмов, пригодных для определения процента идентичности последовательностей и сходства последовательностей, - это алгоритмы BLAST и BLAST 2.0, описанные в Altschul et al., Nuc. Acids Res. 25:3389-3402, 1977; и Altschul et al., J. Mol. Biol. 215:403-410, 1990, соответственно. Программное обеспечение для проведения BLAST-анализа общедоступно через Национальный центр информации по биотехнологии (NCBI). Этот алгоритм включает идентифицирование сначала дающих высокие баллы пар последовательностей (HSPs) путем выявления коротких «слов» длиною W во введенной последовательности, которые либо совпадают, либо удовлетворяют какому-то имеющему положительное значение пороговому показателю Т при выравнивании со «словом» такой же длины в последовательности из базы данных. Величина Т именуется порогом показателя близости «слов» (Altschul et al., supra). Эти найденные «слова» действуют как затравки для запуска поиска содержащих их более длинных HSPs. Встреченные слова наращиваются в обоих направлениях вдоль каждой последовательности до тех пор, пока кумулятивная степень соответствия повышается. Для нуклеотидных последовательностей кумулятивная степень вычисляется с помощью параметров М (награда за каждую пару совпадающих остатков; она всегда >0) и N (штраф за несовпадение остатков; он всегда <0). Для аминокислотных последовательностей при расчете кумулятивной степени используется матрица баллов. Наращивание встреченных «слов» в каждом направлении останавливается, если: кумулятивная степень соответствия падает на величину Х от своего максимального достигнутого значения; кумулятивная степень снижается до нуля или меньше нуля вследствие накопления совмещений одного или нескольких остатков с отрицательными показателями; или если достигнут конец одной из последовательностей. Параметры W, Т и Х алгоритма BLAST определяют чувствительность и скорость выравнивания. В программе BLASTN (для нуклеотидных последовательностей) по умолчанию используется длина «слова» (W)=11, ожидание (Е)=10, М=5, N=-4 и сравнение обеих нитей. Для аминокислотных последовательностей в программе BLASTP по умолчанию используется длина «слова» (W)=3, ожидание (Е)=10 и матрица баллов Blosum62 (см. Henikoff and Henikoff, Proc. Natl. Acad. Sci. USA 89: 10915, 1989).
Алгоритм BLAST также проводит статистический анализ сходства между двумя последовательностями (например, см. Karlin and Altschul, Proc. Natl. Acad. Sci. USA 90: 5873-5787, 1993). Мерой сходства в алгоритме BLAST служит наименьшая сумма вероятностей (P(N)), которая служит показателем того, с какой вероятностью совпадение между двумя нуклеотидными или аминокислотными последовательностями могло бы произойти случайным образом, нуклеиновая кислота считается сходной с референсной последовательностью, если наименьшая сумма вероятностей при сравнении исследуемой нуклеиновой кислоты с референсной нуклеиновой кислотой составляет менее 0,2, более предпочтительно менее 0,01 и наиболее предпочтительно менее 0,001.
Помимо степени идентичности последовательностей, отмеченной выше, другим признаком того, что последовательности двух нуклеиновых кислот или полипептидов являются практически идентичными, служит то, что полипептид, кодируемый первой нуклеиновой кислотой, иммунологически проявляет перекрестную реактивность к антителам против полипептида, кодируемого второй нуклеиновой кислотой, как описано ниже. Таким образом, обычно полипептид считается практически идентичным второму полипептиду, если, к примеру, два пептида отличаются только консервативными заменами. Другим признаком того, что последовательности двух нуклеиновых кислот практически идентичны, служит то, что эти две молекулы или комплементарные им гибридизируются друг с другом в строгих условиях, как описано ниже. Еще одним признаком того, что последовательности двух нуклеиновых кислот практически идентичны, является то, что для амплификации последовательности можно использовать одни и те же праймеры.
Термин "функционально связаны" относится к функциональной взаимосвязи между двумя или нескольким сегментами полинуклеотидов (например, ДНК). Как правило, он относится к функциональной взаимосвязи регулирующей транскрипцию последовательности и транскрибируемой последовательности, последовательность промотора или энхансера функционально связана с кодирующей последовательностью, если она стимулирует или модулирует транскрипцию кодирующей последовательности в соответствующих клетках хозяина или в другой системе экспрессии. Обычно последовательности регулирующих транскрипцию промоторов, которые функционально связанны с транскрибируемой последовательностью, физически прилегают к транскрибируемой последовательности, т.е. работают в цис-положении. Однако некоторые регулирующие транскрипцию последовательности, такие как энхансеры, не обязательно физически прилегают или располагаются в непосредственной близости к той кодирующей последовательности, транскрипцию которой они усиливают.
Термин "вектор" служит для обозначения молекулы полинуклеотида, способного транспортировать другой полинуклеотид, с которым он соединен. Одним типом вектора является "плазмида", что означает кольцевую двухцепочечную петлю ДНК, в которую могут быть лигированы дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, при этом в вирусный геном могут быть лигированы дополнительные сегменты ДНК. Некоторые векторы способны к автономной репликации в тех клетках хозяина, в которые они введены (бактериальные векторы, содержащие бактериальный ориджин репликации, или эписомные векторы млекопитающих). Другие векторы (неэписомные векторы млекопитающих) могут встраиваться в геном клеток хозяина после введения в них и будут реплицироваться вместе с геномом хозяина. Более того, некоторые векторы способны направлять экспрессию тех генов, с которыми они функционально связаны. Такие векторы именуются "рекомбинантными экспрессионными векторами" (или просто "экспрессионными векторами"), В общем, экспрессионные векторы, находящие применение в методах рекомбинантой ДНК, часто имеют вид плазмид. В настоящем описании "плазмида" и "вектор" могут заменять друг друга, так как пламида является наиболее распространенным видом вектора. Однако изобретение охватывает и другие формы экспрессионных векторов, как-то вирусные векторы (например, дефектные по репликации ретровирусы, аденовирусы и аденоассоциированные вирусы), которые выполняют эквивалентные функции.
Термин "рекомбинантная клетка хозяина" (или просто "клетка хозяина") относится к клеткам, в которые был введен рекомбинантный экспрессионный вектор. Следует понимать, что такие термины служат для обозначения не только определенных клеток субъекта, но и потомства таких клеток. Поскольку в ряду поколений могут происходить некоторые модификации в результате мутации или влияния среды, такое потомство фактически может и не быть идентичным исходной клетке, тем не менее, в настоящем изобретении оно охватывается рамками термина "клетки хозяина".
Термин "антиген-мишень" обозначает антиген, против которого был выработан или иным образом получен (например, методом фагового дисплея) исходный иммуно-глобулин.
Термин "немутированный иммуноглобулин" обозначает иммуноглобулин, который не содержит по меньшей мере одну мутацию, представляющую замену на остаток цистеина. В настоящем изобретении немутированный иммуноглобулин может представлять собой гипотетическую конструкцию, служащую для сравнения склонности к олигомеризации или эффективности конъюгации иммуноглобулина с мутацией и без мутации. Для примера: антитело мыши, содержащее гуманизирующие мутации, а также мутации на цистеин в целях конъюгации, не является немутированным иммуно-глобулином. Немутированным иммуноглобулином будет антитело с гуманизирующими мутациями, но без мутации на цистеин. Если мутация служит для выполнения больше чем одной цели, включая обеспечение сайтов для конъюгации, то немутированный иммуноглобулин не должен содержать такие мутации.
Термин "мотив агрегации" относится к группе остатков, сгруппированных вместе на основе следующего процесса. Сначала идентифицируются остатки с SAP (радиусом 5Å) больше 0,15. Затем идентифицируются все остатки в пределах 5Å от каждого остатка, имеющего SAP (радиусом 5Å) больше 0,15. Тогда мотив содержит остаток с SAP (радиусом 5Å) больше 0,15 и все остатки с SAP (радиусом 5Å) больше 0,00 в пределах 5Å от остатка с SAP (радиусом 5Å) больше 0,15. Все такие мотивы, имеющие по меньшей мере один общий остаток, подвергаются итеративному слиянию в больший мотив до тех пор, пока не останется ни одного мотива, имеющего общий остаток. Такие оставшиеся мотивы или группы остатков и составляют мотивы агрегации.
Если остатки иммуноглобулина обозначаются номерами, то номер остатка означает номер соответствующего остатка иммуноглобулина в молекуле IgG1 по Кабату при совмещении данной последовательности иммуноглобулина с иммуноглобулином IgG1 человека. Для справки приводим совмещение константных доменов IgG1, IgG2, IgG3 и IgG4 человека.
Домен CH1

Шарнир

Домен CH2

Домен CH3

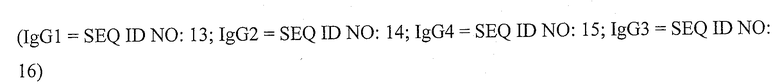
Домен CL

Сопоставления доменов VH и VL приведены в Ewert, Honegger and Pluchthun, Methods 34 (2004) 184-199.
Конъюгаты иммуноглобулинов по изобретению
Настоящее изобретение касается конъюгатов иммуноглобулинов, включающих иммуноглобулины, содержащие по меньшей мере одну мутацию остатка на поверхности иммуноглобулина, причем мутация представляет собой замену на остаток цистеина. Замененный остаток цистеина конъюгируют с атомом или молекулой, которым может быть, к примеру, цитотоксический агент (например, токсин типа доксорубицина или коклюшного токсина), флуорофор типа флуоресцентного красителя вроде флуоресцеина или родамина, хелатирующий агент для интраскопии или радиотерапевтический металл, пептидная или непептидная метка или тэг для детектирования, модифицирующий выведение агент типа различных изомеров полиэтиленгликоля, пептид, который связывается с третьим компонентом, или иной углеводный или липофильный агент. В других воплощениях молекула может представлять собой фермент, пептид, пептидо-миметик, нуклеотид типа молекулы РНК, включая siPHK, микроРНК, и РНК-миметики или аптамеры.
Меченые конъюгаты иммуноглобулинов
В некоторых воплощениях модифицированные иммуноглобулины изобретения могут быть конъюгированы с любой меткой, которая может ковалентно присоединяться к иммуноглобулину через реактивную тиоловую группу цистеина (Singh et al. (2002) Anal. Biochem. 304:147-15; Harlow E. and Lane D. (1999) Using Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.; Lundblad R.L. (1991) Chemical Reagents for Protein Modification, 2nd ed. CRC Press, Boca Raton, Fla.). Присоединенная метка может функционировать, к примеру, для: (i) обеспечения детектируемого сигнала; (ii) взаимодействия со второй меткой для модификации детектируемого сигнала, издаваемого первой или второй меткой, например, методом FRET (резонансного переноса энергии флуоресценции); (iii) стабилизации взаимодействий или повышения сродство связывания с антигеном или лигандом; (iv) воздействия на подвижность, например, электрофоретическую подвижность или клеточную проницаемость, через заряд, гидрофобность, форму или другие физические параметры; или (v) обеспечения захватывающей группировки для модулирования сродства лиганда, связывания антитела/ антигена или комплексирования ионов.
Меченые конъюгаты иммуноглобулинов могут быть полезными в диагностических методах, например, для детектирования экспрессии нужного антигена в специфических клетках, тканях или сыворотке. Для диагностического применения иммуноглобулин обычно метят детектируемой молекулой. Имеются многочисленные метки, которые в общем можно сгруппировать в следующие типичные категории:
(а) Радиоизотопы (радионуклиды), как-то 3H, 11С, 14С, 18F, 32P, 35S, 64Cu, 68Ga, 86Y, 99Tc, 111In, 123I, 124I, 125I, 131I, 133Xe, 177Lu, 211At или 213Bi. Меченые радиоизотопами иммуноглобулины применяются в экспериментах по интраскопии рецепторов-мишеней. Иммуноглобулины можно пометить с помощью лигандов-реагентов, которые связывают, хелатируют или образуют комплекс с радиоизотопным металлом, при этом реагент подвергается реакции с тиолом встроенного в иммуноглобулин цистеина, используя методы, описанные в Current Protocols in Immunology, vol. 1 and 2, Coligen et al., eds. Wiley-Interscience, New York, N.Y., Pubs. (1991). Хелатирующие лиганды, которые могут образовать комплекс с ионом металла, включают DOTA, DOTP, DOTMA, DTPA и ТЕТА (Macrocyclics, Dallas, Тех.). Радионуклиды могут быть нацелены через комплексирование с конъюгатами антитело-лекарство по изобретению (Wu et al. (2005) Nature Biotechnology 23(9):1137-1146).
Хелатные комплексы металлов, подходящие в качестве иммуноглобулиновых меток для экспериментов по интраскопии, приведены в: U.S. патентах 5342606; 5428155; 5316757; 5480990; 5462725; 5428139; 5385893; 5739294; 5750660; 5834456; Hnatowich et al. (1983) J. Immunol. Methods 65:147-157; Meares et al. (1984) Anal. Biochem. 142:68-78; Mirzadeh et al. (1990) Bioconjugate Chem. 1:59-65; Meares et al. (1990) J. Cancer 1990, Suppl. 10:21-26; Izard et al. (1992) Bioconjugate Chem. 3:346-350; Nikula et al. (1995) Nucl. Med. Biol. 22:387-90; Camera et al. (1993) Nucl. Med. Biol. 20:955-62; Kukis et al. (1998) J. Nucl. Med. 39:2105-2110; Verel et al. (2003) J. Nucl. Med. 44:1663-1670; Camera et al. (1994) J. Nucl. Med. 21:640-646; Ruegg et al. (1990) Cancer Res. 50:4221-4226; Verel et al. (2003) J. Nucl. Med. 44:1663-1670; Lee et al. (2001) Cancer Res. 61:4474-4482; Mitchell et al. (2003) J. Nucl. Med. 44:1105-1112; Kobayashi et al. (1999) Bioconjugate Chem. 10:103-111; Miederer et al. (2004) J. Nucl. Med. 45:129-137; DeNardo et al. (1998) Clinical Cancer Research 4:2483-90; Blend et al. (2003) Cancer Biotherapy & Radiopharmaceuticals 18:355-363; Nikula et al. (1999) J. Nucl. Med. 40:166-76; Kobayashi et al. (1998) J. Nucl. Med. 39:829-36; Mardirossian et al. (1993) Nucl. Med. Biol. 20:65-74; Roselli et al. (1999) Cancer Biotherapy & Radiopharmaceuticals, 14:209-20.
(b) Флуоресцентные метки типа хелатов редкоземельных элементов (хелатов европия); метки флуоресцеинового типа, включая FITC, 5-карбоксифлуоресцеин, 6-карбоксифлуоресцеин; родаминового типа, включая TAMRA; дансил; лиссамин; цианины; фикоэритрины; техасский красный; и их аналоги. Флуоресцеиновые метки могут быть конъюгированы с иммуноглобулинами при помощи методов, описанных, к примеру, в Current Protocols in Immunology, supra. Флуоресцентные красители и реагенты для флуоресцентных меток включают те, что коммерчески доступны от Invitrogen/Molecular Probes (Eugene, Oreg.) и Pierce Biotechnology, Inc. (Rockford, I11.).
(c) Различные фермент-субстратные метки, существующие или раскрытые (U.S. патент 4275149). Фермент обычно катализирует химическое изменение хромогенного субстрата, которое можно измерить различными методами. Фермент может катализировать изменение окраски субстрата, которое можно измерить спектрофотометрически. С другой стороны, фермент может изменить флуоресценцию или хемилюминесценцию субстрата. Методы количественной оценки изменений флуоресценции описаны выше. Хемилюминесцентный субстрат становится электронновозбужденным при химической реакции и может затем испускать свет, который можно измерить (к примеру, с помощью хемилюминометра), или передавать энергию на флуоресцентный акцептор. Примеры ферментных меток включают люциферазы (например, люцифераза светлячков или бактериальная люцифераза; U.S. патент 4737456), люциферин, 2,3-дигидрофталазиндионы, малатдегидрогеназу, уреазу, пероксидазу типа пероксидазы хрена (HRP), щелочную фосфатазу (АР), β-галактозидазу, глюкоамилазу, лизоцим, оксидазы сахаридов (например, глюкозооксидаза, галактозооксвдаза и глюкозо-6-фосфат-дегидрогеназа), оксидазы гетероциклов (как-то уриказа и ксантиноксидаза), лактопероксидазу, микропероксидазу и др. Методы конъюгирования ферментов с антителами описаны в O'Sullivan et al. (1981) "Methods for the Preparation of Enzyme-Antibody Conjugates for Use in Enzyme Immunoassay", in Methods in Enzym. (ed J. Langone & H. Van Vunakis), Academic Press, New York, 73:147-166.
Примерами фермент-субстратных комбинаций являются, к примеру: (i) пероксидаза хрена (HRP) с перекисью водорода в качестве субстрата, при этом перекись водорода окисляет предшественник красителя (например, ортофенилендиамин (OPD) или 3,3',5,5'-тетраметилбенизидин гидрохлорид (ТМВ)); (ii) щелочная фосфатаза (АР) с пара-нитрофенилфосфатом в качестве хромогенного субстрата; и (iii) β-D-галактозидаза (β-D-Gal) с хромогенным субстратом (например, пара-нитрофенил-β-D-галактозидом) или флуорогенным субстратом 4-метиллумбелллиферил-β-D-галактозидом. Многочисленные другие фермент-субстратные комбинации доступны специалистам в этой области. См. общие обзоры в U.S. патентах 4275149 и 4318980.
Метка может быть конъюгирована с модифицированными иммуноглобулинами изобретения опосредованно. Иммуноглобулин можно конъюгировать с биотином, а любую из трех обширных категорий меток, приведенных выше, можно конъюгировать с авидином или стрептавидином, или наоборот. Биотин избирательно связывается со стрептавидином, при этом метка может конъюгировать с иммуноглобулином таким непрямым способом. С другой стороны, для достижения непрямой конъюгации метки с вариантом иммуноглобулина этот вариант иммуноглобулина конъюгируют с небольшим гаптеном (например, дигоксином), а одну из различных типов меток, описанных выше, конъюгируют с антигаптеновым вариантом полипептида (например, антителом против дигоксина). Тем самым достигается непрямая конъюгация метки с вариантом иммуноглобулина (Hermanson G. (1996) in Bioconjugate Techniques. Academic Press, San Diego).
Модифицированные иммуноглобулины и конъюгаты иммуноглобулинов настоящего изобретения могут использоваться в любом известном способе определения, таком как ELISA, методы конкурентного связывания, прямые и непрямые методы "сэндвича" и методы иммунопреципитации (Zola (1987) Monoclonal Antibodies: A Manual of Techniques, pp.147-158, CRC Press, Inc.).
Детектирующие метки могут применяться для локализации, визуализации и количественной оценки связывания или распознавания. Меченые конъюгаты иммуноглобулинов изобретения способны детектировать рецепторы на поверхности клетки. Другое применение детектируемых меченых конъюгатов иммуноглобулинов составляет метод иммунозахвата на основе шариков, включающий конъюгирование шариков с флуоресцентно меченым антителом и детектирование флуоресцентного сигнала при связывании лиганда. В подобных методах детекции по связыванию используют эффект поверхностного плазменного резонанса (SRP) для измерения и детектирования взаимодействий антитело-антиген.
Детектирующие метки типа флуоресцентных красителей и хемилюминесцентных красителей (Briggs et al. (1997) "Synthesis of Functionalised Fluorescent Dyes and Their Coupling to Amines and Amino Acids," J. Chem. Soc., Perkin-Trans. 1:1051-1058) издают детектируемый сигнал и в общем применимы для мечения иммуноглобулинов, предпочтительно они обладают следующими свойствами: (i) меченый иммуноглобулин должен давать очень сильный сигнал с низким фоном так, чтобы можно было с высокой чувствительностью детектировать небольшие количества иммуноглобулинов и при бесклеточном определении, и при определении на клетках; и (ii) меченое антитело должно быть светоустойчивым с тем, чтобы можно было наблюдать, отслеживать и регистрировать флуоресцентный сигнал без существенного фотообесцвечивания. Для применений, включающих поверхностное связывание меченых антител с мембранами или поверхностями клеток, в особенности живых клеток, метки предпочтительно (iii) должны обладать хорошей водорастворимостью для получения эффективной концентрации конъюгата и чувствительности детектирования и (iv) не быть токсичными для живых клеток с тем, чтобы не нарушать нормальные процессы метаболизма клеток или не вызывать преждевременной гибели клеток.
Прямая количественная оценка интенсивности клеточной флуоресценции и связанных с флуоресцентной меткой явлений, например, связывания с клеточной поверхностью конъюгатов пептид-краситель, может проводиться на установке FMAT™ 8100 HTS System (Applied Biosystems, Foster City, Calif.), которая в режиме автоматического смешивания и считывания проводит нерадиоактивные анализы на живых клетках или шариках (Miraglia, "Homogeneous cell- and bead-based assays for high throughput screening using fluorometric microvolume assay technology", (1999) J. of Biomolecular Screening 4:193-204). Применение меченых иммуноглобулинов также включает методы связывания с рецепторами клеточной поверхности, методы иммунофиксации, флуоресцентные иммуносорбентные методы (FLISA), расщепление каспазами (Zheng, "Caspase-3 controls both cytoplasmic and nuclear events associated with Fas-mediated apoptosis in vivo" (1998) Proc. Natl. Acad. Sci. USA 95:618-23; U.S. патент 6372907), апоптоз (Vermes, "A novel assay for apoptosis. Flow cytometric detection of phosphatidylserine expression on early apoptotic cells using fluorescein labeled Annexin V" (1995) J. Immunol. Methods 184:39-51) и анализ цитотоксичности. Для идентификации повышающей или понижающей регуляции молекулами, нацеленными на клеточную поверхность, можно применять технологию флуорометрического анализа в микрообъемах (Swartzman, "A homogeneous and multiplexed immunoassay for high-throughput screening using fluorometric microvolume assay technology", (1999) Anal. Biochem. 271:143-51).
Меченые конъюгаты иммуноглобулинов по изобретению применимы в качестве биомаркеров и зондов для интраскопии в различных способах и методах биомедицинской и молекулярной интраскопии, таких как: (i) MRI (магнитно-резонансная интраскопия); (ii) MicroCT (компьютерная томография); (iii) SPECT (однофотонная эмиссионная компьютерная томография); (iv) PET (позитронная эмиссионная томография) (Chen et al. (2004) Bioconjugate Chem. 15:41-49; (v) биолюминесценция; (vi) флуоресценция; и (vii) ультразвук. Иммуносцинтиграфия представляет собой методику интраскопии, при которой антитела, меченые радиоактивными веществами, вводятся животному или больному человеку и делается снимок тех точек в организме, в которых локализуется антитело (U.S. патент 6528624). Биомаркеры для интраскопии можно объективно измерить и оценить в качестве индикатора нормальных биологических процессов, патогенных процессов или фармакологических реакций на терапевтическое вмешательство. Биомаркеры могут быть нескольких типов: тип 0 - это маркеры естественного течения заболевания, которые коррелируют в разные моменты времени с известными клиническими показателями, например, оценкой синовиального воспаления методом MRI при ревматоидном артрите; маркеры I типа фиксируют эффект вмешательства в соответствии с механизмом действия, даже если механизм может быть не связан с клиническим исходом; маркеры II типа функционируют в качестве косвенных конечных точек, в которых изменения биомаркера или сигнала от него предсказывают клиническую пользу для "подтверждения" целевого ответа, например при измерении эрозии костной ткани при ревматоидном артрите методом СТ. Биомаркеры для интраскопии, таким образом, могут давать фармакодинамическую (PD) терапевтическую информацию об: (i) экспрессии белка-мишени, (ii) связывании лекарства с намеченным белком, т.е. избирательности, и (iii) фармакокинетических данных по выведению и времени полужизни. Преимущества биомаркеров для интраскопии in vivo по сравнению с лабораторными биомаркерами включают: не инвазивное лечение, количественный анализ всего организма, повторная дозировка и оценка, т.е. множественность временных точек, и возможность переноса эффектов из доклинических (небольшие животные) на клинические (человек) результаты. При некоторых применениях биоинтраскопия заменяет или сводит к минимуму количество экспериментов на животных в доклинических исследованиях.
Радионуклидные метки для интраскопии включают такие радионуклиды, как 3Н, 11С, 14С, 18F, 32Р, 35S, 64Cu, 68Ga, 86Y, 99Tc, 111In, 123I, 124I, 125I, 131I, 133Xe, 177Lu, 211At или 213Bi. В радионуклиде ион металла может образовать комплекс с хелатирующим линкером типа DOTA. Реагенты для линкеров типа DOTA-малеимида (4-малеимидобутирамидобензил-DOTA) можно получить при реакции аминобензил-DOTA с 4-малеимидомасляной кислотой (Fluka), активированной изопропилхлорформиатом (Aldrich), по методике Axworthy et al. (2000) Proc. Natl. Acad. Sci. USA 97(4): 1802-1807). DOTA-малеимидные реагенты реагируют со свободными аминокислотами цистеина у модифицированных иммуноглобулинов и обеспечивают лиганды для комплексирования с металлом на антителе (Lewis et al. (1998) Bioconj. Chem. 9:72-86). Хелатирующие реагенты для мечения линкеров, такие как DOTA-NHS (моно-N-гидроксисукцинимидный эфир 1,4,7,10-тетра-азациклододекан-1,4,7,10-тетрауксусной кислоты), коммерчески доступны (Macrocyclics, Dallas, Тех.). Прицельная интраскопия рецепторов с помощью меченых радионуклидами антител может служить маркером активации путей при выявлении и количественном измерении прогрессирующего накопления антител в ткани опухоли (Albert et al. (1998) Bioorg. Med. Chem. Lett. 8:1207-1210). Конъюгаты с радиоактивными металлами могут оставаться внутри клетки после деградации в лизосомах.
Способы мечения пептидов хорошо известны. См. Haugland, 2003, Molecular Probes Handbook of Fluorescent Probes and Research Chemicals, Molecular Probes, Inc.; Brinkley, 1992, Bioconjugate Chem. 3:2; Garman (1997) Non-Radioactive Labelling: A Practical Approach, Academic Press, London; Means (1990) Bioconjugate Chem. 1:2; Glazer et al. (1975) Chemical Modification of Proteins. Laboratory Techniques in Biochemistry and Molecular Biology (T.S. Work and E. Work, eds.) American Elsevier Publishing Co., New York; Lundblad R.L. and Noyes C. M. (1984) Chemical Reagents for Protein Modification, vols. I and II, CRC Press, New York; Pfleiderer G. (1985) "Chemical Modification of Proteins", Modem Methods in Protein Chemistry, Н. Tschesche, ed., Walter DeGruyter, Berlin and New York; Wong (1991) Chemistry of Protein Conjugation and Cross-linking, CRC Press, Boca Raton, Fla.); De Leon-Rodriguez et al. (2004) Chem. Eur. J. 10:1149-1155; Lewis et al. (2001) Bioconjugate Chem. 12:320-324; Li et al. (2002) Bioconjugate Chem. 13:110-115; Mier et al. (2005) Bioconjugate Chem. 16:240-237.
Пептиды и белки, меченные двумя молекулами, флуоресцентным репортером и гасителем, при достаточной близости подвергаются резонансному переносу энергии флуоресценции (FRET). Репортерными группами обычно являются флуоресцентные красители, которые возбуждаются светом при определенной длине волны и передают энергию на группу акцептора или гасителя с соответствующим стоксовым сдвигом для эмиссии при максимальной яркости. Флуоресцентные красители включают молекулы с расширенной ароматичностью, такие как флуоресцеин и родамин и их производные. Флуоресцентный репортер может подвергаться частичному или существенному тушению молекулой гасителя в интактном пептиде. При расщеплении пептида пептидазой или протеазой отмечается заметное повышение флуоресценции (Knight С.(1995) "Fluorimetric Assays of Proteolytic Enzymes", Methods in Enzymology, Academic Press, 248:18-34).
Меченые антитела изобретения также могут применяться в качестве средства для аффинной очистки. При этом меченое антитело иммобилизуют на твердой фазе типа смолы Sephadex или фильтровальной бумаги, используя хорошо известные методы. Иммобилизованное антитело приводится в контакт с образцом, содержащим антиген, подлежащий очистке, после чего подложку отмывают подходящим растворителем, удаляющим практически весь материал в образце, за исключением подлежащего очистке антигена, связанного с иммобилизованным вариантом полипептида. Наконец, подложку промывают другим подходящим растворителем типа глицинового буфера, рН 5,0, который высвобождает антиген из варианта полипептида.
Как правило, реагенты для мечения несут реакционноспособную функциональную группу, которая может реагировать (i) непосредственно с тиолом цистеина у модифицированного иммуноглобулина с образованием меченого антитела, (ii) с линкерным реагентом с образованием промежуточного продукта линкер-метка, или (iii) с линкерным антителом с образованием меченого антитела. Реакционноспособные функциональные группы реагентов для мечения включают: малеимид, галоацетил, сукцинимидиловый эфир йодацетамида (например, NHS, N-гидроксисукцинимид), изотиоцианат, сульфонил-хлорид, 2,6-дихлортриазинил, пентафторфениловый эфир и фосфорамидит, хотя могут применяться и другие функциональные группы.
Типичной реакционноспособной функциональной группой является N-гидрокси-сукцинимидиловый эфир (NHS) заместителя карбоксильной группы детектируемой метки, например, биотина или флуоресцентного красителя. NHS-эфир метки может быть получен заранее, выделен, очищен и/или охарактеризован, либо он может образоваться in situ и реагировать с нуклеофильной группой антитела. Как правило, карбоксильная форма метки активируется при реакции с некоторой комбинацией из карбодиимидного реагента, например, дициклогексилкарбодиимида, диизопропилкарбодиимида, или урониевого реагента, например, TSTU (O-(N-сукцинимидил)-N,N,N',N'-тетраметилуроний тетрафторбората, HBTU (O-бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфата) или HATU (O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфата), активатора типа 1-гидроксибензотриазола (HOBt) и N-гидроксисукцинимида с образованием NHS-эфира метки. В некоторых случаях метку и антитело можно конъюгировать при активации метки in situ и реакции с антителом с образованием конъюгата метка-антитело в одну стадию. Другие активирующие и конденсирующие реагенты включают TBTU (2-(1Н-бензотриазо-1-ил)-1-1,3,3-тетраметилуроний гексафторфосфат), TFFH (N,N',N",N'"-тетраметилуроний 2-фтор-гексафторфосфат), РуВОР (бензотриазол-1-ил-окси-трис-пирролидино-фосфоний гексафторфосфат), EEDQ (2-этокси-1-этоксикарбонил-1,2-дигидрохинолин), DCC (дициклогексилкарбодиимид); DIPCDI (диизопропилкарбодиимид), MSNT (1-(мезитилен-2-сульфонил)-3-нитро-1Н-1,2,4-триазол и арилсульфонилгалиды, например, триизопропилбензолсульфонилхлорид.
Соответственно, объектом настоящего изобретения является применение конъюгатов иммуноглобулинов, рассмотренных выше, и всевозможных комбинаций их воплощений в качестве диагностического инструмента.
Соответственно, объектом настоящего изобретения является применение конъюгатов иммуноглобулинов, рассмотренных выше, и всевозможных комбинаций их воплощений в качестве стандарта для высокомолекулярных белков.
Конъюгаты иммуноглобулинов с полимерами
В следующих воплощениях настоящего изобретения также предусмотрены конъюгаты иммуноглобулинов, в которых иммуноглобулин связан с полимером. Как правило, полимер является водорастворимым, так что иммуноглобулиновые компоненты не выпадают в осадок в водной среде типа физиологической среды. Примером подходящего полимера является полимер, который подвергался модификации для получения одной реактивной группы типа активного эфира для ацетилирования или альдегида для алкилирования. Таким образом можно контролировать степень полимеризации. Примером реактивного альдегида является пропионовый альдегид полиэтиленгликоля или его моно-(C1-C10)алкокси- или арилоксипроизводные (см. Harris et al., U.S. патент 5252714). Полимер может быть разветвленным или не разветвленным. Более того, для получения конъюгатов с компонентами антител можно использовать смесь полимеров.
Подходящими водорастворимыми полимерами являются, без ограничения, полиэтиленгликоль (ПЭГ), монометокси-ПЭГ, моно-(С1-С10)алкокси-ПЭГ, арилокси-ПЭГ, поли-(N-винилпирролидон)-ПЭГ, трезилмонометокси-ПЭГ, пропиональдегид ПЭГ, бис-сукцинимидилкарбонат-ПЭГ, гомополимеры пропиленгликоля, сополимеры полипропиленоксида/этиленоксида, полиоксиэтилированные полиоли (например, глицерин), поливиниловый спирт, декстран, целлюлоза или другие полимеры на основе углеводов. Подходящие ПЭГ могут иметь молекулярную массу от 600 до 60,000, включая, к примеру, 5,000, 12,000, 20,000 и 25,000. Конъюгат может содержать и смесь таких водорастворимых полимеров.
В качестве иллюстрации, молекула полиалкилоксида может быть присоединена к N-концу иммуноглобулинового компонента. Одним из подходящих полиалкилоксидов является PEG. Иммуноглобулин может быть модифицирован с помощью PEG, что известно как "пегилирование". Пегилирование иммуноглобулина может проводиться по любой из реакций пегилирования, известных в этой области (к примеру, см. ЕР 0154316, Delgado et al., Critical Reviews in Therapeutic Drug Carrier Systems 9:249 (1992), Duncan and Spreafico, Clin. Pharmacokinet. 27:290 (1994), и Francis et al., Int J Hematol 68:1 (1998)). Пегилирование может проводиться по реакции ацилирования или по реакции алкилирования с реакционноспособной молекулой полиэтиленгликоля. В альтернативном подходе конъюгаты иммуноглобулинов образуются при конденсации активированного ПЭГ, у которого конечная гидрокси- или аминогруппа ПЭГ заменена активированным линкером (см. Karasiewicz et al., U.S. Pat. No. 5382657).
Пегилирование при ацилировании обычно требует проведения реакции активного эфирного производного ПЭГ с иммуноглобулином. Примером активированного эфира ПЭГ является ПЭГ, этерифицированный N-гидроксисукцинимидом. В настоящем изобретении термин "ацилирование" включает следующие типы связей между иммуноглобулином и водорастворимым полимером: амидные, карбаматные, уретановые и т.п. Способы получения пегилированных иммуноглобулинов анти-ВСМА-TACI при помощи ацилирования обычно включают стадии: (а) реакцию иммуноглобулина с ПЭГ (типа реактивного эфира альдегидного производного ПЭГ) в условиях, при которых к иммуно-глобулину присоединяется одна или несколько групп ПЭГ, и (b) получение продукта(ов) реакции. В общем, оптимальные условия для реакций ацилирования определяются, исходя из основы известных параметров и требуемых результатов. Чем большее отношение ПЭГ/компонент антитела, тем выше содержание полипегилированного продукта компонента антитела.
Продуктом пегилирования при ацилировании обычно является полипегилированный продукт иммуноглобулина, у которого ε-аминогруппы лизина пегилированы через соединительную ацильную группу. Примером соединительной связи является амид. Как правило, полученный иммуноглобулиновый компонент будет моно-, ди- или три-пегилирован по меньшей мере на 95%, хотя могут образовываться и разновидности с более высокой степенью пегилирования, в зависимости от условий реакции, пегилированные компоненты иммуноглобулинов можно отделить от неконъюгированных при помощи стандартных методов очистки, как-то диализа, ультрафильтрации, ионообменной хроматографии, аффинной хроматографии и др.
Пегилирование при алкилировании обычно включает проведение реакции терминального производного альдегида ПЭГ с иммуноглобулиновым компонентом в присутствии восстанавливающего реагента. Группы ПЭГ могут присоединяться к полипептиду через группу -CH2-NH.
Получение производных через восстановительное алкилирование с образованием монопегилированного продукта пользуется преимуществом дифференциальной реактивности различных типов первичных аминогрупп, доступных для получения производных. Как правило, реакция проводится при рН, позволяющем воспользоваться разностью рКа между ε-аминогруппами остатков лизина и α-аминогруппой N-концевого остатка белка. При такой избирательной дериватизации можно контролировать присоединение к белку водорастворимого полимера, содержащего реактивную группу типа альдегида. Конъюгирование с полимером происходит преимущественно на N-конце белка без существенной модификации других активных групп типа аминогрупп боковой цепи лизина.
Восстановительное алкилирование для получения практически однородной популяции монополимерных молекул конъюгата компонента антитела может включать следующие стадии: (а) реакцию компонента антитела с реактивным ПЭГ в условиях восстановительного алкилирования при рН, подходящем для избирательной модификации α-аминогрупп на N-конце компонента антитела, и (b) получение продукта(ов) реакции. Восстановительный реагент, используемый для восстановительного алкилирования, должен быть стабильным в водном растворе и предпочтительно способным восстанавливать только шиффово основание, образовавшееся в начале процесса восстановительного алкилирования. Предпочтительными восстановительными реагентами являются борогидрид натрия, цианоборогидрид натрия, диметиламиноборан, триметиламиноборан и пиридиноборан.
Условия восстановительной реакции алкилирования для практически однородной популяции монополимерных конъюгатов иммуноглобулинов должны способствовать избирательному присоединению водорастворимой молекулы полимера к N-концу иммуноглобулина. Такие условия реакции обычно обеспечивают разность рКа между аминогруппами лизина и α-аминогруппой на N-конце. Значение рН также влияет на соотношение полимера к используемому белку. В общем, чем меньшее значение рН, тем больший избыток полимера требуется по отношению к белку, так как чем менее реактивна N-концевая α-группа, тем больше полимера нужно для достижения оптимальных условий. Если же рН выше, то отношение полимер: компонент антитела не должно быть столь высоким, так как доступно больше реактивных групп. Обычно рН попадает в пределы от 3 до 9 или от 3 до 6.
Общие способы получения конъюгатов, содержащих полипептид и водорастворимые молекулы полимеров, известны в данной области, см. Karasiewicz et al., U.S. Pat. No. 5382657; Greenwald et al., U.S. Pat. No. 5738846; Nieforth et al., Clin. Pharmacol. Ther. 59:636 (1996); Monkarsh et al., Anal Biochem. 247:434 (1997).
Конъюгаты иммуноглобулинов с лекарствами
В следующих воплощениях настоящее изобретение охватывает конъюгаты иммуноглобулинов, в которых иммуноглобулин конъюгирован с лекарственной или цитотоксической молекулой. Лекарственные молекулы в конъюгатах иммуноглобулинов с лекарствами могут включать, к примеру, любые соединения, молекулы или группы, обладающие цитотоксическим или цитостатическим эффектом. Лекарственные молекулы включают, без ограничения: (i) химиотерапевтические средства, которые могут действовать как ингибиторы микротрубочек, ингибиторы митоза, ингибиторы топоизомеразы или ДНК-интеркаляторы; (ii) белковые токсины, которые могут действовать энзиматически; и (iii) радиоизотопы.
Типичными лекарственными молекулами являются, без ограничения, майтан-синоиды, ауристатины, доластатины, трихотецены, СС1065, калихеамицин и другие ендииновые антибиотики, таксаны, антрациклины и их стереоизомеры, изомеры, аналоги или производные.
Майтансиновые соединения, пригодные для применения в качестве лекарственных молекул майтансиноидов, хорошо известны в данной области и могут быть выделены из природных источников известными способами, получены методами генной инженерии (см. Yu et al. (2002) Proc. Nat. Acad. Sci. USA 99:7968-7973), или же можно получить майтансинол и аналоги майтансинола синтетически согласно известным методам.
Типичными лекарственными молекулами майтансиноидов являются те, которые содержат модифицированное ароматическое кольцо, как-то С-19-дехлоро (U.S. патент 4256746) (получают восстановлением ансамитоцина Р2 с помощью гидрида алюминия-лития); С-20-гидрокси (или С-20-деметил) ± С-19-дехлоро (U.S. патенты 4361650 и 4307016) (получают деметилированием с помощью Streptomyces или Actinomyces либо дехлорированием с помощью LAH); и С-20-деметокси, С-20-ацилокси (-OCOR) ± дехлоро (U.S. патент 4294757) (получают ацилированием с помощью хлорангидридов), и те, которые содержат модификации в других положениях.
Типичными лекарственными молекулами майтансиноидов также являются те, которые содержат такие модификации, как C-9-SH (U.S. патент 4424219) (получают при реакции майтансинола с H2S или P2S5); С-14-алкоксиметил(деметокси/СН2-OR) (U.S. патент 4331598); С-14-гидроксиметил или ацилоксиметил (CH2OH или CH2OAc) (U.S. патент 4450254) (получают из Nocardia); С-15-гидрокси/ацилокси (U.S. патент 4364866) (получают превращением майтансинола с помощью Streptomyces); С-15-метокси (U.S. патенты 4313946 и 4315929) (выделяют из Trewia nudiflora); С-18-N-деметил (U.S. патенты 4362663 и 4322348) (получают деметилированием майтансинола с помощью Streptomyces); и 4,5-дезокси (U.S. патент 4371533) (получают восстановлением майтансинола с помощью трихлорида титана/LAH). Многие положения в соединениях майтансина известны как полезные в качестве положений для связывания, в зависимости от типа связи. Для образования эфирной связи подходит положение С-3, содержащее гидроксильную группу, положение С-14, модифицированное гидроксиметилом, положение С-15, модифицированное гидроксильной группой, и положение С-20, содержащее гидроксильную группу.
Соединения майтансина ингибируют пролиферацию клеток путем ингибирования образования микротрубочек во время митоза посредством ингибирования полимеризации белка микротрубочек - тубулина (Remillard et al. (1975) Science 189:1002-1005). Майтансины и майтансиноиды сильно цитотоксичны, но их клиническое применение в терапии рака сильно ограничивалось их тяжелыми системными побочными эффектами, которые объясняются главным образом их плохой избирательностью к опухолям. Клинические испытания с майтансином были прерваны из-за серьезных отрицательных эффектов на центральную нервную систему и желудочно-кишечную систему (Issel et al (1978) Can. Treatment. Rev. 5:199-207).
Лекарственные молекулы майтансиноидов привлекательны как молекулы лекарств в конъюгатах иммуноглобулинов с лекарствами, так как они: (i) относительно доступны для получения путем ферментации или химической модификации, преобразования продуктов ферментации, (ii) поддаются образованию производных с функциональными группами, подходящими для конъюгирования с антителами через не-дисульфидные линкеры, (iii) стабильны в плазме и (iv) эффективны против целого ряда раковых клеточных линий (US 2005/0169933; WO 2005/037992; U.S. патент 5208020).
Как и в отношении других лекарственных молекул, в качестве соединений изобретения предусмотрены все стереоизомеры лекарственных молекул майтансиноидов.
Лекарственные молекулы в конъюгатах иммуноглобулинов с лекарствами также включают доластатины и их пептидные аналоги и производные - ауристатины (U.S. патенты 5635483; 5780588). Показано, что доластатины и ауристатины нарушают динамику микротрубочек, гидролиз GTP и деление ядер и клеток (Woyke et al. (2001) Antimicrob. Agents Chemother. 45(12):3580-3584) и обладают противораковой (U.S. патент 5663149) и противогрибковой активностью (Pettit et al. (1998) Antimicrob. Agents Chemother. 42:2961-2965). Различные формы лекарственных молекул доластатина или ауристатина можно ковалентно присоединять к антителам через N-(амино)-конец или С-(карбоксильный)-конец пептидной молекулы лекарства (WO 02/088172; Doronina et al. (2003) Nature Biotechnology 21(7):778-784; Francisco et al. (2003) Blood 102(4):1458-1465).
Типичные воплощения ауристатинов включают связанные по N-концу лекарственные молекулы монометилауристатина DE и DF, раскрытые в WO 2005/081711; Senter et al, Proceedings of the American Association for Cancer Research, Volume 45, Abstract Number 623, presented Mar. 28, 2004, содержание которых прямо включено путем ссылки во всей полноте.
Как правило, лекарственные молекулы на основе пептидов могут быть получены образованием пептидной связи между двумя или несколькими аминокислотами и/или пептидными фрагментами. Такие пептидные связи можно получить, к примеру, методом жидкофазного синтеза (см. Е. Schroder and K. Luibke, "The Peptides", volume 1, pp 76-136, 1965, Academic Press), который хорошо известен в области химии пептидов.
Лекарственные молекулы включают калихеамицин и его аналоги и производные. Антибиотики семейства калихеамицинов способны образовывать разрывы двунитчатой ДНК в суб-пикомолярных концентрациях. Насчет получения конъюгатов семейства калихеамицинов см. U.S. патенты 5712374; 5714586; 5739116; 5767285; 5770701; 5770710; 5773001; 5877296. Структурные аналоги калихеамицина, которые можно использовать, включают, без ограничения, γ1 I, α2 I, α3 I, N-ацетил-γ1 I, PSAG и θI 1 (Hinman et al. Cancer Research 53:3336-3342 (1993); Lode et al. Cancer Research 58:2925-2928 (1998).
Белковые токсины включают, к примеру, А-цепь дифтерийного токсина, не связывающиеся активные фрагменты дифтерийного токсина, А-цепь экзотоксина (из Pseudomonas aeruginosa), А-цепь рицина (Vitetta et al (1987) Science, 238:1098), А-цепь абрина, А-цепь модексина, альфа-сарцин, белки Aleurites fordii, белки диантина, белки Phytolaca americana (PAPI, PAPII и PAP-S), ингибитор Momordica charantia, курцин, кротин, ингибитор Sapaonaria officinalis, гелонин, митогеллин, рестриктоцин, феномицин, еномицин и трихотецены (WO 93/21232).
Терапевтические радиоизотопы включают, к примеру, 32P, 33Р, 90Y, 125I, 131I, 131In, 153Sm 186Re, 188Re, 211At, 212Bi, 212Pb и радиоактивные изотопы Lu.
В конъюгаты могут быть включены радиоизотопы или другие метки известными способами Fraker et al. (1978) Biochem. Biophys. Res. Commun. 80: 49-57; "Monoclonal Antibodies in Immunoscintigraphy" by Chatal, CRC Press, 1989). Типичным хелатирующим агентом для конъюгации радионуклидов с антителами является меченная 14С 1-изотиоцианатобензил-3-метилдиэтилентриаминопентауксусная кислота (MX-DTPA) (WO 94/11026).
Линкеры
В некоторых воплощениях настоящего изобретения конъюгаты иммуноглобулинов включают молекулу линкера, содержащую по меньшей мере два реактивных сайта. Один реактивный сайт связан с замененным остатком цистеина в иммуноглобулине, а другой реактивный сайт связан с атомом или молекулой. "Линкер" - это бифункциональная или мультифункциональная молекула, которая может применяться для соединения одной или нескольких лекарственных молекул и звена иммуноглобулина с образованием конъюгата иммуноглобулина. Конъюгаты иммуноглобулинов удобно получаются с помощью линкера, содержащего реактивную функциональную группу для связывания с лекарством или другой молекулой и с иммуноглобулином. Тиол цистеина в модифицированном иммуноглобулине с заменой на цистеин может образовывать связь с функциональной группой линкерного реагента, лекарственной молекулой или промежуточным продуктом лекарство-линкер.
В одном аспекте линкер содержит реактивный сайт, обладающий электрофильной группой, которая реагирует с нуклеофильным цистеином, находящимся на антителе. Цистеиновый тиол антитела реагирует с электрофильной группой на линкере и образует ковалентную связь с линкером. Полезными электрофильными группами являются, без ограничения, малеимидные и галоацетамидные группы.
Модифицированные иммуноглобулины изобретения реагируют с линкерными реагентами или промежуточными продуктами линкер-лекарство, с электрофильными функциональными группами типа малеимида или α-галокарбонила в соответствии с методом конъюгации, приведенным на стр.766 в Klussman et al. (2004) Bioconjugate Chemistry 15(4):765-773.
Линкер может содержать аминокислотные остатки. Аминокислотное звено, если оно есть, связывает иммуноглобулин с лекарственной молекулой в конъюгатах иммуноглобулинов с лекарствами по изобретению.
Аминокислотный линкер может представлять собой, к примеру, дипептидное, трипептидное, тетрапептидное, пентапептидное, гексапептидное, гептапептидное, октапептидное, нонапептидное, декапептидное, ундекапептидное или додекапептидное звено. Аминокислотные остатки, составляющие аминокислотное звено, включают те, что встречаются в природе, а также минорные аминокислоты и не встречающиеся в природе аналоги аминокислот типа цитруллина.
Аминокислотное звено может энзиматически расщепляться одним или несколькими ферментами, в том числе связанными с раком протеазами, с высвобождением лекарственной молекулы.
В другом воплощении линкером может быть линкер дендритного типа для ковалентного присоединения к антителу больше чем одной лекарственной молекулы через разветвленную мультифункциональную молекулу линкера (Sun et al. (2002) Bioorganic & Medicinal Chemistry Letters 12:2213-2215; Sun et al (2003) Bioorganic & Medicinal Chemistry 11:1761-1768). Дендритные линкеры могут повышать молярное соотношение лекарства к антителу, т.е. нагрузку, которая связана с активностью конъюгата иммуноглобулина с лекарством. Таким образом, если модифицированный иммуноглобулин несет только одну реактивную тиоловую группу цистеина, то через дендритный линкер можно присоединить несколько лекарственных молекул.
В другом воплощении линкер может быть замещен группами, которые модулируют растворимость или реактивность, заряженный заместитель типа сульфоната (-SO3 -) или аммония может повышать водорастворимость реагента и облегчать реакцию связывания линкерного реагента с иммуноглобулином или лекарственной молекулой либо способствовать реакции связывания промежуточного продукта иммуноглобулин-линкер с лекарственной молекулой или промежуточного продукта лекарство-линкер с иммуноглобулином в зависимости от пути синтеза, используемого для получения конъюгата иммуноглобулина.
Соединения по изобретению прямо предусматривают, без ограничения, конъюгаты иммуноглобулинов, образованные с линкерными реагентами: ВМРЕО, BMPS, EMCS, GMBS, HBVS, LC-SMCC, MBS, MPBH, SBAP, SIA, SIAB, SMCC, SMPB, SMPH, сульфо-EMCS, сульфо-GMBS, сульфо-KMUS, сульфо-MBS, сульфо-SIAB, сульфо-SMCC, сульфо-SMPB и SVSB (сукцинимидил-(4-винилсульфон)бензоат), включая бис-малеимидные реагенты: DTME, BMB, BMDB, ВМН, ВМОЕ, ВМ(РЕО)3 и ВМ(РЕО)4, которые коммерчески доступны от Pierce Biotechnology, Inc., Customer Service Department, P.O. Box 117, Rockford, 111., 61105 USA, USA 1-800-874-3723, International +815-968-0747. См. стр.467-498 и 2003-2004 в Applications Handbook и Catalog. Бис-малеимидные реагенты позволяют присоединение тиоловой группы цистеина к тиол-содержащей лекарственной молекуле, метке или промежуточному линкеру последовательным или параллельным образом. Другие функциональные группы, помимо малеимида, которые реагируют с тиоловой группой цистеина, лекарственной молекулой, меткой или промежуточным линкером, включают, без ограничения, йодацетамид, бромацетамид, винилпиридин, дисульфид, пиридилдисульфид, изоцианат и изотиоцианат.
Соответственно, одним объектом настоящего изобретения является получение конъюгатов иммуноглобулинов, содержащих по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL), 25(VH), 125(CH1), 248(CH2), 254(CH2), 286(CH2), 298(CH2) и 326(CH2), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина, и атом или молекулу, которые конъюгированы с остатком цистеина. В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 248(CH2) и 326(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 25(VH) и 286(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 254(CH2) и 298(VH). В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин выбирается из группы, содержащей IgG1, IgG2, IgG3 и IgG4. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает IgG1. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CH1 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CH2 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CH3 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен CL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен VH человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина включает домен VL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина дополнительно включает молекулу линкера, имеющую по меньшей мере два реакционноспособных сайта, причем первый реакционноспособный сайт связан с остатком цистеина иммуноглобулина, а второй реакционноспособный сайт связан с атомом или молекулой. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, содержащими молекулу линкера, молекула линкера выбирается из группы, состоящей из гидразона, дисульфида, пептида, хелатирующего агента и малеимида. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула выбираются из группы, состоящей из радионуклида, химиотерапевтического агента, микробного токсина, растительного токсина, полимера, углевода, цитокина, флуоресцентной метки, люминесцентной метки, фермент-субстратной метки, фермента, пептида, пептидо-миметика, нуклеотида, siPHK, микроРНК, РНК-миметика и аптамера. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула выбираются из группы, состоящей из 90Y, 131I, 67Cu, 177Lu, 213Bi, 211At, калихеамицина, дуокармицина, майтансиноида, ауристатина, антрациклина, экзотоксина A Pseudomonas, дифтерийного токсина, рицина, полиэтиленгликоля, гидроксиэтил-крахмала и остатка маннозила. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула снижает иммуногенность немутированного иммуноглобулина. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, атом или молекула повышает иммуногенность немутированного иммуноглобулина. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина дополнительно обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
Соответственно, другим объектом настоящего изобретения является получение модифицированных или выделенных иммуноглобулинов, содержащих по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL), 25(VH), 125(CH1), 248(CH2), 254(CH2), 286(CH2) и 326(CH2), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина. В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1). В некоторых, воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 248(CH2) и 326(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток, выбранный из группы, состоящей из 25(VH) и 286(CH2). В некоторых воплощениях по меньшей мере одна мутация приходится на остаток 254(CH2). В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин выбирается из группы, содержащей IgG1, IgG2, IgG3 и IgG4. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает IgG1. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CH1 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CH2 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CH3 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен CL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен VH человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, модифицированный или выделенный иммуноглобулин включает домен VL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина дополнительно обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
Получение конъюгатов иммуноглобулинов с лекарствами
В одном аспекте настоящее изобретение включает способы получения конъюгатов иммуноглобулинов. Конъюгаты иммуноглобулинов с лекарствами могут быть получены несколькими путями, используя реакции органической химии, условия и реагенты, известные специалистам, включая: (1) реакцию цистеиновой группы модифицированного иммуноглобулина с линкерным реагентом с образованием промежуточного соединения иммуноглобулин-линкер, через ковалентную связь, с последующей реакцией с активированной молекулой лекарства; и (2) реакцию нуклеофильной группы лекарственной молекулы с линкерным реагентом с образованием промежуточного соединения лекарство-линкер, через ковалентную связь, с последующей реакцией с цистеиновой группой модифицированного иммуноглобулина. Способы конъюгации (1) и (2) могут применяться с различными модифицированными иммуноглобулинами, молекулами лекарств и линкерами для получения конъюгатов иммуноглобулинов с лекарствами.
Тиоловые группы цистеина антител являются нуклеофильными и способны реагировать с образованием ковалентных связей с электрофильными группами на линкерных реагентах и промежуточных соединениях лекарство-линкер, включая: (i) активные эфиры, как-то эфиры NHS, эфиры HOBt, галоформиаты и галоангидриды; (ii) алкил- и бензилгалиды, как-то галоацетамиды; (iii) альдегиды, кетоны, карбоксильные и малеимидные группы; и (iv) дисульфиды, включая пиридилдисульфиды, через обмен сульфидов. Нуклеофильные группы на молекуле лекарства включают, без ограничения: аминогруппы, тиоловые, гидроксильные, гидразидные, оксимные, гидразиновые, тиосемикарбазоновые, гидразинкарбоксилатные и арилгидразидные группы, способные реагировать с образованием ковалентных связей с электрофильными группами на молекулах линкеров и линкерных реагентов.
Майтансины, к примеру, можно преобразовать в May-SSCH3, который можно восстановить до свободного тиола, May-SH, и прореагировать с модифицированным антителом (Chari et al. (1992) Cancer Research 52:127-131), получая иммуноконъюгат майтансиноид-антитело с дисульфидным линкером. Конъюгаты майтансиноид-антитело с дисульфидными линкерами зарегистрированы (WO 04/016801; U.S. патент 6884874; US 2004/039176 A1; WO 03/068144; US 2004/001838 A1; U.S. патенты 6441163, 5208020, 5416064; WO 01/024763). Дисульфидный линкер SPP получали с помощью линкерного реагента N-сукцинимидил-4-(2-пиридилтио)пентаноата.
При определенных условиях модифицированные иммуноглобулины могут стать реактивными для конъюгации с линкерными реагентами при обработке восстанавливающим реагентом типа DTT (Cleland's реагент, дитиотреитол) или ТСЕР (трис(2-карбоксиэтил)фосфин гидрохлорид; Getz et al. (1999) Anal. Biochem. 273:73-80; Soltec Ventures, Beverly, Mass.) или другими восстанвливающими реагентами, известными специалистам в данной области.
Соответственно, объектом настоящего изобретения является обеспечение способов получения конъюгатов иммуноглобулинов путем обеспечения модифицированных или выделенных иммуноглобулинов, как изложено выше, или всевозможных комбинаций их воплощений, восстановления одного или нескольких замененных остатков цистеина восстанавливающим реагентом с образованием восстановленных остатков цистеина и инкубации иммуноглобулина с атомом или молекулой, причем атом или молекула реагирует с восстановленными остатками цистеина с образованием конъюгата иммуноглобулина.
Склонность к пространственной агрегации
В одном аспекте изобретение касается способов отбора остатков на поверхности белка для мутации на цистеин и снижения перекрестного сшивания модифицированного иммуноглобулина или конъюгата иммуноглобулина. Изобретение может применяться для создания иммуноглобулинов и конъюгатов иммуноглобулинов с пониженной склонностью к перекрестному сшиванию, т.е. иммуноглобулин или конъюгат иммуноглобулина в концентрированном растворе остается главным образом в виде мономера, а не в виде агрегированных мультимеров более высокого порядка. Приведенные способы означают прогресс в способности компьютерных методов оценивать склонность белка к перекрестному сшиванию. В частности, методы основываются, по крайней мере частично, на расчете SAA (площади, доступной растворителю. Solvent Accessible Area), которая известна в данной области для характеристики поверхности белка. SAA дает площадь поверхности каждой аминокислоты или структуры белка, находящейся в контакте с растворителем. Как правило, SAA рассчитывают вычислением местоположения центра сферы зонда по мере его качения по белковой поверхности, т.е. поверхности структурной модели белка. Сфера зонда имеет такой же радиус, как и молекула воды: R=1,4 Å. Известны и альтернативные методы расчета SAA, описанные ниже, которые совместимы с описанными здесь методами. Несмотря на то, что величина SAA весьма полезна для характеристики поверхности белка, она оказалась неадекватной для характеристики гидрофобных пятен на поверхности белка, которые потенциально склонны к агрегации из-за следующих недостатков:
1. SAA не делает различий между гидрофобными и гидрофильными участками;
2. SAA не прямо пропорциональна гидрофобности остатка (Met имеет большую площадь поверхности, чем Leu, но он менее гидрофобен);
3. SAA не указывает, что несколько гидрофобных участков находятся рядом и поэтому могут повысить гидрофобность определенного участка. Эти остатки могут находиться рядом либо в первичной последовательности, либо в третичной последовательности, даже если они стоят далеко в первичной последовательности. Так или иначе, они могут повысить гидрофобность определенного участка на поверхности антитела.
Одна величина, описанная здесь, а именно эффективная SAA, получается путем вычисления гидрофобности той части аминокислоты, которая выходит на поверхность, согласно нижеприведенной формуле:

Другое воплощение эффективной SAA дополнительно включает суммирование эффективных значений SAA по меньшей мере через два, через три, через четыре, через пять или через шесть (например, 2. 3, 4, 5, 6 и т.д.) аминокислотных остатков, стоящих рядом в первичной последовательности белка. Хотя эффективная SAA представляет улучшение по сравнению с исходной SAA, тем не менее она не способна полностью объяснить структуру свернутого белка и тот факт, что аминокислоты, которые не стоят рядом в последовательности белка, могут соседствовать друг с другом в свернутой вторичной, третичной или четвертичной структуре белка. Такая укладка белка может формировать склонные к агрегации участки, которые отсутствуют в самой первичной структуре или же определяются только при более пристальном анализе свернутой структуры белка.
Настоящим изобретением предусмотрена новая, более совершенная величина, именуемая склонностью к пространственной агрегации, которая отводит главное место эффективной гидрофобности определенных пятен или участков на поверхности белка. Склонность к пространственной агрегации вычисляется для определенных пространственных участков на или вблизи от атомов структурной модели белка.
В этом плане "определенный пространственный участок" представляет собой трехмерное пространство или объем, выбранный для фиксирования локальной физической структуры и/или химического окружения на или вблизи от белковой структуры. В особенно предпочтительном воплощении склонность к пространственной агрегации вычисляется для сферических участков радиусом R с центром на атомах в белке (например, атомах в структурной модели белка). Склонность к пространственной агрегации можно также рассчитать для сферических участков радиусом R с центром на химических связях или расположенном в пространстве возле структурной модели. Соответственно, в другом воплощении SAP можно рассчитать для заданного пространственного участка с центром возле атома, например, с центром на точке в пространстве, отстоящей на 1-10 Å, 1-5 Å или 1-2 Å от центра определенного атома или химической связи.
В некоторых воплощениях выбранный радиус R составляет от 1Å до 50Å. В предпочтительных воплощениях выбранный радиус составляет по меньшей мере 1Å, по меньшей мере 3Å, по меньшей мере 4Å, по меньшей мере 5Å, по меньшей мере 6Å, по меньшей мере 7Å, по меньшей мере 8Å, по меньшей мере 9Å, по меньшей мере 10Å, по меньшей мере 11Å, по меньшей мере 12Å, по меньшей мере 15Å, по меньшей мере 20Å, по меньшей мере 25Å или по меньшей мере 30Å. В некоторых воплощениях выбранный радиус составляет от 5Å до 15Å, от 5Å до 12Å или от 5Å до 10Å. В конкретных воплощениях выбранный радиус составляет 5Å или 10Å.
В других воплощениях участок, для которого рассчитывается склонность к пространственной агрегации, не является сферическим. Возможная форма участка может также составлять куб, цилиндр, конус, эпилептический сфероид, пирамиду, полусферу или любую другую форму, которую можно использовать для охвата части пространства. В таких воплощениях размер участка можно выбирать, используя другие величины, чем радиус, например, расстояние от центра формы до грани или вершины.
В некоторых воплощениях SAP может применяться для отбора остатков в белке, в частности антителе или иммуноглобулине, которые можно заменить на цистеин без увеличения склонности белка к перекрестному сшиванию. Настоящее изобретение должно упростить процесс идентификации остатков, которые могут быть заменены на цистеин без увеличения склонности к перекрестному сшиванию.
Таким образом, в общих чертах, способ расчета склонности к пространственной агрегации для определенного атома в белке включает: (а) идентификацию одного или нескольких атомов в структурной модели, представляющей белок, причем один или несколько атомов находятся внутри заданного пространственного участка с центром на или вблизи от определенного атома; (b) вычисление, для каждого из одного или нескольких атомов в заданном пространственном участке, отношения доступной для растворителя площади (SAA) атомов к SAA атомов в идентичном остатке, который полностью экспонирован; (с) умножение каждого отношения на гидрофобность одного или нескольких атомов; и (d) суммирование произведений из стадии (с); при этом сумма составляет значение SAP для определенного атома.
В связанном воплощении значение SAP можно рассчитать другим способом, включающим: (а) идентификацию одного или нескольких аминокислотных остатков в структурной модели, представляющей белок, причем один или несколько аминокислотных остатков содержат по меньшей мере один атом внутри заданного пространственного участка с центром на или вблизи от определенного атома; (b) вычисление, для каждого из идентифицированных одного или нескольких аминокислотных остатков, отношения доступной для растворителя площади (SAA) атомов в аминокислоте к SAA атомов в идентичном остатке, который полностью экспонирован; (с) умножение каждого отношения на гидрофобность одного или нескольких аминокислотных остатков, определенную по шкале гидрофобности аминокислот; и (d) суммирование произведений из стадии (с); при этом сумма составляет значение SAP для определенного атома. В предпочтительных воплощениях структурная модель подвергается обработке перед стадией (а), подвергая структурную модель взаимодействию с растворителем на модели молекулярной динамики. Когда аминокислота определяется как содержащая по меньшей мере один атом внутри заданного пространственного участка, то этот по меньшей мере один атом может быть атом, который должен находиться исключительно в боковой цепи аминокислоты. С другой стороны, это может быть атом, который должен находиться в основной цепи.
В других воплощениях этот способ дополнительно может необязательно включать проведение моделирования молекулярной динамики перед стадией (а) и повторение стадий (a)-(d), каждый раз проводя дополнительное моделирование молекулярной динамики на нескольких временных этапах, получая при этом несколько сумм на стадии (d) и рассчитывая среднее значение суммы; при этом рассчитанное среднее значение составляет SAP для определенного атома.
Специалисты в данной области должны понимать, что воплощение настоящего изобретения, в котором используется среднее значение, рассчитанное на модели молекулярной динамики, потребует более интенсивных вычислений. Такое воплощение в некоторых случаях также обеспечит более точную или с более высоким разрешением карту значений склонности к пространственной агрегации. Однако рассматриваемые здесь эксперименты показали, что способ все-таки является очень точным и тогда, когда не применяется усреднение по молекулярной динамике. В одном предпочтительном воплощении значения склонности к пространственной агрегации можно рассчитать для всех белковых структур в базе данных, например, Банке данных по белкам. (Protein Data Bank, PDB), при этом быстро определяются гидрофобные остатки и участки во всех известных белковых структурах. Этот способ позволяет быстрый скрининг больших наборов белков для идентификации потенциально склонных к агрегации участков и/или сайтов взаимодействия белков.
В предпочтительном применении склонность к пространственной агрегации описывается следующей формулой:
SAPатома=∑среднее значение на модели(∑атомы в пределах R от атома((SAA-R/SAA-fe)×hb атома)
где: 1) SAA-R означает SAA атомов боковой цепи в пределах радиуса R, которая рассчитывается по каждому моменту моделирования. SAA предпочтительно рассчитывают на имитационной модели вычислением местоположения центра сферы зонда по мере его качения по поверхности белка. Сфера зонда имеет такой же радиус, как и молекула воды: R=1,4 Å. Специалисты в данной области должны понимать, что другие способы расчета SAA должны быть совместимыми с описанными здесь способами расчета SAP. SAA можно также рассчитать только по атомам основной цепи аминокислоты (т.е. по атомам пептидного остова и связанным с ними водородам). С другой стороны, SAA можно рассчитать только по атомам основной цепи аминокислоты за исключением связанных с ними водородов;
2) SAA-fe означает SAA боковой цепи полностью экспонированного остатка (скажем, для аминокислоты 'X'), которое в предпочтительном воплощении получают вычислением SAA боковых цепей среднего остатка в полностью вытянутой конформации трипептида 'Ala-X-Ala'; и
3) hb атома означает гидрофобность атома, которую получают, как описано выше, по шкале гидрофобности Black and Mould (Black and Mould, Anal. Biochem. 1991, 193, 72-82). Шкалу нормализуют таким образом, чтобы гидрофобность глицина равнялась нулю. Поэтому аминокислоты, более гидрофобные, чем глицин, будут положительными, а менее гидрофобные, чем глицин, будут отрицательными по шкале гидрофобности.
Остаток, который "полностью экспонирован" - это остаток Х в полностью вытянутой конформации трипептида Ala-X-Ala. Специалисты в данной области должны понимать, что такое расположение устроено для того, чтобы вычисление SAA по такому остатку Х давало максимально возможную площадь, доступную для растворителя. Соответственно, предусматривается, что при вычислении можно использовать и другие остатки, помимо аланина, без полного нарушения или изменения результатов.
Как описано выше, способы настоящего изобретения могут применяться к любым структурным моделям белков, включая рентгено структурные, используя ту же формулу, что приведена выше.
Аналогичным образом, если рентгеновская структура недоступна, тот же самый параметр склонности к пространственной агрегации можно применить к структуре, созданной путем моделирования по гомологии, и параметр SAP можно рассчитать по той же формуле, что приведена выше.
В некоторых воплощениях рассчитывается склонность к пространственной агрегации для всех атомов в структурной модели белка. В некоторых воплощениях атомистические значения склонности к пространственной агрегации могут усредняться по каждому индивидуальному остатку белка или по небольшим группам остатков.
Применение методологии SAP
В одном аспекте настоящее изобретение может применяться, как описано выше, для идентификации гидрофобных аминокислотных остатков, участков или пятен в белке. Не придерживаясь каких-то определенных пороговых значений, атомы или аминокислотные остатки со склонностью к пространственной агрегации >0 считаются гидрофобными или находящимися в участке, склонном к агрегации. В зависимости от типа белка, конкретной структуры и растворителя, в котором он существует, может быть желательно идентифицировать атомы или остатки с использованием предела отсечения, который слегка меньше нуля, например, выбирая атомы или остатки, у которых склонность к пространственной агрегации больше -0,1, -0,15, -0,2 и т.д. С другой стороны, может быть желательно использовать более строгий предел отсечения, например, 0, 0,05, 0,1, 0,15, 0,2 и т.д., чтобы отобрать наиболее гидрофобные атомы, остатки или пятна. Кроме того, поскольку алгоритм дает более высокие значения для остатков в центре пятна, то для мутации на менее гидрофобные остатки для снижения агрегации также можно отбирать остатки в пределах 3Å, 4Å, 5Å, 7,5Å или 10Å от остатка, соответствующего пределу отсечения. В другом воплощении может быть предпочтительно просто отбирать атомы или остатки с большей склонностью к пространственной агрегации, чем у атомов или остатков, находящихся рядом последовательно (например, вдоль последовательности белка) или, в предпочтительном воплощении, пространственно (т.е. в трехмерной структуре). Одним из предпочтительных способов отбора атомов или остатков в гидрофобном пятне является картирование расчетных значений склонности к пространственной агрегации, например, по цветной кодировке или цифровой кодировке, на структурной модели белка, из которой они были получены, чтобы визуализировать различия в склонности к пространственной агрегации по всей поверхности белка и тем самым облегчить отбор гидрофобных пятен или остатков. В особенно предпочтительном воплощении расчеты склонности к пространственной агрегации выполняются раздельно с использованием двух значений, выбранных для радиуса, одного с большим разрешением, например, 5Å, и другого с меньшим разрешением, например, 10Å. В таком воплощении на карте с меньшим разрешением будут видны более крупные или широкие гидрофобные пятна на белковой структуре. После отбора представляющих интерес гидрофобных пятен на карте с меньшим разрешением эти пятна можно рассмотреть более детально на карте с большим разрешением, что в некоторых воплощениях позволит специалистам в данной области легче и точнее выбирать остатки для мутации или модификации, при осмотре гидрофобного пятна на карте с большим разрешением может оказаться желательным отобрать для мутации остаток с самым высоким показателем SAP или наиболее гидрофобный (например, самый гидрофобный остаток в пятне по шкале Black and Mould, Anal. Biochem. 1991, 193, 72-82).
В специфическом воплощении способ идентификации склонного к агрегации участка на белке включает: (а) картирование на структурной модели значений SAP для атомов в белке, рассчитанных одним из описанных здесь способов; и (b) идентификацию участка внутри белка, содержащего несколько атомов, у которых SAP>0; при этом участок, склонный к агрегации, составляют аминокислоты, содержащие данные несколько атомов. В таких воплощениях можно рассчитать значения SAP для всех атомов в белке или части атомов. Предусматривается, что можно рассчитать SAP только для определенных остатков или групп остатков, представляющих интерес.
В аналогичном воплощении может оказаться информативным нанесение на график показателей SAP для атомов (или показателей SAP, усредненных по аминокислотным остаткам). Такой график, представляющий показатель SAP вдоль атомов или остатков в белке, позволит легко идентифицировать пики, которые могут означать кандидатов на замену. В особенно предпочтительном воплощении на график наносятся показатели SAP вдоль атомов или остатков в белке и рассчитывается площадь под кривой (AUC) для пиков на графике. В таком воплощении пики с большим значением AUC представляют более крупные или более гидрофобные участки, склонные к агрегации. В предпочтительных воплощениях нужно отобрать для замены один или несколько остатков, идентифицированных как находящиеся в пике или, что более предпочтительно, в пике с большим значением AUC.
В предпочтительных воплощениях настоящее изобретение может применяться для отбора остатков иммуноглобулина для мутации на цистеин. При этом рассчитывается значение SAP первого аминокислотного остатка на поверхности иммуноглобулина. Если значение SAP равно или находится между значениями 0 и -0,11, то первый остаток отбирается для мутации на цистеин. В другом воплощении рассчитываются значения SAP нескольких остатков иммуноглобулина в непосредственной близости от первого остатка. Если несколько остатков имеют значения SAP меньше 0, то первый остаток отбирается для мутации на цистеин.
Варианты иммуноглобулинов могут быть получены любым способом, известным в данной области, включая сайт-направленный мутагенез и другие технологии рекомбинантной ДНК, например, см. US Pat. Nos. 5284760; 5556747; 5789166; 6878531; 5932419; и 6391548.
В предпочтительных воплощениях настоящее изобретение может применяться для получения вариантов иммуноглобулинов, которые можно конъюгировать с атомом или молекулой путем замены по меньшей мере одного остатка аминокислоты, выходящей на поверхность иммуноглобулина и идентифицированной любым из описанных здесь способов, на остаток природной аминокислоты, остаток модифицированой аминокислоты, остаток необычной аминокислоты, остаток не встречающейся в природе аминокислоты или аналог или производное аминокислоты, которые могут использоваться для конъюгирования иммуноглобулина с атомом или молекулой. В предпочтительных воплощениях остаток аминокислоты, выходящей на поверхность иммуноглобулина, заменяется на цистеин. В других воплощениях аминокислотный остаток заменяется на лизин, аспартат или пирорлизин.
Синтез не встречающихся в природе аминокислот известен специалистам в данной области и подробно описан, например, в U.S. патентной публикации №2003-0082575. В общем, для синтеза или включения не встречающихся в природе, модифицированных или необычных аминокислот в белки можно применять любые известные методы, в том числе методы, описанные или приведенные в публикациях Liao J., Biotechnol Prog. 2007 23(1):28-31; Rajesh and Iqbal, Curr Pharm Biotechnol. 2006, 7(4):247-59; Cardillo et al., Mini Rev Med Chem. 2006, 6(3):293-304; Wang et al., Annu Rev Biophys Biomol Struct. 2006, 35:225-49; Chakraborty et al., Glycoconj J. 2005, 22(3):83-93. В качестве дополнительного примера для разработки и введения не встречающихся в природе или необычных аминокислот в белки может применятся технология Ambrx ReCODE™, как указано в описанных здесь способах.
Варианты иммуноглобулинов и конъюгаты иммуноглобулинов по изобретению могут проявлять большую или лучшую стабильность при определении, к примеру, методом SDS-PAGE в невосстанавливающих условиях.
Соответственно, объектом настоящего изобретения является получение выделенных или рекомбинантных полинуклеотидов, кодирующих модифицированные иммуноглобулины, как обсуждалось выше, и всевозможные комбинации их воплощений. В некоторых воплощениях полинуклеотид находится в векторе. В некоторых воплощениях вектор является экспрессионным вектором. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, с полинуклеотидом функционально связан индуцибельный промотор. Следующий аспект охватывает клетки хозяина с вектором из любого из предыдущих воплощений. В некоторых воплощениях клетки хозяина способны экспрессировать иммуноглобулин, кодируемый полинуклеотидом.
Соответственно, объектом настоящего изобретения является обеспечение способов получения иммуноглобулинов с пониженной склонностью к перекрестному сшиванию, включающих обеспечение культуральной среды, содержащей клетки хозяина из предыдущего абзаца, и помещение культуральной среды в условия, при которых экспрессируется иммуноглобулин. В некоторых воплощениях способы включают дополнительную стадию выделения экспрессированного иммуноглобулина.
Соответственно, объектом настоящего изобретения является обеспечение способов отбора остатков иммуноглобулина для мутации на цистеин, включающих вычисление склонности к пространственной агрегации первого аминокислотного остатка на поверхности иммуноглобулина, вычисление склонности к пространственной агрегации нескольких остатков иммуноглобулина в непосредственной близости от первого остатка и отбор первого аминокислотного остатка для мутации на цистеин, если склонность к пространственной агрегации первого аминокислотного остатка равна или находится между значениями 0 и -0,11 и если у нескольких остатков склонность к пространственной агрегации меньше 0. В некоторых воплощениях несколько остатков находятся в пределах 15Å от первого остатка. В некоторых воплощениях несколько остатков находятся в пределах 10Å от первого остатка. В некоторых воплощениях несколько остатков находятся в пределах 7,5Å от первого остатка. В некоторых воплощениях несколько остатков находятся в пределах 5Å от первого остатка. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, вычисление склонности к пространственной агрегации включает вычисление склонности к пространственной агрегации для сферического участка с радиусом из центра атома в остатке. В некоторых воплощениях радиус сферического участка составляет по меньшей мере 5Å.
В некоторых воплощениях изобретение также касается программы рассчета для определения SAP в соответствии со способами изобретения. В других воплощениях изобретение касается компьютера, суперкомпьютера или кластера компьютеров, предназначенных для выполнения способов изобретения. В следующем аспекте изобретением предусмотрена служба на основе веб (сети), сервера или Интернета для отбора остатков белка для мутации на цистеин, причем служба включает прием данных о белке (например, структурной модели белка) от пользователя (напр,, через Интернет) или извлечение таких данных из базы данных с тем, что провайдер службы может генерировать, извлекать или выводить статическую структуру белка, необязательно включая моделирование молекулярной динамики белка для получения динамической структуры белка, определение SAP для атомов или остатков белка на основе полученной при этом статической или динамической структуры, и выдачу данных SAP, к примеру, в виде структурной модели, маркированной этими данными SAP, через провайдера службы пользователю. В некоторых воплощениях пользователем является человек. В других воплощениях пользователем является компьютерная система или автоматизированный компьютерный алгоритм.
В некоторых воплощениях настоящим изобретением предусмотрена система вычисления SAP, включающая: веб-сервер для обеспечения веб-сервиса для расчета SAP на терминале пользователя через Интернет; базу данных для хранения общей информации о способе расчета, гидрофобности аминокислот и т.д., и вычислительный сервер для выполнения расчета SAP на основе информации в базе данных и информации, предоставленной или переданной пользователем через Интернет.
В некоторых воплощениях веб-сервер и вычислительный сервер представляют собой одну и ту же компьютерную систему. В некоторых воплощениях компьютерная система представляет собой суперкомпьютер, кластер компьютеров либо отдельную рабочую станцию или сервер. В связанном с этим воплощении веб-сервер системы вычисления SAP дополнительно включает контроллер для контролирования всей операции, блок выхода в сеть для подключения к Интернету и блок веб-сервиса для предоставления веб-службы для расчета SAP на терминале пользователя, который подключен через интернет.
Кроме того, воплощения настоящего изобретения также касаются устройств хранения данных на машиночитаемом носителе, содержащим управляющую программу для выполнения различных выполняемых компьютером операций, например, вычисления SAP для структурной модели, вычисления SAA, вычисления эффективного значения SAA, обработки структурных моделей, выполнения имитаций молекулярной динамики, организации и хранения соответствующих данных или выполнения других описанных здесь операций. Машиночитаемые носители представляют собой любые устройства для хранения данных, на которых хранятся данные, которые затем могут считываться компьютерной системой. Примеры машиночитаемых носителей включают, без ограничения, жесткие диски, дискеты, флэшки, оптические диски (например, CD, DVD, HD-DVD, диски Blu-Ray и др.) и специально конфигурированные электронные устройства, такие как прикладные интегральные схемы (ASIC) или программируемые логические устройства (PLD). Машиночитаемый носитель также может распространяться как информационный сигнал, воплощенный в виде электромагнитного сигнала передачи модулированной информации через сеть сопряженных компьютерных систем, так что считываемый компьютером код хранится и исполняется рассредоточенным образом. Специалисты должны понимать, что вышеописанное оборудование и программное обеспечение имеют стандартную планировку и конструкцию. Связанные с компьютером, Интернетом, сервером и сервисом воплощения, описанные выше, могут применяться как в отношении SAA и эффективного значения SAA, так и SAP.
Фармацевтические композиции, содержащие иммуноглобулины и конъюгаты иммуноглобулинов
В другом аспекте настоящим изобретением предусмотрены композиции, например, фармацевтические композиции, содержащих один или несколько конъюгатов иммуноглобулинов, полученных способами изобретения и составленных вместе с фармацевтически приемлемым носителем. Фармацевтические композиции изобретения также могут применяться в комбинированной терапии, т.е. в комбинации с другими средствами. К примеру, комбинированная терапия может включать конъюгат иммуноглобулина настоящего изобретения в комбинации по меньшей мере с одним другим противораковым средством.
В настоящем изобретении "фармацевтически приемлемый носитель" включает всевозможные физиологически совместимые растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые средства, изотонические и замедляющие всасывание средства и т.п. Предпочтительно носитель подходит для внутривенного, внутримышечного, подкожного, парентерального, интраспинального или эпидермального введения (например, путем инъекции или вливания). В зависимости от способа применения, активное соединение, т.е. иммуноглобулин или его вариант по изобретению может быть покрыт материалом для защиты соединения от действия кислот и других природных условий, которые могут инактивировать соединение.
Фармацевтические композиции изобретения могут включать одну или несколько фармацевтически приемлемых солей. "Фармацевтически приемлемая соль" означает такую соль, которая сохраняет требуемую биологическую активность исходного соединения и не оказывает каких-либо нежелательных токсикологических эффектов (например, см. Berge S.M. et al. (1977) J. Pharm. Sci. 66:1-19). Примеры таких солей включают соли с кислотами и соли с основаниями. Соли с кислотами включают соли, полученные из нетоксичных неорганических кислот, таких как соляная, азотная, фосфорная, серная, бромистоводородная, иодистоводородная, фосфористая и др., а также из нетоксичных органических кислот, таких как алифатические моно- и дикарбоновые кислоты, фенил-замещенные алкановые кислоты, гидроксиалкановые кислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты и др. Соли с основаниями включают соли, полученные из щелочно-земельных металлов, таких как натрий, калий, магний, кальций и др., а также из нетоксичных органических аминов, таких как N,N'-дибензилэтилендиамин, N-метилглюкамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, прокаин и др.
Фармацевтические композиции изобретения также могут содержать фармацевтически приемлемый антиоксидант. Примеры фармацевтически приемлемых антиоксидантов включают: (1) водорастворимые антиоксиданты, как-то аскорбиновая кислота, цистеин гидрохлорид, бисульфат натрия, метабисульфит натрия, сульфит натрия и др.; (3) жирорастворимые антиоксиданты, как-то аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, альфа-токоферол и др.; и (4) хелаторы металлов, как-то лимонная кислота, этилендиамин-тетрауксусная кислота (EDTA), сорбитол, винная кислота, фосфорная кислота и др.
Примеры подходящих водных и неводных носителей, которые можно применять в фармацевтических композициях изобретения, включают воду, этанол, полиоли (как-то глицерин, пропиленгликоль, полиэтиленгликоль и др.) и их подходящие смеси растительные масла, как-то оливковое масло, и органические эфиры для инъекций, как-то этилолеат. Надлежащая текучесть может поддерживаться, к примеру, с помощью покрывающих материалов типа лецитина, выдерживанием требуемого размера частиц в случае дисперсий и с помощью сурфактантов.
Эти композиции также могут содержать такие адъюванты, как консерванты, смачивающие вещества, эмульгирующие вещества и диспергирующие вещества. Предотвращение присутствия микроорганизмов может обеспечиваться как процедурами стерилизации, так и включением различных антибактериальных и противогрибковых средств, к примеру, парабена, хлорбутанола, фенолсорбиновой кислоты и др. Также может быть желательно включение в композиции изотонических средств, как-то Сахаров, хлорида натрия и др. Кроме того, можно обеспечить продолжительное всасывание лекарственных форм для инъекций включением веществ, замедляющих всасывание, как-то моностеарата алюминия и желатина.
Фармацевтически приемлемые носители включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления ex temporo стерильных растворов или дисперсий для инъекций. Применение таких сред и веществ для фармацевтически активных субстанций известно в этой области. За исключением тех случаев, когда стандартная среда или вещество несовместимы с активным соединением, предусматривается их применение в фармацевтических композициях изобретения. В композиции также можно включать вспомогательные активные соединения.
Типичные лекарственные формы содержат по меньшей мере один конъюгат иммуноглобулина по изобретению и могут содержать стабилизирующие агенты в низких концентрациях, которые в дополнение к приведенным здесь способам могут применяться для предотвращения или снижения перекрестного сшивания иммуноглобулинов. Соответственно, при разработке фармацевтических композиций, содержащих конъюгаты иммуноглобулинов, полученные способами настоящего изобретения, можно использовать традиционные способы, применяемые для предотвращения перекрестного сшивания. К примеру, в фармацевтические композиции изобретения можно включать разнообразные стабилизирующие и дезагрегирующие соединения в зависимости от их предназначения и биологической токсичности. Такие стабилизирующие соединения могут включать, к примеру, циклодекстрин и его производные (U.S. патент 5730969), алкилгликозидные композиции (U.S. Pat. Appl. No. 11/474049), применение молекул шаперонов (например, LEA (Goyal et al., Biochem J. 2005, 388(Pt 1):151-7; способы в U.S. патент 5688651), соединения бетаина (Xiao, Bum, Tolbert, Bioconjug Chem. 2008 May 23), ПАВ (например, Pluronic F127, Pluronic F68, Tween 20 (Wei et al., International Journal of Pharmaceutics, 2007, 338(1-2):125-132), и способы, описанные в U.S. Pat. Nos. 5696090, 5688651 и 6420122.
Кроме того, белки и в частности антитела стабилизируют в лекарственных формах, используя комбинации различных классов эксципиентов, например, (1) дисахариды (например, сахароза, трегалоза) или полиоли (например, сорбитол, маннитол) действуют как стабилизаторы путем предпочтительного исключения и также способны действовать как криопротекторы при лиофилизации; (2) ПАВ (например, Polysorbat 80, Polysorbat 20) действуют путем минимизации взаимодействия белков на границе раздела жидкость/лед, жидкость/материал поверхности и/или жидкость/воздух; и (3) буферы (например, фосфатный, нитратный, гистидиновый) помогают контролировать и поддерживать рН лекарственных форм. Соответственно, такие дисахариды, полиоли, ПАВ и буферы могут применяться в дополнение к способам настоящего изобретения для дополнительной стабилизации иммуноглобулинов и предотвращения их агрегации.
Терапевтические композиции, как правило, должны быть стерильными и стабильными в условиях производства и хранения. Композиции могут быть составлены в виде растворов, микроэмульсий, липосом или других упорядоченных структур, пригодных для высокой концентрации препарата. Носителем может быть растворитель или дисперсионная среда, содержащая, к примеру, воду, этанол, полиоль (к примеру, глицерин, пропиленгликоль, жидкий полиэтиленгликоль и др.) и их подходящие смеси. Надлежащая текучесть может поддерживаться, к примеру, с помощью покрытий типа лецитина, выдерживанием требуемого размера частиц в случае дисперсий и с помощью ПАВ. Во многих случаях предпочтительно включение в композиции изотонических веществ, к примеру, Сахаров, полиспиртов типа маннитола, сорбитола или хлористого натрия. Продолжительное всасывание композиций для инъекций может обеспечиваться включением в композиции веществ, замедляющих всасывание, к примеру, солей моностеарата алюминия и желатина.
Стерильные растворы для инъекций можно приготовить введением активного соединения в требуемом количестве в соответствующий растворитель с одним или комбинацией ингредиентов, перечисленных выше, как потребуется, с последующей стерилизацией микрофильтрованием. Дисперсии обычно получают введением активного соединения в стерильный носитель, содержащий основную дисперсионную среду и необходимые другие ингредиенты из тех, что перечислены выше. В случае стерильных порошков для получения стерильных растворов для инъекций предпочтительными способами получения являются вакуумная сушка и высушивание замораживанием (лиофилизация), которые дают порошок активного ингредиента вместе с любым нужным дополнительным ингредиентом из их предварительно стерилизованных фильтрованием растворов.
Количество активного ингредиента, которое можно сочетать с материалом носителя для получения разовой дозовой формы, будет варьировать в зависимости от подлежащего лечению субъекта и конкретного способа введения. Количество активного ингредиента, которое можно сочетать с материалом носителя для получения разовой дозовой формы, обычно составляет такое количество композиции, которое дает терапевтический эффект. В общем, из расчета на 100% это количество должно составлять от 0,01% до 99% активного ингредиента, предпочтительно от 0,1% до 70%, более предпочтительно от 1% до 30% активного ингредиента в сочетании с фармацевтически приемлемым носителем.
Соответственно, объектом настоящего изобретения является обеспечение способов снижения перекрестного сшивания между выходящими на поверхность цистеинами иммуноглобулина в сильно концентрированной лекарственной форме конъюгатов иммуноглобулина, которые включаюю обеспечение иммуноглобулина, замену остатка, выбранного из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), на остаток цистеина, восстановление одного или нескольких замененных остатков цистеина с помощью восстановителя с образованием восстановленных остатков цистеина, инкубирование иммуноглобулина с атомом или молекулой, причем атом или молекула реагирует с восстановленными остатками цистеина с образованием конъюгата иммуноглобулина, и формирование сильно концентрированной, жидкой лекарственной формы конъюгата иммуноглобулина, в которой концентрация конъюгата иммуноглобулина составляет по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях иммуноглобулин выбирается из группы, содержащей IgG1, IgG2, IgG3 и IgG4. В некоторых воплощениях иммуноглобулин включает IgG1. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CH1 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CH2 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CH3 человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен CL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен VH человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, иммуноглобулин включает домен VL человека. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, конъюгат иммуноглобулина обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
Соответственно, объектом настоящего изобретения является обеспечение лекарственных форм модифицированных иммуноглобулинов, которые могут состоять из конъюгатов иммуноглобулинов, рассмотренных выше, и всевозможных комбинаций их воплощений, в концентрации по меньшей мере 10 мг/мл, по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях конъюгат иммуноглобулина находится в большей концентрации, чем та концентрация, при которой конъюгат иммуноглобулина, обладающий высокой склонностью к олигомеризации, образует олигомеры в концентрированном жидком растворе в тех же условиях. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина составляет неолигомеризованный мономер. В некоторых воплощениях, которые можно комбинировать с любыми из предыдущих воплощений, лекарственная форма включает фармацевтически приемлемый эксципиент. В некоторых воплощениях, которые можно комбинировать с любыми из предыдущих воплощений, лекарственная форма иммуноглобулина содержит по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина, представляющего собой неолигомеризованный мономер.
Соответственно, объектом настоящего изобретения является применение конъюгатов иммуноглобулинов, рассмотренных выше, и всевозможных комбинаций их воплощений в качестве не подверженных олигомеризации фармацевтически активных ингредиентов.
Соответственно, объектом настоящего изобретения является обеспечение фармацевтических композиций, включающих конъюгаты иммуноглобулинов, рассмотренные выше, и всевозможные комбинации их воплощений, и фармацевтически приемлемый эксципиент. В некоторых воплощениях иммуноглобулин находится в концентрации по меньшей мере 10 мг/мл, по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях конъюгат иммуноглобулина находится в большей концентрации, чем та концентрация, при которой конъюгат иммуноглобулина, обладающий высокой склонностью к олигомеризации, образует олигомеры в концентрированном жидком растворе в тех же условиях. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина составляет неолигомеризованный мономер. В некоторых воплощениях, которые можно комбинировать с любыми из предыдущих воплощений, лекарственная форма иммуноглобулина содержит по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина, представляющего собой неолигомеризованный мономер. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, олигомеризация измеряется методом SDS-PAGE в невосстанавливающих условиях.
Схемы дозировки подбирают для обеспечения нужной оптимальной реакции (например, терапевтической реакции). Можно вводить одним болюсом, можно вводить несколькими дробными дозами по времени или же можно пропорционально уменьшать или увеличивать дозу по показаниям тяжести терапевтической ситуации. Особенно предпочтительным является составление парентеральных композиций в виде единичной дозовой формы для удобства введения и единообразия дозировки. Единичная дозовая форма в настоящем изобретении означает физически дискретные единицы, составленные в виде единичных доз для подлежащих лечению субъектов; каждая единица содержит заданное количество активного соединения, рассчитанное для получения нужного терапевтического эффекта вместе с требуемым фармацевтическим носителем. Спецификации для единичных дозовых форм изобретения диктуются и прямо зависят от: (а) уникальных характеристик активного соединения и конкретного терапевтического эффекта, который следует получить, и (b) ограничений, присущих при составлении такого активного соединения для лечения чувствительных лиц.
Для введения конъюгата иммуноглобулина дозировка составляет от 0,0001 до 100 мг/кг, чаще всего от 0.01 до 5 мг/кг веса тела. дозировка может составлять 0,3 мг/кг веса тела, 1 мг/кг веса тела, 3 мг/кг веса тела, 5 мг/кг веса тела или 10 мг/кг веса тела либо в пределах 1-10 мг/кг. Типичный режим лечения требует введения один раз в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в месяц, один раз в 3 месяца или один раз в 3-6 месяцев. Предпочтительные схемы дозировки конъюгатов иммуноглобулина по изобретению включают 1 мг/кг веса тела или 3 мг/кг веса тела путем внутривенного введения, причем антитело вводится по одной из следующих схем дозировки: (i) каждые четыре недели по 6 доз, затем каждые три месяца; (ii) каждые три недели; (iii) 3 мг/кг веса тела один раз, затем 1 мг/кг веса тела раз в три недели.
С другой стороны, конъюгаты иммуноглобулинов изобретения можно вводить в виде лекарственной формы с продолжительным высвобождением, в этом случае требуется менее частое введение. Дозировка и частота варьируют в зависимости от времени полужизни вводимой пациенту субстанции. В общем, человеческие антитела проявляют самое длительное время полужизни, за ними следуют гуманизированные антитела, химерные антитела и антитела не от человека. Дозировка и частота могут варьировать в зависимости от того, является лечение профилактическим или терапевтическим. При профилактическом применении вводится относительно низкая доза через сравнительно редкие интервалы в течение длительного периода времени. Некоторые пациенты продолжают получать лечение на всю оставшуюся жизнь. При терапевтическом применении иногда требуются относительно высокие дозы через сравнительно короткие интервалы, пока не уменьшится или не прекратится прогрессирование заболевания, предпочтительно пока у пациента не проявится частичное или полное улучшение симптомов заболевания. После этого пациента можно перевести на профилактический режим.
Фактический уровень дозировки активных ингредиентов в фармацевтических композициях настоящего изобретения может варьировать с тем, чтобы получить такое количество активного ингредиента, которое эффективно для получения требуемой терапевтической реакции для конкретного пациента, композиции и способа применения, но не будет токсичным для пациента. Выбранный уровень дозы будет зависеть от ряда фармакокинетических факторов, включая активность используемых конкретных композиций настоящего изобретения иди их эфиров, солей или амидов, способа применения, времени введения, скорости выведения данного конкретного соединения, продолжительности лечения, других лекарств, соединений и/или материалов, используемых в комбинации с данными конкретными композициями, возраста, пола, веса, заболевания, общего состояния здоровья и предыдущей медицинской истории подлежащего лечению пациента и других факторов, хорошо известных в области медицины.
"Терапевтически эффективная доза" конъюгата иммуноглобулина по изобретению предпочтительно приводит к снижению тяжести симптомов заболевания, увеличению частоты и продолжительности свободных от болезни периодов или предотвращению ухудшения или инвалидности вследствие заболевания, при лечении опухолей "терапевтически эффективная доза" предпочтительно ингибирует рост клеток или рост опухоли по меньшей мере на 20%, более предпочтительно по меньшей мере на 40%, еще более предпочтительно по меньшей мере на 60% и даже еще более предпочтительно по меньшей мере на 80% относительно не подвергавшихся лечению субъектов. Способность соединения ингибировать рост опухолей можно оценить на животной модели, способной предсказывать эффективность на опухолях человека. С другой стороны, это свойство композиции можно оценить проверкой способности соединения к ингибированию in vitro методами, известными специалистам. Терапевтически эффективное количество терапевтического соединения может уменьшить размер опухоли или иным образом улучшить симптомы у субъекта. Рядовой специалист будет в состоянии определить такие количества, исходя из таких факторов, как размер субъекта, тяжесть симптомов у субъекта и конкретная композиция или выбранный способ применения.
Композиции настоящего изобретения можно вводить одним или несколькими способами введения, используя один или несколько из целого ряда известных способов. Как должно быть известно специалистам, путь и/или способ введения будет варьировать в зависимости от требуемых результатов. Предпочтительными способами введения для связывающих молекул изобретения являются внутривенное, внутримышечное, интрадермальное, внутрибрюшинное, подкожное, интраспинальное или другое парентеральное введение, к примеру, путем инъекции или вливания. Выражение "парентеральное введение" в настоящем изобретении означает способы введения, отличающиеся от энтерального и топического введения, обычно путем инъекции, которые включают, без ограничения, внутривенные, внутримышечные, внутриартериальные, интратекальные, интракапсулярные, интраорбитальные, интракардиальные, интрадермальные, внутри-брюшинные, транстрахеальные, подкожные, внутрикожные, внутрисуставные, субкапсулярные, субарахноидальные, интраспинальные, эпидуральные и интрастернальные инъекции и вливания.
С другой стороны, конъюгаты иммуноглобулинов по изобретению можно вводить и не парентеральным способом, как-то топическим, эпидермальным или мукозальным способом введения, интраназально, перорально, вагинально, ректально, под язык или топически.
Активные соединения можно приготовить с носителями, которые предохранят соединение от быстрого высвобождения, типа лекарственных форм с контролируемым высвобождением, включая импланты, трансдермальные пластыри и системы доставки в микрокапсулах. Можно использовать биоразрушающиеся, биосовместимые полимеры, такие как этилен-винилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие способы приготовления таких лекарственных форм запатентованы или вообще известны специалистам в данной области. Например, см. Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
Терапевтические композиции могут вводиться при помощи медицинских инструментов, известных в данной области, в предпочтительном воплощении терапевтическая композиция изобретения может вводиться с помощью безыгольного инъектора типа устройств, раскрытых в U.S. патентах 5399163; 5383851; 5312335; 5064413; 4941880; 4790824; или 4596556. Примеры хорошо известных имплантов и модулей, применимых в настоящем изобретении, включают: U.S. патент 4487603, в котором раскрыт имплантируемый микроинфузионный насос для дозировки лекарств с контролируемой скоростью; U.S. патент 4486194, в котором раскрыто терапевтическое устройство для введения медикаментов через кожу; U.S. патент 4447233, в котором раскрыт медицинский инфузионный насос для введения лекарств с точной скоростью; U.S. патент 4447224, в котором раскрыт имплантируемый инфузионный аппарат с вариабельным потоком для непрерывного введения лекарств; U.S. патент 4439196, в котором раскрыта осмотическая система доставки лекарств с несколькими отсеками; и U.S. патент 44196, в котором раскрыта осмотическая система доставки лекарств.
Соответственно, объектом настоящего изобретения является применение конъюгатов иммуноглобулинов, рассмотренных выше, и всевозможных комбинаций их воплощений при изготовлении медикаментов, включающих сильно концентрированную жидкую лекарственную форму, в которой концентрация конъюгата иммуноглобулина составляет по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл. В некоторых воплощениях медикамент предназначается для лечения аутоиммунных заболеваний, иммунологических заболеваний, инфекционных заболеваний, воспалительных заболеваний, неврологических заболеваний и онкологических и неопластических заболеваний, включая рак. В некоторых воплощениях медикамент предназначается для лечения застойной сердечной недостаточности (CHF), васкулита, красных угрей, угрей, экземы, миокардита и других заболеваний миокарда, системной красной волчанки, диабета, спондилопатии, потери синовиальных фибробластов и стромы костного мозга, потери костной массы, болезни Паже, остеокластомы; рака молочной железы; остеопении от бездействия; истощения, перидонтальных заболеваний, болезни Гоше, гистиоцитоза клеток Лангерганса, повреждения спинного мозга, острого септического артрита, размягчения костей, синдрома Кушинга, монооссальной фиброзной остеодисплазии, полиоссальной фиброзной остеодисплазии, периодонтальной реконструкция и перелома костей; саркоидоза, остеолитического рака костей, рака молочной железы, рака легких, рака почек и рака прямой кишки; костных метастазов, лечения боли в костях и гуморальной злокачественной гиперкальцемии, анкилозного спондилита и других спондилоартропатий; отторжения трансплантата, вирусных инфекций, гематологических неоплазий и неопластических заболеваний, лимфомы Ходжкина; неходжкинских лимфом (лимфомы Буркитта, мелкоклеточной лимфоцитарной лимфомы/хронического лимфолейкоза, фунгоидной гранулемы, мантиеклеточной лимфомы, фолликулярной лимфомы, диффузной крупно-В-клеточной лимфомы, лимфомы маргинальной зоны, волосковоклеточной лейкемии и лимфоплазмацитарной лейкемии), опухолей клеток-предшественников лимфоцитов, включая В-клеточную острую лимфобластическую лейкемию/лимфому и Т-клеточную острую лимфобластическую лейкемию/лимфому, тимомы, опухолей зрелых Т- и NK- (натуральных киллеров) клеток, включая лейкемию периферических Т-клеток, лейкемию/лимфому взрослых Т-клеток и лейкемию больших гранулярных лимфоцитов, гистиоцитоза клеток Ларгенганса, миелоидных неоплазий типа острой миелогенной лейкемии, включая AML с созреванием, AML без дифференцировки, острую промиелоцитную лейкемию, острую миеломоноцитарную лейкемию и острую моноцитарную лейкемию, миелодиспластических синдромов и хронических миелопролиферативных заболеваний, включая хроническую миелогенную лейкемию, опухолей центральной нервной системы, например, опухолей мозга (глиомы, нейробластомы, астроцитомы, медуллобластомы, эпендимомы и ретинобластомы), солидных опухолей (назофарингеального рака, базальноклеточной карциномы, рака поджелудочной железы, рака желчных протоков, саркомы Капоши, рака яичек, рака матки, влагалища или шейки матки, рака яичников, первичного рака печени или рака эндометрия и опухолей сосудистой системы (ангиосаркомы и гемангиоперицитомы), остеопороза, гепатита, ВИЧ, СПИД, спондилоартрита, ревматоидного артрита, воспалительных заболеваний кишечника (IBD), сепсиса и септического шока, болезни Крона, псориаза, склеродермы, реакции "трансплантат против хозяина" (GVHD), отторжения аллогенных трансплантатов островков, гематологических раковых заболеваний, как-то множестенной миеломы (ММ), миелодиспластическего синдрома (MDS) и острой миелогенной лейкемии (AML), воспаления, связанного с опухолями, повреждения периферических нервов или демиелинизирующих заболеваний. В некоторых воплощениях медикамент предназначается для лечения чешуйчатого псориаза, язвенного колита, неходжкиновской лимфомы, рака молочной железы, рака толстой и прямой кишки, ювенильного идиопатического артрита, дистрофии желтого пятна, респираторно-синцитиального вируса, болезни Крона, ревматоидного артрита, псориазного артрита, анкилозного спондилита, остеопороза, потери костной ткани в результате лечения, костных метастазов, множественной миеломы, болезни Альцгеймера, глаукомы и рассеянного склероза. В некоторых воплощениях, которые можно комбинировать с предыдущими воплощениями, медикамент дополнительно содержит фармацевтически приемлемый эксципиент. В некоторых воплощениях, которые можно комбинировать с любыми из предыдущих воплощений, конъюгат иммуноглобулина в медикаменте содержит по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% неолигомеризованного мономера. В некоторых воплощениях олигомеризация измеряется методом SDS-PAGE в невосстанавливающих условиях.
ПРИМЕРЫ
Описанные здесь примеры относятся к конкретным, не ограничивающим воплощениям изобретения.
Пример 1. Разработка, экспрессирование и конъюгирование цистеиновых вариантов антител
Разработали комплект цистеиновых вариантов IgG1 так, чтобы была представлена каждая складчатая структура в доменах иммуноглобулина (табл.1). Варианты 1-13 были разработаны из рентгеновской структуры антитела-1. Вариант 14 был выбран из структуры другого IgG1, антитела-2, построенного моделированием по гомологии относительно антитела-1. Все сайты выходили на поверхность антитела. Полярные остатки, такие как серин, треонин и аргинин, или заряженные остатки, такие как лизин, заменяли на цистеин. Гены легких и тяжелых цепей субклонировали в вектор gWIZ (Genlantis) и использовали для экспрессии белков путем временной трансфекции клеток млекопитающих. Варианты антител либо синтезировали de novo (GeneArt), либо получали сайт-направленным мутагенезом с помощью ПЦР и проверяли секвенированием. Антитела дикого типа и варианты экспрессировали на уровне 10-100 мг путем временной трансфекции клеток Freestyle HEK 293 (Invitrogen) с помощью полиэтиленимина (Polysciences) как реагента для трансфекции. Через 7-10 дней после трансфекции собирали супернатанты клеточных культур. Антитела очищали на колонке с белком A (GE Healthcare), элюировали 50 мМ цитратным буфером рН 3,5 и заменяли буфер на 100 мМ трис-буфер рН 7,0 для флуоресцентного мечения.
После экспрессии и очистки вариантов антител вставленные на поверхность цистеины были в основном окислены, варианты 4 и 6 содержали меньше 0,3 свободных тиолов на молекулу антитела, в противоположность ожидаемому 2,0 для антител с вставленными на поверхность цистеинами. Мы сравнили эффект мягкого восстанавливающего реагента ТСЕР (трис[2-карбоксиэтил]фосфин гидрохлорида) и более сильного восстанавливающего реагента DTT (дитиотреитола) на один вариант из класса I и один вариант из класса IV. Сначала не олигомеризованный вариант 4 проявлял 0,13 свободных тиолов на антитело, а сильно олигомеризованный вариан 6 содержал 0,25 свободных тиолов на антитело. Аликвоты дикого типа, варианта 4 и варианта 6 обрабатывали при пяти различных условиях: 1) без восстановителя, 2) ТСЕР, 10х, 1 час, 3) ТСЕР, 20х, 1 час, 4) DTT, 5х, 15 мин, и 5) DTT, 10х, 15 мин. После удаления восстановителя образцы разделяли методом PAGE в невосстанавливающих условиях и определяли количество свободного тиола. Сравнение результатов по дикому типу и вариантам показало, что обработка ТСЕР была достаточной для восстановления цистеинов в неолигомеризованной форме (вариант 4) при слабом эффекте на ДТ (дикий тип). Однако цистеины из олигомеров (вариант 6) восстанавливались только после более жесткой обработки. Обработка с DTT даже на низком уровне приводит к фрагментации антител у ДТ и обоих вариантов. Сайты, куда вводились поверхностные цистеины, оказывали сильное влияние на возможность использовать вставленные цистеины для конъюгации.
Испробовали различные способы для специфического восстановления вставленных на поверхность тиолов перед мечением. Использовали два реагента - ТСЕР и DTT, а уровни свободного тиола определяли с помощью реагента Эллмана (Invitrogen). Как оказалось, в наших экспериментах по сайт-специфичному мечению лучше всего работает L-цистеин, поэтому использовали следующую двухстадийную методику. Во-первых, варианты инкубировали со 100-200-кратным избытком L-цистеина в течение 4 часов при 37°С, а затем меняли буфер на 50 мМ трис/EDTA. Во-вторых, образцы инкубировали с 5-10-кратным избытком малеимидного красителя Alexa488 (Invitrogen) в течение 1 ч при комнатной температуре или с 10-кратным избытком пиренового малеимидного красителя (Invitrogen) в течение 12 ч при комнатной температуре. После удаления свободного красителя и замены буфера на 50 мМ фосфатный буфер рН 7,0 рассчитывали эффективность включения метки в молях красителя на моль белка по методике производителя (Invitrogen).
Пример 2. Характеристика сконструированных цистеиновых вариантов антител
Образцы немеченых и меченых антител анализировали методом SDS-PAGE. Для анализа без восстановителя использовали 7,5%, 10% и 12% гели. Для анализа с восстановителем подвергнутых нагреванию с DTT образцов использовали 12% гели. Обычно на дорожку наносили 5-10 мкг образца. Перед окраской Кумасси синим делали флуоресцентные снимки под УФ-светом. Расщепление антител проводили с помощью GluC (фермент: антитело = 1:20 при 25°С в течение 12-24 ч) и проназы (фермент:антитело = 1:20 при 37°С в течение 1 ч).
На гелях без восстановителя проявлялось присутствие мономеров, а также димеров, тримеров и в некоторых случаях даже олигомеров более высокого порядка. На гелях с восстановителем проявлялось исключительное мечение легкой или тяжелой цепи в зависимости от того, куда были вставлены поверхностные цистеины. Меченые и немеченые варианты 1-6 также анализировали на специфичность связывания антигена. Варианты сохраняли активность в пределах 80% и 130% от дикого типа с некоторой потерей активности после мечения. Немеченый вариант 1 сохранял примерно 110% активности дикого типа, тогда как меченый вариант 1 сохранял примерно 80%. Немеченый вариант 2 сохранял примерно 105% активности дикого типа, тогда как меченый вариант 2 сохранял чуть меньше 100% активности. И меченый, и немеченый вариант 3 сохранял примерно 110% активности дикого типа. Немеченый вариант 4 сохранял примерно 125% активности дикого типа, тогда как меченый вариант 4 сохранял примерно 95% активности. Немеченый вариант 5 сохранял примерно 120% активности дикого типа, тогда как меченый вариант 6 сохранял примерно 100% активности. Наконец, немеченый вариант 6 сохранял примерно 115% активности дикого типа, тогда как меченый вариант 6 сохранял примерно 90% активности. Подобно своему немеченому партнеру, меченый вариант 6 проявлял высокую склонность к олигомеризации.
Большинство вариантов метились почти с оптимальной эффективностью 2.0 моль красителя на моль антитела (два идентичных цистеина на молекулу антитела). Эффективность мечения выше 2.0 не желательна, так как это свидетельствует о частичном разрушении и мечении внутрицепочечных дисульфидов. Варианты с высокой склонностью к олигомеризаци, такие как вариант 6, вариант 11 и вариант 5 метились не столь эффективно. Даже среди других вариантов такие условия мечения, как время реакции и отношение красителя к белку приходилось оптимизировать на индивидуальной основе, так как не все вставленные цистеины были одинаково подвержены конъюгации. Варианты 1-14 специфически метились по цепи, несущей вставленный цистеин. Протеолитическая обработка вариантов проназой давала разные профили флуоресценции у большинства вариантов, но у вариантов с соседними заменами, таких как вариант 3 и 12, профили были похожи. Таким образом, большинство вариантов метились эффективно и специфически.
Для этого комплекта цистеиновых вариантов различали пять классов склонности к перекрестному сшиванию (табл.1). Класс I содержит варианты, которые были мономерными и остались стабильными после мечения. Варианты класса II содержали небольшой процент димеров до и после мечения. Варианты класса III обладали более выраженной склонностью к олигомеризациия, включая образование некоторого числа тримеров. Варианты класса IV обладали еще большей склонностью к олигомеризации, о чем свидетельствует присутствие больших агрегатов, чем тримеры, особенно после мечения. Класс V включает варианты с высокой склонностью к олигомеризации, подобно вариантам класса IV, с дополнительными структурными отклонениями типа фрагментации или окрашивания очищенных концентрированных образцов.
Пример 3. Применение сконструированных цистеиновых вариантов антител
Цистеиновые варианты с низкой склонностью к перекрестному сшиванию (варианты 1-4, 7, 10, 12-14) метились с высокой специфичностью и эффективностью и небольшой олигомеризацией. Мечение малемидными красителями является только одним примером сайт-специфичной конъюгации с этими вариантами антител. Точно так же могут присоединяться молекулы со многими другими функциональностями, такими как специфичность связывания или токсичность. Таким образом, данный комплект вариантов распространяется на весь репертуар вариантов антител, служащих носителями полезного груза для прицельной терапии или для флуоресцентного анализа in vitro и in vivo.
Для иллюстрации применения флюоресценции одного из вариантов мы анализировали профиль эмиссии у вариантов, конъюгированных с флуорофором пиреном. Когда две молекулы пирена находятся вблизи друг от друга, возникает характерное усиление эмиссии при 465 нм, известное как эксимерная флуоресценция. Мы пометили варианты 4 и 7 пиреновым малеимидом и проследили спектр излучения. Вариант 4 проявлял базальный уровень эмиссии при 465 нм, тогда как вариант 7 проявлял сильную эксимерную флуоресценцию. Учитывая положение вставленного цистеина в CH1 у варианта 7, на внутренней стороне Fab-доменов, наблюдавшийся результат коррелирует с известным эффектом отсечения Fab относительно Fc. Таким образом, этот вариант может применяться при анализе динамики доменов антител.
Высокая склонность к олигомеризации варианта 6 предполагает другое применение цистеиновых вариантов антител, которое исследовали более подробно. Меченый вариант 6 подвергали гель-фильтрационной хроматографии для того, чтобы отделить мономер от олигомеров, и содержащие белок фракции разделяли методом SDS-PAGE без восстановителя в 7,5% геле и анализировали до и после окрашивания Кумасси голубым. Анализ варианта 6 методом гель-фильтрации указывал на конкуренцию между включением метки и перекрестным сшиванием: чем выше молекулярная масса, тем ниже эффективность мечения (по уровню флуоресценции). При наибольшей молекулярной массе эффективность мечения составляла 0,5, тогда как эффективность мечения у мономеров -1,0, а эффективность мечения исходного меченого образца равна 0,8. Вариант антитела с множественными олигомерами, а именно вариант 6 представляет отличный контроль на олигомеризацию антител и удобный стандарт для высокомолекулярных белков, с дополнительной функциональностью, что его можно пометить сайт-специфичным образом.
Пример 4. Корреляция между склонностью к перекрестному сшиванию (CLP) и склонностью к пространственной агрегации (SAP) у цистеиновых вариантов
Сравнивали склонность к перекрестному сшиванию (CLP) и склонность к пространственной агрегации (SAP) для цистеиновых вариантов, у которых определенные аминокислоты заменяли на цистеин. Каждому варианту приписывали значение CLP на основе анализа методом SDS-PAGE в невосстанавливающих условиях. Значения SAP для мутированных остатков получали из результатов вычисления с радиусом в 5А. На кодируемую SAP структуру антитела-1 накладывали сконструированные цистеиновые варианты.
Наблюдались следующие корреляции. Все аминокислоты, замененные на цистеин, имели отрицательные значения SAP в пределах от -0,27 до 0,00. Это согласуется с выбором полярных или заряженных аминокислот для замены. Все варианты CLP класса I имели значения SAP между 0,00 и -0,11 (варианты 3, 4, 7, 10, 12), а все варианты CLP класса II имели значения SAP между -0,12 и -0,23 (варианты 1, 2, 13). Однако были варианты со значениями SAP в этих пределах и с высоким CLP (к примеру, варианты 8, 9 и 11). Варианты с высоким перекрестным сшиванием, варианты 8 и 11, находятся по соседству с сайтами с высокими значениями SAP. Вариант 5 с CLP III соседствует с сайтами с высоким значением SAP в CH2, тогда как вариант 2 с CLP II - нет. Однако такая корреляция отсутствует между вариантом 6 и вариантом 10 в CH3 и между вариантами 9 и 14 в VH.
Дополнительное наблюдение проводили с вариантом 14. Вариант 14 не экспрессировался, если рядом находился участок с высоким SAP, тогда как он экспрессировался, когда этот участок с высоким SAP заменяли на участок с низким SAP. Наблюдался в 100 раз больший выход варианта 14 в стабилизированном антителе-2 (35,6 мг/л культуры) по сравнению с таковым у варианта 14 на фоне нативного антитела-2 (0,34 мг/л). Относительный выход варианта 14 на различном фоне указывает на структурную проблему, когда цистеин вводится на поверхность белка рядом с участком с высоким значением SAP. Проблема разрешилась, когда две гидрофобные аминокислоты в гидрофобном пятне по соседству со вставленным цистеином заменили на лизин.
В заключение, существуют корреляции между стабильностью цистеиновых вариантов и SAP: 1) цистеиновые варианты с низкой склонностью к перекрестному сшиванию имеют слегка отрицательные SAP (от 0,00 до -0,11); 2) цистеиновые варианты с боле отрицательными SAP (от -0,12 до -0,23) более склонны к перекрестному сшиванию; и 3) цистеиновые варианты в непосредственной близости к пятнам с высоким SAP с большей вероятностью будут подвергаться перекрестному сшиванию или иметь структурные отклонения. Выводы 1 и 2 согласуются с высказанным ранее мнением, что полностью экспонированные остатки могут быть более подвержены перекрестному сшиванию [9].
Пример 5. Выводы
Мы разработали комплект цистеиновых вариантов IgG1 человека, которые широко распределены на молекуле антитела, причем на каждую складчатую стрктуру домена иммуноглобулина приходится по меньшей мере один вариант. Большинство этих вариантов стабильны и могут быть эффективно и специфически конъюгированы без существенной потери антигенсвязывающей активности. Таким образом, стабильные варианты антител дополняют репертуар вариантов для сайт-специфической конъюгации молекул с полезной нагрузкой. Если к вставленным цистеинам присоединить флуорофоры, то можно анализировать динамику определенных доменов. Сильно олигомеризованные варианты тоже полезны, так как многочисленные мультимеры обеспечивают удобный стандарт для агрегатов антител и для высокомолекулярных белков вообще.
Корреляция между склонностью к перекрестному сшиванию описанных здесь цистеиновых вариантов антител и методом SAP показывает, что методология SAP может применяться для скрининга на конъюгацию сайтов с пониженным перекрестным сшиванием. Технология SAP является компьютерной, так что она уменьшает время и экспериментальную работу при разработке вариантов. Сравнение CLP/SAP показало, что замена частично и не совсем экспонированных аминокислот дает наиболее стабильные варианты. Более того, сравнение показало, что следует избегать находящихся по соседству гидрофобных пятен.
Варианты IgG1, со вставленными на поверхность цистеинами, описанные здесь, обеспечивают новые сайты для сайт-специфической конъюгации терапевтических антител и способы идентификации других вариантов. Варианты с небольшой склонностью к перекрестному сшиванию наиболее полезны при разработке антител для прицельной терапии. Приведенные здесь цистеиновые варианты содержат новые сайты в ранее представленных доменах (CL, CH1, CH3), а также и в ранее не представленных (VL, VH, CH2).
Более того, меченые варианты могут применяться в виде комплекта сайт-специфичных маркеров антител для лабораторных исследований in vitro и in vivo. Флуоресцентно меченые продукты могут быть поставлены на коммерческую основу через биотехнологические компании (такие как Thermo Scientific Pierce, GE Healthcare и Invitrogen), обеспечивающие исследовательское сообщество антителами и другими белковыми реагентами.
Вариант 6 с высоким перекрестным связыванием является полезным белковым стандартом для гель-фильтрации или других методов хроматографии. Его могут выпускать компании (к примеру. Invitrogen, Bio-Rad, Pierce), поставляющие белковые реагенты.
Корреляция между CLP и SAP также предполагает коммерческое применение ранее описанной нами технологии SAP. Принятие во внимание SAP может улучшить разработку стабильных цистеиновых вариантов антител для сайт-специфичной конъюгации.
БИБЛИОГРАФИЯ
1. Carter P.J. Potent antibody therapeutics by design. Nat Rev Immunol, 2006. 6(5): p.343-57.
2. Polakis P. Arming antibodies for cancer therapy. Curr Opin Pharmacol, 2005. 5(4): p.382-7.
3. Kaminski M.S. et al. Radioimmunotherapy of B-cell lymphoma with [131I]anti-B1 (anti-CD20) antibody. N Engl J Med, 1993. 329(7): p.459-65.
4. King D.J. et al. Preparation and preclinical evaluation of humanised A33 immunoconjugates for radioimmunotherapy. Br J Cancer, 1995. 72(6): p.1364-72.
5. Khaw В.A. et al. Myocardial infarct imaging of antibodies to canine cardiac myosin with indium-111-diethylenetriamine pentaacetic acid. Science, 1980. 209(4453): p.295-7.
6. Rodwell J.D. et al., Site-specific covalent modification of monoclonal antibodies: in vitro and in vivo evaluations. Proc Natl Acad Sci USA, 1986. 83(8): p.2632-6.
7. Sun M.M. et al. Reduction-alkylation strategies for the modification of specific monoclonal antibody disulfides. Bioconjug Chem, 2005. 16(5): p.1282-90.
8. Junutula J.R. et al. Site-specific conjugation of a cytotoxic drug to an antibody improves the therapeutic index. Nat Biotechnol, 2008. 26(8): p.925-32.
9. Lyons A. et al. Site-specific attachment to recombinant antibodies via introduced surface cysteine residues. Protein Eng, 1990. 3(8): p.703-8.
10. Shopes В. A genetically engineered human IgG mutant with enhanced cytolytic activity. J Immunol, 1992. 148(9): p.2918-22.
11. Shopes В. A genetically engineered human IgG with limited flexibility fully initiates cytolysis via complement. Mol Immunol, 1993. 30(6); p.603-9.
12. Stimmel J.B. et al. Site-specific conjugation on serine right-arrow cysteine variant monoclonal antibodies. J Biol Chem, 2000. 275(39): p.30445-50.
13. Zheng Y. et al. Conformations of IgE bound to its receptor Fc epsilon RI and in solution. Biochemistry, 1991. 30(38): p.9125-32.
14. Zheng Y. et al. Dynamic conformations compared for IgE and IgG1 in solution and bound to receptors. Biochemistry, 1992. 31(33): p.7446-56.
15. Junutula J.R. et al. Rapid identification of reactive cysteine residues for site-specific labeling of antibody-Fabs. J Immunol Methods, 2008. 332(1-2): p.41-52.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОГЛОБУЛИНЫ С УМЕНЬШЕННОЙ АГРЕГАЦИЕЙ | 2009 |
|
RU2532226C2 |
| КОНЪЮГАТЫ ПОЛИПЕПТИДНОГО ТОКСИНА И АНТИТЕЛА, СОЕДИНЕННЫХ КОВАЛЕНТНОЙ СВЯЗЬЮ | 2014 |
|
RU2682754C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ БЕЛКА RGM А И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2524136C2 |
| АНТИТЕЛА К ТЕОФИЛЛИНУ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630664C2 |
| ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА И КОНЪЮГАТЫ АНТИТЕЛО-ПРЕПАРАТ ПРОТИВ CD74 | 2012 |
|
RU2636029C2 |
| АНТИТЕЛА К БИОТИНУ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2630296C2 |
| АНТИТЕЛА К FcRH5, ИХ ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2583270C2 |
| КОВАЛЕНТНО СВЯЗАННЫЕ КОНЪЮГАТЫ ХЕЛИКАР-АНТИТЕЛО ПРОТИВ ХЕЛИКАРА И ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2694981C2 |
| БИСПЕЦИФИЧНЫЕ АНТИТЕЛА ПРОТИВ ГАПТЕНА/ПРОТИВ РЕЦЕПТОРА ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА, ИХ КОМПЛЕКСЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЧЕЛНОКОВ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2014 |
|
RU2693438C2 |
| АНТИТЕЛА ПРОТИВ 5-БРОМ-2'-ДЕЗОКСИУРИДИНА И СПОСОБЫ ПРИМЕНЕНИЯ | 2015 |
|
RU2705299C2 |






Изобретение относится к области молекулярной биологии, биохимии и медицины. Предложен конъюгат иммуноглобулина с уменьшенной склонностью к перекрестному сшиванию, включающий иммуноглобулин, содержащий по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина, и атом или молекулу, причем атом или молекула конъюгированы с остатком цистеина, где конъюгация атома или молекулы с остатком цистеина является прямой или опосредованной, а также рекомбинантный полинуклеотид, экспрессирующий вектор, клетка-хозяин, фармацевтическая композиция, модифицированный иммуноглобулин, способ получения иммуноглобулина и способ получения конъюгата иммуноглобулина. 11 н. и 7 з.п. ф-лы, 1 табл., 5 пр.
1. Конъюгат иммуноглобулина с уменьшенной склонностью к перекрестному сшиванию, включающий иммуноглобулин, содержащий по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина, и атом или молекулу, причем атом или молекула конъюгированы с остатком цистеина, где конъюгация атома или молекулы с остатком цистеина является прямой или опосредованной.
2. Конъюгат иммуноглобулина по п. 1, где конъюгация атома или молекулы с цистеиновым остатком является опосредованной и где конъюгат иммуноглобулина также содержит молекулу линкера, имеющую по меньшей мере два реакционноспособных сайта, причем первый реакционноспособный сайт связан с остатком цистеина иммуноглобулина, а второй реакционноспособный сайт связан с атомом или молекулой.
3. Конъюгат иммуноглобулина по п. 2, в котором молекула линкера выбрана из группы, состоящей из гидразона, дисульфида, пептида, хелатирующего агента и малеимида.
4. Конъюгат иммуноглобулина по п. 1, в котором атом или молекула выбраны из группы, состоящей из радионуклида, химиотерапевтического агента, микробного токсина, растительного токсина, полимера, углевода, цитокина, флуоресцентной метки, люминесцентной метки, фермент-субстратной метки, фермента, пептида, пептидомиметика, нуклеотида, миРНК, микроРНК, РНК-миметика и аптамера.
5. Конъюгат иммуноглобулина по п. 1, в котором атом или молекула выбраны из группы, состоящей из 90Y, 131I, 67Cu, 177Lu, 213Bi, 211At, калихеамицина, дуокармицина, майтансиноида, ауристатина, антрациклина, экзотоксина A Pseudomonas, дифтерийного токсина, рицина, полиэтиленгликоля, гидроксиэтилкрахмала и остатка маннозила.
6. Конъюгат иммуноглобулина по п. 1, в котором конъюгат иммуноглобулина дополнительно обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
7. Модифицированный иммуноглобулин с уменьшенной склонностью к
перекрестному сшиванию, содержащий по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина.
8. Рекомбинантный полинуклеотид, кодирующий иммуноглобулин по п. 7.
9. Экспрессирующий вектор, содержащий полинуклеотид по п. 8, функционально связанный с индуцибельным промотором.
10. Клетка-хозяин, содержащая вектор по п. 9.
11. Способ получения иммуноглобулина, включающий:
(a) обеспечение культуральной среды, содержащей клетку-хозяина по п. 10; и
(b) помещение культуральной среды стадии (а) в условия, при которых экспрессируется иммуноглобулин.
12. Способ получения конъюгата иммуноглобулина, включающий:
(a) обеспечение иммуноглобулина по п. 7;
(b) восстановление одного или нескольких замененных остатков цистеина с помощью восстановителя с образованием восстановленных остатков цистеина; и
(c) инкубирование иммуноглобулина с атомом или молекулой, причем атом или молекула реагирует с восстановленными остатками цистеина с образованием конъюгата иммуноглобулина.
13. Способ получения конъюгата иммуноглобулина со сниженным перекрестным сшиванием между выходящими на поверхность цистеинами иммуноглобулина в сильно концентрированной фармацевтической форме конъюгатов иммуноглобулина, включающий:
(a) обеспечение иммуноглобулина;
(b) замену остатка, выбранного из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), на остаток цистеина;
(c) восстановление одного или нескольких замененных остатков цистеина с помощью восстановителя с образованием восстановленных остатков цистеина;
(d) инкубирование иммуноглобулина с атомом или молекулой, причем атом или молекула реагирует с восстановленными остатками цистеина с образованием конъюгата иммуноглобулина; и
(e) формирование сильно концентрированной жидкой лекарственной формы конъюгата иммуноглобулина, в которой концентрация конъюгата иммуноглобулина составляет по меньшей мере 20 мг/мл, по меньшей мере 30 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл.
14. Способ по п. 13, в котором конъюгат иммуноглобулина обладает антигенсвязывающей активностью, причем эта активность составляет по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 100%, по меньшей мере 110%, по меньшей мере 120% или по меньшей мере 130% от антигенсвязывающей активности немутированного иммуноглобулина.
15. Фармацевтическая композиция, содержащая конъюгат иммуноглобулина по п. 1 в эффективном количестве и фармацевтически приемлемый эксципиент, причем по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% конъюгата иммуноглобулина составляет неолигомеризованный мономер.
16. Фармацевтическая композиция по п. 15, в которой конъюгат иммуноглобулина находится в концентрации по меньшей мере 10 мг/мл, по меньшей мере 20 мг/мл, по меньшей мере 40 мг/мл, по меньшей мере 50 мг/мл, по меньшей мере 75 мг/мл, по меньшей мере 100 мг/мл, по меньшей мере 125 мг/мл или по меньшей мере 150 мг/мл.
17. Модифицированный иммуноглобулин с уменьшенной склонностью к перекрестному сшиванию, содержащий по меньшей мере одну мутацию выходящего на поверхность остатка на цистеин, где мутация выбрана из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), при этом склонность к пространственной агрегации этого остатка равна или находится между значениями 0 и -0,11, а несколько (множество) остатков иммуноглобулина в непосредственной близости от первого остатка имеют значения склонности к пространственной агрегации меньше 0.
18. Конъюгат иммуноглобулина с уменьшенной склонностью к перекрестному сшиванию, включающий иммуноглобулин, содержащий по меньшей мере одну мутацию по остатку, выбранному из группы, состоящей из 7(VH), 20(VL), 22(VL) и 125(CH1), причем по меньшей мере одна мутация представляет собой замену на остаток цистеина, и атом или молекулу, причем атом или молекула конъюгированы с остатком цистеина, где конъюгация атома или молекулы с остатком цистеина является прямой или опосредованной;
где атом или молекула выбрана из группы, включающей радионуклиды, химиотерапевтические агенты, микробные токсины, растительные токсины, полимеры, углеводы, цитокины, флуоресцентные метки, люминесцентные метки, фермент-субстратные метки, ферменты, пептиды, пептидомиметики, нуклеотиды, миРНК, микроРНК, миметики РНК, аптамеры, 90Y, 1311, 67Cu, 177Lu, 213Bi, 211At, калихеамицин, дуокармицин, майтансиноид, ауристатин, антрациклин, экзотоксин A Pseudomonas, дифтерийный токсин, рицин, полиэтиленгликоль, гидрокисэтилированный крахмал и маннозильный остаток.
| US 20060062784 A1, 23.03.2006 | |||
| US 20060286066 A1, 21.12.2006 | |||
| Антенна | 1927 |
|
SU6207A1 |
| ОДНОЦЕПОЧЕЧНЫЕ РЕКОМБИНАНТНЫЕ Т-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ | 2003 |
|
RU2355703C2 |
Авторы
Даты
2015-11-20—Публикация
2010-06-04—Подача