Изобретение относится к новому способу получения дитиинтетракарбоксидиимидов.
Дитиинтетракарбоксидиимиды являются известными соединениями. Известно, что дитиинтетракарбоксидиимиды можно использовать в качестве антигельминтиков для борьбы с внутренними паразитами животных, прежде всего нематодами, причем эти соединения обладают инсектицидным действием (смотри патент США US 3,364,229). Кроме того, известно, что определенные дитиинтетракарбоксидиимиды обладают антибактериальным действием, а также определенным действием против человеческих грибковых заболеваний (смотри II Farmaco, 2005, 60, 944-947). Известно также, что дитиинтетракарбоксидиимиды можно использовать в качестве пигментов в электрофотографических рецепторах или в качестве красителей в лаках и полимерах (смотри японскую заявку на патент JP-A 10-251265, а также патент Польши PL-B 143804).
Дитиинтетракарбоксимиды формулы (I):
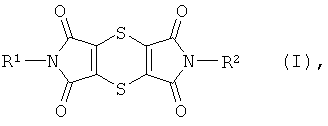
в которой
R1 и R2 одинаковые или разные и означают водород, алкил с 1-8 атомами углерода, при необходимости однократно или многократно замещенный галогеном, -OR3, -COR4, циклоалкил с 3-7 атомами углерода, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода или галогеналкилом с 1-4 атомами углерода, арил, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, -COR4 или сульфониламино, или арил-алкил с 1-4 атомами углерода в алкиле, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, -COR4 или сульфониламино,
R3 означает водород, алкил с 1-4 атомами углерода, алкилкарбонил с 1-4 атомами углерода в алкиле или арил, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода или галогеналкилом с 1-4 атомами углерода,
R4 означает гидрокси, алкил с 1-4 атомами углерода или алкокси с 1-4 атомами углерода,
могут быть получены разными известными методами.
Так, например, на первой стадии одного из известных способов (смотри Synthetic Communications, 2006, 36, 3591-3597) ангидрид янтарной кислоты при необходимости в присутствии разбавителя подвергают превращению с амином формулы (II). Полученные моноамиды янтарной кислоты формулы (III) подвергают последующему превращению со значительным избытком тионилхлорида, осуществляемому при комнатной температуре в присутствии диоксана в качестве разбавителя, причем в результате последовательной реализации множества реакционных стадий получают дитиинтетракарбоксидиимиды формулы (I). Дитиинтетракарбоксидиимиды выделяют фильтрованием либо непосредственно из реакционной смеси, либо после ее смешивания с водой. В зависимости от реакционных условий (разбавителя) и типа остатков R в известных условиях могут быть выделены дитииндиизоимиды формулы (IV), которые затем преобразуют в дитиинтетракарбоксидиимиды формулы (I):
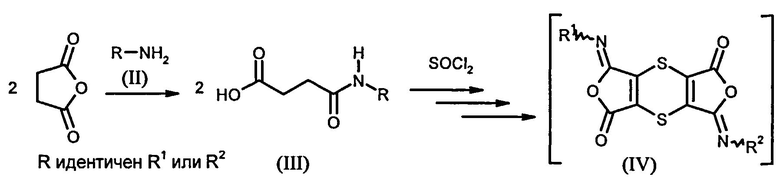
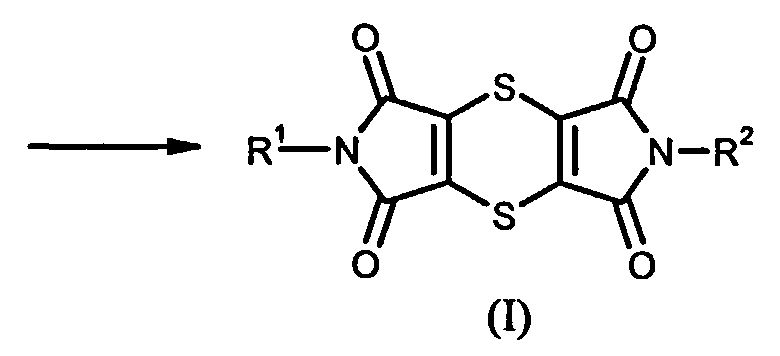
Недостатком указанного способа является длительное время реакций, а также отсутствие возможности обеспечения достаточных выходов от теоретического, которые, как правило, не превышают примерный интервал от 30 до 40%, или отсутствие достаточной степени чистоты выделяемых продуктов. Кроме того, следствием водной переработки реакционной смеси является разрушение значительных количеств тионилхлорида и необходимость удаления образующихся при этом газов (SO2 и HCl). Как показывает опыт, другим недостатком указанного способа является отсутствие возможности получения продукта в виде единственной порции. Напротив, после выполненного путем фильтрования первоначального выделения продукта и последующей длительной выдержки фильтрата из последнего часто выпадает в осадок другой продукт, что требует его выделения путем повторного фильтрования. Иногда эту процедуру приходится выполнять повторно. Подобная технология чрезвычайно сложна и трудоемка.
В соответствии с другим известным способом (смотри патент США US 3,364,229, а также Chem. Bev., 1967,100,1559-70) на первой стадии ангидрид дихлормалеиновой кислоты формулы (V) подвергают превращению с амином формулы (II), которое при необходимости осуществляют в присутствии разбавителя. Полученные на первой стадии имиды дихлормалеиновой кислоты формулы (VI) подвергают дальнейшему превращению с высвобождающим серу соединением (например, сероводородом, тиомочевиной или тиосульфатом натрия):
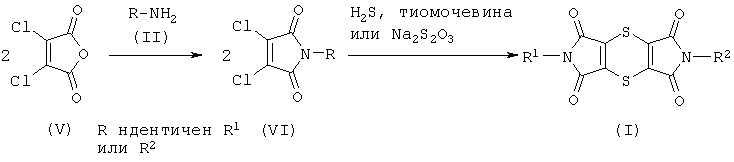
Недостатком данного способа является, например, технически чрезвычайно сложное и трудоемкое обращение с высокотоксичным газообразным сероводородом. В случае использования тиомочевины, кроме целевого продукта, образуются нежелательные побочные продукты, которые могут быть удалены лишь с чрезвычайно большим трудом и обусловливают снижение достижимых выходов. В случае использования тиосульфата натрия достижимый выход недостаточен для технической реализации процесса.
Таким образом существует потребность в технически простом и экономичном способе получения дитиинтетракарбоксидиимидов формулы (I).
Обнаружен новый способ получения дитиинтетракарбоксидиимидов общей формулы (I):

в которой остатки R1 и R2 такие, как указано выше,
отличающийся тем, что имиды дихлормалеиновой кислоты формулы (VI):
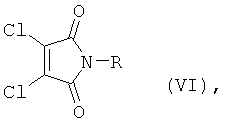
в которой R идентичен остатку R1 или R2,
в растворителе или смеси растворителей подвергают превращению с неорганическим тиосульфатом, причем молярное соотношение тиосульфата к имиду дихлормалеиновой кислоты формулы (VI) составляет от 1,1:1 до 1,8:1.
Имиды дихлормалеиновой кислоты, используемые в качестве исходных веществ при осуществлении предлагаемого в изобретении способа, в общем случае обладают формулой (VI). Остаток R идентичен остатку R1 или R2.
R1 и R2 предпочтительно являются одинаковыми или разными и предпочтительно означают водород, алкил с 1-6 атомами углерода, при необходимости однократно или многократно замещенный фтором, хлором, бромом, -OR3, -COR4, циклоалкил с 3-7 атомами углерода, при необходимости однократно или многократно замещенный хлором, метилом или трифторметилом, фенил, при необходимости однократно или многократно замещенный фтором, хлором, бромом, метилом, трифторметилом, -COR4, сульфониламино, или фенилалкил с 1-4 атомами углерода в алкиле, при необходимости однократно или многократно замещенный фтором, хлором, бромом, метилом, трифторметилом, -COR4 или сульфониламино.
R1 и R2 особенно предпочтительно являются одинаковыми или разными и особенно предпочтительно означают водород, алкил с 1-4 атомами углерода, при необходимости однократно или многократно замещенный фтором, хлором, гидрокси, метокси, этокси, метилкарбонилокси или карбоксилом, циклоалкил с 3-7 атомами углерода, при необходимости однократно или многократно замещенный хлором, метилом или трифторметилом, или фенил, бензил, 1-фенетил, 2-фенетил или 2-метил-2-фенетил, соответственно при необходимости однократно, двукратно или трехкратно замещенный фтором, хлором, бромом, метилом, трифторметилом, -COR4, сульфониламино.
R1 и R2 еще более предпочтительно являются одинаковыми или разными и еще более предпочтительно означают водород, метил, этил, н-пропил, изопропил, 2,2-дифторэтил или 2,2,2-трифторэтил, циклопропил, при необходимости замещенный хлором, метилом или трифторметилом, или циклогексил, при необходимости замещенный хлором, метилом или трифторметилом.
R1 и R2 наиболее предпочтительно являются одинаковыми остатками, означающими метил.
R3 предпочтительно означает водород, метил, этил, метилкарбонил, этилкарбонил или фенил, при необходимости однократно или многократно замещенный фтором, хлором, метилом, этилом, н-пропилом, изопропилом или трифторметилом.
R3 особенно предпочтительно означает водород, метил, метилкарбонил или фенил.
R4 предпочтительно означает гидрокси, метил, этил, метокси или этокси.
R4 особенно предпочтительно означает гидрокси или метокси.
В качестве исходного вещества особенно предпочтительно используют N-метилимид дихлормалеиновой кислоты формулы (VI-1), в которой R означает метил, причем в качестве конечного продукта (1-1) получают 2,6-диметил-1Н,5Н-[1,4]дитиино[2,3-с:5,6-с']дипиррол-1,3,5,7(2Н,6Н)тетрон.
В случае использования в качестве исходного вещества имида дихлормалеиновой кислоты формулы (VI-2), в которой R означает водород, в качестве конечного продукта (1-2) получают 1Н,5Н-[1,4]дитиино[2,3-с:5,6-с']дипиррол-1,3,5)7(2Н,6Н)тетрон.
В качестве тиосульфата в принципе можно использовать любые растворимые неорганические соли тиосерной кислоты, например такие, как тиосульфат лития, тиосульфат натрия, тиосульфат калия, тиосульфат цезия, тиосульфат магния или тиосульфат аммония. Предпочтительно используют тиосульфат натрия, тиосульфат калия или тиосульфат аммония, особенно предпочтительно тиосульфат натрия или тиосульфат аммония. В качестве тиосульфата, очевидно, можно использовать также смеси указанных солей.
Под «тиосульфатом» и «солью тиосерной кислоты» подразумевают также гидраты этих солей.
Молярное соотношение исходного тиосульфата к имиду дихлормалеиновой кислоты формулы (VI) составляет от 1,1:1 до 1,8:1. Молярное соотношение тиосульфата к имиду дихлормалеиновой кислоты формулы (VI) предпочтительно составляет от 1,2:1 до 1,7:1, особенно предпочтительно от 1,3:1 до 1,6:1.
Тиосульфат можно добавлять к реакционной смеси в твердой форме или в виде раствора, например в воде. При необходимости тиосульфат можно добавлять также к реакционной смеси в жидкой форме в виде расплава. Пентагидрат тиосульфата натрия, плавится, например, в температурном интервале от 45 до 50°C. Тиосульфат предпочтительно добавляют в виде раствора в воде.
В соответствии с предлагаемым в изобретении способом температуру реакции можно варьировать в широких пределах (от 0 до 200°C). Для достижения удовлетворительного выхода целевого продукта в расчете на единицу объема и единицу времени реакцию предпочтительно осуществляют в температурном интервале от 20 до 180°C, особенно предпочтительно в интервале от 30 до 150°C.
В соответствии с предлагаемым в изобретении способом время реакции составляет от 10 минут до 24 часов. Реакцию предпочтительно осуществляют в течение промежутка времени от 30 минут до 12 часов, особенно предпочтительно от 1 до 6 часов.
Растворителями, пригодными для осуществления предлагаемого в изобретении способа, являются вода, диметилсульфоксид, сульфолан, спирты, такие как метанол, этанол, пропанол, изопропанол, бутанол, трет-бутанол, циклопентанол, циклогексанол, этиленгликоль или монометиловый эфир этиленгликоля, сложные эфиры, такие как сложный метиловый эфир уксусной кислоты или сложный этиловый эфир уксусной кислоты, амиды, такие как формамид, N,N-диметилформамид, N,N-диметилацетамид или N-метил-пирролидон, простые эфиры, такие как тетрагидрофуран или 1,4-диоксан, нитрилы, такие как ацетонитрил, пропионитрил, бутиронитрил или бензонитрил, кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон или пинаколин, или смеси указанных разбавителей.
Предпочтительно используют воду, диметилсульфоксид, метанол, этанол, пропанол, изопропанол, бутанол, mpem-бутанол, циклогексанол, этиленгликоль, сложный метиловый эфир уксусной кислоты, N,N-диметилформамид, N,N-диметилацетамид, тетрагидрофуран, 1,4-диоксан, ацетонитрил, ацетон, метилэтилкетон, метилизобутилкетон или смеси указанных разбавителей.
Еще более предпочтительно используют смеси воды с метанолом, этанолом, пропанолом, изопропанолом, сложным метиловым эфиром уксусной кислоты, тетрагидрофураном, 1,4-диоксаном, ацетонитрилом или ацетоном.
Приведенные ниже примеры служат для более подробного пояснения предлагаемого в изобретении способа и не ограничивают объем изобретения.
Пример 1
Загружают раствор 90 г [0,5 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 875 мл метанола с комнатной температурой, к которому в течение примерно 10 минут по каплям добавляют раствор 110,7 г [0,7 моля] тиосульфата натрия в 188 мл воды, причем внутренняя температура повышается до 42°C. По завершении добавления указанного раствора температуру повышают до 60°C и реагенты в течение четырех часов перемешивают при этой температуре. Затем реакционную смесь охлаждают до 10°C, твердое вещество отсасывают, промывают тремя порциями воды объемом 150 мл каждая, а затем 100 мл метанола и сушат. Получают 53,7 г зеленого твердого вещества, которое согласно результатам анализа методом жидкостной хроматографии при высоком давлении (ЖХВД) содержит 98,4% соединения (1-1), что соответствует его выходу от теоретического 74,9%.
Пример 2
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл метанола с температурой 65°C, к которому в течение примерно 10 минут по каплям добавляют раствор 29,77 г [0,12 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 65°C. По завершении добавления указанного раствора реагенты в течение часа перемешивают при 65°С.Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл метанола и сушат. Описанным выше методом получают 10,1 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 97,76% масс. соединения (1-1), что соответствует его выходу от теоретического 70%.
Пример 3
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл метанола с температурой 65°C, к которому в течение примерно 10 минут по каплям добавляют раствор 34,73 г [0,14 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 65°C. По завершении добавления указанного раствора реагенты в течение часа перемешивают при 65°C. Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл метанола и сушат. Описанным выше методом получают 11,3 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 95,9% масс. соединения (1-1), что соответствует его выходу от теоретического 76,8%.
Пример 4
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл метанола с температурой 65°C, к которому в течение примерно 10 минут по каплям добавляют раствор 37,22 г [0,15 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 65°C. По завершении добавления указанного раствора реагенты в течение часа перемешивают при 65°С. Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл метанола и сушат. Описанным выше методом получают 10,65 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 98% масс. соединения (1-1), что соответствует его выходу от теоретического 73,9%.
Пример 5
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл метанола с температурой 65°C, к которому в течение примерно 10 минут по каплям добавляют раствор 39,7 г [0,16 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 65°C. По завершении добавления указанного раствора реагенты в течение часа перемешивают при 65°C. Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл метанола и сушат. Описанным выше методом получают 10,4 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 97,3% масс. соединения (1-1), что соответствует его выходу от теоретического 71,7%.
Пример 6
Загружают раствор 360 г [2 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 3500 мл метанола с комнатной температурой, к которому в течение примерно 20 минут по каплям добавляют раствор 442,8 г [2,8 молей] тиосульфата натрия в 750 мл воды. По завершении добавления указанного раствора температуру повышают до 60°C и реагенты в течение последующих четырех часов перемешивают при этой температуре. Затем реакционную смесь охлаждают до 15°C, добавляют 250 мл воды и перемешивают в течение 10 минут. Твердое вещество отсасывают, промывают посредством 1200 мл воды, а затем 600 мл метанола и сушат. Описанным выше методом получают 210,2 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 97,9% масс. соединения (1-1), что соответствует его выходу от теоретического 72,9%.
Пример 7
Загружают раствор 7,2 г [0,04 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 70 мл метанола с комнатной температурой, к которому в течение примерно 10 минут по каплям добавляют раствор 10,74 г [0,068 моля] тиосульфата натрия в 23 мл воды. По завершении добавления указанного раствора температуру повышают до 60°C и реагенты в течение последующих четырех часов перемешивают при этой температуре. Затем реакционную смесь охлаждают до 15°C, добавляют 10 мл воды и перемешивают в течение 10 минут. Твердое вещество отсасывают, промывают посредством 35 мл воды, а затем 10 мл метанола и сушат. Описанным выше методом получают 3,83 г зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 94,7% масс. соединения (1-1), что соответствует его выходу от теоретического 64,2%.
Пример 8
Загружают раствор 7,2 г [0,04 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 70 мл метанола с комнатной температурой, к которому в течение примерно 10 минут по каплям добавляют раствор 12,64 г [0,08 моля] тиосульфата натрия в 27 мл воды. По завершении добавления указанного раствора температуру повышают до 60°C и реагенты в течение последующих четырех часов перемешивают при этой температуре. Затем реакционную смесь охлаждают до 15°C, добавляют 10 мл воды и перемешивают в течение 10 минут. Твердое вещество отсасывают, промывают посредством 35 мл воды, а затем 10 мл метанола и сушат. Описанным выше методом получают 2,5 г зеленого твердого вещества, которое согласно результатам ЖХВД-анализа содержит 83,7% соединения (1-1), что соответствует его выходу от теоретического 37%.
Пример 9
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл этанола с температурой 75°C, к которому в течение примерно 10 минут по каплям добавляют раствор 34,73 г [0,14 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 75°C. По завершении добавления указанного раствора реагенты в течение часа перемешивают при 75°C. Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл этанола и сушат. Описанным выше методом получают 11,0 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 97% масс, соединения (1-1), что соответствует его выходу от теоретического 75,5%.
Пример 10
Загружают раствор 7,2 г [0,04 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 70 мл метанола с комнатной температурой, к которому в течение примерно 10 минут по каплям добавляют раствор 6,52 г [0,044 моля] тиосульфата аммония в 15 мл воды. По завершении добавления указанного раствора температуру повышают до 45°C и реагенты в течение последующих двух часов перемешивают при этой температуре. Затем реакционную смесь охлаждают до 10°C, перемешивают еще в течение 10 минут, твердое вещество отсасывают, промывают посредством 35 мл воды, а затем 10 мл метанола и сушат. Описанным выше методом получают 3,5 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 97,1% масс. соединения (I-1), что соответствует его выходу от теоретического 60,2%.
Пример 11
Загружают раствор 7,2 г [0,04 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 70 мл метанола с комнатной температурой, к которому в течение примерно 10 минут по каплям добавляют раствор 8,3 г [0,056 моля] тиосульфата аммония в 15 мл воды. По завершении добавления указанного раствора температуру повышают до 45°C и реагенты в течение последующих четырех часов перемешивают при этой температуре. Затем реакционную смесь охлаждают до 10°C, перемешивают еще в течение 10 минут, твердое вещество отсасывают, промывают посредством 35 мл воды, а затем 10 мл метанола и сушат. Описанным выше методом получают 3,85 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 98,3% масс. соединения (1-1), что соответствует его выходу от теоретического 67%.
Пример 12
Загружают раствор 6,64 г [0,04 моля] N-метилимида дихлормалеиновой кислоты (VI-2) в 40 мл метанола с температурой 65°C, к которому в течение примерно 10 минут по каплям добавляют раствор 13,89 г [0,056 моля] пентагидрата тиосульфата натрия в 40 мл воды, также нагретый до 65°C. По завершении добавления указанного раствора реагенты в течение часа перемешивают при 65°C. Затем реакционную смесь охлаждают до 15°C, добавляют 10 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 30 мл воды, а затем 15 мл метанола и сушат. Описанным выше методом получают 3,6 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 99,6% соединения (1-2), что соответствует его выходу от теоретического 71%.
Сравнительный пример 1 (в соответствии с примером IX из патента США US 3,364,229; R означает водород)
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл этанола с температурой 75°C, к которому в течение примерно 10 минут по каплям добавляют раствор 24,8 г [0,10 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 75°C. По завершении добавления указанного раствора реагенты перемешивают в течение часа при 75°c. Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл этанола и сушат. Описанным выше методом получают 9,1 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 94,3% соединения (1-1), что соответствует его выходу от теоретического 60,8%.
Сравнительный пример 2
Загружают раствор 18 г [0,1 моля] N-метилимида дихлормалеиновой кислоты (VI-1) в 100 мл метанола с температурой 65°C, к которому в течение примерно 10 минут по каплям добавляют раствор 24,8 г [0,10 моля] пентагидрата тиосульфата натрия в 100 мл воды, также нагретый до 65°C. По завершении добавления указанного раствора реагенты перемешивают в течение часа при 65°C. Затем реакционную смесь охлаждают до 15°C, добавляют 17 мл воды и перемешивают в течение 15 минут. Твердое вещество отсасывают, промывают посредством 70 мл воды, а затем 30 мл метанола и сушат. Описанным выше методом получают 10,4 г темно-зеленого твердого вещества, которое согласно результатам ЖХВД-анализа с использованием эталонного вещества содержит 89,15% масс. соединения (1-1), что соответствует его выходу от теоретического 65,7%.
Общие сведения
Условия выполнения жидкостной хроматографии при высоком давлении: хроматографическая колонка Zorbax Eclipse Plus С18 4,6×50 мм, 1,8 мкм, элюент А: 0,1% H3PO4, элюент В: ацетонитрил, градиент: 90/10, 20%/мин, 5/95 (1,75), скорость потока 2 мл/мин, 55°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СИНТЕЗА ДИТИИН-ТЕТРАКАРБОКСИ-ДИИМИДОВ | 2011 |
|
RU2574393C9 |
| СПОСОБ ПОЛУЧЕНИЯ ДИТИИН-ТЕТРАКАРБОКСИМИДОВ | 2011 |
|
RU2559626C9 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ | 1995 |
|
RU2180335C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗОЛИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2095359C1 |
| АМИДЫ АЛЬФА-АМИНОКИСЛОТ, ИХ ПОЛУЧЕНИЕ И ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 1997 |
|
RU2174511C2 |
| АМИДЫ АЛКОКСИМИНОУКСУСНОЙ КИСЛОТЫ, ФУНГИЦИДНОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ БОРЬБЫ С ГРИБКОВЫМИ ЗАБОЛЕВАНИЯМИ РАСТЕНИЙ | 1996 |
|
RU2167853C2 |
| 2,4,5-ТРИЗАМЕЩЕННЫЕ ФЕНИЛКЕТОЕНОЛЫ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ, СПОСОБ И СРЕДСТВО ДЛЯ БОРЬБЫ С НАСЕКОМЫМИ И ПАУКООБРАЗНЫМИ НА ИХ ОСНОВЕ | 1996 |
|
RU2195449C2 |
| ИНГИБИТОРЫ ФЕРМЕНТА ДИАЦИЛГЛИЦЕРИН О-АЦИЛТРАНСФЕРАЗЫ ТИПА 1 | 2008 |
|
RU2497816C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ АМИНОДИКАРБОНОВЫХ КИСЛОТ, ОБЛАДАЮЩИЕ ФАРМАЦЕВТИЧЕСКИМИ СВОЙСТВАМИ | 2000 |
|
RU2280025C9 |
| АЗОТСОДЕРЖАЩИЕ ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ ВИЧ | 2016 |
|
RU2720145C2 |
Изобретение относится к новому способу получения дитиинтетракарбоксидиимидов общей формулы (I):
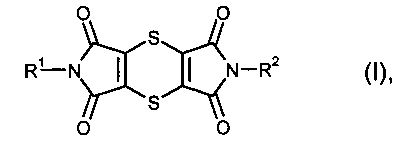
в которой R1 и R2 одинаковые или разные и означают водород, алкил с 1-8 атомами углерода, при необходимости однократно или многократно замещенный галогеном, -OR3, -COR4, циклоалкил с 3-7 атомами углерода, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода или галогеналкилом с 1-4 атомами углерода, арил, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, -COR4 или сульфониламино, или арилалкил с 1-4 атомами углерода в алкиле, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, -COR4 или сульфониламино, R3 означает водород, алкил с 1-4 атомами углерода, алкилкарбонил с 1-4 атомами углерода в алкиле или арил, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода или галогеналкилом с 1-4 атомами углерода, R4 означает гидрокси, алкил с 1-4 атомами углерода или алкокси с 1-4 атомами углерода, отличающийся тем, что имиды дихлормалеиновой кислоты формулы (VI):
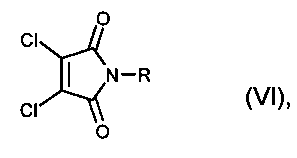
в которой R идентичен остатку R1 или R2, в растворителе или смеси растворителей подвергают превращению с неорганическим тиосульфатом в молярном соотношении тиосульфата между 1,3 и 1,6 моль на моль имида дихлормалеиновой кислоты формулы (VI). 1 з.п. ф-лы, 12 пр.
1. Способ получения дитиинтетракарбоксидиимидов общей формулы (I):

в которой
R1 и R2 одинаковые или разные и означают водород, алкил с 1-8 атомами углерода, при необходимости однократно или многократно замещенный галогеном, -OR3, -COR4, циклоалкил с 3-7 атомами углерода, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода или галогеналкилом с 1-4 атомами углерода, арил, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, -COR4 или сульфониламино, или арилалкил с 1-4 атомами углерода в алкиле, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода, галогеналкилом с 1-4 атомами углерода, -COR4 или сульфониламино,
R3 означает водород, алкил с 1-4 атомами углерода, алкилкарбонил с 1-4 атомами углерода в алкиле или арил, при необходимости однократно или многократно замещенный галогеном, алкилом с 1-4 атомами углерода или галогеналкилом с 1-4 атомами углерода,
R4 означает гидрокси, алкил с 1-4 атомами углерода или алкокси с 1-4 атомами углерода,
отличающийся тем, что имиды дихлормалеиновой кислоты формулы (VI):

в которой R идентичен остатку R1 или R2,
в растворителе или смеси растворителей подвергают превращению с неорганическим тиосульфатом в молярном соотношении тиосульфата между 1,3 и 1,6 моль на моль имида дихлормалеиновой кислоты формулы (VI).
2. Способ по п. 1, отличающийся тем, что в качестве тиосульфата используют растворимые неорганические соли тиосерной кислоты, выбранные из тиосульфата лития, тиосульфата натрия, тиосульфата калия, тиосульфата цезия, тиосульфата магния, тиосульфата аммония или их смеси.
| US 3364229 A, 16.01.1968 | |||
| US 3053853 A1, 11.09.1962 | |||
| RU 2012155464 A, 16.05.2011. |
Авторы
Даты
2015-12-10—Публикация
2011-04-08—Подача