Изобретение относится к комбинации, содержащей в качестве компонентов (а), по меньшей мере, одно соединение 3-(3-диметиламино-1-этил-2-метил-пропил)-фенол и (б), по меньшей мере, одно противоэпилептическое средство, к фармацевтической композиции и к лекарственной форме, содержащей вышеуказанную комбинацию, а также к способу лечения боли, например невропатической боли, посредством которого компоненты (а) и (б) вводят одновременно или последовательно млекопитающему, причем компонент (а) может быть введен до или после компонента (б) и причем компоненты (а) или (б) вводят млекопитающему или через один и тот же, или через другой путь введения.
Лечение состояний хронической и острой боли является исключительно важным в медицине. В настоящее время во всем мире существует потребность в дополнительном, основывающемся не только на опиоидах, но высокоэффективном лечении боли. Крайняя необходимость в действии для ориентированного на пациентов и целенаправленного лечения состояний боли, что означает успешное и удовлетворительное лечение боли у пациента, документально подтверждена в большом количестве научных публикаций, которые появились недавно в области применения анальгетиков и фундаментальной исследовательской работе по ноцицепции.
Даже если анальгетики, которые сейчас используют для лечения боли, например опиоиды, ингибиторы обратного захвата норадреналина и 5НТ, нестероидные противовоспалительные средства и ЦОГ ингибиторы, имеют анальгезирующее действие, тем не менее иногда проявляются побочные эффекты. Заявка WO 01/13904 описывает комбинации веществ, содержащие вещество трамадол и противосудорожное средство, которые в результате применения демонстрируют супераддитивные эффекты. Благодаря супераддитивному эффекту могут быть уменьшены общая доза и соответственно риск нежелательных побочных эффектов.
Таким образом, задача изобретения состояла в том, чтобы разработать дополнительные комбинации, обладающие улучшенными свойствами. К тому же целью изобретения являлась разработка дополнительных комбинаций, пригодных для лечения боли и которые предпочтительно проявляют меньше побочных эффектов в сравнении с их индивидуальными компонентами, если применяют в эффективной дозе.
Было обнаружено, что комбинация, содержащая (а) по меньшей мере, одно соединение 3-(3-диметиламино-1-этил-2-метил-пропил)-фенол и (б) по меньшей мере, одно противоэпилептическое средство, проявляет обезболивающее действие. Если эти компоненты присутствуют в композиции в таком весовом соотношении, что наблюдается супрааддитивный или синергетический эффект при введении пациенту, то общая вводимая доза может быть снижена, так что будет проявляться меньше побочных эффектов.
Следовательно, изобретение относится к фармацевтической комбинации, содержащей в качестве компонентов
(а) 3-(3-диметиламино-1-этил-2-метил-пропил)-фенол формулы (I)
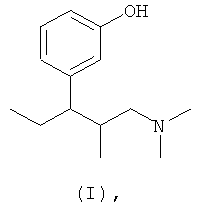
при необходимости в виде одного из его чистых изомеров, в частности энантиомера или диастереомера, рацемата или в виде смеси его стереоизомеров, в частности энантиомеров и/или диастереомеров в любом соотношении компонентов, или любой из его соли присоединения кислоты, и
(б) по меньшей мере, одно противоэпилептическое средство.
В одной форме осуществления комбинации согласно изобретению соединение формулы (I) выбрано из
(1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенола,
(1S,2S)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенола,
(1R,2S)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенола,
(1S,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол, и смеси из этого.
В другой форме осуществления комбинации согласно изобретению соединение формулы (I) выбрано из
(1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенола, и
(1S,2S)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенола, и смеси из этого.
В еще другой форме осуществления комбинация согласно изобретению включает
(а) соединение (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенола формулы (I')
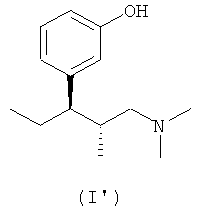
или его соль присоединения кислоты, и
(б) по меньшей мере, одно противоэпилептическое средство.
Соединение 3-(3-диметиламино-1-этил-2-метил-пропил)-фенол формулы (I), его стереоизомеры и соответственно его соли, а также способы его получения являются хорошо известными, например, из US 6,248,737 В1. Таким образом, соответствующие части описания включены путем ссылки и являются частью настоящего раскрытия.
Определение компонента (а), как используется здесь, включает в себя 3-(3-диметиламино-1-этил-2-метил-пропил)-фенол, его производные и его стереоизомеры в любом возможном виде, следовательно, в частности, в том числе сольваты и полиморфы, соли, в частности соли присоединения кислоты и соответствующие сольваты и полиморфы.
Термин производное, как используется здесь, в частности, включает пролекарства, такие как простые и сложные эфиры активного вещества. Пригодные способы селекции и получения пролекарства данного вещества описаны, например, в "Textbook of Drug Design and Discovery", 3-е издание, 2002, глава 14, сс.410-458, изд.: Krogsgaard-Larsen et al., Taylor и Francis, соответствующие части описания приведенного литературного источника включены путем ссылки и являются частью настоящего раскрытия.
Если компонент (а) присутствует в виде смеси энантиомеров, то такая смесь может содержать энантиомеры в рацемической или нерацемической форме. Нерацемическая форма может содержать, например, энантиомеры в соотношении 60±5:40±5, 70±5:30±5, 80±5:20±5 или 90±5:10±5.
Соединение 3-(3-диметиламино-1-этил-2-метил-пропил)-фенол и его стереоизомеры согласно компоненту (а) в фармацевтической композиции согласно изобретению может находиться в виде соли присоединения кислоты, причем может применяться любая пригодная кислота, способная к образованию такой соли присоединения.
Превращение 3-(3-диметиламино-1-этил-2-метил-пропил)-фенола в соответствующую соль присоединения, например, путем реакции с приемлемой кислотой может быть осуществлено способом, общеизвестным для специалиста в данной области техники. Пригодные кислоты включают, но не ограничиваются, соляную кислоту, бромисто-водородную кислоту, серную кислоту, метансульфокислоту, муравьиную кислоту, уксусную кислоту, щавелевую кислоту, янтарную кислоту, винную кислоту, миндальную кислоту, фумаровую кислоту, молочную кислоту, лимонную кислоту, глутаминовую кислоту и/или аспарагиновую кислоту. Образование соли предпочтительно происходит в растворителе, например, простом диэтиловом эфире, диизопропиловом эфире, алкилацетатах, ацетоне и/или 2-бутаноне. Кроме того, триметилхлорсилан в водном растворе также является пригодным для получения гидрохлоридов.
Противоэпилептические средства, которые часто также называются противосудорожными средствами, хорошо известны в данной области техники и включают без ограничения барбитураты и производные, такие как, метилфенобарбитал, фенобарбитал, примидон, барбексаклон и метарбитал; производные гидантоина, такие как, этотоин, фенитоин, амино(дифенилгидантоин) валериановая кислота, мефенитоин и фосфенитоин; производные оксазолидина, такие как, параметадион, триметадион и этадион; производные сукцинимида, такие как, этосуксимид, фенсуксимид и мезуксимид; производные бензодиазепина, такие как, клоназепам; производные карбоксамида, такие как, карбамазепин, окскарбазепин, эсликарбазепин и руфинамид; производные кислоты жирного ряда, такие как, вальпроевая кислота, вальпромид, аминомасляная кислота, вигабатрин, прогабид и тиагабин; или другие противосудорожные средства, такие как, сультиам, фенацемид, ламотригин, фелбамат, топирамат, габапентин, фенетурид, леветирацетам, бриварацетам, селектрацетам, зонизамид, прегабалин, стирипентол, лакозамид и бекламид.
Эти указанные выше классы противоэпилептических средств и большинство из их отдельных представителей перечислены, например, в анатомо-терапевтическо-химической классификации (АТС) под [N03], которая используется ВОЗ для классификации фармацевтически активных ингредиентов (предпочтительное издание: январь 2008 или 2009). Относительно других подробностей индекса АТС делается ссылка на U.Fricke, J.Gunther, Anatomisch-therapeutisch-chemische Klassifikation mit Tagesdosen fur den deutschen Arzneimittelmarkt: Methodik der ATC-Klassifikation und DDD-Festlegung. ATC-lndex mit DDD-Angaben, Wissenschaftliches Institut derAOK; и Swiss Pharmaceutical Society, Index Nominum: International Drug Directory, CRC Press; 18-е изд-е (январь 31, 2004).
Другие пригодные противоэпилептические средства включают в себя, например, мексилетин, ретигабин и ралфинамид.
Некоторые противоэпилептические средства известны как применимые при лечении невропатической боли. В одной форме осуществления изобретения одно или несколько из этих противоэпилептических средств используют в качестве компонента (б).
Также включены стереоизомеры, соли, сольваты, полиморфы и производные противоэпилептического компонента, а также смеси из указанных выше.
В одной форме осуществления комбинации согласно изобретению противоэпилептическое средство согласно компоненту (б) выбрано из группы, содержащей прегабалин, габапентин, топирамат, ламотригин, карбамазепин, оксакарбамазепин, эсликарбазепин, мексилетин, лакозамид, фенитоин, леветирацетам, бриварацетам, селектрацетам, ретигабин, вальпроевую кислоту и ралфинамид.
В другой форме осуществления комбинации согласно изобретению противоэпилептическое средство согласно компоненту (б) выбрано из группы, содержащей прегабалин, габапентин, топирамат, ламотригин, карбамазепин, мексилетин, лакозамид, фенитоин, леветирацетам, ретигабин, вальпроевую кислоту и ралфинамид.
В другой форме осуществления комбинации согласно изобретению противоэпилептическое средство согласно компоненту (б) представляет собой прегабалин.
В еще другой форме осуществления комбинации согласно изобретению противоэпилептическое средство согласно компоненту (б) представляет собой (S)-прегабалин.
Особая форма осуществления изобретения представляет собой комбинацию, включающую (а) (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол, или его соль присоединения кислоты, такую как, гидрохлоридная соль присоединения, и (б) одно или несколько противоэпилептических средств, выбранных из группы, содержащей прегабалин, габапентин, топирамат, ламотригин, карбамазепин, оксакарбамазепин, эсликарбазепин, мексилетин, лакозамид, фенитоин, леветирацетам, бриварацетам, селектрацетам, ретигабин, вальпроевую кислоту и ралфинамид.
Особая форма осуществления изобретения представляет собой комбинацию, включающую (а) (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол, или его соль присоединения кислоты, такую как, гидрохлоридная соль присоединения, и (б) одно или несколько противоэпилептических средств, выбранных из группы, содержащей прегабалин, габапентин, топирамат, ламотригин, карбамазепин, мексилетин, лакозамид, фенитоин, леветирацетам, ретигабин, вальпроевую кислоту и ралфинамид.
Другая особая форма осуществления изобретения представляет собой комбинацию, включающую (а) (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол, или его соль присоединения кислоты, такую как, гидрохлоридная соль присоединения, и (б) прегабалин.
Еще одна другая особая форма осуществления изобретения представляет собой комбинацию, включающую (а) (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол, или его соль присоединения кислоты, такую как, гидрохлоридная соль присоединения, и (б) (S)-прегабалин.
Некоторые противоэпилептические средства содержат функциональные группы, например кислотные группы, такие как, карбокси группы, которые способны образовывать соли с компонентом 3-(3-диметиламино-1-этил-2-метил-пропил)-фенола формулы (I), тем самым объединять оба компонента (а) и (б) в одной и той же соли.
Таким образом, в другой форме осуществления изобретения комбинация согласно изобретению включает компоненты (а) и (б) в виде соли, образованной из этих двух компонентов. Такое образование соли может быть частичным, т.е. композиция согласно изобретению включает один или оба этих компонента к тому же в их не солевой форме, или образование соли, по существу, может быть полным.
Оба компонента (а) и (б) как часть комбинации согласно изобретению могут быть применены в количестве до их максимальной суточной дозы, которая известны специалисту в данной области техники. Предпочтительно соединение прегабалин может быть введено пациенту в суточной дозе от 1 до 1200 мг, соединение габапентин предпочтительно может вводиться пациенту в суточной дозе от 1 до 5000 мг.
Соединение (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол предпочтительно может быть введено пациенту в суточной дозе от 25 до 1000 мг, в частности предпочтительно в дозировке от 50 до 800 мг, в частности более предпочтительно в дозировке от 100 до 600 мг.
Если вводят как часть комбинации согласно изобретению, то вводимое в сутки количество компонента (а) и/или компонента (б) может быть меньшим, чем соответствующий максимум суточной дозы и составлять, например, 75±15 мас.%, 75±10 мас.%, 75±5 мас.%, 50±15 мас.%, 50±10 мас.%, 50±5 мас.%, 25±15 мас.%, 25±10 мас.% и 25±5 мас.% для каждого из компонентов.
В другой форме осуществления изобретения комбинация согласно изобретению может содержать компоненты (а) и (б), по существу, в эквиэффективном соотношении.
В еще одной дополнительной форме осуществления комбинации согласно изобретению компоненты (а) и (б) находятся в таком весовом соотношении, что полученная композиция проявляет супрааддитивный или синергетический эффект при введении пациенту. Приемлемые весовые соотношения могут быть определены способами, хорошо известными специалисту в данной области техники.
Оба компоненты (а) и (б) также могут находиться в комбинации согласно изобретению в соотношениях, отклоняющихся от эквиэффективного соотношения. Например, каждый из компонентов может находиться в пределах от 1/50 эквиэффективного количества до 50 раз эквиэффективного количества, от 1/20 эквиэффективного количества до 20 раз эквиэффективного количества, от 1/10 эквиэффективного количества до 10 раз эквиэффективного количества, от 1/5 эквиэффективного количества до 5 раз эквиэффективного количества, от 1/4 эквиэффективного количества до 4 раз эквиэффективного количества, от 1/3 эквиэффективного количества до 3 раз эквиэффективного количества или от 1/2 эквиэффективного количества до 2 раз эквиэффективного количества.
В другой форме осуществления изобретения компоненты (а) и (б) могут быть введены с особой схемой приема для лечения боли, например невропатической боли. Компоненты (а) и (б) могут применяться одновременно или последовательно один за другим, в каждом случае через тот же самый или другой путь введения.
Вследствие этого другим объектом изобретения является способ лечения боли, отличающийся тем, что компоненты (а) и (б) вводят одновременно или последовательно млекопитающему, причем компонент (а) может быть введен до или после компонента (б) и где компоненты (а) или (б) вводят млекопитающему или через один и тот же, или через другой путь введения.
Понятие боли, употребляемое в данном случае, охватывает, но не ограничивается, воспалительную боль, невропатическую боль, острую боль, хроническую боль, висцеральную боль, боль при мигрени и раковую боль.
Приемлемые пути введения включают, но не ограничиваются, оральное, внутривенное, внутриартериальное, внутрибрюшинное, внутрикожное, чрескожное, интратекальное, внутримышечное, интраназальное, трансмузокальное, подкожное и ректальное введение.
Комбинации согласно изобретению являются безопасными токсикологически и, следовательно, пригодны для лечения млекопитающих, в частности людей, включая младенцев, детей и взрослых.
Таким образом, другой объект изобретения относится к фармацевтической композиции, содержащей комбинацию согласно изобретению, которая описана здесь и одно или несколько вспомогательных средств.
Другой объект изобретения относится к фармацевтической лекарственной форме, содержащей комбинацию согласно изобретению, которая описана здесь и одно или несколько вспомогательных средств.
В одной форме осуществления фармацевтическая лекарственная форма согласно изобретению дополнительно содержит кофеин.
В одной форме осуществления фармацевтическая лекарственная форма согласно изобретению пригодна для введения орально, внутривенно, внутриартериально, внутрибрюшинно, внутрикожно, чрескожно, интратекально, внутримышечно, интраназально, трансмузокально, подкожно или ректально.
Композиции согласно изобретению и лекарственные формы дополнительно могут содержать средства, например носители, наполнители, растворители, разбавители, красители и/или связующие вещества. Выбор используемых вспомогательных средств и их количества зависит, например, от того каким образом применяют лекарственное средство, т.е. орально, внутривенно, внутриартериально, внутрибрюшинно, внутрикожно, чрескожно, внутримышечно, интраназально или локально, например, при заражениях кожи, слизистых оболочек или глаз.
Пригодными вспомогательными средствами в контексте этого изобретения являются, в частности, любые вещества, известные специалисту в данной области техники, которые используют для приготовления галеновых препаратов. Примеры пригодных вспомогательных средств включают, но не ограничиваются, воду, этанол, 2-пропанол, глицерин, этиленгликоль, пропиленгликоль, полиэтиленгликоль, полипропиленгликоль, глюкозу, фруктозу, лактозу, сахарозу, декстрозу, мелассу, крахмал, модифицированный крахмал, желатин, сорбит, инозит, маннит, микрокристаллическую целлюлозу, метилцеллюлозу, карбокисметилцеллюлозу, ацетат целлюлозы, шеллак, цетиловый спирт, поливинипирролидон, парафины, воски, природные и синтетические смолы, аравийскую камедь, альгинаты, декстран, насыщенные и ненасыщенные кислоты жирного ряда, стеариновую кислоту, стеарат магния, стеарат цинка, стеарат глицерина, лаурилсульфат натрия, пищевые масла, кунжутное масло, кокосовое масло, арахисовое масло, соевое масло, лецитин, лактат натрия, полиоксиэтиленовые и полипропиленовые эфиры кислот жирного ряда, эфир сорбита и жирной кислоты, сорбиновую кислоту, бензойную кислоту, лимонную кислоту, аскорбиновую кислоту, дубильную кислоту, хлорид натрия, хлорид калия, хлорид магния, хлорид кальция, оксид магния, оксид цинка, диоксид кремния, оксид титана, диоксид титана, сульфат магния, сульфат цинка, сульфат кальция, поташ, фосфат кальция, фосфат дикальция, бромит калия, иодид калия, тальк, каолин, пектин, кросповидон, агар и бентонит.
Фармацевтические препараты (лекарственные формы) в виде таблеток, шипучих таблеток, жевательных таблеток, драже, капсул, капель, соков или сиропов пригодны, например, для орального применения. Оральные фармацевтические препараты также могут быть в виде множества частиц, таких как, гранул, пилюль, шариков, кристаллов и т.п., при необходимости спрессованных в таблетку, заключенных в капсулу, наполненных в саше или суспендированных в приемлемой жидкой среде. Оральные фармацевтические препараты также могут быть снабжены энтеросолюбильным покрытием.
Фармацевтические препараты, которые пригодны для парентерального, местного и ингаляционного применения, включают, но не ограничиваются, растворы, суспензии, легко ресуспендируемые сухие препараты и спреи.
Суппозитории являются приемлемым фармацевтическим препаратом для ректального введения. Препараты в форме депо, в растворенном виде, например, в пластыре, при необходимости с добавлением агентов для активирования проникновения в кожу, являются приемлемыми препаратами для чрескожного введения.
Один или оба компонента (а) и (б) в фармацевтическом препарате согласно изобретению могут находиться, по меньшей мере, частично в форме с контролируемым высвобождением. Кроме того, любые комбинации с контролируемым/непосредственным высвобождением указанных компонентов также могут присутствовать в фармацевтическом препарате согласно изобретению. Например, один или оба компонента могут высвобождаться из препаратов согласно изобретению с некоторым замедлением, например, если их применяют орально, ректально или чрескожно. Подобные препараты, в частности, пригодны для препаратов «один раз в день» или «два раза в день», которые должны приниматься только раз в день, соответственно, дважды в день. Пригодные вещества с контролируемым высвобождением хорошо известны специалисту в данной области техники.
Фармацевтические препараты согласно изобретению могут быть изготовлены с использованием веществ, средств, устройств и способов, которые хорошо известны из уровня техники фармацевтических препаратов, как описано, например, в "Remington's Pharmaceutical Sciences", A.R.Gennaro (ред.), 17-е издание, Mack Publishing Company, Easton, Pa. (1985), в частности, в части 8, главы с 76 по 93.
Для того, чтобы получить твердый фармацевтический препарат, такой как, таблетка, например, компоненты фармацевтической композиции могут подвергаться гранулированию с фармацевтическим носителем, например, обычными ингредиентами для таблеток, такими как, кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеарат магния, фосфат дикальция или фармацевтически приемлемые смолы, и фармацевтические разбавители, например вода, для того, чтобы получить твердую композицию, которая содержит компоненты с гомогенным распределением. Понятие "гомогенное распределение" означает, что компоненты распределены однородно во всей композиции, так что указанная композиция может быть легко разделена на равным образом эффективные унифицированные лекарственные формы, такие как, таблетки, пилюли или капсулы и т.п. Затем твердые композиции разделяют на унифицированные лекарственные формы. Также таблетки или пилюли фармацевтической композиции в соответствии с изобретением могут быть покрыты или приготовлены различными способами с целью обеспечить лекарственную форму с контролируемым высвобождением.
Если один из компонентов должен быть высвобожден ранее другого компонента, например, по меньшей мере, ранее на 30 мин или на 1 ч, могут быть приготовлены фармацевтические препараты, имеющие соответствующий профиль высвобождения. Примером подобного препарата является осмотически управляемая система высвобождения для достижения замедленного высвобождения одного компонента посредством покрытия, что само содержит другой компонент, который соответственно высвобождается раньше. В системе высвобождения такого рода, которая, в частности, пригодна для орального применения, по меньшей мере, часть, предпочтительно вся поверхность системы высвобождения, предпочтительно те части, которые вступят в контакт с высвобождаемой средой, является/являются полупроницаемыми, предпочтительно снабжены полупроницаемым покрытием, таким образом поверхность (поверхности) является/являются проницаемыми для высвобождаемой среды, но, по существу, предпочтительно всецело непроницаемыми для активного ингредиента, поверхность (поверхности) и/или при необходимости покрытие содержит, по меньшей мере, одно отверстие для высвобождения активного ингредиента. Кроме того, именно та/те поверхность (поверхности), которые находятся в контакте с высвобождаемой средой, снабжены покрытием, которое содержит и высвобождает другой компонент. Предпочтительно имеют в виду систему в таблетированной форме, содержащую высвобождающее отверстие, осмотическое фармацевтическое композиционное ядро, полупроницаемую мембрану и полимерную часть, которая оказывает давление при набухании. Пригодным примером системы подобного рода является система, распространяемая посредством ALZA Corporation, США под торговыми наименованиями OROS®, в частности OROS® Push-Pull™ System, OROS® Delayed Push-Pull™ System, OROS® Multi-Layer Push-Pull™ system, OROS® Push-Stick System и также, в особом случае, L-OROS™.
Формы осуществления и примеры осмотически управляемых систем высвобождения раскрыты, например, в патентах US 4,765,989, 4,783,337 и 4,612,008, все соответствующие содержания которых таким образом включены посредством ссылки и составляют часть раскрытия изобретения.
Дополнительным примером пригодного фармацевтического препарата является таблетка с гелевой матрицей, такие как, продукты разработаны посредством Penwest Pharmaceuticals (например, под TimeRX). Приемлемые примеры представлены в патентах US 5,330,761, 5,399,362, 5,472,711 и 5,455,046, все соответствующие содержания которых таким образом включены посредством ссылки и составляют часть раскрытия изобретения. В частности, пригодной является замедляющий матричный препарат с негомогенным распределением фармацевтически активной композиции, причем, например, один компонент может быть распределен во внешней области (часть, которая входит в соприкосновение с высвобождающейся средой наиболее быстро) матрицы и другой компонент распределяется внутри матрицы. В контакте с высвобождающейся средой внешний матричный слой в начальной стадии (и быстро) набухает и, во-первых, высвобождает первый компонент, за которым следует значительно (более) замедленное высвобождение другого компонента. Примеры приемлемой матрицы включают матрицы с от 1 до 80 мас.% одного или нескольких гидрофильных или гидрофобных полимеров в качестве образователей фармацевтически приемлемой матрицы. Другой пример пригодной матрицы может быть взят из US 4,389,393, соответствующее содержание которого таким образом включено путем ссылки и составляет часть раскрытия изобретения.
Количество фармацевтически активной комбинации согласно изобретению, которое вводят пациенту, может варьироваться в зависимости от различных факторов, хорошо известных специалисту в данной области техники, например от веса пациента, пути введения или от тяжести заболевания.
Другой объект изобретения относится к применению комбинации согласно изобретению, как описано здесь, для лечения боли, вышеуказанная боль предпочтительно охватывает, но не ограничивается, воспалительную боль, невропатическую боль, острую боль, хроническую боль, висцеральную боль, боль при мигрени и раковую боль.
В другом аспекте изобретение относится к применению комбинации согласно изобретению, как описано здесь, для получения лекарственного средства для лечения боли, вышеуказанная боль предпочтительно включает, но не ограничивается, воспалительную боль, невропатическую боль, острую боль, хроническую боль, висцеральную боль, боль при мигрени и раковую боль.
В другом аспекте изобретение относится к способу лечения боли у млекопитающего, предпочтительно человека, который включает введение эффективного количества комбинации согласно изобретению, как описано здесь, млекопитающему.
Фармакологические способы:
Эксперименты in vivo согласно Чангу (Chung)
Весовые соотношения компонентов (а) и (б), которые приведут к супра-аддитивному эффекту/синергетическому эффекту композиций согласно изобретению, могут быть определены в тесте Kim & Chung как описано в Kirn SH, Chung JM. An experimental model for peripheral mononeuropathy produced by segmental spinal nerve ligation in the rat. Pain 1992; 50: 355-63. Настоящим указанная выше ссылка включается в изобретение и составляет часть настоящего раскрытия.
Лигатуры наносили на левые L5/L6 спинальные нервы самцов крыс Sprague-Dawley (140-160 г вес тела, Janvier, Genest St. Isle, Франция). У животных развивалась тактильная аллодиния на ипсилатеральной лапе. Через три или четыре недели после операции тактильной аллодинии пороговый исходный уровень (порог отдергивания) был измерен на ипсилатеральной и контралатеральной задней лапе посредством электронного анестезиометра Фрея (Frey) (Somedic, Швеция). После испытания и измерения исходного уровня (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол гидрохлорид (в дальнейшем именуемый тапентадол гидрохлорид или тапентадол-HCl), (S)-прегабалин, а также комбинацию согласно изобретению тапентадол-HCl и (S)-прегабалина каждый растворяли в 0,9% растворе NaCl и вводили внутривенным путем (i.v.) (объем применения 5 мл/кг). Животных случайным путем распределяли на группы по 10 для каждой тест-дозы и раствора лекарственной основы (0,9% раствор NaCl) и тактильные пороги отдергивания испытывали за 0,5 ч до введения и в отдельные моменты времени (0,5, 1 и 3 ч) после внутривенного введения. Исследовали ипсилатеральные и контралатеральные задние лапы. Срединное значение порога отдергивания каждого животного к каждому моменту времени подсчитывали от пяти индивидуальных стимуляций с помощью электронного филамента Фрея. Пороги отдергивания поврежденных лап выражали как % МРЕ (максимально возможный эффект) сопоставимого пролекарственного порога животных Чанга (Chung) (=0% МРЕ) и контрольного порога имитационных животных (100% МРЕ). Порог установлен при 100% МРЕ. Эффект каждого соединения и лекарственной основы подсчитывали для каждого тестируемого момента времени как интериндивидуальное % МРЕ значение.
Данные (антиаллодинической эффективности (% МРЕ), ипсилатеральный, порог отдергивания лапы (г), ипсилатеральный и контралатеральный) анализированы посредством дисперсионного двухфакторного анализа (ANOVA) с помощью повторных измерений. В случае значимого эффекта условий эксперимента с целью корректировки был произведен вторичный анализ (post hoc) Бонферрони (Bonferroni). Результаты рассматривали статистически существенными, если Р<0,05. EDw значения и 95% доверительных интервалов (95% Cl) определяли регрессивным анализом для антиаллодинической эффективности (% МРЕ) в момент пикового действия для каждого лекарства.
Анализ результатов проводили путем статистического сравнения теоретического добавления ЕОбо-значения с экспериментально определенным ЕОбо-значением так называемой комбинации с фиксированным соотношением (изоболографический анализ согласно Tallarida RJ, Porreca F, и Cowan A. Statistical analysis of drug-drug и site-site interactions with isobolograms. Life Sci 1989; 45: 947-61, который настоящим включен путем ссылки и составляет часть настоящего раскрытия).
Результаты:
Тапентадол гидрохлорид (0,1, 0,316, 1, 3,16 и 10 мг/кг i.v.) показал зависимое от дозы увеличение при пороге отдергивания ипсилатеральной задней лапы с эффективностью 94% МРЕ и ED50-значением (95% доверительный интервал) в 1,65 (1,20-2,35) мг/кг i.v., подсчитанное от пикового действия против контрольных значений в 30 мин после введения.
(S)-прегабалин (0,1, 3,16 и 10 мг/кг i.v.) показал зависимое от дозы увеличение при пороге отдергивания ипсилатеральной задней лапы с эффективностью 67% МРЕ и ED50-значением (95% доверительный интервал) в 4,20 (3,37-5,43) мг/кг i.v., подсчитанное от пикового действия в зависимости от контрольных значений через 30 мин после введения.
Тапентадол гидрохлорид и (S)-прегабалин показывают потенциальную разницу, которая достигает фактор 2.5 на основе ED50 значений через 30 мин после введения. Комбинации с фиксированным соотношением 1:2,5 (тапентадол гидрохлорид: (S)-прегабалин) исследовали в дозах 0,1 мг/кг +0,25 мг/кг; 0,3 мг/кг +0,75 мг/кг, 1 мг/кг+2,5 мг/кг i.v. тапентадол гидрохлорид +(S)-прегабалин соответственно. Эти комбинации показали зависимое от дозы увеличение при пороге отдергивания ипсилатеральной задней лапы. Исследованная комбинация наивысшей дозы показала полную эффективность с 89% МРЕ. Действенность была определена ED50 значением (95% доверительный интервал) в 0,83 (0,74-0,92) мг/кг i.v., подсчитанным от пикового действия в зависимости от контрольных значений через 30 мин после введения.
Результаты изоболографического анализа подытожены в таблице 1.
Экспериментальное ED50 значение (95% доверительный интервал) в 0,83 (0,74-0,92) мг/кг i.v. комбинации согласно изобретению ниже теоретического аддитивного ED50 значения (95% доверительный интервал) в 2,91 (2,28-3,54) мг/кг i.v. и является статистически значимым (р<0,001) по сравнению с линией аддитивности. Таким образом, взаимодействие тапентадола гидрохлорида и (S)-прегабалина является синергетическим.
Исследование контралатеральной лапы порогов отдергивания показывает существенные антиноцицептивные эффекты тапентадола гидрохлорида и (S)-прегабалина при 10 мг/кг i.v. в то время как не был заметен существенный антиноцицептивный эффект при наивысшей дозе комбинации согласно изобретению. Таким образом, синергетическая антиаллодиническая активность тапентадола гидрохлорида и (S)-прегабалина получается вследствие сниженных антиноцицептивных побочных эффектов.
Группа изобретений относится к фармацевтике. Описана синергетическая комбинация для лечения боли, содержащая (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол и противоэпилептическое средство. Противоэпилептическое средство выбирается из группы, включающей топирамат, ламотригин, карбамазепин, лакозамид, леветирацетам и ретигабин. Изобретения относятся к фармацевтическим композициям и лекарственным формам, включающим указанную комбинацию. Также изобретения относятся к применению указанной комбинации для получения лекарственного средства и способу лечения боли. Изобретения обеспечивают реализацию указанного назначения. 5 н. и 6 з.п. ф-лы, 1 табл.
1. Синергетическая комбинация для лечения боли, содержащая в качестве компонента (ов):
(а) (1R,2R)-3-(3-диметиламино-1-этил-2-метил-пропил)-фенол формулы (I′),

или его соль присоединения кислоты, и
(б) противоэпилептическое средство, выбранное из группы, включающей топирамат, ламотригин, карбамазепин, лакозамид, леветирацетам и ретигабин.
2. Комбинация по пункту 1, отличающаяся тем, что соль присоединения кислоты является гидрохлоридной солью.
3. Комбинация по пункту 1 или 2, отличающаяся тем, что компоненты (а) и (б) присутствуют в качестве солей, образованных из этих двух компонентов.
4. Фармацевтическая композиция, содержащая комбинацию по одному из пп.1-3 и вспомогательные средства.
5. Лекарственная форма, содержащая комбинацию по одному из пп.1-3 и вспомогательные средства.
6. Лекарственная форма по п.5, отличающаяся тем, что она пригодна для орального, внутривенного, внутриартериального, внутрибрюшинного, внутрикожного, чрескожного, интратекального, внутримышечного, интраназальноего, трансмукозального, подкожного или ректального введения.
7. Применение комбинации по одному из пп.1-3 для получения лекарственного средства для лечения боли.
8. Применение по п.7, отличающееся тем, что боль выбрана из воспалительной боли, невропатической боли, острой боли, хронической боли, висцеральной боли, боли при мигрени и раковой боли.
9. Способ лечения боли у млекопитающего, который включает введение эффективного количества комбинации по одному из пп.1-3 млекопитающему.
10. Способ по п. 9, отличающийся тем, что компонент (а) и компонент (б) комбинации применяют одновременно или последовательно млекопитающему, причем соединение (а) может быть введено до или после соединения (б) и причем соединения (а) или (б) применяют млекопитающему или через один и тот же, или через другой путь введения.
11. Способ по п. 9 или 10, отличающийся тем, что боль выбрана из воспалительной боли, невропатической боли, острой боли, хронической боли, висцеральной боли, боли при мигрени и раковой боли.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| КОМБИНАЦИИ АЛЬФА-2-ДЕЛЬТА-ЛИГАНДА С СЕЛЕКТИВНЫМ ИНГИБИТОРОМ ЦИКЛООКСИГЕНАЗЫ-2 | 2003 |
|
RU2286151C2 |
Авторы
Даты
2015-12-20—Публикация
2009-09-04—Подача