Объектом настоящей заявки является жидкая композиция, содержащая агонист ГПП-1 и/или его фармакологически приемлемую соль и, необязательно, по меньшей мере один фармакологически приемлемый эксципиент, причем композиция отличается тем, что она содержит метионин.
Следующим объектом является композиция по изобретению для лечения сахарного диабета. Еще одним объектом является применение композиции по изобретению для получения лекарственного средства для лечения сахарного диабета. Следующим объектом настоящей заявки является способ получения композиции по изобретению, содержащей соединение в одной лекарственной форме агониста ГПП-1 или/и его фармакологически приемлемой соли с метионином и, необязательно, по меньшей мере одним фармакологически приемлемым эксципиентом. Еще одним объектом является способ лечения пациента композицией согласно изобретению, содержащий введение композиции пациенту.
Обычные композиции соединений ГПП-1 содержат изотонизирующее вещество, буфер для установки значения pH и консервант.
WO2001/04156 (Zealand Pharmaceuticals) раскрывает жидкую композицию Ser39-эксендин-4(1-39)-NH2, гидрофосфата натрия и консервантов.
WO 2004/035623 (Zealand Pharmaceuticals) раскрывает жидкую композицию, содержащую стабилизированный эксендин, 50 мМ гистидина, 100-200 мМ сахарозы, маннита или другого приемлемого сахара, 20 мМ метионина, 20 мМ аспарагин-глутамина или Asp, c pH 5,3. Стабилизация осуществляется путем определенных модификаций аминокислотных структурных блоков эксендин-4(1-39), например, в позициях Gln13, Met14, Trp25 или Asn28.
WO 2005/021022 (Novo Nordisk) описывает жидкую композицию, содержащую ацетилированный ГПП-1, фенол в качестве консерванта, манит и глицерин в качестве изотонизирующего вещества и, необязательно, буфер.
WO 2006/051110 (Novo Nordisk) раскрывает жидкие композиции, содержащие лираглутид (соединение ГПП-1), полоксамер 188 или полоксамер 407 (Pluronic F-127) в качестве поверхностно-активного вещества, фенол, пропиленгликоль и фосфат натрия (pH 7,7). Добавление полоксамера-188 или полоксамера-407 ведет к стабилизации.
Эксендины представляют собой группу пептидов, которые могут снижать концентрацию глюкозы в крови. Эксендины имеют определенное сходство последовательности с ГПП-1(7-3,6) (53%, Goke et al. J. Biol. Chem. 268, 19650-55). Эксендин-3 и эксендин-4 стимулируют повышение продукции клеточного cAMP в ацинарных клетках поджелудочной железы морских свинок, взаимодействуя с рецепторами эксендина (Raufman, 1996, Reg. Peptides 61:1-18). Эксендин-3, в отличие от эксендина-4, вызывает увеличение выделения амилазы в ацинарных клетках поджелудочной железы. Эксендины действуют как агонисты ГПП-1.
Глюкагоноподобный пептид-1 (ГПП-1) является эндокринным гормоном, который усиливает инсулиновую реакцию после перорального приема глюкозы или жира. Обычно ГПП-1 снижает концентрацию глюкагона, замедляет опорожнение желудка, стимулирует биосинтез (про)инсулина, повышает чувствительность к инсулину и стимулирует инсулинонезависимый биосинтез гликогена (Holst (1999), Curr. Med. Chem 6:1005, Nauck et al. (1997) Exp. Clin. Endocrinol. Diabetes 105: 187, Lopez-Delgado et al. (1998) Endocrinology 139:2811). Человеческий ГПП-1 содержит 37 аминокислотных остатка (Heinrich et al., Endocrinol. 115:2176 (1984), Uttenthal et al., J. Clin. Endocrinol. Metabol. (1985) 61:472). Активные фрагменты ГПП-1 включают ГПП-1(7-36) и ГПП-1(7-37).
Эксендин-3, эксендин-4 и агонисты эксендина предлагались для лечения сахарного диабета и профилактики гипергликемии, причем они снижают двигательную функцию желудка и замедляют опорожнение желудка (US 5424286 и WO98/05351).
Аналоги эксендина могут характеризоваться замещениями аминогруппы и/или C-терминальным усечением естественной последовательности эксендина-4. Такие аналоги эксендина описаны в WO 99/07404, WO 99/25727 и WO 99/25728.
Твердофазный синтез AVE0010 описан в WO 01/0415,6 A1. AVE0010 имеет последовательность: desPro36эксендин-4(1-39)-Lys6-NH2. Это вещество раскрыто в документе WO 01/04156 как SEQ ID NO:93:
H-G-E-G-T-F-T-S-D-L-S-K-Q-M-E-E-E-A-V-R-L-F-I-E-W-L-K-N-G-G-P-S-S-G-A-P-P-S-K-K-K-K-K-K-NH2 (SEQ ID NO:1)
Эксендин-4 (39 AS) имеет последовательность:
H-G-E-G-T-F-T-S-D-L-S-K-Q-M-E-E-E-A-V-R-L-F-I-E-W-L-K-N-G-G-P-S-S-G-A-P-P-P-S-NH2 (SEQ ID NO:2)
Эксендин-3 имеет последовательность (J. Bio. Chem., 267, 1992, 7402-7405):
H-His-Ser-Asp-Gly-Thr-Phe-Thr-Ser-Asp-Leu-Ser-Lys-Gln-Met-Glu-Glu-Glu-Ala-Val-Arg-Leu-Phe-Ile-Glu-Trp-Leu-Lys-Asn-Gly-Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser-NH2 (SEQ ID NO: 3)
ГПП-1 имеет последовательность:
H-A-E-G-T-F-T-S-D-V-S-S-Y-L-E-G-Q-A-A-K-E-F-I-A-W-L-V-K-G-R-NH2 (SEQ ID NO: 4)
Задача настоящего изобретения состоит в том, чтобы повысить стабильность жидких композиций, содержащих агонист ГПП-1. В первую очередь следует улучшить физическую и химическую целостность. Эта задача была решена тем соединением в одной лекарственной форме агониста ГПП-1 с метионином.
Было найдено, что метионин способен повышать стабильность при хранении композиции, содержащей такой агонист ГПП-1, как AVE0010. Метионин не влияет на физическую целостность этих композиций.
Неожиданно было обнаружено, что добавлением метионина можно улучшить стабильность при хранении композиции согласно изобретению, уменьшив долю продуктов окисления метионина, высокомолекулярных белков и всех примесей. Эти параметры являются, по отдельности или вместе, мерой химической целостности композиций.
Далее, неожиданно было найдено, что биологическая активность композиций согласно изобретению повышалась при добавлении метионина.
Стабильность фармацевтически активных полипептидов может ухудшаться вследствие разных механизмов. Сюда входит pH, температура, свет и эффекты некоторых составляющих.
Ряд обычных составляющих композиций агонистов ГПП-1 может отрицательно влиять на химическую или/и физическую целостность и стабильность при хранении композиций, которые содержат агонист ГПП-1. Это, например, полисорбат 20, полисорбат 80, полоксамер 188, хлорид бензалкония и лизин. Поэтому композиции согласно изобретению предпочтительно не содержат этих компонентов.
Объектом настоящего изобретения является жидкая композиция, содержащая агонист ГПП-1 или/и его фармакологически приемлемую соль и, необязательно, по меньшей мере один фармакологически приемлемый эксципиент, причем композиция отличается тем, что она содержит метионин.
Композиция по изобретению предпочтительно содержит метионин в количестве от 0,5 мг/мл до 20 мг/мл, более предпочтительно в количестве от 1 мг/мл до 5 мг/мл. Может использоваться метионин D-форме. Равным образом может использоваться метионин в L-форме. Также могут использоваться смеси D-формы и L-формы в любых желаемых пропорциях.
В частности, композиция согласно изобретению не содержит ПАВов, таких, как полиолы, неполные простые и сложные эфиры многоатомных спиртов и простые и сложные эфиры жирных кислот и многоатомных спиртов, такие, как эфиры глицерина и сорбита. Более конкретно, композиции согласно изобретению не содержат неполных простых и сложных эфиров глицерина и сорбита и простых и сложных эфиров жирных кислот и глицерина и сорбита, выбранных из группы, состоящей из Span®, Tween®, Myrj®, Brij®, Cremophor®. Кроме того, композиции согласно изобретению не содержат, в частности, полиолов, выбранных из группы полипропиленгликолей, полиэтиленгликолей, полоксамеров, плюроников, тетроников. в частности, композиция согласно изобретению не содержит по меньшей мере одно вещество, выбранное из группы, состоящей из полисорбата и полоксамера.
В частности, композиция согласно изобретению по существу не содержит, а предпочтительно совсем не содержит полисорбатов, как, например, полисорбата 20.
В частности, композиция согласно изобретению по существу не содержит, а предпочтительно совсем не содержит полисорбата 80.
В частности, композиция согласно изобретению по существу не содержит, а предпочтительно совсем не содержит полоксамеров, как, например, полоксамер 188.
В частности, композиция согласно изобретению по существу не содержит, предпочтительно совсем не содержит хлорида бензалкония.
В частности, композиция согласно изобретению по существу не содержит, предпочтительно совсем не содержит гистидина.
В частности, композиция согласно изобретению по существу не содержит, предпочтительно совсем не содержит ЭДТА, более конкретно натрий ЭДТА.
Композиция согласно изобретению может содержать одно или несколько веществ, которые обычно используются для буферирования pH (буферные вещества). Примерами таких буферных веществ являются ацетат, цитрат и фосфат, например, в количествах до 5 мг/мл, до 4 мг/мл, до 3 мг/мл или до 2 мг/мл.
Композиция согласно изобретению может также по существу не содержать таких буферных веществ. Равным образом, композиция по изобретению может совсем не содержать таких буферных веществ.
Композиция согласно изобретению может по существу не содержать цитрата, ацетата и/или фосфата или же совсем не содержать цитрата, ацетата и/или фосфата.
В частности, композиция согласно изобретению по существу не содержит, предпочтительно совсем не содержит гистидина и натрий ЭДТА.
Более конкретно, в композиции по изобретению не содержится инсулина.
Фармацевтическая композиция по настоящему изобретению может иметь кислотный или физиологический pH. Кислотный диапазон pH предпочтительно соответствует pH 1-6,8, pH 3,5-6,8 или pH 3,5-5. Физиологический диапазон pH предпочтительно соответствует pH 2,5-8,5, более предпочтительно pH 4,0-8,5, еще более предпочтительно pH 4,0-6,0. Особенно предпочтительно pH составляет примерно 4,5. Для регулирования значений pH подходят физиологически безопасные разбавленные кислоты (типично HCl) или щелочи (типично NaOH).
Композиция по изобретению может включать подходящий консервант. Подходящими консервантами являются, например, фенол, м-крезол, бензиловый спирт и/или сложные эфиры п-гидроксибензойной кислоты. Предпочтителен м-крезол.
Кроме того, композиция по изобретению может содержать подходящие изотонизирующие вещества. Подходят, например, глицерин, декстроза, лактоза, сорбит, маннит, глюкоза, NaCl, соединения кальция или магния, такие, как CaCl2, и т.д. Концентрации глицерина, декстрозы, лактозы, сорбита, маннита и глюкозы обычно лежат в диапазоне 100-250 мМ, NaCl присутствует в концентрации до 150 мМ. Предпочтителен глицерин.
Композиция предназначена, в частности, для парентерального введения. Композиция по изобретению предпочтительно является композицией, годной для инъекций, более предпочтительно для подкожной инъекции. Более конкретно, композиция по настоящему изобретению подходит для инъекций один раз в день.
В частности, композиция согласно изобретению имеет после хранения в течение 1 месяца, 2 месяцев, 4 месяцев или 6 месяцев при температуре +5°C или 25°C активность по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 98% от активности в начальный момент времени.
В настоящей заявке "активность" означает активность агониста ГПП-1, который используется в композиции по изобретению. Способы определения активности агониста ГПП-1 специалисту известны.
Предпочтительно, композиция согласно изобретению имеет биологическую активность агониста ГПП-1 после хранения в течение 6 месяцев при 25°C по меньшей мере 89% или по меньшей мере 90%. Композиция по изобретению предпочтительно имеет биологическую активность агониста ГПП-1 после хранения в течение 6 месяцев при 40°C по меньшей мере 45% или по меньшей мере 50%.
В частности, композиция по изобретению проявляет химическую целостность после хранения в течение 1 месяца, 2 месяцев, 3 месяцев, 4 месяцев или 6 месяцев. Химическая целостность означает, более конкретно, что после хранения при температуре +5°C, 25°C или 40°C композиция содержит по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 98% активного вещества, имевшегося в исходный момент времени, в по существу химически неизменной форме.
Химическая целостность может означать химическую целостность агониста ГПП-1. Агонисты ГПП-1 могут содержать остаточный метиониновый остаток (например, позиция 14 в AVE0010). Химическая целостность агониста ГПП-1 означает, более конкретно, что предотвращается окисление этого метионинового остатка. При этом химическая целостность означает, в частности, что доля окисленного метионина по отношению ко всему содержанию метионина в агонисте ГПП-1 после хранения в течение 1, 2, 3, 4 или 6 месяцев меньше 0,7%, меньше 0,6%, меньше 0,5%, меньше 0,4% или меньше 0,3%. Хранение может быть реализовано, например, при 5°C, 25°C или 40°C. Предпочтительно хранение в течение 6 месяцев при 5°C, при этом доля окисленного метионина ниже 0,3%. Равным образом, предпочтительно хранение в течение 6 месяцев при 25°C, при этом доля окисленного метионина ниже 0,7%, ниже 0,6%, ниже 0,5%, ниже 0,4% или ниже 0,3%. Аналогично, предпочтительно хранение в течение 6 месяцев при 40°C, при этом доля окисленного метионина ниже 1%, ниже 0,7%, ниже 0,6%, ниже 0,5%, ниже 0,4% или ниже 0,3%.
Химическая целостность может означать максимально низкое содержание всех примесей в композиции по изобретению. В частности, полная доля примесей от полной массы агониста ГПП-1, присутствующего в композиции после хранения в течение 6 месяцев при 40°C, составляет менее 50%, менее 10% после хранения при 25°C или/и менее 1,8% после хранения при 5°C.
Химическая целостность может означать как можно меньшее содержание белков высокого молекулярного веса в композиции по изобретению. В частности, доля высокомолекулярных белков от полной массы агониста ГПП-1, присутствующего в композиции после хранения в течение 6 месяцев при 40°C, ниже 5%, ниже 4%, ниже 3% или ниже 2%. В частности, доля высокомолекулярных белков от полной массы агониста ГПП-1, присутствующего в композиции после хранения в течение 6 месяцев при 25°C, составляет менее 0,8%, менее 0,7% или менее 0,6%.
В частности, композиция по изобретению проявляет физическую целостность после хранения в течение 1 месяца, 2 месяцев, 4 месяцев или 6 месяцев. Физическая целостность означает, более конкретно, что после хранения при температуре +5°C, 25°C или 40°C композиция содержит по меньшей мере 80%, по меньшей мере 90%, по меньшей мере 95% или по меньшей мере 98% активного вещества, присутствовавшего в начальный момент времени, в по существу неизменной форме.
Физическая целостность может означать целостность агониста ГПП-1. Более конкретно, физическая целостность означает, что агонист ГПП-1 не образует агрегатов, например, таких, как фибриллы.
Агонист ГПП-1 предпочтительно выбран из группы, состоящей из эксендина-3 и его аналогов и производных, эксендина-4 и его аналогов и производных, причем более предпочтительно агонист ГПП-1 выбран из группы, состоящей из AVE0010 и эксендина-4.
Эксендин-3, аналоги и производные эксендина-3, эксендин-4 и аналоги и производные эксендина-4 можно обнаружить в документах WO 01/04156, WO 98/30231, US 5424286, заявке EP 99 6100434 и в WO 2004/005342. Эти документы введены здесь ссылкой. Описанные в этих документах эксендин-3, эксендин-4 и их аналоги и производные могут быть синтезированы описываемыми здесь способами, причем при необходимости по окончании процесса проводятся модификации.
Последовательности AVE0010 (SEQ ID NO:1), эксендина-4 (SEQ ID NO:2) и эксендина-3 (SEQ ID NO:3) обнаруживают высокую степень сходства. Последовательности AVE0010 и эксендина-4 идентичны в позициях 1-37. Последовательность 1-39 эксендина-4 в 37 из 39 позиций (94%) идентична последовательности эксендина-3 в позициях 48-86. С привязкой к последовательностям, специалист сможет легко преобразовать указанные здесь позиции, которые относятся к определенной последовательности (например, к последовательности AVE0010 или эксендина-4), в другие последовательности.
В частности, аналоги и производные эксендина-3 или/и эксендина-4 содержат модифицированную аминокислотную последовательность. Например, отдельные аминокислоты могут быть удалены (например, desPro36, desPro37, desAsp28, desMet(O)14 в эксендине-4 и соответствующие позиции в эксендине-3). Аналогично, отдельные позиции могут быть заменены (например, Met(O)14, Trp(O2)25, IsoAsp28, Asp28Pro38 в эксендине-4 и соответствующих позициях в эксендине-3), причем могут также использоваться ненатуральные аминокислоты, такие, как Met(O) (метионинсульфоксид или метионинсульфон), Trp(O2) (N-формилкинуренин) или/и IsoAsp (β-аспартат или изоаспартат). Ненатуральные аминокислоты могут быть легко введены в последовательность в форме соответствующих аминокислотных структурных блоков.
Кроме того, можно модифицировать C-терминус или/и N-терминус, например, посредством дополнительной последовательности, такой, как -(Lys)-, -(Lys)2-, -(Lys)3-, -(Lys)4-, -(Lys)5-, -(Lys)6-, -Asn-(Glu)5-, причем предпочтительны -(Lys)4-, -(Lys)5-, -(Lys)6-, -Asn-(Glu)5-. Карбоксильная группа в C-терминусе предпочтительно модифицируется в амидную группу (-NH2). При необходимости модификация C-терминуса или/и N-терминуса проводится как дополнительный этап по завершении синтеза.
Фармацевтически приемлемые соли могут быть получены на следующем этапе по завершении циклов синтеза способа по изобретению. Получение фармацевтически приемлемых солей пептидов специалисту известно. Предпочтительной фармацевтически приемлемой солью является ацетат.
Агонист ГПП-1 предпочтительно выбран из группы, состоящей из эксендина-4, аналогов и производных эксендина-4 и их фармакологически приемлемых солей.
Следующим предпочтительным агонистом ГПП-1 является аналог эксендина-4, выбранный из группы, состоящей из:
H-desPro36-эксендин-4-Lys6-NH2,
H-des(Pro36,37)-эксендин-4-Lys4-NH2,
H-des(Pro36,37)-эксендин-4-Lys5-NH2
и их фармакологически приемлемых солей.
Следующим предпочтительным агонистом ГПП-1 является аналог эксендина-4, выбранный из группы, состоящей из:
desPro36[Asp28]эксендин-4(1-39),
desPro36[IsoAsp28]эксендин-4(1-39),
desPro36[Met(O)14,Asp28]эксендин-4(1-39),
desPro36[Met(O)14,IsoAsp28]эксендин-4(1-39),
desPro36[Trp(O2)25,Asp28]эксендин-2(1-39),
desPro36[Trp(O2)25,IsoAsp28]эксендин-2(1-39),
desPro36[Met(O)14Trp(O2)25,Asp28]эксендин-4(1-39),
desPro36[Met(O)14Trp(O2)25,IsoAsp28]эксендин-4(1-39)
и их фармакологически приемлемых солей.
Следующим предпочтительным агонистом ГПП-1 является аналог эксендина-4, выбранного из группы, описанной в предыдущем абзаце, у которого к С-терминусу присоединен пептид -Lys6-NH2 аналогов of эксендин-4.
Следующий предпочтительный агонист ГПП-1 является аналог эксендина-4, выбранный из группы, состоящей из:
H-(Lys)6-desPro36[Asp28]эксендин-4(1-39)-Lys6-NH2,
desAsp28Pro36,Pro37,Pro38эксендин-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5desPro36,Pro37,Pro38[Asp28]эксендин-4(1-39)-NH2,
desPro36,Pro37,Pro38[Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36[Trp(O2)25,Asp28]эксендин-4(1-39)-Lys6-NH2,
H-desAsp28Pro36,Pro37,Pro38[Trp(O2)25]эксендин-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]эксендин-4(1-39)-NH2,
desPro36,Pro37,Pro38[Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36[Met(O)14,Asp28]эксендин-4(1-39)-Lys6-NH2,
desMet(O)14Asp28Pro36,Pro37,Pro38эксендин-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Met(O)14,Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Asp28]эксендин-4(1-39)-NH2,
desPro36,Pro37,Pro38[Met(O)14,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Met(O)14,Asp28]эксендин-4(1-39)-Lys6-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36[Met(O)14,Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
desAsp28Pro36,Pro37,Pro38[Met(O)14,Trp(O2)25]эксендин-4(1-39)-NH2,
H-(Lys)6-desPro36,Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Asp28]эксендин-4(1-39)-NH2,
desPro36,Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-desPro36Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-desPro36,Pro37,Pro38[Met(O)14,Trp(O2)25,Asp28]эксендин-4(1-39)-(Lys)6-NH2
и их фармакологически приемлемых солей.
Равным образом агонист ГПП-1 может быть выбран из группы, состоящей из ГПП-1 и аналогов и производных ГПП-1. Следующий предпочтительный агонист ГПП-1 выбран из группы, состоящей из Arg34,Lys26(Nε(γ-глутамил(Nα-гексадеканоил)))ГПП-1(7-37) [лираглутид] и его фармакологически приемлемой соли.
Следующим предпочтительным агонистом ГПП-1 является AVE0010. AVE0010 имеет последовательность desPro36эксендин-4(1-39)-Lys6-NH2 (SEQ ID NO:1). Равным образом, предпочтительны фармакологически приемлемые соли AVE0010.
Агонист ГПП-1, например, AVE0010, используется, в частности, в количестве от 0,01 мг/мл до 0,5 мг/мл или от 0,05 мг/мл до 1,5 мг/мл.
В одном частном варианте осуществления композиция по изобретению содержит следующие составляющие:
(a) desPro36эксендин-4(1-39)-Lys6-NH2 (например, примерно 0,1 мг/мл),
(b) ацетат натрия тригидрат (примерно 3,5 мг/мл),
(c) м-крезол (примерно 2,7 мг/мл),
(d) L-метионин (примерно 3 мг/мл),
(e) 85%-ый глицерин (примерно 18 мг/мл),
(f) соляная кислота примерно 0,1 н, если требуется установить pH примерно 4,5,
(g) раствор NaOH примерно 0,1 н, если требуется установить pH примерно 4,5, и
(h) вода.
Более конкретно, композиция по изобретению состоит из компонентов, указанных в пунктах (a)-(h).
В настоящей заявке "примерно" означает, что компонент может находиться в композициях согласно изобретению, например, в пределах диапазона ±10, ±20 или ±30% от указанных значений.
Если композиция по изобретению содержит более одного агониста ГПП-1, то эти агонисты ГПП-1 выбираются независимо друг от друга.
Подходящей упаковкой для композиции согласно изобретению является, например, шприц или стеклянная емкость, подходящим образом закупоренная, из которой по потребности можно отбирать отдельные терапевтически эффективные дозы. Равным образом для введения подходят шприцы карандашного типа (карандаши, ручки), которые содержат емкость (например, картридж), содержащую фармацевтическую композицию по изобретению.
Следующим объектом изобретения является способ лечения пациента композицией по изобретению, содержащий введение композиции пациенту.
Композиция согласно изобретению предназначена для лечения, в первую очередь, сахарного диабета, более конкретно для лечения сахарного диабета типа I или типа II. Следующими возможными показаниями являются симптомы, связанные с сахарным диабетом. Предпочтительно, композиция согласно изобретению применяется для контроля концентрации глюкозы в плазме натощак, после приема пищи или/и после всасывания, для улучшения толерантности к глюкозе, для предупреждения гипогликемии, для предотвращения функциональной потери β-клеток поджелудочной железы, для снижения веса или/и для недопущения повышения веса.
Следующим объектом изобретения является применение композиции по изобретению для получения лекарственного средства для лечения сахарного диабета, в частности, первого или второго типа, или/и связанных с ним симптомов, как описано здесь.
Следующим объектом изобретения является способ получения композиции по изобретению, содержащий соединение в одной лекарственной форме агониста ГПП-1 или/и его фармакологически приемлемой соли с метионином и, необязательно, по меньшей мере одним фармакологически приемлемым эксципиентом.
Следующим объектом изобретения является применение композиции по изобретению вместе с введением метморфина, сульфонилмочевины или глитазонов, инсулина/производного инсулина длительного действия и/или их комбинации, в частности, как дополнительной терапии при применении метморфина.
Следующим объектом изобретения является применение композиции по изобретению пациентами, у которых уровень сахара в крови невозможно контролировать в достаточной степени приемом метморфина, сульфонилмочевины или глитазонов, инсулина/производного инсулина длительного действия и/или их комбинации.
Следующим объектом изобретения является применение композиции по изобретению пациентами с диабетом II типа в качестве добавки к диете для улучшения регулирования/контроля уровня сахара в крови.
Более конкретно, композиция содержит desPro36эксендин-4(1-39)-Lys6-NH2 (AVE0010), лираглутид и/или фармакологически приемлемую соль вместе с метионином и/или фармакологически приемлемой солью.
В частности, в качестве производного инсулина длительного действия можно назвать Lantus®, NεB29-тетрадеканоил (B30)человеческого инсулина или Insuman®.
Особенно предпочтительна дополнительная терапия с метморфином, и/или инсулином/производным инсулина длительного действия, и/или его фармакологически приемлемой соли для лечения диабета II типа и/или ожирения, в частности, у пациентов моложе 50 лет и/или у тех, кто имеет индекс массы тела по меньшей мере 30.
В настоящем изобретение дополнительная терапия включает, в частности, лечение диабета второго типа метморфином и AVE0010. Метморфин и AVE0010 могут вводиться с временным интервалом 24 часа. Метморфин и AVE0010 могут вводиться каждый один раз в сутки. Метморфин и AVE0010 могут вводиться разными способами. Метморфин может вводиться перорально, а AVE0010 подкожно.
Пациенты, получающие дополнительное лечение согласно изобретению, могут иметь уровень гликогемоглобина HbA1c от 7% до 10%. Их возраст предпочтительно составляет от 18 до 50 лет.
Применение в дополнительной терапии согласно изобретению применимо прежде всего к пациентам, у которых диабет второго типа невозможно в достаточной мере контролировать одним метморфином.
В частности, метморфин вводится следующим образом: по меньшей мере 1,0 г/сут, предпочтительно по меньшей мере 1,5 г/сут в течение 3 месяцев.
Далее изобретение поясняется на следующих примерах и фигурах.
Краткое описание фигур
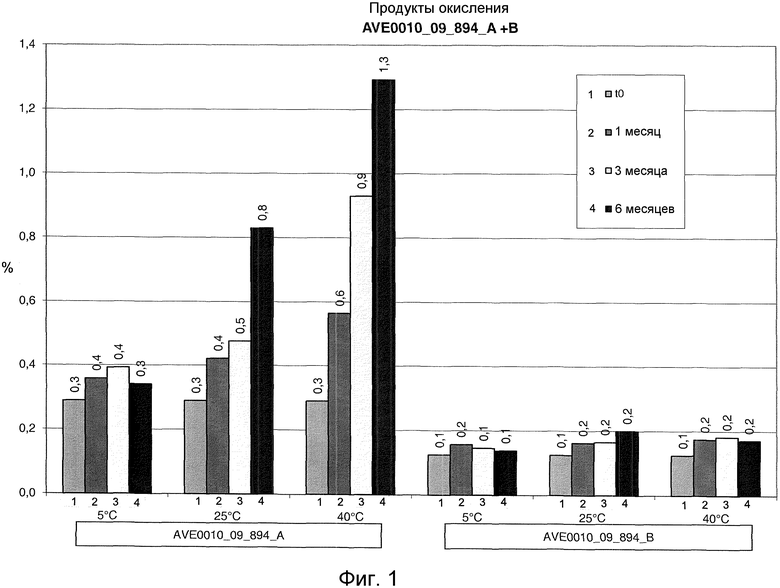
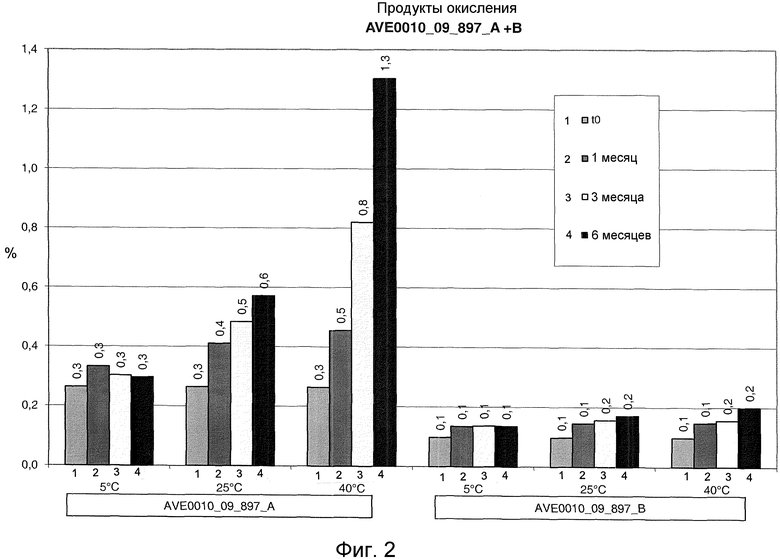
Фиг. 1 и 2 показывают процентное содержание окисленного метионина Met(ox) от полного содержания метионина в AVE0010 после хранения при разных температурах. 1: исходный момент времени t0. 2: хранение в течение 1 месяца. 3: хранение в течение 3 месяцев. 3: хранение в течение 6 месяцев. Фиг. 1: серия 894. Фиг. 2: серия 897.
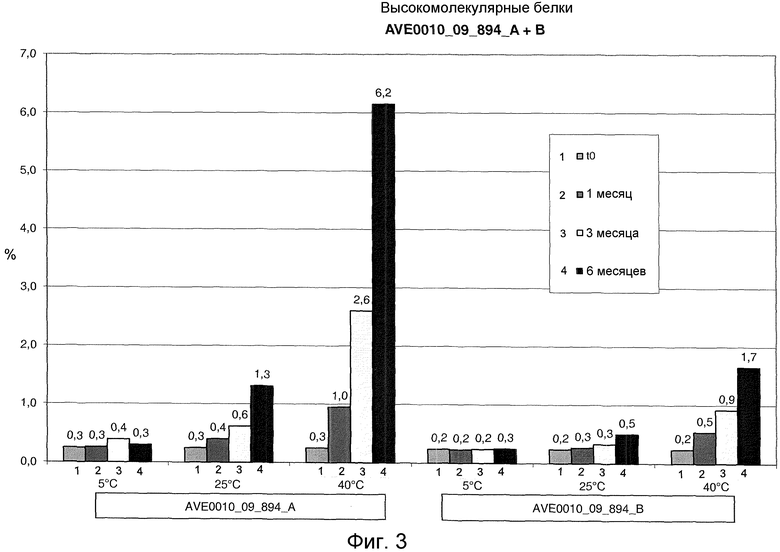
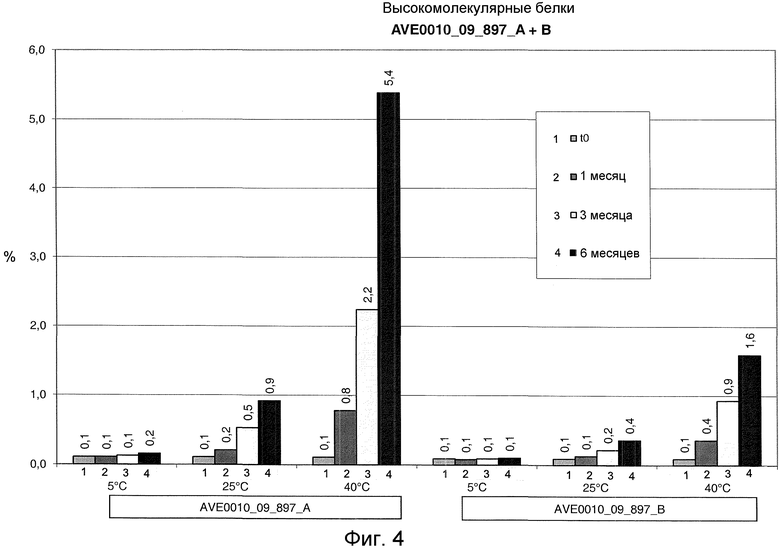
Фиг. 3 и 4 показывают процентное содержание примесных белков высокого молекулярного веса (по отношению к AVE0010) после хранения при разных температурах. 1: исходный момент времени t0. 2: хранение в течение 1 месяца. 3: хранение в течение 3 месяцев. 3: хранение в течение 6 месяцев. Фиг. 3: серия 894. Фиг. 4: серия 897.
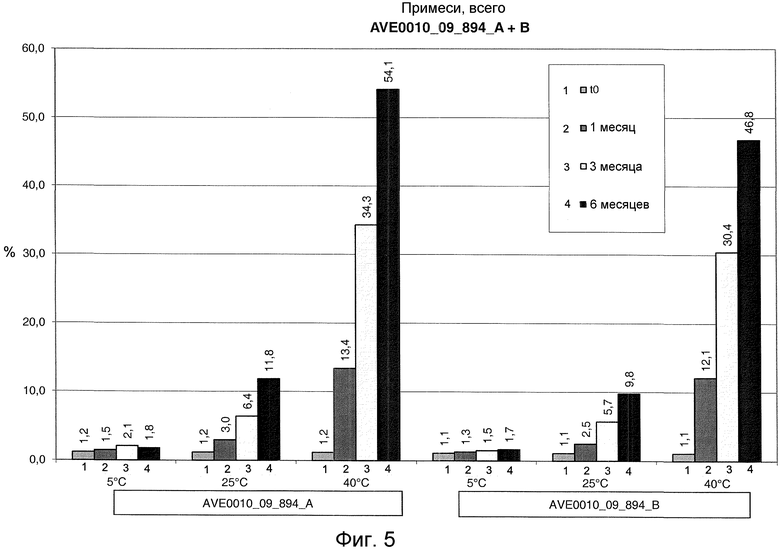
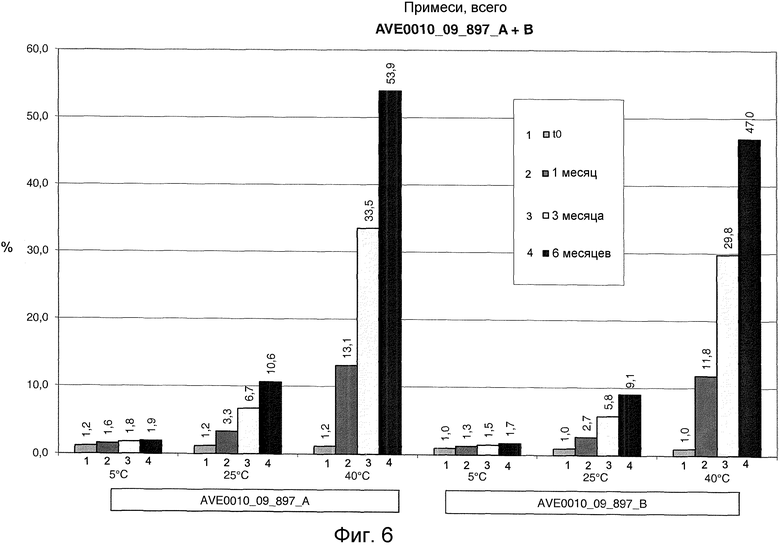
Фиг. 5 и 6 показывают процентное содержание всех примесей (по отношению к AVE0010) после хранения при разных температурах. 1: исходный момент времени t0. 2: хранение в течение 1 месяца. 3: хранение в течение 3 месяцев. 3: хранение в течение 6 месяцев. Фиг. 5: серия 894. Фиг. 6: серия 897.
Пример 1
Жидкая композиция, содержащая AVE0010 и метионин
Целью исследования было оценить химическую или/и физическую стабильность композиций соединения AVE0010 (раствор для инъекции, 0,1 мг/мл) с и без метионина, когда продукт находился в картриджах в условиях длительного хранения и в ускоренных условиях до 6 месяцев.
Испытывались следующие композиции:
Композиция A (2 параллельных серии: AVE0010_09894_A и AVE0010_09897_A)
Композиция B (2 параллельных серии: AVE0010_09894_B и AVE0010_09897_B)
Композиции хранились в блоках, которые предназначаются для клинических исследований и для продажи.
Отбортованная крышка: алюминий
Уплотнительная шайба (снаружи): изопреновый каучук, материал номер 7773/35
Уплотнительная шайба (внутри): бромбутиловый каучук, материал номер 4780/40
Тип I - герметизация (Евр.Фарм./Пат. США)
номер SAP 164571
бромбутиловый каучук, черный
номер SAP 120521
Длительность хранения, условия хранения, временные параметры испытаний в следующей таблице.
Лекарственные формы хранили в лежачем положении. RH означает относительную влажность. Момент времени 0 соответствует началу хранения. Результаты измерения в нулевой момент времени используются как эталон для всех условий тестирования. Во время исследований образцы хранились при +5±3°C.
Физическая и химическая стабильность хранившихся композиций определяется посредством следующих тестов:
- Описание
- Прозрачность раствора и его цвет
- pH
- Химическая стабильность (чистота и примеси, определено по ВЭЖХ), в частности, доля продуктов окисления и полная доля примесей)
- Высокомолекулярные белки, определено по HPSEC
- Видимые частицы
- Биологическая активность композиций
Результаты
Композиции исследовали по отдельности для параллельных серий (894 и 897) в отношении следующих параметров:
Биологическая активность AVE0010 . При 5°C и 25°C активность после 6 месяцев составляла по меньшей мере 96% от исходной активности. Активности композиций по изобретению были выше, чем активности сравнительных композиций. При 40°C активность после 6 месяцев в отсутствие метионина составляла примерно 43%. В присутствии метионина активность составляла примерно 51%, то есть была выше, чем в отсутствие метионина.
Продукты окисления. Измерения проводились на приборе ВЭЖХ (тип: alliance) от Water Systems, причем использовался метод 100%-ной площади пика. Для разделения применялся градиент 0,1% TFA и ацетонитрила в качестве подвижной фазы и колонка C18 с обращением фаз (Jupiter) в качестве стационарной фазы. При 5°C доля окисленного метионина Met(ox) в AVE0010 в отсутствие метионина составляла 0,3%. При 25°C эта доля составляла 0,6-0,8%, и при 40°C 1,3%. Когда композиция содержала метионин, доля окисленного метионина была заметно меньше. При всех условиях эксперимента она составляла не более 0,2%. Так, при 25°C доля составляла всего примерно от 1/4 до 1/3 от содержания в отсутствие метионина, а при 40°C даже всего примерно 1/6 (см. фиг. 1 и 2).
Высокомолекулярные белки. При 5°C их доля составляла от 0,1 до 0,3% и оставалась по существу неизменной в продолжение всего периода хранения. При 25°C доля повышалась в отсутствие метионина до 0,9 и 1,3%, соответственно. В присутствии метионина их доля составляла 0,4-0,5%, то есть более чем вполовину меньше. При 40°C доля составляла в отсутствие метионина 5,4% и 6,2%, соответственно, тогда как в присутствии метионина она составляла всего 1,6 и 1,7%, соответственно, то есть была заметно ниже (см. фиг. 3 и 4).
Все примеси. При 5°C полное содержание примесей незначительно повышалось в течение периода хранения 6 месяцев с 1,2 до 1,8 или до 1,9% (в отсутствие метионина). Когда метионин присутствовал, повышение было несколько меньше. При 25°C наблюдалось повышение до 10,6% и 11,8%, соответственно. В присутствии метионина эти значения лежали ниже 10%. При 40°C доля повышалась до 54% (без метионина). Когда метионин присутствовал, доля примесей составляла всего примерно 47% (см. фиг. 5 и 6).
Процентные величины представляют собой содержание (процентная доля примесей) продуктов окисления, всех примесей и высокомолекулярных белков (HMWP).
Все величины определяли по ВЭЖХ так называемым 100%-ным методом. При этом речь идет, в частности, об обращенно-фазовой ВЭЖХ (колонка C18), в которой для подвижной фазы применялся градиентный метод:
a) 0,1% TFA, 15% ACN и b) 0,1% TFA, 75% ACN.
Обнаружение на 215 нм (УФ)
Высокомолекулярные белки (HMWP) детектировали методом высокоэффективной эксклюзионной хроматографии (HPSEC), описанным в Европейской Фармакопее 6.0 для пригодных для инъекций препаратов инсулина.
Данные сведены в следующих таблицах.
Заключение
Содержание продуктов окисления, высокомолекулярных белков и полное содержание примесей являются, по отдельности или вместе, мерой химической целостности композиций. Из описанных выше результатов с типичными композициями следует, что жидкие композиции по изобретению, содержащие
- агонист ГПП-1 или/и его фармакологически приемлемую соль (более конкретно AVE0010 или/и его фармакологически приемлемую соль),
- необязательно, по меньшей мере один фармакологически приемлемый эксципиент
- и метионин,
имеют улучшенную стабильность или/и химическую целостность. Доля окисленного метионина, всех примесей и высокомолекулярных белков в композициях по изобретению ниже, чем в сравнительных композициях. Композиции по изобретению (серии 894_B и 897_B) отличаются от сравнительных композиций (серии 894_A и 897_A) присутствием метионина. Следовательно, улучшенную стабильность или/и химическую целостность можно объяснить наличием метионина в композициях согласно изобретению.
Пример 2
В следующем эксперименте изучалось, как действуют натрий ЭДТА и гистидин в композиции согласно изобретению.
Композиция B (как в примере 1)
Композиция C
Согласно стандартному планированию эксперимента, кроликов обрабатывали композицией B или C или солевым раствором подкожно (s.c.) или внутримышечно (i.m.). В каждом случае половину кроликов умерщвляли через 24 часа или 120 часов, чтобы гистологически определить острые или подострые эффекты введения. Кроме того, определяли, происходит ли восстановление/регенерация возможных изменений.
При подкожных инъекциях композиции C животные обнаруживали через 24 часа, в отличие от контрольного солевого раствора, воспалительную реакцию, от легкой до умеренной, в подкожной соединительной ткани. Через 120 часов после подкожной инъекции наблюдалась четкая тенденция к восстановлению наблюдаемых изменений путем фибробластной реакции. Таким образом, совместимость можно еще считать умеренной (а не несовместимой).
В случае композиции B животные после подкожной инъекции не обнаруживали никакой или обнаруживали лишь минимальную разницу с контрольным солевым раствором (хорошая совместимость).
После внутримышечной инъекции композиции C животные проявляют мышечный некроз (многоочаговый или рассеянный), четко отличимый от контрольных солевых растворов, в которых только место инъекции было видно как четко ограниченная некротическая зона. В случае композиции C через 120 часов наблюдалась минерализация некротической мышечной ткани, видимая даже при аутопсии животных. Хотя небольшая или очаговая минерализация в разных местах не является для кроликов необычной, минерализация после инъекции композиции C была четко связана с зонами некроза. Таким образом, обратимость поражений, вызванных инъекцией, является более чем сомнительной. Основываясь на этих данных, композиция C после внутримышечной инъекции у кроликов была оценена как несовместимая.
Композиция B после внутримышечной инъекции обнаруживает хорошую совместимость (никакой или минимальная разница с солевым контролем).
Из этих данных следует, что композиция B имеет, по сравнению с композицией C, улучшенную совместимость при внутримышечном или подкожном введении. Подкожная инъекция является предпочтительным способом введения описанных в настоящей заявке композиций, содержащих агонист ГПП-1, более конкретно AVE0010.
Таким образом, композиции согласно изобретению, которые содержат агонист ГПП-1, в частности, AVE0010, могут не содержать ЭДТА или/и гистидина. Равным образом, композиции согласно изобретению могут по существу не содержать ЭДТА и гистидина.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ АГОНИСТ GLP-1, ИНСУЛИН И МЕТИОНИН | 2010 |
|
RU2537239C2 |
| ПРЕПАРАТ ИНСУЛИНА, СОДЕРЖАЩИЙ МЕТИОНИН | 2010 |
|
RU2540485C2 |
| СТАБИЛИЗИРОВАННЫЕ СОЕДИНЕНИЯ ЭКСЕНДИНА-4 | 2003 |
|
RU2376314C2 |
| КОМБИНАЦИЯ ИНСУЛИНА И АГОНИСТА GLP-1 | 2014 |
|
RU2682671C2 |
| КОМБИНАЦИЯ ИНСУЛИНА И АГОНИСТА GLP-1 | 2009 |
|
RU2532378C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИНСУЛИНА С СИЛЬНО ЗАМЕДЛЕННЫМ ПРОФИЛЕМ ВРЕМЯ/ДЕЙСТВИЕ | 2009 |
|
RU2529952C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИНСУЛИНА С ЧРЕЗВЫЧАЙНО ЗАМЕДЛЕННЫМ ПРОФИЛЕМ ВРЕМЯ/ДЕЙСТВИЕ | 2009 |
|
RU2524423C2 |
| ШПРИЦ-РУЧКА С ОКОННЫМ ЭЛЕМЕНТОМ | 2013 |
|
RU2651907C2 |
| УСТРОЙСТВО ПОДАЧИ ЛЕКАРСТВА ДЛЯ ВВЕДЕНИЯ ЗАДАННОЙ ДОЗЫ МЕДИКАМЕНТА | 2012 |
|
RU2603289C2 |
| СИНТЕЗ ЛИКСИСЕНАТИДА С КЭППИРОВАНИЕМ | 2019 |
|
RU2782772C2 |
Группа изобретений раскрывает жидкую композицию, содержащую агонист ГПП-1 или/и его фармакологически приемлемую соль и отличающуюся тем, что композиция содержит метионин, где композиция по существу не содержит гистидина и ЭДТА, и где агонист ГПП-1 присутствует в количестве от 0,01 мг/мл до 1,5 мг/мл, а также ее применение для лечения сахарного диабета и ожирения. Заявленная группа изобретений обладает высокой стабильностью. 8 н. и 21 з.п. ф-лы, 6 ил., 8 табл., 2 пр.
1. Жидкая композиция для лечения сахарного диабета у пациента, содержащая агонист ГПП-1 или/и его фармакологически приемлемую соль и, отличающаяся тем, что композиция содержит метионин, где композиция по существу не содержит гистидина и ЭДТА, и где агонист ГПП-1 присутствует в количестве от 0,01 мг/мл до 1,5 мг/мл.
2. Жидкая композиция по п. 1, где композиция дополнительно содержит по меньшей мере один фармакологически приемлемый эксципиент.
3. Жидкая композиция по п. 1, отличающаяся тем, что она содержит фармакологически приемлемый консервант, в частности, м-крезол.
4. Жидкая композиция по пп. 1, 2 или 3, отличающаяся тем, что она содержит глицерин.
5. Жидкая композиция по п. 1, отличающаяся тем, что она имеет рН в диапазоне от 3,5 до 5.
6. Жидкая композиция по п. 1, отличающаяся тем, что она содержит метионин в количестве от 0,5 мг/мл до 20 мг/мл, предпочтительно от 1 мг/мл до 5 мг/мл.
7. Жидкая композиция по п. 1, отличающаяся тем, что агонист ГПП-1 выбран из группы, состоящей из ГПП-1 и его аналогов и производных, эксендина-3 и его аналогов и производных, эксендина-4 и его аналогов и производных, причем агонист ГПП-1 предпочтительно выбран из группы, состоящей из desPro36эксендин-4(1-39)-Lys6-NH2 и эксендина-4, где аналоги содержат модифицированную аминокислотную последовательность.
8. Жидкая композиция по п. 1, отличающаяся тем, что она содержит следующие компоненты:
(a) desPro36эксендин-4(1-39)-Lys6-NH2,
(b) ацетат натрия,
(c) м-крезол,
(d) L-метионин,
(e) 85%-ый глицерин и
(h) воду.
9. Жидкая композиция по п. 8, где, если требуется установить рН примерно 4,5, композиция дополнительно содержит примерно 0,1 н соляную кислоту.
10. Жидкая композиция по п. 8, где, если требуется установить рН примерно 4,5, композиция дополнительно содержит раствор примерно 0,1 н NaOH.
11. Композиция по п. 1, отличающаяся тем, что она является композицией, годной для инъекций.
12. Композиция по п. 1 для лечения сахарного диабета.
13. Применение композиции по любому из пп. 1-12 для получения лекарственного средства для лечения сахарного диабета.
14. Применение по п. 13, где сахарный диабет представляет собой диабет второго типа.
15. Применение по п. 13 для введения пациенту один раз в день.
16. Применение композиции по пп. 1-12 для введения пациентам с диабетом II типа как дополнение к диете, чтобы улучшить контроль уровня сахара в крови.
17. Применение композиции по пп. 1-12 для введения пациенту один раз в день.
18. Способ получения композиции по любому из пп. 1-12, включающий соединение в одной лекарственной форме агониста ГПП-1 или/и его фармакологически приемлемой соли с метионином.
19. Способ по п. 18, в котором способ дополнительно включает добавление по меньшей мере одного фармакологически приемлемого эксципиента.
20. Способ по п. 18, где композицию вводят пациенту один раз в день.
21. Способ лечения сахарного диабета у пациента с помощью композиции по любому из пп. 1-12, включающий введение композиции пациенту.
22. Способ по п. 21, где композицию вводят пациенту один раз в день.
23. Применение композиции по одному из предыдущих пп. 1-12, вместе с введением метморфина, сульфонилмочевины, глитазона и/или инсулина/производного инсулина длительного действия, и/или их комбинации, и/или фармакологически приемлемой соли для лечения сахарного диабета.
24. Применение по п. 23, включающее дополнительное лечение пациентов, у которых достаточный контроль уровня сахара в крови не может быть достигнут метморфином, сульфонилмочевиной, глитазоном и/или инсулином/производным инсулина длительного действия.
25. Применение по п. 23 или 24, отличающееся тем, что получающие лечение пациенты имеют показатель HbA1c в диапазоне от 7% до 10%.
26. Применение по п. 23 или 24 для лечения диабета II типа и/или ожирения.
27. Применение по п. 25 для лечения диабета II типа и/или ожирения.
28. Применение по п. 23 для введения пациенту один раз в день.
29. Применение по п. 24 для введения пациенту один раз в день.
| US2008260840 A1, 23.10.2008 | |||
| US2008146490 A1, 09.06.2008 | |||
| US2001012829 А1, 09.08.2011 | |||
| US2003104996 A1, 05.06.2003 | |||
| WO2009102467 A2, 20.08.2009 | |||
| WO2004035623 A2, 29.04.2004. |
Авторы
Даты
2016-01-27—Публикация
2010-11-11—Подача