ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка заявляет приоритет предварительной заявки на патент США № 61/410767, поданной 5 ноября 2011 года, раскрытие которой включено в данный документ посредством ссылки во всей своей полноте для любых целей.
ОПИСАНИЕ ТЕКСТОВОГО ФАЙЛА, ПРЕДСТАВЛЕННОГО В ЭЛЕКТРОННОМ ВИДЕ
Содержимое текстового файла, представленного в электронном виде с данным документом, включено в данный документ посредством ссылки во всей своей полноте: копия списка последовательностей в формате, пригодном для ввода в компьютер (имя файла: NOVV_047_01WO_SeqList_ST25.txt, дата записи: 7 ноября 2011 года, размер файла 7 килобайт).
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение в целом относится к вирусоподобным частицам (VLP), содержащим гликопротеины (G-белки) вируса бешенства (RV), и способам их получения и применения, включая иммуногенные композиции, такие как вакцины для лечения и/или профилактики инфекции вируса бешенства.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Вирус бешенства (RV) является несегментированным РНК-вирусом с отрицательной цепью из семейства Rhabdoviridae и вызывает смертельное неврологическое заболевание у людей и животных. Ежегодно регистрируют более чем 70000 человеческих смертей, а миллионам других людей требуется последующее лечение. Несмотря на достижение значительных успехов в профилактике и борьбе с бешенством, данное заболевание остается серьезной угрозой для здоровья населения и продолжает вызывать многочисленные человеческие смерти во всем мире. Представители семейства собачьих остаются наиболее важным резервантом в Азии, Африке и Латинской Америке, где происходит большинство случаев бешенства человека. В развитых странах случаи бешенства человека значительно снизились в течение последних 50 лет, в основном в результате плановой вакцинации домашних животных. Тем не менее, передача бешенства посредством воздействия дикой природы выявляется одной из основных причин заболевания. В Соединенных Штатах в дикой природе было зарегистрировано более чем 90% случаев бешенства животных, представляя постоянную угрозу для здоровья населения. Большинство случаев заболевания человека в последнее десятилетие было связано с RV, обнаруженным у летучих мышей, в частности, у серебристых гладконосов.
Рабдовирусы имеют два основных структурных компонента: спиралеобразное рибонуклеопротеиновое (RNP) ядро и окружающую оболочку. Геном вируса бешенства кодирует пять белков: нуклеопротеин (N), фосфопротеин (P), матричный белок (M), гликопротеин (G) и полимеразу (крупный белок) (L). Порядок генов в геноме вируса бешенства дикого типа 3'-N-P-M-G-L-5'. Белки N, L и P связаны с ядерным RNP-комплексом. RNP-комплекс состоит из РНК-генома, заключенного в капсид с помощью N в сочетании с полимеразой L и белком P. Этот комплекс служит в качестве матрицы для транскрипции и репликации вируса. Компонент вирусной оболочки RV состоит из трансмембранного гликопротеина (G) и матричного белка (M). Гликопротеин образует приблизительно 400 тримерных шипов, которые плотно расположены на поверхности вируса. M-белок связан как с оболочкой, так и с RNP, и, вероятно, является центральным белком сборки рабдовируса.
Как отмечалось выше, бешенство остается серьезной угрозой для здоровья населения во всем мире. Борьба с бешенством и защита людей от бешенства требует нескольких стратегий борьбы, таких как, плановая иммунизация домашних животных и носителей в дикой природе, предварительная иммунизация людей из групп риска и последующее лечение людей, укушенных бешеными животными. Хотя инактивированные вакцины вируса бешенства (RV), подготовленные из клеточной культуры, безопасны и хорошо переносятся, у них есть множество недостатков. Они сложны в изготовлении, сложны в хранении, имеют низкую иммуногенность и требуют многократных инъекций. Более того, они дорогостоящие и, таким образом, недоступны для большинства людей, нуждающихся в вакцинах в развивающихся странах. Кроме того, данные инактивированные вакцины, как правило, содержат адъюванты, которые могут вызвать нежелательные побочные эффекты. Таким образом, необходимы более безопасные, дешевые и более эффективные вакцины RV.
Настоящее изобретение решает данную проблему необходимости путем разработки нового способа получения вирусоподобных частиц (VLP), содержащих гликопротеин (G) вируса бешенства.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к вирусоподобным частицам (VLP) вируса бешенства (RV) для применения в вакцинах для лечения и профилактики инфекции вирусом бешенства. VLP RV по настоящему изобретению обладают потенциалом индуцирования сильных иммунных ответов у субъектов-млекопитающих на вирус бешенства.
В первом аспекте настоящее изобретение обеспечивает VLP RV, содержащие один или несколько гликопротеинов (G-белков) RV. G-белки RV могут быть получены из любого подходящего штамма RV, включая, без ограничения, штаммы RV выделенные из человека, собаки, летучей мыши, енота, скунса и лисицы. В одном варианте осуществления VLP RV, содержащие один или несколько G-белков RV, могут находиться в форме мицелл. В некоторых вариантах осуществления VLP RV могут содержать один или несколько дополнительных белков RV, выбранных из нуклеопротеина (N), фосфопротеина (Р), матричного белка (М) и полимеразы (крупного белка) (L). В конкретном варианте осуществления VLP RV по настоящему изобретению могут содержать матричный белок (М) RV. В одном варианте осуществления М-белок получают из штамма RV человека. В другом варианте осуществления M-белок получают из штамма собачьего RV. В еще одном варианте М-белок получают из штамма RV, выделенного из летучей мыши. В других вариантах осуществления матричный белок может быть М1-белком из штамма вируса гриппа. В одном варианте осуществления штамм вируса гриппа является штаммом вируса птичьего гриппа. В других вариантах осуществления М-белок может быть получен из штамма вируса ньюкаслской болезни (NDV).
В одном варианте осуществления кодирующую последовательность G-белка RV дополнительно оптимизируют для повышения его экспрессии в подходящей клетке-хозяине. В одном варианте осуществления клетка-хозяин является клеткой насекомого. В иллюстративном варианте осуществления клеткой насекомого является клетка Sf9.
VLP RV по настоящему изобретению могут применяться для профилактики и/или лечения инфекции RV. Таким образом, в другом аспекте настоящее изобретение обеспечивает способ индуцирования иммунного ответа на RV. Способ включает этап, на котором субъекту, такому как человек или субъект-животное, вводят иммунологически эффективное количество композиции, содержащей VLP RV.
В другом аспекте настоящее изобретение обеспечивает фармацевтически приемлемые вакцинные композиции, содержащие VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV.
В одном варианте осуществления настоящее изобретение включает иммуногенный состав, содержащий по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. В другом варианте осуществления настоящее изобретение предусматривает фармацевтическую упаковку или набор, содержащий один или несколько контейнеров, заполненных одним или несколькими ингредиентами вакцинных составов по настоящему изобретению.
В другом варианте осуществления настоящее изобретение обеспечивает способ составления вакцины или антигенной композиции, которая индуцирует иммунитет к инфекции или по меньшей мере к одному симптому данного заболевания у млекопитающего, включающий этап, на котором к составу добавляют эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. В предпочтительном варианте осуществления инфекция является инфекцией RV.
VLP RV по настоящему изобретению пригодны для приготовления композиций, которые стимулируют иммунный ответ, обеспечивающий иммунитет или существенный иммунитет к возбудителям инфекции. Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает способ индуцирования иммунитета к инфекции или по меньшей мере одному симптому данного заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV.
В еще одном аспекте настоящее изобретение обеспечивает способ индуцирования существенного иммунитета к инфекции RV или по меньшей мере одному симптому данного заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV.
Композиции по настоящему изобретению могут вызвать существенный иммунитет у позвоночного (например, человека или собачьих) при введении данному позвоночному. Таким образом, в одном варианте осуществления настоящее изобретение обеспечивает способ индуцирования существенного иммунитета к инфекции RV или по меньшей мере одному симптому данного заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. В другом варианте осуществления настоящее изобретение обеспечивает способ вакцинации млекопитающего против RV, включающий этап, на котором указанному млекопитающему вводят индуцирующее защиту количество VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. Профилактический вакцинный состав вводят системно, например, подкожно или внутримышечно с помощью иглы и шприца или безыгольного инъектора. В иллюстративном варианте осуществления вакцинный состав вводят внутримышечно.
В другом варианте осуществления настоящее изобретение включает способ индуцирования защитного ответа антител на инфекцию или по меньшей мере на один из этих симптомов у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV.
В другом варианте осуществления настоящее изобретение включает способ индуцирования защитного клеточного ответа на инфекцию RV или по меньшей мере на один симптом заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV.
В еще одном аспекте настоящее изобретение обеспечивает выделенную нуклеиновую кислоту, кодирующую гликопротеин (G-белок) вируса бешенства. В иллюстративном варианте осуществления выделенная нуклеиновая кислота, кодирующая белок гликопротеина (G-белка) вируса бешенства, является SEQ ID NO: 1.
В еще одном аспекте настоящее изобретение обеспечивает выделенную клетку, содержащую нуклеиновую кислоту, кодирующую гликопротеин (G-белок) вируса бешенства. В иллюстративном варианте осуществления выделенная нуклеиновая кислота, кодирующая белок гликопротеина (G-белка) вируса бешенства, является SEQ ID NO: 1.
В еще одном аспекте настоящее изобретение обеспечивает вектор, содержащий нуклеиновую кислоту, кодирующую гликопротеин (G-белок) вируса бешенства. В иллюстративном варианте осуществления выделенная нуклеиновая кислота, кодирующая белок гликопротеина (G-белка) вируса бешенства, является SEQ ID NO: 1. В одном варианте осуществления вектор представляет собой бакуловирусный вектор.
В еще одном аспекте настоящее изобретение обеспечивает способ получения VLP RV, содержащей один или несколько гликопротеинов (G-белков) вируса бешенства, включающий этап (а), на котором трансформируют клетки-хозяева для экспрессии нуклеиновой кислоты, кодирующей гликопротеин (G-белок) вируса бешенства, и этап (b), на котором культивируют указанные клетки-хозяева в условиях, способствующих продукции указанных VLP RV. В одном варианте осуществления нуклеиновая кислота, кодирующая гликопротеин (G-белок) вируса бешенства, является SEQ ID NO: 1. В другом варианте осуществления клетка-хозяин является клеткой насекомого. В еще одном варианте осуществления клетка-хозяин является клеткой насекомого, трансфицированной бакуловирусным вектором, содержащим гликопротеин (G-белок) вируса бешенства.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На Фигуре 1 изображена карта плазмиды для вектора pFastBac1, содержащего последовательность нуклеиновой кислоты для G-белка (SEQ ID NO: 1) вируса бешенства.
На Фигуре 2 изображены результаты вестерн-блоттинга для G-белков RV с применением сыворотки кролика к RV как в восстановительных условиях (Фигура 2А), так и в условиях, на являющихся восстановительными (Фигура 2B).
На Фигуре 3 представлены изображения частиц очищенного рекомбинантного G-белка RV в форме мицелл, полученные с применением электронной микроскопии с фоновым окрашиванием при увеличении в 150000X.
На Фигуре 4 изображены результаты анализов индуцирования антител у кроликов, которым вводили G-частицы RV, с увеличением разведений.
На Фигуре 5 показана белковая последовательность для вектора pFastBac1, содержащего последовательность нуклеиновой кислоты для G-белка вируса бешенства (SEQ ID NO: 1) (вверху) и последовательность G-белка RV (SEQ ID NO: 2) (внизу).
Фигура 6 представляет собой график, на котором показаны титры антител к вирусу бешенства в разные дни, построенный относительно геометрического среднего для каждого режима иммунизации (n=5 для каждой группы иммунизации).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Как применяется в данном документе, выражение “адъювант” относится к соединению, которое при применении в комбинации с конкретным иммуногеном (например, VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV) в составе будет увеличивать или иным образом изменять или модифицировать результирующий иммунный ответ. Модификация иммунного ответа включает усиление или расширение специфичности одного из или как иммунного ответа с участием антител, так и клеточного иммунного ответа. Модификация иммунного ответа может также означать снижение или подавление определенных антиген-специфических иммунных ответов.
Как применяют в данном документе, выражение “антигенный состав” или “антигенная композиция” относится к препарату, который при введении позвоночному, особенно птице или млекопитающему, будет индуцировать иммунный ответ.
Как применяют в данном документе, выражение “вирус птичьего гриппа” относится к вирусам гриппа, обнаруженным, главным образом, у птиц, но которые также могут инфицировать людей или других животных. В некоторых случаях вирусы птичьего гриппа могут передаваться или распространяться от одного человека к другому. Вирус птичьего гриппа, который инфицирует людей, потенциально может вызвать пандемию гриппа, то есть, заболеваемость и/или смертность у людей. Пандемия возникает тогда, когда появляется новый штамм вируса гриппа (вирус, к которому у человека нет естественного иммунитета), распространяясь за пределы отдельных местностей, возможно, по всему миру, и заражая множество людей одновременно.
Как применяют в данном документе, “эффективная доза” в целом относится к такому количеству VLP RV, содержащей один или несколько гликопротеинов (G-белков) RV, которое достаточно для индуцирования иммунитета для предотвращения и/или уменьшения интенсивности инфекции или уменьшения по меньшей мере одного симптома инфекции или заболевания, и/или для повышения эффективности другой дозы VLP RV, содержащей один или несколько гликопротеинов (G-белков) RV. Эффективная доза может относиться к количеству VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV, достаточному, чтобы задержать или минимизировать проявление инфекции или заболевания. Эффективная доза может также относиться к количеству VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV, которое обеспечивает терапевтическое преимущество при лечении или контроле инфекции или заболевания. Кроме того, эффективная доза представляет собой количество в отношении VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV, отдельно или в комбинации с другими видами терапии, которое обеспечивает терапевтическое преимущество при лечении или контроле инфекции или заболевания. Эффективная доза также может представлять собой количество, достаточное для повышения у субъекта (например, у человека) собственного иммунного ответа на последующее воздействие возбудителя инфекции или заболевания. Уровни иммунитета можно контролировать, например, путем измерения количества нейтрализующих секреторных и/или сывороточных антител, например, путем нейтрализации бляшки, фиксации комплемента, иммуноферментного или микронейтрализационного анализа, или путем измерения клеточных ответов, таких как, без ограничения, цитотоксических Т-клеток, антигенпрезентирующих клеток, хелперных Т-клеток, дендритных клеток и/или других клеточных ответов. Т-клеточные ответы можно контролировать, например, посредством измерения, например, количества присутствующих клеток CD4+и CD8+с применением специфических маркеров методом флуоресцентной проточной цитометрии или Т-клеточных анализов, таких как, без ограничения, анализ Т-клеточной пролиферации, анализ Т-клеточной цитотоксичности, TETRAMER-анализ и/или ELISPOT-анализ. В случае вакцины “эффективная доза” является такой, которая предотвращает заболевание и/или уменьшает тяжесть симптомов.
Как применяют в данном документе, выражение “эффективное количество” относится к количеству VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV, необходимому или достаточному для реализации желаемого биологического эффекта. Эффективное количество композиции будет количеством, которое достигает выбранного результата, и такое количество может быть определено в результате обычного проведения исследований специалистом в данной области техники. Например, эффективное количество для предупреждения, лечения и/или уменьшения интенсивности инфекции, может быть количеством, необходимым для того, чтобы вызвать активацию иммунной системы, приводящую к развитию антиген-специфического иммунного ответа при воздействии VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. Выражение также является синонимом “достаточного количества". В другом варианте осуществления эффективное количество представляет собой количество по весу G-мицеллы RV, которое индуцирует серопротекцию на соответствующей животной модели, у животного или пациента-человека на желаемое количество дней, например, 7, 10, 14 или более дней.
Как применяют в данном документе, выражение “экспрессия” относится к процессу, посредством которого полинуклеиновые кислоты транскрибируются в мРНК и транслируются в пептиды, полипептиды или белки. Если полинуклеиновую кислоту получают из геномной ДНК, экспрессия может включать сплайсинг мРНК, если выбраны соответствующая эукариотическая клетка-хозяин или организм. В контексте настоящего изобретения выражение также охватывает выход мРНК гена G RV и G-белков RV, достигнутый после его экспрессии.
Как применяют в данном документе, выражение “G-белок” или “G-гликопротеин” или “полипептид G-белка” относится к полипептиду или белку, содержащему всю или часть аминокислотной последовательности полипептида G-белка RV.
Как применяют в данном документе, выражения “иммуногены” или “антигены” относятся к веществам, таким как белки, пептиды, пептиды, нуклеиновые кислоты, которые способны вызывать иммунный ответ. Оба выражения также охватывают эпитопы и применяются взаимозаменяемо.
Как применяют в данном документе, выражение “иммунный стимулятор” относится к соединению, которое повышает иммунный ответ через собственные химические мессенджеры организма (цитокины). Данные молекулы включают различные цитокины, лимфокины и хемокины с иммуностимулирующей, иммунопотенцирующей и противовоспалительной активностями, такие как интерфероны (IFN-γ), интерлейкины (например, IL-1, IL-2, IL-3, IL-4, IL-12, IL-13), факторы роста (например, гранулоцитов-макрофагов (GM)-колониестимулирующий фактор (CSF)); и другие иммуностимулирующие молекулы, такие как макрофагальный воспалительный фактор, лиганд Flt3, В7.1, В7.2 и т.д. Молекулы иммунного стимулятора можно вводить в том же составе, что и VLP по настоящему изобретению, или можно вводить отдельно. Для получения иммуностимулирующего эффекта можно вводить либо белок, либо вектор экспрессии, кодирующий данный белок.
Как применяют в данном документе, выражение “иммуногенный состав” относится к препарату, который при введении позвоночному, например млекопитающему, будет индуцировать иммунный ответ.
Как применяют в данном документе, выражение “возбудитель инфекции” относится к микроорганизмам, которые вызывают инфекцию у позвоночных. Как правило, организмы являются вирусами, бактериями, паразитами, простейшими и/или грибами.
Как применяют в данном документе, выражение “поливалентный” относится к композициям, которые имеют один или несколько антигенных белков/пептидов или иммуногенов к множеству типов или штаммов возбудителей инфекции или заболеваний, например, более одного типа, штамма, последовательности G-белка RV и т.д.
Как применяют в данном документе, выражение “фармацевтически приемлемая вакцина” относится к составу, содержащему VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV, находящемуся в форме, которая может быть введена позвоночному, и вызывающему защитный иммунный ответ, достаточный для индуцирования иммунитета для предотвращения и/или уменьшения интенсивности инфекции или заболевания, и/или для уменьшения по меньшей мере одного симптома инфекции или заболевания, и/или для повышения эффективности другой дозы VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. Как правило, вакцина содержит обычный физиологический раствор или среду буферного водного раствора, в которой композицию по настоящему изобретению суспендируют или растворяют. В такой форме композицию по настоящему изобретению можно удобно применять для предотвращения, уменьшения интенсивности или лечения инфекции другим образом. При введении в организм хозяина данная вакцина способна вызвать иммунный ответ, включая, без ограничения, продуцирование антител и/или цитокинов, и/или активацию цитотоксических Т-клеток, антигенпрезентирующих клеток, хелперных Т-клеток, дендритных клеток и/или других клеточных ответов.
Как применяют в данном документе, выражение “защитный иммунный ответ” или “защитный ответ” относится к иммунному ответу, опосредованному антителами, на возбудитель инфекции или заболевание, проявляющееся у позвоночного (например, человека), который предотвращает или уменьшает интенсивность инфекции, или уменьшает по меньшей мере один симптом данного заболевания. VLP RV по настоящему изобретению, которая содержит один или несколько гликопротеинов (G-белков) RV, может стимулировать продуцирование антител, которые, например, нейтрализуют возбудителей инфекции, блокируют проникновение возбудителей инфекции в клетки, блокируют репликацию возбудителей инфекции и/или защищают клетки-хозяева от инфекции и разрушения. Данное выражение может также относиться к иммунному ответу, опосредованному Т-лимфоцитами и/или другими белыми клетками крови, на возбудитель инфекции или заболевание, проявляющееся у позвоночных (например, человека), который предотвращает или уменьшает интенсивность инфекции или заболевания, либо уменьшает по меньшей мере один из его симптомов.
Как применяют в данном документе, выражение “позвоночные” или “субъект” или “пациент” относится к любому члену подтипа хордовых, включая, без ограничения, людей и других приматов, включая любых приматов за исключением человека, таких как шимпанзе и другие виды обезьян. Сельскохозяйственные животные, такие как крупный рогатый скот, овцы, свиньи, козы и лошади; домашние млекопитающие, такие как собаки и кошки; лабораторные животные, включая грызунов, таких как мыши, крысы (включая хлопковых хомяков) и морские свинки; птицы, включая домашних, диких и пернатую дичь, таких как куры, индейки и других куриных, уток, гусей и т.п., также являются неограничивающими примерами. Выражения “млекопитающие” и “животные” включены в данное определение. Охватываются как взрослые, так и новорожденные индивидуумы. В частности, люди, домашние млекопитающие и сельскохозяйственные животные являются подходящими реципиентами вакцины или терапевтического средства RV.
Как применяют в данном документе, выражение “вирусоподобная частица” (VLP), относится к структуре, которая по меньшей мере в одном признаке имеет сходство с вирусом, но которая не продемонстрировала инфекционность. Вирусоподобные частицы в соответствии с настоящим изобретением не несут генетической информации, кодирующей белки вирусоподобных частиц. В целом, вирусоподобные частицы не имеют вирусного генома и, следовательно, не являются инфекционными. Кроме того, вирусоподобные частицы часто могут быть получены в больших количествах путем гетерологичной экспрессии и могут быть легко очищены.
Как применяют в данном документе, выражение “химерная VLP” относится к VLP, которые содержат белки или их части по меньшей мере из двух различных возбудителей инфекции (гетерологичные белки). Как правило, один из белков получают от вируса, который может управлять формированием VLP в клетках-хозяевах. Примерами в иллюстративных целях являются М-белок птичьего гриппа и/или G-белок RV. В случае необходимости, выражения VLP RV и химерные VLP могут применяться взаимозаменяемо.
Как применяют в данном документе, выражение “вакцина” относится к препарату мертвых или ослабленных патогенов, или производных антигенных детерминант, который применяют, чтобы вызвать образование антител или иммунитет к патогену. Вакцину вводят для обеспечения иммунитета к заболеванию, например, гриппу, которое вызвано вирусом гриппа. Кроме того, выражение “вакцина” относится также к суспензии или раствору иммуногена (например, VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV), который вводят позвоночным для получения защитного иммунитета, т.е. иммунитета, который предотвращает или уменьшает тяжесть заболевания, связанного с инфекцией. Настоящее изобретение предусматривает вакцинные композиции, которые являются иммуногенными и могут обеспечить защиту от заболевания, связанного с инфекцией.
Вирусоподобные частицы (VLP) вируса бешенства (RV)
В одном аспекте настоящее изобретение относится к вирусоподобным частицам (VLP) RV, содержащим один или несколько гликопротеинов (G-белков) RV, которые могут быть включены в состав вакцин или антигенных составов для защиты позвоночных (например, человека и домашних животных) от инфекции RV или по меньшей мере одного из симптомов данного заболевания. В некоторых вариантах осуществления VLP, содержащая один или несколько гликопротеинов (G-белков) RV, также содержит дополнительные белки RV, такие как N, P, M и L. В других вариантах осуществления VLP, содержащая один или несколько гликопротеинов (G-белков) RV, дополнительно содержит белки из гетерологичных вирусных штаммов, таких как белки HA, NA и М1 вируса гриппа. В одном варианте осуществления M1-белок вируса гриппа получают из штамма вируса птичьего гриппа (см. заявку на патент США № 13/280043, которая включена в данный документ посредством ссылки во всей своей полноте).
Вакцины против RV
Поскольку инфекция RV может быть предотвращена путем обеспечения нейтрализующих антител позвоночным, вакцина, содержащая VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV, при введении позвоночным может индуцировать нейтрализующие антитела in vivo. VLP RV, которые содержат один или несколько гликопротеинов (G-белков) RV, предпочтительно применяют для профилактики и/или лечения инфекции RV. Таким образом, другой аспект данного раскрытия относится к способу индуцирования иммунного ответа в отношении RV. Способ включает этап, на котором вводят субъекту (такому как человек или субъект-животное) иммунологически эффективное количество композиции, содержащей VLP RV, которая содержит один или несколько гликопротеинов (G-белков) RV. Введение иммунологически эффективного количества композиции вызывает иммунный ответ, специфический в отношении эпитопов, представленных на G-белке RV. Такой иммунный ответ может включать B-клеточные ответы (например, продуцирование нейтрализующих антител) и/или Т-клеточные ответы (например, продуцирование цитокинов). Предпочтительно, иммунный ответ, вызванный G-белком RV, включает в себя элементы, которые являются специфическими в отношении по меньшей мере одного конформационного эпитопа, представленного на G-белке RV. В одном варианте осуществления иммунный ответ является специфическим в отношении эпитопа, представленного на G-белке RV, находящемуся в форме мицеллы. G-белки RV и композиции можно вводить субъекту без усиления вирусного заболевания после контакта с RV. Предпочтительно, G-белки RV, раскрытые в данном документе, и соответствующим образом разработанные иммуногенные композиции вызывают Th1-смещенный иммунный ответ, который снижает или предотвращает инфицирование RV и/или снижает или предотвращает патологический ответ после инфицирования RV.
В одном варианте осуществления G-белки RV по настоящему изобретению находятся в форме мицелл (например, розеток). Смотри пример 2. В одном варианте осуществления мицеллы очищают после экспрессии в клетке-хозяине. В случаях введения субъекту, мицеллы по настоящему изобретению предпочтительно индуцируют нейтрализующие антитела. В некоторых вариантах осуществления мицеллы можно вводить с адъювантом. В других вариантах осуществления мицеллы можно вводить без адъюванта.
В другом варианте осуществления настоящее изобретение охватывает вирусоподобные частицы (VLP) RV, содержащие G-белок RV, которые могут быть включены в состав вакцин или антигенных составов для защиты позвоночных (например, людей) от инфекции RV или по меньшей мере одного симптома данного заболевания. Настоящее изобретение также относится к VLP RV и векторам, содержащим гены RV дикого типа и мутированные гены RV или их комбинацию, полученную из различных штаммов вируса RV, который при трансфекции в клетки-хозяева будет продуцировать вирусоподобные частицы (VLP), содержащие белки RV.
В некоторых вариантах осуществления вирусоподобные частицы RV могут дополнительно содержать по меньшей мере один белок вирусного матрикса (например, М-белок RV). В одном варианте осуществления М-белок получают из штамма RV человека. В другом варианте осуществления М-белок получают из альтернативного штамма RV, такого как штамм RV, выделенный из собаки, летучей мыши, енота или скунса. В других вариантах осуществления матричный белок может быть M1-белком из штамма вируса гриппа. В одном варианте осуществления штамм вируса гриппа является штаммом птичьего гриппа. В иллюстративном варианте осуществления штамм птичьего гриппа является штаммом H5N1 A/Indonesia/5/05. В других вариантах осуществления матричный белок может быть из вируса ньюкаслской болезни (NDV).
В дополнительных вариантах осуществления VLP по настоящему изобретению могут содержать один или несколько гетерологичных иммуногенов, таких как гемагглютинин (HA) и/или нейраминидаза (NA) вируса гриппа.
В некоторых вариантах осуществления настоящее изобретение также включает комбинации различных G, N, P, M и L-белков RV из того же и/или различных штаммов в одной или нескольких VLP. Кроме того, VLP могут включать одну или несколько дополнительных молекул для усиления иммунного ответа.
В другом варианте осуществления настоящего изобретения VLP RV могут переносить средства, такие как нуклеиновые кислоты, siRNA, микроРНК, химиотерапевтические средства, визуализирующие средства и/или другие средства, которые необходимо доставить пациенту.
VLP по настоящему изобретению являются пригодными для получения вакцин и иммуногенных композиций. Одной из важных особенностей VLP является возможность экспрессировать интересующие поверхностные белки так, что иммунная система позвоночных индуцирует иммунный ответ в отношении белка интереса. Однако не все белки могут быть экспрессированы на поверхности VLP. Возможно множество причин, по которым некоторые белки не экспрессируются или слабо экспрессируются на поверхности VLP. Одной из причин является то, что белок не ориентирован на мембрану клетки-хозяина, или, что белок не имеет трансмембранного домена. В качестве примера, последовательности вблизи карбокси-конца гемагглютинина вируса гриппа могут быть важными для включения HA в липидный бислой зрелого вируса гриппа, окружающий нуклеокапсиды, и для сборки тримера HA при взаимодействии с матричным белком M1 гриппа (Ali и соавт., (2000) J. Virol. 74, 8709-19).
Таким образом, один вариант осуществления настоящего изобретения включает химерные VLP, содержащие G-белок из RV и по меньшей мере один иммуноген, который обычно эффективно не экспрессируется на поверхности клетки или не является нормальным белком RV. В одном варианте осуществления G-белок RV может быть гибридизирован с иммуногеном интереса. В другом варианте осуществления G-белок RV связывается с иммуногеном посредством трансмембранного домена и цитоплазматического хвоста гетерологичного поверхностного белка оболочки вируса, например, белка оболочки MMTV.
Другие химерные VLP по настоящему изобретению включают VLP, содержащие G-белок RV и по меньшей мере один белок из гетерологичного возбудителя инфекции. Примеры гетерологичных возбудителей инфекции включают, без ограничения, вирусы, бактерии, простейшие, грибы и/или паразиты. В одном варианте осуществления иммуноген из другого возбудителя инфекции представляет собой гетерологичный вирусный белок. В другом варианте осуществления белок из гетерологичного возбудителя инфекции является связанным с оболочкой белком. В другом варианте осуществления белок из другого гетерологичного возбудителя инфекции экспрессируется на поверхности VLP. В другом варианте осуществления белок из возбудителя инфекции содержит эпитоп, который будет вырабатывать защитный иммунный ответ у позвоночных. В одном варианте осуществления белок из другого возбудителя инфекции коэкспрессируется с G-белком RV. В другом варианте осуществления белок из другого возбудителя инфекции гибридизируют с G-белком RV. В другом варианте осуществления только часть белка из другого возбудителя инфекции гибридизируют с G-белком RV. В другом варианте осуществления только часть белка из другого возбудителя инфекции гибридизируют с частью G-белка RV. В другом варианте осуществления часть белка из другого возбудителя инфекции, гибридизированную с G-белком RV, экспрессируют на поверхности VLP.
Настоящее изобретение также охватывает варианты белков, экспрессированные на или в VLP по настоящему изобретению. Варианты могут содержать изменения в аминокислотных последовательностях составных белков. Выражение “вариант” по отношению к белку относится к аминокислотной последовательности, которая изменена по одной или нескольким аминокислотам по сравнению с эталонной последовательностью. Вариант может иметь “консервативные” замены, где замещенная аминокислота имеет аналогичные структурные и химические свойства, например, замещение лейцина на изолейцин. Альтернативно, вариант может иметь “неконсервативные” замены, например, замена глицина триптофаном. Аналогичные незначительные вариации могут также включать аминокислотную делецию или инсерцию, или и ту, и другую. Руководство в определении того, какие аминокислотные остатки могут быть заменены, вставлены или удалены без устранения биологической или иммунологической активности, можно обнаружить с помощью компьютерных программ, хорошо известных в данной области техники, например, программного обеспечения DNASTAR.
Природные варианты могут возникать вследствие мутаций в белках. Эти мутации могут приводить к антигенной изменчивости в пределах отдельных групп возбудителей инфекции, например, гриппа. Таким образом, у человека, инфицированного, например, штаммом вируса гриппа, вырабатываются антитела в отношении этого вируса, и когда появляются новые штаммы вируса, антитела к старым штаммам больше не распознают новые вирусы, и может произойти повторное инфицирование. Настоящее изобретение охватывает всю антигенную и генетическую изменчивость белков из возбудителей инфекции для получения VLP.
Общие тексты, описывающие молекулярно-биологические методики, которые применимы к настоящему изобретению, такие как клонирование, мутации, клеточная культура и т.п., включают Berger и Kimmel, Guide to Molecular Cloning Techniques, Methods in Enzymology volume 152 Academic Press, Inc., San Diego, Calif. (Berger); Sambrook и соавт, Molecular Cloning--A Laboratory Manual (3rd Ed.), Vol.1-3, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y., 2000 (“Sambrook”) и Current Protocols in Molecular Biology, F. M. Ausubel и соавт., eds., Current Protocols, a joint venture between Greene Publishing Associates, Inc. and John Wiley & Sons, Inc., (“Ausubel”). В данных текстах описывают мутагенез, применение векторов, промоторов и многие другие соответствующие вопросы, связанные, например, с клонированием и мутированием G-молекул RV, и т.д. Таким образом, настоящее изобретение также охватывает применение известных способов инженерии белков и технологии рекомбинантной ДНК для улучшения или изменения характеристик белков, экспрессированных на или в VLP по настоящему изобретению. Для получения и/или выделения вариантных нуклеиновых кислот, которые кодируют белковые молекулы и/или для дальнейшей модификации/мутации белков в или на VLP по настоящему изобретению, могут применяться различные типы мутагенеза. Они включают, без ограничения, сайт-направленный, случайный точечный мутагенез, гомологичную рекомбинацию (перетасовку ДНК), мутагенез с применением урацил-содержащих матриц, олигонуклеотид-направленный мутагенез, мутагенез модифицированной фосфоротиоатом ДНК, мутагенез с применением ДНК-дуплекса, содержащего разрыв, или тому подобное. Дополнительные подходящие способы включают репарацию точечных несоответствий, мутагенез с применением линий клеток-хозяев с недостаточной репарацией, отбор с применением рестрикционных ферментов и очистку с применением рестрикционных ферментов, мутагенез с делецией, мутагенез путем полного синтеза гена, репарация двунитевого разрыва и тому подобное. Мутагенез, например, с участием химерных конструктов, также включен в настоящее изобретение. В одном варианте осуществления при мутагенезе можно руководствоваться известной информацией о природной молекуле или измененной, или мутировавшей, природной молекуле, например, последовательности, сравнении последовательностей, физических свойствах, кристаллической структуре и тому подобным.
Настоящее изобретение дополнительно включает варианты белка, которые демонстрируют значительную биологическую активность, например, способны вызывать эффективный ответ антитела при экспрессии на или в VLP по настоящему изобретению. Такие варианты включают делеции, инсерции, инверсии, повторы и замены, выбранные в соответствии с общими правилами, известными в данной области техники, для того, чтобы оказывать незначительное влияние на активность.
В данной области техники известны способы клонирования белков. Например, ген, кодирующий специфический белок RV, может быть выделен с помощью ПЦР в реальном времени из полиаденилированной мРНК, экстрагированной из клеток, которые были инфицированы вирусом бешенства. Полученный генный продукт может быть клонирован в качестве ДНК-вставки в вектор. Выражение “вектор” относится к средствам, с помощью которых нуклеиновые кислоты можно репродуцировать и/или переносить между организмами, клетками или клеточными компонентами. Векторы включают плазмиды, вирусы и бактериофаги, провирусы, фагмиды, транспозоны, искусственные хромосомы и тому подобное, которые автономно реплицируются или могут интегрироваться в хромосому клетки-хозяина. Вектор также может быть депротеинизированным полинуклеотидом РНК, депротеинизированным полинуклеотидом ДНК, полинуклеотидом, состоящим из ДНК и РНК в пределах одной цепи, соединенной с полилизином ДНК или РНК, соединенной с пептидом ДНК или РНК, соединенной с липосомой ДНК или тому подобным, который не реплицируется автономно. Во многих, но не во всех общих вариантах осуществления, векторы по настоящему изобретению являются плазмидами или бакмидами.
Таким образом, настоящее изобретение включает нуклеотиды, которые кодируют белки, в том числе химерные молекулы, клонированные в вектор экспрессии, который может быть экспрессирован в клетке, индуцирующие образование VLP по настоящему изобретению. “Вектор экспрессии” представляет собой вектор, такой как плазмида, который способен к стимуляции экспрессии, а также репликации нуклеиновой кислоты, включенной в него. Как правило, нуклеиновая кислота, которая должна экспрессироваться, является “функционально связанной” с промотором и/или энхансером, и подлежит регулирующему транскрипцию контролю промотора и/или энхансера. В одном варианте осуществления нуклеотиды кодируют G-белок RV (как обсуждалось выше). В другом варианте осуществления вектор дополнительно содержит нуклеотиды, которые кодируют М-белок RV. В другом варианте осуществления вектор дополнительно содержит нуклеотиды, которые кодируют M и/или N-белки RV. В другом варианте осуществления вектор дополнительно содержит нуклеотиды, которые кодируют M, L и/или N-белки RV. В иллюстративном варианте осуществления вектор экспрессии является бакуловирусным вектором.
В некоторых вариантах осуществления настоящего изобретения белки могут содержать мутации, содержащие изменения, которые производят молчащие замены, добавления или делеции, но не изменяют свойства или активности кодируемого белка или того, как белки получаются. Нуклеотидные варианты могут быть получены по различным причинам, например, для оптимизации кодонов экспрессии для конкретного хозяина (изменение кодонов в мРНК человека на предпочтительные для клеток насекомых, таких как клетки Sf9. См. публикацию патента США № 2005/0118191, включенного в данный документ посредством ссылки во всей своей полноте для любых целей).
Кроме того, нуклеотиды могут быть секвенированы для обеспечения того, чтобы клонировали правильные кодирующие участки, и они не содержали бы каких-либо нежелательных мутаций. Нуклеотиды могут быть субклонированы в вектор экспрессии (например, бакуловирус) для экспрессии в любой клетке. Выше приведен только один пример того, как вирусные белки RV могут быть клонированы. Специалист в данной области техники понимает, что доступны и возможны дополнительные способы.
Настоящее изобретение также предусматривает конструкты и/или векторы, которые содержат нуклеотиды RV, кодирующие структурные гены RV, в том числе G, M, N, L, P или их части, и/или любую химерную молекулу, описанную выше. Вектор может быть, например, фагом, плазмидой, вирусным или ретровирусным вектором. Конструкты и/или векторы, которые содержат структурные гены RV, в том числе G, M, N, L, P или их части, и/или любую химерную молекулу, описанную выше, должны быть функционально связаны с соответствующим промотором, таким как промотор полиэдрина AcMNPV (или другого бакуловируса), промотор фага лямбда PL, lac, phoA и tac промоторы E.coli, ранний и поздний промоторы SV40, и промоторы ретровирусных LTR, которые представляют собой неограничивающие примеры. Другие подходящие промоторы будут известны специалисту в данной области техники в зависимости от клетки-хозяина и/или желаемой скорости экспрессии. Конструкты экспрессии дополнительно содержат сайты инициации, терминации транскрипции, и, в транскрибируемой области, сайт связывания рибосом для трансляции. Кодирующий участок транскриптов, экспрессированный конструктами, предпочтительно включает кодон инициации трансляции в начале и терминирующий кодон, соответствующим образом расположенный в конце транслируемого полипептида.
Векторы экспрессии предпочтительно включают по меньшей мере один селективный маркер. Такие маркеры включают гены дигидрофолатредуктазы, G418 или устойчивости к неомицину для эукариотической клеточной культуры и гены устойчивости к тетрациклину, канамицину или ампициллину для культивирования в E.coli и других бактериях. Среди векторов предпочтительными являются вирусные векторы, такие как бакуловирус, поксвирус (например, вирус коровьей оспы, авипоксвирус, канарипокс вирус, вирус птичьей оспы, вирус оспы енотов, вирус оспы свиней и др.), аденовирус (например, собачий аденовирус), вирус герпеса и ретровирус. Другие векторы, которые можно применять с настоящим изобретением, включают векторы для применения в бактериях, которые включают векторы pQE70, pQE60 и PQE-9, векторы pBluescript, векторы Phagescript, pNH8A, pNH16a, pNH18A, pNH46A, ptrc99A, pKK223-3, pKK233-3, pDR540, pRIT5. Среди предпочтительных эукариотических векторов находятся pFastBac1 pWINEO, pSV2CAT, pOG44, pXT1 и pSG, pSVK3, pBPV, pMSG и pSVL. Другие подходящие векторы будут очевидны специалистам в данной области техники. В одном варианте осуществления вектор, который содержит нуклеотиды, кодирующие гены RV, в том числе гены G RV, а также гены M, N, L, P, или их части, и/или любую химерную молекулу, описанную выше, является pFastBac.
Рекомбинантные конструкты, упомянутые выше, могут применяться для трансфекции, инфицирования или трансформации и могут экспрессировать белки RV, включая G-белки RV и по меньшей мере один иммуноген. В одном варианте осуществления рекомбинантный конструкт включает G, M, N, L, P RV, или их части, и/или любую молекулу, описанную выше, в эукариотических клетках и/или прокариотических клетках. Таким образом, настоящее изобретение предусматривает клетки-хозяева, которые содержат вектор (или векторы), содержащий нуклеиновые кислоты, которые кодируют структурные гены RV, в том числе G RV, и по меньшей мере один иммуноген, такой как, без ограничения, N, L и P RV, или их части, и/или любую молекулу, описанную выше, и обеспечивающий экспрессию генов, в том числе G, N, L или Р RV, или их частей, и/или любой молекулы, описанной выше, в клетке-хозяине в условиях, при которых возможно образование VLP.
Среди эукариотических клеток-хозяев находятся клетки-хозяева дрожжей, насекомых, птиц, растений, C. elegans (или нематоды) и млекопитающих. Неограничивающими примерами клеток насекомых являются клетки Spodoptera frugiperda (Sf), например, Sf9, Sf21, клетки Trichoplusia ni, например, клетки линии High Five и клетки Drosophila S2. Примерами клеток-хозяев грибов (включая дрожжи) являются S. cerevisiae, Kluyveromyces lactis (K. lactis), виды Candida, в том числе C. albicans и C. glabrata, Aspergillus nidulans, Schizosaccharomyces pombe (S. pombe), Pichia pastoris и Yarrowia lipolytica. Примерами клеток млекопитающих являются клетки COS, клетки почки детенышей хомяка, мышиные L-клетки, клетки LNCaP, клетки яичника китайского хомячка (СНО), клетки почки эмбриона человека (НЕК) и клетки африканской зеленой мартышки, клетки CV1, клетки HeLa, клетки MDCK, клетки Vero и Нер-2. Также могут применяться ооциты Xenopus laevis или другие клетки земноводных. Примеры прокариотических клеток-хозяев включают бактериальные клетки, например, E.coli, B. subtilis, Salmonella typhi и микобактерии.
Векторы, например векторы, содержащие полинуклеотиды G-белка RV и по меньшей мере один иммуноген, включая, без ограничения, N, L, P RV или их части, и/или любую химерную молекулу, описанную выше, могут быть трансфицированы в клетки-хозяева в соответствии со способами, хорошо известными в данной области техники. Например, введение нуклеиновых кислот в эукариотические клетки может происходить путем соосаждения фосфатом кальция, электропорации, микроинъекции, липофекции и трансфекции с применением полиаминовых реагентов трансфекции. В одном варианте осуществления вектор представляет собой рекомбинантный бакуловирус. В другом варианте осуществления рекомбинантный бакуловирус трансфецируют в эукариотическую клетку. В предпочтительном варианте осуществления клетка является клеткой насекомого. В другом варианте осуществления клетка насекомого представляет собой клетку Sf9.
Настоящее изобретение также предусматривает конструкты и способы, которые будут повышать эффективность получения VLP. Например, добавление лидерных последовательностей к G, M, N, L, P RV или их частям, и/или любым химерным или гетерологичным молекулам, описанным выше, может улучшить эффективность транспортировки белка в пределах клетки. Например, гетерологичная сигнальная последовательность может быть гибридизирована с G, M, N, L, P RV или их частями, и/или любой химерной или гетерологичной молекулой, описанной выше. В одном варианте осуществления сигнальная последовательность может быть получена из гена клетки насекомого и гибридизирована с G, M, N, L, P RV или их частями, и/или любыми химерными или гетерологичными молекулами, описанными выше. В другом варианте осуществления сигнальный пептид является хитиназной сигнальной последовательностью, которая эффективно функционирует в бакуловирусных системах экспрессии.
Другим способом увеличения эффективности получения VLP является кодон-оптимизация нуклеотидов, которые кодируют RV, включая G-белок RV, M, N, L, P или их части, и/или любые химерные или гетерологичные молекулы, описанные выше, для конкретного типа клеток. В одном варианте осуществления нуклеиновые кислоты кодон-оптимизированы для экспрессии в клетках насекомых. В иллюстративном варианте осуществления клетки насекомых являются клетками насекомых Sf9.
Настоящее изобретение также обеспечивает способы получения VLP, при этом способы включают этап, на котором экспрессируют гены RV, включая G-белок RV, в условиях, обеспечивающих образование VLP. В зависимости от выбранной системы экспрессии и клетки-хозяина VLP продуцируются растущими клетками-хозяевами, трансформированными вектором экспрессии, в условиях, при которых экспрессируются рекомбинантные белки и образуются VLP. В одном варианте осуществления настоящее изобретение включает способ получения VLP, включающий этап, на котором трансфецируют векторы, кодирующие по меньшей мере G-белок RV, в подходящую клетку-хозяина, и этап, на котором экспрессируют G-белок RV в условиях, обеспечивающих образование VLP. В другом варианте эукариотическую клетку выбирают из группы, включающей клетки дрожжей, насекомых, амфибий, птиц или млекопитающих. Выбор подходящих условий роста находится в компетенции специалиста в данной области техники.
Способы выращивания клеток, сконструированных для получения VLP по настоящему изобретению, включают, без ограничения, периодический, периодический с подпиткой, непрерывный и перфузионный методы культивирования клеточной культуры. Культивирование клеточной культуры подразумевает рост и размножение клеток в биореакторе (камере брожения), где клетки размножаются и экспрессируют белок (например, рекомбинантные белки) для очистки и выделения. Как правило, культивирование клеточной культуры проводят в стерильных условиях в биореакторе с контролируемой температурой и атмосферой. Биореактор представляет собой камеру, применяемую для культивирования клеток, в которой можно контролировать условия окружающей среды, такие как температура, атмосфера, перемешивание и/или рН. В одном варианте осуществления биореактор представляет собой камеру из нержавеющей стали. В другом варианте осуществления биореактор представляет собой предварительно стерилизованный пластиковый пакет (например, Cellbag®, Wave Biotech, Бриджуотер, Нью-Джерси). В другом варианте осуществления предварительно стерилизованные пластиковые пакеты представляют собой пакеты от приблизительно 50 л до 1000 л.
VLP затем выделяют с применением способов, которые сохраняют их целостность, например путем центрифугирования в градиенте, например хлорида цезия, сахарозы и иодиксанола, а также стандартных методик очистки, включая, например, ионообменную и гель-фильтрационную хроматографию.
Далее приведен пример того, как VLP по настоящему изобретению могут быть получены, выделены и очищены. Обычно VLP получают из рекомбинантных клеточных линий, сконструированных для создания VLP, в то время как клетки выращивают в клеточной культуре (см. выше). Специалисту в данной области техники должно быть понятно, что существуют дополнительные способы, которые могут применяться для получения и очистки VLP по настоящему изобретению, таким образом, настоящее изобретение не ограничивается описанным способом.
Получение VLP по настоящему изобретению может начинаться с посева клеток Sf9 (неинфицированных) во встряхиваемые колбы, клеткам позволяют увеличиваться в объеме и расширяться по мере того, как клетки растут и размножаются (например, из колбы на 125 мл в пакет на 50 л фирмы Wave). Среду, применяемую для культивирования клеток, составляют для соответствующей клеточной линии (предпочтительно, бессывороточная среда, например, среда для насекомых ExCell-420, JRH). Затем клетки инфицируют рекомбинантным бакуловирусом при наиболее эффективной кратности инфицирования (например, от приблизительно 1 до приблизительно 3 бляшкообразующих единиц на клетку). После того, как произошло инфицирование, G-белок RV и/или любая химерная или гетерологичная молекула, описанная выше, экспрессируются из генома вируса, самостоятельно собираются в VLP и секретируются из клетки от приблизительно 24 до 72 часов после инфицирования. Обычно, инфицирование является наиболее эффективным, когда клетки находятся в середине лаг-фазы роста (4-8×106 клеток/мл) и являются жизнеспособными по меньшей мере на приблизительно 90%.
VLP можно собрать через от приблизительно 48 до 96 часов после инфицирования, когда уровни VLP в среде для культивирования клеток находятся вблизи максимума, но до обширного клеточного лизиса. Плотность и жизнеспособность клеток Sf9 во время сбора может составлять от приблизительно 0,5×106 клеток/мл до приблизительно 1,5×106 клеток/мл с жизнеспособностью по меньшей мере 20%, как показано при помощи метода исключения красителя. Затем среду удаляют и осветляют. Во избежание агрегации VLP, к среде можно добавить NaCl до концентрации от приблизительно 0,4 до приблизительно 1,0 М, предпочтительно до приблизительно 0,5 М. Удаление клеток и продуктов распада клеток из среды клеточной культуры, содержащей VLP по настоящему изобретению, можно выполнить с помощью тангенциальной проточной фильтрации (TFF) с предварительно стерилизованным одноразовым фильтрующим элементом из пористого волокна 0,5 или 1,00 мкм или аналогичным устройством.
Затем VLP в осветленной культуральной среде можно концентрировать с помощью ультрафильтрации с применением предварительно стерилизованного одноразового фильтрующего элемента из пористых волокон с отсеканием молекулярного веса 500000. Концентрированные VLP можно диафильтровать 10 объемами фосфатно-солевого буфера (PBS) с рН от 7,0 до 8,0, содержащего 0,5 М NaCl, для удаления остаточных компонентов среды.
Концентрированные профильтрованные VLP можно дополнительно очистить в 20% до 60% ступенчатом градиенте сахарозы в буфере PBS с рН 7,2 и 0,5 М NaCl путем центрифугирования при 6500×g в течение 18 ч при температуре от приблизительно 4°С до приблизительно 10°C. Обычно VLP образуют характерную видимый слой в диапазоне от приблизительно 30% до приблизительно 40% сахарозы или на границе раздела фаз (в 20% и 60% ступенчатом градиенте), которую можно собрать из градиента и сохранить. Данный продукт можно разбавить до содержания 200 мМ NaCl при подготовке к следующему этапу процесса очистки. Данный продукт содержит VLP и может содержать частицы интактного бакуловируса.
Дополнительной очистки VLP можно достичь с помощью анионообменной хроматографии или изопикнического центрифугирования с применением “подушки” 44% сахарозы. В анионообменной хроматографии образец из градиента сахарозы (см. выше) загружают в колонку, содержащую среду с анионом (например, Matrix Fractogel EMD TMAE) и пропускают через солевой градиент (от приблизительно 0,2 М до приблизительно 1,0 М NaCl), что позволяет отделить VLP от других загрязнений (например, бакуловируса и ДНК/РНК). В способе с сахарозной “подушкой” образец, содержащий VLP, добавляют к 44% сахарозной “подушке” и центрифугируют в течение 18 часов при 30000g. VLP образуют слой в верхней части 44% сахарозы, в то время как бакуловирус осаждается на дно, а другие примесные белки остаются в слое с 0% сахарозы в верхней части. Пик или слой VLP собирают.
Интактный бакуловирус можно инактивировать, если это необходимо. Инактивация может быть выполнена химическими способами, например, формалином или β-пропиолактоном (BPL). Удаление и/или инактивация интактного бакуловируса могут быть выполнены преимущественно способами избирательного осаждения и хроматографии, известными в данной области техники, как проиллюстрировано выше. Способы инактивации включают инкубирование образца, содержащего VLP, в 0,2% BPL в течение 3 часов при температуре от приблизительно 25°С до приблизительно 27°С. Бакуловирус также можно инактивировать путем инкубирования образца, содержащего VLP, в 0,05% BPL при 4°С в течение 3 дней, затем при 37°С в течение одного часа.
После этапа инактивации/удаления продукт, содержащий VLP, можно подавать на другой этап диафильтрации для удаления любого реагента этапа инактивации и/или любую остаточную сахарозу и поместить VLP в желаемый буфер (например, PBS). Раствор, содержащий VLP, можно стерилизовать способами, известными в данной области техники (например, стерилизацией посредством фильтрации), и хранить в холодильнике или в морозильной камере.
Приведенные выше методы могут быть осуществлены на практике в различных масштабах. Например, в Т-колбах, встряхиваемых колбах, вращающихся колбах, вплоть до биореакторов промышленных размеров. Биореакторы могут включать либо резервуар из нержавеющей стали, либо предварительно стерилизованный пластиковый пакет (например, система, поставляемая Wave Biotech, Бриджуотер, Нью-Джерси). Специалист в данной области техники будет знать, что является наиболее желательным для его целей.
Увеличение числа копий и получение векторов экспрессии бакуловируса и инфицирование клеток рекомбинантным бакуловирусом для получения рекомбинантных VLP RV можно выполнять в клетках насекомых, например, клетках насекомых Sf9, как описано ранее. В одном варианте осуществления клетки являются клетками Sf9, инфицированными рекомбинантным бакуловирусом, сконструированным для получения VLP RV.
Фармацевтические или вакцинные составы и введение
Фармацевтические композиции, пригодные по настоящему изобретению, содержат фармацевтически приемлемый носитель, включая любой подходящий разбавитель или наполнитель, который включает любое фармацевтическое средство, само по себе не индуцирующее выработку иммунного ответа, опасного для позвоночного, принимающего композицию, и которое может вводиться без неспецифической токсичности, и VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков). Как применяют в данном документе, выражение “фармацевтически приемлемый” означает одобренный регулирующим органом федерального правительства или правительства штата или зарегистрированный в фармакопее США, европейской фармакопее или другой общепризнанной фармакопее для применения к млекопитающим и, более конкретно, к людям. Данные композиции могут быть пригодны в качестве вакцинных и/или антигенных композиций для индуцирования защитного иммунного ответа у позвоночного.
Настоящее изобретение охватывает фармацевтически приемлемую вакцинную композицию, содержащую VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков). В одном варианте осуществления фармацевтически приемлемая вакцинная композиция содержит VLP, содержащие по меньшей мере один G-белок RV и по меньшей мере один дополнительный иммуноген. В другом варианте осуществления фармацевтически приемлемая вакцинная композиция содержит VLP, содержащие по меньшей мере один G-белок RV и по меньшей мере один М-белок RV. В другом варианте осуществления фармацевтически приемлемая вакцинная композиция содержит VLP, содержащие по меньшей мере один G-белок RV и по меньшей мере один М-белок вируса гриппа. В другом варианте осуществления фармацевтически приемлемая вакцинная композиция содержит VLP, содержащие по меньшей мере один G-белок RV и по меньшей мере один М1-белок вируса птичьего гриппа.
Настоящее изобретение также охватывает набор для иммунизации позвоночного, такого как субъект-человек, включающий VLP, которые содержат по меньшей мере один G-белок RV.
В одном варианте осуществления настоящее изобретение включает иммуногенный состав, содержащий по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков).
Иммуногенный состав по настоящему изобретению содержит VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков), и фармацевтически приемлемый носитель или наполнитель. Фармацевтически приемлемые носители включают, без ограничения, физиологический раствор, буферный солевой раствор, декстрозу, воду, глицерин, стерильный изотонический водный буфер и их комбинации. Подробное обсуждение фармацевтически приемлемых носителей, разбавителей и других наполнителей представлены в Remington's Pharmaceutical Sciences (Mack Pub. Co. N.J., текущее издание). Состав должен соответствовать способу введения. В предпочтительном варианте осуществления состав, являющийся подходящим для введения человеку, предпочтительно является стерильным, незернистым и/или апирогенным.
Композиция, при желании, может также содержать небольшие количества смачивающих или эмульгирующих средств, или средств буферизации рН. Композиция может находиться в твердой форме, такой как лиофилизированный порошок, подходящий для восстановления, жидким раствором, суспензией, эмульсией, таблеткой, пилюлей, капсулой, составом с пролонгированным высвобождением или порошком. Пероральный состав может включать стандартные носители, такие как фармацевтического качества маннит, лактоза, крахмал, стеарат магния, сахарин натрия, целлюлоза, карбонат магния и т.д.
Настоящее изобретение также предусматривает фармацевтическую упаковку или набор, содержащий один или несколько контейнеров, заполненных одним или несколькими ингредиентами вакцинных составов по настоящему изобретению. В одном варианте осуществления набор включает два контейнера, один содержит VLP RV, содержащую один или несколько гликопротеинов RV (G-белков), а другой содержит адъювант. Такой контейнер (контейнеры) может сопровождаться уведомление в форме предписания государственным органом, регулирующим производство, применение или продажу фармацевтических препаратов или биологических продуктов, при этом уведомление отражает одобрение органом производства, применения или продажи для введения человеку.
Настоящее изобретение также предусматривает, что состав должен быть упакован в герметично закрытом контейнере, таком как ампула или саше, с указанием количества композиции. В одном варианте осуществления композицию поставляют в виде жидкости, в другом варианте осуществления в виде сухого стерилизованного лиофилизированного порошка или безводного концентрата в герметично закрытом контейнере, при этом она может быть восстановлена, например, водой или физиологическим раствором до соответствующей концентрации для введения субъекту.
В альтернативном варианте осуществления композицию поставляют в жидкой форме в герметично закрытом контейнере с указанием количества и концентрации композиции. Предпочтительно композиции в жидкой форме поставляют в герметично закрытом контейнере при по меньшей мере приблизительно 50 мкг/мл, более предпочтительно по меньшей мере приблизительно 100 мкг/мл, по меньшей мере приблизительно 200 мкг/мл, по меньшей мере 500 мкг/мл или по меньшей мере 1 мг/мл.
В качестве примера VLP RV, содержащие один или несколько G-белков RV, вводят в эффективном количестве или количестве (как определено выше), достаточном для стимуляции иммунного ответа, каждого ответа в отношении одного или нескольких штаммов RV. Введение VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков), вызывает иммунитет к RV. Как правило, доза может быть откорректирована в пределах этого диапазона на основе, например, возраста, физического состояния, веса тела, пола, диеты, времени введения и других клинических факторов. Профилактический вакцинный состав вводят системно, например, с помощью подкожной или внутримышечной инъекции с применением иглы и шприца или безыгольного инъектора. В иллюстративном варианте осуществления вакцинный состав вводят внутримышечно.
Таким образом, настоящее изобретение также включает способ составления вакцины или антигенной композиции, которая индуцирует иммунитет к инфекции или по меньшей мере одному симптому данного заболевания у млекопитающего, включающий этап, на котором к составу добавляют эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков). В одном варианте осуществления инфекция представляет собой инфекцию RV.
Несмотря на то, что возможна стимуляция иммунитета одной дозой, можно вводить дополнительные дозы одним и тем же или другим путем для достижения желаемого эффекта. Для новорожденных и младенцев, например, может потребоваться многократное введение для того, чтобы вызвать достаточный уровень иммунитета. Введение может продолжаться с интервалами на протяжении всего периода детства, что необходимо для поддержания достаточного уровня защиты в отношении инфекции, например, инфекции RV. Аналогично, взрослым, которые особенно восприимчивы к повторным или серьезным инфекциям, таким как, например, медицинские работники, работники по дневному уходу, члены семей детей младшего возраста, пожилые люди и лица с ослабленной сердечно-легочной функцией, может потребоваться множественная иммунизация для индуцирования и/или поддержания защитных иммунных ответов. Уровни вызванного иммунитета можно контролировать, например, путем измерения количества нейтрализующих секреторных и сывороточных антител, и корректировать дозы или повторять вакцинации по мере необходимости, чтобы индуцировать и поддерживать желаемый уровень защиты.
Способы введения композиции, содержащей VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков), (например, вакцины и/или антигенного состава) включают, без ограничения, парентеральное введение (например, внутрикожное, внутримышечное, внутривенное и подкожное), эпидуральное и чресслизистое (например, интраназальный и пероральный или легочный пути, или посредством суппозиторий). В конкретном варианте осуществления композиции по настоящему изобретению вводят внутримышечно, внутривенно, подкожно, чрескожно или внутрикожно. Композиции можно вводить любым удобным путем, например путем инфузии или болюсной инъекции, путем абсорбции через эпителиальные или кожно-слизистые покровы (например, слизистая рта, толстой кишки, конъюнктивы, носоглотки, ротоглотки, влагалища, уретры, мочевого пузыря и слизистой оболочки кишечника, и т.д.), и можно вводить вместе с другими биологически активными средствами.
Вакцины и/или иммуногенные составы по настоящему изобретению также можно вводить по схеме применения, например, первоначальное введение вакцинной композиции с последующими введениями повторных доз. В конкретных вариантах осуществления вторую дозу композиции вводят в любой момент от двух недель до одного года, предпочтительно от приблизительно 1, приблизительно 2, приблизительно 3, приблизительно 4, приблизительно 5 до приблизительно 6 месяцев после первоначального введения. Кроме того, третья доза может быть введена после второй дозы и от приблизительно трех месяцев до двух лет или даже дольше, предпочтительно от приблизительно 4, приблизительно 5 или приблизительно 6 месяцев, или приблизительно 7 месяцев до приблизительно года после первоначального введения. Необязательно можно вводить третью дозу при отсутствии или низком уровне специфических иммуноглобулинов, обнаруженных в сыворотке крови и/или моче или слизистых выделениях субъекта после второй дозы. В предпочтительном варианте осуществления вторую дозу вводят через приблизительно один месяц после первого введения, а третью дозу вводят через приблизительно шесть месяцев после первого введения. В другом варианте осуществления вторую дозу вводят через приблизительно шесть месяцев после первого введения. В другом варианте осуществления композиции по настоящему изобретению можно вводить как часть комбинированной терапии. Например, композиции по настоящему изобретению могут быть составлены с другими иммуногенными композициями, противовирусными препаратами и/или антибиотиками.
Доза фармацевтической композиции может быть легко определена специалистом в данной области техники, например, путем первоначального выявления эффективных доз для индуцирования профилактического или терапевтического иммунного ответа, например, путем измерения сывороточного титра вирус-специфических иммуноглобулинов или путем измерения ингибирующего соотношения антител в образцах сыворотки или образцах мочи или слизистых выделений. Дозы могут быть определены в исследованиях на животных. Неограничивающий список животных, применяемых для изучения эффективности вакцины, включает морских свинок, хомяков, хорьков, шиншилл, мышей и хлопковых хомяков. Большинство животных не являются природными хозяевами возбудителей инфекции, однако, могут подходить для исследований различных аспектов заболевания. Например, с применением любого из вышеуказанных животных можно получить вакцину-кандидат, например, VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков), для частичной характеристики индуцированного иммунного ответа и/или для определения того, были ли продуцированы нейтрализующие антитела. Например, было проведено множество исследований на мышиной модели, поскольку небольшие размеры мышей и их низкая стоимость позволяют исследователям проведение исследований в более крупном масштабе.
Кроме того, специалистом в данной области техники могут быть выполнены клинические исследования на человеке для определения предпочтительной эффективной дозы для человека. Такие клинические исследования являются общепринятыми и хорошо известны в данной области техники. Точная доза, которая должна применяться, будет также зависеть от пути введения. Эффективные дозы могут быть экстраполированы из кривых доза-реакция, полученных для испытаний in vitro или на животных системах.
Кроме того, как хорошо известно в данной области техники, иммуногенность конкретной композиции может быть повышена путем применения неспецифических стимуляторов иммунного ответа, известных как адъюванты. Адъюванты применялись в эксперименте для стимуляции генерализованного увеличения иммунитета к неизвестным антигенам (например, патент США № 4877611). В протоколах иммунизации применялись адъюванты для стимуляции ответов в течение многих лет, и, таким образом, адъюванты хорошо известны любому специалисту в данной области техники. Некоторые адъюванты влияют на способ, которым презентируются антигены. Например, иммунный ответ увеличивается при осаждении белковых антигенов квасцами. Эмульгирование антигенов также увеличивает продолжительность презентирования антигена. Включение любого адъюванта описано в Vogel и соавт., “A Compendium of Vaccine Adjuvants and Excipients (второе издание)”, включенном в данный документ посредством ссылки во всей полноте для любых целей, предусмотренных в пределах объема данного изобретения.
Иллюстративные адъюванты включают полный адъювант Фрейнда (неспецифический стимулятор иммунного ответа, содержащий убитые Mycobacterium tuberculosis), неполные адъюванты Фрейнда и адъювант на основе гидроксида алюминия. Другие адъюванты включают GMCSP, BCG, гидроксид алюминия, соединения MDP, такие как thur-MDP и nor-MDP, CGP (MTP-PE), липид А, а также рассматривается монофосфориллипид A (MPL). RIBI, который содержит три компонента, извлеченных из бактерий, MPL, димиколат трегалозы (TDM) и скелет клеточной стенки (CWS), в эмульсии 2% сквален/твин 80. Также могут применяться MF-59, Novasomes®, антигены МНС.
В одном варианте осуществления настоящего изобретения адъювант представляет собой однослойную липидную везикулу, содержащую от приблизительно двух до десяти бислоев, расположенных, по сути, в форме сферических оболочек, разделенных водными слоями, окружающими крупную аморфную центральную полость без липидных бислоев. Однослойные липидные везикулы могут участвовать в стимуляции иммунного ответа несколькими путями, как неспецифические стимуляторы, как носители антигена, как носители дополнительных адъювантов и их комбинации. Однослойные липидные везикулы действуют как неспецифические иммунные стимуляторы тогда, когда, например, вакцину получают путем смешивания антигена с предварительно образованными везикулами, так что антиген остается внеклеточным относительно везикул. При инкапсуляции антигена в пределах центральной полости везикулы, везикула действует как иммуностимулятор, так и как носитель антигена. В другом варианте осуществления везикулы первоначально получают из везикул, не содержащих фосфолипиды. В другом варианте осуществления везикулы представляют собой Novasomes®. Novasomes® являются однослойными везикулами, не содержащими фосфолипиды, в диапазоне от приблизительно 100 нм до приблизительно 500 нм. Они содержат Brij 72, холестерин, олеиновую кислоту и сквален. Было показано, что Novasomes являются эффективным адъювантом для антигенов вируса гриппа (см. патенты США №№ 5629021, 6387373 и 4911928, которые включены в данный документ посредством ссылки во всей своей полноте для любых целей).
Композиции по настоящему изобретению также могут быть составлены с “иммунными стимуляторами”. Они представляют собой собственные химические мессенджеры (цитокины) организма для повышения ответа иммунной системы. Иммунные стимуляторы включают, без ограничения, различные цитокины, лимфокины и хемокины с иммуностимулирующей, иммунопотенцирующей и провоспалительной активностями, такие как интерлейкины (например, IL-1, IL-2, IL-3, IL-4, IL-12, IL-13), факторы роста (например, гранулоцитов-макрофагов (GM)-колониестимулирующий фактор (CSF)) и другие иммуностимулирующие молекулы, такие как макрофагальный воспалительный фактор, лиганд Flt3, В7.1, В7.2 и т.д. Иммуностимулирующие молекулы можно вводить в том же составе, что и композиции по настоящему изобретению, или можно вводить отдельно. Для получения иммуностимулирующего эффекта можно вводить либо белок, либо вектор экспрессии, кодирующий белок. Таким образом, в одном варианте осуществления настоящее изобретение включает антигенные и вакцинные составы, содержащие адъювант и/или иммуностимулятор.
Способы стимулирования иммунного ответа
VLP RV, которые содержат один или несколько гликопротеинов RV (G-белков), пригодны для получения композиций, стимулирующих иммунный ответ, который обеспечивает иммунитет или существенный иммунитет к возбудителям инфекции. Настоящее изобретение охватывает способ индуцирования иммунитета к инфекции или по меньшей мере одному симптому данного заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков).
В одном аспекте настоящее изобретение включает способ индуцирования иммунитета к инфекции RV или по меньшей мере одному симптому данного заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков). В одном варианте осуществления субъект является позвоночным. В другом варианте осуществления позвоночное является млекопитающим. В еще одном варианте осуществления млекопитающее является человеком. В еще одном варианте осуществления млекопитающее является домашним животным. В другом варианте осуществления способ включает индуцирование иммунитета к инфекции RV или по меньшей мере одному симптому заболевания путем введения состава в одной дозе. В другом варианте осуществления способ включает индуцирование иммунитета к инфекции RV или по меньшей мере одному симптому заболевания путем введения состава в нескольких дозах.
Композиции по настоящему изобретению могут индуцировать существенный иммунитет у позвоночного (например, человека), при введении этому позвоночному. Существенный иммунитет является результатом иммунного ответа в отношении композиции по настоящему изобретению, который защищает или уменьшает интенсивность инфекции или по меньшей мере уменьшает симптом инфекции у позвоночного. В некоторых случаях, когда позвоночное инфицировано, инфекция будет бессимптомной. Ответ может быть неполным защитным ответом. В этом случае, когда позвоночное инфицировано возбудителем инфекции, позвоночное будет испытывать уменьшенные симптомы или симптомы более короткой продолжительности по сравнению с неиммунизированным позвоночным.
В другом варианте осуществления настоящее изобретение включает способ индуцирования ответа защитных антител в отношении инфекции или по меньшей мере одного из ее симптомов у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков).
Как применяют в данном документе, “антитело” представляет собой белок, содержащий один или несколько полипептидов, по сути или частично кодируемых генами иммуноглобулинов или фрагментами генов иммуноглобулинов. Общепризнанные гены иммуноглобулинов включают каппа-, лямбда-, альфа-, гамма-, дельта-, эпсилон- и мю-гены константных участков, а также множество генов вариабельных участков иммуноглобулинов. Легкие цепи классифицируют как каппа или лямбда. Тяжелые цепи классифицируют как гамма, мю, альфа, дельта или эпсилон, которые в свою очередь определяют класс иммуноглобулинов, IgG, IgM, IgA, IgD и IgE, соответственно. Типичная структурная единица иммуноглобулина (антитела) включает тетрамер. Каждый тетрамер состоит из двух идентичных пар полипептидных цепей, каждая пара имеет одну “легкую” (приблизительно 25 кДа) и одну “тяжелую” цепь (приблизительно 50-70 кДа). N-конец каждой цепи определяет вариабельный участок от приблизительно 100 до 110 или более аминокислот, в первую очередь отвечающих за распознавание антигена. Антитела находятся в виде интактных иммуноглобулинов или в виде ряда хорошо известных фрагментов, полученных расщеплением различными пептидазами.
В одном варианте осуществления настоящее изобретение включает способ индуцирования защитного клеточного ответа в отношении инфекции RV или по меньшей мере одного симптома заболевания у субъекта, включающий этап, на котором вводят по меньшей мере одну эффективную дозу VLP RV, которая содержит один или несколько гликопротеинов RV (G-белков).
Как упоминалось выше, иммуногенные композиции по настоящему изобретению предотвращают или уменьшают по меньшей мере один симптом инфекции RV у субъекта. Симптомы RV хорошо известны в данной области техники. Они включают лихорадку, головную боль и общую слабость или дискомфорт. По мере прогрессирования болезни появляются более специфичные симптомы, которые могут включать бессонницу, беспокойство, спутанность сознания, слабый или частичный паралич, возбуждение, галлюцинации, волнение, повышенное слюноотделение (увеличение количества слюны), затруднение глотания и гидрофобию (боязнь воды). Таким образом, способ по настоящему изобретению включает профилактику или уменьшение по меньшей мере одного симптома, связанного с инфекцией RV. Уменьшение симптома может быть определено субъективно или объективно, например, по самооценке субъекта, по оценке врача или путем проведения соответствующего анализа или измерения (например, температуры тела), включая, например, оценку качества жизни, замедление прогрессирования инфекции RV или дополнительных симптомов, уменьшению тяжести симптомов RV, или подходящим анализам (например, титр антител и/или анализ Т-клеточной активации). Объективная оценка включает оценку как животных, так и человека.
Настоящее изобретение дополнительно иллюстрируется следующими примерами, которые не должны рассматриваться как ограничивающие. Содержание всех ссылок, патентов и опубликованных патентных заявок, приведенных в данной заявке, а также фигуры и перечень последовательностей включены в данный документ посредством ссылки для любых целей.
ПРИМЕРЫ
Пример 1
Очистка G-частиц вируса бешенства для исследования на животных
Целью данного примера является демонстрация того, как очищали G-вирусоподобные частицы RV после экспрессии из бакуловирусных векторов в клетках насекомых Sf9.
Чтобы получить VLP RV, последовательность нуклеиновой кислоты, кодирующую G-белок RV (SEQ ID NO: 2), экспрессировали из бакуловирусного вектора (pFastBac1 G вируса бешенства), показанного на фигуре 1.
Клетки насекомых Sf9 инфицировали при 2,5×106 клеток/мл с MOI 0,2. Клетки собрали через 69 ч после инфицирования с помощью центрифуги при 4000g в течение 15 мин. Клетки промыли 1X PBS, снова центрифугировали и заморозили при -70ºC.
Использовали 23 грамма осадка клеток, полученных из приблизительно 2 л клеточной культуры. Осадок клеток ресуспендировали в 200 мл 25 мМ Трис-Cl с рН 8,0, 50 мМ NaCl, 0,5% NP9, 4 мкг/мл лейпептина. Смесь перемешивали при комнатной температуре в течение 1 ч, центрифугировали при 7000g в течение 60 минут при 4°С и сохранили 200 мл надосадочной жидкости для хроматографии.
После завершения экстракции G839 вируса бешенства из клеточного осадка загружали растворимые белки в хроматографическую колонку Fractogel EMD TMAE Hicap (M). Описание колонки было следующим: производитель колонки: GE Healthcare; тип колонки: XK50f20; производитель смолы: EMD Chemicals; тип смолы: Fractogel EMD TMAE Hicap (M), размеры наполненной колонки: приблизительно 10 см в высоту х 5,0 см в диаметре; объем наполненной колонки: 200 мл; расход при заполнении: 30 мл/мин; заполняющий буфер: 25 мМ Трис с рН 8,0/300 мМ NaCl.
Описание анионообменного процесса было следующим: расход при эксплуатации: 20 мл/мин; буфер для уравновешивания колонки: 25 мМ Трис с рН 8,0, 50 мМ NaCl, 0,02% NP9; элюент А: 25 мМ Трис с рН 8,0, 50 мМ NaCl, 0,02% NP9; элюент B1: 25 мМ Трис с рН 8,0, 180 мМ NaCl, 0,02% NP9; элюент B2: 25 мМ Трис с рН 8,0, 500 мМ NaCl, 0,02% NP9; элюент B3: 25 мМ Трис с рН 8,0, 1500 мМ NaCl, 0,02% NP9; загрузка колонки: 200 мл надосадочной жидкости после экстрагирования G-VLP вируса бешенства; промывка колонки после загрузки: 2 CV элюента А; элюирование колонки: 2 CV элюента BI, 2 CV элюента В2, 2 CV элюента B3.
Сбор основных фракций и объемы были следующими: проточная фракция: 250 мл; элюирование с B1 с 180 мМ NaCl: 175 мл (продукт); элюирование с В2 с 500 мМ NaCl: 100 мл; элюирование с B3 с 1500 мМ NaCl: 100 мл.
Фракцию элюирования 180 мМ NaCl из колонки TMAE загрузили в колонку с лектином чечевицы. Описание колонки было следующим: производитель колонки: GE Healthcare; тип колонки: XKI6/20; производитель смолы: GE Healthcare; тип смолы: сефароза-лектин чечевицы 4B; номер в каталоге смол: 17-0444-01; размеры наполненной колонки: 2,5 см в высоту х 1,6 см в диаметре; объем наполненной колонки: приблизительно 5 мл; расход при заполнении: 2,5 мл/мин; заполняющий буфер: 25 мМ NaHPO4 рН 6,8, 50 мМ NaCl, 0,02% NP9; расход при работе: 2 мл/мин; буфер для уравновешивания колонки: 25 мМ NaHPO4 с рН 6,8, 50 мМ NaCl, 0,02% NP9; элюент А: 25 мМ NaHPO4 с рН 6,8, 50 мМ NaCl, 0,02% NP9, элюент B: 25 мМ NaHPO4 с рН 6,8, 50 мМ NaCl, 0,02% NP9, 500 мМ метил-альфа-D-маннопиранозида (Fisher Scientific); загрузка колонки: 175 мл элюата G839 вируса бешенства из TMAE с 180 мм NaCl; промывка колонки после загрузки: 5 CV с элюентом А; элюирование колонки: 10 CV с элюентом B.
Сбор основных фракций и объемы были следующими: проточная фракция: 180 мл; фракция элюирования: 30 мл (продукт).
Элюат лектина чечевицы загружали в хроматографическую колонку Fractogel EMD SO3 - Hicap (M). Описание колонки было следующим: производитель колонки: GE Healthcare; тип колонки: XK16/20; производитель смолы: EMD Chemicals; тип смолы: Fractogel EMD SO3 - Hicap (M), размеры наполненной колонки: 5 см в высоту х 1,6 см в диаметре; объем наполненной колонки: 10 мл; расход при заполнении: 7,5 мл/мин; заполняющий буфер: 25 мМ NaHPO4 с рН 6,8, 50 мМ NaCl, 0,02% NP9.
Описание катионообменного процесса было следующим: расход при эксплуатации: 5 мл/мин; буфер для уравновешивания колонки: 25 мМ NaHPO4 рН 6,8, 50 мМ NaCl, 0,02% NP9; элюент А: 25 мМ NaHPO4 с рН 6,8; 50 мМ NaCl, 0,02% NP9, элюент B: 25 мм NaHPO4 с рН 6,8, 300 мМ NaCl, 0,02% NP9; загрузка колонки: 30 мл элюата G839 вируса бешенства из колонки с лектином чечевицы; промывка колонки после загрузки: 3 CV с элюентом А; элюирование колонки: 4 CV-этапное элюирование элюентом В; сбор основных фракций и объемы: фракция элюирования: 9 мл (конечный продукт); фильтрация 9 мл продукта элюирования колонки SO3 с 300 мМ NaCl и фильтром 0,2 мкм: производитель фильтра (0,2 мкм): Corning; тип фильтра: 28 мм шприцевой фильтр с мембраной SFCA 0,2 микрона.
Провели вестерн-блоттинг с применением сыворотки кролика к G RV (фигура 2). Чистота G-частиц RV с применением вышеприведенных условий составила 86%. Общее количество белка составило 0,39 мг/мл, и концентрация G-частиц RV составила 0,33 мг/мл с общим количеством 2,97 мг G-частиц RV из 2 л клеточной культуры, с выходом приблизительно 1,5 мг/л клеточной культуры. Важно отметить, что G-частицы RV были стабильны при 4°С в течение по меньшей мере одного месяца (данные не показаны).
Пример 2
Электронная микроскопия для анализа конформации G-белка RV
Очищенный G-белок RV анализировали с помощью электронной микроскопии с применением фонового окрашивания (см. фигуру 3). Средний молекулярный вес G-частиц RV с 0,02% NP9 составил 1,04х10-6. Белковые тримеры имели молекулярный вес 175,5 кДа, а среднее количество тримеров в частице составило 5,9. G-белки RV объединили в форме мицелл (розеток). Тот факт, что G-шипы проявляют морфологию мицелл при электронной микроскопии, означает, что частицы G-белка имеют правильную 3-мерную структуру нативного белка.
Пример 3
Индуцирование высоких уровней антител у кроликов G-частицами RV
Для проверки способности G-частиц RV к индуцированию иммунного ответа кроликам вводили G-частицы RV в различных концентрациях. Результаты этих экспериментов показаны на фигуре 4. G-частицы RV были способны индуцировать высокие уровни антител у кроликов.
Пример 4
Анализ нейтрализации RV и исследования введения RV на мышах
Для проверки эффективности вакцины, содержащей VLP RV, содержащие один или несколько G-белков, в защите от инфекции RV, проводили анализы нейтрализации на мышах. Кратко, в группах мышей внутримышечно вводили VLP RV или VLP RV+адъювант, например на основе алюминия. Кроме того, мышам вводили Rabipur®, коммерчески доступную инактивированную вакцину против вируса бешенства, которую применяли в качестве сравнительного вакцинного средства. VLP RV, содержащие один или несколько G-белков (т.е. G-мицеллы RV), как правило, должны индуцировать более высокие титры нейтрализующих антител по сравнению с Rabipur®.
Пример 5
Сравнение титров против бешенства у мышей Balb/c с введением G-частиц RV или коммерческой вакцины против бешенства Rabipur®
Иммуногенность VLP по настоящему изобретению сравнили с коммерческой вакциной против бешенства Rabipur® на мышиной модели Balb/c. Частицы RV G-VLP сконструировали и очистили, как описано в Примере 1. VLP агрегировали в форме мицелл (фигура 3).
Исследование включило четыре группы (n=5 для каждой группы):
Мышам ввели соответствующий иммуноген в количестве 0,1 мл на день 0, 3 и 7. Брали у мышей образцы сыворотки в дни 0, 4, 7, 10, 14, 21, 28, 35. Сыворотка была проверена на нейтрализующие антитела против бешенства методом ИФА.
Краткое изложение плана клинического исследования приведено в Таблице 1 ниже.
Как обсуждалось выше, нейтрализующие антитела против бешенства измеряли в мышиной сыворотке в моменты времени, предусмотренные выше. Титры указали на графике как среднее геометрическое для каждого измерения (фигура 6). Как показано на Фигуре 6, VLP-мицеллы по настоящему изобретению при каждой дозе обеспечивают более быстрые и более высокие титры антител по сравнению с коммерчески доступной вакциной Rabipur®. В частности, G-VLP RV обеспечивает титр серопротекции (0,5 EU/мл) днями раньше по сравнению с вакциной Rabipur® (фигура 6, таблица 2).
В Таблице 2 также показан процент серопротекции (т.е. титр нейтрализующих антител ≥0,5 EU/мл) для каждой группы иммунизации. В таблице показывается, что серопротекция происходит быстрее у животных, обработанных G-VLP RV по настоящему изобретению (во всех трех дозах), по сравнению с животными, которым вводили вакцину Rabipur®.
Приведенное выше подробное описание дано только для ясности понимания и без необязательных ограничений, при этом следует понимать, что модификации будут очевидны для специалиста в данной области техники. Это не является подтверждением того, что любая предоставленная в данном документе информация, является известным уровнем техники или относится к имеющимся заявленным изобретениям, или, что любые публикации, прямо или косвенно упомянутые, являются известным уровнем техники.
Если не указано иное, все технические и научные выражения, применяемые в данном документе, имеют то же значение, как это обычно понимается специалистом в области техники, к которой относится данное изобретение.
Хотя данная заявка была разбита на разделы, чтобы направить внимание читателя на конкретные варианты осуществления, такие разделы не стоит понимать как разделитель среди вариантов осуществления. Методы в каждом разделе и варианты осуществления, описанные в нем, применимы к другим разделам.
Хотя настоящее изобретение было описано в связи с конкретными вариантами его осуществления, следует понимать, что возможны дополнительные модификации, при этом данная заявка предназначена охватить любые вариации, применения или адаптации настоящего изобретения, в общем, принципы настоящего изобретения и включать такие отклонения от данного раскрытия, которые находятся в пределах известной или обычной практики в области техники, к которой относится настоящее изобретение, и которые могут быть применены к существенным признакам, изложенным выше в данном документе, и как следует из объема прилагаемой формулы изобретения.
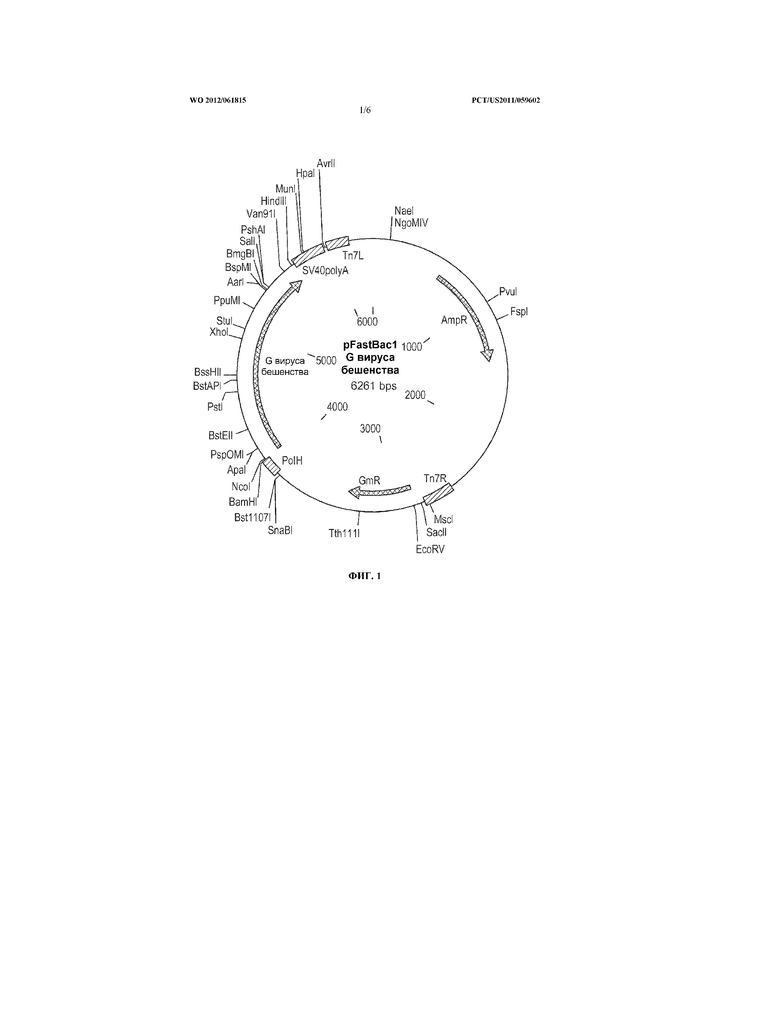


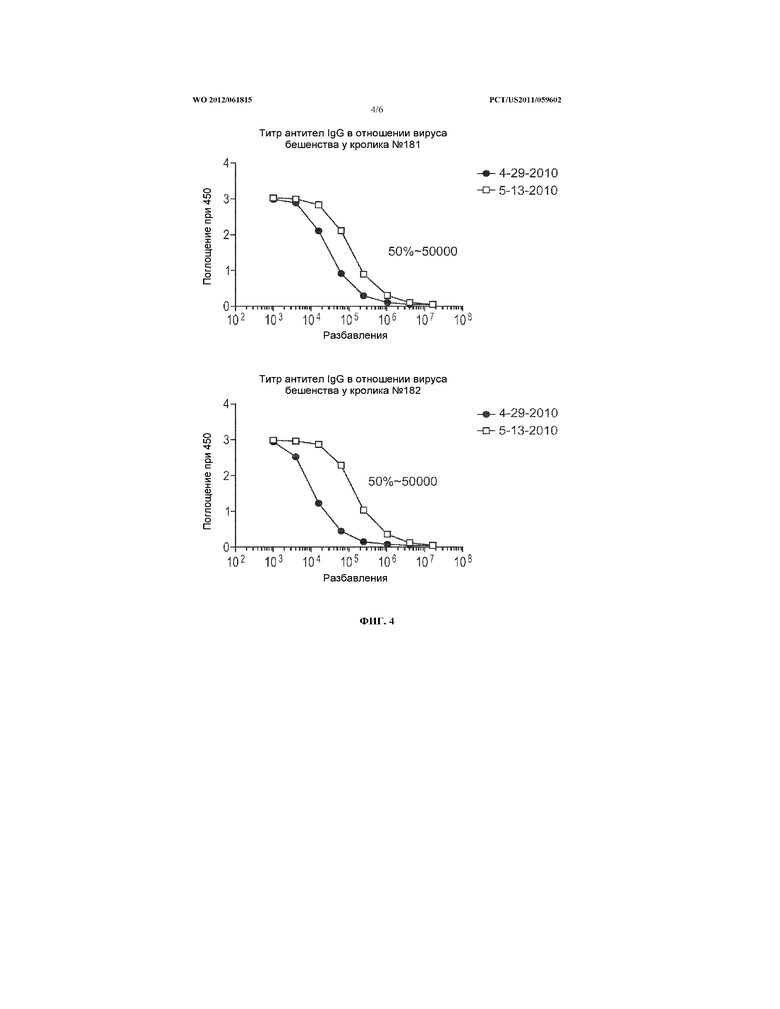

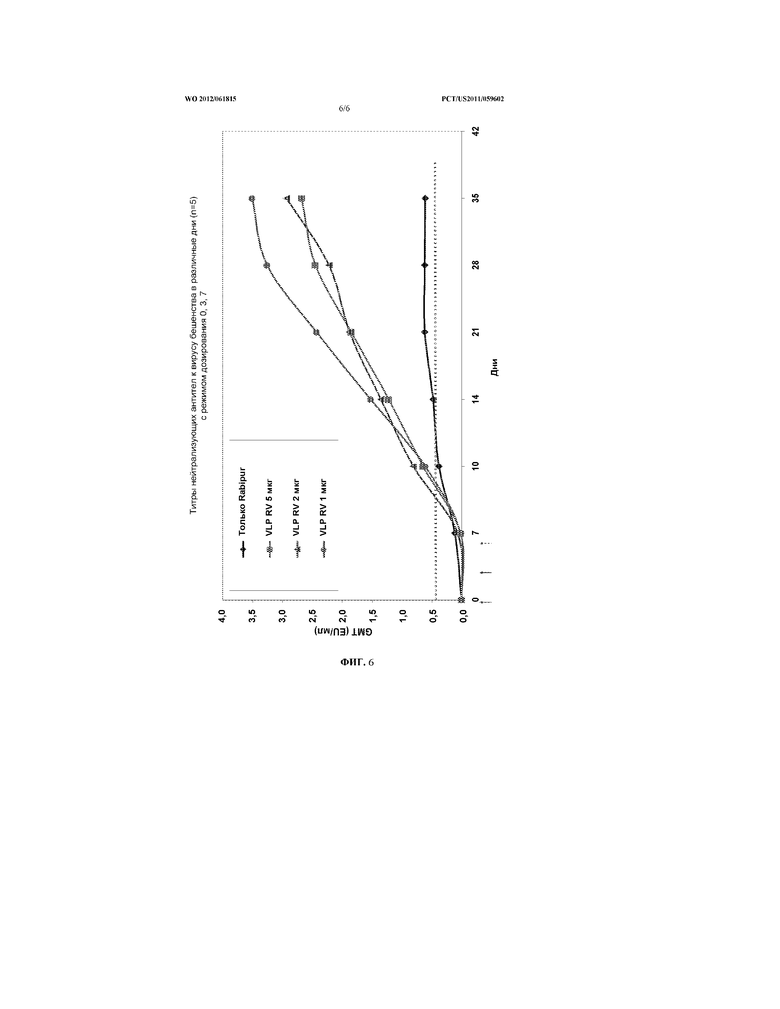
Предложенное изобретение относится к области биотехнологии, а именно к вирусоподобной частице (VLP) для применения в вакцинах или антигенных композициях для лечения или профилактики инфекции вируса бешенства (RV), а также способам их получения и применения. Вирусоподобная частица содержит один или несколько гликопротеинов (G-белков) RV, где G-белки находятся в форме мицеллы и формируют триммер и где указанная мицелла содержит детергент нонилфенол этоксилат 9 (NP-9). Предложенное изобретение позволяет с высокой эффективностью лечить или профилактировать инфекции вируса бешенства. 5 н. и 16 з.п. ф-лы, 6 ил., 2 табл., 5 пр.
1. Вирусоподобная частица (VLP) для применения в вакцинах или антигенных композициях для лечения или профилактики инфекции вируса бешенства (RV), содержащая один или несколько гликопротеинов (G-белков) RV, где G-белки находятся в форме мицеллы и формируют триммер и где указанная мицелла содержит детергент нонилфенол этоксилат 9 (NP-9).
2. VLP по п. 1, где G-белок RV является G-белком, полученным из штамма RV, выделенного из человека, собаки, летучей мыши, енота, скунса и лисицы.
3. VLP по п. 1, где G-белок RV содержит SEQ ID NO: 2.
4. VLP по п. 1, где G-белок RV состоит из SEQ ID NO: 2.
5. Фармацевтически приемлемая вакцинная композиция для лечения или профилактики инфекции вируса бешенства (RV), содержащая эффективное количество VLP по любому из пп. 1-4 и фармацевтически приемлемый носитель или разбавитель, где VLP способна вызывать иммунный ответ в организме-хозяине.
6. Фармацевтическая композиция по п. 5, дополнительно содержащая адъювант.
7. Фармацевтическая композиция по п. 6, где адъювант представляет собой адъювант на основе алюминия.
8. Фармацевтическая композиция по п. 5, где иммунный ответ включает увеличенное продуцирование антител к G-белкам в организме-хозяине.
9. Фармацевтическая композиция по п. 8, где продуцированные антитела к G-белкам представляют собой нейтрализующие антитела.
10. Фармацевтическая композиция по п. 9, где продуцированные антитела к G-белкам являются защитными.
11. Фармацевтическая композиция по п. 8, где антитела к G-белкам индуцированы в организме-хозяине после введения одной дозы.
12. Фармацевтическая композиция по п. 5, где иммунный ответ включает серопротективный титр на 7 дней.
13. Способ получения вирусоподобной частицы (VLP) для применения в вакцинах или антигенных композициях для лечения или профилактики инфекции вируса бешенства (RV), содержащей один или несколько гликопротеинов (G-белков) RV, где G-белки находятся в форме мицеллы и формируют триммер и где указанная мицелла содержит детергент нонилфенол этоксилат 9 (NP-9), включающий этапы, на которых:
(a) трансформируют клетку-хозяина насекомого для экспрессии изолированной нуклеиновой кислоты, кодирующей G-белок RV; и
(b) культивируют указанную клетку-хозяина в условиях, способствующих продуцированию мицеллы; и
(c) восстанавливают мицеллу в присутствии NP-9.
14. Набор для иммунизации субъекта-человека против инфекции вируса бешенства, содержащий один или несколько контейнеров, заполненных вакцинной композицией по любому из пп. 5-7.
15. Способ индуцирования иммунного ответа в отношении вирусной инфекции RV, включающий этап, на котором субъекту вводят эффективное количество фармацевтически приемлемой вакцинной композиции по любому из пп. 5-7.
16. Способ по п. 15, где иммунный ответ включает увеличенное продуцирование антител к G-белкам в организме-хозяине.
17. Способ по п. 16, где продуцированные антитела к G-белкам представляют собой нейтрализующие антитела.
18. Способ по п. 16, где продуцированные антитела к G-белкам являются защитными.
19. Способ по п. 16, где антитела к G-белкам индуцированы в организме-хозяине после введения одной дозы.
20. Способ по п. 15, где иммунный ответ включает серопротективный титр на 7 дней.
21. Способ по п. 15, где субъект является человеком.
| MOREIN B | |||
| ET AL., Subunit vaccines against enveloped viruses: virosomes, micelles and other protein complexes, Vaccine, 1985, v | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Пуговица | 0 |
|
SU83A1 |
| BEREZIN V.E | |||
| ET AL., Controlled organization of multimolecular complexes of enveloped virus glycoproteins: study of immunogenicity, Vaccine, 1988, v | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Двигатель внутреннего горения | 1921 |
|
SU450A1 |
| FEKADU M | |||
| ET AL., An immune | |||
Авторы
Даты
2016-02-20—Публикация
2011-11-07—Подача