Настоящее изобретение относится к вырабатывающим реутерин штаммам Lactobacillus brevis (L. brevis) и к их применению, в частности, для лечения или предотвращения инфекции Helicobacter pylori (H. pylori) и развивающихся вследствие этой инфекции болезней.
Реутерин (3-гидроксипропиональдегид, 3-ГПА) является противомикробным соединением, которое, как считалось изначально, вырабатывается рядом штаммов Lactobacillus reuteri (L. reuteri) при культивировании в анаэробных условиях в присутствии глицерина (TALARICO & DOBROGOSZ, Antimicrob Agents Chemother, 33, 674-9, 1989). Превращение глицерина в реутерин катализируется кобаламин-зависимой глицерин-дегидратазой (Gld; EC 4.2.1.30), которая состоит из трех субъединиц (C, D и E или α, β и γ, соответственно). Существование глицерин-дегидратазного (ГДГ) метаболического пути было обнаружено и в других видах молочнокислых бактерий, таких как Lactobacillus collinoides, Lactobacillus brevis и Lactobacillus hilgardii. Во всех этих видах наличие данного пути меняется от штамма к штамму и зависит от присутствия гена, кодирующего глицерин-дегидратазу или диол-дегидратазу (CADIEUX et al, Appl Environ Microbiol, 74, 4645-9, 2008; SAUVAGEOT et al, FEMS Microbiology Letters, 209, 69-74, 2002; CLAISSE и LONVAUD-FUNEL, Journal of Food Protection, 64, 833-837, 2001). В большей части бактерий, способных усваивать глицерин через ГДГ путь, реутерин в норме является промежуточным соединением метаболизма, которое затем внутриклеточно восстанавливается до 1,3-пропандиола, (1,3-ПД), который выделяется во внеклеточную среду. Только несколько штаммов, обладающих глицерин- или диол-дегидратазой, способны накапливать реутерин в среде для культивирования. Большая часть таких реутерин-накапливающих штаммов принадлежат к виду L. reuteri. Однако было обнаружено, что накапливать реутерин внеклеточно, как правило, в меньшем количестве, чем L. reuteri, способны и некоторые штаммы других видов кисломолочных бактерий: Lactobacillus coryniformis (MARTIN et al, Int J Food Microbiol, 104, 267-77, 2005), Lactobacillus collinoides (GARAI-IBABE et al, International Journal of Food Microbiology 121, 253-261, 2008; SAUVAGEOT et al, International Journal of Food Microbiology, 55, 167-170, 2000) и Lactobacillus hilgardii (PASTERIS and STRASSER DE SAAD, J. Agric. Food Chem., 57 (9), 3853-3858, 2009). Совсем недавно было обнаружено, что один из штаммов Lactobacillus brevis и один из штаммов Lactobacillus pentosus способны накапливать реутерин внеклеточным образом (в 10 раз в меньшей концентрации, однако, чем L. reuteri) (BAUER et al, International Journal of Food Microbiology, 137, 28-31, 2010).
Реутерин обладает широким спектром противомикробного воздействия в отношении потенциально вредоносных микроорганизмов. Реутерин может ингибировать рост дрожжей, грибков, простейших и различных вредоносных бактерий при концентрации, в четыре-пять раз меньшей, чем необходимая для ингибирования роста молочнокислых бактерий концентрация. Ввиду данной избирательной противомикробной активности реутерина, которая позволяет уничтожать ряд патогенных микроорганизмов, не причиняя при этом вреда полезным молочнокислым бактериям кишечной микрофлоры, было предложено применять его для лечения различных нарушений, связанных с пищеварительной системой.
Некоторые штаммы L. reuteri рассматривали как потенциальные пробиотики, в частности, ввиду их защитного действия в отношении патогенов, таких как Salmonella enterica, Escherichia coli, Clostridium difficile и Helicobacter pylori (CLEUSIX et al, BMC Microbiol, 71012007; SPINLER et al, Anaerobe, 14, 166-71, 2008; FRANCAVILLA et al., Helicobacter, 13, 127-34, 2008; PCT WO 2004/031368). Такое действие связывали, по крайней мере частично, с выработкой реутерина.
Среди патогенных микроорганизмов желудочно-кишечного тракта Helicobacter pylori в последние годы вызывает все больший интерес с исследовательской точки зрения. Это грамотрицательные спиралевидные бактерии, которые населяют слизистую оболочку кишечника более чем 50% населения мира. Несмотря на то, что у большинства людей инфекция H. pylori является бессимптомной, хотя в их кишечном эпителии присутствуют признаки воспаления, тем не менее, заболевания развиваются у 15-20% зараженных H. pylori людей. H. pylori является главным фактором заболеваний двенадцатиперстной кишки, хронического активного гастрита, атрофии, метаплазии, дисплазии, рака желудка и лимфомы ткани слизистых оболочек желудка (ТСОЖ) (см. обзор FOX & WANG, J Clin Invest, 117, 60-9, 2007; POLK & PEEK, Nat Rev Cancer, 10, 403-14).
Стандартное лечение пациентов, зараженных H. pylori, включает применение двух антибиотиков и ИПН (ингибитора протонового насоса), т.е. так называемой тройной терапии. Однако уровень эрадикации H. pylori после тройной терапии снижается вследствие устойчивости к антибиотикам или малой восприимчивости. Кроме того, несмотря на ряд исследований, на данный момент на рынке все еще нет эффективной вакцины.
Применение пробиотиков было предложено в качестве альтернативы тройной терапии для лечения или предотвращения инфекции H. pylori. Как указано выше, такие пробиотики включают, в частности, L. reuteri, в частности, вследствие их противомикробных свойств. Некоторые штаммы других молочнокислых бактерий были предложены как потенциально полезные для борьбы с инфекцией H. pylori. Например, SIMOVA et al. (J Appl Microbiol, 106, 692-701, 2009) описывают штамм Lactobacillus delbrueckii (BB18), который вырабатывает ингибирующий пептид (бактериоцин), который оказывает сильное блокирующее воздействие на H. pylori. LINSALATA et al. (Helicobacter, 9, 165-72, 2004) исследуют эффекты отдельного штамма L. brevis (CD2) с высокой активностью аргининовой дезиминазы, влияющей на выживаемость H. pylori в слизистой желудка человека. Они показали снижение количества H. pylori внутри желудка и предположили, что оно может быть связано с повышенной активностью аргининовых дезиминаз, что приводит к снижению аргинина у H. pylori и тормозит их рост и пролиферацию.
Авторы изобретения выделили штамм Lactobacillus brevis, который обладает способностью вырабатывать реутерин и накапливать его в достаточном количестве для проявления противомикробной активности в отношении широкого спектра штаммов H. pylori.
Штамм "способный накапливать реутерин" или "реутерин-накапливающий" штамм, согласно настоящему документу, является штаммом, который способен вырабатывать реутерин и внеклеточно выделять его.
Таким образом, объектом по настоящему изобретению является такой штамм L. brevis, который был депонирован согласно будапештскому соглашению с НККМ (Национальная Коллекция Культур Микроорганизмов, 25, ул. Docteur Roux, Париж) 3 февраля 2011 года, под номером CNCM I-4431.
Помимо способности вырабатывать и накапливать реутерин, этот штамм также обладает следующими характеристиками:
- Морфология: палочкообразные бактерии с однородной окраской, группирующиеся в небольшие цепочки;
- Метаболизм: гетероферментативный;
- Ферментация следующих сахаров (результаты получены с использованием стрипа Api 50 CH и среды API MRS при 37°C за 48 часов): L-арабиноза, D-рибоза, D-ксилоза, D-глюкоза, D-фруктоза, D-мальтоза, D-мелибиоза, калия глюконат, калий 5-цетоглюконат.
Настоящее изобретение также охватывает реутерин-накапливающие штаммы L. brevis, которые были получены вследствие мутагенеза или генетических трансформаций штамма CNCM I-4431, в случае если они сохраняют противомикробные свойства и способность вырабатывать реутерин, присущие родительскому штамму. Это могут быть штаммы, в которых один или несколько эндогенных генов штамма CNCM I-4431 были подвергнуты мутации, например, чтобы изменить их метаболические особенности (например, способность данного штамма метаболизировать сахара, его устойчивость к внутрикишечному транспорту, его устойчивость к кислотности или последующему окислению среды). Это также могут быть штаммы, которые получились в результате генетической трансформации штамма CNCM 1-443 одним или несколькими представляющими интерес генами, что позволит, например, данному штамму приобрести дополнительные физиологические характеристики или вырабатывать белки с терапевтическими или вакцинальными свойствами, которые нужны в ходе лечения с помощью данного штамма.
Эти штаммы можно получать из штамма CNCM I-4431 с помощью общепринятых способов случайного или сайт-специфического мутагенеза и генетической трансформации молочнокислых бактерий, например так, как описано в статье GURY et al. (Arch Microbiol., 182, 337-45, 2004) или VELEZ et al. (Appl Environ Microbiol., 73, 3595-3604, 2007), или с помощью метода, известного как "геномная перетасовка" (PATNAIK et al. Nat Biotechnol, 20, 707-12, 2002; WANG Y. et al, J Biotechnol., 129, 510-15, 2007).
Объектом по настоящему изобретению также является способ получения реутерин-накапливающего штамма Lactobacillus brevis, включающий этап мутагенеза или генетической трансформации штамма CNCM I-4431.
Штамм L. brevis по изобретению можно использовать для получения реутерина. Таким образом, другим объектом по настоящему изобретению является способ для получения реутерина, включающий стадии:
- культивирование штамма L. brevis, предпочтительно, штамма CNCM I-4431, по изобретению указанным выше способом, в присутствии глицерина и
- выделение реутерина, выработанного культурой.
Объектом по настоящему изобретению также является композиция, включающая штамм L. brevis по изобретению, предпочтительно штамм CNCM I-4431.
В композиции по изобретению указанный штамм можно использовать в форме целых, предпочтительно живых бактерий.
Композиции по изобретению может быть представлена в любой подходящей для введения форме, в частности, в форме для перорального введения. Такие формы включают, в том числе, твердые, полутвердые, жидкие формы и порошки. Жидкие композиции, как правило, являются предпочтительными, вследствие простоты введения, например, в виде напитков.
Композиция может содержать по меньшей мере 105 КОЕ, предпочтительно по меньшей мере 106 КОЕ на г сухого веса штамма L. brevis по изобретению.
Композиция может дополнительно содержать другие штаммы бактерий, в частности, пробиотические штамм (штаммы), такие как штаммы Lactobacillus, Bifidobacterium, Streptococcus или Lactococcus.
Композиция может, как правило, содержать от 105 до 1013 колониеобразующих единиц (КОЕ), предпочтительно по меньшей мере 106 КОЕ, более предпочтительно по меньшей мере 107 КОЕ, еще более предпочтительно по меньшей мере 108 КОЕ и наиболее предпочтительно по меньшей мере 109 КОЕ на 1 г сухого веса композиции штамма L. brevis по изобретению. В случае жидкой композиции, это соответствует, как правило, от 104 до 1012 колониеобразующих единицам (КОЕ), предпочтительно по меньшей мере 105 КОЕ, более предпочтительно по меньшей мере 106 КОЕ, еще более предпочтительно по меньшей мере 107 КОЕ и наиболее предпочтительно по меньшей мере 109 КОЕ/мл.
Композиция может быть питательной композицией, в том числе пищевым продуктом, пищевой добавкой или функциональным пищевым продуктом. "Пищевая добавка" подразумевает продукт на основе таких соединений, которые, как правило, используются для получения продуктов питания, но при этом находятся в форме таблеток, порошков, капсул, настоек или в любой другой форме, как правило, не связанной с питанием, и которые оказывают положительное воздействие на здоровье человека. "Функциональный пищевой продукт" является таким пищевым продуктом, который также оказывает положительное воздействие на здоровье человека. В частности, пищевые добавки и функциональные пищевые продукты могут оказывать защищающий или лечащий физиологический эффект в отношении заболеваний, в том числе в отношении хронических заболеваний.
Питательные композиции по изобретению также включают детское питание, детскую молочную смесь для питания с рождения или для питания с полугода. Предпочтительно, настоящая композиция является биологически активной добавкой или фармацевтическим препаратом, питательной добавкой или продуктом лечебного питания.
Композиция может быть молочным продуктом, предпочтительно, ферментированным молочным продуктом. Ферментированный продукт может быть представлен в форме жидкости, или он может быть представлен в форме сухого порошка, полученного путем высушивания ферментированной жидкости. Примеры молочных продуктов включают кисломолочные продукты и/или ферментированную молочную сыворотку в сквашенной, смешанной или питьевой форме, сыр и йогурт.
Ферментированный продукт также может быть ферментированным растительным продуктом, таким как ферментированная соя, злаки и/или фрукты в сквашенной, смешанной или питьевой форме.
В предпочтительном варианте осуществления ферментированный продукт является свежим продуктом. Свежий продукт, не прошедший этапов сильной термической обработки, обладает тем преимуществом, что бактериальные штаммы в нем представлены в живом виде.
Объектом по настоящему изобретению также является штамм L. brevis по изобретению, предпочтительно штамм CNCM I-4431, или композиция по изобретению, подходящий для применения в качестве лекарственного средства. Штамм L. brevis и композиции по изобретению являются особенно подходящими для лечения или предотвращения инфекции H. pylori.
Объектом по настоящему изобретению также является применение штамма L. brevis по изобретению, предпочтительно штамма CNCM I-4431, или композиции по изобретению в качестве лекарственного средства или для получения лекарственного средства, предпочтительно лекарственного средства для лечения или предотвращения инфекции H. pylori.
Объектом по настоящему изобретению также является способ лечения или предотвращения инфекции H. pylori у нуждающегося в этом пациента указанным способом, включающим введение указанному пациенту терапевтически эффективного количества штамма L. brevis по изобретению, предпочтительно штамма CNCM I-4431, или композиции по изобретению.
Настоящее изобретение также охватывает способ для получения лекарственного средства, предпочтительно лекарственного средства для лечения или предотвращения инфекции H. pylori, указанным способом, согласно которому указанный выше штамм L. brevis, предпочтительно штамм CNCM I-4431, помещается по меньшей мере в один фармацевтически приемлемый разбавитель, носитель или эксципиент.
Способы диагностики инфекции H. pylori известны в данной области. В качестве примера, диагностику инфекции H. pylori можно проводить с помощью теста на антитела в крови, теста на антигены в кале или мочевинного дыхательного теста. Также ее можно проводить путем биопсии при эндоскопии, за которой следует уреазный тест, гистологический анализ или культивирование микробов.
Симптомы или заболевания, связанные с инфекцией H. pylori, включают, в частности, боли в желудке, изжогу, кислотный рефлюкс, боли в животе, срыгивание, рвоту, отрыжку, метеоризм, тошноту, эзофагит, гастрит, в том числе хронический активный гастрит, язвенные заболевания желудка, атрофию, метаплазию, дисплазию, рак желудка и лимфому ткани слизистой оболочки желудка (ТСОЖ).
Настоящее изобретение станет более ясным из дальнейшего описания, в котором будут перечислены примеры, демонстрирующие противомикробные иммуномодулирующие и противоинфекционные свойства штамма CNCM I-4431, а также описаны приведенные фигуры.
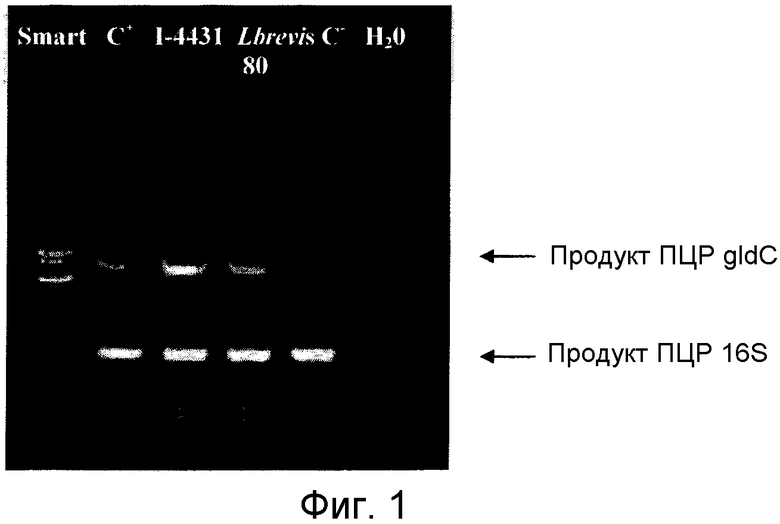
На Фиг. 1 представлен результат проведения ПЦР для штамма Lactobacillus brevis на последовательность gldC. Верхняя полоска на 728 п.н. представляет ожидаемый продукт с использованием генно-специфических праймеров на gldC. Нижняя полоска на 201 п.н. представляет ожидаемый продукт с использованием генно-специфических праймеров на 16S рРНК (положительный контроль ПЦР); Smart: DNA SMART Ladder (Eurogentec); C+: результаты ПЦР, полученные для контрольной ДНК из gldC-положительного штамма Lactobacillus reuteri ATCC 55730; I-4431: результаты ПЦР, полученные для ДНК штамма L. brevis CNCM I-4431; L. brevis 80: результаты ПЦР, полученные для ДНК штамма L. brevis 80 C-: результаты ПЦР, полученные для контрольной ДНК gldC-отрицательного штамма Streptococcus thermophilics; H20: результаты ПЦР, полученные для стерильной воды.
На Фиг. 2 представлен количественный анализ H. pylori (штамма NTCTC 11637) в C. elegans после поглощения H. pylori в отдельности (черная полоска), поглощения H. pylori и штамма L. brevis I-4431, выращенного в среде MRS (темно-серая полоска), поглощения H. pylori и штамма L. brevis I-4431, выращенного в среде MRS в присутствии глицерина (белая полоска) и поглощения H. pylori и среды MRS с глицерином.
Пример 1: Ингибирование роста штаммов H. Pylori in vitro с помощью штамма L. Brevis CNCM I-4431
Материалы и способы
Штаммы Lactobacillus brevis:
- L. brevis CNCM I-4431
- L. brevis 80: стандартный штамм L. brevis
Штаммы Helicobacter pylori:
Использовали три референтных штамма H. pylori, а также пять клинических изолятов.
Референтные штаммы:
- 26695: описан в TOMBS et al. (Nature 388, 539-547, 1997);
- HPAG1: описан в OH et al. (Proc Natl Acad Sci USA., 103, 9999-10004, 2006);
- TN2GF4: получен в Японии от пациента с язвой желудка и адаптирован к монгольской песчанке (штамм описан в WATANABE, et al. Gastroenterol 1998; том 115, стр. 642-648)
Клинические изоляты:
- CR113 и CR114: штаммы получены при биопсии людей с предраковыми повреждениями желудка
- Axcan 342 и Axcan 374: штаммы получены от пациента с гастритом и от пациента с эзофагитом, соответственно; пациенты проходили клиническое исследование на четырехкратную терапию для эрадикации H. pylori (MALFERTHEINER et al, Lancet, 377, 905-913, 2011).
- GC3C: штамм получен от пациента с раком желудка.
Способ:
Штаммы L. brevis выращивали в среде MRS (pH 6,2) в течение 17 часов. Бактериальные суспензии нейтрализовали до pH 6,8 раствором KOH.
Штаммы H. pylori выращивали в течение 48 часов в среде Brucella до получения мутности, эквивалентной стандарту Mac Farland 4. Бактериальные суспензии распределяли по поверхности плашек Mueller Hinton Agar с добавлением 10% (об./об.) овечьей крови, обогащенной 1% (об./об.) добавкой Polyvitex (Biomerieux), и в такой же среде в присутствии глицерина до конечной концентрации 100 мМ для обеспечения выработки реутерина.
На поверхность плашек помещали стерильные бумажные диски. Затем 5 нейтрализованных суспензий L. brevis наносили на каждый бумажный диск. Плашки инкубировали при 37°C в микроаэрофильных атмосферных условиях (газовый распределитель Ruskin Microaerophilic, конечные условия 5% О2, 10% CO2, и 85% N2) в течение от 72 часов до 96 часов.
Чтобы проанализировать воздействие суспензии L. brevis на рост штамма H. pylori, измеряли ширину колец ингибирования роста вокруг бумажных дисков.
Результаты
Результаты представлены ниже в Таблице 1.
Данные результаты демонстрируют то, что в то время как L. brevis 80 оказывает ингибирующее воздействие только на два исследуемых штамма H. pylori, L. brevis I-4431 ингибирует рост восьми из восьми штаммов исследуемых H. pylori. Эти ингибирующие свойства, видимо, связаны с накоплением реутерина, поскольку они наблюдаются только в тех культурах L. brevis, которые выращивали в присутствии глицерина.
Пример 2: ПЦР скрининг гена gldC
Материалы и способы
Наличие у L. brevis CNCM I-4431 гена, кодирующего большую субъединицу глицерин-дегидратазы (GldC), фермента, ответственного за выработку реутерина, исследовали с помощью следующего способа, описанного CADIEUX et al. (2008, ссылка приведена выше).
В кратком изложении, из каждого исследуемого штамма выделяли тотальную ДНК.
В качестве положительного контроля (C+) использовали реутерин-вырабатывающий штамм L. reuterii ATCC 55730. В качестве отрицательного контроля (C-) использовали штамм не вырабатывающего реутерин вида (Streptococcus thermophilus).
Амплификацию фрагмента гена, кодирующего большую субъединицу Gld (gldC), проводили с помощью следующих вырожденных праймеров:
GDCRev: GCRGCYTTSATATCTKSAACCAT (SEQ ID NO: 1) и GDCFor: GCMTAYGCWGAAACCATTTCAGTTTA (SEQ ID NO: 2), оба описаны у CADIEUX et al. Ожидаемый размер амплифицированного фрагмента составлял 728 п.н.
В качестве положительного контроля ПЦР, во всех образцах также амплифицировали фрагмент 16S рРНК с помощью следующих эубактериальных праймеров:
16SFor: ACTCCTACGGGAGGCAGCAG (SEQ ID NO: 3) и
16SRev: GTATTACCGCGGCTGCTGGCAC (SEQ ID NO: 4), оба также описаны CADIEUX et al.
Ожидаемый размер амплифицированного фрагмента 16S рРНК составлял 201 п.н.
Результаты
Результаты анализа ПЦР показаны на Фиг. 1. Штаммы L. brevis CNCM I-4431, L. brevis 80 и (C+) реутерин-вырабатывающий штамм L. reuterii ATCC 55730 оказались положительными в отношении ожидаемого 728-п.н. продукта. Таким образом, штамм L. brevis CNCM I-4431 имеет ген gldC, позволяющий ему вырабатывать реутерин.
Пример 3: Влияние L. Brevis CNCM I-4431 на инфекцию H. Pylori на модели C. elegans
Культивирование L. brevis и H. pylori
Штамм L. brevis CNCM I-4431 выращивали в среде MRS так, как это описано в Примере 1.
Штамм NCTC11637 (ATCC 43504T) H. pylori выращивали в среде BHI (Oxoid), содержащей 5% (об./об.) лошадиной крови (Oxoid).
Супернатанты отделяли от клеток посредством центрифугирования и нейтрализовали NaOH (1M). Затем супернатанты фильтровали (0,22 мкм) и добавляли к клеточному осадку.
В случае культур H. pylori, среду BHI, содержащую лошадиную кровь (Oxoid), удаляли посредством центрифугирования, после чего клетки промывали физиологическим раствором.
В плашки NG Agar, которые применяли для анализа инфекции C. elegans, добавляли по 100 мкл смесей, содержащих культуры LAB с оптической плотностью, составляющей 2,22 (включая клетки и супернатант) и соответствующие клетки штамма H. pylori (оптическая плотность 0,022). В контрольном эксперименте, в котором нематод не кормили LAB, клетки H. pylori ресуспендировали в физиологическом растворе и помещали на плашки.
Анализ инфекции C. elegans
Анализ инфекции проводили со штаммом C. elegans дикого типа (N2). Для заражения нематод использовали штамм H. pylori NCTC 11637. Эксперимент был начат с молодыми взрослыми особями одного возраста (трехдневные нематоды), которых последовательно переносили в разные условия культивирования:
- Среда NG + E. coli OP50 (контроль).
- Среда NG + E. coli OP50 + 100 мкл среды для культивирования LAB (контроль для среды культивирования).
- Среда NG + E. coli OP50 + 100 (H. pylori NCTC 11637T + LAB).
Нематод инкубировали при 25°C в течение 8 суток, перенося их на новые плашки каждые двое суток. Результат выживаемости по популяциям записывали для каждых условий среды.
После инкубационного периода брали образцы из 15 нематод на каждое условие и отмывали их буфером M9, содержащем 0,1% Triton X-100. Нематод затем раздробили с помощью 0,4 г гранул карбида кремния в вортексе.
ДНК зараженных нематод выделяли с помощью коммерческого набора "High Pure PCR Template Preparation Kit" (Roche), затем осаждали и отмывали чистым этиловым спиртом и 5M ацетатом калия. Для выявления наличия H. pylori использовали разведенные образцы ДНК и проводили обратно-траскриптазную ПЦР.
Обратно-транскриптазная ПЦР
Праймеры, которые использовали в данном исследовании, были предназначены для гена vacA (NAYAK & ROSE, J Appl Microbiol, 103, 1931-41, 2007). Они назывались HpylF (5′ CAA TAG CAA TCA AGT GGC TTT G 3′, SEQ ID NO: 5) и HpylR (5′ GCG CGC TTC CAC ATT AGC 3′; SEQ ID NO: 6). Их специфичность заранее проверяли in silico с помощью онлайн-инструмента BLAST и in vitro с помощью кПЦР со штаммами вида H. pylori, разными пробиотическими штаммами и E. coli OP50, которые использовали для кормления C. elegans (см. предыдущий обзор по оптимизации). Использовали мастер-микс "SYBR® Green PCR Master Mix" (Applied Biosystems) и термоциклер StepOne Real-Time (Applied Biosystems). Ниже в Таблице 2 указаны оптимальные условия для проведения кПЦР для H. pylori.
Для построения стандартной кривой ДНК проводили качественный анализ ДНК H. pylori с помощью спектрофотометрии (A260). Число соответствующих геномов рассчитывали следующим способом:
- Число геномов = ДНК (г) × НК/мм
- Размер генома H. pylori = 1,6 м.п.н.
- НК = 6,023×1023
- Число геномов = ДНК (г) × 6,023 × 1023/1,6 × 106 × 2 × 309
Стандартную кривую строили с использованием четырех десятикратных разведений ДНК.
Результаты, полученные со штаммом I-4431, который выращивали на среде MRS или на среде MRS + глицерин, показаны на Фиг. 2. Эти результаты демонстрируют то, что штамм CNCM I-4431 снижает количество H. pylori NCTC 111637Т в C. elegans. Уменьшение инфекции более значительно в том случае, когда штамм I-4431 выращивали на среде MRS + глицерин, что указывает на то, что, по меньшей мере, часть противоинфекционного воздействия является результатом выработки реутерина.


Группа изобретений относится к реутерин-вырабатывающему штамму Lactobacillus brevis и его использованию. Предложен способный накапливать реутерин штамм Lactobacillus brevis CNCM I-4431. Реутерин получают путем культивирования указанного штамма в присутствии глицерина и его выделения. Культуру или нейтрализованную суспензию указанного штамма используют в составе композиции молочного продукта для ингибирования роста Helicobacter pylori. Предложенные штамм в качестве лекарственного средства и композиция могут быть использованы для лечения или предотвращения инфекции H. pylori. Группа изобретений обеспечивает ингибирование роста H. pylori. 6 н. и 2 з.п. ф-лы, 2 ил., 2 табл., 3 пр.
1. Реутерин-накапливающий штамм Lactobacillus brevis, представляющий собой штамм Lactobacillus brevis CNCM I-4431.
2. Применение штамма Lactobacillus brevis по п.1 для выработки реутерина.
3. Композиция молочного продукта для ингибирования роста Helicobacter pylori, содержащая культуру штамма Lactobacillus по п.1 или нейтрализованную суспензию штамма Lactobacillus по п.1.
4. Композиция по п.3, которая характеризуется тем, что содержит по меньшей мере 105 КОЕ, предпочтительно по меньшей мере 106 КОЕ указанного штамма Lactobacillus brevis на грамм сухого веса.
5. Композиция по любому из пп.3 или 4, которая характеризуется тем, что является питательной композицией.
6. Применение штамма Lactobacillus brevis по п.1 в качестве лекарственного средства для лечения или предотвращения инфекции H. pylori.
7. Применение композиции по любому из пп.3-5 для лечения или предотвращения инфекции H. pylori.
8. Способ получения реутерина, включающий стадии:
- культивирования штамма Lactobacillus brevis по п.1 в присутствии глицерина и
- выделение реутерина, выработанного культурой.
| BAUER R | |||
| ET AL | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| // Int J Food Microbiol | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| WO 1988008452 A1, 03.11.1988 | |||
| EP 698347 B1, 12.07.2006 | |||
| ШЕНДЕРОВ Б.А | |||
| Медицинская микробная экология и | |||
Авторы
Даты
2016-03-20—Публикация
2011-11-30—Подача