ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к контролируемой активации системы продуцирования реутерина Lactobacillus reuteri путем добавления глицерина и других веществ при получении клеточных культур и сохранения полученного реутерина в бактериальной клетке во время накопления и хранения. В частности, настоящее изобретение относится к получению больших количеств L.reuteri, нагруженных реутерином, и применению таких нагруженных бактерий для таких целей, как профилактика и лечение заболеваний, в качестве пищевой добавки и т.п.
УРОВЕНЬ ТЕХНИКИ
Обычно клетки прокариот относят к примитивным, хотя некоторые из них содержат необычные оболочки, известные как микрококомпартменты (MCS), которые, как оказалось, представляют собой примитивные органеллы внутри бактериальных клеток. Карбоксисома (которая участвует в фиксации диоксида углерода) в течение почти 30 лет была единственным признанным микрокомпартментом в микробных клетках.
В 2005 профессор Todd O. Yeates и его коллеги открыли первые структурные свойства микрококомпартментов бактерий. При получении первых структур с высоким разрешением бактериальных белков микрококомпартментов были выявлены правила сборки, весьма сходные с таковыми у некоторых вирусов. Шесть идентичных белковых подгрупп объединяются в гексамерную единицу, которая представляет собой элементарное звено при формировании оболочки. Эти гексамерные единицы тесно упакованы друг с другом, образуя молекулярный слой, содержащий только крошечные поры. Такая плотная упаковка, по-видимому, ограничивает перемещение молекул внутрь и наружу микрококомпартментов, за исключением пор.
Кластерный анализ гомологичных веществ микробных микрококомпартментов - специфичных белков, показал, что такие оболочки участвуют не менее чем в семи различных метаболических процессах у бактерий различных видов (Thomas A. Bobik. 2007. Bacterial Microcompartments. Microbe. 1:25-31). Элементарные звенья бактериальных микрококомпартментов состоят исключительно из белков и гликопротеидов. Электронная микроскопия (использованная для исследования микрококомпартментов) показывает отсутствие липидного моно- или би-слоя (как в оболочках эукариот), окружающего такие микрокомпартменты, что делает их единственными известными белковыми метаболическими органеллами в живых клетках. Ряд бактериальных родов, включая Salmonella, Escherichia, Klebsiella, Clostridium, Fusobacterium, Shigella, Listeria и Yersinia, содержат компоненты, необходимые для разложения 1,2-пропандиола (1,2-PD) или этаноламина, в микрокомпартментах (1). Другим свойством микрококомпартментов, как предполагается, является их способность выполнять функции резервуара для токсичных для бактерий субстратов, как в случае c антимикробным реутеринов у L.reuteri.
Поиск в GenBank, проведенный Bobik, по генам оболочки микрококомпартментов показал, что приблизительно 25% (85 из 337) бактериальных геномов содержат гомологичные гены оболочки. У большей части из этих 25% бактериальных геномов, которые несут такие гомологичные гены, гены оболочки формируют кластер с другими генами, кодирующими ферменты, связанные в микрокомпартменты. Это показало, что гены, кодирующие продуцирование реутерина, и гены, кодирующие структуры микрококомпартментов, являются смежными.
В мае 2008 года Sriramulu et al. (Sriramulu DD, Liang M, Hernandez-Romero D, Raux- Deery E, Lunsdorf H, Parsons JB, Warren MJ, Prentice MB: Lactobacillus reuteri DSM 20016 produces cobalamin-dependent diol dehydratase in metabolosomes and metabolizes 1,2-propanediol by disproportionation. J Bacteriol 2008, 190(13):4559-4567) представили первое доказательство того, что продуцирующий антибактериальный агент организм Lactobacillus reuteri имеет возможности для синтеза бактериального микрокомпартмента (карбоксисомы или метаболосомы) при выращивании в модифицированной MRS среде, содержащей 65 мМ 1,2-пропандиола (PD) и малое количество глюкозы. Организм продуцировал кобаламинзависимый фермент диолдегидратазу, индуцированную 1,2-PD. Опероны сопряженного синтеза кобаламина и pdu (утилизация пропандиола) присутствовали в геномной последовательности DSM 20016 L.reuteri, и полный pdu-оперон из лабораторного штамма DSM 20016 L.reuteri был амплифицирован ПЦР, что подтверждает его наличие в пропандиол-метаболизирующем организме. Однако выращивание в модифицированной MRS-среде с 65 мМ 1,2-PD и малым количеством глюкозы, не может использоваться в промышленном масштабе из-за очень низкой скорости роста бактерий в этой среде. В отличие от настоящего изобретения, здесь не раскрывается добавление глицерина во время получения клеточных культур, что обеспечивает нагрузку микрококомпартментов реутерином.
Lactobacillus reuteri представляет собой известную бактерию, продуцирующую антимикробное вещество 3-гидроксипропанальдегид (HPA), также называемый реутерином. Антибактериальная активность реутерина описана, например, в патентах США No 5439678, 5458875, 5534253, 5837238 и 5849289. Реутерин представляет собой низкомолекулярное, нейтральное, водорастворимое соединение, способное ингибировать рост бактерий всех родов и видов, исследованных до настоящего времени, включая: Escherichia, Salmonella, Shigella, Proteus, Pseudomonas, Clostridium, Staphylococcus, Streptococcus и Helicobacter pylori; а также ряда грибов и других микроорганизмов. Используя глицерин в качестве внешнего акцептора электронов, он конвертируется в 1,3-пропандиол, при этом образуется реутерин как интермедиат. Такая реакция проходит совместно с ферментацией сахаров, таких как глюкоза.
Получение реутерина зависит от сложной системы, включающей: фермент глицерин/диол-дегидратазу, катализирующую реакцию; кобаламин (витамин В12), кофактор фермента, который синтезируется сложным путем; факторы, используемые для регенерации фермента; и структур микрококомпартментов, имеющих поперечный размер более чем 100 нм и образованных полипептидами. Все перечисленное закодировано в более чем 50 генах, которые индуцируются в случае, если они необходимы. Добавление 1,2-PD или глицерина в среду для выращивания приводит к созданию большого количества структур микрококомпартментов. Добавление глицерина на более поздней стадии в бактериальную культуру приводит к получению реутерина. Реутерин образуется, накапливается и сохраняется внутри микрококомпартментов, до тех пор, пока они не высвободят вещество. В отсутствие роста и субстрата (включающего глицерин) при нанесении L.reuteri в нормальном состоянии (без полностью нагруженных микрококомпартментов), например, на кожу, высвобождение реутерина обычно не происходит. Таким образом, неожиданным было то, что активированные L.reuteri с реутерином, накопленным в микрокомпартментах, в соответствии с изобретением успешно и быстро высвобождали реутерин в неблагоприятных средах, таких как кожа человека, пищевые продукты или другие подобные места, а также, конечно, в более традиционных местах для пробиотиков, таких как ЖКТ и МВП, рот и нос животных, включая людей.
Рост кожных патогенов, таких как Staphylococcus aureus, Streptococcus pyogenes или Propionibacterium acnes, или некоторых дрожжей может привести к заражению ран и нарушению кожной системы или даже к более серьезным нарушениям кожи или слизистых, таким как экзема, кандидоз, дерматиты, импетиго и т.д. Для лечения этих патогенных агентов известно множество средств. Наиболее традиционными являются антибиотики или химические антибактерильные компоненты. В качестве таковых, например, можно указать композиции на основе альдегидов и их производных.
Другое кожное заболевание, где лечение включает как пероральные, так и местные антибиотики, представляет собой купероз, повреждающий среднюю часть лица, вызывая стойкое покраснение области лица и носа.
Инфекции, вызванные устойчивыми к метициллину Staphylococcus aureus (MRSA) и связанными грамположительными патогенами, являются нарастающей проблемой в медицине. Они включают MRSA, устойчивые к метициллину Staphylococcus epidermidis (MRSE), и устойчивые к метициллину коагулированные отрицательные Staphylococci (MRCNS). Ванкомицин, гликопептидный антибиотик, в настоящее время является средством выбора для борьбы с этими инфекциями. С увеличением использования ванкомицина следует ожидать появления устойчивых к ванкомицину штаммов Staphylococci (VRSA). Таким образом, существует нарастающая потребность в средствах, эффективных против таких патогенов (MRSA/VRSA), но при этом не оказывающих нежелательное побочное действие.
S.aureus обычно колонизируется в ноздрях, хотя дыхательные пути, открытые раны, внутривенные катетеры и мочевые пути также являются потенциальными участками для инфекции. Здоровые индивидуумы могут быть бессимптомными переносчиками MRSA в течение периода от нескольких недель до многих лет.
Другим примером кожного нарушения, трудно поддающегося лечению и которое может быть вызвано широким рядом причин, является контактный дерматит, который у чувствительных субъектов может начаться при контакте кожи с внешним раздражителем/агентом.
Применение Lactobacillus для лечения кожных нарушений уже известно в данной области, например, раскрывается в патентной заявке США No 05/201996. Изобретение относится к области профилактики и/или лечения кожных нарушений при применении препаратов, содержащих пробиотические бактерии, такие как Lactobacillus fermentum штамм VRI-002. Предпочтительным путем введения является пероральный.
Другие бактериальные агенты, такие как Bacillus, также могут быть использованы для кожи или слизистых. Более конкретно, в заявке WO 98/47374 штамм Bacillus использован в композициях, предназначенных для профилактики бактериальных, вирусных или грибковых инфекций кожи.
Однако существует проблема, возникающая при применении молочнокислых бактерий при местном применении или в других неблагоприятных средах с другими бактериями, описанными в уровне техники, которая заключается в коротком сроке жизни бактерий, вызванным неблагоприятной средой на коже или в другом месте. Эта проблема решается настоящим изобретением, посредством введения L.reuteri с нагруженными микрокомпартментами, в режиме “stand by” (ожидания) для секретирования реутерина. Таким образом, L.reuteri осуществляет секрецию реутерина до момента смерти.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение относится к способу контролируемой активации системы продуцирования реутерина L.reuteri путем наполнения системы продуцирования реутерина 1,2 PD или глицерином и затем, при получении клеточных культур, добавления глицерина в культуру бактерий в определенный момент перед накоплением. Данное изобретение также относится к добавлению витамина В12, кобальта и витамина С в среду для выращивания для улучшения условий оптимального роста и формирования микрококомпартментов и реутерина бактериями L.reuteri во время получения.
В частности, это изобретение относится к получению большого количества клеток L.reuteri, которые нагружены реутерином, и применению таких полученных бактерий в композициях, например, для профилактики и лечения заболеваний и в пищевых композициях. Более конкретно, такие композиции предназначены для введения людям, например, местно, для профилактики или лечения нарушений, вызванных патогенами кожной системы. Эти композиции могут также использоваться для назального применения для лечения MRSA. Изобретение преодолевает проблему роста и выживания бактерий L.reuteri в неблагоприятных средах.
Соответственно, перед раскрытием некоторых вариантов выполнения изобретения следует учесть, что изобретение не ограничено в этой заявке до тех деталей конструкции и последовательности компонентов, определенных в нижеследующем описании или показанных на фигурах. Изобретение охватывает и другие варианты выполнения и может быть осуществлено и выполнено различными способами. Кроме того, следует понимать, что фразеология и терминология используется здесь для целей описания и не должна рассматриваться как ограничение.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фиг.1. Показаны гистограммы, иллюстрирующие концентрации реутерина в супернатанте, полученном от штаммов DSM 17938 (незакрашенные прямоугольники) и MM4-1 (черные прямоугольники), выращенных до стационарной фазы в B12-среде в присутствии или отсутствие витамина В12 (наверху) или кобальта (снизу).
Фиг.2. Показаны гистограммы, иллюстрирующие эффекты при концентрациях супернатантов, полученных от штаммов DSM 17938 и MM4-1, выращенных до стационарной фазы в MRS-среде.
Фиг.3a. Показаны гистограммы, иллюстрирующие влияние добавления 1,2-PD на концентрацию реутерина в супернатанте и выживаемость штамма MM4-1, выращенного до стационарной фазы в MRS без добавления кобальта (A, D), витамина В12 (B, E), с добавлением 50 нг/мл кобальта (C, F), 1 мкг/мл витамина В12. Черными прямоугольниками показано отсутствие добавления 1,2-PD. Белыми прямоугольниками показано добавление 65 мМ 1,2-PD. Серыми прямоугольниками показано добавление 200 мМ 1,2-PD. Выживаемость измеряли до начала (0 ч) и после (2 ч) инкубации клеток в 200 мМ глицерин/водный раствор.
Фиг.3b. Показаны гистограммы, иллюстрирующие влияние добавления 1,2-PD на концентрации реутерина в супернатанте и выживаемость штамма DSM 17938, выращенного до стационарной фазы в B12-среде с добавлением 1 мкг/мл витамина В12. Черными прямоугольниками показано отсутствие добавления 1,2-PD. Белыми прямоугольниками показано добавление 65 мМ 1,2-PD. Серыми прямоугольниками показано добавление 200 мМ 1,2-PD. Выживаемость измеряли до начала (0 ч) и после (2 ч) инкубации клеток в 200 мМ глицерин/водный раствор.
Фиг.4. Показано изображение MCS, полученное просвечивающей электронной микроскопией (TEM). Штаммы DSM 17938 (A) и MM4-1A (B) выращивали в MRS. Штаммы DSM 17938 (A) и MM4-1A (B) выращивали в MRS с добавлением витамина В12 (1 мкг/мл) и 200 мМ 1,2-PD. Белые стрелки указывают MCS, образовавшиеся в бактериях.
Фиг.5a. Показаны концентрации реутерина в супернатанте, полученного от клеток MM4-1A, после воздействия 200 мМ глицеринового водного раствора в течение 45 мин. Бактерии выращивали в В12-среде (50 нг/мл кобальт) с добавлением 200 мМ 1,2-PD, 200 мМ глицерина или без добавления этих компонентов.
Фиг.5b. Показаны концентрации реутерина (диаграмма сверху) в супернатанте, полученном от клеток MM4-1, после воздействия 200 мМ глицеринового водного раствора в течение 45 мин. Гистограмма внизу показывает концентрации реутерина в клеточном осадке после воздействия 200 мМ глицеринового водного раствора в течение 45 мин. Бактерии выращивали в MRS (1), в MRS с добавлением 1 мкг/мл витамина В12 (2), в MRS с добавлением 1 мкг/мл витамина В12 и 200 мМ 1,2-PD (3), в MRS с добавлением 1 мкг/мл витамина В12 и 200 мМ глицерина (4) и в MRS с добавлением 1 мкг/мл витамина В12 и 500 мМ глицерина.
Фиг.6. Показан снимок MAS-ЯМР (сверху) обнаруженных веществ, ассоциируемых с клетками MM4-1, после промывки клеток и воздействия 200 мМ глицеринового водного раствора в течение 45 минут. Клетки выращивали в MRS с добавлением 1 мкг/мл витамина В12 и 200 мМ глицерина. Стрелка указывает на альдегидную группу в 3-HPA. На изображениях снизу показаны вещества, ассоциируемые с получением реутерина. Вещества отмеченные звездочкой были обнаружены MAS-ЯМР.
Фиг.7. На гистограмме показано, что наличие сахарозы не влияет на продуцирование реутерина.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Получение культур L.reuteri, которые будут использованы в качестве пробиотиков, проводят без глицерина и затем лиофилизируют. В таких бактериях система, используемая для получения реутерина, не активирована, но в благоприятных условиях система может быть активирована через 30-60 минут после того, как бактерии вступят в контакт с глицерином. В неблагоприятных условиях такая активация может занять намного больше времени или вообще не произойти.
В случаях, когда требуется продукт, содержащий L.reuteri с быстрым продуцированием реутерина, или где условия для роста L.reuteri неблагоприятны, культура L.reuteri может быть улучшена добавлением глицерина во время получения культуры. Глицерин (1-500 мМ) может быть добавлен во время стадии ферментации или он может быть добавлен вместе с криопротекторами после стадии ферментации и промывки, если она требуется, но перед лиофилизацией. Система получения реутерина, включающая формирование микрококомпартментов L.reuteri, может быть улучшена добавлением в систему продуцирования реутерина 1,2 PD или глицерина в начале ферментации.
Продукт клеточной культуры может быть получен несколькими способами, без ограничения включающий три различных варианта, приведенные ниже.
1. Лиофилизированный продукт, содержащий клетки L.reuteri, конвертирующие глицерин в реутерин в конце ферментационной стадии способа получения, но перед стадией лиофилизации. Продукт, полученный таким образом, будет содержать лиофилизированные клетки и реутерин, как внутри, так и вокруг клеток. При таком варианте выполнения способа будут получены бактерии, нагруженные реутерином.
2. Второй вариант аналогичен 1, но к системе продуцирования реутерина бактерий добавляют 1,2 PD или глицерин и, возможно, кобальт или витамин B12 в начале стадии ферментации. В таком варианте выполнения способа будут получены лиофилизированные бактерии, нагруженные реутерином и способные продуцировать и накапливать реутерин.
3. Лиофилизированый продукт, содержащий клетки L.reuteri, конвертирующие глицерин в реутерин после стадии ферментации и промывки, если она требуется, при добавлении глицерина и продуцирующий реутерин в течение приблизительно 30-45 минут при 37°C до стадии лиофилизации. Глицерин для продуцирования реутерина можно, например, добавлять вместе с криопротекторами. Система продуцирования реутерина бактерий заполняется 1,2 PD или глицерином в начале стадии ферментации. Преимущества 3 варианта способа получения по сравнению с 2 заключаются в том, что 3 вариант более удобен для ряда промышленных производственных установок и является более подходящим для контроля образования реутерина.
Добавление 1,2-PD или глицерина в среду для выращивания влияет как на выживание, так и на формирование MCS. Ферментный комплекс PduCDE, отвечающий за конверсию 1,2-PD в пропиональдегид, также отвечает за конверсию глицерина в реутерин, что открывает такую возможность, что MCS, которые образуются при выращивании бактерий в присутствии 1,2-PD, могут также работать как «фабрики» по получению реутерина, при контакте бактерий с глицерином и отсутствии средств для последующего метаболизма реутерина (то есть бактерии находятся в стационарной фазе или подвергаются воздействию глицерина в водном растворе). Реутерин, который образуется в MCS, накапливается в клетках в большем количестве по сравнению с клеткой без MCS. Это позволяет получить "нагруженные" реутерином бактерии, например, до лиофилизации.
Наблюдения Sriramulu et al. для штамма DSM 20016 авторы повторили для штаммов MM4-IA и DSM 17938. Однако выращивание в модифицированной MRS-среде с 65 мМ 1,2-PD и низким количеством глюкозы не подходит для промышленных масштабов из-за очень низкой скорости роста бактерий в этой среде. Вместо этого авторы добавляли 200 мМ 1,2-PD и 1 мкг/мл витамина В12 в немодифицированную MRS-среду и исследовали бактерии на предмет продуцирования видимых MCS после выращивания в течение 24 ч при 37°C (использовали метод электронной микроскопии для визуализации). Как MM4-1A, так и DSM 17938 штаммы продуцировали MCS в этих условиях (Фиг.4).
Глицерин, аналогично 1,2-PD, метаболизируется тем же самым ферментным комплексом, называемым PduCDE, таким образом, также возможно использовать глицерин для индуцирования формирования MCS в бактериях, аналогично к тому, как это наблюдается для 1,2-PD. Рост штамма MM4-1A или в 200 мМ глицерина, или в 1,2-PD приводит к получению клеток, которые ведут себя одинаково при образовании реутерина и его связи с осадком бактериальных клеток, после воздействия в течение 1 ч раствора глицерина на бактерии (Фиг.5a и 5b).
В дополнение к промывке осадка (см. выше, Фиг.5b) авторы также исследовали промытый клеточный осадок на содержание реутерина, используя MAS-ЯМР. Затем штамм MM4-1 выращивали до стационарной фазы в MRS-среде с добавлением B12 (1 мкг/л) и 200 мМ 1,2-PD. Затем выращенные бактерии подвергали воздействию 200 мМ глицерина в водном растворе и инкубировали в течение 1 часа при 37°C. Клетки оставляли на льду и промывали 2 раза дейтериевой водой (D2O), содержащей 200 мМ глицерина. Осадок (приблизительно 20 мкл по массе сырого вещества), полученный на конечной стадии, растворяли в 20 мкл D2O без глицерина и измеряли содержание реутерина методом MAS-ЯМР. Используя эту методику, авторы обнаружили два из трех видов реутерина и некоторые продукты разложения реутерина и 1,2-PD (Фиг.6a и 6b).
Показано, что кроме глицерина и 1,2-PD добавление некоторых других веществ в среду для выращивания может влиять на выживаемость клеток, формирование MCS, продуцирование реутерина и приспособляемость бактерий, такими веществами являются, например, витамин В12, кобальт и витамин С.
Чтобы показать, что добавление витамина В12 или кобальта в среду для выращивания оказывает влияние на приспособляемость L.reuteri, исследовали два различных типа среды для выращивания, MRS (Oxoid) и B12-среду для исследования (Fluka), в отношении продуцирования реутерина и приспособляемости штаммов L.reuteri DSM 17938 и MM4-1 A. Главное отличие между этими двумя средами для выращивания состоит в том, что MRS содержит неопределенный состав витаминов, добавленных в виде дрожжевого экстракта, тогда как B12-среда для исследования (далее называемая B12-среда) содержит определенный состав всех витаминов, необходимых для функционирования бактерий, за исключением B12, который отсутствует. Другое важное отличие в составе витаминов между этими двумя средами, заключается в том, что B12-среда включает витамин С в количестве 4 г/л, возможно, в несколько раз больше, чем в MRS.
Авторы использовали B12-среду как инструмент для наблюдения за реутерином, формированием микрококомпартментов (MCS) и приспособляемостью бактерий при добавлении витамина В12 или кобальта. Витамин В12 является необходимым компонентом ферментного комплекса PduCDE, который отвечает за конверсию глицерина в реутерин. Для реализации своей биологической функции витамину В12 требуется присутствие иона кобальта. Если в среде присутствует кобальт, но отсутствует витамин В12, реутерин может образовываться только в случае, если экспрессированы гены cob-оперона, поскольку они являются основными для образования кобальтсодержащей молекулы B12. Поскольку экспрессия cob-оперона связана с экспрессией расположенного ранее pdu-оперона, вероятно, посредством регулятора PocR (Santos F, Vera JL, van der Heijden R, Valdez G, de Vos WM, Sesma F, Hugenholtz J: The complete coenzyme B 12 biosynthesis gene cluster of Lactobacillus reuteri CRL 1098. Microbiology 2008, 154(Pt 1):81-93; Cheng S, Liu Y, Crowley CS, Yeates TO, Bobik TA: Bacterial microcompartments: their properties and paradoxes. Bioessays 2008, 30(11-12): 1084-1095), авторы исследовали продуцирование реутерина и приспособляемость при добавлении витамина В12 или кобальта в MRS или B12-среду.
Показано значительное влияние на оба штамма (DSM 17938 и MM4-1A) в отношении продуцирования реутерина при выращивании в B12-среде с изменением количества или витамина В12, или кобальта (Фиг.1). Это логично, поскольку продуцирование реутерина не может происходить без воздействия молекул B12, которые или должны быть добавлены непосредственно, или синтезироваться бактериями в присутствии ионов кобальта.
Среда MRS, в отличие от B12-среды, уже содержит некоторое количество витамина В12, поскольку добавленный дрожжевой экстракт содержит смесь витаминов. Измеренное продуцирование реутерина в MM4-1A и DSM 17938, выращенных на простой MRS-среде, совпало с тем, о котором ранее сообщалось в литературе, но при этом у MM4-1 A не было достигнуто такого же уровня продуцирования реутерина, как у штамма DSM 17938 (Фиг.2) (Spinler JK, Taweechotipatr M, Rognerud CL, Ou CN, Tumwasorn S, Versalovic J: Human-derived probiotic Lactobacillus reuteri demonstrate antimicrobial activities targeting diverse enteric bacterial pathogens. Anaerobe 2008, 14(3): 166-171). В отличие от B12-среды, добавление витамина В12 или кобальта в MRS среду не привело к убедительным результатам относительно увеличения продуцирования реутерина MM4-1A и DSM 17938.
Однако при добавлении витамина В12 к MRS-среде проявляется синергетический эффект с 1,2-пропандиолом (1,2-PD) в отношении свойств приспособляемости бактерий MM4-1A (Фиг.3). Усиление приспособляемости штамма MM4-1A, выращенного в MRS с добавлением витаминов В12 и 200 мМ 1,2-PD, коррелирует с уменьшением обнаруженного реутерина в средах, окружающих бактерии (Фиг.3). Авторы указывают, что такой эффект произошел из-за того, что добавление витамина В12 и 1,2-PD к MRS увеличило формирование микрококомпартментов (MCS) в бактериях. Увеличение сформированных MCS привело к тому, что продуцированный реутерин накапливается в образованных MCS, находящихся внутри бактерий.
Для оценки авторы показали, что добавление витамина B12 и 1,2-PD в нормальной MRS:
Создает видимые MCS как в MM4-1A, так и в DSM 17938 (Фиг.4). Увеличение устойчивости к продуцированию реутерина при выращивании MM4-1A в MRS с добавлением витамина В12 (1 мкг/л) и 200 мМ 1,2-PD (Фиг.3). Увеличение устойчивости к продуцированию реутерина при выращивании DSM 17938 в B12-среде с добавлением витамина В12 (1 мкг/л) и 200 мМ 1,2-PD (Фиг.3b).
Авторы также показали, что бактерии MM4-1A, выращенные таким образом (или с добавлением глицерина вместо 1,2-PD), накапливают больше реутерина внутри бактериальной клетки и меньше снаружи (Фиг.5b).
Добавление витамина В12 в MRS с дополнительным 1,2-PD оказывает влияние только на усиление свойств MM4-1 удерживать эндогенно продуцированный реутерин. Насыщение среды для выращивания витамином В12 способствует формированию функционирующих MCS в бактериях при выращивании в присутствии 1,2-PD (Фиг.3 и 3b).
Из полученных L.reuteri, нагруженных активируемыми микрокомпартментами, содержащими реутерин, могут быть приготовлены композиции, обладающие различными формами, как правило, в форме кремов, лосьонов, паст, порошков, капсул, таблеток, мазей, эмульсий, назальных спреев и т.п. Такие препараты могут быть приготовлены известными методами с использованием фармацевтически приемлемых носителей вспомогательных веществ, разбавителей или адъютантов. Такие методики и ингредиенты известны и широко описаны в руководствах и справочниках.
Бактерии по изобретению могут быть использованы для получения композиций, предназначенных, например, для профилактики или лечения нарушений, связанных с патогенами кожной системы, такими как Staphylococcus aureus, Streptococcus pyogenes, Propionibacterium acnes или дрожжи. Такие нарушения кожи могут представлять собой, в частности, акне при атопическом дерматите, кандидозы, импетиго или экзематозную вторичную инфекцию. Нарушения кожи могут также иметь небактериальную причину, например, купероз, псориаз, раны от ожоговых травм, пролежней и других медленно заживающих ран. Бактерии по изобретению могут быть использованы для получения композиции для лечения нарушений, вызванных патогенами кожной системы. В частности, бактерии могут быть использованы для получения композиции для профилактики или лечения MRSA.
Вышеизложенное должно рассматриваться только в качестве иллюстративных основ изобретения. Кроме того, поскольку многочисленные модификации и изменения могут легко быть выполнены специалистом в данной области, то не желательно ограничивать изобретение конкретным выполнением и последовательностью действий, показанными и описанными, и соответственно, все возможные модификации и эквиваленты, подпадающие под объем притязаний, могут быть использованы.
Настоящее изобретение также обеспечивает фармацевтическую композицию, включающую продукт, полученный способом по изобретению, описанным здесь.
ПРИМЕРЫ
ПРИМЕР 1
Получение лиофилизированного порошка L.reuteri с нагруженными микрокомпартментами, содержащими реутерин, активирующимися во время стадии ферментации
Композиция ферментационной среды
Среда центрифугирования
Криопротекторы
Стадии получения лиофилизированного порошка Lactobacillus reuteri.
Двадцать мл среды инокулировали 0,6 мл лиофилизированного порошка Lactobacillus reuteri из рабочей пробирки из банка клеток. Ферментацию проводили в колбе при 37°C в течение 18-20 часов без перемешивания или контроля pH, то есть статически.
Две колбы, каждую с 1 литром среды, инокулировали 9 мл клеточной суспензией на литр. Ферментацию выполняли при 37°C в течение 20-22 часов без перемешивания или контроля pH, то есть статически.
Двумя литровыми клеточными суспензиями со стадии 2 инокулировали 600-литровую емкость. Ферментацию выполняли при 37°C в течение 13 часов при контроле pH и перемешивании. В начале ферментации pH составлял 6,5. Контроль pH начинали, когда pH опускалось ниже 5,4, используя 20% раствор гидроксида натрия. Доводили pH до 5,5.
Четвертую и последнюю стадию ферментации выполняли в 15000-литровой емкости инокуляцией продукта со стадии 3. Ферментацию выполняли при 37°C в течение 9-12 часов с контролем pH и перемешиванием. В начале ферментации pH составлял 6,5. Контроль pH начинали, когда pH опускалось ниже 5,4, используя 20% раствор гидроксида натрия. Доводили pH до 5,5. 100 мМ глицерина добавляли на последней фазе ферментации, непосредственно перед тем, как культура достигнет стационарной фазы. Ферментацию завершали после достижения стационарной фазы культуры, что заметно по уменьшению добавляемого раствора гидроксида натрия. Примерно 930 литров раствора гидроксида натрия было добавлено к 10200 литрам среды и 600 литрам инокулята во время ферментации.
Суспензию клеток с последней стадии ферментации отделяли дважды при 10°C в непрерывной центрифуге от Alfa Laval. После первого центрифугирования объем клеточной суспензии сократился примерно с 11730 литров до 1200 литров. Этот объем промывали 1200 литрами раствора пептона (Пептон 0-24, Orthana) в 3000-литровой емкости и снова разделяли перед смешиванием с криопротекторами. Стадию промывки пептоном выполняли, чтобы предотвратить снижение температуры до точки замерзания при лиофилизации.
После второго центрифугирования объем клеточной суспензии сократился до 495 литров. Этот объем смешивали с 156 кг раствора криопротектора, получая примерно 650 литров клеточной суспензии.
Клеточную суспензию перекачивали в 1000-литровую емкость. Затем емкость перемещали на установку для лиофилизации.
На установке для лиофилизации наливали на каждую пластину для лиофилизации по 2 литра (точно) клеточной суспензии. Максимальная емкость лиофилизатора составляет 600 литров и остатки клеточной суспензии выбрасывали.
Клеточную суспензию Lactobacillus reuteri лиофилизировали в течение четырех-пяти дней и содержание сухого вещества составило 18%.
Во время процесса лиофилизации рабочее давление составляло между 0,176 мбар и 0,42 мбар. Вакуумный насос запускался, когда давление достигало 0,42 мбар. PRT (исследование на герметичность) использовали для определения окончания процесса. Если PRT или увеличение давления составляло менее 0,02 мбар через 120 с, то процесс останавливали.
ПРИМЕР 2
Получение лиофилизированного порошка L.reuteri, с нагруженными микрокомпартментами, содержащими реутерин, наполняемых и активируемых во время стадии ферментации
Способ получения такой же, как описано примере 1, но с добавлением дополнительных 200 мМ 1,2-PD, витамина С (4 г/л) и витамина В12 (1 мкг/мл) в среду для выращивания.
ПРИМЕР 3
Получение лиофилизированного порошка L.reuteri, с нагруженными микрокомпартментами, содержащими реутерин, наполняемых во время стадии ферментации, и активируемых для формирования реутерина перед стадией лиофилизации
Способ получения такой же, как описано примере 1, но с добавлением дополнительных 200 мМ 1,2-PD, витамина С (4 г/л) и витамина В12 (1 мкг/мл) в среду для выращивания. Но 100 мМ глицерина добавляют в клеточную суспензию перед транспортировкой на установку лиофилизации вместо ферментационной фазы.
ПРИМЕР 4
Получение мази с L.reuteri, с активируемой системой продуцирования реутерина
Мазь готовили из следующих компонентов:
Лиофилизированный порошок L.reuteri, с активируемой системой продуцирования реутерина, полученный, например, любым из промышленных способов, описанных выше.
Вспомогательные вещества для продукта (безводное масло стабилизированное твердым жиром или воском). Масло предпочтительно представляет собой растительное масло, например рапсовое или пальмовое масло.
Твердый жир, например пчелиный воск.
Консерванты и стабилизаторы, любые известные в области мазей.
Способ включает плавление твердых компонентов и смешивание с маслом (AkomedPv, AAK) и другими ингредиентами. Лиофилизированный порошок L.reuteri добавляли в смесь при температуре ниже 55°C. Мазь получали при перемешивании смеси до затвердевания.
Тюбики заполняли мазью и закупоривали. Приготовленная мазь содержит приблизительно 10E+08 КОЕ полученной культуры L.reuteri на грамм мази.
ПРИМЕР 5
Лечение купероза человека
Женщину с длительной историей купероза обрабатывали лиофилизированными культурами L.reuteri, полученными в соответствии настоящим изобретением. Субъект обрабатывали два раза в день, утром и на ночь. Каждый раз мазь втирали в кожу, нанося тонким слоем.
После 2 недель купероз заметно улучшился без приема антибиотиков, которые были прописаны для лечения состояния. При отмене лечения L.reuteri состояние возвращалось, но было подавлено при постоянном применение L.reuteri.
ПРИМЕР 6
Получение назального спрея
Назальный препарат, включающий L.reuteri, нагруженные структурами микрококомпартментов, которые готовы к продуцированию реутерина, может быть выполнен в различных формах для введения, например, в форме спрея, капель, геля, мази, крема, порошка или суспензии, используя диспенсер или другое устройство, если необходимо. Различные диспенсеры и средства доставки известны в данной области, включая однодозовые ампулы, распылители, небулайзеры, насосы, назальные пластыри, назальные спонжи, назальные капсулы и т.п.
В общем случае препарат может иметь твердую, полутвердую или жидкую форму. В случае твердой формы компоненты могут быть соединены вместе в блендере, в барабанной мешалке, путем лиофилизации, выпаривания растворителя, совместным размолом, сушкой распылением и другими методами, известными в данной области.
Полутвердые препараты, подходящие для назального применения, могут иметь форму геля на масляной основе или мази.
В предпочтительном варианте выполнения назальный препарат имеет жидкую форму, которая может включать масляный раствор, масляную суспензию. Жидкий препарат может вводиться в форме назального спрея или назальных капель, используя устройства, известные в данной области, включая небулайзеры, которые могут доставлять выбранные объемы препаратов в виде аэрозолей жидких капель. Например, коммерческий распылительный насос с подаваемым объемом 50 мкл или 100 мкл доступен, например, от Valois (Congers, N.Y.), со взрослыми и детскими распылительными наконечниками.
Жидкий препарат может быть получен известными методами. Например, назальный препарат может быть получен путем смешивания L.reuteri, нагруженных реутерином, с маслосодержащим основанием, таким как фармацевтически приемлемое масло, такое как оливковое масло, ланолин, силиконовое масло, глицериновые жирные кислоты и т.п.
Должно быть понятно, что вспомогательные вещества, необходимые для получения препарата, стабильности и/или биодоступности, могут быть включены в препарат. Типичные вспомогательные вещества включают сахара (глюкоза, сорбит, маннит, сахароза), усилители проникновения (хитозан), загустители и агенты, улучшающие стабильность (целлюлоза, поливинилпирролидон, крахмал, и т.д.), буферы, консерванты и/или кислоты и основания для регулирования pH и т.п.
Хотя изобретение было описано со ссылками на конкретные примеры, специалисту в данной области должно быть понятно, что изобретение может быть осуществлено в различных формах.
Группа изобретений относится к области медицины и предназначена для получения клеток культур Lactobacillus reuteri, содержащих реутерин, сохраняемый внутри клеток. Способ включает ферментацию указанных клеточных культур, добавление 1,2-пропандиола или глицерина к реутерин-продуцирующим системам клеток Lactobacillus reuteri в начале ферментации, добавление глицерина к клеточным культурам Lactobacillus reuteri во время получения и сохранение клеток Lactobacillus reuteri. Продукт, полученный заявленным способом, содержит сохраненные клетки Lactobacillus reuteri, при этом реутерин сохраняется в клетках. Заявленная группа изобретений позволяет получить большие количества Lactobacillus reuteri, нагруженных реутерином, которые могут быть использованы для целей профилактики и лечения заболеваний, в качестве пищевой добавки. 2 н. и 7 з.п. ф-лы, 9 ил., 6 пр.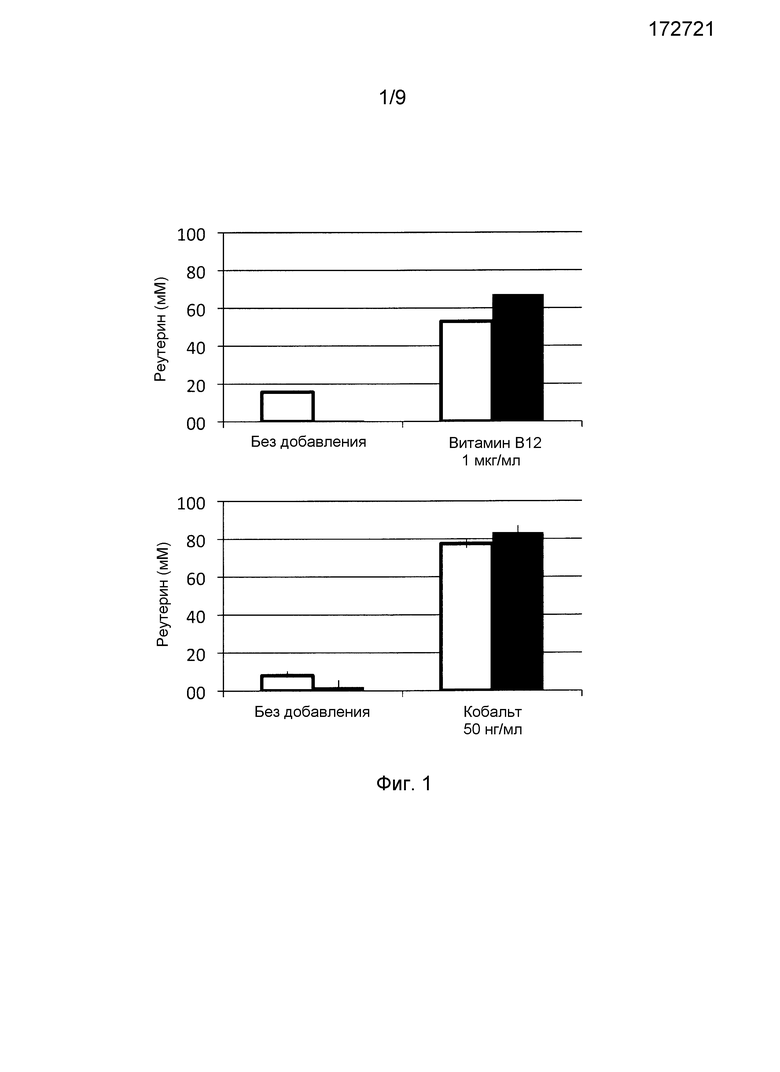
1. Способ получения клеток культур Lactobacillus reuteri, содержащих реутерин, сохраняемый внутри клеток, включающий:
получение клеточных культур Lactobacillus reuteri, где получение включает ферментацию указанных клеточных культур;
добавление 1,2-пропандиола или глицерина к реутерин-продуцирующим системам клеток Lactobacillus reuteri в начале ферментации;
добавление глицерина к клеточным культурам Lactobacillus reuteri во время получения, таким образом получая клетки Lactobacillus reuteri, где реутерин сохраняется внутри клеток; и сохранение клеток Lactobacillus reuteri.
2. Способ по п.1, где ферментация включает добавление глицерина в конце процесса ферментации.
3. Способ по п.1, где сохранение клеток Lactobacillus reuteri включает лиофилизацию клеточных культур после ферментации.
4. Способ по п.2, где сохранение клеток Lactobacillus reuteri включает лиофилизацию клеточных культур после ферментации.
5. Способ по п.3, дополнительно включающий добавление по меньшей мере одного криопротектора вместе с глицерином в клеточные культуры после стадии ферментации, до лиофилизации.
6. Способ по п.3, где от приблизительно 1 до приблизительно 500 мМ глицерина добавляют после стадии ферментации, но до лиофилизации в процессе получения.
7. Способ по любому из пп.2-6, где ферментация клеточных культур Lactobacillus reuteri включает добавление к клеточным культурам по меньшей мере одного из следующих: кобальта, витамина В12, витамина С или их комбинаций в начале стадии ферментации.
8. Продукт, полученный способом по любому из пп.1-7, где продукт содержит сохраненные клетки Lactobacillus reuteri, при этом реутерин сохраняется в клетках.
9. Продукт по п.8 для применения в лечении нарушений, вызванных патогенами кожной системы.
| HIDETOSHI М | |||
| ЕТ AL | |||
| Comparative genome analysis of Lactobacillus reuteri and Lactobacillus fermentum reveal a genomic island for reuterin and cobalamin production | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| CLEUSIX V | |||
| ЕТ AL | |||
| Glycerol induces reuterin production and decreases | |||
Авторы
Даты
2013-09-20—Публикация
2009-06-10—Подача