Область техники
Настоящее изобретение имеет отношение к офтальмологической эмульсии, содержащей циклоспорин, и конкретнее, к устойчивой офтальмологической эмульсии, не вызывающей раздражение при применении, с размером частиц в эмульсии 100 нм или менее, и способу ее приготовления.
Уровень техники
Офтальмологический препарат, содержащий иммуносупрессорное средство, может включать циклоспорин, сиролимус, такролимус или их производное. В их число наряду с циклоспорином, который, как известно, является эффективным при лечении синдрома сухого глаза (сухой кератит), входит циклоспорин A, циклоспорин B, циклоспорин C и циклоспорин D, однако, лучше всего исследованы циклоспорин A и его производные.
Известно, что циклоспорин имеет очень низкую растворимость в воде приблизительно от 20 до 30 мкг/мл, поэтому трудно изготовить содержащее циклоспорин лекарственное средство, которое растворяется в водной среде, и тем не менее такое лекарственное средство является коммерчески доступным Restasis® (офтальмологическая эмульсия циклоспорина 0,05%).
Эмульсией называется дисперсионная система жидкость-жидкость, в которой, по меньшей мере, одна жидкость диспергируется в другой, несмешивающейся с ней жидкости, причем эмульсия имеет, как правило, распределение частиц по размерам в пределах от 0,1 до нескольких десятков микрометров. Микроэмульсии являются термодинамически неустойчивыми и в конечном итоге разделяются разными путями, например флокуляцией (образованием хлопьев), осаждением осадка, образованием отстоя, Оствальдовским созреванием, слипанием и т.д. В связи с этим, когда размеры частиц дисперсной фазы эмульсии уменьшаются до наноразмеров, в кинетическом аспекте, согласно броуновскому движению между частицами, устойчивость эмульсии может быть значительно увеличена, причем коммерчески доступный Restasis® является наноэмульсией, приготовленной путем уменьшения размера частиц дисперсной фазы до наноразмеров.
В то же время, в процессах приготовления известных наноэмульсий, включая Restasis®, используется гомогенизатор высокого давления, который оказывает на эмульсию большое физическое воздействие, или высокоскоростной перемешивающий или режущий агрегат, такой как микрофлюидизатор. Данный способ приготовления требует крупного обогатительного оборудования, несет высокие затраты и применяет энергию высокого уровня к эмульсии, так что температура в процессе получения эмульсии сильно повышается, что затрудняет использование компонента, чувствительного к нагреванию. В дополнение к этому, полученный описанным выше методом Restasis® имеет неоднородный размер частиц в эмульсии, и поэтому наблюдается более выраженная флокуляция и быстро происходит расслаивание, что дает в результате проблему, связанную с длительным хранением. Кроме того, при использовании гомогенизатора высокого давления, вследствие нестабильности фосфолипидов при высокой температуре (например, отделение масла, расслаивание и т.д.), уменьшается устойчивость к изменению запаха или к высокой температуре, и в частности, поскольку распределение частиц дисперсной фазы является относительно широким, трудно гарантировать качество однородного продукта в каждой партии препарата.
В связи с описанной выше проблемой изобретатели разработали метод приготовления офтальмологической композиции в виде наноэмульсии, имеющей средний размер частиц 200 нм или менее, только при помощи простого смешивания и перемешивания масла и водного компонента в процессе получения эмульсии (Korean Patent No. 1008189). Однако при фактическом использовании открытая композиция вызывала сильное раздражение глаз.
Раскрытие изобретения
Техническая проблема
Настоящее изобретение направлено на обеспечение офтальмологической композиции в виде наноэмульсии, содержащей циклоспорин, которую получают путем простого смешивания циклоспорина с солюбилизатором, которая имеет диаметр частиц 100 нм или менее и длительную физиохимическую устойчивость и не вызывает раздражения глаз при применении.
Однако, технические проблемы, решаемые в настоящем изобретении, не ограничиваются описанными выше, при этом другие неописанные проблемы будут понятны среднему специалисту в данной области техники из следующего описания.
Техническое решение
Один аспект настоящего изобретения предоставляет офтальмологическую композицию в виде наноэмульсии, содержащую циклоспорин в количестве от 0,01 до 1 вес.%; полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло в количестве от 0,5 до 9,79 вес.%; и фосфатный буфер в количестве от 90 до 99,29 вес.%, и поскольку в композиции используется полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло в качестве солюбилизатора циклоспорина, особое масло или эмульгатор не является необходимым в наноэмульсионной офтальмологической композиции, при этом данная композиция может быть получена путем простого смешивания.
В одном типичном варианте осуществления настоящего изобретения наноэмульсия имеет средний размер частиц 100 нм или менее и предпочтительно 50 нм или менее.
В другом типичном варианте осуществления настоящего изобретения циклоспорин представляет собой циклоспорин A.
Офтальмологическая композиция настоящего изобретения может дополнительно включать загуститель. Загуститель, используемый в настоящем изобретении, может представлять собой, без ограничения, по меньшей мере, один, выбранный из группы, состоящей из гиалуроновой кислоты или ее соли, хитозана, гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, поливинилпирролидона, карбоксиметилцеллюлозы, карбомера, глицерина и полиэтиленоксида. Предпочтительно, загуститель является гиалуроновой кислотой или ее солью. Загуститель может содержаться в количестве от 0,1 до 5 вес.% относительно общего веса офтальмологической композиции настоящего изобретения.
В еще одном типичном варианте осуществления настоящего изобретения офтальмологическая композиция настоящего изобретения может дополнительно включать этанол в качестве подрастворителя. Этанол может содержаться в количестве от 0,1 до 3 вес.% относительно общего веса офтальмологической композиции.
В еще одном аспекте настоящее изобретение предоставляет способ приготовления не вызывающей раздражения наноэмульсионной офтальмологической композиции, содержащей циклоспорин, который включает следующие действия: приготовление первого раствора путем растворения циклоспорина A в солюбилизаторе; приготовление второго раствора путем растворения загустителя в фосфатном буфере; смешивание первого раствора со вторым раствором и просто перемешивание полученной смеси без использования высокоскоростного перемешивающего или режущего агрегата.
В качестве солюбилизатора может использоваться полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло, и дополнительно в состав солюбилизатора может быть включен этанол. В дополнение к этому, в качестве загустителя может использоваться глицерин и/или гиалуронат натрия.
Полезные эффекты
Настоящее изобретение может успешно предоставить содержащую циклоспорин наноэмульсионную офтальмологическую композицию, не вызывающую раздражение глаз. Кроме того, офтальмологическая композиция настоящего изобретения может быть приготовлена в виде наноэмульсии с меньшим, чем в обычной офтальмологической эмульсии, диаметром частиц и равномерным распределением частиц, полученным путем простого смешивания циклоспорина с солюбилизатором без использования гомогенизатора высокого давления, при этом композиция имеет повышенную физиохимическую устойчивость, что обеспечивает возможность длительного хранения. В дополнение к этому, поскольку эмульсия содержит частицы небольшого диаметра 100 нм или менее с равномерным распределением, не наблюдается нечеткости зрения или раздражения глаз при применении глазных капель.
Описание чертежей
Фиг. 1 - результат измерения размера частиц наноэмульсии, приготовленной согласно типичному варианту осуществления настоящего изобретения.
Фиг. 2 - результат измерения размера частиц коммерчески доступного препарата Restasis®.
Фиг. 3 - результат испытания раздражающего действия офтальмологической композиции согласно типичному варианту осуществления настоящего изобретения и контрольных глазных капель (контроль).
Фиг. 4 - результат испытания эффективности лекарственного средства в тесте Ширмера на слезоотделение, проведенного в отношении офтальмологической композиции согласно типичному варианту осуществления настоящего изобретения и контрольных глазных капель (контроль 1).
Выполнение изобретения
Изобретатели осуществили настоящее изобретение в результате создания наноэмульсии, приготовленной просто путем смешивания и перемешивания циклоспорина и солюбилизатора, имеющей частицы диаметром 100 нм или менее, обладающей продолжительной физиохимической стабильностью и не вызывающей раздражения.
Циклоспорин-содержащая наноэмульсионная офтальмологическая композиция настоящего изобретения представляет собой офтальмологическую композицию в виде наноэмульсий, содержащую циклоспорин в количестве от 0,01 до 1 вес.% полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло в количестве от 0,5 до 9,79 вес.% и фосфатный буфер в количестве от 90 до 99,29 вес.%, причем в данной композиции полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло используется в качестве солюбилизатора циклоспорина, и таким образом, нет необходимости использовать специальное масло и эмульгатор, такую композицию получают путем простого смешивания.
В качестве активного ингредиента в состав может включаться циклоспорин A, производное циклоспорина A, циклоспорин B, циклоспорин С или циклоспорин D. Предпочтительно, в состав настоящего изобретения включается циклоспорин A.
В качестве солюбилизатора для циклоспорина, активного ингредиента офтальмологической композиции настоящего изобретения, может использоваться полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло.
Касторовое масло или гидрогенизированное касторовое масло обладает способностью хорошо растворять циклоспорин, и в коммерчески доступной офтальмологической композиции Restasis® касторовое масло также используется в качестве солюбилизатора. Однако касторовое масло или гидрогенизированное касторовое масло представляет собой триглицерид, полученный путем связывания рицинолевой кислоты или стеариновой кислоты с глицерином и для того, чтобы диспергировать касторовое масло или гидрогенизированное касторовое масло в воде, требуется эмульгатор. Кроме того, для стабильности масляной фазы, диспергированной в воде, частицы эмульсии должны быть измельчены до единиц величиной несколько сотен нанометров с помощью гомогенизатора высокого давления.
В связи с этим, в настоящем изобретении, в отличие от традиционной наноэмульсионной офтальмологической композиции (поскольку в качестве солюбилизатора циклоспорина вместо касторового масла или гидрогенезированного касторового масла используется полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло, в котором гидрофильная группа, то есть этиленоксид, непосредственно модифицируется до жирной кислоты касторового масла или гидрогенизированного касторового масла) может быть предоставлена содержащая циклоспорин офтальмологическая наноэмульсионная композиция, в которой растворимость циклоспорина сохраняется и циклоспорин легко диспергируется в водном растворе. Другими словами, при использовании полиэтоксилированного касторового масла или полиэтоксилированного гидрогенизированного касторового масла, в отличие от известного уровня техники, добавление специального масла или эмульгатора не требуется, и может быть приготовлена наноэмульсионная композиция, имеющая средний размер частиц 100 нм или менее, что обеспечивает офтальмологическую композицию, не вызывающую раздражение или нечеткость зрения при применении.
В одном типичном варианте осуществления настоящего изобретения офтальмологическая композиция настоящего изобретения может дополнительно включать этанол в качестве подрастворителя циклоспорина.
В другом типичном варианте осуществления настоящего изобретения офтальмологическая композиция настоящего изобретения может дополнительно включать загуститель. Загуститель может содержаться в количестве от 0,5 до 5 вес.% относительно веса всей офтальмологической композиции. Использование загустителя в настоящем изобретении не ограничивается, причем могут использоваться загустители, обычно применяемые в лекарственных средствах или пищевых продуктах. Например, загуститель может представлять собой по меньшей мере один выбранный из группы, состоящей из гиалуроновой кислоты или ее соли, глицерина, хитозана, гидроксипропилметилцеллюлозы (HPMC), гидроксипропилцеллюлозы (HPC), гидроксиэтилцеллюлозы (HEC), поливинилпирролидона (PVP), карбоксиметилцеллюлозы (CMC), карбомера и полиэтиленоксида (PEO).
В дополнение к этому, настоящее изобретение предоставляет способ приготовления содержащей циклоспорин наноэмульсионной офтальмологической композиции, при этом данный способ может включать следующие действия:
приготовление первого раствора путем растворения циклоспорина A в солюбилизаторе;
приготовление второго раствора путем растворения загустителя в фосфатном буфере; и
смешивание и простое перемешивание первого раствора и второго раствора.
В качестве солюбилизатора может использоваться полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло, причем в солюбилизатор может быть дополнительно включен этанол.
Способ настоящего изобретения, при необходимости, может дополнительно включать добавление регулятора pH и/или изотонизирующего средства для контролирования значения pH и осмотического давления в глазных каплях.
Далее для лучшего понимания настоящего изобретения будут предоставлены примеры. Однако следующие примеры предоставляются только с целью упрощения понимания настоящего изобретения, при этом рамки настоящего изобретения не ограничиваются следующими примерами.
Примеры
Пример 1. Приготовление наноэмульсии в зависимости от вида солюбилизатора
Циклоспорин смешивали с соответствующими солюбилизаторами согласно соотношению компонентов 1-A-1-J в таблице 1 (первый раствор). Глицерин и полоксамер 188 смешивали в фосфатном буфере, имеющем значение pH 7,2, в соответствии с каждой композицией, и первый раствор диспергировали в полученном растворе, таким образом получая эмульсию. В качестве изотонизирующего средства использовали NaCl, при этом осмолярность была отрегулирована до значения 300 мОсмоль.

Пример 2. Приготовление эмульсионной композиции в зависимости от изменения соотношения компонентов солюбилизатор/этанол
Композиции 2-A-2-I были приготовлены таким же способом, как и композиция 1-A в примере 1, путем регулирования количеств полиэтоксилированного касторового масла и этанола, как показано в таблице 2.

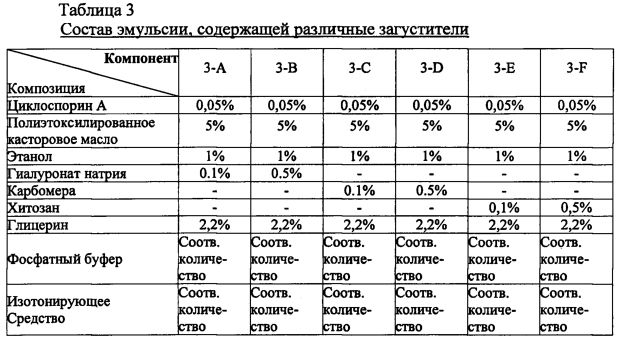
Пример 3. Приготовление эмульсионной композиции, содержащей различные загустители
Композиции 3-A-3-F были приготовлены тем же способом, как и композиция 1-A в примере 1, путем регулирования типа и количества загустителя, как показано в таблице 3.
Пример 4. Приготовление эмульсионной композиции в зависимости от концентрации циклоспорина A
Композиции 4-A-4-E были приготовлены в результате изменения концентрации циклоспорина A, как показано в таблице 4.

Экспериментальный пример 1. Измерение диаметра частиц в эмульсии
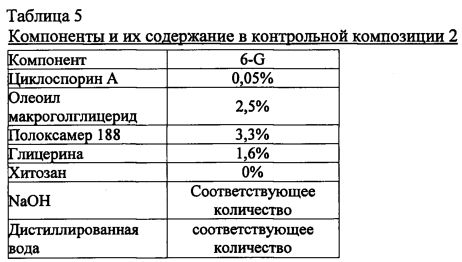
Средний диаметр частиц определяли в эмульсиях, полученных в примерах 1-4, с использованием лазерного анализатора размеров частиц, результаты показаны в таблице 6. В данном случае, коммерчески доступные глазные капли Restasis® 0.05% (произведенные компанией Samil Allergan (Lot No.: 69297)) использовали в качестве контроля (контрольная композиция) 1, а препарат 6-G, раскрытый в качестве примера в Корейском патенте №1008189, использовался как контроль 2.
Как видно из таблицы 6, как и эмульсионный препарат, полученный в примере 1, композиции 1-A-1-B, в которых полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло использовалось в качестве солюбилизатора, могут обеспечить наноэмульсию с диаметром частиц 100 нм или менее без использования отдельного эмульгатора.
В сравнении, композиции 1-C-1-F не образовывали эмульсию без использования эмульгатора, а в композициях 1-G-1-J использовался эмульгатор, в связи с этим наблюдались частицы с очень большим средним диаметром, составляющим несколько микрометров.
В то же время видно, что все композиции 2-A-4-E согласно настоящему изобретению предоставляют наноэмульсии с диаметром частиц 100 нм или менее, и имеют меньший диаметр частиц, чем контроль 1, приготовленный с помощью гомогенизатора с высоким давлением.
В дополнение к этому, как показано на фиг. 1, композиция 2-C настоящего изобретения имела частицы небольшого размера 17,4 нм и даже единообразное распределение частиц, однако, как показано на фиг. 2, в контроле 1 средний размер частиц составлял 328,4 нм и наблюдалось увеличенное распределение частиц, так как небольшие частицы были агломерированы.
В общем, исходя из закона Стокса относительно стабильности эмульсии, по мере уменьшения размера частиц эмульсии вероятность выпадения осадка может уменьшаться.
Исходя из этого результата, поскольку композиция настоящего изобретения включает циклоспорин в виде тонкодисперсных частиц в форме растворенного в воде липида и является однородной, данная композиция потенциально может использоваться в качестве глазных капель, не вызывающих раздражения.

Экспериментальный пример 2. Исследование стабильности эмульсий настоящего изобретения
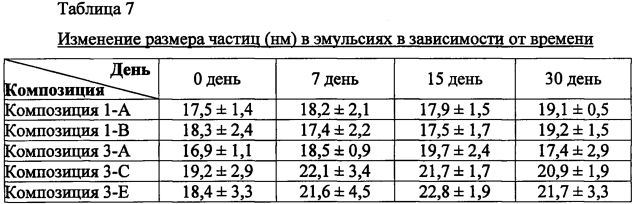
Изменение размера частиц и значения pH композиций 1-A, 1-B, 3-A, 3-C и 3-E настоящего изобретения в зависимости от времени изучали при комнатной температуре, результаты показаны в таблицах 7 и 8. Как видно из таблиц 7 и 8, в композициях настоящего изобретения не наблюдалось значительного изменения размеров частиц и значений pH в эмульсиях с течением времени.
Результаты означают, что композиции настоящего изобретения могут храниться в течение длительного времени в силу того, что они являются физиохимически устойчивыми.

Экспериментальный пример 3. Оценка прозрачности глазных капель
Прозрачность офтальмологических композиций 4-C-4-E, приготовленных в соответствии с настоящим изобретением, и контроля 1 (Restasis®) предварительно была оценена в тесте на прозрачность in vitro.
В частности, для оценки прозрачности невооруженным глазом использовали 2 мл каждой из офтальмологических композиций, добавляя физиологический раствор (0.9% NaCl) вместо слез. Результаты показаны в таблице 9.

Как показано в таблице 9, в случае обычного коммерчески доступного продукта, Restasis®, чтобы он мог стать прозрачным из непрозрачного, при закапывании в глаза, требуется количество физиологического раствора приблизительно в 25 раз больше объема глазных капель (50 мл на 2 мл глазных капель). То есть, когда 0,4 мл обычного продукта закапывают в глаза, можно ожидать, что зрение станет отчетливым после того, как глазные капли разбавятся потоком 10 мл слезной жидкости.
Однако видно, что офтальмологические композиции 4-C-4-E согласно настоящему изобретению были прозрачны с самого начала и сохранили свою прозрачность, поэтому они не оказывали нежелательного действия, такого как нечеткость зрения.
Экспериментальный пример 4. Испытание на раздражающее действие глазных капель
Испытание на раздражающее действие, то есть перекрестный тест 3×3 был проведен на трех группах субъектов по четыре субъекта в группе, как показано в таблице 10. Испытание проводилось в три периода. После применения композиции 2-C, контроля 1 и контроля 2 согласно настоящему изобретению раздражение у субъектов оценивали в баллах, что показано в таблице 11.
Как показано в таблице 11 и на фиг. 3, композиция 2-C, приготовленная согласно настоящему изобретению, почти не вызывала раздражения, показав отличный эффект, контроль 2 вызывал очень тяжелое раздражение, и контроль 1 вызывал раздражение от слабого до умеренного.



Экспериментальный пример 5. Тест на слезоотделение Ширмера
Для оценки эффективности офтальмологической композиции согласно настоящему изобретению было проведено следующее испытание на кроликах-альбиносах.
А именно, кроликов разделили на 2 группы по шесть особей, и 50 мкл 0,1% раствора сульфата атропина наносили три раза в день (в 9 час утра, 2 часа дня и 7 часов вечера) (закапывание 0,1% раствора сульфата атропина в глаза кролика вызывает временный синдром сухого глаза). Через 5 минут правые глаза животных в каждой группе обрабатывали физиологическим раствором, а левые глаза обрабатывали композицией 2-С согласно настоящему изобретению или Restasis® (смотри таблицу 12).

Тест Ширмера проводили в течение 5 дней, измеряя количество слезной жидкости с помощью индикаторной бумаги в 9 часов вечера после 2, 3, 4 и 5 дней проведения теста. Результаты показаны в Таблице 13.

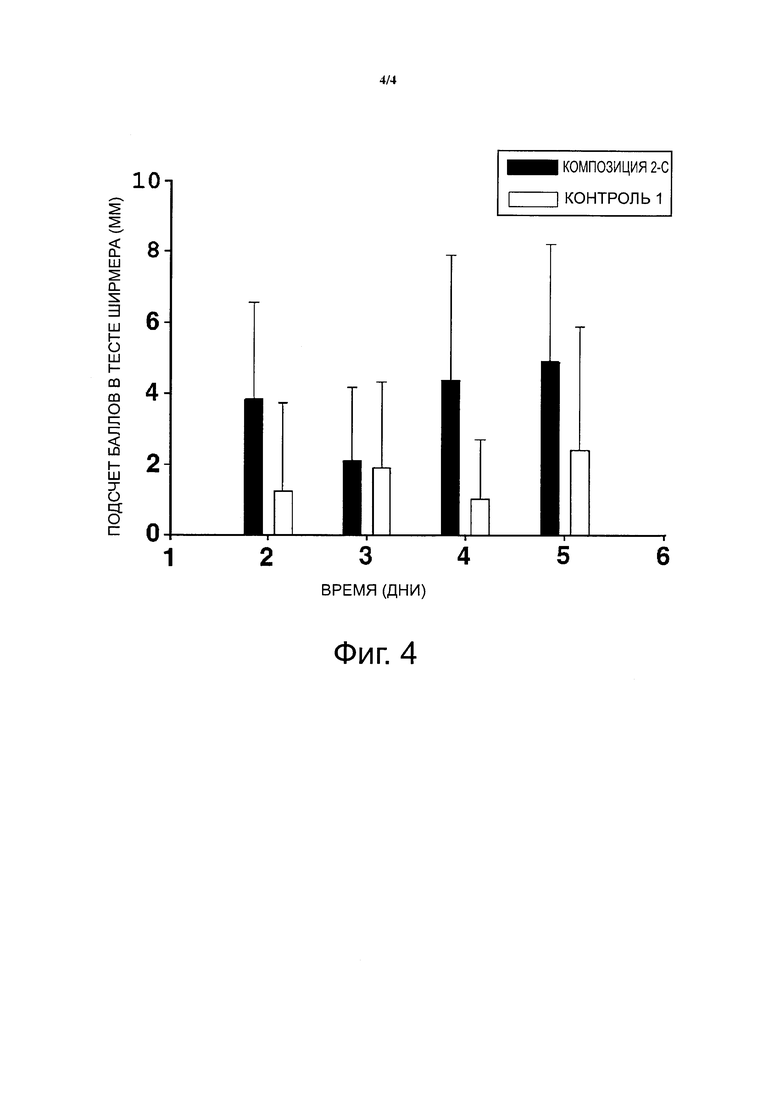
Эффективность офтальмологических композиций настоящего изобретения оценивали по различию количества слезной жидкости между правым глазом (группа с индуцированным синдромом сухого глаза) и левым глазом (группа с индуцированным синдромом сухого глаза, который лечили терапевтическим средством, композицией 2-C или Restasis®) индивидуума, результаты показаны на фиг. 4.
Как можно видеть на фиг. 4, по сравнению с группой, которую лечили контролем 1, в группе, которую лечили композицией 2-С, количество слезной жидкости увеличивалось в 3,1, 1,1, 4,3 и 2,0 раза через 2, 3, 4 и 5 дней проведения теста соответственно.
Результаты означают, что офтальмологическая композиция настоящего изобретения оказывала отличное терапевтическое действие при лечении синдрома «сухого глаза».
Несмотря на то, что изобретение представлено и описано со ссылкой на некоторые типичные варианты его осуществления, специалистам в данной области техники понятно, что могут быть сделаны различные изменения формы и элементов без отступления от существа и объема изобретения, определенного прилагаемой формулой изобретения.
Промышленная применимость
Согласно настоящему изобретению содержащая циклоспорин наноэмульсионная офтальмологическая композиция не вызывает раздражение глаз, например нечеткость зрения, при применении, предоставляет возможность хранения в течение длительного времени благодаря повышенной физиохимической стабильности (так как является стабильной ввиду того, что не используется гомогенизатор высокого давления), так что данная композиция может использоваться в качестве содержащих циклоспорин глазных капель.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОФТАЛЬМИЧЕСКАЯ НАНОЭМУЛЬСИОННАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЦИКЛОСПОРИН, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2014 |
|
RU2683271C2 |
| ОФТАЛЬМОЛОГИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЦИКЛОСПОРИН И ТРЕГАЛОЗУ | 2015 |
|
RU2700927C2 |
| КОМПОЗИЦИЯ КЛОБЕТАЗОЛА В ВИДЕ НАНОЭМУЛЬСИИ МАСЛО В ВОДЕ | 2018 |
|
RU2759901C2 |
| ОФТАЛЬМОЛОГИЧЕСКИЕ КОМПОЗИЦИИ | 2017 |
|
RU2756758C2 |
| ВЗВЕСИ ЦИКЛОСПОРИНА А ФОРМЫ 2 | 2012 |
|
RU2641963C2 |
| ИСКУССТВЕННЫЕ СЛЕЗЫ И ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ | 2010 |
|
RU2589837C2 |
| ВОДНЫЙ ОФТАЛЬМОЛОГИЧЕСКИЙ РАСТВОР НА ОСНОВЕ ЦИКЛОСПОРИНА A | 2013 |
|
RU2634267C2 |
| АНДРОГЕННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОФТАЛЬМОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2012 |
|
RU2599036C2 |
| МИКРОЭМУЛЬСИОННЫЕ КОМПОЗИЦИИ | 2019 |
|
RU2787998C1 |
| ПЭГИЛИРОВАННАЯ ЛИПИДНАЯ НАНОЧАСТИЦА С БИОАКТИВНЫМ ЛИПОФИЛЬНЫМ СОЕДИНЕНИЕМ | 2016 |
|
RU2737893C2 |



Изобретение относится к медицине, а именно к офтальмологии, и предназначено для закапывания в глаз при лечении глазных заболеваний. Офтальмологическая композиция содержит циклоспорин в качестве активного ингредиента, полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло в качестве солюбилизатора циклоспорина и фосфатный буфер. Указанная композиция изготавливается в виде наноэмульсии, имеющей диаметр частиц 100 нм или менее, путем простого смешивания. Использование изобретения обеспечивает композицию, которая не вызывает раздражения глаз, является физиохимически стабильной и может храниться в течение длительного времени. 9 з.п. ф-лы, 13 табл., 4 ил., 9 пр.
1. Наноэмульсионная офтальмологическая композиция, содержащая:
от 0,01 до 1 вес.% циклоспорина;
от 0,5 до 9,79 вес.% полиэтоксилированного касторового масла или полиэтоксилированного гидрогенезированного касторового масла и
от 90 до 99,29 вес.% фосфатного буфера,
отличающаяся тем, что в композиции используется полиэтоксилированное касторовое масло или полиэтоксилированное гидрогенизированное касторовое масло в качестве солюбилизатора циклоспорина, так что особое масло или эмульгатор не требуется, при этом композицию получают путем простого смешивания.
2. Композиция по п. 1, в которой наноэмульсия имеет средний размер частиц 100 нм или менее.
3. Композиция по п. 2, в которой наноэмульсия имеет средний размер частиц 50 нм или менее.
4. Композиция по п. 1, в которой циклоспорин представляет собой циклоспорин A.
5. Композиция по п. 1, дополнительно содержащая загуститель.
6. Композиция по п. 5, в которой загуститель представляет собой по меньшей мере один выбранный из группы, состоящей из гиалуроновой кислоты или ее соли, хитозана, гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, поливинилпирролидона, карбоксиметилцеллюлозы, карбомера, глицерина и полиэтиленоксида.
7. Композиция по п. 6, в которой загуститель является гиалуроновой кислотой или ее солью.
8. Композиция по п. 5, в которой загуститель содержится в количестве от 0,1 до 5 вес.% от всей офтальмологической композиции.
9. Композиция по п. 1, дополнительно содержащая этанол.
10. Композиция по п. 9, в которой этанол содержится в количестве от 0,1 до 3 вес.% от всей офтальмологической композиции.
| KR 100669510 B1, 16.01.2007 | |||
| US 2005196370 A1, 08.09.2005 | |||
| 0 |
|
SU337316A1 | |
| US 2008299206 A1, 04.12.2008 | |||
| ELLIS AG et al | |||
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
| Cancer Chemother Pharmacol., 1996, 38(1), p.81-87. | |||
Авторы
Даты
2016-03-27—Публикация
2013-01-22—Подача