Изобретение относится к средствам, полученным на основе флавоноидов из корней или надземной части Alchemilla vulgaris L. (манжетки обыкновенной), обладающих противовирусной активностью в отношении РНК-геномного вируса (вируса гриппа А) и ДНК-геномных вирусов (ортопоксвирусов: вирусов осповакцины и оспы мышей - эктромелии; и вируса простого герпеса 2-го типа), и может быть использовано в фармацевтике, вирусологии, медицине и ветеринарии.
В настоящее время по своей социальной значимости грипп находится на первом месте среди всех инфекционных болезней человека. Вирус гриппа вызывает ежегодные эпидемии, быстро распространяющиеся из страны в страну, вовлекая в тяжелых случаях (пандемии) значительную часть человеческой популяции земного шара. Наиболее эффективным противоэпидемическим средством против гриппа в настоящее время остается вакцинация, однако вследствие постоянной смены антигенных свойств возбудителя требуется постоянный мониторинг и разработка новых вакцинных штаммов, соответствующих циркулирующим в человеческой популяции в каждый конкретный эпидемический сезон.
Наряду с вакцинацией для предотвращения и лечения гриппа применяются химиопрофилактика и химиотерапия. В настоящее время для этих целей доступен широкий спектр иммуномодулирующих, патогенетических, общеукрепляющих и симптоматических средств и препаратов наряду со средствами специфической противогриппозной терапии. Последние препараты представлены химическими соединениями двух групп, отличающихся по мишеням и механизму действия в жизненном цикле вируса гриппа. Препараты первой группы - римантадин (альфа-метил-1-адамантилметиламина гидрохлорид) и амантадин (1-аминоадамантан) - блокируют белок М2 вируса гриппа, играющий роль ионного канала в вирусной мембране, препятствуя тем самым процессу расщепления гемагглютинина и слияния мембран вируса и лизосомальной вакуоли [Scholtissek C., Quack G., Klenk H.D., Webster R.G. // Antiviral Res. 1998, V. 37, P. 83-95]. Препараты второй группы направлены на ингибирование вирусной нейраминидазы - фермента, необходимого для почкования вирусных частиц. К этой группе соединений относятся озелтамивир ((3R,4R,5S)-этил-4-ацетамидо-5-амино-3-(пентан-3-илокси)циклогекс-1-енкарбоксилат) [Woodhead М., Lavanchy D., Johnston S., Colman P., Fleming D. // Int. J. Clin. Pract. 2000 V. 54(9), P. 604-610], занамивир (5-(ацетиламино)-4-[(аминоиминометил)-амино]-2,6-ангидро-3,4,5-тридезокси-D-глицеро-D-галактонон-2-еноновая кислота) и перамивир ((1S,2S,3S,4R)-3-[(1S)-1-ацетамидо-2-этил-бутил]-4-(диаминометилиденамино)-2-гидрокси-циклопентан-1-карбоновая кислота) [O′Malley Р. // Clin. Nurse Spec. 2010, V. 24(2), Р. 51-53]. Обе группы соединений имеют свои недостатки. В отношении группы производных адамантана можно отметить узкий спектр действия (препараты активны против гриппа A, но не против гриппа B), сравнительно высокую токсичность и быстрое формирование устойчивости штаммов вируса к препаратам. Для ингибиторов нейраминидазы характерны несколько меньшая клиническая эффективность, формирование резистентных вариантов и высокая стоимость синтеза, что делает эти препараты менее доступными для широкого использования. Поэтому поиск наиболее эффективных средств для профилактики и лечения гриппа является чрезвычайно актуальным.
Несмотря на уничтожение вируса натуральной оспы в 1980 г., потенциальная опасность возрождения этой инфекции сохраняется и в наши дни, так как во многих районах Центральной Африки, Южной Америки и Евразии распространены близкие к вирусу натуральной оспы патогенные для человека зоонозные ортопоксвирусы такие, как вирусы осповакцины, оспы коров, оспы буйволов и оспы обезьян, природным резервуаром которых являются разные виды грызунов. Кроме того, у населения отсутствует поствакцинальный иммунитет к вирусу натуральной оспы после прекращения более 30 лет назад вакцинации и производства вакцин по рекомендации ВОЗ, - все это создает риск обострения эпидемической ситуации [Львов Д.К., Зверев В.В, Гинцбург А.Л., Маренникова С.С., Пальцев М.А. Натуральная оспа - дремлющий вулкан // Вопросы вирусологии. - 2008. - №4. - С. 4-8].
В связи с вышеизложенным, а также с тем, что научное сообщество и органы здравоохранения не располагают эффективными адаптированными для массового применения профилактическими и лечебными препаратами против ортопоксвирусов, необходимы исследования по поиску и разработке таких препаратов.
Среди вирусных заболеваний герпетическая инфекция, вызываемая вирусами 1 и 2 типов, занимает одно из лидирующих мест. Так, согласно статистике ВОЗ, в последние годы заражение вирусами простого герпеса (ВПГ) составляет 75,0-95,0% населения Земли, при этом смертность от диссеминированных форм болезни, вызванной ВПГ, составляет 15,8% от всех вирусных заболеваний и занимает 2-е место после показателя смертности от гриппа (35,8%) [Самгин М.А. Простой герпес. Дерматологические аспекты / М.А. Самгин, А.А. Халдин. М.: МЕДпресс информ, 2002. 160 с.]. Герпесвирусная этиология, обусловленная ВПГ-1 и ВПГ-2, прослеживается у 10,0% всех энцефалитов и 20,0% менингоэнцефалитов на территории нашей страны. Летальность при энцефалитах герпетической этиологии составляет 80,0%. В России число госпитализированных больных с диагнозом ВПГ ежегодно превышает 2,5 млн чел, а трудопотери исчисляются более 40 млрд руб. в год. Больные с хроническими поражениями кожных покровов, вызванных вирусами герпеса, а также больные с генитальным герпесом составляют более 10,0% от всего населения России; в 2008 г. заболеваемость составила 18,1 на 100 тыс. населения [Самгин М.А. Простой герпес. Дерматологические аспекты / М.А. Самгин, А.А. Халдин. М.: МЕДпресс информ, 2002. 160 с.].
Для лечения герпетической инфекции используют: химиопрепараты, действующие непосредственно на вирусы; иммуномодуляторы; симптоматические, а также патогенетические средства [Исаков В.А., Архипова Е.И., Исаков Д.В. Герпесвирусные инфекции человека. СПб., 2006; с. 12-150]. Многие из применяемых в настоящее время противогерпетических препаратов имеют ряд существенных недостатков, среди них такие, как низкая биодоступность, высокая нефротоксичность, быстрое развитие устойчивости штаммов ВПГ к препаратам. Все это обусловливает актуальность проблемы создания более эффективных препаратов против герпеса.
Таким образом, одной из главных проблем профилактики и лечения вирусных инфекций является высокая скорость изменчивости многих вирусов, особенно вируса гриппа, что позволяет им, с одной стороны, ускользать от иммунного ответа хозяина, а с другой, - в течение нескольких вирусных поколений вырабатывать устойчивость к противовирусным препаратам. Все вышесказанное свидетельствует о необходимости поиска и разработки эффективных и дешевых противовирусных препаратов возможно более широкого спектра действия.
Предшествующий уровень техники
Известен способ получения суммы флавонолов с адаптогенными свойствами из надземных частей манжетки обыкновенной путем экстракции 96% этиловым спиртом, упаривания экстракта, добавления дистиллированной воды, очистки водного экстракта хлороформом, экстракции очищенного водного остатка этилацетатом, упаривания экстракта и осаждения продукта хлороформом (Патент РФ №2128516 «Способ получения Р-витаминного средства», МПК А61К 35/78, опубл. 10.04.1999).
Однако для полученного таким способом целевого продукта противовирусная активность в отношении РНК- и ДНК-геномных вирусов не исследована и не описана в литературе.
Известно отечественное противовирусное средство гипорамин (Hiporhaminum), получаемое из листьев облепихи крушиновидной - Hippophae rhamnoides L. семейства Лоховые - Elaeagnaceae, представляющее собой сухой очищенный стандартизованный экстракт на основе полифенольного комплекса галлоэллаготаннинов (Вичканова С.А. Изучение листьев облепихи и создание на их основе отечественного противовирусного средства «Гипорамин» // В книге:
«Актуальные проблемы создания новых лекарственных препаратов природного происхождения». V Междунар. съезд. Матер, съезда. - СПб. - 2001. - С. 198-204; Вичканова С.А. «Исследование клинической эффективности гипорамина при вирусных инфекциях у взрослых» // В книге: «Человек и лекарство». - III Рос. нац. конгресс. Тез. докл. - М.: - 1999. - С. 281). Гипорамин обладает выраженной противовирусной активностью в отношении различных штаммов вирусов гриппа А и В, аденовирусов, парамиксовирусов, вирусов простого герпеса, опоясывающего лишая, цитомегаловирусов, респираторно-синцитиального вируса, вирусов иммунодефицита человека (ВИЧ-инфекция).
Однако для гипорамина не показана ингибирующая активность в отношении ортопоксвирусов: вирусов осповакцины и оспы мышей.
Наиболее близким аналогом (прототипом) является новая синергетическая композиция для лечения актуальных вирусных инфекций, включающая водный экстракт из С.sinensis, содержащий 8% дубильных веществ; водный экстракт из Alchemilla vulgaris (манжетка обыкновенная), содержащий 6,5% дубильных веществ; стеарат сорбитана 5,4 г; сквален 2,0 г; октил октаноат 2,0 г; карбомер 0,55 г; пропиленгликоль 0,22 г; стабилизатор на основе парабенов 0,02 г, вода дистиллированная 100 г и другие компоненты. Состав представляет собой косметический крем для профилактики и лечения вируса папилломы, вируса гриппа и герпеса (заявка США №20130028995 А1, 31.01.2013).
Однако синергетическая композиция-прототип содержит несколько водных экстрактов источников танинов (в примере 9, как минимум два - С.Sinensis и Alchemilla vulgaris), вклад каждого из которых в противовирусную активность неизвестен (в заявке не раскрыт), а композиция называется синергетической, т.е. противовирусная активность обусловлена совместным действием обоих водных экстрактов. В этой связи неочевидно, что водный экстракт на основе одной Alchemilla vulgaris (манжетки обыкновенной) будет обладать активностью против вирусов гриппа и герпеса.
Техническим результатом заявляемого изобретения является расширение сырьевой базы и ассортимента противовирусных средств в отношении РНК-содержащего вируса (вируса гриппа А) и ДНК-содержащих вирусов (ортопоксвирусов и вируса простого герпеса 2-го типа).
Указанный технический результат достигается применением суммы флавоноидов из корней или надземной части Alchemilla vulgaris L. (манжетки обыкновенной), полученных путем экстракции корней 50-кратным объемом этилацетата в три приема при нагревании на водяной бане с обратным холодильником по 20 минут, объединения этилацетатного экстракта, концентрирования его упариванием и осаждения концентрата в хлороформе с получением препарата (суммы флавоноидов) или экстракции надземной части манжетки обыкновенной, собранной в начале цветения, 90-96° этиловым спиртом в соотношении 1:10 при комнатной температуре в течение 24 часов с повторением 3-4 раза с последующим объединением и упариванием экстракта, разведения его дистиллированной водой, очистки водного экстракта хлороформом, экстракции очищенного водного остатка этилацетатом, упаривания полученного экстракта и осаждения продукта (суммы флавоноидов) хлороформом в качестве противовирусного средства в отношении РНК-содержащего вируса гриппа А и ДНК-содержащих ортопоксвирусов и вируса простого герпеса 2-го типа.
Указанная сумма флавоноидов, содержащихся в корнях или надземной части манжетки обыкновенной, хорошо растворима в воде.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение суммы флавонолов из надземной части Alchemilla vulgaris L.
К 300 г сырой массы надземной части манжетки обыкновенной, собранной в фазу бутонизации - начала цветения, добавляют 90-96° этиловый спирт (т.к. в сыром материале более 80% воды) в соотношении 1:10, извлечение суммы флавонолов осуществляют при комнатной температуре. При этих условиях оптимальной продолжительностью процесса максимального извлечения суммы флавонолов был период 24 ч, так как увеличение продолжительности процесса до 48 и 72 ч не приводило к статистически достоверному увеличению суммы флавонолов по сравнению с таковой при проведении процесса извлечения в течение 24 ч, а только удлиняло технологический процесс (табл. 1).

Операцию этанольного извлечения повторяют 3-4 раза, объединенный экстракт упаривают в ротационном испарителе под вакуумом до объема, равного массе исходного сырья, после чего добавляют 1/2 часть от массы сырья дистиллированной воды и испаряют до полного испарения этилового спирта. Для очистки от сопутствующих растительных пигментов водный экстракт переносят в делительную воронку и взбалтывают 4-5 раз равными объемами хлороформа до обесцвечивания хлороформенного слоя. Сумму флавонолов из очищенного водного экстракта экстрагируют этилацетатом, взбалтывая в делительной воронке равными объемами этилацетата и экстракта. Эту процедуру повторяют 6 раз. Объединенный этилацетатный экстракт упаривают в ротационном испарителе под вакуумом до 1/2 исходной массы (начало образования осадка). Сгущенный экстракт вливают тонкой струей в шестикратно большее количество хлороформа. Выпавший желтый осадок отфильтровывают на стеклянном фильтре №4, промывают чистыми порциями хлороформа и высушивают в вакуум-сушильном шкафу. Выход целевого продукта 4,5 г, что составляет 1,5%. Содержание флавонолов в осадке 3,2 г, т.е. 71%. Определение качественного состава и количественного содержания проводят методом хроматографии на бумаге, в качестве проявителя используют 10%-ный спиртовый раствор хлористого алюминия. При этом в составе препарата обнаруживается до 4 флавоноловых компонентов.
Пример 2. Получение суммы флаванолов (катехинов и лейкоантоцианов) из корней Alchemilla vulgaris L.
Измельченные и просеянные через сито №1 корни манжетки обыкновенной экстрагируют 50-кратным объемом этилацетата в три приема при нагревании на водяной бане с обратным холодильником по 20 минут. Объединенный этилацетатный экстракт концентрируют на ротационном испарителе в вакууме при температуре не выше 50°C до остатка, превышающего в 3 раза массу сырья. Полученный экстракт вливают тонкой струей при помешивании в 6-кратный объем хлороформа. Выпадает хлопьевидный осадок белого цвета, который отфильтровывают через воронку со стеклянным фильтром №4. Полученный осадок высушивают в вакууме. Выход осадка составляет 5-10% от массы сырья. Количественное содержание определяют спектрофотометрически, при взаимодействии экстракта с 1%-ным раствором ванилина в концентрированной соляной кислоте образуется малиновое окрашивание, плотность раствора определяют на спектрофотометре при длине волны 504 нм. Пересчетный коэффициент рассчитывают по (+)-катехину. Содержание флаванолов в препарате - около 70%.
Пример 3. Характеристика противовирусного средства на основе суммы флавоноидов из Alchemilla vulgaris L.
Новое противовирусное средство представляет собой природную смесь хорошо очищенных и высокоактивных флавоноидных веществ, выделяемых из корней (катехины и лейкоантоцианы) (розоватого цвета) или надземной части (флавонолы) манжетки обыкновенной (Alchemilla vulgaris L.) в виде желтого порошка горьковато-вяжущего вкуса, хорошо растворимого в воде и спирте.
Пример 4. Изучение токсичности препаратов на основе суммы флавоноидов из Alchemilla vulgaris L. на перевиваемых культурах клеток MDCK и Vero
Токсичность препаратов была предварительно изучена в отношении перевиваемых культур клеток MDCK и Vero, полученных из коллекции культур клеток ФБУН ГНЦ ВБ «Вектор». Суспензию с известной концентрацией клеток MDCK или Vero разводили подогретой до температуры 37°C средой RPMI-1640 («Биолот», Санкт-Петербург) или DMEM («Биолот», Санкт-Петербург) соответственно, содержащими 10% сыворотки крови плодов коровы (СКПК) («Gibco», США), до концентрации 1×105 кл./мл и по 100 мкл вносили в лунки 96-луночных планшетов. Планшеты с клетками помещали в термостат на 2-3 сут до образования монослоя при температуре 37°C, 5% CO2 и 100% влажности.
При определении токсических доз для клеток MDCK или Vero препараты разводили в 5, 10, 102, 103, 104, 105, 106 раз средой RPMI-1640 или DMEM соответственно, вносили по 100 мкл/лунку разведений препаратов и ставили в термостат на 2 и 4 соответственно суток при температуре 37°C, 5% CO2 и 100% влажности. Через 2 и 4 сут с помощью инвертированного микроскопа оценивали деструктивные изменения в монослое клеток MDCK или Vero соответственно, инкубированных с разными концентрациями препаратов. В качестве контроля использовали монослои культур клеток MDCK или Vero без препаратов.
Определяли минимально токсическую концентрацию (МТК) и максимально переносимую концентрацию (МПК), равную половине концентрации вещества, не оказывающей на клетки токсического действия, а также для каждого препарата определяли 50%-ную токсическую концентрацию (ТС50), т.е. концентрацию препарата, вызывающую гибель 50% клеток в культуре.
В исследованиях противовирусной активности препаратов использовали МПК или более низкие концентрации [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ / Под ред. Хабриева Р.У. М.: Медицина; 2005; 832].
Как показали исследования токсичности препаратов, полученных из манжетки обыкновенной, препараты №5, №6 и №7 были малотоксичными для перевиваемой культуры клеток MDCK (максимально переносимые концентрации для этих клеток для всех препаратов составили 250 мкг/мл), а для клеток Vero наибольшие токсические свойства из всех препаратов проявил образец №7, полученный из надземной части растения (максимально переносимые концентрации составили 350, 250 и 25 мкг/мл для препаратов №5, №6 и №7 соответственно) (табл. 2).
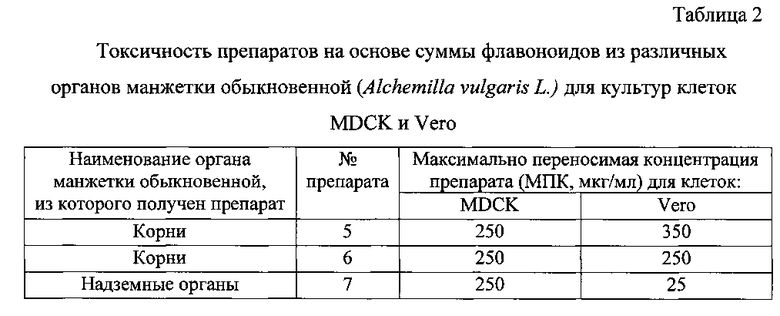
Пример 5. Определение вирулицидной активности средства на основе суммы флавоноидов из Alchemilla vulgaris L. в отношении РНК- и ДНК-геномных вирусов
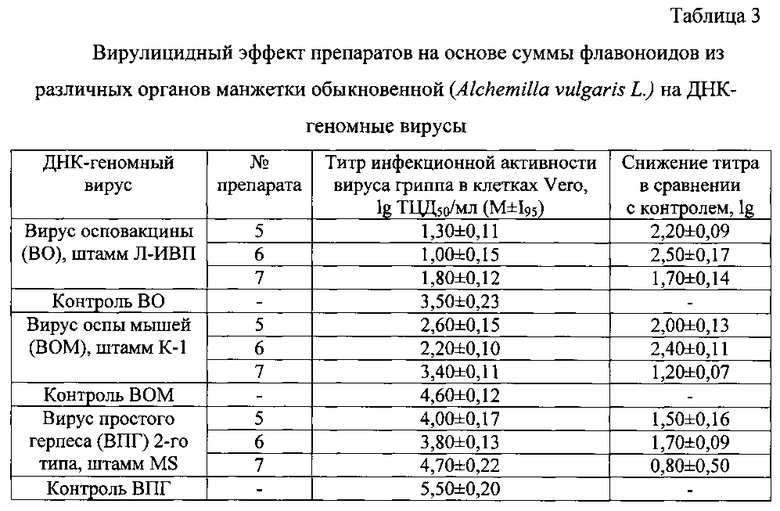
Вирулицидную активность препаратов на основе суммы флавоноидов манжетки обыкновенной исследовали после экспозиции их с вируссодержащим материалом при комнатной температуре в течение 10 минут. Затем титровали инфекционную активность вируса гриппа в каждом варианте опыта в культуре клеток MDCK, а инфекционную активность ДНК-геномных вирусов (вируса осповакцины (ВО), вируса оспы мышей (ВОМ) и вируса простого герпеса (ВПГ)) в культуре клеток Vero. Препарат характеризовался вирулицидной активностью в случае снижения инфекционного титра вируса гриппа для клеток MDCK или титра ДНК-геномных вирусов для клеток Vero после экспозиции в 100 раз и более.
Исследование вирулицидного действия препаратов в отношении ДНК-геномных вирусов показало, что препараты из корней манжетки (№5 и №6) проявляли вирулицидную активность в отношении ортопоксвирусов (снижение инфекционной активности ВО под действием этих препаратов происходит на 2,2 и 2,5 lg, a BOM на 2,0 и 2,4 lg соответственно) и не обнаруживали такого действия в отношении ВПГ 2-го типа, в то время как препарат №7 (из надземных органов растения) вирулицидными свойствами не обладает ни в отношении ортопоксвирусов, ни в отношении вируса герпеса (табл. 3).
Пример 6. Изучение противовирусной активности препаратов на основе суммы флавоноидов из Alchemilla vulgaris L. в отношении РНК- и ДНК-геномных вирусов на перевиваемых культурах клеток
Изучение противовирусной активности препаратов в отношении РНК-геномных вирусов на перевиваемой культуре клеток MDCK.
Культура клеток. Для тестирования противовирусной активности препаратов использовали перевиваемые культуры клеток MDCK и Vero, полученные из коллекции культур клеток ФБУН ГНЦ ВБ «Вектор». По 100 мкл суспензии клеток MDCK в среде RPMI-1640, содержащей 10% сыворотки крови плодов коровы, или суспензии клеток Vero в среде DMEM, содержащей 10% сыворотки крови плодов коровы, вносили в 96-луночные планшеты. Планшеты с клетками MDCK и Vero помещали в термостат при температуре +37°C, 5% СO2 и 100% влажности на 2 и 4 сут соответственно до образования клеточного монослоя.
Определение токсичности препаратов для перевиваемых клеточных культур MDCK и Vero. Для определения токсических концентраций препараты разводили в несколько раз и оценивали наличие токсического действия в монослоях культур клеток MDCK и Vero с помощью инвертированного микроскопа. Для этого препараты растворяли в среде RPMI-1640 или DMEM, содержащей 5% сыворотки крови плодов коровы, делали разведения препаратов в 5 раз, в 10, 100, 1000, 10000, 100000, 1000000 раз средой, вносили по 100 мкл в соответствующие лунки планшета с клетками MDCK и Vero и ставили в термостат при температуре +37°C, 5% CO2 и 100% влажности на 2 и 4 сут соответственно. Через 2 или 4 сут с помощью инвертированного микроскопа оценивали наличие токсического действия в монослое клеток MDCK или Vero, инкубированных с разными концентрациями препаратов из манжетки обыкновенной. В опытах по определению противовирусной активности препаратов на культуре клеток MDCK или Vero использовали предварительно определенные их максимально переносимые концентрации (МПК) для каждой из этих клеточных культур.
Определение противовирусной активности препаратов в отношении вируса гриппа. В работе использовали штамм вируса гриппа птиц A/chicken/Kurgan/05/2005 (H5N1) и штамм вируса гриппа человека A/Aichi/2/68 (H3N2), полученные из Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» (п. Кольцово, Новосибирская обл.).
Наработку вируса гриппа производили на 10-суточных куриных эмбрионах (КЭ), титрование вируса гриппа проводили на культуре клеток MDCK. Концентрация разных субтипов вируса гриппа в вирусаллантоисной жидкости (ВАЖ) составляла от 5,5 до 9,5 lg ТЦД50/мл (десятичных логарифмов 50% тканевых цитопатических доз в мл). В опытах по определению противовирусной активности препаратов из манжетки обыкновенной в отношении вируса гриппа готовили разведения ВАЖ каждого вируса от 1 до 8 с десятикратным шагом с использованием поддерживающей среды RPMI-1640 (ООО «Биолот», Россия), содержащей 2 мкг/мл трипсина ТРСК (Sigma, США).
Для определения противовирусной активности образцов в монослой культуры клеток MDCK вносили по 50 мкл выбранного разведения препарата на поддерживающей среде RPMI-1640, содержащей 2 мкг/мл трипсина, и инкубировали в течение 1 часа при 37°C в атмосфере 5% CO2 в термостате ТС-1/80 СПУ (Россия). Затем в лунки с препаратом добавляли по 50 мкл разведенной поддерживающей средой от 10-1 до 10-8 вирусаллантоисной жидкости (ВАЖ). Клетки инкубировали 2 сут при температуре 37°C в атмосфере 5% CO2. Через 2 сут в каждой лунке с помощью инвертированного микроскопа регистрировали цитопатическое действие (ЦПД) в монослое клеток и определяли наличие вируса в среде культивирования по реакции гемагглютинации (РГА) с 1%-й суспензией эритроцитов кур. За титр вируса в контроле и опыте принимали величину, обратную десятичному логарифму наибольшего разведения исходного вируса, способного вызвать положительную реакцию гемагглютинации в лунке, и выражали в количестве 50% инфекционных доз (ИД50). Титры вируса определяли в lg ТЦД50/мл в контроле (50%-я инфицирующая доза - ИД50 in vitro без препарата) и в опыте (ИД50 in vitro с препаратом). Вирусингибирующее действие исследуемых препаратов оценивали по снижению титра вируса в опыте по сравнению с контролем, для этого высчитывали индекс нейтрализации (ИН) вирусов под влиянием экстракта: ИН = ИД50контроль - ИД50опыт (lg).
На основании полученных данных рассчитывали 50% ингибирующую дозу IC50, т.е. концентрацию препарата, снижающую уровень вирусной репликации вдвое (на 0,3 lg ИД50), и индекс селективности, или химиотерапевтический индекс (SI), представляющий собой отношение ТС50 к IC50.
В качестве контроля использовали следующее.
1. Контроль клеток MDCK, культивируемых в питательной среде RPMI-1640 (ООО «Биолот», С-Петербург), содержащей 2 мкг/мл трипсина ТРСК (Sigma, США).
2. Контроль репродукции штаммов вируса гриппа A/chicken/Kurgan/05/2005 (H5N1) и A/Aichi/2/68 (H3N2) с 1 до 8 разведения с десятикратным шагом без внесения экстрактов.
В процессе исследования ингибирования репродукции вируса гриппа человека A/Aichi/2/68 (H3N2) и вируса гриппа птиц A/chicken/Kurgan/05/2005 (H5N1) препаратами из Alchemilla vulgaris L. и эталонами сравнения (римантадином, тамифлю и рибавирином) по профилактической схеме в монослое клеток MDCK были получены результаты, представленные в таблице 4.
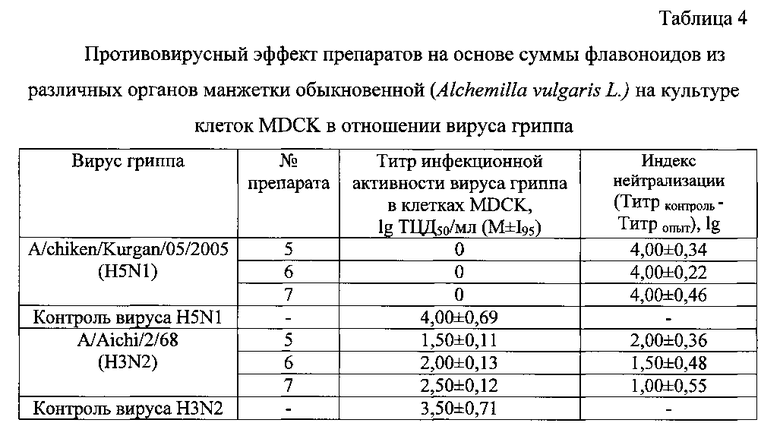
Как видно из таблицы 3, препараты №5 и №6, полученные из корней манжетки обыкновенной, по сравнению с препаратом №7 из надземных органов этого растения в отношении вируса гриппа субтипа H3N2 проявили более выраженный противовирусный эффект (индексы нейтрализации вируса гриппа A/Aichi/2/68 (H3N2) под действием препаратов №5 и №6 составили 2,0 и 1,5 lg соответственно, тогда как под действием препарата №7 - только 1,0 lg). В отношении вируса гриппа птиц A/chicken/Kurgan/05/2005 (H5N1) все исследуемые препараты, полученные из манжетки обыкновенной, обнаружили более выраженную противовирусную активность по сравнению с таковой в отношении вируса гриппа человека субтипа H3N2 (индексы нейтрализации вируса гриппа субтипа H5N1 под действием всех трех препаратов составили 4,0 lg) (табл. 4).
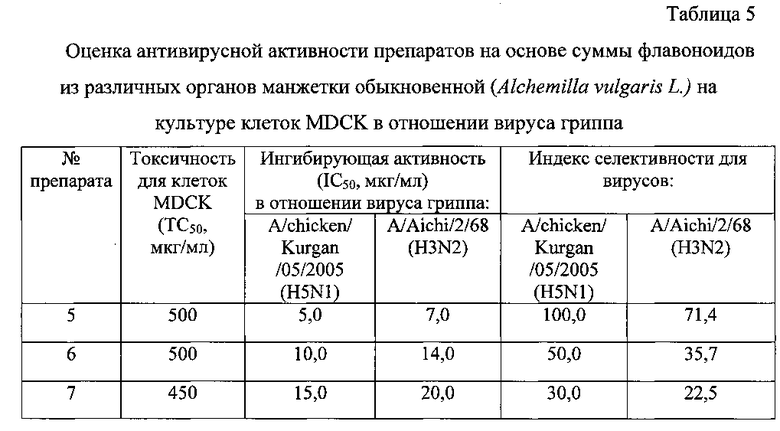
На основании полученных данных были рассчитаны среднетоксические (ТС50) и среднеэффективные вирусингибирующие (IC50) концентрации препаратов из Alchemilla vulgaris L. в отношении используемых штаммов вируса гриппа, снижающие уровень вирусной репликации вдвое (на 0,3 lg ИД50), и индексы селективности, или химиотерапевтические индексы (SI), представляющие собой отношение ТС50 к IC50 (табл. 5).
Представленные в таблице 5 результаты показывают, что препараты №5, №6 и №7, приготовленные из манжетки обыкновенной, подавляют размножение вируса гриппа человека A/Aichi/2/68 (H3N2) в культуре клеток MDCK, при этом среднеэффективные ингибирующие концентрации составляют 7,0, 14,0 и 20,0 мкг/мл, а индексы селективности - 71,4; 35,7 и 22,5 соответственно.
Оценка противовирусной активности этих же препаратов (№5, №6 и №7) по отношению к вирусу гриппа птиц A/chicken/Kurgan/05/2005 (H5N1) показала, что значения среднеэффективных вирусингибирующих концентраций (IC50) для них были ниже по сравнению со значениями данного показателя в отношении вируса гриппа человека и составляли 5,0; 10,0 и 15,0 мкг/мл соответственно, при этом индексы селективности были выше и составляли 100,0; 50,0 и 30,0 соответственно, что говорит о низкой токсичности этих препаратов для эукариотических клеток MDCK.
Таким образом, получены препараты на основе суммы флавоноидов из Alchemilla vulgaris L., обладающие низкой токсичностью и выраженной противовирусной активностью в культуре клеток MDCK. Данные растительные препараты способны ингибировать репликацию вирусов гриппа A/H3N2 и A/H5N1 в концентрациях от нескольких микрограмм до 1,5-2,0-х десятков микрограмм в миллилитре.
Изучение противовирусной активности препаратов в отношении ДНК-геномных вирусов на перевиваемой культуре клеток Vero
Было проведено определение противовирусной активности препаратов в отношении ортопоксвирусов и вируса простого герпеса. В работе использовали штамм Л-ИВП вируса осповакцины (ВО), штамм К-1 вируса оспы мышей (ВОМ) и штамм MS вируса простого герпеса 2-го типа, полученные из Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» (п. Кольцово, Новосибирская обл.).
Наработку и титрование всех ДНК-геномных вирусов проводили на перевиваемой культуре клеток Vero. Концентрация разных вирусов в культуральной вируссодержащей жидкости (КВЖ) составляла от 5,5 до 7,5 lg ТЦД50/мл (десятичных логарифмов 50% тканевых цитопатических доз в мл). В опытах по определению противовирусной активности препаратов из манжетки обыкновенной в отношении ДНК-содержащих вирусов готовили разведения КВЖ каждого вируса от 1 до 8 с десятикратным шагом с использованием поддерживающей среды DMEM (ООО «Биолот», Россия).
Для определения противовирусной активности образцов в монослой культуры клеток Vero вносили по 50 мкл выбранного разведения препарата на поддерживающей среде DMEM и инкубировали в течение 1 часа при 37°C в атмосфере 5% СO2 в термостате ТС-1/80 СПУ (Россия). Затем в лунки с препаратом добавляли по 50 мкл разведенной поддерживающей средой от 10-1 до 10-8 культуральной вируссодержащей жидкости (КВЖ). Клетки инкубировали 4 сут при температуре 37°C в атмосфере 5% CO2. Через 4 сут в каждой лунке с помощью инвертированного микроскопа регистрировали наличие вируса по цитопатическому действию (ЦПД) на монослой клеток. За титр вируса в контроле и опыте принимали величину, обратную десятичному логарифму наибольшего разведения исходного вируса, способного вызвать ЦПД в монослое клеток, и выражали в количестве 50% инфекционных доз (ИД50). Титры вируса определяли в lg ТЦД50/мл в контроле (50%-я инфицирующая доза - ИД50 in vitro без препарата) и в опыте (ИД50 in vitro с препаратом). Вирусингибирующее действие исследуемых препаратов оценивали по снижению титра вируса в опыте по сравнению с контролем, для этого высчитывали индекс нейтрализации (ИН) вирусов под влиянием экстракта: ИН = ИД50контроль - ИД50опыт (lg).
В качестве контроля использовали следующее.
1. Контроль клеток Vero, культивируемых в питательной среде DMEM (ООО «Биолот», С-Петербург).
2. Контроль репродукции вируса простого герпеса 2-го типа, вирусов осповакцины и оспы мышей с 1 до 8 разведения с десятикратным шагом без внесения препаратов.
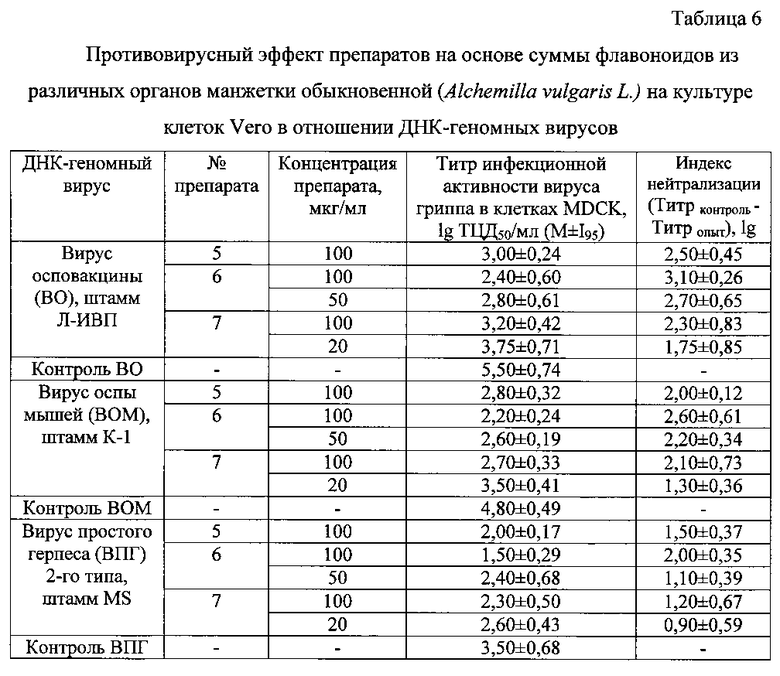
Результаты исследования ингибирования репродукции ДНК-содержащих вирусов в культуре клеток Vero препаратами из Alchemilla vulgaris L. по профилактической схеме представлены в таблице 6.
Как видно из таблицы 6, все препараты, полученные как из корней, так и из надземных органов манжетки обыкновенной, обнаружили противовирусный эффект в отношении используемых в данных экспериментах ДНК-содержащих вирусов. При этом наибольшей антивирусной активностью в отношении этих вирусов обладал препарат №6, полученный из корней растения, в концентрации 100 мкг/мл (индексы нейтрализации вирусов: ВО, ВОМ и ВПГ под действием этого препарата составляли 3,1; 2,6 и 2,0 lg соответственно) (табл. 6).
В целом показано, что полученные препараты на основе суммы флавоноидов из Alchemilla vulgaris L. способны ингибировать репликацию ДНК-геномных вирусов (ортопоксвирусов: вируса осповакцины и вируса оспы мышей, а также вируса простого герпеса 2-го типа) в культуре клеток Vero.
Пример 7. Изучение противовирусной активности препаратов на основе суммы флавоноидов из Alchemilla vulgaris L. в отношении вируса гриппа на модели лабораторных животных
В опытах по изучению протективных свойств препаратов на основе манжетки обыкновенной в отношении вируса гриппа A использовали профилактическую схему: препараты вводили перорально мышам (по 200 мкл/мышь) за час до заражения вирусом гриппа A/Aichi/2/68 (H3N2) или вирусом гриппа A/chicken/Kurgan/05/2005 (H5N1) в дозе 10 ЛД50 (50%-х летальных доз in vivo), далее препараты вводили 1 раз в сутки в течение 5 суток. За животными наблюдали в течение 14 суток. Высчитывали процент выживаемости животных в опыте и контроле и коэффициент защиты (КЗ) мышей. КЗ высчитывали по формуле. % гибели мышей в контроле - % гибели мышей в опыте.
Введение мышам препаратов №5, №6 и №7 до заражения вирусом гриппа A/Aichi/2/68 (H3N2) и после заражения в течение 5 суток вызывало их значительную защиту (выживаемость животных составила 81, 61,0 и 44,0% соответственно). В инфицированной группе сравнения (введение Тамифлю) и контрольной инфицированной группе (введение дистиллированной воды) выжило 100 и 24,1% животных соответственно. Наибольший коэффициент защиты (КЗ), который составлял 56,9%, проявил препарат №5, полученный из корней Alchemilla vulgaris L. (табл. 7).
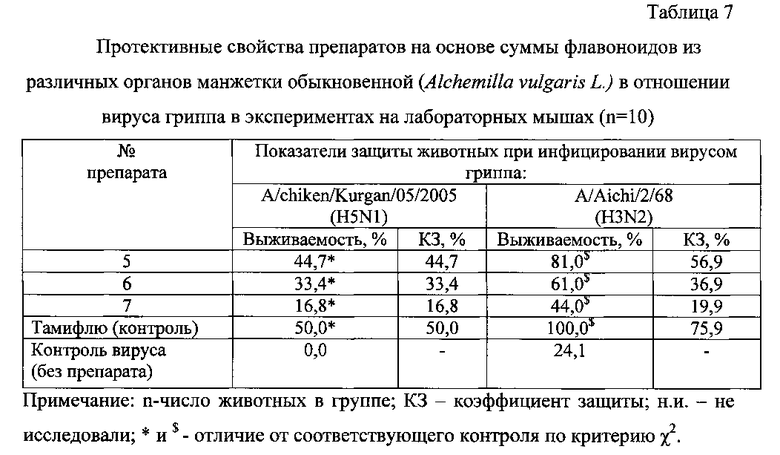
При проведении аналогичных исследований в отношении вируса гриппа птиц A/chicken/Kurgan/05/2005 (H5N1) установлено, что при введении лабораторным мышам препаратов №5, №6, №7 и препарата сравнения Тамифлю процент выживаемости животных составлял 44,7; 33,4, 16,8% и 50,0% соответственно при 100% гибели животных в контроле (введение дистиллированной воды). Наибольший коэффициент защиты (44,7%) в отношении вируса гриппа птиц так же, как и в отношении вируса гриппа человека, обнаружил препарат №5, полученный из корней Alchemilla vulgaris L. (табл. 7).
Таким образом, препараты на основе суммы флавоноидов из манжетки обыкновенной проявляют выраженную противовирусную активность в отношении вируса гриппа в культуре клеток MDCK и в отношении ортопоксвирусов (вируса осповакцины и вируса оспы мышей) и вируса простого герпеса 2-го типа в культуре клеток Vero, а также обнаруживают протективные свойства в модели на лабораторных мышах в отношении вируса гриппа, в связи с чем они могут быть использованы для создания новых эффективных противовирусных препаратов против инфекций, вызванных данными вирусами.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ СУХОГО ЭКСТРАКТА ПЛОДОВОГО ТЕЛА КСИЛОТРОФНОГО БАЗИДИОМИЦЕТА Bjerkandera adusta | 2015 |
|
RU2580296C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ СУХОГО ЭКСТРАКТА ПЛОДОВОГО ТЕЛА БАЗИДИОМИЦЕТА Coprinus comatus | 2015 |
|
RU2584751C1 |
| Способ повышения ингибирующей активности цефтазидима комплексом фенольных соединений | 2024 |
|
RU2839893C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ НУКЛЕАЗЫ БАКТЕРИЙ РОДА SERRATIA | 2014 |
|
RU2580242C2 |
| Штамм бактерий Serratia species, обладающий противовирусной активностью | 2017 |
|
RU2650762C1 |
| Способ получения водного экстракта листьев кипрея узколистного Epilobium angustifolium L., проявляющего ингибирующую активность против коронавируса SARS-CoV-2 и вируса простого герпеса 2-го типа in vitro | 2022 |
|
RU2788172C1 |
| Противовирусное средство на основе экстракта культуры "бородатых корней" ("hairy roots") селитрянки Шобера (Nitraria schoberi L.) | 2016 |
|
RU2615376C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО НА ОСНОВЕ ШТАММА НЕМАТОФАГОВОГО ГРИБА Duddingtonia flagrans F-882 | 2011 |
|
RU2475531C2 |
| Способ получения экстракта из высшего растения Сабельника Залесова (Comarum salesovianum), обладающего противогриппозной активностью | 2024 |
|
RU2838993C1 |
| Способ получения средства с диуретической активностью | 2022 |
|
RU2792378C1 |
Изобретение относится к фармацевтической промышленности, а именно к применению суммы флавоноидов из корней или надземной части Alchemilla vulgaris L. в качестве противовирусного средства в отношении РНК-содержащего вируса гриппа А и ДНК-содержащих ортопоксвирусов и вируса простого герпеса 2-го типа. Применение суммы флавоноидов из корней или надземной части Alchemilla vulgaris L. (манжетки обыкновенной), полученных путем экстракции корней этилацетатом, объединения этилацетатного экстракта, концентрирования его упариванием и осаждения концентрата в хлороформе или экстракции надземной части манжетки обыкновенной, собранной в начале цветения, этиловым спиртом с последующим объединением и упариванием экстракта, разведения его дистиллированной водой, очистки водного экстракта хлороформом, экстракции очищенного водного остатка этилацетатом, упаривания полученного экстракта и осаждения продукта хлороформом при определенных условиях, в качестве противовирусного средства в отношении РНК-содержащего вируса гриппа А и ДНК-содержащих ортопоксвирусов и вируса простого герпеса 2-го типа. Вышеописанная сумма флавоноидов эффективна в качестве противовирусного средства в отношении РНК-содержащего вируса гриппа А и ДНК-содержащих ортопоксвирусов и вируса простого герпеса 2-го типа. 7 табл., 7 пр.
Применение суммы флавоноидов из корней или надземной части Alchemilla vulgaris L. (манжетки обыкновенной), полученных путем экстракции корней 50-кратным объемом этилацетата в три приема при нагревании на водяной бане с обратным холодильником по 20 минут, объединения этилацетатного экстракта, концентрирования его упариванием и осаждения концентрата в хлороформе или экстракции надземной части манжетки обыкновенной, собранной в начале цветения, 90-96° этиловым спиртом в соотношении 1:10 при комнатной температуре в течение 24 часов с повторением 3-4 раза с последующим объединением и упариванием экстракта, разведения его дистиллированной водой, очистки водного экстракта хлороформом, экстракции очищенного водного остатка этилацетатом, упаривания полученного экстракта и осаждения продукта хлороформом, в качестве противовирусного средства в отношении РНК-содержащего вируса гриппа А и ДНК-содержащих ортопоксвирусов и вируса простого герпеса 2-го типа.
| US 20130028995 А1, 31.01.2013 | |||
| WO 2010045969 A1, 29.04.2010 | |||
| СОСТАВ ДЛЯ ЛЕЧЕНИЯ ГРИППА | 1992 |
|
RU2006228C1 |
| Вичканова С.А | |||
| Изучение листьев облепихи и создание на их основе отечественного противовирусного средства "Гипорамин" // В книге: "Актуальные проблемы создания новых лекарственных препаратов природного происхождения" | |||
| V Междунар | |||
| съезд | |||
| Матер | |||
| съезда | |||
| - С.-П | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| - С | |||
| Складная решетчатая мачта | 1919 |
|
SU198A1 |
Авторы
Даты
2016-04-10—Публикация
2015-02-26—Подача