Изобретение относится к области органической химии и медицины, в частности к синтезу новых химических соединений с фармакологической активностью, конкретнее к новому производному 2,6-ди-трет-бутилфенола, обладающему высокой антиоксидантной активностью, низкой токсичностью и выраженным гипогликемическим действием на фоне сахарного диабета. Заявляемое соединение может найти применение в медицине и ветеринарии.
Современная наука насчитывает более 200 заболеваний и патологических состояний, возникновение и развитие которых сопряжено с интенсификацией процессов неферментативного окисления - окислительным стрессом. В число таких патологий входят широко распространенные сердечнососудистые, воспалительные, онкологические и эндокринные заболевания, в частности, сахарный диабет [1. Меньщикова Е.Б., Зенков Н.К., Ланкин В.З., Бондарь И.А., Труфакин В.А. Окислительный стресс: Патологические состояния и заболевания. - Новосибирск: АРТА, 2008. - 284 с.].
Природные и синтетические алкилированные фенолы эффективно нормализуют интенсивность окислительных процессов в живых системах и повышают результативность профилактики и терапии заболеваний, связанных с развитием окислительного стресса [2. Меньщикова Е.Б., Ланкин В.З., Кандалинцева Н.В. Фенольные антиоксиданты в биологии и медицине. - Saarbrücken: LAP LAMBERT, 2012 - 496 с.]. Вместе с тем, в ряду лекарственных препаратов такие антиоксиданты представлены лишь тремя соединениями: 2,6-Ди-трет-бутил-4-метилфенол (ионол, дибунол, (II)) применяется для лечения рака и папилломатоза мочевого пузыря, циститов, ожогов, обморожений, трофических и лучевых язв [3. Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - 1216 с. 721-722].
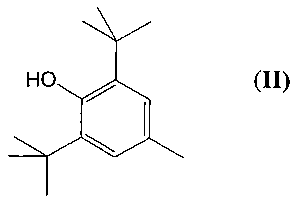
4,4′-(Изопропилидендитио)-бис-(2,6-ди-трет-бутил)фенол (пробукол, (III)) назначается как гиполипидемическое средство при гиперхолестеринемии с риском развития ишемической болезни сердца [3. с. 466].
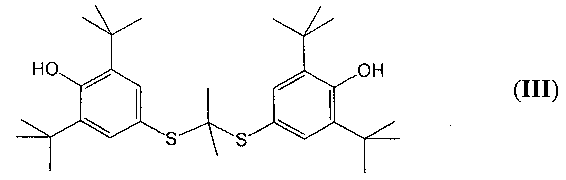
6-Гидрокси-2-метил-2-(4,8,12-триметил-тридецил)хроман(α-токоферол, витамин Е, (IV)):
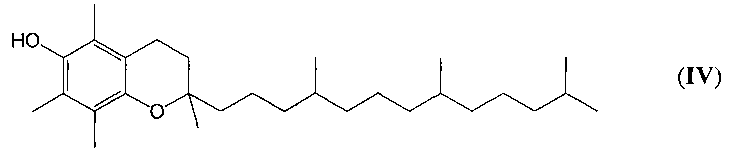
применяют в виде ацетата при мышечных дистрофиях, дерматомиозитах, амиотрофическом боковом склерозе, нарушениях менструального цикла, климаксе, угрозе прерывания беременности, нарушении функции половых желез у мужчин, астеническом и неврастеническом синдромах, склеродермии, системной красной волчанке, ревматоидном артрите, атеросклерозе, а так же при некоторых дерматозах, псориазе, спазмах периферических сосудов. В связи с антиоксидантными свойствами α-токоферола ацетат используется в комплексной терапии глазных болезней, для уменьшения побочных реакций при лечении химиотерапевтическими препаратами и в гериатрической практике. [3. с. 627-628].
Установлено, что указанные антиоксидантные препараты положительно влияют на состояние здоровья экспериментальных животных и пациентов с различными формами сахарного диабета. Так, при моделировании аллоксанового диабета у животных витамин Е стабилизировал мембраны эритроцитов, оказывал гипогликемическое действие, ингибировал процессы перекисного окисления липидов клеточных мембран и гликозирование белков [4. Бобырева Л.Е. Антиоксиданты в комплексной терапии диабетических ангиопатий // Экспер. клин. фармакол. - 1998. - Т. 61, №1. - С. 74-80]. Назначение витамина Е пациентам, страдающим сахарным диабетом I и II типов, приводило к снижению проявлений окислительного стресса [5. Бондарь И.А., Пупышев А.Б., Климонтов В.В. Перекисное окисление липидов и активность лизосомальных ферментов в сыворотке крови при сахарном диабете I типа и их коррекция // Консилиум. - 1999. - №6. - С. 23-26; 6. Wu J.Н., Ward N.С., Indrawan А.P. et al. Effects of α-tocopherol and mixed tocopherol supplementation on markers of oxidative stress and inflammation in type 2 diabetes // Clin. Chem. - 2007. - Vol. 53. - P. 511-519]. В условиях экспериментального аллоксанового диабета у крыс ионол проявлял тенденцию, а пробукол эффективно тормозил развитие гликемии, гиперлипидемии и усиление автоокисления в сосудистой стенке [7. Бобырева Л.Е. Влияние фенольных антиоксидантов на развитие аллоксанового диабета у крыс // Экспер. клин. фармакол. - 1997. - Т. 60, №3. - С. 51-53]. Включение пробукола в комплексную терапию больных сахарным диабетом типа II способствовало существенному снижению проявлений окислительного стресса и позволило стабилизировать состояние компенсации углеводного обмена без увеличения доз сахароснижающих препаратов [8. Недосугова Л.В., Ланкин В.З., Балаболкин М.И., Коновалова Г.Г., Лисина М.О., Антонова К.В., Тихазе А.К., Беленков Ю.Н. Взаимосвязь между компенсацией углеводного обмена и выраженностью проявлений окислительного стресса при сахарном диабете II типа // Бюл. экспер. биол. - 2003. - Т. 138, №8. - С. 152-155].
Широкое распространение сахарного диабета в современном мире (по оценкам ВОЗ 347 миллионов человек в мире больны диабетом [9. Диабет: Информационный бюллетень №312, октябрь 2013 г.// http://www.who.int/mediacentre/factsheets/fs312/ru/], диабет занимает 6 место в ряду ведущих причин смерти [10. 10 ведущих причин смерти в мире: Информационный бюллетень №310, май 2014 г.// http://www.who.int/mediacentre/factsheets/fs310/ru/]) и необходимость использования антиоксидантов в профилактике и терапии данного заболевания при весьма ограниченном их ассортименте обуславливают актуальность создания новых фармацевтических агентов с выраженным антиоксидантным действием.
Изобретение решает задачу разработки нового нетоксичного антиоксиданта, обладающего гипогликемической активностью и расширяющего арсенал антиоксидантных препаратов для использования в комплексной терапии сахарного диабета.
Технический результат достигается предлагаемым новым соединением, а именно, бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)селенидом формулы I:
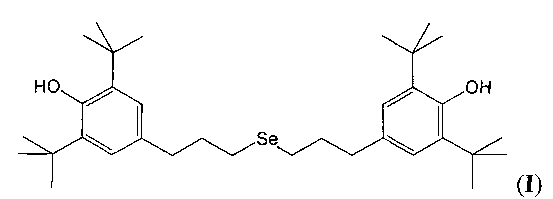
Сущность способа получения заявляемого нового соединения заключается в последовательном превращении 3-(3,5-ди-трет-бутил-4-гидроксифенил)пропилбромида (V) в бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)диселенид (VI) и далее в целевой бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)селенид (I) по следующей схеме:
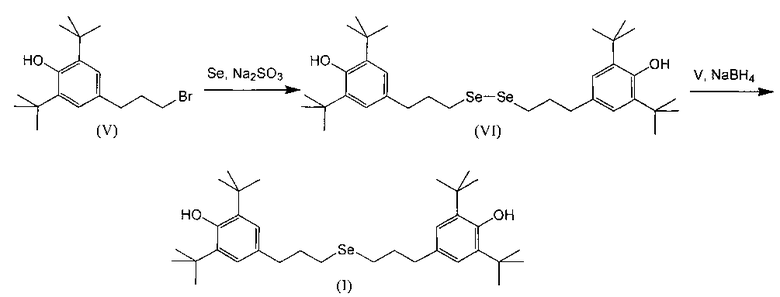
Исходный бромид V получали по ранее описанной методике [11. Пат. РФ 1376511, C07C 39/24, 20.10.1993], способы получения и свойства диселенида VI и селенида I ранее не были описаны. Состав и строение соединений I и VI подтверждены элементным анализом и спектральными данными.
Антиоксидантную активность селенида I тестировали в модельной реакции автоокисления метилолеата (60 С) в сравнении с α-токоферолом. Скорость окисления отслеживали по динамике накопления гидропероксидов, концентрацию которых определяли железороданидным методом по классической методике [12. Лясковская Ю.Н., Пиульская В.И. Методы исследования окислительной порчи жиров. - М.: ГОСИНТИ, 1960. - 50 с.]. Об антиоксидантной активности исследуемых соединений судили по длительности периода индукции автоокисления, за величину которого принимали время достижения пероксидного числа (ПЧ) 0.05% I2 (исходное ПЧ метилолеата составляло 0.003% I2).
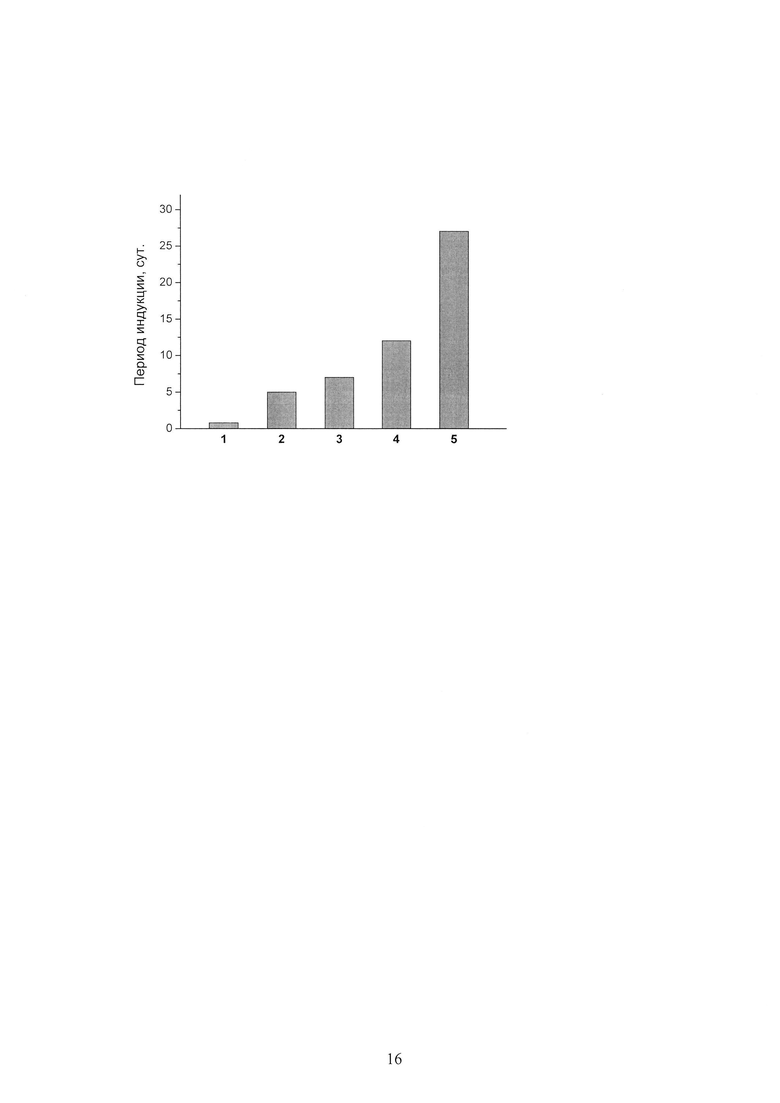
Установлено, что селенид I в диапазоне концентраций 0.25-1.00 мкмоль/г ингибировал автоокисление метилолеата в 1.4-5.4 раза длительнее, чем α-токоферол в концентрации 1.00 мкмоль/г (см. Фиг.). На Фиг. представлены периоды индукции автоокисления метилолеата при 60°C: без ингибитора (1), с добавкой α-токоферола 1 мкмоль/г (2) и селенида I: 0.25 мкмоль/г (3), 0.5 мкмоль/г (4), 1 мкмоль/г (5).
Таким образом, в рассматриваемых условиях селенид I значительно превосходил по противоокислительному действию α-токоферол, который принято считать одним из самых эффективных природных антиоксидантов [2].
Острую токсичность селенида I определяли на белых беспородных мышах массой 20-25 г. при пероральном способе введения [13. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ // Под ред. Р.У. Хабриева - М: ОАО «Издательство «Медицина», 2005. - 832 с.]. Трем группам экспериментальных животных (по 6 особей в каждой) натощак однократно внутрижелудочно вводили масляный раствор селенида I в дозах 150, 500 и 5000 мг/кг (из расчета по 0.2 мл/10 г массы тела). Наблюдение за животными осуществляли в течение 10 дней, за этот период ни одно животное ни в одной группе не погибло (табл. 1). Среднесмертельная доза (ЛД50) селенида I рассчитанная на основе пробит-анализа составила более 5000 мг/кг, по ГОСТ 12.1.007-76 он относится к малоопасным соединениям (IV класс токсичности). Следует отметить, что используемый в медицинской практике ионол (II) относится к умеренно токсичным соединениям: ЛД50 для мышей составляет 2000 мг/кг (III класс токсичности) [14. Пат. РФ 2447888, A61K 31/095, 20.04.2012]. Таким образом, заявляемый селенид I является менее токсичным агентом, чем ионол.
Гипогликемическая активность селенида I была установлена в экспериментах на взрослых самцах крыс линии Wistar. Животные были поделены на четыре группы: первая (9 особей) и вторая (7 особей) группы являлась контрольными, крысам третьей (12 особей) и четвертой (11 особей) групп вводили в межлопаточную область 10% раствор аллоксана из расчета 0.1 мл/100 г массы тела для моделирования сахарного диабета, в то же время животным первой и второй групп вводили физиологический раствор в том же объеме. За неделю до введения аллоксана и на протяжении 1 недели после его инъекции животным 2-й и 4-й групп один раз в сутки перорально вводили селенид I в дозе 100 мг/кг в виде масляного раствора (0.1 мл/100 г массы тела). В течение послеинъекционного периода у всех крыс на 1, 3 и 6 сутки путем надсечки хвоста брали пробы крови (по 0.2 мл), в которых определяли уровень глюкозы пикриновым методом. В конце эксперимента (на 6 сутки) у всех животных под эфирным наркозом забирали образцы тканей печени для определения содержания гликогена методом ШИК-реакции по Мак-Манусу.
Установлено, что у здоровых животных селенид I не оказывает существенного влияния на содержание глюкозы в крови, вместе с тем, на фоне развития аллоксанового диабета достоверно (практически до контрольных значений) снижает ее уровень (таблица 2). У животных 3 группы уровень гликогена в печени был достоверно ниже показателей контрольной группы 1, что, вероятно, обусловлено нарушением синтеза гликогена в результате снижения активности гликогенсинтетазы и ослабления процессов окисления глюкозы вследствие дефекта в пируватдегидрогеназном комплексе [15. Согуйко Ю.Р., Кривко Ю.Я., Крикун Е.Н., Новиков О.О. Морфофункциональная характеристика печени крыс в норме и при сахарном диабете в эксперименте // Современные проблемы науки и образования. - 2013. - №1. - С. 52-59]. В печени обеих групп (2-я и 4-я) животных, получавших селенид I, наблюдалось достоверное увеличение содержания гликогена (таблица 3). Этот результат дает основание полагать, что селенид I активирует синтез гликогена в печени, что может способствовать сохранению углеводного баланса при сахарном диабете. Таким образом, в условиях сахарного диабета селенид I оказывал выраженное гипогликемическое действие, что подтверждает целесообразность его использования в комплексной терапии данной патологии.
Таким образом, новое производное 2,6-ди-трет-бутилфенола - заявляемый бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)селенид I обладает высокой антиоксидантной активностью, низкой токсичностью, выраженным гипогликемическим действием на фоне сахарного диабета, а также способностью активизировать накопление гликогена в печени. Данные свойства заявляемого соединения могут найти применение в медицине, ветеринарии и экспериментальной биологии.
Способ синтеза и свойства соединения I ранее были не известны, в патентной и научной литературе не описаны. Таким образом, предполагаемое техническое решение соответствует критериям патентоспособности изобретения, а именно «новизне», «изобретательскому уровню» и «промышленной применимости».
Сущность изобретения иллюстрируется следующими примерами.
Пример 1. Получение бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)-диселенида (VI) из 3-(3,5-ди-трет-бутил-4-гидроксифенил)пропилбромида (V).
Суспензию селена (0.47 г, 5.95 ммоль) в растворе Na2SO3 (3.02 г, 23.95 ммоль) в 20 мл воды кипятили до полного растворения селена (10 ч). К полученному раствору при 70°C по каплям добавляли раствор (1.75 г, 5.36 ммоль) бромида V в 20 мл этанола, смесь нагревали и кипятили 1 ч. Затем из реакционной массы отгоняли этанол, остаток кипятили еще 3 часа. Далее реакционную массу охлаждали, обрабатывали толуолом (3×10 мл), объединенный экстракт промывали насыщенным раствором NaCl (2×20 мл), сушили Na2SO4, растворитель отгоняли, остаток (1.64 г) кристаллизовали из этанола, получали 1.26 г (72%) диселенида VI в виде светло-желтых игольчатых кристаллов, т.пл. 79.5-81°C.
Найдено (%): С, 62.64; Н, 8.26. C34H54O2Se2. Вычислено (%): С, 62.56; Н, 8.34. УФ-спектр, λmax/нм (lg ε): 277 (3.93). ИК-спектр, ν/см-1: 3646, 2960, 2915, 1435, 1392, 1362, 1316, 1233, 1160, 1121, 1025, 887. Спектр ЯМР 1Н, δ, м.д., J/Гц: 1.42 (с, 36 Н, t-Bu); 2.02 (м, 4 Н, ArCH2CH2); 2.60 (т, 4 Н, ArCH2, J=7.8); 2.91 (т, 4 Н, CH2Se, J=7.8); 4.90 (с, 2 Н, ОН); 6.87 (с, 4 Н, Ar).
Пример 2. Получение бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)-селенида (I).
К раствору бромида V (2.10 г, 6.43 ммоль) и диселенида VI (2.00 г, 3.06 ммоль) в смеси 25 мл этанола (абс.) и 25 мл тетрагидрофурана при комнатной температуре в токе аргона порциями прибавляли NaBH4 (0.46 г, 12.24 ммоль), затем перемешивали 0.5 ч, нагревали и кипятили 3 ч. Далее реакционную массу охлаждали, подкисляли HCl, обрабатывали толуолом (3×20 мл). Объединенный экстракт промывали насыщенным раствором NaCl (3×30 мл), сушили Na2SO4, растворитель отгоняли, остаток (3.53 г) кристаллизовали из гексана, получали 2.91 г (83%) селенида I в виде бесцветных кристаллов, т.пл. 79-80°C.
Найдено (%): С, 71.31; Н, 9.32. C34H54O2Se. Вычислено (%): С, 71.17; Н, 9.49. Спектр УФ, λmax/нм (lg ε): 275 (3.71). ИК-спектр, ν/см-1: 3647, 2959, 1435, 1392, 1362, 1316, 1232, 1160, 1121, 887. Спектр ЯМР 1Н, δ, м.д., J/Гц: 1.43 (с, 36 Н, t-Bu); 1.93 (м, 4 Н, ArCH2CH2); 2.56 (т, 4 Н, ArCH2, J=7.2); 2.60 (т, 4 Н, CH2Se, J=7.2); 4.91 (уш с, 2 Н, ОН); 6.89 (с, 4 Н, Ar). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн (%)): 574 [М]+ (22), 272 (12), 246 (59), 231 (48), 219 (37), 215 (20), 189 (67), 161 (10), 147 (15), 133 (10), 57 (100).
Чистоту полученных образцов контролировали методом ВЭЖХ на приборе «Agilent 1220 Infinity LC» в изократическом режиме, 100% ACN, колонка ZORBAX SB-C18, 5 мкм, 150×4.6 мм, УФ детектор 275 нм. Температуры плавления определяли в капилляре на приборе «МР50 Mettler Toledo», скорость нагрева 0.5°C/мин. УФ спектры записаны в EtOH на спектрометре «Agilent Cary 60 UV-Vis», ИК спектры - в CCl4 на спектрометре «Agilent Cary 600 Series FTIR», спектры ЯМР 1Н - на спектрометре «Bruker DRX600» с рабочей частотой 600 МГц в CDCl3. Масс-спектр получен на хроматографе «Agilent 7890 В» (HP-5MS UI, 30 м × 0.25 мм, газ-носитель -гелий) с масс-детектором «Agilent 5977А» (ЭУ, 70 эВ); в описании масс-спектра приведены пики ионов с интенсивностью ≥10%, включающих наиболее распространенные изотопы.
Пример 3. Изучение антиоксидантной активности селенида I в сравнении с α-токоферолом в модельной реакции автоокисления метилолеата.
Автокисление метилолеата (Acros Organics) проводили на воздухе в условиях термостатирования при 60±0.5°C. В качестве реперного антиоксиданта использовали α-токоферол (Fluka). Масса окисляемой пробы составляла 5 г, концентрация исследуемых соединений: α-токоферола - 1 мкмоль/г, селенида I - 0.25, 0.5 и 1 мкмоль/г. В течение эксперимента из окисляющихся проб отбирали по 0.1 г и определяли содержание пероксидных соединений железороданидным методом [12] с использованием спектрофотометра «Shimadzu UV-1800 UV-Vis». За период индукции принимали время достижения пероксидного числа 0.05% I2. Исходное пероксидное число метилолеата составляло 0.003% I2. Построение и математическую обработку кинетических кривых проводили с использованием программы Origin 6.0. Период индукции неингибированного автоокисления метилолеата составил 19 ч, автоокисления в присутствии 1 мкмоль/г α-токоферола, 0.25, 0.5 и 1 мкмоль/г селенида I - 5, 7, 12 и 27 суток, соответственно.
Пример 4. Изучение острой токсичности селенида I.
Острую токсичность селенида I изучали на беспородных мышах самках массой 20-25 г, содержавшихся в условиях обычного вивария на стандартном корме со свободным доступом к воде. Селенид I вводили экспериментальным животным в виде раствора в подсолнечном масле однократно в дозах 150, 500 и 5000 мг/кг (из расчета по 0.2 мл/10 г массы тела). В каждой группе было по 6 особей. Наблюдения за животными продолжались 10 дней после введения, в течение которых фиксировали количество погибших мышей.
Результаты представлены в таблице 1.
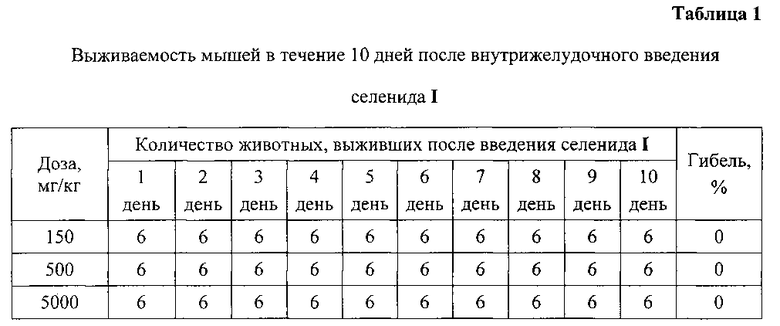
Поскольку в дозе 5000 мг/кг селенид I не вызывает гибели экспериментальных животных по ГОСТ 12.1.007-76 он относится к малоопасным соединениям (IV класс токсичности).
Пример 5. Изучение гипогликемического действия селенида I.
Гипогликемическую активность селенида I изучали в экспериментах на взрослых самцах крыс линии Wistar. Животные были поделены на четыре группы: первая (9 особей) и вторая (7 особей) группы являлась контрольными, крысам третьей (12 особей) и четвертой (11 особей) групп вводили в межлопаточную область 10% раствор аллоксана из расчета 0.1 мл/100 г массы тела для моделирования сахарного диабета, в то же время животным первой и второй групп вводили физиологический раствор в том же объеме. За неделю до введения аллоксана и на протяжении 1 недели после его инъекции животным 2-й и 4-й групп один раз в сутки перорально вводили селенид I в виде раствора в подсолнечном масле по 0.1 мл на 100 г массы тела в дозе 100 мг/кг. Все группы животных находились в стандартных условиях вивария без ограничения потребления воды и пищи.
В течение послеинъекционного периода у всех крыс на 1, 3 и 6 сутки путем надсечки хвоста брали пробы крови (по 0.2 мл), в которых определяли уровень глюкозы пикриновым методом. К 0.1 мл плазмы крови добавляли 0.9 мл дистиллированной воды и 0.5 мл пикриновой кислоты (1.2% р-р), тщательно перемешивали и центрифугировали в течение 15 мин при 3000 об/мин. Затем к 1 мл полученной жидкости приливали 0.2 мл NaOH (20% р-р) и помещали в кипящую водяную баню на 5 мин. После охлаждения растворы фотометрировали при 560 нм на спектрофотоколориметре «Spekol».
В конце эксперимента (на 6 сутки) у всех животных под эфирным наркозом забирали образцы тканей печени для определения содержания гликогена методом ШИК-реакции по Мак-Манусу. Кусочки ткани (50-100 мг) помещали в пробирки с предварительно налитым депротеинизирующим раствором (2 мл) и мелко измельчали. Пробирки закрывали пробками и помещали в кипящую водяную баню на 15 мин. После охлаждения пробы центрифугировали (5 мин при 3000 об/мин), отбирали по 1 мл надосадочной жидкости и добавляли по 3 мл концентрированной серной кислоты. Содержимое пробирок смешивали интенсивным взбалтыванием и нагревали в кипящей водяной бане ровно 6.5 мин. После охлаждения пробы фотометрировали при 520 нм на спектрофотоколориметре «Spekol». Концентрацию гликогена определяли по калибровочной кривой, построенной по стандартным отведениям глюкозы, и пересчитывали в мг/100 г сырой ткани.
Статистический анализ полученных результатов исследования проводили по средним арифметическим (М) и их ошибкам (±m). Различия показателей оценивали методами вариационной статистики по t-критерию Стьюдента для параметрических выборок и считали достоверными при p≤0.05. Расчеты производили по общепринятым формулам с использованием стандартных программ пакета Microsoft Office.
Все эксперименты выполняли в соответствии с Международными рекомендациями по проведению биомедицинских исследований с использованием животных, принятыми Международным советом научных обществ (CIOMS) в 1985 г., со ст. XI Хельсинской декларации Всемирной медицинской ассоциации (1964 г.) и правилами лабораторной практики в РФ (Приказ МЗ РФ от 19.06.2003, №267).
В результате было установлено, что уже на 1-е сутки после инъекции аллоксана содержание глюкозы в крови животных 3-ей группы было достоверно выше, чем в контроле, что свидетельствовало о развитии сахарного диабета у экспериментальных крыс, полученный эффект сохранялся на протяжении всего периода наблюдения (таблица 2).
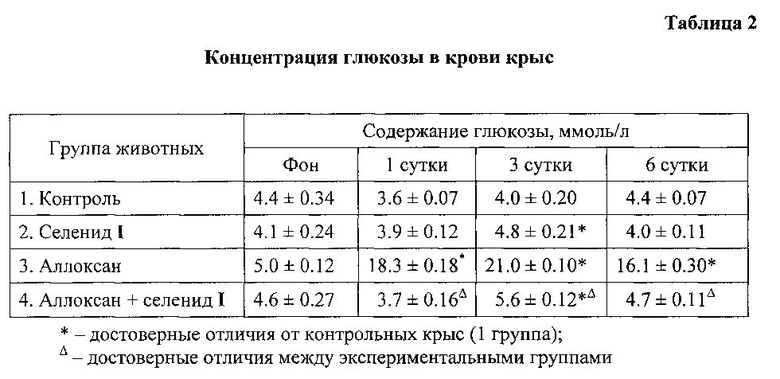
На фоне перорального введения селенида I у крыс 4-ой группы содержание глюкозы в крови было достоверно ниже по сравнению с аналогичными показателями крыс 3-ей группы на протяжении всего исследования. Вместе с тем, во 2-ой группе введение селенида I не вызвало существенных различий показателя от контрольных значений. Как следствие развития аллоксанового диабета уровень гликогена в печени крыс 3-ей группы был достоверно ниже показателей контрольной группы 1 (таблица 3).

Анализируя образцы печени крыс 2-ой и 4-ой групп, получавших селенид I per os, обнаружили достоверное повышение уровня гликогена по сравнению с группами 1 и 3. Таким образом, показано, что селенид I существенно активирует синтез гликогена в печени, что может способствовать сохранению углеводного баланса при сахарном диабете. В целом, полученные результаты свидетельствуют о наличии у селенида I выраженного гипогликемического действия, что может быть использовано в комплексной терапии сахарного диабета.
Таким образом, новое производное 2,6-ди-трет-бутилфенола - заявляемый бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)селенид I обладает высокой антиоксидантной активностью, низкой токсичностью, выраженным гипогликемическим действием на фоне сахарного диабета, а также способностью активизировать накопление гликогена в печени.
Заявляемое новое биологически активное соединение может найти применение в медицине и ветеринарии, в частности, для использования в комплексной терапии сахарного диабета, а также в экспериментальной биологии в качестве антиоксиданта и активатора накопления гликогена.
Источники информации
1. Меньщикова Е.Б., Зенков Н.К., Ланкин В.З., Бондарь И.А., Труфакин В.А. Окислительный стресс: Патологические состояния и заболевания. - Новосибирск: АРТА, 2008. - 284 с.
2. Меньщикова Е.Б., Ланкин В.З., Кандалинцева Н.В. Фенольные антиоксиданты в биологии и медицине. - Saarbrücken: LAP LAMBERT, 2012. - 496 с.
3. Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп.- М.: Новая волна, 2012. - 1216 с.
4. Бобырева Л.Е. Антиоксиданты в комплексной терапии диабетических ангиопатий // Экспер. клин. фармакол. - 1998. - Т. 61, №1. - С. 74-80.
5. Бондарь И.А., Пупышев А.Б., Климонтов В.В. Перекисное оксиление липидов и активность лизосомальных ферментов в сыворотке крови при сахарном диабете I типа и их коррекция // Консилиум. - 1999. - №6. - С. 23-26.
6. Wu J.Н., Ward N.С., Indrawan А.P. et al. Effects of α-tocopherol and mixed tocopherol supplementation on markers of oxidative stress and inflammation in type 2 diabetes // Clin. Chem. - 2007. - Vol. 53. - P. 511-519.
7. Бобырева Л.E. Влияние фенольных антиоксидантов на развитие аллоксанового диабета у крыс // Экспер. клин. фармакол. - 1997. - Т. 60, №3. - С. 51-53.
8. Недосугова Л.В., Ланкин В.З., Балаболкин М.И., Коновалова Г.Г., Лисина М.О., Антонова К.В., Тихазе А.К., Беленков Ю.Н. Взаимосвязь между компенсацией углеводного обмена и выраженностью проявлений окислительного стресса при сахарном диабете II типа // Бюл. экспер. биол. - 2003. - Т. 138, №8. - С. 152-155.
9. Диабет: Информационный бюллетень №312, октябрь 2013 г.// http://www.who.int/mediacentre/factsheets/fs312/ru/.
10. 10 ведущих причин смерти в мире: Информационный бюллетень №310, май 2014 г.// http://www.who.int/mediacentre/factsheets/fs310/ru/.
11. Пат. РФ 1376511, С07С 39/24, 20.10.1993.
12. Лясковская Ю.Н., Пиульская В.И. Методы исследования окислительной порчи жиров. - М.: ГОСИНТИ, 1960. - 50 с.
13. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ // Под ред. Р.У. Хабриева - М.: ОАО «Издательство «Медицина», 2005. - 832 с.
14. Пат. РФ 2447888, A61K 31/095, 20.04.2012.
15. Согуйко Ю.Р., Кривко Ю.Я., Крикун Е.Н., Новиков О.О. Морфофункциональная характеристика печени крыс в норме и при сахарном диабете в эксперименте // Современные проблемы науки и образования. - 2013. - №1. - С. 52-59.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИДИАБЕТИЧЕСКОЕ СРЕДСТВО | 1998 |
|
RU2150952C1 |
| КОМПОЗИЦИЯ ДЛЯ КОРРЕКЦИИ ПАТОЛОГИЧЕСКИХ НАРУШЕНИЙ УГЛЕВОДНОГО, ЛИПИДНОГО ОБМЕНА И АНТИОКСИДАНТНОГО СТАТУСА ОРГАНИЗМА | 2008 |
|
RU2360683C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕФРОАНГИОПАТИИ ПРИ АЛЛОКСАНОВОМ ДИАБЕТЕ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 2008 |
|
RU2372898C1 |
| СРЕДСТВО И СПОСОБ ДЛЯ ПРОФИЛАКТИКИ МЕТАБОЛИЧЕСКИХ НАРУШЕНИЙ КОСТНОЙ ТКАНИ ПРИ ДЛИТЕЛЬНОМ УПОТРЕБЛЕНИИ ГЛЮКОКОРТИКОИДОВ | 2016 |
|
RU2646499C2 |
| N-АЦЕТИЛЦИСТЕИНАТ 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНА, ОБЛАДАЮЩИЙ АНТИОКСИДАНТНЫМИ, ГИПОГЛИКЕМИЧЕСКИМИ, ГИПОЛИПИДЕМИЧЕСКИМИ И ПРОТИВОШОКОВЫМИ СВОЙСТВАМИ | 2006 |
|
RU2357955C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2482868C1 |
| СПОСОБ ДИАГНОСТИКИ И КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ ПРИ СОСУДИСТЫХ ОСЛОЖНЕНИЯХ АЛЛОКСАНОВОГО ДИАБЕТА В ЭКСПЕРИМЕНТЕ | 2010 |
|
RU2455702C1 |
| СБОР, ОБЛАДАЮЩИЙ ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2666398C1 |
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ | 2005 |
|
RU2288258C1 |
| Средство, обладающее гипогликемическим, гиполипидемическим и энергопротективным влиянием | 2016 |
|
RU2630576C1 |
Изобретение относится к селенсодержащему фенольному соединению - бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)селениду формулы:
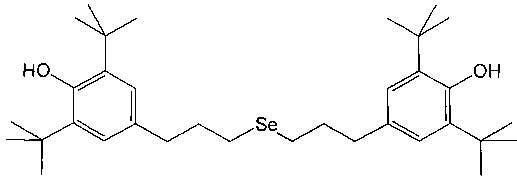 .
.
Заявляемое соединение обладает высокой антиоксидантной активностью, низкой токсичностью и гипогликемическим действием на фоне сахарного диабета, и может найти применение в медицине, ветеринарии и экспериментальной биологии. 1 ил., 3 табл., 5 пр.
Селенсодержащее фенольное соединение - бис-(3-(3,5-ди-трет-бутил-4-гидроксифенил)пропил)селенид формулы:
 , обладающее высокой антиоксидантной активностью, низкой токсичностью и гипогликемическим действием на фоне сахарного диабета для применения в медицине, ветеринарии и экспериментальной биологии.
, обладающее высокой антиоксидантной активностью, низкой токсичностью и гипогликемическим действием на фоне сахарного диабета для применения в медицине, ветеринарии и экспериментальной биологии.
| WO 2012164118 A1, 06.12.2012 | |||
| АНТИОКСИДАНТНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ КАТАРАКТЫ | 2005 |
|
RU2297215C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФУНКЦИОНАЛЬНОГО НАПИТКА АНТИОКСИДАНТНОГО ДЕЙСТВИЯ | 2011 |
|
RU2497415C2 |
Авторы
Даты
2016-06-10—Публикация
2015-04-20—Подача