Изобретение относится к медицине, в частности к офтальмологии, и может быть использовано для лечения эндотелиально-эпителиальной дистрофии (ЭЭД) роговицы.
Эпителиально-эндотелиальная дистрофия роговицы (ЭЭД) является тяжелым, прогрессирующим заболеванием, связанным с декомпенсацией эндотелиального слоя роговой оболочки. После повреждения эндотелия и утраты им функции полупроницаемой мембраны между стромой роговицы и влагой передней камеры постепенно развивается отек стромы роговой оболочки. В дальнейшем влага передней камеры проникает под эпителий роговицы и отслаивает его с развитием рецидивирующих эрозий, вызывающих мучительные для пациента болевые ощущения, светобоязнь и слезотечение.
В настоящее время разработаны различные методы хирургического лечения ЭЭД роговицы: сквозная кератопластика с замещением роговой оболочки аллотрансплантантом (Копаева В.Г. Субтотальная сквозная кератопластика при дистрофии роговой оболочки. Оптикореконструктивные операции и аллопластика в офтальмологии. М., 1974), послойная кератопластика с пересадкой задних слоев роговицы (Волков В.В. К разработке хирургического метода лечения энтотелиально-эпителиальной дистрофии роговицы. Первый съезд офтальмологов Закавказья: Тез. докл. Тбилиси, 1976), интерламеллярная пересадка задней капсулы хрусталика (Авторское свидетельство СССР №810235, кл. A61F 9/007, 1981), послойная кератопластика с использованием желатиновой пленки (Дронов М.М., Каранов К.С., Бобырь А.Б. Способ лечения буллезной кератопатии. - Патент России №2082364, приоритет от 27.06.1997).
Однако перечисленные способы имеют ряд существенных недостатков: техническая сложность операции, высокая частота развития осложнений, вероятность иммунного конфликта с последующим отторжением донорского материала, рецидив заболевания.
Все вышеизложенное послужило основанием для создания нового способа хирургического лечения ЭЭД роговицы путем интрастромальной имплантации полимерных трековых мембран.
Наиболее близким к предлагаемому является способ лечения ЭЭД роговицы, заключающийся в интрастромальной имплантации гидрогелевого диска (Дружинин И.Б. Способ лечения буллезной кератопатии. - Патент России №2405513, приоритет от 13.10.2009).
Согласно этому способу, после обработки операционного поля и местной анестезии, отступив от лимба 1,5-2,0 мм на 12 часах трансконъюнктивально, в направлении глубоких слоев стромы роговицы, формируют тоннель шириной 2,5-3,0 мм и длиной 2,5-3,0 мм, затем расслаивают строму роговицы на глубине 2/3 ее толщины от поверхностных слоев, с последующим формированием интрастромального кармана округлой формы с диаметром 8,5-9,0 мм. Далее, в сформированный интрастромальный карман роговицы имплантируют с помощью стандартного инжектора для имплантации интраокулярных линз гидрогелевый диск, изготовленный из стандартной интраокулярной контактной линзы из сополимера гидрогеля диаметром 8,0 мм и толщиной 0,1 мм. После имплантации гидрогелевого диска края роговичного тоннельного разреза самогерметизируются.
Недостатками этого метода являются: техническая сложность оперативного вмешательства, высокая гидрофильность имплантируемого материала, который в силу физико-химических характеристик не способен уменьшить или предотвратить гидратацию стромы роговицы, относительно большая толщина имплантируемого диска (0,1 мм).
Новый технический результат - снижение травматичности оперативного вмешательства, за счет использования для имплантации гидрофобного материала меньшей толщины
Для решения поставленной задачи в способе лечения эндотелиально-эпителиальной дистрофии (ЭЭД) роговицы, включающем имплантацию диска из полимерного материала мембранного типа в строму роговой оболочки, формируют интрастромальный роговичный карман в глубоких слоях собственного вещества роговой оболочки, для чего на первом этапе выполняют два тоннельных, до глубоких слоев стромы, надреза, на расстоянии 1,5 мм от лимба, шириной 1,2 мм, на 3 и 9 часах, далее, с помощью шпателя, используя оба тоннельных надреза, формируют интрастромальный «карман» в глубоких слоях собственного вещества роговицы, после этого, в один из туннельных надрезов вводят цанговый пинцет, проводя его сквозь расслоенную строму, и выводят через противоположный тоннельный надрез, где браншами пинцета захватывают свернутую валиком полимерную трековую мембрану, выполненную из полиэтиленфталата в виде диска диаметром 8,0 мм, толщиной 7 мкм, с размером пор 0,4 мкм, плотностью 5*106 пор/см2, которую имплантируют в интрастромальный роговичный «карман» во время обратного движения пинцета, после этого трековую мембрану расправляют с помощью шпателя, края тоннельных надрезов гидратируют.
Трековая мембрана представляет собой диск из полиэтилентерефталата (ПЭТФ) диаметром 8,0 мм, толщиной 7 мкм, размер пор составляет 0,4 мкм, плотность 5*106 пор/см2.
Благодаря имплантированной полимерной мембране значительно уменьшается отек ткани роговицы, что способствует восстановлению прозрачности роговой оболочки и улучшению сниженных вследствие заболевания зрительных функций.
Предпосылками предлагаемого способа послужили выполненные на базе ФГАОУ ВО НИ ТПУ и ГБОУ ВПО СибГМУ исследования, доказывающие необходимые для уменьшения отека роговицы физико-химические свойства полимерных трековых мембран.
1. Полимерные трековые мембраны обладают стабильными гидрофобными свойствами поверхности, приобретаемые после их стерилизации. При этом краевой угол смачиваемости Θ с 76,9°±0,5 увеличивается до 102,68±0,5, что является важной характеристикой материала в выполнении барьерной функции для предотвращения избыточной гидратации основного вещества роговицы.
2. Толщина полимерных трековых мембран, измеренная с помощью электронного толщиномера «Tesa Unit» с точностью ±0,1 мкм, составляет 7,0 мкм.
3. Размер пор трековой мембраны составляет 0,4 мкм, плотность 5*106 пор/см2 (фиг. 1).
Полимерные трековые мембраны «ТОМТРЕК» изготавливают из полимера полиэтилентерефталата (ПЭТФ) в лаборатории №16 Физико-Технического Института ТПУ. Ориентированные полимерные пленки из ПЭТФ облучают пучком ионов Ar с максимальной энергией 41 МэВ в специально созданной вакуумной камере с лентопротяжным механизмом. Селективное щелочное травление материала в области трека позволяет получить в исходной пленке пористую систему со сквозными цилиндрическими отверстиями с типичной симметричной структурой. Перед травлением пленку подвергают облучению ультрафиолетовым светом для дополнительной сенсибилизации. Травление осуществляют в водном растворе NaOH с 1,5 N концентрацией при температуре в диапазоне 72-82°C.
Полимерные трековые мембраны «ТОМТРЕК» широко применяются в различных отраслях промышленности, среди которых наиболее значимое их применение - в качестве фильтра различных жидкостей, газов и крови при плазмофорезе. Кроме того, необходимо отметить, что имеется разрешение Федеральной службы по надзору в сфере здравоохранения и социального развития Министерства здравоохранения и социального развития Российской Федерации №01-26718/09 от 28.12.2009 на проведения клинических испытаний трековых мембран из полиэтилентерефталата в качестве эксплантодренажа для лечения глаукомы (Рязанцева Т.В., Кравец Л.И., Елисон В.М. Наноструктурирование в плазме поверхностного слоя трековых мембран с целью получения высокоэффективного биосовместимого эксплантодренажа для хирургического лечения рефрактерной глаукомы / Перспективные материалы. - 2012).
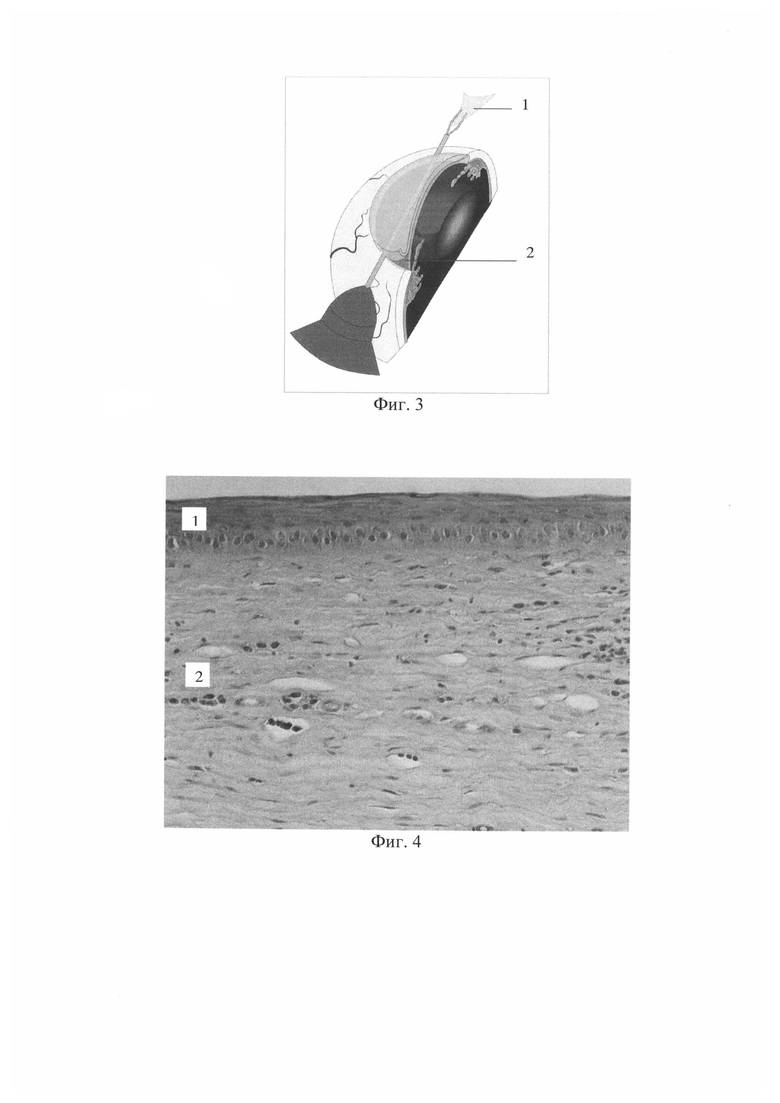
Способ осуществляют следующим образом. В эксперименте, в условиях операционной после наркоза и обработки операционного поля с соблюдением правил асептики и антисептики, животным выполняют операцию: в роговице с предварительно индуцированной ЭЭД формируются два тоннельных - до глубоких слоев стромы - надреза на расстоянии 1,5 мм от лимба шириной 1,2 мм на 3 и 9 часах (фиг. 2). С помощью шпателя через оба тоннельных надреза формируют интрастромальный «карман» в глубоких слоях собственного вещества роговицы. Затем в один из туннельных надрезов вводят цанговый пинцет, проводя его сквозь расслоенную строму, и выводят через противоположный тоннельный надрез, где браншами пинцета захватывают свернутую валиком полимерную трековую мембрану. Во время обратного движения пинцета мембрану имплантируют в интрастромальный роговичный «карман» (фиг. 3). С помощью шпателя трековую мембрану аккуратно расправляют. Края тоннельных надрезов гидратируют.
Способ апробирован на 10 кроликах породы Шиншилла весом 3,5-4,0 кг.
Обзор экспериментального материала: общая продолжительность эксперимента составила 8 недель. На I этапе каждому животному в условиях операционной моделировали ЭЭД путем механического повреждения и удаления эндотелия роговицы одного из глаз. На II этапе спустя 3 недели после развития патологического процесса в роговой оболочке осуществляли имплантацию трековой мембраны описанным способом.
В ходе эксперимента проводили наружный осмотр, фоторегистрацию. Забор материала производили спустя 8 недель от начала эксперимента.
Энуклеированные глаза фиксировали в 12% нейтральном формалине. Фиксацию проводили при комнатной температуре в течение 24 часов. Затем объекты, после 24-часового промывания в проточной воде, подвергали обезвоживанию в спиртах восходящей концентрации, просветляли в О-ксилоле и заливали в парафин. Полученные срезы окрашивали гематоксилином и эозином, а также по методу Ван-Гизона.
Для подсчета различных структурных компонентов и клеточной инфильтрации использовали световой микроскоп ЛОМО Биолам АУ-12 (ок. х7, об. Х40, х90, собственное увеличение микроскопа x1,5), окулярную сетку Автандилова на 50 точек, окулярную вставку с известной площадью.
Полученные данные обработаны с использованием пакета программ "Statistica for Windows".
В ходе морфологических исследований в глазах с интрастромально имплантированной трековой мембраной выявлено следующее.
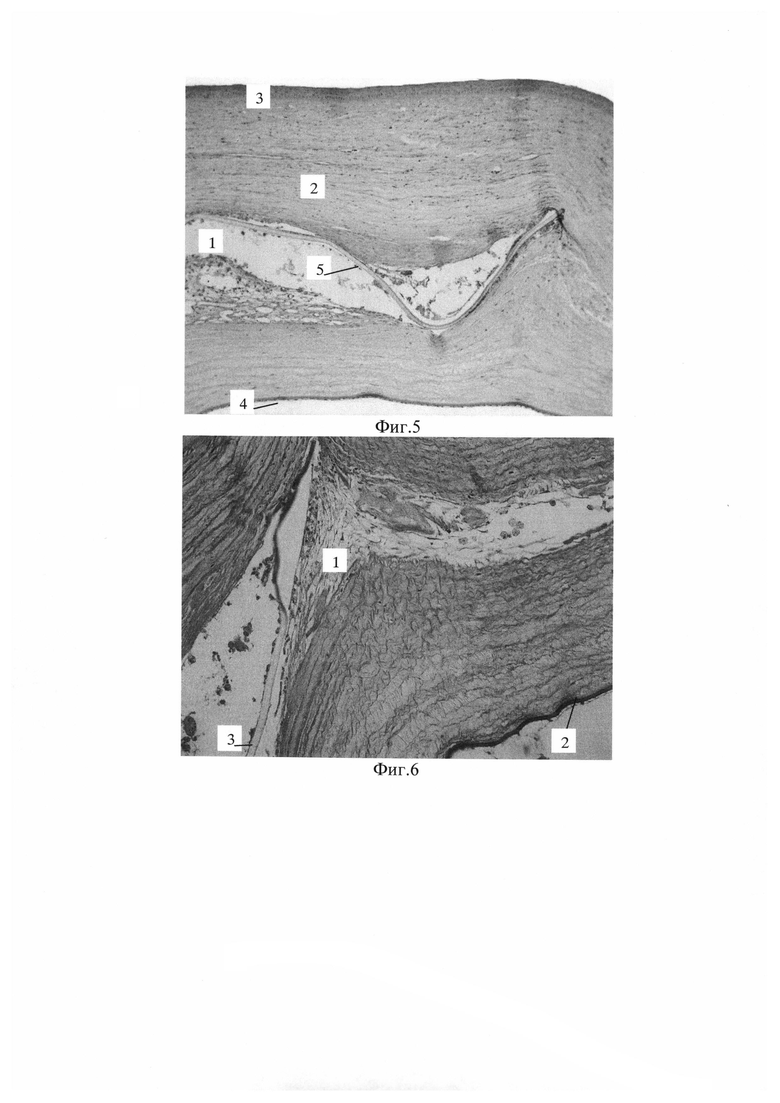
Передний эпителий роговицы представлен 4-5 слоями плоского эпителия с нормохромными ядрами и сохранен на всем протяжении. Боуменова мембрана визуализировалась в виде гомогенной эозинофильной полоски. В собственном веществе роговицы обнаруживались неравномерные умеренные изменения (фиг. 4). В зоне имплантации трековой мембраны выявлялись лимфо-моноцитарная инфильтрация основного вещества и отек, чуть более выраженный в задней трети стромы - между имплантированной мембраной и десцеметовой оболочкой (фиг. 5). Между задней поверхностью имплантированной мембраны и основным веществом роговицы наблюдалось развитие рыхлой соединительной ткани, богатой лимфоцитарными клетками и мелкими тонкостенными сосудами.
В передней части основного вещества, между имплантированной мембраной и боуменовой оболочкой, коллагеновые волокна располагались более компактно (фиг. 6). Среди них встречались единичные клеточные скопления, представленные, преимущественно, лимфоцитами и макрофагами, а также новообразованные сосуды (фиг. 7 и 8).
Задняя пограничная мембрана хорошо визуализировалась на всем протяжении и была представлена гомогенной эозинофильной полоской, чуть более широкой, чем боуменова мембрана.
Анализ полученных в ходе эксперимента данных свидетельствует о том, что имплантация трековой мембраны в строму роговицы при ЭЭД сопровождается развитием умеренно выраженной воспалительно-регенераторной реакции. Отсутствие избыточного фиброгенеза в роговичной ткани в определенной степени может быть объяснено физико-химическими свойствами самого полимера.
Выявленные в ходе гистологического исследования умеренные изменения в передней трети стромы роговицы - между имплантированной трековой мембраны и слоями роговичной ткани - свидетельствуют о стабилизации патологического процесса.
Таким образом, результаты экспериментального исследования показали, что интрастромальная имплантация трековой мембраны в основное вещество роговицы при ЭЭД позволяет компенсировать нарушенную функцию эндотелиального слоя роговой оболочки и стабилизировать течение патологического процесса, благодаря чему уменьшается отек ткани и восстанавливается прозрачность роговицы.
Приложение:
Фиг. 1. Микрофотография фрагмента трековой мембраны, полученной при помощи электронного микроскопа Hitachi ТМ-1000.
Фиг. 2. Роговичные надрезы на 3 и 9 часах:
1 - роговичный надрез.
Фиг. 3. Имплантация трековой мембраны цанговым пинцетом, пропущенным через роговичный «карман»:
1 - трековая мембрана;
2 - роговичный «карман».
Фиг. 4. Сохранный передний эпителий и передняя пограничная мембрана роговицы. Окраска гематоксилином и эозином, x 200:
1 - передний эпителий;
2 - собственное вещество.
Фиг. 5. Изменения собственного вещества роговицы после имплантации мембраны. Окраска гематоксилином и эозином, x 100:
1 - отек в задней части собственного вещества;
2 - собственное вещество роговицы;
3 - передний эпителий роговицы;
4 - задний эпителий роговицы;
5 - трековая мембрана.
Фиг. 6. Изменения собственного вещества роговицы после имплантации мембраны. Окраска гематоксилином и пикрофуксином по Ван-Гизону, x 200:
1 - отек и изменения коллагеновых волокон в задней части собственного вещества;
2 - задний эпителий роговицы;
3 - трековая мембрана.
Фиг. 7. Развитие грануляционной ткани в месте имплантации мембраны в собственное вещество роговицы. Окраска гематоксилином и эозином, x 80:
1 - имплантированная мембрана;
2 - грануляционная ткань;
3 - передний эпителий роговицы;
4 - задний эпителий роговицы;
5 - собственное вещество роговицы.
Фиг. 8. Воспалительная инфильтрация и новообразованные сосуды в собственном веществе роговицы после имплантации мембраны. Окраска гематоксилином и пикрофуксином по Ван-Гизону, x 200:
1 - имплантированная мембрана;
2 - передний эпителий роговицы;
3 - собственное вещество роговицы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РОГОВИЧНОГО СИНДРОМА ПРИ ДАЛЕКОЗАШЕДШЕЙ СТАДИИ ЭНДОТЕЛИАЛЬНО-ЭПИТЕЛИАЛЬНОЙ ДИСТРОФИИ РОГОВИЦЫ | 2015 |
|
RU2600428C1 |
| Способ интраоперационной минимизации степени посткератопластической аметропии | 2021 |
|
RU2773800C1 |
| Способ кератопластики | 2020 |
|
RU2724282C1 |
| СПОСОБ ЛЕЧЕНИЯ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2009 |
|
RU2405513C1 |
| Способ интрастромальной кератопластики при кератоконусе | 2021 |
|
RU2773801C1 |
| СПОСОБ ПРОВЕДЕНИЯ НЕАВТОМАТИЗИРОВАННОЙ ЭНДОКЕРАТОПЛАСТИКИ | 2008 |
|
RU2367392C1 |
| Способ хирургического лечения развитой стадии кератоконуса | 2019 |
|
RU2734951C1 |
| СПОСОБ ЛЕЧЕНИЯ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2013 |
|
RU2544306C2 |
| Способ лечения буллезной кератопатии | 2017 |
|
RU2688795C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ДЕСЦЕМЕТОВОЙ МЕМБРАНЫ | 2015 |
|
RU2600158C1 |


Изобретение относится к медицине, в частности к офтальмологии, и может быть использовано для лечения эндотелиально-эпителиальной дистрофии (ЭЭД) роговицы. Формируют интрастромальный роговичный карман в глубоких слоях собственного вещества роговой оболочки, для чего на первом этапе выполняют два тоннельных надреза до глубоких слоев стромы, на расстоянии 1,5 мм от лимба, шириной 1,2 мм, на 3 и 9 часах, далее, с помощью шпателя, используя оба тоннельных надреза, формируют интрастромальный «карман» в глубоких слоях собственного вещества роговицы. В один из туннельных надрезов вводят цанговый пинцет, проводя его сквозь расслоенную строму, и выводят через противоположный тоннельный надрез, где браншами пинцета захватывают свернутую валиком полимерную трековую мембрану, выполненную в виде диска из полиэтиленфталата диаметром 8,0 мм, толщиной 7 мкм, с размером пор 0,4 мкм, плотностью 5*106 пор/см2, которую имплантируют в интрастромальный роговичный «карман» во время обратного движения пинцета. Трековую мембрану расправляют с помощью шпателя, края тоннельных надрезов гидратируют. Способ позволяет снизить травматичность вмешательства. 8 ил.
Способ лечения эндотелиально-эпителиальной дистрофии (ЭЭД) роговицы, включающий имплантацию диска из полимерного материала мембранного типа в строму роговой оболочки, отличающийся тем, что формируют интрастромальный роговичный карман в глубоких слоях собственного вещества роговой оболочки, для чего на первом этапе выполняют два тоннельных надреза, до глубоких слоев стромы, на расстоянии 1,5 мм от лимба, шириной 1,2 мм, на 3 и 9 часах, далее с помощью шпателя, используя оба тоннельных надреза, формируют интрастромальный «карман» в глубоких слоях собственного вещества роговицы, после этого в один из туннельных надрезов вводят цанговый пинцет, проводя его сквозь расслоенную строму, и выводят через противоположный тоннельный надрез, где браншами пинцета захватывают свернутую валиком полимерную трековую мембрану, выполненную в виде диска из полиэтиленфталата диаметром 8,0 мм, толщиной 7 мкм, с размером пор 0,4 мкм, плотностью 5*106 пор/см2, которую имплантируют в интрастромальный роговичный «карман» во время обратного движения пинцета, после этого трековую мембрану расправляют с помощью шпателя, края тоннельных надрезов гидратируют.
| СПОСОБ ЛЕЧЕНИЯ БУЛЛЕЗНОЙ КЕРАТОПАТИИ | 2009 |
|
RU2405513C1 |
| Способ лечения отечной дистрофииРОгОВицы | 1979 |
|
SU810235A1 |
| АКИМЕНКО С.Н | |||
| и др | |||
| Свойства трековых мембран на основе полиэтиленнафталата | |||
| Серия Критические технологии, Мембраны, 2002, N15, с | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| MUENZLER WS et al | |||
| Lens replacement in pseudophakic bullous keratopathy | |||
| In: Brightbill FS, ed | |||
| Comeal Surgery: Theory, Technique, and Tissue | |||
| St | |||
| Louis: CV Mosby Co, 1986; p.229-236, реферат. | |||
Авторы
Даты
2016-08-20—Публикация
2015-07-30—Подача