Область техники, к которой относится изобретение
Изобретение относится к обнаружению диагностики, и прогнозу рака матки. Изобретение относится к неожиданному открытию того, что биомаркеры, которые соответствуют АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN, дифференциально экспрессируются в контрольных образцах по сравнению с образцами от пациентов, имеющих рак эндометрия, и, которые, следовательно, пригодны для обнаружения рака эндометрия. В особенности эти биомаркеры, имеющие чрезвычайную чувствительность, специфичность, и/или способность отделять пораженных особей от непораженных особей. Кроме того, изобретателями было обнаружено, что дифференциальная экспрессия этих биомаркеров в опухолевой ткани первичного рака эндометрия коррелирует с их уровнем экспрессии в образцах маточной жидкости по сравнению с контрольными значениями. Таким образом, эти биомаркеры являются эффективными, поскольку было обнаружено, что они дифференциально экспрессируются в нескольких различных типах образцов от пораженных и здоровых особей.
Предпосылки создания изобретения
Каждый год в Европе диагностируется около 150 тыс. новых случаев рака эндометрия и около 46 тыс. женщин умирают от этого заболевания (Ferlay и др., (2007) Ann. Onc. 18: 581-592). В США, в год диагностируется около 41 тыс. новых случаев карциномы эндометрия и 7 тыс. 300 женщин умирает каждый год (см. статистику Американского Общества по борьбе с раковыми заболеваниями, доступную в Интернете). Заболеваемость и коэффициент смертности от рака эндометрия возрастают.
Рака эндометрия (ЕС) является наиболее распространенной из инвазивных опухолей женских половых органов и четвертой наиболее встречаемой у женщин в западных странах (Jemal и др.,. (2008) СА Cancer J Clin 58: 71-96). Для борьбы с этим смертельным заболеванием нужны новые методы диагностики, прогнозирования, и классификации рака эндометрия.
Часто рак эндометрия обнаруживается рано, на его начальных стадиях, по наличию симптомов, связанных с заболеванием. К сожалению, 20% пациентов с инвазией миометрия и/или поражением лимфатических узлов, которые являются основными индикаторами, связанными с плохим прогнозом, снижают коэффициент выживаемости, и более прогрессирующим заболеванием. Первоначальным терапевтическим подходом для рака эндометрия является хирургическое лечение.
Обычные симптомы рака матки (например, рака эндометрия) включают необычное вагинальное кровотечение или выделения, нарушения мочеиспускания, боль в области таза, и боль при половом акте. Рак матки обычно развивается после менопаузы. Другими факторами риска для рака эндометрия являются ожирение, прием отдельно эстроген-заместительной гормональной терапии, лечение с применением тамоксифена и наличие генетической предрасположенности к злокачественному новообразованию (например, синдром Линча). Стандартное лечение для рака эндометрия изменяется в зависимости от стадии заболевания. Лечение обычно включает хирургическое вмешательство для удаления матки, которое называется гистерэктомия, хотя другие варианты включают гормональную терапию и лучевую терапию.
Методы, которые общепринято используют в клинических условиях для диагностики рака эндометрия, включают биопсию с последующим цитологическим анализом и/или трансвагинальное ультразвуковое исследование. Диагностика карциномы эндометрия обычно осуществляется путем патологического исследования аспирата эндометрия (20-30%), и путем биопсии при осуществлении гистероскопии (70-80%). Коэффициент успешной диагностики при осуществлении составляет более 90%, с ложноположительными результатами в случае предшествующих поражений аденокарциномы эндометрия (гиперплазии); полипов эндометрия, которые присутствуют в значительном количестве при злокачественном новообразовании (0-4,8%) и должны быть удалены, хотя являются асимптомными или доброкачественными; или в случае диффузных форм аденокарцином эндометрия, которые сложно дифференцировать от гиперплазии эндометрия. Таким образом, существует потребность в менее инвазивном диагностическом тесте на основе молекулярных маркеров. Такой менее инвазивный текст на основе молекулярных маркеров будет предоставлять возможность для более практичного скрининга рака матки. Диагностический тест на основе молекулярных маркеров, который получают менее инвазивным образом и который имеет чувствительность и специфичность сопоставимую с таковыми для биопсии эндометрия, может устранить нецелесообразную гистероскопию.
Карциномы эндометрия можно классифицировать на низкодифференцированные (тип I) и высокодифференцированные (тип 2). Тип I эндометриоидного рака эндометрия (который иногда называют эстроген-зависимым), который составляет приблизительно 80% вновь диагностированных случаев, представляет собой низкодифференцированные опухоли, связанные со стимуляцией эстрогенами, которые обычно развиваются у женщин в пери- или пост-менопаузе и им обычно предшествует гиперплазия эндометрия с атипией или без атипии. Тип II неэндометриоидного рака эндометрия, который обычно поражает более пожилых женщин, является менее дифференцированным и с худшим прогнозом, не связан со стимуляцией эстрогенами, и взаимосвязан с атрофическим эндометрием или, иногда, с полипами эндометрия.
Типично известно, что злокачественные новообразования I типа имеют перестройки в PTEN, KRAS2, дефектах репарации ошибочно спаренных оснований ДНК, CTNNB1, и имеют приблизительно диплоидный кариотип. Злокачественные новообразования II типа типично имеют ТР53 мутации и ErBB2 сверхэкспрессию и в основном не являются диплоидными. Sugiyama и др. ((2003) Clin. Can. Res. 9: 5589-5600) описали, что определенные гены селективно активированы или подавлены при раке эндометрия I типа относительно II типа. Например, ими было обнаружено, что MLH1 подавлен при злокачественных новообразованиях I типа, также как и другие гены, относящиеся к передаче сигналов повреждения и репарации ДНК, такие как О6-метил-гуанин ДНК метилтрансфереза, α каталитическая субъединица ДНК полимеразы, и Ku (р70/р80) антиген. Было обнаружено, что VEGF-C активирован при злокачественных новообразованиях I типа на уровне белка и мРНК по сравнению со злокачественными новообразованиями II типа. Было обнаружено, что KRAS активирован при злокачественных новообразованиях II типа. STAT1 активирован при злокачественных новообразованиях I типа и STAT2 активирован при злокачественных новообразованиях II типа. Konecny и др. ((2009) British Journal рака 100, 89-95) описали, что скорость амплификации HER2 гена, которую измеряли с помощью гибридизации in situ, была повышена при злокачественных новообразованиях II типа, тогда как экспрессия EGFR, которую измеряли с помощью техник IHC, была существенно снижена при злокачественных новообразованиях II типа. Deng и др. ((2005) Clin. Can. Res. том 11, № 23: 8258-8264) описали, что EIG121 является маркером для злокачественных новообразований I типа, связанных с эстрогеном.
Рак матки также классифицируется гистологически в соответствии с типом клеток. Наиболее распространенный тип клеток относится к эндометриоидным и составляет около 80% вновь диагностированных случаев. Другие менее распространенные раки матки относятся к серозным и светлоклеточным ракам. Большинство злокачественных новообразований I типа представляют собой клетки эндометриоидного типа, тогда как злокачественные новообразования II типа, по всей вероятности, являются неэндометриоидным раком матки. Злокачественные новообразования II типа скорее метастазируют и имеют более плохой прогноз по сравнению со злокачественными новообразованиями I типа. Злокачественные новообразования I типа обычно имеют лучший прогноз и лучше отвечают на терапию.
В различных исследованиях анализировали профили экспрессии генов для классификации рака матки. Sugiyama и др. ((2003) din. Canc. Res. 9: 5589-5600) описали, что между типами I и II злокачественных новообразований 45 генов интенсивно экспрессируются при злокачественных новообразованиях I типа и 24 интенсивно экспрессируются при злокачественных новообразованиях I типа. Risinger и др. ((2003) Сапе. Res. 63: 6-11) описали, что микропанельный анализ различных гистологических подтипов рака эндометрия имеет различные профили экспрессии генов. Ими было обнаружено, что 191 генов проявляют более чем 2-кратное отличие в экспрессии между эндометриоидным и неэндометриоидным раками эндометрия.
Были идентифицированы различные биомаркеры рака эндометрия для рака эндометрия. Повышенные уровни СА 125, СА 15-3, и СА 19-9 связаны с более коротким временем выживания. СА 125 коррелирует с размером и стадией опухоли и является независимым прогностическим фактором внематочного распространения.
В литературе были описаны сывороточные маркеры для выявления рака матки. Yurkovetsky и др. ((2007) Gyn. Onc. 107: 58-65) идентифицировали, что пролактин является сывороточным биомаркером с чувствительностью и специфичностью для рака эндометрия. Ими было обнаружено, что сывороточные СА 125 СА 15-3 и СЕА повышены у пациентов с III стадией заболевания по сравнению со стадией I. Панель из пяти биомаркеров пролактин, GH, эотаксин, Е-селектин и TSH различает рак эндометрия от рака яичников и молочной железы.
Другим важным вопросом для клинических врачей для диагностики рака эндометрия являются синхронные злокачественные новообразования. Guirguis и др. (Gyn. Onc. (2008) 108: 370-376) описали, что 10% пациентов с раком яичника имеют опухоль в эндометрии и 5-25% пациентов с раком эндометрия также имеют опухоль в яичнике. Определение первичного сайта злокачественного новообразования имеет важное клиническое значение. Стадия III карциномы эндометрия подвергается хирургическому лечению с последующей химиотерапией и/или лучевой терапией; тогда как двойные первичные стадии I рака яичника и эндометрия имеют лучший прогноз и могут не нуждаться в адъювантной терапии.
Доступные в настоящее время методы диагностики рака эндометрия часто создают дискомфорт для пациента и иногда основаны на субъективной интерпретации визуальных изображений. Существует потребность в менее инвазивных методах для скрининга для рака эндометрия, которые будут менее субъективными при интерпретации. Дополнительно, существует потребность в новых маркерах, которые пригодны для раннего обнаружения рака эндометрия. Доступные в настоящее время методы обнаружения рака эндометрия включают метод дилятации и кюретажа, которые считаются «золотым стандартом», но этот метод является инвазивным, может вызывать существенный дискомфорт, и для него может быть необходим квалифицированный патоморфолог для интерпретации, и, следовательно, он не является пригодным в качестве общих средств для скрининга. Другим менее инвазивным методом для диагностики рака эндометрия является трансвагинальное ультразвуковое исследование, в котором измеряют толщину эндометрия. При исследовании пациентов, имеющих пост-менопаузное кровотечение, используя граничное значение 4 мм, было обнаружено, что трансвагинальное ультразвуковое исследование имеет 100% чувствительность и 60% специфичность (Gull и др. (2003) Am. J.Obstet. Gynecol. 188(2): 401-408). У женщин без вагинального кровотечения, чувствительность измерений толщины эндометрия составила 17% для порогового значения 6 мм и 33% для порогового значения 5 мм (Fleischer и др. (2001) Am. J.Obstet. Gynecol. 184: 70-75). TVS имеет высокий коэффициент ложноположительных результатов, поскольку другие состояния, кроме рака эндометрия, могут продуцировать более толстый эндометрий. Одной из потенциальных проблем при использовании TVS у пре- и пери-менопаузных женщин является то обстоятельство, что толщина эндометрия изменяется в зависимости от фазы менструального цикла. Кроме того, женщины, применяющие тамоксифен, также имеют более толстый эндометрий. Следовательно, существует потребность в технологиях и маркерах, которые могут служить дополнением и/или улучшать способность TVS для диагностики рака эндометрия.
Очевидно, существует возможность улучшения средств, доступных в настоящее время для скрининга для рака эндометрия.
Краткое изложение сущности изобретения
Изобретение относится неожиданному открытию того, что биомаркеры, которые соответствуют АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN дифференциально экспрессируются в контрольных образцах по сравнению с образцами от пациентов, имеющих рак эндометрия, и, которые, следовательно, пригодны для обнаружения рака эндометрия. В особенности эти биомаркеры, имеющие чрезвычайную чувствительность, специфичность, и/или способность отделять пораженных особей от непораженных особей. Кроме того, изобретателями было обнаружено, что дифференциальная экспрессия этих биомаркеров в опухолевой ткани первичного рака эндометрия коррелирует с их уровнем экспрессии в образцах маточной жидкости по сравнению с контрольными значениями. Таким образом, эти биомаркеры являются эффективными, поскольку было обнаружено, что они дифференциально экспрессируются в нескольких различных типах образцов пораженных особей по сравнению с непораженными особями.
Таким образом, настоящее изобретение относится к диагностическому способу in vitro для диагностики рака эндометрия или повышенной вероятности эндометриального, который включает определение уровня
(1) от 1 до 17 биомаркера (ов), выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, и TJP3 в образце от пациента, где повышенный уровень указанных от 1 до 17 биомаркеров по сравнению с контрольным значением указывает на диагноз рака эндометрия или повышенную вероятность рака эндометрия и/или
(2) определение уровня от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где сниженный уровень EFEMP2, SOCS2, и/или DCN по сравнению с контрольным значением указывает на диагноз рака эндометрия или повышенную вероятность рака эндометрия.
Следовательно, настоящее изобретение относится к диагностическому способу in vitro для диагностики рака эндометрия, который включает
(1) определение уровня от 1 до 17 биомаркера (ов), выбранных из Р4НВ, GMIP, IKBKE, FASTKD1, DDR1, SIRT6, PHKG2, АСАА1, АР1М2, EPS8L2, P2RX4, PPFIBP2, PPP1R16A, CGN, RASSF7, RNF183, и TJP3 в образце от пациента, где повышенный уровень указанных от 1 до 17 биомаркеров по сравнению с контрольным значением указывает на существование рака эндометрия и/или
(2) определение уровня от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где сниженный уровень EFEMP2, SOCS2, и/или DCN по сравнению с контрольным значением указывает на существование рака эндометрия.
Было обнаружено, что биомаркеры, представленные в таблице 1, дифференциально экспрессируются между образцами рака эндометрия и нормальными образцами, как определено с помощью микропанельных исследований (см. таблицу 1 в подробном описании изобретения). Изобретателями было обнаружено, что индивидуально каждый из биомаркеров, представленных в таблице 1, имеют прогностическую значимость для диагностики рака эндометрия. Кроме того, уровни комбинаций маркеров, представленных в таблице 1, имеют дополнительную прогностическую значимость для диагностики рака эндометрия (см. пример 5). Например, изобретателями неожиданно было обнаружено, что подгруппы биомаркеров, представленные в таблице 1, имеющие от 2-20 биомаркеров в различных комбинациях, обеспечивают характерные картины фингерпринтов, имеющие чрезвычайно хорошую прогностическую значимость для диагностики или обнаружения рака эндометрия. В целом, если больше, чем один из биомаркеров, представленных в таблице 1, дифференциально экспрессируются в образце, то это повышает вероятность того, что особь имеет рак эндометрия. Кроме того, изобретателями также было обнаружено, что добавление других биомаркеров, вдобавок к тем, которые перечислены в таблице 1, к характерной картине фингерпринтов также может повышать прогностическую значимость, и может являться пригодной для классификации рака эндометрия, для дифференциальной диагностики заболеваний, отличающихся от рака эндометрия, и для прогноза рака эндометрия. В таблице 1 представлены ENSEMBL номера доступов для генов, мРНК, и белков, соответствующие биомаркерам согласно изобретению. Некоторые из биомаркеров имеют альтернативные транскрипты. Изобретение относится к определению дифференциальной экспрессии любого из этих альтернативных транскриптов (или изоформ протеинов) до тех пор, пока их экспрессия коррелирует с отсутствием или наличием рака эндометрия. Предпочтительные транскрипты (или изоформы протеинов) для обнаружения рака эндометрия представляют собой те, которые определяют с матричными зондами, как указано в примерах.
Изобретателями также было обнаружено, что маркеры, представленные в таблице 1, могут быть определены в образцах маточной жидкости и что уровень экспрессии этих маркеров коррелирует в первичной опухоли и маточной жидкости (например, полученной путем промывки матки или аспирации).
Изобретение, таким образом, обеспечивает способы определения уровня от 1 до 20 биомаркеров, перечисленных в таблице 1, в тестируемом образце. Способ может включать обеспечение или получение тестируемого образца от пациента; определение уровня от 1 до 20 биомаркеров, представленных в таблице 1, в образце; и сравнение уровня биомаркера (ов) в тестируемом (ых) образце (ах) с контрольным значением (например, контрольный образец, контрольное значение, или контрольный показатель). Более высокий уровень биомаркера (ов), который (ые), как обнаружено, сверхэкспрессируется (ются) при раке эндометрия, как показано в таблице 1, в тестируемом образце, полученном от пациента, по сравнению с контрольным значением (например, контрольный образец, контрольное значение, и/или контрольный показатель) указывает на рак эндометрия, повышенную вероятность рака эндометрия, и/или предраковое состояние (например, гиперплазия эндометрия). Более низкий уровень биомаркера (ов), который (ые), как обнаружено, недостаточно экспрессируется (ются) при раке эндометрия, как показано в таблице 1, в тестируемом образце, полученном от пациента, по сравнению с уровнем в контрольном значении (например, контрольный образец, контрольное значение, и/или контрольный показатель) указывает на рак эндометрия, повышенную вероятность рака эндометрия, и/или предраковое состояние (например, гиперплазия эндометрия). Уровень биомаркера (ов) можно определить с помощью подходящих исследований, включая ОТ-ПЦР, количественную ПЦР, множественную ПЦР, нозерн гибридизацию, микропанельный анализ, двухгибридные анализы, такие как исследования на основе ДНК-связывающих доменов GAL4, исследования на основе антител, EIA, блоттинг-анализы, сэндвич-анализы, и другие. Уровень биомаркеров, представленных в таблице 1, можно определить в жидкостях и тканях организма для диагностики рака эндометрия. Уровень биомаркеров, представленных в таблице 1, можно определить в опухолевой ткани, полученной, например, путем биопсии. Уровень биомаркеров, представленных в таблице 1, можно определить в образцах, полученных из аспиратов или жидкости матки. Уровень биомаркеров, представленных в таблице 1, можно определить в крови, сыворотке, или плазме.
Биомаркеры, представленные в таблице 1, включают АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, и TJP3, которые, как было обнаружено, активированы при раке эндометрия и DCN, SOCS2, и EFEMP2 которые, как было обнаружено, подавлены при раке эндометрия в этих исследованиях. В одном варианте осуществления, биомаркеры для применения в способе согласно изобретению для обнаружения рака эндометрия или повышенную вероятность рака эндометрия включают от 1 до 17 активированных биомаркеров, перечисленных в таблице 1, и от 1 до 3 подавленных биомаркеров, перечисленных в таблице 1.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня одного или нескольких биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
Следовательно, настоящее изобретение относится к диагностическому способу in vitro для диагностики рака эндометрия, который включает
(1) измерение уровня одного или нескольких биомаркеров, выбранных из Р4НВ, GMIP, IKBKE, FASTKD1, DDR1, SIRT6, PHKG2, АСАА1, АР1М2, EPS8L2, P2RX4, PPFIBP2, PPP1R16A, CGN, RASSF7, RNF183, и TJP3 в образце от пациента, где повышенный уровень указанных одного или нескольких биомаркеров по сравнению с контрольным значением указывает на существование рака эндометрия и/или
(2) измерение уровня одного или нескольких биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где сниженный уровень EFEMP2, SOCS2, и/или DCN по сравнению с контрольным значением указывает на существование рака эндометрия.
В дальнейшем варианте осуществления, настоящее изобретение относится к диагностическому способу in vitro для диагностики рака эндометрия, который включает
(1) определение уровня от 1 до 17 биомаркера (ов), выбранных из Р4НВ, GMIP, IKBKE, FASTKD1, DDR1, SIRT6, PHKG2, АСАА1, АР1М2, EPS8L2, P2RX4, PPFIBP2, PPP1R16A, CGN, RASSF7, RNF183, и TJP3 в образце от пациента, где повышенный уровень указанных от 1 до 17 биомаркеров по сравнению с контрольным значением указывает на существование рака эндометрия и/или
(2) определение уровня от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где сниженный уровень EFEMP2, SOCS2, и/или DCN по сравнению с контрольным значением указывает на существование рака эндометрия.
В одном варианте осуществления, диагностический способ in vitro включает определение уровня Р4НВ. В другом варианте осуществления, диагностический способ in vitro включает определение уровня EFEMP2. В дальнейшем варианте осуществления способ in vitro включает определение уровня IKBKE. В дальнейшем варианте осуществления диагностический способ in vitro включает определение уровня GMIP.
В соответствии с диагностическим способом in vitro согласно изобретению, уровень одного или нескольких GMIP, IKBKE, или EFEMP2 можно определить дополнительно к Р4НВ. Диагностический способ in vitro может дополнительно включать определение уровня одного или нескольких Р4НВ, IKBKE, или GMIP дополнительно к EFEMP2. Диагностический способ in vitro может дополнительно включать определение уровня одного или нескольких GMIP, EFEMP2, или Р4НВ дополнительно к IKBK.E. Также предусматривается, что диагностический способ in vitro может дополнительно включать определение уровня FASTKD1, DDR1, SIRT6, и/или PHKG2. Диагностический способ in vitro может дополнительно включать определение уровня от 1 до 12 биомаркеров, выбранных из АСАА1, АР1М2, EPS8L2, P2RX4, PPFIBP2, PPP1R16A, CGN, RASSF7, RNF183, TJP3, SOCS2 и DCN.
В одном варианте осуществления, пациент имеет фактор риска для рака эндометрия или подвергается скринингу для рака эндометрия. Кроме того, образец от пациента может быть (получен) от пациента с атипичным маточным кровотечением. Другими словами, пациент может страдать от атипичного маточного кровотечения. Образец от указанного пациента также может быть (получен) от пациента, имеющего эндометрий с увеличенной толщиной. Следовательно, пациент может иметь эндометрий с увеличенной толщиной.
Образец от пациента может быть (получен) от пре-менопаузного, пери-менопаузного, или пост-менопаузного пациента. Следовательно, пациент представляет собой пре-менопаузного, пери-менопаузного, или пост-менопаузного пациента. В одном варианте осуществления, пациент является пре-менопаузным. В другом варианте осуществления, пациент является пери-менопаузным. В дальнейшем варианте осуществления, пациент является пост-менопаузным.
Образец может представлять собой образец ткани, крови и/или сыворотки, и/или маточной жидкости.
В одном варианте осуществления, образец представляет собой образец маточной жидкости. Образец маточной жидкости может быть получен путем аспирации.
В одном варианте осуществления, уровень биомаркеров определяют с антителом в соответствии с настоящим изобретением. Уровень биомаркера (ов) также может быть определен с помощью ОТ-ПЦР.
Следующие маркеры можно определить в соответствии с диагностическим способом in vitro согласно настоящему изобретению: Р4НВ, IKBKE, EFEMP2, SOCS2, FASTKD1, GMIP, DDR1, SIRT6, PHKG2, EPS8L2, PPP1R16A, P2RX4, RASSF7, и/или TJP3. Также следующие маркеры можно определить в соответствии с диагностическим способом in vitro согласно настоящему изобретению: Р4НВ, IKBKE, SOCS2, GMIP, DDR1, SIRT6, PHKG2, EPS8L2, PPP1R16A, P2RX4, RASSF7, и/или TJP3.
Маркеры, подлежащие определению, могут представлять собой P2RX4, Р4НВ, PHKG2, PPFIBP2, и/или SOCS2. Маркеры, подлежащие определению, также могут представлять собой Р4НВ, RASSF7, RNF183 и/или IKBKE.
В одном варианте осуществления, диагностический способ in vitro включает определение от 2 до 20 маркеров.
Предпочтительно, определяют комбинацию следующих маркеров: Р4НВ, EFEMP2, SIRT6, GMIP, FASTKD1 и DDR1. Также предпочтительным является определение комбинации следующих маркеров: Р4НВ, EFEMP2, SIRT6, GMIP, FASTKD1 и PHKG2. Также предпочтительным является определение комбинации следующих маркеров: Р4НВ, EFEMP2, SIRT6, АСАА1, АР1М2, EPS8L2, IKBKE, P2RX4, PPFIBP2 и PPP1R16A.
Следующие комбинации маркеров также предпочтительно определяют в соответствии с настоящим изобретением:
GMIP, IKBKE, PFHB, EFEMP2;
DDR1, FASTKD1, GMIP, IKBKE, Р4НВ, PHKG2, SIRT6, EFEMP2;
Р4НВ, EFEMP2, IKBKE, GMIP, FASTKD1.
В контексте настоящего изобретения комбинации маркеров, которые включают комбинацию с Р4НВ (то есть набор маркеров, включающий Р4НВ) являются особенно предпочтительными.
Также в настоящей заявке предусмотрено определение следующей комбинации маркеров:
DDR1, FASTKD1, GMIP, IKBKE, Р4НВ, PHKG2, SIRT6, EFEMP2; SOCS2;
Р4НВ, SOCS2;
GMIP, IKBKE, Р4НВ, SOCS2;
GMIP, IKBKE, Р4НВ, SOCS2, FASTKD1;
GMIP, IKBKE, Р4НВ, SOCS2, DDR1;
GMIP, IKBKE, Р4НВ, SOCS2, PHKG2;
GMIP, IKBKE, Р4НВ, SOCS2, SIRT6;
GMIP, IKBKE, Р4НВ, SOCS2, АСАА1;
GMIP, IKBKE, Р4НВ, SOCS2, АР1М2;
GMIP, IKBKE, Р4НВ, SOCS2, EFEMP2;
GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2;
GMIP, IKBKE, Р4НВ, SOCS2, P2RX4;
GMIP, IKBKE, Р4НВ, SOCS2, PPFIB2;
GMIP, IKBKE, Р4НВ, SOCS2, PPP1R16A;
GMIP, IKBKE, Р4НВ, SOCS2, АСАА1, FASTKD1;
GMIP, IKBKE, Р4НВ, SOCS2, FASTKD1, PHKG2;
GMIP, IKBKE, P4HB, SOCS2, FASTKD1, SIRT6;
GMIP, IKBKE, P4HB, SOCS2.
Один или более дополнительных биомаркеров можно определить в соответствии с раскрытым в настоящей заявке диагностическим способом in vitro. Один или более дополнительных биомаркеров могут быть выбраны из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном варианте осуществления, один или более дополнительных биомаркеров выбирают из дифференциальных диагностических биомаркеров.
Один или более вспомогательных биомаркеров могут быть выбраны из прогностических маркеров. Один или более вспомогательных биомаркеров могут быть выбраны из маркеров классификации рака эндометрия.
В дальнейшем варианте осуществления, настоящее изобретение относится к нуклеиновой кислоте, выбранной из IKBKE мРНК, кДНК, или их комплемента;
P4HB мРНК, кДНК, или их комплемента;
SOCS2 мРНК, кДНК, или их комплемента;
GMIP мРНК, кДНК, или их комплемента;
DDR1 мРНК, кДНК, или их комплемента;
EPS8L2 мРНК, кДНК, или их комплемента; и
PPP1R16A мРНК, кДНК, или их комплемента,
для применения для диагностики рака эндометрия.
Изобретение также относится к нуклеиновой кислоте, выбранной из
Праймеров для IKBKE;
Праймеров для P4HB;
Праймеров для SOCS2;
Праймеров для GMIP;
Праймеров для DDR1;
Праймеров для EPS8L2; и
Праймеров для PPP1R16A;
для применения для диагностики рака эндометрия.
В одном варианте осуществления, изобретение относится к нуклеиновой кислоте, выбранной из
зонда для IKBKE;
зонда для Р4НВ;
зонда для SOCS2;
зонда для GMIP;
зонда для DDR1;
зонда для EPS8L2; и
зонда для PPP1R16A,
для применения для диагностики рака эндометрия.
Также охватывается набор, содержащий два или больше описанных в настоящей заявке зондов для применения для диагностики рака эндометрия, в контексте настоящего изобретения. Кроме того, охватывается набор, содержащие праймеры для двух или более описанных в настоящей заявке Праймеров /пар Праймеров для применения для диагностики рака эндометрия в контексте настоящего изобретения.
В дальнейшем варианте осуществления, настоящее изобретение относится к антителу, выбранному из
антитела к IKBKE;
антитела к Р4НВ;
антитела к SOCS2;
антитела к GMIP;
антитела к DDR1;
антитела к EPS8L2; и
антитела к PPP1R16A,
для применения для диагностики рака эндометрия.
Следовательно, охватывается набор, содержащий антитела к двум или более описанным в настоящей заявке антителам для применения для диагностики рака эндометрия. Изобретение также относится к набору для получения маточной жидкости для применения для диагностики рака эндометрия путем оценки уровней от 1-20 биомаркеров, как определено и раскрыто в настоящей заявке.
Диагностический способ in vitro согласно настоящему изобретению может включать определение/выявление уровня 2 биомаркеров, 3 биомаркеров, 4 биомаркеров, 5 биомаркеров, 7 биомаркеров, 10 биомаркеров, 15 биомаркеров или 20 биомаркеров.
В одном варианте осуществления, настоящее изобретение относится к диагностическому способу in vitro для диагностики рака эндометрия, который включает получение образца аспирата маточной жидкости от пациента, имеющего симптом или фактор риска для рака эндометрия, и определение уровня от 1 до 100 биомаркеров, маркеров, которые дифференциально экспрессируются при раке эндометрия по сравнению с контрольными значениями, характерными для особей, не страдающих от рака эндометрия, где (1) если уровень от 1 до 100 биомаркеров повышен в образце аспирата эндометрия у пациента и в контрольных значениях, то пациент имеет повышенную вероятность наличия рака эндометрия и где (2) если уровень от 1 до 100 биомаркеров понижен в образце аспирата и тогда пациент имеет повышенную вероятность наличия рака эндометрия.
Настоящее изобретение также относится к нуклеиновой кислоте, выбранной из
АСАА1 мРНК, кДНК, или их комплемента;
АР1М2 мРНК, кДНК, или их комплемента;
CGN мРНК, кДНК, или их комплемента;
FASTKD1 мРНК, кДНК, или их комплемента;
P2RX4 мРНК, кДНК, или их комплемента;
RASSF7 мРНК, кДНК, или их комплемента;
RNF183 мРНК, кДНК, или их комплемента;
PHKG2 мРНК, кДНК, или их комплемента;
PPFIBP2 мРНК, кДНК, или их комплемента,
SIRT6 мРНК, кДНК, или их комплемента,
TJP3 мРНК, кДНК, или их комплемента;
EFEMP2 мРНК, кДНК, или их комплемента; и
DCN мРНК, кДНК, или их комплемента,
для применения для диагностики рака эндометрия.
Также объектом настоящего изобретения является нуклеиновая кислота, выбранная из
Праймеров для АСАА1;
Праймеров для АР1М2;
Праймеров для CGN;
Праймеров для FASTKD1;
Праймеров для P2RX4;
Праймеров для RASSSF7;
Праймеров для RNF183;
Праймеров для SIRT6;
Праймеров для PPFIBP2;
Праймеров для PHKG2;
Праймеров для TJP3;
Праймеров для EFEMP2; и
Праймеров для DCN;
для применения для диагностики рака эндометрия.
В дальнейшем варианте осуществления, настоящее изобретение относится к нуклеиновой кислоте, выбранной из
зонда для АСАА1;
зонда для АР1М2;
зонда для CGN;
зонда для FASTKD1;
зонда для P2RX4;
зонда для RASSF7;
зонда для RNF183;
зонда для SIRT6;
зонда для PPFIBP2;
зонда для PKHG2;
зонда для TJP3;
зонда для EFEMP2; и
зонда для DCN,
для применения для диагностики рака эндометрия.
В другом варианте осуществления, изобретение относится к антителу, выбранному из
антитела к АСАА1;
антитела к АР1М2;
антитела к CGN;
антитела к FASTKD1;
антитела к P2RX4;
антитела к RASSF7;
антитела к RNF183;
антитела к SIRT6;
антитела к PPFIBP2;
антитела к PKHG2;
антитела к TJP3;
антитела к EFEMP2; и
антитела к DCN,
для применения для диагностики рака эндометрия.
Антитело/антитела, нуклеиновая (ые) кислота (ы), зонды, праймер (ы)/пара (ы) праймеров, и/или набор (ы), описанные и определенные в настоящей заявке, пригодны для диагностики рака эндометрия в соответствии с настоящим изобретением. Таким образом, антитело/антитела, нуклеиновая (ые) кислота (ы), зонды, праймер (ы)/пара (ы) праймеров, и/или набор (ы), описанные и определенные в настоящей заявке, предназначены для применения для диагностики рака эндометрия. Аналогичным образом, также охватывается применение антитела/антител, нуклеиновой (ых) кислоты (кислот), зондов, праймера (ов)/пары (пар) праймеров, и/или набора (ов) для приготовления диагностической композиции для диагностики рака эндометрия. Также охватывается в контексте настоящего изобретения диагностическая композиция для применения для диагностики рака эндометрия и содержащая описанные и определенные в настоящей заявке антитело /антитела, нуклеиновую (ые) кислоту (ы), зонды, праймер (ы)/пару (ы) праймеров, и/или набор (ы).
Диагностирование рака эндометрия может, в этом контексте, включать или относиться к диагностическому способу, практически осуществляемому на организме человека или животного, который охватывает или включает характерные особенности, относящиеся к
(i) диагностированию с лечебными целями в строгом смысле слова, представляющего дедуктивную медицинскую или ветеринарную фазу принятия решения в качестве исключительно интеллектуального упражнения,
(ii) предшествующим стадиям, которые предназначены для постановки такого диагноза, и
(iii) специфическим взаимодействиям с организмом человека или животного, которые происходят, если осуществляют те из предшествующих стадий, которые имеют техническую природу.
В дальнейшем варианте осуществления, настоящее изобретение относится к диагностическому способу in vitro для диагностики рака эндометрия, который включает обеспечение или получение образца маточной жидкости от пациента-человека, который имеет симптом или фактор риска для рака женских половых органов и определение уровня экспрессии РНК от 2 до 9 биомаркеров, выбранных из Р4НВ, EFEMP2, GMIP, IKBKE, DDR1, FASTKD1, SIRT6, PKHG2, и SOCS2 с помощью количественной ПЦР, где повышенный уровень от 1 до 7 биомаркеров, выбранных из Р4НВ, GMIP, IKBKE, DDR1, FASTKD1, SIRT6, и PKHG2 и/или сниженный уровень EFEMP2 или SOCS2 по сравнению с контролем указывает на существование рака эндометрия. Предпочтительно, рак женских половых органов представляет собой рак эндометрия.
В одном варианте осуществления, может быть определен уровень экспрессии 2-8 биомаркеров, выбранных из Р4НВ, EFEMP2, GMIP, IKBKE, DDR1, FASTKD1, SIRT6, и PKHG2. 2-8 биомаркеров также могут быть выбраны из Р4НВ, GMIP, IKBKE, DDR1, FASTKD1, SIRT6, PKHG2, и SOCS2.
Определение уровня может включать контактирование указанных одного или нескольких биомаркеров с праймерами и реагентами, способными амплифицировать специфически указанные один или несколько биомаркеров и определение уровня указанного амплифицированного одного или нескольких биомаркеров с зондом или зондами, которые гибридизируются с указанным амплифицированным биомаркером. Зонд гибридизируется специфически с указанным амплифицированным биомаркером.
Следующие комбинации биомаркеров могут, в частности, быть определены в соответствии со способом согласно настоящему изобретению: Р4НВ и EFEMP2; Р4НВ и IKBKE; Р4НВ и GMIP; EFEMP2 и IKBKE; EFEMP2 и Р4НВ; Р4НВ, GMIP, и IKBKE; Р4НВ, GMIP, и IKBKE.
Также следующую комбинацию маркеров можно определить в соответствии со способом согласно настоящему изобретению, где указанная комбинация включает IKBKE и Р4НВ; IKBKE и SOCS2; Р4НВ и SOCS2; GMIP и IKBKE; GMIP и Р4НВ; GMIP и SOCS2; GMIP, SOCS2, и IKBKE; GMIP, SOCS2, и Р4НВ; GMIP, IKBKE, и Р4НВ; IKBKE, P4HB, и SOCS2; GMIP, IKBKE, Р4НВ, и SOCS2; GMIP, SOCS2, IKBKE, и EPS8L2; GMIP, SOCS2, Р4НВ, и EPS8L2; GMIP, IKBKE, Р4НВ, и EPS8L2; IKBKE, Р4НВ, SOCS2, и EPS8L2; GMIP, IKBKE, Р4НВ, SOCS2, и DDR1; GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2, и PPP1R16A; GMIP, IKBKE, Р4НВ, SOCS2, PHKG2, и RASSF7; GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2, и DDR1; GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2, PPP1R16A, и DDR1; DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, RASSF7, SIRT6, TJP3, и SOCS2; или DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, RASSF7, SIRT6, TJP3, RNF183 и SOCS2.
Кроме того, можно определить следующую комбинацию маркеров в соответствии со способом согласно настоящему изобретению, где указанная комбинация включает GMIP, IKBKE, Р4НВ, SOCS2 и FASTKD1; GMIP, IKBKE, Р4НВ, SOCS2 и DDR1; GMIP, IKBKE, Р4НВ, SOCS2 и PHKG2; GMIP, IKBKE, Р4НВ, SOCS2 и SIRT6; GMIP, IKBKE, Р4НВ, SOCS2 и АСАА1; GMIP, IKBKE, Р4НВ, SOCS2 и EFEMP2; GMIP, IKBKE, Р4НВ, SOCS2 и EPS8L2; GMIP, IKBKE, Р4НВ, SOCS2 и P2RX4; GMIP, IKBKE, Р4НВ, SOCS2 и PPFIBP2; GMIP, IKBKE, P4HB, SOCS2 и PPP1R16A; GMIP, IKBKE, P4HB, SOCS2, ACAA1 и FASTKD1; GMIP, IKBKE, P4HB, SOCS2, PHKG2 и FASTKD1; GMIP, IKBKE, P4HB, SOCS2, SIRT6 и FASTKD1; ACAA1, AP1M2, EPS8L2, IKBKE, P2RX4, P4HB, PPFIBP2, PPP1R16A, SIRT6, и EFEMP2; GMIP, IKBKE, P4HB, и EFEMP2; DDR1, FASTKD1, PHKG2, SIRT6, SOCS2, GMIP, IKBKE, P4HB, и EFEMP2; DDR1, FASTKD1, PHKG2, SIRT6, GMIP, IKBKE, P4HB, и EFEMP2; или P4HB, EFEMP2, IKBKE, GMIP, и FASTKD1.
Кроме того, можно определить следующую комбинацию маркеров в соответствии со способом согласно настоящему изобретению, где указанная комбинация включает GMIP, IKBKE, P4HB, EFEMP2 и FASTKD1; GMIP, IKBKE, P4HB, EFEMP2 и DDR1; GMIP, IKBKE, P4HB, EFEMP2 и PHKG2; GMIP, IKBKE, P4HB, EFEMP2 и SIRT6; GMIP, IKBKE, P4HB, EFEMP2 и ACAA1; GMIP, IKBKE, P4HB, SOCS2 и EFEMP2; GMIP, IKBKE, P4HB, EFEMP2 и EPS8L2; GMIP, IKBKE, P4HB, EFEMP2 и P2RX4; GMIP, IKBKE, P4HB, EFEMP2 и PPFIBP2; GMIP, IKBKE, P4HB, EFEMP2 и PPP1R16A; GMIP, IKBKE, P4HB, EFEMP2, ACAA1 и FASTKD1; GMIP, IKBKE, P4HB, EFEMP2, PHKG2 и FASTKD1; или GMIP, IKBKE, P4HB, EFEMP2, SIRT6 и FASTKD1.
Способы согласно настоящему изобретению могут дополнительно включать обеспечение образца маточной жидкости, полученного от пациента с помощью устройства Пайпиля или шприца, где пациент имеет фактор риска или симптом рака эндометрия; контактирование указанного образца с агентом, способным предохранять, предотвращать или ослаблять деградацию РНК в указанном образце маточной жидкости; определение в указанном образце уровня экспрессии мРНК, соответствующей от 1 до 20 описанным в настоящей заявке маркерам (предпочтительно 2-8 маркерам) и одного или нескольких эндогенных генов, используя количественную ПЦР; нормализацию уровня экспрессии от 1 до 20 (предпочтительно 2-8 маркеров) описанных в настоящей заявке биомаркеров с одним или несколькими эндогенными генами; сравнение нормализованного уровня от 1 до 20 (предпочтительно 2-8 маркеров) биомаркеров с контрольным значением, где дифференциальная экспрессия от 1 до 20 (предпочтительно 2-8 маркеров) биомаркеров указывает на рак эндометрия или повышенную вероятность рака эндометрия.
Настоящее изобретение дополнительно относится к диагностическому способу in vitro, который включает обеспечение образца маточной жидкости, полученного от пациента с помощью устройства Пайпиля или шприца, где пациент имеет фактор риска или симптом рака эндометрия; контактирование указанного образца с агентом, способным предохранять, предотвращать или ослаблять деградацию РНК в указанном образце маточной жидкости; определение в указанном образце уровня экспрессии мРНК, соответствующей от 1 до 20 описанным в настоящей заявке маркерам (предпочтительно 2-8 маркерам) и одного или нескольких эндогенных генов, используя количественную ПЦР; нормализацию уровня экспрессии от 1 до 20 (предпочтительно 2-8 маркеров) описанных в настоящей заявке биомаркеров с одним или несколькими эндогенными генами; сравнение нормализованного уровня от 1 до 20 (предпочтительно 2-8 маркеров) биомаркеров с контрольным значением, где дифференциальная экспрессия от 1 до 20 (предпочтительно 2-8 маркеров) биомаркеров указывает на рак эндометрия или повышенную вероятность рака эндометрия.
Один или несколько эндогенных генов могут быть выбраны из POLR2A, В2М, PFN1, HMBS, G6PD, и PABPN1.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня от 1-17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, и/или от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В специфическом аспекте этого варианта осуществления, если уровень от 1 до 17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, повышены относительно контрольного значения и/или уровень от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, снижены относительно контрольного значения, то это указывает на рак эндометрия или повышенный шанс наличия рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с другим аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
Из биомаркеров, представленных в таблице 1, было обнаружено, что уровни CGN, P4HB, PPP1R16A, IKBKE, RASSF7, RNF183, и TJP3, имеют наивысший средний уровень сверхэкспрессии в исследованиях ОТ-ПЦР по сравнению с их экспрессией в нормальных образцах (например, не имеющим рака эндометрия). Таким образом, учитывая, что ОТ-ПЦР эксперименты демонстрируют высокий уровень статистически достоверным образом (все р-значения меньше, чем 0,0001 для набора исследуемых образцов) для этих маркеров, они представляют предпочтительные маркеры для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия. Таким образом, уровни CGN, P4HB, PPP1R16A, IKBKE, RASSF7, RNF183, и TJP3 являются очень хорошими предсказателями рака эндометрия и/или повышенной вероятности наличия рака эндометрия. Уровни этих маркеров менее вероятно дают ложноположительные результаты по сравнению с другими маркерами, уровни экспрессии которые не являются настолько высокими и/или настолько достоверными. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня одного или нескольких биомаркеров, выбранных из CGN, P4HB, PPP1R16A, IKBKE, RASSF7, RNF183, и TJP3, где если один или нескольких указанных маркеров дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака. Характерные картины фингерпринтов/профили экспрессии, имеющие от 1-7 биомаркеров, выбранных из CGN, P4HB, PPP1R16A, IKBKE, RASSF7, RNF183, и TJP3 и от 1-13 биомаркеров, выбранных из АСАА1, АР1М2, DDR1, EPS8L2, FASTKD1, GMIP, P2RX4, PHKG2, PPFIBP2, SIRT6, EFEMP2, SOCS2 и DCN, являются одним из примеров наборов предпочтительных профилей для диагностики и/или предсказания повышенной вероятности рака эндометрия. Специфические примеры таких профилей описаны ниже. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
Из биомаркеров, представленных в таблице 1, было обнаружено, что по уровню некоторых биомаркеров можно дифференцировать образцы от пациентов, имеющих злокачественное новообразование, по сравнению с нормальными образцами (или контролем) и образцами от пациентов в секреторной фазе менструального цикла. Таким образом, уровни АСАА1, DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, RASSF7, SIRT6, TJP3, SOCS2 и DCN являются очень хорошими предсказателями рака эндометрия в пре- и пост-менопаузных женщин и в пери-менопаузных женщин, уровни этих маркеров менее вероятно дают ложноположительные результаты по сравнению с другими маркерами, уровни экспрессии которых изменяют в зависимости от цикла. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня одного или нескольких биомаркеров, выбранных из АСАА1, DDR1, EPS8L2, GMIP, IKBKE, LSR, P2RX4, Р4НВ, PHKG2, PPFIBP2, RASSF7, SIRT6, TJP3, SOCS2 и DCN, где, если один или нескольких указанных маркеров дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Характерные картины фингерпринтов/профили экспрессии, имеющие от 1-15 маркеров, выбранных из АСАА1, DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, SIRT6, TJP3, SOCS2 и DCN и от 1 до 5 маркеров, выбранных из АР1М2, CGN, FASTKD1, RNF183, и EFEMP2, являются одним из примеров наборов предпочтительных профилей для диагностики и/или предсказания повышенной вероятности рака эндометрия, поскольку уровень экспрессии по меньшей мере одного из маркеров в профиле не изменяется в зависимости от фазы менструального цикла. Специфические примеры таких профилей описаны ниже. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня одного или нескольких биомаркеров, выбранных из IKBKE, Р4НВ, SOCS2, GMIP, DDR1, EPS8L2, PPP1R16A, P2RX4, PHKG2, RASSF7, SIRT6, TJP3, АР1М2, RNF183, и DCN, где если один или нескольких указанных маркеров дифференциально экспрессируются по сравнению с контрольным значением, то у индивидуума диагностируется эндометриальный и/или повышенная вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня одного или нескольких биомаркеров, выбранных из IKBKE, Р4НВ, SOCS2, GMIP, DDR1, EPS8L2, PPP1R16A, P2RX4, PHKG2, RASSF7, SIRT6, и TJP3, где, если один или нескольких указанных маркеров дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В одном варианте осуществления согласно изобретению, предпочтительные биомаркеры для диагностики рака эндометрия и/или диагностики повышенной вероятности рака эндометрия представляют собой IKBKE, P4HB, SOCS2, GMIP, DDR1, EPS8L2, и PPP1R16A. В одном аспекте, определяют уровень биомаркера в первичной опухоли. В одном аспекте, определяют уровень биомаркера в крови, плазме или сыворотке. В одном аспекте, определяют уровень биомаркера в маточной жидкости. Таким образом, способ в соответствии с этим вариантом осуществления, включает получение образца и определение уровня от 1 до 7 биомаркеров, выбранных из IKBKE, P4HB, SOCS2, GMIP, DDR1, EPS8L2, и PPP1R16A, где дифференциальная экспрессия одного или нескольких из этих биомаркеров по сравнению с контрольным значением указывает на рак эндометрия и/или повышенный риск наличия рака эндометрия. В одном аспекте настоящего изобретения, определяют и/или оценивают уровень белка биомаркера. В другом аспекте, определяют и/или оценивают уровень экспрессии мРНК.
В одном варианте осуществления согласно изобретению, предпочтительные биомаркеры для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия включают GMIP, IKBKE, P4HB, RASSF7, DDR1, RNF183, EFEMP2 и SOCS2. Было обнаружено, что GMIP, IKBKE, P4HB, RASSF7, DDR1, RNF183, EFEMP2 и SOCS2 имеют очень хорошие AUROC значения и таким образом являются неожиданно хорошими классификаторами в исследуемом наборе образцов. В одном аспекте, определяют уровень биомаркера в первичной опухоли. В одном аспекте, определяют уровень биомаркера в крови, плазме или сыворотке. В одном аспекте, определяют уровень биомаркера в маточной жидкости. Таким образом, способ в соответствии с этим вариантом осуществления, включает получение образца и определение уровня от 1 до 8 биомаркеров, выбранных из GMIP, IKBKE, P4HB, RASSF7, DDR1, RNF183, EFEMP2 и SOCS2, где дифференциальная экспрессия одного или нескольких из этих биомаркеров по сравнению с контрольным значением указывает на рак эндометрия и/или повышенный риск наличия рака эндометрия. В одном аспекте настоящего изобретения, определяют и/или оценивают уровень белка биомаркера. В другом аспекте, определяют и/или оценивают уровень экспрессии мРНК.
В одном варианте осуществления согласно изобретению, предпочтительные биомаркеры для диагностики рака эндометрия и/или диагностики повышенной вероятности рака эндометрия включают P2RX4, P4HB, PHKG2, PPFIBP2 и SOCS2. В результате этих исследований, было обнаружено, что P2RX4, P4HB, PHKG2, PPFIBP2 и SOCS2 имеют очень хорошую специфичность для диагностирования рака эндометрия. В одном аспекте, определяют уровень биомаркера в первичной опухоли. В одном аспекте, определяют уровень биомаркера в крови, плазме или сыворотке. В одном аспекте, определяют уровень биомаркера в маточной жидкости. Таким образом, способ в соответствии с этим вариантом осуществления, включает получение образца и определение уровня от 1 до 5 биомаркеров, выбранных из P2RX4, P4HB, PHKG2, PPFIBP2 и SOCS2, где дифференциальная экспрессия одного или нескольких из этих биомаркеров по сравнению с контрольным значением указывает на рак эндометрия и/или повышенный риск наличия рака эндометрия. В одном аспекте настоящего изобретения, определяют и/или оценивают уровень белка биомаркера. В другом аспекте, определяют и/или оценивают уровень экспрессии мРНК.
В одном варианте осуществления согласно изобретению, предпочтительные биомаркеры для диагностики рака эндометрия и/или диагностики повышенной вероятности рака эндометрия включают IKBKE, P4HB, RASSF7, и RNF183. В результате этих исследований, было обнаружено, что IKBKE, P4HB, RASSF7, и RNF183 имеют очень хорошую чувствительность для диагностирования рака эндометрия. В одном аспекте, определяют уровень биомаркера в первичной опухоли. В одном аспекте, определяют уровень биомаркера в крови, плазме или сыворотке. В одном аспекте, определяют уровень биомаркера в маточной жидкости. Таким образом, способ в соответствии с этим вариантом осуществления, включает получение образца и определение уровня от 1 до 4 биомаркеров, выбранных из IKBKE, P4HB, RASSF7, и RNF183, где дифференциальная экспрессия одного или нескольких из этих биомаркеров по сравнению с контрольным значением указывает на рак эндометрия и/или повышенный риск наличия рака эндометрия. В одном аспекте настоящего изобретения, определяют и/или оценивают уровень белка биомаркера. В другом аспекте, определяют и/или оценивают уровень экспрессии мРНК.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня от 2 до 7 биомаркеров, выбранных из GMIP, IKBKE, P4HB, SOCS2, EPS8L2, PPP1R16A, и TJP3, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В результате проведения исследований, описанных в настоящей заявке, неожиданно было обнаружено, что комбинации (например, профили и/или характерные картины фингерпринтов) биомаркеров, выбранных из GMIP, IKBKE, P4HB, SOCS2, EPS8L2, PPP1R16A, и TJP3, имеют очень хорошую чувствительность и специфичность для рака эндометрия и AUROC значения для различных комбинаций этих маркеров свидетельствуют о способности этих маркеров разделять пациентов, имеющих рак эндометрия, от тех пациентов, которые не имеют рака эндометрия.
В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня от 2 до 9 биомаркеров, выбранных из GMIP, IKBKE, P4HB, SOCS2, EFEMP2, PHKG2, SIRT6, DDR1, и FASTKD1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В результате проведения исследований, описанных в настоящей заявке, неожиданно было обнаружено, что комбинации (например, профили и/или характерные картины фингерпринтов) биомаркеров, выбранных из GMIP, IKBKE, P4HB, SOCS2, EFEMP2, PHKG2, SIRT6, DDR1, и FASTKD1 имеют очень хорошую чувствительность и специфичность для рака эндометрия и AUROC значения для различных комбинаций этих маркеров свидетельствуют о способности этих маркеров разделять пациентов, имеющих рак эндометрия, от тех пациентов, которые не имеют рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру. В одном специфическом аспекте этого варианта осуществления, диагностический способ in vitro включает обеспечение образца маточной жидкости, полученного от пациента с помощью устройства Пайпиля или шприца, где пациент имеет фактор риска или симптом рака эндометрия; контактирование указанного образца с агентом, способным предохранять, предотвращать или ослаблять деградацию РНК в указанном образце маточной жидкости; определение в указанном образце уровня экспрессии мРНК, соответствующей указанным от 2 до 9 маркеров, и одного или нескольких эндогенных генов, используя количественную ПЦР; нормализацию уровня экспрессии указанных от 2 до 9 биомаркеров с одним или несколькими эндогенными генами; сравнение нормализованного уровня от 2 до 9 биомаркеров с контрольным значением, где дифференциальная экспрессия от 2 до 9 биомаркеров указывает на рак эндометрия или повышенную вероятность рака эндометрия. В одном специфическом аспекте этого метода, указанные один или нескольких эндогенных генов выбирают из POLR2A, В2М, PFN1, HMBS,G6PD,HPABPN1.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня от 2-8 биомаркеров, выбранных из GMIP, IKBKE, P4HB, EFEMP2, PHKG2, SIRT6, DDR1, и FASTKD1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В результате проведения исследований, описанных в настоящей заявке, неожиданно было обнаружено, что комбинации (например, профили и/или характерные картины фингерпринтов) биомаркеров, выбранных из GMIP, IKBKE, P4HB, EFEMP2, PHKG2, SIRT6, DDR1, и FASTKD1 имеют очень хорошую чувствительность и специфичность для рака эндометрия и AUROC значения для различных комбинаций этих маркеров свидетельствуют о способности этих маркеров разделять пациентов, имеющих рак эндометрия, от тех пациентов, которые не имеют рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру. В соответствии с одним аспектом этого варианта осуществления, уровень от 2 до 8 биомаркеров определяют с помощью количественной ПЦР. В одном специфическом аспекте этого варианта осуществления, диагностический способ in vitro включает обеспечение образца маточной жидкости, полученного от пациента с помощью устройства Пайпиля или шприца, где пациент имеет фактор риска или симптом рака эндометрия; контактирование указанного образца с агентом, способным предохранять, предотвращать или ослаблять деградацию РНК в указанном образце маточной жидкости; определение в указанном образце уровня экспрессии мРНК, соответствующей указанным от 2 до 9 маркеров, и одного или нескольких эндогенных генов, используя количественную ПЦР; нормализацию уровня экспрессии указанных от 2 до 8 биомаркеров с одним или несколькими эндогенными генами; сравнение нормализованного уровня от 2 до 8 биомаркеров с контрольным значением, где дифференциальная экспрессия от 2 до 8 биомаркеров указывает на рак эндометрия или повышенную вероятность рака эндометрия. В одном специфическом аспекте этого метода, указанные один или нескольких эндогенных генов выбирают из POLR2A, В2М, PFN1, HMBS, G6PD, и PABPN1.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от особи и определение уровня от 2-8 биомаркеров, выбранных из GMIP, IKBKE, P4HB, SOCS2, PHKG2, SIRT6, DDR1, и FASTKD1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В результате проведения исследований, описанных в настоящей заявке, неожиданно было обнаружено, что комбинации (например, профили и/или характерные картины фингерпринтов) биомаркеров, выбранных из GMIP, IKBKE, P4HB, SOCS2, PHKG2, SIRT6, DDR1, и FASTKD1 имеют очень хорошую чувствительность и специфичность для рака эндометрия и AUROC значения для различных комбинаций этих маркеров свидетельствуют о способности этих маркеров разделять пациентов, имеющих рак эндометрия, от тех пациентов, которые не имеют рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру. В соответствии с одним аспектом этого варианта осуществления, уровень от 2 до 8 биомаркеров определяют с помощью количественной ПЦР. В одном специфическом аспекте этого варианта осуществления, диагностический способ in vitro включает обеспечение образца маточной жидкости, полученного от пациента с помощью устройства Пайпиля или шприца, где пациент имеет фактор риска или симптом рака эндометрия; контактирование указанного образца с агентом, способным предохранять, предотвращать или ослаблять деградацию РНК в указанном образце маточной жидкости; определение в указанном образце уровня экспрессии мРНК, соответствующей указанным от 2 до 8 маркеров, и одного или нескольких эндогенных генов, используя количественную ПЦР; нормализацию уровня экспрессии указанных от 2 до 8 биомаркеров с одним или несколькими эндогенными генами; сравнение нормализованного уровня от 2 до 8 биомаркеров с контрольным значением, где дифференциальная экспрессия от 2 до 8 биомаркеров указывает на рак эндометрия или повышенную вероятность рака эндометрия. В одном специфическом аспекте этого метода, указанные один или нескольких эндогенных генов выбирают из POLR2A, В2М, PFN1, HMBS, G6PD, и PABPN1.
В одном варианте осуществления, настоящее изобретение обеспечивает способ для характеристики образца, полученного от пациента, для прогностических, диагностических и/или фармакогеномных применений. Характеристику образца, полученного от пациента, путем определения уровней одного или нескольких биомаркеров, представленных в таблице 1, можно использовать для обеспечения информации относительно диагностики рака эндометрия, прогрессирования заболевания, диагностики типа рака эндометрия (и/или подтипа), и выбор подходящего терапевтического лечения. В соответствии со способом согласно изобретению, образец получают от особи. Особь может являться здоровой особью, особью, у которой диагностировано злокачественное новообразование, особью, у которой подозревается наличие злокачественного новообразования, особью, проявляющей один или несколько симптомов рака и/или особью, нуждающейся в скрининге относительно злокачественного новообразования. Способ включает стадию определения уровня биомаркера (ов), представленных в таблице 1, в образце, полученном от пациента. Альтернативные методы для определения биомаркеров в РНК и/или белке (IHC, анализ экспрессии мРНК, и др.) можно использовать в этих методах. Обнаружение повышенных уровней от 1 до 17 биомаркеров, представленных в таблице 1, для которых было обнаружено, что они активированы при раке эндометрия и/или определение сниженных уровней от 1 до 3 биомаркеров, для которых было обнаружено, что они подавлены при раке эндометрия, по сравнению с контрольным значением, указывает на то, что пациент имеет повышенную вероятность наличия рака эндометрия.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака женских половых органов, который включает использование диагностических реагентов для исследования на или обнаружение от 1 до 20 биомаркеров, перечисленных в таблице 1. В более специфическом аспекте этого варианта осуществления, диагностические реагенты используются для определения уровня от 1 до 20 биомаркеров, перечисленных в таблице 1, для диагностики рака эндометрия. В более специфическом аспекте этого варианта осуществления, диагностические реагенты используются для определения уровня от 1 до 20 биомаркеров, перечисленных в таблице 1, для определения рака эндометрия. В одном аспекте этого варианта осуществления, определяют уровень мРНК, соответствующей от 1 до 20 биомаркерам. В одном аспекте этого варианта осуществления, определяют уровень мРНК, соответствующей от 2 до 17 биомаркерам. В одном аспекте этого варианта осуществления, определяют уровень мРНК, соответствующей от 3 до 15 биомаркерам. В одном аспекте этого варианта осуществления, определяют уровень белка или полипептида, соответствующий от 1 до 20 биомаркерам. В одном аспекте этого варианта осуществления, определяют уровень белка или полипептида, соответствующий от 2 до 17 биомаркерам. В одном аспекте этого варианта осуществления, определяют уровень белка или полипептида, соответствующий от 3 до 15 биомаркерам. В одном аспекте этого варианта осуществления, анализируемый образец представляет собой образец опухоли. В одном аспекте этого варианта осуществления, анализируемый образец представляет собой образец маточной жидкости. В одном аспекте этого варианта осуществления, анализируемый образец представляет собой образец сыворотки, крови или плазмы. В одном аспекте, образец, который используют, получен путем применения мягкого, соломинко-подобного устройства (пайпиля), который используют для отсасывания небольшого образца выстилки из матки {например, маточной жидкости). В одном аспекте, образец получен путем применения инструмента с острым краем, который называется кюретка, путем соскребания небольшого образца и его сбора с помощью шприца или отсасывания (например, дилятация и кюретаж). В одном аспекте, образец получен путем применения электронного отсасывающего устройства (например, Vabra аспирация). В одном аспекте, образец получен путем применения распыления жидкости (струйного промывания) для смывания некоторого количества ткани, выстилающей матку. В некоторых аспектах, можно использовать щеточку для удаления некоторого количества выстилки перед осуществлением промывки. В одном аспекте, образец крови, сыворотки или плазмы анализируют относительно от 1 до 20 биомаркеров согласно изобретению.
В микропанельных исследованиях, было обнаружено, что GMIP сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия GMIP коррелирует в первичной опухоли и маточной жидкости. Следовательно, GMIP является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие GMIP, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня GMIP и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, GMIP самостоятельно имеет AUROC значение в таблице 6 0,88 IKBKE самостоятельно имеет AUROC значение 0,90, когда эти два маркера объединяются вместе в профиле, то AUROC значение 0,92 с существенным повышением специфичности (повышенное AUROC значение указывает на повышенную способность разделения популяции). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что IKBKE сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия IKBKE коррелирует в первичной опухоли и маточной жидкости. Следовательно, IKBKE является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие IKBKE, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня IKBKE и от 2 до 19 биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, IKBKE самостоятельно имеет AUROC значение в таблице 6 0,90, Р4НВ самостоятельно имеет AUROC значение 0,97, когда эти два маркера объединяются вместе в профиле, то AUROC значение 0,98 с существенным повышением специфичности до 100% (повышенное AUROC значение указывает на повышенную способность разделения популяции). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что Р4НВ сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия Р4НВ коррелирует в первичной опухоли и маточной жидкости. Следовательно, Р4НВ является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие Р4НВ, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня Р4НВ и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, Р4НВ самостоятельно имеет AUROC значение в таблице 6 0,97, SOCS2 самостоятельно имеет AUROC значение 0,93, когда эти два маркера объединяются вместе в профиле, то AUROC значение 1 с существенным повышением специфичности до 100% (повышенное AUROC значение указывает на повышенную способность разделения популяции). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что экспрессия SOCS2 подавлена в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия SOCS2 коррелирует в первичной опухоли и маточной жидкости. Следовательно, SOCS2 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие SOCS2, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня SOCS2 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, SOCS2 самостоятельно имеет AUROC значение в таблице 6 0,93, GMIP самостоятельно имеет AUROC значение 0,88, когда эти два маркера объединяются вместе в профиле, то AUROC значение 0,999 с существенным повышением чувствительности до 100% (повышенное AUROC значение указывает на повышенную способность разделения популяции). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что EPS8L2 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,002 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия EPS8L2 коррелирует в первичной опухоли и маточной жидкости. Следовательно, EPS8L2 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие EPS8L2, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня EPS8L2 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда EPS8L2 комбинируют с GMIP, IKBKE, P4HB, SOCS2, и DDR1, то значение AUROC равно 1 и чувствительность составляет около 96% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что RASSF7 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0005 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия RASSF7 коррелирует в первичной опухоли и маточной жидкости. Следовательно, RASSF7 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие RASSF7, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня RASSF7 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда RASSF7 комбинируют с DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, SIRT6, TJP3 и SOCS2, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что DDR1 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,02 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия DDR1 коррелирует в первичной опухоли и маточной жидкости. Следовательно, DDR1 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие DDR1, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня DDR1 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда DDR1 комбинируют с EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, SIRT6, TJP3, SOCS2, и RNF183, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что PPP1R16A сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия PPP1R16A коррелирует в первичной опухоли и маточной жидкости. Следовательно, PPP1R16A является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие PPP1R16A, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня PPP1R16A и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда PPP1R16A комбинируют с GMIP, IKBKE, P4HB, SOCS2, и EPS8L2, то значение AUROC приблизительно равно 1 и чувствительность составляет около 92% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что PHKG2 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия PHKG2 коррелирует в первичной опухоли и маточной жидкости. Следовательно, PHKG2 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие PHKG2, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня PHKG2 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда PHKG2 комбинируют с DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PPP1R16A, SIRT6, TJP3, SOCS2, и RNF183, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что P2RX4 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0005 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия P2RX4 коррелирует в первичной опухоли и маточной жидкости. Следовательно, P2RX4 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие P2RX4, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня P2RX4 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда P2RX4 комбинируют с DDR1, EPS8L2, GMIP, IKBKE, P4HB, PHKG2, PPP1R16A, SIRT6, TJP3, SOCS2, и RNF183, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что АСАА1 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия АСАА1 коррелирует в первичной опухоли и маточной жидкости. Следовательно, АСАА1 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие АСАА1, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня АСАА1 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с одним аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В микропанельных исследованиях, было обнаружено, что АР1М2 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия АР1М2 коррелирует в первичной опухоли и маточной жидкости. Следовательно, АР1М2 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие АР1М2, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня АР1М2 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что CGN сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия CGN коррелирует в первичной опухоли и маточной жидкости. Следовательно, CGN является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие CGN, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня CGN и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что FASTKD1 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия FASTKD1 коррелирует в первичной опухоли и маточной жидкости. Следовательно, FASTKD1 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие FASTKD1, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня FASTKD1 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что PPFIBP2 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,02 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия PPFIBP2 коррелирует в первичной опухоли и маточной жидкости. Следовательно, PPFIBP2 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие PPFIBP2, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня PPFIBP2 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что RNF183 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия RNF183 коррелирует в первичной опухоли и маточной жидкости. Следовательно, RNF183 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие RNF183, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня RNF183 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда RNF183 комбинируют с DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, SIRT6, TJP3, и SOCS2, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что SIRT6 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия SIRT6 коррелирует в первичной опухоли и маточной жидкости. Следовательно, SIRT6 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие SIRT6, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня SIRT6 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда SIRT6 комбинируют с DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, TJP3, SOCS2, и RNF183, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что TJP3 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия TJP3 коррелирует в первичной опухоли и маточной жидкости. Следовательно, TJP3 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие TJP3, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня TJP3 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. Например, когда TJP3 комбинируют с DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, SIRT6, SOCS2, и RNF183, то значение AUROC равно 1 и чувствительность составляет 100% и специфичность составляет 100% (см. таблицу 11). В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что EFEMP2 сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,0001 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия EFEMP2 коррелирует в первичной опухоли и маточной жидкости. Следовательно, EFEMP2 является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие EFEMP2, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня EFEMP2 и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В микропанельных исследованиях, было обнаружено, что DCN сверхэкспрессируется в образцах от пациентов, имеющих рак эндометрия, по сравнению с нормальными значениями (непораженных). В ОТ-ПЦР исследованиях этот результат был подтвержден и р-значение меньше чем 0,005 было получено для образцов аспиратов от непораженных особей при сравнении с аспиратами от особей, имеющих рак эндометрия. Также было обнаружено, что экспрессия DCN коррелирует в первичной опухоли и маточной жидкости. Следовательно, DCN является очень хорошим биомаркером для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. Кроме того, полагают, что характерные картины фингерпринтов/профили, имеющие DCN, являются пригодными для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия, который включает получение образца от особи и определение уровня DCN, и от 2 до 19 других биомаркеров, выбранных из таблицы 1, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру.
В одном варианте осуществления, изобретение обеспечивает диагностический способ in vitro для диагностики рака эндометрия или повышенной вероятности эндометриального, который включает определение уровня (1) от 1 до 17 биомаркера (ов), выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, и TJP3 в образце от пациента, где повышенный уровень указанных от 1 до 17 биомаркеров по сравнению с контрольным значением указывает на диагноз рака эндометрия или повышенную вероятность рака эндометрия и/или (2) определение уровня от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где сниженный уровень EFEMP2, SOCS2, и/или DCN по сравнению с контрольным значением указывает на диагноз рака эндометрия или повышенную вероятность рака эндометрия. В одном предпочтительном аспекте, способ диагностирования рака эндометрия или повышенной вероятности рака эндометрия включает применение одного или более активированных биомаркеров и одного или более подавленных биомаркеров в соответствии с таблицей 1.
В одном аспекте этого варианта осуществления, пациент имеет фактор риска для рака эндометрия или подвергается скринингу для рака эндометрия.
В одном аспекте этого варианта осуществления, образец от указанного пациента получен от пациента с атипичным маточным кровотечением.
В одном аспекте этого варианта осуществления, образец от указанного пациента получен от пациента, имеющего эндометрий с увеличенной толщиной.
В одном аспекте этого варианта осуществления, образец от указанного пациента получен от пре-менопаузного, пери-менопаузного, или пост-менопаузного пациента.
В одном аспекте этого варианта осуществления, пациент является пре-менопаузным.
В одном аспекте этого варианта осуществления, пациент является пери-менопаузным.
В одном аспекте этого варианта осуществления, пациент является пост-менопаузным.
В одном аспекте этого варианта осуществления, образец выбирают из образца ткани, крови и/или сыворотки, и маточной жидкости.
В одном аспекте этого варианта осуществления, образец представляет собой образец маточной жидкости.
В одном аспекте этого варианта осуществления, образец маточной жидкости получен путем аспирации.
В одном аспекте этого варианта осуществления, уровень биомаркера (ов) определяют с антителом.
В одном аспекте этого варианта осуществления, уровень биомаркера (ов) определяют с помощью ОТ-ПЦР. В одном специфическом аспекте, уровень биомаркера определяют путем количественной ОТ-ПЦР.
В одном аспекте этого варианта осуществления, маркеры выбирают из IKBKE, Р4НВ, SOCS2, GMIP, DDR1, EPS8L2, PPP1R16A, P2RX4, PHKG2, RASSF7, SIRT6, и TJP3.
В одном аспекте этого варианта осуществления, маркер (ы) выбирают из P2RX4, Р4НВ, PHKG2, PPFIBP2, и SOCS2.
В одном аспекте этого варианта осуществления, маркеры выбирают из Р4НВ, RASSF7, RNF183, и IKBKE.
В одном аспекте этого варианта осуществления, определяют от 2 до 20 маркеров.
В одном аспекте этого варианта осуществления, определяют один или несколько дополнительных вспомогательных биомаркеров.
В одном аспекте этого варианта осуществления, один или более вспомогательных биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и дополнительных биомаркеров для обнаружения рака эндометрия.
В одном аспекте этого варианта осуществления, один или более вспомогательных биомаркеров выбирают из дифференциальных диагностических биомаркеров.
В одном аспекте этого варианта осуществления, один или более вспомогательных биомаркеров выбирают из прогностических маркеров.
В одном аспекте этого варианта осуществления, один или более вспомогательных биомаркеров выбирают из маркеров классификации рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает нуклеиновую кислоту, выбранную из IKBKE мРНК, кДНК, или их комплемента; Р4НВ мРНК, кДНК, или их комплемента; SOCS2 мРНК, кДНК, или их комплемента; GMIP мРНК, кДНК, или их комплемента; DDR1 мРНК, кДНК, или их комплемента; EPS8L2 мРНК, кДНК, или их комплемента; и PPP1R16A мРНК, кДНК, их комплемента, для применения для диагностики рака эндометрия или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает нуклеиновую кислоту, выбранную из АСАА1 мРНК, кДНК, или их комплемента; АР1М2 мРНК, кДНК, или их комплемента; CGN мРНК, кДНК, или их комплемента; P2RX4 мРНК, кДНК, или их комплемента; PPFIBP2 мРНК, кДНК, или их комплемента; RASSF7 мРНК, кДНК, или их комплемента; TJP3 мРНК, кДНК, или их комплемента; DCN мРНК, кДНК, или их комплемента; и RNF183 мРНК, кДНК, или их комплемента, для применения для диагностики рака эндометрия или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает нуклеиновую кислоту, выбранную из EFEMP2 мРНК, кДНК, или их комплемента; PHKG2 мРНК, кДНК, или их комплемента; SIRT6 мРНК, кДНК, или их комплемента; и FASTKD1 мРНК, кДНК, или их комплемента, для применения для диагностики рака эндометрия или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает праймеры, выбранные из праймеров для IKBKE; праймеров для Р4НВ; праймеров для SOCS2; праймеров для GMIP; праймеров для DDR1; праймеров для EPS8L2; и праймеров для PPP1R16A; для применения для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает праймеры, выбранные из праймеров для АСАА1; праймеров для АР1М2; праймеров для CGN; праймеров для P2RX4; праймеров для PPFIBP2; праймеров для RASSF7; праймеров для RNF183; праймеров для TJP3; и праймеров для DCN; для применения для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает праймеры, выбранные из праймеров для EFEMP2; праймеров для SIRT6; праймеров для PHKG2; и праймеров для FASTKD1; для применения для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает нуклеиновую кислоту, выбранную из зонда для IKBKE; зонда для Р4НВ; зонда для SOCS2; зонда для GMIP; зонда для DDR1; зонда для EPS8L2; и зонда для PPP1R16A, для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает нуклеиновую кислоту, выбранную из зонда для АСАА1; зонда для АР1М2; зонда для CGN; зонда для P2RX4; зонда для PPFIBP2; зонда для RASSF7; зонда для RNF183; зонда для TJP3; и зонда для DCN, для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает нуклеиновую кислоту, выбранную из зонда для EFEMP2; зонда для FASTKD1; зонда для SIRT6; зонда для GMIP; и зонда для PHKG2, для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает набор, включающий два или больше зондов к 1-20 биомаркерам согласно изобретению, для диагностики рака эндометрия и/или повышенной вероятности рака.
В одном аспекте этого варианта осуществления, изобретение обеспечивает набор, содержащий праймеры для двух или более из 1-20 биомаркеров согласно изобретению для диагностики рака эндометрия и/или повышенной вероятности рака.
В одном аспекте этого варианта осуществления, изобретение обеспечивает антитело, выбранное из антитела к IKBKE; антитела к Р4НВ; антитела к SOCS2; антитела к GMIP; антитела к DDR1; антитела к EPS8L2; и антитела к PPP1R16A, для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает антитело, выбранное из антитела к АСАА1; антитела к АР1М2; антитела к CGN; антитела к P2RX4; антитела к PPFIBP2; антитела к RASSF7; антитела к RNF183; антитела к TJP3; и антитела к DCN, для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает антитело, выбранное из антитела к EFEMP2; антитела к FASTKD1; антитела к SIRT6; антитела к GMIP; и антитела к PHKG2; для диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия.
В одном аспекте этого варианта осуществления, изобретение обеспечивает набор, содержащий антитела к двум или более биомаркерам, представленным в таблице 1, для диагностики рака эндометрия и/или повышенной вероятности рака.
В аспекте этого варианта осуществления, изобретение обеспечивает набор для получения маточной жидкости для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия путем оценки уровней от 1-20 биомаркеров из таблицы 1.
В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 2 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 3 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 4 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 5 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 5 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 7 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 10 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 15 биомаркеров согласно изобретению. В одном аспекте этого варианта осуществления, диагностический способ in vitro включает определение уровня 20 биомаркеров согласно изобретению.
Если специально не указано иначе, все технические и научные термины, используемые в настоящей заявке, имеют аналогичные значения, которые обычно подразумеваются квалифицированным специалистом в данной области техники, к которой относится настоящее изобретения. Несмотря на то, что материалы и методы, сходные с или эквивалентные тем, которые описаны в настоящей заявке, могут использоваться при практическом осуществлении или тестировании в соответствии с настоящим изобретением, подходящие методы и материалы описаны ниже. В случае конфликта, настоящее описание, включая определения, будет преимущественным. Дополнительно, материалы, методы и примеры являются только иллюстративными и не предназначены для ограничения.
Другие характерные особенности и преимущества в соответствии с изобретением будут понятными из последующего подробного описания, и из пунктов формулы изобретения.
Краткое описание фигур
На фигуре 1 показана корреляция уровней экспрессии биомаркеров в первичной опухоли и в маточной жидкости для биомаркеров, включая биомаркеры согласно изобретению. См. пример 3 для подробного описания.
На фигурах 2А и 2В представлены ящик и диаграмма с усами, на которых указано относительное количество РНК (RQ), присутствующее в образцах аспиратов от пациентов, имеющих рак эндометрия, по сравнению с контрольными образцами для каждого гена, как определено с помощью ОТ-ПЦР. 30 образцов опухолей и 24 контролей представлено на диаграммах. Ящики представляют интерквартильную широту для каждого гена и усы указывают от перцентилей 10 до 90 RQ значений для каждого гена. Черта на ящиках указывает серединное RQ. Белые ящики представляют собой значения для образцов опухолей каждого гена и затененные ящики значения для контрольных образцов. См. пример 4 для более подробного описания.
На фигуре 3 представлен пример уровня экспрессии RNF183, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (RNF183_T), нормальных в секреторной фазе (RNF183_S), нормальных, не имеющих рака эндометрия (RNF183_N), и всех нормальных вместе (RNF183_Nt).
На фигуре 4 представлен пример уровня экспрессии АР1М2, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (АР1М2_Т), нормальных в секреторной фазе (AP1M2_S), нормальных, не имеющих рака эндометрия (AP1M2_N), и всех нормальных вместе (AP1M2_Nt).
На фигуре 5 представлен пример уровня экспрессии CGN, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (CGN_T), нормальных в секреторной фазе (CGN_S), нормальных, не имеющих рака эндометрия (CGN_N), и всех нормальных вместе (CGN_Nt).
На фигуре 6 представлен пример уровня экспрессии FASTKD1, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (FASTKD1_T), нормальных в секреторной фазе (FASTKD1_S), нормальных, не имеющих рака эндометрия (FASTKD1_N), и всех нормальных вместе (FASTKD1_Nt).
На фигуре 7 представлен пример уровня экспрессии IKBKE, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (IKBKE _Т), нормальных в секреторной фазе (IKBKE_S), нормальных, не имеющих рака эндометрия (IKBKE_N), и всех нормальных вместе (IKBKE_Nt).
На фигуре 8 представлен пример уровня экспрессии Р4НВ, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (Р4НВ_Т), нормальных в секреторной фазе (P4HB_S), нормальных, не имеющих рака эндометрия (P4HB_N), и всех нормальных вместе (P4HB_Nt).
На фигуре 9 представлен пример уровня экспрессии SOCS2, как определено с помощью ОТ-ПЦР, в аспиратах, полученных от пациентов, имеющих рак эндометрия, (SOCS2_T), нормальных в секреторной фазе (SOCS2_S), нормальных, не имеющих рака эндометрия (SOCS2_N), и всех нормальных вместе (SOCS2_Nt).
На фигуре 10 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: Р4НВ. Тестируемые образцы включают четыре нормальные ткани (N) и четыре опухолевые ткани (Т). Нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. См. пример 6.
На фигуре 11 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: АР1М2. Тестируемые образцы включают четыре нормальные ткани (N) и четыре опухолевые ткани (Т) от 4 различных пациентов. Согласованные нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. См. пример 6.
На фигуре 12 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: IKBKE. Тестируемые образцы включают нормальную ткань (N) и опухолевую ткань (Т). Согласованные нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. См. пример 6.
На фигуре 13 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: EPS8L2. Тестируемые образцы включают 3 нормальные ткани (N) и 3 опухолевые ткани (Т) от 3 различных пациентов. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия. Согласованные нормальные и опухолевые ткани получали от одного и того же пациента. См. пример 6.
На фигуре 14 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: DDR1. Тестируемые образцы включают нормальную ткань (N) и опухолевую ткань (Т). Согласованные нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. См. пример 6.
На фигуре 15 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: CGN. Тестируемые образцы включают четыре нормальные ткани (N) и четыре опухолевые ткани (Т) от четырех различных пациентов. Согласованные нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. См. пример 6.
На фигуре 16 показан вестерн-блоттинг ткани рака эндометрия с антителом к биомаркеру согласно изобретению: TJP3. Тестируемые образцы включают нормальную ткань (N) и опухолевую ткань (Т). Согласованные нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. См. пример 6.
На фигуре 17 показан рассчитанный риск рака, используя 48 неопухолевых образцов и 33 образцов опухолей, используя АСАА1, АР1М2, EPS8L2, IKBKE, P2RX4, Р4НВ, PPFIBP2, PPP1R16A, SIRT6, EFEMP2. См. пример 5.
На фигуре 18 показан рассчитанный риск рака, используя 48 неопухолевых образцов и 33 образцов опухолей, используя FASTKD1, GMIP, P4HB, EFEMP2, SIRT6, и PHKG2. См. пример 5.
На фигуре 19 показан рассчитанный риск рака, используя 48 неопухолевых образцов и 33 образцов опухолей, используя FASTKD1, GMIP, P4HB, EFEMP2, DDR1, и SIRT6. См. пример 5.
Подробное описание изобретения
Настоящее изобретение основано на выявлении ассоциации изменений уровней экспрессии мРНК биомаркеров, перечисленных в таблице 1, в образцах от пациентов, имеющих рак эндометрия, по сравнению с контрольными значениями (например, нормальной тканью (непораженной) или значением). Эти биомаркеры таким образом представляют биомаркеры рака эндометрия. Дополнительно, изобретатели неожиданно обнаружили, что образцы, полученные из маточной жидкости пациентов с раком эндометрия, проявляют профили экспрессии для биомаркеров, перечисленных в таблице 1, которые в целом коррелируют с профилями экспрессии из первичной опухоли. Кроме того, множество маркеров, обнаруженных изобретателями, как предполагают, обнаружено на клеточных поверхностях и/или в крови в качестве маркеров на основе крови (или в других жидкостях организма, таких как маточная жидкость). Как показано в примере 6, показано, что активированные биомаркеры, представленные в таблице 1, сверхэкспрессируются на уровне белка в первичной ткани по сравнению с нормальной непораженной тканью. Например, уровень белка P4HB с помощью вестерн-блоттинг анализа, указывает на то, что этот биомаркер также сверхэкспрессируется на уровне белка. На фигурах 11-16 показана сверхэкспрессия, на уровне белка, АР1М2, IKBKE, EPS8L2, DDR1, CGN, и TJP3. Кроме того, P4HB, PPP1R16A и EPS8L2 представляет специфическую цитоплазматическую экспрессию в опухолевых клетках во всех гистологических типах и степенях дифференцировки карцином, и отсутствие или слабое цитоплазматическое окрашивание в нормальных эпителиальных железах, как определено с помощью метода тканевых матриц (ТМА) иммуногистохимии (IHC).
Эти исследования обеспечивают диагностические биомаркеры рака эндометрия с очень хорошей прогностической значимостью, отдельно или в комбинациях, которые можно определить с помощью методов, которые являются менее инвазивными по сравнению с современным стандартом лечения. Кроме того, изобретатели идентифицировали специфические поднаборы биомаркеров, которые способны отличать, в образцах аспиратов эндометрия, пациентов, пораженных раком эндометрия от других подгрупп непораженных пациентов.
Некоторые исследования, используемые для идентификации (экспрессионная микропанель) и подтверждения достоверности (ОТ-ПЦР) биомаркеров согласно изобретению описаны вкратце ниже и более подробно в разделе примеров.
Более специфически, изобретатели осуществили анализ экспрессии генов на экспрессионных микропанелях для выявления генов, которые дифференциально экспрессируются при раке эндометрия по сравнению с нормальными тканями. Исследования экспрессионной микропанели генов, раскрытые в настоящей заявке, свидетельствуют о том, что множество генов в образцах рака эндометрия сверхэкспрессированы по сравнению с нормальной тканью эндометрия. Было обнаружено, что АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, и TJP3, сверхэкспрессированы в образцах рака эндометрия и EFEMP2, SOCS2 и DCN снижено экспрессированы, по сравнению с их соответствующими уровнями в нормальной ткани эндометрия, используя микропанельную экспериментальную стратегию. Эти результаты обобщены в таблице 1, в которой представлены общепринятое сокращение для гена, номера доступов ENSMBL (соответствующие гену, транскрипту (ам), и белку, относящимся к биомаркерам согласно изобретению), значения кратности изменения и р-значения для статистической достоверности.
Таблица 1: Дифференциальная экспрессия биомаркеров рака эндометрия в первичной опухоли по сравнению с контрольными значениями (полученными из пула непораженной ткани, см. пример 1).
Как показано на фигуре 1, было обнаружено, что маркеры, представленные в таблице 1, также было обнаружено, что они дифференциально экспрессируются в образцах, полученных из маточной жидкости у пациентов, имеющих рак эндометрия. Маркеры, которые не высоко коррелированы, отделяются или дополнительно отдаляются от корреляционной линии на фигуре 1.
Сверхэкспрессия ACAA1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, и TJP3, и подавленная экспрессия DCN, SOCS2, и EFEMP2 при раке эндометрия подтверждается с помощью ОТ-ПЦР, используя независимый набор образцов. Образцы, используемые в этом исследовании, получали из маточной жидкости особей, имеющих рак эндометрия, и от пациентов, не имеющих рака эндометрия. Эти результаты обобщены в таблице 2 и проиллюстрированы на фигуре 2А и 2В. Эти результаты свидетельствуют о том, что эти маркеры проявляют статистически достоверную дифференциальную экспрессию в образцах рака эндометрия в образцах от особей, имеющих рак эндометрия, по сравнению с нормальными особями и/или образцами (например, контрольным значением).
р-значения рассчитывали, используя непараметричный тест Манна-Уитни. Среднее RQ относится к относительному количеству, и SEM относится к среднеквадратическому отклонению.
Обнаружение корреляции уровней экспрессии этих биомаркеров в первичной ткани и маточной жидкости было неожиданным, учитывая гетерогенность маточной жидкости и обнаружения в исходных микропанельных исследованиях. Полагают, что это впервые, когда было показано, что уровни биомаркеров в первичном раке эндометрия коррелируют статистически достоверным образом с биомаркерами, обнаруженными в маточной жидкости, и таким образом это обеспечивает менее инвазивный и более стандартизированный метод скрининга для рака эндометрия и/или повышенного риска рака эндометрия. Изобретение таким образом обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности рака эндометрия путем получения образца маточной жидкости и определения уровня биомаркеров, дифференциально экспрессируемых при раке эндометрия по сравнению с контрольным значением. В одном аспекте, образец маточной жидкости получен путем аспирации. В одном аспекте, образец маточной жидкости получали путем острожного вымывания и/или промывания полости матки. В одном аспекте, определяют уровень мРНК. В одном аспекте, определяют уровень белка. В одном аспекте, биомаркеры выбирают из 20 перечисленных в таблице 1.
Неожиданно, р-значения для индивидуальных биомаркеров в таблице 1, как определено в микропанельных исследованиях, с одним набором образцов существенно улучшались, чем когда аналогичные биомаркеры анализировали с помощью другой техники (количественной ОТ-ПЦР), используя другой набор образцов, полученных от пациента с помощью другого метода. В целом р-значения были больше чем в 100 раз улучшены по сравнению с микропанельными исследованиями.
Изобретателями было обнаружено, что индивидуально каждый из биомаркеров, представленных в таблице 1, имеют прогностическую значимость для диагностики рака эндометрия. Кроме того, комбинации этих биомаркеров имеют дополнительную прогностическую значимость для диагностики рака эндометрия. Например, изобретателями неожиданно было обнаружено, что различные подгруппы биомаркеров, представленные в таблице 1, имеющие от 2-20 биомаркеров в различных комбинациях, дают характерные картины фингерпринтов, имеющие очень хорошую прогностическую значимость для диагностики или обнаружения рака эндометрия. Дополнительно, изобретателями также было показано, что добавление других биомаркеров, вдобавок к тем, которые перечислены в таблице 1, к характерной картине фингерпринтов также может повышать прогностическую значимость, и может являться пригодной для классификации рака эндометрия, для дифференциальной диагностики заболеваний, отличающихся от рака эндометрия, и для прогноза рака эндометрия.
В одном варианте осуществления, настоящее изобретение обеспечивает способ для характеристики образца, полученного от пациента, для прогностических, диагностических и/или фармакогеномных применений. Характеристика образца, полученного от пациента, в соответствии с уровнями одного или нескольких биомаркеров, представленных в таблице 1, можно использовать для обеспечения информации относительно прогрессирования заболевания, диагностики типа рака эндометрия (и/или подтипа), и выбора подходящего терапевтического лечения. В соответствии со способом согласно изобретению, образец получают от особи. Особь может являться здоровой особью, особью, у которой диагностировано злокачественное новообразование, особью, у которой подозревается наличие злокачественного новообразования, особью, проявляющей один или несколько симптомов рака и/или особью, нуждающейся в скрининге относительно злокачественного новообразования. Способ включает стадию определения уровня биомаркера (ов), представленных в таблице 1, в образце, полученном от пациента. Альтернативные методы определения биомаркеров (IHC, анализ экспрессии мРНК, и др.) можно использовать в этих методах.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия и/или повышенной вероятности наличия рака эндометрия, который включает получение образца от особи и определение уровня от 1 до 20 биомаркеров, представленных в таблице 1, в образце. Если уровень от 1 до 17 активированных биомаркеров повышен относительно контрольного значения и/или уровень от 1 до 3 подавленных биомаркеров снижен по сравнению с контрольным значением, то пациент имеет повышенную вероятность наличия рака эндометрия.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от пациента, имеющего симптом рака эндометрия и определение уровня от 1 до 20 биомаркеров, представленных в таблице 1, в образце. В одном аспекте этого варианта осуществления, симптом рака эндометрия выбирают из вагинального кровотечения и/или кровомазания у пост-менопаузных женщин, атипичного маточного кровотечения, атипичных менструальных периодов, кровотечения между нормальными периодами у пременопаузных женщин у женщин старше 40 лет, чрезвычайно длинных, тяжелых, или частых эпизодов кровотечения, анемии, вызванной хронической кровопотерей, боли в нижней части живота или тазовых судорог, жидких белых или прозрачных влагалищных выделений у пост-менопаузных женщин, и подозрительных симптомов в пери-менопаузных. Следовательно, в одном аспекте этого варианта осуществления, изобретение относится к способу диагностики рака эндометрия, который включает получение или обеспечение образца от особи, имеющей вагинальное кровотечение и/или кровомазание у пост-менопаузных женщин, атипичное маточное кровотечение, атипичные менструальные периоды, кровотечение между нормальными периодами у пременопаузных женщин у женщин старше 40 лет, чрезвычайно длинные, тяжелые, или частые эпизоды кровотечения, анемию, вызванную хронической кровопотерей, боли в нижней части живота или тазовые судороги, жидкие белые или прозрачные влагалищные выделение у пост-менопаузных женщин, или подозрительные симптомы в пери-менопаузных и определение уровня от 1-17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, и/или от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В специфическом аспекте этого варианта осуществления, если уровень от 1 до 17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, повышены относительно контрольного значения и/или уровень от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, снижены относительно контрольного значения, то это указывает на рак эндометрия или повышенный шанс наличия рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, уровни одного или нескольких биомаркеров для обнаружения рака эндометрия нормализованы к одному или более эндогенным биомаркерам или генам. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с другим аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от пациента, имеющего фактор риска для рака эндометрия и определение уровня от 1 до 20 биомаркеров, представленных в таблице 1, в образце. В одном аспекте этого варианта осуществления, фактор риска для рака эндометрия выбирают из высоких уровней эстрогена, гиперплазии эндометрия, ожирения, повышенного кровяного давления, синдрома поликистоза яичников, неспособности к деторождению, бесплодия, раннего менархе, поздней менопаузы, полипов эндометрия или других доброкачественных ростовых процессов выстилки матки, диабета, приема тамоксифена, гиперплазии, потребления больших количеств животных жиров, лучевой терапии тазовой области, рака молочной железы, рака яичника, ежедневного потребления алкоголя в больших количествах, семейного анамнеза рака, семейного анамнеза HNPCC, и наличия HNPCC мутации носителя. В одном аспекте этого варианта осуществления, биомаркеры выбирают для различения пациентов, имеющих опухоль, от тех пациентов, которые находятся в секреторной фазе менструального цикла. Следовательно, в одном аспекте этого варианта осуществления, изобретение относится к способу диагностики рака эндометрия, который включает получение или обеспечение образца от особи, имеющий фактор риска для рака, который представляет собой высокие уровни эстрогена, гиперплазию эндометрия, ожирение, повышенное кровяное давление, синдром поликистоза яичников, неспособность к деторождению, бесплодие, раннее менархе, позднюю менопаузу, полипы эндометрия или другие доброкачественные ростовые процессы выстилки матки, диабет, прием тамоксифена, гиперплазию, потребление больших количеств животных жиров, лучевую терапию тазовой области, рак молочной железы, рак яичника, ежедневное потребление алкоголя в больших количествах, семейный анамнез рака, семейный анамнез HNPCC, или наличие HNPCC мутации носителя, который представляет собой и определение уровня от 1-17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, и/или от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В специфическом аспекте этого варианта осуществления, если уровень от 1 до 17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, повышены относительно контрольного значения и/или уровень от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, снижены относительно контрольного значения, то это указывает на рак эндометрия или повышенный шанс наличия рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, уровни одного или нескольких биомаркеров для обнаружения рака эндометрия нормализованы к одному или более эндогенным биомаркерам или генам. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с другим аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру. В предпочтительном аспекте этого варианта осуществления, способ включает определение уровня от 1-17 активированных биомаркеров, представленные в таблице 1, и от 1-3 подавленных маркеров из таблицы 1 с помощью количественной ПЦР в образце маточной жидкости.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает получение образца от пациента, имеющего эндометрий с повышенной толщиной. В одном аспекте этого варианта осуществления, толщина эндометрия измеряется путем трансвагинального ультразвукового исследования. "Повышенная толщина" относится к толщине, превышающей значение, которое общепринято используется в данной области для идентификации пациентов, которые нуждаются в дальнейшей обработке или исследовании. Способ согласно этому варианту осуществления включает определение уровня определение уровня от 1 до 20 биомаркеров, представленных в таблице 1, в образце, полученном от пациента, имеющего эндометрий с повышенной толщиной. В соответствии с аспектом этого варианта осуществления, образец представляет собой образец маточной жидкости. В другом аспекте этого варианта осуществления, определяют уровень от 1-20 мРНК биомаркеров. В другом аспекте этого варианта осуществления, определяют уровень от 1-20 белков биомаркеров. В одном аспекте этого варианта осуществления, биомаркеры выбирают из тех, которые способны отличить образцы от пациентов, пораженных раком эндометрия, и от тех пациентов, которые имеют другое состояние, при котором повышается толщина эндометрия. Состояния, при которых повышается толщина эндометрия, но необязательно представляют собой рак эндометрия у пациентов, включают, но не ограничиваясь только ими, прием тамоксифена, прием гормонов, фазу менструального цикла (в целом, толщина эндометрия повышается при переходе из пролиферативной в секреторную фазу). Некоторые предпочтительные биомаркеры, которые хорошо себя зарекомендовали для разделения образцов от пациентов, пораженных раком эндометрия, от пациентов, не пораженных раком эндометрия, в секреторной фазе представлены в таблице 9 в примерах. Следовательно, в одном аспекте этого варианта осуществления, изобретение относится к способу диагностики рака эндометрия, который включает получение или обеспечение образца от особи, имеющей повышенную толщину эндометрия, и определение уровня от 1-17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, и/или от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, где, если указанные маркеры дифференциально экспрессируются по сравнению с контрольным значением, то у особи диагностируют рак эндометрия и/или повышенную вероятность рака эндометрия. В специфическом аспекте этого варианта осуществления, если уровень от 1 до 17 биомаркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, повышены относительно контрольного значения и/или уровень от 1 до 3 биомаркеров, выбранных из EFEMP2, SOCS2 и DCN, снижены относительно контрольного значения, то это указывает на рак эндометрия или повышенный шанс наличия рака эндометрия. В соответствии с одним аспектом этого варианта осуществления, уровни одного или нескольких биомаркеров для обнаружения рака эндометрия нормализованы к одному или более эндогенным биомаркерам или генам. В соответствии с одним аспектом этого варианта осуществления, образец выбирают из образца ткани и образца жидкости. В одном аспекте, образец жидкости представляет собой образец маточной жидкости или аспират из матки. В соответствии с одним аспектом этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркеру. В соответствии с другим аспектом этого варианта осуществления, определяют уровень белка, соответствующего биомаркеру. В предпочтительном аспекте этого варианта осуществления, способ включает определение уровня от 1-17 активированных биомаркеров, представленные в таблице 1, и от 1-3 подавленных маркеров из таблицы 1 с помощью количественной ПЦР в образце маточной жидкости.
Профили, характерные картины фингерпринтов, и комбинации
Исходные микропанельные исследования, раскрытые в настоящей заявке, свидетельствуют о том, что каждый из биомаркеров из таблицы 1, в качестве независимых биомаркеров, имеет прогностическую значимость для диагностики рака эндометрия. Кроме того, было обнаружено, что комбинации маркеров (например, профили или характерные картины фингерпринтов) имеют повышенную прогностическую значимость для рака эндометрия. Следовательно, дополнительно к применению этих маркеров в качестве индивидуальных маркеров, они могут использоваться в комбинации от 2 до 20 биомаркеров для диагностики рака эндометрия. В некоторых вариантах осуществления дополнительные маркеры могут быть включены в профиль или характерную картину фингерпринтов для дифференциальной диагностики (исключения или подтверждения заболевания или состояний, отличающихся от рака эндометрия (например, гиперплазия эндометрия, эндометриоз, рак яичника, фиброиды, и др.)), классификации типа рака эндометрия (например, типа I относительно типа II), классификации клеточного типа рака эндометрия, и прогноза.
В одном варианте осуществления, изобретение обеспечивает профили и/или характерные картины фингерпринтов, имеющие 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20, биомаркеров из таблицы 1. В одном аспекте этого варианта осуществления, определяют уровень мРНК, соответствующей биомаркерам в профиле, для применения для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном аспекте этого варианта осуществления, определяют уровень белка, соответствующей биомаркерам в профиле, для применения для диагностики рака эндометрия и/или повышенной вероятности рака эндометрия. В одном аспекте этого варианта осуществления, уровень биомаркеров определяют в образце, полученном из маточной жидкости. В одном аспекте этого варианта осуществления, уровень биомаркеров определяют в образце, полученном из сыворотки, крови, или плазмы.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня АСАА1 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие АСАА1, представляют собой АСАА1 и АР1М2; АСАА1 и CGN; АСАА1 и DDR1; АСАА1 и EPS8L2; АСАА1 и FASTKD1; АСАА1 и GMIP; АСАА1 и IKBKE; АСАА1 и P2RX4; АСАА1 и Р4НВ; АСАА1 и PHKG2; АСАА1 и PPFIBP2; АСАА1 и PPP1R16A; АСАА1 и RASSF7; АСАА1 и RNF183; АСАА1 и SIRT6; АСАА1 и TJP3; АСАА1 и EFEMP2; АСАА1 и SOCS2; или АСАА1 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня АР1М2 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, P4HB, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие АР1М2, представляют собой АР1М2 и АСАА1; АР1М2 и CGN; AP1M2 и DDR1; АР1М2 и EPS8L2; АР1М2 и FASTKD1; АР1М2 и GMIP; АР1М2 и IKBKE; АР1М2 и P2RX4; АР1М2 и P4HB; АР1М2 и PHKG2; АР1М2 и PPFIBP2; АР1М2 и PPP1R16A; АР1М2 и RASSF7; АР1М2 и RNF183; АР1М2 и SIRT6; АР1М2 и TJP3; АР1М2 и EFEMP2; АР1М2 и SOCS2; или АР1М2 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня CGN биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, P4HB, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие CGN, представляют собой CGN и АР1М2; АСАА1 и CGN; CGN и DDR1; CGN и EPS8L2; CGN и FASTKD1; CGN и GMIP; CGN и IKBKE; CGN и P2RX4; CGN и Р4НВ; CGN и PHKG2; CGN и PPFIBP2; CGN и PPP1R16A; CGN и RASSF7; CGN и RNF183; CGN и SIRT6; CGN и TJP3; CGN и EFEMP2; CGN и SOCS2; или CGN и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня DDR1 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является DDR1 и Р4НВ; DDR1 и GMIP; DDR1 и IKBKE; DDR1 и EFEMP2; DDR1 и SOCS2; DDR1, Р4НВ, и GMIP; DDR1, Р4НВ, GMIP, и IKBKE; DDR1, Р4НВ, GMIP, IKBKE и EFEMP2; или DDR1, GMIP, IKBKE, Р4НВ, и SOCS2. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня EPS8L2 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие EPS8L2, представляют собой EPS8L2 и АР1М2; EPS8L2 и CGN; EPS8L2 и DDR1; EPS8L2 и EPS8L2; EPS8L2 и FASTKD1; EPS8L2 и GMIP; EPS8L2 и IKBKE; EPS8L2 и P2RX4; EPS8L2 и Р4НВ; EPS8L2 и PHKG2; EPS8L2 и PPFIBP2; EPS8L2 и PPP1R16A; EPS8L2 и RASSF7; EPS8L2 и RNF183; EPS8L2 и SIRT6; EPS8L2 и TJP3; EPS8L2 и EFEMP2; EPS8L2 и SOCS2; EPS8L2 и АСАА1; или EPS8L2 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня FASTKD1 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является FASTD1 и Р4НВ; FASTKD1 и GMIP; FASTKD1 и IKBKE; FASTKD1 и EFEMP2; FASTKD1 и SOCS2; FASTD1 и DDR1; FASTKD1 и SIRT6; FASTKD1 и PHKG2; FASTKD1, Р4НВ, и GMIP; FASTKD1, Р4НВ и IKBKE; FASTKD1, Р4НВ, и EFEMP2; FASTKD1, Р4НВ, EFEMP2, IKBKE, и GMIP; FASTKD1, Р4НВ, EFEMP2, SIRT6, DDR1, и GMIP; или FASTKD1, Р4НВ, EFEMP2, SIRT6, PHKG2, и GMIP. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня GMIP биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является GMIP и Р4НВ; FASTKD1 и GMIP; GMIP и IKBKE; GMIP и EFEMP2; GMIP и SOCS2; GMIP и DDR1; GMIP и SIRT6; GMIP и PHKG2; GMIP, Р4НВ, и IKBKE; GMIP, SOCS2, и IKBKE; GMIP, SOCS2, и Р4НВ; GMIP, IKBKE, Р4НВ, и EFEMP2; GMIP, IKBKE, Р4НВ, и SOCS2; GMIP, Р4НВ, EFEMP2, IKBKE, и FASTKD1; GMIP, Р4НВ, EFEMP2, SIRT6, DDR1, и FASTKD1; или GMIP, Р4НВ, EFEMP2, SIRT6, PHKG2, и FASTKD1. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня IKBKE биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является IKBKE и Р4НВ; IKBKE и GMIP; IKBKE и FASTKD1; IKBKE и EFEMP2; IKBKE и SOCS2; IKBKE и DDR1; IKBKE и SIRT6; IKBKE и PHKG2 ; IKBKE, Р4НВ, и GMIP; IKBKE, Р4НВ, и EFEMP2; IKBKE, GMIP, и EFEMP2; IKBKE, Р4НВ, и SOCS2; IKBKE, GMIP, Р4НВ, и SOCS2; IKBKE, GMIP, Р4НВ, и EFEMP2; IKBKE, Р4НВ, EFEMP2, GMIP, и FASTKD1; или IKBKE, DDR1, GMIP, Р4НВ, PHKG2, SIRT6, и EFEMP2. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня P2RX4 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P4HB, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие P2RX4, представляют собой P2RX4 и АР1М2; P2RX4 и CGN; P2RX4 и DDR1; P2RX4 и EPS8L2; P2RX4 и FASTKD1; P2RX4 и GMIP; P2RX4 и IKBKE; P2RX4 и P4HB; P2RX4 и PHKG2; P2RX4 и PPFIBP2; P2RX4 и PPP1R16A; P2RX4 и RASSF7; P2RX4 и RNF183; P2RX4 и SIRT6; P2RX4 и TJP3; P2RX4 и EFEMP2; P2RX4 и SOCS2; P2RX4 и АСАА1; или P2RX4 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня Р4НВ биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является FASTD1 и Р4НВ; Р4НВ и GMIP; Р4НВ и IKBKE; Р4НВ и EFEMP2; Р4НВ и SOCS2; Р4НВ и DDR1; Р4НВ и SIRT6; Р4НВ и PHKG2; Р4НВ, GMIP, и IKBKE; Р4НВ, GMIP, и SOCS2; Р4НВ, GMIP, и EFEMP2; Р4НВ, IKBKE, GMIP, и SOCS2; Р4НВ, IKBKE, GMIP, и EFEMP2; Р4НВ, EFEMP2, IKBKE, GMIP, и FASTKD1; Р4НВ, EFEMP2, SIRT6, GMIP, DDR1, и FASTKD1; Р4НВ, EFEMP2, SIRT6, GMIP, PHKG2, и FASTKD1; или DDR1, FASTKD1, GMIP, IKBKE, Р4НВ, PHKG2, SIRT6, и EFEMP2. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня PHKG2 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является PHKG2 и Р4НВ; PHKG2 и GMIP; PHKG2 и IKBKE; PHKG2 и EFEMP2; PHKG2 и SOCS2; PHKG2 и DDR1; PHKG2 и SIRT6; FASTKD1 и PHKG2; PHKG2, Р4НВ, и EFEMP2; PHKG2, Р4НВ, GMIP; PHKG2, Р4НВ, IKBKE, и EFEMP2; PHKG2, Р4НВ, IKBKE, и SOCS2; Р4НВ, EFEMP2, SIRT6, GMIP, PHKG2, и FASTKD1; или DDR1, FASTKD1, GMIP, IKBKE, Р4НВ, PHKG2, SIRT6, и EFEMP2 В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня PPFIBP2 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие PPFIBP2, представляют собой PFIBP2 и АР1М2; PPFIBP2 и CGN; PPFIBP2 и DDR1; PPFIBP2 и EPS8L2; PPFIBP2 и FASTKD1; PPFIBP2 и GMIP; PPFIBP2 и IKBKE; PPFIBP2 и P2RX4; PPFIBP2 и Р4НВ; PPFIBP2 и PHKG2; PPFIBP2 и PPP1R16A; PPFIBP2 и RASSF7; PPFIBP2 и RNF183; PPFIBP2 и SIRT6; PPFIBP2 и TJP3; PPFIBP2 и EFEMP2; PPFIBP2 и SOCS2; PPFIBP2 и АСАА1; или PPFIBP2 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня PPP1R16A биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие PPP1R16A, представляют собой PPP1R16A и АР1М2; PPP1R16A и CGN; PPP1R16A и DDR1; PPP1R16A и EPS8L2; PPP1R16A и FASTKD1; PPP1R16A и GMIP; PPP1R16A и IKBKE; PPP1R16A и P2RX4; PPP1R16A и Р4НВ; PPP1R16A и PHKG2; PPFIBP2 и PPP1R16A; PPP1R16A и RASSF7; PPP1R16A и RNF183; PPP1R16A и SIRT6; PPP1R16A и TJP3; PPP1R16A и EFEMP2; PPP1R16A и SOCS2; PPP1R16A и АСАА1; или PPP1R16A и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня RASSF7 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие RASSF7, представляют собой RASSF7 и АР1М2; RASSF7 и CGN; RASSF7 и DDR1; RASSF7 и EPS8L2; RASSF7 и FASTKD1; RASSF7 и GMIP; RASSF7 и IKBKE; RASSF7 и P2RX4; RASSF7 и Р4НВ; RASSF7 и PHKG2; RASSF7 и PPP1R16A; RASSF7 и RNF183; RASSF7 и SIRT6; RASSF7 и TJP3; RASSF7 и EFEMP2; RASSF7 и SOCS2; RASSF7 и АСАА1; или RASSF7 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня RNF183 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие RNF183, представляют собой RNF183 и АР1М2; RNF183 и CGN; RNF183 и DDR1; RNF183 и EPS8L2; RNF183 и FASTKD1; RNF183 и GMIP; RNF183 и IKBKE; RNF183 и P2RX4; RNF183 и Р4НВ; RNF183 и PHKG2; RNF183 и PPP1R16A; RASSF7 и RNF183; RNF183 и SIRT6; RNF183 и TJP3; RNF183 и EFEMP2; RNF183 и SOCS2; RNF183 и АСАА1; или RNF183 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня SIRT6 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является SIRT6 и Р4НВ; SIRT6 и GMIP; SIRT6 и IKBKE; SIRT6 и EFEMP2; SIRT6 и SOCS2; SIRT6 и DDR1; FASTKD1 и SIRT6; SIRT6 и PHKG2; SIRT6, Р4НВ, и EFEMP2; SIRT6, Р4НВ, и IKBKE; SIRT6, IKBKE, и EFEMP2; SIRT6, Р4НВ, и SOCS2; SIRT6, Р4НВ, IKBKE, и GMIP; SIRT6, Р4НВ, EFEMP2, GMIP, DDR1, и FASTKD1; SIRT6, Р4НВ, EFEMP2, GMIP, PHKG2, и FASTKD1; или SIRT6, Р4НВ, EFEMP2, GMIP, IKBKE, PHKG2, DDR1, и FASTKD1. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня TJP3 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, P4HB, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, EFEMP2, SOCS2 и DCN. Комбинации или субкомбинации, включающие TJP3 are TJP3 и АР1М2; TJP3 и CGN; TJP3 и DDR1; TJP3 и EPS8L2; TJP3 и FASTKD1; TJP3 и GMIP; TJP3 и IKBKE; TJP3 и P2RX4; TJP3 и P4HB; TJP3 и PHKG2; TJP3 и PPP1R16A; TJP3 и RNF183; TJP3 и SIRT6; TJP3 и RASSF7;TJP3 и EFEMP2; TJP3 и SOCS2; TJP3 и АСАА1; или TJP3 и DCN. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня EFEMP2 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, P4HB, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, SOCS2 и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является EFEMP2 и P4HB; EFEMP2 и GMIP; EFEMP2 и IKBKE; FASTKD1 и EFEMP2; EFEMP2 и SOCS2; EFEMP2 и DDR1; EFEMP2 и SIRT6; EFEMP2 и PHKG2; EFEMP2, Р4НВ, и IKBKE; EFEMP2, IKBKE, и GMIP; EFEMP2, IKBKE, и FASTKD1; EFEMP2, GMIP, и DDR1; EFEMP2, SIRT6, и FASTKD1; EFEMP2, IKBKE, GMIP, и Р4НВ; EFEMP2, Р4НВ, IKBKE, GMIP, и FASTKD1; EFEMP2, Р4НВ, SIRT6, DDR1, GMIP, и FASTKD1; EFEMP2, Р4НВ, SIRT6, PHKG2, GMIP, и FASTKD1; или EFEMP2, Р4НВ, IKBKE, GMIP, DDR1, PHKG2, SIRT6, и FASTKD1; В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня SOCS2 биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7. RNF183, SIRT6, TJP3, EFEMP2, и DCN. Предпочтительной комбинацией или субкомбинацией, пригодной для обнаружения рака эндометрия или повышенной вероятности рака эндометрия, является SOCS2 и Р4НВ; SOCS2 и GMIP; SOCS2 и IKBKE; SOCS2 и EFEMP2; FASTKD1 и SOCS2; SOCS2 и DDR1; SOCS2 и SIRT6; SOCS21 и PHKG2; SOCS2, Р4НВ, и IKBKE; SOCS2, GMIP, и Р4НВ; SOCS2, Р4НВ, и IKBKE; GMIP, Р4НВ, IKBKE, и SOCS2; SOCS2, GMIP, IKBKE, Р4НВ, и DDR1; или SOCS2, DDR1, FASTKD1, GMIP, IKBKE, Р4НВ, PHKG2, SIRT6, и EFEMP2. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В одном варианте осуществления, изобретение обеспечивает способ диагностики рака эндометрия, который включает определение уровня DCN биомаркера в комбинации с уровнем одного или нескольких биомаркеров. В специфическом аспекте этого варианта осуществления один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из дифференциальных диагностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, и биомаркеров, пригодных для классификации рака эндометрия. В одном аспекте этого варианта осуществления, один или несколько биомаркеров, пригодных для обнаружения рака эндометрия, выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, и SOCS2. Комбинации или субкомбинации, включающие DCN, представляют собой DCN и АР1М2; DCN и CGN; DCN и DDR1; DCN и EPS8L2; DCN и FASTKD1; DCN и GMIP; DCN и IKBKE; DCN и P2RX4; DCN и Р4НВ; DCN и PHKG2; DCN и PPP1R16A; DCN и RNF183; DCN и SIRT6; DCN и RASSF7; DCN и EFEMP2; DCN и SOCS2; или DCN и АСАА1. В одном аспекте этого варианта осуществления, определяют уровень (и) экспрессии гена биомаркера. В другом аспекте этого варианта осуществления, определяют уровень (и) экспрессии белка. В одном аспекте этого варианта осуществления, анализируют опухоль или подозрительный образец. В другом аспекте анализируют образец жидкости. В другом аспекте этого варианта осуществления, анализируют образец, полученный из маточной жидкости. В еще другом аспекте этого варианта осуществления, анализируют образцы сыворотки или крови. В одном аспекте, анализируемый образец получен из клетки.
В предпочтительном аспекте диагностического способа in vitro согласно изобретению уровни определяют комбинацию маркеров, где указанная комбинация включает IKBKE и Р4НВ; IKBKE и SOCS2; Р4НВ и SOCS2; GMIP и IKBKE; GMIP и Р4НВ; GMIP и SOCS2; GMIP, SOCS2, и IKBKE; GMIP, SOCS2, и Р4НВ; GMIP, IKBKE, и Р4НВ; IKBKE.P4HB, и SOCS2; GMIP, IKBKE, Р4НВ, и SOCS2; GMIP, SOCS2, IKBKE, и EPS8L2; GMIP, SOCS2, Р4НВ, и EPS8L2; GMIP, IKBKE, Р4НВ, и EPS8L2; IKBKE, Р4НВ, SOCS2, и EPS8L2; GMIP, IKBKE, Р4НВ, SOCS2, и DDR1; GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2, и PPP1R16A; GMIP, IKBKE, Р4НВ, SOCS2, PHKG2, и RASSF7; GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2, и DDR1; GMIP, IKBKE, Р4НВ, SOCS2, EPS8L2, PPP1R16A, и DDR1; DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, RASSF7, SIRT6, TJP3, и SOCS2; или DDR1, EPS8L2, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPP1R16A, RASSF7, SIRT6, TJP3, RNF183 и SOCS2.
В другом предпочтительном аспекте диагностического способа in vitro согласно изобретению определяют уровни комбинации маркеров, где указанная комбинация включает GMIP, IKBKE, Р4НВ, SOCS2 и FASTKD1; GMIP, IKBKE, Р4НВ, SOCS2 и DDR1; GMIP, IKBKE, Р4НВ, SOCS2 и PHKG2; GMIP, IKBKE, Р4НВ, SOCS2 и SIRT6; GMIP, IKBKE, Р4НВ, SOCS2 и АСАА1; GMIP, IKBKE, Р4НВ, SOCS2 и EFEMP2; GMIP, IKBKE, Р4НВ, SOCS2 и EPS8L2; GMIP, IKBKE, Р4НВ, SOCS2 и P2RX4; GMIP, IKBKE, Р4НВ, SOCS2 и PPFIBP2; GMIP, IKBKE, Р4НВ, SOCS2 и PPP1R16A; GMIP, IKBKE, Р4НВ, SOCS2, АСАА1 и FASTKD1; GMIP, IKBKE, Р4НВ, SOCS2, PHKG2 и FASTKD1; GMIP, IKBKE, Р4НВ, SOCS2, SIRT6 и FASTKD1; АСАА1, АР1М2, EPS8L2, IKBKE, P2RX4, P4HB, PPFIBP2, PPP1R16A, SIRT6, и EFEMP2; GMIP, IKBKE, Р4НВ, и EFEMP2; DDR1, FASTKD1, PHKG2, SIRT6, SOCS2, GMIP, IKBKE, Р4НВ, и EFEMP2; DDR1, FASTKD1, PHKG2, SIRT6, GMIP, IKBKE, Р4НВ, и EFEMP2; или Р4НВ, EFEMP2, IKBKE, GMIP, и FASTKD1.
В другом предпочтительном аспекте диагностического способа in vitro согласно изобретению уровни определяют комбинацию маркеров, где указанная комбинация включает GMIP, IKBKE, Р4НВ, EFEMP2 и FASTKD1; GMIP, IKBKE, Р4НВ, EFEMP2 и DDR1; GMIP, IKBKE, Р4НВ, EFEMP2 и PHKG2; GMIP, IKBKE, Р4НВ, EFEMP2 и SIRT6; GMIP, IKBKE, Р4НВ, EFEMP2 и АСАА1; GMIP, IKBKE, Р4НВ, SOCS2 и EFEMP2; GMIP, IKBKE, Р4НВ, EFEMP2 и EPS8L2; GMIP, IKBKE, Р4НВ, EFEMP2 и P2RX4; GMIP, IKBKE, Р4НВ, EFEMP2 и PPFIBP2; GMIP, IKBKE, Р4НВ, EFEMP2 и PPP1R16A; GMIP, IKBKE, Р4НВ, EFEMP2, АСАА1 и FASTKD1; GMIP, IKBKE, Р4НВ, EFEMP2, PHKG2 и FASTKD1; или GMIP, IKBKE, Р4НВ, EFEMP2, SIRT6 и FASTKD1.
Вспомогательные биомаркеры
"Вспомогательные биомаркеры" относятся к биомаркерам, которые могут применяться в сочетании с одним или несколькими биомаркерами из таблицы 1. Вспомогательные биомаркеры могут применяться в способах согласно изобретению для обеспечения дальнейшей характеристики заболевания или состояния, которое может иметь пациент.
Дифференциальные диагностические биомаркеры пригодны для отличия между заболеваниями, которые могут проявлять сходные клинические симптомы. Например, пациент может иметь симптомы рака эндометрия (например, вагинальное кровотечение и/или боль в области таза), но эти симптомы также могут вызываться другими заболеваниями (например, раком яичника). Таким образом, дифференциальные диагностические биомаркеры обеспечивают информацию для характеристики заболевания. Примеры заболеваний, при которых могут проявляться сходные симптомы, как и при раке эндометрия, включают фибромы матки, эндометриоз, гиперплазию эндометрия, саркому матки - другой тип злокачественного новообразования матки, лейомиомы матки, полипы эндометрия (тип полипов), рак шейки матки, атрофический эндометрий, аденомиоз, атрофический вагинит, опухоль яичника, лейомиосаркома, и пролиферация эндометрия.
В соответствии с открытием изобретателями, что уровень биомаркеров в первичной ткани рака эндометрия может коррелировать с их уровнями в маточной жидкости, предполагают, что образцы маточной жидкости могут использоваться для дифференциальной диагностики состояний, отличающихся от рака эндометрия. Следовательно, в одном аспекте, изобретение обеспечивает способ для дифференциальной диагностики рака эндометрия путем получения образца маточной жидкости от пациента и определения уровня одного или нескольких биомаркеров, которые способны отличить рак эндометрия от нерака эндометрия. Дифференциальные диагностические биомаркеры для эндометриоза пригодны для различения эндометриоза от рака эндометрия. Дифференциальные диагностические биомаркеры для рака яичника пригодны для различения рака яичника от рака эндометрия. Примеры биомаркеров, пригодных для различения рака эндометрия от рака яичника, включают, но не ограничиваясь только ими, те, которые описаны в Yurkovetsky и др. (Gyn. Onc. (2007) 107:58-65), где они описали панель из пяти биомаркеров пролактина, GH, эотаксина, Е-селектина, и TSH для дифференцировки рака эндометрия от рака яичников и рака молочной железы.
Идентифицированы различные биомаркеры рака эндометрия. СА 125 коррелирует с размером и стадией опухоли и является независимым предсказателем внематочного распространения.
B литературе описаны сывороточные маркеры для определения рака матки.
Прогностические биомаркеры: Повышенные уровни СА 125, СА 15-3, и СА 19-9 связаны с более коротким временем выживания. Они обнаружили, что сывороточные СА 125 СА 15-3 и СЕА являются более высокими у пациентов на стадии заболевания III по сравнению со стадией I. Другая группа прогностических маркеров включает рецептор эстрогена, рецептор прогестерона, и HER2.
Биомаркеры для классификации рака эндометрия включают биомаркеры для оценки стадии злокачественного новообразования, клеточного типа, и/или типа рака эндометрия (например, тип I относительно типа II). Примеры биомаркеров для классификации рака эндометрия включают, но не ограничиваясь только ими, те биомаркеры, которые описаны в Sugiyama и др. (2003) Clin. Can. Res. 9:5589-5600. Гены, проявляющие повышенную экспрессию при типе I по сравнению с типом II, включают ММР11, RHOG, и предшественник В субъединицы фактора роста тромбоцитов, STAT2, октамер-связывающий транскрипционный фактор 1, и GATA-6, предшественник фактора роста VEGF-С, каспаза (каспаза 1/IL-1β превращающий фермент). Гены, проявляющие повышенную экспрессию при типе II по сравнению с типом I, включают PIRIN, EGR1, STAT1, IFN регуляторный фактор 1, и KRAS. Konecny и др. ((2009) British Journal рака 100, 89-95) описали, что скорость амплификации HER2 гена, как измерено с помощью флуоресценции гибридизации in situ, является более высокой при злокачественных новообразованиях II типа, тогда как EGFR экспрессия, как измерено с помощью IHC техник, является существенно более низкой при злокачественных новообразованиях II типа. Deng и др. ((2005,) Clin. Can. Res. том 11, № 23:8258-8264) описали, что EIG121 представляет собой маркер для эстроген-связанных злокачественных новообразований I типа. Маркеры для классификации рака эндометрия также могут использоваться для различия разных гистологических типов рака эндометрия, таких как серозный и эндометриоидный рак. Risinger и др. ((2003) Canc. Res. 63:6-11) идентифицировали биомаркеры, которые могут отличать папиллярный серозный рак от эндометриоидного рака. Например, было обнаружено, что AGR2, TFF3, DUSP6, IGF2, FOLR1, и UCHL1 дифференциально экспрессируются между папиллярным серозным и эндометриоидным раком, как было обнаружено с помощью микропанели и подтверждено с помощью ОТ-ПЦР. Было обнаружено, что AGR2, TFF3, DUSP6 активированы при эндометриоидных типах рака, в то время как было обнаружено, что IGF2, FOLR1 и UCHL1 активированы при папиллярных серозных раках.
В соответствии с открытием изобретателями, что уровень биомаркеров в первичной ткани рака эндометрия может коррелировать с их уровнями в маточной жидкости, полагают, что образцы маточной жидкости могут использоваться для классификации типа рака эндометрия. Классификация типа рака эндометрия может относиться к отличию злокачественных новообразованиях типа I и типа II. Классификация типа рака эндометрия также может относиться к определению гистологического типа и/или подтипа рака эндометрия. Следовательно, в одном аспекте, изобретение обеспечивает способ для классификации рака эндометрия путем получения образца маточной жидкости от пациента и определения уровня одного или нескольких биомаркеров, которые способны классифицировать рак эндометрия.
"Вспомогательные биомаркеры для обнаружения рака эндометрия" относятся к биомаркерам, которые можно использовать дополнительно к биомаркерам, представленным в таблице 1, для диагностики рака эндометрия и/или повышенный риск наличия рака эндометрия: Yurkovetsky и др. (Gyn. Onc. (2007) 107:58-65) идентифицировали, что пролактин является сывороточным биомаркером с чувствительностью и специфичностью для рака эндометрия. Yurkovetsky и др. обнаружили, что пролактин, GH, эотаксин, Е-селектин, и TSH являются пригодными маркерами для диагностики рака эндометрия.
В некоторых аспектах этих вариантов осуществления, один или несколько вспомогательных биомаркеров исследуют для определения изменения в образце от пациента, у которого подозревают наличие рака эндометрия. В специфическом аспекте, вспомогательные биомаркеры выбирают из сывороточных биомаркеров. В более специфическом аспекте сывороточные биомаркеры представляют собой один или несколько белков, выбранных из СА 125, СА 15-3, СА 19-9, СЕА, AFP, СА 72-4, VEGF, bFGF, IGFBPI, HGF, ErbB2, EGFR, TGFα, Fas, FasL, Cyfra 21-1, MMP-1, MMP-2, MMP-3, MMP-7, MMP-8, MMP-9, MMP-12, MMP-13, tPAI, sICAM, sVCAM, sE-селектина, адипонектина, резистина, IL-6, IL-8, TNFα, TNFR I, G-CSF, CD40L, IL-2R, IP-10, MCP-1, MIP-1α, MIP-1β, MIF, эотаксина, RANTES, FSH, LH, TSH, ACTH, пролактина, GH, βHCG, hK8, hK10, активного РАМ, ULBP-1, ULBP-2, ULBP-3, MICA, антиостатина, SCC, сывороточного амилоида A, TTR, S100, мезотелина , и миелопероксидазы (МРО). В более специфическом аспекте, сывороточные биомаркеры выбирают из пролактина, GH, эотаксина, е-селектина и FSH. В еще более специфическом аспекте, сывороточный биомаркер представляет собой пролактин. В некоторых аспектах, вспомогательный (е) биомаркер (ы) могут анализироваться в аспиратах из матки (например, уровень мРНК и/или уровни белка).
Образцы
Изобретение, в некоторых вариантах осуществления, относится к характеристике одного или нескольких биомаркеров, представленных в таблице 1, из образца от пациента, у которого подозревают наличие рака эндометрия или который нуждается в скрининге рака. Примеры таких образцов, которые можно использовать в изобретении, представляют собой жидкости, образцы тканей, и/или клетки. В зависимости от специфического маркера, способы, используемые для характеристики биомаркеров в соответствии с изобретением, могут включать, например, исследование количества копий ДНК гена, который соответствует биомаркеру, выявление белка, связанного с биомаркером, определение уровней экспрессии мРНК биомаркера, и др. Изобретение пригодно для различных применений, включая диагностику, прогнозирование, определение стадии, предсказание ответа на терапию. Изобретателями были обнаружены доказательства дифференциальной экспрессии биомаркеров, представленных в таблице 1, в многочисленных различных образцах, включая мРНК в первичной опухоли, белка в первичной опухоли, и мРНК в аспиратах, и белка в аспиратах. Биомаркеры, представленные в таблице 1, включают те биомаркеры, которые сверхэкспрессируются в образцах рака эндометрия от пациентов по сравнению с нормальными уровнями. Дополнительно некоторые биомаркеры, представленные в таблице 1, сниженно экспрессируются в образцах рака эндометрия от пациентов по сравнению с нормальными уровнями.
Изобретение, в некоторых вариантах осуществления, относится к характеристике одного или нескольких биомаркеров, представленных в таблице 1, от образца пациента (например, опухоль, раковая клетка, образец, для которого подозревают злокачественность, жидкость организма (например, маточная жидкость), кровь, сыворотка, плазма, и вагинальная кровь /выделения) и/или из "нормальной" клетки, от особи (или альтернативно контрольное значение может использоваться вместо нормального значения из клетки).
В одном аспекте, анализируемый образец получают от пациента, который имеет факторы риска для рака эндометрия. Факторы риска для рака эндометрия включают, но не ограничиваясь только ими, имеющие синдром Линча, генетически связанного с особью, имеющей синдром Линча, страдающей ожирением, принимающей гормонально-заместительную терапию только с эстрогеном, и предшествующее лечение тамоксифеном.
В одном аспекте этого варианта осуществления, анализируемый образец представляет собой образец маточной жидкости. В одном аспекте, образец, который используют, получен путем применения мягкого, соломинко-подобного устройства (пайпиля) для отсасывания небольшого образца выстилки из матки. В одном аспекте, образец получен путем применения инструмента с острым краем, который называется кюретка, путем соскребания небольшого образца и его сбора с помощью шприца или отсасывания (например, дилятация и кюретаж). В одном аспекте, образец получен путем применения электронного отсасывающего устройства (например, Vabra аспирация). В одном аспекте, образец получен путем применения распыления жидкости (струйного промывания) для смывания некоторого количества ткани, выстилающей матку. В некоторых аспектах, можно использовать щеточку для удаления некоторого количества выстилки перед осуществлением промывки.
В одном варианте осуществления, образец для анализа биомаркеров получают с помощью шприца или устройства типа пайпиля. В одном варианте осуществления, устройство для сбора образца маточной жидкости из внутренней полости (например, матки) пациента, включает цилиндр, имеющий отверстие на одном его конце, поршень, работающего аксиально с цилиндром, цилиндр и поршень, разграничивающий камеру для жидкости, имеющий объем, который изменяется при аксиальном движении поршня в цилиндре, и углубление, удлиненную трубку, расположенную от камеры для жидкости через отверстие в цилиндре, трубка функционально связана с цилиндром для аксиального движения для выдвижения и втягивания трубки по отношению к цилиндру при аксиальном движении поршня, и трубка находится в жидком соединении с камерой для жидкости для обеспечения пути для тока жидкости в и из камеры для жидкости через полую трубку. В одном аспекте этого варианта осуществления, после получения образца с помощью устройства, его хранят в средстве, которое сохраняет целостность биомаркеров, представляющих интерес. Например, когда анализируемый биомаркер представляет собой нуклеиновую кислоту, такую как РНК, образец может храниться в средстве, которое предотвращает разложение молекул РНК в образце, или если биомаркер представляет собой белок, то образец можно хранить, например, в агенте, который сохраняет белок. Примерами агентов, которые предотвращают разложение молекул РНК в образце, являются ингибиторы РНКазы {например, RNeasy от Qiagen, SUPERase·ln™ от Ambion или ингибитор РНКазы ScriptGuard™ RNase Inhibitor из эпицентра биотехнологий) или молекулы, который осаждают РНК из биологических растворов (например, трифенилметановые красители (например, метиловый зеленый, кристаллический фиолетовый, и парарозанилин), крезиловый фиолетовый, полиамины, и ионы кобальта). Примеры агентов, которые предотвращают разложение белков, включают ингибиторы протеазы (например, PMSF (фенилметансульфонил фторид, полный коктейль ингибиторов протеаз от Roche, или Пепстатин) или агенты, которые фиксируют ткани (формалин).
Следовательно, изобретение обеспечивает в одном варианте осуществления, диагностический способ in vitro для рака эндометрия, который включает получение образца аспирата маточной жидкости от пациента, имеющего симптом или фактор риска для рака эндометрия, и определение уровня от 1 до 100 биомаркеров, маркеров, которые дифференциально экспрессируются при раке эндометрия по сравнению с контрольными значениями, характерными для особей, не страдающих от рака эндометрия, где (1) если уровни 1-100 биомаркеры повышен в образце аспирата эндометрия у пациента и в контрольных значениях, то пациент имеет повышенную вероятность наличия рака эндометрия и где (2) если уровень 1-100 биомаркеров снижены в образце аспирата и тогда пациент имеет повышенную вероятность наличия рака эндометрия. Биомаркеры согласно этому аспекту могут представлять собой любые биомаркеры, которые дифференциально представлены в образцах рака эндометрия пациентов по сравнению с образцами от пациентов, которые не поражены раком эндометрия, и являются пригодными для диагностики рака эндометрия или повышенной вероятность рака эндометрия. Предпочтительные биомаркеры представляют собой биомаркеры 1-20, раскрытые в настоящей заявке в таблице 1.
Способы определения биомаркеров
Изобретение относится к идентификации биомаркеров, которые пригодны для диагностики рака эндометрия. Изобретение обеспечивает способы определения одного или нескольких биомаркеров, представленных в таблице 1, для диагностики рака эндометрия. Способ согласно изобретению может применяться для определения одного или нескольких белков, соответствующих биомаркерам, представленным в таблице 1, для диагностики рака эндометрия. Способ согласно изобретению может применяться для определения одной или нескольких мРНК, соответствующих биомаркерам, представленным в таблице 1, для диагностики рака эндометрия. Биомаркеры могут быть определены в образце, полученном от пациента, например, образце, полученном из ткани матки, маточной жидкости, или крови.
В некоторых вариантах осуществления, способ согласно изобретению включает получение образца и определение уровня 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20, биомаркеров, представленных в таблице 1, в образце. В специфическом аспекте, способ включает определение уровня 2 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 3 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 4 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 5 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 6 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 7 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 8 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 9 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 10 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 11 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 12 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 13 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 14 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 15 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня от 2 до 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня от 3 до 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня от 3 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня от 4 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня от 5 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня от 10 до 17 биомаркеров, перечисленных в таблице 1. В одном аспекте этого варианта осуществления, способ включает определение уровня меньше, чем 500 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня меньше, чем 250 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня меньше, чем 100 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня меньше, чем 50 различных биомаркеров. Повышенные уровни одного или нескольких биомаркеров, представленных в таблице 1, которые сверхэкспрессируются и/или снижены уровни одного или нескольких биомаркеров, представленных в таблице 1, экспрессия которых подавлена, указывают на то, что существует повышенная вероятность рака эндометрия. Подразумевается, что в некоторых аспектах этого варианта осуществления, анализируемые биомаркеры включают больше биомаркеров, чем перечислено в таблице 1.
В некоторых аспектах этих вариантов осуществления, способ включает получение образца и определение уровня мРНК 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20, биомаркеров, представленных в таблице 1, в образце. В специфическом аспекте, способ включает определение уровня мРНК 2 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 3 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 4 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 5 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 6 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 7 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 8 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 9 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 10 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 11 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 12 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 13 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 14 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 15 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК от 2 до 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК от 3 до 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК от 3 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК от 4 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК от 5 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня мРНК от 10 до 20 биомаркеров, перечисленных в таблице 1. В одном аспекте этого варианта осуществления, способ включает определение уровня мРНК меньше, чем 500 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня мРНК меньше, чем 250 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня мРНК меньше, чем 100 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня мРНК меньше, чем 50 различных биомаркеров. Повышенные уровни одной или нескольких мРНК, соответствующих биомаркерам, представленных в таблице 1, которые сверхэкспрессируются и/или снижены уровни одного или нескольких биомаркеров, представленных в таблице 1, экспрессия которых подавлена, указывают на то, что существует повышенная вероятность рака эндометрия. Подразумевается, что в некоторых аспектах этого варианта осуществления, анализируемые биомаркеры включают больше биомаркеров, чем перечислено в таблице 1.
В некоторых аспектах этих вариантов осуществления, способ включает получение образца и определение уровня белка 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20, биомаркеров, представленных в таблице 1, в образце. В специфическом аспекте, способ включает определение уровня белка 2 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 3 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 4 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 5 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 6 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 7 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 8 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 9 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 10 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 11 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 12 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 13 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 14 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 15 или более биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка от 2 до 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка от 3 до 20 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка от 3 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка от 4 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка от 5 до 17 биомаркеров, перечисленных в таблице 1. В специфическом аспекте, способ включает определение уровня белка от 10 до 17 биомаркеров, перечисленных в таблице 1. В одном аспекте этого варианта осуществления, способ включает определение уровня белка, меньше, чем 500 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня белка, меньше, чем 250 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня белка, меньше, чем 100 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня белка, меньше, чем 50 различных биомаркеров. В одном аспекте этого варианта осуществления, способ включает определение уровня белка от 1 до 10 различных биомаркеров. Повышенные уровни одного или нескольких белков, соответствующих биомаркерам, представленным в таблице 1, указывают на то, что существует повышенная вероятность рака эндометрия. Подразумевается, что в некоторых аспектах этого варианта осуществления, анализируемые биомаркеры включают больше биомаркеров, чем перечислено в таблице 1.
В одном варианте осуществления, изобретение обеспечивает способ определения одного или нескольких белков биомаркеров в сыворотке, крови, и/или плазмы. В специфическом аспекте этого варианта осуществления, один или несколько биомаркеров выбирают из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN. В более специфическом аспекте, один или несколько биомаркеров выбирают из IKBKE, P4HB, SOCS2, GMIP, DDR1, EPS8L2, PPP1R16A, P2RX4, PHKG2, RASSF7, SIRT6, TJP3, АР1М2, RNF183, и DCN. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня IKBKE. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня P4HB. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня SOCS2. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня GMIP. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня АР1М2. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня EPS8L2. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня DDR1. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня CGN. В другом специфическом аспекте этого варианта осуществления, способ включает определение уровня TJP3.
В некоторых аспектах этих вариантов осуществления, способ включает определение уровня 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, или 50 или больше биомаркеров, дополнительно к одному или нескольким биомаркерам, перечисленным в таблице 1. Эти маркеры могут представлять собой те маркеры, для которых известно, что уровень их экспрессии изменен у пациентов, имеющих рак эндометрия. Альтернативно, дополнительные биомаркеры могут использоваться для дифференциальной диагностики других заболеваний (например, эндометриоза, рака яичника, и фиброидов), для классификации типа рака, прогностической информации и/или для обеспечения информации для выбора терапии. В специфическом аспекте этого варианта осуществления, дополнительные биомаркеры анализируют в образцах маточной жидкости.
В специфическом аспекте согласно изобретению, один или несколько биомаркеров, перечисленных в таблице 1, определяют на матрице, имеющей различные зонды на матрице, которые представляют собой олигонуклеотиды, имеющие от приблизительно 5 до 200 оснований в длину. В другом специфическом аспекте, каждый из различных зондов на матрице представляют собой олигонуклеотид, имеющий от приблизительно 15 до 200, 15-150, 15-100, 15-75, 15-60, или 20-55 оснований в длину. В одном аспекте, матрица имеет зонды к 2 или более биомаркерам, перечисленным в таблице 1. В одном аспекте, матрица имеет зонды к 3 или более биомаркерам, перечисленным в таблице 1. В одном аспекте, матрица имеет зонды к 4 или более биомаркерам, перечисленным в таблице 1. В одном аспекте, матрица имеет зонды к 5 или более биомаркерам, перечисленным в таблице 1. В одном аспекте, матрица имеет зонды к 6 или более биомаркерам, перечисленным в таблице 1. В одном аспекте, матрица имеет зонды к 7 или более биомаркерам, перечисленным в таблице 1. В одном аспекте, матрица имеет зонды к менее чем 1000 различных генов. В одном аспекте, матрица имеет зонды к менее чем 500 различных генов. В одном аспекте, матрица имеет зонды к менее чем 100 различных генов.
В некоторых аспектах этих вариантов осуществления, определяют количество копий одного или нескольких биомаркеров, перечисленных в таблице 1. В другом аспекте этого варианта осуществления, определяют профиль количества копий 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20 биомаркеров, представленных в таблице 1, (или локуса, соответствующего биомаркеру) для обнаружения рака эндометрия.
В одном аспекте, изобретение обеспечивает праймеры, которые могут гибридизоваться с нуклеиновой кислотой, соответствующей биомаркеру, представленному в таблице 1, и использоваться для амплификации нуклеиновой кислоты или ее фрагмента, соответствующего указанному биомаркеру для диагностики рака эндометрия в соответствии со способами согласно изобретению. В более специфическом аспекте, праймеры создают для амплификации одного или нескольких экзонов биомаркера. В другом аспекте, праймеры создают для амплификации фрагмента одного или нескольких экзонов биомаркера. В одном аспекте, праймеры пригодны для ОТ-ПЦР анализа. В одном аспекте, способ согласно изобретению охватывает применение праймеров для амплификации нуклеиновой кислоты, соответствующей биомаркеру из таблицы 1, и обнаружение продукта амплификации с зондом к амплификованному продукту. В другом аспекте, способ согласно изобретению охватывает применение праймеров для амплификации нуклеиновой кислоты, соответствующей биомаркеру из таблицы 1, и обнаружение амплификованного продукта с красителем, который предоставляет возможность количественного определения амплификованного продукта.
В одном аспекте, изобретение обеспечивает зонды к биомаркерам, представленные в таблице 1, для обнаружения нуклеиновой кислоты или ее фрагмента, соответствующей биомаркеру. Зонды могут использоваться в способах согласно изобретению, например, для диагностики рака эндометрия. В специфическом аспекте, зонд представляет собой зонд для мРНК или нуклеиновой кислоты биомаркера, полученный из мРНК, соответствующей биомаркеру. В специфическом аспекте, зонд соответствует двум смежным экзонам биомаркера из таблицы 1, (или фрагментам двух или больше смежных экзонов). В специфическом аспекте, зонд соответствует экзону биомаркера или его фрагменту. В специфическом аспекте, зонд соответствует по меньшей мере порции промоторного региона биомаркера и по меньшей мере порции экзона 1 биомаркера.
В одном аспекте согласно изобретению, анализ путем множественной ПЦР используют для оценки уровни от 2 до 20 биомаркеров, представленных в таблице 1, для определения наличия или отсутствия рака эндометрия. В более специфическом аспекте, уровни от 3 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 4 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 5 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 6 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 7 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 8 до 20 или больше биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 9 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 10 до 20 или больше биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 15 до 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР. В более специфическом аспекте, уровни от 20 биомаркеров, представленных в таблице 1, оценивают с помощью множественной ПЦР.
Количественная ПЦР
В некоторых вариантах осуществления, изобретение основано на количественной ПЦР для определения уровня одного или нескольких биомаркеров из таблицы 1. В специфическом аспекте способ количественной ПЦР представляют собой количественную ОТ-ПЦР. Способы могут быть полуколичественными или полностью количественными.
Способы согласно изобретению для определения биомаркеров согласно изобретению могут включать конкурентную количественную ПЦР или количественную ПЦР в реальном времени, которые обе оценивают концентрацию целевого гена в образце путем сравнения со стандартными кривыми, построенными из амплификации серийных разведений стандартной ДНК. Количественная ПЦР или количественная ПЦР в реальном времени по существу отличаются способом создания стандартных кривых. В конкурентной КПЦР, внутренний конкурент ДНК добавляют к известной концентрации как серийно разведенных стандартных образцов, так и к неизвестным (например, полученным от пациента) образцам. После со-амплификации, соотношения внутреннего конкурента и целевых ПЦР продуктов рассчитывают как для стандартных разведений, так и для неизвестных образцов, и строят стандартную кривую, которая представляет собой график соотношений конкурент-целевой ПЦР продукт относительно исходной концентрации целевой ДНК стандартных разведений. Учитывая равную эффективность амплификации конкурента и целевой ДНК, их этой стандартной кривой можно экстраполировать концентрацию целевой ДНК в образцах пациентов.
В КПЦР в реальном времени, накопление амплифицированного продукта измеряют непрерывно как в стандартных разведениях целевой ДНК, так и в образцах, содержащих неизвестные количества целевой ДНК. Стандартную кривую строят путем корреляции исходной концентрации матрицы в стандартных образцах с количеством циклов ПЦР (Ct), необходимых для получения специфической пороговой концентрации продукта. В тестируемых образцах, накопление целевого ПЦР продукта изменяют после аналогичного d, что предоставляет возможность интерполяции концентрации целевой ДНК из стандартной кривой. Несмотря на то, что КПЦР в реальном времени позволяет осуществить более быстрое и легкое измерение целевой ДНК при осуществлении стандартных анализов, конкурентная КПЦР остается важной альтернативной для целевого количественного определения в окружающих образцах. Со-амплификация известного количества конкурента ДНК с целевой ДНК представляет собой интуитивный путь для коррекции отклонений вариаций между образцами эффективности амплификации вследствие присутствия ингибирующих субстратов и больших количество фоновой ДНК, что, очевидно, отсутствует из стандартных разведений.
Другим типом КПЦР является применение количественной ПЦР. Часто обозначаемая как "относительная количественная ПЦР," в этом методе определяют относительные концентрации специфических нуклеиновых кислот. В контексте согласно настоящему изобретению, ОТ-ПЦР осуществляют на видах мРНК, выделенных от пациентов. Посредством определения такой концентрации специфических видов мРНК, можно определить, будет ли ген, кодирующий специфические виды мРНК, дифференциально экспрессироваться.
В одном варианте осуществления, изобретение обеспечивает способ, включающий получение тестируемого образца из клеток, ткани, или жидкости пациента; определение уровня одного или нескольких биомаркеров, представленных в таблице 1, и сравнение уровня биомаркера (ов) в образце с уровнем, предполагаемым для нормального образца (или контрольным значением).
В одном варианте осуществления, изобретение обеспечивает способ, включающий получение предполагаемого образца опухоли от пациента; определение уровня одного или более биомаркеров, перечисленных в таблице 1, и сравнение уровня биомаркера (ов) в образце с уровнем, предполагаемым для нормального непораженного образца (или контрольным значением).
В одном варианте осуществления, изобретение обеспечивает способ, включающий получение образца от пациента, содержащий клетку; определение уровня одного или нескольких биомаркеров, представленных в таблице 1, в указанной клетке и сравнение уровня биомаркера (ов) в клетке с уровнем, предполагаемым для нормальной непораженной клетки (или контрольным значением).
В одном варианте осуществления, изобретение обеспечивает способ, включающий получение тестируемого образца из жидкости пациента; определение уровня одного или нескольких биомаркеров, представленных в таблице 1, и сравнение уровня биомаркера (ов) в образце с уровнем, предполагаемым для нормального непораженного образца. В одном аспекте этого варианта осуществления, жидкость представляет собой маточную жидкость, полученную путем аспирации. В одном аспекте этого варианта осуществления, жидкость представляет собой маточную жидкость, полученную путем аспирации с помощью жесткого пайпиля. В одном аспекте этого варианта осуществления, жидкость представляет собой маточную жидкость. В другом аспекте этого варианта осуществления, жидкость представляет собой вагинальные выделения. В одном варианте осуществления, изобретение обеспечивает способ, включающий получение тестируемого образца из образца крови или сыворотки от пациента; и определение уровня одного или нескольких биомаркеров, представленных в таблице 1, и сравнение уровня биомаркера (ов) в образце с уровнем, предполагаемым для нормального непораженного образца.
В одном варианте осуществления, изобретение обеспечивает способ, включающий получение тестируемого образца из мочи пациента; определение уровня одного или нескольких биомаркеров, представленных в таблице 1, и сравнение уровня биомаркеров в моче с уровнем, предполагаемым для контрольного значения.
В одном варианте осуществления, изобретение обеспечивает способ, включающий получение тестируемого образца из матки пациента, используя щетку; и определение уровня одного или нескольких биомаркеров, представленных в таблице 1, и сравнение уровня биомаркеров в образце с уровнем, предполагаемым для нормального образца.
Наличие повышенных уровней одного или нескольких биомаркеров, представленных в таблице 1, может указывать на рак эндометрия или предраковое состояние в ткани, например, гиперплазию эндометрия. В одном аспекте этого варианта осуществления, способ включает идентификацию пациента, нуждающегося в анализе одного или нескольких биомаркеров, представленных в таблице 1.
В другом аспекте этого варианта осуществления, настоящее изобретение обеспечивает способы диагностики или предсказания рака эндометрия. Способ согласно этому аспекту может включать (1) получение тестируемого образца из клеток, ткани, и/или жидкости (2) получение контрольного образца из клеток, ткани, или жидкости, которая является нормальной, или получение нормального контрольного значения, и (3) определение или измерение в обоих образца - в тестируемом образце и в контрольном образце - уровня одного или нескольких мРНК транскриптов, соответствующих одному или нескольким биомаркерам, представленным в таблице 1. Если уровень одного или нескольких транскриптов повышен в тестируемом образце по сравнению с контрольным образцом, то это указывает на рак эндометрия (и/или и повышенный риск наличия рака эндометрия) или предраковое состояние в тестируемом образце клеток или ткани. В другом аспекте контрольный образец может быть получен от другой особи или представлять собой нормализованное значение на основе исходных данных, полученных из популяции. В одном аспекте этого варианта осуществления, способ включает идентификацию пациента, нуждающегося в анализе одного или нескольких биомаркеров, представленных в таблице 1. В одном аспекте, пациент, нуждающийся в анализе одного или нескольких биомаркеров, представленных в таблице 1, представляет собой пациента, который имеет наличие рака эндометрия, у которого подозревают наличие рака эндометрия, или и/или который подвергается скринингу.
В еще другом аспекте этого варианта осуществления, способ включает получение тестируемого образца из клеток, ткани, или жидкости; определение количества копий ДНК одного или нескольких биомаркеров, представленных в таблице 1, ((например, на клетку) в образце; и сравнение количества копий ДНК, обнаруженного (например, количественно и/или качественно) в образце, с контрольным образцом или известным значением (или контрольным значением), таким образом определяя, амплифицировано ли количество копий биомаркера (ов) в тестируемом образце. В одном аспекте этого варианта осуществления, способ включает идентификацию пациента, нуждающегося в анализе одного или нескольких биомаркеров, представленных в таблице 1. В одном аспекте, пациент, нуждающийся в анализе одного или нескольких биомаркеров, представленных в таблице 1, представляет собой пациента, который имеет наличия рака эндометрия, у которого подозревают наличие рака эндометрия, или и/или который подвергается скринингу.
В еще другом аспекте этого варианта осуществления, способ включает (1) получение тестируемого образца из клеток, ткани, или жидкости; контактирование образца с антителом к белку или его фрагменту, соответствующему одному или нескольким биомаркерам, представленным в таблице 1, и определение в тестируемом образце, уровня биомаркера (ов), где повышенный уровень биомаркера (ов), по сравнению с контрольным значением указывает на то, что пациент может иметь предраковое или раковое состояние. В другом аспекте, контрольное значение может быть получено от другой особи или представлять собой нормализованное значение на основе исходных данных, полученных из популяции. Альтернативно, данный уровень биомаркера, характерный для популяции без рака эндометрия, который был установлен ранее на основании измерений от нормальных пациентов, без рака эндометрия, может использоваться в качестве контрольного значения. Контрольные данные, полученные из сравнительной базы данных, исходя из данных, полученных из контрольных образцов, характерных для популяции без рака эндометрия, также можно использовать в качестве контрольного значения. В одном аспекте этого варианта осуществления, способ включает идентификацию пациента, нуждающегося в анализе одного или нескольких биомаркеров, представленных в таблице 1. В одном аспекте, пациент, нуждающийся в анализе биомаркера (ов) представляет собой пациента, который имеет наличия рака эндометрия, у которого подозревают наличие рака эндометрия, или и/или который подвергается скринингу.
В некоторых вариантах осуществления, способ согласно изобретению включает сравнение экспрессия биомаркера согласно изобретению с эндогенным биомаркером. Например, уровень экспрессии одного или нескольких биомаркеров, перечисленных в таблице 1, нормализируют к уровню экспрессии эндогенного биомаркера. Следовательно, в одном специфическом аспекте, эндогенный биомаркер выбирают из POLR2A, В2М, PFN1, HMBS, G6PD, и PABPN1. Идентификационные номера ENSMBL представлены ниже для этих эндогенных биомаркеров.
Диагностические и прогностические реагенты
Изобретение обеспечивает реагенты для обнаружения биомаркеров согласно изобретению (например, тех, которые представлены в таблице I). Реагенты пригодны для обнаружения уровней белков и нуклеиновых кислот биомаркеров, представленных в таблице 1, для обнаружения и/или диагностики рака эндометрия. Регенты, описанные ниже, могут использоваться для обнаружения комбинаций биомаркеров для диагностики рака эндометрия. Специфические примеры нуклеиновых кислот, зондов, праймеров и т.д., относящихся к каждому из индивидуальных биомаркеров, представлены в примерах.
В одном варианте осуществления, изобретение обеспечивает АСАА1 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации АСАА1 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с АСАА1 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с АСАА1 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает АСАА1 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает АСАА1 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает АР1М2 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации АР1М2 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с АР1М2 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с АР1М2 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает АР1М2 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает АР1М2 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает CGN нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации CGN нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с CGN нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с CGN белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает CGN полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает CGN полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает DDR1 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации DDR1 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с DDR1 нуклеиновой кислотой для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с DDR1 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает DDR1 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает DDR1 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает EPS8L2 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации EPS8L2 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с EPS8L2 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с EPS8L2 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает EPS8L2 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает EPS8L2 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает FASTKD1 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации FASTKD1 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с FASTKD1 нуклеиновой кислотой для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с FASTKD1 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает FASTKD1 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает FASTKD1 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает GMIP нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации GMIP нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с GMIP нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с GMIP белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает GMIP полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает GMIP полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает IKBKE нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации IKBKE нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с IKBKE нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с IKBKE белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает IKBKE полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает IKBKE полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает P2RX4 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации P2RX4 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с P2RX4 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с P2RX4 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает P2RX4 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает P2RX4 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает Р4НВ нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации Р4НВ нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с Р4НВ нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с Р4НВ белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает Р4НВ полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает Р4НВ полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает PHKG2 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации PHKG2 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с PHKG2 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с PHKG2 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает PHKG2 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает PHKG2 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает PPFIBP2 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации PPFIBP2 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с PPFIBP2 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с PPFIBP2 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает PPFIBP2 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает PPFIBP2 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает PPP1R16A нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации PPP1R16A нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с PPP1R16A нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с PPP1R16A белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает PPP1R16A полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает PPP1R16A полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает RASSF7 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации RASSF7 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с RASSF7 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с RASSF7 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает RASSF7 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает RASSF7 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает RNF183 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации RNF183 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с RNF183 нуклеиновой кислотой для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с RNF183 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает RNF183 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает RNF183 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает SIRT6 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации SIRT6 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с SIRT6 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с SIRT6 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает SIRT6 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает SIRT6 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает TJP3 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации TJP3 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с TJP3 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с TJP3 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает TJP3 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает TJP3 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает EFEMP2 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации EFEMP2 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с EFEMP2 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с EFEMP2 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает EFEMP2 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает EFEMP2 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает SOCS2 нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации SOCS2 нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с SOCS2 нуклеиновой кислотой, для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с SOCS2 белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает SOCS2 полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает SOCS2 полипептид для создания иммунного ответа на маркер.
В одном варианте осуществления, изобретение обеспечивает DCN нуклеиновую кислоту для обнаружения рака эндометрия. В связанном аспекте, изобретение обеспечивает праймеры для амплификации DCN нуклеиновой кислоты для обнаружения рака эндометрия. В другом связанном аспекте изобретение обеспечивает зонд, который может гибридизоваться с DCN нуклеиновой кислотой для обнаружения рака эндометрия.
В другом связанном аспекте, изобретение обеспечивает антитело, которое связывается иммунологически с DCN белком, для обнаружения рака эндометрия. В связанном аспекте изобретение обеспечивает DCN полипептид для создания антитела. В еще другом связанном аспекте, изобретение обеспечивает DCN полипептид для создания иммунного ответа на маркер.
Наборы
Изобретение также обеспечивает наборы для обнаружения одного или нескольких биомаркеров, представленных в таблице 1. В одном варианте осуществления, набор пригоден для обнаружения и/или диагностики рака женских половых органов. В другом варианте осуществления, набор пригоден для обнаружения и/или диагностики рака эндометрия. В одном аспекте, набор содержит реагенты для обнаружения CGN. В одном аспекте, набор содержит средства для обнаружения CGN. В одном аспекте, набор содержит реагенты для обнаружения АР1М2. В одном аспекте, набор содержит средства для обнаружения АР1М2. В одном аспекте, набор содержит реагенты для обнаружения EPS8L2. В одном аспекте, набор содержит средства для обнаружения EPS8L2. В одном аспекте, набор содержит реагенты для обнаружения IKBKE. В одном аспекте, набор содержит средства для обнаружения IKBKE. В одном аспекте, набор содержит реагенты для обнаружения PPP1R16A. В одном аспекте, набор содержит средства для обнаружения PPP1R16A. В одном аспекте, набор содержит реагенты для обнаружения RASSF7. В одном аспекте, набор содержит средства для обнаружения RASSF7. В одном аспекте, набор содержит реагенты для обнаружения TJP3. В одном аспекте, набор содержит средства для обнаружения TJP3. В одном аспекте, набор содержит реагенты для обнаружения P2RX4. В одном аспекте, набор содержит средства для обнаружения P2RX4. В одном аспекте, набор содержит реагенты для обнаружения RNF183. В одном аспекте, набор содержит средства для обнаружения RNF183. В одном аспекте, набор содержит реагенты для обнаружения GMIP. В одном аспекте, набор содержит средства для обнаружения GMIP. В одном аспекте, набор содержит реагенты для обнаружения PHKG2. В одном аспекте, набор содержит средства для обнаружения PHKG2. В одном аспекте, набор содержит реагенты для обнаружения Р4НВ. В одном аспекте, набор содержит средства для обнаружения Р4НВ. В одном аспекте, набор содержит реагенты для обнаружения PPFIBP2. В одном аспекте, набор содержит средства для обнаружения PPFIBP2. В одном аспекте, набор содержит реагенты для обнаружения FASTKD1. В одном аспекте, набор содержит средства для обнаружения FASTKD1. В одном аспекте, набор содержит реагенты для обнаружения DDR1. В одном аспекте, набор содержит средства для обнаружения DDR1. В одном аспекте, набор содержит реагенты для обнаружения SIRT6. В одном аспекте, набор содержит средства для обнаружения SIRT6. В одном аспекте, набор содержит реагенты для обнаружения АСАА1. В одном аспекте, набор содержит средства для обнаружения АСАА1. В одном аспекте, набор содержит реагенты для обнаружения DCN. В одном аспекте, набор содержит средства для обнаружения DCN. В одном аспекте, набор содержит реагенты для обнаружения SOCS2. В одном аспекте, набор содержит средства для обнаружения SOCS2. В одном аспекте, набор содержит реагенты для обнаружения EFEMP2. В одном аспекте, набор содержит средства для обнаружения EFEMP2.
В одном аспекте, набор содержит реагенты для обнаружения от 2 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 2 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 3 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 3 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 4 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 4 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 5 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 5 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 6 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 6 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 7 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 7 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 8 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 8 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для обнаружения от 9 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 9 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 10 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 10 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для обнаружения от 15 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для ОТ-ПЦР оценки от 1 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для ОТ-ПЦР оценки от 1 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для микропанельной оценки от 1 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для микропанельной оценки от 1 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит реагенты для оценки на основе антитела от 1 до 20 биомаркеров из таблицы 1. В одном аспекте, набор содержит средства для оценки на основе антитела от 1 до 20 биомаркеров из таблицы 1. В одном аспекте, набор имеет реагенты для обнаружения различных биомаркеров дополнительно к одному или нескольким биомаркерам, которые перечислены в таблице 1. В одном аспекте, набор имеет средства для обнаружения различных биомаркеров дополнительно к 1-20 биомаркерам, которые перечислены в таблице 1. В одном аспекте, набор имеет реагенты для множественной ПЦР от 2 до 20 маркеров из таблицы 1. В одном аспекте, набор имеет средства для множественной ПЦР от 2 до 20 маркеров из таблицы 1.
В некоторых аспектах, набор имеет устройство для получения образца для анализа. В одном аспекте устройство представляет собой пайпиль. В другом аспекте, устройство представляет собой устройство, как описано в патенте US № 7,207,951, выданном 24 апреля 2007 г., который полностью включен в настоящую заявку в качестве ссылки. В другом аспекте, устройство представляет собой кюретаж. В другом аспекте, устройство представляет собой щетку. Одним примером устройства в виде щетки является тао-щетка.
В некоторых аспектах, набор имеет средства для стабилизации образцов, полученных от пациентов. Например, в специфическом аспекте, средство представляет собой буфер для стабилизации образца, полученного от пациента, содержащий раствор, сохраняющий РНК. В другом аспекте, средство пригодно для стабилизации образов крови или сыворотки.
Диагностические антитела к биомаркерам, представленным в таблице 1
Диагностические антитела к одному или нескольким биомаркерам, представленным в таблице 1, (также обозначаются как целевой белок) для диагностических применений могут быть получены с помощью любого из возможных путей. Кроме того, антитела к некоторым биомаркерам, представленным в таблице 1, являются коммерчески доступными или описаны в литературе. Эти известные антитела могут использоваться в способах согласно изобретению и/или в качестве базиса для конструирования новых антител. Техники фагового дисплея можно использовать для создания антител к одному или нескольким биомаркерам, представленным в таблице 1. Стандартные гибридомные технологии можно использовать для создания антител к одному или нескольким биомаркера, представленным в таблице 1. Антитела к некоторым биомаркерам, представленным в таблице 1, известны в данной области (см. примеры). В некоторых аспектах, антитело к одному или нескольким биомаркерам, представленным в таблице 1, имеет происхождение из животного источника (например, мыши, крысы, или кролика).
Поликлональные антитела
Антитела к целевым белкам могут содержать поликлональные антитела. Способы получения поликлональных антител известны специалисту в данной области техники. Поликлональные антитела могут вырабатываться в млекопитающем, например, путем одной или нескольких инъекций иммунизирующего средства и, при необходимости, адъюванта. Типично, иммунизирующее средство и/или адъювант будут инъецировать млекопитающему путем множественных подкожных или внутрибрюшинных инъекций. Иммунизирующее средство может включать полипептид целевого белка (или его фрагмент) или его слитый белок. Может быть пригодным конъюгирование иммунизирующего средства в белку, для которого известно, что он является иммуногенным для млекопитающего, подвергающегося иммунизации. Примеры таком иммуногенных белков включают, но не ограничиваясь только ими, гемоцианин лимфы улитки, сывороточный альбумин, бычий тиреоглобулин, и соевый ингибитор трипсина. Примеры адъювантов, которые могут применяться, включают полный адъювант Фрейнда и М PL-TDM адъювант (монофосфорил липид А, синтетический трегалоза дикориномиколат). Протокол иммунизации может быть выбран квалифицированным специалистом в данной области техники без дополнительных экспериментов.
Моноклональные антитела
Антитела к целевым белкам могут представлять собой, альтернативно, моноклональные антитела. Моноклональные антитела могут быть получены с помощью методов гибридом, таких как методы, описанные Kohler и Milstein (1975) Nature 256:495. В методе гибридом, мышь, хомячка, или другое подходящее животное-хозяин, обычно иммунизируют с помощью иммунизирующего средства для раздражения лимфоцитов, которые продуцируют или способны продуцировать антитела, которые будут специфически связываться с иммунизирующим средством. Альтернативно, лимфоциты могут быть иммунизированы in vitro.
Иммунизирующее средство обычно будет включать полипептид целевого белка (или его фрагмента) или его слитого белка. В целом, либо лимфоциты периферической крови ("PBL") используются, если желательными являются клетки человеческого происхождения, или используются клетки селезенки или клетки лимфатических узлов, если желательными являются источники-млекопитающие, отличающиеся от человека. После этого лимфоциты сливают с иммортализированной клеточной линией, используя подходящее средство для слияния, такое как полиэтиленгликоль, с образованием гибридомной клетки (Goding, Monoclonal Antibodies: Principles and Practice, Academic Press, (1986) pp.59-103). Иммортализованные клеточные линии обычно представляют собой трансформированные клетки млекопитающих, в частности миеломные клетки грызунов, бычьего и человеческого происхождения. Обычно, используют миеломные клеточные линии крыс или мышей. Гибридомные клетки могут культивироваться в подходящей культуральной среде, которая предпочтительно содержит одно или несколько веществ, которые ингибируют рост или выживание неслитых, иммортализованных клеток. Например, если в родительских клетках отсутствует фермент гипоксантин-гуанинфосфорибозилтрансфераза (HGPRT или HPRT), то культуральная среда для гибридом обычно будет включать гипоксантин, аминоптерин, и тимидин ("HAT среда"), где эти вещества предотвращают рост HGPRT-дефицитных клеток.
Предпочтительные иммортализованные линии клеток представляют собой те линии, которые сливаются эффективно, поддерживают стабильно высокий уровень экспрессии антитела путем выбранных антитело-продуцирующих клеток, и являются чувствительными к среде, такой как HAT среда. Более предпочтительные иммортализованные линии клеток представляют собой мышиные миеломные линии, которые могут быть получены, например, из Salk Institute Cell Distribution Center, San Diego, Calif, и Американской коллекции типовых культур (American Type Culture Collection), Manassas, Va. Также были описаны линии клеток миеломы человека и гетеромиеломы мышь-человек для продукции человеческих моноклональных антител (Kozbor (1984) J.Immunol. 133:3001; Brodeur и др., Monoclonal Antibody Production Techniques and Applications, Marcel Dekker, Inc., New York, (1987) cc.51-63).
После этого культуральная среда, в которой культивируются гибридомные клетки, может подвергаться анализу для определения наличия моноклональных антител к целевому белку. Предпочтительно, специфичность связывания моноклональных антител, продуцируемых гибридомными клетками, определяют с помощью иммунопреципитации или путем анализа связывания in vitro, такого как радиоиммунологический анализ (RIA) или иммуносорбентный ферментный анализ (ELISA). Такие техники и исследования известны в данной области. Специфичность связывания моноклонального антитела можно определить, например, с помощью анализа Скэтчарда Munson и Pollard (1980) Anal. Biochem. 107:220.
После того как, были идентифицированы желательные гибридомные клетки, клоны можно субклонировать с помощью процедур серийных разведений и выращивать с помощью стандартных методов [Monoclonal Antibodies: Principles and Practice, (1986) cc.59-103]. Подходящие культуральные среды для этой цели включают, например, модифицированную по способу Дульбекко среду Игла и RPMI-1640 среду. Альтернативно, гибридомные клетки можно выращивать in vivo в виде асцитов у млекопитающего.
Моноклональные антитела, секретируемые субклонами, можно выделять или очищать из культуральной среды или асцитной жидкости с помощью общепринятых техник очистки иммуноглобулинов, таких как, например, протеин А-Сефароза, гидроксилапатит хроматография, гель-электрофорез, диализ, или аффинная хроматография.
Моноклональные антитела также могут быть получены с помощью методов рекомбинантной ДНК, таких как методы, описанные в патенте US № 4,816,567. ДНК, кодирующая Моноклональные антитела согласно изобретению, легко может быть выделена и секвенирована, используя общепринятые процедуры (например, используя олигонуклеотидные зонды, которые способны специфически связываться с генами, кодирующими тяжелые и легкие цепи мышиных антител). Гибридомные клетки согласно изобретению служат в качестве предпочтительного источника такой ДНК. После выделения, ДНК можно помещать в экспрессионные векторы, которые затем трансфектируют в клетки-хозяева, такие как COS клетки обезьян, клетки яичника китайского хомячка (СНО), или миеломные клетки, которые только как предусмотрено продуцируют белок иммуноглобулина, получая синтез моноклональных антител в рекомбинантных клетках-хозяевах. ДНК также может быть модифицирована, например, путем замены кодирующей последовательности для константных доменов тяжелых и легких цепей человека вместо гомологичных мышиных последовательностей [патент US № 4,816,567; Morrison и др., выше] или путем ковалентного присоединения к кодирующей последовательности иммуноглобулина всей или части кодирующей последовательности для полипептида, неиммуноглобулина. Такой полипептид, не представляющий собой иммуноглобулин, может быть заменен на константные домены антитела согласно изобретению, или может быть заменен на вариабельные домены одного антиген-связывающего сайта антитела согласно изобретению для создания химерного двухвалентного антитела.
Антитела могут представлять собой моновалентные антитела. Способы получения моновалентных антител хорошо известны в данной области техники. Например, один из методов включает рекомбинантную экспрессию легкой цепи иммуноглобулина и модифицированной тяжелой цепи. Тяжелая цепь усечена в целом в любой точке в Fc участке для того, чтобы предотвратить перекрестное связывание тяжелых цепей. Альтернативно, релевантные остатки цистеина заменены другим аминокислотным остатком или удалены для того, чтобы предотвратить поперечное связывание.
Методы in vitro также пригодны для получения моновалентных антител. Расщепление антител для получения их фрагментов, в частности, Fab фрагментов, может осуществляться с помощью общепринятых методик, известных в данной области.
Фаговый дисплей
Антитела к биомаркерам согласно изобретению также могут быть получены путем применения комбинаторных библиотек для скрининга клонов синтетических антител с желательной активностью или активностями. В принципе, клоны синтетических антител отбирают путем скрининга фагов библиотек, содержащих фаг, который проявляет различные фрагменты вариабельного участка антитела (Fv), слитого с белком оболочки фага. Такие фаговые библиотеки прогоняют с помощью аффинной хроматографии относительно желательного антигена. Клоны, экспрессирующие Fv фрагменты, способные связываться с желательным антигеном, адсорбируются на антигене и таким образом отделяются от несвязанных клонов в библиотеке. После этого связанные клоны элюируются с антигена, и в дальнейшем могут обогащаться путем дополнительных циклов адсорбция антигеном /элюция. Антитела к биомаркерам согласно изобретению могут быть получены путем создания подходящей процедуры скрининга антигена для выбора клона фага, представляющего интерес, с последующим конструированием клона полноразмерного антитела, используя Fv последовательности из клона фага, представляющего интерес, и подходящих последовательностей константного участка (Fc), описанных в Kabat и др., Sequences of Proteins of Immunological Interest, пятое издание, NIH Publication 91-3242, Bethesda MD (1991), тома 1-3.
Конъюгаты антител
Антитела (и их фрагменты) согласно изобретению могут быть конъюгированы с молекулами для диагностических целей. Например, антитело к биомаркеру, представленному в таблице 1, может быть конъюгировано с обнаруживаемой меткой (например, для визуализации) для диагностики или обнаружения рака эндометрия. Подходящие обнаруживаемые маркеры включают, но не ограничиваясь только ими, радиоактивный изотоп, наночастицу, флуоресцирующее соединение, биолюминесцентное соединение, хемилюминесцентное соединение, металлохелат или фермент. Техники для конъюгирования диагностических средств к антителам хорошо известны (Holmes и др. (2001) Curr Protoc Cytom. May; раздел 4: секция 4.2; Kumar и др (2008) ACS Nano. Mar; 2(3):449-56; Rosenthal и др. (2006) Laryngoscope Sep; 116(9): 1636-41). Дополнительно наборы для конъюгации средств к диагностическим антител являются коммерчески доступными.
Данные и информация
В одном аспекте согласно изобретению, настоящее изобретение относится к способу для сравнения и компилирования данных, где данные хранятся в электронном или бумажном формате. Электронный формат может быть выбран из группы, включающей электронную почту, диск, компакт-диск (CD), компакт-диск формата DVD (DVD), карту памяти, схему памяти, ROM или RAM, магнитный оптический диск, ленту, видео, видеоклип, микрофильм, Интернет, сеть совместного пользования, сервер совместного пользования и другие; где данные представляются, передаются или анализируются с помощью электронной пересылки, представления видео, телекоммуникации, или путем применения любого из вышеописанных форматов хранения; где данные сравниваются и компилируются в сайте отбора образцов или в расположении, где данные транспортируются с помощью процесса, как описано выше. Данные согласно этому варианту осуществления представляют собой информации относительно результатов анализа биомаркеров из таблицы 1.
Биомаркеры, реагенты, мишени, исследования, тесты, обследования и методологии, описанные в настоящей заявке, могут применяться в различных контекстах, включая диагностическое открытие, диагностическую разработку, мониторинг безопасности и эффективности, сравнительные исследования, маркетинг и другие. Информация, обеспечиваемая изобретением, может быть сообщена регуляторным органам, лечащим врачам и другим медицинским работникам, производителям, владельцам, инвесторам, пациентам, и/или широкой общественности. Эта и другая информация могут использоваться, например, в поисковых исследованиях, доклинических и клинических действиях, мечения, продукции, рекламировании, и продажах.
Определения
Как используется в настоящей заявке, "АСАА1 биомаркер" относится к "АСАА1 нуклеиновой кислоте" или "АСАА1 белку", которые могут быть специфически обнаружены. АСАА1 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену АСАА1 человека или его фрагменту. Например, АСАА1 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле АСАА1 мРНК. АСАА1 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном АСАА1. Примеры АСАА1 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения АСАА1 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "АР1М2 биомаркер" относится к "АР1М2 нуклеиновой кислоте" или "АР1М2 белку", которые могут быть специфически обнаружены. АР1М2 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену АР1М2 человека или его фрагменту. Например, АР1М2 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле АР1М2 мРНК. АР1М2 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном АР1М2. Примеры АР1М2 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения АР1М2 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "CGN биомаркер" относится к "CGN нуклеиновой кислоте" или "CGN белку", которые могут быть специфически обнаружены. CGN нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену CGN человека или его фрагменту. Например, CGN нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле CGN мРНК. CGN белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном CGN. Примеры CGN биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения CGN биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "DDR1 биомаркер" относится к "DDR1 нуклеиновой кислоте" или "DDR1 белку", которые могут быть специфически обнаружены. DDR1 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену DDR1 человека или его фрагменту. Например, DDR1 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле DDR1 мРНК. DDR1 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном DDR1. Примеры DDR1 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения DDR1 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "EPS8L2 биомаркер" относится к "EPS8L2 нуклеиновой кислоте" или "EPS8L2 белку", которые могут быть специфически обнаружены. EPS8L2 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену EPS8L2 человека или его фрагменту. Например, EPS8L2 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле EPS8L2 мРНК. EPS8L2 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном EPS8L2. Примеры EPS8L2 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения EPS8L2 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "FASTKD1 биомаркер" относится к "FASTKD1 нуклеиновой кислоте" или "FASTKD1 белку", которые могут быть специфически обнаружены. FASTKD1 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену FASTKD1 человека или его фрагменту. Например, FASTKD1 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле FASTKD1 мРНК. А FASTKD1 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном FASTKD1. Примеры FASTKD1 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения FASTKD1 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "GMIP биомаркер" относится к "GMIP нуклеиновой кислоте" или "GMIP белку", которые могут быть специфически обнаружены. GMIP нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену GMIP человека или его фрагменту. Например, GMIP нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле GMIP мРНК. А GMIP белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном GMIP. Примеры GMIP биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения GMIP биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "IKBKE биомаркер" относится к "IKBKE нуклеиновой кислоте" или "IKBKE белку", которые могут быть специфически обнаружены. IKBKE нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену IKBKE человека или его фрагменту. Например, IKBKE нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле IKBKE мРНК. IKBKE белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном IKBKE. Примеры IKBKE биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения IKBKE биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "P2RX4 биомаркер" относится к "P2RX4 нуклеиновой кислоте" или "P2RX4 белку", которые могут быть специфически обнаружены. P2RX4 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену P2RX4 человека или его фрагменту. Например, P2RX4 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле P2RX4 мРНК. А P2RX4 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном P2RX4. Примеры P2RX4 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения P2RX4 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "Р4НВ биомаркер" относится к "Р4НВ нуклеиновой кислоте" или "Р4НВ белку", которые могут быть специфически обнаружены. Р4НВ нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену Р4НВ человека или его фрагменту. Например, Р4НВ нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле Р4НВ мРНК. А Р4НВ белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном Р4НВ. Примеры Р4НВ биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения Р4НВ биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "PHKG2 биомаркер" относится к "PHKG2 нуклеиновой кислоте" или "PHKG2 белку", которые могут быть специфически обнаружены. PHKG2 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену АР1М2 человека или его фрагменту. Например, PHKG2 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле PHKG2 мРНК. А PHKG2 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном PHKG2. Примеры PHKG2 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения PHKG2 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "PPFIBP2 биомаркер" относится к "нуклеиновой кислоте биомаркера PPFIBP2" или "белку биомаркера PPFIBP2", которые могут быть специфически обнаружены. Нуклеиновая кислота биомаркера PPFIBP2 может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену PPFIBP2 биомаркера человека или его фрагменту. Например, нуклеиновая кислота биомаркера PPFIBP2 может представлять собой кДНК, или ее фрагмент, соответствующий молекуле мРНК биомаркера PPFIBP2. Белок биомаркера PPFIBP2 относится к белку (или его фрагменту), который кодируется или экспрессируется геном биомаркера PPFIBP2. Примеры биомаркеров PPFIBP2 биомаркера представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения биомаркеров PPFIBP2 биомаркера, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "PPP1R16A биомаркер" относится к "PPP1R16A нуклеиновой кислоте" или "PPP1R16A белку", которые могут быть специфически обнаружены. PPP1R16A нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену PPP1R16A человека или его фрагменту. Например, PPP1R16A нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле PPP1R16A мРНК. PPP1R16A белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном PPP1R16A. Примеры PPP1R16A биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения PPP1R16A биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "TJP3 биомаркер" относится к "TJP3 нуклеиновой кислоте" или "TJP3 белку", которые могут быть специфически обнаружены. TJP3 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену TJP3 человека или его фрагменту. Например, TJP3 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле TJP3 мРНК. TJP3 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном TJP3. Примеры TJP3 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения TJP3 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "RASSF7 биомаркер" относится к "RASSF7 нуклеиновой кислоте" или "RASSF7 белку", которые могут быть специфически обнаружены. RASSF7 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену RASSF7 человека или его фрагменту. Например, RASSF7 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле RASSF7 мРНК. RASSF7 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном RASSF7. Примеры RASSF7 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения RASSF7 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "RNF183 биомаркер" относится к "RNF183 нуклеиновой кислоте" или "RNF183 белку", которые могут быть специфически обнаружены. RNF183 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену RNF183 человека или его фрагменту. Например, RNF183 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле RNF183 мРНК. RNF183 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном RNF183. Примеры RNF183 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения RNF183 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "SIRT6 биомаркер" относится к "SIRT6 нуклеиновой кислоте" или "SIRT6 белку", которые могут быть специфически обнаружены. SIRT6 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену SIRT6 человека или его фрагменту. Например, SIRT6 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле SIRT6 мРНК. SIRT6 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном SIRT6. Примеры SIRT6 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения SIRT6 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "DCN биомаркер" относится к "DCN нуклеиновой кислоте" или "DCN белку", которые могут быть специфически обнаружены. DCN нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену DCN человека или его фрагменту. Например, DCN нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле DCN мРНК. DCN белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном DCN. Примеры LSR биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения DCN биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "SOCS2 биомаркер" относится к "SOCS2 нуклеиновой кислоте" или "SOCS2 белку", которые могут быть специфически обнаружены. SOCS2 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену SOCS2 человека или его фрагменту. Например, SOCS2 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле SOCS2 мРНК. SOCS2 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном SOCS2. Примеры SOCS2 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения SOCS2 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, "EFEMP2 биомаркер" относится к "EFEMP2 нуклеиновой кислоте" или "EFEMP2 белку", которые могут быть специфически обнаружены. EFEMP2 нуклеиновая кислота может представлять собой РНК молекулу, ДНК молекулу, или другую нуклеиновую кислоту, которая соответствует гену EFEMP2 человека или его фрагменту. Например, EFEMP2 нуклеиновая кислота может представлять собой кДНК, или ее фрагмент, соответствующий молекуле EFEMP2 мРНК. An EFEMP2 белок относится к белку (или его фрагменту), который кодируется или экспрессируется геном EFEMP2. Примеры EFEMP2 биомаркеров представлены в примерах, также как и некоторые реагенты, пригодные для обнаружения EFEMP2 биомаркеров, нуклеиновых кислот, и белков.
Как используется в настоящей заявке, термин "чувствительность" относится к соотношению субъектов с положительным сравнительным тестом (больных), у кого тест положительный со скрининговым тестом.
Как используется в настоящей заявке, термин "специфичность" относится к пропорций субъектов с отрицательным сравнительным тестом (здоровых), у кого тест отрицательный со скрининговым тестом.
Как используется в настоящей заявке, термин "секреторная фаза" относится к фазе менструального цикла, которая может быть отличена от других фаз менструального цикла с помощью стандартных процедур в данной области, например, патологического исследования ткани, полученной из эндометрия или матки. Секреторная фаза связана с кровотечением (менструация).
Как используется в настоящей заявке, термин "ROC" или "зависимость чувствительности от частоты ложноположительных заключений" относится к графическому изображению чувствительности относительно (1-специфичности) или другими словами график коэффициента истинно-положительных результатом относительно фракции ложноположительных. Площадь под ROC, или AUROC, кривой может изменяться в диапазоне от 0 до 1. Площадь под ROC кривой 1 представляет собой совершенный текст или разделение групп, тогда как площадь под кривой ROC 0,5 указывает на то, что классификатор по существу неспособен разделить группы и, таким образом, является непригодным.
"Рак" у животного относится к наличию клеток, обладающих типичными характеристиками клеток, вызывающих рак, например, неконтролируемой пролиферацией, потерей специализированных функций, бессмертием, существенным метастатическим потенциалом, существенным повышением анти-апоптотической активности, быстрым ростом и скоростью пролиферации, и определенными характерными морфологическими и клеточными маркерами.
Фраза "обнаружение рака" или "диагностика рака" относится к определению наличия или отсутствия рака или предракового состояния у животного. "Обнаружение рака" также может относиться к получению подтверждений относительно вероятности наличия предраковых или раковых клеток у животного или оценки предрасположенности пациента к развитию рака. Обнаружение рака может осуществляться с применением способов в соответствии с настоящим изобретением отдельно, в комбинации с другими методами, или с учетом другой информации относительно состояния здоровья животного.
"Опухоль," как используется в настоящей заявке, относится к росту и пролиферации всех опухолевых клеток, независимо от того, являются ли они злокачественными или доброкачественными, и всех предраковых и раковых клеток и тканей.
Термин "предраковый" относится к клеткам или тканям, имеющим характеристики, относящиеся к изменениям, которые могут приводить к злокачественности или раку.
В целом, "ген" представляет собой участок генома, который способен транскрибировать в РНК, которая имеет либо регуляторную функцию, каталитическую функцию, и/или кодирует белок. Эукариотический ген обычно имеет интроны и экзоны, которые могут организовываться и продуцировать различные варианты РНК сплайсов, которые кодируют альтернативные версии зрелого белка. Для квалифицированного специалиста в данной области техники будет понятным, что настоящее изобретение охватывает все кодирующие транскрипты, которые могут быть обнаружены, включая варианты сплайсинга, аллельные варианты и транскрипты, которые возникают вследствие альтернативные промоторных сайтов или альтернативных сайтов полиаденилирования биомаркеров, как перечислено в таблице 1. "Полноразмерный" ген или РНК таким образом охватывает любые встречающиеся в природе варианты сплайсинга, аллельные варианты, другие альтернативные транскрипты, варианты сплайсинга, созданные с помощью рекомбинантных технологий, которые выполняют аналогичную функцию, что и встречающиеся в природе варианты, и образованные молекулы РНК. "Фрагмент" гена, включая онкоген, может представлять собой любую порцию из гена, которые может представлять или может не представлять собой функциональный домен, например, каталитический домен, ДНК-связывающий домен, и т.д. Фрагмент предпочтительно может включать нуклеотидные последовательности, которые кодируют по меньшей мере 25 смежных аминокислот, и предпочтительно по меньшей мере приблизительно 30, 40, 50, 60, 65, 70, 75 или больше непрерывных аминокислот или любое целое число около или внутри этого диапазона. В некоторых аспектах согласно изобретению, для квалифицированного специалиста в данной области техники будет понятно, что термин ген используется взаимозаменяемо с термином "локус", который относится в общем к геномной ДНК, несмотря на то, что кодирует ли он РНК, белок, или регуляторный элемент.
"Дифференциально экспрессируемый транскрипт гена", как используется в настоящей заявке, относится к гену, транскрипт которого обнаружен на различном уровне в различных типах клеток или тканей организма, имеющего опухоль или рак, по сравнению с уровнем или состоянием транскрипта гена, обнаруженным в клетках аналогичной ткани в здоровом организме, или в клетках аналогичной ткани в том же организме. Множественные копии транскриптов генов могут быть обнаружены в организме, имеющем опухоль или рак, в то время как несколько копий аналогичного транскрипта гена обнаруживают в здоровом организме или здоровых клетках той же ткани в том же организме, или наоборот для генов, экспрессия которых подавлена. В целом, дифференциально экспрессируемые транскрипты представляют собой такие транскрипты, которые, при измерении в пораженном образце или образце от пораженного пациента, имеют определяемый другой уровень экспрессии по сравнению с контрольным значением, который является характерным для непораженного образца или образца от непораженного пациента. Примеры дифференциальной экспрессии включают изменение на 10% или больше, 20% или больше 30% или больше, 40% или больше, или 50% или больше в пораженном по сравнению с непораженным.
Как используется в настоящей заявке термин "полипептид" обозначает последовательность аминокислот, соединенных вместе с помощью пептидных связей. Аминокислотная последовательность полипептида может определяться последовательностью ДНК оснований, которые кодируют аминокислоты полипептидной цепи. Полипептиды, описанные в настоящей заявке, включают, но не ограничиваясь только ими, полные белки, фрагменты полных белков, эпитопы белков и др. Как используется в настоящей заявке, термин полипептид, пептид, и белок относится к молекуле, имеющей два или больше аминокислотных остатков (природных или неприродных), соединенных вместе с помощью одной или нескольких пептидных связей.
"Дифференциально экспрессируемый ген" может представлять собой целевой ген, ген фингерпринта, или ген пути метаболизма. Например, "ген фингерпринта", как используется в настоящей заявке, относится к дифференциально экспрессируемому гену, характер экспрессии которого может использоваться в качестве прогностического или диагностического маркера для оценки опухолей и рака, или который может использоваться для идентификации соединений, пригодных для идентификации соединений, пригодных для лечения опухолей и рака, например, рака эндометрия. Гены фингерпринта могут представлять собой один или несколько генов (или соответствующих биомаркеров например, белка), соответствующим биомаркерам из таблицы 1.
"Характерная картина фингерпринтов", как используется в настоящей заявке, относится к характерной картине, полученной, когда определяют характер экспрессии серий (которые могут находиться в диапазоне от двух до всех генов фингерпринта, которые существуют для данного состояния) генов фингерпринта. Характерная картина фингерпринтов также может обозначаться как "профиль экспрессии". Характерная картина фингерпринтов или профиль экспрессии, имеющий от 1 до 20 биомаркеров, представленных в таблице 1, могут использоваться в аналогичных диагностических, прогностических, и методах согласно изобретению.
"Гены метаболических путей", как используется в настоящей заявке, представляют собой гены, которые кодируют белки или полипептиды, которые взаимодействуют с другими генными продуктами, задействованными в опухоли и рак. Гены метаболических путей также могут проявлять характеристики целевого гена и/или гена фингерпринта.
"Обнаруживаемый" уровень экспрессии РНК, как используется в настоящей заявке, обозначает уровень, который обнаруживается с помощью стандартных техник, известных в настоящее время в данной области техники или тех, которые станут стандартными в ближайшем будущем, и включают, например, сравнительный анализ, полимеразную цепную реакцию (ПЦР), связанную с ОТ (обратная транскриптаза), нозерн-блоттинг, и/или анализы защиты от РНКазы.
Молекулы нуклеиновой кислоты согласно изобретению, например, те, которые соответствуют одному или больше биомаркерам из таблицы 1, и их последовательности /альтернативные транскрипты, могут быть вставлены в вектор, как описано ниже, который будет облегчать экспрессию вставки. Молекулы нуклеиновой кислоты и полипептиды, которые они кодируют, могут использоваться непосредственно к качестве диагностических средств, или могут использоваться (непосредственно в случае полипептида или опосредованно в случае молекулы нуклеиновой кислоты) для создания антител, которые, в свою очередь, клинически пригодны в качестве диагностического средства. Следовательно, векторы, содержащие нуклеиновые кислоты согласно изобретению, клетки, трансфектированные этими векторами, экспрессируемые полипептиды, и антитела, созданные либо к целому полипептиду или его антигенному фрагменту, составляют аспекты согласно изобретению.
"Выделенная молекула ДНК" представляет собой фрагмент ДНК, который отделен от хромосомной или геномной ДНК организма. Выделение также определяется для дополнительного обозначения степени выделения из оригинального источника или окружающих условий.
"Комплементарная ДНК" (кДНК), часто обозначается как "копия ДНК", представляет собой одноцепочечную молекулу ДНК, которая образуется из матрицы мРНК с помощью фермента обратная транскриптаза. Специалисты в данной области также используют термин "кДНК" для обозначения двухцепочечной молекулы ДНК, которая содержит одноцепочечную молекулу ДНК и ее комплементарную ДНК цепь.
Термин "экспрессия" относится к биосинтезу продукта гена.
"Клонирующий вектор" представляет собой молекулу нуклеиновой кислоты, например, плазмиду, космиду или бактериофаг, который способен автономно реплицироваться в клетке-хозяине. Клонирующие векторы обычно содержат (i) один или небольшое количество сайтов распознавания рестрикционной эндонуклеазой, в которые могут быть вставлены последовательности чужеродной ДНК определяемым образом без потери существенной биологической функции вектора, и (ii) маркерный ген, который пригоден для применения для идентификации и отбора клеток, трансформированных или трансфектированных клонирующим вектором. Маркерные гены могут включать, но не ограничиваясь только ими, гены, которые обеспечивают резистентность к тетрациклину или резистентность к ампициллину.
"Экспрессионный вектор" представляет собой конструкцию нуклеиновой кислоты, созданную рекомбинантно или синтетически, несущую серии заданных элементов нуклеиновых кислот, которая способна осуществлять транскрипцию конкретного гена в клетке-хозяине. Обычно, экспрессию гена устанавливают под контролем определенных регуляторных элементов, включая конститутивные или индуцибельные промоторы, регуляторные элементы, предпочтительные для ткани, и энхансеры.
"Рекомбинантный хозяин" может представлять собой любую прокариотическую или эукариотическую клетку, которая содержит либо клонирующий вектор или экспрессионный вектор. Этот термин также охватывает те прокариотические или эукариотические клетки, которые были генетически сконструированы таким образом, что они содержат клонированный (ые) ген (ы) в хромосоме или геноме клетки-хозяина.
Термин "функционально связанный" используется для описания соединения между регуляторными элементами и геном или его кодирующим участком. Это обозначает, что экспрессия гена обычно находится под контролем определенных регуляторных элементов, включая конститутивные или индуцибельные промоторы, ткане-специфические регуляторные элементы, и энхансеры. Такой ген или кодирующий участок считается "функционально связанным с" или "функционирующе связан с" или "функционально ассоциирован с" регуляторными элементами, обозначает, что ген или кодирующий участок контролируется или находится под влиянием регуляторного элемента.
"Гомология последовательностей" используется для описания взаимоотношения последовательностей между двумя или больше нуклеиновых кислот, полинуклеотидов, белков, или полипептидов, и понимается в контексте и в сочетании с терминами, включая: (а) сравнительная последовательность, (b) окно сравнения, (с) идентичность последовательностей, (d) процент идентичности последовательностей, и (е) существенная идентичность или "гомология."
"Сравнительная последовательность" представляет собой известную последовательность, которая используется как основание для сравнения последовательностей. Сравнительная последовательность может представлять собой подгруппу или целую специфическую последовательность; например, сегмент полноразмерной кДНК или последовательности гена, или полную кДНК или последовательность гена. Для полипептидов, длину сравнительной последовательности полипептида можно выбирать из по меньшей мере приблизительно 16 аминокислот, по меньшей мере приблизительно 20 аминокислот, по меньшей мере приблизительно 25 аминокислот, и приблизительно 35 аминокислот, приблизительно 50 аминокислот, или приблизительно 100 аминокислот. Для нуклеиновых кислот, длину сравнительной последовательности нуклеиновых кислот можно выбирать из по меньшей мере приблизительно 50 нуклеотидов, по меньшей мере приблизительно 60 нуклеотидов, по меньшей мере приблизительно 75 нуклеотидов, и приблизительно 100 нуклеотидов или приблизительно 300 нуклеотидов или любого целого числа около или в указанном диапазоне.
"Окно сравнения" включает ссылку на непрерывный соприкасающийся и заданный сегмент полинуклеотидной последовательности, где полинуклеотидная последовательность может быть сравнена со сравнительной последовательностью и где часть полинуклеотидной последовательности в окне сравнения может включать добавления, замещения, или делеции (то есть, бреши) по сравнению со сравнительной последовательностью (которая не содержит добавлений, замещений, или делеции) для оптимального выравнивания двух последовательностей. В целом, окно сравнения составляет по меньшей мере 20 смежных нуклеотидов в длину, и необязательно может быть 30, 40, 50, 100, или больше. Для специалиста в данной области техники понятно, как избежать ошибочного высокого сходства со сравнительной последовательностью благодаря включению брешей в полинуклеотидную последовательность штраф за брешь обычно включают и отнимают от количества совпавших пар.
Методы выравнивания последовательностей для сравнения хорошо известны в данной области техники. Оптимальное выравнивание последовательностей для сравнения может быть осуществлено путем алгоритма локальной гомологии Smith и Waterman (1981) Adv. Appl. Math., 2: 482,; путем алгоритма гомологичного выравнивания и Wunsch (1970) J.Mol.Biol., 48: 443; путем поиска сходства по методу Pearson и Lipman (1988) Proc. Natl. Acad. Sci. USA, 8: 2444; путем компьютеризированного выполнения этих алгоритмов, включая, но не ограничиваясь только ими: CLUSTAL в программе PC/Gene от Intelligenetics, Mountain View, Calif., GAPS, BESTFIT, BLAST, FASTA, и TFASTA в Wisconsin Genetics Software Package, Genetics Computer Group (GCG), 7 Science Dr., Madison, Wise., USA; программа CLUSTAL хорошо описана Higgins и Sharp (1988) Gene 73: 237-244; Corpet и др. (1988) Nucleic Acids Research, 16:881-90; Huang, и др., Computer Applications in the Biosciences, 8:1-6, 1992; и Pearson, и др. (1994) Methods in Molecular Biology, 24:7-331. Семейство программ BLAST, которые может использоваться для поиска сходства в базах данных, включает: BLASTN для нуклеотидных поисковых последовательностей относительно нуклеотидных последовательностей из баз данных; BLASTX для нуклеотидных поисковых последовательностей относительно белковых последовательностей из баз данных; BLASTP для белковых поисковых последовательностей относительно белковых последовательностей из баз данных; TBLASTN для белковых поисковых последовательностей относительно нуклеотидных последовательностей из баз данных; и TBLASTX для нуклеотидных поисковых последовательностей относительно нуклеотидных последовательностей из баз данных. См., Current Protocols in Molecular Biology, часть 19, Ausubel, и др., ред., Greene Publishing и Wiley-Interscience, New York, 1995. Новые версии вышеописанных программ или сами новые программы, несомненно, появятся в будущем, и могут использоваться в соответствии с настоящим изобретением.
Если специально не указано иначе, значения идентичности /сходства последовательностей, представленные в настоящем изобретении, относятся к значениям, полученным с использованием набора программ BLAST 2.0, или их правопреемников, используя параметры по умолчанию. Altschul и др. (1997) Nucleic Acids Res, 2:3389-3402. Подразумевается, что настройки по умолчанию этих параметров легко могут быть изменены, при необходимости, в будущем.
Как будет очевидно для квалифицированного специалиста в данной области техники, BLAST поиски предполагают, что белки могут моделироваться в качестве случайных последовательностей. Тем не менее, многие настоящие белки содержат участки неслучайных последовательностей, которые могут представлять собой гомополимерные участки, повторы с коротким периодом, или участки, обогащенные одной или больше аминокислотами. Такие участки с низкой сложностью могут выравниваться между неродственными белками, даже если другие участки белка являются полностью несходными. Различные программы фильтрования низкой сложности могут применяться для уменьшения такого низкосложного выравнивания. Например, фильтры для низкой сложности SEG (Wooten и Federhen, (1993) Comput. Chem. 17:149-163) и XNU (Claverie и States (1993) Comput. Chem., 17:191-1) могут применяться отдельно или в комбинации.
"Идентичность последовательностей" или "идентичность" в контексте двух последовательностей нуклеиновых кислот или полипептидов включает ссылки на остатки в двух последовательностям, которые являются одинаковыми при выравнивании для максимального соответствия в указанном окне сравнения, и может учитывать добавления, делеции и замещения. Если используется процент идентичности последовательностей по отношению к белкам, то общепризнано, что положения остатков, которые не являются идентичными, часто отличаются консервативными аминокислотными заменами, где аминокислотные остатки замещены другими аминокислотными остатками со сходными химическими свойствами (например, заряд или гидрофобность) и таким образом не оказывают разрушительного влияния на изменение функциональных свойств молекулы. Если последовательности отличаются консервативными заменами, то процент идентичности последовательностей может быть скорректирован вверх для коррекции консервативной природы замены. Считается, что последовательности, которые отличаются такими консервативными заменами, имеют сходные последовательности. Подходы для осуществления такой подгонки хорошо известны специалистам в данной области техники. Обычно это включает подсчет консервативных замен в виде частичного, а не полного ошибочного спаривания, таким образом повышая процент идентичность последовательностей. Следовательно, например, если идентичная аминокислота имеет показатель 1 и неконсервативная замена имеет показатель ноль, то консервативная замена имеет показатель между нулем и 1. Оценку консервативных замен рассчитывают, например, в соответствии с алгоритмом Meyers и Miller (1988) Computer Applic. Biol. Sci., 4: 11-17 например, как реализовано в программе PC/GENE (Intelligenetics, Mountain View, Calif., USA).
"Процент идентичности последовательностей" обозначает значение, определенное путем сравнение двух оптимально выравненных последовательностей через окно сравнения, где часть полинуклеотидной последовательности в окне сравнения может содержать добавления, замены, или делеции (то есть, бреши) по сравнению со сравнительной последовательностью (которая не содержит добавлений, замен, или делеции) для оптимального выравнивания двух последовательностей. Процент рассчитывается путем определения количества положений, в которых расположены идентичные основания нуклеиновых кислот или аминокислотные остатки в обеих последовательностях с получением количества спаренных положений, разделения количества спаренных положений в окне сравнения и умножения результата на 100 для получения процента идентичности последовательностей.
Термин "существенная идентичность" или "гомология" в их различных грамматических формах в контексте полинуклеотидов обозначает, что полинуклеотид содержит последовательность, которая имеет желательную идентичность, например, по меньшей мере 60% идентичность, предпочтительно по меньшей мере 70% идентичность последовательностей, более предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95%, по сравнению со сравнительной последовательностью, используя одну из описанных программ выравнивая с применением стандартных параметров. Для специалиста в данной области техники будет понятным, что эти значения могут быть подходяще откорректированы для определения соответствующей идентичности белков, кодируемых двумя нуклеотидными последовательностями, принимая во внимание вырожденность кодона, сходство аминокислот, положение открытой рамки считывания и другие. Существенная идентичность аминокислотных последовательностей обычно обозначает идентичность последовательностей по меньшей мере 60%, более предпочтительно по меньшей мере 70%, 80%, 90%, и наиболее предпочтительно по меньшей мере 95%.
Другим свидетельством того, что нуклеотидные последовательности являются существенно идентичными, является то, что молекулы двух последовательностей гибридизируются друг с другом в жестких условиях. Тем не менее, нуклеиновые кислоты, которые не гибридизируются друг с другом в жестких условиях, еще являются существенно идентичными, если полипептиды, которые они кодируют, являются существенно идентичными. Это может происходить, например, когда копия нуклеиновой кислоты создается с использованием максимальной вырожденности кодонов, разрешенных генетическим кодом. Одним из свидетельств, что две последовательности нуклеиновых кислот является существенно идентичными, является то, что полипептид, который кодируется первой нуклеиновой кислотой, иммунологически перекрестие реагирует с полипептидом, кодируемым второй нуклеиновой кислотой, хотя такая перекрестная реактивность не является необходимой для двух полипептидов, которые, предположительно, являются существенно идентичными.
Термин "существенная идентичность" или "гомология" в их различных грамматических формах в контексте пептидов указывает на то, что пептид содержит последовательность, которая имеет желательную идентичность, например, по меньшей мере 60% идентичность, предпочтительно по меньшей мере 70% идентичность последовательностей со сравнительной последовательностью, более предпочтительно 80%, еще более предпочтительно 85%, наиболее предпочтительно по меньшей мере 90% или 95% идентичность последовательностей со сравнительной последовательностью в указанном окне сравнения. Предпочтительно, оптимальное выравнивание осуществляют с использованием алгоритма выравнивания гомологии Needleman и Wunsch (1970) J.Mol.Biol., 48:443. Свидетельством того, что две пептидные последовательности являются существенно идентичными является то, что один полипептид иммунологически реагирует с антителами, выработанными к другому пептиду, хотя такая перекрестная реактивность не является необходимой для двух полипептидов, которые, предположительно, являются существенно идентичными. Следовательно, пептид является существенно идентичным со вторым пептидом, например, если два пептида отличаются только консервативной заменой. Пептиды, которые представляют собой "существенно идентичные" совместно используют последовательности, как указано выше, за исключением того, что оставшиеся положения, которые не являются идентичными, могут отличаться консервативными аминокислотными изменениями. Консервативные замены обычно включают, но не ограничиваясь только ими, замены в пределах следующих групп: глицин и аланин; валин, изолейцин, и лейцин; аспарагиновая кислота и глутаминовая кислота; аспарагин и глутамин; серии и треонин; лизин и аргинин; и фенилаланин и тирозин, и другие, как известно специалисту в данной области техники.
"Биологический субъект", как используется в настоящей заявке, относится к целевому биологическому объекту, полученному, достигнутому, или собранному in vivo, ex-vivo, или in situ, который содержит или подозревается в содержании нуклеиновых кислот или полипептидов, соответствующих биомаркеру из таблицы 1.
"Биологический образец", как используется в настоящей заявке, относится к образцу, полученному от биологического субъекта, включая образец биологической ткани или жидкости, которая имеет происхождение, получена, достигнута, или собрана in vivo, ex-vivo, или in situ, которая содержит или подозревается в содержании нуклеиновых кислот или полипептидов, соответствующих биомаркеру из таблицы 1. Биологический образец также включает образцы из участка биологического субъекта, содержащего предраковые или раковые клетки или ткани. Такими образцами могут быть, но не ограничиваясь только ими, органы, ткани, фракции и клетки, выделенные из млекопитающих, включая людей, таких как пациенты. Биологические образцы могут включать срезы биологических образцов, включая ткани, например, замороженные срезы, взятые для гистологических целей. Биологический образец, как описано в настоящей заявке, может представлять собой: "контроль" или "контрольный образец" или "тестируемый образец". Биологический образец может быть получен из матки, используя общепринятые клинические практики (например, аспирация, щетка, кюретаж, или гистероскопии).
"Контроль" или "контрольное значение" относится к характерному здоровому, без рака эндометрия биологическому субъекту или информации, полученной из отличающегося нормализованного индивидуального или нормализованного значения, которое может быть на основе исходных данных, полученных из популяции или других приемлемых источников. Контроль также может относиться к заданному уровню биомаркера из таблице 1, характерному для популяции без рака эндометрия, которое было установлено ранее на основе измерений от нормальных особей, без рака эндометрия. Контроль также может представлять собой сравнительную точку данных в базе данных на основе данных, полученных из контрольных образцов, типичных для популяции без рака. Кроме того, контроль может быть установлен согласно специфическим возрастным параметрам, полу, этническим параметрам или другим демографическим параметрам. В определенном контексте, контроль предполагают в конкретном измерении. Контрольное значение или контроль также может относиться к "контрольному показателю". Контрольные показатели могут представлять собой значения, полученные при определении уровня экспрессии одного или больше биомаркеров согласно изобретению. Например, коммерчески доступные различные программы и алгоритмы для создания формул, которые обеспечивают получение значения показателя на основе измерения уровней одного или нескольких биомаркеров, которые могут указывать на то, имеет ли, вероятно, индивидуум состояние или нет. В другом примере, значение выше или ниже определенного порога, которое может указывать на повышенную (или сниженную) вероятность наличия заболевания. Значение контрольного показателя может основываться на единичном маркере или комбинации маркеров.
"Контрольный образец" относится к образцу биологического материала, характерному для здоровых, не имеющих рака животных или нормальному биологическому субъекту, полученному из популяции без рака. Уровень биомаркера из таблицы 1, в контрольном образце является желательно типичным для общей популяции нормальных без рака животных аналогичных видов. Этот образец либо может быть собран от животного для использования в способах, раскрытых в настоящем изобретении, или он может представлять собой любой биологический материал, характерный для нормальных животных без рака, пригодный для применения в способах согласно настоящему изобретению. Контрольный образец также может быть получен из нормальной ткани животного, которое имеет рак, или подозревается в наличии рака.
"Тестируемый образец", как используется в настоящей заявке, относится к биологическому образцу, включая образец биологической ткани или жидкости, имеющий происхождение, полученный, достигнутый, или собранный in vivo, ех-vivo, или in situ, который содержит или подозревается в содержании нуклеиновых кислот или полипептидов, соответствующих биомаркеру из таблицы 1. Тестируемый образец также включает биологические образцы, содержащие предраковые или раковые клетки или ткани. Тестируемый образец также может включать срезы биологического образца, включая ткани, например, замороженные срезы, приготовленные для гистологических целей.
"Обеспечение биологического субъекта, биологического образца, или тестируемого образца" обозначает получение биологического субъекта in vivo, ex-vivo, или in situ, включая образец ткани или клетки для применения в способах, раскрытых в настоящем изобретении. Более часто, это осуществляется путем удаления образца клеток из животного, но также может осуществляться in vivo, ex-vivo, или in situ, или путем использования выделенных ранее клеток (например, выделенных из другой особи, в другое время, и/или для другой цели). Образец также может быть получен из таких источников, как кровь, сыворотка, и маточная жидкость.
"Данные" включают, но не ограничиваясь только ими, полученную информацию, которая относится к "биологическому образцу", "тестируемому образцу", "контрольному образцу", и/или "контролю", как описано выше, где информация применяется для создания тестового уровня для диагностического, профилактического, наблюдательного или терапевтического применения. Настоящее изобретение относится к методам для сравнения и компилирования данных, где данные хранятся в электронном или бумажном формате. Электронный формат может быть выбран из группы, включающей электронную почту, диск, компакт-диск (CD), компакт-диск формата DVD (DVD), карту памяти, схему памяти, ROM или RAM, магнитный оптический диск; ленту, видео, видеоклип, микрофильм, Интернет, сеть совместного использования, сервер совместного использования и другие; где данные представляются, передаются или анализируются с помощью электронной пересылки, представления видео, телекоммуникации, или путем применения любого из вышеописанных форматов хранения; где данные сравниваются и компилируются в сайте отбора образцов или в расположении, где данные транспортируются с помощью процесса, как описано выше.
"Сверхэкспрессия" гена или "повышенный," или "увеличенный," уровень рибонуклеотида или белка относится к уровню гена, рибонуклеотида или полипептида, который, по сравнению с контрольных уровнем /значением гена, рибонуклеотидов или полипептида, является обнаружимо выше. Сравнение можно осуществлять с помощью статистических анализов при различных измерениях экспрессии; или, может осуществляться путем визуального исследования результатов экспериментов с помощью квалифицированных исследователей. Примеры сверхэкспрессии включают изменение на 10% или больше, 20% или больше 30% или больше, 40% или больше, или 50% или больше у пораженных по сравнению с непораженными.
"Подавленная экспрессия" гена или "сниженный," или "более низкий," уровень рибонуклеотида или белка относится к уровню гена, рибонуклеотида или полипептида, который по сравнению с контрольным уровнем гена, рибонуклеотидов или полипептида, является обнаружимо ниже. Сравнение можно осуществлять с помощью статистических анализов при различных измерениях экспрессии; или, может осуществляться путем визуального исследования результатов экспериментов с помощью квалифицированных исследователей. Примеры подавленной экспрессии включают изменение на 10% или больше, 20% или больше 30% или больше, 40% или больше, или 50% или больше у пораженных по сравнению с непораженными.
Уровень рибонуклеотида или полипептида, который "экспрессируется" в контрольном образце, относится к уровню, который представляет типичный, образец без рака, и из повышенного, или диагностического, наличия полипептида или полинуклеотида, может быть различен. Предпочтительно, "предполагаемый" уровень будет контролироваться такими факторами, как возраст, пол, медицинский анамнез и т.д. млекопитающего, а также для конкретного биологического субъекта, подвергаемого тестированию.
Термины "выделенный," "очищенный," или "биологический чистый" относится к материалу, который не содержит в различных количествах компоненты, которые в обычном состоянии его сопровождают, как он находится в нативном состоянии. "Выделенный" обозначает степень разделения от исходного источника или окружающей среды. "Очищенный" обозначает степень разделения, которая превышается таковую для выделения. "Очищенный" или "биологически чистый" белок достаточно свободен от других материалов, таких как любые примеси, которые по существу оказывают влияния на биологические свойства белка или вызывают другие нежелательные последствия. Таким образом, нуклеиновая кислота или пептид согласно настоящему изобретению очищен, если он по существу не содержит клеточного материала, вирусного материала, или культуральной среды, когда он получен с помощью технологий рекомбинантных ДНК, или химических предшественников или других химических веществ, когда он синтезирован химически. Чистоту и гомогенность обычно определяют с помощью методик аналитической химии, например, электрофореза в полиакриламидном геле или высокоэффективная жидкостная хроматография. Термин "очищенный" может обозначать, что такая нуклеиновая кислота или белок будет образовывать по существу одну полосу в электрофоретическом геле. Для белка, который может быть подвержен модификациям, например, фосфорилированию или гликозилирования, различные модификации могут приводить к различным выделенным белкам, которые могут быть отдельно очищены. Различные уровни чистоты могут применяться, при необходимости, в соответствии с настоящим изобретением, в различных методологиях, указанных в настоящей заявке выше; можно использовать общепринятые стандарты очистки, известные в данной области, если другой стандарт не указан иначе.
"Выделенная молекула нуклеиновой кислоты" может относиться к молекуле нуклеиновой кислоты, в зависимости от обстоятельств, которая отделена от 5' и 3' кодирующих последовательностей генов или фрагментов генов, смежных во встречающемся в природе геноме организма. Термин "выделенная молекула нуклеиновой кислоты" также включает молекулы нуклеиновой кислоты, которые не встречаются в природе, например, молекулы нуклеиновой кислоты, созданные с помощью технологий рекомбинантных ДНК.
"Нуклеиновая кислота" относится к дезоксирибонуклеотидам или рибонуклеотидам и их полимерам либо в одноцепочечной или двухцепочечной форме. Термин охватывает нуклеиновые кислоты, содержащие известные нуклеотидные аналоги или модифицированные скелетные остатки или связи, которые являются синтетическими, встречающимися в природе, и невстречающимися в природе, которые имеют сходные свойства связывания, как и сравнительная нуклеиновая кислота, и которые метаболизируются сходным образом со сравнительными нуклеотидами. Примеры таких аналогов включают, без ограничений, фосфоротиоаты, фосфороамидаты, метилфосфонаты, хиральные метилфосфонаты, 2-O-метил рибонуклеотиды, и пептид-нуклеиновые кислоты (PNA).
Если специально не указано иначе, конкретная последовательность нуклеиновой кислоты также неявно охватывает их консервативные, модифицированные варианты (например, замены с вырожденными кодонами) и комплементарные последовательности, а также последовательности, однозначно указанные. Специфически, замены с вырожденным кодоном можно получать путем создания последовательностей, в которых третье положение одного или больше выбранных (или всех) заменено подходящим смешанным основанием и/или дезоксиинозиновым основанием (Batzer и др. (1991) Nucleic Acid Res, 19:081; Ohtsuka и др. (1985) J.Biol.Chem., 260: 2600-2608; Rossolini и др. (1994) Mol.Cell Probes, 8:91-98). Термин нуклеиновая кислота может использоваться взаимозаменяемо с геном, кДНК, мРНК, олигонуклеотидом, и полинуклеотидом.
"Метка" или "обнаруживаемая часть" представляет собой композицию, которая, когда связана с молекулой нуклеиновой кислоты или белка, представляет собой интерес, придает последней обнаруживаемость, с помощью спектроскопического, фотохимического, биохимического, иммунохимического, или химического методов. Например, пригодные метки включают радиоактивные изотопы, магнитные шарики, металлические шарики, коллоидные частицы, флуоресцентные красители, электронно-плотные реагенты, ферменты (например, как обычно используется в ELISA), биотин, дигоксигенин, или гаптены. "Меченная нуклеиновая кислота или олигонуклеотидный зонд" представляет собой структуру, которая, связана, либо ковалентно, с помощью линкера или химической связи, или нековалентно, с помощью ионных связей, ван-дер-ваальсовых сил, электростатического притяжения, гидрофобных взаимодействий, или водородных связей, с меткой, таким образом, что присутствие нуклеиновой кислоты или зонда можно определить путем обнаружения присутствия метки, связанной с нуклеиновой кислотой или зондом.
Как используется в настоящей заявке, "нуклеиновокислотный или олигонуклеотидный зонд" определяется как нуклеиновая кислота, способная связываться с целевой нуклеиновой кислотой комплементарной последовательности посредством одного или нескольких типов химических связей, обычно путем комплементарного спаривания оснований, обычно путем образования водородных связей. Как используется в настоящей заявке, зонд может включать природные (то есть, A, G, С, или Т) или модифицированные основания (7-дезазагуанозин, инозин, и др.). Дополнительно, основания в зонде могут быть соединены с помощью связи, отличающейся от фосфодиэфирной связи, при условии, что они не будут чрезмерно препятствовать гибридизации. Для специалиста в данной области техники будет понятным, что для зондов, которые могут связывать целевые последовательности, отсутствует полная комплементарность с последовательностью зонда, в зависимости от жесткости умов гибридизации. Зонды предпочтительно непосредственно метят с помощью изотопов, например, хромофоров, люминофоров, хромогенов, или опосредованно метят с помощью биотина, с которым позже может связываться стрептавидиновый комплекс. Путем анализа наличия или отсутствия зонда, можно определить наличие или отсутствие целевого гена, представляющего интерес.
Фраза "селективно (или специфически) гибридизируется с" относится к связыванию, дуплексированию, или гибридизации молекулы только в конкретной нуклеотидной последовательностью при жестких условиях гибридизации, когда такая последовательность представляет собой комплексную смесь (например, общую клеточную или библиотечную ДНК или РНК).
Фраза "жесткие условия гибридизации" относятся к условиям, при которых зонд будет гибридизоваться с его целевой комплементарной последовательностью, обычно в комплексной смеси нуклеиновых кислот, но не с другими последовательностями. Жесткие условия зависят от последовательностей и от обстоятельство; например, более длинные последовательности могут гибридизируется со специфичностью при более высоких температурах. Подробное описание гибридизации нуклеиновых кислот представлено в in Tijssen (1993) Techniques in Biochemistry and Molecular Biology-Hybridization with Nucleic Probes, "Overview of principles of hybridization and the strategy of nucleic acid assays". В контексте настоящего изобретения, как используется в настоящей заявке, термин "гибридизируется в жестких условиях" предназначен для описания условий для гибридизации и промывания, при которых нуклеотидные последовательности с по меньшей мере 60% гомологией друг к другу обычно остаются гибридизированными друг с другом. Предпочтительно, условия являются такими, что последовательности с по меньшей мере приблизительно 65%, более предпочтительно по меньшей мере приблизительно 70%, и наиболее предпочтительно по меньшей мере приблизительно 75% или больше гомологией друг к другу обычно остаются гибридизированными друг с другом.
В целом, жесткие условия выбирают приблизительно на 5-10°С ниже, чем температурная точка плавления (Tm) для специфической последовательности при определенной ионной силе рН. Tm представляет собой температуру (при определенной ионной силе, рН, и нуклеиновой концентрации), при которой 50% зондов, комплементарных с мишенью, гибридизируются с целевой последовательностью при равновесии (поскольку целевые последовательности присутствуют в избытке, при Tm, 50% зондов заняты при равновесии). Жесткие условия будут представлять собой такие условия, при которых концентрация соли составляет меньше, чем приблизительно 1,0 М ионов натрия, обычно приблизительно 0,01-1,0 М концентрации ионов натрия (или других солей) при рН 7,0-8,3 и температура равна по меньшей мере приблизительно 30°С для коротких зондов (например, 10-50 нуклеотидов) и по меньшей мере приблизительно 60°С для длинных зондов (например, больше, чем 50 нуклеотидов). Жесткие условия также могут достигаться путем добавления дестабилизирующих средств, например, формамида. Для селективной или специфической гибридизации, положительный сигнал по меньшей мере в два раза превышает фоновый, предпочтительно в 10 раз превышает фоновую гибридизацию.
Примерами жестких условий гибридизации могут быть следующие условия, например: 50% формамид, 5×SSC и 1% SDS, инкубирование при 42°С, или 5×SSC и 1% SDS, инкубирование при 65°С, с промыванием в 0,2×SSC и 0,1% SDS при 65°С. Альтернативные условия включают, например, условия по меньшей мере такой жесткости, как и гибридизация при 68°С в течение 20 часов, с последующим промыванием в 2×SSC, 0,1% SDS, два раза в течение 30 минут при 55°С и три раза в течение 15 минут при 60°С.Другим альтернативным набором условий является гибридизация в 6×SSC приблизительно при 45°С, с последующими одним или больше промываниями в 0,2×SSC, 0,1% SDS при 50-65°С. Для ПЦР, температура около 36°С является типичной для амплификации при низкой жесткости, хотя температуры отжига могут изменяться в диапазоне до приблизительно 32°С до 48°С в зависимости от длины праймера. Для ПЦР амплификации с высокой жесткостью, типичной является температура приблизительно 62°С, хотя температуры отжига с высокой жесткостью могут находиться в интервале от приблизительно 50°С до приблизительно 65°С, в зависимости от длины и специфичности праймера. Типичные условия циклизации для амплификации как с высокой, так и с низкой жесткостью, включают фазу денатурации от 90°С до 95°С в течение 30 сек. до 2 минут, фазу отжига, продолжающуюся 30 секунд до 2 минут, и фазу удлинения при приблизительно 72°С в течение 1-2 минут.
Нуклеиновые кислоты, которые не гибридизируются друг с другом в жестких условиях, все еще могут быть по существу идентичными, если полипептиды, которые они кодируют, являются по существу идентичными. Это происходит, например, когда копия нуклеиновой кислоты создается с использованием максимальной вырожденности кодонов, разрешенных генетическим кодом. В таких случаях, нуклеиновые кислоты обычно гибридизируются в умеренно жестких условиях гибридизации. Примеры "умеренно жестких условий гибридизации" включают гибридизацию в буфере 40% формамид, 1 М NaCl, 1% SDS при 37 С, и промывку в 1×SSC при 45 С. Положительная гибридизация по меньшей мере в раза превышает фоновую. Для специалистов в данной области техники будет очевидным, что могут использоваться альтернативные условия гибридизации и промывки для обеспечения условий аналогичной жесткости.
Термин "целевой ген" или "целевой биомаркер" или "целевая нуклеиновая кислота" или "целевой белок" может относиться к целевой нуклеиновой кислоте (ДНК и РНК) или белку (или полипептиду), (например, соответствующим биомаркерам в таблице 1) и могут включать их полиморфные варианты, аллели, мутанты, и межвидовые гомологи, которые имеют (i) существенную гомологию нуклеотидной последовательности (например, по меньшей мере 60% идентичность, предпочтительно по меньшей мере 70% идентичность последовательностей, более предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95%) с нуклеотидной последовательностью, указанной в базе данных Ensembi для указанного номера ID; или (ii) по меньшей мере 65% гомологию последовательности с аминокислотной последовательностью, как указано в записи Ensembi; или (hi) существенную гомологию нуклеотидной последовательности (например, по меньшей мере 60% идентичность, предпочтительно по меньшей мере 70% идентичность последовательностей, более предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95%) с нуклеотидной последовательностью, как указано в Ensembi записи, с существенной гомологией последовательности с кодируемой аминокислотной последовательностью. Как используется в настоящей заявке, и если специально не указано иначе, эти термины относятся к последовательности целого гена, последовательности мРНК, и/или белковой последовательности, а также к фрагментам этих последовательностей. В более специфическом определении, эти термины относятся к минимальному количеству последовательности нуклеиновых кислот или аминокислот, которые могут использоваться для идентификации биомаркера специфическим образом. Для специалиста в данной области техники понятно, что целевые гены/биомаркер могут иметь различные сплайсинговые формы и варианты. При ссылке на специфический целевой ген или локус с помощью регистрационного номера (например, Entrez gene ID или Ensembi), все сплайсинговые формы и варианты включены в различные варианты осуществления согласно изобретению. Целевой ген/биомаркер также может включать регуляторный элемент. Эти последовательности являются характерными для каждого отдельного индивидуума в популяции людей. Люди отличаются друг от друга последовательностями их генов. Эти вариации чрезвычайно минимальны, иногда происходят с частотой около 1-10 нуклеотидов на ген. Различные формы любого конкретного гена существуют в пределах человеческой популяции. Эти различные формы называются аллельными вариантами. Аллельные варианты очень часто не изменяют аминокислотную последовательность кодируемого белка; такие варианты называются синонимическими. Если даже они изменяют кодируемую аминокислоту (несинонимические), то функция белка типично не изменяется. Такие изменения являются эволюционно или функционально нейтральными. Если ссылка на ID гена (например, genbank или Ensembi) представлена в настоящей заявке, то подразумевается, что все аллельные варианты охватываются этим термином. Последовательности ID гена, представленные для биомаркера, обеспечиваются только в качестве репрезентативных примеров последовательности человека дикого типа. Изобретение не ограничивается единичной аллельной формой амплифицированных генов или участков (и белками, которые они кодируют).
Примеры
Последующие примеры включены для демонстрации предпочтительных вариантов осуществлений изобретения. Для специалистов в данной области техники будет понятным, что техники, раскрытые в примерах, которые сопровождают репрезентативные техники, используемые изобретателем, функционируют хорошо при практическом осуществлении изобретения, и, таким образом, могут рассматриваться как предпочтительные варианты его практического осуществления. Тем не менее, квалифицированные специалисты в данной области техники, с учетом представленного раскрытия, должны принять во внимание, что могут быть осуществлены различные изменения в специфических вариантах осуществления, которые раскрыты, и все еще получают сходный или аналогичный результат без отклонения от сущности и объема изобретения.
Пример 1: Идентификация биомаркеров рака эндометрия Для идентификации биомаркеров для предсказания и/или диагностики рака эндометрия, уровень экспрессии генов из пятидесяти шести первичных опухолей эндометрия на различных стадиях дифференциации сравнивали с 10 нормальными (то есть, не имеющими рака эндометрия) эндометриальными тканями с помощью техники ДНК микропанели. Эта техника предоставляет нам возможность проверить экспрессию целого генома в конкретном типе клеток, ткани, органа, или в этом случае, проверить дифференциальную экспрессию генов между раком эндометрия и здоровой тканью эндометрия. Микропанельный чип содержит небольшие последовательности ДНК, упорядоченные в регулярную структуру со специфическими адресами для зондов для типично тысячи генов.
Количество специфической мРНК в образце может быть оценено с помощью ее сигнала гибридизации на панели.
Описание образцов
Образцы опухолей получали от пациентов, подвергнутых хирургическому вмешательству, и контрольная ткань было получена из непораженных участков ткани эндометрия от тех же пациентов. При приготовлении образцов, особое внимание уделяли макроскопическому отрезанию рака от любого смежного миометрия.
Использовали десять контрольных образцов (девять из них были спарены с их соответствующими образцами опухолей и десятый представлял собой атрофический эндометрий) и основные характеристики других тестируемых образцов обобщены в таблице 3 ниже.
Общую РНК экстрагировали с помощью мини-набора RNeasy (Qiagen, Hilden, Germany), согласно инструкциям, предоставленным производителем. Количество и качество полученной РНК измеряли с помощью Nanodrop (Nandrop ND-1000, Agilent 2100 Bioanalyzer) и РНК низкого качества выбраковывали из процесса панельной гибридизации.
План микропанели
Микропанели для экспрессии генов были созданы с помощью алгоритма Tethysc использованием ENSEMBL базы данных. Для последовательностей, где мы не могли обнаружить зондов высокого качества, мы дополняли план с помощью зондов Oryzon Optimized Agilent. Синтез ДНК микропанелей осуществлялся Agilent.
Панель для экспрессии генов целого генома содержала:
• 20148 Oryzon High Quality зонды от ENSEMBL базы данных.
• 5698 Oryzon Tm оптимизированные Agilent зонды.
Общее количество зондов составило 25846.
Мечение аРНК
Су3 и Су5 меченную аРНК получали с помощью набора MessageAmplification от Ambion (ссылка: 1819 для 96х набора или ссылка: 1751 для 20х набора). Эти наборы использовали с некоторыми модификациями, которые были введены Oryzon геномикой. Мечение РНК осуществляли, по существу используя Eberwine протокол (Van Gelder, 1992), промышленно внедренный Ambion с MessageAmplification набором (Ambion/Applied Biosystems) с небольшими модификациями. 500 нг общей РНК обратно транскрибировали в присутствии олиго(dT)24, осуществляли двухцепочечный синтез и приготавливали транскрипт этой дцДНК, используя СТР_Су3 или СТР_Су5 (PerkinElmer). Амплифицированную кРНК количественно определяли с помощью Nanodrop ND-1000 и кРНК качество контролировали с помощью Agilent RNA Bionalyzer 2100.
Микропанельная гибридизация
Микропанельную гибридизацию осуществляли при 60°С и времени гибридизации 17 часов в соответствии с указаниями Agilent, используя Agilent прокладки (G2534-60002), Agilent камеры для гибридизации (G2534A) и в Agilent ДНК гибридизационной печи (G2545A). Контроли гибридизации Oryzon также использовали в процессе гибридизации. Контроли для процесса гибридизации, соответствующие 3 кДНК клонов кукурузы (Xet, Zm42,Exp), включали во все анализы. Ехр использовали в качестве отрицательного пикового контроля и его ни амплифицировали, ни метили. Для Xet и Zm42 получали ПЦР фрагменты путем ПЦР амплификации из вектора с универсальными праймерами и создавали кРНК, используя системы транскрипции in vitro (T7 или Т3 Megascript набор; Ambion) с СТР_Су3 или СТР_Су5 (PerkinElmer). Оба положительных пиковых контроля Xet и Zm42 были с обоими Су5 и Су3 флуофорами.
Получение данных
Начальные необработанные данные получали, используя Agilent DNA Microarray Scanner (G2505B) и Agilent программное обеспечение сбора данных(Feature Extraction Software). В осуществленном протоколе экстракции не использовали вычитание фона, расчет систематической ошибки оценки красителей и коэффициент поправки.
Анализ данных
В план исследования с помощью микропанелей включали большое количество контролей для наблюдения сканирования и характеристики группы и для контроля пространственной однородности и исправленных отклонений. Таким образом, суммарная погрешность при измерении микромассива данных может быть оценена путем развернутого анализа данных от контролей.
Среднее значение кратности изменения или М значения могут быть классифицированы на основе их вероятности, отличающейся от 0, в соответствии с абсолютным значением упорядоченной t-статистики (Baldi и Long, 2001), где используют байесовский метод для получения модифицированной и улучшенной статистики t-стьюдента. Для осуществления отбора на основе кратности изменения, использовали среднее значение М распределения. Это распределение корректировали до нормального распределения и итерационный процесс использовали для определения средних М чисел, которые находятся за пределами распределения. Разделение выбирали в виде n времен стандартных отклонений (σ) от среднего значения. В этом способе получают функциональное среднее значение и стандартное отклонение и предоставляется возможность корректировки значений разделения до распределения шумов данных. Типично, отбирали значения со средним FC>3σ или средним FC<-3σ распределения данных образцов.
Непрямой сравнительный анализ, где уровни экспрессии конкретных биомаркеров в образцах опухолей сравнивали со сравнительным пулом РНК, полученным из группы свыше 20 клеточных линий (меланома, рак легких, рак яичника, рак ободочной кишки, и несколько нераковых клеточных линий). Уровни экспрессии конкретных генов в нормальных образцах (контроли) сравнивали с аналогичным сравнительным пулом и кратность изменений конечной экспрессии между опухолью и нормальной тканью эндометрия получали in silico, элиминируя сравнительный пул.
Кандидатные гены отбирали в качестве биомаркеров для рака эндометрия на основе кратности сверхэкспрессии, р-значения, и других факторов. В таблице 1 в подробном описании изобретения представлены 17 сверхэкспрессируемых генов и 3 генов с подавленной экспрессией, идентифицированных с использованием этой процедуры. Сверхэкспрессия этих генов подтверждается с помощью ОТ-ПЦР, как описано в следующих примерах.
Результаты микропанельных исследований обобщены в таблице 1 в подробном описании изобретения, где представлены общепринятое сокращение, используемое для гена, номера доступов ENSMBL гена, транскрипта и белка, а также кратность сверхэкспрессии и рассчитанные р-значения.
Пример 2: Приготовления образца маточной жидкости
Аспираты эндометрия собирали с помощью шероховатого пайпиля, после того, как полное информированное согласие было получено от всех пациентов. Аспират (маточной жидкости) сразу переносили в пробирки Эппендорфа, содержащие 500 микролитров раствора для сохранения РНК (RNA later, Ambion). Образцы центрифугировали и осадок после центрифугирования, содержащий характерную популяцию клеток из полости матки, в дальнейшем обрабатывали для экстрагирования РНК (Qiagen). Проверку качества (Bioanalyzer) осуществляли перед анализом экспрессии генов с помощью Taqman технологии для выбранных маркеров карциномы эндометрия.
Пример 3: Корреляция биомаркеров в первичной опухоли и в маточной жидкости
Уровни биомаркеров из образца первичной опухоли и образца маточной жидкости, полученного с помощью процедуры, описанной в примере 2, сравнивали с помощью ОТ-ПЦР с последующим общим протоколом ОТ-ПЦР, как описано в примере 4. Биомаркеры в этом исследовании включали АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN, для которых неожиданно было обнаружено, что их экспрессия коррелирует между первичной опухолью и аспиратами эндометрия (маточной жидкости). См. фигуру 1. Как можно увидеть на фигуре 1, уровня экспрессии различных биомаркеров рака эндометрия коррелируют в маточной жидкости и первичной опухоли. В особенности, было обнаружено, что существует высокий уровень корреляции экспрессии биомаркеров, которые соответствуют АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN в образце опухоли и в образцах, полученных из маточной жидкости. Следовательно, изобретатели неожиданно обнаружили группу генов, которые могут использоваться для диагностики или предсказания повышенной вероятности рака эндометрия на основе их уровней экспрессии в образцах, полученных из маточной жидкости. Кроме того, изобретателями было показано, что маточная жидкость может использоваться для оценки биомаркеров для рака эндометрия. Например, прогностические биомаркеры для рака эндометрия, биомаркеры для определения стадии рака эндометрия, биомаркеры для определения типа рака эндометрия (например, тип 1 относительно типа II) или тип (эндометриоидный, прозрачных клеток, серозный, и т.д.), вспомогательные диагностические биомаркеры, дифференциальные диагностические биомаркеры, могут быть оценены в маточной жидкости для характеристики рака.
Пример 4: Подтверждение сверхэкспрессии биомаркеров с помощью количественной ОТ-ПЦР
После получения массива данных, группу с повышенной и пониженной активностью генов в образцах опухолей по сравнению с нормальной тканью отбирали частично на основе их р-значений и стандартных отклонений. Эти кандидаты отбирали для определения их уровней экспрессии с помощью независимой методики, используя другой набор образцов опухолей.
Микрожидкостные карты (MFC) от Applied Biosystems использовали для осуществления ОТ-ПЦР с РНК, выделенной из опухолей и образцов нормальной ткани эндометрия. В этом случае, оба типа тканей, здоровые и канцерогенные, получали от одного и того же пациента с помощью микрохирургической процедуры. Эти исследования подтверждали микропанельные результаты для большинства маркеров из таблицы 1. Другой набор ОТ-ПЦР исследований осуществляли, используя аспираты, полученные от пациентов с раком эндометрия (подтвержденные) и аспираты от непораженных особей. Эти исследования с использованием образцов аспиратов описаны более подробно ниже.
Образцы аспиратов получали с помощью процедуры, аналогичной описанной в примере 2. Описание характеристик пациентов для пораженных и непораженных образцов представлено в таблице 4 и в таблице 5 ниже.
Вкратце, лунки микрожидкостной карты содержали Applied Biosystems пробы флуорогенной 5' нуклеазы, которые определяют амплификацию в реальном времени матрицы выбранных мишеней. Относительные уровни экспрессии генов определяли на основе флуоресцентных данных, созданных при осуществлении ПЦР, используя программное обеспечение ABI PRISM® 7900HT Sequence Detection System (7900HT SDS) Relative Quantification.
Анализ данных осуществляли с помощью сравнительного ΔΔCt метода относительного количественного определения. Дифференциально экспрессируемые гены подтверждали путем всестороннего статистического анализа, используя модифицированный Т-тест.
Образцы, используемые в исследовании, описанном в этом примере, включали: образцы от 30 пациентов, имеющие рак эндометрия: 25 эндометриоидных карцином в 9 в G3, 9 в G2 и 7 в G1, и 5 образцов опухолей из другого типа II карцином (4 в G3 и 1 в G2).
Образцы от 24 пациентов, не имеющих рака эндометрия ("контроли" или "нормальные"). Они представляли собой гетерогенную смесь образов, некоторые из них от пациентов с другими неопухолевыми патологиями, такими как полипы: 4 образцов от пациентов с атрофическим эндометриоидом, 4 нормальных образцов, два от пациентов, имеющих полипы от постменопаузных женщин, и 11 образцов от пре-менопаузных женщин (7 из них в секреторной фазе и 4 в пролиферативной фазе цикла). См. таблицу ниже для обобщенных данных относительно образцов.
Экспериментальные процедуры
Образцы РНК выделяли из образцов аспиратов согласно процедуре, как описано выше, и осуществляли контроль качества перед конечным отбором образцов. Образцы аспиратов собирали, как описано в примере 2.
ОТ-ПЦР осуществляли согласно стандартному протоколу Applied Biosystem для 7900НТ системы. Протокол состоял из двухстадийного метода, где первой стадией являлось создание кДНК из образцов РНК, используя набор High Capacity cDNA, и второй стадией являлась амплификация кДНК, после загрузки на MFC, с помощью ABI PRISM® 7900 НТ системы.
Данные ОТ-ПЦР собрали для набора из 20 генов, идентифицированных в примере 1, и количественно определяли относительно уровней POLR2A. RQ значения для аспиратов, соответствующие 30 образцам опухолей и 24 образцам, которые не являлись раком эндометрия (нормальные), проиллюстрированы в ящике и диаграмме с усами, см. фигуру 2А и 2В. В таблице 2 в подробном описании изобретения представлены обобщенные данные относительно средних RQ значений, среднеквадратического отклонения и р-значений, рассчитанных для этих маркеров в этом наборе образцов. Как можно увидеть из представленных данных, р-значения, полученные с использованием набора контрольных образцов в микропанельных исследованиях (таблица 1), были существенно улучшены в другом наборе образцов, используя другие техники (микропанель относительно ОТ-ПЦР) и другие источники образцов (аспираты относительно первичной опухоли). В большинстве случаев, р-значение улучшено больше чем в 100 раз для биомаркеров. Это связано частично с обоснованной природой схемы микропанельного эксперимента и полноценным отбором маркеров на основе критериев изобретателей.
В последующей таблице представлены чувствительность и специфичность для каждого индивидуального гена в патентной заявке и площадь под ROC (AUROC) кривой для каждого гена, при сравнении RQ значений из 30 опухолевых образцов и 24 контрольных образцов. Для расчета данных использовали программу на основе метода опорных векторов (SVM). Как можно увидеть из таблицы, представленной ниже, маркеры, идентифицированные в этих исследованиях, имеют очень хорошую чувствительность и/или специфичность для предсказания повышенной вероятности и/или диагностики рака эндометрия. Кроме того, AUROC значения для этих биомаркеров указывают на то, что эти маркеры чрезвычайно пригодны для диагностики рака эндометрия.
Контрольные образцы представляли собой гетерогенную группу из пре- и пост-менопаузных женщин. В то же время, аспираты от пре-менопаузных женщин могут быть разделены на две категории в зависимости от фазы цикла эндометрия матки, когда отбирались образцы: пролиферативная или секреторная. Характеристика секреторной относительно пролиферативной фазы для пациентов осуществляется патологоанатомом с использованием стандартных техник.
Некоторые из тестируемых генов могут давать ложноположительный результат для рака эндометрия, если аспират отбирали от пре-менопаузных женщин в секреторной фазе. Для проверки того, какие из генов могут давать ложноположительные результаты в зависимости от фазы цикла или которые по-другому могут различаться между опухолевыми образцами и секреторной фазы, мы осуществляли статистический анализ, сравнивая опухоли с различными контрольными группами.
• опухоли относительно контрольных образцов (все контрольные образцы: 24 образцов)
• опухоли относительно контрольных образцов минус образцы в секреторной фазе: 17 образцов
• опухолевые образцы относительно контрольных образцов в секреторной фазе: 7 образцов
• опухолевые образцы относительно контрольных образцов от пост-менопаузных женщин: 11 образцов
Рассчитывали площадь ROC для каждого сравнения с помощью программы GraphPad Prism и применяли дисперсионный анализ для выяснения того, являются ли отличия между этими группами достоверными.
В таблицах, представленных ниже, используются следующие сокращения для р-значений:
*** р<0,0001
** р<0,001
* р<0,01
нд (не достоверно).
Как видно из результатов, представленных в таблицах, существуют гены, такие как Р4НВ или SOCS2, которые разделяют опухолевые образцы от контрольных независимо от природы контрольных образцов (пост-менопаузные, пре-менопаузные в секреторной или пролиферативной фазе). Другие гены, такие как P2RX4 или PPFIBP2, могут различать между опухолевым образцом (пораженным) и образцом в секреторной фазе лучше по сравнению с контролями от пост-менопаузных женщин.
Эти наблюдения открывают возможности использования различных алгоритмов и/или различных наборов генов, в зависимости от того, в тесте детально исследуются пре-менопаузные или пост-менопаузные женщины. Кроме того, первичной тактикой исследования для скрининга проблем эндометрия является трансвагинальное ультразвуковое исследование, которое используют для оценки толщины эндометрия, где пациенты, имеющие более толстый эндометрий (по сравнению с определенным пороговым значением), вероятно, имеют рак эндометрия или другое заболевание или состояние. Толщина эндометрия также изменяется в зависимости от фазы менструального цикла, где индивидуумы в секреторной фазе имеют более толстый эндометрий по сравнению с индивидуумами в пролиферативной фазе. Следовательно, эти данные исследования указывают на то, что способы и биомаркеры согласно изобретению можно использовать для помощи и улучшения способности трансвагинального ультразвукового исследования идентифицировать рак эндометрия.
Таблица 7: Обобщенные данные для ОТ-ПЦР исследований сравнения уровней экспрессии биомаркеров в аспиратах (30) от пациентов, пораженных раком эндометрия, и аспиратов, полученных индивидуально от всех пациентов, не пораженных раком эндометрия (24).
В таблице 7 показано, что 20 биомаркеров способны отличать аспираты от пациентов, пораженных раком эндометрия, от аспиратов всех контрольных непораженных пациентов с высокими ROC значениями и/или очень хорошей статистической достоверностью.
В таблице 8 представлена классификация 20 биомаркеров согласно изобретению, способных отличать аспираты от пациентов, пораженных раком эндометрия, от аспиратов всех контрольных непораженных пациентов, исключая пациентов в секреторной фазе. В таблице 7 представлены биомаркеры согласно изобретению, которые имеют высокие ROC значения и/или очень хорошую статистическую достоверность для разделения этих популяций.
Как можно видеть, в таблице 9 предпочтительные маркеры, способные отличать аспираты от пациентов, пораженных раком эндометрия, от аспиратов пациентов, не пораженных раком эндометрия, в секреторной фазе, включают Р4НВ, SOCS2 P2RX4, IKBKE, PPFIB2, DDR1 и DCN которые имеют высокие ROC значения и/или очень хорошую статистическую достоверность.
Как можно увидеть из данных, представленных в таблицах 7 и 9 выше, примеры генов, способных дифференцировать между аспиратами от пациентов, имеющих опухоль, и аспиратами от всех непораженных пациентов (включая секреторную фазу) и/или между аспиратами от пациентов, имеющими опухоль, и аспиратами от непораженных пациентов в секреторной фазе, включают Р4НВ, SOCS2, и IKBKE, которые имеют высокую статистическую достоверность и ROC значения.
Как можно увидеть, в таблице 10 предпочтительные маркеры, способные отличать аспираты от пациентов, пораженных раком эндометрия, от пост-менопаузных пациентов, непораженных раком эндометрия, включают PHKG2, Р4НВ, EFEMP2, RNF183, и SOCS2, которые имеют высокие ROC значения и/или очень хорошую статистическую достоверность.
Со ссылкой на фигуры 2А и 2В (ящик и диаграмма с усами), RQ: относительная величина, представляет собой относительное количество РНК для специфического гена, присутствующего в образцах опухолей по сравнению с количеством, присутствующим в контрольном образце для одного и того же гена.
Для расчета RQ, Ct значения каждого гена нормализовали по отношению к Ct эндогенного гена с получением дельта Ct. Использовали формулу 2-(дельта aCt) для расчета RQ.
Различные эндогенные гены можно использовать в качестве контроля для нормализации, а также другие контроли для нормализации. В одном примере, предпочтительный эндогенный ген имеет следующие характеристики: он представляет собой ген, который конститутивно экспрессируется в той же ткани в различных условиях, таких как, например, развитие рака. Следовательно, его можно использовать для нормализации отличий в количествах кДНК, при загрузке образцов или вариаций вследствие экспериментальных обоснований для кОТ-ПЦР.
Нами было протестировано четыре различных конститутивных гена в качестве возможных эндогенных генов для нормализации: 18S, В2М, PFN-1 и POLR2A. В конечном итоге, POLR2A является наиболее стабильным геном из всех этих генов и все расчеты и статистики осуществляли, используя его в качестве эндогенного. Его уровень экспрессии является подобным генам, используемым в нашем тесте, и отличает по сравнению с 18 S, экспрессия которого является немного выше по сравнению с генами, используемыми для теста. Предполагается, что эндогенные биомаркеры, такие как POLR2A, В2М, PFN1, HMBS, G6PD, или PABPN1 или другой стабильный ген можно использовать для нормализации в способах согласно изобретению, при необходимости.
Пример 5: Профили для диагностики рака эндометрия
Алгоритм на основе метода опорных векторов использовали для идентификации комбинаций маркеров из таблицы 1, которые пригодны для предсказания рака эндометрия и/или повышенной вероятности наличия рака эндометрия. В частности, для анализа данных использовали свободно доступную программу DTREG (см. www на DTREG.COM).
Алгоритм на основе метода опорных векторов можно использовать для различных применений, включая идентификацию профилей экспрессии генов для разделения популяций, имеющих различные фенотипические характеристики. В основу алгоритма положена идея многомерного представления данных, например, каждый маркер представляют на диаграмме в различном измерении и определяют плоскость, которая проходит через такое многомерное представление данных, которая может разделять фенотипы. Проекция через "середину" относится к разделительной гиперплоскости и представляет решение: ответы (например, уровень экспрессии выше данного порогового значения), которые приходятся на одну сторону линии, включаются в одну категорию (например, рак) и ответы (например, уровень экспрессии выше данного порогового значения), которые находятся на другой стороне линии, соответствуют другой категории (например, без рака). Несколько разделяющих гиперплоскостей возможно для каждого набора данных. Предстоит определить, какая из них является наилучшей разделяющей гиперплоскостью. В теории метода опорных векторов, наилучшее решение относится к максимально предельной гиперплоскости. Эта максимально предельная гиперплоскость представляет собой гиперплоскость, которая разделяет две группы и занимает максимальное расстояние от любой другой для данных профилей экспрессии.
Несмотря на то, что индивидуальные гены проявляют высокую чувствительность и специфичность, эти параметры еще повышаются при комбинировании определенных генов. Некоторые примеры чувствительности, специфичности и AUROC генов, комбинированных два на два, три на три, четыре на четыре, пять на пять, шесть на шесть, семь на семь и всех их вместе. См. таблицу ниже для обобщенных результатов этих данных.
Как можно увидеть из таблицы, представленной выше, очень высокие чувствительность и специфичности получены для комбинаций биомаркеров согласно изобретению и AUROC значения являются очень высокими. Следовательно, эти результаты свидетельствуют о том, что комбинации 2 или больше маркеров, выбранных из АСАА1, АР1М2, CGN, DDR1, EPS8L2, FASTKD1, GMIP, IKBKE, P2RX4, Р4НВ, PHKG2, PPFIBP2, PPP1R16A, RASSF7, RNF183, SIRT6, TJP3, EFEMP2, SOCS2 и DCN, обеспечивают неожиданно высокую чувствительность и специфичность для предсказания повышенной вероятности и/или диагностики рака эндометрия. Эти результаты получены из образцов из маточной жидкости и указывают на то, что комбинации биомаркеров, обнаруженных в маточной жидкости, могут являться пригодными для диагностики и/или характеристики рака эндометрия. Кроме того, эти результаты получены в образцах от пре- и пост-менопаузных женщин и таким образом представляют набор маркеров, которые можно исследовать для этих типов пациентов. Следует отметить, что различные программы и алгоритмы можно использовать для создания профилей или характерных картин фингерпринтов. Изобретение отхватывает профили и/или характерные картины фингерпринтов, с применением программ и алгоритмов, отличающихся от DTREG, как используется в настоящей заявке. Профили, идентифицированные в таблице 11, представляют собой неограничивающие примеры, используемые для иллюстрации того, что комбинации биомаркеров, представленных в таблице 1, имеют очень хорошую чувствительность и специфичность для рака эндометрия.
Дополнительные комбинации
Значения чувствительности и специфичности, несмотря на то, что полностью охарактеризованы валидностью диагностического теста, имеют недостаток необеспечения релевантной информации, если клинический вывод производится на основе частного результата теста. Тем не менее, у нас есть преимущество получения собственных свойств для теста и определения его валидности независимо от распространения заболевания в исследуемой популяции.
Чувствительность
Представляет собой вероятность правильной классификации индивидуального пациента или вероятность того, что индивидуум с раком получит положительный результат при применении диагностического теста.
Специфичность
Представляет собой вероятность правильной классификации здорового индивидуума или вероятность того, что здоровый индивидуум получит отрицательный результат при применении диагностического теста Чувствительность и специфичность, таким образом, можно использовать для оценки валидности диагностического теста. Тем не менее, такие представления не очень помогают в клинической практике. Если пациент подвергается диагностическому тесту, то у доктора отсутствует априорная информация относительно их диагноза, таких образом, возникает следующий вопрос: задавать положительный (или отрицательный) при тесте? Что обозначает вероятность, что тестируемый индивидуум имеет заболевание (или нет)? Эти вероятности известны в качестве положительной прогностической значимости и отрицательной прогностической значимости конкретного теста. Положительная прогностическая значимость представляет вероятность наличия заболевания, если индивидуум имеет положительный результат при применении диагностического теста. Отрицательная прогностическая значимость представляет вероятность того, что индивидуум, который получил отрицательный результат при тесте, является по существу здоровым.
Практикующие врачи отдают предпочтение диагностическим тестам с высокой отрицательной прогностической значимостью, поскольку они не допускают возможности для людей с раком получать неправильных диагноз. Из этих соображений, нами были отданы предпочтения тем комбинациям, которые обеспечивают нам наивысшие отрицательные прогностические значимости.
Следующие значения в таблице 12 рассчитывали, используя указанные маркеры, как определено с помощью ОТ-ПЦР, в образцах маточной жидкости.
Комбинации, показанные на фигуре 18 (Р4НВ, EFEMP2, SIRT6, DDR1, GMIP, и FASTKD1) и фигуре 19 (Р4НВ, EFEMP2, SIRT6, PHKG2, GMIP, и FASTKD1), и комбинации всех 20 маркеры имеют чувствительности, специфичности, NPV, и PPV равные 100%, и AUROC равно 1.
Максимизация отрицательной прогностической значимости: Новые образцы: три новых образца рака и 24 образцов без опухолей обеспечивали общее количество образцов в дальнейшем анализе (33Т и 48 без опухоли) с дополнительным образцом, имеющим следующие характеристики:
Рассчитанный риск рака для 48 образцов без опухолей и 33 образцов опухолей, используя следующие комбинации генов АСАА1, АР1М2, EPS8L2, IKBKE, P2RX4, Р4НВ, PPFIBP2, PPP1R16A, SIRT6, и EFEMP2 результат представлен на фигуре 17.
На фигуре 18 показан рассчитанный риск рака для 48 образцов без опухолей и 33 образцов опухолей, используя FASTKD1, GMIP, Р4НВ, EFEMP2, DDR1, и SIRT6.
На фигуре 19 показан рассчитанный риск рака для 48 образцов без опухолей и 33 образцов опухолей, используя FASTKD1, GMIP, Р4НВ, EFEMP2, PHKG2, и SIRT6.
Как показано на фигуре 17, первая комбинация способна классифицировать все образцы правильно, но процент нескольких здоровых образов, и имеющих рак, очень близок к 50%: некоторые образцы рака являются слишком близко к неправильной классификации при использовании этой комбинации. В заключение, риск неправильной классификаций пациентов с раком с ложным диагнозом. Несмотря на то, комбинации, представленные на фигуре 18 и фигуре 19, ошибочно классифицировали один и два образца здоровых пациентов соответственно, обе эти комбинации правильно классифицировали всех пациентов с раком и они осуществляют это с более высоким процентом риска рака по сравнению с предыдущей комбинацией. Поэтому указанные комбинации являются ценными с клинической точки зрения.
Пример 6: Обнаружение белка, соответствующего биомаркерам из таблицы 1
Обнаружение белка, соответствующего биомаркерам, представленным в таблице 1, можно осуществлять в соответствии с любым из методов, доступных для специалиста в данной области техники. В соответствии с этим методом, получают образцы из контролей (или контрольное значение устанавливают) и пораженных особей (например, сыворотки, ткани, и маточной жидкости) и зонд для антител, селективный или специфический к конкретному биомаркеру. Одним из методов обнаружения белок является вестерн-блоттинг анализ и он проиллюстрирован, как в случае Р4НВ.
Вестерн-блоттинг анализ для образцов человека из нормальной ткани эндометрия и опухолевой ткани рака эндометрия для определения уровня белка Р4НВ (около 60 кДа) в этих образцах.
Гели загружали с 40 мкг общих белковых экстрактов из каждого образца. Как можно увидеть на фигуре 10, образцы опухолей окрашивались значительно более интенсивно для Р4НВ по сравнению с нормальной тканью.
Тестируемые образцы включают четыре нормальные ткани (N) и четыре опухолевые ткани (Т). Нормальные и опухолевые ткани получали от одного и того же пациента. В качестве положительного контроля: общий белковый экстракт из клеточной линии опухоли эндометрия Isikawa. Используемое антитело: LS-C38385 от LifeSpan.
Результаты подтверждали на уровне белка результаты, полученные в опытах экспериментах на панели и TaqMan.
Вестерн-блоттинг анализ осуществляли для АР1М2, IKBKE, EPS8L2, DDR1, CGN, и TJP3. См. фигура Х - фигура X. Эти результаты подтверждают на уровне белка результаты, полученные в экспериментах на панели и TaqMan для этих биомаркеров.
Для иммуногистохимической валидации, конструировали микропанели тканей. Для охвата полного диапазона от нормальной ткани до различных типов и степеней дифференцировки карцином эндометрия, репрезентативные площади от 70 зафиксированных в парафине карцином (56 эндометриоидных, 6 серозно-папиллярных, 1 слизеобразующей, 4 светлоклеточных раков, 3 карциносарком), и 11 неопухолевых эндометриев (4 атрофических, 3 пролиферативных, 1 секреторный эндометрий и 3 гиперплазии), осторожно отбирали и метили на индивидуальных парафиновых блоках. Две центральные массы тканей диаметром 1 мм получали из каждого парафинового блока и точно встраивали в новый парафиновый блок. Получали срезы 5 мкм из всех тканей микропанелей парафиновых блоков. Протокол был одобрен экспертным советом организации при госпитале Vall D'Hebron, и письменное согласие было получено от всех пациентов. Р4НВ, PPP1R16A и EPS8L2 обнаруживали с помощью непрямого анализа иммунопероксидазы с цитратным буфером рН 7,3 для извлечения антигена. Срезы инкубировали с первичным антителом к Р4НВ (LS-C38385) и PPP1R16A (Н00084988-М06) в течение 1 часа при комнатной температуре, используя разведение 1:500 и 1:100, соответственно, и EPS8L2 (Н00064787-В01) в течение ночи при разведении 1:100. После этого срезы инкубировали с конъюгированным с пероксидазой козьим антимышиным иммуноглобулином (EnVision Dual System, DAKO, Glostrup, Denmark). Эндогенную активность пероксидазы блокировали с помощью 3% H2O2. Срезы промывали, и реакции развивали с диаминобензидином, с последующим контрастным окрашиванием с гематоксилином. Полуколичественную оценку белков осуществляли с тремя независимыми исследователями, подсчитывая интенсивность окрашивания и процент положительных клеток.
ТМА иммуногистохимия подтверждала дифференциальную экспрессию трех белков в опухолевых уплотнениях по сравнению с уплотнениями нормального эндометрия. Р4НВ, PPP1R16A и EPS8L2 представляли специфическую цитоплазматическую экспрессию в опухолевых клетках во всех гистологических типах и степенях дифференцировки карцином, и отсутствие или слабое цитоплазматическое окрашивание в нормальных эпителиальных железах. Эти результаты подтверждают на уровне белка результаты, полученные для этих белков в экспериментах на микропанелях и количественной ПЦР, описанные в настоящей заявке.
Пример 7: АСАА1
Было обнаружено, что АСАА1 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что АСАА1 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что АСАА1 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способов, описанных в примерах 2-4. В примере 5 показано, что АСАА1 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая АСАА1, приведена в ENSEMBL per. № ENST00000333167 и имеет последовательность, как представлено в SEQ ID NO:1

Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000333664 и имеет последовательность, как представлено в SEQ ID NO:2

Праймеры для амплификации последовательности АСАА1 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации АСАА1 включают приведенные в
Прямой SEQ ID NO:3 GAGCTTCTCTCGGCAGTCAT
Обратный SEQ ID NO:4 CTCAGAAACTGGGCGATTC
Прямой SEQ ID NO:5 GCAATCATGGCCCGAATC
Обратный SEQ ID NO:6 CCCCGACGAACACTGTCTAT
Прямой SEQ ID NO:7 GTGCCTTTGTCCACTGTCAA
Обратный SEQ ID NO:8 ACAGGCCATGCCAATGTC
Прямой SEQ ID NO:9 TCACGGGAGAAGCAGGATAC
Обратный SEQ ID NO:10 CTCTTGGTGCCCTTGTCATC
Прямой SEQ ID NO:11 GGCTGACAGTGAGTGACGTG
Обратный SEQ ID NO:12 AGGGGGTTCACCTTCTCAG
Прямой SEQ ID NO:13 GTGGCATCAGAAATGGGTCT
Обратный SEQ ID NO:14 CTCTGGCCTTCTCCTTCTCC
Прямой SEQ ID NO:15 ATTACTTCGCGCTTGATGGA
Обратный SEQ ID NO:16 AGGGCAAAGGTATCCTGCTT
Прямой SEQ ID NO:17 GCCTGCCTTCAAGAAAGATG
Обратный SEQ ID NO:18 TAAGACCTCAGGACCCCAAG
Прямой SEQ ID NO:19 TGGGGTCCTGAGGTCTTATG
Обратный SEQ ID NO:20 TCTCGAAGATGTCCACGTCA
Прямой SEQ ID NO:21 GTGGCATCAGAAATGGGTCT
Обратный SEQ ID NO:22 AGGGCAAAGGTATCCTGCTT
Прямой SEQ ID NO:23 TGACCCAGGATGAGGGTATC
Обратный SEQ ID NO:24 TCTCGAAGATGTCCACGTCA
Прямой SEQ ID NO:25 GGAGACTGTGCCTTTGTCCA
Обратный SEQ ID NO:26 CTCTGTCAGCCAGGGACAT
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения АСАА1 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:27 CGGTTCTCAAGGACGTGAAT
SEQ ID NO:28 AGTGACATCCCGGAGACTGT
SEQ ID NO:29 GTGGCATCAGAAATGGGTCT
SEQ ID NO:30 AGCTGAGATTGTGCCTGTGA
SEQ ID NO:31 ATCAATGAGGCCTTTGCAAG
SEQ ID NO:32 ACAGAGGGAACCCTGGAAAT
SEQ ID NO:33 GATTGCCTGATTCCTATGGG
SEQ ID NO:34 GTCCAAGGCAGAAGAGTTGG
SEQ ID NO:35 ATGCCATCCCAGTAGCTTTG
SEQ ID NO:36 GCCTGTGGGATAACCTCTGA
SEQ ID NO:37 AAACTGAAGCCTGCCTTCAA
SEQ ID NO:38 ATAGACAGTGTTCGTCGGGG
Зонд для обнаружения АСАА1 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как представлено в SEQ ID NO:39 GCTACGCAGACAGTCCTGCTGCTCTAGCAGCAAGGCAGTAACACCACAAAA GCAAAACCA
Другие зонды к АСАА1 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к АСАА1 включают, но не ограничиваясь только ими. Кроличье поликлональное анти-АСАА1 № каталога НРА006764 от atlas антител (только распознан первый транскрипт); и мышиное поликлональное антитело, выработанное к полноразмерному белку АСАА1 человека. № каталога: Н00000030-В01 от abnova (MaxPab).
Пример 8: АР1М2
Было обнаружено, что АР1М2 (связанный с адаптером белковый комплекс 1, mu 2 субъединица) также известен как D9Ertd818e, HSMU1B, MU-1B, MU1B), сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что АР1М2 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что АР1М2 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что АР1М2 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
АР1М2 представляет собой субъединицу гетеротетрамерного клатрин связанного с адаптером белкового комплекса 1 (АР-1), который играет решающую роль во многих путях миграции везикул в клетке. Этот белок способен взаимодействовать с сортирующими сигналами на основе тирозина. AP1 экспрессируется исключительно в эпителиальных клетках. Все АР комплексы содержат две большие субъединицы 100-130 кДа (α и β1 в API), среднюю субъединицу 50 кДа (µ1 в AP1), и маленькую субъединицу 17-20 кДа (σ1 вАР1). PMID: 10338135
В везикулах, покрытых клатрином, АР-2 расположен между липидным бислоем и клатриновой сеткой, и, предположительно, заякоривает клатрин в мембрану. АР1М2 является представителем семейства адаптеров со средней длиной цепи, обозначаемой MulB, который специфически экспрессируется в поляризованных эпителиальных клетках и некоторых экзокринных клетках. MulB наиболее близкородственный убиквитарно-экспрессируемой MulA субъединице АР-1 (79% идентичность на аминокислотном уровне).
Последовательность мРНК, соответствующая АР1М2, представлена в ENSEMBL номер доступа ENST00000250244 и имеет последовательность, как представлено в SEQ ID NO:40

Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000250244 и имеет последовательность, как представлено в SEQ ID NO:41

Праймеры для амплификации последовательности ENST00000250244 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc.
Примеры пар праймеров для амплификации АР1М2 включают:
Прямой SEQ ID NO:42 CGCCACCATGTCCGCCTCGGCTG
Обратный SEQ ID NO:43 GCTCAATCTTGCTCATGGCCAC (Ex2)
Прямой SEQ ID NO:44 CAGGTCCACTTCCTATGGATC (ex2)
Обратный SEQ ID NO:45 CAAAGTTGTCCCGGATGCTC (Ex4)
Прямой SEQ ID NO:46 CGCTCCGAGGGTATCAAG (EX5)
Обратный SEQ ID NO:47 CTTGCTGCGGCCAGTGAGC (ex6-7)
Прямой SEQ ID NO:48 GACTTTGAGCTCATGTCATACC (Ex7)
Обратный SEQ ID NO:49 CTTAATACTCCAAATCACGACG (Ex9)
Прямой SEQ ID NO:50 GTTTGAGATCCCCTACTTC (Ex10)
Обратный SEQ ID NO:51 GCCTGGTAACCACTTTTCTCAATG (Ex11)
Прямой SEQ ID NO:52 CTGGGTTCGCTACATCACC (Ex11)
Обратный SEQ ID NO:53 GCCCCGTGTTCAAGC (Ex12)
Прямой SEQ ID NO:54 CATGCCTTTGCTGGTACAG (Ex2)
Обратный SEQ ID NO:55 GAGTACACCAGGGAGGCATTG (Ex3)
Прямой SEQ ID NO:56 CTCCCTGGTGTACTCCTTC (Ex3)
Обратный SEQ ID NO:57 GCTGTCGGTGGTCTGCGGGAAG (Ex4)
Прямой SEQ ID NO:58 CAGCAAGATCCTGCAGGAG (Ex4-5)
Обратный SEQ ID NO:59 CAGGTTGACAGACTCTATG (Ex5)
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения АР1М2 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Примеры зондов включают:
SEQ ID NO:60
ATGAAGAAATAGAAGAGGGGCTTGAAGTCCTCCTCGCGAGTGCCTTCTTGCAATTACCTG
SEQ ID NO:61
CCAGGTCCACTTCCTATGGATCAAACACAGCAACCTCTACTTGGTGGCCACCACATCG
SEQ ID NO:62 GACAATAGAGGTATTCTGCGAATACTTCAAGGAGCTGGAGGAG
SEQ ID NO:63
CAATGACCGCGTGCTCTTCGAGCTCACTGGCCGCAGCAAGAACAAATCAGTAGA
SEQ ID NO:64
TTTCCCGGGGGGCAAGGAGTACTTGATGCGAGCCCACTTTGGCCTCCCCAGTGTGG
Другие зонды к АР1М2 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к АР1М2 включают, но не ограничиваясь только ими, Proteintech Group, Inc. № каталога 10618-1-АР, который представляет собой аффинное очищенное кроличье поликлональное антитело с антигеном, который представляет собой рекомбинантный АР1М2 белок, которые включает аминокислоты 1-320 белка и от № каталога Abnova H00010053-B01, который представляет собой мышиное поликлональное антитело к полноразмерному белку.
Пример 9: CGN
Было обнаружено, что CGN (также известен как DKFZp779N1112, FLJ39281, и KIAA1319) сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что CGN сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что CGN сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что CGN можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая CGN, представлена в ENSEMBL номер доступа ENST00000271636 и имеет последовательность, как представлено в SEQ ID NO:65


Старт- и стоп-кодоны выделены жирным шрифтом.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000271636 и имеет последовательность, как представлено в SEQ ID NO:66

Праймеры для амплификации последовательности CGN могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc. Примеры пар праймеров для амплификации CGN включают приведенные в
Прямой SEQ ID NO:67 GCTTTAGCCGTTCTCGTCA
Обратный SEQ ID NO:68 CTGGTCTCGAAGGAGGTCTG
Прямой SEQ ID NO:69 CAGACCTCCTTCGAGACCAG
Обратный SEQ ID NO:70 TTCCTCCTCACAGAGGTTTCA
Прямой SEQ ID NO:71 TACAGCGAAAGCTGGATGAA
Обратный SEQ ID NO:72 AGTCGGCTGCACTCTTCTGT
Прямой SEQ ID NO:73 TGCAGAACAAGCTGAAACAT
Обратный SEQ ID NO:74 GCTGCTCCTCTACTCGCTGT
Прямой SEQ ID NO:75 GGGCATTGGCAGAGTATGTT
Обратный SEQ ID NO:76 TTCCATCTCCTCCTTCTCCA
Прямой SEQ ID NO:77 CAGCAACTGCGACAGGACT
Обратный SEQ ID NO:78 CATTTTCCTCCTGGGTCTCC
Прямой SEQ ID NO:79: CTGAGCTGGAGGAGCAGAAG
Обратный SEQ ID NO:80 TGCAGGGCTTGCTTAGAGTC
Прямой SEQ ID NO:81 TGGAGCAAGAGGCAGAGAAC
Обратный SEQ ID NO:82 ACTCTGTTTCCAGCCGTGAG
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения CGN могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:83 CAGGACTGGGTCCTTCAGAG
SEQ ID NO:84 CAGGCAGTGTGGACCATATG
SEQ ID NO:85 GCTAGAGCCATCCCAAGTTG
SEQ ID NO:86 TGAGCCTGCTAAGGAGGTGT
SEQ ID NO:87 TAGAGCCACCAAGCAGGAAC
SEQ ID NO:88 TTCCAAGGCTAAGATGGTGG
SEQ ID NO:89 GACAGGACTGTGGACCGACT
SEQ ID NO:90 TGAAGGGTCTCGAGGAAAAA
Зонд для матрицы SEQ ID NO:91
GGGAAGAGGTAAGGGGGATGATTCACCTCCATATTTCCTAAGCAGGTTGTATAGGGAGCC
Антитела к CGN включают, но не ограничиваясь только ими, кроличье античеловеческое цингулин (CGN) поликлональное, неконъюгированное № каталога LS-C22229-100, от lifespan bioscience (С-концевой участок); и мышиное античеловеческое цингулин (CGN) моноклональное, неконъюгированное, клон 6а40 № каталога LS-C22230-100, от Lifespan Bioscience (С-концевой участок).
Пример 10: DDR1
Было обнаружено, что DDR1 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что DDR1 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что DDR1 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что DDR1 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая DDR1, приведена в ENSEMBL per. № ENST00000376570 и имеет последовательность, как представлено в SEQ ID NO:92


Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ЕР0000365754 и имеет последовательность, как представлено в SEQ ID NO:93

Праймеры для амплификации последовательности DDR1 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации DDR1 включают приведенные в
Прямой SEQ ID NO:94 CATCTCTGCTTCCAGCTCCT
Обратный SEQ ID NO:95 TACTCCTCCTCCTTGGGAAA
Прямой SEQ ID NO:96 AGCTACCGGCTGCGTTACT
Обратный SEQ ID NO:97 CTTCAGCACCACTCCCTCAG
Прямой SEQ ID NO:98 CGTCTGTCTGCGGGTAGAG
Обратный SEQ ID NO:99 CCGTCATAGGTGGAGTCGTT
Прямой SEQ ID NO:100 CAACGACTCCACCTATGACG
Обратный SEQ ID NO:101TGCTCCATCCCACATAGTCA
Прямой SEQ ID NO:102 TGACTATGTGGGATGGAGCA
Обратный SEQ ID NO: 103 CCAGCGTGTGCATGTTGTTA
Прямой SEQ ID NO:104 TGTCTCAGTGCCCCTTGG
Обратный SEQ ID NO:105 GTGCCGGAGAGGAATTGTT
Прямой SEQ ID NO:106 ACCTCCCACCAACTTCAGC
Обратный SEQ ID NO:107 CAGCAGGAGCAGGATGATG
Прямой SEQ ID NO:108 CATCATCCTGCTCCTGCTG
Обратный SEQ ID NO:109 CCAGGGACAGAGAGGTGAAC
Прямой SEQ ID NO:110 ACCGCCCAGGTCCTAGAG
Обратный SEQ ID NO:111 CGGTAGGCTGGATTGGAGA
Прямой SEQ ID NO:112 CACCCTTTGCTGGTAGCTGT
Обратный SEQ ID NO:113 CGAATGATGTTTGGGTCCTT
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения DDR1 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:114 ACAGCAGGTTGGAGAGCAGT
SEQ ID NO:115 GTCAGGAGGTGATCTCAGGC
SEQ ID NO:116 CTCTATGGCTGCCTCTGGAG
SEQ ID NO:117 GTGGGGCTGGATGACTTTAG
SEQ ID NO:118 AGTTTGAGTTTGACCGGCTG
SEQ ID NO:119 CCCTGGTTACTCTTCAGCGA
SEQ ID NO:120 CTTGGAGCTGGAGCCCAG
SEQ ID NO:121 AGGGTGTTGGAAGAGGAGCT
SEQ ID NO:122 ACTCTGCTCCCTGTGTCCC
SEQ ID NO:123 GCCAGGAATGATTTCCTGAA
Зонд, используемый для обнаружения DDR1 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как представлено в SEQ ID NO:124
ATTGGGATTGGGGGGAAAGAGGGAGCAACGGCCCATAGCCTTGGGGTTGGACAT CTCTAG
Другие зонды к DDR1 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к DDR1 включают, но не ограничиваясь только ими, кроличье поликлональное антитело к МСК10 от abcam № каталога ab5508 эпитоп: аа31-47; и мышиное анти-человеческое DDR1 поликлональное антитело, неконъюгированное от № каталога Abnova H00000780-A01 по отношению к полноразмерному.
Пример 11: EPS8L2
Было обнаружено, что EPS8L2 (EPSS-подобный 2, также известен как AI042819, AW545405, Eps812_прогностический, Eps812 прогностический, EPS8R2, FLJ16738, FLJ21935, FLJ22171, MGC126530, MGC3088) сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что EPS8L2 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что EPS8L2 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что EPS8L2 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Ген EPS8L2 кодирует белок, который относится к субстрату 8 пути передачи сигналов рецептора фактора роста эпидермиса 8 (EPS8), субстрату для рецептора фактора роста эпидермиса. eps8Ls определяет новое семейство белков, отвечающих за функциональную избыточность в RTK-активированному пути передачи сигналов, приводящему к ремоделированию актина. Представители этого семейства связывают стимуляцию фактора роста с организацией актина. Представители eps8 семейства совместно используют модульную организацию, состоящую из предполагаемого РТВ домена, центрального SH3 домена и С-концевого эффекторного участка. SH3 домены eps8L проявляют уникальные предпочтения связывания для пептидов, содержащих пролин-Х-Х-аспартат-тирозин (pXXDY) консенсус и составляют филогенетически отличающееся подсемейство в пределах семейства SH3 домена. (PMID: 14565974).
Несмотря на то, что EPS8L2 функция неизвестна, при анализах экспрессии генов рака молочной железы и щитовидной железы, идентифицирован Eps8, другой представитель семейства, в качестве нового предполагаемого онкогена и также он вовлечен в миграцию опухолевых клеток в клетки фибросаркомы. (PMID: 16618726) (PMID: 17075124) (PMID: 15289329)
Последовательность мРНК, соответствующая EPS8L2, приведена в ENSEMBL per. № ENST00000318562 и SEQ ID NO:125

Старт- и стоп-кодоны выделены жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000320828 и имеет последовательность, как представлено в SEQ ID NO:126

Праймеры для амплификации последовательности ENST00000318562 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3. Примеры пар праймеров для амплификации EPS8L2 включают:
Прямой SEQ ID NO:127 GAG ACC TGG CGC CCC GGC (Ex1)
Обратный SEQ ID NO:128 GTG GCC CCG GTC TGA GGC (Ex2)
Прямой SEQ ID NO:129 GAG CCA GTC CGG GGC CGT G (Ex2)
Обратный SEQ ID NO:130 CTT GGG GCT CAT CTT GGC (Ex3)
Прямой SEQ ID NO:131 CGA CGG TGT GGC CAA GAT GAG (Ex3
Обратный SEQ ID NO:132 CGT GGT ACT GCG AGG TC (Ex4)
Прямой SEQ ID NO:133 CTCCAACGTCATCATGCAC (Ex4)
Обратный SEQ ID NO:134 GATGGCGTCGTCCACAGAC (Ex5)
Прямой SEQ ID NO:135 CAGTCGCTGCGGCTGCTGG (Ex5)
Обратный SEQ ID NO:136 GGACCGTCTGGCTGCGCTG (Ex6)
Прямой SEQ ID NO:137 GATGTCCACTTCTTCCACTGC (Ex6)
Обратный SEQ ID NO:138 CCGAATCTTCTCCTGGTGTC (Ex8)
Прямой SEQ ID NO:139 GAGGCCAAGAATCGCGTGGGC (Ex8)
Обратный SEQ ID NO:140 GTCCAGGGCGCAGTTGAGG (Ex10)
Прямой SEQ ID NO:141 CGACTGCTTCCAGAAAATC (Ex11)
Обратный SEQ ID NO:142 CGAAGAGGAAGTGCACGAG (Ex12)
Прямой SEQ ID NO:143 GATGTCGCTGTGGGAGTCAC (Ex13)
Обратный SEQ ID NO:144 GAGGGGCACCTGTGGCTC (Ex14)
Прямой SEQ ID NO:145 GGTGGAGGGGCTGGCGTC (Ex14)
Обратный SEQ ID NO:146 GGCTCTGAAGTG GGGCTGTG (Ex15)
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения EPS8L2 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя праймеры, описанные выше, и подходящие реагенты).
Примеры зондов включают:
SEQ ID NO:147
GCTTCCCGGGGAACAAAGACGAGCTCATGCAGCACATGGACGAGGTCAACGACGAGCTCA
SEQ ID NO:148
GCAGAGCTGGTGCACGAGGACATCGAGAGCGCGTTGGCCGACTGCCGG
SEQ ID NO:149
GCCGTCGGGAGTCGCAGGAGGAGCCGCGGGCCGTGCTGGCTCAGAAGATAG
SEQ ID NO:150
GCTCGTGTGCCAGGACTCGGAGCAGAGCAAGCCGGATGTCCAC
SEQ ID NO:151
GTACAGCCAGCTCACCATGCAGAAGGCCTTCCTGGAGAAGCAGCAAAG
Другие зонды к EPS8L2 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к EPS8L2 включают, но не ограничиваясь только ими, № каталога Abnova H00064787-M01, которое представляет собой мышиное моноклональное антитело, выработанное по отношению к неполностью рекомбинантному EPS8L2 (615 а/к ~ 715 а/к) и № каталога Abnova H00064787-B01, которое представляет собой мышиное поликлональное антитело, выработанное к полноразмерному белку человека EPS8L2 белок.
Пример 12: FASTKD1
Было обнаружено, что FASTKD1 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что FASTKD1 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что FASTKD1 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что FASTKD1 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая FASTKD1, приведена в ENSEMBL per. № ENST00000260971 и имеет последовательность, как представлено в SEQ ID NO:152


Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000260971 и имеет последовательность, как представлено в SEQ ID NO:153

Праймеров для амплификации последовательности нуклеиновых кислот FASTKD1 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации нуклеиновой кислоты FASTKD1 включают приведенные в
Прямой: SEQ ID NO:154 TGAATGACGATACCCTGGTG
Обратный: SEQ ID NO:155 AGCCTTCTCCATGCTTCTGT
Прямой: SEQ ID NO:156 CCATGACCCGCTAGTTGAAG
Обратный: SEQ ID NO:157 TGATCTGCTAGGCAAGAGGAA
Прямой: SEQ ID NO:158 TTCCTCTTGCCTAGCAGATCA
Обратный: SEQ ID NO:159 TGTTGACCATCAAGACAGACA
Прямой: SEQ ID NO:160 TCCTCTGTGTAATCATCCTGCT
Обратный: SEQ ID NO:161 CTCGCCAGTTAGGTCCTCTG
Прямой: SEQ ID NO:162 GGAGCAATGGGAGATATGGA
Обратный: SEQ ID NO:163 TTCCTTTGGAAATGCAGAAAA
Прямой: SEQ ID NO:164 TGCATTTCCAAAGGAAGGAG
Обратный: SEQ ID NO:165 CAAGTGAGGAGAAGGGAGCA
Прямой: SEQ ID NO:166 AAATGTTGGGGAGATTGCAT
Обратный: SEQ ID NO:167 TCAATACGCTGAATGGACGA
Прямой: SEQ ID NO:168 GATCCACCTCAAAGGGATGA
Обратный: SEQ ID NO:169 GGCCAAAGAGAAACCAAGAA
Прямой: SEQ ID NO:170 GTGTTTCTTGGTTTCTCTTTGG
Обратный: SEQ ID NO:171 CTGTTGTGTTCCATCCATGC
Прямой: SEQ ID NO:172 GCATTGGGACAACTACCAGAA
Обратный: SEQ ID NO:173 GTATGGGAGCGCAAAAGAAG
Прямой: SEQ ID NO:174 TGTGTTGCTTCATATTTGTACCC
Обратный: SEQ ID NO:175 CATAGCAGATTTTCCTTTCATGTG
Прямой: SEQ ID NO:176 TGACCGCTTCTGTCAACAAT
Обратный: SEQ ID NO:177 TGAATCCAAAAATTCCAAAGC
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения FASTK.D1 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:178 GACCCGCTAGTTGAAGCACT
SEQ ID NO:179 ACAGAAGCATGGAGAAGGCT
SEQ ID NO:180 GAACTTGGAAACCACACAGGA
SEQ ID NO:181 TTGTAGCATTGGGACCCATT
SEQ ID NO:182 TGCATAAACATTTGGATGGC
SEQ ID NO:183 TTCTGGTCCGTGCTATTTCC
SEQ ID NO:184 GTGGCTGTTCAGCAGATTGA
SEQ ID NO:185 GAACTTGCGTGCAACATCTT
SEQ ID NO:186 CCAGAAGATCTGCTAAAGGCA
SEQ ID NO:187 TGCCCTGGGAATCAAATATC
SEQ ID NO:188 GGATTGCTTTGGAATTTTTGG
SEQ ID NO:189 ATGGATGGAACACAACAGCA
Зонд для обнаружения FASTKD1 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как представлено в SEQ ID NO:190 TGAATGGAACTCTATGGCACTGTCAACAAAGGATGCTCGGATGGACTACCTG AGAGA
Другие зонды к FASTKD1 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к FASTKD1 включают, но не ограничиваясь только ими, мышиное античеловеческое FLJ21901 поликлональное антитело № каталога Н00079675-А01 к N-концу (от а/к 2-100).
Пример 13: IKBKE
Было обнаружено, что IKBKE (ингибитор энхансера гена полипептида каппа-легкой цепи в В-клетках, киназа эпсилон), также известен как IKK-I; IKKE; IKKI; KIAA0151; MGC125294; MGC125295; MGC125297, сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что IKBKE сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что IKBKE сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что IKBKE можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
IKBKE является представителем большого киназного комплекса IkB, способного фосфорилировать IkB. IKK фосфорилирует только один из двух остатков серина в IκВα, необходимых для убиквитинилирования и разложения IκВα. Тем не менее, разложение IkBα освобождает расположенные в ядре сигналы на NF-kB, что приводит к их транслокации в ядро, где они связываются со специфическими промоторами и активируют транскрипцию. (PMID: 10882136).
Последовательность мРНК, соответствующая IKBKE, приведена в ENSEMBL per. № ENST00000367120 и имеет последовательность, как представлено в SEQ ID NO:191

Старт- и стоп-кодоны выделены жирным шрифтом.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000356087 и имеет последовательность, как представлено в SEQ ID NO:192

Праймеры для амплификации последовательности ENST00000367120 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации IKBKE включают:
Прямой SEQ ID NO:193 GTGCCACAGACAGAAAGCATAAC (EX2)
Обратный SEQ ID NO:194 GGCTGTGCTCTGCATCTC (ex3)
Foward SEQ ID NO:195 GGGGCCACTGCCAGTGTG (ex3)
Обратный SEQ ID NO:196 GCAGGTAGCTGGTAGTGTTGAAG (ex4)
Прямой SEQ ID NO:197 GAGGTCCTGCGGAAGCTGAAC (ex4)
Обратный SEQ ID NO:198 CACTCAGCAGGCTCCCACTG (ex5)
Прямой SEQ ID NO:199 CCTGAGGATGAGTTCCTGGTG (ex5)
Обратный SEQ ID NO:200 GTCGCGATGCACAATGCCGTTC (ex6)
Прямой SEQ ID NO:201 GGATGATGATGAGAAGTTCGTCTC
Обратный SEQ ID NO:202 GAACGCTTTTTGCTGGGGC (ex7)
Прямой SEQ ID NO:203 CATCCCCTTTGGTGGGCCAC (ex7)
Обратный SEQ ID NO:204 CCGTTCTCCCGCCTCTGG (ex8)
Прямой SEQ ID NO:205 CCTGGAGTGGAGCTACACC (ex8)
Обратный SEQ ID NO:206 CACTTGGCCTGCTCCACCTC (ex9)
Прямой SEQ ID NO:207 GTCCCAGGCAGTCCTGCAC (ex9)
Обратный SEQ ID NO:208 GACGCTGGGCTCGAGGACAC (ex10)
Прямой SEQ ID NO:209 GACCCTCTTCAGCACAGCCAT С
Обратный SEQ ID NO:210 GCCGCAGGGCCTGGTAGC (ex 12)
Прямой SEQ ID NO:211 GATCCAGGAACTGAAGGCGGC (ex 14)
Обратный SEQ ID NO:212 CCTGATCCCGGCTCTTCAC (exl5)
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения IKBK-E могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя праймеры, описанные выше, и подходящие реагенты).
Другие примеры зондов включают:
SEQ ID NO:213
CTCCTGTTCTTTCTATGCTTGGTCTGACTGAGCCTAAAGTTGAGAAAATGGGTGGCCAAG
SEQ ID NO:214
CATCACCTGCCAGCTGTCACTGGGGCTGCAGAGCC
SEQ ID NO:215
CTATATCCATGCCCACAACACGATAGCCATTTTCC
SEQ ID NO:216
GGACGTCCCCAAGTTCGTCCCCAAAGTGGACCTGCAGGCG
SEQ ID NO:217
GGTCCAGGAGAGTCTCAGCAAGCTCCTGGAAGAGCTATCTCAC
Другие зонды к IKBKE известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к IKBKE включают, но не ограничиваясь только ими, Abcam № каталога ab37596, которое представляет собой кроличье поликлональное антитело с антигеном, который представляет собой KLH конъюгированный синтетический пептид, выбранный в пределах а/к 700-800 IKKE человека; и № каталога Abcam abl2142, которое представляет собой мышиное моноклональное антитело к синтетическому пептиду, соответствующему а/к остаткам 175-188, 525-540, или 567-580 IKK йота/IKK эпсилон человека.
Пример 14: PHKG2
Было обнаружено PHKG2, что сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что PHKG2 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что PHKG2 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что PHKG2 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая PHKG2, приведена в ENSEMBL per. № ENST00000328273 и имеет последовательность, как представлено в SEQ ID NO:218

Старт- и стоп-кодоны выделены жирным шрифтом.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000329968 и имеет последовательность, как представлено в SEQ ID NO:219

Праймеры для амплификации последовательности PHKG2 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc.
Примеры пар праймеров для амплификации PHKG2 включают приведенные в
прямой SEQ ID NO:220 CCGCCAAAGAGTTTTACCAG
обратный SEQ ID NO:221 TCCATAATCTTCACCGCAAA
прямой SEQ ID NO:222 GGCGAGAGACACACATCCTT
обратный SEQ ID NO:223 CAAACACCAGGAACATGAAGC
прямой SEQ ID NO:224 GCTTCATGTTCCTGGTGTTTG
обратный SEQ ID NO:225 TTTTCAGAGAGGGCCACCTT
прямой SEQ ID NO:226 GGAAGGGAGAGCTGTTTGACT
обратный SEQ ID NO:227 TGTTGTTGGCATGGAGAAAG
прямой SEQ ID NO:228 TCAGATTTCGGGTTCTCCTG
обратный SEQ ID NO:229 ATAGCCTGGGTGGGTTTCAT
прямой SEQ ID NO:230 ATGAAACCCACCCAGGCTAT
обратный SEQ ID NO:231 TGCGTAACATCAGGATCTGC
прямой SEQ ID NO:232 CGTTCCAGCACTGTCAAAGA
обратный: SEQ ID NO:233 CCTTCACAACGCTCAAAGAA
прямой SEQ ID NO:234 ACCCCTTCTTTGAGCGTTGT
обратный SEQ ID NO:235 CGTACACGATGGGTGCTTAG
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения PHKG2 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:236 CCGTTGTGTTCATCGAGCTA
SEQ ID NO:237 CATCACCCTCATCGATTCCT
SEQ ID NO:238 GGAAGGGAGAGCTGTTTGACT
SEQ ID NO:239 AGGAAACCAGGTCCATCATG
SEQ ID NO:240 CAGGGTATCTAGCGCCAGAG
SEQ ID NO:241 CCTGTGGGGTGATCTTGTTC
SEQ ID NO:242 ACAGCTGAGCAGGCCCTAC
SEQ ID NO:243 GTTGTGGCAGTGTGGACAGT
Зонд для обнаружения PHKG2 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как указано в
SEQ ID NO:244
CTCAACCCCAGGGATTCCCAGGAAGCAGAACTCTCCAGAAGAAGGGTTTTGATCATTCCA
Другие зонды к PHKG2 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к PHKG2 включают, но не ограничиваясь только ими, мышиное моноклональное антитело анти-РНКС2 к полноразмерному белку № каталога WH0005261M1 от SIGMA; PHKG2 антитело - N-концевое № каталога ab71129 от abcam; и PHKG2 антитело № каталога ab28642 к участку между аминокислотами 8-57 PHKG2 человека от abcam.
Пример 15: Р4НВ
Было обнаружено, что Р4НВ сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что Р4НВ сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия и неожиданно было обнаружено, что Р4НВ сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примерах 2-4. В примере 5 показано, что Р4НВ можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая Р4НВ, приведена в ENSEMBL per. № ENST00000331483 и имеет последовательность, как представлено в SEQ ID NO:245

Старт- и стоп-кодоны выделены жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000327801 и имеет последовательность, как представлено в SEQ ID NO:246

Праймеры для амплификации последовательности Р4НВ могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации Р4НВ включают приведенные в
Прямой SEQ ID NO:247: GCTGCGGAAAAGCAACTTC
Обратный SEQ ID NO:248 CTGATCTCGGAACCTTCTGC
Прямой SEQ ID NO:249 GGCTATCCCACCATCAAGTT
Обратный SEQ ID NO:250 TCTTCAGCCAGTTCACGATG
Прямой SEQ ID NO:251 GCAGAGTCCTTGGTGGAGTC
Обратный SEQ ID NO:252 TGGAAGTGATCCCAAATGGT
Прямой SEQ ID NO:253 ACCATTTGGGATCACTTCCA
Обратный SEQ ID NO:254 GGTGACCTCCCCTTCAAAGT
Прямой SEQ ID NO:255 CCCCTTGTCATCGAGTTCAC
Обратный SEQ ID NO:256 TGCTCAGTTTGCCGTCATAG
Прямой SEQ ID NO:257 TCACATCCTGCTGTTCTTGC
Обратный SEQ ID NO:258 GTCGCTGTCGATGAAGATGA
Прямой SEQ ID NO:259 GACGGCAGAGAGGATCACAG
Обратный SEQ ID NO:260 TTCTTCCCAACAAGCACCTT
Прямой SEQ ID NO:261 AGCCTGTCAAGGTGCTTGTT
Обратный SEQ ID NO:262 CAAATGGGAGCCAACTGTTT
Прямой SEQ ID NO:263 ACAGCTTCCCCACACTCAAG
Обратный SEQ ID NO:264 CACCGCTCTCCAGGAATTT
Прямой SEQ ID NO:265 GCACGCTGGATGGTTTTAAG
Обратный SEQ ID NO:266 TCATCGTCTTCCTCCATGTCT
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения Р4НВ могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:267 CACAAGTACCTGCTGGTGGA
SEQ ID NO:268 GGCTTCCCCCAAGGAATATA
SEQ ID NO:269 GCTTCTTCAAGGACGTGGAG
SEQ ID NO:270 CTCGACAAAGATGGGGTTGT
SEQ ID NO:271 TCACATCCTGCTGTTCTTGC
SEQ ID NO:272 CTATGACGGCAAACTGAGCA
SEQ ID NO:273 AAAATCAAGCCCCACCTGAT
SEQ ID NO:274 TGAAGACGTGGCTTTTGATG
SEQ ID NO:275 GGTCATTGATTACAACGGGG
SEQ ID NO:276 ATGACGATCTCGAGGACCTG
Зонд для обнаружения Р4НВ нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как указано в
SEQ ID NO:277
GGCATTTCTATTTCACAATCGAATTGAACACATTGGCCAAATAAAGTTGAAATTTTCCCC
Другие зонды к Р4НВ известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к Р4НВ включают, но не ограничиваясь только ими, анти Р4НВ № каталога ab31811 от abcam (кроличье поликлональное) к остаткам 400-500; и PDI (Р4НВ) Мышиное античеловеческое моноклональное антитело от Lifespan Biosciences № каталога LS-C38385.
Пример 16: P2RX4
Было обнаружено, что P2RX4 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что P2RX4 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что P2RX4 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что P2RX4 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
P2RX4
(также известен как Р2Х4; P2X4R; P2RX4)
Р2Х пуринорецептор 4 (Р2Х4)(АТР рецептор)(Пуринергический рецептор
ENSG00000135124
Последовательность мРНК, соответствующая P2RX4, приведена в ENSEMBL per. № ENST00000337233 и имеет последовательность, как представлено в SEQ ID NO:278


Старт- и стоп-кодоны выделены жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000336607 и имеет последовательность, как представлено в SEQ ID NO:279

Примеры пар праймеров для амплификации P2RX4 включают:
Прямой SEQ ID NO:281 AACTGCTCATCCTGGCCTAC
Обратный SEQ ID NO:282 GTCGTAACGGAGCTGACCAC
Прямой SEQ ID NO:283 GGATGTGGCGGATTATGTG
Обратный SEQ ID NO:284 CCTGTGTCTGGTTCATGGTG
Прямой SEQ ID NO:285 AGATTCCAGATGCGACCACT
Обратный SEQ ID NO:286 CAGACCCGTTGAAAGCTACG
Прямой SEQ ID NO:287 TCTGTCAAGACGTGTGAGGTG
Обратный SEQ ID NO:288 CCAAAAGAGTGAAGTTTTCTGC
Прямой SEQ ID NO:289 TTTTGGTTAAGAACAACATCTGG
Обратный SEQ ID NO:290 ATATGGGGCAGAAGGGATCT
Прямой SEQ ID NO:291 CGCTTCGACATCATTGTGTT
Обратный SEQ ID NO:292 TAGCAGTGCCAGGCCAGAG
Прямой SEQ ID NO:293 GAAAAGACTCTACTATCGGGAGAA
Обратный SEQ ID NO:294 CTGTTCTTTGATGGGGCTGT
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения P2RX4 получены из многих источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты).
Другие примеры зондов включают:
SEQ ID NO:295 TTGTGTGGGAAAAGGGCTAC
SEQ ID NO:296 TTCGTCATGACCAACGTGAT
SEQ ID NO:297 TCAGATGCCAGCTGTACTGC
SEQ ID NO:298 GTGGAGGATGACACACACGT
SEQ ID NO:299 TCCTTCCCAACATCACCACT
SEQ ID NO:300 GAAGGCAGGGAAATTTGACA
SEQ ID NO:301 GGGTCTTGCTAGTGAGCTGG
Зонд для обнаружения P2RX4 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как указано в
SEQ ID NO:302
CTCCTCAGAGAAGCGCTGTGCTAAGGTGATCGAGGACCAGACATTAAAGCGTGATTTTCT
Другие зонды к P2RX4 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к P2RX4, включают, но не ограничиваясь только ими, мышиное античеловеческое P2RX4 Maxpab поликлональное, неконъюгированное от Novus Biologicals, P2RX4 (1 а/к ~ 388 а/к) полноразмерный белок человека, Н00005025-В01, и козье Anti-P2RX4 поликлональное, неконъюгированное от Novus Biologicals, NBP1-00141, Синтетический пептид, SEQ ID NO:303 YREKKYKYVEDYEQ, представляющий С конец последовательности в соответствии с NP_002551.2
Пример 17: PPFIBP2
Было обнаружено, что PPFIBP2 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что PPFIBP2 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что PPFIBP2 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что PPFIBP2 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
PPPFIBP2
Последовательность мРНК, соответствующая PPPFIBP2, приведена в ENSEMBL per. № ENST00000299492 и имеет последовательность, как представлено в SEQ ID NO:304


Старт- и стоп-кодоны выделены жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000299492 и имеет последовательность, как представлено в SEQ ID NO:305

Праймеры для амплификации последовательности ENST00000299492 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации PPFIBP2 включают:
1) Прямой SEQ ID NO:306 GCTAGTCATGCGCTGGAAG
Обратный SEQ ID NO:307 GAAGCTCCAGCATCTCCAAG
2) Прямой SEQ ID NO:308 CCCAGGTAAACCACCACAGT
Обратный SEQ ID NO:309 CTGGTGTCCTTCCAGACACA
3) Прямой SEQ ID NO:310 TGTGTCTGGAAGGACACCAG
Обратный SEQ ID NO:311 TCCTCCTGCTCTCTCTGCTC
4) Прямой SEQ ID NO:312 AAGAGCTCAGGCACCTCAAA
Обратный SEQ ID NO:313 CTCACTGTGGAGAGCTGCTG
5) Прямой SEQ ID NO:314 AAACTTTGCTGCTTGCCAAT
Обратный SEQ ID NO:315 TTGAGTGACCATCACAATCTCC
6) Прямой SEQ ID NO:316 TCTCTCAATCAATGAAGAAGAACC
Обратный SEQ ID NO:317 TCCAGTGATTTCTGTGGCAAT
7) Прямой SEQ ID NO:318 GCCTCCAAGATGTAGCTCTCC
Обратный SEQ ID NO:319 TCCACAGATTCACTTCTCAAGTC
8) Прямой SEQ ID NO:320 CGGAGCACAAATATCCCACT
Обратный SEQ ID NO:321 CTTTGGGATTCCGTTTACCA
9) Прямой SEQ ID NO:322 TGGTAAACGGAATCCCAAAG
Обратный SEQ ID NO:323 TTGGAGTCCCTGGTCCTAGA
10) Прямой SEQ ID NO:324 TCTAGGACCAGGGACTCCAA
Обратный SEQ ID NO:325 GGGTGGCTGTCAATAAGGTG
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения PPFIBP2 получены из многих источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты).
Другие примеры зондов включают:
Зонд:
SEQ ID NO:326 CAGGCACTAAAACAGGTGCA
SEQ ID NO:327 AGGGGATAAGGAGTCCCTCA
SEQ ID NO:328 TTGAGACCCAGAAGCTCGAT
SEQ ID NO:329 GAAATTGAGCGTCTGCACAG
SEQ ID NO:330 TTACGGGGCTGTTAAACCAG
SEQ ID NO:331 CAGCAAGTGGAACGCTACAA
SEQ ID NO:332 TGCCACAGAAATCACTGGAA
SEQ ID NO:333 ACACAGAAAGTGGCTGGGAC
SEQ ID NO:334 TTCTACACTGACACGCTGGG
SEQ ID NO:335 GGCCTGGCTCAGTATGTGAT
Зонд для обнаружения PPFIBP2 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как представлено в SEQ ID NO:336
AGATCAAAGGGATGAGCAACAGGGACTTCTGCCACAGTGACAATGGAATTGTGTTGTGCC
Другие зонды к PPP1R16A известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
1) Антитела:
2) Мышиное античеловеческое PPFIBP2 моноклональное антитело,
неконъюгированное, клон ЗА5, Abnova Corporation, PPFIBP2 (NP_003612, 1 а/к ~ 101 а/к) неполностью рекомбинантный белок с GST меткой. MM GST метки отдельно составляет 26 кДа.
3) Кроличье анти-человеческое PPFIBP2 очищенное - MaxPab поликлональное антитело, неконъюгированное, Abnova Corporation, PPFIBP2 (NP_003612.1,1 а/к ~ 876 а/к полноразмерный белок человека.
Пример 18: PPP1R16A
Было обнаружено, что PPP1R16A (белковая фосфатаза 1, регуляторная (ингибиторная) субъединица 16А) также известен как MGC14333 и MYPT3 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что PPP1R16A сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что PPP1R16A сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что PPP1R16A можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
PPP1R16A, также называется как миозин фосфатаза нацеленная субъединица 3 (MYPT3) представляет собой расположенный в мембране белок, который имеет 524 аминокислотных остатка, в которых пять анкириновых повторов и консенсусный РР1 связывающий сайт расположены в пределах N-концевых 300 аминокислотных остатках. С-концевой участок с 224 остатками содержит две возможные Src гомологии 3 связывающих сайта и мотив пренилирования (СааХ). Эти структурные особенности свидетельствуют о том, что R16A может представлять собой каркасный белок регулирующий белок-белковые взаимодействия, а также передачу сигналов в клетках. (PMID: 18202305)
Последовательность мРНК, соответствующая PPP1R16A, приведена в ENSEMBL per. № ENST00000292539 и имеет последовательность, как представлено в SEQ ID NO:337


Старт- и стоп-кодоны выделены жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000292539 и имеет последовательность, как представлено в SEQ ID NO:338

Праймеры для амплификации последовательности ENST00000292539 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации PPP1R16A включают:
Прямой SEQ ID NO:339 GTGTTGTCCTTCTGGAGGCCG (Ex2)
Обратный SEQ ID NO:340 GCCGTCAGGCCGTCCTCGTTG (Ех3)
Прямой SEQ ID NO:341 GCTGCCCGAAATGACCTGG (Ех3)
Обратный SEQ ID NO:342 CGGAAATCATCAATGCAGC (Ex5)
Прямой SEQ ID NO:343 GACGCCTCTGCATGCTGCGG (Ex5)
Обратный SEQ ID NO:344 CACAGGTCATAGGGCATGTTC (Ex6)
Прямой SEQ ID NO:345 GATGAGCAGACGCTGGACTG (Ex6)
Обратный SEQ ID NO:346 CTCCGGATGTCGTCCAGC (Ex7)
Прямой SEQ ID NO:347 CAGGCCGGGGCAGACCTC
Обратный SEQ ID NO:348 GGCTCGGTGTTCCAGCAGCAG
Прямой SEQ ID NO:349 GGGAGCCGCTGCACGCC
Обратный SEQ ID NO:350 CCCGCACCTCCTCGTCCC
Прямой SEQ ID NO:351 CTGCGCGCCCAGAGCCGC
Обратный SEQ ID NO:352 GCGTGCTGCTTGCGGTAC
Прямой SEQ ID NO:353 GCCAGACAGGCGCAGAGCTC
Обратный SEQ ID NO:354 CTACTCGGCCATTGTGCG
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения PPP1R16A получены из многих источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты).
Другие примеры зондов включают:
SEQ ID NO:355
TCTACTGTACAGGACACTGGCCCCTCTCAGGTCAGAAGACATGCCTGGAGGGATGTCTGGCTGCAAAGACTATTTTTATCC
SEQ ID NO:356
CTGACGGCCCTGCACCAGTGCTGCATTGATGATTTCC
SEQ ID NO:357
GACTGCCATGGCCGACCGTGGCATCACCCAG
SEQ ID NO:358
GCTCGTGGCGCACGGGGCCGACCTGAACGC
SEQ ID NO:359
GCGCCGGCAGCCGCGGGAAGGTGGTGAGG
Другие зонды к PPP1R16A известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к PPP1R16A включают, но не ограничиваясь только ими, № каталога Abnova Corporation H00084988-M06, которое представляет собой мышиное моноклональное антитело, выработанное к неполностью рекомбинантному PPP1R16A: 429 а/к ~ 529 а/к; и от № каталога Abnova H00084988-B01, которое представляет собой мышиное поликлональное, выработанное к полноразмерному белку человека PPP1R16A белок.
Пример 19: RASSF7
Было обнаружено, что RASSF7, представитель 7 семейства Ras ассоциированного (RalGDS/AF-6) домена (N-концевой) также известен как 2400009 В 11RIK, AW210608, C110RF13, HRAS1, HRC1, MGC126069, MGC 126070, и RGD 1306244 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что RASSF7 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что RASSF7 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что RASSF7 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
RASSF7 является представителем нового Ras эффекторного семейства, характеризующегося наличием RA домена в их последовательности. Несмотря на то, что они взаимодействуют либо непосредственно или опосредованно с активированным Ras, их роль в опосредовании его биологических эффектов остается невыясненной. Установлено, что они, возможно, модулируют некоторые ростовые ингибиторные ответы, опосредованные Ras, и могут служить в качестве опухолевых супрессорных генов. Действительно, было описано, что представители семейства являются молчащими в опухолях путем метилирования их промоторов. (PMID: 17692468).
Последовательность мРНК, соответствующая RASSF7, приведена в ENSEMBL per. № ENST00000344375 и имеет последовательность, как представлено в SEQ ID NO:360

Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000344226 и имеет последовательность, как представлено в SEQ ID NO:361

Праймеры для амплификации последовательности ENST00000344375 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации RASSF7 включают:
Прямой SEQ ID NO:362 CTGCCAGGAAGTGGTCAT С (Ex1)
Обратный SEQ ID NO:363 GCCGCTGCACAAGCACA (ex2)
Прямой SEQ ID NO:364 CATGGAGCTGAAGGTG (ex1)
Обратный SEQ ID NO:365 CTCAGGACAAACTGGAC (ex2)
Прямой SEQ ID NO:366 GCCACTGAGCGCCTGC (Ex2)
Обратный SEQ ID NO:367 GTCTGCTGGATGAACTG (EX3)
Прямой SEQ ID NO:368 CAG CAG AGC GAG CCT TGC AG
Обратный SEQ ID NO:369 CTG AGT GCC AGG AGG GC (Ex3)
Прямой SEQ ID NO:370 CAC GGC CTG АСА GGG GCC (Ex3)
Обратный SEQ ID NO:371 GCC TAG GCT GGG CAC (EX4)
Прямой SEQ ID NO:372 CTCTGAGTCCCATGCTGG (EX4)
Обратный SEQ ID NO:373 GACACCACTCTGGGGC (EX5)
Прямой SEQ ID NO:374 TGCCCAGCCTAGGCCC (EX4)
Обратный SEQ ID NO:375 GCCAGAGGACACCACTC (EX5)
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения RASSF7 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают:
SEQ ID NO:376
GAGAGGTCCTTCACTGTGTGTACACAGCAAGAGCATGTGTGTGCCACTTC
SEQ ID NO:377
AGTGTCCTCCGAGCCAGGACAGGCATGTTGTTGGGACTGGCGGCCATGGAG
SEQ ID NO:378
GAGCCGGGCCCTGGAGGCAGCAGAGCGAGCCTTGCAGGCTCAGGCTCAGGAGCTG
SEQ ID NO:379
CGGCCTGACAGGGGCCCTCCTGGCACTCAGGGCCCTCTGCCTCCAGCCAGAGAGGAG
SEQ ID NO:380
GAGGAGCTGGGCCATGAGGCCTTCTGGGAGCAAGAGCTGCGCCGGGAGCAGGCCCGGGAG
Другие зонды к RASSF7 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к RASSF7 включают, но не ограничиваясь только ими, № каталога LifeSpan BioSciences. LS-C31793-100, которое представляет собой кроличье поликлональное антитело; и от Novus Biologivals № каталога NB 100-93434, которое представляет собой козье поликлональное анти-RASSF7 к эпитопу SEQ ID NO:381 CTDLRGLELRVQRN.
Пример 20: RNF183
Было обнаружено, что RNF183 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что RNF183 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что RNF183 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что RNF183 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая RNF183, приведена в ENSEMBL per. № ENST00000297894 и имеет последовательность, как представлено в SEQ ID NO:382

Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000297894 и имеет последовательность, как представлено в SEQ ID NO:383

Праймеры для амплификации последовательности RNF183 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc.
Примеры пар праймеров для амплификации RNF183 включают приведенные в
Прямой SEQ ID NO:384 GAGAAGCTGGGCTGGAG (ЭКЗОН 3)
Обратный SEQ ID NO:385 CAGCCACACACGGGGA (ЭКЗОН 4)
Прямой SEQ ID NO:386 CAGCTGTGTGCTAAGAACAAAG (ЭКЗОН 3)
Обратный SEQ ID NO:387 GCCCTGCTGCTCAGCCATC (ЭКЗОН 4)
Прямой SEQ ID NO:388 GCAGAAGGCAGCGAGGAC (ЭКЗОН 3)
Обратный SEQ ID NO:389 GGCAGCAATCCAGCATTTTG (ЭКЗОН 4)
Прямой SEQ ID NO:390 CTGCGTGGAATGTCTGGCC (ЭКЗОН 4)
Обратный SEQ ID NO:391 CAAGTCAGTGACAGGCTGC (ЭКЗОН 4)
Прямой SEQ ID NO:392 GTCTACACGCTGGACCTTG (ЭКЗОН 4)
Обратный SEQ ID NO:393 GATGCGGAACTGAGGGTTG (ЭКЗОН 4)
Прямой SEQ ID NO:394 CTACCTGATGGCCGTCATC (ЭКЗОН 4)
Обратный SEQ ID NO:395 CCAGCAGCAACCGAAAAAG (ЭКЗОН 4)
Прямой SEQ ID NO:396 CATGCGTGCAGGGCTGCA (ЭКЗОН 1)
Обратный SEQ ID NO:397 GTGCTGCTCTCCCAGGG (ЭКЗОН 2)
Прямой SEQ ID NO:398 CCG TGGAATCGATTCCCAG (ЭКЗОН 2)
Обратный SEQ ID NO:399 CTGTTTCTCATATGGGTCATTCG (ЭКЗОН 3)
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения RNF183 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:400 ATGGCTGAGCAGCAGGGCCGGGAGCTTGAGGCTGAGTGCCC
SEQ ID NO:401 GCCCACGGACACTGCCATGCTCGCCCTGCTCC
SEQ ID NO:402 GGACCAGCCCAAGAGCCGCTACTTCCTGCGCCAGCCT
SEQ ID NO:403 CGCTGGACCTTGGCCCCCAGCCTGGGGGCCAG
SEQ ID NO:404 GTTCCTTTGGGGTGTGGGGTGAGTGCTG
Зонд для обнаружения RNF183 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как представлено в SEQ ID NO:405
CAGTGGTATCCAGGAACCTGACTAGCCCAAATAGCAAGTTGCATTTCTCACT GGAGCTGC
Другие зонды к RNF183 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Пример 21: SIRT6
Было обнаружено, что SIRT6 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что SIRT6 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что SIRT6 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что SIRT6 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая SIRT6, приведена в ENSEMBL per. № ENST00000269860 и имеет последовательность, как представлено в SEQ ID NO:406

Старт- и стоп-кодоны выделены жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000269860 и имеет последовательность, как представлено в SEQ ID NO:407

Праймеры для амплификации последовательности SIRT6 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации SIRT6 включают приведенные в
Прямой SEQ ID NO:408 TTGTGGAAGAATGTGCCAAG
Обратный SEQ ID NO:409CCTTAGCCACGGTGCAGAG
Прямой SEQ ID NO:410 TCTTCCAGTGTGGTGTTCCA
Обратный SEQ ID NO:411 TTGGCACATTCTTCCACAAA
Прямой SEQ ID NO:412 AGCTGAGGGACACCATCCTA
Обратный SEQ ID NO:413 GCAGGTTGACGATGACCAG
Прямой SEQ ID NO:414 GCTTCCTGGTCAGCCAGA
Обратный SEQ ID NO:415 ATGTACCCAGCGTGATGGAC
Прямой SEQ ID NO:416 GCTTCCTGGTCAGCCAGA
Обратный SEQ ID NO:417 CTAGGATGGTGTCCCTCAGC
Прямой SEQ ID NO:418 GAGAGCTGAGGGACACCATC
Обратный SEQ ID NO:419 GTACCCAGCGTGATGGACAG
Прямой SEQ ID NO:420 AGGATGTCGGTGAATTACGC
Обратный SEQ ID NO:421 AAAGGTGGTGTCGAACTTGG
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения SIRT6 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
SEQ ID NO:422 TGTAAGACGCAGTACGTCCG
SEQ ID NO:423 GACTTCAGGGACAAACTGGC
SEQ ID NO:424 ACTGGGAGGACTCCCTGC
SEQ ID NO:425 TGTAAGACGCAGTACGTCCG
SEQ ID NO:426 TGTAAGACGCAGTACGTCCG
SEQ ID NO:427 TAGACTGGGAGGACTCCCTG
SEQ ID NO:428 GAGTCTGGACCATGGAGGAG
Зонд для обнаружения SIRT6 нуклеиновой кислоты, который используется в микропанели, имеет последовательность, как представлено в SEQ ID NO:429 GAAGTGGGGGATCAGTAGAGGCTTGCACTGCCTTTGGGGCTGGAGGGAGA
Другие зонды к SIRT6 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к SIRT6 включают, но не ограничиваясь только ими, кроличье поликлональное анти- SIRT6 к С-концу № каталога 2590 от Cell Signalling Technology; и мышиное моноклональное антитело, выработанное к неполностью рекомбинантному SIRT6 141 а/к ~ 251 а/к № каталога:Н00051548-М01 от abnova.
Пример 22: TJP3
Было обнаружено, что TJP3, белок 3 плотного сочленения (запирающая зона 3) также известен как MGC119546, ZO-3, Z03 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что TJP3 сверхэкспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что TJP3 сверхэкспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что TJP3 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
TJP3 (ZO-3) впервые идентифицирован в виде белка 130 кДа, которые образует иммунопреципитат совместно с ZO-1. Он является представителем MAGUK белков (МЕМБРАНО-ассоциированные гуанилат киназа-подобные гомологи). Эти белки вовлечены в образование и поддержание надмолекулярных комплексов в специфических участках клеточной поверхности, называемых плотным сочленением. Плотные сочленения расположены главным образом в апикальной части латеральных мембран простых эпителиальных клеток, и считаются вовлеченными в барьерные и ограждающие функции.
Клонирование и секвенирование кДНК, кодирующих MAGUK белки, показало, что все они имеют три PDZ домена (PDZ 1-3), один SH3 домен, и один гуанилат киназа-подобный (GUK) домен в указанном это порядке от их NH2 конца (PMID: 10966866). Из этих доменов, PDZ домены связываются с СООН-концевыми областями различных белков, в особенности интегральными мембранными белками, большинство из них оканчивается валином. Следовательно, MAGUK может перекрестно связывать множественные интегральные мембранные белки на цитоплазматической поверхности плазматических мембран для создания специализированных мембранных доменов. Также описано, что ZO-3 ассоциирован с ZO-1, но не с ZO-2, хотя домены, отвечающие за ZO-3/ZO-1 взаимодействия, остаются не идентифицированными. Также показано, что ZO-3 непосредственно связывается с цитоплазматическим доменов окклюдина (Haskins и др. 1998).
Последовательность мРНК, соответствующая TJP3, приведена в ENSEMBL per. № ENST00000262968 и имеет последовательность, как представлено в SEQ ID NO:430


Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000262968 и имеет последовательность, как представлено в SEQ ID NO:431

Праймеры для амплификации последовательности ENST00000262968 могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3.
Примеры пар праймеров для амплификации TJP3 включают:
Прямой SEQ ID NO:432 CCCTCGACCAGGTGGCTGAC (Экзон 1)
Обратный SEQ ID NO:433 CCTCCAGAGATCGCAATGC (Экзон 2)
Прямой SEQ ID NO:434 GTATCTGACGTGGTACCTG (Экзон 2)
Обратный SEQ ID NO:435 GGCAAACGCGGAGGTGGCATT С (Экзон 3)
Прямой SEQ ID NO:436 CGGGGTTTCCATGGAGAATG (Экзон 3)
Обратный SEQ ID NO:437 GCGGGCAGGTGGATCCTCC (Экзон 4)
Прямой SEQ ID NO:438 GCAGGACGTGCAGATGAAGC (Экзон 4)
Обратный SEQ ID NO:439 CCCGAATCTGTAATGTGCTTG (Экзон 5)
Прямой SEQ ID NO:440 GTGGGCTGCAGGAAGGAGATC (Экзон 5)
Обратный SEQ ID NO:441 GAACTGCCCACGATCTCTCAGC (Экзон 6)
Прямой SEQ ID NO:442 GATCGTGGGCAGTTCCTGG (Экзон 6)
Обратный SEQ ID NO:443 GATGTCTGCAGGGGGAGAGG (Экзон 7)
Прямой SEQ ID NO:444 CACCCCGGCATGCTCAGCG (Экзон 7)
Обратный SEQ ID NO:445 CCGAGATGGTTCTGGAATC (Экзон 8)
Прямой SEQ ID NO:446 GAGTCCCCGGCTTCGGCGG (Экзон 8)
Обратный SEQ ID NO:447 CGATCCTCCATGCTCTGACTG (Экзон 9)
Прямой SEQ ID NO:448 GTG CAG GCG GGC AGC CCG (Экзон 10)
Обратный SEQ ID NO:449 GTC CTG CTT CCT CTG CGT С (Экзон 11)
Прямой SEQ ID NO:450 CGAGAGCAGCAGACGCGGCC
Обратный SEQ ID NO:451 GAGGTCAGCGGAGCTGTCG
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения TJP3 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты).
Другие примеры зондов включают:
SEQ ID NO:452
CAGGGACAGTGGCGACAGGACAGCATGCGAACCTATGAACGGGAAGCCCTGAAGAAAAAG
SEQ ID NO:453
GAACAGCACACGGCCACACTGTCCAAGGACCCCCGCCGGGGC
SEQ ID NO:454
ACCAAGATGGCCAACATCACAGTGAAACGTCCCCGGAGGATCCACCTGCCCGCC
SEQ ID NO:455
CAGTGACAGCGACAGCTCGCCATTGGAGGAAGGCGTGACCATGGCTGATGAGAT
SEQ ID NO:456
CGAGTGGTGTTGCGAGAAGCCAGTTTCAAGCGCCCGGTAGTGATCCTGGGACCC
Другие зонды к TJP3 известны в данной области и/или легко могут быть созданы специалистом в данной области техники.
Антитела к включают, но не ограничиваясь только ими, TJP3 коммерчески доступны от, например, № каталога Abnova H00027134-A01, которое представляет собой мышиное поликлональное антитело, выработанное к неполностью рекомбинантному TJP3, имеющее последовательность SEQ ID NO:457
DEPPAPALARSSEPVQADESQSPRDRGRISAHQGAQVDSRHPQGQWRQDSMRTYEREALKKKFMRVHDAESSDEDGYDWGPATDL (NP_055243, 868 а/к ~ 953 а/к); от LifeSpanBiosciences № каталога LS-C 18593, которое представляет собой кроличье поликлональное к синтетическому пептиду, имеющему происхождение из С-конца TJP3 белка (ZO-3) человека; и от LifeSpanBiosciences № каталога LS-C50518, которое представляет собой кроличье поликлональное к синтетическому пептиду, имеющему происхождение их С-конца TJP3 белка (ZO-3) человека.
Пример 23: EFEMP2
Было обнаружено, что экспрессия EFEMP2, также известного как FBLN4, МВР1, и UPH1, подавлена в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что EFEMP2 снижено экспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что EFEMP2 снижено экспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что EFEMP2 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
ENSG00000172638: Только один транскрипт
Последовательность мРНК, соответствующая EFEMP2, представлена в ENSEMBL номер доступа ENST00000307998 и имеет последовательность, как представлено в SEQ ID NO:458.

Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000309953 и имеет последовательность, как представлено в SEQ ID NO:459

Примеры пар праймеров для амплификации EFEMP2 включают приведенные в
Прямой SEQ ID NO:460 TGCTCTTGGGATCAGCTTCT
Обратный SEQ ID NO:461 CCTCAGGGATGGTCAGACAC
Прямой SEQ ID NO:462 TGCCCACCAGGCTATGAG
Обратный SEQ ID NO:463 CAGGCAAGTTATGGCAGTCC
Прямой SEQ ID NO:464 AACTTGCCTGGCTCCTATCA
Обратный SEQ ID NO:465 GTGCTGGCAGTAGCGGTAG
Прямой SEQ ID NO:466 GGCCTAACAACCGCTCCT
Обратный SEQ ID NO:467 CGACACAGGAAGGTCCCATA
Прямой SEQ ID NO:468 TATGGGACCTTCCTGTGTCG
Обратный SEQ ID NO:469 GATGCAGCGGTACTGACAGA
Прямой SEQ ID NO:470 GTCAGTACCGCTGCATCAAC
Обратный SEQ ID NO:471 CGCACCAGACTCACACTCAT
Прямой SEQ ID NO:472 GTGGAGCCCTACATCCAGGT
Обратный SEQ ID NO:473 TCCGAGGTGATGGTCATGTA
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения EFEMP2 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
Зонд, используемый на микропанели, имеет последовательность, как представлено в
SEQ ID NO:474
TTCATCCATTGTGCACCGCTACATGACCATCACCTCGGAGCGGAGCGTGC
SEQ ID NO:475 GAAGAGCCCGACAGCTACAC
SEQ ID NO:476 CAGGCAAGTTATGGCAGTCC
SEQ ID NO:477 CCTGATGGTTACCGCAAGAT
SEQ ID NO:478 GTGAACGAGTGTGACATGGG
SEQ ID NO:479 ATGGCTTCTCCTGCAGTGAT
SEQ ID NO:480 ACGCCTCTGCCAAGACATT
SEQ ID NO:481 ATGTCGAGAGCAGCCTTCAT
Антитела к EFEMP2 включают мышиное античеловеческое EFEMP2 MaxPab® поликлональное антитело, неконъюгированное № каталога Н00030008-В01 к полноразмерному EFEMP2 человека; анти-EFEMP2 моноклональное антитело, неконъюгированное, клон 2С8 № каталога Н00030008-М01к неполному белку, 26 а/к - 443 а/к; и кроличье анти-человеческое EFEMP2 поликлональное антитело, неконъюгированное № каталога ab74873 к синтетическому пептиду, имеющему происхождение из внутреннего участка EFEMP2 человека.
Пример 24: SOCS2
Было обнаружено, что экспрессия SOCS2, также известного как CIS2, Cish2, SOCS-2, SSI-2, SSI2, и STATI2, подавлена в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что SOCS2 снижено экспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что SOCS2 снижено экспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что SOCS2 можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Последовательность мРНК, соответствующая SOCS2, представлена в ENSEMBL номер доступа ENST00000340600 и имеет последовательность, как представлено в SEQ ID NO:482


Старт- и стоп-кодоны выделены жирным шрифтом.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000339428 и имеет последовательность, как представлено в SEQ ID NO:483

Примеры пар праймеров для амплификации SOCS2 включают приведенные в
Прямой SEQ ID NO:484 AGTCACCAAGCCCCTTCC
Обратный SEQ ID NO:485 GCTCTTTCTCCCCAGATCCT
Прямой SEQ ID NO:486 GGGACTGCCTTTACCAACAA
Обратный SEQ ID NO:487 TTTACATAGCTGCATTCGGAGA
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области (например, используя Oligo Calc и/или Primer 3).
Зонды для обнаружения SOCS2 могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
Зонд, используемый на микропанели, имеет последовательность, как представлено в
SEQ ID NO:488
AGTGTGGTTCATCTGATCGACTACTATGTTCAGATGTGCAAGGATAAGCGGACAGGTCCA
SEQ ID NO:489 GACTTTGTCATCCGTCCTCC
SEQ ID NO:490 ACTTGGAAGAATATAAATTCCAGGT
Антитела к SOCS2 включают, но не ограничиваясь только ими, мышиное античеловеческое SOCS2 поликлональное антитело, неконъюгированное № каталога Н00008835-А01 к неполному белку: 99 а/к - 198 а/к; мышиное античеловеческое SOCS2 моноклональное антитело, неконъюгированное, клон ЗЕ7 № каталога Н00008835-М01 к неполному белку: 99 а/к - 198 а/к; кроличье анти-человеческое SOCS2 поликлональное антитело, неконъюгированное № каталога ab74533 к С-концевой части белка.
Пример 25: DCN
Было обнаружено, что экспрессия DCN, также известного как CSCD, DSPG2, PG40, PGII, PGS2, и SLRR1B, подавлена в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия с помощью микропанельного эксперимента, описанного в примере 1. В дальнейших исследованиях с использованием ОТ-ПЦР было показано, что DCN снижено экспрессируется в первичной ткани рака эндометрия по сравнению с нормальной тканью эндометрия, как описано в примере 2. Неожиданно было обнаружено, что DCN снижено экспрессируется в образцах, полученных из маточной жидкости (например, аспиратах) от пациентов, имеющих рак эндометрия, с помощью способа, описанного в примере 4. В примере 5 показано, что DCN можно комбинировать с другими биомаркерами с получением очень хорошей прогнозирующей способности для диагностики рака эндометрия.
Шесть транскриптов из гена ENSG00000011465, но только 4 из них гибридизируется с нашим матричным зондом, включая следующие:
Последовательность мРНК, соответствующая DCN, представлена в ENSEMBL номер доступа ENST00000052754 и имеет последовательность, как представлено в SEQ ID NO:491


Стоп-кодон выделен жирным шрифтом, также как и положение, соответствующее микроматричному зонду.
Соответствующая аминокислотная последовательность приведена в ENSEMBL per. № ENSP00000052754 и имеет последовательность, как представлено в SEQ ID NO:492

Праймеры для амплификации последовательности DCN могут быть созданы с помощью программного обеспечения для создания праймеров, такого как Oligo Calc и/или Primer 3. Примеры пар праймеров для амплификации DCN включают приведенные в
Прямой SEQ ID NO:493 AGCTTTGAGGGCTCCTGTG
Обратный SEQ ID NO:494 GCAAGCAGAAGGAGGATGAT
Прямой SEQ ID NO:495 AATGCCATCTTCGAGTGGTC
Обратный SEQ ID NO:496 TGCAGGTCTAGCAGAGTTGTG
Прямой SEQ ID NO:497 AACCGAAATCAAAGATGGAGA
Обратный SEQ ID NO:498 GTCCAGGTGGGCAGAAGTC
Прямой SEQ ID NO:499 AATGCCATCTTCGAGTGGTC
Обратный SEQ ID NO:500 CTGCTGATTTTGTTGCCATC
Прямой SEQ ID NO:501 TGGCAACAAAATCAGCAGAG
Обратный SEQ ID NO:502 GCCATTGTCAACAGCAGAGA
Прямой SEQ ID NO:503 GGGCTGGCAGAGCATAAGTA
Обратный SEQ ID NO:504 GTCCAGGTGGGCAGAAGTC
Прямой SEQ ID NO:505 AACCGAAATCAAAGATGGAGA
Обратный SEQ ID NO:506 CCAAAGGTGTAAATGCTCCAG
Прямой SEQ ID NO:507 GAGATCACCAAAGTGCGAAA
Обратный SEQ ID NO:508 AAAGCCCCATTTTCAATTCC
Прямой SEQ ID NO:509 AATGCCATCTTCGAGTGGTC
Обратный SEQ ID NO:510 AAAGCCCCATTTTCAATTCC
Другие наборы праймеров легко могут быть созданы специалистом в данной области техники и/или известны в данной области.
Зонды для обнаружения DCN могут быть получены из любых многочисленных источников в зависимости от желательного применения (например, используя вышеописанные праймеры и подходящие реагенты). Другие примеры зондов включают
Зонд, используемый на микропанели, имеет последовательность, как представлено в SEQ ID NO:511
TTTAACTGTGCTATGGAGTAGAAGCAGGAGGTTTTCAACCTAGTCACAGAGCAGC ACC
SEQ ID NO:512 TTCCCGGATTAAAAGGTTCC
SEQ ID NO:513 AAGTGCCAAAGGATCTTCCC
SEQ ID NO:514 CCTGAAGAACCTTCACGTTG
SEQ ID NO:515 TCCTCCTTCCCTTACGGAAT
SEQ ID NO:516 ATGCAGCTAGCCTGAAAGGA
SEQ ID NO:517 CATCCAGGTTGTCTACCTTCA
SEQ ID NO:518 TGAAGAACCTTCACGCATTG
SEQ ID NO:519 TGTCATAGAACTGGGCACCA
SEQ ID NO:520 GTTCTGATTTGGAACTGGGC
Антитела к DCN включают, но не ограничиваясь только ими, мышиное античеловеческое декорин моноклональное антитело, неконъюгированное № каталога ab54728, к рекомбинантному полноразмерному белку; и анти-DCN моноклональное антитело, неконъюгированное. Clone 2B5-G5 № каталога Н00001634-М02, к рекомбинантному полноразмерному белку.
Дополнительные праймеры для биомаркеры согласно изобретению:
АСАА1
SEQ ID NO:521 tcacgggagaagcaggatac
SEQ ID NO:522 cttgctctgggctcttgc
SEQ ID NO:523 ccagagattgcctgattcct
SEQ ID NO:524 cctgcttctcccgtgaaat
SEQ ID NO:525 agctgggggacatctgtgt
SEQ ID NO:526 cactcagaaactgggcgatt
AP1M2
SEQ ID NO:527 cacatcgaagaatgccaatg
SEQ ID NO:528 gctccttgaagtattcgcaga
SEQ ID NO:529 tgctcttcgagctcactgg
SEQ ID NO:530 cacgcactggtggaatttt
SEQ ID NO:531 gttcgctacatcacccagagt
SEQ ID NO:532 gtaaggaagccccgtgttc
CGN
SEQ ID NO:533 gagcttacccgaaaagtgga
SEQ ID NO:534 tctagcttctgccgcttctt
SEQ ID NO:535 ggagatactcgccaggttga
SEQ ID NO:536 ccttaagctcctcctgtgtcc
SEQ ID NO:537 cctctgtgaggaggaaggttag
SEQ ID NO:538 ttagtagaaccagaagaaaccatcac
DDR1
SEQ ID NO:539 tagagagccacccccgta
SEQ ID NO:540 ccatatagtccccactgtaggc
SEQ ID NO:541 ccactctgctccctgtgtc
SEQ ID NO:542 ctggcttctcaggctccata
SEQ ID NO:543 tggggactattaccgtgtgc
SEQ ID NO:544 acgtcactcgcagtcgtg
EPS8L2
SEQ ID NO:545 gcagctcttctccctcaaca
SEQ ID NO:546 cccactttgctgcttctcc
SEQ ID NO:547 caagatgagccccaaggac
SEQ ID NO:548 tgatgacgttggagttggaa
SEQ ID NO:549 caaggatgaggtcctagaggtg
SEQ ID NO:550 gatgttgcagggcacgta
FASTKD1
SEQ ID NO:551 tggaaattctggggtatcgt
SEQ ID NO:552 gcatcctttgttgacagtgc
SEQ ID NO:553 cctgggaatcaaatatcgaaatag
SEQ ID NO:554 ccaaaaattccaaagcaatcc
SEQ ID NO:555 aagaattaacttttctgcatttcca
SEQ ID NO:556 cagaacagacacctcagttggt
GMIP
SEQ ID NO:557 aaccctggccatggagac
SEQ ID NO:558 ccgccacttctcaatctcag
SEQ ID NO:559 cccagcaccacagtaccc
SEQ ID NO:560 ctctgtggagttggaatctcg
SEQ ID NO:561 ctggtggcccatctgttc
SEQ ID NO:562 ggttgttggcagacatcttgt
IKBKE
SEQ ID NO:563 acagttcaagaagtctaggatgagg
SEQ ID NO:564 tggctaaatgactgaaattcacc
SEQ ID NO:565 ggacatccctcctctacctca
SEQ ID NO:566 ggatctcaggcgttccag
SEQ ID NO:567 ctgcctgaggatgagttcct
SEQ ID NO:568 gatgcacaatgccgttctc
P2RX4
SEQ ID NO:569 ccgttacgaccaaggtcaag
SEQ ID NO:570 tgacgaagagggagttttcc
SEQ ID NO:571 tctgtcaagacgtgtgaggtg
SEQ ID NO:572 agtgaagttttctgcagccttta
SEQ ID NO:573 tctcctggctacaatttcagg
SEQ ID NO:574 atgccataggccttgatgag
P4HB
SEQ ID NO:575 gcttcccccaaggaatataca
SEQ ID NO:576 tcttcagccagttcacgatg
SEQ ID NO:577 gcaggggatgatgacgat
SEQ ID NO:578 cgtcttcctccatgtctgg
SEQ ID NO:579 ctggagggcaaaatcaagc
SEQ ID NO:580 ttcttcccaacaagcacctt
PHKG2
SEQ ID NO:581 gcagatccgactttcagatttc
SEQ ID NO:582 ggggtcccacacaactctc
SEQ ID NO:583 ttccagcactgtcaaagacct
SEQ ID NO:584 aaagaaggggtgctgtaggg
SEQ ID NO:585 aggctatggcaaggaggtc
SEQ ID NO:586 tgcgtaacatcaggatctgc
PPFIBP2
SEQ ID NO:587 aggggataaggagtccctca
SEQ ID NO:588 ctggtgtccttccagacaca
SEQ ID NO:589 gaatggaagctaaaggccact
SEQ ID NO:590 atctttcagggccacctgtt
SEQ ID NO:591 aatcttcgagggagtggagtc
SEQ ID NO:592 cagggtgtccccagtgaa
PPP1R16A
SEQ ID NO:593 ccctcccagtgttgtcctt
SEQ ID NO:594 ccccactcccaaggaact
SEQ ID NO:595 gagtgctggacgcctctg
SEQ ID NO:596 ttgaccgccaggagattg
SEQ ID NO:597 atgccctatgacctgtgtgat
SEQ ID NO:598 gatgctgtcctgggtgatg
RASSF7
SEQ ID NO:599 cactagcccaagcaataggc
SEQ ID NO:600 cactcttgtggcagcaactg
SEQ ID NO:601 cagcctggctctggtgag
SEQ ID NO:602 ggagctctcggttcagctc
SEQ ID NO:603 tctgcctccagccagaga
SEQ ID NO:604 ctccaggagttctgcgtcat
RNF183
SEQ ID NO:605 tccagagtagtctgcctgacc
SEQ ID NO:606 catcctcagccacacacg
SEQ ID NO:607 tccagagtagtctgcctgacc
SEQ ID NO:608 tgttgttgaaggggttccag
SEQ ID NO:609 tctgccaccgtgtctacg
SEQ ID NO:610cggaaacactccctcaaaga
SIRT6
SEQ ID NO:611 agctgagggacaccatccta
SEQ ID NO:612 atgtacccagcgtgatggac
SEQ ID NO:613 aggatgtcggtgaattacgc
SEQ ID NO:614 agaccagcctcgccagtt
SEQ ID NO:615 ggtcagccagaacgtgga
SEQ ID NO:616 gtggagctctgccagtttgt
TJP3
SEQ ID NO:617 gtgggcatcttcgtgtcc
SEQ ID NO:618 gaatggcacgtcattcacc
SEQ ID NO:619 atctggacggcggaagat
SEQ ID NO:620 ggtgagggaggtctaggttgt
SEQ ID NO:621 tcatcaagcacattacagattcg
SEQ ID NO:622 ggctagacaccccgttgat
EFEMP2
SEQ ID NO:623 actcgcagggggacttttac
SEQ ID NO:624 catgagggaattcatggtga
SEQ ID NO:625 atcgggatggcttctcct
SEQ ID NO:626 tgatgcagcggtactgaca
SEQ ID NO:627 agtaccgctgcatcaacga
SEQ ID NO:628 cgcaccagactcacactcat
SOCS2
SEQ ID NO:629 ggagctcggtcagacagg
SEQ ID NO:630 ctaatcaagaaagttccttctggtg
SEQ ID NO:631 cagtcaccaagccccttc
SEQ ID NO:632 aagggatggggctctttct
SEQ ID NO:633 ggagctcggtcagacagg
SEQ ID NO:634 gttccttctggtgcctctttt
DCN
SEQ ID NO:635 ggagactttaagaacctgaagaacc
SEQ ID NO:636 cgttccaacttcaccaaagg
SEQ ID NO:637 ctgtcaatgccatcttcgag
SEQ ID NO:638 gatcctttggcactttgtcc
SEQ ID NO:639 caatatcaccagcattcctcaag
SEQ ID NO:640 ctgctgattttgttgccatc
Все публикации и патентные заявки, указанные в описании, свидетельствуют об уровне тех специалистов в области техники, к которой относится настоящее изобретение. Все публикации и патентные заявки включены в настоящую заявку в качестве ссылки в той же степени, как и если 6 каждая отдельная публикация или патентная заявка была специфически и индивидуально включена в качестве ссылки. Только указание публикаций и патентных заявок не обязательно является признанием того, что они являются уровнем техники для настоящего изобретения.
Несмотря на то, что вышеуказанное изобретение было более подробно описано с помощью иллюстраций и примеров для четкого понимания, очевидно, что при практическом осуществлении изобретения могут быть осуществлены различные изменения и модификации, охватываемые объемом приложенной формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ РАКА ТЕЛА МАТКИ | 2014 |
|
RU2558059C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ НАРУШЕНИЙ ПОЧЕК У СОБАК | 2010 |
|
RU2546016C2 |
| СПОСОБ И НАБОР ДЛЯ ДИАГНОСТИКИ ГЛОМЕРУЛОНЕФРИТА У КОШКИ | 2011 |
|
RU2564122C2 |
| ПАНЕЛЬ БИОМАРКЕРОВ И СПОСОБЫ ВЫЯВЛЕНИЯ МИКРОСАТЕЛЛИТНОЙ НЕСТАБИЛЬНОСТИ ПРИ РАЗНЫХ ВИДАХ РАКА | 2019 |
|
RU2795410C2 |
| БИОМАРКЕР | 2009 |
|
RU2573925C2 |
| СПОСОБ ДИАГНОСТИКИ КОЛОРЕКТАЛЬНОГО РАКА ИЗ ОБРАЗЦА КАЛА ЧЕЛОВЕКА С ПОМОЩЬЮ КОЛИЧЕСТВЕННОЙ ПЦР, ПРАЙМЕРОВ И НАБОРА | 2015 |
|
RU2692555C2 |
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С СИРТУИНОМ (SIRT), ПУТЕМ ИНГИБИРОВАНИЯ ПРИРОДНОГО АНТИСМЫСЛОВОГО ТРАНСКРИПТА К СИРТУИНУ (SIRT) | 2011 |
|
RU2693462C2 |
| КОГОРТЫ БИОМАРКЕРОВ МОЧИ, ПРОФИЛЬ ЭКСПРЕССИИ ГЕНОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2668164C2 |
| АНТИТЕЛА АНТИ-PD-L1 И СПОСОБЫ ИХ ДИАГНОСТИЧЕСКОГО ПРИМЕНЕНИЯ | 2015 |
|
RU2715038C2 |
| УЛУЧШЕННЫЙ СПОСОБ СКРИНИНГА, ДИАГНОСТИКИ И/ИЛИ МОНИТОРИНГА КОЛОРЕКТАЛЬНОЙ НЕОПЛАЗИИ НА ПОЗДНЕЙ СТАДИИ, АДЕНОМЫ НА ПОЗДНЕЙ СТАДИИ И/ИЛИ КОЛОРЕКТАЛЬНОГО РАКА | 2020 |
|
RU2834789C2 |
































































































































































































































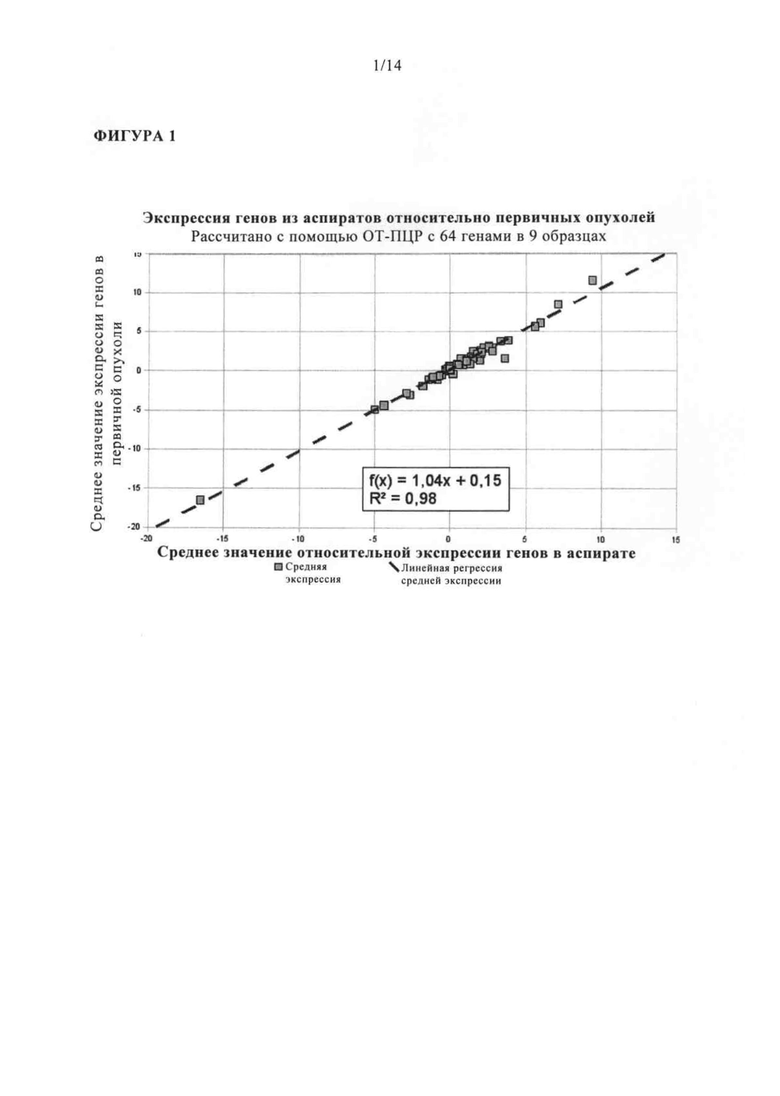
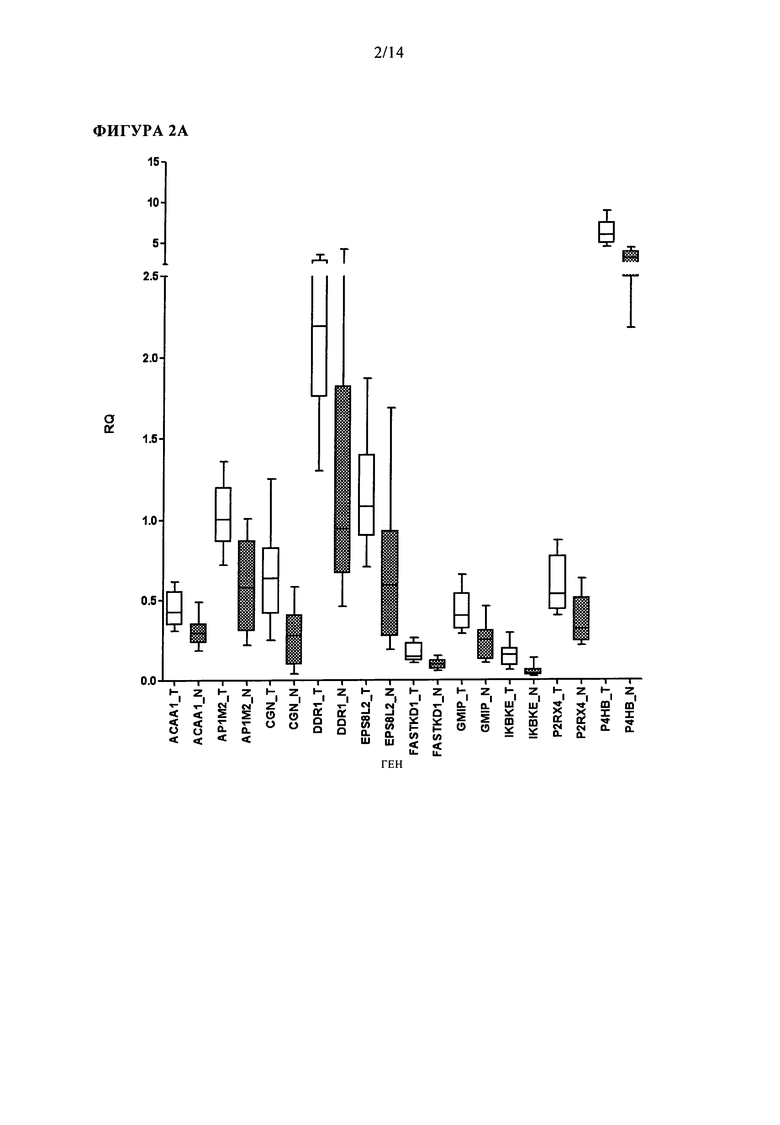
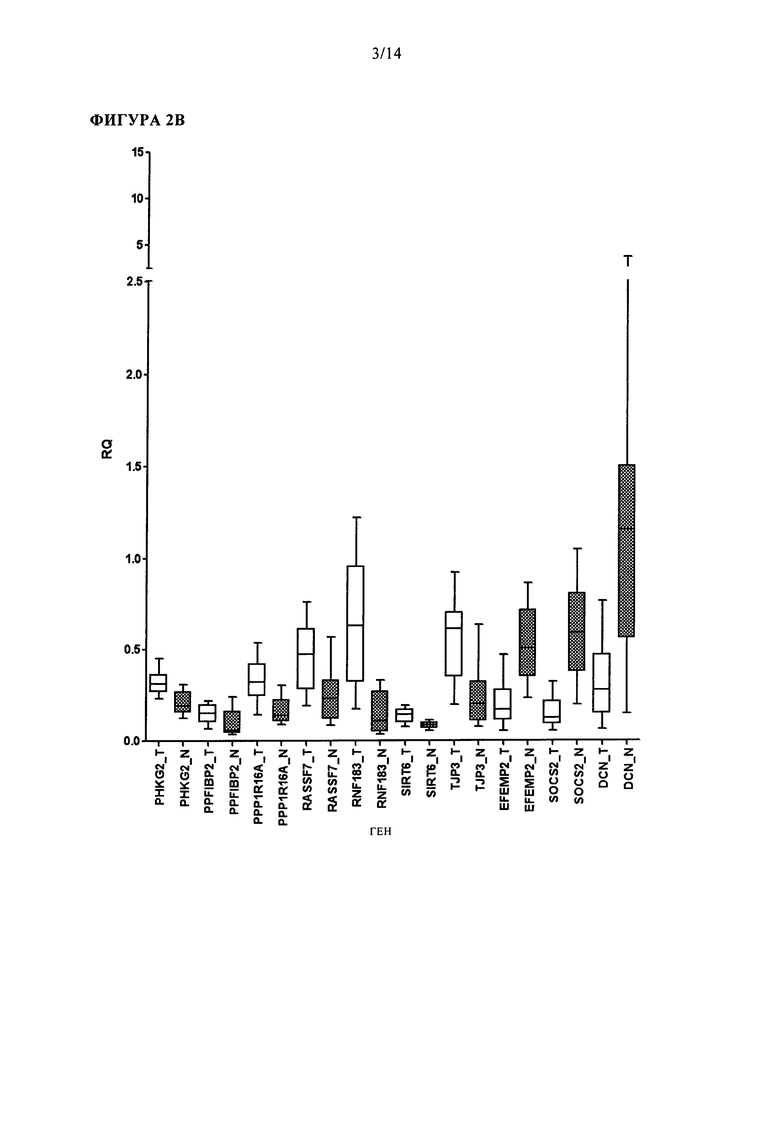
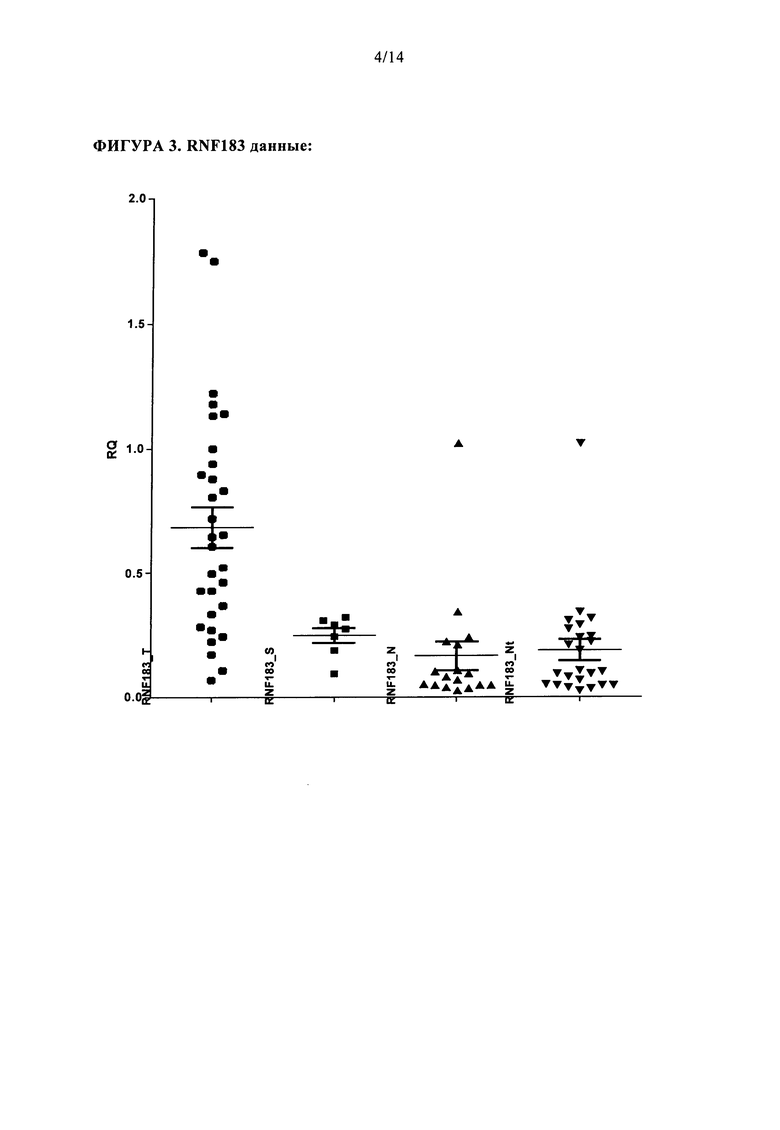
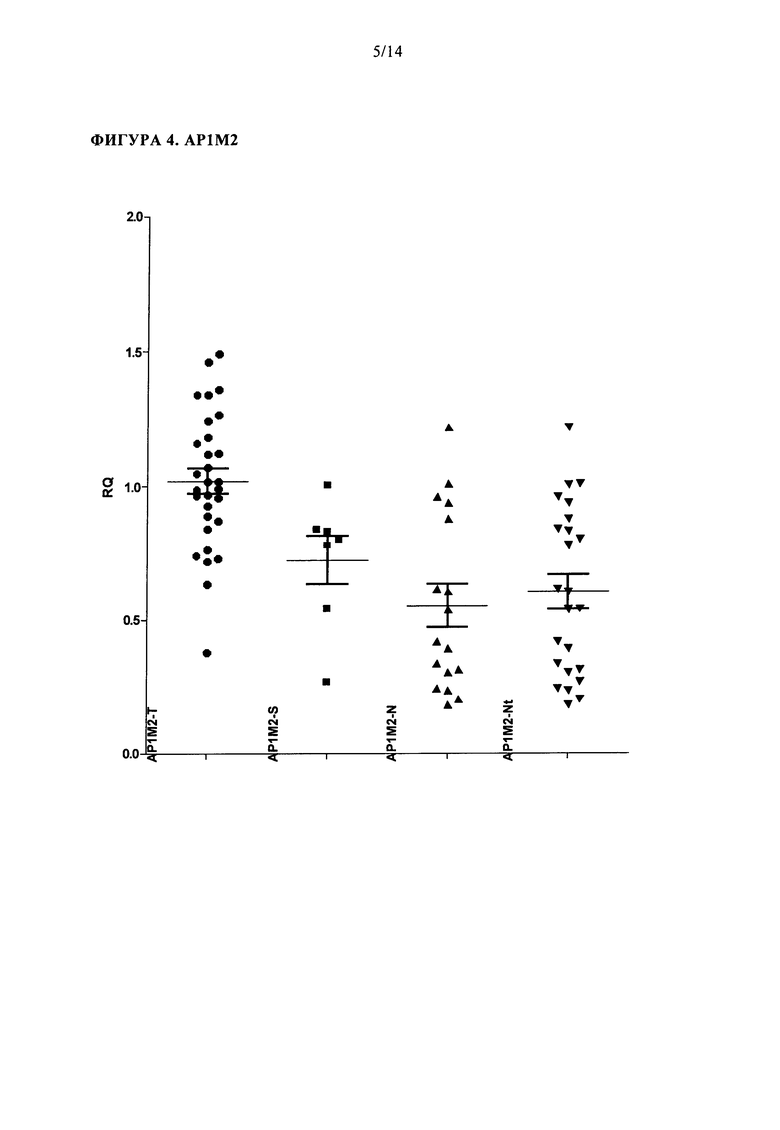
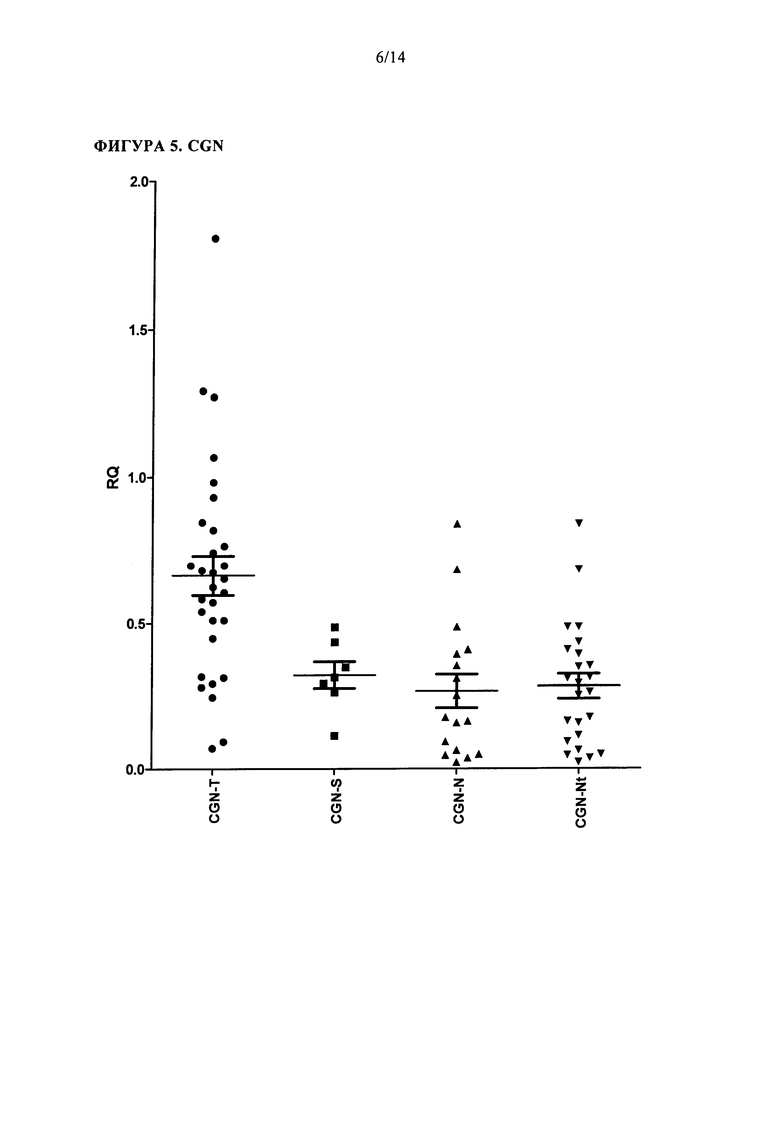
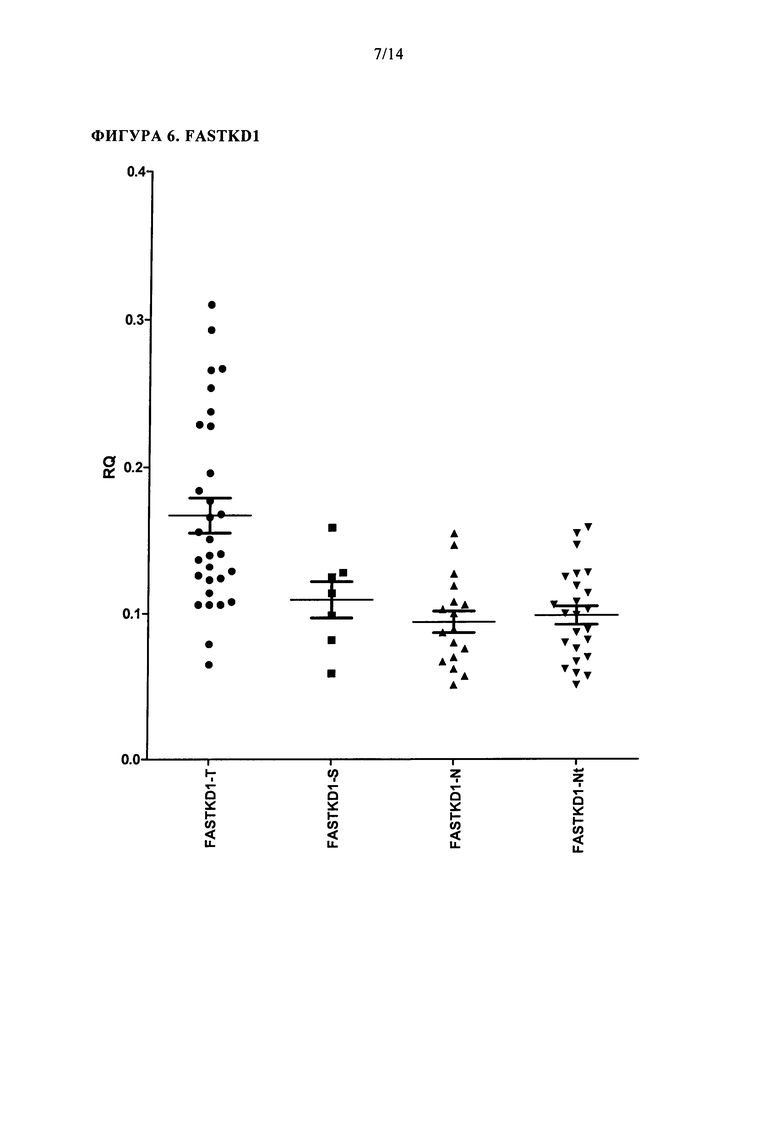
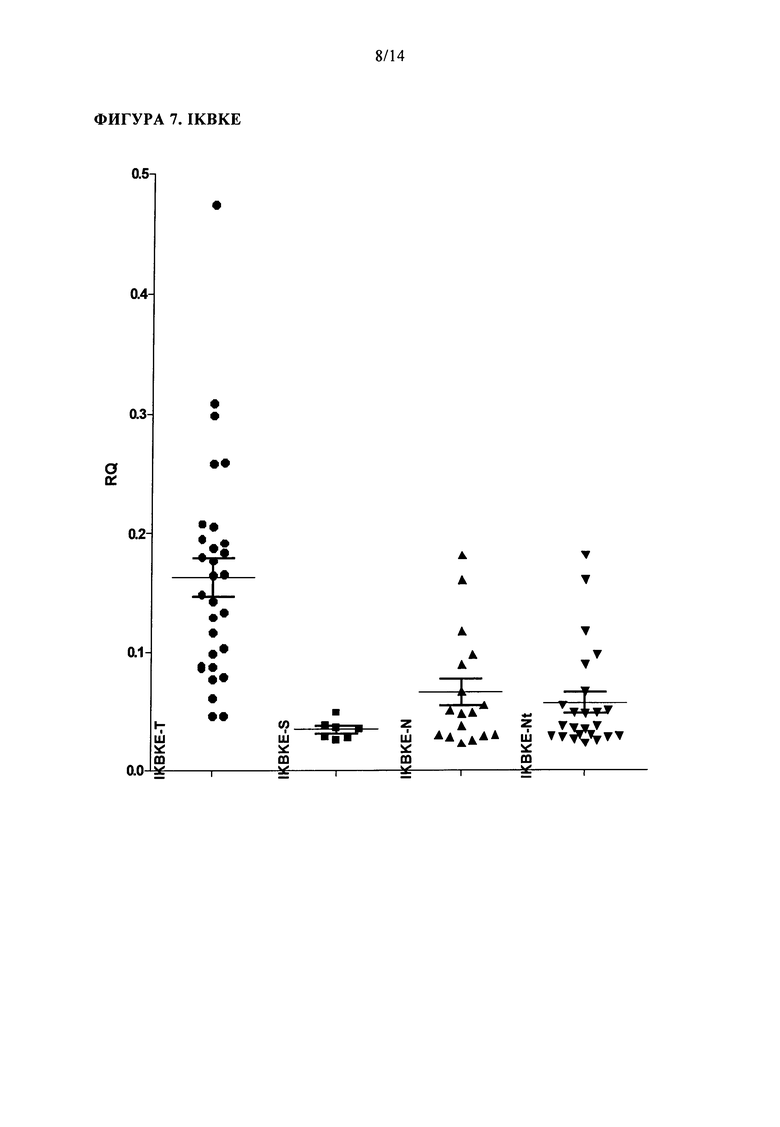
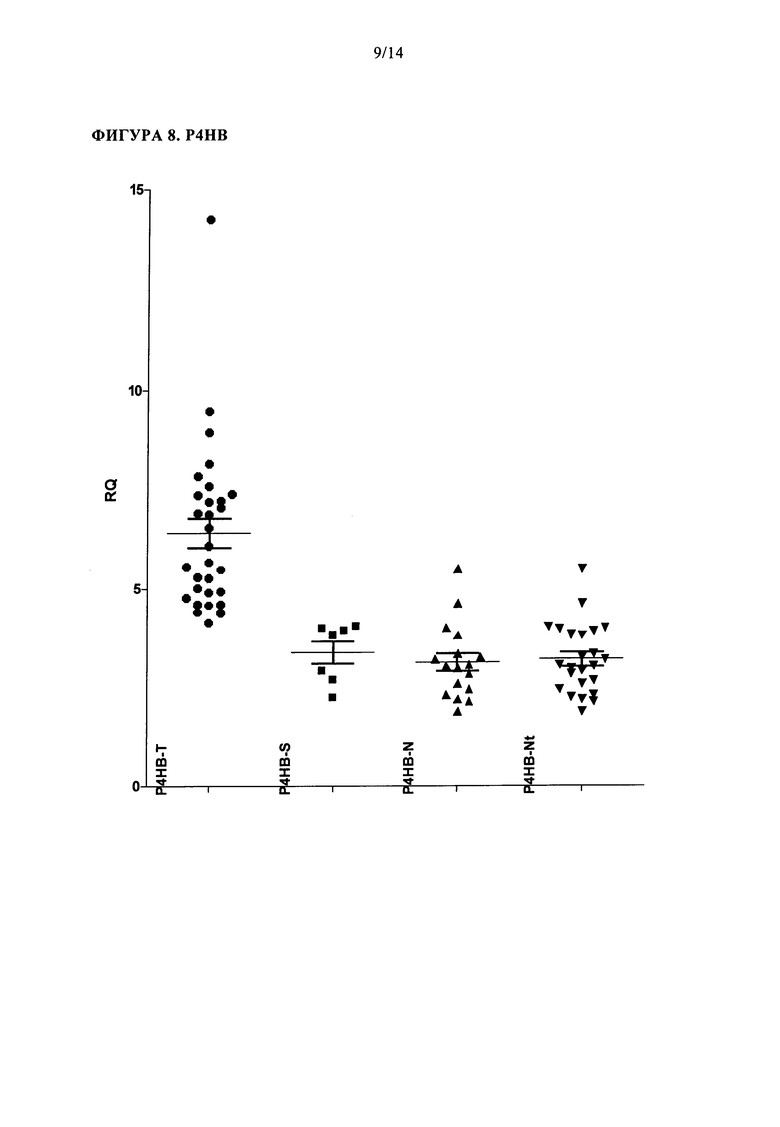

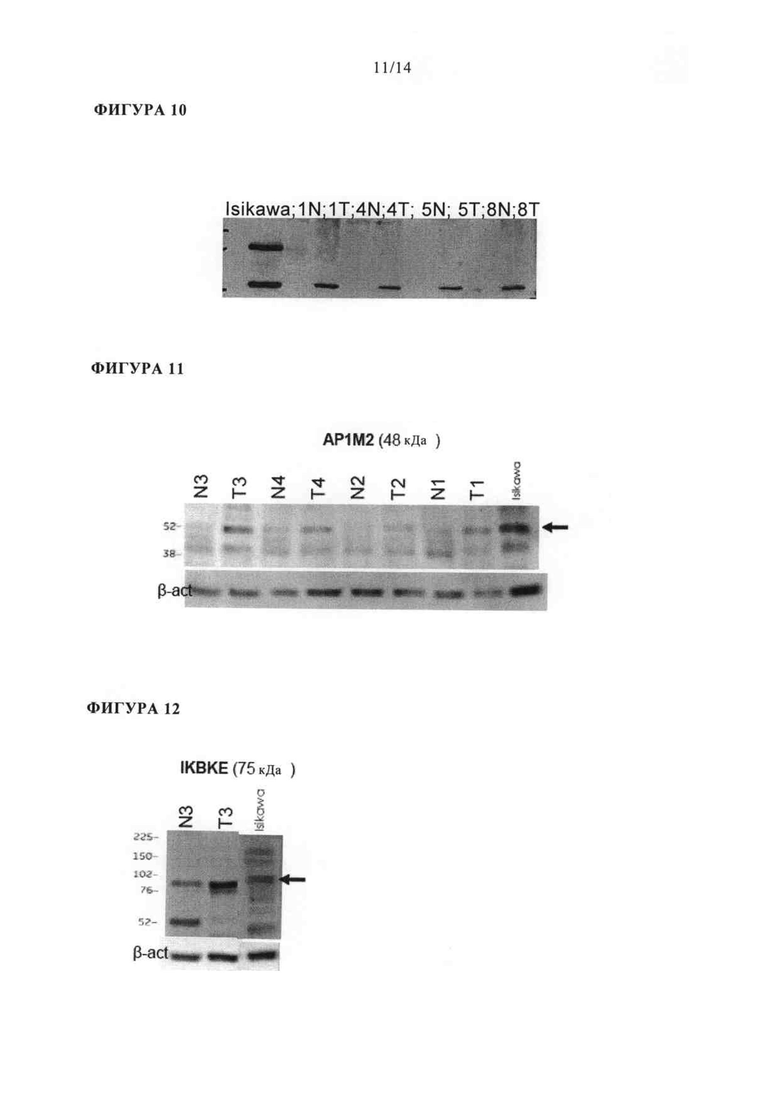
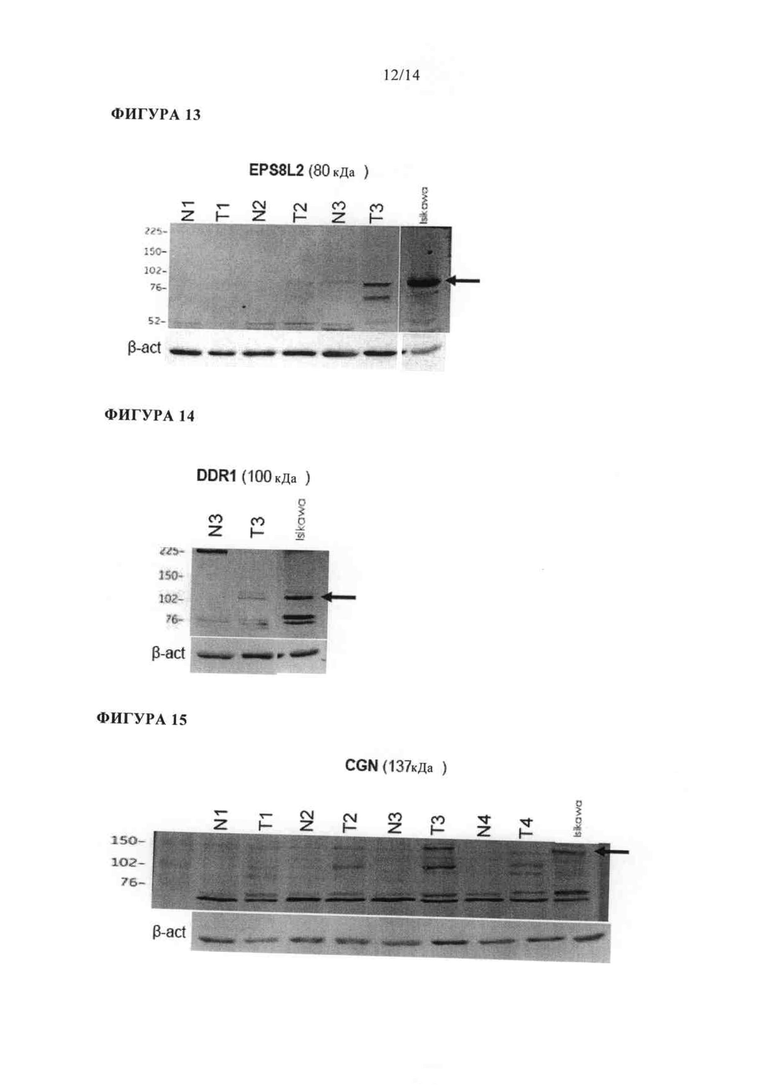
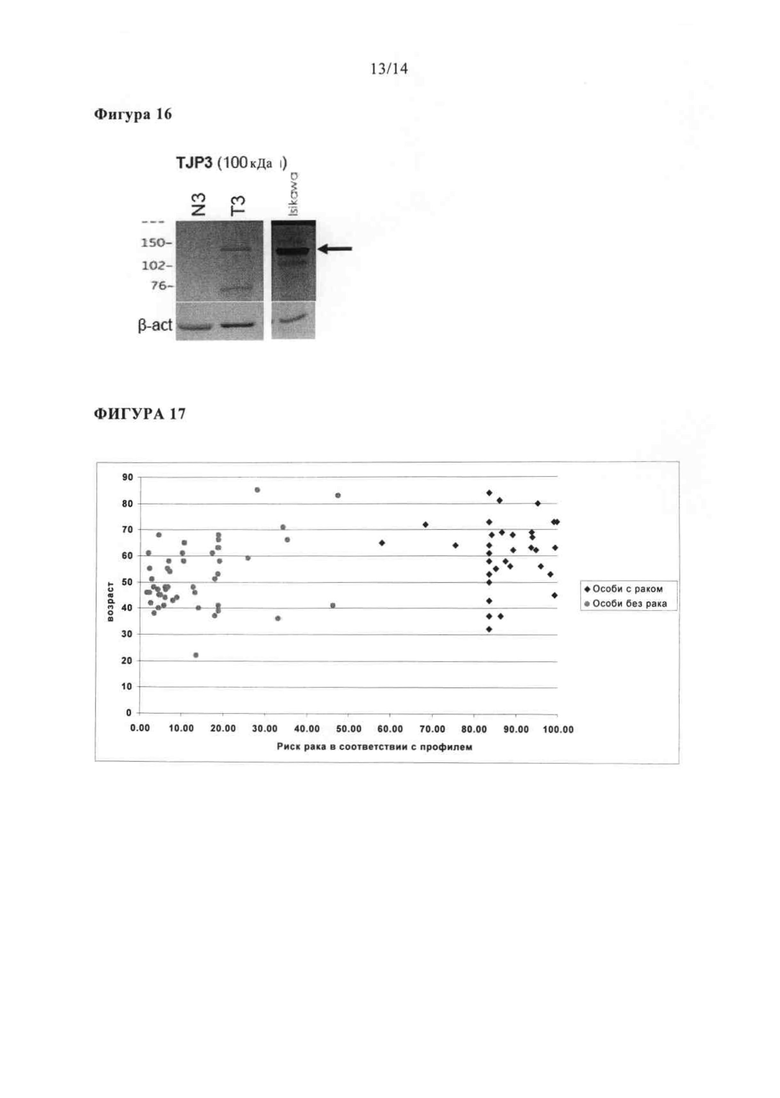
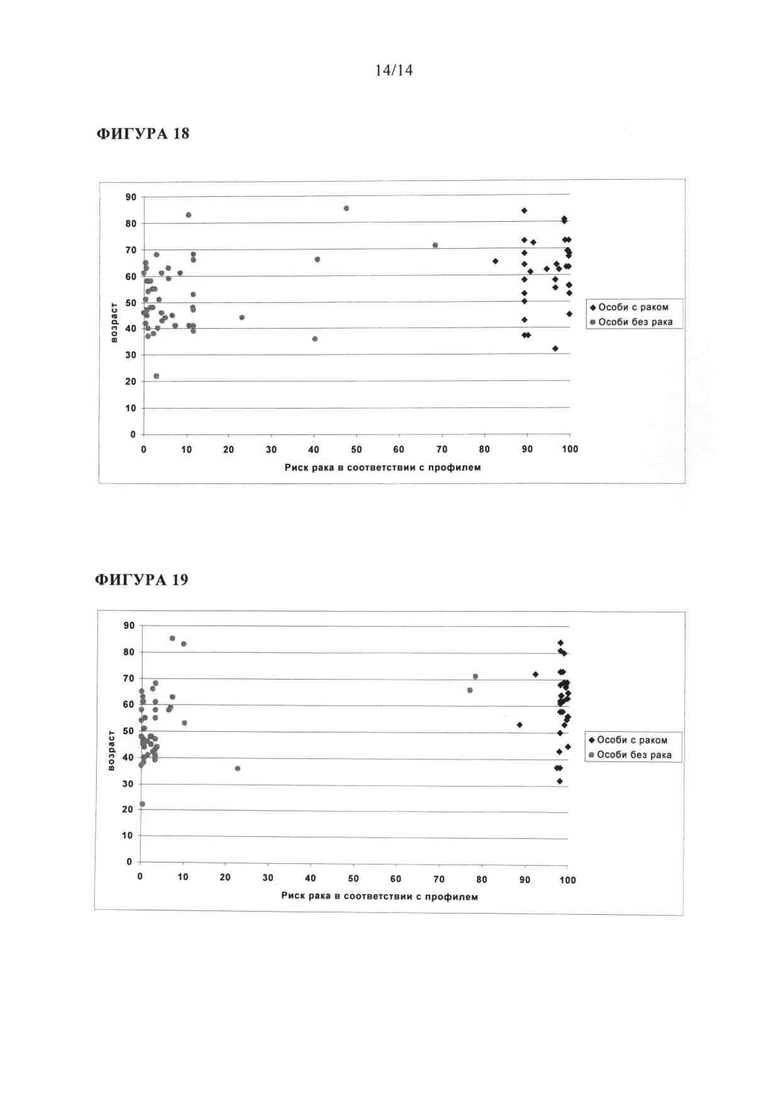
Изобретение относится к области биотехнологии. Описан диагностический способ in vitro диагностики рака эндометрия. Способ предусматривает определение уровня биомаркера P4HB в образце от пациента. Было обнаружено, что дифференциальная экспрессия этого биомаркера в опухолевой ткани первичного рака эндометрия коррелирует с его уровнем экспрессии в образцах маточной жидкости по сравнению с контрольными значениями. Таким образом, этот биомаркер является эффективным, поскольку было обнаружено, что он дифференциально экспрессируется в нескольких различных типах образцов от пораженных особей. Изобретение может быть использовано в медицине. 9 н. и 45 з.п. ф-лы, 20 ил., 12 табл., 25 пр.
1. Диагностический способ in vitro для диагностики рака эндометрия, который включает определение уровня биомаркера Р4НВ в образце от пациента, где повышенный уровень Р4НВ по сравнению с контрольным значением указывает на существование рака эндометрия.
2. Диагностический способ in vitro по п. 1, который дополнительно включает определение уровня одного или нескольких GMIP, IKBKE или EFEMP2.
3. Диагностический способ in vitro по п. 1, который дополнительно включает определение уровня FASTKD1.
4. Диагностический способ in vitro по п. 1, который дополнительно включает определение уровня DDR1.
5. Диагностический способ in vitro по п. 1, который дополнительно включает определение уровня SIRT6.
6. Диагностический способ in vitro по п. 1, который дополнительно включает определение уровня PHKG2.
7. Диагностический способ in vitro по п. 1, который дополнительно включает определение уровня от 1 до 12 биомаркеров, выбранных из АСАА1, АР1М2, EPS8L2, P2RX4, PPFIBP2, PPP1R16A, CGN, RASSF7, RNF183, TJP3, SOCS2 и DCN.
8. Диагностический способ in vitro по п. 1, где указанный пациент имеет фактор риска для рака эндометрия или подвергается скринингу в отношении рака эндометрия.
9. Диагностический способ in vitro по п. 1, где указанный образец от указанного пациента получают от пациента с атипичным маточным кровотечением или где указанный пациент страдает от атипичного маточного кровотечения.
10. Диагностический способ in vitro по п. 1, где указанный образец от указанного пациента получают от пациента, имеющего эндометрий с повышенной толщиной, или где указанный пациент имеет эндометрий с повышенной толщиной.
11. Диагностический способ in vitro по п. 1, где указанный образец от указанного пациента получают от пре-менопаузного, пери-менопаузного или пост-менопаузного пациента или где указанный пациент представляет собой пре-менопаузного, пери-менопаузного или пост-менопаузного пациента.
12. Диагностический способ in vitro по п. 11, где указанный пациент является пре-менопаузным.
13. Диагностический способ in vitro по п. 11, где указанный пациент является пери-менопаузным.
14. Диагностический способ in vitro по п. 11, где указанный пациент является пост-менопаузным.
15. Диагностический способ in vitro по п. 1, где указанный образец выбирают из образца ткани, крови и/или сыворотки и маточной жидкости.
16. Диагностический способ in vitro по п. 15, где указанный образец представляет собой образец маточной жидкости.
17. Диагностический способ in vitro по п. 16, где указанный образец маточной жидкости получают путем аспирации.
18. Диагностический способ in vitro по п. 1, где определяют уровень экспрессии белка биомаркера(ов).
19. Диагностический способ in vitro по п. 18, где уровень биомаркеров определяют с помощью антитела.
20. Диагностический способ in vitro по п. 1, где определяют уровень мРНК, соответствующей биомаркеру.
21. Диагностический способ in vitro по п. 1, где уровень биомаркера(ов) определяют с помощью ОТ-ПЦР.
22. Диагностический способ in vitro по п. 1, где определяют от 2 до 20 маркеров.
23. Диагностический способ in vitro по п. 1, где определяют комбинацию следующих маркеров: Р4НВ, EFEMP2, SIRT6, GMIP, FASTKD1 и DDR1.
24. Диагностический способ in vitro по п. 1, где определяют комбинацию следующих маркеров: Р4НВ, EFEMP2, SIRT6, GMIP, FASTKD1 и PHKG2.
25. Диагностический способ in vitro по п. 1, где определяют комбинацию следующих маркеров: Р4НВ, EFEMP2, SIRT6, АСАА1, АР1М2, EPS8L2, IKBKE, P2RX4, PPFIBP2 и PPP1R16A.
26. Диагностический способ in vitro по п. 1, где определяют один или несколько дополнительных биомаркеров.
27. Диагностический способ in vitro по п. 26, где указанные один или несколько дополнительных биомаркеров выбирают из дифференциальных диагностических биомаркеров, прогностических биомаркеров, биомаркеров, пригодных для обнаружения рака эндометрия, биомаркеров для классификации рака эндометрия и вспомогательных биомаркеров для обнаружения рака эндометрия.
28. Диагностический способ in vitro по п. 26, где один или несколько дополнительных биомаркеров выбирают из дифференциальных диагностических биомаркеров.
29. Диагностический способ in vitro по п. 26, где один или несколько вспомогательных биомаркеров выбирают из прогностических маркеров.
30. Диагностический способ in vitro по п. 26, где один или несколько вспомогательных биомаркеров выбирают из маркеров классификации рака эндометрия.
31. Диагностический способ in vitro по п. 1, включающий определение уровня биомаркера Р4НВ в образце аспирата маточной жидкости от пациента, который имеет симптом или фактор риска для рака эндометрия, и где биомаркер Р4НВ дифференциально экспрессируется в раке эндометрия по сравнению с контрольными значениями, характерными для особей, не страдающих от рака эндометрия, где уровень биомаркера Р4НВ повышен в образце аспирата эндометрия у пациента, который имеет повышенную вероятность наличия рака эндометрия.
32. Диагностический способ in vitro по п. 1, включающий определение уровня РНК, экспрессирующей биомаркер Р4НВ с помощью количественного ПЦР в образце аспирата маточной жидкости от пациента, который имеет симптом или фактор риска для рака эндометрия, и где повышенный уровень биомаркера Р4НВ по сравнению с контрольными значениями указывает на наличие рака эндометрия.
33. Диагностический способ in vitro по п. 32, где уровень РНК, экспрессирующих 2-8 биомаркеров, выбирается из Р4НВ и одного или более EFEMP2, GMIP, IKBKE, DDR1, FASTKD1, SIRT6 и PKHG2.
34. Диагностический способ in vitro по п. 32, где уровень РНК, экспрессирующих 2-8 биомаркеров, выбирается из Р4НВ и одного или более GMIP, IKBKE, DDR1, FASTKD1, SIRT6, PKHG2 и SOCS2.
35. Диагностический способ in vitro по п. 1, где указанное определение уровня включает контактирование указанных биомаркеров Р4НВ с праймерами и реагентами, способными амплифицировать специфически указанные биомаркеры, и определение уровня указанных амплифицированных биомаркеров с зондом или зондами, которые гибридизируются с указанным амплифицированным биомаркером.
36. Диагностический способ in vitro по п. 35, где указанный зонд гибридизируется специфически с указанным амплифицированным биомаркером.
37. Диагностический способ in vitro по любому из пп. 1-36, где определяют Р4НВ и EFEMP2.
38. Диагностический способ in vitro по любому из пп. 1-36, где определяют Р4НВ и IKBKE.
39. Диагностический способ in vitro по любому из пп. 1-36, где определяют Р4НВ и GMIP.
40. Диагностический способ in vitro по любому из пп. 1-36, где определяют EFEMP2 и Р4НВ.
41. Диагностический способ in vitro по любому из пп. 1-36, где определяют Р4НВ, GMIP и IKBKE.
42. Диагностический способ in vitro по любому из пп. 1-36, где определяют комбинацию маркеров, где указанная комбинация включает IKBKE и Р4НВ; Р4НВ и SOCS2; GMIP и Р4НВ; GMIP, SOCS2 и Р4НВ; GMIP, IKBKE и Р4НВ; IKBKE, Р4НВ и SOCS2; GMIP, IKBKE, Р4НВ и SOCS2; GMIP, SOCS2, Р4НВ и EPS8L2; GMIP, IKBKE, Р4НВ и EPS8L2; IKBKE, Р4НВ, SOCS2 и EPS8L2; GMIP, IKBKE, P4HB, SOCS2 и DDR1; GMIP, IKBKE, P4HB, SOCS2, EPS8L2 и PPP1R16A; GMIP, IKBKE, P4HB, SOCS2, PHKG2 и RASSF7; GMIP, IKBKE, P4HB, SOCS2, EPS8L2 и DDR1; GMIP, IKBKE, P4HB, SOCS2, EPS8L2, PPP1R16A и DDR1; DDR1, EPS8L2, GMIP, IKBKE, P2RX4, P4HB, PHKG2, PPP1R16A, RASSF7, SIRT6, TJP3 и SOCS2; или DDR1, EPS8L2, GMIP, IKBKE, P2RX4, P4HB, PHKG2, PPP1R16A, RASSF7, SIRT6, TJP3, RNF183 и SOCS2.
43. Диагностический способ in vitro по любому из пп. 1-36, где определяют комбинацию маркеров, где указанная комбинация включает GMIP, IKBKE, Р4НВ, SOCS2 и FASTKD1; GMIP, IKBKE, Р4НВ, SOCS2 и DDR1; GMIP, IKBKE, P4HB, SOCS2 и PHKG2; GMIP, IKBKE, P4HB, SOCS2 и SIRT6; GMIP, IKBKE, P4HB, SOCS2 и ACAA1; GMIP, IKBKE, P4HB, SOCS2 и EFEMP2; GMIP, IKBKE, P4HB, SOCS2 и EPS8L2; GMIP, IKBKE, P4HB, SOCS2 и P2RX4; GMIP, IKBKE, P4HB, SOCS2 и PPFIBP2; GMIP, IKBKE, P4HB, SOCS2 и PPP1R16A; GMIP, IKBKE, P4HB, SOCS2, ACAA1 и FASTKD1; GMIP, IKBKE, P4HB, SOCS2, PHKG2 и FASTKD1; GMIP, IKBKE, P4HB, SOCS2, SIRT6 и FASTKD1; ACAA1, AP1M2, EPS8L2, IKBKE, P2RX4, P4HB, PPFIBP2, PPP1R16A, SIRT6 и EFEMP2; GMIP, IKBKE, P4HB и EFEMP2; DDR1, FASTKD1, PHKG2, SIRT6, SOCS2, GMIP, IKBKE, P4HB и EFEMP2; DDR1, FASTKD1, PHKG2, SIRT6, GMIP, IKBKE, P4HB и EFEMP2; или P4HB, EFEMP2, IKBKE, GMIP и FASTKD1.
44. Диагностический способ in vitro по любому из пп. 1-36, где определяют комбинацию маркеров, где указанная комбинация включает GMIP, IKBKE, Р4НВ, EFEMP2 и FASTKD1; GMIP, IKBKE, Р4НВ, EFEMP2 и DDR 1; GMIP, IKBKE, P4HB, EFEMP2 и PHKG2; GMIP, IKBKE, P4HB, EFEMP2 и SIRT6; GMIP, IKBKE, P4HB, EFEMP2 и ACAA1; GMIP, IKBKE, P4HB, SOCS2 и EFEMP2; GMIP, IKBKE, P4HB, EFEMP2 и EPS8L2; GMIP, IKBKE, P4HB, EFEMP2 и P2RX4; GMIP, IKBKE, P4HB, EFEMP2 и PPFIBP2; GMIP, IKBKE, P4HB, EFEMP2 и PPP1R16A; GMIP, IKBKE, P4HB, EFEMP2, ACAA1 и FASTKD1; GMIP, IKBKE, P4HB, EFEMP2, PHKG2 и FASTKD1; или GMIP, IKBKE, P4HB, EFEMP2, SIRT6 и FASTKD1.
45. Диагностический способ in vitro по любому из пп. 1-36, который включает обеспечение образца маточной жидкости, полученного от пациента с помощью устройства Пайпиля или шприца, где пациент имеет фактор риска или симптом рака эндометрия; контактирование указанного образца с агентом, способным предохранять, предотвращать или ослаблять деградацию РНК в указанном образце маточной жидкости; определение в указанном образце уровня экспрессии мРНК, соответствующего маркера Р4НВ и одного или нескольких эндогенных генов, используя количественную ПЦР; нормализацию уровня экспрессии указанного биомаркера Р4НВ с одним или несколькими эндогенными генами; сравнение нормализованного уровня биомаркера Р4НВ с контрольным значением, где дифференциальная экспрессия биомаркера Р4НВ указывает на рак эндометрия или повышенную вероятность рака эндометрия.
46. Диагностический способ in vitro по п. 45, где указанные один или несколько эндогенных генов выбирают из POLR2A, В2М, PFN1, HMBS, G6PD и PABPN1.
47. Применение нуклеиновой кислоты, которой является мРНК Р4НВ, кДНК или ее комплемент, для диагностики рака эндометрия.
48. Применение нуклеиновой кислоты, которой являются праймеры для Р4НВ, для диагностики рака эндометрия.
49. Применение нуклеиновой кислоты, которой является зонд для Р4НВ, для диагностики рака эндометрия.
50. Набор, включающий зонды, которые охарактеризованы в п. 49, для применения для диагностики рака эндометрия.
51. Набор, включающий праймеры, которые охарактеризованы в п. 48, для применения для диагностики рака эндометрия.
52. Применение антитела к Р4НВ для диагностики рака эндометрия.
53. Набор, содержащий антитело, которое охарактеризовано в п. 52, для диагностики рака эндометрия.
54. Набор для диагностики рака эндометрия, включающий устройство для отбора образца жидкости из матки и зонды или праймеры для оценки уровней биомаркеров Р4НВ.
| DOMENYUK V.P | |||
| et al., "Identification of new DNA markers of endometrial cancer in patients from the Ukrainian population", Exp Oncol | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| US 2004063120 A1, 01.04.2004 | |||
| US 2006271309 A1, 30.11.2006 | |||
| US 2009075299 A1, 19.03.2009 | |||
| WO 2009021338 A1, 19.02.2009 | |||
| FIEGL H | |||
| et al., "Methylated DNA collected by tampons--a new tool to | |||
Авторы
Даты
2016-09-10—Публикация
2010-07-23—Подача