Область изобретения
Настоящее изобретение относится к стимулирующим регенерацию тканей средствам, которые вводят в ткань, отличную от ткани, нуждающейся в регенерации.
Уровень техники
Регенеративная медицина нацелена на функциональную и структурную регенерацию поврежденных органов с использованием клеток или тканей, культивированных и обработанных ex vivo. Например, культивируемый слой кожи получают взятием клеток кожи от пациента или другого индивидуума, культивированием их вне организма и преобразованием их в форму слоя, а затем трансплантируют на поврежденную кожу. В регенеративной медицине для получения клеток, используемых для лечения, требуются культивирование или пролиферация клеток ex vivo. Поскольку методика культивирования может вызывать повреждение клеток (старение, генез опухолей или контаминация бактериями, вирусами и т.д.), для поддерживания безопасности необходимо, чтобы получение проводили на оборудовании, сертифицированном как удовлетворяющее стандартам Good Manufacturing Practice (GMP). Ожидается, что это приведет к проблеме высокой стоимости лечения.
Между тем, живой организм имеет механизмы регенерации для репарации повреждений в случае повреждения органов. Однако известно, что, если поврежденная область является крупной, они заполняются нефункциональными рубцовыми тканями. Заживление повреждения такими рубцовыми тканями становится ингибирующим фактором для регенерации нервов при инфаркте головного мозга или повреждении спинного мозга, становится этиологическим фактором для разрыва сердца при инфаркте миокарда, или приводит к образованию келоидного рубца в хирургических ранах или при обширных ожогах, тем самым приводя к в высокой степени плохому прогнозу и качеству жизни (QOL) в косметическом аспекте. Если бы можно было активировать собственные регенерационные механизмы организма для репарации повреждения ткани, то можно ожидать, что возможно индуцировать регенерацию поврежденных тканей (органов) с функциональными тканями, а не рубцевание.
Известно, что костный мозг содержит мезенхимальные стволовые клетки, которые могут дифференцироваться в кость, хрящ, жировую ткань и другие, а также гемопоэтические стволовые клетки, которые дифференцируются в лейкоциты, эритроциты и т.п. Недавно было установлено, что костный мозг также содержит плюрипотентные стволовые клетки, которые могут дифференцироваться в эпителиальные и нервные клетки.
Документы уровня техники
Патентные документы
Патентный документ 1: WO 2008/053892
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Задачи, решаемые изобретением
Задачей настоящего изобретения является разработка нового терапевтического способа, посредством которого активируется механизм физиологической регенерации/репарации для индукции заживления поврежденных тканей, тем самым осуществляя лечение трудноизлечимых заболеваний, таких как обширное изъязвление кожи, трудноизлечимые переломы костей и инфаркт головного мозга, которые трудно лечить общепринятыми способами терапии.
Средства для решения задач
Эффект HMGB-1 и S100A8 при привлечении происходящих из костного мозга клеток на язву кожи в процессе заживления язвы кожи оценивали с использованием мышей. Результат продемонстрировал, что введение HMGB-1 или S100A8 в венозную кровь, которая была нецелевой областью, отдаленной от изъязвления кожи, приводило к привлечению происходящих из костного мозга клеток к язве кожи. Затем оценивали эффект внутривенного введения HMGB-1 и S100A8 на стимуляцию заживления язвы кожи. В результате, заживление язвы кожи успешно стимулировалось HMGB-1 и S100A8, вводимыми в кровеносный сосуд, который был нецелевой областью, отдаленной от области изъязвления. Кроме того, оценка их эффекта стимуляции заживления язвы кожи без рубцов показала, что внутривенное введение HMGB-1 может стимулировать раннее закрытие и заживление без рубцов язвы кожи путем усиления дальнейшего привлечения происходящих из костного мозга клеток в область изъязвления.
Более того, тестировали модель инфаркта головного мозга у мышей на присутствие происходящих из костного мозга клеток в их головном мозге. В результате в головном мозге мышей, которым после индукции инфаркта головного мозга внутривенно вводили HMGB-1, были выявлены происходящие из костного мозга клетки, экспрессирующие маркеры нервных клеток. Затем оценка эффекта уменьшения инфаркта головного мозга продемонстрировала значительное улучшение у мышей после инфаркта головного мозга, которым внутривенно вводили HMGB-1, по сравнению с контрольными мышами. Кроме того, оценка улучшения уровня выживания после инфаркта головного мозга показала, что внутривенное введение HMGB-1 приводило к увеличению уровня выживаемости мышей.
Дальнейшую оценку проводили с использованием мышей для установления того, были ли плюрипотентные стволовые клетки костного мозга из областей, отличных от области перелома костей, вовлечены в процесс заживления перелома. Результат показал, что происходящие из костного мозга клетки мигрировали из областей, отдаленных от поврежденной области, в область перелома кости для репарации поврежденной ткани.
Более того, для оценки активности внутривенно вводимого HMGB-1 при привлечении мезенхимальных стволовых клеток костного мозга в поврежденную область проводили тест с использованием модели перелома костей на мышах. Было выявлено, что внутривенное введение HMGB-1 приводило к накоплению мезенхимальных стволовых клеток, привлеченных в кровь в области перелома кости.
Исходя из этих открытий, настоящая заявка относится к следующим изобретениям:
[1] средство, стимулирующее регенерацию тканей, содержащее любое из:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
где средство вводят в ткань, отличную от ткани, нуждающейся в регенерации.
[2] средство согласно [1], которое вводят парентерально;
[3] средство согласно [2], которое вводят путем инъекции;
[4] средство согласно [1], которое вводят внутрисосудистым путем, внутримышечно, подкожно, внутрикожным путем или внутрибрюшинно;
[5] средство согласно любому из [1]-[4], где экстракт клеток или тканей получают способом, включающим стадию погружения клетки или ткани в растворитель;
[6] средство согласно любому из [1]-[4], где связывающую гепарин фракцию экстракта клеток или тканей получают способом, включающим стадии:
(a) погружения клетки или ткани в растворитель;
(b) контактирования иммобилизованного гепарина с экстрактом, полученным на стадии (a); и
(c) элюирования связывающей гепарин фракции с иммобилизованного гепарина;
[7] средство согласно любому из [1]-[6] для применения в стимуляции регенерации нервной, костной или кожной ткани;
[8] набор для стимуляции регенерации ткани, который содержит композицию, содержащую любое из:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
где композицию вводят в ткань, отличную от ткани, нуждающейся в регенерации.
[9] набор согласно [8], который вводят парентерально;
[10] набор согласно [9], который вводят путем инъекции;
[11] набор согласно [8], который вводят внутрисосудистым путем, внутримышечно, подкожно, внутрикожным путем или внутрибрюшинно;
[12] набор согласно любому из [8]-[11], который используют для стимуляции регенерации нервной, костной или кожной ткани;
[13] способ стимуляции регенерации ткани, который включает стадию введения эффективного количества композиции в ткань, отличную от ткани, нуждающейся в регенерации, где композиция содержит любое из:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
[14] способ согласно [13], где введение представляет собой парентеральное введение;
[15] способ согласно [14], где введение представляет собой инъекцию;
[16] способ согласно [13], где введение представляет собой внутрисосудистое, внутримышечное, подкожное, внутрикожное или внутрибрюшинное введение;
[17] способ согласно любому из [13]-[16], который стимулирует регенерацию нервной, костной или кожной ткани;
[18] применение композиции для продуцирования средства, стимулирующего регенерацию тканей, где композиция содержит любое из:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
где средство вводят в ткань, отличную от ткани, нуждающейся в регенерации;
[19] применение согласно [18], где средство вводят парентерально;
[20] применение согласно [19], где введение представляет собой инъекцию;
[21] применение согласно [18], где средство вводят внутрисосудистым путем, внутримышечно, подкожно, внутрикожным путем или внутрибрюшинно;
[22] применение согласно любому из [18]-[21], где средство представляет собой средство для стимуляции регенерации нервной, костной или кожной ткани;
[23] композиция для применения в способе стимуляции регенерации тканей, содержащая любое из:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
где композицию вводят в ткань, отличную от ткани, нуждающейся в регенерации;
[24] композиция согласно [23], которую вводят парентерально;
[25] композиция согласно [24], которую вводят путем инъекции;
[26] композиция согласно [23], которую вводят внутрисосудистым путем, внутримышечно, подкожно, внутрикожным путем или внутрибрюшинно; и
[27] композиция согласно любому из [23]-[26], где способ стимуляции регенерации ткани представляет собой способ стимуляции регенерации нервной, костной или кожной ткани.
Эффекты изобретения
Клеточные факторы роста, такие как HGF, EGF, VEGF и FGF известные как фармацевтические средства для регенерации поврежденных тканей. Их используют, ожидая, что они будут стимулировать рост клеток при введении непосредственно в поврежденную область и окружающие ее ткани.
HMGB1, HMGB2, HMGB3, S100A8 и S100A9 обладают активностью привлечения плюрипотентных стволовых клеток костного мозга. Плюрипотентные стволовые клетки костного мозга могут дифференцироваться в эпителиальные и нервные клетки, а также в мезенхимальные клетки. В случае обширного повреждения тканей, ожидается, что если бы можно было привлечь плюрипотентные стволовые клетки костного мозга в поврежденную область через кровоток, они будут стимулировать функциональную регенерацию/репарацию поврежденных тканей.
Настоящее изобретение относится к способам стимуляции репарации поврежденных тканей, в которых HMGB1, HMGB2, HMGB3, S100A8 и S100A9, которые являются факторами для привлечения плюрипотентных стволовых клеток костного мозга, вводят в область, отдаленную от поврежденной области, путем внутривенного введения или сходным с ним, тем самым привлекая плюрипотентные стволовые клетки костного мозга в периферическую кровь. Например, при лечении заболевания глубоко расположенного органа, такого как инфаркт головного мозга, трудно вводить лекарственное средство непосредственно в поврежденную область (головной мозг). С другой стороны, в настоящем изобретении, такое лечение можно проводить путем внутривенного введения, которое широко используют в общей медицинской практике. Таким образом, возможно вводить лекарственное средство в любой концентрации и с любой частотой безопасным и простым образом. Этот эффект является лучшим по сравнению с общепринятыми способами терапии.
Между тем, недавно разработанный способ на основе клеток костного мозга, который, как известно, является эффективным для лечения инфаркта головного мозга, вовлекает сбор клеток из костного мозга пациента и повторное введение клеток в кровоток. Этот способ неизбежно ассоциирован с тяжелой инвазией, поскольку клетки костного мозга необходимо аспирировать ширококанальной иглой, помещенной в костный мозг, который расположен глубоко в организме. Напротив, настоящее изобретение позволяет привлечение клеток костного мозга непосредственно в кровоток путем внутривенного введения средства, и таким образом, не вовлекает тяжелую инвазию, даже когда средство часто вводят пациентам с инфарктом головного мозга.
Плюрипотентные стволовые клетки костного мозга обладают потенциальной способностью дифференцироваться в различные типы клеток, такие как мезенхимальные клетки, эпителиальные клетки и нервные клетки. После миграции в поврежденную область они могут дифференцироваться, в зависимости среды ниши, окружающей поврежденную область, а затем индуцировать репарацию ткани. В регенеративной медицине и клеточной терапии плюрипотентные стволовые клетки костного мозга, которые являются редкими клетками, размножаются путем культивирования ex vivo перед применением для лечения. Однако это требует надлежащего контроля безопасности, поскольку, в отличие от общепринятых фармацевтических средств, существует риск повреждения клеток (перерождение в злокачественные и контаминация бактериями, вирусами и т.д.), которое может возникнуть в процессе культивирования. В настоящем изобретении плюрипотентные стволовые клетки костного мозга привлекаются в периферический кровоток путем введения HMGB1, HMGB2, HMGB3, S100A8 и/или S100A9. Это является в высокой степени безопасным терапевтическим способом, поскольку клетки не удаляются из организма для искусственного манипулирования.
Краткое описание чертежей
На фиг.1 представлен набор фотографий, демонстрирующих процесс очистки HMGB1. HEK293 трансфицировали экспрессирующим вектором, содержащим GST-метку, 6XHis-метку и последовательность расщепления HRV3C на N-конце HMGB1. Культуральный супернатант наносили на никелевую колонку и связывающуюся фракцию элюировали имидазолом. Связавшуюся с никелевой колонкой фракцию обрабатывали HRV3C для отщепления GST-метки и 6XHis-метки от HMGB1. Затем фракции позволяли связаться с аффинной колонкой с гепарином и элюировали хлоридом натрия. Связавшуюся с гепарином фракцию наносили на Q-колонку и элюировали хлоридом натрия. Для детекции степени очистки на каждой стадии очистки каждую связавшуюся с колонкой фракцию подвергали SDS-PAGE, а затем окрашиванию Кумасси.
На фиг.2 представлен набор фотографий, демонстрирующих сигналы GFP в коже и тонких срезах кожи после закрытия язвы. Кожную язву создавали на спине мышей с трансплантированным костным мозгом с GFP, и мышам внутривенно вводили HMGB1 или S100A8. По сравнению с контролем, в коже мышей, которым внутривенно вводили HMGB1 или S100A8, было выявлено много GFP-положительных происходящих из костного мозга клеток.
На фиг.3 представлен график, демонстрирующий площадь язвы кожи, измеренную с течением времени. Язву кожи создавали на спине мышей и мышам внутривенно вводили HMGB1 или S100A8. Через 3 суток после создания язвы наблюдали эффект уменьшения язвы кожи в группе введения HMGB1 по сравнению с контрольной группой. Через 7 суток после создания язвы в группе введения S100A8 наблюдали эффект уменьшения язвы кожи по сравнению с контрольной группой (вертикальная ось, [площадь язвы]/[площадь язвы во время создания]×100; горизонтальная ось, сутки после создания язвы).
На фиг.4 представлен набор фотографий, демонстрирующий результаты окрашивания гематоксилином-эозином (HE) и окрашивания трихромной краской Массона (MT) тонких срезов кожи после закрытия язвы кожи. Язву кожи создавали на спине мышей, и мышам внутривенно вводили HMGB1. У контрольных мышей наблюдали аномальное увеличение коллагеновых волокон, в то время как такое аномальное увеличение коллагеновых волокон было снижено у мышей, которым внутривенно вводили HMGB1.
На фиг.5 представлен набор фотографий, демонстрирующих результат детекции клеток, экспрессирующих нестин (маркер нервных стволовых клеток) и β III тубулин (маркер нейронов). У мышей с трансплантированным костным мозгом с GFP создавали инфаркт головного мозга, а затем проводили им внутривенное введение HMGB1. После введения получали срезы головного мозга и подвергали их иммуногистохимии. На левой фотографии стрелки указывают на GFP-положительные, нестин-положительные клетки. На правой панели стрелки указывают на GFP-положительные, β III тубулин-положительные клетки. Было продемонстрировано, что происходящие из костного мозга клетки экспрессируют маркеры нейронов.
На фиг.6 представлен набор фотографий, демонстрирующих результат детекции областей инфаркта. Получали модель заболевания на мышах для инфаркта головного мозга, а затем им внутривенно вводили HMGB1. После введения получали тонкие срезы головного мозга и подвергали их окрашиванию Ниссля. В случае введения PBS (контроль), в коре наблюдали некротические ткани. В случае введения HMGB1 в коре не было выявлено некротической ткани.
На фиг.7 представлен набор графиков, демонстрирующий уровни выживания в течение 7 суток после создания инфаркта головного мозга. Получали модель заболевания на мышах для инфаркта головного мозга (путем 45-минутной или 60-минутной ишемии), а затем проводили им внутривенное введение HMGB1. Было показано, что введение HMGB1 увеличивает уровень выживаемости в случае как ишемии в течение 45 минут, так и ишемии в течение 60 минут.
На фиг.8 представлен набор фотографий, демонстрирующий, что, когда мышь с трансплантированным костным мозгом с GFP соединяли через кожу с мышью дикого типа, клетки костного мозга мигрировали из химерной мыши с костным мозгом с GFP в область перелома кости правой задней конечности мыши дикого типа и дифференцировались в остеобласты. Мышь с костным мозгом с GFP соединяли через кожу с мышью дикого типа. Затем у мыши дикого типа создавали перелом кости. После заживления перелома кости, было выявлено, что некоторые экспрессирующие остеокальцин остеобласты являются положительными по GFP клетками. Это указывает на то, что в процессе заживления перелома кости, клетки, происходящие из костного мозга, отдаленные от поврежденной области, мигрируют в область перелома кости, а затем дифференцируются в остеобласты для физиологического заживления повреждения.
На фиг.9 представлены фотографии, демонстрирующие накопление флуоресценции GFP, наблюдаемой в трансплантате кожи после трансплантации кожи на спину мышей с трансплантированным костным мозгом с GFP. Сверху слева представлено изображение области трансплантации кожи, наблюдаемое невооруженным глазом, сверху по центру представлено изображение окрашенной HE ткани кожи реципиента вблизи границы между пересаженной кожей и кожей реципиента (показано стрелкой), и сверху справа представлено изображение окрашенной HE ткани трансплантата кожи. Более того, на изображении снизу слева представлено накопление флуоресценции GFP в трансплантированной коже, снизу по центру представлено увеличенное изображение области трансплантации кожи, и снизу справа представлено увеличенное изображение, демонстрирующее накопление флуоресценции GFP на том же увеличенном изображении трансплантата кожи.
На фиг.10 представлен набор фотографий, демонстрирующих происходящие из костного мозга эпидермальные клетки и происходящие из костного мозга дермальные фибробласты, которые накапливались в трансплантированной коже на спине мышей с трансплантированным костным мозгом с GFP. В первом ряду сверху представлены изображения кожи области трансплантации при низком увеличении (× 100), в среднем ряду представлены увеличенные изображения того же самого, демонстрирующие границу эпидермис/дермис при высоком увеличении (× 200), и в нижнем ряду представлены далее увеличенные изображения того же самого, демонстрирующие волосяной фолликул при высоком увеличении (× 200). В крайней левой колонке представлено окрашивание DAPI (ядерное окрашивание), во второй слева колонке представлены флуоресцентные изображения GFP соответствующих областей первого ряда. На третьей колонке слева представлены изображения, демонстрирующие иммуноокрашивание по кератинину 5 (K5). В четвертой колонке слева представлены объединенные изображения для каждого из этих типов флуоресценции. Наблюдали большие количества положительных по GFP эпидермальных клеток и дермальных фибробластов.
На фиг.11 представлен набор фотографий, демонстрирующих результаты анализа способности к миграции/активности происходящих из костного мозга мезенхимальных стволовых клеток в экстракте кожи с использованием камеры Бойдена. На верхнем левом изображении представлены мезенхимальные стволовые клетки, прикрепленные к силиконовой мембране, на нижней стороне камеры, мигрировавшие из верхнего отделения камеры Бойдена в отделение кожного экстракта (нижнее отделение камеры) через тонкие поры в силиконовой мембране, которые окрашены синим пигментом. Окрашенные изображения представлены непосредственно после культивирования (0 ч), после 12 часов (12 ч) и после 24 часов (24 ч) (четыре лунки для каждого случая) сверху. Верхнее правое изображение представляет собой изображение для 0 ч при высоком увеличении. Снизу слева представлено изображение для 12 ч при высоком увеличении. Снизу справа представлено изображение для 24 ч при высоком увеличении.
На фиг.12 представлена фотография, демонстрирующая результат способности к миграции/активности происходящих из костного мозга мезенхимальных стволовых клеток, исследованных в препаратах очищенных фракций кожных экстрактов с использованием камеры Бойдена, и соответствие результату SDS-PAGE-электрофореза для каждого препарата очищенной фракции. Слева, дорожка 1 (М.М.): маркер молекулярной массы; дорожка 2 (C.E.): неочищенный экстракт кожи, дорожка 3 (H.A.): связывающаяся с аффинной колонкой с гепарином фракция (полуочищенная фракция); и дорожки 4-13 (A.E.): связывающиеся с анионообменной колонкой фракции (конечная очищенная фракция), элюированные различными концентрациями NaCl, все из которых были окрашены серебром после электрофореза. Кроме того, в конечной очищенной фракции No. 4, которая продемонстрировала наиболее сильную активность миграции происходящих из костного мозга мезенхимальных стволовых клеток, окрашенные полосы в окрашенном серебром электрофоретическом геле (дорожка 7) вырезали, а затем подвергали масс-спектрометрии и анализу баз данных. Результат показал, что полоса, указанная стрелкой, представляет собой HMGB1.
На фиг.13 представлена фотография, демонстрирующая результат оценки активности HMGB1 в отношении индукции миграции происходящих из костного мозга мезенхимальных стволовых клеток с использованием камеры Бойдена. Два изображения сверху представляют собой окрашенные изображения происходящих из костного мозга мезенхимальных стволовых клеток, которые мигрировали в экстракт кожи. Средние два изображения представляют собой окрашенные изображения происходящих из костного мозга мезенхимальных стволовых клеток, которые мигрировали в очищенный препарат HMGB1. Снизу представлены окрашенные изображения происходящих из костного мозга мезенхимальных стволовых клеток, которые мигрировали в очищенный препарат HMGB1, который использовали для центральных изображений, но который был нейтрализован добавлением поликлонального антитела против HMGB1 (активность миграции была практически полностью утрачена).
На фиг.14 представлен набор фотографий, демонстрирующий активность HMGB1 в отношении мобилизации происходящих из костного мозга мезенхимальных стволовых клеток in vivo. Фракция HMGB1 (конечная очищенная фракция No. 4) продемонстрировала активность мобилизации, приблизительно в три раза превышающую активность мобилизации контроля (конечная очищенная фракция No.1).
На фиг.15 представлена фотография, демонстрирующая клетки, мобилизованные in vivo фракцией HMGB1 (конечная очищенная фракция No. 4) при высоком увеличении.
На фиг.16 представлен набор фотографий, демонстрирующих изображения сразу после начала культивирования клеток, которые мигрировали в силиконовую трубку. Слева представлено изображение светового поля с мигрирующими клетками, инокулированными в среду, и справа представлено их GFP-флуоресцентное изображение в темном поле.
На фиг.17 представлен набор фотографий, демонстрирующих изображения через 24 часа после начала культивирования клеток, которые мигрировали в силиконовую трубку. На левом изображении представлено изображение в световом поле подобных фибробластам клеток и подобных эпителиальным клеток, которые пролиферировали и прикрепились на пластмассовую чашку для культивирования, и на правом изображении представлено их GFP-флуоресцентное изображение в темном поле.
На фиг.18 представлен набор фотографий, демонстрирующих изображения через 2 недели после начала культивирования клеток, которые мигрировали в силиконовую трубку. На фотографиях слева и справа представлено одно и то же поле зрения, причем слева представлены изображения для светового поля, в то время как справа представлены изображения через флуоресцентный фильтр (флуоресценция GFP выявлена в B и D и флуоресценция кератина 5 выявлена в F). Подобную волосу линейную форму (указана треугольником (стрелка)) наблюдают слева от положительной по костному мозгу с GFP популяции клеток, образующих круговые колонии на пластмассовой чашке для культивирования. F указывает на то, что происходящие из костного мозга клетки морфологически трансформированы в подобную волосу форму, и, кроме того, экспрессируют кератин 5 (указано треугольником (стрелкой)).
На фиг.19 представлен набор фотографий, демонстрирующих семейство HMGB в экстракте кожи новорожденных мышей, детектированное способом вестерн-блоттинга.
На фиг.20 представлена иллюстрация карты экспрессирующего вектора для семейства HMGB в клетках млекопитающих, которое имеет, ниже промотора, энхансер цитомегаловируса и промотор β-актина курицы, для синтеза большого количества мРНК, кодируемой кДНК (комплементарной ДНК) семейства HMGB.
На фиг.21 представлен набор фотографий, демонстрирующих результат вестерн-блоттинга очищенных рекомбинантных слитых белков Flag-метка - семейство HMGB, экспрессироанных в клетках HEK293.
На фиг.22 представлен набор графиков, демонстрирующих активность рекомбинантных HMGB1/HMGB2/HMGB3 в отношении индукции миграции мезенхимальных клеток костного мозга в камере Бойдена. Все рекомбинантные белки продемонстрировали более высокую активность индукции миграции по сравнению с контрольными группами.
На фиг.23 представлен набор графиков, демонстрирующих результат лечения на моделях лечения кожных язв с использованием семейства HMGB. Все из HMGB1, HMGB2 и HMGB3 продемонстрировали значительные эффекты в отношении снижения площади язвы по сравнению с контрольными группами.
На фиг.24 представлена фотография, демонстрирующая оценку активности HMGB1 человека и экстракта кожи человека в отношении индукции миграции происходящих из костного мозга мезенхимальных стволовых клеток, проведенную с использованием камеры Бойена.
На фиг.25 представлен набор фотографий, демонстрирующий оценку активности веществ, привлекающих мезенхимальные клетки костного мозга, в экстрактах сердца, головного мозга и кожи мыши, проведенную с использованием камеры Бойдена после очистки веществ с помощью колонки с гепарином.
На фиг.26 представлен набор фотографий, демонстрирующих оценку активности экстракта HEK293 и экстракта HeLa в отношении индукции миграции мезенхимальных стволовых клеток костного мозга человека, проведенную с использованием камеры Бойдена. Обе культивированные клеточные линии продемонстрировали активность миграции в отношении мезенхимальных стволовых клеток костного мозга человека.
На фиг.27A представлена фотография, на которой показана мышь, фиксированная к стереотаксическому устройству для головного мозга с разрезом головы по средней линии скальпелем, с последующей трепанацией с использованием бура. На фиг.27B представлена фотография, на которой показан головной мозг, к которому применяют отрицательное давление с использованием шприца для аспирирования части ткани головного мозга. На фиг.27C представлена фотография после инъекции 5 мкл очищенной на колонке с гепарином фракции экстракта кожи, растворенного в фибриновом адгезивном составе (фибриноген) в головной мозг, и последующей инъекции 5 мкл состава фибринового клея (тромбин). На фиг.27D и фиг.27E представлены фотографии модели повреждения головного мозга, полученные через 2 недели после лечения. Более высокое накопление положительных по GFP клеток наблюдали в группе лечения с использованием очищенной на колонке с гепарином фракции экстракта кожи, на E, по сравнению с контролем, на D. На фиг.27F и фиг.27G представлены фотографии модели повреждения головного мозга, полученные через 6 недель после лечения. Более высокое накопление GFP-положительных клеток наблюдали в группе лечения с использованием очищенной на колонке с гепарином фракции экстракта кожи, на G, по сравнению с контролем, на F.
На фиг.28 представлена диаграмма, демонстрирующая введение экстракта кожи (SE) мыши через хвостовую вену и взятие периферической крови.
На фиг.29 представлена диаграмма, демонстрирующая введение HMGB1 мыши через хвостовую вену и взятие периферической крови.
На фиг.30 представлен набор диаграмм, демонстрирующих фракционирование проточной цитометрией фракций мононуклеарных клеток периферической крови мыши, которые были получены через 12 часов после введения экстракта кожи (SE), а затем флуоресцентно мечены антителом против PDGFRα мыши и антителом против CD44 мыши. На верхних трех панелях показана группа введения PBS в качестве отрицательного контроля (n=3), и на нижних трех панелях показана группа введения экстракта кожи (SE) (n=3). Вертикальные и горизонтальные оси указывают на уровни экспрессии CD44 и PDGFRα, соответственно. Область, заключенная в рамку синего цвета соответствует популяции CD44-положительных, PDGFRα-положительных клеток, которая была увеличена в экстракте коже группы введения (SE) по сравнению с группой PBS.
На фиг.31 представлен набор диаграмм, демонстрирующих фракционирование проточной цитометрии фракций мононуклеарных клеток периферической крови мыши, которые были получены через 12 часов после введения HMGB1, а затем флуоресцентно мечены антителом против PDGFRα мыши и антителом против CD44 мыши. На верхней панели представлены мыши, которым вводили PBS, в качестве отрицательного контроля, и на правой панели представлены мыши, которым вводили HMGB1. Вертикальные и горизонтальные оси указывают на уровни экспрессии CD44 и PDGFRα, соответственно. Область, заключенная в рамку синего цвета соответствует популяции CD44-положительных, PDGFRα-положительных клеток, которая была увеличена у мышей, которым вводили HMGB1, по сравнению с мышами, которым вводили PBS.
На фиг.32A представлена диаграмма результата проточной цитометрии, которая демонстрирует присутствие клеток, имеющих CD44 и PDGFRα. Введение HMGB1 увеличивало обе популяции из PDGFRα- и CD44-двойных положительных клеток, и PDGFRα-положительных CD44-отрицательных клеток в периферической крови. На фиг.32B и 32C представлены результаты сравнения между группами введения PBS и HMGB1 на присутствие PDGFRα- и CD44-двойных положительных клеток, и PDGFRα-положительных CD44-отрицательных клеток в периферической крови, соответственно. Обе популяции клеток были статистически значимо увеличены в группе введения HMGB1.
На фиг.33 в наборе фотографий представлено накопление флуоресценции GFP в пересаженной коже, наблюдаемое после трансплантации кожи на спину мышей с трансплантированным костным мозгом с GFP. На левой фотографии (A) представлено окрашивание ядер с помощью DAPI. На средней фотографии (B) представлена зеленая флуоресценция положительных по GFP происходящих из костного мозга клеток, накопленных в области трансплантата кожи. На правой фотографии (C) представлено объединенное изображение фотографий (A) и (B). Происходящие из костного мозга клетки реконструируют ткани кожи.
На фиг.34 представлена фотография, на которой показан результат анализа измерения активности миграции происходящих из костного мозга мезенхимальных стволовых клеток в экстрактах кожи с использованием камеры Бойдена. На этом изображении показаны окрашенные синим цветом мезенхимальные стволовые клетки костного мозга, мигрировавшие из верхнего отделения камеры Бойдена через микропоры размером 8 мкм мембранного фильтра из поликарбоната в нижнее отделение, содержащее экстракты кожи, и прикрепившиеся к мембране со стороны нижнего отделения. В нижние отделения были помещены экстракты кожи, взятой от мышей в возрасте двух дней или шести недель.
На фиг.35 представлен набор фотографий детекции посредством вестерн-блоттинга белков S100A8 и S100A9 в экстрактах кожи.
На фиг.36 представлена фотография, на которой показано элюирование гепарин-связывающего белка кожных экстрактов, элюированного с аффинной колонки с гепарином посредством градиента концентрации NaCl. Белки в каждой фракции разделяли посредством SDS-PAGE и подвергали детекции окрашиванием серебром.
На фиг.37 представлена фотография, на которой показаны результаты анализа по измерению активности в отношении миграции происходящих из костного мозга мезенхимальных стволовых клеток в экстракты кожи с использованием камеры Бойдена. На изображении показаны окрашенные синим цветом мезенхимальные стволовые клетки костного мозга, которые мигрировали из верхнего отделения камеры Бойдена через микропоры фильтра к каждой гепарин-связывающей фракции в экстрактах (в нижнее отделение) и прикреплялись к мембране со стороны нижнего отделения.
На фиг.38 представлен набор фотографий, на которых показана детекция вестерн-блоттингом белков S100A8 и S100A9 в каждой гепарин-связывающей фракции экстрактов кожи.
На фиг.39 представлена схема экспрессирующего вектора для S100A8 или S100A9.
На фиг.40 представлена фотография, на которой показан результат анализа активности миграции происходящих из костного мозга мезенхимальных стволовых клеток в экстракты кожи с использованием камеры Бойдена. На этих изображениях показаны окрашенные синим цветом мезенхимальные стволовые клетки костного мозга, которые мигрировали из верхнего отделения камеры Бойдена через микропоры фильтра в нижнее отделение, содержащее рекомбинантный GST-S100A8, GST-S100A9 или экстракты кожи, и прикреплялись к мембране со стороны нижнего отделения.
На фиг.41A представлен набор диаграмм, демонстрирующих результат FACS для CD44, PDGFRα и PDGFRα во фракции CD45-отрицательных клеток в периферической крови через 12 часов после введения GST-S100A8 или GST-S100A9 через хвостовую вену мыши. На фиг.41B представлен набор графиков, полученных путем количественного анализа популяции CD45-отрицательных, CD44-положительных, PDGFRα-положительных клеток (слева), или CD45-отрицательных, CD44-положительных, PDGFRα-положительных клеток (справа).
На фиг.42 представлен набор фотографий клеток, полученных после сортировки происходящих из костного мозга прикрепляющихся клеток у мыши со вставкой рецептора PDGF α-GFP с использованием гранул MACS с антителом против CD11b. Экспрессия GFP практически не выявлялась в CD11b-положительных клетках. Напротив, экспрессию GFP наблюдали практически во всех CD11b-отрицательных клетках. Это указывает на то, что CD11b-положительные клетки являются отрицательными по рецептору PDGF α, в то время как CD11b-отрицательные клетки являются положительными по рецептору PDGF α.
На фиг.43 представлена фотография, демонстрирующая, что HMGB1 имеет активность индукции миграции мезенхимальных стволовых клеток, которые представляют собой CD11b-отрицательные клетки, одновременно проявляя малую активность индукции миграции макрофагов, которые являются CD11b-положительными клетками.
На фиг.44 представлена фотография, демонстрирующая результат выявления флуоресценции GFP (зеленая флуоресценция) в мезенхимальных клетках костного мозга, накопленных в области перелома кости, созданного у мыши с рецептором PDGF α-GFP. На ней показано, что у мыши, которой внутривенно вводили HMGB1, в области перелома кости накапливалось больше мезенхимальных клеток костного мозга, чем у мышей, которым вводили отрицательный контроль.
Способ осуществления изобретения
Настоящее изобретение относится к средствам, стимулирующим регенерацию ткани, содержащим любое из следующих веществ, которые вводят в ткань, отличную от ткани, нуждающейся в регенерации:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
Средства, стимулирующие регенерацию тканей, отличаются тем, что, при введении в ткань, отличную от ткани, нуждающейся в регенерации, они привлекают (также говорят "притягивают" или "локально притягивают") костномозговые клетки из костного мозга в ткань, нуждающуюся в регенерации, через периферическую циркуляцию. В рамках настоящего изобретения, "периферическую циркуляцию" также называют "кровотоком" или "циркулирующим периферическим кровотоком".
Средства, стимулирующие регенерацию тканей по настоящему изобретению, предпочтительно подавляют рубцовое заживление и индуцируют заживление без рубцов. Рубцовое заживление относится к состоянию, при котором фибриллярный коллаген заменяет функциональные ткани. С другой стороны, заживление без рубцов относится к состоянию, при котором поврежденная область регенерирует функциональные ткани, состоящие из клеточных компонентов, и оно функционально и эстетически превосходит рубцовое заживление. Стимулирующие регенерацию тканей средства по настоящему изобретению включают такие средства, стимулирующие регенерацию без рубцов.
Таким образом, средства по настоящему изобретению также могут называться следующим образом:
стимулирующие регенерацию тканей средства, которые вводят в ткань, отличную от ткани, нуждающейся в регенерации, и которые стимулируют регенерацию тканей путем привлечения клеток костного мозга в периферическую кровь из костного мозга и, в результате, привлечения происходящих из костного мозга клеток в ткань, нуждающуюся в регенерации, через систему периферической циркуляции;
средства, стимулирующие регенерацию ткани без рубцов, которые вводят в ткань, отличную от ткани, нуждающейся в регенерации; или
средства, стимулирующие регенерацию тканей без рубцов, которые вводят в ткань, отличную от ткани, нуждающейся в регенерации, и которые стимулируют регенерацию тканей путем привлечения клеток костного мозга в периферическую кровь из костного мозга и, в результате, привлечения происходящих из костного мозга клеток в ткань, нуждающуюся в регенерации, через систему периферической циркуляции.
Ткань, нуждающаяся в регенерации, включает, например, поврежденные ткани, некротические ткани, ткани после хирургической операции, ткани со сниженной функцией, фиброзирующие ткани, стареющие ткани и пораженные заболеванием ткани. Примеры тканей включают живые ткани кожи и поврежденные ткани, полученные внутренней биопсией (хирургической операцией) (головного мозга, легкого, сердца, печени, желудка, тонкого кишечника, толстого кишечника, поджелудочной железы, почки, мочевого пузыря, селезенки, матки, семенников, крови и т.д.).
В настоящем изобретении введение в ткань, отличную от ткани, нуждающейся в регенерации, относится к введению в область, которая не является областью, нуждающейся в регенерации (область, отличная от области, нуждающейся в регенерации). Таким образом, "ткань, отличная от ткани, нуждающейся в регенерации" также может называться следующим образом:
область, отличная от ткани, нуждающейся в регенерации; область, отличная от области, нуждающейся в регенерации; область, отдаленная от ткани, нуждающейся в регенерации; область, отдаленная от области, нуждающейся в регенерации; область, удаленная от области, нуждающейся в регенерации; ткань, удаленная от ткани, нуждающейся в регенерации; удаленная область; или удаленная ткань.
В частности, средства по настоящему изобретению эффективно используют для регенерации тканей (головного мозга, сердца и т.д.), в которые трудно прямо вводить фармацевтические средства извне организма.
Происходящие из костного мозга клетки, привлеченные в ткань, нуждающуюся в регенерации, дифференцируются в различные типы клеток, обеспечивая функциональную регенерацию ткани, нуждающейся в регенерации и поддержании/усилении функций. В настоящем изобретении, примеры ткани, нуждающейся в регенерации, включают, но не ограничиваются ими, ткани, поврежденные различными патологическими состояниями вследствие ишемических/гипоперфузионных/гипоксических состояний, травмы, ожогов, воспаления, аутоиммунитета, генных аномалий и т.п.
Ткани в настоящем изобретении конкретно не ограничены, при условии, что они представляют собой ткани, в которые могут дифференцироваться происходящие из костного мозга клетки. Их примеры включают все типы тканей в живом организме, такие как кожная ткань, костная ткань, хрящевая ткань, мышечная ткань, жировая ткань, ткань сердечной мышцы, неврологическая ткань, легочная ткань, желудочно-кишечные ткани, печеночные/билиарные/панкреатические ткани и органы мочеполовой системы. Более того, при использовании указанных выше стимулирующих регенерацию тканей средств, лечение для индукции функциональной регенерации тканей становится возможным не только при кожных заболеваниях, таких как трудноизлечимые кожные язвы, кожные раны, буллез и алопеция, но также в тканях, нуждающихся в регенерации, таких как ткани после инфаркта головного мозга, инфаркта миокарда, перелома кости, инфаркта легких, желудочных язв и энтерита. Виды животных, подлежащих введению описанного выше стимулирующего регенерацию тканей средства, конкретно не ограничены и включают млекопитающих, птиц, рыб и т.п. Млекопитающие включают человека и не являющихся человеком животных, примерами которых являются, но не ограничиваясь ими, люди, мыши, крысы, обезьяны, свиньи, собаки, кролики, хомяки, морские свинки, лошади, овцы и киты.
Примеры ткани, отличной от ткани, нуждающейся в регенерации, включают ткани крови, мышечные ткани, подкожные ткани, внутрикожные ткани, ткани брюшной полости и т.п.
Таким образом, средства по настоящему изобретению включают средства для стимуляции регенерации описанных выше тканей.
Средства по настоящему изобретению предпочтительно включают средства для стимуляции регенерации нервных тканей, костных тканей и кожных тканей, но не ограничиваются ими. Такие средства, стимулирующие регенерацию нервной ткани, включают средства для стимуляции регенерации тканей центральной нервной системы, но не ограничиваются ими. Средства, стимулирующие регенерацию нервной ткани, также можно использовать для лечения, например, но не ограничиваясь ими, инфаркта головного мозга, кровоизлияния в мозг и ушиба головного мозга. Более того, средства, стимулирующие регенерацию костной ткани, можно использовать для лечения, например, но не ограничиваясь этим, перелома кости. Кроме того, средства, стимулирующие регенерацию кожной ткани, можно использовать для лечения, например, но не ограничиваясь ими, кожных язв, недостаточного закрытия швами хирургических ран, ожогов, разрезов, синяков, эрозий кожи и ссадин.
В рамках настоящего изобретения, "клетки костного мозга" и "происходящие из костного мозга клетки" представляют собой клетки, отличные от гемопоэтических стволовых клеток, или клетки, происходящие из них, такие как лейкоциты, эритроциты и тромбоциты, и представляют собой стволовые клетки, которые соответствуют клеткам, называемым в настоящем описании мезенхимальными стволовыми клетками костного мозга, стромальными плюрипотентными стволовыми клетками костного мозга или плюрипотентными стволовыми клетками костного мозга. "Клетки костного мозга" включают клетки, содержащие популяции клеток-предшественников тканей, существующие в костном мозге. "Клетки костного мозга" и "происходящие из костного мозга клетки можно выделять взятием костного мозга (взятием клеток костного мозга) или взятием периферической крови. Гемопоэтические стволовые клетки являются не прикрепляющимися, в то время как некоторые из "клеток костного мозга" и "происходящих из костного мозга клеток" получают в качестве прикрепляющихся клеток путем культивирования фракции моноцитов крови, полученной взятием костного мозга (взятием клеток костного мозга) или взятием периферической крови. Более того, "клетки костного мозга" и "происходящие из костного мозга клетки" включают мезенхимальные стволовые клетки, и имеют потенциал к дифференцировке, предпочтительно, в остеобласты (индукцию дифференцировки можно идентифицировать путем выявления кальцификации), хондроциты (которые можно идентифицировать по положительному окрашиванию альциановым синим, по положительному окрашиванию сафранином O, или сходными с ними), адипоциты (которые можно идентифицировать по положительному окрашиванию суданом III), и другие мезенхимальные клетки, такие как фибробласты, гладкомышечные клетки, стромальные клетки и клетки сухожилий; и, кроме того, нервные клетки, эпителиальные клетки (например, эпидермальные кератиноциты и эпителиальные клетки кишечника экспрессируют семейство цитокератинов), и сосудисто-эндотелиальные клетки. Клетки, в которые может происходить дифференцировка, не ограничиваются указанными выше клетками, и также они включают клетки, имеющие потенциал к дифференцировке в клетки паренхиматозных органов, таких как печень, почка и поджелудочная железа.
В рамках настоящего изобретения, "клетки костного мозга" относятся к клеткам, существующим в костном мозге, в то время как "происходящие из костного мозга клетки" относятся к "клеткам костного мозга", привлеченным извне костного мозга.
В рамках настоящего изобретения, "мезенхимальные клетки костного мозга", "стромальные плюрипотентные клетки костного мозга" или "плюрипотентные стволовые клетки костного мозга" относятся к клеткам, существующим в костном мозге, которые отбирают непосредственно из костного мозга или отбирают непрямо из других тканей (крови, кожи, жировой ткани и других тканей), и они могут культивироваться и пролиферировать в качестве прикрепляющихся клеток на чашке для культивирования (изготовленной из пластмассы или стекла). Эти клетки отличаются наличием потенциала к дифференцировке в мезенхимальные ткани, такие как кость, хрящ и жировая ткань (мезенхимальные стволовые клетки), или в ткань скелетной мышцы, нервные ткани и эпителиальные ткани (плюрипотентные стволовые клетки), и их можно получать путем взятия клеток костного мозга. "Мезенхимальные стволовые клетки костного мозга", "стромальные плюрипотентные клетки костного мозга" или "плюрипотентные стволовые клетки костного мозга", привлеченные из костного мозга, представляют собой клетки, которые можно получать путем взятия из периферической крови, мезенхимальных тканей, таких как жировая ткань, эпителиальные ткани, такие как кожа, или нервные ткани, такие как ткань головного мозга. Мезенхимальные стволовые клетки костного мозга, стромальные плюрипотентные стволовые клетки костного мозга, плюрипотентные стволовые клетки костного мозга или эти клетки, привлеченные из костного мозга, также отличаются наличием потенциала к дифференцировке в эпителиальные ткани, такие как кератиноциты, составляющие кожу, или нервные ткани, которые составляют головной мозг, при введении в очаг повреждения в живом организме непосредственно после взятия или после прикрепления на чашку для культивирования. Примеры мезенхимальных стволовых клеток костного мозга, стромальных плюрипотентных стволовых клеток костного мозга, плюрипотентных стволовых клеток костного мозга или этих клеток, привлеченных из костного мозга, включают, но не ограничиваются ими, клетки, имеющие свойство быть CD11b-отрицательными.
Мезенхимальные стволовые клетки костного мозга, костномозговые стромальные плюрипотентные стволовые клетки, плюрипотентные стволовые клетки костного мозга, или эти клетки, привлеченные из костного мозга, предпочтительно имеют потенциал к дифференцировке в: остеобласты (индукцию дифференцировки можно идентифицировать путем выявления кальцификации), хондроциты которые можно идентифицировать по положительному окрашиванию альциановым синим, по положительному окрашиванию сафранином O, или сходными с ними), адипоциты (которые можно идентифицировать по положительному окрашиванию суданом III), и другие мезенхимальные клетки, такие как фибробласты, гладкомышечные клетки, клетки скелетных мышц, стромальные клетки и клетки сухожилий; нервные клетки, пигментные клетки, эпидермальные клетки, клетки волосяных фолликулов (которые экспрессируют семейство цитокератинов, семейство кератина волос или сходные с ними), эпителиальные клетки (например, эпидерамльные кератиноциты и эпителиальные клетки кишечника экспрессируют семейство цитокератинов или сходные с ними), и эндотелиальные клетки; и, кроме того, предпочтительно в клетки паренхиматозных органов, таких как печень, почка и поджелудочная железа. Однако дифференцированные клетки не ограничиваются описанными выше клетками.
Более того, примерами мезенхимальных стволовых клеток костного мозга, стромальных плюрипотентных стволовых клеток костного мозга, плюрипотентных стволовых клеток костного мозга человека, или этих клеток, привлеченных из костного мозга, могут являться, но не ограничиваясь ими, клетки, которые можно прямо получать взятием костного мозга (клеток), периферической крови или жировой ткани, или получать в качестве прикрепляющихся клеток путем культивирования выделенной фракции моноцитов. Маркеры мезенхимальных стволовых клеток костного мозга, стромальных плюрипотентных стволовых клеток костного мозга, плюрипотентных стволовых клеток костного мозга человека или этих клеток, привлеченных из костного мозга, могут быть, например, все или некоторые из следующих, но не ограничиваясь ими: Lin-отрицательные, CD45-отрицательные, CD44-положительные, CD90-положительные и CD29-положительные.
Более того, примерами мезенхимальных стволовых клеток костного мозга, стромальных плюрипотентных стволовых клеток костного мозга, плюрипотентных стволовых клеток костного мозга мыши или этих клеток, привлеченных из костного мозга, могут являться, но не ограничиваясь ими, клетки, которые можно получать способами, описанными в примерах. Маркерами для мезенхимальных стволовых клеток костного мозга, стромальных плюрипотентных стволовых клеток костного мозга, плюрипотентных стволовых клеток костного мозга мыши или этих клеток, привлеченных из костного мозга, могут быть, например, все или некоторые из следующих, но не ограничиваясь ими: CD44-положительные, PDGFRα-положительные, PDGFRβ-положительные, CD45-отрицательные, Lin-отрицательные, Sca-1-положительные, c-kit-отрицательные, CD90-положительные и CD29-положительные.
Клетки-предшественники ткани определяют как недифференцированные клетки, обладающие однонаправленной способностью дифференцироваться в клетки конкретной ткани, отличной от системы крови, и включают недифференцированные клетки, обладающие способностью дифференцироваться в мезенхимальные ткани, эпителиальные ткани, нервные ткани, паренхиматозные органы и эндотелий сосудов, как упоминалось выше.
Для средств, стимулирующих регенерацию ткани, не существует конкретного ограничения веществ, отличных от по меньшей мере одного из веществ (a)-(q), упомянутых выше, при условии, что они не ингибируют привлечение происходящих из костного мозга клеток и стимуляцию регенерации ткани. Например, в дополнение по меньшей мере к одному из веществ (a)-(q), упомянутых выше, стимулирующие регенерацию тканей средства по настоящему изобретению могут содержать: родственную молекулу(ы), усиливающую функцию веществ (a)-(q), упомянутых выше, состоящую в индукции функциональной регенерации тканей; молекулу(ы), которая ингибирует непредвиденные действия веществ (a)-(q), упомянутых выше; факторы, которые регулируют пролиферацию и дифференцировку происходящих из костного мозга клеток; и другие факторы, которые усиливают/поддерживают эти факторы или клеточные функции.
Виды животных, которые служат в качестве источника белка HMGB1, HMGB2, HMGB3, S100A8 или S100A9, экстракта, упомянутого выше, или связывающей гепарин фракции, упомянутой выше, для стимулирующих регенерацию тканей средств по настоящему изобретению, включают человека и не являющихся человеком животных, таких как люди, мыши, крысы, обезьяны, свиньи, собаки, кролики, хомяки и морские свинки, но предпочтительно являются такими же, как и виды животных, подлежащих введению веществ и сходных с ними.
Белок HMGB1 по настоящему изобретению может быть проиллюстрирован, но не ограничиваясь этим, белками, содержащими аминокислотную последовательность SEQ ID NO: 1, 3 или 5. Белки HMGB1 по настоящему изобретению также могут включать белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3 или 5. Примеры таких белков включают 1) выделенные белки, которые содержат аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 1, 3 или 5, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3 или 5; и 2) выделенные белки, которые кодируются ДНК, которые гибридизуются в строгих условиях с ДНК, содержащими нуклеотидную последовательность SEQ ID NO: 2, 4 или 6, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3 или 5.
Белок HMGB2 по настоящему изобретению может быть проиллюстрирован, но не ограничиваясь этим, белками, содержащими аминокислотную последовательность SEQ ID NO: 7, 9 или 11. Белки HMGB2 по настоящему изобретению также могут включать белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 7, 9 или 11. Примеры таких белков включают 1) выделенные белки, которые содержат аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 7, 9 или 11 и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 7, 9 или 11; и 2) выделенные белки, которые кодируются ДНК, которые гибридизуются в строгих условиях с ДНК, содержащими нуклеотидную последовательность SEQ ID NO: 8, 10 или 12, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 7, 9 или 11.
Белок HMGB3 по настоящему изобретению может быть проиллюстрирован, но не ограничиваясь этим, белками, содержащими аминокислотную последовательность SEQ ID NO: 13 или 15. Белки HMGB3 по настоящему изобретению также могут включать белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 13 или 15. Примеры таких белков включают 1) выделенные белки, которые содержат аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 13 или 15, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 13 или 15; и 2) выделенные белки, которые кодируются ДНК, которые гибридизуются в строгих условиях с ДНК, содержащими нуклеотидную последовательность SEQ ID NO: 14 или 16, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 13 или 15.
Белок S100A8 по настоящему изобретению может быть проиллюстрирован, но не ограничиваясь этим, белками, содержащими аминокислотную последовательность SEQ ID NO: 17, 19 или 21. Белки S100A8 по настоящему изобретению также могут включать белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 17, 19 или 21. Примеры таких белков включают 1) выделенные белки, которые содержат аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 17, 19 или 21, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 17, 19 или 21; и 2) выделенные белки, которые кодируются ДНК, которые гибридизуются в строгих условиях с ДНК, содержащими нуклеотидную последовательность SEQ ID NO: 18, 20 или 22, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 17, 19 или 21.
Белок S100A9 по настоящему изобретению может быть проиллюстрирован, но не ограничиваясь этим, белками, содержащими аминокислотную последовательность SEQ ID NO: 23, 25 или 27. Белки S100A9 по настоящему изобретению также могут включать белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 23, 25 или 27. Примеры таких белков включают 1) выделенные белки, которые содержат аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 23, 25 или 27, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 23, 25 или 27; и 2) выделенные белки, которые кодируются ДНК, которые гибридизуются в строгих условиях с ДНК, содержащими нуклеотидную последовательность SEQ ID NO: 24, 26 или 28, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 23, 25 или 27.
Выделенные белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, могут быть гомологами или паралогами белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27. Специалисты в данной области могут выделять белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, известными способами (дополнительный том "Jikken Igaku (Experimental Medicine), Idenshi Kougaku Handbook (Genetic Engineering Handbook)", pp. 246-251, опубликованный Yodosha Co., Ltd., 1991).
Примеры белков, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, включают белки, обладающие активностью привлечения происходящих из костного мозга клеток в ткани, нуждающиеся в регенерации, или активность миграции происходящих из костного мозга клеток.
Белки, которые содержат аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, включают встречающиеся в природе белки. Как правило, эукариотические гены имеют полиморфизм, как известно для генов интерферонов и сходных с ними. Изменения нуклеотидной последовательности, вызванные полиморфизмом, могут привести к одной или нескольким аминокислотным заменам, делециям, инсерциям и/или вставкам. Встречающиеся в природе белки, такие как белки, содержащие аминокислотную последовательность с одной или несколькими аминокислотными заменами, делециями, инсерциями и/или вставками в аминокислотной последовательности SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, включены в белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9 по настоящему изобретению.
Настоящее изобретение также включает искусственно продуцированные мутантные белки при условии, что они функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27. Известные способы, которые приводят к случайной мутации данной нуклеотидной последовательности, включают замену(ы) пары(пар) оснований посредством обработки ДНК азотистой кислотой (Hirose, S. et al., Proc. Natl. Acad. Sci. USA, 79: 7258-7260, 1982). Этот способ обеспечивает случайное внесение замены(замен) пары(пар) оснований в конкретный сегмент посредством обработки азотистой кислотой желательного для мутации сегмента. Альтернативно, технологии для сайт-направленной мутации мишени включают способ дуплекса с брешью (Kramer W. and Fritz H.J., Methods in Enzymol., 154: 350-367, 1987) и т.п. Замкнутый двухцепочечный вектор, в который клонируют ген, подлежащий встраиванию мутации, разделяют на отдельные цепи. Эти отдельные цепи гибридизуют с синтетическим олигонуклеотидом с мутацией в участке-мишени. Происходящую из вектора комплементарную отдельную цепь ДНК, линеаризованную ферментом рестрикции, подвергают отжигу с циклическим одноцепочечным вектором, и разрыв между олигонуклеотидом и вектором достраивают с использованием ДНК-полимеразы, которую затем преобразовывают в полный двухцепочечный вектор лигированием.
Количество аминокислот, подлежащих модификации, как правило, составляет 50 или менее, предпочтительно 30 или менее, и более предпочтительно 5 аминокислот или менее (например, одна аминокислота).
Когда аминокислоту заменяют искусственно, замена аминокислотой, имеющей сходные свойства, приводит к сохранению активности исходного белка. Белки по настоящему изобретению включают белки, полученные в результате консервативной замены при указанной выше замене аминокислоты(аминокислот), и которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27. Консервативную замену считают важной в случае замены аминокислоты(аминокислот) доменов, важных для активности белка. Такая консервативная замена аминокислоты(аминокислот) хорошо известна специалистам в данной области.
Примеры групп аминокислот, пригодных для консервативной замены, включают основные аминокислоты (такие как лизин, аргинин и гистидин), кислотные аминокислоты (такие как аспарагиновая кислота и глутаминовая кислота), незаряженные полярные аминокислоты (такие как глицин, аспарагин, глутамин, серин, треонин, тирозин и цистеин), неполярные аминокислоты (такие как аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин и триптофан), β-разветвленные аминокислоты (такие как треонин, валин и изолейцин) и ароматические аминокислоты (такие как тирозин, фенилаланин, триптофан и гистидин).
Более того, неконсервативная замена может повышать активность белка (например, конститутивно активированные белки).
Кроме того, белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, можно получать способами, в которых используется гибридизация. Иными словами, ДНК, кодирующую белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9 по настоящему изобретению, как показано в SEQ ID NO: 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26 или 28, или ее фрагмент используют в качестве зонда, и затем выделяют ДНК, которые могут гибридизоваться с ними. Реакция гибридизации, проведенная в строгих условиях, приводит к выбору высоко гомологичной ДНК в качестве нуклеотидной последовательности. Это повышает вероятность того, что выделенные белки содержат белки, которые функционально эквивалентны белку HMGB1, HMGB2, HMGB3, S100A8 или S100A9. Примеры высоко гомологичной нуклеотидной последовательности включают последовательности, обладающие 70% или более, и желательно 90% или более идентичностью.
В конкретном примере термин "строгие условия" относится к условиям гибридизации с 6xSSC, 40% формамидом при 25°C и последующему промыванию 1xSSC при 55°C. Строгость зависит от таких условий, как концентрация соли, концентрация формамида или температура; однако специалистам в данной области понятно, как устанавливать условия, чтобы получить необходимую строгость.
С использованием гибридизации, например, можно выделять ДНК, кодирующие гомологи белков HMGB1, HMGB2, HMGB3, S100A8 или S100A9, отличные от белков, содержащих аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27.
Белки, которые функционально эквивалентны белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, обычно имеют высокую гомологию с аминокислотной последовательностью SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27. Термин "высокая гомология" относится к идентичности последовательностей, составляющей по меньшей мере 30% или более, предпочтительно 50% или более, более предпочтительно 80% или более (например, 95% или более). Идентичность нуклеотидных последовательностей и аминокислотных последовательностей можно определять с использованием сайта поиска гомологии через интернет (например, программы поиска гомологии, такие как FASTA, BLAST, PSI-BLAST и SSEARCH, можно использовать в DNA Data Bank of Japan (DDBJ) [примеры которого включают страницу поиска гомологии (Search and Analysis) на web-сайте DNA Data Bank of Japan (DDBJ); http://www.ddbj.nig.ac.jp/E-mail/homology-j.html]). Более того, поиск с использованием BLAST можно проводить через web-сайт National Center for Biotechnology Information (NCBI) (примеры которого включают страницу BLAST на домашней странице web-сайта NCBI; http://www.ncbi.nlm.nih.gov/BLAST/; Altschul, S.F. et al., J. Mol. Biol., 1990, 215(3): 403-10; Altschul, S.F. & Gish, W., Meth. Enzymol., 1996, 266: 460-480; Altschul, S.F. et al., Nucleic Acids Res., 1997, 25: 3389-3402)).
Например, при вычислении идентичности аминокислотных последовательностей с использованием Advanced BLAST 2.1, величину идентичности (%) можно получить следующим образом: в качестве программы используют blastp, ожидаемое значение устанавливают на 10, все фильтры устанавливают на OFF, в качестве матрицы используют BLOSUM62, и штраф за наличие пропуска, штраф пропуска остатка, и отношение лямбда устанавливают на 11, 1 и 0,85, соответственно (параметры по умолчанию) (Karlin, S. and S.F. Altschul (1990) Proc. Natl. Acad. Sci. USA 87: 2264-68; Karlin, S. и S.F. Altschul (1993) Proc. Natl. Acad. Sci. USA 90: 5873-7).
Кроме того, белки, функционально эквивалентные белку, содержащему аминокислотную последовательность SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27, могут представлять собой фрагменты аминокислотной последовательности SEQ ID NO: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25 или 27.
Белки по настоящему изобретению или белки, функционально эквивалентные им, могут представлять собой белки, подвергнутые различным модификациям, таким как физиологическая модификация сахарными цепями и т.п., мечение флуоресцентными или радиоактивными веществами, или слияние с другими белками. В частности, в рекомбинантных молекулах, описанных ниже, модификация сахарной цепи может варьировать в зависимости от хозяев, используемых для экспрессии. Однако даже если существуют отличия в модификации сахарных цепей, все белки, имеющие свойства, сходные со свойствами белков HMGB1, HMGB2, HMGB3, S100A8 или S100A9, описанных в настоящем документе, представляют собой белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9 по настоящему изобретению или белки, функционально эквивалентные им.
Белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9 можно получать не только из материалов живых организмов, но также в форме рекомбинантных белков, путем встраивания генов, которые кодируют эти белки, в соответствующую экспрессирующую систему. Для получения белков HMGB1, HMGB2, HMGB3, S100A8 или S100A9 способами генной инженерии указанные выше ДНК, которые кодируют белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9, можно встраивать в соответствующую экспрессирующую систему, а затем они могут экспрессироваться. Примеры систем хозяин/вектор, применимых для настоящего изобретения, включают экспрессирующий вектор pGEX и E. coli. В случае pGEX, чужеродные гены могут быть экспрессированы в качестве слитого с глутатион-S-трансферазой белка (GST) (Gene, 67: 31-40, 1988). pGEX, в который встроен ген, кодирующий белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9, вводят в штамм E. coli, такой как BL21, посредством теплового шока, инкубируют в течение подходящего периода времени, а затем добавляют изопропилтио-β-D-галактозид (IPTG) для индукции слитого с GST белка HMGB1, слитого с GST белка HMGB2, слитого с GST белка HMGB3, слитого с GST белка S100A8 или слитого с GST белка S100A9. Поскольку GST по настоящему изобретению адсорбируется на глутатион-сефарозу 4B, продукт экспрессии легко выделять и очищать аффинной колоночной хроматографией.
Кроме того, в качестве систем хозяин/вектор для получения рекомбинантных белков HMGB1, HMGB2, HMGB3, S100A8 или S100A9 можно использовать следующее. Прежде всего, когда в качестве хозяев используют бактерии, экспрессирующие векторы для слитых белков, в которых используется гистидиновая метка, HA-метка, FLAG-метка и сходные с ними, являются коммерчески доступными. Рекомбинантные белки по настоящему изобретению также включают рекомбинантные белки, с которыми связана метка или ее неполный пептид. Что касается дрожжей, известно, что дрожжи, относящиеся к роду Pichia, являются эффективными для экспрессии содержащих сахарную цепь белков. С точки зрения добавления сахарных цепей, также являются пригодными экспрессирующие системы, в которых используется бакуловирусный вектор с клетками насекомых в качестве клеток-хозяев (Bio/Technology, 6: 47-55, 1988). Кроме того, при использовании клеток млекопитающих, трансфекцию вектора проводят с использованием промоторов, таких как CMV, RSV и SV40. Любые из этих систем хозяин/вектор можно использовать в качестве экспрессирующей системы для белков HMGB1, HMGB2, HMGB3, S100A8 или S100A9. Более того, гены также можно вводить с использованием вирусных векторов, таких как ретровирусные векторы, аденовирусные векторы и векторы на основе аденоассоциированных вирусов.
Полученные таким образом белки по настоящему изобретению можно выделять из внутреннего содержимого клетки или извне клеток (среда и т.п.), и их можно очищать в качестве белков, которые являются по существу чистыми и гомогенными. Белки можно разделять и очищать с использованием способов разделения и очитки, которые обычно используют при очистке белков, и они конкретно не ограничены. Например, белки можно разделять и очищать путем надлежащего выбора и комбинирования хроматографических колонок, фильтров, ультрафильтрации, высаливания, осаждения растворителем, экстракции растворителем, дистилляции, иммунопреципитации, SDS-полиакриламидного гель-электрофореза, электрофореза с изоэлектрическим фокусированием, диализа, перекристаллизации и т.п.
Примеры хроматографии включают аффинную хроматографию, ионообменную хроматографию, гидрофобную хроматографию, гель-фильтрацию, обращенно-фазовую хроматографию и адсорбционную хроматографию (Marshak et al., Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Cold Spring Harbor Laboratory Press, 1996). Эти типы хроматографии можно проводить с использованием жидкофазной хроматографии, такой как ВЭЖХ и FPLC.
Более того, белки по настоящему изобретению предпочтительно представляют собой по существу очищенные белки. В настоящем документе, термин "по существу очищенный" означает, что чистота белка по настоящему изобретению (доля белка по настоящему изобретению в общих белковых компонентах) составляет 50% или более, 60% или более, 70% или более, 80% или более, 90% или более, 95% или более, 100% или близко к 100%. Верхний предел для выражения "близко к 100%" зависит от способов очистки и аналитических способов специалистов в данной области, и его примерами являются 99,999%, 99,99%, 99,9%, 99% и т.п.
Более того, по существу очищенный белок включает любой белок, очищенный любым способом очистки при условии, что чистота белка является такой, как указано выше. Примеры включают, но не ограничиваются ими, белки, по существу очищенные посредством надлежащего выбора и комбинирования указанных выше хроматографических колонок, фильтров, ультрафильтрации, высаливания, осаждения растворителем, экстракции растворителем, дистилляции, иммунопреципитации, SDS-полиакриламидного гель-электрофореза, электрофореза с изоэлектрическим фокусированием, диализа, перекристаллизации и т.п.
Клетки, где высвобождаются или секретируются белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9 по настоящему изобретению, в основном включают все типы происходящих из тканей клеток in vivo. Примерами клеток, которые можно легко собирать и культивировать, являются, но они не ограничиваются ими, фибробласты (такие как нормальные фибробласты кожи и клеточные линии, происходящие из них). Более того, клетки, секретирующие белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9 также можно получать следующим образом. Получают вектор встраиванием ДНК, кодирующей белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9, или ДНК, кодирующей HMGB1, HMGB2, HMGB3, S100A8 или S100A9, связанной с ДНК, кодирующей сигнальную последовательность для секреции (ATG CAG ACA GAC ACA CTC CTG CTA TGG GTA CTG CTG CTG TGG GTT CCA GGT TCC ACT GGT GAC; SEQ ID NO: 29), в известный экспрессирующий вектор или вектор генной терапии. Полученный вектор вводят в клетки млекопитающих, такие как фибробласты (такие как нормальные фибробласты кожи и клеточные линии, происходящие из них), клетки насекомых и другие клетки. Примеры ДНК, кодирующих сигнальные последовательности для секреции, включают, но не ограничиваются ими, ДНК с описанными выше последовательностями. Более того, не существует конкретных ограничений типа животных, из которых эти клетки происходят, хотя предпочтительно используют клетки из типа животных, к которому относится животное-мишень, которому вводят вектор, клетки из самого животного-мишени или клетки, происходящие из близкого родственника животного-мишени, которому вводят вектор.
ДНК, которые кодируют белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9 индукторов или средств, стимулирующих регенерацию тканей, по настоящему изобретению, могут представлять собой кДНК, геномные ДНК, природные ДНК или искусственно синтезированные ДНК, при условии, что они кодируют белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9. ДНК, которые кодируют белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9, обычно вводят в форме, встроенной в векторы.
Примеры векторов по настоящему изобретению включают, но не ограничиваются ими, плазмидные векторы, ретровирусные векторы, лентивирусные векторы, аденовирусные векторы, векторы на основе аденоассоциированного вируса, векторы на основе вируса Сендай, векторы на основе оболочки вируса Сендай и векторы на основе вируса папилломы. Векторы могут содержать промоторные последовательности ДНК, которые эффективно индуцируют экспрессию генов, факторы, которые регулируют экспрессию генов, и молекулы, которые необходимы для поддержания стабильности ДНК.
В настоящем изобретении также можно использовать следующие векторы: неполные пептиды белка HMGB1, HMGB2, HMGB3, S100A8 или S100A9, которые обладают активностью привлечения происходящих из костного мозга клеток; клетки, секретирующие эти неполные пептиды; или векторы, в которые встроена ДНК, кодирующая эти неполные пептиды.
Экстракты клеток или тканей, используемые в настоящем изобретении, можно получать способами, включающими стадию погружения клеток или тканей в растворитель.
Клетки и ткани, подлежащие погружению в растворитель, конкретно не ограничены, но включают, например, происходящие из ткани клетки, клетки клеточных линий, полученных из происходящих из ткани клеток (включая, но не ограничиваясь ими, например, HeLa и HEK293), выделенные клетки, не выделенные клетки (например, клетки в выделенных тканях), и клетки, трансфицированные ДНК, кодирующей белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9. Указанные выше ткани могут представлять собой ткани любого типа, и они включают, но не ограничиваются ими, например, живые ткани кожи и ткани, полученные внутренней биопсией (хирургической операцией) (головного мозга, легкого, сердца, печени, желудка, тонкого и толстого кишечника, поджелудочной железы, почки, мочевого пузыря, селезенки, матки, семенников, крови и т.д.).
Примеры указанного выше растворителя включают, но не ограничиваются ими, физиологический раствор, фосфатно-солевой буфер (PBS) и забуференный Tris солевой раствор (TBS). Более того, время погружения клеток или ткани в растворитель должно иметь продолжительность, необходимую и достаточную для индукции некроза клеток, т.е. от 1 часа до 48 часов (например, от 6 до 48 часов), и предпочтительно от 12 часов до 24 часов, но оно не ограничивается этим. Таким образом, "стадию погружения клеток в растворитель" можно перефразировать как "стадию погружения клеток в растворитель на период времени, необходимый и достаточный для индукции некроза" или "стадию обеспечения некроза клеток". Более того, примеры температуры для погружения клеток или ткани в растворитель включают, но не ограничиваются этим, от 4°C до 25°C (например, от 4°C до 8°C), и предпочтительно 4°C. Кроме того, примеры pH для погружения клеток или ткани в растворитель включают, но не ограничиваются этим, pH от 7 до 8, и предпочтительно pH 7,5. Примеры буфера включают, но не ограничиваются этим, фосфатно-солевой буфер в концентрации от 10 мМ до 50 мМ, предпочтительно от 10 до 20 мМ.
Более того, в настоящем изобретении после погружения клеток или тканей в растворитель их можно извлекать из растворителя. Способы извлечения клеток или тканей из растворителя конкретно не ограничены, при условии, что способ известен специалистам в данной области. Например, клетки или ткани можно удалять из растворителя центрифугированием при гравитационном ускорении от 10 G до 100000 G (например, 440 G) при от 4°C до 25°C (например, 4°C), с последующим отделением супернатанта, однако способ удаления не ограничивается этим способом. Супернатант можно использовать в качестве экстракта клеток или тканей.
Экстракты клеток или тканей в настоящем изобретении включают, например, но не ограничиваются ими, экстракт кожи и экстракт мононуклеарных клеток периферической крови (экстракт периферической крови).
Экстракт периферической крови получают следующим способом: после сбора крови шприцом или сходными с ним клетки замораживают в морозильной камере или в жидком азоте, на сухом льду, или сходными способами, а затем размораживают при температуре 0°C или более. Затем для удаления нерастворимых клеточных компонентов образец центрифугируют, например, при силе тяжести от 10 до 100000 G (например, при 440 G) и при от 4°C до 25°C (например, при 4°C), и полученный супернатант собирают. Нерастворимые клеточные компоненты можно удалять из растворителя способом, описанным выше. Однако способы удаления нерастворимых клеточных компонентов не ограничены указанным выше примером. Полученный супернатант можно использовать в качестве экстракта клеток или тканей. Альтернативно, вместо центрифугирования нерастворимые клеточные компоненты можно удалять фильтрацией через фильтр из нитроцеллюлозы с микропорами 0,45 мкм, или сходные с ним. Альтернативно, собранной периферической крови можно позволять стоять в течение от трех до 48 часов при 4°C для индукции некроза клеток. При такой обработке из клеток периферической крови могут высвобождаться внутриклеточные компоненты. Затем для удаления из растворителя нерастворимых клеточных компонентов, образец центрифугируют при силе тяжести от 10 до 100000 G (например, при 440 G), и полученный супернатант собирают. Нерастворимые клеточные компоненты можно удалять из растворителя способом, описанным выше, но не ограничиваясь им. Полученный супернатант можно использовать в качестве экстракта клеток или тканей. Альтернативно, вместо центрифугирования нерастворимые клеточные компоненты можно удалять фильтрацией через фильтр из нитроцеллюлозы с микропорами 0,45 мкм или т.п.
Между тем, способ получения клеточного экстракта из периферических мононуклеарных клеток является следующим: периферическую цельную кровь отбирают с использованием шприца или сходных с ним, а затем разбавляют PBS до общего объема 4 мл. Затем в центрифужную пробирку помещают 3 мл Ficoll-Paque Plus (GE), и разбавленную кровь наслаивают на него. После центрифугирования в течение 40 минут при 400 G (18°C), мононуклеарные клетки, содержащие средний слой, собирают в новую центрифужную пробирку, и к ним добавляют 45 мл PBS. После центрифугирования в течение 5 минут при 800 G (18°C), супернатант удаляют, и к клеткам добавляют 45 мл PBS. После центрифугирования в течение 5 минут при 800 G (18°C) супернатант удаляют и добавляют 200 мкл PBS для суспендирования выпавших в осадок клеток. Суспензию клеток замораживают в течение 30 минут при -80°C в морозильном камере, а затем извлекают из морозильной камеры и размораживают на льду. Эту обработку замораживанием-размораживанием повторяют три раза, и суспензию центрифугируют при 800 G (4°C) в течение 15 минут для взятия супернатанта. Вместо замораживания клетки можно помещать в холодильник при 4°C на от 3 до 48 часов для индукции некроза клеток и высвобождения внутриклеточных компонентов. Альтернативно внутриклеточные компоненты можно высвобождать из клеток разрушением их с использованием обработки ультразвуком при охлаждении на льду. После любой из этих обработок для высвобождения внутриклеточных компонентов из клеток, образец центрифугируют при гравитационном ускорении от 440 G до 1000000 G, предпочтительно от 20000 G до 100000 G, и супернатант собирают в качестве клеточного экстракта. Вместо центрифугирования образец можно фильтровать через фильтр из нитроцеллюлозы с микропорами 0,45 мкм, ацетат целлюлозы или сходные с ними для удаления нерастворимых компонентов и получения клеточного экстракта.
Гепарин-связывающие фракции из экстрактов клеток или тканей, подлежащие применению в настоящем изобретении, можно продуцировать способом, включающим следующие стадии:
(a) погружение клетки или ткани в растворитель;
(b) контактирование экстракта, полученного на стадии (a), с иммобилизованным гепарином; и
(c) элюирование гепарин-связывающей фракции (также она может называться очищенной гепарином фракцией или очищенной на колонке с гепарином фракцией) с иммобилизованного гепарина.
"Иммобилизованный гепарин" относится к гепарину, ковалентно связанному с нерастворимым носителем. Примеры нерастворимого носителя включают, но не ограничиваются ими, гранулы сефарозы (такие как сефароза 4B, сефароза 6B и т.п.: GE Healthcare). В настоящем изобретении также можно использовать коммерчески доступный иммобилизованный гепарин (колонка Hitrap Heparin HP: GE Healthcare).
Примеры условий для контактирования экстракта клеток или тканей с иммобилизованным гепарином включают, но не ограничиваются ими, pH приблизительно от 7 до 8 (предпочтительно pH 7,5), и концентрацию соли от 0 до 200 мМ, и предпочтительно приблизительно от 100 до 200 мМ. Время, в течение которого экстракт контактирует с иммобилизованным гепарином, конкретно не ограничено, однако контакт предпочтительно продолжается в течение 5 минут или более для достаточной адсорбции гепарин-связывающей фракции на иммобилизованный гепарин. Примеры температуры включают, но не ограничиваются ими, от 4 до 8°C, и предпочтительно 4°C. Кроме того, примеры условий элюирования гепарин-связывающей фракции, адсорбированной на иммобилизованный гепарин, включают, но не ограничиваются ими, pH приблизительно от 7 до 8 и концентрацию соли от 200 до 1000 мМ (предпочтительно приблизительно 1000 мМ).
Способы введения стимулирующих регенерацию тканей средств по настоящему изобретению включают парентеральное введение, более конкретно, они включают введение путем инъекции, но не ограничиваются этим. Кроме того, способы введения стимулирующих регенерацию тканей средств по настоящему изобретению конкретно не ограничены, при условии, что они позволяют стимулирующим регенерацию тканей средствам проникнуть в кровоток не оставаясь в области введения. Способы введения стимулирующих регенерацию тканей средств по настоящему изобретению включают, например, внутрисосудистое введение (внутриартериальное введение, внутривенное введение и т.д.), введение в кровь, внутримышечное введение, подкожное введение, внутрикожное введение и внутрибрюшинное введение, но не ограничиваются ими.
Способ введения можно пригодным образом выбирать согласно возрасту и симптомам пациента. Когда вводят белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9, однократную дозу белка можно выбирать из диапазона от 0,0000001 мг до 1000 мг на кг массы тела пациента. Альтернативно дозу можно выбирать, например, из диапазона от 0,00001 мг до 100000 мг на массу тела пациента. При введении клеток, секретирующих белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9, или векторов для генной терапии, в которые встроена ДНК, кодирующая белки HMGB1, HMGB2, HMGB3, S100A8 или S100A9, их можно вводить так, чтобы количества белка HMGB1, HMGB2, HMGB3, S100A8 или S100A9 в тканях, нуждающихся в регенерации, находились в пределах указанного выше диапазона. Однако дозировка стимулирующих регенерацию тканей средств по настоящему изобретению не ограничивается этим.
Стимулирующие регенерацию тканей средства по настоящему изобретению можно изготавливать согласно обычным способам (например, Remington's Pharmaceutical Science, последнее издание, Mark Publishing Company, Easton, США), и они могут содержать фармацевтически приемлемые носители и добавки. Их примеры включают поверхностно-активные вещества, эксципиенты, красители, отдушки, консерванты, стабилизаторы, буферы, суспендирующие вещества, обеспечивающие изотоничность средства, связующие вещества, дезинтегрирующие вещества, смазывающие вещества, средства, обеспечивающие текучесть, и вкусовые добавки, хотя они не ограничены ими, и можно надлежащим образом использовать другие распространенные носители. Конкретные примеры включают легкую безводную кремниевую кислоту, лактозу, кристаллическую целлюлозу, маннит, крахмал, кармеллозу кальция, кармеллозу натрия, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилацетальдиэтиламиноацетат, поливинилпирролидон, желатин, триглицерид жирной кислоты средней длины цепи, полиоксиэтилен-гидрогенизированное касторовое масло 60, белый сахар, карбоксиметилцеллюлозу, кукурузный крахмал и неорганические соли.
Также настоящее изобретение относится к наборам для стимуляции регенерации тканей, содержащим композицию, содержащую вещество согласно любому из (a)-(q), описанных ниже, где композицию вводят в ткань, отличную от ткани, нуждающейся в регенерации:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей.
Наборы для стимуляции регенерации тканей отличаются тем, что, при введении в ткань, отличную от ткани, нуждающейся в регенерации, они привлекают клетки костного мозга из костного мозга в ткань, нуждающуюся в регенерации, через периферическую циркуляцию.
Наборы по настоящему изобретению также включают наборы для лечения тканей, нуждающихся в регенерации, как указано выше. Наборы по настоящему изобретению предпочтительно включают наборы для парентерального введения, более предпочтительно наборы для введения путем инъекции. Наборы по настоящему изобретению также предпочтительно включают наборы для внутрисосудистого, внутримышечного, подкожного, внутрикожного или внутрибрюшинного введения.
Более того, наборы по настоящему изобретению предпочтительно включают наборы, используемые для стимуляции регенерации нервной, костной или кожной тканей.
Наборы для стимуляции регенерации тканей включают, например, наборы, содержащие: (1) описанное выше вещество, растворенное в фибриногене и (2) тромбин; или (1) описанное выше вещество, (2) фибриноген и (3) тромбин. В настоящем изобретении возможно использовать коммерчески доступные фибриноген и тромбин, включая, например, фибриноген HT-Wf (Benesis-Mitsubishi Pharma), Beriplast (ZLB Behring), Tisseel (Baxter), Bolheal (KAKETSUKEN), и TachoComb (ZLB Behring); однако они не ограничиваются этими примерами.
Между тем, использование описанных выше клеточного экстракта или экстракта ткани, связывающей гепарин фракции клеточного экстракта или экстракта ткани; белка HMGB1, HMGB2, HMGB3, S100A8 или S100A9; клеток, экспрессирующих белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9; вектора, в который встроена ДНК, кодирующая белок HMGB1, HMGB2, HMGB3, S100A8 или S100A9; неполного пептида белка HMGB1, HMGB2, HMGB3, S100A8 или S100A9; клетки, экспрессирующей неполный пептид; или вектора, в который встроена ДНК, кодирующая неполный пептид, может быть описан следующим образом:
(1) способ стимуляции регенерации тканей, который включает стадию введения эффективного количества композиции, содержащей вещество согласно любой из (a)-(q) ниже, в ткань, отличную от ткани, нуждающейся в регенерации:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
(2) применение композиции, содержащей вещество согласно любому из (a)-(q) ниже, для продуцирования средства, стимулирующего регенерацию тканей, где стимулирующее регенерацию тканей средство вводят в ткань, отличную от ткани, нуждающейся в регенерации:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей;
(3) композиция для применения в способе стимуляции регенерации тканей, которая содержит вещество согласно любому из (a)-(q) ниже и которую вводят в ткань, отличную от ткани, нуждающейся в регенерации:
(a) белок HMGB1;
(b) клетка, которая секретирует белок HMGB1;
(c) вектор, в который встроена ДНК, кодирующая белок HMGB1;
(d) белок HMGB2
(e) клетка, которая секретирует белок HMGB2;
(f) вектор, в который встроена ДНК, кодирующая белок HMGB2;
(g) белок HMGB3;
(h) клетка, которая секретирует белок HMGB3;
(i) вектор, в который встроена ДНК, кодирующая белок HMGB3;
(j) белок S100A8;
(k) клетка, которая секретирует белок S100A8;
(l) вектор, в который встроена ДНК, кодирующая белок S100A8;
(m) белок S100A9;
(n) клетка, которая секретирует белок S100A9;
(o) вектор, в который встроена ДНК, кодирующая белок S100A9;
(p) экстракт клеток или тканей; и
(q) связывающая гепарин фракция экстракта клеток или тканей.
Все документы уровня техники, включенные в настоящее описание, включены в настоящее описание в качестве ссылок.
Пример 1
Очистка HMGB-1 и S100A8
Из кожи новорожденных мышей экстрагировали РНК с использованием Trizol (Invitrogen), а затем синтезировали кДНК с использованием набора для синтеза кДНК SuperScript III (Invitrogen). С использованием этой кДНК в качестве матрицы, кДНК HMGB1 амплифицировали полимеразной цепной реакцией (ПЦР). Полученную кДНК встраивали в pCAGGS, плазмидный вектор для экспрессии белка в клетках млекопитающих, так чтобы вектор экспрессировал белок, с которым связаны последовательности GST-метки и 6XHis-метки на N-конце этой аминокислотной последовательности, для удобства очистки.
pCAGGS-Flag-His-S100A8 трансфицировали в культивируемую клеточную линию, происходящую из клеток почки эмбриона человека, HEK 293 с использованием полиэтиленимина (PEI). Через 48 часов клетки и культуральный супернатант по отдельности собирали центрифугированием при 4400 G при 4°C в течение пяти минут. Затем собранный супернатант фильтровали через фильтр из ацетата целлюлозы, имеющий поры диаметром 0,8 мкм, а затем через фильтр из нитроцеллюлозы, имеющий поры диаметром 0,45 мкм, для получения образца, из которого удалены нерастворимые фракции. Образец наносили на 5-мл HisTrap FF (GE), уравновешенную 50 мл 50 мМ Tris HCl (pH 8,0) содержавшим 50 мМ NaCl, а затем адсорбированные компоненты промывали 50 мМ Tris HCl (pH 8,0), содержавшим 50 мМ NaCl и 10 мМ имидазола, для удаления не специфически адсорбированных компонентов. Специфично адсорбированные компоненты элюировали с колонки с использованием 50 мМ Tris HCl (pH 8,0), содержавшего 50 мМ NaCl и 100 мМ имидазола. Адсорбированные фракции фракционировали в покрытые силиконом пластмассовые пробирки (500 мкл/пробирка). Содержавшие белок фракции объединяли, а затем имидазол удаляли с использованием колонки для обессоливания PD10 (GE). Фракции элюировали с использованием 50 мМ Tris HCl (pH 7,5), содержавшего 150 мМ NaCl. К элюированным образцам добавляли HRV3C (Novagen) и смесь инкубировали при 4°C в течение восьми часов. После расщепления образец наносили на 1-мл колонку с гепарином HiTrap Heparin column (GE), уравновешенную 50 мМ Tris HCl (pH 7,5), содержавшим 150 мМ NaCl. Внутри колонку промывали 50 мМ Tris HCl (pH 7,5), содержавшим 150 мМ NaCl. Белок, связавшийся с колонкой, элюировали 50 мМ Tris HCl (pH 7,5), содержавшим 1000 мМ NaCl. Элюированный образец разбавляли в 50 раз 50 мМ Tris HCl (pH 8,8), содержавшим 20 мМ NaCl, и адсорбировали на 1-мл HiTrap Q FF (GE), уравновешенную тем же буфером. Адсорбированный белок элюировали посредством 50 мМ Tris HCl (pH 8,8), содержавшего 500 мМ NaCl, постепенно увеличивая концентрацию NaCl. Присутствие белка, связанного с никелевой колонкой, колонкой с гепарином, и колонкой Q, подтверждали посредством SDS-PAGE, а затем окрашиванием кумасси бриллиантовым голубым.
В результате очищали в высокой степени чистый HMGB-1, как представлено на фиг.1. В представленных ниже примерах использовали HMGB-1, очищенный этим способом очистки.
Из кожи новорожденных мышей экстрагировали РНК с использованием Trizol (Invitrogen), а затем синтезировали кДНК с использованием набора для синтеза кДНК SuperScript III (Invitrogen). С использованием этой кДНК в качестве матрицы, амплифицировали кДНК S100A8 способом полимеразной цепной реакции (ПЦР). Полученную кДНК встраивали в pCAGGS, плазмидный вектор для экспрессии белка в клетках млекопитающих, так чтобы вектор экспрессировал белок, связанный с последовательностью GST-метки (SEQ ID NO: 31 (аминокислотная последовательность); SEQ ID NO: 32 (последовательность ДНК)) (фиг.39).
В культивируемую клеточную линию, происходящую из клеток почки эмбриона человека, HEK 293 трансфицировали pCAGGS-GST-S100A8 с использованием реагента для липофекции (Invitrogen) и клетки и культуральный супернатант собирали через 48 часов. Клетки и культуральный супернатант центрифугировали при 4400 g в течение 5 минут при 4°C для отбора супернатанта (супернатант A) и клеток по отдельности. К клеткам добавляли PBS, содержавший 0,1% Tween 20 и подвергали их обработке ультразвуком в течение 30 секунд на льду для разрушения клеточных мембран. После центрифугирования при 4400 g в течение 5 минут при 4°C супернатант собирали (супернатант B). Супернатанты A и B объединяли и наносили на колонку HiTrap GST FF (GE healthcare; 5 мл), в которой буфер был заранее заменен на 30 мл PBS. После нанесения колонку промывали 100 мл PBS, и адсорбированный белок элюировали 20 мМ фосфатным буфером (pH 8), содержавшим восстановленный глутатион. Для удаления глутатиона буфер заменяли PBS с использованием колонки для гель-фильтрации PD-10 (GE).
Пример 2
Эффект внутривенного введения HMGB-1 и S100A8 на привлечение происходящих из костного мозга клеток в область изъязвления кожи в процессе заживления язвы кожи
Самцов мышей C57BL/6 (в возрасте 6 недель) облучали летальной дозой (10 Гр). Сразу после этого через хвостовую вену трансплантировали клетки костного мозга (5×106 клеток/0,1 мл физиологический фосфатный буфер (pH 7,4)), полученного от трансгенных мышей с зеленым флуоресцентным белком (GFP) (Okabe M. et al., FEBS Lett. 407, 313-319, 1997). Через 8 недель на спине создавали округлую язву кожи диаметром 6 мм. Для предотвращения стягивания кожи мышей к области язвы прикрепляли силиконовое кольцо с наружным диаметром 10 мм, внутренним диаметром 6 мм и толщиной 1 мм с использованием двухсторонней клейкой ленты и медицинского адгезива Aron alpha A (Sankyo). Язву закрывали силиконовым диском диаметром 10 мм и толщиной 1 мм для предотвращения обезвоживания и бактериальной инфекции в язве. Кроме того, язву закрывали Tegaderm (3M) для защиты.
HMGB-1 (40 мкг) или S100A8 (250 нг) вводили через хвостовую вену пять раз с 24-часовыми интервалами, начиная с дня создания язвы кожи. Через две недели после создания язвы кожи, мышам давали анестезию путем ингаляции изофлурана, а затем выявляли степень флуоресценции GFP в области язвы кожи, созданной на спине, с использованием флуоресцентного стереоскопического микроскопа. Затем из области созданной язвы вырезали кожу округлой формы и фиксировали ее в PBS (фосфатный буфер; Nacalai), содержавшем 4% параформальдегид. После погружения в состав OCT, кожу нарезали на 8-мкм срезы с использованием микротома с охлаждающим устройством (Leica). Срезы фиксировали на предметных стеклах. Затем состав смывали с помощью PBS и ядра окрашивали с помощью DAPI. Далее срезы промывали PBS для удаления избытка DAPI, и заливали средой для заливки, содержащей реагент против обесцвечивания. Детекцию флуоресценции GFP каждого образца проводили с использованием флуоресцентного микроскопа.
Результат представлен на фиг.2. Было выявлено, что у мышей, которым вводили HMGB-1 или S100A8, происходящие из костного мозга клетки (положительные по GFP клетки) по сравнению с контролем накапливаются в дермисе, в частности, в верхнем слое, после закрытия язвы кожи.
Плюрипотентные стволовые клетки костного мозга могут дифференцироваться в остеобласты, хондроциты, адипоциты и другие. Также полагают, что в кожных тканях они способны дифференцироваться в эпидермальные клетки, клетки волосяных фолликулов, дермальные фибробласты и т.п. Уже было выявлено, что HMGB-1 и S100A8 обладают активностью привлечения плюрипотентных стволовых клеток костного мозга и имеют эффект уменьшения язвы кожи у мышей при введении их прямо в область язвы кожи. Однако данный результат впервые продемонстрировал, что происходящие из костного мозга клетки привлекаются в область изъязвления кожи путем введения HMGB-1 и S100A8 в венозную кровь, которая не является целевой областью и отдалена от области изъязвления.
Пример 3
Эффект внутривенного введения HMGB-1 и S100A8 на стимуляцию заживления язвы кожи
У самцов мышей C57BL/6 (в возрасте 6 недель) на спине создавали округлую язву кожи диаметром 6 мм. Для предотвращения стягивания кожи мышей к области язвы прикрепляли силиконовое кольцо с наружным диаметром 10 мм, внутренним диаметром 6 мм и толщиной 1 мм с использованием двухсторонней клейкой ленты и медицинского адгезива Aron alpha A (Sankyo). Язву закрывали силиконовым диском диаметром 10 мм и толщиной 1 мм для предотвращения обезвоживания и бактериальной инфекции в язве. Кроме того, язву закрывали Tegaderm (3M) для защиты.
HMGB-1 (40 мкг) или S100A8 (250 нг) вводили через хвостовую вену пять раз с 24-часовыми интервалами, начиная с дня создания язвы кожи. Размер язвы измеряли на 3, 5, и 10 сутки после создания язвы.
Результат представлен на фиг.3. HMGB-1 снижал размер язвы на 3 сутки после создания язвы по сравнению с отрицательным контролем (введение PBS). Между тем, S100A8 снижал размер язвы на 7 сутки после создания язвы по сравнению с отрицательным контролем (введение PBS).
Эффекта заживления язвы кожи традиционно достигали путем введения HMGB-1 или S100A8 непосредственно в область язвы кожи. Однако настоящее исследование впервые оказалось успешным в отношении стимуляции заживления язвы кожи путем введения HMGB-1 или S100A8 в кровеносный сосуд, который был нецелевой областью и был отдален от области изъязвления. Настоящее изобретение обеспечивает лечение язв кожи без прямого введения в область изъязвления. Таким образом, возможно разработать фармацевтические средства, которые можно использовать даже для условий, где прямое введение в область изъязвления является трудным, таким как обширная язва кожи, язва, ассоциированная с потерей кожи, инфицированные очаги повреждения или некротизирующие очаги повреждения и т.п.
Пример 4
Эффект внутривенного введения HMGB-1 на стимуляцию заживления язвы кожи без рубца
У самцов мышей C57BL/6 (в возрасте 8 недель) на спине создавали округлую язву кожи диаметром 6 мм. Для предотвращения стягивания кожи мышей к области язвы прикрепляли силиконовое кольцо с наружным диаметром 10 мм, внутренним диаметром 6 мм и толщиной 1 мм с использованием двухсторонней клейкой ленты и медицинского адгезива Aron alpha A (Sankyo). Язву закрывали силиконовым диском диаметром 10 мм и толщиной 1 мм для предотвращения обезвоживания и бактериальной инфекции в язве. Кроме того, язву закрывали Tegaderm (3M) для защиты.
HMGB-1 (40 мкг) вводили через хвостовую вену пять раз с 24-часовыми интервалами, начиная с дня создания кожной язвы. Через четыре недели после создания язвы брали образец части язвы и фиксировали его в 10% забуференном формальдегиде. Образцы погружали в парафин, а затем нарезали на тонкие срезы с использованием микротома. После депарафинизации срезы обрабатывали окрашиванием гематоксилином-эозином (HE) и окрашиванием трихромной краской Массона (MT).
Результат представлен на фиг.4. На коже мышей, которым вводили HMGB-1, в верхнем слое дермы наблюдали область, строго положительную по окрашиванию трихромной краской Массона по сравнению с контрольными мышами (введение PBS).
Известно, что в процессе заживления язвы кожи, язва закрывается рубцовым заживлением, если восстановление кожных тканей является недостаточным. Рубцовое заживление относится к закрытию язвы неклеточными компонентами, такими как коллагеновое волокно, секретируемое фибробластами, и т.п. Поскольку рубец не имеет функциональной тканевой структуры, в отличие от нормальных тканей, он ассоциирован с уплотнением и стягиванием ткани даже после заживления. Таким образом, подавление образования рубца является важной задачей с функциональной и косметической точки зрения. Данный результат демонстрирует, что возможно стимулировать раннее закрытие и заживление язвы кожи без рубца путем введения HMGB-1 внутривенно и, тем самым, привлечения происходящих из костного мозга в область изъязвления.
Пример 5
Наблюдение происходящих из костного мозга клеток в головном мозге модельных животных с инфарктом головного мозга, которым внутривенно вводили HMGB-1
Инфаркт головного мозга создавали у мышей с трансплантированным костным мозгом с GFP (модель окклюзии средней мозговой артерии внутрипросветной нитью). В частности, мышам с трансплантированным костным мозгом с GFP, полученным способом согласно упомянутому выше примеру, проводили анестезию путем ингаляции изофлурана. Затем кожу головы открывали и зонд лазерного допплеровского измерителя скорости кровотока присоединяли непосредственно к кости черепа для мониторинга кровотока головного мозга. Далее проводили срединный надрез кожи от грудины к нижней челюсти. Правую общую сонную артерию отделяли и лигировали слабо шелковым швом #4. Правую наружную сонную артерию лигировали в дистальном положении с использованием шелкового шва #6. На правой наружной сонной артерии делали прокол в проксимальном положении при натяжении шва вокруг общей сонной артерии. В область прокола помещали шов из нейлоновой мононити #6 (внутрипросветная нить), причем в область прокола помещали кончик размером 700 мкм, сформированный нагреванием. Нить продвигали вдоль внутренней сонной артерии, пока не был помещен кончик шва размером приблизительно 8 мм. Затем шов вокруг общей сонной артерии ослабляли. Было подтверждено, что показатели лазерного допплеровского измерителя скорости кровотока были снижены в 10 раз после блокирования кровотока.
Через 30 минут после блокирования кровотока внутрипросветную нить удаляли для восстановления кровотока. Через 12 часов, через хвостовую вену полученной мыши с моделью заболевания вводили HMGB-1 (100 мкг), разбавленного 500 мкл PBS. Затем HMGB-1 вводили четыре раза с 24-часовыми интервалами аналогичным образом. Контрольным мышам вводили PBS.
Через две недели после последнего дня введения проводили перфузионную фиксацию с использованием 2% параформальдегида под ингаляционной анестезией изофлураном. Головной мозг извлекали из черепной кости и дегидратировали путем погружения в 10% раствор сахарозы на 12 часов, а затем в 20% раствор сахарозы на 24 часа. После дегидратации головной мозг помещали в состав OTC и замораживали на сухом льду для приготовления блока. Блок нарезали на 8-мкм срезы с помощью микротома для изготовления срезов из замороженных образцов, и срезы укладывали на покрытые силаном предметные стекла. После укладывания срезы тщательно сушили и промывали PBS для удаления состава.
PBS, содержавшему 2% обезжиренное молоко, позволяли пропитать образцы, а затем антителу против нестина мыши и антителу против βIII тубулина, разбавленным в 500 раз в PBS, содержавшем 2% обезжиренное молоко, позволяли пропитать образцы при 4°C в течение 8 часов. После тщательного промывания образцов PBS в течение 5 минут пять раз, меченному PE антителу против IgG крысы, разбавленному в 500 раз PBS, содержавшему 2% обезжиренное молоко, позволяли пропитать образцы в течение одного часа при комнатной температуре. После тщательного промывания PBS аналогичным образом, раствору DAPI позволяли пропитать образцы в течение 10 минут при комнатной температуре. Затем образцы тщательно промывали PBS. Образцы заливали средой для заливки, содержавшей средство против обесцвечивания, и наблюдали в отношении флуоресценции GFP, DAPI и PE с использованием конфокального лазерного микроскопа.
Результат представлен на фиг.5. В головном мозге мышей, которым вводили HMGB-1, было выявлено много происходящих из костного мозга клеток (положительных по GFP клеток), и некоторые происходящие из костного мозга клетки были положительными по нестину (желтые клетки на правой панели), в то время как другие были положительны по βIII тубулину (желтые клетки на левой панели). Происходящие из костного мозга клетки также наблюдали в группе введения PBS; однако ни одна из клеток не экспрессировала нестин или βIII-тубулин (фотографии не представлены).
Известно, что происходящие из костного мозга клетки дифференцируются в нервные клетки in vitro (в культуральной системе). Более того, известно, что происходящие из костного мозга клетки in vivo (в организме) редко экспрессируют нейрональные маркеры в головном мозге. Однако неясно, имеют ли такие происходящие из костного мозга клетки неврологические функции в головном мозге. Между тем, было показано, что невоспалительные клетки костного мозга, такие как мезенхимальные стволовые клетки костного мозга, вызывают терапевтический эффект при введении при патологичном состоянии инфаркта головного мозга. Однако механизм заживления еще предстоит установить.
Данный результат показал, что происходящие из костного мозга клетки, экспрессирующие маркеры нервных клеток, присутствовали в головном мозге мышей, которым проводили внутривенное введение HMGB-1 после создания инфаркта головного мозга. Эти положительные по GFP клетки предположительно происходят из невоспалительных клеток, таких как мезенхимальные стволовые клетки костного мозга.
Пример 6
Эффект введения HMGB-1 на снижение размера инфаркта головного мозга
Самок мышей C57/Bl6 в возрасте восьми недель подвергали анестезии путем ингаляции изофлурана. Затем кожу головы открывали и зонд лазерного допплеровского измерителя скорости кровотока присоединяли непосредственно к кости черепа для мониторинга кровотока головного мозга. Далее проводили срединный надрез кожи от грудины к нижней челюсти. Правую общую сонную артерию отделяли и лигировали слабо шелковым швом #4. Правую наружную сонную артерию лигировали в дистальном положении с использованием шелкового шва #6. На правой наружной сонной артерии делали прокол в проксимальном положении при натяжении шва вокруг общей сонной артерии. В область прокола помещали шов из нейлоновой мононити #6 (внутрипросветная нить), причем в область прокола помещали кончик размером 700 мкм, сформированный нагреванием. Нить продвигали вдоль внутренней сонной артерии, пока не был помещен кончик шва размером приблизительно 8 мм. Затем шов вокруг общей сонной артерии ослабляли. Было подтверждено, что показатели лазерного допплеровского измерителя скорости кровотока были снижены в 10 раз после блокирования кровотока.
Через 30 минут после блокирования кровотока внутрипросветную нить удаляли для восстановления кровотока. Через 12 часов, через хвостовую вену полученной мыши с моделью заболевания вводили HMGB-1 (10 мкг), разбавленного 500 мкл PBS. Затем HMGB-1 вводили четыре раза с 24-часовыми интервалами аналогичным образом. Контрольным мышам вводили PBS.
Через пять суток после последнего дня введения проводили перфузионную фиксацию с использованием 2% параформальдегида под ингаляционной анестезией изофлураном. Головной мозг извлекали из черепной кости. После дегидратации головной мозг помещали в состав OTC и замораживали на сухом льду для приготовления блока. Блок нарезали на 8-мкм срезы с помощью микротома для изготовления срезов из замороженных образцов, и срезы укладывали на покрытые силаном предметные стекла. После укладывания срезы тщательно сушили и промывали PBS для удаления состава OCT. После фиксации в течение 10 минут PBS, содержавшего 4% параформальдегид, срезы промывали фосфатным буфером в течение 5 минут и погружали в дистиллированную воду на 10 минут. Затем образцы окрашивали в течение 13 минут 0,5% раствором крезилового фиолетового. После промывания в течение одной минуты дистиллированной водой срезы погружали в 50% этанол, 75% этанол, 95% этанол и 100% этанол на 10 секунд в каждом случае, два раза в ксилол на две минуты и, наконец, заливали с использованием Entellan.
Результат представлен на фиг.6. У мышей, которым вводили HMGB-1, наблюдали значительное улучшение после инфаркта головного мозга по сравнению с мышами, которым вводили PBS.
В описанном выше эксперименте эффект уменьшения инфаркта головного мозга обеспечивали путем внутривенного введения HMGB-1 после создания инфаркта головного мозга. Ранее было показано, что внутривенное введение собственных клеток костного мозга пациента после инфаркта головного мозга обеспечивает эффект смягчения инфаркта головного мозга. Поскольку HMGB-1 обладает активностью привлечения происходящих из костного мозга плюрипотентных стволовых клеток, можно ожидать, что он вызовет тот же эффект, что и внутривенное введение клеток костного мозга. Кроме того, поскольку прямое введение HMGB-1 в область инфаркта головного мозга может потенциально вызывать повреждения и воспаление в тканях головного мозга, введение в нецелевую область, например, внутрисосудистое введение и подкожное введение, как используют в описанных выше экспериментах, является превосходным способом введения, который обеспечивает терапевтическое лечение инфаркта головного мозга.
Пример 7
Улучшение уровня выживаемости после инфаркта головного мозга путем введения HMGB-1
Самцов мышей C57/Bl6 в возрасте восьми недель подвергали анестезии путем ингаляции изофлурана. Затем кожу головы открывали и зонд лазерного допплеровского измерителя скорости кровотока присоединяли непосредственно к кости черепа для мониторинга кровотока головного мозга. Далее проводили срединный надрез кожи от грудины к нижней челюсти. Правую общую сонную артерию отделяли и лигировали слабо шелковым швом #4. Правую наружную сонную артерию лигировали в дистальном положении с использованием шелкового шва #6. На правой наружной сонной артерии делали прокол в проксимальном положении при натяжении шва вокруг общей сонной артерии. В область прокола помещали шов из нейлоновой мононити #6 (внутрипросветная нить), причем в область прокола помещали кончик размером 700 мкм, сформированный нагреванием. Нить продвигали вдоль внутренней сонной артерии, пока не был помещен кончик шва размером приблизительно 8 мм. Затем шов вокруг общей сонной артерии ослабляли. Было подтверждено, что показатели лазерного допплеровского измерителя скорости кровотока были снижены в 10 раз после блокирования кровотока.
После блокирования кровотока в течение определенного периода времени (45 или 60 минут) у каждой мыши, внутрипросветную нить удаляли для восстановления кровотока. Через 12 часов, через хвостовую вену полученной мыши с моделью заболевания вводили очищенный HMGB-1 (10 мкг), разбавленного 500 мкл PBS. Затем HMGB-1 вводили четыре раза с 24-часовыми интервалами аналогичным образом. Контрольным мышам вводили PBS. Мониторинг уровня выживаемости проводили в течение 7 суток после создания инфаркта.
Результат представлен на фиг.7. Все мыши, которых подвергали инфаркту в течение 30 минут, выжили в течение 7 суток (N=3) (фигура не представлена). У мышей, подвергнутых инфаркту в течение 45 минут, уровень выживаемости в течение 7 суток составил 40% в группе введения PBS, в то время как в группе введения HMGB-1 выжили все мыши. У мышей, которых подвергали инфаркту в течение 60 минут, уровень выживаемости в течение 7 суток составил 50% в группе введения PBS, в то время как в группе введения HMGB-1 выжили все мыши.
В моделях инфаркта как в течение 45 минут и 60 минут, только приблизительно половина мышей в контрольной группе (группа введения PBS) выжили в течение 7 суток. Когда введение HMGB-1 начинали через 12 часов после создания инфаркта головного мозга, уровень выживаемости в течение 7 суток после создания инфаркта увеличивался. Инфаркт головного мозга влияет на прогноз выживания, в зависимости от области, площади и длительности инфаркта. Более того, инфаркт головного мозга часто вовлекает паралич, утрату сознания и т.п., которые могут вызывать задержку лечения медицинским учреждением. Современные фармацевтические средства с продемонстрированной эффективностью, такие как препарат t-PA, должны быть введены в пределах от 3 до 4 часов после начала. Таким образом, только очень небольшая доля всех случаев инфаркта головного мозга являются показаниями для таких препаратов. На сегодняшний день мало лекарственных средств, которые можно вводить и которые являются эффективными, даже после того, как пройдет длительный период времени после возникновения инфаркта головного мозга. Настоящее изобретение может улучшить прогноз выживания путем внутривенного введения, которое является очень простым менее инвазивным способом, даже когда введение начинают через длительный период (12 часов) после возникновения инфаркта головного мозга. Таким образом, возможно разработать новые лекарственные средства для лечения инфаркта головного мозга, которые можно вводить при многих случаях инфаркта головного мозга.
Пример 8
Вовлечение плюрипотентных стволовых клеток костного мозга из областей, отличных от области перелома кости, в процесс заживления перелома кости
Самцов мышей C57BL/6 (в возрасте 6 недель) облучали летальной дозой (10 Гр). Сразу после этого через хвостовую вену трансплантировали клетки костного мозга (5×106 клеток/0,1 мл физиологический фосфатный буфер (pH 7,4)), полученного от трансгенных мышей с зеленым флуоресцентным белком (GFP) (химерная мышь с костным мозгом с GFP). Через 8 недель химерную мышь с костным мозгом с GFP (мышь слева на фиг.8) и мышь дикого типа (мышь справа на фиг.8) соединяли через кожу для парабиоза. Затем на правой задней конечности мыши дикого типа (мышь справа на фиг.8) создавали перелом кости. После заживления перелома кости получали срезы тканей. Срезы тканей блокировали PBS, содержащим 4% обезжиренное молоко, а затем подвергали реакции с антителом против остеокальцина мыши, разбавленным PBS, содержащим 4% обезжиренное молоко. После промывания PBS срезы подвергали реакции при комнатной температуре в течение одного часа с меченным PE антителом против IgG крысы, разбавленным PBS, содержащим 4% обезжиренное молоко. После промывания PBS, ядра окрашивали с помощью DAPI. Затем образцы промывали PBS. После заливки наблюдали флуоресценцию с использованием конфокального лазерного микроскопа.
Результат представлен на фиг.8. Остеокальцин (OC) визуализируют в качестве красной флуоресценции, а положительные по GFP клетки, т.е. происходящие из костного мозга клетки визуализируют в качестве зеленой флуоресценции. На изображении с наложением (Merge), желтые клетки представляют собой положительные по остеокальцину происходящие из костного мозга клетки. Таким образом, на фиг.8 продемонстрировано, что клетки костного мозга химерной мыши с костным мозгом с GFP слева мигрировали в область перелома кости в правой задней конечности мыши дикого типа и дифференцировались в остеобласты.
Ранее полагали, что в процессе заживления перелома костей, остеобласты вблизи поврежденной области накапливаются в поврежденной области и стимулируют заживление. Однако данный результат демонстрируют, что происходящие из костного мозга клетки, отдаленные от поврежденной области, мигрируют в область перелома кости и восстанавливают поврежденные ткани. Мышь справа имеет подкожную и внутрикожную сосудистую связь с мышью слева. Таким образом, если значительное количество костномозговых плюрипотентных стволовых клеток костного мозга, таких как мезенхимальные стволовые клетки костного мозга, могут успешно привлекаться в кровь из костного мозга по всему организму, можно ожидать, что они будут стимулировать заживление в области перелома кости.
Пример 9
Задачи: оценка внутривенно вводимого HMGB1 в отношении активности привлечения мезенхимальных стволовых клеток костного мозга в поврежденную область у модельных мышей с переломом кости
Способы: исследования проводили следующими способами для осуществления описанной выше задачи:
(1) В эксперименте использовали мышей, в геном которых был встроен GFP ниже промотора рецептора PDGF α (мыши PDGFRα-GFP) (ссылка: Hamilton et al., Mol Cell Biol. 2003 Jun; 23(11):4013-25). Мыши экспрессируют GFP в клетках, экспрессирующих PDGF рецептор α, который можно выявлять в качестве зеленой флуоресценции при наблюдении с помощью флуоресцентного микроскопа.
(2) Клетки костного мозга отбирали у мышей PDGFRα-GFP и высевали в чашки для культивирования клеток. Клетки культивировали в α-MEM, содержавшей 10% FBS. Среду заменяли каждые трое или четверо суток, и прикрепившиеся клетки собирали приблизительно через 14 суток. Собранные клетки сортировали на положительные по CD11b клетки и отрицательные по CD11b клетки с использованием гранул MACS с антителом против CD11b. Флуоресцентная микроскопия продемонстрировала, что положительные по CD11b клетки были отрицательными по GFP (фиг.42, A1 и A2), в то время как отрицательные по CD11b клетки были положительными по GFP (фиг.42, B1 и B2). Для тестирования того, индуцирует ли HMGB1 миграцию этих клеток, проводили способ с камерой Бойдена. Положительные по CD11b клетки или отрицательные по CD11b клетки помещали в верхний уровень камеры Бойдена. HMGB1 разбавляли до 0, 50, или 100 мкг/мл посредством DMEM, содержавшей 10% FBS, и добавляли в нижний уровень. Камере позволяли стоять при 37°C в 5% CO2 в инкубаторе. Через четыре часа мембрану удаляли из камеры и клетки, которые мигрировали в нижний уровень, выявляли путем окрашивания (фиг.43).
(3) Самцов мышей PDGFRα-GFP в возрасте 12 недель подвергали общей анестезии с использованием изофлурана и на большеберцовой кости левой нижней конечности осуществляли модель перелома кости. Десять мкг HMGB1, разбавленного в 500 мкл PBS, вводили через хвостовую вену сразу, через 24 часа и 48 часов после создания перелома кости. У отрицательных контролей 500 мкл PBS вводили через хвостовую вену (N=6).
(4) Через 72 часа после создания перелома кости левую большеберцовую кость удаляли и оставляли ее на 24 часа в PBS, содержавшем 4% параформальдегид, для фиксации ткани. Кость промывали PBS, а затем наблюдали под флуоресцентным стереоскопическим микроскопом для детекции флуоресценции GFP (фиг.44).
Результаты: CD11b-положительные клетки были отрицательными по GFP, что указывает на то, что эти клетки не экспрессируют рецептор PDGF α (фиг.42; A1 и A2). Отрицательные по CD11b клетки были положительными по GFP, указывая на то, что они экспрессируют рецептор PDGF α (фиг.42; B1 и B2). HMGB1 не индуцировали миграцию CD11b-положительных (рецептор PDGF α-отрицательных) клеток; однако они индуцировали миграцию CD11b-отрицательных (рецептор PDGF α-положительных) клеток (фиг.43).
По сравнению с отрицательными контрольными мышами группы введения PBS (фиг.44; D1), у четырех из шести мышей группы введения HMGB1 (фиг.44; D2), были выявлены GFP-положительные (рецептор PDGF α-положительные) клетки в кости вокруг области перелома кости.
Обсуждение: в настоящем эксперименте мышей (мышей PDGFRα-GFP), клетки которых, положительные по рецептору для PDGF α, который является одним из маркеров мезенхимальных стволовых клеток костного мозга, экспрессируют GFP, использовали для выявления живых мезенхимальных стволовых клеток костного мозга. Клетки костного мозга включают кроветворные клетки (эритроциты, лейкоциты, макрофаги и т.д.) и мезенхимальные клетки. Известно, что среди них макрофаги (CD11b-положительные) и мезенхимальные стволовые клетки костного мозга (CD11b-отрицательные) прикрепляются к чашкам для культивирования клеток. Между тем, поскольку рецептор PDGF α является маркером мезенхимальных стволовых клеток костного мозга, CD11b-отрицательные, GFP-положительные (рецептор PDGF α-положительные) клетки, выявленные в этом эксперименте, могут быть мезенхимальными стволовыми клетками костного мозга. Результат способа с камерой Бойдена продемонстрировал, что HMGB1 индуцировал миграцию мезенхимальных стволовых клеток костного мозга (рецептор PDGF α-положительные, CD11b-отрицательные) без индукции миграции макрофагов (CD11b-положительные клетки). Кроме того, в модели перелома кости с использованием мышей PDGFRα-GFP, было выявлено, что GFP-положительные клетки (рецептор PDGF α-положительные клетки) собираются вокруг области перелома кости в группе введения HMGB1, по сравнению с группой отрицательного контроля. Эти GFP-положительные клетки считаются мезенхимальными стволовыми клетками костного мозга, привлеченными HMGB1.
Известно, что мезенхимальные стволовые клетки костного мозга являются плюрипотентными стволовыми клетками, которые дифференцируются в остеобласты, хондроциты, адипоциты и прочие. Между тем, в основном, полагают, что перелом кости заживляется остеобластами, мигрирующими из области перелома кости или окружающих областей. Однако, как показано с помощью результата эксперимента с парабиозом в примере 8 мезенхимальные стволовые клетки костного мозга в костях, отличных от области перелома кости, могут участвовать в регенерации области перелома кости.
Данный экспериментальный результат показал, что мезенхимальные стволовые клетки костного мозга, которые привлекались в кровь путем внутривенного введения HMGB1, накопленного в область перелома кости. Это указывает на то, что HMGB1 можно использовать в качестве лекарственного средства при переломе кости.
Макрофаги, которые являются CD11b-положительными (рецептор PDGF α-отрицательными), являются воспалительными клетками. Таким образом, не позволение макрофагам мигрировать обеспечит предупреждение чрезмерного воспаления. Чрезмерное воспаление является нежелательным для регенерации ткани, поскольку оно может увеличить повреждение ткани и длительность заживления. Описанный выше результат демонстрирует, что HMGB1 обладает активностью специфической индукции миграции мезенхимальных стволовых клеток, которые являются эффективными для регенерации тканей.
Традиционно, перелом костей, главным образом, лечат путем неинвазивного восстановления, хирургической операции и иммобилизацией. Фармацевтических средств для активной стимуляции заживления перелома кости существует мало. Поскольку настоящий способ осуществляют путем внутривенного введения средства, он также применим для трудноизлечимых переломов костей, переломов костей, которые трудно лечить хирургической операцией и т.п. Таким образом, настоящий способ обеспечивает новое достижение в терапии.
Справочный пример 1
Задача: оценка вклада происходящих из костного мозга клеток в функциональную регенерацию ткани кожи, трансплантированной в живой организм.
Способы: ввиду указанной выше задачи исследования проводили с помощью следующих способов.
1) C использованием системы трансплантата живой кожи у мышей с трансплантированным костным мозгом с GFP, исследовали степень вклада происходящих из костного мозга в функциональную регенерацию трансплантированной кожи. В частности, самцов мышей C57BL/6 в возрасте от 6 до 8 недель облучали летальной дозой радиационного излучения (10 Гр), и сразу после этого через хвостовую вену трансплантировали полученные от трансгенной мыши с GFP (зеленый флуоресцентный белок) клетки костного мозга (5×106 клеток/0,1 мл физиологического фосфатно-солевого буфера при pH 7,4).
2) Трансплантированным клеткам костного мозга позволяли прижиться (в течение 6 недель), и в результате получали мышей с трансплантированным костным мозгом с GFP. Затем кожу новорожденной мыши (самки) трансплантировали на кожу спины мышей с трансплантированным костным мозгом с GFP.
3) Трансплантату кожи позволяли прижиться и после удовлетворительной регенерации ткани кожи (4 недели), степень накопления флуоресценции GFP в области трансплантированной кожи наблюдали с использованием флуоресцентного стереоскопического микроскопа.
4) Под ингаляционной анестезией, трансплантат кожи извлекали путем биопсии. Затем получали замороженные срезы кожи (6 мкм) с использованием микротома с охлаждающим устройством, а затем фиксировали 4% параформальдегидом (в течение 30 минут). Ядра клеток в ткани окрашивали с помощью DAPI. Иммунное окрашивание проводили с использованием антитела против эпидермального специфичного к клеткам кератина 5. Ткань закрепляли для исследования присутствия GFP-положительных происходящих из костного мозга клеток с помощью конфокального лазерного микроскопа. Часть образца окрашивали с помощью HE для исследования конструкции его ткани.
Результаты: в системе трансплантата живой кожи у мышей с трансплантированным костным мозгом с GFP, наблюдали значительное накопление флуоресценции GFP, соответствующее области регенерировавшей кожи (фиг.9). Более того, при гистологическом наблюдении с использованием окрашенного образца HE трансплантата кожи, наблюдали функциональную регенерацию ткани кожи, содержащей большое количество волосяных фолликулов (фиг.9). При исследовании с использованием конфокального лазерного микроскопа, флуоресценцию GFP наблюдали во многих экспрессирующих кератин 5 эпидермальных кератиноцитах, дермальных фибробластах и, кроме того, в гладкомышечных клетках и адипоцитах, демонстрируя, что эти клетки происходят из костного мозга (фиг.10). Следовательно, впервые было выявлено, что многие эпителиальные и мезенхимальные клетки, требуемые для функциональной регенерации трансплантированной кожи, были образованы из происходящих из костного мозга стволовых клеток.
Обсуждение: впервые эти результаты исследования явно демонстрируют крупное открытие, что происходящие из костного мозга клетки вносят значительный вклад в регенерацию кожи после трансплантации кожи, что является общепринятой клинической процедурой.
Описано, что костный мозг имеет две системы стволовых клеток: гемопоэтические стволовые клетки и мезенхимальные стволовые клетки. Трудно представить, что большое количество происходящих из костного мозга эпителиальных клеток и мезенхимальных клеток, которые были мобилизованы в трансплантированную кожу (как показано с помощью настоящего исследования) поступали только из происходящих из костного мозга гемопоэтических стволовых клеток. Это строго предполагает о возможном вкладе происходящих из костного мозга мезенхимальных стволовых клеток в функциональную регенерацию трансплантированных тканей. Следовательно, было предсказано, что сразу после трансплантации кожи фактор для мобилизации происходящих из костного мозга мезенхимальных стволовых клеток высвобождается из ткани кожи реципиента, направляясь в область гипоперфузии/некроза, в которой мезенхимальные стволовые клетки мобилизуются из костного мозга через периферический кровоток в трансплантированный фрагмент кожи, и, таким образом, индуцируя функциональную регенерацию ткани кожи.
Справочный пример 2
Задача: идентификация фактора, привлекающего происходящие из костного мозга стволовые клетки, в экстракте кожной ткани
Способы: имея задачу идентификации фактора, мобилизующего происходящие из костного мозга мезенхимальные стволовые клетки, который, как ожидается, будет высвобождаться из вырезанной кожи в условиях гипоперфузии, исследования проводили следующими способами.
1) Для получения происходящих из костного мозга мезенхимальных стволовых клеток мыши, клетки костного мозга собирали из кости бедра или голени мышей C57BL/6, а затем распределяли на планшете для культивирования клеток, имеющем 10% эмбриональную телячью сыворотку, содержащую D-MEM (Nacalai), в качестве клеточной культуральной среды, а затем культивировали в условиях 5% CO2 при 37°C. Когда клетки пролиферировали до состояния, когда они занимали от 70 до 100% дна планшета для культивирования, клетки снимали с планшета для культивирования с использованием 0,25% трипсина 1m MEDTA (Nacalai), а затем культивировали в описанных выше условиях. Этот процесс пассирования и культивирования повторяли по меньшей мере пять раз. Далее, эти прикрепляющиеся клетки выделяли и культивировали, а затем проводили анализ антигенов клеточной поверхности с использованием проточной цитометрии для подтверждения того, что эти клетки являются Lin-отрицательными, CD45-отрицательными, CD44-положительными, Sca-1-положительными и c-kit-отрицательными. Было подтверждено, что эти клетки способны дифференцироваться в клетки костей и адипоциты и обладают свойствами мезенхимальных стволовых клеток костного мозга.
2) Свободные фрагменты кожи, полученные от 400 новорожденных мышей, погружали в 400 мл физиологического фосфатно-солевого буфера при pH 7,4 (PBS). Раствор инкубировали при 4°C в течение 24 часов, а затем центрифугировали при 440 G при 4°C в течение 10 минут для удаления ткани. Супернатант собирали с получением экстракта кожи.
3) Чтобы подтвердить, что полученный таким образом экстракт ткани кожи обладает активностью привлечения происходящих из костного мозга мезенхимальных стволовых клеток, его активность индукции миграции происходящих из костного мозга мезенхимальных стволовых клеток мыши C57BL6, которые уже были получены в качестве клеточной линии авторами настоящего изобретения, исследовали с использованием камеры Бойдена. В частности, экстракт кожи (25 мкл) помещали в нижнее отделение (объем: 25 мкл) камеры Бойдена, и на него помещали поликарбонатную мембрану, имеющую поры размером 8 мкм. Далее на него помещали верхнее отделение (объем: 50 мкл) камеры Бойдена, чтобы они соприкасались, и заполняли суспензией происходящих из костного мозга мезенхимальных стволовых клеток (5×104 клеток/50 мл раствора для культивирования: DMEM/10% эмбриональная телячья сыворотка). Камеру инкубировали в инкубаторе с CO2 при 37°C в течение от 4 до 24 часов. После культивирования верхнее отделение удаляли и силиконовую мембрану удаляли. Количество происходящих из костного мозга мезенхимальных стволовых клеток, которые мигрировали в нижнее отделение через тонкие поры, количественно исследовали окрашиванием.
4) Для очистки факторов, имеющих активность мобилизации происходящих из костного мозга мезенхимальных стволовых клеток в экстракте кожи, проводили аффинную колоночную хроматографию с гепарином и хроматографию на анионообменной колонке (колонка Q). Экстракт кожи разбавляли в 10 раз 9 объемами 20 мМ фосфатного буфера при pH 7,5 при 4°C (разбавленный раствор A). В колонку HiTrap Heparin HP (объем колонки: 5 мл, GE Healthcare) заранее вливали 20 мМ фосфатный буфер при pH 7,5 (30 мл) для уравновешивания колонки. Далее разбавленному раствору A позволяли связаться с колонкой. Затем колонку промывали 20-мМ фосфатным буфером при pH 7,5 с помощью 100 мМ NaCl (30 мл). Для элюирования абсорбированных белков, в колонку вливали 20 мМ фосфатный буфер при pH 7,5 с 1000 мМ NaCl, для элюирования фракций в пробирки. Фракции, обладающие способностью индуцировать миграцию согласно способу оценки активности с использованием камеры Бойдена, описанной в 2), собирали из каждой абсорбированной фракции. Ее разбавляли 9 объемами 50 мМ Tris HCl pH 8,0 (разбавленный раствор B). В колонку HiTrap mono Q (объем колонки: 1 мл, GE Healthcare) заранее вливали 50 мМ Tris HCl pH 8,0 (30 мл) для уравновешивания колонки. Далее разбавленному раствору B позволяли связаться с колонкой. Для элюирования абсорбированных белков в колонку вливали Tris HCl, pH 8,0, и 1000 мМ NaCl, элюируя фракции в пробирки. Весь описанный выше процесс очистки можно проводить при от 4 до 16°C, однако предпочтительно его проводят при от 4 до 8°C, и более предпочтительно при 4°C. Элюаты оценивали способом оценки активности миграции с использованием камеры Бойдена, как описано в 2).
5) Полученные из экстракта кожи очищенные препараты, обладающие активностью мобилизации происходящих из костного мозга мезенхимальных клеток, которые получали путем комбинирования оценки активности миграции с использованием камеры Бойдена и колоночной хроматографии, подвергали SDS-PAGE электрофорезу для разделения в геле на основе молекулярной массы, и полосы мигрировавших белков выявляли окрашиванием серебром.
6) Среди групп полученных из экстракта кожи белков, которые подвергали SDS-PAGE электрофорезу и которые разделялись в геле в качестве отдельных полос окрашиванием серебром согласно 5), все белковые полосы, полученные из очищенных хроматографией препаратов, обладающие наиболее сильной активностью мобилизации происходящих из костного мозга мезенхимальных клеток вырезали, а затем проводили идентификацию этих белков масс-спектрометрией и анализ баз данных.
7) Среди идентифицированных групп белков, отбирали белки-кандидаты, обладающие активностью мобилизации происходящих из костного мозга мезенхимальных стволовых клеток. Очищенные препараты, включающие такие белки-кандидаты, обрабатывали нейтрализующими антителами (100 мкл раствора очищенного препарата инкубировали на льду в течение 30 минут с разбавленным в 100 раз поликлональным антителом белка-кандидата. Затем исследовали степень ингибирования активности мобилизации происходящих из костного мозга стволовых клеток путем оценки способности к миграции с использованием камеры Бойдена.
8) Полученные препараты происходящих из костного мозга мезенхимальных стволовых клеток смешивали с матригелем в объеме приблизительно 10%. Силиконовую трубку, имеющую диаметр приблизительно 1 мм и длину 5 мм заполняли матригелем, а затем подкожно трансплантировали в спину мышей с трансплантированным костным мозгом с GFP. Через две недели установленную трубку извлекали и количественно анализировали флуоресценцию GFP, испускаемую из происходящих из костного мозга клеток, которые мигрировали в трубку, с помощью флуориметра. Далее, мигрировавшие клетки отбирали из трубки и инокулировали в среду DMEM/10% эмбриональная телячья сыворотка, а затем культивировали в инкубаторе с CO2 для исследования активности мобилизации происходящих из костного мозга мезенхимальных стволовых клеток in vivo. Эти клетки, которые непрерывно культивировали в течение 2 недель, фиксировали с помощью 2% параформальдегида при 25°C в течение 10 минут и промывали PBS четыре раза, по 5 минут каждый, чтобы смыть параформальдегид. Затем их обрабатывали 2% раствором обезжиренного молока, и позволяли реагировать с антителом против кератина 5 мыши в 1000-кратном разведении (разбавленным 2% обезжиренным молоком, содержавшим 0,5% tween 20) при 4°C в течение 16 часов. Антитело смывали с помощью PBS четыре раза, каждый в течение 5 минут. Затем смеси позволяли реагировать с меченным Alexa546 антителом против IgG кролика, разбавленным в 1000 раз (разбавленным 2% обезжиренным молоком) при 25°C в течение 1 часа.
Результаты: начиная с раствора экстракта вырезанной кожи новорожденной мыши в PBS, белки, обладающие активностью мобилизации происходящих из костного мозга мезенхимальных стволовых клеток, подвергали идентификации и функциональному анализу упомянутыми выше способами. Оценка активности миграции с использованием камеры Бойдена показала, что экстракт кожи имеет чрезвычайно высокую активность привлечения происходящих из костного мозга мезенхимальных клеток (фиг.11). С использованием этой активности в качестве показателя, аффинную колонку с гепарином и анионообменную колонку (колонка Q) использовали для продолжения очистки целевого фактора. Каждую из полученных фракций анализировали SDS-PAGE электрофорезом. В результате, высокая активность мобилизации происходящих из костного мозга стволовых клеток была показана окрашиванием серебром в очищенном препарате, содержавшем несколько белков, которые разделялись в геле в форме отдельных полос (дорожка 7 на фиг.12). Полученные окрашенные серебром полосы вырезали, а затем подвергали масс-спектрометрии и анализу баз данных. В результате, было выявлено, что белок, обладающий молекулярной массой, приблизительно 25000, указанный стрелкой, представлял собой HMGB1 (фиг.12). Для проверки того, что HMGB1, содержащийся в этой очищенной фракции (дорожка 7) имеет предполагаемую активность мобилизации происходящих из костного мозга мезенхимальных стволовых клеток, проводили эксперимент по ингибированию миграции с использованием поликлонального антитела против MGB1. В результате, было выявлено, что поликлональное антитело против HMGB1 в высокой степени ингибирует активность очищенного препарата в отношении индукции миграции происходящих из костного мозга мезенхимальных стволовых клеток (фиг.13) и что фактор, мобилизующий происходящие из костного мозга стволовые клетки, в экстракте костного мозга представляет собой HMGB1.
Кроме того, для подтверждения того, что HMGB1 обладает активностью мобилизации происходящих из костного мозга мезенхимальных клеток in vivo, силиконовую трубку, содержащую этот очищенный препарат, подкожно помещали в спину мыши с трансплантированным костным мозгом с GFP. Через две недели исследовали свойства клеток, мобилизованных в трубку. В результате очищенный препарат HMGB1 мобилизовал большее количество GFP-положительных происходящих из костного мозга клеток в трубку (приблизительно в три раза) по сравнению с контролем (очищенный препарат, использованный для дорожки 4 в SDS-PAGE на фиг.12) (фиг.14). На фиг.15 представлено изображение с высоким увеличением, полученное с помощью флуоресцентного стереоскопического микроскопа. Кроме того, GFP-положительные клетки, мобилизованные в трубку, отбирали и культивировали в среде DMEM/10% эмбриональная телячья сыворотка. В результате, сразу после культивирования наблюдали плавающие клетки округлой формы (фиг.16), однако через 24 часа после этого было подтверждено, что GFP-положительные происходящие из костного мозга клетки прикреплялись на культуральную чашку и пролиферировали в форме веретеновидных подобных фибробластам клеток и, кроме того, в форме цилиндроидных подобных эпителиальным клеток (фиг.17). Когда эти клетки непрерывно культивировали в течение других 2 недель, среди GFP-положительных происходящих из костного мозга клеток наблюдали клетки, образующие волосяные фолликулы (фиг.18A; световое поле, низкое увеличение, фиг.18B; флуоресценция GFP, низкое увеличение, фиг.18C; световое поле, высокое увеличение, фиг.18D; флуоресценция GFP, высокое увеличение). Более того, когда иммуногистохимические способы использовали для кератина 5, маркера эпителиальных кератиноцитов, среди GFP-положительных происходящих из костного мозга клеток наблюдали положительные по кератину 5 клетки (фиг.18E; световое поле, фиг.18F; флуоресценция положительных по кератину 5 клеток).
Обсуждение: в этот раз, авторы настоящего изобретения впервые в мире открыли, что: свободные фрагменты кожи продуцируют HMGB1; продуцированный HMGB1 обладает активностью мобилизации большого количества происходящих из костного мозга мезенхимальных стволовых клеток во фрагменты кожи; происходящие из костного мозга мезенхимальные стволовые клетки, мобилизованные во фрагменты кожи, дифференцируются в мезенхимальные клетки, такие как фибробласты, адипоциты, гладкомышечные клетки в кожной ткани, и, кроме того, дифференцируются в клетки, которые формируют волосяные фолликулы из эпидермальных клеток, для индукции функциональной регенерации трансплантированных кожных тканей. Можно легко предсказать, что эта мобилизация происходящих из костного мозга мезенхимальных стволовых клеток посредством HMGB1 и получаемые в результате функции функциональной регенерации тканей, существуют не только для регенерации трансплантированной кожи, но также в качестве механизма индукции функциональной регенерации тканей в различных поврежденных органах/тканях, сопровождающего гипоперфузию/некроз. Авторы настоящего изобретения твердо верят, что, если разработка лекарственного средства с использованием состава HMGB1 обеспечивает мобилизацию происходящих из костного мозга мезенхимальных стволовых клеток в локальную область в процессе регенерации поврежденных тканей, она обеспечит терапию, индуцирующую функциональную регенерацию тканей для жизненно важных функциональных органов без того, чтобы органы стали дисфункциональными вследствие заживления с фиброзным рубцом.
Справочный пример 3
Задача: идентификация семейства HMGB1 в экстракте кожи и исследование активности привлечения мезенхимальных стволовых клеток.
Способы: наличие или отсутствие в неонатальном экстракте кожи мыши семейства белков HMGB подтверждали с использованием способа вестерн-блоттинга. Десять мкл экстракта кожи, полученного согласно справочному примеру 2 использовали в качестве образца и подвергали SDS-PAGE электрофорезу. Белки, разделенные в геле, переносили на PVDF-мембрану с использованием устройства для блоттинга (ATTO). Мембрану инкубировали с PBS, содержащим 3% обезжиренное молоко и 0,1% Tween 20 (S-T-PBS) при комнатной температуре в течение 1 часа, и затем ей позволяли реагировать с каждым из антитела кролика против HMGB1 мыши, антитела кролика против HMGB2 мыши, или антитела кролика против HMGB3 мыши, которые разбавляли в 1000 раз посредством S-T-PBS, при 4°C в течение 16 часов. После реакции мембрану PVDF промывали посредством S-T-PBS пять раз в течение 5 минут. Затем мембрану PVDF инкубировали с разбавленным в 2000 раз (разбавленным посредством S-T-PBS) меченным пероксидазой антителом козы против IgG кролика (GE Healthcare) при 25°C в течение 1 часа. Кроме того, после промывания посредством S-T-PBS пять раз в течение 5 минут мембране PVDF позволяли реагировать с системой для детекции вестерн-блоттингом ECL (GE Healthcare). Пленку ECL экспонировали и проявляли для детекции присутствия белков HMGB1, HMGB2 и HMGB3.
РНК экстрагировали из кожи новорожденной мыши с использованием Trizol (Invitrogen), и далее синтезировали кДНК с использованием набора SuperScript III cDNA Synthesis Kit (Invitrogen). С использованием этой кДНК в качестве матрицы амплифицировали кДНК HMGB1, HMGB2 и HMGB3 способом ПЦР (полимеразная цепная реакция). кДНК встраивали в плазмидный вектор pCAGGS для экспрессии белков в клетках млекопитающих, так чтобы могли экспрессироваться белки с дополнительной последовательностью Flag-метки (Asp-Tyr-Lys-Asp-Asp-Asp-Lys; SEQ ID NO: 30) на N-конце аминокислотной последовательности. Эти плазмидные векторы вводили в HEK293 (культуру клеточной линии, происходящую из почки эмбриона человека) и культивировали в течение 48 часов для экспрессии белков. Клетки, экспрессирующие каждый из белков HMGB1, HMGB2 и HMGB3 и культуральный супернатант, инкубировали при 4°C в течение 16 часов, а затем их центрифугировали при 4400 g в течение 5 минут для сбора супернатанта. 100 мкл геля антитела против Flag (Sigma) смешивали с 50 мл этого супернатанта, а затем инкубировали при 4°C в течение 16 часов. Затем проводили центрифугирование для сбора геля и промывание PBS пять раз. Кроме того, белок элюировали с использованием пептида 3x Flag (конечная концентрация 100 мкг/мл). Экспрессию рекомбинантных белков исследовали способом вестерн-блоттинга с использованием разбавленного в 1000 раз (разбавленного S-T-PBS) антитела мыши против Flag и разбавленного в 2000 раз (разбавленного S-T-PBS) меченного пероксидазой антитела против IgG мыши (GE Healthcare). Активность этих очищенных рекомбинантных белков в отношении индукции миграции мезенхимальных стволовых клеток костного мозга мыши оценивали аналогично справочному примеру 2 с использованием камеры Бойдена. Более того, для исследования лекарственной эффективности средства на основе семейства HMGB in vivo, из кожи спины мышей C57BL/6 в возрасте 8 недель вырезали круг, имеющий диаметр 8 мкм, для осуществления моделей кожных язв. Каждый из очищенных HMGB1, HMGB2 и HMGB3 (100 нг) смешивали с тем же количеством раствора гиалуроновой кислоты в концентрации 1 г/100 мл PBS, и 100 мкл его вводили на поверхность язвы. Поверхность язвы покрывали прозрачной клейкой повязкой на рану/защитным материалом Tegaderm (3M Healthcare), чтобы избежать высыхания, и площадь раны измеряли с течением времени для определения терапевтического эффекта.
Кроме того, для исследования того, обладает ли экстракт кожи человека и очищенный HMGB1 человека активностью обеспечения миграции мезенхимальных стволовых клеток костного мозга человека, использовали камеру Бойдена аналогично тому, как в справочном примере 2. Кожу человека, имеющую площадь 1 см2, погружали в 1 мл PBS, а затем инкубировали при 4°C в течение 16 часов, а затем центрифугировали при 440 G при 4°C в течение 10 минут. Супернатант отдельно собирали для применения в качестве экстракта кожи человека. Более того, мезенхимальные стволовые клетки костного мозга человека (Cambrex) использовали в качестве клеток, помещаемых в верхнее отделение камеры Бойдена (в результате анализа поверхностных антигенов проточной цитометрией было подтверждено, что эти клетки являются CD105-положительными, CD166-положительными, CD29-положительными, CD44-положительными, CD34-отрицательными и CD45-отрицательными. Также с помощью тестов индукции дифференцировки было выявлено, что они дифференцируются в адипоциты, хондроциты и костные клетки). Более того, 100 нг/лунка HMGB1 человека (R&D) и экстракта кожи человека разбавляли в 10 раз PBS и помещали в нижнее отделение. В качестве контроля использовали PBS.
Результаты: в результате вестерн-блоттинга, были выявлены полосы HMGB2 и HMGB3, а также полоса HMGB1. Таким образом, было подтверждено, что экстракт кожи новорожденной мыши содержит, помимо HMGB1, белки семейства HMGB2 и HMGB3 (фиг.19). Получали экспрессирующие векторы HMGB1/HMGB2/HMGB3, имеющие Flag-метку, добавленную на N-конец каждого белка (фиг.20). Эти экспрессирующие векторы вводили в клетки HEK293, и экспрессированные белки очищали с использованием Flag-метки, и для выявления этих белков проводили вестерн-блоттинг (фиг.21). Активность миграции мезенхимальных стволовых клеток костного мозга мыши определяли с использованием этих очищенных белков, и активность была подтверждена для всех из этих белков (фиг.22). Площадь язвы, сформированной на спине мыши, измеряли каждые 7 суток, и в группах введения HMGB1, 2 и 3, был подтвержден значительный эффект в отношении снижения площади язвы по сравнению с группой без введения (фиг.23). Аналогично случаю с мышью, было выявлено, что HMGB1 человека и экстракт кожи человека обладает активностью миграции мезенхимальных стволовых клеток костного мозга (фиг.24).
Обсуждение: HMGB2 и HMGB3 известны в качестве белков, обладающих высокой гомологией с HMGB1. Также предполагается, что эти белки имеют свойства, сходные с HMGB1. Было подтверждено, что HMGB2 и HMGB3 семейства HMGB1 также выделяются из экстракта свободного среза кожи. Кроме того, продуцировали рекомбинантные белки HMGB1/HMGB2/HMGB3, и также были подтверждены их хемотаксическая активность в отношении мезенхимальных стволовых клеток костного мозга in vitro и терапевтический эффект на кожную язву in vivo. Было выявлено, что семейство HMGB (HMGB1/HMGB2/HMGB3) и рекомбинантное семейство HMGB в свободном срезе кожи новорожденной мыши обладают активностью привлечения мезенхимальных стволовых клеток костного мозга и активностью локального привлечения происходящих из костного мозга стволовых клеток, которые могут дифференцироваться в эпителий и таким образом привлеченная группа происходящих из костного мозга клеток дифференцируется в различные клетки, такие как эпидермальные кератиноциты, волосяные фолликулы и фибробласты в поврежденной ткани, обеспечивая восстановление поврежденной ткани. Более того, поскольку мезенхимальные стволовые клетки костного мозга представляют собой плюрипотентные стволовые клетки, авторы настоящего изобретения полагают, что также аналогично можно ожидать терапевтических эффектов путем систематического введения или местного введения семейства HMGB для лечения повреждений в других тканях, например, повреждений тканей, таких как повреждение головного мозга, инфаркт миокарда и перелом кости.
Более того, известно, что между человеком и мышью гомология аминокислотных последовательностей для HMGB1 составляет 98% (213/215), 96% (202/210) для HMGB2, и 97% (195/200) для HMGB3. Таким образом, считается, что HMGB человека и HMGB мыши имеют сходную активность, и результаты настоящих справочных примеров показали, что экстракт кожи человека и HMGB1 человека обладают активностью привлечения мезенхимальных стволовых клеток костного мозга, аналогичной активности экстракта кожи мыши и HMGB1 мыши.
Справочный пример 4
Задача: установление способа продукции экстракта тканей, содержащего факторы, привлекающие мезенхимальные стволовые клетки костного мозга.
Способы: головной мозг, сердце, кишечник, почку и печень мыши C57BL6 в возрасте 6 недель и кожу новорожденной мыши погружали в 1 мл физиологического фосфатно-солевого буфера (PBS) при pH 7,4. Растворы инкубировали при 4°C в течение 24 часов, а затем центрифугировали при 440 G при 4°C в течение 10 минут для удаления тканей. Супернатанты собирали с получением экстрактов тканей. Для подтверждения того, обладает ли полученный таким образом экстракт активностью привлечения происходящих из костного мозга мезенхимальных стволовых клеток, исследовали его активность индукции миграции происходящих из костного мозга мезенхимальных стволовых клеток с использованием камеры Бойдена, аналогично тому, как в справочном примере 2. Более того, измеряли концентрацию HMGB1, содержащегося в этих образцах, с использованием набора HMGB1 ELISA Kit (Shino-Test). Кроме того, экстрактам тканей головного мозга, сердца и кожи позволяли связываться с аффинной колонкой с гепарином аналогично тому, как в справочном примере 2, и активность привлечения происходящих из костного мозга мезенхимальных стволовых клеток в связанной с белком фракции подтверждали с использованием камеры Бойдена.
Результаты: экстракт головного мозга мыши содержал количество HMGB1, эквивалентное экстракту кожи новорожденной мыши. Кроме того, активность привлечения мезенхимальных стволовых клеток костного мозга также наблюдали в головном мозге мыши, как и в коже. Хотя экстракт кишечника мыши и экстракт сердца мыши содержали мало HMGB1, также наблюдали активность привлечения мезенхимальных стволовых клеток костного мозга. Более того, связанные с колонкой с гепарином фракции головного мозга мыши и сердца мыши, а также связанная с колонкой с гепарином фракция кожи мыши, показали активность привлечения мезенхимальных стволовых клеток костного мозга (фиг.25). В таблице 1 представлены результаты измерения концентрации HMGB1 и активности привлечения мезенхимальных стволовых клеток костного мозга в каждом из экстрактов тканей мыши.
Обсуждение: разработан способ, которым HMGB1 можно удобным образом экстрагировать не только из кожи, но также из головного мозга посредством прямого погружения этих органов в физиологический буфер. Этот способ также применим к другим органам, таким как печень и почка. Более того, хотя экстракты из кишечника и сердца содержат мало HMGB1, наблюдали активность привлечения мезенхимальных стволовых клеток костного мозга. Это указывает на то, что эти экстракты содержат другое вещество(а), привлекающее мезенхимальные стволовые клетки костного мозга, помимо HMGB1. Такие вещества, содержавшиеся в этих экстрактах, исходно присутствуют в каждой ткани, и полагают, что они в физиологических условиях привлекают мезенхимальные стволовые клетки костного мозга в поврежденную ткань, когда ткань повреждена. С помощью настоящего изобретения разработан новый способ удобной и функциональной экстракции множества веществ, привлекающих мезенхимальные стволовые клетки костного мозга, включая HMGB1, из различных органов. Кроме того, также разработан способ очистки веществ, привлекающих мезенхимальные стволовые клетки костного мозга, из экстракта ткани с использованием связывания с колонкой с гепарином. Эти вещества, обладающие активностью привлечения мезенхимальных стволовых клеток костного мозга, можно очищать из головного мозга и сердца, также как и из кожи, с использованием колонки с гепарином.
Справочный пример 5
Задача: установление способа экстракции активаторов миграции мезенхимальных стволовых клеток из культивированных клеток.
Способы: происходящую из почки эмбриона человека клеточную линию HEK293 и клеточную линию карциномы шейки матки человека HeLa культивировали в D-MEM (Nacalai), содержащей 10% эмбриональную телячью сыворотку. Эти клетки промывали PBS, а затем 107 клеток погружали в 5 мл PBS (Nacalai) при 4°C в течение 16 часов. Раствор центрифугировали при 440 G (гравитационное ускорение) при 4°C в течение 5 минут, а затем супернатант собирали. Мезенхимальные стволовые клетки костного мозга человека помещали в верхнее отделение камеры Бойдена, и разбавленный в 5 раз (посредством DMEM) экстракт клеток помещали в нижнее отделение, для подтверждения миграционной активности мезенхимальных стволовых клеток костного мозга человека.
Результаты: как экстракт HEK293, так и экстракт HeLa, показали сходную активность в отношении миграции мезенхимальных стволовых клеток костного мозга (фиг.26).
Обсуждение: активаторы миграции мезенхимальных стволовых клеток костного мозга успешно экстрагированы удобным способом погружения культивируемых клеток в PBS.
Справочный пример 6
Задача: исследование того, можно ли индуцировать регенерацию нервных клеток, путем создания моделей дефекта головного мозга мышей, которым вводят очищенную на колонке с гепарином фракцию экстракта кожи способом замедленного высвобождения локально в область повреждения, обеспечивая миграцию стволовых клеток, содержащихся в миелоидной системе, локально в область повреждения.
Способы:
(1) Получение очищенной на колонке с гепарином фракции экстракта кожи
Вырезанный срез кожи новорожденной мыши инкубировали в PBS (мышь/мл) при 4°C в течение 16 часов, и получали экстракт кожи. Экстракт кожи разбавляли в 10 раз 9 объемами 20 мМ фосфатного буфера при pH 7,5 при 4°C. Предварительно для уравновешивания колонки в колонку HiTrap Heparin HP (объем колонки: 5 мл, GE Healthcare) выливали 20 мМ фосфатный буфер, pH 7,5 (30 мл). Затем разбавленному раствору позволяли связаться с колонкой. Затем колонку промывали 20 мМ фосфатным буфером при pH 7,5 и 100 мМ NaCl (30 мл). Для элюирования адсорбированных белков, в колонку выливали 20 мМ фосфатный буфер с pH 7,5 и 1000 мМ NaCl, и фракции элюировали в пробирки. Каждую из адсорбированных фракций оценивали в отношении хемотаксической активности для происходящих из костного мозга клеток мыши с использованием способа с камерой Бойдена, представленного выше, и собирали фракцию(и), имеющую способность к хемотаксису. Раствор(ы), обладающий этой активностью, использовали в качестве очищенной на гепарине фракции(ий) экстракта кожи в эксперименте, представленном ниже.
(2) Получение мышей с подавлением костного мозга
Мышей облучали однократной дозой рентгеновского излучения, составляющей 10 Гр, для получения мышей с подавлением костного мозга.
(3) Трансплантат костного мозга мыши с GFP мышам с подавлением костного мозга
Клетки костного мозга собирали из обеих бедренных костей и костей голени мышей GFP. Эти клетки вводили мышам с подавлением костного мозга через хвостовую вену через 24 часа после облучения. Введение проводили под ингаляционной анестезией с использованием изофлурана.
(4) Получение модели дефекта головного мозга (дефекта тканей головного мозга) на мышах
Мышей с подавлением костного мозга, которым трансплантировали клетки костного мозга мыши с GFP, подвергали ингаляционной анестезии с использованием изофлурана и пентобарбитала (45 мг/кг), которые мышам инъецировали внутрибрюшинно. Мышей фиксировали к стереотактическому устройству для головного мозга и проводили срединный разрез головы скальпелем. Трепанацию проводили на 2,5 мм латерально справа и 12,5 мм спереди брегмы с использованием бура (фиг.27A). На глубине 3 мм от этого участка помещали и фиксировали иглу 20 G Surflow. Затем применяли отрицательное давление с использованием шприца для отсасывания части ткани головного мозга (фиг.27B).
(5) Введение очищенной на колонке с гепарином фракции экстракта кожи в область дефекта ткани головного мозга
Пять мкл очищенной на колонке с гепарином фракции экстракта кожи, растворенной в фибриногене адгезивного состава для тканей на основе фибрина (Bolheal (Kaketsuken)) инъецировали в указанную выше область, а затем инъецировали 5 мкл тромбина адгезивного состава для тканей на основе фибрина (Bolheal (Kaketsuken)) с использованием шприца Hamilton и шприца 26 G (фиг.27C). Задачей этого действия было обеспечение эффекта замедленного высвобождения для очищенной на колонке с гепарином фракции экстракта кожи.
(6) Оценка эффекта регенерации нервных клеток в областях дефекта тканей головного мозга
Для оценки использовали мышей контрольной группы и группы введения. Определяли параметры в соответствующие периоды времени (с течением времени), мышам проводили перфузию 4% параформальдегидом, а затем их фиксировали и вырезали головной мозг. Кроме того, проводили наружную фиксацию 4% параформальдегидом. Затем его дегидратировали в 15% и 30% градиенте сахарозы с получением замороженных срезов.
Ядра окрашивали раствором DAPI (4',6-диамидино-2-фенилиндол, дигидрохлорид) и срез закрывали с использованием средства против обесцвечивания. Накопление GFP-положительных клеток в области повреждения (области дефекта ткани головного мозга) оценивали с использованием конфокального лазерного микроскопа.
Результаты: качественно показано накопление GFP-положительных клеток в течение 2 недель и в течение 6 недель после введения. Накопление GFP-положительных клеток имеет тенденцию к тому, чтобы быть более высоким в областях повреждения группы введения, а не в контрольной группе, как через 2 недели (контроль; фиг.27D, фракция очищенного на колонке с гепарином экстракта кожи; фиг.27E), так и через 6 недель (контроль; фиг.27F, фракция очищенного на колонке с гепарином экстракта кожи; фиг.27G) после введения.
Обсуждение: введение очищенной на колонке с гепарином фракции экстракта кожи приводило к накоплению происходящих из костного мозга клеток в области дефекта ткани головного мозга, которые имели форму нервных клеток. Известно, что происходящие из костного мозга мезенхимальные стволовые клетки также дифференцируются в нервные клетки и результат показал, что очищенная на колонке с гепарином фракция экстракта кожи способна индуцировать регенерацию нервных клеток поврежденной области головного мозга. Более того, это также применимо к регенерации нейронов поврежденных областей в тканях головного мозга при ишемических заболеваниях головного мозга и контузиях головного мозга.
Справочный пример 7
Задача: Мобилизация стволовых клеток ткани костного мозга в периферическую кровь с использованием факторов, привлекающих происходящие из ткани костного мозга стволовые клетки, в экстракте кожной ткани
Способы: для достижения указанной выше задачи проводили исследование способом, описанным ниже.
(1) Получение фактора, привлекающего происходящие из ткани костного мозга стволовые клетки. Свободные фрагменты кожи, полученные от 25 новорожденных мышей (в возрасте двух суток) погружали в 25 мл фосфатно-солевого буфера (PBS), pH 7,4. После инкубации в течение 24 часов при 4°C образец центрифугировали при 440 G при 4°C в течение десяти минут для удаления ткани. Супернатант собирали в качестве экстракта кожи (SE).
Тем временем из кожи новорожденных мышей C57/Bl6 экстрагировали РНК с использованием Trizol (Invitrogen), а затем синтезировали кДНК с использованием набора SuperScript III cDNA Synthesis Kit (Invitrogen). С использованием этой кДНК в качестве матрицы проводили полимеразную цепную реакцию (ПЦР) для амплификации кДНК HMGB1. кДНК HMGB1 встраивали в плазмидный вектор для экспрессии белков клеток млекопитающих, pCAGGS, для экспрессии белка, в котором с N-концом аминокислотной последовательности связана последовательность Flag-метки (Asp-Tyr-Lys-Asp-Asp-Asp-Lys, SEQ ID NO: 30) (фиг.20). Плазмидный вектор трансфицировали в HEK293 (культивированная клеточная линия, происходящая из клеток почки эмбриона человека). Клетки культивировали в течение 48 часов для экспрессии белка. Каждый образец клеток, экспрессирующих белок HMGB1, и культуральный супернатант инкубировали при 4°C в течение 16 часов, а затем центрифугировали при 4400×g в течение пяти минут. Супернатант собирали и к нему добавляли гель с антителом против Flag (Sigma) в количестве 100 мкл на 50 мл супернатанта. Смесь инкубировали при 4°C в течение 16 часов. Гель собирали центрифугированием, а затем пять раз промывали PBS. Затем гель элюировали 3х пептидом Flag (конечная концентрация 100 мкг/мл). Концентрацию элюированного белка определяли с использованием набора HMGB1 ELISA Kit (Shino-Test Co.). После лиофилизации концентрацию белка доводили до 200 мкг/мл с помощью PBS.
(2) Мышам в возрасте восьми недель (C57/Bl6) вводили 500 мкл описанного выше экстракта кожи (SE), или 500 мкл PBS в качестве группы отрицательного контроля, через хвостовую вену с использованием шприцов, к которым присоединена игла для инъекций 30G 1/2 (фиг.28). Через шесть, 12, 24 и 48 часов после введения из сердца мышей отбирали 1 мл периферической крови под ингаляционной анестезией с помощью изофлурана с использованием покрытого гепарином 1-мл шприца. Каждый из образцов крови смешивали с 3 мл PBS, а затем осторожно наслаивали на 3 мл Ficoll (GE healthcare). Полученные образцы центрифугировали с использованием центрифуги при 400×g при 25°C в течение 40 минут. Клетки мутного среднего слоя собирали в качестве фракции мононуклеарных клеток. К собранным клеткам добавляли 1 мл раствора HLB (Immuno-Biological Laboratories Co., Ltd.), гемолитического средства. Клетки инкубировали при комнатной температуре в течение пяти минут. Эту гемолитическую обработку повторяли дважды. После добавления 10 мл PBS клетки центрифугировали при 440×g при 25°C в течение пяти минут. Супернатанты удаляли и клетки собирали. 1000000 клеток инкубировали при комнатной температуре в течение 20 минут с антителами, каждое из которых разбавлено 100-кратно PBS, включающим меченное PE антитело против PDGFRα мыши (e-Bioscience), меченное PE антитело против PDGFRβ мыши (e-Bioscience) и меченное PerCy5 антитело против CD44 мыши (BD biosciences). После инкубации клетки центрифугировали при 440×g при 25°C в течение пяти минут. Супернатант удаляли. К клеткам добавляли 400 мкл PBS, содержащего 1% параформальдегид, для подготовки образцов для анализа проточной цитометрией.
Мышам в возрасте восьми недель (C57/Bl6) вводили 250 мкл HMGB1 мыши (1 мкг/мкл), или 250 мкл PBS в качестве группы отрицательного контроля, через хвостовую вену с использованием шприцов, к которым присоединена игла для инъекций 30G 1/2 (фиг.29). Через 12 часов после введения отбирали 1 мл периферической крови из сердца мышей под ингаляционной анестезией с помощью изофлурана с использованием покрытого гепарином 1-мл шприца. Каждый из образцов крови смешивали с 3 мл PBS, а затем осторожно наслаивали на 3 мл Ficoll (GE healthcare). Полученные образцы центрифугировали с использованием центрифуги при 400×g при 25°C в течение 40 минут. Клетки мутного среднего слоя собирали в качестве фракции мононуклеарных клеток. К собранным клеткам добавляли 1 мл раствора HLB (Immuno-Biological Laboratories Co., Ltd.), гемолитического средства. Клетки инкубировали при комнатной температуре в течение пяти минут. Эту гемолитическую обработку повторяли дважды. После добавления 10 мл PBS клетки центрифугировали при 440×g при 25°C в течение пяти минут. Супернатанты удаляли и клетки собирали. 1000000 клеток инкубировали при комнатной температуре в течение 20 минут с антителами, каждое из которых 100-кратно разбавлено PBS, включающим меченное PE антитело против PDGFRα мыши (e-Bioscience) и меченное PerCy5 антитело против CD44 мыши (BD biosciences). После инкубации клетки центрифугировали при 440×g при 25°C в течение пяти минут. Супернатант удаляли. К клеткам добавляли 400 мкл PBS, содержащего 1% параформальдегид, для подготовки образцов для анализа проточной цитометрией.
Результаты: было показано, что двойные положительные по PDGFRα и CD44 клетки в значительной степени вовлекаются в периферическую кровь через 12 часов после инъекции экстракта кожи (SE) (фиг.30). Более того, было показано, что двойные положительные по PDGFRα и CD44 клетки в значительной степени вовлекаются в периферическую кровь через 12 часов после инъекции HMGB1 (фиг.31).
Справочный пример 8
Задача: тестирование того, вовлекаются ли мезенхимальные стволовые клетки в периферическую кровь посредством внутривенного введения рекомбинантного белка HMGB1.
Способы: мышам C57BL6 (возраст от восьми до десяти недель, самцы) вводили 400 мкл физиологического раствора, содержащего 100 мкг/мл рекомбинантного белка HMGB1 (40 мкг HMGB1) или 400 мкл физиологического раствора отдельно через хвостовую вену. Через 12 часов у мышей проводили взятие периферической крови. Образцы крови разбавляли PBS до общего объема 4 мл. Разбавленные образцы крови наслаивали на 3 мл Ficoll-Paque Plus (GE), помещенного в центрифужные пробирки. Образцы центрифугировали при 400 G при 18°C в течение 40 минут. Средний слой, содержавший мононуклеарные клетки, переносили в свежую центрифужную пробирку и в нее добавляли 45 мл PBS. Пробирку центрифугировали при 800 G при 18°C в течение пяти минут. Супернатант удаляли. Снова добавляли 45 мл PBS и пробирку центрифугировали при 800 G при 18°C в течение пяти минут. Супернатант удаляли. Полученные мононуклеарные клетки инкубировали с меченным фикоэритробилином (PE) антителом против PDGFRα мыши и меченным флуоресцеинизотиоцианатом (FITC) антителом против CD44 мыши. Затем оценивали увеличение содержания двойных положительных по PDGFRα и CD44 клеток во фракции мононуклеарных клеток с помощью проточной цитометрии (Facscan; Becton, Dickinson and Company).
Результаты: было показано, что количество двойных положительных по PDGFRα и CD44 клеток, и PDGFRα-положительных, CD44-отрицательных клеток во фракции мононуклеарных клеток периферической крови значительно возрастало через 12 часов после введения HMGB1 (фиг.32). Конкретно, было продемонстрировано, что HMGB1 обладает активностью вовлечения PDGFRα-положительных клеток в периферическую кровь из костного мозга. PDGFRα известен в качестве маркера мезенхимальных стволовых клеток.
Обсуждение: PDGFRα и CD44 известны в качестве поверхностных маркеров мезенхимальных стволовых клеток костного мозга, которые являются иллюстративными для происходящих из костного мозга плюрипотентных стволовых клеток. Мезенхимальные стволовые клетки костного мозга представляют собой плюрипотентные стволовые клетки, способные дифференцироваться в нервные клетки, эпителиальные клетки или сходные с ними, а также в остеоциты, хондроциты и адипоциты. Тем временем, фрагменты кожи, использованные в этом эксперименте, находятся в ишемизированном состоянии. Таким образом, происходит постепенный некроз тканей и внутриклеточные белки, такие как ядерные белки, а также белки клеточной поверхности, высвобождаются наружу. HMGB1 представляет собой белок, содержащийся в экстракте кожи. При трансплантации кожи или сходных с ней, такие белки служат в качестве сигнала для привлечения происходящих из ткани костного мозга стволовых клеток в пересаженную кожу. Таким образом, предполагается, что функциональная регенерация кожи в трансплантате кожи достигается восстановлением эпидермиса, гиподермы, фолликулярных тканей или сходных с ними, обусловленным клетками костного мозга. Исходя из этого эксперимента, в настоящем изобретении было успешно открыто, что происходящие из ткани костного мозга стволовые клетки вовлекаются в периферический кровоток внутривенным введением HMGB1 или экстракта кожи, как описано выше. Это открытие обеспечивает новые терапевтические способы для лечения трудноизлечимых заболеваний с повреждениями тканей, таких как инфаркт головного мозга, инфаркт миокарда, перелом кости и кожная язва, которые основаны на вовлечении происходящих из костного мозга плюрипотентных стволовых клеток в периферическую кровь. Кроме того, клетки, вовлеченные в периферическую кровь, можно собирать общепринятым способом сбора крови. Таким образом, настоящее изобретение обеспечивает более простые и более безопасные способы сбора происходящих из ткани костного мозга стволовых клеток по сравнению с общепринятым способом лечения инфаркта головного мозга, в случае которого клетки собирают из костного мозга.
Справочный пример 9
Задача: Оценить вклад происходящих из костного мозга клеток в функциональную регенерацию трансплантированной ткани кожи in vivo
Способы: для достижения указанной выше задачи проводили исследование.
(1) Степень, с которой происходящие из костного мозга клетки участвуют в функциональной регенерации трансплантированной кожи оценивали с использованием системы трансплантации кожи in vivo у мышей с трансплантированным костным мозгом с GFP. В частности, самцов мышей C57BL/6 (в возрасте от шести до восьми недель) облучали летальной дозой (10 Гр), и сразу после облучения мышам через хвостовую вену трансплантировали клетки костного мозга с зеленым флуоресцентным белком (GFP) (5×106 клеток/0,1 мл физиологического фосфатно-солевого буфера, pH 7,4).
(2) После подтверждения приживления трансплантированных клеток костного мозга (шесть недель), кожу новорожденной мыши (самки) трансплантировали на кожу спины полученных мышей с трансплантированным костным мозгом с GFP.
(3) После подтверждения приживления трансплантированной кожи и достаточной регенерации ткани кожи (четыре недели), степень накопления флуоресценции GFP в области трансплантированной кожи наблюдали под флуоресцентным стереомикроскопом.
(4) Трансплантированную кожу получали путем биопсии под ингаляционной анестезией. Получали срезы замороженной кожи (6 мкм) с использованием микротома с охлаждающим устройством, и фиксировали их в течение 30 минут 4% параформальдегидом. Затем ядра клеток в тканях окрашивали DAPI. После заливки ткани с использованием среды для заливки, содержащей средство против обесцвечивания, ткани наблюдали под конфокальным лазерным микроскопом для оценки присутствия GFP-положительных происходящих из костного мозга клеток.
Результаты: в системе для трансплантации кожи in vivo у мышей с трансплантированным костным мозгом с GFP, флуоресценцию GFP наблюдали в большинстве эпидермальных кератиноцитов и дермальных фибробластов, а также в гладкомышечных клетках и адипоцитах регенерированных тканей кожи, указывая на то, что эти клетки происходили из костного мозга (Фиг.33). В частности, происходящие из костного мозга стволовые клетки служили в качестве источника большинства эпителиальных клеток и мезенхимальных клеток, требуемых для функциональной регенерации трансплантированных тканей.
Обсуждение: результаты, описанные выше, указывают на то, что при повреждении кожи клетки костного мозга накапливаются в поврежденной области и дифференцируются в различные типы органов, составляющих кожу, тем самым участвуя в функциональной регенерации кожи. Между тем, полагают, что трансплантированная кожа содержит вещества, которые привлекают клетки костного мозга, которые способны дифференцироваться в различные типы органов.
Было описано, что костный мозг содержит два типа систем стволовых клеток: гемопоэтические стволовые клетки и мезенхимальные стволовые клетки. Было бы трудным ожидать, что большое количество происходящих из костного мозга эпителиальных клеток и мезенхимальных клеток, мобилизованных в трансплантированную кожу, обеспечиваются происходящими из костного мозга гемопоэтическими стволовыми клетками, как показано с помощью настоящего исследования. Это строго указывает на возможность того, что происходящие из костного мозга мезенхимальные стволовые клетки вносят вклад в функциональную регенерацию трансплантированных тканей. В частности, ожидается, что сразу после трансплантации кожи факторы, которые мобилизуют происходящие из костного мозга мезенхимальные стволовые клетки, высвобождаются из трансплантированной кожи в состоянии гемостаза/некроза, и мобилизуют мезенхимальные стволовые клетки в трансплантированную кожу из костного мозга через периферический кровоток, тем самым индуцируя функциональную регенерацию кожной ткани.
Справочный пример 10
Задача: идентифицировать факторы привлечения происходящих из ткани костного мозга стволовых клеток в экстрактах тканей кожи.
Способы: способом, описанным ниже, проводили исследование для идентификации факторов, ответственных за привлечение мезенхимальных стволовых клеток костного мозга, которые предположительно высвобождаются из вырезанной кожи в условиях гемостаза.
(1) Клетки костного мозга собирали из бедренных костей или костей голени мышей C57BL/6 для получения происходящих из костного мозга мезенхимальных стволовых клеток мыши. Клетки высевали в чашку для культивирования клеток с D-MEM (Nacalai), дополненной 10% эмбриональной телячьей сывороткой в качестве культуральной среды, и культивировали при 37°C под 5% газообразным диоксидом углерода. Когда клетки вырастали, чтобы занимать площадь от 70 до 100% относительно дна культуральной чашки, клетки отделяли от культуральной чашки с использованием 0,25% трипсина/1 мМ ЭДТА (Nacalai). Затем клетки пассировали в тех же условиях культивирования. После по меньшей мере пяти пассажей прикрепляющиеся клетки выделяли и далее культивировали и анализировали в отношении антигенов клеточной поверхности проточной цитометрией. Результат показал, что клетки были положительными по CD44 и Sca-1, и отрицательными по Lin, CD45 и c-kit. Было подтверждено, что клетки могут дифференцироваться в остеоциты и адипоциты и, таким образом, они имеют характеристики мезенхимальных стволовых клеток костного мозга.
(2) Свободные фрагменты кожи, полученные от пяти новорожденных мышей (в возрасте двух суток), погружали в 5 мл физиологического фосфатно-солевого буфера (PBS, pH 7,4). После инкубации в течение 24 часов при 4°C образец центрифугировали при 440 G при 4°C в течение десяти минут для удаления тканей. Супернатант собирали в качестве экстракта кожи. Кроме того, аналогично, свободные фрагменты кожи от мыши в возрасте шести недель погружали в 5 мл физиологического фосфатно-солевого буфера (PBS, pH 7,4). После инкубации при 4°C в течение 24 часов образцы центрифугировали при 440 G при 4°C в течение десяти минут для удаления тканей. Супернатанты собирали в качестве экстракта кожи.
(3) Для подтверждения того, обладает ли полученный экстракт кожи активностью привлечения мезенхимальных стволовых клеток костного мозга, авторы настоящего изобретения использовали камеру Бойдена для исследования хемотаксической активности ранее клонированных происходящих из костного мозга мезенхимальных клеток, полученных от мышей C57BL6. Конкретно, смесь DMEM (20 мкл) и экстракта кожи (5 мкл) от мышей в возрасте двух суток или шести недель добавляли в нижнее отделение (объем 25 мкл) камеры Бойдена, и сверху помещали поликарбонатную мембрану с микропорами 8 мкм. Затем верхнее отделение (объем 50 мкл) камеры Бойдена контактировали с мембраной, а в верхнее отделение помещали суспензию происходящих из костного мозга мезенхимальных стволовых клеток (5×104 клеток/50 мл культуральной среды (DMEM, дополненная 10% эмбриональной телячьей сывороткой)). Камеру инкубировали в инкубаторе с CO2 при 37°C в течение от четырех до 24 часов. После инкубации верхнее отделение камеры удаляли. Тонкую силиконовую пленку открепляли, и посредством окрашивания клеток определяли количество происходящих из костного мозга мезенхимальных стволовых клеток, мигрировавших в нижнее отделение через микропоры (фиг.34).
(4) Образцы кожи размером примерно 2 см2 вырезали от мышей в возрасте двух суток и в возрасте шести недель и сразу замораживали в жидком азоте. Образцы кожи растирали в ступке. Из образцов вырезали и очищали РНК с использованием RNeasy (Qiagen). С использованием очищенных РНК проводили анализ на микрочипах для скрининга мРНК, экспрессирующейся на более высоких уровнях у мышей в возрасте двух суток. 767 генов показали в два или более раз более высокие показатели у мышей в возрасте двух суток. Среди этих генов исследовали белки с высокой аффинностью к гепарину, потенциальные секреторные белки, и гены, показатели для которых в шесть или более раз были более высокими у мышей в возрасте двух суток, и S100A9 был выявлен в качестве 57 гена по счету сверху. Таким образом, вестерн-блоттингом были выявлены S100A9 и S100A8, который, как известно, формирует гетеродимер с S100A9 в экстракте кожи от мышей в возрасте двух суток. Конкретно, 5 мкл экстракта кожи от мышей в возрасте двух суток смешивали с 5 мкл буфера для образца SDS-PAGE (Bio-Rad). Смесь нагревали в термоблоке при 98°C в течение пяти минут, а затем охлаждали до 25°C. Полученный образец наносили на 12,5% акриламидный гель e-PAGEL (ATTO) и подвергали электрофорезу при 40 мА в течение 75 минут с использованием устройства для электрофореза (ATTO). Гель собирали после электрофореза. С использованием устройства для блоттинга (ATTO) белки в геле переносили в мембрану PVDF (7 см на 9 см, Millipore), предварительно обработанную 100% метанолом. После переноса белка в течение 75 минут при 120 мА мембрану PVDF удаляли и встряхивали при комнатной температуре в течение 30 минут в PBS (Nacalai), содержащем 4% обезжиренное молоко. Затем удаленную мембрану PVDF погружали в 5 мкл антитела против S100A8 (R&D) или антитела против S100A9 (R&D), каждое из которых было разбавлено 10 мл PBS, содержащего 4% обезжиренного молока, и встряхивали при комнатной температуре в течение 60 минут. После удаления раствора антитела мембрану встряхивали в 30 мл PBS, содержащего 0,1% Tween20 при комнатной температуре в течение пяти минут. Это промывание повторяли пять раз. Затем мембрану пропитывали 5 мкл меченного HRP антитела против IgG козы (GE healthcare), разбавленного 10 мл PBS, содержащего 4% обезжиренное молоко, и встряхивали при комнатной температуре в течение 45 минут. После удаления раствора антитела, мембрану промывали 30 мл PBS, содержащего 0,1% Tween20 при комнатной температуре в течение пяти минут при встряхивании. Это промывание повторяли пять раз. Мембрану обрабатывали для люминесценции с использованием набора ECL Detection Kit (GE healthcare), а затем экспонировали на пленку. Сигналы для белков S100A8 и S100A9 получали путем проявки пленки в проявочном устройстве (фиг.35).
(5) Факторы, обладающие активностью привлечения происходящих из костного мозга мезенхимальных стволовых клеток в экстрактах кожи, очищали аффинной колоночной хроматографией с гепарином. Эксперимент, описанный ниже, проводили с использованием устройства FPLC (GE healthcare). Прежде всего, экстракт кожи мышей в возрасте двух суток разбавляли в 10 раз девятью объемами 20 мМ фосфатного буфера (pH 7,5) при 4°C (раствор для разбавления A). Предварительно через колонку HiPrep 16/10 Heparin FF (GE Healthcare) пропускали 300 мл 20 мМ фосфатного буфера (pH 7,5) для уравновешивания колонки, и в колонку помещали раствор для разбавления A. Затем колонку промывали 300 мл 20 мМ фосфатного буфера (pH 7,5). Для элюирования адсорбированного белка получали 20 мМ фосфатный буфер (pH 7,5), содержащий 10 мМ NaCl (раствор A) и 20 мМ фосфатный буфер (pH 7,5), содержащий 500 мМ NaCl (раствор B). Элюирование начинали с [100% раствор A + 0% раствор B], а затем долю раствора B постепенно увеличивали. Наконец, колонку элюировали посредством [0% раствор A + 100% раствор B]. Общий элюированный объем составил 150 мл. Элюат фракционировали в покрытые силиконом пробирки (3 мл/пробирка). 5 мкл каждого из фракционированных образцов смешивали с 5 мкл буфера для образца SDS-PAGE (Bio-Rad). Смеси нагревали в термоблоке при 98°C в течение пяти минут, а затем охлаждали до 25°C. Образцы наносили на акриламидный гель e-PAGEL (5-20% градиент, ATTO), и подвергали электрофорезу при 40 мА в течение 75 минут с использованием устройства для электрофореза. После электрофореза проводили детекцию подвергнутого электрофорезу белка с использованием набора Dodeca Silver Stain Kit (Bio-Rad) (фиг.36).
Хемотаксическую активность фракционированных образцов оценивали аналогично тому, как описано выше, с использованием камеры Бойдена (фиг.37).
Присутствие белков S100A8 и S100A9 во фракционированных образцах выявляли аналогично тому, как описано выше, вестерн-блоттингом (фиг.38).
(6) РНК экстрагировали из кожи новорожденной мыши с использованием Trizol (Invitrogen), а затем с РНК синтезировали кДНК с использованием набора SuperScript III cDNA Synthesis Kit (Invitrogen). кДНК S100A8 и S100A9 амплифицировали способом полимеразной цепной реакции (ПЦР) с использованием кДНК в качестве матрицы. Каждую из этих кДНК встраивали в плазмидный вектор для экспрессии белка в клетках млекопитающих pCAGGS, для экспрессии белков, в которых с N-концом их аминокислотных последовательностей связана последовательность GST-метки (аминокислотная последовательность/SEQ ID NO: 31; последовательность ДНК/SEQ ID NO: 32) (фиг.39). Каждый из pCAGGS-GST-S100A8 или pCAGGS-GST-S100A9 трансфицировали в культивированную клеточную линию, происходящую из почки эмбриона человека, HEK293 с использованием реагента для липофекции (Invitrogen). Через 48 часов после трансфекции, клетки и культуральный супернатант собирали и центрифугировали при 4400 G при 4°C в течение пяти минут. Супернатант (супернатант A) и клетки собирали по отдельности. К клеткам добавляли PBS, содержащий 0,1% Tween20, и суспензию обрабатывали ультразвуком на льду в течение 30 секунд для разрушения клеточной мембраны. После центрифугирования при 4400×g при 4°C в течение пяти минут полученный супернатант собирали (супернатант B). Супернатанты A и B объединяли и помещали в колонку HiTrap GST FF (5 мл; GE Healthcare), буфер которой предварительно заменяли 30 мл PBS. После загрузки колонку промывали 100 мл PBS и адсорбированный белок элюировали 20 мМ фосфатным буфером (pH 8), содержащим восстановленный глутатион. Хемотаксическую активность рекомбинантных S100A8 и S100A9 в отношении мезенхимальных стволовых клеток костного мозга оценивали с использованием камеры Бойдена. Образцы получали растворением очищенного белка S100A8 или S100A9 в концентрации 0,1 нг/мкл в DMEM, или путем разбавления экстракта кожи мышей в возрасте двух суток четырьмя объемами DMEM, и их добавляли в нижнее отделение камеры Бойдена. Аналогично использовали отрицательный контроль, полученный следующим образом: белок экстрагировали из клеток, трансфицированных контрольным вектором, который не несет кДНК S100A8 или S100A9 в качестве вставки; а затем фракцию элюировали с колонки HiTrap GST FF. После добавления образца в нижнее отделение сверху помещали поликарбонатную мембрану с микропорами 8 мкм. Затем верхнее отделение (объем 50 мкл) камеры Бойдена контактировали с мембраной и в верхнюю камеру добавляли суспензию происходящих из костного мозга мезенхимальных стволовых клеток (5×104 клеток/50 мл культуральной среды (DMEM, дополненная 10% эмбриональной телячьей сывороткой)). Камеру инкубировали в инкубаторе с CO2 при 37°C в течение от четырех до 24 часов. После инкубации верхнее отделение камеры удаляли. Тонкую поликарбонатную мембрану открепляли и посредством окрашивания клеток определяли количество происходящих из костного мозга мезенхимальных стволовых клеток, мигрировавших в нижнее отделение через микропоры (фиг.40).
(7) Мышам в возрасте восьми недель инъецировали 250 мкл описанных выше очищенных рекомбинантных белков GST-S100A8 или S100A9 (1 нг/мкл) через хвостовую вену. Через 12 часов после инъекции 1 мл периферической крови отбирали из сердца мышей под ингаляционной анестезией с изофлураном с использованием 1-мл покрытого гепарином шприца. Каждый из образцов крови смешивали с 3 мл PBS, а затем наслаивали на 3 мл Ficoll (GE healthcare). Полученные образцы центрифугировали с использованием центрифуги при 400×g при 25°C в течение 40 минут. Клетки мутного среднего слоя собирали в качестве фракции мононуклеарных клеток. К собранным клеткам добавляли 1 мл раствора HLB (Immuno-Biological Laboratories Co., Ltd.), гемолитического средства, и клетки инкубировали при комнатной температуре в течение пяти минут. Эту гемолитическую обработку повторяли дважды. После добавления 10 мл PBS, клетки центрифугировали при 440×g при 25°C в течение пяти минут. Полученные супернатанты удаляли и клетки собирали. 1000000 клеток инкубировали при комнатной температуре в течение 20 минут с меченным PE антителом против PDGFRα мыши (e-Bioscience), меченным PE антителом против PDGFRβ мыши (e-Bioscience), меченным FITC антителом против CD45 мыши (BD biosciences) и меченным PerCy5 антителом против CD44 мыши (BD biosciences), каждое из которых разбавлено в 100 раз PBS. Затем клетки центрифугировали при 440×g при 25°C в течение пяти минут. Супернатанты удаляли. К клеткам добавляли 400 мкл PBS, содержащего 1% параформальдегид, для подготовки образцов для анализа проточной цитометрией. Антитела использовали в следующих комбинациях:
(I) PDGFRα/CD45/CD44
(II) PDGFβ/CD45/CD44
Исходя из результата анализа определяли отношение клеток, экспрессирующих PDGFRα (или β) и CD44, к клеткам, которые были слабо положительными или отрицательными по CD45 (фиг.41A и B).
Результаты: образцы кожи, вырезанные у мышей в возрасте двух суток и шести недель, оценивали в отношении активности привлечения мезенхимальных стволовых клеток костного мозга. Было показано, что активность экстракта кожи от мышей в возрасте двух суток была более высокой, чем активность экстракта кожи от мыши в возрасте шести недель. Сильная экспрессия S100A9 в коже от мышей в возрасте двух суток была выявлена посредством анализа ДНК на микрочипах. Неочищенные образцы экстрактов кожи, очищенные на колонке с гепарином, проявляли корреляцию между активностью миграции мезенхимальных стволовых клеток и содержанием S100A9 и S100A8. Экспрессирующие векторы для этих белков конструировали, и рекомбинантные белки продуцировали с использованием HEK293 и очищали. Активность в отношении миграции мезенхимальных стволовых клеток костного мозга подтверждали в очищенных образцах S100A8 и S100A9 посредством анализов с использованием камеры Бойдена. Более того, при внутривенном введении мышам белки также проявляли активность привлечения популяции двойных положительных по PDGFRα и CD44 клеток в периферическую кровь (фиг.41).
Обсуждение: авторы настоящего изобретения впервые в мире открыли в настоящем изобретении, что свободные фрагменты кожи продуцируют S100A8 и S100A9, и продуцированные белки S100A8 и S100A9 имели выраженную активность привлечения происходящих из костного мозга мезенхимальных стволовых клеток. Тем временем, мезенхимальные стволовые клетки костного мозга известны в качестве плюрипотентных стволовых клеток, которые дифференцируются в костные ткани, жировые ткани, хрящевые ткани, фибробласты и т.п. Недавно было показано, что происходящие из костного мозга клетки также включают плюрипотентные стволовые клетки, которые дифференцируются в ткани, такие как сердечная мышца, нервные клетки и эпидермальные клетки. Поскольку настоящее изобретение демонстрирует, что эпидермальные клетки, клетки волосяных фолликулов, фибробласты подкожных тканей и т.п. в пересаженной коже формируются из происходящих из костного мозга клеток, можно предположить, что S100A8 и S100A9 ответственны за привлечение происходящих из ткани костного мозга стволовых клеток к трансплантату кожи для индукции функциональной репарации поврежденных тканей. Даже при внутривенной инъекции, S100A8 и S100A9 могут вовлекать мезенхимальные стволовые клетки костного мозга в периферическую кровь. Таким образом, S100A8 и S100A9 также можно вводить через периферический кровоток в ткани, расположенные глубоко в организме, где местное введение является трудным (головной мозг, сердце, спинной мозг и т.д.). Авторы настоящего изобретения полагают, что эффекты, такие как укорочение времени заживления, функциональная регенерация поврежденных тканей и т.п. можно ожидать в процессе заживления не только поврежденных тканей кожи, но также различных других поврежденных тканей, таких как головной мозг, мышца и кость, при использовании настоящего изобретения в фармацевтических средствах, которые обеспечивают местное привлечение происходящих из ткани костного мозга стволовых клеток, включающих мезенхимальные стволовые клетки, для регенерации поврежденных тканей.













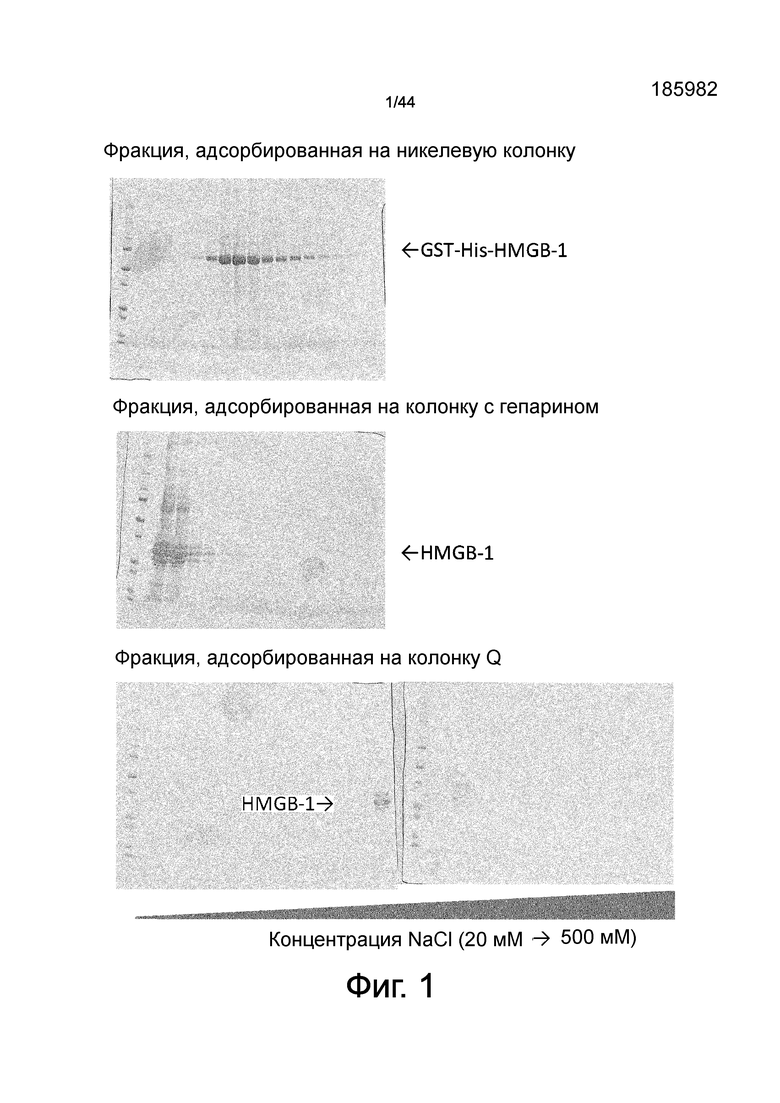


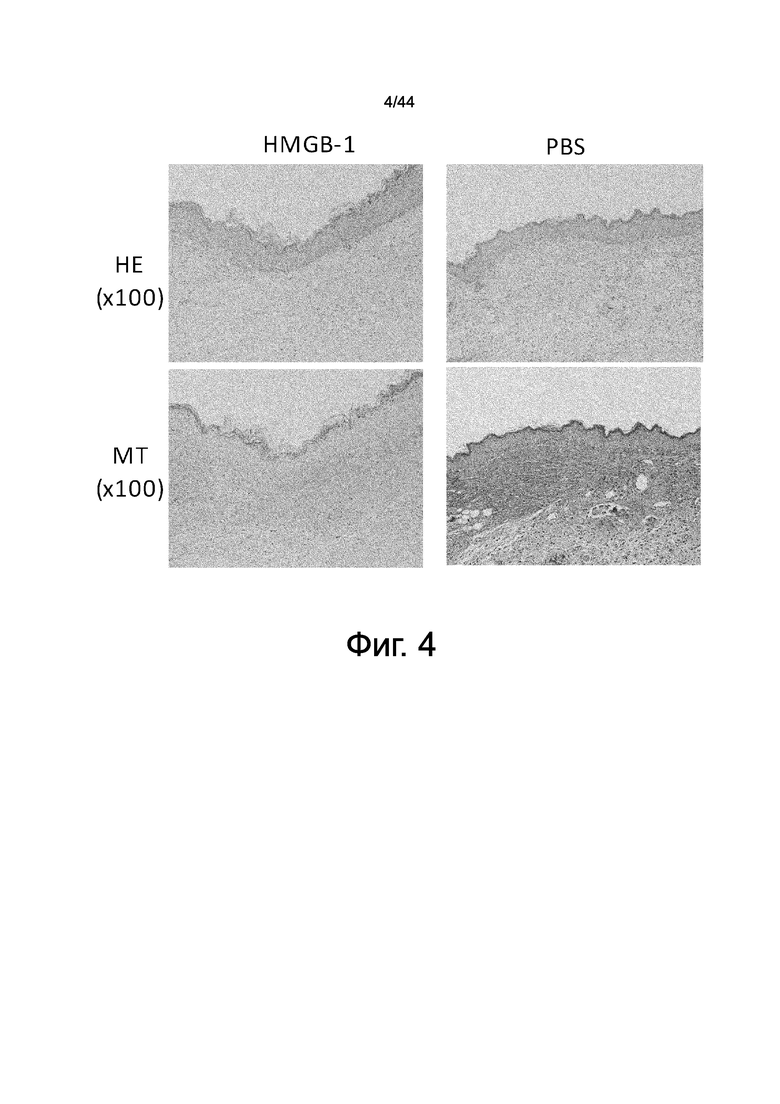

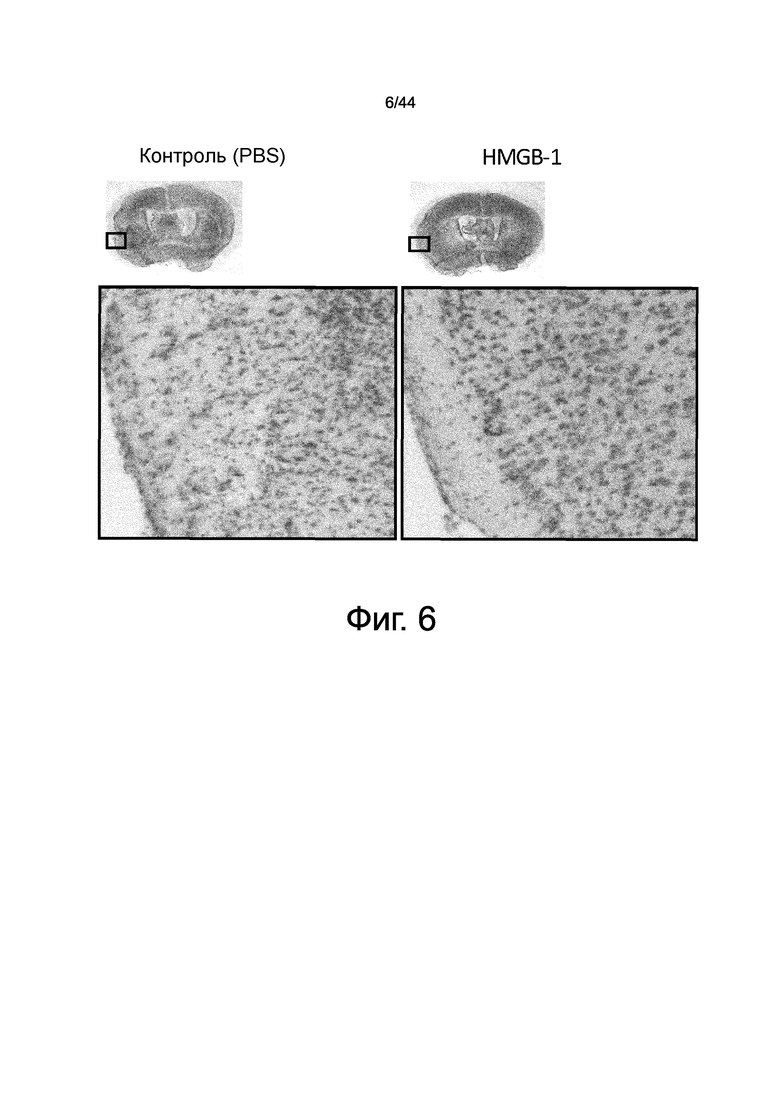
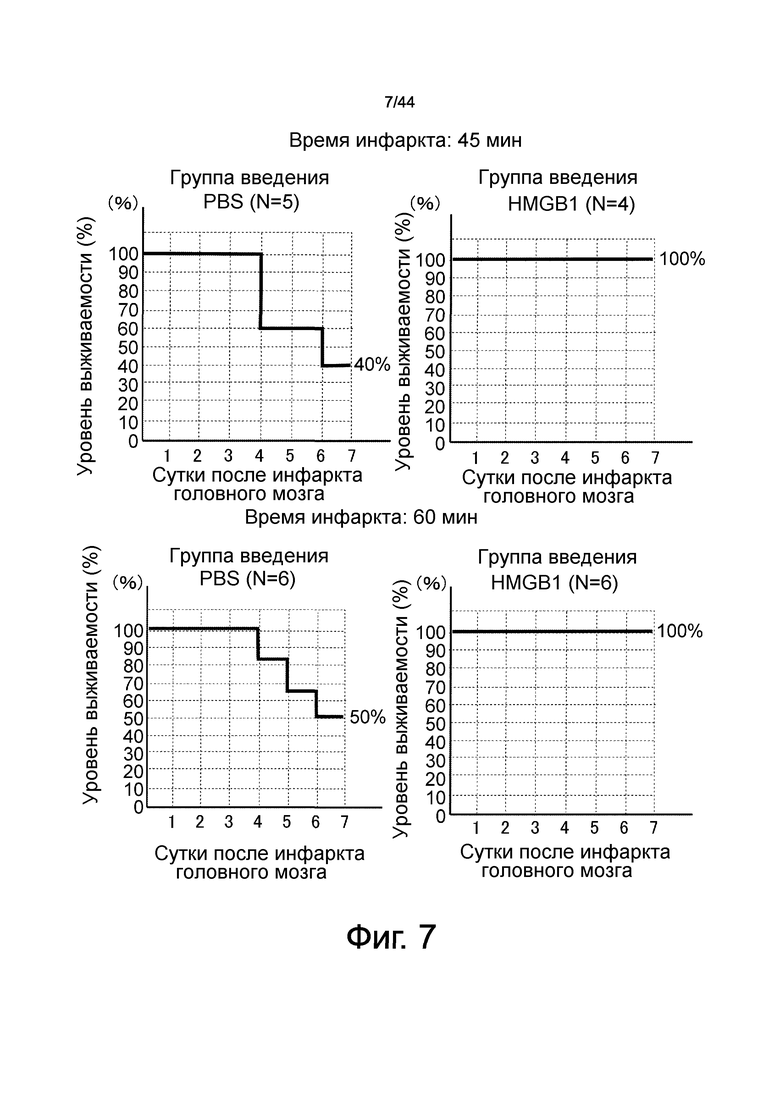
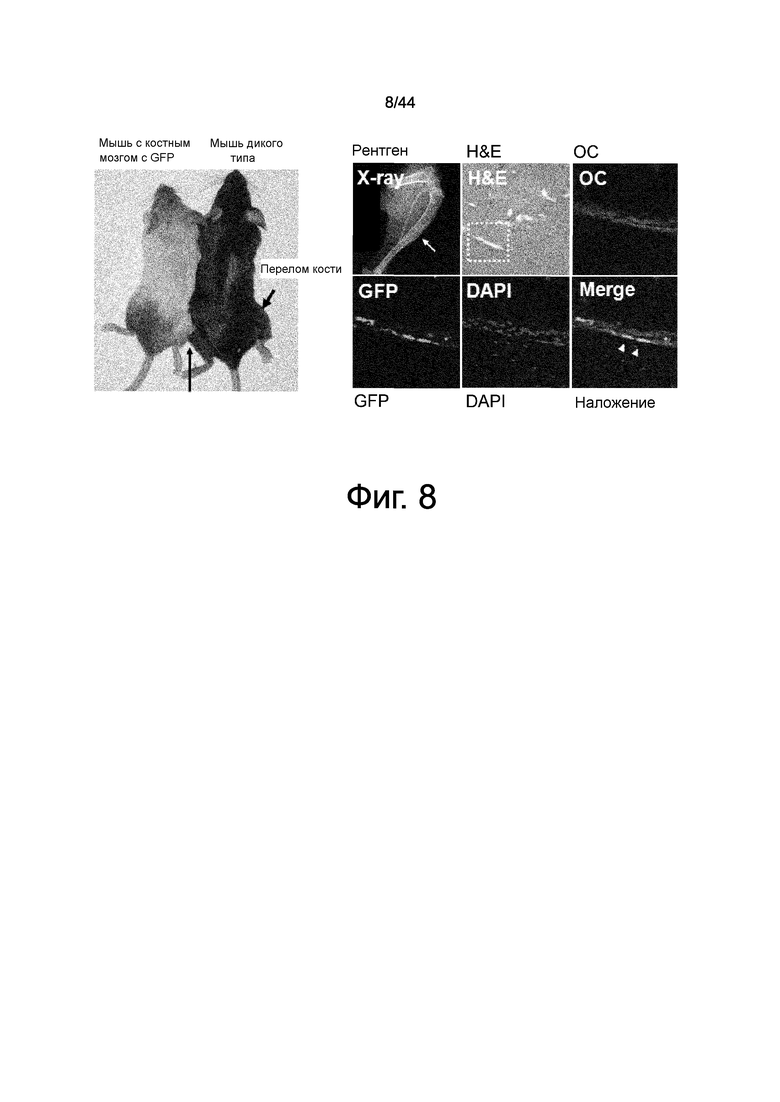
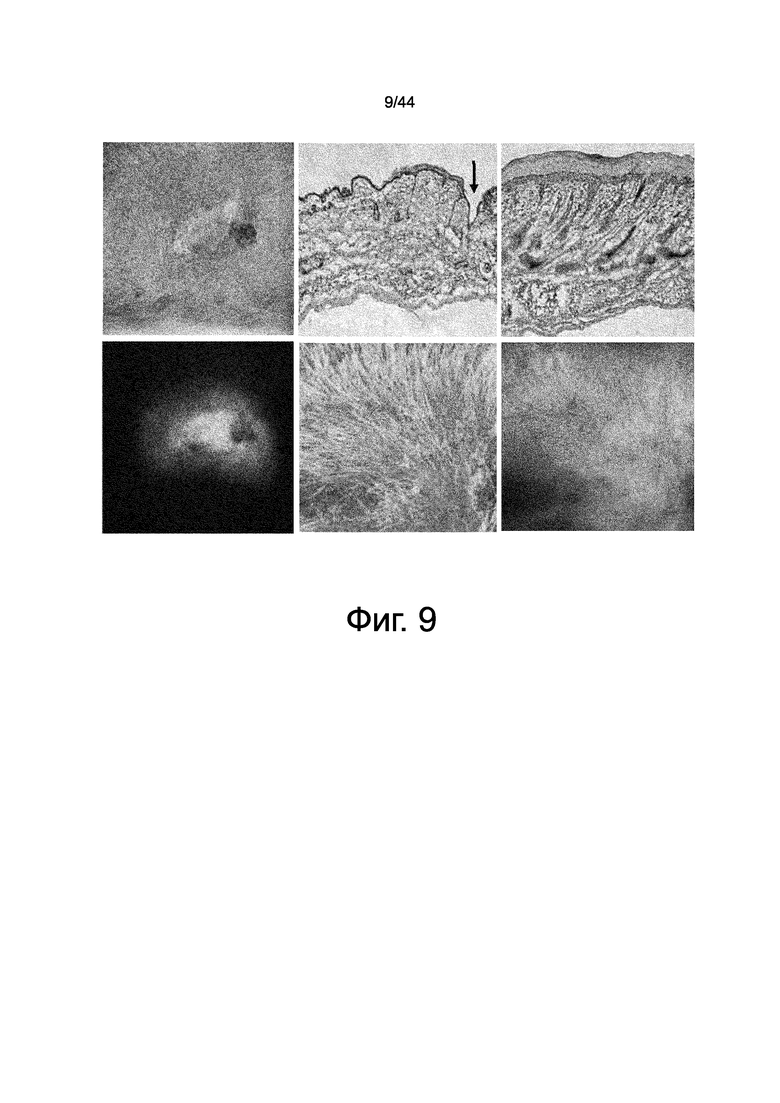
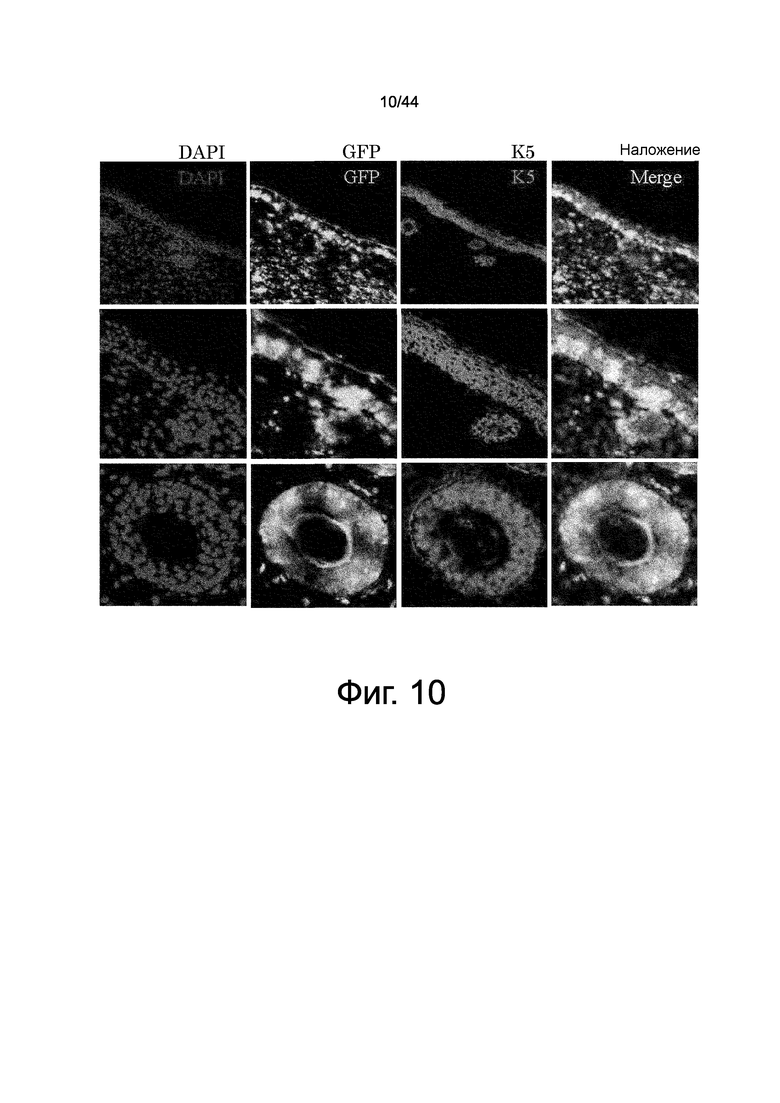
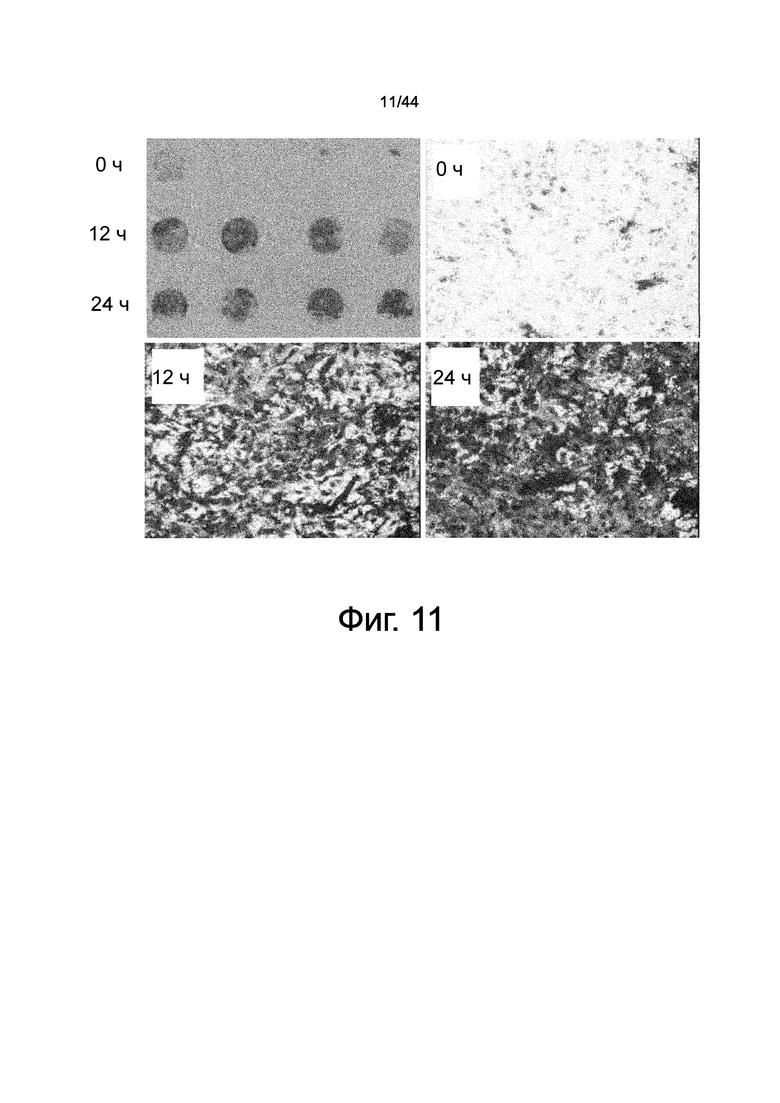
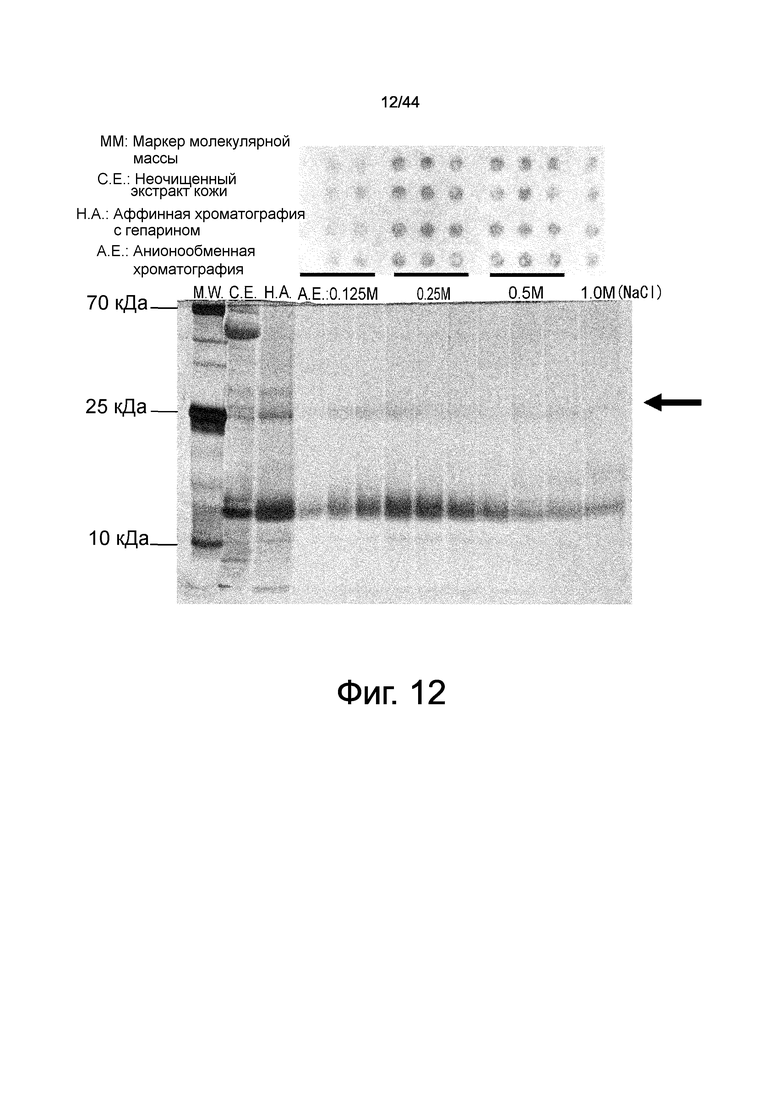
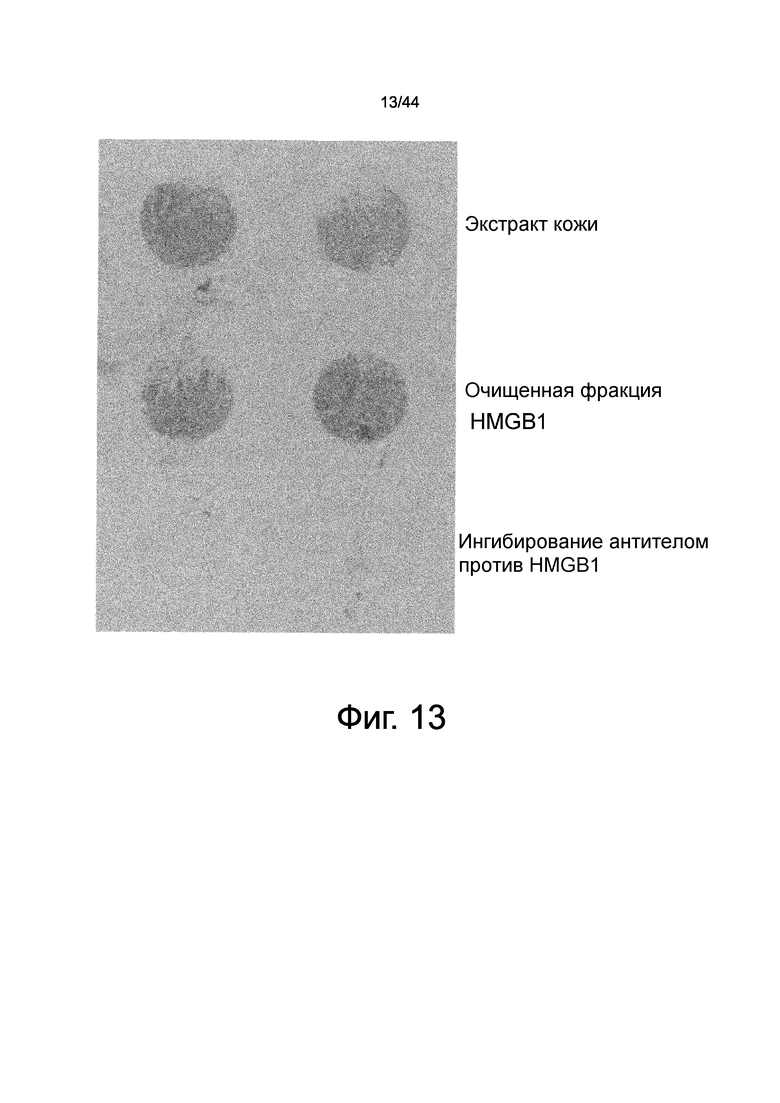

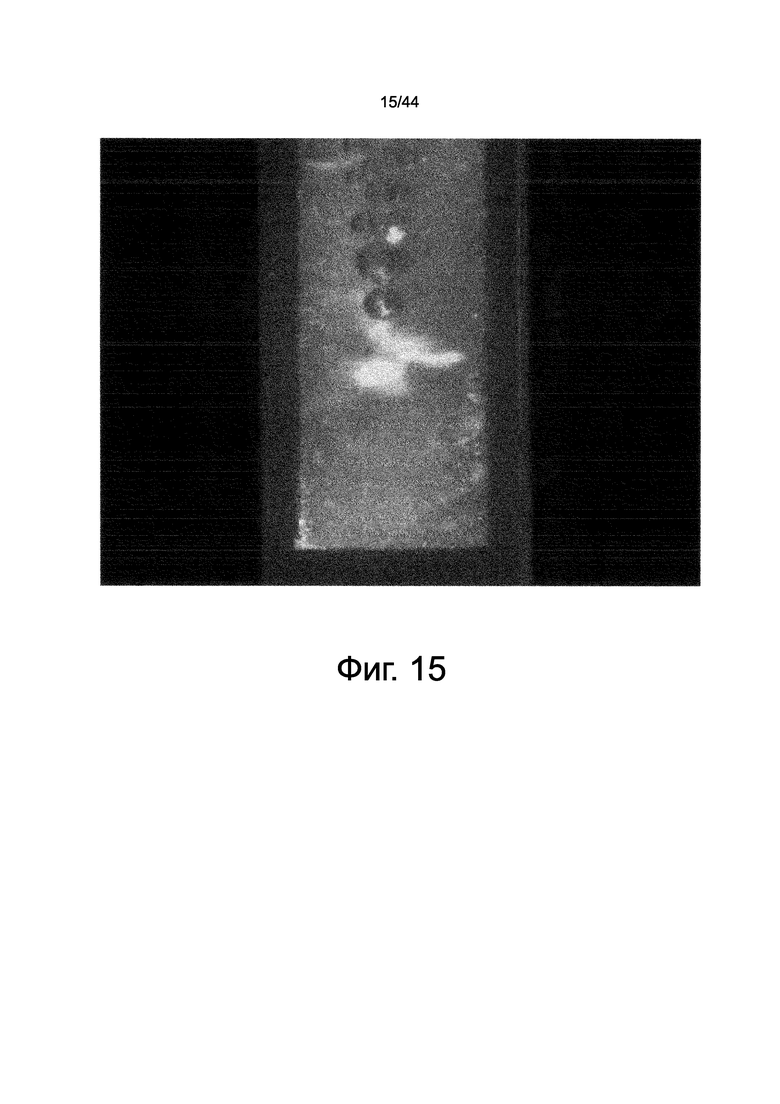

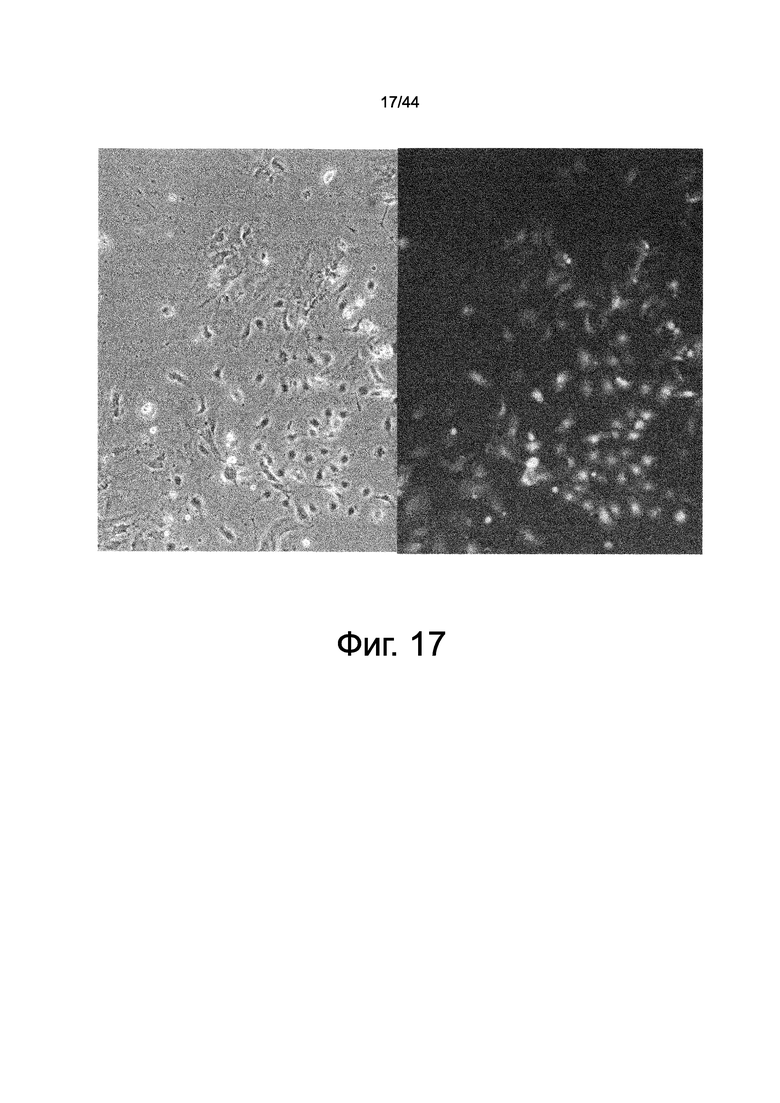
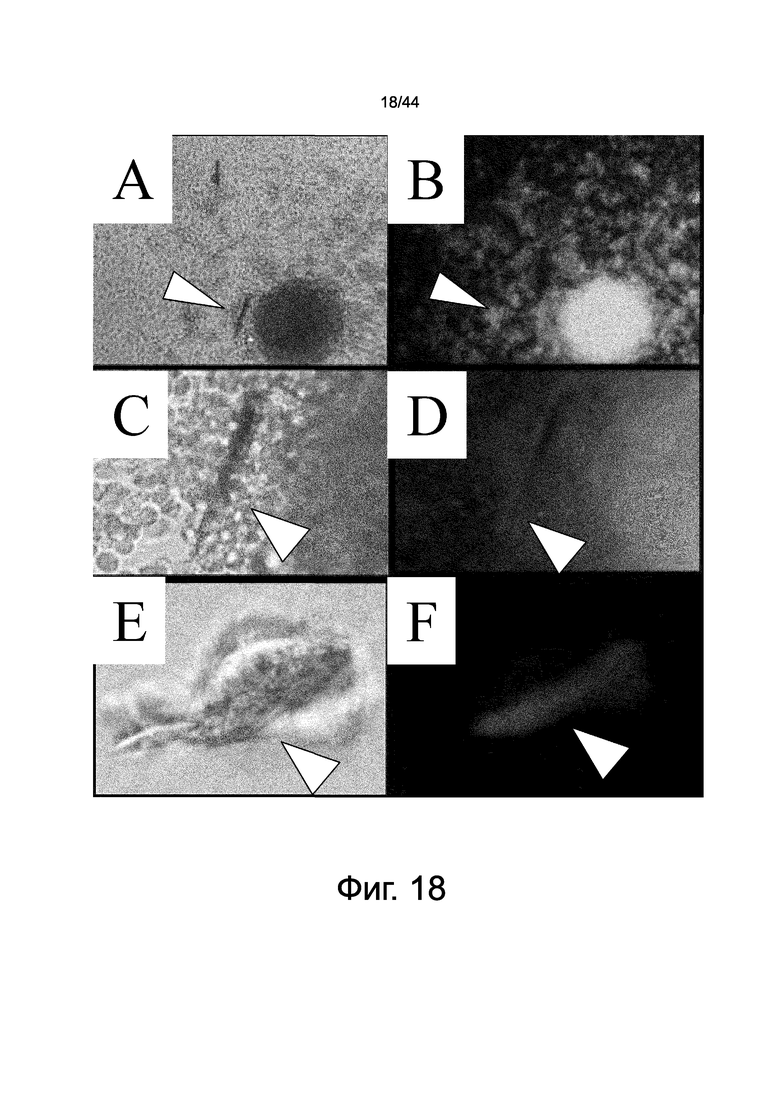

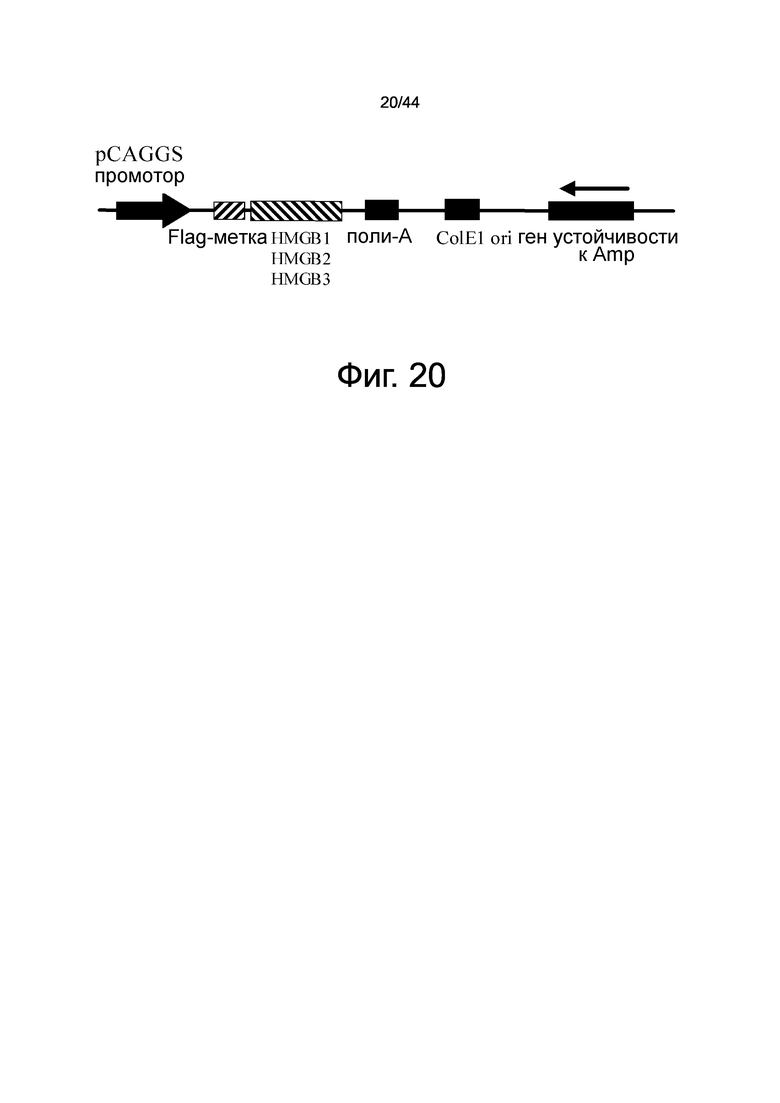
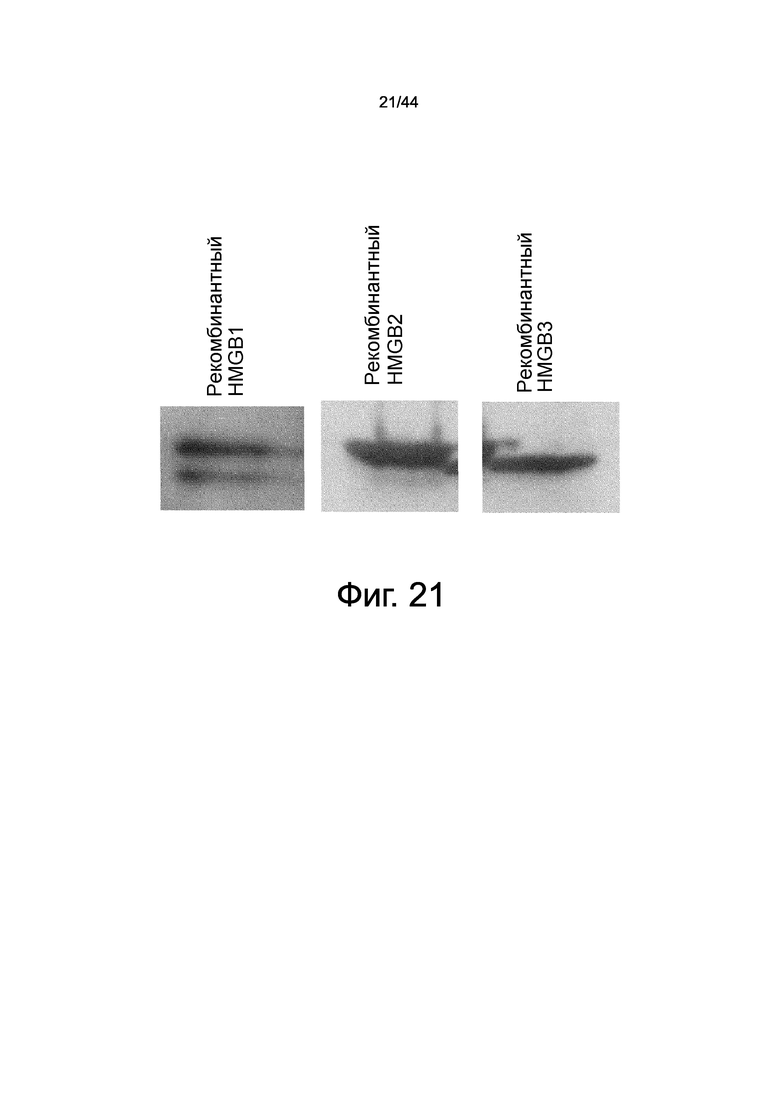
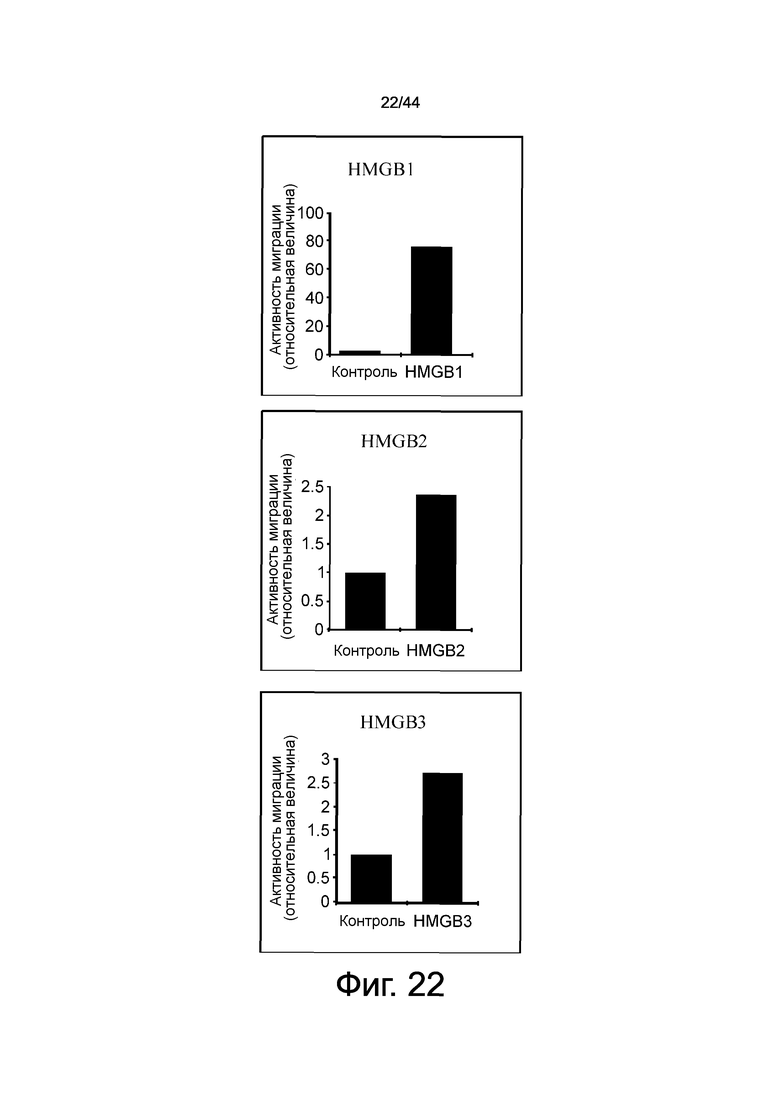
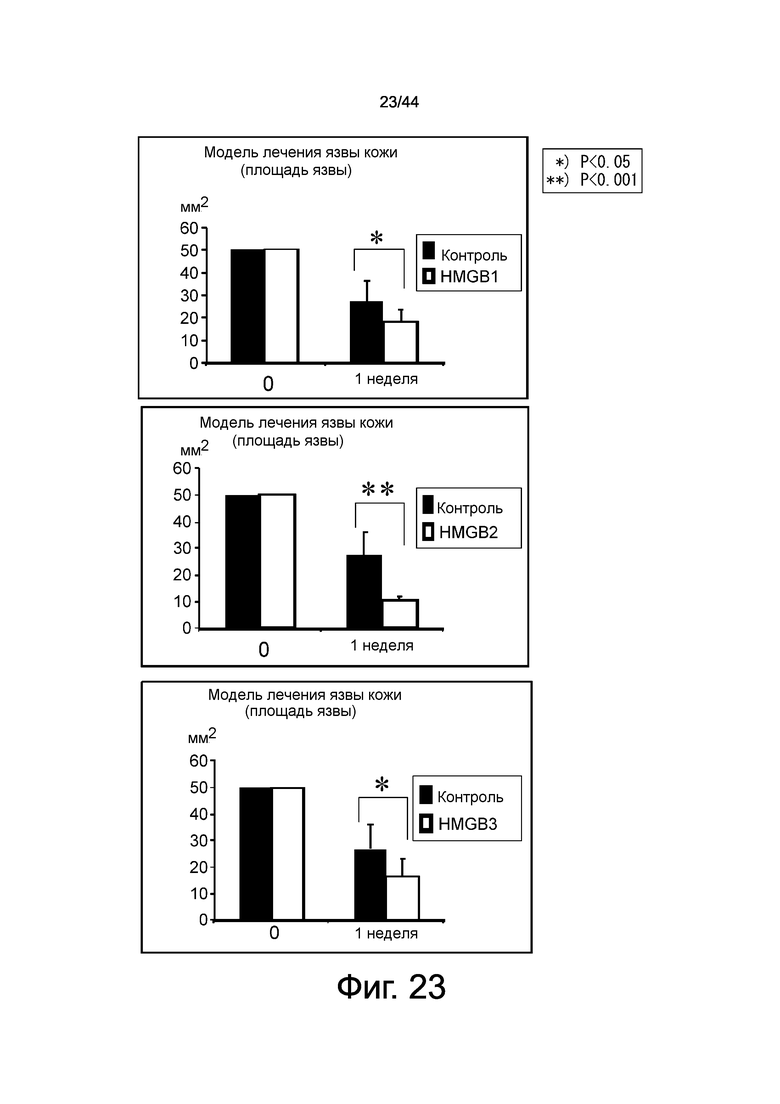
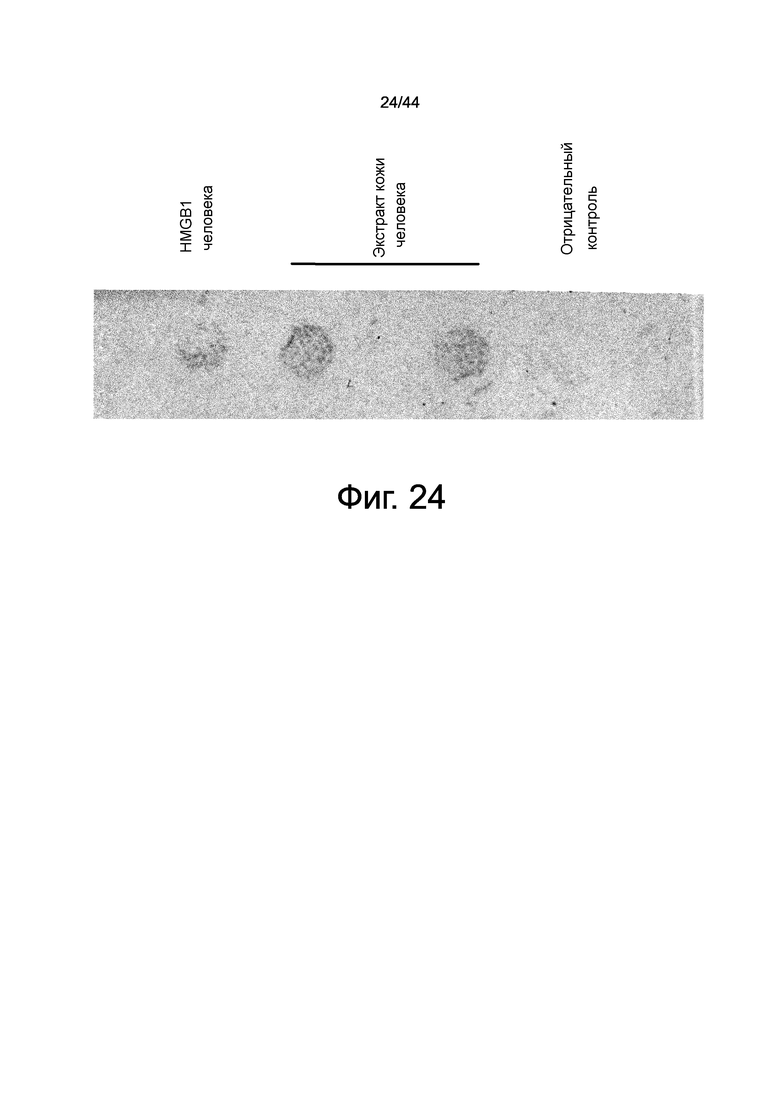
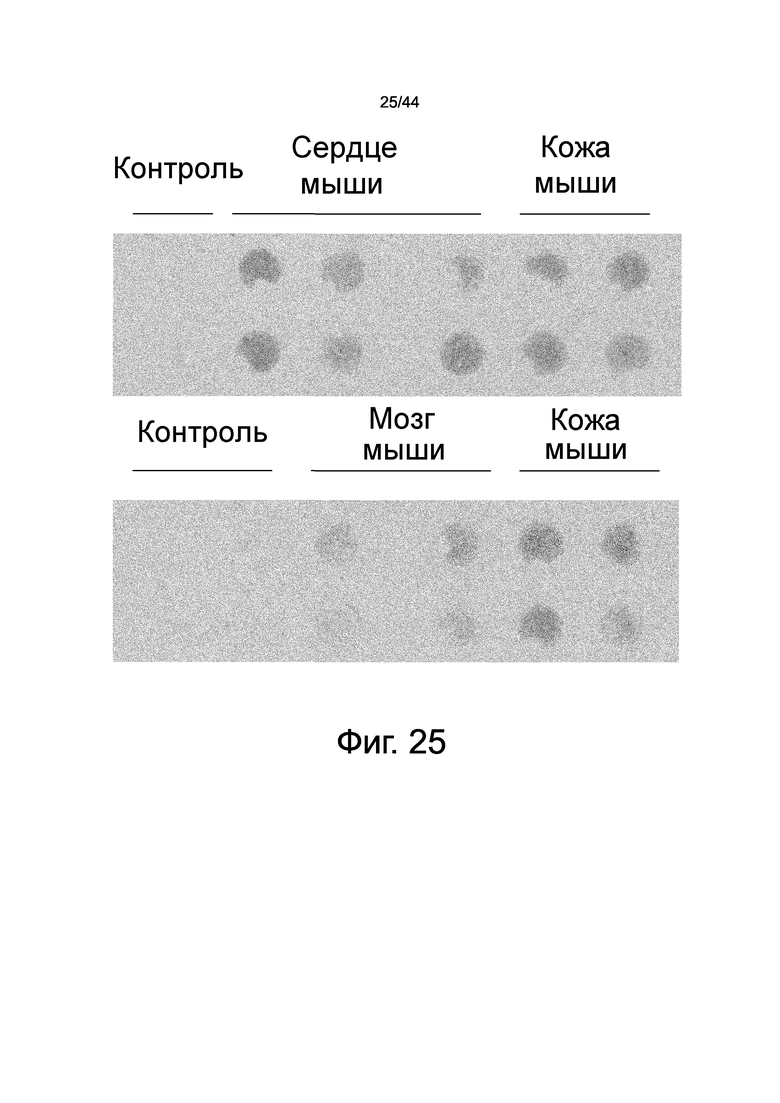


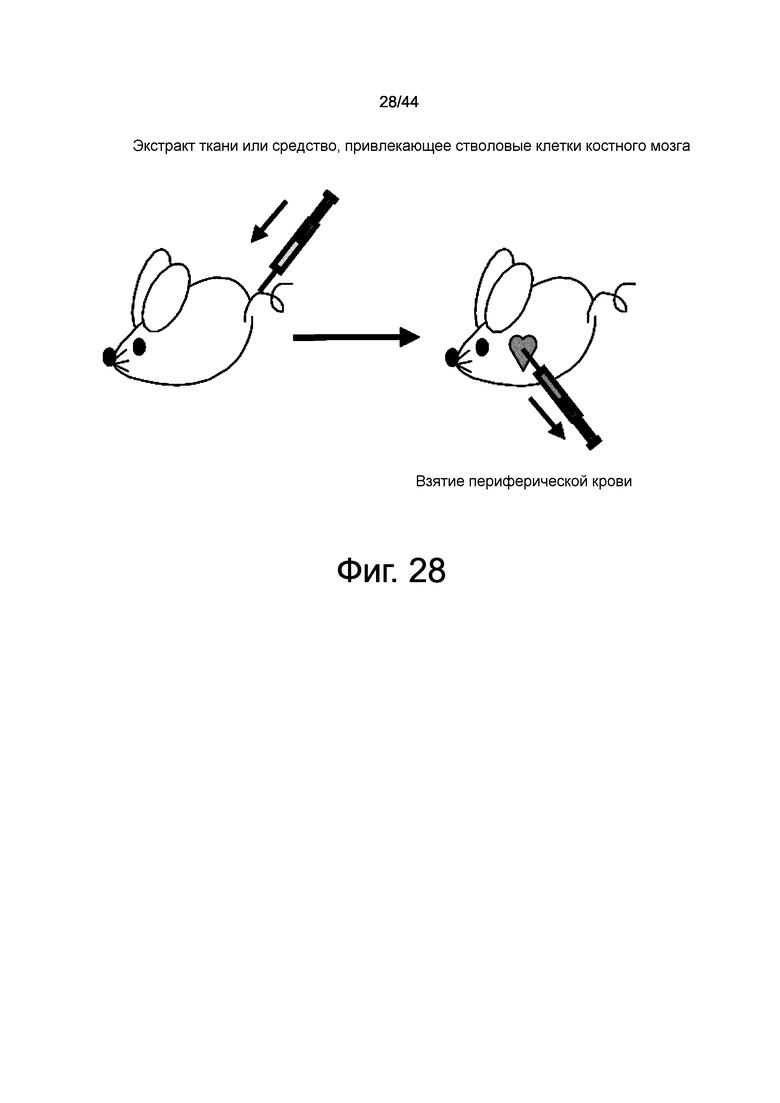
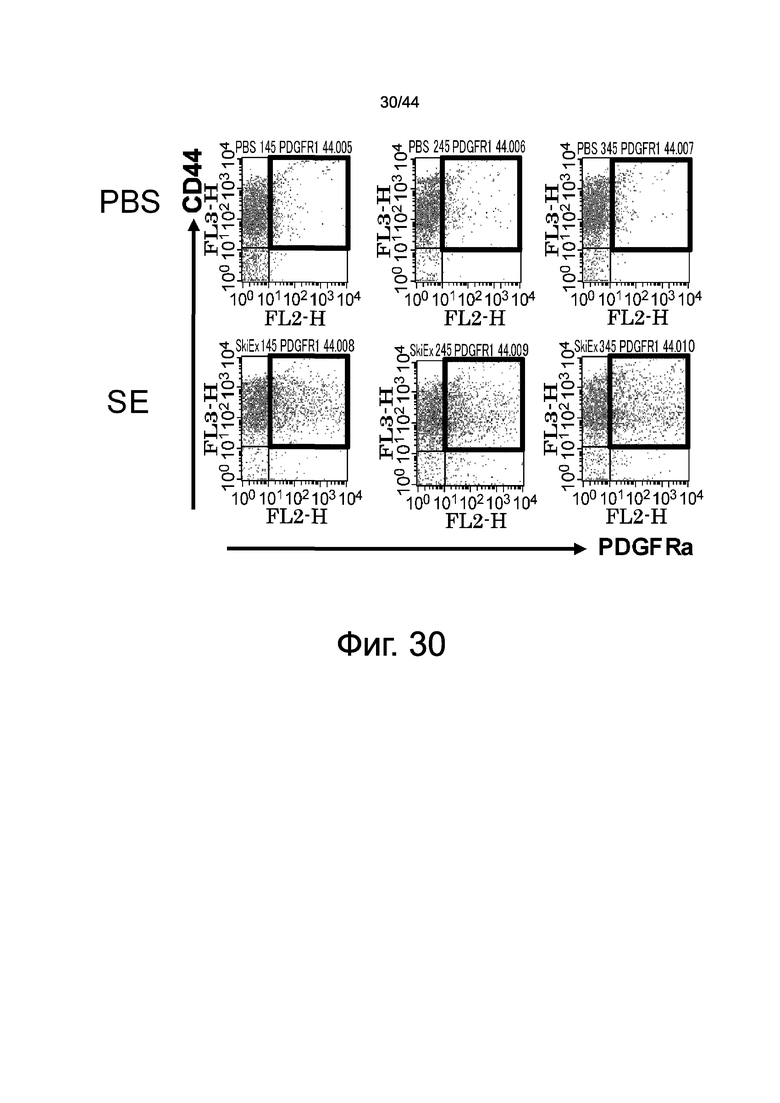
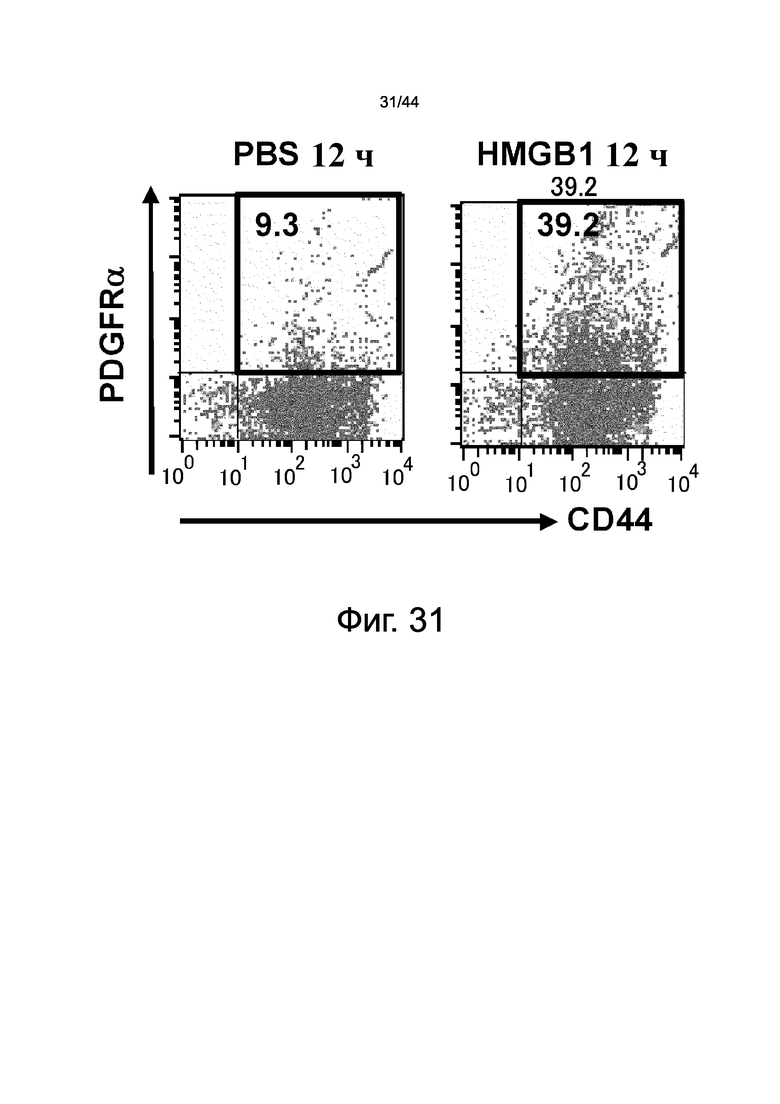
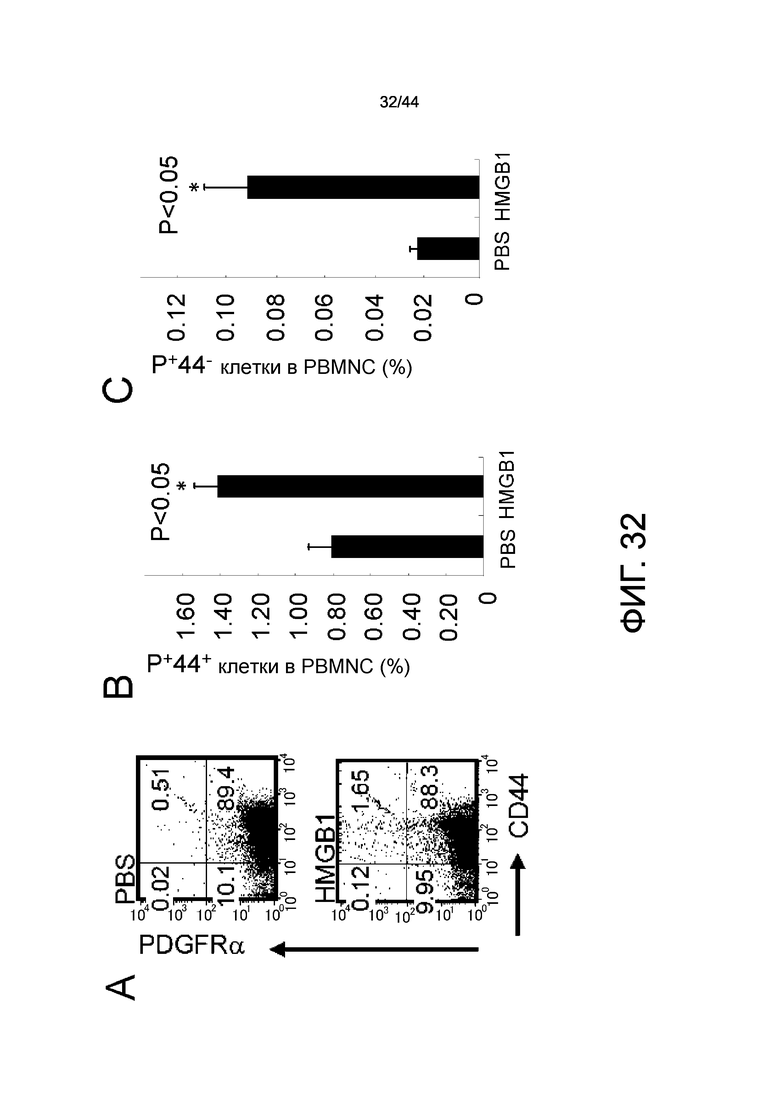

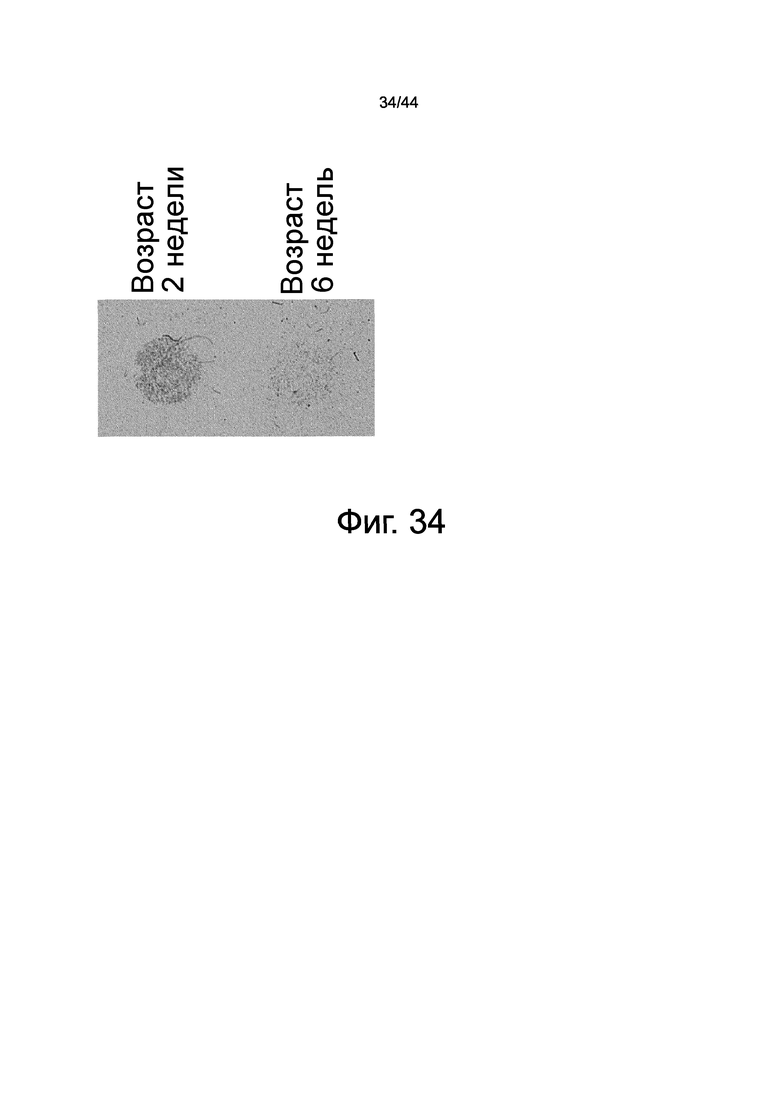

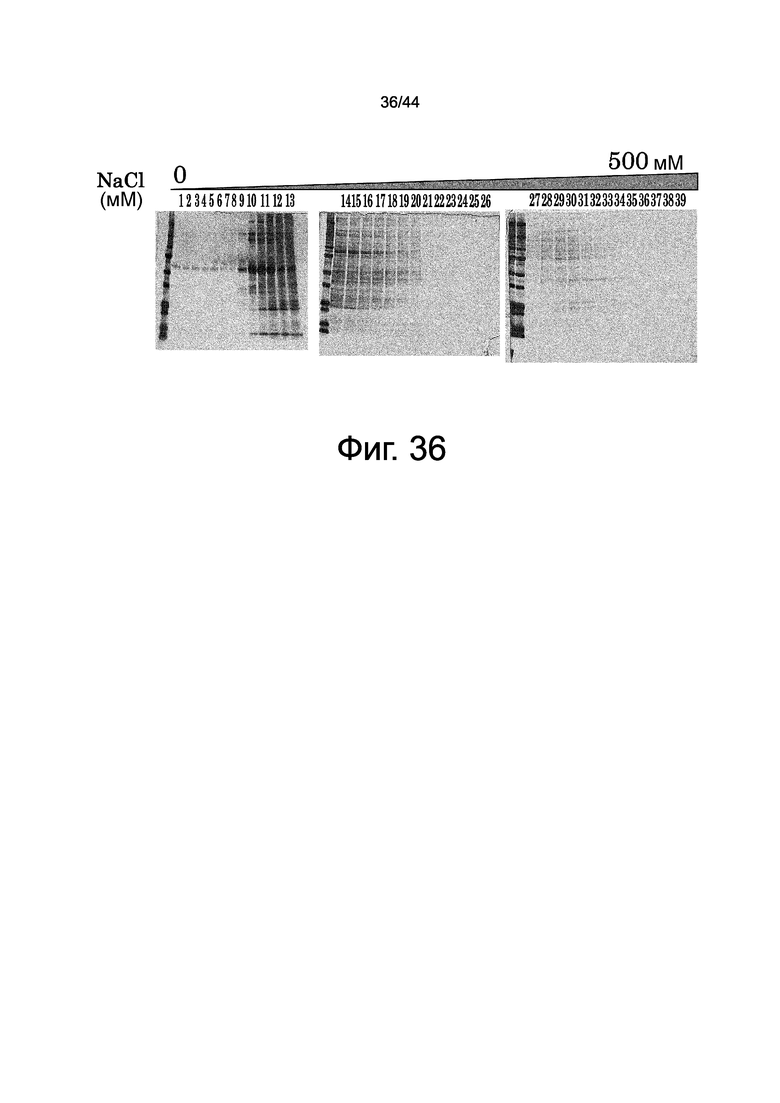


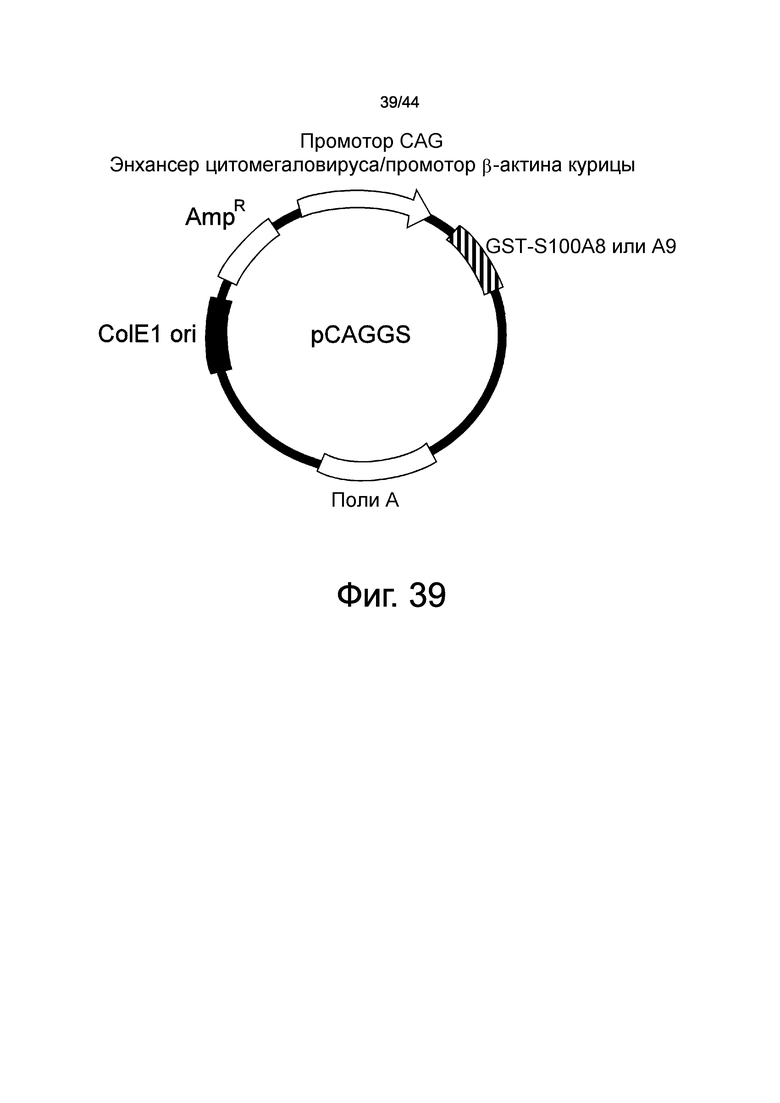
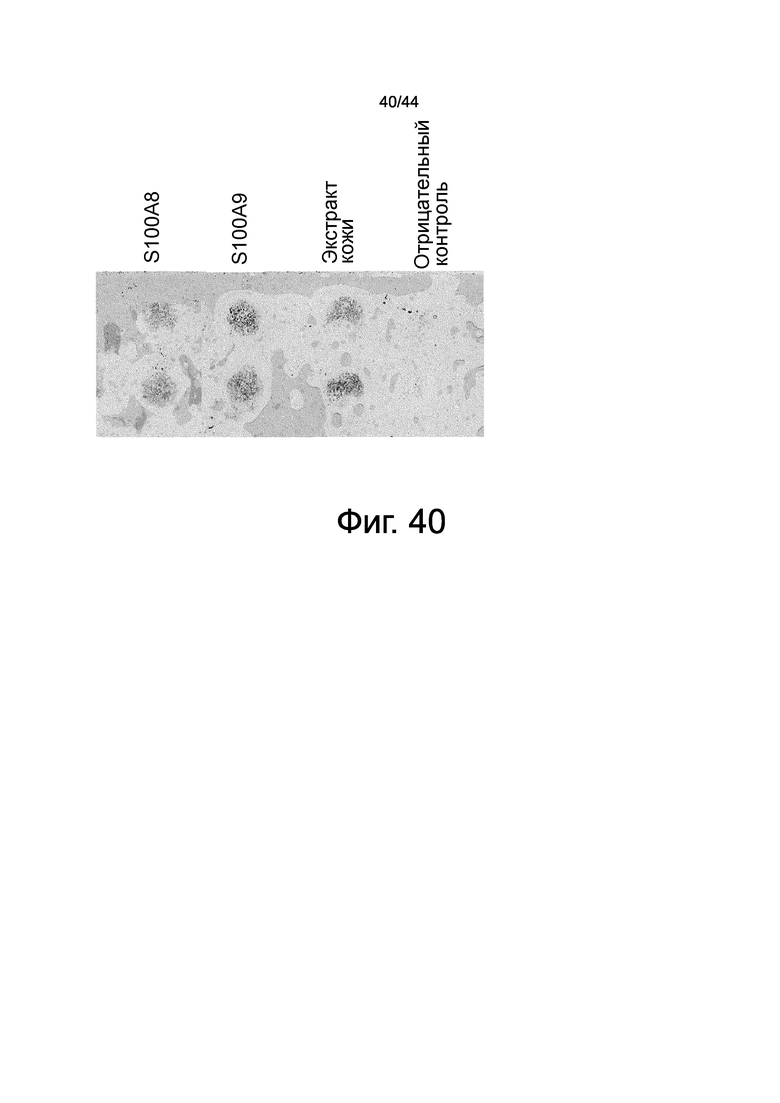



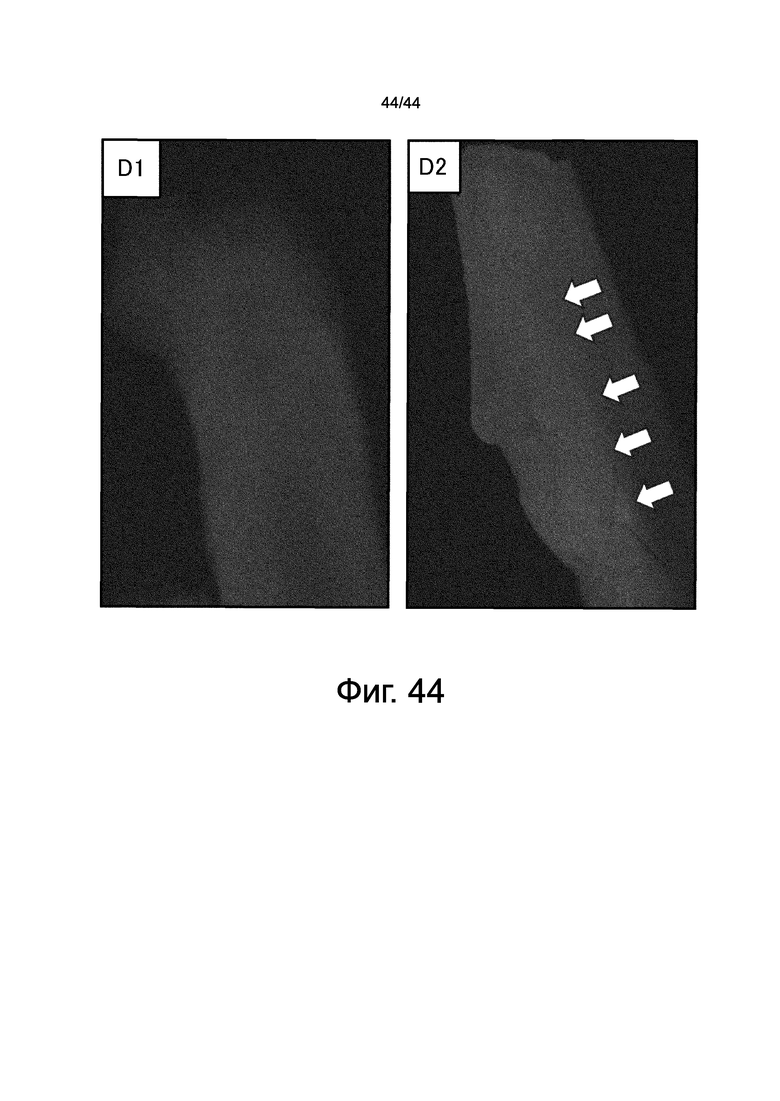
Представленные изобретения касаются применения средства, стимулирующего регенерацию тканей, и способа стимуляции регенерации мезенхимальных, эпителиальных или неврологических тканей путем введения такого средства. Охарактеризованное средство представляет собой белок S100A8, клетку, которая секретирует белок S100A8, вектор, в который встроена ДНК, кодирующая белок S100A8, белок S100A9, клетку, которая секретирует белок S100A9 или вектор, в который встроена ДНК, кодирующая белок S100A8-9. Представленные изобретения могут быть использованы для индукции заживления поврежденных тканей путем привлечения происходящих из костного мозга клеток в область повреждения, тем самым осуществляя лечение таких заболеваний, как обширное изъязвление кожи, переломы костей, инфаркта головного мозга. 2 н. и 5 з.п. ф-лы, 44 ил., 1 табл., 9 пр.
1. Способ стимуляции регенерации мезенхимальных тканей, эпителиальных тканей или неврологической ткани, который включает стадию введения в ткань, отличную от ткани, нуждающейся в регенерации, эффективного количества средства, стимулирующего регенерацию тканей, выбранного из группы:
(a) белок S100A8;
(b) клетка, которая секретирует белок S100A8;
(c) вектор, в который встроена ДНК, кодирующая белок S100A8;
(d) белок S100A9;
(e) клетка, которая секретирует белок S100A9;
(f) вектор, в который встроена ДНК, кодирующая белок S100A9.
2. Способ по п. 1, где введение представляет собой парентеральное введение.
3. Способ по п. 2, где введение представляет собой инъекцию.
4. Способ по п. 1, где введение представляет собой внутрисосудистое, внутримышечное, подкожное, внутрикожное или внутрибрюшинное введение.
5. Способ по любому из пп. 1-4, в котором ткань представляет собой нервную, костную или кожную ткань.
6. Применение средства, стимулирующего регенерацию тканей для стимуляции регенерации мезенхимальных тканей, эпителиальных тканей или неврологической ткани, выбранного из группы:
(a) белок S100A8;
(b) клетка, которая секретирует белок S100A8;
(c) вектор, в который встроена ДНК, кодирующая белок S100A8;
(d) белок S100A9;
(e) клетка, которая секретирует белок S100A9;
(f) вектор, в который встроена ДНК, кодирующая белок S100A9.
7. Применение по п. 6, где ткань представляет собой нервную, костную или кожную ткань.
| ROBINSON MJ et al., The S100 Family Heterodimer, MRP-8/14, Binds with High Affinity to Heparin and Heparan Sulfate Glycosaminoglycans on Endothelial Cells, J.Biol.Chem., 2002, Vol.277, No.5, pp.3658-3665. | |||
| WO 2008053892 A1, 08.05.2008 | |||
| RU 2005102593 A, 10.10.2005. |
Авторы
Даты
2016-10-10—Публикация
2010-10-28—Подача