ССЫЛКА НА СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей в считываемой с помощью компьютера форме. Считываемая с помощью компьютера форма включена в настоящее описание в качестве ссылки.
ССЫЛКА НА ДЕПОЗИТ БИОЛОГИЧЕСКОГО МАТЕРИАЛА
Настоящая заявка содержит ссылку на депозит биологического материала, которая включена в настоящее описание в качестве ссылки. Для полной информации см. таблицу 1.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выделенным штаммам бактерий и к способу выбора штаммов бактерий, имеющих характеристики увеличенной конкурентоспособности и эффективности.
УРОВЕНЬ ТЕХНИКИ, К КОТОРОМУ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Для поддержания здорового роста растения должны извлекать множество элементов из почвы, в которой они растут. Эти элементы включают азот и так называемые микроэлементы (например, медь, железо и цинк), однако многие почвы имеют дефицит таких элементов или они содержат их только в формах, которые не могут легко быть поглощены растениями (в целом, полагают, что необходимые элементы не могут быть легко поглощены растениями, если они не присутствуют в почве в растворенной форме). Азот является необходимым элементом для большинства растений, поскольку он участвует в синтезе аминокислот, белков, нуклеотидов, нуклеиновых кислот, хлорофилла, коферментов и в росте и здоровье растения в целом. Чтобы устранять такой дефицит, источники дефицитных элементов часто вносят в почву для увеличения скорости роста и выхода, получаемого из сельскохозяйственных растений. Например, часто в почву добавляют нитрат и/или аммоний для устранения дефицита доступного азота.
В области растениеводства хорошо известно, что для многих возделываемых культур требуется, чтобы почва предоставляла относительно большие количества азота растению. Примечательными исключениями из этих растений, требующих азот через почву, являются растения семейства бобовых.
В частности, бобовые растения являются уникальными относительно небобовых растений их способностью фиксировать атмосферный азот в форме аммиака. Способность фиксировать атмосферный азот в форме пригодного источника азота для растения устраняет необходимость получения растением азота из почвы. Однако фиксация азота требует симбиотических взаимоотношений между бобовым растением и нативными бактериями в почве. Одними из наиболее широко исследованных партнеров в этих симбиотических взаимоотношениях являются бактерии, принадлежащие роду Bradyrhizobium или Rhizobium. Gresshoff, P. (1999). Identification of Plant Genes Involved in Plant-Microbe Interactions. Stacey, G. & Keen, T. (Ed.), Plant-Microbe Interactions (4th ed.) (Ch. 6). St. Paul: APS Press.
Симбиоз обычно достигается путем обмена комплексом двунаправленных сигналов между растением и микроорганизмом, и микроорганизмом и растением. Как правило, растительные факторы, такие как флавоноиды и флавоноид-подобные вещества, индуцируют колонизацию бактерий в корневом клубеньке бобового растения. (Gresshoff, 1999). После колонизации бактериями корневого клубенька, бактерии осуществляют морофологические изменения в растении, а именно, закручивание корневых волосков и развитие нового корневого органа - клубенька (Gresshoff, 1999). Клубенек позволяет установление новых физиологических условий для дифференцировки индуцирующих клубеньки бактерий в азотфиксирующий эндосимбионт, или бактероид, для колонизированного растения. (Gresshoff, 1999).
Хорошо известно, что подвижность и хемотаксис Rhizobial являются важными признаками для конкурентоспособности штаммов. Например, в Althabegoiti, et al., 2008, FEMS Microbiol. Lett. 282: 115-123 обсуждается получение самопроизвольного мутантного штамма из USDA 110, имеющего увеличенную подвижность, который усиливает образование клубеньков по сравнению со штаммом дикого типа. Кроме того, в Maier, et al., 1990, Appl. Environ. Microbiol. 56 (8): 2341-2346 обсуждается роль молибдена в процессе биологической фиксации азота. Более того, в Alves, et al., 2003, Plant and Soil 252: 1-9 обсуждаются инокуляты сои, используемые в Бразилии, и важность конкурентоспособности для эффективной фиксации азота. Наконец, в Bloem, J.F., et al., 2001, Bio Fertil. Soils 33: 181-189 описана важность конкурентоспособности при выборе штаммов. В этом исследовании исследователи используют способы генетической инженерии для помещения репортерного гена (GUS) в их маркерный штамм для определения конкурентоспособности штаммов. (Bloem, et al. 2001). Поскольку проведенное исследование (Bloem, et al. 2001) требовало широкого применения химического окрашивания и технологии микроскопии, описанный способ остается непрактичным подходом для скрининга большой выборки микроорганизмов.
Задачей настоящего изобретения является предоставление сверхконкурентоспособного изолята(ов) бактерий из рода Bradyrhizobia для колонизации бобовых растений, который превосходит по способности к колонизации коммерчески доступные штаммы, например, коммерческий штамм USDA 532C. Следующей задачей настоящего изобретения является предоставление сверхконкурентоспособного изолята(ов) бактерий из рода Bradyrhizobia для колонизации бобовых растений, способного повышать эффективность стимуляции роста бобового растения по сравнению с коммерчески доступными штаммами, например, коммерческим штаммом USDA 532C.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Для улучшения общего здоровья растения и доступности пригодного источника азота для растений существует потребность в штаммах бактерий, которые являются лучшими в отношении колонизации растений и усиления общего роста растений. Выделенные штаммы по настоящему изобретению реализуют эти преимущества.
Настоящее изобретение относится к выделенным штаммам бактерий, имеющим по меньшей мере следующие улучшенные характеристики по сравнению с коммерчески доступными штаммами, например, коммерческим штаммом USDA 532C, где улучшенные характеристики включают, но не ограничиваются ими:
a. увеличенную конкурентоспособность для колонизации растения; и
b. увеличенную эффективность стимуляции роста растения.
Настоящее изобретение относится к биологически чистой культуре(ам) штамма(ов) Bradyrhizobia japonicum
штамм, имеющий номер доступа депозита NRRL B-50592 (также депонированный как NRRL B-59571);
штамм, имеющий номер доступа депозита NRRL B-50593 (также депонированный как NRRL B-59572);
штамм, имеющий номер доступа депозита NRRL B-50586 (также депонированный как NRRL B-59565);
штамм, имеющий номер доступа депозита NRRL B-50588 (также депонированный как NRRL B-59567);
штамм, имеющий номер доступа депозита NRRL B-50587 (также депонированный как NRRL B-59566);
штамм, имеющий номер доступа депозита NRRL B-50589 (также депонированный как NRRL B-59568);
штамм, имеющий номер доступа депозита NRRL B-50591 (также депонированный как NRRL B-59570);
штамм, имеющий номер доступа депозита NRRL B-50590 (также депонированный как NRRL B-59569);
штамм, имеющий номер доступа депозита NRRL B-50594 (также депонированный как NRRL B-50493);
штамм, имеющий номер доступа депозита NRRL B-50726;
штамм, имеющий номер доступа депозита NRRL B-50727;
штамм, имеющий номер доступа депозита NRRL B-50728;
штамм, имеющий номер доступа депозита NRRL B-50729; и
штамм, имеющий номер доступа депозита NRRL B-50730, или комбинация по меньшей мере двух или более из указанных выше депонированных штаммов.
Настоящее изобретение также относится к выделенному штамму(ам) бактерий по настоящему изобретению, который включает штамм(ы), который является близкородственным любому из описанных выше штаммов, исходя из идентичности последовательности 16S рДНК, и который является по меньшей мере на 95% идентичным любому из описанных выше штаммов, исходя из идентичности последовательности 16S рДНК.
Кроме того, настоящее изобретение относится к способу усиления роста растений, включающему применение к растениям, семенам растений или почве, окружающей растения или семена растений, композиции, содержащей по меньшей мере один из штаммов по настоящему изобретению или комбинацию по меньшей мере двух или более из указанных выше депонированных штаммов.
Кроме того, изобретение относится к композициям, содержащим один или несколько штаммов по настоящему изобретению, в том числе с агрономически приемлемым носителем.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1A представлено изображение геля ПЦР, на котором показан уникальный праймер 209, специфичный к USDA 532C.
На фиг.1B представлено изображение геля ПЦР, на котором показана специфичность праймера 209 с использованием USDA 532C и нативных штаммов.
На фиг.2A представлено изображение геля ПЦР, на котором показан штамм Bradyrhizobia japonicum USDA 532C в качестве конкурентно доминирующего штамма для образования клубеньков сои.
На фиг.2B представлено изображение геля ПЦР, на котором показаны штаммы, отличные от штамма Bradyrhizobia japonicum USDA 532C, в качестве конкурентно доминирующего штамма для образования клубеньков сои.
На фиг.3A представлена дендрограмма отпечатков ДНК выделенных штаммов и USDA 532C:
138 - NRRL B-50589 (также депонированный как NRRL B-59568);
13 - NRRL B-50586 (также депонированный как NRRL B-59565);
p140 - USDA 532C;
184 - NRRL B-50594 (также депонированный как NRRL B-50493);
142 - NRRL B-50590 (также депонированный как NRRL B-59569);
130 - NRRL B-50587 (также депонированный как NRRL B-59566);
65 - NRRL B-50588 (также депонированный как NRRL B-59567);
198 - NRRL B-50592 (также депонированный как NRRL B-59571);
135 - NRRL B-50591 (также депонированный как NRRL B-59570); и
48 - NRRL B-50593 (также депонированный как NRRL B-59572).
На фиг.3B представлена дендрограмма отпечатков ДНК выделенных штаммов и USDA 532C:
138 - NRRL B-50589 (также депонированный как NRRL B-59568);
13 - NRRL B-50586 (также депонированный как NRRL B-59565);
140 - USDA 532C;
184 - NRRL B-50594 (также депонированный как NRRL B-50493);
142 - NRRL B-50590 (также депонированный как NRRL B-59569);
130 - NRRL B-50587 (также депонированный как NRRL B-59566);
65 - NRRL B-50588 (также депонированный как NRRL B-59567);
198 - NRRL B-50592 (также депонированный как NRRL B-59571);
135 - NRRL B-50591 (также депонированный как NRRL B-59570);
48 - NRRL B-50593 (также депонированный как NRRL B-59572)
318 - NRRL B-50727,
278 - NRRL B-50726,
727 - NRRL B-50730,
370 - NRRL B-50728; и
518 - NRRL B-50729.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выделенным штаммам бактерий, имеющим по меньшей мере следующие улучшенные характеристики по сравнению с коммерчески доступными штаммами, например, коммерческим штаммом USDA 532C, где улучшенные характеристики включают, но не ограничиваются ими:
a. увеличенную конкурентоспособность для колонизации растения; и
b. увеличенную эффективность в отношении стимуляции роста растения.
“Штамм(ы) бактерий”, как используют в рамках изобретения, означает штаммы бактерий, которые являются диазотрофами. Это означает бактерии, которые являются симбиотическими азотфиксирующими бактерии. Неограничивающие примеры штаммов бактерий, как используют в рамках изобретения, включают, но не ограничиваются ими бактерии рода Rhizobium spp. (например, R. cellulosilyticum, R. daejeonense, R. etli, R. galegae, R. gallicum, R. giardinii, R. hainanense, R. huautlense, R. indigoferae, R. leguminosarum, R. loessense, R. lupini, R. lusitanum, R. mongolense, R. miluonense, R. sullae, R. tropici, R. undicola и/или R. yanglingense), Bradyrhizobium spp. (например, B. bete, B. canariense, B. elkanii, B. iriomotense, B. japonicum, B. jicamae, B. liaoningense, B. pachyrhizi и/или B. yuanmingense), Azorhizobium spp. (например, A. caulinodans и/или A. doebereinerae), Sinorhizobium spp. (например, S. abri, S. adhaerens, S. americanum, S. aboris, S. fredii, S. indiaense, S. kostiense, S. kummerowiae, S. medicae, S. meliloti, S. mexicanus, S. morelense, S. saheli, S. terangae и/или S. xinjiangense), Mesorhizobium spp (M. albiziae, M. amorphae, M. chacoense, M. ciceri, M. huakuii, M. loti, M. mediterraneum, M. pluifarium, M. septentrionale, M. temperatum, M. tianshanense). В одном конкретном варианте осуществления штамм(ы) бактерий по изобретению дополнительно включают штаммы Bradyrhizobium japonicum, имеющие номера доступа депозитов NRRL B-50592 (также депонированный как NRRL B-59571), NRRL B-50593 (также депонированный как NRRL B-59572), NRRL B-50586 (также депонированный как NRRL B-59565), NRRL B-50588 (также депонированный как NRRL B-59567), NRRL B-50587 (также депонированный как NRRL B-59566), NRRL B-50589 (также депонированный как NRRL B-59568), NRRL B-50591 (также депонированный как NRRL B-59570); NRRL B-50590 (также депонированный как NRRL B-59569); NRRL B-50594 (также депонированный как NRRL B-50493); NRRL B-50726; NRRL B-50727; NRRL B-50728; NRRL B-50729; NRRL B-50730, или комбинацию по меньшей мере двух или более из указанных выше депонированных штаммов, включая два из указанных выше штаммов, по меньшей мере три из указанных выше штаммов, по меньшей мере четыре из указанных выше штаммов, по меньшей мере пять из указанных выше штаммов, по меньшей мере шесть из указанных выше штаммов, по меньшей мере семь из указанных выше штаммов, по меньшей мере восемь из указанных выше штаммов, по меньшей мере девять из указанных выше штаммов, по меньшей мере десять из указанных выше штаммов, по меньшей мере одиннадцать из указанных выше штаммов, по меньшей мере двенадцать из указанных выше штаммов, по меньшей мере тринадцать из указанных выше штаммов, вплоть до и включая все из указанных выше штаммов.
Термин “коммерчески доступный штамм(ы)” означает коммерчески доступные штаммы бактерий, например, USDA 532C, USDA 110, USDA 123, USDA 127, USDA 129, и т.д. Cregan, P.B., et al., 1989, Appl. and Enviro. Microbiol. 55 (10): 2532-2536.
Как используют в рамках изобретения, “увеличенная конкурентоспособность” и/или “увеличенное образование клубеньков” означают штамм(ы), обладающие доминирующей процентной заполненностью клубеньков, например, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99%, вплоть до 100% заполненности клубеньков. “Увеличеную конкурентоспособность” определяли согласно детальному анализу(ам), описанному ниже (см. Материалы и способы: “Протокол первичного скрининга” и “Протокол испытания конкуренции”).
Как используют в рамках изобретения, термин “клубенек” включает, но не ограничивается ими, детерминантные клубеньки, индетерминантные клубеньки или их комбинацию. Примеры детерминантных клубеньков и индетерминантных клубеньков хорошо известны в данной области и описаны в Denison, R. F., 2000, The Amer. Naturalist. 156 (6): 567-576. Детерминантные клубеньки встречаются в видах Glycine, Lotus или Phaseolus и имеют округлую или сферическую форму. (Denison, 2000). Детерминантные клубеньки растут только в течение ограниченного периода времени, как правило, несколько недель. (Denison, 2000). В противоположность детерминантным клубенькам, индетерминантные клубеньки встречаются в видах Medicago, Trifolium и Pisium, имеют вытянутую форму и растут постоянно. (Denison, 2000).
“Заполненность клубеньков” представляет собой термин, известный в данной области. McDermott T.R. & Graham, P.H., Appl. and Environ. Microbiol. 55(10): 2493-2498. Как используют в рамках изобретения, “заполненность клубеньков” означает процент клубеньков, занятых штаммом(ами) бактерий, отличным от коммерчески доступного штамма Bradyrhizobium, например USDA 532C, и/или количество клубеньков, содержащих конкретный штамм(ы) бактерий, отличный от коммерчески доступного штамма Bradyrhizobium, например USDA 532C, деленное на общее количество клубеньков, содержащих все штаммы бактерий. “Заполненность клубеньков” определяли в соответствии с детальным анализом(ами), описанным ниже (см. Материалы и способы: “Протокол первичного скрининга” и “Протокол испытания конкуренции”), и ее можно определить из анализа клубеньков растений, полученных из образцов либо из теплицы, либо с поля. В качестве примера, процентная заполненность клубеньков = A/(A+B) где A представляет собой количество клубеньков, содержащих конкретный штамм(ы) бактерий, отличный от коммерчески доступного штамма Bradyrhizobium, например, USDA 532C, и B представляет собой количество клубеньков, содержащих коммерчески доступный штамм Bradyrhizobium, например, USDA 532C. В данной области хорошо известно, что, за редким исключением, один клубенек содержит только один штамм бактерий. Johnston, A.W.B., et al., 1974, J. Gen. Microbiol 87: 343-350; Dunham, D. H. & Baldwin, I.L., 1931, Soil Science 32: 235-249; Johnson, H.W., et al., 1963, Agrono. J. 55: 269-271; Dudman, W.F. & Brockwell, J., 1968, J. Agricul. Res. 19: 739-747; Nicol, H. & Thorton, H.G., 1941, Proc. Roy. Soc. B 130, 32-59; Hughes, D.Q., & Vincent, J.M., 1942, Proc. of the Linnenan Soc. of New South Wales 67: 142-152; и Vincent, J.M. & Waters, L.M., 1953, J. Gen. Microbiol. 9: 357-370.
Как используют в рамках изобретения, “увеличенная эффективность стимуляции роста” включает по меньшей мере одно из увеличенного выхода растений, измеряемого в значениях бушель/акр, увеличенного количества плодов, увеличенного количества корней, увеличенной длины корней, увеличенной массы корней, увеличенного объема корней, увеличенной площади листьев, увеличенной густоты стояния растений, увеличенной мощности растений и/или увеличенной способности фиксировать азот (N2). “Увеличенную эффективность стимуляции роста” определяли в соответствии с детальным анализом(ами), описанным ниже (см. Материалы и способы: “Протокол первичного скрининга” и “Протокол испытания эффективности”) и ее можно определять из анализа растений, полученных из образцов либо из теплицы, либо с поля.
Как используют в рамках изобретения “увеличенное количество плодов” означает увеличенное общее количество соевых бобов на соевом растении и/или увеличенную общую сухую массу соевых бобов на соевом растении.
Как используют в рамках изобретения “общая масса сухого вещества” означает массу растительного материала (например, плоды растений, стручки растений, корни растений, клубеньки растений, цельные растения, части растений, и т.д.) после инкубации при 80°C в течение определенного периода времени, например, по меньшей мере 4 часов, по меньшей мере 8 часов, по меньшей мере 12 часов, по меньшей мере 24 часов, по меньшей мере 48 часов и т.д., или любого периода времени, необходимого для высушивания растительного материала. Следует понимать, что время высушивания для определения “общей массы сухого вещества” зависит от многих факторов. Неограничивающие факторы, которые могут повлиять на время высушивания, включают материал, подлежащий высушиванию, массу материала, подлежащего высушиванию, количество материала, подлежащего высушиванию, и/или их комбинации. Инкубацию можно проводить в любом устройстве с контролируемой температурой, используемом в данной области. Для целей настоящего изобретения “общую массу сухого вещества определяли с помощью инкубатора Eppendorf Innova® 42R.
Термин “увеличенная способность фиксации азота (N2)”, как используют в рамках изобретения, означает, что выделенные бактерии могут увеличивать фиксацию азота (N2). В соответствии с “Протоколом испытания эффективности”, предоставленным ниже (Материалы и способы), относительную способность фиксации азота (N2) бактериями можно количественно определять путем измерения общего содержания азота в растении с использованием стандартных способов количественного определения азота, известных специалисту в данной области (например, способ Kjeldahl и т.д.). См. Takahashi, M., et al., 2007. Uptake, Assimilation, and Novel Metabolism of Nitrogen Dioxide in Plants, p. 109-118. N. Willey (ed.), Phytoremediation: Methods and Reviews, vol. 23. Humana Press, New York; Bremner, J. M. 1965. Total nitrogen, p. 1149-1178. C.A. Black (ed.), Methods of soil analysis, vol. 2. American Society for Agronomy, Madison; Schank, S.C., et al., 1981, App. and Enviro. Microbiol., 41 (2): 342-345.
В другом аспекте настоящего изобретения выделенный штамм(ы) бактерий имеет увеличенную температурную устойчивость. “Увеличенная температурная устойчивость” означает диапазон температур, при котором выделенный бактериальный штамм(ы) способен расти, например, максимальные и минимальные температуры, при которых выделенный штамм(ы) Bradyrhizobium может расти. В одном аспекте “увеличенную температурную устойчивость” определяли в соответствии с “Протоколом профиля температур”, рассмотренным ниже (Материалы и способы).
В другом аспекте настоящего изобретения выделенный штамм(ы) бактерий естественным образом устойчив к глифосату. В одном аспекте “увеличенную температурную устойчивость” определяли в соответствии с “Протоколом профиля устойчивости к глифосату”, рассмотренным ниже (Материалы и способы).
В другом аспекте выделенный штамм(ы) бактерий по настоящему изобретению включает штамм(ы), который является близкородственным любому из описанных выше штаммов, исходя из идентичности последовательности 16S рДНК. См. Stackebrandt E, et al., “Report of the ad hoc committee for the re-evaluation of the species definition in bacteriology,” Int J Syst Evol Microbiol. 52(3):1043-7 (2002) в отношении использования идентичности последовательностей 16S рДНК для определения родства в бактериях. В одном варианте осуществления по меньшей мере один штамм по меньшей мере на 95% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК, по меньшей мере на 96% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК, по меньшей мере на 97% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК, по меньшей мере на 98% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК, по меньшей мере на 98,5% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК, по меньшей мере на 99% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК или по меньшей мере на 99,5% идентичен любому из описанных выше штаммов, исходя из идентичности последовательностей 16S рДНК.
В другом варианте осуществления настоящее изобретение относится к способу выделения штамма(ов) бактерий, имеющих увеличенную конкурентоспособность для занятия клубеньков бобового растения и увеличенную эффективность стимуляции роста бобового растения. Как используют в рамках изобретения, термин “изолят, изоляты, выделение и/или выделенный, и т.д.” означает, что указанный материал извлечен из окружающей среды, в которой он обычно находится. Способ включает, среди прочего,
a. получение штамма(ов) бактерий из образца почвы;
b. воздействие штаммом(ами) бактерий и коммерчески доступным штаммом на бобовое растение;
с. выбор штамма(ов) бактерий, которые являются более конкурентоспособными, чем коммерчески доступный штамм, в отношении занятия клубеньков бобового растения;
d. анализ выбранного штамма(ов) бактерий, который является более конкурентоспособным в отношении занятия клубеньков бобового растения, чем коммерчески доступный штамм, на тот бактериальный штамм(ы), который имеет увеличенную эффективность стимуляции роста бобового растения; и
e. выделение штамма(ов) бактерий, имеющего увеличенную эффективность стимуляции роста бобового растения.
В одном аспекте выделенный штамм(ы) бактерий представляет собой штаммы рода Bradyrhizobium. В другом аспекте способ дополнительно включает стадию скрининга штамма(ов) Bradyrhizobium с использованием специфического праймера, уникального для коммерчески доступного штамма Bradyrhizobia, например, коммерческого штамма USDA 532C.
В другом аспекте, способ включает выделение культуры Bradyrhizobia japonicum, выбранной из группы, состоящей из:
штамм, имеющий номер доступа депозита NRRL B-50592 (также депонированный как NRRL B-59571);
штамм, имеющий номер доступа депозита NRRL B-50593 (также депонированный как NRRL B-59572);
штамм, имеющий номер доступа депозита NRRL B-50586 (также депонированный как NRRL B-59565);
штамм, имеющий номер доступа депозита NRRL B-50588 (также депонированный как NRRL B-59567);
штамм, имеющий номер доступа депозита NRRL B-50587 (также депонированный как NRRL B-59566);
штамм, имеющий номер доступа депозита NRRL B-50589 (также депонированный как NRRL B-59568);
штамм, имеющий номер доступа депозита NRRL B-50591 (также депонированный как NRRL B-59570);
штамм, имеющий номер доступа депозита NRRL B-50590 (также депонированный как NRRL B-59569);
штамм, имеющий номер доступа депозита NRRL B-50594 (также депонированный как NRRL B-50493);
штамм, имеющий номер доступа депозита NRRL B-50726;
штамм, имеющий номер доступа депозита NRRL B-50727;
штамм, имеющий номер доступа депозита NRRL B-50728;
штамм, имеющий номер доступа депозита NRRL B-50729; и
штамм, имеющий номер доступа депозита NRRL B-50730, или комбинация по меньшей мере двух или более из указанных выше депонированных штаммов, включая более двух, как например, по меньшей мере три из описанных выше штаммов, по меньшей мере четыре из описанных выше штаммов, по меньшей мере пять из описанных выше штаммов, по меньшей мере шесть из описанных выше штаммов, по меньшей мере семь из описанных выше штаммов, по меньшей мере восемь из описанных выше штаммов, по меньшей мере девять из описанных выше штаммов, по меньшей мере десять из описанных выше штаммов, по меньшей мере одиннадцать из описанных выше штаммов, по меньшей мере двенадцать из описанных выше штаммов, по меньшей мере тринадцать из описанных выше штаммов, в том числе, вплоть до всех из описанных выше штаммов.
В другом аспекте способ включает выделение штамма(ов) бактерий, имеющего увеличенную температурную устойчивость. См. Материалы и способы: “Протокол профиля температур”.
Более того, способ включает выделение штамма(ов) бактерий, имеющего природную устойчивость к глифосату. См. Материалы и способы: “Протокол профиля устойчивости к глифосату”.
В другом предпочтительном аспекте способ включает выделение штамма(ов) бактерий, выбранного из рода, состоящего из Rhizobium и Bradyrhizobium, способного усиливать образование клубеньков бобового растения.
Композиция
Настоящее изобретение относится к композиции, содержащей по меньшей мере один выделенный бактериальный штамм(ы) по настоящему изобретению или комбинацию по меньшей мере двух или более из указанных выше депонированных штаммов, в том числе более двух, как например, по меньшей мере три из описанных выше штаммов, по меньшей мере пять из описанных выше штаммов, по меньшей мере шесть из описанных выше штаммов, по меньшей мере семь из описанных выше штаммов, по меньшей мере восемь из описанных выше штаммов, по меньшей мере девять из описанных выше штаммов, по меньшей мере десять из описанных выше штаммов, по меньшей мере одиннадцать из описанных выше штаммов, по меньшей мере двенадцать из описанных выше штаммов, по меньшей мере тринадцать из описанных штаммов, в том числе вплоть до всех из описанных выше штаммов, и агрономически приемлемый носитель.
В некоторых вариантах осуществления композиция может представлять собой композицию инокулята. Как используют в рамках изобретения и в данной области, термин “композиция инокулята” относится, главным образом, к композициям или материалам, которые вносят совместимые бактериальные штаммы либо на внешнюю поверхность семян, либо в борозду для семян.
Композиция может содержать один или несколько агрономически приемлемых носителей. В случаях, когда используют несколько агрономически приемлемых носителей, агрономически приемлемые носители могут быть одинаковыми или могут отличаться. Как используют в рамках изобретения применительно к термину "носитель", термин “агрономически приемлемый” относится к любому материалу, который можно использовать для доставки активных веществ в семена, почву или растение, и предпочтительно этот носитель можно добавлять (к семенам, в почву или в растение) без неблагоприятного эффекта на рост растения, структуру почвы, осушение почвы и т.п. Пригодные носители включают, но не ограничиваются ими, чешуи пшеницы, отруби, измельченную пшеничную солому, торфяные порошки или гранулы, гранулы на основе гипса и глины (например, каолин, бентонит, монтмориллонит). Составы в качестве жидкости, торфа или смачиваемого порошка пригодны для покрытия семян. При использовании для покрытия семян, материал можно смешивать с водой, наносить на семена и позволять ему высохнуть. Примеры других носителей включают влажные отруби, высушенные, просеянные и нанесенные на семена перед покрытием адгезивным веществом, например, гуммиарабиком. В вариантах осуществления, которые охватывают состав активных веществ, агрономически приемлемый носитель может быть водным. Если используют жидкий носитель, жидкий (например, вода) носитель, как правило, включает среду для культивирования штаммов бактерий. Неограничивающие примеры подходящих сред для роста штаммов бактерий включают дрожжевой экстракт с маннитом, дрожжевой экстракт с глицерином, или любую среду, о которой специалистам в данной области известно, что она совместима и/или обеспечивает питательные вещества для роста штаммов бактерий.
Также композиции по настоящему изобретению охватывают композиции, включающие одну или несколько сигнальных молекул. Неограничивающие примеры сигнальных молекул растений включают факторы nod (т.е. липохитоолигосахариды), хитоолигосахариды, хитиновые соединения, флавоноиды, жасмоновую кислоту или ее производные, линолеиновую кислоту или ее производные, линоленовую кислоту или ее производные, каррикины или их комбинации.
Соединения липохитоолигосахаридов (LCO), также известные в данной области как симбиотические сигналы Nod или факторы Nod, состоят из олигосахаридной основной цепи из β-1,4-связанных остатков N-ацетил-D-глюкозамина ("GlcNAc") с N-связанной жирной ацильной цепью, конденсированной на невосстанавливающем конце. LCO отличается количеством остатков GlcNAc в основной цепи, длиной и степенью насыщенности жирной ацильной цепи, и замещениями восстанавливающих и невосстанавливающих остатков сахаров. Пример LCO представлен ниже в качестве формулы I:

на которой:
G представляет собой гексозамин, который может быть замещен, например, ацетильной группой на азоте, сульфатной группой, ацетильной группой и/или простой эфирной группой на кислороде,
R1, R2, R3, R5, R6 и R7, которые могут быть идентичными или могут отличаться, обозначают H, CH3 CO-, CxHyCO-, где x представляет собой целое число от 0 до 17, и y представляет собой целое число от 1 до 35, или любую ацильную группу, например, такую как карбамил,
R4 обозначает моно-, ди- или триненасыщенную алифатическую цепь, содержащую по меньшей мере 12 атомов углерода, и n представляет собой целое число от 1 до 4.
LCO можно получать (выделять и/или очищать) из бактерий, таких как Rhizobia, например, Rhizobium spp., Bradyrhizobium spp., Sinorhizobium spp. и Azorhizobium spp. Структура LCO является характерной для каждого из вида бактерий, и каждый штамм может продуцировать множество LCO с различными структурами. Например, конкретные LCO из S. meliloti также описаны в патенте США 5549718, имеющие формулу II:

в которой R обозначает H или CH3CO- и n равно 2 или 3.
Более конкретные LCO включают NodRM, NodRM-1, NodRM-3. Когда они являются ацетилированными (R=CH3CO-), они становятся AcNodRM-1 и AcNodRM-3, соответственно (патент США 5545718).
LCO из Bradyrhizobium japonicum описаны в патентах США 5175149 и 5321011. В общем, они представляют собой пентасахаридные фитогормоны, содержащие метилфукозу. Описан ряд этих происходящих из B. japonicum LCO: BjNod-V (C18:1); BjNod-V (AC, C18:1), BjNod-V (C16:1); и BjNod-V (AC, C16:0), где "V" указывает на присутствие пяти N-ацетилглюкозаминов; "Ac" обозначает ацетилирование; число после "C" указывает на количество атомов углерода в боковой цепи жирной кислоты; и число после ":" обозначает количество двойных связей.
LCO, используемые в композициях по изобретению, можно получать (т.е. выделять и/или очищать) из штаммов бактерий, которые продуцируют LCO, таких как штаммы Azorhizobium, Bradyrhizobium (включая B. japonicum), Mesorhizobium, Rhizobium (включая R. leguminosarum), Sinorhizobium (включая S. meliloti), и штаммы бактерий, модифицированные способами генетической инженерии так, чтобы они продуцировали LCO.
Также настоящее изобретение охватывает композиции, в которых используются LCO, полученные (т.е. выделенные и/или очищенные) из микоризного гриба, такого как грибы группы Glomerocycota, например, Glomus intraradicus. Структуры репрезентативных LCO, получаемых из этих грибов, описаны в WO 2010/049751 и WO 2010/049751 (LCO, описанные в них, также называют "факторами Myc").
Кроме того, композиции по настоящему изобретению охватывают применение синтетических соединений LCO, таких как соединения, описанные в WO 2005/063784, и рекомбинантных LCO, полученных способами генетической инженерии. Основная встречающаяся в природе структура LCO может содержать модификации или замены, встречающиеся во встречающихся в природе LCO, такие как модификации и замены, описанные в Spaink, Crit. Rev. Plant Sci. 54:257-288 (2000) и D'Haeze, et al., Glycobiology 12:79R-105R (2002). Олигосахаридные молекулы-предшественники (CO, которые, как описано ниже, также пригодны в качестве сигнальных молекул растений согласно настоящему изобретению) для конструирования LCO также могут синтезироваться модифицированными способами генетической инженерии организмами, например, как описано в Samain, et al., Carb. Res. 302:35-42 (1997); Samain, et al., J. Biotechnol. 72:33-47 (1999).
LCO можно использовать в различных формах в отношении чистоты и их можно использовать отдельно или в форме культуры продуцирующих LCO бактерий или грибов. Способы предоставления по существу чистых LCO включают простое удаление клеток микроорганизмов из смеси LCO и микроорганизмов, или с последующим выделением или очисткой молекул LCO посредством разделения фаз растворителей LCO с последующей хроматографией ВЭЖХ, как описано, например, в патенте США 5549718. Очистку можно улучшать путем повторения ВЭЖХ, и очищенные молекулы LCO можно сушить сублимационной сушкой для длительного хранения.
Хитоолигосахариды (CO) известны в данной области как связанные β-1-4-связями структуры N-ацетилглюкозамина, идентифицированные в качестве хитиновых олигомеров, а также в качестве N-ацетилхитоолигосахаридов. CO имеют уникальные и отличающиеся конструкции боковых цепей, которые делают их отличающимися от молекул хитина [(C8H13NO5)n, CAS № 1398-61-4], и молекул хитозана [(C5H11NO4)n, CAS № 9012-76-4]. Репрезентативные источники литературы, в которых описана структура и получение CO, являются следующими: Van der Holst, et al., Current Opinion in Structural Biology, 11:608-616 (2001); Robina, et al., Tetrahedron 58:521-530 (2002); Hanel, et al., Planta 232:787-806 (2010); Rouge, et al. Chapter 27, "The Molecular Immunology of Complex Carbohydrates", Advances in Experimental Medicine and Biology, Springer Science; Wan, et al., Plant Cell 21:1053-69 (2009); PCT/F100/00803 (9/21/2000); и Demont-Caulet, et al., Plant Physiol. 120(1):83-92 (1999). CO могут быть синтетическими или рекомбинантными. Способы получения рекомбинантных CO известны в данной области. См., например, Samain, et al. (выше); Cottaz, et al., Meth. Eng. 7(4):311-7 (2005) и Samain, et al., J. Biotechnol. 72:33-47 (1999).
Композиции по настоящему изобретению также могут включать хитиновые соединения (отличные от CO), флавоноиды, жасмоновую кислоту, линолеиновую кислоту и линоленовую кислоту и их производные и каррикины.
Хитины и хитозаны, которые являются главными компонентами клеточных стенок грибов и экзоскелетов насекомых и ракообразных, также состоят из остатков GlcNAc. Хитиновые соединения включают хитин, (IUPAC: N-[5-[[3-ацетиламино-4,5-дигидрокси-6-(гидроксиметил)оксан-2-ил]метоксиметил]-2-[[5-ацетиламино-4,6-дигидрокси-2-(гидроксиметил)оксан-3-ил]метоксиметил]-4-гидрокси-6-(гидроксиметил)оксан-3-ил]этанамид) и хитозан (IUPAC: 5-амино-6-[5-амино-6-[5-амино-4,6-дигидрокси-2(гидроксиметил)оксан-3-ил]окси-4-гидрокси-2-(гидроксиметил)оксан-3-ил]окси-2-(гидроксиметил)оксан-3,4-диол). Эти соединения можно получать из коммерческих источников, например, от Sigma-Aldrich, или получать из насекомых, панциря ракообразных или клеточных стенок грибов. Способы получения хитина и хитозана известны в данной области и описаны, например, в патенте США 4536207 (получение из панцирей ракообразных), Pochanavanich, et al., Lett. Appl. Microbiol. 35:17-21 (2002) (получение из клеточных стенок грибов) и патенте США 5965545 (получение из панцирей крабов и гидролиз коммерческого хитозана). Можно получать деацетилированные хитины и хитозаны, которые имеют диапазон ацетилирования от менее чем 35% до более чем 90%, и охватывают широкий спектр молекулярных масс, например, низкомолекулярные олигомеры хитозана массой менее 15 кДа и олигомеры хитина массой от 0,5 до 2 кДа; хитозан "практической категории" с молекулярной массой приблизительно 15 кДа; и высокомолекулярный хитозан массой вплоть до 70 кДа. Также являются коммерчески доступными композиции хитина и хитозана, составленные для обработки семян. Коммерческие продукты включают, например, ELEXA® (Plant Defense Boosters, Inc.) и BEYONDTM (Agrihouse, Inc.).
Флавоноиды представляют собой фенольные соединения, имеющие общую структуру из двух ароматических колец, связанных мостиком из трех атомов углерода. Флавоноиды продуцируются растениями и имеют множество функций, например, в качестве полезных сигнальных молекул, и в качестве защиты от насекомых, животных, грибов и бактерий. Классы флавоноидов включают халконы, антоцианидины, кумарины, флавоны, флаванолы, флавонолы, флаваноны и изофлавоны. См. Jain, et al., J. Plant Biochem. & Biotechnol. 11:1-10 (2002); Shaw, et al., Environmental Microbiol. 11:1867-80 (2006).
Репрезентативные флавоноиды, которые могут быть пригодными в композициях по настоящему изобретению, включают генистеин, даидзеин, формононетин, нарингенин, гесперетин, лутеолин и апигенин. Флавоноидные соединения являются коммерчески доступными, например, от Natland International Corp., Research Triangle Park, NC; MP Biomedicals, Irvine, CA; LC Laboratories, Woburn MA. Флавоноидные соединения можно выделять из растений или семян, например, как описано в патентах США 5702752; 5990291 и 6146668. Флавоноидные соединения также можно получать с помощью модифицированных способами генетической инженерии организмов, таких как дрожжи, как описано в Ralston, et al., Plant Physiology 137:1375-88 (2005).
Также в композициях по настоящему изобретению можно использовать жасмоновую кислоту (JA, [1R-[1α,2β(Z)]]-3-оксо-2-(пентенил)циклопентануксусная кислота) и ее производные, линолеиновую кислоту ((Z,Z)-9,12-октадекадиеновая кислота) и ее производные и линоленовую кислоту ((Z,Z,Z)-9,12,15-октадекатриеновая кислота) и ее производные. Жасмоновая кислота и ее метиловый эфир, метилжасмонат (MeJA), в совокупности известные как жасмонаты, представляют собой соединения на основе октадеканоидов, которые встречаются в природе в растениях. Жасмоновая кислота продуцируется корнями побегов пшеницы и грибковыми микроорганизмами, такими как Botryodiplodia theobromae и Gibbrella fujikuroi, дрожжами (Saccharomyces cerevisiae) и патогенными и непатогенными штаммами Escherichia coli. Линолеиновая кислота и линоленовая кислота образуются в процессе биосинтеза жасмоновой кислоты. Сообщается, что жасмонаты, линолеиновая кислота и линолеиновая кислота (и их производные) являются индукторами экспрессии генов nod или продукции LCO ризобактериями. См., например, Mabood, Fazli, Jasmonates induce the expression of nod genes in Bradyrhizobium japonicum, May 17, 2001; и Mabood, Fazli, "Linoleic and linolenic acid induce the expression of nod genes in Bradyrhizobium japonicum", USDA 3, May 17, 2001.
Пригодные производные линолеиновой кислоты, линоленовой кислоты и жасмоновой кислоты, которые могут быть пригодными в композициях по настоящему изобретению, включают сложные эфиры, амиды, гликозиды и соли. Репрезентативные сложные эфиры представляют собой соединения, в которых карбоксильная группа линолеиновой кислоты, линоленовой кислоты или жасмоновой кислоты заменена группой -COR, где R представляет собой группу -OR1, в которой R1 представляет собой: алкильную группу, такую как C1-C8 неразветвленная или разветвленная алкильная группа, например, метильная, этильная или пропильная группа; алкенильную группу, такую как C2-C8 неразветвленная или разветвленная алкенильная группа; алкинильную группу, такую как C2-C8 неразветвленная или разветвленная алкинильная группа; арильную группу, имеющую, например, от 6 до 10 атомов углерода; или гетероарильную группу, имеющую, например, от 4 до 9 атомов углерода, где гетероатомы в гетероарильной группе могут представлять собой, например, N, O, P или S. Репрезентативные амиды представляют собой соединения, в которых карбоксильная группа линолеиновой кислоты, линоленовой кислоты или жасмоновой кислоты заменена группой -COR, где R представляет собой группу NR2R3, в которой R2 и R3 независимо представляют собой: водород; алкильную группу, такую как C1-C8неразветвленная или разветвленная алкильная группа, например, метильную, этильную или пропильную группу; алкенильную группу, такую как C2-C8 неразветвленная или разветвленная алкенильная группа; алкинильную группу, такую как C2-C8неразветвленная или разветвленная алкинильная группа; арильную группу, имеющую, например, от 6 до 10 атомов углерода; или гетероарильную группу, имеющую, например, от 4 до 9 атомов углерода, где гетероатомы в гетероарильной группе могут представлять собой, например, N, O, P или S. Сложные эфиры можно получать известными способами, такими как катализируемое кислотой нуклеофильное присоединение, где карбоновую кислоту подвергают реакции со спиртом в присутствии каталитического количества минеральной кислоты. Амиды также можно получать известными способами, такими как реакция карбоновой кислоты с подходящим амином в присутствии агента реакции сочетания, такого как дициклогексилкарбодиимид (DCC), в нейтральных условиях. Пригодные соли линолеиновой кислоты, линоленовой кислоты и жасмоновой кислоты включают, например, основно-аддитивные соли. Основания, которые можно использовать в качестве реагентов для получения метаболически приемлемых основных солей этих соединений, включают основания, происходящие из катионов, таких как катионы щелочных металлов (например, калий и натрий) и катионы щелочноземельных металлов (например, кальций и магний). Эти соли можно легко получать путем смешения раствора линолеиновой кислоты, линоленовой кислоты или жасмоновой кислоты с раствором основания. Соль можно осаждать из раствора и собирать фильтрацией или ее можно выделять другими способами, такими как выпаривание растворителя.
Каррикины представляют собой винилогические 4H-пироны, например, 2H-фуро[2,3-c]пиран-2-оны, включая их производные и аналоги. Примеры этих соединений соответствуют следующей структуре:

где Z представляет собой O, S или NR5; каждый из R1, R2, R3 и R4 независимо представляет собой H, алкил, алкенил, алкинил, фенил, бензил, гидрокси, гидроксиалкил, алкокси, фенилокси, бензилокси, CN, COR6, COOR=, галоген, NR6R7 или NO2; и каждый из R5, R6 и R7 независимо представляет собой H, алкил или алкенил, или их биологически приемлемую соль. Примеры биологически приемлемых солей этих соединений могут включать кислотно-аддитивные соли, образованные с биологически приемлемыми кислотами, примеры которых включают гидрохлорид, гидробромид, сульфат или бисульфат, фосфат или гидрофосфат, ацетат, бензоат, сукцинат, фумарат, малеат, лактат, цитрат, тартрат, глюконат; метансульфонат, бензолсульфонат и п-толуолсульфоновую кислоту. Дополнительные биологически приемлемые соли металлов могут включать соли щелочных металлов с основаниями, примеры которых включают соли натрия или калия. Примеры соединений, охватываемых структурой и которые могут быть пригодными для применения в рамках настоящего изобретения, включают следующие: 3-метил-2H-фуро[2,3-c]пиран-2-он (где R1=CH3, R2, R3, R4=H), 2H-фуро[2,3-c]пиран-2-он (где R1, R2, R3, R4=H), 7-метил-2H-фуро[2,3-c]пиран-2-он (где R1, R2, R4=H, R3=CH3), 5-метил-2H-фуро[2,3-c]пиран-2-он (где R1, R2, R3=H, R4=CH3), 3,7-диметил-2H-фуро[2,3-c]пиран-2-он (где R1, R3=CH3, R2, R4=H), 3,5-диметил-2H-фуро[2,3-c]пиран-2-он (где R1, R4=CH3, R2, R3=H), 3,5,7-триметил-2H-фуро[2,3-c]пиран-2-он (где R1, R3, R4=CH3, R2=H), 5-метоксиметил-3-метил-2H-фуро[2,3-c]пиран-2-он (где R1=CH3, R2, R3=H, R4=CH2OCH3), 4-бром-3,7-диметил-2H-фуро[2,3-c]пиран-2-он (где R1, R3=CH3, R2=Br, R4=H), 3-метилфуро[2,3-c]пиридин-2(3H)-он (где Z=NH, R1=CH3, R2, R3, R4=H), 3,6-диметилфуро[2,3-c]пиридин-2(6H)-он (где Z=N-CH3, R1=CH3, R2, R3, R4=H). См. патент США 7576213. Эти молекулы также известны как каррикины. См., Halford, выше.
Композиции по настоящему изобретению, кроме того, могут включать полезный с сельскохозяйственной/агрономической точки зрения агент. Неограничивающие примеры таких агентов, которые могут быть пригодными для применения на практике этого изобретения, включают гербициды, фунгициды и инсектициды.
Пригодные гербициды включают бентазон, ацифлуорфен, хлоримурон, лактофен, кломазон, флуазифоп, глуфосинат, глифосат, сетоксидим, имазетапир, имазамокс, фомесейф, флумиклорак, имазаквин и клетодим. Коммерческие продукты, содержащие каждое из этих соединений, являются доступными. Концентрация гербицида в композиции, как правило, может соответствовать указанному уровню применения для конкретного гербицида.
"Фунгицид", как используют в рамках изобретения и в данной области, представляет собой средство, которое уничтожает или ингибирует рост грибов. Как используют в рамках изобретения, фунгицид "проявляет активность против" конкретного вида грибов, если обработка фунгицидом приводит к уничтожению или ингибированию роста популяции грибов (например, в почве) относительно необработанной популяции. Эффективные фунгициды в соответствии с изобретением надлежащим образом проявляют активность против широкого диапазона патогенов, включая, но не ограничиваясь ими Phytophthora, Rhizoctonia, Fusarium, Pythium, Phomopsis или Selerotinia и Phakopsora и их комбинации.
Коммерческие фунгициды могут быть пригодными для применения в рамках настоящего изобретения. Пригодные коммерчески доступные фунгициды включают PROTÉGÉ, RIVAL или ALLEGIANCE FL или LS (Gustafson, Plano, TX), WARDEN RTA (Agrilance, St. Paul, MN), APRON XL, APRON MAXX RTA или RFC, MAXIM 4FS или XL (Syngenta, Wilmington, DE), CAPTAN (Arvesta, Guelph, Ontario) и PROTREAT (Nitragin Argentina, Buenos Ares, Argentina). Активные ингредиенты в этих и других коммерческих фунгицидах включают, но не ограничиваются ими, флудиоксонил, мефеноксам, азоксистробин и металаксил. Коммерческие фунгициды наиболее пригодным образом используют в соответствии с инструкциями изготовителя в рекомендованных концентрациях.
Как используют в рамках изобретения, инсектицид "проявляет активность против" конкретного вида насекомых, если обработка инсектицидом приводит к уничтожению или ингибированию популяции насекомых относительно необработанной популяции. Эффективные инсектициды в соответствии с изобретением надлежащим образом проявляют активность против широкого диапазона насекомых, включая, но не ограничиваясь ими, проволочников, совок, личинок, кукурузного корневого жука, личинок мухи ростковой, земляных блошек, земляных клопов, афид, листоедов и щитников.
Для применения в рамках настоящего изобретения могут быть пригодными коммерческие инсектициды. Пригодные коммерчески доступные инсектициды включают CRUISER (Syngenta, Wilmington, DE), GAUCHO и PONCHO (Gustafson, Plano, TX). Активные ингредиенты в этих и других коммерческих инсектицидах включают тиаметоксам, клотианидин и имидаклоприд. Коммерческие инсектициды наиболее пригодным образом используют в соответствии с инструкциями производителя в рекомендованных концентрациях.
Композиции по настоящему изобретению также включают применение одного или нескольких растворяющих фосфаты агентов. Как используют в рамках изобретения, растворяющие фосфаты агенты включают, но не ограничиваются ими, растворяющие фосфаты микроорганизмы. Как используют в рамках изобретения, “растворяющий фосфат микроорганизм” представляет собой микроорганизм, который способен увеличивать количество фосфора, доступного для растения. Растворяющие фосфаты микроорганизмы включают штаммы грибов и бактерий. В одном варианте осуществления растворяющий фосфаты микроорганизм представляет собой спорогенный микроорганизм.
Неограничивающие примеры растворяющих фосфаты микроорганизмов включают виды рода, выбранного из группы, состоящей из Acinetobacter, Arthrobacter, Arthrobotrys, Aspergillus, Azospirillum, Bacillus, Burkholderia, Candida Chryseomonas, Enterobacter, Eupenicillium, Exiguobacterium, Klebsiella, Kluyvera, Microbacterium, Mucor, Paecilomyces, Paenibacillus, Penicillium, Pseudomonas, Serratia, Stenotrophomonas, Streptomyces, Streptosporangium, Swaminathania, Thiobacillus, Torulospora, Vibrio, Xanthobacter и Xanthomonas.
Неограничивающие примеры растворяющих фосфаты микроорганизмов выбраны из группы, состоящей из Acinetobacter calcoaceticus, Acinetobacter spp., Arthrobacter spp., Arthrobotrys oligospora, Aspergillus niger, Aspergillus spp., Azospirillum halopraeferans, Bacillus amyloliquefaciens, Bacillus atrophaeus, Bacillus circulans, Bacillus licheniformis, Bacillus subtilis, Burkholderia cepacia, Burkholderia vietnamiensis, Candida krissii, Chryseomonas luteola, Enterobacter aerogenes, Enterobacter asburiae, Enterobacter spp., Enterobacter taylorae, Eupenicillium parvum, Exiguobacterium spp., Klebsiella spp., Kluyvera cryocrescens, Microbacterium spp., Mucor ramosissimus, Paecilomyces hepialid, Paecilomyces marquandii, Paenibacillus macerans, Paenibacillus mucilaginosus, Pantoea aglomerans, Penicillium expansum, Pseudomonas corrugate, Pseudomonas fluorescens, Pseudomonas lutea, Pseudomonas poae, Pseudomonas putida, Pseudomonas stutzeri, Pseudomonas trivialis, Serratia marcescens, Stenotrophomonas maltophilia, Streptomyces sp., Streptosporangium spp., Swaminathania salitolerans, Thiobacillus ferrooxidans, Torulospora globosa, Vibrio proteolyticus, Xanthobacter agilis и Xanthomonas campestris.
В одном варианте осуществления растворяющий фосфаты микроорганизм представляет собой штамм гриба Penicillium. Штаммы гриба Penicillium, которые могут быть пригодными для применения на практике настоящего изобретения, включают P. bilaiae (ранее известный как P. bilaii), P. albidum, P. aurantiogriseum, P. chrysogenum, P. citreonigrum, P. citrinum, P. digitatum, P. frequentas, P. fuscum, P. gaestrivorus, P. glabrum, P. griseofulvum, P. implicatum, P. janthinellum, P. lilacinum, P. minioluteum, P. montanense, P. nigricans, P. oxalicum, P. pinetorum, P. pinophilum, P. purpurogenum, P. radicans, P. radicum, P. raistrickii, P. rugulosum, P. simplicissimum, P. solitum, P. variabile, P. velutinum, P. viridicatum, P. glaucum, P. fussiporus и P. expansum.
В другом варианте осуществления растворяющий фосфаты микроорганизм вида Penicillium представляет собой P. bilaiae, P. gaestrivorus и/или их комбинацию. В другом варианте осуществления штаммы P. bilaiae выбраны из группы, состоящей из ATCC 20851, NRRL 50169, ATCC 22348, ATCC 18309, NRRL 50162 (Wakelin, et al., 2004. Biol Fertil Soils 40:36-43) и штамм P. gaestrivorus представляет собой NRRL 50170 (см., Wakelin, выше.).
В соответствии с композициями по изобретению, предусматривается, что можно использовать более одного растворяющего фосфаты микроорганизма, как например, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять, по меньшей мере 6, включая любую комбинацию Acinetobacter, Arthrobacter, Arthrobotrys, Aspergillus, Azospirillum, Bacillus, Burkholderia, Candida Chryseomonas, Enterobacter, Eupenicillium, Exiguobacterium, Klebsiella, Kluyvera, Microbacterium, Mucor, Paecilomyces, Paenibacillus, Penicillium, Pseudomonas, Serratia, Stenotrophomonas, Streptomyces, Streptosporangium, Swaminathania, Thiobacillus, Torulospora, Vibrio, Xanthobacter и Xanthomonas, включая один вид, выбранный из следующей группы: Acinetobacter calcoaceticus, Acinetobacter spp., Arthrobacter spp., Arthrobotrys oligospora, Aspergillus niger, Aspergillus spp., Azospirillum halopraeferans, Bacillus amyloliquefaciens, Bacillus atrophaeus, Bacillus circulans,Bacillus licheniformis, Bacillus subtilis, Burkholderia cepacia, Burkholderia vietnamiensis, Candida krissii, Chryseomonas luteola, Enterobacter aerogenes, Enterobacter asburiae, Enterobacter spp., Enterobacter taylorae, Eupenicillium parvum, Exiguobacterium spp., Klebsiella spp., Kluyvera cryocrescens, Microbacterium spp., Mucor ramosissimus, Paecilomyces hepialid, Paecilomyces marquandii, Paenibacillus macerans, Paenibacillus mucilaginosus, Pantoea aglomerans, Penicillium expansum, Pseudomonas corrugate, Pseudomonas fluorescens, Pseudomonas lutea, Pseudomonas poae, Pseudomonas putida, Pseudomonas stutzeri, Pseudomonas trivialis, Serratia marcescens, Stenotrophomonas maltophilia, Streptomyces spp., Streptosporangium spp., Swaminathania salitolerans, Thiobacillus ferrooxidans, Torulospora globosa, Vibrio proteolyticus, Xanthobacter agilis и Xanthomonas campestris.
В другом варианте осуществления настоящее изобретение относится к способу усиления роста растения, включающему применение к растению, семенам растения или почве, окружающей растение или семена растения, одного или нескольких штамма(ов) бактерий по настоящему изобретению (включая композицию, содержащую по меньшей мере один выделенный штамм(ы) по настоящему изобретению и агрономически приемлемый носитель). Один или несколько штаммов бактерий могут включать только один штамм бактерий или комбинацию по меньшей мере двух или более штаммов по настоящему изобретению, включая более двух, как например, по меньшей мере три из описанных выше штаммов, по меньшей мере четыре из описанных выше штаммов, по меньшей мере пять из описанных выше штаммов, по меньшей мере шесть из описанных выше штаммов, по меньшей мере семь из описанных выше штаммов, по меньшей мере восемь из описанных выше штаммов, по меньшей мере девять из описанных выше штаммов, по меньшей мере десять из описанных выше штаммов, по меньшей мере одиннадцать из описанных выше штаммов, по меньшей мере двенадцать из описанных выше штаммов, по меньшей мере тринадцать из описанных выше штаммов, в том числе вплоть до всех из описанных выше штаммов.
Применение
Способы по изобретению включают стадию обработки для применения по меньшей мере одного из выделенных штаммов и/или композиций, содержащих по меньшей мере один из выделенных штаммов, к семенам, проросткам, корням, растениям, почвам или их комбинациям. “Проведение обработки” или “обработка” в качестве терминов, используемых в рамках настоящего изобретения и в данной области, относятся к любому применению, которое приводит к контакту семян, проростков, корней или растений с эффективным количеством композиции или компонентов для обработки для повышения конкурентоспособности для колонизации растения и эффективности стимуляции роста растения.
Эффективное количество и/или пригодные уровни нанесения варьируют, в зависимости от типа почвы, типа растений, количеств источников питательных микроэлементов, присутствующих в почве или добавленных в нее и т.д., и пригодный уровень может быть выявлен без труда с помощью простых экспериментов методом проб и ошибок для каждого конкретного случая. Обычно уровень применения по меньшей мере одного из выделенных штаммов и/или композиций, содержащих по меньшей мере один из выделенных штаммов, попадает в диапазон 1×102-1×108 колониеобразующих единиц (к.о.е.) на семя (когда используют покрытые семена). В конкретном варианте осуществления уровень применения находится в диапазоне 1×104-1×105 колониеобразующих единиц (к.о.е.) на семя (когда используют покрытые семена). В случае гранулярного носителя, уровень применения находится в диапазоне 1×108-1×1013 к.о.е. на гектар. В конкретном варианте осуществления уровень применения для гранулярного носителя находится в диапазоне 2×1011-6×1011 к.о.е. на гектар. Даже несмотря на то, что композиции инокулята и/или композиции, используемые в соответствии с настоящим изобретением, могут включать смесь/комбинацию по меньшей мере двух или более различных штаммов бактерий, на протяжении настоящей заявки указывается общее количество колониеобразующих единиц в комбинированной смеси. Эффективное количество LCO и/или CO, используемое в композиции по изобретению для обработки семян прямо, выражают в единицах концентрации и, как правило, оно находится в диапазоне от приблизительно 10-5 до приблизительно 10-14 M (молярная концентрация), и в некоторых вариантах осуществления от приблизительно 10-5 до приблизительно 10-11 M, и в некоторых других вариантах осуществления от приблизительно 10-7 до приблизительно 10-8 M. Выражаемое в единицах массы, эффективное количество, как правило, находится в диапазоне от приблизительно 1 до приблизительно 400 мкг/американский центнер (cwt) (45,4 кг) семян, и в некоторых вариантах осуществления от приблизительно 2 до приблизительно 70 мкг/cwt, и в некоторых других вариантах осуществления, от приблизительно 2,5 до приблизительно 3,0 мкг/cwt семян.
Для непрямой обработки семян, т.е. обработки в борозде, эффективное количество LCO или CO, главным образом, находится в диапазоне от 1 мкг/акр до приблизительно 70 мкг/акр, и в некоторых вариантах осуществления от приблизительно 50 мкг/акр до приблизительно 60 мкг/акр. Для применения к растениям, эффективное количество LCO или CO, как правило, находится в диапазоне от 1 мкг/акр до приблизительно 30 мкг/акр, и в некоторых вариантах осуществления от приблизительно от 11 мкг/акр до приблизительно 20 мкг/акр.
Обработку проводили прямо, т.е. путем применения прямо к семенам, проросткам, корням или растениям (включая листья), или ее можно проводить непрямо, т.е. путем применения к почве (в том числе в борозде).
Как будет понятно, обработку каждым компонентом можно проводить последовательно или одновременно. Например, если используют жидкий носитель, компоненты можно совместно суспендировать в емкости для смешения коммерческого протравливателя семян, а затем применять к семенам любым подходящим способом нанесения покрытия, например, способом пленочного покрытия. В процессе нанесения пленочного покрытия взвесь распыляют на семена в непрерывном процессе нанесения покрытия. Альтернативно, например, если используют носитель в виде пыли или порошка, компоненты можно применять последовательно. Таким образом, обработка также может охватывать применение к листве и/или применение композиции в борозде.
Неограничивающие примеры растений, подлежащих обработке выделенными штаммами и/или композициями, содержащими по меньшей мере один из выделенных штаммов, включают бобовые культуры. Неограничивающие примеры бобовых культур включают, но не ограничиваются ими, такие растения, как соя, люцерна, арахис, горох, чечевица, бобы и клевер. Как будет понятно, термин "сельскохозяйственная культура" охватывает любое растение, которое может быть собрано в качестве урожая.
Культура
Настоящее изобретение относится к биологически чистой культуре штамма(ов) Bradyrhizobia japonicum:
штамм, имеющий номер доступа депозита NRRL B-50592 (также депонированный как NRRL B-59571);
штамм, имеющий номер доступа депозита NRRL B-50593 (также депонированный как NRRL B-59572);
штамм, имеющий номер доступа депозита NRRL B-50586 (также депонированный как NRRL B-59565);
штамм, имеющий номер доступа депозита NRRL B-50588 (также депонированный как NRRL B-59567);
штамм, имеющий номер доступа депозита NRRL B-50587 (также депонированный как NRRL B-59566);
штамм, имеющий номер доступа депозита NRRL B-50589 (также депонированный как NRRL B-59568);
штамм, имеющий номер доступа депозита NRRL B-50591 (также депонированный как NRRL B-59570);
штамм, имеющий номер доступа депозита NRRL B-50590 (также депонированный как NRRL B-59569);
штамм, имеющий номер доступа депозита NRRL B-50594 (также депонированный как NRRL B-50493);
штамм, имеющий номер доступа депозита NRRL B-50726;
штамм, имеющий номер доступа депозита NRRL B-50727;
штамм, имеющий номер доступа депозита NRRL B-50728;
штамм, имеющий номер доступа депозита NRRL B-50729; и
штамм, имеющий номер доступа депозита NRRL B-50730.
Как используют в рамках изобретения, выражение "биологически частая культура" означает культуру, по существу свободную от биологического загрязнения и имеющую генетическое единообразие, так что различные подкультуры, полученные из них, проявляют по существу идентичные генотипы и фенотипы (например, культуры имеют чистоту по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99%, вплоть до 100%). Такие культуры могут быть полезными в крупномасштабной ферментации или для других коммерческих целей. Таким образом, в объем изобретения входят мутанты, трансконъюганты, рекомбинанты и полученные способами генетической инженерии варианты, которые происходят из штаммов Bradyrhizobium japonicum, имеющих номера доступа депозитов NRRL B-50592 (также депонированный как NRRL B-59571), NRRL B-50593 (также депонированный как NRRL B-59572), NRRL B-50586 (также депонированный как NRRL B-59565), NRRL B-50588 (также депонированный как NRRL B-59567), NRRL B-50587 (также депонированный как NRRL B-59566), NRRL B-50589 (также депонированный как NRRL B-59568), NRRL B-50591 (также депонированный как NRRL B-59570); NRRL B-50590 (также депонированный как NRRL B-59569); NRRL B-50594 (также депонированный как NRRL B-50493); NRRL B-50726; NRRL B-50727; NRRL B-50728; NRRL B-50729; NRRL B-50730 и их культуры.
В одном варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50592 (также депонированный как NRRL B-59571). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50593 (также депонированный как NRRL B-59572). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50586 (также депонированный как NRRL B-59565). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50588 (также депонированный как NRRL B-59567). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50587 (также депонированный как NRRL B-59566). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50589 (также депонированный как NRRL B-59568). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50591 (также депонированный как NRRL B-59570). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50590 (также депонированный как NRRL B-59569). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50594 (также депонированный как NRRL B-50493). В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50726. В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50727. В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50728. В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50729. В другом варианте осуществления культура представляет собой штамм, имеющий номер доступа депозита NRRL B-50730.
Депозит биологического материала
Следующий биологический материал депонирован согласно условиям Будапештского договора в American Type Culture Collection (ATCC), 10801 University Blvd., Manassas, VA 20108, USA, и Microbial Genomics and Bioprocessing Research Unit (NRRL) National Center for Agricultural Utilization Research 1815 N. University Street, Peoria, IL 61604, USA, и получал следующий номер доступа:
Депозит биологического материала
NRRL B-59571
8 марта 2011 года
NRRL B-59572
8 марта 2011 года
NRRL B-59565
8 марта 2011 года
NRRL B-59567
8 марта 2011 года
NRRL B-59566
8 марта 2011 года
NRRL B-59568
8 марта 2011 года
NRRL B-59570
8 марта 2011 года
NRRL B-59569
8 марта 2011 года
NRRL B-50493
8 марта 2011 года
Штамм депонирован согласно условиям, которые гарантируют, что доступ к культуре будет доступен в ходе рассмотрения настоящей заявки лицу, установленному комиссаром по патентам и торговым знакам, уполномоченным согласно 37 C.F.R. §1.14 и 35 U.S.C. §122. Депозит представляет собой чистую культуру депонированного штамма. Депозит доступен в соответствии с требованиями иностранных патентных законов в странах, где подан эквивалент рассматриваемой заявки или происходящие из нее заявки. Однако следует понимать, что доступность депозита не определяет разрешение для применения на практике настоящего изобретения для нарушения патентных прав, предоставленных действиями со стороны правительства.
Представленные ниже примеры включены только для иллюстративных целей и не предназначены для ограничения объема изобретения.
ПРИМЕРЫ
Материалы и способы
Среда
Агар YEM (YEMA): (10 г/л D-маннита; 0,50 г/л дрожжевого экстракта Oxoid; 0,10 г/л NaCl; 0,50 г/л K2HPO4; 0,20 г/л MgSO4·7H2O; 12,0 г/л агара; pH≈6,8).
Жидкая YEM: (10 г/л D-маннита; 0,50 г/л дрожжевого экстракта Oxoid; 0,10 г/л NaCl; 0,50 г/л K2HPO4; 0,20 г/л MgSO4·7H2O; pH≈6,8).
Протокол выделения ДНК
Для штаммов, выращенных на чашках, петлю с 1 мкл каждого штамма из чашек добавляли по отдельности в 100 мкл раствора для выделения ДНК PrepMan® Ultra DNA Isolation solution от Applied Biosystems. Раствор нагревали до 100°C в течение 10 минут. Выделенную ДНК использовали для анализа способом ПЦР.
Для ДНК, выделенной из клубеньков, клубеньки извлекали с помощью пинцета из корней сои и промывали diH2O. Клубеньки помещали по отдельности в 100 мкл раствора для выделения ДНК PrepMan® Ultra DNA Isolation solution от Applied Biosystems, разделяли и нагревали при 100°C в течение 10 минут с использованием 96-луночного планшета для ПЦР, также от Applied Biosystems. Чтобы избежать перекрестной контаминации для раскрытия клубеньков использовали одноразовые зубочистки. Выделенную ДНК использовали для анализа способом ПЦР.
Протокол ПЦР
Полимеразную цепную реакцию (ПЦР) проводили с использованием 96-луночного термоблока Applied Biosystems Veriti® 96-well Fast Thermal Cycler. ПЦР адаптировали для каждого штамма. 2 мкл ДНК добавляли к 0,5 мкл 3’-праймера, 0,5 мкл 5’-праймера, 0,5 мкл Taq-полимеразы (New England Biolabs, Inc.) и 21,5 мкл Platinum Blue PCR Supermix® (Invitrogen). Смесь для ПЦР нагревали до 94°C в течение 4 минут. После денатурации ПЦР проводили в течение 35 циклов по следующей программе: 94°C в течение 1 минуты, 68°C или зависимая от отжига праймеров температура(ы) в течение 1 минуты, и удлинение в реакционной смеси при 72°C в течение 1 минут. После завершения программы ПЦР 5 мкл смеси для ПЦР разделяли с помощью системы Lonza® FlashGel®.
Протокол выделения штаммов
Для выделения штаммов клубеньки подвергали поверхностной стерилизации с помощью 10% хозяйственного отбеливателя в течение 2 минут. Клубеньки промывали в стерильной воде, а затем помещали в микроцентрифужную пробирку с 250 мкл стерильной воды. Клубеньки измельчали стерильными зубочистками и штаммы Rhizobium высвобождали в воду. Две петли с 10 мкл воды наносили штрихами для единичных колоний на чашки YEMA. Все чашки заворачивали в Parafilm® и выращивали при 30°C в инкубаторе Eppendorf Innova® 42R. Время выращивания на изолят отличалось.
Протокол первичного скрининга
Штаммы подвергали первичному скринингу с помощью двух различных протоколов, т.е. “Протокол для сои в полевой почве (USDA 532C обработанное поле)” и “Протокол необработанного (контрольного) поля”. Каждый протокол описан.
Протокол для сои в полевой почве (USDA 532C, обработанное поле)
Семена сои, покрытые USDA 532C, высевали в различные почвы в регионах выращивания сои в США, например, в Южной Дакоте, Северной Дакоте, Джорджии, Айове, Небраске, Иллинойсе, Индиане, Техасе, Канзасе, Миннесоте и т.д. Семена сои, обработанные штаммом Bradyrhizobium japonicum USDA 532C, выращивали в этой почве, собирали их урожай, и клубеньки сои анализировали непосредственно с использованием анализа способом ПЦР. Из каждого образца почвы собирали сорок (40) клубеньков. Индивидуальные клубеньки сои наносили в единичную лунку 96-луночного микропланшета для титрования. ДНК из этих индивидуальных клубеньков сои выделяли непосредственно из клубеньков на основе методики, описанной выше, (см. Материалы и способы: Протокол выделения ДНК).
Анализ способом ПЦР с использованием специфического праймера 209 для USDA 532C проводили непосредственно в 96-луночном планшете (см. Материалы и способы: Протокол ПЦР). Амплификацию праймера 209 (полоса размером 0,9 т.п.н.) из 40 клубеньков вычисляли для определения процентной амплификации. Если амплификация ДНК размером 0,9 т.п.н. была меньшей или равной 30% (т.е. больше или равно 70% образцов ПЦР были негативными по амплификации праймера 209), тогда образец почвы содержал штаммы Bradyrhizobium japonicum с большей конкурентоспособностью, чем у штамма USDA 532C. Клубеньки сои с амплификацией, меньшей или равной 30%, содержали нативные штаммы, идентифицированные в качестве более конкурентоспособных, чем USDA 532C, исходя из описанной методики (см. Материалы и способы: Протокол выделения штаммов).
Если более 30% клубеньков сои были колонизированы Bradyrhizobia japonicum штамма USDA 532C, тогда почва считалась непригодной для выделения нового штамма и образец почвы отбраковывали.
Протокол необработанного (контрольного) поля
Клубеньки получали с полей с соей, не обработанных USDA 532C, в следующих штатах: Арканзас, Джорджия, Иллинойс, Индиана, Айова, Оклахома, Небраска, Каназас, Миссури и Техас. Штамм Bradyrhizobium japonicum выделяли непосредственно из этих клубеньков в соответствии с протоколом, описанным выше (см. материалы и способы: Протокол выделения штаммов). Выделенные штаммы помещали в условия прямой конкуренции со штаммом Bradyrhizobia japonicum USDA 532C в соответствии с “Протоколом испытания конкуренции” (см. Материалы и способы: Протокол испытания конкуренции). Выделенные штаммы, которые занимали более 70% клубеньков сои по сравнению со штаммом Bradyrhizobia japonicum USDA 532C, выбирали для оценки эффективности (см. Материалы и способы: Протокол испытания эффективности).
Протокол испытания конкуренции
Определяли оптическую плотность. (Спектрофотометр Nanodrop® ND1000) Получали соотношение в инокуляте 1:1 USDA 532C и штамма каждого изолята. USDA 532C разбавляли или концентрировали до оптической плотности 0,5 при 600 нм, и 0,5 мл инокулята USDA 532C отделяли для каждого изолята. Штаммы всех изолятов либо концентрировали, либо разбавляли до оптической плотности 0,5 при 600 нм с использованием следующего подсчета: (оптическая плотность 0,5 для USDA 532C)×(0,5 мл USDA 532C)=(оптическая плотность штамма изолята)×(мл штамма изолята). 0,5 мл USDA 532C добавляли к 0,5 мл каждого изолята в качестве отдельной обработки. Семена сои покрывали смесью инокулята в количестве 0,5 мл смеси инокулята на 12 семян сои. Семенам позволяли пропитываться в течение 30 минут. 5 из 12 обработанных семян сои высевали в смеси Fafard® 3B Potting mix вы горшке объемом 1 галлон (3785 см3). Для посева семян надевали перчатки и их меняли между обработками. После посева 7 оставшихся семян сои отбрасывали.
При проращивании горшки прореживали до 3 растений. Растения выращивали в течение 6-7 недель в теплице и избегали перекрестного загрязнения в процессе орошения. Температура находилась в диапазоне приблизительно 23°C-32°C. Орошение проводили по принципу “по необходимости”. Собирали клубеньки после каждой обработки и использовали их для выделения ДНК и анализа ПЦР со специфичным для USDA 532C праймером 209. См. Материалы и способы: Протокол выделения ДНК и Протокол ПЦР.
Протокол испытания эффективности
Испытание эффективности является прямым сравнением эффективности от штамма к штамму между отдельным выделенным штаммом и коммерчески доступным штаммом Bradyrhizobium japonicum USDA 532C. Выделенный штамм и контрольный штамм (штамм Bradyrhizobium japonicum USDA 532C) наносили штрихами одновременно на отдельные чашки YEMA. Выделенный штамм и контрольный штамм по отдельности инокулировали в 5 мл жидкой среды YEM до получения первоначальной оптической плотности 0,03 при 600 нм в пробирке с каждым инокулятом (спектрофотометр Nanodrop® ND1000). Выделенный штамм и контрольный штамм инкубировали по отдельности при 30°C в течение 3 суток. После инкубации инокулят выделенного штамма и контрольного штамма далее разбавляли или концентрировали до конечной оптической плотности 0,5 при 600 нм в каждой пробирке с инокулятом (спектрофотометр Nanodrop® ND1000) с получением раствора для исследуемой обработки (выделенный штамм) и контрольной обработки (контрольный штамм Bradyrhizobium japonicum USDA 532C).
0,75 мл раствора для исследуемой обработки добавляли к 32 семенам сои. Обработанным семенам позволяли пропитаться в течение 30 минут. Через 30 минут по 2 семя высевали в 15 отдельных горшков (4”×4”×6”) в смеси для посева в горшок Fafard® 3B Potting mix. Для посева семян одевали перчатки и их меняли между обработками. После посева 2 оставшихся обработанных семени сои отбрасывали. Этот процесс повторяли для контрольной обработки.
При прорастании горшки для исследуемой обработки и контрольной обработки прореживали до одного растения. Растения выращивали в течение 8-10 недель в теплице и избегали перекрестного загрязнения в процессе орошения. Температура находилась в диапазоне приблизительно 23°C-32°C. Орошение проводили по принципу “по необходимости”. Через 8-10 недель проводили сбор с горшков и сушили в течение ночи при 80°C. Анализ с помощью статистического программного обеспечения JMP® (SAS Institute, Inc.) использовали для определения статистически значимого повышения эффективности по сравнению со штаммом Bradyrhizobium japonicum USDA 532C.
Протокол температурного профиля
Выделенные штаммы Bradyrhizobium japonicum наносили штрихами на планшеты YEMA (10 г/л D-маннита; 0,50 г/л дрожжевого экстракта Oxoid; 0,10 г/л NaCl; 0,50 г/л K2HPO4; 0,20 г/л MgSO4·7H2O; 12,0 г/л агара; pH≈6,8) и инкубировали при 30°C и 35°C, соответственно, в течение 7 суток. Выделенные штаммы анализировали в отношении их способности расти до выделенных колоний.
Протокол профиля устойчивости к глифосату
Выделенные штаммы Bradyrhizobium japonicum наносили штрихами на чашки YEMA (10 г/л D-маннит; 0,50 г/л дрожжевой экстракт Oxoid; 0,10 г/л NaCl; 0,50 г/л K2HPO4; 0,20 г/л MgSO4·7H2O; 12,0 г/л агара; pH≈6,8) с 1 мМ глифосатом и 2 мМ глифосатом. Чашки инкубировали при 30°C в течение 7 суток и штаммы анализировали в отношении их способности расти до выделенных колоний.
Протокол профиля устойчивости к антибиотикам
Выделенные штаммы Bradyrhizobium japonicum наносили T-штрихами на YEMA с гентамицином (50 мг/л), YEMA с хлорамфениколом (50 мг/л), YEMA с полимиксином B (100 мг/л), YEMA с карбенициллином (100 мг/л), YEMA с неомицином (50 мг/л) и YEMA с налидиксовой кислотой (50 мг/л). Чашки инкубировали при 30°C в течение 7 суток и штаммы анализировали в отношении их способности расти до выделенных колоний.
Протокол ПЦР Diversilab®
ПЦР Diversilab® ПЦР проводили с использованием набора Diversilab Pseudomonas Kit® от BioMerieux. Этот набор содержал запатентованные праймеры, предназначенные для амплификации различных частей генома для получения отпечатка множества амплификаций ДНК. Каждый штамм имеет уникальный отпечаток и процентное сходство между штаммами можно определять с использованием программного обеспечения Diverilab.
ПЦР проводили следующим образом. 2 мкл ДНК добавляли к 18,0 мкл Re-PCR MM1, 2,0 мкл смеси праймеров, 0,5 мкл Taq-полимеразы (New England Biolabs, Inc.) и 2,5 мкл буфера для Taq-полимеразы (New England Biolabs, Inc.) в общем объеме 25 мкл. ПЦР нагревали до 94°C в течение 2 минут, а затем проводили 35 циклов следующим образом: 94°C в течение 0,5 минут, затем 50°C в течение 0,5 минут, и наконец 70°C в течение 1,5 минуты. После завершения 35 циклов всю реакцию поддерживали при 70°C в течение 3 минут. После завершения анализа способом ПЦР, продукт ПЦР анализировали с помощью Agilent® 2100 Series Bioanalyzer. Набор Diversilab® DNA Reagents & Supplies Kit от BioMerieux использовали для нанесения продукта ПЦР на чипы Diversilab® System. Набор хранили в соответствии с инструкциями. Перед применением набор выдерживали при комнатной температуре в течение 30 минут перед нанесением на чип Diversilab®. Нанасение на чип Diversilab® проводили в соответствии со всеми предоставленными протоколами и инструкциями. После завершения нанесения на чип Diversilab®, чип помещали в Agilent® 2100 Series Bioanalyzer и проводили анализ до завершения.
Пример 1
Уникальная конструкция праймера для коммерческого штамма Bradyrhizobium USDA 532C
Был разработан способ генетической идентификации для оценки конкурентоспособности коммерческого штамма Bradyrhizobium japonicum USDA 532C против нативных штаммов в полевых условиях. Был идентифицирован праймер, специфичный к USDA 532C, и технологию ПЦР использовали, чтобы эффективно оценить конкурентоспособность USDA 532C в полевых условиях.
Полное секвенирование генома USDA 532C проводили в Novozymes Davis. Было выявлено, что двадцать пять различных фрагментов ДНК имеют низкую гомологию с общедоступными последовательностями Bradyrhizobium japonicum. ДНК выделяли из штаммов B. japonicum (USDA 532C, P152, Br173, Br187, P190 и P194), выращенных на чашках в соответствии с методикой, описанной выше (см. Материалы и способы: Протокол выделения ДНК). Дополнительный анализ последовательностей проводили для этих двадцати пяти фрагментов ДНК. Были выбраны предполагаемые уникальные праймеры для штамма USDA 532C, и их использовали для скрининга специфических для USDA 532C праймеров способом ПЦР против некоторых репрезентативных штаммов Bradyrhizobium japonicum. После оценки способом ПЦР был идентифицирован один уникальный праймер для USDA 532C, и он был обозначен как p209.
Последовательность праймера 209 была следующей:
SEQ ID NO: 1 - P209p5-TTGGGTTGAGCATGCCCACCCGGACGG,
SEQ ID NO: 2 - P209p3-gtctcagttgccgagcccacggcgc
Специфичность праймеров
Двадцать пять праймеров исследовали по отдельности для положительной идентификации USDA 532C. Праймеры далее исследовали в отношении специфичности к USDA 532C способом ПЦР с использованием USDA 532C и 5 различных нативных штаммов B. japonicum (P152, Br173, Br187, P190 и P194) для сравнения. Секвенирование генома показало, что Br187 и USDA 532C были генетически одинаковыми.
Обобщение скрининга праймеров
В таблице 2 обобщены данные (“+” указывает на положительную идентификацию полосы амплификации ПЦР в геле, “-” указывает на отсутствие амплификации ДНК).
Ссылаясь на ФИГ.1A, было продемонстрировано, что выделенный праймер 209 является специфичным к USDA 532C и Br187. Дальнейшее генетическое исследование показало, что USDA 532C и штамм Bradyrhizobium japonicum P187 являются идентичными (результаты не представлены). Содержимое лунок (слева направо) указывает на следующие нативные штаммы USDA 532C, P152, Br173, Br187, Br190, Br194 и контрольный маркер. См. фиг.1A.
Специфичность праймера 209 исследовали против нативных штаммов P152, Br173, Br187, Br190, Br194 и USDA 532C. См. фиг.1B. ПЦР с праймером 209 проводили для 100 штаммов, полученных из необработанных участков в поле в соответствии с описанным выше способом (см. Материалы и способы: Протокол необработанного (контрольного) поля). Штамм Bradyrhizobium japonicum USDA 532C не добавляли в эти участки. Из исследованных штаммов только 3% нативных штаммов могли амплифицироваться с получением полосы размером 0,9 т.п.н., специфической для праймера 209. Этот результат продемонстрировал, что праймер 209 можно использовать для специфической детекции USDA 532C.
Пример 2
Анализ и выделение новых штаммов
Праймер 209 использовали в качестве маркера для указания на присутствие или отсутствие колонизации штаммом Bradyrhizobia japonicum USDA 532C в корневых клубеньках растений сои. Полосы (т.е. полоса размером 0,9 т.п.н.), указывающие на присутствие праймера 209, отражают положительную идентификацию Bradyrhizobia japonicum штамма USDA 532C. См. фиг.2A. На фиг.2A представлен пример случая, где штамм Bradyrhizobia japonicum USDA 532C является доминантным конкурирующим штаммом для колонизации клубеньков растений сои по сравнению с другими нативными штаммами Rhizobial. На фиг.2B количество полос, указывающих на положительную идентификацию праймера 209, и, таким образом, присутствие штамма Bradyrhizobia japonicum USDA 532C, снижено по сравнению с общим количеством полос, присутствующих для праймера 209 на фиг.2A. На фиг.2A и фиг.2B продемонстрировано, что присутствие или отсутствие праймера 209 можно использовать для определения того, является ли USDA 532C доминирующим конкурирующим штаммом в клубеньках растения сои.
Выделенные штаммы Bradyrhizobium japonicum выбирали из клубеньков в соответствии с обоими протоколами скрининга (см. Материалы и способы: протокол первичного скрининга). Выбранные штаммы выделяли из клубеньков в соответствии с методикой выделения (см. Материалы и способы: Протокол выделения штаммов).
Пример 3
Оценка конкуренции друг против друга
Все выделенные штаммы подвергали программе скрининга, предназначенной для прямого сравнения конкурентоспособности изолята относительно штамма Bradyrhizobium japonicum USDA 532C в отношении способности колонизировать клубеньки (см. Материалы и способы: Протокол испытания конкуренции).
Выделенный праймер 209, специфичный к USDA 532C, использовали в качестве маркера, указывающего на присутствие или отсутствие колонизации штамма Bradyrhizobia japonicum USDA 532C в корневых клубеньках растений сои. Положительная идентификация праймера 209 указывала на колонизацию штаммом Bradyrhizobia japonicum USDA 532C корневых клубеньков растений сои. Напротив, отсутствие полос, указывающих на положительную идентификацию праймера 209, указывало на колонизацию нативным штаммом корневых клубеньков растений сои, отличным от штамма Bradyrhizobia japonicum USDA 532C. Выделенные штаммы, которые проявляли более чем 70% колонизацию проанализированных клубеньков, были выбраны для второй оценки для подтверждения. Штаммы подвергали по меньшей мере двум раундам оценки конкуренции. С помощью этой методики был проведен скрининг более чем 1000 изолятов в отношении усиленной конкурентоспособности.
Пример 4
Оценка эффективности
Исследование эффективности представляет собой прямое сравнение от штамма к штамму выделенных штаммов USDA 532C. Увеличенную эффективность можно измерять в качестве функции сухой массы стручков (г). См. Материалы и способы: Протокол испытания эффективности. Результаты представлены в таблицах 3A-3D.
Увеличенная эффективность в качестве
функции сухой массы стручков (г)
Процентную колонизацию подтверждали в испытаниях в трех экземплярах и увеличенную сухую массу стручков подтверждали в испытаниях в двух экземплярах для всех штаммов.
Увеличенная эффективность в качестве функции
сухой массы стручков (г)
Процентную колонизацию подтверждали в испытаниях в трех экземплярах и увеличенную сухую массу стручков подтверждали в испытаниях в двух экземплярах для всех штаммов.
Увеличенная эффективность в качестве функции
сухой массы стручков (г)
Процентную колонизацию подтверждали в испытаниях в трех экземплярах и увеличенную сухую массу стручков подтверждали в испытаниях в двух экземплярах для всех штаммов.
Увеличенная эффективность в качестве функции сухой массы стручков (г)
Процентную колонизацию и увеличенную сухую массу стручков подтверждали в испытаниях в двух экземплярах для всех штаммов, за исключением NRRL B-50730*, для которого проводили только один раунд испытания.
Коммерчески доступный штамм USDA 532C использовали в качестве контроля для каждой оценки. Результаты в таблицах 3A-3D указывают на то, что все выделенные штаммы, кроме одного, имели увеличенную эффективность по сравнению с контролем USDA 532C.
Пример 5
Испытание по охарактеризации
Выделенные штаммы Bradyrhizobium japonicum далее охарактеризовывали, исходя из профилей температуры, устойчивости к глифосату и устойчивости к антибиотикам (см. Материалы и способы: протоколы температурного профиля, профиля устойчивости к глифосату и профиля устойчивости к антибиотикам). Результаты представлены в таблице 4.
Охарактеризация выделенных штаммов в качестве функции температурного профиля, устойчивости к глифосату и устойчивости к антибиотикам
50493
В таблице 4 обобщенно представлены результаты (“+” указывает на рост выделенных колоний, “-” указывает на отсутствие роста, и “+-” указывает на небольшой рост выделенных колоний/минимальный и спорадический рост). Результаты указывают на то, что штаммы NRRL B-59570, NRRL B-59568, NRRL B-59565, NRRL B-59566 и NRRL B-50493 в основном являются толерантными к температуре 35°C. Кроме того, результаты указывают на то, что выделенные штаммы NRRL B-59569, NRRL B-59568, NRRL B-59565 и NRRL B-50493 являются естественным образом устойчивыми к глифосату. Было выявлено, что штаммы NRRL B-59566 и NRRL B-59569 обладают устойчивостью к налидиксовой кислоте.
Пример 5
Получение отпечатков ДНК
Изоляты с наилучшей эффективностью подвергали анализу отпечатков ДНК Diversilab® (см. Материалы и способы: протокол ПЦР Diversilab®). ДНК выделяли из каждого штамма в соответствии с описанными способами (см. Материалы и способы: Протокол выделения ДНК). Выделенную ДНК использовали для анализа способом ПЦР.
Результаты анализа отпечатков ДНК Diversilab представлены на фиг.3A-3B. Результаты демонстрируют, что выделенные штаммы являются уникальными штаммами и штаммами, отличными от USDA 532C.
Настоящее изобретение описано, по меньшей мере частично, с помощью следующих пронумерованных положений:
1. Биологически чистая культура Bradyrhizobia japonicum, выбранная из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50592;
штамма, имеющего номер доступа депозита NRRL B-50593;
штамма, имеющего номер доступа депозита NRRL B-50586;
штамма, имеющего номер доступа депозита NRRL B-50588;
штамма, имеющего номер доступа депозита NRRL B-50587;
штамма, имеющего номер доступа депозита NRRL B-50589;
штамма, имеющего номер доступа депозита NRRL B-50591;
штамма, имеющего номер доступа депозита NRRL B-50590;
штамма, имеющего номер доступа депозита NRRL B-50594;
штамма, имеющего номер доступа депозита NRRL B-50726;
штамма, имеющего номер доступа депозита NRRL B-50727;
штамма, имеющего номер доступа депозита NRRL B-50728;
штамма, имеющего номер доступа депозита NRRL B-50729; и
штамма, имеющего номер доступа депозита NRRL B-50730.
2. Штаммы Bradyrhizobium согласно положению 1, где указанные штаммы способны обеспечивать фиксацию азота растением.
3. Штаммы Bradyrhizobium согласно любому из положений 1-2, где указанные штаммы являются устойчивыми при температуре выращивания, по существу равной 35°C.
4. Штаммы Bradyrhizobium согласно любому из положений 1-3, где указанные штаммы выбраны из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50591;
штамма, имеющего номер доступа депозита NRRL B-50589;
штамма, имеющего номер доступа депозита NRRL B-50586;
штамма, имеющего номер доступа депозита NRRL 50594; и комбинация по меньшей мере двух или более из штаммов.
5. Штаммы Bradyrhizobium согласно любому из положений 1-4, где указанные штаммы Bradyrhizobium являются естественным образом устойчивыми к глифосату.
6. Штаммы Bradyrhizobium согласно положению 5, где указанные штаммы выбраны из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50590;
штамма, имеющего номер доступа депозита NRRL B-50594; и комбинация по меньшей мере двух или более штаммов.
7. Штаммы Bradyrhizobium согласно любому из положений 1-6, где указанные штаммы имеют увеличенную конкурентоспособность в отношении колонизации растения.
8. Штаммы Bradyrhizobium согласно любому из положений 1-7, где указанные штаммы имеют увеличенную эффективность стимуляции роста растений.
9. Штаммы Bradyrhizobium согласно любому из положений 1-8, где увеличенная конкурентоспособность включает по меньшей мере 51% заполненность клубеньков, например, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, по меньшей мере 99% или 100% заполненность клубеньков.
10. Штаммы Bradyrhizobium согласно любому из абзацев 1-9, где увеличенная эффективность стимуляции роста растений включает по меньшей мере одно из увеличенного выхода, измеряемого в бушелях/акр, увеличенного количества плодов, увеличенного количества корней, увеличенной длины корней, увеличенной массы корней, увеличенного объема корней, увеличенной площади листьев, увеличенной густоты стояния листьев, увеличенной мощности растения и/или увеличенной способности фиксировать азот (N2) по сравнению с коммерчески доступным штаммом, например, USDA 532C.
11. Штаммы Bradyrhizobium согласно любому из положений 1-10, где увеличенная эффективность стимуляции роста сои включает увеличение общей сухой массы стручков сои на указанном растении сои, когда указанную общую сухую массу стручков сои сравнивают с общей сухой массой стручков сои на растении сои, подвергнутом воздействию коммерчески доступного штамма, например, коммерческого штамма USDA 532C.
12. Композиция, содержащая штамм Bradyrhizobia japonicum, выбранный из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50592;
штамма, имеющего номер доступа депозита NRRL B-50593;
штамма, имеющего номер доступа депозита NRRL B-50586;
штамма, имеющего номер доступа депозита NRRL B-50588;
штамма, имеющего номер доступа депозита NRRL B-50587;
штамма, имеющего номер доступа депозита NRRL B-50589;
штамма, имеющего номер доступа депозита NRRL B-50591;
штамма, имеющего номер доступа депозита NRRL B-50590;
штамма, имеющего номер доступа депозита NRRL B-50594;
штамма, имеющего номер доступа депозита NRRL B-50726;
штамма, имеющего номер доступа депозита NRRL B-50727;
штамма, имеющего номер доступа депозита NRRL B-50728;
штамма, имеющего номер доступа депозита NRRL B-50729;
штамма, имеющего номер доступа депозита NRRL B-50730; и комбинация по меньшей мере двух или более штаммов и агрономически приемлемого носителя.
13. Композиция согласно положению 12, где указанная композиция включает одну или несколько сигнальных молекул.
14. Композиция согласно положению 13, где сигнальная молекула растений представляет собой липохитоолигосахарид (LCO).
15. Композиция согласно любому из положений 13-14, где LCO является синтетическим.
16. Композиция согласно любому из положений 13-15, где LCO является рекомбинантным.
17. Композиция согласно любому из положений 13-16, где LCO является встречающимся в природе.
18. Композиция согласно любому из положений 13-17, где LCO получен из вида Rhizobia, выбранного из Rhizobium spp., Bradyrhizobium spp., Sinorhizobium spp. и Azorhizobium spp.
19. Композиция согласно любому из положений 13-18, где LCO получен из Bradyrhizobium japonicum.
20. Композиция согласно любому из положений 13-19, где LCO получают из древовидного микоризного гриба.
21. Композиция согласно положению 13, где сигнальной молекулой растения является хитиновое соединение.
22. Композиция согласно положению 22, где хитиновое соединение представляет собой хитоолигомер (CO).
23. Композиция согласно любому из положений 21-22, где CO является синтетическим.
24. Композиция согласно любому из положений 21-23, где CO является рекомбинантным.
25. Композиция согласно любому из положений 21-24, где CO является встречающимся в природе.
26. Композиция согласно положению 13, где сигнальной молекулой растения является флавоноид.
27. Композиция согласно положению 13, где сигнальной молекулой растения является жасмоновая кислота или ее производное.
28. Композиция согласно положению 13, где сигнальной молекулой растения является линолеиновая кислота или ее производное.
29. Композиция согласно положению 13, где сигнальной молекулой растения является линоленовая кислота или ее производное.
30. Композиция согласно положению 13, где сигнальной молекулой растения является каррикин.
31. Композиция согласно любому из положений 12-30, где композиция включает по меньшей мере две различных сигнальных молекулы растения.
32. Композиция согласно любому из положений 12-31, где композиция включает по меньшей мере одно агрономически полезный агент.
33. Композиция согласно положению 32, где агрономически полезным агентом является гербицид, инсектицид или фунгицид.
34. Композиция согласно положению 33, где агронмически полезным средством является по меньшей мере один растворяющий фосфаты микроорганизм.
35. Композиция согласно положению 34, где по меньшей мере один растворяющий фосфат микроорганизм включает штамм гриба Penicillium.
36. Композиция согласно положению 35, где по меньшей мере один растворяющий фосфат микроорганизм включает штамм P. bilaiae.
37. Композиция согласно положению 36, где штамм P. bilaiae выбран из группы, состоящей из NRRL 50162, NRRL 50169, ATCC 20851, ATCC 22348 и ATCC 18309.
38. Композиция согласно положению 34, где по меньшей мере один растворяющий фосфат микроорганизм включает штамм P. gaestrivorus.
39. Композиция согласно положению 38, где штаммом P. gaestrivorus является NRRL 50170.
40. Способ выделения штамма(ов) бактерий, выбранного из рода, состоящего из Rhizobium и Bradyrhizobium, имеющего увеличенную конкурентоспособность в отношении колонизации бобового растения и увеличенную эффективность стимуляции роста бобового растения, включающий:
a. получение штамма(ов) бактерий из образца почвы;
b. воздействие указанным штаммом(ы) бактерий и коммерчески доступным штаммом(ами), например, коммерческий штамм USDA 532C, на бобовое растение;
c. выбор указанного штамма(ов) бактерий, который является более конкурентоспособным, чем коммерчески доступный штамм, в отношении занятия клубеньков бобового растения;
d. анализ выбранного штамма(ов) бактерий, который является более конкурентоспособным в отношении занятия клубеньков бобового растения, чем коммерчески доступный штамм, на тот штамм(ы) бактерий, который имеет увеличенную эффективность стимуляции роста бобового растений; и
f. выделение указанного штамма(ов) бактерий, имеющего увеличенную эффективность стимуляции роста бобовых растений.
40. Выделенный штамм бактерий согласно положению 40, где указанный штамм бактерий представляет собой штамм Bradyrhizobium spp.
41. Выделенный штамм Bradyrhizobium согласно положению 41, где указанный штамм Bradyrhizobium spp. представляет собой штамм Bradyrhizobium japonicum.
42. Выделенный штамм Bradyrhizobium согласно любому из положений 41-42, где указанный штамм представляет собой штамм Bradyrhizobia japonicum, выбранный из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50592;
штамма, имеющего номер доступа депозита NRRL B-50593;
штамма, имеющего номер доступа депозита NRRL B-50586;
штамма, имеющего номер доступа депозита NRRL B-50588;
штамма, имеющего номер доступа депозита NRRL B-50587;
штамма, имеющего номер доступа депозита NRRL B-50589;
штамма, имеющего номер доступа депозита NRRL B-50591;
штамма, имеющего номер доступа депозита NRRL B-50590;
штамма, имеющего номер доступа депозита NRRL B-50594;
штамма, имеющего номер доступа депозита NRRL B-50726;
штамма, имеющего номер доступа депозита NRRL B-50727;
штамма, имеющего номер доступа депозита NRRL B-50728;
штамма, имеющего номер доступа депозита NRRL B-50729;
штамма, имеющего номер доступа депозита NRRL B-50730; и комбинация по меньшей мере двух или более штаммов.
44. Способ согласно любому из положений 40-43, где выделенный штамм Bradyrhizobia japonicum способен к фиксации азота в растении.
45. Способ согласно любому из положений 40-44, где выделенный штамм Bradyrhizobia japonicum является устойчивым при температуре выращивания, по существу равной 35°C.
46. Способ согласно положению 45, где выделенный штамм Bradyrhizobia japonicum выбран из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50591;
штамма, имеющего номер доступа депозита NRRL B-50589;
штамма, имеющего номер доступа депозита NRRL B-50586;
штамма, имеющего номер доступа депозита NRRL 50594; и комбинация по меньшей мере двух или более штаммов.
47. Способ согласно любому из положений 40-46, где штамм Bradyrhizobia japonicum имеет природную устойчивость к глифосату.
48. Способ согласно положению 47, где выделенный штамм Bradyrhizobia japonicum выбран из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL B-50590;
штамма, имеющего номер доступа депозита NRRL B-50594; и комбинация по меньшей мере двух или более штаммов.
49. Способ улучшения роста растений, включающий обработку семени, проростка, корня, растения, почвы или их комбинации композицией в соответствии с любым из положений 1-39.
50. Способ согласно положению 49, где семя, проросток, корень или растение принадлежат бобовой культуре.
51. Способ согласно положению 50, где семя, проросток, корень или растение представляют собой семя, проросток, корень или растение сои.
52. Способ согласно любому из положений 49-51, где указанную композицию добавляют в почву в количестве от 1×108 до 1×1013 колониеобразующих единиц на гектар, предпочтительно, от 2×1011 до 6×1011 колониеобразующих единиц на гектар.
53. Способ согласно любому из положений 49-52, где указанную композицию применяют в качестве покрытия семян, содержащего от 1×102 до 1×108, предпочтительно от 1×104 до 1×105 колониеобразующих единиц на семя.
Изобретение, описанное и заявленное в настоящем описании, не ограничивается по объему конкретными вариантами осуществления, описанными в настоящем описании, поскольку эти варианты осуществления приведены в качестве иллюстраций нескольких аспектов изобретения. Любые эквивалентные варианты осуществления находятся в объеме настоящего изобретения. Действительно, различные модификации изобретения в дополнение к модификациям, представленным и описанным в настоящем описании, будут понятными специалистам в данной области, исходя из представленного выше описания. Такие модификации также считаются относящимися к объему прилагаемой формулы изобретения. В случае противоречий, настоящее описание, включая определение, будет иметь приоритет.
В настоящем описании цитированы различные ссылки, описание которых включено в качестве ссылок в полном объеме.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ BRADYRHIZOBIUM ДЛЯ УЛУЧШЕНИЯ РОСТА РАСТЕНИЙ (ВАРИАНТЫ), КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ УКАЗАННЫЙ ШТАММ, И СЕМЯ, ПОКРЫТОЕ КОМПОЗИЦИЕЙ | 2012 |
|
RU2588483C2 |
| СПОСОБ ОБРАБОТКИ СЕМЕНИ РАСТЕНИЯ | 2012 |
|
RU2646138C1 |
| КОМПОЗИЦИИ И СПОСОБЫ УСИЛЕНИЯ РОСТА РАСТЕНИЙ | 2014 |
|
RU2659000C2 |
| КОМПОЗИЦИИ И СПОСОБЫ УСИЛЕНИЯ СТАБИЛЬНОСТИ МИКРОБОВ | 2014 |
|
RU2658994C2 |
| СТАБИЛЬНЫЕ КОМПОЗИЦИИ С ИНОКУЛЯНТОМ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2730863C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ОБРАБОТКИ ОТ ВРЕДИТЕЛЕЙ | 2014 |
|
RU2660673C2 |
| МИКРОБНЫЕ ШТАММЫ, КОМПОЗИЦИИ И СПОСОБЫ УВЕЛИЧЕНИЯ ДОСТУПНОГО ФОСФАТА ДЛЯ РАСТЕНИЙ | 2013 |
|
RU2668832C2 |
| СМЕСИ, ВКЛЮЧАЮЩИЕ ШТАММ BACILLUS И ПЕСТИЦИД | 2015 |
|
RU2689686C2 |
| СПОСОБЫ ОБРАБОТКИ СЕМЯН И КОМПОЗИЦИИ | 2012 |
|
RU2640425C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ТРИАЗОЛЬНОЕ СОЕДИНЕНИЕ И БИОПЕСТИЦИД | 2014 |
|
RU2669997C2 |





Предложена композиция инокулята для усиления роста растения, подходящая для покрытия семян. Указанная композиция содержит агрономически приемлемый носитель и по меньшей мере один штамм Bradyrhizobia japonicum. При этом по меньшей мере один штамм Bradyrhizobia japonicum выбран из группы, состоящей из штамма Bradyrhizobia japonicum NRRL В-50592, штамма Bradyrhizobia japonicum NRRL В-5059, штамма Bradyrhizobia japonicum NRRL В-50586, штамма Bradyrhizobia japonicum NRRL В-50588, штамма Bradyrhizobia japonicum NRRL В-50587, штамма Bradyrhizobia japonicum NRRL В-50589, штамма Bradyrhizobia japonicum NRRL В-50591, штамма Bradyrhizobia japonicum NRRL В-50590, штамма Bradyrhizobia japonicum NRRL В-50594, штамма Bradyrhizobia japonicum NRRL В-50726, штамма Bradyrhizobia japonicum NRRL В-50727, штамма Bradyrhizobia japonicum NRRL В-50728, штамма Bradyrhizobia japonicum NRRL В-50729 и/или штамма Bradyrhizobia japonicum NRRL В-50730. Предложено также покрытое семя бобового растения, причем покрытие содержит композицию инокулята. Указанное семя предназначено для получения бобового растения, содержащего композицию инокулята и имеющего усиленный рост. Группа изобретений обеспечивает увеличение эффективности стимуляции роста бобовых растений. 3 н. и 57 з.п. ф-лы, 6 ил., 7 табл., 5 пр.
1. Композиция инокулята для усиления роста растения, подходящая для покрытия семян, где указанная композиция содержит агрономически приемлемый носитель и по меньшей мере одну биологически чистую культуру штамма Bradyrhizobia japonicum, где указанная по меньшей мере одна биологически чистая культура штамма Bradyrhizobia japonicum выбрана из группы, состоящей из:
штамма, имеющего номер доступа депозита NRRL В-50592;
штамма, имеющего номер доступа депозита NRRL В-50593;
штамма, имеющего номер доступа депозита NRRL В-50586;
штамма, имеющего номер доступа депозита NRRL В-50588;
штамма, имеющего номер доступа депозита NRRL В-50587;
штамма, имеющего номер доступа депозита NRRL В-50589;
штамма, имеющего номер доступа депозита NRRL В-50591;
штамма, имеющего номер доступа депозита NRRL В-50590;
штамма, имеющего номер доступа депозита NRRL В-50594;
штамма, имеющего номер доступа депозита NRRL В-50726;
штамма, имеющего номер доступа депозита NRRL В-50727;
штамма, имеющего номер доступа депозита NRRL В-50728;
штамма, имеющего номер доступа депозита NRRL В-50729; и/или
штамма, имеющего номер доступа депозита NRRL В-50730.
2. Композиция инокулята по п.1, где рост по крайней мере одного из указанных штаммов Bradyrhizobia japonicum является устойчивым при температуре, по существу, равной 35°С.
3. Композиция инокулята по любому из пп.1, 2, где рост по крайней мере одного из указанных штаммов Bradyrhizobia japonicum является устойчивым в присутствии 1,0 мМ глифосата.
4. Композиция инокулята по любому из пп.1, 2, где рост по крайней мере одного из указанных штаммов Bradyrhizobia japonicum является устойчивым в присутствии 2,0 мМ глифосата.
5. Композиция инокулята по любому из пп.1, 2, где рост по крайней мере одного из указанных штаммов Bradyrhizobia japonicum является устойчивым в присутствии 50 мг/л налидиксовой кислоты.
6. Композиция инокулята по любому из пп.1, 2, где по крайней мере один из указанных штаммов Bradyrhizobia japonicum имеет увеличенную конкурентоспособность в отношении колонизации растения по сравнению с одним или более коммерчески доступными штаммами Bradyrhizobia.
7. Композиция инокулята по п.6, где увеличенная конкурентоспособность включает по меньшей мере 51% заполненности клубеньков.
8. Композиция инокулята по любому из пп.1, 2, 6, где по крайней мере один из указанных штаммов Bradyrhizobia japonicum имеет увеличенную эффективность стимуляции роста растений по сравнению с одним или более коммерчески доступными штаммами Bradyrhizobia.
9. Композиция инокулята по п.8, где увеличенная эффективность стимуляции роста растений включает по меньшей мере одно из увеличенного выхода растений, измеряемого в значениях бушель/акр, увеличенного количество плодов, увеличенного количество корней, увеличенной длины корней, увеличенной массы корней, увеличенного объема корней, увеличенной площади листьев, увеличенной густоты стояния растений, увеличенной мощности растений и/или увеличенной способности фиксации азота (N2) по сравнению с одним или более коммерчески доступными штаммами Bradyrhizobia.
10. Композиция инокулята по п.8, где указанным растением является растение сои, и где увеличенная эффективность стимуляции роста растения включает увеличение общей сухой массы стручков сои на растении сои, когда указанную общую сухую массу сравнивают с общей сухой массой стручков сои на растении сои, подвергнутом воздействию одним или более коммерчески доступными штаммами Bradyrhizobia.
11. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, где указанный по крайней мере один штамм Bradyrhizobia japonicum содержит:
штамм, имеющий номер доступа депозита NRRL В-50591;
штамм, имеющий номер доступа депозита NRRL В-50589;
штамм, имеющий номер доступа депозита NRRL В-50586; и/или
штамм, имеющий номер доступа депозита NRRL 50594.
12. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, где указанный по крайней мере один штамм Bradyrhizobia japonicum содержит:
штамм, имеющий номер доступа депозита NRRL В-50590; и/или
штамма, имеющий номер доступа депозита NRRL В-50594.
13. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, где указанный по крайней мере один штамм Bradyrhizobia japonicum содержит штамм, имеющий номер доступа депозита NRRL В-50728.
14. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, дополнительно содержащая по меньшей мере одну сигнальную молекулу растения.
15. Композиция инокулята по п.14, где указанная по крайней мере одна сигнальная молекула растений содержит по крайней мере один липохитоолигосахарид (LCO).
16. Композиция инокулята по п.15, где указанная по крайней мере одна LCO содержит по крайней мере одну синтетическую LCO.
17. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну рекомбинантную LCO.
18. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну встречающимся в природе LCO.
19. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из штамма Azorhizobium, Bradyrhizobium, Mesorhizobium, Rhizobium и/или Sinorhizobium.
20. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из штамма Bradyrhizobium japonicum.
21. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из штамма Sinorhizobium meliloti.
22. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из штамма Rhizobium leguminosaruym.
23. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из микоризного гриба.
24. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из штамма Glomerocycota.
25. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит по крайней мере одну LCO, полученную из штамма Glomus intraradicus.
26. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO содержит одну или несколько LCO, представленных формулой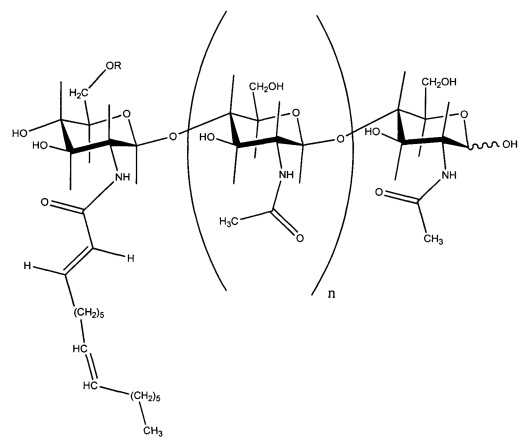
в которой R обозначает Н или СН3СО- и n равно 2 или 3.
27. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO присутствует в концентрации от примерно 10-5 до примерно 10-14 моль.
28. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO присутствует в концентрации от примерно 10-5 до примерно 10-11 моль.
29. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна LCO присутствует в концентрации от примерно 10-7 до примерно 10-8 моль.
30. Композиция инокулята по любому из пп.15, 16, где указанная по крайней мере одна сигнальная молекула растений содержит по меньшей мере один хитоолигосахарид (СО).
31. Композиция инокулята по п.30, где указанный по меньшей мере один СО присутствует в концентрации от примерно 10-5 до примерно 10-14 моль.
32. Композиция инокулята по п.30, где указанный по меньшей мере один СО присутствует в концентрации от примерно 10-5 до примерно 10-11 моль.
33. Композиция инокулята по п.30, где указанный по меньшей мере один СО присутствует в концентрации от примерно 10-7 до примерно 10-8 моль.
34. Композиция инокулята по любому из пп.15, 16, 31-33, где указанная по крайней мере одна сигнальная молекула растений содержит по меньшей мере одно хитиновое соединение.
35. Композиция инокулята по п.34, где указанное по крайней мере одно хитиновое соединение содержит хитин.
36. Композиция инокулята по любому из п.35, где указанное по крайней мере одно хитиновое соединение содержит хитозан.
37. Композиция инокулята по любому из пп.15, 16, 31-33, 35, 36, где указанная по крайней мере одна сигнальная молекула растений содержит по меньшей мере один флавоноид.
38. Композиция инокулята по п.37, где указанный по крайней мере один флавоноид содержит генистеин.
39. Композиция инокулята по любому из пп.15, 16, 31-33, 35, 36, 38, где указанная по крайней мере одна сигнальная молекула растений содержит жасмоновую кислоту или ее эфир, амид, гликозид или соль, линолеиновую кислоту или ее эфир, амид, гликозид или соль, и/или линоленовую кислоту или ее эфир, амид, гликозид или соль, и/или каррикин.
40. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, дополнительно содержащая один или более гербицидов, инсектицидов и/или фунгицидов.
41. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, дополнительно содержащая по меньшей мере один растворяющий фосфаты микроорганизм.
42. Композиция инокулята по п.41, где указанный по меньшей мере один растворяющий фосфаты микроорганизм содержит по меньшей мере один штамм Penicillium.
43. Композиция инокулята по п.41, где указанный по меньшей мере один растворяющий фосфаты микроорганизм содержит по меньшей мере один штамм P. bilaiae.
44. Композиция инокулята по п.43, где указанный по крайней мере один штамм P. bilaiae содержит:
штамм, имеющий номер доступа депозита NRRL В-50162;
штамм, имеющий номер доступа депозита NRRL В-50169;
штамм, имеющий номер доступа депозита NRRL В-20851;
штамм, имеющий номер доступа депозита NRRL 22348; и/или
штамм, имеющий номер доступа депозита NRRL 18309.
45. Композиция инокулята по любому из пп.42-44, где указанный по меньшей мере один растворяющий фосфаты микроорганизм содержит по меньшей мере один штамм Р. gaestrivorus.
46. Композиция инокулята по п.45, где указанный по крайней мере один штамм P. gaestrivorus содержит штамм, имеющий номер доступа депозита NRRL В-50170.
47. Композиция инокулята по п.41, где указанный по меньшей мере один растворяющий фосфаты микроорганизм содержит по меньшей мере один штамм Streptomyces.
48. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, 42-44, 46, 47, где указанный агрономически приемлемый носитель представляет собой жидкость не на водной основе.
49. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, 42-44, 46, 47, где указанный агрономически приемлемый носитель представляет собой жидкость на водной основе.
50. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, 42-44, 46, 47, где указанный агрономически приемлемый носитель представляет собой смачиваемый порошок.
51. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, 42-44, 46, 47, где указанный агрономически приемлемый носитель содержит торфяные порошки или гранулы.
52. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, 42-44, 46, 47, где указанный агрономически приемлемый носитель содержит гранулы на основе гипса.
53. Композиция инокулята по любому из пп.1, 2, 6, 9, 10, 15, 16, 31-33, 35, 36, 38, 42-44, 46, 47, где указанный агрономически приемлемый носитель содержит глину.
54. Покрытое семя бобового растения для получения бобового растения, имеющего усиленный рост, отличающееся тем, что покрытие содержит композицию инокулята по любому из пп.1-53.
55. Покрытое семя по п.54, где указанное семя представляет собой семя сои.
56. Покрытое семя по п.54, где указанное семя представляет собой семя люцерны.
57. Покрытое семя по п.54, где указанное семя представляет собой семя гороха.
58. Покрытое семя по п.54, где указанное семя представляет собой семя чечевицы.
59. Покрытое семя по п.54, где указанное семя представляет собой семя фасоли.
60. Бобовое растение, имеющее усиленный рост, где растение содержит композицию инокулята по любому из пп.1-53.
| WO 2001038492 A1, 31.05.2001 | |||
| US 0006606822 В2, 19.08.2003 | |||
| US 0005300127 А1,05.04.1994 | |||
| Способ инокуляции бобовых растенийпРЕпАРАТАМи КлубЕНьКОВыХ бАКТЕРий | 1979 |
|
SU843914A1 |
| ZHANG H | |||
| ET AL | |||
| Low temperature tolerant Bradyrhizobium japonicum strains allowing improved nodulation and nitrogen fixation of soybean in a short season (cool spring) area // Europ | |||
| J | |||
| Agronomy, 2003, vol | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Автоматическая акустическая блокировка | 1921 |
|
SU205A1 |
Авторы
Даты
2017-02-21—Публикация
2012-03-30—Подача