Изобретение относятся к травматологии и ортопедии, а именно к способам профилактики и лечения поражений деформирующим остеоартрозом голеностопного сустава.
Профилактика, а также лечение различных поражений суставов являются актуальными направлениями в современной травматологии и ортопедии.
Дегенеративные и воспалительные заболевания поражают суставы разных возрастных групп, а после 60-летнего возраста - примерно у 60% мужчин и 70% женщин. При этом суставы нижних конечностей, постоянно находящиеся под нагрузкой массы тела, поражаются намного чаще суставов верхних конечностей. Заболеваемость деформирующим остеоартрозом (далее OA) голеностопного сустава (крузартроз) составляет до 25% в структуре заболеваемости OA (Завгородний Н.В., Терешкова В.П., 2008), при этом в 60% случаев OA развивается после различных травм, занимая третье место после артроза коленного и тазобедренного суставов (Плоткин Г.Л. с соавт., 2006, Ежов М.Ю., 2011), встречается преимущественно у лиц молодого трудоспособного возраста и протекает наиболее тяжело вследствие максимальной весовой нагрузки на эти отделы. Крузартроз является прогрессирующим заболеванием, которое характеризуется снижением амплитуды движений, нарастанием болевого синдрома, особенно при физической нагрузке, отеком сустава, стопы и голени. В последующем присоединяются трофические нарушения. По данным внутрикостной флебографии выявляются выраженные признаки нарушения венозного оттока. В норме внутрикостное давление в теле таранной кости составляет 10 мм водн. ст., в дистальном отделе большеберцовой и малоберцовой костей 26 и 23 соответственно. При OA давление в таранной кости увеличивается в 4 раза, в большеберцовой кости - в 3 раза.
Все это приводит, как правило, к выраженным повреждениям суставного хряща, субхондральной кости и капсульно-связочного аппарата суставов.
Важную роль в патогенезе заболеваний играют неблагоприятные изменения трибологических характеристик суставных хрящей, нарушающие их скольжение и должное функционирование. Развивающаяся в результате указанных заболеваний воспалительная реакция вызывает также резкое усиление свободнорадикальных процессов с образованием токсичных продуктов, усугубляющих повреждения суставных тканей.
Процессы, обеспечивающие адекватную биологическую смазку и поддержание физиологического уровня свободнорадикальных процессов в суставах в мировой практике до конца не изучены. Причины и патогенез отмеченных нарушений в функционировании суставов до сих пор не установлены, что препятствует разработке и поиску патогенетически обоснованных способов лечения и профилактики заболеваний суставов.
Имеющиеся в настоящее время способы лечения не направлены на устранение исходных причин заболеваний и оказывают, зачастую, лишь симптоматическое лечение.
Известно также, что внутрисуставное введение препаратов на основе гиалуроната, предложенное в изобретении, не способно полноценно восстановить трибологические показатели больных суставов (пат. US №5143724).
Использование фосфолипидов также проблематично, ввиду неясности участия фосфолипидов в суставном трении (пат. US №6133249).
Для лечения воспалительных заболеваний суставов, в частности для облегчения болей, раскрыто применение синтетического катализатора, ускоряющего элиминацию токсичных радикалов кислорода. Однако такой подход не устраняет причин, вызывающих активизацию свободнорадикальных процессов в пораженных суставах (пат. US №6980620).
Для лечения артритов предложены растительные липидные экстракты, оказывающие благоприятное действие благодаря входящим в их состав природным антиоксидантам, что является, по сути, компенсаторным лечением, восполняющим имеющийся в тканях суставов недостаток эндогенных антиоксидантов (пат. US №6346278).
Применение ингибиторов циклооксигеназы-2, индуцируемой синтазы окиси азота - iNOS, а также ингибиторов активности цитокинов снижает воспалительную реакцию в больных суставах (пат. US №6248745, US №6492516). Однако и в указанных источниках информации причины, обусловливающие возникновение воспалительной реакции, не устраняются.
Так известен способ лечения дефектов суставного хряща инъекцией эмбриональной ткани (пат. РФ №2195940). Недостатками данного способа являются риски, связанные с применением аллогеной ткани - возможным отторжением, инфекцией, существуют и проблемы с наличием донорского материала.
Известен способ имплантации аутологичных хондроцитов (АО), культивированных in vitro, затем пересаженных в зону дефекта и закрепленных с помощью надкостницы, или искусственной мембраны. К недостаткам данного способа относятся: длительные сроки получения культуры клеток (порядка 3 недель), расширение хирургической агрессии при заборе надкостницы, кроме того, искусственная мембрана является чужеродным материалом, высока и стоимость такого лечения (Brittberg М. Treatment of deep cartilage defects in the knee with autologous chondrocyte transplantation / M. Brittberg, A. Lindahl, A. Nilsson et al. // N. Engl. J. Med. - 1994. - Vol. 331, №14. - P. 889-895).
В настоящее время не вызывает сомнения тот факт, что источником эмбрионального развития хрящевых тканей является мезенхима, в составе которой ведущую роль играют полипотентные мезенхимные стволовые клетки. Мезенхимным стволовым клеткам посвящен ряд исследований, из которых следует, что потомками этой клеточной популяции во взрослом организме человека являются мультипотентные мезенхимальные стромальные клетки костного мозга. Они отличаются от стволовых кроветворных клеток, так как не экспрессируют антигены гемопоэтических клеток - CD34, CD14, CD45. Часть мультипотентных мезенхимальных стромальных клеток, при определенных условиях (соответствующее микроокружение, цитокиновое влияние, действие факторов роста и пр.), способна дифференцироваться по хондробластическому пути в хондрогенные клетки - прехондробласты, хондробласты, хондроциты (Мазуров В.М. Болезни суставов. Спецлит, 2008, 397 с.).
Рядом исследователей показано, что клетки стромально-васкулярного фенотипа, полученные из жировой ткани, могут являться источником клеток-предшественников хрящевой ткани. Стромальные клетки жировой ткани представляют собой популяцию клеток, обладающих высокой степенью пластичности и высокой интенсивностью пролиферации (Трактуев Д.О. Стромальные клетки жировой ткани - пластический тип клеток, обладающий высоким терапевтическим потенциалом / Д.О. Трактуев, Е.Б. Парфенова, В.А. Ткачук, К.Л. Марч // Цитология. - 2006. - Т. 48, №2 - с. 83-93).
Известен способ восстановления дефектов гиалинового хряща коленного суставова, включающий введение мезенхимальных стволовых клеток, полученных липосакцией подкожно-жировой клетчатки из различных тканей с последующей ферментной обработкой, после проведения абразивной хондроплатики и микрофрактуринга методом артроскопии (Стадников А.А. и др. Новые методы лечения дефектов гиалинового хряща коленного сустава у больных гонантрозом. Научно-практическая ревматология, 2009, №3, с. 1-5). В данном способе речь идет только о восстановлении коленного сустава.
Известен способ восстановления дефектов гиалинового хряща суставных поверхностей голеностопного сустава, при котором применяют инъекционное введение смеси клеток стромальной сосудистой фракции одновременно с фибриновым клеем без вскрытия сустава под контролем электронно-оптического преобразователя под местной или общей анестезией, позволяющий добиться точной доставки смеси к зоне дефекта и надежного крепления (пат. РФ №2559089).
На более поздних стадиях заболевания и выраженных повреждениях суставов широко распространенным способом восстановления пораженных суставов является имплантация искусственных суставов. Основным недостатком эндопротезирования является более травматичный хирургический метод. Кроме того, он уничтожает все структуры сустава (суставные поверхности, суставную капсулу), не дает шанса суставу на восстановление репаративных процессов в нем.
Для максимального использования ресурсов организма пациента, минимизирования хирургического вмешательства, а также расширения возможности для лечения заболеваний суставов, восстановления и создания артромедуллярной связи используют различные канюлированные устройства для отбора и подачи жидкой фракции костного мозга (костного жира) из внутрикостного пространства в суставную полость для смазки суставных поверхностей (пат. РФ. №2329775).
Известны также различные варианты имплантатов артромедуллярных (пат. РФ на ПМ №№91843, 92320, 92321), выполненных канюлированными, которые обеспечивают соединения полости кости с суставной полостью для поступления костного жира из внутрикостного пространства в полость сустава, что обеспечивает снижение коэффицента трения суставных поверхностей.
Ни в одном из источников информации не было указания на установку канюлированных имплантатов артромедуллярных конкретно в голеностопный сустав для смазки суставных поверхностей костным жиром, находящимся в составе костного мозга, из-за его анатомической особенности.
Голеностопный сустав - сочленение костей голени со стопой - подвижное соединение большеберцовой, малоберцовой и таранной костей человека. Сложный по строению, блоковидный по форме, образован суставными поверхностями дистальных эпифизов обеих берцовых костей, охватывающими «вилкой» блок таранной кости. К верхней суставной поверхности таранной кости прилежит большеберцовая кость, а по бокам - суставные поверхности наружной и внутренней лодыжек. В суставе возможны движения: фронтальная ось - сгибание и разгибание стопы; сагиттальная ось - супинация и пронация, вертикальная ось - отведение и приведение. Движения по осям сопряжены и выполняются по составляющей линии.
Техническим результатом, на достижение которого направлено данное техническое решение, является создание таких способов профилактики и лечения поражений суставов и разработка методики лечения голеностопного сустава, которые обеспечивали бы смазывание, восстановление пораженных суставов, исключая при подаче костного мозга в полость сустава попадание мелких костей и частей мягких тканей при рассверливании костной ткани. Кроме того, способствовали бы восстановлению трибологических характеристик, нормализации в них окислительных и воспалительных процессов с использованием костного жира пациента с помощью миниинвазивно устанавливаемых известных канюлированных устройств артроскопическим или открытым способами.
Технический результат достигается за счет использования способа лечения и профилактики деформирующего остеоартроза голеностопного сустава, отличающегося тем, что осуществляют продольный разрез кожи при доступе по передне-внутренней поверхности большеберцовой кости в проекции голеностопного сустава, далее разрез проводят в проекции суставной щели по внутреннему контуру медиальной лодыжки, затем выделяют зону доступа у основания внутренней лодыжки по переднему краю большеберцовой кости, под контролем ЭОП проводят спицу Киршнера интрамедуллярно и канюлированным сверлом формируют канал, в который устанавливают артромедуллярный шунт с внутренним каналом заподлицо под хрящ до полного погружения его вровень с костным передним краем большеберцовой кости, соединяя внутрикостное пространство, образующее костномозговую полость трубчатой кости с суставной полостью, после извлечения спицы производят очистку канала шунта от возможного попадания костной стружки и обрабатывают хрящ в зоне выходного отверстия зенковкой.
Также можно осуществлять доступ по передне-наружному краю большеберцовой кости в проекции голеностопного сустава, далее разрез проводят по внутреннему контуру латеральной лодыжки и выделяют зону доступа, формируя искусственную ямку у основания наружной лодыжки по переднему краю большеберцовой кости.
Из приведенного сопоставительного анализа следует, что заявляемый способ соответствует критерию патентоспособности "новизна", так как из источников информации не было найдено аналогичного решения применительно для голеностопного сустава, не описана методика проведения операции по установке артромедуллярного полого шунта в голеностопный сустав.
Способ, составляющий заявляемое изобретение, предназначен для использования в здравоохранении. Возможность его осуществления подтверждена описанными в заявке приемами и средствами. Заявленный способ обеспечивает достижение усматриваемого заявителем технического результата, а именно обеспечение высокой репаративной способности регенерации суставного хряща и укорочение сроков реабилитации больных с заболеваниями суставов, отсутствует вероятность попадания мелких костей и частей мягких тканей при рассверливании костной ткани в костный мозг.
Из изложенного следует, что заявляемое изобретение соответствует условию патентоспособности "промышленная применимость".
При анализе известных способов было выявлено в них отсутствие сведений о влиянии отличительных признаков способа на достижение технического результата, следовательно, изобретение соответствует требованию "изобретательский уровень".
Таким образом, в настоящее время отсутствует эффективный, малотравматичный способ лечения дегенеративно-дистрофических заболеваний голеностопного сустава с использованием костного мозга пациента, постоянно поступающего на поверхность пораженных суставов.
Профилактику и лечение поражений голеностопного сустава (ГСС) в начальной и в последующих стадиях поражения сустава осуществляют за счет соединения внутрикостного пространства, образующего сустав кости, заполненного костным мозгом, с суставной полостью. Это обеспечивает поступление компонентов костного мозга, в том числе костного жира в суставную полость за счет повышения внутрикостного давления в результате упругой деформации кости при осуществлении нагрузки на кость, в том числе возникающей при движении. Кроме того, при OA давление в таранной кости увеличивается в 4 раза, а в большеберцовой кости - в 3 раза. Костный мозг способен постоянно и достаточно легко проникать по созданному каналу в суставную щель. Из-за разницы в давлениях возникает градиент давления, обеспечивающий направление перемещения жидкости из области с большим давлением в область с меньшим давлением. При этом исключается возможность спонтанного выдавливания костного мозга в кровяное русло, что могло бы послужить причиной жировой эмболии.
Компоненты костного мозга, в том числе костного жира, поступают также на трущиеся поверхности сустава и обеспечивают их смазывание, тем самым снижения трение между ними. Для этого используют миниинвазивно устанавливаемое устройство артроскопическим или открытым способами - имплантат, или канюлированное устройство, выполненное в виде трубки или выполненное в виде шунта.
Установку используемых устройств осуществляют различными способами с помощью наборов инструментов, применяемых в хирургии, миниинвазивно, и/или с помощью артроскопической техники.
Техника операции
При проведении операции возможен как передне-внутренний доступ, так и передне-наружный доступ.
Операция осуществляется с применением регионарной анестезии (спинномозговая, проводниковая, эпидуральная). Положение больного лежа на спине.
Проведение операции при передне-внутреннем доступе. После трехкратной обработки операционного поля раствором антисептика и обкладывания стерильными простынями передний отдел стопы располагаем в положении максимальной пронации и отведения стопы кнаружи.
Осуществляют продольный разрез кожи до 3,5 см при доступе по передне-внутренней поверхности большеберцовой кости в проекции голеностопного сустава, далее разрез продолжают в проекции суставной щели по внутреннему контуру медиальной лодыжки. Тупо и остро выделяем зону доступа у основания внутренней лодыжки по переднему краю большеберцовой кости, где имеется собственная анатомическая ямка или выемка.
Под контролем ЭОП проводится спица Киршнера, интрамедуллярно (снизу-вверх, спереди-назад, изнутри-кнаружи), до ощущения «проваливания». Канюлированным сверлом 0 4,5 мм формируется канал, в который по спице ввинчивается артромедуллярный шунт («заподлицо» под хрящ) до полного погружения его вровень с костным передним краем большеберцовой кости. Типы и размеры шунта подбираются заранее или определяем измерительной линейкой интраоперационно.
После извлечения спицы производится очистка канала шунта от возможного попадания костной стружки, других включений. Появление костного жира в зоне головки шунта свидетельствует о надлежащей установке шунта. Завершающим этапом обрабатывается хрящ в зоне выходного отверстия (зенковка) с целью профилактики зарастания канала. Гемостаз. Послойно - швы на рану.
В послеоперационном периоде: холод - местно, обезболивающие по показаниям, физиолечение. ЛФК при отсутствии болевого синдрома. Дозированная нагрузка на конечность с 1 суток, с продолжением в последующие 2-3 суток и полная опора на ногу с 3-4 дня.
Проведение операции по передне-наружному краю большеберцовой кости
Операция выполняется передне-наружным доступом, под регионарной анестезий (спинномозговая, проводниковая, эпидуральная). Положение больного лежа на спине.
После трехкратной обработки операционного поля раствором антисептика и обкладывания стерильными простынями за передний отдел стопы руками хирурга приводим, суппинируем и выводим в положение подошвенной флексии всю стопу. Проводится продольный разрез кожи до 3,5 см, доступ осуществляют по передне-наружному краю большеберцовой кости в проекции голеностопного сустава, далее разрез проводят по внутреннему контуру латеральной лодыжки. Тупо и остро выделяем зону доступа, у основания наружной лодыжки по переднему краю большеберцовой кости создаем искусственную анатомическую ямку.
Под контролем ЭОП проводится спица Киршнера, интрамедуллярно (снизу-вверх, спереди-назад, изнутри-кнаружи), до ощущения «проваливания». Канюлированным сверлом ∅ 4,5 мм формируется канал, в который по спице ввинчивается артромедуллярный шунт («заподлицо» под хрящ) до полного погружения его вровень с костным передним краем большеберцовой кости. Типы и размеры шунта подбираются заранее или определяем измерительной линейкой интраоперационно.
После извлечения спицы производится очистка канала шунта от возможного попадания костной стружки, других включений. Появление костного жира в зоне головки шунта свидетельствует о надлежащей установке шунта. Завершающим этапом обрабатывается хрящ в зоне выходного отверстия (зенковка) с целью профилактики зарастания канала. Гемостаз. Послойно - швы на рану.
В послеоперационном периоде: холод - местно, обезболивающие по показаниям, физиолечение. ЛФК при отсутствии болевого синдрома. Дозированная нагрузка на конечность с 1 суток, с продолжением в последующие 2-3 суток и полная опора на ногу с 3-4 дня.
ПОКАЗАНИЯ:
- остеоартроз I-II, II-III стадии;
- длительный болевой синдром (более 6 месяцев);
- импиджмент-синдром переднего и заднего отделов голеностопного сустава;
- период ожидания протезирования;
- пациенты, которые не могут или не хотят протезироваться.
Клинический пример. Больная Н.,76 л. ДЗ: Посттравматический деформирующий остеоартроз (ДОА) левого голеностопного сустава 2 ст., состояние после операции металлоостеосинтеза н/з костей голени (по первичным показаниям).
Жалобы при поступлении: на боли при ходьбе, быструю утомляемость, отек в области голеностопного сустава.
История заболевания: травма бытовая, падение на улице 15.01.2014, первично обратились в ГКБ №12, рентгеновские снимки, установлен диагноз перелом нижней трети костей левой голени. Операция 30.01.2014 - открытый остеосинтез костей левой голени, фиксация пластинами и винтами.
Местный статус: ходит без дополнительной опоры, прихрамывая на левую ногу. Кожа обеих голеней чистая. Правая голень и стопа без патологии. На левой голени имеются послеоперационные рубцы на уровне нижней трети. Цвет кожи на этом участке изменен. Разгибание и сгибание в левом голеностопном суставе ограничены, около 25°. Чувствительность сохранена.
На R-грамме: костные разрастания по краям суставных поверхностей большеберцовой и шейки таранной костей, консолидированный перелом лодыжек. При биомеханическом исследовании выявлена скрытая хромота, выраженная асимметрия временных параметров (7%, при норме менее 5%), увеличено время двойной опоры. Также отчетливо снижена частота шага и скорость ходьбы. Кроме того, как компенсация функции голеностопного сустава, резко снижена амплитуда сгибательно-разгибательных движений в коленном суставе, его рекурвация и внутрипронационная установка тазобедренного сустава.
Пациентке, после удаления позиционных винтов из голени, проведена операция по вышеописанной методике по передне-внутренней поверхности голеностопного сустава, установка артромедуллярного шунта. Послеоперационный период без особенностей. Заживление ран первичным натяжением.
При контрольном осмотре через 3 месяца: боли нет. Походка обычная, не хромает. Объем движений в голеностопном суставе увеличился до нормы. На R-грамме положение артромедуллярного шунта (АМШ) стабильно, миграции имплантата и резорбции косной ткани вокруг него не определяется.
При повторном биомеханическом исследовании выявлено, что параметры асимметрии пришли в норму (3%), периоды опоры выровнялись, повысилась сила заднего толчка левой стопы. При этом увеличилась частота шага и скорость ходьбы. Кроме того, уменьшилась варусная девиация левой стопы, рекурвация левого коленного сустава и внутрипронационная установка в тазобедренном суставе. Восстановился практически нормальный объем движений в коленном и тазобедренном суставах.
Предлагаемый способ лечения предназначен для профилактики и лечения голеностопного сустава и позволяет сохранить амплитуду движений в голеностопном суставе, продлить на многие годы (десятки лет) способность человека передвигаться самостоятельно без болевого синдрома, кроме того, в некоторых случаях возможна замена эндопротезирования проведением лечения пораженного сустава за счет использования внутренних резервов организма, таких как смазывающая способность и способность восстанавливать запасы жировой смазки в костях.
Предлагаемый способ лечения найдет широкое применение в клинической практике.
На рис. 1 в качестве имплантата представлено канюлированное устройство, выполненное со сквозным каналом, с входным и выходным отверстиями, оболочка, которого изготавливается из применяемых в ортопедии материалов и снабжена резьбовыми элементами, перфорационными отверстиями различной формы и конфигурации. Типоразмеры устройства позволяют осуществлять подбор для конкретного варианта на основании таких данных, как, например, ширина суставной щели, стадия заболевания. Для достижения указанного технического результата возможно использование различных известных устройств, устанавливаемых инвазивно, а именно канюлированное устройство, выполненное в виде трубки или выполненное в виде шунта.
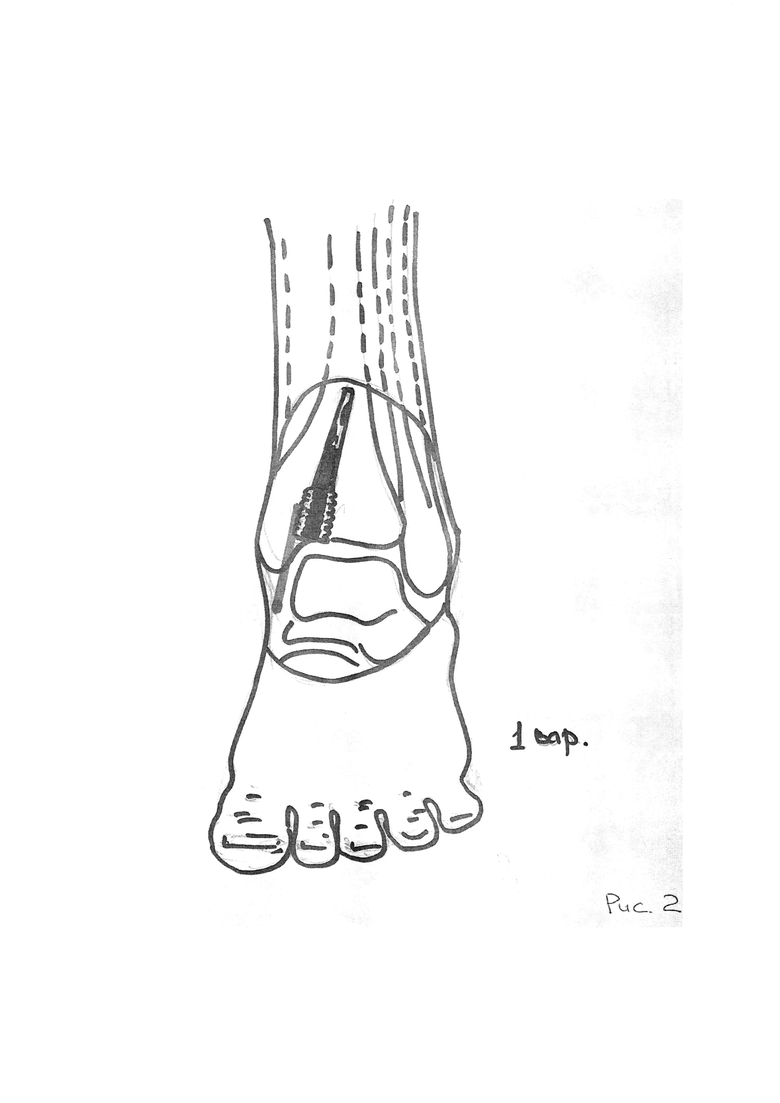
На рис. 2 и 3 представлена схематично методика операции соответственно по 1 варианту (проведение операции при передне-внутреннем доступе) и 2 варианту (проведение операции по передне-наружному краю большеберцовой кости).
Вышеуказанный способ обеспечивает ускорение процесса восстановления пораженных хрящевых тканей сустава, трущихся поверхностей суставов путем смазывание трущихся поверхностей суставов компонентами костного мозга, включающими костный жир.
Предлагаемый способ позволит предупредить или существенно замедлить развитие различных поражений суставов, в том числе посттравматических артрозов, улучшить восстановление работоспособности пораженных суставов человека, в том числе пораженных артрозом голеностопного сустава, в начальной и последующих стадиях поражений, в том числе травм или заболеваний, отдалить сроки возможного последующего эндопротезирования суставов и тем самым продлить срок функционирования собственных суставов человека. Используют в предлагаемом изобретении особенные свойства костного жира, входящего в состав костного мозга, которые обладают уникальными смазывающими свойствами, а также тот факт, что костный жир содержит в своем составе антиоксидант - витамин Е, который блокирует радикалобразующую активность частиц изнашивания трущихся поверхностей.
Таким образом, достигнут технический результат, который способствовал восстановлению трибологических характеристик натуральных и искусственных суставов, нормализации в них окислительных и воспалительных процессов для обеспечения длительного надлежащего функционирования естественных и искусственных суставов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ АРТРОДЕЗА СУСТАВОВ ЗАДНЕГО ОТДЕЛА СТОПЫ | 2014 |
|
RU2549296C1 |
| ИМПЛАНТАТЫ АРТРОМЕДУЛЛЯРНЫЕ (ВАРИАНТЫ) | 2020 |
|
RU2743407C1 |
| Способ хирургического замещения полнослойных костно-хрящевых дефектов суставной поверхности таранной кости с хондропатией и асептическим некрозом | 2021 |
|
RU2766042C1 |
| МАЛОИНВАЗИВНЫЙ АРТРОДЕЗ ПОДТАРАННОГО СУСТАВА | 2014 |
|
RU2549297C1 |
| Способ выполнения артродеза голеностопного сустава с использованием трех спонгиозных винтов | 2016 |
|
RU2633945C1 |
| СПОСОБ АРТРОДЕЗА ГОЛЕНОСТОПНОГО СУСТАВА ПРИ НЕПРАВИЛЬНО СРОСШИХСЯ ПЕРЕЛОМАХ МАЛОБЕРЦОВОЙ КОСТИ И ЗАДНЕГО КРАЯ БОЛЬШЕБЕРЦОВОЙ КОСТИ | 2003 |
|
RU2243737C2 |
| СПОСОБ КОМПРЕССИОННОГО АРТРОДЕЗА ГОЛЕНОСТОПНОГО СУСТАВА ПРИ ТРАВМАТИЧЕСКОМ ОСТЕОАРТРОЗЕ | 2008 |
|
RU2368342C1 |
| СПОСОБ РЕКОНСТРУКЦИИ ЗАДНЕГО ОТДЕЛА СТОПЫ ПРИ УТРАТЕ ПЯТОЧНОЙ КОСТИ | 2012 |
|
RU2488360C1 |
| СПОСОБ ОПЕРАТИВНОГО ДОСТУПА К МЕДИАЛЬНОЙ ЧАСТИ СУСТАВНОЙ ПОВЕРХНОСТИ ТАРАННОЙ КОСТИ | 2016 |
|
RU2638280C1 |
| СПОСОБ АРТРОДЕЗА ГОЛЕНОСТОПНОГО И ПОДТАРАННОГО СУСТАВОВ | 2006 |
|
RU2334480C2 |


Группа изобретений относится к травматологии и ортопедии и может быть применима для лечения и профилактики деформирующего остеоартроза голеностопного сустава. Под контролем ЭОП проводят спицу Киршнера интрамедуллярно, и канюлированным сверлом формируют канал, в который устанавливают артромедуллярный шунт с внутренним каналом заподлицо под хрящ до полного погружения его вровень с костным передним краем большеберцовой кости, соединяя внутрикостное пространство, образующее костномозговую полость трубчатой кости с суставной полостью. После извлечения спицы производят очистку канала шунта от возможного попадания костной стружки и обрабатывают хрящ в зоне выходного отверстия зенковкой. Группа изобретений позволяет ускорить восстановление хрящевых тканей сустава, предотвратить их изнашивание. 2 н.п. ф-лы, 3 ил., 1 пр.
1. Способ лечения и профилактики деформирующего остеоартроза голеностопного сустава, отличающийся тем, что осуществляют продольный разрез кожи при доступе по передне-внутренней поверхности большеберцовой кости в проекции голеностопного сустава, далее разрез продолжают в проекции суставной щели по внутреннему контуру медиальной лодыжки, затем выделяют зону доступа у основания внутренней лодыжки по переднему краю большеберцовой кости, под контролем ЭОП проводят спицу Киршнера интрамедуллярно и канюлированным сверлом формируют канал, в который устанавливают артромедуллярный шунт с внутренним каналом заподлицо под хрящ до полного погружения его вровень с костным передним краем большеберцовой кости, соединяя внутрикостное пространство, образующее костномозговую полость трубчатой кости с суставной полостью, после извлечения спицы производят очистку канала шунта от возможного попадания костной стружки и обрабатывают хрящ в зоне выходного отверстия зенковкой.
2. Способ лечения и профилактики деформирующего остеоартроза голеностопного сустава, отличающийся тем, что осуществляют продольный разрез кожи при доступе по передне-наружному краю большеберцовой кости в проекции голеностопного сустава далее разрез проводят по внутреннему контуру латеральной лодыжки и выделяют зону доступа, формируя искусственную ямку у основания наружной лодыжки по переднему краю большеберцовой кости, под контролем ЭОП проводят спицу Киршнера интрамедуллярно и канюлированным сверлом формируют канал, в который устанавливают артромедуллярный шунт с внутренним каналом заподлицо под хрящ до полного погружения его вровень с костным передним краем большеберцовой кости, соединяя внутрикостное пространство, образующее костномозговую полость трубчатой кости с суставной полостью, после извлечения спицы производят очистку канала шунта от возможного попадания костной стружки и обрабатывают хрящ в зоне выходного отверстия зенковкой.
| УСТРОЙСТВО ДЛЯ ВОССТАНОВЛЕНИЯ И СОЗДАНИЯ АРТРОМЕДУЛЛЯРНОЙ СВЯЗИ, ОТБОРА КОСТНОГО ЖИРА, ВНУТРИСУСТАВНОГО ВВЕДЕНИЯ ИНГРЕДИЕНТОВ ДЛЯ ЛЕЧЕНИЯ ПОРАЖЕННЫХ СУСТАВОВ | 2006 |
|
RU2329775C2 |
| US 20130296267 A1, 07.11.2013 | |||
| САМОШКИН И.Б | |||
| и др | |||
| Артро-медуллярное шунтирование при лечении дефектов суставного хряща у животных | |||
| РВЖ МДЖ, 2011, N 3, c.22-27 | |||
| YANG X | |||
| et al | |||
| Intraarticular Injection of Allogenic Mesenchymal Stem Cells has a Protective Role for the Osteoarthritis (Abstract) | |||
| Chin Med J (Engl) | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| PMID:26365972 [PubMed - indexed for MEDLINE]. | |||
Авторы
Даты
2017-03-01—Публикация
2016-01-27—Подача