ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Данная заявка содержит Перечень последовательностей, который был представлен в формате ASCII с помощью EFS-Web и полностью включен в данную заявку посредством отсылки. Указанная копия ASCII, созданная 14 сентября 2011 г., называется 16395US1.txt, и этот файл имеет объем 3295858 байт.
РОДСТВЕННАЯ ЗАЯВКА
Данная заявка притязает на приоритет предварительной заявки №61/384,015, поданной 17 сентября 2010 г., содержание которой полностью включено в данную заявку посредством отсылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к области фаговой терапии для лечения и контроля бактериальных инфекций. В частности, настоящее изобретение предусматривает новые бактериофаги F387/08, F391/08, F394/08, F488/08, F510/08, F44/10, F125/10, выделенные фаговые полипептиды, композиции, содержащие один или более новых бактериофагов и/или выделенных полипептидов; и способы лечения и профилактики бактериальных инфекций, вызванных, например, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Escherichia coli и/или Pseudomonas aeruginosa, с помощью этих бактериофагов, которые применяются сами по себе или в комбинации с другими терапевтическими средствами, например, антибиотиками или другими фагами.
УРОВЕНЬ ТЕХНИКИ
Бактериофаги (фаги) представляют собой вирусы, которые специфически инфицируют бактерии и вызывают их лизис. Фаговая терапия, способ применения вирусов фага для лечения бактериальных инфекций, были разработаны в 20-е годы 19 века Феликсом д’Эрелем. Первоначально фаговая терапия интенсивно изучалась, были предприняты многочисленные исследования с целью оценки потенциала фаговой терапии при лечении бактериальной инфекции у людей и животных. Достигнутые вскоре успехи ускорили создание многочисленных коммерческих фаговых препаратов. Например, в 1940 г. компания Eli Lilly Company получила 7 фаговых препаратов для лечения людей, включая фаговые препараты для лечения различных болезней, вызванных Staphylococcus sp., E.coli и другими патогенными бактериями. Эти препараты были использованы, например, для лечения инфекций, которые вызывают абсцессы, гнойные раны, вагинит, острые хронические инфекции верхних дыхательных путей и мастоидит.
Однако с развитием антибиотиков в 40-х годах 19 века интерес к фаговым терапевтическим средствам в западном мире снизился. Одним из наиболее важных факторов этого падения интереса было отсутствие стандартизованных протоколов испытаний и способов получения фагов. Неудача с созданием мировых стандартов для проведения испытаний фаговых препаратов мешала документации результатов исследований, что приводило к ощутимому отсутствию эффективности, а также к возникновению проблем с доверием к этим препаратам с учетом стоимости фаговой терапии. Кроме того, проблемы, связанные с производством образцов/видов фагов, затрудняли начальные исследования и разработки. Для повышения жизнеспособности фаговых терапевтических препаратов вначале применяли различные стабилизаторы и консерванты. Однако из-за того, что биология и фагов, и различных стабилизаторов была плохо изучена, многие ингредиенты, добавляемые с целью увеличения жизнеспособности фаговых препаратов, оказались или токсичными для людей, или отрицательно влияли на срок хранения этих препаратов. Другой проблемой при производстве фагов была степень чистоты коммерческих фаговых препаратов. В то время препараты фаговой терапии обычно состояли из неочищенных лизатов бактерий хозяина, которые были обработаны нужным фагом. Таким образом, многие препараты содержали ингредиенты, которые в настоящее время считаются нежелательными бактериальными компонентами, например, эндотоксины. Поэтому неблагоприятные эффекты часто были связаны с препаратами, особенно при их внутривенном введении пациентам. Тем не менее, в Восточной Европе и в бывшем Советском Союзе, где доступ к антибиотикам был ограничен, разработка и применение методов фаговой терапии продолжались вместе с развитием антибиотиков или вместо антибиотиков.
Однако с появлением штаммов многих бактерий, резистентных к антибиотикам, в западном мире снова увеличился интерес к терапии, основанной на применении фагов. Хотя могут быть созданы новые классы антибиотиков, перспектива того, что бактерии могут стать резистентными к новым лекарствам, привела к ускорению поиска не химиотерапевтических средств для контролирования, профилактики и лечения бактериальных инфекций.
Существуют три основных подхода к применению фаговой терапии в клинических условиях: 1) введение вирулентного фага; 2) применение эндолизинов или очищенных лизинов, кодируемых бактериофагом; 3) применение структурных белков фага в качестве метаболических ингибиторов ключевых бактериальных ферментов, таких как ферменты, которые синтезируют пептидогликан.
Следовательно, существует необходимость создания новых бактериофагов и фаговых продуктов в качестве потенциальных терапевтических и профилактических агентов для применения in vivo против патогенных бактерий. В частности, существует необходимость создания бактериофагов, способных вызывать лизис нозокомиальных бактерий, включая Styphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Escherichia coli и/или Pseudomonas aeruginosa. Поскольку большинство фагов и фаговых пептидов, изученных к настоящему времени, проявляют активность, направленную специфически против видов (или подвидов) бактерий, из которых они выделены, новый метод терапии, основанный на применении фагов, может найти особое применение в больничных условиях при селективном нацеливании на нозокомиальные патогены без воздействия на окружающую флору.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Данное изобретение предусматривает выделенные бактериофаги и выделенные антибактериальные полипептиды бактериофагового происхождения для применения при лечении, профилактике или регулировании состояний, связанных с инфекцией, вызванной грамположительными или грамотрицательными бактериями. В частности, выделенные бактериофаги или полипептиды по изобретению могут быть использованы в фармацевтических композициях для лечения, профилактики или регулировании инфекции, вызванной нозокомиальными патогенами, например, грамотрицательными бактериями, включая, но без ограничения, Klebsiella pneumoniae, Acinetobacter baumannii, Escherichia coli и Pseudomonas aeruginosa; и грамположительными бактериями, включая, но без ограничения, Staphylococcus aureus. Согласно некоторым вариантам фармацевтические композиции по изобретению пригодны для лечения состояний, связанных с инфекцией, вызванной резистентными к антибиотикам штаммами бактерий, например, резистентными к метициллину штаммами Staphylococcus aureus (MRSA). Согласно конкретным вариантам выделенные бактериофаги или полипептиды по изобретению применяются для топического лечения инфекции, вызванной нозокомиальными патогенами, у субъектов, которые нуждаются в этом. Согласно другим вариантам выделенные бактериофаги или полипептиды по изобретению применяются для диагностики инфицирующего агента в образце (например, в ткани, крови, моче, образце мокроты), взятом у пациента. Согласно другим вариантам выделенные бактериофаги или полипептиды по изобретению применяются в качестве профилактических дезинфицирующих средств или противоинфекционных агентов для обработки твердых поверхностей, включая кожу и другие эпидермальные поверхности.
Согласно некоторым вариантам данное изобретение предусматривает выделенный бактериофаг, F391/08, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:1 (ФИГУРЫ 15A-15III), и проявляющий антибактериальную активность в отношении одного или более штаммов Klebsiella pneumoniae. Согласно другим вариантам изобретение предусматривает выделенный бактериофаг, F394/08, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:2 (ФИГУРЫ 16A-16Q) и проявляющий антибактериальную активность в отношении одного или более штаммов Acinetobacter baumannii. Согласно другим вариантам данное изобретение предусматривает выделенный бактериофаг, F488/08, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:3 (ФИГУРЫ 17А-17КККК) и проявляющий антибактериальную активность в отношении одного или более штаммов Escherichia coli. Согласно другим вариантам данное изобретение предусматривает выделенный бактериофаг, F510/08, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:4 (ФИГУРЫ 18А-18Х) и проявляющий антибактериальную активность в отношении одного или более штаммов Pseudomonas aeruginosa. Согласно другим вариантам данное изобретение предусматривает выделенный бактериофаг, F44/10, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:560 (ФИГУРЫ 19А-19UUU) и проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus. Согласно другим вариантам данное изобретение предусматривает выделенный бактериофаг, F387/08, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:781 (ФИГУРЫ 20А-20КККК) и проявляющий антибактериальную активность в отношении одного или более штаммов Klebsiella pneumoniae. Согласно другим вариантам данное изобретение предусматривает выделенный бактериофаг, F125/10, включающий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:1074 (ФИГУРЫ 21A-21ZZZ) и проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus.
Данное изобретение охватывает также выделенные бактерии, инфицированные одним или более бактериофагами по изобретению. Согласно некоторым вариантам данное изобретение предусматривает выделенные бактерии К. Pneumonia, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1. Согласно другим вариантам данное изобретение предусматривает выделенные бактерии А. baumannii, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2. Согласно другим вариантам данное изобретение предусматривает выделенные бактерии Е.coli, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3. Согласно другим вариантам данное изобретение предусматривает выделенные бактерии Р. aeruginosa, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4. Согласно другим вариантам данное изобретение предусматривает выделенные бактерии S. aureus, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560. Согласно другим вариантам данное изобретение предусматривает выделенные бактерии К. pneumonia, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:781. Согласно другим вариантам данное изобретение предусматривает выделенные бактерии S. aureus, инфицированные бактериофагом, включающим геном, содержащий последовательность нуклеиновой кислоты или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1074.
Данное изобретение охватывает полипептиды, выделенные из бактериофагов F387/08, F391/08, F394/08, F488/08, F510/08, F44/10 и/или F125/10, при этом такие полипептиды проявляют антибактериальную активность в отношении одного или более видов или штаммов грамположительных и грамотрицательных бактерий, например, К. pneumoniae, A. baumannii, Е.coli, P. aeruginosa и/или S. aureus. Согласно конкретным вариантам полипептиды по изобретению, выделенные или полученные из фагов F387/08 и F3910/08 проявляют антибактериальную или антимикробную активность, например, лизирующую киллерную активность против, по меньшей мере, К. pneumoniae; полипептиды, выделенные или полученные из F394/08, активны против, по меньшей мере, А. baumannii; полипептиды, выделенные или полученные из F488/08, активны против, по меньшей мере, Е.coli; полипептиды, выделенные или полученные из F510/08, активны в отношении, по меньшей мере, Р. aeruginosa; полипептиды, выделенные или полученные из F44/10 и F125/10, активны в отношении, по меньшей мере, S. aureus.
Согласно некоторым вариантам полипептид по изобретению содержит выделенный лизин или состоит из выделенного лизина или его фрагмента (например, домена CHAP), который проявляет антибактериальную активность в отношении одного или более видов или штаммов грамположительных бактерий, таких как S. aureus; и/или грамотрицательных бактерий, таких как К. pneumoniae, A. baumannii, Е.coli и Р. aeruginosa. Согласно конкретным вариантам полипептид по изобретению представляет собой выделенный лизиновый белок, например, эндолизин или лизин хвостового отростка, содержащий аминокислотные последовательности SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:1216 или SEQ ID NO:1261, или состоящий из них. Предсказанными функциями указанных лизиновых белков являются, например, Ig-подобный белок вириона (SEQ ID NO:20), гидролаза клеточной стенки (SEQ ID NO:80), N-ацетилмурамил-L-аланинамидаза (SEQ ID NO:192), растворимый лизоцим (SEQ ID NO:282), Т4-подобный лизоцим (SEQ ID NO:547), эндолизин (SEQ ID NO:556), лямбда-Rzl-подобный белок (SEQ ID NO:557), эндолизин (SEQ ID NO:598), эндолизин (SEQ ID NO:1216) и лизин хвостового отростка (SEQ ID NO:1261).
Согласно другим вариантам полипептид по изобретению содержит фрагмент, вариант или производное с последовательностями SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:1216 или SEQ ID NO:1261, причем указанные фрагмент, вариант или производное проявляют антибактериальную или антимикробную активность, например, лизирующую киллерную активность, в отношении одного или более штаммов К. pneumonia, A. baumannii, Е.coli, P. aeruginosa и/или S. aureus. Согласно конкретным примерам в соответствии с этим аспектом вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:20 и/или SEQ ID NO:80 проявляют антибактериальную или антимикробную активность, (например, лизирующую киллерную активность), в отношении одного или более штаммов К. Pneumonia, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1. Согласно другим примерам в соответствии с этим аспектом вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:192 проявляют антибактериальную или антимикробную активность (например, лизирующую киллерную активность), в отношении одного или более штаммов А. baumannii, например, в отношении бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2. Согласно другим примерам в соответствии с этим аспектом вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:282 проявляют антибактериальную или антимикробную активность (например, лизирующую киллерную активность), в отношении одного или более штаммов Е.coli, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3. Согласно другим примерам в соответствии с этим аспектом изобретения вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:547, SEQ ID NO:556 и/или SEQ ID NO:557 проявляют антибактериальную или антимикробную активность (например, лизирующую киллерную активность), в отношении одного или более штаммов Р. aerugmosa, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4. Согласно дальнейшим примерам в соответствии с этим аспектом вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:598, SEQ ID NO:1216 и/или SEQ ID NO:1261 проявляют антибактериальную или антимикробную активность (например, лизирующую киллерную активность), в отношении одного или более штаммов S. aureus, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560 или SEQ ID NO:1074.
Согласно конкретным вариантам данного изобретения выделенный полипептид по изобретению содержит или состоит из домена CHAP последовательностей SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557 или SEQ ID NO:598. Согласно другим вариантам полипептид по изобретению содержит фрагмент, вариант или производное домена CHAP последовательностей SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557 или SEQ ID NO:598, при этом указанные фрагмент, вариант или производное проявляют антибактериальную или антимикробную активность, например, лизирующую киллерную активность, в отношении одного или более штаммов К. pneumonia, A. baumannii, Е.coli, Р. aerugmosa и/или S. aureus.
Согласно другим вариантам полипептид по изобретению содержит или состоит из выделенного белка хвостового отростка (например, хвостового компонента, белка хвостовой нити, белка рулетки хвостового отростка, белка хвостовой части в месте адсорбции, основного белка хвостовой части, основного белка чехла хвостового отростка, субъединицы конусовидной базальной пластинки) или его фрагмента, биологическая функция которых связана с бактериофагом, из которого они получены, например это может быть антимикробная или антибактериальная активность (например, литическая киллерная активность, направленная в отношении по меньшей мере одного или более видов или штаммов бактерий К. pneumoniae, A. baumannii, Е.coli, P. aeruginosa и/или S. aureus.
Согласно конкретным вариантам полипептид по изобретению является выделенным белком хвостового отростка, содержащим или состоящим из аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266. Согласно другим вариантам полипептид по изобретению содержит фрагмент, вариант или производное SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266, при этом указанные фрагмент, вариант или производное обладают биологической функцией, связанной с бактериофагом, из которого они получены, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), и эта функция направлена в отношении одного или более штаммов К. pneumoniae, А. baumannii, Е.coli, Р. aerugmosa и/или S. aureus.
Предсказанные функции указанных белков хвостового отростка включают, например, рецептор-связывающий хвостовой белок (SEQ ID NO:15), основной хвостовой белок (SEQ ID NO:26 и SEQ ID NO:1077), минорный хвостовой белок (SEQ ID NO:30), порообразующий белок наконечника хвостового отростка (SEQ ID NO:30), хвостовой белок (SEQ ID NO:32-33), минорный хвостовой белок (SEQ ID NO:34), белок хвостового отростка фага (SEQ ID NO:35), белок чехла хвостового отростка (SEQ ID NO:180), белок рулетки хвостового отростка (SEQ ID NO:183), хвостовой белок (SEQ ID NO:185), белок хвостовых нитей (SEQ ID NO:190), белок трубки хвостового отростка (SEQ ID NO:231), мономер чехла хвостового отростка (SEQ ID NO:232), стабилизирующий и завершающий белок хвостового отростка (SEQ ID NO:235), короткие хвостовые волокна (SEQ ID NO:239), завершающий белок конусовидной базальной пластинки наконечника хвостового отростка (SEQ ID NO:240-241), завершающий белок кармана конусовидной базальной пластинки хвостового отростка (SEQ ID NO:242), субъединица конусовидной базальной пластинки (SEQ ID NO:243), инициатор конусовидной базальной пластинки (SEQ ID NO:244), конусовидная базальная пластинка (SEQ ID NO:245), субъединица хаба базальной пластинки и хвостового лизоцима, приспособление, прокалывающее клетки (SEQ ID NO:248), завершение конусовидной базальной пластинки (SEQ ID NO:249), белок, завершающий хвостовой отросток и стабилизирующий чехол хвостового отростка (SEQ ID NO:252), шаперон сборки длинных и коротких хвостовых нитей (SEQ ID NO:254), белок хвостовых нитей (SEQ ID NO:433), белок хвостовых нитей (SEQ ID NO:434), длинные хвостовые нити шарнирного соединителя (SEQ ID NO:435), шарнир хвостовых нитей (SEQ ID NO:436), проксимальная субъединица хвостовых волокон (SEQ ID NO:437), инициатор базальной пластинки-трубки хвостового отростка (SEQ ID NO:489), базальная пластинка (SEQ ID NO:490), субъединица хаба базальной пластинки, детерминатор длины хвостового отростка (SEQ ID NO:491), субъединица дистального хаба базальной пластинки (SEQ ID NO:492), субъединица хаба базальной пластинки (SEQ ID NO:493), катализатор сборки хабов базальной пластинки (SEQ ID NO:494), субъединица хаба базальной пластинки (SEQ ID NO:495), субъединица конусовидной базальной пластинки (SEQ ID NO:496), белок трубки хвостового отростка (SEQ ID NO:544-545), белок хвостовых нитей (SEQ ID NO:549 и SEQ ID NO:551), основной белок чехла хвостового отростка (SEQ ID NO:629 и SEQ ID NO:1250), основной хвостовой белок (SEQ ID NO:686), белок трубки хвостового отростка (SEQ ID NO:789),
фибритин (SEQ ID NO:796), короткие хвостовые волокна (SEQ ID NO:797), наконечник завершения базальной пластинки хвостового отростка (SEQ ID NO:798), субъединица конусовидной базальной пластинки и наконечник хвостового отростка (SEQ ID NO:799), соединитель хвостовых нитей базальной пластинки (SEQ ID NO:800), субъединица хаба базальной пластинки и лизоцима (SEQ ID NO:806), лизоцим (SEQ ID NO:854), холин (SEQ ID NO:999 и SEQ ID NO:1217), дистальный катализатор сборки длинных хвостовых нитей (SEQ ID NO:1000), L-образный белок хвостовых нитей (SEQ ID NO:1001), дистальный соединитель шарнирного соединения длинных хвостовых волокон (SEQ ID NO:1002), проксимальный соединитель шарнирного соединения длинных хвостовых волокон (SEQ ID NO:1003), проксимальная субъединица длинных хвостовых нитей (SEQ ID NO:1004), инициатор трубки базальной пластинки хвостового отростка (SEQ ID NO:1053), завершение трубки базальной пластинки (SEQ ID NO:1054), субъединица хаба базальной пластинки, детерминатор длины хвостового отростка (SEQ ID NO:1055), субъединица дистального хаба базальной пластинки (SEQ ID NO:1056), субъединица хаба базальной пластинки (SEQ ID NO:1057 и 1059), катализатор сборки хабов базальной пластинки (SEQ ID NO:1058), субъединица конусовидной базальной пластинки (SEQ ID NO:1060) и белок базальной пластинки (SEQ ID NO:1266).
Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30 или SEQ ID NO:32-35, которые имеют биологическую функцию, связанную с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, например, антимикробную или антибактериальную активность, (например, лизирующую киллерную активность), причем эта функция направлена в отношении одного или более штаммов К. pneumoniae. Согласно другим вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185 или SEQ ID NO:190, которые имеют биологическую функцию, связанную с бактериофагом, содержащим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2, например, антимикробную или антибактериальную активность, (например, лизирующую киллерную активность), причем эта функция направлена в отношении одного или более штаммов А. baumannii.
Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-495 или SEQ ID NO:496, которые имеют биологическую функцию, связанную с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3, например, антимикробную или антибактериальную активность, (например, лизирующую киллерную активность), причем эта функция направлена в отношении одного или более штаммов Е.coli. Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549 или SEQ ID NO:551, которые имеют биологическую функцию, связанную с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4, например, антимикробную или антибактериальную активность, (например, лизирующую киллерную активность), причем эта функция направлена против одного или более штаммов Р. aeruginosa. Согласно другим вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:629 или SEQ ID NO:686, которые имеют биологическую функцию, связанную с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560, например, антимикробную или антибактериальную активность, (например, лизирующую киллерную активность), причем эта функция направлена против одного или более штаммов S. aureus. Согласно другим вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004 или SEQ ID NO:1053-1060, которые имеют биологическую функцию, связанную с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:781, например, антимикробную или антибактериальную активность, (например, лизирующую киллерную активность), причем эта функция направлена против одного или более штаммов К. pneumoniae. Согласно другим вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266, которые имеют биологическую функцию, связанную с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1074, например, антимикробную или антибактериальную активность (например, лизирующую киллерную активность), причем эта функция направлена против одного или более штаммов S. aureus.
Согласно некоторым вариантам данное изобретение предусматривает выделенные полипептиды, которые проявляют антимикробную или антибактериальную активность, (например, лизирующую киллерную активность) против одного или более штаммов бактерий, например, грамположительных бактерий (таких как S. aureus), грамотрицательных бактерий (например, К. pneumoniae, A. baumannii, E.coli и Р. aeruginosd) или бактерий, не классифицированных ни как грамположительные, ни как грамотрицательные, при этом указанные выделенные полипептиды имеют аминокислотную последовательность, которая по меньшей мере на 60%, 65%, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентична второй аминокислотной последовательности с той же длиной (например, состоящей из того же количества остатков), при этом этой второй аминокислотной последовательностью является SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261, SEQ ID NO:1266 и/или ее фрагмент.
Данное изобретение предусматривает также выделенные полипептиды, содержащие или состоящие из любой аминокислотной последовательности из SEQ ID NO:5-176, SEQ ID NO:177-223, SEQ ID NO:224-506, SEQ ID NO:507-559, SEQ ID NO:561-780, SEQ ID NO:782-1073 и SEQ ID NO:1075-1300. Согласно другим вариантам предусмотрены выделенные полипептиды по изобретению, рекомбинантно слитые или химически соединенные (например, соединенные ковалентно или не ковалентно) с терапевтическими агентами (например, гетерологичными полипептидами или малыми молекулами).
Данное изобретение охватывает также полинуклеотиды, которые кодируют полипептиды по изобретению. Согласно конкретному варианту данное изобретение предусматривает выделенную нуклеиновую кислоту, содержащую последовательность нуклеиновой кислоты, кодирующей полипептид, из SEQ ID NO:5-176, SEQ ID NO:177-223, SEQ ID NO:224-506, SEQ ID NO:507-559, SEQ ID NO:561-780, SEQ ID NO:782-1073 и SEQ ID NO:1075-1300. Согласно другим вариантам данное изобретение предусматривает выделенную нуклеиновую кислоту, содержащую любую последовательность нуклеиновой кислоты, кодирующей полипептид, из SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261 или SEQ ID NO:1266, или ее активные фрагмент, вариант или производное, при этом эти фрагмент, вариант или производное проявляют биологическую функцию, связанную с бактериофагом, из которого они выделены, например, антимикробную или антибактериальную активность (например, лизирующую киллерную активность). Настоящее изобретение относится также к вектору, который содержит одну или более таких нуклеиновых кислот. Согласно одному из вариантов указанный вектор представляет собой экспрессионный вектор. Далее, настоящее изобретение предусматривает также хозяйские клетки, содержащие вектор, включающий один или более полинуклеотидов, которые кодируют полипептиды по изобретению.
Данное изобретение охватывает также способы получения полипептидов по изобретению или их активных фрагментов, в особенности, для применения в составе фармацевтических композиций, а именно, антимикробных композиций. Например, полипептиды по изобретению могут быть выделены непосредственно из клеточных культур (например, бактериальных клеточных культур), инфицированных бактериофагами F387/08, F391/08, F394/08, F488/08, F510/08, F44/10 и/или F125/10. Или же полипептиды по изобретению могут быть получены рекомбинантными способами с помощью экспрессионных векторов, содержащих последовательность нуклеиновой кислоты, кодирующей полипептиды по изобретению, например, SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557,, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261 или SEQ ID NO:1266, или ее активные фрагменты, производные или варианты. Полипептиды по изобретению могут быть получены любым способом, известным из уровня техники, в частности, путем химического синтеза или методом рекомбинантной экспрессии.
Согласно конкретным вариантам данное изобретение относится к способу рекомбинантного получения фагового белка, например, лизинового белка, белка хвостового чехла или их активного фрагмента, варианта или производного, причем этот способ включает: (i) культивирование в условиях, подходящих для экспрессии указанного белка в окружающей среде, клетки-хозяина, содержащей вектор, включающий последовательность нуклеиновой кислоты, кодирующей аминокислотную последовательность SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, or SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261 или SEQ ID NO:1266 или ее фрагмент, и (ii) выделение указанного белка из указанной среды. Согласно некоторым вариантам данного изобретения последовательность нуклеиновой кислоты, кодирующая полипептид по изобретению, функционально связана с гетерологичным промотором.
Настоящее изобретение охватывает также способы диагностики возбудителя инфекции в случае клинического проявления бактериальной инфекции. Выделенный бактериофаг или выделенные полипептиды по изобретению могут быть использованы для облегчения определения видов бактерий в образце, отобранном у пациента, путем определения чувствительности бактерий в образце к бактериофагу и/или полипептидам по изобретению. Эти способы включают также оценку антибактериальной активности бактериофага и/или полипептидов по изобретению. Антибактериальная активность бактериофага и/или полипептидов по изобретению или чувствительность неизвестного образца к такой активности можно оценить любым методом, известным из уровня техники и/или описанным в данной заявке. Согласно некоторым вариантам антибактериальная активность и/или чувствительность оцениваются путем культивирования известных бактерий и/или образцов ткани, крови, жидкости или мазка, взятых у пациента, в соответствии со стандартными методиками (например, в культуральной жидкости или на агаровых пластинах), контактирования культуры с бактериофагом и/или полипептидами по изобретению и мониторинга роста клеток после указанного контактирования. Например, в культуральной жидкости бактерии (например, К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и/или S. aureus) могут быть выращены до достижения оптической плотности ("OD"), представляющей среднюю точку экспоненциального роста культуры; эта культура подвергается воздействию одной или более концентраций одного или более бактериофагов и/или полипептидов по изобретению, и затем осуществляют мониторинг OD относительно контрольной культуры. Уменьшение OD относительно плотности контрольной культуры свидетельствует о проявлении антибактериальной активности бактериофагом и/или полипептидом по изобретению (например, о проявлении лизирующей киллерной активности) в отношении испытуемого образца или видов бактерий и/или штамма в указанной культуре. Подобным образом дают колониям бактерий образоваться на агаровых пластинах, эти пластины подвергают действию бактериофага и/или полипептида по изобретению и оценивают последующий рост колоний по сравнению с контрольными пластинами. Уменьшение размеров бактериальной колонии или уменьшение общего числа колоний показывает, что бактериофаг и/или полипептид обладают антибактериальной активностью против испытуемого образца и/или культивированных видов бактерий или штамма.
Данное изобретение предусматривает также фармацевтические композиции, содержащие и/или состоящие из бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074. Согласно некоторым вариантам фармацевтическая композиция по изобретению содержит бактериофаг, имеющий геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074, в добавление к одному или более другим бактериофагам. Один или более других бактериофагов могут быть одним или несколькими бактериофагами по изобретению (например, имеющими геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074), одним или несколькими его штаммами или могут быть одним или несколькими бактериофагами, известными из уровня техники и отличающимися от бактериофага, имеющего геном, соответствующий последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781, or SEQ ID NO:1074. Кроме того, один или более бактериофагов в фармацевтической композиции по изобретению может быть нацелен на один и тот же или на разные виды или штаммы бактерий. Согласно некоторым вариантам фармацевтические композиции по изобретению, содержащие один или более бактериофагов по изобретению, содержат также один или более полипептидов по изобретению и/или другие фаговые продукты, которые описаны в данной заявке или известны из уровня техники.
Согласно некоторым вариантам данное изобретение предусматривает фармацевтические композиции, содержащие полипептиды или их активные фрагменты, в частности, те, которые обладают антимикробной и/или антибактериальной активностью, которые выделены из бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074. Согласно конкретным вариантам фармацевтические композиции по изобретению содержат один или более полипептидов, имеющих аминокислотную последовательность из SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261 или SEQ ID NO:1266. Согласно другим вариантам фармацевтические композиции по изобретению содержат полипептид, который является вариантом или производным или фрагментом последовательности SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261 или SEQ ID NO:1266, где указанные вариант, производное или фрагмент сохраняют биологическую функцию полипептида, из которого они получены, например, антимикробную или антибактериальную активность (например, лизирующую киллерную активность) предпочтительно в отношении одного или более штаммов К. pneumoniae, A. baumannii, Е.coli, P. aeruginosa, and/or S. aureus.
Фармацевтические композиции по изобретению могут дополнительно содержать фармацевтически приемлемые носитель, эксципиент или стабилизатор. Согласно некоторым вариантам фармацевтические композиции по изобретению являются антибиотическими композициями (они проявляют антибактериальную активность) или терапевтическими композициями для лечения, профилактики и/или ослабления симптомов болезни или расстройства, связанных с инфекцией, вызванной бактериями, у субъекта, нуждающегося в этом. Согласно конкретным вариантам фармацевтические композиции по изобретению являются антибактериальными композициями или терапевтическими композициями для лечения, профилактики и/или ослабления симптомов болезни или расстройства, связанных с инфекцией, вызванной К. pneumoniae, A. baumannii, Е.coli, P. aeruginosa и/или S. aureus. Согласно некоторым вариантам субъектом, получающим фармацевтическую композицию по изобретению, является млекопитающее (например, быки, овцы, козы, непарнокопытные животные, приматы (например, люди), грызуны, зайцеобразные и птицы (например, цыплята, утки, гуси)).
Данное изобретение предусматривает способы лечения или профилактики бактериальной инфекции, включающие введение субъекту, нуждающемуся в этом, фармацевтической композиции, содержащей один или более бактериофагов или фаговых продуктов (например, выделенного полипептида бактериофага или его фрагмента, варианта или производного), возможно, в дополнение к одному или более бактериофагам или другим фаговым продуктам, которые описаны в данной заявке. В контексте данного изобретения термин "лечение" относится как к терапевтическому лечению, так и к профилактическим или предупредительным мерам, при этом цель лечения состоит в устранении, ослаблении, уменьшении тяжести, замедлении развития или отсрочки или профилактики симптомов или причин (например, бактериальной инфекции), связанных с патологическим состоянием или расстройством. Фармацевтические композиции по изобретению могут быть использованы при лечении или сдерживании развития инфекций, относящихся к любой бактериальной инфекции, включая, но без ограничения, инфекции, вызванные К. pneumoniae, А. baumannii, Е.coli, P. aeruginosa и/или S. aureus, а также, согласно некоторым вариантам, S. epidermidis, S. auricularis, S. capitis, S. haemolyticus, S. hominis, S. saprophyticus, S. simulans, S. xylosis, M. luteus, B. subtilis, B. pumilus, Е. faecalis, Е. hirae, Е. faecium, Е. avium и их комбинациями. Согласно некоторым вариантам фармацевтические композиции могут быть использованы для лечения состояний или расстройств, связанных с бактериальными инфекциями, включая, но без ограничения, послеоперационный эндофтальмит, эндокардит, инфекции центральной нервной системы, пневмонию, остеомиелит, раневые инфекции (например, диабетические язвы стопы), мастит, септицемию, пищевое отравление, менингит, кожные инфекции, абсцессы, синдром токсического шока, бактериемию и/или другие состояния, связанные с нозокомиальными бактериальными инфекциями.
Согласно некоторым вариантам данное изобретение предусматривает применение бактериофага или выделенного фагового продукта (например, выделенного фагового полипептида или его активного варианта или его производного) при проведении монотерапии. Согласно другим вариантам настоящее изобретение предусматривает применение бактериофага или выделенного фагового продукта (например, выделенного фагового полипептида или его активного фрагмента, варианта или производного) в комбинации со стандартными или экспериментальными методами лечения. Примеры терапевтических агентов, которые особенно полезны в комбинации с бактериофагом и/или полипептидом по изобретению, представляют собой противовоспалительные агенты, стандартные химиотерапевтические антибиотические агенты (например, пенициллин, синтетические пенициллины, бацитрацин, метициллин, нафциллин, оксацилин, клоксациллин, ванкомицин, тейкопланин, клиндамицин, ко-тримоксазол, цефалоспорин, полимиксин, цефахлор, цефадроксил, цефамандола нафат, цефазолин, цефиксим, цефметазол, цефониоид, цефоперазон, цефоранид, цефотиам, цефотаксим, цефотетан, цефокситин, цефподоксима проксетил, цефтазидим, цефтизоксим, цефтриаксон, цефтриаксона моксалактам, цефуроксим, цефалексин, цефалоспорин С, натриевая соль цефалоспорина С, цефалотин, натриевая соль цефалотина, цефапирин, цефрадин, цефуроксимеаксетил, цефалотина дигидрат, моксалактам, лоракарбефа мафат и хелатирующие агенты), местные анестезирующие агенты и/или кортикостероиды. Согласно еще одному варианту композиции по данному изобретению могут быть соединены с одним или более бактериофагами или фаговыми продуктами, известными из уровня техники. Комбинационные терапевтические средства, охваченные данным изобретением, могут быть в виде одной фармацевтической композиции или же могут вводиться в виде отдельных композиций, но как часть общей схемы лечения.
Фармацевтические композиции по изобретению могут вводиться любым методом, известным из уровня техники, который подходит для введения антибактериального вещества, например, оральным или парентеральным (например, путем ингаляции, внутримышечным, внутривенным или эпидермальным путем). Согласно предпочтительным вариантам фармацевтические композиции по изобретению могут вводиться топическим путем, например, в виде топического состава. Композиции по изобретению могут быть использованы топически для лечения и/или профилактики обычных нозокомиальных инфекций, таких как инфекции в местах хирургических надрезов или инфекций, связанных с применением катетеров или дренажа. Согласно другим вариантам изобретения композиции применяют для лечения бактериальных кожных инфекций или инфекций верхних слоев кожи (например, инфекций, вызванных диабетическими язвами стопы или карбункулов).
Фармацевтические композиции по изобретению могут быть также использованы для традиционно не терапевтических целей, например, в качестве антибактериальных агентов в косметике или в составе спреев или растворов для нанесения на твердые поверхности для предотвращения колонизации бактерий (то есть, как дезинфектанты).
Данное изобретение направлено также на способы скрининга пептидов на антибактериальную активность. Согласно одному из вариантов такой способ включает скрининг заменимых аминокислотных последовательностей длиной из по меньшей мере 6, 10, 15, 20 или 25 остатков, которые кодируются открытыми рамками считывания последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074, для выявления антибактериальной активности, при этом антибактериальная активность оценивается по способности пептидов ингибировать рост бактерий, например, на агаре или в жидкой культуре.
ОПРЕДЕЛЕНИЯ
Применяемый в данной заявке термин "фрагмент" относится к пептиду или полипептиду, содержащему аминокислотную последовательность, состоящую из, по меньшей мере, 5 остатков заменимых аминокислот, по меньшей мере 10 остатков заменимых аминокислот, по меньшей мере 15 остатков заменимых аминокислот, по меньшей мере 20 остатков заменимых аминокислот, по меньшей мере 25 остатков заменимых аминокислот, по меньшей мере 40 остатков заменимых аминокислот, по меньшей мере 50 остатков заменимых аминокислот, по меньшей мере 60 остатков заменимых аминокислот, по меньшей мере 70 остатков заменимых аминокислот, по меньшей мере 80 остатков заменимых аминокислот, по меньшей мере 90 остатков заменимых аминокислот, по меньшей мере 100 остатков заменимых аминокислот, по меньшей мере 125 остатков заменимых аминокислот, по меньшей мере 150 остатков заменимых аминокислот, по меньшей мере 175 остатков заменимых аминокислот, по меньшей мере 200 остатков заменимых аминокислот, по меньшей мере 250 остатков заменимых аминокислот белка. Согласно конкретному варианту фрагмент является функциональным, что означает, что он сохраняет по меньшей мере одну функцию белка, из которого он выделен (например, антимикробную или антибактериальную активность (например, лизирующую киллерную активность)).
Применяемые в данной заявке термины "активные бактериофаги" и "бактериофаговые продукты" относятся к полипептидам, или их фрагментам, вариантам или производным, выделенным из бактериофага по изобретению, причем эти полипептид или его фрагмент, вариант или производное проявляют биологическую функцию или активность, связанную с бактериофагом, из которого они выделены или произведены (например, антимикробную активность или антибактериальную активность, (в том числе лизирующую киллерную активность).
Применяемый в данной заявке термин "выделенный" в отношении пептида, полипептида или белка слияния относится к пептиду, полипептиду или к белку слияния, которые по существу не содержат клеточного материала или загрязняющих белков из клетки или тканевого источника, из которых они получены, или по существу не содержат химических предшественников или других химических веществ, если они получены путем химического синтеза. Выражение "по существу не содержат клеточного материала" относится к препаратам пептида, полипептида или белка слияния, в которых пептид, полипептид или белок слияния отделены от компонентов клеток, из которых они выделены или получены рекомбинантным методом. Таким образом, пептид, полипептид или белок слияния, которые по существу не содержат клеточного материала, представляют собой препараты пептида, полипептида или белка слияния, содержащие менее примерно 30%, 20%, 10% или 5% (на сухой вес) гетерологичного белка (который в данной заявке называется также "загрязняющим белком"). Когда пептид, полипептид или белок слияния получается рекомбинантным путем, он не содержит также культуральной среды, а именно, культуральная среда составляет менее примерно 30%, 20%, 10% или 5% от объема белкового препарата. Когда пептид, полипептид или белок слияния получаются методом химического синтеза, они по существу не содержат химических предшественников или других химических веществ, то есть они отделены от химических предшественников или других химических веществ, которые участвовали в процессе синтеза пептида, полипептида или белка слияния. Соответственно, препараты пептида, полипептида, белка слияния или антитела содержат менее примерно 30%, 20%, 10% или 5% (на сухой вес) химических предшественников или соединений, не являющихся нужными пептидом, полипептидом или белком слияния.
Применяемый в данной заявке термин "выделенные" в отношении молекул нуклеиновой кислоты относится к первой молекуле нуклеиновой кислоты, которая отделена от других молекул нуклеиновой кислоты, которые содержатся в природном источнике первой молекулы нуклеиновой кислоты. Более того, "выделенная" молекула нуклеиновой кислоты, такая как молекула кДНК, при получении этой кислоты рекомбинантным методом по существу не содержит другого клеточного материала или культуральной среды или по существу не содержит химических предшественников или других химических веществ при получении этой кислоты методом химического синтеза, или может не содержать других кДНК или других молекул геномных ДНК, например, когда эта кислота была выделена из других клонов в библиотеке нуклеиновых кислот.
Термин "очищенный(-ая)" означает, что концентрация пептида, полипептида, белка слияния или молекулы нуклеиновой кислоты была заметно увеличена путем осуществления любого способа очистки, включая, но без ограничения, методы колоночной хроматографии, ЖХВР (HPLC), осаждения, электрофореза и т.д., когда частично, по существу почти полностью или полностью удаляются примеси, такие как предшественники или другие химические вещества, участвующие в получении пептида, полипептида, белка слияния или молекулы нуклеиновой кислоты. Специалисту в данной области известно, как определить степень очистки, необходимую для данного применения. Например, термин "выделенный белок", в отношении белка, предназначенного для применения в терапевтических композициях для введения людям, означает, что белок обычно должен иметь высокую степень чистоты в соответствии с регулятивными нормами и эффективными способами получения.
Применяемый в данной заявке термин "производное" в отношении полипептидов относится к полипептиду, который содержит аминокислотную последовательность, которая была изменена путем введения замен, делеций или добавлений аминокислотных остатков. Термин "производное", применяемый в данной заявке, относится также к полипептиду, который был модифицирован, например, путем ковалентного присоединения молекулы любого типа к полипептиду. Например, но без ограничения, полипептид может быть модифицирован, например, путем гликозилирования, ацетилирования, пэгилирования, фосфорилирования, амидирования, дериватизации при помощи известных защитных/блокирующих групп, протеолитического расщепления, связывания с клеточным лигандом или другим белком и т.д. Производное полипептида может быть получено путем химических модификаций способами, известными специалистам в данной области, включая, но без ограничения, специфичное химическое расщепление, ацетилирование, формилирование, метаболический синтез туникамицина и т.д. Кроме того, производное полипептида может содержать остаток одной или более неклассических аминокислот. Производное полипептида обладает такой же или идентичной функцией, что и полипептид, на основе которого он был получен. Термин "полученный на основе", использованный в отношении полипептида, произведенного из организма, может также относиться к выделению полипептида непосредственно из указанного организма (например, бактериальных клеток или фага).
Применяемый в данной заявке термин "клетка-хозяин" относится к конкретной клетке субъекта, трансфецированной молекулой нуклеиновой кислоты, и к потомству или потенциальному потомству такой клетки, которые содержат молекулу нуклеиновой кислоты или ее хромосомную интегрированную версию. Потомство такой клетки может быть не идентичным родительской клетке, трансфецированной молекулой нуклеиновой кислоты, из-за мутаций или влияния окружающей среды, которые могут возникнуть у последующих поколений, или интегрирования молекулы нуклеиновой кислоты в геном клетки-хозяина. При осуществлении экспрессии белков и полипептидов бактериофага клетка-хозяин предпочтительно не является клеткой того же самого вида или штамма бактерий, из которого бактериофаг выделен или культивирован.
Применяемый в данной заявке термин "в комбинации" относится к применению более чем одного профилактического и/или терапевтического агента. Применение термина "в комбинации" не ограничивает порядок, в котором профилактический и/или терапевтический агенты вводятся субъекту, страдающему от болезни или расстройства. Первый профилактический и/или терапевтический агент может быть введен субъекту, нуждающемуся в этом, например, субъекту, страдающему от болезни или расстройства, до (например, за 5 мин, 15 мин, 30 мин, 45 мин, 1 ч, 2 ч, 4 ч, 6 ч, 12 ч, 24 ч, 48 ч, 72 ч, 96 ч, 1 нед, 2 нед, 3 нед, 4 нед, 5 нед, 6 нед, 8 нед или 12 нед), вместе с или после (например, через 5 мин, 15 мин, 30 мин, 45 мин, 1 ч, 2 ч, 4 ч, 6 ч, 12 ч, 24 ч, 48 ч, 72 ч, 96 ч, 1 нед, 2 нед, 3 нед, 4 нед, 5 нед, 6 нед, 8 нед или 12 нед) введения второго профилактического и/или терапевтического агента (отличающегося от первого профилактического и/или терапевтического агента).
Применяемые в данной заявке термины "нуклеиновые кислоты" и "нуклеотидные последовательности" относятся к молекулам однонитевых и двунитевых ДНК и/или РНК или их комбинациям. Применяемый в данной заявке термин "кодируемая нуклеиновой кислотой" относится к аминокислотной последовательности, которая получается в результате трансляции прямой, обратной, комплементарной или обратимо-комплементарной последовательности нуклеиновой кислоты с использованием стандартного генетического кода (то есть, стандартных кодонов (триплетов)), что хорошо известно из уровня техники.
Применяемые в данной заявке термины "профилактический агент" и "профилактические агенты" относятся к бактериофагу и/или полипептидам по изобретению, которые могут быть использованы для профилактики, лечения, сдерживания развития или облегчения одного или более симптомов болезни или расстройства, в частности, болезни или расстройства, связанных с бактериальной инфекцией.
Применяемые в данной заявке термины "терапевтический агент" и "терапевтические агенты" относятся к бактериофагу и/или полипептидам по изобретению, которые могут быть использованы для профилактики, лечения, сдерживания развития или облегчения одного или более симптомов болезни или расстройства, в частности, болезни или расстройства, связанных с бактериальной инфекцией.
Используемый в данной заявке термин "терапевтически эффективное количество" относится к такому количеству терапевтического агента, которое является достаточным для облегчения одного или более симптомов болезни или расстройства, в частности, болезни или расстройства, связанных с бактериальной инфекцией.
Применяемые в данной заявке термины "лечить", "лечение" и "лечащий" относятся к облегчению одного или более симптомов болезни или расстройства, в частности, болезни или расстройства, связанных с бактериальной инфекцией, которое возникает после введения одного или более бактериофагов и/ил полипептидов по изобретению. Как отмечено выше, термин "лечение" и родственные ему термины относятся как к терапевтическому лечению, так и к профилактическим или предупредительным мерам, при этом цель такого лечения состоит в устранении, уменьшении, ослаблении тяжести, замедлении развития или задержке или профилактике симптомов или вызывающей их причины (например, бактериальной инфекции), связанных с патологическим состоянием или расстройством.
Применяемые в данной заявке термины "антибактериальная активность" и "антимикробная активность" в отношении бактериофага, выделенного бактериофагового белка (или его варианта, производного или фрагмента) или бактериофагового продукта используются как взаимозаменяемые для обозначения способности вызывать киллинг и/или ингибировать рост или репродукцию микроорганизма, в частности, бактерий или штаммов бактерий, которые инфицируются бактериофагом. Согласно некоторым вариантам антибактериальная или антимикробная активность оценивается при культивировании бактерий, например, грамположительных бактерий (в том числе, S. aureus), грамотрицательных бактерий (например, К. pneumoniae, A. baumannii, E.coli и/или Р. aeruginosa) или бактерий, которые не классифицируются ни как отрицательные, ни как положительные, стандартными методами (например, в жидкой культуре или на агаровых пластинах), контактировании полученной культуры с бактериофагом или полипептидом согласно изобретению и мониторинге клеточного роста после указанного контактирования. Например, в жидкой культуре бактерии могут вырасти до достижения оптической плотности ("OD"), отражающей среднюю точку на кривой экспоненциального роста культуры; эта культура подвергается действию одного или более бактериофагов или полипептидов по изобретению в одной или более концентрациях и затем осуществляют мониторинг OD относительно контрольной культуры. Уменьшение OD относительно плотности контрольной культуры свидетельствует о проявлении антибактериальной активности бактериофагом и/или полипептидами по изобретению (например, о проявлении лизирующей киллерной активности) против испытуемого образца или вида бактерий и/или штамма в указанной культуре. Подобным образом дают колониям бактерий образоваться на агаровых пластинах, эти пластины подвергают действию бактериофага и/или полипептидов по изобретению и оценивают последующий рост колоний по сравнению с контрольными пластинами. Уменьшение размеров бактериальной колонии или уменьшение общего числа колоний показывает, что бактериофаг и/или полипептид обладают антибактериальной активностью.
Применяемый в данной заявке термин "домен CHAP" относится к консервативному домену амидазы, обнаруженному в нескольких кодированных фагом пептидогликан-гидролазах и обозначает "цистеин, гистидин-зависимые амидогидролазы/пептидазы." См., например, источник Rigden D, et. al., Trends Biochem Sci. 2003 May 28(5): 230-4. Этот домен обнаружен в суперсемействе амидаз, включая GSP-амидазу и пептидогликан-гидролазы. Это семейство обладает по меньшей мере двумя разными типами активности, расщепляющей пептидогликаны: активностью L-мурамил-L-аланинамидазы и активностью D-аланилглицил-эндопептидазы. Домены CHAP обычно содержат консервативные остатки цистеина и гистидина и гидролизуют γ-глутамилсодержащие субстраты. Полагают, что эти цистеиновые остатки являются существенными для проявления активности нескольких указанных амидаз, и их тиольные группы действуют как нуклеофилы в каталитических механизмах всех ферментов, содержащих этот домен. Домены CHAP часто находятся в ассоциации с другими доменами, которые расщепляют пептидогликан, например, действуя вместе с ними при расщеплении специфических субстратов. См., также источник Bateman A, et al., Trends Biochem Sci. 2003 May 28(5): 234-7.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На ФИГУРАХ 1А-1В показана схематически структура генома F391/08, содержащего последовательность нуклеиновой кислоты SEQ ID NO:1. Открытые рамки считывания ("ORF"), примерно находящиеся в геноме 113 Т.П.О., показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на ФИГУРЕ, показана также в табличной форме на ФИГУРЕ 2.
ФИГУРЫ 2A-2II: Характеристики генома F391/08 бактериофага, включая генные продукты и указание предполагаемых функций. На указанных ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции. ORF 1-172, перечисленные на ФИГУРЕ 2, кодируют аминокислотные последовательности SEQ ID NO:5-176, соответственно.
На ФИГУРЕ 3 показана схематически организация генома F394/08, содержащего аминокислотную последовательность SEQ ID NO:2. Открытые рамки считывания ("ORF"), находящиеся примерно в геноме 31Т.П.О. показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на этой Фигуре, показана также в табличной форме на ФИГУРЕ 4.
ФИГУРЫ 4А-4К: Характеристики генома F394/08 бактериофага, включая генные продукты и указание предполагаемых функций. На указанных ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции. ORF 1-47, перечисленные на ФИГУРЕ 4, кодируют аминокислотные последовательности SEQ ID NO:177-223, соответственно.
ФИГУРЫ 5А-5В: показана схематически структура генома F488/08, содержащего последовательность нуклеиновой кислоты SEQ ID NO:3. Открытые рамки считывания ("ORF"), находящиеся примерно в геноме 167 Т.П.О. показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на этой ФИГУРЕ, показана также в табличной форме на ФИГУРЕ 6.
ФИГУРЫ 6A-6DDD: Характеристики генома F488/08 бактериофага, включая генные продукты и указание предполагаемых функций. На этих ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции. ORF 1-283, перечисленные на Фигуре 6, кодируют аминокислотные последовательности SEQ ID NO:224-506, соответственно.
ФИГУРА 7: показана схематически структура генома F510/08, содержащего последовательность нуклеиновой кислоты SEQ ID NO:4. Открытые рамки считывания ("ORF"), находящиеся примерно в геноме 43 Т.П.О. показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на этой ФИГУРЕ, показана также в табличной форме на ФИГУРЕ 8.
ФИГУРЫ 8A-8S: характеристики генома F510/08 бактериофага, включая генные продукты и указание предполагаемых функций. На ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции. ORF 1-53, перечисленные на ФИГУРЕ 8, кодируют аминокислотные последовательности SEQ ID NO:507-559, соответственно.
ФИГУРА 9: показана схематически структура генома F44/10, содержащего последовательность нуклеиновой кислоты SEQ ID NO:560. Открытые рамки считывания ("ORF"), находящиеся примерно в геноме 137Т.П.О. показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на этой ФИГУРЕ, показана также в табличной форме на ФИГУРЕ 10.
ФИГУРЫ 10A-10QQ: характеристики генома F44/10 бактериофага, включая генные продукты и указание предполагаемых функций. На ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции.
ORF 1-216, включая ORF 1a, 1b, 82a, 82b, 82c, 114a и 114b, перечисленные на ФИГУРЕ 10, кодируют аминокислотные последовательности SEQ ID NO: 561-780, соответственно.
ФИГУРА 11: показана схематически структура генома F3 87/08, содержащего последовательность нуклеиновой кислоты SEQ ID NO: 781. Открытые рамки считывания ("ORF"), находящиеся примерно в геноме 167Т.П.О. показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на этой ФИГУРЕ, показана также в табличной форме на ФИГУРЕ 12.
ФИГУРЫ 12A-12UUU: характеристики генома F387/08 бактериофага, включая генные продукты и указание предполагаемых функций. На этих ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции.
ORF 1-292, перечисленные на ФИГУРЕ 12, кодируют аминокислотные последовательности SEQ ID NO: 782-1073, соответственно.
ФИГУРЫ 13А-13В: показана схематически структура генома F125/10, содержащего последовательность нуклеиновой кислоты SEQ ID NO: 1074. Открытые рамки считывания ("ORF"), находящиеся примерно в геноме 145Т.П.О. показаны стрелками и пронумерованы цифрами черного цвета. Направление стрелки показывает направление транскрипции. Цветовые обозначения: черный цвет - ORF, для которых продукты функционального назначения могут быть получены на основе известных функций гомологичных белков; серый цвет - ORF, кодирующие продукты, которые похожи на белки с неизвестной функцией; незакрашенные ORF, кодирующие белки, которые не гомологичны белкам, содержащимся в доступных базах данных. ORF с предсказанной функциональностью также перечислены на этой ФИГУРЕ. Информация, приведенная на этой ФИГУРЕ, показана также в табличной форме на ФИГУРАХ 14A-14ZZZ.ФИГУРЫ 14A-14ZZZ: характеристики генома F 125/10 бактериофага, включая генные продукты и указание предполагаемых функций. На этих ФИГУРАХ приведен перечень ORF генома и для каждой ORF указано: (i) ее положение в геноме, (ii) кодирующая аминокислотная последовательность, (iii) перечень гомологичных белков и консервативных доменов в кодированном полипептиде и (iv) указание предполагаемой функции. ORF 1b-221, 1a, перечисленные на этой Фигуре, кодируют аминокислотные последовательности SEQ ID NO:1075-1300, соответственно, включая 36а и 36b, 68а и 68b, и 153а и 153b.
ФИГУРЫ 15A-15III: нуклеотидная последовательность генома бактериофага F391/08 (SEQ ID NO:1).
ФИГУРЫ 16A-16Q: нуклеотидная последовательность генома бактериофага F394/08 (SEQ ID NO:2).
Фигуры 17А-17КККК: нуклеотидная последовательность генома бактериофага F488/08 (SEQ ID NO:3).
ФИГУРЫ 18А-18Х: нуклеотидная последовательность генома бактериофага F510/08 (SEQ ID NO:4).
ФИГУРЫ 19A-19UUU: нуклеотидная последовательность генома бактериофага F44/10 (SEQ ID NO:560).
ФИГУРЫ 20А-20КККК: нуклеотидная последовательность генома бактериофага F387/08 (SEQ ID NO:781).
ФИГУРЫ 21A-21ZZZ: нуклеотидная последовательность генома бактериофага F125/10 (SEQ ID NO:1074).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Данное описание предусматривает выделенные бактериофаги и их выделенные полипептиды, обладающие антибактериальной активностью против одного или более видов или штаммов нозокомиальных патогенов Klebsiella pneumoniae, Acinetobacter baumannii, Escherichia coli, Pseudomonas aeruginosa и S. aureus. Согласно одному из вариантов предусмотрены выделенные бактериофаги или полипептиды, которые проявляют антибактериальную или антимикробную активность против резистентных к метициллину штаммов S. aureus (MRSA). Кроме того, бактериофаги и полипептиды согласно данному изобретению могут проявлять антибактериальную или антимикробную активность в отношении одного или более видов или штаммов патогенных бактерий, включая, но без ограничения, S. epidermidis, S. auricularis, S. capitis, S. haemolyticus, S. hominis, S. saprophyticus, S. simulans, S. xylosis, Micrococcus luteus, Bacilus subtilis, B. pumilus, E. hirae и E. avium.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F391/08, который может быть нацелен на ряд штаммов бактерий вида Klebsiella, включая К. pneumoniae и К. oxytoca. Схематическая организация генома F391/08, включающего последовательность нуклеиновой кислоты SEQ ID NO:1, показана на ФИГУРЕ 1. Открытые рамки считывания (ORF) в геноме F391/08 представлены на ФИГУРЕ 2. Показаны также положения ORF в геноме, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-172, перечисленные на ФИГУРЕ 2, кодируют аминокислотные последовательности SEQ ID NO:5-176, соответственно.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:781. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F387/08, который может быть нацелен на ряд штаммов бактерий вида Klebsiella, включая К. pneumoniae и К. oxytoca. Схематическая организация генома F387/08, включающего последовательность нуклеиновой кислоты SEQ ID NO:781, показана на ФИГУРЕ 11. Открытые рамки считывания (ORF) в геноме F387/08 представлены на ФИГУРЕ 12. Показаны также положения ORF в геноме F387/08, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-292, перечисленные на Фигуре 12, кодируют аминокислотные последовательности SEQ ID NO:782-1073, соответственно.
Бактерия Klebsiella pneumonia представляет собой неподвижную грамотрицательную бактерию палочковидной формы, обнаруженную в нормальной флоре полости рта, кожи и кишечника. Как инкапсулированный факультативный анаэроб, бактерия также имеется в природе в почве и около 30% штаммов могут удерживать азот в анаэробных условиях. Клинически, эта бактерия является наиболее важным членом рода Klebsiella семейства Enterobacteriaceae и также тесно связана с видом К. oxytoca. Инфекции, вызванные Klebsiella, возникают у людей с ослабленной иммунной системой из-за неправильного питания, например, у алкоголиков и диабетиков. Бактерия Klebsiella является также условно патогенным микроорганизмом у пациентов с хронической легочной болезнью, энтеральной патогенностью, атрофией слизистой оболочки носа и риносклеромой. С течением времени появляются новые резистентные к антибиотикам штаммы К. pneumonia и все чаще появляются инфекции, вызванные нозокомиальными бактериями, например, вследствие контакта с загрязненным инструментарием.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F394/08, который может быть нацелен на ряд штаммов бактерий вида Acinetobacter, включая A. baumanni, A. calcoaceticus и A. Iwoffi. Схематическая организация генома F391/08, включающего последовательность нуклеиновой кислоты SEQ ID NO:2, показана на ФИГУРЕ 3. Открытые рамки считывания (ORF) в геноме F394/08 представлены на ФИГУРЕ 4. Показаны также положения ORF в геноме, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-47, перечисленные на ФИГУРЕ 4, кодируют аминокислотные последовательности SEQ ID NO:177-223, соответственно.
Acinetobacter baumannii представляет собой вид бактерий, которые вызывают ряд серьезных клинических инфекций, особенно у индивидуумов с нарушенным иммунитетом. А. baumannii является плеоморфной аэробной грамотрицательной палочковидной бактерией, которая обычно выделяется из больничной среды и из организма госпитализированных пациентов. Бактерия часто попадает в открытые раны, катетеры или дыхательные трубки. А. baumannii обычно образует колонии в водной среде и часто культивируется в мокроте госпитализированных пациентов или в секреции органов дыхания, в ранах и в моче. В больнице A. baumannii обычно образует колонии в растворах для промывки и в растворах для внутривенного введения. Известно также, что эта бактерия устойчива к действию многих антибиотиков, и количество нозокомиальных инфекций, вызванных A. Baumanni, в последние годы растет.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F488/08, который может быть нацелен на ряд штаммов бактерий вида Escherichia, включая Е.coli. Схематическая организация генома F488/08, включающего последовательность нуклеиновой кислоты SEQ ID NO:3, показана на ФИГУРЕ 5. Открытые рамки считывания (ORF) в геноме F488/08 представлены на ФИГУРЕ 6. Показаны также положения ORF в геноме, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-283, перечисленные на ФИГУРЕ 6, кодируют аминокислотные последовательности SEQ ID NO:224-506, соответственно.
Бактерия Escherichia coli представляет собой грамотрицательную палочковидную бактерию, которая обычно обнаруживается в нижней части кишечника млекопитающих, являясь основной факультативной анаэробной бактерией желудочно-кишечного тракта. Большая часть штаммов Е.coli является безвредной и может входить в состав нормальной флоры кишечника, где они могут быть благоприятными для клеток-хозяев, например, за счет продуцирования витамина К2 и/или предотвращения появления патогенных бактерий в кишечнике. Однако некоторые вирулентные штаммы Е.coli могут вызывать пищевое отравление, обычно проявляющееся как периодический понос. Другие вирулентные штаммы, такие как 0157:Н7, могут вызывать серьезные заболевания и даже смерть у пожилых людей, очень молодых людей или людей с плохим иммунитетом. Штаммы, такие как 0157:Н7, а также 0121 и 0104:Н21, продуцируют потенциально летальные токсины. Вирулентные штаммы Е.coli могут также вызывать гастроэнтерит, инфекции мочевого тракта и неонатальный менингит, а также, в более редких случаях, гемолитико-уремический синдром (BUS), перитонит, мастит, септицемию и пневмонию, вызванную грамотрицательным и бактериями. Кроме того, если бактерии Е.coli покидают кишечный тракт через перфорацию в тканях (например, из лопнувшего аппендицита и лопнувшей язвы или вследствие хирургической ошибки) и попадают в брюшинную полость, они обычно вызывают перитонит, который без неотложного лечения может стать фатальным. При воспалительных заболеваниях кишечника, при болезни Крона и язвенном колите, в слизистой оболочке кишечника также наблюдаются Е.Coli.
Антибиотики, которые могут быть использованы при лечении инфекции, вызванной Е.coli, включают амоксициллин, а также другие полусинтетические пенициллины, многие цефалоспорины, карбапенемы, азтреонам, триметоприм-сульфаметоксазол, ципрофлоксацин, нитрофурантоин и аминогликозиды. Тем не менее, являясь грамотрицательными организмами, Е.coli резистентны ко многим антибиотикам, которые являются эффективными против грамположительных организмов, такая резистентность к антибиотикам представляет собой растущую проблему. Например, резистентность к бета-лактамным антибиотикам в последнее время стала особенной проблемой, так как штаммы бактерий, которые продуцируют бета-лактамазы расширенного спектра, стали более распространенными. Эти ферменты бета-лактамазы могут превращать многие, если не все, пенициллины и/или цефалоспорины в терапевтически неэффективные антибиотики. Штаммы Е.coli, продуцирующие бета-лактамазы расширенного спектра, которые резистентны ко многим антибиотикам, приводят к возникновению инфекций, которые особенно трудно поддаются лечению.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F510/08, который может быть нацелен на ряд штаммов бактерий вида Pseudomonas species, including P. aeruginosa. Схематическая организация генома F510/08, включающего последовательность нуклеиновой кислоты SEQ ID NO:4, показана на ФИГУРЕ 7. Открытые рамки считывания (ORF) в геноме F510/08 представлены на ФИГУРЕ 8. Показаны также положения ORF в геноме, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-53, перечисленные на ФИГУРЕ 8, кодируют аминокислотные последовательности SEQ ID NO:507-559, соответственно.
Pseudomonas aeruginosa представляет собой распространенную грамотрицательную палочковидную бактерию, обнаруженную в почве, воде, бактериальной флоре кожи и в созданной человеком окружающей среде. Она прекрасно разрастается не только в обычной среде, но также при наличии небольшого количества кислорода как факультативный анаэроб и может инфицировать поврежденные ткани или индивидуумов с ослабленным иммунитетом. Когда такие колонии образуются в органах, имеющих первостепенное значение, таких как легкие, мочевой тракт и почки, результаты могут быть фатальными. Поскольку эта бактерия размножается на поверхностях, ее находят также на медицинском оборудовании и внутри него, таком как катетеры, что вызывает перекрестные инфекции в больницах и клиниках. Р. aeruginosa является одним из многих релевантных условно-патогенных, нозокомиальных патогенов, было установлено, что один из десяти приобретенных в больнице видов инфекций вызван именно Pseudomonas. P. aeruginosa является наиболее распространенной причиной инфекций от ожоговых травм и инвазивным микробом, наиболее часто встречающимся в медицинских инструментах, таких как катетеры.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F44/10, который может быть нацелен на ряд штаммов бактерий вида Staphylococcus species, including S. aureus. Схематическая организация генома F44/10, включающего последовательность нуклеиновой кислоты SEQ ID NO:560, показана на ФИГУРЕ 9. Открытые рамки считывания (ORF) в геноме F44/10 представлены на ФИГУРЕ 10. Показаны также положения ORF в геноме, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-216, включая 1a, 1b, 82a, 82b, 82с, 114а и 114b, перечисленные на ФИГУРЕ 10, кодируют аминокислотные последовательности SEQ ID NO:561-780, как показано на этой ФИГУРЕ.
Согласно некоторым вариантам данное изобретение предусматривает бактериофаг, содержащий геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1074. Конкретным примером согласно данному варианту изобретения является выделенный бактериофаг F125/10, который может быть нацелен на ряд штаммов бактерий вида Staphylococcus species, including S. aureus. Схематическая организация генома F125/10, включающего последовательность нуклеиновой кислоты SEQ ID NO:1074, показана на ФИГУРЕ 13. Открытые рамки считывания (ORF) в геноме F125/10 представлены на ФИГУРЕ 14. Показаны также положения ORF в геноме, аминокислотные последовательности, кодированные ORF, гомологичные или похожие белки и консервативные домены в кодированном полипептиде и предполагаемые функции. ORF 1-221, включая 1a, 1b, 36a, 36b, 68а, 68b, 153a и 153b, перечисленные на ФИГУРЕ 14, кодируют аминокислотные последовательности SEQ ID NO:1075-1300, как показано на ФИГУРЕ.
Staphylococcus aureus представляет собой грамположительную факультативную бактерию сферической формы, которая растет в виде гроздеподобных кластеров с характерным золотистым цветом, и является наиболее распространенной причиной стафилококковых инфекций. Часто она входит в состав бактериальной флоры человеческой кожи и отвечает за ряд инфекций, включая сыпь, карбункулы, токсический некроз эпидермиса, пневмонию, гастроэнтерит, менингит, остеомиелит, эндокардит, синдром токсического шока, бактериемию и сепсис. Она остается одной из пяти наиболее распространенных причин нозокомиальных инфекций, часто вызывая раневые инфекции после хирургического вмешательства. Было подсчитано, что около 50000 пациентов в американских больницах подхватывают стафилококковую инфекцию. Особенную проблему представляют штаммы Staphylococcus aureus, резистентные к метициллину (MRSA). MRSA оставались нечастой причиной возникновения инфекций в больнице до 90-х годов 20-го века, когда произошло резкое увеличение количества случаев заболеваний, преобладающих в больничной обстановке, где теперь они считаются эндемическими, особенно в Соединенном Королевстве. См., Johnson A.P., et al., J. Antimicrobial Chemotherapy, 48(1): 143-144 (2001). S. aureus оказалась очень выносливой бактерией и в одном исследовании было показано, что она может выжить на поверхности полиэфира в течение почти трех месяцев, такой полиэфир является основным материалом, применяемым для изготовления разделительных штор в больнице. См., Neely, A.N., et al., J. Clin. Microbiol., 38(2): 724-726 (2000).
16 сентября 2011 г. в коллекции NCIMB Limited (Национальной коллекции промышленных, пищевых и морских бактерий), расположенной в Ferguson Building, Craibstone Estate, Bucksbum, Aberdeen, AB21 9YA, Scotland, Соединенное Королевство, по условиям Будапештского договора о международном признании депонирования микроорганизмов для целей патентной процедуры (("Будапештский договор") были депонированы следующие указанные ниже организмы, и NCIMB присвоила им следующие номера доступа для поддерживаемых культур: штамм-хозяин Pseudomonas aeruginosa 433/07 В2, NCIMB 41861; штамм-хозяин Staphylococcus aureus 743/06 B1, NCIMB 41862; штамм-хозяин Acinetobacter baumannii 1305/05 B3, NCIMB 41863; фаг F770/05 Pseudomonas aeruginosa, NCIMB 41864; фаг F1245/05 Acinetobacter baumannii, NCIMB 41865; фаг F125/10 Staphylococcus aureus, NCIMB 41866; фаг F44/10 Staphylococcus aureus, NCIMB 41867; и фаг F510/08 Pseudomonas aeruginosa, NCIMB 41868, все из которых включены в данную заявку посредством отсылок.
Согласно некоторым вариантам бактериофаг по изобретению содержит или состоит из генома, содержащего последовательность, идентичную по меньшей мере на 85%, 90%, 95%, 96%, 97%, 98% или по меньшей мере на 99% последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074, при этом указанный бактериофаг проявляет по меньшей мере один вид биологической активности, например, антимикробную или антибактериальную активность (например, лизирующую киллерную активность) одного или более бактериофагов F391/08, F394/08, F488/08, F510/08, F387/08, FF44/10 и F125/10. Альтернативно или в дополнение, бактериофаг по изобретению может содержать геном, содержащий функциональный фрагмент последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074, включая последовательности любой из открытых рамок считывания, показанных на ФИГУРАХ 2, 4, 6, 8, 10, 12 и/или 14.
Данное изобретение предусматривает также выделенные бактерии, инфицированные одним или более бактериофагами по изобретению. Согласно некоторым вариантам данное изобретение предусматривает выделенные бактерии К. pneumonia, инфицированные бактериофагом, содержащим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1 и/или SEQ ID NO:781. Согласно некоторым вариантам данное изобретение предусматривает выделенные бактерии A. baumannii, инфицированные бактериофагом, содержащим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2. Согласно некоторым вариантам данное изобретение предусматривает выделенные бактерии Е.coli, инфицированные бактериофагом, содержащим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3. Согласно некоторым вариантам данное изобретение предусматривает выделенную бактерию Р. aeruginosa, инфицированную бактериофагом, содержащим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4. Согласно некоторым вариантам данное изобретение предусматривает выделенную бактерию S. Aureus, инфицированную бактериофагом, содержащим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560 и/или SEQ ID NO:1074.
Настоящее изобретение предусматривает способы получения и выделения бактериофага, имеющего геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074.
Согласно некоторым вариантам данное изобретение предусматривает способы получения и выделения бактериофага, имеющего геном, включающий или состоящий из последовательности нуклеиновой кислоты из SEQ ID NO:1 и/или SEQ ID NO:781, включающие (i) получение культуры К. pneumoniae, (ii) ее инфицирование бактериофагом, имеющим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2; (iii) культивирование клеток до появления сильного лизиса культуры; и (iv) выделение бактериофага из этой культуры. Согласно другим вариантам данное изобретение предусматривает способ получения и выделения бактериофага, имеющего геном, который содержит или состоит из последовательности нуклеиновой кислоты SEQ ID NO:3, включающий (i) получение культуры Е.coli, (ii) ее инфицирование бактериофагом, имеющим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3; (iii) культивирование клеток до появления сильного лизиса культуры; и (iv) выделение бактериофага из этой культуры. Согласно другим вариантам данное изобретение предусматривает способ получения и выделения бактериофага, имеющего геном, который содержит или состоит из последовательности нуклеиновой кислоты SEQ ID NO:4, включающий (i) получение культуры Р. aeruginosa, (ii) ее инфицирование бактериофагом, имеющим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4; (iii) культивирование клеток до появления сильного лизиса культуры; и (iv) выделение бактериофага из этой культуры.
Согласно другим вариантам данное изобретение предусматривает способ получения и выделения бактериофага, имеющего геном, который содержит или состоит из последовательности нуклеиновой кислоты SEQ ID NO:560 и/или SEQ ID NO:1074, включающий (i) получение культуры S. aureus, (ii) ее инфицирование бактериофагом, имеющим геном, включающий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560 и/или SEQ ID NO:1074; (iii) культивирование клеток до появления сильного лизиса культуры; и (iv) выделение бактериофага из этой культуры.
Бактериофаг может быть выделен из бактериального образца с помощью любого метода, описанного в данной заявке или известного из уровня техники (см., например, Carlson, "Working with bacteriophage: common techniques and methodological approaches," In, Kutter and Sulakvelidze (Eds) Bacteriophage: Biology and Applications, 5th ed. CRC Press (2005); этот источник полностью включен в данную заявку посредством отсылки).
Данное изобретение предусматривает также полипептиды, выделенные из бактериофага по изобретению. Выделенные полипептиды могут быть бактериофаговыми белками полной длины или могут быть фрагментами, вариантами или производными бактериофаговых белков при условии, что указанные фрагмент, вариант или производное проявляют по меньшей мере один вид биологической активности, характерной для бактериофага или полипептида, из которого они произведены.
Согласно некоторым вариантам полипептиды по изобретению выделены из бактериофага F387/08 или F391/08 (который обычно инфицирует К. pneumoniae), бактериофага F394/08 (который обычно инфицирует A. baumannii), бактериофага F488/08 (который обычно инфицирует Е.coli), бактериофага F510/08 (который обычно инфицирует Р. aeruginosd) или бактериофагов F44/10 или F 125/40 (которые обычно инфицируют S. aureus).
Согласно конкретным вариантам полипептид по изобретению представляет собой лизин, выделенный из бактериофага, имеющего геном, содержащий или состоящий из SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074 (например, бактериофагов F391/08, F394/08, F488/08, F510/08, F44/10, F387/08 или or F125/10, соответственно). Согласно конкретным вариантам полипептид по изобретению представляет собой лизиновый белок, например, эндолизин или хвостовой лизин, содержащий аминокислотную последовательность, включающую или состоящую из SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:1216 или SEQ ID NO:1261. Предсказанные функции указанных лизинов включают, например, Ig-подобный вирионный белок (SEQ ID NO:20), гидролазу клеточной стенки (SEQ ID NO:80), эндолизин; N-ацетилмурамил-L-аланинамидазу (SEQ ID NO:192), растворимый лизоцим (SEQ ID NO:282), Т4-подобный лизоцим (SEQ ID NO:547), эндолизин (SEQ ID NO:556), лямбда-Rzl-подобный белок (SEQ ID NO:557), эндолизин (SEQ ID NO:598), эндолизин (SEQ ID NO:1216) и хвостовой лизин (SEQ ID NO:1261).
Согласно другим вариантам выделенный полипептид по изобретению представляет собой фрагмент, вариант или производное эндолизина или лизина, выделенного из бактериофага по изобретению, при этом эти фрагмент, вариант или производное проявляют по меньшей мере один вид биологической активности, предпочтительно, антибактериальной активности (например, лизирующей киллерной активности), характерной для эндолизина, лизина или бактериофага, из которого они выделены или произведены. Соответственно, согласно некоторым вариантам изобретение предусматривает выделенные полипептиды, которые представляют собой фрагменты, варианты или производные эндолизинов или лизинов, которые выделены из бактериофага по изобретению, при этом эти фрагменты, варианты или производные проявляют антимикробную или антибактериальную активность (например, лизирующую киллерную активность), в отношении одного или более видов бактерий К. pneumoniae, A. baumannii, E.coli, P. aeruginosa или S. aureus. Согласно другим вариантам выделенные полипептиды представляют собой фрагменты, варианты или производные эндолизинов или лизинов, которые выделены из бактериофага по изобретению, которые проявляют антимикробную или антибактериальную активность (например, лизирующую киллерную активность), в отношении одного или более видов бактерий, отличающихся от К. pneumoniae, A. baumannii, E.coli, P. aeruginosa или S. aureus. Согласно некоторым вариантам полипептид по изобретению включает или состоит из аминокислотной последовательности SEQ ID NO:20 и/или SEQ ID NO:80 или ее фрагмента, варианта или производного, при этом этот полипептид проявляет антимикробную или антибактериальную активность в отношении одного или более штаммов К. pneumoniae, например, против бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1. Согласно другим вариантам полипептид по изобретению включает или состоит из аминокислотной последовательности SEQ ID NO:192 или ее фрагмента, варианта или производного, при этом этот полипептид проявляет антимикробную или антибактериальную активность в отношении одного или более штаммов A. baumannii, например, против бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2. Согласно другим вариантам полипептид по изобретению включает или состоит из аминокислотной последовательности SEQ ID NO:282 или ее фрагмента, варианта или производного, при этом этот полипептид проявляет антимикробную или антибактериальную активность в отношении одного или более штаммов E.coli,, например, в отношении бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3. Согласно другим вариантам полипептид по изобретению включает или состоит из аминокислотной последовательности SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557 или ее фрагмента, варианта или производного, при этом этот полипептид проявляет антимикробную или антибактериальную активность в отношении одного или более штаммов Р. aeruginosa, например, против бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4. Согласно другим вариантам полипептид по изобретению включает или состоит из аминокислотной последовательности SEQ ID NO:598 или ее фрагмента, варианта или производного, при этом этот полипептид проявляет антимикробную или антибактериальную активность в отношении одного или более штаммов S. aureus, например, в отношении бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560. Согласно другим вариантам полипептид по изобретению включает или состоит из аминокислотной последовательности SEQ ID NO:1216 и/или SEQ ID NO:1261 или ее фрагмента, варианта или производного, при этом этот полипептид проявляет антимикробную или антибактериальную активность в отношении одного или более штаммов S. aureus, например, в отношении бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1074.
Согласно некоторым вариантам полипептид по изобретению содержит или состоит из домена CHAP, выделенного из эндолизина или лизина бактериофагов F387/08, F391/08, F394/08, F488/08, F510/08, F44/10 или F125/10. Выделенные домены CHAP, как это было показано, сохраняют антибактериальную активность (например, лизирующую киллерную активность) эндолизина или лизина, из которых они произведены; домены CHAP могут быть идентифицированы и выделены стандартными методами, известными из уровня техники (см., например, источники Rigden et al., 2003, Trends Biochem. Sci. 28:230-234; Bateman et al., 2003, Trends Biochem. Sci. 28:234-237, каждый из которых полностью включен в данную заявку посредством отсылок). Согласно конкретным вариантам полипептид по изобретению содержит или состоит из домена CHAP, выделенного из полипептида, имеющего аминокислотную последовательность SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:1216 или SEQ ID NO:1261. Согласно другим вариантам данное изобретение предусматривает фрагмент, вариант или производное домена CHAP, выделенного из эндолизина или лизина бактериофага F387/08, F391/08, F394/08, F488/08, F510/08, F44/10, F125/10, при этом эти фрагмент, вариант или производное проявляют по меньше мере один вид биологической активности, например, лизирующую киллерную активность, домена CHAP, из которого они произведены.
Согласно некоторым вариантам полипептид по изобретению содержит или состоит из хвостового белка (например, хвостового компонента, хвостового волоконного белка, хвостового белка, связанного с адсорбцией, белка рулетки хвостового отростка, субъединицы белка клиновидной базальной пластинки) или его фрагмента, варианта или производного, выделенных из бактериофага, который имеет геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074 (например, бактериофага F391/08, F394/08, F488/08, F510/08, F44/10, F387/08 или F125/10, соответственно), при этом хвостовой белок или его фрагмент, вариант или производное обладает биологической функцией, связанной с бактериофагом, из которого он выделен, например, антимикробной активностью или антибактериальной активностью (например, лизирующей киллерной активностью). Согласно конкретным вариантам антимикробная или антибактериальная активность хвостового белка направлена в отношении по меньшей мере одного или более видов или штаммов бактерий К. pneumoniae, A. baumannii, Е.coli, Р. Aeruginos или S. aureus. Согласно конкретным вариантам полипептид по изобретению представляет собой хвостовой белок, содержащий аминокислотную последовательность, содержащую или состоящую из SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629; SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266. Согласно другим вариантам выделенный полипептид по изобретению является фрагментом, вариантом или производным аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629; SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266, при этом указанные фрагмент, вариант или производное проявляют по меньшей мере один вид биологической активности или функции бактериофага, из которого они выделены или произведены, например, антимикробную активность или антибактериальную активность (например, лизирующую киллерную активность). Согласно предпочтительным вариантам по меньшей мере один вид биологической активности или функция фрагмента, варианта или производного направлена против одного или более штаммов К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и S. aureus.
Предсказанные функции указанных хвостовых белков включают, например, рецептор-связывающий хвостовой белок (SEQ ID NO:15), основной хвостовой белок (SEQ ID NO:26), минорный хвостовой белок (SEQ ID NO:26), минорный хвостовой белок (SEQ ID NO:27), порообразующий белок наконечника молекулы (SEQ ID NO:30), хвостовой белок (SEQ ID NO:32-33), минорный хвостовой белок (SEQ ID NO:34), белок хвостового отростка фага (SEQ ID NO:35), белок чехла хвостового отростка (SEQ ID NO:180), белок рулетки хвостового отростка (SEQ ID NO:183), хвостовой белок (SEQ ID NO:185), фибриллярный хвостовой белок (SEQ ID NO:190), белок белковой трубки хвостового отростка (SEQ ID NO:231), мономер чехла хвостового отростка (SEQ ID NO:232), стабилизирующий и завершающий белок чехла хвостового отростка (SEQ ID NO:235), короткие нити хвостового отростка (SEQ ID NO:239), завершающий и стабилизирующий белок клиновидной базальной пластинки (SEQ ID NO:240-241), фибриллярный хвостовой завершающий белок кармана базальной пластинки (SEQ ID NO:242), субъединицу белка клиновидной базальной пластинки (SEQ ID NO:243), инициатор клиновидной базальной пластинки (SEQ ID NO:244), клиновидную базальную пластинку (SEQ ID NO:245), лизоцим субъединицы хаба базальной пластинки хвостового отростка, стержень, прокалывающий клетку (SEQ ID NO:248), завершение клиновидной базальной пластинки (SEQ ID NO:249), завершающий стабилизирующий белок чехла хвостового отростка (SEQ ID NO:252), шапероны сборки длинных и коротких хвостовых нитей (SEQ ID NO:254), фибриллярный хвостовой белок (SEQ ID NO:433), фибриллярный хвостовой белок (SEQ ID NO:434), длинные хвостовые нити шарнирного соединения (SEQ ID NO:435), шарнир хвостовой нити (SEQ ID NO:436), проксимальная субъединица нити хвостового отростка (SEQ ID NO:437), белок инициатора трубки базальной пластинки (SEQ ID NO:489), базальную пластинку (SEQ ID NO:490), субъединицу хаба базальной пластинки, детерминатор длины хвоста (SEQ ID NO:491), субъединицу дистального хаба базальной пластинки (SEQ ID NO:492), субъединицу хаба базальной пластинки (SEQ ID NO:493), катализатор сборки хабов базальной пластинки (SEQ ID NO:494), субъединицу хаба базальной пластинки (SEQ ID NO:495), субъединицу конусовидной базальной пластинки (SEQ ID NO:496), белок трубки хвостового отростка (SEQ ID NO:544-545), хвостовой фибриллярный белок (SEQ ID NO:549 и SEQ ID NO:551), основной белок чехла хвостового отростка (SEQ ID NO:629); основной хвостовой белок (SEQ ID NO:686); белок трубки хвостового отростка (SEQ ID NO:789); фибритин (SEQ ID NO:796); короткие хвостовые нити (SEQ ID NO:797); завершающий и стабилизирующий белок конца молекулы клиновидной базальной пластинки (SEQ ID NO:798); субъединицу конусовидной базальной пластинки и наконечник хвостового отростка (SEQ ID NO:799); фибриллярный линкер конусовидной базальной пластинки хвостового отростка (SEQ ID NO:800); субъединицу хаба базальной пластинки и лизоцим (SEQ ID NO:806); лизоцим (SEQ ID NO:854); холин (SEQ ID NO:999); катализатор сборки дистальных длинных хвостовых нитей (SEQ ID NO:1000); L-образный белок нитей хвостового отростка (SEQ ID NO:1001); шарнирный линкер дистального линкера длинных хвостовых нитей (SEQ ID NO:1002); шарнирный линкер проксимального линкера длинных хвостовых нитей (SEQ ID NO:1003); проксимальную субъединицу длинных хвостовых нитей (SEQ ID NO:1004); инициатор трубки базальной пластинки хвостового отростка (SEQ ID NO:1053); завершение трубки базальной пластинки (SEQ ID NO:1054); субъединицу хаба базальной пластинки, детерминатор длины хвостового отростка (SEQ ID NO:1055); субъединицу дистального хаба базальной пластинки (SEQ ID NO:1056); субъединицу хаба базальной пластинки (SEQ ID NO:1057 и 1059); катализатор сборки хабов базальной пластинки (SEQ ID NO:1058); субъединицу конусовидной базальной пластинки (SEQ ID NO:1058); субъединицу конусовидной базальной пластинки (SEQ ID NO:1060); основной хвостовой белок (SEQ ID NO:1077); холин (SEQ ID NO:1217); основной белок чехла хвостового отростка (SEQ ID NO:1250); и белок базальной пластинки (SEQ ID NO:1266).
Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30 или SEQ ID NO:32-35, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена против одного или более штаммов К. pneumoniae.
Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004 или SEQ ID NO:1053-1060, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:781, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена в отношении одного или более штаммов К. pneumoniae. Согласно другим вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185 или SEQ ID NO:190, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий ли состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена против одного или более штаммов А. baumannii.
Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-495 или SEQ ID NO:496, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена в отношении одного или более штаммов Е.coli. Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549 или SEQ ID NO:551, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена в отношении одного или более штаммов Р. aeruginosa. Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:629 или SEQ ID NO:686, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена в отношении одного или более штаммов S. aureus. Согласно некоторым вариантам данное изобретение охватывает вариант, фрагмент или производное аминокислотной последовательности SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261 или SEQ ID NO:1266, которые обладают биологической функцией, связанной с бактериофагом, включающим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1074, например, антимикробной или антибактериальной активностью (например, лизирующей киллерной активностью), причем эта функция направлена в отношении одного или более штаммов S. aureus.
Согласно некоторым вариантам выделенный полипептид по изобретению представляет собой вариант бактериофагового полипептида, при этом указанный вариант включает или состоит из аминокислотной последовательности, которая идентична по меньшей мере на 60%, 65%, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более второй аминокислотной последовательности с той же длиной (то есть состоящей из такого же количества остатков), при этом вторая аминокислотная последовательность является SEQ ID NO:15, SEQ ID NO:20, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:80, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:192, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:282, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:547, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1216, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1261, SEQ ID NO:1266 и/или ее фрагментом, и этот вариант обладает по меньшей мере одной биологической функцией или активностью бактериофага, из которого он произведен (например, антимикробной активностью или антибактериальной активностью (такой как литическая киллерная активность)) в отношении одного или более штаммов бактерий, например, грамположительных бактерий (например, S. aureus), грамотрицательных бактерий (например, К. pneumoniae, A baumannii, Е.coli, P. aeruginosd) или бактерий, не проклассифицированных как грамотрицательные или грамположительные.
Согласно некоторым вариантам данное изобретение предусматривает выделенный полипептид, включающий любую аминокислотную последовательность из SEQ ID NO:5-176, SEQ ID NO:177-223, SEQ ID NO:224-506, SEQ ID NO:507-559, SEQ ID NO:561-780, SEQ ID NO:782-1073 и SEQ ID NO:1075-1300 и ее биологически активные фрагменты. Согласно предпочтительным вариантам вариантный полипептид по изобретению обладает по меньшей мере одним видом биологической активности, связанной с полипептидом или бактериофагом, из которых он выделен или произведен, например, лизирующей активностью, направленной в отношении по меньшей мере одного или более штаммов К. pneumoniae, A. baumannii, Е.coli, P. aeruginosa и/или S. aureus.
Согласно другим вариантам данное изобретение предусматривает выделенную последовательность нуклеиновой кислоты, кодирующую аминокислотную последовательность одной из SEQ ID NO:5-176, SEQ ID NO:177-223, SEQ ID NO:224-506, SEQ ID NO:507-559, SEQ ID NO:561-780, SEQ ID NO:782-1073 и SEQ ID NO:1075-1300, и ее активные фрагменты. Согласно другим вариантам данное изобретение предусматривает выделенную последовательность нуклеиновой кислоты, кодирующую любую из открытых рамок считывания, показанных на ФИГУРАХ 2, 4, 6, 8,10, 12 и/или 14.
Согласно некоторым вариантам полипептиды по данному изобретению являются слитыми рекомбинантным способом или химически конъюгированными (включая ковалентное или не ковалентное конъюгирование) с терапевтическими агентами, например, гетерологичными полипептидами или малыми молекулами с получением белков слияния или химерных полипептидов. Слияние необязательно должно быть прямым, а может происходить через линкерные последовательности или путем химического конъюгирования. Неограничивающие примеры терапевтических агентов, с которыми могут быть конъюгированы полипептиды по изобретению, включают пептидные и не пептидные цитотоксины (включающие антимикробные агенты и/или антибиотики), молекулы меток/маркеров (например, радионуклиды и флуорофоры) и другие антибиотические или антибактериальные агенты, известные из уровня техники.
АНТИБИОТИЧЕСКИЕ КОМПОЗИЦИИ
Выделенные бактериофаги или полипептиды по данному изобретению могут быть введены сами по себе в фармацевтическую композицию для лечения или профилактики бактериальных инфекций, например, инфекций, вызванных бактериями, включая, но без ограничения, К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и S. aureus. Полипептиды могут быть соединены с фармацевтически приемлемым носителем, эксципиентом и стабилизатором. Примеры фармацевтически приемлемых носителей, эксципиентов и стабилизаторов включают, но без ограничения, буферные вещества, такие как фосфат, цитрат и другие органические кислоты, антиоксиданты, включая, но без ограничения, аскорбиновую кислоту; низкомолекулярные полипептиды; белки, такие как сывороточный альбумин и желатин; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; сахарные спирты, такие как маннит или сорбит; солеобразующие противоионы, такие как ион натрия; и/или неионные поверхностно-активные вещества, такие как TWEEN™, полиэтиленгликоль (PEG) и PLURONICS™. В добавление к перечисленным выше компонентам фармацевтические композиции по данному изобретению (например, антибактериальные композиции) могут также включать смазывающий агент, смачиватель, подсластитель, ароматизирующее вещество, эмульгатор, суспендирующий агент и консервант.
Бактериофаги и/или полипептиды согласно данному изобретению также могут быть соединены с одним или более терапевтическими и/или профилактическими агентами, пригодными для лечения бактериальной инфекции, как описано в данной заявке и/или известно из уровня техники (например, с одним или более лизинами). Следовательно, фармацевтические композиции согласно изобретению могут содержать два или более бактериофагов по изобретению (с антибактериальной активностью против тех же самых или разных видов или штаммов бактерий), комбинацию бактериофага и полипептида по изобретению или комбинацию бактериофага и/или полипептида по изобретению и бактериофага и/или полипептида, известных из уровня техники. Согласно конкретным вариантам терапевтические компоненты такой комбинации могут быть нацелены на два или более видов или штаммов бактерий или проявлять разную ферментативную активность. Например, лизины в общем проявляют одну из активностей амидазы, эндопептидазы, мурамидазы или глюкозамидазы. Соответственно, комбинация лизинов, обладающих разными видами активности, может обеспечить синергическое повышение терапевтической активности фармацевтической композиции по изобретению.
Согласно некоторым вариантам ряд различных бактериофагов соединяют с целью получения "фагового коктейля." Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере 2 фага, по меньшей мере 3 фага, по меньшей мере 4 фага, по меньшей мере 5 фагов, по меньшей мере 6 фагов, по меньшей мере 7 фагов, по меньшей мере 8 фагов, по меньшей мере 9 фагов, по меньшей мере 10 фагов или более. Согласно некоторым вариантам фаговый коктейль содержит 2-20 фагов, 2-15 фагов, 2-10 фагов, 3-8 фагов или 4-6 фагов.
Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля представляет собой фаг с антибактериальной активностью в отношении по меньшей мере одного вида грамотрицательных бактерий, включая, но без ограничения, Klebsiella pneumoniae, Acinetobacter baumannii, Escherichia coli и Pseudomonas aeruginosa; и/или в отношении по меньшей мере одного вида грамположительных бактерий, включая, но без ограничения, Staphylococcus aureus. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F391/08, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:1 и проявляющий антибактериальную активность в отношении одного или более штаммов Klebsiella pneumoniae. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F394/08, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:2 и проявляющий антибактериальную активность в отношении одного или более штаммов Acinetobacter baumannii. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F488/08, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:3 и проявляющий антибактериальную активность в отношении одного или более штаммов Escherichia coli. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F510/08, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:4 и проявляющий антибактериальную активность в отношении одного или более штаммов Pseudomonas aeruginosa. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F44/10, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:560 и проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F387/08, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:781 и проявляющий антибактериальную активность в отношении одного или более штаммов Klebsiella pneumoniae. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F125/10, имеющим геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:1074 и проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F170/08, имеющим геном, описанный в международной заявке WO 2010/090542, и проявляющим антибактериальную активность в отношении одного или более штаммов Enterococcus faecalis или faecium. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F168/08, имеющим геном, описанный в международной заявке WO 2010/090542, и проявляющим антибактериальную активность в отношении одного или более штаммов Enterococcus faecalis или faecium. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F770/05, имеющим геном, описанный в международной заявке WO 2010/090542, и проявляющим антибактериальную активность в отношении одного или более штаммов Pseudomonas aeruginos. Согласно некоторым вариантам по меньшей мере один фаг в составе коктейля является фагом F1245/05, имеющим геном, описанный в международной заявке WO 2010/090542, и проявляющим антибактериальную активность в отношении одного или более штаммов Acinetobacter baumannii.
Согласно некоторым предпочтительным вариантам коктейль содержит фаг, обладающий активностью в отношении Acinetobacter. Например, коктейль может содержать фаг F394/08 и/или F1245/05, обладающий активностью в отношении одного или более штаммов Acinetobacter baumannii. Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере один фаг, проявляющий активность в отношении одного или более штаммов Acinetobacter baumannii и по меньшей мере один фаг, проявляющий активность в отношении другого вида бактерий. Например, согласно некоторым вариантам фаговый коктейль содержит фаги F394/08 и/или F1245/05 в сочетании с, по меньшей мере, одним другим фагом, выбранным из F391/08, F488/08, F510/08, F44/10, F387/08, F170/08, F168/08, F770/05 и F125/10. Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность в отношении одного или более штаммов Klebsiella pneumonia и по меньшей мере один фаг, проявляющий антибактериальную активность в отношении другого вида бактерий. Например, согласно некоторым вариантам фаговый коктейль содержит фаг F391/08 и/или F387/08 в комбинации с по меньшей мере одним другим фагом, выбранным из F394/08, F488/08, F510/08, F44/10, F1245/05, F170/08, F168/08, F770/05, и F125/10. Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность в отношении одного или более штаммов Escherichia coli и по меньшей мере один фаг, проявляющий антибактериальную активность в отношении другой бактерии. Например, согласно некоторым вариантам фаговый коктейль содержит F488/08 в комбинации с по меньшей мере одним другим фагом, выбранным из F391/08, F510/08, F44/10, F394/08, F387/08, F170/08, F168/08, F1245/05, F770/05 и F125/10. Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность в отношении одного или более штаммов Pseudomonas aeruginosa и по меньшей мере один фаг, проявляющий антибактериальную активность в отношении другого вида бактерий. Например, согласно некоторым вариантам фаговый коктейль содержит фаг F510/08 и/или F770/05 в комбинации с по меньшей мере одним другим фагом, выбранным из F391/08, F394/08, F488/08, F44/10, F387/08, F170/08, F168/08, F1245/05, и F125/10. Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность против одного или более штаммов Staphylococcus aureus и по меньшей мере один фаг, проявляющий антибактериальную активность против другого вида бактерий. Например, согласно некоторым вариантам фаговый коктейль содержит F44/10 и/или F125/10 в комбинации с по меньшей мере одним другим фагом, выбранным из F391/08, F394/08, F488/08, F510/08, F387/08, F170/08, F168/08, F770/05 и F1245/05. Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность против одного или более штаммов Enterococcus faecalis или faecium в комбинации с по меньшей мере одним другим фагом, выбранным из F391/08, F394/08, F488/08, F510/08, F44/10, F387/08, F770/05, F1245/05 и F125/10.
Согласно некоторым вариантам фаговый коктейль содержит по меньшей мере четыре (4) фага, выбранные из группы, состоящей из F391/08, F394/08, F488/08, F510/08, F44/10, F387/08, F170/08, F168/08, F770/05, F1245/05 и F125/10. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F488/08 и F510/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F44/10, F387/08, F170/08 и F168/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F770/05 и F1245/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F510/08 и/или F44/10. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F44/10, и/или F387/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F387/08 и/или F170/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F170/08 и F168/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F168/08 и/или F770/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F391/08, F394/08, F770/05 и F1245/05.
Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F391/08, F394/08 и F488/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F394/08, F488/08 и F510/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F488/08, F510/08 и F44/10. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F44/10, F387/08 и F170/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F170/08, F168/08 и F770/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F770/05, F1245/05 и F391/08. Согласно некоторым вариантам фаговый коктейль содержит в добавление к перечисленным выше компонентам фаги F125/10, F510/08, F44/10, F387/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F387/08, F170/08, F168/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F168/08, F770/05 и F1245/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F125/10, F1245/05, F391/08 и F394/08.
Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, F510/08 и/или F44/10. Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, F44/10 и/или F387/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, F387/08 и/или F170/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, F170/08 и/или F168/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, F168/08 и/или F770/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, FF770/05 и/или F1245/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F394/08, F488/088, F1245/05 и/или F391/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F44/10 и/или F387/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F387/08 и/или F170/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F170/08 и/или F168/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F168/08 /или F770/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F770/05 и/или F1245/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F1245/05 и/или F391/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F488/08, F510/08, F391/08 и/или F394/08.
Согласно некоторым вариантам фаговый коктейль содержит фаги F387/08, F170/08, F168/08 и/или F770/05. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F770/05 и/или F1245/05. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F1245/05 и/или F391/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F391/08 и/или F394/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F394/08 и/или F488/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F488/08 и/или F510/08. Согласно некоторым вариантам фаговый коктейль содержит F387//08, F170/08, F510/08 и/или F44/10. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F44/10 и/или F387/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F387/08 и/или F170/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F170/08 и/или F168/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F168/08 и/или F770/05. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F770/05 и/или F1245/05. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F1245/05 и/или F391/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F391/08 и/или F394/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F394/08 и/или F488/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F488/08 и/или F510/08. Согласно некоторым вариантам фаговый коктейль содержит F387/08, F170/08, F510/08 и/или F44/10.
Согласно некоторым вариантам фаговый коктейль содержит фаги F510/08, F44/10, F387/08, и/или F170/08. Согласно некоторым вариантам фаговый коктейль содержит F510/08, F44/10, F170/08 и/или F168/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F510/08, F44/10, F168/08 и/или F770/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F510/08, F44/10, F770/05 и/или F1245/05. Согласно некоторым вариантам фаговый коктейль содержит фаги F510/08, F44/10, F1245/05 и/или F391/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F510/08, F44/10, F391/08 и/или F394/08. Согласно некоторым вариантам фаговый коктейль содержит фаги F510/08, F44/10, F394/08 и/или F488/08.
Согласно некоторым вариантам фаговый коктейль содержит фаги F44/10, F387/08, F170/08 и/или F168/08. Согласно некоторым вариантам фаговый коктейль содержит F44/10, F387/08, F168/08 и/или F770/05. Согласно некоторым вариантам фаговый коктейль содержит F44/10, F387/08, F770/05 и/или F1245/05. Согласно некоторым вариантам фаговый коктейль содержит F44/10, F387/08, F1245/05 и/или F391/08. Согласно некоторым вариантам фаговый коктейль содержит F44/10, F387/08, F391/08 и/или F394/08. Согласно некоторым вариантам фаговый коктейль содержит F44/10, F387/08, F394/08 and/or F488/08. Согласно некоторым вариантам фаговый коктейль содержит F44/10, F387/08, F488/08 и/или F510/08.
Согласно некоторым вариантам фаговый коктейль может содержать или не содержать фаг, выбранный для увеличения in vivo периода полужизни, например, фаги, описанные в патенте США №5,688,501, содержание которого включено в данную заявку посредством отсылки.
Согласно некоторым вариантам фаговый коктейль содержит один или более полипептидов, выделенных из одного или более фагов, и/или их фрагмент, вариант или производное, в частности, полипептид, его фрагмент, вариант или производное, которые имеют антибактериальную или антимикробную активность. Согласно некоторым вариантам полипептид, его фрагмент, вариант или производное включает или состоит из лизина (или его фрагмента, например, домена CHAP) и/или хвостового белка. Согласно конкретным вариантам такой полипептид соответствует выделенному полипептиду, его фрагменту, варианту или производному, которые описаны в данной заявке и/или в заявке WO 2010/090542, содержание которой включено в данную заявку посредством отсылки. Согласно некоторым вариантам коктейль вводится в отсутствие выделенного полипептида, такого как лиаза.
Дополнительные примеры других терапевтических агентов, которые могут быть использованы в комбинации с полипептидом по изобретению, включают, но без ограничения, стандартные антибиотики, противовоспалительные агенты, противовирусные агенты, местные анестетики и кортикостероиды. В некоторых случаях коктейль вводят в отсутствие антибиотика.
Стандартные антибиотики, которые могут быть использованы в фармацевтических композициях по изобретению, содержащих бактериофаг и/или полипептид по изобретению, включают, но без ограничения, амикацин, гентамицин, канамицин, неомицин, нетилмицин, паромомицин, родострептомицин, стрептомицин, тобрамицин, апрамицин, рифамицин, нафтомицин, мупироцин, гелданамицин, ансамитоцин, карбацефемы, имипенем, меропенем, эртапенем, фаропенем, дорипенем, панипенем/бетамипрон, биапенем, PZ-601, цефалоспорины, цефацетрил, цефадроксил, цефалексин, цефалоглицин, цефалоний, цефалоридин, цефалотин, цефапирин, цефатризин, цефазафлур, цефазедон, цефазолин, цефрадин, цефроксадин, цефтезол, цефаклор, цефоницид, цефпрозил, цефуроксим, цефузонам, цефметазол, цефотетан, цефокситин, цефкапен, цефдалоксим, цефдинир, цефдиторен, цефетамет, цефиксим, цефменоксим, цефтерам, цефтибутен, цефтиофур, цефтиолен, цефтизоксим, цефтриаксон, цефоперазон, цефтазидима латамоксеф, цефклидин, цефепим, цефлупренам, цефоселис, цефозопран, цефпиром, цефквином, фломоксеф, цефтобипрол, азитромицин, кларитромицин, диритромицин, эритромицин, рокситромицин, азтреонам, пенициллин и производные пенициллина, актиномицин, бацитрацин, колистин, полимиксин В, циноксацин, флумеквин, налидиксовую кислоту, оксолиновую кислоту, пиромидиновую кислоту, пипемидиновую кислоту, росоксацин, ципрофлоксацин, эноксацин, флероксацин, ломефлоксацин, надифлоксацин, норфлоксацин, офлоксацин, пефлоксацин, руфлоксацин, балофлоксацин, гатифлоксацин, грепафлоксацин, левофлоксацин, моксифлоксацин, пазуфлоксацин, спарфлоксацин, темафлоксацин, тосуфлоксацин, клинафлоксацин, гареноксацин, гемифлоксацин, стифлоксацин, тровалфлоксацин, прулифлоксацин, ацетазоламид, бензоламид, буметанид, целекоксиб, хлорталидон, клопамид, дихлорфенамид, дорзоламид, этоксизоламид, фуросемид, гидрохлортиазид, индапамид, мафендид, мефрусид, метолазон, пробенецид, сульфацетамид, сульфадиметоксин, сульфадоксин, сульфаниламиды, сульфаметоксазол, сульфасалазин, сультиам, суматриптан, ксипамид, тетрациклин, хлортетрациклин, окситетрациклин, доксициклин, лимециклин, меклоциклин, метациклин, миноциклин, ролитетрациклин, метициллин, нафциллин, оксацилин, клоксациллин, ванкомицин, тейкопланин, клиндамицин, ко-тримоксазол и их любые комбинации в количествах, которые эффективны для аддитивного или синергического улучшения терапевтического эффекта бактериофага и/или полипептида по изобретению для данной инфекции.
Местные анестетики, которые могут быть использованы в фармацевтических композициях по данному изобретению, включают тетракаин, тетракаина гидрохлорид, лидокаин, лидокаина гидрохлорид, диметизоквина гидрохлорид, дибукаин, дибукаина гидрохлорид, бутамбенпикрат и прамоксина гидрохлорид.
Кортикостероиды, которые могут быть использованы в комбинации с полипептидами, бактериофагами и/или фармацевтическими композициями по изобретению включают бетаметазон, дипропионат, флуоцинолона актинид, бетаметазона валерат, триамцинолона актинид, клобетазола пропионат, дезоксиметазон, дифлоразона диацетат, амцинонид, флурандренолид, гидрокортизона валерат, гидрокортизона бутират и десонид. Примерная концентрация кортикостероида составляет примерно от 0,01% до примерно 1% в расчете на вес всей композиции.
Согласно некоторым вариантам состав, содержащий бактериофаг и/или полипептид по изобретению, включает также буфер SM (0,05 М Трис-HCl (pH 7,4-7,5); 0,1 М NaCl; 10 мМ MgSO4). Согласно другим вариантам состав содержит также буфер SM и 10 мМ MgCl2.
Согласно другим вариантам состав содержит также буфер SM и примерно 20% или примерно 30% этанола. Фармацевтические композиции, содержащие бактериофаг и/или полипептид согласно данному изобретению, могут быть изготовлены в виде одноразовых или многоразовых лекарственных форм. Подходящие составы могут быть в виде мазей, растворов, суспензий или эмульсий, экстрактов, порошков, гранул, спреев, пастилок, таблеток или капсул и дополнительно могут включать диспергирующий агент или стабилизирующий агент.
Фармацевтические композиции по изобретению могут быть введены путем ингаляции, в виде суппозитория или маточного кольца, топически (например, в виде лосьона, раствора, крема, мази или присыпки), эпи- или транс-дермально (например, путем наложения пластыря на кожу), орально (например, в виде таблетки, которая может содержать эксципиенты, такие как крахмал или лактоза), в виде капсулы, суппозитория, эликсиров, растворов или суспензий (каждый из них может содержать ароматизирующие вещества, красители и/или эксципиенты), или они могут быть введены в виде инъекций парентерально (например, внутривенно, внутримышечно или подкожно). При парентеральном введении композиция может быть использована в виде стерильного водного раствора, который может содержать другие вещества, например, достаточное количество соли или моносахарида для придания раствору изотоничности крови. При буккальном или подъязычном введении композиции могут быть в виде таблеток или пастилок, которые получают известными методами. Согласно предпочтительному варианту бактериофаг и/или полипептид по изобретению вводится топически или в виде единственного агента или в комбинации с другими видами антибиотиков, как описано в данной заявке или известно из уровня техники.
Бактериофаг и/или полипептид по данному изобретению могут быть также введен дермально или трансдермально. При топическом нанесении на кожу бактериофаги и/или полипептиды по данному изобретению могут быть соединены с одним носителем или с комбинацией носителей, которые включают, но без ограничения, водную жидкость, жидкость на спиртовой основе, водорастворимый гель, лосьон, мазь, неводную жидкую основу, минеральную основу масел, смесь минерального масла и петролатума, ланолин, липосомы, белковые носители, такие как сывороточный альбумин или желатин, порошкообразную целлюлозу фирмы Carmel и их комбинации. Топический способ доставки может включать применение вязкого состава, спрея, повязки, пластыря с пролонгированным высвобождением, влажных салфеток с абсорбированной жидкостью или их комбинаций. Бактериофаг и/или полипептид по данному изобретению может быть нанесен на пластырь, салфетку, повязку и т.д. или непосредственно, или с носителем (носителями). Пластыри, салфетки, повязки и т.д. могут быть влажными или сухими, при этом фаг и/или полипептид (например, полипептид, содержащий лизин) на поверхности пластыря находится в лиофилизированной форме. Носители топических композиций могут представлять собой полутвердые и гелеподобные средства, которые включают полимерный загуститель, воду, консерванты, активные поверхностно-активные вещества или эмульгаторы, антиоксиданты, солнцезащитные вещества и растворитель или смеси растворителей. В патенте США №5,863,560 описан ряд различных комбинаций носителей, которые могут способствовать действию медикамента на кожу, содержание этого источника включено в данную заявку посредством отсылки. Носитель может включать или не включать состав с регулируемым высвобождением, например, описанный в заявке США на патент №2008/0260697, содержание которой включено в данную заявку посредством отсылки. Носитель может включать или не включать фаг, адсорбированный на матрице, например, как описано в любом из следующих источников: в заявках США на патент №№2008/0038322, 2008/0138311, 2009/0130196, в патентах EP 1812025, EP 1817043 и EP 1833497, содержание которых включено в данную заявку посредством отсылок. Согласно некоторым вариантам носитель может быть или не быть вязким составом, например, гелем, таким как описанный в заявке США №2009/0191254, содержание которой включено в данную заявку посредством отсылки.
При интраназальном введении или при введении путем ингаляции бактериофаг и/или полипептид по изобретению обычно доставляется с помощью порошкового ингалятора или путем распыления в виде аэрозоля из резервуара со сжатым воздухом, с помощью насоса, распылителя или небулайзера при помощи пропеллента, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, гидрофторалкана, в том числе 1,1,1,2-тетрафторэтана (HFA 134A.TM.) или 1,1,1,2,3,3,3-гептафторпропана (HFA 227EA.TM.), двуокиси углерода или другого подходящего газа. В случае аэрозоля под давлением единица дозирования может быть определена с помощью клапана для доставки отмеренного количества. Контейнер под давлением, насос, распылитель или небулайзер может содержать раствор или суспензию активного соединения, например, в смеси этанола и пропеллента в качестве растворителя, которые дополнительно могут содержать смазывающий агент, например, триолеат сорбитана. Капсулы и картриджи (изготовленные, например, из желатина), используемые в ингаляторе или в порошковдувателе, могут содержать порошковую смесь бактериофага и/или полипептида по изобретению и подходящей порошкообразной основы, такой как лактоза или крахмал. Для введения в виде суппозитория или вагинального суппозитория терапевтическая композиция может быть топической в виде геля, гидрогеля, лосьона, раствора, крема, мази или присыпки. Композиции по изобретению могут также вводиться офтальмологическим путем. В случае офтальмологического применения композиции по изобретению могут быть получены в виде микронизированных суспензий в изотоническом стерильном физиологическом растворе с регулируемым pH или же в растворах в изотоническом стерильном физиологическом растворе с регулируемым pH, возможно в комбинации с консервантом, таким как бензалконийхлорид. Или же они могут быть в виде мази, например, на основе петролатума.
Дозы и желательные концентрации фармацевтических композиций по данному изобретению могут сильно меняться в зависимости от конкретного применения. Определение соответствующих доз или способа их введения находится в компетенции обычного специалиста в данной области. Эксперименты на животных могут обеспечить надежное руководство по определению эффективных доз при лечении людей. Межвидовой перенос эффективных доз может осуществляться средним специалистом в данной области с применением принципов, описанных Mordenti, J. and Chappell, W. "The use of interspecies scaling in toxicokinetics" in Toxicokinetics and New Drug Development, Yacobi et al., Eds., Pergamon Press, New York 1989, p.p.42-96.
ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ
Бактериофаги и полипептиды по данному изобретению обладают активностью в отношении многих штаммов К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и/или S. aureus, как показано в Таблицах 1-7 и следующих ниже примерах. Следовательно, композиции по изобретению могут найти применение при осуществлении способов профилактики и/или лечения инфекций, связанных с инфекцией, вызванной К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и/или S. aureus, как у людей, так и у животных. Согласно другим вариантам композиции по изобретению могут быть использованы для лечения инфекции, связанной с родственными видами или штаммами этих бактерий, включая, но без ограничения, S. epidermidis, S. auricularis, S. capitis, S. haemolyticus, S. hominis, S. saprophyticus, S. simulans, S. xylosis, Micrococcus luteus, Bacilus subtilis, B. pumilus, E. hirae.
Согласно конкретным вариантам субъектом, получающим фармацевтическую композицию по данному изобретению, является млекопитающее (например, жвачные животные, овцы и козы, непарнокопытные животные, приматы (например, люди), грызуны, зайцеобразные или птицы (например, куры, утки, гуси)). В контексте данного изобретения термин "лечение" относится к терапевтическому лечению, цель которого состоит в устранении, облегчении, уменьшении тяжести, ослаблении, замедлении развития или предотвращении симптомов или причин (например, бактериальной инфекции), связанной с патологическим состоянием или расстройством. Термин "лечение" относится и к терапевтическому лечению, и к профилактическим или предупредительным мерам, при этом цель заключается в устранении, облегчении, уменьшении тяжести, ослаблении, замедлении развития или предотвращении симптомов или причин (например, бактериальной инфекции), связанной с патологическим состоянием или расстройством. Предполагается также, что бактериофаг или полипептид по изобретению действует как профилактическое или предупредительное средство, предотвращая вспышку инфекции, вызванной одним или несколькими видами бактерий.
Бактерии К. pneumoniae, A. baumannii, E.coli, P. aerugmosa и S. aureus отвечают за многие серьезные оппортунистические (вызываемые условно-патогенными организмами) инфекции, особенно у субъектов с ослабленной иммунной системой. Фармацевтические композиции по данному изобретению предназначены для лечения любой инфекции, связанной с К. pneumoniae, A. baumannii, E.coli, Р. aerugmosa и/или S. aureus или с другими видами или штаммами бактерий, включая, но без ограничения, кожные инфекции (включая, но без ограничения, кожные язвы, карбункулы, пролежни и диабетические язвы стопы), инфекции в ранах и вокруг них, послеоперационные инфекции, инфекции, обусловленные применением катетеров и дренажных трубок, и инфекции в крови.
Диабетическая язва стопы является одним из основных осложнений при сахарном диабете, возникающим у примерно 15% всех диабетических больных и являющимся причиной ампутаций голени примерно в 85% случаев. (См., Brem, et al., J. Clinical Invest., 2007, 117(5): 1219-1222). Сахарный диабет препятствует нормальному заживлению ран. Незаживающие хронические диабетические язвы часто подвергают лечению методами внеклеточной заместительной терапии, современной терапии с увлажнением раны, биоинженерного замещения ткани или кожи, методом с применением факторов роста, удаления омертвевших частей раны, артериальной реваскуляризации и/или методом заживления ран при отрицательном давлении. (См., (Blume et.al, Diabetes Care, 2008, 31: 631-636). Язвы могут инфицироваться оппортунистическими бактериями, которые затем обостряют состояние больного. Соответственно, язвы на стопах при диабете часто также требуют применения антибиотиков, например, против инфекции, вызванной Staphylococcus, a также другими анаэробными бактериями, такими как Klebsiella pneumonia, Escherchia coli и/или Pseudomonas aerugmosa.
Одна или более композиций по данному изобретению находят применение при лечении диабетических язв стопы. Например, выделенный бактериофаг или полипептид по изобретению могут быть применены при лечении инфекций, связанных с диабетическими язвами стопы у субъекта, нуждающегося в этом. Согласно конкретным вариантам композиция, используемая для лечения диабетических язв стопы, является топической, полученной для топического введения, например, композицией для непосредственного нанесения на язву, рану, повреждения и/или нагноение, связанные с диабетической язвой стопы.
Согласно некоторым вариантам композиция для лечения диабетической язвы стопы включает выделенный фаг F44/10, имеющий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:560 и проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus. Согласно некоторым вариантам применяется композиция, содержащая полипептид, выделенный из бактериофага F44/10, или его фрагмент, вариант или производное, при этом указанные полипептид, его фрагмент, вариант или производное проявляют антибактериальную активность в отношении одного или более штаммов S. aureus. Согласно некоторым таким вариантам полипептид, его фрагмент, вариант или производное содержат лизин, домен CHAP или хвостовой белок, проявляющие антибактериальную активность в отношении одного или более штаммов S. aureus. Согласно некоторым вариантам композиция, используемая для лечения диабетической язвы стопы, содержит выделенный фаг F125/10, имеющий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:1074 и проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus. Согласно некоторым вариантам применяют композицию, содержащую полипептид, выделенный из бактериофага F125/10, или его фрагмент, вариант или производное, при этом указанные полипептид, его фрагмент, вариант или производное проявляют антибактериальную активность в отношении одного или более штаммов S. Aureus. Согласно некоторым таким вариантам полипептид, его фрагмент, вариант или производное содержат лизин, домен CHAP или хвостовой белок, проявляющие антибактериальную активность в отношении одного или более штаммов S. aureus.
Согласно некоторым вариантам применяют композицию, содержащую фаговый коктейль, например, когда этот фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность в отношении одного или более штаммов Staphylococcus aureus и по меньшей мере один фаг, проявляющий антибактериальную активность в отношении других бактерий. Согласно конкретным вариантам фаговый коктейль содержит фаги F44/10 и/или F125/10 в комбинации с по меньшей мере одним другим фагом, выбранным из F391/08, F394/08, F488/08, F510/08, F387/08, F170/08, F168/08, F770/05 и F1245/05. Согласно особенно предпочтительным вариантам фаговый коктейль содержит фаги F44/10 и/или F125/10 в комбинации с одним, двумя, тремя или более фагами, выбранными из F391/08, F387/08, F488/08, F510/08 и/или F770/05.
Согласно некоторым вариантам для лечения диабетической язвы стопы применяют композицию, содержащую выделенные фаги F391/08 и/или F387/08, имеющие геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:1 или SEQ ID NO:781, соответственно, и проявляющий антибактериальную активность в отношении одного или более штаммов Klebsiella pneumoniae. Согласно некоторым вариантам применяют композицию, содержащую полипептид, выделенный из бактериофагов F391/08 и/или F3 87/08, или его фрагмент, вариант или производное, при этом указанные полипептид, его фрагмент, вариант или производное проявляют антибактериальную активность против одного или более штаммов К. pneumoniae. Согласно некоторым таким вариантам полипептид, его фрагмент, вариант или производное содержат лизин, домен CHAP или хвостовой белок, проявляющие антибактериальную активность против одного или более видов и штаммов К. pneumoniae. Согласно некоторым вариантам применяют композицию, содержащую фаговый коктейль, при этом, например, фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность против одного или более штаммов Klebsiella pneumonia, и по меньшей мере один фаг, проявляющий антибактериальную активность против других бактерий. Согласно конкретным вариантам фаговый коктейль содержит фаги F391/08 и/или F387/08 в комбинации с по меньшей мере одним другим фагом, выбранным из F394/08, F488/08, F510/08, F44/10, F170/08, F168/08, F770/05, F1245/05 и F125/10. Согласно особенно предпочтительным вариантам фаговый коктейль содержит фаги F391/08 и/или F387/08 в комбинации с по меньшей мере одним другим фагом, выбранным из F44/10, F488/08, F510/08 и/или F770/05.
Согласно некоторым вариантам композиция, применяемая для лечения диабетических язв стопы, содержит выделенный фаг F488/08, имеющий геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:3, проявляющий антибактериальную активность против одного или более штаммов Escherichia coli. Согласно нескольким вариантам применяют композицию, содержащую полипептид, выделенный из бактериофага F488/08, или его фрагмент, вариант или производное, проявляющий антибактериальную активность против одного или более штаммов Escherichia coli. Согласно некоторым таким вариантам полипептид, его фрагмент, вариант или производное содержат лизин, домен CHAP или хвостовой белок, проявляющие антибактериальную активность против одного или более видов и штаммов Escherichia coli. Согласно некоторым вариантам применяют композицию, содержащую фаговый коктейль, при этом фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность против одного или более штаммов Escherichia coli и по меньшей мере один фаг, проявляющий антибактериальную активность против других бактерий. Согласно конкретным вариантам фаговый коктейль содержит фаг F488/08 в комбинации с по меньшей мере одним другим фагом, выбранным из F394/08, F510/08, F44/10, F170/08, F168/08, F770/05, F1245/05, F391/08 F387/08 и F125/10. Согласно особенно предпочтительным вариантам фаговый коктейль содержит фаг F488/08 в комбинации с одним, двумя, тремя или более фагами, выбранными из F391/08, F387/08, F44/10, F125/10, F510/08 и/или F770/05.
Согласно некоторым вариантам для лечения диабетической язвы стопы применяют композицию, содержащую выделенные фаги F510/08 и/или F770/05, имеющие геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO:4, такую как описанную в международной заявке № WO 2010/090542, проявляющий антибактериальную активность против одного или более штаммов Pseudomonas aeruginosa. Согласно нескольким вариантам применяют композицию, содержащую полипептид, выделенный из бактериофагов F510/08 и/или F770/05, или его фрагмент, вариант или производное, проявляющие антибактериальную активность против одного или более штаммов Р. aeruginosa. Согласно некоторым таким вариантам полипептид, его фрагмент, вариант или производное содержат лизин, домен CHAP или хвостовой белок, проявляющие антибактериальную активность против одного или более видов и штаммов Pseudomonas aeruginosa. Согласно некоторым таким вариантам применяют композицию, содержащую фаговый коктейль, при этом фаговый коктейль содержит по меньшей мере один фаг, проявляющий антибактериальную активность против одного или более штаммов Pseudomonas aeruginosa и по меньшей мере один фаг, проявляющий антибактериальную активность против других бактерий. Согласно конкретным вариантам фаговый коктейль содержит фаги F510/08 и/или F770/05 в комбинации с по меньшей мере одним другим фагом, выбранным из F394/08, F488/08, F44/10, F170/08, F168/08, F1245/05, F391/08, F387/08 и F125/10. Согласно особенно предпочтительным вариантам фаговый коктейль содержит фаги F510/08 и/или F770/05 в комбинации с одним, двумя, тремя или более фагами, выбранными из F44/10, F488/08, F391/08 и/или F387/08.
Штаммы К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и S. aureus ассоциируются также с инфекциями, которые затрагивают системы органов, которые имеют высокое содержание жидкости, подразумевается, что бактериофаги и/или полипептиды по изобретению терапевтически пригодны для профилактики и лечения этих инфекций. Например, фармацевтические композиции по изобретению можно применять для профилактики и лечения инфекций дыхательного тракта, спинномозговой жидкости, перитонеальной жидкости и мочевого тракта. Композиции по изобретению можно также применять для профилактики и лечения нозокомиальной пневмонии, инфекций, связанных с непрерывным амбулаторным перитонеальным диализом (CAPD), бактериемии, связанной с применением катетеров, и нозокомиального менингита.
Согласно предпочтительному варианту бактериофаги и/или полипептиды по изобретению применяют профилактически в больницах, особенно для предотвращения инфекций, связанных с ранами, язвами и отверстиями в коже, например, из-за катетеризации и применения любых других медицинских процедур и устройств.
Согласно некоторым вариантам бактериофаг и/или полипептид по изобретению применяют в качестве единственного агента для лечения или профилактики инфекций, связанных с К. pneumoniae, А. baumannii, Е.coli, P. aeruginosa и/или S. aureus и/или с другими видами бактерий. Согласно другим вариантам изобретения бактериофаг и/или полипептид по изобретению применяют в комбинации с другими агентами, включая, но без ограничения, другие бактериофаги (например, нацеленные на другие виды или штаммы бактерий) или с антибиотиками, которые нацелены на те же самые или другие виды бактерий, включая бактерии, выбранные из любых грамположительных бактерий, любых грамотрицательных бактерий или любых других бактерий, которые не классифицированы как грамположительные или грамотрицательные. Композиции по данному изобретению могут также применяться в комбинации с любым другим средством для лечения бактериальной инфекции, известным специалисту в данной области.
Данное изобретение предусматривает также способы профилактики и способы лечения инфекции, вызванной бактериями, включая, но без ограничения, бактерии К. pneumoniae, A. baumannii, Е.coli, P. aeruginosa и/или S. aureus, которые включают введение млекопитающему, нуждающемуся в этом, композиции, содержащей лизин, включающий или состоящий из аминокислотной последовательности SEQ ID NO:20, SEQ ID NO:80, SEQ ID NO:192, SEQ ID NO:282, SEQ ID NO:547, SEQ ID NO:556, SEQ ID NO:557, SEQ ID NO:598, SEQ ID NO:1216, SEQ ID NO:1261, или его фрагмент, вариант или производное, при этом указанные фрагмент, вариант или производное проявляют антибактериальную или антимикробную активность в отношении видов бактерий, из которых выделен родительский бактериофаг. Согласно конкретному примеру в соответствии с этим вариантом данное изобретение предусматривает способы профилактики или лечения инфекции, вызванной бактериями, включая, но без ограничения, К. pneumoniae, A. baumannii, E.coli, Р. aeruginosa и/или S. aureus, которые включают введение млекопитающему, нуждающемуся в этом, композиции, содержащей выделенный домен CHAP лизина или его фрагмент, вариант или производное, которые проявляют по меньшей мере один вид биологической активности домена CHAP, из которого они выделены (например, лизирующую киллерную активность).
Согласно некоторым вариантам данное изобретение предусматривает способы профилактики и/или лечения инфекции, вызванной бактериями, включая, но без ограничения, К. pneumoniae, A. baumannii, E.coli, P. aeruginosa и/или S. aureus, которые включают введение млекопитающему, нуждающемуся в этом, композиции, содержащей хвостовой белок, содержащий или состоящий из аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629 или SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250, SEQ ID NO:1266, или его фрагмент, вариант или производное, при этом указанные фрагмент, вариант или производное проявляют по меньшей мере один вид биологической активности, связанной с бактериофагом, из которого они выделены.
Согласно другим вариантам данное изобретение предусматривает способы профилактики и/или лечения инфекции, вызванной бактериями, включая, но без ограничения, К. pneumoniae, A. baumannii, E.coli, P. Aeruginosa и/или S. aureus, которые включают введение млекопитающему, нуждающемуся в этом, композиции, содержащей бактериофаг, имеющий геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 и/или SEQ ID NO:1074. Комбинации лизинов (или их фрагментов, вариантов или производных, описанных выше) возможно, с одним или более бактериофагами согласно данному изобретению или с другими терапевтическими агентами, такими как антибиотики, также предусмотрены данным изобретением, как и способы лечения и/или способы профилактики бактериальной инфекции с применением одной или более комбинаций, описанных в данной заявке.
Применяемый в данной заявке термин "в комбинации" относится к применению более чем одного профилактического и/или терапевтического агента. Применение термина "в комбинации" не ограничивает порядок, в котором профилактический и/или терапевтический агенты вводятся субъекту, страдающему от болезни или расстройства. Первый профилактический и/или терапевтический агент может быть введен субъекту, страдающему от болезни или расстройства, перед введением второго профилактического и/или терапевтического агента (например, за 5 мин, 15 мин, 30 мин. 45 мин, 1 ч, 2 ч, 4 ч, 6 ч, 12 ч, 24 ч, 48 ч, 72 ч, 96 ч, 1 нед, 2 нед, 3 нед, 4 нед, 5 нед, 6 нед, 8 нед или 12 нед), одновременно с ним или после введения второго профилактического и/или терапевтического агента (например, через 5 мин, 15 мин, 30 мин. 45 мин, 1 ч, 2 ч, 4 ч, 6 ч, 12 ч, 24 ч, 48 ч, 72 ч, 96 ч, 1 нед, 2 нед, 3 нед, 4 нед, 5 нед, 6 нед, 8 нед или 12 нед), который отличается от первого профилактического и/или терапевтического агента.
ПРИМЕНЕНИЕ В КАЧЕСТВЕ ДЕЗИНФИЦИРУЮЩЕГО И ПРОТИВОИНФЕКЦИОННОГО СРЕДСТВА
Бактериальные патогены чаще всего инфицируют какой-либо участок в мембране слизистой оболочки (например, в верхних и нижних дыхательных путях, в кишечнике, в мочеполовом тракте, в глазах и т.п.). Мембраны слизистой оболочки сами по себе часто являются резервуаром, иногда только резервуаром, для многих патогенных бактерий, обнаруженных в окружающей среде (например, пневмококков, стафилококков и стрептококков). Имеются очень немногие противоинфекционные средства, которые предназначены для контролирования состояния носительства патогенных бактерий. Однако исследования показали, что путем уменьшения размера этого резервуара в окружающей среде, такой как больницы и интернаты для престарелых, возможность возникновения инфекций будет значительно снижена. Профилактика нозокомиальных инфекций включает регулярную и повторяющуюся процедуру очистки зараженных поверхностей.
Бактериофаги и/или полипептиды по данному изобретению могут быть использованы в противоинфекционных композициях для контролирования роста бактерий (например, грамположительных бактерий (в том числе, S. aureus), грамотрицательных бактерий (например, К. pneumoniae, A. baumannii, E.coli и Р. aeruginosa) или бактерий, не проклассифицированных как грамположительные или грамотрицательные) для того, чтобы предотвратить или снизить количество нозокомиальных инфекций. Кроме того, в дополнение к применению в композициях для нанесения на слизистые мембраны, бактериофаг и/или полипептид по данному изобретению может быть также введен в составы, такие как гели, кремы, мази или спреи, для регулирования или предотвращения колонизации бактерий на поверхности тела (например, на коже или слизистой оболочке) (например, для стерилизации поверхности рук при хирургическом вмешательстве и кожи работников здравоохранения и/или пациентов) и на других твердых поверхностях (например, инструментах, рабочих поверхностях кухни и, в особенности, больничном оборудовании).
ПРИМЕНЕНИЕ В НАНОТЕХНОЛОГИИ
Бактериофаги и/или полипептиды по данному изобретению могут быть также использованы в нанотехнологии, например, при создании наноустройств. Комбинация нанотехнологии и молекулярной биологии привела к появлению нового поколения наноустройств, таких как нанопроводники. Биологические системы функционируют на основе структуры макромолекул, в основном белков и нуклеиновых кислот, которые структурно организованы на наноуровне. Соответственно, биологические макромолекулы могут найти применение на наноуровне для различных целей. В частности, белки, имеющие в высшей степени организованные структуры, могут быть использованы при создании наноустройств.
Согласно некоторым вариантам полипептид по изобретению, содержащий или состоящий из хвостового белка (например, компонента хвостового отростка, хвостового фибриллярного белка, хвостового белка, связанного с адсорбцией, белка рулетки хвостового отростка, субъединицы конусовидной базальной пластинки) или его фрагмента, варианта или производного, выделенных из бактериофага, имеющего геном, содержащий или состоящий из SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781 или SEQ ID NO:1074 (например, бактериофага F391/08, F394/08, F488/08, F510/08, F44/10, F387/08 или F125/10, соответственно), может быть применен в нанотехнологии. Например, белки хвостового отростка из хвостовых нитей фага могут быть в высшей степени организованными и могут найти применение в нанопроводниках. Такие проводники могут быть использованы, например, для осаждения золота и/или других ионов.
Согласно конкретным вариантам полипептид по данному изобретению, используемый в нанотехнологии, представляет собой выделенный белок хвостового отростка, содержащий или состоящий из аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NOs:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266. Согласно другим вариантам полипептид по данному изобретению представляет собой фрагмент, вариант или производное SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266, при этом указанные фрагмент, вариант или производное имеют высокоорганизованную структуру. Такие полипептиды находят применение, например, в нанопроводниках, как указано выше.
ДИАГНОСТИЧЕСКИЕ СПОСОБЫ
Данное изобретение предусматривает также диагностические способы определения возбудителя бактериальной инфекции. Согласно некоторым вариантам диагностика возбудителя бактериальной инфекции проводится путем: (i) культивирования образцов ткани, крови или жидкости пациента по стандартной методике; (ii) контактирования полученной культуры с одним или более бактериофагами и/или полипептидами по изобретению; и (iii) наблюдения (мониторинга) за ростом клеток и/или появлением лизиса после указанного контактирования. Поскольку активность бактериофага и/или выделенных из него продуктов (например, полипептидов или биологически активных фрагментов, вариантов или производных) специфична к видам или штаммам бактерий, наличие или отсутствие чувствительности к одному или более бактериофагам и/или полипептидам по изобретению может служить показателем наличия вида или штамма инфекционных бактерий. Например, уменьшенный рост испытуемых культур после контактирования с бактериофагом, имеющим геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1 или 781, или с выделенным из него полипептидом может быть показателем наличия испытуемого образца, содержащего К. pneumoniae. Подобным образом, бактериофаг, имеющий геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2, или выделенный или полученный из него полипептид могут быть использованы для идентификации инфекции, вызванной A. baumannii; бактериофаг, имеющий геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3, или выделенный или полученный из него полипептид могут быть использованы для идентификации инфекции, вызванной Е.coli; в то время как бактериофаг, имеющий геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4, или выделенный или полученный из него полипептид могут быть использованы для идентификации инфекции, вызванной Р. aeruginosa; а бактериофаг, имеющий геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560 или 1074, или выделенный или полученный из него полипептид могут быть использованы для идентификации инфекции, вызванной S. aureus.
Кроме того, согласно некоторым вариантам бактериофаги и/или полипептиды по изобретению могут быть использованы в биосенсорах в целях диагностики. Применяемый в данной заявке термин "биосенсор" относится к аналитическому прибору для детектирования аналита, в котором биологический компонент соединяется с физико-химическим компонентом детектора. В частности, белки, участвующие в распознавании бактериальных рецепторов, могут быть использованы при создании диагностических биосенсоров.
Согласно некоторым вариантам полипептид по изобретению, содержащий или состоящий из белка хвостового отростка (например, компонента хвостового отростка, хвостового фибриллярного белка, хвостового белка, связанного с адсорбцией, белка рулетки хвостового отростка, субъединицы конусовидной базальной пластинки) или его фрагмента, варианта или производного, выделенных из бактериофага, имеющего геном, содержащий или состоящий из последовательности SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:560, SEQ ID NO:781, SEQ ID NO:1074 (например, из бактериофага F391/08, F394/08, F488/08, F510/08, F44/10, F387/08 или F125/10, соответственно), могут быть использованы в биосенсорах. Например, белок хвостового отростка фага может специфически распознавать один или более видов и/или штаммов бактерий и поэтому может найти применение в биосенсорной диагностике. Детектирование некоторых видов и/или штаммов бактерий с помощью одного или более бактериофагов и/или полипептидов по изобретению может служить показателем наличия вида или штамма инфекционных бактерий.
Согласно некоторым вариантам полипептид по изобретению, используемый в биосенсорах, представляет собой выделенный блок хвостового отростка, содержащий или состоящий из аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266. Согласно другим вариантам полипетид по изобретению содержит фрагмент, вариант или производное SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30, SEQ ID NO:32-35, SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185, SEQ ID NO:190, SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-496, SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549, SEQ ID NO:551, SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004, SEQ ID NO:1053-1060, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250, or SEQ ID NO:1266, при этом указанные фрагмент, вариант или производное способны специфически распознавать вид бактерий, например, специфический вид и/или один или более специфических штаммов бактерий. Такие полипептиды найдут применение, например, в биосенсорах для детектирования специфических бактерий и/или диагностики некоторых инфекций, как описано выше.
Обычно хвостовой белок фага, применяемый в биосенсорах, будет детектировать свою хозяйскую бактерию или один или более специфических видов и/или специфических штаммов бактерии-хозяина. Соответственно, согласно некоторым вариантам данное изобретение предусматривает хвостовой белок, соответствующий аминокислотной последовательности SEQ ID NO:15, SEQ ID NO:26, SEQ ID NO:27, SEQ ID NO:30 или SEQ ID NO:32-35, или его фрагмент, вариант или производное, которые распознают и могут обнаружить один или более штаммов К. pneumoniae. Такое обнаружение может быть показателем инфекции, вызванной К. pneumoniae. Согласно некоторым вариантам данное изобретение предусматривает хвостовой белок, соответствующий аминокислотной последовательности SEQ ID NO:180, SEQ ID NO:183, SEQ ID NO:185 или SEQ ID NO:190, или его фрагмент, вариант или производное, которые распознают и могут обнаружить один или более штаммов A. baumannii. Такое обнаружение может быть показателем инфекции, вызванной A. baumannii. Согласно некоторым вариантам данное изобретение предусматривает хвостовой белок, соответствующий аминокислотной последовательности SEQ ID NO:231, SEQ ID NO:232, SEQ ID NO:235, SEQ ID NO:239-245, SEQ ID NO:248, SEQ ID NO:249, SEQ ID NO:252, SEQ ID NO:254, SEQ ID NO:433-437, SEQ ID NO:489-495 или SEQ ID NO:496, его фрагмент, вариант или производное, которые распознают и могут обнаружить один или более штаммов Е.coli. Такое обнаружение может быть показателем инфекции, вызванной Е.coli.
Согласно некоторым вариантам данное изобретение предусматривает хвостовой белок, соответствующий аминокислотной последовательности SEQ ID NO:544, SEQ ID NO:545, SEQ ID NO:549 или SEQ ID NO:551, его фрагмент, вариант или производное, которые распознают и могут обнаружить один или более штаммов Р. aeruginosa. Такое обнаружение может быть показателем инфекции, вызванной Р. aeruginosa. Согласно некоторым вариантам данное изобретение предусматривает хвостовой белок, соответствующий аминокислотной последовательности SEQ ID NO:629, SEQ ID NO:686, SEQ ID NO:1077, SEQ ID NO:1217, SEQ ID NO:1250 или SEQ ID NO:1266, его фрагмент, вариант или производное, которые распознают и могут обнаружить один или более штаммов S. aureus. Такое обнаружение может быть показателем инфекции, вызванной S. aureus. Согласно некоторым вариантам данное изобретение предусматривает хвостовой белок, соответствующий аминокислотной последовательности SEQ ID NO:789, SEQ ID NO:796-800, SEQ ID NO:806, SEQ ID NO:854, SEQ ID NO:999-1004 или SEQ ID NO:1053-1060, его фрагмент, вариант или производное, которые распознают и могут обнаружить один или более штаммов К. pneumoniae. Такое обнаружение может быть показателем инфекции, вызванной К. pneumoniae.
Согласно некоторым вариантам данное изобретение охватывает применение более чем одного хвостового белка, например, комбинации двух или более хвостовых белков, описанных выше, для биосенсоров с целью детектирования более чем одного вида и/или штамма бактерий. В состав биосенсора могут входить дополнительные белки и/или другие агенты для детектирования тех же самых или других видов бактерий.
ВАРИАНТЫ ПО АМИНОКСЛОТНЫМ ПОСЛЕДОВАТЕЛЬНОСТЯМ
По данному изобретению могут быть созданы варианты аминокислотных последовательностей полипептидов. Согласно нескольким вариантам они могут быть замещенными, инсерционными и/или делеционными вариантами. В делеционных вариантах отсутствует один или более остатков нативного (неизмененного) белка, которые обычно не существенны для функции аминокислот (например, антимикробной или антибактериальной активности). Инсерционные мутанты включают добавление остатков в неконцевую область полипептида. Замещающие варианты обычно включают замену одного остатка аминокислоты на другой в одном или более участках полипептида и могут быть сконструированы для модулирования одного или более свойств полипептида, таких как стабильность к протеолитическому расщеплению, предпочтительно без потери (или значительной потери) других функций или свойств. Замены этого вида предпочтительно являются консервативными, то есть остаток одной аминокислоты заменяется остатком похожей формы и с похожим зарядом. Консервативные замены хорошо известны из уровня техники и включают, например, следующие замены: аланина на серии, аргинина на лизин, аспарагина на глутамин или гистидин, аспартата на глутамат, цистеина на серин, глутамина на аспарагин, глутамата на аспартат, глицина на пролин, гистидина на аспарагин или глутамин, изолейцина на лейцин или валин, лейцина на валин или изолейцин, лизина на аргинин, метионина на лейцин или изолейцин, фенилаланина на тирозин, лейцин или метионин, серина на треонин, треонина на серии, триптофана на тирозин, тирозина на триптофан или фенилаланин и валина на изолейцин или лейцин.
Как только ареалы генов будут проидентифицированы как гены, придающие конкретную антибактериальную активность, например, как лизин, описанный в данной заявке, можно применять точечный мутагенез для определения со всей точностью, какие аминокислотные остатки являются важными для наличия антибактериальной активности. Таким образом, специалист в данной области может проводить, например, единичные замены оснований в пределах нити ДНК для получения измененного кодона и/или миссенс-мутации, которые сохраняют желаемое свойство.
Предпочтительно, когда мутация аминокислот белка приводит к созданию эквивалентной или даже улучшенной молекулы второго поколения. Например, некоторые аминокислоты могут быть заменены на другие аминокислоты в белковой структуре без различимой или существенной потери функции белка (например, антибактериальной или антимикробной активности). При осуществлении таких изменений следует учитывать гидропатический индекс аминокислот. Значение гидропатического индекса аминокислот в придании интерактивной биологической функции белка в данной области общеизвестно. Принято считать, что относительно гидропатический характер аминокислоты содействует образованию вторичной структуры получаемого белка, что в свою очередь определяет взаимодействие белка с другими молекулами, например, взаимодействие с пептидогликаном во внешней оболочке грамположительной бактерии. Каждая аминокислота имеет свой гидропатический индекс на основе ее гидрофобности и характеристик заряда, например: изолейцин (+4.5); валин (+4.2); лейцин (+3.8); фенилаланин (+2.8); цистеин/цистин (+2.5); метионин (+1.9); аланин (+1.8); глицин(-0.4); треонин (-0.7); серии (-0.8); триптофан (-0.9); тирозин (-1.3); пролин (-1.6); гистидин (-3.2); глутамат (-3.5); глутамин (-3.5); аспартат (-3.5); аспарагин (-3.5); лизин (-3.9); и аргинин (-4.5). Из уровня техники известно также, что подобные замены аминокислот могут эффективно производиться на основе гидрофильности. Как и в случае гидрофобности, каждая аминокислота получила свой индекс гидрофильности: аргинин (+3.0); лизин (+3.0); аспартат (+3.0±1); глутамат (-0.5±1); аланин (-0.5); гистидин (-0.5); цистеин (-1.0); метионин (-1.3); валин (-1.5); лейцин (-1.8); изолейцин (-1.8); тирозин (-2.3); фенилаланин (-2.5) и триптофан (-3.4). Эквивалентные молекулы могут быть получены путем замены одной аминокислоты на другую, при этом их гидропатические индексы и/или их индексы гидрофильности отличаются друг от друга на ±2, предпочтительно на ±1, или наиболее предпочтительно, на ±5.
Согласно некоторым вариантам данное изобретение охватывает выделенные полипептиды, которые содержат 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более модификаций аминокислот (например, инсерций, замен, делеций и т.д.) относительно аминокислотных последовательностей, описанных в данной заявке. Согласно предпочтительным вариантам мутация (мутации) осуществляется(-ются) таким образом, что биологическая активность конкретного полипептида сохраняется или практически сохраняется. Например, данное изобретение предусматривает полипептиды, выделенные из бактериофагов F387/08, F391/08, F394/08, F488/08, F510/068, F44/10 и/или F125/10, которые мутированы так, что они содержат 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 или более модификаций относительно аминокислотных последовательностей, описанных в данной заявке, и которые проявляют антибактериальную активность в отношении одного или более видов или штаммов грамположительных или грамотрицательных бактерий, например, против К. pneumoniae, A. baumannii, E.coli, Р. aeruginosa и/или S. aureus. Согласно конкретным вариантам полипептиды, полученные из фагов F387/08 или F391/08, проявляют антибактериальную или антимикробную активность, например, лизирующую киллерную активность, против по меньшей мере К. Pneumonia; полученные из фага F394/08 - против по меньшей мере А. baumannii; полученные из фага F488/08 - против по меньшей мере E.coli; полученные из фага F510/08 - против по меньшей мере Р. aeruginosa, и полученные из фагов F44/10 или F 125/10 - против по меньшей мере S. aureus.
ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ПОЛИПЕПТИДЫ ПО ИЗОБРЕТЕНИЮ
Данное изобретение предусматривает также полинуклеотиды, содержащие нуклеотидную последовательность, кодирующую полипептид по изобретению. Настоящее изобретение охватывает также полинуклеотиды, которые гибридизуются в строгих условиях, в промежуточных условиях и в условиях пониженной жесткости, например, как указано выше, с полинуклеотидами, которые кодируют полипептид по изобретению и которые кодируют модифицированные полипептиды, которые обладают антибиотической и/или другой биологической активностью.
Полинуклеотиды могут быть получены, а нуклеотидная последовательность полинуклеотидов определена, любым способом, известным из уровня техники. Например, полинуклеотид, кодирующий полипептид по изобретению, может быть получен из нуклеиновой кислоты из подходящего источника (например, бактериофагов F387/08, F391/08, F394/08, F488/08, F510/08, F44/10 и/или F125/10). Нуклеотидные последовательности могут быть выделены из фаговых геномов обычными методами, известными из уровня техники (см., например, источники Carlson, "Working with bacteriophage: common techniques and methodological approaches," In, Kutter and Sulakvelidze (Eds) Bacteriophage: Biology and Applications, 5th ed. CRC Press (2005); которые включены полностью в данную заявку посредством отсылки). Если источник, содержащий нуклеиновую кислоту, кодирующую определенный полипептид, не доступен, но аминокислотная последовательность полипептида по изобретению известна, нуклеиновая кислота, кодирующая полипептид, может быть получена химическим способом и клонирована в реплицирующихся клонирующих векторах способом, хорошо известным из уровня техники.
Как только нуклеотидная последовательность полипептида по изобретению определена, нуклеотидной последовательностью полипептида можно управлять, используя методы манипулирования нуклеотидными последовательностями, известные из уровня техники, например, технологию рекомбинантных ДНК, сайт-направленный мутагенез, ПЦР и т.д. (см., например, методы, описанные в источниках Sambrook et al., 1990, Molecular Cloning, A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory, Cold Spring Harbor, NY и Ausubel et al., eds., 1998, Current Protocols in Molecular Biology, John Wiley & Sons, NY, которые оба полностью включены в данную заявку посредством отсылки), для получения полипептидов, содержащих различные аминокислотные последовательности, например, для введения аминокислотных замен, делеций и/или инсерций.
Согласно некоторым вариантам предусмотрена нуклеотидная последовательность, кодирующая одну или более ORF, показанных на ФИГУРАХ 2, 4, 6, 8, 10, 12 и 14. Согласно некоторым вариантам предусмотрена нуклеотидная последовательность, кодирующая вариант, фрагмент или производное одной или более ORF, показанных на ФИГУРАХ 2, 4, 6, 8, 10, 12 и 14, при этом эти вариант, фрагмент или производное проявляют антибактериальную или антимикробную активность (например, лизирующую киллерную активность) в отношении одного или более штаммов К. pneumoniae, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:1 или SEQ ID NO:781; и/или в отношении одного или более штаммов A. baumannii, например, в отношении бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:2; и/или в отношении одного или более штаммов Е.coli, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:3; и/или в отношении одного или более штаммов Р. aeruginosa, например, в отношении бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:4; и/или в отношении одного или более штаммов S. aureus, например, против бактериофага, имеющего геном, содержащий или состоящий из последовательности нуклеиновой кислоты SEQ ID NO:560 или SEQ ID NO:1074.
РЕКОМБИНАНТНАЯ ЭКСПРЕССИЯ МОЛЕКУЛ ПО ИЗОБРЕТЕНИЮ
После получения последовательности нуклеиновой кислоты, кодирующей молекулу по данному изобретению (например, полипептид), методом рекомбинантных ДНК, хорошо известным из уровня техники, может быть получен вектор для получения молекул. Методы, хорошо известные специалистам в данной области, могут быть применены для конструирования экспрессионных векторов, содержащих кодирующие последовательности для молекул по изобретению и соответствующих сигналов транскрипции и трансляции. Эти методы включают, например, in vitro технологию рекомбинантных ДНК, методы синтеза и in vivo генетическую рекомбинацию. (См., например, методы, описанные Sambrook et al., 1990, Molecular Cloning, A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory, Cold Spring Harbor, NY и Ausubel et al. eds., 1998, Current Protocols in Molecular Biology, John Wiley & Sons, NY).
Данное изобретение предусматривает векторы экспрессии, кодирующие полипептиды по изобретению. Вектор экспрессии, содержащий нуклеотидную последовательность молекулы, идентифицированную способами по изобретению, может быть перенесен в клетку-хозяина обычными методами (например, электропорацией, липосомальной трансфекцией и методом осаждения из растворов фосфата кальция) и затем трансфецированные клетки культивируют обычными методами для получения молекул по изобретению. Согласно предпочтительным вариантам клетка-хозяин отличается от клеток родительских бактерий, из которых бактериофаг, содержащий указанную последовательность, произведен. Согласно конкретным вариантам экспрессия молекул по изобретению регулируется конститутивным, индуцируемым или ткане-специфическим промотором. Согласно конкретным вариантам экспрессионный вектор представляет собой pQE-30 (Qiagen) или рЕТ-29(а) (Novagen).
Клетки хозяина, применяемые для экспрессии молекул, идентифицируемых способами по изобретению, могут быть бактериальными клетками (предпочтительно, не чувствительными к белку бактериофага или его варианту, производному или фрагменту по изобретению). Для экспрессии молекул, идентифицированных по изобретению, могут быть использованы различные системы экспрессии хозяин-вектор. Такие системы экспрессии хозяин-вектор представляют собой носители, с помощью которых могут быть получены и затем очищены молекулы согласно данному изобретению, но также представляют собой клетки, которые, после трансформирования или трансфекции при помощи соответствующей нуклеотидной кодирующей последовательности, экспрессируют in situ молекулы по изобретению. Они включают, но без ограничения, микроорганизмы, такие как бактерии, которые не чувствительны к белку бактериофага или его варианта, производного или фрагмента (например, В. subtilis), и трансформированы с помощью векторов экспрессии рекомбинантной ДНК бактериофага, плазмидной ДНК, космидной ДНК, содержащих кодирующие последовательности для молекул, идентифицированных способами по изобретению; дрожжи (например, Saccharomyces Pichid), трансформированные с помощью рекомбинантных векторов экспрессии дрожжей, содержащих кодирующие последовательности для молекул, идентифицированных способами по изобретению; системы клеток насекомых, инфицированных рекомбинантными вирусными векторами экспрессии (например, baculovirus), содержащими кодирующие последовательности для молекул, идентифицированных способами по изобретению; системы растительных клеток, инфицированных рекомбинантными вирусными векторами экспрессии (например, вирусом мозаики цветной капусты (CaMV) и вирусом мозаики табака (TMV) или трансформированных с помощью рекомбинантных плазмидных векторов экспрессии (например, Ti плазмиды), содержащих кодирующие последовательности для молекул, идентифицированных способами по изобретению; или систем клеток млекопитающего (например, клеток COS, СНО, ВНК, 293, 293Т, 3Т3, лимфатических клеток (см. патент США №5,807,715), клеток С.6 (человеческие ретинальные клетки, полученные Cnicell), содержащих рекомбинантные конструкты экспрессии, содержащие промоторы, полученные из генома человека (например, металлотионеиновый промотор) или из человеческих вирусов (например, поздний промотор аденовируса; промотор вируса 7.5К вирусной вакцины), содержащих последовательности, кодирующие молекулы, идентифицированные способами по изобретению.
В бактериальных системах, не чувствительных к белку фага или его варианту, производному или фрагменту по изобретению, в зависимости от желаемого применения, предназначенного для экспрессируемой молекулы, может быть выбран ряд экспрессионных векторов. Например, когда должно быть получено большое количество такого белка с целью получения фармацевтических композиций полипептида по изобретению, желательными являются экспрессионные векторы, которые направляют высокий уровень экспрессии слитых белков, которые легко очищаются. Такие векторы включают, но без ограничения, экспрессионный вектор pUR278 E.coli (Ruther et al., 1983, EMBO J. 2:1791), в котором белковая последовательность может быть лигирована индивидуально в векторе в рамку с кодирующей областью lac Z таким образом, что образуется слитый белок; векторы pIN (Inouye & Inouye, 1985, Nucleic Acids Res. 13: 3101-3109; Van Heeke & Schuster, 1989, J. Biol. Chem. 24: 5503-5509); и т.п. Для экспрессии чужеродных полипептидов, таких как белки слияния с глютатион-S-трансферазой (GST), могут быть также использованы векторы pGEX. В общем, такие белки слияния являются растворимыми и могут быть легко очищены из лизированных клеток путем адсорбции и связывания с гранулами матриксной глютатион-агарозы с последующим элюированием в присутствии свободного глютатиона. Векторы pGEX сконструированы так, что включают сайты расщепления протеазы тромбином или фактором Ха, и клонированный целевой генный продукт может быть высвобожден из GST. В системе клеток насекомых в качестве вектора экспрессии чужеродных генов используется вирус ядерного полиэдроза Autographa californica (AcNPV). Этот вирус предпочтительно выращивать в клетках Spodoptera frugiperda. Последовательность, кодирующая полипептид, может быть индивидуально клонирована в областях вируса, относящихся к незаменимым (например, в гене полиэдрина) и помещена под контроль промотора AcNPV (например, промотора полиэдрина). Как только молекула по изобретению (например, полипептиды) подверглась рекомбинантной экспрессии, она может быть очищена любым методом очистки полипептидов, известным из уровня техники, например, методом хроматографии (в том числе, методами ионообменной, аффинной хроматографии и хроматографии на колонке), центрифугирования, методом дифференциальной растворимости или любым другим обычным методом очистки полипептидов или антител. После ознакомления с приведенным выше описанием специалист в данной области может произвести некоторые модификации и усовершенствования. Очевидно, что все такие модификации и усовершенствования не включены в данное описание в целях сжатости и четкости изложения, но они входят в объем данного изобретения, определенный формулой изобретения.
ПРИМЕРЫ
Следует иметь в виду, что следующие примеры и приведенные варианты изобретения описаны только с целью иллюстрации изобретения и что специалистам в данной области известно, как осуществить различные модификации или изменения в свете этого описания, эти модификации или изменения входят в объем данного изобретения, который определяется приведенной ниже формулой изобретения. Все публикации, патенты и заявки на патенты, ссылки на которые приведены в тексте описания, включены в данную заявку посредством отсылок полностью для всех целей.
Если иное не указано, бактериофаги по изобретению были выделены, обработаны и проанализированы в соответствии со следующими методами.
ОЧИСТКА ФАГОВ
Исходные препараты бактериофагов, выделенные из клинических образцов, готовили в соответствии с протоколами, описанными в публикации Carlson, "Working with bacteriophage: common techniques and methodological approaches," In, Kutter and Sulakvelidze (Eds) Bacteriophage: Biology and Applications, 5th ed. CRC Press (2005) ("Carlson," эта публикация включена в данную заявку полностью посредством отсылки). Исходные бактериофаги концентрировали путем осаждения с помощью ПЭГ согласно протоколу, описанному в публикации Carlson and Yamamoto et al., 2004, PNAS 101:6415-6420. Вкратце, исходный препарат инкубировали в 1 М NaCl в течение 1 ч при перемешивании при температуре 4°C. Затем постепенно добавляли ПЭГ 8000 (AppliChem, Cheshire, MA) до получения конечной концентрации равной 10% (вес/об). Затем смесь инкубировали в течение ночи при температуре 4°C. После этого осадок снова суспендировали в буфере SM (0,05 М Tris-HCE при pH 7,4, 0,1 М NaCl, 10 мМ MgSO4) с желатином (1% вес/об) и центрифугировали при 1000 об/мин в течение 10 мин при температуре 4°C. Надосадочную жидкость, содержащую суспендированный фаг, сохраняли для последующей очистки. Надосадочную жидкость очищали, используя градиент CsCl, в соответствии с методикой Carlson.
CsCl удаляли из очищенного и концентрированного фага путем диализа. Диализная мембрана Cellu.Sep H1 High Grade Regenerated Cellulose Tubular Membrane (Cellu.Sep, River Street, USA) была подготовлена в соответствии с инструкциями производителя. Диализ включал первую инкубацию в течение 30 мин в 100 мМ Tris-HCl и 3 М NaCl (pH 7,4) при температуре 4°C. Затем следовала вторая стадия инкубации в течение 30 мин в 100 мМ Tris-HCl и 0,3 М NaCl (pH 7,4) при температуре 4°C. После диализа суспендированный фаг удаляли из диализного мешка и хранили при температуре 4°C.
ЭКСТРАКЦИЯ ДНК ФАГА
К 5 мл очищенного и концентрированного фага добавляли 20 мМ ЭДТА при pH 8,0, ДСН 0,5% (ч/об) и протеиназу Proteinase К до получения конечной концентрации, равной 40 мкг/мл. Смесь инкубировали при температуре 56°C в течение 1 ч. Осуществляли последовательные экстракции смесью фенол:хлороформ:спирт в соотношении 25:24:1 до появления четкой границы раздела водной и органической фаз. Водную фазу обрабатывали равным объемом хлороформа и центрифугировали (13000 g) в течение 10 мин при температуре 4°C. Водную фазу снова удаляли и осаждали ДНК путем добавления двух объемов абсолютного этилового спирта и инкубирования в течение 30 мин при температуре 20°C. Затем образцы центрифугировали (11000 g) в течение 30 мин при температуре 4°C. Осадок промывали 70%-ным этиловым спиртом при комнатной температуре и вновь суспендировали в 50 мкл ультрачистой воды (Gibco, California). Концентрация ДНК была определена путем измерения абсорбции при длине волны 260 нм в спектрофотометре ND-1000. Целостность выделенной ДНК фага определяли методом электрофореза в 1%-ном геле агарозы.
АНАЛИЗ ГЕНОМОВ ФАГА
Секвенирование генома бактериофага позволило идентифицировать потенциальные открытые рамки считывания (ORF) в геноме. Предполагаемые ORF были использованы для поиска гомологичных последовательностей ДНК в базе данных коллекции нуклеотидов NCBI с помощью программы BLASTN (см, например, Zhang et al., 2000, J. Comput. Biol. 7:203-214).
ПРИМЕР 1: БАКТЕРИОФАГ F391/08
Сравнение предполагаемых ORF генома бактериофага F391/08 с последовательностями в базе данных NCBI по нуклеотидам показало, что только небольшие части генома (≤ 11% перекрытия генома) были гомологичны известным последовательностям. Схематическая организация генома фага F391/08 показана на ФИГУРЕ 1. ORF фага F391/08, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 2. Предсказание orf проводили путем интегрирования результатов, полученных с использованием программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологичных белков выполняли с помощью программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных NCBI по статистически неопределимым белковым последовательностям. Консервативные домены белков были предсказаны с помощью специализированной программы NCBI BLAST (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240). orf, продукты которых были гомологичны тем же самым белкам (белку) указаны тем же номером с добавлением буквы нижнего регистра, что показано на ФИГУРЕ 2. Идентификацию предполагаемых генов транспортной РНК (тРНК) проводили, применяя программу tRNAscan-SE progam (Lowe, T.M. et al., 1997. Nucleic Acids Res., 25: 955-964).
В Таблице 1 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F391/08 в отношении 100 штаммов Klebsiella sp. (86 штаммов К. pneumoniae; 12 штаммов К. oxytoca и 2 штамма Klebsiella sp.), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, приготовленной из очищенного CsCl лизата. Чувствительность каждого штамма к фагу оценивали на основе относительной шкалы ранжирования от мутного ореола лизиса (+) до прозрачного ореола (++++). Стерильные пятна, возникшие из бляшек выделенного фага, указаны в бляшкообразующих единицах (б.о.е.), а устойчивость к фаговой инфекции - как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
ПРИМЕР 2: БАКТЕРИОФАГ F394/08
Сравнение предполагаемых ORF генома бактериофага F394/08 с последовательностями в базе данных NCBI по нуклеотидам не показало значительной гомологии с известными последовательностями, в отличие от наблюдаемого для небольших частей генома (≤ 1% перекрытия генома). Схематическая организация генома F394/08 показана на ФИГУРЕ 3. ORF в F394/08, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 4. Предсказание ORF осуществляли путем интегрирования результатов, полученных с помощью программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологии белков проводили при помощи программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных NCBI статистически неопределимых белковых последовательностей. Домены консервативных белков предсказывали, используя специальную программу NCBI BLAST (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240). Orfs, которые были гомологичны тем же самым белкам (тому же белку) обозначены на ФИГУРЕ 4 тем же самым номером с добавлением буквы нижнего регистра,. Идентификация предполагаемых генов транспортной РНК (тРНК) проводилась с помощью программы tRNAscan-SE (Lowe, T.M. et al., 1997. Nucleic Acids Res., 25: 955-964).B Таблице 2 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F394/08 в отношении 100 штаммов Acinetobacter sp. (93 штаммов A. baumannii; 6 штаммов A. calcoaceticus; и 1 штамм A. lwqffi), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, полученной из лизата, очищенного CsCl. Чувствительность каждого штамма к фагу оценивали на основе шкалы относительного ранжирования от мутного (+) до прозрачного (++++) ореола лизиса. Пятна, возникшие от бляшек выделенного фага, показаны в бляшкообразующих единицах (б.о.е.), а стойкость к инфекции, вызванной фагом, показана как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
ПРИМЕР 3: Бактериофаг F488/08
Сравнение предполагаемых ORF генома бактериофага F488/08 с последовательностями в базе данных NCBI по нуклеотидам показало, что около 94% ДНК фага F488/08 подобны ДНК фага Enterobaceria RB14, со степенью идентичности индивидуальных ORF в интервале от 70 до 100%. Схематическая организация генома фага F488/08 показана на ФИГУРЕ 5. ORF фага F488/08, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 6. Предсказание ORF осуществляли путем интегрирования результатов, полученных с помощью программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологии белков проводили при помощи программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных NCBI по статистически неопределимым белковым последовательностям. Домены консервативных белков предсказывали, используя специальную программу NCBI BLAST (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240). ORF которые были гомологичны тем же самым белкам (тому же белку) обозначены на ФИГУРЕ 6 тем же самым номером с добавлением строчной буквы. Идентификация предполагаемых генов транспортной РНК (тРНК) проводилась с помощью программы tRNAscan-SE (Lowe, T.M. et al., 1997. Nucleic Acids Res., 25: 955-964). В Таблице 3 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F488/08 в отношении 100 штаммов Escherichia coli (ECO), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, полученной из лизата, очищенного CsCl. Чувствительность каждого штамма к фагу оценивали на основе шкалы относительного ранжирования от мутного (+) до прозрачного (++++) ореола лизиса.
Пятна, возникшие от бляшек выделенного фага, показаны в бляшкообразующих единицах (б.е), а стойкость к инфекции, вызванной фагом показана как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
ПРИМЕР 4: Бактериофаг F510/08
Сравнение предполагаемых ORF генома бактериофага F510/08 с последовательностями в базе данных NCBI по нуклеотидам показало, что около 95% ДНК фага F510/08 подобны в высшей степени ДНК фага Pseudomonas LUZ19, со степенью идентичности индивидуальных ORF в интервале от 89 до 97%. Схематическая организация генома фага F510/08 показана на ФИГУРЕ 7. ORF фага F510/08, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 8. Предсказание ORF осуществляли путем интегрирования результатов, полученных с помощью программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологии белков проводили при помощи программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных NCBI статистически неопределимых белковых последовательностей. Домены консервативных белков предсказывали, используя специальную программу NCBI BLAST (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240). ORF, которые были гомологичны тем же самым белкам (тому же белку) обозначены на ФИГУРЕ 8 тем же самым номером с добавлением строчной буквы. Идентификация предполагаемых генов транспортной РНК (тРНК) проводилась с помощью программы tRNAscan-SE (Lowe, T.M. et al., 1997. Nucleic Acids Res., 25: 955-964). В Таблице 4 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F510/08 против 100 штаммов Pseudomonas aeruginosa (PSA), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, полученной из лизата, очищенного CsCl. Чувствительность каждого штамма к фагу оценивали на основе шкалы относительного ранжирования от мутного (+) до прозрачного (++++) ореола лизиса.
Пятна, возникшие от бляшек выделенного фага, приведены в бляшкообразующих единицах (б/е), а стойкость к инфекции, вызванной фагом показана как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
ПРИМЕР 5: Бактериофаг F44/10
Сравнение предполагаемых ORF генома бактериофага F44/10 с последовательностями в базе данных NCBI по нуклеотидам показало, что около 81% ДНК фага F44/10 подобны ДНК фага Staphylococcus К, со степенью идентичности индивидуальных ORF в интервале от 80 до 99%. Схематическая организация генома фага F44/10 показана на ФИГУРЕ 9. ORF фага F44/10, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 10. Предсказание от/осуществляли путем интегрирования результатов, полученных с помощью программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологии белков проводили при помощи программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных статистически неопределимых белковых последовательностей NCBI. Домены консервативных белков предсказывали, используя специальную программу NCBI BLAST (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240). Orfs, которые были гомологичны тем же самым белкам (тому же белку) обозначены на ФИГУРЕ 10. тем же самым номером с добавлением буквы нижнего регистра. Как ранее сообщалось для фага Staphylococcus К, предполагаемый ген полимеразы (orf1 14a, orf1 14b) может содержать интрон-подобную последовательность. См. (O’Flaherty et al., 2004). Идентификация предполагаемых генов транспортной РНК (тРНК) проводилась с помощью программы tRNAscan-SE (Lowe, T.M. et al., 1997. Nucleic Acids Res., 25: 955-964). В Таблице 5 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F44/10 против 100 штаммов Staphylococcus aureus (STA), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, полученной из лизата, очищенного CsCl. Чувствительность каждого штамма к фагу оценивали на основе шкалы относительного ранжирования от мутного (+) до прозрачного (++++) ореола лизиса.
Пятна, возникшие от бляшек выделенного фага, показаны в бляшкообразующих единицах (б.е), а стойкость к инфекции, вызванной фагом показана как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
ПРИМЕР 6: Бактериофаг F387/08
Сравнение предполагаемых ORF генома бактериофага F387/08 с последовательностями в базе данных NCBI по нуклеотидам NCBI не показало значительной гомологии с известными последовательностями, в отличие от наблюдаемого для небольших частей генома (≤ 12% перекрытия генома). Схематическая организация генома F387/08 показана на ФИГУРЕ 11. ORF фага F387/08, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 12. Предсказание orf осуществляли путем интегрирования результатов, полученных с помощью программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологии белков проводили при помощи программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных NCBI. статистически неопределимых белковых последовательностей Домены консервативных белков предсказывали, используя специальную программу BLAST NCBI (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240).
В Таблице 6 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F387/08 против 100 штаммов Klebsiella sp.(86 штаммов К. pneumoniae; 12 штаммов К. oxytoca; и 2 штамма Klebsiella sp.), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, полученной из лизата, очищенного CsCl. Чувствительность каждого штамма к фагу оценивали на основе шкалы относительного ранжирования от мутного (+) до прозрачного (++++) ореола лизиса. Пятна, возникшие от бляшек выделенного фага, показаны в бляшкообразующих единицах (б.о.е.), а устойчивость к инфекции, вызванной фагом, показана как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
ПРИМЕР 7: Бактериофаг F125/10
Сравнение предполагаемых ORF генома бактериофага F125/10 с последовательностями в базе данных по нуклеотидам NCBI показало, что около 87% ДНК фага F125/10 подобны в высшей степени ДНК фага Staphylococcus A5W, со степенью идентичности индивидуальных ORF в интервале от 77 до 99%. Схематическая организация генома фага F125/10 показана на ФИГУРЕ 13. ORF фага F125/10, их кодированные аминокислотные последовательности и известные гомологичные белки показаны на ФИГУРЕ 14. Предсказание orf осуществляли путем интегрирования результатов, полученных с помощью программ GeneMark.hmm и MetaGeneAnnotator programs (Besemer, J. and Borodovsky, M. 1999. Nucleic Acids Res., 27: 3911-3920; Noguchi, H. et al., 2008. DNA Res., 15: 387-396). Поиски гомологии белков проводили при помощи программы BLASTP (Alschul, S.F. et al., 1997. Nucleic Acids Res., 25: 3389-33402), используя базу данных NCBI статистически неопределимых белковых последовательностей NCBI. Домены консервативных белков предсказывали, используя специальную программу NCBI BLAST (Marchler-Bauer, A. et al., 2007. Nucleic Acids Res. 35: 237-240). Orf, которые были гомологичны тем же самым белкам (тому же белку) обозначены на ФИГУРЕ 14 тем же самым номером с добавлением буквы нижнего регистра. Как ранее сообщалось для фага Staphylococcus К (O’Flaherty et al., 2004, J. of Bacteriology 186(9):2862-2871), и фага Twort (Landthaler et al., 2002, Nucleic Acids Research 30(9):1935-1943), были обнаружены гены, прерывающие интроны, участвующие в метаболизме ДНК; и предполагаемая большая субъединица гена терминазы (orf153a, orf153b) может содержать интрон-подобную последовательность (orf154*). В Таблице 7 ниже приведены результаты спот-тестов, которые оценивали круг хозяев и активность бактериофага F125/10 против 98 штаммов Staphylococcus aureus (STA), выделенных из клинических образцов. Каждая проба содержала 5 мкл суспензии бактериофага с указанными титрами, полученной из лизата, очищенного CsCl. Чувствительность каждого штамма к фагу оценивали на основе шкалы относительного ранжирования от мутного (+) до прозрачного (++++) ореола лизиса.
Пятна, возникшие от бляшек выделенного фага, показаны в бляшкообразующих единицах (б.о.е.), а устойчивость к инфекции, вызванной фагом, показана как (-). Показано также количество штаммов, обладающих фенотипом особенной чувствительности.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ КОКТЕЙЛЯ, СОДЕРЖАЩИЕ АНТИБАКТЕРИАЛЬНЫЕ ФАГИ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2654596C2 |
| БАКТЕРИОФАГИ, БЕЛКИ БАКТЕРИОФАГОВ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2671110C2 |
| БАКТЕРИОФАГ, ОБЛАДАЩИЙ АКТИВНОСТЬЮ ПРОТИВ PSEUDOMONAS AERUGINOSA, БЕЛКИ БАКТЕРИОФАГА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2580248C9 |
| Штамм бактериофага Pseudomonas phage Ka1 для лечения и/или профилактики инфекционных заболеваний, вызываемых Pseudomonas aeruginosa | 2024 |
|
RU2831173C1 |
| ЛИЗИНЫ АЦИНЕТОБАКТЕРОВ | 2015 |
|
RU2725809C2 |
| ПОЛИНУКЛЕОТИДЫ И ПОЛИПЕПТИДЫ ФАГА φ-mru, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2520738C2 |
| СИСТЕМА ЭКСПРЕССИИ И СЕКРЕЦИИ | 2013 |
|
RU2670491C2 |
| ГЕНЫ И БЕЛКИ ДЛЯ БИОСИНТЕЗА ЛАНТИБИОТИКА 107891 | 2007 |
|
RU2441915C9 |
| Новые способы дисплея циклических пептидов на частицах бактериофага | 2015 |
|
RU2702087C2 |
| КОМПОЗИЦИЯ АНТИБАКТЕРИАЛЬНАЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ (ВАРИАНТЫ), ШТАММЫ БАКТЕРИОФАГОВ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ | 2015 |
|
RU2628312C2 |
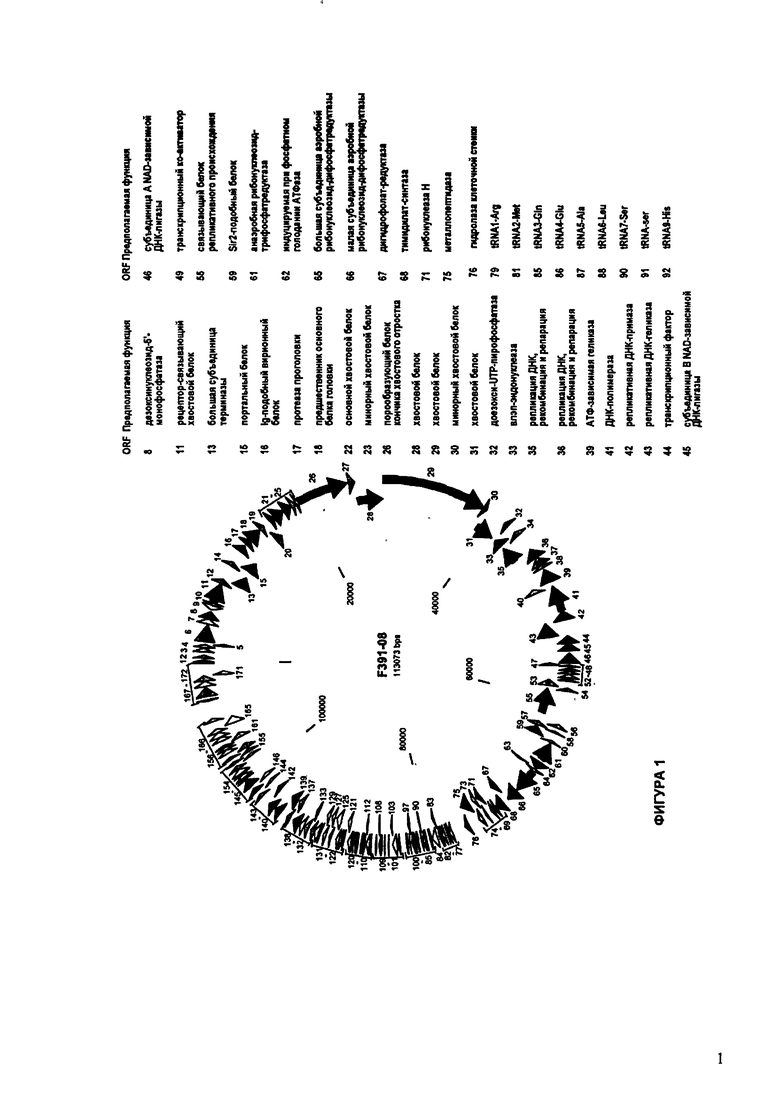
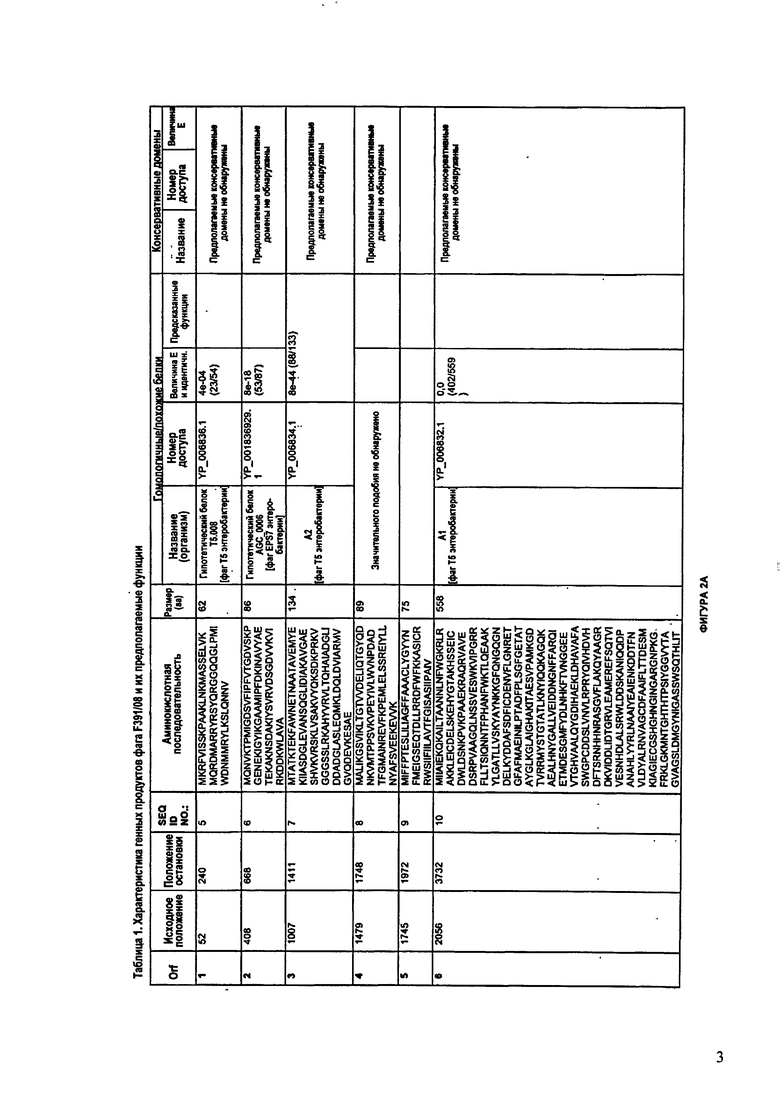
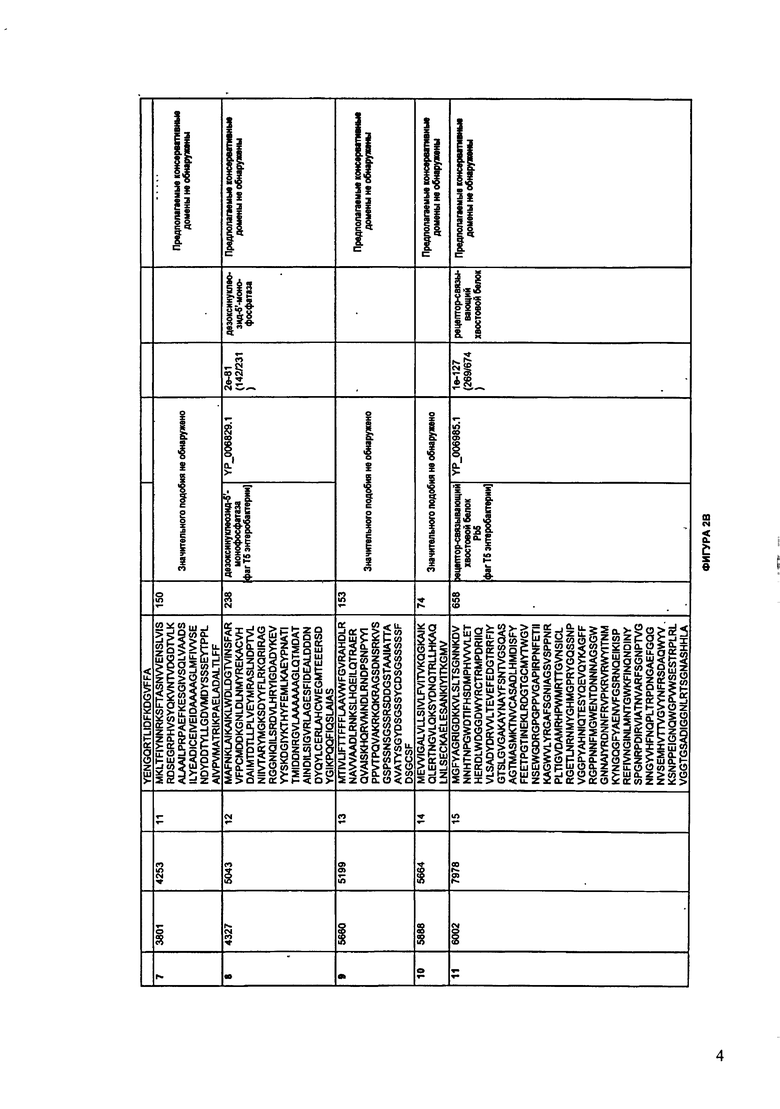
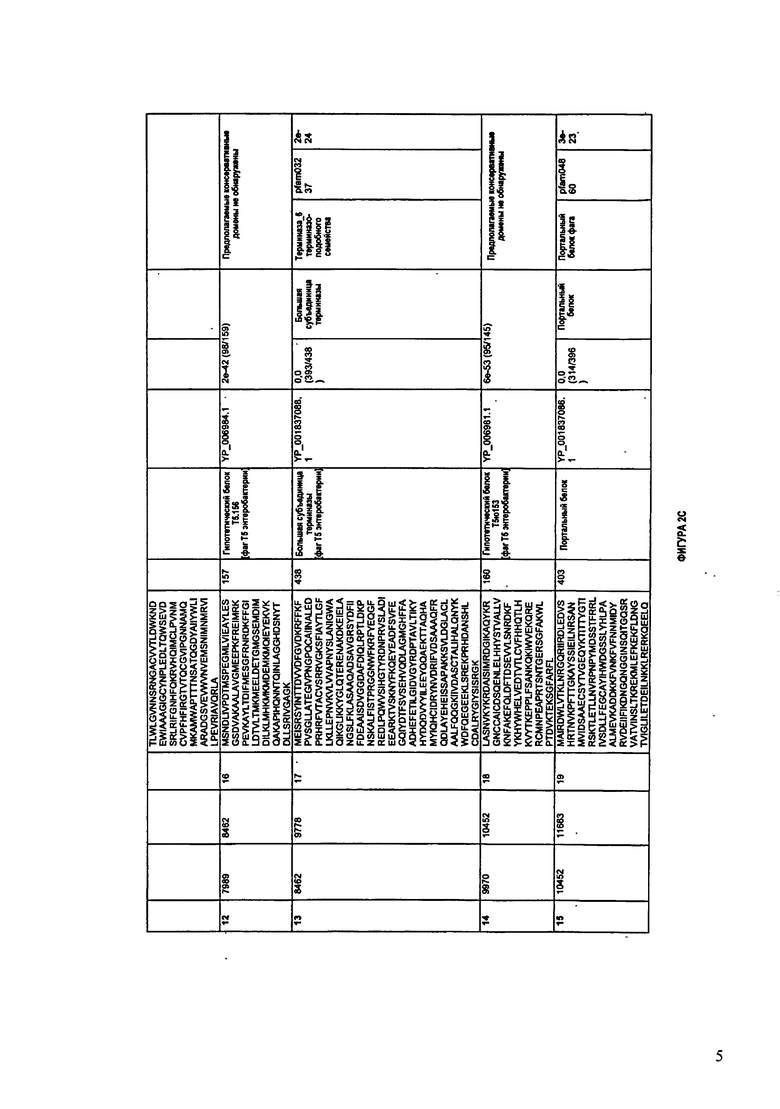
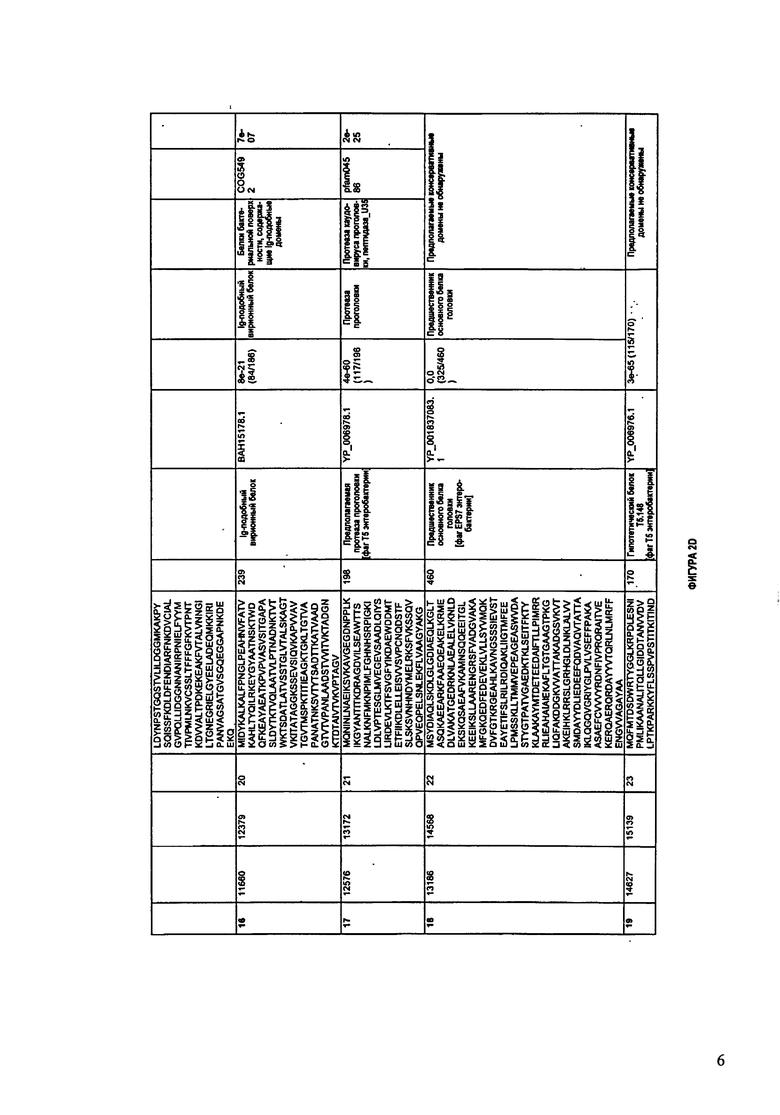







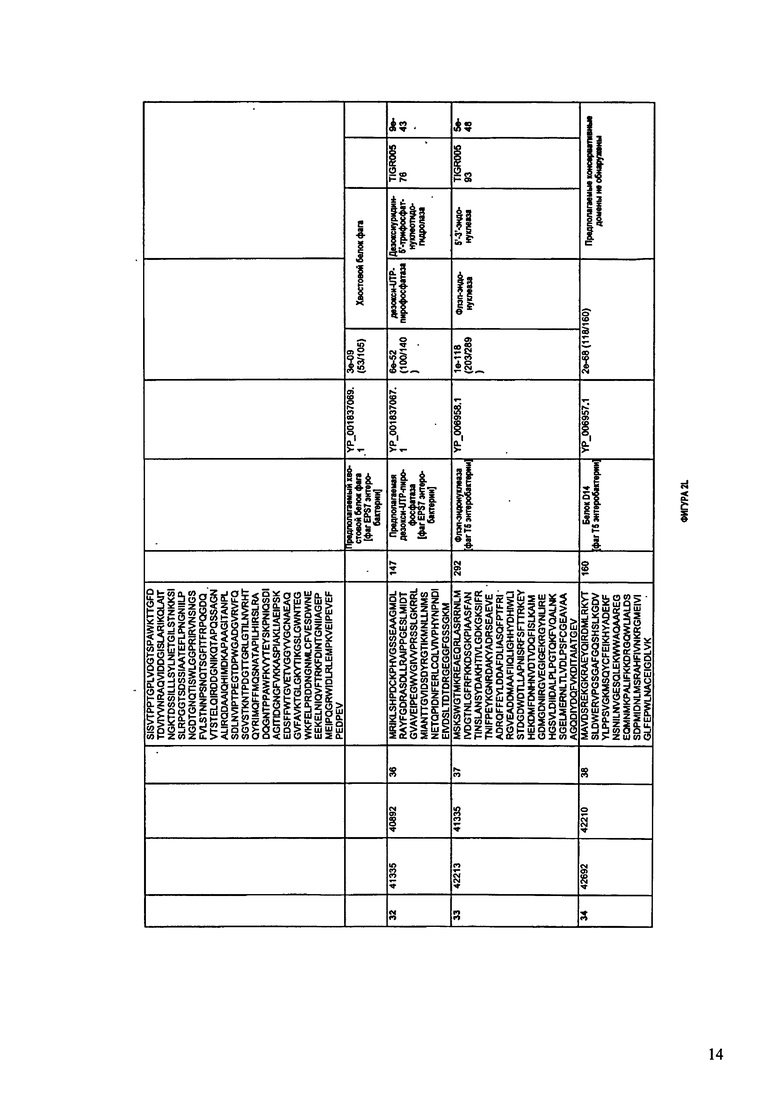

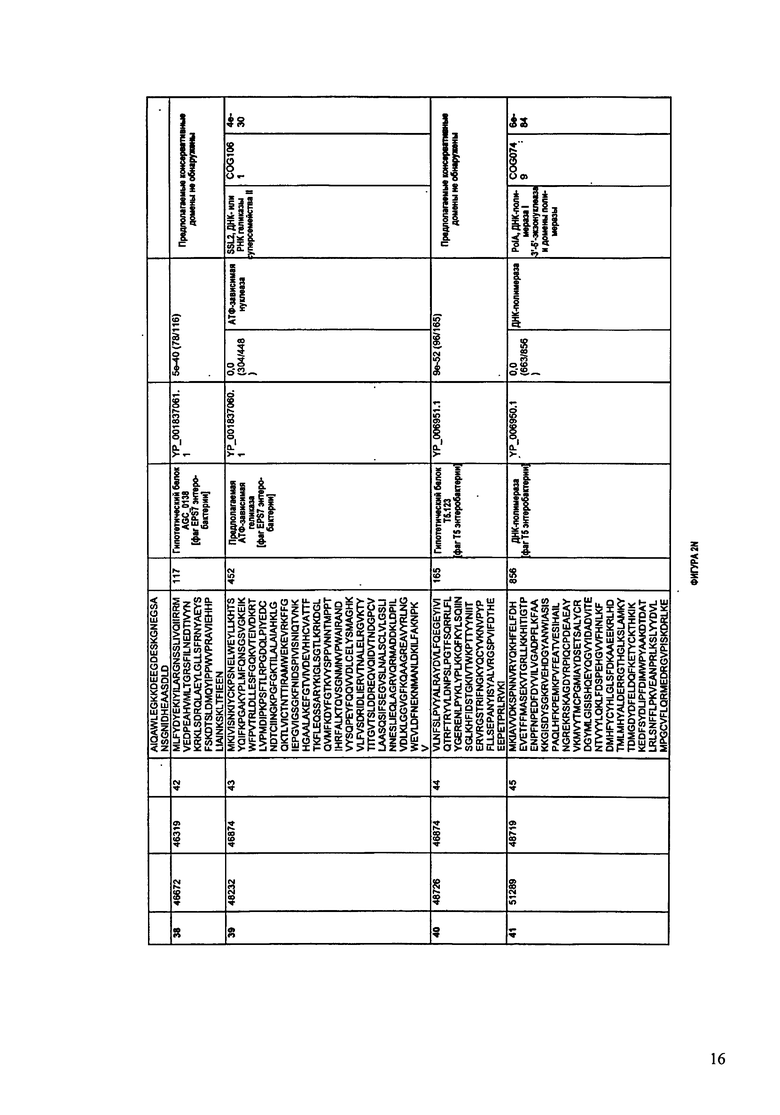
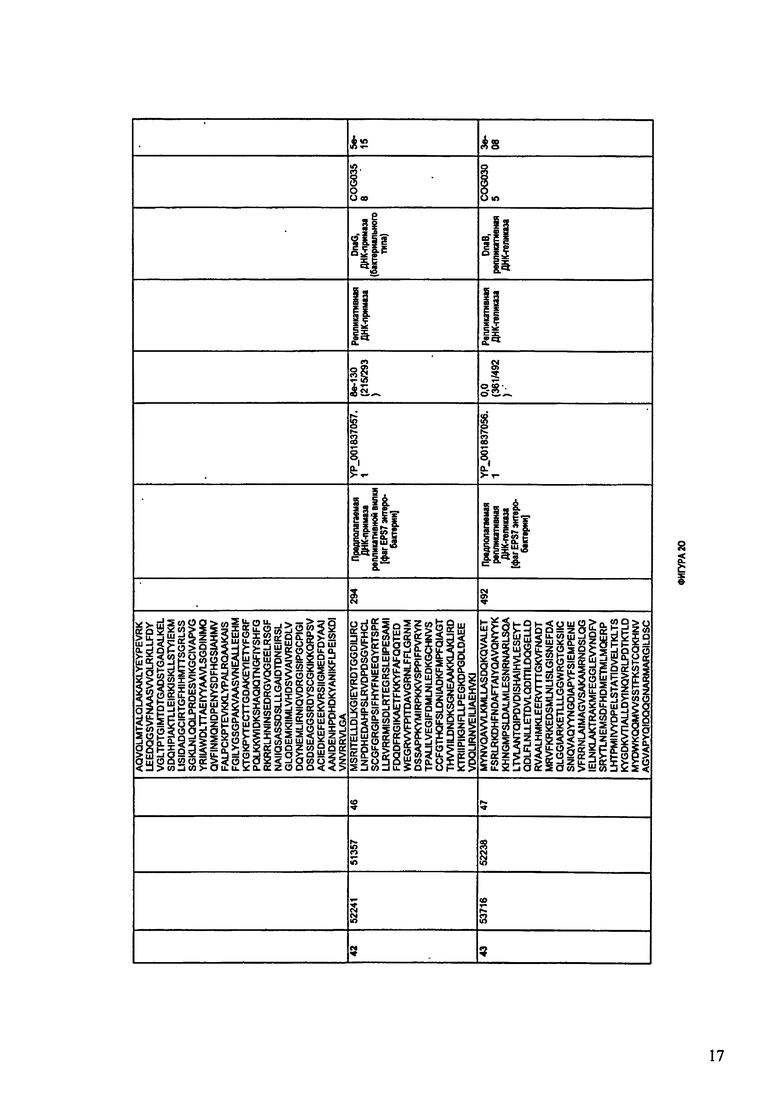
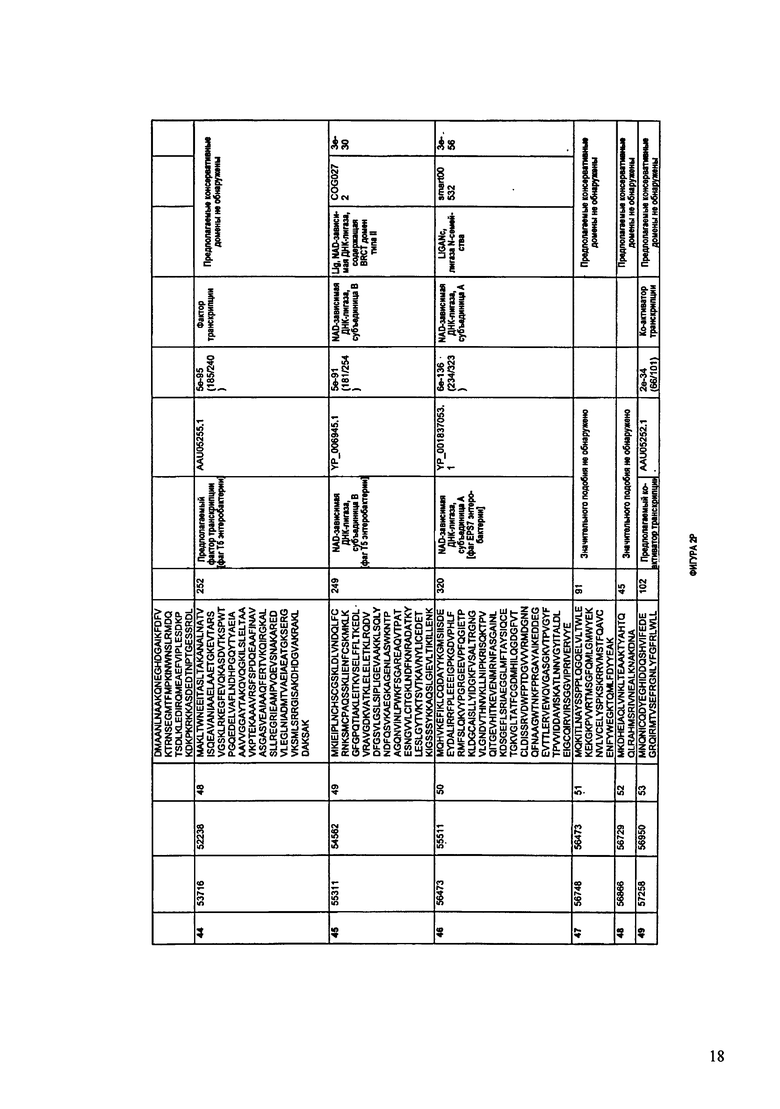

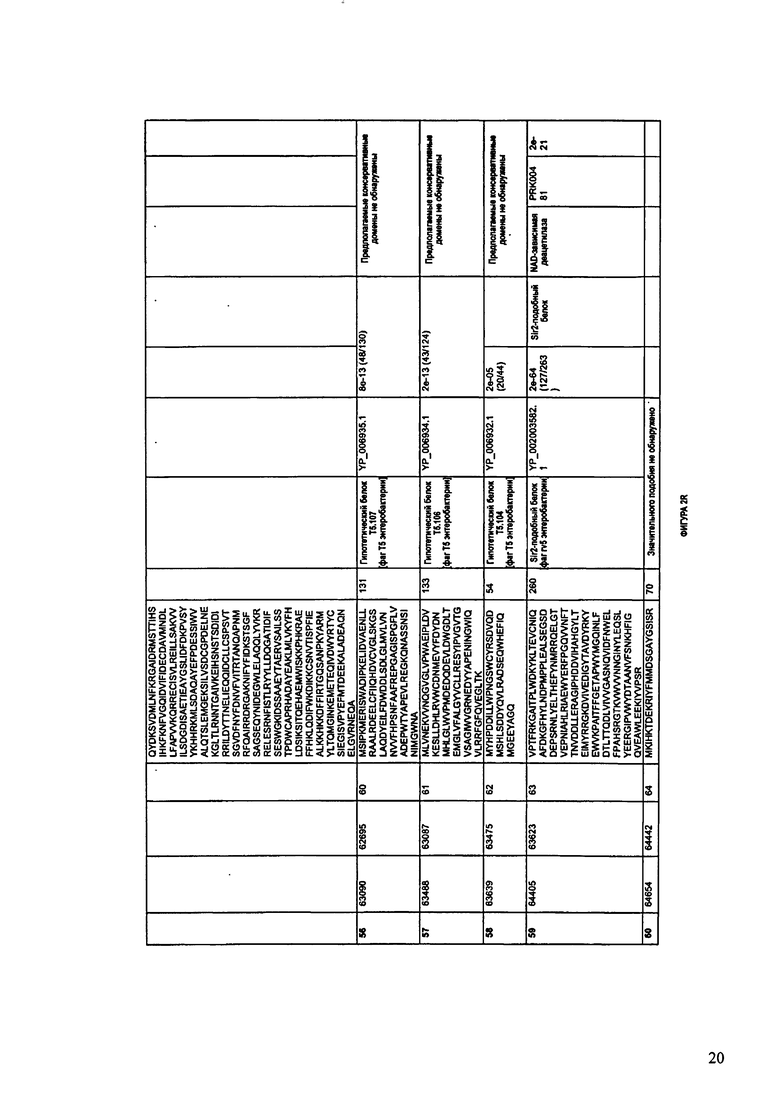


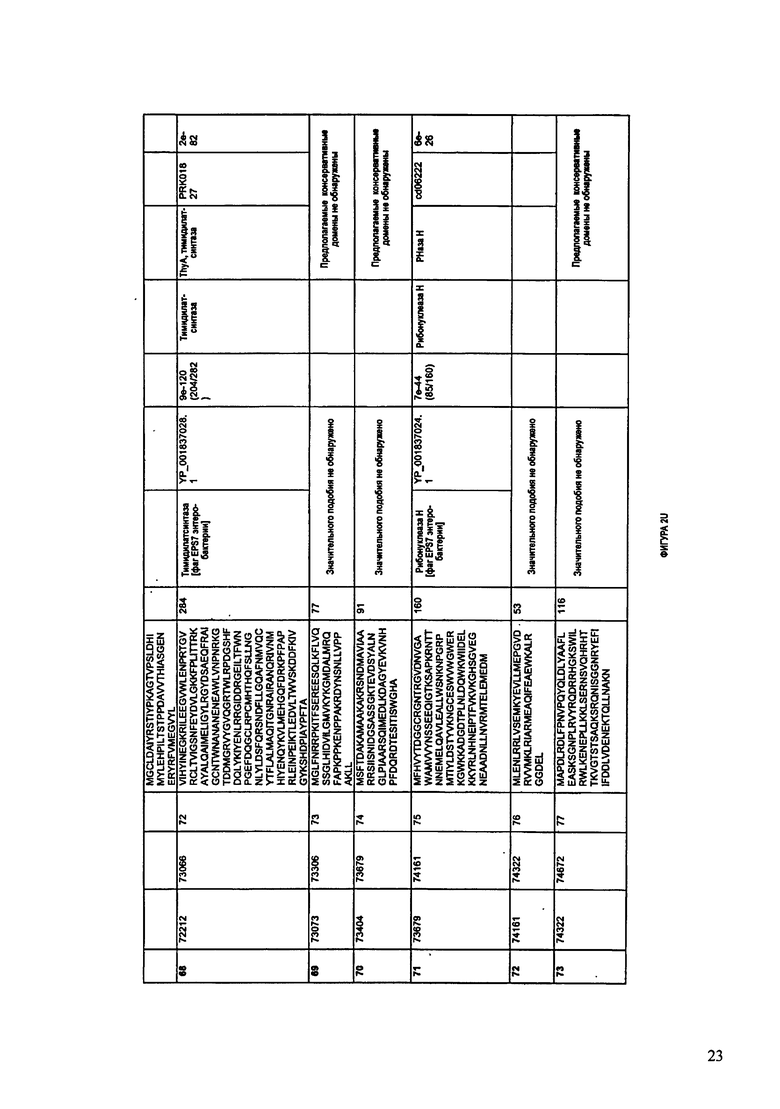

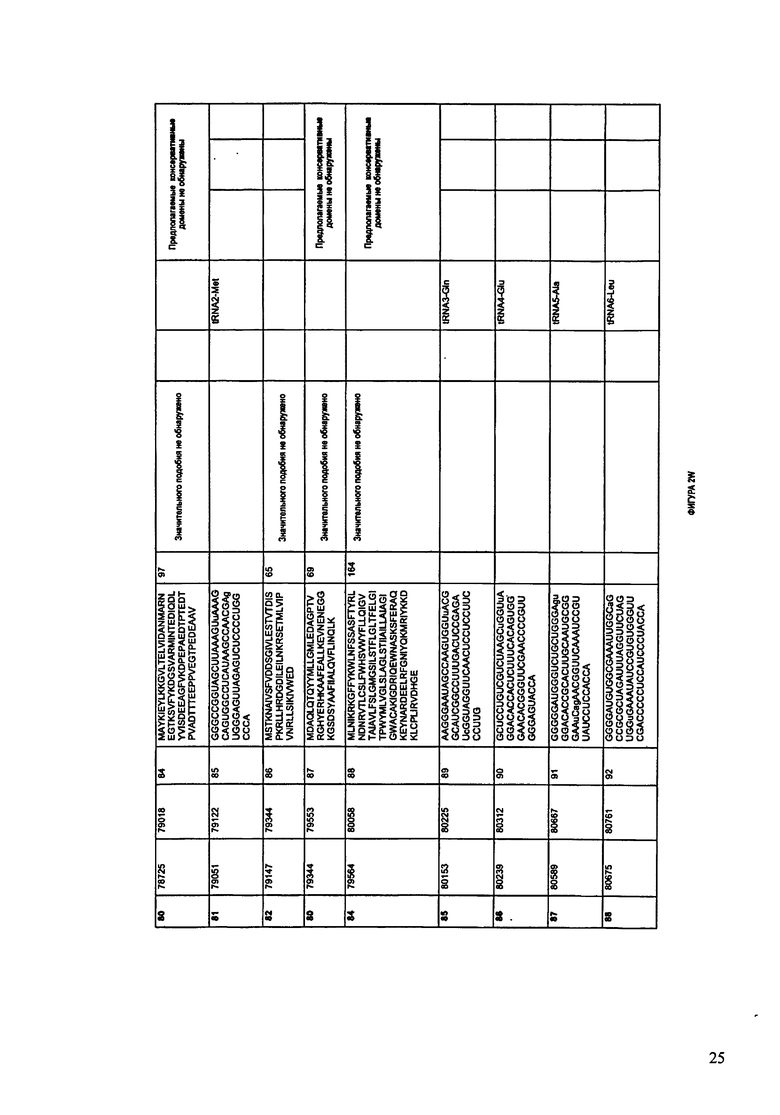
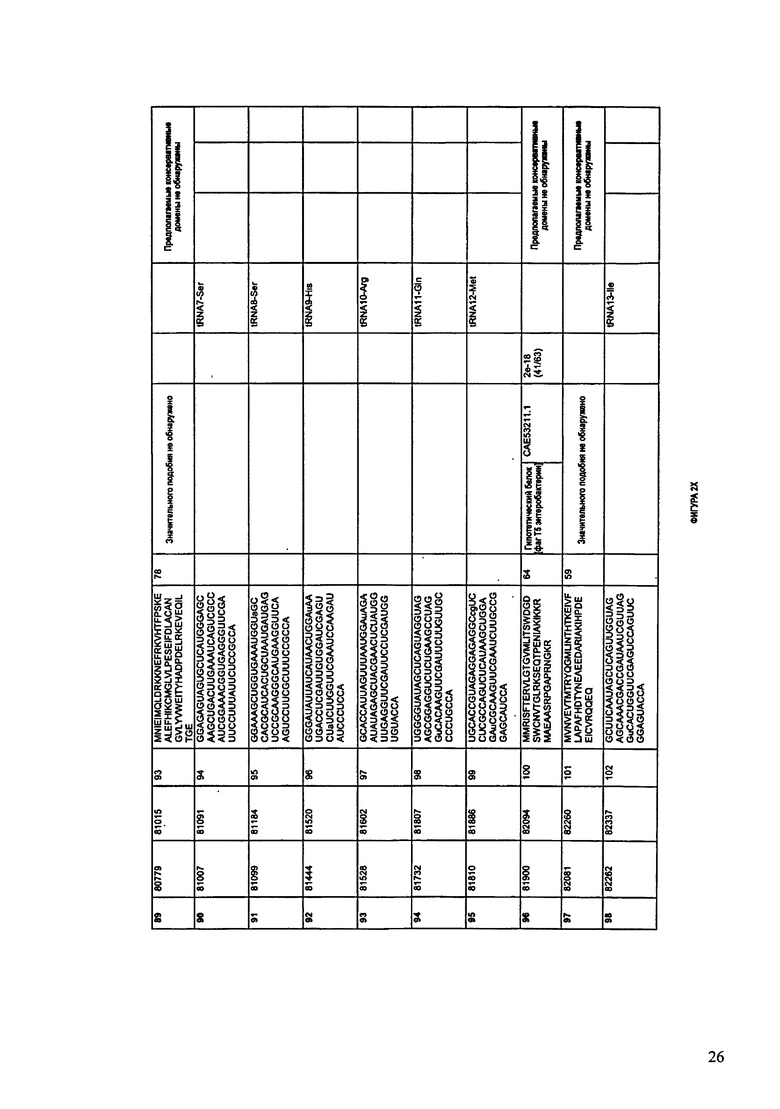
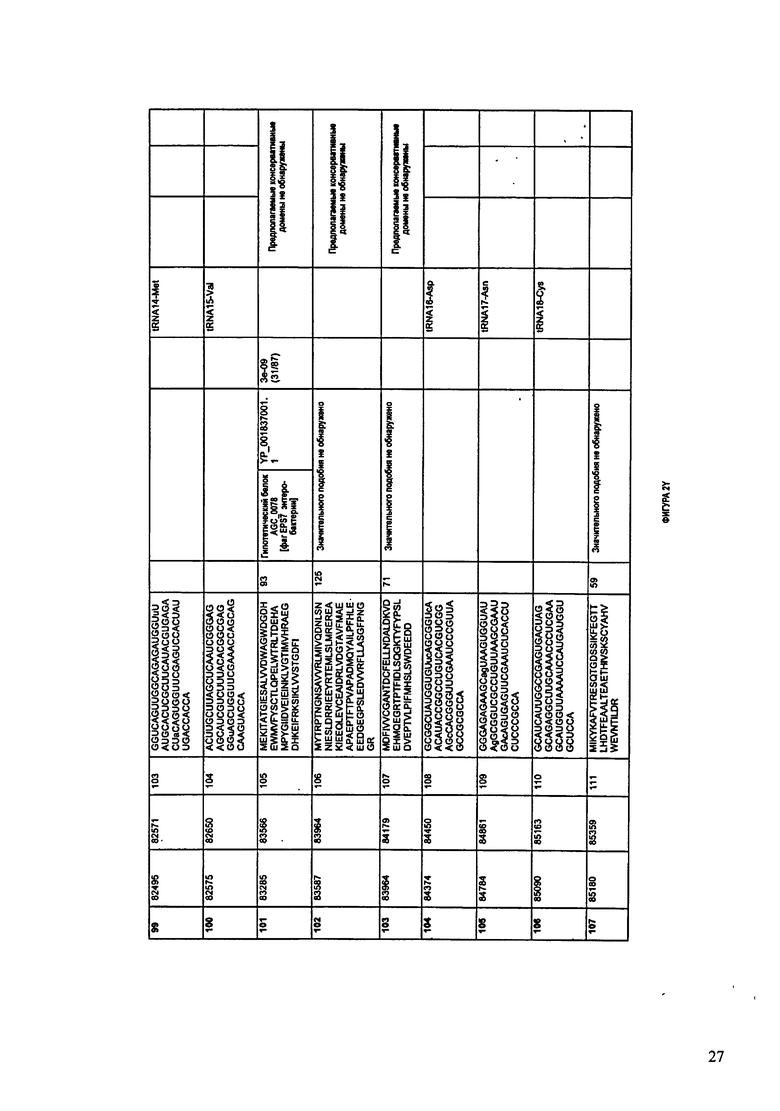
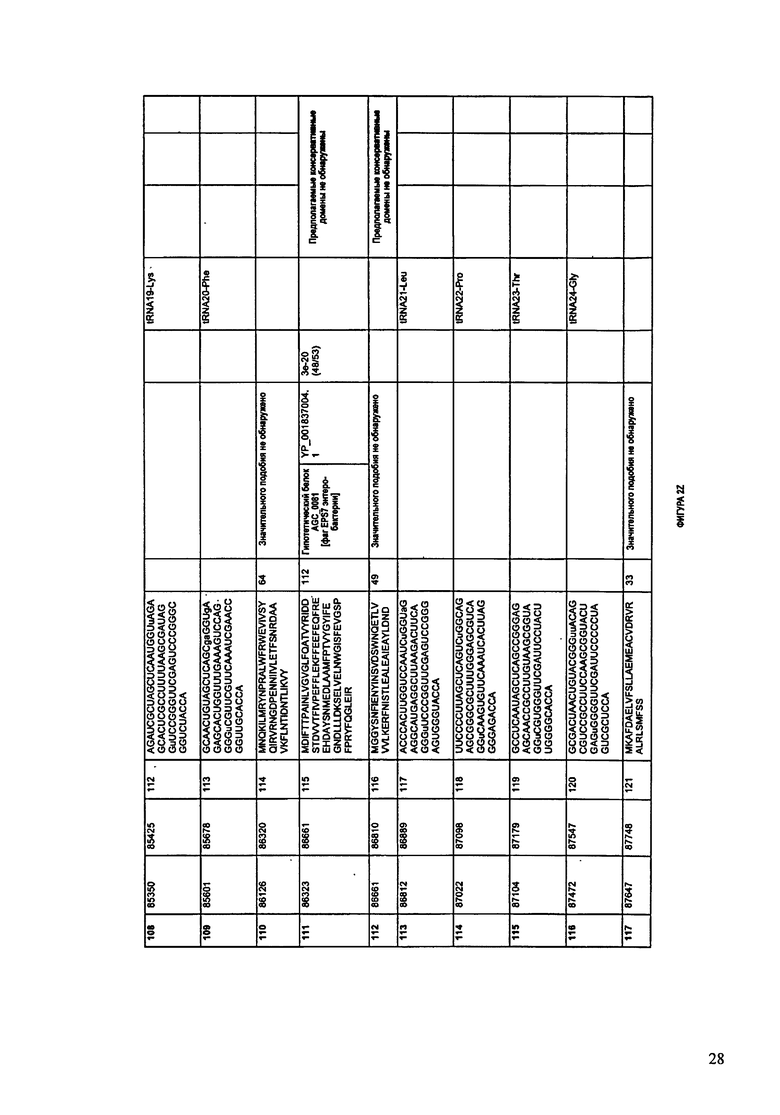
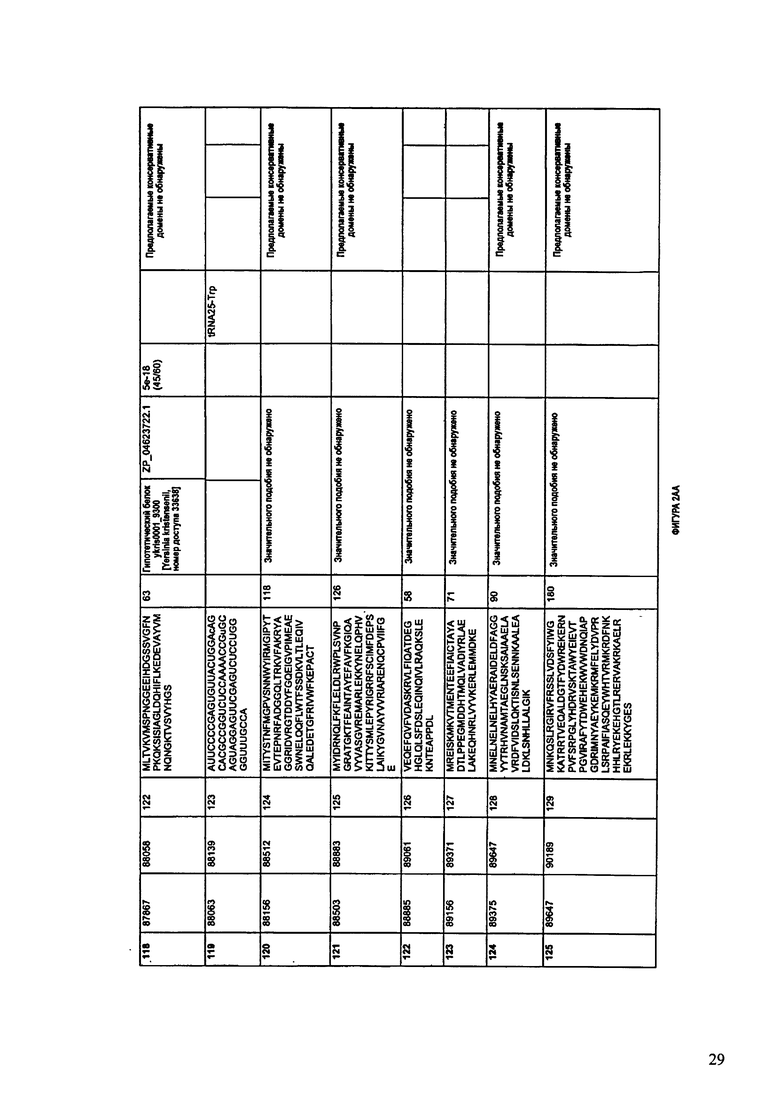
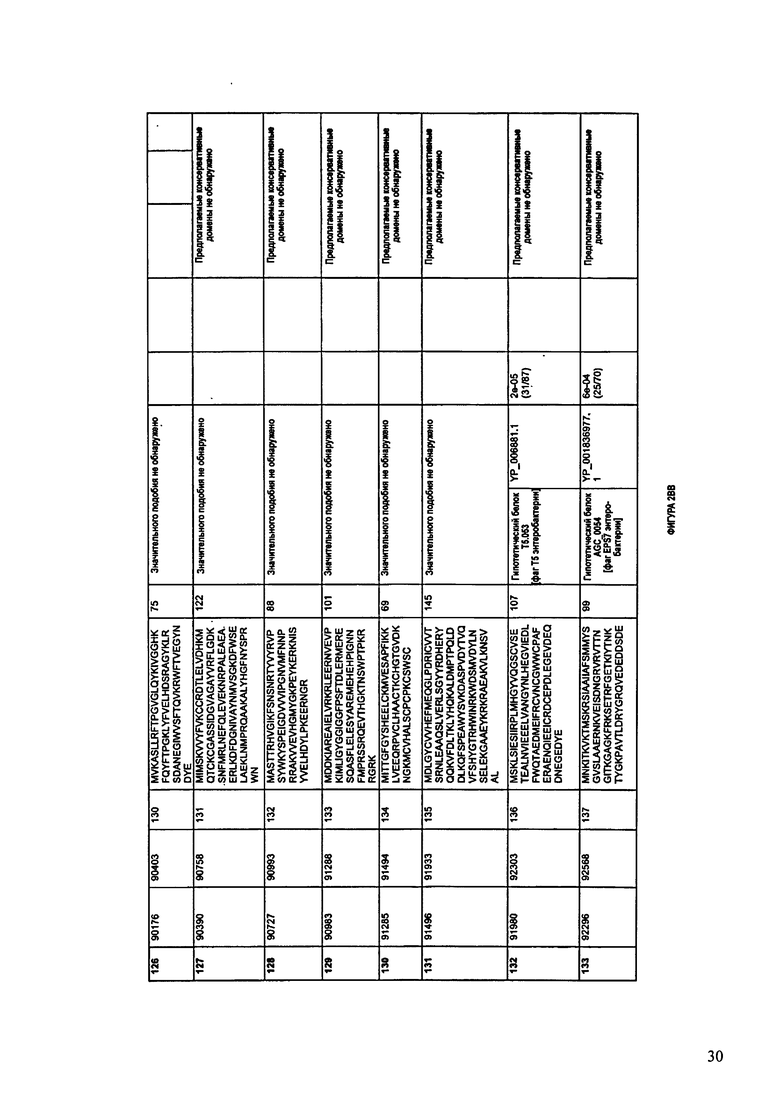
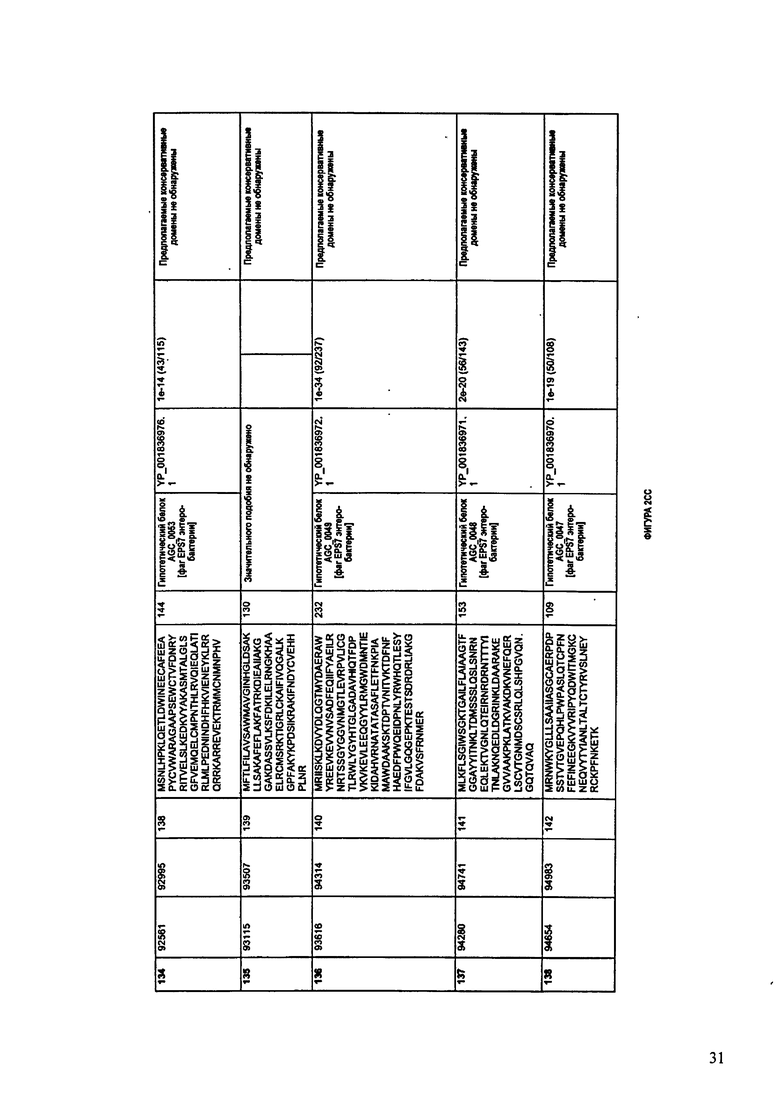
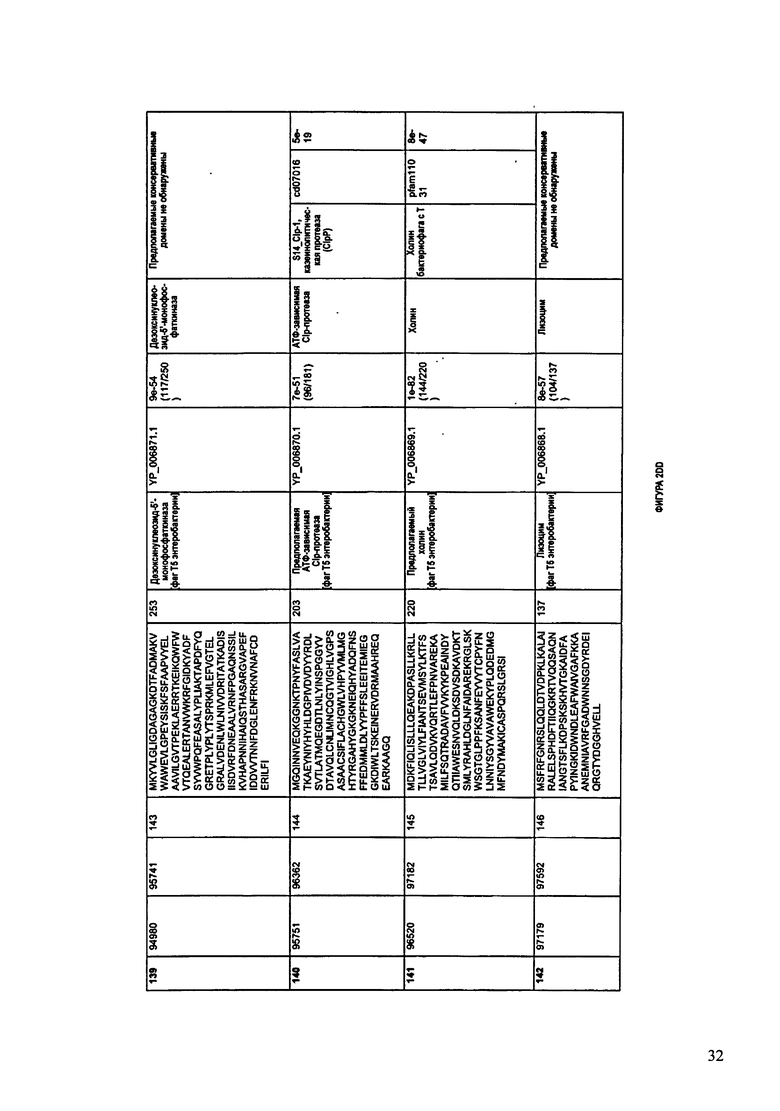

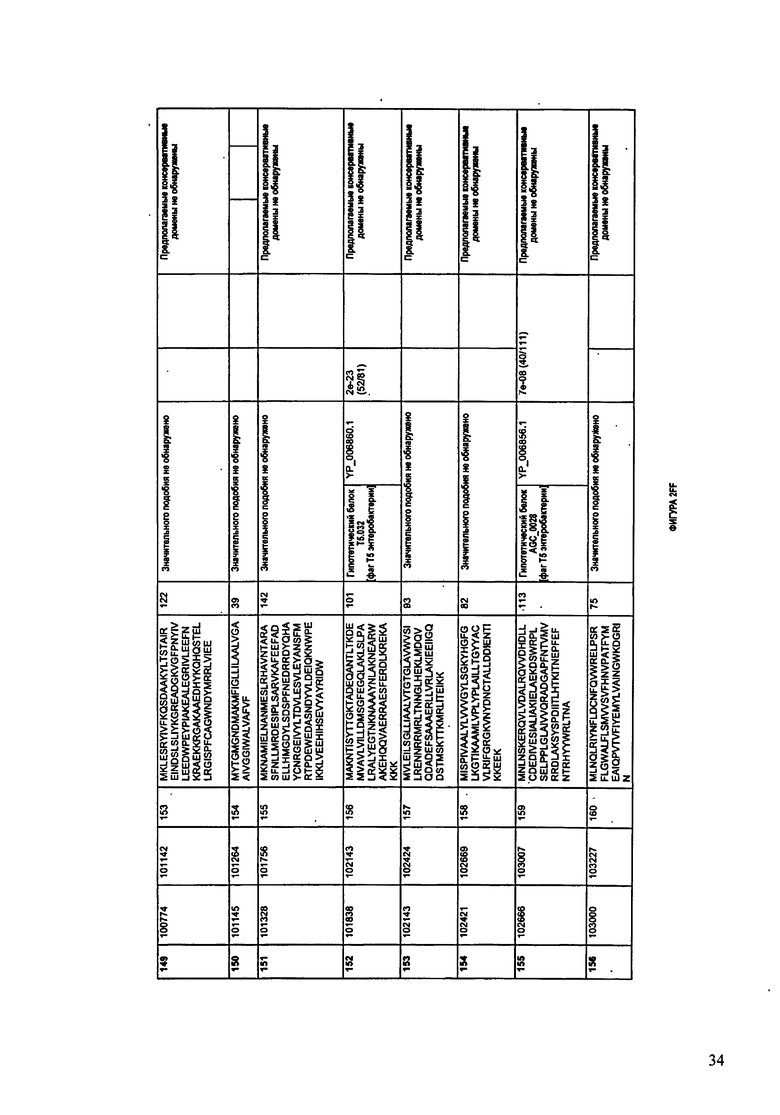
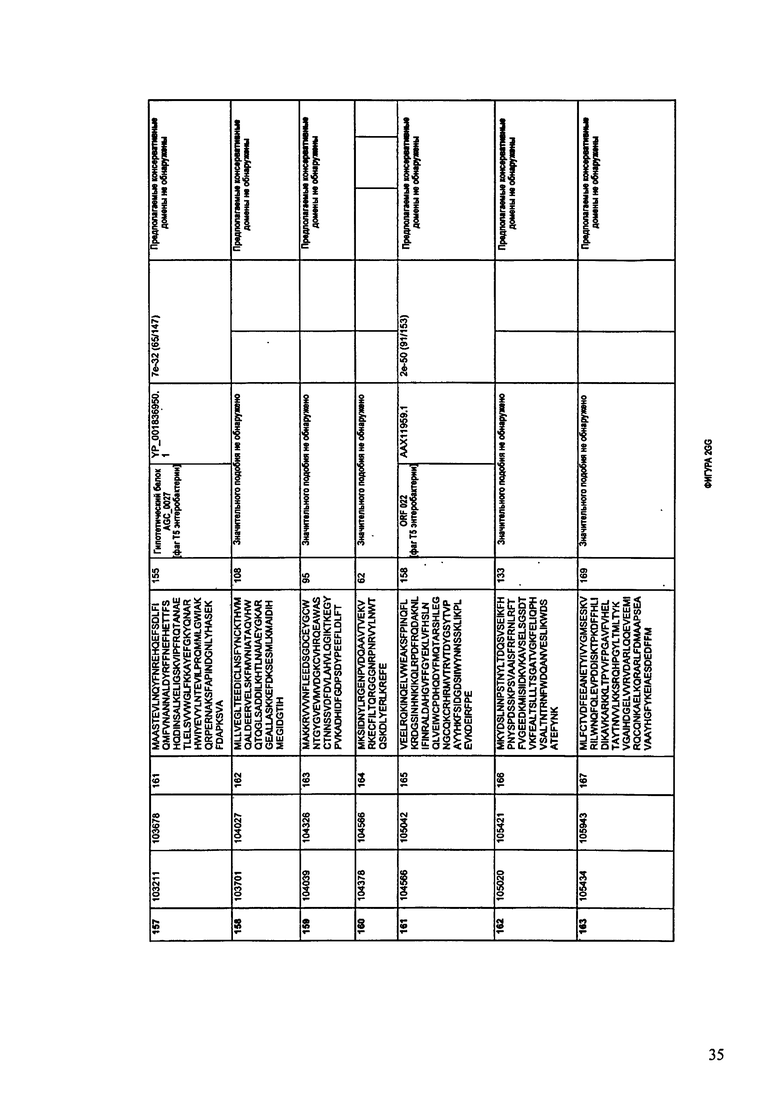
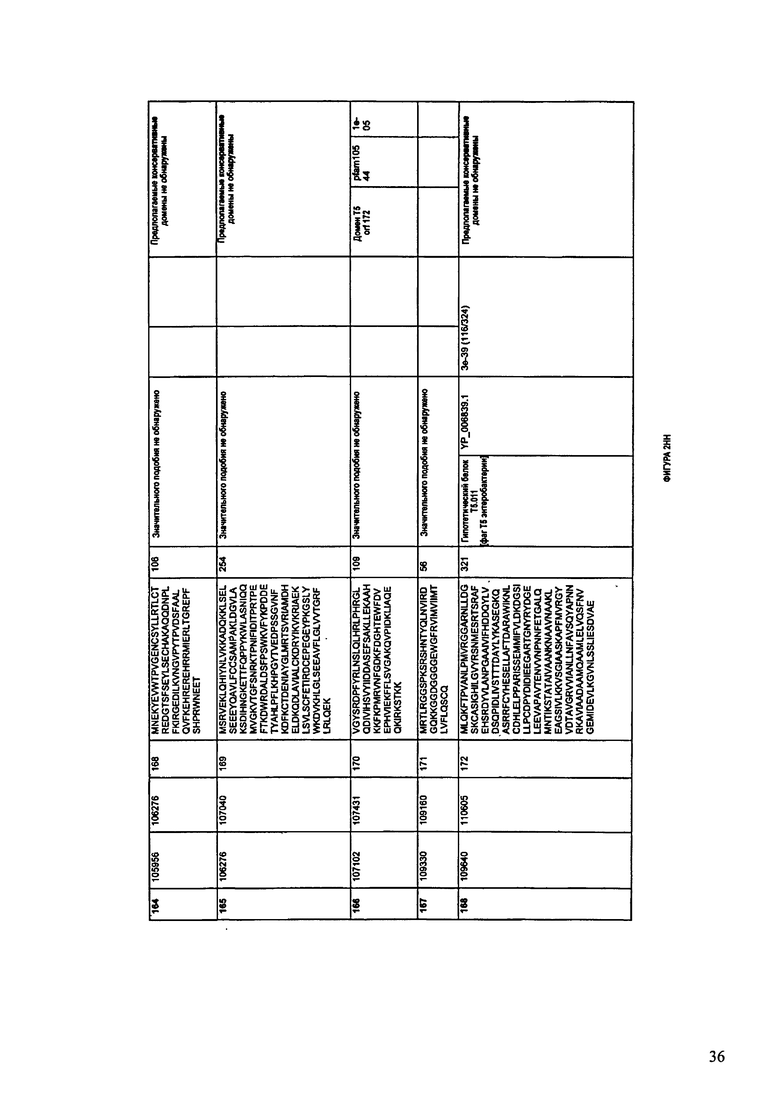




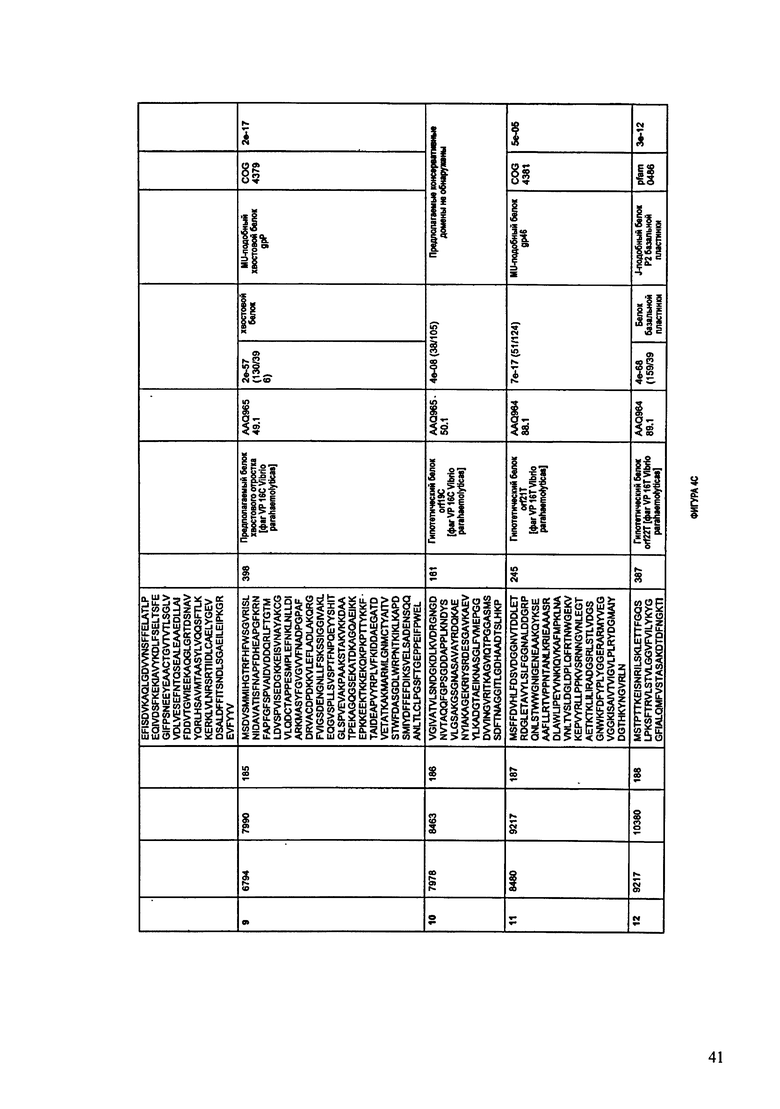


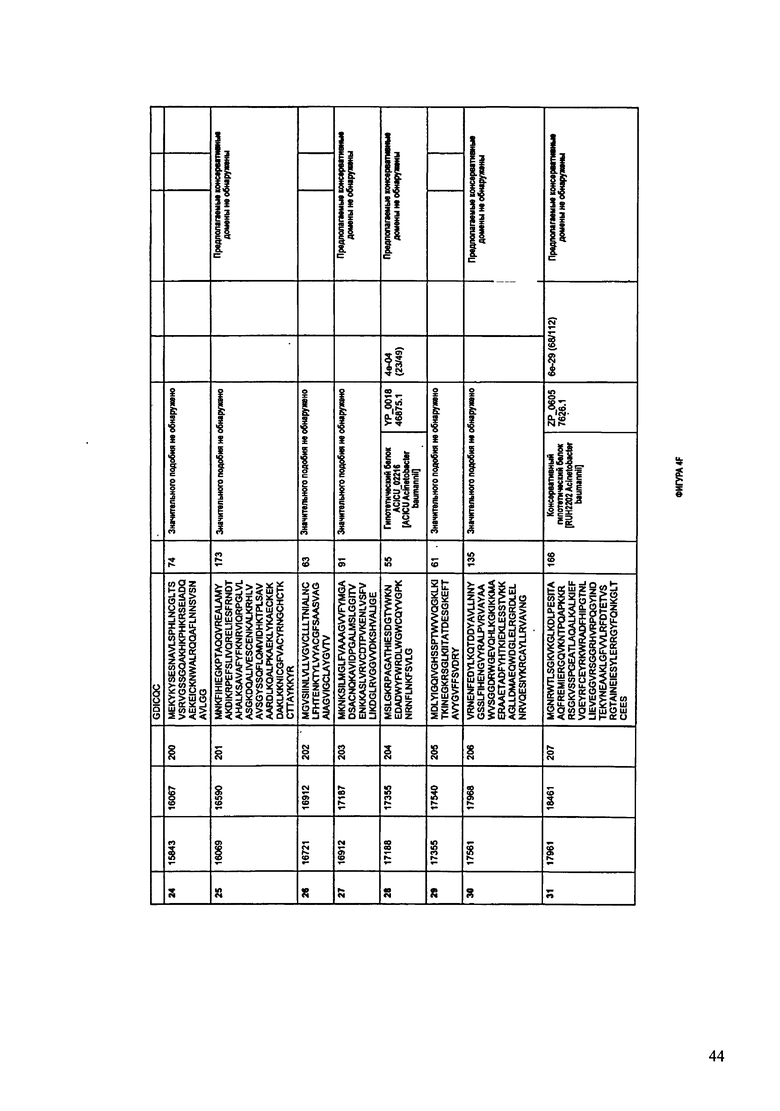
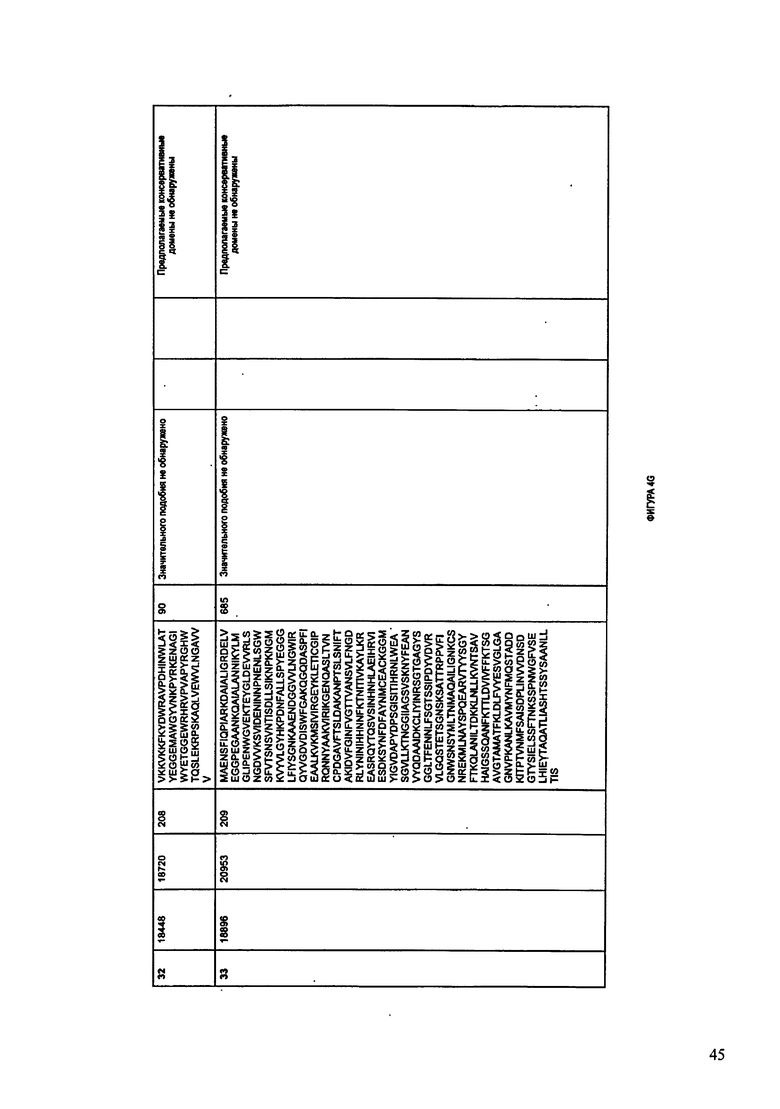

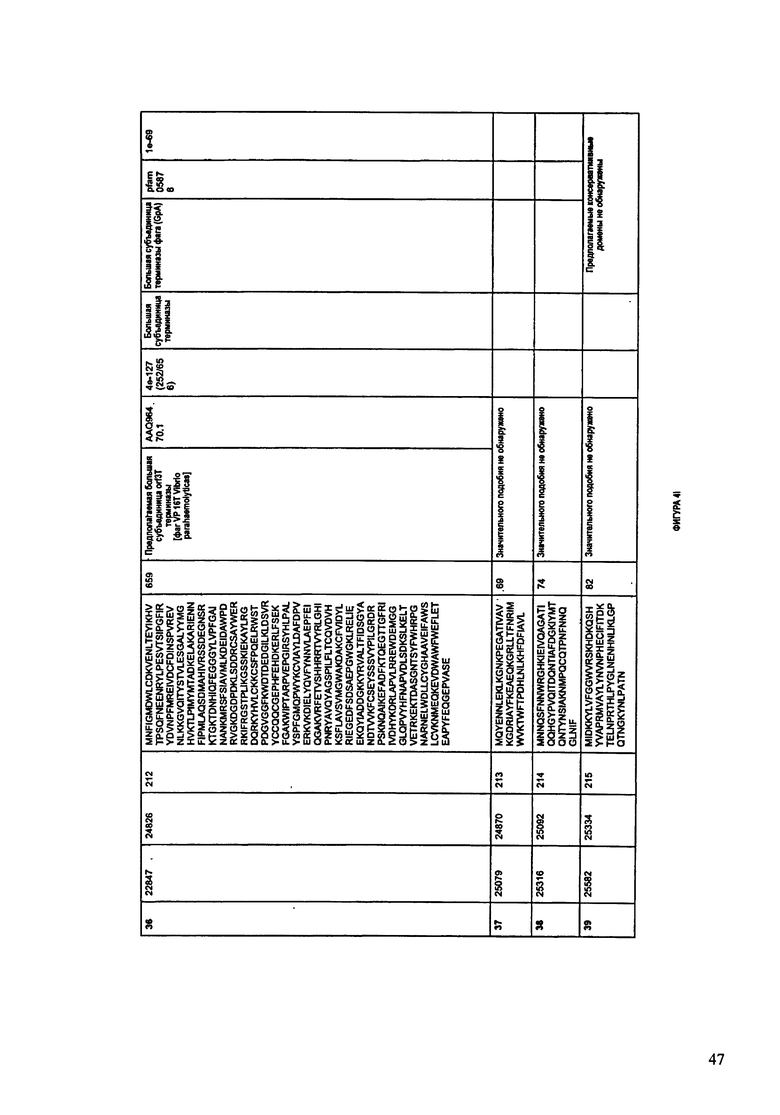

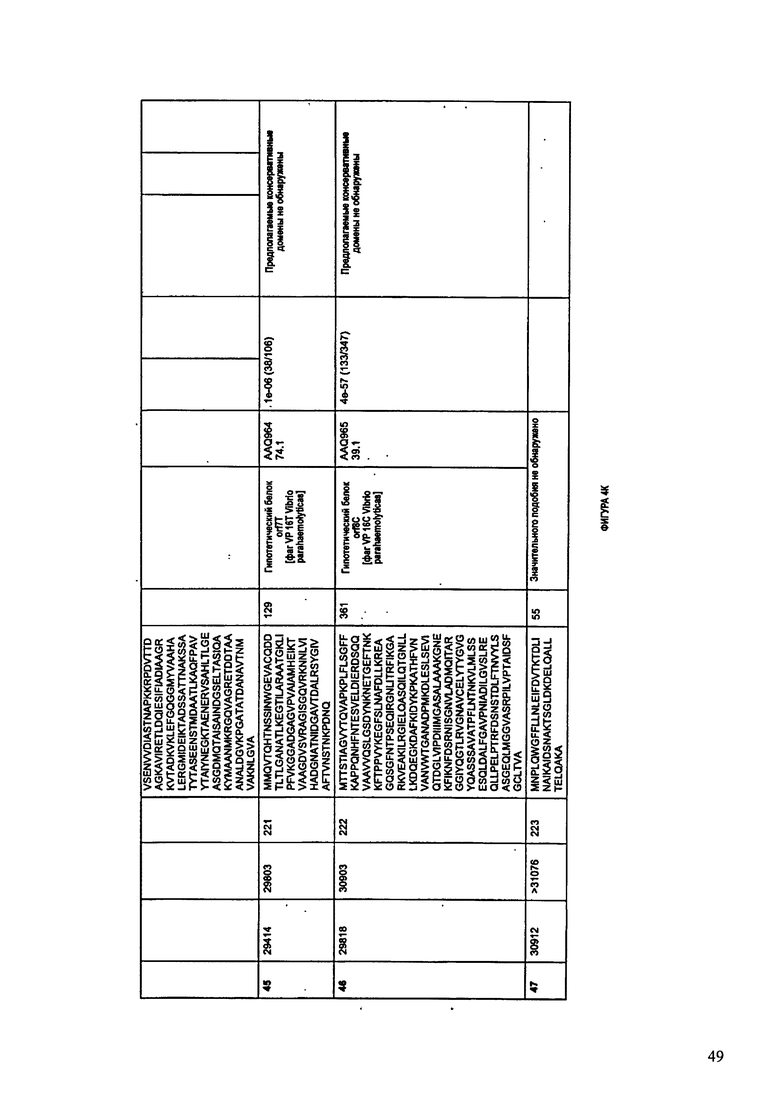



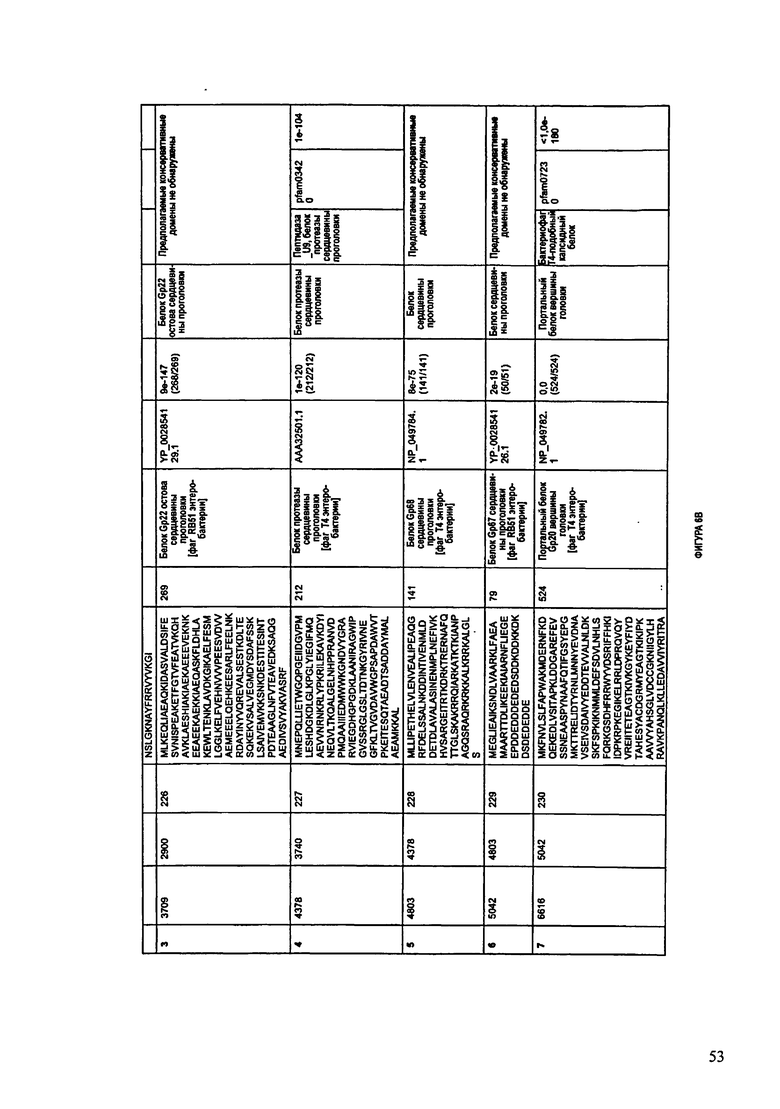

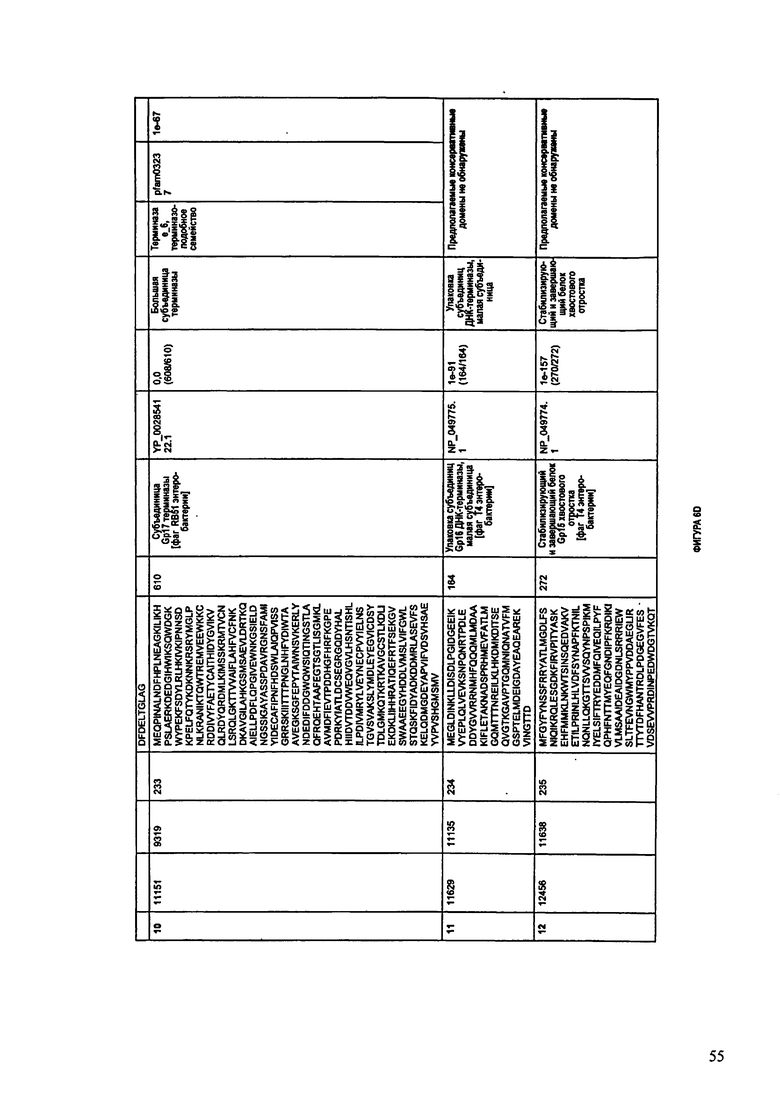
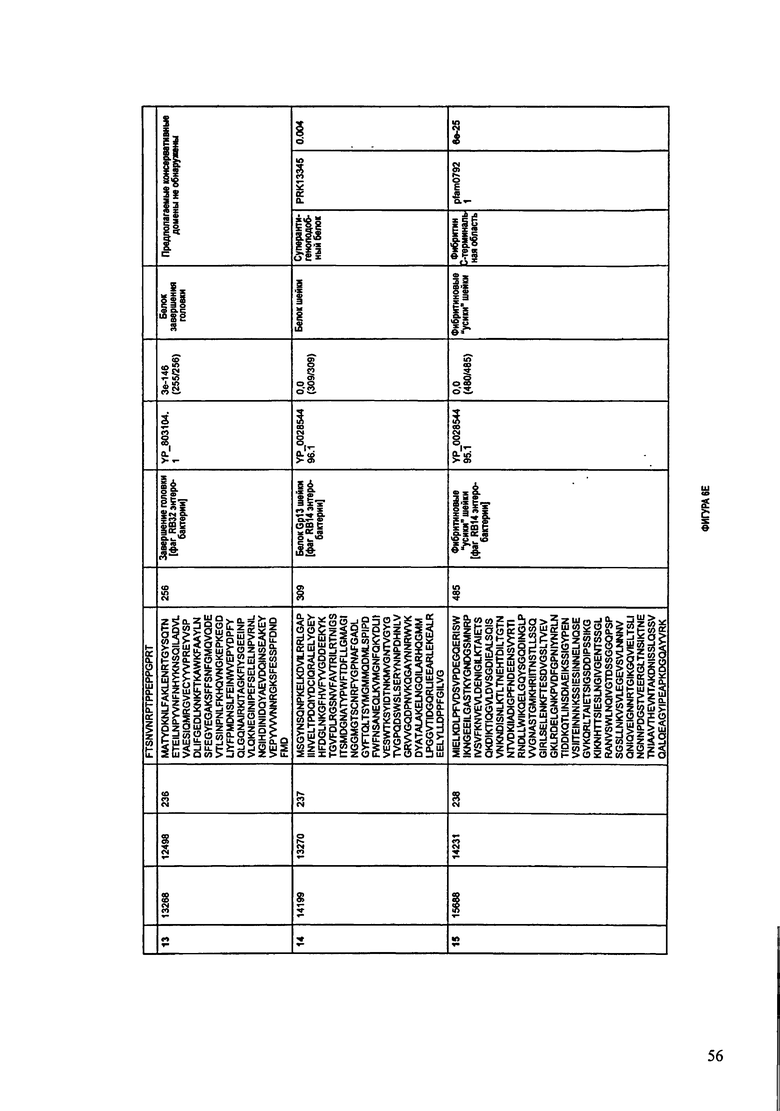

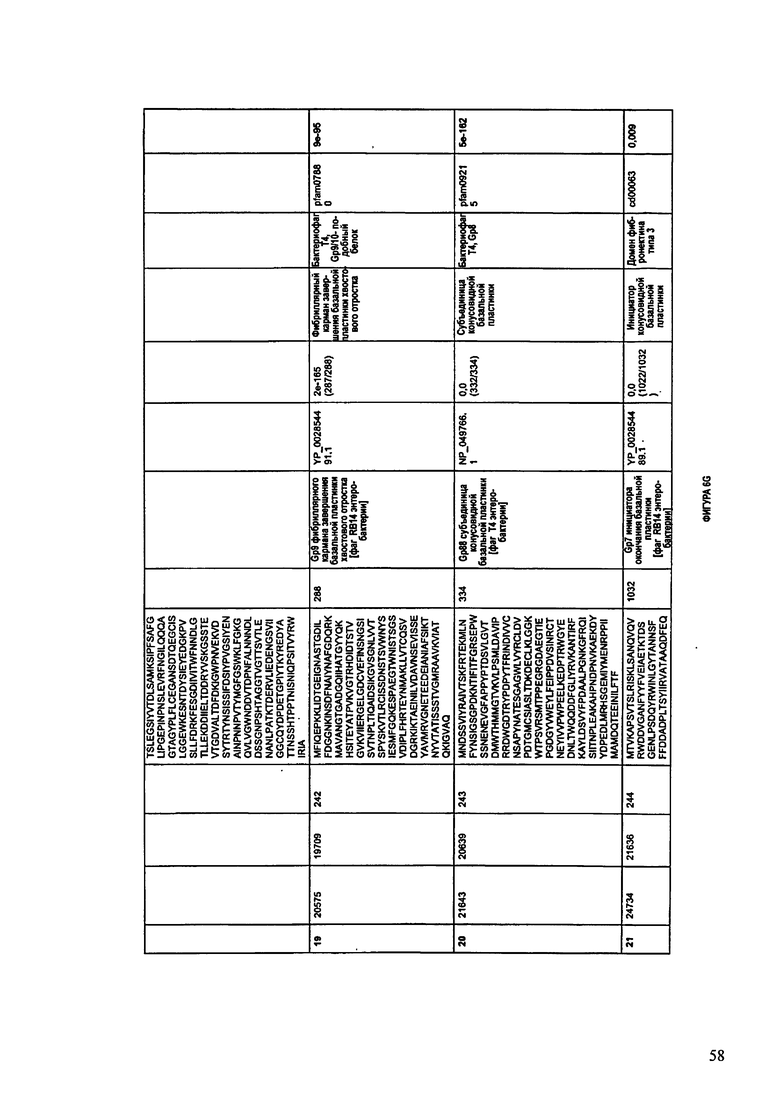

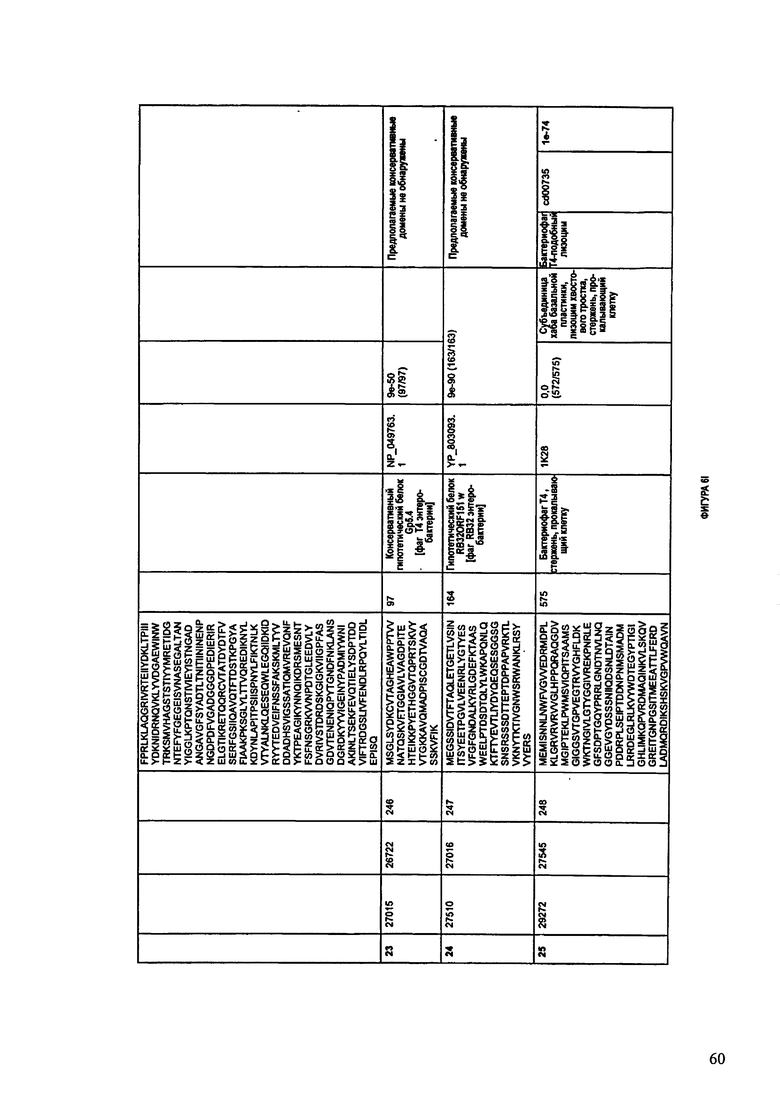
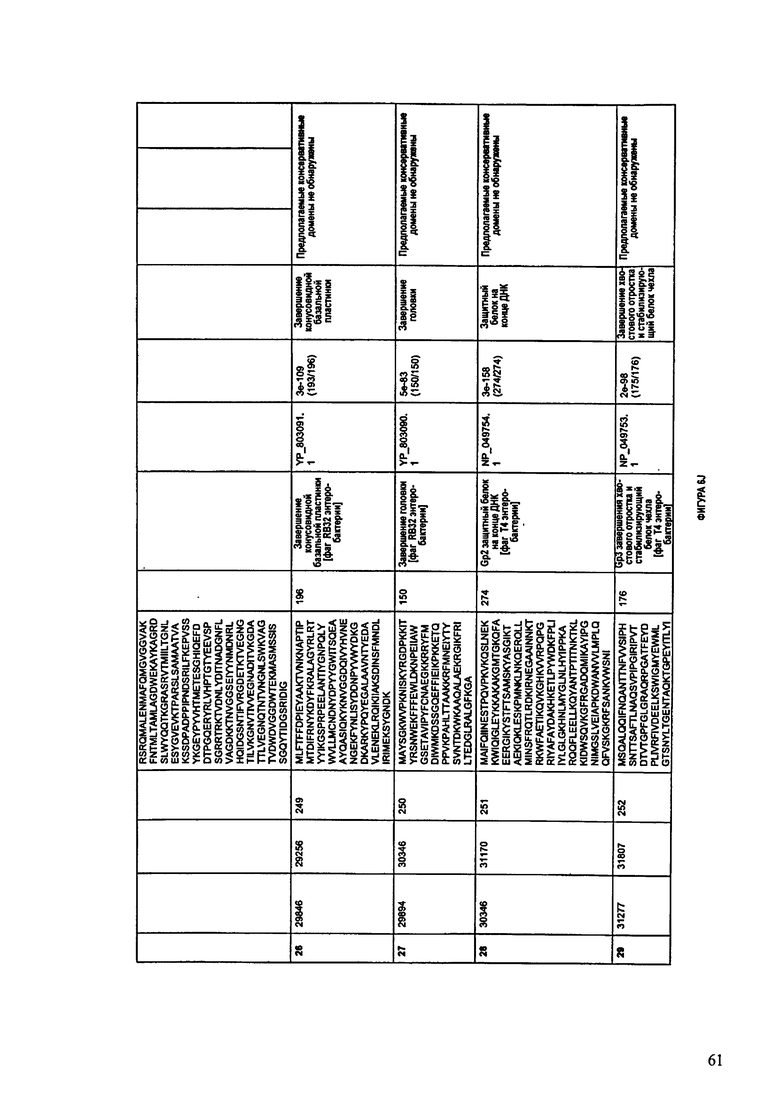
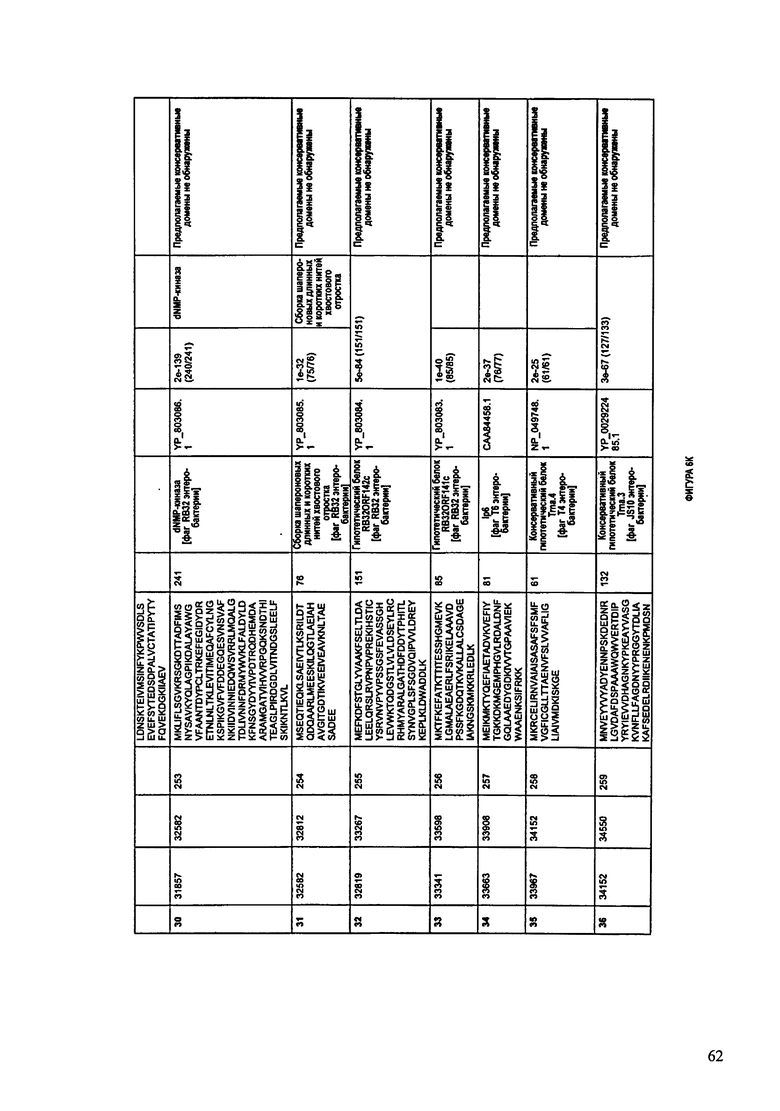
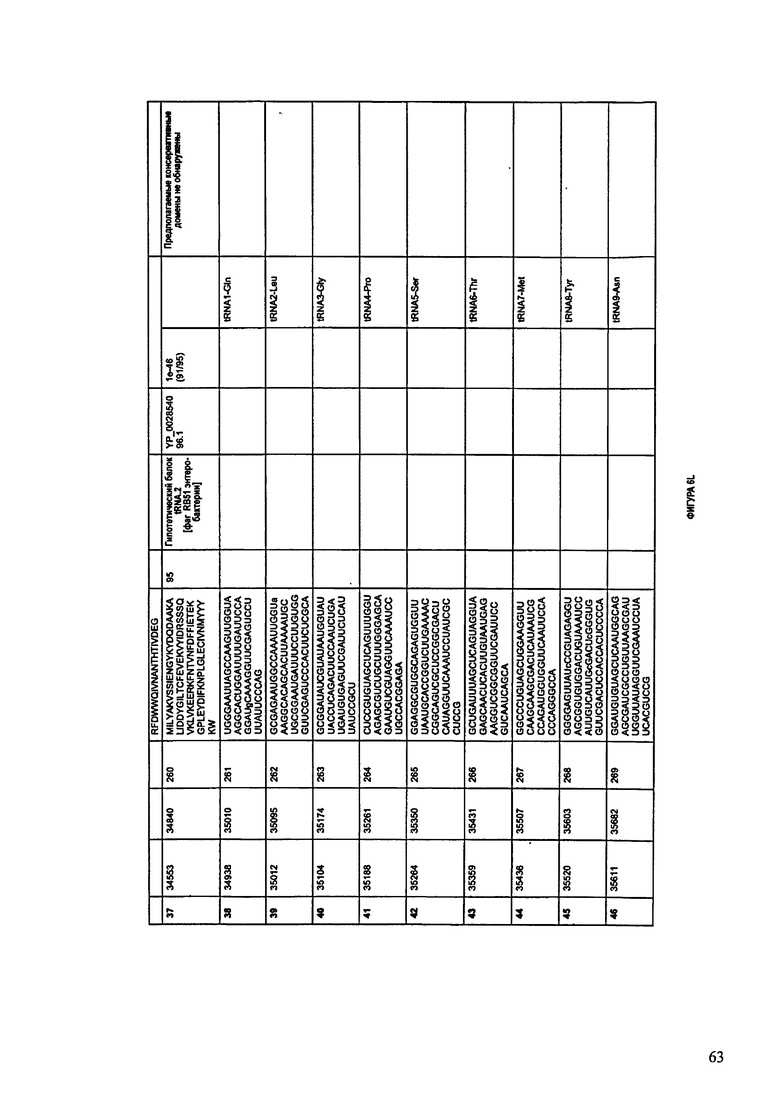
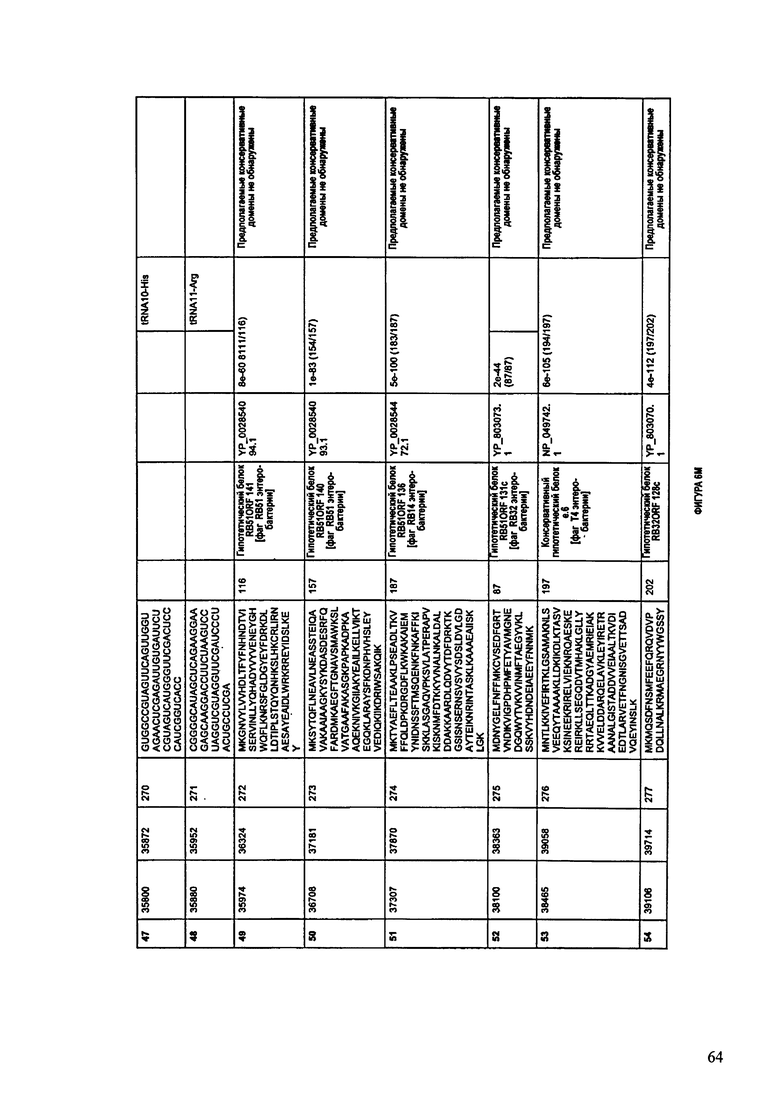
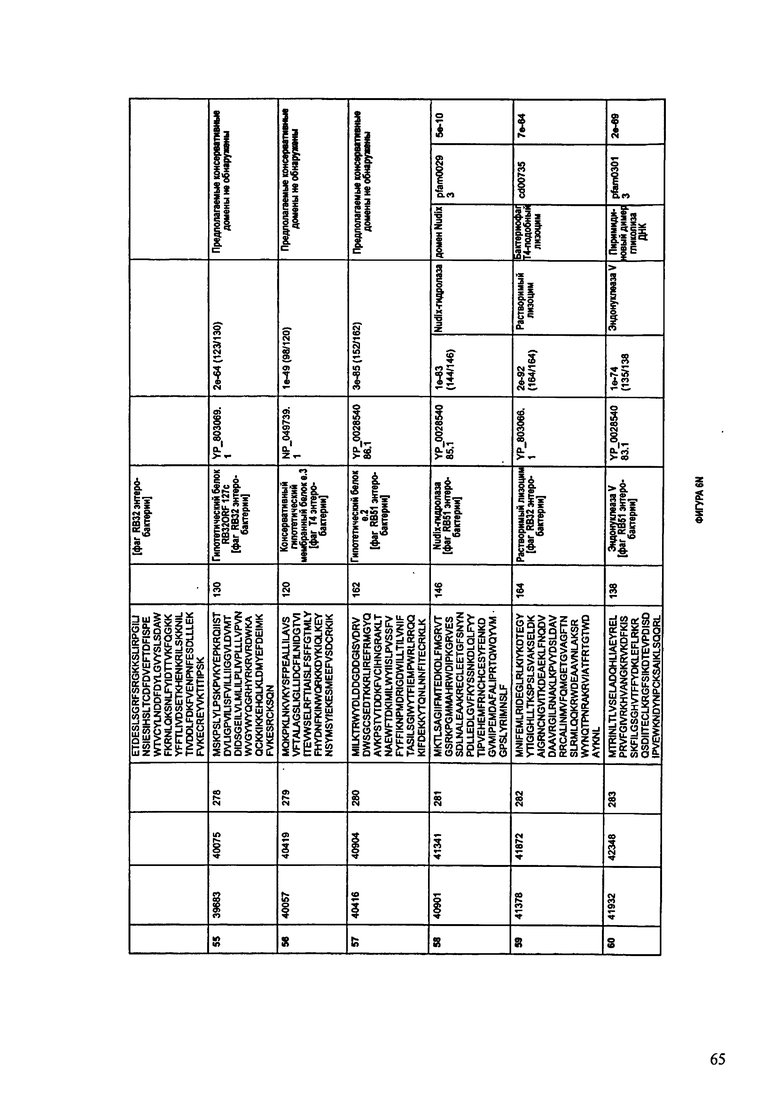

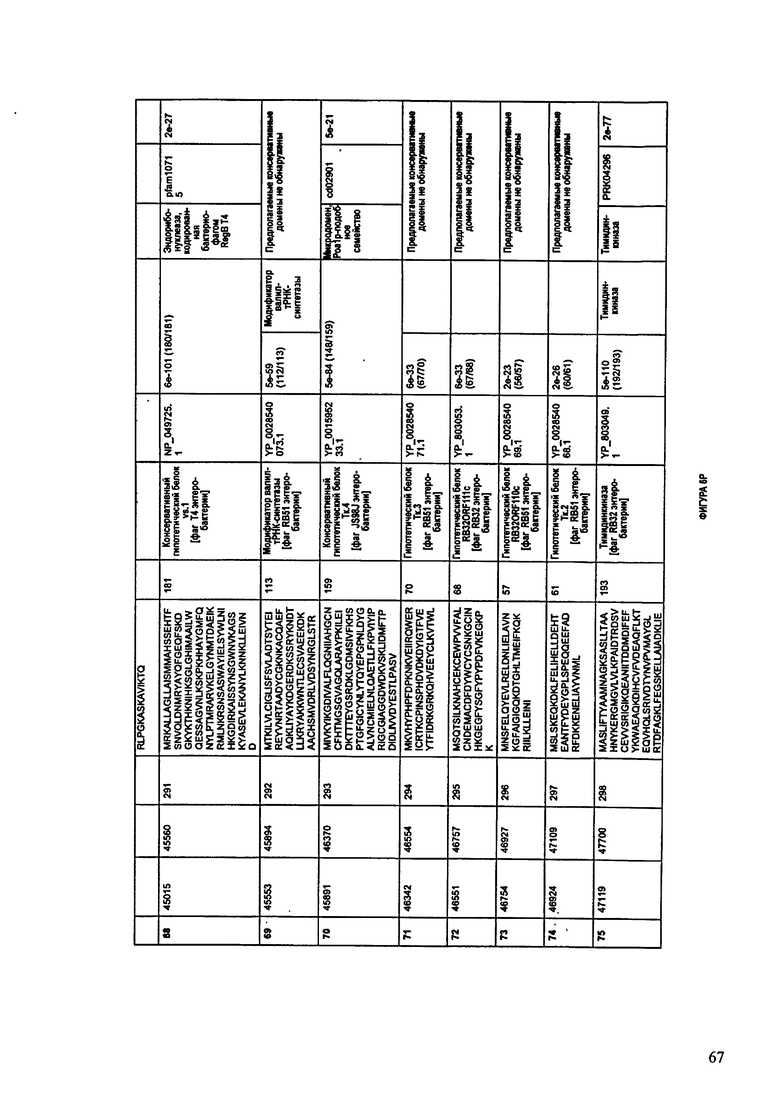
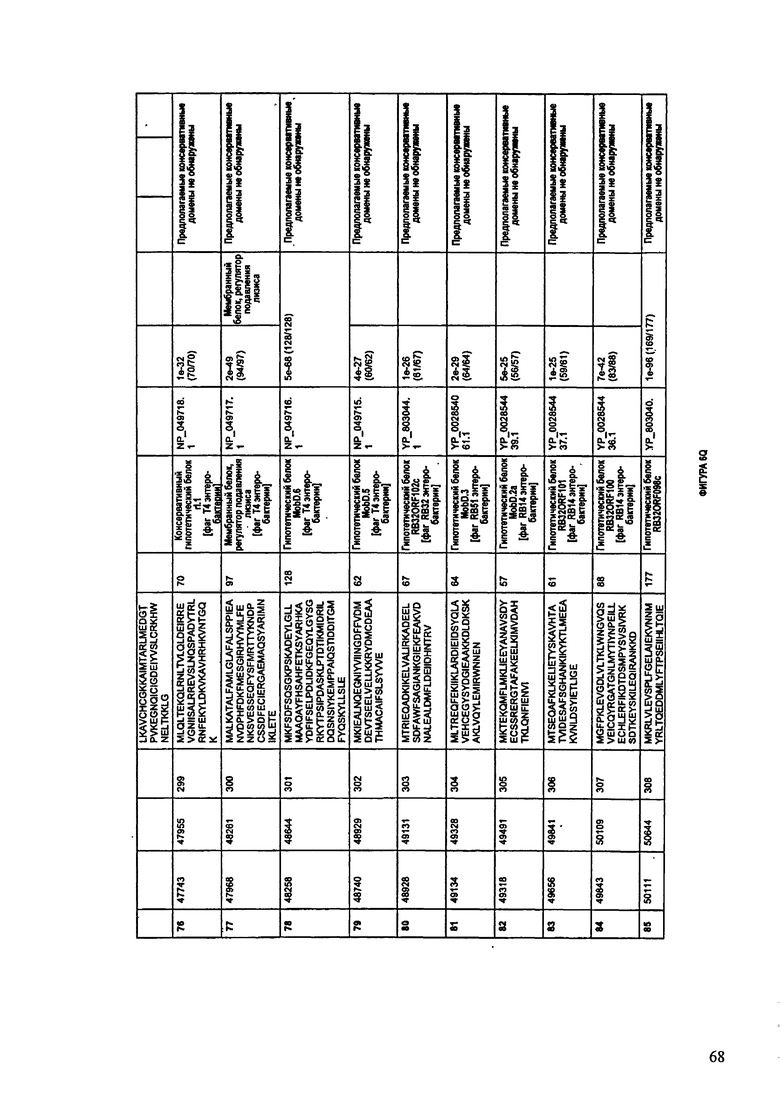
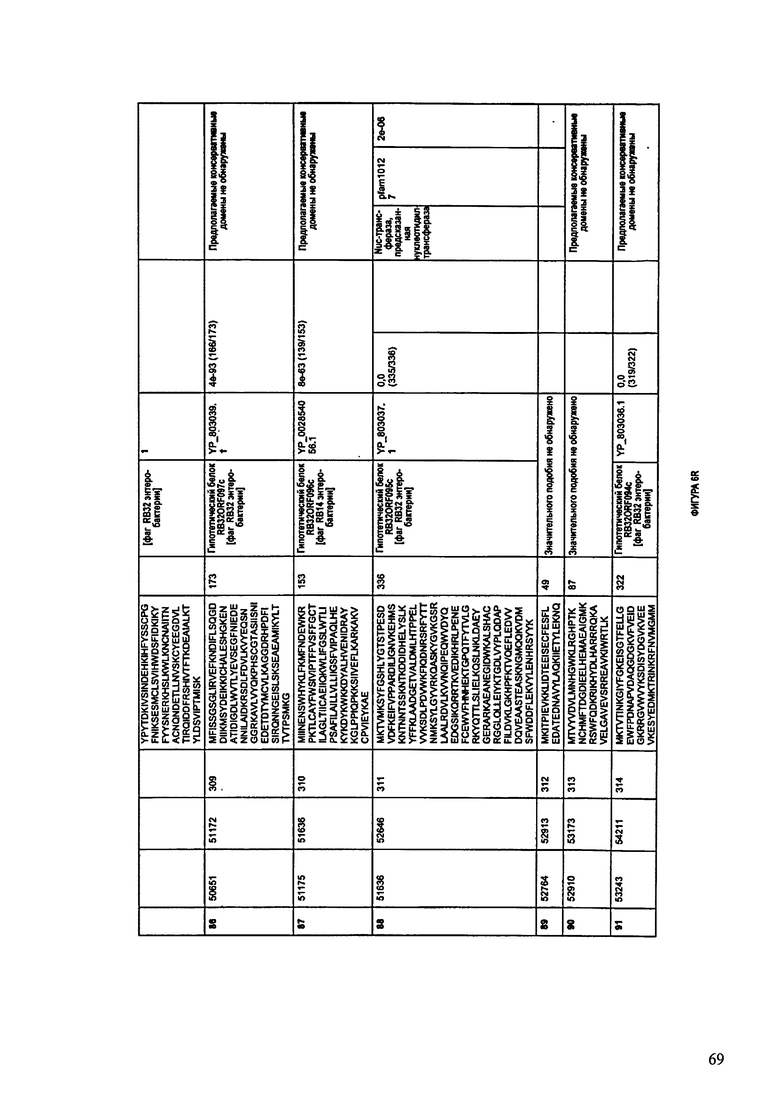
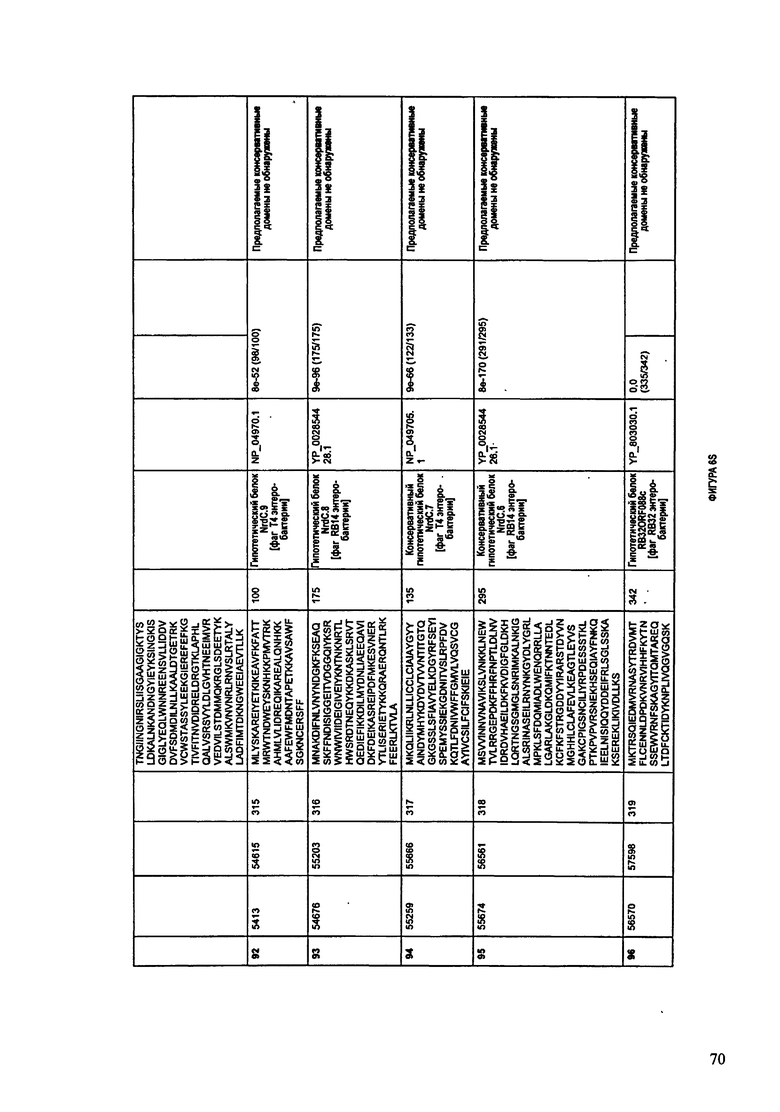

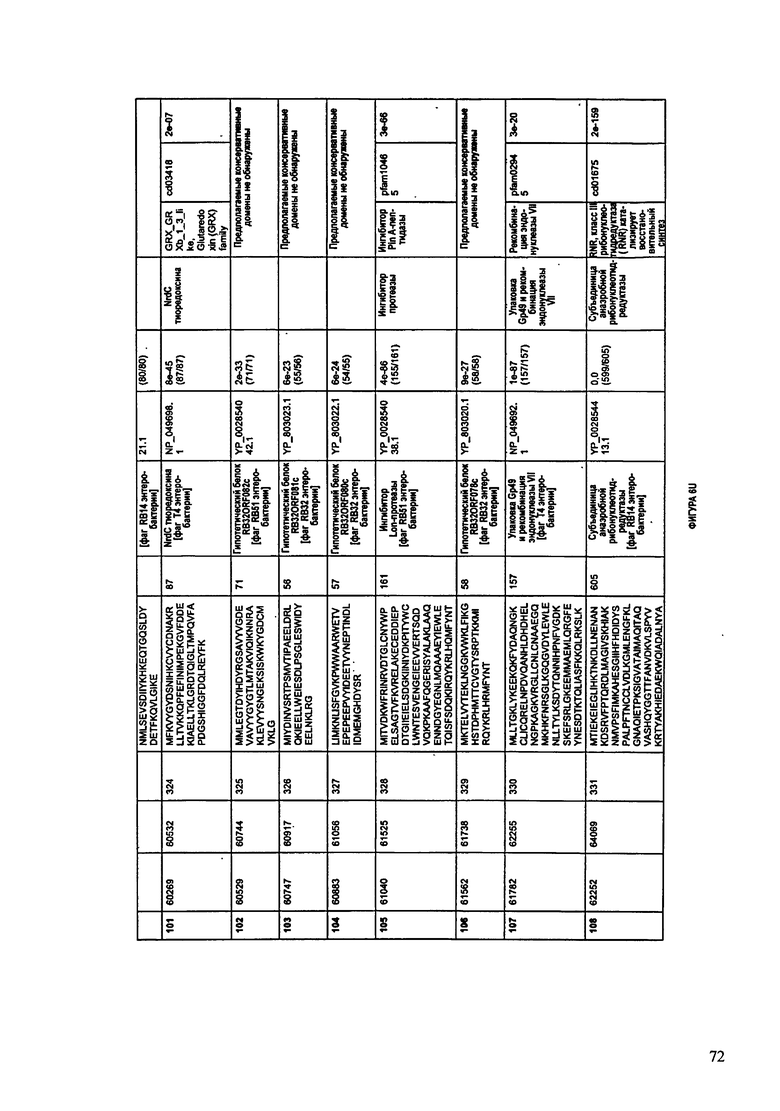
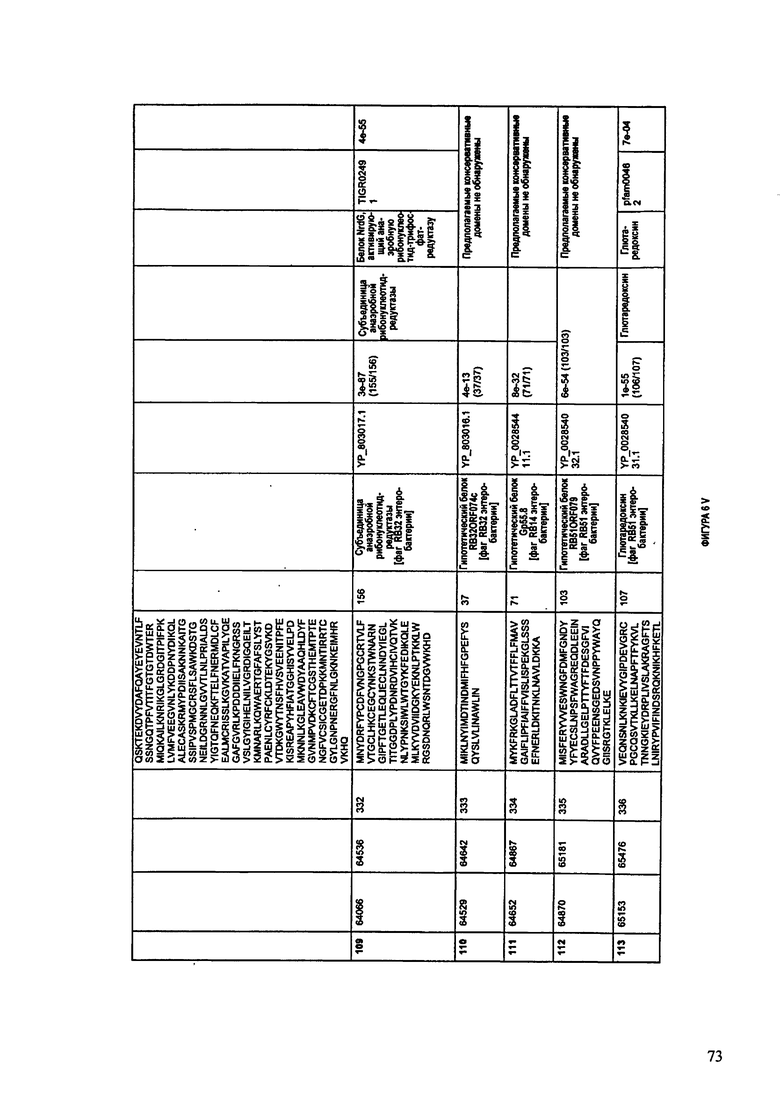
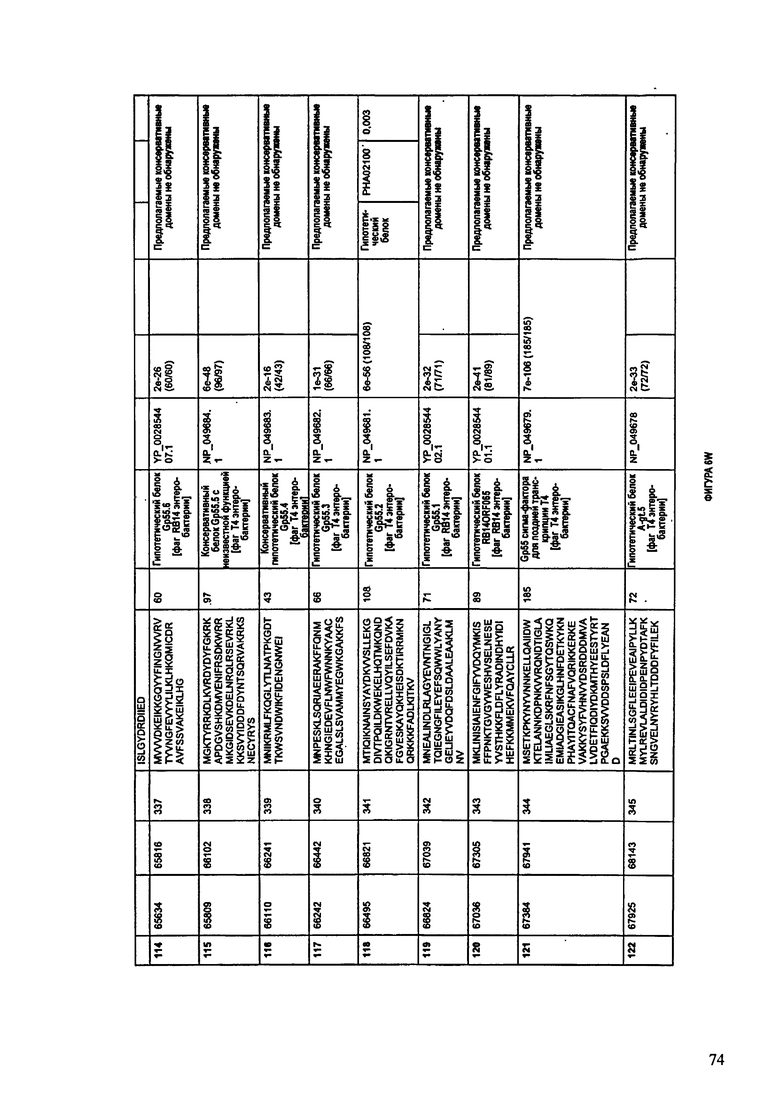





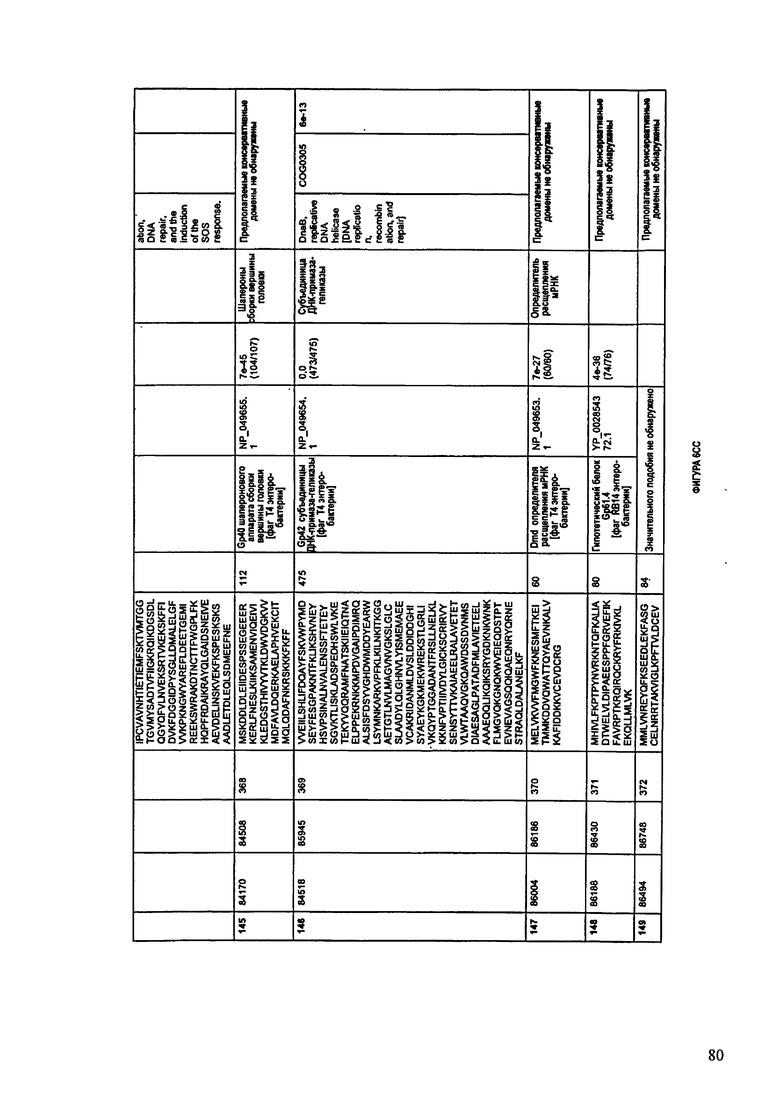
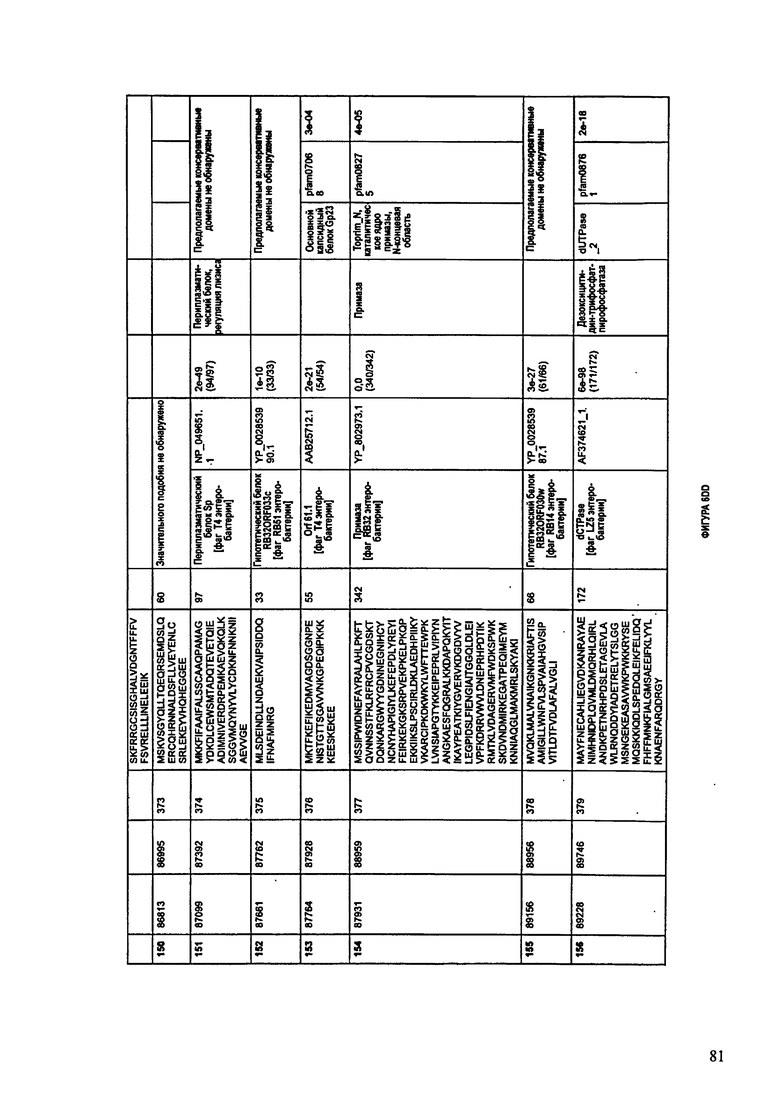
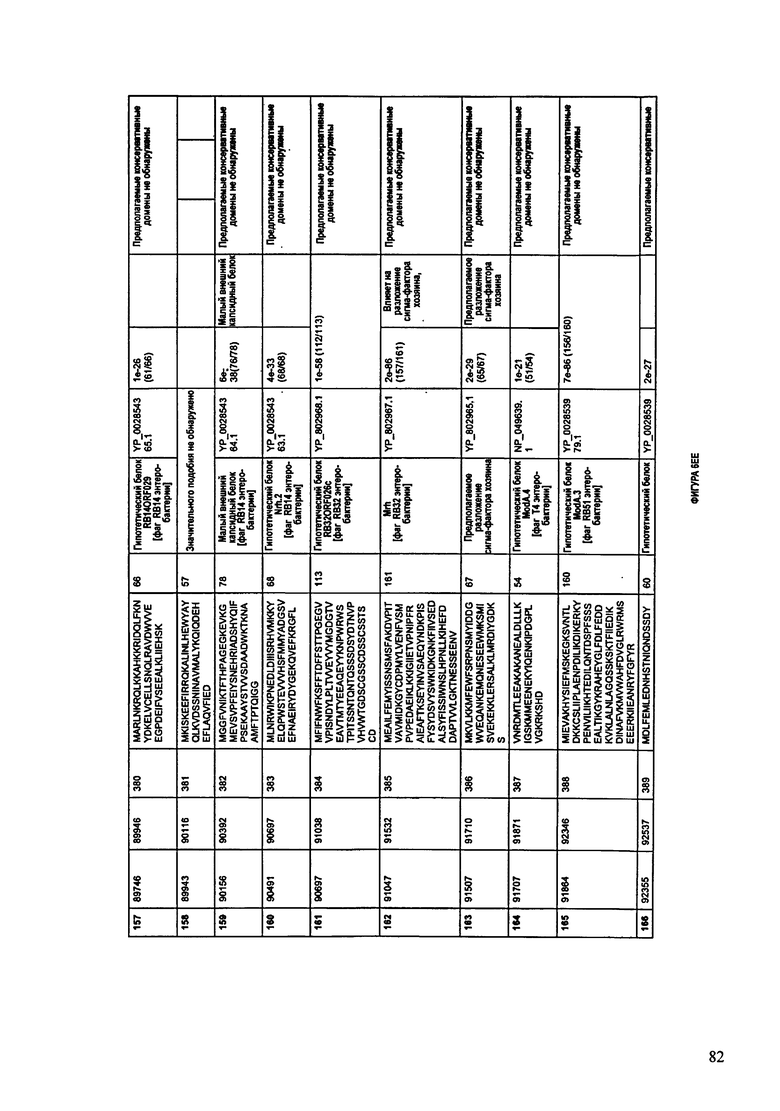
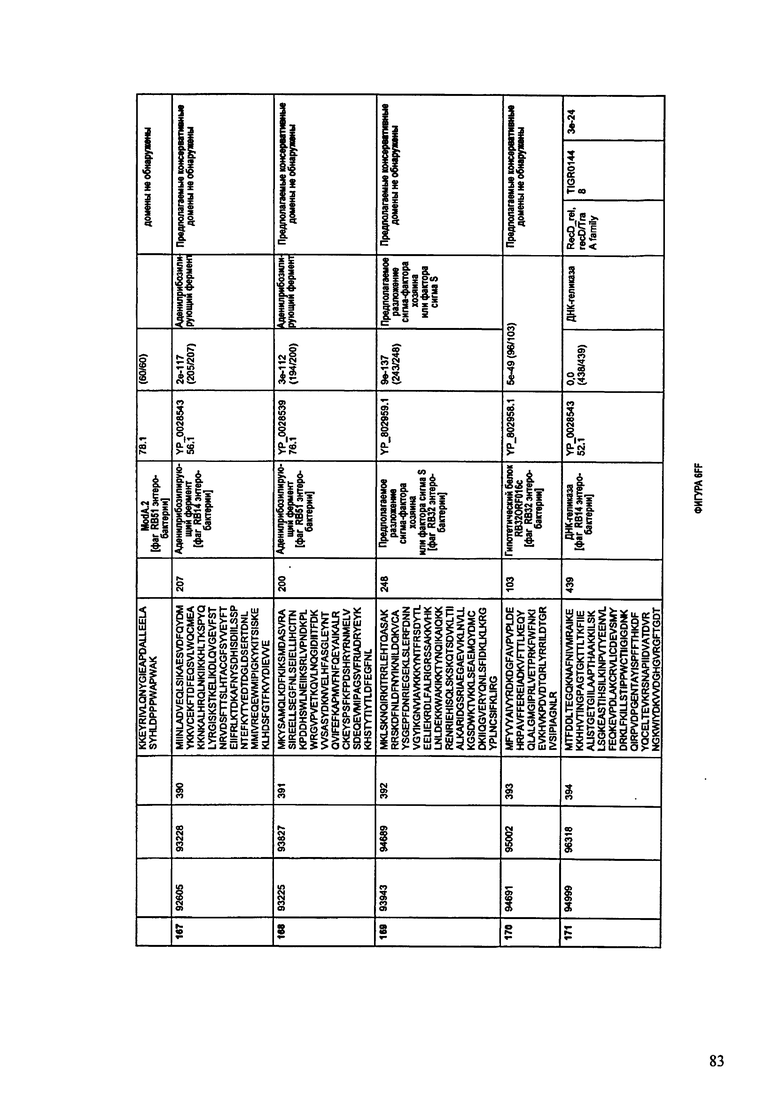
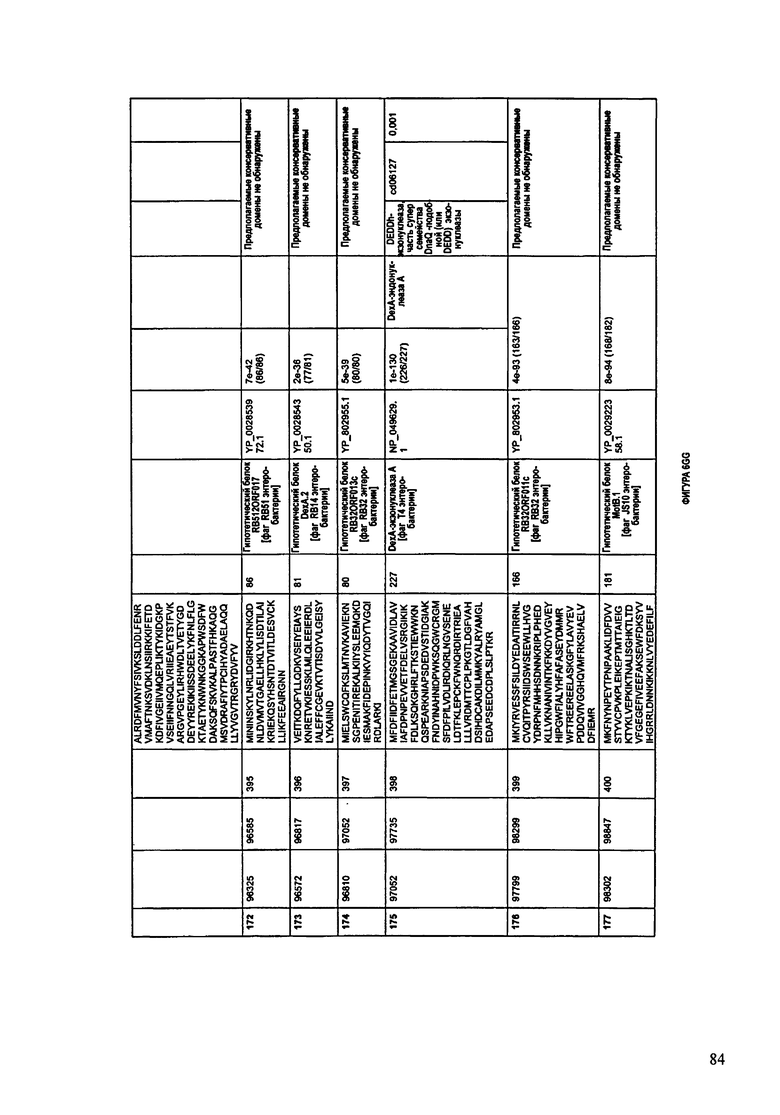
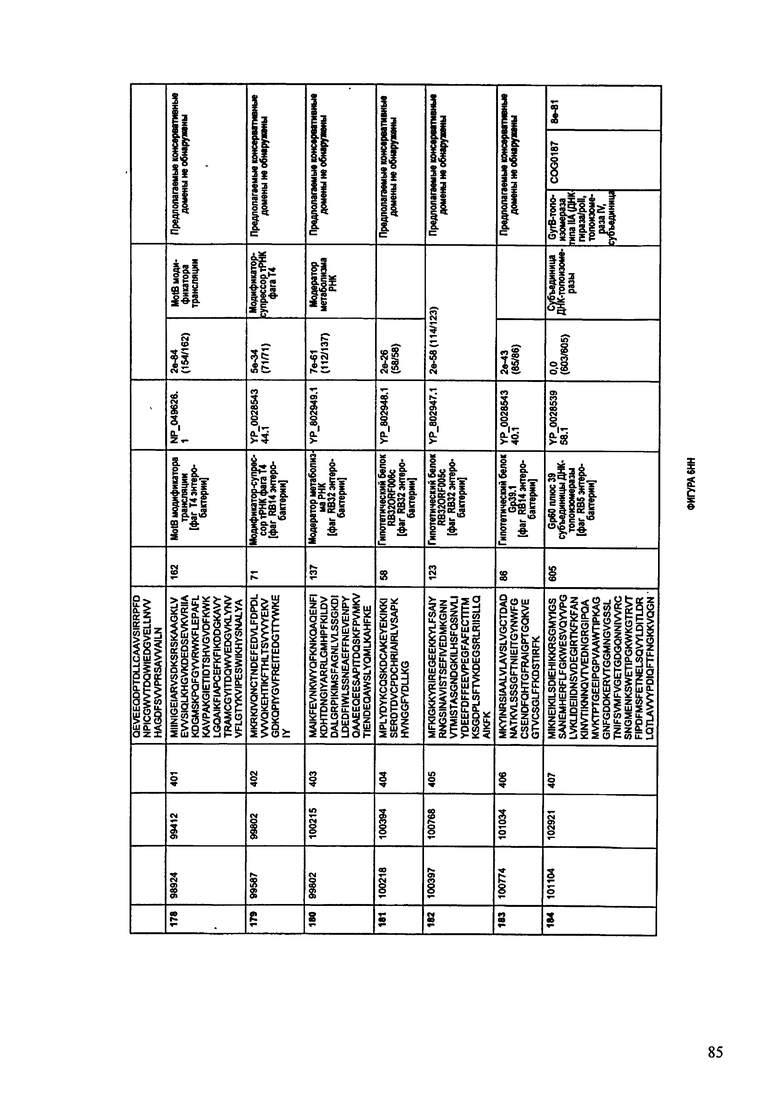

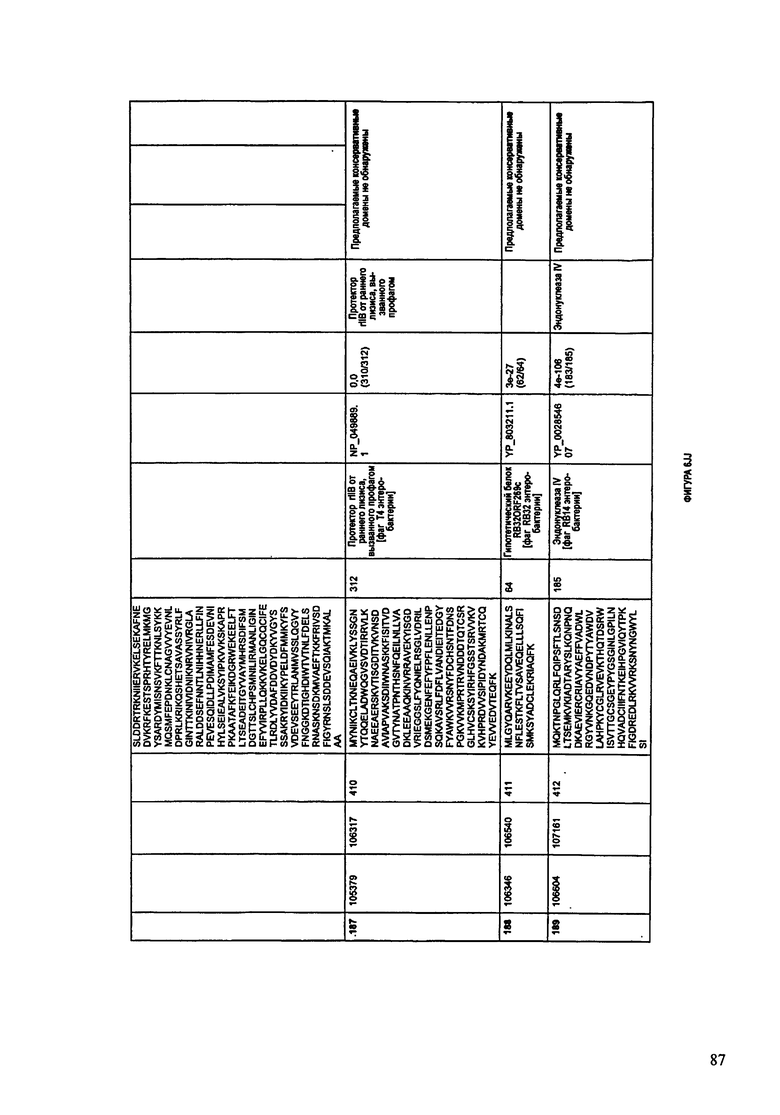
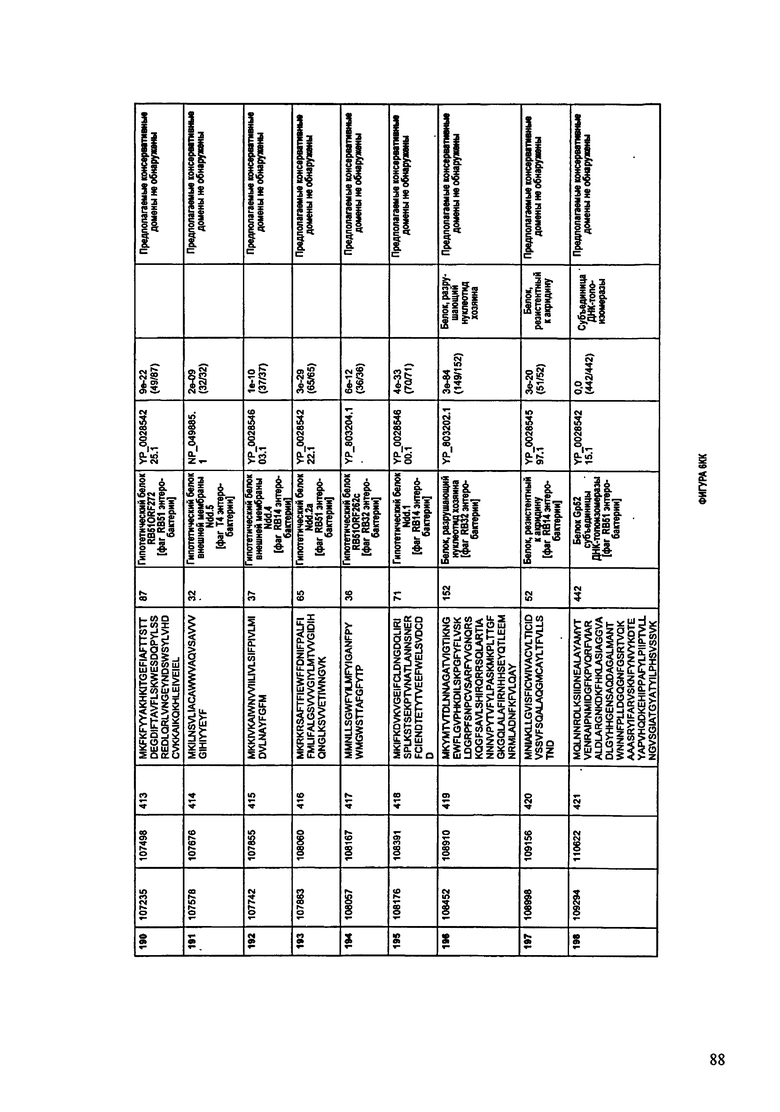
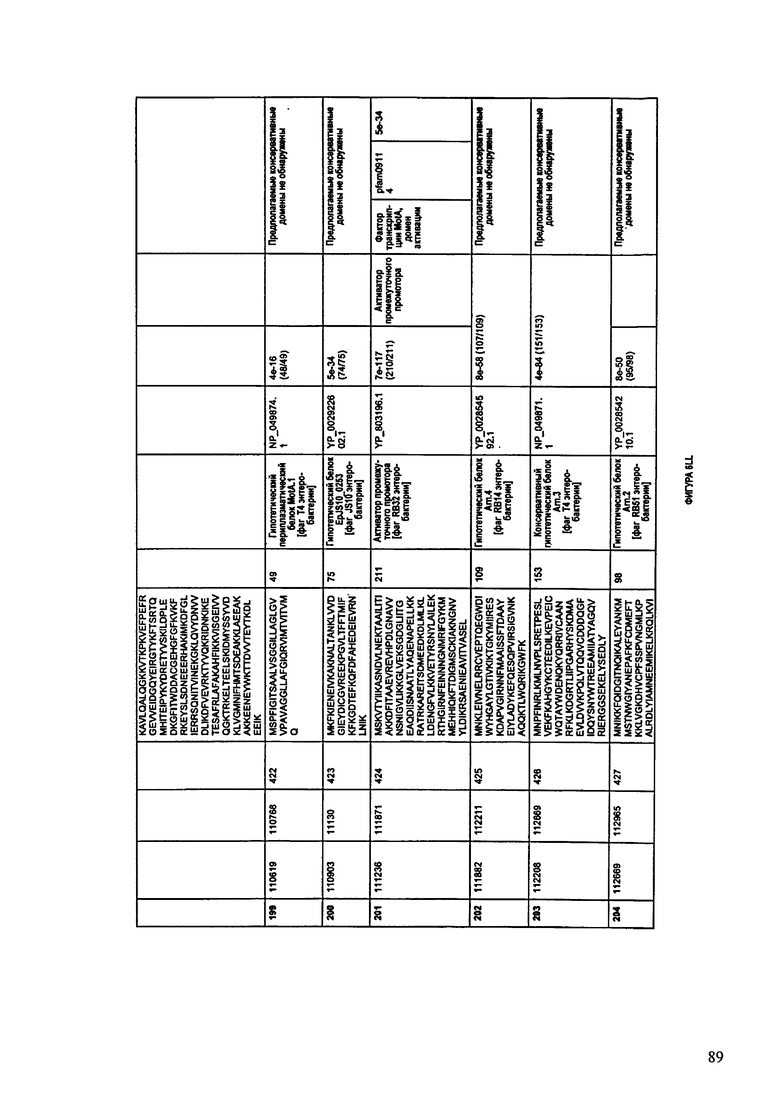
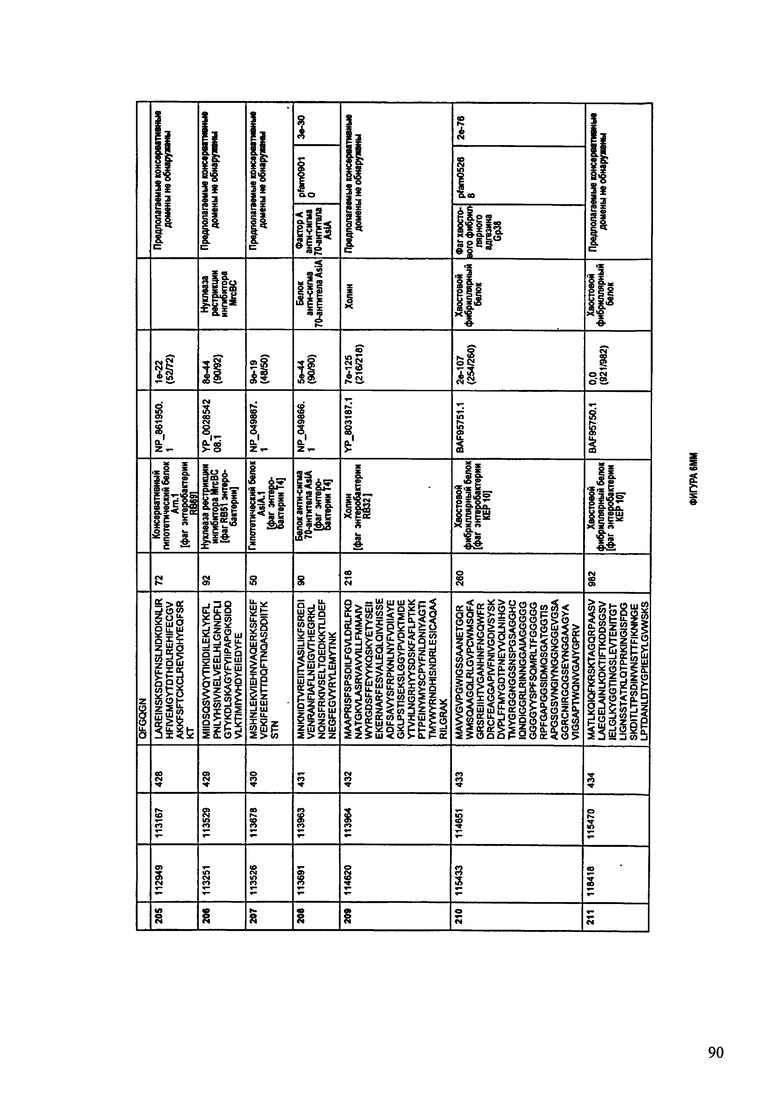


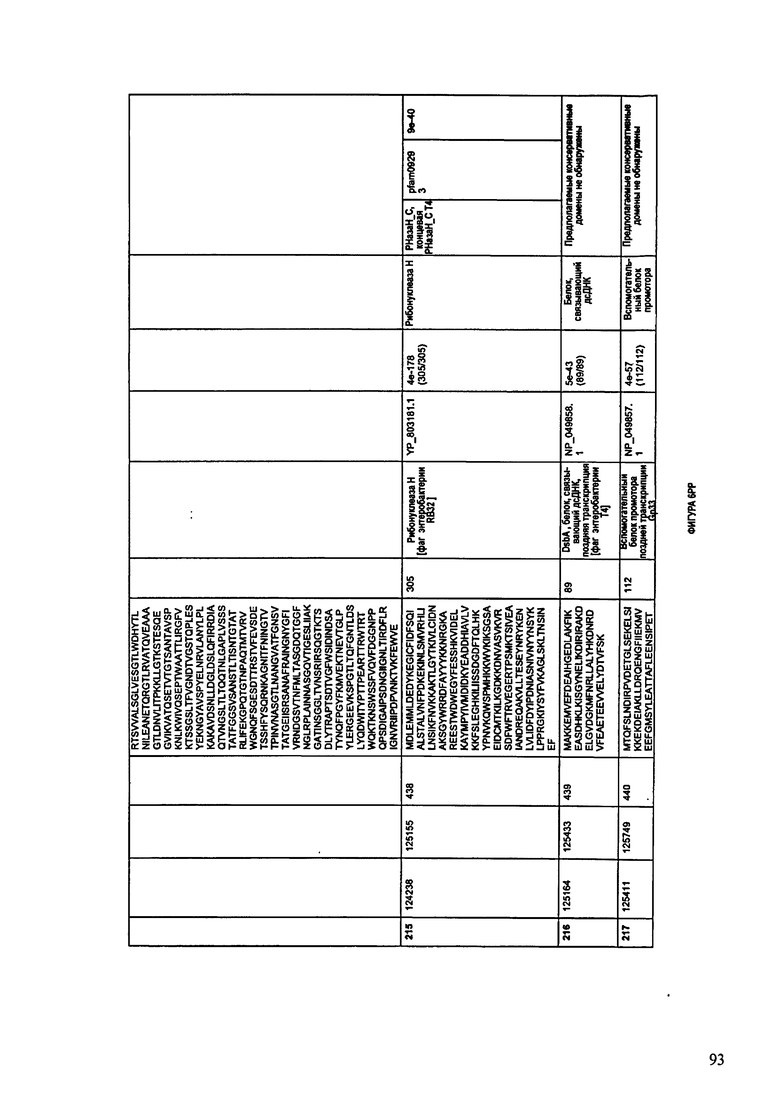
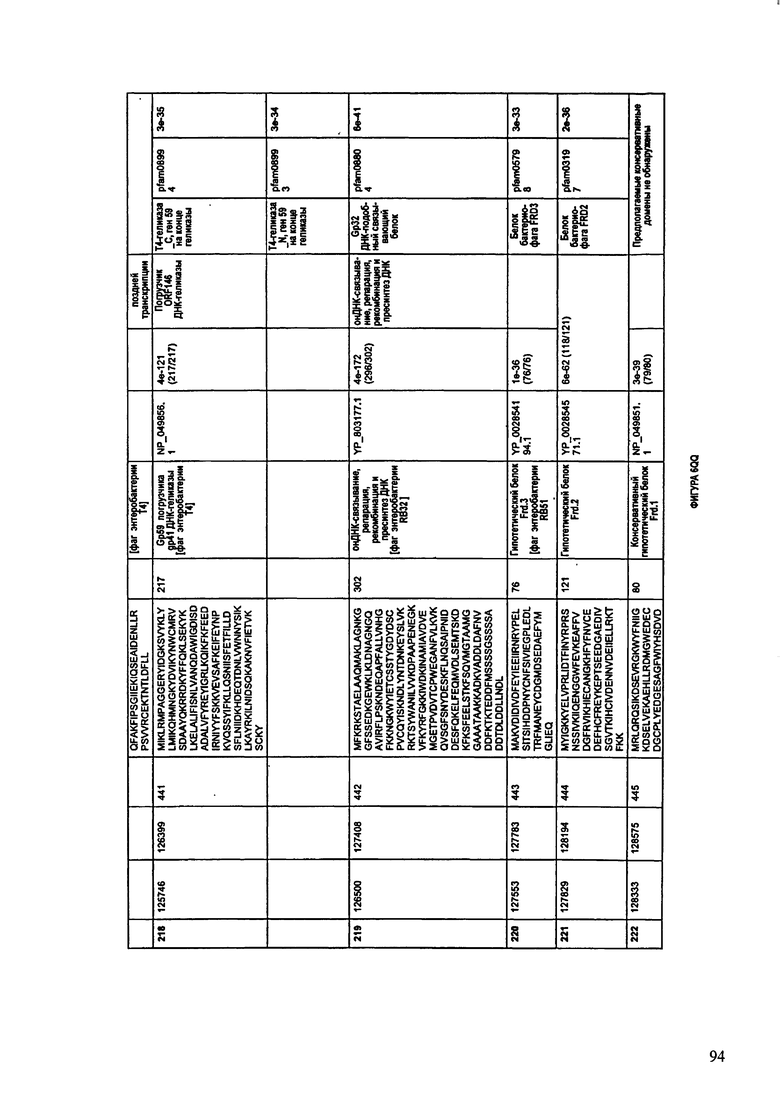
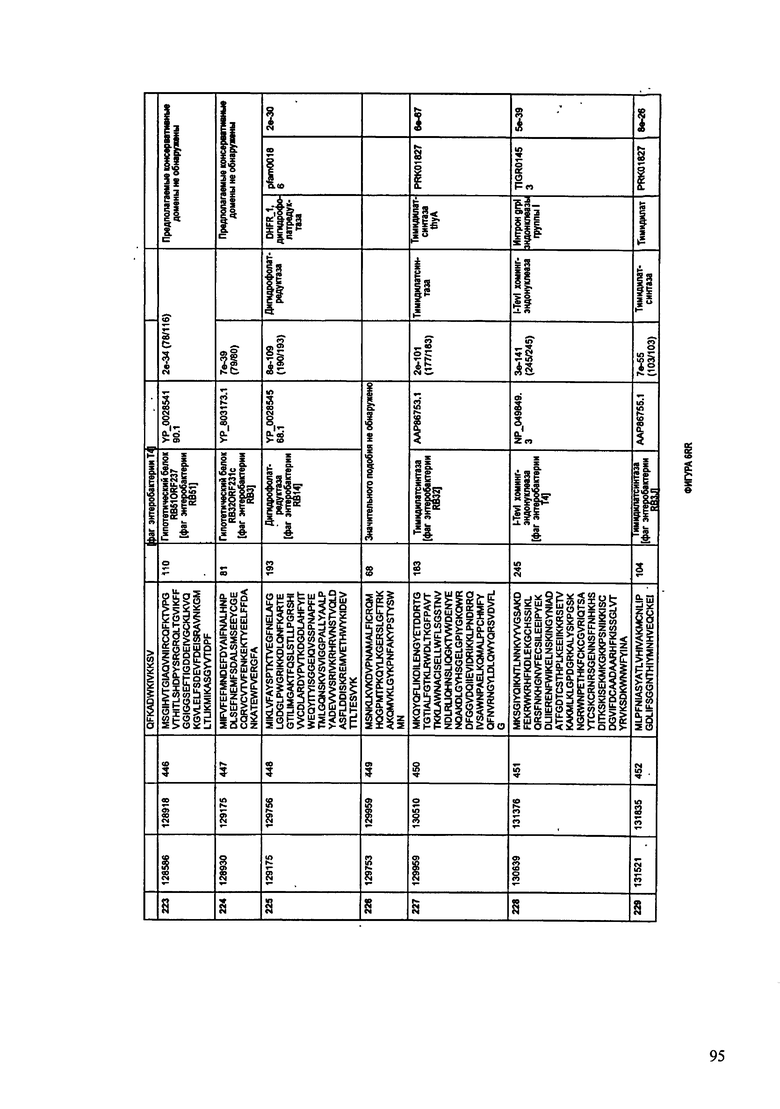

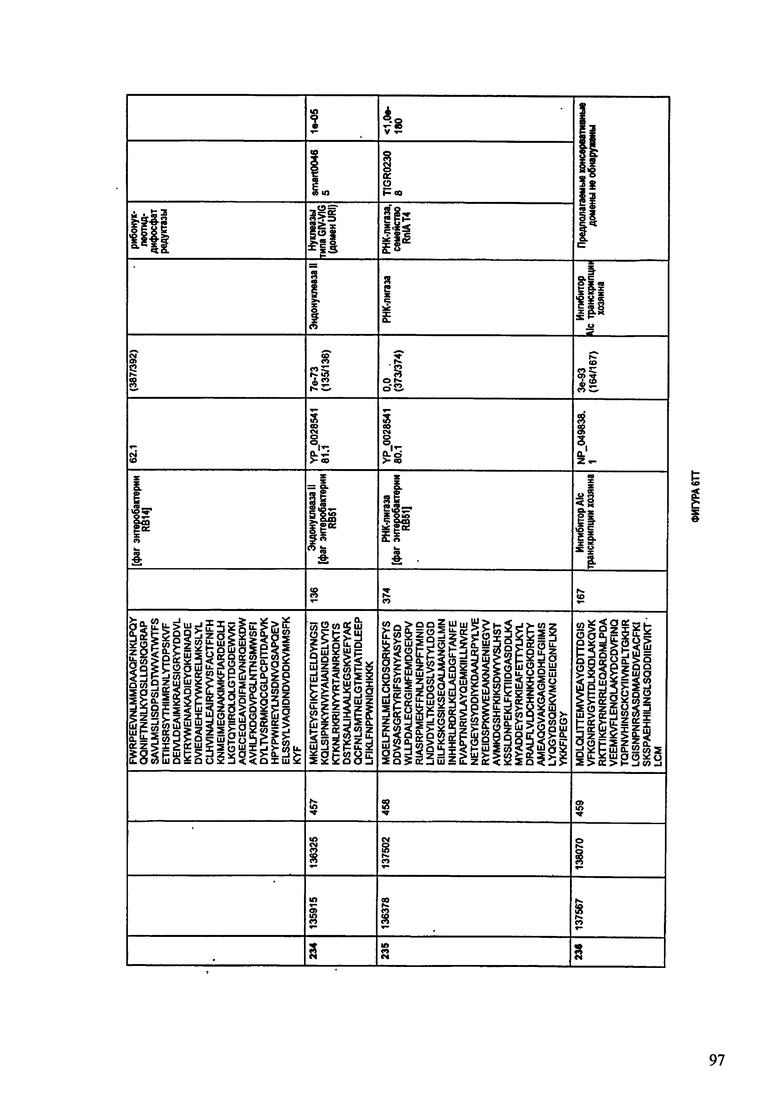


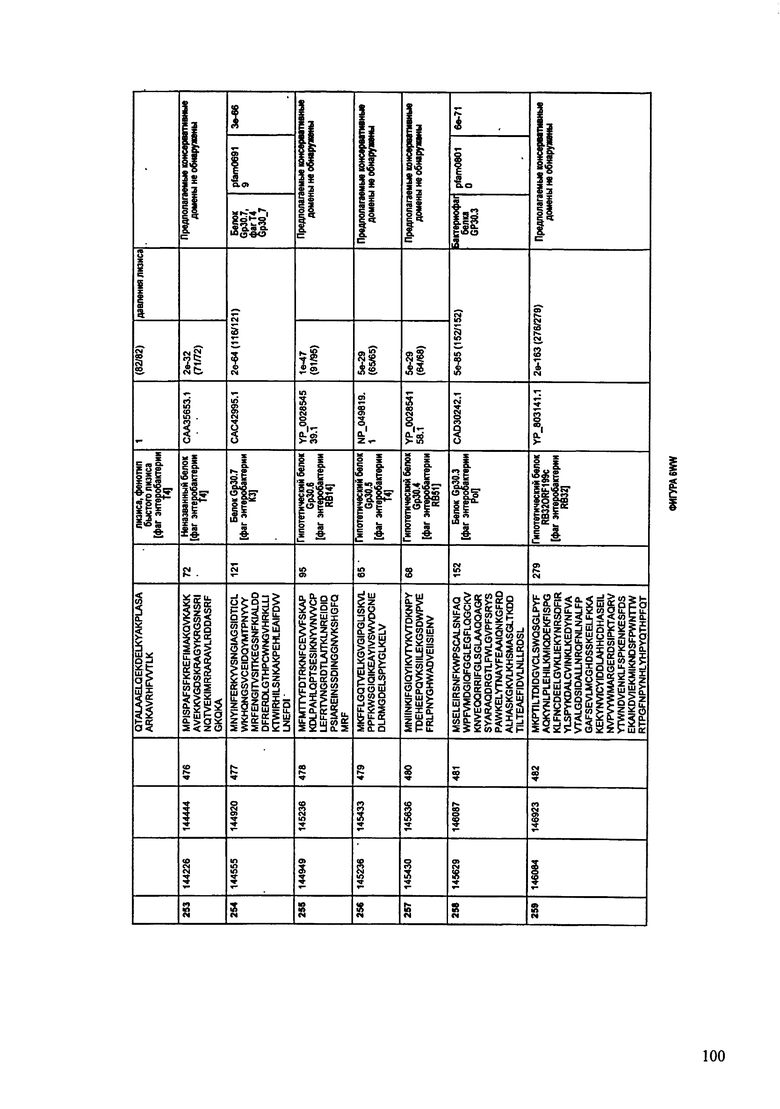
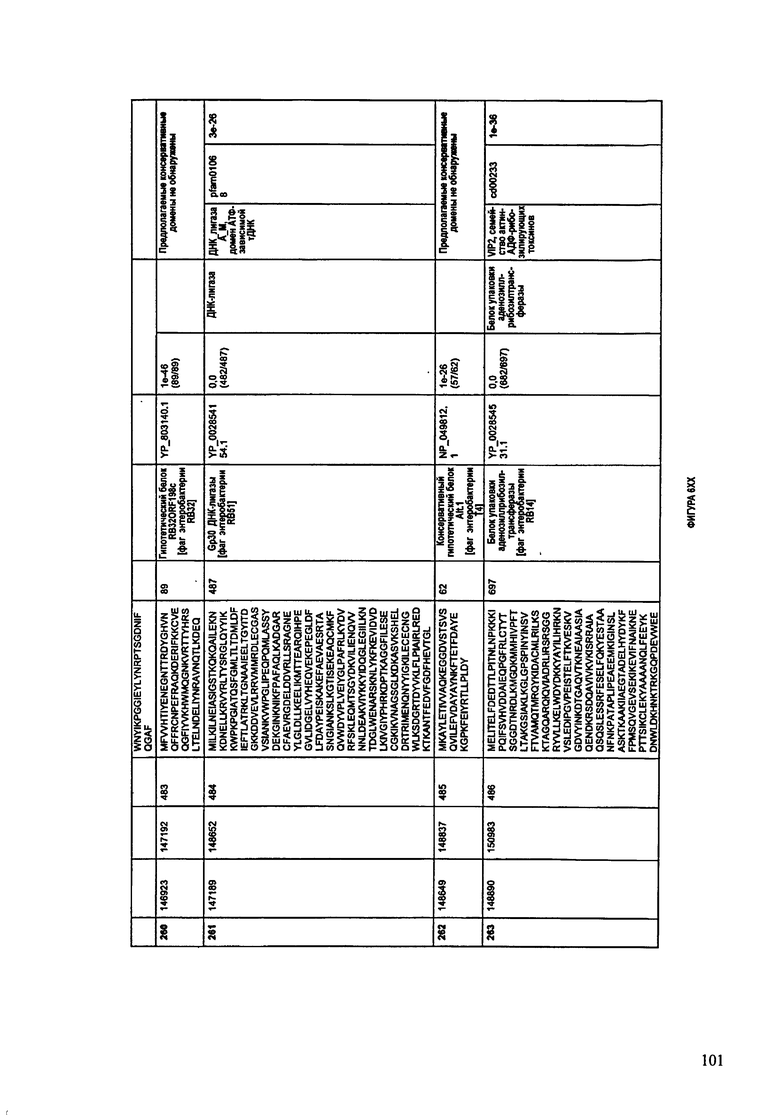

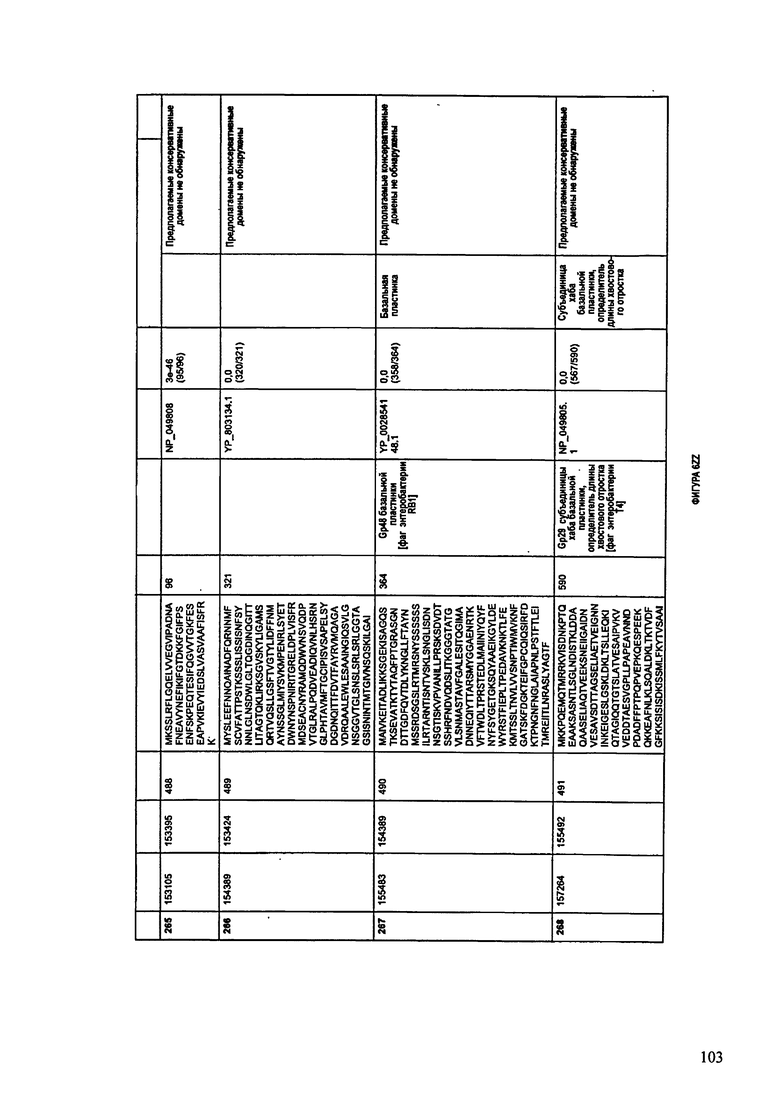
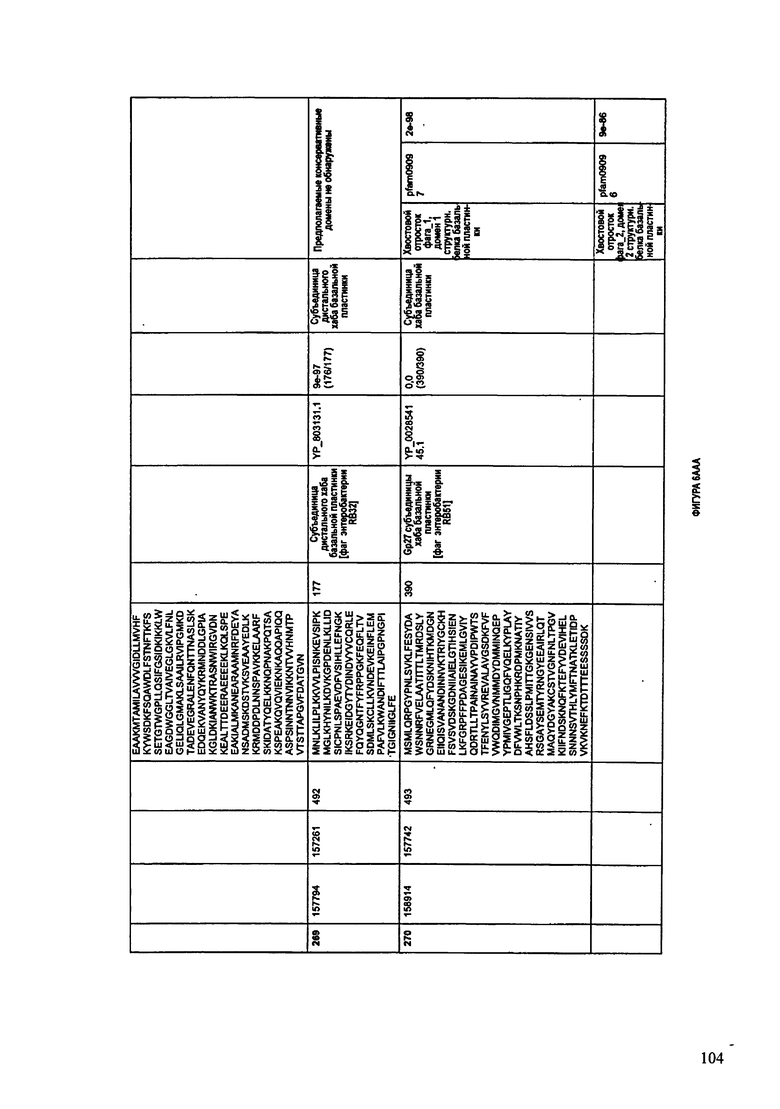
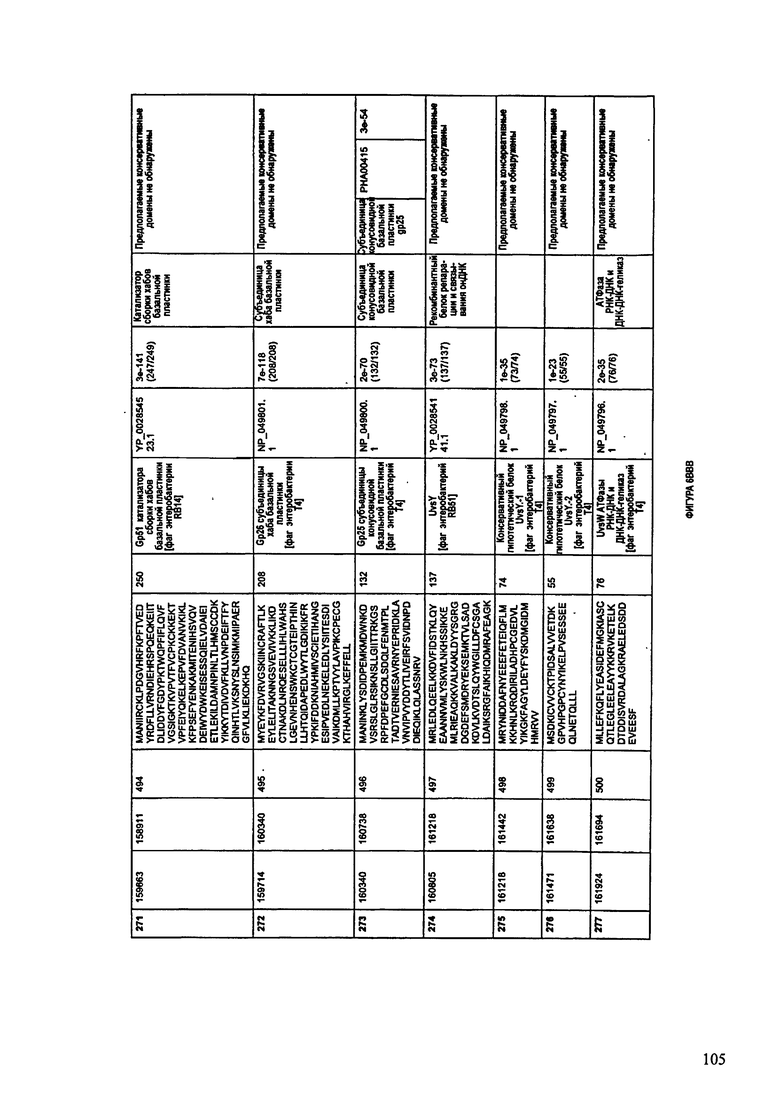

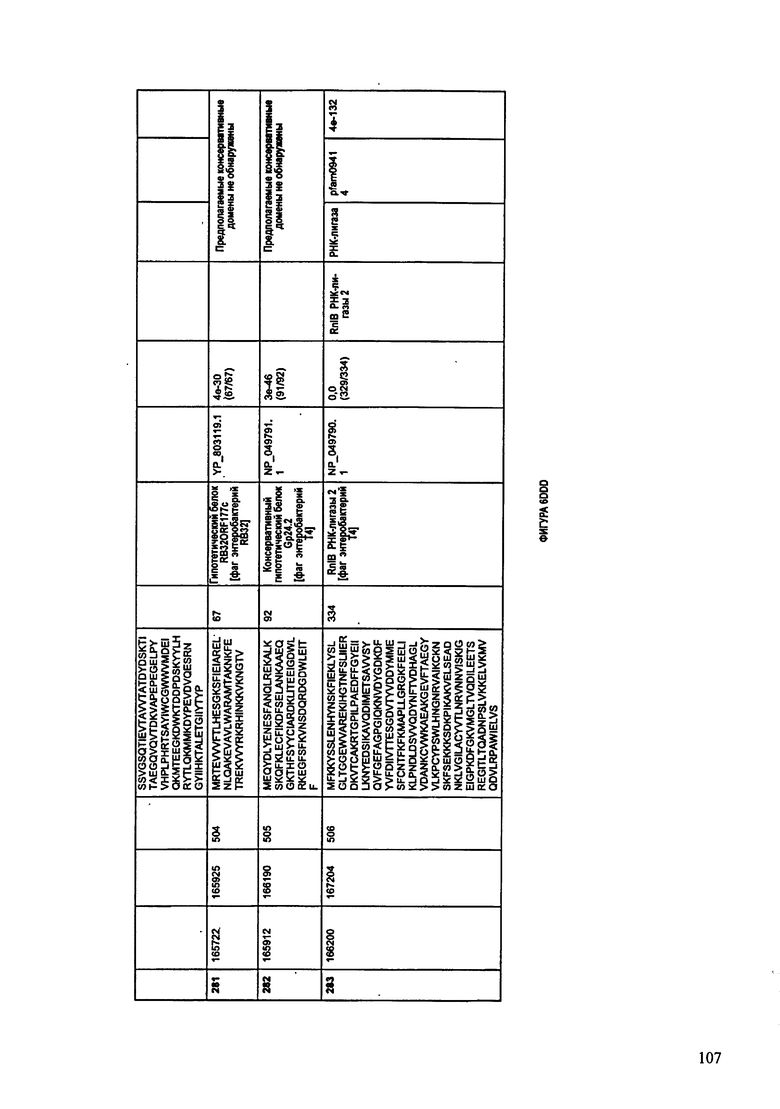

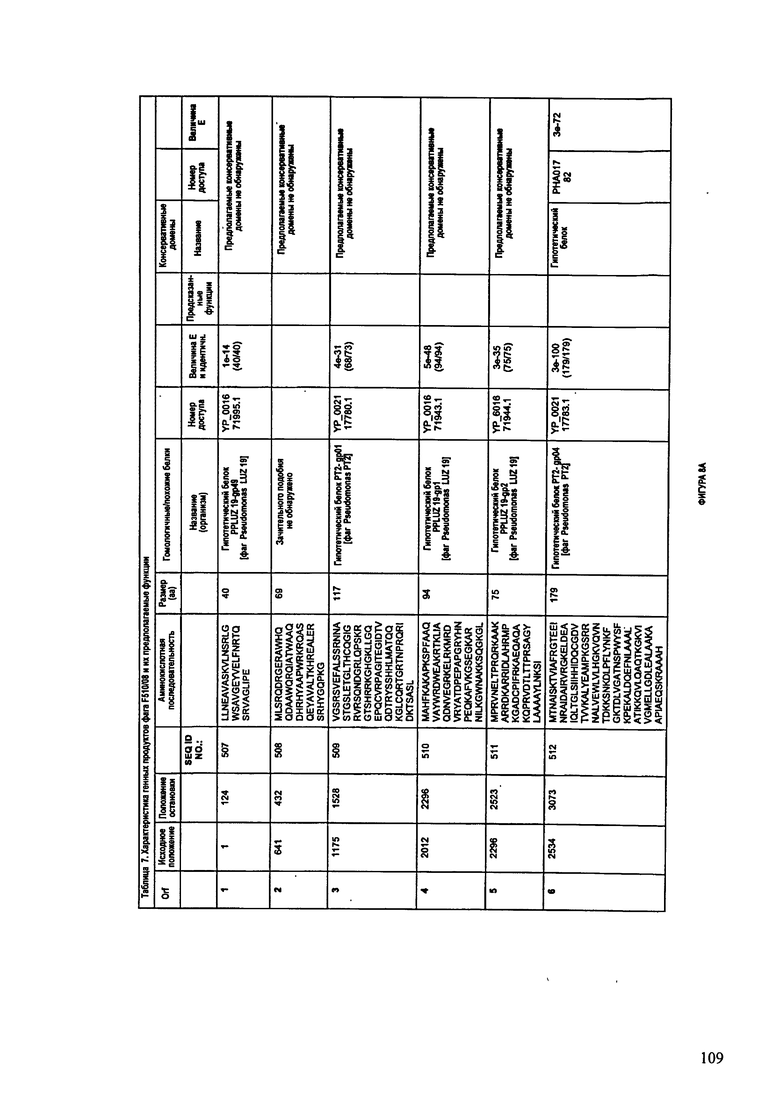
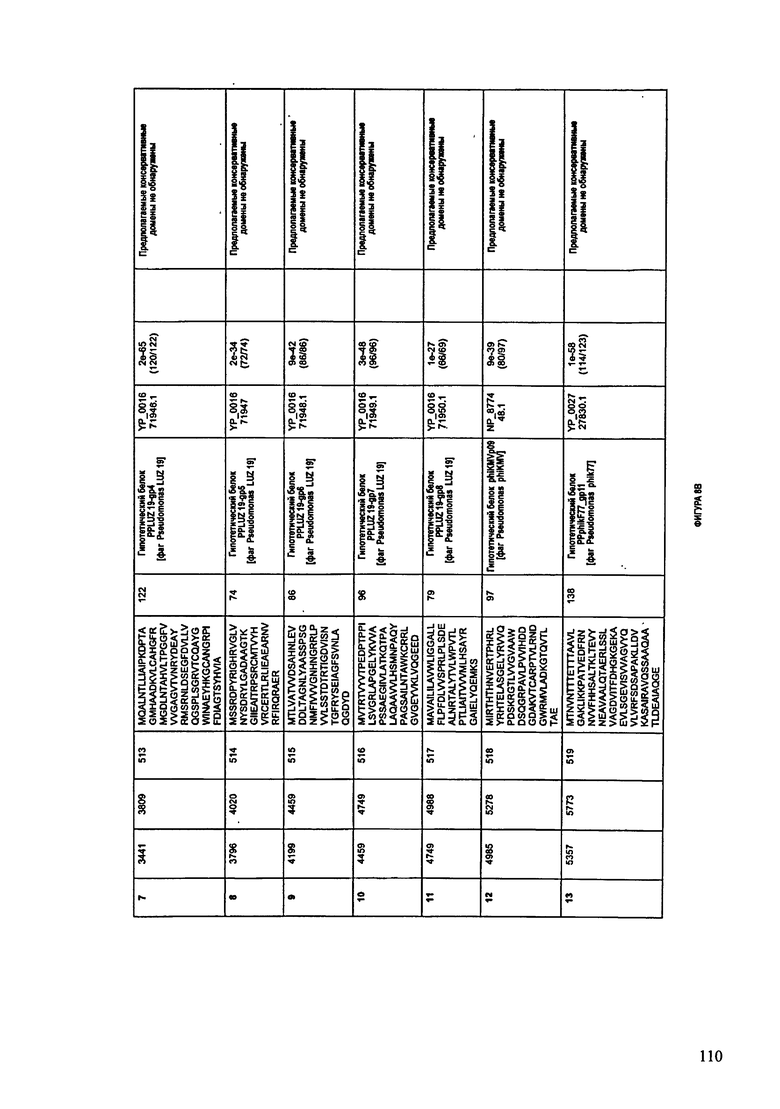
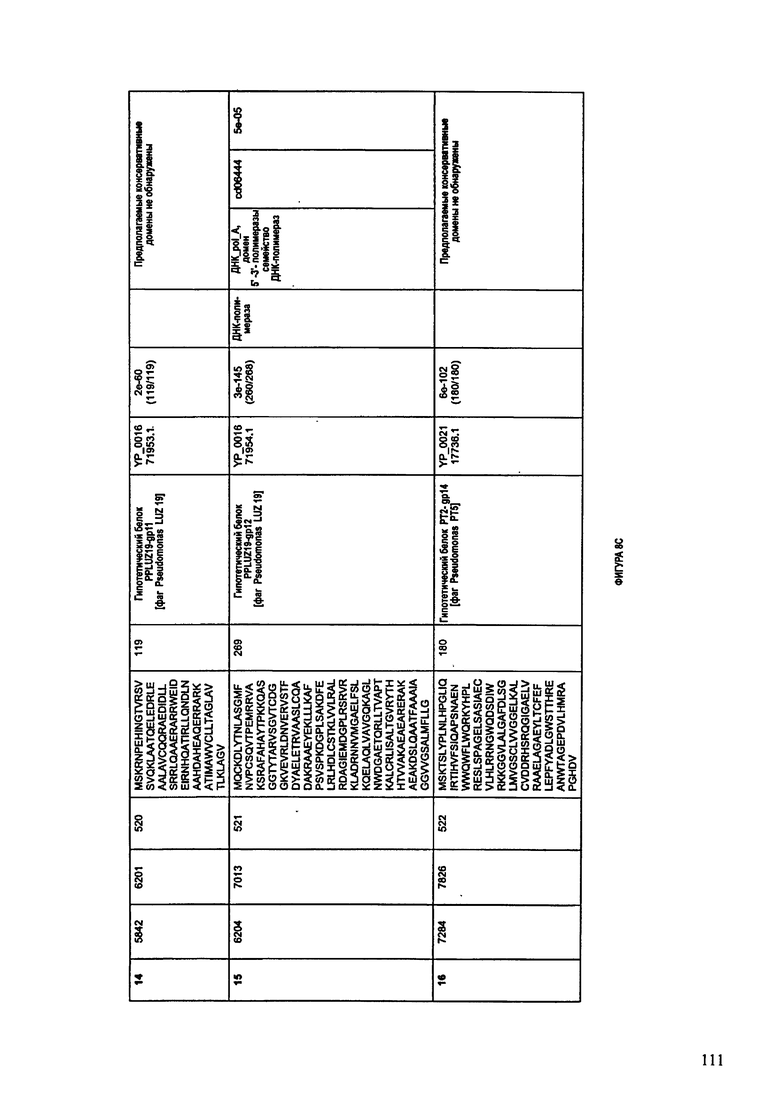
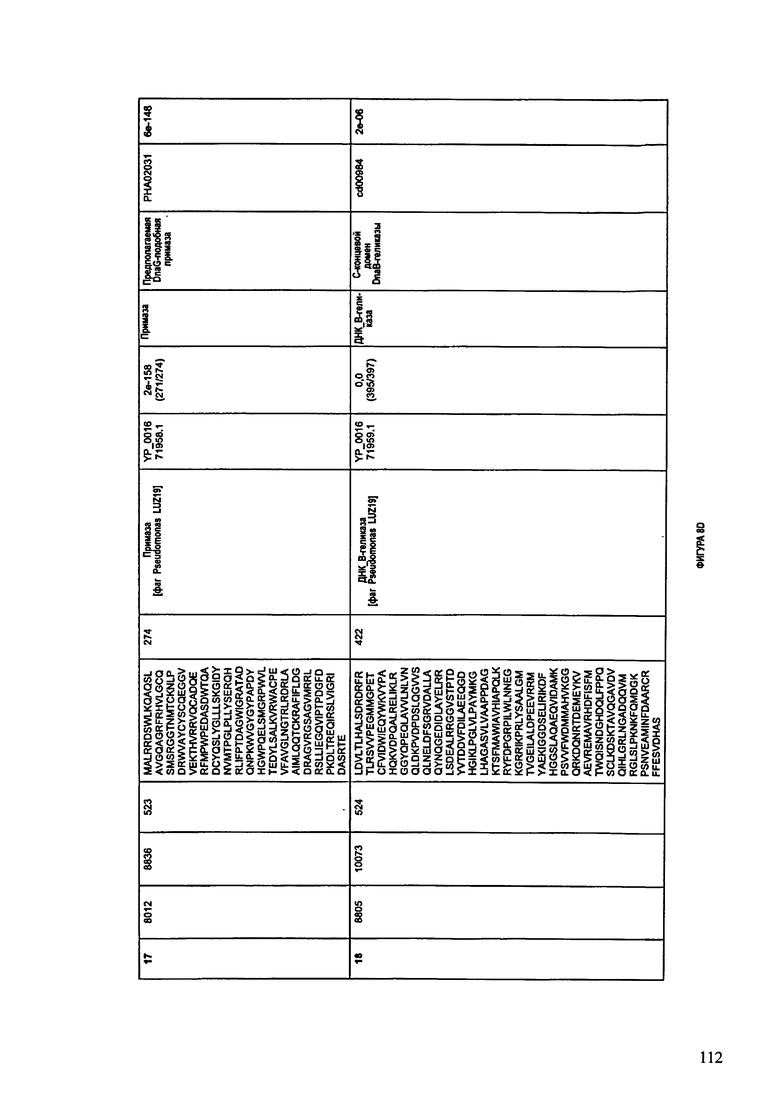
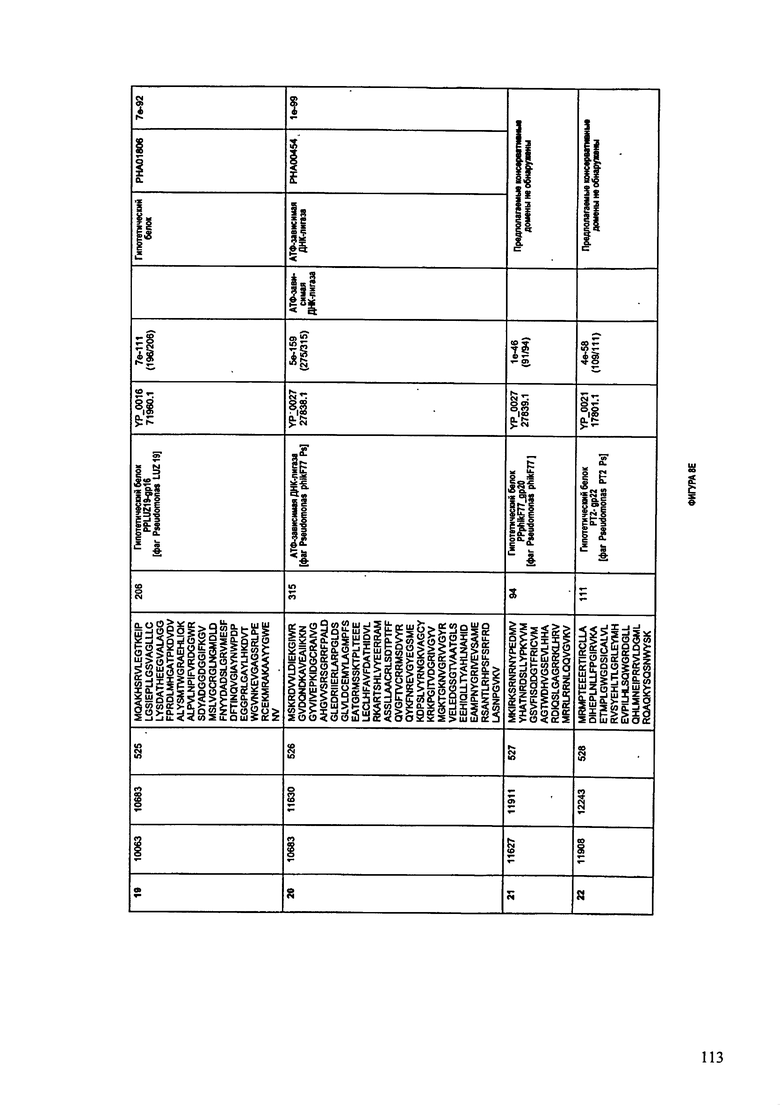

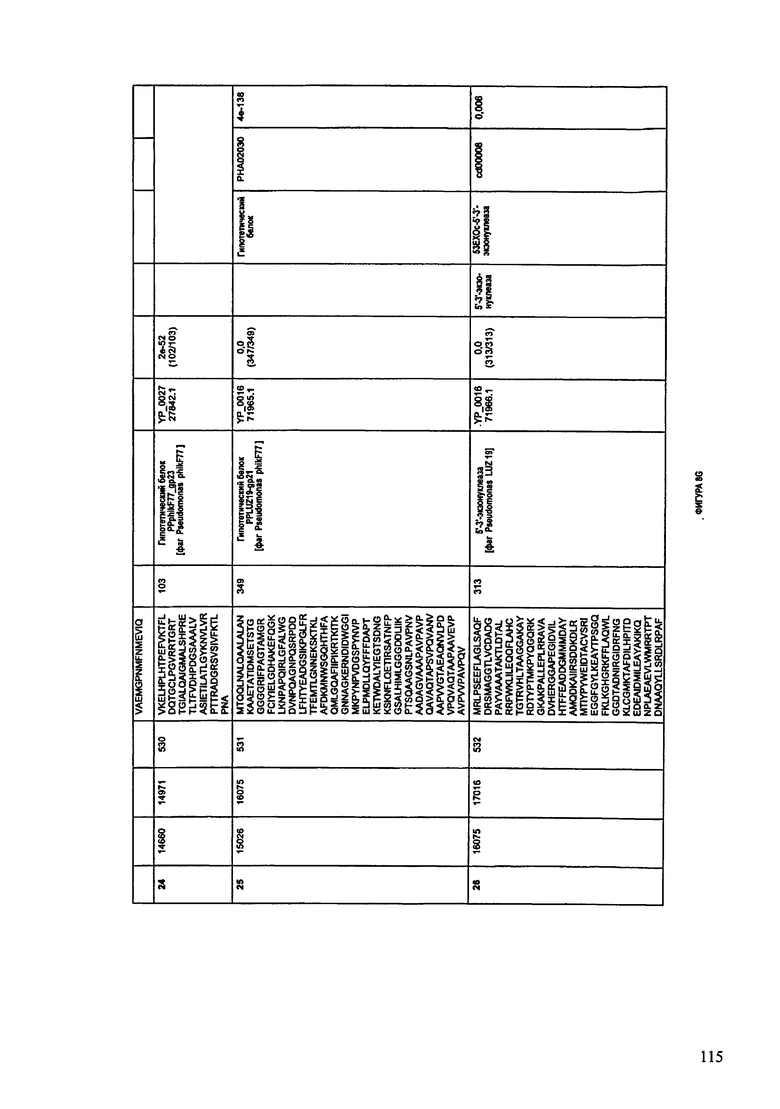
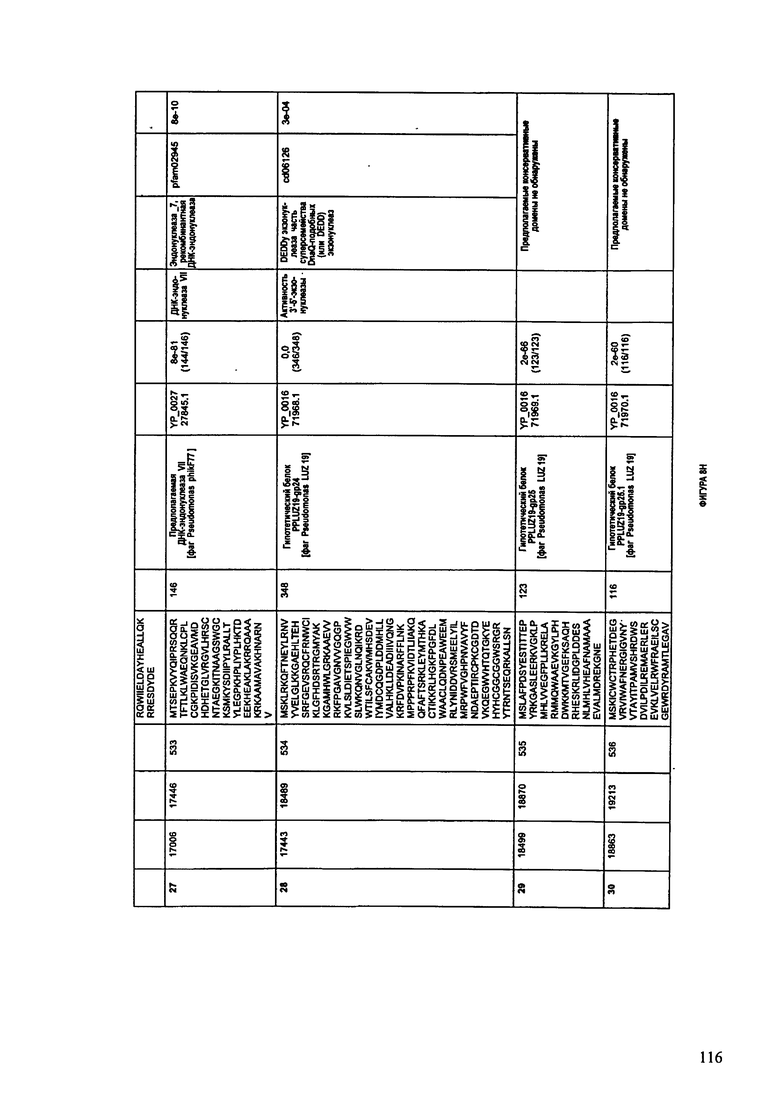

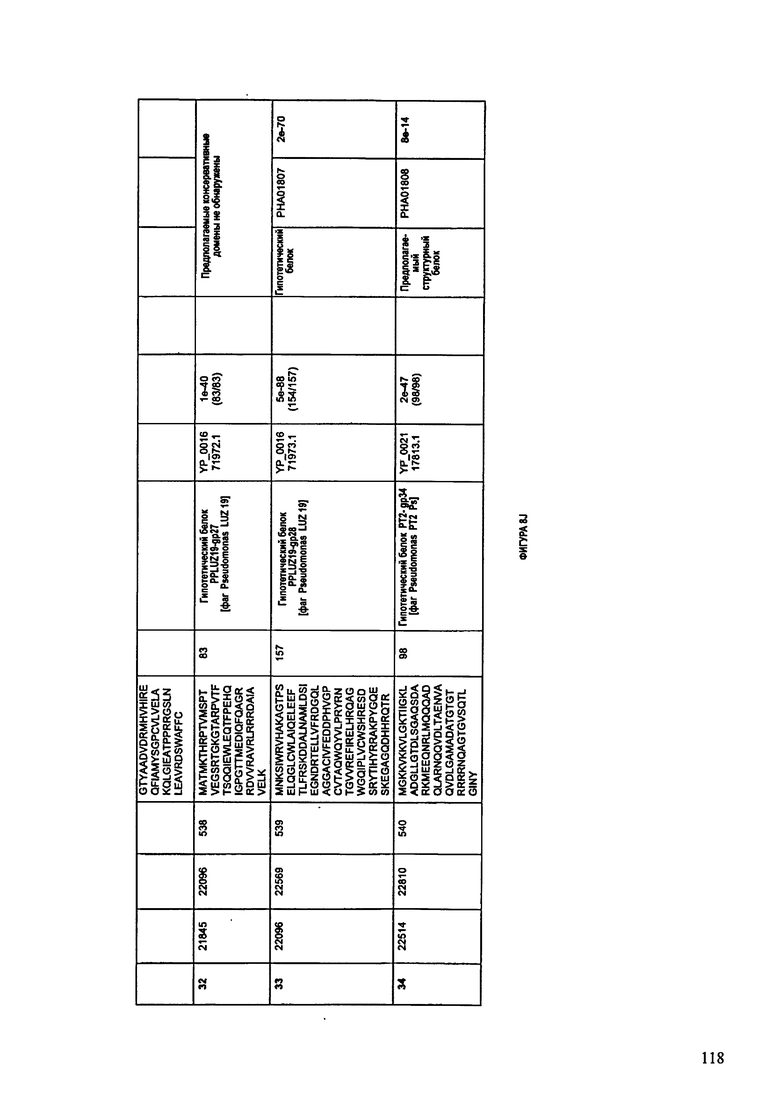

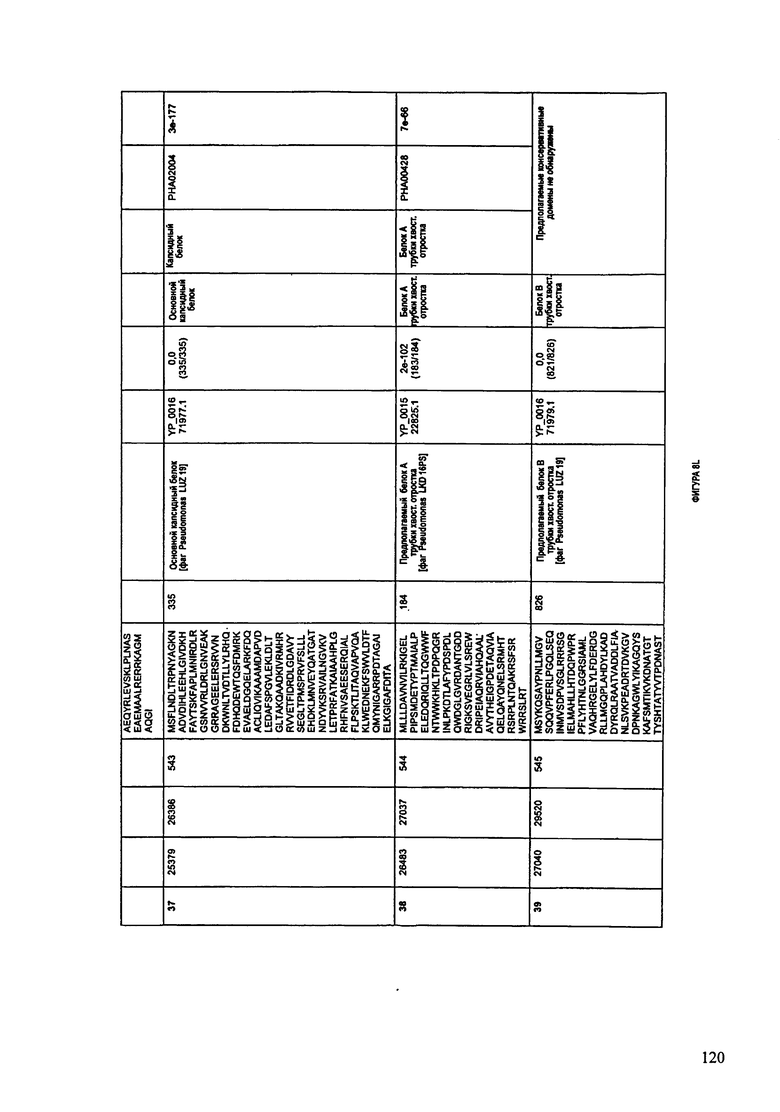




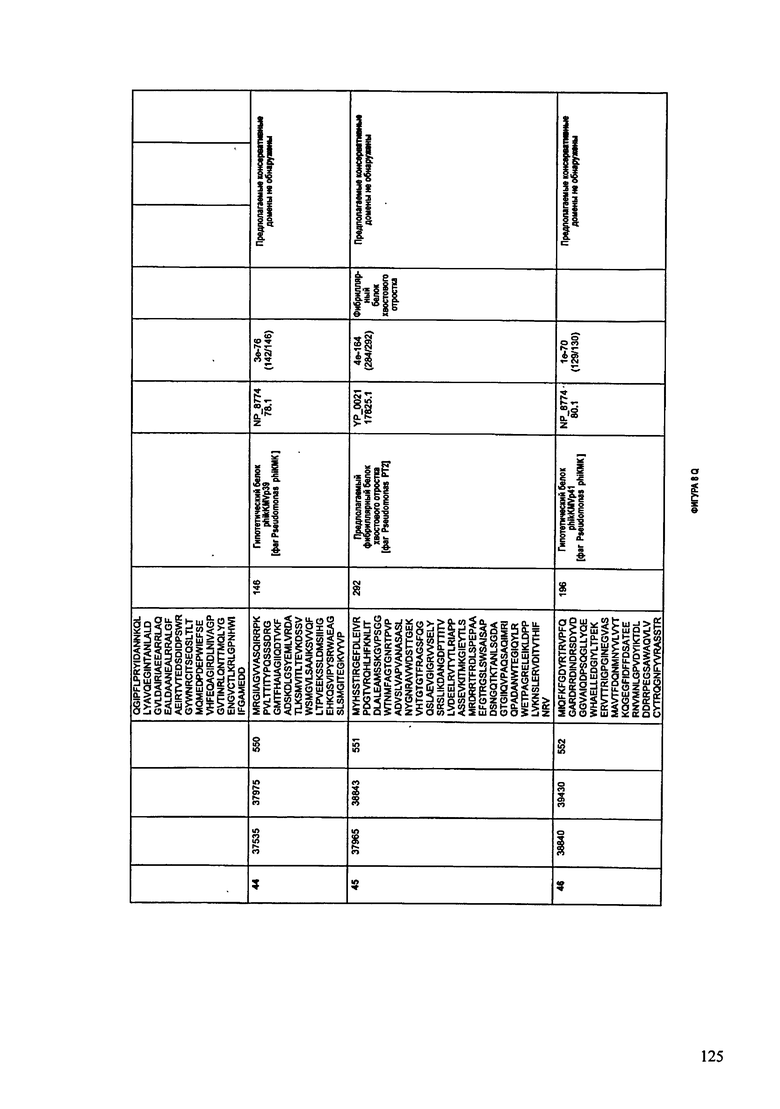
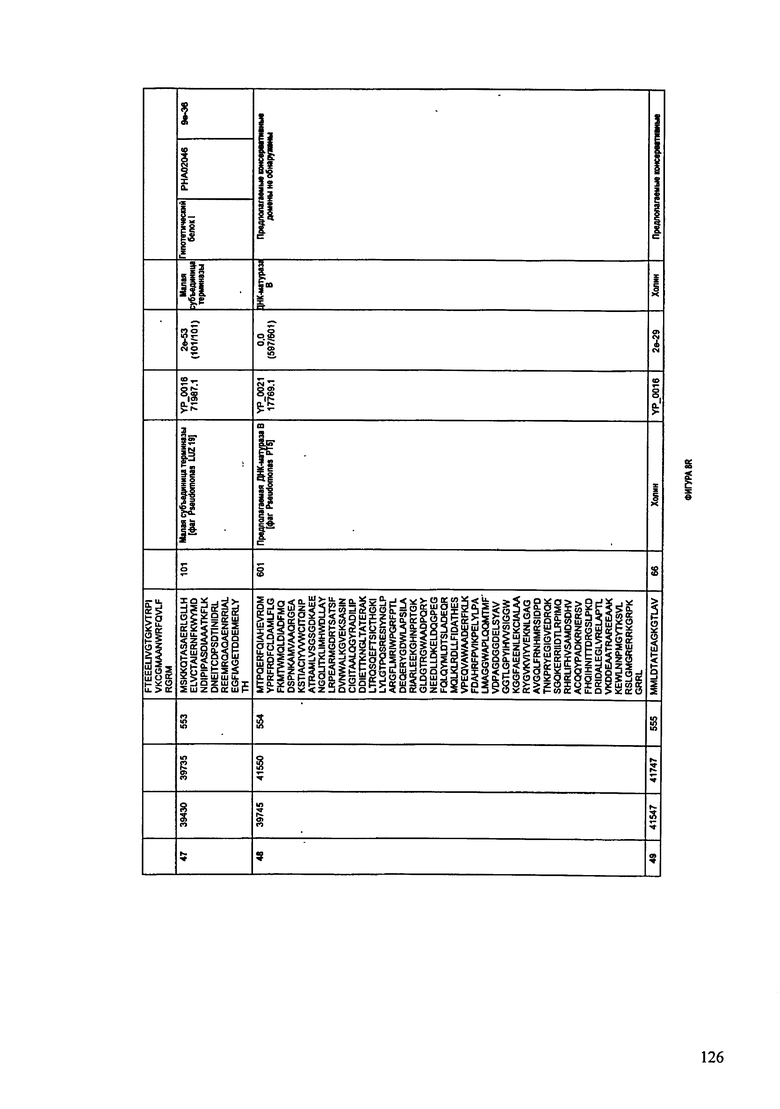
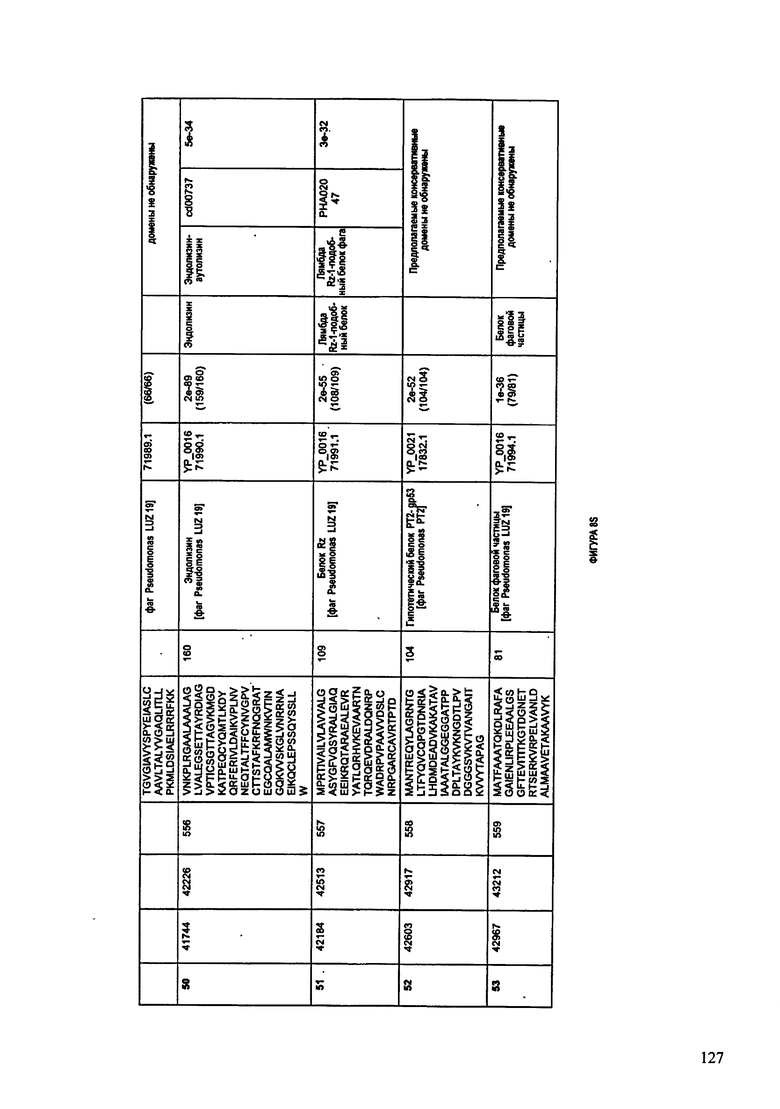
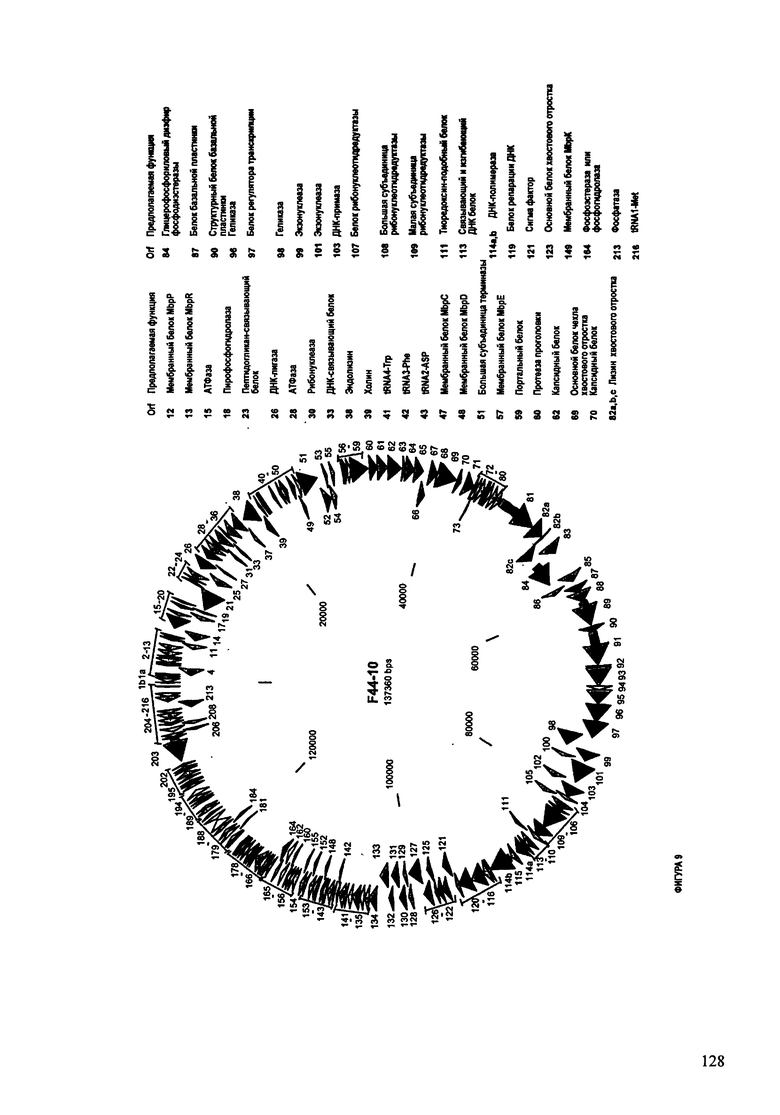
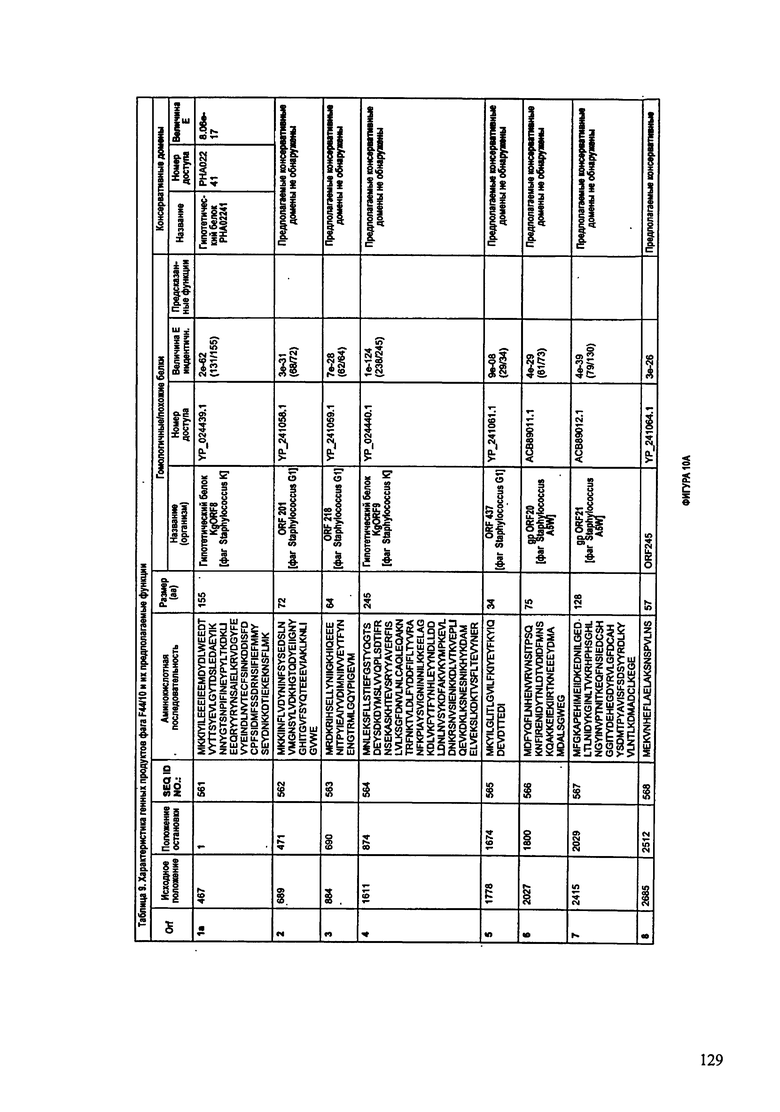
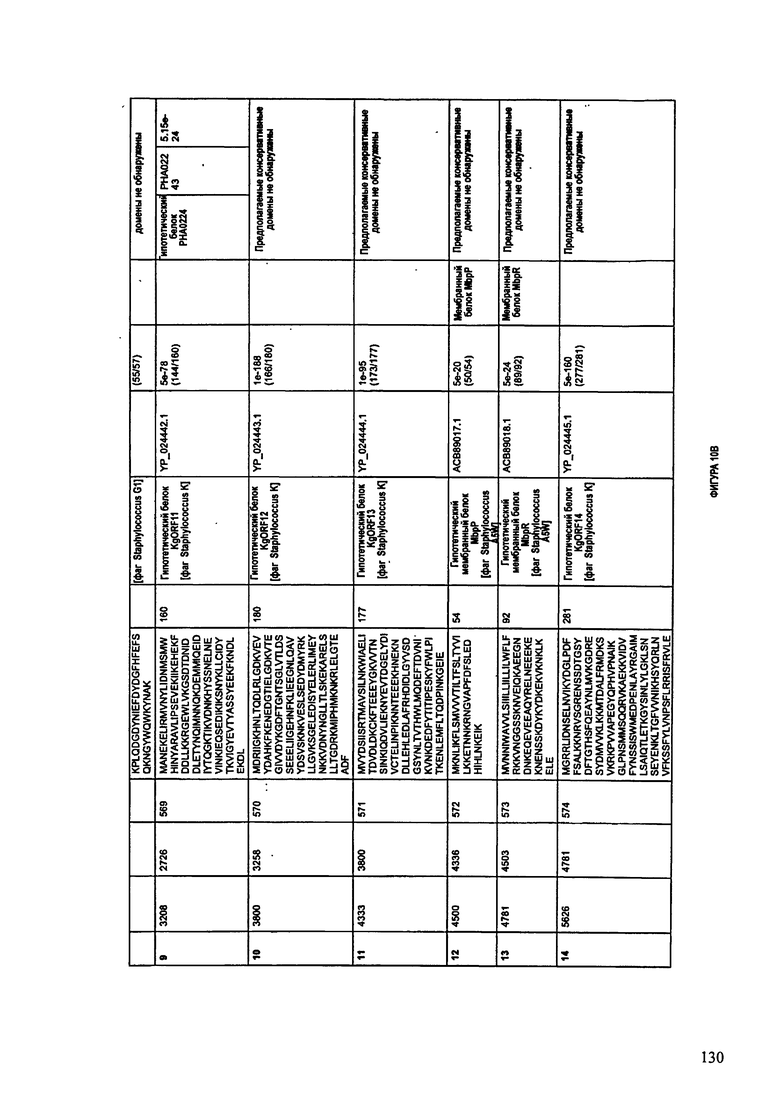
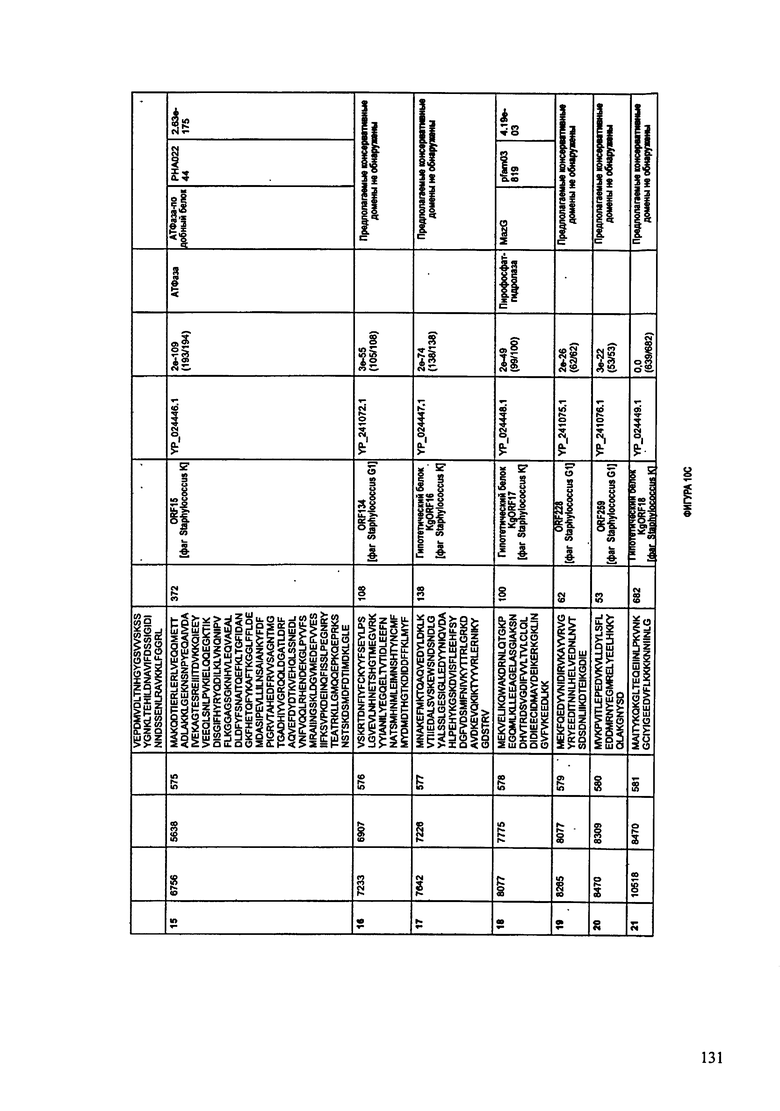

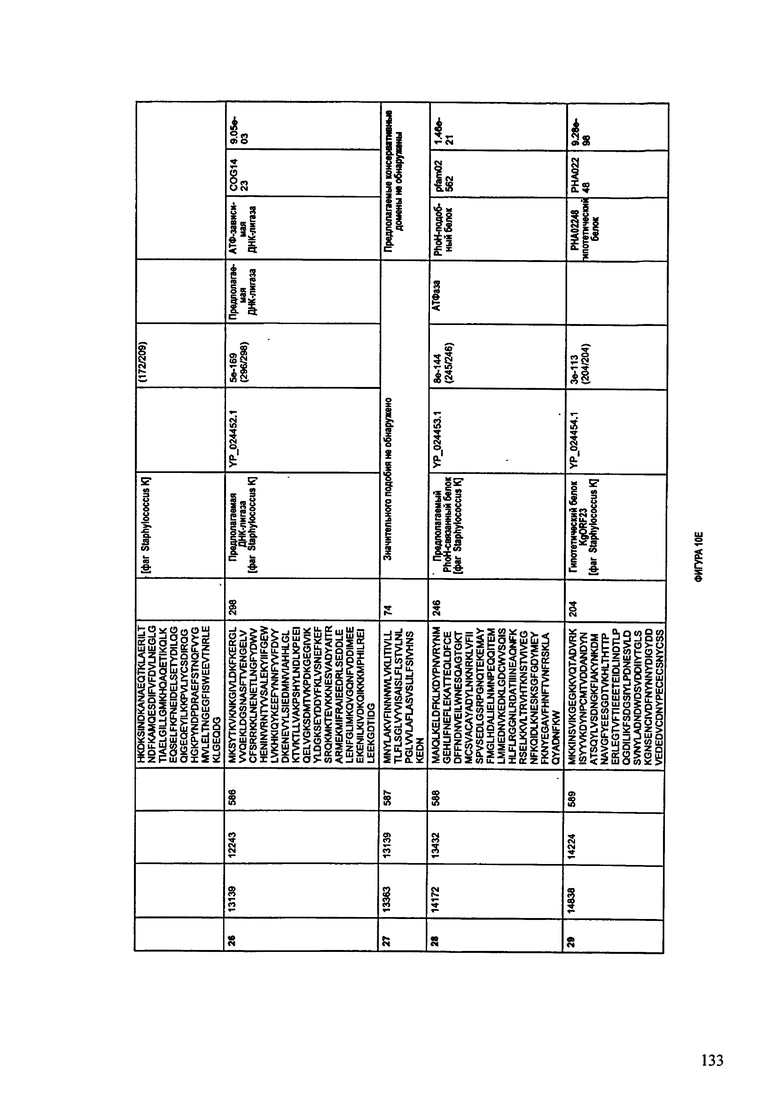
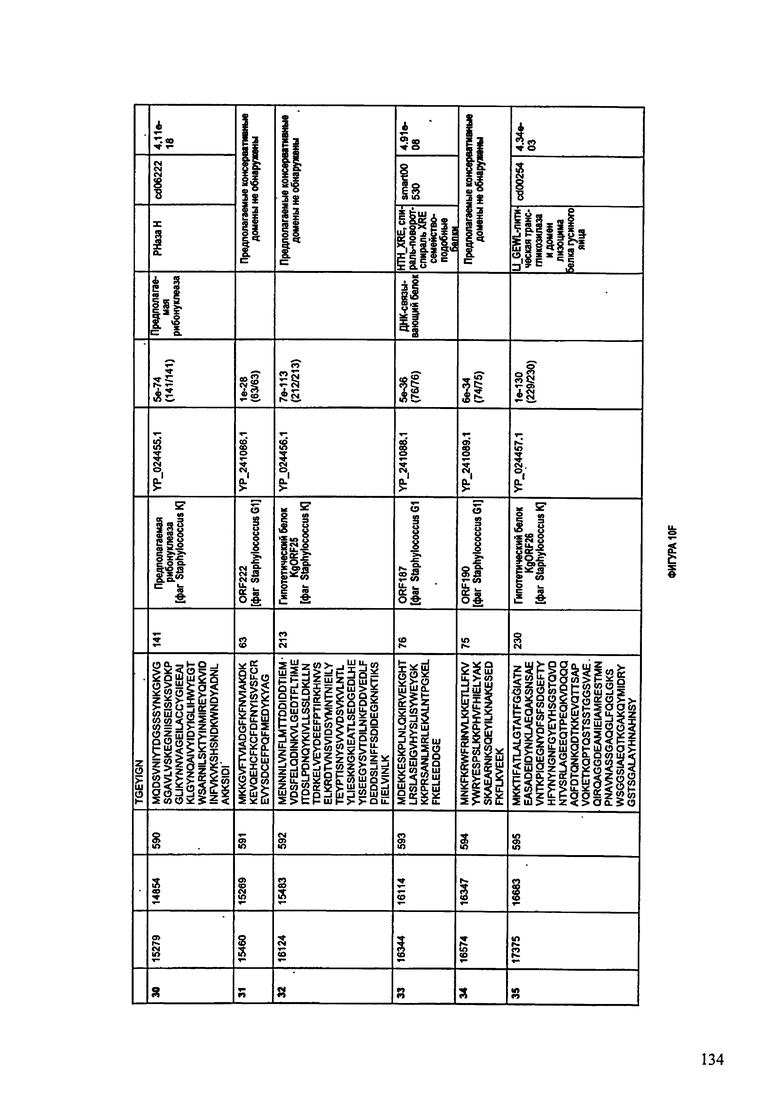

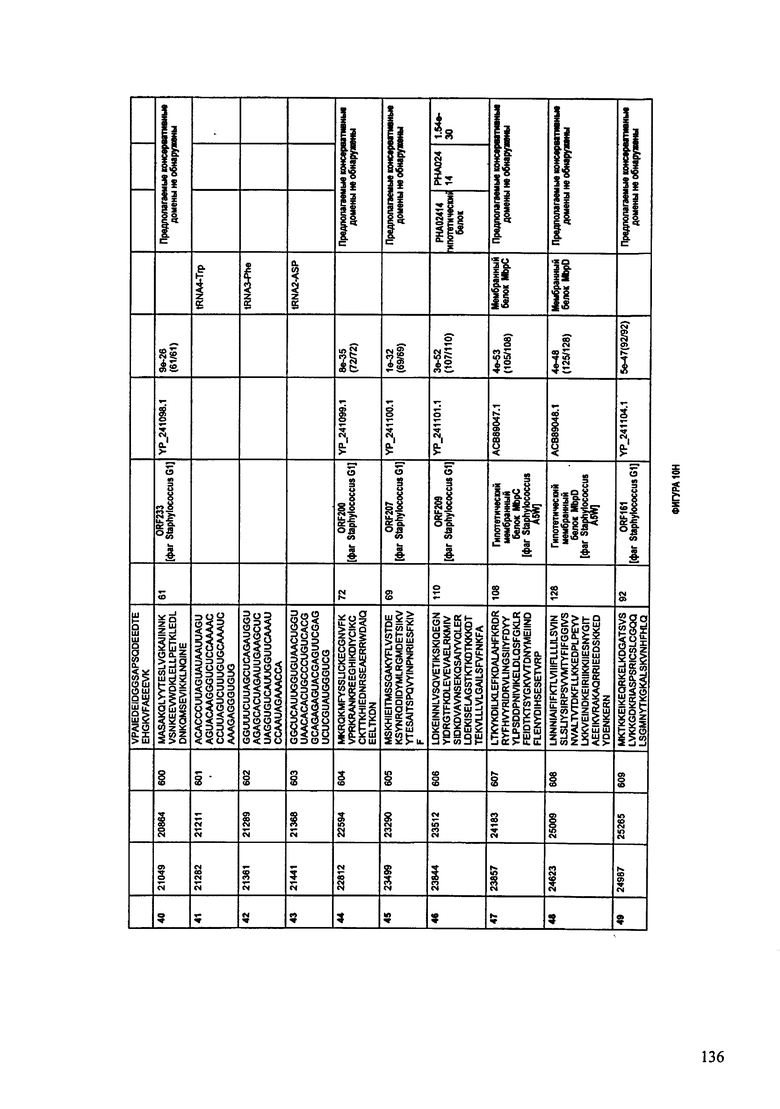

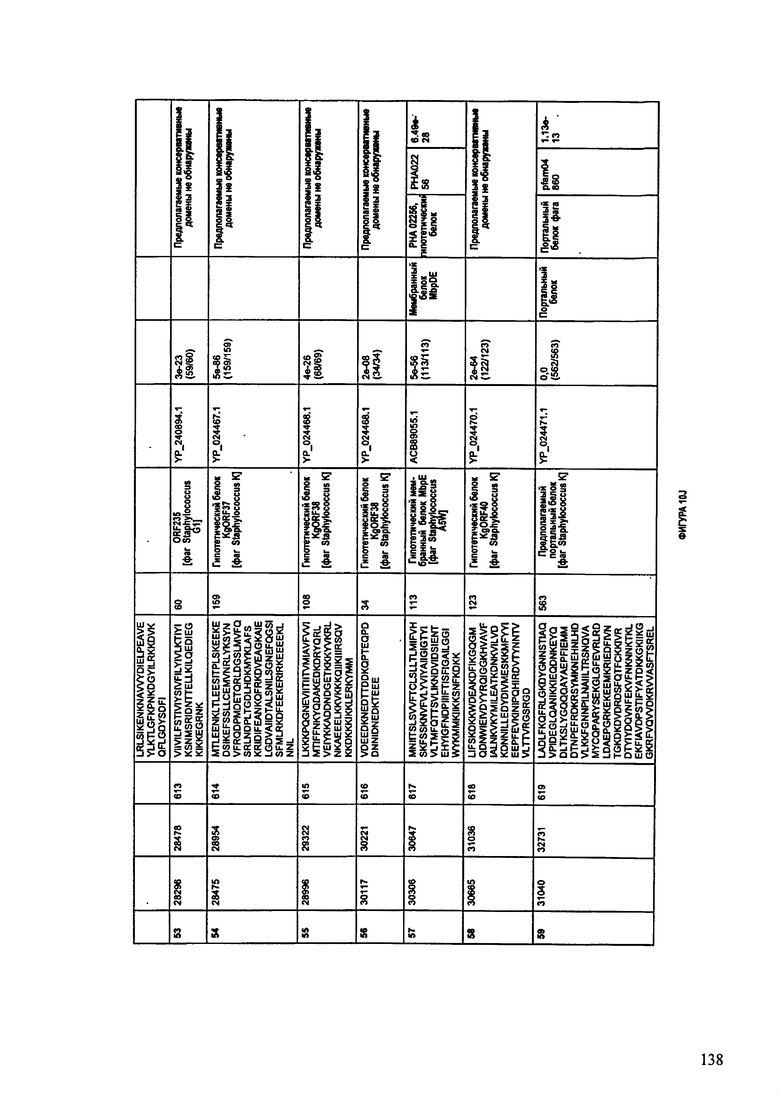



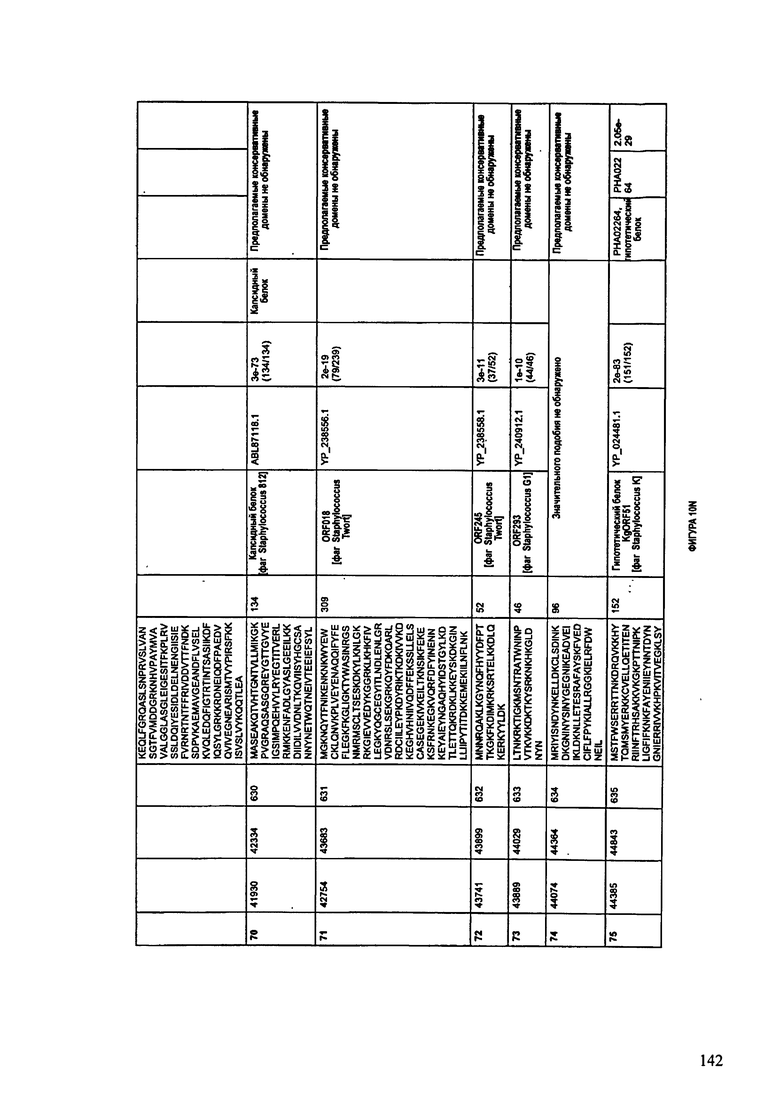
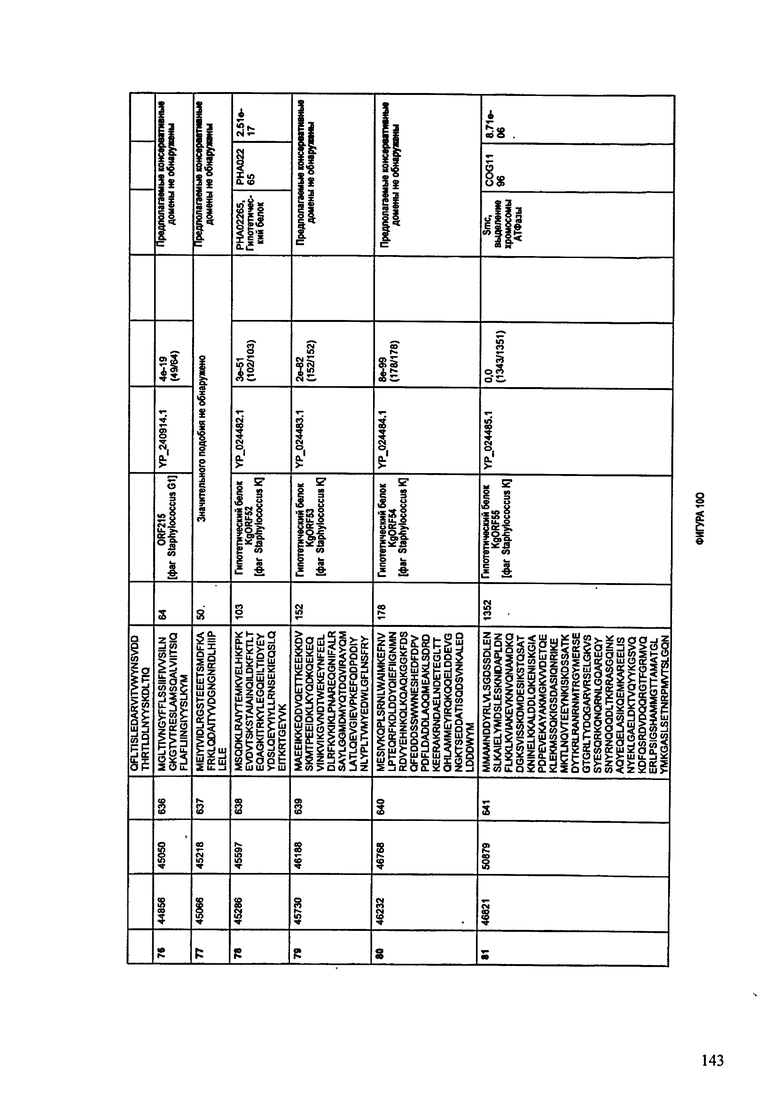

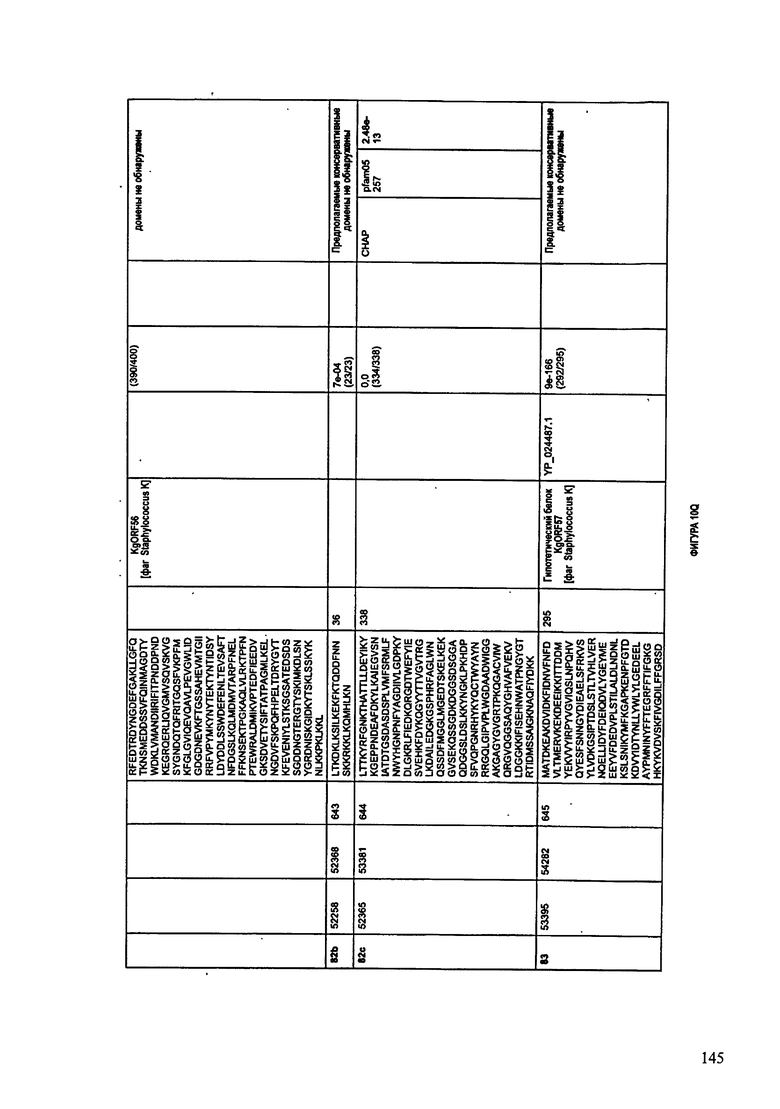

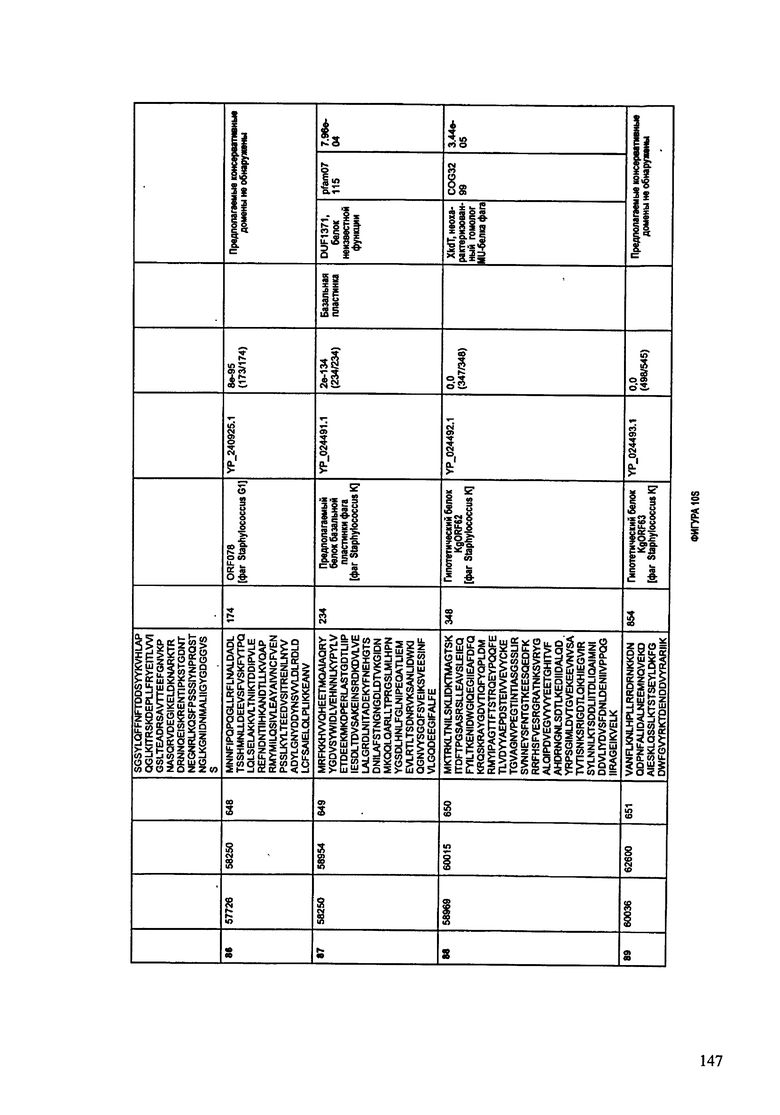


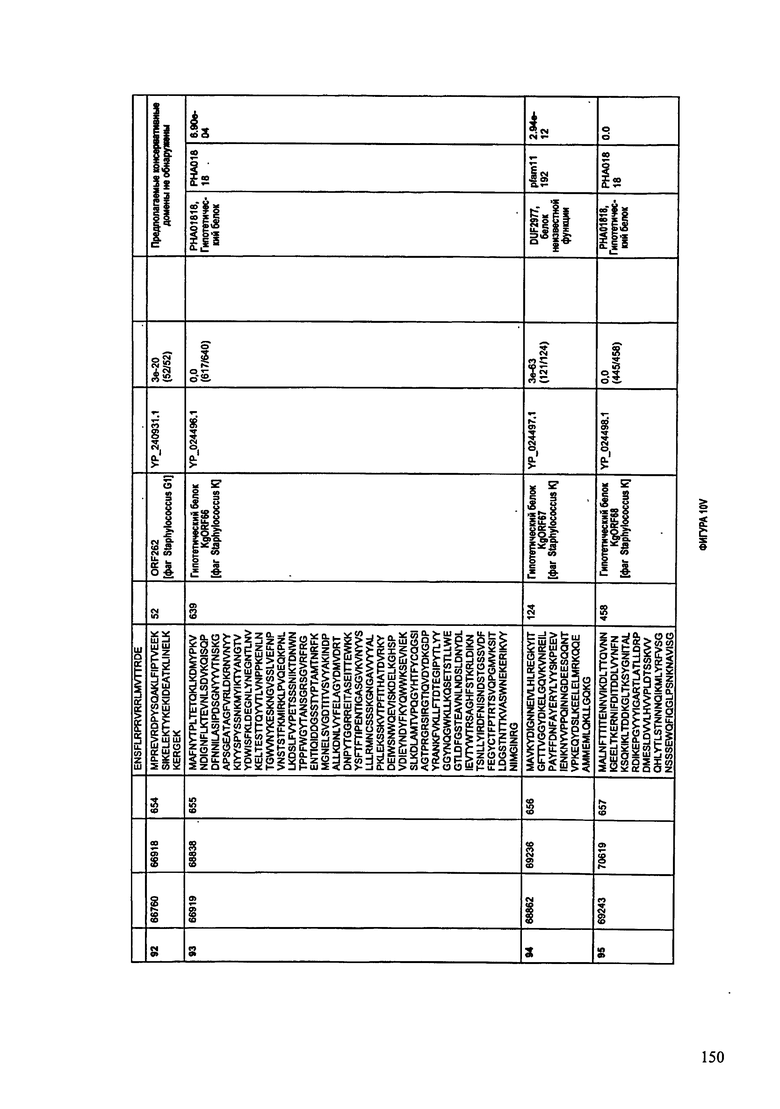
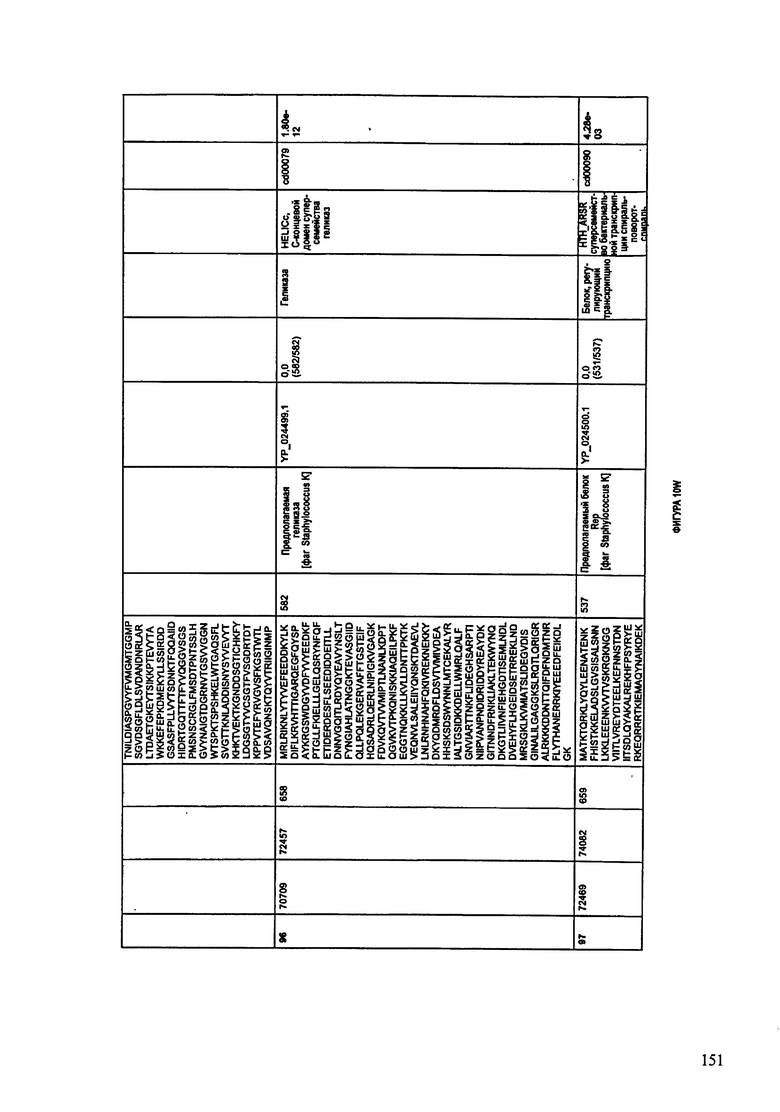


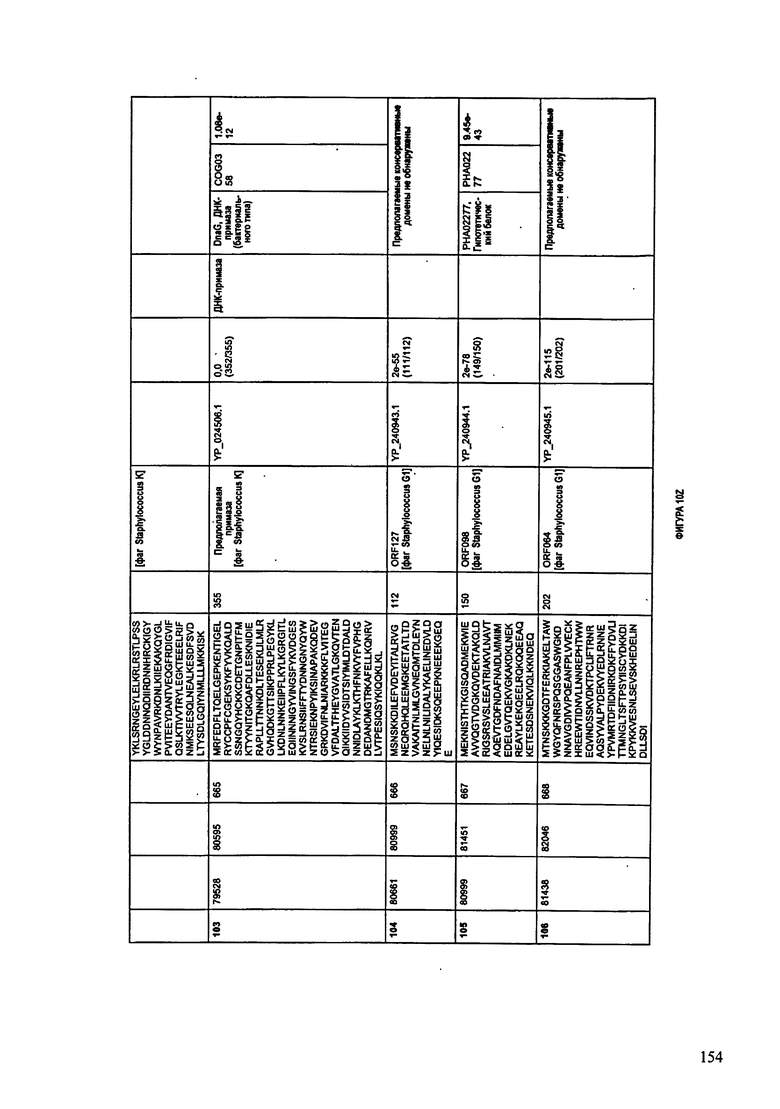

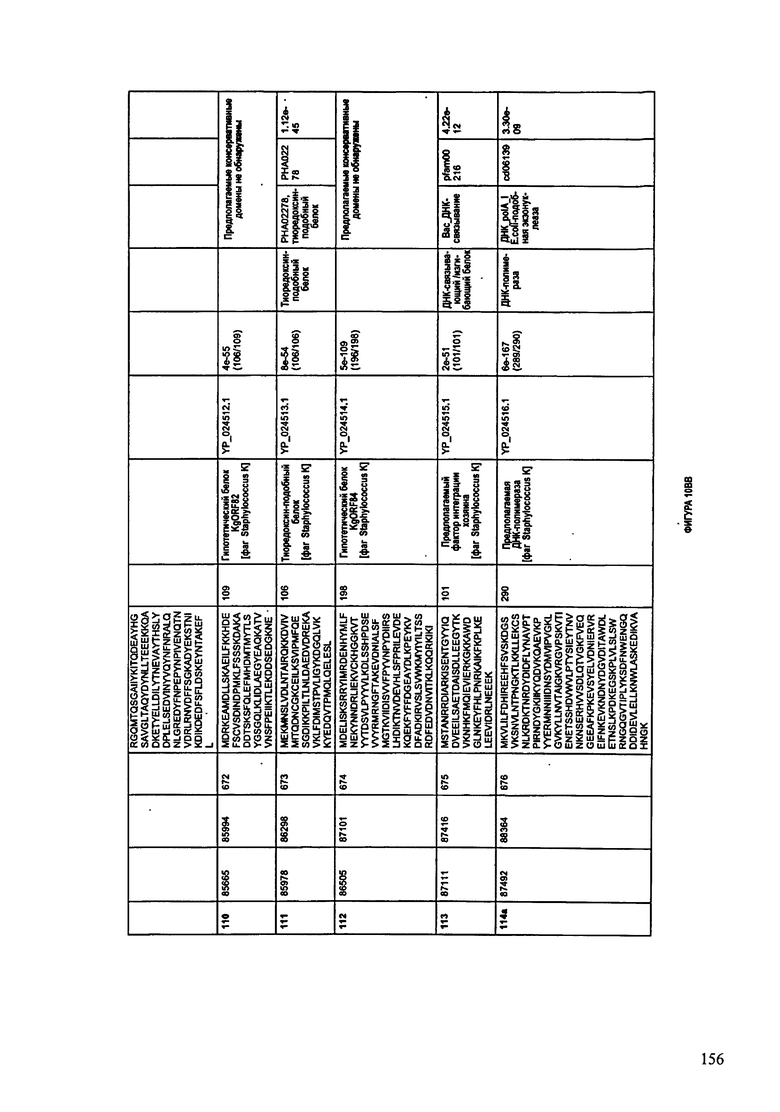

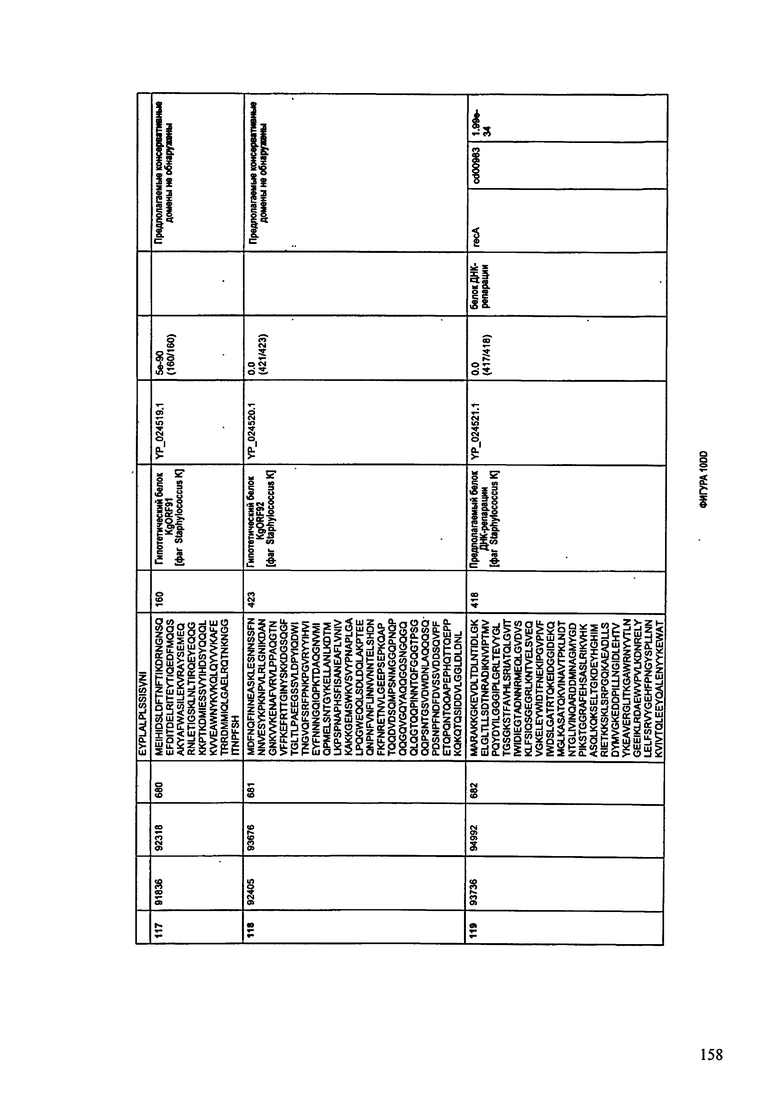
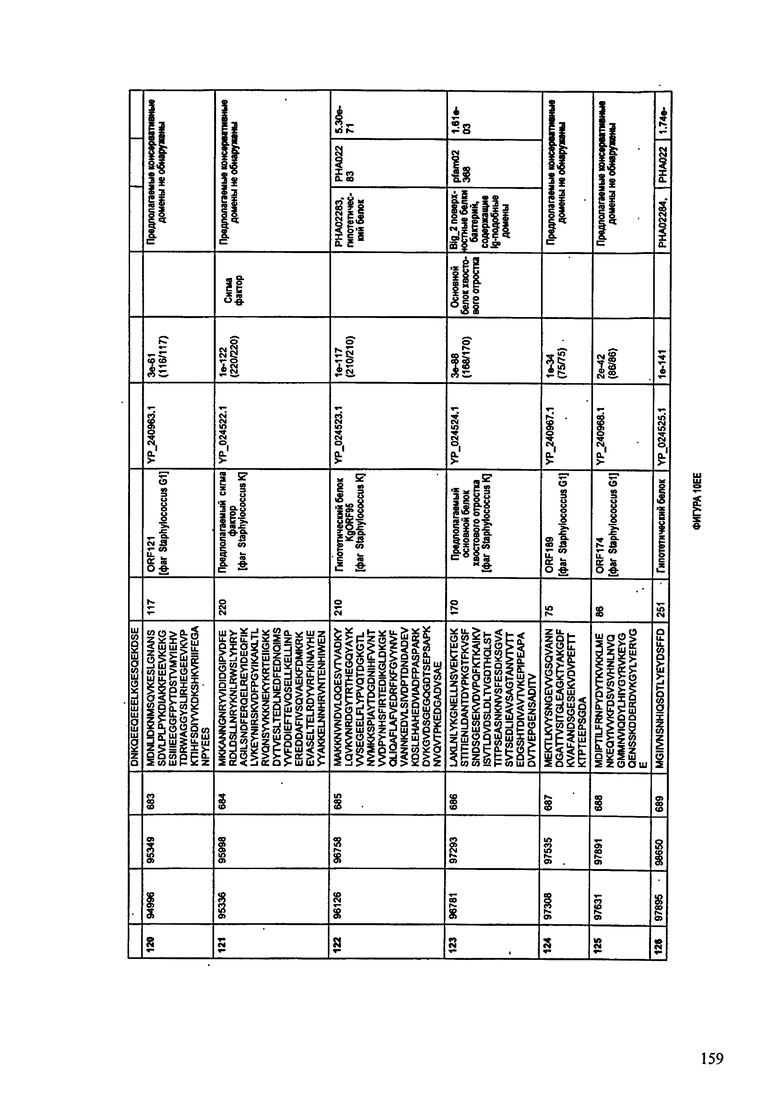
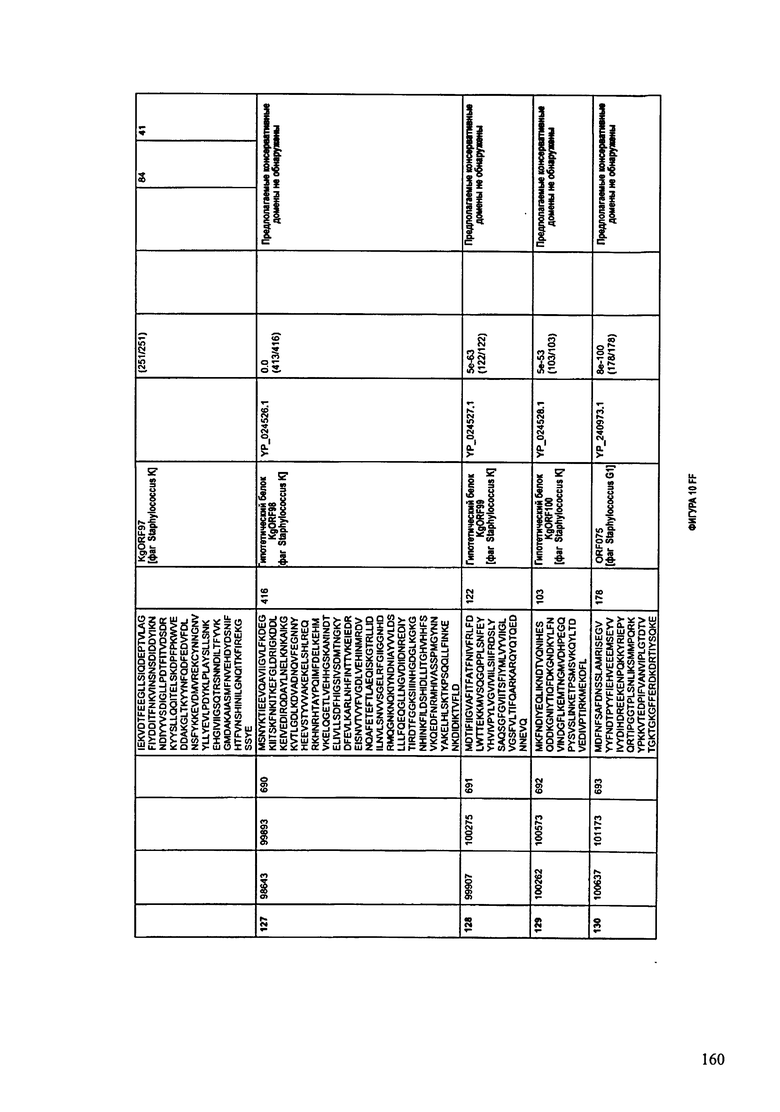
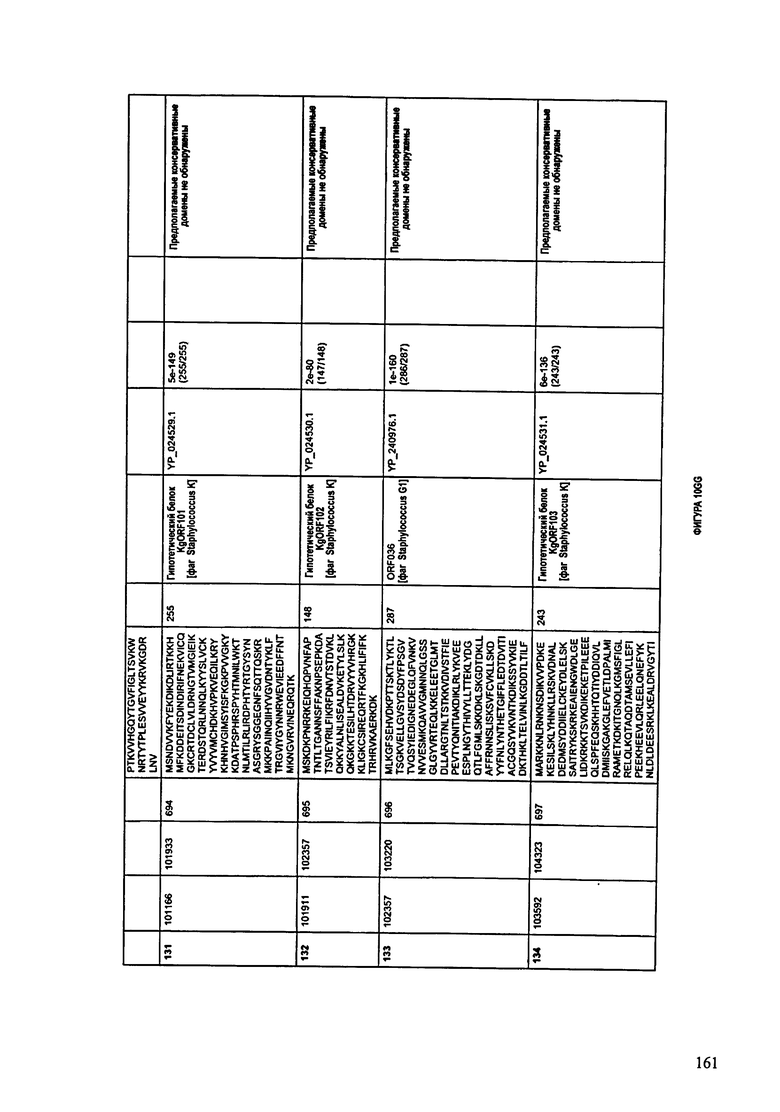
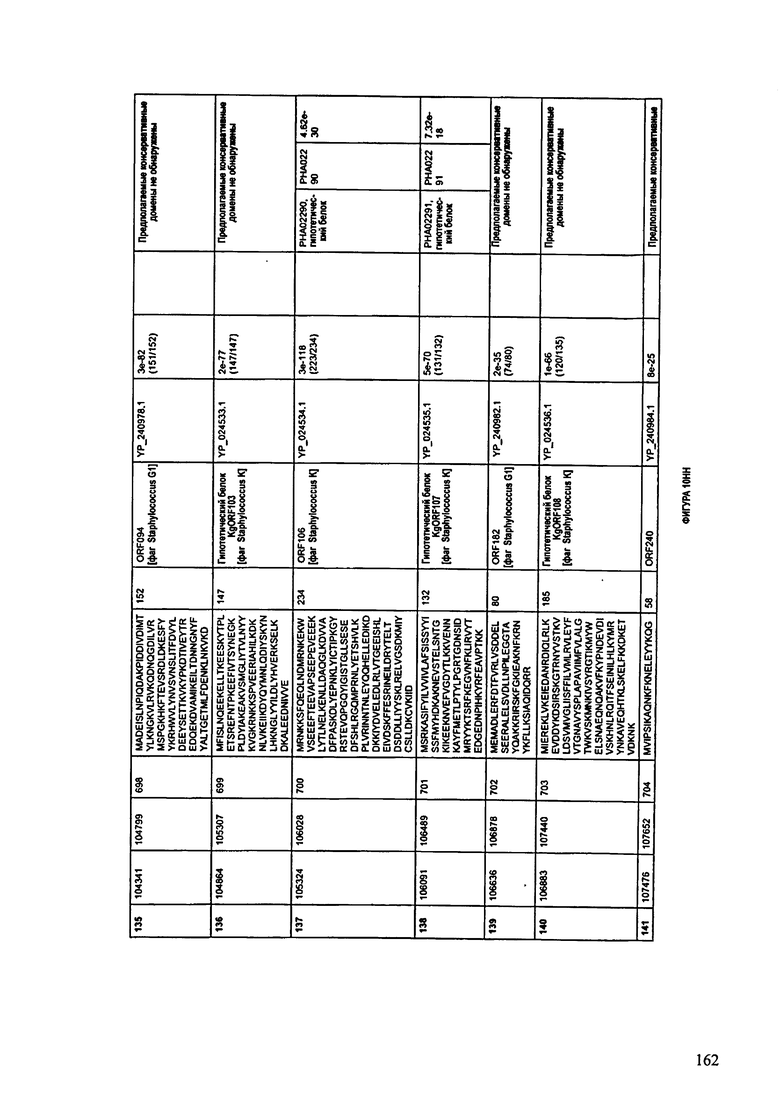
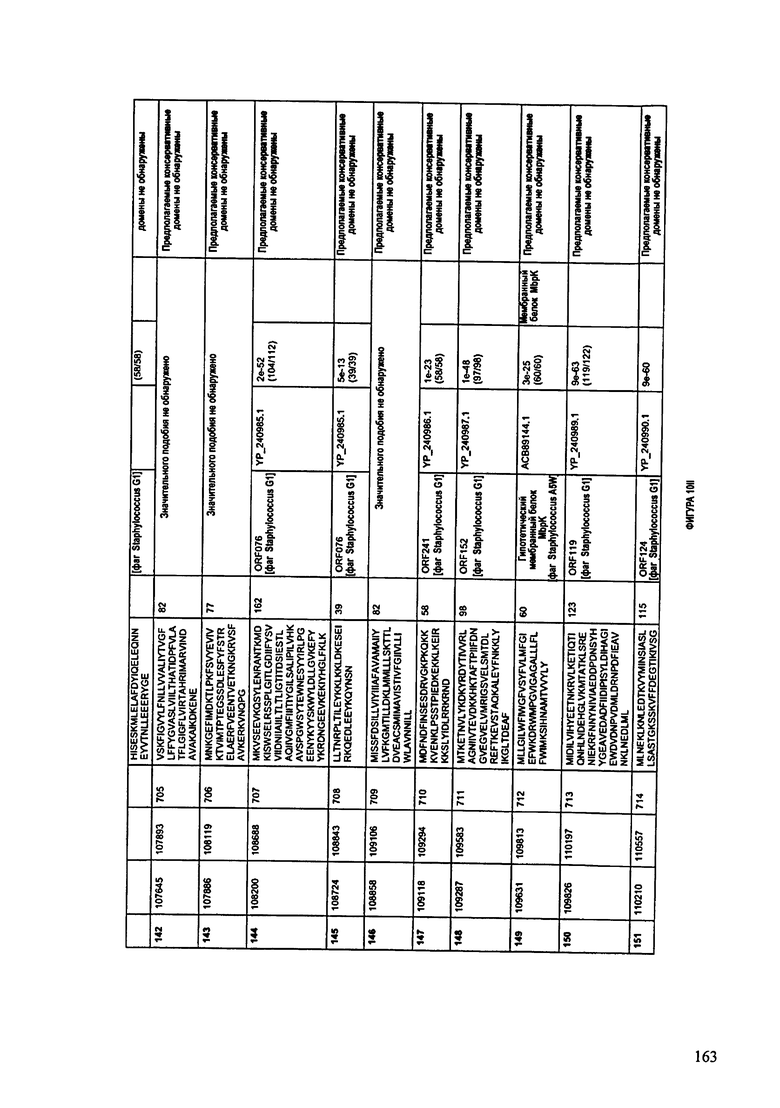
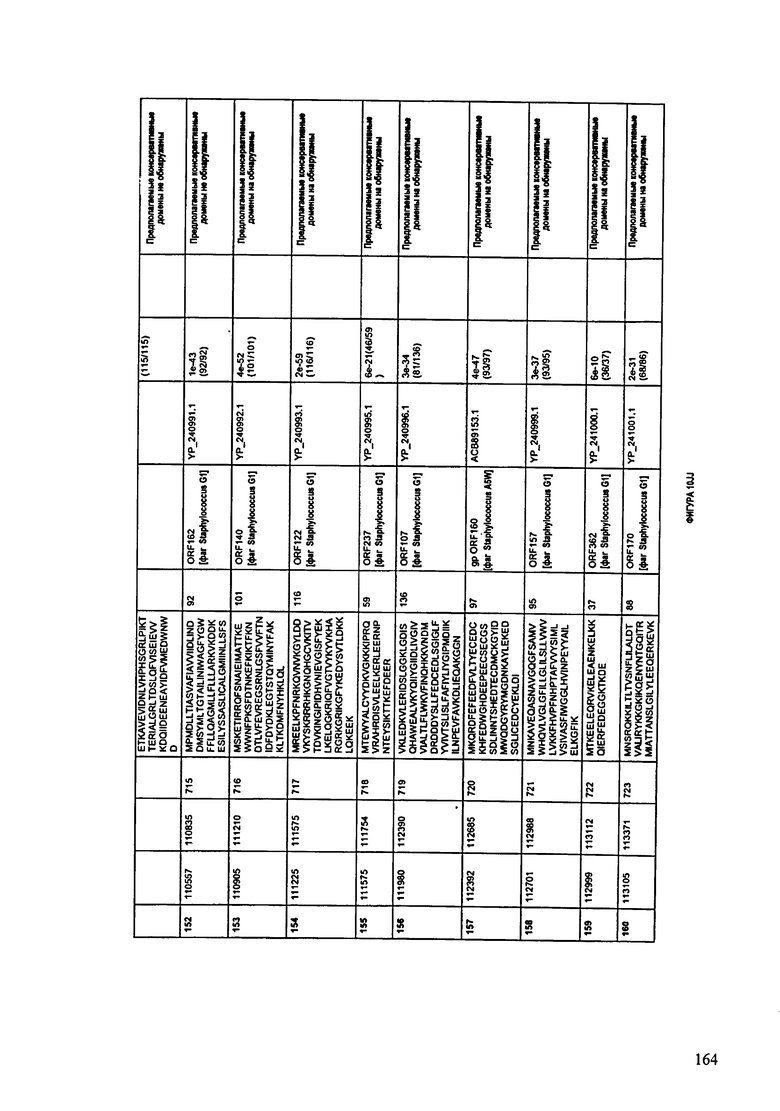
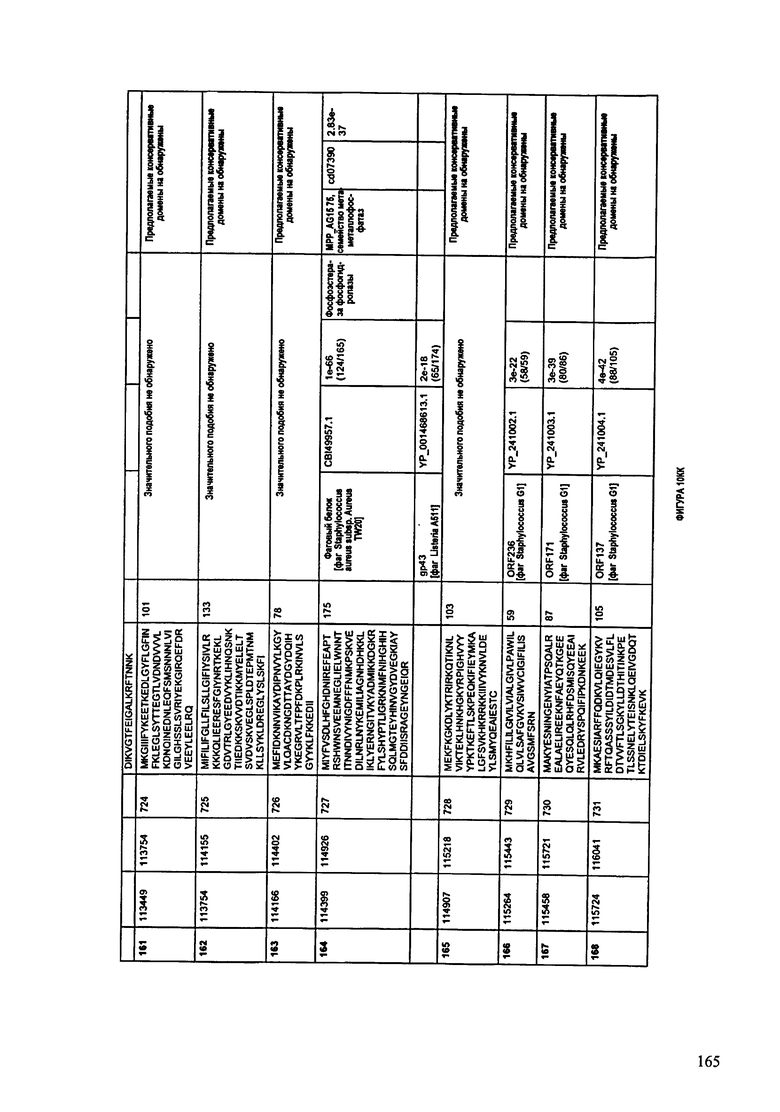
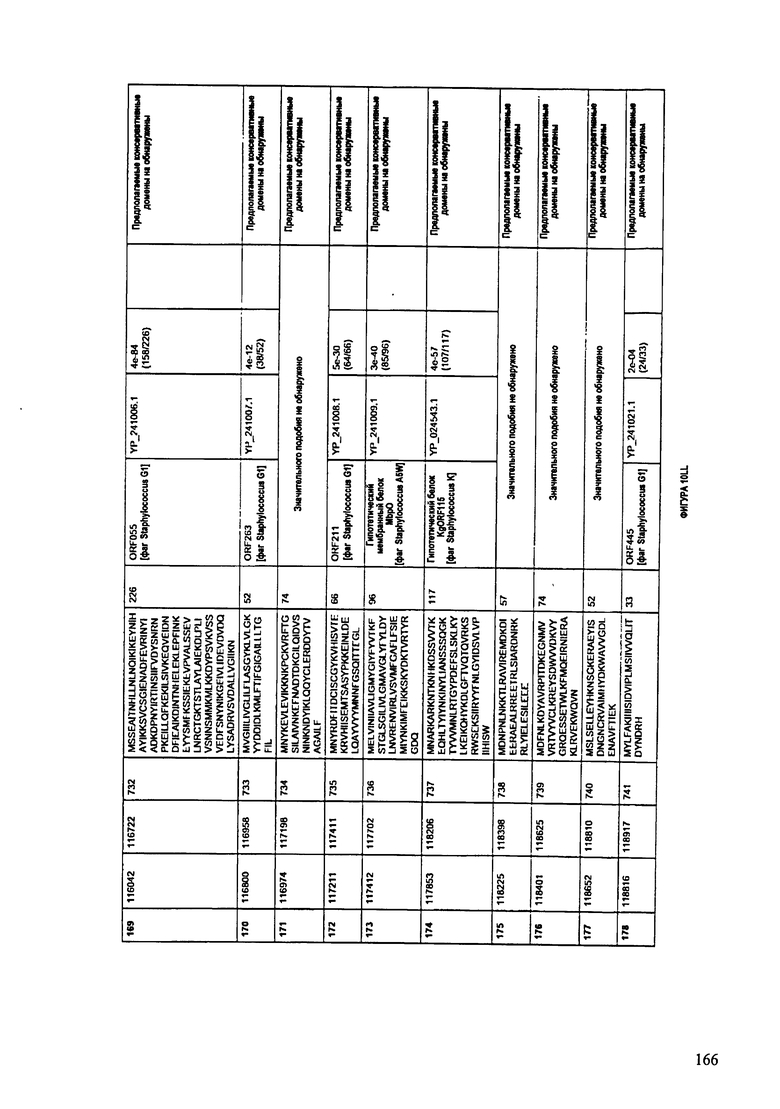
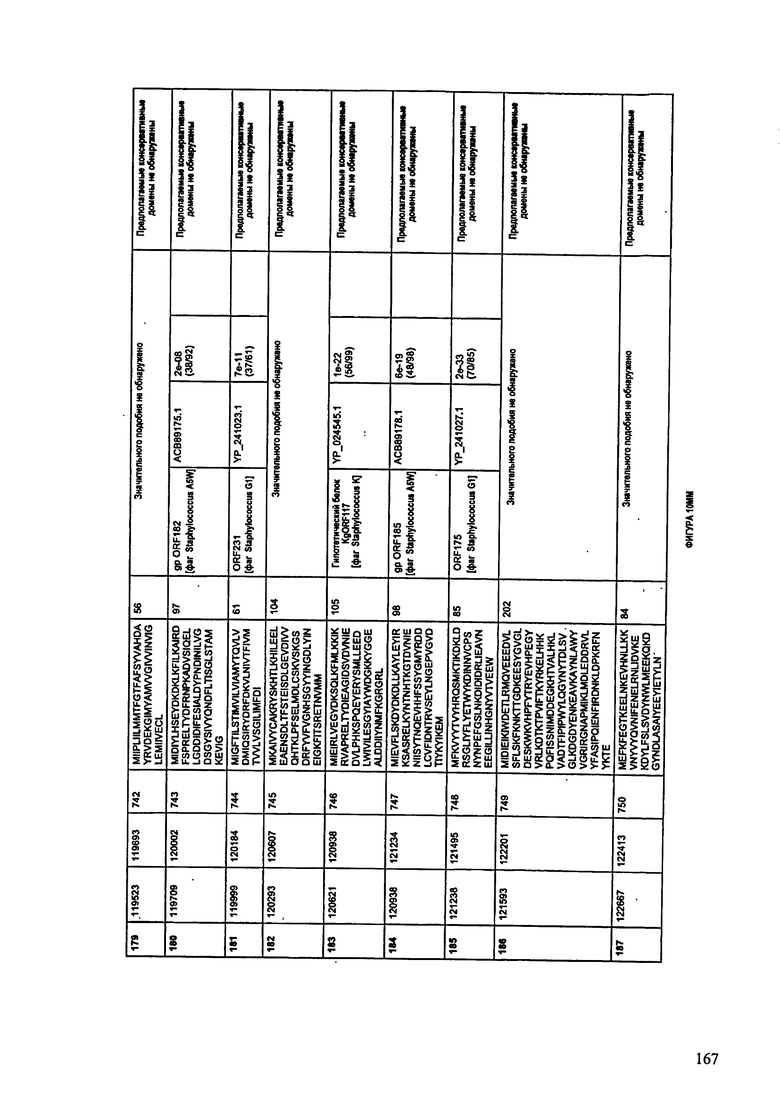
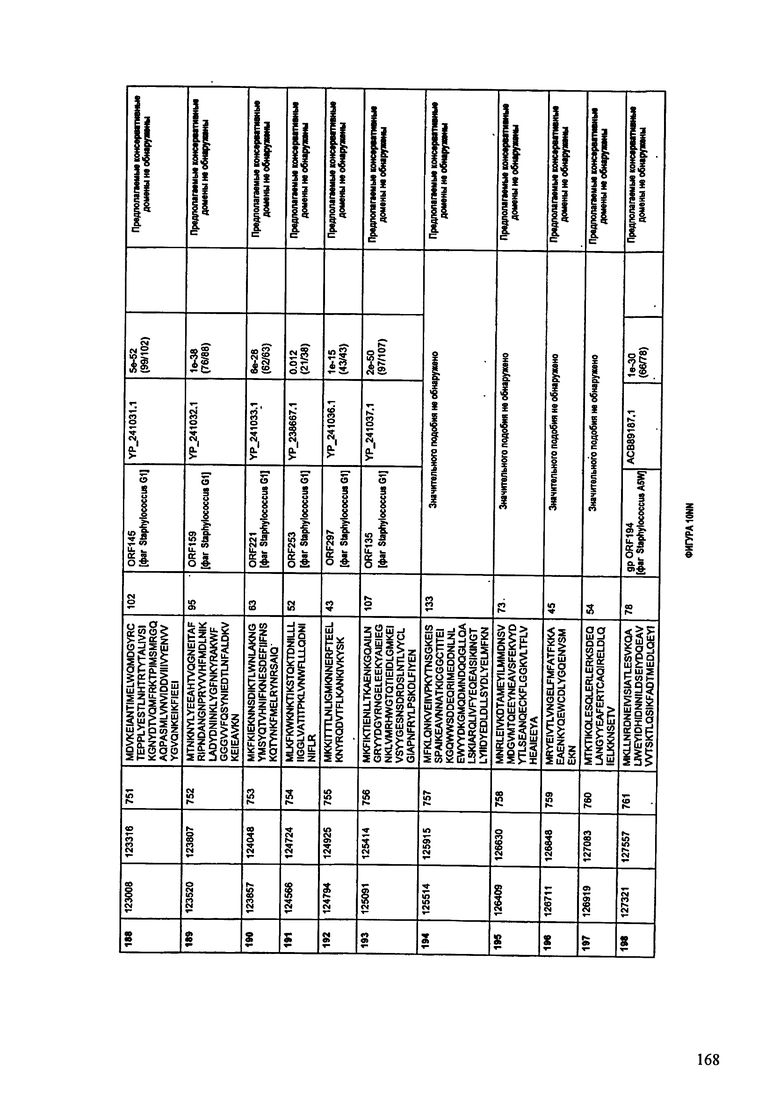

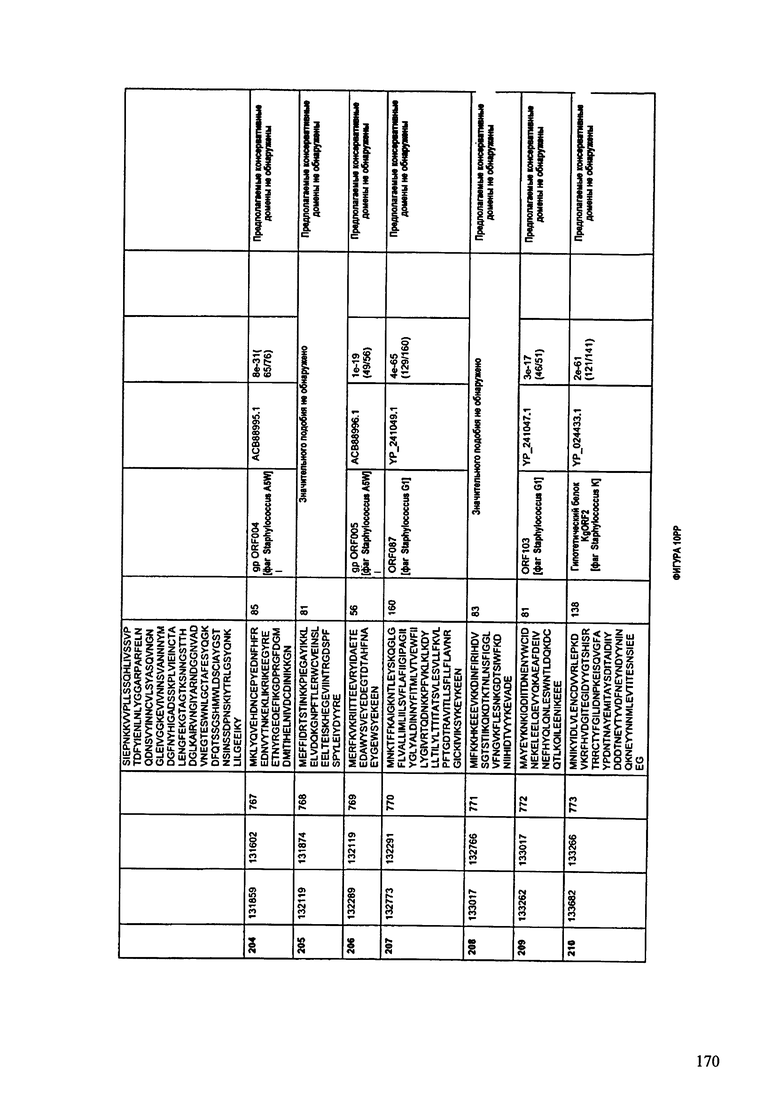
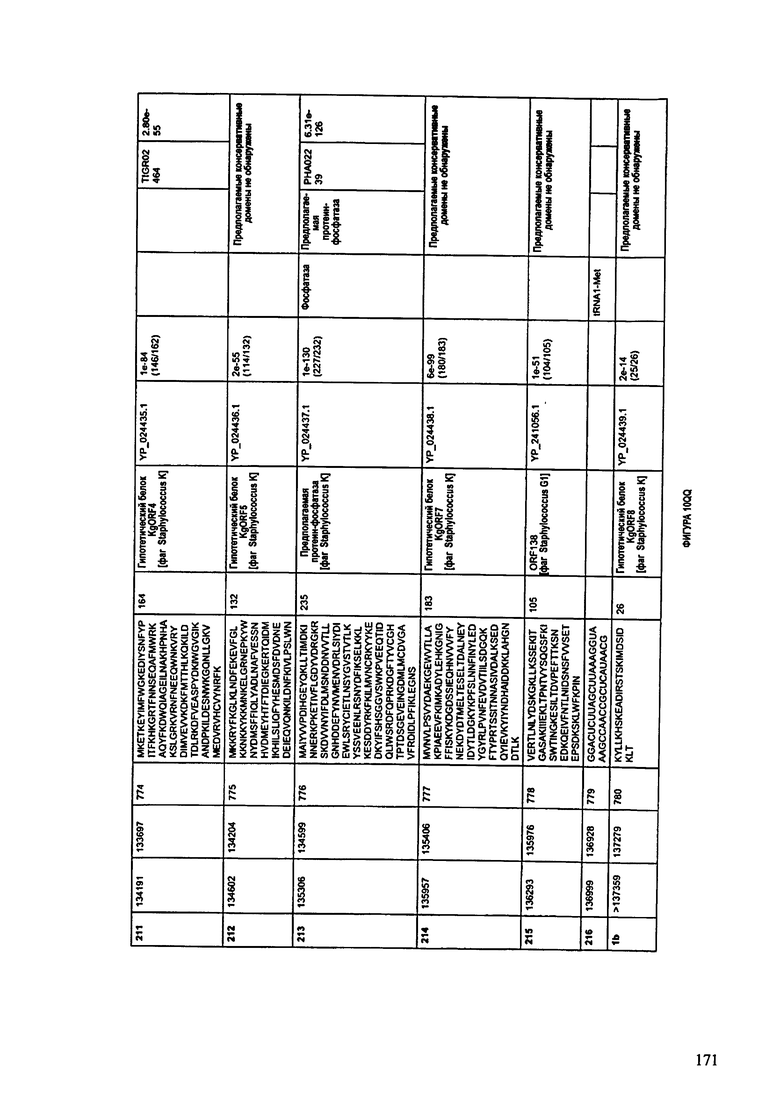
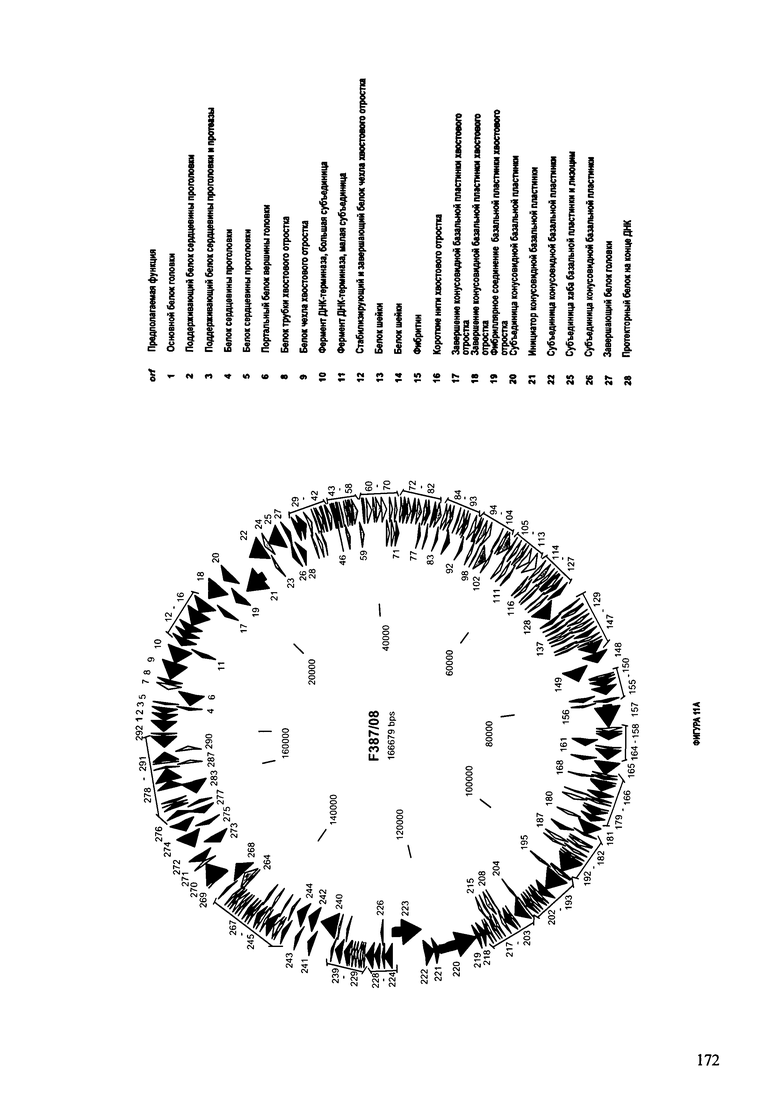




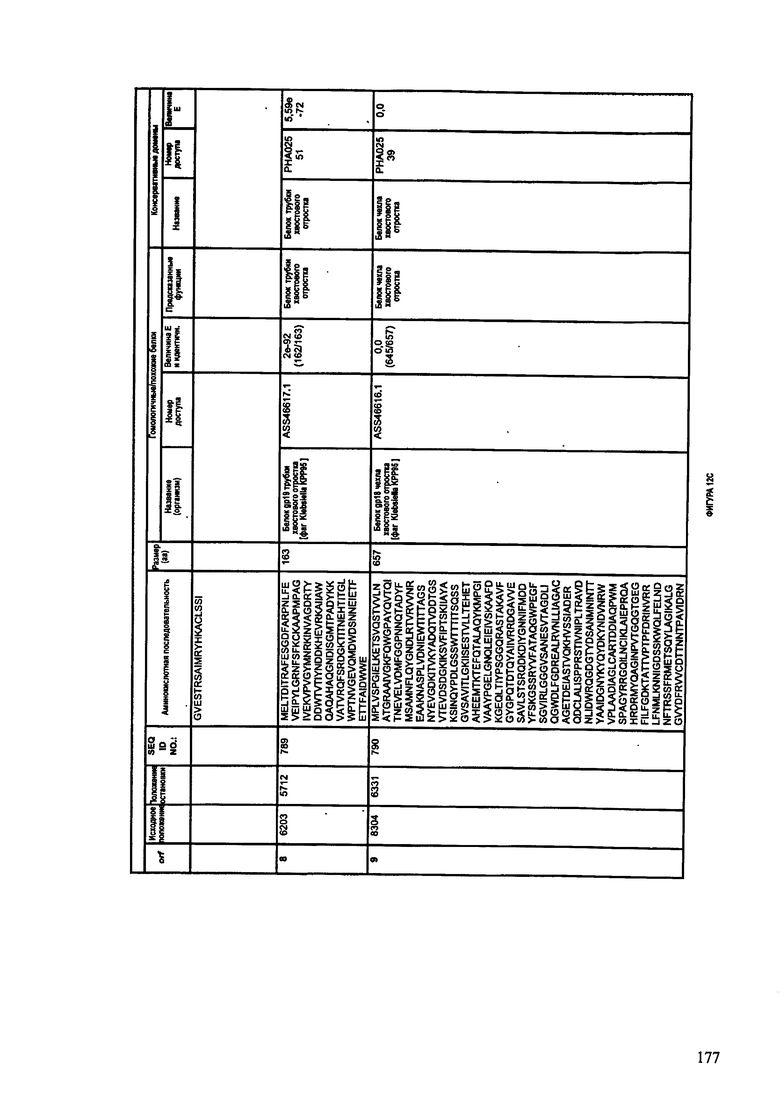
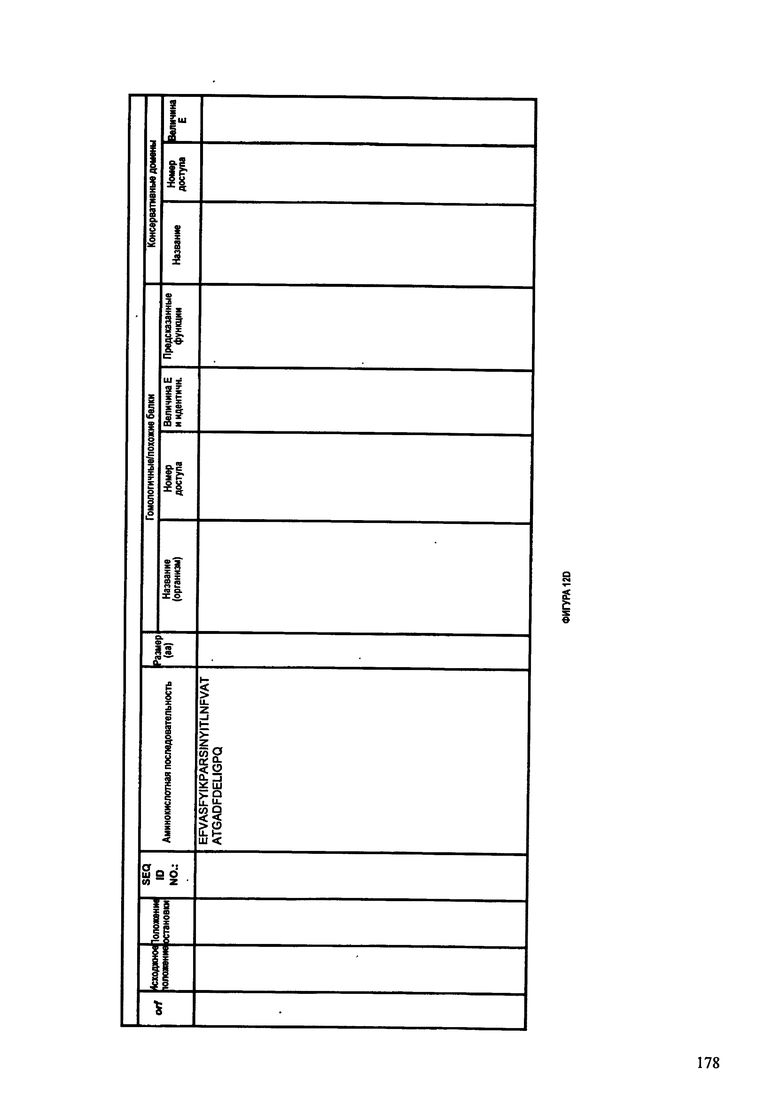

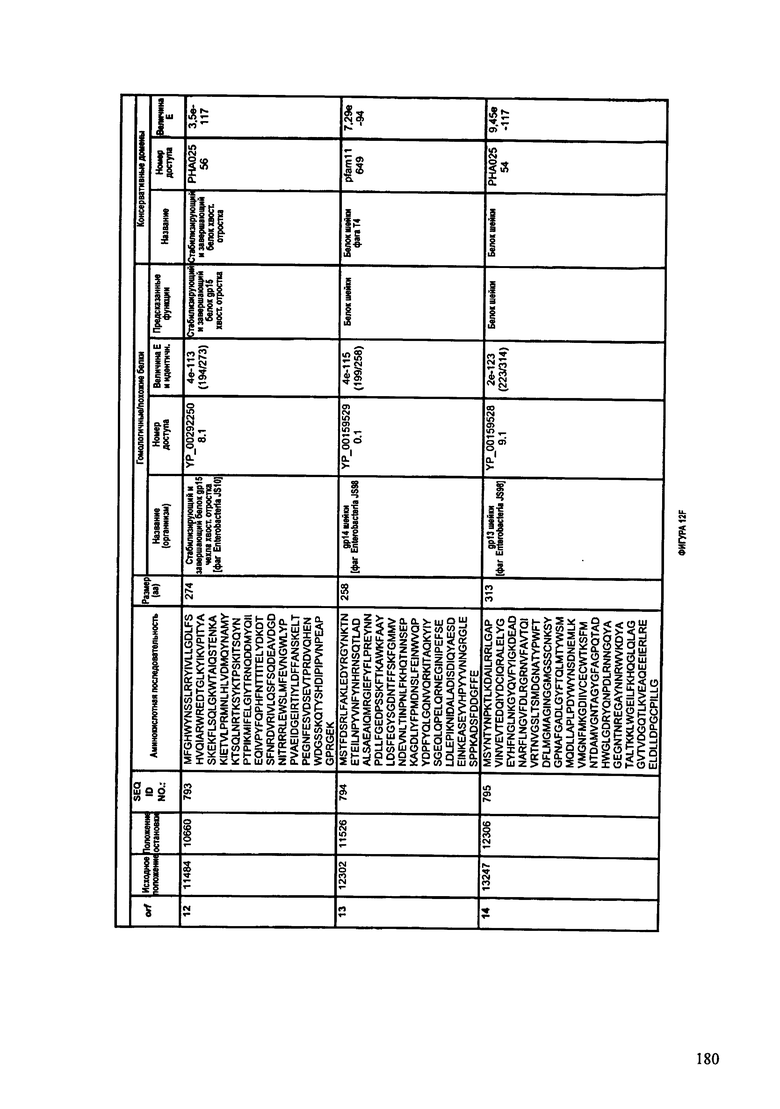
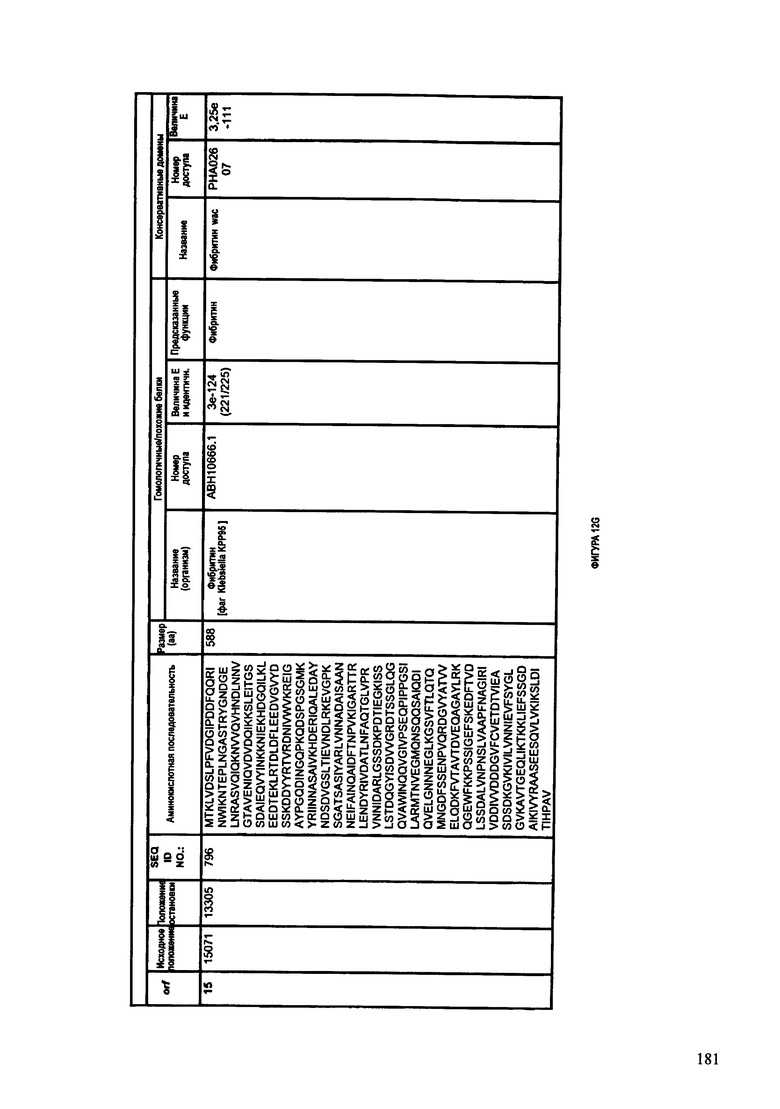



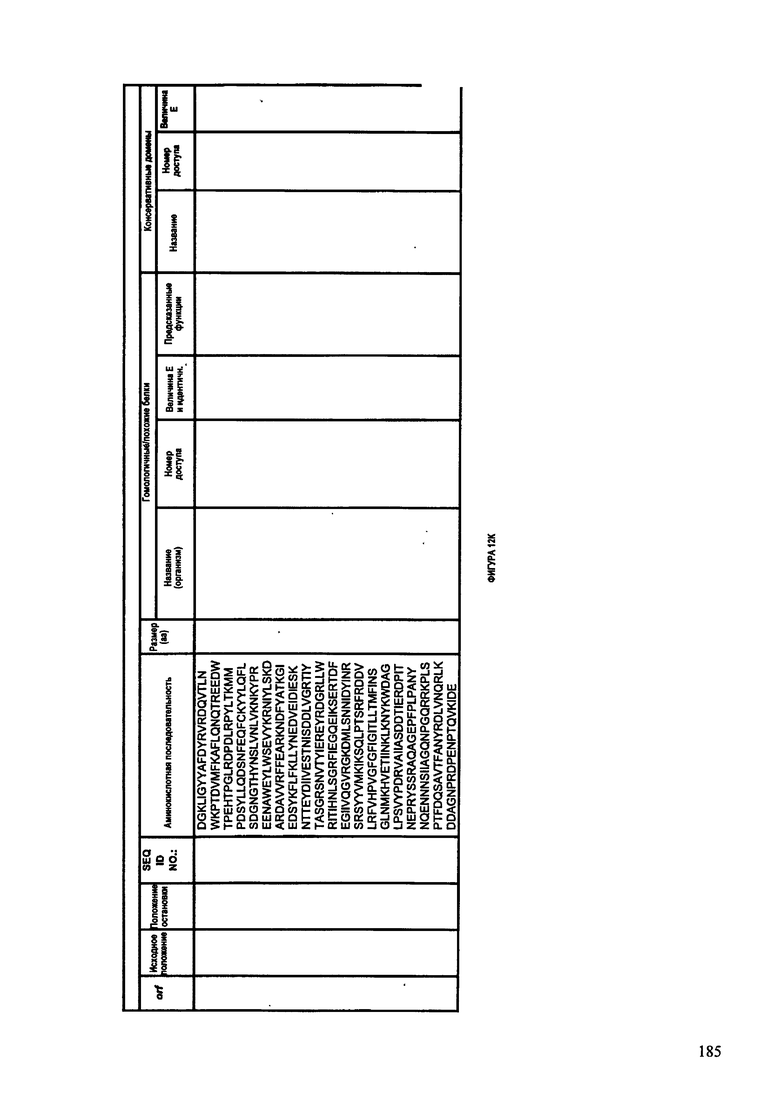


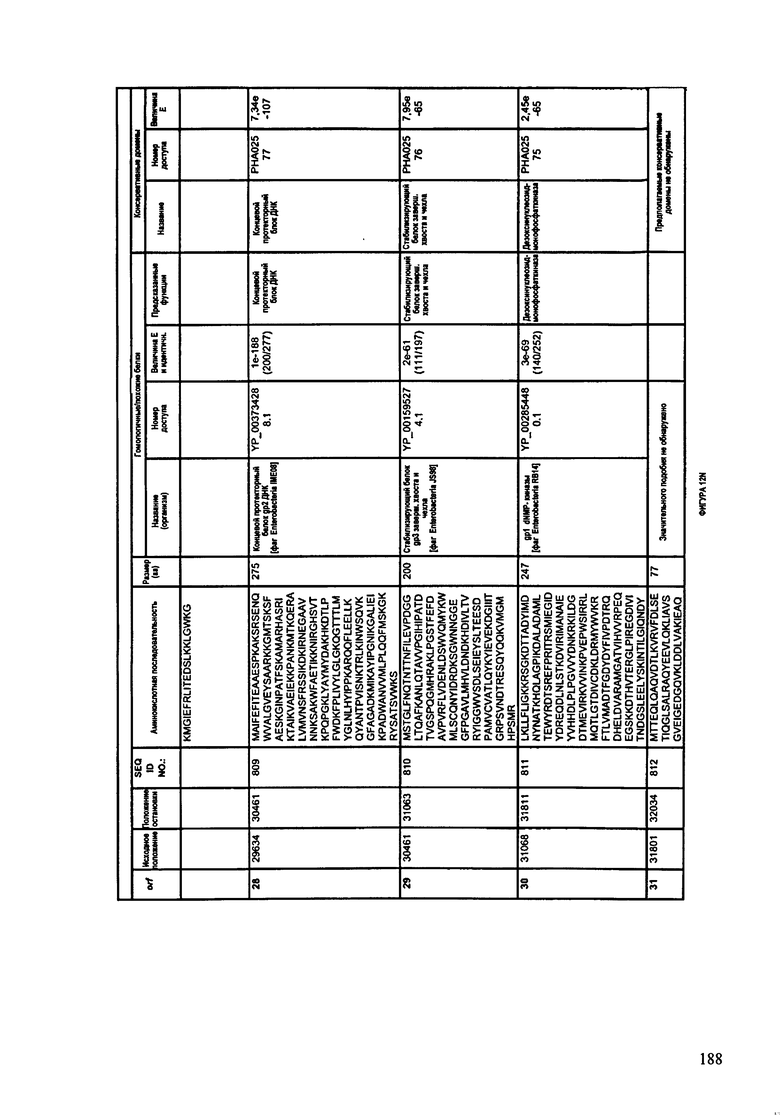
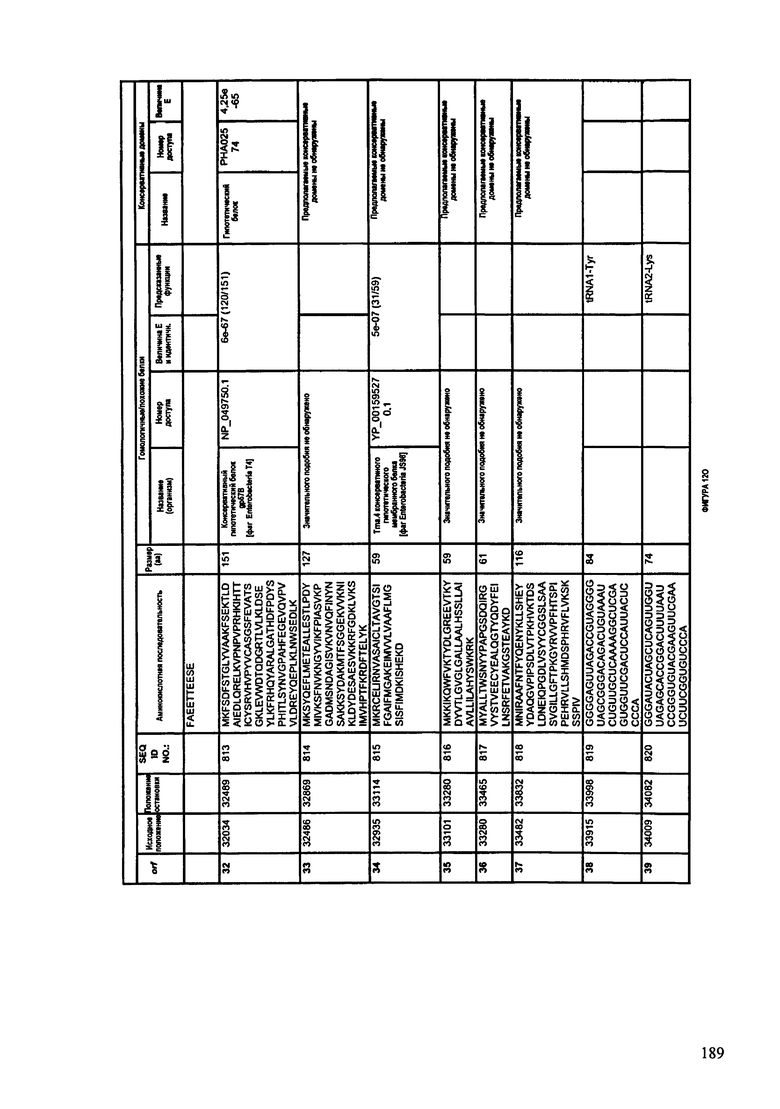
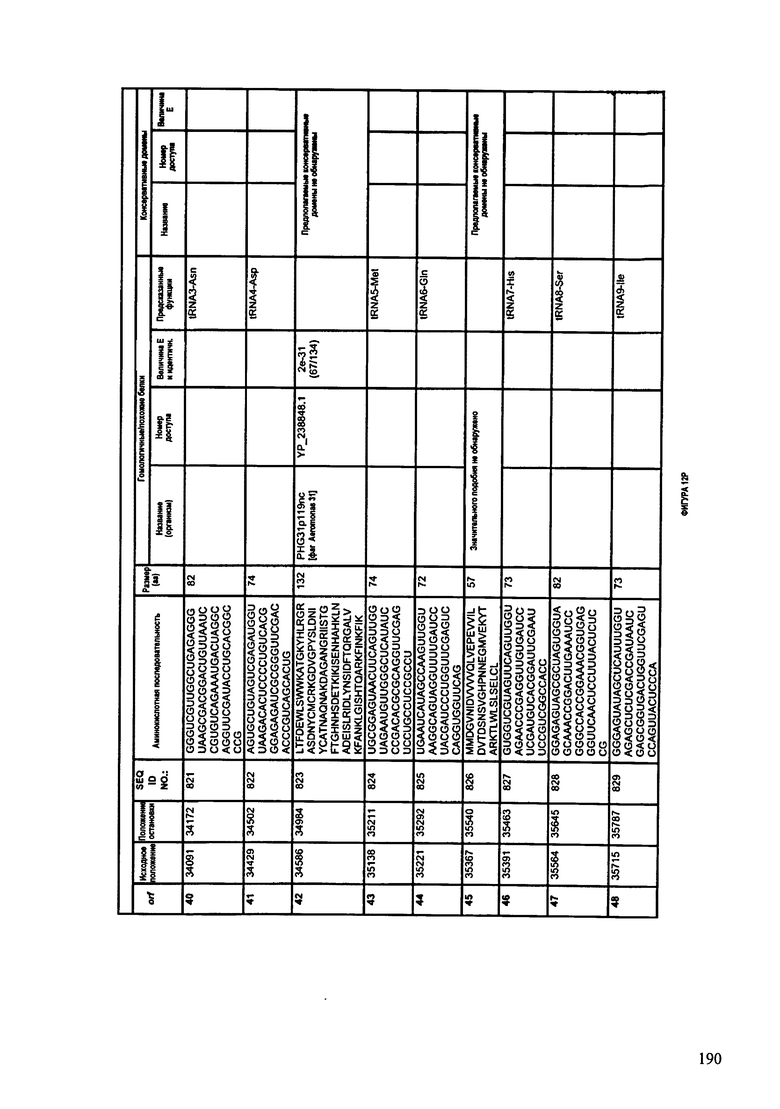
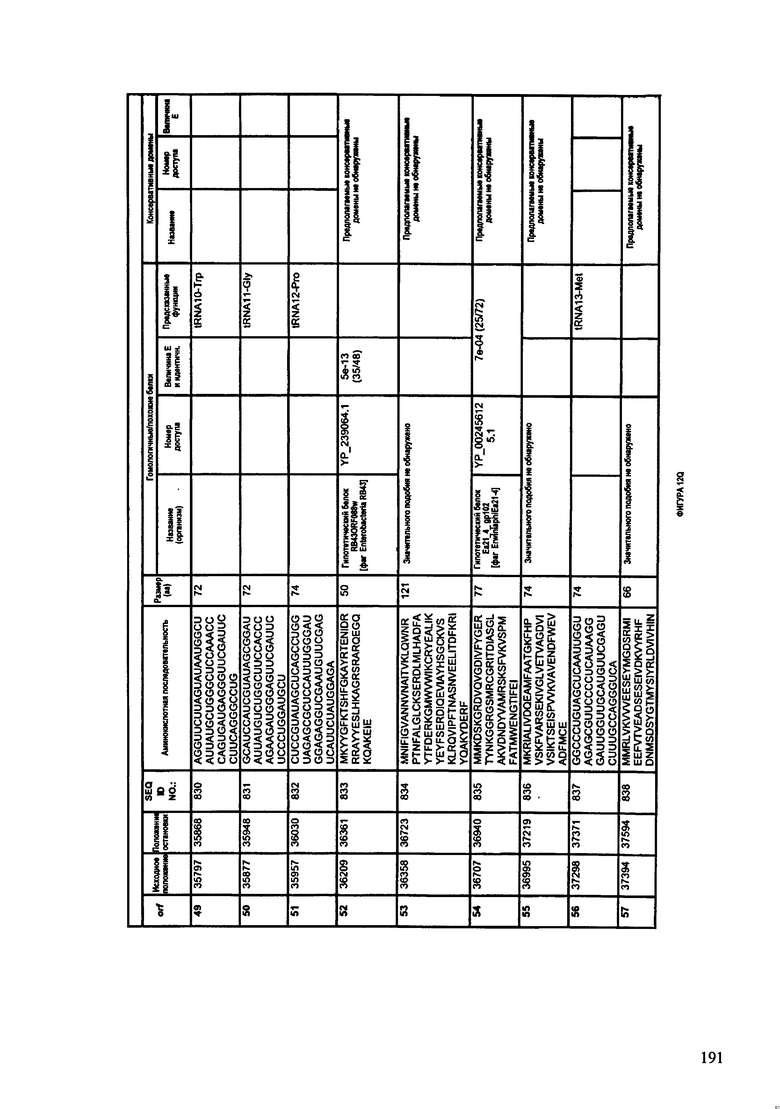
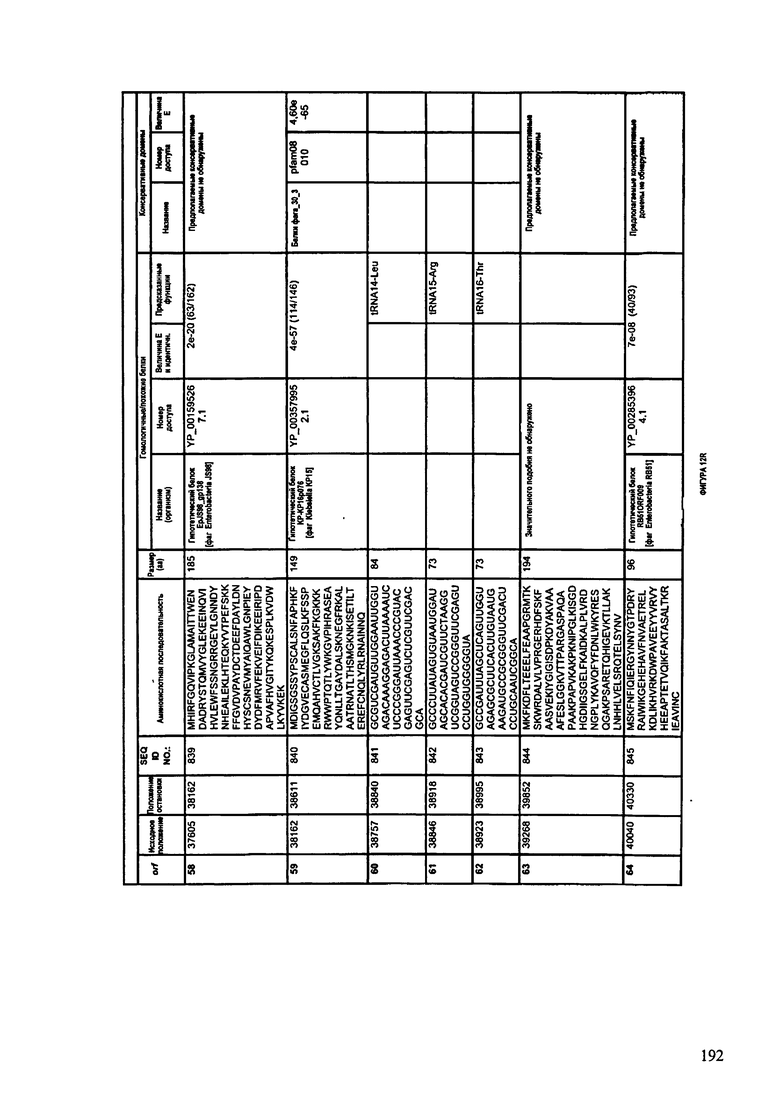
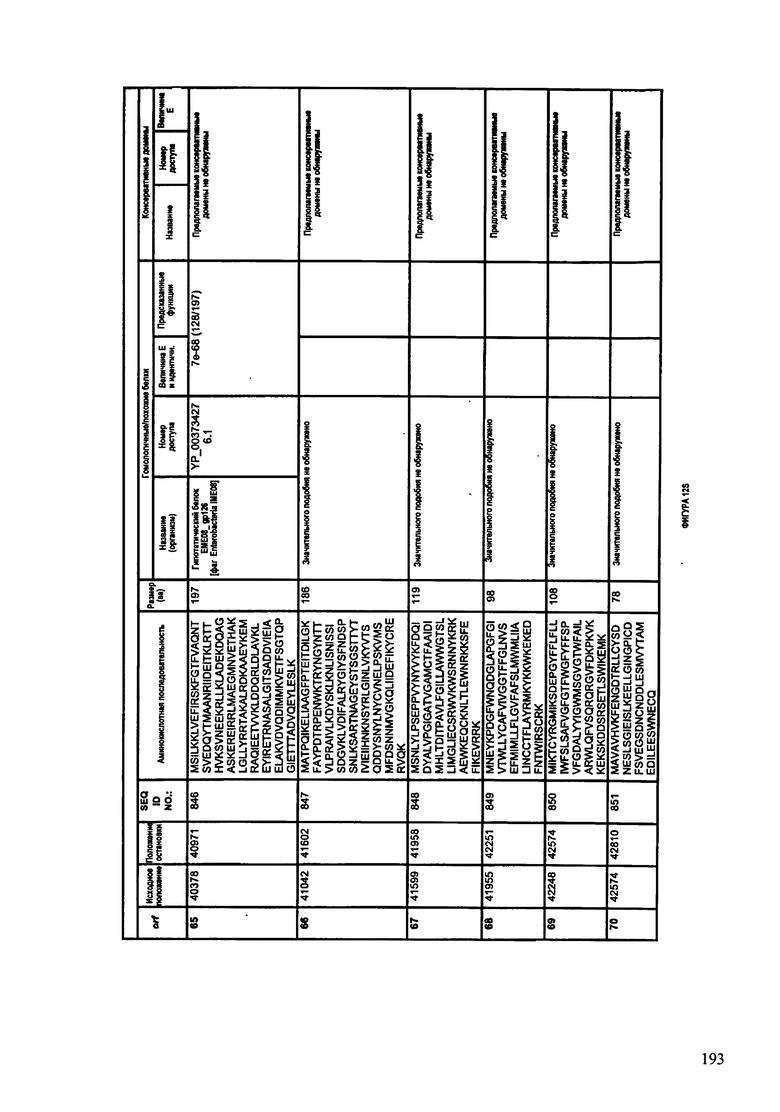

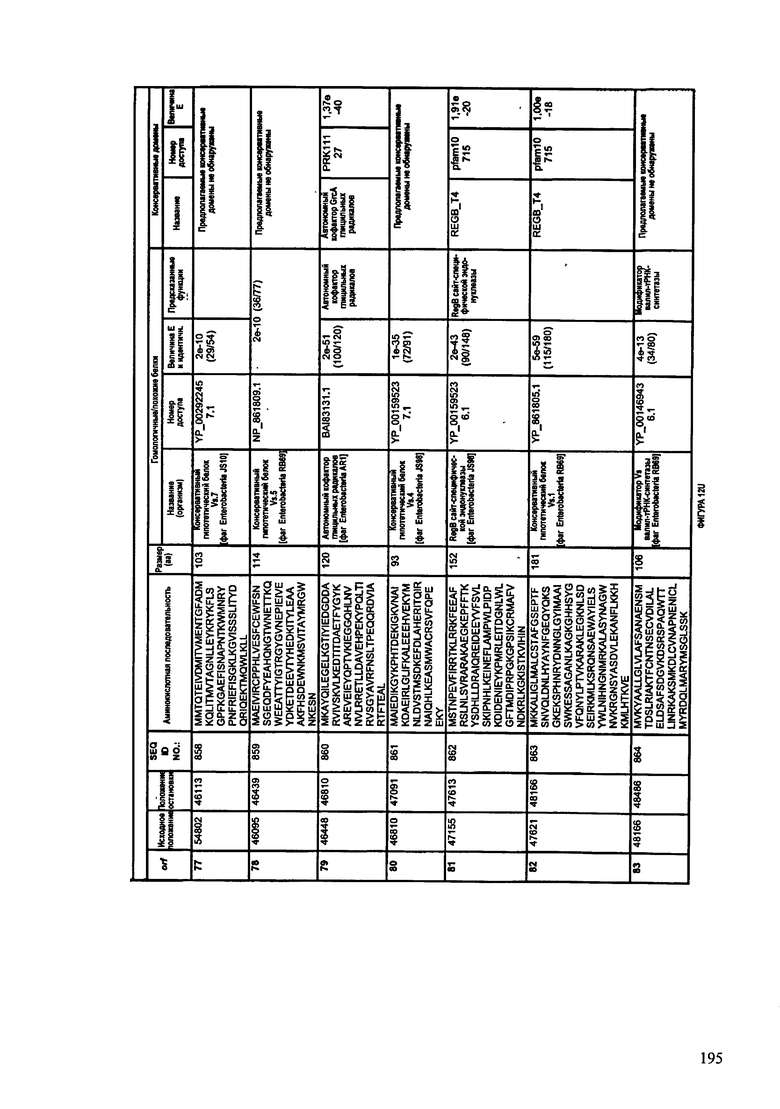
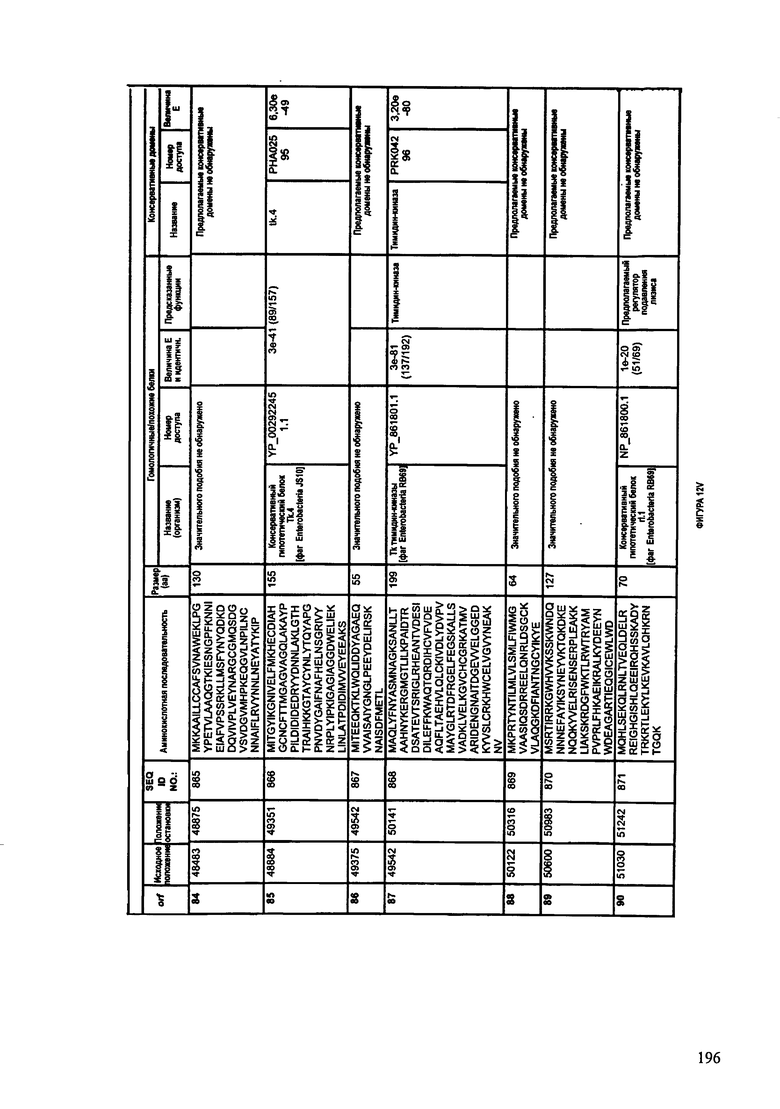
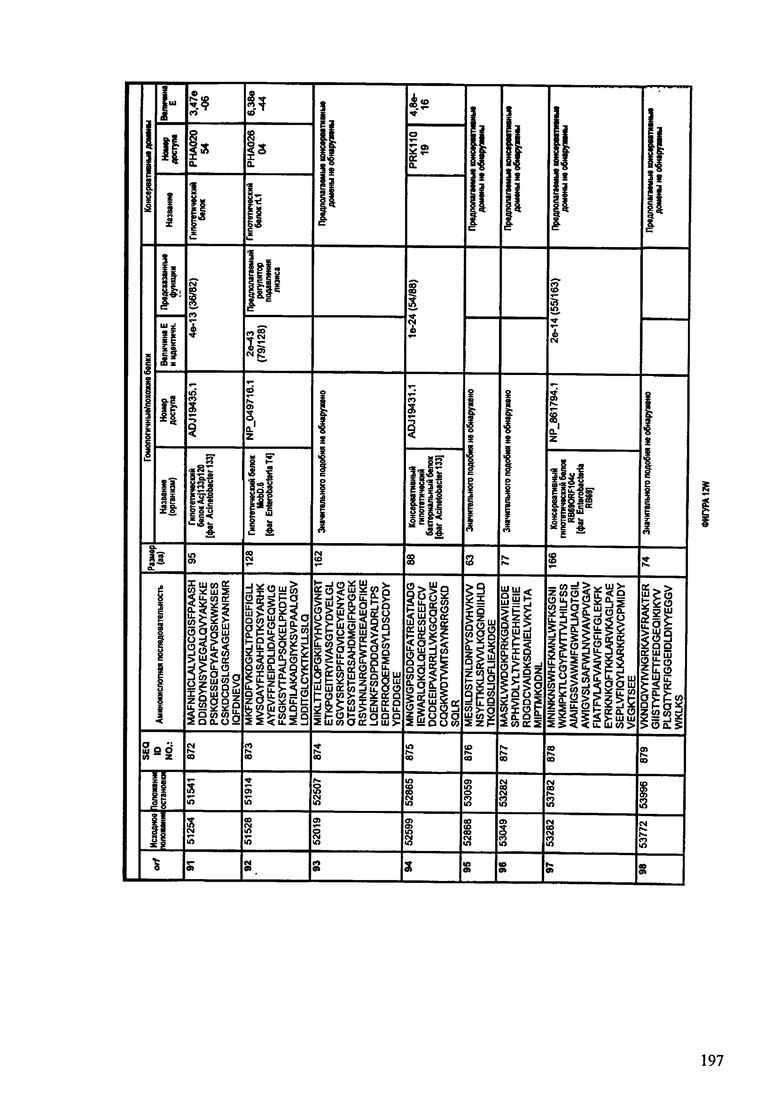
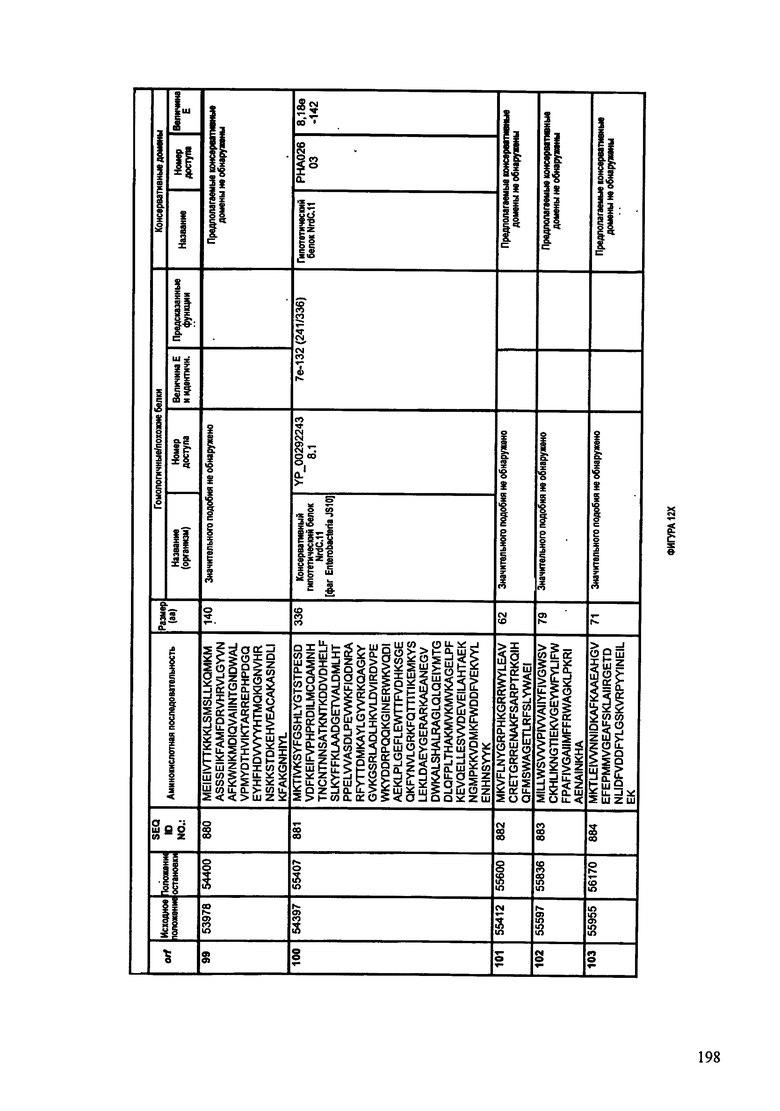
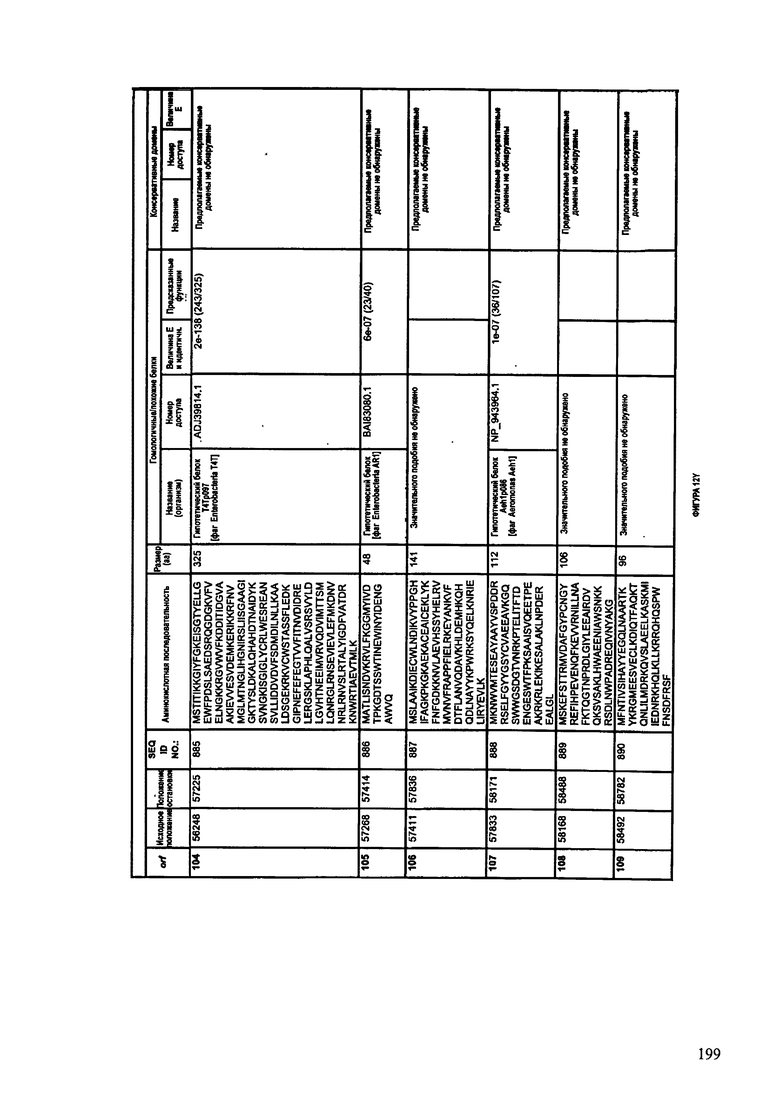

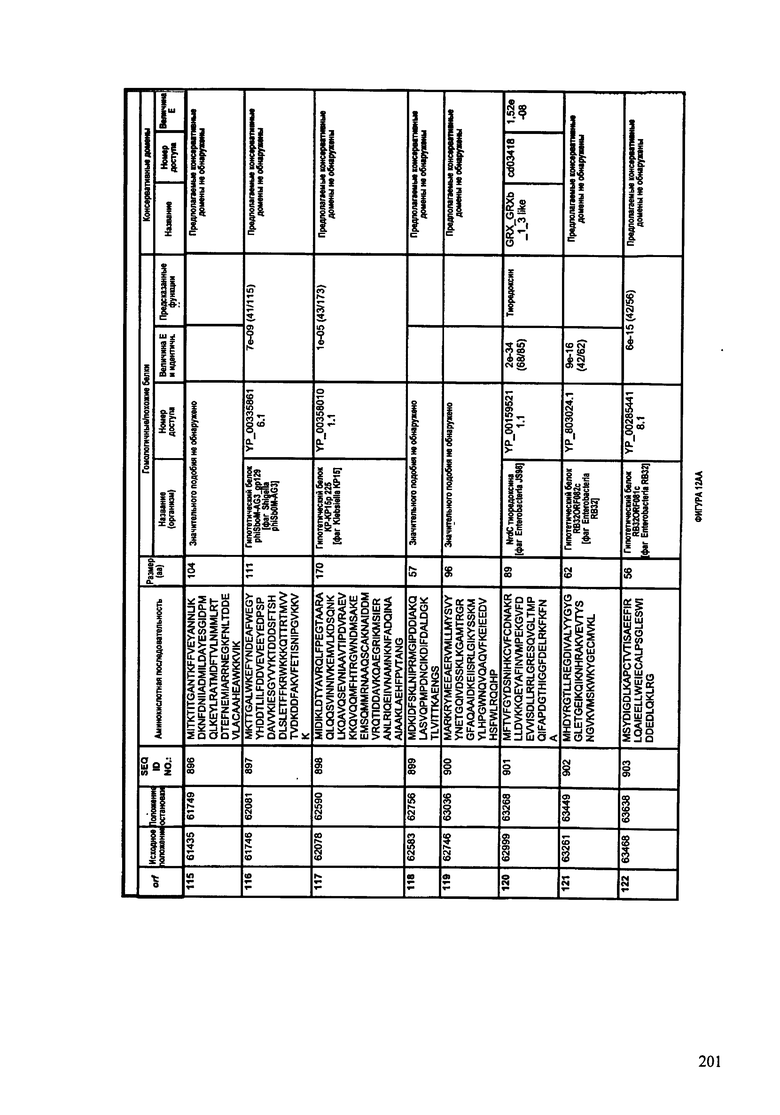
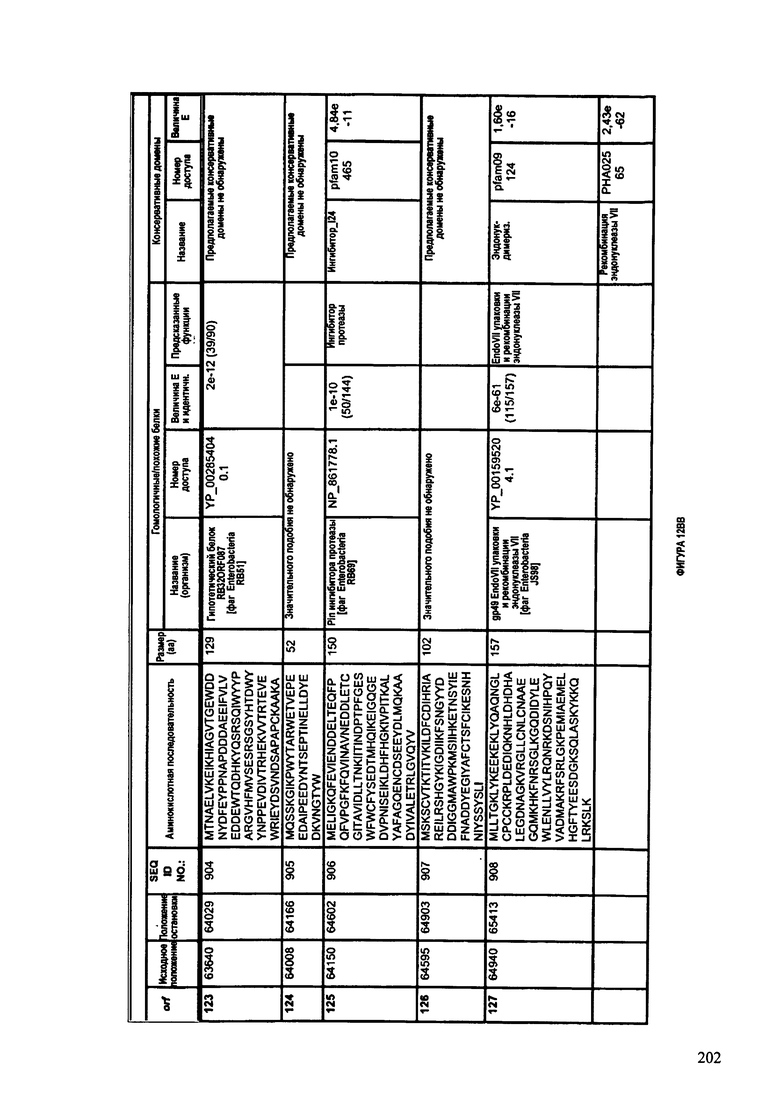

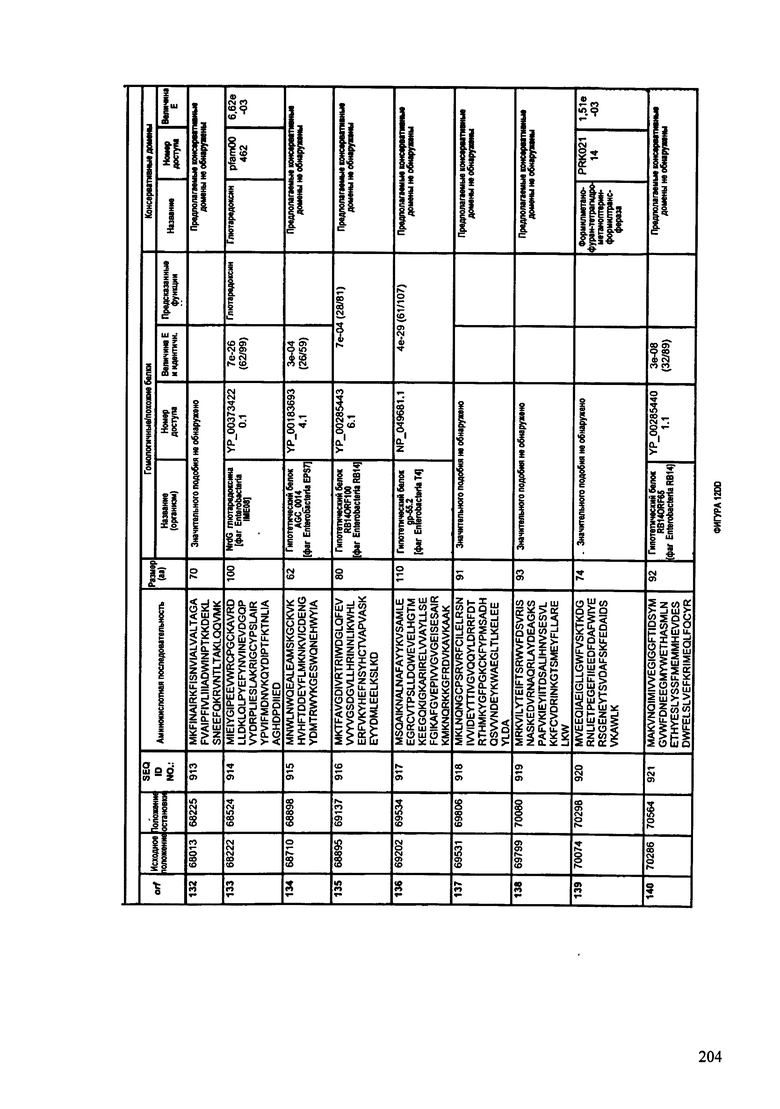
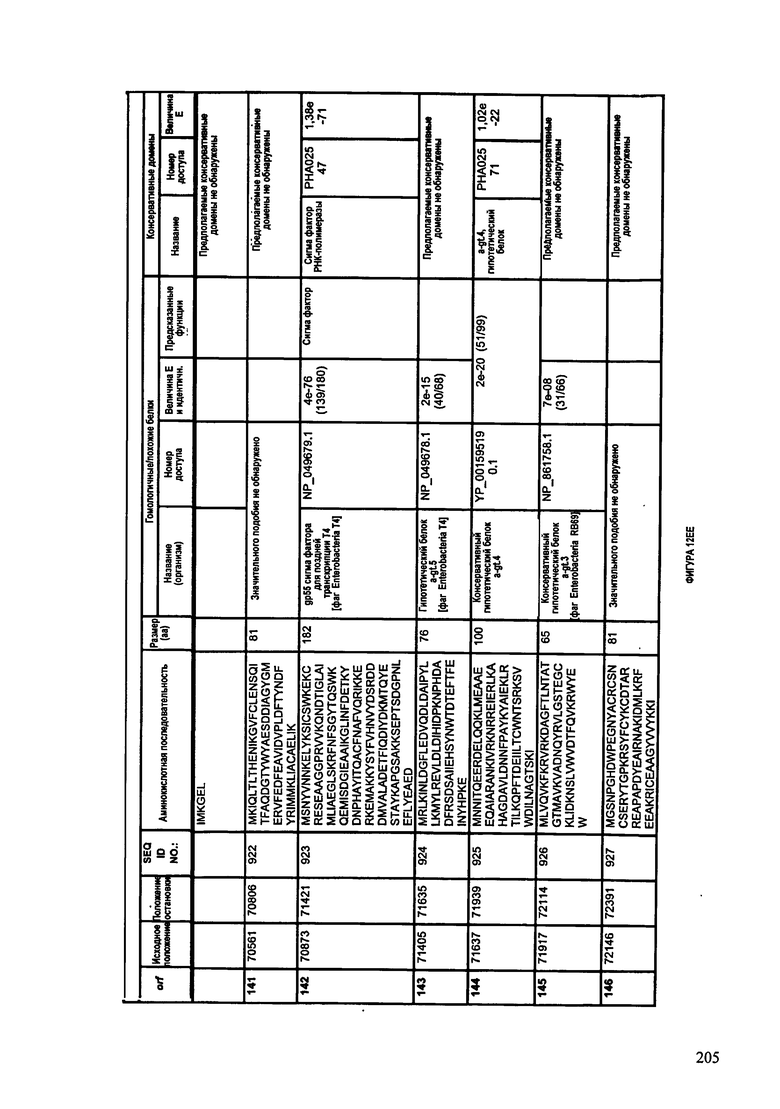
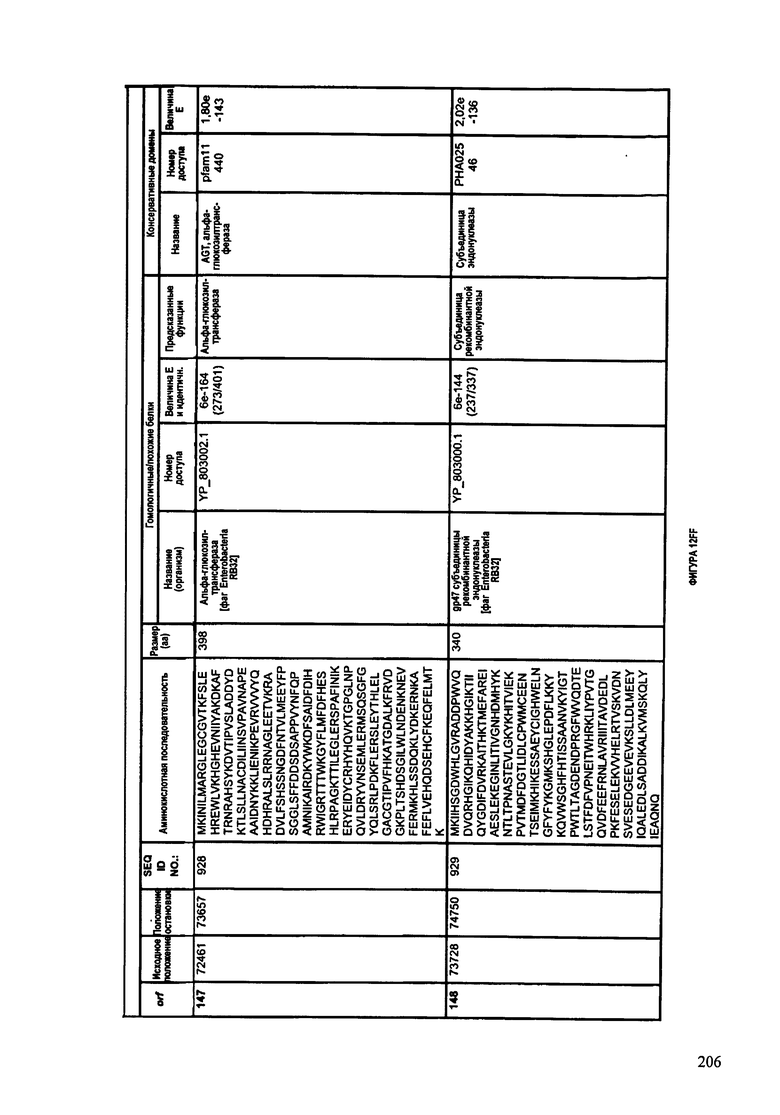

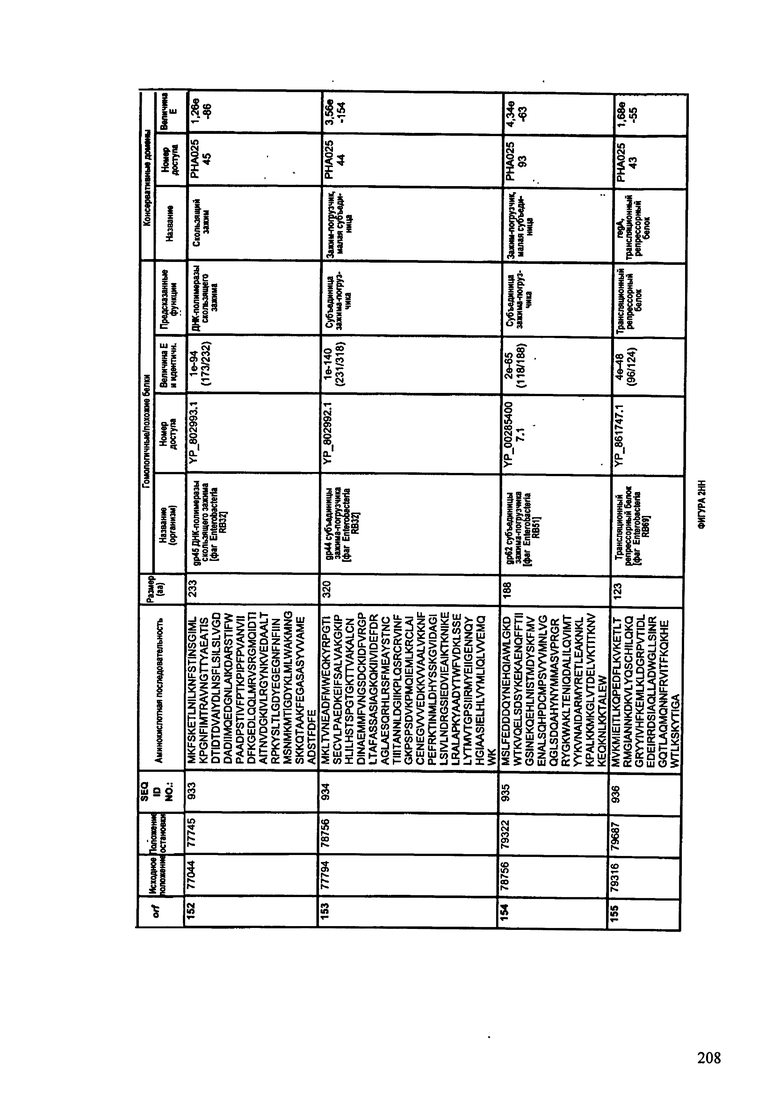


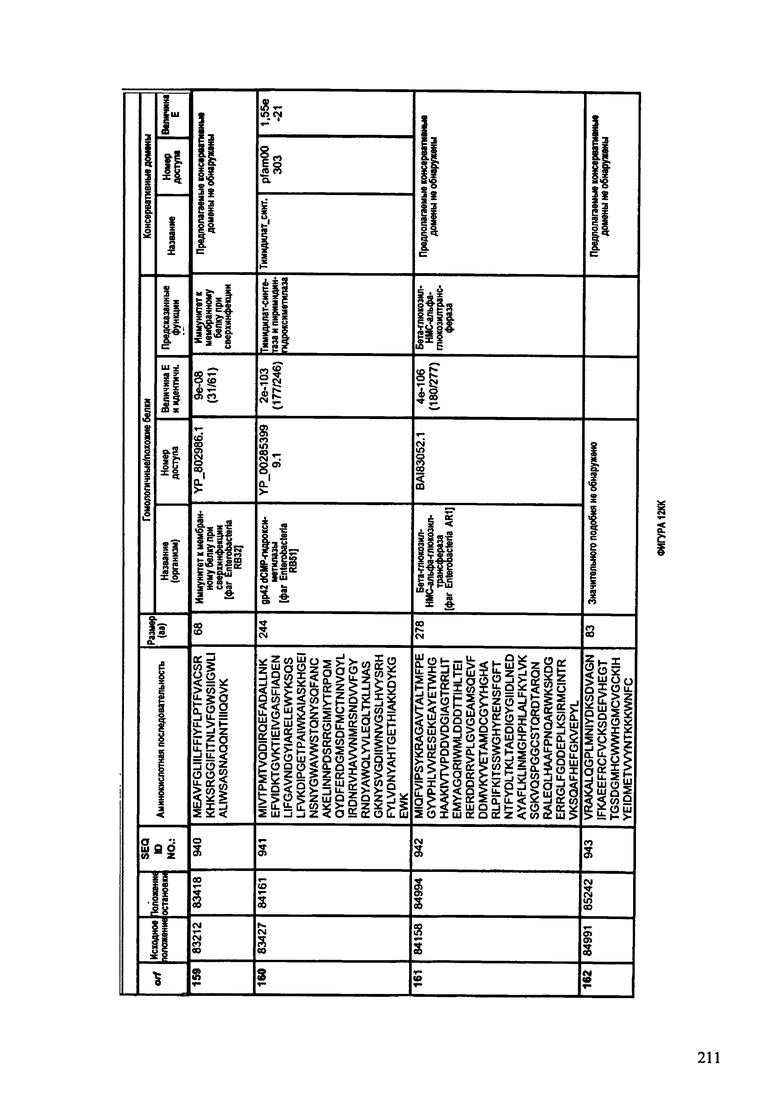



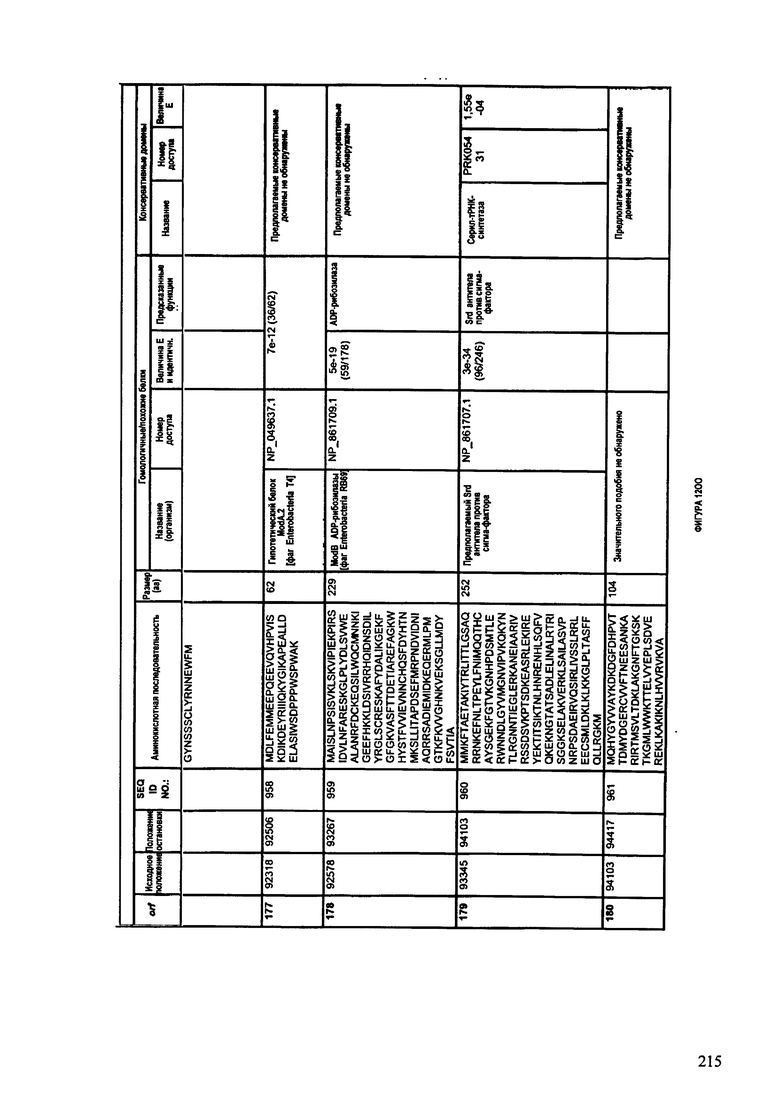

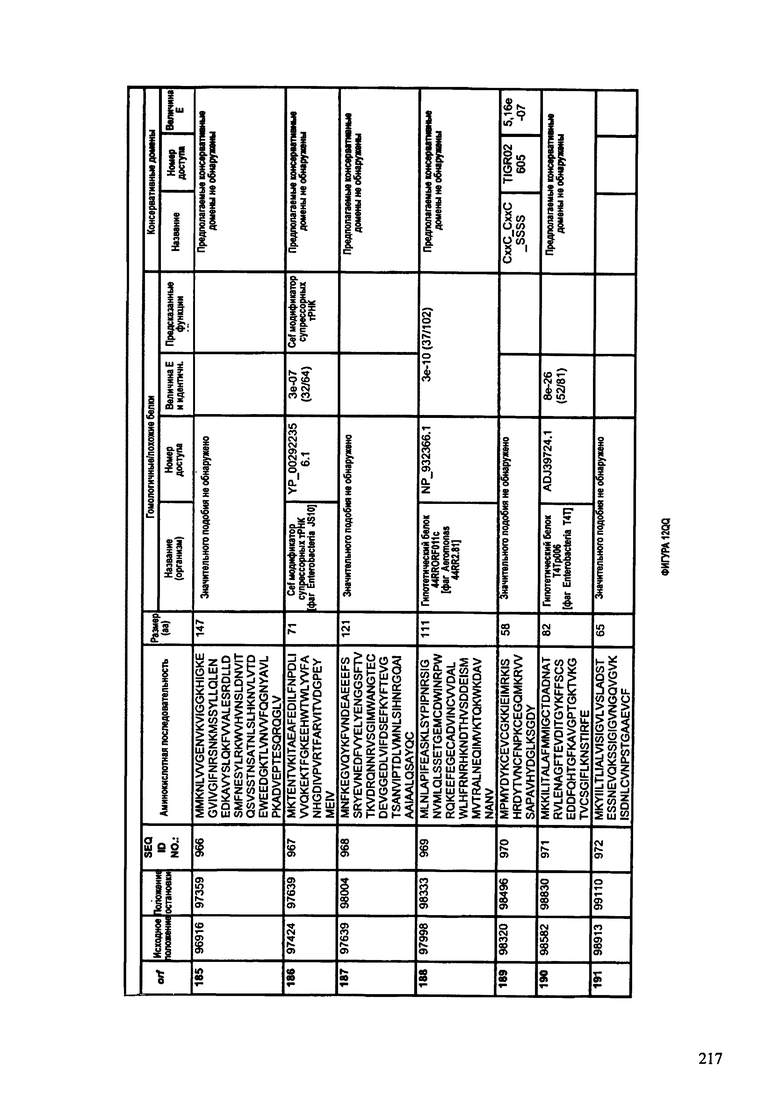


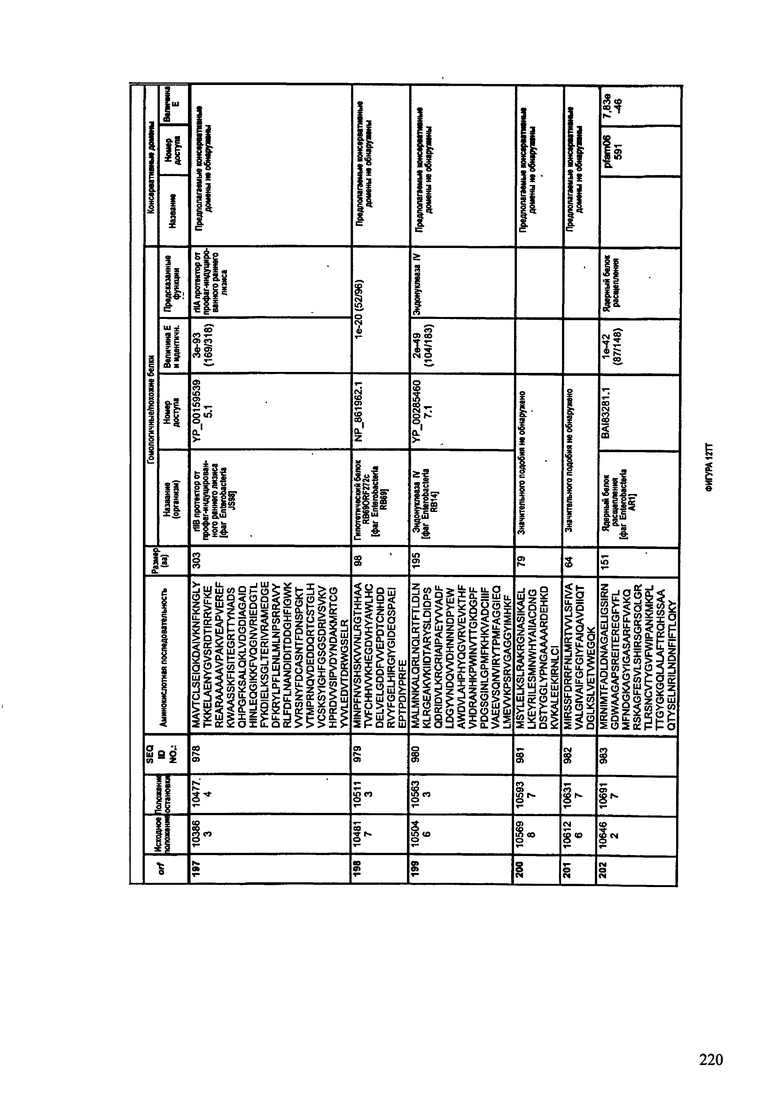

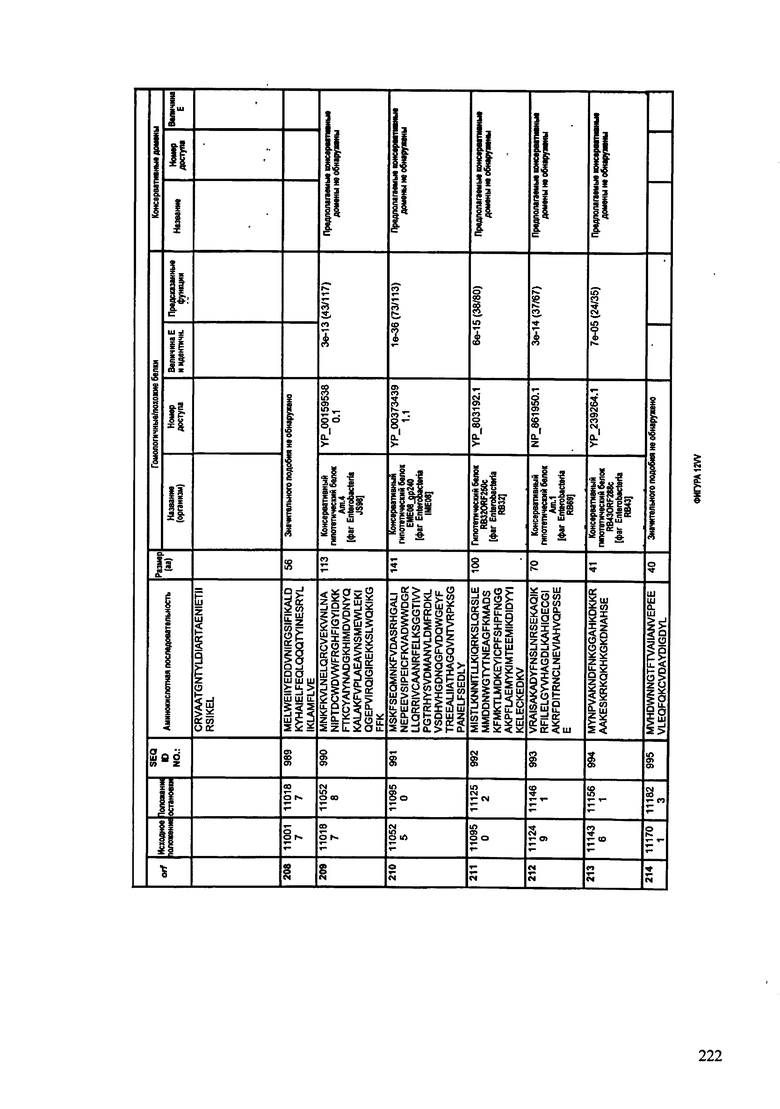
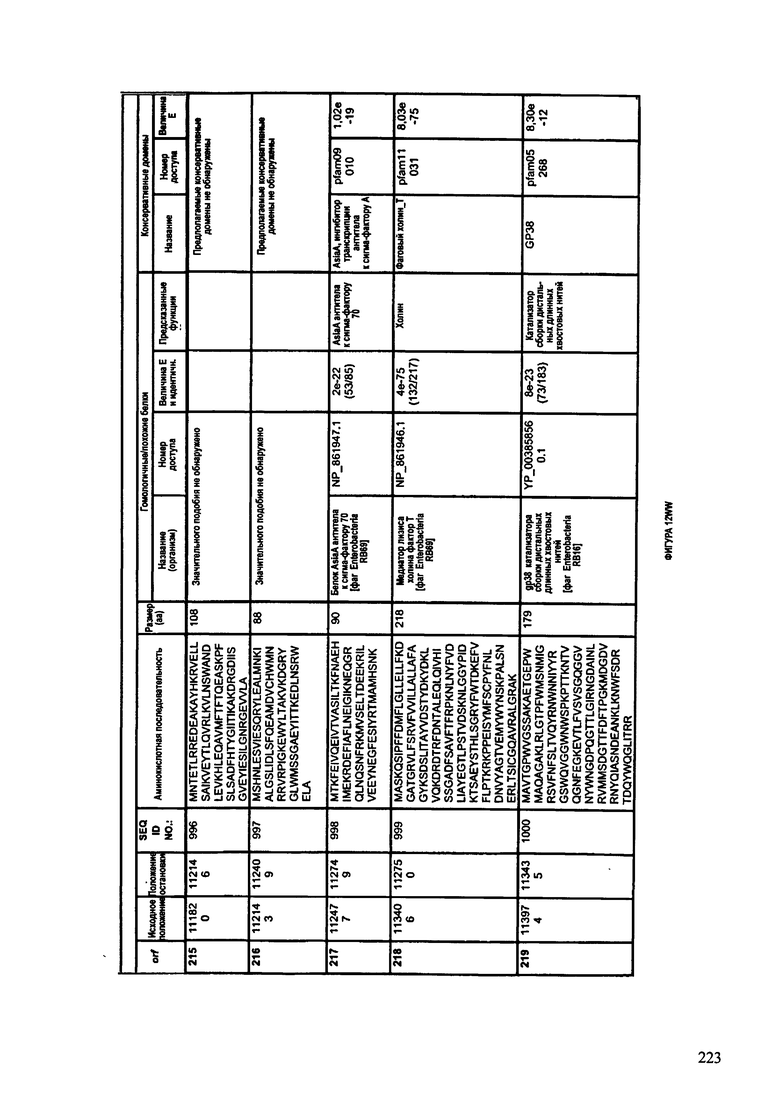
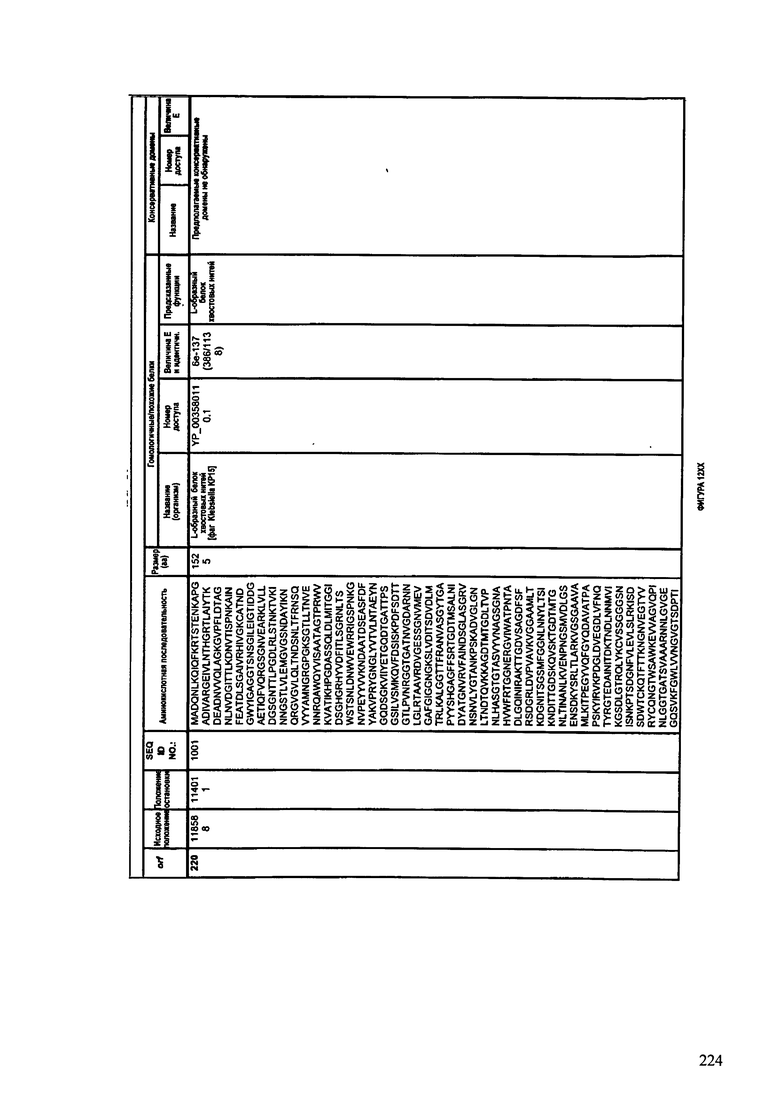
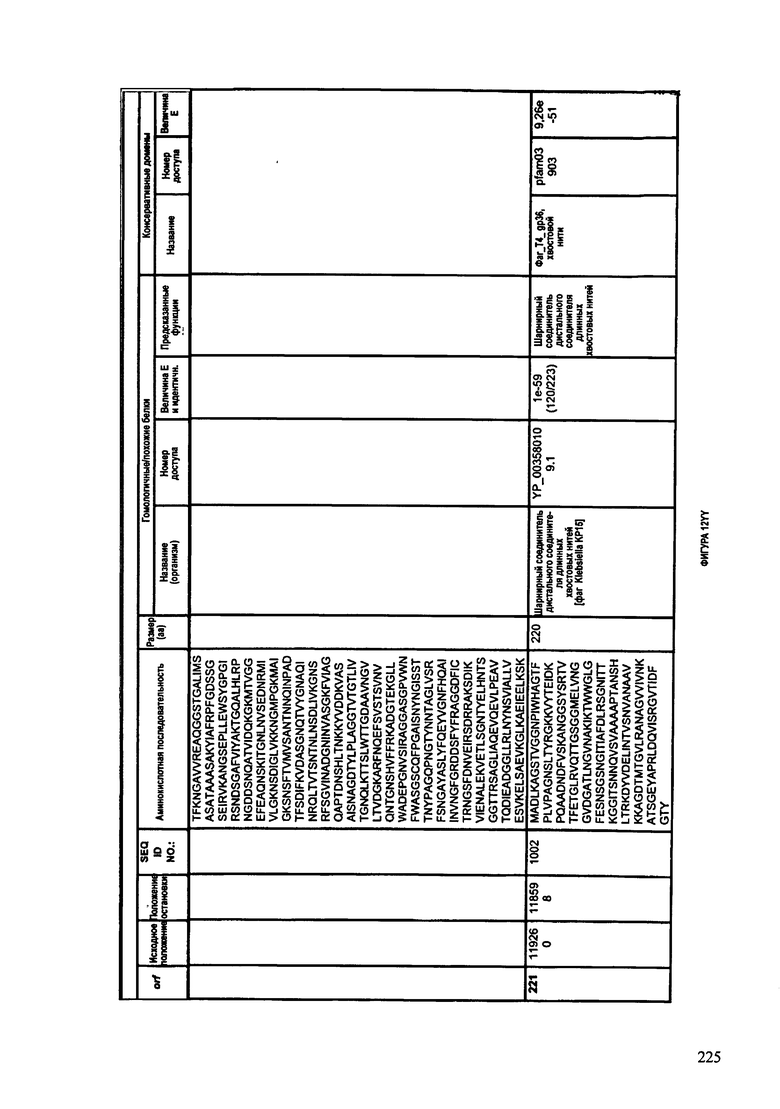



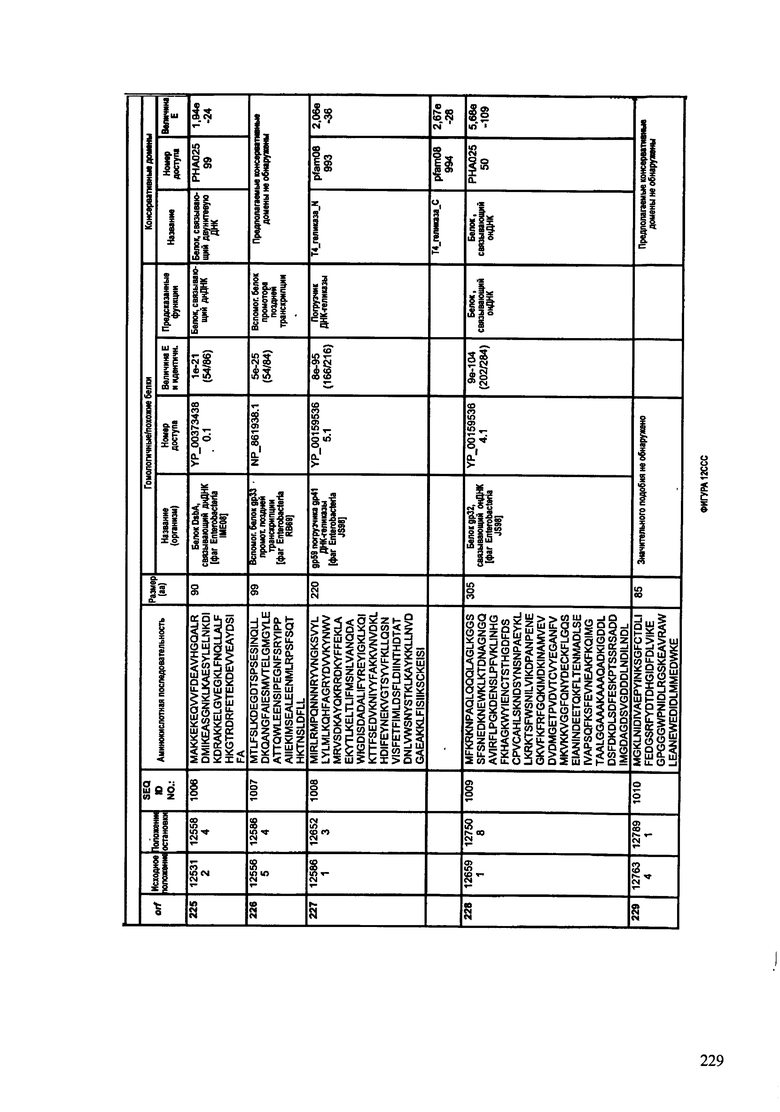
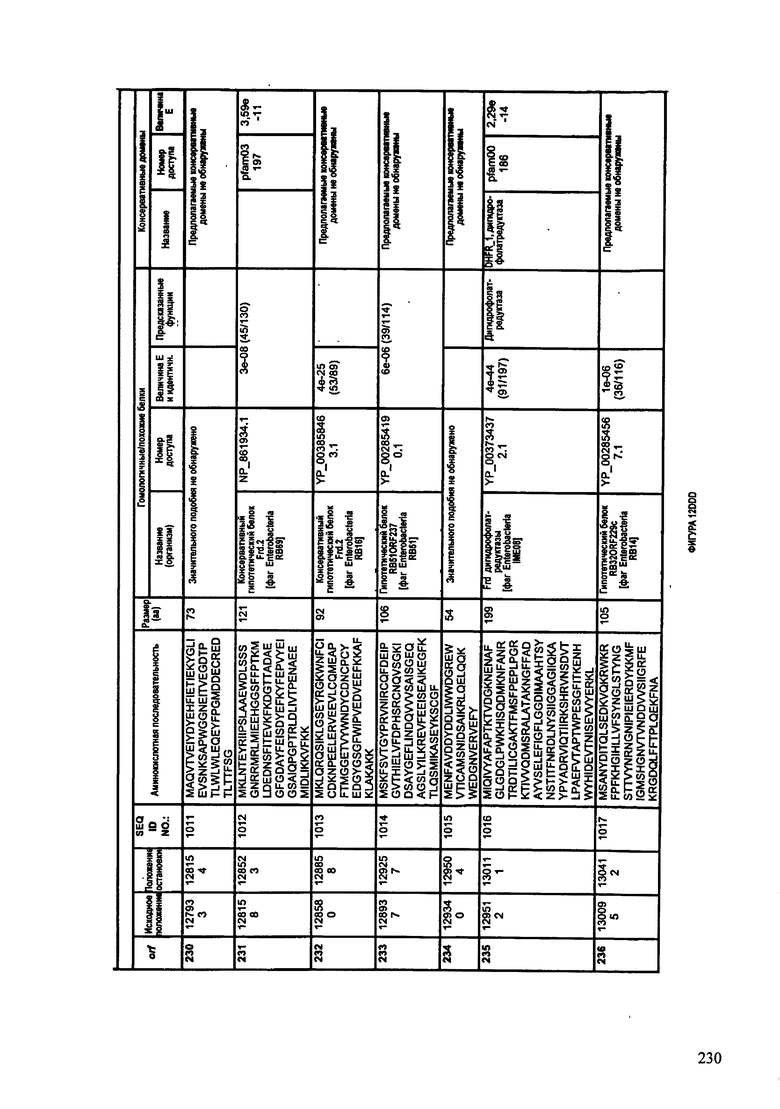
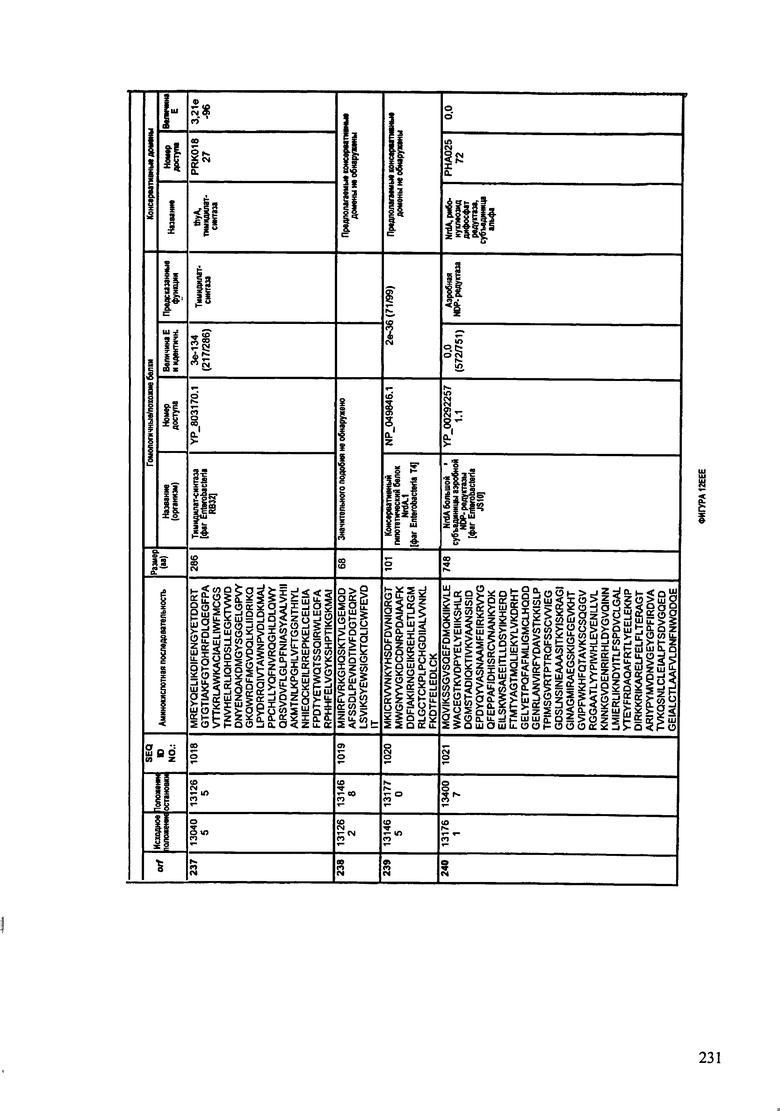



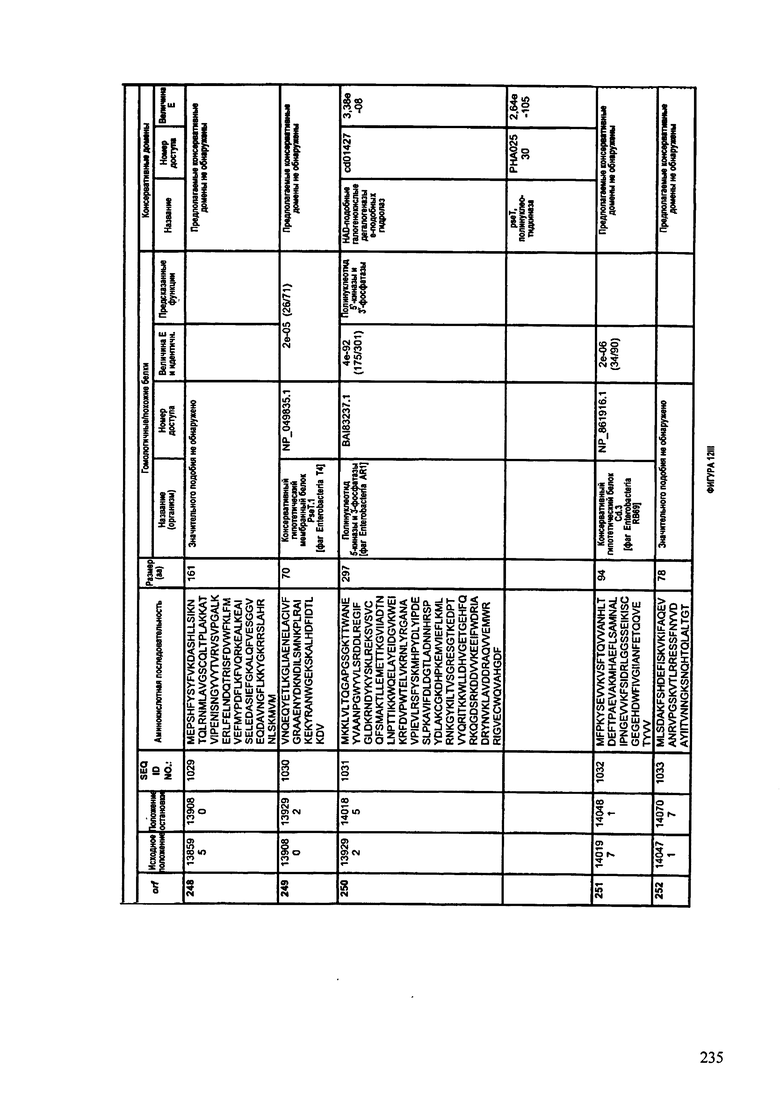




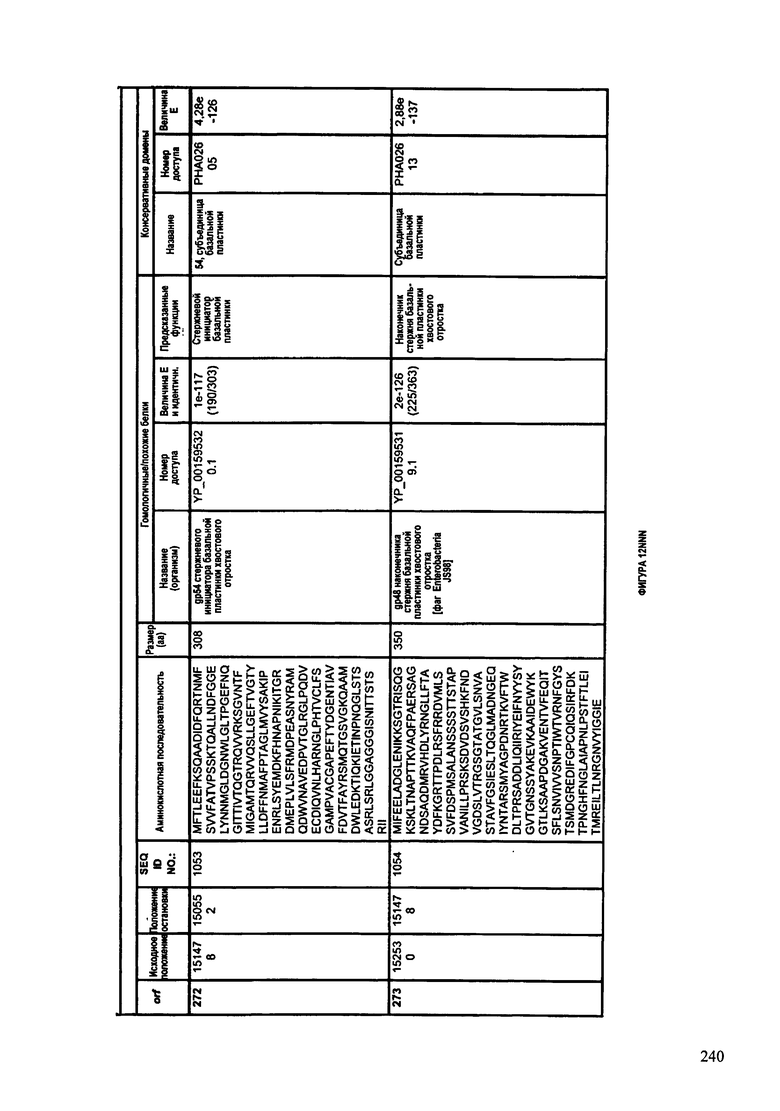

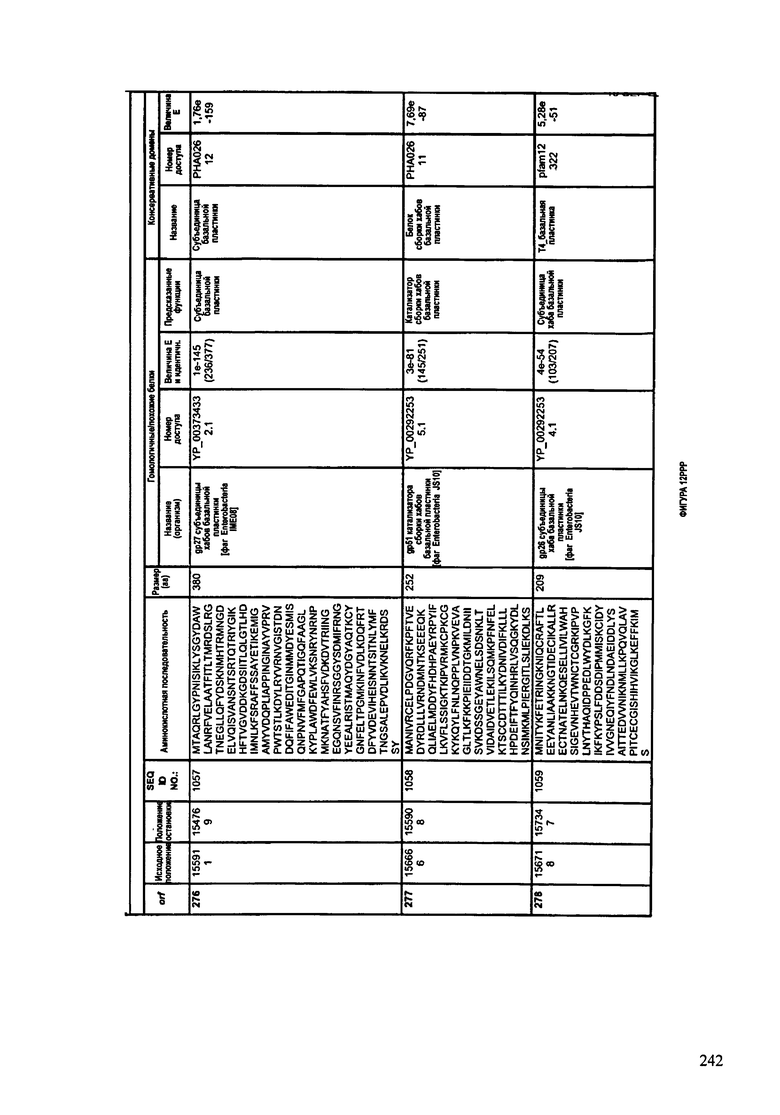
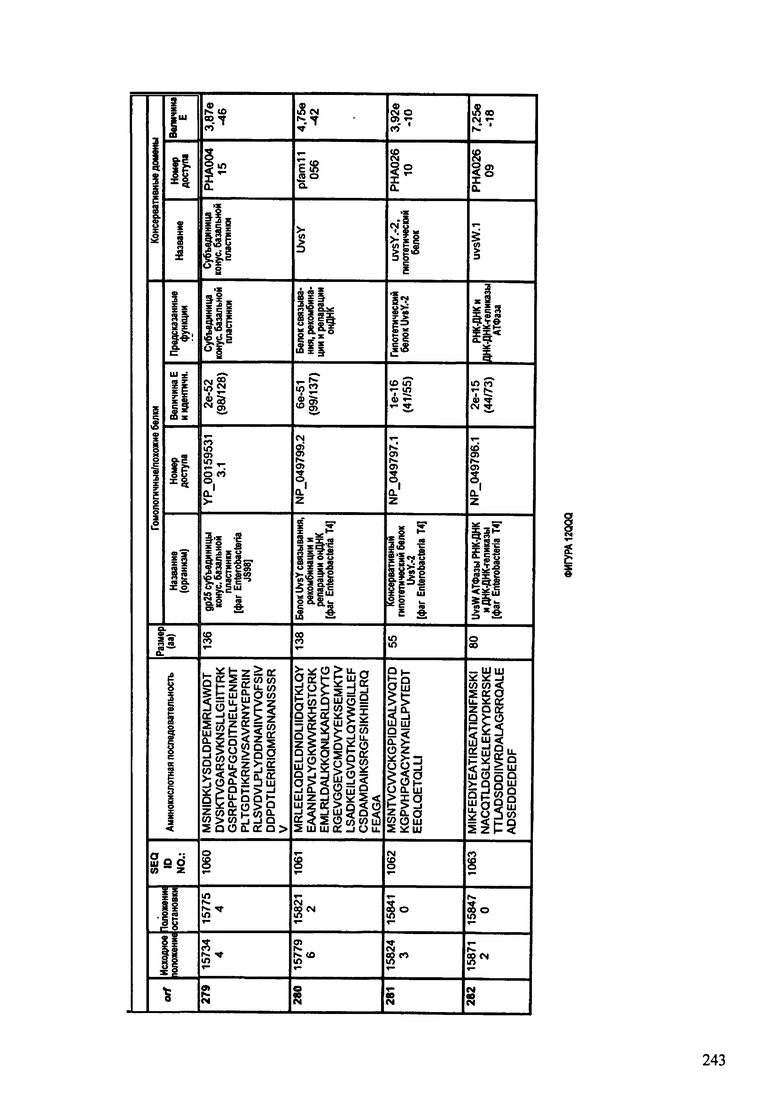
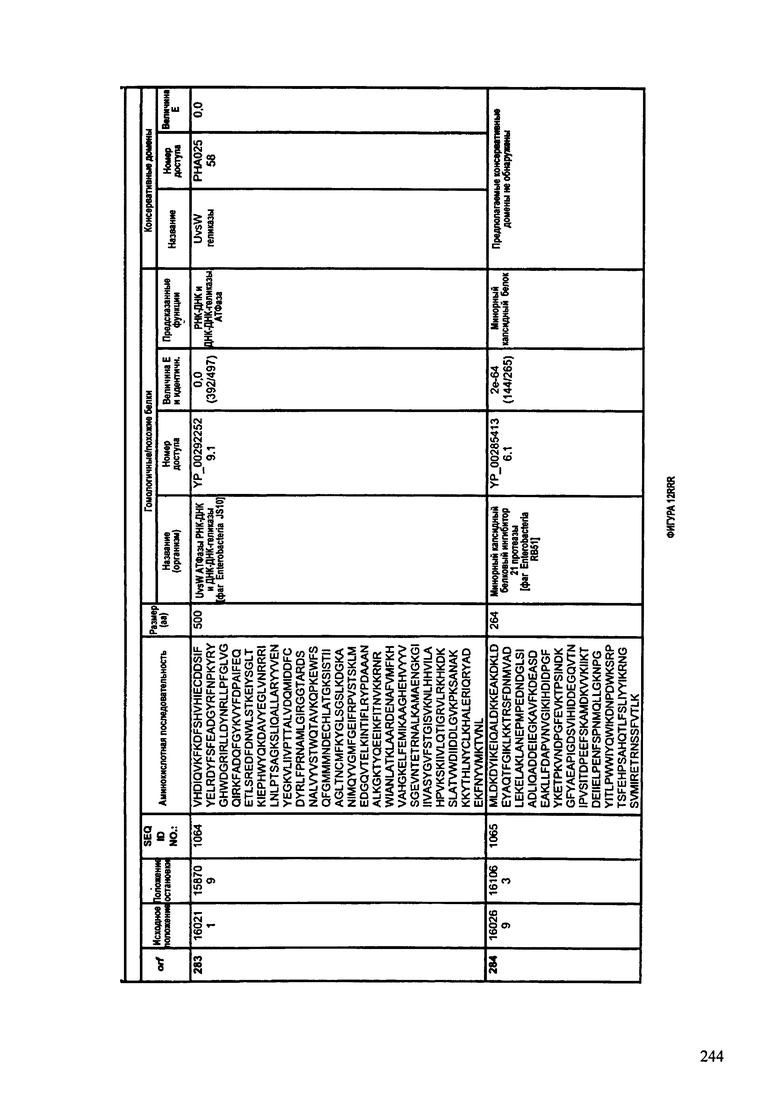


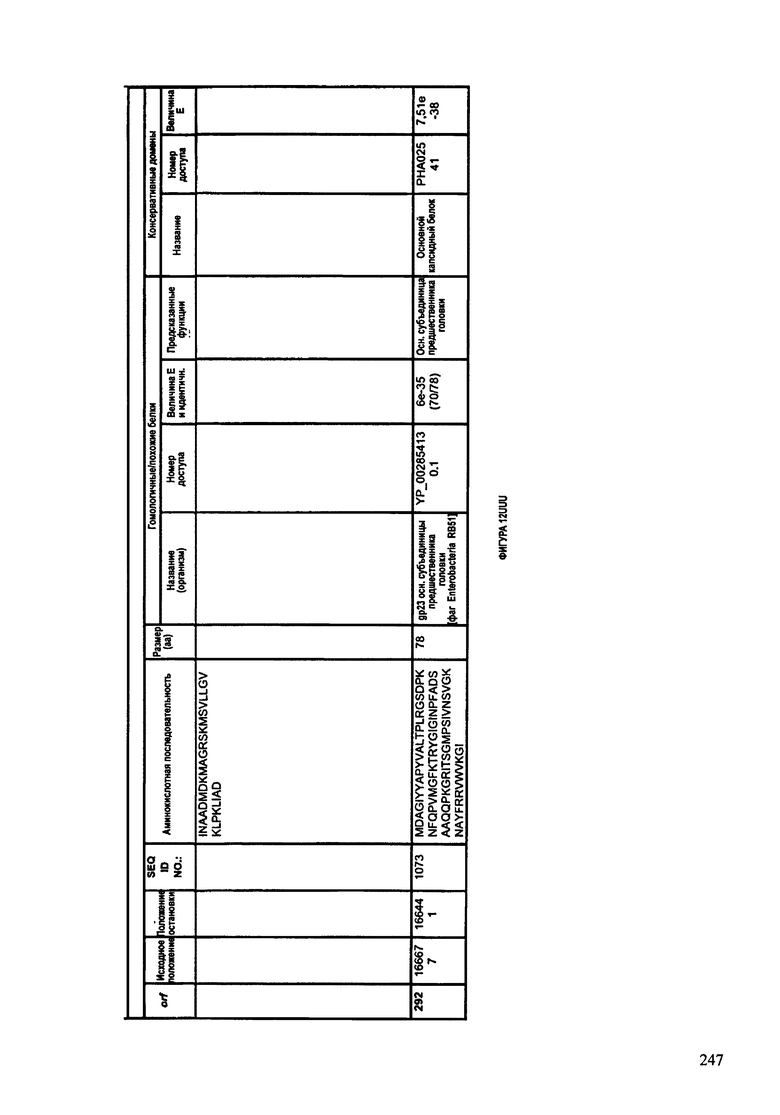
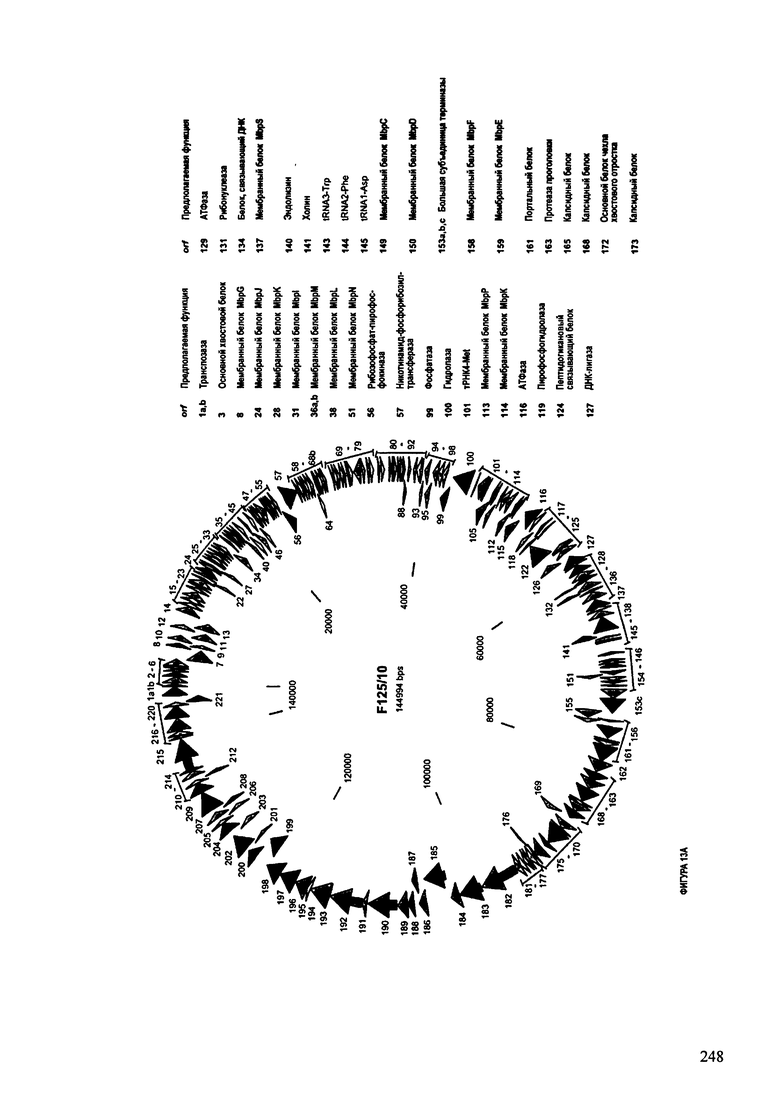
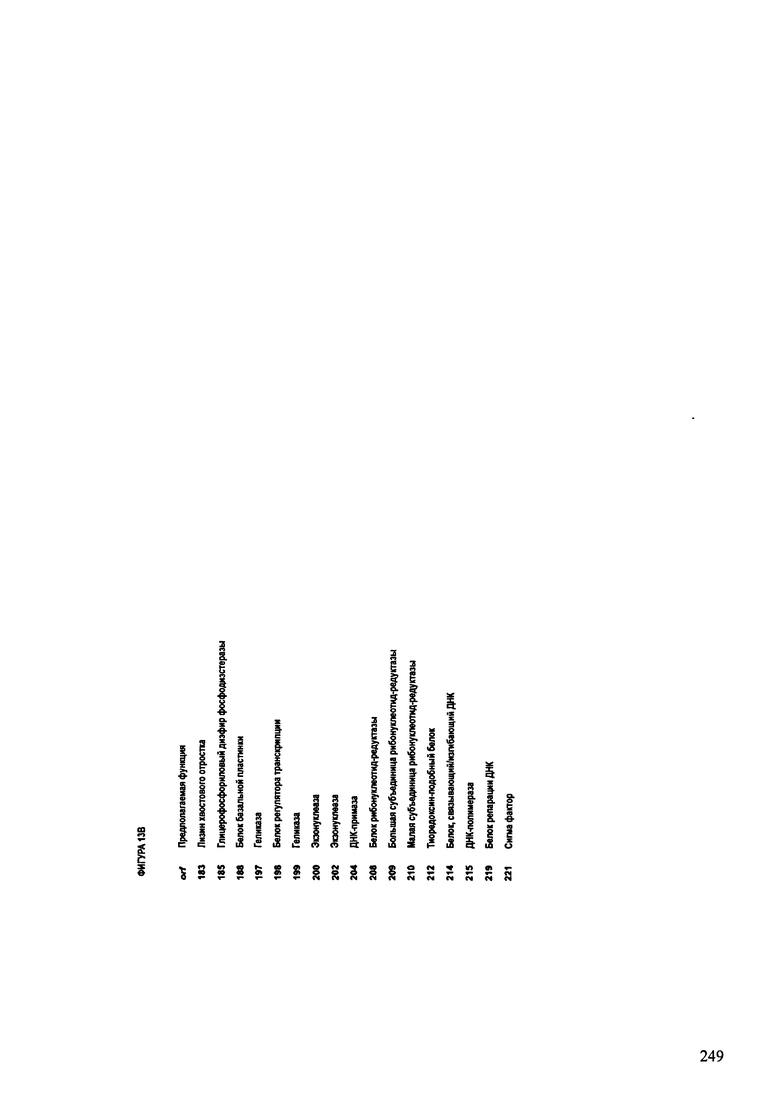
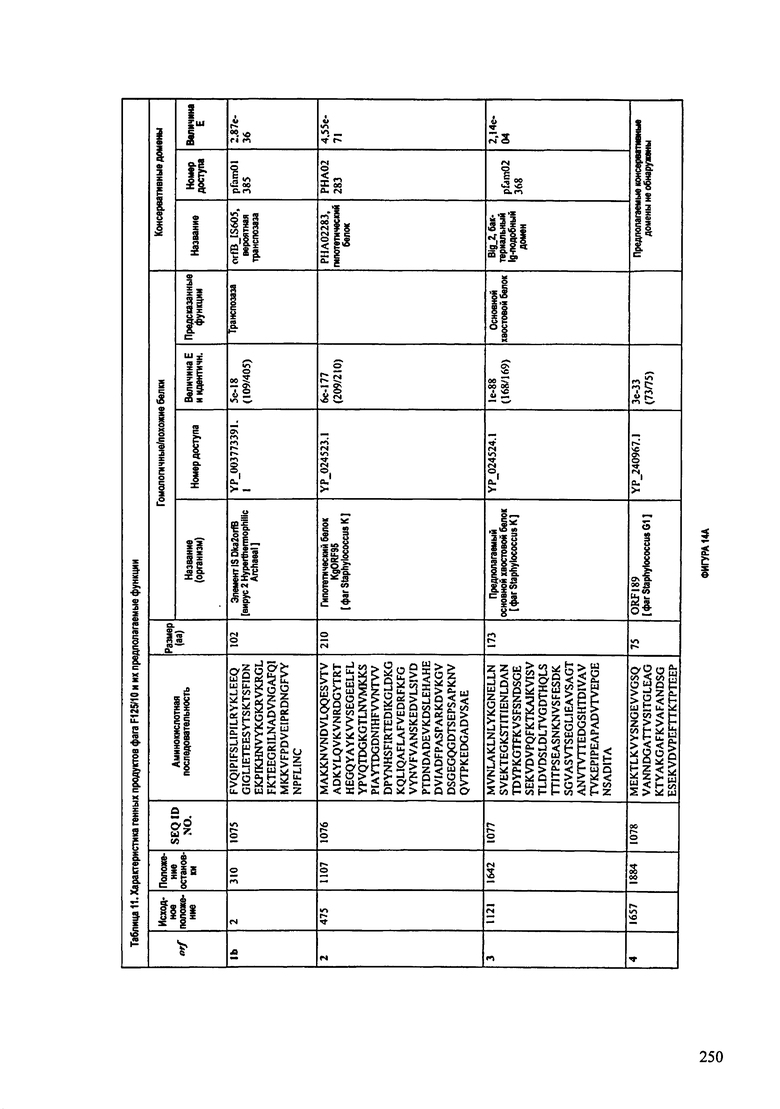
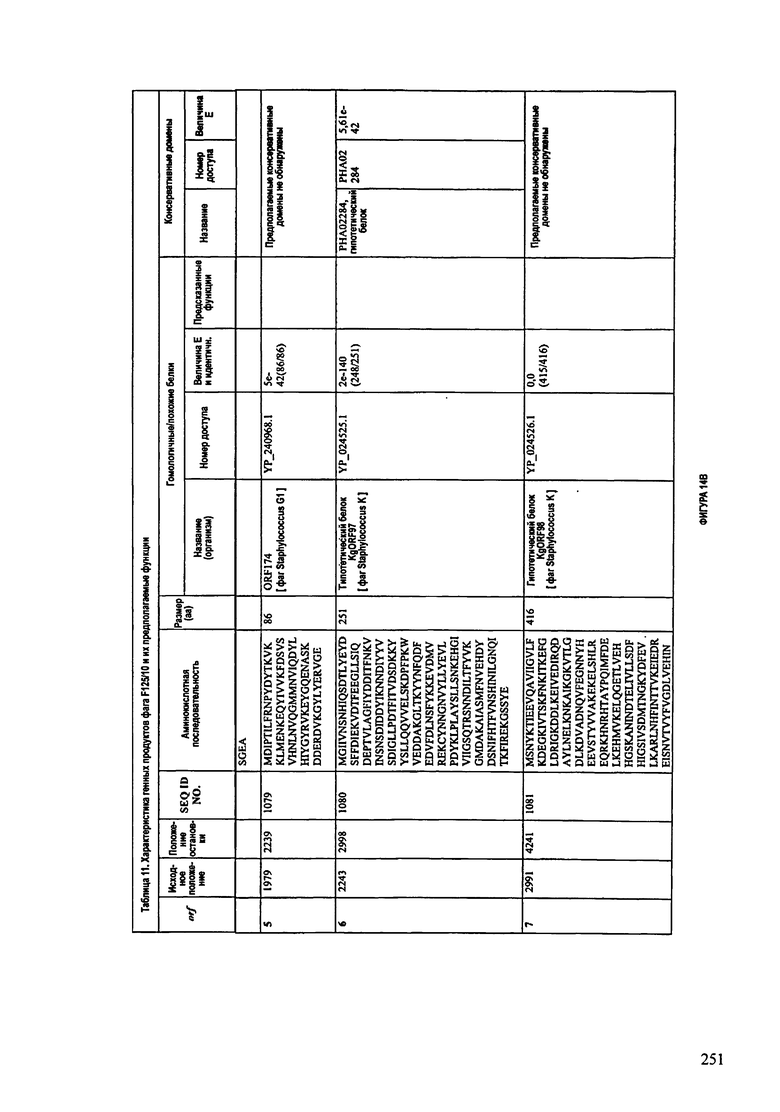
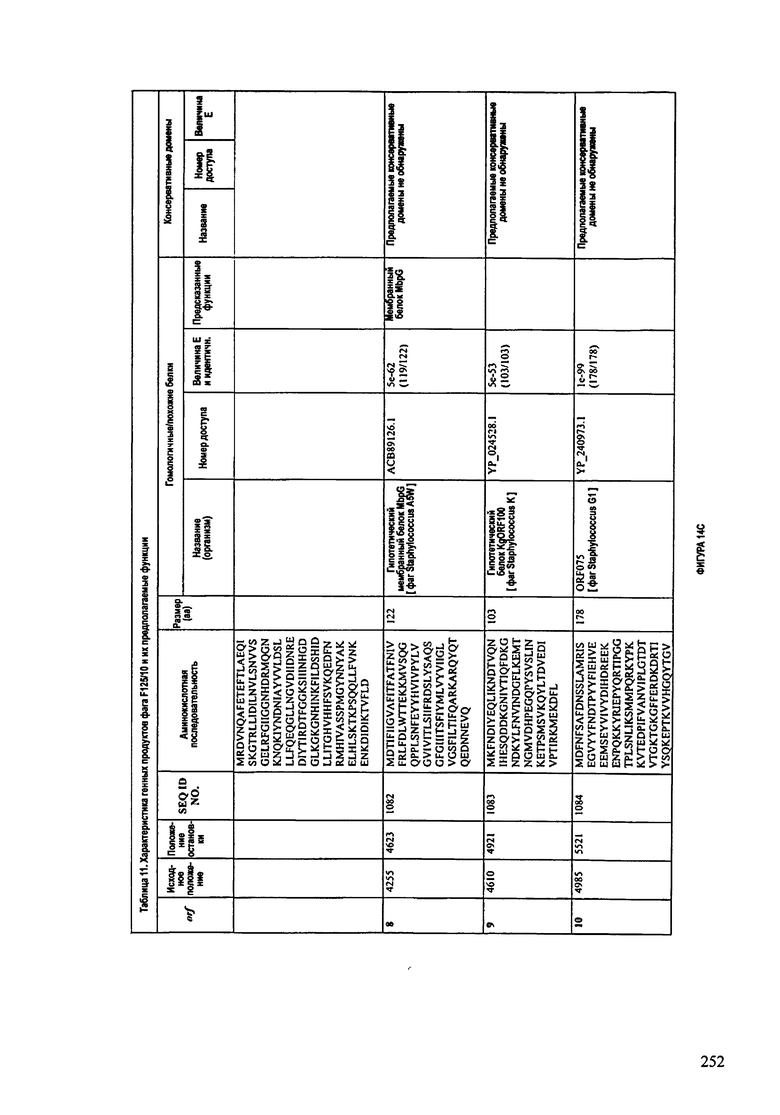
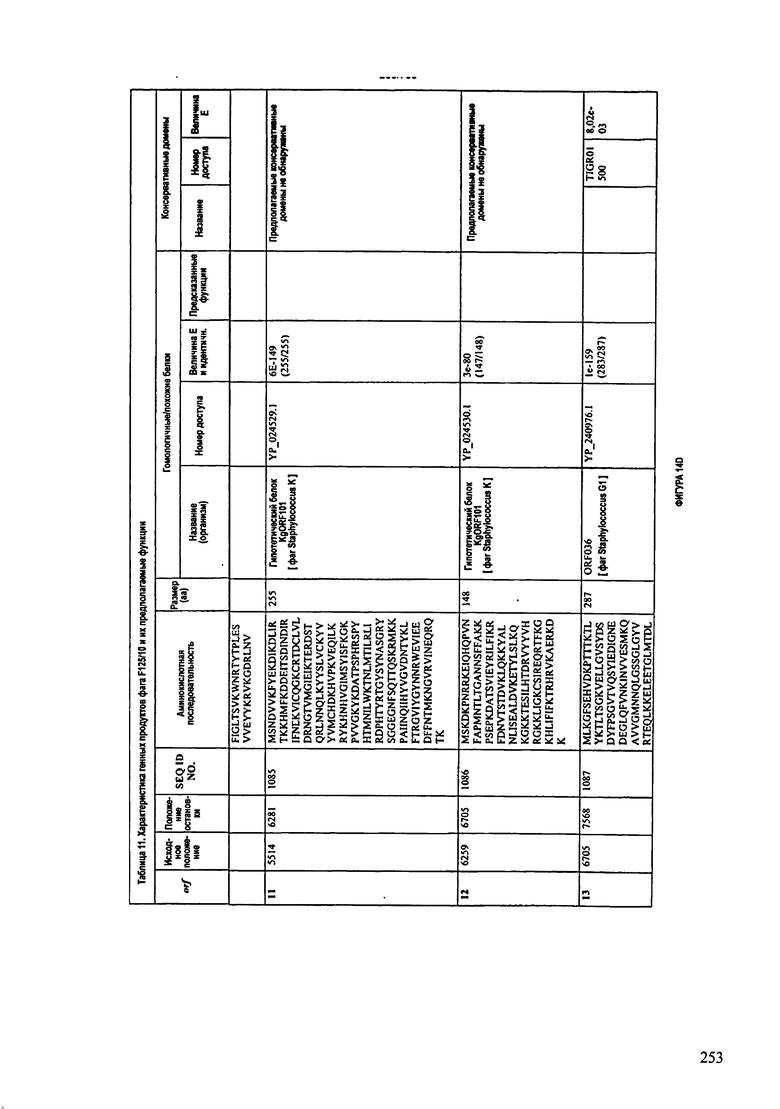
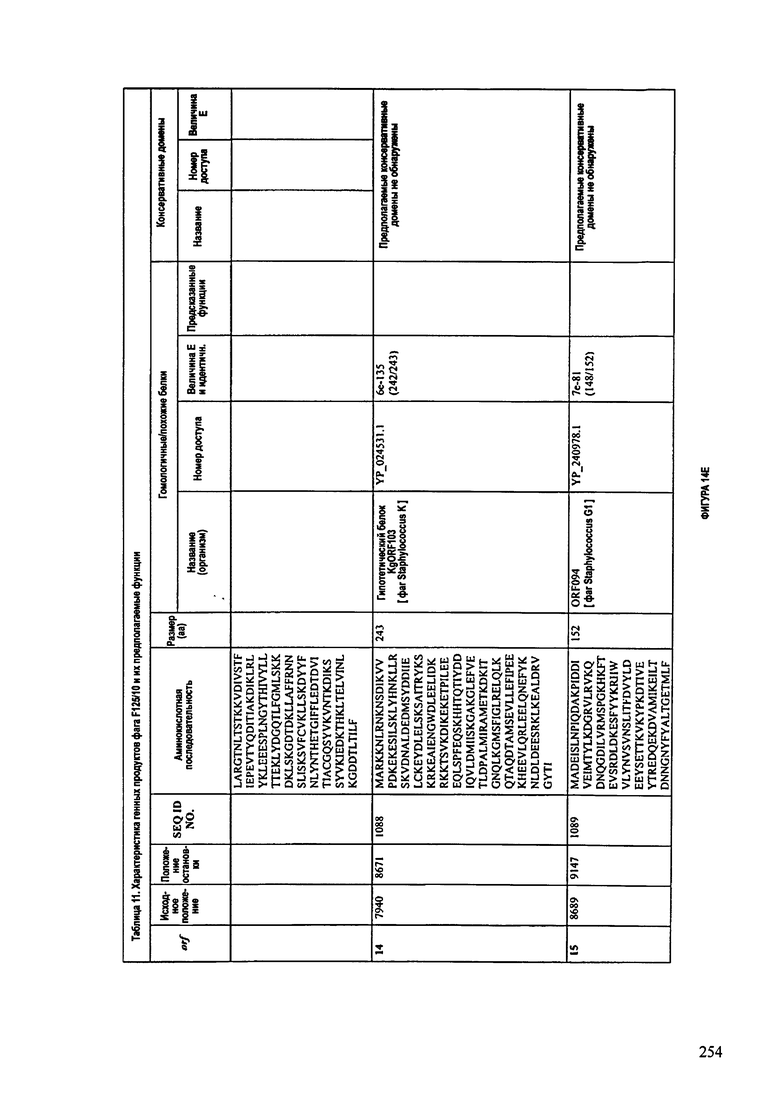
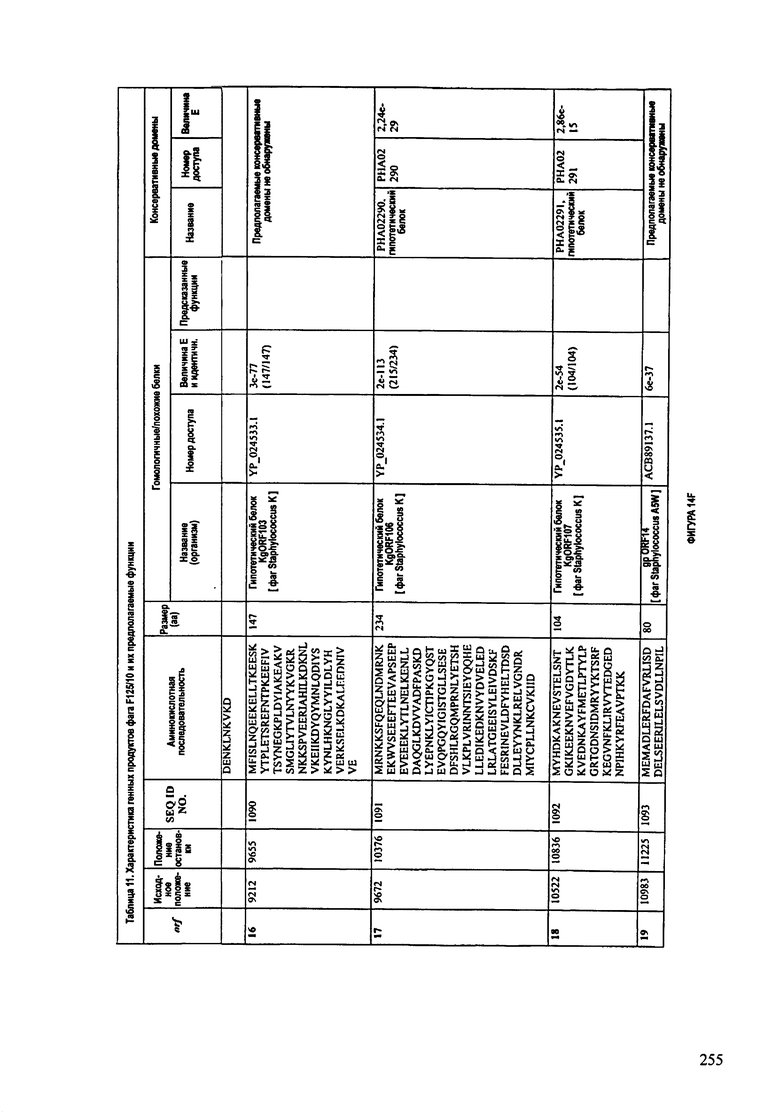
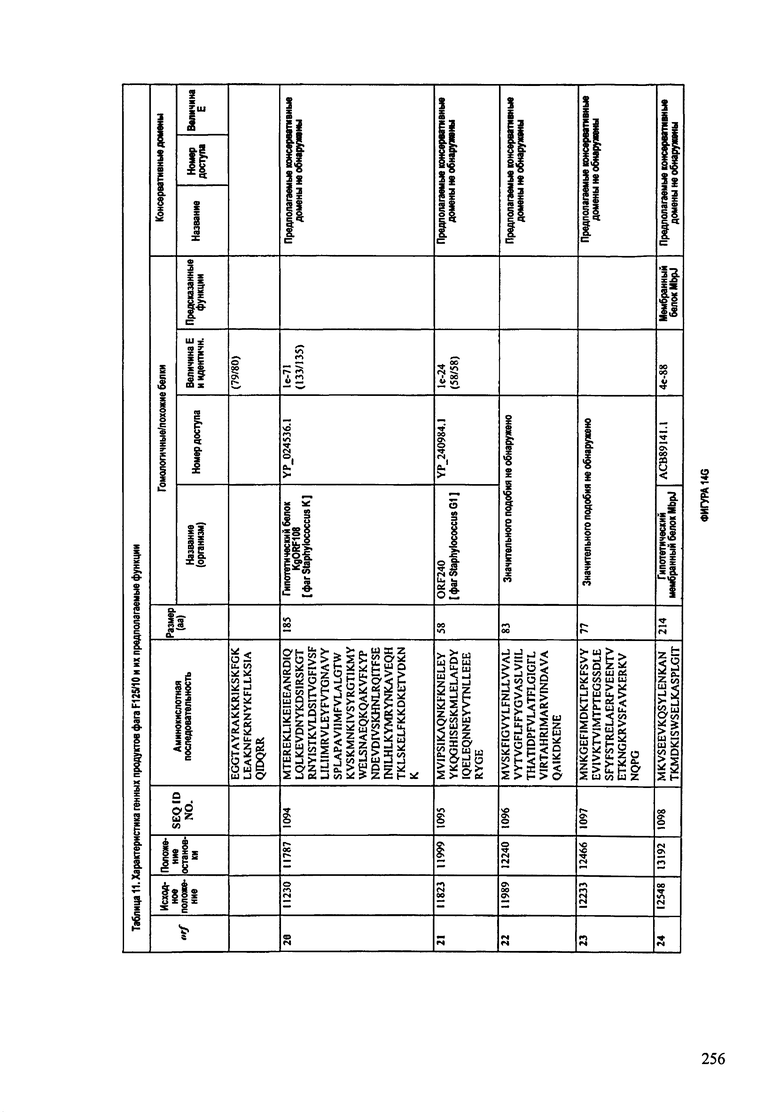
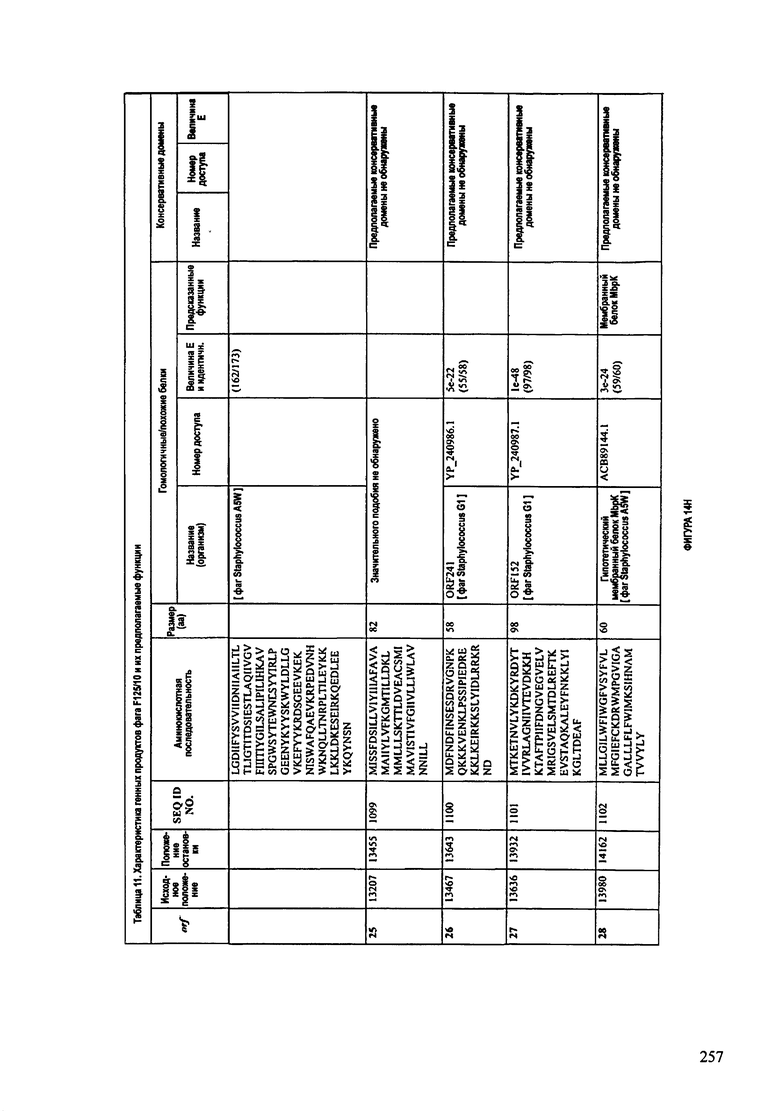
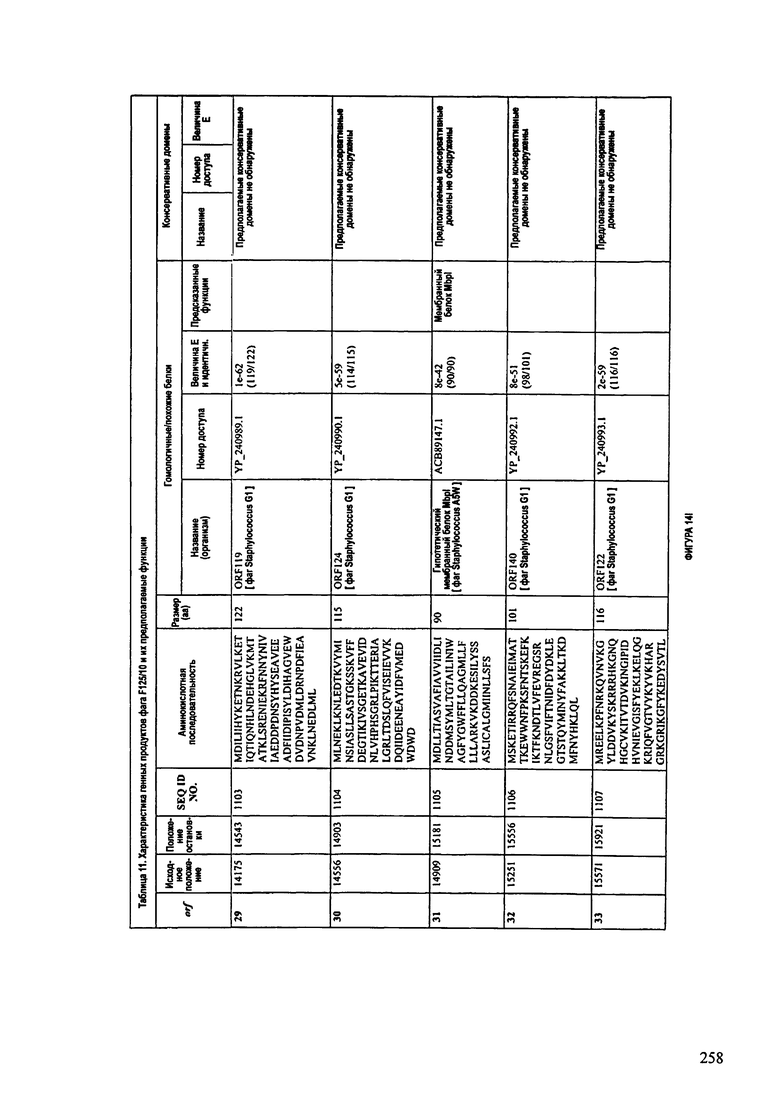
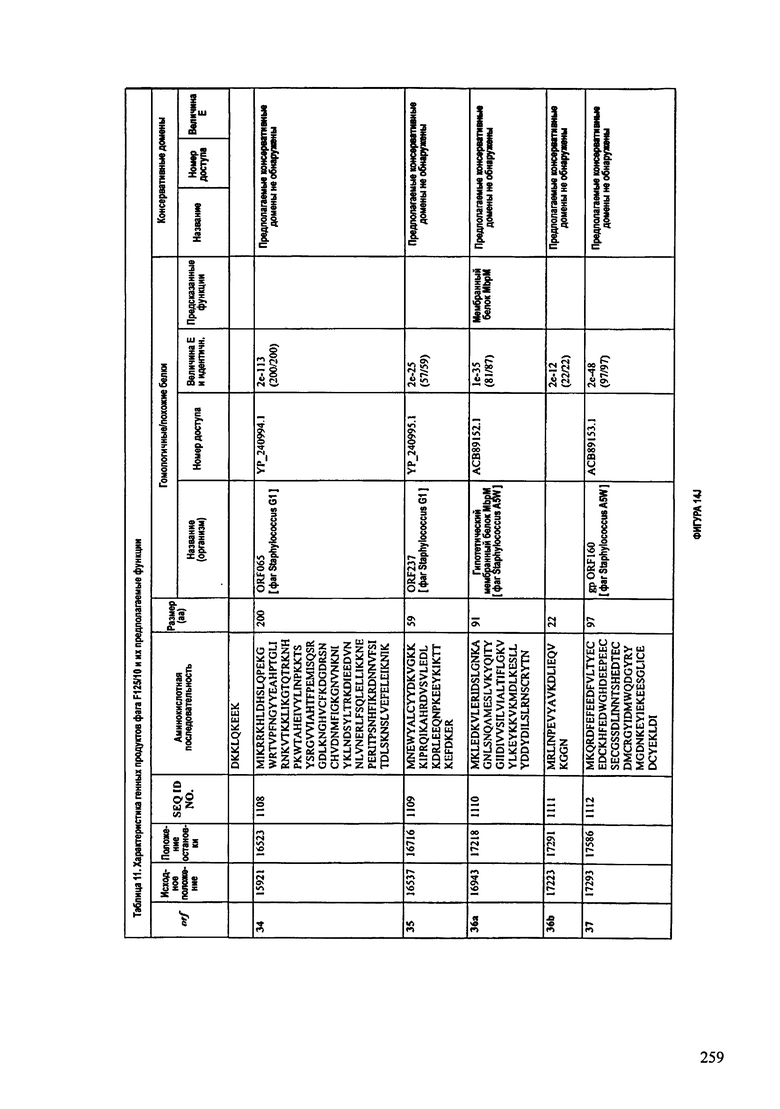
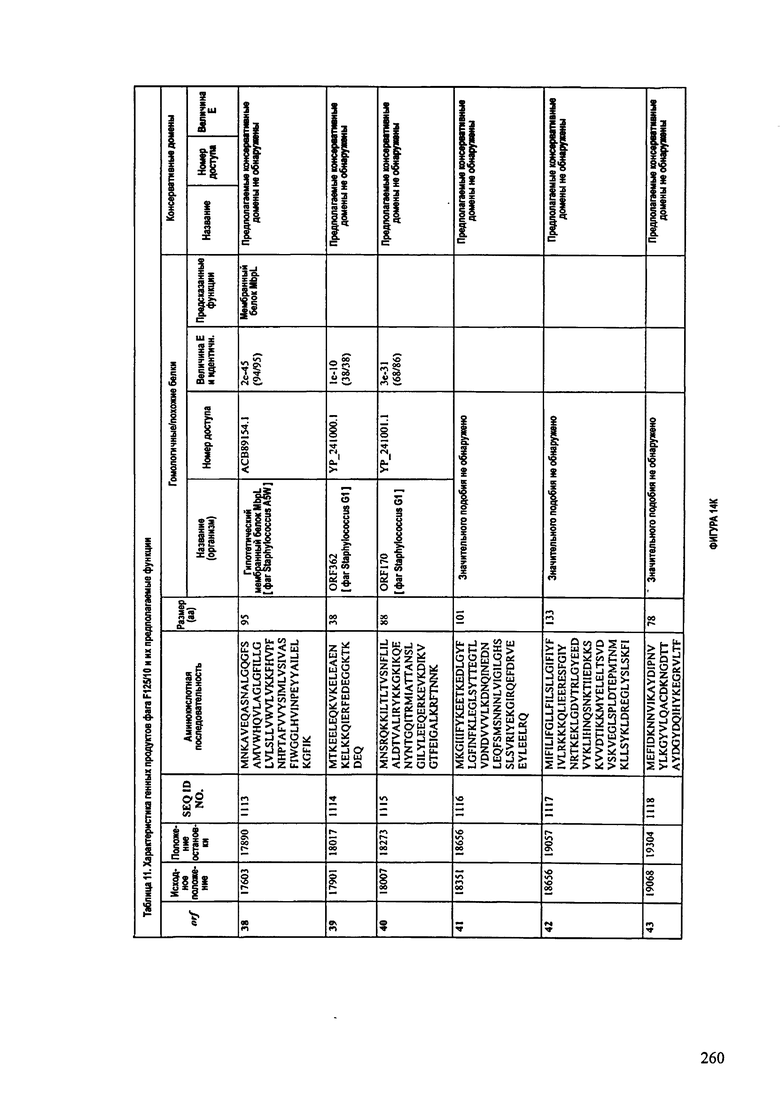
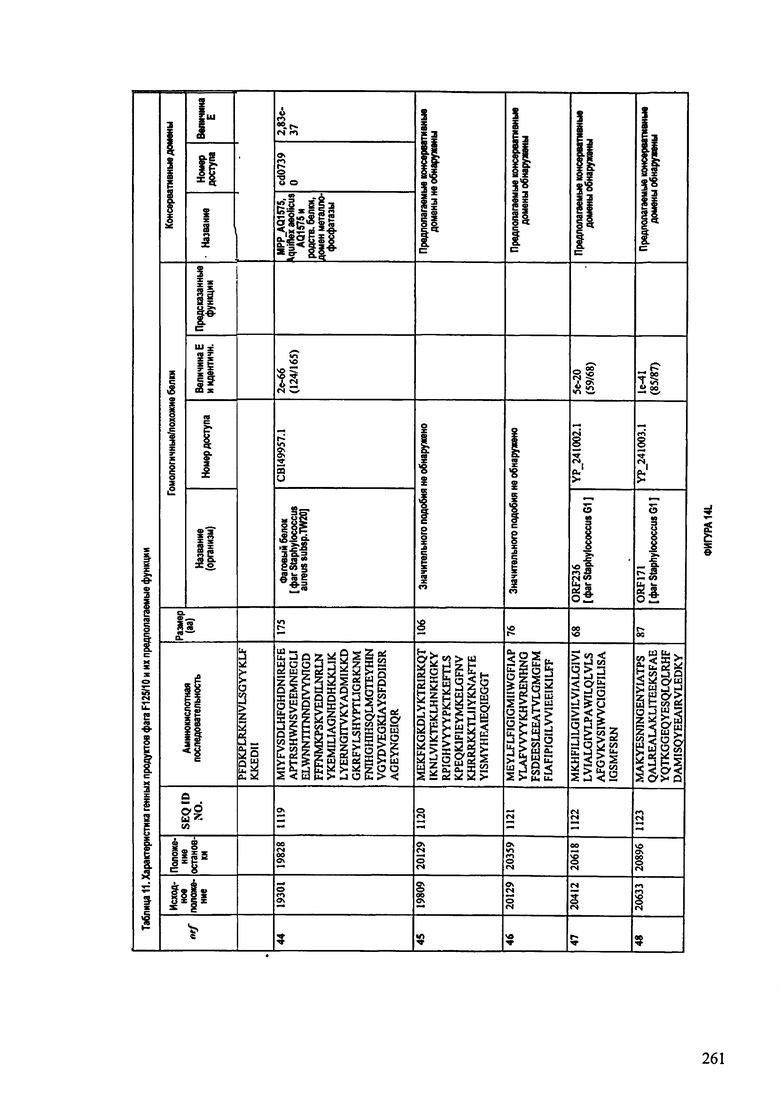
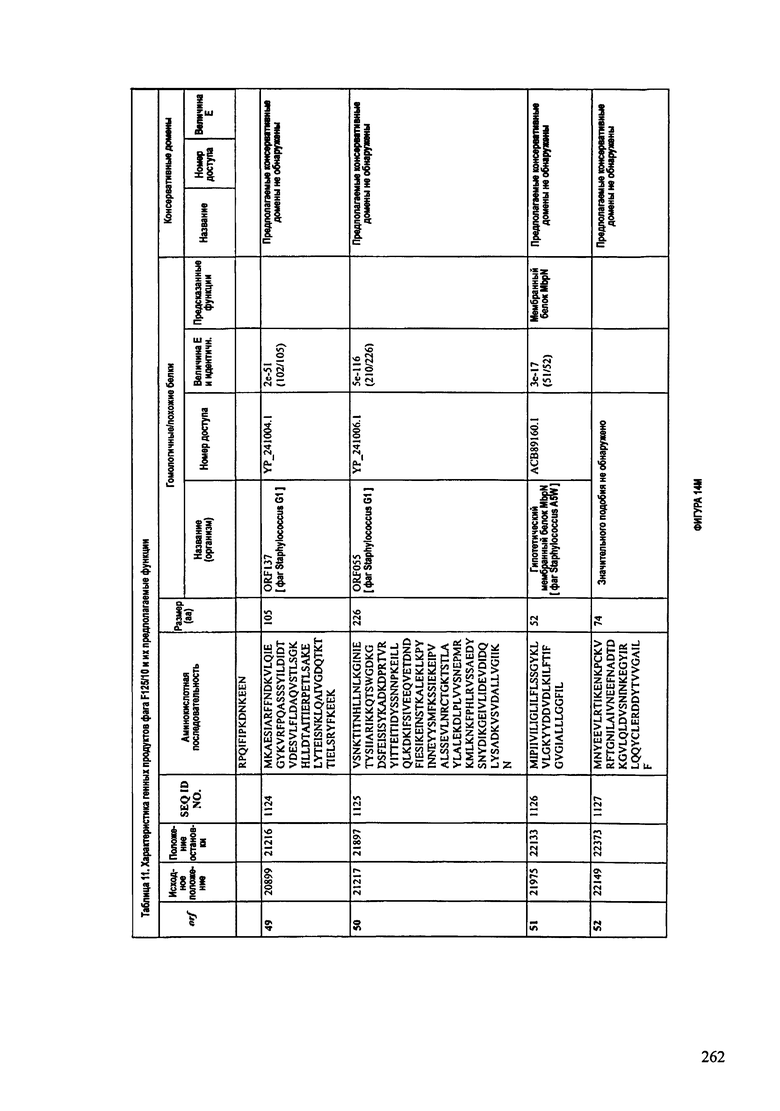
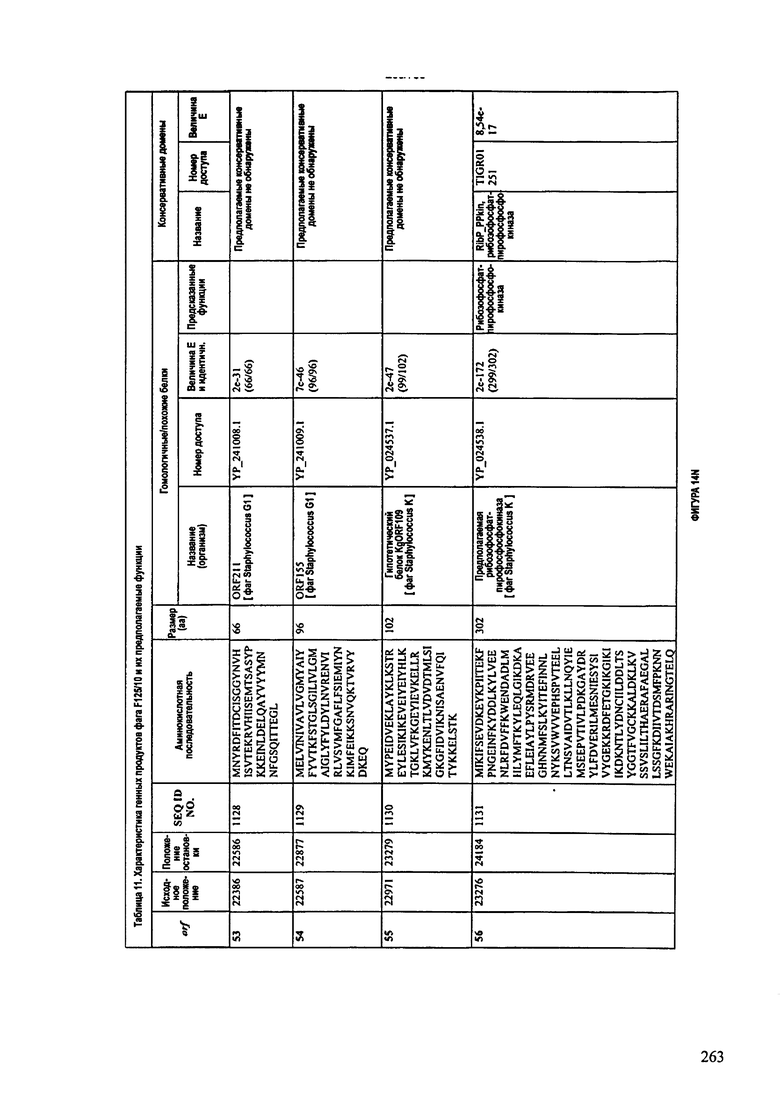

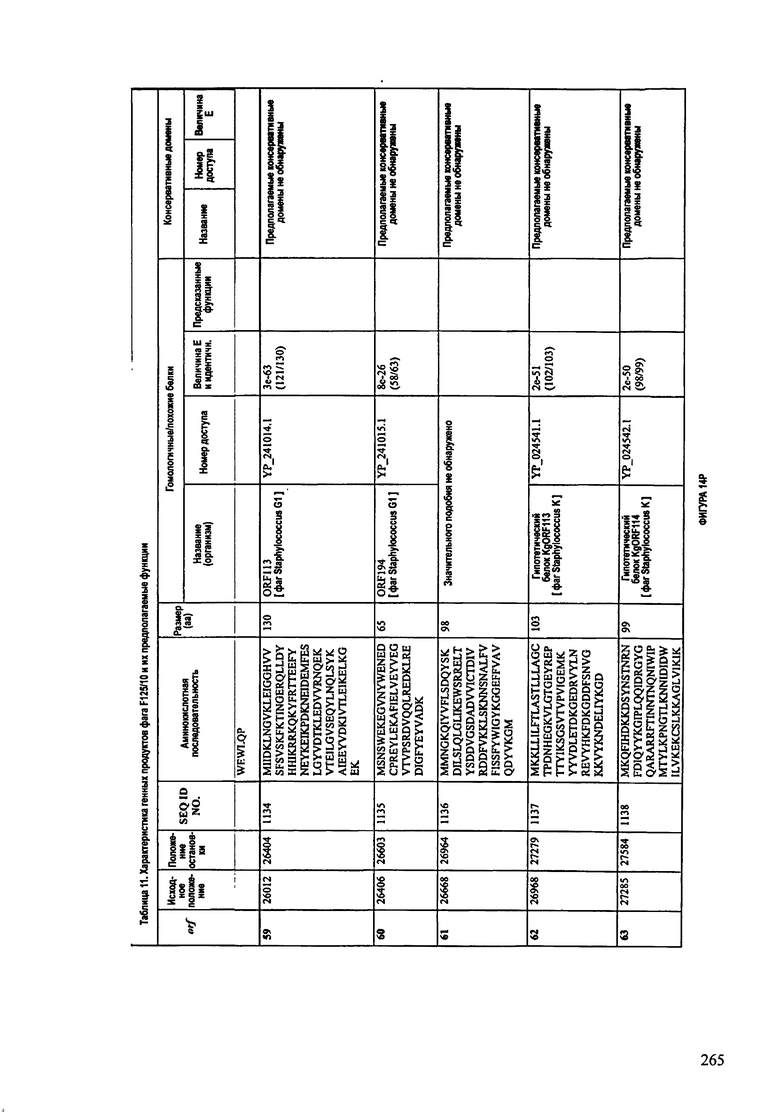
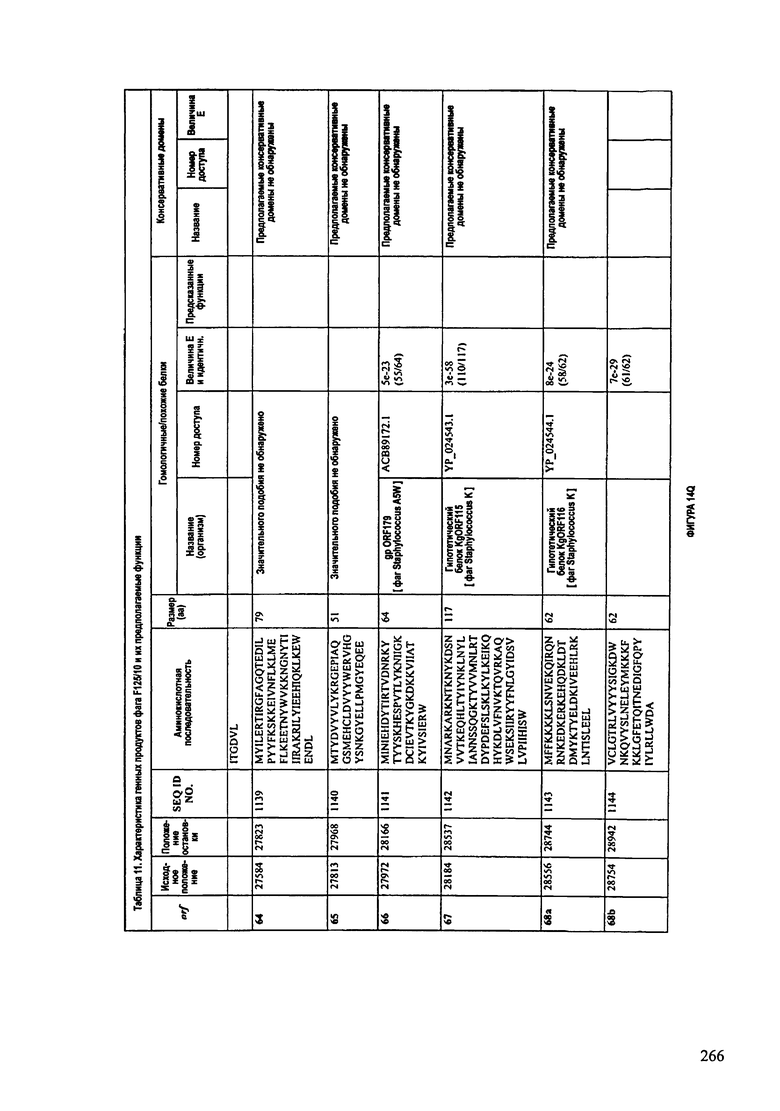
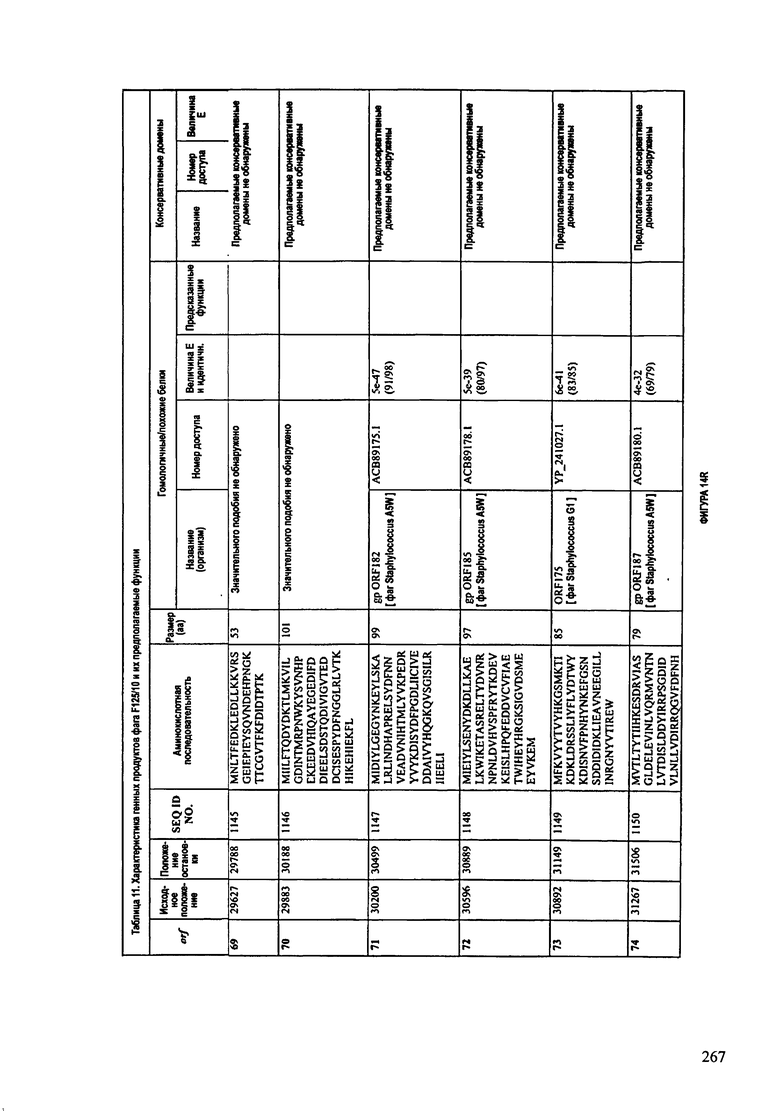
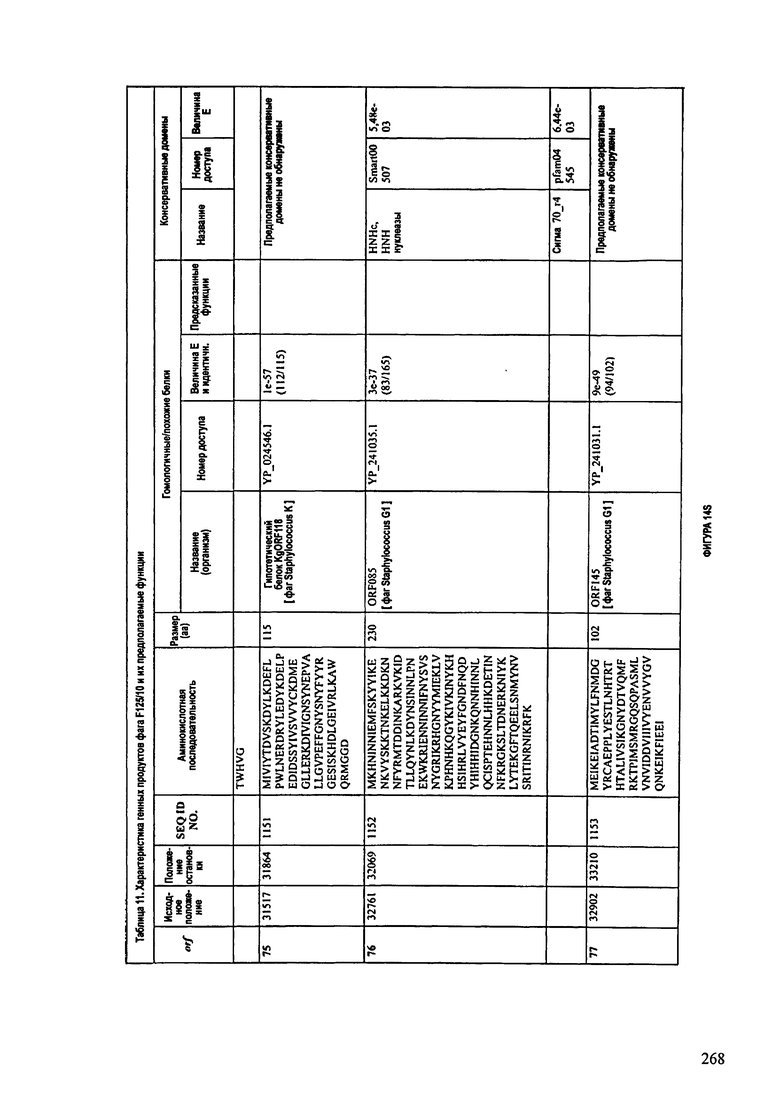
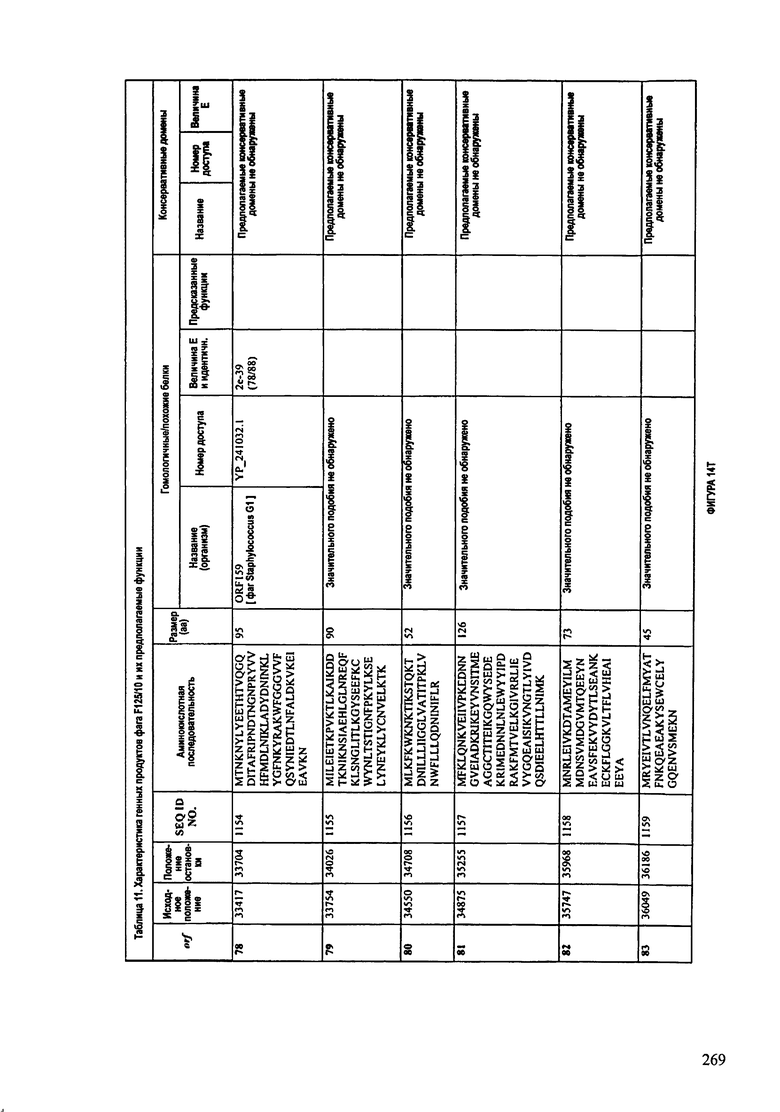
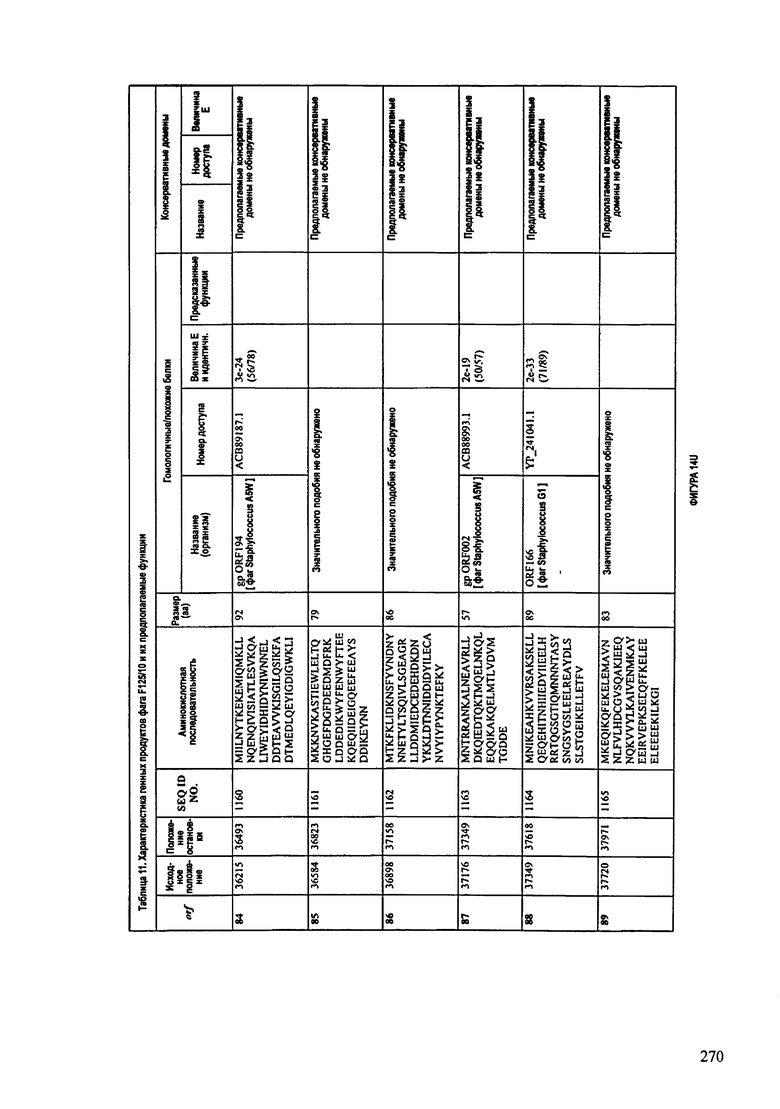
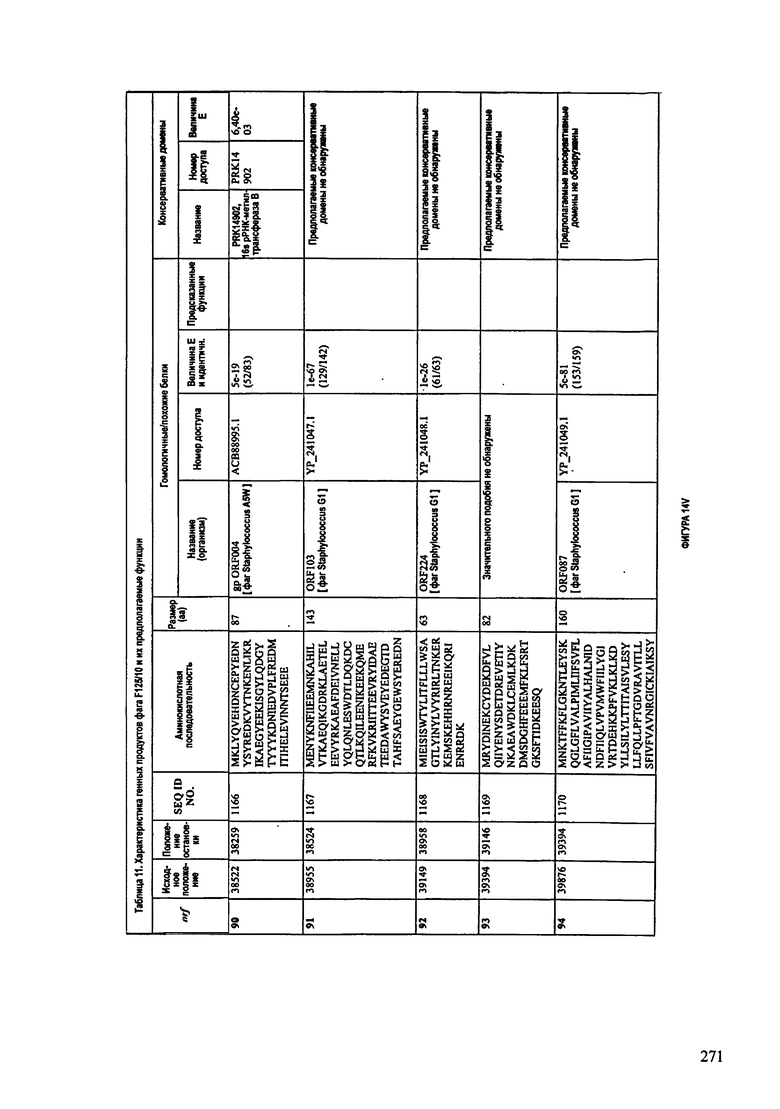
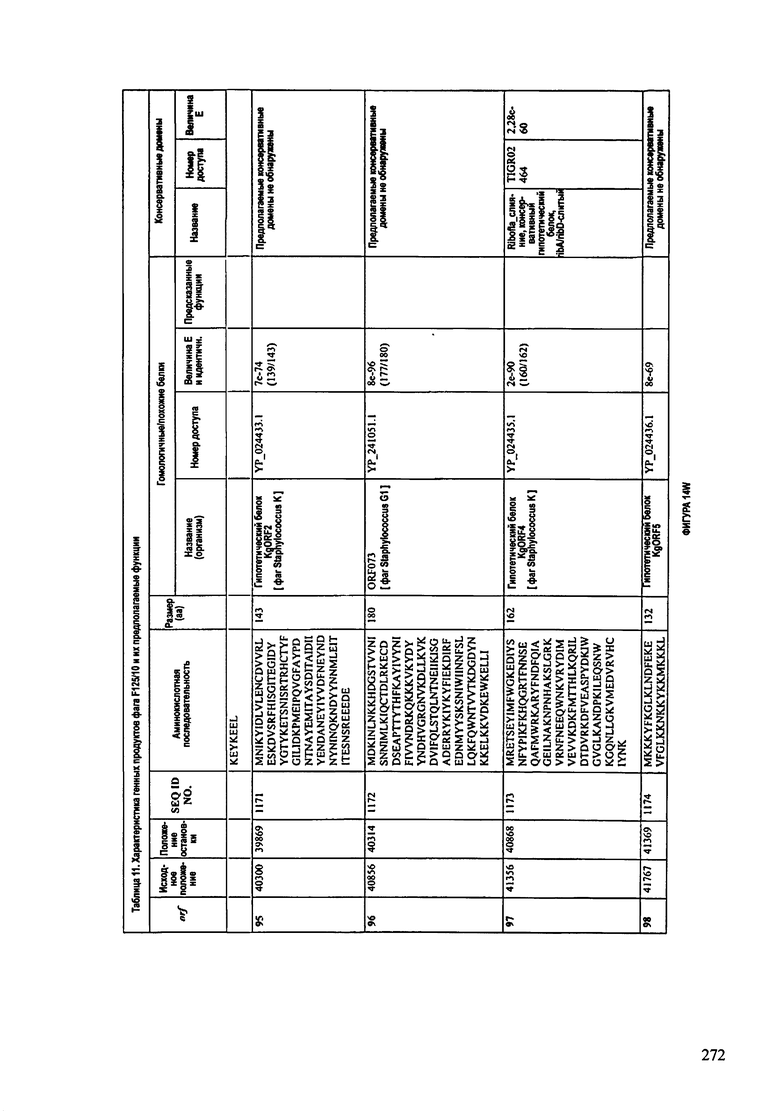
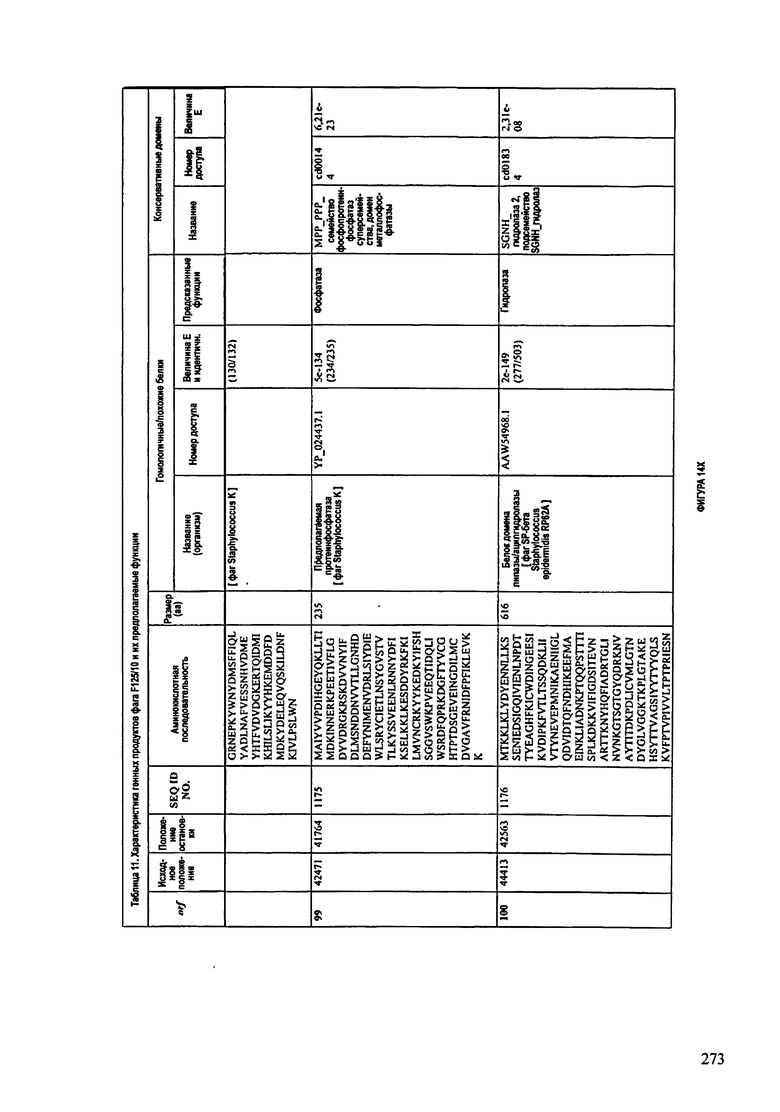

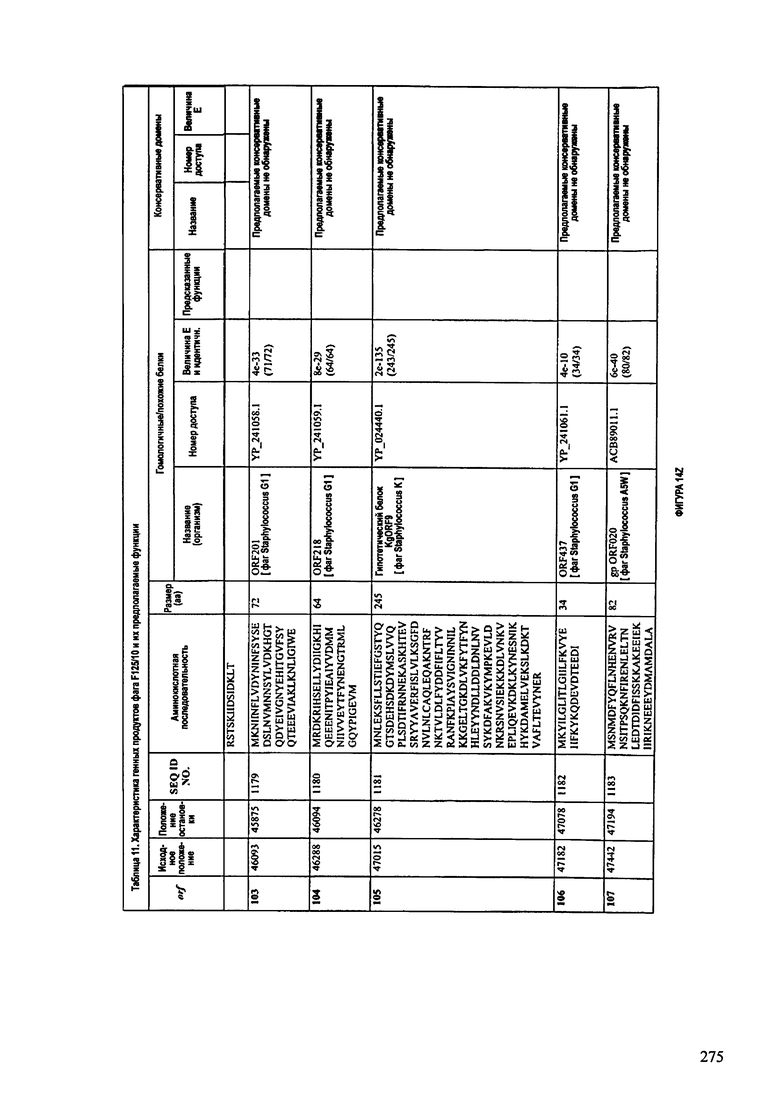
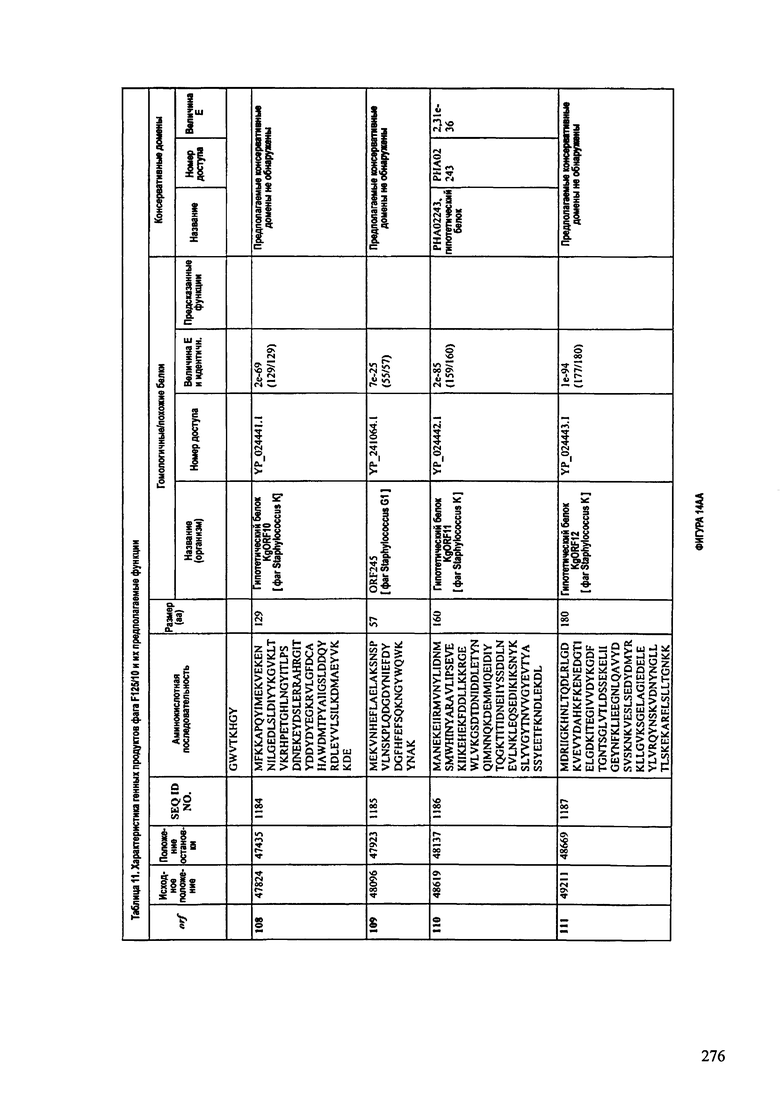
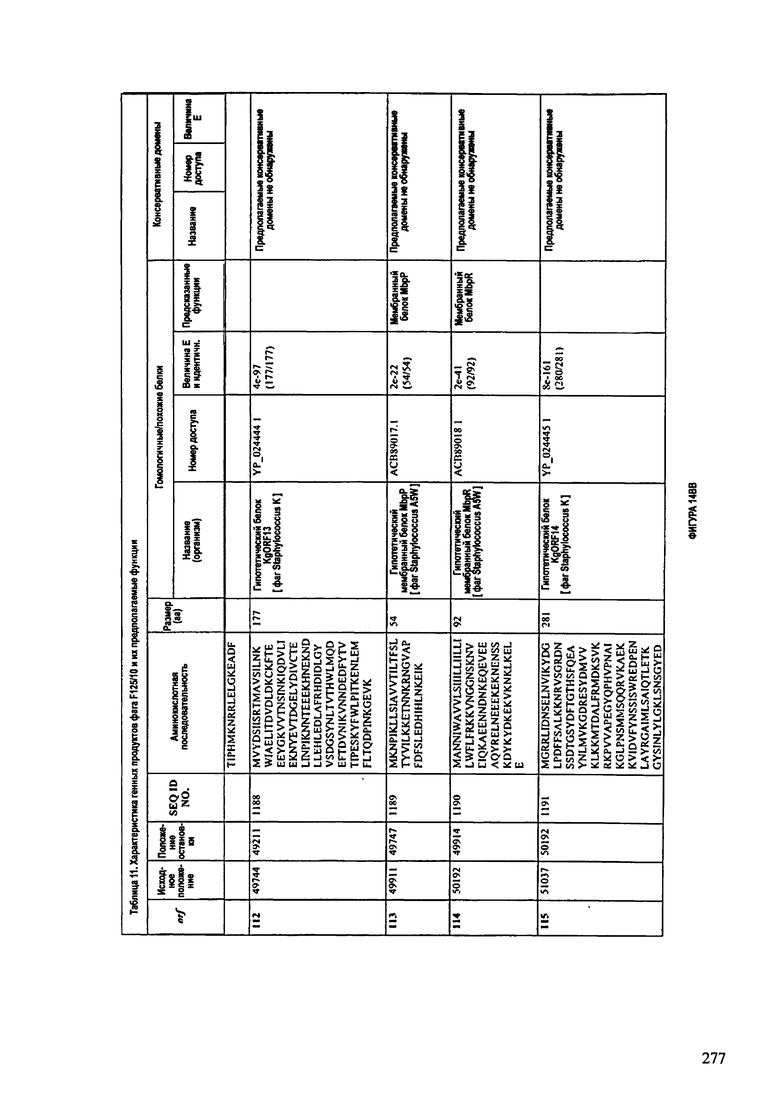

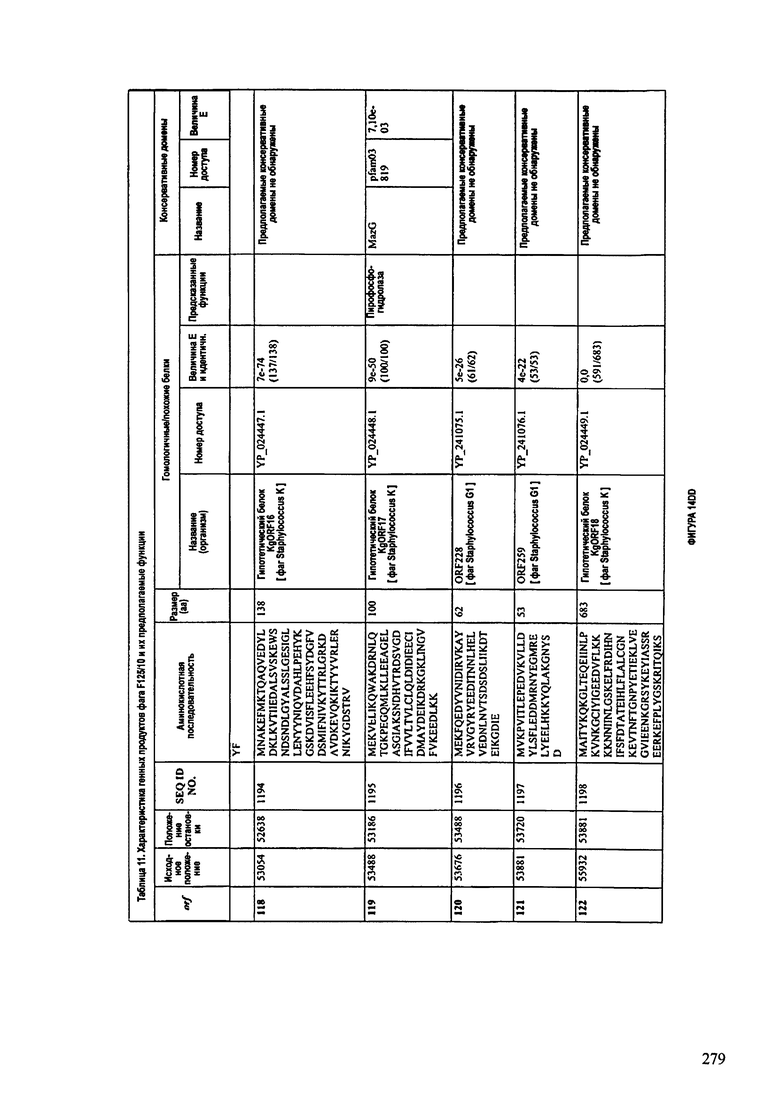

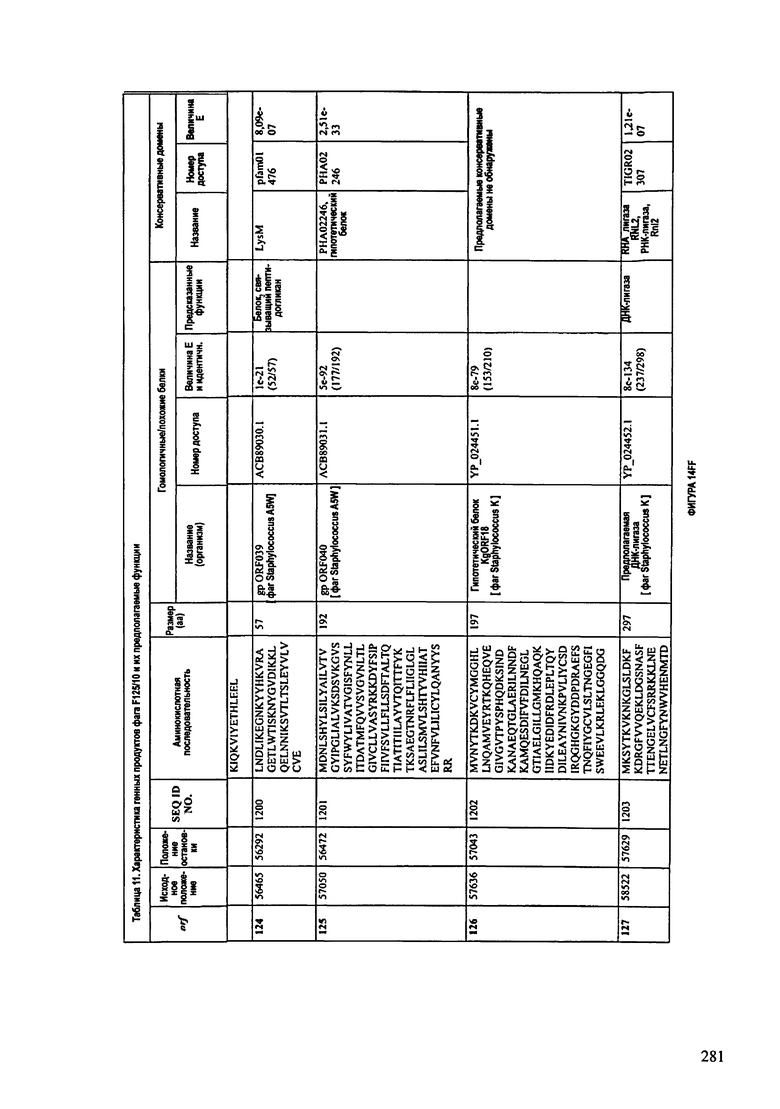
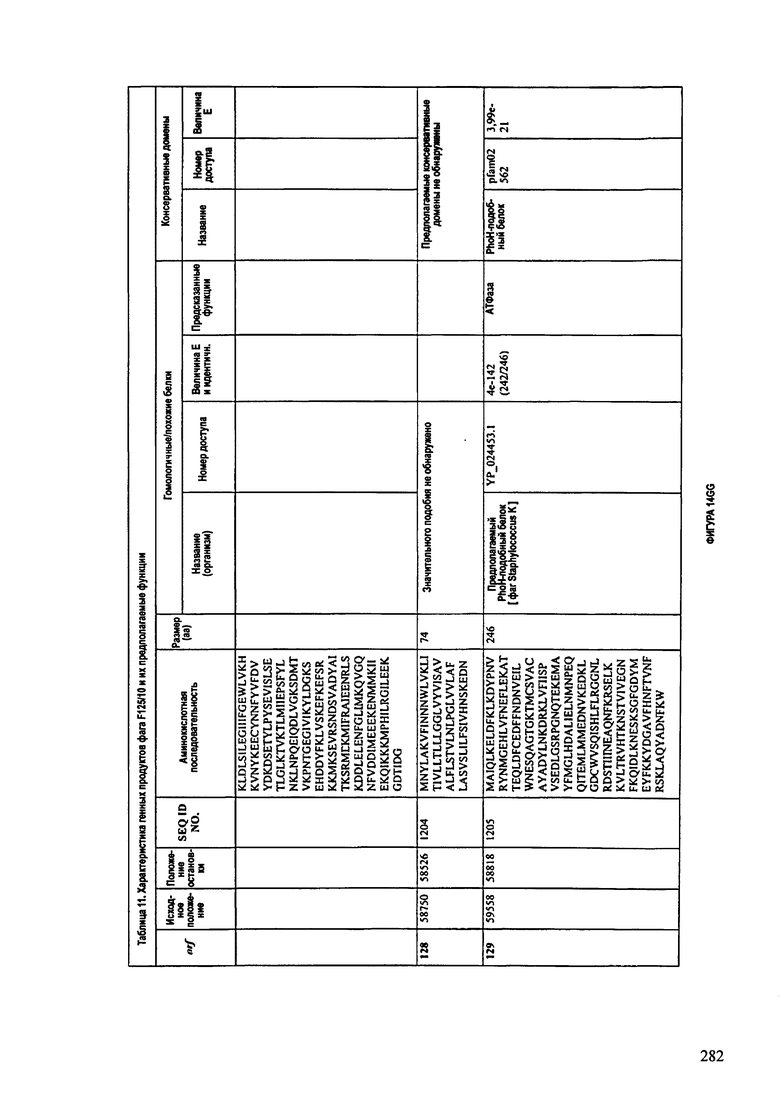
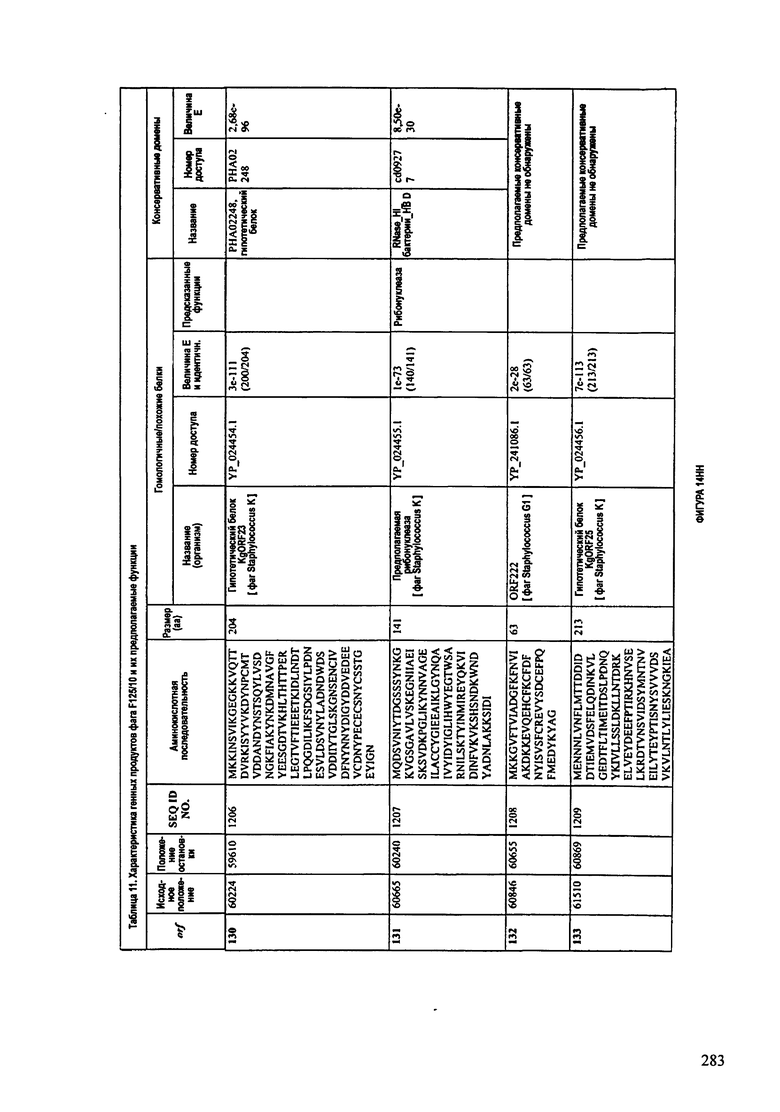



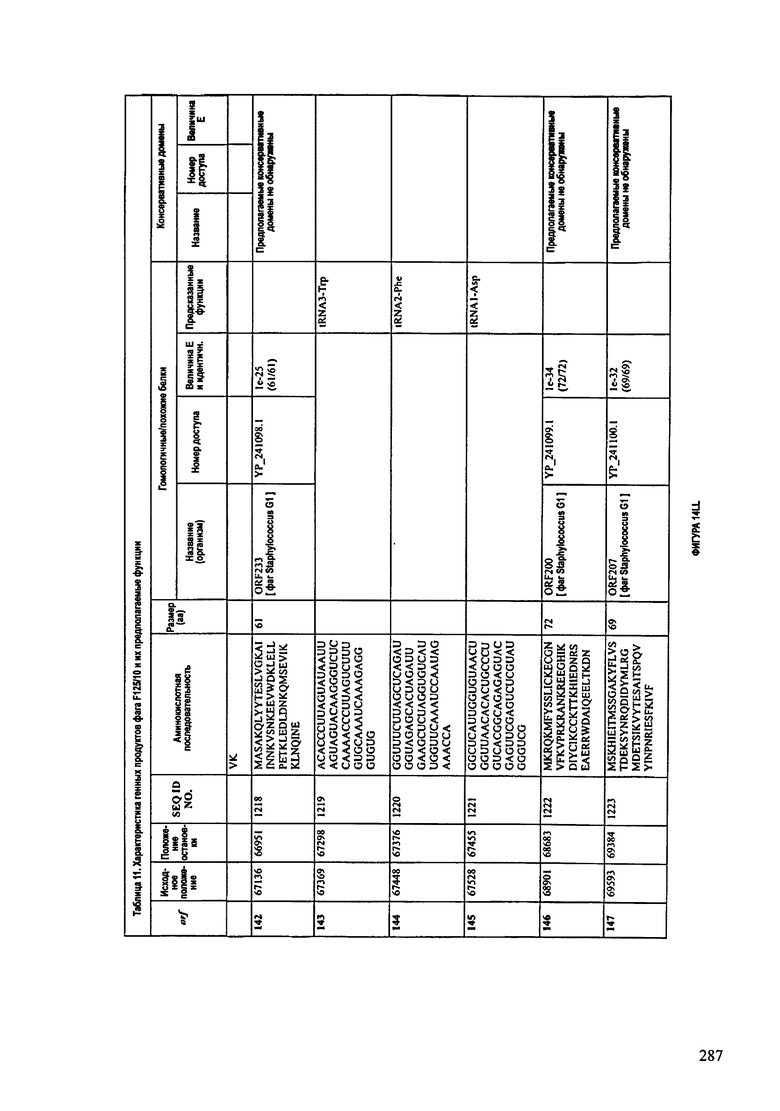
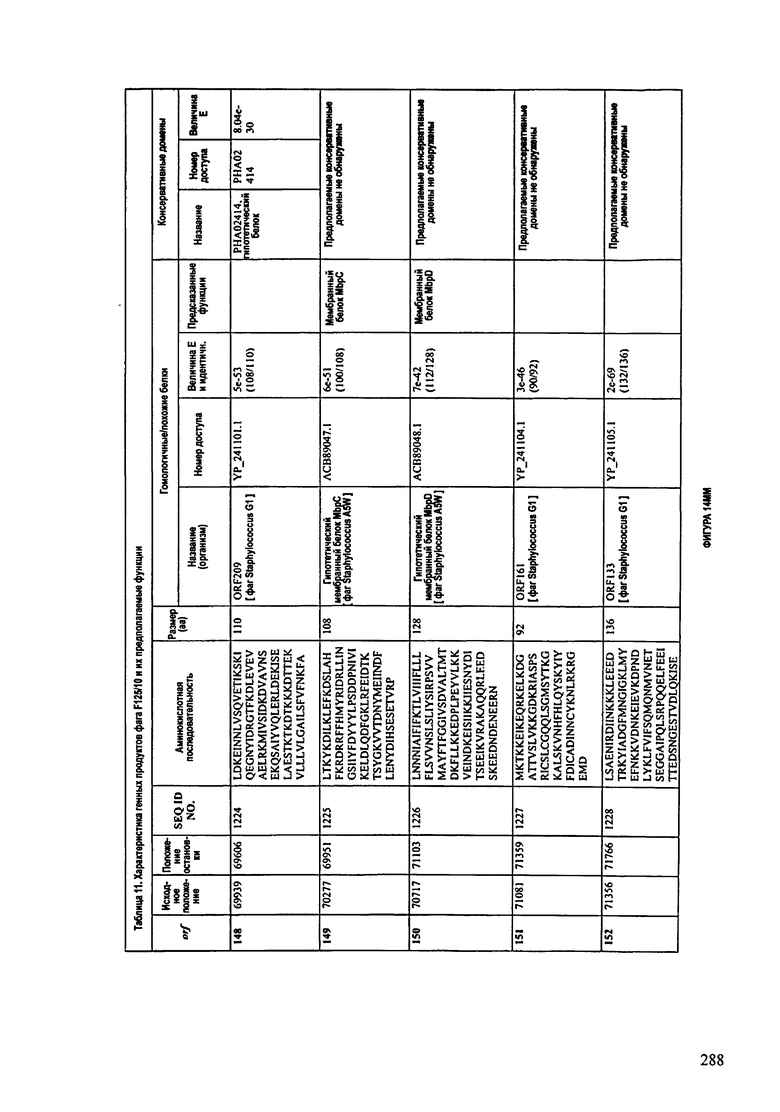
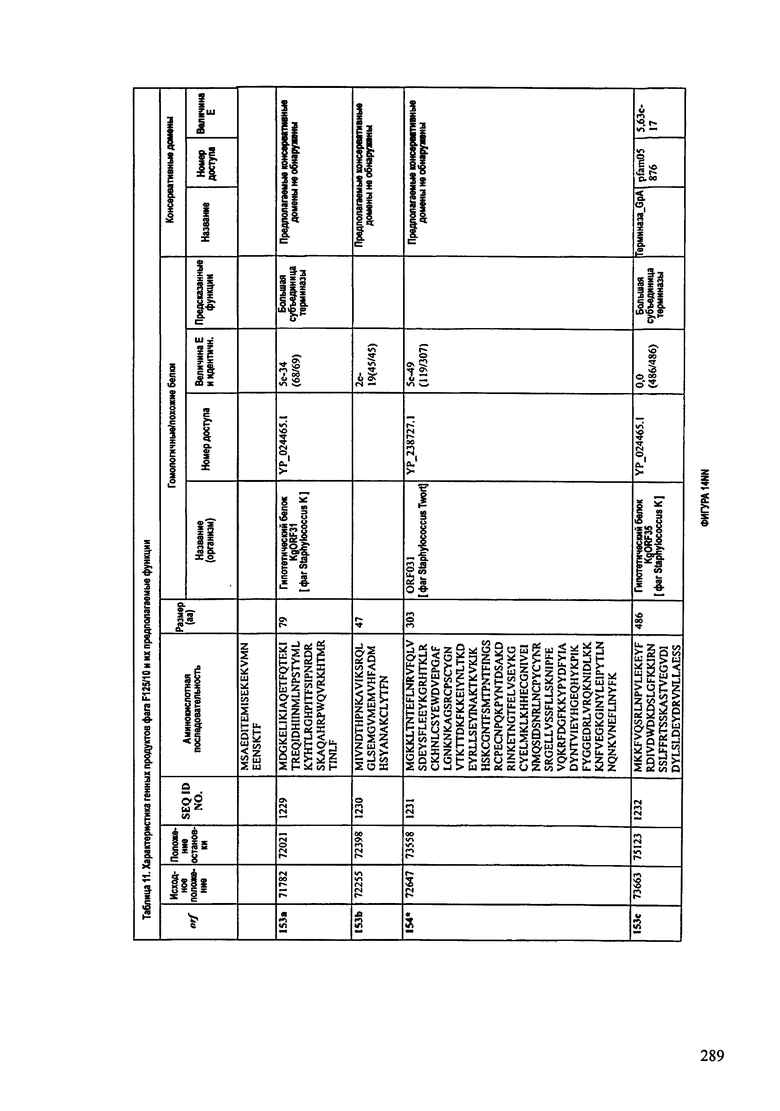

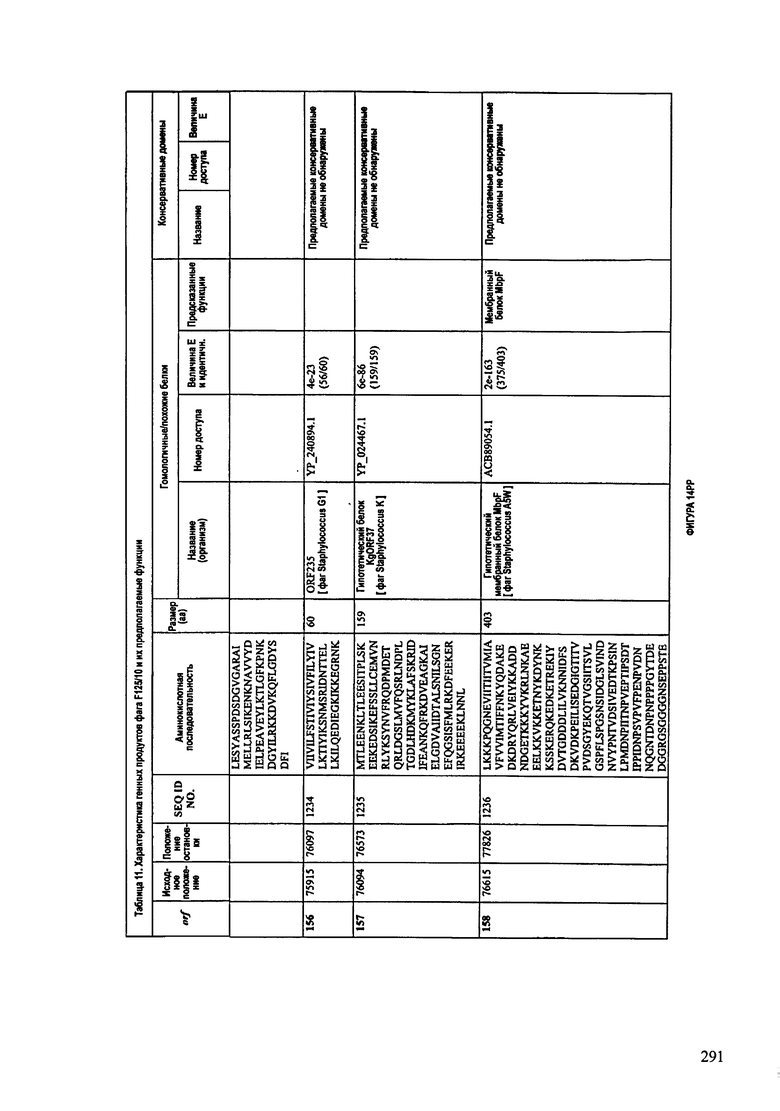
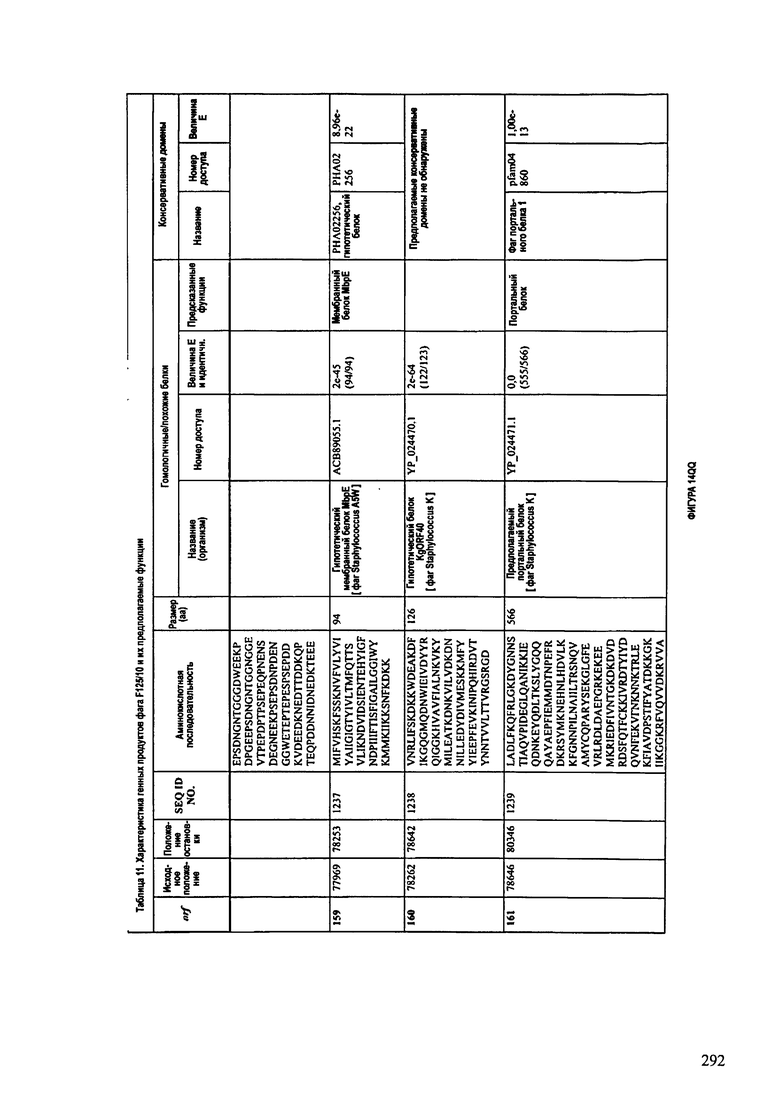



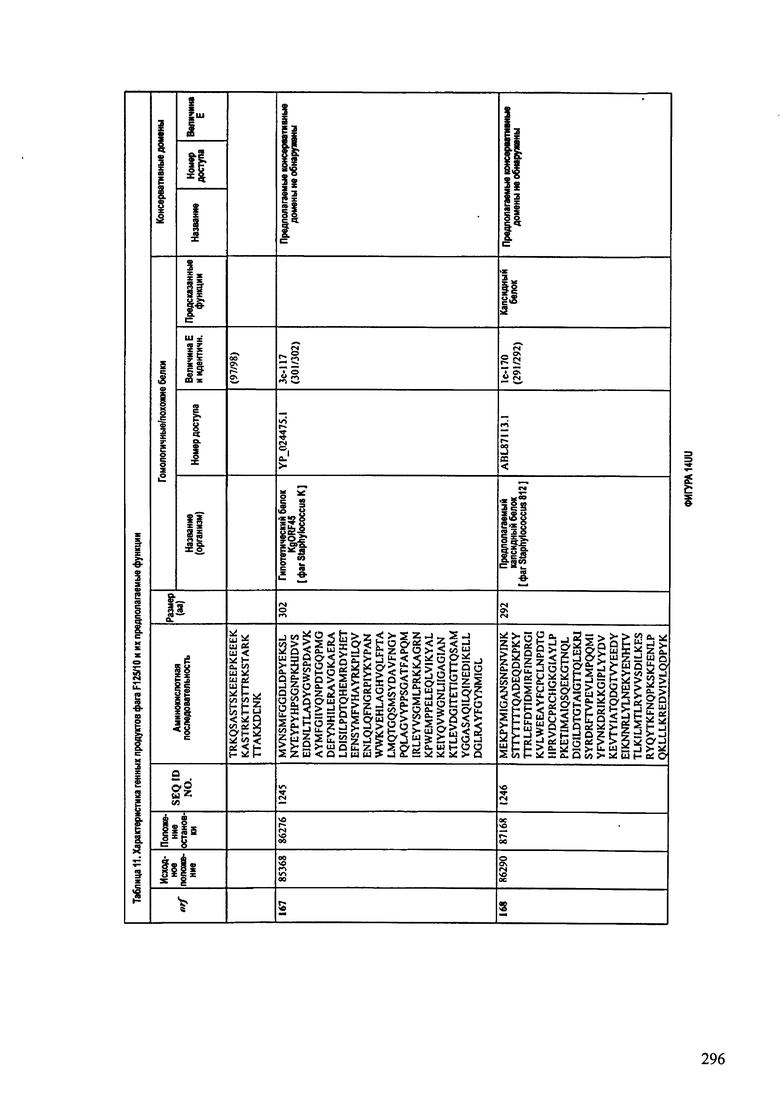


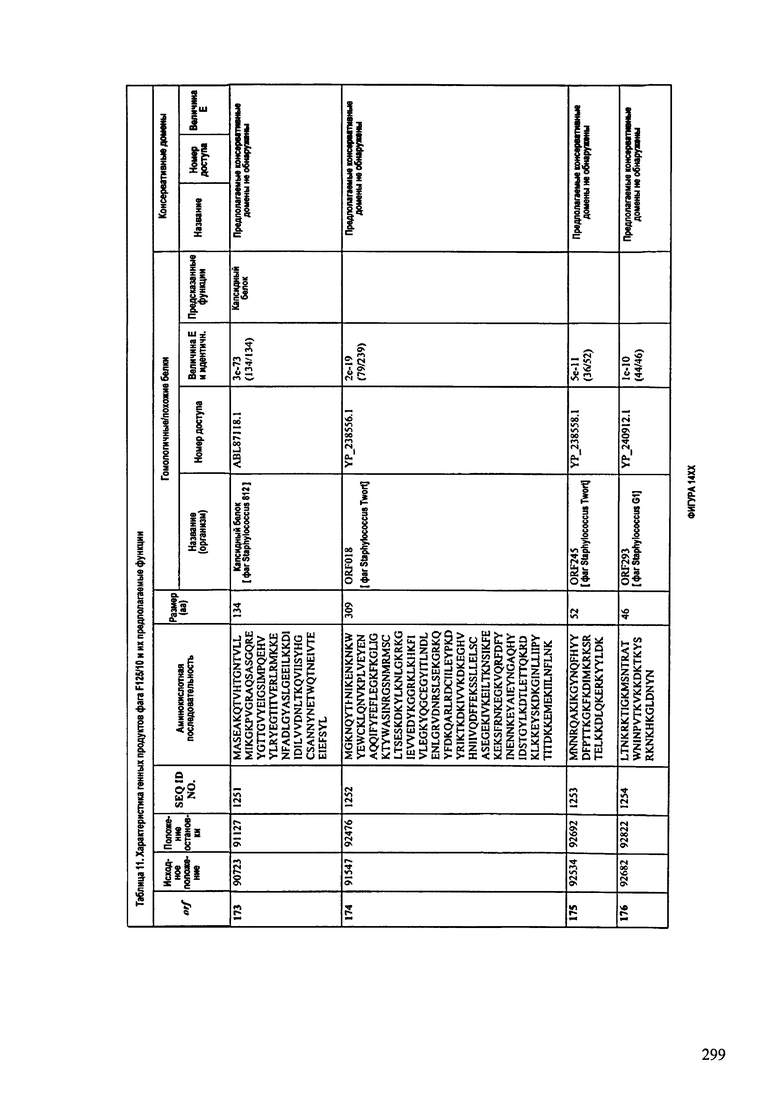
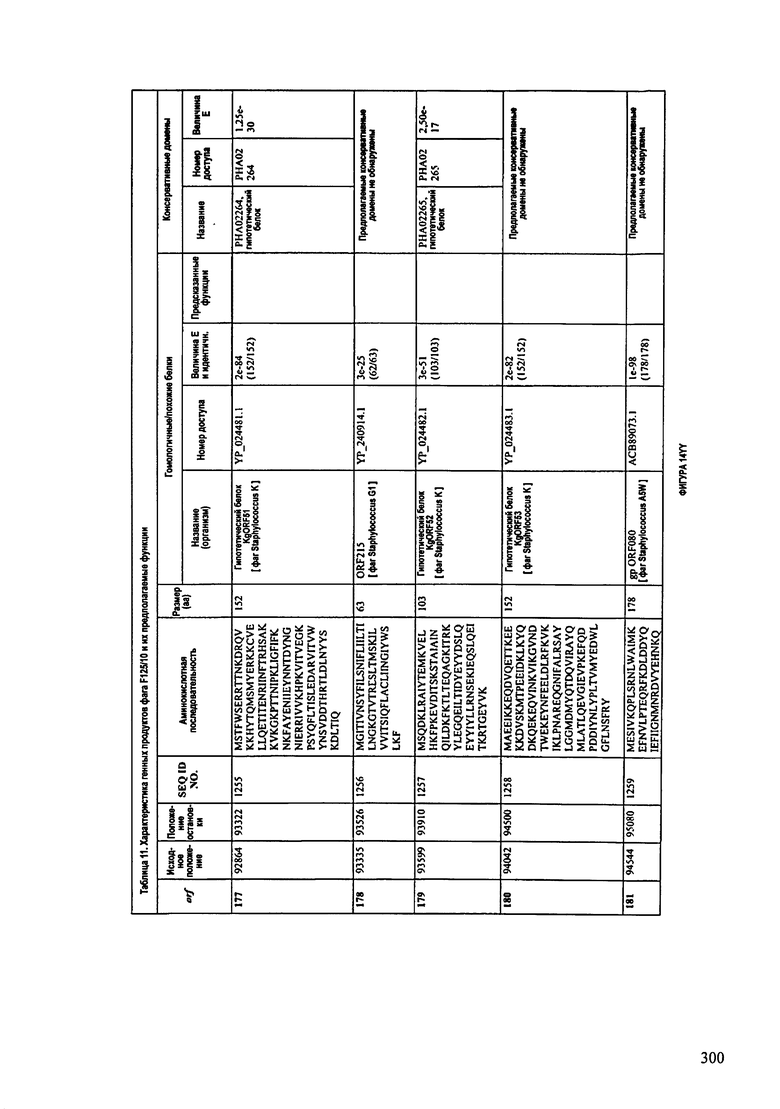



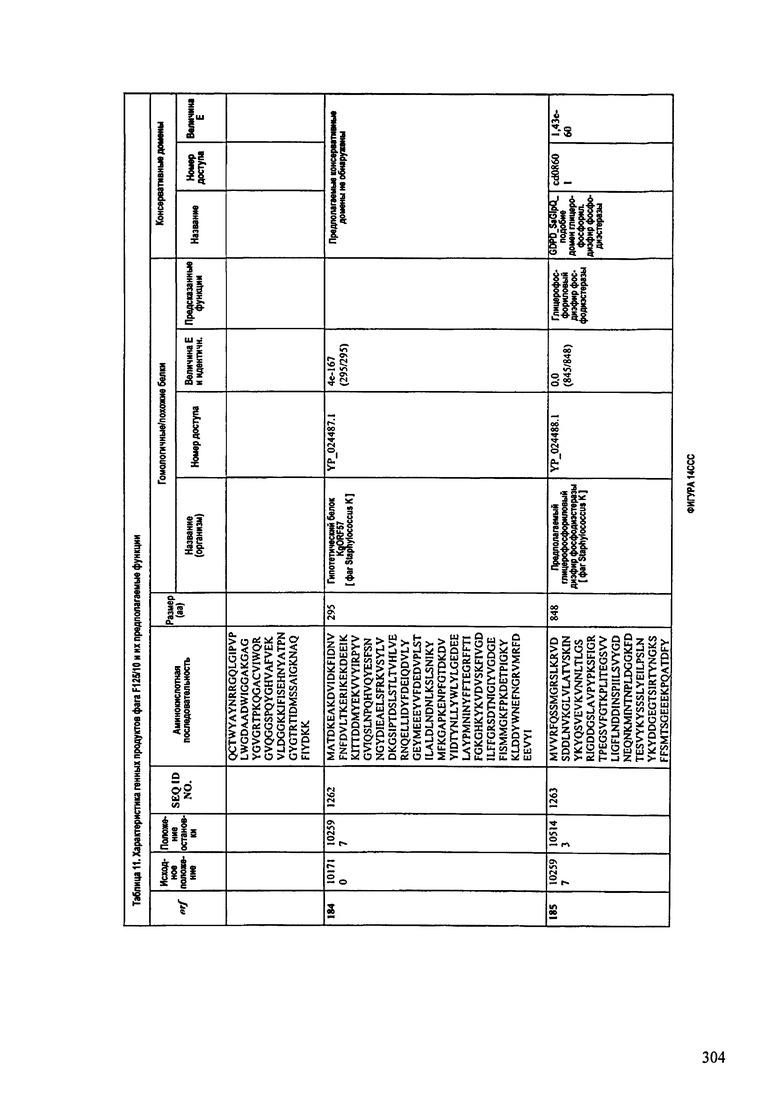

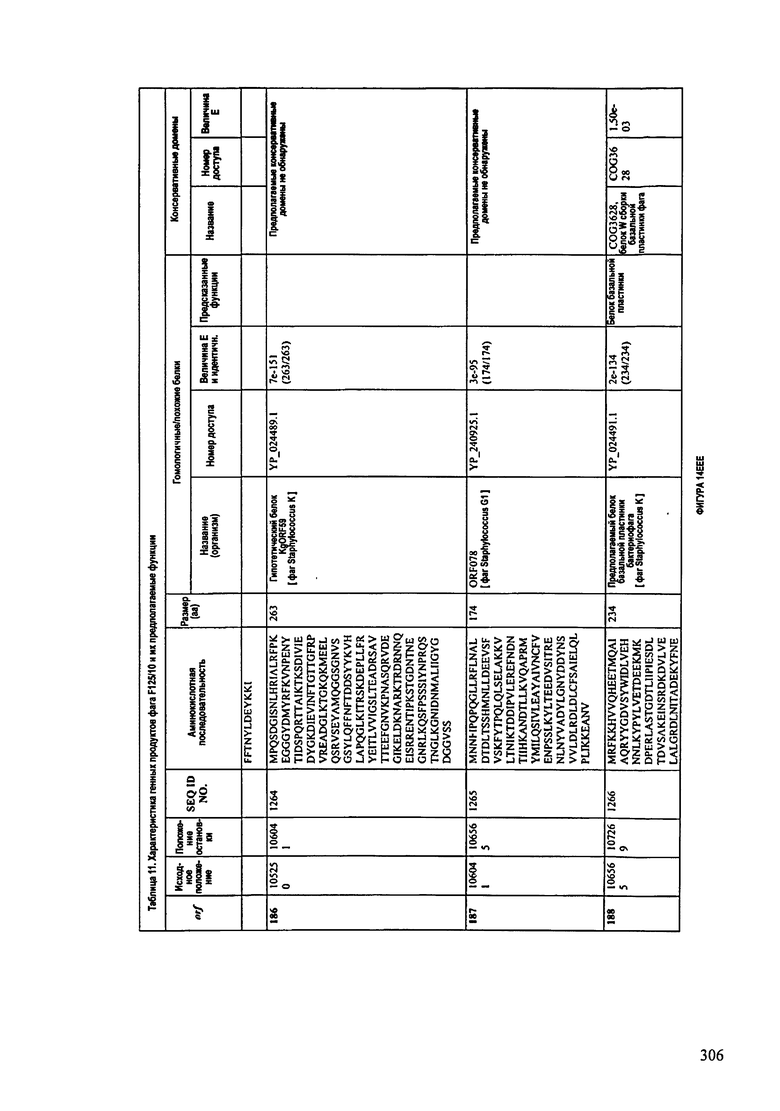





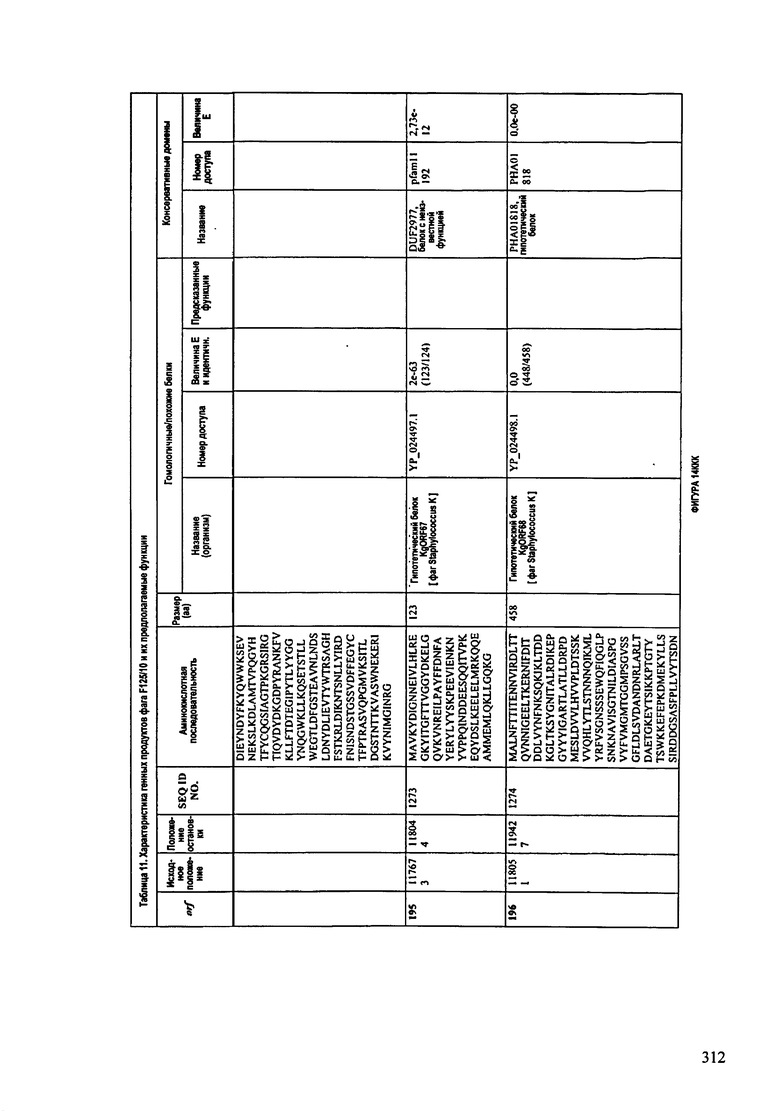



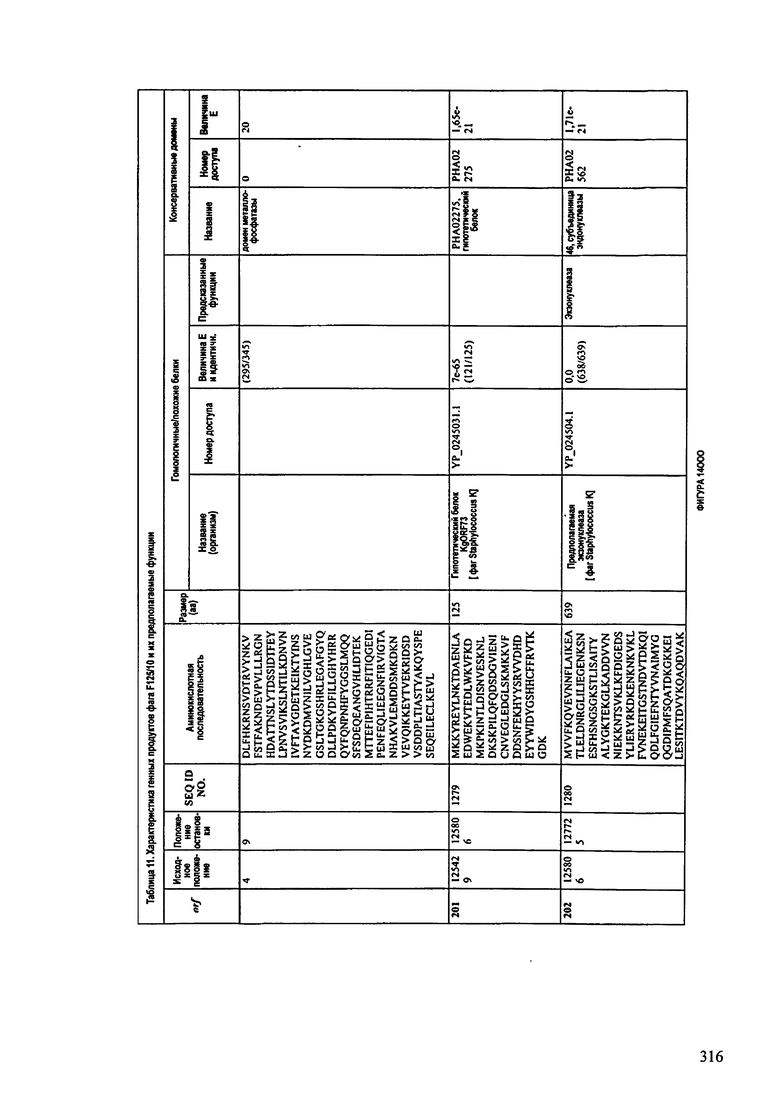

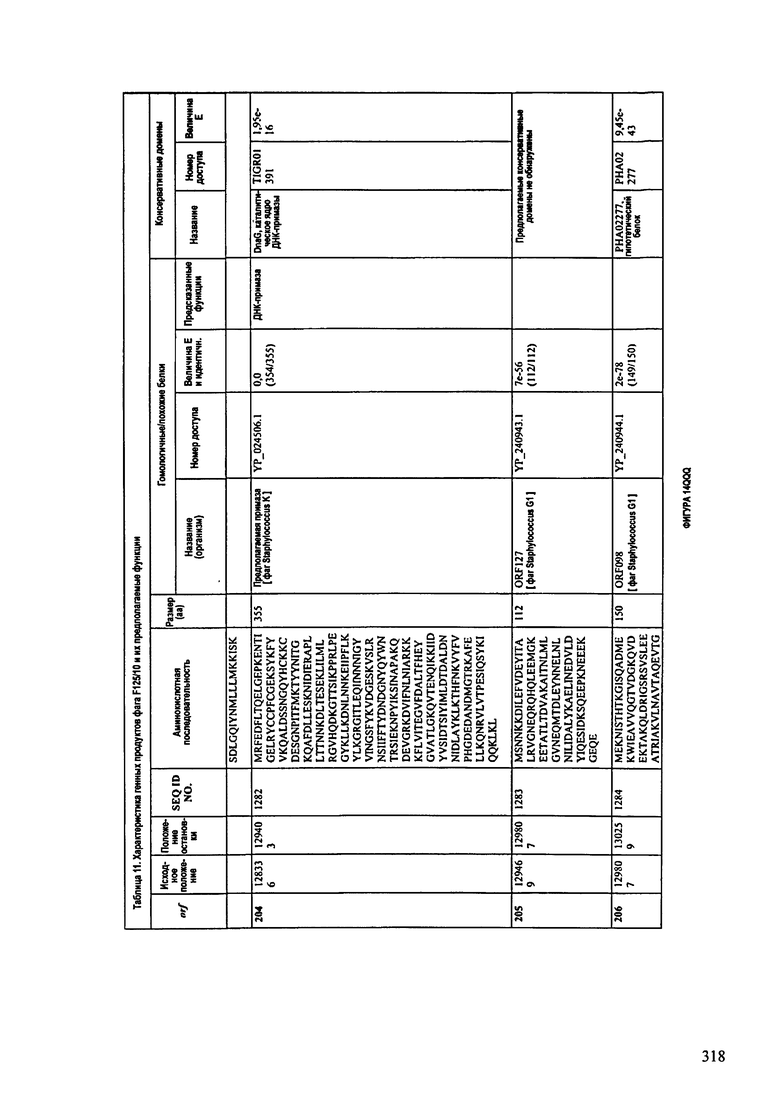
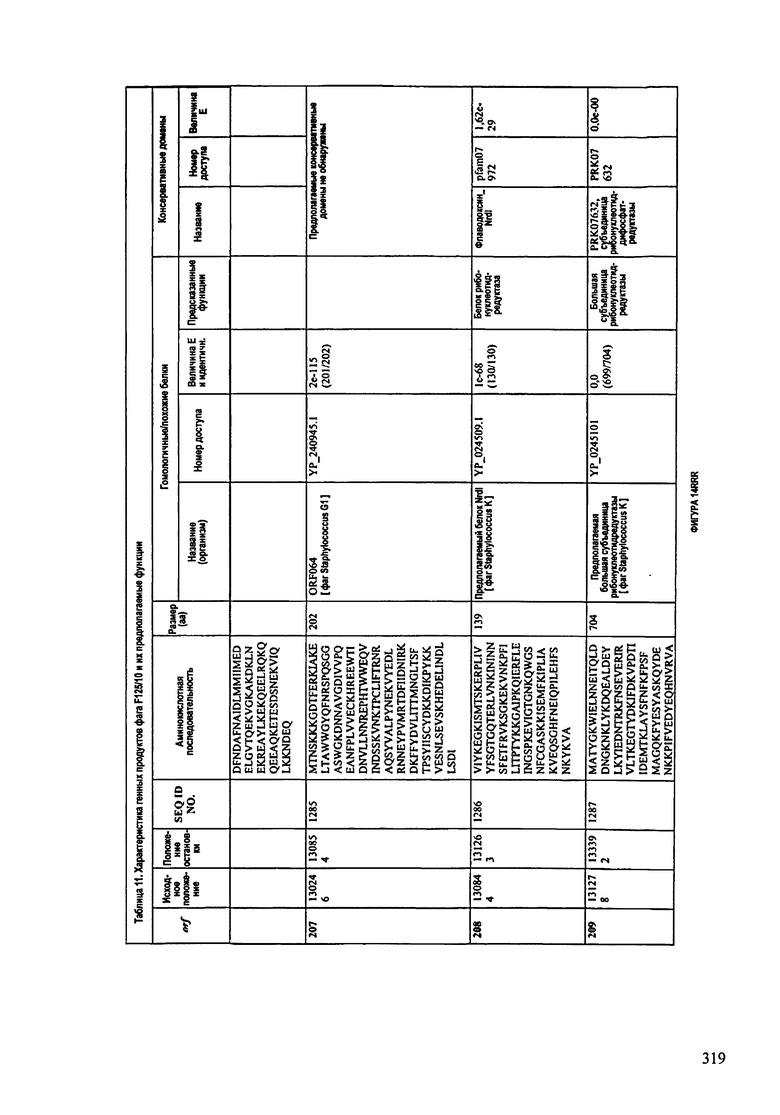

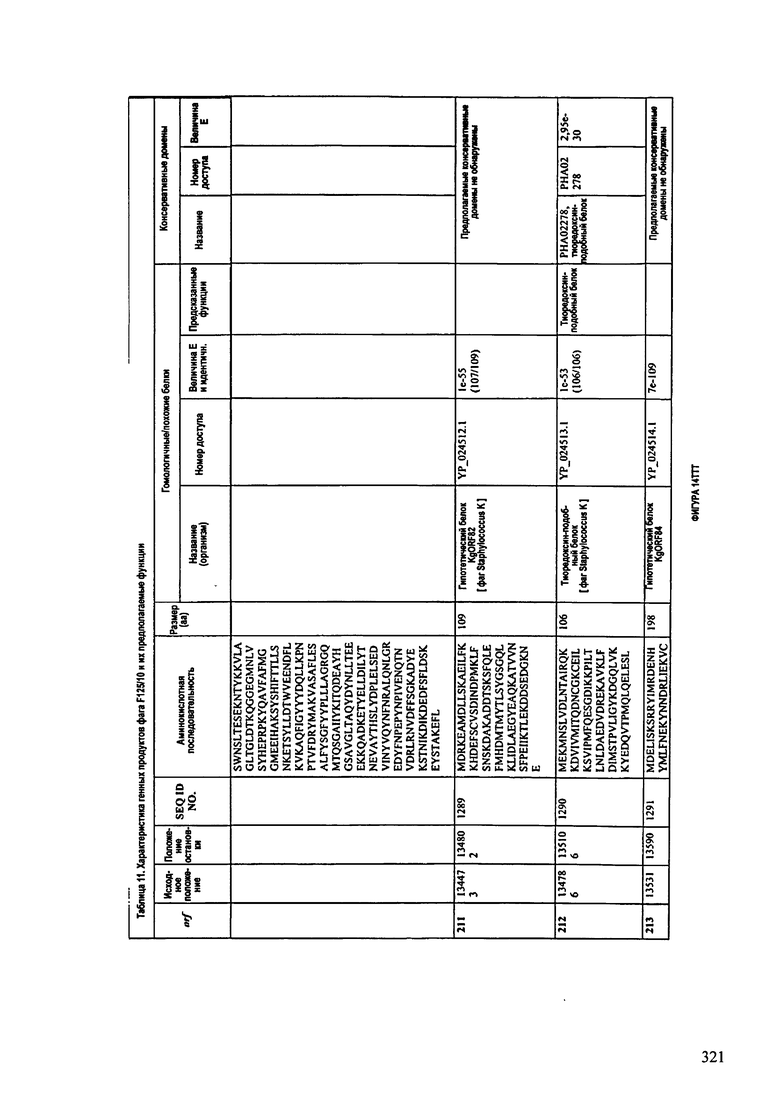
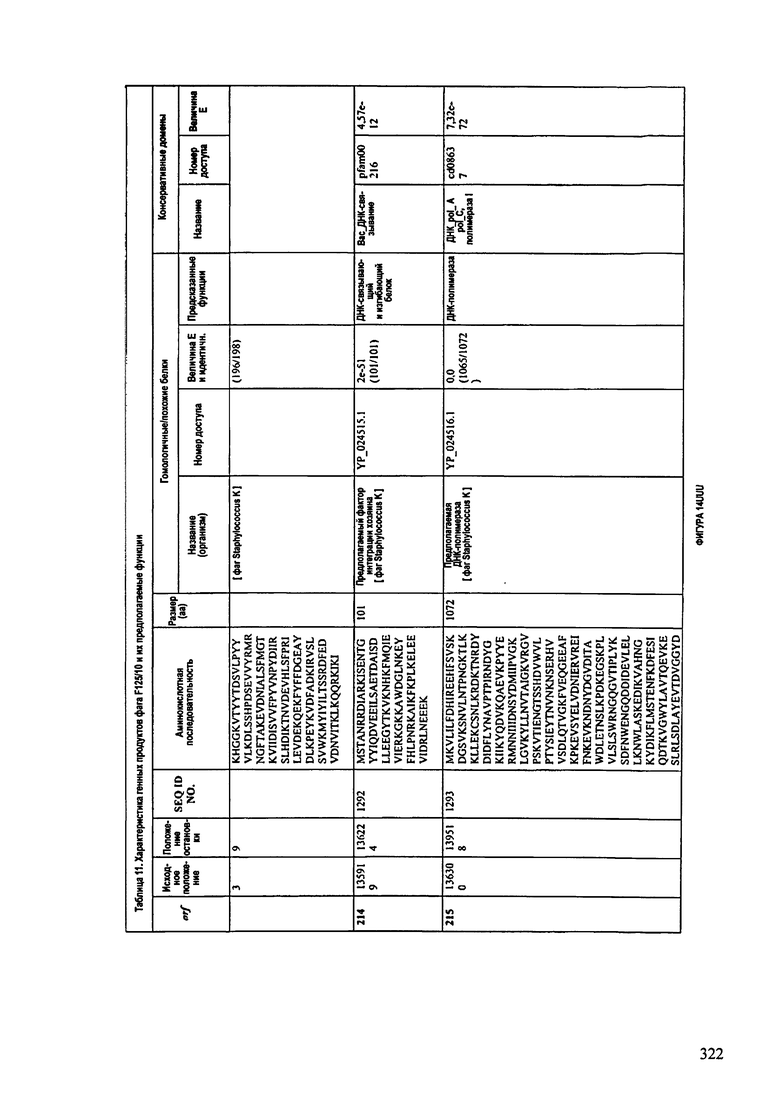

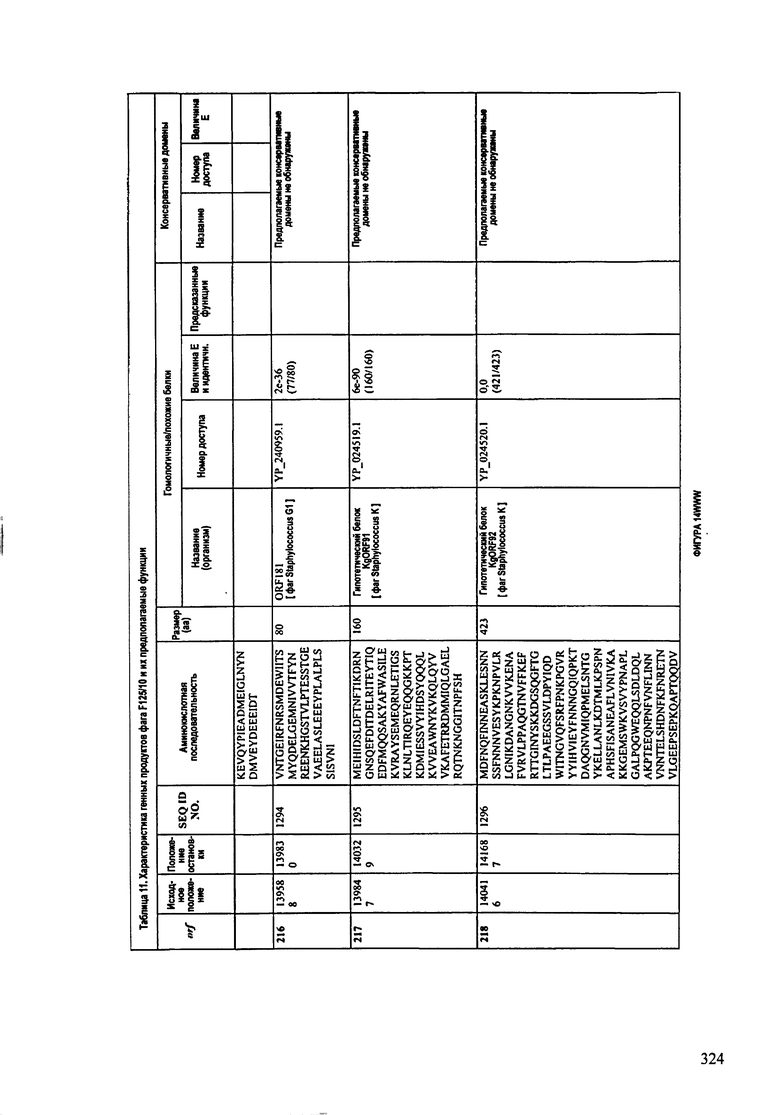



































































































































































































































































































































































































































































































































































































































































































Изобретение относится к области биотехнологии и вирусологии. Описан бактериофаг F510/08, имеющий геном, который содержит последовательность нуклеиновой кислоты SEQ ID NO:4. Бактериофаг проявляет активность в отношении Pseudomonas aeruginosa. Также описаны варианты фармацевтической композиции, содержащей такой бактериофаг, и способы терапии для лечения и профилактики бактериальной инфекции. Предложенная группа изобретений может быть использована в медицине. 12 н. и 11 з.п. ф-лы, 327 ил., 7 табл., 7 пр.
1. Выделенный бактериофаг, имеющий геном, который содержит последовательность нуклеиновой кислоты SEQ ID NO: 4, причем указанный бактериофаг проявляет активность в отношении Pseudomonas aeruginosa.
2. Фармацевтическая композиция, проявляющая активность в отношении Pseudomonas aeruginosa, содержащая эффективное количество бактериофага по п. 1 и фармацевтически приемлемый носитель.
3. Фармацевтическая композиция по п. 2, дополнительно содержащая один или более дополнительных штаммов бактериофага, эффективных в отношении Pseudomonas aeruginosa.
4. Фармацевтическая композиция по п. 2, дополнительно содержащая один или более дополнительных штаммов бактериофага, эффективных в отношении бактерий, отличных от Pseudomonas aeruginosa.
5. Белок лизин, имеющий аминокислотную последовательность, выбранную из SEQ ID NO: 547, SEQ ID NO: 556 и SEQ ID NO: 557, обладающий активностью в отношении Pseudomonas aeruginosa и кодируемый последовательностью нуклеиновой кислоты генома бактериофага по п. 1.
6. Хвостовой белок, имеющий аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 544, SEQ ID NO: 545, SEQ ID NO: 549 и SEQ ID NO: 551, обладающий активностью в отношении Pseudomonas aeruginosa и кодируемый последовательностью нуклеиновой кислоты генома бактериофага по п. 1.
7. Белок, обладающий активностью в отношении Pseudomonas aeruginosa, причем белок имеет аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 547, SEQ ID NO: 556 или SEQ ID NO: 557, соответствующий белку лизину, кодируемому последовательностью нуклеиновой кислоты генома бактериофага по п. 1.
8. Белок, обладающий активностью в отношении Pseudomonas aeruginosa, причем белок имеет аминокислотную последовательность, которая по меньшей мере на 90% идентична аминокислотной последовательности SEQ ID NO: 544, SEQ ID NO: 545, SEQ ID NO: 549 или SEQ ID NO: 551, соответствующий хвостовому белку, кодируемому последовательностью нуклеиновой кислоты генома бактериофага по п. 1.
9. Фармацевтическая композиция, проявляющая активность в отношении Pseudomonas aeruginosa, содержащая эффективное количество выделенного белка по любому из пп. 5-8 и фармацевтически приемлемый носитель.
10. Фармацевтическая композиция по п. 9, которая содержит по меньшей мере один выделенный белок, выбранный из группы, состоящей из SEQ ID NO: 544, SEQ ID NO: 545, SEQ ID NO; 547, SEQ ID NO: 549, SEQ ID NO: 551, SEQ ID NO: 556 и SEQ ID NO: 557, обладающая активностью в отношении Pseudomonas aeruginosa.
11. Фармацевтическая композиция по п. 9 или 10, дополнительно содержащая один или более бактериофагов или дополнительных белков, кодируемых геномом бактериофага, причем один или более бактериофагов или дополнительных белков являются эффективными против Pseudomonas aeruginosa и/или являются эффективными против бактерий, отличных от Pseudomonas aeruginosa.
12. Фармацевтическая композиция по любому из пп. 2-4, дополнительно содержащая по меньшей мере три дополнительных фага, выбранных из группы, состоящей из F391/08, F394/08, F488/08, F44/10, F387/08, F125/10, F170/08, F168/08, F770/05 и F1245/05; предпочтительно по меньшей мере три дополнительных фага, выбранных из группы, состоящей из F44/10, F391/08, F387/08, F488/08 и F770/05; предпочтительно F394/08, F44/10 и/или F1245/05; и/или
которая составлена для топического нанесения;
причем
F391/08 имеет геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO: 1;
F394/08 имеет геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO: 2;
F488/08 имеет геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO: 3;
F44/10 имеет геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO: 560;
F387/08 имеет геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO: 781; и
F125/10 имеет геном, содержащий последовательность нуклеиновой кислоты SEQ ID NO: 1074.
13. Выделенная нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую белок по любому из пп. 5-8, причем белок имеет активность в отношении Pseudomonas aeruginosa.
14. Применение терапевтически эффективного количества фармацевтической композиции по пп. 2-4 или 9-12 для изготовления лекарственного средства для лечения или уменьшения возможности возникновения инфекции, связанной с Pseudomonas aeruginosa; и/или
инфекция является нозокомиальной инфекцией; и/или
где указанным субъектом является млекопитающее, предпочтительно человек; и/или
композиция вводится топическим путем.
15. Применение по п. 14, причем инфекция является инфекцией кожи; и/или
инфекция является инфекцией, вызванной ожоговой травмой, или поврежденными тканями кожи, или диабетической язвой стопы; и/или
композиция вводится топическим путем.
16. Применение по п. 14, причем инфекция представляет собой инфекцию легких.
17. Применение по п. 16, причем фармацевтическая композиция вводится путем ингаляции; и/или
причем введение путем ингаляции осуществляется с помощью насоса, распылителя или небулайзера; и/или
причем фармацевтическая композиция для введения путем ингаляции включает сухой порошок или аэрозоль.
18. Применение по п. 14, причем инфекция представляет собой инфекцию мочевого тракта или почек.
19. Применение по п. 18, причем фармацевтическая композиция вводится с помощью катетера.
20. Применение по п. 14, причем лекарственное средство дополнительно содержит по меньшей мере один из:
(i) антибиотик для лечения бактериальной инфекции, вызванной Pseudomonas aeruginosa;
(ii) один или более дополнительных бактериофагов, имеющих активность в отношении Pseudomonas aeruginosa; и
(iii) один или более дополнительных бактериофагов, имеющих активность в отношении бактерии, отличной от Pseudomonas aeruginosa.
21. Способ диагностики бактериальной инфекции, вызванной Pseudomonas aeruginosa, включающий:
(i) культивирование образца ткани, отобранного у пациента;
(ii) приведение в контакт культуры со стадии (i) с бактериофагом по п. 1 или белком по пп. 5-8, имеющим активность в отношении Pseudomonas aeruginosa; и
(iii) мониторинг наличия роста или лизиса культуры, причем наличие лизиса культуры показывает, что культура содержит Pseudomonas aeruginosa;
где предпочтительно образец ткани представляет собой образец крови, мочи, мокроты, поврежденной кожи, биопсии ткани или мазок, взятые у пациента.
22. Способ уменьшения или ингибирования колонизации или роста Pseudomonas aeruginosa на твердой поверхности, включающий приведение указанной поверхности в контакт с бактериофагом по п. 1 или белком по пп. 5-8, имеющих активность в отношении Pseudomonas aeruginosa,
где предпочтительно указанная поверхность представляет собой поверхность больничных инструментов или предмета больничного оборудования, предпочтительно хирургических инструментов или предмета хирургического оборудования.
23. Применение бактериофага по п. 1 или белка по одному из пп. 5-8, имеющих активность в отношении Pseudomonas aeruginosa, для изготовления лекарственного средства для уменьшения или ингибирования инфекции, связанной с колонизацией или ростом Pseudomonas aeruginosa на биологической поверхности, контактировавшей с Pseudomonas aeruginosa;
причем указанная поверхность предпочтительно представляет собой собой кожу, поврежденную кожу или слизистую оболочку млекопитающего или кожу, или поврежденную кожу, или слизистую оболочку человека.
| WO 2010041970 A2, 15.04.2010;US 2010172918 A1, 08.07.2010;WO 03080823 A2, 02.10.2003;WO 02076483 A2, 03.10.2002;RU 2112800 C1, 10.06.1998. |
Авторы
Даты
2017-03-22—Публикация
2011-09-19—Подача