Предлагаемое изобретение относится к области биохимии и микробиологии, может быть использовано в биотехнологиях производства лекарственных средств для применения в медицине и ветеринарии для лечения и/или профилактики инфекционных заболеваний, вызываемых Pseudomonas aeruginosa.
Штамм бактериофага Pseudomonas phage Ka1 выделен из воды притока озера Байкал, в районе сброса очищенных сточных вод г. Слюдянка (Россия).
Штамм бактериофага Pseudomonas phage Ka1 задепонирован в Биоресурсном центре Всероссийской коллекции промышленных микроорганизмов (Регистрационный номер ВКПМ: Ph-1631).
К роду Pseudomonas относят возбудителей, обитающих в окружающей среде и при определенных условиях, вызывающих инфекционный процесс у человека (оппортунистичекие инфекции). Наиболее патогенной бактерией считают Pseudomonas aeruginosa. Быстрее всего прогрессируют инфекционные поражения роговицы и наружный отит. Воротами инфекции могут быть ожоговые и раневые поверхности, при этом возможно развитие вторичной септицемии - частой причины смерти пациентов с нейтропенией. Некоторые штаммы вызывают деструкцию кожных покровов и гангренозную эктиму. В дальнейшем может развиться остеомиелит, септический артрит и менингит (особенно после хирургических операций). Хронический муковисцидоз приводит к прогрессирующему ухудшению функции легких [https://meduniver.com/Medical/Microbiology/infekciipseudomonas_aeroginosa.html].
Штамм бактериофага Pseudomonas phage Ka1 является вирулентным, то есть обладает природной способностью лизировать (разрушать) клетки P. aeruginosa и не способен к лизогенному пути развития.
В результате аннотации генома штамма бактериофага Pseudomonas phage Ka1 выявлена 71 кодирующая последовательность. Из них 27 кодируют гипотетические полипептиды с неизвестной функцией. Выявлено 6 генов метаболизма аминокислот, 4 гена кодируют белки с нуклеазной активностью, И генов участвуют в обмене нуклеиновых кислот, 20 генов кодируют структурные белки капсида и хвоста, 3 гена отвечают за синтез тРНК. При этом в геноме отсутствуют гены интегразы, транспозазы и рекомбиназы - потенциальных белков, связанных с переходом к лизогенному жизненному циклу, что делает его перспективным для бактериальной терапии, в том числе в сочетании терапии с имеющимися противобактериальными препаратами.
Использованные в описании сокращения, термины и пояснения
Бактериофаги - вирусы, поражающие и уничтожающие только бактерии. Фармацевты научились использовать во благо свойства этих крошечных помощников борьбы с болезнями путем создания на их основе лечебно-профилактических антибактериальных препаратов [https://naked-science.ru/article/column/bakterij-net-kak-fagi-vliyayut-na-organizm? Бактерий.нет: как фаги влияют на организм (naked-science.ru)];
МПА - мясо-пептонный агар;
LA - твердая агаризованная среда Лурии-Бертани;
Лизис - в клинической медицине (греч, lysis) - растворение, разложение, ослабление, развязка клеток и их систем, в том числе микроорганизмов, под влиянием различных агентов, например ферментов, бактериолизинов, бактериофагов, противобактериальных препаратов;
мкл - микролитр;
мкм - микрометр;
NaCl - хлорид натрия;
Клинические изоляты - потенциально болезнетворные микроорганизмы, в основном стафилококки и энтеробактерии, которые выделены не из природной среды, а из организма животных или людей, в том числе пациентов стационаров.
КОЕ - колониеобразующая единица - единица измерения, оценивающая количество микробных клеток.
БОЕ - бляшкообразующая единица - наименьшее количество вируса или бактериофага, способное вызвать образование одной негативной колонии (бляшки) соответственно на однослойной культуре клеток позвоночных или на агаровой культуре бактерий.
МПК - минимальная концентрация, подавляющая видимый рост исследуемого микроорганизма в бульонной культуре или на плотной среде.
Заявителем выполнен анализ уровня техники. Из исследованного уровня техники заявителем выявлены аналоги предлагаемого изобретения. При описании аналогов использована терминология их (аналогов) описаний.
Характеристики аналогов
Известно предлагаемое изобретение «Антибактериальное средство» по заявке на патент России RU 2010140760/10 (приоритет от 06.10.2010).
Сущность известного предлагаемого изобретения заключается в том, что: 1. Антибактериальное средство, содержащее концентрат бактериофагов, гелеобразователь в виде неионогенного или анионогенного высокомолекулярного соединения, неионогенное поверхностно-активное вещество (ПАВ), любой консервант, кроме относящихся к производным четвертичных аммониевых оснований, к производным тяжелых металлов, к окислителям, к бром- или йодсодержащим, к формальдегидвыделяющим консервантам, регулятор рН и воду при следующем соотношении компонентов, мас. %:
2. Антибактериальное средство по п. 1, отличающееся тем, что оно содержит карбомер в качестве гелеобразователя, сополимер силикона и гликоля (предпочтительнее ПЭГ 12 диметикон) в качестве ПАВ, триэтаноламин в качестве регулятора рН и комплекс бензилового спирта, метилхлоризотиазолинона, метилизотиазолинона в качестве консерванта при следующем соотношении компонентов, мас. %:
3. Антибактериальное средство по п. 1, отличающееся тем, что оно содержит гипромеллозу в качестве гелеобразователя, ПАВ, выбранное из группы этоксилированных растительных масел, и/или этоксилированных жирных кислот, и/или этоксилированных спиртов, фосфатный буфер в качестве регулятора рН и комплекс бензоата натрия и сорбата калия в качестве консерванта при следующем соотношении компонентов, мас. %:
4. Антибактериальное средство по п. 1, отличающееся тем, что оно содержит глюкоманнан в качестве гелеобразователя, ПЭГ 40 гидрогенизированное касторовое масло в качестве ПАВ, натрия гидроксид в качестве регулятора рН, комплекс бензоат натрия и феноксиэтанола в качестве консерванта при следующем соотношении компонентов, мас. %:
5. Антибактериальное средство по п. 1, отличающееся тем, что оно содержит повидон в качестве гелеобразователя, ПАВ из группы полиоксиэтиленсорбитанов жирных кислот (предпочтительно твин 80), натрия гидроксид в качестве регулятора рН и сорбат калия в качестве консерванта при следующем соотношении компонентов, мас. %:
вода до 100
6. Антибактериальное средство по п. 1, отличающееся тем, что оно содержит повидон в качестве гелеобразователя, ПАВ, выбранные из группы этоксилированных растительных масел, и/или этоксилированных жирных кислот, и/или этоксилированных спиртов, натрия гидроксид в качестве регулятора рН и комплекс натриевых солей метилпарабена и пропилпарабена в качестве консерванта при следующем соотношении компонентов, мас. %:
7. Антибактериальное средство по любому из пп. 1-6, отличающееся тем, что оно содержит увлажнитель из группы многоатомных спиртов и/или солей органических кислот в количестве 0,5-6,0 мас. %.
8. Антибактериальное средство по любому из пп. 1-6, отличающееся тем, что оно содержит вещество с пребиотическим эффектом в отношении нормофлоры в количестве 0,5-10,0 мас. %.
9. Антибактериальное средство по любому из пп. 1-6, отличающееся тем, что оно содержит подсластитель и/или ароматизатор в количестве 0,01-5,0 мас. %.
10. Антибактериальное средство по любому из пп. 1-6, отличающееся тем, что оно содержит фармацевтические неионогенные субстанции, обладающие местно анестезирующими и/или гипосенсибилизирующими свойствами (предпочтительно бензокаин, новокаин, димедрол, ментол) в количестве 0,05-5,0 мас. %.
11. Антибактериальное средство по любому из пп. 1 -6, отличающееся тем, что оно содержит прооксиданты и/или генераторы активных форм кислорода (предпочтительно аргинин, перекись водорода, аскорбиновая кислота, лактоферрин, глюкозооксидаза, лактопероксидаза) в количестве не выше 0,02 мас. %.
Существенным недостатком известного антибактериального средства является его многокомпонентность (более 15 наименований компонентов, например - концентрат бактериофагов с литической активностью по Аппельману не менее 10-4 для каждого вида бактериофага; гелеобразователь; ПАВ; регулятор рН; карбомер; сополимер силикона и гликоля; консервант; триэтаноламин; консервант; вода; гипромеллоза; ПЭГ 40; гидрогенизированное касторовое масло; повидон; лаурет-9; подсластитель и/или ароматизатор) известного средства. Кроме того, при изготовлении известного антибактериального средства каждый из его множества компонентов необходимо с высокой точностью (например, для концентрата бактериофагов для каждого вида бактериофага или для ПАВ - точность 0,001 мас. %) взвешивать с существенной затратой времени, для чего требуются высокоточное измерительное оборудование и высококвалифицированный персонал.
Недостатки существенно ограничивают возможность промышленного производства и область использования известного технического решения.
Известно изобретение «Композиция антибактериальная для профилактики или лечения госпитальных инфекций (варианты), штаммы бактериофагов, используемые для получения такой композиции» по патенту России RU 2628312 (опубликовано 15.08.2017. Бюл. №23. Приоритет от 16.03.2015).
По существу «Композиция антибактериальная для профилактики и лечения госпитальных инфекций...», включает комбинацию фильтратов фаголизатов бактерий, характеризуется тем, что она обладает литической активностью не ниже 10-4 по Аппельману в отношении тест-штаммов и выделенных из клинического материала изолятов бактерий и включает фильтрат фаголизата Staphylococcus aureus, полученный с использованием штамма бактериофага Staphylococcus aureus, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером SCH1, фильтрат фаголизата Staphylococcus aureus, полученный с использованием штамма бактериофага Staphylococcus aureus, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером SCH111, фильтрат фаголизата Klebsiella pneumoniae, полученный с использованием штамма бактериофага Klebsiella pneumoniae, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером KPV15, фильтрат фаголизата Klebsiella pneumoniae, полученный с использованием штамма бактериофага Klebsiella pneumoniae, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером KPV811, фильтрат фаголизата Pseudomonas aeruginosa, полученный с использованием штамма бактериофага Pseudomonas aeruginosa, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером РА5, фильтрат фаголизата Pseudomonas aeruginosa, полученный с использованием штамма бактериофага Pseudomonas aeruginosa, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером РА10, фильтрат фаголизата Acinetobacter baumannii, полученный с использованием штамма бактериофага Acinetobacter baumannii, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером АМ24, и целевые добавки в количестве 0,01÷99,99 мас. % от массы композиции.
2. Композиция антибактериальная для профилактики и лечения госпитальных инфекций, включающая комбинацию фильтратов фаголизатов бактерий, отличающаяся тем, что она обладает литической активностью не ниже 10-4 по Аппельману в отношении тест-штаммов и выделенных из клинического материала изолятов бактерий и включает фильтрат фаголизата Staphylococcus aureus, полученный с использованием штамма бактериофага Staphylococcus aureus, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером SCH1, фильтрат фаголизата Staphylococcus aureus, полученный с использованием штамма бактериофага Staphylococcus aureus, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером SCH111, фильтрат фаголизата Klebsiella pneumoniae, полученный с использованием штамма бактериофага Klebsiella pneumoniae, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером KPV15, фильтрат фаголизата Klebsiella pneumoniae, полученный с использованием штамма бактериофага Klebsiella pneumoniae, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером KPV811, фильтрат фаголизата Pseudomonas aeruginosa, полученный с использованием штамма бактериофага Pseudomonas aeruginosa, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером РА5, фильтрат фаголизата Pseudomonas aeruginosa, полученный с использованием штамма бактериофага Pseudomonas aeruginosa, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером РА10, фильтрат фаголизата Acinetobacter baumannii, полученный с использованием штамма бактериофага Acinetobacter baumannii, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером АМ24, фильтрат фаголизата Acinetobacter baumannii, полученный с использованием штамма бактериофага Acinetobacter baumannii, депонированного в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером АР22, и целевые добавки в количестве 0,01÷99,99 мас. % от массы композиции.
3. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 0,01-95,0 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: сироп корня солодки, пектин яблочный, натрий-фосфатный буфер, HEPES-буфер, хинозол и представлена в виде суспензии.
4. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 50,0-95,0 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: глицин, цистеин, гистидин, альбумин, масло касторовое, ланолин, кондитерский жир, пищевой жир, спермацет, вазелин, глюкоза, твердые жиры (SolPro), эмульгатор Т-2, парафин, какао-масло, вода, витебсол, хинозол, желатин, глицерин, кальций глюконат, полиэтиленоксид 400, полиэтиленоксид 1500 и соли, способные образовывать фосфатный, или ацетатный, или трис-буферный растворители, и представлена в виде суппозитория.
5. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 50,0-95,0 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: соли, образующие буферный раствор, глицин, цистеин, гистидин, хинозол, полиглюкин, воск, саломас, комбижир, ланолин, спермацет, вазелин, глицерин, церезин, вазелиновое масло, искусственный вазелин, пальмитин, гидрированный жир, кондитерский жир, пальмовый олеин, пальмовый стеарин, полиэтиленоксид 1500, полиэтиленоксид 400, масло какао, масло касторовое, персиковое масло, льняное масло, конопляное масло, пропиленгликоль, гексиленгликоль и представлена в виде мази.
6. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 99,99 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: карбапол ЕТД, экстракт календулы, эфирное масло лаванды, нипазол (пропилпарабен), NaOH, марка РД, вода очищенная, и представлена в виде косметического геля.
7. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 99,99 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: повидон, ПЭГ 40 гидрогенизированное касторовое масло, лаурет-9, гидроокись натрия, бензоат натрия, сорбат калия, метилпарабен, вода, лактат магния, D-пантенол, бензокаин, ментол, пропиленгликоль, АСД фракция 2, и представлена в виде геля при ожогах.
8. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 99,99 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: повидон, ПЭГ 40 гидрогенизированное касторовое масло, гидроокись натрия, бензат натрия, сорбат калия, вода, фруктоолигосахарид, лактулоза, лактат калия, D-пантенол, ароматизатор, и представлена в виде спрея для полости рта.
9. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 99,99 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: гипромеллоза, ПЭГ 40 гидрогенизированное касторовое масло, бензоат натрия, сорбат калия, фосфатный буфер, вода, отдушка, аргинин, ментол, пропиленгликоль, и представлена в виде геля для повязок.
10. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она содержит целевые добавки в количестве 99,99 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: карбомер, триэтаноламип, бензиловый спирт, метилхлоризотиазолинон, метилизотиазолинон, ПЭГ 12 диметикон, хинозол, вода, отдушка, и представлена в виде дезинфицирующего средства.
11. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 1 или 2, отличающаяся тем, что она включает комбинацию фильтратов фаголизатов бактерий в виде сухой биомассы.
12. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 11, отличающаяся тем, что она содержит целевые добавки в количестве 30,0-94,0 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: аэросил, сахароза, лактоза, глюкоза, мальтоза, манит, фруктоза, кислота аскорбиновая, кислота лимонная, кислота янтарная, глицин, тиомочевина, полиглюкин, пектин, декстрин, альбумин, желатин, соли, образующие буферный раствор, кальция стеарат, титана двуокись, лактулоза, поливинилпирролидон, целлюлоза микрокристаллическая, крахмал, тальк, цистеин, гистидин, хинозол, и представлена в виде лиофилизированного порошка.
13. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 11, отличающаяся тем, что она содержит целевые добавки в количестве 50,0-94,0 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: аэросил, сахароза, лактоза, глюкоза, мальтоза, манит, фруктоза, кислота аскорбиновая, кислота лимонная, кислота янтарная, глицин, тиомочевина, полиглюкин, пектин, декстрин, альбумин, желатин, соли, образующие буферный раствор, кальция стеарат, титана двуокись, лактулоза, поливинилпирролидон, целлюлоза микрокристаллическая, крахмал, тальк, целлюлоза, метилцеллюлоза, ацетатфталатцеллюлоза, натрий карбоксиметилцеллюлоза, натрий кроскармеллоза, натрия гликолят крахмал, воск, твин, гистидин, цистеин, хинозол, и представлена в виде таблетки с кишечнорастворимым покрытием.
14. Композиция антибактериальная для профилактики и лечения госпитальных инфекций по п. 11, отличающаяся тем, что она содержит целевые добавки в количестве 30,0-94,0 мас. % от массы композиции в виде смеси ингредиентов, выбранных из ряда: аэросил, сахароза, лактоза, глюкоза, мальтоза, манит, фруктоза, кислота аскорбиновая, кислота лимонная, кислота янтарная, глицин, тиомочевина, полиглюкин, пектин, декстрин, альбумин, желатин, соли, образующие буферный раствор, кальция стеарат, титана двуокись, лактулоза, поливинилпирролидон, целлюлоза микрокристаллическая, крахмал, тальк, целлюлоза, метилцеллюлоза, ацетатфталатцеллюлоза, кросповидон, хинозол, и представлена в виде капсулы.
15. Штамм бактериофага Staphylococcus aureus, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером SCH1.
16. Штамм бактериофага Staphylococcus aureus SCH1, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 1.
17. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 1.
18. Штамм бактериофага Staphylococcus aureus, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером SCH111.
19. Штамм бактериофага Staphylococcus aureus SCH111, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 2.
20. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 2.
21. Штамм бактериофага Klebsiella pneumoniae, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером KPV15.
22. Штамм бактериофага Klebsiella pneumoniae KPV15, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 3.
23. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 3.
24. Штамм бактериофага Klebsiella pneumoniae, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером KPV811.
25. Штамм бактериофага Klebsiella pneumonia KPV811, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 4.
26. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%>, 93%, 96%, 99% или 100% идентична SEQ ID NO: 4.
27. Штамм бактериофага Pseudomonas aeruginosa, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером РА5.
28. Штамм бактериофага Pseudomonas aeruginosa РА5, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%, 99% или 100%>идентична SEQ ID NO: 5.
29. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 5.
30. Штамм бактериофага Pseudomonas aeruginosa, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером РА10.
31. Штамм бактериофага Pseudomonas aeruginosa РА10, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%>, 99% или 100% идентична SEQ ID NO: 6.
32. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 6.
33. Штамм бактериофага Acinetobacter baumannii, используемый для получения композиции антибактериальной по п. 1 или 2, депонированный в коллекции музея микроорганизмов Федерального бюджетного учреждения науки «Государственный научный центр прикладной микробиологии и биотехнологии» Федеральной службы по надзору в сфере защиты нрав потребителей и благополучия человека (ФБУН ГНЦ ПМБ Роспотребнадзора) под номером АМ24.
34. Штамм бактериофага Acinetobacter baumannii АМ24, включающий нуклеотидную последовательность, которая на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 7.
35. Нуклеотидная последовательность, кодирующая геном бактериофага, и на 90%, 93%, 96%, 99% или 100% идентична SEQ ID NO: 7.
Существенным недостатком известной антибактериальной композиции является сложность ее состава, состоящего из химических и биологических компонентов (например, п. 12: в составе композиции химических компонентов (29 наименований) -аэросил; сахароза; лактоза; глюкоза; мальтоза; манит; фруктоза; кислота аскорбиновая; кислота лимонная; кислота янтарная; глицин; тиомочевина; полиглюкин; пектин; декстрин; альбумин; желатин; соли, образующие буферный раствор; кальция стеарат; титана двуокись; лактулоза; поливинилпирролидон; целлюлоза микрокристаллическая; крахмал; тальк; цистеин; гистидин; хинозол) и задепонированных в России штаммов бактериофагов (7 наименований), а именно - Staphylococcus aureus; Staphylococcus aureus SCH111; Klebsiella pneumoniae KPV15; Klebsiella pneumonia KPV811; Pseudomonas aeruginosa PA5; Pseudomonas aeruginosa РА10; Acinetobacter baumannii AM24 композиции. При изготовлении известной композиции каждый из его множества компонентов необходимо с высокой точностью (до 0,01 мас. %) взвешивать с существенной затратой времени, для чего требуются высокоточное измерительное оборудование и высококвалифицированный персонал со знанием химии и микробиологии.
Недостатки технического решения существенно ограничивают возможности промышленного производства известной композиции и область ее использования.
Известно изобретение по патенту России «Бактериофаг, обладающий активностью против Pseudomonas aeruginosa, белки бактериофага и способы их применения» по патенту России RU 2580248 (Конвенционный приоритет: 06.02.2009 US 61/150,585; 18.06.2009 РТ 61/218,345).
Сущность известного предлагаемого изобретения заключается в том, что:
1. Выделенный бактериофаг с геномом, содержащим последовательность нуклеиновых кислот SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 760.
2. Фармацевтическая композиция, включающая бактериофаг по п. 1 и фармацевтически приемлемый носитель.
3. Фармацевтическая композиция, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 1 или SEQ ID NO: 2, и дополнительно один или более дополнительных бактериофагов, эффективных против Enterococcus faecalis или Enterococcus faecium.
4. Фармацевтическая композиция, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 1 или SEQ ID NO: 2, и дополнительно один или более дополнительных бактериофагов, эффективных по отношению к бактериям, отличным от Enterococcus faecalis или Enterococcus faecium.
5. Фармацевтическая композиция по п. 2, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 3, и дополнительно один или несколько дополнительных бактериофагов, эффективных против Pseudomonas aeruginosa.
6. Фармацевтическая композиция по п. 2, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 3, и дополнительно один или более дополнительных бактериофагов, эффективных по отношению к бактериям, отличным от Pseudomonas aeruginosa.
7. Фармацевтическая композиция по п. 2, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6 или SEQ ID NO: 7, и дополнительно один или несколько дополнительных бактериофагов, эффективных против Staphylococcus aureus.
8. Фармацевтическая композиция по п. 2, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6 или SEQ ID NO: 7, и дополнительно один или более дополнительных бактериофагов, эффективных по отношению к бактериям, отличным от Staphylococcus aureus.
9. Фармацевтическая композиция по п. 2, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 760, и дополнительно один или более дополнительных бактериофагов, эффективных по отношению к Acinetobacter baumannii.
10. Фармацевтическая композиция по п. 2, включающая бактериофаг с геномом, который содержит последовательность нуклеиновых кислот SEQ ID NO: 760, и дополнительно один или более дополнительных бактериофагов, эффективных по отношению к бактериям, отличным от Acinetobacter baumannii.
11. Белок лизин, выделенный из бактериофага F1245/05, F168/08, F170/08, F197/08, F86/06, F87S/06 или F91a/06 или его фрагмент, вариант или производное, обладающее антибактериальной или антимикробной активностью по отношению к одному или более видам бактерий из числа Acinetobacter baumanii, Enterococcus faecalis, Enterococcus faecium и Staphylococcus aureus.
12. Выделенный белок лизин по п. П, который имеет последовательность аминокислот SEQ ID NO: 68, SEQ ID NO: 184, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 446, SEQ ID NO: 447, SEQ ID NO: 448, SEQ ID NO: 575, SEQ ID NO: 641, SEQ ID NO: 712, SEQ ID NO: 797, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью по отношению к одному или более видам бактерий из числа Enterococcus faecalis, Enterococcus faecium, Staphylococcus aureus и Acinetobacter baumanii.
13. Выделенный первый белок, по меньшей мере на 85% идентичный по последовательности второму белку того же размера, причем указанный первый белок обладает антибактериальной или антимикробной активностью по отношению к одному или более видам бактерий из Acinetobacter baumanii, Enterococcus faecalis, Enterococcus faecium и Staphylococcus aureus и указанный второй белок содержит последовательность аминокислот SEQ ID NO: 797, SEQ ID NO: 68, SEQ ID NO: 184, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 446, SEQ ID NO: 447, SEQ ID NO: 448, SEQ ID NO: 575, SEQ ID NO: 641, SEQ ID NO: 712 или ее фрагмент.
14. Выделенный первый белок по п. 13, по меньшей мере на 95% идентичный по последовательности аминокислот указанному второму белку.
15. Фрагмент по п. П, который представляет собой домен CHAP, выделенный из полипептида с последовательностью аминокислот SEQ ID NO: 68, SEQ ID NO: 184, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 446, SEQ ID NO: 447, SEQ ID NO: 448, SEQ ID NO: 575, SEQ ID NO: 641 или SEQ ID NO: 712.
16. Фрагмент по п. 15, который содержит последовательность аминокислот SEQ ID NO: 755, SEQ ID NO: 756, SEQ ID NO: 757, SEQ ID NO: 758 или SEQ ID NO: 759.
17. Белок «рулетка» хвостового отростка (tail tape measure protein) или белок хвостового отростка, выделенный из бактериофага F168/08, F170/08, F770/05, F197/08, F86/06, F87S/06, F91a/06 или F1245/05, или его фрагмент, вариант или производное, обладающие биологической активностью, обусловленной бактериофагом, из которого они выделены.
18. Выделенный «рулетка» хвостового отростка или белок хвостового отростка по п. 17, имеющий последовательность аминокислот SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 204, SEQ ID NO: 214, SEQ ID NO: 435, SEQ ID NO: 438, SEQ ID NO: 440, SEQ ID NO: 525, SEQ ID NO: 526, SEQ ID NO: 527, SEQ ID NO: 528, SEQ ID NO: 529, SEQ ID NO: 530, SEQ ID NO: 531, SEQ ID NO: 532, SEQ ID NO: 533, SEQ ID NO: 534, SEQ ID NO: 535, SEQ ID NO: 536, SEQ ID NO: 537, SEQ ID NO: 538, SEQ ID NO: 539, SEQ ID NO: 567, SEQ ID NO: 568, SEQ ID NO: 632, SEQ ID NO: 633, SEQ ID NO: 700, SEQ ID NO: 701, SEQ ID NO: 702, SEQ ID NO: 703, SEQ ID NO: 704, SEQ ID NO: 795 или его фрагмент, вариант или производное, обладающие биологической активностью, обусловленной бактериофагом, из которого они выделены.
19. Выделенный первый белок, по меньшей мере на 85% идентичный по последовательности аминокислот второму белку того же размера, причем первый белок обладает биологической активностью, обусловленной бактериофагом F168/08, F170/08, F770/05, F197/08, F86/06, F87S/06, F91a/06 или F1245/05, а указанный второй белок имеет последовательность аминокислот SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 204, SEQ ID NO: 214, SEQ ID NO: 435, SEQ ID NO: 438, SEQ ID NO: 440, SEQ ID NO: 525, SEQ ID NO: 526, SEQ ID NO: 527, SEQ ID NO: 528, SEQ ID NO: 529, SEQ ID NO: 530, SEQ ID NO: 531, SEQ ID NO: 532, SEQ ID NO: 533, SEQ ID NO: 534, SEQ ID NO: 535, SEQ ID NO: 536, SEQ ID NO: 537, SEQ ID NO: 538, SEQ ID NO: 539, SEQ ID NO: 567, SEQ ID NO: 568, SEQ ID NO: 632, SEQ ID NO: 633, SEQ ID NO: 700, SEQ ID NO: 701, SEQ ID NO: 702, SEQ ID NO: 703, SEQ ID NO: 704, SEQ ID NO: 795 или его фрагмент.
20. Выделенный первый белок по п. 19, по меньшей мере на 95% идентичный по последовательности аминокислот указанному второму белку.
21. Фармацевтическая композиция, содержащая выделенный белок по п. П или 17 и фармацевтически приемлемый носитель.
22. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 68, SEQ ID NO: 184, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 204 или SEQ ID NO: 214, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью по отношению к Enterococcus faecalis или Enterococcus faecium, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных по отношению к Enterococcus faecalis или Enterococcus faecium.
23. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NO: 61, SEQ ID NO: 63, SEQ ID NO: 68, SEQ ID NO: 184, SEQ ID NO: 202, SEQ ID NO: 203, SEQ ID NO: 204 или SEQ ID NO: 214, или его фрагмент, вариант или производное, которые обладают антибактериальной или антимикробной активностью по отношению к Enterococcus faecalis или Enterococcus faecium, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных по отношению к бактериям, отличным от Enterococcus faecalis или Enterococcus faecium.
24. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NO: 435 или SEQ ID NO: 438, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью против Pseudomonas aeruginosa, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных против Pseudomonas aeruginosa.
25. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NO: 435 или SEQ ID NO: 438, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью против Pseudomonas aeruginosa, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных против бактерий, отличных от Pseudomonas aeruginosa.
26. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NO: 440, SEQ ID NO: 525, SEQ ID NO: 526, SEQ ID NO: 527, SEQ ID NO: 528, SEQ ID NO: 529, SEQ ID NO: 530, SEQ ID NO: 531, SEQ ID NO: 532, SEQ ID NO: 533, SEQ ID NO: 534, SEQ ID NO: 535, SEQ ID NO: 536, SEQ ID NO: 537, SEQ ID NO: 538, SEQ ID NO: 539, SEQ ID NO: 567, SEQ ID NO: 568, SEQ ID NO: 632, SEQ ID NO: 633, SEQ ID NO: 700, SEQ ID NO: 701, SEQ ID NO: 702, SEQ ID NO: 703, SEQ ID NO: 704, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью по отношению к Staphylococcus aureus, и дополнительно включающая один иди более бактериофагов или дополнительных белков, эффективных по отношению к Staphylococcus aureus.
27. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NO: 440, SEQ ID NO: 525, SEQ ID NO: 526, SEQ ID NO: 527, SEQ ID NO: 528, SEQ ID NO: 529, SEQ ID NO: 530, SEQ ID NO: 531, SEQ ID NO: 532, SEQ ID NO: 533, SEQ ID NO: 534, SEQ ID NO: 535, SEQ ID NO: 536, SEQ ID NO: 537, SEQ ID NO: 538, SEQ ID NO: 539, SEQ ID NO: 567, SEQ ID NO: 568, SEQ ID NO: 632, SEQ ID NO: 633, SEQ ID NO: 700, SEQ ID NO: 701, SEQ ID NO: 702, SEQ ID NO: 703, SEQ ID NO: 704, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью по отношению к Staphylococcus aureus, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных по отношению к бактериям, отличным от Staphylococcus aureus.
28. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NOS: 761-816, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью по отношению к Acinetobacter baumannii, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных по отношению к Acinetobacter baumannii.
29. Фармацевтическая композиция по п. 21, включающая выделенный белок, имеющий последовательность аминокислот SEQ ID NOS: 761-816, или его фрагмент, вариант или производное, обладающие антибактериальной или антимикробной активностью по отношению к Acinetobacter baumannii, и дополнительно включающая один или более бактериофагов или дополнительных белков, эффективных по отношению к бактериям, отличным от Acinetobacter baumannii.
30. Выделенная нуклеиновая кислота, содержащая последовательность нуклеотидов, кодирующую белок по п. 11 или 17.
31. Способ лечения или профилактики бактериальной инфекции у пациента, который в этом нуждается, включающий введение указанному пациенту терапевтического количества фармацевтической композиции по п. 2 или 21.
32. Способ по п. 31, в котором бактериальная инфекция вызвана одной или более бактериями из числа Acinetobacter baumanni, Enterococcus faecalis, Enterococcus faecium, Pseudomonas aeruginosa и Staphylococcus aureus.
33. Способ по п. 31, в котором бактериальная инфекция вызвана бактериями, отличными от Acinetobacter baumanni, Enterococcus faecalis, Enterococcus faecium, Pseudomonas aeruginosa и Staphylococcus aureus.
34. Способ по п. 31, в котором инфекция является нозокомиальной.
35. Способ по п. 31, в котором композицию вводят местно.
36. Способ по п. 31, в котором пациентом является млекопитающее.
37. Способ по п. 36, в котором млекопитающее является человеком.
38. Способ по п. 31, в котором инфекция, которую надо излечить, является кожной инфекцией.
39. Способ по п. 38, в котором указанная инфекция кожи связана с диабетической стопой.
40. Способ диагностики возбудителя бактериальной инфекции, включающий
(i) культивирование образца ткани, взятой у пациента;
(ii) контактирование культуры со стадии (i) с бактериофагом или белком по пп. 1, 11 или 17;
(iii) мониторинг роста или лизиса культуры,
причем свидетельство лизиса культуры указывает на то, что культура включает вид или штамм бактерий, которые известны как чувствительные к бактериофагу или полипептиду, использованным на стадии (ii).
41. Способ по п. 40, в котором образец ткани представляет собой образец крови, жидкости, биопсии ткани или мазок, взятый у указанного пациента.
42. Способ уменьшения или ингибирования колонизации или роста бактерий на поверхности, включающий приведение указанной поверхности в контакт с бактериофагом или полипептидом по пп. 1, 11 или 17.
43. Способ по п. 42, в котором указанная поверхность является кожей или слизистой оболочкой млекопитающего.
44. Способ по п. 43, в котором указанное млекопитающее является человеком.
45. Способ по п. 42, в котором указанная поверхность является поверхностью больничной аппаратуры или частью больничного оборудования.
46. Способ по п. 45, в котором указанная аппаратура или оборудование является аппаратурой или частью оборудования для хирургии.
Известно изобретение по патенту России RU 2770222 «Способ лечения язвенных кератитов у лошадей препаратом с бактериофагами». По сущности «Способ лечения язвенных кератитов у лошадей препаратом с бактериофагами», включает введение бактериофагового препарата «Фагодерм» в конъюнктивальную полость больного глаза в дозе 0,5 мл 4 раза в день в течение 25-30 дней до формирования лейкомы роговицы.
Недостатком известного способа лечения является его ограниченная функциональность, а именно - из описания этого технического решения следует:
«Способ лечения язвенных кератитов у лошадей препаратом с бактериофагами….
Применение препарата с бактериофагами улучшает состояние глаз у лошадей без применения антибиотиков». Видимо поэтому в описании известного изобретения отсутствует информация о применении бактериофагов совместно (вместе) с антибиотиками, так, как это осуществляют в медицине при лечении людей, страдающих от болезней бактериального происхождения, свойственных только людям и несвойственных лошадям, например - болезней ожогового происхождения.
Недостаток существенно ограничивает область применения технического решения по патенту RU 2770222.
Известно изобретение по патенту России RU 2808830 «Штамм бактериофага Pseudomonas phage Ка2 для профилактики и лечения инфекционных заболеваний, вызываемых Pseudomonas aeruginosas.
Сущность известного технического решения: Штамм бактериофага Pseudomonas phage Ка2 ВКПМ: Ph-1630 для профилактики и лечения инфекционных заболеваний, вызываемых Pseudomonas aeruginosa.
По совокупности совпадающих признаков это техническое решение по мнению заявителя наиболее близко к заявленному техническому решению и принят заявителем в качестве прототипа.
Недостатком прототипа является ограниченность области действия штамма бактериофага Ph-1630, а именно - штамм Ph-1630 не осуществляет лизис (растворение, разложение, ослабление, развязку клеток и их систем, в том числе микроорганизмов), некоторых типичных клинических изолятов инфекционных заболеваний, вызываемых Pseudomonas aeruginosa, например - являющихся вероятной (возможной) причиной возникновения остеомиелита, септического артирита.
Техническим результатом заявленного решения является штамм бактериофага Pseudomonas phage Ka1, обладающий литической активностью в отношении бактерий Р. aeruginosa, для профилактики и лечения инфекционных заболеваний, в том числе в сочетании с известными антибиотиками - противобактериальными препаратами. При этом достигается более высокий лечебный эффект по сравнению с использованием известных противобактериальных препаратов. Заявленное техническое решение способствует расширению известного перечня применяемых в медицине лекарственных средств.
Сущностью заявленного технического решения является штамм бактериофага Pseudomonas phage Ka1 для лечения и профилактики инфекционных заболеваний, вызываемых Pseudomonas aeruginosa.
Заявленное техническое решение иллюстрируют Фиг. 1, Фиг. 2, Фиг. 3.
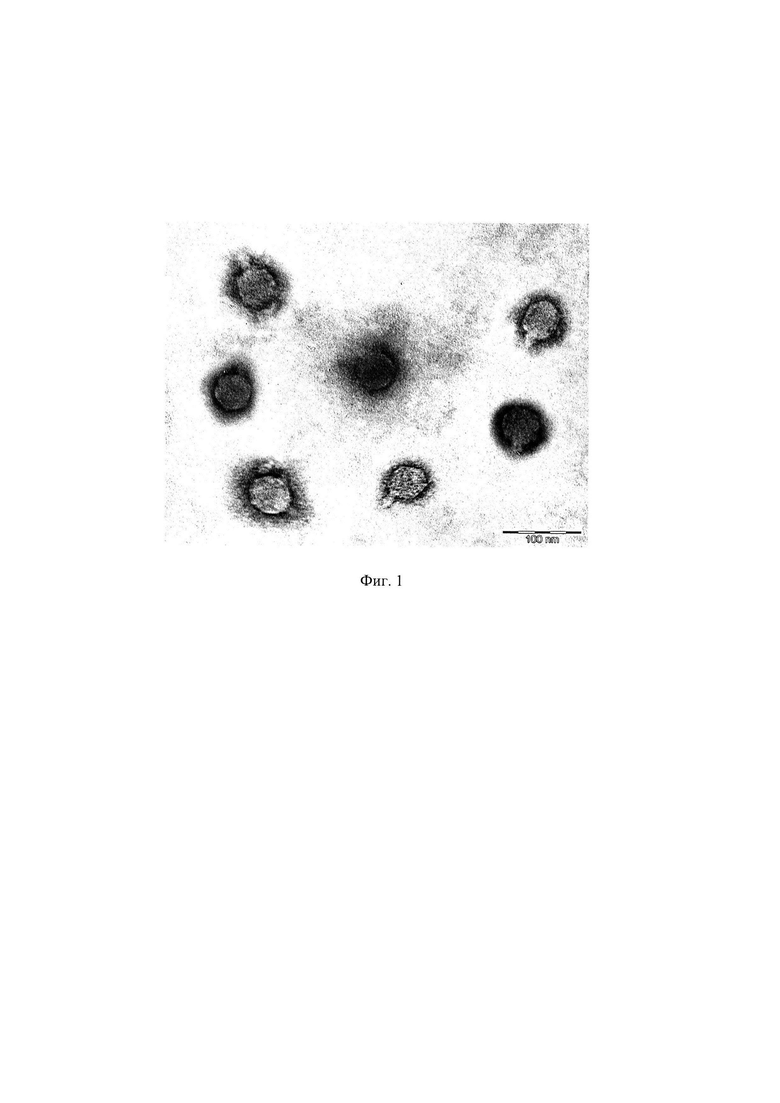
На Фиг. 1 представлена морфология изолированного штамма бактериофага Pseudomonas phage Ka1, полученная с помощью трансмиссионной электронной микроскопии.
На Фиг. 2 представлены зоны лизиса на газоне монокультуры P. aeruginosa. Фиг. 2 демонстрирует полный лизис бактериальной культуры в зоне соприкосновения с бактериофагом Pseudomonas phage Ka1.
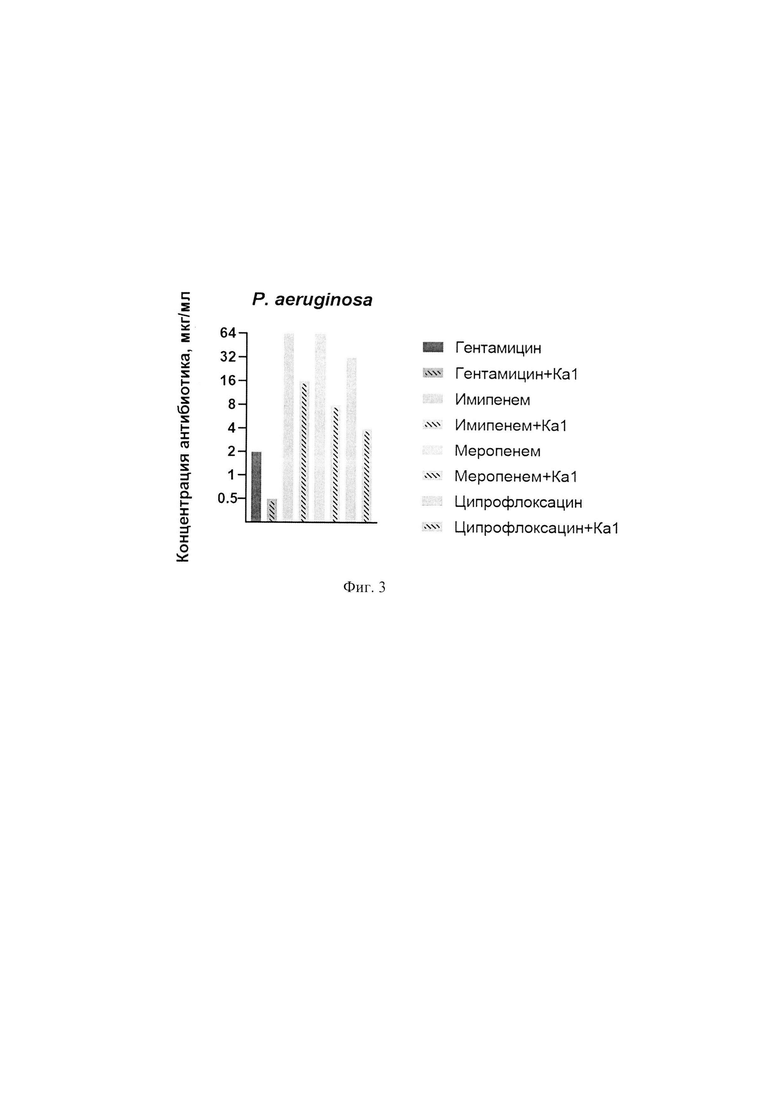
На Фиг. 3 представлена минимальная подавляющая концентрация известных и применяемых в практической медицине противобактериальных препаратов без и со штаммом бактериофага Pseudomonas phage Ka1 против монокультуры P. aeruginosa.
Далее заявителем приведено описание заявленного технического решения Характеристика заявленного штамма бактериофага Pseudomonas phage Ka1.
Штамм бактериофага Pseudomonas phage Ka1 найден в естественных условиях, выделен из воды притока озера Байкал, в районе сброса очищенных сточных вод г. Слюдянка. На Фиг. 1 представлена морфология изолированного штамма бактериофага Pseudomonas phage Ka1, полученная с помощью трансмиссионной электронной микроскопии.
Культивирование штамма проводили по известной методике Грациа.
Средой для культивирования штамма бактериофага Pseudomonas phage Ka1 является твердая агаризованная среда Лурии-Бертани (LA), состав среды LA (г/100 мл дистиллированной воды): триптон - 1,0; дрожжевой экстракт - 0,5; NaCl - 0,5; агар - 2,0.
Штамм бактериофага Pseudomonas phage Ka1 выращивают на среде LA на бактериальном газоне методом двойного слоя агара в чашке Петри в условиях термостата при температуре плюс (37,0±0,5)°С в течение 24 ч. Полужидкую LA с 0,6% агара используют для верхнего слоя. Наличие бактериофага Pseudomonas phage Ka1 и титр в супернатанте определяют по появлению бляшек на бактериальном газоне. Для получения бактериофага Pseudomonas phage Ka1 из зоны лизиса наконечником пипетки соскабливают слой бактериофагов Pseudomonas phage Ka1 и опускают в 0,9% раствор NaCl объемом 15 мл. Полученный раствор обрабатывают хлороформом 30 мкл/мл в течение 30 минут при плюс 4°С, центрифугируют, чтобы осадить клеточный дебрис при 4500 об/мин в течение 10 мин и надосадочную жидкость фильтруют через мембранный фильтр с диаметром пор 0,22 мкм. Для длительного хранения бактериофага Pseudomonas phage Ka1 500 мкл свежего фаголизата смешивают с 500 мкл стерильного глицерина и помещают в морозильную камеру при минус 86°С.
Для измерения концентрации бактериофагов в фаголизате в стерильный 96-луночный планшет в лунки вносили по 90 мкл 0,9% NaCl. В первую лунку добавляли 10 мкл фаголизата, следующие лунки содержали двукратно уменьшающиеся концентрации фаголизата. Готовили серийные 10-кратные разведения жидкой фаговой культуры из каждой лунки в 0,9% NaCl и по 15 мкл суспензии переносили на чашки с LA, предварительно содержащие ночную культуру P. aeruginosa. БОЕ подсчитывали из капель, содержащих минимум 5 бляшек, умножая на число разведения.
Культурально-морфологические признаки бактериофага Pseudomonas phage Ka1
Штамм бактериофага Pseudomonas phage Ka1 является вирулентным, то есть обладает природной способностью лизировать (разрушать) клетки P. aeruginosa и не способен к лизогенному пути развития.
В результате аннотации генома штамма бактериофага Pseudomonas phage Ka1 выявлена 71 кодирующая последовательность. Из них 27 кодируют гипотетические полипептиды с неизвестной функцией. Выявлено 6 генов метаболизма аминокислот, 4 гена кодируют белки с нуклеазной активностью, 11 генов участвуют в обмене нуклеиновых кислот, 20 генов кодируют структурные белки капсида и хвоста, 3 гена отвечают за синтез тРНК. При этом в геноме отсутствуют гены интегразы, транспозазы и рекомбиназы - потенциальных белков, связанных с переходом к лизогенному жизненному циклу, что делает его перспективным для противомикробной терапии, в том числе в сочетании терапии с имеющимися противобактериальными препаратами.
При высеве заявленного штамма на МПА образуются бляшкообразующие единицы с четким краем и прозрачным центром различного диаметра в диапазоне 0,15±0,1 мм.
Штамм бактериофага Pseudomonas phage Ka1 способен лизировать (разрушать) клетки P. aeruginosa PAO1. С помощью просвечивающего электронного микроскопа выявлено, что фаг имеет икосаэдрическую головку диаметром 70±10 нм и короткий сократительный хвост размером 20±5 нм (Фиг. 1).
ДНК изолята выделена с помощью коммерческого набора Viral RNA/DNA Mini Kit (Invitrogen by Thermo Fisher Scientific) и проведено shotgun-секвенирование в режиме парноконцевых прочтений с длиной 300 п. о. на платформе Illumina MiSeq. Собран кольцевой геном размером 46092 п.о. с 50% ГЦ-составом. Выравнивание с базой данных GenBank выявило максимальную идентичность с геномом бактериофага Pseudomonas phage phiPA01_EW (98% идентичности при покрытии 76%). Геном депонирован в GenBank под номером (ОР455935.1) [https://www.ncbi.nlm.nih.gov/nucleotide/OP455935.1?report=genbank&log$=nucltop&blast_га nk=9&RID=R0741S58016]. Бактериофаг Pseudomonas phage Ka1 задепонирован в Биоресурсном центре Всероссийской коллекции промышленных микроорганизмов (Регистрационный номер ВКПМ: Ph-1631).
В результате аннотации генома штамма бактериофага Pseudomonas phage Ka1 выявлена 71 кодирующая последовательность. Из них 27 последовательностей кодируют гипотетические полипептиды с неизвестной функцией. Выявлено 6 генов метаболизма аминокислот, 4 гена кодируют белки с нуклеазной активностью (нуклеазы способствуют расщеплению нуклеиновых кислот), 11 генов участвуют в обмене нуклеиновых кислот, 20 генов кодируют структурные белки капсида и хвоста (с помощью этих белков происходит лизис клетки и высвобождаются новообразованные вирусные частицы), 3 гена отвечают за синтез тРНК (тРНК обеспечивает взаимодействие аминокислоты, рибосомы и матричной РНК (мРНК) в ходе трансляции). При этом в геноме отсутствуют гены интегразы, транспозазы и рекомбиназы - потенциальных белков, связанных с переходом к лизогенному жизненному циклу, что делает его перспективным для противомикробной терапии, в том числе в сочетании имеющимися противобактериальными препаратами.
Далее заявителем представлены примеры конкретного выполнения заявленного технического решения.
Пример 1. Использование заявленного штамма бактериофага Pseudomonas phage Ka1 для оценки лизиса культуры P. aeruginosa PAQ1.
Для оценки лизиса культуры P. aeruginosa PAO1 с использованием заявленного штамма бактериофага Pseudomonas phage Ka1 получают ночную культуру P. aeruginosa PAO1l. На чашку с питательной средой LA наносили 3 мл полужидкого LA, содержащего 30 мкл ночной культуры P. aeruginosa (107 КОЕ/мл). После застывания среды наносили капли фагового лизата объемом 15 мкл с концентрацией 108 БОЕ/мл, просушивали 15 мин и инкубировали при плюс 37°С в течение 24 ч.
Получают зону лизиса на газоне монокультуры P. aeruginosa.
Полученный результат представлен на Фиг. 2 - представлены зоны лизиса на газоне монокультуры P. aeruginosa. Фиг. 2 демонстрирует полный лизис бактериальной культуры в зоне соприкосновения.
Пример 2. Использование заявленного штамма бактериофага Pseudomonas phage Ka1 для оценки его совместного действия с противомикробными препаратами.
Оценку совместного действия штамма бактериофага Pseudomonas phage Ka1 с известными противобактериальными препаратами проводят с помощью метода серийных разведений противобактериального препарата в 96-луночных стерильных полистироловых планшетах и определяют минимальную подавляющую концентрацию противобактериального препарата без добавления штамма бактериофага Pseudomonas phage Ka1 и с добавлением штамма бактериофага Pseudomonas phage Ka1.
Сначала получают разведения противобактериального препарата (например, мирамистин, бензалкония хлорид) в питательной среде Мюллера-Хинтона (Sigmaaldrich). В первую лунку вносят противобактериальный препарат в среде Мюллера-Хинтона в концентрации, в 2 раза превышающую максимальную, в объеме 200 мкл. В остальные лунки вносят чистую питательную среду Мюллера-Хинтона в объеме 100 мкл. Далее из первой лунки 100 мкл переносят во вторую лунку, тщательно перемешивают. Из второй лунки 100 мкл переносят в третью лунку и так далее. В результате, последовательным двукратным разведением доводят концентрацию противобактериального препарата до 0,5 мкг/мл. Затем в каждую лунку вносят приготовленный инокулюм (100 мкл суспензии ночной культуры микроорганизмов P. aeruginosa с содержанием КОЕ 106 клеток в мл), разводя тем самым вдвое концентрацию противобактериального препарата. В результате максимальная финальная концентрация противобактериального препарата составляет 64 мкг/мл. В следующих лунках содержатся двукратно уменьшающиеся концентрации противобактериального препарата - 64-0,5 мкг/мл.
В качестве контроля включают лунки, не содержащие противобактериального препарата (контроль роста культуры). Кроме того, ставят контроль чистоты питательных сред и растворителей.
Аналогично готовят серию разведений противобактериального препарата, в которую дополнительно вместе с инокулюмом вносят суспензию штамма бактериофага Pseudomonas phage Ka1 до конечной концентрации 108 БОЕ/мл.
Планшеты инкубируют в термостате при плюс 37°С в течение 24 часов.
Оценку роста культур проводят с помощью окрашивания 0,1% водным раствором резазурина, внося по 5 мкл в каждую лунку. Сравнивают рост микроорганизмов Р. aeruginosa в присутствии противобактериального препарата. Образование розовой окраски резазурина свидетельствовало о том, что данная концентрация исследуемого противобактериального препарата недостаточна, чтобы подавить жизнеспособность микроорганизмов P. aeruginosa. Первую, наименьшую, концентрацию исследуемого противобактериального препарата (из серии последовательных разведений), где не происходит образования розового продукта трансформации резазурина, считали МПК. В каждом опыте присутствовал положительный (бульон с растущей культурой Р. aeruginosa) и отрицательный (бульон без растущей культуры P. aeruginosa) контроли. В качестве МПК соединения принимают его медианное значение, полученное в трех независимых экспериментах (биологические повторное™).
Полученные результаты опытов показаны на Фиг. 3, где представлена минимальная подавляющая концентрация противобактериальных препаратов без и с бактериофагом Pseudomonas phage Ka1 против монокультуры P. aeruginosa. Показано, что в присутствии бактериофага Pseudomonas phage Ka1 минимальная подавляющая концентрация гентамицина, имипенема снижается в 4 раза (четырехкратно), а ципрофлоксацина и меропенема снижается в 8 раз (восьмикратно) по сравнению с МПК чистого антибиотика, что свидетельствует о синергизме бактериофага с данными противомикробными препаратами. Следовательно, повышается эффективность противобактериальной терапии инфекций, вызываемых P. aeruginosa.
Таким образом, из описанного выше можно сделать вывод, что заявителем достигнут заявленный технический результат, а именно: выделен штамм бактериофага Pseudomonas phage Ka1, обладающий литической активностью в отношении бактерий Р. aeruginosa, обеспечивающий возможность лечения и профилактики инфекционных заболеваний, в том числе - в сочетании с имеющимися противобактериальными препаратами. При этом достигнут более высокий лечебный эффект при совместном использовании штамма бактериофага Pseudomonas phage Ka1 с противобактериальными препаратами по сравнению с использованием одних противобактериальных препаратов против монокультуры P. aeruginosa.
Предлагаемое изобретение позволяет расширить ассортимент средств, содержащих в качестве действующего начала высокоселективный природный антибактериальный компонент (бактериофаг), обеспечить биологическую стабильность и активность бактериофага в составе композиции лечебного средства. Кроме того, композиция обладает низким риском токсических и побочных эффектов, позволяет расширить варианты и способы практического применения средств, содержащих бактериофаги, обеспечивает стабильность при хранении и эффективность применения в широком диапазоне температур.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ АНТИБАКТЕРИАЛЬНАЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ГОСПИТАЛЬНЫХ ИНФЕКЦИЙ (ВАРИАНТЫ), ШТАММЫ БАКТЕРИОФАГОВ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ | 2015 |
|
RU2628312C2 |
| КОМПОЗИЦИЯ АНТИБАКТЕРИАЛЬНАЯ, ШТАММ БАКТЕРИОФАГА Escherichia coli, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ТАКОЙ КОМПОЗИЦИИ. | 2012 |
|
RU2518303C2 |
| Штамм бактериофага Pseudomonas phage Ka2 для профилактики и лечения инфекционных заболеваний, вызываемых Pseudomonas aeruginosa | 2023 |
|
RU2808830C1 |
| Композиция антибактериальная для продления срока годности охлажденной рыбы и снижения риска возникновения инфекций, передаваемых пищевым путем, штаммы бактериофагов, используемые для ее получения | 2016 |
|
RU2644667C1 |
| ШТАММ БАКТЕРИОФАГА Citrobacter freundii CF17, СПОСОБНЫЙ ЛИЗИРОВАТЬ ПАТОГЕННЫЕ ШТАММЫ CITROBACTER FREUNDII | 2014 |
|
RU2565559C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730614C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Salmonella typhi и Staphylococcus haemolyticus (варианты) | 2019 |
|
RU2730613C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против грамотрицательных бактерий: Pseudomonas aeruginosa, Acinetobacter baumannii, Klebsiella pneumoniae и Salmonella typhi (варианты) | 2019 |
|
RU2730615C1 |
| ВИДОСПЕЦИФИЧЕСКИЙ ВИРУЛЕНТНЫЙ ШТАММ БАКТЕРИОФАГА, ОБЛАДАЮЩИЙ ЛИТИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ Staphylococcus aureus, ВКЛЮЧАЯ МУЛЬТИРЕЗИСТЕНТНЫЕ ШТАММЫ | 2012 |
|
RU2503716C1 |
| Антибактериальная композиция (варианты) и применение белка в качестве антимикробного средства, направленного против бактерий Acinetobacter baumannii, (варианты) | 2019 |
|
RU2730616C1 |

Изобретение относится к биохимии и микробиологии и представляет собой штамм бактериофага Pseudomonas phage Ka1 для лечения и профилактики инфекционных заболеваний, вызываемых Pseudomonas aeruginosa. Изобретение может быть использовано в биотехнологиях производства лекарственных средств для применения в медицине и ветеринарии для лечения и/или профилактики инфекционных заболеваний, вызываемых Pseudomonas aeruginosa. 3 ил., 2 пр.
Штамм бактериофага Pseudomonas phage Ka1 ВКПМ: Ph-1631 для лечения и профилактики инфекционных заболеваний, вызываемых Pseudomonas aeruginosa.
| KAMYAB H | |||
| et al., Isolation, characterization, and genomic analysis of vB_PaeS_TUMS_P81, a lytic bacteriophage against Pseudomonas aeruginosa, Virus Genes, 2023, vol | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения нерастворимых лаков основных красителей в субстанции и на волокнах | 1923 |
|
SU132A1 |
| Штамм бактериофага Pseudomonas phage Ka2 для профилактики и лечения инфекционных заболеваний, вызываемых Pseudomonas aeruginosa | 2023 |
|
RU2808830C1 |
| АЛЕКСАНИНА Н | |||
| В., Чувствительность к бактериофагам антибиотикорезистентных нозокомиальных штаммов Pseudomonas aeruginosa, Социально | |||
Авторы
Даты
2024-12-02—Публикация
2024-02-21—Подача