ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Эта заявка притязает на приоритет предварительной заявки на патент США с № 61/668397, поданной 5 июля 2012, предварительной заявки на патент США с № 61/852483, поданной 15 марта 2013, и предварительной заявки на патент США с № 61/819063, поданной 3 мая 2013, все из которых включены сюда посредством ссылки в их полном объеме.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к системе экспрессии и секреции и способам ее применения для экспрессии и секреции одного слитого с Fab белка в случае трансформации нуклеиновой кислотой прокариотической клетки для фагового дисплея и отличного или идентичного слитого с Fab белка в случае трансфекции нуклеиновой кислотой эукариотической клетки для экспрессии и очистки. Здесь также обеспечиваются молекулы нуклеиновых кислот, векторы и клетки-хозяева, включающие такие векторы и молекулы нуклеиновых кислот.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Фаговый дисплей пептидов или белков на частицах нитчатых фагов является in vitro технологией, которая позволяет отобрать пептиды или белки с желаемыми свойствами из больших совокупностей вариантов пептидов или белков (McCafferty et al., Nature, 348: 552-554 (1990); Sidhu et al., Current Opinion in Biotechnolosv, 11: 610-616 (2000); Smith et al., Science, 228: 1315-1317 (1985)). Фаговый дисплей может использоваться для представления разнообразных библиотек пептидов или белков, включая фрагменты антител, такие как Fab, в области отыскания антител на поверхности частицы нитчатого фага, которые затем отбирают по связыванию с конкретным антигеном, представляющим интерес. Фрагмент антитела можно представить на поверхности частицы нитчатого фага посредством слияния гена для фрагмента антитела с геном белка оболочки фага, что приводит к фаговой частице, которая представляет кодируемый фрагмент антитела на своей поверхности. Эта технология позволяет выделить фрагменты антител с желаемой аффинностью ко многим антигенам из большой библиотеки фагов.
В случае отыскания основанных на фагах антител для оценки отобранных фрагментов антител и свойств родственных им IgG в функциональных анализах (таких как анализы связывания мишени, клеточные анализы активности, in vivo полупериод существования) требуется изменение Fab-формата последовательностей тяжелой цепи (HC) и легкой цепи (LC) на полноразмерный IgG посредством субклонирования последовательностей ДНК, кодирующих HC и LC, из вектора, использованного для фагового дисплея, в векторы для экспрессии в клетках млекопитающих для экспрессии IgG. Трудоемкий процесс субклонирования дюжим или сотен отобранных пар HC/LC представляет собой основное «узкое место» в процессе отыскания основанных на фагах антител. Кроме того, поскольку значительная часть отобранных Fab, после изменения формата, не имеет удовлетворительные эксплуатационные свойства в первоначальных скрининговых исследованиях, увеличение количества клонов, которые проводят через этот процесс изменения формата/скрининга, сильно увеличивает наибольшую вероятность успеха.
Здесь описывается создание системы экспрессии и секреции для осуществления экспрессии слияния Fab-фаговый полипептид в случае трансформации E. coli и осуществления экспрессии полноразмерного IgG, содержащего тот же самый Fab-фрагмент, в случае трансфекции клеток млекопитающих. Авторы настоящего изобретения демонстрируют, что сигнальная последовательность млекопитающего из мышиного связывающего иммуноглобулинового белка (mBiP) (Haas et al., Immunoglobulin heavy chain binding protein, Nature, 306: 387-389 (1983); Munro et al., An Hsp70-like protein in the ER: identify with the 78 kd glucose-regulated protein and immunoglobulin heavy chain binding protein, Cell 4: 291-300 (1986) может приводить к эффективной экспрессии белков как в прокариотических, так и в эукариотических клетках. Используя сплайсинг мРНК млекопитающих для удаления синтетического интрона, содержащего фаговый пептид слияния, вставленный в шарнирную область НС IgG1 человека, авторы настоящего изобретения способны создать два различных белка зависимым от клетки-хозяина образом: Fab-фрагмент, слитый с адаптерным пептидом для фагового дисплея в E. coli, и природного IgG1 человека в клетках млекопитающих. Эта технология позволяет отобрать Fab-фрагменты, которые связываются с представляющим интерес антигеном, из библиотеки фагового дисплея с последующей экспрессией и очисткой родственных полноразмерных IgG в клетках млекопитающих без необходимости в субклонировании.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В одном аспекте настоящее изобретение основано, частично, на экспериментальных данных, показывающих, что (1) сигнальные последовательности непрокариотического происхождения функционируют в прокариотических клетках, и (2) различные слитые с Fab белки экспрессируются с одной и той же молекулы нуклеиновой кислоты зависимым от клетки-хозяина образом, когда процессирование мРНК происходит в эукариотических клетках, но не в прокариотических клетках (слитые Fab-фаговый полипептид белки в прокариотических клетках и слитые Fab-Fc белки в эукаритических клетках). Соответственно, здесь описываются молекулы нуклеиновых кислот для экспрессии и секреции Fab-фрагмента, слитого с белком фаговой частицы, белком оболочки или адаптерным белком, для фагового дисплея в бактериях, когда нуклеиновой кислотой трансформируют прокариотические клетки-хозяева (например, E. coli), и Fab-фрагмента, слитого с Fc, когда нуклеиновой кислотой трансформируют эукариотические клетки (например, клетки млекопитающих), без необходимости в субклонировании, и способы применения.
В одном варианте осуществления настоящим изобретением обеспечивается молекула нуклеиновой кислоты, кодирующая первый полипептид, включающий VH-HVR1, VH-HVR2 и HVR3 вариабельного домена тяжелой цепи (VH), и/или второй полипептид, включающий VL-HVR1, VL-HVR2 и VL-HVR3 вариабельного домена легкой цепи (VL), и причем молекула нуклеиновой кислоты, кроме того, кодирует сигнальную последовательность, которая является функциональной как в прокариотических, так и в эукариотических клетках и кодируется последовательностью нуклеиновой кислоты, которая функционально связана с последовательностью первого и/или второго полипептида, и причем полноразмерное антитело получается из первого и/или второго полипептида молекулы нуклеиновой кислоты. В другом варианте осуществления первый и/или второй полипептид, кроме того, включает вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL). В дальнейшем варианте осуществления VH-домен связан с CH1, а VL-домен связан с CL.
В одном аспекте настоящим изобретением обеспечивается молекула нуклеиновой кислоты, кодирующая VH-HVR1, VH-HVR2 и VH-HVR3 вариабельного домена тяжелой цепи (VH) и VL-HVR1, VL-HVR2 и VL-HVR3 вариабельного домена легкой цепи (VL) и включающая прокариотический промотор и эукариотический промотор, которые функционально связаны с HVR-участками VH и/или HVR-участками VL для допуска экспрессии HVR-участков VH и HVR-участков VL в прокариотической и эукариотической клетке, и причем HVR-участки VH и/или VL связаны с полезным пептидом при экспрессии эукариотической клеткой, и причем нуклеиновая кислота, кроме того, кодирует сигнальную последовательность, которая является функциональной как в прокариотической, так и в эукариотической клетке.
В другом аспекте настоящим изобретением обеспечивается молекула нуклеиновой кислоты, кодирующая вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL) и включающая прокариотический промотор и эукариотический промотор, которые функционально связаны с VH-доменом и/или VL-доменом для допуска экспрессии VH-домена и/или VL-домена в прокариотической и эукариотической клетке, и причем VH-домен и/или VL-домен связаны с полезным пептидом при экспрессии эукариотической клеткой, и причем нуклеиновая кислота, кроме того, кодирует сигнальную последовательность, которая функционирует как в прокариотической, так и в эукариотической клетке.
В одном варианте осуществления VL и VH связаны с полезными пептидами. В дальнейшем варианте осуществления VH, кроме того, связан с CH1, а VL связан с CL. Полезный пептид выбирают из группы, состоящей из Fc, маркера, метки и контрольного белка. В одном варианте осуществления VL связан с контрольным белком, а VH связан с Fc. Например, контрольным белком является белок gD, или его фрагмент.
В еще одном дополнительном варианте осуществления первый и/или второй полипептид настоящего изобретения слит с белком оболочки (например, pI, pII, pIII, pIV, pV, pVI, pVII, pVIII, pIX и pX бактериофага M13, f1 или fd, или его фрагментом, таким как аминокислоты 267-421 или 262-418 белка pIII, («pI», «pII», «pIII», «pIV», «pV», «pVI», «pVII», «pVIII», «pIX» и «pX» при использовании здесь относится к полноразмерному белку или его фрагментам, кроме особо оговоренных случаев)) или адаптерным белком (например, белком «лейциновая молния» или полипептидом, включающим аминокислотную последовательность SEQ ID NO: 12 (cJUN(R): ASIARLEEKV KTLKAQNYEL ASTANMLREQ VAQLGGC) или SEQ ID NO: 13 (FosW(E): ASIDELQAEVEQLEERNYAL RKEVEDLQKQ AEKLGGC), или его вариантом (аминокислоты в SEQ ID NO: 12 и SEQ ID NO: 13, которые могут быть модифицированы, включают, но без ограничения, те, которые подчеркнуты и выделены полужирным шрифтом), причем вариант содержит аминокислотную модификацию, причем в результате модификации сохраняется или увеличивается сродство адаптерного белка к другому адаптерному белку, или с полипептидом, включающим аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO: 6 (ASIARLRERVKTLRARNYELRSRANMLRERVAQLGGC) или SEQ ID NO: 7 (ASLDELEAEIEQLEEENYALEKEIEDLEKELEKLGGC)), или полипептидом, включающим аминокислотную последовательность SEQ ID NO: 8 (GABA-R1: EEKSRLLEKENRELEKIIAEKEERVSELRHQLQSVGGC) или SEQ ID NO: 9 (GABA-R2: TSRLEGLQSENHRLRMKITELDKDLEEVTMQLQDVGGC), или SEQ ID NO: 14 (Cys: AGSC), или SEQ ID NO: 15 (Шарнир: CPPCPG). Молекула нуклеиновой кислоты, кодирующая белок оболочки или адаптерный белок, включена в синтетический интрон. Синтетический интрон расположен между нуклеиновой кислотой, кодирующей VH-домен, и нуклеиновой кислотой, кодирующей Fc. Синтетический интрон, кроме того, включает нуклеиновую кислоту, кодирующую встречающийся в природе интрон из IgG1, причем встречающийся в природе интрон можно выбрать из группы, включающей интрон 1, интрон 2 или интрон 3 из IgG1.
В одном варианте осуществления настоящим изобретением обеспечивается молекула нуклеиновой кислоты, причем в прокариотических клетках экспрессируется первый слитый белок, а в эукариотических клетках экспрессируется второй слитый белок. Первый слитый белок и второй слитый белок могут быть одинаковыми или различными. В дальнейшем варианте осуществления первым слитым белком может быть слитый Fab-фаговый полипептид белок (например, слитый Fab-фаговый полипептид белок включает VH/CH1, слитый с pIII), а вторым слиянием может быть слитый Fab-Fc или Fab-шарнир-Fc белок (например, слитый Fab-Fc или Fab-шарнир-Fc белок включает VH/CH1, слитый с Fc).
В одном варианте осуществления настоящим изобретением обеспечивается молекула нуклеиновой кислоты, причем сигнальная последовательность приводит к секреции белка в эндоплазматический ретикулум или наружную часть клетки в случае эукариотических клеток, и/или причем сигнальная последовательность приводит к секреции белка в периплазму или наружную часть клетки в случае прокариотических клеток. Кроме того, сигнальная последовательность может кодироваться последовательностью нуклеиновой кислоты, которая кодирует аминокислотную последовательность, включающую аминокислотную последовательность SEQ ID NO: 10 (XMKFTWAAALLLLGAVRA, где X=0 аминокислот или 1 или 2 аминокислотам (например, X=M (SEQ ID NO: 3; MMKFTWAAALLLLGAVRA; mBIP дикого типа) или X=MT (SEQ ID NO: 19; MTMKFTWAAALLLLGAVRA), или X отсутствует (SEQ ID NO: 20; MKFTWAAALLLLGAVRA), или последовательностью нуклеиновой кислоты, которая кодирует mBIP (SEQ ID NO: 4; ATG ATG AAA TTT ACC GTG GTG GCG GCG GCG CTG CTG CTG CTG GGC GCG GTC CGC GCG), и ее вариантами, или последовательностью нуклеиновой кислоты, которая кодирует аминокислотную последовательность, идентичную на по крайней мере 90% аминокислотной последовательности, выбираемой из SEQ ID NO: 3 (аминокислотной последовательности mBIP), и причем сигнальная последовательность функционирует как в прокариотических, так и в эукариотических клетках, или последовательностью нуклеиновой кислоты SEQ ID NO: 11 (консенсусной для mBIP последовательностью, X ATG AAN TTN ACN GTN GTN GCN GCN GCN CTN CTN CTN CTN GGN GCN GTN CGN GCN, причем N=A, T, C или G, где X=ATG (SEQ ID NO: 5; ATG ATG AAN TTN ACN GTN GTN GCN GCN GCN CTN CTN CTN CTN GGN GCN GTN CGN GCN), X=ATG ACC (SEQ ID NO: 21; ATG ACC ATG AAN TTN ACN GTN GTN GCN GCN GCN CTN CTN CTN CTN GGN GCN GTN CGN GCN), или X = отсутствует (SEQ ID NO: 22; ATG AAN TTN ACN GTN GTN GCN GCN GCN CTN CTN CTN CTN GGN GCN GTN CGN GCN), или последовательностью нуклеиновой кислоты, выбираемой из группы SEQ ID NO: 16 (mBIP.Opt1: ATG ATG AAA TTT ACC GTT GTT GCT GCT GCT CTG CTA CTT CTT GGA GCG GTC CGC GCA), SEQ ID NO: 17 (mBIP.Opt2: ATG ATG AAA TTT ACT GTT GTT GCG GCT GCT CTT CTC CTT CTT GGA GCG GTC CGC GCA) и SEQ ID NO: 18 (mBIP.Opt3: ATG ATG AAA TTT ACT GTT GTC GCT GCT GCT CTT CTA CTT CTT GGA GCG GTC CGC GCA).
В дальнейшем варианте осуществления синтетический интрон в молекуле нуклеиновой кислоты фланкирован нуклеиновой кислотой, кодирующей CH1, на его 5'-конце и нуклеиновой кислотой, кодирующей Fc, на его 3'-конце. Кроме того, нуклеиновая кислота, кодирующая CH1-домен, включает часть природной донорной последовательности сплайсинга, а нуклеиновая кислота, кодирующая Fc, включает часть природной акцепторной последовательности сплайсинга. Альтернативно, нуклеиновая кислота, кодирующая CH1-домен, включает часть модифицированной донорной последовательности сплайсинга, причем модифицированная донорная последовательность сплайсинга включает модификацию по крайней мере одного остатка нуклеиновой кислоты, и причем модификация увеличивает сплайсинг.
В одном варианте осуществления прокариотическим промотором является промотор phoA, Tac, Tphac или Lac, и/или эукариотическим промотором является CMV или SV40, или U3-район вируса лейкоза у мышей Молони, или U3-район вируса артроэнцефалита козлов, или U3-район вируса висны, или последовательность U3-района ретровируса. Экспрессия с помощью прокариотического промотора происходит в бактериальной клетке, а экспрессия с помощью эукариотического промотора происходит в клетке млекопитающего. В дальнейшем варианте осуществления бактериальной клеткой является клетка E. coli, а эукариотической клеткой является дрожжевая клетка, клетка CHO, клетка 293 или клетка NSO.
В другом варианте осуществления настоящим изобретением обеспечивается вектор, включающий молекулы нуклеиновых кислот, описанные здесь, и/или клетка-хозяин, трансформированная такими векторами. Клеткой-хозяином может быть бактериальная клетка (например, клетка E. coli) или эукариотическая клетка (например, дрожжевая клетка, клетка CHO, клетка 293 или клетка NSO).
В другом варианте осуществления настоящим изобретением обеспечивается способ продуцирования антитела, включающий культивирование клетки-хозяина, описанной здесь, так что нуклеиновая кислота экспрессируется. Способ, кроме того, включает выделение антитела, экспрессируемого клеткой-хозяином, и причем антитело выделяют из среды для культивирования клетки-хозяина.
В одном аспекте настоящим изобретением обеспечивается адаптерный белок, включающий модификацию по крайней мере одного остатка аминокислотной последовательности SEQ ID NO: 8, 9, 12, 13, 14 или 15. В одном варианте осуществления аминокислотную последовательность выбирают из группы, состоящей SEQ ID NO: 6 (ASIARLRERVKTLRARNYELRSRANMLRERVAQLGGC) или SEQ ID NO: 7 (ASLDELEAEIEQLEEENYALEKEIEDLEKELEKLGGC). В одном варианте осуществления настоящим изобретением обеспечиваются нуклеиновые кислоты, кодирующие такой адаптерный белок.
В одном аспекте настоящим изобретением обеспечивается молекула нуклеиновой кислоты, кодирующая полипептид mBIP, включающий аминокислотную последовательность SEQ ID NO: 3, или ее варианты, которая является функциональной как в прокариотических, так и в эукариотических клетках, или полипептид, имеющий аминокислотную последовательность, гомологичную на 85% аминокислотной последовательности SEQ ID NO: 3. В одном варианте осуществления настоящим изобретением обеспечивается способ экспрессии полипептида mBIP, включающего аминокислотную последовательность SEQ ID NO: 3, или ее варианты, как в прокариотических, так и в эукариотических клетках. В одном варианте осуществления настоящим изобретением обеспечивается бактериальная клетка, которая экспрессирует последовательность mBIP, включающую аминокислотную последовательность SEQ ID NO: 3, или ее варианты.
В одном аспекте в настоящем изобретении предусматривается, что синтетический интрон расположен между нуклеиновой кислотой, кодирующей VH-домен, и нуклеиновой кислотой, кодирующей Fc или шарнирную область антитела, посреди нуклеиновой кислоты, кодирующей CH2- и CH3-домены антитела, посреди нуклеиновой кислоты, кодирующей шарнирную область и CH2-домен антитела.
В одном аспекте настоящее изобретение включает полипептид, включающий сигнальную последовательность, включающую аминокислотную последовательность SEQ ID NO: 3, или ее варианты, вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), причем VH-домен соединен с N-концом VL-домена, или полипептид, включающий сигнальную последовательность, включающую аминокислотную последовательность SEQ ID NO: 3, или ее варианты, вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), причем VH-домен соединен с C-концом VL-домена, или полипептид, включающий сигнальную последовательность, включающую аминокислотную последовательность SEQ ID NO: 3, и VH-HVR1, VH-HVR2 и VH-HVR3 вариабельного домена тяжелой цепи (VH), или полипептид, включающий сигнальную последовательность, включающую аминокислотную последовательность SEQ ID NO: 3, и VL-HVR1, VL-HVR2 и VL-HVR3 вариабельного домена легкой цепи (VL), или полипептид, включающий сигнальную последовательность, включающую аминокислотную последовательность SEQ ID NO: 3, или ее варианты, VH-HVR1, VH-HVR2 и VH-HVR3 вариабельного домена тяжелой цепи (VH) и VL-HVR1, VL-HVR2 и VL-HVR3 вариабельного домена легкой цепи (VL). В одном варианте осуществления полипептидом настоящего изобретения является антитело или фрагмент антитела. Антитело или фрагмент антитела настоящего изобретения можно выбрать из группы, состоящей из F(ab')2- и Fv-фрагментов, диател и молекул одноцепочечных антител.
В одном аспекте настоящее изобретение включает мутантный фаг-помощник для увеличения фагового дисплея белков. В одном варианте осуществления нуклеотидная последовательность фага-помощника включает амбер-мутацию в pIII, причем фаг-помощник, включающий амбер-мутацию, увеличивает дисплей белков, слитых с pIII, на фаге. В дальнейшем варианте осуществления предусматривается нуклеотидная последовательность по пункту 70, причем амбер-мутацией является мутация в нуклеотидах 2613, 2614 и 2616 нуклеиновой кислоты для M13KO7. Еще в одном дальнейшем варианте осуществления предусматривается нуклеотидная последовательность по пункту 71, причем мутация в нуклеотидах 2613, 2614 и 2616 нуклеиновой кислоты для M13KO7 привносит стоп-кодон амбер.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1. (A) Специфический для экспрессирующих Her фагов ELISA очищенного фага с дисплеем Fab против Her2 под контролем четырех различных эукариотических сигнальных последовательностей (mBiP, Gaussia princeps, yBGL2, hGH). Прокариотическая сигнальная последовательность из термостабильного энтеротоксина II (STII), обычно используемая в фагемидах, служит в качестве этанола сравнения. (B) Фаговый дисплей Fab против Her2, слитого с эукариотической сигнальной последовательностью из mBiP дикого типа (mBiP.wt), и вариантами с оптимизацией кодонов, полученными в результате пэннинга библиотеки фагов (mBiP.Opt1, mBiP.Opt2 и mBip.Opt3 (SEQ ID NO: 16-18)).
Фиг. 2. (A) Выходы продуктов экспрессии из 30-мл суспензионных культур клеток 293 для отдельных клонов и (B) суммарная статистика для клонов hIgG1, экспрессированных в виде слияний или с эукариотической сигнальной последовательностью из mBiP, или с прокариотической сигнальной последовательностью из НС природного IgG (VHS).
Фиг. 3. (A) Геномная структура НС IgG1, содержащая три природных интрона. Интрон 1 находится непосредственно перед шарнирной областью. (B) Конструкция для HC, содержащая синтетический интрон, происходящий из интрона 1 или 3 и содержащий фаговый адаптерный пептид слияния. Синтетический интрон фланкирован природной донорной последовательностью сплайсинга интрона (D) и акцепторной последовательностью сплайсинга интрона (A) из интрона 1 или 3. (C) Конструкция для HC, содержащая синтетический интрон, происходящий из интрона 1 или 3 и содержащий фаговый оболочечный белок слияния. Синтетический интрон фланкирован природной донорной последовательностью сплайсинга интрона (D) и акцепторной последовательностью сплайсинга интрона (A) из интрона 1 или 3. Обе конструкции (B) и (C) содержат стоп-кодон на 3'-конце последовательности адаптерного пептида или белка оболочки фага.
Фиг. 4. (A) Уровни экспрессии IgG h4D5 с конструкции, или не содержащей интрон, или содержащей синтетический интрон, содержащий фаговый адаптерный пептид (см. фиг. 3B), или синтетический интрон, содержащий белок оболочки фага (ген-III, см. фиг. 3C). (B) ПЦР в режиме реального времени НС hIgG1 из трансфецированных клеток. Предсказанный размер подвергнутой надлежащему сплайсингу мРНК для HC составляет 1650 нуклеотидов. Верхняя полоса в случае конструкции адаптер + интрон 1 представляет собой не подвергнутую сплайсингу мРНК-предшественник. Нижняя полоса в случае содержащих адаптер и ген-III конструкций подвергнута ненадлежащему сплайсингу с использованием скрытой донорной последовательности сплайсинга в VH.
Фиг. 5. (A) Точечные мутации, введенные в природную донорную последовательности сплайсинга интрона 1 для увеличения соответствия консенсусной донорной последовательности сплайсинга для мРНК млекопитающих. (B) Оптимизация донорной последовательности сплайсинга интрона устраняет накопление не подвергнутой сплайсингу или подвергнутой ненадлежащему сплайсингу мРНК для HC и (C) увеличивает экспрессию в клетках млекопитающих до уровней, отмечаемых в случае отсутствия интрона.
Фиг. 6. (A) Модуляция дисплея, используя pDV.5.0 и либо KО7 дикого типа (одновалентный дисплей), либо адаптер-KО7 (поливалентный дисплей). (B) Экспрессия четырех различных мАт с pDV.5.0 в трех различных линиях клеток млекопитающих.
Фиг. 7. Схема вектора для экспрессии и секреции полипептидов в прокариотических и эукариотических клетках. Синтетический интрон может содержать или адаптерную последовательность, или последовательность белка оболочки фага вместе с любой из встречающихся в природе последовательностей интронов из hIgG1. И HC, и LC могут иметь или: 1) промоторы бактерий и млекопитающих 5' от ORF (открытой рамки считывания, 2) только бактериальный промотор 5' от ORF (см. также фиг. 14), или 3) только промотор млекопитающих 5' от ORF. Представлена конструкция, в которой и HC, и LC имеют оба типа промоторов. Кассета, содержащая слияние гена-III с адаптерным пептидом, (представлен pDV5.0) присутствует только, когда синтетический интрон содержит слияние с адаптерным пептидом, но не когда слияние с белком оболочки фага присутствует в синтетическом интроне.
Фиг. 8. Нуклеотидная последовательность pIII (нуклеотиды 1579-2853 (SEQ ID NO: 24)) мутантного фага-помощника Amber KО7 для увеличения дисплея белков, слитых с pIII, на фаге M13. Amber KО7 содержит амбер-кодон, введенный в геном фага-помощника M13KO7 с помощью сайт-направленного мутагенеза. Подчеркнутые остатки представляют собой мутации в нуклеотидах 2613, 2614 и 2616 (T2613C, C2614T и A2616G), которые привносят стоп-кодон амбер (TAG) в кодон 346 и молчащую мутацию для рестрикционного сайта для AvrII в кодон 345 гена III М13КО7. Нуклеотид 1 M13KO7 является третьим остатком уникального рестрикционного сайта для HpaI.
Фиг. 9. Увеличенный дисплей Fab-фрагментов на pIII фага M13 при использовании фага-помощника Amber-KО7. Обычная фагемида с высоким уровнем дисплея вместе с M13KO7 дикого типа (открытые ромбы) приводит к уровням дисплея Fab, значительно превышающим таковые, достигаемые с помощью фагемидного вектора с низким уровнем дисплея (замкнутые квадраты), когда M13KO7 дикого типа используется для продукции фагов. Использование модифицированного M13KO7, содержащего амбер-мутацию в pIII, (Amber KО7) увеличивает уровень дисплея фагемидой с низким уровнем дисплея (замкнутые треугольники) до уровня, достигаемого при использовании фагемиды с высоким уровнем дисплея вместе с M13KO7 дикого типа (открытые ромбы).
Фиг. 10 представляет собой столбчатую диаграмму, на которой продемонстрировано связывание (измеренное с помощью ELISA для фагов) клонов, отобранных в результате сортировки библиотеки фагов - библиотеки двойственных векторов Fab-фагов на основе не иммунизированных источников примера 5 против иммобилизованного VEGF. Отдельные клоны были отобраны после четырех циклов отбора, и содержащие фаги супернатанты были проверены в отношении связывания с иммобилизованным антигеном (VEGF) и с нерелевантным белком (Her2) для оценки специфичности связывания.
На фиг. 11 продемонстрирован скрининг отобранных фаговых клонов в IgG-формате с помощью BIAcore на предмет связывания с антигеном - VEGF, определяемому с помощью анализа захвата Fc, используя прибор BIAcore T100. 96 клонов, которые были отобраны для анализа последовательности и ELISA для фагов, были трансфецированы в клетки 293S (1 мл) и подвергнуты культивированию в течение семи дней для экспрессии IgG. Супернатанты пропускали через 0,2-мкм фильтр и использовали для оценки связывания с антигеном VEGF с помощью анализа захвата Fc, используя прибор BIAcore T100.
На фиг. 12 представлены последовательности позитивных связующих веществ из эксперимента по пэннингу против VEGF примера 5. Представлена последовательность CDR тяжелой цепи для восьми клонов (VEGF50 (SEQ ID NO: 25-27, соответственно, в порядке представления), VEGF51 (SEQ ID NO: 28-30, соответственно, в порядке представления), VEGF52 (SEQ ID NO: 31-33, соответственно, в порядке представления), VEGF59 (SEQ ID NO: 34-36, соответственно, в порядке представления), VEGF55 (SEQ ID NO: 37-39, соответственно, в порядке представления), VEGF60 (SEQ ID NO: 40-42, соответственно, в порядке представления), VEGF61 (SEQ ID NO: 43-45, соответственно, в порядке представления) и VEGF64 (SEQ ID NO: 46-48, соответственно, в порядке представления)). Все клоны имеют одинаковую последовательность CDR легкой цепи.
На фиг. 13 продемонстрирована способность отобранных IgG против VEGF, отобранных в результате сортировки фагов против VEGF, к ингибированию связывания VEGF с одним из его природных рецепторов, VEGF-R1. Антитела, отобранные в результате сортировки против VEGF, были экспрессированы в клетках CHO, и очищенный IgG использовали для определения способности отобранных клонов к ингибированию связывания VEGF с VEGF-R1. Один клон (VEGF55) ингибировал связывание VEGF-R1 с IC50, которая была в 3,5-кратных пределах таковой для бевацизумаба (Avastin).
На фиг. 14 представлена схема вектора для экспрессии и секреции полипептидов в прокариотических и эукариотических клетках, причем синтетический интрон содержит pIII, вместе с любой из встречающихся в природе последовательностей интронов из hIgG1, и причем LC имеет бактериальный промотор 5' от ORF, а HC имеет и промотор млекопитающего, и бактериальный промотор 5' от ORF. В отличие от вектора, представлено на фиг. 7, этому вектору (pDV6.5) не требуется дополнительная кассета gIII для слияния с фаговыми частицами. Белки, являющиеся результатом экспрессии в E. coli и клетках млекопитающих, представлены под схемой вектора. Пунктирные линии означают интроны в транскрипте для тяжелой цепи, вырезаемые в клетках млекопитающих. Обратите внимание, что часть последовательности, кодирующей шарнирную область IgG1, повторена в этом векторе для допуска включения в экспрессируемые и в E. coli, и в клетках млекопитающих белки.
На фиг. 15 представлены характеристики полноразмерных IgG против VEGF, экспрессированных с pDV6.5. IgG были экспрессированы в 100-мл культурах трансфецированных клеток CHO и подвергнуты очистке с помощью хроматографии с использованием белка A. Конечные выходы очищенного IgG указаны вместе с оценкой в ELISA для бакуловирусов, использованного для измерения неспецифического связывания. Также указано позитивное или негативное связывание каждого клона в фаговом формате (в ELISA для фагов) или IgG-формате (BIAcore).
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
I. ОПРЕДЕЛЕНИЯ
Термин «синтетический интрон», как здесь используется, определяет сегмент нуклеиновой кислоты, который расположен между нуклеиновой кислотой, кодирующей CH1, и нуклеиновой кислотой, кодирующей шарнирную область-Fc или Fc. «Синтетический интрон» может быть любой нуклеиновой кислотой, которая не кодирует синтез белка, любой нуклеиновой кислотой, которая действительно кодирует синтез белка, такого как белок фаговой частицы или белок оболочки (например, pI, pII, pIII, pIV, pV, pVI, pVII, pVIII, pFX, pX), или адаптерный белок (например, белок «лейциновая молния» и т.д.), или любая их комбинация. В одном варианте осуществления «синтетический интрон» включает часть донорной последовательности сплайсинга и акцепторной последовательности сплайсинга, которые делают возможным событие сплайсинга. Донорная и акцепторная последовательности сплайсинга делают возможным событие сплайсинга и могут включать природные или синтетические последовательности нуклеиновых кислот.
Термин «полезный полипептид», как здесь используется, относится к полипептиду, который применим для ряда мероприятий, например, применим для очистки белка, маркировки белка, мечения белка (например, мечения обнаруживаемым соединением или композицией (например, радиоактивной меткой, флуоресцентной меткой или ферментной меткой). Метка может быть непосредственно конъюгирована с боковой цепью аминокислоты, активированной боковой цепью аминокислоты, антителом с созданным цистеином и т.п. Например, антитело можно конъюгировать с биотином, и любую из трех широких классов меток, отмеченных выше, можно конъюгировать с авидином или стрептавидином, или наоборот. Биотин связывается селективно со стрептавидином, и таким образом, метку можно конъюгировать с антителом таким опосредованным образом. Альтернативно, для достижения опосредованного конъюгирования метки с вариантом полипептида, вариант полипептида конъюгируют с небольшим гаптеном (например, дигоксином), и один из различных типов меток, упомянутых выше, конъюгируют с направленным против гаптена вариантом полипептида (например, антителом против дигоксина). Таким образом, можно достичь опосредованного конъюгирования метки с вариантом полипептида (Hermanson, G. (1996) in Bioconjugate Techniques Academic Press, San Diego).
Нуклеиновая кислота является «функционально связанной», когда она находится в функциональной связи с другой последовательностью нуклеиновой кислоты. Например, ДНК для предпоследовательности или секреторной лидерной последовательности является функционально связанной с ДНК для полипептида, если она экспрессируется в виде белка-предшественника, который участвует в секреции полипептида; промотор или энхансер является функционально связанным с кодирующей последовательностью, если он влияет на транскрипцию последовательности; сайт связывания рибосомы является функционально связанным с кодирующей последовательностью, если он размещен, чтобы способствовать трансляции. Как правило, «функционально связанные» означает, что связанные последовательности ДНК существуют в молекуле нуклеиновой кислоты таким образом, что они имеют функциональную связь друг с другом как нуклеиновые кислоты или как белки, которые экспрессируются ими. Они могут быть смежными или нет. В случае секреторной лидерной последовательности они часто являются смежными и находятся в фазе считывания. Однако энхансеры не должны быть смежными. Связывание выполняют посредством лигирования в подходящих рестрикционных сайтах. Если такие сайты не существуют, могут использоваться синтетические олигонуклеотидные адаптеры или линкеры.
VH- или VL-домены «связаны» с фагом, когда нуклеиновая кислота, кодирующая гетерологичную белковую последовательность (например, VH- или VL-домены), вставлена непосредственно в нуклеиновую кислоту, кодирующую белок оболочки фага (например, pII, pVI, pVII, pVIII или pIX). После введения в прокариотическую клетку будет продуцироваться фаг, белок оболочки которого может демонстрировать VH- или VL-домены. В одном варианте осуществления получающиеся фаговые частицы осуществляют дисплей фрагментов антител, слитых с амино-концом или карбоксильным концом белков оболочки фагов.
Используемые здесь термины «связанные» или «связи», или «связь», как подразумевается, относятся к ковалентному соединению двух аминокислотных последовательностей или двух последовательностей нуклеиновых кислот вместе с помощью пептидных или фосфодиэфирных связей, соответственно, такое соединение может включать любое количество дополнительных аминокислотных или нуклеотидных последовательностей между двумя аминокислотными последовательностями или последовательностями нуклеиновых кислот, которые соединяют. Например, между первой и второй аминокислотными последовательностями может существовать прямая связь в виде пептидной связи или связь, в которую вовлечена одна или более аминокислотных последовательностей между первой и второй аминокислотными последовательностями.
Под «линкером», как здесь используется, подразумевается аминокислотная последовательность длиной две или более аминокислот. Линкер может состоять из нейтральных полярных или неполярных аминокислот. Длина линкера может составлять, например, 2-100 аминокислоты, например, 2-50 аминокислот, например, 3, 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50 аминокислот. Линкер может быть «расщепляемым», например, в результате саморасщепления, или ферментативного или химического расщепления. Сайты расщепления в аминокислотных последовательностях, и ферменты и химические вещества, которые осуществляют расщепление в таких сайтах, хорошо известны в данной области техники, а также здесь описаны.
Термин «функции сигнальной последовательности» относится к биологической активности сигнальной последовательности, направляющей секретируемые белки в ER (у эукариот) или периплазму (у прокариот) или наружную часть клетки.
«Контрольный белок», как здесь используется, относится к белковой последовательности, экспрессию которой измеряют для количественного определения уровня дисплея белковой последовательности. Например, белковой последовательностью может быть «эпитопная метка», которая позволяет легко очистить VH или VL с помощью аффинной очистки, используя антитело против метки или другой тип аффинной матрицы, который связывается с эпитопной меткой. Примеры полипептидов-меток и соответствующих им антител, которые являются подходящими, включают: полигистидиновые (поли-His) метки или метки в виде поли(гистидин-глицин) (поли-His-gly); полипептид-метка в виде HA гриппа и антитело против него 12CA5 [Field et al, Mol. Cell. Biol., 8:2159-2165 (1988)]; метка c-myc и антитела против нее 8F9, 3C7, 6E10, G4, B7 и 9E10 [Evan et al., Molecular and Cellular Biology, 5: 3610-3616 (1985)]; и метка в виде гликопротеина D (gD) вируса простого герпеса и антитело против нее [Paborsky et al., Protein Engineering, 3(6): 547-553 (1990)]. Другие полипептиды-метки включают Flag-пептид [Hopp et al., BioTechnology, 6: 1204-1210 (1988)]; пептидный эпитоп KT3 [Martin et al., Science, 255: 192-194 (1992)]; пептидный эпитоп α-тубулина [Skinner et al., J. Biol. Chem., 266: 15163-15166 (1991)]; и пептидная метка гена 10 T7 [Lutz-Freyermuth et al., Proc. Natl. Acad. Sci. USA, 87: 6393-6397 (1990)].
«Белок оболочки», как здесь используется, относится к любому из пяти капсидных белков, которые являются компонентами фаговых частиц, включая pIII, pVI, pVII, pVIII и pIX. В одном варианте осуществления «белок оболочки» может использоваться для дисплея белков или пептидов (см. Phage Display, A Practical Approach, Oxford University Press, edited by Clackson and Lowman, 2004, p. 1-26). В одном варианте осуществления белком оболочки может быть белок pIII или какой-либо его вариант, часть и/или производное. Например, может использоваться C-концевая часть белка оболочки pIII бактериофага M13 (cP3), такая как последовательность, кодирующая C-концевые остатки 267-421 белка III фага M13. В одном варианте осуществления последовательность pIII включает аминокислотную последовательность SEQ ID NO:

В одном варианте осуществления фрагмент pIII включает аминокислотную последовательность SEQ ID NO: 2  «Адаптерный белок», как здесь используется, относится к последовательности белка, которая специфически взаимодействует с другой последовательностью адаптерного белка в растворе. В одном варианте осуществления «адаптерный белок» включает домен гетеромультимеризации. В одном варианте осуществления адаптерным белком является белок cJUN или белок Fos. В другом варианте осуществления адаптерный белок включает последовательность SEQ ID NO: 6 (ASIARLRERVKTLRARNYELRSRANMLRERVAQLGGC) или SEQ ID NO: 7 (ASLDELEAEIEQLEEENYALEKEIEDLEKELEKLGGC).
«Адаптерный белок», как здесь используется, относится к последовательности белка, которая специфически взаимодействует с другой последовательностью адаптерного белка в растворе. В одном варианте осуществления «адаптерный белок» включает домен гетеромультимеризации. В одном варианте осуществления адаптерным белком является белок cJUN или белок Fos. В другом варианте осуществления адаптерный белок включает последовательность SEQ ID NO: 6 (ASIARLRERVKTLRARNYELRSRANMLRERVAQLGGC) или SEQ ID NO: 7 (ASLDELEAEIEQLEEENYALEKEIEDLEKELEKLGGC).
Как здесь используется, «домен гетеромультимеризации» относится к изменениям биологической молекулы или добавлениям к ней, чтобы способствовать образованию гетеромультимера или препятствовать образованию гомомультимера. Любой домен гетеродимеризации со строгим предпочтением образования гетеродимеров относительно гомодимеров находится в объеме настоящего изобретения. Иллюстративные примеры включают, но без ограничения, например, заявку на патент США с № 20030078385 (Arathoon et al. - Genentech; в которой описывается выступ во впадины); WO 2007147901 (Kjasrgaard et al. - Novo Nordisk: в которой описываются ионные взаимодействия); WO 2009089004 (Kannan et al. - Amgen: в которой описываются эффекты электростатического наведения); WO2011/034605 (Christensen et al. - Genentech; в которой описываются суперспирали). См. также, например, Pack, P. & Plueckthun, A., Biochemistry 31, 1579-1584 (1992), в котором описывается лейциновая молния, или Pack et al., Bio/Technology 11, 1271-1277 (1993), в котором описывается мотив спираль-петля-спираль. Выражения «домен гетеромультимеризации» и «домен гетеродимеризации» используются здесь взаимозаменяемо.
Термин «слитый с Fab белок», как здесь используется, относится к слитому Fab-фаговый полипептид белку в прокариотических клетках и/или слитому Fab-Fc белку в эукариотических клетках. Слиянием Fab-Fc может также быть слияние Fab-шарнир-Fc.
Термин «антитело» используется здесь в самом широком значении и охватывает различные структуры антител, включающие, но без ограничения, моноклональные антитела, поликлональные антитела, полиспецифические антитела (например, биспецифические антитела) и фрагменты антител, если они проявляют желаемую активность связывания с антигеном.
«Фрагмент антитела» относится к молекуле, отличной от интактного антитела, которая включают часть интактного антитела, которая связывается с антигеном, с которым связывается интактное антитело. Примеры фрагментов антител включают, но без ограничения, Fv, Fab, Fab', Fab'-SH, F(ab')2; диатела; линейные антитела; одноцепочечные молекулы антител (например, scFv); и полиспецифические антитела, образованные из фрагментов антител.
«Класс» антитела относится к типу константного домена или константной области, который имеет его тяжелая цепь. Существует пять основных классов антител: IgA, IgD, IgE, IgG и IgM - и некоторые из них можно, кроме того, подразделить на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелой цепи, соответствующие различным классам иммуноглобулинов, называют α, δ, ε, γ и μ, соответственно.
Термин «Fc-область» здесь используется для определения C-концевой области тяжелой цепи иммуноглобулина, которая содержит по крайней мере часть константной области. Этот термин включает Fc-области со встречающимися в природе последовательностями и варианты Fc-областей. В одном варианте осуществления Fc-область тяжелой цепи IgG человека простирается от Cys226, или от Pro230, до карбоксильного конца тяжелой цепи. Однако C-концевой лизин (Lys447) Fc-области может присутствовать или может не присутствовать. Кроме случаев, оговоренных здесь особо, нумерация аминокислотных остатков в Fc-области или константной области соответствует EU системе нумерации, также называемой EU индексом, описанной в Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD, 1991.
«Каркасная область» или «FR» относится к остаткам вариабельного домена, отличным от остатков гипервариабельного участка (HVR). FR вариабельного домена, как правило, состоит из четырех FR-доменов: FR1, FR2, FR3 и FR4. Соответственно, последовательности HVR и FR, как правило, обнаруживаются в следующем порядке в VH (или VL): FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4.
Термины «полноразмерное антитело», «интактное антитело» или «полное антитело» используются здесь взаимозаменяемо для ссылки на антитело, имеющее структуру, в значительной степени сходную со структурой встречающегося в природе антитела, или имеющее тяжелые цепи, которые содержат Fc-область, определенную здесь.
Термины «клетка-хозяин», «линия клеток-хозяев» и «культура клеток-хозяев» используются взаимозаменяемо и относятся к клеткам, в которые была введена экзогенная нуклеиновая кислота, в том числе потомству таких клеток. Клетки-хозяева включают «трансформанты» и «трансформированные клетки», которые включают первичные трансформированные клетки и происходящее от них потомство независимо от числа пассажей. Потомство может быть полностью идентично по содержимому нуклеиновых кислот родительской клетке, но может содержать мутации. Мутантные потомки, которые имеют функцию или биологическую активность, одинаковую с той, которая была отобрана для первоначально трансформированной клетки, включены сюда.
Используемый здесь термин «гипервариабельный участок» или «HVR» относится к каждому из участков вариабельного домена антитела, которые является гипервариабельными по последовательности и/или образуют структурно определяемые петли («гипервариабельные петлевые участки»). Как правило, встречающиеся в природе четырехцепочечные антитела включают шесть HVR; три в VН (Н1, Н2, Н3) и три в VL (L1, L2, L3). HVR, как правило, включают аминокислотные остатки из гипервариабельных петлевых участков и/или из «определяющих комплементарность участков» (CDR), при этом последние характеризуются наибольшей вариабельностью последовательности и/или вовлечены в распознавание антигена. Приводимые в качестве примера гипервариабельные петлевые участки встречаются в положениях аминокислотных остатков 26-32 (L1), 50-52 (L2), 91-96 (L3), 26-32 (H1), 53-55 (H2) и 96-101 (H3) (Chothia and Lesk, J. Mol. Biol. 196: 901-917 (1987)). Приводимые в качестве примера CDR (CDR-L1, CDR-L2, CDR-L3, CDR-H1, CDR-H2 и CDR-H3) встречаются в положениях аминокислотных остатков 24-34 L1, 50-56 L2, 89-97 L3, 31-35B H1, 50-65 H2 и 95-102 H3. (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991)). За исключением CDR1 в VH, CDR, как правило, включают аминокислотные остатки, которые образуют гипервариабельные петлевые участки. CDR также включают «определяющие специфичность остатки» или «SDR», которые являются остатками, которые контактируют с антигеном. SDR содержатся в участках CDR, называемых укороченными-CDR или a-CDR. Приводимые в качестве примера a-CDR (a-CDR-L1, a-CDR-L2, a-CDR-L3, a-CDR-H1, a-CDR-H2 и a-CDR-H3) встречаются в положениях аминокислотных остатков 31-34 L1, 50-55 L2, 89-96 L3, 31-35B H1, 50-58 H2 и 95-102 H3. (См. Almagro and Fransson, Front. Biosci. 13: 1619-1633 (2008).) За исключением особо оговоренных случаев, остатки HVR и другие остатки в вариабельном домене (например, остатки FR) пронумерованы здесь в соответствии с Kabat и др., выше.
«Индивидуумом» или «субъектом» является млекопитающее. Млекопитающие включают, но без ограничения, одомашненных животных (например, коров, овец, кошек, собак и лошадей), приматов (например, людей и не являющихся людьми приматов, таких как обезьяны), кроликов и грызунов (например, мышей и крыс). В некоторых вариантах осуществления индивидуумом или субъектом является человек.
«Изолированным антителом» является антитело, которое было отделено от компонента его природного окружения. В некоторых вариантах осуществления антитело очищено до степени чистоты, превышающей 95% или 99%, как определено, например, с помощью электрофоретических способов (например, электрофореза в SDS-ПААГ, изоэлектрофокусировки (IEF), капиллярного электрофореза) или хроматографических способов (например, ионообменной HPLC или HPLC с обращенной фазой). Для обзора способов оценки степени чистоты антител см., например, Flatman et al., J. Chromatogr. B 848: 79-87 (2007).
«Выделенная» нуклеиновая кислота относится к молекуле нуклеиновой кислоты, которая была отделена от компонента ее природного окружения. Выделенная нуклеиновая кислота включает молекулу нуклеиновой кислоты, содержащуюся в клетках, которые обычно содержат молекулу нуклеиновой кислоты, но молекула нуклеиновой кислоты присутствует экстрахромосомно или в положении в хромосоме, которое отличается от ее природного положения в хромосоме.
«Выделенная нуклеиновая кислота, кодирующая антитело», относится к одной или более молекул нуклеиновых кислот, кодирующих тяжелую и легкие цепи антитела (или их фрагменты), в том числе такой молекуле(ам) нуклеиновой кислоты в одном векторе или отдельных векторах, и такой молекуле(ам) нуклеиновой кислоты, присутствующей в одном или более положений в клетке-хозяине.
Используемый здесь термин «моноклональное антитело» относится к антителу, полученному из популяции по существу гомогенных антител, т.е. отдельные антитела, составляющие популяцию, являются идентичными и/или связываются с одним и тем же эпитопом, за исключением возможных вариантов антител, например, содержащих встречающиеся в природе мутации или возникающих во время приготовления препарата моноклональных антител, при этом такие варианты, как правило, присутствуют в незначительных количествах. В отличие от препаратов поликлональных антител, которые типично включают различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело препарата моноклональных антител направлено против одной антигенной детерминанты. Таким образом, определение «моноклональное» указывает на то, что характеристикой антитела является то, что его получают из по существу гомогенной популяции антител, и не должно рассматривается как требование продукции антитела каким-либо конкретным способом. Например, моноклональные антитела, используемые в соответствии с настоящим изобретением, можно создать с помощью ряда методов, включающих, но без ограничения, гибридомную технологию, методы рекомбинантных ДНК, методы фагового дисплея и методы с использованием трансгенных животных, содержащих все или часть иммуноглобулиновых локусов человека, при этом такие методы и другие, приводимые в качестве примера методы создания моноклональных антител описываются здесь.
«Не конъюгированное антитело» относится к антителу, которое не конъюгировано с гетерологичной составляющей (например, цитотоксической составляющей) или радиоактивной меткой. Не конъюгированное антитело может присутствовать в фармацевтическом препарате.
«Природные антитела» относятся к встречающимся в природе молекулам иммуноглобулинов с изменяющимися структурами. Например, природные антитела класса IgG представляют собой гетеротетрамерные гликопротеины с М.м., составляющей приблизительно 150000 Дальтон, состоящие из двух идентичных легких цепей и двух идентичных тяжелых цепей, которые соединены посредством дисульфидных связей. От N- к C-концу, каждая тяжелая цепь содержит вариабельную область (VH), также называемую вариабельным доменом тяжелой цепи, за которой следуют три константных домена (CH1, CH2 и CH3). Так же, от N- к C-концу, каждая легкая цепь содержит вариабельную область (VL), также называемую вариабельным доменом легкой цепи, за которой следует константный домен легкой цепи (CL). Легкую цепь антитела можно отнести к одному из двух типов, называемых каппа (κ) и лямбда (λ), на основе аминокислотной последовательности ее константного домена.
Термин «листовка-вкладыш», как используется, относится к инструкциям, обычно включаемым в промышленные упаковки терапевтических продуктов, которые содержат информацию о показаниях, применении, дозе, введении, комбинированной терапии, противопоказаниях и/или предостережениях в отношении применения таких терапевтических продуктов.
Термин «вариабельная область» или «вариабельный домен» относится к домену тяжелой или легкой цепи антитела, который участвует в связывания антитела с антигеном. Вариабельные домены тяжелой цепи и легкой цепи (VH и VL, соответственно) природного антитела, как правило, имеют схожие структуры, при этом каждый домен включает четыре консервативные каркасные области (FR) и три гипервариабельных участка (HVR). (См., например, Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007).) Одного VH- или VL-домена может быть достаточно для придания специфичности связывания с антигеном. Кроме того, антитела, которые связываются с конкретным антигеном, можно выделить, используя VH- или VL-домен из антитела, которое связывается с антигеном, для скрининга библиотеки комплементарных VL- или VH-доменов, соответственно. См., например, Portolano et al., J. Immunol. 150: 880-887 (1993); Clarkson et al., Nature 352: 624-628 (1991).
Используемый здесь термин «вектор» относится к молекуле нуклеиновой кислоты, способной репродуцировать другую нуклеиновую кислоту, с которой она связана. Термин включает вектор в виде самореплицирующейся полинуклеотидной структуры, а также вектор, включаемый в геном клетки-хозяина, в которую он был введен. Некоторые векторы способны управлять экспрессией нуклеиновых кислот, с которыми они функционально связаны. Такие векторы называют здесь «экспрессионными векторами».
II. ПОДРОБНОЕ ОПИСАНИЕ
В процессе отыскания антител, основанных на фагах, используется технология фагового дисплея для отбора Fab-фрагментов с желаемыми специфичностями связывания из больших совокупностей отдельных фаговых клонов1-3. В этом подходе создают библиотеки фагов, состоящие из Fab-фрагментов, слитых с частицами нитчатых фагов M13, или непосредственно, или опосредованного через один из основных белков оболочки, и содержащие разнообразные определяющие комплементарность участки (CDR), используя широко известные методы молекулярной биологии и приспособленные для фагового дисплея векторы (Tohidkia et al., Journal of drus targeting, 20: 195-208 (2012); Bradbury et al., Nature biotechnology, 29: 245-254 (2011); Qi et al., Journal of molecular biology, 417: 129-143 (2012)). Хотя теоретическое разнообразие таких библиотек может легко превышать 1025 уникальных последовательностей, практические ограничения при создании совокупностей фагов типично ограничивают фактическое разнообразие до ≤1011 клонов в случае конкретной библиотеки (Sidhu et al., Methods in enzymology, 328: 333-363 (2000)).
Принимая во внимание значительное количество уникальных последовательностей, которое может содержать исходная библиотека, пропускная способность скрининга отобранных клонов имеет решающее значение. В случае отыскания основанных на фагах антител для тщательной оценки отбираемых Fab-фрагментов и свойств родственных им полноразмерных IgG в функциональных анализах (анализах связывания мишени, клеточных анализах активности, при определении in vivo полупериода существования) требуется изменение Fab-формата последовательностей тяжелой цепи (HC) и легкой цепи (LC) на полноразмерный IgG посредством субклонирования последовательностей ДНК, кодирующих HC и LC, из фагемидного вектора, использованного для дисплея, в векторы для экспрессии в клетках млекопитающих для экспрессии IgG. Трудоемкий процесс субклонирования дюжим или сотен отобранных пар HC/LC представляет собой основное «узкое место» в процессе отыскания основанных на фагах антител. Кроме того, поскольку значительная часть отобранных Fab, после изменения формата, не имеет удовлетворительные эксплуатационные свойства в первоначальных скрининговых исследованиях, увеличение количества клонов, которые проводят через этот процесс изменения формата/скрининга, сильно увеличивает наибольшую вероятность успеха.
Здесь описывается создание системы экспрессии и секреции для экспрессии и секреции одного слитого с Fab белка в прокариотических клетках и отличного (или идентичного) слитого с Fab белка в эукариотических клетках. Например, система экспрессии и секреции осуществляет экспрессию слияния Fab-фаговый полипептид в случае трансформации E. coli и осуществляет экспрессию полноразмерного IgG, содержащего тот же самый Fab-фрагмент, в случае трансфекции клеток млекопитающих. Авторы настоящего изобретения демонстрируют, что сигнальная последовательность млекопитающего из мышиного связывающего иммуноглобулинового белка (mBiP)8,9 может приводить к эффективной экспрессии белков как в прокариотических, так и в эукариотических клетках. Используя сплайсинг мРНК млекопитающих для удаления синтетического интрона, содержащего фаговый пептид слияния, вставленный в шарнирную область НС IgG1 человека, авторы настоящего изобретения способны создать два различных белка зависимым от клетки-хозяина образом: Fab-фрагмент, слитый с адаптерным пептидом для фагового дисплея в E. coli, и природный IgG1 человека в клетках млекопитающих. Эта технология позволяет отобрать Fab-фрагменты, которые связываются с представляющим интерес антигеном, из библиотеки фагового дисплея с последующей экспрессией и очисткой родственных полноразмерных IgG в клетках млекопитающих без необходимости в субклонировании.
Настоящее изобретение основано, частично, на экспериментальных данных, показывающих, что (1) сигнальные последовательности небактериального происхождения функционируют в прокариотических клетках на уровнях, достаточных для сортировки библиотек фагов, без подрыва экспрессии IgG в эукариотических клетках, и (2) различные слитые с Fab белки экспрессируются с одной и той же молекулы нуклеиновой кислоты зависимым от клетки-хозяина образом, когда процессирование мРНК происходит в эукариотических клетках, но не в прокариотических клетках (слитые Fab-фаговый полипептид белки в прокариотических клетках и слитые Fab-Fc белки в эукариотических клетках). Соответственно, здесь описывается система экспрессии и секреции для экспрессии и секреции Fab-фрагмента, слитого с белком фаговой частицы, белком оболочки или адаптерным белком, для фагового дисплея в прокариотических клетках-хозяевах (например, E. coli) и Fab-фрагмента, слитого с Fc, в эукариотических клетках (например, клетках млекопитающих), без необходимости в субклонировании, и способы, относящиеся к созданию и применению системы экспрессии и секреции. В частности, здесь описываются векторы для экспрессии и секреции слитого Fab-фаговый полипептид белка в прокариотических клетках и слитого Fab-Fc белка в эукариотических клетках, молекулы нуклеиновых кислот для экспрессии и секреции белков или пептидов в прокариотических и эукариотических клетках, и клетки-хозяева, включающие такие векторы. Кроме того, здесь описываются способы применения системы экспрессии и секреции, в том числе способы применения системы экспрессии и секреции для скрининга и отбора новых антител против представляющих интерес белков.
Варианты осуществления настоящего изобретения
При осуществлении на практике настоящего изобретения будут использоваться, кроме особо оговоренных случаев, обычные методы молекулярной биологии (включая рекомбинантные методы), микробиологии, клеточной биологии, биохимии и иммунологии, которые находятся в пределах знаний в данной области техники. Такие методы полностью объяснены в литературе, например, "Molecular Cloning: A Laboratory Manual", 2nd edition (Sambrook et al., 1989); "Oligonucleotide Synthesis" (M.J. Gait, ed., 1984); "Animal Cell Culture" (R.I. Freshney, ed., 1987); "Methods in Enzymology" (Academic Press, Inc.); "Handbook of Experimental Immunology", 4th edition (D.M. Weir & C.C. Blackwell, eds., Blackwell Science Inc., 1987); "Gene Transfer Vectors for Mammalian Cells" (J.M. Miller & M.P. Calos, eds., 1987); "Current Protocols in Molecular Biology" (F.M. Ausubel et al., eds., 1987); "PCR: The Polymerase Chain Reaction", (Mullis et al., eds., 1994); и "Current Protocols in Immunology" (J.E. Coligan et al, eds., 1991).
Система экспрессии и секреции для прокариотических и эукариотических клеток
Система экспрессии и секреции для прокариотических и эукариотических клеток включает вектор, который содержит регуляторные и кодирующие последовательности для представляющего интерес белка (например, тяжелой или легкой цепи молекулы IgG), причем прокариотические и эукариотические промоторы (например, CMV (эукариотический) и PhoA (прокариотический)) расположены последовательно 5' от представляющего интерес гена(ов), и одинаковые сигнальные последовательности управляют экспрессией представляющего интерес белка в прокариотических и эукариотических клетках. Настоящим изобретением обеспечивается возможность в случае этого вектора создания двух различных слитых форм представляющего интерес белка зависимым от клетки-хозяина образом посредством использования синтетического интрона, расположенного между VH/CH1 и шарнирной областью-Fc-областью IgG1, причем синтетический интрон вырезается во время процессирования мРНК в эукариотических клетках.
А. Сигнальная последовательность, которая функционируют как в прокариотических, так и в эукариотических клетках.
Одна проблема при конструировании вектора, способного к экспрессии представляющих интерес белков как в прокариотических (E. coli), так и эукариотических клетках (млекопитающих) является результатом различий в сигнальных последовательностях, встречающихся в этих типах клеток. Хотя некоторые особенности сигнальных последовательностей являются, как правило, консервативными и в прокариотических, и в эукариотических клетках (например, участок гидрофобных остатков, расположенный в середине последовательности, и полярные/заряженные остатки вблизи сайта расщепления на N-конце зрелого полипептида), другие более характерны для одного типа клеток, чем другого. Кроме того, в данной области техники известно, что различные сигнальные последовательности могут оказывать значительное влияние на уровни экспрессии в клетках млекопитающих, даже если все последовательности происходят от млекопитающих (Hall et al., J of Biological Chemistry, 265: 19996-19999 (1990); Humphreys et al., Protein Expression and Purification, 20: 252-264 (2000)). Например, бактериальные сигнальные последовательности типично содержат положительно заряженные остатки (чаще всего лизин) непосредственно после инициирующего метионина, тогда как они не всегда присутствуют в сигнальных последовательностях млекопитающих. Хотя существуют известные сигнальные последовательности, способные управлять секрецией в обоих типах клеток, такие сигнальные последовательности типично приводят к высоким уровням секреции белков только в одном типе клеток или другом.
Хотя бактериальные сигнальные последовательности, как было установлено, очень редко проявляют какую-либо функциональность в клетках млекопитающих, были сообщения о сигнальных последовательностях, происходящих от млекопитающих, которые способны приводить к транслокации в периплазму бактерий (Humphreys et al., The Protein Expression and Purification, 20: 252-264 (2000)). Однако сама по себе функциональность сигнальной последовательности не является достаточной для использования сильной двойственной экспрессионной системы для фагового дисплея и экспрессии IgG. Точнее, выбранная сигнальная последовательность должна функционировать хорошо в обеих экспрессионных системах, в частности, для фагового дисплея, в случае которого низкие уровни дисплея будут подрывать возможность использования системы для выполнения экспериментов по пэннингу фагов.
Настоящее изобретение основано частично на обнаружении того, что сигнальные последовательности небактериального происхождения функционируют в прокариотических клетках на уровнях, достаточных для сортировки библиотек фагов, без подрыва экспрессии IgG в эукариотических клетках.
В настоящем изобретении предусматривается, что может использоваться любая сигнальная последовательность (в том числе консенсусные сигнальные последовательности), которая направляет представляющий интерес полипептид в периплазму в случае прокариот и эндоплазматический ретикулум в случае эукариот. Сигнальные последовательности, которые могут использоваться, включают, но без ограничения, сигнальную последовательность из мышиного связывающего иммуноглобулинового белка (mBiP) (UniProtKB: идентификационный № P20029), сигнальные последовательности из гормона роста человека (hGH) (UniProtKB: идентификационный № BIA4G6), люциферазы Gaussia princeps (UniProtKB: идентификационный № Q9BLZ2), дрожжевой эндо-1,3-глюканазы (yBGL2) (UniProtKB: идентификационный № P15703). В одном варианте осуществления сигнальной последовательностью является природная или синтетическая сигнальная последовательность. В дальнейшем варианте осуществления синтетическая сигнальная последовательность является оптимизированной последовательностью секреторного сигнала, которая приводит к уровням дисплея на оптимизированном уровне по сравнению с соответствующей ей неоптимизированной природной сигнальной последовательностью.
Подходящее исследование для определения способности сигнальных последовательностей к управлению дисплеем представляющих интерес полипептидов в прокариотических клетках включает, например, ELISA для фагов, описанный здесь.
Подходящее исследование для определения способности сигнальных последовательностей к управлению экспрессией представляющих интерес полипептидов в эукариотических клетках включает, например, трансфекцию культивируемых клеток млекопитающих векторами для экспрессии в клетках млекопитающих, кодирующими представляющие интерес полипептиды с представляющей интерес сигнальной последовательностью, выращивание клеток в течение периода времени, сбор супернатантов подвергнутых культивированию клеток и очистку IgG их супернатантов с помощью аффинной хроматографии, как описано здесь.
B. Синтетический интрон, который приводит к экспрессии зависимых от хозяина слитых белков с одной и той же нуклеиновой кислоты
Настоящее изобретение основано, частично, на обнаружении того, что различные слитые с Fab белки можно экспрессировать с одной и той же молекулы нуклеиновой кислоты зависимым от клетки-хозяина образом при использовании природного процесса вырезания интронов, который происходит во время процессирования мРНК в эукариотических клетках, но не в прокариотических клетках.
Геномная последовательность константной области НС hIgG1 содержит три природных интрона (фиг. 3A), интрон 1, интрон 2 и интрон 3. Интрон 1 представляет собой интрон размером 391 пар оснований, расположенный между вариабельным доменом HC/CH1 (VH/CHl) и шарнирной областью. Интрон 2 представляет собой интрон размером 118 пар оснований, расположенный между шарнирной областью и CH2. Интрон 3 представляет собой интрон размером 97 пар оснований, расположенный между CH2 и CH3.
Настоящим изобретением обеспечивается вектор, который включает интрон 1, расположенный между VH/CH1 и шарнирной областью. Другие примеры включают интрон 2 или интрон 3, расположенный между VH/CH1 и шарнирной областью. В случае некоторых векторов нуклеиновая кислота, кодирующая белок оболочки или адаптерный белок, вставлена в интрон, расположенный между VH/CH1 и шарнирной областью, с природной донорной последовательностью сплайсинга для интрона на его 5'-конце и природной акцепторной последовательностью сплайсинга на его 3'-конце. Другие примеры включает мутантную донорную последовательность сплайсинга с заменами в положениях 1 и 5 из 8 положений донорной последовательности сплайсинга.
Например, ELISA для фагов может использоваться для анализа системы экспрессии и секреции в прокариотических клетках.
Например, очистка IgG из супернатантов культур с использованием белка A и гель-хроматографии может использоваться для анализа системы экспрессии и секреции в эукариотических клетках. Кроме того, ПЦР в режиме реального времени может использоваться для анализа сплайсинга содержащей синтетический интрон кассеты для HC в эукариотических клетках.
C. Вектор для экспрессии и секреции полипептидов в прокариотических и эукариотических клетках
Система экспрессии и секреции для экспрессии и секреции слитых с Fab белков в прокариотических и эукариотических клетках может быть создана, используя ряд методов, которые находятся в пределах знаний данной области техники.
В одном аспекте система экспрессии и секреции включает вектор, включающий: (1) промотор млекопитающего, (2) кассету для LC, включающую (в порядке от 5' к 3') бактериальный промотор, сигнальную последовательность, последовательность для легкой цепи антитела, контрольный белок (gD); (3) синтетическую кассету, включающую (в порядке от 5' к 3') сигнал полиаденилирования/сигнал терминации транскрипции млекопитающего, последовательность терминатора транскрипции для прекращения транскрипции в прокариотических клетках, промотор млекопитающего и бактериальный промотор для управления экспрессией HC; (4) кассету для HC, включающую сигнальную последовательность и последовательность для тяжелой цепи антитела; и (5) вторую синтетическую кассету, включающую сигнал полиаденилирования/сигнал терминации транскрипции млекопитающего и последовательность терминатора транскрипции для прекращения транскрипции в прокариотических клетках. Последовательность секреторного сигнала, предшествующая LC и HC, может быть одинаковой сигнальной последовательностью, которая функционирует и в прокариотических, и в эукариотических клетках (например, сигнальной последовательностью mBiP млекопитающего). В одном варианте осуществления последовательность для тяжелой цепи антитела включает синтетический интрон. Синтетический интрон расположен вместе с VH/CH1-доменом (на его 5'-конце) и шарнирной областью (на его 3'-конце). В одном варианте осуществления синтетический интрон фланкирован оптимизированной донорной последовательностью сплайсинга на 5'-конце и природной акцепторной последовательностью сплайсинга интрона 1 на 3'-конце. В одном варианте осуществления синтетический интрон включает нуклеотидную последовательность, которая кодирует белок оболочки фага (например, pIII) для прямого дисплея слияния (см. фиг. 14) или адаптерный белок, слитый на нуклеотидном уровне с интроном 1 для непрямого дисплея слияния (см. фиг. 7). Для непрямого дисплея слияния вектор, кроме того, включает отдельную бактериальную экспрессионную кассету, включающую (в порядке от 5' к 3') бактериальный промотор, бактериальную сигнальную последовательность, белок оболочки фага (например, pIII) с адаптерным пептидом-партнером, слитым на нуклеотидном уровне с N-концом белка оболочки, и последовательность терминатора транскрипции (см. фиг. 7). Кроме того, возможны отличные варианты осуществления вышеизложенных конструкций, в которых и HC, и LC контролируются промоторами млекопитающего и бактерии последовательно (см. фиг. 7), или только одна кассета (например, для HC) контролируется расположенными последовательно промоторами млекопитающего и бактерии, тогда как другая кассета (например, для LC) контролируется только бактериальным промотором (см. фиг. 14).
Кроме того, вектор включает бактериальное начало репликации, начало репликации млекопитающих, нуклеиновую кислоту, кодирующую полипептиды, применимые в качестве контроля (например, белок gD) или применимые для таких мероприятий, как очистка белка, маркировка белка, мечение белка (например, мечение обнаруживаемым соединением или композицией (например, радиоактивной меткой, флуоресцентной меткой или ферментной меткой).
В одном варианте осуществления промоторы млекопитающего и бактерии и сигнальные последовательности функционально связаны с последовательностью для легкой цепи антитела, и промоторы млекопитающего и бактерии и сигнальные последовательности функционально связаны с последовательностью для тяжелой цепи антитела.
D. Отбор и скрининг антител против представляющих интерес антигенов
Настоящим изобретением обеспечивается способ скрининга и отбора антител против представляющих интерес белков с помощью фагового или бактериального дисплея основанных на Fab библиотек или для оптимизации существующих антител с помощью схожих методов. Двойственный вектор, описанный выше, может использоваться для скрининга и отбора Fab-фрагментов в прокариотических клетках, и отбора Fab, которые можно легко экспрессировать в виде полноразмерных молекул IgG, для дальнейшего тестирования без необходимости в субклонировании.
Антитела настоящего изобретения
В дальнейшем аспекте настоящего изобретения антителом в соответствии с любым из вышеизложенных вариантов осуществления является моноклональное антитело, включая химерное, гуманизированное антитело или антитело человека. В одном варианте осуществления антителом является фрагмент антитела, например, Fv, Fab, Fab', scFv, диатело или F(ab')2-фрагмент. В другом варианте осуществления антителом является полноразмерное антитело, например, интактное антитело изотипа IgG1, IgG2, IgG3 или IgG4 или другой класс или изотип антитела, описанный здесь.
В дальнейшем аспекте антитело в соответствии с любым из вышеизложенных вариантов осуществления может включать любое из свойств, отдельно или в сочетании, описанных в разделах 1-7 ниже:
1. Аффинность антитела
В некоторых вариантах осуществления предусмотренное здесь антитело характеризуется константой диссоциации (Kd) ≤1 мкМ, ≤100 нМ, ≤10 нМ, ≤1 нМ, ≤0,1 нМ, ≤0,01 нМ или ≤0,001 нМ (например, 10-8 M или менее, например, от 10-8 M до 10-13 M, например, от 10-9 M до 10-13 M).
В одном варианте осуществления Kd определяют с помощью анализа связывания меченного радиоактивным изотопом антигена (RIA), выполняемого с использованием Fab-варианта представляющего интерес антитела и его антигена, как описано, с помощью следующего анализа. Аффинность Fab к антигену в растворе определяют путем приведения Fab в равновесие с минимальной концентрацией (125I)-меченного антигена в присутствии титрационного ряда немеченого антигена, затем захвата связанного антигена на планшет, покрытый антителом против Fab (см. Chen et al., (1999) J. Mol. Biol 293: 865-881). Для установки условий для анализа титрационные микропланшеты MICROTITER® (Thermo Scientific) покрывают в течение ночи 5 мкг/мл захватывающего антитела против Fab (Cappel Labs) в 50 мМ карбонате натрия (рН 9,6) и впоследствии блокируют 2% (в отношении веса к объему) бычьим сывороточным альбумином в PBS в течение двух-пяти часов при комнатной температуре (приблизительно 23°С). В планшете без адсорбирующего агента (Nunc #269620) 100 пМ или 26 пМ [125I]-антигена смешивают с последовательными разведениями представляющего интерес Fab (например, в соответствии с оценкой антитела против VEGF, Fab-12, в Presta et al., (1997) Cancer Res. 57: 4593-4599). Представляющий интерес Fab затем инкубируют в течение ночи, однако инкубация может продолжаться в течение более длительного периода (например, 65 часов) для того, что гарантировать достижение равновесия. После этого смесь переносят в захватывающий планшет для инкубации при комнатной температуре (например, в течение одного часа). Раствор затем удаляют, и планшет промывают восемь раз 0,1% полисорбата 20 (Tween-20®) в PBS. После высыхания планшетов добавляют 150 мкл/лунку сцинтиллятора (MicroScint-20™, Packard), и планшеты считают с помощью счетчика гамма-квантов Topcount™ (Packard) в течение десяти минут. Для использования в анализах конкурентного связывания выбирают концентрации каждого Fab, которые обеспечивают связывание, составляющее менее или равное 20% от максимального связывания.
В соответствии с другим вариантом осуществления Kd определяют с помощью анализов с использованием поверхностного плазмонного резонанса, используя BIAcore™-2000 или BIAcore™-3000 (BIAcore, Inc., Piscataway, NJ) при 25°С с использованием чипов СМ5 с иммобилизованным антигеном при ~10 единиц ответа (ЕО). Вкратце, биосенсорные чипы со слоем, модифицированным карбоксиметилированным декстраном, (CM5, BIACORE, Inc.) активируют с использованием N-этил-N'-(3-диметиламинопропил)-карбодиимида гидрохлорида (EDC) и N-гидроксисукцинимида (NHS) в соответствии с инструкциями поставщика. Антитело разводят 10 мМ ацетатом натрия, pH 4,8, до 5 мкг/мл (~0,2 мкМ) до инъекции со скоростью потока, составляющей 5 мкл/минуту, для достижения приблизительно 10 единиц ответа (ЕО) связанного белка. После инъекции антигена инъецируют 1 M этаноламин для блокирования не вступивших в реакцию групп. Для кинетических измерений двукратные последовательные разведения Fab (0,78 нМ - 500 нМ) инъецируют в PBS с 0,05% полисорбата 20 (TWEEN-20™) - поверхностно-активного вещества (PBST) при 25°C со скоростью потока, составляющей приблизительно 20 мкл/мин. Скорости ассоциации (kon) и скорости диссоциации (koff) рассчитывают, используя ленгмюровскую модель простого связывания в соотношении один к одному (версию 3.2 программного обеспечения для оценки BIACORE®), посредством одновременного построения сенсограмм, соответствующих ассоциации и диссоциации. Равновесную константу диссоциации (Kd) рассчитывают как отношение koff/kon. См., например, Chen et al., J. Mol. Biol. 293: 865-881 (1999). Если скорость ассоциации превышает 106 М-1 сек-1 при вышеуказанном анализе с использованием поверхностного плазмонного резонанса, то скорость ассоциации можно определить, используя метод гашения флуоресценции, с помощью которого определяется увеличение или уменьшение интенсивности эмиссии флуоресценции (возбуждение = 295 нм; эмиссия = 340 нм; полоса пропускания = 16 нм) при 25°С 20 нМ антитела против антигена (формы Fab) в PBS, pH 7,2, в присутствии увеличивающихся концентраций антигена, что измеряется в спектрометре, таком как спектрофотометр, оснащенный прекращением-потоком, (Avin Instruments) или спектрофотометр SLM-AMINCO™ 8000-серии (ThermoSpectronic) с кюветой с мешалкой.
2. Фрагменты антитела
В некоторых вариантах осуществления предусмотренным здесь антителом является фрагмент антитела. Фрагменты антител включают, но без ограничения, Fab-, Fab'-, Fab'-SH, F(ab')2-, Fv- и scFv-фрагменты, и другие фрагменты, описываемые ниже. Для обзора некоторых фрагментов антител см. Hudson et al. Nat. Med. 9: 129-134 (2003). Для обзора scFv-фрагментов см., например, Pluckthun, in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., (Springer-Verlag, New York), pp. 269-315 (1994); см. также WO 93/16185; и патенты США с № 5571894 и 5587458. Ради обсуждения Fab- и F(ab')2-фрагментов, включающих остатки эпитопа связывания рецептора реутилизации и имеющих увеличенный полупериод существования in vivo, см. патент США с № 5869046.
Диатела представляют собой фрагменты антител с двумя антигенсвязывающими сайтами, которые могут быть двухвалентными или полиспецифическими. См., например, EP 404097; WO 1993/01161; Hudson et al, Nat. Med. 9: 129-134 (2003); и Hollinger et al, Proc. Natl. Acad. Sci. USA 90: 6444-6448 (1993). Триатела и тетратела также описаны в Hudson et al., Nat. Med. 9: 129-134 (2003).
Однодоменные антитела представляют собой фрагменты антител, включающие весь вариабельный домен тяжелой цепи или его часть или весь вариабельный домен легкой цепи антитела или его часть. В некоторых вариантах осуществления однодоменным антителом является однодоменное антитело человека (Domantis, Inc., Waltham, MA; см., например, патент США с № 6248516 B1).
Фрагменты антител можно создать с помощью различных методов, включающих, но без ограничения, протеолитическое расщепление интактного антитела, а также продукцию с помощью рекомбинантных клеток-хозяев (например, E. coli или фага), как описано здесь.
3. Химерные и гуманизированные антитела
В некоторых вариантах осуществления предусмотренное здесь антитело является химерным антителом. Некоторые химерные антитела описаны, например, в патенте США с № 4816567 и в Morrison et al., Proc. Natl. Acad. Sci. USA, 81: 6851-6855 (1984)). В одном примере химерное антитело включает нечеловеческую вариабельную область (например, вариабельную область, происходящую от мыши, крысы, хомяка, кролика или не являющегося человеком примата, такого как обезьяна) и человеческую константную область. В дальнейшем примере химерное антитело представляет собой антитело со «сменой класса», в случае которого класс или изотип был изменен по сравнению с таковым родительского антитела. Химерные антитела включают их антигенсвязывающие фрагменты.
В некоторых вариантах осуществления химерным антителом является гуманизированное антитело. Типично нечеловеческое антитело подвергают гуманизации для уменьшения иммуногенности у людей, при сохранении специфичности и аффинности родительского нечеловеческого антитела. Как правило, гуманизированное антитело включает один или более вариабельных доменов, в которых HVR, например, CDR, (или их части) происходят из нечеловеческого антитела, а FR (или их части) происходят из последовательностей антител человека. Необязательно гуманизированное антитело будет также включать по крайней мере часть константной области человека. В некоторых вариантах осуществления некоторые остатки FR в гуманизированном антителе заменены соответствующими остатками из нечеловеческого антитела (например, антитела, из которого происходят остатки HVR), например, для восстановления или увеличения специфичности или аффинности антитела.
Гуманизированные антитела и способы их получения рассматриваются, например, в Almagro and Fransson, Front. Biosci. 13: 1619-1633 (2008) и, кроме того, описываются, например, в Riechmann et al., Nature 332: 323-329 (1988); Queen et al., Proc. Nat'l Acad. Sci. USA 86: 10029-10033 (1989); патентах США с № 5821337, 7527791, 6982321 и 7087409; Kashmiri et al., Methods 36: 25-34 (2005) (где описывается пересадка SDR (a-CDR)); Padlan, Mol. Immunol. 28: 489-498 (1991) (где описывается «изменение поверхности»); Dall'Acqua et al., Methods 36: 43-60 (2005) (где описывается «перетасовка FR»); и Osbourn et al., Methods 36: 61-68 (2005) и Klimka et al., Br. J. Cancer, 83: 252-260 (2000) (где описывается способ «направляемого отбора» для перетасовки FR).
Человеческие каркасные области, которые могут использоваться для гуманизации, включают, но без ограничения, каркасные области, отобранные с использованием метода «наилучшей подгонки» (см., например, Sims et al. J. Immunol. 151: 2296 (1993)); каркасные области, полученные на основе консенсусной последовательности для антител человека конкретной подгруппы вариабельных областей легкой или тяжелой цепи (см., например, Carter et al. Proc. Natl. Acad. Sci. USA, 89: 4285 (1992); и Presta et al. J. Immunol, 151: 2623 (1993)); каркасные области созревших (соматически мутированных) иммуноглобулинов человека или каркасные области иммуноглобулинов зародышей линии человека (см., например, Almagro and Fransson, Front. Biosci. 13: 1619-1633 (2008)); и каркасные области, полученные в результате скрининга библиотек FR (см., например, Baca et al., J. Biol. Chem. 272: 10678-10684 (1997) и Rosok et al., J. Biol. Chem. 271: 22611-22618 (1996)).
4. Антитела человека
В некоторых вариантах осуществления предусмотренное здесь антитело является антителом человека. Антитела человека можно продуцировать, используя различные методы, известные в данной области техники. Антитела человека описаны в общих чертах в van Dijk and van de Winkel, Curr. Opin. Pharmacol. 5: 368-74 (2001) и Lonberg, Curr. Opin. Immunol. 20: 450-459 (2008).
Антитела человека можно приготовить посредством введения иммуногена трансгенному животному, которое было изменено для продукции интактных антител человека или интактных антител с вариабельными областями человека в ответ на антигенное воздействие. Такие животные типично содержат все локусы иммуноглобулинов человека или их часть, которые замещают эндогенные локусы иммуноглобулинов, или которые присутствуют экстрахромосомно или интегрированы по случайному закону в хромосомы животного. У таких трансгенных мышей эндогенные локусы иммуноглобулинов, как правило, инактивированы. Для обзора способов получения антител человека из трансгенных животных см. Lonberg, Nat. Biotech. 23: 1117-1125 (2005). См. также, например, патенты США с № 6075181 и 6150584, в которых описывается технология XENOMOUSE™; патент США с № 5770429, в котором описывается технология HUMAB®; патент США с № 7041870, в котором описывается технология K-M MOUSE®, и публикацию заявки на патент США с № US 2007/0061900, в которой описывается технология VELOCIMOUSE®. Вариабельные области человека из интактных антител, созданных с помощью таких животных, можно далее модифицировать, например, посредством объединения с отличной константной областью человека.
Антитела человека можно также продуцировать с помощью методов на основе гибридомы. Были описаны линии клеток миеломы человека и гетеромиеломы мыши-человека для продукции моноклональных антител человека. (См., например, Kozbor J. Immunol, 133: 3001 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications, pp. 51-63 (Marcel Dekker, Inc., New York, 1987); и Boerner et al., J. Immunol, 147: 86 (1991).) Антитела человека, созданные благодаря гибридомной технологии с использованием В-клеток человека, также описываются в Li et al., Proc. Natl. Acad. Sci. USA, 103: 3557-3562 (2006). Дополнительные способы включают те, которые описаны, например, в патенте США с № 7189826 (где описывается продукция моноклональных антител человека класса IgM за счет линий гибридомных клеток) и в Ni, Xiandai Mianyixue, 26(4): 265-268 (2006) (где описываются гибридомы человек-человек). Технология получения гибридом человека (технология Trioma) также описывается в Vollmers and Brandlein, Histology and Histopathology, 20(3): 927-937 (2005) и Vollmers and Brandlein, Methods and Findings in Experimental and Clinical Pharmacology, 27(3): 185-91 (2005).
Антитела человека можно также создать с помощью выделения последовательностей вариабельных доменов Fv-клонов, отбираемых из библиотек фагового дисплея человеческого происхождения. Такие последовательности вариабельных доменов можно затем объединить с желаемым константным доменом человека. Методы отбора антител человека из библиотек антител описываются ниже.
5. Получаемые из библиотек антитела
Антитела настоящего изобретения можно выделить посредством скрининга комбинаторных библиотек на предмет антител с желаемой активностью или активностями. Например, в данной области техники известен ряд способов создания библиотек фагового дисплея и скрининга таких библиотек на предмет антител, обладающих желаемыми характеристиками связывания. Такие способы рассматриваются, например, в Hoogenboom et al. in Methods in Molecular Biology 178: 1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, 2001) и, кроме того, описываются, например, в McCafferty et al., Nature 348: 552-554; Clackson et al., Nature 352: 624-628 (1991); Marks et al., J. Mol. Biol. 222: 581-597 (1992); Marks and Bradbury, in Methods in Molecular Biology 248: 161-175 (Lo, ed., Human Press, Totowa, NJ, 2003); Sidhu et al., J. Mol. Biol. 338(2): 299-310 (2004); Lee et al., J. Mol. Biol. 340(5): 1073-1093 (2004); Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004); и Lee et al., J. Immunol. Methods 284(1-2): 119-132(2004).
В некоторых методах фагового дисплея наборы генов VH и VL клонируют отдельно с помощью полимеразной цепной реакции (ПЦР) и рекомбинируют по случайному закону в библиотеки фагов, которые затем можно скринировать на предмет антигенсвязывающего фага, как описано в Winter et al., Ann. Rev. Immunol., 12: 433-455 (1994). Фаги типично представляют на своей поверхности фрагменты антител, в виде либо одноцепочечных Fv-(scFv) фрагментов, либо Fab-фрагментов. Библиотеки на основе иммунизированных источников обеспечивают антитела с высокой аффинностью к иммуногену без необходимого условия конструирования гибридом. Альтернативно, можно клонировать набор генов из не иммунизированного источника (например, человека) для обеспечения одного источника антител против широкого ряда антигенов, не являющихся аутоантигенами, а также аутоантигенов без какой-либо иммунизации, как описано в Griffiths et al., EMBO J, 12: 725-734 (1993). Наконец, библиотеки на основе не иммунизированных источников можно также приготовить синтетически посредством клонирования сегментов не подвергнутых реаранжировке V-генов из стволовых клеток и использования праймеров, имеющих случайную последовательность, для ПЦР, чтобы кодировать в высокой степени вариабельные CDR3-участки и завершить реаранжировку in vitro, как описано в Hoogenboom and Winter, J. Mol. Biol, 227: 381-388 (1992). Публикации патентов и заявок на патенты, в которых описываются библиотеки антител человека в фагах, включают, например, патент США с № 5750373 и публикации заявок на патенты с № 2005/0079574, 2005/0119455, 2005/0266000, 2007/0117126, 2007/0160598, 2007/0237764, 2007/0292936 и 2009/0002360.
Антитела или фрагменты антител, выделенные из библиотек антител человека, считаются здесь антителами человека или фрагментами антител человека.
6. Полиспецифические антитела
В некоторых вариантах осуществления предусмотренное здесь антитело является полиспецифическим антителом, например, биспецифическим антителом. Полиспецифические антитела представляют собой моноклональные антитела, которые обладают специфичностями связывания с по крайней мере двумя различными сайтами. В некоторых вариантах осуществления одной из специфичностей связывания является таковая в отношении первого антигена, а другая - в отношении любого другого антигена. В некоторых вариантах осуществления биспецифические антитела могут связываться с двумя различными эпитопами первого антигена. Биспецифические антитела могут также использоваться для сосредоточения цитотоксических агентов в клетках, которые экспрессируют первый антиген. Биспецифические антитела можно приготовить в виде полноразмерных антител или фрагментов антител.
Методы продукции полиспецифических антител включают, но без ограничения, рекомбинантную коэкспрессию пар тяжелая цепь-легкая цепь двух иммуноглобулинов, имеющих различные специфичности (см. Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829 и Traunecker et al., EMBO J. 10: 3655 (1991)) и инженерию «выступы-во-впадины» (см., например, патент США с № 5731168). Полиспецифические антитела можно также получить посредством создания эффектов электростатического наведения для получения гетеродимерных молекул из Fc антител (WO 2009/089004A1); сшивания двух или более антител или фрагментов (см., например, патент США с № 4676980 и Brennan et al., Science, 229: 81 (1985)); использования «лейциновых молний» для получения биспецифических антител (см., например, Kostelny et al., J. Immunol., 148(5): 1547-1553 (1992)); использования технологии получения «диател» для создания фрагментов биспецифических антител (см., например, Hollinger et al., Proc. Natl. Acad. Sci. USA, 90: 6444-6448 (1993)), и использования димеров одноцепочечных Fv (sFv) (см., например, Gruber et al., J. Immunol, 152: 5368 (1994)); и приготовления триспецифических антител, как описано, например, в Tutt et al. J. Immunol. 147: 60 (1991).
Сюда также включены сконструированные антитела с тремя или более функциональными антигенсвязывающими сайтами, включающие «антитела-осьминоги» (см., например, US 2006/0025576 A1).
Антитело или фрагмент здесь также включает «Fab двойственного действия» или «DAF», включающий антигенсвязывающий сайт, который связывается с первым антигеном, а также с другим отличным антигеном (см. US 2008/0069820, например).
7. Варианты антител
В некоторых вариантах осуществления предусматриваются варианты по аминокислотным последовательностям антител, предусмотренных здесь. Например, может быть желательным увеличение аффинности и/или улучшение других биологических свойств антитела. Варианты по аминокислотной последовательности антитела можно приготовить путем введения соответствующих модификаций в нуклеотидную последовательность, кодирующую антитело, или путем пептидного синтеза. Такие модификации включают, например, делеции и/или вставки и/или замены остатков в пределах аминокислотных последовательностей антитела. Для получения конечной конструкции может быть осуществлена любая комбинация делеции, вставки и замены при условии, что конечная конструкция обладает желаемыми свойствами, например, связыванием с антигеном.
а) Варианты с заменой(ами), инсерционные и делеционные варианты
В некоторых вариантах осуществления обеспечиваются варианты антител, содержащие одну или более замен аминокислот. Представляющие интерес места для мутагенеза с заменой включают HVR и FR. Консервативные замены представлены в таблице 1 под заголовком «консервативные замены». Более существенные изменения представлены в таблице 1 под заголовком «примеры замен» и дополнительно описаны ниже со ссылкой на классы боковых цепей аминокислот. Аминокислотные замены можно ввести в представляющее интерес антитело, а продукты подвергнуть скринингу на предмет желаемой активности, например, сохранения/увеличения связывания с антигеном, уменьшения иммуногенности или увеличения ADCC или CDC.
Аминокислоты можно подразделить на группы в соответствии с общими свойствами боковых цепей:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, оказывающие влияние на ориентацию цепи: Gly, Pro; и
(6) ароматические: Trp, Tyr, Phe.
Неконсервативные замены повлекут за собой замену члена одного из этих классов на другой класс.
Один тип варианта с заменой(ами) включает замену одного или более остатков гипервариабельных участков родительского антитела (например, гуманизированного антитела или антитела человека). Как правило, получаемый в результате вариант(ы), отбираемый для дальнейшего исследования, будет иметь изменения (например, улучшения) некоторых биологических свойств (например, увеличение аффинности, уменьшение иммуногенности) относительно родительского антитела, и/или у него будут сохранены в значительной степени определенные биологические свойства родительского антитела. Приводимым в качестве примера вариантом с заменой(ами) является антитело с созревшей аффинностью, которое можно беспрепятственно создать, например, используя методы созревания аффинности на основе фагового дисплея, такие как те, которые здесь описаны. Вкратце, один или более остатков HVR мутируют, и варианты антител представляют на поверхности фагов и скринируют на предмет конкретной биологической активности (например, аффинности).
Изменения (например, замены) можно ввести в HVR, например, для увеличения аффинности антитела. Такие изменения можно ввести в «горячие точки» HVR, т.е. остатки, кодируемые кодонами, которые подвергаются мутации с высокой частотой во время соматического процесса созревания (см., например, Chowdhury, Methods Mol. Biol. 207: 179-196 (2008)), и/или SDR (a-CDR), при этом результирующий вариант VH или VL проверяют на аффинность. Созревание аффинности с помощью конструирования вторичных библиотек и выбора заново из них было описано, например, в Hoogenboom et al. in Methods in Molecular Biology 178: 1-37 (O'Brien et al, ed., Human Press, Totowa, NJ, (2001).) В некоторых вариантах осуществления созревания аффинности в гены вариабельных областей, которые выбраны для созревания, вносят разнообразие с помощью любого из множества способов (например, ПЦР с внесением ошибок, перетасовки цепей или мутагенеза с использованием олигонуклеотидов). Затем создают вторичную библиотеку. Затем библиотеку скринируют для идентификации любых вариантов антитела с желаемой аффинностью. Другой способ внесения разнообразия включает направленные на HVR подходы, в которых рандомизируют несколько остатков HVR (например, 4-6 остатков за один раз). Остатки HVR, вовлеченные в связывание антигена, можно, в частности, идентифицировать, например, используя сканирующий аланином мутагенез или моделирование. В особенности CDR-H3 и CDR-L3 часто становятся мишенями.
В некоторых вариантах осуществления замены, вставки или делеции могут встречаться в одном или более HVR при условии, что такие изменения не уменьшают существенно способность антитела к связыванию антигена. Например, консервативные изменения (например, консервативные замены, представленные здесь), которые не уменьшают существенно аффинность, могут быть внесены в HVR. Такие изменения могут находиться вне «горячих точек» HVR или SDR. В некоторых вариантах осуществления вариантов последовательностей VH и VL, представленных выше, каждый HVR либо является неизмененным, либо содержит не более одной, двух или трех аминокислотных замен.
Пригодный способ идентификации остатков или районов антитела, которые могут быть намечены для мутагенеза, называют «сканирующим аланином мутагенезом», как описано Cunningham и Wells (Science, 244: 1081-1085 (1989)). В этом способе остаток или группу остатков-мишеней (например, заряженные остатки, такие как arg, asp, his, lys и glu) идентифицируют и замещают нейтральной или отрицательно заряженной аминокислотой (например, аланином или полиаланином) для определения того, оказывается ли влияние на взаимодействие антитела с антигеном. Затем замены могут быть введены в положения аминокислот, демонстрирующие функциональную чувствительность к первоначальным заменам. Альтернативно или дополнительно, может использоваться кристаллическая структура комплекса антиген-антитело для идентификации точек контакта между антителом и антигеном. Такие точки контакта и соседние остатки могут быть намечены в качестве кандидатов на замену или исключены. Варианты можно подвергнуть скринингу для определения того, обладают ли они желаемыми свойствами.
Вставки в аминокислотную последовательность, длина которых находится в диапазоне от одного остатка до полипептидов, содержащих сотню или более остатков, включают слияния с амино-концом и/или карбоксильным концом, а также вставки внутрь последовательности одного или множества аминокислотных остатков. Примеры концевых вставок включают антитело с метионильным остатком на N-конце. Другие инсерционные варианты молекулы антитела включают слияние фермента (например, для ADEPT) или полипептида, который увеличивает полупериод существования антитела в сыворотке, с N- или С-концом антитела.
b) Варианты гликозилирования
В некоторых вариантах осуществления предусмотренное здесь антитело изменяют для увеличения или уменьшения степени гликолизирования антитела. Добавление к антителу сайтов гликозилирования или их исключение можно легко осуществить путем изменения аминокислотной последовательности, так что создается или исключается один или более сайтов гликозилирования.
Если антитело включает Fc-область, углевод, присоединяемый к нему, может быть изменен. Встречающиеся в природе антитела, продуцируемые клетками млекопитающих, типично включают разветвленный, биантеннальный олигосахарид, который, как правило, присоединен с помощью N-связи к Asn297 CH2-домена Fc-области. См., например, Wright et al. TIBTECH 15: 26-32 (1997). Олигосахарид может включать различные углеводы, например, маннозу, N-ацетилглюкозамин (GlcNAc), галактозу и сиаловую кислоту, а также фукозу, присоединенную к GlcNAc в «стволе» биантеннальной олигосахаридной структуры. В некоторых вариантах осуществления модификации олигосахарида в антителе настоящего изобретения могут осуществляться с целью создания вариантов антитела с определенными улучшенными свойствами.
В одном варианте осуществления обеспечиваются варианты антител с углеводной структурой, в которой недостает фукозы, присоединенной (непосредственно или опосредованно) к Fc-области. Например, количество фукозы в таком антителе может составлять от 1% до 80%, от 1% до 65%, от 5% до 65% или от 20% до 40%. Количество фукозы определяют путем расчета среднего количества фукозы в сахарной цепи, присоединенной к Asn297, относительно суммы всех гликоструктур, присоединенных к Asn 297 (например, сложных, гибридных структур и структур с высоким количеством маннозы), определяемых с помощью MALDI-TOF масс-спектрометрии, как описано в WO 2008/077546, например. Asn297 относится к остатку аспарагина, находящемуся приблизительно в положении 297 в Fc-области (EU-нумерация остатков Fc-области); однако Asn297 может также находится на приблизительно ±3 аминокислоты выше или ниже положения 297, т.е. между положениями 294 и 300, вследствие незначительных вариаций последовательностей антител. Такие варианты фукозилирования могут характеризоваться улучшенной функцией в виде ADCC. См., например, публикации заявок на патенты США с № US 2003/0157108 (Presta, L.); US 2004/0093621 (Kyowa Hakko Kogyo Co., Ltd). Примеры публикаций, относящихся к «дефукозированным» или «с недостатком фукозы» вариантам антител, включают: US 2003/0157108; WO 2000/61739; WO 2001/29246; US 2003/0115614; US 2002/0164328; US 2004/0093621; US 2004/0132140; US 2004/0110704; US 2004/0110282; US 2004/0109865; WO 2003/085119; WO 2003/084570; WO 2005/035586; WO 2005/035778; WO 2005/053742; WO 2002/031140; Okazaki et al. J. Mol. Biol. 336: 1239-1249 (2004); Yamane-Ohnuki et al. Biotech. Bioeng. 87: 614 (2004). Примеры линий клеток, способных к продукции дефукозированных антител, включают клетки Lec13 CHO с недостаточной способностью к фукозилированию белков (Ripka et al. Arch. Biochem. Biophys. 249: 533-545 (1986); заявка на патент США с № US 2003/0157108 A1, Presta, L; и WO 2004/056312 Al, Adams et al., особенно в примере 11), и линии клеток с выключенным геном, такие как клетки СНО с выключенным геном альфа-1,6-фукозилтрансферазы, FUT8, (см., например, Yamane-Ohnuki et al., Biotech. Bioeng. 87: 614 (2004); Kanda, Y. et al, Biotechnol. Bioeng., 94(4): 680-688 (2006); и WO2003/085107).
Кроме того обеспечиваются варианты антител с биссекторными олигосахаридами, например, в которых GlcNAc делит пополам биантеннальный олигосахарид, присоединенный к Fc-области антитела. Такие варианты антител могут иметь уменьшенное фукозилирование и/или улучшенную функцию в виде ADCC. Примеры таких вариантов антител описаны, например, в WO 2003/011878 (Jean-Mairet et al.); патенте США с № 6602684 (Umana et al.) и US 2005/0123546 (Umana et al). Также обеспечиваются варианты антител с по крайней мере одним остатком галактозы в олигосахариде, присоединенном к Fc-области. Такие варианты антител могут иметь улучшенную функцию в виде CDC. Такие варианты антител описаны, например, в WO 1997/30087 (Patel et al.); WO 1998/58964 (Raju, S.) и WO 1999/22764 (Raju, S.).
c) Варианты Fc-области
В некоторых вариантах осуществления одна или более модификаций аминокислот может быть введена в Fc-область предусмотренного здесь антитела, создавая тем самым вариант Fc-области. Вариант Fc-области может включать последовательность Fc-области человека (например, Fc-области IgG1, IgG2, IgG3 или IgG4 человека), включающую модификацию аминокислоты (например, замену) в одном или нескольких положениях аминокислот.
В некоторых вариантах осуществления настоящим изобретением предусматривается вариант антитела, который обладает некоторыми, но не всеми эффекторными функциями, что делает его желательным кандидатом на такие применения, когда важен полупериод существования антитела in vivo, однако же некоторые эффекторные функции (такие как комплемент и ADCC) являются ненужными или вредными. In vitro и/или in vivo анализы цитотоксичности можно провести для подтверждения уменьшения/истощения активностей CDC и/или ADCC. Например, можно провести анализы связывания с Fc-рецептором (FcR) для гарантии того, что антитело не связывает FcγR (следовательно, у него, вероятно, отсутствует активность ADCC), но у него сохраняется способность связывать FcRn. Основные клетки, опосредующие ADCC, NK-клетки, экспрессируют только FcγRIII, в то время как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR в гемопоэтических клетках резюмирована в таблице 3 на странице 464 Ravetch and Kinet, Annu. Rev. Immunol. 9: 477-492 (1991). Неограничивающие примеры in vitro анализов для оценки активности ADCC представляющей интерес молекулы описаны в патенте США С № 5500362 (см., например, Hellstrom, I. et al. Proc. Nat'l Acad. Sci. USA 83: 7059-7063 (1986)) и Hellstrom, I et al., Proc. Nat'l Acad. Sci. USA 82: 1499-1502 (1985); патент США с № 5821337 (см. Bruggemann, M. et al., J. Exp. Med. 166: 1351-1361 (1987)). Альтернативно могут использоваться нерадиоактивные анализы (см., например, нерадиоактивный анализ цитотоксичности ACTI™ вместо проточной цитометрии (CellTechnology, Inc. Mountain View, CA; и нерадиоактивный анализ цитотоксичности CytoTox 96® (Promega, Madison, WI). Применимые для таких анализов клетки-эффекторы включают мононуклеарные клетки периферической крови (PBMC) и природные киллеры (NK). Альтернативно или дополнительно, активность ADCC представляющей интерес молекулы можно оценить in vivo, например, в модели на животном, такой как модель, описанная в Clynes et al., Proc. Nat'l Acad. Sci. USA 95: 652-656 (1998)). Можно также провести анализы связывания C1q для подтверждения того, что антитело не способно связывать C1q и, следовательно, не обладает активностью CDC. См., например, ELISA для оценки связывания C1q и C3c в WO 2006/029879 и WO 2005/100402. Для оценки активации комплемента можно провести анализ CDC (см., например, Gazzano-Santoro et al., J. Immunol. Methods 202: 163 (1996); Cragg, M.S. et al., Blood 101: 1045-1052 (2003); и Cragg, M.S. and M.J. Glennie, Blood 103: 2738-2743 (2004)). Определения связывания с FcRn и in vivo клиренса/периода полувыведения можно также провести с использованием способов, известных в данной области техники (см., например, Petkova, S.B. et al., Int'l. Immunol. 18(12): 1759-1769 (2006)).
Антитела со сниженной эффекторной функцией включают антитела с заменой одного или более остатков в положениях 238, 265, 269, 270, 297, 327 и 329 Fc-области (патент США с № 6737056). Такие Fc-мутанты включают Fc-мутанты с заменами в двух или более положениях аминокислот 265, 269, 270, 297 и 327, включающие так называемый Fc-мутант «DANA» с заменой остатков 265 и 297 на аланин (патент США с № 7332581).
Описаны определенные варианты антител с увеличенным или уменьшенным связыванием с FcR (см., например, патент США с № 6737056; WO 2004/056312 и Shields et al., J. Biol. Chem. 9(2): 6591-6604 (2001).)
В некоторых вариантах осуществления вариант антитела включает Fc-область с одной или более аминокислотных замен, которые увеличивают ADCC, например, заменами в положениях 298, 333 и/или 334 Fc-области (EU-нумерация остатков).
В некоторых вариантах осуществления осуществляют изменения в Fc-области, которые приводят к изменению (т.е. либо увеличению, либо уменьшению) связывания C1q и/или комплементзависимой цитотоксичности (CDC), например, как описано в патенте США с № 6194551, WO 99/51642 и в Idusogie et al. J. Immunol. 164: 4178-4184 (2000).
Антитела с увеличенным полупериодом существования и увеличенным связыванием с неонатальным Fc-рецептором (FcRn), который ответственен за перенос материнских IgG плоду (Guyer et al., J. Immunol. 117: 587 (1976) и Kim et al., J. Immunol. 24: 249 (1994)), описаны в US 2005/0014934 A1 (Hinton et al.). Эти антитела включают Fc-область с одной или более замен в ней, которые увеличивают связывание Fc-области с FcRn. Такие варианты Fc-области включают Fc-области с заменами в одном или более остатков Fc-области, выбираемых из 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 и 434, например, заменой остатка 434 Fc-области (патент США с № 7371826).
См. также Duncan & Winter, Nature 322: 738-740 (1988); патент США с № 5648260; патент США с № 5624821 и WO 94/29351, касающиеся других примеров вариантов Fc-области.
d) Варианты антител с генно-инженерным цистеином(ами)
В некоторых вариантах осуществления желательным может быть создание антител с генно-инженерным цистеином(ами), например, «тиомАт», в которых один или более остатков антитела заменены остатками цистеина. В конкретных вариантах осуществления замещенные остатки встречаются в открытых для доступа местах антитела. В результате замещения этих остатков цистеином реакционно-способные тиольные группы располагаются таким образом в доступных местах антитела и могут использоваться для конъюгации антитела с другими составляющими, такими как составляющие в виде лекарственных средств или составляющие линкер-лекарственное средство, для создания иммуноконъюгата, как описывается далее здесь. В некоторых вариантах осуществления на цистеин может быть заменен любой один или более из следующих остатков: V205 (нумерация Kabat) легкой цепи; A118 (EU-нумерация) тяжелой цепи и S400 (EU-нумерация) Fc-области тяжелой цепи. Антитела с генно-инженерным цистеином(ами) можно создать, как описано, например, в патенте США с № 7521541.
e) Производные антител
В некоторых вариантах осуществления предусмотренное здесь антитело можно, кроме того, модифицировать так, чтобы оно содержало дополнительные небелковоподобные составляющие, которые известны в данной области техники и легкодоступны. Составляющие, подходящие для дериватизации антитела, включают, но без ограничения, водорастворимые полимеры. Неограничивающие примеры водорастворимых полимеров включают, но без ограничения, полиэтиленгликоль (ПЭГ), сополимеры этиленгликоля и пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена и малеинового ангидрида, полиаминокислоты (или гомополимеры, или произвольные сополимеры) и декстран или поли(н-винилпирролидон)полиэтиленгликоль, гомополимеры пропропиленгликоля, сополимеры пролипропиленоксида и этиленоксида, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт и их смеси. Полиэтиленгликольпропиональдегид может иметь преимущества при производстве вследствие его устойчивости в воде. Полимер может быть любой молекулярной массы и может быть разветвленным или неразветвленным. Число полимеров, присоединяемых к антителу, может варьировать, и если присоединяется больше одного полимера, они могут представлять собой одинаковые или различные молекулы. Как правило, число и/или тип используемых для дериватизации полимеров можно определить на основе принятия во внимание, например, но без ограничения, конкретных свойств или функций антитела, которые необходимо улучшить, того, будет ли производное антитела использоваться для лечения при определенных условиях и т.д.
В другом варианте осуществления обеспечиваются конъюгаты антитела и небелковоподобной составляющей, которую можно избирательно нагреть посредством подвергания воздействию излучения. В одном варианте осуществления небелковоподобной составляющей является углеродная нанотрубка (Kam et al., Proc. Natl. Acad. Sci. USA 102: 11600-11605 (2005)). Излучение может быть любой длины волны и включает, но без ограничения, длины волн, которые не наносят вред обычным клеткам, но которые нагревают небелковоподобную составляющую до температуры, при которой уничтожаются клетки, находящиеся близко к антителу - небелковоподобной составляющей.
Рекомбинантные методы и композиции
Антитела можно продуцировать, используя рекомбинантные методы и композиции, например, как описано в патенте США с № 4816567. В одном варианте осуществления обеспечивается выделенная нуклеиновая кислота, кодирующая антитело, описываемое здесь. Такая нуклеиновая кислота может кодировать аминокислотную последовательность, включающую VL, и/или аминокислотную последовательность, включающую VH антитела, (например, легкую и/или тяжелую цепи антитела). В дальнейшем варианте осуществления обеспечивается один или более векторов (например, экспрессионных векторов), включающих такую нуклеиновую кислоту. В дальнейшем варианте осуществления обеспечивается клетка-хозяин, включающая такую нуклеиновую кислоту. В одном таком варианте осуществления клетка-хозяин включает (например, была трансформирована им(и)): (1) вектор, включающий нуклеиновую кислоту, которая кодирует аминокислотную последовательность, включающую VL антитела, и аминокислотную последовательность, включающую VH антитела, или (2) первый вектор, включающий нуклеиновую кислоту, которая кодирует аминокислотную последовательность, включающую VL антитела, и второй вектор, включающий нуклеиновую кислоту, которая кодирует аминокислотную последовательность, включающую VH антитела. В одном варианте осуществления клетка-хозяин является эукариотической, например, клеткой яичника китайского хомячка (CHO) или лимфоидной клеткой (например, клеткой Y0, NSO, Sp20). В одном варианте осуществления обеспечивается способ продуцирования антитела, который включает культивирование клетки-хозяина, включающей нуклеиновую кислоту, кодирующую антитело, предусмотренное выше, в условиях, подходящих для экспрессии антитела, и необязательно извлечение антитела из клетки-хозяина (или среды для культивирования клетки-хозяина).
Для рекомбинантной продукции антитела нуклеиновую кислоту, кодирующую антитело, например, описанную выше, выделяют и встраивают в один или более векторов для дальнейшего клонирования и/или экспрессии в клетке-хозяине. Такую нуклеиновую кислоту можно без труда выделить и секвенировать, используя обычные процедуры (например, используя олигонуклеотидные зонды, которые способны к специфическому связыванию с генами, кодирующими тяжелую и легкую цепи антитела).
Клетки-хозяева, подходящие для клонирования или экспрессии кодирующих антитела векторов, включают прокариотические или эукариотические клетки, описываемые здесь. Например, антитела можно продуцировать в бактериях, в частности, когда гликозилирование и эффекторная функция Fc не требуются. Ради экспрессии фрагментов антител и полипептидов в бактериях см., например, патенты США с № 5648237, 5789199 и 5840523. (См. также Charlton, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ, 2003), pp. 245-254, где описывается экспрессия фрагментов антител в E. coli.) После экспрессии антитело можно выделить из массы бактериальных клеток в растворимой фракции и можно в дальнейшем очистить.
Хозяевами, подходящими для клонирования или экспрессии кодирующих антитела векторов, являются, помимо прокариот, эукариотические микробы, такие как нитчатые грибы или дрожжи, включающие штаммы грибов и дрожжей, пути гликозилирования которых были «гуманизированы», приводя к продукции антитела с частично или полностью человеческим профилем гликозилирования. См. Gerngross, Nat. Biotech. 22: 1409-1414 (2004) и Li et al, Nat. Biotech. 24: 210-215 (2006).
Клетки-хозяева, подходящие для экспрессии гликозилированного антитела, также получены от многоклеточных организмов (беспозвоночных и позвоночных). Примеры клеток беспозвоночных включают клетки растений и насекомых. Были идентифицированы многочисленные штаммы бакуловирусов, которые могут использоваться совместно с клетками насекомых, в частности, для трансфекции клеток Spodoptera frugiperda.
Культуры клеток растений могут также использоваться в качестве хозяев. См., например, патенты США с № 5959177, 6040498, 6420548, 7125978 и 6417429 (где описывается технология PLANTIBODIES™ для продукции антител в трансгенных растениях).
Клетки позвоночных могут также использоваться в качестве хозяев. Например, могут применяться линии клеток млекопитающих, которые адаптированы к росту в суспензии. Другими примерами применимых линий клеток млекопитающих-хозяев являются линия CV1 почки обезьяны, трансформированная SV40 (COS-7); линия клеток эмбриональной почки человека (293 или клетки 293, описанные в Graham et al., J. Gen Virol. 36: 59 (1977)); клетки почки детеныша хомячка (BHK); клетки опухоли Сертоли мыши (клетки TM4, описанные, например, в Mather, Biol. Reprod. 23: 243-251 (1980)); клетки почки обезьяны (CV1); клетки почки африканской зеленой мартышки (VERO-76); клетки карциномы шейки матки человека (HELA); клетки почки собаки (MDCK); клетки печени крысы Buffalo (BRL 3A); клетки легкого человека (W138); клетки печени человека (Hep G2); опухоль молочной железы мыши (MМT 060562); клетки TRI, описанные, например, в Mather et al., Annals N.Y. Acad. Sci. 383: 44-68 (1982); клетки MRC 5 и клетки FS4. Другие применимые линии клеток млекопитающих-хозяев включают клетки яичника китайского хомячка (CHO), включающие клетки DHFR- CHO (Urlaub et al., Proc. Natl. Acad. Sci. USA 77: 4216 (1980)); и линии клеток миеломы, такие как Y0, NS0 и Sp2/0. Для обзора некоторых линий клеток млекопитающих-хозяев, подходящих для продукции антител, см., например, Yazaki and Wu, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, NJ), pp. 255-268 (2003).
Анализы
Предусмотренные здесь антитела можно идентифицировать, отобрать или охарактеризовать в отношении их физических/химических свойств и/или биологических активностей с помощью различных анализов, известных в данной области техники.
1. Анализы связывания и другие анализы
В одном аспекте проверяют антигенсвязывающую активность антитела настоящего изобретения, например, с помощью известных способов, таких как ELISA, Вестерн-блоттинг и т.д.
В другом аспекте анализы конкуренции могут использоваться для идентификации антитела, которое конкурирует за связывание с представляющим интерес антигеном с антителом настоящего изобретения. В некоторых вариантах осуществления такое конкурирующее антитело связывается с тем же эпитопом (например, линейным или конформационным эпитопом), с которым связывается антитело настоящего изобретения. Изложенные подробно, приводимые в качестве примера способы картирования эпитопа, с которым связывается антитело, представлены в Morris (1996) "Epitope Mapping Protocols," in Methods in Molecular Biology vol. 66 (Humana Press, Totowa, NJ).
В приводимом в качестве примера анализе конкуренции иммобилизованный представляющий интерес антиген инкубируют в растворе, включающем первое меченое антитело, которое связывается с представляющим интерес антигеном, (например, антитело настоящего изобретения) и второе немеченое антитело, способность которого к конкуренции с первым антителом за связывание с представляющим интерес антигеном проверяют. Второе антитело может присутствовать в супернатанте гибридомы. В качестве контроля, иммобилизованный представляющий интерес антиген инкубируют в растворе, включающем первое меченое антитело, но не второе немеченое антитело. После инкубации в условиях, допускающих связывание первого антитела с представляющим интерес антигеном, избыточное количество не связавшегося антитела удаляют, и определяют количество метки, связавшейся с иммобилизованным представляющим интерес антигеном. Если количество метки, связавшейся с иммобилизованным представляющим интерес антигеном, является существенно уменьшенным в исследуемом образце относительно контрольного образца, то это означает, что второе антитело конкурирует с первым антителом за связывание с представляющим интерес антигеном. См. Harlow and Lane (1988) Antibodies: A Laboratory Manual ch.14 (Cold Spring Harbor Laboratory, Cold Spring Harbor, NY).
2. Анализы активности
В одном аспекте обеспечиваются анализы для идентификации антител, обладающих биологической активностью. Также обеспечиваются антитела, обладающие такой биологической активностью in vivo и/или in vitro.
В некоторых вариантах осуществления антитело настоящего изобретения проверяют в отношении такой биологической активности.
Следующие примеры представлены лишь с иллюстративной целью и, как предполагается, не ограничивают объем настоящего изобретения никоим образом.
Все патентные и справочные материалы, на которые ссылаются в описании настоящего изобретения, включены таким образом намеренно в их полном объеме посредством ссылки.
III. ПРИМЕРЫ
Ниже приведены примеры способов и композиций настоящего изобретения. Понятно, что различные другие варианты можно осуществить на практике, принимая во внимание общее описание, приведенное выше.
Фаг-помощник M13KO7 был от New England Biolabs. Бычий сывороточный альбумин (BSA) и Tween 20 были от Sigma. Казеин был от Pierce. Конъюгированное с пероксидазой хрена (HRP) антитело протии М13 было от Amersham Pharmacia. Иммунопланшеты Maxisorp были от NUNC. Субстрат тетраметилбензидин (TMB) был от Kirkegaard и Perry Laboratories. Все другие белковые антигены были созданы научно-исследовательскими группами в Genentech, Inc.
Пример 1: Выбор сигнальной последовательности для экспрессии в прокариотических и эукариотических клетках
Для разрешения вопроса, способен ли вектор экспрессировать представляющие интерес белки и в Escherichia coli, и в эукариотических клетках (млекопитающих), были выбраны четыре сигнальных последовательности небактериального происхождения, для которых существовали отдельные примеры, подтверждающие представление, что они могут функционировать в клетках млекопитающих. Авторы настоящего изобретения проверили эти сигнальные последовательности в отношении их способности стимулировать дисплей Fab против Her2 (h4D5) на фаге M13, используя ELISA для фагов (фиг. 1A). Уровни дисплея оценивали относительно сигнальной последовательности бактериального термостабильного энтеротоксина II (STII). Способность сигнальных последовательностей к стимулированию фагового дисплея Fab сильно варьировала, и одна сигнальная последовательность, из мышиного связывающего иммуноглобулинового белка (mBiP), приводила к уровням дисплея, которые могли бы, наверное, допускать эффективные уровни дисплея Fab.
Для дальнейшего увеличения эффективности сигнальной последовательности из mBiP, авторы настоящего изобретения использовали подход к оптимизации кодонов на основе фагов, поскольку ранее было установлено, что на функцию эукариотических сигнальных последовательностей в бактериях оказывает сильное влияние частота использования кодона (Humphreys et al, The Protein Expression and Purification, 20: 252-264 (2000). Была сконструирована библиотека фагов, в которой сигнальная последовательность из mBiP была слита с N-концом НС Fab h4D5 в стандартном фагемидном векторе. В последовательность ДНК сигнального пептида mBiP вносили разнообразие в третье основание каждого кодона после первых двух метионинов, что допускало только молчащие мутации. После четырех циклов твердофазного пэннинга против иммобилизованного Her2, отдельные клоны были отобраны и подвергнуты секвенированию. Авторы настоящего изобретения установили, что в консенсусной последовательности отобранных клонов оказывалось сильное предпочтение аденину или тимину в рандомизированных положениях, а не гуанину или цитозину. Этот результат подчеркивается тем фактом, что 15 из 17 кодонов в последовательности mBiP дикого типа содержат гуанин или цитозин в положении третьего основания, но каждый из 17 кодонов в подвергнутой сортировке библиотеке содержал аденин или тимин в этих положениях в 60-90% случаев. После проверки в ELISA для фагов, оптимизированная сигнальная последовательность из mBiP приводит к дисплею Fab h4D5 на уровнях, соизмеримых с таковыми в случае прокариотической сигнальной последовательностью STII, что говорит о том, что сигнальная последовательность mBiP может использоваться для фагового дисплея и экспериментов по пэннингу вместо прокариотической сигнальной последовательности STII без какого-либо видимого уменьшения эффективности (фиг. 1B).
Затем была оценена способность сигнальной последовательности mBiP к поддержке экспрессии и секреции IgG в клетках млекопитающих. Векторы для экспрессии в клетках млекопитающих, кодирующие HC и LC hIgG1 h4D5, каждый с сигнальной последовательностью mBiP, слитой с N-концом, были котрансфецированы в клетки 293S в суспензии и подвергнуты выращиванию в течение пяти дней, после чего супернатанты собирали, и IgG очищали с помощью аффинной хроматографии. Выход IgG из одной 30-мл культуры составлял регулярно ~2,0 мг, что соизмеримо с выходами, полученными, используя природную сигнальную последовательность HC (VHS) для обеих цепей (не представленные данные). Интересно, что использование сигнальной последовательности mBiP дикого типа в сравнении с ее подвергнутой оптимизации кодонов формой не оказывало заметный эффект на уровни экспрессии IgG (не представленные данные). Гель-хроматография и масс-спектрометрия подтвердили, что очищенный белок был на >90% мономерным в растворе, и что сигнальная последовательность mBiP полностью отщеплялась в правильном положении и в HC, и в LC (не представленные данные). Поскольку h4D5, как известно, является хорошим экспрессером, авторы настоящего изобретения проверили эффективность mBiP относительно VHS на совокупности не охарактеризованных клонов, произвольно отобранных в результате эксперимента по пэннингу фагов. Средний выход из этих клонов составлял ~1,0 мг из 30-мл суспензионной культуры, и значимые различия не отмечались между двумя сигнальными последовательностями (фиг. 2A и B).
В заключение, последовательность секреторного сигнала млекопитающего из mBiP была способна к экспрессии IgG в клетках млекопитающих на уровнях, достаточных для скрининга, и после оптимизации кодонов также была способна к стимулированию устойчивого дисплея Fab на фаге без подрыва уровней экспрессии IgG.
Пример 2: Экспрессия альтернативных слияний с Fab в прокариотических и эукариотических клетках
Для продуцирования различных слитых с Fab белков зависимым от клетки-хозяина образом авторы настоящего изобретения попытались использовать природный процесс вырезания интронов, который происходит во время процессирования мРНК в эукариотических, но не в прокариотических клетках. Геномная последовательность константной области НС hIgG1 содержит три природных интрона (фиг. 3A). Первый из них (интрон 1) является интроном размером 384 пар оснований, расположенным между вариабельным доменом HC (VH) и шарнирной областью. Вектор для экспрессии HC, содержащий интрон 1 и оптимизированную донорную последовательность сплайсинга, экспрессировал полностью сплайсированную мРНК, как определено с помощью ПЦР в режиме реального времени и секвенирования транскриптов, и, после котрансфекции с использованием вектора для LC, экспрессировал IgG1 на уровнях, соизмеримых с вектором без интрона (фиг. 5).
Для определения того, допускает ли слияние Fab-фрагмента с фаговым адаптерным пептидом, введенным в последовательность интрона 1, и дисплей ли фаге, и экспрессию IgG в бактериальных клетках и клетках млекопитающих, соответственно, адаптерный пептид (фиг. 3B) или ген-III белка оболочки фага (фиг. 3C) был вставлен в конструкцию h4D5 HC.интрон 1 на 5'-конце интрона 1 или интрона 3. Природная донорная последовательность сплайсинга из интрона 1 или 3 была перемещена непосредственно 5' от адаптерного пептида. Когда конструкцию HC-адаптер.интрон 1 коэспрессировали с LC h4D5 в клетках млекопитающих, экспрессия IgG h4D5 составляла приблизительно 40% (в случае содержащего адаптер интрона) или 5% (в случае содержащего ген-III интрона) от таковой контрольной конструкции без интрона (фиг. 4A). ПЦР в режиме реального времени показала, что хотя часть мРНК для HC-адаптера была подвергнута надлежащему сплайсингу (фиг. 4B, серединная полоса), значительное количество мРНК или не подвергнуто сплайсингу (фиг. 4B, верхняя полоса), или подвернуто ненадлежащему сплайсингу из скрытой донорной последовательности сплайсинга в VH-области (фиг. 4B, нижняя полоса). мРНК HC-ген-III почти полностью подвергалась сплайсингу из скрытой донорной последовательности сплайсинга. Молчащая мутация скрытой донорной последовательности сплайсинга приводили только к накоплению по подвергнутой сплайсингу мРНК (не представлено).
Ввиду неспособности интрона к эффективному сплайсингу в случае вставки адаптерной последовательности, авторы настоящего изобретения сравнили природную донорную последовательность сплайсинга с известной консенсусной донорной последовательностью сплайсинга для мРНК млекопитающих (Stephens et al., J. of Molecular Biology, 228: 1124-1136 (1992)). Как показано на фиг. 5, природная донорная последовательность сплайсинга из интрона 1 hIgG1 отличается от консенсусной донорной последовательности в трех из восьми положений. Замены в положениях 1 и 5 были проанализированы дополнительно, поскольку эти положения являются более консервативными, чем положение 8. Была создана мутантная донорная последовательность сплайсинга (донор 1), в которой основания в положениях 1 и 5, были изменены, чтобы соответствовать консенсусной последовательности (фиг. 5A), и была проверена способность этих модифицированных донорных последовательностей к опосредованию сплайсинга синтетического интрона в HC. Эта оптимизированная донорная последовательность сплайсинга полностью восстанавливала сплайсинг синтетического интрона (фиг. 5B) с сопутствующим увеличением экспрессии IgG h4D5 до уровня, который соответствовал таковому контрольной конструкции, не содержащей интрон (фиг. 5C). Увеличение сплайсинга и экспрессии IgG отмечалось независимо от того, содержит ли синтетический интрон адаптерный пептид или ген-III, а также независимо от того, основан ли синтетический интрон на интроне 1 или интроне 3 hIgG1.
Пример 3: Создание системы экспрессии и секреции для прокариотических и эукариотических клеток
Для создания двойственной векторной плазмиды авторы настоящего изобретения использовали происходящий из pBR322 фагемидный вектор, в настоящее время используемый для фагового дисплея, pRS. Этот бицистронный вектор состоит из бактериального промотора PhoA, регулирующего экспрессию кассеты для легкой цепи антитела со связанной с ней сигнальной последовательностью STII, за которой следует кассета для тяжелой цепи антитела со связанной с ней сигнальной последовательностью STII. На конце последовательности легкой цепи находится эпитопная метка gD для обнаружения дисплея Fab на фаговых частицах. В обычных фагемидах последовательность тяжелой цепи состоит только из VH- и CH1-доменов hIgG и слита на нуклеотидном уровне с полезным пептидом, таким как белок слияния фага, чаще всего геном-III, который кодирует белок оболочки фага pIII, или адаптерный пептид. 3'-Конец кассет для легкой цепи и тяжелой цепи содержит последовательность терминатора транскрипции лямбда для прекращения транскрипции в E. coli. Поскольку этот вектор порождает легкую цепь и тяжелую цепь-pIII с одного мРНК-транскрипта, между последовательностями LC и HC нет регулирующих транскрипцию элементов. Вектор также содержит ген бета-лактамазы (bla) для придания устойчивости к ампициллину, начало репликации pMB1 в E. coli и начало f1 для экспрессии пилуса на бактериальной поверхности, что делает возможным инфицирование фагом M13. Другая форма этого вектора также включает начало репликации SV40 для эписомной репликации плазмиды в соответствующих линиях клеток млекопитающих.
Для конструирования исходного двойственного вектора (называемого здесь «pDV.6.0») авторы настоящего изобретения вставили промотор CMV млекопитающих из pRK (вектора для экспрессии в клетках млекопитающих, используемого для экспрессии IgG и других белков) 5' от промотора PhoA, управляющего экспрессией цистрона LC-HC. В конце кодирующей LC антитела последовательности авторы настоящего изобретения вставили стоп-кодон амбер, за которым следовала эпитопная метка gD, позволяющая обнаружить меченные LC на фаге после дисплея в являющемся амбер-супрессором штамме E. coli. Эпитопная метка отсутствует при экспрессии вектора в клетках млекопитающих. Таким образом, кассета для LC включает (в порядке от 5' к 3') эукариотический промотор, бактериальный промотор, сигнальную последовательность, кодирующую легкую цепь антитела (LC) последовательность и эпитопную метку (gD).
Затем, между кассетами для HC и LC авторы настоящего изобретения вставили синтетическую кассету, включающую (в порядке от 5' к 3') сигнал полиаденилирования/сигнал терминации транскрипции SV40 млекопитающих, последовательность терминатора лямбда для терминации транскрипции в E. coli, промотор CMV и промотор PhoA.
Затем сигнал полиаденилирования/сигнал терминации транскрипции SV40 млекопитающих и последовательность терминатора лямбда были вставлены после кассеты для HC. Кассета для HC включает сигнальную последовательность и кодирующую тяжелую цепь антитела (HC) последовательность.
Чтобы сделать возможной секрецию слитого белка(ов), представляющего интерес, и в прокариотических, и в эукариотических клетках, авторы настоящего изобретения заменили сигнальную последовательность STII, предшествующую LC и HC, эукариотической сигнальной последовательностью из мышиного связывающего иммуноглобулинового белка (mBiP). Скрининг нескольких сигнальных последовательностей-кандидатов привел авторов настоящего изобретения к обнаружению того, что эта сигнальная последовательность способна функционировать в приложениях, в которых требуется прокариотическая экспрессия (т.е. фаговый дисплей) и/или эукариотическая экспрессия (т.е. экспрессия IgG в клетках млекопитающих), и что сигнальная последовательность из mBiP функционирует настолько же хорошо в обоих из этих окружений, как и соответствующие сигнальные последовательности, которые использовались до этой работы.
Чтобы сделать возможной экспрессию слияния Fab-фаговый полипептид в E. coli и IgG в клетках млекопитающих авторы настоящего изобретения создали синтетический интрон в кассете для HC. Авторы настоящего изобретения модифицировали природный интрон из интрона 1 или интрона 3 IgG1 человека для создания синтетического интрона, содержащего белок слияния (ген-III) для дисплея на фаговых частицах. Геномную последовательность интрона 1 (или интрона 3) из IgG1 человека вставляли непосредственно после последовательности гена-III, отделенной с помощью стоп-кодона для образования слияний Fab HC-p3 в E. coli. Для размещения природного донорного октануклеотида сплайсинга в 5' фланкирующем районе синтетического интрона потребовались две аминокислотных мутации в шарнирной области в случае экспрессии в E. coli (E212G и P213K, в соответствии с нумераций по Kabat), и мутации для создания оптимизированной донорной последовательности сплайсинга приводят к тому, что оба из этих остатков мутируются с заменой на лизин. Эти мутации не оказывают воздействие на уровни дисплея на фаге (не представленные данные) и, поскольку шарнирная область фага удается во время процесса сплайсинга, будут отсутствовать в полноразмерном IgG, экспрессируемом в клетках млекопитающих.
Альтернативно, в случае использования фагового дисплея адаптера, авторы настоящего изобретения сконструировали вектор, схожий с вектором pDV6.0, описанным выше, с отличным синтетическим интроном, (называемый здесь pDV5.0, представленный на фиг. 7). Последовательность гена-III заменяли одним из двух членов пары «лейциновая молния» (называемым здесь «адаптером»). В этом синтетическом интроне за последовательностью адаптерного пептида следует стоп-кодон и геномная последовательность интрона 1 или 3. В случае этой конструкции авторы настоящего изобретения также вставили отдельную бактериальную экспрессионную кассету, состоящую из гена-III, слитого с узнаваемым членом пары «лейциновая молния». Эта отдельная бактериальная экспрессионная кассета была вставлена 5' от промотора CMV для LC и контролируется промотором PhoA, содержит сигнальную последовательность STII для ограничения экспрессии слияния адаптер-ген-III в E. coli, и содержит терминатор лямбда непосредственно 3'. При экспрессии в E. coli тяжелая и легкая цепи собираются в периплазме с образованием Fab, и адаптер, слитый с тяжелой цепью, устойчиво связывается с узнаваемым адаптером на белке pIII-адаптер. Упаковка этого собранного комплекса Fab-адаптер-pIII в фаговые частицы будет приводить к фаговому дисплею представляющего интерес Fab. Кроме того, авторы настоящего изобретения создали специально разработанный мутант фага-помощника KО7, в котором являющийся партнером адаптер слит с N-концом гена-III (адаптер-KО7). Инфицирование E. coli, содержащей pDV.5.0, фагом-помощником адаптер-KО7 приводит к тому, что все копии pIII, присутствующие на зрелой фагемиде, слиты с адаптером. В результате все копии pIII доступны для ассоциации со слиянием Fab-адаптер, а не только те копии pIII, которые произошли от pDV5. Однако в некоторых случаях боле низкие уровни дисплея могут быть желательны, когда пытаются найти редкие клоны с высокой аффинностью (например, в приложениях, относящихся к созреванию аффинности). В этом случае инфицирование E. coli, содержащей pDV.5.0, обычным фагом-помощником KО7 будет приводить к тому, что смесь слияния адаптер-pIII (из pDV.5.0) и pIII дикого типа (из фага-помощника KО7) будет представлена на фаговых частицах. В этом сценарии, поскольку лишь подсовокупность всей совокупности pIII может соединяться с адаптер-Fab, результирующие уровни дисплея будут ниже, чем в случае использования фага-помощника адаптер-KО7. Эта возможность модулировать уровни дисплея просто посредством выбора соответствующего фага-помощника является уникальным преимуществом настоящего изобретения.
Авторы настоящего изобретения оценили способность pDV5.0 экспрессировать различные IgG в клетках млекопитающих. HC и LC из четырех различных IgG человека были субклонированы в pDV5.0 и экспрессированы в клетках 293. Немного неожиданно, что общие выходы от pDV были последовательно в ~10 раз меньше таковых от двухплазмидной системы. Однако же выходы являются выходами порядка ~0,1-0,4 мг на 30 мл культуры (фиг. 6B). Это количество материала является более чем достаточным для обычных скрининговых исследований и может быть легко увеличено до 0,1-1 л или более, если требуется большее количество материала. Было установлено с помощью гель-хроматографии, что IgG являются на >90% мономерными в растворе.
Пример 4: Создание мутантного фага-помощника, M13KO7 с амбер-мутацией в гене-III (AMBER KO7)
Для увеличения дисплея белков, слитых с pIII, на фаге M13 авторы настоящего изобретения создали мутантный фаг-помощник, Amber KО7, используя сайт-направленный мутагенез Amber KО7 содержит амбер-кодон, введенный в геном фага-помощника M13KO7 с помощью сайт-направленного мутагенеза. Нуклеотидная последовательность pIII (нуклеотиды 1579-2853) мутантного фага-помощника Amber KО7 представлена на фиг. 8.
Для создания Amber KО7 фаг-помощник M13KO7 использовали для инфицирования штамма CJ236 Escherichia coli (генотип dut-/lung-), и вирионы потомства собирали для очистки оцДНК, используя набор для очистки оцДНК (QIAGEN). Синтетический олигонуклеотид (последовательность 5'-GTGAATTATCACCGTCACCGACCTAGGCCATTTGGGAATTAGAGCCA-3') (SEQ ID NO: 23) использовали для мутирования гена-III в M13KO7 с помощью сайт-направленного мутагенеза с использованием олигонуклеотида. Подвергнутую мутагенезу ДНК использовали для трансформации клеток E. coli XLl-Blue (Agilent Technologies) и засевали на газон неинфицированных клеток XLl-Blue на чашках с мягким агаром. Бляшки отбирали по отдельности, и клетки выращивали в среде LB, содержащей 50 мкг/мл канамицина. Двухцепочечную ДНК репликационной формы (RF) экстрагировали с помощью набора DNA Miniprep kit и секвенировали для подтверждения присутствия амбер-мутации. Гомогенность популяции подтверждали посредством расщепления эндонуклеазой рестрикции AvrII и электрофореза в агарозном геле ДНК RF. Все стадии манипулирования рекомбинантной ДНК выполняли, как описано (Sambrook, J. et al., A Laboratory Manual, Third Edition, Cold Spring Harbor Laboratroy Press, Cold Spring Harbor, NY, 2001).
Уровень дисплея Fab на фаговых частицах, продуцированных, используя Amber KО7, определяли с помощью ELISA для фагов. Антиген (Her2) подвергали иммобилизации на иммунопланшетах, и фаги, содержащие Fab против Her2, продуцировали в клетках XL1-Blue, используя фаг-помощник или KО7 дикого типа (WT K07), или модифицированный M13KO7, содержащий амбер-мутацию в pIII (Amber KО7). Связывание детектировали посредством инкубации с конъюгатом мышиное антитело против M13-HRP, а затем субстратом TMB с последующим измерением ОП при 450 нм. Использование Amber KО7 привело к более высоким уровням дисплея фагемидой с низким уровнем дисплея (замкнутые треугольники) по сравнению с уровнями, достигнутыми с помощью той же фагемиды, когда KО7 дикого типа использовали для продукции фагов (замкнутые квадраты) (фиг. 9). Уровень дисплея Fab фагемидой с низким уровнем дисплея, используя Amber KО7 (замкнутые треугольники), был также схож с уровнем дисплея Fab, отмечаемым при использовании фагемиды с высоким уровнем дисплея с KО7 дикого типа (открытые ромбы) (фиг. 9).
Пример 5: Создание системы экспрессии и секреции для прокариотических и эукариотических клеток с целью создания библиотек только HC на основе не иммунизированных источников и использование системы для пэннинга фагов
Помимо векторов прямых и непрямых слияний, характерными чертами которых являются прокариотические и эукариотические промоторы и для HC, и для LC (pDV5.0 и pDV6.0), описанных в примере 3, авторы настоящего изобретения создали модифицированную двойственную векторную конструкцию прямого слияния (pDV.6.5, представленную на фиг. 14), в которой LC Fab слита с сигнальной последовательностью STII и управляется только бактериальным промотором PhoA, тогда как НС Fab (содержащая последовательности ген-III-синтетический интрон и Fc hIgG для экспрессии НС полноразмерного hIgG1 в клетках млекопитающих) управлялась как эукариотическим промотором CMV, так и прокариотическим промотором PhoA. Эту конструкцию использовали для повтора библиотеки синтетических Fab человека, ранее описанной (Lee, et al., Journal of Molecular Biology, 340. 1073-1093 (2004)), в которой разнообразие внесено только в HC. Для экспрессии полноразмерного IgG с этого вектора требуется котрансфекция вектором для экспрессии в клетках млекопитающих, который кодирует LC.
Библиотеки фагового дисплея были созданы, используя мутагенез с использованием олигонуклеотидов (Kunkel) и вариантов pDV.6.5 «стоп-матрица», в которых стоп-кодоны (TAA) были помещены во все три CDR тяжелой цепи. Эти стоп-кодоны подвергались репарации во время реакции мутагенеза с использованием смеси олигонуклеотидов, которые подвергались отжигу вдоль участков, кодирующих CDRH1, H2 и H3, и заменяли кодоны в положениях, выбранных для рандомизации, вырожденными кодонами. Реакции мутагенеза подвергали электропорации в клетки XL1-Blue, и культуры выращивали, используя протокол изменения температуры (37°C в течение 4 часов, а затем 36 часов при 30°C) в бульоне 2YT, дополненном фагом-помощником Amber.KО7, 50 мкг/мл карбенициллина и 25 мкг/мл канамицина. Фаги собирали из культуральной среды посредством преципитации с использованием ПЭГ/NaCl. Для каждой реакции электропорации использовали ~5 мкг ДНК, и она давала 1×108-7×108 трансформантов.
Пэннинг библиотеки фагов, созданной в этом векторе на основе не иммунизированных источников, выполняли против фактора роста эндотелия сосудов (VEGF). Для сортировки библиотеки фагов белковые антигены подвергали иммобилизации на иммунопланшетах Maxisorp, и библиотеки подвергали четырем-пяти циклам отборов по связыванию. Альтернативно лунки блокировали, используя BSA или казеин, в альтернативных циклах. Случайные клоны, отобранные в результате циклов с 3 по 5 включительно, исследовали, используя ELISA для фагов, для сравнения связывания с антигеном-мишенью (VEGF) и нерелевантным белком (Her2) для проверки неспецифического связывания. Вкратце, фаговые клоны выращивали в течение ночи в 1,6 мл бульона 2YT, дополненного фагом-помощником Amber.KО7 (пример 4). Супернатанты связывали с планшетами с иммобилизованным антигеном или планшетами, покрытыми нерелевантным белком, в течение 1 часа при комнатной температуре. После промывки связавшийся фаг детектировали, используя конъюгированное с HRP антитело против M13 (в течение 20 минут при комнатной температуре) с последующим детектированием с использованием субстрата TMB. Авторы настоящего изобретения изолировали множество клонов, которые были позитивными в ELISA по VEGF, но не по нерелевантному контрольному белку (Her2) (фиг. 10 - столбчатая диаграмма).
ДНК из этих клонов, которые продемонстрировали специфичность в отношении VEGF, затем использовали для экспрессии полноразмерного IgG посредством котрансфекции вектором для экспрессии в клетках млекопитающих, кодирующим общую LC, клеток 293 в маломасштабных суспензионных культурах для экспрессии полноразмерного hIgG1. Культуры объемом 1 мл трансфецировали, используя Expifectamine или JetPEI в соответствии с инструкциями производителя, и инкубировали при 37°C/8% CО2 в течение 5-7 дней. Трансфекции в увеличенном масштабе выполняли в 30 мл клеток 293.
Супернатанты культур затем использовали для скрининга IgG на предмет связывания с VEGF в анализе захвата Fc, используя прибор BIAcore T100 (фиг. 11). Содержащие IgG супернатанты от культур объемом 1 мл использовали для скрининга на предмет связывания с антигеном. Антитело против Fc человека для захвата подвергали иммобилизации на сенсорном чипе СМ5 серии S (~10000 единиц ответа (RU)). Супернатанты последовательно пропускали через проточные ячейки 2, 3 и 4 (5 мкл/мин в течение 4 минут) для допуска захвата IgG из супернатанта (50-150 RU), после чего пропускали антиген (100-1000 нМ) над иммобилизованными IgG (30 мкл/мин в течение 2 минут) для измерения ответа связывания.
Секвенирование позитивных связующих веществ выявляет восемь уникальных последовательностей (последовательности CDR тяжелой цепи представлены на фиг. 12) с позитивными характеристиками связывания (фиг. 12). Данные секвенирования (фиг. 12) в сочетании с ELISA для фагов (фиг. 10) и полученными с использованием BiaCore данными (фиг. 11) использовали для отбора совокупности из восьми анти-VEGF клонов для дальнейшего анализа.
В случае этих восьми клонов масштаб экспрессии был увеличен до 100-мл культур клеток яичника китайского хомячка (СНО) (см. фиг. 15), и очищенный материал использовали для оценки способности анти-VEGF клонов блокировать связывание VEGF с одним из узнаваемых им рецепторов (VEGFR1) с помощью ELISA блокирования рецептора. Биотинилированный hVEGF165 (2 нМ) инкубировали с последовательно разведенными в 3 раза антителами против VEGF (200 нМ максимальная концентрация) в PBS/0,5% BSA/0,05% Tween-20. После инкубации в течение 1-2 часа при комнатной температуре смеси переносили в планшеты с иммобилизованным VEGFR1 и инкубировали в течение 15 минут. Связавшийся с VEGFR-1 VEGF затем детектировали с использованием стрептавидина-HRP в течение 30 минут с последующим развитием реакции с использованием субстрата TMB, и определяли значения IC50.
Авторы настоящего изобретения идентифицировали один клон (VEGF55) с IC50, соизмеримой с таковой для бевицизумаба, коммерческого антитела против VEGF (фиг. 13). Таким образом авторы настоящего изобретения смогли перейти напрямую от пэннинга фагов к экспрессии IgG и отсортировать совокупность клонов вплоть до одного кандидата, все без потребности в субклонировании.
В заключение, этот модифицированный двойственный вектор прямого слияния (pDV.6.5) смогли использовать для конструирования библиотек фагового дисплея с рандомизированными тяжелыми цепями и неизменными легкими цепями в E. coli и смогли использовать для последующей экспрессии отобранных клонов в виде природных IgG1 в клетках млекопитающих без субклонирования при совместном применении с вектором для экспрессии легкой цепи. Поскольку промотор CMV млекопитающих присутствуют только 5' от HC, pDV экспрессировал и LC Fab, и HC Fab-pIII в E. coli, но экспрессировал только hIgG1HC в клетках млекопитающих. Этот вектор использовали для отбора Fab-фрагментов из библиотеки синтетических Fab, связывающихся с множеством антигенов, на основе не иммунизированных источников и затем для экспрессии полноразмерного природного hIgG1 из отобранных клонов в клетках 293 и CHO млекопитающих посредством котрансфекции клонов, содержащих модифицированный двойственный вектор прямого слияния, вектором для экспрессии в клетках млекопитающих, кодирующим общую LC. Природный IgG1 был получен в результате этих экспериментов по экспрессии для проведения нескольких анализов, так что из совокупности 8 уникальных анти-VEGF клонов, демонстрирующих активность связывания в ELISA и BIAcore, авторы настоящего изобретения смогли произвести отбор вплоть до одного кандидата на оценку поведения в растворе, неспецифического связывания и биологической активности кандидатов в IgG-формате без необходимости в субклонировании последовательностей HC из первоначальных клонов фаговых векторов.
Хотя вышеприведенное изобретение было описано подробно ради иллюстрации и примера для целей четкости понимания, описание и примеры не следует рассматривать как ограничение объема настоящего изобретения. Описание всей патентной и научной литературы, на которую здесь ссылаются, включено намеренно в ее полном объеме посредством ссылки.























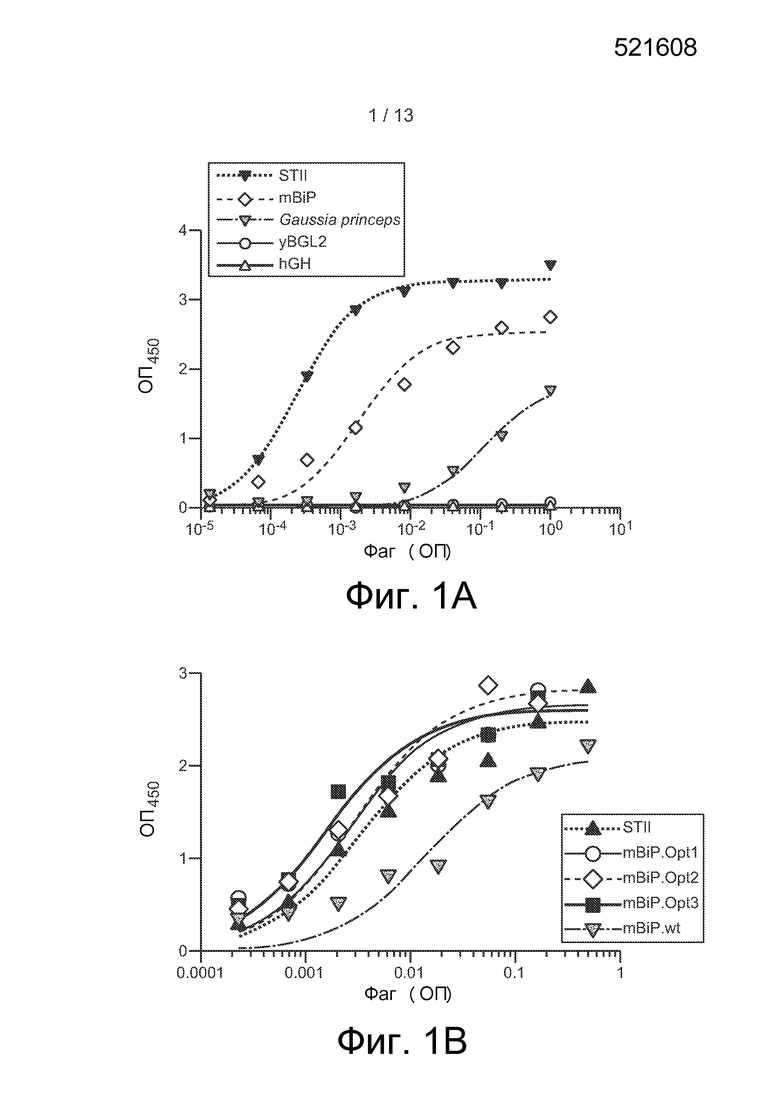
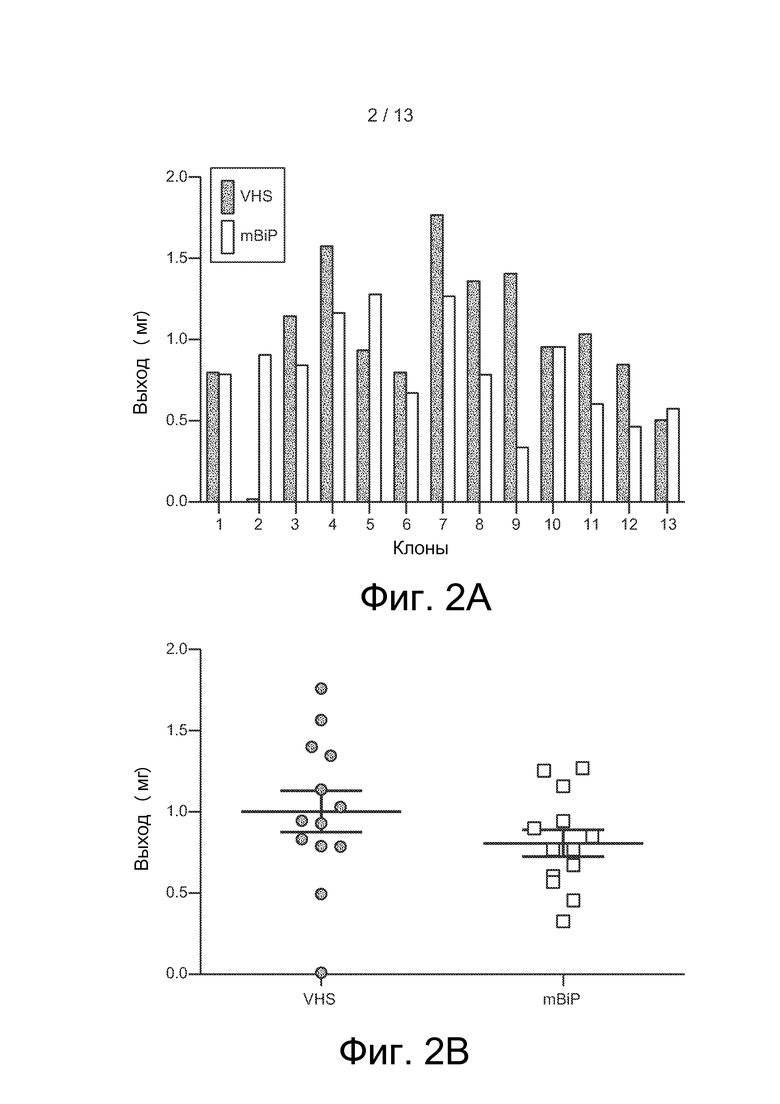

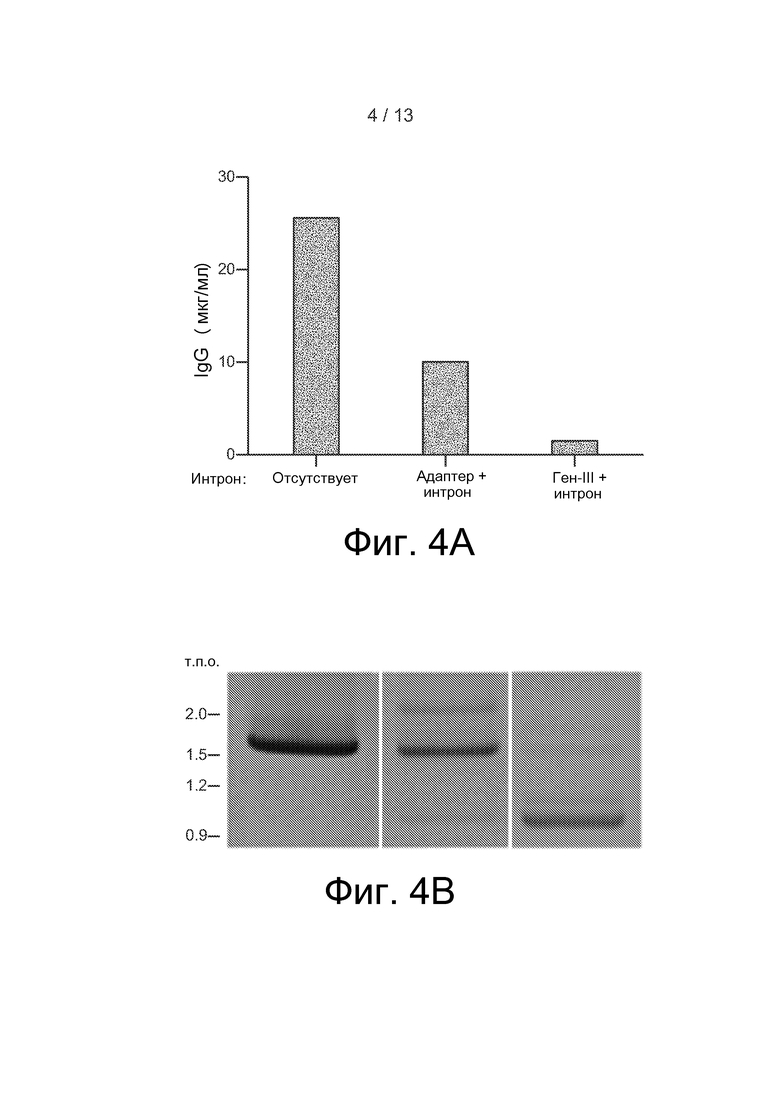

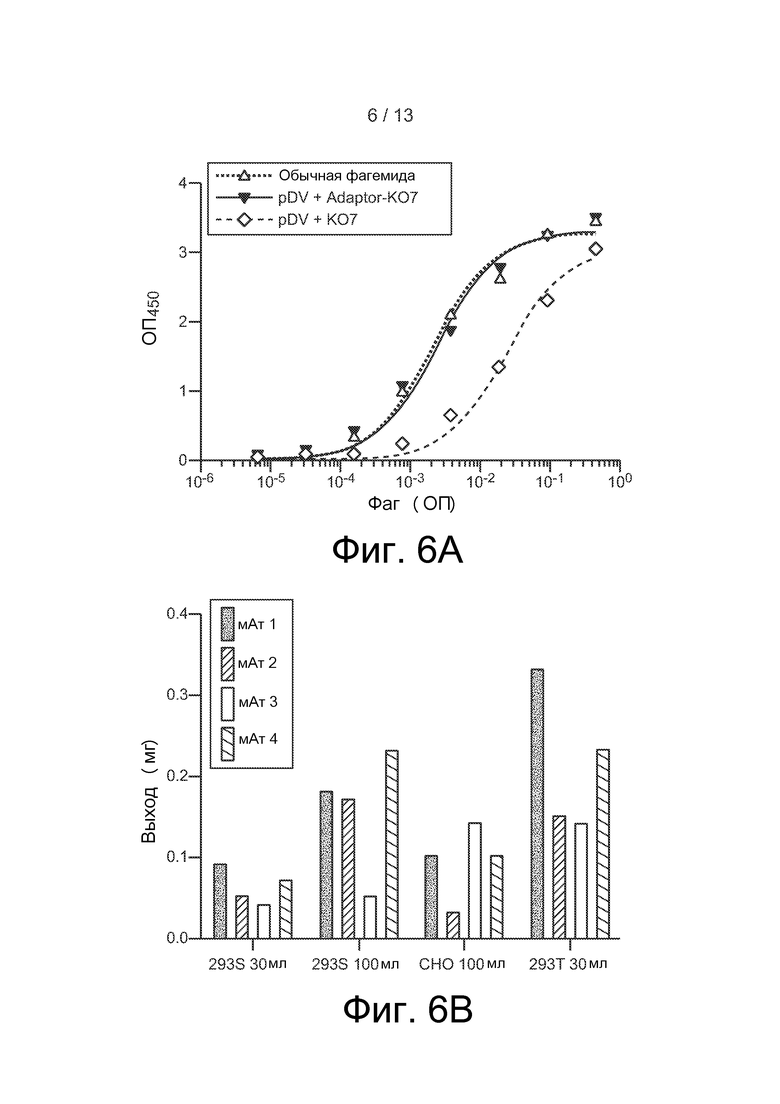
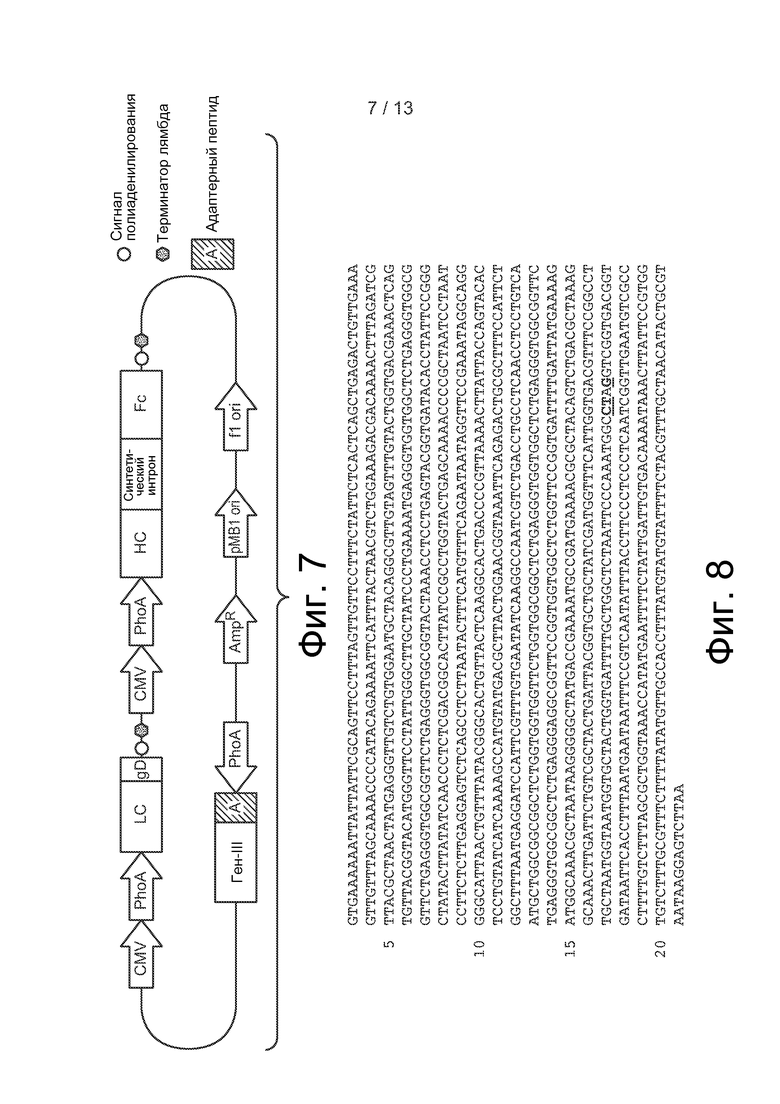

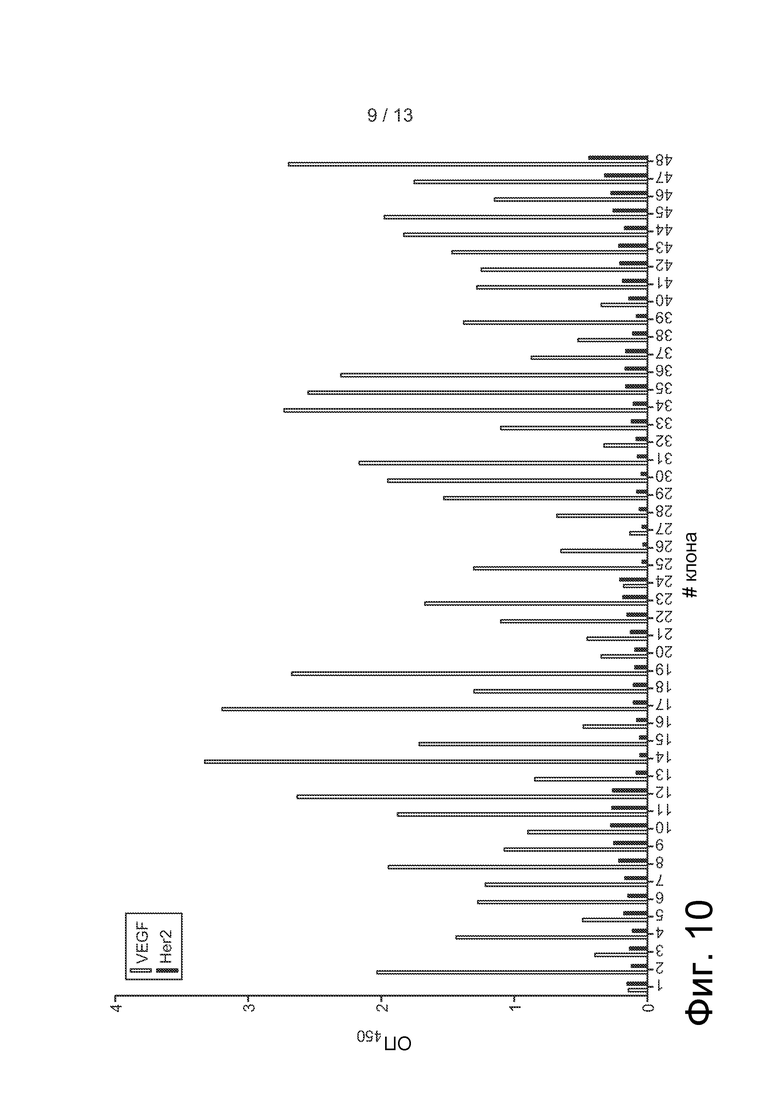
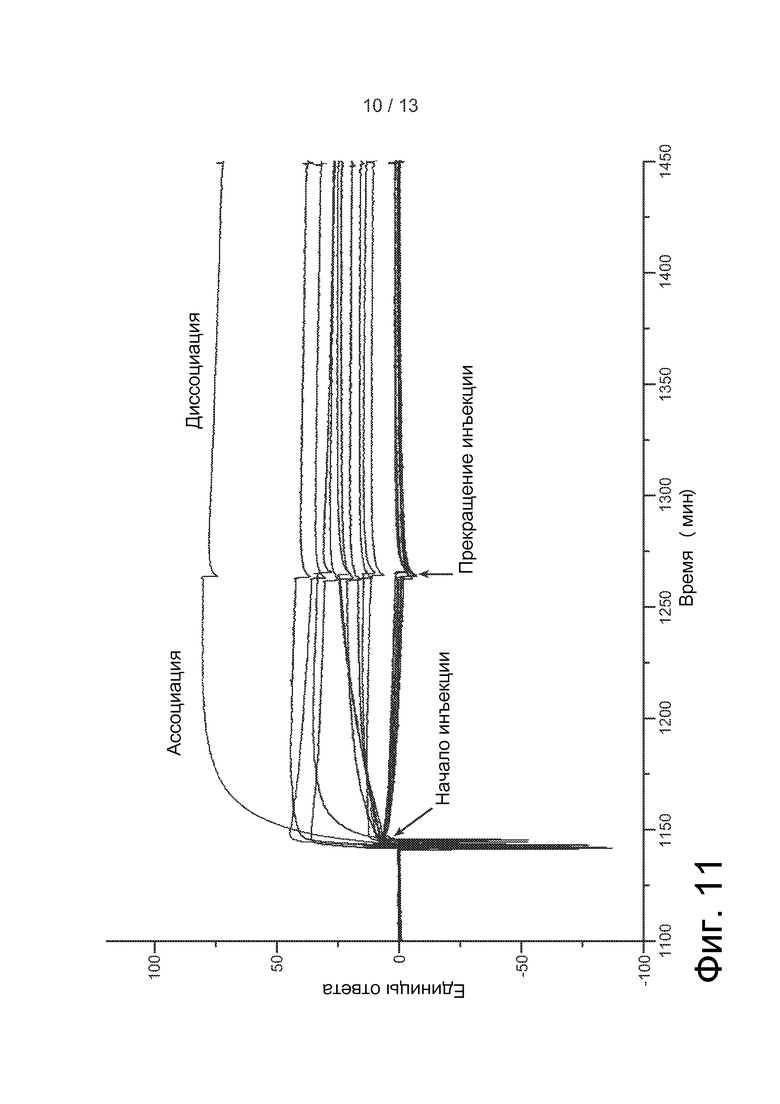
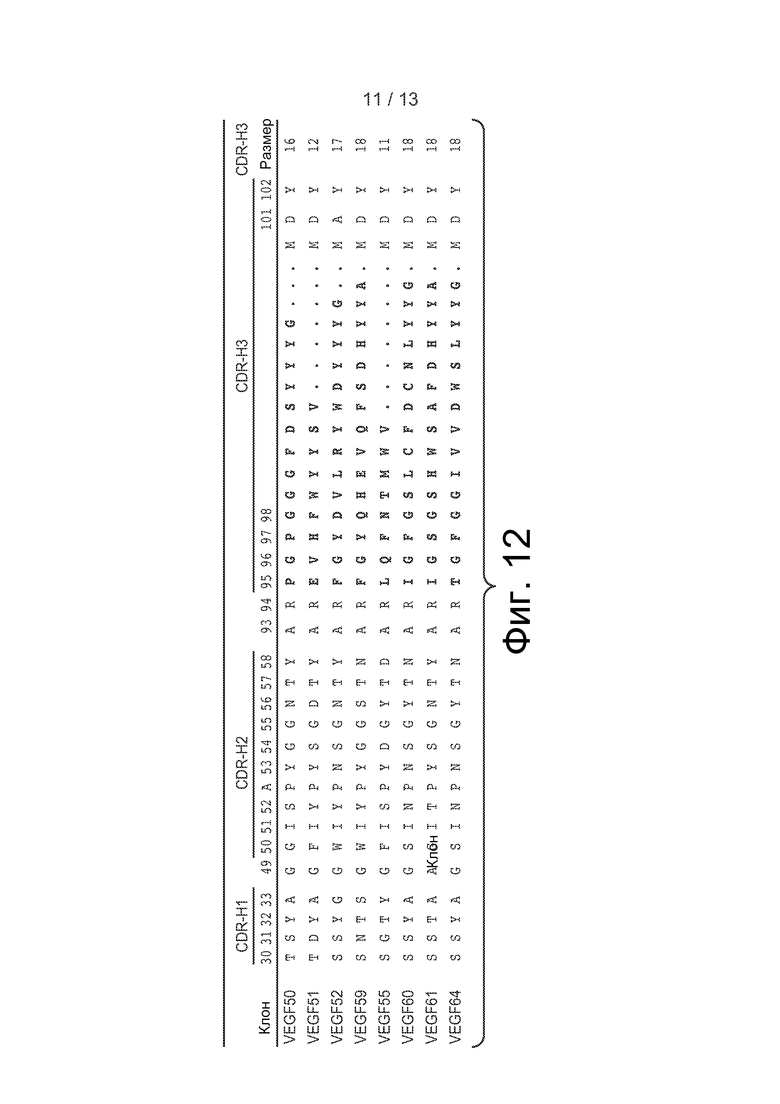
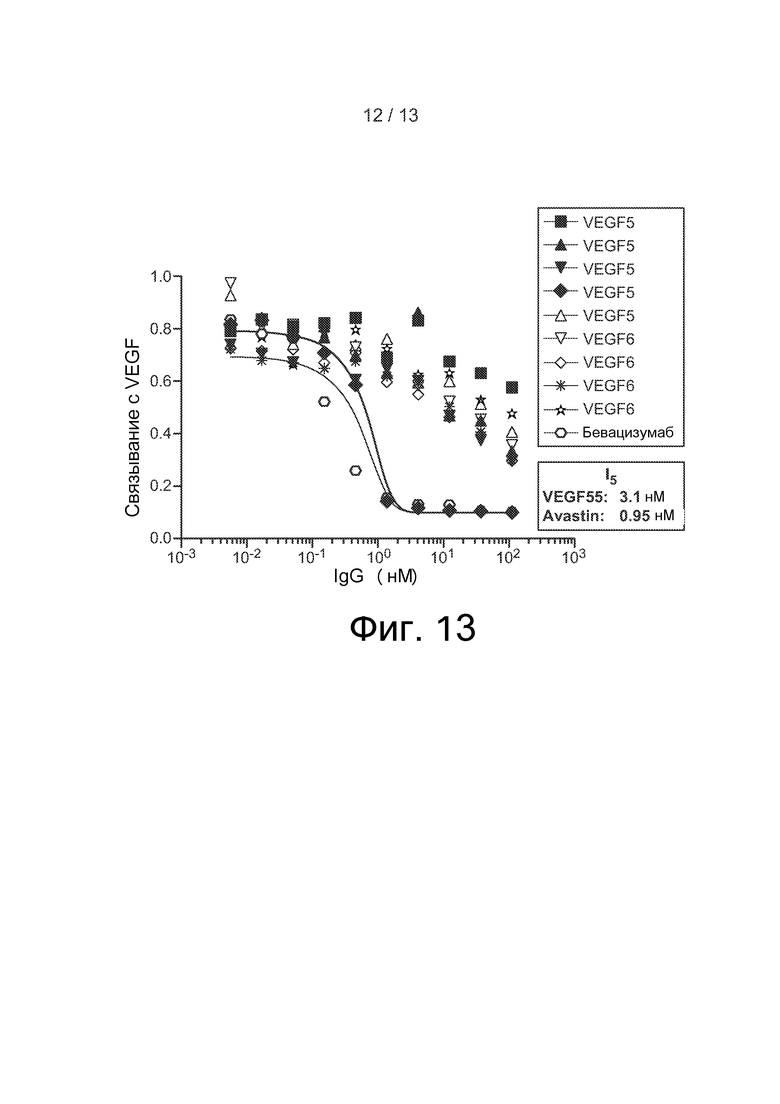
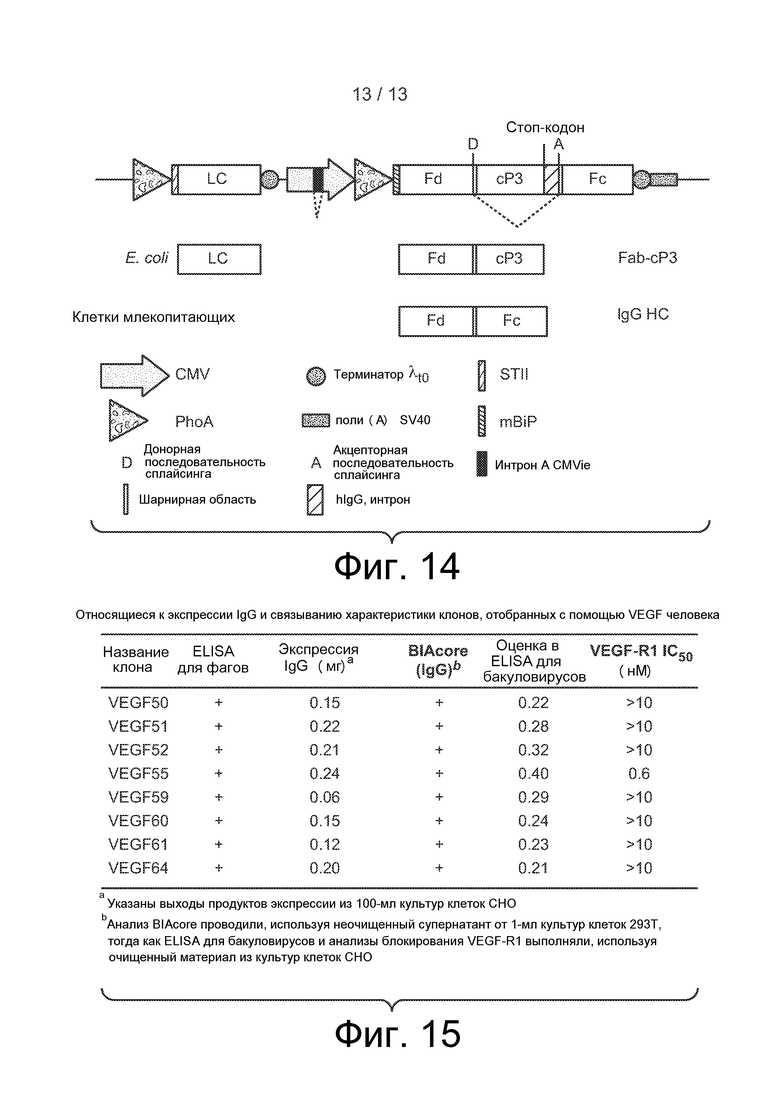
Изобретение относится к области биохимии, в частности к молекуле нуклеиновой кислоты, кодирующей первый полипептид, второй полипептид, сигнальную последовательность mBIP и либо белок оболочки, либо адаптерный белок. Изобретение также относится к экспрессионному вектору, включающему вышеуказанную молекулу нуклеиновой кислоты и клетке-хозяину для продуцирования антитела, трансформированную вышеуказанным экспрессионным вектором. Кроме того, раскрыт способ продуцирования антитела, включающий культивирование вышеуказанной клетки-хозяина, где экспрессируется антитело. Изобретение позволяет получать высокоэффективную систему экспрессии и секреции слитого с Fab белка в прокариотической и эукариотической клетке. 4 н. и 20 з.п. ф-лы, 1 табл., 23 ил., 5 пр.
1. Молекула нуклеиновой кислоты, кодирующая первый полипептид, второй полипептид, сигнальную последовательность mBIP и либо белок оболочки, либо адаптерный белок, где
(a) первый полипептид содержит вариабельный домен тяжелой цепи (VH), включающий VH-HVR1, VH-HVR2 и VH-HVR3,
(b) второй полипептид включает вариабельный домен легкой цепи (VL), включающий VL-HVR1, VL-HVR2 и VL-HVR3,
(c) сигнальная последовательность mBIP является функциональной как в прокариотической, так и в эукариотической клетке и кодируется последовательностью нуклеиновой кислоты SEQ ID NO: 11, где сигнальная последовательность mBIP кодируется последовательностью нуклеиновой кислоты, функционально связанной с последовательностью нуклеиновой кислоты, кодирующей первый полипептид и последовательностью нуклеиновой кислоты, кодирующей второй полипептид, и
(d) первый полипептид и второй полипептид образуют полноразмерное антитело, где первый полипептид или второй полипептид слиты с указанным белком оболочки или указанным адаптерным белком.
2. Молекула нуклеиновой кислоты по п.1, где VL-домен связан с белком gD или его фрагментом и VH-домен связан с Fc.
3. Молекула нуклеиновой кислоты по п.1, где сигнальная последовательность (a) направляет секрецию белка в эндоплазматический ретикулум или вовне клетки у эукариотических клеток, и (b) направляет секрецию белка в периплазму или вовне клетки у прокариотических клеток.
4. Молекула нуклеиновой кислоты по п.2, где VH-домен дополнительно связан с CH1-доменом, а VL-домен связан с CL-доменом.
5. Молекула нуклеиновой кислоты по п.1, где
(a) нуклеиновую кислоту, кодирующую белок оболочки или адаптерный белок, содержит синтетический интрон;
(b) адаптерный белок представляет собой «лейциновую молнию»;
(c) адаптерный белок включает аминокислотную последовательность SEQ ID NO: 8, 9, 12, 13, 14 или 15;
(d) адаптерный белок включает аминокислотную последовательность с по меньшей мере одной модификацией аминокислоты SEQ ID NO: 8, 9, 12, 13, 14 или 15, где указанная модификация сохраняет или увеличивает сродство адаптерного белка к другому адаптерному белку;
(e) белок оболочки выбирают из группы, состоящей из pI, pII, pIII, pIV, pV, pVI, pVII, pVIII, pIX и pX бактериофага M13, f1 или fd; или
(f) адаптерный белок включает аминокислотную последовательность SEQ ID NO: 6 (ASIARLRERVKTLRARNYELRSRANMLRERVAQLGGC) SEQ ID NO: 7 (ASLDELEAEIEQLEEENYALEKEIEDLEKELEKLGGC).
6. Молекула нуклеиновой кислоты по п.1, где нуклеиновую кислоту, кодирующую белок оболочки или адаптерный белок, содержит синтетический интрон и указанный синтетический интрон расположен между нуклеиновой кислотой, кодирующей VH-домен, и нуклеиновой кислотой, кодирующей Fc или шарнир.
7. Молекула нуклеиновой кислоты по п.6, где синтетический интрон дополнительно включает нуклеиновую кислоту, кодирующую встречающийся в природе интрон из IgG1.
8. Молекула нуклеиновой кислоты по п.7, где встречающийся в природе интрон из IgG1 представляет собой интрон 1, интрон 2 или интрон 3 из IgG1.
9. Молекула нуклеиновой кислоты по п.1, где белок оболочки представляет собой pIII или его фрагмент бактериофага M13, f1 или fd.
10. Молекула нуклеиновой кислоты по п.1, где белок оболочки выбирают из группы, состоящей из pI, pII, pIII, pIV, pV, pVI, pVII, pVIII, pIX и pX бактериофага M13, f1 или fd; и
в прокариотических клетках экспрессируется первый слитый белок, а в эукариотических клетках экспрессируется второй слитый белок.
11. Молекула нуклеиновой кислоты по п.10, где
(a) первый слитый белок и второй слитый белок являются одинаковыми; или
(b) первый слитый белок и второй слитый белок являются различными.
12. Молекула нуклеиновой кислоты по п.11, где первый слитый белок представляет собой слитый Fab-фаговый полипептид белок.
13. Молекула нуклеиновой кислоты по п.12, где слитый Fab-фаговый полипептид белок включает VH/CH1 домен, слитый с pIII.
14. Молекула нуклеиновой кислоты по п.13, где второй слитый белок представляет собой слитый белок Fab-Fc или Fab-шарнир-Fc.
15. Молекула нуклеиновой кислоты по п.14, где слитый белок Fab-Fc или Fab-шарнир-Fc включает VH/CH1, слитый с Fc.
16. Молекула нуклеиновой кислоты по п.3, дополнительно включающая нуклеиновую кислоту, кодирующую CH1-домен, и нуклеиновую кислоту, кодирующую Fc, где
(a) нуклеиновая кислота, кодирующая CH1-домен, включает часть природной донорной последовательности сплайсинга или часть модифицированной донорной последовательности сплайсинга.
17. Молекула нуклеиновой кислоты по п.3, где сигнальная последовательность mBIP кодируется последовательностью нуклеиновой кислоты, выбираемой из группы SEQ ID NO: 16, SEQ ID NO: 17 и SEQ ID NO: 18.
18. Экспрессионный вектор, включающий молекулу нуклеиновой кислоты по любому из пп.1-17.
19. Клетка-хозяин для продуцирования антитела, где указанная клетка-хозяин трансформирована экспрессионным вектором по п.18.
20. Клетка-хозяин по п.19, где клетка-хозяин представляет собой бактериальную клетку или эукариотическую клетку.
21. Клетка-хозяин по п.20, где бактериальная клетка представляет собой клетку E. coli.
22. Клетка-хозяин по п.20, где эукариотическая клетка представляет собой дрожжевую клетку, клетку CHO, клетку НЕК 293 или клетку NSO.
23. Способ продуцирования антитела, включающий культивирование клетки-хозяина по п.19, где экспрессируется антитело.
24. Молекула нуклеиновой кислоты по п.1, причем молекулу нуклеиновой кислоты, кодирующую белок оболочки или адаптерный белок, содержит синтетический интрон, и указанный синтетический интрон расположен между нуклеиновыми кислотами, кодирующими
(a) CH2-домен и CH3-домен антитела, или
(b) шарнирную область и CH2-домен антитела.
| Y HUMPHREYS D | |||
| P | |||
| et al., High-level periplasmic expression in Escherichia coli using a eukaryotic signal peptide: importance of codon usage at the 5 end of the coding sequence, Protein expression and purification, 2000, Т | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| JOHANSSON D | |||
| X | |||
| et al., Efficient expression of recombinant human monoclonal antibodies in Drosophila S2 cells, Journal of immunological methods, 2007, Т | |||
| Способ изготовления фасонных резцов для зуборезных фрез | 1921 |
|
SU318A1 |
| MAZOR Y | |||
| et al., Isolation of engineered, full-length antibodies from libraries expressed in Escherichia coli, Nature biotechnology, 2007, Т | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| WO 2004063343 A2, 29.07.2004 | |||
| РЕКОМБИНАНТНЫЕ АНТИТЕЛА ПРОТИВ CD4 ДЛЯ ТЕРАПИИ ЧЕЛОВЕКА | 1996 |
|
RU2232773C2 |
Авторы
Даты
2018-10-23—Публикация
2013-07-03—Подача