Настоящая заявка испрашивает приоритет на основании заявки на патент Китая №201210258175,3, поданной 24 июля 2012 г., под названием «Комбинированный препарат лерканидипина и аторвастатина» («Compound Preparation of Lercanidipine and Atorvastatin»), содержание которой полностью включено в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области медицины, в частности, относится к комбинированному препарату лерканидипина и аторвастатина.
УРОВЕНЬ ТЕХНИКИ
Гипертензия являлась наиболее распространенным сердечно-сосудистым заболеванием среди населения Китая и была основной причиной инсульта и серьезным фактором риска развития ишемической болезни сердца. В ноябре 2009 года Американское общество гипертензии (ASH) обновило определение гипертензии как "сложного и прогрессирующего сердечно-сосудистого (СС) синдрома, вызванного различными причинами заболевания, включая взаимодействия между ними». В результате исследований было обнаружено, что гипертензия является видом синдрома нарушения метаболизма, при этом наиболее часто встречаются сопровождающиеся артериальной гипертензией нарушения метаболизма глюкозы и липидов. Гиперлипидемия тесно коррелирует с заболеваемостью и смертностью от ишемической болезни сердца и других атеросклеротических заболеваний, а также является фактором риска развития инсульта, ишемической болезни сердца, инфаркта миокарда и внезапной смерти, а также является серьезным фактором риска развития гипертензии, нарушенной толерантности к глюкозе и диабета. Согласно данным эпидемиологической статистики, заболеваемость гиперлипидемией в Китае в настоящее время составляет более 10%, при этом более 100 миллионов людей по всей стране нуждаются в терапии, регулирующей количество липидов, а в Европе и Соединенных Штатах уровни дислипидемии и уровни холестерина у людей выше, чем среди населения Китая. Многочисленные исследования подтвердили, что существует положительная корреляция между уровнем холестерина в крови и артериальным давлением. В исследовании с участием 1032 пациентов с гипертензией, 147 пациентов страдали только гипертензией, что составляло лишь 14,3%, а 885 пациентов страдали гипертензией, сопровождающейся различными нарушениями, что составляло 85,7%, из которых 15,0% приходились на пациентов с гипертензией, сопровождающейся дислипидемией. В популяциях старше 35 лет число пациентов, страдающих гипертензией, сопровождающейся дислипидемией, составляло до 37 миллионов человек (у 30%~50% из них гипертензия сопровождалась гиперлипидемией). При одном и том же уровне артериального давления существовала положительная корреляция между, уровнем холестерина в крови и кровяным давлением.
В исследовании, проведенном в Тромсе (Tromso), исследовалось состояние 8081 мужчин в возрасте 20-54 лет и 7663 женщин в возрасте 20-49 лет, и было обнаружено, что и у мужчин, и у женщин уровни как общего холестерина, так и не относящегося к липопротеинам высокой плотности холестерина были значительно увеличены при увеличении систолического и диастолического кровяного давления. Риск сердечно-сосудистых заболеваний у пациентов с гипертензией, сопровождающихся дислипидемией, был не просто суммой рисков данных явлений, а иллюстрировал ситуацию «1+1>2». В настоящее время опасность гиперлипидемии, сопровождающейся гипертензией, полностью осознана, и, таким образом, лечение, обеспечивающее положительные результаты в отношении антигипертензивного действия, должно быть объединено с гиполипидемическим лечением.
Лерканидипин, разработанный итальянской компанией Recordati, является дигидропиридиновым антагонистом кальциевых каналов третьего поколения. Механизм действия лерканидипина гидрохлорида аналогичен механизму действия лерканидипина, то есть представляет собой обратимую блокировку поступления Ca2+ в кальциевые каналы L-типа, находящиеся в мембранах клеток гладкой мускулатуры сосудов, и расширение периферических сосудов с обеспечением таким образом снижения кровяного давления. Лерканидипина гидрохлорид имеет высокую липофильность и, соответственно, более замедленное начало действия при большей продолжительности действия. Испытания, проведенные in vivo и in vitro, показывают, что отрицательное инотропное действие, вызываемое селективным расширением кровеносных сосудов, у лерканидипина гидрохлорида слабее, чем у нифедипина, нитрендипина и фелодипина, в то время как его селективность в отношении сосудов выше, чем у амлодипина, фелодипина, нитрендипина и лацидипина. Кроме того, лерканидипина гидрохлорид также обладает антиатеросклеротическим и защитным действием по отношению к органам-мишеням. Лерканидипина гидрохлорид в терапевтической дозе не препятствовал бы нормальной возбудимости и проводимости сердечной мышцы у пациентов, страдающих гипертензией. Эксперименты на животных показали, что данный продукт обладал защитным действием в отношении почек, и его механизм действия может быть не связан с гемодинамикой. По сравнению с лекарственными средствами того же вида лерканидипина гидрохлорид имеет более высокую селективность в отношении сосудов, а его особая липoфильнoсть обеспечивает более медленное и длительное антигипертензивное действие, которое хорошо переносится пациентами. Данный продукт имеет высокий уровень безопасности и не оказывает кардиотонического действия, не влияет на частоту сердечных сокращений и в то же время обладает хорошим антиатеросклеротическим действием, что является особенно подходящим для пациентов с атеросклерозом, сопровождающимся гипертензией.
Аторвастатин представляет собой ингибитор 3-гидрокси-3-метилглутарил-кофермент А-редуктазы (ГМГ-коА-редуктазы), основная функция которого заключается в уменьшении уровня холестерина липопротеинов низкой плотности (Х-ЛПНП) в плазме, и является основным современным лекарственным средством для снижения уровня липидов в крови, которое в настоящее время используется в клиническом лечении гиперхолестеринемии (ГХ) и смешанной гиперлипидемии, характеризующейся повышенными уровнями общего холестерина (ОХ) и Х-ЛПНП. Данное вещество само по себе не обладает активностью, но после перорального приема и всасывания его гидролизаты обеспечивают конкурентное ингибирование in vivo гидроксиметилглутарилкофермент А-редуктазы, которая является ферментом, лимитирующим скорость процесса синтеза холестерина, и сокращают синтез холестерина, а также увеличивают синтез рецептора липопротеинов низкой плотности. Главным местом действия аторвастатина является печень, и в результате его действия снижаются уровни холестерина и холестерина ЛПНП в крови, умеренно снижается уровень триглицеридов в сыворотке и повышается уровень липопротеинов высокой плотности в крови, таким образом, аторвастатин служит для предотвращения и лечения атеросклероза и ишемической болезни сердца.
Таблетки аторвастатина кальция во всем мире являются наиболее широко используемым лекарственным средством для снижения уровня холестерина. Аторвастатин может снизить уровень липидов в крови более эффективно, чем другие статиновые лекарственные средства. По сравнению с той же дозой симвастатина, правастатина и ловастатина, гиполипидемическое действие аторвастатина кальция эффективнее на 38%, 46% и 51%, соответственно. Аторвастатин кальция представляет собой новое синтетическое статиновое лекарственное средство, которое в настоящее время является наиболее эффективным в отношении снижения уровня общего холестерина. Для пациентов с ишемической болезнью сердца таблетки аторвастатина кальция снижают уровень холестерина жировых отложений, повышают уровень кристаллизованного холестерина и увеличивают механическую прочность бляшки и делает его устойчивой, чтобы ее было нелегко сломать. В то же время аторвастатин кальция также может, ингибировать пролиферацию клеток гладкой мускулатуры и их миграцию к внутренней оболочке сосуда, что снижает риск разрыва бляшки и, следовательно, уменьшает число острых коронарных явлений и обеспечивает высокие темпы снижения уровня липидов.
Комбинированное введение лерканидипина и аторвастатина для лечения гипертензии не описано.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Технической задачей, решаемой посредством настоящего изобретения, является создание комбинированного препарата лерканидипина и аторвастатина кальция, содержащего в одной единице дозы 5-20 мг лерканидипина гидрохлорида и 10-80 мг аторвастатина кальция. Комбинированный препарат согласно настоящему изобретению может обеспечивать эффективное регулирование кровяного давления и уровня липидов у пациентов с гипертензией, сопровождающейся гиперлипидемией, удобен в применении и характеризуется хорошей соблюдаемостью режима введения для животных.
Клинические исследования и эксперименты на животных показали, что аторвастатин оказывает действие по регулированию кровяного давления и защите сердца. Чем выше кровяное давление, тем более заметно антигипертензивное действие, и при этом, антигипертензивное действие аторвастатина не зависит от гиполипидемического действия. Статиновые лекарственные средства не являются антигипертензивными лекарственными средствами, и их действие в основном направлено на снижение риска сердечно-сосудистого заболевания и повышение антигипертензивного действия антигипертензивных лекарственных средств. Для пациентов с гипертензией лечение статиновыми лекарственными средствами совместно с лечением, обеспечивающим положительные результаты в отношении антигипертензивного действия, позволяет предотвратить возникновение патологических состояний, связанных с сердечно-сосудистой системой.
Предпочтительно массовое отношение лерканидипина гидрохлорида к аторвастатину кальция составляет 1:1-8.
Более предпочтительно массовое отношение лерканидипина гидрохлорида к аторвастатину кальция составляет 1:2-4.
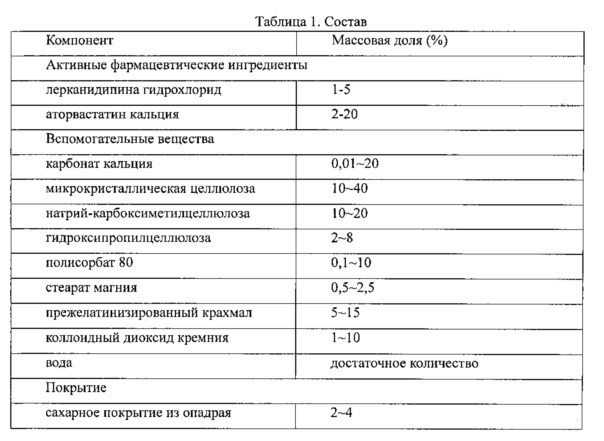
Предпочтительно комбинированный препарат содержит 1-5% лерканидипина гидрохлорида, 2-20% аторвастатина кальция и 0,01-20% карбоната кальция, 10-40% микрокристаллической целлюлозы, 10-20% натрий-карбоксиметилцеллюлозы, 2-8% гидроксипропилцеллюлозы, 0,1-10% полисорбата 80, 0,5-2,5% стеарата магния, 5-15% прежелатинизированного крахмала и 1-10% коллоидного диоксида кремния в качестве вспомогательных веществ.
Предпочтительно сахарное покрытие из опадрая применяют в количестве, составляющем 2-4% от комбинированного препарата.
В настоящем изобретении также предложен способ получения указанного комбинированного препарата, включающий следующие этапы:
этап 1: активный фармацевтический ингредиент лерканидипина гидрохлорид и активный фармацевтический ингредиент аторвастатин кальция взвешивают и просеивают, перемешивают до гомогенного состояния с карбонатом кальция, микрокристаллической целлюлозой, натрий-карбоксиметилцеллюлозой, гидроксипропилцеллюлозой, полисорбатом 80, стеаратом магния, прежелатинизированным крахмалом и коллоидным диоксидом кремния, подвергают вакуумному прессованию, измельчают и просеивают с получением гранул и прессуют с получением таблеток при регулировании твердости ядра таблетки;
этап 2: опадрай добавляют к этанолу при перемешивании и проводят перемешивание до получения дисперсии, затем добавляют очищенную воду и перемешивают с получением раствора изолирующего покрытия, который далее применяют для нанесения пленочного покрытия на ядро таблетки, полученное на этапе 1, с получением тонкого пленочного покрытия;
этап 3: опадрай добавляют к этанолу при перемешивании, добавляют очищенную воду и перемешивают с получением раствора изолирующего покрытия, который далее применяют для нанесения покрытия на ядра полученных таблеток с получением таблетки с тонким пленочным покрытием;
этап 4: опадрай добавляют к этанолу и перемешивают до гомогенного состояния с получением раствора кишечнорастворимого покрытия, который далее применяют для нанесения покрытия на таблетки с тонким пленочным покрытием с получением кишечнорастворимого покрытия.
Предпочтительно регулируемая на этапе 1 твердость ядра составляет 2-10 кг.
Предпочтительно концентрация этанола на этапах 2 и 3 составляет 75-100%.
Предпочтительно продолжительность добавления и перемешивания очищенной воды на этапе 2 и продолжительность перемешивания на этапе 3 составляют 20-100 мин.
Предпочтительно опадрай на этапе 2 представляет собой Y-1-7000, а опадрай на этапе 3 представляет собой OY-P типа 91S.
Эксперименты на животных, проведенные в отношении настоящего изобретения, показали, что комбинированное введение лерканидипина с аторвастатином позволяет; одновременно значительно снизить кровяное давление и уровни липидов у крыс с гипертензией, сопровождающейся дислипидемией, и каждый из эффектов был несколько больше, чем эффект соответствующего отдельного компонента, что демонстрирует синергическое действие данных двух компонентов.
Результаты клинических испытаний показали, что комбинированное введение лерканидипина и аторвастатина обеспечивает активность, заключающуюся как в антигипертензивном, так и в гиполипидемическом действии. По сравнению со значениями до введения, различие является статистически значимым (p<0,05), а указанная активность немного превышает соответствующую активность отдельного лекарственного средства. Группа, получавшая однокомпонентный препарат, характеризовалась наличием симптомов со стороны желудочно-кишечного тракта, головокружения и других нежелательных реакций; в то время как в группе, которой производили комбинированное введение, значительных побочных реакций не появлялось.
Вышеуказанные результаты показывают, что, комбинированный препарат лерканидипина и аторвастатина оказывает значительное антигипертензивное и гиполипидемическое действие одновременно, обладая более высокой эффективностью при уменьшенной фармацевтической дозировке по сравнению с комбинированным введением таблетки амлодипина безилата и таблетки симвастатина, при этом у пациентов снижена частота нежелательных реакций, а также достигается хорошая переносимость и соблюдаемость режима лечения пациентами.
Приготовление лерканидипина и аторвастатина в виде комбинированного препарата может обеспечивать синергический эффект, заключающийся в увеличении антигипертензивной и гиполипидемической эффективности при одновременном снижении нежелательных реакций, вызванных указанными лекарственными средствами, а также увеличении переносимости и улучшении соблюдаемости режима лечения пациентами. Комбинированный препарат удобен для введения пациенту и имеет хорошие перспективы клинического применения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении предложен комбинированный препарат лерканидипина и аторвастатина, который может быть получен специалистом в данной области техники на основании настоящего описания посредством соответствующего улучшения технологических параметров. Следует особо отметить, что все подобные замены и модификации очевидны для специалиста в данной области техники и считаются входящими в объем настоящего изобретения. Продукты и применения согласно настоящему изобретению описаны посредством предпочтительных примеров. Для реализации и применения методик согласно настоящему изобретению специалистом в данной области техники без отхода от содержания, сущности и объема настоящего изобретения могут быть очевидным образом сделаны, изменения, соответствующие модификации и комбинации приведенных в настоящем описании способов и применений.
Настоящее изобретение далее описано более подробно путем объединения следующих конкретных вариантов реализации настоящего изобретения, чтобы техническое решение согласно настоящему изобретению могло быть лучше понято специалистами в данной области техники.
Пример 1: Состав комбинированного препарата согласно настоящему изобретению
Комбинированный препарат содержит лерканидипина гидрохлорид и аторвастатин кальция в качестве активных фармацевтических ингредиентов, а вспомогательные вещества включают карбонат кальция, натрий-карбоксиметилцеллюлозу, микрокристаллическую целлюлозу, прежелатинизированный крахмал, полисорбат 80, гидроксипропилцеллюлозу, очищенную воду, коллоидный диоксид кремния, стеарат магния и сахарное покрытие из опадрая.
Пример 2: Получение комбинированного препарата согласно настоящему изобретению
(1) Активный фармацевтический ингредиент: лерканидипина гидрохлорид - и активный фармацевтический ингредиент: аторвастатин кальция - взвешивали и просеивали для применения.
(2) Карбонат кальция, микрокристаллическую целлюлозу, натрий-карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, полисорбат 80, стеарат магния, прежелатинизированный крахмал и коллоидный диоксид кремния взвешивали и гомогенизировали с указанными активными фармацевтическими ингредиентами; при этом вспомогательные вещества содержали 0,01-20% карбоната кальция, 10-40% микрокристаллической целлюлозы, 10-20% натрий-карбоксиметилцеллюлозы, 2-8% гидроксипропилцеллюлозы, 0,1-10% полисорбата 80, 0,5-2,5% стеарата магния, 5-15% прежелатинизированного крахмала и 1-10% коллоидного диоксида кремния.
(3) Указанную смесь подвергали вакуумному прессованию, измельчали и просеивали с получением гранул и прессовали с получением таблеток при регулировании твердости ядра таблетки 2-10 кг.
(4) Нанесение тонкого пленочного покрытия: опадрай (Y-1-7000) добавляли к этанолу при перемешивании до получения дисперсии, после чего добавляли очищенную воду и проводили перемешивание в течение 20-100 мин с получением раствора изолирующего покрытия (концентрация этанола составляла 75-100%), который применяли для нанесения покрытия на ядра таблеток с получением таблетки с тонким пленочным покрытием.
(5) Нанесение кишечнорастворимого покрытия: опадрай (OY-P типа 91S) в заданном количестве добавляли к этанолу при перемешивании, далее проводили перемешивание в течение 20-100 мин и получали раствор кишечнорастворимого покрытия (концентрация этанола составляла 75-100%), который применяли для нанесения покрытия на таблетки с тонким пленочным покрытием с получением кишечнорастворимого покрытия. Каждая полученная таблетка комбинированного препарата содержала 5-10 мг лерканидипина гидрохлорида и 10-80 мг аторвастатина кальция.
Пример 3: Методика исследования качества
Исследование качества включало описание, идентификацию, обнаружение (связанных веществ, потери при сушке, хлорида, тяжелых металлов, определение скорости растворения и однородности содержимого) и определения содержания и т.п. Определение содержания лерканидипина гидрохлорида проводили следующим образом:
Определение содержания: метод ВЭЖХ, использованные стационарная фаза и подвижная фаза приведены в следующей таблице.
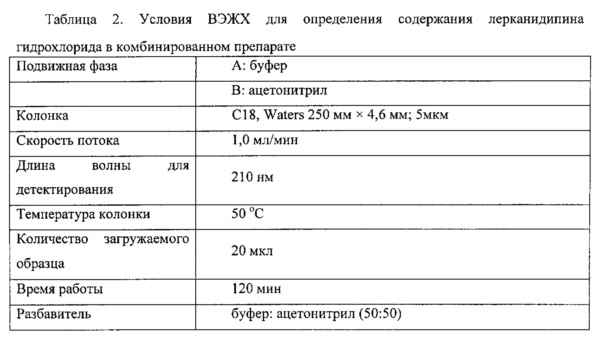
Приготовление буфера А: 1,36 г дигидрофосфата калия растворяли в 1 л воды и после его растворения добавляли 1 г натриевой соли октансульфоновой кислоты. Смесь подвергали ультразвуковой обработке и доводили pH до 2,5±0,05 с применением 10%-й фосфорной кислоты (об./об.).
Пример 4: Эксперименты по определению антигипертензивного и гиполипидемического действия на крысах со спонтанной гипертензией, сопровождающейся дислипидимией
5-месячным крысам со спонтанной гипертензией (взрослые крысы линии MHS), половина из которых были самцами, а половина самками, давали каждый день корм с высоким содержанием жиров (1,0% холестерина, 0,2% пропилтиоурацила, 0,5% холата натрия, 5,0% свиного жира, 1,0% метионина и 92,3% основного рациона) в течение четырех недель; через четыре недели у крыс весом 200-240 г измеряли базальное систолическое давление и уровень липидов. Крыс с артериальной гипертензией, сопровождающиеся дислипидемией, равномерно разделяли на 4 группы по 12 крыс в каждой группе. Данные четыре группы были, соответственно, следующими: (А) контрольная группа, получавшая растворитель, (В) группа лерканидипина (лерканидипина гидрохлорид, 0,4 мг/кг), (С) группа аторвастатина (аторвастатин кальция, 0,8 мг/кг) и (D) группа комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,4 мг/кг + 0,8 мг/кг). Лекарственные средства каждой группы готовили в составах с физиологическим раствором и вводили крысам через желудочный зонд один раз в день в течение 4 недель подряд. Измерения систолического давления, уровней общего холестерина в сыворотке и т.п. у крыс проводили через 2 часа после введения в конце каждой недели.
Изменения систолического давления в каждой группе приведены в таблице 3, при этом показано, что систолическое давление в группах B и D значительно изменилось (p<0,01), и было снижено до нормальных уровней кровяного давления, и степень указанного снижения в группе D была больше, чем в группе В. В группе А существенных изменений систолического давления не было. Изменения общего холестерина в каждой группе приведены в таблице 4. Снижение наблюдалось в группах B, C и D, при этом снижение в группах C и D было значимым (p<0,05). В группе В уровень общего холестерина был снижен (p>0,05), в то время как в группе А никаких существенных изменений не произошло.
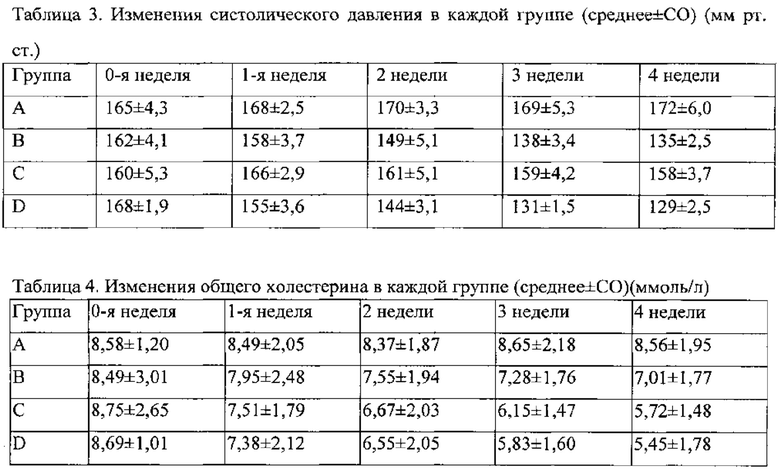
Как можно видеть, комбинированное введение лерканидипина и аторвастатина в нормальной дозировке может одновременно и эффективно регулировать кровяное давление и уровень липидов в крови у крыс с гипертензией, сопровождающейся гиперлипидемией, и указанная комбинация удобна для введения и характеризуется хорошей соблюдаемостью режима введения для животных.
Пример 5: Эксперименты по определению антигипертензивного и гиполипидемического действия на подопытных крысах с гипертензией, сопровождающейся дислипидемией
Крыс линии Спрег-Доули (SD) весом 150-180 г анестезировали путем внутрибрюшинной инъекции хлоралгидрата (320 мг/кг). Вскрывали брюшную полость, отделяли левую почечную артерию, и ограничивали ее серебряной клипсой размером 0,2 мм. На 8-10-ю неделю после указанной процедуры крыс с систолическим давлением ≥140 мм рт.ст. считали крысами с гипертензией. Крысам с гипертензией вводили витамин D3 через желудочный зонд в общей дозе 600000 Ед/кг в течение трех дней, а затем давали каждый день корм с высоким содержанием жиров (1,0% холестерина, 0,2% пропилтиоурацила, 0,5% холата натрия, 5,0% свиного жира, 1,0% метионина, 92,3% основного рациона). Крысам в нормальной контрольной группе давали корм, соответствующий обычному рациону. Через четыре недели у крыс измеряли систолическое давление, а также измеряли уровни общего холестерина (ОХ) и триглицеридов (ТГ) в сыворотке путем взятия крови из хвостовой вены.
140 крыс с гипертензией, сопровождающейся дислипидемией, равномерно разделяли на 7 групп по 20 крыс в каждой группе согласно кровяному давлению и уровням липидов, и данные группы соответственно представляли собой: контрольную группу, получавшую растворитель, группу лерканидипина (лерканидипина гидрохлорид, 0,5 мг/кг), группу аторвастатина (аторвастатин кальция, 1,0 мг/кг), группу 1 комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 0,5 мг/кг), группу 2 комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 1,0 мг/кг), группу 3 комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 2,0 мг/кг) и группу положительного контроля (амлодипина безилат + аторвастатин кальция, 0,5 мг/кг + 1,0 мг/кг).
Остальные 20 нормальных крыс составляли нормальную контрольную группу. Крысам с гипертензией продолжали давать корм с высоким содержанием жиров, а крысам в нормальной группе давали обычный рацион. Лекарственные средства каждой группы готовили в составах с физиологическим раствором, крысам нормальной контрольной группы и контрольной группы, получавшей растворитель, вводили такой же объем физиологического раствора. Введение осуществляли через желудочный зонд один раз в день в течение 20 недель подряд. Крыс взвешивали раз в неделю и корректировали дозу в зависимости от веса. Кровяное давление измеряли в различные моменты времени до и после введения, соответственно, для вычисления величины снижения артериального давления (систолическое давление до введения - систолическое давление после введения). Через 20 недель отбирали образцы из крыс и определяли уровни общего холестерина (OX) и триглицеридов (ТГ) в сыворотке. Соответствующие параметры для каждой группы были представлены в виде среднего ± стандартное отклонение (среднее ± CO) и для сравнения различных групп использовали t-критерий.
Как показано в таблице 5, в конце недели 20, по сравнению с крысами нормальной группы, у крыс контрольной группы, получавшей растворитель, значительно увеличилось систолическое давление; по сравнению с крысами контрольной группы, получавшей растворитель, систолическое давление в группе аторвастатина (1,0 мг/кг) было улучшено, систолическое давление во всех остальных группах, а именно группе лерканидипина (0,5 мг/кг), группе комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 0,5/1,0/2,0 мг/кг), группе положительного контроля (амлодипина безилат + аторвастатин кальция, 0,5 мг/кг + 1,0 мг/кг), было значительно снижено (p<0,01) до нормального уровня, а по сравнению с группой лерканидипина (0,5 мг/кг), крысы группы комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 0,5/1,0/2,0 мг/кг) имели несколько большую степень снижения систолического давления, что, однако, не было статистически значимым. К концу недели 20, по сравнению с крысами в нормальной группе, уровень ОХ и ТГ у крыс в контрольной группе, получавшей растворитель, значительно увеличился, и по сравнению с контрольной группой растворителей, ОХ и ТГ в группе лерканидипина (0,5 мг/кг) были улучшены, ОХ и ТГ в группе аторвастатина (1,0 мг/кг), группе комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 0,5/1,0/2,0 мг/кг), группе положительного контроля (амлодипина безилат + аторвастатин кальция, 0,5 мг/кг + 1,0 мг/кг) значительно уменьшились (p<0,01), а по сравнению с группой аторвастатина (1,0 мг/кг), крысы в группе 2 комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 1,0 мг/кг) имели большую степень снижения уровней ОХ и ТГ. По сравнению с группой положительного контроля (амлодипина безилат + аторвастатин кальция, 0,5 мг/кг + 1,0 мг/кг), антигипертензивное и гиполипидемическое действия группы 2 комбинаций лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5, мг/кг + 1,0 мг/кг) были несколько выше (что, однако, не имело высокую статистическую значимость) и, скорее всего, связаны с усилением действия лерканидипина по предотвращению накопления излишнего жира в печени.
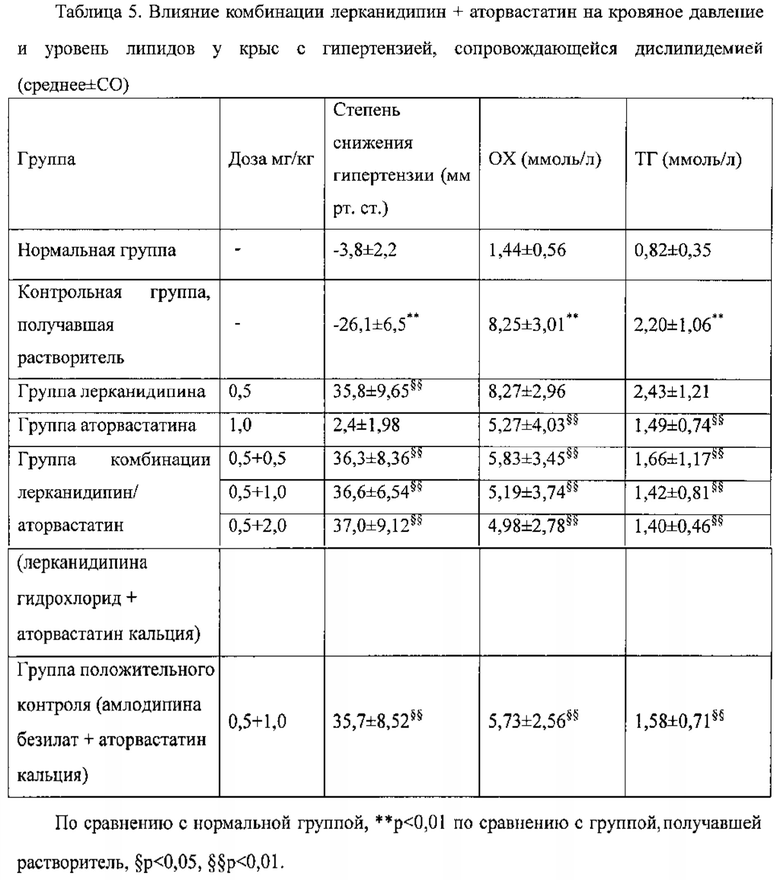
Как можно видеть, введение комбинации лерканидипин/аторвастатин (лерканидипина гидрохлорид + аторвастатин кальция, 0,5 мг/кг + 0,5/1,0/2,0 мг/кг) снизило кровяное давление и уровни липидов у крыс с гипертензией, сопровождающейся дислипидемией, сразу же и значительно, и каждое действие было сильнее, чем соответствующее действие отдельного компонента. Указанные два компонента обладали несомненным синергическим действием.
Пример 6: Терапевтическое действие при введении лерканидипина и аторвастатина по отдельности и при их комбинированном введении, оказываемое на пациентов с артериальной гипертензией, сопровождающейся гиперлипидемией
Проводили двойное слепое параллельное рандомизированное исследование действия комбинированного введения лерканидипина и аторвастатина по одновременному регулированию гипертензии и гиперлипидемии у пациентов с умеренной гипертензией и гиперлипидемией.
Критерий включения субъектов: субъекты представляли собой взрослых мужчин или женщин в возрасте от 18 до 80 лет, страдающих одновременно умеренной гипертензией и гиперлипидемией.
Наличие гиперлипидемии может быть подтверждено путем оценки уровня липопротеинов низкой плотности (ЛПНП) у субъекта, связанного с определенными положительными факторами риска. Если субъект не страдал ишемической болезнью сердца (ИБС) и имел менее двух положительных факторов риска, и если уровень ЛПНП субъекта был больше или равен 190 мг/дл, субъект считался страдающим гиперлипидемией, нуждающейся в лекарственной терапии; если субъект не имел ИБС и имел два или более факторов риска, и если уровень ЛПНП субъекта был больше или равен 160 мг/дл, субъект считался страдающим гиперлипидемией, нуждающейся в лекарственной терапии; и если субъект страдал ИБС, и если уровень ЛПНП субъекта был больше или равен 130 мг/дл, субъект считался страдающим гиперлипидемией. Положительные факторы риска включают: (1) мужчины старше 45 лет, (2) женщины старше 55 лет, причем данные женщины не подвергались заместительной гормональной терапии (ЗГТ), (3) раннее начало сердечно-сосудистых заболеваний в семейном анамнезе, (4) субъект является регулярным курильщиком, (5) субъект страдает диабетом, (6) ЛПВП менее 45 мг/дл, и (7) субъект страдает гипертензией. Уровень ЛПВП более 60 мг/дл считался отрицательным фактором риска, который могут противостоять одному из представленных выше положительных факторов риска.
Когда кровяное давление в состоянии покоя составляет от 105 до 114 мм рт.ст., считается, что субъект страдает умеренной гипертензией. Все значения кровяного давления представляли собой среднее из трех измерений с 5-минутным интервалом.
Субъекты, которые соответствовали критерию включения, переставали принимать текущие антигипертензивные и гиполипидемические лекарственные средства и позволяли почти всем лекарствам вывестись из организма. Вновь диагностированные субъекты, как правило, не получали лечения до начала испытания. Через 4 недели проводили измерение исходного уровня кровяного давления и уровня липидов натощак у субъектов, при оценке липидов определяли уровень общего холестерина, холестерина ЛПНП, холестерина ЛПВП, триглицеридов, липопротеина очень низкой плотности (ЛОНП) и т.п.
После этого субъектов случайным образом разделяли на следующие три группы:
(1) группа лерканидипина (таблетки лерканидипина гидрохлорида, Recordati S.P.A., 10 мг на таблетку);
(2) группа аторвастатина (таблетки аторвастатина кальция, Pfizer Ireland Pharmaceuticals, 40 мг на таблетку);
(3) группа лерканидипин + аторвастатин (комбинированные таблетки лерканидипина/аторвастатина 10 мг/40 мг, полученные согласно описанному выше способу получения).
В каждой группе, состоящей из 50 субъектов, субъекты принимали по одной таблетке соответствующих препаратов один раз в день за полчаса до обеда в течение 8 недель. Во время исследования субъекты должны были придерживаться нормальной диеты, не принимая никаких других лекарств. Через восемь недель пациенты возвращались в исследовательские центры, и у них снова измеряли кровяное давление и уровень липидов. Записывали нежелательные реакции, которые субъекты испытывали в период приема препаратов, и до и после испытания для пациентов было проведено полное исследование, включая электрокардиограмму, обычные анализы крови и мочи, анализ функции печени и почек, уровня глюкозы в крови и электролитов крови. Рассчитывали среднее значение и стандартное отклонение параметров кровяного давления и липидов для каждой группы (см. таблицу 6) и для определения различия между уровнями до и после введения использовали t-критерий.
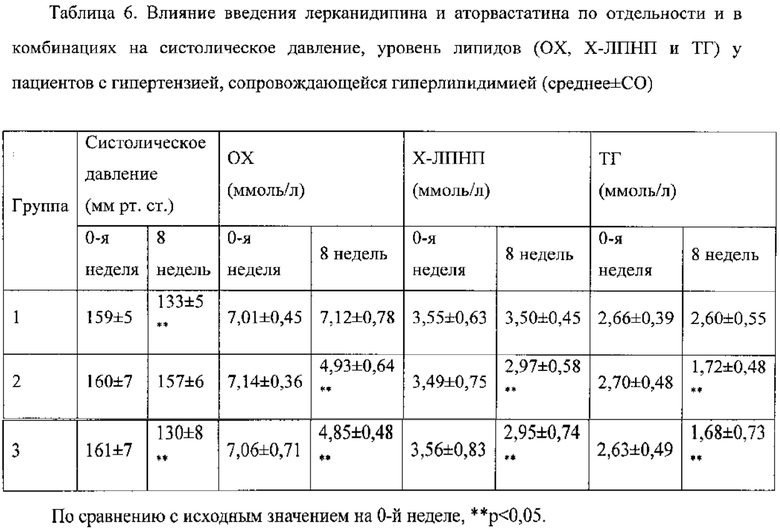
Результаты исследования показали, что комбинированное введение лерканидипина и аторвастатина одновременно проявляло и антигипертензивную, и гиполипидемическую активность, и различие было статистически значимым по сравнению со значениями до введения (P<0,05), и данная активность была немного сильнее, чем соответствующая активность единственного лекарственного средства. В группе, которой вводили только лерканидипин, был 1 случай возникновения симптомов со стороны желудочно-кишечного тракта, 1 случай головокружения; в группе, которой вводили только аторвастатин, был 1 случай сухости во рту и 1 случай боли в животе, обе реакции были незначительными и не повлияли на дальнейшее введение. В группе комбинированного введения существенных нежелательных реакций показано не было. Через восемь недель лечения существенного, различия в отношении изменений результатов лабораторных анализов и электрокардиограммы между тремя группами пациентов показано не было.
Пример 7: Сравнение действия комбинированного препарата лерканидипина и аторвастатина и действия при комбинированном введении
Комбинированное введение: введение двух лекарственных средств, таблетки амлодипина безилата (Zhejiang Weikang Pharmaceutical Co. Ltd., 5 мг на таблетку) и таблетки симвастатина (Merck Sharp & Dohme (Австралия) Pty Ltd., 20 мг на таблетку), в комбинации.
Была проведена оценка действия комбинированного препарата лерканидипина и аторвастатина и указанного выше комбинированного введения на пациентов с умеренной гепертензией, сопровождающейся гиперлипидемией.
Критерий включения субъектов: субъекты представляли собой взрослых мужчин или женщин в возрасте от 18 до 80 лет, страдающих одновременно умеренной гипертензией и гиперлипидемией. Оцениваемые показатели были такими же, как в предыдущем примере.
Субъекты, которые соответствовали критерию включения, переставали принимать текущие антигипертензивные и гиполипидемические лекарственные средства и позволяли почти всем лекарствам вывестись из организма. Вновь диагностированные субъекты, как правило, не получали лечения до начала испытания. Через 4 недели проводили измерение исходного значения кровяного давления и уровня липидов натощак у субъектов, при оценке липидов определяли уровень общего холестерина, холестерина ЛПНП, холестерина ЛПВП, триглицеридов, липопротеина очень низкой плотности (ЛОНП) и т.п. В исследовании принимали участие в общей сложности 98 пациентов. Субъектов случайным образом разделяли на следующие две группы в зависимости от кровяного давления и уровня липидов (по 49 пациентов в каждой группе):
(1) группа комбинированного препарата лерканидипина и аторвастатина (комбинированные таблетки лерканидипина/аторвастатина 10 мг/20 мг, полученные согласно описанному выше способу получения);
(2) группа комбинированного введения таблетки амлодипина безилата и таблетки симвастатина.
Субъекты каждой группы принимали соответствующие препараты один раз в день за полчаса до обеда в течение 8 недель. Группа комбинированного препарата получала каждый раз по одной таблетке, в то время как в группе комбинированного введения субъекты каждый раз принимали по одной таблетке каждого препарата (по 2 таблетки в общей сложности). Во время исследования субъекты должны были придерживаться нормальной диеты, не принимая никаких других лекарств. Через восемь недель пациенты возвращались в исследовательские центры, и у них снова измеряли кровяное давление и уровень липидов. Записывали нежелательные реакции, которые субъекты испытывали в период введения препаратов. Рассчитывали среднее значение и стандартное отклонение параметров кровяного давления и липидов для каждой группы (см. таблицу 7) и для определения различия между уровнями до и после введения, а также различия между двумя указанными группами использовали t-критерий.
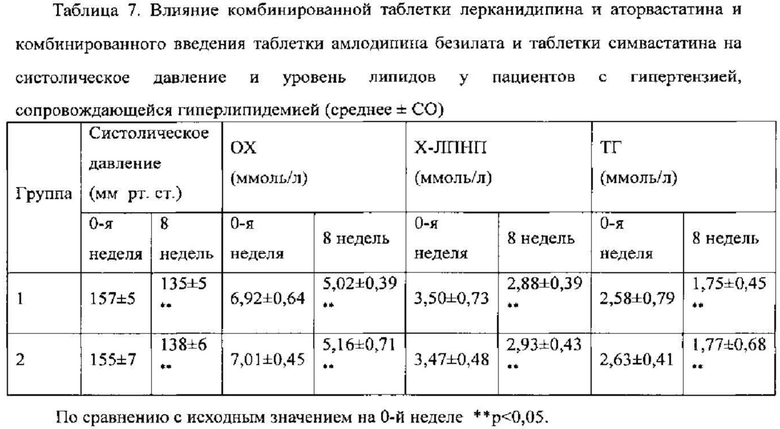
Амлодипин используется в качестве примера блокатора кальциевых каналов, в частности дигидропиридинового блокатора кальциевых каналов. Его сочетание, с симвастатином, гиполипидемическим статиновым лекарственным средством, является наиболее широко назначаемым составом. Результаты испытаний показали, что и комбинированная таблетка лерканидипина и аторвастатина, и комбинированное введение таблетки амлодипина безилата и таблетки симвастатина обеспечивают значительное снижение кровяного давления и уровня липидов у пациентов с умеренной гипертензией, сопровождающейся гиперлипидемией. Для группы комбинированного препарата был зафиксирован только один случай мягкого отека лодыжки, ни один из субъектов не прекратил исследование из-за непереносимости нежелательных реакций; а в случае группы комбинированного введения был зафиксирован один случай умеренного отека, один случай слабой головной боли, и один субъект прекратил исследование из-за нежелательных реакций на лекарственные средства. Несмотря на то, что различие в эффективности между двумя группами не было статистически значимым, лучшее антигипертензивное и гиполипидемическое действие было достигнуто в группе комбинированного препарата лерканидипина и аторвастатина, и в данной группе были достигнуты лучшая переносимость и соблюдаемость режима введения пациентами.
В заключение следует отметить, что комбинированный препарат лерканидипина/аторвастатина одновременно обладает существенным антигипертензивным и гиполипидемическим действием, имея более высокую эффективность при меньшей дозе по сравнению с комбинированным введением таблетки амлодипина безилата и таблетки симвастатина, и характеризуется пониженной частотой нежелательных реакций, а также хорошей переносимостью и соблюдаемостью режима введения пациентами.
Вышеупомянутые сведения являются только описанием предпочтительных вариантов реализации настоящего изобретения. Следует отметить, что средние специалисты в данной области техники также могут без отхода от принципа настоящего изобретения сделать ряд усовершенствований и модификаций, которые следует рассматривать как подпадающие под объем притязаний согласно настоящему изобретению.
Группа изобретений относится к области медицины и фармации. Предложены комбинированный препарат лерканидипина гидрохлорида и аторвастатина кальция для лечения гипертензии, сопровождающейся гиперлипидемией, который содержит на единичную дозу 5-20 мг лерканидипина гидрохлорида и 10-80 мг аторвастатина кальция, при этом массовое соотношение лерканидипина гидрохлорида к аторвастатину кальция составляет 1:2-4, и способ получения содержащей их таблетки с покрытием. Технический результат: комбинированный препарат лерканидипина и аторвастатина кальция согласно настоящему изобретению имеет более высокую эффективность при меньшей дозе по сравнению с комбинированным введением таблеток в отношении существенного уменьшения гипертензии и снижения уровня липидов; характеризуется снижением терапевтической дозы и снижением числа нежелательных эффектов, а также хорошей переносимостью и соблюдаемостью режима лекарственной терапии пациентами. 2 н. и 6 з.п. ф-лы, 7 табл.
1. Комбинированный препарат лерканидипина и аторвастатина кальция для лечения гипертензии, сопровождающейся гиперлипидемией, характеризующийся тем, что указанный препарат содержит 5-20 мг лерканидипина гидрохлорида и 10-80 мг аторвастатина кальция на единичную лекарственную форму, при этом массовое отношение лерканидипина гидрохлорида к аторвастатину кальция составляет 1:2-4.
2. Комбинированный препарат по п. 1, характеризующийся тем, что он содержит 1-5% лерканидипина гидрохлорида, 2-20% аторвастатина кальция и 0,01-20% карбоната кальция, 10-40% микрокристаллической целлюлозы, 10-20% натрий-карбоксиметилцеллюлозы, 2-8% гидроксипропилцеллюлозы, 0,1-10% полисорбата 80, 0,5-2,5% стеарата магния, 5-15% прежелатинизированного крахмала и 1-10% коллоидного диоксида кремния в качестве вспомогательных веществ.
3. Комбинированный препарат по п. 2, характеризующийся тем, что указанный комбинированный препарат представляет собой таблетку с покрытием и в нем используется сахарное покрытие из опадрая в количестве, составляющем 2-4% от комбинированного препарата.
4. Способ получения таблетки с покрытием по п. 3, характеризующийся тем, что он включает следующие этапы:
этап 1: активный фармацевтический ингредиент лерканидипина гидрохлорид и активный фармацевтический ингредиент аторвастатин кальция взвешивают и просеивают, перемешивают до гомогенного состояния с карбонатом кальция, микрокристаллической целлюлозой, натрий-карбоксиметилцеллюлозой, гидроксипропилцеллюлозой, полисорбатом 80, стеаратом магния, прежелатинизированным крахмалом и коллоидным диоксидом кремния, подвергают вакуумному прессованию, измельчают, просеивают с получением гранул и прессуют с получением таблеток при регулировании твердости ядра таблетки;
этап 2: опадрай добавляют к этанолу при перемешивании, добавляют очищенную воду и перемешивают с получением отдельного раствора покрытия, который далее применяют для нанесения покрытия на ядра полученных таблеток с получением таблетки с тонким пленочным покрытием;
этап 3: опадрай добавляют к этанолу и перемешивают до гомогенного состояния с получением раствора кишечнорастворимого покрытия, который далее применяют для нанесения покрытия на таблетки с тонким пленочным покрытием с получением кишечнорастворимого покрытия.
5. Способ получения по п. 4, характеризующийся тем, что регулируемая на этапе 1 твердость ядра составляет 2-10 кг.
6. Способ получения по п. 4, характеризующийся тем, что концентрация этанола на этапе 2 составляет 75-100%.
7. Способ получения по п. 4, характеризующийся тем, что продолжительность добавления и перемешивания очищенной воды на этапе 2 составляет 20-100 мин.
8. Способ получения по п. 4, характеризующийся тем, что опадрай на этапе 2 представляет собой Y-1-7000, а опадрай на этапе 3 представляет собой OY-P типа 91S.
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Прибор с двумя призмами | 1917 |
|
SU27A1 |
| ПОДЪЯЗЫЧНАЯ ТАБЛЕТКА, ПОКРЫТАЯ ОБОЛОЧКОЙ | 2006 |
|
RU2403043C2 |
| CN 102579453 A, 18.07.2012 | |||
| CN 101690816 A, 07.04.2010 | |||
| CN 101716159 B, 04.01.2012 | |||
| CN 102294032 A, 28.12.2011 | |||
| ТЕХНОЛОГИЯ ЛЕКАРСТВЕННЫХ ФОРМ | |||
| Под ред | |||
| Л.А.Ивановой | |||
| М.: Медицина, 1991, т.2, с.142, глава 9.4, с.145, 2-й абзац, с.183, глава 9.6, с.187 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2017-04-19—Публикация
2013-02-25—Подача