Предпосылки создания изобретения
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым соединениям, обладающим неприлизин-ингибирующей активностью. Настоящее изобретение относится также к фармацевтическим композициям, содержащим такие соединения, способам и промежуточным продуктам для получения таких соединений и способам применения таких соединений при лечении заболеваний, таких как гипертензия, сердечная недостаточность, легочная гипертензия и болезнь почек.
Уровень техники
Неприлизин (нейтральная эндопептидаза, EC 3.4.24.11) (NEP), является эндотелиальной мембраной Zn2+ металлопептидазы, обнаруженной во многих органах и тканях, включая мозг, почки, легкие, желудочно-кишечный тракт, сердце и периферийные сосуды. NEP разлагает и инактивирует ряд эндогенных пептидов, таких как энкефалины, циркулирующий брадикинин, пептиды группы ангиотензина и натрийуретические пептиды, причем последние обладают некоторыми эффектами, включая, например, вазодилатацию и натриурез/диурез, а также ингибируют гипертрофию сердца и вентрикулярный фиброз. Таким образом, NEP играет важную роль в гомеостазе артериального давления и сердечно-сосудистых заболеваний.
В качестве возможных лекарственных средств были исследованы ингибиторы NEP, такие как тиорфан, кандоксатрил и кандоксатрилат. Также известны соединения, которые ингибируют как NEP, так и ангиотензин-I преобразующий фермент (ACE), и они включают омапатрилат, гемпатрилат и сампатрилат. Что касается ингибиторов вазопептидазы, то последний указанный класс соединений описан в работе Robl et al. (1999) Exp. Opin. Ther. Patents 9(12): 1665-1677.
Сущность изобретения
Настоящее изобретение относится к новым соединениям, которые, как было обнаружено, обладают ингибирующей фермент неприлизин (NEP) активностью. В соответствии с этим, было предположено, что соединения по изобретению могут быть использованы и являться полезными в качестве лекарственных средств при лечении состояний, таких как гипертензия и сердечная недостаточность.
Один аспект изобретения относится к соединению формулы I:

где:
R1 выбран из -OR7 и -NR8R9;
R2 представляет собой H или -P(O)(OH)2, или R2, взятый вместе с R7, образует -CR18R19-, или, взятый вместе с R8, образует -C(O)-;
X представляет собой -C1-9гетероарил;
R3 отсутствует или выбран из H; галогена; -C0-5алкилен-OH; -NH2; -C1-6алкила; -CF3; -C3-7циклоалкила; -C0-2алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -C(O)NR22R23; -NHC(O)R24; =O; -NO2; -C(CH3)=N(OH); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -OH, -CF3, -OCH3, -NHC(O)CH3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, необязательно замещенного метилом; тиофенила, необязательно замещенного метилом или галогеном; фуранила и -CH2-морфолинила; и R3, когда присутствует, присоединен к атому углерода;
R4 отсутствует или выбран из H; -OH; -C1-6алкила; -C1-2алкилен-COOR35; -CH2OC(O)CH(R36)NH2; -OCH2OC(O)CH(R36)NH2; -OCH2OC(O)CH3; -CH2OP(O)(OH)2; -CH2CH(OH)CH2OH; -CH[CH(CH3)2]-NHC(O)O-C1-6алкила; пиридинила; и фенила или бензила, необязательно замещенных одной или более группами, выбранными из галогена, -COOR35, -OCH3, -OCF3 и -SCF3; и R4, когда присутствует, присоединен к атому углерода или азота;
или R3 и R4 взяты вместе с образованием -фенилен-O-(CH2)1-3- или -фенилен-O-CH2-CHOH-CH2-;
a равно 0 или 1; R5 выбран из галогена, -CH3, -CF3 и -CN;
b равно 0 или целому числу от 1 до 3; каждый R6 независимо выбран из галогена, -OH, -CH3, -OCH3 и -CF3;
R7 выбран из H, -C1-8алкила, -C1-3алкилен-C6-10арила, -C1-3алкилен-C1-9гетероарила, -C3-7циклоалкила, -[(CH2)2O]1-3CH3, -C1-6алкилен-OC(O)R10, -C1-6алкилен-NR12R13, -C1-6алкилен-C(O)R31, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила,
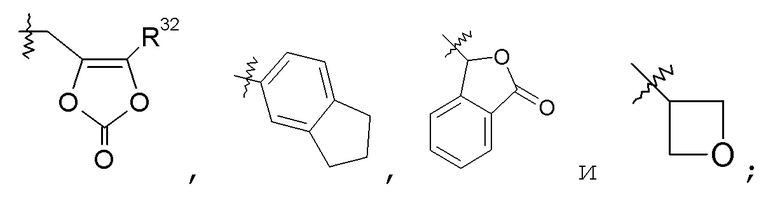
R10 выбран из -C1-6алкила, -O-C1-6алкила, -C3-7циклоалкила, -O-C3-7циклоалкила, фенила, -O-фенила, -NR12R13, -CH[CH(CH3)2]-NH2, -CH[CH(CH3)2]-NHC(O)O-C1-6алкила и -CH(NH2)CH2COOCH3; и R12 и R13 независимо выбраны из H, -C1-6алкила и бензила; или R12 и R13 взяты вместе как -(CH2)3-6-, -C(O)-(CH2)3- или -(CH2)2O(CH2)2-; R31 выбран из -O-C1-6алкила, -O-бензила и -NR12R13; и R32 представляет собой -C1-6алкил или -C0-6алкилен-C6-10арил;
R8 выбран из H, -OH, -OC(O)R14, -CH2COOH, -O-бензила, -пиридила и -OC(S)NR15R16; R14 выбран из H, -C1-6алкила, -C6-10арила, -OCH2-C6-10арила, -CH2O-C6-10арила и -NR15R16; и R15 и R16 независимо выбраны из H и -C1-4алкила;
R9 выбран из H, -C1-6алкила и -C(O)-R17; и R17 выбран из H, -C1-6алкила, -C3-7циклоалкила, -C6-10арила и -C1-9гетероарила;
R18 и R19 независимо выбраны из H, -C1-6алкила и -O-C3-7циклоалкила, или R18 и R19 взяты вместе с образованием =O;
R20 выбран из H и -C1-6алкила;
R21 и R35 независимо выбраны из H, -C1-6алкила, -C1-3алкилен-C6-10арила, -C1-3алкилен-C1-9гетероарила, -C3-7циклоалкила, -[(CH2)2O]1-3CH3, -C1-6алкилен-OC(O)R25; -C1-6алкилен-NR27R28, -C1-6алкилен-C(O)R33, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила,
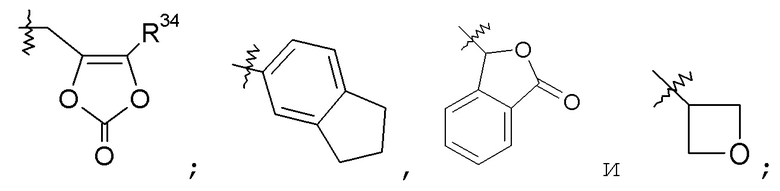
R25 выбран из -C1-6алкила, -O-C1-6алкила, -C3-7циклоалкила, -O-C3-7циклоалкила, фенила, -O-фенила, -NR27R28, -CH[CH(CH3)2]-NH2, -CH[CH(CH3)2]-NHC(O)O-C1-6алкила и -CH(NH2)CH2COOCH3; R27 и R28 независимо выбраны из H, -C1-6алкила и бензила; или R27 и R28 взяты вместе как -(CH2)3-6-, -C(O)-(CH2)3- или -(CH2)2O(CH2)2-; R33 выбран из -O-C1-6алкила, -O-бензила и -NR27R28; и R34 представляет собой -C1-6алкил или -C0-6алкилен-C6-10арил;
R22 и R23 независимо выбраны из H, -C1-6алкила, -CH2COOH, -(CH2)2OH, -(CH2)2OCH3, -(CH2)2SO2NH2, -(CH2)2N(CH3)2, -C0-1алкилен-C3-7циклоалкила и -(CH2)2-имидазолила; или R22 и R23 взяты вместе с образованием насыщенного или частично ненасыщенного -C3-5гетероцикла, необязательно замещенного галогеном, -OH, -COOH или -CONH2; и необязательно содержащего в кольце атом кислорода;
R24 выбран из -C1-6алкила; -C0-1алкилен-O-C1-6алкила; фенила, необязательно замещенного галогеном или -OCH3; и -C1-9гетероарила; и
R36 выбран из H, -CH(CH3)2, фенила и бензила;
где каждая алкильная группа в R1, R3 и R4 необязательно замещена 1-8 атомами фтора; и
где метиленовый линкер на бифениле необязательно замещен одной или двумя -C1-6алкильными группами или циклопропилом;
или его фармацевтически приемлемая соль.
Другой аспект изобретения относится к фармацевтическим композициям, содержащим фармацевтически приемлемый носитель и соединение по изобретению. Такие композиции необязательно могут содержать другие терапевтические агенты. В соответствии с этим, в еще одном аспекте изобретения фармацевтическая композиция содержит соединение по изобретению в качестве первого терапевтического агента, один или более вторых терапевтических агентов и фармацевтически приемлемый носитель. Другой аспект изобретения относится к комбинации активных агентов, содержащих соединение по изобретению и второй терапевтический агент. Соединение по изобретению может быть введено в состав вместе или раздельно с дополнительным(ми) агентом(ами). При введении в состав раздельно, фармацевтически приемлемый носитель может быть включен вместе с дополнительным(ми) агентом(ами). Таким образом, еще один аспект изобретения относится к комбинации фармацевтических композиций, где указанная комбинация включает: первую фармацевтическую композицию, содержащую соединение по изобретению и первый фармацевтически приемлемый носитель; и вторую фармацевтическую композицию, содержащую второй терапевтический агент и второй фармацевтически приемлемый носитель. В другом аспекте настоящее изобретение относится к набору, содержащему такие фармацевтические композиции, например, где первая и вторая фармацевтические композиции являются отдельными фармацевтическими композициями.
Соединения по изобретению обладают ингибирующей фермент неприлизин (NEP) активностью и, следовательно, как ожидается, могут быть использованы в качестве лекарственных средств при лечении пациентов, страдающих заболеванием или нарушением, которые могут быть подвергнуты лечению путем ингибирования фермента NEP или путем повышения уровней его пептидных субстратов. Таким образом, один аспект изобретения относится к способу лечения пациентов, страдающих заболеванием или нарушением, которые могут быть подвергнуты лечению путем ингибирования фермента NEP, включающему введение пациенту терапевтически эффективного количества соединения по изобретению. Другой аспект изобретения относится к способу лечения гипертензии, сердечной недостаточности или болезни почек, включающему введение пациенту терапевтически эффективного количества соединения по изобретению. Также еще один аспект изобретения относится к способу ингибирования фермента NEP у млекопитающего, включающему введение млекопитающему ингибирующего фермент NEP количества соединения по изобретению.
Поскольку соединения по изобретению обладают ингибирующей NEP активностью, они также могут быть использованы в качестве исследовательских инструментов. В соответствии с этим, один аспект изобретения относится к способу применения соединения по изобретению в качестве исследовательского инструмента, включающему проведение биологического анализа с использованием соединения по изобретению. Соединения по изобретению также могут быть использованы для оценки новых химических соединений. Таким образом, другой аспект изобретения относится к способу оценки исследуемых соединений в биологическом анализе, включающему: (a) проведение биологического анализа с исследуемым соединением для осуществления первой аналитической оценки; (b) проведение биологического анализа с соединением по изобретению для осуществления второй аналитической оценки; где стадию (a) проводят либо до, после, либо одновременно со стадией (b); и (c) сравнение первой аналитической оценки со стадии (a) со второй аналитической оценкой со стадии (b). Примеры биологических анализов включают анализ ингибирования фермента NEP. Также еще один аспект изобретения относится к способу исследования биологической системы или образца, содержащего фермент NEP, включающему: (a) приведение в контакт биологической системы или образца с соединением по изобретению; и (b) определение эффектов, вызванных соединением в биологической системе или образце.
Еще один аспект изобретения относится к способам и промежуточным соединениям, используемым при получении соединения по изобретению. В соответствии с этим, другой аспект изобретения относится к способу получения соединений формулы I, включающему стадию сочетания соединения формулы 1 с соединением формулы 2:
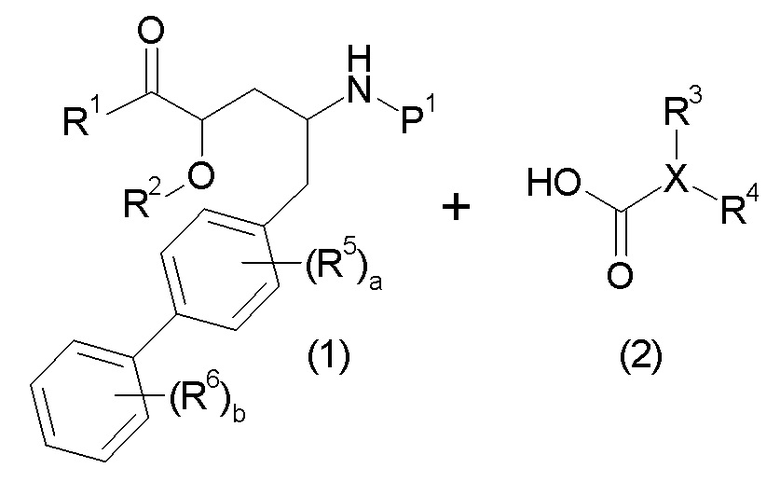
с получением соединения формулы I; где P1 представляет собой H или аминозащитную группу, выбранную из трет-бутоксикарбонила, тритила, бензилоксикарбонила, 9-флуоренилметоксикарбонила, формила, триметилсилила и трет-бутилдиметилсилила; и где способ далее включает удаление защиты у соединения формулы 1, когда P1 представляет собой аминозащитную группу; и где R1-R6, a, b и X имеют значения, указанные для формулы I. Другой аспект изобретения относится к способу получения фармацевтически приемлемой соли соединения формулы I, включающему приведение в контакт соединение формулы I в форме свободной кислоты или основания с фармацевтически приемлемым основанием или кислотой. В других аспектах настоящее изобретение относится к продуктам, полученным любым способом, описанным в данном описании, а также к новым промежуточным соединениям, используемых в таком способе. В одном аспекте изобретения новые промежуточные соединения имеют формулу 1, 6, 7, 8 или 9, или их соли, как определено в данном описании.
Еще один аспект изобретения относится к применению соединения формулы I или его фармацевтически приемлемой соли при получении лекарственного средства, в частности, при получении лекарственного средства, используемого при лечении гипертензии, сердечной недостаточности или болезни почек. Другой аспект изобретения относится к применению соединения по изобретению для ингибирования фермента NEP у млекопитающего. Также еще один аспект изобретения относится к применению соединения по изобретению в качестве исследовательского инструмента. Другие аспекты и варианты осуществления изобретения описаны в данном описании.
Подробное описание изобретения
Определения
При описании соединений, композиций, методов и способов по изобретению следующие термины имеют указанные далее значения, если не указано иное. Кроме того, как используется в данном описании, форма единственного числа включает соответствующие формы множественного числа, если из контекста явно не следует обратное. Термины "содержащий", "включающий" и "имеющий" предназначены для включения и означают, что могут быть дополнительные элементы, отличные от перечисленных элементов. Все числа, выражающие количества ингредиентов, свойства, такие как молекулярная масса, условия реакции и т.д., используемые в данном описании, следует понимать как модифицированные во всех случаях термином "примерно", если не указано иное. В соответствии с этим, значения, приведенные в настоящем описании, являются приблизительными и могут изменяться в зависимости от желаемых свойств, которые должны быть достигнуты согласно настоящему изобретению. По меньшей мере, но не в качестве попытки ограничить применение доктрины эквивалентов к объему формулы изобретения, каждое значение должно восприниматься, по меньшей мере, в свете сообщенных значащих цифр и с применением обычных методов округления.
Термин "алкил" означает моновалентную насыщенную углеводородную группу, которая может быть линейной или разветвленной. Если не указано иное, такие алкильные группы обычно содержат от 1 до 10 атомов углерода и включают, например, -C1-4алкил, -C1-5алкил, -C2-5алкил, -C1-6алкил, -C1-8алкил и -C1-10алкил. Иллюстративные алкильные группы включают, в качестве примера, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил и тому подобное.
Когда определенное количество атомов углерода предназначено для конкретного используемого в данном описании термина, число атомов углерода указано как предшествующий символ в виде индекса. Например, термин "-C1-6алкил" означает алкильную группу, содержащую от 1 до 6 атомов углерода, и термин "-C3-7циклоалкил" означает циклоалкильную группу, содержащую от 3 до 7 атомов углерода, соответственно, где атомы углерода образуют любую приемлемую конфигурацию.
Термин "алкилен" означает двухвалентную насыщенную углеводородную группу, которая может быть линейной или разветвленной. Если не указано иное, такие алкиленовые группы обычно содержат от 0 до 10 атомов углерода и включают, например, -C0-1алкилен-, -C0-6алкилен-, -C1-3алкилен- и -C1-6алкилен-. Иллюстративные алкиленовые группы включают, в качестве примера, метилен, этан-1,2-диил ("этилен"), пропан-1,2-диил, пропан-1,3-диил, бутан-1,4-диил, пентан-1,5-диил и тому подобное. Понятно, что, когда термин алкилен включает ноль атомов углерода, такой как -C0-1алкилен-, то такие термины предназначены для указания на отсутствие атомов углерода, то есть, алкиленовая группа не представлена, присутствует только ковалентная связь, соединяющая группы, разделенные термином алкилен.
Термин "арил" означает моновалентный ароматический углеводород, содержащий единственное кольцо (то есть, фенил) или одно или несколько конденсированных колец. Конденсированные кольцевые системы включают такие, которые являются полностью ненасыщенными (например, нафталин), а также такие, которые являются частично ненасыщенными (например, 1,2,3,4-тетрагидронафталин). Если не указано иное, такие арильные группы обычно содержат от 6 до 10 кольцевых атомов углерода и включают, например, -C6-10арил. Иллюстративные арильные группы включают, в качестве примера, фенил и нафталин-1-ил, нафталин-2-ил и тому подобное.
Термин "циклоалкил" означает моновалентную насыщенную карбоциклическую углеводородную группу. Если не указано иное, такие циклоалкильные группы обычно содержат от 3 до 10 атомов углерода и включают, например, -C3-5циклоалкил, -C3-6циклоалкил и -C3-7циклоалкил. Иллюстративные циклоалкильные группы включают, в качестве примера, циклопропил, циклобутил, циклопентил, циклогексил и тому подобное.
Термин "галоген" означает фтор, хлор, бром и йод.
Термин "гетероцикл" предназначен для включения моновалентных ненасыщенных (ароматических) гетероциклов, содержащих единственное кольцо или два конденсированных кольца, а также моновалентных насыщенных и частично ненасыщенных групп, содержащих единственное кольцо или несколько конденсированных колец. Гетероциклическое кольцо может содержать всего от 3 до 15 кольцевых атомов, из которых 1-14 являются атомами углерода кольца, и 1-4 являются гетероатомами, выбранными из азота, кислорода или серы. Обычно, однако, гетероциклическое кольцо содержит всего от 3 до 10 кольцевых атомов, из которых 1-9 являются атомами углерода кольца, и 1-4 являются гетероатомами. Точка присоединения может быть на любом доступном атоме углерода или азота кольца. Примеры гетероциклов включают, например, -C1-7гетероцикл, -C3-5гетероцикл, -C2-6гетероцикл, -C3-12гетероцикл, -C5-9гетероцикл, -C1-9гетероцикл, -C1-11гетероцикл и -C1-14гетероцикл.
Моновалентные ненасыщенные гетероциклы часто указываются также как "гетероарильные" группы. Если не указано иное, гетероарильные группы обычно содержат в общем от 5 до 10 кольцевых атомов, из которых 1-9 являются атомами углерода кольца, и 1-4 являются гетероатомами, и включают, например, -C1-9гетероарил и -C5-9гетероарил. Иллюстративные гетероарильные группы включают, в качестве примера, пиррол (например, 3-пирролил и 2H-пиррол-3-ил), имидазол (например, 2-имидазолил), фуран (например, 2-фурил и 3-фурил), тиофен (например, 2-тиенил), триазол (например, 1,2,3-триазолил и 1,2,4-триазолил), пиразол (например, 1H-пиразол-3-ил), оксазол (например, 2-оксазолил), изоксазол (например, 3-изоксазолил), тиазол (например, 2-тиазолил и 4-тиазолил) и изотиазол (например, 3-изотиазолил), пиридин (например, 2-пиридил, 3-пиридил и 4-пиридил), пиридилимидазол, пиридилтриазол, пиразин, пиридазин (например, 3-пиридазинил), пиримидин (например, 2-пиримидинил), тетразол, триазин (например, 1,3,5-триазинил), индолил (например, 1H-индол-2-ил, 1H-индол-4-ил и 1H-индол-5-ил), бензофуран (например, бензофуран-5-ил), бензотиофен (например, бензо[b]тиен-2-ил и бензо[b]тиен-5-ил), бензимидазол, бензоксазол, бензотиазол, бензотриазол, хинолин (например, 2-хинолил), изохинолин, хиназолин, хиноксалин и тому подобное.
Моновалентные насыщенные гетероциклы обычно содержат в общем от 3 до 10 кольцевых атомов, из которых 2-9 являются атомами углерода кольца, и 1-4 являются гетероатомами, и включают, например, -C3-5гетероцикл. Иллюстративные моновалентные насыщенные гетероциклы включают, в качестве примера, моновалентные группы пирролидина, имидазолидина, пиразолидина, пиперидина, 1,4-диоксана, морфолина, тиоморфолина, пиперазина, 3-пирролина и тому подобное. В некоторых случаях, группы могут быть описаны как взятые вместе с образованием насыщенного -C3-5гетероцикла, необязательно содержащего в кольце атом кислорода. Такие группы включают:
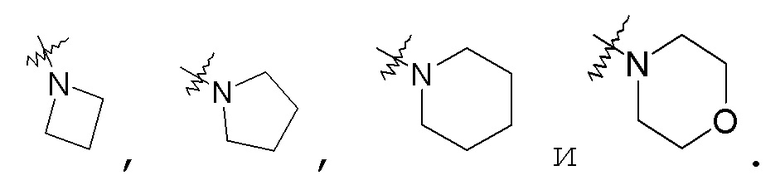
Моновалентные частично ненасыщенные гетероциклы обычно содержат в общем от 3 до 10 кольцевых атомов, из которых 2-11 являются атомами углерода кольца, и 1-3 являются гетероатомами, и включают, например, -C3-5гетероцикл и -C2-12гетероцикл. Иллюстративные моновалентные частично ненасыщенные гетероциклы включают, в качестве примера, пиран, бензопиран, бензодиоксол (например, бензо[1,3]диоксол-5-ил), тетрагидропиридазин, 2,5-дигидро-1H-пиррол, дигидроимидазол, дигидротриазол, дигидрооксазол, дигидроизоксазол, дигидротиазол, дигидроизотиазол, дигидрооксадиазол, дигидротиадиазол, тетрагидропиридазин, гексагидропирролохиноксалин и дигидрооксадиазабензо[e]азулен. В некоторых случаях, группы могут быть описаны как взятые вместе с образованием частично ненасыщенного -C3-5гетероцикла. Такие группы включают:

Термин "необязательно замещенный" означает, что группа, о которой идет речь, может быть незамещенной или может быть замещенный один или более раз, как 1-3 раза или 1-5 раз, или 1-8 раз. Например, фенильная группа, которая "необязательно замещена" атомами галогена, может быть незамещенной, или она может содержать 1, 2, 3, 4 или 5 атомов галогена; и алкильная группа, которая "необязательно замещена" атомами фтора, может быть незамещенной, или она может содержать 1, 2, 3, 4, 5, 6, 7 или 8 атомов фтора. Подобным образом, группа, которая является "необязательно замещенной" одной или двумя -C1-6алкильными группами, может быть незамещенный, или она может содержать одну или две -C1-6алкильные группы.
Как используется в данном описании, фраза "имеющий формулу" или "имеющий структуру" не предназначена для ограничения и используется таким же образом, как и обычно используемый термин "содержащий". Например, если изображена одна структура, понятно, что охватываются все стереомерные и таутомерные формы, если не указано иное.
Термин "фармацевтически приемлемый" относится к веществу, которое не является биологически или иным образом неприемлемым для использования по настоящему изобретению. Например, термин "фармацевтически приемлемый носитель" относится к веществу, которое может быть включено в композицию и может быть введено пациенту без проявления нежелательных биологических эффектов или взаимодействия неприемлемым образом с другими компонентами композиции. Такие фармацевтически приемлемые вещества обычно отвечают требуемым стандартам токсикологического тестирования и производства, и включают такие материалы, которые приняты как подходящие неактивные ингредиенты согласно требованиям агентства U.S. Food и Drug Administration.
Термин "фармацевтически приемлемая соль" означает соль, полученную из основания или кислоты, которые являются приемлемыми для введения пациенту, такому как млекопитающее (например, соли, имеющие приемлемую безопасность для млекопитающих при данном режиме дозирования). Однако, понятно, что соли, охватываемые настоящим изобретением, необязательно должны быть фармацевтически приемлемыми солями, такими как соли промежуточных соединений, не предназначенные для введения пациенту. Фармацевтически приемлемые соли могут быть производными фармацевтически приемлемых неорганических или органических оснований и фармацевтически приемлемых неорганических или органических кислот. Кроме того, когда соединение формулы I содержит как группу основания, такого как амин, пиридин или имидазол, так и группу кислоты, такую как карбоновая кислота или тетразол, могут образовываться цвиттерионы, и они охватываются термином "соль", как используется в данном описании. Соли, полученные из фармацевтически приемлемых неорганических оснований, включают соли аммония, кальция, меди, железа(II), железа(III), лития, магния, марганца(II), марганца(IV), калия, натрия и цинка, и тому подобное. Соли, полученные из фармацевтически приемлемых органических оснований, включают соли первичных, вторичных и третичных аминов, включая замещенные амины, циклические амины, природные амины и тому подобное, такие как аргинин, бетаин, кофеин, холин, N,N'-дибензилэтилендиамин, диэтиламин, 2-диэтиламиноэтанол, 2-диметиламиноэтанол, этаноламин, этилендиамин, N-этилморфолин, N-этилпиперидин, глюкамин, глюкозамин, гистидин, гидрабамин, изопропиламин, лизин, метилглюкамин, морфолин, пиперазин, пиперадин, полиаминовые смолы, прокаин, пурины, теобромин, триэтиламин, триметиламин, трипропиламин, трометамин и тому подобное. Соли, полученные из фармацевтически приемлемых неорганических кислот, включают соли борной, карбоновой, галогеноводородной (бромистоводородной, хлористоводородной, фтористоводородной или йодистоводородной), азотной, фосфорной, сульфаминовой и серной кислот. Соли, полученные из фармацевтически приемлемых органических кислот, включают соли алифатических гидроксильных кислот (например, лимонной, глюконовой, гликолевой, молочной, лактобионовой, яблочной и винной кислот), алифатических монокарбоновых кислот (например, уксусной, бутановой, муравьиной, пропионовой и трифторуксусной кислот), аминокислот (например, аспарагиновой и глютамовой кислот), ароматических карбоновых кислот (например, бензойной, п-хлорбензойной, дифенилуксусной, гентизиновой, гиппуровой и трифенилуксусной кислот), ароматических гидроксильных кислот (например, о-гидроксибензойной, п-гидроксибензойной, 1-гидроксинафталин-2-карбоновой и 3-гидроксинафталин-2-карбоновой кислот), аскорбиновой, дикарбоновых кислот (например, фумаровой, малеиновой, щавелевой и янтарной кислот), глюкуроновой, миндальной, слизевой, никотиновой, оротовой, памовой, пантотеновой, сульфоновых кислот (например, бензолсульфоновой, камфосульфоновой, 1,2-этандисульфоновой, этансульфоновой, изетионовой, метансульфоновой, нафталинсульфоновой, нафталин-1,5-дисульфоновой, нафталин-2,6-дисульфоновой и п-толуолсульфоновой кислот), ксинафоевой кислоты и тому подобное.
Как используется в данном описании, термин "пролекарство" предназначен для обозначения неактивного (или по существу менее активного) предшественника лекарственного средства, которое в физиологических условиях в организме преобразуется в свою активную форму, например, путем обычных процессов метаболизма. Такие соединения могут не обладать фармакологической активностью в отношении NEP, но могут быть введены перорально или парентерально и затем в организме подвергнуться метаболизму с образованием соединений, которые являются фармакологически активными в отношении NEP. Примеры пролекарств включают сложные эфиры, такие как сложные C1-6алкиловые эфиры и сложные арил-C1-6алкиловые эфиры. В одном варианте осуществления изобретения активное соединение имеет свободный карбоксил, и пролекарство представляет собой его сложноэфирное производное, то есть, пролекарство является сложным эфиром, таким как -C(O)OCH2CH3. Такие сложноэфирные пролекарства далее преобразуются путем сольволиза или в физиологических условиях, с получением свободного карбоксильного соединения. Термин предназначен также для включения некоторых защищенных производных соединений формулы I, которые могут быть получены перед заключительной стадией удаления защиты. Таким образом, все защищенные производные и пролекарства соединений формулы I включены в объем настоящего изобретения.
Термин "терапевтически эффективное количество" означает количество, достаточное для осуществления лечения при введении пациенту, нуждающемуся в этом, то есть, количество лекарственного средства, необходимое для достижения желаемого терапевтического эффекта. Например, терапевтически эффективное количество для лечения гипертензии представляет собой количество соединения, необходимое, например, для того, чтобы уменьшить, подавить, устранить или предотвратить симптомы гипертензии, или для лечения основных причин гипертензии. В одном варианте осуществления изобретения терапевтически эффективное количество является таким количеством лекарственного средства, которое необходимо для снижения артериального давления, или количеством лекарственного средства, необходимым для поддержания нормального кровяного давления. С другой стороны, термин "эффективное количество" означает количество, достаточное для достижения желаемого результата, которое необязательно может являться терапевтическим результатом. Например, при исследовании системы, содержащей фермент NEP, "эффективное количество" может представлять собой количество, необходимое для ингибирования фермента.
Термин "лечение" или "терапия", как используется в данном описании, означает лечение или терапию заболевания или медицинского состояния (такого как гипертензия) у пациента, такого как млекопитающее (в частности, человека), которое включает одно или более из следующих: (a) предотвращение протекания заболевания или медицинского состояния, то есть, предотвращение повторения заболевания или медицинского состояния, или профилактическое лечение пациента, предрасположенного к заболеванию или медицинскому состоянию; (b) улучшение заболевания или медицинского состояния, то есть, устранение или регрессию заболевания или медицинского состояния у пациента; (c) подавление заболевания или медицинского состояния, то есть, замедление или остановку развития заболевания или медицинского состояния у пациента; или (d) облегчение симптомов заболевания или медицинского состояния у пациента. Например, термин "лечение гипертензии" может включать предотвращение протекания гипертензии, улучшение гипертензии, подавление гипертензии и облегчение симптомов гипертензии (например, снижение кровяного давления). Термин "пациент" предназначен для включения таких млекопитающих, как человек, нуждающихся в лечении или предотвращении заболевания, или которые в настоящее время подвергаются лечению заболевания или профилактике лечения конкретного заболевания или медицинского состояния, а также изучаемых субъектов, на которых оценивают соединения по изобретению или которые используют в анализах, например, животную модель.
Все другие термины, используемые в данном описании, предназначены для использования в их обычном значении, как понятно специалистам в области техники, к которой они имеют отношение.
В одном аспекте настоящее изобретение относится к соединениям формулы I:

или их фармацевтически приемлемым солям.
Как используется в данном описании, термин "соединение по изобретению" включает все соединения, охватываемые формулой I, такие как охватываемые формулами Ia-d, а также соединения, охватываемые формулами II и III, и их аналоги. Кроме того, соединения по изобретению также могут содержать несколько групп оснований или кислот (например, амино- или карбоксильные группы), и поэтому указанные соединения могут существовать в виде свободного основания, свободной кислоты или в различных солевых формах. Все такие солевые формы включены в объем изобретения. Далее, соединения по изобретению также могут существовать в виде пролекарств. В соответствии с этим, специалистам в данной области понятно, что ссылка на соединение в данном описании, например, ссылка на "соединение по изобретению" или на "соединение формулы I" включают соединение формулы I, а также фармацевтически приемлемые соли и пролекарства указанного соединения, если не указано иное. Далее, термин "или его фармацевтически приемлемая соль и/или пролекарство" предназначен для включения всех производных солей и пролекарств, таких как фармацевтически приемлемая соль пролекарства. Кроме того, в объем настоящего изобретения включены сольваты соединений формулы I.
Соединения формулы I могут иметь один или несколько хиральных центров, и поэтому указанные соединения могут быть получены и использованы в различных стереоизомерных формах. В соответствии с этим, настоящее изобретение также относится к рацемическим смесям, чистым стереоизомерам (например, энантиомерам и диастереоизомерам), смесям, обогащенным стереоизомером, и тому подобное, если не указано иное. Когда химическая структура изображена в данном описании без указания какой-либо стереохимии, понятно, что такой структурой охватываются все возможные стереоизомеры. Таким образом, например, термины "соединение формулы I", "соединения формулы II" и т.д. предназначены для включения всех возможных стереоизомеров соединения. Подобным образом, когда конкретный стереоизомер показан или назван в настоящем описании, специалисту в данной области будет понятно, что в композициях по изобретению могут присутствовать незначительные количества других стереоизомеров, если не указано иное, при условии, что полезность композиции в целом не исключает присутствие других таких изомеров. Отдельные стереоизомеры могут быть получены различными способами, которые хорошо известны в данной области, включая хиральную хроматографию с использованием подходящей хиральной стационарной фазы или подложки, или путем их химического преобразования в диастереоизомеры, разделением диастереоизомеров обычными средствами, такими как хроматография или перекристаллизация, с последующей регенерацией первоначального стереоизомера.
Кроме того, когда приемлемо, все цис-транс или E/Z изомеры (геометрические изомеры), таутомерные формы и топоизомерные формы соединений по изобретению включены в объем изобретения, если не указано иное. Например, если X изображен как (R4 представляет собой водород):
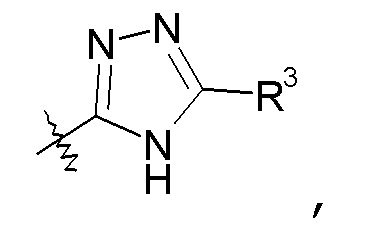
понятно, что соединение также может существовать в таутомерной форме, такой как:
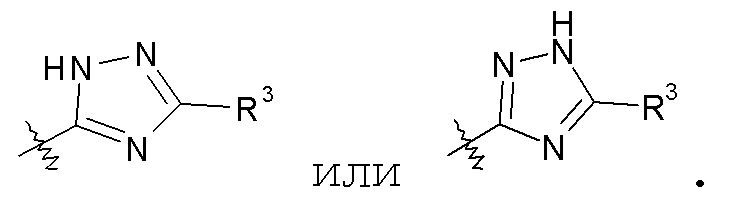
Более конкретно, соединения формулы I могут иметь, по меньшей мере, два хиральных центра, указанные на следующей формуле символами * и **:

В одном стереоизомере оба атома углерода, помеченные символами * и **, имеют (R) конфигурацию. Этот вариант осуществления изобретения показан формулой Ia:
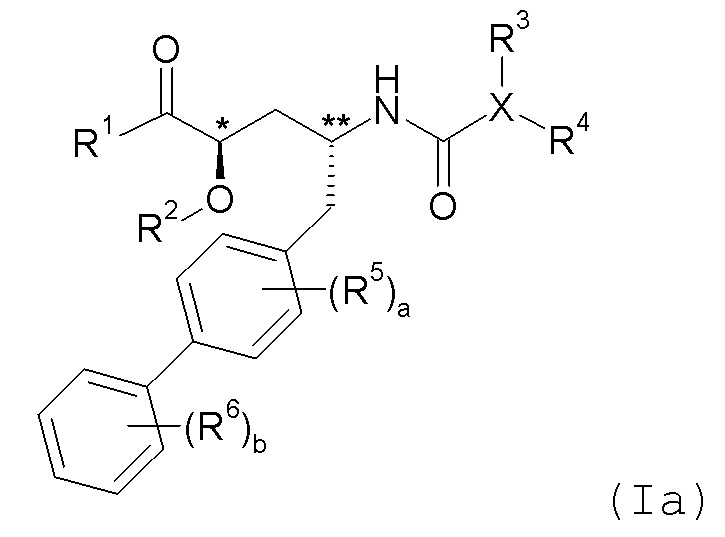
В данном варианте осуществления изобретения, соединения имеют (R,R) конфигурацию на атомах углерода * и ** или обогащены стереоизомерной формой, имеющей (R,R) конфигурацию на указанных атомах углерода.
В другом стереоизомере оба атома углерода, помеченные символами * и **, имеют (S) конфигурацию. Этот вариант осуществления изобретения показан формулой Ib:

В данном варианте осуществления изобретения соединения имеют (S,S) конфигурацию на атомах углерода * и ** или обогащены стереоизомерной формой, имеющей (S,S) конфигурацию на указанных атомах углерода.
В еще одном стереоизомере атом углерода, помеченный символом *, имеет (S) конфигурацию, и атом углерода, помеченный символом **, имеет (R) конфигурацию. Этот вариант осуществления изобретения показан формулой Ic:

В данном варианте осуществления изобретения соединения имеют (S,R) конфигурацию на атомах углерода * и ** или обогащены стереоизомерной формой, имеющей (S,R) конфигурацию на указанных атомах углерода.
В еще одном стереоизомере атом углерода, помеченный символом *, имеет (R) конфигурацию, и атом углерода, помеченный символом **, имеет (S) конфигурацию. Этот вариант осуществления изобретения показан формулой Id:
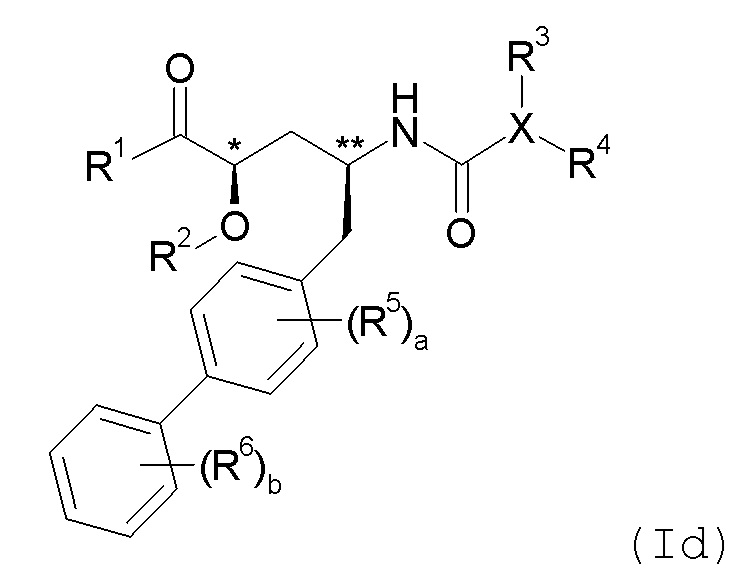
В данном варианте осуществления изобретения соединения имеют (R,S) конфигурацию на атомах углерода * и ** или обогащены стереоизомерной формой, имеющей (R,S) конфигурацию на указанных атомах углерода.
Соединения формулы Ia и Ib представляют собой энантиомеры, и поэтому, в отдельных аспектах, настоящее изобретение относится к каждому отдельному энантиомеру (то есть, Ia или Ib), рацемической смеси Ia и Ib или обогащенной энантиомером смеси Ia и Ib, содержащей преимущественно Ia или преимущественно Ib. Подобным образом, соединения формулы Ic и Id представляют собой энантиомеры, и поэтому, в отдельных аспектах настоящее изобретение относится к каждому отдельному энантиомеру (то есть, Ic или Id), рацемической смеси Ic и Id или обогащенной энантиомером смеси Ic и Id, содержащей преимущественно Ic или преимущественно Id.
В некоторых вариантах осуществления изобретения, с целью оптимизации терапевтической активности соединений по изобретению, например, для лечения гипертензии, может быть желательным, чтобы атомы углерода, помеченные символами * и **, имели конкретную (R,R), (S,S), (S,R) или (R,S) конфигурацию или были обогащены стереоизомерной формой, имеющей такую конфигурацию. Например, в одном варианте осуществления изобретения соединения по изобретению имеют (S,R) конфигурацию формулы Ic или обогащены стереоизомерной формой, имеющей (S,R) конфигурацию, и в другом варианте осуществления соединения по изобретению имеют (R,S) конфигурацию формулы Id или обогащены стереоизомерной формой, имеющей (R,S) конфигурацию. В других вариантах осуществления соединения по изобретению представлены в виде рацемических смесей, например, в виде смеси энантиомеров формулы Ia и Ib, или в виде смеси энантиомеров формулы Ic и Id.
Соединения по изобретению, а также такие соединения, которые используются в их синтезе, также могут включать изотопно-меченные соединения, то есть, такие, где одно или несколько атомов обогащены атомами, имеющими атомную массу, отличающуюся от атомной массы атомов, преимущественно встречающихся в природе. Примеры изотопов, которые могут входить в состав соединений формулы I, например, включают, но, не ограничиваясь ими, 2H, 3H, 13C, 14C, 15N, 18O, 17O, 35S, 36Cl и 18F. Особый интерес представляют собой соединения формулы I, обогащенные тритием или углеродом-14, которые могут быть использованы, например, при исследованиях распределения в ткани; соединения формулы I, обогащенные дейтерием, особенно на участке метаболизма, дают, например, соединения, имеющие более высокую метаболическую стабильность; и соединения формулы I, обогащенные излучающим позитрон изотопом, таким как 11C, 18F, 15O и 13N, которые могут быть использованы, например, в исследованиях путем позитронной эмиссионной томографии (PET).
Номенклатура, используемая в данном описании для названия соединений по изобретению, проиллюстрирована в примерах данного описания. Эта номенклатура была получена с использованием коммерчески доступного программного обеспечения AutoNom (MDL, San Leandro, California).
Иллюстративные варианты осуществления изобретения
Следующие заместители и их значения предназначены для демонстрации иллюстративных примеров различных аспектов и вариантов осуществления изобретения. Эти иллюстративные значения предназначены для дальнейшего определения и иллюстрирования таких аспектов и вариантов осуществления, но не предназначены для исключения других вариантов осуществления или для ограничения объема изобретения. В этом отношении, представление, что конкретное значение или заместитель является предпочтительным, не предназначено каким-либо образом для исключения других значений или заместителей по настоящему изобретению, если это специально не указано.
В одном аспекте настоящее изобретение относится к соединениям формулы I:

R1 выбран из -OR7 и -NR8R9. Группа R7 выбрана из:
H;
-C1-8алкила, например, -CH3, -CH2CH3, -(CH2)2CH3, -CH(CH3)2, -CH2CH(CH3)2, -(CH2)3CH3, -(CH2)4CH3, -(CH2)2CH(CH3)2, -(CH2)5CH3 и -(CH2)6CH3;
-C1-3алкилен-C6-10арила, например, бензила;
-C1-3алкилен-C1-9гетероарила, например, -CH2-пиридинила и -(CH2)2-пиридинила;
-C3-7циклоалкила, например, циклопентила;
-[(CH2)2O]1-3CH3, например, -(CH2)2OCH3 и -[(CH2)2O]2CH3;
-C1-6алкилен-OC(O)R10, например, -CH2OC(O)CH3, -CH2OC(O)CH2CH3, -CH2OC(O)(CH2)2CH3, -CH2CH(CH3)OC(O)CH2CH3, -CH2OC(O)OCH3, -CH2OC(O)OCH2CH3, -CH(CH3)OC(O)OCH2CH3, -CH(CH3)OC(O)O-CH(CH3)2, -CH2CH(CH3)OC(O)-циклопентила, -CH2OC(O)O-циклопропила, -CH(CH3)-OC(O)-O-циклогексила, -CH2OC(O)O-циклопентила, -CH2CH(CH3)OC(O)-фенила, -CH2OC(O)O-фенила, -CH2OC(O)-CH[CH(CH3)2]-NH2, -CH2OC(O)-CH[CH(CH3)2]-NHC(O)OCH3 и -CH(CH3)OC(O)-CH(NH2)CH2COOCH3;
-C1-6алкилен-NR12R13, например, -(CH2)2-N(CH3)2,

-C1-6алкилен-C(O)R31, например, -CH2C(O)OCH3, -CH2C(O)O-бензил, -CH2C(O)-N(CH3)2 и
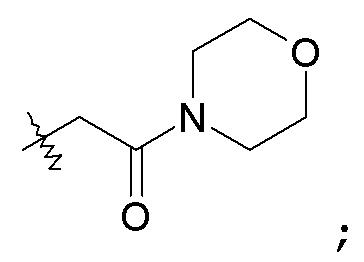
-C0-6алкиленморфолинила, например, -(CH2)2-морфолинила и -(CH2)3-морфолинила:

-C1-6алкилен-SO2-C1-6алкила, например, -(CH2)2SO2CH3;

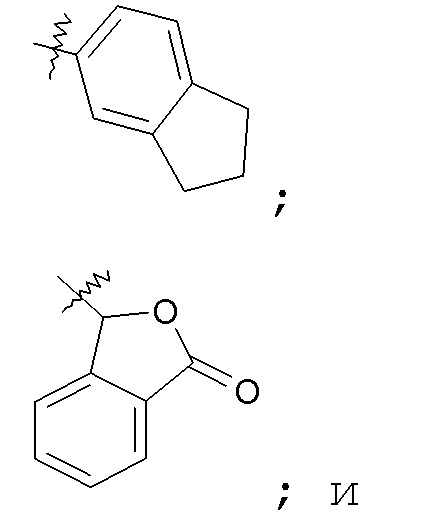
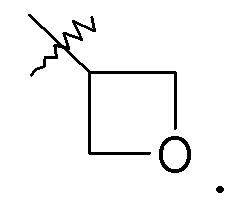
Группа R10 выбрана из:
-C1-6алкила, например, -CH3 и -CH2CH3;
-O-C1-6алкила, например, -OCH3, -O-CH2CH3 и -O-CH(CH3)2;
-C3-7циклоалкила, например, циклопентила;
-O-C3-7циклоалкила, например, -O-циклопропила, -O-циклогексила и -O-циклопентила;
фенила;
-O-фенила;
-NR12R13;
-CH[CH(CH3)2]-NH2;
-CH[CH(CH3)2]-NHC(O)O-C1-6алкила, например, -CH[CH(CH3)2]-NHC(O)OCH3; и
-CH(NH2)CH2COOCH3.
Группы R12 и R13 независимо выбраны из H, -C1-6алкила (например, CH3) и бензила. Альтернативно, группы R12 и R13 могут быть взяты вместе как -(CH2)3-6-, -C(O)-(CH2)3- или -(CH2)2O(CH2)2-, например, с образованием группы, такой как:

Группа R31 выбрана из -O-C1-6алкила, например, -OCH3, -O-бензила и -NR12R13, например, -N(CH3)2, и
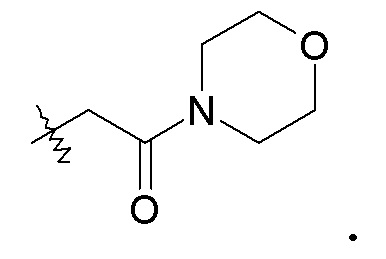
Группа R32 представляет собой -C1-6алкил (например, -CH3 и -C(CH3)3) или -C0-6алкилен-C6-10арил.
Группа R8 выбрана из:
H;
-OH;
-OC(O)R14, например, -OC(O)CH3, -OC(O)-фенила, -OC(O)-OCH2-фенила, -OC(O)-CH2O-фенила, -OC(O)(NH2) и -OC(O)[N(CH3)2;
-CH2COOH;
-O-бензила;
пиридила и
-OC(S)NR15R16, например, -OC(S)NH2 и -OC(S)N(CH3)2.
Группа R14 выбрана из:
H;
-C1-6алкила, например, -CH3;
-C6-10арила, например, фенила;
-OCH2-C6-10арила, например, -OCH2-фенила;
-CH2O-C6-10арила, например, -CH2O-фенила; и
-NR15R16, например, -NH2 и N(CH3)2.
Группы R15 и R16 независимо выбраны из H и -C1-4алкила.
R9 представляет собой группу, выбранную из H, -C1-6алкила (например, -CH3) и -C(O)R17 (например, -C(O)H). Группа R17 выбрана из H, -C1-6алкила (например, -CH2CH3), -C3-7циклоалкила (например, циклопропила), -C6-10арила (например, фенила) и -C1-9гетероарила (например, пиридина).
Кроме того, каждая алкильная группа в R1 необязательно замещена 1-8 атомами фтора. Например, когда R1 представляет собой -OR7, и R7 представляет собой -C1-8алкил, R1 также может представлять собой группу, такую как -OCH(CH3)CF3, -OCH2CF2CF3, -OCH(CF3)2, -O(CH2)2CF3, -OCH(CH2F)2, -OC(CF3)2CH3 и -OCH(CH3)CF2CF3.
В одном варианте осуществления изобретения R1 выбран из -OR7, где R7 выбран из H, -C1-8алкила, -C1-6алкилен-OC(O)R10, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила и
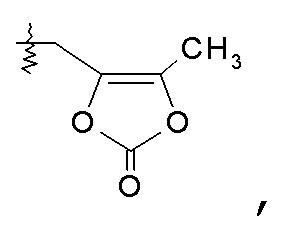
где R10 представляет собой -O-C3-7циклоалкил; и -NR8R9, где R8 представляет собой H, и R9 представляет собой H. В другом варианте осуществления указанные соединения имеют формулу III.
В одном варианте осуществления изобретения R1 выбран из -OR7 и -NR8R9, где R7 представляет собой H, R8 представляет собой H или -OH, и R9 представляет собой H. В другом варианте осуществления указанные соединения имеют формулу III.
В другом варианте осуществления R1 представляет собой -OR7, где R7 выбран из -C1-8алкила, -C1-3алкилен-C6-10арила, -C1-3алкилен-C1-9гетероарила, -C3-7циклоалкила, -[(CH2)2O]1-3CH3, -C1-6алкилен-OC(O)R10, -C1-6алкилен-NR12R13, -C1-6алкилен-C(O)R31, -C0-6алкиленморфолинила; -C1-6алкилен-SO2-C1-6алкила;
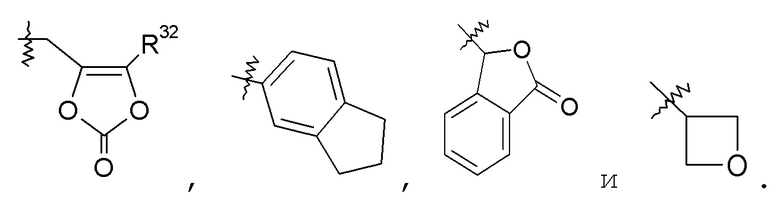
В еще одном варианте осуществления изобретения R1 представляет собой -NR8R9; где R8 выбран из -OC(O)R14, -CH2COOH, -O-бензила, пиридила и -OC(S)NR15R16; и R9 представляет собой H. В еще одном варианте осуществления изобретения R1 представляет собой -NR8R9, где R8 представляет собой H или -OH; и R9 представляет собой -C1-6алкил или -C(O)R17. В еще одном варианте осуществления изобретения R1 представляет собой -NR8R9, где R8 выбран из -OC(O)R14, -CH2COOH, -O-бензила, пиридила и -OC(S)NR15R16; и R9 представляет собой -C1-6алкил или -C(O)R17. В другом варианте осуществления указанные соединения имеют формулу III. В одном аспекте изобретения указанные соединения могут найти конкретное применение в качестве пролекарств или в качестве промежуточных соединений в способах синтеза, описанных в данном описании. Например, в одном варианте осуществления изобретения R1 представляет собой -OR7, и R7 представляет собой -C1-6алкилен-OC(O)R10, такой как -O-CH(CH3)OC(O)-O-циклогексил:
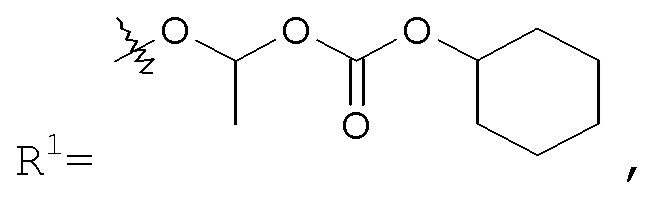
образуя соединение сложный эфир цилексетила; или R1 представляет собой -OR7, и R7 представляет собой -C0-6алкиленморфолинил, такой как -O-(CH2)2-морфолинил:

образуя соединение сложный эфир 2-морфолиноэтила или мофетила; или R1 представляет собой -OR7, и R7 представляет собой

такой как -O-CH2-5-метил[1,3]диоксол-2-он:
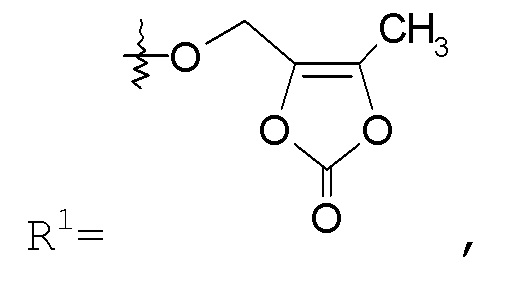
образуя соединение сложный эфир медоксомил.
R2 представляет собой H или -P(O)(OH)2. R2 также может быть взят вместе с R7 с образованием -CR18R19- или, взятый вместе с R8, образует -C(O)-. R18 и R19 независимо выбраны из H, -C1-6алкила и -O-C3-7циклоалкила, или R18 и R19 могут быть взяты вместе с образованием =O. В одном варианте осуществления изобретения R2 представляет собой H. В другом варианте осуществления указанное соединение имеет формулу III.
Когда R2, взятый вместе с R7, образует -CR18R19-, данный вариант осуществления может быть изображен как:
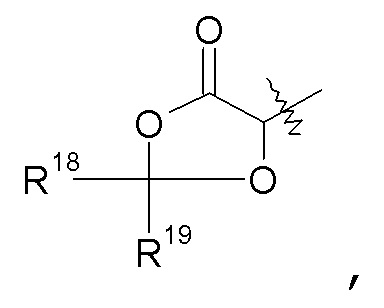
и, когда R18 и R19 взяты вместе с образованием =O, данный вариант осуществления может быть изображен как:

Когда R2, взятый вместе с R8, образует -C(O)-, данный вариант осуществления может быть изображен как:

В одном аспекте изобретения указанные соединения могут найти конкретное применение в качестве пролекарств или в качестве промежуточных соединений в способах синтеза, описанных в данном описании. В другом варианте осуществления указанные соединения имеют формулу III. Соединения, где R2 представляет собой -P(O)(OH)2, также могут найти конкретное применение в качестве пролекарств.
Группа "X" представляет собой -C1-9гетероарил, и точкой присоединения является любой доступный атом углерода или азота. Следует учесть, что в некоторых вариантах осуществления изобретения R3 и/или R4 могут отсутствовать. Когда присутствует, R3 находится на любом доступном атоме углерода. Когда присутствует, R4 находится на любом доступном атоме углерода или азота. Примеры -C1-9гетероарильных колец включают, в качестве иллюстрации, но не ограничения:
пиразольные кольца, такие как:
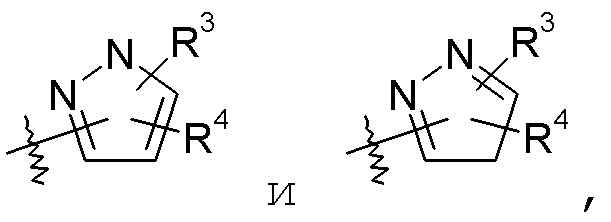
конкретные примеры которых включают:

имидазольные кольца, такие как:

конкретные примеры которых включают:
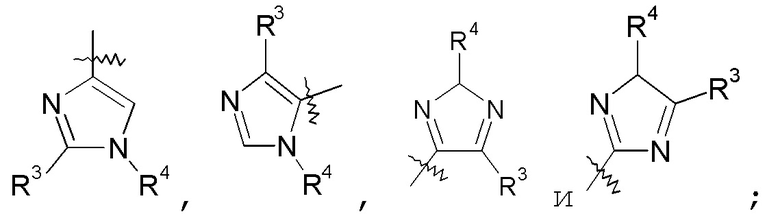
триазольные кольца, включая 1,2,3-триазол, такой как:

а также 1,2,4-триазол, такой как:

бензотриазольные кольца, такие как:
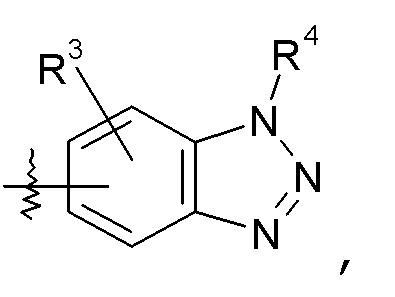
конкретные примеры которых включают:
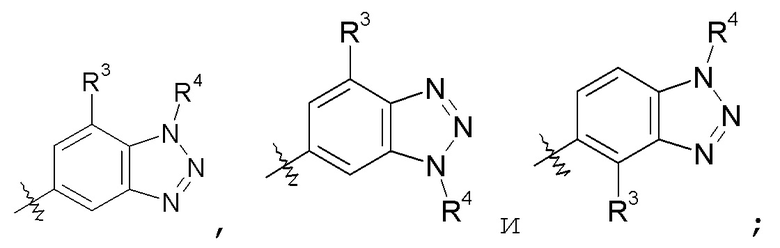
фурановые кольца:

конкретные примеры которых включают:
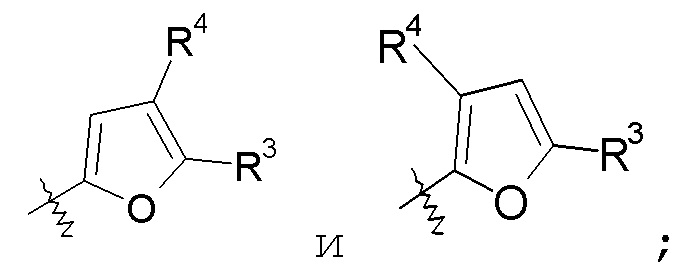
пиррольные кольца:
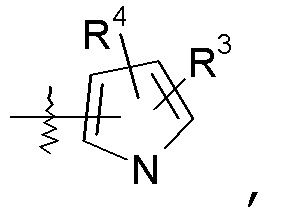
конкретные примеры которых включают:

тетразольные кольца, такие как:
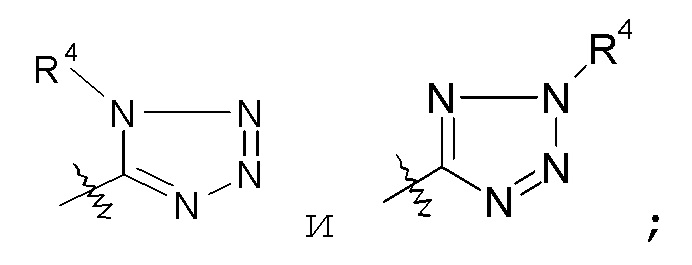
пиразиновые кольца:
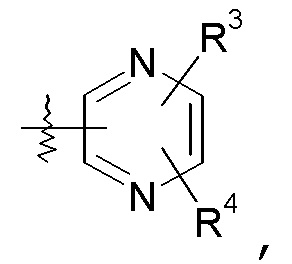
конкретный пример которого включает:

тиофеновые кольца:
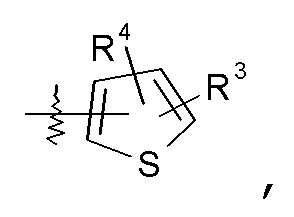
конкретные примеры которых включают:

оксазольные кольца:

конкретные примеры которых включают:

изоксазольные кольца:
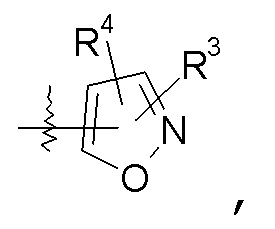
конкретные примеры которых включают:

тиазольные кольца:

конкретные примеры которых включают:
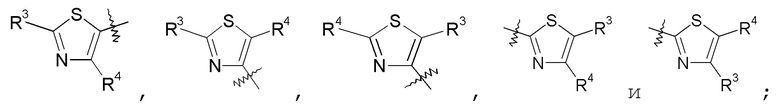
изотиазольные кольца:

оксадиазольные кольца, включая [1,2,4]оксадиазол, такой как:
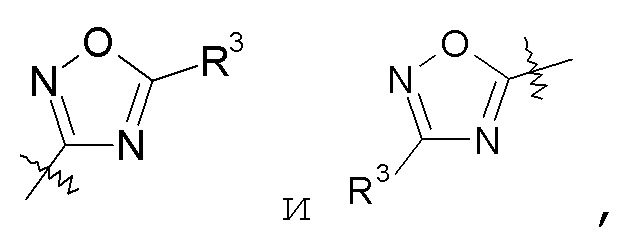
а также [1,2,3]оксадиазол, такой как:

и [1,3,4]оксадиазол:

тиадиазольные кольца, включая [1,2,4]тиадиазол, такой как:

а также [1,2,3]тиадиазол, такой как:

и [1,3,4]тиадиазол:
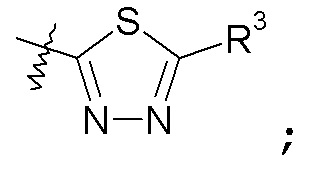
пиридазиновые кольца:
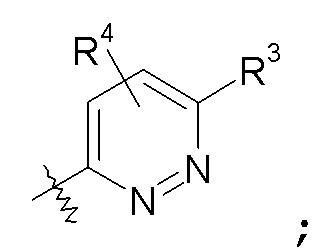
пиридиновые кольца:

конкретные примеры которых включают:

пиримидиновые кольца:
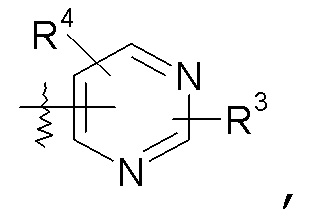
конкретные примеры которых включают:

пирановые кольца, такие как

бензимидазольные кольца, такие как:
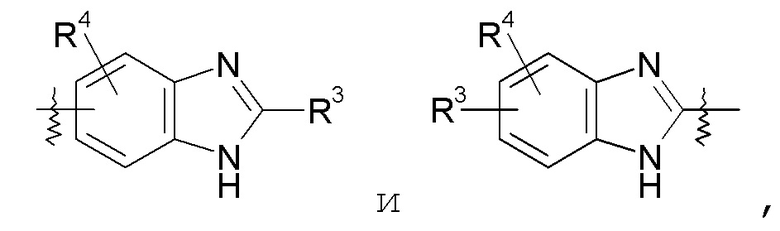
конкретные примеры которых включают:
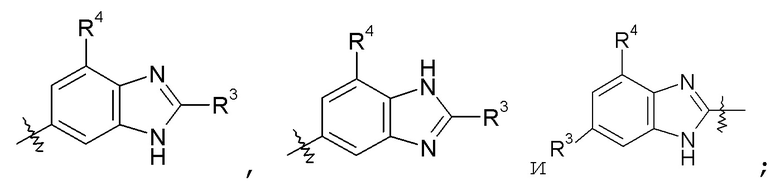
бензоксазольные кольца, такие как:

конкретные примеры которых включают:
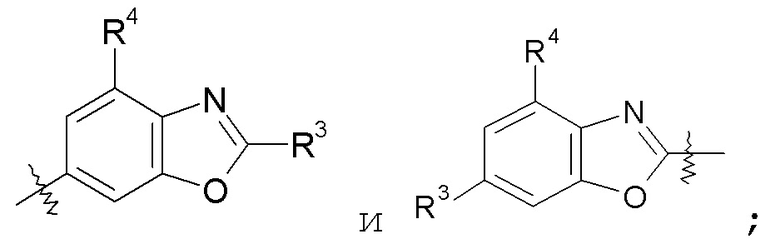
бензотиазольные кольца, такие как:

конкретные примеры которых включают:

пиридилимидазольные кольца, такие как:
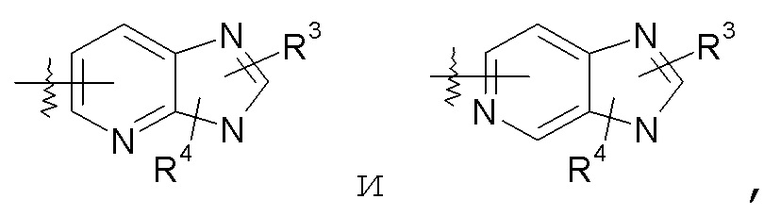
конкретный пример которого включает:

пиридилтриазольные кольца, такие как:

конкретные примеры которых включают:

В одном конкретном варианте осуществления X выбран из пиразола, имидазола, триазола, бензотриазола, фурана, пиррола, тетразола, пиразина, тиофена, оксазола, изоксазола, тиазола, изотиазола, оксадиазола, тиадиазола, пиридазина, пиридина, пиримидина, пирана, бензимидазола, бензоксазола, бензотиазола, пиридилимидазола и пиридилтриазола.
Следует понимать, что некоторые -C1-9гетероарильные кольца могут существовать в таутомерной форме, и что такие таутомерные формы представляют собой часть изобретения и охватываются термином "гетероарил". Таким образом, если соединение изображено с -C1-9гетероарильным кольцом, понятно, что соединение также может существовать в таутомерной форме и, наоборот, что обе формы охватываются настоящим изобретением.
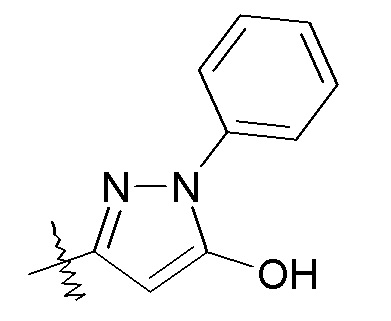






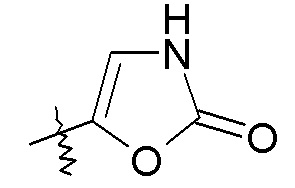


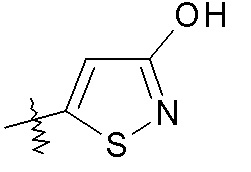
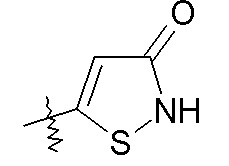

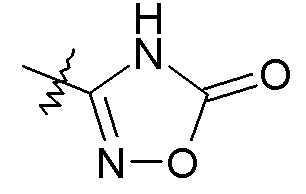
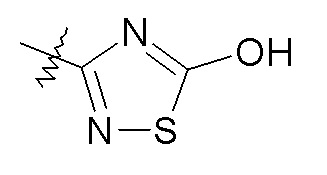
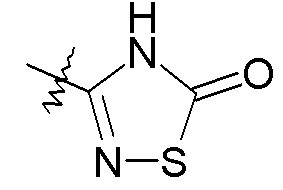


В одном конкретном варианте осуществления X выбран из пиразола, триазола, бензотриазола, фурана, тетразола, пиразина, тиофена, оксазола, изоксазола, тиазола, оксадиазола, пиридазина, пиридина, пиримидина, бензоксазола, пиридилимидазола и пиридилтриазола. В другом варианте осуществления X выбран из пиразола, триазола, бензотриазола, изоксазола, пиридазина, пиримидина и пиридилтриазола. В еще одном варианте осуществления изобретения X представляет собой изоксазол, и в одном конкретном варианте осуществления имеет формулу III:

где R1-R6, a и b имеют значения, указанные для формулы I. В еще одном варианте осуществления изобретения соединения по изобретению имеют формулу IIIa:

где R1, R5, R6, a и b имеют значения, указанные для формулы I. В еще одном варианте осуществления изобретения соединения по изобретению имеют формулу IIIb:
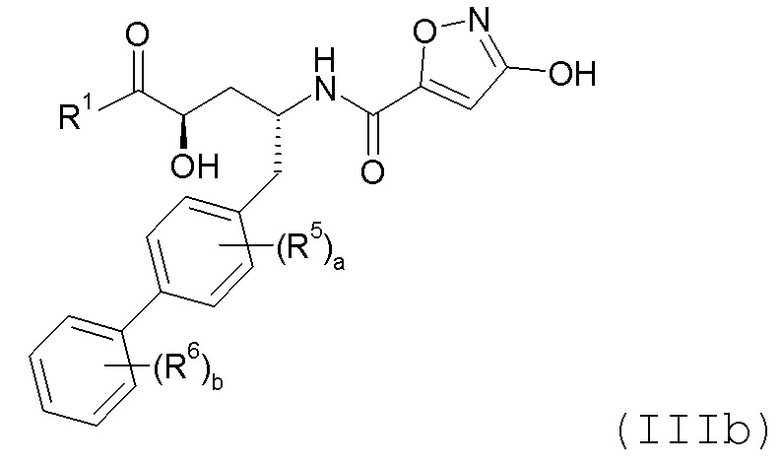
где R1, R5, R6, a и b имеют значения, указанные для формулы I.
Группа R3 может отсутствовать. Когда присутствует, R3 присоединен к атому углерода в группе "X" и выбран из:
H;
галогена, например, хлора и фтора;
-C0-5алкилен-OH, например, -OH, -CH2OH, -CH(OH)CH3 и -C(CH3)2-OH;
-NH2;
-C1-6алкила, например, -CH3, -(CH2)2CH3, -CH(CH3)2 и -(CH2)3-CH3;
-CF3;
-C3-7циклоалкила, например, циклопропила и циклогексила;
-C0-2алкилен-O-C1-6алкила, например, -OCH3, -OCH2CH3, -CH2-OCH3 и -(CH2)2-OCH3;
-C(O)R20, например, -C(O)H и -C(O)CH3;
-C0-1алкилен-COOR21, например, -COOH, -CH2-COOH, -C(O)O-CH2CH3, -C(O)O-(CH2)2OCH3 -C(O)O-CH2OC(O)CH3, -CH2-C(O)O-CH2OC(O)CH3, -C(O)O-CH2OC(O)O-CH3, -CH2-C(O)O-CH2OC(O)O-CH3, -C(O)O-CH(CH3)OC(O)O-CH2CH3, -C(O)O-CH(CH3)OC(O)O-CH(CH3)2, -C(O)O-CH2CH(CH3)OC(O)-циклопентила, -C(O)O-CH2OC(O)O-циклопропила, -C(O)O-CH(CH3)-OC(O)-O-циклогексила, -C(O)O-CH2OC(O)O-циклопентила, -C(O)O-CH2CH(CH3)OC(O)-фенила, -C(O)O-CH2OC(O)O-фенила, -C(O)O-CH2-пиридина, -C(O)O-CH2-пирролидина, -C(O)O-(CH2)2-морфолинила, -C(O)O-(CH2)3-морфолинила и -C(O)O-(CH2)2-SO2-CH3;
-C(O)NR22R23, например, -C(O)NH2, -C(O)NHCH3, -C(O)N(CH3)2, -C(O)NH-(CH2)2CH3, -C(O)NH-CH2COOH, -C(O)NH-(CH2)2-OH, -C(O)NH-(CH2)2-N(CH3)2, -C(O)NH-циклопропила, -C(O)NH-(CH2)2-имидазолила, -C(O)N(CH3)-CH2CH(CH3)2 и -C(O)N(CH3)[(CH2)2OCH3];
-NHC(O)R24, например, -NHC(O)-CH2CH3, -NHC(O)-(CH2)3CH3, -NHC(O)O-CH2CH3, -NHC(O)-CH2-OCH3, -NHC(O)-2-метоксифенил, -NHC(O)-2-хлорфенила и -NHC(O)-2-пиридина;
=O;
-NO2;
-C(CH3)=N(OH);
фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -OH, -CF3, -OCH3, -NHC(O)CH3 и фенила (например, фенила, 2-хлорфенила, 2-фторфенила, 2-гидроксифенила, 2-трифторметилфенила, 2-метоксифенила, 3-хлорфенила, 3-фторфенила, 3-метоксифенила, 3-NHC(O)CH3-фенила, 4-хлорфенила, 4-фторфенила, 4-метоксифенила, 4-бифенила, 2,5-дихлорфенила, 2,5-диметоксифенила, 2,4-дихлорфенила, 2-метокси, 5-фторфенила и 3,4-дихлорфенил);
нафталенила;
пиридинила;
пиразинила;
пиразолила, необязательно замещенного метилом;
тиофенила, необязательно замещенного метилом или галогеном (например, хлором);
фуранила и
-CH2-морфолинила.
Группа R20 выбрана из H и -C1-6алкила (например, -CH3). Группа R21 выбрана из:
H;
-C1-6алкила, например, -CH3 и -CH2CH3;
-C1-3алкилен-C6-10арила;
-C1-3алкилен-C1-9гетероарила, например, -CH2-пиридина;
-C3-7циклоалкила;
-[(CH2)2O]1-3CH3, например, -(CH2)2OCH3;
-C1-6алкилен-OC(O)R25, например, -CH2OC(O)CH3, -CH2OC(O)O-CH3, -CH2OC(O)O-CH3, -CH(CH3)OC(O)O-CH2CH3, -CH(CH3)OC(O)O-CH(CH3)2, -CH2CH(CH3)OC(O)-циклопентила, -CH2OC(O)O-циклопропила, -CH(CH3)-OC(O)-O-циклогексила, -CH2OC(O)O-циклопентила, -CH2CH(CH3)OC(O)-фенила и -CH2OC(O)O-фенила;
-C1-6алкилен-NR27R28, например, -CH2-пирролидина;
-C1-6алкилен-C(O)R33;
-C0-6алкиленморфолинила, например, -(CH2)2-морфолинила и -(CH2)3-морфолинила:
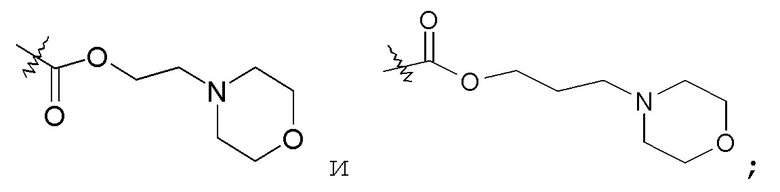
-C1-6алкилен-SO2-C1-6алкила, например, -(CH2)2-SO2-CH3;
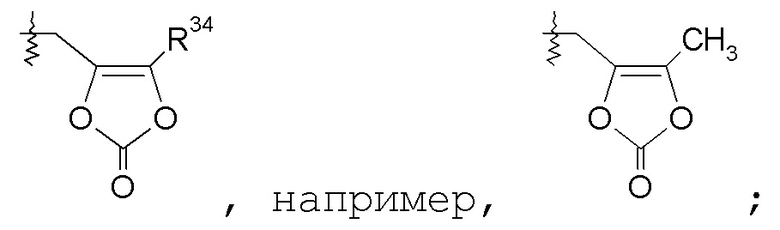

Группы R22 и R23 независимо выбраны из:
H;
-C1-6алкила, например, -CH3 и -(CH2)2CH3;
-CH2COOH;
-(CH2)2OH;
-(CH2)2OCH3;
-(CH2)2SO2NH2;
-(CH2)2N(CH3)2;
-C0-1алкилен-C3-7циклоалкила, например, циклопропила и -CH2-циклопропила; и
-(CH2)2-имидазолила.
R22 и R23 также могут быть взяты вместе с образованием насыщенного или частично ненасыщенного -C3-5гетероцикла, необязательно замещенного галогеном, -OH, -COOH или -CONH2, и необязательно содержащего в кольце атом кислорода. Насыщенные -C3-5гетероциклы включают азетидин, пирролидин, пиперидин и морфолин, так что примеры R3 группы включают:

Частично ненасыщенные -C3-5гетероциклы включают 2,5-дигидро-1H-пиррол, так что примеры R3 группы включают:

Группа R24 выбрана из:
-C1-6алкила, например, -CH2CH3 и -(CH2)3CH3;
-C0-1алкилен-O-C1-6алкила, например, -O-CH2CH3 и -CH2-OCH3;
фенила, необязательно замещенного галогеном или -OCH3, например, -2-хлорфенила или -2-метоксифенила; и
-C1-9гетероарила, например, 2-пиридина.
R25 выбран из:
-C1-6алкила, например, -CH3, -CH2CH3 и -(CH2)3CH3;
-O-C1-6алкила, например, -OCH3, -OCH2CH3 и -OCH(CH3)2;
-C3-7циклоалкила, например, циклопентила;
-O-C3-7циклоалкила, например, -O-циклопропила, -O-циклопентила и -O-циклогексила;
фенила;
-O-фенила;
-NR27R28;
-CH[CH(CH3)2]-NH2;
-CH[CH(CH3)2]-NHC(O)O-C1-6алкила, например, -CH[CH(CH3)2]-NHC(O)OCH3; и
-CH(NH2)CH2COOCH3.
R27 и R28 независимо выбраны из H, -C1-6алкила и бензила, или R27 и R28 взяты вместе как -(CH2)3-6-, -C(O)-(CH2)3- или -(CH2)2O(CH2)2-; R33 выбран из -O-C1-6алкила, -O-бензила и -NR27R28; и R34 представляет собой -C1-6алкил (например, -CH3 и -C(CH3)3) или -C0-6алкилен-C6-10арил.
Кроме того, каждая алкильная группа в R3 необязательно замещена 1-8 атомами фтора. Например, когда R3 представляет собой -C0-1алкилен-COOR21, и R21 представляет собой -C1-6алкил, R3 также может быть таким, как -COOCH(CH3)CF3, -COOCH2CF2CF3, -COOCH(CF3)2, -COO(CH2)2CF3, -COOCH(CH2F)2, -COOC(CF3)2CH3 и -COOCH(CH3)CF2CF3.
В одном варианте осуществления изобретения R3 отсутствует или выбран из H; галогена; -C0-5алкилен-OH; -NH2; -C1-6алкила; -CF3; -C3-7циклоалкила; -C0-2алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -C(O)NR22R23; -NHC(O)R24; =O; -C(CH3)=N(OH); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -OH, -CF3, -OCH3, -NHC(O)CH3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, замещенного метилом; тиофенила, замещенного метилом или галогеном; фуранила; и -CH2-морфолинила; R20 представляет собой -C1-6алкил; R21 выбран из H и -C1-6алкила; R22 выбран из H и -C1-6алкила; и R23 выбран из H, -C1-6алкила, -CH2COOH, -(CH2)2OH, -(CH2)2OCH3, -(CH2)2N(CH3)2, -C3-7циклоалкила и -(CH2)2-имидазолила; или R22 и R23 взяты вместе с образованием азетидина, пирролидина, пиперидина или морфолина, все необязательно замещены -OH или -CONH2; и R24 выбран из -C1-6алкила; -C0-1алкилен-O-C1-6алкила; фенила, замещенного галогеном или -OCH3; и пиридина. В других вариантах осуществления указанные соединения имеют формулу III.
В одном варианте осуществления изобретения R3 отсутствует или выбран из H; галогена; -C0-5алкилен-OH; -NH2; -C1-6алкила; -CF3; -C3-7циклоалкила; -C0-2алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -C(O)NR22R23; -NHC(O)R24; =O; -NO2; -C(CH3)=N(OH); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -OH, -CF3, -OCH3, -NHC(O)CH3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, необязательно замещенного метилом; тиофенила, необязательно замещенного метилом или галогеном; фуранила; и -CH2-морфолинила; и R21 представляет собой H. В других вариантах осуществления указанные соединения имеют формулу III.
В другом варианте осуществления R3 представляет собой -C0-1алкилен-COOR21, и R21 выбран из -C1-6алкила, -C1-3алкилен-C6-10арила, -C1-3алкилен-C1-9гетероарила, -C3-7циклоалкила, -[(CH2)2O]1-3CH3, -C1-6алкилен-OC(O)R25; -C1-6алкилен-NR27R28, -C1-6алкилен-C(O)R33, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила,
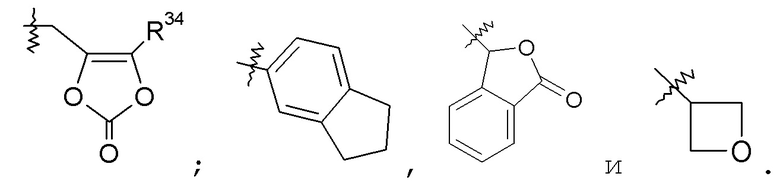
В одном аспекте изобретения указанные соединения могут найти конкретное применение в качестве пролекарств или в качестве промежуточных соединений в способах синтеза, описанных в данном описании. В других вариантах осуществления указанные соединения имеют формулу III.
Группа R4 может отсутствовать. Когда присутствует, R4 присоединен к атому углерода или азота в группе "X" и выбран из:
H;
-OH;
-C1-6алкила, например, -CH3;
-C1-2алкилен-COOR35, например, -CH2COOH и -(CH2)2-COOH;
-CH2OC(O)CH(R36)NH2, например, -CH2OC(O)CH[CH(CH3)2]NH2;
-OCH2OC(O)CH(R36)NH2, например, -OCH2OC(O)CH[CH(CH3)2]NH2;
-OCH2OC(O)CH3;
-CH2OP(O)(OH)2;
-CH2CH(OH)CH2OH;
-CH[CH(CH3)2]-NHC(O)O-C1-6алкила;
пиридинила; и
фенила или бензила, необязательно замещенных одной или более группами, выбранными из галогена, -COOR35, -OCH3, -OCF3 и -SCF3 (например, 4-хлорфенила, 3-метоксифенила, 2,4-дихлорфенила, 3,4-дихлорфенила, 2-хлора, 5-фторфенила, 3-трифторметокси, 4-хлорфенила, 3-трифторметилсульфанила, 4-хлорфенила, 2,6-дифтора, 4-хлорфенила, 2-хлорбензила, 3-хлорбензила, 4-хлорбензила, 3-карбоксибензила, 4-карбоксибензила, 3-метоксибензила, 2-хлора, 5-фторбензила, 3-хлора, 5-фторбензила, 2-фтора, 4-хлорбензила, 3-хлора, 4-фторбензила, 3-OCF3, 4-хлорбензила, 3-SCF3, 4-хлорбензила, 2,6-дифтора, 3-хлорбензила, 2,6-дифтора, 4-хлорбензила и 2,3,5,6-тетрафтора, 4-метоксибензила).
Группа R35 выбрана из:
H;
-C1-6алкила, например, -CH3 и -CH2CH3;
-C1-3алкилен-C6-10арила;
-C1-3алкилен-C1-9гетероарила, например, -CH2-пиридина;
-C3-7циклоалкила;
-[(CH2)2O]1-3CH3, например, -(CH2)2OCH3;
-C1-6алкилен-OC(O)R25, например, -CH2OC(O)CH3, -CH2OC(O)O-CH3, -CH2OC(O)O-CH3, -CH(CH3)OC(O)O-CH2CH3, -CH(CH3)OC(O)O-CH(CH3)2, -CH2CH(CH3)OC(O)-циклопентила, -CH2OC(O)O-циклопропила, -CH(CH3)-OC(O)-O-циклогексила, -CH2OC(O)O-циклопентила, -CH2CH(CH3)OC(O)-фенила и -CH2OC(O)O-фенила;
-C1-6алкилен-NR27R28, например, -CH2-пирролидина;
-C1-6алкилен-C(O)R33;
-C0-6алкиленморфолинила, например, -(CH2)2-морфолинила и -(CH2)3-морфолинила:

-C1-6алкилен-SO2-C1-6алкила, например, -(CH2)2-SO2-CH3;

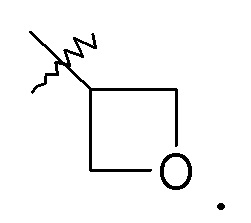
Группы R25, R27, R28, R33 и R34 определены выше. Группа R36 выбрана из H, -CH(CH3)2, фенила и бензила.
Кроме того, каждая алкильная группа в R4 необязательно замещена 1-8 атомами фтора. Например, когда R4 представляет собой -C1-2алкилен-COOR35, и R35 представляет собой -C1-6алкил, R4 также может быть таким, как -COOCH(CH3)CF3, -COOCH2CF2CF3, -COOCH(CF3)2, -COO(CH2)2CF3, -COOCH(CH2F)2, -COOC(CF3)2CH3 и -COOCH(CH3)CF2CF3.
Группа R4 также может быть взята вместе с R3 с образованием -фенилен-O-(CH2)1-3- или -фенилен-O-CH2-CHOH-CH2-. Только в целях иллюстрации, указанные варианты осуществления изобретения изображены далее с X, представляющим собой пиразол. Следует понимать, что также могут быть использованы другие группы X.
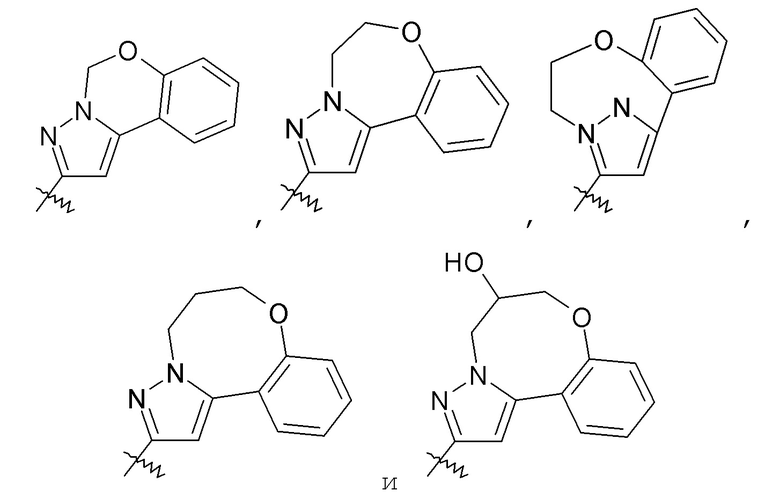
В другом конкретном варианте осуществления R4 отсутствует или выбран из H; -OH; -C1-6алкила; -C1-2алкилен-COOR35; -CH2OC(O)CH(R36)NH2; -CH2CH(OH)CH2OH; пиридинила; фенила, необязательно замещенного одной группой галогена; и бензила, необязательно замещенного одной или более группами, выбранными из галогена, -COOH, -OCH3, -OCF3 и -SCF3; R35 представляет собой H; и R36 представляет собой -CH(CH3)2; или R3 и R4 взяты вместе с образованием -фенилен-O-(CH2)1-3- или -фенилен-O-CH2-CHOH-CH2-. В других вариантах осуществления указанные соединения имеют формулу III.
В одном варианте осуществления изобретения R4 отсутствует или выбран из H; -OH; -C1-6алкила; -C1-2алкилен-COOR35; -CH2OC(O)CH(R36)NH2, -CH2CH(OH)CH2OH; пиридинила; и фенила или бензила, необязательно замещенных одной или более группами, выбранными из галогена, -COOR35, -OCH3, -OCF3 и -SCF3; и R35 представляет собой H. В других вариантах осуществления указанные соединения имеют формулу III.
В другом варианте осуществления R4 выбран из -OCH2OC(O)CH3; -CH2OP(O)(OH)2; -C1-2алкилен-COOR35; и фенила или бензила, замещенного, по меньшей мере, одной группой -COOR35; где R35 выбран из -C1-6алкила, -C1-3алкилен-C6-10арила, -C1-3алкилен-C1-9гетероарила, -C3-7циклоалкила, -[(CH2)2O]1-3CH3, -C1-6алкилен-OC(O)R25; -C1-6алкилен-NR27R28, -C1-6алкилен-C(O)R33, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила,
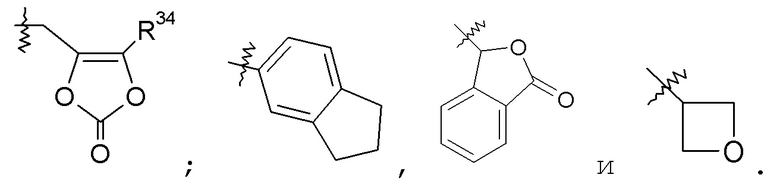
В одном аспекте изобретения указанные соединения могут найти конкретное применение в качестве пролекарств или в качестве промежуточных соединений в способах синтеза, описанных в данном описании. В других вариантах осуществления указанные соединения имеют формулу III.
Нумерация для R5 и R6 группы является следующей:
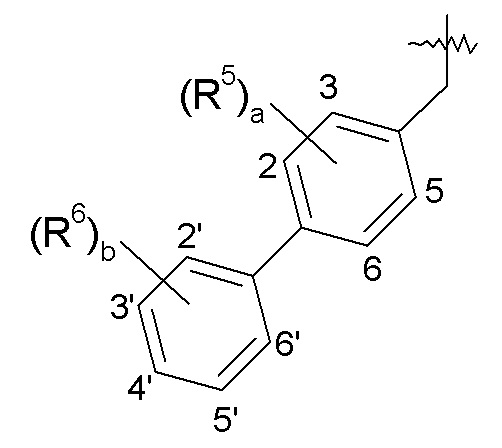
Целое число "a" равно 0 или 1. Группа R5, когда присутствует, выбрана из галогена, -CH3, -CF3 и -CN. В одном варианте осуществления изобретения a равно 0. В другом варианте осуществления a равно 1, и R5 представляет собой галоген, такой как 3-хлор или 3-фтор. Целое число "b" равно 0 или целому числу от 1 до 3. Группа R6, когда присутствует, независимо выбрана из галогена, -OH, -CH3, -OCH3 и -CF3. В одном варианте осуществления изобретения b равно 0. В другом варианте осуществления b равно 1, и R6 выбран из Cl, F, -OH, -CH3, -OCH3 и -CF3, такой как 2'-хлор, 3'-хлор, 2'-фтор, 3'-фтор, 2'-гидрокси, 3'-гидрокси, 3'-метил, 2'-метокси или 3'-трифторметил. В другом варианте осуществления b равно 1, и R6 представляет собой галоген, -CH3 или -OCH3, такой как 3'-хлор, 3'-метил или 2'-метокси. В одном варианте осуществления изобретения b равно 2, и R6 представляет собой 2'-фтор-5'-хлор, 2',5'-дихлор, 2',5'-дифтор, 2'-метил-5'-хлор, 3'-фтор-5'-хлор, 3'-гидрокси-5'-хлор, 3',5'-дихлор, 3',5'-дифтор, 2'-метокси-5'-хлор, 2'-метокси-5'-фтор, 2'-гидрокси-5'-фтор, 2'-фтор-3'-хлор, 2'-гидрокси-5'-хлор или 2'-гидрокси-3'-хлор; и в другом варианте осуществления b равно 2, и каждый R6 независимо представляет собой галоген, например, 2'-фтор-5'-хлор и 2',5'-дихлор. В другом варианте осуществления b равно 3, и каждый R6 независимо представляет собой галоген или -CH3, такой как 2'-метил-3', 5'-дихлор или 2'-фтор-3'-метил-5'-хлор. В еще одном варианте осуществления изобретения, a равно 1, и b равно 1, и R5 и R6 независимо представляют собой галоген, например, 3-хлор и 3'-хлор. В других вариантах осуществления указанные соединения имеют формулу III. Особый интерес представляют собой соединения формул:

Метиленовый линкер на бифениле необязательно замещен одним или двумя -C1-6алкильными группами или циклопропилом. Например, в одном варианте осуществления изобретения метиленовый линкер на бифениле является незамещенным; в другом варианте осуществления метиленовый линкер на бифениле замещен одной -C1-6алкильной группой (например, -CH3); и в еще одном варианте осуществления изобретения метиленовый линкер на бифениле замещен двумя -C1-6алкильными группами (например, двумя -CH3 группами); в другом варианте осуществления метиленовый линкер на бифениле замещен циклопропильной группой. Указанные варианты осуществления изобретения изображены, соответственно, следующим образом:
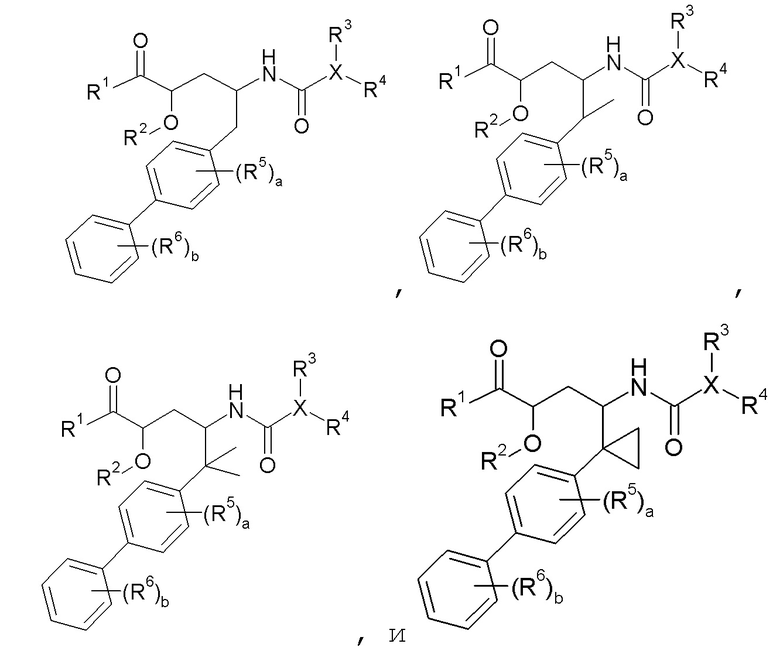
В другом варианте осуществления R7 выбран из H, -C1-8алкила, -C1-6алкилен-OC(O)R10, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила и
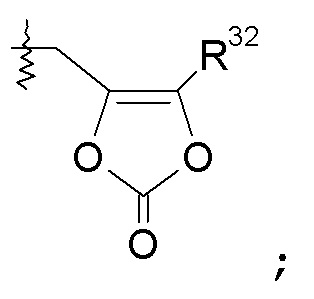
R10 представляет собой -O-C3-7циклоалкил; R8 представляет собой H; R9 представляет собой H; R2 представляет собой H; R3 отсутствует или выбран из H; галогена; -C0-5алкилен-OH; -NH2; -C1-6алкила; -CF3; -C3-7циклоалкила; -C0-2алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -C(O)NR22R23; -NHC(O)R24; =O; -C(CH3)=N(OH); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -OH, -CF3, -OCH3, -NHC(O)CH3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, замещенного метилом; тиофенила, замещенного метилом или галогеном; фуранила и -CH2-морфолинила; R20 представляет собой -C1-6алкил; R21 представляет собой H или -C1-6алкил; R22 представляет собой H или -C1-6алкил; и R23 выбран из H, -C1-6алкила, -CH2COOH, -(CH2)2OH, -(CH2)2OCH3, -(CH2)2N(CH3)2, -C3-7циклоалкила и -(CH2)2-имидазолила; или R22 и R23 взяты вместе с образованием азетидина, пирролидина, пиперидина или морфолина, все необязательно замещены -OH или -CONH2; и R24 выбран из -C1-6алкила; -C0-1алкилен-O-C1-6алкила; фенила, замещенного галогеном или -OCH3; и пиридинила; R4 отсутствует или выбран из H; -OH; -C1-6алкила; -C1-2алкилен-COOR35; -CH2OC(O)CH(R36)NH2; -CH2CH(OH)CH2OH; пиридинила; фенила, необязательно замещенного одной группой галогена; и бензила, необязательно замещенного одной или более группами, выбранными из галогена, -COOH, -OCH3, -OCF3 и -SCF3; R35 представляет собой H; и R36 представляет собой -CH(CH3)2; или R3 и R4 взяты вместе с образованием -фенилен-O-(CH2)1-3- или -фенилен-O-CH2-CHOH-CH2-; a равно 0; или a равно 1, и R5 представляет собой 3-хлор; b равно 0; или b равно 1, и R6 представляет собой 3'-хлор, 3'-метил или 2'-метокси; или b равно 2, и R6 представляет собой 2'-фтор-5'-хлор, 2',5'-дихлор, 2'-метил-5'-хлор или 3'-хлор-5'-гидрокси; и метиленовый линкер на бифениле необязательно замещен 2 метильными группами. В одном варианте осуществления изобретения X выбран из пиразола, триазола, бензотриазола, фурана, тетразола, пиразина, тиофена, оксазола, изоксазола, тиазола, оксадиазола, пиридазина, пиридина, пиримидина, бензоксазола, пиридилимидазола и пиридилтриазола.
В еще одном варианте осуществления изобретения R1 представляет собой -OR7; R2 представляет собой H; X выбран из пиразола, триазола, бензотриазола, изоксазола, пиридазина, пиримидина и пиридилтриазола; R3 выбран из H; галогена; -C0-5алкилен-OH; -C1-6алкила; -CF3; -C3-7циклоалкила; -C0-2алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -C(O)NR22R23; -NHC(O)R24; =O; -C(CH3)=N(OH); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -OH и -OCH3; пиридинила; пиразинила; и тиофенила, замещенного метилом или галогеном; R4 выбран из H; -OH; -C1-6алкила; -C1-2алкилен-COOR35; -CH2CH(OH)CH2OH; пиридинила; и фенила, необязательно замещенного одной группой галогена; или R3 и R4 взяты вместе с образованием -фенилен-O-(CH2)1-3-; a равно 0; или a равно 1, и R5 представляет собой 3-хлор; b равно 0; или b равно 1, и R6 представляет собой 3'-хлор, 3'-метил или 2'-метокси; или b равно 2, и R6 представляет собой 2'-фтор-5'-хлор, 2',5'-дихлор, 2'-метил-5'-хлор или 3'-хлор-5'-гидрокси; R20 представляет собой -C1-6алкил; R21 представляет собой H; R22 выбран из H и -C1-6алкила; и R23 выбран из -C1-6алкила, -(CH2)2OCH3 и -C3-7циклоалкила; или R22 и R23 взяты вместе с образованием азетидина, пирролидина или пиперидина, все необязательно замещены -OH или -CONH2; R24 представляет собой фенил, замещенный галогеном или -OCH3; R35 представляет собой H; метиленовый линкер на бифениле необязательно замещен 2 метильными группами; и R7 имеет значения, указанные для формулы I.
Конкретная группа соединений формулы I является такой, которая описана в предварительной заявке США №61/423180, поданной 15 декабря, 2010. Данная группа включает соединения формулы II:
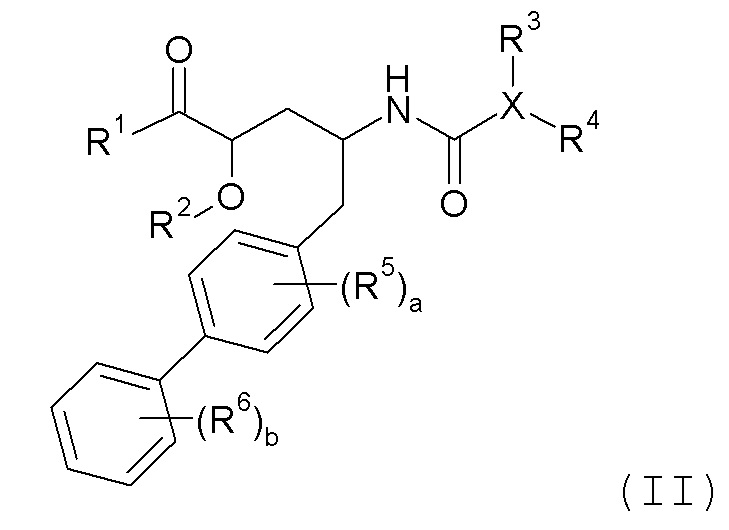
где R1 выбран из -OR7 и -NR8R9; R7 выбран из H; -C1-6алкила; -C1-3алкилен-C6-10арила; -C1-3алкилен-C1-9гетероарила; -C3-7циклоалкила; -(CH2)2OCH3; -C1-6алкилен-OC(O)R10; -CH2-пиридина; -CH2-пирролидина; -C0-6алкиленморфолина; -C1-6алкилен-SO2-C1-6алкила;

где R10 выбран из -C1-6алкила, -O-C1-6алкила, -C3-7циклоалкила, -O-C3-7циклоалкила, фенила, -O-фенила, -NR12R13 и -CH(NH2)CH2COOCH3; и R12 и R13 независимо выбраны из H, -C1-6алкила и бензила, или R12 и R13 взяты вместе как -(CH2)3-6-; R8 выбран из H; -OH; -OC(O)R14; -CH2COOH; -O-бензила; пиридила и -OC(S)NR15R16; где R14 выбран из H, -C1-6алкила, -C6-10арила, -OCH2-C6-10арила, -CH2O-C6-10арила и -NR15R16; и R15 и R16 независимо выбраны из H и -C1-4алкила; R9 выбран из H; -C1-6алкила и -C(O)R17; где R17 выбран из H; -C1-6алкила; -C3-7циклоалкила; -C6-10арила и -C1-9гетероарила; R2 представляет собой H или, взятый вместе с R1, образует -OCHR18R19- или -NHC(O)-; где R18 и R19 независимо выбраны из H, -C1-6алкила и -O-C3-7циклоалкила, или R18 и R19 взяты вместе с образованием =O; X представляет собой -C1-9 гетероарил или частично ненасыщенный -C3-5гетероцикл; R3 отсутствует или выбран из H; галогена; -C0-5алкилен-OH; -NH2; -C1-6алкила; -C3-7циклоалкила; -C0-1алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-C(O)OR21; -C(O)NR22R23; -NHC(O)R24; фенила, необязательно замещенного одной группой, выбранной из галогена, -CF3, -OCH3, -NHC(O)CH3 и фенила; нафтила; пиридина; пиразина; пиразола, необязательно замещенного метилом; тиофена, необязательно замещенного метилом; и фурана; и R3, когда присутствует, присоединен к атому углерода, R20 выбран из H и -C1-6алкила; R21 выбран из H; -C1-6алкила; -C1-3алкилен-C6-10арила; -C1-3алкилен-C1-9гетероарила; -C3-7циклоалкила; -(CH2)2OCH3; -C1-6алкилен-OC(O)R25; -CH2-пиридина; -CH2-пирролидина; -C0-6алкиленморфолина; -C1-6алкилен-SO2-C1-6алкила;
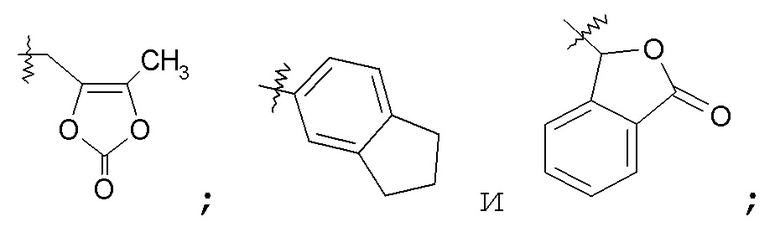
где R25 выбран из -C1-6алкила, -O-C1-6алкила, -C3-7циклоалкила, -O-C3-7циклоалкила, фенила, -O-фенила, -NR27R28 и -CH(NH2)CH2COOCH3; и R27 и R28 независимо выбраны из H, -C1-6алкила и бензила, или R27 и R28 взяты вместе как -(CH2)3-6-; R22 и R23 независимо выбраны из H; -C1-6алкила; -CH2COOH; -(CH2)2OH; -(CH2)2OCH3; -(CH2)2SO2NH2; -(CH2)2N(CH3)2; -C3-7циклоалкила и -(CH2)2-имидазола; или R22 и R23 взяты вместе с образованием насыщенного или частично ненасыщенного -C3-5гетероцикла, необязательно замещенного -OH, -COOH или -CONH2; и необязательно содержащего в кольце атом кислорода; R24 выбран из -C1-6алкила; -O-C1-6алкила; -CH2-O-C1-6алкила; фенила, замещенного -OCH3; и пиридина; R4 выбран из H; -C1-6алкила; фенила или бензила, замещенного одной или более группами, выбранными из галогена, -COOH, -OCH3, -OCF3 и -SCF3; и R4 присоединен к атому углерода или азота; a равно 0 или 1; R5 представляет собой галоген или -CF3; и b равно 0 или 1; R6 представляет собой галоген; или его фармацевтически приемлемую соль.
Кроме того, конкретные соединения формулы I, представляющие интерес, включают такие, которые приведены в примерах далее, а также их фармацевтически приемлемые соли.
Общие способы синтеза
Соединения по изобретению могут быть получены из легкодоступных исходных продуктов с использованием следующих общих методов, способов, представленных в примерах, или с использованием других способов, реагентов и исходных продуктов, которые известны специалисту в данной области. Хотя следующие способы могут иллюстрировать конкретный вариант осуществления изобретения, следует понимать, что другие варианты осуществления изобретения могут быть получены подобным образом с использованием тех же самых или подобных методов или с использованием других методов, реагентов и исходных продуктов, известных специалистам в данной области. Следует понимать также, что, когда указаны обычные или предпочтительные условия способа (например, температура реакции, время, мольные соотношения реагентов, растворители, давление и т.д.), также могут быть использованы другие условия способа, если не указано иное. В некоторых случаях, реакции можно проводить при комнатной температуре и какого-либо фактического измерения температуры не было предпринято. Следует понимать, что комнатная температура может означать температуру в диапазоне, обычно связанном с температурой окружающей среды в лабораторных условиях, и обычно находится в интервале от около 18°C до около 30°C. В других случаях, реакции можно осуществлять при комнатной температуре, и температуру фактически измеряли и регистрировали. Несмотря на то, что оптимальные условия реакции будут обычно меняться в зависимости от различных параметров реакции, таких как конкретные реагенты, растворители и используемые величины, специалист в данной области может легко определить подходящие условия реакции, используя стандартные методы оптимизации.
Кроме того, как будет понятно специалисту в данной области, могут быть необходимыми или желательными обычные защитные группы для предохранения некоторых функциональных групп от нежелательных реакций. Выбор подходящих защитных групп для конкретной функциональной группы, а также подходящих условий и реагентов для введения и удаления защиты у таких функциональных групп хорошо известны в данной области. Могут быть использованы защитные группы, иные, чем те, которые проиллюстрированы в способах, описанных в данном описании, если желательно. Например, разнообразные защитные группы и их введение и удаление описаны в обзоре T. W. Greene and G. M. Wuts, Protecting Groups in Organic Synthesis, Fourth Edition, Wiley, New York, 2006, и в цитированных там ссылках.
Карбоксизащитные группы являются подходящими для предотвращения нежелательных реакций по карбоксигруппе, и примеры включают, но, не ограничиваясь ими, метил, этил, трет-бутил, бензил (Bn), п-метоксибензил (PMB), 9-флуоренилметил (Fm), триметилсилил (TMS), трет-бутилдиметилсилил (TBDMS), дифенилметил (бензгидрил, DPM) и тому подобное. Аминозащитные группы являются подходящими для предотвращения нежелательных реакций по аминогруппе, и примеры включают, но, не ограничиваясь ими, трет-бутоксикарбонил (BOC), тритил (Tr), бензилоксикарбонил (Cbz), 9-флуоренилметоксикарбонил (Fmoc), формил, триметилсилил (TMS), трет-бутилдиметилсилил (TBDMS) и тому подобное. Гидроксилзащитные группы являются подходящими для предотвращения нежелательных реакций по гидроксильной группе, и примеры включают, но, не ограничиваясь ими, C1-6алкилы, силильные группы, включая триС1-6алкилсилильные группы, такие как триметилсилил (TMS), триэтилсилил (TES) и трет-бутилдиметилсилил (TBDMS); сложные эфиры (ацильные группы), включая C1-6алканоильные группы, такие как формил, ацетил и пивалоил, и ароматические ацильные группы, такие как бензоил; арилметильные группы, такие как бензил (Bn), п-метоксибензил (PMB), 9-флуоренилметил (Fm) и дифенилметил (бензгидрил, DPM); и тому подобное.
Для удаления защитных групп используются стандартные методики снятия защиты и реагенты, и они могут изменяться в зависимости от используемой группы. Например, когда карбоксизащитной группой является метил, обычно используется гидроксид натрия или лития, когда карбоксизащитной группой является этил или трет-бутил, обычно используется кислота, такая как ТФУ или HCl, и когда карбоксизащитной группой является бензил, может быть использован H2/Pd/C. BOC аминозащитную группу можно удалить с помощью кислотного реагента, такого как ТФУ в DCM или HCl в 1,4-диоксане, и Cbz аминозащитную группу можно удалить, используя условия каталитического гидрирования, такие как H2 (1 атм) и 10% Pd/C в спиртовом растворителе ("H2/Pd/C"). H2/Pd/C обычно используется, когда гидроксилзащитной группой является бензил, и NaOH обычно используется, когда гидроксилзащитной группой является ацильная группа.
Подходящие основания для использования в данных схемах включают, в качестве иллюстрации, но не ограничения, карбонат калия, карбонат кальция, карбонат натрия, триэтиламин, пиридин, 1,8-диазабицикло[5,4,0]ундец-7-ен (DBU), N,N-диизопропилэтиламин (DIPEA), 4-метилморфолин, гидроксид натрия, гидроксид калия, трет-бутоксид калия и гидриды металлов.
Подходящие инертные разбавители или растворители для использования в данных схемах включают, в качестве иллюстрации, но не ограничения, тетрагидрофуран (ТГФ), ацетонитрил (MeCN), N,N-диметилформамид (ДМФ), N,N-диметилацетамид (DMA), диметилсульфоксид (ДМСО), толуол, дихлорметан (DCM), хлороформ (CHCl3), тетрахлорид углерода (CCl4), 1,4-диоксан, метанол, этанол, воду и тому подобное.
Подходящие агенты сочетания карбоновая кислота/амин включают гексафторфосфат бензотриазол-1-илокситрис(диметиламино)фосфония (BOP), гексафторфосфат бензотриазол-1-илокситрипирролидинофосфония (PyBOP), гексафторфосфат N,N,N',N'-тетраметил-O-(7-азабензотриазол-1-ил)урония (HATU), 1,3-дициклогексилкарбодиимид (DCC), N-(3-диметиламинопропил)-N'-этилкарбодиимид (EDCI), карбонилдиимидазол (CDI), 1-гидроксибензотриазол (HOBt) и тому подобное. Реакции сочетания проводят в инертном разбавителе в присутствии основания, такого как DIPEA, и осуществляют в обычных условиях образования амидной связи.
Все реакции обычно осуществляют при температуре в интервале от около -78°C до 100°C, например, при комнатной температуре. Реакции могут быть отслежены с использованием тонкослойной хроматографии (ТСХ), высокоэффективной жидкостной хроматографии (ВЭЖХ) и/или ЖХМС до полного завершения реакции. Реакции могут завершаться за минуты или могут потребоваться часы, обычно от 1-2 часов и до 48 часов. После завершения реакции полученную смесь или продукт реакции затем могут быть подвергнуты обработке с целью получения желаемого продукта. Например, полученная смесь или продукт реакции могут быть подвергнуты одной или нескольким из следующих процедур: концентрирование или распределение (например, между EtOAc и водой или между 5% ТГФ в EtOAc и 1M фосфорной кислотой); экстракция (например, с помощью EtOAc, CHCl3, DCM, хлороформа); промывка (например, насыщенным водным раствором NaCl, насыщенным водным раствором NaHCO3, Na2CO3 (5%), CHCl3 или 1M NaOH); сушка (например, над MgSO4, над Na2SO4 или в вакууме); фильтрование; кристаллизация (например, из EtOAc и гексана); упаривание (например, в вакууме); и/или очистка (например, хроматография на силикагеле, флэш-хроматография, препаративная ВЭЖХ, ВЭЖХ с обращенной фазой или кристаллизация).
Соединения формулы I, а также их соли, могут быть получены как показано на схеме I:
Схема I
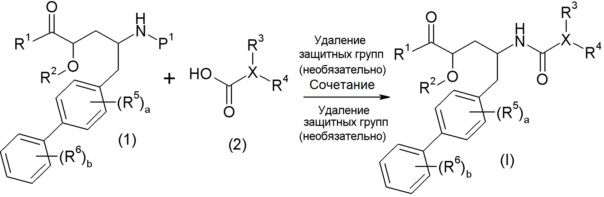
Способ включает стадию сочетания соединения 1 с соединением 2, где R1-R6, X, a и b имеют значения, указанные для формулы I, и P1 представляет собой H или подходящую аминозащитную группу, примеры которой включают трет-бутоксикарбонил, тритил, бензилоксикарбонил, 9-флуоренилметоксикарбонил, формил, триметилсилил и трет-бутилдиметилсилил. Когда P1 представляет собой аминозащитную группу, способ далее включает удаление защиты у соединения формулы 1, до или в процессе осуществления стадии сочетания.
В случаях, когда R1 представляет собой группу, такую как -OCH3 или -OCH2CH3, стадия сочетания может следовать за стадией удаления защиты, с получением соединения формулы I, где R1 представляет собой группу, такую как -OH. Таким образом, один способ получения соединения по изобретению включает сочетание соединения 1 и 2 с необязательной стадией удаления защиты, с образованием соединения формулы I или его фармацевтически приемлемой соли.
Способы получения соединения 1 описаны в примерах. Соединение 2 обычно является коммерчески доступным или может быть получено с использованием способов, которые известны в данной области.
Соединения формулы I, а также их соли, также могут быть получены, как показано на схеме II:
Схема II
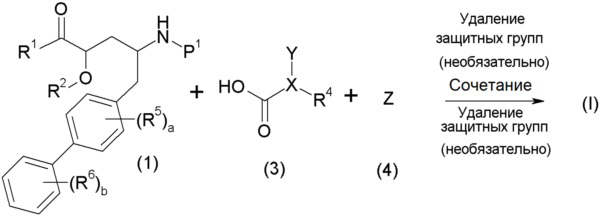
На первой стадии, соединение 1 подвергают сочетанию с соединением 3 и соединение 3 подвергают сочетанию с соединением 4, где Y и Z непосредственно взаимодействуют, образуя группу R3. Например, когда R3 представляет собой -C(O)NR22R23, Y представляет собой -COOH, и Z представляет собой HNR22R23. Альтернативно, соединение 3 сначала подвергают сочетанию с соединением 4, и полученное соединение затем подвергают сочетанию с соединением 1. Как и на схеме I, в случаях, когда R1 представляет собой группу, такую как -OCH3 или -OCH2CH3, стадия сочетания может сопровождаться стадией удаления защиты, с получением соединения формулы I, где R1 представляет собой группу, такую как -OH. Таким образом, один способ получения соединения по изобретению включает сочетание соединения 1, 2 и 3 с необязательной стадией удаления защиты, с образованием соединения формулы I или его фармацевтически приемлемой соли.
Соединения 3 и 4 обычно являются коммерчески доступными или могут быть получены с использованием способов, которые известны в данной области.
Соединения формулы I, а также их соли, также могут быть получены, как показано на схеме III: {На основе примера 9}
Схема III

Вновь, как и на схемах I и II, реакция представляет собой обычную реакцию сочетания между соединением формулы I, где R1 представляет собой -OH, и соединением 5, с получением соединения формулы I, где R1 представляет собой -NR8R9.
Некоторые промежуточные соединения, описанные в данном описании, как полагают, являются новыми и, в соответствии с этим, такие соединения являются следующим аспектом настоящего изобретения, включая, например, соединения формулы 1 или их соли:
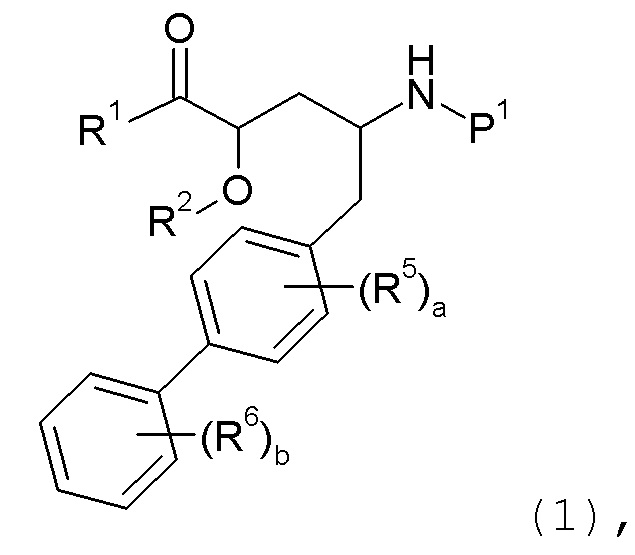
где P1 представляет собой H или аминозащитную группу, выбранную из трет-бутоксикарбонила, тритила, бензилоксикарбонила, 9-флуоренилметоксикарбонила, формила, триметилсилила и трет-бутилдиметилсилила; и R1, R2, R5, R6, a и b имеют значения, указанные для формулы I. Другое промежуточное соединение по изобретению или его соль имеет формулу 6:

где R1P выбран из -O-P3, -NHP2 и -NH(O-P4); где P2 представляет собой аминозащитную группу, выбранную из трет-бутоксикарбонила, тритила, бензилоксикарбонила, 9-флуоренилметоксикарбонила, формила, триметилсилила и трет-бутилдиметилсилила; P3 представляет собой карбоксизащитную группу, выбранную из метила, этила, трет-бутила, бензила, п-метоксибензила, 9-флуоренилметила, триметилсилила, трет-бутилдиметилсилила и дифенилметила; P4 представляет собой гидроксилзащитную группу, выбранную из -C1-6алкила, триС1-6алкилсилила, -C1-6алканоила, бензоила, бензила, п-метоксибензила, 9-флуоренилметила и дифенилметила; и R2, R3, R4, R5, R6, a, b и X имеют значения, указанные для формулы I. Другое промежуточное соединение по изобретению или его соль имеет формулу 7:
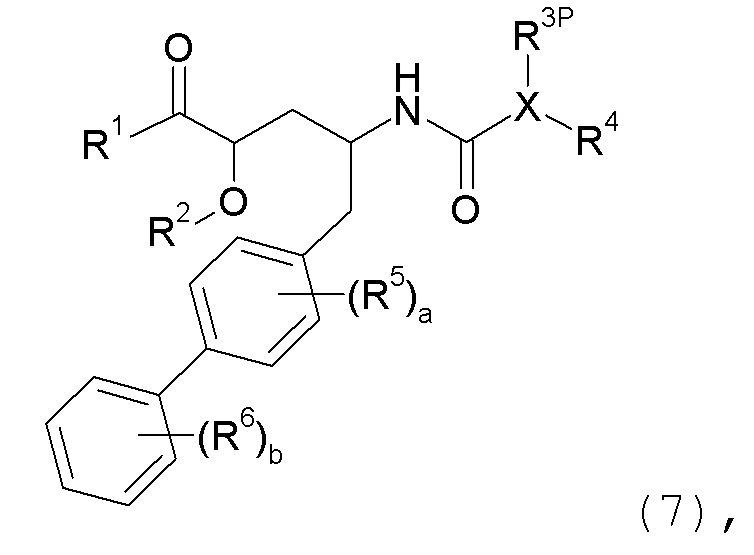
где R3P выбран из -C0-5алкилен-O-P4, -C0-1алкилен-COO-P3 и фенила, замещенного -O-P4; P3 представляет собой карбоксизащитную группу, выбранную из метила, этила, трет-бутила, бензила, п-метоксибензила, 9-флуоренилметила, триметилсилила, трет-бутилдиметилсилила и дифенилметила; P4 представляет собой гидроксилзащитную группу, выбранную из -C1-6алкила, триС1-6алкилсилила, -C1-6алканоила, бензоила, бензила, п-метоксибензила, 9-флуоренилметила и дифенилметила; и R1, R2, R4, R5, R6, a, b и X имеют значения, указанные для формулы I. Еще одно промежуточное соединение по изобретению или его соль имеет формулу 8:

где R4P выбран из -O-P4; -C1-2алкилен-COO-P3; и фенила или бензила, замещенного -COO-P3; P3 представляет собой карбоксизащитную группу, выбранную из метила, этила, трет-бутила, бензила, п-метоксибензила, 9-флуоренилметила, триметилсилила, трет-бутилдиметилсилила и дифенилметила; P4 представляет собой гидроксилзащитную группу, выбранную из -C1-6алкила, триС1-6алкилсилила, -C1-6алканоила, бензоила, бензила, п-метоксибензила, 9-флуоренилметила и дифенилметила; и R1, R2, R3, R5, R6, a, b и X имеют значения, указанные для формулы I. Еще одно промежуточное соединение по изобретению или их соль имеет формулу 9:
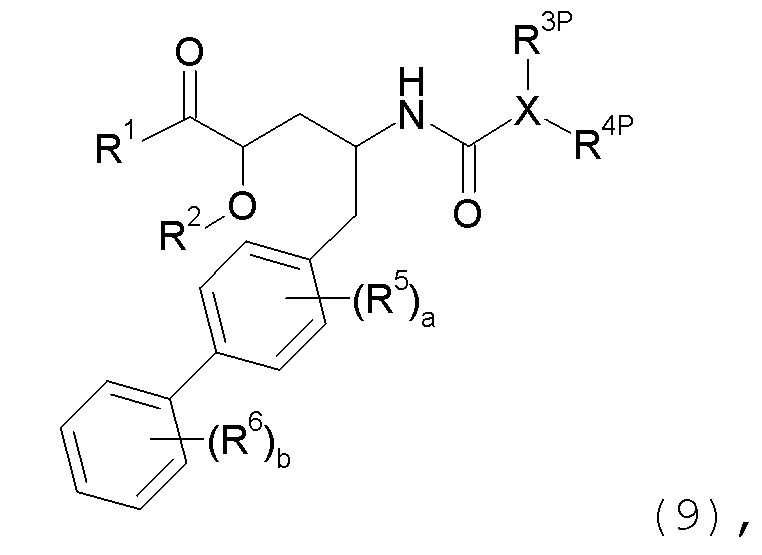
где R3P выбран из -C0-5алкилен-O-P4, -C0-1алкилен-COO-P3 и фенила, замещенного -O-P4; R4P выбран из -O-P4; -C1-2алкилен-COO-P3; и фенила или бензила, замещенного -COO-P3; P3 представляет собой карбоксизащитную группу, выбранную из метила, этила, трет-бутила, бензила, п-метоксибензила, 9-флуоренилметила, триметилсилила, трет-бутилдиметилсилила и дифенилметила; P4 представляет собой гидроксилзащитную группу, выбранную из -C1-6алкила, триС1-6алкилсилила, -C1-6алканоила, бензоила, бензила, п-метоксибензила, 9-флуоренилметила и дифенилметила; и R1, R2, R5, R6, a, b и X имеют значения, указанные для формулы I. Таким образом, другой способ получения соединения по изобретению включает удаление защиты у соединений формулы 1, 6, 7, 8, 9 или их солей.
Дополнительные подробности, касающиеся конкретных условий реакций и других способов получения иллюстративных соединений по изобретению или их промежуточных соединений, описаны в примерах, изложенных ниже.
Полезность
Соединения по изобретению обладают ингибирующей неприлизин (NEP) активностью, то есть, соединения способны ингибировать каталитическую активность фермента. В другом варианте осуществления соединения не демонстрируют значительную ингибирующую активность ангиотензин-превращающего фермента. Одним из показателей способности соединения ингибировать активность NEP является константа ингибирования (pKi). Значение pKi представляет собой отрицательный логарифм с основанием 10 константы диссоциации (Ki), который обычно представляется в молярных единицах. Особый интерес представляют собой соединения по изобретению, которые имеют pKi при NEP больше или равный 6,0, особенно такие, которые имеют pKi больше или равный 7,0, и даже более конкретно такие, которые имеют pKi больше или равный 8,0. В одном варианте осуществления изобретения представляющие интерес соединения имеют pKi в интервале 6,0-6,9; в другом варианте осуществления изобретения представляющие интерес соединения имеют pKi в интервале 7,0-7,9; в еще одном варианте осуществления изобретения, представляющие интерес соединения имеют pKi в интервале 8,0-8,9; и в еще одном варианте осуществления изобретения, представляющие интерес соединения имеют pKi в интервале от более чем или равный 9,0. Такие значения могут быть определены методами, которые хорошо известны в данной области, а также с помощью анализов, описанных в данном описании.
Другой мерой способности соединения ингибировать активность NEP является наблюдаемая константа ингибирования (IC50), которая является молярной концентрацией соединения, которая приводит к половине максимального ингибирования преобразования субстрата с помощью фермента NEP. Значение pIC50 является отрицательным логарифмом с основанием 10 IC50. Соединения по изобретению, которые представляют особый интерес, включают такие, которые проявляют pIC50 для NEP больше или равный около 5,0. Представляющие интерес соединения также включают такие, которые имеют pIC50 для NEP≥ около 6,0 или pIC50 для NEP≥ около 7,0. В другом варианте осуществления представляющие интерес соединения имеют pIC50 для NEP в интервале приблизительно 7,0-11,0; и в другом варианте осуществления в интервале приблизительно 8,0-11,0, такое как в интервале приблизительно 8,0-10,0.
Следует отметить, что в некоторых случаях соединения по изобретению могут обладать слабой ингибирующей NEP активностью. В таких случаях, специалистам в данной области техники будет понятно, что указанные соединения по-прежнему обладают полезностью в качестве исследовательских инструментов.
Примеры анализов для определения свойств соединений по изобретению, таких как ингибирующая активность NEP, описаны в примерах и включают в качестве иллюстрации, но не ограничения, анализы, в которых определяют ингибирование NEP (описано в анализе 1). Используемые вторичные анализы включают анализы по определению ингибирования ACE (также описано в анализе 1) и ингибирования аминопептидазы P (APP) (описано Sulpizio et al. (2005) JPET 315:1306-1313). Фармакодинамический анализ для оценки in vivo ингибирующей способности ACE и NEP у крыс под наркозом описан в анализе 2 (см. также Seymour et al. (1985) Hypertension 7 (Suppl I): I-35-I-42 и Wigle et al. (1992) Can. J. Physiol. Pharmacol. 70:1525-1528), где ингибирование ACE определяется как процент ингибирования ответа артериального давления на ангиотензин I, и ингибирование NEP определяется как повышение экскреции циклического гуанозин-3',5'-монофосфата (cGMP).
Существует много анализов in vivo, которые могут быть использованы для дальнейшего определения полезности соединений по изобретению. Моделью на находящихся в сознании крысах со спонтанной гипертензией (SHR) является ренин зависимая модель гипертензии, и описана в анализе 3. См. также Intengan et al. (1999) Circulation 100(22):2267-2275 и Badyal et al. (2003) Indian Journal of Pharmacology 35:349-362. Модель на находящихся в сознании крысах при использовании ацетата дезоксикортикостерона (DOCA-соль) является зависимой от объема моделью гипертензии, которая используется для измерения активности NEP и описана в анализе 4. См. также Trapani et al. (1989) J. Cardiovasc. Pharmacol. 14:419-424, Intengan et al. (1999) Hypertension 34(4):907-913, и Badyal et al. (2003) supra). Модель DOCA-соль является особенно полезной для оценки способности исследуемого соединения понижать кровяное давление, а также для определения способности исследуемого соединения предотвращать или задерживать повышение артериального давления. Чувствительная к Dahl соли (DSS) модель гипертензии на крысах представляет собой модель гипертензии, которая чувствительна к потребляемой соли (NaCl) и описана в анализе 5. См. также Rapp (1982) Hypertension 4:753-763. Модель монокроталиновой формы артериально-легочной гипертензии у крыс описанная, например, в работе Kato et al. (2008) J. Cardiovasc. Pharmacol. 51(1):18-23, является надежным показателем клинической эффективности при лечении артериальной легочной гипертензии. Модели сердечной недостаточности на животных включают DSS модель на крысах с сердечной недостаточностью и модель с коронарно-легочной фистулой (анастомоз AV), последняя из которых описана, например, в работе Norling et al. (1996) J. Amer. Soc. Nephrol. 7:1038-1044. Для определения анальгезирующих свойств соединений по изобретению могут быть использованы другие модели на животных, такие как тест горячей пластины, тест отдергивания хвоста и формалиновый тест, а также модель нейропатической боли с перевязкой спинального нерва (SNL). См., например, Malmberg et al. (1999) Current Protocols in Neuroscience 8.9.1-8.9.15.
Предполагается, что соединения по изобретению ингибируют фермент NEP в анализах, перечисленных выше, или анализах подобной природы. Таким образом, вышеуказанные анализы могут быть использованы при определении терапевтической полезности соединений по изобретению, например, их полезность в качестве антигипертензивных агентов или антидиарейных агентов. Другие свойства и полезность соединений по изобретению могут быть продемонстрированы с использованием других in vitro и in vivo анализов, хорошо известных специалистам в данной области. Соединения формулы I могут быть активными лекарственными средствами, а также пролекарствами. Таким образом, когда обсуждается активность соединений по изобретению, понятно, что такие пролекарства могут не проявлять предполагаемую активность в анализе, но ожидается, что они проявят желаемую активность при метаболизме.
Предполагается, что соединения по изобретению могут быть использованы для лечения и/или профилактики медицинских состояний, реагирующих на ингибирование NEP. Таким образом, предполагается, что пациенты, страдающие заболеванием или нарушением, на которое можно благотворно воздействовать путем ингибирования фермента NEP или повышением уровней его пептидных субстратов, могут быть подвергнуты лечению путем введения терапевтически эффективного количества соединения по изобретению. Например, предполагается, что путем ингибирования NEP соединения потенцируют биологические эффекты эндогенных пептидов, которые метаболизируются с помощью NEP, таких как натрийуретические пептиды, бомбезин, брадикинины, кальцитонин, эндотелины, энкефалины, нейротензин, субстанция Р и вазоактивный интестинальный пептид. Таким образом, ожидается, что указанные соединения обладают другими физиологическими действиями, например, на почки, центральную нервную систему, желудочно-кишечную и репродуктивные системы.
Согласно одному варианту осуществления изобретения, пациенты, страдающие заболеванием или нарушением, на которое благотворно воздействует фермент NEP, могут быть подвергнуты лечению путем введения соединения по изобретению, которое находится в своей активной форме, то есть, соединения формулы I, где R1 выбран из -OR7 и -NR8R9, R7 представляет собой H, R8 представляет собой H или -OH, R9 представляет собой H, и R2-R6, a, b и X имеют значения, указанные для формулы I.
В другом варианте осуществления пациентов подвергают лечению путем введения соединения, которое метаболизируется in vitro с образованием соединения формулы I, где R1 выбран из -OR7 и -NR8R9, R7 представляет собой H, R8 представляет собой H или -OH, R9 представляет собой H, и R2-R6, a, b и X имеют значения, указанные для формулы I. В примерах варианта осуществления изобретения пациентов подвергают лечению путем введения соединения, которое метаболизируется in vitro с образованием соединения формулы III, где R1 представляет собой -OR7, и R7 представляет собой H.
В другом варианте осуществления пациентов подвергают лечению путем введения соединения по изобретению, которое представлено в форме его пролекарства по группе R1, то есть, соединения формулы I где:
R1 представляет собой -OR7; и R7 выбран из -C1-8алкила, -C1-3алкилен-C6-10арила, -C1-3алкилен-C1-9гетероарила, -C3-7циклоалкила, -[(CH2)2O]1-3CH3, -C1-6алкилен-OC(O)R10, -C1-6алкилен-NR12R13, -C1-6алкилен-C(O)R31, -C0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила,

R1 представляет собой -NR8R9; R8 выбран из -OC(O)R14, -CH2COOH, -O-бензила, пиридила и -OC(S)NR15R16; и R9 представляет собой H; или
R1 представляет собой -NR8R9; R8 выбран из -OC(O)R14, -CH2COOH, -O-бензила, пиридила и -OC(S)NR15R16; и R9 представляет собой -C1-6алкил или -C(O)R17;
R1 представляет собой -NR8R9; R8 выбран из H или -OH; и R9 выбран из -C1-6алкила и -C(O)R17;
R1 представляет собой -OR7, и R2, взятый вместе с R7, образует -CR18R19-; или
R1 представляет собой -NR8R9, и R2, взятый вместе с R8, образует -C(O)-;
и R10, R12-R17, R31, R32, R3-R6, a, b и X имеют значения, указанные для формулы I. В примерах варианта осуществления изобретения пациентов подвергают лечению путем введения соединения по изобретению, которое представлено в форме его пролекарства по группе R1 и имеет формулу III.
Сердечно-сосудистые заболевания
Предполагается, что соединения по изобретению могут быть использованы для лечения и/или предотвращения медицинских состояний, таких как сердечно-сосудистые заболевания, путем усиления действия вазоактивных пептидов, подобных натрийуретическим пептидам и брадикинину. См., например, Roques et al. (1993) Pharmacol. Rev. 45:87-146 и Dempsey et al. (2009) Amer. J. of Pathology 174(3):782-796. Представляющие интерес сердечно-сосудистые заболевания включают гипертензию и сердечную недостаточность. Гипертензия включает, в качестве иллюстрации, но не ограничения: первичную гипертензию, на которую ссылаются также как на эссенциальную гипертензию или идиопатическую гипертензию; вторичную гипертензию; гипертензию с сопутствующей болезнью почек; сильную гипертензию с сопутствующей болезнью почек или без сопутствующей болезни почек; легочную гипертензию, включая легочную артериальную гипертензию; и резистентную гипертензию. Сердечная недостаточность включает, в качестве иллюстрации, но не ограничения: застойную сердечную недостаточность, острую сердечную недостаточность, хроническую сердечную недостаточность, например, со сниженной фракцией выброса левого желудочка (также называемой систолической сердечной недостаточностью) или с сохраненной фракцией выброса левого желудочка (также называемой диастолической сердечной недостаточностью); и острую и хроническую декомпенсированную сердечную недостаточность, с сопутствующей болезнью почек или без сопутствующей болезни почек. Таким образом, один вариант осуществления изобретения относится к способу лечения гипертензии, в частности, первичной гипертензии или легочной артериальной гипертензии, включающему введение пациенту терапевтически эффективного количества соединения по изобретению.
При лечении первичной гипертензии, терапевтически эффективное количество обычно является количеством, которое достаточно для понижения кровяного давления у пациента. Это включает как слабую до средней силы гипертензию, так и сильную гипертензию. При применении для лечения гипертензии, соединение может быть введено в комбинации с другими терапевтическими агентами, такими как антагонисты альдостерона, ингибиторы альдостеронсинтазы, ингибиторы ангиотензин-превращающего фермента и ингибиторы двойного действия ангиотензин-превращающий фермента/неприлизина, активаторы и стимуляторы ангиотензин-превращающего фермента 2 (ACE2), ангиотензин-II вакцины, антидиабетические агенты, антилипидные агенты, антитромботические агенты, антагонисты рецептора АТ1 и ингибиторы двойного действия антагониста рецептора АТ1/неприлизина, антагонисты β1-адренергического рецептора, антагонист β-адренергического рецептора/антагонисты α1-рецептора двойного действия, блокаторы кальциевых каналов, диуретики, антагонисты эндотелинового рецептора, ингибиторы эндотелин превращающего фермента, ингибиторы неприлизина, натрийуретические пептиды и их аналоги, антагонисты очистки рецептора натрийуретического пептида, доноры оксида азота, нестероидные противовоспалительные агенты, ингибиторы фосфодиэстеразы (в частности, ингибиторы PDE-V), агонисты рецептора простагландина, ингибиторы ренина, стимуляторы и активаторы растворимой гуанилатциклазы и их комбинациями. В одном конкретном варианте осуществления изобретения, соединение по изобретению объединено с антагонистом рецептора AT1, блокатором кальциевых каналов, диуретиком или их сочетанием, и используется для лечения первичной гипертензии. В другом конкретном варианте осуществления изобретения соединение по изобретению объединено с антагонистом AT1 рецептора и используется для лечения гипертензии с сопутствующей болезнью почек. Когда оно используется для лечения резистентной гипертензии, соединение может быть введено в комбинации с другими терапевтическими агентами, такими как ингибиторы альдостеронсинтазы.
При лечении легочной артериальной гипертензии терапевтически эффективное количество обычно представляет собой такое количество, которое является достаточным для понижения легочного сосудистого сопротивления. Другими целями терапии являются улучшение толерантности к способности переносить физическую нагрузку у пациента. Например, в клинических условиях терапевтически эффективное количество может представлять собой такое количество, которое улучшает способность пациента удобно ходить в течение периода от 6 минут (покрывая дистанцию приблизительно в 20-40 метров). При лечении легочной артериальной гипертензии соединение может быть введено в комбинации с другими терапевтическими агентами, такими как антагонисты α-адренергического рецептора, антагонисты β1-адренергического рецептора, агонисты β2-адренергического рецептора, ингибиторы ангиотензин-превращающего фермента, антикоагулянты, блокаторы кальциевых каналов, диуретики, антагонисты эндотелинового рецептора, ингибиторы PDE-V, аналоги простагландина, ингибиторы селективного серотонинового ответа и их комбинациями. В одном конкретном варианте осуществления изобретения соединение по изобретению объединено с ингибитором PDE-V или ингибитором селективного серотонинового ответа и используется для лечения легочной артериальной гипертензии.
Другой вариант осуществления изобретения относится к способу лечения сердечной недостаточности, в частности застойной сердечной недостаточности (включая как систолическую, так и диастолическую застойную сердечную недостаточность), включающему введение пациенту терапевтически эффективного количества соединения по изобретению. Обычно, терапевтически эффективным количеством является такое количество, которое достаточно для понижения кровяного давления и/или улучшения функции почек. В клинических условиях терапевтически эффективным количеством может быть такое количество, которое является достаточным для улучшения динамики кровообращения сердца, такой как, например, снижение давления заклинивания, давления в правом предсердии, давления наполнения и сосудистое сопротивление. В одном варианте осуществления изобретения соединение вводят в виде внутривенной лекарственной формы. При лечении сердечной недостаточности, соединение может быть введено в комбинации с другими терапевтическими агентами, такими как антагонисты аденозинового рецептора, прерыватели усиленного гликозилирования конечных продуктов, антагонисты альдостерона, антагонисты AT1 рецептора, антагонисты β1-адренергического рецептора, антагонисты β-адренергического рецептор/антагонисты α1-рецептора двойного действия, ингибиторы химазы, дигоксин, диуретики, ингибиторы эндотелин превращающего фермента (ECE), антагонисты эндотелинового рецептора, натрийуретические пептиды и их аналоги, антагонисты очистки рецептора натрийуретического пептида, доноры оксида азота, аналоги простагландина, ингибиторы PDE-V, активаторы и стимуляторы растворимой гуанилатциклазы и антагонисты рецептора вазопрессина. В одном конкретном варианте осуществления изобретения соединение по изобретению объединено с антагонистом альдостерона, антагонистом β1-адренергического рецептора, антагонистом AT1 рецептора или диуретиком, и используются для лечения застойной сердечной недостаточности.
Диарея
Предполагается, что в качестве ингибиторов NEP, соединения по изобретению ингибируют деградацию эндогенных энкефалинов, и, таким образом, данные соединения могут также найти применение при лечении диареи, включая инфекционную и секреторную/водянистую диарею. См., например, Baumer et al. (1992) Gut 33:753-758; Farthing (2006) Digestive Diseases 24:47-58; и  -Collado (1987) Eur. J. Pharmacol. 144(2):125-132. При лечении диареи, соединения по изобретению могут быть объединены с одним или более дополнительными антидиарейными агентами.
-Collado (1987) Eur. J. Pharmacol. 144(2):125-132. При лечении диареи, соединения по изобретению могут быть объединены с одним или более дополнительными антидиарейными агентами.
Болезни почек
Предполагается, что соединения по изобретению улучшают функции почек путем усиления действия вазоактивных пептидов, подобных натрийуретическим пептидам и брадикининам (см., Chen et al. (1999) Circulation 100:2443-2448; Lipkin et al. (1997) Kidney Int. 52:792-801; и Dussaule et al. (1993) Clin. Sci. 84:31-39) и найдут применение при лечении и/или в профилактике болезни почек. Представляющие интерес болезни почек включают диабетическую нефропатию, хроническое заболевание почек, протеинурию и, в частности, острую травму почек или острую почечную недостаточность (см., Sharkovska et al. (2011) Clin. Lab. 57:507-515 и Newaz et al. (2010) Renal Failure 32:384-390). При лечении болезни почек, соединение может быть введено в комбинации с другими терапевтическими агентами, такими как ингибиторы ангиотензин-превращающего фермента, антагонисты AT1 рецептора и диуретики.
Профилактическая терапия
Предполагается, что соединения по изобретению могут быть также использованы в профилактической терапии путем усиления действия натрийуретических пептидов в связи с антигипертрофическим и антифиброзным действием натрийуретических пептидов (см., Potter et al. (2009) Handbook of Experimental Pharmacology 191:341-366), например, при профилактике прогрессирования сердечной недостаточности после инфаркта миокарда, при профилактике артериального рестеноза после ангиопластики, при профилактике утолщения стенок кровеносных сосудов после операций на сосудах, при профилактике атеросклероза и при профилактике диабетической ангиопатии.
Глаукома
Предполагается, что соединения по изобретению могут быть использованы при лечении глаукомы путем усиления действия натрийуретических пептидов. См., например, Diestelhorst et al. (1989) International Ophthalmology 12:99-101. При лечении глаукомы, соединения по изобретению могут быть объединены с одним или более дополнительными антиглаукомными агентами.
Облегчение боли
Предполагается, что соединения по изобретению в качестве ингибиторов NEP, ингибируют разложение эндогенных энкефалинов, и, таким образом, указанные соединения могут также найти применение в качестве анальгетиков. См., например, Roques et al. (1980) Nature 288:286-288 и Thanawala et al. (2008) Current Drug Targets 9:887-894. При лечении боли, соединения по изобретению могут быть объединены с одним или нескольким дополнительными антиноцицептивными лекарственными средствами, такими как ингибиторы аминопептидазы N или дипептидилпептидазы III, нестероидные противовоспалительные агенты, ингибиторы повторного захвата моноамина, мышечные релаксанты, антагонисты NMDA рецептора, агонисты опиоидного рецептора, агонисты серотонинового рецептора 5-HT1D и трициклические антидепрессанты.
Другие применения
Предполагается, что соединения по изобретению могут быть использованы благодаря своим ингибирующим NEP свойствам в качестве противокашлевых агентов, а также найдут применение при лечении портальной гипертензии, связанной с циррозом печени (см., Sansoe et al. (2005) J. Hepatol. 43:791-798), злокачественной опухоли (см., Vesely (2005) J. Investigative Med. 53:360-365), депрессии (см., Noble et al. (2007) Exp.Opin. Ther. Targets 11:145-159), менструальных нарушений, преждевременных родов, преэклампсии, эндометриоза, репродуктивных нарушений (например, мужское и женское бесплодие, поликистозный синдром яичников, неудачная имплантация) и мужской и женской сексуальной дисфункции, включая мужскую эректильную дисфункцию и женское сексуальное расстройство возбуждения. Более конкретно, предполагается, что соединения по изобретению могут быть использованы при лечении женской сексуальной дисфункции (см., Pryde et al. (2006) J. Med. Chem. 49:4409-4424), которая часто определяется как трудность или неспособность получить удовлетворение в сексуальном выражении у пациента женщины. Это охватывает множество разнообразных женских сексуальных расстройств, включая, в качестве иллюстрации, но не ограничения, гипоактивное расстройство сексуального желания, расстройство сексуального возбуждения, расстройство оргазма и расстройство сексуальной боли. При лечении таких нарушений, особенно женской сексуальной дисфункции, соединения по изобретению могут быть объединены с одним или более из следующих вторых агентов: ингибиторами PDE-V, агонистами допамина, агонистами и/или антагонистами рецептора эстрогена, андрогенами и эстрогенами. Полагают, что благодаря своим ингибирующим NEP свойствам, соединения по изобретению также обладают противовоспалительными свойствами, ожидается, что они будут иметь полезность сами по себе, в частности, когда используются в комбинации со статинами.
Недавние исследования предполагают, что NEP играет роль в регуляции нервной деятельности при инсулин-дефицитном диабете и диетах, вызванных ожирением. Coppey et al. (2011) Neuropharmacology 60:259-266. Таким образом, благодаря своим ингибирующим NEP свойствам предполагается, что соединения по изобретению могут быть использованы для обеспечения защиты от нервных поражений, вызванных диабетом, или диетой, вызванной ожирением.
Количество соединения по изобретению, вводимое в виде дозы или все введенное количество в день может быть определено заранее или его можно определить для отдельного пациента, принимая во внимание различные факторы, включая природу и серьезность состояния пациента, подвергаемого лечению состояния, возраста, массы и общего состояния здоровья пациента, восприимчивости пациента к активному средству, пути введения, фармакологических показателей, таких как активность, эффективность, фармакокинетические данные и профили токсичности соединений и второго вводимого агента, и тому подобное. Лечение пациента, страдающего заболеванием или медицинским состоянием (таким как гипертензия), может быть начато с предварительно определенной дозы или дозы, установленной лечащим врачом, и продолжаться в течение периода времени, необходимого для предотвращения, улучшения, подавления или облегчения симптомов заболевания или медицинского состояния. Пациенты, подвергаемые такому лечению, обычно находятся под контролем на регулярной основе с целью определения эффективности терапии. Например, при лечении гипертензии, измерение кровяного давления может быть использовано для определения эффективности лечения. Подобные индикаторы для других заболеваний и состояний, описанные в данном описании, хорошо известны и являются легкодоступными для лечащего врача. Непрерывный контроль со стороны врача гарантирует, что оптимальное количество соединения по изобретению будет введено в любой момент времени, а также упрощает процедуру определения продолжительности лечения. Это имеет особое значение, когда также вводятся вторые агенты, а также может потребоваться корректировка выбора, дозировки и длительности терапии. Таким образом, режим лечения и режим дозирования могут быть скорректированы в течение курса терапии таким образом, чтобы вводилось самое низкое количество активного агента, который проявляет желаемую эффективность, и, кроме того, чтобы введение продолжалось только до тех пор, пока это необходимо для полного лечения заболевания или медицинского состояния.
Исследовательские инструменты
Поскольку соединения по изобретению обладают ингибирующей фермент неприлизин (NEP) активностью, такие соединения также могут быть полезными в качестве исследовательских инструментов для исследования или изучения биологических систем или образцов, содержащих фермент NEP, например, для изучения заболеваний, в которых играют роль фермент NEP или его пептидные субстраты. В таких изучениях может быть использована подходящая биологическая система или образец, содержащие фермент NEP, и они могут быть осуществлены либо in vitro, либо in vivo. Иллюстративные биологические системы или образцы, подходящие для таких изучений включают, но, не ограничиваясь ими, клетки, клеточные экстракты, плазменные мембраны, образцы ткани, изолированные органы, млекопитающие (такие как мыши, крысы, морские свинки, кролики, собаки, свиньи, люди и т.д.) и тому подобное, и млекопитающие представляют интерес.В одном конкретном варианте осуществления изобретения активность фермента NEP у млекопитающего ингибируется путем введения количества соединения по изобретению, ингибирующего NEP. Соединения по изобретению также могут быть использованы в качестве исследовательских инструментов путем проведения биологических анализов с использованием таких соединений.
При использовании в качестве исследовательского инструмента биологическую систему или образец, содержащий фермент NEP, обычно подвергают контакту с ингибирующим фермент NEP количеством соединения по изобретению. После воздействия на биологическую систему или образец соединением, действие по ингибированию фермента NEP определяют с использованием общеизвестных способов и оборудования, таких как определение связывания рецептора путем анализа связывания или определение лиганд-опосредованных изменений в функциональном анализе. Воздействие охватывает контакт клетки или ткани с соединением, введение соединения млекопитающему, например, с помощью внутрибрюшинного, перорального, внутривенного, подкожного или ингаляционного введения и т.д. Такая определяющая стадия может включать определение ответа (количественный анализ) или может включать наблюдения (качественный анализ). Определение ответа включает, например, определение воздействия соединения на биологические системы или образец с использованием общеизвестных способов и оборудования, таких как анализы ферментативной активности и определение субстрата фермента или опосредованного продуктом изменений в функциональном анализе. Для определения уровня активности, а также количества соединения, необходимого для достижения желаемого результата, то есть количества, ингибирующего фермент NEP, могут быть использованы результаты анализа. Обычно, определяющая стадия будет включать определение эффектов по ингибированию фермента NEP.
Кроме того, соединения по изобретению могут быть использованы в качестве средств исследования для оценки других химических соединений и, следовательно, могут быть также использованы в анализах скрининга, чтобы обнаружить, например, новые соединения, обладающие ингибирующей NEP активностью. Таким образом, соединение по настоящему изобретению может быть использовано в качестве стандарта в тесте для получения сравнимых результатов, полученных с помощью исследуемого соединения и с соединениями по изобретению для идентификации тех исследуемых соединений, которые обладают приблизительно равной или большей активностью, если таковые имеются. Например, данные pKi для исследуемого соединения или группы исследуемых соединений сравнивают с данными pKi для соединения по настоящему изобретению для идентификации таких исследуемых соединений, которые обладают желаемыми свойствами, например, исследуемых соединений, имеющих значение pKi приблизительно равное или большее относительно соединения по настоящему изобретению, если таковые имеются. Этот аспект настоящего изобретения включает, в виде отдельных вариантов осуществления, как накопление данных сравнения (с использованием соответствующих анализов), так и анализ данных испытаний для идентификации представляющих интерес исследуемых соединений. Таким образом, исследуемое соединение может быть оценено в биологическом анализе способом, включающем следующие стадии: (а) проведение биологического анализа с исследуемым соединением, с получением первого значения анализа, (b) проведение биологического анализа с соединением по изобретению для получения второго значения анализа; в котором стадию (а) проводят до, после или одновременно со стадией (b); и (c) сравнение первого значения анализа, полученного на стадии (а), со вторым значением анализа, полученного на стадии (b). Примеры биологических анализов включают анализ ингибирования фермента NEP.
Фармацевтические композиции и препараты
Соединения по настоящему изобретению обычно вводят пациенту в виде фармацевтической композиции или препарата. Такие фармацевтические композиции могут быть введены пациенту любым приемлемым способом введения, включая, но, не ограничиваясь ими, пероральный, ректальный, вагинальный, назальный, ингаляционный, местный (включая трансдермальный), через глаз и парентеральный способы введения. Кроме того, соединения по изобретению могут быть введены, например, перорально, в виде многократных доз в день (например, два, три или четыре раза в день) в виде однократной суточной дозы или однократной недельной дозы. Следует учесть, что любая форма соединений по изобретению (т.е. свободное основание, свободная кислота, фармацевтически приемлемая соль, сольват и т.д.), которая подходит для конкретного способа введения, может быть использована в фармацевтических композициях, описанных в настоящем описании.
Соответственно, в одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель и соединение по настоящему изобретению. Композиции могут содержать другие терапевтические и/или формулирующие агенты, если это необходимо. При рассмотрении композиций, "соединение по настоящему изобретению" может также быть обозначено в настоящем описании как "активный агент", чтобы отличать его от других компонентов композиции, таких как, например, носитель. Таким образом, следует учесть, что термин "активный агент" включает соединения формулы I, а также их фармацевтически приемлемые соли, сольваты и пролекарства.
Фармацевтические композиции по изобретению обычно содержат терапевтически эффективное количество соединения по настоящему изобретению. Тем не менее, специалисту в данной области будет понятно, что фармацевтическая композиция может содержать большее терапевтически эффективное количество соединения, например, в суммарном составе, или меньшее терапевтически эффективное количество, то есть отдельные однократные дозы, предназначенные для многократного введения для получения терапевтически эффективного количества. Обычно композиция будет содержать около 0,01-95% масс. активного вещества, включая примерно 0,01-30% масс., например, около 0,01-10% масс., при этом фактическое количество зависит от самого препарата, способа введения, частоты введения и так далее. В одном варианте осуществления композиция, пригодная для пероральной лекарственной формы, например, может содержать около 5-70% масс. или около 10-60% масс. активного вещества.
Любой обычный носитель или эксципиент может быть использован в фармацевтических композициях по изобретению. Выбор конкретного носителя или эксципиента или комбинаций носителей или эксципиентов, будет зависеть от способа введения, используемого для лечения конкретного пациента, или вида медицинского состояния или заболевания. В связи с этим, получение подходящей композиции для конкретного способа введения находится в пределах области знаний специалиста в данной области фармацевтики. Кроме того, носители или эксципиенты, используемые в таких композициях, являются коммерчески доступными. В качестве дополнительной иллюстрации, обычные методы получения лекарственных средств описаны в Remington: The Science and Practice of Pharmacy, 20th Edition, Lippincott Williams & White, Baltimore, Maryland (2000); и H. C. Ansel et al., Pharmaceutical Dosage Forms and Drug Delivery Systems, 7th Edition, Lippincott Williams & White, Baltimore, Maryland (1999).
Иллюстративные примеры материалов, которые могут служить в качестве фармацевтически приемлемых носителей, включают, но не ограничиваются, ими, следующие: сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал, целлюлозу, такую как микрокристаллическая целлюлоза и ее производные, такие как натрийкарбоксиметилцеллюлоза, этилцеллюлоза и ацетат целлюлозы; порошкообразный трагакант; солод; желатин; тальк; эксципиенты, такие как масло какао и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль, полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные агенты, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический солевой раствор, раствор Рингера, этиловый спирт; фосфатные буферные растворы; сжатые газы-вытеснители, такие как хлорфторуглероды и гидрофторуглероды, а также другие нетоксичные совместимые вещества, используемые в фармацевтических композициях.
Фармацевтические композиции обычно получают путем тщательного и однородного перемешивания или смешивания активного агента с фармацевтически приемлемым носителем и одним или более дополнительными ингредиентами. Затем полученная равномерно перемешанная смесь может быть формована или загружена в таблетки, капсулы, пилюли, контейнеры, картриджи, дозаторы и тому подобное с использованием обычных процедур и оборудования.
В одном варианте осуществления фармацевтические композиции пригодны для перорального введения. Подходящие композиции для перорального введения могут быть в виде капсул, таблеток, пилюль, лепешек, облаток, драже, порошков, гранул, растворов или суспензий в водной или неводной жидкости, жидких эмульсий типа масло-в-воде или вода-в-масле, эликсиров или сиропов и подобного, каждый из которых содержит определенное количество активного агента.
В случае перорального введения в виде твердой лекарственной формы (капсулы, таблетки, пилюли и тому подобное), композиции обычно содержат активный агент и один или более фармацевтически приемлемых носителей, таких как цитрат натрия или дикальцийфосфат. Твердые дозированные формы могут также включать: наполнители или разбавители, такие как крахмал, микрокристаллическая целлюлоза, лактоза, сахароза, глюкоза, маннит и/или кремниевая кислота; связующие, такие как карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и/или аравийская камедь, увлажнители, такие как глицерин; разрыхляющие агенты, такие как агар-агар, карбонат кальция, картофельный крахмал или маниоковый крахмал, альгиновая кислота, некоторые силикаты и/или карбонат натрия; замедляющие растворение агенты, такие как парафин, ускорители абсорбции, такие как четвертичные аммониевые соединения, смачивающие агенты, такие как цетиловый спирт и/или глицеринмоностеарат; абсорбенты, такие как каолин и/или бентонит, лубриканты, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия и/или их смеси, красители и буферирующие агенты.
Разделяющие агенты, смачивающие агенты, покрывающие агенты, подсластители, вкусовые добавки и ароматизаторы, консерванты и антиоксиданты также могут присутствовать в фармацевтических композициях. Примеры покрывающих агентов для таблеток, капсул, пилюль и подобного, включают агенты, которые используются для энтеросолюбильных покрытий, например, ацетат-фталат целлюлозы, поливинилацетат-фталат, фталат гидроксипропилметилцеллюлозы, сополимеры эфира метакриловой кислоты и метакриловой кислоты, ацетаттримеллитат целлюлозы, карбоксиметилэтилцеллюлоза, ацетатсукцинат гидроксипропилметилцеллюлозы и тому подобное. Примеры фармацевтически приемлемых антиоксидантов включают: водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфат натрия, сульфит натрия и т.п.; растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, лецитин, пропилгаллат, альфа-токоферол и тому подобное, и хелаты металлов, такие, как лимонная кислота, этилендиаминтетрауксусная кислота, сорбит, винная кислота, фосфорная кислота и тому подобное.
Композиции могут быть также получены с тем, чтобы обеспечить медленное или контролируемое высвобождение активного агента с использованием, в качестве примера, гидроксипропилметилцеллюлозы в различных пропорциях или другие полимерные матрицы, липосомы и/или микросферы. Кроме того, фармацевтические композиции, согласно изобретению, могут содержать опалесцирующие агенты и могут быть получены таким образом, чтобы они высвобождали активный агент только или предпочтительно в определенной части желудочно-кишечного тракта, необязательно с замедлением. Примеры «встраиваемых» композиций, которые могут быть использованы, включают полимерные вещества и воски. Активный агент может быть также в микроинкапсулированной форме, необязательно с одним или более из вышеописанных эксципиентов.
Подходящие жидкие лекарственные формы для перорального введения включают, в качестве иллюстрации, фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Жидкие лекарственные формы обычно содержат активное вещество и инертный разбавитель, такой как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, масла (например, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбитана и их смеси. Суспензии могут содержать суспендирующие агенты, такие как, например, этоксилированные изостеариловые спирты, полиоксиэтиленсорбит и сложные эфиры сорбита, микрокристаллическую целлюлозу, метагидроксид алюминия, бентонит, агар-агар и трагакант, и их смеси.
В случае перорального введения, фармацевтические композиции по изобретению могут быть упакованы в стандартные лекарственные формы. Термин "единичная дозированная форма" относится к физически дискретной единице, подходящей для дозирования пациенту, то есть каждая единица содержит заданное количество активного вещества, рассчитанное на получение желаемого терапевтического эффекта, по отдельности или в комбинации с одним или более дополнительными единицами. Например, такие стандартные лекарственные формы могут быть в виде капсул, таблеток, пилюль и тому подобное.
В другом варианте осуществления композиции по изобретению пригодны для ингаляционного введения и, как правило, могут быть в виде аэрозоля или порошка. Обычно такие композиции вводят с использованием известных устройств для доставки, таких как распылитель, сухой порошок или дозирующий ингалятор. Распылительные устройства создают поток воздуха с высокой скоростью, что вызывает распыление композиции в виде тумана, который доставляется в дыхательные пути пациента. Обычная распыляемая композиция содержит активный агент, растворенный в носителе с образованием раствора, или микронизированный и комбинированный с носителем с образованием суспензии микронизированных частиц с размером, пригодным для дыхания. Сухие порошковые ингаляторы вводят активный агент в виде сыпучего порошка, который диспергирован в потоке воздуха во время вдоха пациента. Обычная композиция сухого порошка содержит активный агент, смешанный в сухом виде с эксципиентом, таким как лактоза, крахмал, маннит, декстроза, полимолочная кислота, сополимер лактида и гликолида, и их комбинацией. Дозирующие ингаляторы выпускают определенные количества активного агента с использованием сжатого газа-пропеллента. Обычная дозированная композиция содержит раствор или суспензию активного агента в сжиженном пропелленте, таком как фреон или гидрофторалкан. Необязательные компоненты таких композиций включают сорастворители, такие как этанол или пентан, и поверхностно-активные вещества, такие как сорбитантриолеат, олеиновая кислота, лецитин, глицерин и лаурилсульфат натрия. Такие композиции обычно получают добавлением охлажденного или сжатого гидрофторалкана в подходящий контейнер, содержащий активный агент, этанол (если присутствует) и поверхностно-активное вещество (если присутствует). Для получения суспензии, активный агент тонко микронизируют и затем объединяют с пропеллентом. Кроме того, суспензии могут быть получены распылительной сушкой покрытия поверхностно-активных веществ на микронизированные частицы активного агента. Затем композицию загружают в аэрозольный контейнер, который образует часть ингалятора.
Соединения по изобретению могут быть также введены парентерально (например, подкожно, внутривенно, внутримышечно или с помощью внутрибрюшинной инъекции). Для такого применения активный агент представлен в виде стерильного раствора, суспензии или эмульсии. Примеры растворителей для получения таких композиций включают воду, физиологический раствор, низкомолекулярные спирты, такие как пропиленгликоль, полиэтиленгликоль, масло, желатин, эфиры жирных кислот, такие как этилолеат, и тому подобное. Парентеральные композиции могут также содержать один или более антиоксидантов, солюбилизаторов, стабилизаторов, консервантов, смачивающих агентов, эмульгаторов и диспергирующих агентов. Поверхностно-активные вещества, дополнительные стабилизирующие агенты или рН-регулирующие агенты (кислоты, основания или буферы) и антиоксиданты являются особенно полезными для обеспечения стабильности композиции, например, чтобы свести к минимуму или избежать гидролиза сложноэфирных и амидных связей, которые могут присутствовать в соединениях. Такие композиции могут быть стерилизованы с использованием стерильной среды для инъекций, стерилизующего агента, фильтрации, облучения или нагревания. В одном конкретном варианте осуществления парентеральный препарат содержит водный раствор циклодекстрина в качестве фармацевтически приемлемого носителя. Подходящие циклодекстрины включают циклические молекулы, содержащие шесть или более единиц α-D-глюкопиранозы, которые в 1,4-положениях связаны так же, как в амилазе, β-циклодекстрине или циклогептаамилозе. Конкретные циклодекстрины включают производные циклодекстринов, такие как гидроксипропилцеллюлоза, и сульфобутиловый эфир циклодекстринов, таких как гидроксипропил-β-циклодекстрин и сульфобутиловый эфир β-циклодекстрина. Конкретные буферы для таких композиций, включают буферы на основе карбоновой кислоты, такие как буферные растворы цитрата, лактата и малеата.
Соединения по настоящему изобретению также можно вводить трансдермально с использованием известных трансдермальных систем доставки и эксципиентов. Например, соединение может быть смешано с усилителями проницаемости, такими как пропиленгликоль, монолаурат полиэтиленгликоля, азациклоалкан-2-оны и тому подобное, и включены в пластырь или аналогичной системы доставки. В таких трансдермальных композициях, если это необходимо, могут быть использованы дополнительные эксципиенты, включая желирующие агенты, эмульгаторы и буферы.
Вторые агенты
Соединения по изобретению могут быть использованы как единственные при лечении заболевания или могут быть объединены с одним или более дополнительными терапевтическими агентами с целью достижения терапевтического действия. Таким образом, в одном варианте осуществления изобретения фармацевтические композиции по изобретению содержат другие лекарственные средства, которые вводятся вместе с соединением по изобретению. Например, композиция может дополнительно содержать одно или более лекарственных средств (также указываемые как "второй(ые) агент(ы)"). Такие терапевтические агенты хорошо известны в данной области и включают антагонисты аденозинового рецептора, антагонисты α-адренергического рецептора, антагонисты β1-адренергического рецептора, агонисты β2-адренергического рецептора, антагонисты β-адренергического рецептора/антагонисты α1-рецептор двойного действия, прерыватели усиленного гликозилирования конечных продуктов, антагонисты альдостерона, ингибиторы альдостеронсинтазы, ингибиторы аминопептидазы N, андрогены, ингибиторы ангиотензин-превращающего фермента и ингибиторы двойного действия ангиотензин-превращающего фермента/неприлизина, активаторы и стимуляторы ангиотензин-превращающего фермента активаторы и стимуляторы ангиотензин-превращающего фермента 2, ангиотензин-II вакцины, антикоагулянты, антидиабетические агенты, антидиарейные агенты, антиглаукомные агенты, антилипидные агенты, антиноцицептивные агенты, антитромботическиес агенты, антагонисты AT1 рецептора и ингибиторы двойного действия антагониста AT1 рецептора/неприлизина и мультифункциональной ангиотензин рецептор блокаторы, антагонисты рецептора брадикинина, блокаторы кальциевых каналов, ингибиторы химазы, дигоксин, диуретики, агонисты допамина, ингибиторы эндотелин превращающего фермента, антагонисты эндотелинового рецептора, HMG-CoA ингибиторы редуктазы, эстрогены, агонисты и/или антагонисты рецептора эстрогена, ингибиторы повторного захвата моноамина, мышечные релаксанты, натрийуретический пептиды и их аналоги, антагонисты очистки рецептора натрийуретического пептида, ингибиторы неприлизина, доноры оксида азота, нестероидные противовоспалительные агенты, антагонисты рецептора N-метил d-аспартата, агонисты опиоидного рецептора, ингибиторы фосфодиэстеразы, аналоги простагландина, агонисты рецептора простагландина, ингибиторы ренина, селективные ингибиторы серотонинового ответа, блокатор натриевых каналов, стимуляторы и активаторы растворимой гуанилатциклазы, трициклические антидепрессанты, антагонисты рецептора вазопрессина и их комбинации. Конкретные примеры указанных агентов описаны подробно далее.
В соответствии с этим, согласно еще одному аспекту изобретения, фармацевтическая композиция содержит соединение по изобретению, второй активный агент и фармацевтически приемлемый носитель. В композицию могут быть также включены третий, четвертый и т.д. активные агенты. В комбинационной терапии, количество соединения по изобретению, которое вводится, а также количество вторых агентов может быть меньше, чем количество обычно вводимых в монотерапии.
Соединения по изобретению могут быть физически смешаны со вторым активным агентом с образованием композиции, содержащей оба агента; или каждый агент может быть представлен в отдельных и различных композициях, которые вводятся пациенту одновременно или в разное время. Например, соединение по изобретению может быть объединено со вторым активным агентом с помощью общеизвестных способов и оборудования, с получением комбинации активных агентов, содержащей соединение по изобретению и второй активный агент. Кроме того, активные агенты могут быть объединены с фармацевтически приемлемым носителем с образованием фармацевтической композиции, содержащий соединение по изобретению, второй активный агент и фармацевтически приемлемый носитель. В данном варианте осуществления изобретения компоненты композиции обычно смешивают или измельчают, чтобы получить физическую смесь. Физическую смесь затем вводят в терапевтически эффективном количестве, используя какой-либо путь введения, описанный в данном описании.
Альтернативно, активные агенты могут оставаться отдельно или раздельно перед введением пациенту. В данном варианте осуществления изобретения агенты не являются физически смешанными вместе перед введением, а вводятся одновременно или в разное время в виде отдельных композиций. Такие композиции могут быть расфасованы отдельно или могут быть расфасованы совместно в наборе. При введении в разное время, второй агент обычно вводят менее чем 24 часа спустя после введения соединения по изобретению, в интервале от почти одновременного введения соединения по изобретению до около 24 часов последующей дозой. Это также указывается как последовательное введение. Таким образом, соединение по изобретению может быть введено перорально одновременно или последовательно с другим активным агентом, используя две таблетки, одну таблетку для каждого активного агента, где последующая может быть введена сразу после введения соединения по изобретению или через некоторое определенное время (например, спустя один час или через три часа). Также может быть предусмотрено, что второй агент может быть введен более чем через 24 часа после введения соединения по изобретению. Альтернативно, комбинация может быть введена различными путями введения, то есть, один компонент перорально и другой путем ингаляции.
В одном варианте осуществления изобретения набор содержит первую дозированную форму, содержащую соединение по изобретению и, по меньшей мере, одну дополнительную дозированную форму, содержащую один или несколько вторых агентов, указанных выше, в количестве, достаточном для осуществления способов по изобретению. Первая дозированная форма и вторая (или третья и т.д.) дозированная форма вместе содержат терапевтически эффективное количество активных агентов для лечения или профилактики заболевания или медицинского состояния у пациента.
Второй(ые) агент(ы), когда он(они) включены, представлены в таком терапевтически эффективном количестве, как они обычно вводятся, чтобы произвести терапевтически благоприятное воздействие при совместном введении с соединением по изобретению. Второй агент может быть в виде фармацевтически приемлемой соли, сольвата, оптически чистого стереоизомера и т.д. Второй агент также может быть в виде пролекарства, например, соединение, имеющее группу карбоновой кислоты, которая была этерифицирована. Таким образом, вторые агенты, перечисленные в данном описании, предназначены для включения всех таких форм и являются коммерчески доступными или могут быть получены с использованием обычных способов и реагентов.
В одном варианте осуществления изобретения соединения по изобретению вводятся в комбинации с антагонистом рецептора аденозина, иллюстративные примеры которого включают, но, не ограничиваясь ими, наксфиллин, ролофиллин, SLV-320, теофиллин и тонапофиллин.
В одном варианте осуществления изобретения соединения по изобретению вводятся в комбинации с антагонистом α-адренергического рецептора, иллюстративные примеры которого включают, но, не ограничиваясь ими, доксазозин, празозин, тамсулозин и теразозин.
Соединения по изобретению также могут быть введены в комбинации с антагонистом β1-адренергического рецептора ("β1-блокаторы»). Иллюстративные β1-блокаторы включают, но, не ограничиваясь ими, ацебутолол, альпренолол, амосулалол, аротинолол, атенолол, бефунолол, бетаксолол, бевантолол, бисопролол, бопиндолол, буциндолол, букумолол, буфетолол, буфуралол, бунитролол, бупранолол, бубридин, бутофилолол, каразолол, картеолол, карведилол, целипролол, цетамолол, клоранолол, дилевалол, эпанолол, эсмолол, инденолол, лабетолол, левобунолол, мепиндолол, метипранолол, метопролол, такой как метопролола сукцинат и метопролола тартрат, мопролол, надолол, надоксолол, небивалол, нипрадилол, окспренолол, пенбутолол, пербутолол, пиндолол, практолол, пронетгалол, пропранолол, соталол, суфиналол, талиндол, тертатолол, тилизолол, тимолол, толипролол, ксибенолол и их комбинации. В одном конкретном варианте осуществления β1-антагонист выбран из атенолола, бисопролола, метопролола, пропранолола, соталола и их комбинаций. Обычно, β1-блокатор вводится в количестве, достаточном, чтобы обеспечить около 2-900 мг на дозу.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с агонистом β2-адренергического рецептора, иллюстративные примеры которого включают, но, не ограничиваясь ими, альбутерол, битолтерол, фенотерол, формотерол, индакатерол, изоэтарин, левалбутерол, метапротеренол, пирбутерол, сальбутамол, сальмефамол, сальметерол, тербуталин, вилантерол и тому подобное. Обычно, агонист β2-адренергического рецептора вводится в количестве, достаточном для обеспечения дозы около 0,05-500 мкг.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с прерывателем усиленного гликозилирования конечных продуктов (AGE), примеры которого включают, в качестве иллюстрации, но не ограничения, алагебриум (или ALT-711) и TRC4149.
В другом варианте осуществления соединения по изобретению вводят в комбинации с антагонистом альдостерона, иллюстративные примеры которого включают, но, не ограничиваясь ими, эплеренон, спиронолактон и их комбинации. Обычно, антагонист альдостерона вводят в количестве, достаточном для обеспечения около 5-300 мг в день.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с ингибитором аминопептидазы N или дипептидил пептидазы III, примеры которого включают, в качестве иллюстрации, но не ограничения, бестатин и РС18 (2-амино-4-метилсульфонилбутантиол, метионинтиол).
Соединения по изобретению также могут быть введены в комбинации с ингибитором ангиотензин-превращающего фермента (АСЕ). Иллюстративные АСЕ ингибиторы включают, но, не ограничиваясь ими, аккуприл, алацеприл, беназеприл, беназеприлат, каптоприл, церанаприл, цилазаприл, делаприл, эналаприл, эналаприлат, фозиноприл, фозиноприлат, имидаприл, лизиноприл, моэксиприл, моноприл, мовелтиприл, пентоприл, периндоприл, хинаприл, хинаприлат, рамиприл, рамиприлат, саралазина ацетат, спираприл, темокаприл, трандолаприл, зофеноприл и их комбинации. В конкретном варианте осуществления изобретения, ингибитор АСЕ выбран из: беназеприла, каптоприла, эналаприла, лизиноприла, рамиприла и их комбинаций. Обычно, ингибитор АСЕ вводят в количестве, достаточном для обеспечения около 1-150 мг в день.
В другом варианте осуществления соединения по изобретению вводят в комбинации с ингибитором двойного действия ангиотензин-превращающего фермента/неприлизина (ACE/NEP), примеры которого включают, но, не ограничиваясь ими: AVE-0848 ((4S,7S,12bR)-7-[3-метил-2(S)-сульфанилбутирамидо]-6-оксо-1,2,3,4,6,7,8,12b-октагидропиридо[2,1-а][2]бензазепин-4-карбоновая кислота); AVE-7688 (илепатрил) и его родоначальное соединение; BMS-182657 (2-[2-оксо-3(S)-[3-фенил-2(S)-сульфанилпропионамидо]-2,3,4,5-тетрагидро-1H-1-бензазепин-1-ил]уксусная кислота); CGS-26303 ([N-[2-(бифенил-4-ил)-1(S)-(1H-тетразол-5-ил)этил]амино]метилфосфоновая кислота); CGS-35601 (N-[1-[4-метил-2(S)-сульфанилпентанамидо]циклопентилкарбонил]-L-триптофан); фазидотрил; фазидотрилат; энаприлат; ER-32935 ((3R,6S,9aR)-6-[3(S)-метил-2(S)-сульфанилпентанамидо]-5-оксопергидротиазоло[3,2-a]азепин-3-карбоновая кислота); гемпатрилат; MDL-101264 ((4S,7S,12bR)-7-[2(S)-(2-морфолиноацетилтио)-3-фенилпропионамидо]-6-оксо-1,2,3,4,6,7,8,12b-октагидропиридо[2,1-a][2]бензазепин-4-карбоновая кислота); MDL-101287 ([4S-[4α,7α(R*),12bβ]]-7-[2-(карбоксиметил)-3-фенилпропионамидо]-6-оксо-1,2,3,4,6,7,8,12b-октагидропиридо[2,1-a][2]бензазепин-4-карбоновая кислота); омапатрилат; RB-105 (N-[2(S)-(меркаптометил)-3(R)-фенилбутил]-L-аланин); сампатрилат; SA-898 ((2R,4R)-N-[2-(2-гидроксифенил)-3-(3-меркаптопропионил)тиазолидин-4-илкарбонил]-L-фенилаланин); Sch-50690 (N-[1(S)-карбокси-2-[N2-(метансульфонил)-L-лизиламино]этил]-L-валил-L-тирозин); и также могут быть включены их комбинации. В одном конкретном варианте осуществления ингибитор ACE/NEP выбран из: AVE-7688, энаприлата, фазидотрила, фазидотрилата, омапатрилата, сампатрилата и их комбинаций.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с активатором или стимулятором ангиотензин-превращающего фермента 2 (ACE2).
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с вакциной ангиотензин-II, примеры которой включают, но, не ограничиваясь ими, ATR12181 и CYT006-AngQb.
В одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с антикоагулянтом, иллюстративные примеры которого включают, но, не ограничиваясь ими: кумарины, такие как варфарин, гепарин и прямые ингибиторы тромбина, такие как аргатробан, бивалирудин, дабигатран и лепирудин.
В еще одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с антидиабетическим агентом. Иллюстративные антидиабетические агенты включают инъектируемые лекарственные средства, а также перорально эффективные лекарственные средства и их комбинации. Примеры инъектируемых лекарственных средств включают, но, не ограничиваясь ими, производные инсулина и инсулин. Примеры перорально эффективных лекарственных средств включают, но, не ограничиваясь ими: бигуаниды, такие как метформин; антагонисты глюкагона; ингибиторы α-глюкозидазы, такие как акарбоз и миглитол; ингибиторы дипептидил пептидазы IV (ингибиторы DPP-IV), такие как алоглиптин, денаглиптин, линаглиптин, саксаглиптин, ситаглиптин и вильдаглиптин; меглитиниды, такие как репаглинид; оксадиазолидиндионы; сульфонилмочевины, такие как хлорпропамид, глимепирид, глипизид, глибурид и толазамид; тиазолидинедионы, такие как пиоглитазон и росиглитазон; и их комбинации.
В другом варианте осуществления соединения по изобретению вводят в комбинации с антидиарейным лечением. Иллюстративные варианты лечения включают, но, не ограничиваясь ими, пероральные регидратирующие растворы (ORS), лоперамид, дифеноксилат и субсалицилат висмута.
В еще одном варианте осуществления изобретения, соединение по изобретению вводят в комбинации с антиглаукомным агентом. Иллюстративные антиглаукомные агенты включают, но, не ограничиваясь ими: α-адренергические агонисты, такие как бримонидин; антагонисты β1-адренергического рецептора; местные β1-блокаторы, такие как бетаксолол, левобунолол и тимолол; ингибиторы карбон ангидразы, такие как ацетазоламид, бринзоламид или дорзоламид; холинергические агонисты, такие как цевимелин и DMXB-анабазин; соединения эпинефрина; миотики, такие как пилокарпин; и аналоги простагландина.
В еще одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с антилипидным агентом. Иллюстративные антилипидные агенты включают, но, не ограничиваясь ими: ингибиторы белка переносчика эфиров холестерина (СЕТР), такие как анацетрапиб, дальцетрапиб и торсетрапиб; статины, такие как аторвастатин, флувастатин, ловастатин, правастатин, розувастатин и симвастатин; и их комбинации.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с антитромботическим агентом. Иллюстративные антитромботические агенты включают, но, не ограничиваясь ими: аспирин; антитромбоцитные агенты, такие как клопидогрел, прасугрел и тиклопидин; гепарин и их комбинации.
В одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с антагонистом AT1 рецептора, также известного как блокатор рецептора 1 ангиотензина типа II (ARB). Иллюстративные ARB включают, но, не ограничиваясь ими, абитесартан, азилсартан (например, азилсартан медоксомил), бензиллосартан, кандесартан, кандесартан цилексетил, элисартан, эмбусартан, енолтазосартан, эпросартаном EXP3174, фонсартан, форасартан, глициллосартан, ирбесартан, изотеолин, лозартан, медоксимил, милфасартан, олмесартан (например, олмесартан медоксомил), опомисартан, пратосартан риписартан, саприсартан, саралазин, сармезин, TAK-591, тазосартан, телмисартан, валсартан, золасартан и их комбинации. В конкретном варианте осуществления изобретения ARB выбран из азилсартан медоксимила, кандесартан цилексетила, эпросартана, ирбесартана, лозартана, олмесартан медоксимила, ирбесартана, саприсартана, тазосартана, телмисартана, валсартана и их комбинаций. Примеры соли и/или пролекарства включают кандесартан цилексетил, эпросартан мезилат, калиевую соль лосартана и олмесартан медоксимил. Обычно, ARB вводят в количестве, достаточном для обеспечения около 4-600 мг на дозу, примеры суточных доз находятся в интервале 20-320 мг в день.
Соединения по изобретению также могут быть введены в комбинации с агентом двойного действия, таким как ингибитор антагониста AT1 рецептора/ингибитор неприлизина (ARB/NEP), примеры которого включают, но, не ограничиваясь ими, соединения, описанные в публикациях патентов США №№2008/0269305 и 2009/0023228, оба на имя Allegretti et al., поданных 23 апреля, 2008, такие как соединение 4'-{2-этокси-4-этил-5-[((S)-2-меркапто-4-метилпентаноиламино)метил]имидазол-1-илметил}-3'-фторбифенил-2-карбоновая кислота.
Соединения по изобретению также могут быть введены в комбинации с мультифункциональными блокаторами рецептора ангиотензина, как описано в работе Kurtz & Klein (2009) Hypertension Research 32:826-834.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с антагонистом рецептора брадикидина, например, икатибантом (HOE-140). Предполагается, что такая комбинационная терапия может иметь успех в профилактике ангионевротического аллергического отека или других нежелательных последствий повышенного уровня брадикинина.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с блокатором кальциевых каналов. Иллюстративные блокаторы кальциевых каналов включают, но, не ограничиваясь ими, амлодипин, анипамил, аранипин, барнидипин, бенциклан, бенидипин, бепридил, клентиазем, цилнидипин, циннаризин, дилтиазем, эфонидипин, элгодипин, этафенон, фелодипин, фендилин, флунаризин, галлопамил, исрадипин, лацидипин, лерканидипин, лидофлазин, ломеризин, манидипин, мибефрадил, никардипин, нифедипин, нигулдипин, нилудипин, нилвадипин, нимодипин, низолдипин, нитрендипин, нивалдипин, пергексилин, прениламин, риозидин, семотиадил, теродилин, тиапамил, верапамил и их комбинации. В конкретном варианте осуществления изобретения блокатор кальциевых каналов выбран из амлодипина, бепридила, дилтиазема, фелодипина, исрадипина, лацидипина, никардипина, нифедипина, нигулдипина, нилудипина, нимодипина, низолдипина, риозидина, верапамила и их комбинаций. Обычно, блокатор кальциевых каналов вводят в количестве, достаточном для обеспечения около 2-500 мг на дозу.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с ингибитором химазы, таким как ТРС-806 и 2-(5-формиламино-6-оксо-2-фенил-1,6-дигидропиримидин-1-ил)-N-[{3,4-диоксо-1-фенил-7-(2-пиридилокси)}-2-гептил]ацетамид (NK3201).
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с диуретиком. Иллюстративные диуретики включают, но, не ограничиваясь ими: ингибиторы карбон ангидразы, такие как ацетазоламид и дихлорфенамид; петлевые диуретики, которые включают сульфонамидные производные, такие как ацетазоламид, амбузид, азосемид, буметанид, бутазоламид, хлораминофенамид, клофенамид, клопамид, клорексолон, дисульфамид, этоксзоламид, фуросемид, мефлузид, метазоламид, пиретанид, торсемид, трипамид и ксипамид, а также несульфонамидные диуретики, такие как этакриновая кислота, и другие соединения феноксиуксусной кислоты, такие как тиениловая кислота, индакринон и хинкарбат; осмотические диуретики, такие как маннит; диуретики, удерживающие калий, которые включают антагонисты альдостерона, такие как спиронолактон, и ингибиторы Na+ каналов, такие как амилорид и триамтерен; тиазид и подобные тиазиду диуретики, такие как алтиазид, бендрофлуметиазид, бензилгидрохлортиазид, бензтиазид, бутиазид, хлорталидон, хлортиазид, циклопентиазид, циклотиазид, эпитиазид, этиазид, фенхизон, флюметиазид, гидрохлортиазид, гидрофлуметиазид, индапамид, метилклотиазид, метикран, метолазон, парафлутизид, политиазид, хинетазон, теклотиазид и трихлорметиазид; и их комбинации. В конкретном варианте осуществления изобретения диуретик выбран из амилорида, буметанида, хлортиазида, хлорталидона, дихлорфенамида, этакриновой кислоты, фуросемида, гидрохлортиазида, гидрофлуметиазида, индапамида, метилклотиазида, метозалона, торсемида, триамтерена и их комбинаций. Диуретик вводят в количестве, достаточном для обеспечения около 5-50 мг в день, более обычно 6-25 мг в день, в общей дозе 6,25 мг, 12,5 мг или 25 мг в день.
Соединения по изобретению также могут быть введены в комбинации с ингибитором эндотелин превращающего фермента (ECE), примеры которого включают, но, не ограничиваясь ими, фосфорамидон, CGS 26303 и их комбинации.
В конкретном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с антагонистом эндотелинового рецептора. Иллюстративные антагонисты эндотелинового рецептора включают, но, не ограничиваясь ими: селективные антагонисты эндотелинового рецептора, которые воздействуют на рецепторы эндотелина A, такие как авозентан, амбрисентан, атрасентан, BQ-123, клазосентан, дарузентан, ситаксетан и зиботентан; и двойные антагонисты эндотелинового рецептора, которые воздействуют на оба эндотелина A и B, такие как бозентан, мацитентан, тезосентан).
В еще одном варианте осуществления изобретения, соединение по изобретению вводят в комбинации с одним или более ингибиторами HMG-CoA редуктазы, которые также известны как статины. Иллюстративные статины включают, но, не ограничиваясь ими, аторвастатин, флувастатин, ловастатин, питавастатин, правастатин, розувастатин и симвастатин.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с ингибитором обратного захвата моноамина, примеры которого включают, в качестве иллюстрации, но не ограничения, ингибиторы обратного захвата норэфедрина, такие как атомоксетин, бупроприон и метаболит бупроприона гидроксибупроприон, мапротилин, ребоксетин и вилоксазин; селективные ингибиторы серотонинового ответа (SSRI), такие как циталопрам и метаболит циталопрама десметилциталопрам, дапоксетин, эсциталопрам (например, эсциталопрам оксалат), флуоксетин и метаболит десметилфлуоксетина норфлуоксетин, флувоксамин (например, флувоксамин малеат), пароксетин, сертралин и метаболит сертралина деметилсертралин; двойные ингибиторы обратного захвата серотонина-норэфедрин (SNRI), такие как бицифадин, дулоксетин, милнаципран, нефазодон и венлафаксин; и их комбинации.
В другом варианте осуществления соединения по изобретению вводят в комбинации с мышечным релаксантом, примеры которого включают, но, не ограничиваясь ими: каризопродол, хлорзоксазон, циклобензаприн, дифлунизал, метаксалон, метокарбамол и их комбинации.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с натрийуретическим пептидом или аналогом, примеры которого включают, но, не ограничиваясь ими: карпетитид, CD-NP (Nile Therapeutics), CU-NP, незиритид, PL-3994 (Palatin Technologies, Inc.), уларитид, цендеритид и соединения, описанные в работе Ogawa et al (2004) J. Biol. Chem. 279:28625-31. Указанные соединения также называют агонистами рецептора-A натрийуретических пептидов (NPR-A). В другом варианте осуществления соединения по изобретению вводят в комбинации с антагонистом рецептора очистки натрийуретических пептидов (NPR-C), таким как SC-46542, cANF (4-23) и AP-811 (Veale (2000) Bioorg Med Chem Lett 10:1949-52). Например, AP-811 проявляет синергизм, когда объединен с ингибитором NEP, тиорфаном (Wegner (1995) Clin. Exper. Hypert. 17:861-876).
В другом варианте осуществления соединения по изобретению вводят в комбинации с ингибитором неприлизина (NEP). Иллюстративные ингибиторы NEP включают, но, не ограничиваясь ими: AHU-377; кандоксатрил; кандоксатрилат; дексекадотрил (бензиловый эфир (+)-N-[2(R)-(ацетилтиометил)-3-фенилпропионил]глицина); CGS-24128 (3-[3-(бифенил-4-ил)-2-(фосфонометиламино)пропионамидо]пропионовая кислота); CGS-24592 ((S)-3-[3-(бифенил-4-ил)-2-(фосфонометиламино)пропионамидо]пропионовая кислота); CGS-25155 (бензиловый эфир N-[9(R)-(ацетилтиометил)-10-оксо-1-азациклодекан-2(S)-илкарбонил]-4(R)-гидрокси-L-пролина); производные 3-(1-карбамоилциклогексил)пропионовой кислоты, описанные в WO 2006/027680, Hepworth et al. (Pfizer Inc.); JMV-390-1 (2(R)бензил-3-(N-гидроксикарбамоил)пропионил-L-изолейцил-L-лейцин); экадотрил; фосфорамидон; ретротиорфан; RU-42827 (2-(меркаптометил)-N-(4-пиридинил)бензолпропионамид); RU-44004 (N-(4-морфолинил)-3-фенил-2-(сульфанилметил)пропионамид); SCH-32615 ((S)-N-[N-(1-карбокси-2-фенилэтил)-L-фенилаланил]-β-аланин) и его пролекарство SCH-34826 ((S)-N-[N-[1-[[(2,2-диметил-1,3-диоксолан-4-ил)метокси]карбонил]-2-фенилэтил]-L-фенилаланил]-β-аланин); сиалорфин; SCH-42495 (этиловый эфир N-[2(S)-(ацетилсульфанилметил)-3-(2-метилфенил)пропионил]-L-метионина); спинорфин; SQ-28132 (N-[2-(меркаптометил)-1-оксо-3-фенилпропил]лейцин); SQ-28603 (N-[2-(меркаптометил)-1-оксо-3-фенилпропил]-β-аланин); SQ-29072 (7-[[2-(меркаптометил)-1-оксо-3-фенилпропил]амино]гептановая кислота); тиорфан и его пролекарство рацецадотрил; UK-69578 (цис-4-[[[1-[2-карбокси-3-(2-метоксиэтокси)пропил]циклопентил]карбонил]амино]циклогексанкарбоновая кислота); UK-447841 (2-{1-[3-(4-хлорфенил)пропилкарбамоил]циклопентилметил}-4-метоксибутановая кислота); UK-505749 ((R)-2-метил-3-{1-[3-(2-метилбензотиазол-6-ил)пропилкарбамоил]циклопентил}пропионовая кислота); 5-бифенил-4-ил-4-(3-карбоксипропиониламино)-2-метилпентановая кислота и этиловый эфир 5-бифенил-4-ил-4-(3-карбоксипропиониламино)-2-метилпентановой кислоты (WO 2007/056546); даглутрил [(3S,2'R)-3-{1-[2'-(этоксикарбонил)-4'-фенилбутил]циклопентан-1-карбониламино}-2,3,4,5-тетрагидро-2-оксо-1H-1-бензазепин-1-уксусная кислота], описанный в WO 2007/106708, Khder et al. (Novartis AG); и их комбинации. В конкретном варианте осуществления изобретения, ингибитор NEP выбран из AHU-377, кандоксатрила, кандоксатрилата, CGS-24128, фосфорамидона, SCH-32615, SCH-34826, SQ-28603, тиорфана и их комбинаций. В конкретном варианте осуществления изобретения, ингибитор NEP представляет собой соединение, такое как даглутрил, которое также обладает активностью как ингибитор эндотелии превращающего фермента (ЕСЕ), так и NEP. Могут быть использованы также другие соединения ECE/NEP двойного действия. Ингибитор NEP вводят в количестве, достаточном для обеспечения около 20-800 мг в день, при обычном интервале суточных доз 50-700 мг в день, чаще 100-600 или 100-300 мг в день.
В одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с донором оксида азота, примеры которого включают, но, не ограничиваясь ими, никорандил; органические нитраты, такие как пентаэритритола тетранитрат; и синдоимины, такие как линзидомин и молзидомин.
В еще одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с нестероидными противовоспалительными агентами (NSAID). Иллюстративные NSAID включают, но, не ограничиваясь ими: ацеметацин, ацетил салициловую кислоту, алклофенак, алминопрофен, амфенак, амиприлоз, алоксиприн, аниролак, апазон, азапропазон, бенорилат, беноксапрофен, безпиперилон, броперамол, буклоксовую кислоту, карпрофен, клиданак, диклофенак, дифлунизал, дифталон, эноликам, этодолак, эторикоксиб, фенбуфен, фенклофенак, фенклозиновую кислоту, фенопрофен, фентиазак, фепразон, флуфенамовую кислоту, флуфенизал, флупрофен, флурбипрофен, фурофенак, ибуфенак, ибупрофен, индометацин, индопрофен, изоксепак, изоксикам, кетопрофен, кеторолак, лофемизол, лорноксикамом, меклофенамат, меклофенамовую кислоту, мефенамовую кислоту, мелоксикам, мезаламин, миропрофен, мофебутазон, набуметон, напроксен, нифлумовую кислоту, оксапрозин, окспинак, оксифенбутазон, фенилбутазон, пироксикам, пирпрофен, пранопрофен, салсалат, судоксикам, сульфазалазин, сулиндак, супрофен, теноксикам, тиопинак, тиапрофеновую кислоту, тиоксапрофен, толфенамовую кислоту, толметина трифлумидат, зидометацин, зомепирак и их комбинации. В конкретном варианте осуществления изобретения НПВП выбран из этодолака, флурбипрофена, ибупрофена, индометацина, кетопрофена, кеторолака, мелоксикама, напроксена, оксапрозина, пироксикам и их комбинаций.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с антагонистом рецептора N-метил d-аспартата (NMDA), примеры которого включают, в качестве иллюстрации, но не ограничения, амантадин, декстрометорфан, декстропропоксифен, кетамин, кетобемидон, мемантин, метадон и т.д.
В еще одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с агонистом опиоидного рецептор (также указываемые как опиоидные анальгетики). Иллюстративные агонисты опиоидного рецептора включают, но, не ограничиваясь ими: бупренорфин, буторфанол, кодеин, дигидрокодеин, фентанил, гидрокодон, гидроморфон, леваллорфан, леворфанол, меперидин, метадон, морфин, налбуфин, налмефен, налоприн, налоксон, налтрексон, налорфин, оксикодон, оксиморфон, пентазоцин, пропоксифен, трамадол и их комбинации. В некоторых вариантах осуществления изобретения агонист опиоидного рецептора выбран из кодеина, дигидрокодеина, гидрокодона, гидроморфона, морфина, оксикодона, оксиморфона, трамадола и их комбинаций.
В конкретном варианте осуществления изобретения соединения по изобретению вводят в комбинации с ингибитором фосфодиэстеразы (PDE), в частности, ингибитором PDE-V. Иллюстративные PDE-V ингибиторы включают, но, не ограничиваясь ими, аванафил, лоденафил, мироденафил, силденафил (Revatio®), тадалафил (Adcirca®), варденафил (Levitra®) и уденафил.
В другом варианте осуществления соединения по изобретению вводят в комбинации с аналогом простагландина (также указываемые как простаноиды или аналоги промтациклина). Иллюстративные аналоги простагландина включают, но, не ограничиваясь ими, берапрост натрия, биматопрост, эпопростенол, илопрост, латанопрост, тафлупрост и трепростинил, из которых представляют интерес биматопрост, латанопрост и тафлупрост.
В еще одном варианте осуществления изобретения, соединения по изобретению вводят в комбинации с агонистом рецептора простагландина, примеры которого включают, но, не ограничиваясь ими, биматопрост, латанопрост, травопрост и т.д.
Соединения по изобретению также могут быть введены в комбинации с ингибитором ринина, примеры которого включают, но, не ограничиваясь ими, алискирен, эналкирен, ремикирен и их комбинации.
В другом варианте осуществления соединения по изобретению вводят в комбинации с селективным ингибитором серотонинового ответа (SSRI). Иллюстративные SSRI включают, но, не ограничиваясь ими: циталопрам и метаболит циталопрама десметилциталопрам, дапоксетин, эсциталопрам (например, эсциталопрам оксалат), флуоксетин и метаболит флуоксетина десметил норфлуоксетин, флувоксамин (например, флувоксамин малеат), пароксетин, сертралин и метаболит сертралина деметилсертралин и их комбинации.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с агонистом серотонинового рецептора 5-HT1D, примеры которого включают, в качестве иллюстрации, но не ограничения, триптаны, такие как алмотриптан, авитриптан, элетриптан, фловатриптан, наратриптан, ризатриптан, суматриптан и золмитриптан.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с блокатором натриевых каналов, примеры которого включают, в качестве иллюстрации, но не ограничения, карбамазепин, фосфенитоин, ламотригин, лидокаин, мексилетин, окскарбазепин, фенитоин и их комбинации.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации со стимулятором и активатором растворимой гуанилатциклазы, примеры которого включают, но, не ограничиваясь ими, атацикват, риоцикват и их комбинации.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с трициклическим антидепрессантом (ТСА), примеры которого включают, в качестве иллюстрации, но не ограничения, амитриптилин, амитриптилиноксид, бутриптилин, кломипрамин, демексиптилин, дезипрамин, дибензепин, диметакрин, дозулепин, доксепин, имипрамин, имипраминоксид, лофепрамин, мелитрацен, метапрамин, нитроксазепин, нортриптилин, ноксиптилин, пипофезин, пропизепин, протриптилин, хинкпрамин и их комбинации.
В одном варианте осуществления изобретения соединения по изобретению вводят в комбинации с антагонистом рецептора вазопрессина, примеры которого включают, в качестве иллюстрации, но не ограничения, кониваптан и толваптан.
Объединенные вторые терапевтические агенты также могут быть полезными в дальнейшей комбинационной терапии с соединением по изобретению. Например, соединения по изобретению могут быть объединены с диуретиком и ARB, или блокатором кальциевых каналов и ARB, или диуретиком и ингибитором ACE, или блокатором кальциевых каналов и статина. Конкретные примеры включают комбинацию ингибитора ACE энелаприла (в виде малеатной соли) и диуретика гидрохлортиазида, который продается под маркой Vaseretic®, или комбинацию блокатора кальциевых каналов амлодипина (в виде безилатной соли) и ARB олмесартана (в форме пролекарства медоксомил), или комбинацию блокатора кальциевых каналов и статина, все также могут быть использованы с соединениями по изобретению. Другие терапевтические агенты, такие как агонисты рецептора α2-адренергического и антагонисты рецептора вазопрессина также могут быть полезными в комбинационной терапии. Примеры α2-адренергического рецептора агонисты включают клонидин, дексмедетомидин и кванфацин.
Следующие препараты иллюстрируют иллюстративные фармацевтические композиции по изобретению.
Примеры твердых желатиновых капсул для перорального введения
Соединение по изобретению (50 г), 440 г высушенную распылением лактозу и 10 г стеарата магния тщательно перемешивают. Полученную композицию затем загружают в твердые желатиновые капсулы (500 мг композиции на капсулу). Альтернативно, соединение по изобретению (20 мг) тщательно перемешивают с крахмалом (89 мг), микрокристаллической целлюлозой (89 мг) и стеаратом магния (2 мг). Смесь затем пропускают через сито №45 меш США и загружают в твердые желатиновые капсулы (200 мг композиции на капсулу).
Альтернативно, соединение по изобретению (30 г), вторичный агент (20 г), 440 г высушенной распылением лактозы и 10 г стеарата магния тщательно перемешивают и обрабатывают, как описано выше.
Примеры желатиновых капсул для перорального введения
Соединение по изобретению (100 мг) тщательно перемешивают с моноолеатом полиоксиэтиленсорбитана (50 мг) и порошком крахмала (250 мг). Смесь затем загружают в желатиновые капсулы (400 мг композиции на капсулу). Альтернативно, соединение по изобретению (70 мг) и второй агент (30 мг) тщательно смешивают с моноолеатом полиоксиэтиленсорбитана (50 мг) и порошком крахмала (250 мг), и полученную смесь загружают в желатиновую капсулу (400 мг композиция на капсулу).
Альтернативно, соединение по изобретению (40 мг) тщательно перемешивают с микрокристаллической целлюлозой (Avicel PH 103; 259,2 мг) и стеаратом магния (0,8 мг). Смесь затем загружают в желатиновую капсулу (размер №1, белая, непрозрачная) (300 мг композиции на капсулу).
Примеры препарата в виде таблеток для перорального введения
Соединение по изобретению (10 мг), крахмал (45 мг) и микрокристаллическую целлюлозу (35 мг) пропускают через сито №20 меш США и тщательно смешивают. Полученные таким образом гранулы сушат при температуре 50-60°С и пропускают через сито №16 меш США. Раствор поливинилпирролидона (4 мг в виде 10%-ного раствора в стерильной воде) смешивают с натрийкарбоксиметилкрахмалом (4,5 мг), стеаратом магния (0,5 мг) и тальком (1 мг), и полученную смесь затем пропускают через сита №16 меш США. Затем добавляют в гранулы натрийкарбоксиметилкрахмал, стеарат магния и тальк. После перемешивания смесь прессуют на таблеточной машине, с получением таблеток массой 100 мг.
Альтернативно, соединение по изобретению (250 мг) тщательно перемешивают с микрокристаллической целлюлозой (400 мг), тонкодисперсным диоксидом кремния (10 мг) и стеариновой кислотой (5 мг). Смесь затем прессуют в таблетки (665 мг композиции на таблетку).
Альтернативно, соединение по изобретению (400 мг) тщательно перемешивают с кукурузным крахмалом (50 мг), тонкоизмельченной натрийкроскармеллозой (25 мг), лактозой (120 мг) и стеаратом магния (5 мг). Смесь затем прессуют в форме таблеток (600 мг композиции на таблетку).
Альтернативно, соединение по изобретению (100 мг) тщательно перемешивают с кукурузным крахмалом (100 мг) и водным раствором желатина (20 мг). Смесь сушат и измельчают в мелкий порошок. Микрокристаллическую целлюлозу (50 мг) и стеарат магния (5 мг) затем смешивают с желатиновым препаратом, гранулируют, и полученную смесь прессуют в таблетки (100 мг соединения по изобретению на таблетку).
Примеры суспензионного препарата для перорального введения
Следующие ингредиенты смешивают с образованием суспензии, содержащей 100 мг соединения по изобретению на 10 мл суспензии:
Примеры жидкого препарата для перорального введения
Подходящий жидкий препарат представляет собой кислотно-основной буфер, такой как цитратный, лактатный и малеатный буферные растворы. Например, соединения по изобретению (которые могут быть предварительно смешаны с ДМСО) смешивают с 100 мМ буфером цитрата аммония и доводят pH до pH 5, или смешивают со 100 мМ раствором лимонной кислоты и pH доводят до pH 2. Такие растворы также могут включать солюбилизирующий эксципиент, такой как циклодекстрин, например, раствор может содержать 10% масс. гидроксипропил-β-циклодекстрина.
Другие подходящие препараты включают 5%-ный раствор NaHCO3 с циклодекстрином или без него.
Примеры инъекционного препарата для введения путем инъекции
Соединение по изобретению (0,2 г) смешивают с 0,4M буферным раствором ацетата натрия (2,0 мл). pH полученного раствора доводят до pH 4 с использованием 0,5н водной хлористоводородной кислоты или 0,5н водного гидроксида натрия, что необходимо, и затем добавляют достаточное количество воды для инъекции до достижения общего объема в 20 мл. Смесь затем фильтруют через стерильный фильтр (0,22 микрон), с получением стерильного раствора, подходящего для введения путем инъекции.
Примеры композиций для введения путем ингаляции
Соединение по изобретению (0,2 мг) микронизируют и затем смешивают с лактозой (25 мг). Полученную смешанную смесь затем загружают в желатиновый картридж для ингаляции. Содержимое картриджа вводят, например, с использованием сухого порошкового ингалятора.
Альтернативно, микронизированное соединение по изобретению (10 г) диспергируют в растворе, полученном растворением лецитина (0,2 г) в деминерализованной воде (200 мл). Полученную суспензию подвергают распылительной сушке и затем измельчают до образования микронизированной композиции, содержащий частицы, имеющие средний диаметр менее чем около 1,5 мкм. Микронизированную композицию затем загружают в дозированные картриджи ингалятора, содержащие под давлением 1,1,1,2-тетрафторэтан в количестве, достаточном, чтобы обеспечить от около 10 мкг до около 500 мкг соединения по изобретению на дозу при введении в ингалятор.
Альтернативно, соединение по изобретению (25 мг) растворяют в цитратном буфере (pH 5) изотонического солевого раствора (125 мл). Смесь перемешивают и подвергают воздействию ультразвуком до растворения соединения. pH раствора контролируют и доводят, если необходимо, до pH 5 медленным добавлением 1н водного раствора NaOH. Раствор вводят с использованием распылительного устройства, которое обеспечивает от около 10 мкг до около 500 мкг соединения по изобретению на дозу.
ПРИМЕРЫ
Следующие получения и примеры предназначены для иллюстрации конкретных вариантов осуществления изобретения. Указанные конкретные варианты осуществления изобретения, однако, не предназначены для ограничения объема изобретения каким-либо образом, если специально не указано иное.
Следующие аббревиатуры имеют следующие значения, если не указано иное, и другие используемые и не определенные здесь аббревиатуры имеют свои стандартные, общепринятые значения:
AcOH уксусная кислота
(Boc)2O ди-трет-бутилдикарбонат
DCC дициклогексилкарбодиимид
DCM дихлорметан или метиленхлорид
DIBAL гидрид диизобутилалюминия
DIPEA N,N-диизопропилэтиламин
DMAP 4-диметиламинопиридин
ДМФ N,N-диметилформамид
ДМСО диметилсульфоксид
Dnp 2,4-динитрофенил
EDCI N-(3-диметиламинопропил)-N'-этилкарбодиимид
Et3N триэтиламин
Et2O диэтиловый эфир
EtOAc этилацетат
EtOH этанол
HATU гексафторфосфат N,N,N',N'-тетраметил-O-(7-азабензотриазол-1-ил)урония
HCTU (гексафторфосфат 2-(6-хлор-1H-бензотриазол-1-ил)-1,1,3,3-тетраметиламиния)
HEPES 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота
HOAt 1-гидрокси-7-азабензотриазол
LiHMDS гексаметилдисилазид лития
Mca (7-метоксикумарин-4-ил)ацил
MeCN ацетонитрил
MeOH метанол
Pd(PPh3)4 тетракис(трифенилфосфин)палладий(0)
SilicaCat®DPP-Pd катализатор дифенилфосфинпалладий(II) на основе диоксида кремния
SilicaCat®Pd(0) катализатор палладий (0) на основе диоксида кремния
ТФУ трифторуксусная кислота
ТГФ тетрагидрофуран
Если не указано иное, все материалы, такие как реагенты, исходные продукты и растворители, были приобретены у коммерческих поставщиков (таких как Sigma-Aldrich, Fluka Riedel-de  и тому подобное) и были использованы без дополнительной очистки.
и тому подобное) и были использованы без дополнительной очистки.
Реакции проводили в атмосфере азота, если не указано иное. Протекание реакции контролировали с помощью тонкослойной хроматографии (ТСХ), аналитической высокоэффективной жидкостной хроматографии (аналитическая ВЭЖХ) и масс-спектрометрии, детали которых приведены в конкретных примерах. Растворители, используемые в аналитической ВЭЖХ были следующими: растворитель A представлял собой 98% H2O/2% MeCN /1,0 мл/л ТФУ; растворитель B представлял собой 90% MeCN/10% H2O/1,0 мл/л ТФУ.
Реакционные смеси обрабатывали, как описано конкретно для каждого получения, например: обычно реакционные смеси очищали путем экстракции и другими способами очистки, такими как зависящая от температуры и растворителей кристаллизация и осаждение. Кроме того, реакционные смеси обычно очищали препаративной ВЭЖХ, обычно используя упаковки колонок Microsorb C18 и Microsorb BDS и общепринятые элюенты. Протекание реакции обычно определяли с помощью жидкостной хроматографии с масс-спектрометрией (ЖХМС). Изомеры охарактеризовывали с помощью спектроскопии ядерного эффекта Оверхаузера (NOE). Продукты реакции охарактеризовывали обычным образом с помощью масс и 1H-ЯМР спектрометрии. Для получения данных ЯМР, образцы растворяли в дейтерированном растворителе (CD3OD, CDCl3 или ДМСО-d6), и 1H-ЯМР спектр регистрировали на приборе Varian Gemini 2000 (400 МГц) в стандартных условиях наблюдения. Масс-спектрометрическую идентификацию соединений обычно осуществляли, используя способ ионизации электрораспылением (ESMS) на приборе Applied Biosystems (Foster City, CA) модель API 150 EX или на приборе Agilent (Palo Alto, CA) модель 1200 LC/MSD.
Получение 1
Оксодипероксимолибден(пиридин)(гексаметилфосфорнойтриамид)

Оксид молибдена (MoO3; 30 г, 0,2 моль) и 30%-ный пероксид водорода (150 мл) объединяли при перемешивании. Реакционный сосуд помещали на масляную баню, уравновешенную при температуре 40°C, и нагревали до достижения внутренней температуры 35°C. Нагревательную баню затем отставляли и заменяли водяной баней для контроля экзотермической реакции средней силы таким образом, чтобы поддерживалась внутренняя температура 35-40°C. После начального экзотермического периода (~30 минут) реакционный сосуд снова помещали на масляную баню при температуре 40°C и перемешивали в течение всего 3,5 часов с образованием желтого раствора с небольшим количеством суспендированного белого твердого вещества. После охлаждения до температуры 20°C раствор фильтровали, и полученный желтый фильтрат охлаждали до температуры 10°C (ледяная баня, при перемешивании) и в течение 5 минут добавляли по каплям гексаметилфосфортриамид ((Me2N)3PO; HMPA; 37,3 г, 0,2 моль), что приводило к получению кристаллического желтого осадка. Перемешивание продолжали в течение всего около 15 минут при температуре 10°C, и продукт фильтровали и сушили отжатием. После 30 минут выдерживания в вакууме осадок на фильтре объединяли с MeOH (20 мл) и перемешивали при температуре 40°C. Медленно добавляли дополнительное количество MeOH до растворения твердых продуктов. Насыщенный раствор охлаждали в холодильнике, с получением желтого твердого вещества (выделяется в виде игл). Твердую массу механически дробили, фильтровали и промывали холодным MeOH (20-30 мл), с получением продукта оксодипероксимолибден(водный)(гексаметилфосфортриамида) (MoO5·H2O·HMPA, 46-50 г).
MoO5·H2O·HMPA сушили над оксидом фосфора в вакуумном эксикаторе, экранируя от воздействия света, в течение 24 часов при давлении 0,2 мм рт. ст., с получением слегка гигроскопичного желтого твердого вещества, MoO5·HMPA. MoO5·HMPA (36,0 г, 0,1 моль) растворяли в ТГФ (150 мл), и раствор фильтровали для удаления осадка. Фильтрат затем перемешивали при температуре 20°C, при этом в течение 10 минут добавляли сухой пиридин (8,0 г, 0,1 моль). Кристаллический продукт желтого цвета собирали, промывали сухим ТГФ (25 мл) и безводным эфиром (200 мл) и сушили в вакуумном эксикаторе (1 час, 0,2 мм рт. ст.), с получением указанного в заголовке соединения, оксодипероксимолибден(пиридин)(гексаметилфосфортриамида) (MoO5·Py·HMPA) в виде тонкоизмельченного желтого твердого вещества (36-38 г).
Получение 2
трет-Бутиловый эфир (S)-2-бифенил-4-илметил-5-оксопирролидин-1-карбоновой кислоты

В перемешиваемый раствор (R)-3-бифенил-4-ил-2-трет-бутоксикарбониламинопропионовой кислоты (50 г, 146,5 ммоль), кислоты Мельдрума (23,3 г, 161,1 ммоль) и DMAP (27,8 г, 227 ммоль) в безводном DCM (500 мл) в атмосфере азота добавляли раствор DCC (33,3 г, 161,1 ммоль) в безводном DCM (200 мл) в течение 1 часа при температуре -5°C. Смесь перемешивали при температуре -5°C в течение 8 часов, затем охлаждали в течение ночи, при этом выпадали крошечные кристаллы дициклогексилмочевины. После фильтрования смесь промывали 5% KHSO4 (4×200 мл), насыщенным водным раствором NaCl (1×200 мл) и сушили над MgSO4 в течение ночи. Полученный раствор упаривали, с получением неочищенного соединения 1 (68 г) в виде светло-желтого твердого вещества). ЖХ-МС: [M+Na]:490, [2M+Na]:957.

В раствор неочищенного соединения 1 (68 г, 146,5 ммоль) в безводном DCM (1000 мл) в атмосфере азота добавляли AcOH (96,8 г, 1,6 моль) при температуре -5°C. Полученную смесь перемешивали при температуре -5°C в течение 0,5 часов, затем в течение 2 часов небольшими порциями добавляли NaBH4 (13,9 г, 366 ммоль). После перемешивания в течение еще часа при температуре -5°C добавляли насыщенный водный раствор NaCl (300 мл). Органический слой промывали насыщенным водным раствором NaCl (2×300 мл), затем водой (2×300 мл), сушили над MgSO4, фильтровали и упаривали, с получением неочищенного соединения 2, которое затем очищали хроматографией (гексан:EtOAc=5:1), с получением очищенного соединения 2 (46 г) в виде светло-желтого твердого вещества. ЖХ-МС: [M+Na]:476, [2M+Na]:929.
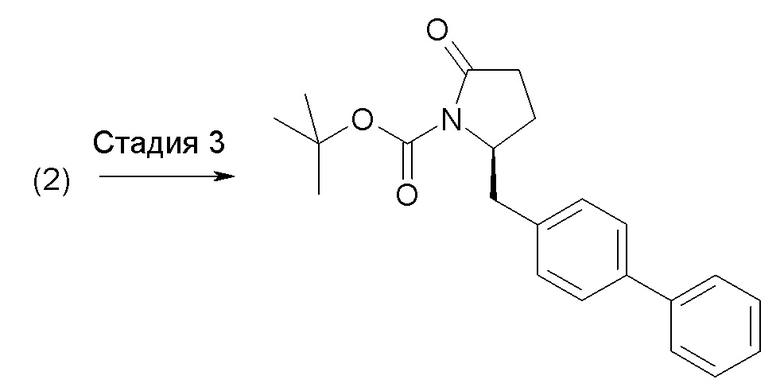
Перемешиваемый раствор очищенного соединения 2 (46 г, 101 ммоль) в безводном толуоле (300 мл) нагревали при кипячении с обратным холодильником в атмосфере азота в течение 3 часов. После упаривания растворителя остаток очищали хроматографией (гексан:EtOAc=10:1), с получением указанного в заголовке соединения (27 г) в виде светло-желтого твердого вещества.
ЖХ-МС: [M+Na]: 374, [2M+Na]: 725;
1H ЯМР (300 МГц, CDCl3): (7,64-7,62 (м, 4H), 7,51-7,46 (м, 2H), 7,42-7,39 (м, 1H), 7,39-7,30 (м, 2H), 4,50-4,43 (м, 1H), 3,27-3,89 (м, 1H), 2,88-2,80 (м, 1H), 2,48-2,42 (м, 2H), 2,09-1,88 (м, 2H), 1,66 (с, 9H).
Получение 3
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты и этиловый эфир (2R,4S)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты
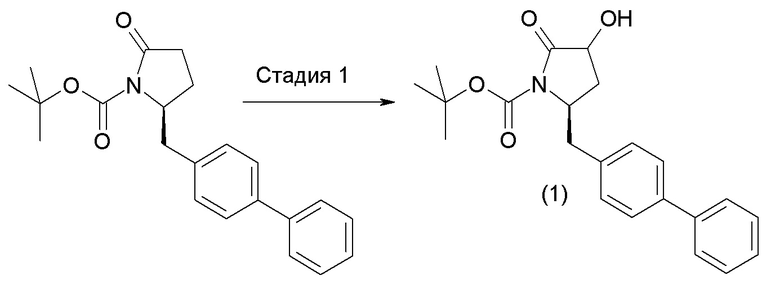
Стадия 1: В перемешиваемый раствор трет-бутилового эфира (S)-2-бифенил-4-илметил-5-оксопирролидин-1-карбоновой кислоты (4,4 г, 12,4 ммоль) в безводном ТГФ (70 мл) в течение 15 минут в атмосфере азота добавляли раствор 1M LiHMDS в ТГФ (28 мл) при температуре -65°C. После перемешивания в течение 3 часов при температуре -65°C добавляли оксодипероксимолибден(пиридин)(гексаметилфосфортриамид) (9 г, 18,6 ммоль). Смесь перемешивали в течение еще 2 часов при температуре -35°C, затем добавляли насыщенный водный раствор Na2S2O3 (60 мл). Органический слой собирали и промывали насыщенным водным раствором NH4Cl (60 мл ×3) и насыщенным водным раствором NaCl (60 мл ×2), затем сушили над Na2SO4 и растворитель удаляли при пониженном давлении, с получением неочищенного продукта, который затем очищали хроматографией (гексан:EtOAc=5:1), с получением соединения 1 в виде белого твердого вещества (1,8 г). ЖХ-МС: [2M+Na]:757.

Стадия 2: В раствор соединения 1 (1,8 г, 5,0 ммоль) в безводном DCM (50 мл) при температуре 0°C в атмосфере азота добавляли DMAP (122 мг, 1 ммоль) и Et3N (1,5 г, 14,9 ммоль). После перемешивания в течение 0,5 час при температуре 0°C, в течение 15 минут добавляли бензилхлорид (1,0 г, 7,4 ммоль). Смесь перемешивали в течение дополнительных 2 часов при температуре 0°C, затем добавляли насыщенный водный раствор NaHCO3 (50 мл). Органический слой собирали и промывали насыщенным водным раствором NaHCO3 (50 мл ×2) и насыщенным водным раствором NaCl (50 мл ×1), затем сушили над Na2SO4. Твердые продукты отфильтровывали, и фильтрат концентрировали, с получением неочищенного продукта, который затем очищали хроматографией (гексан:EtOAc=4:1), с получением соединения 2A (471 мг) и соединения 2B (883 мг) в виде белого твердого вещества. ЖХ-МС: [M+Na]:494; [2M+Na]:965.
Соединение 2A: 1H ЯМР (300 МГц, CDCl3): ((м.д.)=8,02 (м, 2H), 7,57-7,25 (м, 12H), 5,42 (м, 1H), 4,50 (м, 1H), 3,26-3,21 (м, 1H), 2,90 (м, 1H), 2,58 (м, 1H), 2,15-2,05 (м, 1H), 1,62 (м, 9H)
Соединение 2B: 1H ЯМР (300 МГц, CDCl3): ((м.д.)=8,06 (м, 2H), 7,58-7,18 (м, 12H), 5,53-5,41 (м, 1H), 4,39 (м, 1H), 3,57-3,54 (м, 1H), 2,87-2,80 (м, 1H), 2,48-2,44 (м, 1H),1,98 (м, 1H), 1,63 (м, 9H).

Стадия 3: В перемешиваемый раствор соединения 2A (471 мг, 1 ммоль) в безводном EtOH (10 мл) при комнатной температуре в атмосфере азота добавляли безводный K2CO3 (691 мг, 5 ммоль). После перемешивания в течение 20 часов при комнатной температуре, твердые продукты отфильтровывали. В фильтрат добавляли воду (30 мл), DCM (30 мл) и насыщенный водный раствор NaCl (5 мл). Водный слой отделяли и экстрагировали DCM (30 мл ×3). Объединенные органические слои промывали насыщенным водным раствором NaCl (50 мл), сушили над Na2SO4 и концентрировали, с получением неочищенного продукта, который затем очищали хроматографией (гексан:EtOAc=6:1), с получением соединения 3 в виде белого твердого вещества (275 мг). ЖХ-МС: [M+Na]: 436, [2M+Na]: 849.

Стадия 4: В EtOH (5 мл) при температуре -30°C добавляли ацетилхлорид (685 мг). После перемешивания в течение 1 час при температуре -30°C добавляли раствор соединения 3 (275 мг, 665 мкмоль) в безводном EtOH (5 мл). Смесь нагревали до 25°C и перемешивали в течение 3 часов при температуре 25°C. После упаривания растворителя остаток промывали холодным безводным Et2O (10 мл), с получением этилового эфира (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты в виде белого твердого вещества, HCl соль (207 мг). ЖХ-МС: [M+H]:314, [2M+Na]:649.
1H ЯМР (300 МГц, CDCl3): ((м.д.)=7,99 (м, 3H), 7,66-7,64 (м, 4H), 7,48-7,35 (м, 5H), 6,08 (м, 1H), 4,21 (м, 1H), 4,09-4,05 (м, 2H), 3,52 (м, 1H), 2,97-2,95 (м, 2H), 1,89-1,87 (м, 2H), 1,19-1,14 (м, 3H).

Стадия 5: В перемешиваемый раствор соединения 2B (883 мг, 1,9 ммоль) в безводном EtOH (15 мл) при комнатной температуре добавляли безводный K2CO3 (1293 мг, 9,4 ммоль) в атмосфере азота. После перемешивания в течение 20 часов при комнатной температуре твердые продукты отфильтровывали. В фильтрат добавляли воду (30 мл), DCM (30 мл) и насыщенный водный раствор NaCl (5 мл). Водный слой отделяли и экстрагировали DCM (30 мл ×3). Объединенные органические слои промывали насыщенным водным раствором NaCl (50 мл), сушили над Na2SO4 и концентрировали, с получением неочищенного продукта, который затем очищали хроматографией (гексан:EtOAc=6:1), с получением соединения 4 в виде белого твердого вещества (524 мг). ЖХ-МС: [M+Na]: 436, [2M+Na]: 849.

Стадия 6: В EtOH (8 мл) при температуре -30°C добавляли ацетилхлорид (1300 мг). После перемешивания в течение 1 час при температуре -30°C добавляли раствор соединения 4 (524 мг, 1,3 ммоль) в безводном EtOH (8 мл). Смесь нагревали до 25°C и перемешивали в течение 3 часов при температуре 25°C. После упаривания растворителя остаток промывали холодным безводным Et2O (10 мл), с получением этилового эфира (2R,4S)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты в виде белого твердого вещества, HCl соль (395 мг). ЖХ-МС: [M+H]:314, [2M+Na]:649.
1H ЯМР (300 МГц, CDCl3): ((м.д.)=8,14 (м, 3H), 7,66-7,62 (м, 4H), 7,47-7,31 (м, 5H), 5,87-5,85 (м, 1H), 4,34 (м, 1H), 4,08-4,00 (м, 2H), 3,48 (м, 1H), 3,09 (м, 1H), 2,85-2,81 (м, 1H), 1,88 (м, 1H), 1,76 (м, 1H), 1,15-1,10 (м, 3H).
Альтернативный синтез
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты
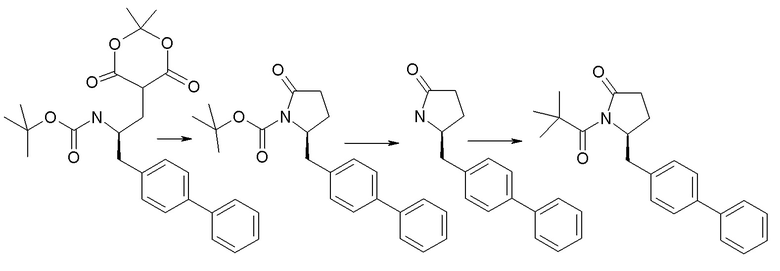
Раствор трет-бутилового эфира [(S)-2-бифенил-4-ил-1-(2,2-диметил-4,6-диоксо[1,3]диоксан-5-илметил)этил]карбаминовой кислоты (143 г, 320 ммоль) в безводном толуоле (1 л) нагревали при кипячении с обратным холодильником в атмосфере азота в течение ночи. Растворитель удаляли при пониженном давлении, с получением трет-бутилового эфира (S)-2-бифенил-4-илметил-5-оксопирролидин-1-карбоновой кислоты, который использовали напрямую без дополнительной очистки и добавляли в раствор 3н HCl в EtOAc (1,2 л). Полученную смесь перемешивали в течение 3 часов при комнатной температуре. Растворитель удаляли в вакууме. Остаток перекристаллизовывали из EtOAc (300 мл), с получением первой партии соединения с удаленными защитными группами (56 г). Маточную жидкость подвергали колоночной хроматографии (элюировали смесью EtOAc и гексана от 1:1 до 100% EtOAc), с получением второй партии соединения с удаленными защитными группами (8 г). В суспензию соединения с удаленными защитными группами (64 г, 250 ммоль) в безводном ТГФ (500 мл) добавляли по каплям BuLi (100 мл, 2,5М в гексане) при температуре -78°C. После перемешивания в течение 0,5 час добавляли по каплям пивалоилхлорид (34 г, 0,28 моль). Смесь перемешивали в течение 1 часа при температуре -78°C. Реакцию затем гасили насыщенным водным раствором NH4Cl, и смесь экстрагировали EtOAc. Экстракт сушили над MgSO4 и концентрировали, с получением (S)-5-бифенил-4-илметил-1-(2,2-диметилпропионил)пирролидин-2-она (85 г) в виде белого твердого вещества.

(S)-5-Бифенил-4-илметил-1-(2,2-диметилпропионил)пирролидин-2-он (40 г, 120 ммоль) растворяли в безводном ТГФ (400 мл) и перемешивали при температуре -78°C в атмосфере азота. В раствор в течение 5 минут добавляли по каплям 1,5 экв. 2,0M раствора натрия бис(триметилсилил)амида в ТГФ. Смесь светло-желтого цвета перемешивали в течение 20 минут в атмосфере азота при температуре -78°C, затем медленно по каплям добавляли оксазиридин (53 г, 180 ммоль) в виде 200 мл раствора в ТГФ. Смесь перемешивали в течение 0,5 час. Реакцию гасили насыщенным водным раствором NH4Cl, и смесь экстрагировали EtOAc (1 л). Экстракт промывали 1н HCl (1 л), сушили над MgSO4 и концентрировали до объема в 500 мл. Выпавший твердый белый продукт отфильтровывали, после добавления силикагеля (200 г) фильтрат концентрировали для удаления растворителя. Остаток помещали на колонку (8×80 см) с силикагелем (900 г), которую предварительно набивали в гексане. Элюирование проводили сначала смесью DCM:гексан (1:1). Когда оксазиридин и имин были полностью собраны, колонку элюировали DCM, с получением (3R,5R)-5-бифенил-4-илметил-1-(2,2-диметилпропионил)-3-гидроксипирролидин-2-она (21 г, 98%-ная чистота) в виде желтого масла.
(3R,5R)-5-Бифенил-4-илметил-1-(2,2-диметилпропионил)-3-гидроксипирролидин-2-он (56 г, 0,156 моль) растворяли в EtOH (700 мл) и 12н HCl (700 мл). Смесь нагревали при 90~95°C в течение 20 часов. Смесь концентрировали на водяной бане с температурой 80°C при пониженном давлении. К остатку добавляли EtOH (100 мл), и полученную смесь фильтровали, с получением желтого твердого вещества. Данный твердый продукт суспендировали в смеси 3н HCl/EtOH (800 мл). Смесь кипятили с обратным холодильником в течение 3 часов. Раствор концентрировали для уменьшения объема (объем ~200 мл), и добавляли эфир (200 мл). Полученное желтоватое твердое вещество отфильтровывали и сушили при пониженном давлении, с получением этилового эфира (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (43 г).
Получение 4
Бутиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты

1-Бутанол (40 мл, 400 ммоль) охлаждали на ледяной бане и добавляли по каплям ацетилхлорид до достижения концентрации 4н HCl. Смесь нагревали до комнатной температуры. К подкисленному бутанолу (15 мл) добавляли этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 250 мг, 710 мкмоль), и смесь герметически закрывали и нагревали при 80°C в течение 3 часов. Полученный продукт сушили в вакууме, с получением указанного в заголовке соединения в виде хлопьевидного белого/оранжевого твердого продукта, HCl соль (220 мг).
ПРИМЕР 1

A. Этиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-CH2CH3)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 500 мг, 1 ммоль, 1,0 экв.), 5-ацетил-2H-пиразол-3-карбоновую кислоту (330,4 мг, 2,1 ммоль, 1,5 экв.) и HATU (820 мг, 2,1 ммоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (750 мкл), и смесь перемешивали в течение 1 часа. Смесь сушили в вакууме, и продукт очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением указанного в заголовке соединения (300 мг, чистота 98%) в виде соли с ТФУ. МС m/z [M+H]+ вычислено для C25H27N3O5, 450,20; найдено 450,2.
B. (2R,4R)-4-[(5-Ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановая кислота (R7=H)
Часть (200 мг) очищенного этилового эфира (соединение A) растворяли в EtOH (~10 мл) и добавляли 10н NaOH, для подщелачивания раствора (~200 мкл). Смесь контролировали в течение 1 часа до полного удаления защитных групп. Смесь подкисляли равным объемом (~200 мкл) AcOH и сушили в вакууме. Продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (160 мг; чистота 100%). МС m/z [M+H]+ вычислено для C23H23N3O5, 422,16; найдено 422,2.
C. Бутиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-(CH2)3CH3)
Бутиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 500 мг, 1 ммоль, 1,0 экв.), 3-ацетил-1H-пиразол-5-карбоновую кислоту (330,4 мг, 2,1 ммоль, 1,5 экв.) и HATU (820 мг, 2,1 ммоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (750 мкл), и смесь перемешивали в течение 1 часа. Смесь сушили в вакууме, и продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (45 мг; чистота 95%). МС m/z [M+H]+ вычислено для C27H31N3O5, 478,23; найдено 478,4.
D. 2-Метоксиэтиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-(CH2)2OCH3)
Насыщенный раствор HCl в 2-метоксиэтаноле получали путем добавления по каплям ацетилхлорида (~400 мкл) к 10 мл безводного спирта. К полученному раствору добавляли этиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (21,3 мг, 47,4 мкмоль), и полученную смесь нагревали при 60°C в течение 1-2 часов. Продукт сушили в вакууме. Продукт затем очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (10 мг; чистота 100%) МС m/z [M+H]+ вычислено для C26H29N3O6, 480,21; найдено 480,4.
E. 5-Метил-2-оксо[1,3]диоксол-4-илметиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-CH2-5-метил[1,3]диоксол-2-он)
(2R,4R)-4-[(5-Ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановую кислоту (20 мг, 50 мкмоль) растворяли в сухом ДМФ (2 мл). Добавляли карбонат дицезия (50 мг, 0,2 ммоль), и полученную смесь перемешивали при температуре 0°C в течение 1 часа. Добавляли 4-хлорметил-5-метил-1,3-диоксол-2-он (20 мг, 0,1 ммоль), и полученную смесь перемешивали при комнатной температуре в течение ночи. Добавляли EtOAc (20 мл), и смесь промывали насыщенным водным раствором NaCl (100 мл), затем сушили в вакууме. Продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (5 мг, чистота 100%). МС m/z [M+H]+ вычислено для C28H27N3O8, 534,18; найдено 534,4.
F. 2-Морфолин-4-илэтиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-(CH2)2-морфолин)
(2R,4R)-4-[(5-Ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановую кислоту (50 мг, 120 мкмоль, 1,1 экв.) и HATU (42 мг, 110 мкмоль, 1,0 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли 4-морфолинэтанол (73 мг, 560 мкмоль, 5,0 экв.), затем добавляли DIPEA. Полученную смесь перемешивали в течение 1 часа, затем продукт сушили в вакууме. Далее продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (приблизительно 4 мг, чистота 95%). МС m/z [M+H]+ вычислено для C29H34N4O6, 535,25; найдено 535,4.
G. 2-Метансульфонилэтиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-(CH2)2-SO2-CH3)
2-(Метилсульфонил)этанол (690 мг, 5,6 ммоль) нагревали при 40°C и при перемешивании в течение 5 минут добавляли 0,5 экв. ацетилхлорида. Добавляли этиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты (50 мг, 110 мкмоль), и реакционный сосуд герметически закрывали и нагревали при 70°C в течение 2 часов. Продукт затем очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (приблизительно 28 мг, чистота 95%). МС m/z [M+H]+ вычислено для C26H29N3O7S, 528,17; найдено 528,4.
Получение 5
Этиловый эфир ацетокси(диэтоксифосфорил)уксусной кислоты
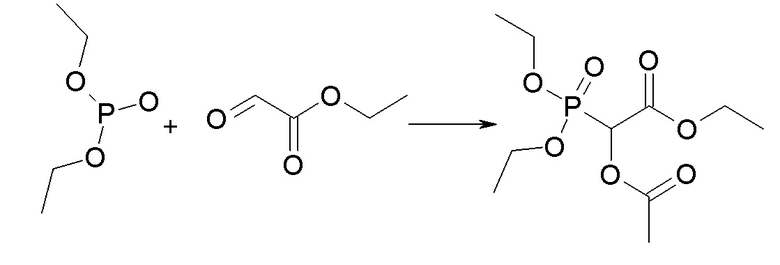
В раствор диэтилгидрофосфита (50 г, 362,1 ммоль, 1,0 экв.) в толуоле (100 мл) при перемешивании в атмосфере азота добавляли по каплям этил 2-оксоацетат (50%) (74 г, 724,8 ммоль, 1,0 экв.) при температуре 0°C. При перемешивании добавляли по каплям Et3N (110 г, 1,1 моль, 3,0 экв.) при температуре 0°C. Полученный раствор перемешивали в течение 1 часа при комнатной температуре. В смесь по каплям при перемешивании добавляли уксусный ангидрид (37 г, 362,4 ммоль, 1,0 экв.) при температуре 0°C. Полученный раствор перемешивали в течение ночи при комнатной температуре. pH раствора доводили до 6 с использованием 2н HCl. Полученный раствор экстрагировали DCM (3×150 мл), и органические слои объединяли, сушили над Na2SO4 и концентрировали в вакууме. Остаток помещали на колонку с силикагелем с помощью смеси EtOAc:гексан (1:2~1:5), с получением указанного в заголовке соединения (52 г) в виде светло-желтой жидкости.
Получение 6
трет-Бутиловый эфир [(R)-2-бифенил-4-ил-1-(метоксиметилкарбамоил)этил]карбаминовой кислоты
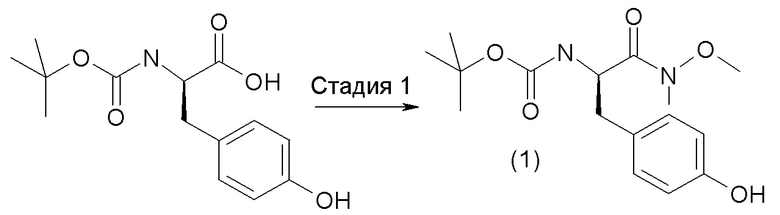
Стадия 1: N-трет-Boc-D-тирозин (80,0 г, 284,4 ммоль, 1,0 экв.), гидрохлорид O,N-диметилгидроксиламина (33,3 г, 341,4 ммоль, 1,2 экв.), гидрохлорид 1-этил-3-((3-диметиламино)пропил)карбодиимида (81,8 г, 426,7 ммоль, 1,5 экв.), гидроксибензотриазол (57,6 г, 426,4 ммоль, 1,5 экв.) и DCM (высушенный) (800 мл) объединяли при перемешивании в атмосфере азота. Полученную смесь охлаждали до температуры 0°C, и при перемешивании в течение 40 минут добавляли по каплям Et3N (44,0 г, 434,8 ммоль, 1,53 экв.). Полученный раствор перемешивали в течение ночи при комнатной температуре, затем промывали насыщенным водным раствором NaHCO3 (2×300 мл). Органический слой отделяли, и водный слой снова экстрагировали DCM (200 мл). Органические фазы объединяли, сушили над Na2SO4 и концентрировали в вакууме, с получением неочищенного соединения 1 (100 г) в виде желтого твердого вещества.

Стадия 2: Соединение 1 (100,0 г, неочищенное, 308,3 ммоль, 1,0 экв.), пиридин (61,0 г, 771,2 ммоль, 2,5 экв.) и DCM (высушенный) (1000 мл) объединяли при перемешивании в атмосфере азота. Полученную смесь охлаждали до температуры -20°C, и затем при перемешивании в течение 30 минут добавляли по каплям ангидрид трифторметансульфоновой кислоты (104,0 г, 368,6 ммоль, 1,2 экв.) при температуре -20°C. Полученный раствор затем перемешивали в течение 30 минут при температуре -20~-15°C. Реакцию затем гасили путем добавления воды (250 мл). Полученную смесь промывали 0,5н раствором NaOH (2×300 мл) и 15%-ным раствором лимонной кислоты (2×300 мл). Основной водный слой снова экстрагировали DCM (200 мл), и органические фазы объединяли, сушили над Na2SO4 и концентрировали в вакууме. Остаток помещали на колонку с силикагелем со смесью EtOAc:гексан (0~1:5), с получением соединения 2 (97,7 г) в виде масла бледно-желтого масла.

Стадия 3: Фенилбороновую кислоту (53,0 г, 434,7 ммоль, 2,03 экв.), карбонат калия (45,0 г, 325,6 ммоль, 1,52 экв.), тетракис(трифенилфосфин)палладий(0) (12,5 г, 10,8 ммоль, 0,05 экв.) и толуол (перегнанный) (800 мл) объединяли при перемешивании в атмосфере азота. Полученную суспензию дегазировали и нагревали при 80°C, затем добавляли 200 мл толуольного раствора соединения 2 (97,7 г, 214,1 ммоль, 1,0 экв.). Тонкую суспензию перемешивали в течение ночи при температуре 80°C. Ход реакции отслеживали с помощью ЖХМС, что указывало на завершение реакции. После выделения смеси неочищенный продукт/исходное вещество с помощью хроматографии, добавляли дополнительное количество фенилбороновой кислоты (21,2 г), карбоната калия (18,0 г), тетракис(трифенилфосфин)палладия(0) (5,0 г), и полученную смесь суспендировали в толуоле (перегнанный) (700 мл). Полученную смесь нагревали при 80°C и перемешивали в течение ночи. После завершения реакции ее гасили путем добавления воды (300 мл). Смесь экстрагировали EtOAc (2×300 мл), и органические слои объединяли. Органическую фазу промывали насыщенным водным раствором NaCl (1×300 мл), сушили над Na2SO4 и концентрировали в вакууме. Остаток помещали на колонку с силикагелем со смесью EtOAc:гексан (0~1:3), с получением указанного в заголовке соединения (50,0 г) в виде белого твердого вещества.
Получение 7
трет-Бутиловый эфир ((R)-2-бифенил-4-ил-1-формилэтил)карбаминовой кислоты

трет-Бутиловый эфир [(R)-2-бифенил-4-ил-1-(метоксиметилкарбамоил)этил]карбаминовой кислоты (7,5 г, 19,5 ммоль, 1,0 экв.) в атмосфере азота объединяли с ТГФ (перегнанный) (100 мл). К полученному перемешиваемому раствору в течение 30 минут несколькими порциями добавляли литийалюминийгидрид (750 мг, 19,8 ммоль, 1,0 экв.) при температуре -5~0°C. Полученный раствор перемешивали в течение 30 минут при температуре -5-0°C. Реакцию затем гасили путем добавления раствора KHSO4 (6,6 г) в воде (35 мл). Полученный раствор объединяли с 1н раствором HCl (75 мл) и перемешивали в течение пяти минут. Добавляли EtOAc (100 мл), и полученный раствор экстрагировали EtOAc (3×100 мл), и органические слои объединяли, с получением указанного в заголовке соединения (6,3 г) в виде желтого масла.
Получение 8
Этиловый эфир (R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты

Стадия 1: Раствор этилового эфира ацетокси(диэтоксифосфорил)уксусной кислоты (15,6 г, 55,3 ммоль, 1,2 экв.) в ТГФ (высушенный) (150 мл), в атмосфере азота, охлаждали до температуры -78°C. При перемешивании добавляли по каплям LiHMDS (1M в ТГФ) (55,3 мл, 1,2 экв.) при температуре -78°C. После перемешивания в течение 30 минут при этой температуре в течение 15 минут добавляли по каплям раствор трет-бутилового эфира ((R)-2-бифенил-4-ил-1-формилэтил)карбаминовой кислоты (15,0 г, неочищенный, 1,0 экв.) в ТГФ (высушенный) (30 мл). Перемешивание продолжали в течение 1,5 часов при температуре -78°C, затем смесь выливали в холодный раствор воды (200 мл) и EtOAc (200 мл). Органический слой повторно отделяли, и водный слой вновь экстрагировали EtOAc (2×100 мл). Объединенные органические слои сушили над Na2SO4, фильтровали и упаривали, и остаток очищали флэш-хроматографией (EtOAc/гексан=0~1:10), с получением соединения 1 (10,5 г) в виде белого твердого вещества.

Стадия 2: Перемешиваемый раствор соединения 1 (10,5 г, 23,2 ммоль, 1,0 экв.) в EtOH (безводный) (100 мл) в атмосфере азота объединяли с палладием на углероде (1,0 г). Смесь продували четыре раза водородом и затем барботировали водород в течение 2 часов при комнатной температуре. Палладий на углероде отфильтровывали, и фильтрат концентрировали в вакууме, с получением неочищенного соединения 2 (10,0 г) в виде бледно-желтого масла, которое использовали без дополнительной очистки.
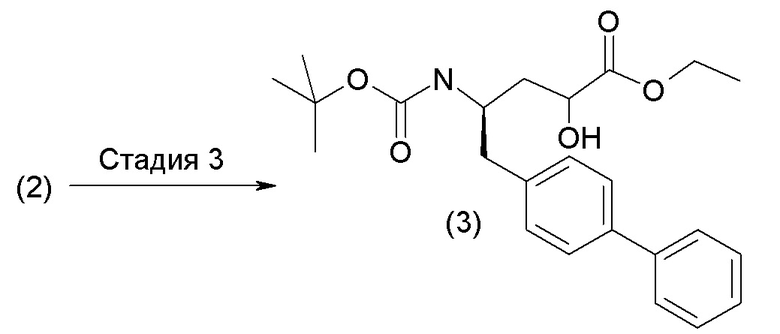
Стадия 3: Соединение 2 (10,0 г, 22,0 ммоль, 1,0 экв.) в EtOH (безводный) (100 мл) объединяли с карбонатом калия (6,1 г, 44,1 ммоль, 2,0 экв.), и полученный раствор перемешивали в течение 2 часов при комнатной температуре. Твердые продукты отфильтровывали, и фильтрат концентрировали в вакууме. Остаток помещали на колонку с силикагелем (EtOAc/гексан=0~1:5), с получением соединения 3 (6,0 г) в виде белого твердого вещества.
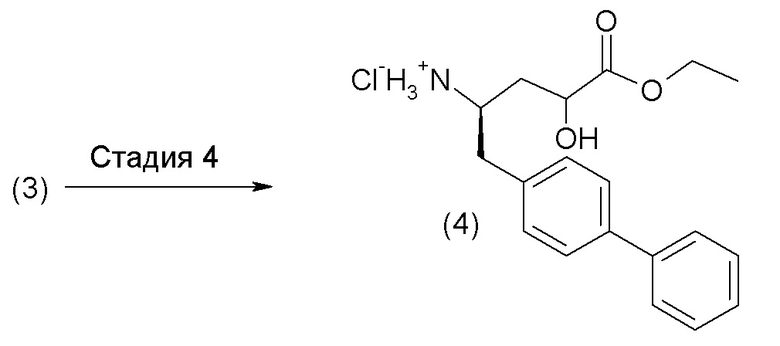
Стадия 4: Соединение 3 (6,0 г, 14,5 ммоль, 1,0 экв.) растворяли в DCM (высушенный) (120 мл), и в смесь в течение 5~6 часов барботировали HCl при комнатной температуре. Наблюдалось образование твердого осадка. Смесь концентрировали до половины объема, затем фильтровали. Твердые продукты собирали и промывали холодным EtOAc, и сушили при пониженном давлении, с получением указанного в заголовке соединения (4,2 г) в виде не совсем белого твердого вещества, HCl соль. ЖХ-МС (ES, m/z): 314 [M-HCl+H]+.
1H ЯМР (300 МГц, ДМСО): ((м.д.)=8,07 (с, 1,9H), 7,96 (с, 1,2H), 7,65-7,69 (м, 4,0H), 7,45-7,50 (м, 2,0H), 7,33-7,39 (м, 3,0H), 6,05-6,07 (м, 0,63H), 5,88-5,90 (м, 0,88H), 4,32-4,38 (м, 0,80H), 4,18-4,31 (м, 0,51H), 4,05-4,11 (м, 2H), 3,50 (с, 1H), 2,75-3,05 (м, 2,8H), 1,83-1,94 (м, 1H), 1,71-1,82 (м, 1H), 1,10-1,20 (м, 3,3H).
ПРИМЕР 2

A. 5-((1R,3S)-1-Бифенил-4-илметил-3-этоксикарбонил-3-гидроксипропилкарбамоил)-2H-пиразол-3-карбоновая кислота (R7=-CH2CH3)
B. 5-((1R,3R)-1-Бифенил-4-илметил-3-этоксикарбонил-3-гидроксипропилкарбамоил)-2H-пиразол-3-карбоновая кислота (R7=-CH2CH3)
C. 5-((1R,3S)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2H-пиразол-3-карбоновая кислота (R7=H)
D. 5-((1R,3R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2H-пиразол-3-карбоновая кислота (D; R7=H)
Этиловый эфир (R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (500 мг, 1,6 ммоль, 1,0 экв.), 3,5-пиразолдикарбоновую кислоту (250 мг, 1,6 ммоль, 1,6 экв.) и HATU (610 мг, 1,6 ммоль, 1,0 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (1 мл), и смесь перемешивали в течение 1 часа. Смесь сушили в вакууме, и продукт очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением 5-((R)-1-бифенил-4-илметил-3-этоксикарбонил-3-гидроксипропилкарбамоил)-2H-пиразол-3-карбоновой кислоты в виде соли с ТФУ.
Полученное вещество отделяли препаративной ВЭЖХ, очищали с использованием хроматографии с обращенной фазой и сушили в вакууме, с получением соединений A и B в виде солей с ТФУ. Соединения A и B, каждое, растворяли в EtOH (~100 мл), и добавляли 10н NaOH для подщелачивания раствора (~200 мкл). Каждую смесь отслеживали в течение 1 часа до полного удаления защитных групп. Каждую смесь подкисляли равным объемом (~200 мкл) AcOH и сушили в вакууме. Продукты очищали с использованием хроматографии с обращенной фазой, с получением соединения C (52 мг; чистота 100%; МС m/z [M+H]+ вычислено для C22H21N3O6, 424,14; найдено 424,2) и соединения D (65 мг; чистота 100%; МС m/z [M+H]+вычислено для C22H21N3O6, 424,14; найдено 424,2) в виде солей с ТФУ.
E. 5-((1R,3R)-1-Бифенил-4-илметил-3-бутоксикарбонил-3-гидроксипропилкарбамоил)-1H-пиразол-3-карбоновая кислота (R7=-(CH2)3CH3)
Бутиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 108 мг, 286 мкмоль, 1,0 экв.), 3,5-пиразолдикарбоновую кислоту (66,9 мг, 429 мкмоль, 1,5 экв.) и HATU (160 мг, 430 мкмоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (150 мкл), и смесь перемешивали в течение 1 часа. Смесь сушили в вакууме, и продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (60 мг; чистота 98%). МС m/z [M+H]+ вычислено для C26H29N3O6, 480,21; найдено 480,4).
ПРИМЕР 3

A. Этиловый эфир (2S,4R)-5-бифенил-4-ил-2-гидрокси-4-({5-[(2-метоксиэтил)метилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановой кислоты (R7=-CH2CH3)
B. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-({5-[(2-метоксиэтил)метилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановой кислоты (R7=-CH2CH3)
C. (2S,4R)-5-Бифенил-4-ил-2-гидрокси-4-({5-[(2-метоксиэтил)метилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановая кислота (R7=H)
D. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-({5-[(2-метоксиэтил)метилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановая кислота (R7=H)
Этиловый эфир (R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (900 мг, 3,0 ммоль, 1,0 экв.), 3,5-пиразолдикарбоновую кислоту (448 мг, 2,9 ммоль, 1,0 экв.), N-(2-метоксиэтил)метиламин (256 мг, 2,9 ммоль, 1,0 экв.) и HATU (1090 мг, 2,9 ммоль, 1,0 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (1 мл), и смесь перемешивали в течение 1 часа. Смесь сушили в вакууме, и продукт очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением этилового эфира (R)-5-бифенил-4-ил-2-гидрокси-4-({5-[(2-метоксиэтил)метилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановой кислоты (25 мг) в виде соли с ТФУ.
Данный продукт отделяли препаративной ВЭЖХ, очищали с использованием хроматографии с обращенной фазой и сушили в вакууме, с получением соединений A и B в виде солей с ТФУ. Соединения A и B, каждое, растворяли в EtOH (~10 мл), и добавляли 10н NaOH для подщелачивания раствора (~200 мкл). Каждую смесь отслеживали в течение 1 часа до полного удаления защитных групп. Каждую смесь подкисляли равным объемом (~200 мкл) AcOH и сушили в вакууме. Продукты очищали с использованием хроматографии с обращенной фазой, с получением соединений C (20,6 мг; чистота 100%; МС m/z [M+H]+ вычислено для C26H30N4O6, 495,22; найдено 495,22) и D (8,3 мг; чистота 100%; МС m/z [M+H]+ вычислено для C26H30N4O6, 495,22; найдено 495,22) в виде солей с ТФУ.
ПРИМЕР 4

A. Этиловый эфир (2R,4R)-4-{[5-(азетидин-1-карбонил)-2H-пиразол-3-карбонил]амино}-5-бифенил-4-ил-2-гидроксипентановой кислоты (R7=-CH2CH3)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 100 мг, 286 мкмоль, 1,0 экв.), 3,5-пиразолдикарбоновую кислоту (66,9 мг, 429 мкмоль, 1,5 экв.) и HATU (160 мг, 430 мкмоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (150 мкл), и смесь перемешивали в течение 1 часа. Добавляли гидрохлорид азетидина (40,0 мг, 429 мкмоль, 1,5 экв.) со вторым эквивалентом HATU, и смесь быстро перемешивали. Добавляли дополнительное количество DIPEA (2,0 экв.), и смесь перемешивали. Смесь сушили в вакууме, затем очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением указанного в заголовке соединения в виде соли с ТФУ (20 мг; чистота 95%). МС m/z [M+H]+ вычислено для C27H30N4O5, 491,22; найдено 491,4.
B. (2R,4R)-4-{[5-(Азетидин-1-карбонил)-2H-пиразол-3-карбонил]амино}-5-бифенил-4-ил-2-гидроксипентановая кислота (R7=H)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 50 мг, 0,1 ммоль, 1,0 экв.), моногидрат 3,5-пиразолдикарбоновой кислоты (29,9 мг, 173 мкмоль, 1,2 экв.) и HATU (82 мг, 210 мкмоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (75 мкл), и смесь перемешивали в течение 1 часа. Добавляли гидрохлорид азетидина (20,0 мг, 214 мкмоль, 1,5 экв.) со вторым эквивалентом HATU, и смесь быстро перемешивали. Смесь сушили в вакууме, с получением неочищенного сложного эфира. Неочищенный сложный эфир растворяли в EtOH (~10 мл), и добавляли 10н NaOH для подщелачивания раствора (~200 мкл). Смесь отслеживали в течение 1 часа до полного удаления защитных групп. Смесь подкисляли равным объемом (~200 мкл) AcOH и сушили в вакууме. Продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (17 мг; чистота 95%). МС m/z [M+H]+ вычислено для C25H26N4O5, 463,19; найдено 463,4.
ПРИМЕР 5

A. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(пирролидин-1-карбонил)-2H-пиразол-3-карбонил]амино}пентановой кислоты (R7=-CH2CH3)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 85 мг, 240 мкмоль, 1,0 экв.), моногидрат 3,5-пиразолдикарбоновой кислоты (40 мг, 0,2 ммоль, 1,0 экв.) и HATU (90 мг, 0,2 ммоль, 1,0 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (150 мкл), и смесь перемешивали в течение 1 часа. Добавляли второй эквивалент HATU, затем пирролидин (20,3 мкл, 243 мкмоль, 1,0 экв.) (1н в ТГФ) и второй эквивалент DIPEA. После завершения реакции смесь сушили в вакууме, затем очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением указанного в заголовке соединения в виде соли с ТФУ (65 мг; чистота 98%). МС m/z [M+H]+ вычислено для C28H32N4O5, 505,24; найдено 505,4.
B. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(пирролидин-1-карбонил)-2H-пиразол-3-карбонил]амино}пентановая кислота (R7=H)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 50 мг, 0,1 ммоль, 1,0 экв.), моногидрат 3,5-пиразолдикарбоновой кислоты (20,0 мг, 0,1 ммоль, 1,0 экв.) и HATU (50 мг, 0,1 ммоль, 1,0 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (75 мкл), и смесь перемешивали в течение 1 часа. Добавляли второй эквивалент HATU, затем пирролидин (20,0 мг, 280 мкмоль, 2,0 экв.) и второй эквивалент DIPEA. Смесь сушили в вакууме, с получением неочищенного сложного эфира. Неочищенный сложный эфир растворяли в EtOH (~10 мл), и добавляли 10н NaOH для подщелачивания раствора (~200 мкл). Смесь контролировали в течение 1 часа до полного удаления защитных групп. Смесь подкисляли равным объемом (~200 мкл) AcOH и сушили в вакууме. Продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (25 мг; чистота 95%). МС m/z [M+H]+ вычислено для C26H28N4O5, 477,21; найдено 477,0.
ПРИМЕР 6
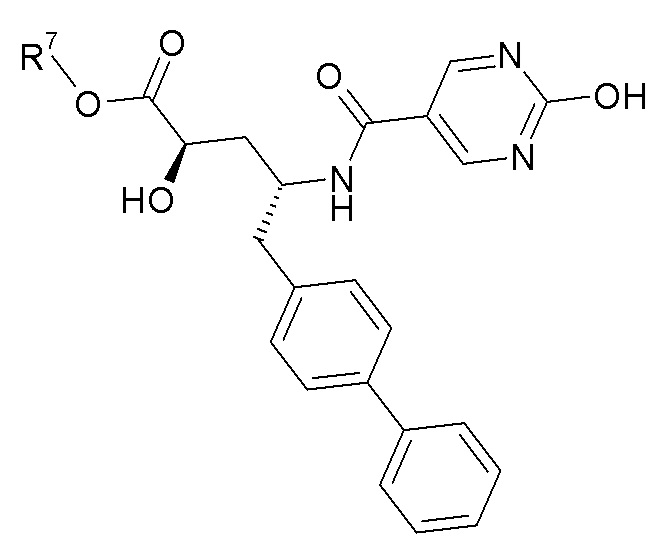
A. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(2-гидроксипиримидин-5-карбонил)амино]пентановой кислоты (R7=-CH2CH3)
B. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(2-гидроксипиримидин-5-карбонил)амино]пентановая кислота (R7=H)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 200 мг, 572 мкмоль, 1,0 экв.) и 2-гидроксипиримидин-5-карбоновую кислоту (88,1 мг, 629 мкмоль) суспендировали в ДМФ (5,0 мл). Добавляли HATU (239 мг, 629 мкмоль), затем DIPEA (299 мкл), и полученную смесь перемешивали при комнатной температуре до завершения реакции (~2 часов). Смесь разделяли на две равные части, и оба раствора концентрировали. Одну часть очищали препаративной ВЭЖХ (10-70% MeCN/H2O), с получением соединения A в виде соли с ТФУ (59,2 мг). МС m/z [M+H]+ вычислено для C24H25N3O5, 436,18; найдено 436,4. Оставшуюся часть растворяли в ТГФ (2,0 мл). Добавляли моногидрат LiOH (120 мг, 2,9 ммоль) в воде (2,0 мл), и смесь перемешивали при комнатной температуре в течение ~1 часа. Реакцию гасили добавлением AcOH, и раствор концентрировали. Неочищенный продукт очищали препаративной ВЭЖХ (10-70% MeCN/H2O), с получением соединения B в виде соли с ТФУ (27,8 мг). МС m/z [M+H]+ вычислено для C22H21N3O5, 408,15; найдено 408,4.
ПРИМЕР 7
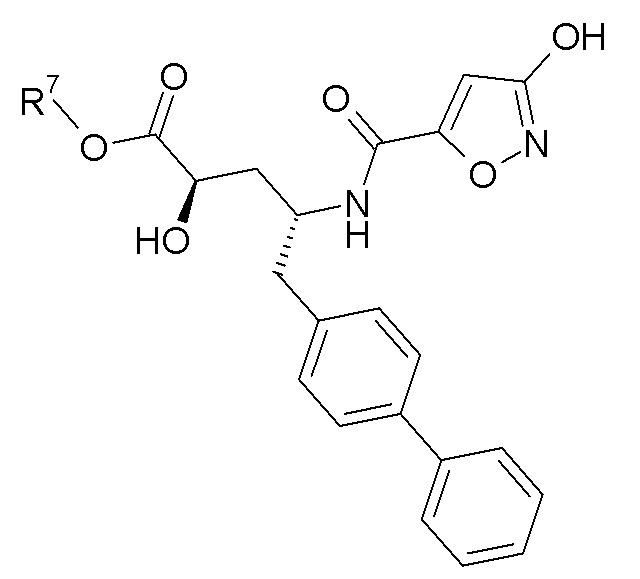
A. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(3-гидроксиизоксазол-5-карбонил)амино]пентановой кислоты (R7=-CH2CH3)
3-Гидроксиизоксазол-5-карбоновую кислоту (81,2 мг, 629 мкмоль, 1,1 экв.) растворяли в ДМФ (5,0 мл). Добавляли DIPEA (299 мкл) и HOAt (85,6 мг, 629 мкмоль, 1,1 экв.), затем EDCI (111 мкл, 1,1 экв.). Раствор перемешивали в течение 5 минут. Затем добавляли этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 200 мг, 572 мкмоль, 1,0 экв.), и полученную смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали, и неочищенный продукт очищали препаративной ВЭЖХ (10-70% MeCN/H2O), с получением указанного в заголовке соединения в виде соли с ТФУ (50,8 мг, 98%-ная чистота). МС m/z [M+H]+ вычислено для C23H24N2O6, 425,16; найдено 425,4.
B. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(3-гидроксиизоксазол-5-карбонил)амино]пентановая кислота (R7=H)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 200 мг, 572 мкмоль, 1,0 экв.) и 3-гидроксиизоксазол-5-карбоновую кислоту (81,2 мг, 629 мкмоль) суспендировали в ДМФ (5,0 мл). Добавляли HATU (239 мг, 629 мкмоль), затем DIPEA (299 мкл), и полученную смесь перемешивали при комнатной температуре в течение ночи. Смесь концентрировали, и неочищенное соединение использовали без очистки. Неочищенный продукт растворяли в ТГФ (3,0 мл). Добавляли моногидрат LiOH (240 мг, 5,7 ммоль) в воде (3,0 мл), и смесь перемешивали при комнатной температуре в течение ~1 часа. Смесь концентрировали, и неочищенный продукт очищали препаративной ВЭЖХ (10-70% MeCN/H2O), с получением указанного в заголовке соединения в виде соли с ТФУ (36,6 мг, 97%-ная чистота). МС m/z [M+H]+ вычислено для C21H20N2O6, 397,13; найдено 397,2.
C. 5-Метил-2-оксо[1,3]диоксол-4-илметиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(3-гидроксиизоксазол-5-карбонил)амино]пентановой кислоты (R7=-CH2-5-метил[1,3]диоксол-2-он)
Гидрохлорид этилового эфира (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты; (1,6 г, 4,6 ммоль, 1,0 экв.) растворяли в DCM (100 мл) и охлаждали до температуры 0°C. Добавляли в виде твердого вещества ди-трет-бутилдикарбонат (1,2 г, 5,4 ммоль, 1,2 экв.), затем DIPEA (1,6 мл, 9,1 ммоль). Полученную смесь перемешивали в течение ночи при комнатной температуре. Продукт очищали флэш-хроматографией (0-75% EtOAc/гексан), затем растворяли в EtOH и достаточном количестве эквивалентов 10н NaOH для подщелачивания раствора (pH=14). Реакцию отслеживали до полного удаления защитных групп (~1 час). Добавляли EtOAc (200 мл), и смесь промывали 1н HCl (100 мл), затем насыщенным водным раствором NaCl (100 мл). Органический слой отделяли и сушили над безводным MgSO4 в течение 10 минут, затем фильтровали и упаривали в вакууме досуха, с получением (2R,4R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-гидроксипентановой кислоты (1,2 г).
(2R,4R)-5-Бифенил-4-ил-4-трет-бутоксикарбониламино-2-гидроксипентановую кислоту (500 мг, 1,0 ммоль, 1,0 экв.) растворяли в сухом ДМФ (10,0 мл). Раствор охлаждали до температуры 0°C, и добавляли карбонат дицезия (465 мг, 1,4 ммоль, 1,1 экв.). Смесь перемешивали в течение 30 минут, и добавляли 4-хлорметил-5-метил-1,3-диоксол-2-он (212 мг, 1,4 ммоль, 1,1 экв.). Полученную смесь перемешивали в течение еще 1 часа при температуре 0°C, затем нагревали до комнатной температуры при перемешивании. Смесь затем перемешивали в течение ночи. Добавляли EtOAc (20 мл), затем промывали насыщенным водным раствором NaCl (100 мл). Продукт сушили в вакууме и очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением 5-метил-2-оксо[1,3]диоксол-4-илметилового эфира (2R,4R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-гидроксипентановой кислоты. Данный продукт растворяли в 4н HCl в диоксане и перемешивали в течение 2 часов при комнатной температуре. Продукт сушили в вакууме, затем подвергали азеотропной отгонке с толуолом, с получением 5-метил-2-оксо[1,3]диоксол-4-илметилового эфира (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты, который использовали на следующей стадии без дополнительной очистки.
5-Метил-2-оксо[1,3]диоксол-4-илметиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (100 мг, 0,3 ммоль, 1,0 экв.) и 3-гидроксиизоксазол-5-карбоновую кислоту (50,5 мг, 391 мкмоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA, и полученную смесь перемешивали в течение 1 часа. Продукт сушили в вакууме, затем очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения (40 мг, 98%-ная чистота). МС m/z [M+H]+ вычислено для C26H24N2O9, 509,15; найдено 509,4.
ПРИМЕР 8

A. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(1-гидрокси-1-метилэтил)-1H-пиразол-3-карбонил]амино}пентановой кислоты (R7=-CH2CH3)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 100 мг, 0,3 ммоль, 1,0 экв.), 5-(1-гидрокси-1-метилэтил)-1H-пиразол-3-карбоновую кислоту (73 мг, 429 мкмоль, 1,5 экв.) и HATU (160 мг, 430 мкмоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (149 мкл), и смесь перемешивали в течение 1 часа. После завершения реакции смесь сушили в вакууме, затем очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением указанного в заголовке соединения в виде соли с ТФУ (50 мг). МС m/z [M+H]+ вычислено для C26H31N3O5, 466,23; найдено 466,4.
B. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(1-гидрокси-1-метилэтил)-1H-пиразол-3-карбонил]амино}пентановая кислота (R7=H)
Этиловый эфир (2R,4R)-4-амино-5-бифенил-4-ил-2-гидроксипентановой кислоты (HCl соль; 60 мг, 0,2 ммоль, 1,0 экв.), 5-(1-гидрокси-1-метилэтил)-1H-пиразол-3-карбоновую кислоту (43,8 мг, 257 мкмоль, 150 экв.) и HATU (98 мг, 260 мкмоль, 1,5 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли DIPEA (89,6 мкл), и смесь перемешивали в течение 1 часа. Смесь сушили в вакууме, с получением неочищенного сложного эфира. Неочищенный сложный эфир растворяли в EtOH (~10 мл), и добавляли 10н NaOH для подщелачивания раствора (~200 мкл). Смесь контролировали в течение 1 часа до полного удаления защитных групп. Смесь подкисляли равным объемом (~200 мкл) AcOH и сушили в вакууме. Продукт очищали с использованием хроматографии с обращенной фазой, с получением указанного в заголовке соединения в виде соли с ТФУ (30 мг). МС m/z [M+H]+ вычислено для C24H27N3O5, 438,20; найдено 438,4.
ПРИМЕР 9
((1R,3R)-1-Бифенил-4-илметил-3-карбамоил-3-гидроксипропил)амид 2-гидроксипиримидин-5-карбоновой кислоты
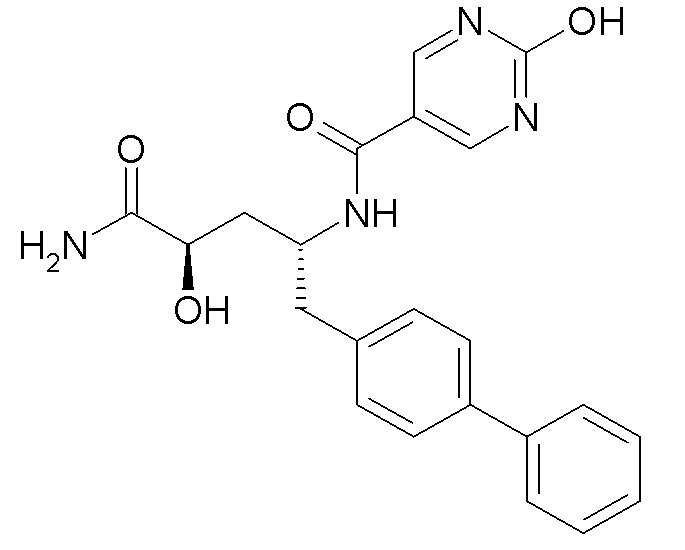
(2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(2-гидроксипиримидин-5-карбонил)амино]пентановую кислоту (14,5 мг, 35,6 мкмоль, 1,0 экв.) и HATU (13,5 мг, 35,6 мкмоль, 1,0 экв.) объединяли в ДМФ (5 мл), и полученную смесь перемешивали в течение 2 минут. Добавляли 0,5М аммиак в диоксане, затем DIPEA (12,4 мкл). Полученную смесь перемешивали в течение 1 часа, затем сушили в вакууме. Продукт очищали с использованием хроматографии с обращенной фазой (10-70% MeCN/H2O; 0,05% ТФУ в течение 70 минут), с получением указанного в заголовке соединения (2 мг). МС m/z [M+H]+ вычислено для C22H22N4O4, 407,16; найдено 407,4.
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, также получали соединения примеров 10-15, имеющие следующую формулу:
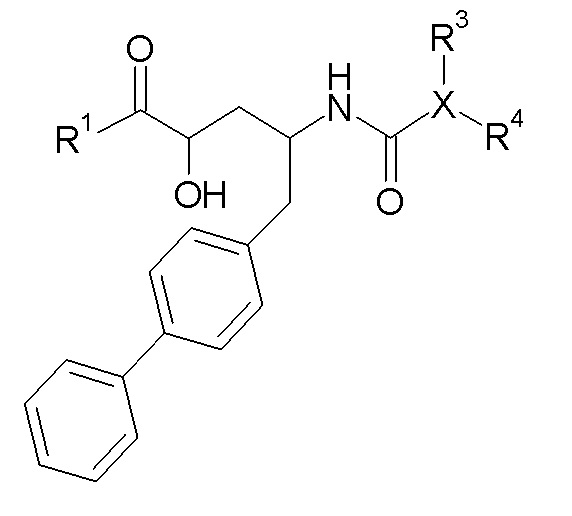
ПРИМЕР 10
Указанные соединения получали в виде родоначального соединения или в виде соли с ТФУ.

2. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(3H-[1,2,3]триазол-4-карбонил)амино]пентановая кислота (соль с ТФУ)

4. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты (соль с ТФУ)
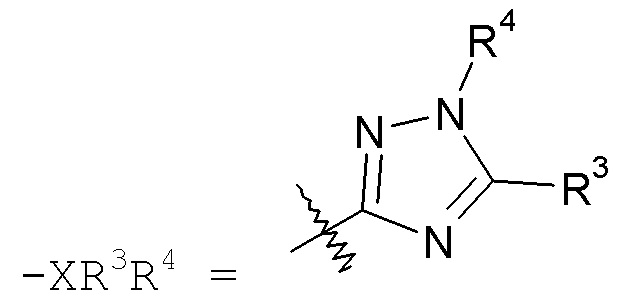
6. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(1H-[1,2,4]триазол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
7. (R)-5-Бифенил-4-ил-4-{[1-(4-хлорфенил)-5-метил-1H-[1,2,4]триазол-3-карбонил]амино}-2-гидроксипентановая кислота (соль с ТФУ)
8. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(5-гидрокси-1H-[1,2,4]триазол-3-карбонил)амино]пентановой кислоты (соль с ТФУ)
9. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-гидрокси-1H-[1,2,4]триазол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
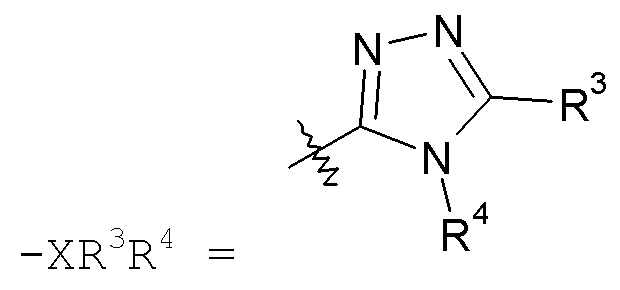

12. (2R,4R)-5-Бифенил-4-ил-4-[(5-хлор-2H-[1,2,4]триазол-3-карбонил)амино]-2-гидроксипентановая кислота
ПРИМЕР 11
Все указанные соединения получали в виде солей с ТФУ.

2. 4-[5-((1R,3S)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)бензотриазол-1-илметил]бензойная кислота
3. (R)-4-[(1H-Бензотриазол-5-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановая кислота
4. (R)-5-Бифенил-4-ил-4-[(7-фтор-1H-бензотриазол-5-карбонил)амино]-2-гидроксипентановая кислота
5. Этиловый эфир (R)-5-бифенил-4-ил-4-[(7-хлор-1H-бензотриазол-5-карбонил)амино]-2-гидроксипентановой кислоты

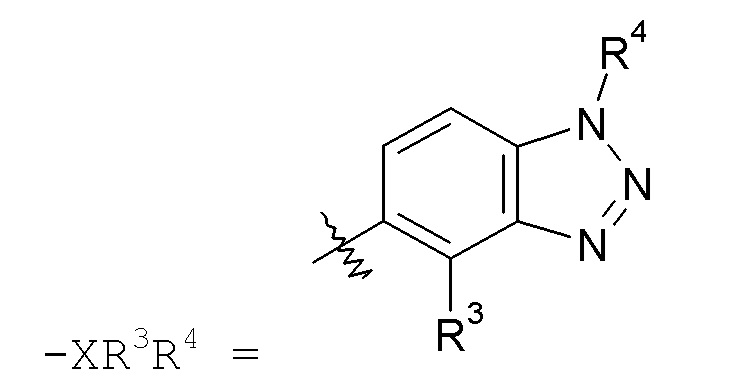



11. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(1H-[1,2,3]триазоло[4,5-b]пиридин-6-карбонил)амино]пентановая кислота
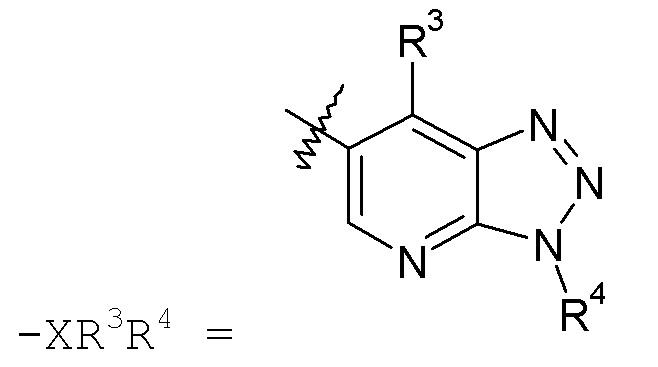
13. (2S,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(3H-[1,2,3]триазоло[4,5-b]пиридин-6-карбонил)амино]пентановая кислота
14. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(3H-[1,2,3]триазоло[4,5-b]пиридин-6-карбонил)амино]пентановой кислоты
15. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(3H-[1,2,3]триазоло[4,5-b]пиридин-6-карбонил)амино]пентановая кислота
ПРИМЕР 12
Указанные соединения получали в виде родоначального соединения или в виде соли с ТФУ.
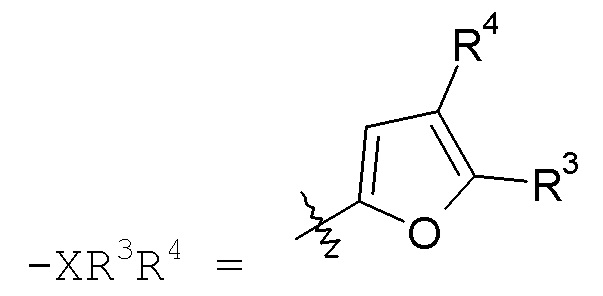

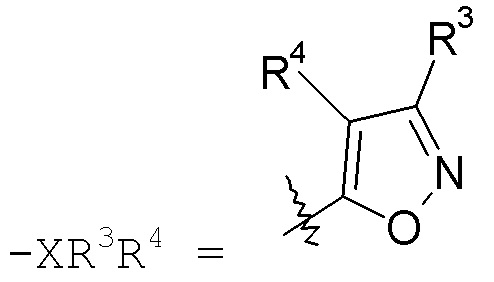


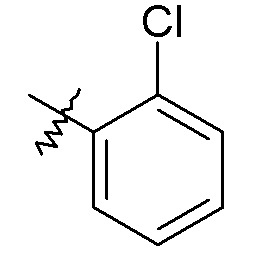
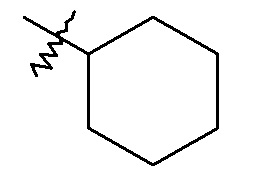

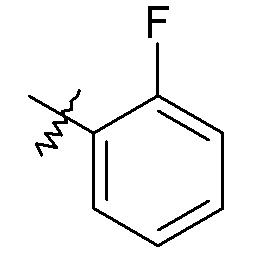


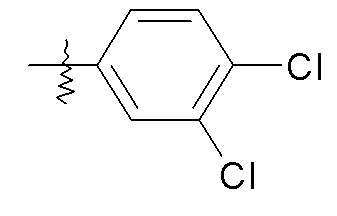
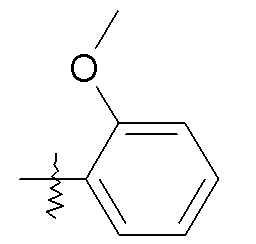
4. (2R,4R)-5-Бифенил-4-ил-4-{[3-(4-хлорфенил)изоксазол-5-карбонил]амино}-2-гидроксипентановая кислота (соль с ТФУ)
5. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[3-(2-метоксибензоиламино)изоксазол-5-карбонил]амино}пентановая кислота (соль с ТФУ)
6. (2R,4R)-5-Бифенил-4-ил-4-{[3-(2-хлорфенил)изоксазол-5-карбонил]амино}-2-гидроксипентановая кислота (соль с ТФУ)
7. (2R,4R)-5-Бифенил-4-ил-4-[(3-циклогексилизоксазол-5-карбонил)амино]-2-гидроксипентановая кислота (соль с ТФУ)
8. (2R,4R)-5-Бифенил-4-ил-4-{[3-(3-фторфенил)изоксазол-5-карбонил]амино}-2-гидроксипентановая кислота
9. (2R,4R)-5-Бифенил-4-ил-4-{[3-(2-фторфенил)изоксазол-5-карбонил]амино}-2-гидроксипентановая кислота
10. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[3-(1-метил-1H-пиразол-4-ил)изоксазол-5-карбонил]амино}пентановая кислота (соль с ТФУ)
11. (2R,4R)-5-Бифенил-4-ил-4-{[3-(2,5-дихлорфенил)изоксазол-5-карбонил]амино}-2-гидроксипентановая кислота
12. (2R,4R)-5-Бифенил-4-ил-4-{[3-(3,4-дихлорфенил)изоксазол-5-карбонил]амино}-2-гидроксипентановая кислота
13. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[3-(2-метоксифенил)изоксазол-5-карбонил]амино}пентановая кислота
14. 5-((1R,3R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)изоксазол-3-карбоновая кислота
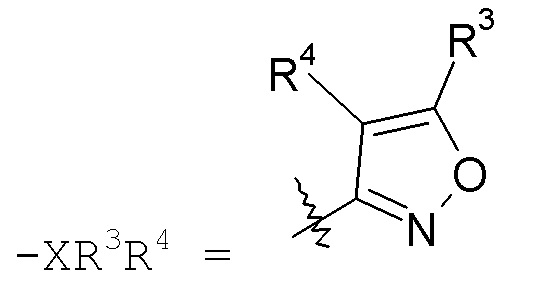
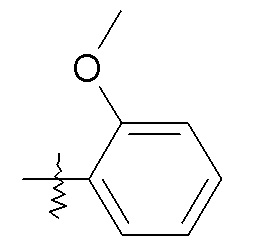
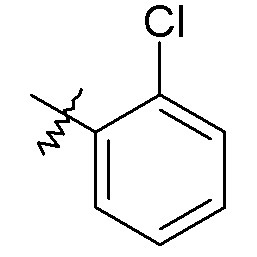
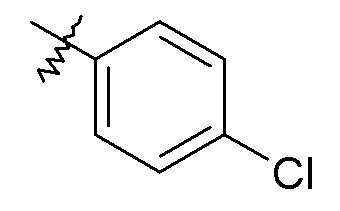
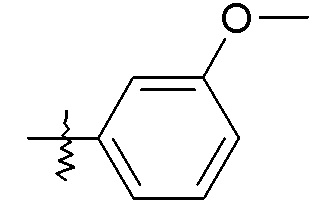




16. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2-хлорфенил)изоксазол-3-карбонил]амино}-2-гидроксипентановая кислота (соль с ТФУ)
17. (2R,4R)-5-Бифенил-4-ил-4-{[5-(4-хлорфенил)изоксазол-3-карбонил]амино}-2-гидроксипентановая кислота (соль с ТФУ)
18. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(3-метоксифенил)изоксазол-3-карбонил]амино}пентановая кислота (соль с ТФУ)
19. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-морфолин-4-илметилизоксазол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
20. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(4-метоксифенил)изоксазол-3-карбонил]амино}пентановая кислота (соль с ТФУ)
21. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(2-гидроксифенил)изоксазол-3-карбонил]амино}пентановая кислота (соль с ТФУ)
22. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2-хлорбензоиламино)изоксазол-3-карбонил]амино}-2-гидроксипентановая кислота (соль с ТФУ)
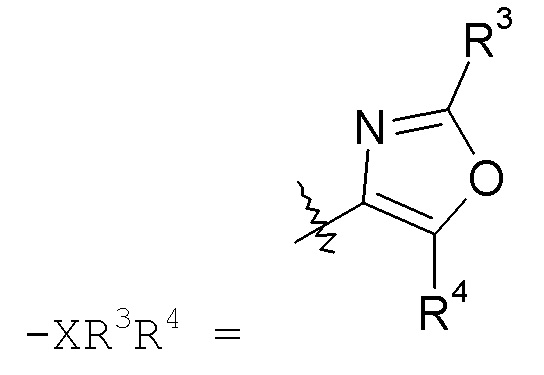




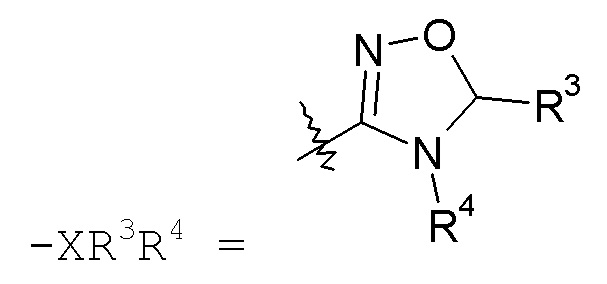
ПРИМЕР 13
Указанные соединения получали в виде родоначального соединения или в виде соли с ТФУ.

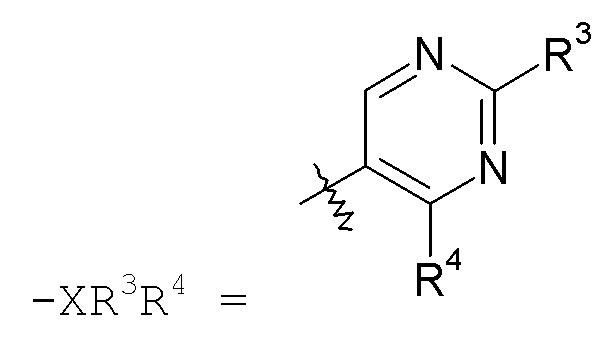

4. Этиловый эфир (R)-5-бифенил-4-ил-2-гидрокси-4-[(6-гидроксипиридазин-3-карбонил)амино]пентановой кислоты
5. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(6-гидроксипиридазин-3-карбонил)амино]пентановая кислота (соль с ТФУ)

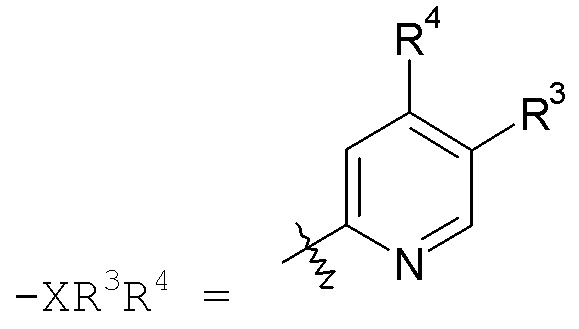

ПРИМЕР 14
Указанное соединение получали в виде родоначального соединения.
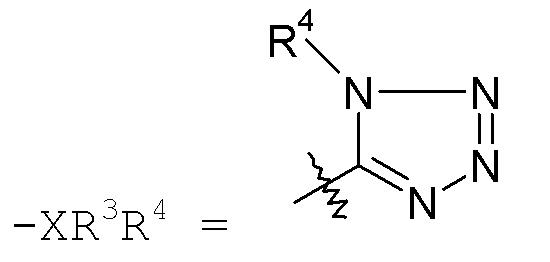
ПРИМЕР 15
Указанные соединения получали в виде солей с ТФУ.
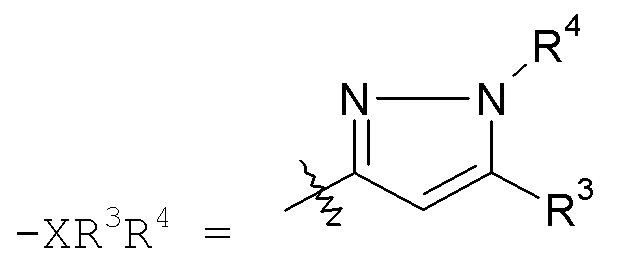


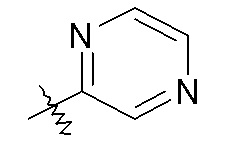
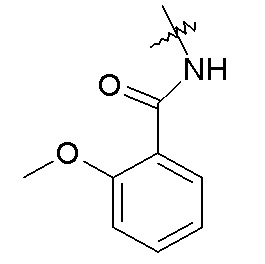

2. (2R,4R)-5-Бифенил-4-ил-4-[(5-карбоксиметил-1H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
3. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-гидроксиметил-1H-пиразол-3-карбонил)амино]пентановая кислота
4. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-метоксиметил-1H-пиразол-3-карбонил)амино]пентановая кислота
5. 5-((1R,3R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-метил-2H-пиразол-3-карбоновая кислота
6. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(4-хлор-3-трифторметилсульфанилбензил)-2H-пиразол-3-карбоновая кислота
7. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(3-хлорбензил)-2H-пиразол-3-карбоновая кислота
8. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(4-хлор-2,6-дифторбензил)-2H-пиразол-3-карбоновая кислота
9. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(2-хлорбензил)-2H-пиразол-3-карбоновая кислота
10. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(2-хлор-5-фторбензил)-2H-пиразол-3-карбоновая кислота
11. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(3-хлор-5-фторбензил)-2H-пиразол-3-карбоновая кислота
12. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(4-хлор-3-трифторметоксибензил)-2H-пиразол-3-карбоновая кислота
13. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(4-хлор-2-фторбензил)-2H-пиразол-3-карбоновая кислота
14. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(3-хлор-4-фторбензил)-2H-пиразол-3-карбоновая кислота
15. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(4-хлорбензил)-2H-пиразол-3-карбоновая кислота
16. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(3-хлор-2,6-дифторбензил)-2H-пиразол-3-карбоновая кислота
17. 5-((R)-1-Бифенил-4-илметил-3-карбокси-3-гидроксипропилкарбамоил)-2-(3-метоксибензил)-2H-пиразол-3-карбоновая кислота
18. Этиловый эфир 5-((R)-1-бифенил-4-илметил-3-этоксикарбонил-3-гидроксипропилкарбамоил)-2H-пиразол-3-карбоновой кислоты
19. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-метил-1H-пиразол-3-карбонил)амино]пентановая кислота
20. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пиридин-4-ил-1H-пиразол-3-карбонил)амино]пентановая кислота
21. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пиридин-3-ил-1H-пиразол-3-карбонил)амино]пентановая кислота
22. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пиразин-2-ил-1H-пиразол-3-карбонил)амино]пентановая кислота
23. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(1'-метил-2H,1'H-[3,4']biпиразолил-5-карбонил)амино]пентановая кислота
24. (R)-5-Бифенил-4-ил-4-{[5-(2-хлорфенил)-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
25. (2R,4R)-5-Бифенил-4-ил-4-{[5-(3-хлорфенил)-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
26. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2,4-дихлорфенил)-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
27. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2,5-дихлорфенил)-1H-пиразол-3-карбонил]амино}-2- гидроксипентановая кислота
29. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(2-гидроксифенил)-1H-пиразол-3-карбонил]амино}пентановой кислоты
30. (2R,4R)-5-Бифенил-4-ил-4-{[1-(2,3-дигидроксипропил)-5-(2-гидроксифенил)-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
31. (R)-4-{[5-(3-Ацетиламинофенил)-1H-пиразол-3-карбонил]амино}-5-бифенил-4-ил-2-гидроксипентановая кислота
32. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(2-метоксибензоиламино)-1H-пиразол-3-карбонил]амино}пентановая кислота
33. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-фенил-1H-пиразол-3-карбонил)амино]пентановая кислота
34. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(1-метил-5-фенил-1H-пиразол-3-карбонил)амино]пентановая кислота
35. (2R,4R)-5-Бифенил-4-ил-4-[(1-карбоксиметил-5-фенил-1H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
36. (2R,4R)-5-Бифенил-4-ил-4-{[1-(2-карбоксиэтил)-5-фенил-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
37. (R)-5-Бифенил-4-ил-4-[(5-фуран-2-ил-1H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
38. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-нафталин-2-ил-1H-пиразол-3-карбонил)амино]пентановая]амино}пентановой кислоты
39. (R)-5-Бифенил-4-ил-4-[(5-бифенил-4-ил-1H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
40. (R)-5-Бифенил-4-ил-4-{[5-(4-хлорфенил)-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
41. 5-Метил-2-оксо[1,3]диоксол-4-илметиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(1-гидрокси-1-метилэтил)-1H-пиразол-3-карбонил
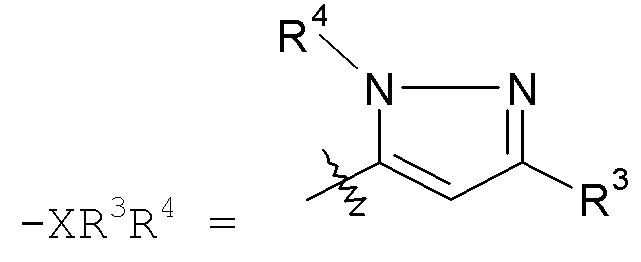
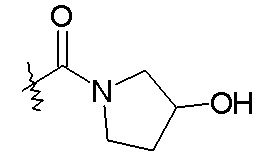


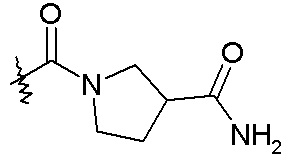
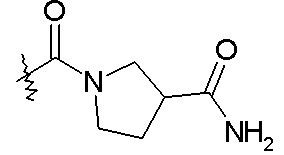

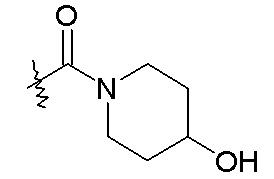


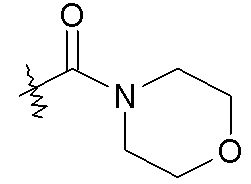
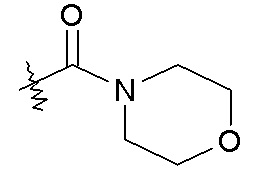
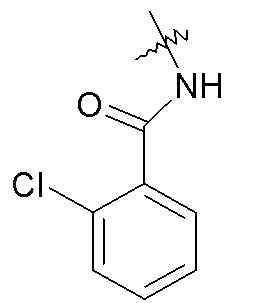
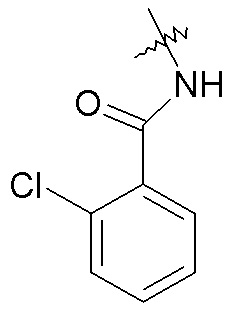
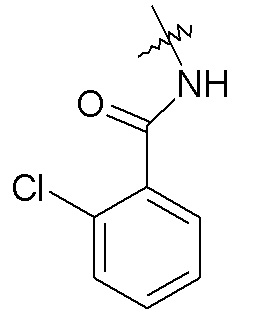
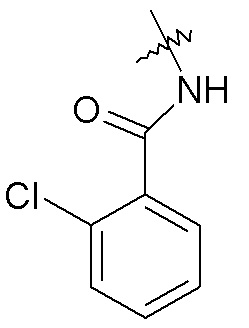



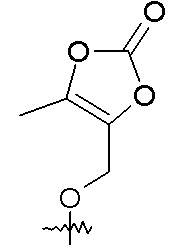
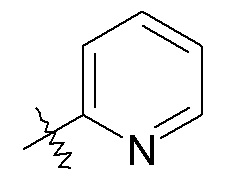
=N(OH)
43. Этиловый эфир (2S,4R)-5-бифенил-4-ил-4-{[5-(3-карбамоилпирролидин-1-карбонил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
44. (2S,4R)-5-Бифенил-4-ил-4-{[5-(3-карбамоилпирролидин-1-карбонил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
45. Этиловый эфир (2R,4R)-5-бифенил-4-ил-4-{[5-(3-карбамоилпирролидин-1-карбонил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
46. (2R,4R)-5-Бифенил-4-ил-4-{[5-(3-карбамоилпирролидин-1-карбонил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
47. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(4-гидроксипиперидин-1-карбонил)-2H-пиразол-3-карбонил]амино}пентановой кислоты
49. Этиловый эфир (2S,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(4-гидроксипиперидин-1-карбонил)-2H-пиразол-3-карбонил]амино}пентановой кислоты
50. (2S,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(4-гидроксипиперидин-1-карбонил)-2H-пиразол-3-карбонил]амино}пентановая кислота
51. Этиловый эфир (R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(морфолин-4-карбонил)-2H-пиразол-3-карбонил]амино}пентановой кислоты
52. Этиловый эфир (2S,4R)-5-бифенил-4-ил-4-[(5-циклопропилкарбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановой кислоты
53. (R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(морфолин-4-карбонил)-2H-пиразол-3-карбонил]амино}пентановая кислота
54. Этиловый эфир (2R,4R)-5-бифенил-4-ил-4-[(5-циклопропилкарбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановой кислоты
55. (2S,4R)-5-Бифенил-4-ил-4-[(5-циклопропилкарбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
56. (R)-5-Бифенил-4-ил-4-{[5-(карбоксиметилкарбамоил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
57. (2R,4R)-5-Бифенил-4-ил-4-[(5-циклопропилкарбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
58. Этиловый эфир (R)-5-бифенил-4-ил-4-[(5-карбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановой кислоты
60. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-метилкарбамоил-2H-пиразол-3-карбонил)амино]пентановая кислота
61. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пропилкарбамоил-2H-пиразол-3-карбонил)амино]пентановая кислота
62. Этиловый эфир (2R,4R)-5-бифенил-4-ил-4-[(5-диметилкарбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановой кислоты
63. (2R,4R)-5-Бифенил-4-ил-4-[(5-диметилкарбамоил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
64. Этиловый эфир (2S,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(изобутилметилкарбамоил)-2H-пиразол-3-карбонил]амино}пентановой кислоты
65. (2S,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(изобутилметилкарбамоил)-2H-пиразол-3-карбонил]амино}пентановая кислота
66. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-{[5-(изобутилметилкарбамоил)-2H-пиразол-3-карбонил]амино}пентановой кислоты
67. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(изобутилметилкарбамоил)-2H-пиразол-3-карбонил]амино}пентановая кислота
68. Этиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-({5-[2-(1H-имидазол-4-ил)-этилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановой кислоты
69. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-({5-[2-(3H-имидазол-4-ил)этилкарбамоил]-2H-пиразол-3-карбонил}амино)пентановая кислота
71. (R)-5-Бифенил-4-ил-4-{[5-(2-диметиламиноэтилкарбамоил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
72. (R)-5-Бифенил-4-ил-4-[(5-циклопропил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
73. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-изопропил-2H-пиразол-3-карбонил)амино]пентановая кислота
74. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пропил-2H-пиразол-3-карбонил)амино]пентановая кислота
75. (R)-5-Бифенил-4-ил-4-[(5-бутил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
76. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-фенил-2H-пиразол-3-карбонил)амино]пентановая кислота
77. (2R,4R)-5-Бифенил-4-ил-4-{[2-(2-карбоксиэтил)-5-фенил-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
78. (2R,4R)-5-Бифенил-4-ил-4-{[2-(2,3-дигидроксипропил)-5-(2-гидроксифенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
79. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(2-метоксифенил)-2H-пиразол-3-карбонил]амино}пентановая кислота
80. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2,5-диметоксифенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
82. (R)-5-Бифенил-4-ил-4-{[5-(4-фторфенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
83. (2R,4R)-5-Бифенил-4-ил-4-{[5-(4-хлорфенил)-2H-пиразол-3-карбонил]-2-гидроксипентановая кислота
84. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2-хлорфенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
85. Этиловый эфир (2R,4R)-5-бифенил-4-ил-4-{[5-(2-хлорфенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
86. (2R,4R)-5-Бифенил-4-ил-4-{[5-(5-фтор-2-метоксифенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
87. Изопропиловый эфир (2R,4R)-5-Бифенил-4-ил-4-{[5-(5-фтор-2-метоксифенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты (HCl соль)
88. Этиловый эфир (2R,4R)-5-Бифенил-4-ил-4-{[5-(5-фтор-2-метоксифенил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
89. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(5-метилтиофен-2-ил)-2H-пиразол-3-карбонил]амино}пентановая кислота
90. (2R,4R)-5-Бифенил-4-ил-4-{[5-(5-хлортиофен-2-ил)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
91. (R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пропиониламино-2H-пиразол-3-карбонил)амино]пентановая кислота
93. (R)-5-Бифенил-4-ил-4-[(5-этоксикарбониламино-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
94. (R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(2-метоксиацетиламино)-2H-пиразол-3-карбонил]амино}пентановая кислота
95. (R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-(2-метоксибензоиламино)-2H-пиразол-3-карбонил]амино}пентановая кислота
96. (2R,4R)-5-Бифенил-4-ил-4-{[5-(2-хлорбензоиламино)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
97. Этиловый эфир (2R,4R)-5-бифенил-4-ил-4-{[5-(2-хлорбензоиламино)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
98. Изобутиловый эфир (2R,4R)-5-бифенил-4-ил-4-{[5-(2-хлорбензоиламино)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
99. Изопропиловый эфир (2R,4R)-5-бифенил-4-ил-4-{[5-(2-хлорбензоиламино)-2H-пиразол-3-карбонил]амино}-2-гидроксипентановой кислоты
100. (R)-5-Бифенил-4-ил-2-гидрокси-4-({5-[(пиридин-2-карбонил)амино]-2H-пиразол-3-карбонил}амино)пентановая кислота
101. (R)-4-[(5-Амино-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановая кислота
102. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановая кислота
104. Изобутиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты
105. 5-Метил-2-оксо[1,3]диоксол-4-илметиловый эфир (2R,4R)-5-бифенил-4-ил-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты
106. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-пиразин-2-ил-2H-пиразол-3-карбонил)амино]пентановая кислота
107. 1-Циклогексилоксикарбонилоксиэтиловый эфир (2R,4R)-4-[(5-ацетил-2H-пиразол-3-карбонил)амино]-5-бифенил-4-ил-2-гидроксипентановой кислоты
108. 5-Ацетил-2H-пиразол-3-карбоновая кислота ((1R,3R)-1-бифенил-4-илметил-3-карбамоил-3-гидроксипропил)амид
109. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-((S)-1-гидроксиэтил)-2H-пиразол-3-карбонил]амино}пентановая кислота
110. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-{[5-((R)-1-гидроксиэтил)-2H-пиразол-3-карбонил]амино}пентановая кислота
111. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-{1-[(E)-гидроксиимино]этил}-2H-пиразол-3-карбонил)амино]пентановая кислота
112. (2R,4R)-5-Бифенил-4-ил-4-[(5-бутил-2H-пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
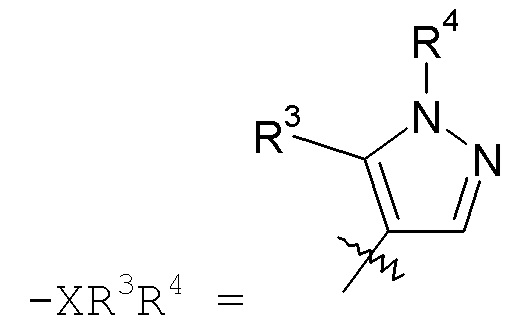
ПРИМЕР 16
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде солей с ТФУ.

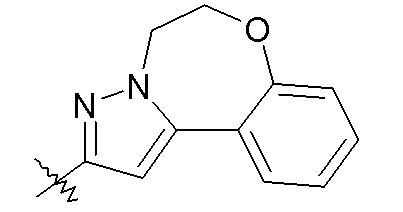


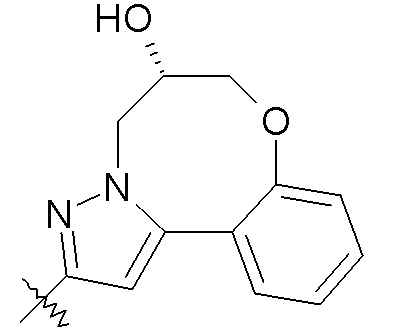


2. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(8-окса-11,14-диазатрицикло[9,2,1,02,7]тетрадека-1(14),2,4,6,12-пентаен-12-карбонил)амино]пентановая кислота
3. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(10-окса-5,6-диазатрицикло[9,4,0,02,6]пентадека-1(15),2,4,11,13-пентаен-4-карбонил)амино]пентановая кислота
4. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[((S)-8-гидрокси-10-окса-5,6-диазатрицикло[9,4,0,02,6]пентадека-1(15),2,4,11,13-пентаен-4-карбонил)амино]пентановая кислота
5. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[((R)-8-гидрокси-10-окса-5,6-диазатрицикло[9,4,0,02,6]пентадека-1(15),2,4,11,13-пентаен-4-карбонил)амино]пентановая кислота
6. (2R,4R)-5-Бифенил-4-ил-2-гидрокси-4-[(5-окса-3,3a-диазациклопента[a]нафталин-2-карбонил)амино]пентановая кислота
Получение 9
трет-Бутиловый эфир (S)-2-(4-бромбензил)-5-оксопирролидин-1-карбоновой кислоты

В раствор (R)-2-амино-3-(4-бромфенил)пропионовой кислоты (50 г, 0,2 моль) в MeCN (700 мл) добавляли раствор NaOH (16,4 г, 0,4 моль) в воде (700 мл) при температуре -5°C. После перемешивания в течение 10 минут добавляли раствор (Boc)2O (44,7 г, 0,2 моль) в MeCN (100 мл). Смесь нагревали до комнатной температуры и перемешивали в течение ночи. После упаривания MeCN остаток разбавляли DCM (800 мл) и подкисляли 1M HCl до pH=2 при температуре -5°C. Водный слой экстрагировали DCM (3×200 мл). Объединенные органические слои промывали насыщенным водным раствором NaCl (500 мл), сушили над Na2SO4 и концентрировали, с получением соединения 1 (66,5 г) в виде белого твердого вещества. ЖХ-МС: 366 (M+Na), 709 (2M+Na).
В раствор соединения 1 (66,5 г, 193 мкмоль), кислоты Мельдрума (33,4 г, 232 ммоль) и DMAP (37,7 г, 309 ммоль) в безводном DCM (600 мл) в атмосфере азота добавляли в течение 1 часа по каплям раствор DCC (47,9 г, 232 ммоль) в безводном DCM (200 мл) при температуре -5°C. Смесь перемешивали при температуре -5°C в течение 8 часов, затем охлаждали в течение ночи. Наблюдалось образование кристаллов дициклогексилмочевины. Смесь фильтровали, промывали 5% KHSO4 (5×200 мл), насыщенным водным раствором NaCl (200 мл) и сушили над безводным MgSO4 при охлаждении в холодильнике в течение ночи. Затем раствор упаривали, с получением неочищенного соединения 2 (91 г) в виде светло-желтого твердого вещества. ЖХ-МС: 492(M+Na), 961(2M+Na).

В раствор неочищенного соединения 2 (91 г, 193 ммоль) в безводном DCM (1 л) при температуре -5°C в атмосфере азота добавляли AcOH (127,5 г, 2,1 моль). Смесь перемешивали при температуре -5°C в течение 30 минут, затем небольшими порциями добавляли NaBH4 (18,3 г, 483 ммоль) в течение 1 часа. После перемешивания в течение еще 1 часа при температуре -5°C добавляли насыщенный водный раствор NaCl (500 мл). Органический слой промывали насыщенным водным раствором NaCl (2×300 мл) и водой (2×300 мл), сушили над MgSO4, фильтровали и концентрировали, с получением неочищенного продукта, который затем очищали промыванием Et2O, с получением соединения 3 (68 г) в виде светло-желтого твердого вещества. ЖХ-МС: 478 (M+Na), 933 (2M+Na).
Раствор соединения 3 (68 г, 149 ммоль) в безводном толуоле (500 мл) кипятили с обратным холодильником в атмосфере азота в течение 3 часов. После упаривания растворителя остаток очищали хроматографией (гексан:EtOAc=10:1), с получением указанного в заголовке соединения (38 г) в виде светло-желтого масла. ЖХ-МС: 376 (M+Na), 729 (2M+Na).
Получение 10
Этиловый эфир (2R,4R)-4-амино-5-(4-бромфенил)-2-гидроксипентановой кислоты

В раствор трет-бутилового эфира (S)-2-(4-бромбензил)-5-оксопирролидин-1-карбоновой кислоты (38 г, 107 ммоль) в безводном DCM (250 мл) при температуре -5°C в атмосфере азота добавляли ТФУ (20 мл, 0,27 моль). Смесь нагревали до комнатной температуры и перемешивали в течение ночи. После упаривания растворителя остаток разбавляли EtOAc (300 мл) и промывали насыщенным водным раствором NaHCO3 (3×200 мл), водой (200 мл), насыщенным водным раствором NaCl (250 мл), сушили над Na2SO4 и концентрировали, с получением неочищенного соединения 1 (24 г) в виде светло-желтого твердого вещества. ЖХ-МС: 254 (M+H).
В раствор NaH (8,6 г, 250 ммоль) в безводном ТГФ (200 мл) в течение 30 минут в атмосфере азота добавляли по каплям раствор соединения 1 (24 г, 94 ммоль) в безводном ТГФ (200 мл) при температуре 0°C. Смесь нагревали до комнатной температуры и перемешивали в течение 2 часов. После охлаждения до температуры 0°C добавляли по каплям пивалоилхлорид (18 г, 150 ммоль) в течение 30 минут. Смесь нагревали до комнатной температуры и перемешивали в течение ночи. Реакцию гасили насыщенным водным раствором NH4Cl (300 мл) и экстрагировали EtOAc (3×200 мл). Объединенные органические слои промывали насыщенным водным раствором NaCl (300 мл), сушили над MgSO4, фильтровали и концентрировали, с получением неочищенного продукта, который затем очищали хроматографией (гексан:EtOAc=25:1), с получением соединения 2 (18 г) в виде светло-желтого твердого вещества. ЖХ-МС: 360(M+Na).
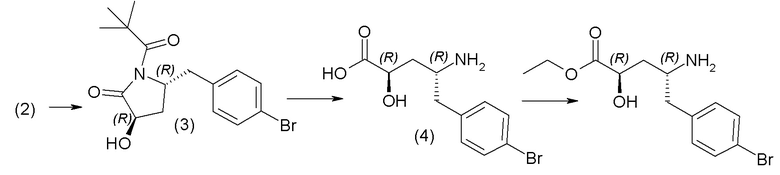
В раствор соединения 2 (18 г, 53 ммоль) в безводном ТГФ (250 мл) в течение 30 минут в атмосфере азота добавляли по каплям HMDSNa (47,7 мл, 96 ммоль) при температуре -78°C. После перемешивания в течение 90 минут при температуре -78°C добавляли по каплям раствор (+)-(8,8-дихлоркамфорилсульфонил)оксазиридина (31,6 г, 106 ммоль) в течение 30 минут. После перемешивания при температуре -78°C в течение 2 часов реакцию гасили насыщенным водным раствором NH4Cl (400 мл) и экстрагировали EtOAc (3×300 мл). Объединенные органические слои промывали насыщенным водным раствором NaCl (300 мл), сушили над MgSO4, фильтровали и концентрировали, с получением неочищенного продукта, который затем очищали хроматографией (гексан:EtOAc=15:1), с получением соединения 3 (8,9 г) в виде светло-желтого твердого вещества. ЖХ-МС: 376(M+Na).
Раствор соединения 3 (8,9 г, 25 ммоль) в концентрированной HCl (81 мл, 81 ммоль) нагревали при температуре 100°C в течение 16 часов. Смесь затем концентрировали, с получением неочищенного продукта, который затем очищали промыванием Et2O, с получением соединения 4 (7 г) в виде светло-желтого твердого вещества, HCl соль. ЖХ-МС: 323 (M+H).
Раствор соединения 4 (7 г, 22 ммоль) в EtOH (10 мл) при комнатной температуре объединяли с 8M HCl в EtOH (120 мл, 960 ммоль). Смесь нагревали при температуре 50°C в течение 16 часов, затем концентрировали. Неочищенный продукт затем очищали промыванием Et2O, с получением указанного в заголовке соединения (6 г) в виде светло-желтого твердого вещества, HCl соль. ЖХ-МС: 352 (M+H).
Получение 11
1-Гидрокси-1H-1,2,3-триазол-4-карбоновая кислота

Этиловый эфир 1-гидрокси-1H-[1,2,3]триазол-4-карбоновой кислоты (2,0 г, 13 ммоль) и EtOH (25 мл) объединяли с предварительно полученным раствором моногидрата гидроксида лития (1,6 г, 38,2 ммоль) в воде (10 мл) и перемешивали при комнатной температуре в течение 4 часов. Смесь частично концентрировали и подкисляли HCl для вызывания образования осадка. Твердый продукт фильтровали и сушили в вакууме, с получением указанного в заголовке соединения (1,3 г).
Получение 12
Этиловый эфир (2R,4R)-5-(4-бромфенил)-2-гидрокси-4-[(1-гидрокси-1H-1,2,3-триазол-4-карбонил)амино]пентановой кислоты

1-Гидрокси-1H-1,2,3-триазол-4-карбоновую кислоту (163 мг, 1,3 ммоль), HCTU (523 мг, 1,3 ммоль) и ДМФ объединяли и перемешивали в течение 5 минут при комнатной температуре. Добавляли DIPEA (661 мкл, 3,8 ммоль) и этиловый эфир (2R,4R)-4-амино-5-(4-бромфенил)-2-гидроксипентановой кислоты (4 мг, 1,3 ммоль), и полученную смесь перемешивали в течение 10 минут. Реакционную смесь упаривали при пониженном давлении и очищали (колонка C18; 20-70% MeCN в воде с 0,05% ТФУ), с получением указанного в заголовке соединения (330 мг).
ПРИМЕР 17
A. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановая кислота
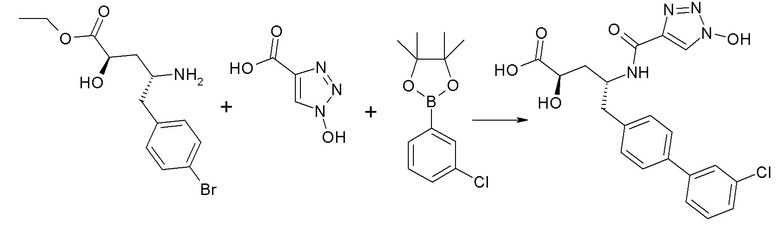
1-Гидрокси-1H-1,2,3-триазол-4-карбоновую кислоту (17,6 мг, 136 мкмоль) и HCTU (56,4 мг, 136 мкмоль) объединяли в ДМФ и перемешивали в течение 5 минут при комнатной температуре. Добавляли DIPEA (71,2 мкл, 409 мкмоль) и этиловый эфир (2R,4R)-4-амино-5-(4-бромфенил)-2-гидроксипентановой кислоты (43 мг, 140 мкмоль), и полученную смесь перемешивали в течение 10 минут. Реакционную смесь упаривали при пониженном давлении и очищали (колонка C18 с обращенной фазой). Очищенное вещество объединяли с пинаконовым эфиром 3-хлорфенилбороновой кислотой, (48,1 мг, 202 мкмоль), K2CO3 (41,8 мг, 302 мкмоль), EtOH (1 мл) и водой (0,3 мл). Кислород удаляли (высокий вакуум), и в атмосфере азота быстро добавляли SilicaCat®Pd(0) (загрузка 0,09 ммоль/г; 112 мг, 10,1 мкмоль). Смесь подвергали воздействию микроволнового излучения при температуре 100°C в течение 20 минут, затем концентрировали. Продукт вновь растворяли в AcOH и очищали препаративной ВЭЖХ, с получением указанного в заголовке соединения (12 мг; чистота 95%). МС m/z [M+H]+ вычислено для C20H19ClN4O5, 431,10; найдено 431,4.
B. Этиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты

Этиловый эфир (2R,4R)-5-(4-бромфенил)-2-гидрокси-4-[(1-гидрокси-1H-1,2,3-триазол-4-карбонил)амино]пентановой кислоты (120 мг, 281 мкмоль) и пинаконовый эфир 3-хлорфенилбороновой кислоты (120 мг, 506 мкмоль) объединяли с K2CO3 (116 мг, 842 мкмоль), EtOH (3 мл) и водой (0,8 мл). Затем добавляли SilicaCat®DPP-Pd (загрузка 280 мкмоль/г; 1 мг, 28 мкмоль), и смесь нагревали при температуре 90°C, и протекание реакции контролировали ЖХ/МС. Реакцию останавливали через 2 часа, и смесь фильтровали, концентрировали и очищали (колонка C18 с обращенной фазой; 30-70% MeCN в воде с 0,05% ТФУ). Добавляли EtOH (5,0 мл, 86 ммоль) и 4М HCl в диоксане (1,5 мл, 6,0 ммоль), и полученную смесь перемешивали при комнатной температуре в течение 40 минут, затем концентрировали и очищали (колонка C18 с обращенной фазой; 30-90% MeCN в воде с 0,05% ТФУ), с получением указанного в заголовке соединения (20 мг; чистота 95%). МС m/z [M+H]+ вычислено для C22H23ClN4O5, 459,14; найдено 459,4.
ПРИМЕР 18
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде родоначального соединения или в виде соли с ТФУ.
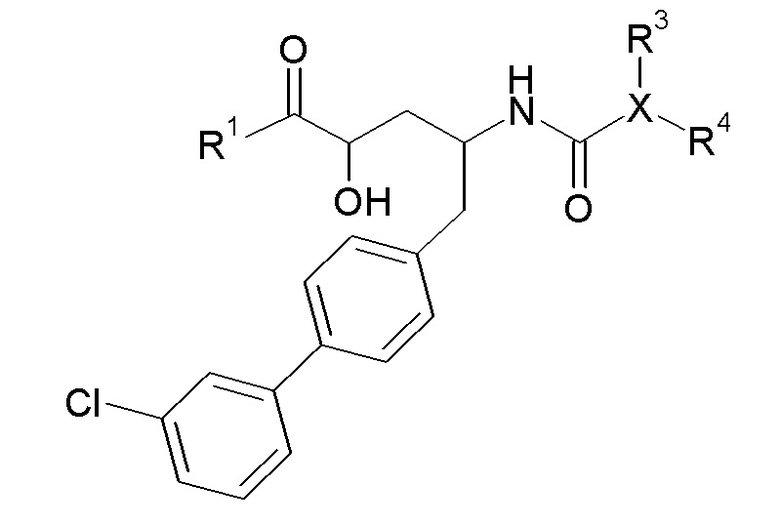

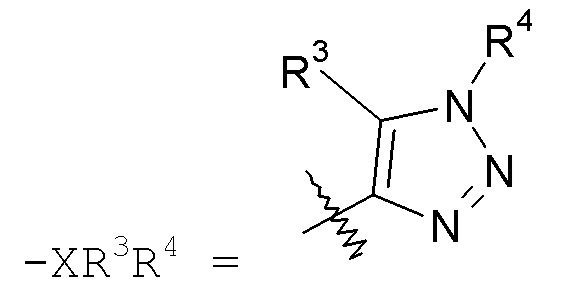

4. Этиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты

6. Изопропиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты
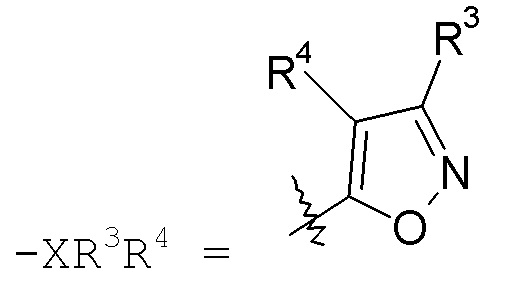
8. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(3-метоксиизоксазол-5-карбонил)амино]пентановая кислота
9. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-4-[(3-хлоризоксазол-5-карбонил)амино]-2-гидроксипентановая кислота
10. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(3-изопропилизоксазол-5-карбонил)амино]пентановая кислота
11. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(3-пропилизоксазол-5-карбонил)амино]пентановая кислота
12. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(3-изобутилизоксазол-5-карбонил)амино]пентановая кислота
13. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-{[3-(1-гидрокси-1-метилэтил)изоксазол-5-карбонил]амино}пентановая кислота
14. (2R,4R)-4-[(3-трет-Бутилизоксазол-5-карбонил)амино]-5-(3'-хлорбифенил-4-ил)-2-гидроксипентановая кислота
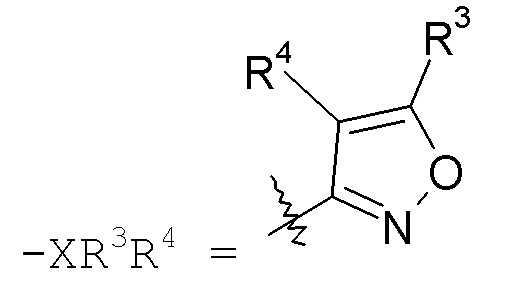
16. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-{[5-(2-гидроксифенил)изоксазол-3-карбонил]амино}пентановая кислота

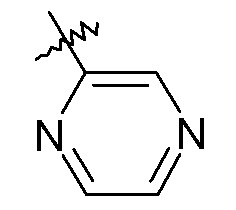



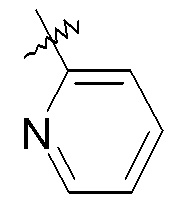

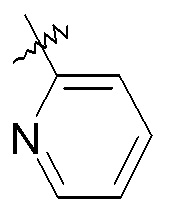
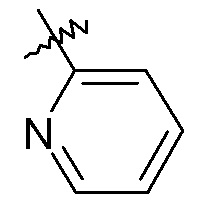

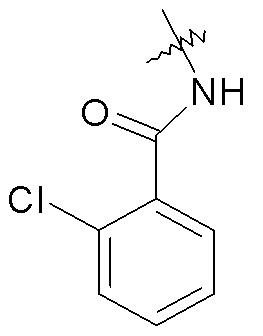



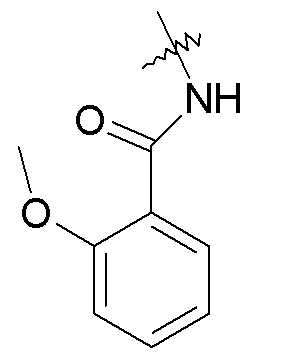

18. Этиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-{[5-(2-гидроксифенил)-2H-пиразол-3-карбонил]амино}пентановой кислоты (соль с ТФУ)
19. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиразин-2-ил-2H-пиразол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
21. Изобутиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиразин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты
22. 5-Метил-2-оксо[1,3]диоксол-4-илметиловый эфир (2S,4S)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиразин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты (соль с ТФУ)
23. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
24. Этиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты
25. Изобутиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты
26. Изопропиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты
27. (2R,4R)-4-{[5-(2-Хлорбензоиламино)-2H-пиразол-3-карбонил]амино}-5-(3'-хлорбифенил-4-ил)-2-гидроксипентановая кислота (соль с ТФУ)
28. Этиловый эфир (2R,4R)-4-{[5-(2-хлорбензоиламино)-2H- пиразол-3-карбонил]амино}-5-(3'-хлорбифенил-4-ил)-2-гидроксипентановой кислоты (соль с ТФУ)
30. Изобутиловый эфир (2R,4R)-4-{[5-(2-хлорбензоиламино)-2H-пиразол-3-карбонил]амино}-5-(3'-хлорбифенил-4-ил)-2-гидроксипентановой кислоты (соль с ТФУ)
31. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-{[5-(2-метоксибензоиламино)-2H-пиразол-3-карбонил]амино}пентановая кислота
32. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-{[5-(1-гидроксиэтил)-2H-пиразол-3-карбонил]амино}пентановая кислота
33. Этиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-3-ил-2H-пиразол-3-карбонил)амино]пентановой кислоты (соль с ТФУ)

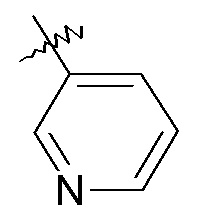

35. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-гидрокси-1-метил-1H-пиразол-3-карбонил)амино]пентановая кислота
36. Изобутиловый эфир (2R,4R)-5-(3'-хлорбифенил-4-ил)-2-гидрокси-4-[(5-гидрокси-1-метил-1H-пиразол-3-карбонил)амино]пентановой кислоты
37. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-гидрокси-1-пиридин-2-ил-1H-пиразол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
38. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-4-{[1-(2-фторфенил)-5-гидрокси-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
39. (2R,4S)-5-(3'-Хлорбифенил-4-ил)-4-{[1-(3-хлорфенил)-5-гидрокси-1H-пиразол-3-карбонил]амино}-2-гидроксипентановая кислота
40. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-4-[(5-этокси-1H- пиразол-3-карбонил)амино]-2-гидроксипентановая кислота
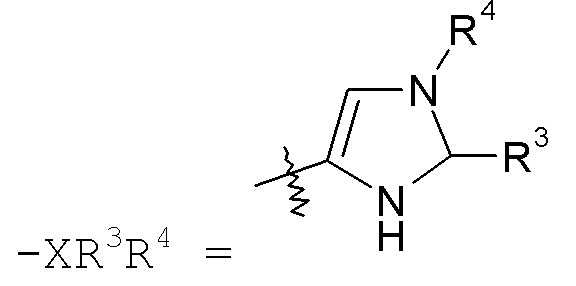
42. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-4-{[1-(3-хлорфенил)-5-оксо-4,5-дигидро-1H-[1,2,4]триазол-3-карбонил]амино}-2-гидроксипентановая кислота
43. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-4-{[1-(2-хлорфенил)-5-оксо-4,5-дигидро-1H-[1,2,4]триазол-3-карбонил]амино}-2-гидроксипентановая кислота
44. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-4-{[1-(4-фторфенил)-5-оксо-4,5-дигидро-1H-[1,2,4]триазол-3-карбонил]амино}-2-гидроксипентановая кислота



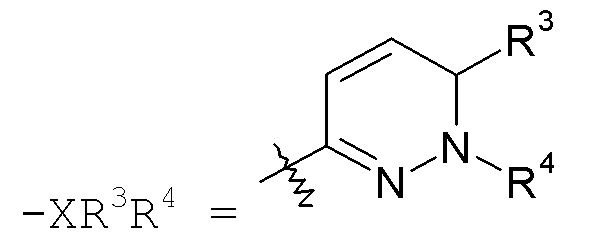
49. (2R,4R)-5-(3'-Хлорбифенил-4-ил)-2-гидрокси-4-[(6-оксо-1-фенил-1,6-дигидропиридазин-3-карбонил)амино]пентановая кислота (соль с ТФУ)
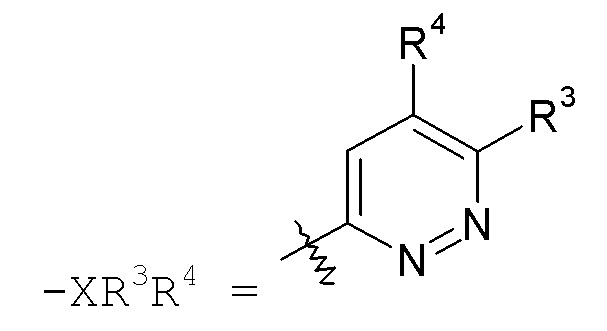
ПРИМЕР 19
Следуя способам, описанным в примерах данного документа, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде родоначального соединения.


2. Изобутиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
3. Изобутиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
4. Этиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
5. Гептиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
6. (2R,4R)-5-(5'-Хлор-2'-фторбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановая кислота
7. Изобутиловый эфир (2R,4R)-5-(5'-хлор-2'-фторбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
8. Изобутиловый эфир (2R,4R)-5-(5'-хлор-2'-фторбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
9. Этиловый эфир (2R,4R)-5-(5'-хлор-2'-фторбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
10. Гептиловый эфир (2R,4R)-5-(5'-хлор-2'-фторбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
12. (2R,4R)-5-(5'-Хлор-2'-метилбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановая кислота
13. Изобутиловый эфир (2R,4R)-5-(5'-хлор-2'-метилбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
14. Изобутиловый эфир (2R,4R)-5-(5'-хлор-2'-метилбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
15. Этиловый эфир (2R,4R)-5-(5'-хлор-2'-метилбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
16. Гептиловый эфир (2R,4R)-5-(5'-хлор-2'-метилбифенил-4-ил)-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]пентановой кислоты
17. (2R,4R)-2-Гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]-5-(2'-метоксибифенил-4-ил)пентановая кислот
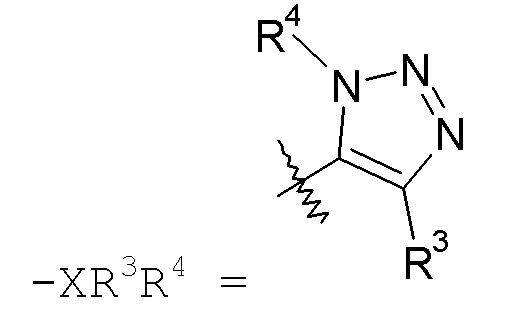
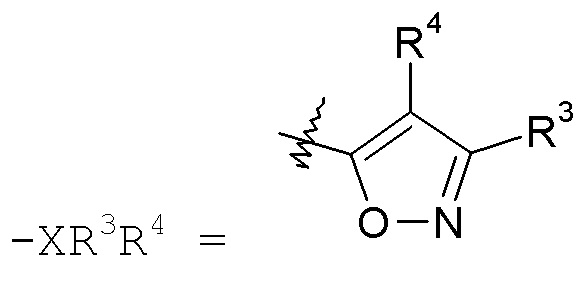
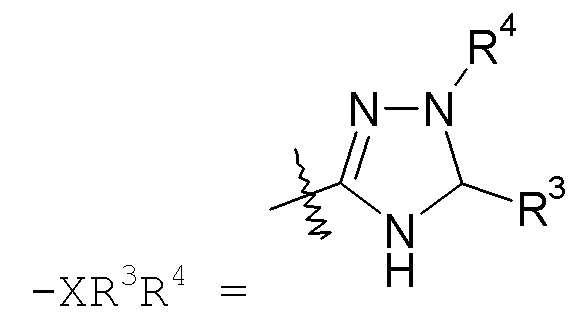

22. Изобутиловый эфир (2R,4R)-4-{[3-((S)-2-амино-3-метилбутирилоксиметокси)-3H-бензотриазол-5-карбонил]амино}-5-(3'-хлорбифенил-4-ил)-2-гидроксипентановой кислоты
ПРИМЕР 20
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде родоначального соединения или в виде соли с ТФУ.

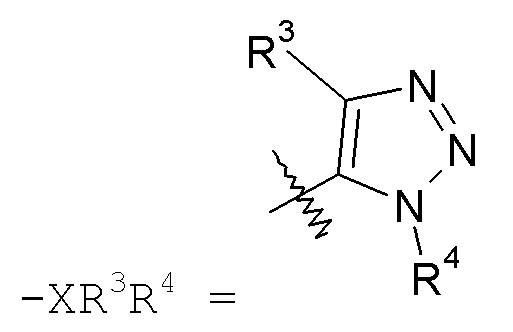

4. (2R,4R)-5-(3-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-оксо-1-фенил-4,5-дигидро-1H-[1,2,4]триазол-3-карбонил)амино]пентановая кислота
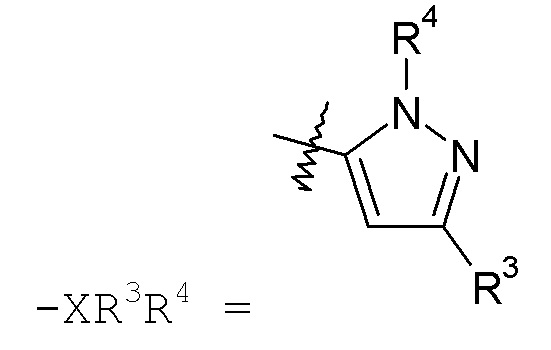
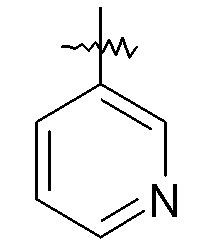

6. (2R,4R)-5-(3-Хлорбифенил-4-ил)-2-гидрокси-4-({5-[(2-метоксиэтил)метилкарбамоил]-2H-пиразол-3- карбонил}амино)пентановая кислота
7. (2R,4R)-4-[(5-Ацетил-2H-пиразол-3-карбонил)амино]-5-(3-хлорбифенил-4-ил)-2-гидроксипентановая кислота
8. (2R,4R)-5-(3-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-3-ил-2H-пиразол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
9. (2R,4R)-5-(3-Хлорбифенил-4-ил)-2-гидрокси-4-[(5-пиридин-2-ил-2H-пиразол-3-карбонил)амино]пентановая кислота (соль с ТФУ)
ПРИМЕР 21
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде родоначального соединения.
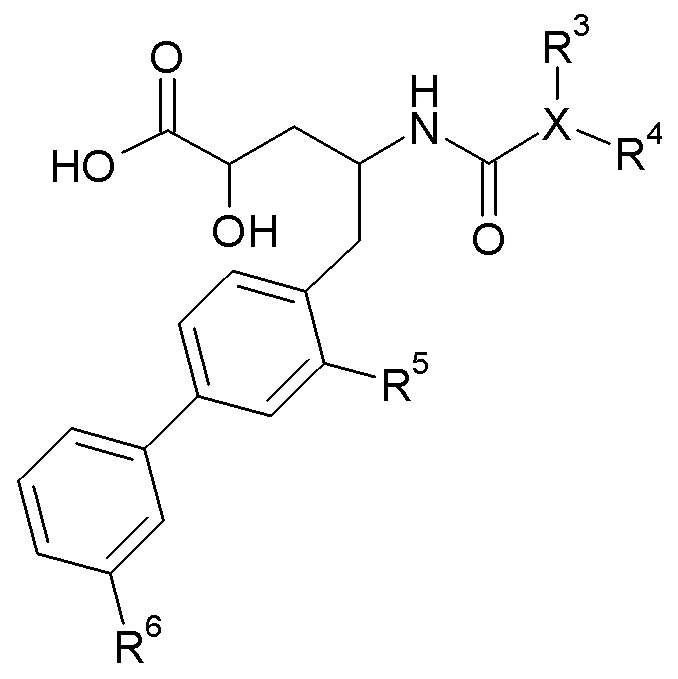
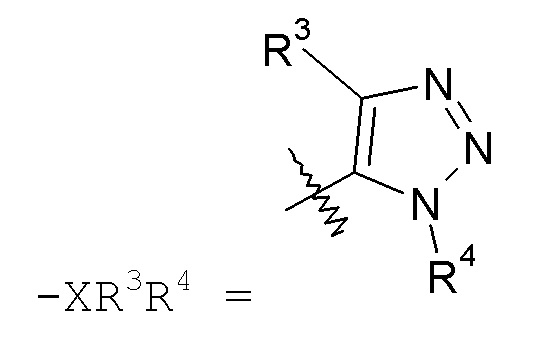

Получение 13
Этиловый эфир (2R,4R)-5-(4-бромфенил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты

В раствор 1-гидрокси-1H-1,2,3-бензотриазол-6-карбоновой кислоты (362 мг, 2,0 ммоль) добавляли HCTU (837 мг, 2,0 ммоль), и смесь перемешивали при комнатной температуре в течение 10 минут. Затем добавляли DIPEA (529 мкл, 3,0 ммоль) и этиловый эфир (2R,4R)-4-амино-5-(4-бромфенил)-2-гидроксипентановой кислоты (320 мг, 1,0 ммоль), и полученную смесь перемешивали при комнатной температуре в течение 15 минут. Смесь концентрировали в вакууме, и полученный осадок очищали (колонка C18, 55 г, 20-70% MeCN в воде с 5% ТФУ), с получением указанного в заголовке соединения в виде белого твердого вещества 365 мг).
ПРИМЕР 22
(2R,4R)-5-(5'-Хлор-2'-фторбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановая кислота

В раствор этилового эфира (2R,4R)-5-(4-бромфенил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты (50,0 мг, 105 мкмоль), фенилбороновой кислоты (157 мкмоль, 1,5 экв.) и K2CO3 (43,4 мг, 314 мкмоль) в EtOH (500 мкл) и воде (150 мкл) добавляли SilicaCat®DPP-Pd (загрузка 0,3 ммоль/г; 37,4 мг, 10 мкмоль), и реакционную смесь нагревали при температуре 100°C в течение 10 минут. Смеси давали охладиться до комнатной температуры, после чего добавляли 1,0М LiOH в воде (838 мкл, 838 мкмоль), и смесь перемешивали в течение 30 минут. Смесь фильтровали, фильтрат концентрировали в вакууме и очищали препаративной ВЭЖХ, с получением указанного в заголовке соединения (17,9 мг; чистота 98%). МС m/z [M+H]+ вычислено для C24H20ClFN4O5, 499,11; найдено 499,2.
ПРИМЕР 23
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде родоначального соединения или в виде соли с ТФУ.
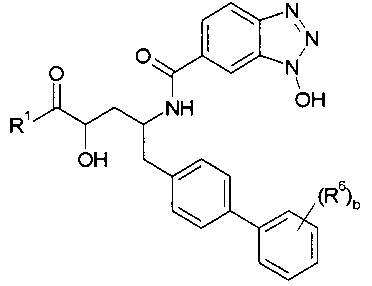
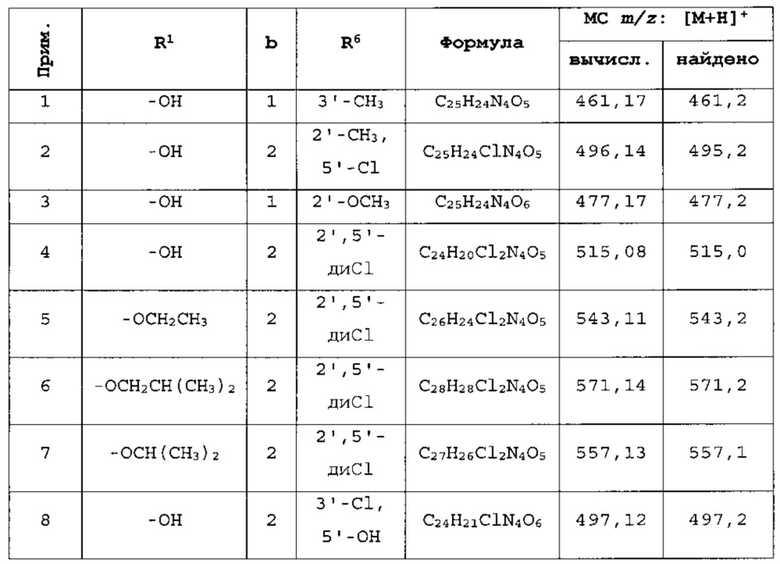
2. (2S,4S)-5-(5'-Хлор-2'-метилбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-1Н-бензотриазол-5-карбонил)амино]пентановая кислота
3. (2S,4S)-2-Гидрокси-4-[(3-гидрокси-3Н-бензотриазол-5-карбонил)амино]-5-(2'-метоксибифенил-4-ил)пентановая кислота
4. (2S,4S)-5-(2',5'-Дихлорбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановая кислота
5. Этиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты
6. Изобутиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты
7. Изопропиловый эфир (2R,4R)-5-(2',5'-дихлорбифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановой кислоты (соль с ТФУ)
8. (2S,4S)-5-(3'-Хлор-5'-гидроксибифенил-4-ил)-2-гидрокси-4-[(3-гидрокси-3H-бензотриазол-5-карбонил)амино]пентановая кислота
Получение 14
трет-Бутиловый эфир (S)-2-(1-бифенил-4-ил-1-метилэтил)-5-оксопирролидин-1-карбоновой кислоты

В раствор 2-(4-бромфенил)ацетонитрила (130,0 г, 0,7 моль) и йодметана (103,9 мл, 1,7 моль) в ТГФ (1,0 л) при температуре 10°C небольшими порциями добавляли NaH (60% дисперсия в минеральном масле, 66,7 г, 1,7 моль). После завершения добавления смесь перемешивали при температуре 10°C в течение еще 2 часов. Смесь выливали в ледяную воду (2,0 л) и экстрагировали EtOAc (1,5 л). Органический слой промывали насыщенным водным раствором NaCl, сушили над безводным MgSO4 и концентрировали, с получением соединения 1 (175 г, содержащее минеральное масло) в виде желтого масла, которое использовали напрямую без дополнительной очистки.
1H ЯМР (CDCl3, 300 МГц) (7,52 (д, J=9,0 Гц, 2H), 7,38 (д, J=9,0 Гц, 2H), 1,72 (с, 6H).
В раствор соединения 1 (175 г, содержащее минеральное масло) в DCM (1,0 л) при температуре -78°C по каплям добавляли DIBAL (1,0М раствор в DCM, 700 мл, 0,70 моль). Реакционную смесь перемешивали при температуре -78°C в течение 1,5 часа и затем осторожно гасили 3,0н HCl (1,0 л). Полученную смесь перемешивали при комнатной температуре в течение ночи, и органический слой промывали насыщенным водным раствором NaCl, сушили над безводным Na2SO4 и концентрировали, с получением соединения 2 (180 г) в виде желтого масла, которое использовали напрямую без дополнительной очистки.
1H ЯМР (CDCl3, 300 МГц) (9,48 (с, 1H), 7,53 (д, J=11,0 Гц, 2H), 7,17 (д, J=11,0 Гц, 2H), 1,46 (с, 6H).
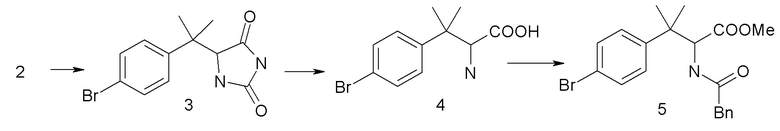
В водный раствор NaCN (32,7 г в 1,0 л H2O, 0,7 моль) добавляли (NH4)2CO3 (380 г, 4,0 моль) и соединение 2 (180 г). Реакционную смесь кипятили с обратным холодильником в течение ночи и затем концентрировали при пониженном давлении при температуре 75°C. К остатку добавляли воду (350 мл), и смесь снова концентрировали. Остаток суспендировали в петролейном эфире (700 мл) и воде (250 мл), и полученную смесь перемешивали при комнатной температуре в течение 15 минут. Выпавший осадок собирали фильтрованием и сушили, с получением соединения 3 (150 г) в виде белого твердого вещества.
1H ЯМР (ДМСО-d6, 300 МГц) (10,39 (с, 1H), 8,05 (с, 1H), 7,48 (д, J=9,0 Гц, 2H), 7,28 (д, J=9,0 Гц, 2H), 4,17 (с, 1H), 1,42 (с, 3H), 1,34 (с, 3H).
Суспензию соединения 3 (150 г, 0,51 моль) в 6,0н NaOH (400 мл) и этан-1,2-диоле (300 мл) перемешивали при температуре 120°C в течение 38 часов. Смесь охлаждали до комнатной температуры и нейтрализовали раствором HCl. Выпавший осадок собирали фильтрованием и сушили, с получением соединения 4 (250 г, содержащее NaCl соль) в виде белого твердого вещества.
1H ЯМР (ДМСО-d6, 300 МГц) (7,35 (д, J=9,0 Гц, 2H), 7,17 (д, J=9,0 Гц, 2H), 3,22 (с, 1H), 1,16 (с, 3H), 1,15 (с, 3H).
В суспензию соединения 4 (250 г, содержащее NaCl соль) в MeOH (1,0 л) добавляли по каплям тионилхлорид (72,0 мл, 1,0 моль) при температуре 5°C. Смесь кипятили с обратным холодильником в течение ночи, и растворитель удаляли при пониженном давлении. Остаток распределяли между DCM (1,0 л) и насыщенным водным раствором NaHCO3 (1,5 л). Органический слой промывали насыщенным водным раствором NaCl, сушили над безводным Na2SO4 и концентрировали, с получением соответствующего метилового эфира (90,0 г). При температуре 0°C добавляли по каплям 2-фенилацетилхлорид (48,6 г, 0,32 моль) в растворе эфира (90,0 г) и Et3N (56,5 мл, 0,41 моль) в DCM (1,0 л), и смесь перемешивали при температуре 0°C в течение 30 минут. Смесь промывали 1,0н HCl (500 мл) и насыщенным водным раствором NaCl, соответственно. Органический слой сушили над безводным Na2SO4 и концентрировали, с получением соединения 5 (120 г).
1H ЯМР (CDCl3, 300 МГц) (7,32 (м, 5H), 7,18 (м, 2H), 6,95 (м, 2H), 5,68 (ушир.с, 1H), 4,76 (д, J=9,0 Гц, 1H), 3,57 (с, 3H), 3,53 (д, J=5,0 Гц, 2H), 1,30 (с, 3H), 1,25 (с, 3H).

В раствор соединения 5 (120 г, 0,30 моль) в MeOH (500 мл) добавляли 4,0н NaOH (200 мл). Смесь перемешивали при комнатной температуре в течение 4 часов, и затем доводили pH до pH=1 3,0н HCl. Полученную смесь экстрагировали EtOAc (2×300 мл). Объединенные экстракты промывали насыщенным водным раствором NaCl, сушили над безводным Na2SO4 и концентрировали при пониженном давлении. Остаток перекристаллизовывали из смеси EtOAc/гексан, с получением соединения 6 (82,0 г).
1H ЯМР (ДМСО-d6, 300 МГц) (7,41 (д, J=6,0 Гц, 2H), 7,22 (м, 5H), 6,99 (д, J=6,0 Гц, 2H), 4,65 (д, J=9,0 Гц, 1H), 3,52 (д, J=14,0 Гц, 1H), 3,36 (д, J=14,0 Гц, 1H), 1,34 (с, 3H), 1,30 (с, 3H).
Доводили pH суспензии соединения 6 (82,0 г, 0,21 моль) до pH=8,5 в дистиллированной воде (3,0 л) 3,0н LiOH, и образовывался прозрачный раствор. Добавляли иммобилизованную пенициллиназу (20,0 г), и полученную смесь перемешивали при температуре 37°C в течение 60 часов. Смесь фильтровали, и pH фильтрата доводили до pH=1 3,0н HCl и экстрагировали EtOAc. Объединенные экстракты промывали насыщенным водным раствором NaCl, сушили над безводным Na2SO4 и концентрировали, с получением соединения 7 (59,0 г, 80% эи, содержащего 2-фенилуксусную кислоту).
Суспензию соединения 7 (59,0 г, содержащую 2-фенилуксусную кислоту) в 6,0н HCl (500 мл) кипятили с обратным холодильником в течение ночи. Смесь промывали EtOAc (300 мл), и водную фазу концентрировали при пониженном давлении, с получением соответствующей аминокислоты в виде ее гидрохлоридной соли. Соль растворяли в воде (300 мл), и pH раствора доводили до pH=11. Добавляли раствор (Boc)2O (33,0 г, 0,2 моль) в ацетоне (200 мл), и смесь перемешивали при комнатной температуре в течение 2 часов. Смесь промывали гексаном (200 мл), и pH водной фазы доводили до pH=2. Полученную смесь экстрагировали EtOAc (2×300 мл). Объединенные экстракты промывали насыщенным водным раствором NaCl, сушили над безводным Na2SO4 и концентрировали, с получением соединения 8 (37,0 г) в виде белого твердого вещества.
1H ЯМР (CDCl3, 300 МГц) (9,48 (ушир.с, 1H), 7,46 (д, J=7,0 Гц, 2H), 7,26 (д, J=7,0 Гц, 2H), 5,02 (ушир.с, 1H), 4,56 (д, J=9,0 Гц, 1H), 1,39 (с, 9H).

Смесь соединения 8 (37,0 г, 0,1 моль) в диоксане (200 мл) и 1,0н K2CO3 (200 мл) дегазировали в течение 30 минут азотом, затем добавляли фенилбороновую кислоту (13,4 г, 0,1 моль) и Pd(PPh3)4 (1,6 г, 1,4 ммоль). Смесь нагревали при температуре 75°C в течение 8 часов и затем охлаждали до комнатной температуры. Смесь промывали раствором EtOAc/гексан (150 мл, 1:1), и pH водной фазы доводили до pH=2 и экстрагировали EtOAc (2×300 мл). Объединенные экстракты промывали насыщенным водным раствором NaCl, сушили над безводным Na2SO4 и концентрировали, с получением соединения 9 (31,0 г, 84%-ный выход) в виде белого твердого вещества.
Раствор соединения 9 (31,0 г, 84 ммоль), кислоты Мельдрума (13,3 г, 92 ммоль) и DMAP (15,4 г, 0,13 моль) в DCM (400 мл) охлаждали до температуры -5°C, и в течение 1 часа добавляли раствор DCC (19,0 г, 92 ммоль) в DCM (200 мл). Смесь перемешивали при температуре -5°C в течение ночи. Выпавший осадок отфильтровывали, и фильтрат промывали 1,0н HCl (2×700 мл) и насыщенным водным раствором NaCl, соответственно. После сушки органического слоя, содержащего соединение 10, над безводным MgSO4, его использовали напрямую на следующей стадии без концентрирования.
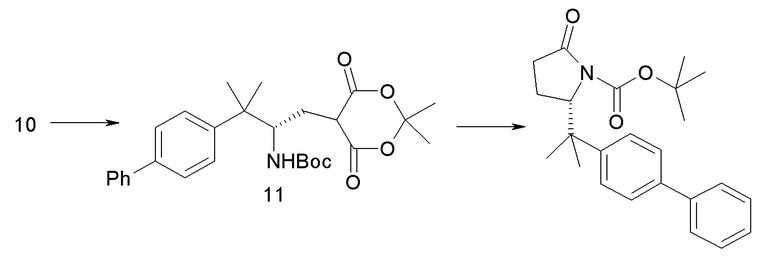
Раствор соединения 10 в DCM (600 мл) охлаждали до температуры -5°C и добавляли AcOH (45,0 мл). Затем в течение 30 минут небольшими порциями добавляли NaBH4 (7,0 г, 0,2 моль), и смесь перемешивали при температуре -5°C в течение 3 часов. Добавляли по каплям воду (50,0 мл), затем добавляли насыщенный водный раствор NaCl (450 мл). Органический слой промывали водой (2×300 мл) и насыщенным водным раствором NaHCO3 (2×300 мл), сушили над безводным MgSO4 и концентрировали, с получением соединения 11 (32,0 г, 75% эи) в виде не совсем белого твердого вещества. После перекристаллизации из EtOH получали хирально чистое соединение 11 (13,0 г).
1H ЯМР (CDCl3, 300 МГц) (7,61 (м, 10H), 4,46 (ушир.с, 1H), 4,26 (м, 1H), 3,72 (ушир.с, 1H), 2,23 (м, 1H), 1,79 (с, 3H), 1,76 (с, 3H), 1,48 (с, 6H), 1,39 (с, 9H).
Раствор соединения 11 (13,0 г, 27,0 ммоль) в толуоле (100,0 мл) кипятили с обратным холодильником в течение 3 часов. После упаривания растворителя остаток перекристаллизовывали из смеси гексан/EtOAc (3:1), с получением указанного в заголовке соединения (8,0 г) в виде белого твердого вещества.
Получение 15
Этиловый эфир (2R,4S)-4-амино-5-бифенил-4-ил-2-гидрокси-5-метилгексановой кислоты
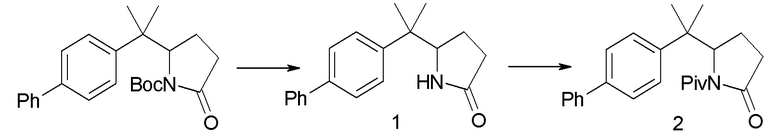
Смесь трет-бутилового эфира (S)-2-(1-бифенил-4-ил-1-метилэтил)-5-оксопирролидин-1-карбоновой кислоты (14,0 г, 36,9 ммоль, рацемический) в 3,0н растворе HCl-EtOAc (150 мл) перемешивали при комнатной температуре в течение 3 часов. Растворитель удаляли при пониженном давлении, с получением соединения 1 (10,0 г) в виде белого твердого вещества.
В раствор соединения 1 (10,0 г, 35,8 ммоль) в ТГФ (80,0 мл) добавляли по каплям BuLi (2,5М в гексане, 15,0 мл) при температуре -78°C. После перемешивания смеси в течение 30 минут добавляли по каплям пивалоилхлорид (4,8 мл, 39,4 ммоль). Смесь перемешивали при температуре -78°C в течение 1 часа и затем гасили насыщенным водным раствором NH4Cl. Полученную смесь экстрагировали EtOAc, и объединенные экстракты промывали насыщенным водным раствором NaCl, сушили над безводным MgSO4 и концентрировали. Остаток очищали колоночной флэш-хроматографией на силикагеле, с получением соединения 2 (9,0 г) в виде белого твердого вещества.

В раствор соединения 2 (9,0 г, 24,7 ммоль) в ТГФ (50,0 мл) при температуре -78°C добавляли по каплям бис(триметилсилил)амид натрия (2,0М в ТГФ, 18,5 мл, 37,0 ммоль). Смесь перемешивали в течение 20 минут, и добавляли по каплям раствор производного оксазиридина (10,8 г, 37,0 ммоль) в ТГФ (30,0 мл). Смесь перемешивали при температуре -78°C в течение 30 минут, и затем гасили насыщенным водным раствором NH4Cl. Полученную смесь экстрагировали EtOAc (1,0 л), и экстракт промывали 1,0н HCl и насыщенным водным раствором NaCl, сушили над безводным MgSO4 и упаривали для удаления большей части растворителя. Выпавший осадок отфильтровывали, и фильтрат концентрировали. Остаток очищали колоночной флэш-хроматографией на силикагеле (от DCM:гексан=1:1 до DCM), с получением соединения 3 (4,3 г, рацемический). Указанный рацемат подвергали хиральной AD-колоночной хроматографии, с получением хирально чистого соединения 3 (1,4 г).
1H ЯМР (ДМСО-d6, 300 МГц) (7,63 (м, 4H), 7,49 (м, 4H), 4,83 (д, 1H), 3,29 (м, 1H), 2,31 (м, 2H), 1,40 (с, 3H), 1,36 (с, 3H), 1,28 (с, 9H). ЖХ-МС (ESI): m/z 380,1 [M+H]+.
Раствор соединения 3 (1,7 г, 160 ммоль) в EtOH (15,0 мл) и 12,0н HCl (15,0 мл) нагревали при температуре 90~95°C в течение 20 часов. Растворитель удаляли, и остаток обрабатывали 3,0н раствором HCl-EtOH (25,0 мл) при кипячении с обратным холодильником в течение еще 3 часов. После удаления растворителя остаток очищали препаративной ВЭЖХ, с получением указанного в заголовке соединения (0,6 г) в виде пенообразного твердого вещества HCl соли.
1H ЯМР (ДМСО-d6, 300 МГц) (7,88 (ушир.с, 3H), 7,68 (м, 4H), 7,49 (м, 4H), 7,35 (м, 1H), 6,11 (ушир.с, 1H), 4,11 (ушир.с, 1H), 4,05 (кв, 2H), 3,61 (ушир.с, 1H), 1,67 (м, 2H), 1,40 (с, 3H), 1,36 (с, 3H), 1,09 (т, 3H). ЖХ-МС (ESI): m/z 342,1 [M+H]+.
ПРИМЕР 24
5-[(S)-2-Бифенил-4-ил-1-((R)-2-карбокси-2-гидроксиэтил)-2-метилпропилкарбамоил]-1H-пиразол-3-карбоновая кислота
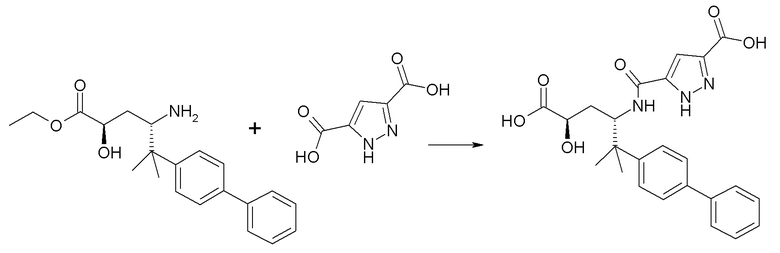
Этиловый эфир (2R,4S)-4-амино-5-бифенил-4-ил-2-гидрокси-5-метилгексановой кислоты (70 мг, 0,2 ммоль), 3,5-пиразолдикарбоновую кислоту (32 мг, 0,2 ммоль) и HCTU (85 мг, 0,2 ммоль) объединяли в ДМФ (5 мл) и перемешивали в течение 2 минут. Добавляли DIPEA (79 мг, 0,6 ммоль), и полученную смесь перемешивали в течение 1 часа при температуре 50°C. Реакционную смесь упаривали при пониженном давлении. Неочищенный продукт растворяли в EtOH, и добавляли достаточное количество эквивалентов 10н NaOH для подщелачивания смеси. Реакцию внимательно отслеживали в течение 1 часа до полного удаления защитных групп. Смесь затем вновь подкисляли равным количеством уксусной кислоты и упаривали при пониженном давлении. Продукт очищали с использованием хроматографии с обращенной фазой (градиент 10-70% MeCN), с получением указанного в заголовке соединения в виде соли с ТФУ (14 мг; чистота 90%). МС m/z [M+H]+ вычислено для C24H25N3O6, 452,17; найдено 452,2.
ПРИМЕР 25
Следуя способам, описанным в примерах данного описания, и заменяя соответствующие исходные продукты и реагенты, получали соединения, имеющие следующую формулу, в виде родоначального соединения или в виде соли с ТФУ.
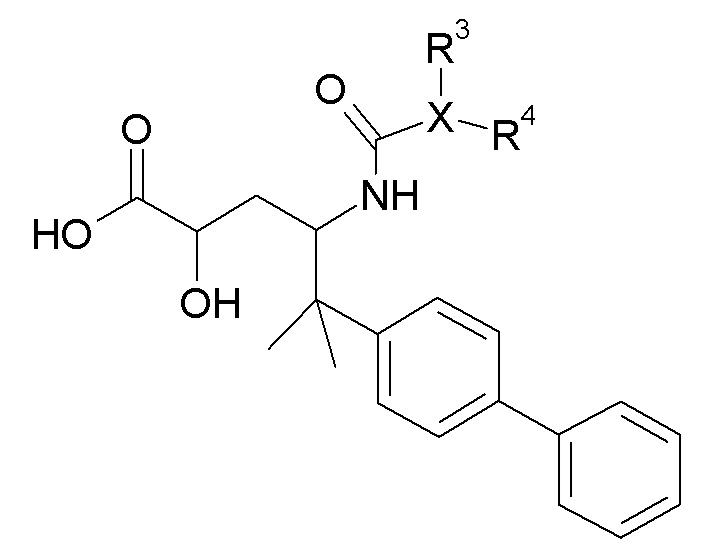
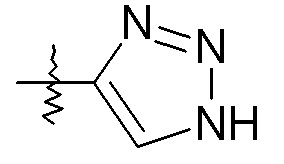
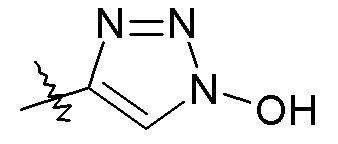

2. (2R,4S)-5-Бифенил-4-ил-2-гидрокси-4-[(1-гидрокси-1H-[1,2,3]триазол-4-карбонил)амино]-5-метилгексановая кислота (соль с ТФУ)
3. (2R,4S)-5-Бифенил-4-ил-2-гидрокси-4-[(3-гидроксиизоксазол-5-карбонил)амино]-5-метилгексановая кислота
АНАЛИЗ 1
Анализы in vitro для количественной оценки силы ингибиторов для NEP человека и крысы и ACE человека
Ингибирующую неприлизин активность соединений для человека и крыс (EC 3.4.24.11; (NEP) и ингибитора ангиотензин-превращающего фермента человека (ACE) определяли с использованием анализов in vitro, как описано ниже.
Выделение активного NEP из почек крысы
NEP крысы получали из почек взрослых крыс Sprague Dawley. Цельные почки промывали в холодном забуференном фосфатом физиологическом растворе PBS и переносили в ледяной буфер для лизиса (1% Triton X-114, 150 мМ NaCl, 50 мМ трис(гидроксиметил)аминометан pH 7,5; Bordier (1981) J. Biol. Chem. 256: 1604-1607) в соотношении 5 мл буфера на каждый грамм почки. Образцы гомогенизировали с использованием ручного гомогенизатора тканей polytron на льду. Гомогенаты центрифугировали при 1000g в роторе с качающимися стаканами в течение 5 минут при 3°C. Осадок вновь суспендировали в 20 мл ледяного буфера для лизиса и инкубировали на льду в течение 30 минут. Затем образцы (15-20 мл) наслаивали на подушку 25 мл ледяного буфера (6% масс./об. сахарозы, 50 мМ pH 7,5 Трис, 150 мМ NaCl, 0,06%, Triton X-114), нагревали до 37°C в течение 3-5 минут и центрифугировали при 1000×g на роторе с качающимися стаканами при комнатной температуре в течение 3 минут. Два верхних слоя аспирировали, оставляя вязкий масляный осадок, содержащий обогащенную мембранную фракцию. Глицерин добавляли до концентрации 50%, и образцы хранили при -20°C. Концентрации белка оценивали количественно с использованием системы детекции BCA с альбумином бычьей сыворотки (BSA) в качестве стандарта.
Анализы ингибирования ферментов
Рекомбинантный человеческий NEP и рекомбинантный человеческий ACE получали из коммерческих источников (R&D Systems, Minneapolis, MN, каталожные номера 1182-ZN и 929-ZN, соответственно). Флуорогенный пептидный субстрат Mca-D-Arg-Arg-Leu-Dap-(Dnp)-OH (Medeiros et al. (1997) Braz. J. Med. Biol. Res. 30:1157-62; Anaspec, San Jose, CA) и Abz-Phe-Arg-Lys(Dnp)-Pro-OH (Araujo et al. (2000) Biochemistry 39:8519-8525; Bachem, Torrance, CA) использовали для анализов NEP и ACE, соответственно.
Анализы проводили на 384-луночных непрозрачных белых планшетах при 37°C с использованием субстратов флуорогенных пептидов в концентрации 10 мкм в буфере для анализа (NEP: 50 мМ HEPES pH 7,5, 100 мМ NaCl, 0,01% полиэтиленгликоль сорбитан монолаурат (Tween-20), 10 мкМ ZnSO4; ACE: 50 мМ HEPES, pH 7,5, 100 мМ NaCl, 0,01% Tween-20, 1 мкМ ZnSO4). Соответствующие ферменты использовали в концентрациях, приводящих к количественному протеолизу 1 мкм субстрата через 20 минут при 37°C.
Исследуемые соединения анализировали в интервале концентраций от 10 мкМ до 20. Исследуемые соединения добавляли к ферментам и инкубировали в течение 30 мин при 37°C до инициирования взаимодействия добавлением субстрата. Взаимодействия прекращали через 20 минут инкубации при 37°C добавлением ледяной уксусной кислоты до конечной концентрации, составляющей 3,6% (об./об.).
Планшеты считывали на флуориметре с длинами волн возбуждения и испускания, установленными на 320 нм и 405 нм, соответственно. Константы ингибирования получали нелинейным регрессом данных, используя уравнение (GraphPad Software, Inc., San Diego, CA):
v=v0/[1+(I/K′)]
где v - скорость реакции, v0 - скорость неингибируемой реакции, I - концентрация ингибитора, и K′ - истинная константа ингибирования.
Соединения по изобретению исследовали в данном анализе и было обнаружено, что значения pKi для NEP человека, были следующие. Обычно, либо пролекарства соединения не ингибировали фермент в этом in vitro анализе, либо пролекарства не определяли (н.о.), поскольку активность не ожидалась.
АНАЛИЗ 2
Фармакодинамический (PD) анализ активности ACE и NEP у подвергнутых анестезии крыс
Самцов нормотензивных крыс, Sprague Dawley, подвергали анестезии с помощью 120 мг/кг (i.p.) инактина. После анестезии вставляли канюли в яремную вену, сонную артерию (трубки PE 50) и мочевой пузырь (расширяющиеся трубки PE 50) и проводили трахеотомию (тефлоновая игла, размер 14) для облегчения самостоятельного дыхания. Затем животных оставляли стабилизироваться в течение 60 минут и содержали их при постоянной инфузии по всем отделам 5 мл/кг/час солевого раствора (0,9%) для поддержания их гидратации и обеспечения продукции мочи. Температуру тела поддерживали на протяжении эксперимента с использованием грелки-подушки. В конце периода стабилизации 60 минут животным вводили внутривенно (i.v.) две дозы AngI (1,0 мкг/кг, в случае активности ингибитора ACE) с интервалом 15 минут. Через 15 минут после второй дозы AngI животных обрабатывали носителем или исследуемым соединением. Через пять минут животных дополнительно обрабатывали с помощью болюсной i.v. инъекции предсердного натрийуретического пептида (ANP; 30 мкг/кг). Сбор мочи (в предварительно взвешенные пробирки eppendorf) начинали сразу после обработки ANP и продолжали в течение 60 минут. На 30 и 60 минутах при сборе мочи животных повторно стимулировали AngI. Измерения кровяного давления проводили с использованием системы Notocord (Kalamazoo, MI). Образцы мочи замораживали при -20°C до использования для анализа cGMP. Концентрации cGMP в моче определяли иммуноферментным анализом с использованием коммерческого набора (Assay Designs, Ann Arbor, Michigan, Cat. No. 901-013). Объем мочи определяли гравиметрически. Выход cGMP с мочой рассчитывали как выход продукции мочи и концентрацию cGMP в моче. Ингибирование ACE оценивали количественным определением % ингибирования прессорной реакции на AngI. Ингибирование NEP оценивали количественным определением стимуляции индуцированного ANP-повышения выхода cGMP с мочой.
АНАЛИЗ 3
Оценка in vivo антигипертензивного действия на модели контролируемой гипертензии SHR
Крыс со спонтанной гипертензией (SHR, возраст 14-20 недель) оставляли адаптироваться в течении минимум 48 часов после прибытия на место тестирования со свободным доступом к корму и воде. Для регистрации кровяного давления этим животным хирургически имплантировали небольшие радиопередатчики для грызунов (модуль телеметрии; DSI модели TA11PA-C40 или C50-PXT DSI, Data Science Inc., США). Наконечник катетера, связанного с передатчиком, вставляли в нисходящую аорту выше подвздошной бурификации и закрепляли на месте тканевым клеем. Передатчик удерживали внутрибрюшинно и прикрепляли к брюшной стенке, закрывая лапаротомию не рассасывающимися нитями. Эпидермис закрывали швом и скобами. Животных оставляли выздоравливать при соответствующем послеоперационном уходе. В день эксперимента животных в их клетках помещали на модули телеметрических приемников для акклиматизации к обстановке проведения исследований и записи исходных данных. Через по меньшей мере, 2 часа осуществляли измерения исходных данных, затем животным вводили дозы носителя или исследуемого соединения и проводили измерения кровяного давления через 24 часа после введения дозы. Данные записывали непрерывно в течение проведения исследования с использованием программного обеспечения Notocord (Kalamazoo, MI) и сохраняли в виде электронных цифровых сигналов. Измеряемые параметры представляли собой кровяное давление (систолическое, диастолическое и среднее артериальное давление) и частоту сердечных сокращений.
АНАЛИЗ 4
Оценка in vivo антигипертензивного действия на DOCA-солевой модели контролируемой гипертензии у крыс
Крысам CD (самцы, взрослые, 200-300 г, Charles River Laboratory, USA) давали адаптироваться в течение 48 часов по прибытии на место тестирования перед тем, как их переводили на высоко солевую диету. Через неделю после начала высоко солевой диеты, имплантировали подкожно шарик (8% в корме или 1% NaCl в питьевой воде) дезоксикортикостеронацетата (DOCA) (100 мг, время высвобождения 90 дней, Innovative Research of America, Sarasota, FL) и проводили одностороннюю нефректомию. На этом этапе для регистрации кровяного давления животным также хирургически имплантировали небольшие радиопередатчики для грызунов (см. анализ 3 более подробно). Животных оставляли выздоравливать при соответствующем послеоперационном уходе. План исследования, регистрация данных и измеряемые параметры аналогичны описанным в анализе 3.
АНАЛИЗ 5
Оценка in vivo антигипертензивного действия на модели контролируемой гипертензии у крыс линии Dahl/SS
Чувствительных к соли самцов крыс Dahl (Dahl/SS, возраст 6-7 недель, от Charles River Laboratory, USA) оставляли адаптироваться в течение, по меньшей мере, 48 часов по прибытии на место тестирования перед тем, как их переводили на высоко солевую диету с 8% NaCl (TD.92012, Harlan, USA), затем для измерения кровяного давления животным хирургически имплантировали небольшие радиопередатчики для грызунов (см. анализ 3 более подробно). Животных оставляли выздоравливать при соответствующем послеоперационном уходе. Приблизительно на 4-5 неделе с начала диеты с высоким содержанием соли, животные, как ожидалось, становились гипертензивными. Как только уровень гипертензии подтверждался, животных использовали для исследования при продолжении диеты с высоким содержанием соли для поддержания у них уровня гипертензии. План исследования, регистрация данных и измеряемые параметры аналогичны описанным в анализе 3.
В то время как настоящее изобретение описано по отношению к его конкретным аспектам или вариантам осуществления, специалистам в данной области будет понятно, что можно осуществлять различные изменения или можно заменять эквиваленты без отклонения от истинной сущности и объема изобретения. Кроме того, до степени, допустимой применяемыми патентными законодательными актами и нормативами, полное содержание всех публикаций, патентов и патентных заявок, процитированных в настоящем описании, таким образом, приведено посредством ссылки до такой же степени, как если бы каждый документ являлся отдельно приведенным посредством ссылки в настоящем описании.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ НЕПРИЛИЗИНА | 2013 |
|
RU2663618C2 |
| ЗАМЕЩЕННЫЕ АМИНОМАСЛЯНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ НЕПРИЛИЗИНА | 2012 |
|
RU2604522C2 |
| ИНГИБИТОРЫ НЕПРИЛИЗИНА | 2012 |
|
RU2629930C2 |
| НОВОЕ ФОСФОРАМИДАТНОЕ ПРОИЗВОДНОЕ НУКЛЕОЗИДА И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2621709C2 |
| ИНГИБИТОРЫ НЕПРИЛИЗИНА | 2011 |
|
RU2605557C2 |
| ИНГИБИТОРЫ НЕПРИЛИЗИНА | 2013 |
|
RU2650114C2 |
| КАРБАПЕНЕМОВЫЕ СОЕДИНЕНИЯ | 2017 |
|
RU2772909C2 |
| N-(2-ЦИАНОГЕТЕРОЦИКЛИЛ)ПИРАЗОЛОПИРИДОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ЯНУС-КИНАЗЫ | 2014 |
|
RU2669922C2 |
| АНТИГИПЕРТЕНЗИВНЫЕ СОЕДИНЕНИЯ ДВОЙНОГО ДЕЙСТВИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2008 |
|
RU2476427C2 |
| НОВЫЕ СОЕДИНЕНИЯ, КОТОРЫЕ ЯВЛЯЮТСЯ ИНГИБИТОРАМИ ERK | 2013 |
|
RU2660429C2 |
Изобретение относится к соединению формулы I, где R1 выбран из -OR7 и -NR8R9; R2 представляет собой Н; X представляет собой -C1-9гетероарил, выбранный из пиразола, имидазола, триазола, бензотриазола, фурана, тетразола, пиразина, тиофена, оксазола, изоксазола, тиазола, оксадиазола, пиридазина, пиридина, пиримидина, бензоксазола, пиридилимидазола и пиридилтриазола; R3 отсутствует или выбран из Н; галогена; -С0-5алкилен-ОН; -NH2; -C1-6алкила; -CF3; -С3-7циклоалкила; -С0-2алкилен-О-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -С(О)NR22R23; -NHC(O)R24; =O; -NO2; -С(СН3)=N(ОН); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -ОН, -CF3, -ОСН3, -NHC(O)СН3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, необязательно замещенного метилом; тиофенила, необязательно замещенного метилом или галогеном; фуранила; и -СН2-морфолинила; и R3, когда присутствует, присоединен к атому углерода; R4 отсутствует или выбран из Н; -ОН; -C1-6алкила; -C1-2алкилен-COOR35; -ОСН2ОС(О)СН(R36)NH2; -ОСН2ОС(О)СН3; -СН2СН(ОН)СН2ОН; и фенила или бензила, необязательно замещенных 1-3 группами, выбранными из галогена, -COOR35, -ОСН3, -OCF3 и -SCF3; и R4, когда присутствует, присоединен к атому углерода или азота; или R3 и R4 взяты вместе с образованием -фенилен-О-(СН2)1-3- или -фенилен-O-СН2-СНОН-СН2-; а равен 0 или 1; R5 представляет собой галоген; b равен 0 или целому числу от 1 до 3; каждый R6 независимо выбран из галогена, -ОН, -СН3 и -ОСН3; R7 выбран из Н, -C1-8алкила, -[(СН2)2O]1-3CH3, -C1-6алкилен-OC(O)R10, -С0-6алкиленморфолинила, -С1-6алкилен-SO2-C1-6алкила и структуры формулы (а); R10 представляет собой -O-С3-7циклоалкил; и R32 представляет собой -C1-6алкил; R8 и R9 представляют собой Н; R20, R21 и R35 независимо выбраны из Н и -C1-6алкила; R22 и R23 независимо выбраны из Н, -C1-6алкила, -СН2СООН, -(СН2)2ОН, -(СН2)2ОСН3, -(CH2)2SO2NH2, -(СН2)2N(СН3)2, -С0-1алкилен-С3-7циклоалкила и -(СН2)2-имидазолила; или R22 и R23 взяты вместе с образованием цикла; R24 выбран из -C1-6алкила; -С0-1алкилен-О-C1-6алкила; фенила, необязательно замещенного галогеном или -ОСН3; и пиридинила; и R36 представляет собой -СН(СН3)2; и где метиленовый линкер на бифениле необязательно замещен одной или двумя -C1-6алкильными группами; или его фармацевтически приемлемая соль. Соединения формулы (I) получают путем сочетания соединения формулы 1 с соединением формулы 2 с получением соединения формулы I; где Р1 представляет собой Н. Также изобретение относится к промежуточному соединению формулы 1, где Р1 представляет собой Н. Соединения формулы (I) предназначены для получения лекарственного средства или фармацевтической композиции, обладающих ингибирующей активностью в отношении неприлизина (NEP). Технический результат – соединения, обладающие ингибирующей фермент неприлизин (NEP) активностью. 7 н. и 21 з.п. ф-лы, 61 табл., 25 пр.
 ,
,  (а),
(а), 
1. Соединение формулы I:
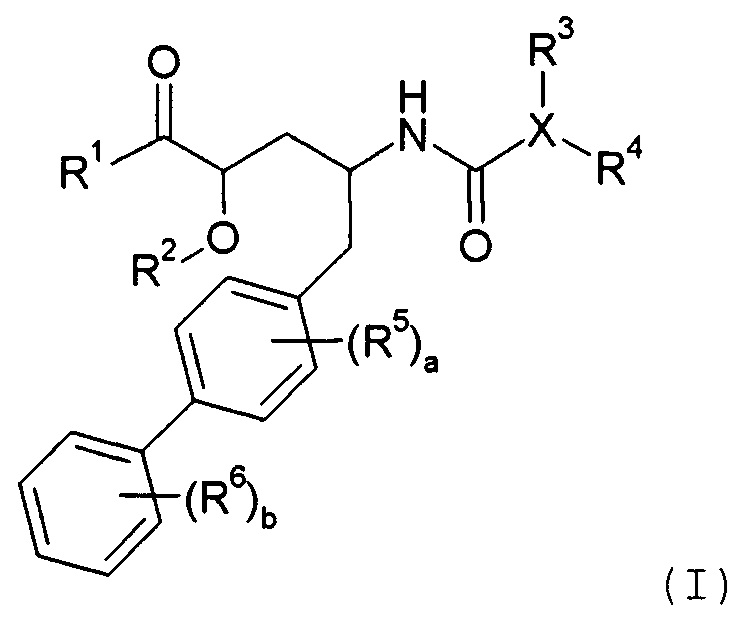
где:
R1 выбран из -OR7 и -NR8R9;
R2 представляет собой Н;
X представляет собой -C1-9гетероарил, выбранный из пиразола, имидазола, триазола, бензотриазола, фурана, тетразола, пиразина, тиофена, оксазола, изоксазола, тиазола, оксадиазола, пиридазина, пиридина, пиримидина, бензоксазола, пиридилимидазола и пиридилтриазола;
R3 отсутствует или выбран из Н; галогена; -С0-5алкилен-ОН; -NH2; -C1-6алкила; -CF3; -С3-7циклоалкила; -С0-2алкилен-О-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -С(О)NR22R23; -NHC(O)R24; =O; -NO2; -С(СН3)=N(ОН); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -ОН, -CF3, -ОСН3, -NHC(O)СН3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, необязательно замещенного метилом; тиофенила, необязательно замещенного метилом или галогеном; фуранила; и -СН2-морфолинила; и R3, когда присутствует, присоединен к атому углерода;
R4 отсутствует или выбран из Н; -ОН; -C1-6алкила; -C1-2алкилен-COOR35; -ОСН2ОС(О)СН(R36)NH2; -ОСН2ОС(О)СН3; -СН2СН(ОН)СН2ОН; и фенила или бензила, необязательно замещенных 1-3 группами, выбранными из галогена, -COOR35, -ОСН3, -OCF3 и -SCF3; и R4, когда присутствует, присоединен к атому углерода или азота;
или R3 и R4 взяты вместе с образованием -фенилен-О-(СН2)1-3- или -фенилен-O-СН2-СНОН-СН2-;
а равен 0 или 1; R5 представляет собой галоген;
b равен 0 или целому числу от 1 до 3; каждый R6 независимо выбран из галогена, -ОН, -СН3 и -ОСН3;
R7 выбран из Н, -C1-8алкила, -[(СН2)2O]1-3CH3, -C1-6алкилен-OC(O)R10, -С0-6алкиленморфолинила, -С1-6алкилен-SO2-C1-6алкила и
 ;
;
R10 представляет собой -O-С3-7циклоалкил; и R32 представляет собой -C1-6алкил;
R8 и R9 представляют собой Н;
R20 выбран из Н и -C1-6алкила;
R21 и R35 независимо выбраны из Н и -C1-6алкила;
R22 и R23 независимо выбраны из Н, -C1-6алкила, -СН2СООН, -(СН2)2ОН, -(СН2)2ОСН3, -(CH2)2SO2NH2, -(СН2)2N(СН3)2, -С0-1алкилен-С3-7циклоалкила и -(СН2)2-имидазолила; или R22 и R23 взяты вместе с образованием цикла, выбранного из азетидинила, пирролидинила, пиперидинила или морфолинила, каждый из которых необязательно замещен -ОН или -CONH2;
R24 выбран из -C1-6алкила; -С0-1алкилен-О-C1-6алкила; фенила, необязательно замещенного галогеном или -ОСН3; и пиридинила; и
R36 представляет собой -СН(СН3)2;
и
где метиленовый линкер на бифениле необязательно замещен одной или двумя -C1-6алкильными группами;
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, имеющее формулу III:

3. Соединение по любому из пп. 1 или 2, где R7 представляет собой Н, R8 представляет собой Н.
4. Соединение по любому из пп. 1 или 2, где:
R1 представляет собой -OR7; и R7 выбран из -С1-8алкила, -[(СН2)2О]1-3СН3, -C1-6алкилен-ОС(О)R10, -С0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила и
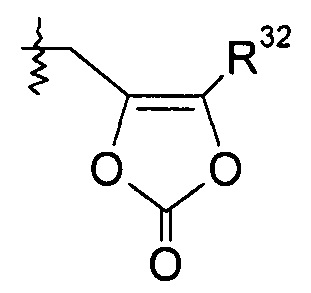 .
.
5. Соединение по любому из пп. 1 или 2, где R1 представляет собой -OR7, и R7 выбран из Н, -C1-8алкила, -C1-6алкилен-ОС(О)R10, -С0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила и
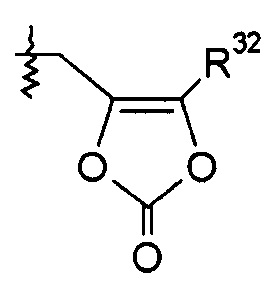 ;
;
R10 представляет собой -O-С3-7циклоалкил; и R32 представляет собой -СН3.
6. Соединение по любому из пп. 1 или 2, где R3 представляет собой -С0-1алкилен-COOR21 и R21 представляет собой Н.
7. Соединение по любому из пп. 1 или 2, где R3 представляет собой -С0-1алкилен-COOR21; и R21 представляет собой -C1-6алкил.
8. Соединение по любому из пп. 1 или 2, где R20 представляет собой -C1-6алкил и R22 выбран из Н и -C1-6алкила.
9. Соединение по любому из пп. 1 или 2, где R4 отсутствует или выбран из Н; -ОН; -C1-6алкила; -C1-2алкилен-COOR35; -ОСН2ОС(O)CH(R36)NH2; -СН2СН(ОН)СН2ОН; фенила или бензила, необязательно замещенных 1-3 группами, выбранными из галогена, -COOR35, -ОСН3, -OCF3 и -SCF3; и R35 представляет собой Н.
10. Соединение по любому из пп. 1 или 2, где R4 выбран из -ОСН2ОС(О)СН3; -C1-2алкилен-COOR35; фенила или бензила, замещенных, по меньшей мере, одной группой -COOR35; где R35 представляет собой -C1-6алкил.
11. Соединение по любому из пп. 1 или 2, где R4 отсутствует или выбран из Н; -ОН; -C1-6алкила; -С1-2алкилен-COOR35; -ОСН2ОС(O)CH(R36)NH2; -СН2СН(ОН)CH2OH; фенила, необязательно замещенного одной группой галогена; и бензила, необязательно замещенного 1-3 группами, выбранными из галогена, -СООН, -ОСН3, -OCF3 и -SCF3; R35 представляет собой Н; и R36 представляет собой -СН(СН3)2; или R3 и R4 взяты вместе с образованием -фенилен-О-(CH2)1-3- или -фенилен-O-СН2-СНОН-СН2-.
12. Соединение по любому из пп. 1 или 2, где а равен 0; или а равен 1, и R5 представляет собой 3-хлор.
13. Соединение по любому из пп. 1 или 2, где b равен 0; или b равен 1, и R6 представляет собой 3'-хлор, 3'-метил или 2'-метокси; или b равен 2, и R6 представляет собой 2'-фтор-5'-хлор, 2',5'-дихлор, 2'-метил-5'-хлор или 3'-хлор-5'-гидрокси.
14. Соединение по любому из пп. 1 или 2, где метиленовый линкер на бифениле замещен 2 метильными группами.
15. Соединение по п. 1, где
R1 представляет собой -OR7; R7 выбран из Н, -C1-8алкила, -C1-6алкилен-ОС(О)R10, -С0-6алкиленморфолинила, -C1-6алкилен-SO2-C1-6алкила и
 ;
;
R10 представляет собой -O-С3-7циклоалкил; R32 представляет собой -СН3;
R2 представляет собой Н;
X выбран из пиразола, триазола, бензотриазола, фурана, тетразола, пиразина, тиофена, оксазола, изоксазола, тиазола, оксадиазола, пиридазина, пиридина, пиримидина, бензоксазола, пиридилимидазола и пиридилтриазола;
R3 отсутствует или выбран из Н; галогена; -С0-5алкилен-ОН; -NH2; -C1-6алкила; -CF3; -С3-7циклоалкила; -С0-2алкилен-O-C1-6алкила; -C(O)R20; -C0-1алкилен-COOR21; -С(О)NR22R23; -NHC(O)R24; =O; С(СН3)=N(ОН); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -ОН, -CF3, -ОСН3, -NHC(O)СН3 и фенила; нафталенила; пиридинила; пиразинила; пиразолила, замещенного метилом; тиофенила, замещенного метилом или галогеном; фуранила и -СН2-морфолинила;
R4 отсутствует или выбран из Н; -ОН; -C1-6алкила; -C1-2алкилен-COOR35; -ОСН2ОС(О)СН(R36)NH2; -СН2СН(ОН)СН2ОН; фенила, необязательно замещенного одной группой галогена; и бензила, необязательно замещенного одной или более группами, выбранными из галогена, -СООН, -ОСН3, -OCF3 и -SCF3;
или R3 и R4 взяты вместе с образованием -фенилен-О-(СН2)1-3- или -фенилен-O-СН2-СНОН-СН2-;
а равен 0; или а равен 1, и R5 представляет собой 3-хлор;
b равен 0; или b равен 1, и R6 представляет собой 3'-хлор, 3'-метил или 2'-метокси; или b равен 2, и R6 представляет собой 2'-фтор-5'-хлор, 2',5'-дихлор, 2'-метил-5'-хлор или 3'-хлор-5'-гидрокси;
R20 представляет собой -C1-6алкил;
R21 выбран из Н и - C1-6алкила;
R22 выбран из Н и -C1-6алкила; и R23 выбран из Н, -C1-6алкила, -СН2СООН, -(СН2)2ОН, -(СН2)2ОСН3, -(СН2)2N(СН3)2, -С0-10алкилен-С3-7циклоалкила и -(СН2)2-имидазолила; или R22 и R23 взяты вместе с образованием азетидина, пирролидина, пиперидина или морфолина, все необязательно замещены -ОН или -CONH2;
R24 выбран из -C1-6алкила; -O-C1-6алкила; -СН2-O-С1-6алкила; фенила, замещенного галогеном или -ОСН3; и пиридинила;
R35 представляет собой Н;
R36 представляет собой -СН(СН3)2; и
метиленовый линкер на бифениле необязательно замещен 2 метильными группами.
16. Соединение по п. 1, где
R1 представляет собой -OR7;
R2 представляет собой Н;
X выбран из пиразола, триазола, бензотриазола, изоксазола, пиридазина, пиримидина и пиридилтриазола;
R3 выбран из Н; галогена; -С0-5алкилен-ОН; -C1-6алкила; -CF3; -С3-7циклоалкила; -С0-2алкилен-О-C1-6алкила; -C(O)R20; -С0-1алкилен-COOR21; -C(O)NR22R23; -NHC(O)R24; =O; -С(СН3)=N(ОН); фенила, необязательно замещенного одной или двумя группами, независимо выбранными из галогена, -ОН и -ОСН3; пиридинила; пиразинила; и тиофенила, замещенного метилом или галогеном;
R4 выбран из Н; -ОН; -C1-6алкила; -C1-2алкилен-COOR35; -СН2СН(ОН)СН2ОН; фенила, необязательно замещенного одной группой галогена; или R3 и R4 взяты вместе с образованием -фенилен-O-(СН2)1-3-;
а равен 0; или а равен 1, и R5 представляет собой 3-хлор;
b равен 0; или b равен 1, и R6 представляет собой 3'-хлор, 3'-метил или 2'-метокси; или b равен 2, и R6 представляет собой 2'-фтор-5'-хлор, 2',5'-дихлор, 2'-метил-5'-хлор или 3'-хлор-5'-гидрокси;
R20 представляет собой -C1-6алкил;
R21 представляет собой Н;
R22 выбран из Н и -C1-6алкила; и R23 выбран из -C1-6алкила, -(СН2)2OCH3 и -С0-1алкилен-С3-7циклоалкила; или R22 и R23 взяты вместе с образованием азетидина, пирролидина или пиперидина, все необязательно замещены -ОН или -CONH2;
R24 представляет собой фенил, замещенный галогеном или -ОСН3;
R35 представляет собой Н; и
метиленовый линкер на бифениле необязательно замещен 2 метильными группами.
17. Способ получения соединения по любому из пп. 1-16, включающий стадию сочетания соединения формулы 1 с соединением формулы 2:

с получением соединения формулы I; где Р1 представляет собой Н.
18. Промежуточное соединение, используемое в синтезе соединения по любому из пп. 1-16, имеющее формулу 1:
 ,
,
где Р1 представляет собой Н.
19. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении неприлизина (NEP), содержащая в качестве активного ингредиента терапевтически эффективное количество соединения по любому из пп. 1-16 и фармацевтически приемлемый носитель.
20. Фармацевтическая композиция по п. 19, дополнительно содержащая терапевтический агент, выбранный из ингибиторов ангиотензин-преобразующего фермента и ингибиторов двойного действия ангиотензин-преобразующего фермента/неприлизина, антагонистов АТ1 рецептора и ингибиторов двойного действия АТ1 рецептора антагониста/неприлизина, блокаторов кальциевых каналов, диуретиков, ингибиторов неприлизина, ингибиторов фосфодиэстеразы, ингибиторов ренина, стимуляторов и активаторов растворимой гуанилатциклазы и их сочетания.
21. Фармацевтическая композиция по п. 20, где терапевтический агент представляет собой антагонист AT1 рецептора.
22. Соединение по любому из пп. 1-16 для применения в качестве ингибитора неприлизина (NEP).
23. Соединение по п. 22 для применения при лечении гипертензии, сердечной недостаточности или болезни почек.
24. Применение соединения по любому из пп. 1-16 для получения лекарственного средства для лечения гипертензии, сердечной недостаточности или болезни почек.
25. Соединение формулы I
 ,
,
где R1 представляет собой -OR7; R7 представляет собой Н;
R2 представляет собой Н;
X представляет собой оксазол;
R3 представляет собой фенил;
R4 представляет собой Н;
а равен 0;
b равен 0;
или его фармацевтически приемлемая соль.
26. Соединение по п. 25, в котором X представляет собой
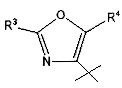 .
.
27. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении неприлизина (NEP), содержащая в качестве активного агента терапевтически эффективное количество соединения по п. 25 и фармацевтически приемлемый носитель.
28. Фармацевтическая композиция по п. 27, дополнительно содержащая антагонист АТ1 рецептора.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| KSANDER G | |||
| M | |||
| et al | |||
| "Dicarboxylic acid dipeptide neutral endopeptidase inhibitors", Journal of Medicinal Chemistry, 1995, vol.38, no.10, p.1689-1700 | |||
| RU 2005119167, 20.01.2006. | |||
Авторы
Даты
2017-06-14—Публикация
2011-12-14—Подача