УРОВЕНЬ ТЕХНИКИ
В данной заявке описаны способы фазоселективного гелеобразования с применением алкилированных ароматических кислот.
Проблема фазоселективного гелеобразования привлекла современное внимание из-за потенциальных сфер применений для улучшения состояния окружающей среды, как, например, локализация разливов нефти, фазоселективная изоляция токсичных органических жидкостей из сложных смесей и тому подобное. Проектирование фазоселективных гелеобразующих соединений часто представляет собой проблему из-за высокой способности воды участвовать в образовании водородных связей, которые могут препятствовать процессу гелеобразования.
Полимерные гели также использовались в качестве разделителей для нефти и воды. Полимерные гели, однако, могут требовать значительной загрузки гелеобразующего соединения и, как правило, не являются термообратимыми, и восстановление нефтяной фазы из гелеобразователя или наоборот, является сложным, если не невозможным. По причине возможности повторной переработки гелеобразующего соединения, низкомолекулярное соединение является предпочтительным.
Органогель представляет собой трехмерную сетку нековалентно взаимодействующих молекул с заполненным органической жидкостью внутренним пространством между узлами. Низкомолекулярные органогели представляют собой быстро развивающийся класс таких материалов, в которых структурные элементы из молекул малых размеров самостоятельно формируются в ансамбли, соединенные водородными связями, которые могут образовывать трехмерную сетку, способную придавать жесткость всей жидкости при очень низких концентрациях. Использование органогелевых материалов разнообразно и охватывает множество областей применений, таких как медицина, электроника, полиграфия, товары личной гигиены и восстановление окружающей среды.
Самосборка по методу "снизу вверх" молекулярных структурных элементов в наноструктурированные материалы привлекла значительный интерес к исследованию передовых материалов. Наноструктурированные материалы с контролируемым размером, формой и функцией важны для многочисленных промышленных областей применений. Низкомолекулярные органогели представляют собой быстро развивающийся класс таких материалов, в которых структурные элементы из молекул малых размеров самостоятельно формируются в ансамбли, соединенные водородными связями, которые могут образовывать трехмерную сетку, способную придавать жесткость всей жидкости при очень низких концентрациях.
Применение материалов на основе органогелей разнообразно и охватывает множество областей, таких как медицина, электроника, полиграфия, товары личной гигиены и восстановление окружающей среды. Несмотря на то, что большое количество органических гелеобразующих соединений было описано многими исследователями, рациональное проектирование и синтез новых органических гелеобразующих соединений остается важной проблемой, так как свойства геля в данной жидкости не могут быть спрогнозированы единственно на основании молекулярных структур. К тому же, не все самоорганизующиеся наноструктуры образуют гели при контакте с жидкостью.
В то время как известные композиции и способы являются подходящими для их областей применения, сохраняется необходимость в материалах и способах для разделения смесей нефть-вода. Кроме того, сохраняется необходимость в материалах и способах для локализации, разделения и восстановления желательной или нежелательной фазы из смеси двух несмешиваемых жидких фаз, таких как нефтяное пятно на поверхности воды. Также сохраняется необходимость в таких материалах и способах, в которых материалы, применяемые для разделения фаз, могут быть повторно использованы.
Дополнительно сохраняется необходимость в таких материалах и способах, в которых материалы имеют самокомплементарные функциональные группы, которые могут легко самостоятельно формироваться с помощью метода производства "снизу-вверх" для получения отчетливо выраженных наноструктур и сетчатых структур потенциально более высокого порядка; методы производства "снизу-вверх" вызывают растущие структуры желаемой формы и размеров из меньших структурных элементов, также называемые самосборкой. Также сохраняется необходимость в таких материалах и способах, где в некоторых вариантах осуществления способ разделения, т.е. гелеобразование, может быть инициировано внешним воздействием, таким как тепло, свет, ультразвук, химическое воздействие, механическое воздействие и тому подобное. Кроме того, сохраняется необходимость в таких материалах и способах, где в некоторых вариантах осуществления способ восстановления является обратимым, что облегчает восстановление нефти, воды и гелеобразующего вещества.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В данной заявке описывается способ, который включает смешивание алкилированной ароматической кислоты со смесью, содержащей первую жидкость и вторую жидкость, тем самым вызывая образование органогеля, содержащего алкилированную ароматическую кислоту и первую жидкость. Также в данной заявке описывается способ экстрагирования первой жидкости из второй жидкости, который включает: (а) получение смеси, содержащей первую жидкость и вторую жидкость, и (b) контактирование смеси с алкилированной ароматической кислотой при условиях, эффективных, чтобы вызвать образование органогеля, содержащего алкилированную ароматическую кислоту и первую жидкость, извлекая, таким образом, по меньшей мере, некоторое количество первой жидкости из второй жидкости. Дополнительно в данной заявке описывается способ обработки органического загрязнения, который включает внесение алкилированной ароматической кислоты в нефть указанного нефтяного загрязнения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗРОБРЕТЕНИЯ
Описанные в данной заявке соединения алкилированной ароматической кислоты образуют гели путем растворения в органической жидкости при нагревании и последующего охлаждения полученного в результате раствора, что приводит к образованию геля. Этот способ обусловлен иерархической самосборкой молекул алкилированной ароматической кислоты в пористую наноразмерную гелевую сетку, которая может захватывать молекулы растворителя и придавать жесткость всему объему жидкости.
Способ, описанный в данной заявке, включает смешивание алкилированной ароматической кислоты со смесью двух жидкостей, которые, в одном варианте осуществления являются несмешиваемыми, вызывая тем самым образование геля, и в одном варианте осуществления отделение, по меньшей мере, некоторого количества одной жидкости от другой. Смесь содержит, по меньшей мере, две жидкости и может содержать более двух, как, например, смеси двух или более взаимосмешиваемых материалов в одной или в обеих фазах двухфазной смеси, при этом смеси содержат три или более несмешиваемых фаз, и тому подобное.
Алкилированные ароматические кислоты включают кислоты с общими формулами
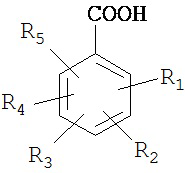 ,
,
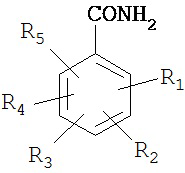 ,
,
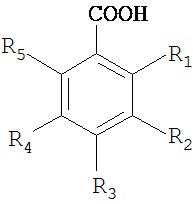
или их смеси, где R1, R2, R3, R4 и R5, каждый, независимо от остальных, представляет собой:
атомы водорода;
алкильные группы, включая линейные, разветвленные, насыщенные, ненасыщенные, циклические, замещенные и незамещенные алкильные группы, и в которых гетероатомы, такие как кислород, азот, сера, кремний, фосфор, бор, и тому подобное как могут, так и не могут присутствовать в алкильной группе, в одном варианте осуществления, по меньшей мере, с 1 атомом углерода, в другом варианте осуществления, по меньшей мере, с 6 атомами углерода, и еще в другом варианте осуществления, по меньшей мере, с 12 атомами углерода, и в одном варианте осуществления не более чем со 100 атомами углерода, в другом варианте осуществления не более чем с 50 атомами углерода, и еще в другом варианте осуществления не более чем с 36 атомами углерода;
арильные группы, включая замещенные и незамещенные арильные группы, в которых гетероатомы, такие как кислород, азот, сера, кремний, фосфор, бор, и тому подобное как могут, так и не могут присутствовать в арильной группе, в одном варианте осуществления, по меньшей мере, с 5 атомами углерода, в другом варианте осуществления, по меньшей мере, с 6 атомами углерода, и еще в другом варианте осуществления, по меньшей мере, с 12 атомами углерода, и в одном варианте осуществления не более чем со 100 атомами углерода, в другом варианте осуществления не более чем с 50 атомами углерода, и еще в другом варианте осуществления не более чем с 36 атомами углерода, такие как фенил и тому подобное;
арилалкильные группы, включая замещенные и незамещенные арилалкильные группы, в которых алкильная часть арилалкильной группы может быть линейной, разветвленной, насыщенной, ненасыщенной, и/или циклической, и в которых гетероатомы, такие как кислород, азот, сера, кремний, фосфор, бор, и тому подобное как могут, так и не могут присутствовать в одной из двух или обеих алкильной части и арильной части арилалкильной группы, в одном варианте осуществления, по меньшей мере, с 6 атомами углерода, в другом варианте осуществления, по меньшей мере, с 7 атомами углерода, и еще в другом варианте осуществления, по меньшей мере, с 12 атомами углерода, и в одном варианте осуществления не более чем со 100 атомами углерода, в другом варианте осуществления не более чем с 50 атомами углерода, и еще в другом варианте осуществления не более чем с 32 атомами углерода, такие как бензил и тому подобное; или
алкиларильные группы, включая замещенные и незамещенные алкиларильные группы, в которых алкильная часть алкиларильной группы может быть линейной, разветвленной, насыщенной, ненасыщенной, и/или циклической, и в которых гетероатомы, такие как кислород, азот, сера, кремний, фосфор, бор, и тому подобное как могут, так и не могут присутствовать в одной из двух или обеих алкильной части и арильной части алкиларильной группы, в одном варианте осуществления, по меньшей мере, с 6 атомами углерода, в другом варианте осуществления, по меньшей мере, с 7 атомами углерода, и еще в другом варианте осуществления, по меньшей мере, с 12 атомами углерода, и в одном варианте осуществления не более чем со 100 атомами углерода, в другом варианте осуществления не более чем с 50 атомами углерода, и еще в другом варианте осуществления не более чем с 32 атомами углерода, такие как бензил и тому подобное;
при условии, что, по меньшей мере, один из R1, R2, R3, R4, и R5 представляет собой -X-Rc, где:
(f) -Х- представляет собой связывающую группу между Rc и ароматической группой с примерами, включающими (но не ограничиваясь ими):
(i) -O-;
(ii) -S-;
(iii) -SO-;
(iv) -SO2-;
(v) -NH-(C=O)-;
(vi) -(C=O)-NH-;
(vii) -NH-(C=S)-;
(viii) -(C=S)-NH-;
(ix) -NH-;
(x) -NH-(C=O)-NH-;
(xi) -NH-(C=S)-NH-;
(xii) -NH-(C=O)-O-;
(xiii) -NH-(C=O)-S-;
(xiv) -O-(C=O)-NH-;
(xv) -S-(C=O)-NH-;
(xvi) -NH-(C=S)-O-;
(xvii) -NH-(C=S)-S-;
(xviii) -O-(C=S)-NH-;
(xix) -S-(C=S)-NH-;
(xx) -(C=O)-O-;
(xxi) -(C=O)-S-;
(xxii) -O-(C=O)-;
(xxiii) -S-(C=O)-;
(xxiv) -(C=S)-O-;
(xxv) -(C=S)-S-;
(xxvi) -O-(C=S)-;
(xxvii) -S-(C=S)-;
(xxviii) -O-(C=O)-O-;
(xxix) -O-(C=S)-O-;
и тому подобное, а также их комбинации; и
Rc представляет собой алкильную группу, включая линейные, разветвленные, насыщенные, ненасыщенные, циклические, замещенные, и незамещенные алкильные группы, и в которой гетероатомы, такие как кислород, азот, сера, кремний, фосфор, бор, и тому подобное как могут, так и не могут присутствовать в этой алкильной группе, в одном варианте осуществления, по меньшей мере, с 6 атомами углерода, в другом варианте осуществления, по меньшей мере, с 12 атомами углерода, и еще в другом варианте осуществления, по меньшей мере, с 18 атомами углерода, и в одном варианте осуществления не более чем со 100 атомами углерода, в другом варианте осуществления не более чем с 50 атомами углерода, и еще в другом варианте осуществления не более чем с 32 атомами углерода;
где замещающие группы в замещенных алкильных, арильных, арилалкильных и алкиларильных группах могут быть (но не ограничиваясь ими) гидроксильными группами, атомами галогенов, аминогруппами, иминогруппами, аммониевыми группами, циано группами, пиридин группами, пиридиния группами, группами простых эфиров, альдегидными группами, кетоновыми группами, группами сложных эфиров, амидными группами, карбонил группами, тиокарбонил группами, сульфатными группами, сульфонатными группами, группами сульфоновой кислоты, сульфидными группами, сульфоксид группами, фосфин группами, группами фосфония, фосфатными группами, нитрильными группами, меркапто группами, нитро группами, нитрозо группами, сульфоновыми группами, ацил группами, группами ангидрида кислоты, азид группами, азо группами, цианатными группами, изоцианатными группами, тиоцианатными группами, изотиоцианатными группами, карбоксилатными группами, группами карбоновой кислоты, уретановыми группами, группами мочевины, силиловыми группами, силоксил группами, силан группами, их смесями, и тому подобное, в которых два или более заместителя могут быть соединены друг с другом с образованием кольца.
В одном конкретном варианте осуществления только один из R1, R2, R3, R4, и R5 представляет собой -X-Rc. В другом конкретном варианте осуществления два из R1, R2, R3, R4, и R5 каждый, независимо от остальных, представляет собой -X-Rc группу. В другом конкретном варианте осуществления один из R1, R2, R3, R4, и R5 представляет собой -X-Rc и один из R1, R2, R3, R4, и R5 представляет собой -СООН или -CONH2.
В одном конкретном варианте осуществления соединение имеет формулы
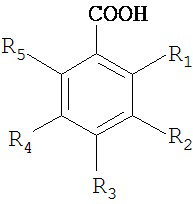 ,
,
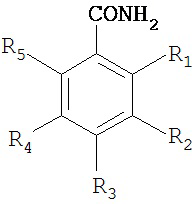 ,
,
или их смеси, где R1, R3, и R5 каждый представляет собой атомы водорода. В другом конкретном варианте осуществления R1, R3, и R5 каждый представляет собой атомы водорода, R2 представляет собой -X1-Rc1 и R4 представляет собой -СООН, -CONH2 или -X2-Rc2, где X1 и Х2 могут быть или одинаковыми, или отличаться друг от друга, и Rc1 и Rc2 могут быть или одинаковыми, или отличаться друг от друга. В другом конкретном варианте осуществления соединение имеет формулу
 ,
,
R1, R3, и R5 каждый представляет собой атомы водорода, R2 представляет собой -X1-Rc1 и R4 представляет собой -СООН или -X2-Rc2, где X1 и Х2 могут быть или одинаковыми, или отличаться друг от друга, и Rc1 и Rc2 могут быть или одинаковыми, или отличаться друг от друга.
Приведенные выше формулы включают структуры формулы
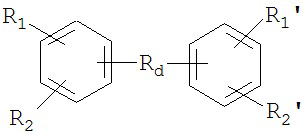
в которой R1’ имеет такое же определение, как R1, и может быть или таким же, или отличаться от R1, R2’ имеет такое же определение, как R2, и может быть или таким же, или отличаться от R2, и Rd представляет собой бифункциональную группу, которая соединяет мостиком две или более группы ароматической кислоты, с примерами подходящих rd групп, включая (но не ограничиваясь ими):
(а) -(СН2)n-;
(b) -X-(CH2)n-X’-;
(с) -[(ХСН2СН2)n]Х’-;
(d) -[(C=O)-(CH2)n-(C=O)]-;
(e) -Х-[(C=О)-(CH2)n-(С=O)]-Х’-;
(f) -X-[(C=O)-X’-(CH2)n-X"-(C=O)]-X’’’-;
(g) -[(C=O)-X-(CH2)n-X’-(C=O)]-;
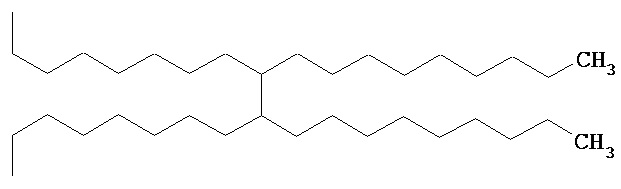
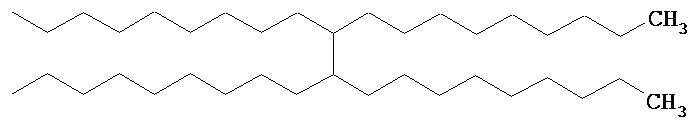
и тому подобное, где X, X’, X" и X’’’ каждый, независимо от остальных, определен как О, S или NH, и n представляет собой целое число, в одном варианте осуществления, по меньшей мере, 1, и в одном варианте осуществления не более чем 50. Конкретные примеры Rd также включают большие разветвленные алкилированные функциональные группы, такие как
 ,
,
 ,
,
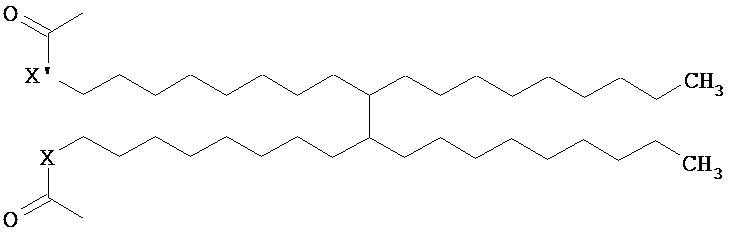 ,
,
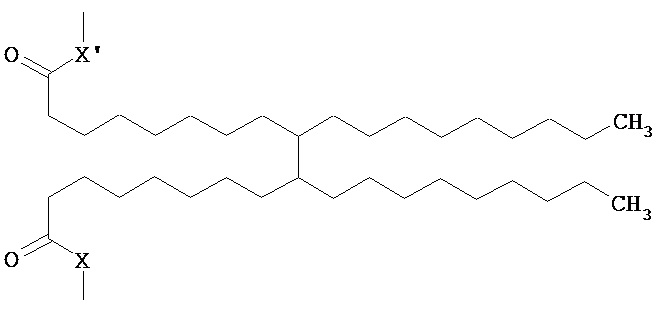 ,
,
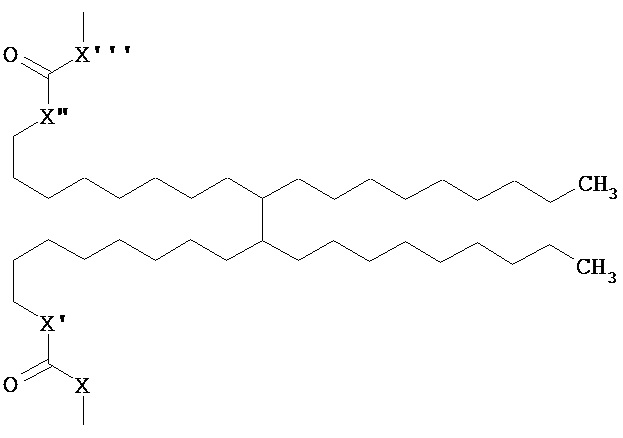 ,
,
и тому подобное, а также их смеси, где X, X’, X" и X’’’ каждый, независимо от остальных, определен как О, S или NH.
Конкретные примеры Rc групп включают (но не ограничиваются ими):
(а) линейные незамещенные алкильные группы формулы -(СН2)nCH3, в которой n представляет собой в одном варианте осуществления, по меньшей мере, 5, в другом варианте осуществления, по меньшей мере, 10, и еще в другом варианте осуществления, по меньшей мере, 15, и в одном варианте осуществления не более чем 50, в другом варианте осуществления не более чем 40, и еще в другом варианте осуществления не более чем 25, включая конкретные значения, такие как:
(i) 17;
(ii) 15;
(iii) 11;
и тому подобное; и
(b) разветвленные незамещенные алкильные группы формулы
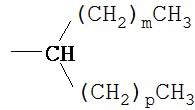
где m представляет собой в одном варианте осуществления 0, в другом варианте осуществления, по меньшей мере, 1, и еще в другом варианте осуществления, по меньшей мере, 3, и в одном варианте осуществления не более чем 17, в другом варианте осуществления не более чем 11, и еще в другом варианте осуществления не более чем 5, и где р представляет собой в одном варианте осуществления 0, в другом варианте осуществления, по меньшей мере, 1, и еще в другом варианте осуществления, по меньшей мере, 3, и в одном варианте осуществления не более чем 17, в другом варианте осуществления не более чем 11, и еще в другом варианте осуществления не более чем 5, включая конкретные значения, такие как:
(i) m=11, p=9;
(ii) m=5, p=3;
(iii) m=7, p=5;
(c) разветвленные незамещенные алкильные группы формулы
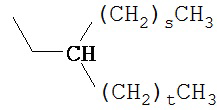
где s представляет собой целое число, в одном варианте осуществления 0, в другом варианте осуществления, по меньшей мере, 1, и еще в другом варианте осуществления, по меньшей мере, 3, и в одном варианте осуществления не более чем 49, в другом варианте осуществления не более чем 11, и еще в другом варианте осуществления не более чем 5, и где t представляет собой целое число, в одном варианте осуществления 0, в другом варианте осуществления, по меньшей мере, 1, и еще в другом варианте осуществления, по меньшей мере, 3, и в одном варианте осуществления не более чем 59, в другом варианте осуществления не более чем 11, и еще в другом варианте осуществления не более чем 5;
(d) разветвленные незамещенные алкильные группы формулы
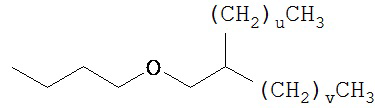
где и представляет собой целое число, в одном варианте осуществления 0, в другом варианте осуществления, по меньшей мере, 1, и еще в другом варианте осуществления, по меньшей мере, 3, и в одном варианте осуществления не более чем 49, в другом варианте осуществления не более чем 11, и еще в другом варианте осуществления не более чем 5, и где v представляет собой целое число, в одном варианте осуществления 0, в другом варианте осуществления, по меньшей мере, 1, и еще в другом варианте осуществления, по меньшей мере, 3, и в одном варианте осуществления не более чем 59, в другом варианте осуществления не более чем 11, и еще в другом варианте осуществления не более чем 5;
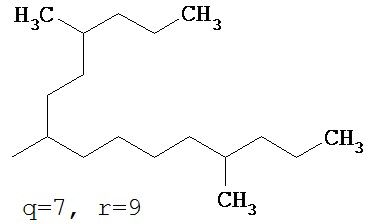
(е) мультиразветвленные незамещенные алкильные группы формулы
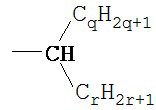
где q представляет собой целое число, в одном варианте осуществления, по меньшей мере, 1, в другом варианте осуществления, по меньшей мере, 4, и еще в другом варианте осуществления, по меньшей мере, 6, и в одном варианте осуществления не более чем 18, в другом варианте осуществления не более чем 12, и еще в другом варианте осуществления не более чем 10, и где r представляет собой целое число, в одном варианте осуществления, по меньшей мере, 1, в другом варианте осуществления, по меньшей мере, 4, и еще в другом варианте осуществления, по меньшей мере, 6, и в одном варианте осуществления не более чем 18, в другом варианте осуществления не более чем 12, и еще в другом варианте осуществления не более чем 10, включая конкретные значения, такие как:
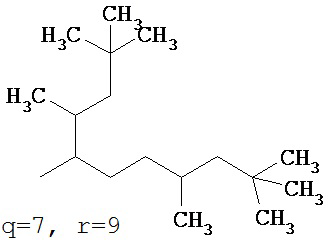 ;
;
 ;
;
и тому подобное, а также их смеси.
Некоторые конкретные примеры подходящих соединений включают соединения формулы

в которой R1, R2 и R3 каждый представляет собой атомы водорода и:
(a) R2 представляет собой -СООН, и R4 представляет собой
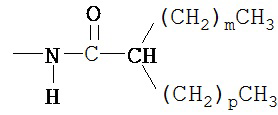
в которой m представляет собой 11, и р представляет собой 9;
(b) R2 представляет собой -СООН, и R4 представляет собой
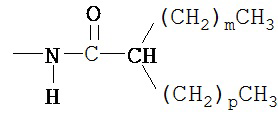
в которой m представляет собой 5, и р представляет собой 3;
(c) R2 представляет собой -СООН, и R4 представляет собой
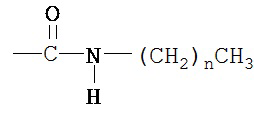
в которой n представляет собой 17;
(d) R2 представляет собой -СООН, и R4 представляет собой

в которой m представляет собой 7, и р представляет собой 5;
(e) R2 представляет собой -СООН, и R4 представляет собой
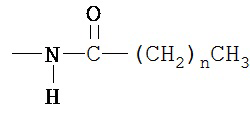
в которой n представляет собой 15;
(f) R2 представляет собой -СООН, и R4 представляет собой
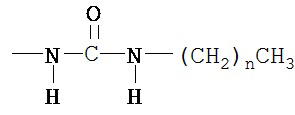
в которой n представляет собой 11;
(g) R2 представляет собой -СООН, и R4 представляет собой
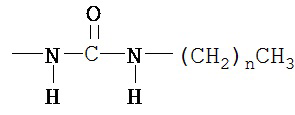
в которой n представляет собой 17;
(h) R2 представляет собой

в которой m представляет собой 11, и р представляет собой 9, и R4 представляет собой

в которой m представляет собой 11, и р представляет собой 9;
(i) R2 представляет собой
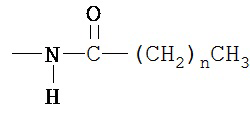
в которой n представляет собой 17, и R4 представляет собой
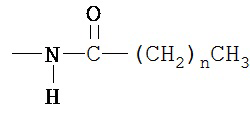
в которой n представляет собой 17; и тому подобное.
Алкилированные соединения ароматической кислоты могут быть получены, как описано, например, в патенте США U.S. 7,905,954 и одновременно находящейся на рассмотрении заявке США №.12/820,497.
Алкилированная ароматическая кислота или ее смесь смешивается или контактирует со смесью, содержащей первую жидкость и вторую жидкость, тем самым вызывая образование органогеля, содержащего алкилированную ароматическую кислоту и эту первую жидкость. В некоторых вариантах первая и вторая жидкости являются не смешиваемыми.
Любая желаемая или эффективная органическая жидкость может быть использована в качестве первой жидкости, включая (но не ограничиваясь ими) углеводороды, включая алифатические и ароматические углеводороды, спирты, амины, сложные эфиры, простые эфиры, меркаптаны, кислоты (включая карбоновые кислоты, сульфоновые кислоты и тому подобное, а также их смеси), сульфоны, ангидриды, галоидангидриды, силоксаны, полимерные жидкости, ионные жидкости, и тому подобное, а также их смеси.
Конкретные примеры подходящих органических жидкостей включают (но не ограничиваются ими):
линейные, разветвленные, и/или циклические незамещенные алифатические углеводороды, такие как бутаны, пентаны, такие как n-пентан, изопентан, неопентан, циклопентан, и тому подобное, гексаны, такие как n-гексан, изогексан, неогексан, циклогексан, и тому подобное, гептаны, такие как n-гептан, изогептан, неогептан, циклогептан, и тому подобное, октаны, такие как n-октан, изооктан, неооктан, циклооктан, и тому подобное, нонаны, деканы, такие как n-декан, изодекан, неодекан, декадегидронафталин, и тому подобное, ундеканы, додеканы, такие как n-додекан, изододекан, неододекан, и тому подобное, а также их смеси; линейные, разветвленные, и/или циклические замещенные алифатические углеводороды, такие как хлорметан, бромметан, иодметан, дихлорметан, дибромметан, бромхлорметан, дихлорфторметан, трихлорфторметан, хлордифторметан, хлороформ, бромоформ, тетрахлорид углерода, дихлорэтаны, дибромэтаны, трихлорэтаны, йодистый этил, йодистые пропилы, йодистые бутилы, тетрахлорэтаны, тетрахлорэтине более, чемлен, и тому подобное, а также их смеси;
незамещенные ароматические и гетероароматические углеводороды, такие как бензол, толуол, ксилол, мезитилен, стирол, пиридин, пиррол, фуран, пиразин, и тому подобное, а также их смеси;
замещенные ароматические и гетероароматические углеводороды, такие как фторбензол, хлорбензол, бромбензол, иодбензол, нитробензол, и тому подобное, а также их смеси;
линейные, разветвленные, и/или циклические незамещенные алифатические спирты, такие как метанол, этанол, пропанолы, бутанолы, пентанолы, гексанолы, гептанолы, октанолы, нонанолы, деканолы, ундеканолы, додеканолы, и тому подобное, а также их смеси;
алифатические и ароматические амины, такие как метиламин, этиламин, пропиламин, бутиламин, пентиламин, гексиламин, октиламин, дециламин, додециламин, триэтиламин, диизопропилэтиламин, анилин, метилантранилат, и тому подобное, а также их смеси;
жирные кислоты, такие как каприловая кислота, лауриловая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, ненасыщенные жирные кислоты, такие как олеиновая кислота и линолевая кислота, масла жирных кислот, такие как соевое масло, масло канолы, оливковое масло, тунговое масло, подсолнечное масло, сафлоровое масло, конопляное масло, хлопковое масло, пальмовое масло, кукурузное масло, и тому подобное, а также их смеси;
алифатические и ароматические сложные эфиры, такие как метилацетат, этилацетат, бутилацетат, амилацетат, метиловый эфир капроновой кислоты, метиловый эфир каприловой кислоты, метилмиристат, метилолеат, метиллинолеат, метилбензоат, этилбензоат, бензилбензоат, и тому подобное, а также их смеси;
алифатические и ароматические простые эфиры, такие как простой диэтиловый эфир, дипропиловые эфиры, дибутиловые эфиры, дипентиловые эфиры, анизол, дифениловый эфир, и тому подобное, а также их смеси;
с примерами подходящих заместителей, включая (но не ограничиваясь ими) гидроксильные группы, атомы галогенов, аминогруппы, иминогруппы, аммониевые группы, циано группы, пиридиновые группы, группы пиридиния, группы простых эфиров, альдегидные группы, кетонные группы, группы сложных эфиров, амидные группы, карбонильные группы, тиокарбонильные группы, сульфатные группы, сульфонатные группы, группы сульфоновой кислоты, сульфидные группы, сульфоксидные группы, фосфиновые группы, группы фосфония, фосфатные группы, нитрильные группы, меркапто группы, нитро группы, нитрозо группы, сульфон группы, ацил группы, группы ангидридов кислот, азид группы, азо группы, цианато группы, изоцианатные группы, тиоцианатные группы, изотиоцианатные группы, карбоксилатные группы, группы карбоновой кислоты, уретановые группы, группы мочевины, силиловые группы, силоксиловые группы, силановые группы, их смеси, и тому подобное, в которых два или более заместителя могут быть объединены в кольцо;
и тому подобное, а также их смеси.
В некоторых вариантах осуществления вторая жидкость является несмешиваемой с первой жидкостью. Примеры включают воду и тому подобное.
Соединение алкилированный бензимидазолон смешивается с первой жидкостью в любом желаемом или эффективном количестве для образования органогеля, в одном варианте осуществления, по меньшей мере, 0.05% по массе, в другом варианте осуществления, по меньшей мере, 0.1% по массе, и еще в другом варианте осуществления, по меньшей мере, 1% по массе, и в одном варианте осуществления не более чем 20% по массе, в другом варианте осуществления не более чем 10% по массе, и еще в другом варианте осуществления не более чем 5% по массе.
Первая жидкость и вторая жидкость могут присутствовать в любых желаемых или эффективных относительных количествах, в одном варианте осуществления, по меньшей мере, 0.1 массовая часть первой жидкости на каждую 1 массовую часть второй жидкости, в другом варианте осуществления, по меньшей мере, 0.2 массовые части первой жидкости на каждую 1 массовую часть второй жидкости, и еще в другом варианте осуществления, по меньшей мере, 0.5 массовых частей первой жидкости на каждую 1 массовую часть второй жидкости, и в одном варианте осуществления не более 1 массовой части первой жидкости на каждую 1 массовую часть второй жидкости.
Загрязненные жидкости могут быть удалены из полученного геля для повторной переработки с помощью любого желаемого или эффективного способа, такого как дистилляция и тому подобное.
Способы фазоселективного гелеобразования, описанные в данной заявке, имеют ряд областей применений, включая способы восстановления окружающей среды, такие как локализация и/или очистка химических разливов, рекультивация нефтяных разливов, и тому подобное.
Соединения в Примерах I и II применялись в гелеобразных органических жидкостях с помощью метода переворачивания пробирки, как описано, например, в Fages, F. Low Molecular Mass Gelators, Vol.256, 2005 in Topics in Current Chemistry. Гели получали путем помещения определенного количества гелеобразующего порошка в пробирку с подходящим органическим растворителем. Смеси затем нагревали до определенной температуры в течение некоторого периода времени до получения однородной смеси или прозрачного раствора с последующим охлаждением и выдерживанием при комнатной температуре в течение, по меньшей мере, 30 мин. Гели затем качественно оценивали, используя "тест инверсии", который включает переворачивание образца геля и наблюдение за характером изменения текучести. Если материал не вытекал или не выпадал под собственным весом под действием силы тяжести, материал классифицировался как гель.
ПРИМЕР I
Синтез 5-(2’-децилтетрадеканамидо)изофталевой кислоты
Этап 1: Синтез 2-децилтетрадеканоил хлорида
2-Децилтетрадекановую кислоту (ISOCARB 24, полученную от Sasol America, TX, 7.65 г, 20.8 ммоль) и каталитическое количество N,N’-диметилформамида (0.28 мл, 3.62 ммоль) растворяли в сухом тетрагидрофуране (100 мл) в инертной атмосфере. Смесь охлаждали до 0°С и медленно добавляли по каплям оксалил хлорид (7.3 мл, 83.7 ммоль, полученный от Sigma-Aldrich, Milwaukee, WI) и давали возможность перемешиваться в течение, по меньшей мере, 10 мин, пока не прекращалось выделение газообразного хлористого водорода. Смеси давали возможность медленно нагреваться до комнатной температуры более 3 ч перед тем, как удаляли растворитель путем роторного выпаривания, с получением соединения хлорангидрида в виде вязкого, бледно-желтого сиропа, который применяли на следующем этапе без дополнительной очистки.
Этап 2: Синтез 5-(2’-децилтетрадеканамидо)изофталевой кислоты
Суспензию 2-децилтетрадеканоил хлорида из Этапа 1 в сухом тетрагидрофуране (80 мл) медленно добавляли по каплям к суспензии диметил 5-аминоизофталата (Aldrich, 4.40 г, 21.0 ммоль), триэтиламина (4.4 мл, 31.5 ммоль) и сухого тетрагидрофурана (100 мл) в инертной атмосфере при 0°С. Реакции давали возможность медленно нагреваться до комнатной температуры и перемешивали в течение ночи. Добавляли деионизированную воду (10 мл) и удаляли тетрагидрофуран путем роторного выпаривания. Сырой остаток затем растворяли в 250 мл этилацетата и последовательно промывали 3 порциями по 100 мл деионизированной воды. Затем из органической фазы удаляли этилацетат путем роторного выпаривания и продукт высушивали in vacuo с получением сырого диметил 5-(2’-децилтетрадеканамидо)изофталата (12.56 г) в виде бледно-желтого твердого вещества.
Этап 3: Омыление Диметил 5-(2’-децилтетрадеканамидо)изофталата
Диметил 5-(2’-децилтетрадеканамидо)изофталат (12.56 г) из Этапа 2, гидроксид калия (4.67 г, 0.0832 моль) и метанол (100 мл) добавляли в 500 мл колбу и смесь нагревали и выдерживали с обратным холодильником в течение ночи. Реакцию затем охлаждали до комнатной температуры с получением мутной красно-оранжевой смеси. Смесь далее окисляли соляной кислотой (7 мл) с получением белого осадка, который собирали путем фильтрования с отсасыванием, промывали деионизированной водой и затем высушивали in vacuo с получением грязно-белого порошка (11.7 г). Продукт идентифицировали с помощью 1Н и 13С ЯМР спектроскопии и ESI-MS, и он был удовлетворительной чистоты. Продукт, как полагали, имел формулу
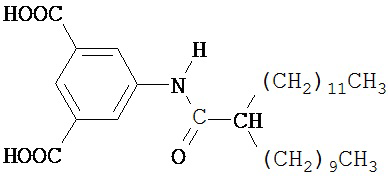 .
.
Гелеобразование керосина
5-(2’-Децилтетрадеканамидо)изофталевую кислоту применяли для желатинирования жидкого керосина. Соединение, которое получено на вышеприведенных этапах (10.1 мг), и керосин (1 мл) помещали в герметично закрытый сосуд и перемешивали и нагревали до тех пор, пока не получали прозрачный, гомогенный раствор. После медленного охлаждения и оставления сосуда при комнатной температуре в течение, по меньшей мере, 30 мин, образовывался прозрачный гель, который не выпадал и не вытекал при переворачивании сосуда.
Фазоселективное гелеобразование керосина из смесей керосин-вода
Соединение 5-(2’-децилтетрадеканамидо)изофталевая кислота, полученное на вышеприведенных этапах (10.9 мг), керосин (1 мл) и деионизированную воду (1 мл) герметично закрывали в 4 мл пробирке с завинчивающейся пробкой. Затем смесь нагревали тепловой пушкой с легким встряхиванием до получения двух прозрачных фаз раствора. После того, как смеси давали возможность охлаждаться и оставаться при комнатной температуре в течение, по меньшей мере, 30 мин, верхняя керосиновая фаза, по наблюдению, образовывала непрозрачную твердую фазу, которая при переворачивании пробирки была достаточно твердой, чтобы локализовать и поддерживать вес нижней прозрачной водной фазы.
Фазоселективное гелеобразование керосина из смесей керосин-вода с применением ультразвуковой ванны
Соединение 5-(2’-децилтетрадеканамидо)изофталевая кислота, полученное на вышеприведенных этапах (10.4 мг), добавляли поверх смеси керосина (1 мл) и деионизированной воды (1 мл) и герметично закрывали в 4 мл пробирке с завинчивающейся пробкой. Затем смесь помещали в ультразвуковую ванну (100 Вт, 42 кГц, Bransonic Ultrasonic Cleaner, Branson Ultrasonics Corporation) в течение 5 мин. В дальнейшем, в результате выстаивания наблюдали, что верхняя керосиновая фаза образовывала непрозрачную твердую фазу, которая при переворачивании пробирки была достаточно твердой, чтобы локализовать и поддерживать вес нижней прозрачной водной фазы.
Фазоселективное гелеобразование керосина из смесей керосин-вода с вихревым смешиванием
Соединение 5-(2’-децилтетрадеканамидо)изофталевая кислота, полученное на вышеприведенных этапах, (9.6 мг) добавляли поверх смеси керосина (1 мл) и деионизированной воды (1 мл) и герметично закрывали в 4 мл пробирке с завинчивающейся пробкой. Затем смесь помещали в вихревую мешалку Fisher Scientific на 5 мин. После выстаивания в течение нескольких дней наблюдали, что верхняя керосиновая фаза образовала непрозрачную твердую фазу, которая при переворачивании пробирки была достаточно твердой, чтобы локализовать и поддерживать вес нижней прозрачной водной фазы.
ПРИМЕР II
Синтез 5-(2’-бутилоктанамидо)изофталевой кислоты
Этап 1: Синтез 2-бутилоктаноил хлорида
2-Гексилдекановую кислоту (ISOCARB 12, полученную от Sasol America, TX, 11.43 г, 57.1 ммоль) и сухой тетрагидрофуран (200 мл) добавляли в 500 мл одногорлую круглодонную колбу в инертной атмосфере. Затем добавляли каталитическое количество N,N’-диметилформамида (0.3 мл, 3.87 ммоль) с последующим медленным добавлением по каплям оксалил хлорида (7.0 мл, 80.2 ммоль). Смесь перемешивали в течение 10 мин, пока не прекращалось выделение газообразного хлористого водорода, затем медленно нагревали до комнатной температуры в течение 2 ч. Роторным выпариванием THF получали хлорангидрид 2-бутилоктаноил хлорида в виде коричневого масла, которое высушивали in vacua перед применением на Этапе 2.
Этап 2: Синтез диметил 5-(2’-бутилоктанамидо)изофталевой кислоты
Раствор 2-бутилоктаноил хлорида из Этапа 1 в сухом тетрагидрофуране (50 мл) медленно добавляли по каплям к другому раствору диметил 5-аминоизофталата (Aldrich Chemical Co., 11.08 г, 53.0 ммоль) и триэтиламина (11.0 мл, 78.9 ммоль) в тетрагидрофуране (250 мл) в инертной атмосфере при 0°С. Затем смеси давали возможность медленно нагреваться до комнатной температуры и перемешивали в течение ночи. Добавляли деионизированную воду (10 мл) и удаляли тетрагидрофуран путем роторного выпаривания. Сырой остаток затем растворяли в 200 мл диэтилового эфира и последовательно промывали насыщенным бикарбонатом натрия (60 мл), деионизированной водой (60 мл) и рассолом (60 мл). Органическую фазу затем высушивали над сульфатом натрия и фильтровали перед удалением диэтилового эфира путем роторного выпаривания. Сырую диметил 5-(2-бутилоктанамидо)изофталевую кислоту (21.71 г) получали в виде янтарного масла после высушивания in vacuo.
Этап 3: Омыление диметил 5-(2’-бутилоктанамидо)изофталата
Диметил 5-(2’-бутилоктанамидо)изофталат из Этапа 2, гидроксид калия (85%, 29.61 г, 0.0527 моль) и метанол (200 мл) нагревали и выдерживали с обратным холодильником в течение ночи. Реакцию затем охлаждали до комнатной температуры с получением мутной красно-оранжевой смеси. Смесь за тем окисляли соляной кислотой с получением белого осадка, который собирали путем фильтрования с отсасыванием, промывали деионизированной водой и затем высушивали in vacuo с получением белого порошка (18.94 г). Продукт идентифицировали с помощью 1H и 13С ЯМР спектроскопии и ESI-MS, и он был удовлетворительной чистоты. Продукт, как полагали, имел формулу
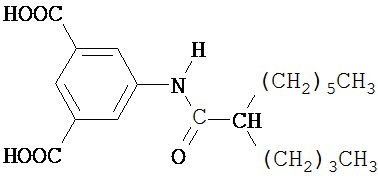 .
.
Гелеобразование ксилола с применением 5-(2’-бутилоктанамидо)изофталевой кислоты
0.56 М этанольный раствор 5-(2’-бутилоктанамидо)изофталевой кислоты из предыдущих этапов (50 μл, 28.0 μмоль, 10.1 мг) добавляли в ксилол (1 мл) и осторожно встряхивали в течение нескольких секунд. В результате выстаивания смесь затвердевала в мутный гель, который не выпадал или не вытекал при переворачивании сосуда.
Фазоселективное гелеобразование ксилола из смесей ксилол: вода с применением 5-(2’-бутилоктанамидо)изофталевой кислоты
0.56 М этанольный раствор 5-(2’-бутилоктанамидо)изофталевой кислоты из предыдущих этапов (50 μл, 28.0 μмоль, 10.1 мг) добавляли к смеси ксилола (1 мл) и воды (1 мл) и встряхивали в течение нескольких секунд. В результате выстаивания верхний ксилольный слой избирательно затвердевал в непрозрачный гель, который локализовывал и поддерживал вес прозрачного нижнего водного слоя при переворачивании сосуда.
ПРИМЕР III
Синтез 3,5-бис(2’-децилтетрадеканамидо)бензойной кислоты
Этап 1: Синтез 2-децилтетрадеканоил хлорида
2-Децилтетрадекановую кислоту (ISOCARB 24, полученную от Sasol America, 1.15 г, 3.13 ммоль) и сухой тетрагидрофуран (20 мл) смешивали в 100 мл сосуде с перемешиванием в инертной атмосфере. Смесь охлаждали до 0°С в течение, по меньшей мере, 30 мин, после чего добавляли каталитическое количество N,N’-диметилформамида (4 капли) с последующим медленным добавлением по каплям оксалил хлорида (1 мл, 12.6 ммоль). Реакции затем давали возможность медленно нагреваться до комнатной температуры и давали возможность перемешиваться в течение 30 мин перед удалением растворителя путем роторного выпаривания. Соединение хлорангидрид, полученный таким образом, применяли на следующем этапе без дополнительной очистки.
Этап 2: Синтез метил 3,5-бис(2’-децилтетрадеканамидо)бензоата
3,5-Диаминобензойную кислоту (Sigma-Aldrich) этерифицировали, применяя общеизвестные способы (Electrochimica Acta 2001, 46, 3955-3962), тионил хлоридом и безводным метанолом с получением соответствующего метилового сложного эфира, метил 3,5-диаминобензоата. Метил 3,5-диаминобензоат (260.8 мг, 1.9 ммоль) растворяли в сухом тетрагидрофуране (5 мл) в 100 мл сосуде в инертной атмосфере. Затем добавляли триэтиламин (0.7 мл, 4.99 ммоль) и раствор охлаждали до 0°С. Затем медленно добавляли по каплям раствор 2-децилтетрадеканоил хлорида из Этапа 1 в сухом тетрагидрофуране (10 мл). Реакции затем давали возможность медленно нагреваться до комнатной температуры. После перемешивания в течение ночи, реакцию останавливали водой и удаляли тетрагидрофуран путем роторного выпаривания. Остаток сырого продукта затем растворяли в диэтиловом эфире (50 мл) и промывали деионизированной водой (20 мл). Слой эфира отделяли и концентрировали с получением метил 3,5-бис(2’-децилтетрадеканамидо)бензоата в виде бледно-розового твердого вещества (1.17 г).
Этап 3: Омыление метил 3,5-бис(2’-децилтетрадеканамидо)бензоата
Метил 3,5-бис(2’-децилтетрадеканамидо)бензоат из Этапа 2, гидроксид калия (0.38 г, 5.77 ммоль) и метанол (20 мл) добавляли в 50 мл сосуд и нагревали с обратным холодильником. Затем добавляли деионизированную воду (10 мл), и реакцию выдерживали с обратным холодильником в течение ночи. Реакцию затем охлаждали до комнатной температуры, что приводило в результате к образованию масляной фазы. Добавляли диэтиловый эфир (20 мл) и водную фазу удаляли. Органическую фазу затем последовательно промывали 1М соляной кислотой (30 мл), 0.1М соляной кислотой (30 мл) и дважды деионизированной водой (30 мл каждая), перед концентрированием эфирного слоя путем роторного выпаривания и высушивания in vacua с получением 3,5-бис(2’-децилтетрадеканамидо)бензойной кислоты в виде светло-коричневого воскообразного твердого вещества (1.33 г, 99%). Продукт идентифицировали с помощью 1Н и 13С ЯМР спектроскопии и ESI-MS, и он был удовлетворительной чистоты. Продукт, как полагали, имел формулу
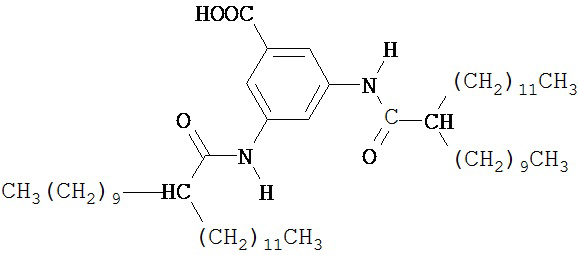
ПРИМЕР IV
Синтез 5-(октадецилуреидо)изофталата
Этап 1: Синтез диметил 5-(октадецилуреидо)изофталата
Диметил 5-аминоизофталат (полученный от Aldrich Chemical Co., Milwaukee, WI, 0.441 г, 2.12 ммоль) растворяли в сухом N,N-диметилформамиде (8 мл) в 50 мл круглодонной колбе в инертной атмосфере. Затем добавляли по каплям 2.12 М раствор октадецилизоцианата (2.12 ммоль) в сухом N,N-диметилформамиде (1 мл). Остаточный раствор октадецилизоцианата количественно переносили 2 порциями N,N-диметилформамида (1 мл каждая), и реакцию перемешивали в течение ночи при комнатной температуре. Реакцию за тем нагревали до 100°С в течение 22 ч и вслед за этим охлаждали до комнатной температуры с получением суспензии белого цвета. Твердое вещество затем отфильтровывали под вакуумом, промывали свежим N,N-диметилформамидом и затем промывали деионизированной водой. Фильтрат концентрировали путем роторного выпаривания с получением белого твердого вещества.
Этап 2: Омыление диметил 5-(октадецилуреидо)изофталата
Сырой диметил 5-(октадецилуреидо)изофталат из Этапа 1 (330 мг, 0.654 ммоль) суспендировали в метаноле (15 мл). Затем добавляли гидроксид калия (0.1983 мг, 3.53 ммоль), и смесь нагревали с обратным холодильником в течение 2 ч. После охлаждения до комнатной температуры суспендированное белое твердое вещество извлекали путем фильтрации и промывали холодным метанолом. Сырое твердое вещество затем суспендировали в 1 М соляной кислоте и перемешивали в течение 2 дней, после чего продукт собирали путем фильтрации, промывали деионизированной водой и высушивали in vacuo с выходом белого порошка (124.8 мг). Продукт идентифицировали с помощью 1Н и 13С ЯМР спектроскопии и ESI-MS, и он был удовлетворительной чистоты. Продукт, как полагали, имел формулу
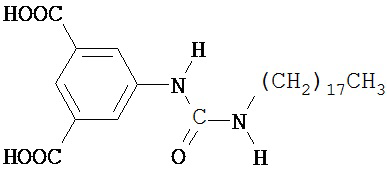 .
.
ПРИМЕР V
Синтез 9,10-динонилоктадеканамидодиизофталевой кислоты
Этап 1: Синтез тетрахлорида 9,10-динонилоктадекандикарбоновой кислоты
PRIPOL® 1006 (96%, 3.23 г, 5.70 ммоль, полученный от Uniqema) и сухой тетрагидрофуран (50 мл) добавляли в 250 мл круглодонную колбу в инертной атмосфере. Раствор затем охлаждали до 0°С в течение, по меньшей мере, 30 мин перед тем, как добавляли каталитическое количество N,N’-диметилформамида (0.10 мл, 1.3 ммоль) с последующим медленным добавлением по каплям оксалил хлорида (2.0 мл, 23.3 ммоль). Смеси затем давали возможность медленно нагреваться до комнатной температуры и перемешивали в течение 3.5 ч перед тем, как удаляли растворитель путем роторного выпаривания с получением бесцветной жидкости с суспендированным белым твердым веществом. Соединение тетрахлорангидид, полученное таким образом, применяли на следующем этапе без дополнительной очистки.
Этап 2: Синтез тетраметил
9,10-динонилоктадеканамидодиизофталевой кислоты
Тетрахлорид 9,10-динонилоктадекандиларбоновой кислоты из Этапа 1 и сухой тетрагидрофуран (50 мл) смешивали в инертной атмосфере и смесь охлаждали до 0°С в течение, по меньшей мере, 30 мин. Затем медленно, по каплям, добавляли диметил 5-аминоизофталат (Aldrich, 2.65 г, 12.7 ммоль) в виде раствора в сухом N,N’-диметилформамиде (15 мл) в колбу, содержащую тетрахлорангидид. Проводили два последовательных промывания тетрагидрофураном (10 мл), чтобы количественно перенести весь амин в колбу с хлорангидридом. Затем добавляли триэтиламин (2.6 мл, 18.7 ммоль), и реакции после этого давали возможность медленно нагреваться до комнатной температуры и перемешиваться в течение ночи. После удаления тетрагидрофурана путем роторного выпаривания, сырой остаток растворяли в 140 мл диэтилового эфира и промывали деионизированной водой (40 мл), насыщенным бикарбонатом натрия (40 мл), 5% лимонной кислотой (40 мл) и рассолом (40 мл). Слой диэтилового эфира затем высушивали над сульфатом натрия и фильтровали через стекловату, после чего удаляли растворитель путем роторного выпаривания, и продукт высушивали т vacua с получением сырого тетраметилбисизофталата (5.61 г) в виде вязкого желтого сиропа. Сложный диэфир, полученный таким образом, применяли на следующем этапе без дополнительной очистки.
Этап 3: Омыление тетраметил
9,10-динонилоктадеканамидо-диизофталата
Тетраметил 9,10-динонилоктадеканамидо-диизофталат из Этапа 2, гидроксид калия (15.38 г, 233 ммоль), метанол (200 мл) и деионизированную воду (100 мл) добавляли в 500 мл сосуд и смесь нагревали с обратным холодильником в течение 1 ч. Реакцию затем охлаждали до комнатной температуры и окисляли 5 М соляной кислотой (50 мл) с получением белого осадка, который собирали путем фильтрования с отсасыванием, промывали деионизированной водой и затем высушивали in vacuo с получением бледного оранжево-желтого порошка (4.62 г, 91%). Продукт идентифицировали с помощью 1Н и 13С ЯМР спектроскопии и ESI-MS, и он был удовлетворительной чистоты. Продукт, тетраметил 9,10-динонилоктадеканамидодиизофталевая кислота, как полагали, имел формулу
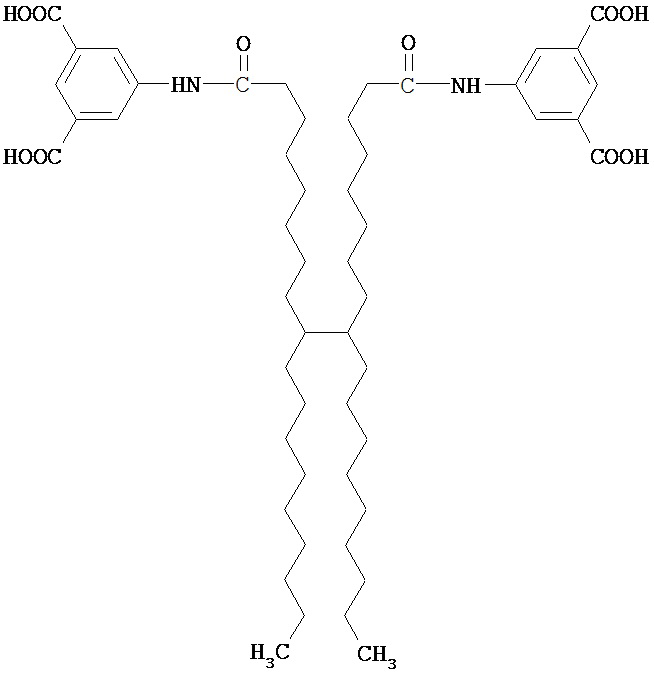 .
.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИМЕТИНОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФЛУОРЕСЦЕНТНЫХ МЕТОК | 2016 |
|
RU2696562C1 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2808165C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2665571C2 |
| НЕЙРОАКТИВНЫЕ СОЕДИНЕНИЯ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2764702C2 |
| ЗАМЕЩЕННЫЕ ПИРРОЛО [2,3-b] ПИРИДИН И ПИРАЗОЛО [3,4-b] ПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2020 |
|
RU2824583C2 |
| ЗАМЕЩЕННЫЕ (2-АЗАБИЦИКЛО[3.1.0]ГЕКСАН-2-ИЛ)ПИРАЗОЛО[1.5-a]ПИРИМИДИНОВЫЕ И ИМИДАЗО[1.2-b]ПИРИДАЗИНОВЫЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ КИНАЗ TRK | 2019 |
|
RU2781618C2 |
| ПРОТИВОМИКРОБНЫЕ СОЕДИНЕНИЯ И КОМПОЗИЦИИ | 2014 |
|
RU2630693C2 |
| КАТАЛИЗАТОРЫ НА ОСНОВЕ ПЕРЕХОДНОГО МЕТАЛЛА 8 ГРУППЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ИХ ПРИМЕНЕНИЯ В РЕАКЦИИ МЕТАТЕЗИСА | 2014 |
|
RU2674471C2 |
| МУЛЬТИПЛЕКСНОЕ ФЛУОРЕСЦЕНТНОЕ ОБНАРУЖЕНИЕ АНАЛИТОВ | 2020 |
|
RU2816515C2 |
| ДИГИДРОПТЕРИДИНОНОВЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2673944C2 |
Изобретение относится к способу, включающему смешивание ароматической кислоты со смесью, содержащей первую жидкость и вторую жидкость, вызывая тем самым образование органогеля, содержащего ароматическую кислоту и первую жидкость, причем ароматическая кислота имеет формулу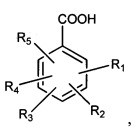 где R1, R3 и R5 представляют собой водород, R2 представляет собой -X1-Rc1, R4 представляет собой -СООН или -X2-Rc2, X1, Х2 представляют собой -NH-C(O)-, Rc1 и Rc2 представляют собой разветвленную незамещенную алкильную группу или линейную незамещенную группу формулы -(СН2)nCH3, где n представляет собой целое число, которое составляет по меньшей мере 15; либо ароматическая кислота имеет формулу:
где R1, R3 и R5 представляют собой водород, R2 представляет собой -X1-Rc1, R4 представляет собой -СООН или -X2-Rc2, X1, Х2 представляют собой -NH-C(O)-, Rc1 и Rc2 представляют собой разветвленную незамещенную алкильную группу или линейную незамещенную группу формулы -(СН2)nCH3, где n представляет собой целое число, которое составляет по меньшей мере 15; либо ароматическая кислота имеет формулу: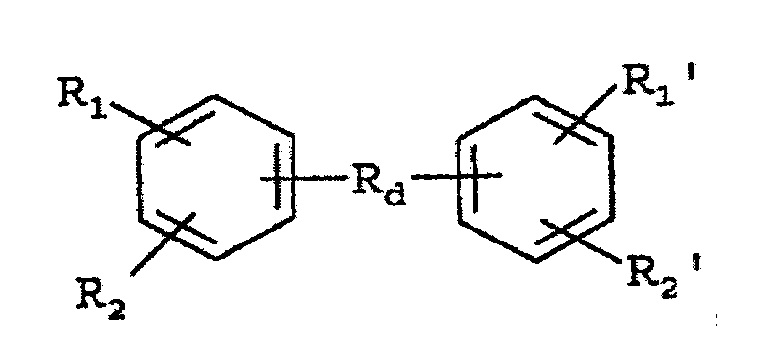 , где R1, R2, R1', R2' представляет собой СООН группу, a Rd представляет собой бифункциональную группу, которая соединяет мостиком группы ароматической кислоты. Изобретение также относится к способу экстрагирования и к способу обработки органического загрязнения, включающему внесение ароматической кислоты в нефть нефтяного загрязнения. 3 н. и 9 з.п. ф-лы, 5 пр.
, где R1, R2, R1', R2' представляет собой СООН группу, a Rd представляет собой бифункциональную группу, которая соединяет мостиком группы ароматической кислоты. Изобретение также относится к способу экстрагирования и к способу обработки органического загрязнения, включающему внесение ароматической кислоты в нефть нефтяного загрязнения. 3 н. и 9 з.п. ф-лы, 5 пр.
1. Способ, включающий смешивание ароматической кислоты со смесью, содержащей первую жидкость и вторую жидкость, вызывая тем самым образование органогеля, содержащего ароматическую кислоту и первую жидкость, причем ароматическая кислота имеет формулу
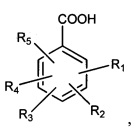
где R1, R3 и R5 представляют собой водород,
R2 представляет собой -X1-Rc1, R4 представляет собой -СООН или -X2-Rc2,
X1, Х2 представляют собой -NH-C(O)-,
Rc1 и Rc2 представляют собой разветвленную незамещенную алкильную группу или линейную незамещенную группу формулы -(СН2)nCH3, где n представляет собой целое число, которое составляет по меньшей мере 15;
либо ароматическая кислота имеет формулу:
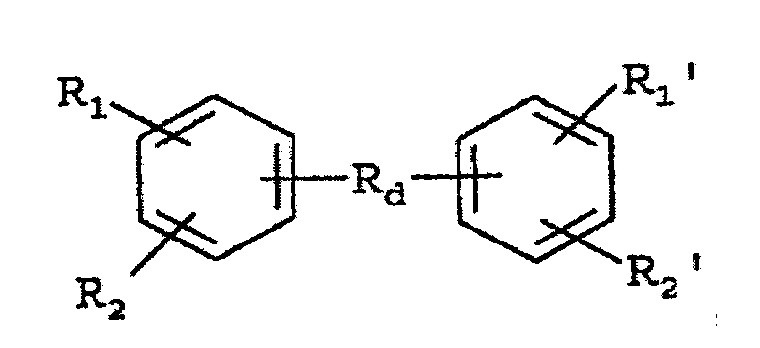
где R1, R2, R1', R2' представляет собой СООН группу, a Rd представляет собой бифункциональную группу, которая соединяет мостиком группы ароматической кислоты.
2. Способ по п. 1, в котором образование органогеля вызывает отделение, по меньшей мере, некоторого количества первой жидкости от второй жидкости.
3. Способ по п. 1, в котором первая жидкость и вторая жидкость являются несмешиваемыми.
4. Способ по п. 1, в котором ароматическая кислота смешивается с первой жидкостью в количестве от 0,05% до 20% по массе от первой жидкости.
5. Способ по п. 1, в котором ароматическая кислота смешивается с первой жидкостью в количестве не более чем около 20% по массе от первой жидкости.
6. Способ по п. 1, в котором первая жидкость и вторая жидкость присутствуют в относительных количествах от около 0,1 до около 1 массовой части первой жидкости на каждую 1 массовую часть второй жидкости.
7. Способ по п. 1, дополнительно включающий отделение органогеля от смеси.
8. Способ по п. 7, в котором способ отделения включает дистилляцию.
9. Способ по п. 1, в котором Rc1 и Rc2 представляют собой:
(а) разветвленную незамещенную алкильную группу формулы
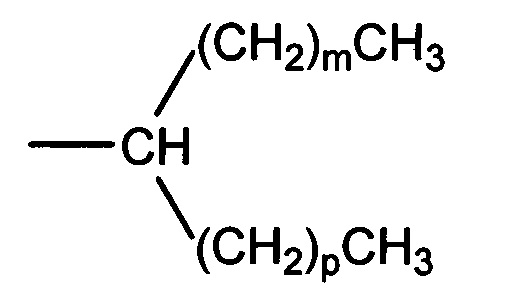
в которой m представляет собой целое число и p представляет собой целое число;
b) разветвленную незамещенную алкильную группу формулы
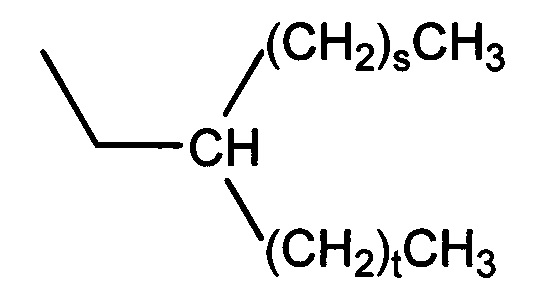
в которой s представляет собой целое число и t представляет собой целое число;
(c) разветвленную незамещенную алкильную группу формулы
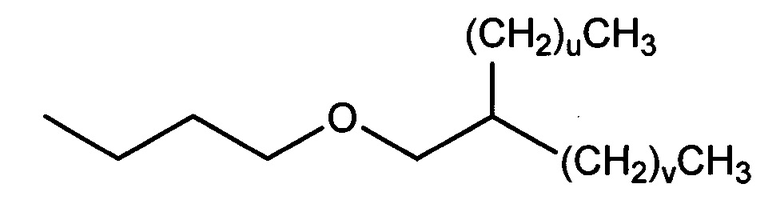
в которой u представляет собой целое число и v представляет собой целое число;
(d) мультиразветвленную незамещенную алкильную группу формулы
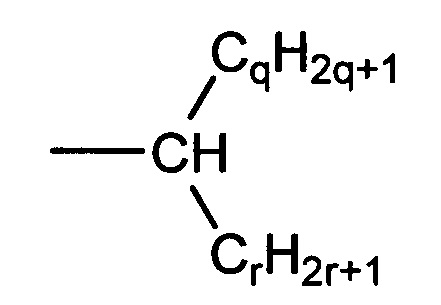
в которой q представляет собой целое число и r представляет собой целое число;
или их смеси,
причем Rc1 и Rc2 могут быть или одинаковыми или отличаться друг от друга.
10. Способ по п. 1, в котором ароматическая кислота представляет собой
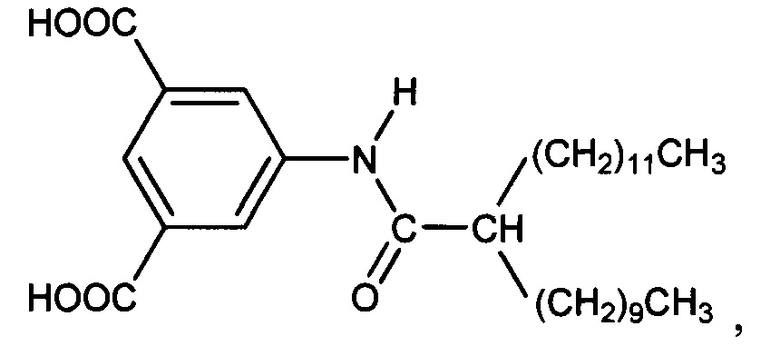
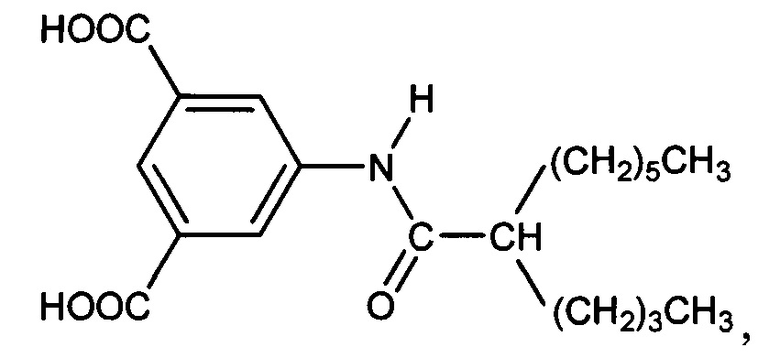
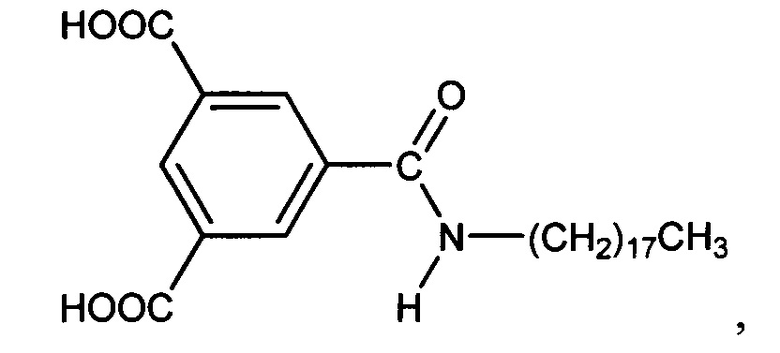
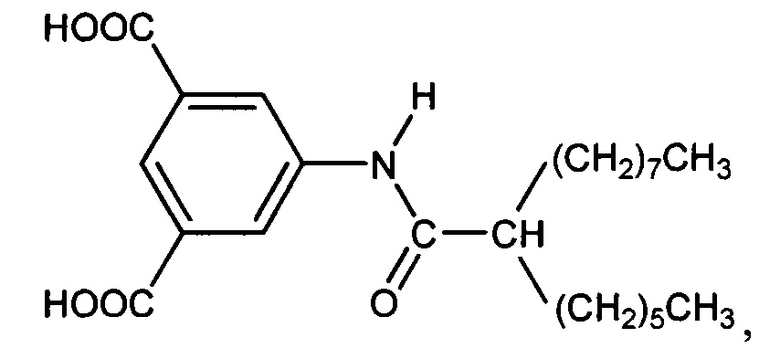
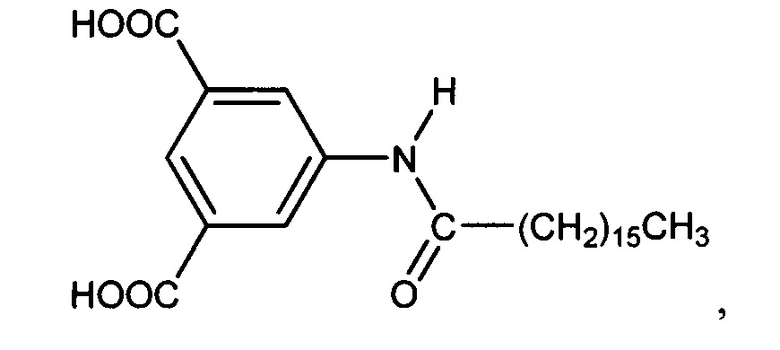
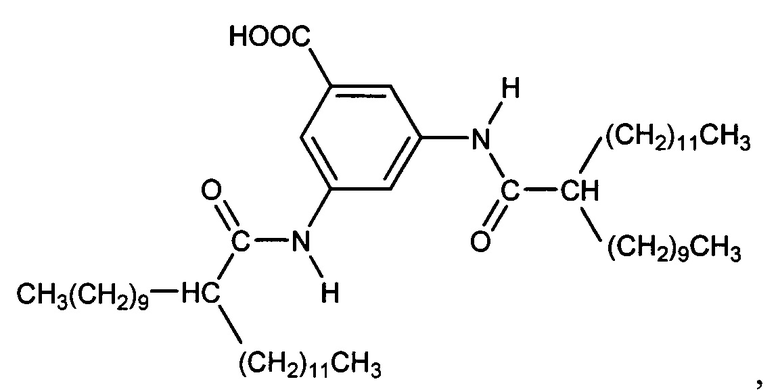
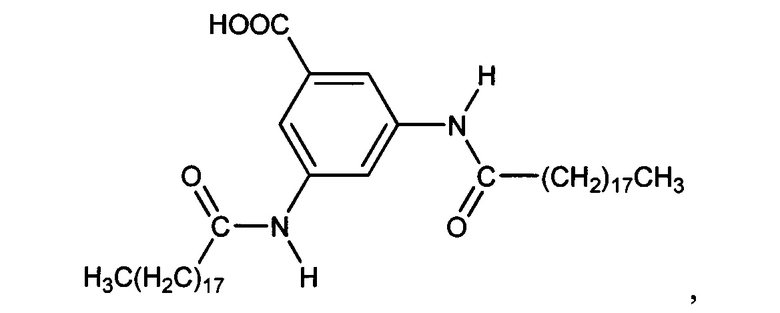
или их смеси.
11. Способ экстрагирования первой жидкости из второй жидкости, включающий:
(a) получение смеси, содержащей первую жидкость и вторую жидкость, и
(b) контактирование смеси с ароматической кислотой при условиях, эффективных для того, чтобы вызвать образование органогеля, содержащего алкилированную ароматическую кислоту и первую жидкость, таким образом извлекая, по меньшей мере, некоторое количество первой жидкости из второй жидкости,
причем ароматическая кислота имеет формулу
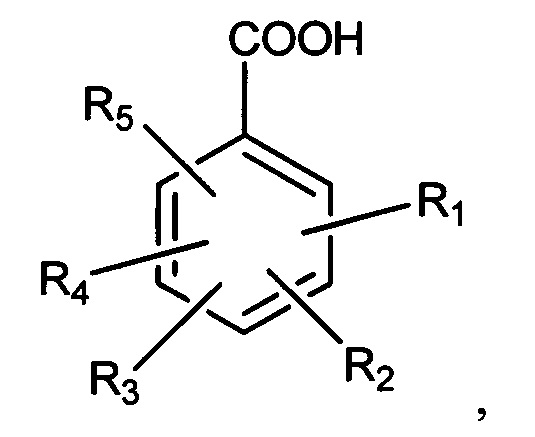
где R1, R3 и R5 представляют собой водород,
R2 представляет собой -X1-Rc1, R4 представляет собой -СООН или -X2-Rc2,
X1, Х2 представляют собой -NH-C(O)-,
Rc1 и Rc2 представляют собой разветвленную незамещенную алкильную группу или линейную незамещенную группу формулы -(СН2)nCH3, где n представляет собой целое число, которое составляет по меньшей мере 15;
либо ароматическая кислота имеет формулу:
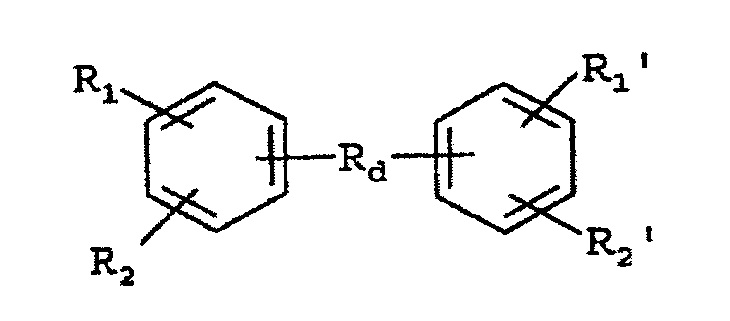
где R1, R2, R1', R2' представляет собой СООН группу, a Rd представляет собой бифункциональную группу, которая соединяет мостиком группы ароматической кислоты.
12. Способ обработки органического загрязнения, включающий внесение ароматической кислоты в нефть указанного нефтяного загрязнения и включающий:
(а) смешивание ароматической кислоты с загрязнением для образования органогеля; и
(b) сбор полученного в результате органогеля,
причем ароматическая кислота имеет формулу
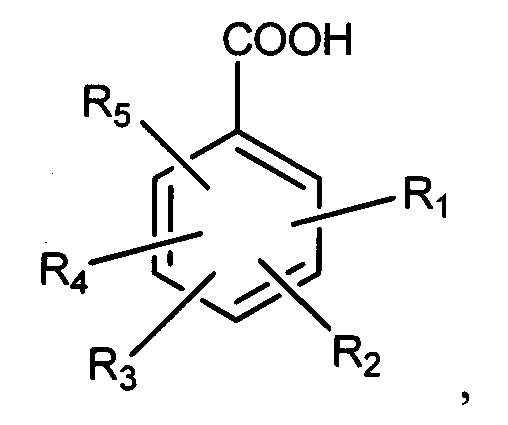
где R1, R3 и R5 представляют собой водород,
R2 представляет собой -X1-Rc1, R4 представляет собой -СООН или -X2-Rc2,
X1, Х2 представляют собой -NH-C(O)-,
Rc1 и Rc2 представляют собой разветвленную незамещенную алкильную группу или линейную незамещенную группу формулы -(СН2)nCH3, где n представляет собой целое число, которое составляет по меньшей мере 15;
либо ароматическая кислота имеет формулу:
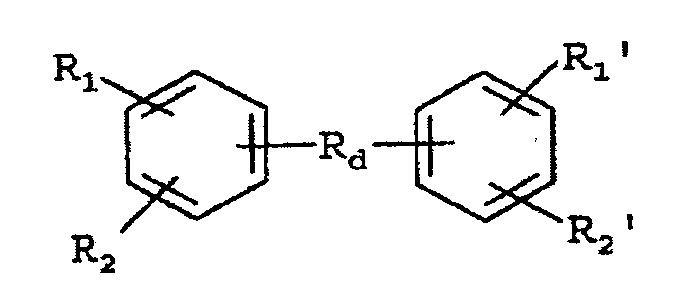
где R1, R2, R1', R2' представляет собой СООН группу, a Rd представляет собой бифункциональную группу, которая соединяет мостиком группы ароматической кислоты.
| Ho Yong Lee et al | |||
| "Microtubule Formation Using Two-Component Gel System" JACS, 2007, 129, pp | |||
| ВИСЯЧИЙ ШКВОРНЕВОЙ ЗАМОК | 1924 |
|
SU1040A1 |
| СПОСОБ ПЛАСТИКИ КОНЪЮНКТИВЫ | 1995 |
|
RU2113196C1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| СРЕДСТВО ДЛЯ ОЧИСТКИ ПОВЕРХНОСТИ ВОДЫ ОТ НЕФТИ И НЕФТЕПРОДУКТОВ | 1999 |
|
RU2148025C1 |
Авторы
Даты
2017-07-06—Публикация
2012-12-13—Подача