Изобретение относится к биотехнологии, молекулярной биологии и может быть использовано для определения нуклеотидной последовательности фрагмента гена 28S рРНК и идентификации медицински значимых микромицетов в пробах чистых культур специалистами учреждений практического здравоохранения, Роспотребнадзора и в научно-исследовательских лабораториях.
Причиной заболевания микозами миллионов людей во всем мире могут являться первично-патогенные микромицеты - возбудители кокцидиоидомикоза, гистоплазмоза, бластомикоза, паракокцидиоидомикоза, эндемического пенициллиоза, дерматофитий и некоторых других заболеваний, а также условно-патогенные микромицеты, имеющие повсеместное распространение - Candida spp., Aspergillus spp. и т.д. За последние десятилетия отмечается постоянный рост заболеваемости микотическими инфекциями, в том числе, вызываемыми условно-патогенными микромицетами, на фоне увеличения числа пациентов с поражениями иммунной системы (первичные или вторичные иммунодефициты).
Идентификация медицински значимых микромицетов чрезвычайно важна для проведения своевременного лечения, поскольку клинические симптомы не всегда позволяют дифференцировать микозы как между собой, так и от многих бактериальных и вирусных инфекций.
Согласно данным большинства исследователей для идентификации микромицетов и изучения их филогенетического родства на видовом уровне наиболее часто применяют анализ ядерной рибосомальной ДНК (18S-5.8S-28S), обладающей большой копийностью в геноме [Redecker D. Phylogenetic analysis of a dataset of fungal 5.8S rDNA sequences shows that highly divergent copies of internal transcribed spacers reported from Scutellospora castanea are of ascomycete origin / D. Re-decker, M. Hijri, H. Dulieu, I.R. Sanders // Fungal Genetics and Biology. - 1999 - Vol. 28. - №3. - P. 238-244.]. Исследователями установлена высокая вариабельность нуклеотидного состава входящих в данный регион участков и показана потенциальная возможность применения рибосомальной ДНК в качестве маркерной области для анализа широкого спектра микроскопических грибов [Eberhardt U. Methods for DNA barcoding of fungi. / U. Eberhardt // Methods Mol Biol. - 2012. - Vol. - 858. - P. 183-205. doi: 10.1007/978-1-61779-591-6_9]. Уникальность кластера рибо-сомальных генов в том, что он состоит из последовательно расположенных генов и межгенных промежутков различной степени генетической вариабельности 18S-ITS1-5,8S-ITS2-28S. На основе сравнительного анализа секвенированных последовательностей нуклеотидов описываемых участков генома изучаемого микроорганизма с последовательностями ДНК, представленными в генетических базах данных, возможно определить его видовую принадлежность, а также проанализировать степень родства обнаруженных микромицетов с использованием филогенетического исследования.
Наиболее близким аналогом является набор для секвенирования ДНК микромицетов MicroSeq® D2 LSU rDNA Fungal Identification Kit, производства компании «Applied Biosystems» (США). В основе метода лежит амплификация и последующее секвенирование региона D2 LSU рибосомальной ДНК. Однако данный набор рекомендован для проведения научных исследований и для его работы производитель настоятельно рекомендует оборудование и реактивы собственного производства, что не позволяет использовать приборы и реагенты других производителей (в том числе российских) для сокращения затрат на проведение анализа.
Целью настоящего изобретения является разработка набора олигонуклеотидных праймеров для идентификации медицински значимых микромицетов путем амплификации и последующего секвенирования фрагмента гена 28S pРНК.
Цель достигается конструированием набора олигонуклеотидных праймеров для идентификации медицински значимых микромицетов методом секвенирования ДНК путем амплификации и последующего определения нуклеотидной последовательности вариабельного фрагмента гена 28S рРНК, содержащего пару олиго-нуклеотидов, обладающих активностью прямого и обратного праймеров, комплементарных нуклеотидным последовательностям консервативных участков региона гена 28S pРНК микромицетов и имеющих следующую структуру:
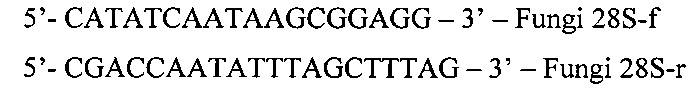
Характеристика олигонуклеотидных праймеров.
При выборе олигонуклеотидных затравок основывались на данных, представленных в различных генетических базах данных (GenBank, EMBL, DDBJ и Broad Institute). Для идентификации медицински значимых микромицетов были подобраны праймеры, обозначенные Fungi 28S-f/Fungi 28S-r, комплементарные консервативным фрагментам гена 28S рРНК и обеспечивающие амплификацию и секвенирование вариабельного участка ДНК различных микромицетов, который ограничен данными праймерами. Длина специфического фрагмента ДНК микромицетов составляла около 300 п.н.
Эксперименты проводили на коллекционных штаммах микромицетов II-IV групп патогенности, используя для выделения ДНК обеззараженные суспензии грибов. Апробация разработанного набора олигонуклеотидных праймеров была осуществлена на наборе штаммов различных возбудителей микозов лаборатории коллекционных штаммов ФКУЗ Волгоградский научно-исследовательский противочумный институт Роспотребнадзора. По результатам амплифицикации и секвенирования фрагментов гена 28S рРНК опытных образцов с помощью разработанного набора олигонуклеотидных праймеров, построены дендрограммы сравнения с последовательностями микромицетов, представленными в генетической базе данных GenBank, Broad Institute. На основе выявленных отличий в нуклеотидных последовательностях подтверждена видовая принадлежность исследуемых микромицетов.
Примеры конкретного выполнения.
Пример 1. Конструирование набора олигонуклеотидных праймеров для идентификации медицински значимых микромицетов методом секвенирования ДНК путем амплификации и последующего определения нуклеотидной последовательности фрагмента гена 28S рРНК.
На основе анализа in silico нуклеотидных последовательностей возбудителей микозов, представленных в базах данных (Broad Institute - http://www.broadinstitute.org/scientific-community/data, GenBank, США - www.ncbi.nlm.nih.gov, EMBL - European Bioinformatics Institute, или EBI - www.ebi.ac.uk, DDBJ, Япония - www.ddbj.nig.ac.jp, а также International Nucleotide Sequence Database (INSD), возникшей в результате сотрудничества между GenBank, EMBL и DDBJ), для конструирования прямого Fungi 28S-f и обратного Fungi 28S-r праймеров были выбраны участки, комплементарные консервативным фрагментам, фланкирующим вариабельный участок гена 28S рРНК, кодирующего рибосомальную РНК большой субъединицы рибосомы микромицетов (GenBank NCBI). Расчетная длина предполагаемого ампликона составляла около 300 п.н. Ее размер может варьировать, например для микромицетов порядка Onygenales, включающего большинство первично-патогенных микромицетов длина фрагмента, амплифицируемого праймерами Fungi 28S-f/Fungi 28S-r может варьировать от 289 до 294 п.н. у Blastomyces dermatitidis, от 293 до 295 п.н. у Histoplasma capsulatum, от 295 до 298 п.н. у Trichophyton spp., 295-296 п.н. у Arthroderma spp., 295 п.н. у Coccidioides spp. и 296 п.н. у Microsporum spp.
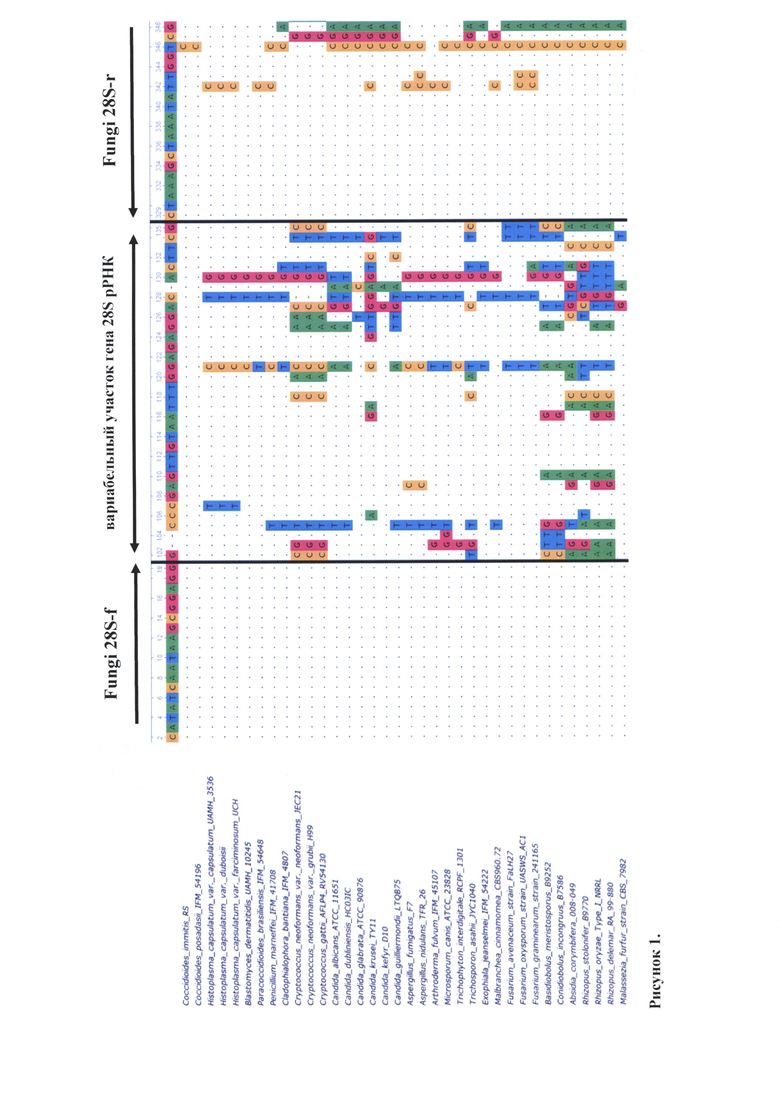
При конструировании праймеров из доступных баз данных были выбраны нуклеотидные последовательности различных видов медицински значимых микромицетов, проведено их множественное выравнивание и, с помощью программного обеспечения или вручную, выполнен поиск участков для отжига праймеров, локализованных в консервативных областях, разделенных вариабельным регионом гена 28S рРНК, пригодным для идентификации методом секвенирования ДНК (рис. 1).
На рисунке 1 отображена схема выравнивания последовательностей и выбор вариабельного региона гена 28S рРНК при конструировании праймеров для идентификации исследуемых микромицетов методом секвенирования.
При выборе последовательностей праймеров руководствовались общими требованиями к олигонуклеотидным затравкам, используемым в ПЦР и секвенировании. С помощью компьютерного моделирования была проанализирована структура выбранных пар праймеров (образование димеров, шпилек и других вторичных структур) и показана их теоретическая пригодность для успешной инициации реакции амплификации и секвенирования нуклеотидной последовательности фрагмента гена 28S pPHК медицински значимых микромицетов.
Праймеры Fungi 28S-f/Fungi 28S-r были проанализированы с использованием компьютерных программ BLAST (http://www.ncbi.nlm.nih.gov/BLAST/) и Primer-Blast (http://www.ncbi.nlm.nih.gov/tools/primer-blast) на web-сервере Национального Центра Биотехнологической Информации (NCBI) для установления гомологии праймеров и нуклеотидных последовательностей гетерологичных микромицетов, представленных в генетических базах данных. На момент проведения компьютерного анализа выявлена лишь специфическая гомология праймеров Fungi 28S-f/Fungi 28S-r для широкого спектра медицински значимых микромицетов.
Пример 2. Амплификация и электрофоретическая детекция специфичных фрагментов ДНК гена 28S рРНК с использованием разработанного набора праймеров Fungi 28S-f/Fungi 28S-r для идентификации медицински значимых микромицетов.
Обеззараживание исследуемых образцов проводили согласно требованиям СП 1.3.3118-13 «Безопасность работы с микроорганизмами I-II групп патогенности (опасности)» и МУ 1.3. 2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности». Выделение ДНК из чистых культур микромицетов осуществляли методом гуанидинтиоцианат-фенольной экстракции с переосаждением ДНК изопропанолом [Sandhu G.S. et al., 1995].
В состав реакционной смеси для амплификации входили ДНК анализируемых микромицетов, разработанные комплементарные специфическому фрагменту ДНК прямой Fungi 28S-f и обратный Fungi 28S-r праймеры, дезоксирибонуклеозидтрифосфаты (дНТФ), MgCl2, буфер, фермент Taq-полимераза (ФБУН ЦНИИ Эпидемиологии Роспотребнадзора, Москва). Амплификацию проводили с использованием «горячего старта», который обеспечивали разделением реакционной смеси воском на два слоя. В «нижнем» слое находились дезоксирибонуклеозидтрифосфаты и праймеры, «верхний» слой содержал ДНК-матрицу и буферный раствор с ионами Mg2+ и ферментом Taq-полимеразой. Плавление воска и перемешивание реакционных компонентов происходило на этапе предварительной денатурации ДНК при 95°С. Для предотвращения испарения смеси сверху наслаивали по 30 мкл минерального масла. В качестве отрицательного контрольного образца использовали ТЕ-буфер.
Амплификацию проводили на приборе «Терцик» (НПФ «ДНК-технология», Россия). Условия проведения реакции ПЦР: предварительная денатурация 95°С - 5 мин, затем денатурация 95°С - 10 с, отжиг 60°С - 10 с, элонгация 72°С - 30 с, в течение 45 циклов.
Присутствие специфического ПЦР-продукта детектировали электрофоретическим разделением амплификационной смеси в 1,5% агарозном геле, приготовленном на трис-боратном буфере, при градиенте напряжения 5 В/см. Время проведения электрофореза составляло 30 мин.
Окрашивание гелей для визуализации в проходящем ультрафиолетовом свете (трансиллюминатор фирмы «LKB», Швеция) проводили бромистым этидием (0,5 мкг/мл). Результаты оценивали по наличию или отсутствию в геле ампликонов микромицетов необходимого размера (рис. 2).
На рисунке 2 отображены результаты амплификации ДНК различных видов медицински значимых микромицетов с помощью разработанного набора праймеров Fungi 28S-f/Fungi 28S-r (1. Coccidioides posadasii 36-S; 2. Coccidioides immitis 158; 3. Histoplasma capsulation 6652; 4. Blastomyces dermatitidis 6/85; 5. Cryptococcus neoformans 9/22; 6. Candida parapsilosis BKMY-58; 7. Candida glabrata BKM Y-1481; 8. Candida kefyr BKM Y-257; 9. Candida guilliermondii BKM Y-41; 10. Rhodotorula mucilaginosa BKM Y-339; 11. Geotrichum fermentans BKM Y-813; 12. Fusarium javanicum (solani) BKM F-134; 13. Absidia hyalospora BKM F-1435; 14. Aspergillus fumigatus BKM F-753; 15. Rhizopus microsporia var. microsporus BKM F-774; 16. Fusarium culmorum BKM F-1017; 17. Gymnoascus reesii BKM F-1707; 18. Mucor racemosus var. racemosus BKM F-1128; 19. Phialophora verrucosa BKM F-1990; 20. Scopulariopsis brevicaulis BKM F-406; 21. Отрицательный контроль, К-).
Пример 3. Определение нуклеотидной последовательности ДНК с помощью разработанного набора праймеров Fungi 28S-f/Fungi 28S-r для идентификации медицински значимых микромицетов методом секвенирования ДНК.
После проведения ПЦР амплифицированные фрагменты вырезали из агарозного геля и проводили очистку от агарозы центрифугированием в спин-колонках при 8000 об/мин в течение 8 мин. Элюент высушивали и подвергали дальнейшей очистке добавлением экзонуклеазы и щелочной фосфатазы (ExoI/SAP, «Thermo Fisher Scientific», США). Реакцию секвенирования проводили с использованием BigDye® Terminator v3.1 Cycle Sequencing Kit («Thermo Fisher Scientific», США). Термоциклирование проводили в соответствие со стандартной программой.
Далее добавляли в каждую пробирку по 1 мкл 2,2% SDS (додецил сульфат натрия) и термоциклировали (95°С - 5 мин; 25°С - 10 мин). Определение нуклеотидной последовательности проводили на приборе ABI 3130 («Applied Biosystems», США).
После проведения секвенирования осуществляли сравнение анализируемой последовательности ДНК со всеми известными последовательностями ДНК микромицетов в режиме «on-line» с помощью программы BLASTn на сервере (http://www.ncbi.nlm.nih.gov/BLAST/), депонированными в базе данных GenBank. На основе установления гомологии определяли видовую принадлежность исследуемых микромицетов.
С использованием разработанного набора олигонуклеотидных праймеров Fungi 28S-f/Fungi 28S-r было проведено секвенирование ДНК 40 штаммов из коллекции ФКУЗ Волгоградский научно-исследовательский противочумный институт Роспотребнадзора, среди которых представители группы особо опасных микромицетов: 6 штаммов Coccidioides immitis, 2 штамма Coccidioides posadasii, 9 штаммов Histoplasma capsulatum, 3 штамма Blastomyces dermatitidis, а также условно-патогенные микромицеты: 5 штаммов Cryptococcus neoformans и по 1 штамму Candida parapsilosis BKM Y-58, Candida glabrata BKM Y-1481, Candida kefyr BKM Y-257, Candida guilliermondii BKM Y-41, Rhodotorula mucilaginosa BKM Y-339, Geotrichum fermentans BKM Y-813, Fusarium javanicum (solani) BKM F-l34, Absidia hyalospora (syn. Mycocladus hyalospora) BKM F-1435, Aspergillus fumigatus BKM F-753, Rhizopus microsporia var. microsporus BKM F-774, Fusarium culmorum BKM F-1017, Gymnoascus reesii BKM F-1707, Mucor racemosus var. racemosus BKM F-l128, Phialophora verrucosa BKM F-l990, Scopulariopsis brevicaulis BKM F-406.
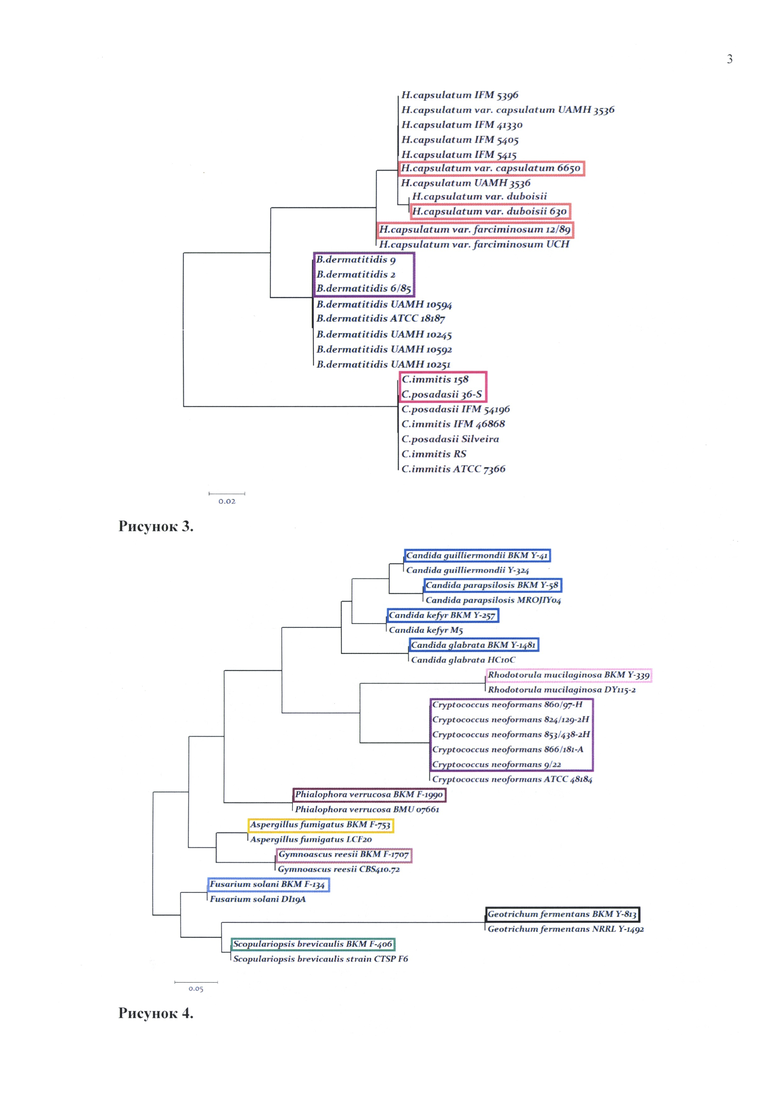
В результате сравнительного анализа секвенированных последовательностей ДНК с гомологичными нуклеотидными последовательностями доступных генетических баз данных подтверждена видовая принадлежность коллекционных штаммов исследуемых микромицетов. На основании полученных данных построены филогенетические деревья, отражающие степень родства изучаемых микроскопических грибов. Показана 100% точность в процессе идентификации 40 исследуемых штаммов микромицетов II-IV групп патогенности (рис. 3 и 4).
Рисунок 3 отображает дендрограмму сходства, построенную на основе сравнения секвенированных с помощью разработанного набора олигонуклеотидных праймеров последовательностей фрагментов гена 28S рРНК исследуемых штаммов возбудителей особо опасных микозов и последовательностей, депонированных в генетической базе данных GenBank. Рамкой выделены штаммы коллекции живых культур ФКУЗ Волгоградский научно-исследовательский противочумный институт Роспотребнадзора.
Рисунок 4 отображает дендрограмму сходства, построенную на основе сравнения секвенированых с помощью разработанного набора олигонуклеотидных праймеров фрагмента гена 28S рРНК исследуемых штаммов микромицетов III-IV групп и последовательностей, представленных в базе данных GenBank. Рамкой выделены штаммы коллекции живых культур ФКУЗ Волгоградский научно-исследовательский противочумный институт Роспотребнадзора
Таким образом, разработанный набор праймеров Fungi 28S-f/Fungi 28S-r может быть использован для амплификации и секвенирования фрагмента гена 28S рибосомальной РНК различных видов возбудителей микозов для анализа нуклеотидных последовательностей, установления видовой принадлежности чистых культур микромицетов, изучения их филогенетического родства на видовом уровне и идентификации медицински значимых микромицетов.

Настоящее изобретение относится к биохимии, биотехнологии, молекулярной биологии, в частности к набору олигонуклеотидных праймеров для идентификации медицински значимых микромицетов методом секвенирования ДНК путём амплификации и последующего определения нуклеотидной последовательности фрагмента гена 28S рРНК. Указанный набор содержит пару олигонуклеотидов, обладающих активностью прямого и обратного праймеров, комплементарных нуклеотидным последовательностям консервативных участков региона гена 28S рРНК микромицетов. Олигонуклеотидные праймеры имеет следующую структуру: 5'-CATATCAATAAGCGGAGG-3' (прямой праймер Fungi 28S-f) и 5'-CGACCAATATTTAGCTTTAG-3' (обратный праймер Fungi 28S-r). Настоящее изобретение позволяет расширить арсенал средств для амплификации и секвенирования фрагмента гена 28S рибосомальной РНК различных видов возбудителей микозов для анализа нуклеотидных последовательностей, установления видовой принадлежности чистых культур микромицетов, изучения их филогенетического родства на видовом уровне и идентификации медицински значимых микромицетов. 4 ил., 3 пр.
Набор олигонуклеотидных праймеров для идентификации медицински значимых микромицетов методом секвенирования ДНК путем амплификации и последующего определения нуклеотидной последовательности вариабельного фрагмента гена 28S рРНК, содержащий пару олигонуклеотидов, обладающих активностью прямого и обратного праймеров, комплементарных нуклеотидным последовательностям консервативных участков региона гена 28S рРНК микромицетов и имеющих следующую структуру:
5'-CATATCAATAAGCGGAGG-3'-Fungi 28S-f
5'-CGACCAATATTTAGCTTTAG-3'-Fungi 28S-r
| ОЛИГОНУКЛЕОТИДНЫЕ ПРАЙМЕРЫ ДЛЯ ИДЕНТИФИКАЦИИ Coccidioides posadasii | 2007 |
|
RU2346045C1 |
| US 9238831 B2, 19.01.2016 | |||
| НАЖДАЧНАЯ ОБОЙКА | 1950 |
|
SU92088A1 |
| ЛЕМАСОВА Л.В | |||
| и др., Анализ праймеров и зондов, позволяющих дифференциацировать Burkholderia mallei и Burkholderia pseudomallei методом ПЦР, Дальневосточный Журнал Инфекционной Патологии, 2014, No.25, с.132-134. | |||
Авторы
Даты
2017-09-28—Публикация
2016-08-04—Подача