Изобретение относится к химическим средствам обработки воды из природных источников для использования в быту, в полевых условиях, в чрезвычайных ситуациях (наводнения, техногенные аварии на производствах и системах водоподготовки и центрального водоснабжения, в туристических походах, в условиях военных действий и т.д.).
В реагентной технологии водоподготовки и водоочистки эффективность процесса определяется степенью очистки воды от примесей, длительностью процесса осаждения примесей, продолжительностью цикла фильтрования очищаемой воды и другими факторами.
Одним из основных является доза реагента, которая должна быть минимальной для достижения достаточной степени очистки, что определяется не только экономическими соображениями, но и требованиями инспектирующих органов к качеству очищенной воды, а также санитарными нормами в отношении остаточного количества реагента в очищенной воде [1].
Известно также, что обработка воды коагулянтами - самый распространенный метод очистки больших объемов воды от грубодисперсных, коллоидных, органических и химических загрязнений.
Масштабы применения метода коагуляции в централизованной водоподготовке для бытовых и производственных целей общеизвестны и в последние годы постоянно совершенствуются. В связи с этим быстро растет ассортимент коагулянтов и сопутствующих им реагентов, предлагаемых для очистки природных вод с целью улучшения качества питьевой воды.
Традиционно используемый коагулянт сульфат алюминия - Al2(SO4)3 не во всех случаях обеспечивает требуемое качество очистки. Особенно затруднительно его использование при температурах ниже 8αC, так как при данных температурах образуются такие высокодисперсные осадки продуктов гидролиза коагулянта, что их трудно отделить от очищаемой воды методами отстаивания и фильтрации.
Для интенсификации процессов реагентной очистки мягких вод с низким содержанием естественных взвесей необходимо дополнительное применение водорастворимых высокомолекулярных полиэлектролитов - флокулянтов. Флокулянты позволяют повысить эффективность коагуляции и седиментации примесей воды, снизить дозу коагулянта.
Так, коагулянтами для водоподготовки технической воды систем горячего водоснабжения могут служить гидрохлориды алюминия - Al(OH)Cl2 и Al(OH)2Cl. Однако эти коагулянты обычно используются для перевода солей «временной» жесткости в соли «постоянной» жесткости, но для получения питьевой воды непригодны.
В последнее время все более широкое распространение находит коагулянт - высокоосновный оксихлорид алюминия (ОХА), Al2(OH)5Cl. Другие названия: гидроксихлорид алюминия, полиалюминий хлорид (по международной номенклатуре непатентованное название «РАС») является перспективным и экономичным коагулянтом нового поколения, выбранным нами за прототип.
Оксихлорид алюминия широко применяется для очистки природных, оборотных и сточных вод от взвешенных веществ, тяжелых металлов, нефтепродуктов, фосфатов, синтетических поверхностно-активных веществ, для снижения цветности, мутности и пр.
Практика применения коагулянта «Бопак-Е» [2] показала ряд преимуществ его использования в сравнении с традиционно используемым сульфатом алюминия.
1. Дозировка данного препарата меньше, чем сульфата алюминия (в пересчете на Al2O3) и затраты на водоподготовку меньше, чем при использовании других неорганических флокулянтов.
2. Применение продукта приводит к стремительному хлопьеобразованию, получению крупных хлопьев и их осаждению, в результате чего образуется быстро выпадающий и хорошо фильтруемый осадок.
3. Оксихлорид алюминия может применяться в расширенном диапазоне температуры воды, обладает хорошей растворимостью.
4. Снижает содержание хлорорганических соединений.
5. Обладает малой коррозийной активностью.
6. Имеет расширенный диапазон оптимальных (pH) и фактически не изменяет щелочность воды.
Выбор коагулянта, учитывающий особенности исходной воды и сезонных изменений ее качества - основа для получения воды, соответствующей нормативным требованиям.
В полевых условиях и в чрезвычайных ситуациях необходимый предварительный контроль качества воды из природных источников не реализуем, а доставка качественной воды населению многократно усложняется. Кроме того требуется очень строгий контроль дозирования реагентов для предотвращения избыточного содержания алюминия в питьевой воде (ПДК 0,02 мг/л. ГОСТ 18165-2014).
Указанных недостатков лишен экспресс-метод приготовления питьевой воды из природных источников в полевых условиях и в чрезвычайных ситуациях, включающий обработку воды химическими реагентами, коагулянтом и содой, отличающийся тем, что сначала к воде при перемешивании прибавляют раствор коагулянта - высокоосновного оксихлорида алюминия Al2(OH)5Cl, а затем - пищевую соду NaHCO3, в эквимолярном соотношении к коагулянту.
В испытаниях очистки природной воды были использованы следующие реагенты и аппаратура:
1. Коагулянт - ОХА, Al2(OH)5Cl, ТУ 216-350-002-39928758-02.
2. Сода пищевая - NaHCO3, ГОСТ 2156-76.
3. Вода питьевая и жесткая - по НПБ 304-2001.
4. pH-Meter, РН-009(1) СЕ.
5. TDS-Meter, 139 TDS Testers CE.
Реагенты 1 и 2 могут раздельно храниться неограниченно долго в виде водных растворов в пластиковой таре.
Согласно требованиям Управления по охране окружающей среды (ЕРА) максимально допустимый уровень загрязнения воды составляет 500 мг/литр или 500 частиц на миллион (parts per million, ppm) к общему количеству растворенных в воде твердых частиц.

Жесткость воды отражает содержание в ней ионов кальция и магния.
Жесткость, обусловленная наличием в воде гидрокарбонатов кальция и магния, Ca(HCO3)2; Mg(HCO3)2 называется временной или карбонатной (Жвр).
Жесткость, обусловленная хлоридами и сульфатами этих металлов (CaCl2, MgCl2, CaSO4, MgSO4,), называется постоянной (Жп). Суммарная жесткость воды носит название общей жесткости.
Жесткость воды (степень жесткости принято выражать в миллимолях ионов Ca2+ или Mg2+ (или обоих ионов) в 1 дм3 или 1 кг воды - ммоль/дм3 или ммоль/кг. В технической литературе встречается единица измерения степени жесткости воды - мг экв/дм3 или мг-экв/л.
Общая жесткость воды, используемой для питья, согласно СанПиН 2.1.4.599-96 должна находиться в пределах - от 1,5 до 7 мг-экв/л, при этом кальция должно быть не более 140 мг/л, а магния - не более 85 мг/л.
Питьевая вода в разных регионах отличается по своему составу, по содержанию вредных примесей солей и требует использования специальных реагентов для ее очистки.
Так, в Дагестане не соответствует гигиеническим нормативам около 40% проб водопроводной воды. Наиболее низкое качество воды отмечено в столице республики, Избербаше, Хасавюрте, Буйнакске, Дагестанских Огнях, Дербенте.
К неблагополучным районам можно причислить - Ахтынский, Акушинский, Бабаюртовский, Каякентский, Казбековский, Карабудахкентский, Левашинский, Новолакский, Кизилюртовский, Хасавюртовский, Буйнакский, Цумадинский, Лакский, Сулейман-Стальский, Гергебильский, Гунибский, Дахадаевский, Сергокалинский.
Проведенный специальными службами республики анализ состояния водоснабжения городов и районов Дагестана показывает, что ситуация с питьевым водоснабжением неудовлетворительна.
Причины неудовлетворительного качества воды, как и во многих регионах России, - недоочистка стоков и требующие реконструкции водопроводные трубы.
(Источник: Акваэксперт (http://www.aquaexpert.ru/news/2008/08/15/dagestan/). Все испытания по очистке воды экспресс-методом проводят на водопроводной и природной воде г.Хасавюрт, Республики Дагестан.
В таблице 1, приведены данные протокола испытаний питьевой воды городского водоснабжения г. Хасавюрт.
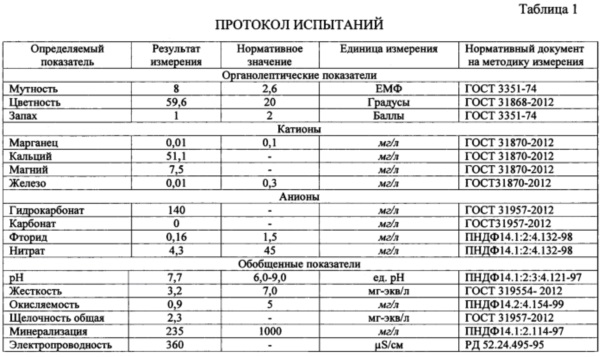
По данным анализа проба воды по исследованиям санитарно-химических показателей не соответствует СанПиН 2.1.4.10745-01 «Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения» по следующим показателям: Цветность, Мутность.
Исходя из результатов исследования установлено, что проба из источника не соответствует нормам, применяемым как к питьевой воде, так и к бытовой.
Поэтому было необходимо на основании протокола исследования подобрать комплексную систему водоподготовки, для исключения негативного влияния такой воды на здоровье.
Реагенты коагулянт - ОХА и пищевая сода были сбалансированы так, что их используют поэтапно в равных расчетных эквимолярных соотношениях.
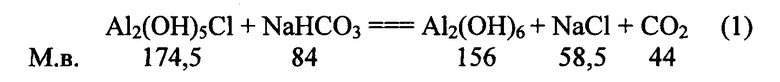
Реакция (1) позволяет в любых условиях применения реагентов избежать избытка коагулянта, ограниченного требованиями ПДК (0,02 мг/л).
В соответствии с техническими условиями ТУ 216-350-002-39928758-02 коагулянт ОХА содержит не менее 34% основного продукта - Al2(OH)5Cl. В примерах описания изобретения для удобства практического применения и дозирования в малые объемы контейнеров (1,5 л), ОХА разбавляют водой в 2 раза (17%) для использования в полевых условиях или чрезвычайных ситуациях в паре с раствором пищевой соды в воде (8,7%) в равном объемном соотношении 1:1, вместо 0,5:1. Иными словами, при любом разбавлении взаимодействующих компонентов необходимо учитывать лишь требование их эквимолярного соотношения по реакции (1).
Возможные варианты применения Na2CO3 и NaOH, вместо пищевой соды, по соображениям доступности и безопасности в бытовых условиях не рассматривались.
Предварительные исследования показали, что мелкодисперсный золь гидроокиси алюминия, образующийся в первый момент времени коагуляции, характеризуется максимально высокой сорбционной активностью. Поэтому особенно важно обеспечить быстрое и равномерное смешение коагулянта со всем объемом очищаемой воды.
Ниже приведены примеры таких испытаний.
Пример 1.
В полиэтиленовую емкость объемом 6 литров с водопроводной водой прибавляют 1 мл коагулянта ОХА с содержанием 0,17 г Al2(OH)5Cl и тщательно перемешивают встряхиванием. Наблюдается коагуляция примесей и хлопьеобразование. При этом происходит химическое взаимодействие ОХА с солями временной жесткости и перевод их в осадок CaCO3 и MgCO3.
Одновременно протекает взаимодействие ОХА с солями постоянной жесткости, сульфатами CaSO4 и MgSO4 с образованием нерастворимого осадка - [Al2(OH)5]2SO4.
Очищенная вода практически не содержит сульфатов металлов.
Далее в объем воды добавляют 1 мл насыщенного раствора пищевой соды и также тщательно перемешивают для связывания избытка коагулянта и ускорения образования осадка.
Пример 2.
Отличался от примера 1 лишь объемами очищаемой водопроводной воды - 60 литров и соответственно объемами используемых реагентов ОХА и соды по 10 мл каждого.
Пример 3.
Отличался от примера 1 лишь объемами очистки природной воды - 1,5 л и соответственно используемых реагентов ОХА и соды по 0,25 мл каждого.
Учитывая столь малые объемы применяемых реагентов, было определено содержание капель в 1 мл раствора из стандартного одноразового шприца (с калибровкой на - 2 миллилитра), без использования иглы. Измерения показали, что в 1 миллилитре воды содержится 20 капель по 0,05 мл.
Таким образом, для получения 1,5 л питьевой воды из природных источников в походных условиях или в чрезвычайных ситуациях, достаточно использовать по 5 капель соответствующих реагентов для обеспечения безопасности воды для здоровья.
Наличие в аптечке флаконов по 20 мл каждого из реагентов может обеспечить питьевую воду из природных источников объемом 120 литров.
Результаты анализа питьевой воды представлены в таблице 2.
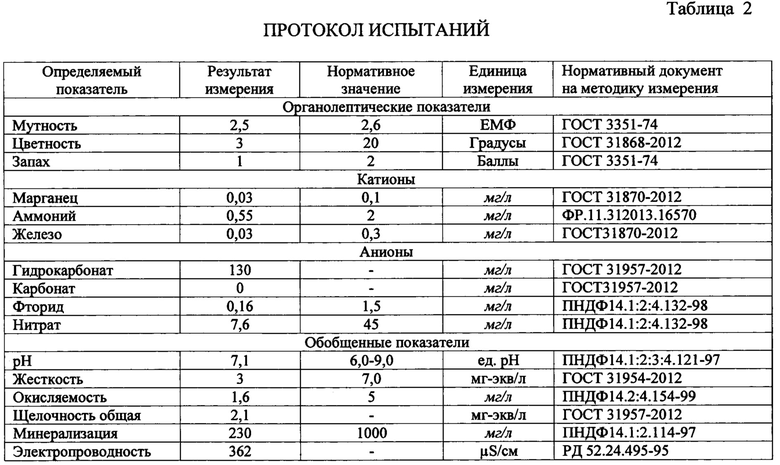
Проба воды по исследованным санитарно-химическим показателям соответствует СанПиН 2.1.4.10745-01 «Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения».
Результаты анализов образца говорят о высоком качестве воды, переданной для анализа.
Дополнительные меры по водоподготовке не требуются, вода может быть использована как питьевая без ограничений (ХАЦ ф-та почвоведения МГУ им. М.В. Ломоносова).
Технический результат заявленного изобретения заключается в обеспечении приготовления питьевой воды, соответствующей нормативным требованиям в походных условиях и чрезвычайных ситуациях.
К важным преимуществам применения экспресс-метода следует также отнести отсутствие необходимости в проведении предварительного аппаратурного анализа качества природной воды и возможной передозировки используемых химических реагентов.
Литература
1. Ксенофонтов Б.С. Водопользование и очистка промстоков // Безопасность жизнедеятельности. - 2003. - №9. - С. 1-10.
2. Алексеева Л.П. Оценка эффективности применения оксихлорида алюминия по сравнению с другими коагулянтами. Журнал «ВСТ» №2, 2003 г.
Изобретение относится к химическим средствам обработки воды из природных источников и может быть использовано в питьевом водоснабжении в быту или в полевых условиях. Экспресс-метод приготовления воды из природных источников в полевых условиях и в чрезвычайных ситуациях включает обработку воды коагулянтом и содой. Сначала к воде при перемешивании прибавляют раствор коагулянта - высокоосновного оксихлорида алюминия - Al2(ОН)5Cl, а затем - пищевую соду NaHCO3 в эквимолярном соотношении к коагулянту. Изобретение позволяет обеспечить приготовление питьевой воды, соответствующей нормативным требованиям, в походных условиях и чрезвычайных ситуациях. 2 табл., 3 пр.
Экспресс-метод приготовления питьевой воды из природных источников в полевых условиях и в чрезвычайных ситуациях, включающий обработку воды химическими реагентами, коагулянтом и содой, отличающийся тем, что сначала к воде при перемешивании прибавляют раствор коагулянта - высокоосновного оксихлорида алюминия Al2(OH)5Cl, а затем - пищевую соду NaHCO3, в эквимолярном соотношении к коагулянту.
| КИЧИГИН А., БАТКИБЕКОВА М.Б., ДЖУНУШЛИЕВА Т.Ш., Быстрый метод очистки питьевой воды, Известия КГТУ им | |||
| И | |||
| Раззакова, 2014, N 31, c | |||
| Приспособление для подачи воды в паровой котел | 1920 |
|
SU229A1 |
| СОСТАВ ДЛЯ ОБРАБОТКИ ПРОМЫШЛЕННЫХ И БЫТОВЫХ СТОЧНЫХ ВОД | 1997 |
|
RU2114068C1 |
| DE 0019704953 A1, 13.08.1998 | |||
| ЕВСЮТИН А.В., Исследование и совершенствование технологии предварительной очистки воды с использованием оксихлоридов алюминия, Автореферат диссертации на соискание ученой степени кандидата технических наук, Москва, 2009, с | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ДОМНИН К.В | |||
| и др., Обеспечение населения качественной питьевой водой в условиях чрезвычайной ситуации, Водоснабжение и санитарная техника, 2007, N6, ч | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
Авторы
Даты
2017-10-19—Публикация
2016-01-18—Подача