Предлагаемое изобретение относится к исследованиям биологических образцов с применением оптической микроскопии и нанотехнологий и может быть использовано для определения локализации одиночных фосфоресцентных наночастиц или их дискретных агрегатов, нанесенных на биологические образцы, и времени жизни их фотолюминесценции при мультиплексном маркировании.
В настоящее время широкое распространение получили микроскопические исследования различных биологических образцов с целью получения информации о молекулярных процессах, происходящих в них, например, таких как перемещение отдельных молекул при передаче клеточных сигналов. Общий алгоритм исследования включает маркировку биообразца фосфоресцентными метками, их визуализацию с использованием лазерной сканирующей микроскопии и определение времени жизни фотолюминесценции. Однако актуальной остается разработка новых способов исследования для получения более точной и ценной научной информации.
Известен способ микроскопического исследования биологических образцов, основанный на применении флуоресцентного маркирования с молекулярной специфичностью, которое обычно реализуется с использованием органических флуоресцентных красителей. Использование флуоресцентных зондов позволяет визуализировать клеточные и тканевые компоненты, такие как внеклеточный матрикс, органеллы и биомолекулы, проводить исследования белок-белковых взаимодействий, а также анализировать перемещения отдельных молекул при передаче клеточных сигналов [Moerner, W.Е. Proceedings of the National Academy of Sciences, 2007, 104, 12596].
Однако многие известные молекулярные флуорофоры весьма чувствительны к биохимическому окружению. При этом взаимодействие с окружением может приводить к уширению спектров, мерцанию или тушению флуоресценции. Эти недостатки существенно ограничивают применение таких молекулярных маркеров [Gomez, D.Е.; van Embden, J.; Jasieniak, J.; Smith, T.A.; Mulvaney, P. Small, 2006, 2, 204].
Для частичного решения указанных проблем применяют фотолюминесцентные наночастицы, такие как квантовые точки и наноалмазы. Однако применяемые квантовые точки обладают высокой квантовой эффективностью, узкими и перестраиваемыми спектрами, но при этом испускание квантовых точек характеризуется мерцанием и сами они имеют высокую биологическую токсичность [Edmonds, А.М.; Sobhan, М.А.; Sreenivasan, V.K.A.; Grebenik, Е.A.; Rabeau, J.R.; Goldys, E.M; Zvyagin, A.V. Particle & Particle Systems Characterization, 2013, 30]; наноалмазы нетоксичны, но интенсивность их излучения намного слабее интенсивности излучения квантовых точек [Yu, S.J.; Kang, М.W.; Chang, H.С; Chen, K.М.; Yu, Y.С. Journal of the American Chemical Society, 2005, 127, 17604; Sreenivasan, V.; Zvyagin, A.; Goldys, E. Journal of physics. Condensed matter: an Institute of Physics journal, 2013, 25, 194101].
Известно фотолюминесцентное маркирование с использованием молекулярных флуорофоров и наночастиц. К недостаткам их использования можно отнести наличие сильного фонового излучения клеток и биологических тканей. Известно, что вклад автофлуоресценции может быть частично подавлен при использовании спектральной фильтрации. Однако этого недостаточно для исследования бимолекулярных процессов, таких как перемещение отдельных молекул при передаче клеточных сигналов.
Известно использование наноразмерных антистоксовых 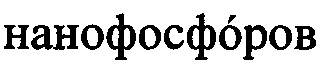 (НАФ) для маркирования биологических объектов. В отличие от традиционных молекулярных флуорофоров НАФ имеют практически неограниченную фотостабильность, уникальные фотофизические свойства, позволяющие преодолеть шумовой вклад автофлуоресценции за счет апконверсии - преобразования энергии света средней интенсивности, поглощенного в инфракрасной области, в свет с большей энергией в видимом и ближнем инфракрасном диапазонах. Кроме того, НАФ имеют большие времена жизни фотолюминесценции, превышающие времена жизни флуоресценции органических красителей и эндогенных флуорофоров. Причем время жизни фотолюминесценции НАФ является параметром, зависящим от окружения наночастиц. Это позволяет эффективно использовать НАФ при мультиплексном маркировании [Lu, Y.Q.; Zhao, J.В.; Zhang, R; Liu, Y.J.; Liu, D.M; Goldys, E.M; Yang, X.S.; Xi, P.; Sunna, A.; Lu, J.; Shi, Y.; Leif, R.C; Huo, Y.J.; Shen, J.; Piper, J.A.; Robinson, J.P.; Jin, D.Y. Nature Photonics, 2014, 8, 33].
(НАФ) для маркирования биологических объектов. В отличие от традиционных молекулярных флуорофоров НАФ имеют практически неограниченную фотостабильность, уникальные фотофизические свойства, позволяющие преодолеть шумовой вклад автофлуоресценции за счет апконверсии - преобразования энергии света средней интенсивности, поглощенного в инфракрасной области, в свет с большей энергией в видимом и ближнем инфракрасном диапазонах. Кроме того, НАФ имеют большие времена жизни фотолюминесценции, превышающие времена жизни флуоресценции органических красителей и эндогенных флуорофоров. Причем время жизни фотолюминесценции НАФ является параметром, зависящим от окружения наночастиц. Это позволяет эффективно использовать НАФ при мультиплексном маркировании [Lu, Y.Q.; Zhao, J.В.; Zhang, R; Liu, Y.J.; Liu, D.M; Goldys, E.M; Yang, X.S.; Xi, P.; Sunna, A.; Lu, J.; Shi, Y.; Leif, R.C; Huo, Y.J.; Shen, J.; Piper, J.A.; Robinson, J.P.; Jin, D.Y. Nature Photonics, 2014, 8, 33].
Однако ввиду того, что НАФ имеют очень большие времена жизни фотолюминесценции (в масштабе миллисекунд), поточечная запись сигнала при получении изображения образцов, маркированных НАФ, требует накопления фотолюминесцентного сигнала в каждой точке (пикселе) в течение времени, сравнимого со временем жизни НАФ, т.е. в масштабе миллисекунд. Это делает общее время записи сканированного изображения непрактично долгим. А при более быстром сканировании изображения наночастиц имеют вид вытянутых вдоль быстрой оси сканирования пятен, в результате чего теряется информативность при маркировании.
Наиболее близким к предлагаемому способу по совокупности существенных признаков и техническому результату, выбранному в качестве прототипа предлагаемого изобретения, является способ микроскопического исследования биологических образцов, маркированных фосфоресцентными зондами in vitro, включающий мультиплексное маркирование биологического образца фосфоресцентными материалами, их визуализацию и определение времени жизни фотолюминесценции с использованием лазерной сканирующей микроскопии [Pominova D.V., Ryabova A.V., Grachev P.V., Romanishkin I.D., Kuznetsov S.V., Rozhnova J.A., Yasyrkina D.S., Fedorov P.P., Loschenov V.B. Upconversion microparticles as time-resolved luminescent probes for multiphoton microscopy: desired signal extraction from the streaking effect // J. Biomed. Optics. 2016. Vol. 21(9). 096002-1-9].
Известный способ осуществляют следующим образом.
Антистоксовые микрочастицы, основанные на фторидной матрице, легированной 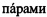 редкоземельных ионов Yb3+-Er3+ и Yb3+-Tm3+, наносят на исследуемый биобразец. Осуществляют визуализацию антистоксовых микрочастиц с использованием лазерного сканирующего микроскопа (LSM-710 NLO, Carl Zeiss, Германия). При этом возбуждение микрочастиц осуществляют импульсным фемтосекундным лазером (Chameleon Ultra II, Coherent, США) на длине волны 980 нм. Далее с использованием воздушного неиммерсионного объектива с 20-кратным увеличением сканируют образец, при скорости сканирования в диапазоне 1.27-3.15 мкс/пикс. Регистрацию фотолюминесцентного сигнала осуществляют с использованием недесканирующих детекторов (NDD) в трех спектральных диапазонах: 400-490 нм, 490-560 нм и 565-700 нм соответственно. Полученное изображение раскладывают на строки с шагом в один пиксель вдоль быстрой оси сканирования. В каждой строке определяют положение микрочастицы как точку с максимальной яркостью и границы ее сигнала. Полученную последовательность (профиль сигнала, заключающийся в указанных пределах) аппроксимируют с использованием функции рассеяния точки (ФРТ) вида:
редкоземельных ионов Yb3+-Er3+ и Yb3+-Tm3+, наносят на исследуемый биобразец. Осуществляют визуализацию антистоксовых микрочастиц с использованием лазерного сканирующего микроскопа (LSM-710 NLO, Carl Zeiss, Германия). При этом возбуждение микрочастиц осуществляют импульсным фемтосекундным лазером (Chameleon Ultra II, Coherent, США) на длине волны 980 нм. Далее с использованием воздушного неиммерсионного объектива с 20-кратным увеличением сканируют образец, при скорости сканирования в диапазоне 1.27-3.15 мкс/пикс. Регистрацию фотолюминесцентного сигнала осуществляют с использованием недесканирующих детекторов (NDD) в трех спектральных диапазонах: 400-490 нм, 490-560 нм и 565-700 нм соответственно. Полученное изображение раскладывают на строки с шагом в один пиксель вдоль быстрой оси сканирования. В каждой строке определяют положение микрочастицы как точку с максимальной яркостью и границы ее сигнала. Полученную последовательность (профиль сигнала, заключающийся в указанных пределах) аппроксимируют с использованием функции рассеяния точки (ФРТ) вида:
h(x,y)=(-Aexp(-y/vτr)+Bexp(-y/vτd))∫δ(x)dx,
где v - скорость сканирования вдоль быстрой оси сканирования, τr и τd - времена роста и спада антистоксовой фотолюминесценции, А и В - коэффициенты, δ(х) - дельта функция Дирака. Определяют параметры ФРТ, затем осуществляют восстановление изображения методом Люси-Ричардсона.
Однако известный способ имеет следующие недостатки:
- большой размер антистоксовых микрочастиц осложняет и/или препятствует их проникновению внутрь клетки;
- чувствительность известного способа ограничена, с одной стороны, за счет увеличения вклада автофлуоресценции, возбуждаемой фемтосекундным лазером, используемым для возбуждения антистоксовой люминесценции, с другой стороны, низкоапертурный воздушный объектив, используемый в известном способе, имеет низкое разрешение, которое не позволяет наблюдать одиночные наноразмерные и даже субмикронные частицы;
- получаемые изображения имеют большую зашумленность, так как в известном способе сканирование осуществляют со скоростью 1.27-3.15 мкс/пикс, превышающей оптимальную скорость, применяемую для достижения оптимального соотношения сигнал/шум (около 10 мкс/пикс).
Вышеуказанные недостатки снижают точность и достоверность определения времени жизни фотолюминисценции и локализации наночастиц.
Задачей предлагаемого изобретения является создание способа микроскопического исследования биологических образцов, маркированных фосфоресцентными зондами in vitro, лишенного недостатков прототипа.
Технический результат предлагаемого способа заключается в:
- увеличении чувствительности при визуализации фосфоресцентных наночастиц, нанесенных на биологические образцы;
- уменьшении вклада шумовой компоненты (увеличении отношения сигнал/шум);
- увеличении точности определения локализации дискретных фосфоресцентных наночастиц и их агрегатов на биологических образцах;
- увеличении точности определения времени жизни фотолюминесценции дискретных фосфоресцентных наночастиц и их агрегатов, нанесенных на биологические образцы по изображению.
Технический результат достигается тем, что в известном способе микроскопического исследования биологических образцов, маркированных фосфоресцентными зондами in vitro, включающем мультиплексное маркирование биологического образца фосфоресцентным материалом, их визуализацию и определение времени жизни фотолюминесценции с использованием лазерной сканирующей микроскопии, для мультиплексного маркирования биологического образца используют наноразмерные антистоксовые 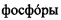 (НАФ), имеющие размер, не превышающий 200 нм, которые возбуждают непрерывным ИК-лазером с длиной волны 980 нм, полученное с использованием лазерного сканирующего микроскопа изображение обрабатывают в два этапа, на первом этапе обработку осуществляют вдоль медленной оси сканирования, на втором этапе обработку осуществляют вдоль быстрой оси сканирования.
(НАФ), имеющие размер, не превышающий 200 нм, которые возбуждают непрерывным ИК-лазером с длиной волны 980 нм, полученное с использованием лазерного сканирующего микроскопа изображение обрабатывают в два этапа, на первом этапе обработку осуществляют вдоль медленной оси сканирования, на втором этапе обработку осуществляют вдоль быстрой оси сканирования.
Предлагаемое изобретение отвечает критериям «новизна» и «изобретательский уровень», так как проведенные патентно-информационные исследования не выявили источников научно-технической литературы и патентной документации, которые бы прочили новизну предлагаемого способа, равно как и технических решений с существенными признаками предлагаемого способа.
Технический результат предлагаемого способа заключается в:
- увеличении чувствительности при визуализации фосфоресцентных наночастиц, нанесенных на биологические образцы;
- уменьшении вклада шумовой компоненты (увеличении отношения сигнал/шум);
- увеличении точности определения локализации дискретных фосфоресцентных наночастиц и их агрегатов на биологических образцах;
- увеличении точности определения времени жизни фотолюминесценции дискретных фосфоресцентных наночастиц и их агрегатов нанесенных на биологические образцы по изображению.
Предлагаемый способ поясняется графическим материалом.
На фиг. 1 на примере одномерного сигнала фотолюминесценции ряда антистоксовых 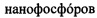 представлены результаты работы заявленного способа микроскопического исследования биологических образцов, основанного на определении времени жизни фотолюминесценции и локализации антистоксовых
представлены результаты работы заявленного способа микроскопического исследования биологических образцов, основанного на определении времени жизни фотолюминесценции и локализации антистоксовых 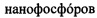 по их изображению.
по их изображению.
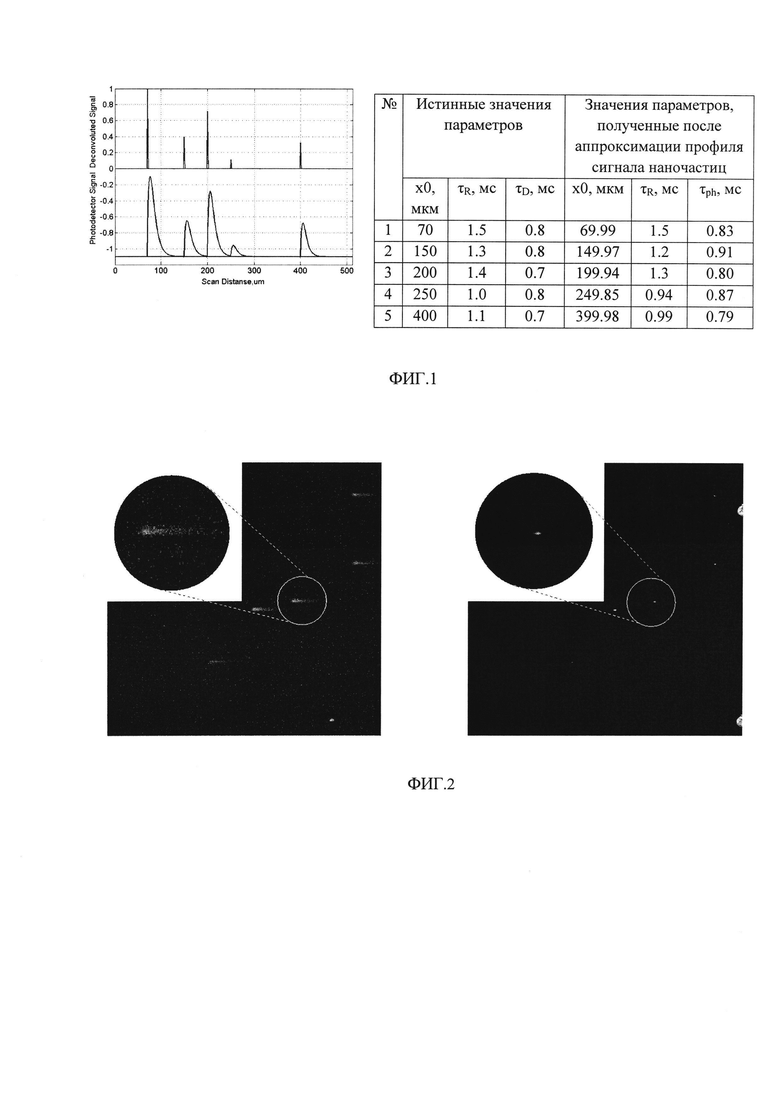
На фиг. 2 представлено двумерное изображение смоделированного сигнала фотолюминесценции ряда дискретных фосфоресцентных наночастиц (левая панель) и восстановленное с использованием заявляемого способа изображение (правая панель). Во вставках показаны увеличенные изображения областей, обведенных на изображении белыми окружностями. Чтобы продемонстрировать чувствительность используемого алгоритма восстановления к изображению, был добавлен случайный шум. Следует отметить, что в результате деконволюции существенно уменьшается размер изображения и наблюдается значительное увеличения отношения сигнал/шум. Последний эффект демонстрируется отсутствием шума на восстановленном изображении.
На фиг. 3 представлены результаты работы заявляемого способа исследования биологических образцов, маркированных фосфоресцентными наноматериалами, на примере изображения среза печени (пример конкретного исполнения). Получение изображений осуществлялось при сканировании лазерного луча со скоростью около 10 см/с и времени записи сигнала с одной точки около 10 мкс. Рассматриваемый образец представлял собой тонкий срез ткани печени, выделенной из лабораторной мыши через три часа после инъекции биологически-совместимых нанокомплексов антистоксовых 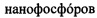 , подготовленных в фосфатно-солевом растворе.
, подготовленных в фосфатно-солевом растворе.
После выделения ткань печени фиксировалась 10% нейтральным забуференным формалином на протяжении 48 часов. После этого ткань дегидратировалась в серии спиртовых растворов, помещалась в парафин и нарезалась на срезы с толщиной около 5 мкм.
На фиг. 3а представлено наложение изображения среза печени, полученного в режиме проходящего света (показано серым цветом) и фотолюминесцентного изображения 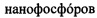 (показаны зеленым цветом), локализовавшихся в печени после внутривенной инъекции. Масштабный отрезок - 50 мкм. На фиг. 3b, с показаны графики поверхности исходного (b) и восстановленного в результате деконволюции (с) изображения тех же фотолюминесцентных наночастиц на печени, что и на (а). Полученное время жизни фотолюминесценции наночастиц, накопившихся в печени лабораторной мыши, составляло 0,4-0,8 мс.
(показаны зеленым цветом), локализовавшихся в печени после внутривенной инъекции. Масштабный отрезок - 50 мкм. На фиг. 3b, с показаны графики поверхности исходного (b) и восстановленного в результате деконволюции (с) изображения тех же фотолюминесцентных наночастиц на печени, что и на (а). Полученное время жизни фотолюминесценции наночастиц, накопившихся в печени лабораторной мыши, составляло 0,4-0,8 мс.
Предлагаемый способ осуществляют следующим образом.
Биологически .овместимые нанокомплексы антистоксовых 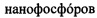 , имеющие размер, не превышающий 200 нм, наносят на исследуемый образец (срез ткани или культуру клеток) и возбуждают непрерывным ИК-лазером с длиной волны 980 нм. При этом наночастицы распределяются по образцу, связываясь с определенными участками. Взаимодействие наночастиц с окружающими молекулами сопровождается изменением времени жизни их фотолюминесценции.
, имеющие размер, не превышающий 200 нм, наносят на исследуемый образец (срез ткани или культуру клеток) и возбуждают непрерывным ИК-лазером с длиной волны 980 нм. При этом наночастицы распределяются по образцу, связываясь с определенными участками. Взаимодействие наночастиц с окружающими молекулами сопровождается изменением времени жизни их фотолюминесценции.
Полученные биологические образцы исследуют с помощью лазерного сканирующего микроскопа.
Изображения получают при следующих настройках микроскопа:
Антистоксовые 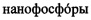 возбуждают непрерывным ИК-лазером с длиной волны 980 нм.
возбуждают непрерывным ИК-лазером с длиной волны 980 нм.
Сигнал фотолюминесценции антистоксовых нанофосфоров регистрируют с использованием недесканирующего режима детектирования (NDD-режим).
При помощи оптических фильтров выделяют спектральный диапазон детектирования, соответствующий спектральному диапазону испускания фотолюминесценции используемых для маркирования антистоксовых наночастиц. При использовании наночастиц, легированных Tm3+, регистрацию сигнала осуществляют в спектральных диапазонах 445-485 нм и 790-810 нм, при легировании Er3+ - 500-550 нм.
При этом для получения изображений отдельных наночастиц и их агрегатов, распределенных по исследуемому биологическому образцу, используют высокоапертурный иммерсионный объектив (например, Apochromat 63х/1.2 W).
Для получения информации о морфологии образца используют лазер с длиной волны 405 нм, который эффективно возбуждает эндогенные флуорофоры. Сигнал автофлуоресценции исследуемого биологического образца собирают в отдельном треке, чтобы исключить наложение сигналов автофлуоресценции и фотолюминесценции наночастиц.
Размер получаемого изображения ограничивают задаваемым количеством пикселей (например, 512×512 пикс).
Выбирают оптимальную скорость сканирования (около 10 мкс/пикс), при которой достигается максимальное соотношение сигнал/шум. Сканирование с такой скоростью реализуют при возбуждении лазерным лучом с интенсивностью большей, чем плотность энергии насыщения антистоксовых нанофосфоров (>0.1 Дж × см-2).
Полученные изображения сохраняют в доступном формате и экспортируют для последующей обработки с использованием специального алгоритма, реализованного в программном пакете Матлаб.
Исходя из того, что время сканирования одной строки соизмеримо либо гораздо больше времени жизни используемых для маркирования антистоксовых 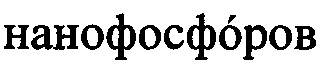 , в предлагаемом способе изображение представляют в виде массива, состоящего из последовательности строк, каждая из которых содержит одномерный профиль сигнала вдоль быстрой оси сканирования.
, в предлагаемом способе изображение представляют в виде массива, состоящего из последовательности строк, каждая из которых содержит одномерный профиль сигнала вдоль быстрой оси сканирования.
К полученному таким образом массиву применяют последовательную двухэтапную обработку с использованием алгоритма деконволюции. При этом обработку осуществляют сначала вдоль медленной (варьируя номер строки), затем вдоль быстрой оси сканирования (варьируя номер столбца).
Обработка вдоль медленной оси сканирования включает деконволюцию с использованием Гауссиана в качестве импульсной функции, описывающей нормальное распределение сигнала вдоль медленной оси сканирования. Данная процедура позволяет ограничить строки, в которых содержится сигнал фотолюминесценции наночастиц и существенно уменьшить вклад шумовой компоненты.
Обработку изображения вдоль быстрой оси сканирования осуществляют в выбранных строках с использованием следующего алгоритма:
1) выполняют поиск локальных максимумов среди элементов строки. При этом для осуществления поиска точного расположения наночастиц задают порог, представляющий собой минимальную интенсивность пика (МРН, Min Peak Height);
2) ограничивают (находят начало и конец) каждый из обнаруженных пиков;
3) выполняют аппроксимацию каждого из пиков с использованием функции рассеяния точки (ФРТ), описывающей рост и последующий спад фотолюминесцентного сигнала. При этом сигнал фотолюминесценции 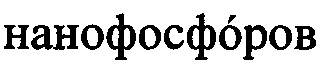 аппроксимируется функцией, представленной в общем виде как:
аппроксимируется функцией, представленной в общем виде как:
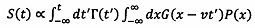 ,
,
где G представляет собой распределение интенсивности возбуждающего лазерного луча и описывает распространение бегущей волны в положительном направлении оси x со скоростью v. Данное распределение интенсивности описывается функцией Гаусса с перетяжкой пучка w, которая равна диаметру сфокусированного луча:
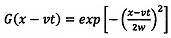 ;
;
Р(х) - исследуемый профиль сигнала фотолюминесценции; Г(t) - зависимость фотолюминесценции наночастиц от времени, описываемая функцией вида [Hehlen, М.P.; Kuditcher, A.; Lenef, A.L.; Ni, Н.; Shu, Q.; Rand, S.С; Rai, J.; Rai, S. Physical Review В 2000, 61, 1116]:
Г(t)=-A exp(-t/τR)+В exp(-t/τph),
где τR - характерное время апконверсионного переноса энергии; τph - время жизни фотолюминесценции антистоксовых 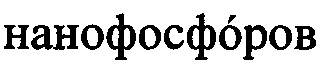 .
.
Таким образом, детектируемый сигнал S(t) является наложением поверхностного профиля сигнала наночастиц и функции временного спада интенсивности фотолюминесценции Г(t):
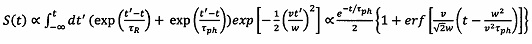 ,
,
где erƒ - функция ошибки.
Функция S является более точной импульсной функцией по сравнению с используемой в известном способе, которую используют для дальнейшей деконволюции.
4) используя полученные в результате аппроксимации профиля сигнала параметры (tR и τph), выполняют деконволюцию профиля с использованием алгоритма Лиси-Ричардсона, реализованного в среде Матлаб;
5) сохраняют параметры в таблицу с результатами и переходят к следующей строке. Для предотвращения потери сигнала крупных частиц, а также вклада долговременного шума контролируют наличие корреляции между соседними строками.
Пример конкретного исполнения дан в виде выписки из протокола эксперимента.
Биологически совместимые нанокомплексы антистоксовых 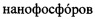 , имеющие размер, не превышающий 200 нм, наносят на исследуемый образец (печень белой мыши) и возбуждают непрерывным ИК-лазером с длиной волны 980 нм. При этом наночастицы распределяются по образцу, связываясь с определенными участками. Взаимодействие наночастиц с окружающими молекулами сопровождается изменением времени жизни их фотолюминесценции.
, имеющие размер, не превышающий 200 нм, наносят на исследуемый образец (печень белой мыши) и возбуждают непрерывным ИК-лазером с длиной волны 980 нм. При этом наночастицы распределяются по образцу, связываясь с определенными участками. Взаимодействие наночастиц с окружающими молекулами сопровождается изменением времени жизни их фотолюминесценции.
Полученные биологические образцы исследуют с помощью лазерного сканирующего микроскопа.
Изображения получают при следующих настройках микроскопа:
Антистоксовые 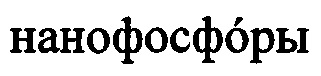 возбуждают непрерывным ИК-лазером с длиной волны 980 нм.
возбуждают непрерывным ИК-лазером с длиной волны 980 нм.
Сигнал фотолюминесценции антистоксовых нанофосфоров регистрируют с использованием недесканирующего режима детектирования (NDD-режим).
При помощи оптических фильтров выделяют спектральный диапазон детектирования, соответствующий спектральному диапазону испускания фотолюминесценции используемых для маркирования антистоксовых наночастиц. При использовании наночастиц, легированных Tm3 , регистрацию сигнала осуществляют в спектральных диапазонах 445-485 нм и 790-810 нм, при легировании Er3+ - 500-550 нм.
При этом для получения изображений отдельных наночастиц и их агрегатов, распределенных по исследуемому биологическому образцу, используют высокоапертурный иммерсионный объектив (например, Apochromat 63x/1.2 W).
Для получения информации о морфологии образца используют лазер с длиной волны 405 нм, который эффективно возбуждает эндогенные флуорофоры. Сигнал автофлуоресценции исследуемого биологического образца собирают в отдельном треке, чтобы исключить наложение сигналов автофлуоресценции и фотолюминесценции наночастиц.
Размер получаемого изображения ограничивают задаваемым количеством пикселей (например, 512×512 пикс).
Выбирают оптимальную скорость сканирования (около 10 мкс/пикс), при которой достигается максимальное соотношение сигнал/шум. Сканирование с такой скоростью реализуют при возбуждении лазерным лучом с интенсивностью большей, чем плотность энергии насыщения антистоксовых 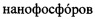 (>0.1 Дж × см-2).
(>0.1 Дж × см-2).
Полученные изображения сохраняют в доступном формате и экспортируют для последующей обработки с использованием специального алгоритма, реализованного в программном пакете Матлаб.
Исходя из того, что время сканирования одной строки соизмеримо либо гораздо больше времени жизни используемых для маркирования антистоксовых 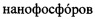 , в предлагаемом способе изображение представляют в виде массива, состоящего из последовательности строк, каждая из которых содержит одномерный профиль сигнала вдоль быстрой оси сканирования.
, в предлагаемом способе изображение представляют в виде массива, состоящего из последовательности строк, каждая из которых содержит одномерный профиль сигнала вдоль быстрой оси сканирования.
К полученному таким образом массиву применяют последовательную двухэтапную обработку с использованием алгоритма деконволюции. При этом обработку осуществляют сначала вдоль медленной (варьируя номер строки), затем вдоль быстрой оси сканирования (варьируя номер столбца).
Обработка вдоль медленной оси сканирования включает деконволюцию с использованием Гауссиана в качестве импульсной функции, описывающей нормальное распределение сигнала вдоль медленной оси сканирования. Данная процедура позволяет ограничить строки, в которых содержится сигнал фотолюминесценции наночастиц и существенно уменьшить вклад шумовой компоненты.
Обработку изображения вдоль быстрой оси сканирования осуществляют в выбранных строках с использованием следующего алгоритма:
1) выполняют поиск локальных максимумов среди элементов строки. При этом для осуществления поиска точного расположения наночастиц задают порог, представляющий собой минимальную интенсивность пика (МРН, Min Peak Height);
2) ограничивают (находят начало и конец) каждый из обнаруженных пиков;
3) выполняют аппроксимацию каждого из пиков с использованием функции рассеяния точки (ФРТ), описывающей рост и последующий спад фотолюминесцентного сигнала. При этом сигнал фотолюминесценции 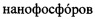 аппроксимируется функцией, представленной в общем виде как:
аппроксимируется функцией, представленной в общем виде как:
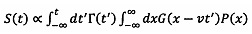 ,
,
где G представляет собой распределение интенсивности возбуждающего лазерного луча и описывает распространение бегущей волны в положительном направлении оси x со скоростью v. Данное распределение интенсивности описывается функцией Гаусса с перетяжкой пучка w, которая равна диаметру сфокусированного луча:
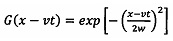 ;
;
Р(х) - исследуемый профиль сигнала фотолюминесценции 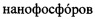 ; Г(t) -зависимость фотолюминесценции наночастиц от времени, описываемая функцией вида [Hehlen, М.P.; Kuditcher, A.; Lenef, A.L.; Ni, Н.; Shu, Q.; Rand, S.С; Rai, J.; Rai, S. Physical Review В 2000, 61, 1116]:
; Г(t) -зависимость фотолюминесценции наночастиц от времени, описываемая функцией вида [Hehlen, М.P.; Kuditcher, A.; Lenef, A.L.; Ni, Н.; Shu, Q.; Rand, S.С; Rai, J.; Rai, S. Physical Review В 2000, 61, 1116]:
Г(t)=-А ехр(-t/τR)+В exp(-t/τph),
где τR - характерное время апконверсионного переноса энергии; τph - время жизни фотолюминесценции антистоксовых 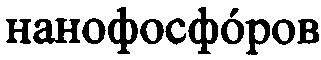 .
.
Таким образом, детектируемый сигнал S(t) является наложением поверхностного профиля сигнала наночастиц и функции временного спада интенсивности фотолюминесценции Г(t):
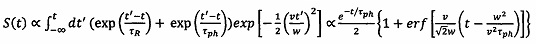 ,
,
где erƒ - функция ошибки.
Функция S является более точной импульсной функцией, по сравнению с используемой в известном способе, которую используют для дальнейшей деконволюции.
4) используя полученные в результате аппроксимации профиля сигнала параметры (τR и τph), выполняют деконволюцию профиля с использованием алгоритма Лиси-Ричардсона, реализованного в среде Матлаб;
5) сохраняют параметры в таблицу с результатами и переходят к следующей строке. Для предотвращения потери сигнала крупных частиц, а также вклада долговременного шума контролируют наличие корреляции между соседними строками.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ВИЗУАЛИЗАЦИИ ПАТОЛОГИЧЕСКИХ ОЧАГОВ | 2012 |
|
RU2544094C2 |
| Способ получения функционализированных визуализирующих агентов с антистоксовой фотолюминесценцией на основе полиакролеиновых дисперсий | 2014 |
|
RU2607587C2 |
| СПОСОБ МНОГОАНАЛИТНОГО ИММУНОАНАЛИЗА С ИСПОЛЬЗОВАНИЕМ МИКРОЧАСТИЦ | 2008 |
|
RU2379691C1 |
| СПОСОБ ДИАГНОСТИКИ ДЕФЕКТОВ НА МЕТАЛЛИЧЕСКИХ ПОВЕРХНОСТЯХ | 2014 |
|
RU2581441C1 |
| СПОСОБ МНОГОАНАЛИТНОГО ИММУНОАНАЛИЗА С ИСПОЛЬЗОВАНИЕМ МИКРОЧАСТИЦ | 2007 |
|
RU2339953C1 |
| ПРИБОР ДЛЯ ФОТОЛЮМИНЕСЦЕНТНОГО КАРТОГРАФИРОВАНИЯ ПОЛУПРОВОДНИКОВЫХ ПЛАСТИН (ВАРИАНТЫ) | 2000 |
|
RU2172946C1 |
| МНОГОКАНАЛЬНЫЙ ОПТОВОЛОКОННЫЙ НЕЙРОИНТЕРФЕЙС ДЛЯ МУЛЬТИМОДАЛЬНОЙ МИКРОСКОПИИ МОЗГА ЖИВОТНЫХ | 2014 |
|
RU2584922C1 |
| СПОСОБ ЗАЩИТЫ ОТ ПОДДЕЛОК И КОНТРОЛЯ ПОДЛИННОСТИ ЦЕННЫХ ИЗДЕЛИЙ | 2006 |
|
RU2359328C2 |
| СПОСОБ ПРИМЕНЕНИЯ ФИКОБИЛИПРОТЕИНОВ В КАЧЕСТВЕ ОПТИЧЕСКИХ СЕНСОРОВ ЛОКАЛЬНОЙ ТЕМПЕРАТУРЫ В ЖИВЫХ КЛЕТКАХ И ТКАНЯХ | 2021 |
|
RU2780954C1 |
| СПОСОБ ДЕТЕКЦИИ ЛОКАЛЬНОЙ ТЕМПЕРАТУРЫ В ЖИВЫХ КЛЕТКАХ И ПОСТРОЕНИЯ ТЕМПЕРАТУРНЫХ КАРТ ЖИВЫХ КЛЕТОК | 2022 |
|
RU2799016C1 |

Изобретение относится к медицине и может быть использовано для микроскопического исследования биологических образцов, маркированных фосфоресцентными зондами in vitro. При этом проводят мультиплексное маркирование биологического образца фосфоресцентным материалом, их визуализацию и определение времени жизни фотолюминесценции с использованием лазерной сканирующей микроскопии. Для мультиплексного маркирования биологического образца используют наноразмерные антистоксовые фосфоры (НАФ), имеющие размер, не превышающий 200 нм. НАФ возбуждают непрерывным ИК-лазером с длиной волны 980 нм. Полученное с использованием лазерного сканирующего микроскопа изображение обрабатывают в два этапа. На первом этапе обработку осуществляют вдоль медленной оси сканирования. На втором этапе обработку осуществляют вдоль быстрой оси сканирования. Изобретение позволяет увеличить чувствительность при визуализации фосфоресцентных наночастиц, увеличить точность определения локализации и времени жизни фотолюминесценции дискретных фосфоресцентных наночастиц и их агрегатов, нанесенных на биологические образцы. 3 ил.
Способ микроскопического исследования биологических образцов, маркированных фосфоресцентными зондами in vitro, включающий мультиплексное маркирование биологического образца фосфоресцентным материалом, их визуализацию и определение времени жизни фотолюминесценции с использованием лазерной сканирующей микроскопии, отличающийся тем, что для мультиплексного маркирования биологического образца используют наноразмерные антистоксовые фосфоры (НАФ), имеющие размер, не превышающий 200 нм, которые возбуждают непрерывным ИК-лазером с длиной волны 980 нм, полученное с использованием лазерного сканирующего микроскопа изображение обрабатывают в два этапа, на первом этапе обработку осуществляют вдоль медленной оси сканирования, на втором этапе обработку осуществляют вдоль быстрой оси сканирования.
| POMINOVA D.V | |||
| et al | |||
| Upconversion microparticles as time-resolved luminescent probes for multiphoton microscopy: desired signal extraction from the streaking effect, J Biomed Opt | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ВИЗУАЛИЗАЦИИ ПАТОЛОГИЧЕСКИХ ОЧАГОВ | 2012 |
|
RU2544094C2 |
| US 2008105568 A1, 08.05.2008 | |||
| ГРЕБЕНИК Е.А.и др | |||
| Специфическая визуализация опухолевых клеток с помощью антистоксовых нанофосфоров | |||
| Acta Naturae, 2014, т | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
Авторы
Даты
2017-12-05—Публикация
2016-12-07—Подача