Изобретение относится к медицине, а именно к экспериментальной кардиофармакологии, и может быть использовано в комплексной оценке кардиопротективной активности фармакологических средств в экспериментальных группах животных.
Известна оценка влияния кардиотоксичности некоторых лекарственных препаратов с помощью методики регистрации поглощения ионов кальция изолированным сердцем крысы (Заложных Е.А., Пискунова К.А., Гардиенко Т.О//Международный студенческий научный вестник. – 2016. –№ 4 (часть 2)– С. 148-149), которая заключается в регистрации поглощения ионов кальция изолированным сердцем, позволяющей проводить оценку влияния лекарственных средств на работу сердца.
Основным недостатком данного способа является влияние ряда препаратов (пирацетам, верапамил и др.), имеющих высокую чувствительность на процесс Nа+-Ca2+ обмена в сердце крыс, что снижает достоверность результатов.
Также существует способ оценки кардиопротективного действия препаратов при проведении пробы на нагрузку сопротивлением (Меерсон Ф.З. Метаболизм и функция кардиомиоцита, 1984; Кузнецов В.И. Сократительная функция, экстракардиальная регуляция и морфологические изменения в сердце крыс в динамике длительной непрерывно действующей стрессорной ситуации, 1990).
Недостатком этого способа является оценка функциональных возможностей миокарда in vivo по результатам абсолютных показателей левожелудочкового давления (ЛЖД), что при моделировании артериальной гипертензии, сердечной недостаточности, стресса и т.д. неминуемо запускает системные механизмы поддержания гомеостаза и, следовательно, является малоинформативным.
Неинвазивная оценка систолической функции сердца с помощью постоянноволновой допплерэхокардиографии у собак с митральной регургитацией (K. Asano,Y. Masui, K. Masuda, T. Fujinaga.К. // Кардиология. – 2003. – С. 28-30), которая заключалась в том, что хорду митрального клапана дважды рассекли биотомом, введенным в ЛЖ через наружную сонную артерию. С помощью левосторонней вентрикулографии у всех собак оценили выраженность митральной регургитации согласно классификации Seller. Результаты в эксперименте оценивали не ранее чем через 6 месяцев после формирования митральной регургитации.
Недостатком этого способа является длительное время эксперимента, сложность хирургических манипуляций и высокая стоимость оборудования.
Известен способ оценки кардиопротективного действия лекарственных средств по результатам измерения левожелудочкового давления при моделировании артериальной гипертензии (RU № 2194436, опубл. 20.12.2002). Основным недостатком данного способа является то, что данная модель не дает возможности оценить основные важные пути связанные с кардиопротективным эффектом, и не исключает влияние экстракардиальных факторов на сократимость миокарда, и выявляемые нарушения сократительной функции сердца могут быть обусловлены повреждениями самого сердца. Кроме того, в данном способе используется сложная математическая модель.
Известен способ оценки сократимости и метаболизма изолированных сердец при токсических дозах ингибиторов АПФ (Яцинюк Б.Б., Сенцов В.Г., Долгих В.Т., Брусин К.М.//Вестник Уральской медицинской академии наук. – 2010. – № 1– С. 71-75), который заключается в изучении сократимости и метаболизма изолированного сердца крысы по Лангендорфу, при введении токсических доз энапа, с навязыванием сердцу высокого ритма сокращений и гиперкальциевой нагрузкой. Однако дефект диастолы оценивали лишь по показателям сократимости и метаболизма миокарда, не определяя площадь под кривой, как один из информативных и точных показателей, характеризующий повреждение сердца.
Задачей изобретения является создание способа оценки кардиопротективной активности фармакологических средств, позволяющего объективно оценить степень кардиопротективной активности в экспериментальных группах животных.
Поставленная задача решается с помощью предлагаемого способа оценки кардиопротективной активности фармакологических средств, включающего моделирование патологии кардиомиопатии путем введения доксорубицина внутрибрюшинно в дозе 20 мг/кг, через 48 ч оценку показателей сократимости левого желудочка в условиях высокого ритма сокращений 480 уд./мин в течение 15 с на фоне увеличения концентрации Са2+ до 5 ммоль в перфузате на изолированном сердце крыс, кроме того, в качестве дополнительного критерия оценки кардиопротективной активности фармакологических средств используют коэффициент SТТI, отражающий дефект диастолы - площади под кривой подъема конечно-диастолического давления.
Техническим результатом изобретения является информативность и повышение достоверности показателей оценки степени кардиопротективной активности фармакологических средств с помощью коэффициента SТТI.
Для оценки резервных возможностей миокарда использовали индекс «напряжения по времени» Тension-Тime Index (TTI) — показатель изменения механического напряжения миокарда, вычисляемый по кривой динамики внутрижелудочкового давления методом планиметрирования (т.е. измерением площади, заключенной под кривой). Площадь под кривой рассчитывали путем складывания площадей трапеций и которая равна произведению ее высоты на среднюю линию. Коэффициент диастолической дисфункции или дефект диастолы (SТТI) выражали в усл. ед.
В экспериментах на изолированном сердце крыс проводили оценку кардиотоксического действия на доксорубициновой модели патологии (20 мг/кг, внутрибрюшинно) путем навязывания сердцу высокой частоты сокращений (480 уд./мин) в условиях увеличения концентрации Са2+ до 5 ммоль в перфузате. В качестве критерия использован коэффициент STTI. Для этого рассчитывали площадь дефекта диастолы (SТТI) путем оценки площади под кривой подъема конечно-диастолического давления в течение 15 с с навязыванием сердцу высокого ритма сокращений. При этом у интактных крыс STTI равен 1,4±0,1 усл.ед., а у крыс с моделированием патологии 8,3±0,3 усл.ед.
Изобретение поясняется фиг. 1 и 2.
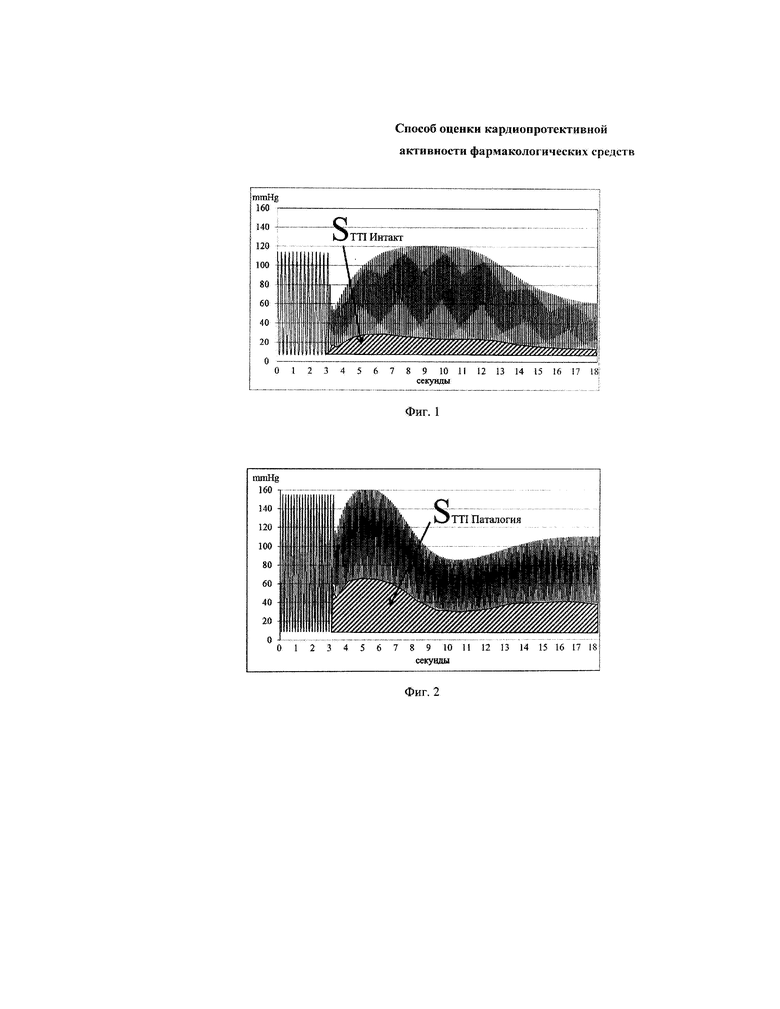
На фиг. 1 продемонстрирована динамика показателей сократимости: левожелудочковое давление (ЛЖД, мм рт.ст.), частота сердечных сокращений (ЧСС, уд./мин), максимальная скорость сокращения (+dP/dtmax, мм рт.ст./c), максимальная скорость расслабления миокарда (-dP/dtmax, мм рт.ст./c), показатели конечного-диастолического давления (КДД) на изолированном сердце у интактных животных путем навязывания сердцу высокого ритма сокращений (480 уд./мин) в условиях увеличения концентрации Са2+ до 5 ммоль в перфузате.
На фиг. 2 продемонстрирована динамика показателей сократимости: левожелудочковое давление (ЛЖД, мм рт.ст.), частота сердечных сокращений (ЧСС, уд./мин), максимальная скорость сокращения (+dP/dtmax, мм рт.ст./c), максимальная скорость расслабления миокарда (-dP/dtmax, мм рт.ст./c), показатели конечно-диастолического давления (КДД) у животных на фоне кардиотоксического действия на доксорубицина (через 48 ч после в/б введения 20 мг/кг) в условиях навязывания сердцу высокого ритма сокращений (480 уд./мин) при увеличении концентрации Са2+ до 5 ммоль в перфузате.
Технический результат достигается тем, что при оценке результатов в интактной группе при навязывания сердцу высокого ритма сокращений (480 уд./мин) в условиях увеличения концентрации Са2+ до 5 ммоль в перфузате, дефект диастолы был в пределах физиологических значений (SТТI - 1,4±0,1 усл.ед.) (фиг. 1).
При оценке результатов в группе на фоне кардиотоксического влияния доксорубицина у всех сердец было отмечено снижение ЛЖД, отрицательные инотропные эффекты и значительное повышение диастолического давления, что свидетельствует о нарушении расслабления миокарда. При этом коэффициент SТТI составил 8,3±0,3 усл.ед. (фиг. 2).
Способ осуществлялся следующим образом.
Исследование проводили на изолированных сердцах крыс Wistar с массой тела 300 ±20 г. Все крысы были разделены на 4 опытные группы по 8 животных. Первая группа, контрольная, которой внутрибрюшинно вводили физиологический раствор. Второй группе внутрибрюшинно вводили доксорубицин (Teva) в кумулятивной дозе 20 мг/кг, однократно. Животных из эксперимента выводили через 48 ч. Сердца извлекали у животных под золетиловым наркозом (30 мг/кг) и помещали в «ледяной» (2–4°С) раствор Кребса-Хензеляйта следующего состава (ммоль): NaCl – 118,5; KCl – 4,7; MgSO4/7Н2О – 1,2; KH2PO4 – 1,2; CaCl2 – 1,5; глюкоза – 11,1; NaHCO3 –25,0. Уровень pH раствора в ходе всего эксперимента составлял 7,4. После прекращения спонтанных сокращений выделяли аорту и отделяли соединительную ткань. Затем аорту канюлировали и производили ретроградную перфузию сердца методом Лангендорфа в режиме проточной перфузии в течение 20 мин раствором Кребса-Хензеляйта, насыщенным карбогеном (95 % О2 + 5 % СО2) при 37°С и при давлении 100 мм рт.ст. и скорости перфузата 10 мл/мин. Сократительную функцию сердца регистрировали с помощью введенного в полость левого желудочка латексного баллончика, соединенного с датчиком давления, встроенного в аппарат для физиологических исследований МР150 компании «Biopac Systems, Inc» (California, USA). Баллончик заполняли дистиллированной водой, объем которой был достаточным для создания конечно-диастолического давления в левом желудочке на уровне 3-5 мм Hg. С помощью оригинальной прикладной программы Acq Knowledge компании «Biopac Systems, Inc» (California, USA) у всех крыс проводили регистрацию показателей сократимости: левожелудочковое давление (ЛЖД, мм рт.ст.), частоту сердечных сокращений (ЧСС, уд./мин), максимальную скорость сокращения (+dP/dtmax, мм рт.ст./c), максимальную скорость расслабления миокарда (-dP/dtmax, мм рт.ст./c). Затем для определения динамики диастолического напряжения сердца использовали прием увеличения частоты до 480 уд./мин в условиях концентрации Са2+(2,5 ммоль/л) и увеличения его содержания в 2 раза до 5 ммоль/л. Для создания высокой частоты (480 уд./мин) на металлизированную канюлю присоединяли коннектор-земля электрического стимулятора, а на ушко левого предсердия присоединяется коннектор-плюс. После 20 мин перфузии раствором с высоким содержанием Са2+ (5 ммоль/л) сердце подвергалось стимуляции электрическими импульсами с помощью прибора STM 200-1 компании «Biopac Systems, Inc» (California, USA) в течение 15 с.
Пример конкретного выполнения
Показатели сократительной функции сердец всех исследуемых групп в исходном состоянии и при повышении концентрации Са2+ до 5 ммоль/л представлены в таблицах 1 и 2.
Исследования показали, что в условиях данной патологии изменения сократимости характеризуется отрицательным инотропным действием (таблица 1).
Показатели сократительной функции сердца крыс (M±m; n=8) 2,5 ммоль Са2+ в перфузате
Таблица 1
мм рт.ст.
мм рт.ст./c
мм рт.ст./c
Примечание: * - р<0,05 в сравнении с группой интактных животных;
** - р<0,05 в сравнении с группой контроля
Показатели сократительной функции сердца крыс (M±m; n=8) 5 ммоль Са2+ в перфузате при стимуляции (480 уд./мин)
Таблица 2
мм рт.ст.
мм рт.ст./c
мм рт.ст./c
за 48 ч (20 мг/кг)
Примечание: * - р<0,05 в сравнении с группой интактных животных;** - р<0,05 в сравнении с группой контроля
Дальнейшим этапом экспериментов явилось повышение концентрации ионов Са2+ до 5 ммоль/л в перфузионном растворе. После 20 мин перфузии раствором с высоким содержанием Са2+ (5 ммоль/л) сердце подвергалось стимуляции электрическими импульсами в течение 15 с. Перфузия интактных сердец и сердец в группе контроля, раствором с повышенной концентрацией ионов кальция в течение 1-й мин проявлялась положительным инотропным эффектом, что выражалось в возрастании систолического давления и его скоростных характеристик. При этом конечно-диастолическое давление увеличивалось до 20-25 мм рт.ст. и формировало дефект диастолы. В цифровом выражении коэффициент SТТI составил SТТI - 1,4±0,1 усл.ед. (фиг. 1) (таблица 3).
В группе с моделированием доксорубициновой кардиомиопатии при навязывании высокого ритма сокращений (480 уд./мин) положительный инотропный эффектне развивался, а происходило увеличение конечно-диастолического давления до 40-60 мм рт.ст. Дефект диастолы и в цифровом выражении SТТI составил SТТI - 8,3±0,3 усл.ед. (фиг.2) (таблица 3).
Коэффициент дефекта диастолы SТТI, усл.ед. (при доксорубициновой модели кардиомиопатии)
Таблица 3
за 48 ч (20 мг/кг)
Примечание: * - р<0,05 в сравнении с группой интактных животных;** - р<0,05 в сравнении с группой контроля
Таким образом, приведенные результаты наглядно демонстрируют, что для оценки кардиопротективной активности фармакологических средств цифровым значением является коэффициент дефекта диастолы SТТI в виде планиметрического измерения площади под кривой конечно-диастолического давления.
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-ГИДРОКСИНИКОТИНАТ КАЛИЯ, ОБЛАДАЮЩИЙ КАРДИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2640580C1 |
| 3-(1Н-бензимидазол-2-ил)-1,2,2-триметилциклопентанкарбоновая кислота, обладающая кардиопротекторной активностью | 2017 |
|
RU2645356C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ КАРДИОТОНИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2521213C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ КАРДИОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ В УСЛОВИЯХ СТРЕССОРНОГО ВОЗДЕЙСТВИЯ | 2013 |
|
RU2531082C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ КАРДИОПРОТЕКТОРНЫМИ, АНТИАГРЕГАНТНЫМИ, АНТИКОАГУЛЯНТНЫМИ И МЕМБРАНОПРОТЕКТОРНЫМИ СВОЙСТВАМИ В УСЛОВИЯХ СТРЕССОРНОГО ВОЗДЕЙСТВИЯ | 2013 |
|
RU2531080C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2014 |
|
RU2567827C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИШЕМИИ МИОКАРДА | 2002 |
|
RU2241463C2 |
| СУППОЗИТОРИИ ДЛЯ ЛЕЧЕНИЯ СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ | 2000 |
|
RU2191001C2 |
| КАРДИОПЛЕГИЧЕСКИЙ РАСТВОР "АСН-БОКЕРИЯ-БОЛДЫРЕВА" | 2009 |
|
RU2413502C1 |
| КРИСТАЛЛОИДНЫЙ КАРДИОПЛЕГИЧЕСКИЙ РАСТВОР | 2009 |
|
RU2423135C2 |
Изобретение относится к медицине, а именно к экспериментальной кардиофармакологии, и может быть использовано в комплексной оценке активности фармакологических средств на изолированном сердце крысы. Для этого способ включает регистрацию показателей сократимости в условиях навязывания сердцу высокого ритма сокращений и гиперкальциевой нагрузки. При этом регистрируют показатели сократительной функции левого желудочка, затем для определения динамики диастолического напряжения проводят 20-минутную перфузию сердца раствором, содержащим 5 ммоль/л Са2+ В последующим навязывают частоту сокращения до 480 уд./мин в течение 15 сек с помощью электрического стимулятора. После чего рассчитывают коэффициент STTI (площадь дефекта диастолы) в усл.ед. путем складывания площадей трапеций под кривой подъема конечно-диастолического давления и оценивают сократительную функцию сердца с учетом показателей физиологических значений STTI. Способ обеспечивает информативность и повышение достоверности показателей оценки степени кардиопротективной или кардиотоксической активности фармакологических средств с помощью коэффициента SТТI. 2 ил.,3 табл., 1 пр.
Способ оценки сократительной функции изолированного сердца крысы, включающий регистрацию показателей сократимости в условиях навязывания сердцу высокого ритма сокращений и гиперкальциевой нагрузки, отличающийся тем, что регистрируют показатели сократительной функции левого желудочка, затем для определения динамики диастолического напряжения проводят 20-минутную перфузию сердца раствором, содержащим 5 ммоль/л Са2+, с последующим навязыванием частоты сокращения до 480 уд./мин в течение 15 с с помощью электрического стимулятора, после чего рассчитывают коэффициент STTI (площадь дефекта диастолы) в усл.ед. путем складывания площадей трапеций под кривой подъема конечно-диастолического давления и оценивают сократительную функцию сердца с учетом показателей физиологических значений STTI.
| ЯЦИНЮК Б.Б | |||
| и др | |||
| Вестник Уральской медицинской академии наук, 2010, N 1, С | |||
| Контрольный стрелочный замок | 1920 |
|
SU71A1 |
| СПОСОБ ОЦЕНКИ КАРДИОПРОТЕКТИВНОГО ДЕЙСТВИЯ ФАРМАКОЛОГИЧЕСКИХ СРЕДСТВ ПО РЕЗУЛЬТАТАМ ИЗМЕРЕНИЯ ЛЕВОЖЕЛУДОЧКОВОГО ДАВЛЕНИЯ ПРИ МОДЕЛИРОВАНИИ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 2000 |
|
RU2194436C2 |
| УСТАНОВКА ДЛЯ ПЕРФУЗИИ ИЗОЛИРОВАННОГО СЕРДЦА ПО ЛАНГЕНДОРФУ | 2012 |
|
RU2491963C1 |
| СПОСОБ ДИАГНОСТИКИ СИНДРОМА КАРДИОСТИМУЛЯТОРА | 1998 |
|
RU2167597C2 |
| CN 102608089 A, 25.07.2012 | |||
| US 20020143259 A1, 03.10.2002 | |||
| ГУБАРЕВА И.В | |||
| Способ диагностики диастолической дисфункции левого желудочка у больных с артериальной гипертонией | |||
| Известия Самарского научного центра Российской академии наук, том 16, N 5(4), 2014, с.1266-1268 | |||
| YAO YY et al | |||
| Activation of Akt and cardioprotection against reperfusion injury are maximal with only five minutes of sevoflurane postconditioning in isolated rat hearts | |||
| J Zhejiang Univ Sci B | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2018-01-30—Публикация
2017-02-21—Подача