ОБЛАСТЬ ПРИМЕНЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение по существу относится к средствам и устройствам для обеспечения гемостаза и уплотнения тканей и, более конкретно, к гемостатическим прокладкам, содержащим биологически абсорбируемые каркасы, несущие лиофилизированные белки, способствующие гемостазу, такие как фибриноген и тромбин.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Кровь представляет собой жидкую ткань, которая включает в себя эритроциты, лейкоциты, форменные элементы крови и тромбоциты, растворенные в жидкой фазе. Жидкая фаза представляет собой плазму, которая включает в себя кислоты, липиды, растворенные электролиты и белки. Особым белком, который находится во взвешенном состоянии в жидкой фазе, является фибриноген. При возникновении кровотечения фибриноген взаимодействует с водой и тромбином (фермент) и образует фибрин, вещество, нерастворимое в крови, которое образует сгустки при полимеризации.
В самых разных случаях у животных, включая людей, могут возникать кровотечения, связанные с ранами или хирургическими процедурами. В некоторых случаях кровотечение является сравнительно слабым и нормальных функций свертывания крови вместе с применением простых приемов оказания первой помощи оказывается достаточно. В иных случаях может возникать существенное кровотечение. В данных случаях обычно требуется специализированное оборудование и материалы, а также персонал с навыками оказания соответствующей помощи.
Для решения описанных выше проблем были разработаны материалы для контроля чрезмерного кровотечения. Топические биологически абсорбируемые гемостатические средства (TAH) широко используются в хирургической практике. TAH включают в себя продукты на основе различных тканых или нетканых материалов или губок, как правило, изготовленных из по меньшей мере частично рассасываемых материалов, варьирующихся от натуральных до синтетических полимеров и их комбинаций, включая сополимеры на основе лактида-гликолида, такие как полиглактин 910, окисленная целлюлоза (ОЦ), окисленная регенерированная целлюлоза (ОРЦ), желатин, коллаген, хитин, хитозан и т.п. Для улучшения гемостатических характеристик каркасы на основе указанных выше материалов могут быть скомбинированы с факторами свертывания крови биологического происхождения, такими как тромбин и/или фибриноген.
В ряде гемостатических составов, которые в настоящее время доступны в продаже или находятся в процессе разработки, используется лиофилизированный фибриноген, часто в комбинации с лиофилизированным тромбином, причем гемостатические составы применяются в виде сухого порошка, полужидкой пасты, жидкого состава или, необязательно, помещаются на опорный каркас, такой как биологически абсорбируемый тканевой каркас.
В случае гемостатических пластырей или прокладок, содержащих лиофилизированные тромбин и фибриноген на биологически абсорбируемых каркасах, существует потребность в улучшении эксплуатационных характеристик и свойств таких устройств, причем особенно необходимы улучшения, связанные с повышением смачиваемости прокладок, которая способствует более быстрому восстановлению лиофилизированных белков и более быстрому гемостазу, а также с уменьшением осыпаемости, т.е. рыхлости активных порошков при манипуляциях с прокладками и/или при их разрезании; и улучшением свойств, обеспечивающих адгезию к тканям и закрытие раны.
В патенте США № 7320962 под названием «Гемоактивные композиции и способы их производства и применения» описан обезвоженный гемоактивный материал для подавления кровотечения или выделения средства, содержащий: поперечносшитый биологически совместимый полимер, который при контакте с кровью образует гидрогель; и непоперечносшитый биологически совместимый полимер, который растворяется при контакте с кровью; причем поперечносшитый полимер распределен в обезвоженной матрице непоперечносшитого полимера. Дополнительно в ссылке описан пластификатор, присутствующий по меньшей мере в непоперечносшитом полимере; и утверждается, что пластификатор выбран из группы, состоящей из полиэтиленгликоля, сорбита и глицерина.
В патенте США № 6706690 под названием «Гемоактивные композиции и способы их производства и применения» описан обезвоженный материал, который при контакте с кровью образует гидрогель, причем указанный материал содержит: поперечносшитый биологически совместимый полимер, который при контакте с кровью образует гидрогель; непоперечносшитый биологически совместимый полимер, который растворяется при контакте с кровью; пластификатор, присутствующий в непоперечносшитом биологически совместимом полимере; и причем поперечносшитый полимер распределен в обезвоженной матрице непоперечносшитого полимера, причем непоперечносшитый биологически совместимый полимер растворяется при контакте с кровью за 15 или менее минут. Дополнительно в ссылке описан пластификатор, присутствующий в непоперечносшитом полимере в количестве от 1% вес. до 20% вес. материала; и утверждается, что пластификатор выбран из группы, состоящей из полиэтиленгликоля, сорбита и глицерина.
В заявке на патент США № 2011/0071499A1 под названием «СВОБОДНО РАСПОЛАГАЮЩИЙСЯ БИОДЕГРАДИРУЕМЫЙ ПЛАСТЫРЬ» описано устройство, содержащее: пленку, содержащую смесь твердого фибриногена и твердого тромбина, причем пленка расположена свободно и выполнена с возможностью образовывать при контакте с влагой фибриновый пластырь; дополнительно утверждается, что пленка дополнительно содержит пластификатор. Дополнительно в патенте описано устройство, в котором пленка содержит от приблизительно 5 до приблизительно 30% вес. полиэтиленгликоля.
В заявке на патент США № 2009/0053288 A1 под названием «Гемостатический тканый материал» описан тканый материал, имеющий модифицированное переплетение «воронья лапа» (саржевое) и дополнительно содержащий гемостатическое средство. Дополнительно в ссылке описан тканый материал, дополнительно содержащий консервант, выбранный из группы, состоящей из глицерина, пропандиола, полиоксиэтиленгликоля (PEG), трегалозы и их комбинаций.
В заявке на патент США № 2007/0160653 A1 под названием «Гемостатическая ткань» описана гемостатическая ткань, содержащая: материал, содержащий стекловолокно и одно или более вторичных волокон, выбранных из группы, состоящей из шелковых волокон; полиэфирных волокон; нейлоновых волокон; керамических волокон; исходных или регенерированных бамбуковых волокон; хлопковых волокон; гидратцеллюлозных волокон; льняных волокон; полимеров лактида и/или гликолида; сополимеров лактида и гликолида; тромбина или фракции, содержащей тромбин; и одно или более гемостатических средств, выбранных из группы, состоящей из тромбоцитов в растворе Рингера с лактатом, клеток крови в растворе Рингера с лактатом; фибрина и фибриногена; при контакте с раневой поверхностью указанная гемостатическая ткань способна активировать системы гемостаза в организме. Дополнительно в ссылке описана гемостатическая ткань, дополнительно содержащая консервант, выбранный из группы, состоящей из глицерина, пропандиола, полиоксиэтиленгликоля (PEG), трегалозы и их комбинаций.
В патентной публикации № WO 1997028832 A1, опубликованной в рамках Договора о патентной кооперации (PCT), под названием «КОМПОЗИЦИЯ ДЛЯ УПЛОТНЕНИЯ РАН» описан гемостатический бандаж, который содержит порошкообразные фибриноген и тромбин, адгезивно прикрепленные к волокнистой матрице вязким безводным адгезивом, таким как вязкий полисахарид, гликоль или вазелин. Безводный адгезив препятствует протеканию гидролитической реакции между фибриногеном и тромбином до тех пор, пока бандаж не вступит в контакт с жидкостью организма, такой как кровь; также утверждается, что бандаж можно изготовить и хранить в течение длительных периодов времени с сохранением гемостатической активности. Дополнительно в ссылке описана композиция для уменьшения кровотечения из раны, содержащая: носитель; компоненты, способствующие коагуляции и прикрепленные к носителю адгезивом, выбранным из группы, состоящей из воды с таким показателем pH, при котором тромбин и фибриноген не взаимодействуют с образованием фибрина, и вязкого безводного биосовместимого адгезива; причем компоненты, способствующие коагуляции, содержатся в количестве, терапевтически эффективном для свертывания и уменьшения кровотечения из раны в случаях, когда композиция вступает в контакт с жидкостями организма, которые активируют коагуляцию. Дополнительно в ссылке описана композиция, в которой адгезив представляет собой безводную жидкость при температуре 20°C, удерживающую компоненты, способствующие коагуляции, на носителе. Дополнительно в ссылке описана композиция, в которой безводный адгезив выбран из группы, состоящей из пропиленгликоля, глицерина, вазелина и полиэтиленгликоля.
Дополнительно в ссылке описана гемостатическая раневая повязка, содержащая: волокнистую матрицу, подходящую для размещения в качестве прокладки, которую накладывают поверх раны или вводят в открытую кровоточащую рану; смесь перемешанных частиц порошкообразных факторов коагуляции, присутствующих на поверхности матрицы, причем частицы располагаются достаточно близко друг от друга для образования сгустка при контакте с водной средой, имеющей физиологические значения pH; причем частицы прикрепляются к матрице вязким безводным адгезивом, вязкость которого составляет по меньшей мере 100 сантипуаз при температуре 20°C, что подавляет реакцию коагуляции между перемешанными частицами до тех пор, пока частицы не подвергнутся воздействию водной среды при физиологических значениях pH.
Дополнительно в ссылке описана гемостатическая раневая повязка, содержащая: волокнистую матрицу, подходящую для размещения в качестве прокладки, которую накладывают поверх раны или вводят в открытую кровоточащую рану; смесь перемешанных частиц порошкообразных факторов коагуляции, расположенных по всей матрице достаточно близко друг от друга для образования сгустка при контакте с водной средой, имеющей физиологические значения pH; причем частицы прикрепляются к матрице вязким безводным адгезивом, который подавляет реакцию коагуляции между перемешанными частицами до тех пор, пока частицы не подвергнутся воздействию водной среды при физиологических значениях pH, причем адгезив выбран из группы, состоящей из полисахарида, полиэтиленгликоля, пропиленгликоля, глицерина и вазелина, причем адгезив наносят на матрицу в жидкой форме, содержащей менее 3% вес. воды.
ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Вкратце, в одном варианте осуществления настоящее изобретение относится к гемостатической прокладке, имеющей улучшенные характеристики осыпаемости и смачиваемости, а также к способу производства такой гемостатической прокладки, содержащей: биологически абсорбируемый или биологически рассасывающийся каркасный материал; порошок лиофилизированного тромбина, порошок лиофилизированного фибриногена и порошок полиэтиленгликоля (PEG), каждый из которых помещен на биологически абсорбируемый каркасный материал; причем порошок PEG связывает порошок лиофилизированного тромбина и порошок лиофилизированного фибриногена с биологически абсорбируемым каркасным материалом, но полностью не обволакивает частицы порошка лиофилизированного тромбина и/или лиофилизированного фибриногена. В настоящем документе термины «биологически абсорбируемый» и «биологически рассасывающийся» являются взаимозаменяемыми и означают материалы, которые могут распадаться в организме и не требуют механического удаления.
В одном варианте осуществления настоящее изобретение относится к способу производства гемостатической прокладки, содержащему этапы (a) формирования суспензии из порошка лиофилизированного тромбина, порошка лиофилизированного фибриногена и порошка полиэтиленгликоля в безводной текучей среде; (b) нанесения суспензии на каркас из биологически рассасывающегося материала; (c) выпаривания текучей среды, после которого на каркасе остается часть порошка тромбина, часть порошка фибриногена и часть порошка полиэтиленгликоля; (d) нагревания каркаса до температуры, превышающей температуру плавления полиэтиленгликоля, но не превышающей температуру существенной денатурации тромбина и фибриногена; (e) охлаждения каркаса до температуры окружающей среды для формирования гемостатической прокладки.
В одном варианте осуществления настоящее изобретение относится к способу обеспечения гемостатического лечения или уплотнения тканей в месте расположения раны, содержащему этапы: (a) формирования гемостатической прокладки в соответствии с представленным выше описанием; и (b) нанесения гемостатической прокладки на место расположения раны.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 представлены данные испытания на отслаивание ткани и эффекты добавления PEG.
На фиг. 2 представлены данные испытания на отсутствие утечек для нескольких исследованных систем.
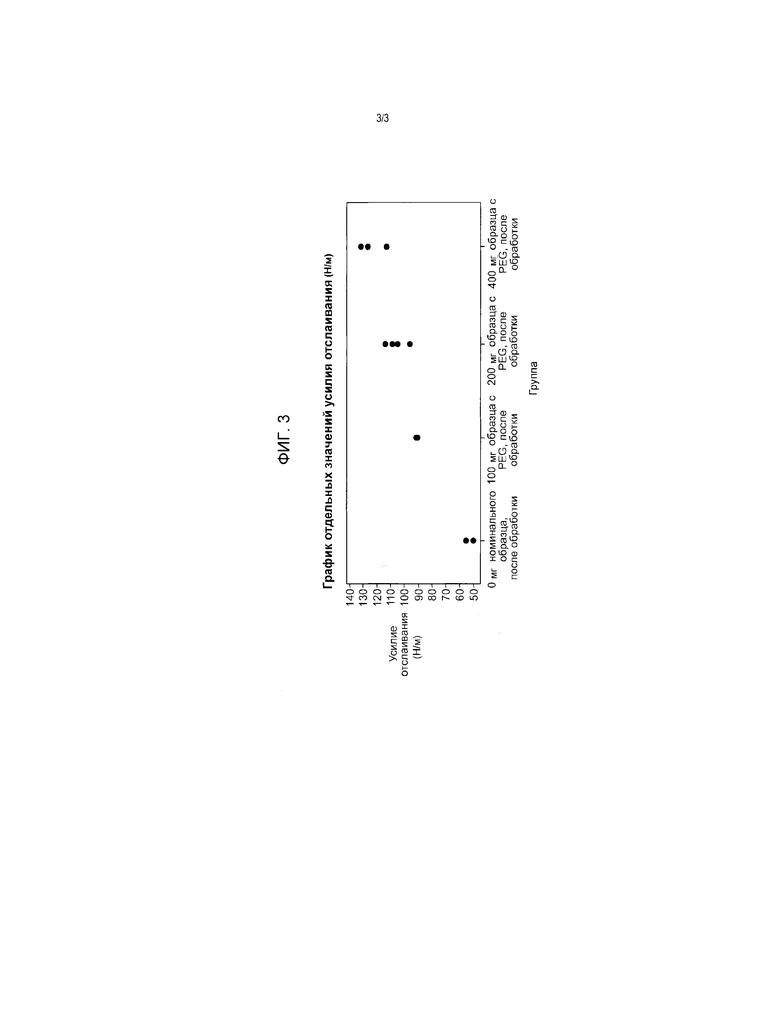
На фиг. 3 представлены результаты испытания на осыпаемость при различных концентрациях PEG3.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Вкратце, в одном варианте осуществления настоящее изобретение относится к гемостатической прокладке, имеющей улучшенные характеристики осыпаемости и смачиваемости, а также к способу производства такой гемостатической прокладки, содержащей: биологически абсорбируемый каркасный материал; порошок лиофилизированного тромбина, порошок лиофилизированного фибриногена и порошок полиэтиленгликоля, каждый из которых помещен на биологически абсорбируемый каркасный материал; причем порошок PEG связывает порошок лиофилизированного тромбина и порошок лиофилизированного фибриногена с биологически абсорбируемым каркасным материалом, но полностью не обволакивает частицы порошка лиофилизированного тромбина и лиофилизированного фибриногена.
В соответствии с одним вариантом осуществления настоящего изобретения плавкий PEG, необязательно в присутствии карбоксиметилцеллюлозы (КМЦ), используется для создания более прочной адгезии лиофилизированных белков к биологически абсорбируемому каркасному материалу и лучшей смачиваемости/клейкости полученной гемостатической прокладки, где расплавленный и повторно отвердевший PEG связывает проксимально расположенные частицы или порошки с волокнами каркаса, но полностью не покрывает или не обволакивает такие порошки/частицы, позволяя жидкости вступать в контакт и быстро активировать данные биологические средства в условиях хирургической практики. Это позволяет получить недорогое решение, направленное на снижение осыпаемости и улучшение адгезии к тканям и их уплотнения.
В одном варианте осуществления настоящее изобретение относится к гемостатическому или уплотняющему ткань материалу или прокладке. В другом варианте осуществления настоящее изобретение также относится к способу обеспечения гемостатического лечения или уплотнения тканей в месте расположения раны, содержащему этапы: (а) формирования гемостатического или уплотняющего ткань материала или прокладки, как описано выше, и (b) нанесения гемостатического или уплотняющего ткань материала на место расположения раны.
Гемостатическая прокладка, содержащая лиофилизированные фибриноген и тромбин
В соответствии с вариантом осуществления настоящее изобретение относится к гемостатической прокладке, содержащей способствующие гемостазу лиофилизированные или необязательно лиофилизированные средства на биологически абсорбируемом каркасе или матрице. Предпочтительные гемостатические каркасы являются натуральными, или модифицированными методами генной инженерии биологически абсорбируемыми полимерами, или синтетическими биологически абсорбируемыми полимерами, или их смесями.
Примерами натуральных или модифицированными методами генной инженерии биологически абсорбируемых полимеров являются белки, полисахариды и их комбинации. Полисахариды включают в себя, без ограничений, целлюлозу, окисленную целлюлозу, окисленную регенерированную целлюлозу (ОРЦ), алкилцеллюлозу, например метилцеллюлозу, алкилгидроксиалкилцеллюлозу, гидроксиалкилцеллюлозу, сульфатцеллюлозу, соли карбоксиметилцеллюлозы, карбоксиметилцеллюлозу, карбоксиэтилцеллюлозу, хитин, карбоксиметилхитин, гиалуроновую кислоту, соли гиалуроновой кислоты, альгинат, альгиновую кислоту, альгинат пропиленгликоля, гликоген, декстран, сульфат декстрана, курдлан, пектин, пуллулан, ксантан, хондроитин, хондроитинсульфаты, карбоксиметилдекстран, карбоксиметилхитозан, хитозан, крахмал, амилозу, амилопектин, поли-N-глюкозамин, полиманнуроновую кислоту, полиглюкуроновую кислоту, полигулуроновую кислоту и производные любых из указанных выше веществ.
Примерами синтетических биологически абсорбируемых полимеров являются полиэфирные полимеры, сополимеры и/или их комбинации. Полиэфиры, как правило, синтезируют путем полимеризации с раскрытием цикла мономеров, включая, без ограничений, молочную кислоту, лактид (включая L-, D-, мезо- и D-, L-смеси), гликолевую кислоту, гликолид, ε-капролактон, п-диоксанон (1,4-диоксан-2-он) и триметиленкарбонат (1,3-диоксан-2-он).
Средства, способствующие гемостазу, включают в себя белки, протромбин, тромбин, фибриноген, фибрин, фибронектин, гепариназу, фактор X/Xa, фактор VII/VIIa, фактор IXa/IXa, фактор XI/XIa, фактор XII/XIIa, тканевой фактор, батроксобин, анкрод, экарин, фактор фон Виллебранда, коллаген, эластин, альбумин, желатин, поверхностные гликопротеины тромбоцитов, вазопрессин, аналоги вазопрессина, адреналин, селектин, прокоагулянтный яд, ингибитор активатора плазминогена, средства, активирующие тромбоциты, синтетические пептиды, обладающие гемостатической активностью, и/или их комбинации.
Гемостатическая прокладка, содержащая лиофилизированные тромбин и фибриноген на биологически абсорбируемом каркасе, используемом при испытаниях образцов, составляющих предмет настоящего изобретения, упоминается как усовершенствованная гемостатическая прокладка, содержащая биологические препараты и состоящая из композитной матрицы на основе волокон полиглактина 910 (PG910), вшитых иглопробивным способом в защитный слой из окисленной регенерированной целлюлозы (ОРЦ). Сторона матрицы, содержащая PG910, покрыта порошками человеческого фибриногена и тромбина в обезвоженном непрореагировавшем состоянии. Когда усовершенствованную гемостатическую прокладку, содержащую биологические препараты, накладывают на кровоточащее место, белки быстро (в течение нескольких секунд) гидратируются, в результате чего происходит превращение фибриногена в фибрин, образующий фибриновый сгусток. Образование фибрина на поверхности ткани способствует гемостазу и адгезии к ткани. Важно, что до нанесения на ткань белки остаются в непрореагировавшем состоянии. Преждевременное превращение фибриногена в фибрин (предварительная активация) из-за контакта с водой при производстве или хранении может оказывать негативное влияние на характеристики изделия и его стабильность.
Патент США № 7,666,803, выданный Shetty и соавторам, под названием «Армированная биологически абсорбируемая многослойная ткань для применения в медицинских устройствах» полностью включен в настоящий документ во всех отношениях путем ссылки и описывает многослойную ткань, содержащую первый биологически абсорбируемый нетканый материал и второй биологически абсорбируемый тканый или трикотажный материал, содержащий окисленные полисахариды.
Заявка на патент США № 2009/0246238 A1, поданная Gorman и соавторами, под названием «АРМИРОВАННАЯ БИОЛОГИЧЕСКИ АБСОРБИРУЕМАЯ МНОГОСЛОЙНАЯ ГЕМОСТАТИЧЕСКАЯ РАНЕВАЯ ПОВЯЗКА» полностью включена в настоящий документ во всех отношениях путем ссылки и описывает способ получения многослойной раневой повязки, имеющей первый биологически абсорбируемый нетканый материал, один или более вторых биологически абсорбируемых тканых или трикотажных материалов, тромбин и/или фибриноген, причем способ содержит этапы: (a) сгибания волокон биологически абсорбируемого полимера или пряжи в диапазоне приблизительно от 3,94 до 11,8 сгибов на один см (10-30 сгибов на дюйм); (b) разрезания извитых волокон или пряжи по длине штапельного волокна в диапазоне приблизительно от 0,26 до 6,35 сантиметра (0,1-2,5 дюйма); (c) прочесывания штапельного волокна для формирования первого биологически абсорбируемого нетканого материала при одновременном поддержании влажности в диапазоне приблизительно 20-60% при комнатной температуре, составляющей приблизительно 15-24°C; (d) прикрепления первого биологически абсорбируемого нетканого материала ко второму биологически абсорбируемому тканому или трикотажному материалу; (e) нанесения тромбина и/или фибриногена на первый биологически абсорбируемый нетканый материал. Дополнительно в ссылке описан способ получения раневой повязки, содержащей биологически абсорбируемый нетканый материал, тромбин и/или фибриноген, который содержит этапы: (a) суспендирования тромбина и/или фибриногена в перфторированном углеводороде для образования суспензии; и (b) нанесения суспензии на биологически абсорбируемый нетканый материал.
Европейский патент № EP 2052746 A2 под названием «Способ получения биологически абсорбируемого гемостатического средства», подан Gorman и соавторами, полностью включен в настоящий документ во всех отношениях путем ссылки и описывает способ получения раневой повязки, содержащий: суспендирование порошка тромбина и/или фибриногена в жидком перфторированном углеводороде-носителе, в котором они нерастворимы, и нанесение полученной суспензии на первый биологически абсорбируемый нетканый материал.
Опубликованная заявка на патент США № 2006/0088589 A1 под названием «Способ получения абсорбируемого гемостатического средства», Gorman и соавторы, полностью включена в настоящий документ во всех отношениях путем ссылки и описывает способ получения раневой повязки, содержащий: суспендирование порошка тромбина и/или фибриногена в жидком перфторированном углеводороде-носителе, в котором они не растворимы, и нанесение полученной суспензии на первый абсорбируемый нетканый материал.
Гемостатические прокладки, содержащие биологические препараты и полученные в соответствии с описанием в указанных выше ссылках, использовали в экспериментах, проведенных во время практического применения настоящего изобретения.
Матричный компонент гемостатической прокладки, содержащей биологические препараты, состоит из трикотажного защитного слоя ОРЦ, расположенного под слоем нетканых волокон полиглактина 910 (PG910). При производстве матрицы волокна PG910 вводят в войлок посредством кардования и пришивают иглопробивным способом к защитному слою ОРЦ для получения матрицы усовершенствованной гемостатической прокладки, содержащей биологические препараты.
Биологические компоненты гемостатической прокладки, содержащей биологические препараты, предпочтительно представляют собой лиофилизированные формы таких лекарственных средств, как человеческий фибриноген и человеческий тромбин. В альтернативном варианте осуществления такие вещества, как фибриноген и тромбин, могут быть получены из отличных от человека животных источников или синтезированы известным способом. Композиция гемостатической прокладки, содержащей биологические препараты, которую использовали в экспериментах, будет описана с помощью представленных ниже данных. В дополнение к определенным количествам активных порошков, как описано ниже, обладающие признаками изобретения гемостатические прокладки, содержащие биологические препараты, также необязательно покрывали различными количествами PEG 3000 и КМЦ, как описано ниже в настоящем документе. Биологические компоненты прокладки, содержащей фибриноген, предпочтительно представляют собой лиофилизированные формы человеческого фибриногена и человеческого тромбина. Соответственно, они содержат биологически активные компоненты, такие как фибриноген и тромбин, а также другие эксципиенты. Композиции человеческого фибриногена и человеческого тромбина, наносимые на прокладку, содержащую фибриноген, содержат 2-20 мг/см2 фибриногена и 1-150 МЕ/см2 тромбина. Композиция каркасного или матричного компонента гемостатической прокладки, содержащей биологические препараты, содержала приблизительно 5-30 мг/см2 ОРЦ (в качестве защитного слоя); и 5-30 мг/см2 PG910 (в качестве несущего слоя), причем общий вес матрицы составлял приблизительно 10-60 мг/см2.
Композиции человеческого фибриногена и человеческого тромбина, которые наносили на прокладку, содержащую фибриноген, содержали 2-20 мг/см2 фибриногена и 1-150 МЕ/см2 тромбина в присутствии других эксципиентов, таких как хлорид кальция, необязательно аргинин, глицин, альбумин, манит, буферные соли и другие необязательные белковые компоненты, традиционно присутствующие в продуктах, полученных из плазмы крови.
Пример 1. Производство образцов для испытания гемостатической прокладки, содержащей биологические препараты
Следующие процедуры аналогичны процедурам, описанным в указанной выше заявке на патент США № 2009/0246238 A1 и европейском патенте № EP 2052746 A2, где сополимер лактида и гликолида (PGLA, 90/10 моль/моль) получили прядением из расплава в волокно. Мультифиламентную пряжу с весовым номером 80 денье объединили в консолидированную пряжу с весовым номером 800 денье. Консолидированную пряжу извили при температуре приблизительно 110°C. Извитую пряжу разрезали на штапельное волокно, имеющее длину приблизительно 3,18 см (1,25 дюйма); 20 грамм извитого штапельного волокна точно взвесили и равномерно уложили на транспортерную ленту кардочесальной машины с множественными валками. Контролировали соответствующие условия окружающей среды (температура 21°C и относительная влажность 55%). Затем штапельное волокно подвергли кардованию для создания нетканого войлока. Войлок извлекли из захватывающего валка и разрезали на 4 равные части. Их повторно загрузили в кардочесальную машину перпендикулярно направлению выхода волокон. После второго прогона войлок взвесили (19,8 г: выход ткани 99%) и затем спрессовали в войлочное полотно. Спрессованное войлочное полотно точно расположили на ткани ОРЦ и прочно скрепили иглопробивным способом. Многослойный материал обрезали и промыли в 3-х раздельных ваннах с изопропиловым спиртом для удаления замасливателя и следов машинного масла. Промытый многослойный материал сушили в печи при температуре 70ºC в течение 30 минут, охладили и взвесили.
Затем промытую многослойную ткань разрезали на части размером 10,2×10,2 сантиметра (4×4 дюйма). 1,70 грамма BAC-2 (производство компании Omrix Biopharmaceuticals, Inc.), имеющего специфическую активность (по Клауссу) 0,3 г/г, а также 0,30 г тромбинсодержащего порошка (также производство компании Omrix Biopharmaceuticals, Inc.), необязательно 0,40 г полиэтиленгликоля (PEG) и необязательно 0,30 г порошка карбоксиметилцеллюлозы (КМЦ) тщательно перемешали с приблизительно 14 миллилитрами безводной текучей среды гидрофторэфир HFE-7000. Для дальнейшего размещения ткани суспензию влили в лоток с лункой, размер которой был немного больше 10,2×10,2 сантиметра (4×4 дюйма). Чтобы порошки по существу отложились на ткани, ее затем погрузили в суспензию. Полученную многослойную гемостатическую прокладку сушили на воздухе в течение по меньшей мере 15 минут.
Затем образцы для испытания, содержащие PEG, и несколько образцов, также необязательно содержащих КМЦ, подвергли термической обработке при температуре, превышающей температуру плавления PEG. Образцы расположили в стандартной вакуумной печи с температурой 65-70°C и нагревали в течение приблизительно 15 минут. Таким образом, частицы лиофилизированного тромбина и фибриногена, покрывающие биологически абсорбируемый каркас, и необязательно частицы КМЦ вплавили в каркас благодаря нагреванию до температуры, превышающей температуру плавления PEG. Затем образцам для испытания дали остыть до комнатной температуры.
Текучая среда на основе гидрофторэфира (HFE) представляла собой 3M Novec™ Engineered Fluid HFE-7000, 1-метоксигептафторпропан, поставляемый в продажу компанией 3M Corporation. HFE-7000 является инертной невоспламеняющейся текучей средой с низкой температурой кипения. HFE-7000 применяется при производстве в качестве инертной несущей среды для порошков тромбина и фибриногена и необязательно PEG и/или КМЦ, а также по существу полностью удаляется путем выпаривания в ходе производственного процесса. При изготовлении обладающих признаками изобретения гемостатических прокладок в качестве инертной несущей среды для порошков тромбина и фибриногена и необязательно PEG и/или КМЦ можно использовать любую другую инертную невоспламеняющуюся безводную текучую среду с низкой температурой кипения.
Во время практического использования настоящего изобретения можно применять любой плавкий биологически совместимый и биологически абсорбируемый порошок с условием, что при температуре окружающей среды он является твердым и температура его плавления ниже температуры существенной денатурации лиофилизированных белков. Предпочтительным связующим веществом является PEG, имеющий среднюю молекулярную массу от 1000 до 20 000 дальтон, более предпочтительно - PEG с молекулярной массой от 3000 до 8000 дальтон. В данном примере использовали PEG 3000 производства компании Fluka с температурой плавления приблизительно 56-59°C и средним размером частиц 45 микрон. В предпочтительном варианте осуществления по меньшей мере 95% (в количественном отношении) частиц связующего вещества имеют размер в диапазоне приблизительно 25-60 микрон, более предпочтительно - в диапазоне 35-55 микрон.
КМЦ (30 000 PA Clear and Stable) была получена от компании Dow Wolff Cellulosics и имела средний размер частиц 20 микрон.
BAC-2 (биологически активный компонент 2) представляет собой полученный из крови препарат, который содержит главным образом фибриноген; остальная часть включает в себя альбумин, буферные соли и другие белковые компоненты, традиционно присутствующие в продуктах, полученных из плазмы крови.
В соответствии с описанным выше способом изготовили и затем подвергли испытаниям три типа образцов гемостатических прокладок, содержащих биологические препараты:
a) гемостатические прокладки с биологическими препаратами, содержащие фибриноген и тромбин;
b) гемостатические прокладки с биологическими препаратами, содержащие фибриноген, тромбин и PEG;
c) гемостатические прокладки с биологическими препаратами, содержащие фибриноген, тромбин, PEG и КМЦ.
Гемостатические прокладки с биологическими препаратами, содержащие небольшие количества PEG, неожиданно продемонстрировали усовершенствованные характеристики, включая повышенную прочность при отслаивании, улучшенные характеристики осыпаемости и смачиваемости. Функциональный результат данных усовершенствований заключается в улучшении уплотняющих свойств и адгезии к ткани, а также снижении осыпаемости активных веществ.
Пример 2. Испытание на отслаивание от ткани
При испытаниях использовали следующие различные концентрации активных компонентов.
Фибриногенсодержащий порошок BAC-2: 5,0 и 6,7 мг/см2 фибриногена или 1,27 грамма и 1,7 грамма фибриногенсодержащего порошка BAC-2 на один образец гемостатической прокладки с биологическими препаратами размером 10,2 ×10,2 см (4×4 дюйма).
Тромбинсодержащий порошок: 300 мг тромбинсодержащего порошка на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма).
PEG: 0; 100, 400 мг на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма).
КМЦ: 0; 300 мг на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма).
Испытание на отслаивание от ткани проводили следующим образом. Образец для испытания гемостатической прокладки с биологическими препаратами, имеющий ширину 1,9 сантиметра и длину приблизительно 10,2 сантиметра (0,75 дюйма и приблизительно 4 дюйма), поместили на влажную бычью дерму. Сразу же после этого к верхней части образца для испытания гемостатической прокладки с биологическими препаратами приложили давление 23,9 кПа (180 мм рт. ст.), развиваемое компрессионным весом, воздействие которого продолжалось три минуты для инкубации и сцепления с тканью. После инкубации вес удалили, а образец гемостатической прокладки с биологическими препаратами прикрепили к поперечнику и затем отслоили от ткани дермы под углом 90 градусов; силу отслаивания измеряли с помощью тензиометра.
В табл. 1 и на фиг. 1 представлены результаты испытания на отслаивание от ткани.
Результаты испытания на отслаивание от ткани
Анализ данных, представленных в табл. 1, указывает на то, что присутствие PEG 3000 в количестве от 100 до 400 мг существенно увеличивает усилие отслаивания от ткани гемостатической прокладки с биологическими препаратами, причем более высокое содержание PEG приводит к большему усилию отслаивания. Дополнительный анализ данных свидетельствует о том, что аналогичным образом, за исключением одного испытания, присутствие КМЦ 30k в количестве 300 мг увеличивает усилие отслаивания от ткани гемостатической прокладки с биологическими препаратами.
На фиг. 1 представлены отдельные точки на графике, а также средние значения, полученные при испытании на отслаивание от ткани, которые конкретно демонстрируют влияние 400 мг PEG на отслаивание от ткани. График отражает данные, полученные для гемостатической прокладки с биологическими препаратами, которая имеет номинальное количество фибриногена и тромбина (1700 мг и 300 мг соответственно) по сравнению с гемостатической прокладкой с биологическими препаратами, дополнительно имеющей 400 мг PEG 3000. Анализ данных указывает на то, что присутствие PEG 3000 существенно увеличивало усилие отслаивания от ткани гемостатической прокладки с биологическими препаратами.
Пример 3. Испытание на отсутствие утечек
Испытание на отсутствие утечек проводили следующим образом. Образец для испытания гемостатической прокладки с биологическими препаратами подвергли инкубации в плазме крови свиньи в течение трех минут при одновременном воздействии компрессионного веса. Затем образец поместили на плоскую металлическую подставку с отверстием диаметром 4,5 мм, и поверх гемостатической прокладки с биологическими препаратами закрепили прозрачную пластиковую крышку, совместимую с отверстием. После этого образец подвергали воздействию свиной плазмы, подававшейся через отверстие с постоянной скоростью в виде гидравлической текучей среды. Следовательно, утечка была единственным возможным вариантом неудовлетворительного результата, а пиковые значения давления фиксировались как выходной сигнал.
В табл. 2 и на фиг. 2 представлены результаты испытания на отсутствие утечек для двух разных количеств BAC-2: 1,7 г и 1,27 г фибриногенсодержащего порошка BAC-2 на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма); 0 и 400 мг PEG 3000; и 0 и 300 мг КМЦ 30k; все количества указаны из расчета на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма).
Результаты испытания на отсутствие утечек
Анализ данных указывает на то, что при испытании на отсутствие утечек присутствие PEG 3000 существенно улучшает свойства гемостатической прокладки с биологическими препаратами (образцы 12, 13, 24) по сравнению с гемостатической прокладкой с биологическими препаратами без добавления PEG (образец 14). Значение среднего давления при испытании на отсутствие утечек увеличилось в диапазоне от приблизительно 6 до приблизительно 14 раз.
Пример 4. Испытание на осыпаемость
В табл. 3 и на фиг. 3 представлены результаты испытания на осыпаемость при четырех различных концентрациях PEG 3000 (0, 100, 200 и 400 мг; все концентрации указаны из расчета на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма)) после манипуляций с гемостатической прокладкой с биологическими препаратами.
Испытание на осыпаемость для определения уменьшения веса порошка после обработки проводили следующим образом. Образец для испытания гемостатической прокладки с биологическими препаратами подвергли интенсивной обработке, применяемой на практике. Сначала зафиксировали вес гемостатической прокладки с биологическими препаратами размером 10,2×10,2 сантиметра (4×4 дюйма). Затем гемостатическую прокладку держали одной рукой над рабочей поверхностью стола на высоте приблизительно 7,6 сантиметра (три дюйма) так, что сторона прокладки с покрытием была обращена вниз. Прокладку разрезали с помощью хирургических ножниц на две части размером приблизительно 5,1×10,2 сантиметра (2×4 дюйма). Отрезанной части позволили упасть на хирургическую салфетку на поверхности стола. Затем каждую из двух частей размером 5,1×10,2 сантиметра (2×4 дюйма) подняли на высоту 30,5 сантиметра (12 дюймов) над хирургической салфеткой, расположенной на поверхности стола, после чего каждую из них уронили три раза. Две части взвесили на весах и выполнили уравновешивание для расчета процента снижения веса порошка по сравнению с первоначальным образцом размером 10,2×10,2 сантиметра (4×4 дюйма). Использованные образцы содержали различные количества PEG и не содержали КМЦ. Результаты представлены в табл. 3.
Испытание на осыпаемость: уменьшение веса порошка после обработки
Анализ данных, представленных в табл. 3, указывает на то, что при выполнении испытания на осыпаемость присутствие PEG 3000 приводило к существенному уменьшению осыпаемости гемостатической прокладки с биологическими препаратами (образцы 6, 7, 8) по сравнению с гемостатической прокладкой с биологическими препаратами без добавления PEG (образец 5), причем вес осыпавшегося порошка уменьшился в диапазоне от приблизительно 11 раз при самом высоком содержании PEG, равном 400 мг, до приблизительно 6 раз при самом низком количестве PEG, соответствующем 100 мг.
Затем образцы, которые подвергали интенсивной обработке, описанной выше, подвергли испытанию на отслоение от ткани в соответствии с процедурой, описанной в примере 2. Данное испытание продемонстрировало синергичный эффект пониженной осыпаемости, а также повышенной смачиваемости и силы отслаивания от ткани у образцов, содержавших PEG в количествах 100, 200 и 400 мг, в устройстве размером 10,2×10,2 см (4×4 дюйма) по сравнению с образцами, содержавшими 0 мг PEG. Усилие отслаивания от ткани измеряли на образцах гемостатических прокладок с биологическими препаратами, которые подвергали стандартизированной описанной выше интенсивной обработке. Результаты отражают синергичный эффект снижения осыпаемости и улучшения адгезии. Анализ результатов эксперимента, представленных на фиг.3, указывает на то, что присутствие PEG 3000 существенно увеличивало усилие отслаивания от ткани после того, как образцы подвергали интенсивной обработке. Результаты испытания на отслаивание от ткани свидетельствовали о положительном дозозависимом эффекте PEG, в соответствии с которым при увеличении содержания PEG увеличивалось и усилие отслаивания, причем образцы, содержащие 400 мг PEG, показали результат в 2-2,5 раза лучше, чем образцы, не содержащие PEG.
Пример 5. Испытание на образование фибринового геля
Испытание на образование фибринового геля, предназначенное для измерения времени, в течение которого в образце из раствора фибрина образуется сгусток (способ переворачивания пробирки), проводили следующим образом. Фибриноген (ERL FIB3) растворили в 200 мМ ТРИС-буферного физиологического раствора в концентрации 10 мг/мл. Образец обладающей признаками изобретения гемостатической прокладки с биологическими препаратами либо контрольной гемостатической прокладки с биологическими препаратами размером приблизительно 1 см2 поместили на дно пробирки из боросиликатного стекла размером 12×75 мм. Образец разместили таким образом, чтобы поверхность с покрытием была обращена вверх. Затем в пробирку добавили 2 мл раствора фибриногена в концентрации 10 мг/мл, после чего ее закрыли, а пробирочный штатив немедленно поместили в водяную баню с температурой 37°C. Каждые десять секунд пробирку вручную переворачивали и ставили обратно в штатив, находящийся в водяной бане. Наблюдения проводили при каждом переворачивании, причем конечной точкой считали время полного гелеобразования, т.е. отсутствия перемещения текучей среды в пробирке.
Результаты испытания заключаются в следующем. При испытании образца контрольной гемостатической прокладки с биологическими препаратами, не содержащей PEG и КМЦ, время образования сгустка из раствора фибрина в двух испытаниях составило 230 и 270 секунд. В случае обладающей признаками изобретения гемостатической прокладки с биологическими препаратами, содержащей 400 мг PEG 3000 и 300 мг КМЦ, для всех концентраций из расчета на один образец гемостатической прокладки с биологическими препаратами размером 10,2×10,2 см (4×4 дюйма) время образования сгустка из раствора фибрина в двух испытаниях составило 90 и 120 секунд.
Результаты указывают на более быстрое загущение раствора фибрина и, следовательно, более быструю смачиваемость, менее выраженную гидрофобность и лучшую доступность тромбина в гемостатических прокладках с биологическими препаратами, которые содержат PEG и КМЦ.
Пример 6. Исследование на проникновение воды
Исследование на проникновение воды проводили следующим образом. Образец гемостатической прокладки с биологическими препаратами размером приблизительно 1 см2 подвергли капельному воздействию воды, подаваемой через шприц на поверхность прокладки с активным покрытием. Затем измерили время впитывания капли воды в образец.
Результаты испытания заключаются в следующем. При испытании номинальной гемостатической прокладки с биологическими препаратами, не содержащей PEG, время впитывания капли воды в образец исчислялось минутами, т.е. составляло более приблизительно 1-2 минут. В случае обладающей признаками изобретения гемостатической прокладки с биологическими препаратами, содержащей 400 мг PEG 3000 и 300 мг КМЦ, время впитывания капли воды в образец исчислялось миллисекундами.
Результаты указывают на более быстрое смачивание и менее выраженную гидрофобность гемостатических прокладок с биологическими препаратами, содержащими PEG и КМЦ.
Хотя в описанных выше примерах демонстрируются определенные варианты осуществления настоящего изобретения, их следует рассматривать не как ограничивающие объем настоящего изобретения, а как дополнительное средство для полного описания настоящего изобретения.


Гемостатическая прокладка, содержащая биологически абсорбируемый каркасный материал; порошок лиофилизированного тромбина, порошок лиофилизированного фибриногена и порошок плавкого связующего вещества, причем все порошки размещены на биологически абсорбируемом каркасном материале. Плавкое связующее вещество, такое как PEG, связывает порошок лиофилизированного тромбина и порошок лиофилизированного фибриногена с биологически абсорбируемым каркасным материалом для улучшения характеристик осыпаемости, смачиваемости и эффективности при применении, таком как гемостатическое лечение или уплотнение тканей в месте расположения раны. 11 з.п. ф-лы, 3 ил., 3 табл. 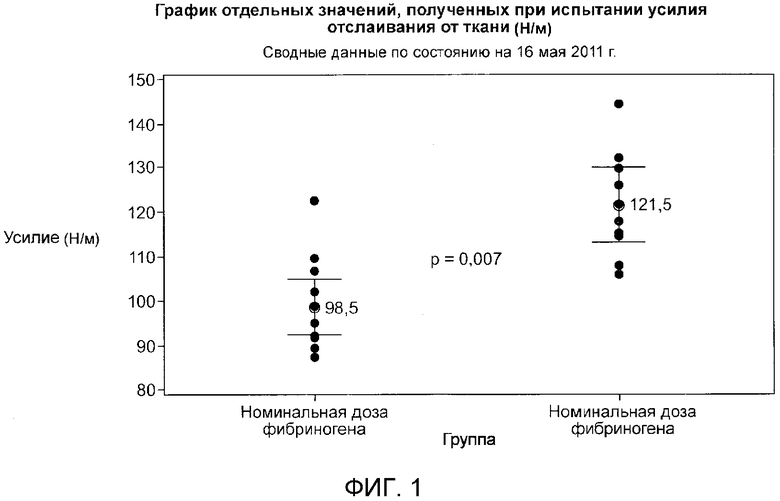
1. Гемостатическая прокладка, содержащая:
a) биологически абсорбируемый материал,
b) порошок лиофилизированного тромбина,
c) порошок лиофилизированного фибриногена, и
d) порошок плавкого связующего вещества, являющегося гидрофильным, биологически совместимым и биологически абсорбируемым материалом, имеющим температуру плавления от приблизительно 25°C до приблизительно 100°C;
причем указанные порошки тромбина и фибриногена распределены на биологически абсорбируемом каркасном материале и порошок плавкого связующего вещества связывает порошок тромбина и порошок фибриногена с биологически абсорбируемым каркасным материалом, но полностью не покрывает или не обволакивает порошок лиофилизированного тромбина и/или порошок лиофилизированного фибриногена.
2. Гемостатическая прокладка по п.1, в которой плавкое связующее вещество содержит полимер полиэтиленгликоля, имеющий среднюю молекулярную массу от приблизительно 1500 до приблизительно 20000 дальтон.
3. Гемостатическая прокладка по п.1, в которой плавкое связующее вещество состоит по существу из полимера полиэтиленгликоля, имеющего среднюю молекулярную массу от приблизительно 2500 до приблизительно 8000 дальтон, более предпочтительно - от приблизительно 2500 до приблизительно 4000 дальтон.
4. Гемостатическая прокладка по п.3, в которой средняя молекулярная масса полимера полиэтиленгликоля в составе порошка связующего вещества составляет приблизительно 3000 дальтон.
5. Гемостатическая прокладка по п.2, в которой частицы связующего вещества имеют средний размер частиц приблизительно 45 микрон.
6. Гемостатическая прокладка по п.2, в которой весовая доля порошка лиофилизированного тромбина составляет приблизительно 10-15%, порошка лиофилизированного фибриногена - приблизительно 55-85%, а полиэтиленгликоля - 2-20%, все из расчета от общего веса порошков тромбина, фибриногена и полиэтиленгликоля на гемостатической прокладке.
7. Гемостатическая прокладка по п.2, в которой биологически абсорбируемый каркасный материал представляет собой тканый или нетканый синтетический или натуральный материал либо их комбинации.
8. Гемостатическая прокладка по п.2, в которой биологически абсорбируемый каркасный материал представляет собой двухслойный материал, содержащий слой нетканых волокон полиглактина 910, вшитый иглопробивным способом в слой трикотажной окисленной регенерированной целлюлозы, причем указанные порошки распределены только на указанном слое нетканых волокон полиглактина 910.
9. Гемостатическая прокладка по п.2, в которой указанный порошок лиофилизированного тромбина и указанный порошок лиофилизированного фибриногена связаны с биологически абсорбируемым каркасным материалом посредством повышения температуры гемостатической прокладки до уровня, превышающего температуру плавления полимера полиэтиленгликоля.
10. Гемостатическая прокладка по п.2, в которой указанная гемостатическая прокладка содержит приблизительно 200-600 МЕ тромбина на 6,45 см2 (квадратный дюйм) указанной гемостатической прокладки в соответствии с измерениями при нанесении, содержит фибриноген в количестве приблизительно 20-80 мг на 6,45 см2 (квадратный дюйм) указанной гемостатической прокладки в соответствии с измерениями при нанесении; и полиэтиленгликоль присутствует в количестве приблизительно 6-25 мг на 6,45 см2 (квадратный дюйм) указанной гемостатической прокладки.
11. Гемостатическая прокладка по п.2, дополнительно содержащая порошок карбоксиметилцеллюлозы (КМЦ).
12. Гемостатическая прокладка по п.11, в которой указанный порошок КМЦ имеет средний размер частиц приблизительно 20 микрон, и причем указанный порошок КМЦ присутствует в количестве приблизительно 15-20 мг на 6,45 см2 (квадратный дюйм) указанной гемостатической прокладки.
| US 20060088589 A1, 27.04.2006 | |||
| US 20110071499 A1, 24.03.2011 | |||
| US 20090246238 A1, 01.10.2009 | |||
| US 4427650 A, 24.01.1984. |
Авторы
Даты
2018-03-06—Публикация
2012-11-28—Подача