Изобретение относится к области медицины и, в частности, к процессам экспериментального моделирования терапевтического воздействия фокусированного ультразвука на сосуды животных для выявления закономерностей, применимых в процессе лечения человека, например, в случае варикозной болезни вен нижних конечностей.
В настоящее время для лечения заболевания сосудов, в частности варикозной болезни вен нижних конечностей, широко применяются малоинвазивные методы - склеротерапия, радиочастотная и эндоваскулярная лазерная абляция. Однако даже эти минимально инвазивные методы требуют хирургического вмешательства, не исключая при этом риск различных осложнений. В последние годы все больше внимания уделяется изучению возможности использования неинвазивного высокоинтенсивного фокусированного ультразвука (HIFU) при венозной патологии.
Основные механизмы действия HIFU на сосуды включают термические эффекты (нагревание свыше 60°C) и механические, связанные с кавитацией, акустическими потоками и т.д. В зависимости от параметров облучения эффекты воздействия HIFU могут быть различными: образование окклюзирующего и неокклюзирующего тромба, разрыв, повреждение отдельных слоев сосудистой стенки без нарушения проходимости, облитерация. В клинике HIFU-технология для лечения варикозных вен еще не получила широкого применения, так как остаются невыясненными условия, определяющие оптимальный эффект. Одним из таких условий является сохранность кровотока в вене, на которую воздействует (HIFU). С другой стороны, важным является изучение влияния выключенного кровотока на характер повреждения стенок вены при воздействии (HIFU).
Первоначально HIFU был предложен для склеротерапии поверхностных вен диаметром менее 2 мм. Объектом воздействия являлись открытые хирургическим способом бедренные вены у крыс. По данным доплеровского обследования все обработанные ультразвуком вены оказались закупоренными тромбами в отличие от контрольных вен, которые остались проходимыми. Гистологические исследования не обнаружили разрушений окружающих нормальных тканей [Delon-Martin and other. Venous thrombosis generation by means of HIFU//Ultrasaund Med. Biol. 1995. v. 1. P 113-119].
По данным работы Хининена [Hininen R. Focused ultrasound surgery guided by MKI//Science and Medicine. 1996. Sept/Oct. V. 3. №5. P. 62-71] результат воздействия HIFU на кровеносные сосуды существенно зависит от размеров сосуда, скорости и объема кровотока (а следовательно, и способности крови уносить тепловую энергию от места воздействия) и от параметров ультразвука (интенсивности, частоты, длительности импульса и т.п.). Объектом исследования были бедренные артерии и вены кроликов. Ультразвуковое воздействие приводило к уменьшению кровотока в сосудах с диаметрами 1-1,3 мм или к сужению сосудов.
В качестве экспериментальных моделей сосудов для исследования воздействия на них HIFU используются кровеносные сосуды различных животных, например, крыс, кроликов, собак и свиней. Крысы неудобны слишком малыми размерами. Использование собак и свиней сопряжено с дополнительными финансовыми трудностями, получением разрешений, созданием особых условий. Кроме того, у всех экспериментальных животных нет системы подкожных вен, подобных венам нижних конечностей, которые есть у человека.
В опытах на кроликах обычно используют вены ушей. Они расположены поверхностно, хорошо визуализируются, доступны, их отключение практически не влияет на жизнедеятельность животного. Но при этом имеется несколько отрицательных моментов. Вена идет непосредственно под кожей и поэтому отсутствует жировая прослойка. Рядом с ней, как правило, расположена артерия, что является причиной передаточной пульсации. Сосуды расположены на хряще и их диаметр не превышает 2 мм. Для четкой УЗИ-визуализации необходимо сбривать волосы на коже над веной, что сопровождается повреждением и отеком окружающих тканей. Все эти факторы затрудняют проведение экспериментов по применению HIFU для облитерации вен. Кроме того, для получения достоверных данных, свидетельствующих об облитерации вены, нужен сосуд диаметром больше, чем 2,5-3 мм. Если воздействовать на сосуд диаметром около 2 мм, то не удастся четко понять механизм облитерации, что лежит в основе повреждения - поражение сосудистой стенки или крови в просвете сосуда.
Таким образом, все многообразие задач, требующих решения при исследовании процесса воздействия HIFU на сосуды, сводится к двум направлениям, а именно воздействию на сосуд с сохраненным кровотоком и воздействию на сосуд с выключенным кровотоком. Важным обстоятельством является то, что в хроническом эксперименте необходимо остановить кровоток для создания условий облитерации сосуда. При этом кролик должен оставаться живым в течение месяца и более. Если учесть, что для получения достоверных данных требуется сосуд диаметром больше, чем 2,5-3 мм, а наиболее пригодные для эксперимента сосуды кролика имеют диаметры не более 2 мм, то эксперименты с сохраненным и выключенным кровотоками не гарантируют в любом из этих случаев достоверных данных. Кроме того, ограниченность диаметров ушных вен кроликов не дает возможность осуществить эксперименты с использованием HIFU на моделях, вены которых были хотя бы сопоставимы с большой подкожной веной человека, что значительно увеличило бы достоверность получаемых данных. Следует также отметить, что в экспериментальной практике неизвестны факты использования одной и той же вены, которая применялась для работы как с открытым, так и выключенным кровотоками. Наличие такой возможности способно значительно расширить диапазон экспериментальных возможностей.
Таким образом, задачей изобретения является повышение достоверности экспериментальных данных, способствующих лучшему пониманию механизмов воздействия HIFU на сосуды, а также расширение диапазона экспериментальных возможностей.
Поставленная задача решается за счет того, что в способе экспериментальной оценки эффективности терапевтического воздействия фокусированного ультразвука на сосуды животных, включающем использование экспериментальной модели в виде сосудистой системы кролика, в качестве модели используют его каудальную вену, которую прошивают в продольном направлении, образуя пару параллельных каналов с сохранением кровотока, по меньшей мере, в одном из них, при этом один из каналов выполняют с просветом не более 70% общего просвета вены и длиной не менее 1 см. Кровоток выключают в канале с большим просветом.
Технический результат изобретения состоит в том, что в качестве экспериментальной модели используют каудальную вену кролика, по своим размерам сопоставимую с большой подкожной веной человека, что уже значительно повышает достоверность исследований, проводимых на сосудах с использованием HIFU. Продольная прошивка вены дает возможность проведения хронических экспериментов с включенным и выключенным кровотоками на одном животном.
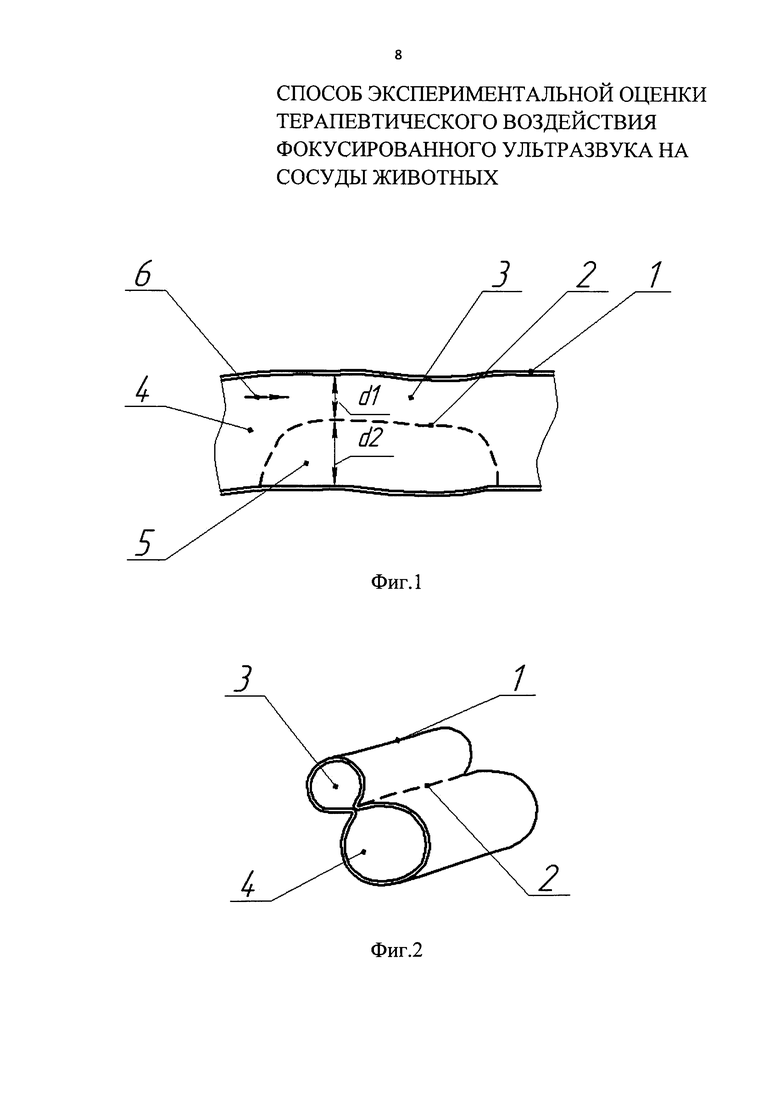
На фиг. 1 дано схематическое изображение каудальной вены кролика, а на фиг. 2 дано 3D-изображения последней, на которых 1 - каудальная вена, 2 - непрерывный шов из атравматичной не рассасывающейся нити, 3 - канал с сохраненным кровотоком, 4 - канал с выключенным кровотоком и внутренней замкнутой полостью 5, 6 - стрелка, указывающая направление кровотока, d1 и d2 - диаметры каналов с сохраненным и выключенным кровотоками соответственно.
Предлагаемый способ реализуется следующим образом.
Каудальная вена 1 у кролика имеет диаметр около 10-12 мм и протяженность вены такого диаметра составляет 2-3 см. Под эндотрахеальной анестезией выполняют верхнесрединную лапаротомию. Все петли тонкой и толстой кишок выводят из брюшной полости влево и укрывают влажной марлевой салфеткой. При этом открывается доступ к каудальной вене на протяжении 4-5 см от нижнего края печени до бифуркации. На этом участке в нее впадают почечные вены, при этом у мест их впадения расположены правый и левый надпочечники. Над каудальной веной рассекают париетальную брюшину, что делать необязательно, так как стенка вены становится тоньше, а это может затруднить УЗИ-визуализацию. Затем под каудальную вену подводят лигатуру 2 и прошивают ее в продольном направлении, образуя пару параллельных каналов 3 и 4 с сохранением кровотока с направлением 6 в одном из них (3), а другой (4) блокируют, что приводит к остановке в нем кровотока и образованию замкнутой полости 5. Выключенный кровоток создает условия для облитерации сосуда. Подвергнутый воздействию HIFU участок с выключенным кровотоком вместе с окружающими тканями иссекают для гистологического исследования. Материал фиксируют в 10% нейтральном формалине на фосфатном буфере (pН 7,4) в течение суток, обезвоживая в серии этанола возрастающей концентрацией и заливая в парафиновые блоки по стандартной гистологической методике. Следует отметить, что эксперимент с выключенным кровотоком целесообразно проводить на максимально возможном диаметре сосуда, т.е. на канале 4, для чего диаметр его просвета выбирался не более 70% общего просвета вены, а длина канала выбиралась не менее 1 см.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования портальной гипертензии у свиньи | 2021 |
|
RU2770735C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ВАРИКОЦЕЛЕ | 1991 |
|
RU2045228C1 |
| Способ деструкции эмбологенного матрикса в эксперименте. | 2020 |
|
RU2739669C1 |
| СРЕДСТВО, УСИЛИВАЮЩЕЕ ЭФФЕКТ ОБРАБОТКИ ФОКУСИРОВАННЫМ УЛЬТРАЗВУКОМ ВЫСОКОЙ ИНТЕНСИВНОСТИ, И СПОСОБ СКРИНИНГА ДАННОГО СРЕДСТВА | 2005 |
|
RU2363494C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ КОРРЕКЦИИ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ У ЖИВОТНЫХ | 1991 |
|
RU2033642C1 |
| Способ моделирования хронической ишемии у экспериментальных животных. | 2022 |
|
RU2777184C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЦИРРОЗА ПЕЧЕНИ В ЭКСПЕРИМЕНТЕ | 2014 |
|
RU2570526C1 |
| СПОСОБ ЛЕЧЕНИЯ ИШЕМИЧЕСКИХ НАРУШЕНИЙ ПЕЧЕНИ | 2014 |
|
RU2563796C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ВАРИКОЗНОЙ БОЛЕЗНИ ВЕН НИЖНИХ КОНЕЧНОСТЕЙ У СОБАК | 2023 |
|
RU2823139C1 |
| СПОСОБ ПРОВЕДЕНИЯ ПЕРВОГО ЭТАПА ЛЕЧЕНИЯ БОЛЬНЫХ СОЧЕТАННЫМИ СТРИКТУРАМИ ПИЩЕВОДА И АНТРАЛЬНОГО ОТДЕЛА ЖЕЛУДКА | 2006 |
|
RU2316271C1 |
Изобретение относится к экспериментальной медицине, в частности к изучению терапевтического воздействия фокусированного ультразвука на сосуды. Способ экспериментальной оценки эффективности воздействия ультразвука включает использование каудальной вены кролика. Для этого, при выполнении верхнесрединной лапаротомии, открывают доступ к каудальной вене, подводят под нее лигатуру и прошивают участок вены в продольном направлении, образуя пару параллельных каналов с сохранением кровотока, по меньшей мере, в одном из них. Технический результат изобретения состоит в том, что модель сосуда, по своим размерам сопоставимая с большой подкожной веной человека, значительно повышает достоверность исследований, а продольная прошивка вены дает возможность проведения хронических экспериментов с включенным и выключенным кровотоками на одном животном. 1 з.п. ф-лы, 2 ил.
1. Способ экспериментальной оценки эффективности терапевтического воздействия фокусированного ультразвука на сосуд, включающий использование вены кролика, отличающийся тем, что в качестве модели используют каудальную вену кролика, для этого при выполнении верхнесрединной лапаротомии открывают доступ к каудальной вене, подводят под нее лигатуру и прошивают участок вены в продольном направлении, образуя пару параллельных каналов с сохранением кровотока, по меньшей мере, в одном из них.
2. Способ по п. 1, в котором один из каналов выполняют с просветом не более 70% общего просвета вены и длиной не менее 1 см и этот канал используют для эксперимента с выключенным кровотоком.
| HININEN R | |||
| Focused ultrasound surgery guided by MKI | |||
| Science and Medicine | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| Sept/Oct | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ВАРИКОЗНОГО РАСШИРЕНИЯ ВЕН ПИЩЕВОДА И ЖЕЛУДКА В ЭКСПЕРИМЕНТЕ НА СОБАКАХ | 2004 |
|
RU2282900C1 |
| RU 2012128416 A, 20.01.2014 | |||
| US 20140188102 A1, 03.07.2014 | |||
| US 6436061 B1, 20.08.2002 | |||
| CN 102406982 A, 11.04.2012 | |||
| DELON-MARTIN C Venous thrombosis generation by means of high-intensity focused ultrasound | |||
| Ultrasound Med Biol | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
Авторы
Даты
2018-03-15—Публикация
2016-12-27—Подача