Изобретение относится к области ветеринарной вирусологии, в частности к способу диагностики вируса нодулярного дерматита КРС.
Известен способ обнаружения специфических антител к вирусам оспы овец и коз методом ингибирования твердофазного иммуноферментного анализа, предусматривающий взаимодействие исследуемой сыворотки крови с антигеном вируса оспы овец и последующую детекцию иммобилизированного на твердой фазе комплекса антитело - специфический антиген поликлональным пероксидазным конъюгатом, где на первом этапе реакции происходит взаимодействие исследуемой сыворотки с культуральным антигеном вируса оспы овец, на втором этапе не вступивший в реакцию антиген взаимодействует с иммобилизированными на твердой фазе моноклональными антителами клона 08.3, обладающими специфичностью к антигенной детерминанте полипептида молекулярной массы 36-40 кД вируса оспы овец штамма "НИСХИ", а образовавшийся комплекс моноклональное антитело - антиген выявляют специфическим пероксидазным конъюгатом поликлональных антител, выделенных из гипериммунной сыворотки животных-реконвалесцентов (патент РФ №2202112, кл. A61K 39/275, G12Q 1/68).
Известен метод диагностики оспы коз и овец (Орлова Е.С. Совершенствование методов диагностики оспы овец и оспы коз: автореф. дис.канд. биол. наук / Е.С.Орлова. - Владимир, 2007 г. - 25 с.), включающий проведение ПЦР в реакционной смеси следующего состава: 2,5 мкл 10х буфера для Taq-полимеразы, 3 мМ Mg2+0,2 мМ dNTPs, 1,0 ед. Taq-полимеразы, по 10 пмоль праймеров, 3 мкл раствора вирусной ДНК и вода до конечного объема 25 мкл на ДНК-амплификаторе РТС-100 (MJ Research, США) при следующем температурном режиме: 2 мин предварительной денатурации при 94°С, 35 циклов амплификации (30 с денатурации при 94°С, 30 с отжига праймеров при 55°С, 30 с элонгации при 72°С) и 2 мин заключительной элонгации, с возможным (при необходимости) проведением второго этапа амплификации с внутренними праймерами в смеси аналогичного состава в течение 20-25 циклов, далее продукты реакции анализировали с помощью электорофореза в 2,0% агарозном геле, содержащем 0,001% бромистого этидия, при силе тока 50 мА.
Недостатком данного способа является то, что он дает только качественный результат.
Известно техническое решение (Касьян Ж.А. и др. «Разработка тест-системы для дифференциации видов бруцелл методом ПНР с учетом результатов в режиме реального времени. Проблемы особо опасных инфекций. 2016, вып. 3, с. 47-51. http://ioumal.microbe.ru/iour - прототип) отбор проб патологического материала из очага инфекционного заболевания, экстракцию ДНК бактерий инфекционного заболевания из полученных проб, идентификацию видовой принадлежности возбудителя болезни методом полимеразной цепной реакции с флуоресцентным учетом результатов в режиме реального времени с применением термоциклера типа RotorGene на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией.
Недостатком данного способа является ограниченная применимость только к возбудителю бруцеллеза и отсутствие возможности диагностирования раннего развития заболевания.
Техническим результатом является расширение функциональных возможностей способа, предотвращение массового распространения заболевания и перехода его в тяжелую запущенную форму.
Технический результат достигается тем, что в способе экспресс-диагностики нодулярного дерматита крупного рогатого скота, включающем отбор проб патологического материала из очага инфекционного заболевания, экстракцию ДНК бактерий инфекционного заболевания из полученных проб, идентификацию видовой принадлежности возбудителя болезни методом полимеразной цепной реакции с флуоресцентным учетом результатов в режиме реального времени с применением термоциклера типа RotorGene на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией, согласно изобретению в качестве патологического материала используют пробы из очага инфекционного заболевания нодулярного дерматита, при этом отбор проб патологического материала осуществляют от всех животных, находящихся в очаге инфекционного заболевания, и проводят экспресс-диагностику полученного патологического материала в течение суток для выявления животных-носителей вируса нодулярного дерматита на начальной стадии инфицирования, при этом учет результатов полимеразной цепной реакции проводят по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, если наблюдают рост специфического сигнала, то образец считают положительным - вирус нодулярного дерматита крупного рогата скота присутствует, при этом значения контрольных образцов находятся в пределах нормы, если не наблюдают рост специфического сигнала, то образец считают отрицательным - вирус нодулярного дерматита крупного рогата скота отсутствует и значения контрольных образцов также находятся в пределах нормы.
Новизна заявляемого способа экспресс-диагностики нодулярного дерматита крупного рогата скота состоит в идентификации вируса нодулярного дерматита в пробах патологического материала с помощью полимеразной цепной реакции (ПНР) с флуоресцентной детекцией в режиме реального времени, что в свою очередь позволяет выявить животных-носителей вируса заболевания на начальной стадии инфицирования животных.
Признаки, отличающие заявляемое техническое решение от прототипа, направлены на достижение технического результата и не выявлены при изучении данной и смежной областей науки и техники и, следовательно, соответствуют критерию «изобретательский уровень».
Заявляемый способ экспресс-диагностики вируса нодулярного дерматита крупного рогатого скота рекомендовано использовать в специализированных ветеринарных, санитарно-эпидемиологических, животноводческих, сельскохозяйственных предприятиях, что соответствует критерию «промышленная применимость».
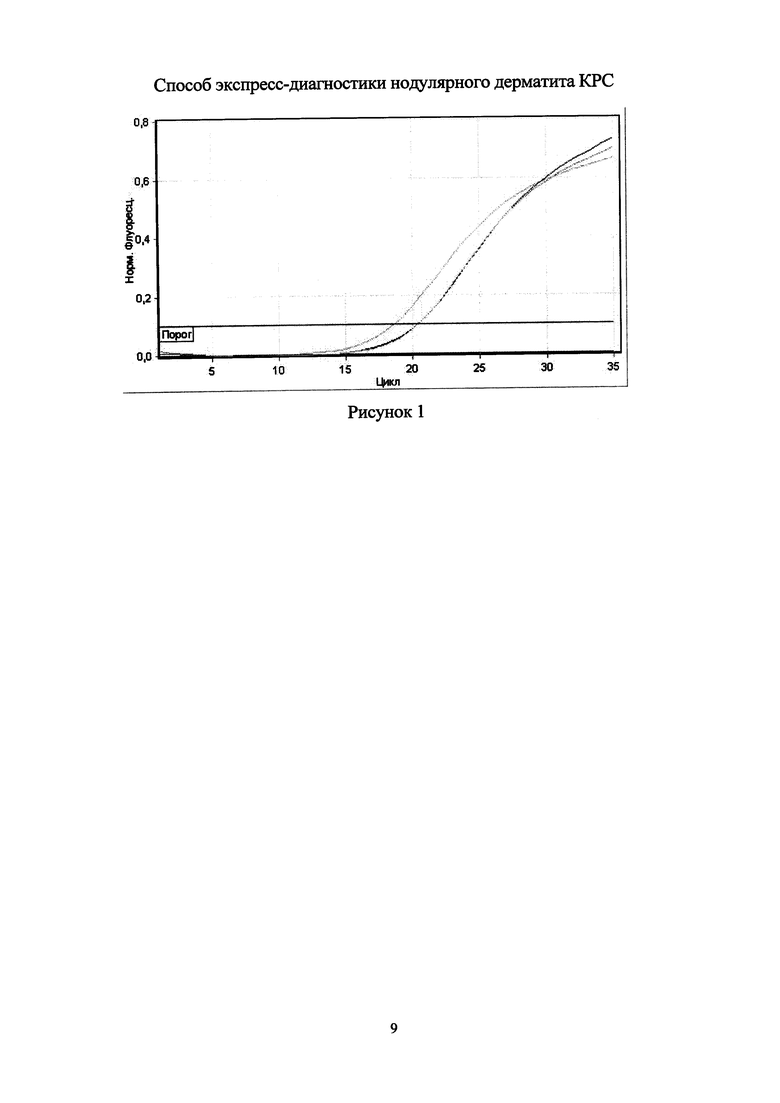
Сущность изобретения поясняется чертежом, где на рисунке 1 представлен график результатов экспресс-диагностики нодулярного дерматита.
Способ экспресс-диагностики нодулярного дерматита крупного рогатого скота осуществляют следующим образом.
В стаде овец или коз осуществляют отбор проб патологического материала от каждого животного из очага инфекционного заболевания нодулярного дерматита. При отборе проб и подготовке проб для исследования соблюдают меры, предупреждающие обсеменение объектов внешней среды. Материал от каждого животного отбирают отдельными инструментами.
Цельная кровь забирается в пробирку с 6% ЭДТА из расчета 50 мкл раствора ЭДГА на 1 мл крови, закрытую пробирку с кровью несколько раз переворачивают. Для получения сыворотки забирают кровь в пробирку без антикоагулянта. Помимо крови, в качестве исследуемого материала также используют фрагменты тканей и органов (нодулы, селезенка, лимфатические узлы), которые отбирают в стерильный контейнер. Для подготовки пробы к проведению полимеразной цепной реакции используют различные методики, с помощью которых осуществляют экстракцию ДНК из полученных образцов сыворотки крови животных и удалении или нейтрализации посторонних примесей для получения препарата ДНК с чистотой, пригодной для проведения полимеразной цепной реакции.
После подготовки исследуемого материала приступают к проведению анализа, состоящего из 3 этапов:
- экстракция ДНК;
- проведение полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени;
- учет результатов анализа.
ПЦР с флуоресцентной детекцией в режиме реального времени имеет ряд значительных преимуществ:
- объединение этапов амплификации и детекции результатов. Появляется возможность оценить кинетику процесса, которая зависит от начального количества исследуемого материала;
- существенное снижение риска контаминации и ошибок при анализе результатов;
- высокая специфичность реакции за счет использования высокоспецифичных флуоресцентных зондов;
- высокая производительность;
- упрощение требований к организации ПЦР-лаборатории;
- возможность количественной оценки исходной ДНК матрицы;
- регистрация и учет данных в электронном формате.
ПЦР в реальном времени характеризуется возможностью проведения качественного и количественного анализа. Регистрируемое в процессе амплификации нарастание сигнала от отделенного флуорофора прямо пропорционально увеличению концентрации синтезированных специфических продуктов и отражает концентрацию ДНК в исходной матрице.
Экстракция ДНК
Перед выделением ДНК осуществляют подготовку исследуемых проб с помощью набора реагентов «ПЦР-НОДУЛЯРНЫЙ ДЕРМАТИТ КРС-ФАКТОР», состоящий из 2 комплектов (таблица 1 и 2).
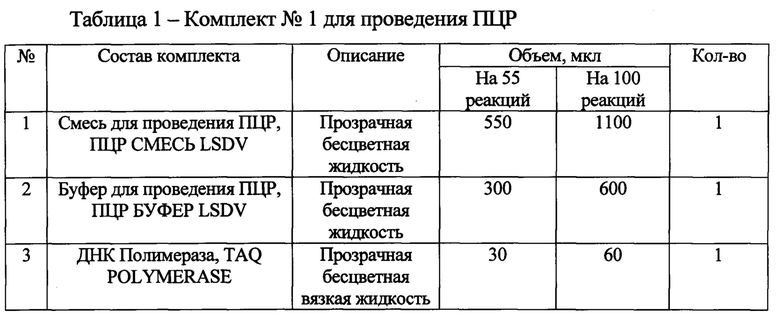
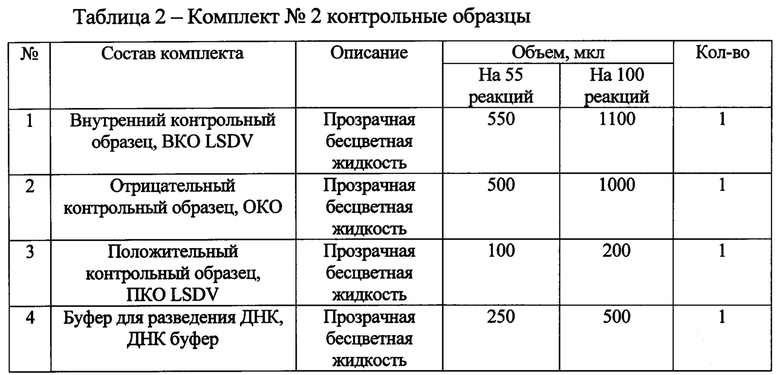
При подготовке образцов в отдельной пробирке смешивают компоненты набора из расчета на каждую реакцию: 10 мкл ПЦР СМЕСЬ LSDV, 5 мкл смеси ПЦР БУФЕР LSDV, 0,5 мкл TAQ POLYMERASE, данную смесь перемешивают и сбрасывают капли кратковременным центрифугированием. Затем отбирают необходимое количество пробирок для амплификации ДНК исследуемых и контрольных проб, вносят по 15 мкл приготовленной реакционной смеси. Используя наконечники с фильтром, в подготовленные пробирки добавляют:
1) отрицательный контроль ПЦР (К-) - вносят в пробирку по 10 мкл отрицательного контрольного образца;
2) по 10 мкл ДНК из исследуемых образцов (включая ОКО) в соответствующие пробирки;
3) положительный контроль ПЦР (К+) - вносят в пробирку 10 мкл положительного контрольного образца LSDV.
При этом не наносят маркировку на крышку пробирок, т.к. это затрудняет процесс считывания амплификатором.
Проведение полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени.
Устанавливают пробирки в реакционный модуль прибора «Rotor-Gene 3000/6000» (Q), в котором осуществляют полимеразную цепную реакцию с флуоресцентным детектором в режиме реального времени. В соответствии с протоколом анализа прибор программируют, устанавливают параметры температурно-временного режима амплификации, детекцию флуоресцентного сигнала назначают после стации отжига праймеров, после чего начинают процесс амплификации с флуоресцентной детекцией в режиме реального времени. В его основе лежит принцип флуоресцентной детекции продуктов полимеразной цепной реакции непосредственно в ходе амплификации. Детекция продуктов амплификации проводится прямо в реакционной среде через стенки или крышку закрытой пробирки.
Учет результатов полимеразной цепной реакции проводят по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией (рисунок 1). Образец считают положительным (вирус нодулярного дерматита крупного рогатого скота присутствует), если наблюдают рост специфического сигнала, при этом значения контрольных образцов находятся в пределах нормы (таблица 3). Образец считают отрицательным (вирус нодулярного дерматита крупного рогатого скота отсутствует), если не наблюдают рост специфического сигнала, при этом значения контрольных образцов находятся в пределах нормы.
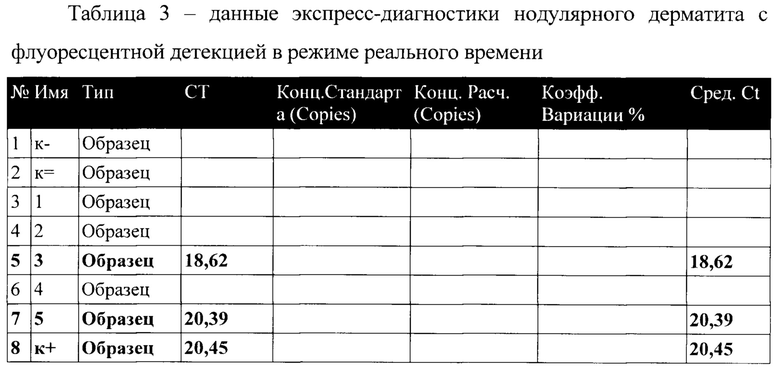
Таким образом, результаты исследований показывают, что заявляемый способ экспресс-диагностики нодулярного дерматита КРС, состоящий из идентификации вируса нодулярного дерматита в пробах патологического материала с помощью полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени позволяет выявить животных-носителей вируса нодулярного дерматита на начальной стадии их инфицирования, что в свою очередь не позволит заболеванию массово распространиться, перейти в более тяжелую и запущенную форму.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ профилактики нодулярного дерматита КРС | 2016 |
|
RU2619337C1 |
| Способ выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных с помощью полимеразной цепной реакции в режиме реального времени | 2019 |
|
RU2719719C1 |
| Способ определения ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле | 2019 |
|
RU2728660C1 |
| Способ профилактики оспы овец и коз | 2016 |
|
RU2619336C1 |
| Способ профилактики африканской чумы свиней | 2016 |
|
RU2629399C1 |
| Способ экспресс-диагностики оспы овец и коз | 2016 |
|
RU2648845C2 |
| Олигонуклеотидные праймеры и флуоресцентно-меченый зонд, способ и тест-система для выявления генома полевых изолятов вируса заразного узелкового дерматита (нодулярного дерматита) КРС в реакции полимеразной цепной реакции в режиме реального времени | 2017 |
|
RU2668398C1 |
| Олигонуклеотидные праймеры и флуоресцентно-меченый зонд, способ и тест-система для выявления генома вируса заразного узелкового дерматита (нодулярного дерматита) КРС в реакции полимеразной цепной реакции в режиме реального времени | 2019 |
|
RU2714045C1 |
| Тест-система для выявления ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных с помощью полимеразной цепной реакции в режиме реального времени | 2019 |
|
RU2726242C1 |
| Тест-система для определения ДНК вируса нодулярного дерматита (LSDV) в биологическом материале животных методом ПЦР с электрофоретической детекцией продуктов амплификации в агарозном геле | 2019 |
|
RU2726432C1 |
Изобретение относится к области ветеринарной вирусологии, в частности к способу экспресс-диагностики нодулярного дерматита крупного рогатого скота (КРС). Способ экспресс-диагностики вируса нодулярного дерматита КРС включает отбор проб патологического материала из очага инфекционного заболевания от всех животных, находящихся в очаге инфекционного заболевания, и проведение экспресс-диагностики полученного патологического материала в течение суток методом ПЦР с флуоресцентным учетом результатов в режиме реального времени с применением термоциклера типа RotorGene для выявления животных-носителей вируса нодулярного дерматита на начальной стадии инфицирования, при этом учет результатов ПЦР проводят по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, если наблюдают рост специфического сигнала, то образец считают положительным - вирус нодулярного дерматита КРС присутствует, при этом значения контрольных образцов находятся в пределах нормы, если не наблюдают рост специфического сигнала, то образец считают отрицательным - вирус нодулярного дерматита крупного рогата скота отсутствует, и значения контрольных образцов также находятся в пределах нормы. 3 табл., 1 ил.
Способ экспресс-диагностики вируса нодулярного дерматита крупного рогатого скота, включающий отбор проб патологического материала из очага инфекционного заболевания, экстракцию ДНК бактерий инфекционного заболевания из полученных проб, идентификацию видовой принадлежности возбудителя болезни методом полимеразной цепной реакции с флуоресцентным учетом результатов в режиме реального времени с применением термоциклера типа RotorGene на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией, отличающийся тем, что в качестве патологического материала используют пробы из очага инфекционного заболевания нодулярного дерматита крупного рогата скота, при этом отбор проб патологического материала осуществляют от всех животных, находящихся в очаге инфекционного заболевания, и проводят экспресс-диагностику полученного патологического материала в течение суток для выявления животных-носителей вируса нодулярного дерматита на начальной стадии инфицирования, при этом учет результатов полимеразной цепной реакции проводят по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, если наблюдают рост специфического сигнала, то образец считают положительным - вирус нодулярного дерматита крупного рогата скота присутствует, при этом значения контрольных образцов находятся в пределах нормы, если не наблюдают рост специфического сигнала, то образец считают отрицательным - вирус нодулярного дерматита крупного рогата скота отсутствует, и значения контрольных образцов также находятся в пределах нормы.
| Mohammed Body et al | |||
| Clinico-Histopathological Findings and PCR Based Diagnosis of Lumpy Skin Disease in the Sultanate of Oman | |||
| Pakistan Veterinary Journal, 2012, vol | |||
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| СПОСОБ ОБНАРУЖЕНИЯ СПЕЦИФИЧЕСКИХ АНТИТЕЛ К ВИРУСАМ ОСПЫ ОВЕЦ И ОСПЫ КОЗ МЕТОДОМ ДВУХФАЗНОГО ИНГИБИРОВАНИЯ ТВЕРДОФАЗНОГО ИММУНОФЕРМЕНТНОГО АНАЛИЗА НА ОСНОВЕ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ | 2001 |
|
RU2202112C1 |
| Е.С.Орлова | |||
| Совершенствование методов диагностики оспы овец и оспы коз | |||
| Автореферат дис | |||
| на соиск | |||
| уч | |||
| степ | |||
| к.б.н, Владимир, 2007. | |||
Авторы
Даты
2018-03-28—Публикация
2016-08-08—Подача