Изобретение относится к ортотопическому искусственному эндопротезу мочевого пузыря.
Применение изобретения заключается в замене мочевого пузыря пациента, если последний страдает от серьезных неизлечимых заболеваний, которые нарушают его нормальное функционирование.
Известные эндопротезы мочевого пузыря содержат оболочку баллона, изготовленную из непроницаемой многослойной силиконовой мембраны.
Такая оболочка является достаточно жесткой для того, чтобы стабильно поддерживать свою форму, и гибкой для того, чтобы была возможность сжать ее вручную для обеспечения опорожнения.
Оболочка имеет соединительный элемент, расположенный на нижней части оболочки для соединения с уретрой пациента. Кроме того, два соединительных тела находятся в верхней части для того, чтобы обеспечить соединение с мочеточниками.
Само соединение производится путем наложения швов или простого сцепления.
После имплантации эндопротеза пациенту происходит формирование слоя (ненепроницаемого) мышечно-волокнистой ткани вокруг оболочки. Таким образом, вокруг эндопротеза создается неоцистис.
Поскольку эндопротезы известного типа являются постоянными, осложнения могут возникать даже после окончания реабилитации пациента.
Действительно, спонтанно или после катетеризации может произойти инфицирование неоцистиса.
В таком случае, необходимо соответствующее лечение антибиотиком. Такие лекарственные средства являются эффективными в уничтожении скопления бактерий, локализованных в биологической ткани, и имеют низкое или даже нулевое воздействие в отношении скопления бактерий, локализованных в искусственных материалах, таких как те, из которых изготовлена оболочка. Следовательно, неблагоприятным является то, что эндопротезы известного типа могут являться препятствием для эффективного лечения антибиотиками.
В этом контексте, техническая задача, лежащая в основе настоящего изобретения, заключается в предложении ортотопического искусственного эндопротеза мочевого пузыря, который преодолевает этот недостаток вышеуказанного предшествующего уровня техники.
В частности, цель настоящего изобретения состоит в том, чтобы предоставить ортотопический искусственный эндопротез мочевого пузыря, который снижает риски, связанные с бактериальными инфекциями.
Указанная техническая задача и указанная цель, по существу, достигаются посредством ортотопического искусственного эндопротеза мочевого пузыря, содержащего технические признаки, изложенные в одном или нескольких пунктах прилагаемой формулы изобретения.
Дополнительные характеристики и преимущества настоящего изобретения выявятся более четко из следующего неограничивающего описания предпочтительного, но не исключительного варианта осуществления ортотопического искусственного эндопротеза мочевого пузыря, как показано на прилагаемых чертежах, на которых:
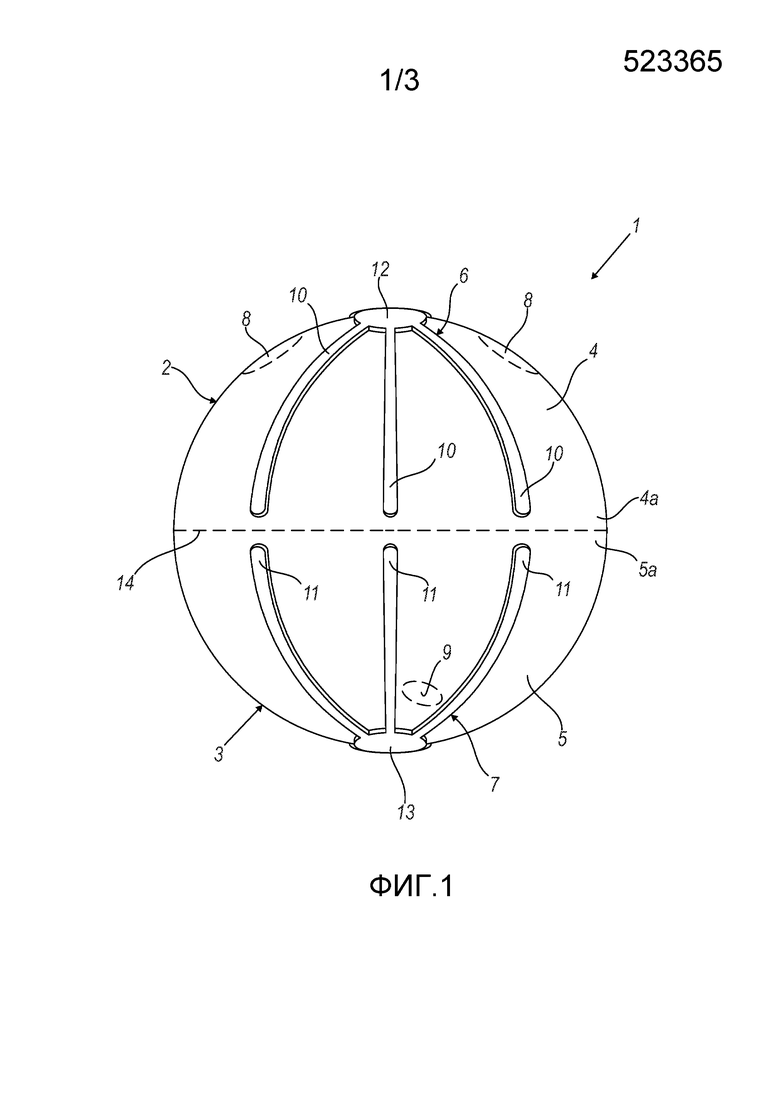
- на фиг. 1 представлен схематический вид сбоку ортотопического искусственного эндопротеза мочевого пузыря в соответствии с настоящим изобретением, согласно первому варианту осуществления;
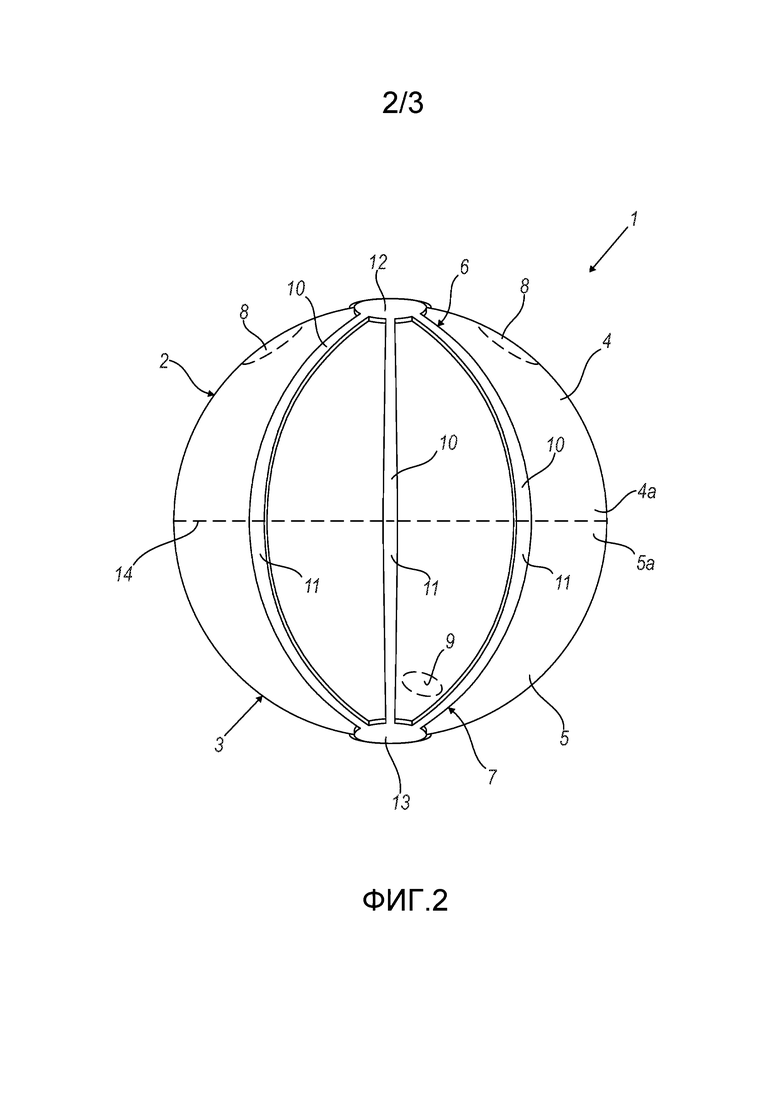
- на фиг. 2 представлен схематический вид сбоку ортотопического искусственного эндопротеза мочевого пузыря в соответствии с настоящим изобретением, согласно второму варианту осуществления;
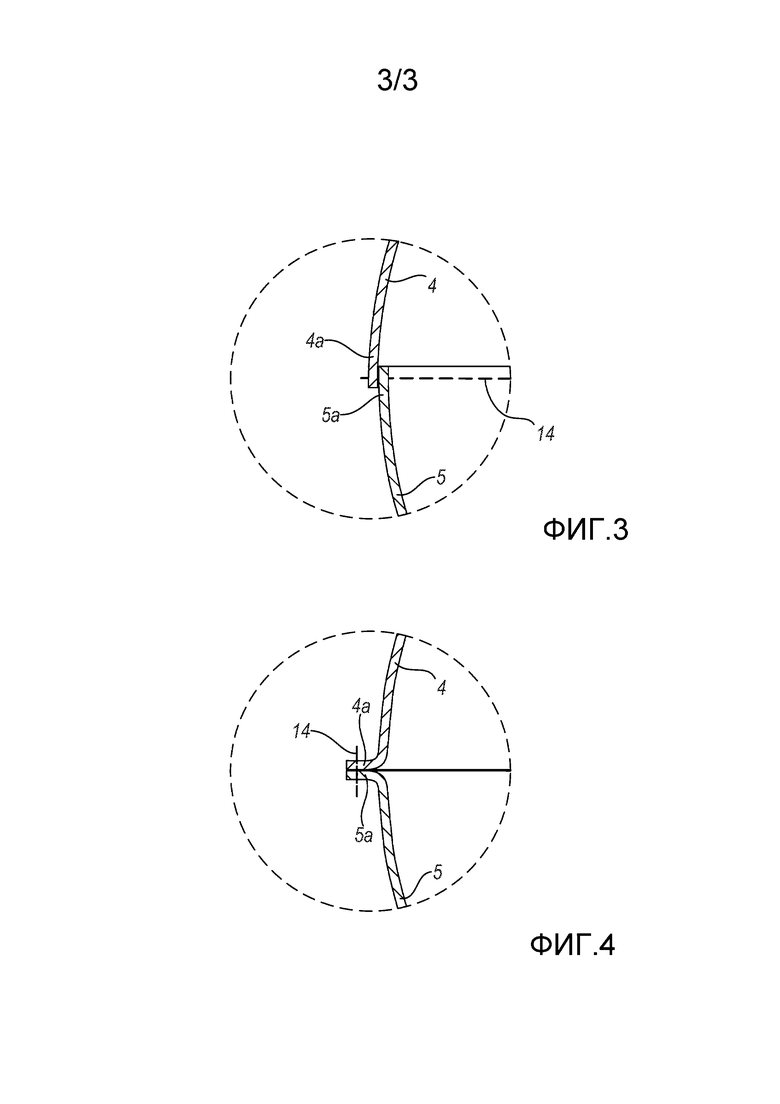
- на фиг. 3 и 4 представлены виды в разрезе соответствующих вариантов осуществления детали эндопротеза, показанной на фиг. 1.
Как показано на прилагаемых чертежах, ссылочная позиция 1 указывает ортотопический искусственный эндопротез мочевого пузыря в соответствии с настоящим изобретением. Эндопротез 1 содержит две части 2, 3, которые соединены друг с другом. Предпочтительно части 2, 3 эквивалентны друг другу. Предпочтительно части 2,3 соединены друг с другом с помощью рассасывающегося шовного материала.
Части 2, 3 имеют, по существу, полусферическую форму и соединены таким образом, что их вогнутости обращены друг на друга. Таким образом, две соединенные части 2, 3 определяют замкнутую полость для содержания мочи. Объем полости лежит по существу в диапазоне между 100 см3 и 900 см3, предпочтительно составляет 400 см3. Первая часть 2 предназначена для подсоединения к мочеточникам пациента. Вторая часть 3 предназначена для подсоединения к уретре патента.
Каждая из частей 2, 3 содержит способную рассасываться чашу 4, 5. Чаши 4, 5 соединены друг с другом.
В частности, чаша 4 первой части 2 и чаша 5 второй части 3 соединены друг с другом вдоль соответствующих краев 4a, 5b.
Соединение между чашами 4, 5 достигается с помощью рассасывающегося шовного материала 14.
В соответствии с вариантом осуществления, показанном на фиг. 3, соединение осуществляется путем совмещения внутренней стороны края 4а чаши 4 первой части 2 к внешней стороне края 5а чаши 5 второй части 3.
В соответствии с непоказанным вариантом осуществления, соединение осуществляется путем совмещения внешней стороны края 4а чаши 4 первой части 2 к внутренней стороне края 5а чаши 5 второй части 3.
В соответствии с вариантом осуществления, показанном на фиг. 4, соединение осуществляется путем совмещения внутренней стороны края 4а чаши 4 первой части 2 к внутренней стороне края 5а чаши 5 второй части 3.
Каждая из чаш 4, 5 получается с помощью материала по существу круглой, плоской формы. Кроме того, каждая из частей 2, 3 содержит каркас 6, 7, прикрепленный к материалу.
Каркас 6, 7 действует как несущая конструкция для материала, что позволяет ему принимать куполообразную форму, которая поддерживается как таковая даже под тяжестью новообразования фиброзной капсулы.
Материал чаш 3, 4 изготовлен с применением сверхлегкой нити или хирургической мононити, производной предпочтительно из волокон на основе гомополимера PGA (полигликолида или полигликолиевой кислоты). PGA имеет высокую биосовместимость, является способным рассасываться полимером и устойчива к моче. В частности, время рассасывания PGA составляет приблизительно один месяц. Предпочтительно использование PGA волокон в получении материала для чаш 3, 4 делает возможным формирование мышечно-волокнистой соединительной ткани в течение фазы резорбции эндопротеза 1.
Кроме того, всегда во время резорбции имеет место формирование переходного эпителиального слоя, который также называют уротелий. Преимущественно слой уротелия является непроницаемым, существенный факт для того, чтобы обеспечить правильное функционирование протеза и неоцистиса, который в это время формируется.
Кроме того, как только эндопротез 1 вставлен, материал чаш 4, 5 покрытия пропитывается кровью, и, в частности, плазмой, которая обеспечивает эффективность антибиотиков на эндопротезе. Материал чаш 3, 4 может быть получен с помощью плетения PGA нити различными способами, порождая трикотажное полотно, тканый материал или нетканый материал.
Предпочтительно, материал является трикотажным полотном, еще более предпочтительно основосвязанным полотном.
В этом случае, материал имеет грубую поверхность, способную приобрести сетчатое строение с достаточно маленькими ячейками.
В деталях, ее уток такой, что ее межуточное пространство меньше чем 200 мкм, предпочтительно около 160 пм, что соответствует средней площади отверстий, равных приблизительно 0,02 мм2. Это гарантирует непроницаемость для мочи, предотвращая утечки.
Кроме того, предпочтительно, чтобы материал был текстурирован таким образом, чтобы придать ему еще большую шероховатость его поверхности и большую жесткость и непроницаемость. Большая шероховатость материала ограничивает риск адгезии фиброзной капсулы.
Исключительно в качестве примера, материал имеет диаметр, по существу, в диапазоне между 8 и 20 см.
Еще в качестве примера, материал имеет толщину, по существу, в диапазоне между 0,3 и 0,6 мм, более предпочтительно в диапазоне между 0,4 и 0,53 мм, еще более предпочтительно, по существу, 0,45 мм.
На материале чаши 4 первой части 2 имеются две области 8 соединения, предназначенные для подсоединения мочеточников пациента к эндопротезу 1. В частности, когда эндопротез 1 имплантируется, хирург делает отверстие в чаше 4 в областях 8 соединения в соответствии с диаметром мочеточников, раздвигает свободные концы мочеточников и сшивает такие концы с чашей 4. Аналогично, на материале чаши 5 второй части 3, область 9 соединения, о которой идет речь, предназначена для подсоединения уретры пациента к эндопротезу 1. В частности, когда эндопротез 1 имплантирован, хирург делает отверстие в чаше 5 в области 9 соединения, чтобы оно соответствовало диаметру уретры, раздвигает свободный конец уретры и сшивает такой конец с чашей 5.
Каждый из каркасов 6, 7 содержит множество ответвлений 10, 11, расположенных в виде звезды и определяющих профиль купола. Более подробно, все ответвления 10, 11 имеют изогнутую форму и скреплены вместе в соединяющей части 12, 13, расположенной вверху каждой части 2, 3.
Каркасы 6, 7 расположены снаружи чаш 4, 5. В частности, каждый из каркасов 6, 7 крепится к материалу с помощью рассасывающегося шовного материала.
Как правило, толщина каркасов 6, 7, т.е. ответвления 10, 11 и соединяющие части 12, 13, находится в диапазоне между 0,1 и 10 мм, предпочтительно между 0,5 и 2 мм. В предпочтительном варианте осуществления толщина по существу составляет 1 мм.
Каркасы 6, 7 получают путем инъекции сополимера молочной кислоты и гликолевой кислот, обозначаемого как PGA/PLA (сополимер молочной и гликолевой кислот), чья куполообразная форма сообщается при нагревании посредством термоформования.
Поскольку молекула молочной кислоты является хиральной, существуют различные типы полимеров, PDLA, PLLA, PDLLA, где D и L представляют собой два стереоизомера. PLLA имеет степень кристалличности 37%, температуру перехода в стеклообразное состояние в диапазоне между 50 и 80°С и температуру плавления в диапазоне между 173 и 178°С, в то время как полимер, получающийся при полимеризации рацемической смеси, PDLLA, является неупорядоченным.
Термин поли(молочная) кислота здесь предназначен для определения всех различных вышеупомянутых типов PLA.
PGA/PLA-сополимер, с которым выполнен каркас 9, образуется количеством PGA, составляющим от 20 до 30% и количеством PLA, соответственно, составляющим от 70 до 80%.
Особенно предпочтительный PGA/PLA (сополимер молочной и гликолевой кислот) сополимер является сополимером L-молочной и гликолевой кислот) (PLLA/PGA), в котором молярный процент L-молочной кислоты составляет от 82-88% в молях, тогда как молярное процент гликолевой кислоты составляет от 18-12%. Этот сополимер известен под коммерческим названием Resomer® LG855S.
Согласно показанному на фиг. 1, ответвления 10 первой части 2 и ответвления 11 второй части 3 являются раздельными и размещены с промежутками.
Свободные концы ответвлений 10 первой части 2 и ответвления 11 второй части 3 соответствуют друг другу.
В непоказанном варианте осуществления, свободные концы ответвления 10 первой части 2 и ответвления 11 второй части 3 смещены относительно друг друга и чередуются.
В соответствии с показанным на фиг. 2, ответвления 10 первой части 2 и ответвления 11 второй части 3 выполнены в виде единой детали для того, чтобы придать дополнительную жесткость эндопротезу 1.
Заявитель неожиданно обнаружил, что чаши 4, 5, изготовленные с помощью PGA материала как описано выше, в частности текстурированного, в сочетании с PGA/PLA каркасами 6, 7, показывают хорошую механическую целостность и достаточную жесткость даже в присутствии мочи, и поэтому они способны обеспечить правильную деформацию мочевого пузыря при опорожнении и/или его заполнении, вместе с этим показывая хорошую устойчивость к утечкам мочи. Кроме того, было доказано, что чаши 4, 5 и каркасы 6, 7 являются нейтральными при контакте с растущей новой тканью. Это включает в себя быстрое заселение устройства клетками окружающей растущей ткани. В то же время было доказано, что сращение уменьшается благодаря уменьшению взаимодействия между полимерами, которые составляют чаши 4, 5 и каркасами 6, 7 и биологическими молекулами, таким образом, обеспечивая адгезию к внутренним тканям пациента.
Описанное изобретение достигает заранее установленной цели.
Действительно, так как эндопротез после имплантации полностью пропитывается кровью и плазмой, антибиотики являются полностью эффективными и риск осложнений, вызванных бактериальной инфекцией, значительно снижается.
Кроме того, следует отметить, что эндопротез, являющийся предметом настоящего изобретения, способен полностью рассасываться. Таким образом, никакое инородное тело не остается у пациента после операции.
Изобретение относится к области медицины, хирургии. Протез ортотопического искусственного мочевого пузыря состоит из двух частей, соединенных друг с другом в замкнутую полость. Каждая из частей содержит каркас и рассасывающуюся чашу из материала из PGA волокон. Каркас, выполненный из PGA/PLA-сополимера, связан с чашей. Протез позволяет заменить естественный пузырь, обеспечивает биологическую совместимость при формировании слоя мышечно-волокнистой ткани неоцистиса вокруг оболочки эндопротеза. 8 з.п. ф-лы, 4 ил.
1. Ортотопический искусственный эндопротез мочевого пузыря, отличающийся тем, что он содержит две части (2, 3), соединенные друг с другом; причем каждая часть (2, 3) содержит соответствующую рассасываемую чашу (4, 5), изготовленную из материала из PGA волокон, и соответствующий каркас (6, 7), связанный с указанной чашей (4, 5) и полученный с использованием PGA/PLA-сополимера, содержащий множество ответвлений (10, 11) расположенных в виде звезды и образующих куполообразный профиль; при этом указанные части (2, 3) соединены друг с другом для образования замкнутой полости.
2. Эндопротез по п.1, отличающийся тем, что указанные части (2, 3) соединены друг с другом с помощью рассасывающегося шовного материала.
3. Эндопротез по п.1 или 2, отличающийся тем, что указанные чаши (4, 5) соединены друг с другом на своих краях (4а, 5а).
4. Эндопротез по п.1, отличающийся тем, что ответвления (10) первой части (2) прикреплены к ответвлениям (11) второй части (3).
5. Эндопротез по п.1, отличающийся тем, что ответвления (10) первой части (2) отделены от ответвлений (10, 11) второй части (3).
6. Эндопротез по п. 1, отличающийся тем, что материал указанных чаш (4, 5) основосвязанного типа и/или предпочтительно текстурированный.
7. Эндопротез по п. 1, отличающийся тем, что PGA/PLA-сополимер состоит на 30% из PGA и на 70% из PLA.
8. Эндопротез по п. 1, отличающийся тем, что толщина материала находится в диапазоне между 0,1 мм и 2 мм, предпочтительно между 0,3 мм и 0,6 мм, более предпочтительно между 0,4 мм и 0,53 мм, еще более предпочтительно 0,45 мм.
9. Эндопротез по п. 1, отличающийся тем, что материал получен с помощью нити, имеющий плотность, находящуюся в диапазоне между 50 и 200 денье.
| WO 2007095193 A2, 23.08.2007 | |||
| МАГНИТНЫЙ СЕПАРАТОР | 1997 |
|
RU2116838C1 |
| 0 |
|
SU159502A1 | |
| WO 2011064110 A1, 03.06.2011 | |||
| WO 2009077047 A1, 25.06.2009 | |||
| ВОЛКОВ В.А | |||
| Синтетические биоматериалы на основе полимеров органических кислот в тканевой инженерии | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
Авторы
Даты
2018-04-03—Публикация
2013-10-10—Подача