Настоящее изобретение относится к молекуле нуклеиновой кислоты, содержащей двухцепочечную структуру, молекуле нуклеиновой кислоты, содержащей двухцепочечную структуру для применения в способе лечения и/или профилактики заболевания, молекуле нуклеиновой кислоты, содержащей двухцепочечную структуру для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству, применению молекулы нуклеиновой кислоты, содержащей двухцепочечную структуру, для получения лекарственного средства, применению молекулы нуклеиновой кислоты, содержащей двухцепочечную структуру, в получееении средства для восстановления чувствительности злокачественных клеток к лекарственному средству, наноэмульсии, содержащей молекулу нуклеиновой кислоты, содержащую двухцепочечную структуру, наноэмульсии для применения в способе лечения и/или профилактики заболевания, наноэмульсии для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству, применению наноэмульсии структуры для получения лекарственного средства, применению наноэмульсии в получении средства для восстановления чувствительности злокачественных клеток к лекарственному средству, фармацевтической композиции, содержащей молекулу нуклеиновой кислоты, содержащую двухцепочечную структуру, фармацевтической композиции для применения в способе лечения и/или профилактики заболевания, фармацевтической композиции для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству, способу лечения и/или профилактики заболевания, включающему введение молекулы нуклеиновой кислоты, содержащей двухцепочечную структуру, способу восстановления чувствительности злокачественных клеток к лекарственному средству, включающему введение молекулы нуклеиновой кислоты, содержащей двухцепочечную структуру, набору, содержащему молекулу нуклеиновой кислоты, содержащую двухцепочечную структуру, набору для применения в способе лечения и/или профилактики заболевания, набору для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству, набору, содержащему наноэмульсию, набору для применения в способе лечения и/или профилактики заболевания и набору для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
Notch 1 является геном, кодирующим однопроходный трансмембранный рецептор, также классифицируемый как трансмембранный белок типа 1. Notch 1 человека впервые описан Ellisen LW et al. (Ellisen LW et al., Cell 66(4), 649-661 (1991)). Notch 1 является членом семейства Notch. Члены этого семейства обладают структурными характеристиками, включающими внеклеточный домен, состоящий из множества подобных эпидермальному фактору роста (EGF) повторов, и внутриклеточный домен, состоящий из множества различных типов доменов. Члены семейства Notch играют роль во множестве процессов развития, контролируя предопределение судьбы клеток. Сигнальная сеть Notch является эволюционно консервативным межклеточным путем передачи сигнала, регулирующим взаимодействия между физически близкими клетками. Notch 1 и продукт его трансляции представляют собой мишень для лекарственных средств при многих опухолях. Информацию о последовательности, включающую нуклеотидную последовательность кДНК Notch 1 человека, например, можно получать в GenBank под регистрационным номером NM_017617.3.
В этой области существует постоянная потребность в средствах сайленсинга или нокдауна уровней экспрессии Notch 1 in vitro и in vivo, включая использование миРНК для лечения заболевания, которое можно лечить или подвергать профилактике, снижая экспрессию гена Notch 1, и более конкретно, снижая трансляцию мРНК, кодирующей Notch 1. Одной группой заболеваний, которые можно лечить таким образом, являются различные опухоли и злокачественные новообразования.
Таким образом, задачей, лежащей в основе настоящего изобретения, является получение средств для сайленсинга или нокдауна Notch 1, и более предпочтительно - сайленсинга или нокдауна уровней экспрессии Notch 1 in vitro и in vivo. Дополнительной задачей, лежащей в основе настоящего изобретения, является разработка способа лечения заболевания, более предпочтительно - заболевания, которое можно лечить или подвергать профилактике, снижая экспрессию гена Notch 1, и более конкретно, снижая трансляцию мРНК, кодирующей Notch 1, и средств, применимых в таком способе. Еще одной задачей, лежащей в основе настоящего изобретения, является разработка способа восстановления чувствительности злокачественных клеток к лекарственному средству и средств, применимых в таком способе. Наконец, задачей, лежащей в основе настоящего изобретения, является разработка способа вспомогательной терапии в лечении злокачественного новообразования и средств, применимых в таком способе.
Эти и другие задачи, лежащие в основе настоящего изобретения, решают посредством объекта прилагаемых независимых пунктов формулы изобретения. Предпочтительные варианты осуществления можно вывести из прилагаемых зависимых пунктов формулы изобретения.
Конкретные варианты осуществления будут очевидны специалисту в этой области с учетом описания, включающего эти варианты осуществления, приведенные ниже. Эти варианты осуществления, приведенные ниже, в равной степени решают указанные выше и другие проблемы, лежащие в основе настоящего изобретения.
Вариант осуществления 1: Молекула нуклеиновой кислоты, содержащая двухцепочечную структуру,
где двухцепочечная структура образована первой цепью и второй цепью,
где первая цепь содержит первый фрагмент смежных нуклеотидов, и вторая цепь содержит второй фрагмент смежных нуклеотидов,
где первый фрагмент смежных нуклеотидов содержит
a) нуклеотидную последовательность, где нуклеотидная последовательность является по меньшей мере на 63% идентичной по отношению к
(i) нуклеотидной последовательности 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидной последовательности 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8); или
b) нуклеотидную последовательность, где нуклеотидная последовательность содержит по меньшей мере фрагмент из 8 или 9 нуклеотидов из
(i) нуклеотидной последовательности 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидной последовательности 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8)
и
где молекула нуклеиновой кислоты способна вызывать посттранскрипционный сайленсинг гена.
Вариант осуществления 2: Молекула нуклеиновой кислоты по варианту осуществления 1, где посттранскрипционный сайленсинг гена является РНК-интерференцией.
Вариант осуществления 3: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-2, где ген является Notch 1, предпочтительно, Notch 1 человека.
Вариант осуществления 4: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-3, где молекула нуклеиновой кислоты способна вызывать деградацию мРНК, кодирующей ген или предшественник указанной мРНК, предпочтительно, в клетке.
Вариант осуществления 5: Молекула нуклеиновой кислоты по варианту осуществления 4, где нуклеотидная последовательность кДНК мРНК доступна в GenBank под регистрационным номером NM_017617.3.
Вариант осуществления 6: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-5, где кДНК состоит из нуклеотидной последовательности SEQ ID NO: 2.
Вариант осуществления 7: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-6, где второй фрагмент смежных нуклеотидов является по меньшей мере частично комплементарным части первого фрагмента смежных нуклеотидов.
Вариант осуществления 8: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-7, где второй фрагмент смежных нуклеотидов является по меньшей мере частично комплементарным первому фрагменту смежных нуклеотидов.
Вариант осуществления 9: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-8, где первый фрагмент смежных нуклеотидов содержит от 13 до 29 нуклеотидов, предпочтительно от 17 до 25 или от 19 до 25 нуклеотидов, и более предпочтительно от 19 до 23 нуклеотидов.
Вариант осуществления 10: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-9, где второй фрагмент смежных нуклеотидов содержит от 13 до 29 нуклеотидов, предпочтительно от 17 до 25 или от 19 до 25 нуклеотидов, и более предпочтительно от 19 до 23 нуклеотидов.
Вариант осуществления 11: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-10, где первый фрагмент смежных нуклеотидов и второй фрагмент смежных нуклеотидов содержит от 13 до 29 нуклеотидов, предпочтительно от 17 до 25 или от 19 до 25 нуклеотидов, и более предпочтительно от 19 до 23 нуклеотидов.
Вариант осуществления 12: Молекула нуклеиновой кислоты по любому из вариантов осуществления 9-11, где нуклеотиды являются последовательными нуклеотидами.
Вариант осуществления 13: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-12, где первая цепь состоит из первого фрагмента смежных нуклеотидов.
Вариант осуществления 14: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-13, где вторая цепь состоит из второго фрагмента смежных нуклеотидов.
Вариант осуществления 15: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-14, где первая цепь состоит из первого фрагмента смежных нуклеотидов, и вторая цепь состоит из второго фрагмента смежных нуклеотидов.
Вариант осуществления 16: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-14, где двухцепочечная структура содержит от 13 до 29 пар оснований, предпочтительно от 16 до 27 или от 19 до 25 пар оснований, и более предпочтительно от 19 до 23 пар оснований.
Вариант осуществления 17: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-16, где первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8).
Вариант осуществления 18: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-17, где второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGU-3' (SEQ ID NO: 3) или
(ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCG-3' (SEQ ID NO: 9).
Вариант осуществления 19: Молекула нуклеиновой кислоты по любому из вариантов осуществления 17-18, где первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8), и
второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGU-3' (SEQ ID NO: 3) или
(ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCG-3' (SEQ ID NO: 9).
Вариант осуществления 20: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-19, где молекула нуклеиновой кислоты имеет тупой конец по меньшей мере на одном конце.
Вариант осуществления 21: Молекула нуклеиновой кислоты по варианту осуществления 20, где молекула нуклеиновой кислоты имеет тупой конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи.
Вариант осуществления 22: Молекула нуклеиновой кислоты по варианту осуществления 20, где молекула нуклеиновой кислоты имеет тупой конец на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
Вариант осуществления 23: Молекула нуклеиновой кислоты по любому из вариантов осуществления 20-22, где молекула нуклеиновой кислоты имеет тупой конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи, и на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
Вариант осуществления 24: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-19, где молекула нуклеиновой кислоты имеет липкий конец по меньшей мере на одном конце.
Вариант осуществления 25: Молекула нуклеиновой кислоты по варианту осуществления 24, где молекула нуклеиновой кислоты имеет липкий конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи.
Вариант осуществления 26: Молекула нуклеиновой кислоты по варианту осуществления 25, где липкий конец является липким 5'-концом.
Вариант осуществления 27: Молекула нуклеиновой кислоты по варианту осуществления 25, где липкий конец является липким 3'-концом.
Вариант осуществления 28: Молекула нуклеиновой кислоты по варианту осуществления 24, где молекула нуклеиновой кислоты имеет липкий конец на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
Вариант осуществления 29: Молекула нуклеиновой кислоты по варианту осуществления 28, где липкий конец является липким 5'-концом.
Вариант осуществления 30: Молекула нуклеиновой кислоты по варианту осуществления 28, где липкий конец является липким 3'-концом.
Вариант осуществления 31: Молекула нуклеиновой кислоты по варианту осуществления 24, где молекула нуклеиновой кислоты имеет липкий конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи, и на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
Вариант осуществления 32: Молекула нуклеиновой кислоты по варианту осуществления 31, где липкий конец является липким 5'-концом.
Вариант осуществления 33: Молекула нуклеиновой кислоты по варианту осуществления 32, где липкий конец является липким 3'-концом.
Вариант осуществления 34: Молекула нуклеиновой кислоты по любому из вариантов осуществления 24-33, где липкий конец состоит из одного, двух, трех, четырех или пяти нуклеотидов.
Вариант осуществления 35: Молекула нуклеиновой кислоты по варианту осуществления 34, где липкий конец состоит из двух нуклеотидов.
Вариант осуществления 36: Молекула нуклеиновой кислоты по любому из вариантов осуществления 34-35, где нуклеотид является dT.
Вариант осуществления 37: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-19 и 24-36, где первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUCdTdT-3' (SEQ ID NO: 4) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGUdTdT-3' (SEQ ID NO: 10).
Вариант осуществления 38: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-19 и 24-37, где второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGUdTdT-3' (SEQ ID NO: 5) или
(ii) нуклеотидная последовательность 5'-ACCAGUGGUCCAGCUCGdTdT-3' (SEQ ID NO: 11).
Вариант осуществления 39: Молекула нуклеиновой кислоты по любому из вариантов осуществления 37-38, где
первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUCdTdT-3' (SEQ ID NO: 4) или
(i) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGUdTdT-3' (SEQ ID NO: 10), и
второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGUdTdT-3' (SEQ ID NO: 5) или
(Ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCGdTdT-3' (SEQ ID NO: 11).
Вариант осуществления 40: Молекула нуклеиновой кислоты по любому из предшествующих вариантов осуществления, где первая цепь и вторая цепь ковалентно связаны друг с другом, предпочтительно, 3'-конец первой цепи ковалентно связан с 5'-концом второй цепи.
Вариант осуществления 41: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-40, где один или несколько нуклеотидов, образующих первый фрагмент смежных нуклеотидов, являются модифицированными.
Вариант осуществления 42: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-41, где один или несколько нуклеотидов, образующих второй фрагмент смежных нуклеотидов, являются модифицированными.
Вариант осуществления 43: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41 и 42, где один или несколько нуклеотидов, образующих первый фрагмент смежных нуклеотидов, являются модифицированными, и один или несколько нуклеотидов, образующих второй фрагмент смежных нуклеотидов, являются модифицированными.
Вариант осуществления 44: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-43, где один или несколько нуклеотидов, образующих первую цепь, являются модифицированными.
Вариант осуществления 45: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-44, где один или несколько нуклеотидов, образующих вторую цепь, являются модифицированными.
Вариант осуществления 46: Молекула нуклеиновой кислоты по любому из вариантов осуществления 44-45, где один или несколько нуклеотидов, образующих первую цепь, являются модифицированными, и один или несколько нуклеотидов, образующих вторую цепь, являются модифицированными.
Вариант осуществления 47: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41-46, где модификация одного или нескольких нуклеотидов является модификацией сахарного остатка одного или нескольких нуклеотидов и/или модификацией фосфатного остатка одного или нескольких нуклеотидов.
Вариант осуществления 48: Молекула нуклеиновой кислоты по варианту осуществления 47, где модификация сахарного остатка выбрана из группы, содержащей 2'O-метил и 2'-F.
Вариант осуществления 49: Молекула нуклеиновой кислоты по любому из вариантов осуществления 47-48, где модификация фосфатного остатка является такой, что между двумя нуклеотидами образуется фосфотиоатная связь.
Вариант осуществления 50: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41-43 и 47-49, где один или несколько нуклеотидов в зависимости от положения во фрагменте являются модифицированными.
Вариант осуществления 51: Молекула нуклеиновой кислоты по варианту осуществления 50, где по всей длине первого и/или второго фрагмента или его части нуклеотид в четном положении фрагмента является модифицированным.
Вариант осуществления 52: Молекула нуклеиновой кислоты по любому из вариантов осуществления 50 и 51, где по всей длине первого и/или второго фрагмента или его части нуклеотид в нечетном положении фрагмента является модифицированным.
Вариант осуществления 53: Молекула нуклеиновой кислоты по любому из вариантов осуществления 51-52, где по всей длине первого и/или второго фрагмента или его части нуклеотид в четном положении фрагмента является модифицированным, и где по всей длине первого и/или второго фрагмента или его части нуклеотид в четном положении фрагмента является модифицированным, где модификация нуклеотидов в четном положении отличается от модификации нуклеотидов в нечетном положении.
Вариант осуществления 54: Молекула нуклеиновой кислоты по любому из вариантов осуществления 51-53, где (a) модификация нуклеотидов в четном положении является 2'-O-метильной модификацией, и модификация нуклеотидов в нечетном положении является 2'-F-модификацией, или (b) модификация нуклеотидов в нечетном положении является 2'-O-метильной модификацией, и модификация нуклеотидов в четном положении является 2'-F-модификацией.
Вариант осуществления 55: Молекула нуклеиновой кислоты по любому из вариантов осуществления 44-50, где один или несколько нуклеотидов является модифицированным в зависимости от положения в цепи.
Вариант осуществления 56: Молекула нуклеиновой кислоты по варианту осуществления 55, где по всей длине первой и/или второй цепи или ее части нуклеотид в четном положении цепи является модифицированным.
Вариант осуществления 57: Молекула нуклеиновой кислоты по любому из вариантов осуществления 55 и 56, где по всей длине первой и/или второй цепи или ее части нуклеотид в нечетном положении цепи является модифицированным.
Вариант осуществления 58: Молекула нуклеиновой кислоты по любому из вариантов осуществления 56-57, где по всей длине первой и/или второй цепи или ее части нуклеотид в четном положении цепи является модифицированным, и где по всей длине первой и/или второй цепи или ее части нуклеотид в четном положении цепи является модифицированным, где модификация нуклеотидов в четном положении отличается от модификации нуклеотидов в нечетном положении цепи.
Вариант осуществления 59: Молекула нуклеиновой кислоты по любому из вариантов осуществления 56-58, где (a) модификация нуклеотидов в четном положении является 2'-O-метильной модификацией, и модификация нуклеотидов в нечетном положении является 2'-F-модификацией, или (b) модификация нуклеотидов в нечетном положении является 2'-O-метильной модификацией, и модификация нуклеотидов в четном положении является 2'-F-модификацией.
Вариант осуществления 60: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41-54, где первый фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным.
Вариант осуществления 61: Молекула нуклеиновой кислоты по варианту осуществления 60, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'O-метил-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
Вариант осуществления 62: Молекула нуклеиновой кислоты по любому из вариантов осуществления 60 и 61, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
Вариант осуществления 63: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41-55 и 60-62, где второй фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 64: Молекула нуклеиновой кислоты по варианту осуществления 63, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине второго фрагмента или его части.
Вариант осуществления 65: Молекула нуклеиновой кислоты по любому из вариантов осуществления 63 и 64, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'O-метил-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
Вариант осуществления 66: Молекула нуклеиновой кислоты по любому из вариантов осуществления 60-65, где первый фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первого фрагмента или его части, где второй фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'O-метил-модифицированным, и где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'O-метил-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
Вариант осуществления 67: Молекула нуклеиновой кислоты по любому из вариантов осуществления 60-66, где первый фрагмент содержит на своем 3'-конце два dT нуклеотида, и второй фрагмент содержит на своем 3'-конце два dT нуклеотида, где два dT нуклеотида ковалентно связаны посредством фосфотиоатной связи.
Вариант осуществления 68: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41-49 и 55-59, где первая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным.
Вариант осуществления 69: Молекула нуклеиновой кислоты по варианту осуществления 68, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'O-метил-модифицированным нуклеотидом по всей длине первой цепи или ее части.
Вариант осуществления 70: Молекула нуклеиновой кислоты по любому из вариантов осуществления 68 и 69, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первой цепи или ее части.
Вариант осуществления 71: Молекула нуклеиновой кислоты по любому из вариантов осуществления 41-49, 55-59 и 68-70, где вторая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 72: Молекула нуклеиновой кислоты по варианту осуществления 71, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине второй цепи или ее части.
Вариант осуществления 73: Молекула нуклеиновой кислоты по любому из вариантов осуществления 71 и 72, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'O-метил-модифицированным нуклеотидом по всей длине первой цепи или ее части.
Вариант осуществления 74: Молекула нуклеиновой кислоты по любому из вариантов осуществления 68-73, где первая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первой цепи или ее части, где вторая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'O-метил-модифицированным, и где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'O-метил-модифицированным нуклеотидом по всей длине первой цепи или ее части.
Вариант осуществления 75: Молекула нуклеиновой кислоты по любому из вариантов осуществления 68-74, где первая цепь содержит на своем 3'-конце два dT нуклеотида, и вторая цепь содержит на своем 3'-конце два dT нуклеотида, где два dT нуклеотида ковалентно связаны посредством фосфотиоатной связи.
Вариант осуществления 76: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-75, где
нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) модифицируют следующим образом:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
нуклеотидную последовательность 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8) модифицируют следующим образом:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 77: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-76, где
нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGU-3' (SEQ ID NO: 3) модифицируют следующим образом
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), и
нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCG-3' (SEQ ID NO: 9) модифицируют следующим образом
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 78: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-77, где первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6) или
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 79: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-78, где второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7) или
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 80: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-79, где
a) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
b) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
c) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14), или
d) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 81: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-80, где молекула нуклеиновой кислоты состоит из
a) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
b) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
c) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14), или
d) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 82: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-81, где молекула нуклеиновой кислоты состоит из
a) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
b) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
c) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14), или
d) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным.
Вариант осуществления 83: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-81, где молекула нуклеиновой кислоты состоит из
a) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuCdTsdT-3' (SEQ ID NO: 69), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGudTsdT-3' (SEQ ID NO: 70), или
b) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgUdTsdT-3' (SEQ ID NO: 71), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGudTsdT-3' (SEQ ID NO: 70), или
c) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuCdTsdT-3' (SEQ ID NO: 69), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCgdTsdT-3' (SEQ ID NO: 72), или
d) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgUdTsdT-3' (SEQ ID NO: 71), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCgdTsdT-3' (SEQ ID NO: 72),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным и
где dTsdT указывает на то, что на 3'-конце присоединен динуклеотид, состоящий из двух dT, где указанные два dT ковалентно связаны посредством фосфотиоатной связи.
Вариант осуществления 84: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-83 для применения в способе лечения и/или профилактики заболевания.
Вариант осуществления 85: Молекула нуклеиновой кислоты по варианту осуществления 84, где заболевание является заболеванием, которое можно лечить, снижая экспрессию гена Notch 1 и, более конкретно, снижая трансляцию мРНК, кодирующей Notch 1.
Вариант осуществления 86: Молекула нуклеиновой кислоты по любому из вариантов осуществления 84-85, где заболевание выбрано из группы, включающей рак пищевода, плоскоклеточный рак полости рта, рак головы и шеи, рак языка, лейкоз, почечноклеточную карциному, рак желудка, аденокарциному толстого кишечника, рак эндометрия/тела матки, рак шейки матки, внутрипеченочную холангиокарциному, печеночноклеточную карциному, остеосаркому, карциному мочевого пузыря, злокачественную меланому, рак щитовидной железы, аденокарциному легких, рак предстательной железы, рак молочной железы, рак яичников, рак поджелудочной железы и глиому.
Вариант осуществления 87: Молекула нуклеиновой кислоты по любому из вариантов осуществления 84-86, где способ включает дополнительное введение фармацевтически активного средства.
Вариант осуществления 88: Молекула нуклеиновой кислоты по варианту осуществления 87, где фармацевтически активное средство является цитостатическим средством.
Вариант осуществления 89: Молекула нуклеиновой кислоты по варианту осуществления 88, где фармацевтически активное средство выбрано из группы, содержащей гемцитабин, доцетаксел, цисплатин, оксалиплатин, 5-фторурацил, иринотекан, паклитаксел, дексаметазон и темозоломид.
Вариант осуществления 90: Молекула нуклеиновой кислоты по любому из вариантов осуществления 1-83, для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
Вариант осуществления 91: Молекула нуклеиновой кислоты по варианту осуществления 90, где чувствительность к лекарственному средству является чувствительностью к лекарственному средству, опосредуемой и/или включающей каскад NF-kappaB.
Вариант осуществления 92: Применение молекулы нуклеиновой кислоты по любому из вариантов осуществления 1-83 для получения лекарственного средства для лечения и/или профилактики заболевание.
Вариант осуществления 93: Применение по варианту осуществления 92, где заболевание является заболеванием, которое можно лечить, снижая экспрессию гена Notch 1 и, более конкретно, снижая трансляцию мРНК, кодирующей Notch 1.
Вариант осуществления 94: Применение по любому из вариантов осуществления 92-93, где заболевание выбрано из группы, включающей рак пищевода, плоскоклеточный рак полости рта, рак головы и шеи, рак языка, лейкоз, почечноклеточную карциному, рак желудка, аденокарциному толстого кишечника, рак эндометрия/тела матки, рак шейки матки, внутрипеченочную холангиокарциному, печеночноклеточную карциному, остеосаркому, карциному мочевого пузыря, злокачественную меланому, рак щитовидной железы, аденокарциному легких, рак предстательной железы, рак молочной железы, рак яичников, рак поджелудочной железы и глиому.
Вариант осуществления 95: Применение по любому из вариантов осуществления 92-94, где лекарственное средство предназначено для введения вместе с дополнительным фармацевтически активным средством.
Вариант осуществления 96: Применение по варианту осуществления 95, где фармацевтически активное средство является цитостатическим средством.
Вариант осуществления 97: Применение по варианту осуществления 96, где фармацевтически активное средство выбрано из группы, включающей гемцитабин, доцетаксел, цисплатин, оксалиплатин, 5-фторурацил, иринотекан, паклитаксел, дексаметазон и темозоломид.
Вариант осуществления 98: Применение молекулы нуклеиновой кислоты по любому из вариантов осуществления 1-83 в получении средства для восстановления чувствительности злокачественных клеток к лекарственному средству.
Вариант осуществления 99: Применение по варианту осуществления 98, где чувствительность к лекарственному средству является чувствительностью к лекарственному средству, опосредуемой и/или включающей каскад NF-kappaB.
Вариант осуществления 100: Наноэмульсия, содержащая дискретную фазу, и непрерывную водную фазу, и молекулу нуклеиновой кислоты по любому из вариантов осуществления 1-83.
Вариант осуществления 101: Наноэмульсия по варианту осуществления 100, где дискретная фаза содержит перфторуглеродную фазу.
Вариант осуществления 102: Наноэмульсия по любому из вариантов осуществления 1-101, где наноэмульсия содержит усиливающую эндоцитоз поверхность, предпочтительно, усиливающая эндоцитоз поверхность содержит усиливающий эндоцитоз компонент, где усиливающий эндоцитоз компонент выбран из группы, содержащей по меньшей мере одно соединение, индуцирующее клеточный захват наноэмульсии или частиц наноэмульсии посредством эндоцитоза.
Вариант осуществления 103: Наноэмульсия по любому из вариантов осуществления 100-102 для применения в лечении и/или профилактике заболевания.
Вариант осуществления 104: Наноэмульсия по любому из вариантов осуществления 100-102 для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
Вариант осуществления 105: Применение наноэмульсии по любому из вариантов осуществления 100-102 для получения лекарственного средства для лечения и/или профилактики заболевания.
Вариант осуществления 106: Применение наноэмульсии по любому из вариантов осуществления 100-102 в получении средства для восстановления чувствительности злокачественных клеток к лекарственному средству.
Вариант осуществления 107: Фармацевтическая композиция, содержащая молекулу нуклеиновой кислоты по любому из вариантов осуществления 1-83 и/или наноэмульсию по любому из вариантов осуществления 100-102 и фармацевтически приемлемый эксципиент.
Вариант осуществления 108: Фармацевтическая композиция по варианту осуществления 107 для применения в лечении и/или профилактике заболевания.
Вариант осуществления 109: Фармацевтическая композиция по варианту осуществления 107 для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
Вариант осуществления 110: Способ лечения и/или профилактики заболевания, где способ включает введение индивидууму нуклеиновой кислоты по любому из вариантов осуществления 1-3, наноэмульсии по любому из вариантов осуществления 100-102 и/или фармацевтической композиции по варианту осуществления 107.
Вариант осуществления 111: Способ восстановления чувствительности злокачественных клеток к лекарственному средству, где способ включает введение индивидууму нуклеиновой кислоты по любому из вариантов осуществления 1-83, наноэмульсии по любому из вариантов осуществления 100-02 и/или фармацевтической композиции по варианту осуществления 107, где индивидуум страдает злокачественным новообразованием, и клетки злокачественного новообразования являются резистентными к лекарственному средству.
Авторы настоящего изобретения неожиданно обнаружили, что молекула нуклеиновой кислоты, содержащая двухцепочечную структуру,
где двухцепочечная структура образована первой цепью и второй цепью,
где первая цепь содержит первый фрагмент смежных нуклеотидов, и вторая цепь содержит второй фрагмент смежных нуклеотидов,
где первый фрагмент смежных нуклеотидов содержит
a) нуклеотидную последовательность, где нуклеотидная последовательность является по меньшей мере на 63% идентичной по отношению к
(i) нуклеотидной последовательности 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидной последовательности 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8); или
b) нуклеотидную последовательность, где нуклеотидная последовательность содержит, по меньшей мере, фрагмент из 8 или 9 нуклеотидов из
(i) нуклеотидной последовательности 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидной последовательности 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8)
способна вызывать, в частности, посттранскрипционный сайленсинг гена и РНК-интерференцию. Эту нуклеиновую кислоту, включающую все эти варианты осуществления, будут обозначать в настоящем описании как молекула нуклеиновой кислоты по изобретению.
В объем изобретения входит то, что молекула нуклеиновой кислоты по изобретению является малой интерферирующей РНК (миРНК). Такая миРНК является особенно предпочтительным вариантом осуществления молекулы нуклеиновой кислоты по изобретению. В варианте осуществления миРНК направлена против экспрессируемого транскрипта РНК Notch 1 (иногда обозначаемого в настоящем описании как "нуклеиновая кислота-мишень"). Как предпочтительно применяют в настоящем описании, термины "сайленсинг" и "нокдаун" по отношению к экспрессии гена означают снижение экспрессия гена. Настоящее изобретение дополнительно относится к способам получения молекулы нуклеиновой кислоты по изобретению.
В варианте осуществления изобретения нуклеиновая кислота-мишень является РНК, экспрессирующейся с гена Notch 1 млекопитающего. В одном из вариантов осуществления нуклеиновая кислота-мишень является РНК, экспрессирующейся с Notch 1 мыши. В другом варианте осуществления нуклеиновая кислота-мишень является РНК, экспрессирующейся с Notch 1 человека. В другом варианте осуществления нуклеиновая кислота-мишень является мРНК Notch 1 человека. В другом варианте осуществления нуклеиновая кислота-мишень является гяРНК Notch 1 человека. В другом варианте осуществления нуклеиновая кислота-мишень является мРНК, содержащей последовательность SEQ ID NO: 12.
В варианте осуществления настоящего изобретения молекула нуклеиновой кислоты не образует двухцепочечную структуру. В таком варианте осуществления молекула нуклеиновой кислоты образована двумя отдельными одиночными цепями, которые могут присутствовать отдельно, т.е. в негибридизованном состоянии таким образом, что двухцепочечная структура не образуется, или в гибридизованной форме, когда образуется двухцепочечная структура, отличающаяся от двухцепочечной структуры, необходимой для опосредования или запуска РНК-интерференции. Альтернативно, молекула нуклеиновой кислоты, образующая двухцепочечную структуру, является одноцепочечной молекулой нуклеиновой кислоты, где молекула нуклеиновой кислоты не сворачивается обратно самостоятельно таким образом, что образуется двухцепочечная структура, или таким образом, что образуется двухцепочечная структура, отличающаяся от двухцепочечной структуры, необходимой для опосредования или запуска РНК-интерференции. В более предпочтительном варианте осуществления двухцепочечная структура образуется в условиях in vivo и, более конкретно, после введения молекулы нуклеиновой кислоты индивидууму, предпочтительно, млекопитающему или клетке млекопитающего.
МиРНК по настоящему изобретению подходит для ингибирования экспрессии Notch 1. Таким образом, миРНК по настоящему изобретению подходит для запуска ответа с РНК-интерференцией, приводящему к снижению мРНК Notch 1 в клетке млекопитающего. МиРНК по настоящему изобретению дополнительно подходит для снижения экспрессии белка Notch 1, снижая экспрессию гена на уровне мРНК.
Дизайн миРНК: МиРНК по настоящему изобретению содержит две цепи нуклеиновой кислоты, первую цепь, также обозначаемую как антисмысловая цепь, содержащую первый фрагмент смежных нуклеотидов, также обозначаемый как антисмысловой фрагмент, и вторую цепь, также обозначаемую как смысловая цепь, содержащую второй фрагмент смежных нуклеотидов, также обозначаемый как смысловой фрагмент. Как правило, нуклеиновая кислота состоит из рибонуклеотидов или модифицированных рибонуклеотидов, однако, нуклеиновая кислота может содержать дезоксинуклеотиды (ДНК), как представлено в настоящем описании. МиРНК дополнительно содержит часть двухцепочечной нуклеиновой кислоты или дуплексную область, образованную всей или частью антисмысловой цепи или антисмыслового фрагмента и всей или частью смысловой цепи или смыслового фрагмента. Такую часть двухцепочечной нуклеиновой кислоты или дуплексную область в настоящем описании также обозначают как двухцепочечную структуру. Часть антисмысловой цепи или антисмыслового фрагмента, образующая дуплексную область со смысловой цепью или с антисмысловым фрагментом, является дуплексной областью антисмысловой цепи или областью антисмыслового фрагмента или, просто, антисмысловой дуплексной областью, и часть смысловой цепи или смыслового фрагмента, образующая дуплексную область с антисмысловой цепью или антисмысловым фрагментом, является дуплексной областью смысловой цепи, является дуплексной областью смыслового фрагмента или, просто, смысловой дуплексной областью. Дуплексную область определяют как начинающуюся с первой пары оснований, образовавшихся между антисмысловой цепью или антисмысловым фрагментом и смысловой цепью или смысловым фрагментом, и заканчивающуюся последней парой оснований, образовавшихся между антисмысловой цепью или антисмысловым фрагментом и смысловой цепью или смысловым фрагментом, включительно. Часть миРНК на любой стороне дуплексной области является фланкирующими областями. Часть антисмысловой цепи или антисмыслового фрагмента на любой стороне антисмысловой дуплексной области является антисмысловыми фланкирующими областями. Часть антисмысловой цепи или антисмыслового фрагмента в 5'-направлении к антисмысловой дуплексной областью является антисмысловой 5'-фланкирующей областью. Часть антисмысловой цепи или антисмыслового фрагмента в 5'-направлении к антисмысловой дуплексной области является антисмысловой 3'-фланкирующей областью. Часть смысловой цепи или смыслового фрагмента на любой стороне смысловой дуплексной области является смысловыми фланкирующими областями. Часть смысловой цепи или смыслового фрагмента в 5'-направлении к смысловой дуплексной области является смысловой 5'-фланкирующей областью. Часть смысловой цепи или смыслового фрагмента в 5'-направлении к смысловой дуплексной области является смысловой 3'-фланкирующей областью.
Идентичность: В варианте осуществления идентичность одной нуклеотидной последовательности по отношению к другой нуклеотидной последовательности является показателем того, насколько много нуклеотидов является общими между одной нуклеотидной последовательностью и другой нуклеотидной последовательностью. Идентичность выражают как соотношение количества нуклеотидов одной последовательности, общих с другой нуклеотидной последовательностью, и общего количества нуклеотидов другой нуклеотидной последовательности. Максимальное значение идентичности составляет 100%. Специалисту в этой области известно, что, в зависимости от длины одной нуклеотидной последовательности и другой нуклеотидной последовательности с одной стороны и количества нуклеотидов, общих между одной нуклеотидной последовательностью и другой нуклеотидной последовательностью, - с другой, идентичность не всегда является целым числом. Если такое вычисленное соотношение не является целым числом, идентичность, несмотря на это, предпочтительно указывают как целое число, наиболее близкое к вычисленному соотношению и имеющее технический смысл. По настоящему изобретению идентичность может составлять 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%,92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100%.
Комплементарность: По изобретению антисмысловая дуплексная область и смысловая дуплексная область могут являться полностью комплементарными и являются, по меньшей мере, частично комплементарными друг другу. Такая комплементарность основана на спаривании оснований по Уотсону-Крику (т.е. спаривании оснований A:U и G:C). В зависимости от длины молекулы нуклеиновой кислоты по изобретению и миРНК, в частности, полное совпадение в терминах комплементарности оснований между антисмысловой и смысловой дуплексными областями не является необходимым, однако, антисмысловые и смысловые цепи должны быть способными к гибридизации в физиологических условиях.
В одном из вариантов осуществления комплементарность между антисмысловой цепью и смысловой цепью является полной, т.е. без несовпадений нуклеотидов или дополнительных/делетированных нуклеотидов в любой цепи.
В одном из вариантов осуществления комплементарность между антисмысловым фрагментом и смысловым фрагментом является полной, т.е. без несовпадений нуклеотидов или дополнительных/делетированных нуклеотидов в любом фрагменте.
В одном из вариантов осуществления комплементарность между антисмысловой дуплексной областью и смысловой дуплексной областью является полной, т.е. без несовпадений нуклеотидов или дополнительных/делетированных нуклеотидов в дуплексной области любой цепи.
В другом варианте осуществления комплементарность между антисмысловой дуплексной областью и смысловой дуплексной областью не является полной. В одном из вариантов осуществления идентичность между антисмысловой дуплексной областью и комплементарной последовательностью смысловой дуплексной области выбрана из группы, состоящей из по меньшей мере 75%, 80%, 85%, 90% и 95%; где миРНК, содержащая антисмысловую дуплексную область и смысловую дуплексную область, подходит для снижения экспрессии Notch 1. В другом варианте осуществления, где идентичность между антисмысловой дуплексной областью и комплементарной последовательностью смысловой дуплексной области выбрана из группы, состоящей из по меньшей мере 75%, 80%, 85%, 90% и 95%, миРНК способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50% или 75% от сравнительной миРНК, имеющей дуплексную область с полной идентичностью между антисмысловой дуплексной областью и смысловой дуплексной областью. Как применяют в настоящем описании, термин "сравнительная миРНК" означает миРНК, идентичную миРНК, с которой ее сравнивают, за исключением определенного различия, и которую тестируют в идентичных условиях.
РНКи с использованием миРНК включает образование дуплексной области между всей или частью антисмысловой цепи или антисмыслового фрагмента и частью нуклеиновой кислоты-мишени. Часть нуклеиновой кислоты-мишени, образующая дуплексную область с антисмысловой цепью или антисмысловым фрагментом, определяемым как начинающийся с первой пары оснований, образованной между антисмысловой цепью или антисмысловым фрагментом и последовательностью-мишенью, и заканчивающийся последней парой, образованной между антисмысловой цепью или антисмысловым фрагментом и последовательностью-мишенью, включительно, является последовательностью нуклеиновой кислоты-мишени или просто последовательностью-мишенью. Дуплексная область, образующаяся между антисмысловой цепью или антисмысловым фрагментом и смысловой цепью или смысловым фрагментом, необязательно, может являться той же, что и дуплексная область, образующаяся между антисмысловой цепью или антисмысловым фрагментом и последовательностью-мишенью. Т.е. смысловая цепь или смысловой фрагмент может иметь последовательность, отличающуюся от последовательности-мишени, однако, антисмысловая цепь или антисмысловой фрагмент могут быть способными образовывать дуплексную структуру со смысловой цепью или смысловым фрагментом и последовательностью-мишенью.
В одном из вариантов осуществления комплементарность между антисмысловой цепью или антисмысловым фрагментом и последовательностью-мишенью является полной, т.е. без несовпадений нуклеотидов или дополнительных/делетированных нуклеотидов в любой нуклеиновой кислоте.
В одном из вариантов осуществления комплементарность между антисмысловой дуплексной областью, т.е. частью антисмысловой цепи или антисмыслового фрагмента, образующей дуплексную область со смысловой цепью или смысловым фрагментом, и последовательностью-мишенью является полной, т.е. без несовпадений нуклеотидов или дополнительных/делетированных нуклеотидов в любой нуклеиновой кислоте.
В другом варианте осуществления комплементарность между антисмысловой дуплексной областью и последовательностью-мишенью не является полной. В одном из вариантов осуществления идентичность между антисмысловой дуплексной областью и комплементарной последовательностью последовательности-мишени выбрана из группы, состоящей из по меньшей мере 75%, 80%, 85%, 90% или 95%, где миРНК, содержащая антисмысловую дуплексную область, подходит для снижения экспрессии Notch 1. В другом варианте осуществления, где идентичность между антисмысловой дуплексной областью и комплементарной последовательностью последовательности-мишени выбрана из группы, состоящей из по меньшей мере 75%, 80%, 85%, 90% и 95%, миРНК способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50% или 75% от сравнительной миРНК с полной идентичностью по отношению к антисмысловой цепи или антисмысловому фрагменту и последовательностью-мишенью.
В другом варианте осуществления миРНК по изобретению содержит дуплексную область, где антисмысловая дуплексная область имеет количество нуклеотидов, выбранное из группы, состоящей из 1, 2, 3, 4 и 5, не спаривающихся с нуклеотидом в смысловой дуплексной области, и где указанная миРНК подходит для снижения экспрессии Notch 1. Отсутствие спаривания оснований является результатом отсутствия комплементарности между основаниями, т.е. отсутствия спаривания оснований по Уотсону-Крику, или отсутствия соответствующего нуклеотида в антисмысловой дуплексной области или смысловой дуплексной области таким образом, что образуется петля. В одном из вариантов осуществления миРНК, содержащая антисмысловую дуплексную область, имеющую количество нуклеотидов, выбранное из группы, состоящей из 1, 2, 3, 4 и 5, не спаривающихся со смысловой дуплексной областью, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК, где все нуклеотиды указанной антисмысловой дуплексной области спариваются со всеми нуклеотидами указанной смысловой дуплексной области.
В другом варианте осуществления антисмысловая цепь или антисмысловой фрагмент имеет количество нуклеотидов, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, не спаривающихся со смысловой цепью или смысловым фрагментом, и где миРНК, содержащая указанную антисмысловую цепь, подходит для снижения экспрессии Notch 1. Отсутствие комплементарности является результатом отсутствия комплементарности между основаниями или отсутствия соответствующего нуклеотида в антисмысловой цепи, или антисмысловом фрагменте, или смысловой цепи, или смысловом фрагменте. Отсутствие соответствующего нуклеотида приводит к образованию одноцепочечного липкого конца или петли (если в дуплексной области) в антисмысловой цепи, или антисмысловом фрагменте, или смысловой цепи, или смысловом фрагменте. В одном из вариантов осуществления миРНК, содержащая антисмысловую цепь или антисмысловой фрагмент, имеющий количество нуклеотидов, выбранной из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, не спаривающихся со смысловой цепью или смысловым фрагментом, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК, где все нуклеотиды указанной антисмысловой цепи или указанного антисмыслового фрагмента являются комплементарными всем нуклеотидам смысловой цепи или смыслового фрагмента. В одном из вариантов осуществления миРНК, содержащая антисмысловую цепь или антисмысловой фрагмент, имеющий количество нуклеотидов, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, не совпадающих с последовательностью-мишенью, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК, где все нуклеотиды указанной антисмысловой цепи или указанной антисмысловой цепи являются комплементарными всем нуклеотидам указанной смысловой цепи или указанного смыслового фрагмента. В другом варианте осуществления все несовпадающие нуклеотиды находятся вне дуплексной области.
В другом варианте осуществления антисмысловая дуплексная область имеет количество нуклеотидов, выбранное из 1, 2, 3, 4 или 5, не спаривающихся со смысловой дуплексной областью, и где миРНК, содержащая указанную антисмысловую дуплексную область, подходит для снижения экспрессии Notch 1. Отсутствие комплементарности является результатом отсутствия комплементарности между основаниями или отсутствия соответствующего нуклеотида в антисмысловой дуплексной области или смысловой дуплексной области таким образом, что образуется петля в антисмысловой дуплексной области или смысловой дуплексной области. В одном из вариантов осуществления миРНК, содержащая антисмысловую дуплексную область, имеющую количество нуклеотидов, выбранное из группы, состоящей из 1, 2, 3, 4 и 5, не спаривающихся со смысловой дуплексной областью, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК, где все нуклеотиды указанной антисмысловой дуплексной области являются комплементарными всем нуклеотидам указанной смысловой дуплексной области.
В другом варианте осуществления антисмысловая цепь имеет количество нуклеотидов, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, не спаривающихся с последовательностью-мишенью, и где миРНК, содержащая указанную антисмысловую цепь, подходит для снижения экспрессии Notch 1. Отсутствие комплементарности является результатом отсутствия комплементарности между основаниями или отсутствия соответствующего нуклеотида в антисмысловой цепи, или антисмысловом фрагменте, или последовательности-мишени. Отсутствие соответствующего нуклеотида приводит к образованию петли в антисмысловой цепи, или антисмысловом фрагменте, или последовательности-мишени. В одном из вариантов осуществления миРНК, содержащая антисмысловую цепь или антисмысловой фрагмент, имеющий количество нуклеотидов, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, не спаривающихся с последовательностью-мишенью, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК, где все нуклеотиды указанной антисмысловой цепи или антисмыслового фрагмента являются комплементарными всем нуклеотидам указанной последовательности-мишени. В одном из вариантов осуществления миРНК, содержащая антисмысловую цепь или антисмысловой фрагмент, имеющий количество нуклеотидов, выбранных из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, не совпадающих с последовательностью-мишенью, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50% или 75% от сравнительной миРНК, где все нуклеотиды указанной антисмысловой цепи или указанного антисмыслового фрагмента являются комплементарными всем нуклеотидам указанной последовательности-мишени.
В другом варианте осуществления комплементарность между антисмысловой дуплексной областью и смысловой дуплексной областью и последовательностью-мишенью миРНК является такой, что антисмысловая дуплексная область и смысловая дуплексная область или последовательность-мишень гибридизуются друг с другом в физиологических условиях (37°C в физиологическом буфере), и миРНК подходит для снижения экспрессии Notch 1. В одном из вариантов осуществления миРНК, содержащая антисмысловую дуплексную область, гибридизующуюся со смысловой дуплексной областью и последовательностью-мишенью в физиологических условиях, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК с полной комплементарностью между антисмысловой цепью или антисмысловым фрагментом и последовательностью-мишенью.
В другом аспекте комплементарность между антисмысловой дуплексной областью и смысловой дуплексной областью миРНК является такой, что антисмысловая дуплексная область и смысловая дуплексная область гибридизуются в следующих условиях: 400 мМ NaCl, 40 мМ PIPES, pH 6,4, 1 мМ ЭДТА, 70°C, и подходит для снижения экспрессии Notch 1. В одном из вариантов осуществления миРНК, содержащая антисмысловую дуплексную область и смысловую дуплексную область, гибридизующиеся друг с другом в условиях 400 мМ NaCl, 40 мМ PIPES, pH 6,4, 1 мМ ЭДТА, 70°C, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК с полной комплементарностью между антисмысловой дуплексной областью и смысловой дуплексной областью.
В другом варианте осуществления комплементарность между антисмысловой цепью или антисмысловым фрагментом миРНК и последовательностью-мишенью является такой, что антисмысловая цепь или антисмысловой фрагмент и последовательность-мишень гибридизуются в следующих условиях: 400 мМ NaCl, 40 мМ PIPES, pH 6,4, 1 мМ ЭДТА, 70°C, и где миРНК подходит для снижения экспрессии Notch 1. В одном из вариантов осуществления миРНК, содержащая антисмысловую цепь или антисмысловой фрагмент, гибридизующиеся с последовательностью-мишенью в следующих условиях: 400 мМ NaCl, 40 мМ PIPES, pH 6,4, 1 мМ ЭДТА, 70°C, способна снижать экспрессию Notch 1 по меньшей мере на 25%, 50%, 75% от сравнительной миРНК с полной комплементарностью между антисмысловой цепью или антисмысловым фрагментом и последовательностью-мишенью.
Длина: РНК-интерференцию наблюдают при использовании длинных молекул нуклеиновой кислоты, содержащих несколько десятков или сотен пар оснований, хотя предпочтительными, как правило, являются более короткие молекулы РНКи.
В одном из вариантов осуществления длина дуплексной области миРНК выбрана из группы, состоящей из от приблизительно 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 пар оснований. В одном из вариантов осуществления длина дуплексной области миРНК выбрана из группы, состоящей из от приблизительно 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 последовательных пар оснований. В другом варианте осуществления длина дуплексной области миРНК выбрана из группы, состоящей из 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 пар оснований. В другом варианте осуществления длина дуплексной области миРНК выбрана из группы, состоящей из 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 последовательных пар оснований.
В одном из вариантов осуществления длина антисмысловой цепи выбрана из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов. В одном из вариантов осуществления длина антисмысловой цепи выбрана из группы, состоящей из 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов.
В одном из вариантов осуществления длина антисмыслового фрагмента выбрана из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов. В одном из вариантов осуществления длина антисмыслового фрагмента выбрана из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов.
В одном из вариантов осуществления длина смысловой цепи выбрана из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов. В одном из вариантов осуществления длина смысловой цепи выбрана из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов.
В одном из вариантов осуществления длина смыслового фрагмента выбрана из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов. В одном из вариантов осуществления длина смыслового фрагмента выбрана из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов.
В одном из вариантов осуществления длина антисмысловой цепи и длина смысловой цепи независимо выбраны из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов. В одном из вариантов осуществления длина антисмысловой цепи и длина смысловой цепи независимо выбраны из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов. В одном из вариантов осуществления антисмысловая цепь и смысловая цепь равны по длине. В другом варианте осуществления антисмысловая цепь и смысловая цепь равны по длине, где длина выбрана из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов.
В одном из вариантов осуществления длина антисмыслового фрагмента и длина смыслового фрагмента независимо выбраны из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов. В одном из вариантов осуществления длина антисмыслового фрагмента и длина смыслового фрагмента независимо выбраны из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов. В одном из вариантов осуществления антисмысловой фрагмент и смысловой фрагмент равны по длине. В другом варианте осуществления антисмысловой фрагмент и смысловой фрагмент равны по длине, где длина выбрана из группы, состоящей из 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов.
В одном из вариантов осуществления длина антисмысловой цепи или антисмыслового фрагмента выбрана из группы, состоящей из от приблизительно 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов, где антисмысловая цепь или антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1.
В одном из вариантов осуществления длина антисмысловой цепи или антисмыслового фрагмента выбрана из группы, состоящей из приблизительно 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов, где антисмысловая цепь или антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1.
В одном из вариантов осуществления длина смысловой цепи или смыслового фрагмента выбрана из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов, где смысловая цепь или смысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В одном из вариантов осуществления длина смысловой цепи или смыслового фрагмента выбрана из группы, состоящей из приблизительно 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов, где смысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В одном из вариантов осуществления длина антисмысловой цепи или антисмыслового фрагмента и длина смысловой цепи или смыслового фрагмента независимо выбраны из группы, состоящей из от приблизительно 13 до 35, от 16 до 35, от 16 до 30, от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов, где антисмысловая цепь или антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловая цепь или смысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В одном из вариантов осуществления длина антисмысловой цепи и длина смысловой цепи независимо выбрана из группы, состоящей из 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов, где антисмысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В одном из вариантов осуществления длина антисмыслового фрагмента и длина смыслового фрагмента независимо выбраны из группы, состоящей из 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов, где антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В одном из вариантов осуществления антисмысловая цепь и смысловая цепь равны по длине, где антисмысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В одном из вариантов осуществления антисмысловой фрагмент и смысловой фрагмент равны по длине, где антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В другом варианте осуществления антисмысловая цепь и смысловая цепь равны по длине, где длина выбрана из группы, состоящей из от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов, где антисмысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В другом варианте осуществления антисмысловой фрагмент и смысловой фрагмент равны по длине, где длина выбрана из группы, состоящей из от 17 до 35, от 17 до 30, от 17 до 25, от 17 до 24, от 18 до 29, от 18 до 25, от 18 до 24, от 18 до 23, от 19 до 25, от 19 до 24, от 19 до 23, от 20 до 25, от 20 до 24, от 21 до 25 и от 21 до 24 нуклеотидов, где антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В другом варианте осуществления антисмысловая цепь и смысловая цепь равны по длине, где длина выбрана из группы, состоящей из 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов, где антисмысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловая цепь содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
В другом варианте осуществления антисмысловой фрагмент и смысловой фрагмент равны по длине, где длина выбрана из группы, состоящей из 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35 нуклеотидов, где антисмысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 8 или 1, и где смысловой фрагмент содержит нуклеотидную последовательность SEQ ID NO: 9 или 3.
Конкретные варианты осуществления представляют собой комбинации антисмысловой и смысловой цепи (указанных по SEQ ID NO:): 8 и 9; 1 и 3; 4 и 5; 6 и 7; и 10 и 11.
Конкретные варианты осуществления представляют собой комбинации антисмыслового и смыслового фрагмента (указанных по SEQ ID NO:): 8 и 9; 1 и 3; 4 и 5; 6 и 7; и 10 и 11.
Концы (липкие и тупые концы): МиРНК по настоящему изобретению может содержать липкие или тупые концы. Как применяют в настоящем описании, "липкий конец" имеет свое нормальное и общепринятое в этой области значение, т.е. одноцепочечной части нуклеиновой кислоты, выходящей за пределы концевого нуклеотида комплементарной цепи или фрагмента в двухцепочечной нуклеиновой кислоте. Термин "тупой конец" включает двухцепочечную нуклеиновую кислоту, в которой обе цепи или фрагмента заканчиваются в одном положении, независимо от того являются ли концевые нуклеотиды спаренными. В одном из вариантов осуществления концевой нуклеотид антисмысловой цепи или антисмыслового фрагмента и смысловой цепи или смыслового фрагмента на тупом конце являются спаренными. В другом варианте осуществления концевой нуклеотид антисмысловой цепи или антисмыслового фрагмента и смысловой цепи или смыслового фрагмента на тупом конце являются неспаренными. В другом варианте осуществления концевые два нуклеотида антисмысловой цепи или антисмыслового фрагмента и смысловой цепи или смыслового фрагмента на тупом конце являются спаренными. В другом варианте осуществления концевые два нуклеотида антисмысловой цепи или антисмыслового фрагмента и смысловой цепи или смыслового фрагмента на тупом конце являются неспаренными.
В одном из вариантов осуществления миРНК имеет липкий конец на одном конце и тупой конец на другом. В другом варианте осуществления миРНК имеет липкий конец на обоих концах. В другом варианте осуществления миРНК имеет тупой конец на обоих концах. В одном из вариантов осуществления миРНК имеет тупой конец на одном конце. В другом варианте осуществления миРНК имеет тупой конец на конце 5'-конца антисмысловой цепи или антисмыслового фрагмента и 3'-конца смысловой цепи или смыслового фрагмента. В другом варианте осуществления миРНК имеет тупой конец на конце 3'-конца антисмысловой цепи или антисмыслового фрагмента и 5'-конца смысловой цепи или смыслового фрагмента. В другом варианте осуществления миРНК имеет тупой конец на обоих концах.
В другом варианте осуществления миРНК содержит липкий конец на 3'- или 5'-конце. В одном из вариантов осуществления миРНК имеет липкий 3'-конец на антисмысловой цепи или антисмысловом фрагменте. В другом варианте осуществления миРНК имеет липкий 3'-конец на смысловой цепи или смысловом фрагменте. В другом варианте осуществления миРНК имеет липкий 5'-конец на антисмысловой цепи или антисмысловом фрагменте. В другом варианте осуществления миРНК имеет липкий 5'-конец на смысловой цепи или смысловом фрагменте. В другом варианте осуществления миРНК имеет липкий конец на 5'-конце и 3'-конце антисмысловой цепи или антисмыслового фрагмента. В другом варианте осуществления миРНК имеет липкий конец на 5'-конце и 3'-конце смысловой цепи или смыслового фрагмента. В другом варианте осуществления миРНК имеет липкий 5'-конец на антисмысловой цепи или антисмысловом фрагменте и липкий 3'-конец на смысловой цепи или смысловом фрагменте. В другом варианте осуществления миРНК имеет липкий 3'-конец на антисмысловой цепи или антисмысловом фрагменте и липкий 5'-конец на смысловой цепи или смысловом фрагменте. В другом варианте осуществления миРНК имеет липкий 3'-конец на антисмысловой цепи или антисмысловом фрагменте и липкий 3'-конец на смысловой цепи или смысловом фрагменте. В другом варианте осуществления миРНК имеет липкий 5'-конец на антисмысловой цепи или антисмысловом фрагменте и липкий 5'-конец на смысловой цепи или смысловой цепи.
В одном из вариантов осуществления липкий конец на 3'-конце антисмысловой цепи или антисмыслового фрагмента имеет длину, выбранную из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов. В одном из вариантов осуществления липкий конец на 3'-конце смысловой цепи или смыслового фрагмента имеет длину, выбранную из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов. В одном из вариантов осуществления липкий конец на 5'-конце антисмысловой цепи или антисмыслового фрагмента имеет длину, выбранную из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов. В одном из вариантов осуществления липкий конец на 5'-конце смысловой цепи или смыслового фрагмента имеет длину, выбранную из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов.
Модификация: Другой аспект относится к модификациям миРНК, и по этому аспекту молекулу нуклеиновой кислоты по изобретению можно модифицировать, как описано ниже. В объем настоящего изобретения входит, что каждая и любая модификация и паттерн, представленные в настоящем описании, и любое обсуждение в настоящем описании, относящееся к такой модификации и паттерну, в частности, относящееся к миРНК, также может быть применимо и, таким образом, реализовано в отношении молекулы нуклеиновой кислоты по изобретению. В объем настоящего изобретения также входит, что, в той мере, в которой оно относится к антисмысловой цепи и/или смысловой цепи, особенно когда это касается модификации антисмысловой цепи и/или смысловой цепи и нуклеотидов, образующих такую антисмысловую цепь и/или смысловую цепь, такое обсуждение в равной степени применимо к антисмысловому фрагменту и/или смысловому фрагменту, особенно когда это касается модификации антисмыслового фрагмента и/или смыслового фрагмента и нуклеотидов, образующих такой антисмысловой фрагмент и/или смысловой фрагмент.
МиРНК по изобретению является рибонуклеиновой кислотой или модифицированной рибонуклеиновой кислотой. Химические модификации миРНК по настоящему изобретению относятся к мощному инструменту для преодоления потенциальных ограничений, включая, в качестве неограничивающих примеров, стабильность in vitro и in vivo и биодоступность, свойственные нативным молекулам РНК. С помощью химически-модифицированных миРНК также можно минимизировать возможность активации активности интерферона у людей. Химическая модификация может дополнительно повышать функциональную доставку миРНК в клетку-мишень. Модифицированная миРНК по настоящему изобретению может содержать один или несколько химически модифицированных рибонуклеотидов антисмысловой цепи или смысловой цепи или и той, и другой. Рибонуклеотид может содержать химическую модификацию основания, сахарного или фосфатного остатков.
Модификации остатка основания: Вторичный аспект относится к модификациям остатка основания. Один или несколько нуклеотидов миРНК по настоящему изобретению может содержать модифицированное основание. Термин "модифицированное основание" означает основание нуклеотида, иное, чем аденин, гуанин, цитозин или урацил в 1'-положении.
В одном из аспектов миРНК содержит по меньшей мере один нуклеотид, содержащий модифицированное основание. В одном из вариантов осуществления модифицированное основание находится на антисмысловой цепи. В другом варианте осуществления модифицированное основание находится на смысловой цепи. В другом варианте осуществления модифицированное основание находится в дуплексной области. В другом варианте осуществления модифицированное основание находится вне дуплексной области, т.е. в одноцепочечной области. В другом варианте осуществления модифицированное основание находится на антисмысловой цепи и вне дуплексной области. В другом варианте осуществления модифицированное основание находится на смысловой цепи и вне дуплексной области. В другом варианте осуществления 3'-концевой нуклеотид антисмысловой цепи является нуклеотидом с модифицированным основанием. В другом варианте осуществления 3'-концевой нуклеотид смысловой цепи является нуклеотидом с модифицированным основанием. В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи является нуклеотидом с модифицированным основанием. В другом варианте осуществления 5'-концевой нуклеотид смысловой цепи является нуклеотидом с модифицированным основанием.
В одном из вариантов осуществления миРНК имеет 1 модифицированное основание. В другом варианте осуществления миРНК имеет приблизительно 2-4 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 4-6 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 6-8 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 8-10 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 10-12 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 12-14 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 14-16 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 16-18 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 18-20 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 20-22 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 22-24 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 24-26 модифицированных оснований. В другом варианте осуществления миРНК имеет приблизительно 26-28 модифицированных оснований. В каждом случае миРНК, содержащая указанные модифицированные основания, сохраняет по меньшей мере 50% своей активности по сравнению с той же миРНК, но без указанных модифицированных оснований.
В одном из вариантов осуществления модифицированное основание является пурином. В другом варианте осуществления модифицированное основание является пиримидином. В другом варианте осуществления, по меньшей мере, половина пуринов являются модифицированными. В другом варианте осуществления, по меньшей мере, половина пиримидинов являются модифицированными. В другом варианте осуществления все пурины являются модифицированными. В другом варианте осуществления все пиримидины являются модифицированными.
В другом варианте осуществления миРНК содержит нуклеотид, содержащий модифицированное основание, где основание выбрано из группы, состоящей из 2-аминоаденозина, 2,6-диаминопурина, инозина, пиридин-4-она, пиридин-2-она, фенила, псевдоурацила, 2,4,6-триметоксибензола, 3-метилурацила, дигидроуридина, нафтила, аминофенила, 5-алкилцитидина (например, 5-метилцитидина), 5-алкилуридина (например, риботимидина), 5-галогенуридина (например, 5-бромуридина), 6-азапиримидина, 6-алкилпиримидина (например 6-метилуридина), пропина, квеуозина, 2-тиоуридина, 4-тиоуридина, вибутозина, вибутоксозина, 4-ацетилцитидина, 5-(карбоксигидроксиметил)уридина, 5'-карбоксиметиламинометил-2-тиоуридина, 5-карбоксиметиламинометилуридина, бета-D-галактозилквеуозина, 1-метиладенозина, 1-метилинозина, 2,2-диметилгуанозина, 3-метилцитидина, 2-метиладенозина, 2-метилгуанозина, N6-метиладенозина, 7-метилгуанозина, 5-метоксиаминометил-2-тиоуридина, 5-метиламинометилуридина, 5-метилкарбонилметилуридина, 5-метилоксиуридина, 5-метил-2-тиоуридина, 2-метилтио-N6-изопентениладенозина, бета-D-маннозилквеуозина, уридин-5-оксиуксусной кислоты и 2-тиоцитидина.
В другом аспекте миРНК по настоящему изобретению содержит нуклеотид без основания. Как применяют в настоящем описании, термин "без основания" относится к остаткам, в которых отсутствует основание или имеющим другие химические группы вместо основания в 1'-положении, например, 3',3'-связанное или 5',5'-связанное дезоксиабазическое производное рибозы. Как применяют в настоящем описании нуклеотид с модифицированным основанием не включает нуклеотиды без основания. В одном из аспектов миРНК содержит по меньшей мере один нуклеотид без основания. В одном из вариантов осуществления нуклеотид без основания находится на антисмысловой цепи. В другом варианте осуществления нуклеотид без основания находится на смысловой цепи. В другом варианте осуществления нуклеотид без основания находится в дуплексной области. В другом варианте осуществления нуклеотид без основания находится вне дуплексной области. В другом варианте осуществления нуклеотид без основания находится на антисмысловой цепи и вне дуплексной области. В другом варианте осуществления нуклеотид без основания находится на смысловой цепи и вне дуплексной области. В другом варианте осуществления 3'-концевой нуклеотид антисмысловой цепи является нуклеотидом без основания. В другом варианте осуществления 3'-концевой нуклеотид смысловой цепи является нуклеотидом без основания. В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи является нуклеотидом без основания. В другом варианте осуществления 5'-концевой нуклеотид смысловой цепи является нуклеотидом без основания. В другом варианте осуществления миРНК содержит ряд нуклеотидов без основания, выбранных из группы, состоящей из 1, 2, 3, 4, 5 и 6.
Модификации сахарного остатка: Другой вторичный аспект относится к модификациям сахарного остатка. Один или несколько нуклеотидов миРНК по настоящему изобретению может содержать модифицированный остаток рибозы.
Модификации в 2'-положении, где 2'-OH является замещенным, включают неограничивающие примеры, выбранные из группы, состоящей из алкила, замещенного алкила, алкиларила, аралкила, -F, -Cl, -Br, -CN, -CF3, -OCF3, -OCN, -O-алкила, -S-алкила, HS-алкил-O, -O-алкенила, -S-алкенила, -N-алкенила, -SO-алкила, -алкил-OSH, -алкил-OH, -O-алкил-OH, -O-алкил-SH, -S-алкил-OH, -S-алкил-SH, -алкил-S-алкила, -алкил-O-алкила, -ONO2, -NO2, -N3, -NH2, алкиламиногруппы, диалкиламиногруппы, аминоалкила, аминоалкоксигруппы, аминокислоты, аминоацила, -ONH2, -O-аминоалкила, -O-аминокислоты, -O-аминоацила, гетероциклоалкила, гетероциклоалкиларила, аминоалкиламиногруппы, полиалкиламиногруппы, замещенного силила, метоксиэтила (MOE), алкенила и алкинила. "Замкнутые" нуклеиновые кислоты (ЗНК), в которых 2'-гидроксил соединен, например, метиленовым мостиком, с 4'-углеродом того же сахара рибозы, дополнительно включены в качестве 2'-модификации по настоящему изобретению. Предпочтительными заместителями являются 2'-метоксиэтил, 2'-OCH3, 2'-O-аллил, 2'-C-аллил и 2'-фтор.
В одном из вариантов осуществления миРНК содержит 1-5 2'-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 5-10 2'-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 15-20 2'-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 20-25 2'-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 25-30 2'-модифицированных нуклеотидов.
В одном из вариантов осуществления антисмысловая цепь содержит 1-2 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 2-4 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 4-6 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 6-8 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 8-10 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 10-12 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 12-14 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 14-16 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 16-18 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 18-20 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 22-24 2'-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 24-26 2'-модифицированных нуклеотидов.
В одном из вариантов осуществления смысловая цепь содержит 1-2 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 2-4 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 4-6 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 6-8 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 8-10 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 10-12 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 12-14 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 14-16 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 16-18 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 18-20 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 22-24 2'-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 24-26 2'-модифицированных нуклеотидов.
В одном из вариантов осуществления миРНК содержит 1-5 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 5-10 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 15-20 2'-OCH3-модифицированнов нуклеотиды. В другом варианте осуществления миРНК содержит 20-25 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК содержит 25-30 2'-OCH3-модифицированных нуклеотидов.
В одном из вариантов осуществления антисмысловая цепь содержит 1-2 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 2-4 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 4-6 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 6-8 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 8-10 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 10-12 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 12-14 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 14-16 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 16-18 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 18-20 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 22-24 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая цепь содержит приблизительно 24-26 2'-OCH3-модифицированных нуклеотидов.
В одном из вариантов осуществления смысловая цепь содержит 1-2 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 2-4 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 4-6 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 6-8 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 8-10 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 10-12 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 12-14 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 14-16 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 16-18 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 18-20 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 22-24 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления смысловая цепь содержит приблизительно 24-26 2'-OCH3-модифицированных нуклеотидов.
В одном из вариантов осуществления миРНК дуплексная область содержит 1-5 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК дуплексная область содержит 5-10 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК дуплексная область содержит 15-20 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК дуплексная область содержит 20-25 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления миРНК дуплексная область содержит 25-30 2'-OCH3-модифицированных нуклеотидов.
В одном из вариантов осуществления антисмысловая дуплексная область содержит 1-2 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 2-4 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 4-6 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 6-8 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 8-10 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 10-12 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 12-14 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 14-16 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 16-18 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 18-20 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 22-24 2'-OCH3-модифицированных нуклеотидов. В одном из вариантов осуществления антисмысловая дуплексная область содержит приблизительно 24-26 2'-OCH3-модифицированных нуклеотидов.
В одном из вариантов осуществления смысловая дуплексная область содержит 1-2 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 2-4 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 4-6 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 6-8 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 8-10 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 10-12 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 12-14 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 14-16 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 16-18 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 18-20 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 22-24 2'-OCH3-модифицированных нуклеотидов. В другом варианте осуществления смысловая дуплексная область содержит приблизительно 24-26 2'-OCH3-модифицированных нуклеотидов.
В одном из вариантов осуществления миРНК содержит антисмысловую цепь из 19 нуклеотидов в длину и смысловую цепь из 19 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 1, 3, 5, 7, 9, 11, 13, 15, 17 и 19, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 2, 4, 6, 8, 10, 12, 14, 16 и 18, где указанную антисмысловую цепь нумеруют в 5'-3'-направлении и указанную смысловую цепь нумеруют в 3'-5'-направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 20 нуклеотидов в длину и смысловую цепь из 20 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 1, 3, 5, 7, 9, 11, 13, 15, 17 и 19, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 2, 4, 6, 8, 10, 12, 14, 16, 18 и 20, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 21 нуклеотидов в длину и смысловая цепь 21 нуклеотиды в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 1, 3, 5, 7, 9, 11, 13, 15, 17, 19 и 21, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 2, 4, 6, 8, 10, 12, 14, 16, 18 и 20, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 22 нуклеотидов в длину и смысловую цепь из 22 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 1, 3, 5, 7, 9, 11, 13, 15, 17, 19 и 21, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 2, 4, 6, 8, 10, 12, 14, 16, 18, 20 и 22, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 23 нуклеотидов в длину и смысловую цепь из 23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21 и 23, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 2, 4, 6, 8, 10, 12, 14, 16, 18, 20 и 22, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении.
В другом варианте осуществления миРНК содержит антисмысловую цепь из 18-23 нуклеотидов в длину и смысловую цепь из 18-23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 3, 5, 7, 9, 11, 13, 15 и 17, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 4, 6, 8, 10, 12, 14 и 16, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 18-23 нуклеотидов в длину и смысловую цепь из 18-23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 5, 7, 9, 11, 13 и 15, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 6, 8, 10, 12 и 14, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 18-23 нуклеотидов в длину и смысловую цепь из 18-23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 7, 9, 11, 13 и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 8, 10 и 12, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 18-23 нуклеотидов в длину и смысловую цепь из 18-23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 7, 9 и 11, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 8, 10 и 12, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 18-23 нуклеотидов в длину и смысловую цепь из 18-23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 7 и 9, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 8 и 10, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении. В другом варианте осуществления миРНК содержит антисмысловую цепь из 18-23 нуклеотидов в длину и смысловую цепь из 18-23 нуклеотидов в длину, где указанная антисмысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 9 и 11, и где указанная смысловая цепь содержит 2'-OCH3-модификации в нуклеотидах 8 и 10, где указанную антисмысловую цепь нумеруют в 5'-3' направлении и указанную смысловую цепь нумеруют в 3'-5' направлении.
В дополнительных вариантах осуществления миРНК содержит следующие нуклеотидные последовательности, где последовательности содержат 2'-OCH3-модификации в нуклеотидах, указанных заглавными буквами:
В другом варианте осуществления антисмысловая цепь содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 2'-дезоксинуклеотидов.
В другом варианте осуществления смысловая цепь содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 2'-дезоксинуклеотидов.
В другом варианте осуществления антисмысловая цепь содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 2'-фтор-нуклеотидов.
В другом варианте осуществления смысловая цепь содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 или 25 2'-фтор-нуклеотидов.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловой цепи являются 2'-O-метилпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловой цепи являются 2'-O-метилпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловой цепи являются 2'-дезоксипиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловой цепи являются 2'-дезоксипуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловой цепи являются 2'-фторпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловой цепи являются 2'-фторпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловой цепи являются 2'-O-метилпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловой цепи являются 2'-O-метилпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловой цепи являются 2'-дезоксипиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловой цепи являются 2'-дезоксипуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловой цепи являются 2'-фторпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловой цепи являются 2'-фторпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловой дуплексной области являются 2'-O-метилпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловой дуплексной области являются 2'-O-метилпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловой дуплексной области являются 2'-дезоксипиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловой дуплексной области являются 2'-дезоксипуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловой дуплексной области являются 2'-фторпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловой дуплексной области являются 2'-фторпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловой дуплексной области являются 2'-O-метилпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловой дуплексной области являются 2'-O-метилпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловой дуплексной области являются 2'-дезоксипиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловой дуплексной области являются 2'-дезоксипуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловой дуплексной области являются 2'-фторпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловой дуплексной области являются 2'-фторпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловых фланкирующих дуплекс областях являются 2'-O-метилпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловых фланкирующих дуплекс областях являются 2'-O-метилпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловых фланкирующих дуплекс областях являются 2'-дезоксипиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловых фланкирующих дуплекс областях являются 2'-дезоксипуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в антисмысловых фланкирующих дуплекс областях являются 2'-фторпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в антисмысловых фланкирующих дуплекс областях являются 2'-фторпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловых фланкирующих дуплекс областях являются 2'-O-метилпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловых фланкирующих дуплекс областях являются 2'-O-метилпуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловых фланкирующих дуплекс областях являются 2'-дезоксипиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловых фланкирующих дуплекс областях являются 2'-дезоксипуриновыми нуклеотидами.
В другом варианте осуществления пиримидиновые нуклеотиды в смысловых фланкирующих дуплекс областях являются 2'-фторпиримидиновыми нуклеотидами.
В другом варианте осуществления пуриновые нуклеотиды в смысловых фланкирующих дуплекс областях являются 2'-фторпуриновыми нуклеотидами.
Паттерн: В объем настоящего изобретения входит, что любое обсуждение, относящееся к паттерну, представленному в настоящем описании, особенно в отношении антисмысловой цепи, в равной степени применимо к антисмысловому фрагменту, и любое обсуждение, относящееся к паттерну, представленному в настоящем описании, особенно в отношении смысловой цепи, в равной степени применимо к смысловому фрагменту.
В одном из вариантов осуществления антисмысловая дуплексная область содержит множество групп модифицированных нуклеотидов, обозначаемых в настоящем описании как "модифицированные группы", где каждая модифицированная группа состоит из одного или нескольких идентично модифицированных нуклеотидов, где каждую модифицированную группу на одной или обеих сторонах фланкирует вторая группа нуклеотидов, обозначаемая в настоящем описании как "фланкирующая группа", где каждая указанная фланкирующая группа состоит из одного или нескольких нуклеотидов, являющихся немодифицированными или модифицированными способом, отличающимся от нуклеотидов указанной модифицированной группы. В одном из вариантов осуществления каждая модифицированная группа в антисмысловой дуплексной области является идентичной, т.е. каждая модифицированная группа состоит из равного количества идентично модифицированных нуклеотидов. В другом варианте осуществления каждая фланкирующая группа содержит равное количество нуклеотидов. В другом варианте осуществления каждая фланкирующая группа является идентичной. В другом варианте осуществления нуклеотиды указанных модифицированных групп в антисмысловой дуплексной области содержат модифицированное основание. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированный фосфатный остов. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированное 2'-положение.
В другом аспекте смысловая дуплексная область содержит множество групп модифицированных групп, где каждая модифицированная группа состоит из одного или нескольких идентично модифицированных нуклеотидов, где каждую модифицированную группу с одной или обеих сторон фланкирует фланкирующая группа, где каждая указанная фланкирующая группа состоит из одного или нескольких нуклеотидов, являющихся немодифицированными или модифицированными способом, отличающимся от нуклеотидов указанной модифицированной группы. В одном из вариантов осуществления каждая модифицированная группа в смысловой дуплексной области является идентичной. В другом варианте осуществления каждая фланкирующая группа содержит равное количество нуклеотидов. В другом варианте осуществления каждая фланкирующая группа является идентичной. В другом варианте осуществления нуклеотиды указанных модифицированных групп в смысловой дуплексной области содержат модифицированное основание. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированный фосфатный остов. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированное 2'-положение.
В другом аспекте каждая из антисмысловой дуплексной области и смысловой дуплексной области содержит множество модифицированных групп, где каждая модифицированная группа состоит из одного или нескольких идентично модифицированных нуклеотидов, где каждую модифицированную группу с одной или обеих сторон фланкирует фланкирующая группа, где каждая указанная фланкирующая группа состоит из одного или нескольких нуклеотидов, являющихся немодифицированными или модифицированными способом, отличающимся от нуклеотидов указанной модифицированной группы. В одном из вариантов осуществления каждая модифицированная группа в антисмысловой дуплексной области и смысловой дуплексной области является идентичной. В другом варианте осуществления каждая фланкирующая группа в антисмысловой дуплексной области и смысловой дуплексной области содержит равное количество нуклеотидов. В другом варианте осуществления каждая фланкирующая группа в антисмысловой дуплексной области и в смысловой дуплексной области является идентичной. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой дуплексной области и смысловой дуплексной области содержит одинаковые модифицированные группы и одинаковые фланкирующие группы. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой дуплексной области и смысловой дуплексной области содержит модифицированное основание. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой дуплексной области и смысловой дуплексной области содержит модифицированный фосфатный остов. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой дуплексной области и смысловой дуплексной области содержат модифицированное 2'-положение.
В одном из аспектов антисмысловая цепь содержит множество групп модифицированных нуклеотидов, обозначаемых в настоящем описании как "модифицированные группы", где каждая модифицированная группа состоит из одного или нескольких идентично модифицированных нуклеотидов, где каждую модифицированную группу с одной или обеих сторон фланкирует вторая группа нуклеотидов, обозначаемая в настоящем описании как "фланкирующая группа", где каждая указанная фланкирующая группа состоит из одного или нескольких нуклеотидов, являющихся немодифицированными или модифицированными способом, отличающимся от нуклеотидов указанной модифицированной группы. В одном из вариантов осуществления каждая модифицированная группа в антисмысловой цепи является идентичной, т.е. каждая модифицированная группа состоит из равного количества идентично модифицированных нуклеотидов. В другом варианте осуществления каждая фланкирующая группа содержит равное количество нуклеотидов. В другом варианте осуществления каждая фланкирующая группа является идентичной. В другом варианте осуществления нуклеотиды указанных модифицированных групп в антисмысловой цепи содержат модифицированное основание. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированный фосфатный остов. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированное 2'-положение.
В другом аспекте смысловая цепь содержит множество групп модифицированных групп, где каждая модифицированная группа состоит из одного или нескольких идентично модифицированных нуклеотидов, где каждую модифицированную группу с одной или обеих сторон фланкирует фланкирующая группа, где каждая указанная фланкирующая группа состоит из одного или нескольких нуклеотидов, являющихся немодифицированными или модифицированными способом, отличающимся от нуклеотидов указанной модифицированной группы. В одном из вариантов осуществления каждая модифицированная группа в смысловой цепи является идентичной. В другом варианте осуществления каждая фланкирующая группа содержит равное количество нуклеотидов. В другом варианте осуществления каждая фланкирующая группа является идентичной. В другом варианте осуществления нуклеотиды указанных модифицированных групп в смысловой цепи содержат модифицированное основание. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированный фосфатный остов. В другом варианте осуществления нуклеотиды указанных модифицированных групп содержат модифицированное 2'-положение.
В другом аспекте каждая из антисмысловой цепи и смысловой цепи содержит множество модифицированных групп, где каждая модифицированная группа состоит из одного или нескольких идентично модифицированных нуклеотидов, где каждую модифицированную группу с одной или обеих сторон фланкирует фланкирующая группа, где каждая указанная фланкирующая группа состоит из одного или нескольких нуклеотидов, являющихся немодифицированными или модифицированными способом, отличающимся от нуклеотидов указанной модифицированной группы. В одном из вариантов осуществления каждая модифицированная группа в антисмысловой цепи и смысловой цепи является идентичной. В другом варианте осуществления каждая фланкирующая группа в каждой из антисмысловой цепи и смысловой цепи содержит равное количество нуклеотидов. В другом варианте осуществления каждая фланкирующая группа в антисмысловой цепи и смысловой цепи является идентичной. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой цепи и смысловой цепи содержит одинаковые модифицированные группы и одинаковые фланкирующие группы. В другом варианте осуществления нуклеотиды указанных модифицированных групп в каждой из антисмысловой цепи и смысловой цепь содержат модифицированной основание. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой цепи и смысловой цепи содержит модифицированный фосфатный остов. В другом варианте осуществления каждый нуклеотид указанных модифицированных групп в антисмысловой цепи и смысловой цепи содержит модифицированное 2'-положение.
В другом аспекте модифицированные группы и фланкирующие группы образуют регулярный паттерн на антисмысловой цепи. В другом аспекте модифицированные группы и фланкирующие группы образуют регулярный паттерн на смысловой цепи. В одном из вариантов осуществления модифицированные группы и фланкирующие группы образуют регулярный паттерн и на антисмысловой цепи, и на смысловой цепи. В другом варианте осуществления модифицированные группы и фланкирующие группы образуют регулярный паттерн в антисмысловой дуплексной области. В другом аспекте модифицированные группы и фланкирующие группы образуют регулярный паттерн в смысловой дуплексной области. В одном из вариантов осуществления модифицированные группы и фланкирующие группы образуют регулярный паттерн и в антисмысловой дуплексной области, и в смысловой дуплексной области.
В другом аспекте паттерн является пространственным или позиционным паттерном. Пространственный или позиционный паттерн означает, что (a) нуклеотиды являются модифицированными в зависимости от их положения в нуклеотидной последовательности двухцепочечной части. Таким образом, не имеет значения, является ли нуклеотид, подлежащий модификации, пиримидином или пурином. Положение модифицированного нуклеотида скорее зависит от: (a) его номерного положения на цепи нуклеиновой кислоты, где нуклеотиды пронумерованы с 5'-конца до 3'-конца, при этом 5'-концевой нуклеотид цепи имеет положение один (антисмысловая цепь и смысловая цепь пронумерованы относительно их 5'-концевого нуклеотида), или (b) положения модифицированной группы относительно фланкирующей группы. Таким образом, по этому варианту осуществления паттерн модификации всегда будет одинаковым, независимо от последовательности, подлежащей модификации.
В другом варианте осуществления количество модифицированных групп на антисмысловой цепи выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество модифицированных групп на смысловой цепи выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество фланкирующих групп на антисмысловой цепи нуклеиновой кислоты выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество фланкирующих групп на смысловой цепи нуклеиновой кислоты выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В одном из вариантов осуществления количество модифицированных групп и количество фланкирующих групп на любой или обеих из антисмысловой цепи и смысловой цепи является одинаковым.
В другом варианте осуществления количество модифицированных групп в антисмысловой дуплексной области выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество модифицированных групп в смысловой дуплексной области выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество фланкирующих групп в антисмысловой дуплексной области нуклеиновой кислоты составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество фланкирующих групп в смысловой дуплексной области нуклеиновой кислоты выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В одном из вариантов осуществления количество модифицированных групп и количество фланкирующих групп на любой или обеих из антисмысловой цепи и смысловой цепи является одинаковым.
В одном из вариантов осуществления количество модифицированных групп и количество фланкирующих групп на цепи или в дуплексной области является одинаковым. В другом варианте осуществления количество модифицированных групп и количество фланкирующих групп на цепи или в дуплексной области является одинаковым, где количество выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14.
В другом варианте осуществления количество нуклеотидов в модифицированной группе выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14. В другом варианте осуществления количество нуклеотидов во фланкирующей группе выбрано из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14.
В одном из вариантов осуществления каждая модифицированная группа на антисмысловой цепи и смысловой цепи является идентичной. В одном из вариантов осуществления каждая модифицированная группа в антисмысловой дуплексной области и смысловой дуплексной области является идентичной. В другом варианте осуществления каждая модифицированная группа и каждая фланкирующая группа на антисмысловой цепи и смысловой цепи является идентичной. В одном из вариантов осуществления каждая модифицированная группа и каждая фланкирующая группа в антисмысловой дуплексной области и смысловой дуплексной области является идентичной.
В одном из вариантов осуществления каждая модифицированная группа, положение каждой модифицированной группы, каждая фланкирующая группа и положение каждой фланкирующей группы на антисмысловой цепи и смысловой цепи являются идентичными. В одном из вариантов осуществления каждая модифицированная группа, положение каждой модифицированной группы, каждая фланкирующая группа и положение каждой фланкирующей группы в антисмысловой дуплексной области и смысловой дуплексной области являются идентичными. В другом варианте осуществления модифицированные группы на антисмысловой цепи комплементарны модифицированным группам на смысловой цепи (модифицированные группы на антисмысловой цепи и смысловой цепи полностью выровнены относительно друг друга). В другом варианте осуществления в модифицированных группах отсутствуют несовпадения таким образом, что каждая модифицированная группа на антисмысловой цепи спарена с каждой модифицированной группой на смысловой цепи. В другом варианте осуществления каждая модифицированная группа на смысловой цепи сдвинута на 1, 2, 3, 4 или 5 нуклеотидов относительно модифицированных групп на антисмысловой цепи. Например, если каждая модифицированная группа на смысловой цепи сдвинута на один нуклеотид и модифицированная группа начинается с положения один на антисмысловой цепи, модифицированная группа на смысловой цепи будет начинаться с положения два. В другом варианте осуществления модифицированные группы антисмысловой цепи не перекрываются с модифицированными группами смысловой цепи, т.е. нуклеотид модифицированной группы на антисмысловой цепи не спарен с нуклеотидом модифицированной группы на смысловой цепи.
В одном из вариантов осуществления дезоксирибонуклеотиды на конце цепи нуклеиновой кислоты не учитывают при определении положения модифицированной группы, т.е. позиционная нумерация начинается с первого рибонуклеотида или модифицированного рибонуклеотида. В другом варианте осуществления нуклеотиды без основания на конце цепи нуклеиновой кислоты не учитывают при определении положения модифицированной группы.
В одном из аспектов модифицированная группа содержит 5'-концевой нуклеотид любой или обеих из антисмысловой цепи и смысловой цепи. В другом варианте осуществления фланкирующая группа содержит 5'-концевой нуклеотид любой или обеих из антисмысловой цепи и смысловой цепи. В другом варианте осуществления 5'-концевой нуклеотид любой или обеих из антисмысловой цепи и смысловой цепи является немодифицированным. В другом варианте осуществления модифицированная группа содержит наиболее близкий к 5'-концу нуклеотид любой или обеих из антисмысловой дуплексной области и смысловой дуплексной области. В другом варианте осуществления фланкирующая группа содержит наиболее близкий к 5'-концу нуклеотид любой или обеих из антисмысловой дуплексной области и смысловой дуплексной области. В другом варианте осуществления наиболее близкий к 5'-концу нуклеотид любой или обеих из антисмысловой дуплексной области и смысловой дуплексной области является немодифицированным. В другом варианте осуществления нуклеотид в положении 10 антисмысловой цепи является немодифицированным. В другом варианте осуществления нуклеотид в положении 10 смысловой цепи является модифицированным. В другом варианте осуществления модифицированная группа содержит нуклеотид в положении 10 смысловой цепи.
В одном из вариантов осуществления модификация в 2'-положении выбрана из группы, содержащей аминогруппу, фтор, метоксигруппу, алкоксигруппу и C1-C3-алкил. В другом варианте осуществления модификация представляет собой 2'-O-метил.
В другом аспекте каждая модифицированная группа состоит из одного нуклеотида, и каждая фланкирующая группа состоит из одного нуклеотида. В одном из вариантов осуществления каждую модифицированную группу на антисмысловой цепи выравнивают с фланкирующей группой на смысловой цепи.
В другом аспекте каждая модифицированная группа состоит из одного 2'-O-метилмодифицированного нуклеотида, и каждая фланкирующая группа состоит из одного нуклеотида. В одном из вариантов осуществления каждая фланкирующая группа состоит из одного немодифицированного нуклеотида. В одном из вариантов осуществления каждая фланкирующая группа состоит из одного 2'-O-метилмодифицированного нуклеотида. В другом варианте осуществления каждая модифицированная группа и на антисмысловой цепи, и на смысловой цепи состоит из одного 2'-O-метилмодифицированного нуклеотида, и каждая фланкирующая группа и на антисмысловой цепи, и на смысловой цепи состоит из одного нуклеотида, где ни одна из модифицированных групп на одной цепи не выровнена или не выровнена и не спарена с другой модифицированной группой на другой цепи, и ни одна из фланкирующих групп на одной цепи не выровнена или не выровнена и не спарена с фланкирующей группой на другой цепи. В другом варианте осуществления, исключая любые необязательные липкие концы, каждая модифицированная группа на каждой цепи выровнена или выровнена и спарена с фланкирующей группой на другой цепи. В одном из вариантов осуществления фланкирующая группа является немодифицированной. В другом варианте осуществления нуклеотид в положении один на антисмысловой цепи является 2'O-метил-модифицированным. В другом варианте осуществления наиболее близкий к 5'-концу нуклеотид антисмысловой дуплексной области является 2'-O-метил-модифицированным.
Схемы позиционной модификации описывают в международной патентной заявке WO 2004/015107, включенной в настоящее описание в полном объеме в качестве ссылки.
Модификации фосфатного остова:
В объем настоящего изобретения входит, что любое обсуждение, относящееся к модификации фосфатного остова, представленного в настоящем описании, конкретно относящееся к антисмысловой цепи или нуклеотидам, образующим такую антисмысловую цепь, в равной степени применимо к антисмысловому фрагменту или нуклеотидам, образующим такой антисмысловой фрагмент, и любое обсуждение, относящееся к модификации фосфатного остова, представленного в настоящем описании, конкретно относящееся к смысловой цепи или нуклеотидам, образующим такую смысловую цепь, в равной степени применимо к смысловому фрагменту или нуклеотидам, образующим такой смысловой фрагмент.
В одном из вариантов осуществления молекула нуклеиновой кислоты по изобретению и миРНК по изобретению, в частности, несут, имеют или демонстрируют одну или несколько модификаций фосфатного остова, таким образом, такая модификация, предпочтительно, является модификацией, представленной в настоящем описании.
Все или часть нуклеотидов миРНК по изобретению можно соединять посредством фосфодиэфирных связей, как обнаруживают в немодифицированной нуклеиновой кислоте. Однако миРНК по настоящему изобретению может содержать модифицированную фосфодиэфирную связь. Фосфодиэфирные связи антисмысловой цепи или смысловой цепи можно модифицировать так, чтобы они независимо включали по меньшей мере один гетероатом, выбранный из группы, состоящей из азота и серы. В одном из вариантов осуществления фосфоэфирную группу, соединяющую рибонуклеотид со смежным рибонуклеотидом, заменяют модифицированной группой. В одном из вариантов осуществления модифицированная группа, заменяющая фосфоэфирную группу, выбрана из группы, состоящей из фосфотиоатной, метилфосфонатной или фосфоамидатной группы.
В одном из вариантов осуществления все нуклеотиды антисмысловой цепи соединяют посредством фосфодиэфирных связей. В другом варианте осуществления все нуклеотиды антисмысловой дуплексной области соединяют посредством фосфодиэфирных связей. В другом варианте осуществления все нуклеотиды смысловой цепи соединяют посредством фосфодиэфирных связей. В другом варианте осуществления все нуклеотиды смысловой дуплексной области соединяют посредством фосфодиэфирных связей. В другом варианте осуществления антисмысловая цепь содержит количество модифицированным фосфодиэфирных групп, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. В другом варианте осуществления антисмысловая дуплексная область содержит количество модифицированных фосфодиэфирных групп, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. В другом варианте осуществления смысловая цепь содержит количество модифицированных фосфодиэфирных групп, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. В другом варианте осуществления смысловая дуплексная область содержит количество модифицированных фосфодиэфирных групп, выбранное из 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
В другом варианте осуществления один или несколько нуклеотидов, образующих антисмысловую дуплексную область, смысловую дуплексную область или липкие концы соединяют посредством фосфотиоатных связей. В предпочтительном варианте осуществления нуклеотиды, образующие липкий конец, соединены друг с другом посредством одной или нескольких фосфотиоатных связей.
Модификации 5'- и 3'-конца:
В объем настоящего изобретения входит, что любое обсуждение, относящееся к модификациям 5'- и 3'-конца, представленным в настоящем описании, конкретно относящееся к антисмысловой цепи или нуклеотидам, образующим такую антисмысловую цепь, в равной степени применимо к антисмысловому фрагменту или нуклеотидам, образующим такой антисмысловой фрагмент, и любое обсуждение, относящееся к модификациям 5'- и 3'-конца, представленным в настоящем описании, конкретно относящееся к смысловой цепи или нуклеотидам, образующим такую смысловую цепь, в равной степени применимо к смысловому фрагменту или нуклеотидам, образующим такой смысловой фрагмент.
В одном из вариантов осуществления молекула нуклеиновой кислоты по изобретению и миРНК по изобретению, в частности, несут, имеют или демонстрируют модификацию 5' и/или 3', таким образом, такая модификация, предпочтительно, является модификацией, представленной в настоящем описании.
миРНК по настоящему изобретению может включать молекулы нуклеиновой кислоты, содержащие один или несколько модифицированных нуклеотидов, нуклеотидов без основания, ациклических или дезоксирибонуклеотидов на 5'- или 3'-конце любой или обеих из смысловой или антисмысловой цепей. В одном из вариантов осуществления 5'- и 3'-концевые нуклеотиды смысловой и антисмысловой цепей являются немодифицированными. В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи является модифицированным. В другом варианте осуществления 5'-концевой нуклеотид смысловой цепи является модифицированным. В другом варианте осуществления 3'-концевой нуклеотид антисмысловой цепи является модифицированным. В другом варианте осуществления 3'-концевой нуклеотид смысловой цепи является модифицированным. В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи и 5'-концевой нуклеотид смысловой цепи являются модифицированными. В другом варианте осуществления 3'-концевой нуклеотид антисмысловой цепи и 3'-концевой нуклеотид смысловой цепи являются модифицированными. В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи и 3'-концевой нуклеотид смысловой цепи являются модифицированными. В другом варианте осуществления 3'-концевой нуклеотид антисмысловой цепи и 5'-концевой нуклеотид смысловой цепи являются модифицированными. В другом варианте осуществления 3'-концевой нуклеотид антисмысловой цепи и 5'- и 3'-концевые нуклеотиды смысловой цепи являются модифицированными. В другом варианте осуществления 5'- и 3'-концевые нуклеотиды антисмысловой цепи являются модифицированными. В другом варианте осуществления 5'- и 3'-концевые нуклеотиды смысловой цепи являются модифицированными.
В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи является фосфорилированным. В другом варианте осуществления 5'-концевой нуклеотид смысловой цепи является фосфорилированным. В другом варианте осуществления 5'-концевые нуклеотиды антисмысловой цепи и смысловой цепи являются фосфорилированными. В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи является фосфорилированным, и 5'-концевой нуклеотид смысловой цепи имеет свободную гидроксильную группу (5'-OH). В другом варианте осуществления 5'-концевой нуклеотид антисмысловой цепи является фосфорилированным, и 5'-концевой нуклеотид смысловой цепи является модифицированным.
Модификации 5'- и 3'-концевых нуклеотидов не ограничены 5'- и 3'-положениями этих концевых нуклеотидов. Неограничивающие примеры модификаций концевых нуклеотидов включают биотин, инвертированные дезоксинуклеотиды без оснований, аминогруппу, фтор, хлор, бром, CN, CF, метоксигруппу, имидазол, карбоксилат, тиоат, C1-C10-низший алкил, замещенный низший алкил, алкиларил или аралкил, OCF3, OCN, O-, S-, или N-алкил; O-, S-, или N-алкенил; SOCH3; SO2CH3; ONO2; NO2, N3; гетероциклоалкил; гетероциклоалкиларил; аминоалкиламиногруппу; полиалкиламиногруппу или замещенный силил, как, помимо прочего, описывают, например, в патентной заявке PCT WO 99/54459, европейских патентах EP 0 586 520 B1 или EP 0 618 925 B1, включенных в настоящее описание в качестве ссылки в полном объеме. Как применяют в настоящем описании, термин "алкил" означает C1-C12-алкил, и термин "низший алкил" означает C1-C6-алкил, включая C1-, C2-, C3-, C4-, C5- и C6-алкил.
В другом аспекте 5'-конец антисмысловой цепи, 5'-конец смысловой цепи, 3'-конец антисмысловой цепи или 3'-конец смысловой цепи ковалентно соединяют с остатком пролекарства. В одном из вариантов осуществления остаток расщепляется в эндосоме. В другом варианте осуществления остаток расщепляется в цитоплазме.
Различные возможные неограничивающие варианты осуществления миРНК по настоящему изобретению, имеющие различные типы модификации концов, представлены в следующей таблице.
Различные варианты осуществления интерферирующей рибонуклеиновой кислоты по настоящему изобретению
3'-конец
свободная OH-группа
свободная OH-группа
3'-конец
концевая модификация
концевая модификация
3'-конец
свободная OH-группа
концевая модификация
3'-конец
концевая модификация
свободная OH-группа
3'-конец
свободная OH-группа
свободная OH-группа
3'-конец
концевая модификация
свободная OH-группа
3'-конец
свободная OH-группа
концевая модификация
3'-конец
концевая модификация
концевая модификация
В другом варианте осуществления концевой 3'-нуклеотид или два концевых 3'-нуклеотида на любой или обеих из антисмысловой цепи или смысловой цепи является 2'-дезоксинуклеотидом. В другом варианте осуществления 2'-дезоксинуклеотид является 2'-дезоксипиримидином. В другом варианте осуществления 2'-дезоксинуклеотид является 2'-дезокситимидином.
shRNA и связанная миРНК:
В объем настоящего изобретения входит, что любое обсуждение, относящееся к shRNA и связанной миРНК, представленным в настоящем описании, конкретно относящееся к антисмысловой цепи или нуклеотидам, образующим такую антисмысловую цепь, в равной степени применимо к антисмысловому фрагменту или нуклеотидам, образующим такой антисмысловой фрагмент, и любое обсуждение, относящееся к модификациям 5'- и 3'-конца, представленным в настоящем описании, конкретно относящееся к смысловой цепи или нуклеотидам, образующим такую смысловую цепь, в равной степени применимо к смысловому фрагменту или нуклеотидам, образующим такой смысловой фрагмент.
В одном из вариантов осуществления молекула нуклеиновой кислоты по изобретению и миРНК по изобретению, в частности, являются shRNA и/или связанной миРНК, таким образом, такая shRNA и/или связанная миРНК, предпочтительно, представлены в настоящем описании.
В объем настоящего изобретения входит, что двухцепочечная структура образована двумя отдельными цепями, т.е. антисмысловой цепью и смысловой цепью. Однако в объем настоящего изобретения также входит, что антисмысловая цепь и смысловая цепь ковалентно связаны друг с другом. Такое соединение может происходить между любыми из нуклеотидов, образующих антисмысловую цепь и смысловую цепь, соответственно. Такое соединение может образовываться посредством ковалентной или нековалентной связей. Ковалентная связь может образовываться посредством соединения обеих цепей один или несколько раз и в одном или нескольких положениях, соответственно, соединением, предпочтительно выбранным из группы, содержащей метиленовый синий и бифункциональные группы. Такие бифункциональные группы, предпочтительно, выбраны из группы, содержащей бис(2-хлорэтил)амин, N-ацетил-N'-(p-глиоксилбензоил)цистамин, 4-тиоурацил и псорален.
В одном из вариантов осуществления антисмысловая цепь и смысловая цепь соединены петлевой структурой. В другом варианте осуществления петлевая структура состоит из полимера, не являющегося нуклеиновой кислотой. В другом варианте осуществления полимером, не являющимся нуклеиновой кислотой, является полиэтиленгликоль. В другом варианте осуществления 5'-конец антисмысловой цепи соединяют с 3'-концом смысловой цепи. В другом варианте осуществления 3'-конец антисмысловой цепи соединяют с 5'-концом смысловой цепи.
В другом варианте осуществления петля состоит из нуклеиновой кислоты. Как применяют в настоящем описании, замкнутую нуклеиновую кислоту (ЗНК) (Elayadi and Corey (2001) Curr Opin Investig Drugs. 2(4):558-61) и пептид-нуклеиновую кислоту (ПНК) (обзор в Faseb J. (2000) 14:1041-1060) считают нуклеиновыми кислотами, и их также можно использовать в качестве полимеров, образующих петлю. В одном из вариантов осуществления нуклеиновая кислота является рибонуклеиновой кислотой. В одном из вариантов осуществления 5'-конец антисмысловой цепи соединяют с 3'-концом смысловой цепи. В другом варианте осуществления 3'-конец антисмысловой цепи соединяют с 5'-концом смысловой цепи. Петля состоит из минимум четырех нуклеотидов или аналогов нуклеотидов. В одном из вариантов осуществления петля состоит из количества нуклеотидов или аналогов нуклеотидов, выбранного из 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15. В одном из вариантов осуществления длина петли является достаточной для ковалентного соединения двух цепей таким образом, что обратный фолдинг может происходить благодаря петлевой структуре или аналогичной структуре. Конструкции рибонуклеиновой кислоты можно встраивать в подходящие векторные системы. Предпочтительно вектор содержит промотор для экспрессии РНКи. Предпочтительно, соответствующим промотором является pol III, и более предпочтительными промоторами являются промоторы U6, H1, 7SK, как описано в Good et al. (1997) Gene Ther. 4, 45-54.
В другом варианте осуществления нуклеиновая кислота по настоящему изобретению содержит фосфотиоатную межнуклеотидную связь. В одном из вариантов осуществления фосфотиоатная межнуклеотидная связь находится в пределах 5 нуклеотидов от 3'-конца или 5'-конца любой или обеих из антисмысловой цепи и смысловой цепи. Антисмысловая цепь может содержать от приблизительно одной до приблизительно пяти фосфотиоатных межнуклеотидных связей.
Комбинации вариантов осуществления:
В объем настоящего изобретения входит, что любое обсуждение, относящееся к комбинациям вариантов осуществления, представленных в настоящем описании, конкретно относящееся к антисмысловой цепи или нуклеотидам, образующим такую антисмысловую цепь, в равной степени применимо к антисмысловому фрагменту или нуклеотидам, образующим такой антисмысловой фрагмент, и любое обсуждение, относящееся к модификациям 5'- и 3'-конца, представленным в настоящем описании, конкретно относящееся к смысловой цепи или нуклеотидам, образующим такую смысловую цепь, в равной степени применимо к смысловому фрагменту или нуклеотидам, образующим такой смысловой фрагмент.
В одном из вариантов осуществления липкий конец на 3'-конце смысловой цепи выбран из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов в длину. В одном из вариантов осуществления липкий конец на 5'-конце антисмысловой цепи выбран из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов в длину. В одном из вариантов осуществления липкий конец на 5'-конце смысловой цепи выбран из группы, состоящей из 1, 2, 3, 4 и 5 нуклеотидов в длину.
В одном из вариантов осуществления молекула миРНК имеет тупой конец на обоих концах и имеет длину, выбранную из группы, состоящей из 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28 или 29 последовательных нуклеотидов.
В одном из вариантов осуществления молекула миРНК имеет тупой конец на одном конце, и двухцепочечная часть молекулы миРНК имеет длину, выбранную из группы, состоящей из 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28 или 29 последовательных нуклеотидов.
В одном из вариантов осуществления молекула миРНК имеет липкие концы на обоих концах, и двухцепочечная часть молекулы миРНК имеет длину, выбранную из группы, состоящей из 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28 или 29 последовательных нуклеотидов.
В одном из вариантов осуществления молекула миРНК содержит липкий конец, содержащий по меньшей мере один дезоксирибонуклеотид. В одном из вариантов осуществления молекула миРНК содержит липкий конец, содержащий два дезоксирибонуклеотида.
В одном из вариантов осуществления молекула миРНК имеет липкие концы на 3'-конце антисмысловой цепи и на 3'-конце смысловой цепи, содержащие по меньшей мере один дезоксирибонуклеотид. В одном из вариантов осуществления молекула миРНК имеет липкие концы на 3'-конце антисмысловой цепи и на 3'-конце смысловой цепи, содержащие два дезоксирибонуклеотида.
Нуклеотиды, образующие липкий конец, могут являться (a) дезоксирибонуклеотидами, (a) рибонуклеотидами или их комбинацией. В одном из вариантов осуществления антисмысловая цепь и/или смысловая цепь содержат динуклеотид TT на 3'-конце.
Как применяют в настоящем описании, в предпочтительном варианте осуществления dT указывает на дезоксирибонуклеотид, а именно T, в молекуле, в ином случае являющейся РНК или состоящей из рибонуклеотидов, которые могут, например, являться модифицированными, как указано в настоящем описании.
Способы получения: Нуклеиновую кислоту по настоящему изобретению можно получать общепринятыми способами в этой области, включающими химический синтез или экспрессию нуклеиновой кислоты in vitro (например, способ транскрипции обрезанной ДНК) или in vivo. В одном из вариантов осуществления миРНК получают с использованием твердофазного химического синтеза. В другом варианте осуществления нуклеиновую кислоту получают с использованием экспрессирующего вектора. В одном из вариантов осуществления экспрессирующий вектор продуцирует нуклеиновую кислоту по изобретению в клетке-мишени. Таким образом, такой вектор можно использовать для производства лекарственного средства. Способы синтеза молекулы нуклеиновой кислоты, представленные в настоящем описании, известны специалистам в этой области. Такие способы, помимо прочего, описывают в Caruthers et al., 1992, Methods in Enzymology 211, 3-19, Thompson et al., международной публикации PCT № WO 99/54459, Wincott et al., 1995, Nucleic Acids Res. 23, 2677-2684, Wincott et al., 1997, Methods Mol. Bio., 74, 59, Brennan et al., 1998, Biotechnol Bioeng., 61, 33-45 и патенте США № 6001311 на имя Brennan (каждый из которых включен в настоящее описание в качестве ссылки в полном объеме).
Как применяют в настоящем описании в отношении любого аспекта изобретения, формулировка, определяющая пределы диапазона длин, такого как, например, "от 13 до 35" означает любое целое число от 13 до 35, т.е. 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 и 35. Другими словами, любой диапазон, определяемый двумя целыми четко указанными числами, предназначен для содержания и описания любого целого числа, определяющего указанные пределы, и любого целого числа, содержащегося в указанном диапазоне.
Доставка/составы:
миРНК можно доставлять в клетки in vitro и in vivo множеством способов, известных специалистам в этой области, включая непосредственный контакт с клетками ("депротеинизированная" миРНК) или использование комбинации с одним или несколькими средствами, облегчающими нацеливание или доставку в клетки. Такие средства и способы включают наноэмульсии (WO 2009/141257 A1), липоплексы, липосомы, ионтофорез, гидрогели, циклодекстрины, нанокапсулы, микро- и наносферы и белковые векторы (например, Bioconjugate Chem. (1999) 10:1068-1074 и WO 00/53722). Комбинацию нуклеиновая кислота/наполнитель можно доставлять местно in vivo посредством прямой инъекции или с использованием инфузионного насоса. МиРНК по изобретению можно доставлять in vivo различными способами, включая внутривенную, подкожную, внутримышечную или внутрикожную инъекцию или ингаляцию. Молекулы по настоящему изобретению можно использовать в качестве фармацевтических средств. Предпочтительно, с помощь фармацевтических средств предотвращают, модулируют частоту или лечат (облегчают симптом до некоторой степени, предпочтительно, все симптомы) стадии заболевания у индивидуума. Таким образом, в дополнительном аспекте настоящее изобретение относится к композиции, содержащей молекулу нуклеиновой кислоты по изобретению и одно из таких средств; предпочтительно, такая композиция предназначена для доставки молекулы нуклеиновой кислоты по изобретению в любом из способов, представленных в настоящем описании.
Наноэмульсия, как описано в международной патентной заявке WO 2009/141257 A1, является стабильной перфторуглеродной наноэмульсией, содержащей усиливающую эндоцитоз поверхность, таким образом, наноэмульсия имеет дискретную перфторуглеродную фазу и забуференную непрерывную водную фазу и содержит (a) перфторуглеродный компонент, содержащий по меньшей мере одно перфторуглеродное соединение; (b) эмульгирующий компонент; и (c) усиливающий эндоцитоз компонент, содержащий по меньшей мере одно соединение, индуцирующее клеточный захват наноэмульсии посредством эндоцитоза. Наноэмульсия может иметь размер частиц менее 100 нм, предпочтительно, наноэмульсия состоит из частиц, имеющих средний размер приблизительно 50 нм. Способы измерения размера частиц известны в этой области и, например, описаны в Murdock RC et al. (R. C. Murdock, et al., "Characterization of nanomaterial dispersion in solution prior to in vitro exposure using dynamic light scattering technique," Toxicol. Sci. 101(2), 239 (2008)) или в Bootz et al. (A. Bootz, V. Vogel, D. Schubert, and J. Kreuter, "Comparison of scanning electron microscopy, dynamic light scattering and analytical ultracentrifugation for the sizing of poly(butyl cyanoacrylate) nanoparticles," Eur. J. Pharm. Biopharm. 57(2), 369 (2004)). Как правило, забуференная водная фаза представляет собой от 25 до 60% по массе наноэмульсии. В варианте осуществления по меньшей мере одно соединение, индуцирующее клеточный захват посредством эндоцитоза, выбрано из трансферрина, аполипопротеин A1, гликозилфосфатидилинозитол(GIP)-заякоренные белки, мегалин-связывающие белки, белки Antennapedia, фрагменты и производные указанных соединений и соединения, имеющие аналогичный эффект, наиболее предпочтительно, указанное соединение является трансферрином или его фрагментом или производным. В другом варианте осуществления по меньшей мере, один перфторуглеродное соединение выбрано из CmF2m+1X, XCmF2mX, XCnF2nOCoF2oX, N(CoF2oX)3 и N(CoF2o+1)3 (где m является целым числом от 3 до 10, n и 0 являются целыми числами от 1 до 5, и X независимо выбран из CI, Br и I), предпочтительно, перфторуглерод выбран из перфтороктилбромида и перфтортрибутиламина и их смесей. Эмульгирующий компонент может содержать по меньшей мере один фосфолипид в качестве важного эмульгирующего компонента и один или несколько вспомогательных липидов. По меньшей мере один фосфолипид выбран из соединений, представленных формулой I
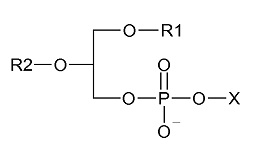
(формула I)
где R1 и R2 независимо выбраны из H и C16-24-ацильных остатков, которые могут являться насыщенными или ненасыщенными и могут нести от 1 до 3 остатков R3, и где один или несколько из атомов углерода могут являться замещенными 0 или NR4, и X выбран из H, -(CH2)p-N(R4)3+, -(CH2)p-CH(N(R4)3+)-COO-, -(CH2)p-CH(OH)-CH2OH и -CH2(CHOH)p-CH2OH (где p является целым числом от 1 до 5; R3 независимо выбран из H, низшего алкила, F, Cl, CN и OH; и R4 независимо выбран из H, CH3 и CH2CH3) или его фармакологически приемлемой соли, предпочтительно, R1 и R2 независимо выбраны из H и незамещенных C16-24-ацильных остатков, которые могут являться насыщенными или ненасыщенными, и X выбран из остатка холина, серина, этаноламина и инозитола, наиболее предпочтительно, фосфолипидный компонент выбран из фосфатидилхолина, лизофосфатидилхолина, фосфатидилэтаноламина и их смесей. Вспомогательный липид можно выбирать из жирных кислот, стероидов, витаминов и их смесей. В предпочтительном варианте осуществления наноэмульсия содержит перфтороктилбромид в качестве перфторуглеродного компонента (a), эмульгирующий компонент (b), содержащий фосфатидилхолин, сфингомиелин, холестерин и лизофосфатидилхолин в качестве фосфолипида и трансферрин в качестве усиливающего эндоцитоз компонента (c).
Липидные наночастицы, содержащие фосфатидилхолин, которые также можно использовать в составлении и доставке молекулы нуклеиновой кислоты по изобретению, например, описывают в Torchilin VP (V. P. Torchilin, "Recent advances with liposomes as pharmaceutical carriers," Nat. Rev. Drug Discov. 4(2), 145 (2005)), Ozpolat B et al. (B. Ozpolat, A. K. Sood, and G. Lopez-Berestein, "Nanomedicine based approaches for the delivery of siRNA in cancer," J. Intern. Med. 267(1), 44 (2010)) or Abbasalipourkabir R et al. (R. Abbasalipourkabir, A. Salehzadeh, and R. Abdullah, "Characterization and stability of nanostructured lipid carriers as drug delivery system," Pak. J. Biol. Sci. 15(3), 141 (2012)).
Другими средствами, которые можно использовать для составления и/или доставки молекулы нуклеиновой кислоты по изобретению, являются липосомы с модифицированной поверхностью, содержащие полиэтиленгликолевые липиды (PEG-модифицированные или длительно циркулирующие липосомы или стелс-липосомы). Эти составы представляют собой способ повышения стабильности растворов липосом или липоплексов, предотвращая их агрегацию и слияние. Составы также обладают дополнительным преимуществом in vivo резистентности опсонизации и элиминации системой мононуклеарных фагоцитов (MPS или RES), таким образом, делая возможным большее время циркуляции в кровотоке и повышенное воздействие на ткань в случае инкапсулированного лекарственного средства. Показано, что такие липосомы избирательно накапливаются в опухолях, предположительно, посредством экстравазации и захвата в неоваскуляризированных тканях-мишенях (Lasic et al., Science 19952671275-1276; Oku et al., 1995, Biochim. Biophys. Acta, 1238, 86-90). Длительно циркулирующие липосомы повышают фармакокинетику и фармакодинамику ДНК и РНК, особенно, по сравнению с общепринятыми катионными липосомами, которые, как известно, накапливаются в тканях MPS (Liu et al., J. Biol. Chem. 1995,42,24864-24780; международная публикация PCT № WO 96/10391 на имя Choi et al.; международная публикация PCT № WO 96/10390 на имя Ansell et al.; международная публикация PCT № WO 96/10392 на имя Holland et al.). Длительно циркулирующие липосомы также защищают миРНК от деградации нуклеазами.
Дополнительными средствами, которые можно использовать в составлении и/или доставке молекулы нуклеиновой кислоты по изобретению, являются липоплексы, например, как описано в WO 2005/105152. В предпочтительном варианте осуществления такой липоплекс является положительно заряженной липосомой, состоящей из:
(a) приблизительно 50 моль% β-аргинил-2,3-диаминопропионовая кислота-N-пальмитил-N-олеил-амида тригидрохлорида, предпочтительно β-(L-аргинил)-2,3-L-диаминопропионовая кислота-N-пальмитил-N-олеил-амида тригидрохлорида, (b) от приблизительно 48 до 49 моль% 1,2-дифитаноил-sn-глицеро-3-фосфоэтаноламина (DPhyPE) и (c) от приблизительно 1 до 2 моль% 1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин-полиэтилeнгликоля, предпочтительно, натриевой соли N-(карбонил-метоксиполиэтиленгликоль-2000)-1,2-дистеароил-sn-глицеро-3-фосфоэтаноламина.
Фармацевтические композиции
Молекулу нуклеиновой кислоты по изобретению можно составлять в виде фармацевтических композиций. Фармацевтические композиции можно использовать в качестве лекарственных средств или диагностических средств в отдельности или в комбинации с другими средствами. Фармацевтические композиции можно использовать в любом способе по изобретению.
Например, одну или несколько молекул нуклеиновой кислоты и/или одну или несколько миРНК по изобретению можно комбинировать со средством доставки (например, наноэмульсией или липосомами) и эксципиентами, такими как носители, дилюенты. В предпочтительном варианте осуществления фармацевтическая композиция является композицией, как описано в разделе "Доставка/составы" в настоящем описании.
Также можно добавлять другие средства, такие как консерванты и стабилизаторы. Способы доставки молекул нуклеиновой кислоты известны в этой области и описаны, например, в Akhtar et al., 1992, Trends Cell Bio., 2, 139; Delivery Strategies for Antisense Oligonucleotide Therapeutics, ed. Akhtar, 1995, Maurer et al., 1999, Mol. Memb. Biol., 16, 129-140; Hofland and Huang, 1999, Handb. Exp. Pharmacol., 137, 165-192; and Lee et al., 2000, ACS Symp. Ser., 752, 184-192, патенте США № 6395713 и PCT WO 94/02595 (каждый из которых включен в настоящее описание в качестве ссылки в полном объеме). МиРНК по настоящему изобретению также можно вводить в комбинации с другими терапевтическими соединениями, вводимыми раздельно или одновременно, например, в качестве комбинированной однократной дозы. В одном из вариантов осуществления изобретение включает фармацевтическую композицию, содержащую одну или несколько миРНК по настоящему изобретению в физиологически/фармацевтически приемлемом эксципиенте, таком как стабилизатор, консервант, дилюент, буфер и т.п.
Специалисты в этой области могут определять уровни доз для лекарственного средства и фармацевтических композиций по изобретению посредством рутинного экспериментирования. В одном из вариантов осуществления однократная доза содержит от приблизительно 0,01 мг/кг до приблизительно 100 мг/кг массы тела миРНК. В одном из вариантов осуществления доза миРНК составляет приблизительно 10 мг/кг до приблизительно 25 мг/кг массы тела. В одном из вариантов осуществления доза миРНК составляет приблизительно 1 мг/кг до приблизительно 10 мг/кг массы тела. В одном из вариантов осуществления доза миРНК составляет приблизительно 0,05 мг/кг до приблизительно 5 мг/кг массы тела. В другом варианте осуществления доза миРНК составляет приблизительно 0,1 мг/кг до приблизительно 5 мг/кг массы тела. В другом варианте осуществления доза миРНК составляет приблизительно 0,1 мг/кг до приблизительно 1 мг/кг массы тела. В другом варианте осуществления доза миРНК составляет приблизительно 0,1 мг/кг до приблизительно 0,5 мг/кг массы тела. В другом варианте осуществления доза миРНК составляет приблизительно 0,5 мг/кг до приблизительно 1 мг/кг массы тела.
В одном из аспектов фармацевтическая композиция является стерильной инъецируемой водной суспензией или раствором. В одном из аспектов фармацевтическая композиция находится в лиофилизированной форме. В одном из вариантов осуществления фармацевтическая композиция содержит наноэмульсию, содержащую молекулу миРНК по изобретению. В одном из вариантов осуществления фармацевтическая композиция содержит лиофилизированные липоплексы, где липоплексы содержат миРНК по настоящему изобретению. В другом варианте осуществления фармацевтическая композиция содержит водную суспензию липоплексов, где липоплексы содержат миРНК по настоящему изобретению.
Фармацевтические композиции и лекарственные средства по настоящему изобретению можно вводить индивидууму (млекопитающему) в описываемых способах лечения. В одном из вариантов осуществления млекопитающее выбрано из группы, состоящей из людей, собак, кошек, лошадей, верблюда, свиньи, козы, овцы, мыши, крысы, хомяка и морской свинки. В одном из вариантов осуществления млекопитающее является человеком. В другом варианте осуществления млекопитающее является не принадлежащим человеку млекопитающим.
Наборы
В дополнительном аспекте изобретение относится к набору. Набор содержит молекулу нуклеиновой кислоты по изобретению, предпочтительно, миРНК по изобретению, и по меньшей мере одно, выбранное из группы, состоящей из контейнера, вкладыша с инструкцией, буфера, положительного контроля, отрицательного контроля или средства доставки, при этом средство доставки, предпочтительно, является средством доставки, представленным в настоящем описании, и реакционной смеси. Набор применим/подходит для практического осуществления любого способа по изобретению. В варианте осуществления набор предназначен для применения в любом способе по изобретению.
Способы лечения
Молекула нуклеиновой кислоты по изобретению применима и ее можно использовать в лечении и/или профилактике заболевания. В варианте осуществления способ включает введение нуклеиновой кислоты индивидууму. Предпочтительно, индивидуум страдает заболеванием или имеет риск развития заболевания. Предпочтительно, индивидуум представляет собой млекопитающего. Как предпочтительно применяют в настоящем описании, млекопитающее является животным, выбранным из группы, содержащей человека, примата, обезьяну, мышь, крысу, кролика, кошку, собаку, верблюда, лошадь, домашнее животное, рабочее животное и животное-компаньона. Более предпочтительно, индивидуум является человеком.
Молекулу нуклеиновой кислоты по изобретению вводят индивидууму в эффективном количестве. Предпочтительно, такое эффективное количество является фармацевтически эффективным количеством или терапевтически эффективным количеством.
Молекулу нуклеиновой кислоты по изобретению можно вводить, по существу, в любой форме, известной специалистам в этой области. Предпочтительным путем введения является системное введение, более предпочтительно - парентеральное введение, предпочтительно - посредством инъекции. Альтернативно, лекарственное средство можно вводить местно. Другие пути введения включают внутримышечный, интраперитонеальный и подкожный, пероральный, интраназальный, интратрахеальный или легочный, при этом предпочтение отдают путю введения, являющемуся наименее инвазивным, в то же время обеспечивающему эффективность.
Парентеральное введение, как правило, используют для подкожных, внутримышечных или внутривенных инъекций и инфузий. Дополнительно, в одном подходе парентерального введения используют имплантацию систем с замедленным высвобождением, обеспечивающих поддержание постоянного уровня дозы, что хорошо известно специалисту в этой области.
Кроме того, предпочтительные лекарственные средства по настоящему изобретению можно вводить в интраназальной форме посредством местного использования подходящих интраназальных наполнителей, ингалянтов или трансдермальными путями с использованием форм трансдермальных пластырей, хорошо известных специалистам в этой области. Для введения в форме трансдермальной системы доставки введение дозы, разумеется, будет непрерывным, а не прерывающимся на всем протяжении режима дозирования. Другие предпочтительные местные препараты включают кремы, мази, лосьоны, аэрозольные спреи и гели.
В предпочтительном варианте осуществления молекула нуклеиновой кислоты по изобретению является миРНК по изобретению.
В варианте осуществления способ лечения и/или профилактики заболевания представляет собой заболевание, которое можно лечить, снижая экспрессию гена Notch 1 и, более конкретно, снижая трансляцию мРНК, кодирующей Notch 1. Конкретные заболевания и состояния, попадающие в эту группу заболеваний, известны специалисту в этой области. Кроме того, определения этого типа заболевания в равной степени известны специалисту в этой области. Предпочтительным заболеванием является злокачественное новообразование, предпочтительно, те формы злокачественного новообразования, при которых Notch 1 положительно регулируется, Notch 1 экспрессируется с изменением по сравнению с неповрежденной тканью или непораженной тканью, и/или при которых терапевтического эффекта можно достигать, снижая экспрессию гена Notch 1 и, более конкретно, снижая трансляцию мРНК, кодирующей Notch 1.
В варианте осуществления заболевание является одним из следующей группы, в которой показано участие Notch 1 и, соответственно, Notch 1 идентифицирован как мишень для лекарственного средства: рак пищевода (см. Streppel, E. A. Montgomery, and A. Maitra, "New Advances in the Pathogenesis and Progression of Barrett's Esophagus," Curr. Mol. Med. (2013)), плоскоклеточный рак полости рта (см. R. Yoshida, et al., "The pathological significance of Notch1 in oral squamous cell carcinoma," Lab Invest (2013)), рак головы и шеи (см. J.T. Lin, et al., "Association of high levels of Jagged-1 and Notch-1 expression with poor prognosis in head and neck cancer," Ann. Surg. Oncol. 17(11), 2976 (2010)), рак языка (см. Y. H. Joo, C. K. Jung, M. S. Kim, and D. I. Sun, "Relationship between vascular endothelial growth factor and Notch1 expression and lymphatic metastasis in tongue cancer," Otolaryngol. Head Neck Surg. 140(4), 512 (2009)), лейкоз (см. E. Kanamori, et al., "Flow cytometric analysis of Notch1 and Jagged1 expression in normal blood cells and leukemia cells," Exp. Ther. Med.4(3), 397 (2012); и Zhang J et al. (J. Zhang, et al., "Prognostic impact of delta-like ligand 4 and Notch1 in acute myeloid leukemia," Oncol. Rep. 28(4), 1503 (2012)), почечноклеточная карцинома (см. Q. Ai, et al., "High-level expression of Notch1 increased the risk of metastasis in T1 stage clear cell renal cell carcinoma," PLoS. One. 7(4), e35022 (2012) и Sjolund, et al., "The notch and TGF-beta signaling pathways contribute to the aggressiveness of clear cell renal cell carcinoma," PLoS. One. 6(8), e23057 (2011)), рак желудка (см. T. S. Yeh, et al., "The activated Notch1 signal pathway is associated with gastric cancer progression through cyclooxygenase-2," Cancer Res. 69(12), 5039 (2009) и Y. Sun, et al., "Differential Notch1 and Notch2 expression and frequent activation of Notch signaling in gastric cancers," Arch. Pathol. Lab Med. 135(4), 451 (2011)), аденокарциному толстого кишечника (см. M. Reedijk, et al., "Activation of Notch signaling in human colon adenocarcinoma," Int J. Oncol. 33(6), 1223 (2008) и M. Reedijk, et al., "Activation of Notch signaling in human colon adenocarcinoma," Int J. Oncol. 33(6), 1223 (2008)), рак эндометрия/тела матки (см. Y. Mitsuhashi, et al., "Prognostic significance of Notch signalling molecules and their involvement in the invasiveness of endometrial carcinoma cells," Histopathology 60(5), 826 (2012)), рак шейки матки (см. L. Santos, et al., "Identification of differential expressed transcripts in cervical cancer of Mexican patients," Tumour. Biol. 32(3), 561 (2011)), внутрипеченочная холангиокарцинома (см. Q. Zhou, et al., "The roles of Notch1 expression in the migration of intrahepatic cholangiocarcinoma," BMC. Cancer 13, 244 (2013) и S. Zender, et al., "A critical role for notch signaling in the formation of cholangiocellular carcinomas," Cancer Cell 23(6), 784 (2013)), печеночноклеточная карцинома (см. A. Villanueva, et al., "Notch signaling is activated in human hepatocellular carcinoma and induces tumor formation in mice," Gastroenterology 143(6), 1660 (2012) и R. Fan, et al., "Cooperation of deregulated Notch signaling and Ras pathway in human hepatocarcinogenesis," J. Mol. Histol. 42(5), 473 (2011)), остеосаркома (см. J. Yang and W. Zhang, "New molecular insights into osteosarcoma targeted therapy," Curr. Opin. Oncol. 25(4), 398 (2013)), карцинома мочевого пузыря (см. A. G. Abdou, et al., "Immunohistochemical analysis of the role and relationship between Notch-1 and Oct-4 expression in urinary bladder carcinoma," APMIS (2013)), злокачественная меланома (см. C. S. Muller, "Notch signaling and malignant melanoma," Adv. Exp. Med. Biol. 727, 258 (2012)), рак щитовидной железы (см. H. S. Park, et al., "Notch1 receptor as a marker of lymph node metastases in papillary thyroid cancer," Cancer Sci. 103(2), 305 (2012)), аденокарцинома легких (см. K. A. Hassan, et al., "Notch pathway activity identifies cells with cancer stem cell-like properties and correlates with worse survival in lung adenocarcinoma," Clin. Cancer Res. 19(8), 1972 (2013) и B. Westhoff, et al., "Alterations of the Notch pathway in lung cancer," Proc. Natl. Acad. Sci. U. S. A 106(52), 22293 (2009)), рак предстательной железы (см. H. Zhu, et al., "Elevated Jagged-1 and Notch-1 expression in high grade and metastatic prostate cancers," Am. J. Transl. Res. 5(3), 368 (2013)) и M. Kashat, et al., "Inactivation of AR and Notch-1 signaling by miR-34a attenuates prostate cancer aggressiveness," Am. J. Transl. Res. 4(4), 432 (2012)), рак молочной железы (см. J. Speiser, et al., "Notch-1 and Notch-4 biomarker expression in triple-negative breast cancer," Int J. Surg. Pathol. 20(2), 139 (2012) и S. Mittal, et al., "Cooperation of Notch and Ras/MAPK signaling pathways in human breast carcinogenesis," Mol. Cancer 8, 128 (2009)), рак яичников (см. S. L. Rose, M. Kunnimalaiyaan, J. Drenzek, and N. Seiler, "Notch 1 signaling is active in ovarian cancer," Gynecol. Oncol. 117(1), 130 (2010)), рак поджелудочной железы (см. F. H. Sarkar, S. Banerjee, and Y. Li, "Pancreatic cancer: pathogenesis, prevention and treatment," Toxicol. Appl. Pharmacol. 224(3), 326 (2007), O. JP De La, et al., "Notch and Kras reprogram pancreatic acinar cells to ductal intraepithelial neoplasia," Proc. Natl. Acad. Sci. U. S. A 105(48), 18907 (2008), E. Ristorcelli and D. Lombardo, "Targeting Notch signaling in pancreatic cancer," Expert. Opin. Ther. Targets. 14(5), 541 (2010), Z. Wang, et al., "Notch-1 down-regulation by curcumin is associated with the inhibition of cell growth and the induction of apoptosis in pancreatic cancer cells," Cancer 106(11), 2503 (2006), P. Buchler, et al., "The Notch signaling pathway is related to neurovascular progression of pancreatic cancer," Ann. Surg. 242(6), 791, discussion (2005), Z. Wang, et al., "Down-regulation of Notch-1 contributes to cell growth inhibition and apoptosis in pancreatic cancer cells," Mol. Cancer Ther. 5(3), 483 (2006), Z. Wang, et al., "Down-regulation of notch-1 inhibits invasion by inactivation of nuclear factor-kappaB, vascular endothelial growth factor, and matrix metalloproteinase-9 in pancreatic cancer cells," Cancer Res. 66(5), 2778 (2006)) и глиома (см. X. Zhang, et al., "Notch1 promotes glioma cell migration and invasion by stimulating beta-catenin and NF-kappaB signaling via AKT activation," Cancer Sci. 103(2), 181 (2012), L. Jiang, et al., "Notch1 expression is upregulated in glioma and is associated with tumor progression," J. Clin. Neurosci. 18(3), 387 (2011), J. Li, et al., "Notch1 is an independent prognostic factor for patients with glioma," J. Surg. Oncol. 103(8), 813 (2011) и S. Puget, et al., "Candidate genes on chromosome 9q33-34 involved in the progression of childhood ependymomas," J. Clin. Oncol. 27(11), 1884 (2009)).
В объем настоящего изобретения входит, что в дополнение к молекуле нуклеиновой кислоты по изобретению в способах лечения используют по меньшей мере одно дополнительное терапевтически или фармацевтически активное средство (также обозначаемое в настоящем описании как "второе дополнительное средство"). Такой способ лечения также обозначают как комбинированное лечение.
"Комбинированное лечение" (или "котерапия") включает введение молекулы нуклеиновой кислоты по изобретению и по меньшей мере второго или дополнительного средства как части конкретной схемы лечения, предназначенной для обеспечения положительного воздействия в результате совместного действия этих терапевтических средств, т.е. лекарственного средства по настоящему изобретению и указанного второго или дополнительного средства. Положительное воздействие комбинации включает, в качестве неограничивающих примеров, фармакокинетическое или фармакодинамическое совместное действие, являющееся результатом комбинации терапевтических средств. Введение этих терапевтических средств в комбинации, как правило, осуществляют в течение определенного периода времени (как правило, минут, часов, дней или недель в зависимости от выбранной комбинации).
Термин "комбинированное лечение" может быть предназначен, но, как правило, нет, для включения введения двух или более из этих терапевтических средств как части раздельных монотерапевтических схем лечения. Термин "комбинированное лечение" предназначен для включения последовательного введения этих терапевтических средств, т.е. где каждое терапевтическое средство вводят в разное время, а также, по существу, одновременного введения этих терапевтические средства или по меньшей мере двух из терапевтических средств. По существу, одновременное введение можно осуществлять, например, посредством введения индивидууму одной капсулы, имеющей фиксированное соотношение каждого терапевтического средства, или множества отдельных капсул для каждого из терапевтических средств.
Последовательное или, по существу, одновременное введение каждого терапевтического средства можно осуществлять любым подходящим путем, включая, в качестве неограничивающих примеров, местные пути, пероральные пути, внутривенные пути, внутримышечные пути и прямую абсорбцию через ткани слизистой оболочки. Терапевтические средства можно вводить одним и тем же путем или разными путями. Например, первое терапевтическое средство из выбранной комбинации можно вводить посредством инъекции, в то время как другие терапевтические средства из комбинации можно вводить местно.
Альтернативно, например, все терапевтические средства можно вводить местно или все терапевтические средства можно вводить посредством инъекции. Последовательность, в которой вводят терапевтические средства, не является критичной, если не указано иначе. "Комбинированное лечение" также может включать введение терапевтических средств, как описано выше, в дополнительной комбинации с другими биологически активными ингредиентами. Если комбинированное лечение дополнительно включает немедикаментозное лечение, немедикаментозное лечение можно осуществлять в любое подходящее время при условии достижения положительного воздействия в результате совместного действия комбинации терапевтических средств и немедикаментозного лечения. Например, в соответствующих случаях положительного воздействия все равно достигают, если немедикаментозное лечение временно удаляют из схемы лечения с введением терапевтических средств, возможно, на дни или даже недели.
В соответствии с этим такое дополнительное терапевтически или фармацевтически активное средство также вводят индивидууму. В варианте осуществления дополнительное терапевтически или фармацевтически активное средство вводят до, совместно или после молекулы нуклеиновой кислоты по изобретению. В варианте осуществления дополнительное терапевтически или фармацевтически активное средство является средством, выбранным из группы, содержащей производные таксана, такие как доцетаксел, паклитаксел (см. Q. F. Ye, et al., "siRNA-mediated silencing of Notch-1 enhances docetaxel induced mitotic arrest and apoptosis in prostate cancer cells," Asian Pac. J. Cancer Prev. 13(6), 2485 (2012), C. C. Zhang, et al., "Synergistic effect of the gamma-secretase inhibitor PF-03084014 and docetaxel in breast cancer models," Stem Cells Transl. Med. 2(3), 233 (2013), K. A. Hassan, et al., "Notch pathway activity identifies cells with cancer stem cell-like properties and correlates with worse survival in lung adenocarcinoma," Clin. Cancer Res. 19(8), 1972 (2013), Y. P. Liu, et al., "Cisplatin selects for multidrug-resistant CD133+ cells in lung adenocarcinoma by activating Notch signaling," Cancer Res. 73(1), 406 (2013) и S. Zang, et al., "RNAi-mediated knockdown of Notch-1 leads to cell growth inhibition and enhanced chemosensitivity in human breast cancer," Oncol. Rep. 23(4), 893 (2010)), производные платины, такие как цисплатин и оксалиплатин (см. K. A. Hassan, et al., "Notch pathway activity identifies cells with cancer stem cell-like properties and correlates with worse survival in lung adenocarcinoma," Clin. Cancer Res. 19(8), 1972 (2013) and Z. P. Zhang, et al., "Correlation of Notch1 expression and activation to cisplatin-sensitivity of head and neck squamous cell carcinoma," Ai. Zheng. 28(2), 100 (2009)), аналоги нуклеозидов, такие как 5-фторурацил (см. R. D. Meng, et al., "gamma-Secretase inhibitors abrogate oxaliplatin-induced activation of the Notch-1 signaling pathway in colon cancer cells resulting in enhanced chemosensitivity," Cancer Res. 69(2), 573 (2009)), ингибиторы топоизомеразы I, такие как иринотекан (см. R. D. Meng, et al., "gamma-Secretase inhibitors abrogate oxaliplatin-induced activation of the Notch-1 signaling pathway in colon cancer cells resulting in enhanced chemosensitivity," Cancer Res. 69(2), 573 (2009)), вещества-интеркаляторы, такие как доксорубицин (см. Y. P. Liu, et al., "Cisplatin selects for multidrug-resistant CD133+ cells in lung adenocarcinoma by activating Notch signaling," Cancer Res. 73(1), 406 (2013)), аналоги нуклеозидов, такие как гемцитабин (см. X. Du, et al., "Notch1 contributes to chemoresistance to gemcitabine and serves as an unfavorable prognostic indicator in pancreatic cancer," World J. Surg. 37(7), 1688 (2013), S. Yabuuchi, et al., "Notch signaling pathway targeted therapy suppresses tumor progression and metastatic spread in pancreatic cancer," Cancer Lett. 335(1), 41 (2013) и S. Richter, et al., "A phase I study of the oral gamma secretase inhibitor R04929097 in combination with gemcitabine in patients with advanced solid tumors (PHL-078/CTEP 8575)," Invest New Drugs (2013)), синтетические глюкокортикоиды, такие как дексаметазон (см. Q. Zhou, et al., "The roles of Notch1 expression in the migration of intrahepatic cholangiocarcinoma," BMC. Cancer 13, 244 (2013)), и алкилирующие средства, такие как темозоломид (см. C. A. Gilbert, M. C. Daou, R. P. Moser, and A. H. Ross, "Gamma-secretase inhibitors enhance temozolomide treatment of human gliomas by inhibiting neurosphere repopulation and xenograft recurrence," Cancer Res. 70(17), 6870 (2010)).
Вариант осуществления способа по изобретению, при условии, что способ лечения является комбинированным лечением, является способом, где вместо введения по меньшей мере одного дополнительного фармацевтически или терапевтически активного средства индивидууму проводят лучевую терапию.
Лучевая терапия (также обозначаемая как "облучение") представляет собой использование ионизирующей радиации для уничтожения злокачественных клеток. Лучевую терапию используют в медицине для лечения почти каждого типа солидной опухоли. Облучение также используют для лечения лейкоза и лимфомы. Лучевая терапия повреждает или уничтожает клетки в области, подвергаемой лечению, повреждая их генетический материал, делая невозможным продолжение роста и деления этих клеток. Эффекты лучевой терапии являются локализованными и ограничены областью, подвергаемой лечению. Доза радиации для каждого участка зависит от ряда факторов, включающих радиочувствительность каждого типа злокачественного новообразования и то, находятся ли рядом ткани и органы, которые радиация может повреждать. Целью лучевой терапии является повреждение наибольшего возможного количества злокачественных клеток с одновременным ограничением повреждения близлежащих здоровых тканей.
В дополнительном варианте осуществления способа лечения и/или профилактики заболевания по изобретению, включающего введение молекулы нуклеиновой кислоты по изобретению, предпочтительно миРНК по изобретению, индивидууму, притом, что заболевание, предпочтительно, является злокачественным новообразованием, и более предпочтительно - злокачественным новообразованием, как представлено в настоящем описании, способ, по существу, является вспомогательной терапией. Целью такой вспомогательной терапии является содействие первичному лечению, предпочтительно, первичному лечению злокачественных опухолей.
Молекула нуклеиновой кислоты по изобретению применима и ее можно использовать в способе восстановления чувствительности злокачественных клеток к лекарственному средству. В варианте осуществления способ включает введение нуклеиновой кислоты по изобретению индивидууму, при условии, что индивидуум страдает заболеванием, предпочтительно, злокачественным новообразованием, и злокачественные клетки, вовлеченные в заболевание, и/или клетки, подлежащие воздействию, повреждению и/или уничтожению посредством любой терапии, проводимой индивидууму или посредством любого фармацевтически или терапевтически активного средства, вводимого индивидууму при лечении заболевания, не являются или более не являются восприимчивыми к такой терапии и/или такому фармацевтически или терапевтически активному средству. Как правило, после введения молекулы нуклеиновой кислоты по изобретению указанные клетки снова становятся восприимчивыми к такой терапии и/или фармацевтически или терапевтически активному средству, по меньшей мере, до терапевтически и/или фармацевтически важного уровня. Такая терапия предпочтительно является терапией злокачественного новообразования, включая, в качестве неограничивающих примеров, терапию на основе цитостатических средств и лучевую терапию, и такое фармацевтически или терапевтически активное средство является средством, используемым в терапии злокачественных новообразований. Предпочтительно, молекула нуклеиновой кислоты по изобретению является миРНК по изобретению.
Таким образом, способ восстановления чувствительности злокачественных клеток к лекарственному средству является способом ресенсибилизации злокачественных клеток, не являющихся или более не являющихся восприимчивыми к терапии злокачественных новообразований и/или фармацевтически или терапевтически активному средству, используемому в терапии злокачественных новообразований. Также следует признать, что способ восстановления чувствительности злокачественных клеток к лекарственному средству представляет собой вспомогательную терапию для способа лечения злокачественного новообразования.
Следует признать, что представленное в настоящем описании в отношении способа лечения и/или профилактики заболевания в равной степени применимо к способу восстановления чувствительности злокачественных клеток к лекарственному средству. В частности, это применимо к аспектам такого способа, относящимся к предмету способа, введению и способам введения нуклеиновой кислоты по изобретению и т.п. Таким образом, способ восстановления чувствительности злокачественных клеток к лекарственному средству является вариантом осуществления способа лечения и/или профилактики заболевания. Предпочтительные формы злокачественного новообразования, у которых может развиваться резистентность к терапии, как правило, проводимой индивидууму, страдающему такими формами злокачественных новообразований, являются следующими:
Рак пищевода (см. Streppel, E. A. Montgomery, and A. Maitra, "New Advances in the Pathogenesis and Progression of Barrett's Esophagus," Curr. Mol. Med. (2013)), плоскоклеточный рак полости рта (см. R. Yoshida, et al., "The pathological significance of Notch1 in oral squamous cell carcinoma," Lab Invest (2013)), рак головы и шеи (см. J.T. Lin, et al., "Association of high levels of Jagged-1 and Notch-1 expression with poor prognosis in head and neck cancer," Ann. Surg. Oncol. 17(11), 2976 (2010)), рак языка (см. Y. H. Joo, C. K. Jung, M. S. Kim, and D. I. Sun, "Relationship between vascular endothelial growth factor and Notch1 expression and lymphatic metastasis in tongue cancer," Otolaryngol. Head Neck Surg. 140(4), 512 (2009)), лейкоз (см. E. Kanamori, et al., "Flow cytometric analysis of Notch1 and Jagged1 expression in normal blood cells and leukemia cells," Exp. Ther. Med. 4(3), 397 (2012); и Zhang J et al. (J. Zhang, et al., "Prognostic impact of delta-like ligand 4 and Notch1 in acute myeloid leukemia," Oncol. Rep. 28(4), 1503 (2012)), почечноклеточная карцинома (см. Q. Ai, et al., "High-level expression of Notch1 increased the risk of metastasis in T1 stage clear cell renal cell carcinoma," PLoS. One. 7(4), e35022 (2012) и J. Sjolund, et al., "The notch and TGF-beta signaling pathways contribute to the aggressiveness of clear cell renal cell carcinoma," PLoS. One. 6(8), e23057 (2011)), рак желудка (см. T. S. Yeh, et al., "The activated Notch1 signal pathway is associated with gastric cancer progression through cyclooxygenase-2," Cancer Res. 69(12), 5039 (2009) и Y. Sun, et al., "Differential Notch1 and Notch2 expression and frequent activation of Notch signaling in gastric cancers," Arch. Pathol. Lab Med. 135(4), 451 (2011)), аденокарцинома толстого кишечника (см. M. Reedijk, et al., "Activation of Notch signaling in human colon adenocarcinoma," Int J. Oncol. 33(6), 1223 (2008) и M. Reedijk, et al., "Activation of Notch signaling in human colon adenocarcinoma," Int J. Oncol. 33(6), 1223 (2008)), рак эндометрия/тела матки (см. Y. Mitsuhashi, et al., "Prognostic significance of Notch signalling molecules and their involvement in the invasiveness of endometrial carcinoma cells," Histopathology 60(5), 826 (2012)), рак шейки матки (см. L. Santos, et al., "Identification of differential expressed transcripts in cervical cancer of Mexican patients," Tumour. Biol. 32(3), 561 (2011)), внутрипеченочная холангиокарцинома (см. Q. Zhou, et al., "The roles of Notch1 expression in the migration of intrahepatic cholangiocarcinoma," BMC. Cancer 13, 244 (2013) и S. Zender, et al., "A critical role for notch signaling in the formation of cholangiocellular carcinomas," Cancer Cell 23(6), 784 (2013)), печеночноклеточная карцинома (см. A. Villanueva, et al., "Notch signaling is activated in human hepatocellular carcinoma and induces tumor formation in mice," Gastroenterology 143(6), 1660 (2012) и R. Fan, et al., "Cooperation of deregulated Notch signaling and Ras pathway in human hepatocarcinogenesis," J. Mol. Histol. 42(5), 473 (2011)), остеосаркома (см. J. Yang and W. Zhang, "New molecular insights into osteosarcoma targeted therapy," Curr. Opin. Oncol. 25(4), 398 (2013)), карцинома мочевого пузыря (см. A. G. Abdou, et al., "Immunohistochemical analysis of the role and relationship between Notch-1 and Oct-4 expression in urinary bladder carcinoma," APMIS (2013)), злокачественная меланома (см. C. S. Muller, "Notch signaling and malignant melanoma," Adv. Exp. Med. Biol. 727, 258 (2012)), рак щитовидной железы (см. H. S. Park, et al., "Notch1 receptor as a marker of lymph node metastases in papillary thyroid cancer," Cancer Sci. 103(2), 305 (2012)), аденокарцинома легких (см. K. A. Hassan, et al., "Notch pathway activity identifies cells with cancer stem cell-like properties and correlates with worse survival in lung adenocarcinoma," Clin. Cancer Res. 19(8), 1972 (2013) и B. Westhoff, et al., "Alterations of the Notch pathway in lung cancer," Proc. Natl. Acad. Sci. U. S. A 106(52), 22293 (2009)), рак предстательной железы (см. H. Zhu, et al., "Elevated Jagged-1 and Notch-1 expression in high grade and metastatic prostate cancers," Am. J. Transl. Res. 5(3), 368 (2013)) и M. Kashat, et al., "Inactivation of AR and Notch-1 signaling by miR-34a attenuates prostate cancer aggressiveness," Am. J. Transl. Res. 4(4), 432 (2012)), рак молочной железы (см. J. Speiser, et al., "Notch-1 and Notch-4 biomarker expression in triple-negative breast cancer," Int J. Surg. Pathol. 20(2), 139 (2012) и S. Mittal, et al., "Cooperation of Notch and Ras/MAPK signaling pathways in human breast carcinogenesis," Mol. Cancer 8, 128 (2009)), рак яичников (см. S. L. Rose, M. Kunnimalaiyaan, J. Drenzek, and N. Seiler, "Notch 1 signaling is active in ovarian cancer," Gynecol. Oncol. 117(1), 130 (2010)), рак поджелудочной железы (см. F. H. Sarkar, S. Banerjee, and Y. Li, "Pancreatic cancer: pathogenesis, prevention and treatment," Toxicol. Appl. Pharmacol. 224(3), 326 (2007), O. JP De La, et al., "Notch and Kras reprogram pancreatic acinar cells to ductal intraepithelial neoplasia," Proc. Natl. Acad. Sci. U. S. A 105(48), 18907 (2008), E. Ristorcelli and D. Lombardo, "Targeting Notch signaling in pancreatic cancer," Expert. Opin. Ther. Targets. 14(5), 541 (2010), Z. Wang, et al., "Notch-1 down-regulation by curcumin is associated with the inhibition of cell growth and the induction of apoptosis in pancreatic cancer cells," Cancer 106(11), 2503 (2006), P. Buchler, et al., "The Notch signaling pathway is related to neurovascular progression of pancreatic cancer," Ann. Surg. 242(6), 791, discussion (2005), Z. Wang, et al., "Down-regulation of Notch-1 contributes to cell growth inhibition and apoptosis in pancreatic cancer cells," Mol. Cancer Ther. 5(3), 483 (2006), Z. Wang, et al., "Down-regulation of notch-1 inhibits invasion by inactivation of nuclear factor-kappaB, vascular endothelial growth factor, and matrix metalloproteinase-9 in pancreatic cancer cells," Cancer Res. 66(5), 2778 (2006)) и глиома (см. X. Zhang, et al., "Notch1 promotes glioma cell migration and invasion by stimulating beta-catenin and NF-kappaB signaling via AKT activation," Cancer Sci. 103(2), 181 (2012), L. Jiang, et al., "Notch1 expression is upregulated in glioma and is associated with tumor progression," J. Clin. Neurosci. 18(3), 387 (2011), J. Li, et al., "Notch1 is an independent prognostic factor for patients with glioma," J. Surg. Oncol. 103(8), 813 (2011) и S. Puget, et al., "Candidate genes on chromosome 9q33-34 involved in the progression of childhood ependymomas," J. Clin. Oncol. 27(11), 1884 (2009)).
Резистентность злокачественных клеток, которую можно преодолевать способом восстановления чувствительности к лекарственному средству, является Notch 1-индуцированной резистентностью и, в частности, Notch 1-индуцированной хеморезистентностью. Таким образом, способ восстановления чувствительности злокачественных клеток к лекарственному средству является способом реверсирования Notch 1-индуцированной резистентности и, в частности, Notch 1-индуцированной хеморезистентности. Является ли клетка и, в частности, злокачественная клетка резистентной к химиотерапевтическим средствам можно определять посредством рутинных тестов, известных специалисту в этой области, такого как анализ MMT (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромид) и проточная цитометрия.
С помощью анализа MMT (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида) измеряют восстановление MTT клеточными ферментами. Измеряя эту метаболическую активность с помощью NAD(P)H-зависимых ферментов можно оценивать количество жизнеспособных клеток. Анализы тетразолиевых красителей делают возможными измерение цитотоксичности и цитостатической активности химиотерапевтических средств.
При проточной цитометрии клетки суспендируют в потоке жидкости и пропускают через детектор. Используя лазерную технологию, можно определять количество клеток и идентифицировать маркеры. Большое количество частиц можно анализировать одновременно по биофизическим и химическим параметрам. Используя этот способ, можно отделять жизнеспособные клетки от апоптотических клеток для измерения эффектов фармацевтических средств.
Notch 1-индуцированную хеморезистентность описывают, например, в K. M. Capaccione and S. R. Pine (K. M. Capaccione and S. R. Pine, "The Notch signaling pathway as a mediator of tumor survival," Carcinogenesis 34(7), 1420 (2013)). Исходя из этой и других ссылок, вполне вероятно, что можно преодолевать Notch 1-индуцированную хеморезистентность посредством ингибирования экспрессии Notch 1 и, таким образом, посредством использования молекулы нуклеиновой кислоты по изобретению. Такие другие ссылки включают, в качестве неограничивающих примеров, Ye, QF et al. (Q. F. Ye, et al., "siRNA-mediated silencing of Notch-1 enhances docetaxel induced mitotic arrest and apoptosis in prostate cancer cells," Asian Pac. J. Cancer Prev. 13(6), 2485 (2012)) в случае рака предстательной железы, Zhang CC et al. (C. C. Zhang, et al., "Synergistic effect of the gamma-secretase inhibitor PF-03084014 and docetaxel in breast cancer models," Stem Cells Transl. Med. 2(3), 233 (2013)) или Zang S et al. (S. Zang, et al., "RNAi-mediated knockdown of Notch-1 leads to cell growth inhibition and enhanced chemosensitivity in human breast cancer," Oncol. Rep. 23(4), 893 (2010)) в случае рака молочной железы, Hassan KA et al. (K. A. Hassan, et al., "Notch pathway activity identifies cells with cancer stem cell-like properties and correlates with worse survival in lung adenocarcinoma," Clin. Cancer Res. 19(8), 1972 (2013)) в случае рака легких, Zhang ZP et al. (Z. P. Zhang, et al., "Correlation of Notch1 expression and activation to cisplatin-sensitivity of head and neck squamous cell carcinoma," Ai. Zheng. 28(2), 100 (2009)) в случае плоскоклеточных карцином, Meng RD et al. (R. D. Meng, et al., "gamma-Secretase inhibitors abrogate oxaliplatin-induced activation of the Notch-1 signaling pathway in colon cancer cells resulting in enhanced chemosensitivity," Cancer Res. 69(2), 573 (2009)) в случае рака толстого кишечника, Liu YP et al. (Y. P. Liu, et al., "Cisplatin selects for multidrug-resistant CD133+ cells in lung adenocarcinoma by activating Notch signaling," Cancer Res. 73(1), 406 (2013)) в случае немелкоклеточного рака легких, Du X et al. (X. Du, et al., "Notch1 contributes to chemoresistance to gemcitabine and serves as an unfavorable prognostic indicator in pancreatic cancer," World J. Surg. 37(7), 1688 (2013)) или Yabuuchi S et al (S. Yabuuchi, et al., "Notch signaling pathway targeted therapy suppresses tumor progression and metastatic spread in pancreatic cancer," Cancer Lett. 335(1), 41 (2013)) в случае рака поджелудочной железы, Zhou Q et al. (Q. Zhou, et al., "The roles of Notch1 expression in the migration of intrahepatic cholangiocarcinoma," BMC. Cancer 13, 244 (2013)) в случае лейкоза и, в частности, острого T-клеточного лимфобластного лейкоза и Gilbert CA et al. (C. A. Gilbert, M. C. Daou, R. P. Moser, and A. H. Ross, "Gamma-secretase inhibitors enhance temozolomide treatment of human gliomas by inhibiting neurosphere repopulation and xenograft recurrence," Cancer Res. 70(17), 6870 (2010)) в случае глиомы.
Помимо преодоления Notch 1-индуцированной резистентности молекула нуклеиновой кислоты по изобретению также подходит для преодоления резистентности к радиации, как это видно из Hovinga KE (K. E. Hovinga, et al., "Inhibition of notch signaling in glioblastoma targets cancer stem cells via an endothelial cell intermediate," Stem Cells 28(6), 1019 (2010)) и Wang J et al. (J. Wang, et al., "Notch promotes radioresistance of glioma stem cells," Stem Cells 28(1), 17 (2010)).
Настоящее изобретение дополнительно проиллюстрировано посредством фигур, примеров и списка последовательностей, из которых можно брать дополнительные признаки, варианты осуществления и преимущества, где
Фиг. 1 является диаграммой, на которой показана относительная экспрессия Notch 1 после трансфекции клеток C4-2 с использованием различных миРНК;
Фиг. 2 является диаграммой для различных миРНК, на которой показана остаточная относительная экспрессия мРНК Notch 1 как функция концентрации отдельных миРНК, что делает возможным определение значения IC50 для каждой миРНК;
Фиг. 3A и 3B являются диаграммами, на которых показана относительная экспрессия мРНК Notch 1 после подвергания клеток C4-2 клетки воздействию миРНК XD-00404 (фиг. 3A) или XD-00409 (фиг. 3B) в их немодифицированной, промежуточной или полностью модифицированной форме в концентрации 10 нМ, 1 нм и 0,1 нМ;
Фиг. 4 является диаграммой, на которой показано относительное увеличение объема опухоли (указанное как %±SEM) в модели ксенотрансплантата мыши с использованием клеток PANC-1; и
Фиг. 5 является диаграммой, на которой показано количество животных в модели ортотопической опухоли PANC-1 без метастазов, с несколькими метастазами и с отдельными метастазами после введения модели на животных контроля, гемцитабина или комбинации гемцитабина и наноносителя, содержащего миРНК по изобретению.
Пример 1: Материалы и способы
МиРНК
МиРНК, представленные в таблице 1, получали с использованием стандартного химического синтеза:
Приведенная выше таблица 1 снова представлена в виде таблицы 1a, включающей идентификаторы последовательностей.
(SEQ ID NO: 73)
(SEQ ID NO: 74)
(SEQ ID NO: 75)
(SEQ ID NO: 76)
(SEQ ID NO: 77)
(SEQ ID NO: 78)
(SEQ ID NO: 79)
(SEQ ID NO: 80)
(SEQ ID NO: 81)
(SEQ ID NO: 82)
(SEQ ID NO: 83)
(SEQ ID NO: 84)
(SEQ ID NO: 85)
(SEQ ID NO: 86)
(SEQ ID NO: 87)
(SEQ ID NO: 88)
(SEQ ID NO: 89)
(SEQ ID NO: 90)
(SEQ ID NO: 91)
(SEQ ID NO: 92)
(SEQ ID NO: 93)
(SEQ ID NO: 94)
(SEQ ID NO: 95)
(SEQ ID NO: 96)
(SEQ ID NO: 97)
(SEQ ID NO: 98)
(SEQ ID NO: 99)
(SEQ ID NO: 100)
(SEQ ID NO: 101)
(SEQ ID NO: 102)
(SEQ ID NO: 103)
(SEQ ID NO: 104)
(SEQ ID NO: 105)
(SEQ ID NO: 106)
(SEQ ID NO: 107)
(SEQ ID NO: 108)
(SEQ ID NO: 109)
(SEQ ID NO: 110)
(SEQ ID NO: 111)
(SEQ ID NO: 112)
(SEQ ID NO: 113)
(SEQ ID NO: 114)
(SEQ ID NO: 115)
(SEQ ID NO: 116)
(SEQ ID NO: 117)
(SEQ ID NO: 118)
(SEQ ID NO: 119)
(SEQ ID NO: 120)
(SEQ ID NO: 121)
(SEQ ID NO: 122)
(SEQ ID NO: 123)
(SEQ ID NO: 124)
(SEQ ID NO: 125)
(SEQ ID NO: 126)
Из этой группы модифицировали несколько следующих миРНК. Модифицированные миРНК указаны в таблице 2.
Таблица 2:
a) XD-00395
смысловая цепь: 5'-GGACCCAACACUUACACCUdTdT-3' (SEQ ID NO: 87)
антисмысловая цепь: 5'-AGGUGUAAGUGUUGGGUCCdTdT-3' (SEQ ID NO: 88)
b) XD-00404
смысловая цепь: 5'-GACAUCGCACAGGAGCGCAdTdT-3' (SEQ ID NO: 105)
антисмысловая цепь: 5'-UGCGCUCCUGUGCGAUGUCdTdT-3' (SEQ ID NO: 106)
c) XD-00406
смысловая цепь: 5'-CAUGGUGCCGAACCAAUACdTdT-3' (SEQ ID NO: 109)
антисмысловая цепь: 5'-GUAUUGGUUCGGCACCAUGdTdT-3' (SEQ ID NO: 110)
d) XD-00407
смысловая цепь: 5'-UGGUGCCGAACCAAUACAAdTdT-3' (SEQ ID NO: 111)
антисмысловая цепь: 5'-UUGUAUUGGUUCGGCACCAdTdT-3' (SEQ ID NO: 112)
e) XD-00409
смысловая цепь: 5'-GACCAGUGGUCCAGCUCGUdTdT-3' (SEQ ID NO: 115)
антисмысловая цепь: 5'-ACGAGCUGGACCACUGGUCdTdT-3' (SEQ ID NO: 116)
f) XD-00410
смысловая цепь: 5'-CAUUCCAACGUCUCCGACUdTdT-3' (SEQ ID NO: 117)
антисмысловая цепь: 5'-AGUCGGAGACGUUGGAAUGdTdT-3' (SEQ ID NO: 118)
Полностью стабилизированные миРНК
МиРНК XD-00404 и XD-00409 из таблицы 2 подвергали полной стабилизации. Таким образом, полностью стабилизированные миРНК являлись следующими.
a) XD-00409
смысловая цепь: 5'-GAcCaGuGgUcCaGcUcGudTSdT-3' (SEQ ID NO: 70)
антисмысловая цепь: 5'-acGaGcUgGaCcAcUgGuCdTSdT-3'(SEQ ID NO: 69)
b) XD-00404
смысловая цепь: 5'-GAcAuCgCaCaGgAgCgCadTSdT-3' (SEQ ID NO: 128)
антисмысловая цепь: 5'-ugCgCuCcUgUgCgAuGuCdTSdT-3'(SEQ ID NO: 127),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'O-метил-модифицированным и
где dTsdT указывает на то, что на 3'-конце присоединен динуклеотид, состоящий из двух dT, где указанные два dT ковалентно связаны посредством фосфотиоатной связью.
Промежуточно стабилизированные миРНК
Промежуточно стабилизированные миРНК отличаются от полностью стабилизированной миРНК таким образом, что в ней отсутствует липкий конец dTsdT, и в ней не наблюдают какую-либо 2'-F модификацию.
Культивирование клеток C4-2
Клетки C4-2 культивировали стандартными способами, описанными для этой клеточной линии, с использованием среды RPMI 1640.
Трансфекция клеток C4-2
Клетки C4-2 трансфицировали с использованием различных концентраций миРНК с использованием Lipofectamine 2000. В эксперименте по трансфекции концентрации миРНК составляли 50 нМ, 10 нМ, 1 нМ или 0,1 нМ. Время инкубации составляло 24 ч. В ином случае использовали стандартный протокол. Определяли эффективность трансфекции посредством измерения миРНК "домашнего хозяйства"; эффективность трансфекции составляла по меньшей мере 93% во всех случаях.
Определение IC50 миРНК
Значения IC50 определяли стандартными способами. Более конкретно, определяли концентрацию миРНК, при которой экспрессия мРНК Notch 1 снижалась до 50% с использованием клеток C4-2, трансфицированных, как описано, с использованием различных указанных миРНК.
Наноноситель
Для получения наноносителя, являющегося перфторуглеродным наноносителем, перфтороктилбромид (Perflubron) эмульгировали со смесью фосфолипидов. Один грамм смеси содержит фосфатидилхолин (980 мг), сфингомиелин (10 мг), холестерин (5 мг), Лизофосфатидилхолин (5 мг) в дистиллированной воде и буфере 75 мМ дигидрофосфат натрия (NaH2PO4). Для получения 1000 мкл перфторуглеродного наноносителя использовали 475 мкл перфтороктилбромида, 36 мг фосфолипидов, 200 мкл 75 мМ NaH2PO4 при pH 7,4 и 325 мкл дистиллированной воды.
Сначала смешивали фосфолипиды, буфер дигидрофосфата натрия и дистиллированную воду, а затем добавляли раствор перфторуглерода (PFC). Через 40 секунд смесь необходимо смешать с помощью шейкера в течение 60 сек и незамедлительно дважды гомогенизировать с помощью ультразвукового устройства с частотой 1100 кГц в течение 120 сек с интервалами 30 сек. Ультразвуковой модуль держат при температуре 4°C. Для конечной эмульсии в ином случае нерастворимого PFC смесь помещают в гомогенизатор высокого давления. После шести гомогенизаций при 2500×105 Па мутная смесь становится прозрачной, голубоватой эмульсией. Это превращение в прозрачную эмульсию является макроскопическим признаком того, что размер перфторуглеродных частиц становится меньше видимых длин волн. При наименьшей видимой длине волны (синяя/фиолетовая область) λ=400 нм размер частиц определяют как λ/2, если смесь становится прозрачной. На этом этапе добавляют четыре дополнительных цикла гомогенизации. Размер частиц измеряли посредством электронной микроскопии как 50 нм (среднее), при этом все частицы имели размер менее 100 нм. Для получения функционального наноносителя 4 мг холотрансферрина растворяют в 60 мкл стерильного 0,9% NaCl. Непосредственно после этого, трансферрин гомогенизируют в течение 2 сек с помощью охлаждаемого ультразвукового устройства. Растворенный трансферрин добавляют к 1000 мкл перфторуглеродной эмульсии для получения конечной концентрации 4 мг/мл. И снова, соединение незамедлительно помещали в шейкер на 30 сек.
Этот наноноситель также обозначают как ненагруженный носитель или NCf4.
Наноносители, нагруженные миРНК Notch
Получали наноносители, нагруженные миРНК Notch, с учетом описанного в разделе "Наноноситель" выше. Для нагрузки желаемые типы миРНК добавляли в наноносители и, таким образом, полученную смесь подвергали гомогенизации с помощью ультразвука с использованием 500 Вт в течение 15 сек.
Исследование на животных - модель ксенотрансплантата
Шестьдесят самок безтимусных мышей Foxn1nu, несущих опухоли из подкожно инокулированных опухолей поджелудочной железы человека PANC-1, выбирали из совокупности 112. Эта модель на животных является моделью на животных, разработанной для рака поджелудочной железы и опухоли поджелудочной железы, соответственно, с использованием линии клеток PANC-1, впервые описанной Lieber M et al. (M. Lieber, et al., "Establishment of a continuous tumor-cell line (panc-1) from a human carcinoma of the exocrine pancreas," Int J. Cancer 15(5), 741 (1975)), и биохимически, а также морфологически, охарактеризованной Madden ME и Sarras MP (M. E. Madden and M. P. Sarras, Jr., "Morphological and biochemical characterization of a human pancreatic ductal cell line (PANC-1)," Pancreas 3(5), 512 (1988)). Такую линию клеток и модель на животных, разработанную с использованием такой линии клеток, используют в оценке противоопухолевых средств Schultz RM et al. (R. M. Schultz, et al., "Evaluation of new anticancer agents against the MIA PaCa-2 and PANC-1 human pancreatic carcinoma xenografts," Oncol. Res. 5(6-7), 223 (1993)).
Через тридцать три дня после инокуляции мышей рандомизировали по размеру опухоли на шесть групп по десять (день 0).
Мышам в каждой группе дважды в неделю вводили контрольный наполнитель (ненагруженный наноноситель, NCf4), или гемцитабин в дозе 60 мг/кг посредством интраперитонеальной инъекции, или комбинацию Notch/гемцитабин, каждый - описываемым образом, при этом Notch представлял собой наноносители, нагруженные миРНК Notch (полученные, как описано в примере 1, с использованием полностью стабилизированного XD-00409), вводимые посредством внутривенной инъекции.
Введение начинали в день 0 и вводили семь доз. Ежедневно осуществляли клиническое наблюдение. Измерения массы тела и размера опухоли осуществляли три раза в неделю в течение исследования.
После окончания исследования (день 24) собирали опухоли из всех мышей во всех исследуемых группах, взвешивали и разрезали пополам. Одну часть фиксировали в растворе RNAlater для выделения РНК и анализа qRT-ПЦР. Оставшуюся часть фиксировали в формалине для заключения в парафин и микроскопической оценки некроза.
Исследование на животных - ортотопическая модель
Шестидесяти самкам безтимусных мышей Foxn1nu ортотопически инокулировали опухолевые клетки поджелудочной железы человека PANC-1. Частоту приживления оценивали у трех мышей в дни 20 и 27 после инокуляции. Через тридцать два дня после инокуляции оставшихся 60 мышей рандомизировали по массе тела на шесть групп по десять (день 0).
Мышам в каждой группе дважды в неделю вводили контрольный наполнитель (ненагруженный наноноситель, NCf4), гемцитабин в дозе 60 мг/кг посредством интраперитонеальной инъекции, или комбинацию Notch/гемцитабин, каждый - описываемым образом, при этом Notch представлял собой наноносители, нагруженные миРНК Notch (полученные, как описано в примере 1, с использованием полностью стабилизированного XD-00409), вводимые посредством внутривенной инъекции.
Введение начинали в день 0 и вводили пять доз.
Ежедневно осуществляли клиническое наблюдение. Измерения массы тела и размера опухоли осуществляли три раза в неделю в течение исследования.
После окончания исследования (день 18) интактную опухоль и поджелудочную железу из всех мышей во всех исследуемых группах и взвешивали. Опухоли удаляли из поджелудочной железы и разрезали пополам. Одну часть фиксировали в растворе RNAlater для необязательного выделения РНК и анализа qRT-ПЦР (не осуществляли). Оставшуюся часть фиксировали в формалине для заключения в парафин и микроскопической оценки некроза. Легкие и печень собирали из всех мышей по окончании исследования. Их взвешивали и оценивали на поверхностные метастазы. Легкие и печени фиксировали в формалине для заключения в парафин. Печени оценивали на наличие микрометастазов.
Пример 2: Эффективность немодифицированных миРНК против Notch 1 человека
Клетки C4-2 культивировали и трансфицировали с использованием различных миРНК, указанных в таблице 1, как описано в примере 1, при этом концентрация миРНК составляла 50 нМ. Результаты представлены на фиг. 1. Фиг. 1 является диаграммой, на которой показана относительная экспрессия Notch 1 после трансфекции клеток C4-2 с использованием различных миРНК. Экспрессию нормализуют по экспрессии Notch 1 в клетках C4-2 с использованием контроля. Контролем являлась миРНК, не направленная против какой-либо известной мРНК, кодирующей белок.
Как видно на фиг. 1, лучшая миРНК демонстрирует нокдаун мРНК Notch 1 почти на 80%. Так же на фиг. 1 видно, что существует значимое различие в эффективности различных миРНК.
6 миРНК, демонстрирующих лучший нокдаун, представлены в таблице 2. Эти миРНК дополнительно охарактеризовывали в терминах их IC50. Результаты представлены на фиг. 2.
Фиг. 2 является диаграммой для каждой миРНК из таблицы 2, на которой показана остаточная относительная экспрессия мРНК Notch 1 как функция концентрации каждой миРНК. Из указанных диаграмм вычисляли IC50 для каждой из указанных миРНК. Значения IC50 для указанных молекул миРНК представлены в таблице 3.
Как видно из фиг. 2 и таблицы 3, лучшей молекулой миРНК в терминах IC50 является XD-00409, имеющая IC50 4,3 пМ.
Пример 3: Эффективность модифицированной миРНК против Notch 1 человека
Молекулы миРНК XD00404 и XD-00409 из таблиц 1 и 2 подвергали промежуточной стабилизации и полной стабилизации, как описано в примере 1. Таким образом, модифицированные молекулы миРНК являлись следующими
a) XD-00404 с промежуточной стабилизацией (также обозначаемая как XD-00751);
b) XD-00404 с полной стабилизацией (также обозначаемая как XD-00752);
c) XD-00409 с промежуточной стабилизацией (также обозначаемая как XD-00753);
d) XD-00409 с полной стабилизацией (также обозначаемая как XD-00754).
Эти молекулы миРНК тестировали на их эффективность в клетках C4-2 после трансфекции указанных клеток C4-2, как описано в примере 1, при этом в эксперименте по трансфекции концентрация миРНК составляла 10 нМ, 1 нМ или 0,1 нМ.
Результаты таких экспериментов представлены на фиг. 3A для миРНК XD-00404 в ее немодифицированной, промежуточной или полностью модифицированной форме и для миРНК XD-00409 в ее немодифицированной, промежуточной или полностью модифицированной форме и на фиг. 3B в виде относительной экспрессии мРНК с использованием контроля. Контролем являлась миРНК, не направленная против какой-либо известной мРНК, кодирующей белок.
Как видно из фиг. 3, хотя модификация молекулы миРНК является благоприятной в терминах стабильности, очевидно, что модификация обеих миРНК (XD-00404 и XD-00409) снижает их эффективность нокдауна экспрессии мРНК Notch 1. Однако неожиданно обнаруживали, что влияние модификации на XD-00409 является менее выраженным и, фактически, не существует по сравнению с влиянием модификации на XD-00404. Таким образом, миРНК DX-00409 демонстрирует неожиданные эффекты.
Пример 4: Эффект миРНК против Notch 1 человека в модели ксенотрансплантата опухоли поджелудочной железы
Осуществляли исследование на животных с использованием опухолей поджелудочной железы человека PANC-1, как описано в примере 1. Используемым типом миРНК являлась полностью модифицированная XD-00409.
Результаты исследования можно обобщать следующим образом:
- Потеря массы тела не являлась очевидной. Небольшая масса присутствовала под передней лапой всего у 10 мышей в исследовании.
- Наблюдали слабое ингибирование опухоли после использования монотерапии гемцитабином и комбинации Notch/гемцитабин, определяемое посредством измерения процентной доли роста опухоли и массы опухоли, но только введение комбинации Notch/гемцитабин значимо отличалось от наполнителя в отношении массы опухоли. При введении комбинации Notch/гемцитабин наблюдали синергичный ответ, относящийся к ингибированию опухоли, измеряемый по процентной доле роста опухоли.
- Мыши, которым проводили монотерапию гемцитабином и вводили комбинацию Notch/гемцитабин, имели наименьшую частоту некроза опухоли.
Результат указанного исследования на животных также представлен на фиг. 4. Фиг. 4 является диаграммой, на которой показано относительное повышение объема опухоли (указанное как %±SEM) с течение времени при использовании контроля ("наполнитель (NCF4)"), гемцитабин ("гемцитабин") и комбинации гемцитабина и наноносителя, нагруженного миРНК Notch ("Notch/гемцитабин"). Каждое из средств или комбинацию средств вводили дважды в неделю.
Пример 5: Эффект миРНК против Notch 1 человека в модели ортотопической опухоли поджелудочной железы
Осуществляли исследование на животных с использованием опухолей поджелудочной железы PANC-1 человека, как описано в примере 1. Используемым типом миРНК являлась полностью стабилизированная XD-00409.
Результаты исследования можно обобщать следующим образом:
Количество животных без метастазов на основе клеток PANC-1 значимо снижалось, как показано на фиг. 5 в случае животных, которым вводили комбинацию гемцитабина и наноносителя, нагруженного миРНК Notch, по сравнению с животными, которым вводили контроль или только гемцитабин. Более конкретно, после введения десяти животным только наполнителя три животных имели несколько метастазов, три животных имели отдельные метастазы, и у четырех животных отсутствовали метастазы; после введения десяти животным только гемцитабина два животных имели несколько метастазов, четыре животных имели отдельные метастазы, и у четырех животных отсутствовали метастазы; и после введения десяти животным гемцитабина и наноносителей, нагруженных миРНК, с использованием полностью модифицированной XD-00409 одно животное имело несколько метастазов, одно животное имело отдельный метастаз, и у восьми животных отсутствовали метастазы.
Кроме того, введение гемцитабина в комбинации с Notch 1-специфичной миРНК (полностью стабилизированной XD-00409) ассоциировано со значимой средней потерей массы тела и с ухудшением физического состояния у двух мышей.
Содержание и описание различных ссылок, процитированных в настоящем описании, включено в настоящее описание в качестве ссылок в полном объеме.
Признаки настоящего изобретения, представленные в описании, формуле изобретения и/или чертежах раздельно и в любой их комбинации, могут являться материалом для реализации изобретения в различных его формах.
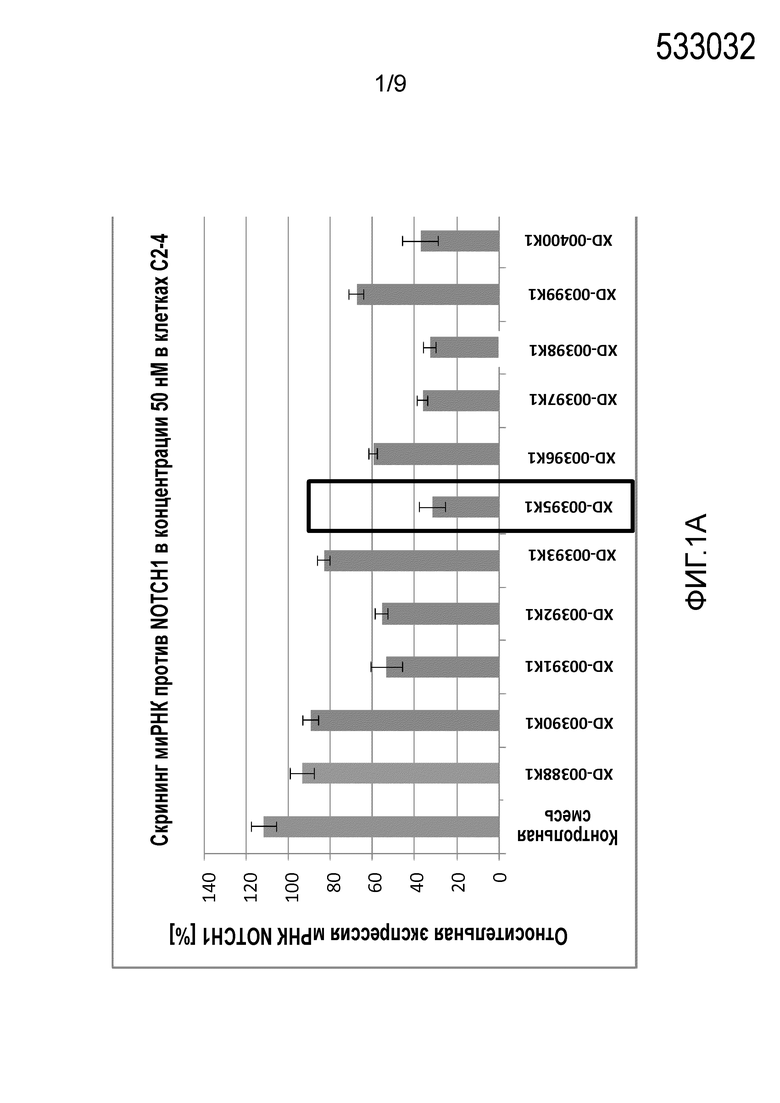
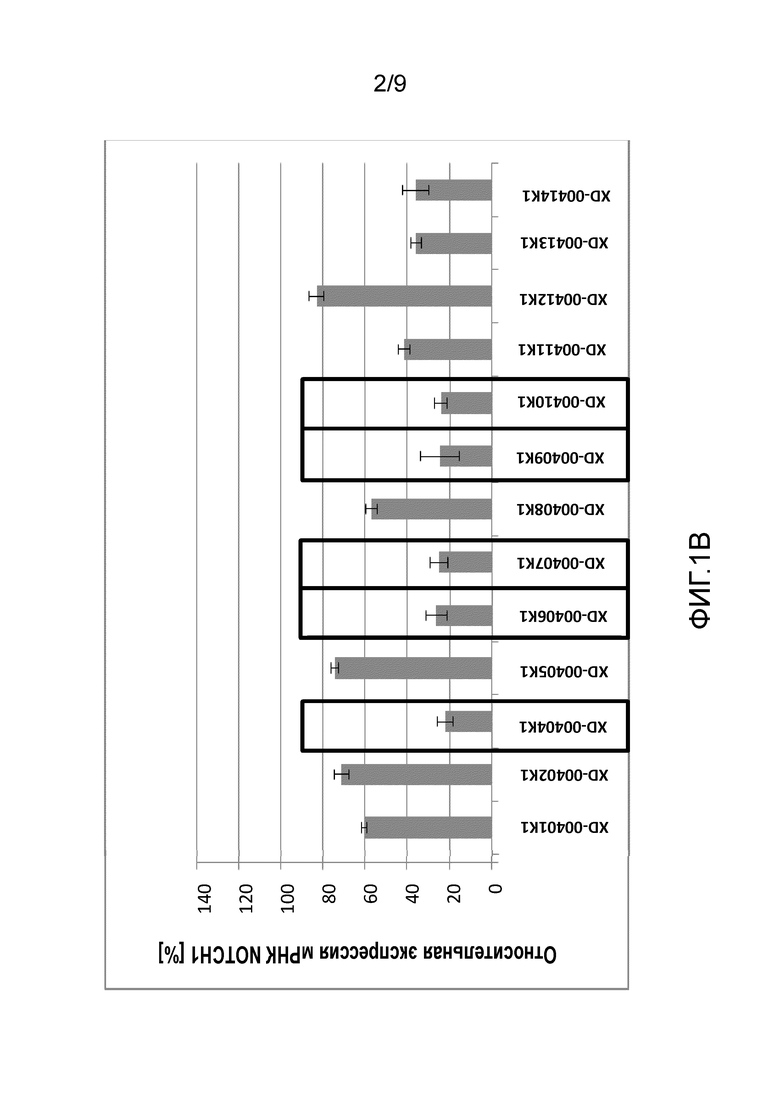
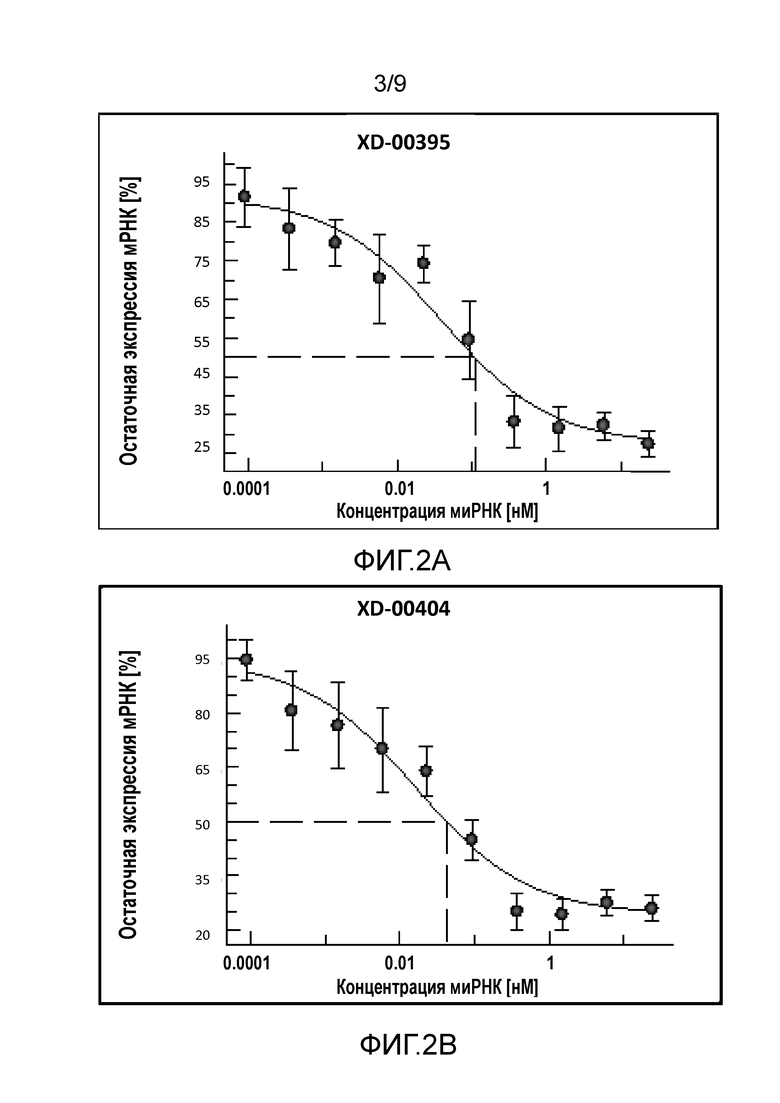
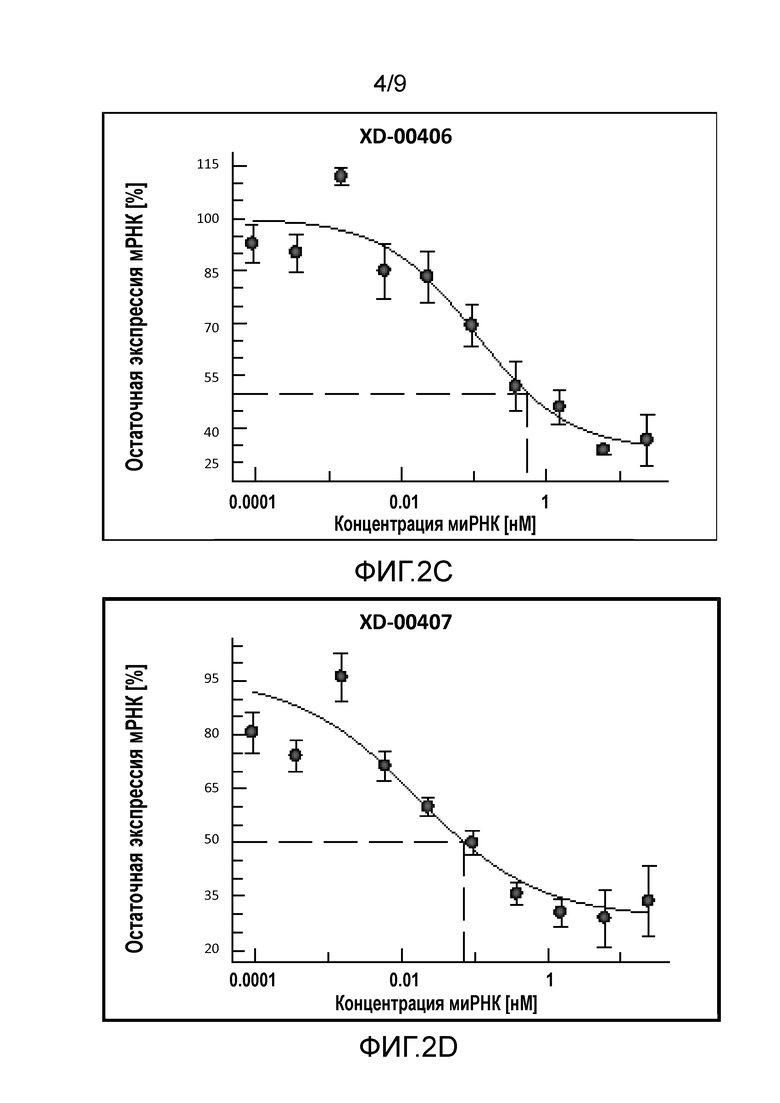
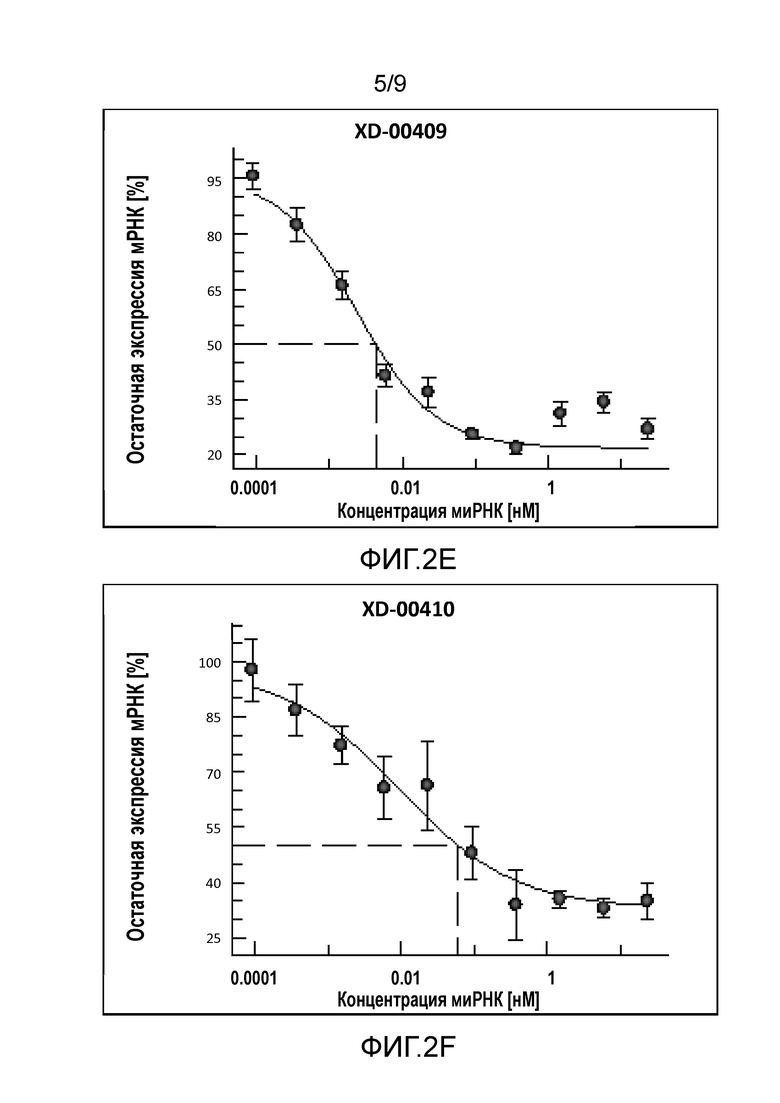
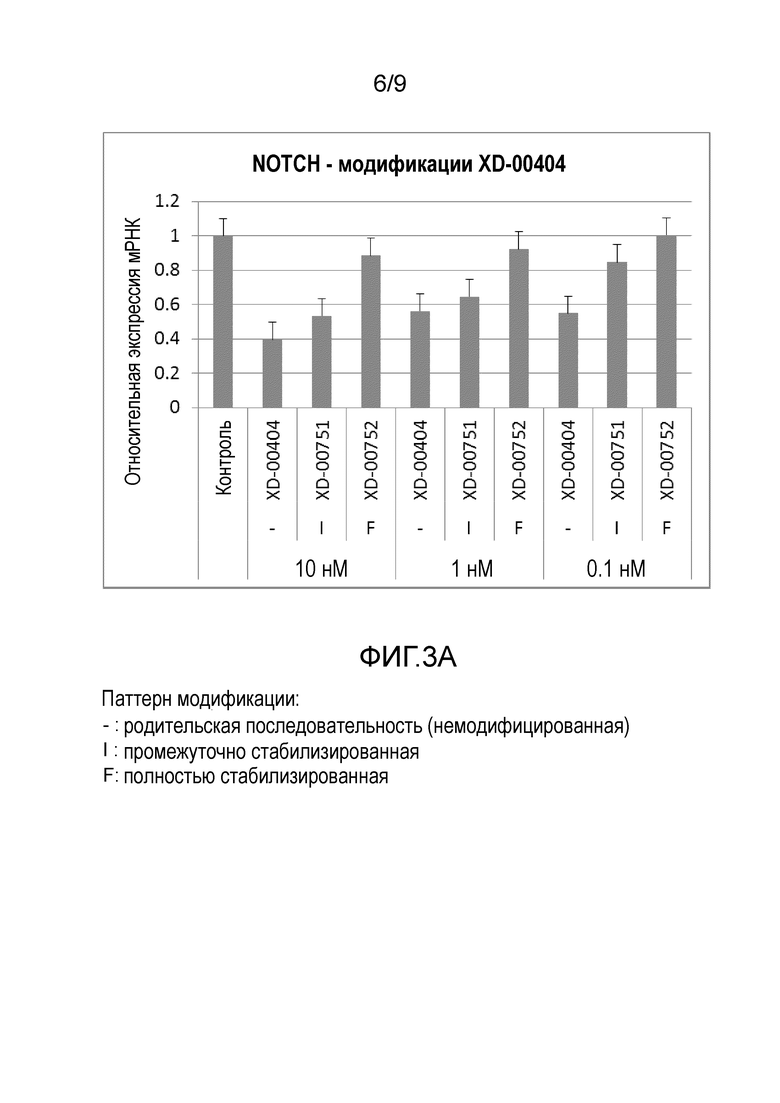
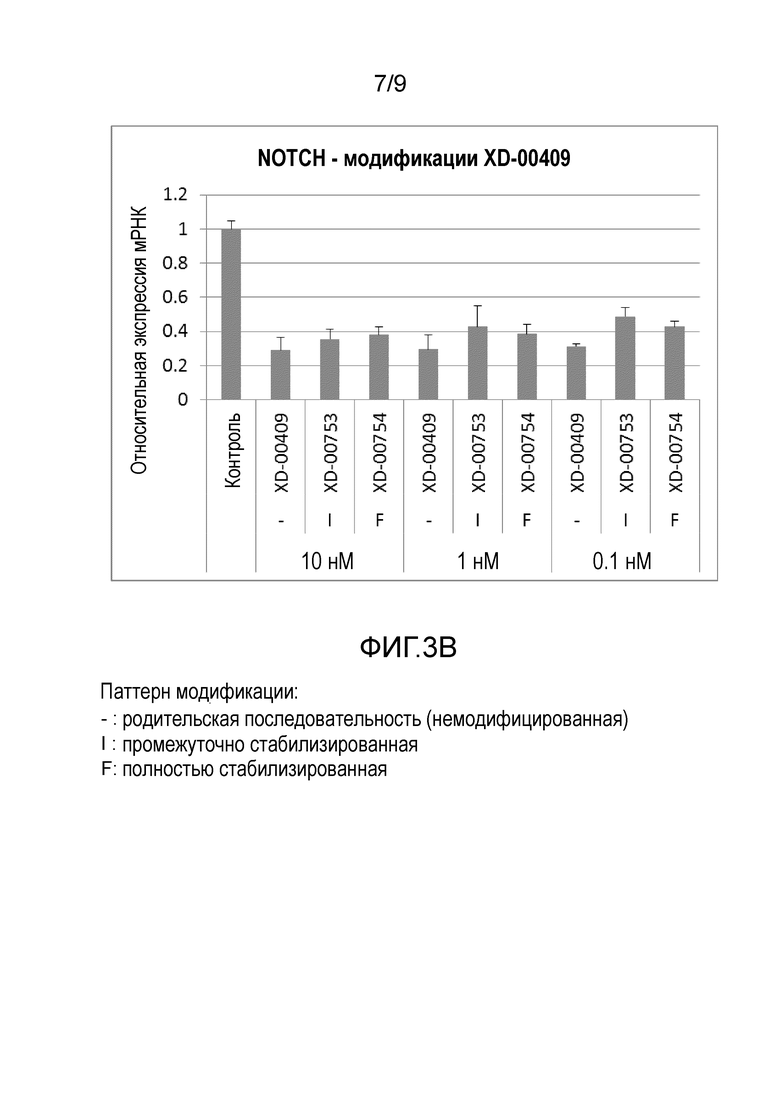
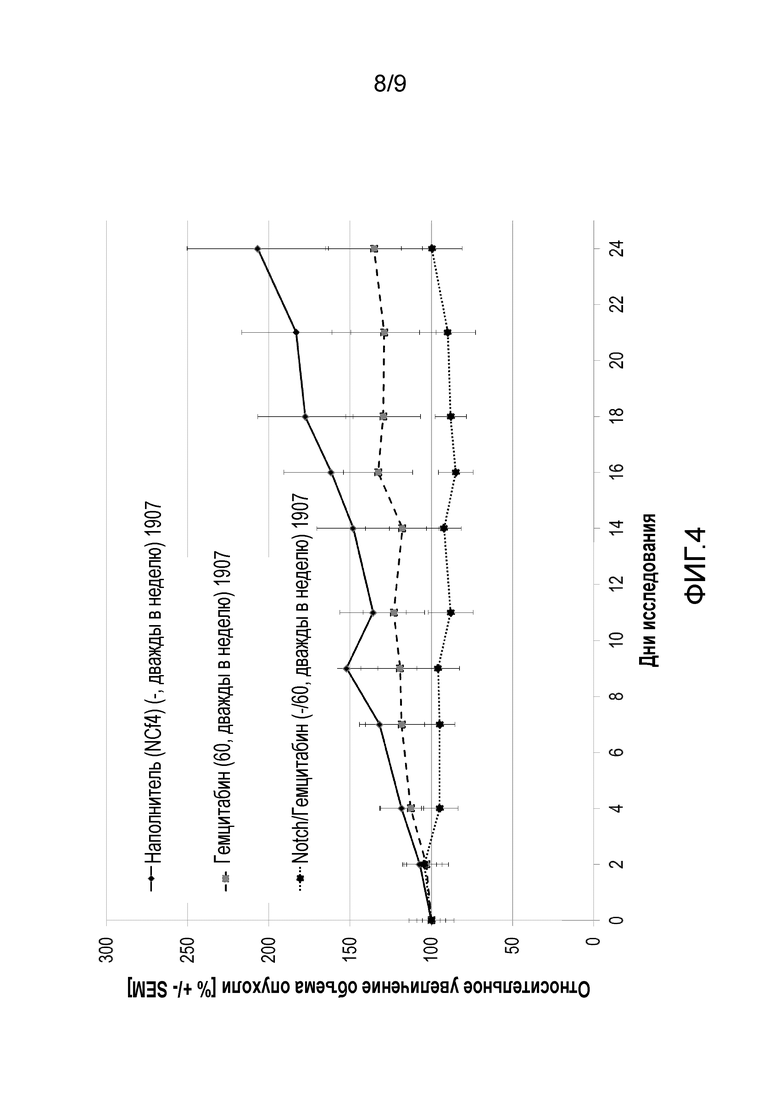
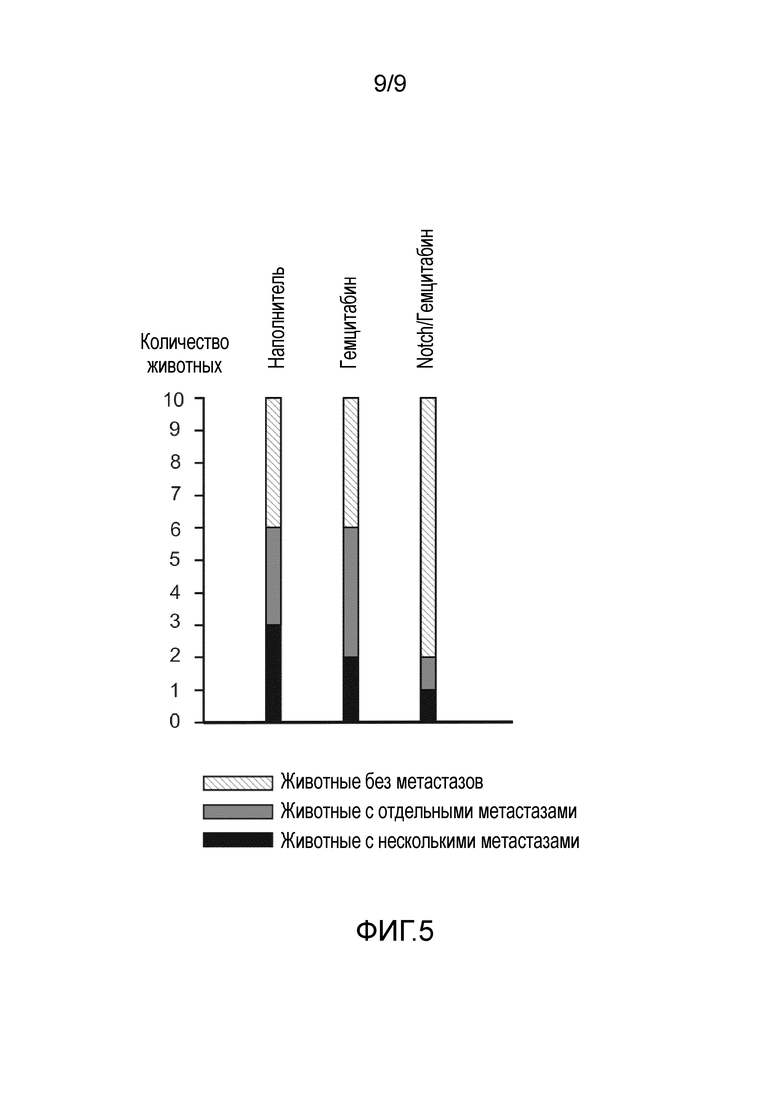
Изобретение относится к биотехнологии. Описана молекула нуклеиновой кислоты, содержащая двухцепочечную структуру,
где двухцепочечная структура образована первой цепью и второй цепью, где первая цепь состоит из следующей нуклеотидной последовательности:
5'-acGaGcUgGaCcAcUgGuCdTSdT-3' и вторая цепь состоит из следующей нуклеотидной последовательности:
5'-GAcCaGuGgUcCaGcUcGudTSdT-3', где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным и где dTSdT указывает на то, что на 3'-конце присоединен динуклеотид, состоящий из двух нуклеотидов dT, где указанные два dT ковалентно связаны посредством фосфотиоатной связи. Описано применение описанной молекулы нуклеиновой кислоты в получении средства для восстановления чувствительности злокачественных клеток к лекарственному средству и для лечения и/или профилактики заболевания. Представлены фармацевтическая композиция и наноэмульсия, содержащие описанную молекулу нуклеиновой кислоты. 7 н. и 104 з.п. ф-лы, 5 ил., 3 табл., 5 пр.
1. Молекула нуклеиновой кислоты, содержащая двухцепочечную структуру,
где двухцепочечная структура образована первой цепью и второй цепью,
где первая цепь содержит первый фрагмент смежных нуклеотидов и вторая цепь содержит второй фрагмент смежных нуклеотидов,
где первый фрагмент смежных нуклеотидов содержит
a) нуклеотидную последовательность, где нуклеотидная последовательность является по меньшей мере на 63% идентичной по отношению к
(i) нуклеотидной последовательности 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидной последовательности 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8); или
b) нуклеотидную последовательность, где нуклеотидная последовательность содержит, по меньшей мере, фрагмент из 8 или 9 нуклеотидов из
(i) нуклеотидной последовательности 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидной последовательности 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8)
и
где молекула нуклеиновой кислоты способна вызывать посттранскрипционный сайленсинг гена.
2. Молекула нуклеиновой кислоты по п.1, где посттранскрипционный сайленсинг гена является РНК-интерференцией.
3. Молекула нуклеиновой кислоты по п.1, где ген является Notch 1, предпочтительно Notch 1 человека.
4. Молекула нуклеиновой кислоты по п.1, где молекула нуклеиновой кислоты способна вызывать деградацию мРНК, кодирующую ген или предшественник указанной мРНК, предпочтительно в клетке.
5. Молекула нуклеиновой кислоты по п.4, где нуклеотидная последовательность кДНК мРНК доступна в GenBank под регистрационным номером NM_017617.3.
6. Молекула нуклеиновой кислоты по п.5, где кДНК состоит из нуклеотидной последовательности SEQ ID NO: 2.
7. Молекула нуклеиновой кислоты по п.1, где второй фрагмент смежных нуклеотидов является по меньшей мере частично комплементарным части первого фрагмента смежных нуклеотидов.
8. Молекула нуклеиновой кислоты по п.1, где второй фрагмент смежных нуклеотидов является по меньшей мере частично комплементарным первому фрагменту смежных нуклеотидов.
9. Молекула нуклеиновой кислоты по п.1, где первый фрагмент смежных нуклеотидов содержит от 13 до 29 нуклеотидов, предпочтительно от 17 до 25 или от 19 до 25 нуклеотидов и более предпочтительно от 19 до 23 нуклеотидов.
10. Молекула нуклеиновой кислоты по п.1, где второй фрагмент смежных нуклеотидов содержит от 13 до 29 нуклеотидов, предпочтительно от 17 до 25 или от 19 до 25 нуклеотидов и более предпочтительно от 19 до 23 нуклеотидов.
11. Молекула нуклеиновой кислоты по п.1, где первый фрагмент смежных нуклеотидов и второй фрагмент смежных нуклеотидов содержит от 13 до 29 нуклеотидов, предпочтительно от 17 до 25 или от 19 до 25 нуклеотидов и более предпочтительно от 19 до 23 нуклеотидов.
12. Молекула нуклеиновой кислоты по п.9, где нуклеотиды являются последовательными нуклеотидами.
13. Молекула нуклеиновой кислоты по п.1, где первая цепь состоит из первого фрагмента смежных нуклеотидов.
14. Молекула нуклеиновой кислоты по п.1, где вторая цепь состоит из второго фрагмента смежных нуклеотидов.
15. Молекула нуклеиновой кислоты по п.1, где первая цепь состоит из первого фрагмента смежных нуклеотидов и вторая цепь состоит из второго фрагмента смежных нуклеотидов.
16. Молекула нуклеиновой кислоты по п.1, где двухцепочечная структура содержит от 13 до 29 пар оснований, предпочтительно от 16 до 27 или от 19 до 25 пар оснований и более предпочтительно от 19 до 23 пар оснований.
17. Молекула нуклеиновой кислоты по п.1, где первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8).
18. Молекула нуклеиновой кислоты по п.1, где второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGU-3' (SEQ ID NO: 3) или
(ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCG-3' (SEQ ID NO: 9).
19. Молекула нуклеиновой кислоты по любому из пп. 17 или 18, где первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8) и
второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGU-3' (SEQ ID NO: 3) или
(ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCG-3' (SEQ ID NO: 9).
20. Молекула нуклеиновой кислоты по п.1, где молекула нуклеиновой кислоты имеет тупой конец по меньшей мере на одном конце.
21. Молекула нуклеиновой кислоты по п.20, где молекула нуклеиновой кислоты имеет тупой конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи.
22. Молекула нуклеиновой кислоты по п.20, где молекула нуклеиновой кислоты имеет тупой конец на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
23. Молекула нуклеиновой кислоты по п.20, где молекула нуклеиновой кислоты имеет тупой конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи, и на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
24. Молекула нуклеиновой кислоты по п.1, где молекула нуклеиновой кислоты имеет липкий конец по меньшей мере на одном конце.
25. Молекула нуклеиновой кислоты по п.24, где молекула нуклеиновой кислоты имеет липкий конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи.
26. Молекула нуклеиновой кислоты по п.25, где липкий конец является липким 5'-концом.
27. Молекула нуклеиновой кислоты по п.25, где липкий конец является липким 3'-концом.
28. Молекула нуклеиновой кислоты по п.24, где молекула нуклеиновой кислоты имеет липкий конец на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
29. Молекула нуклеиновой кислоты по п.28, где липкий конец является липким 5'-концом.
30. Молекула нуклеиновой кислоты по п.28, где липкий конец является липким 3'-концом.
31. Молекула нуклеиновой кислоты по п.24, где молекула нуклеиновой кислоты имеет липкий конец на конце, определяемом 5'-концом первой цепи и 3'-концом второй цепи, и на конце, определяемом 3'-концом первой цепи и 5'-концом второй цепи.
32. Молекула нуклеиновой кислоты по п.31, где липкий конец является липким 5'-концом.
33. Молекула нуклеиновой кислоты по п.31, где липкий конец является липким 3'-концом.
34. Молекула нуклеиновой кислоты по п.24, где липкий конец состоит из одного, двух, трех, четырех или пяти нуклеотидов.
35. Молекула нуклеиновой кислоты по п.34, где липкий конец состоит из двух нуклеотидов.
36. Молекула нуклеиновой кислоты по п.34 или 35, где нуклеотид является dT.
37. Молекула нуклеиновой кислоты по п.1, где первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUCdTdT-3' (SEQ ID NO: 4) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGUdTdT-3' (SEQ ID NO: 10).
38. Молекула нуклеиновой кислоты по п.1, где второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGUdTdT-3' (SEQ ID NO: 5) или
(ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCGdTdT-3' (SEQ ID NO: 11).
39. Молекула нуклеиновой кислоты по п.37 или 38, где
первый фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUCdTdT-3' (SEQ ID NO: 4) или
(ii) нуклеотидную последовательность 5'-CGAGCUGGACCACUGGUdTdT-3' (SEQ ID NO: 10) и
второй фрагмент смежных нуклеотидов содержит
(i) нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGUdTdT-3' (SEQ ID NO: 5) или
(ii) нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCGdTdT-3' (SEQ ID NO: 11).
40. Молекула нуклеиновой кислоты по п.1, где первая цепь и вторая цепь ковалентно связаны друг с другом, предпочтительно 3'-конец первой цепи ковалентно связан с 5'-концом второй цепи.
41. Молекула нуклеиновой кислоты по п.1, где один или несколько нуклеотидов, образующих первый фрагмент смежных нуклеотидов, являются модифицированными.
42. Молекула нуклеиновой кислоты по п.1, где один или несколько нуклеотидов, образующих второй фрагмент смежных нуклеотидов, являются модифицированными.
43. Молекула нуклеиновой кислоты по п.41 или 42, где один или несколько нуклеотидов, образующих первый фрагмент смежных нуклеотидов, являются модифицированными и один или несколько нуклеотидов, образующих второй фрагмент смежных нуклеотидов, являются модифицированными.
44. Молекула нуклеиновой кислоты по п.1, где один или несколько нуклеотидов, образующих первую цепь, являются модифицированными.
45. Молекула нуклеиновой кислоты по п.1, где один или несколько нуклеотидов, образующих вторую цепь, являются модифицированными.
46. Молекула нуклеиновой кислоты по п.44 или 45, где один или несколько нуклеотидов, образующих первую цепь, являются модифицированными и один или несколько нуклеотидов, образующих вторую цепь, являются модифицированными.
47. Молекула нуклеиновой кислоты по любому из пп. 41 или 42, где модификация одного или нескольких нуклеотидов является модификацией сахарного остатка одного или нескольких нуклеотидов и/или модификацией фосфатного остатка одного или нескольких нуклеотидов.
48. Молекула нуклеиновой кислоты по п.47, где модификация сахарного остатка выбрана из группы, содержащей 2'-O-метил и 2'-F.
49. Молекула нуклеиновой кислоты по п.47, где модификация фосфатного остатка является такой, что между двумя нуклеотидами образуется фосфотиоатная связь.
50. Молекула нуклеиновой кислоты по п.41 или 42, где один или несколько нуклеотидов в зависимости от положения во фрагменте являются модифицированными.
51. Молекула нуклеиновой кислоты по п.50, где по всей длине первого и/или второго фрагмента или его части нуклеотид в четном положении фрагмента является модифицированным.
52. Молекула нуклеиновой кислоты по п.50, где по всей длине первого и/или второго фрагмента или его части нуклеотид в нечетном положении фрагмента является модифицированным.
53. Молекула нуклеиновой кислоты по п.50, где по всей длине первого и/или второго фрагмента или его части нуклеотид в четном положении фрагмента является
модифицированным и где по всей длине первого и/или второго фрагмента или его части нуклеотид в четном положении фрагмента является модифицированным, где модификация нуклеотидов в четном положении отличается от модификации нуклеотидов в нечетном положении.
54. Молекула нуклеиновой кислоты по п.50, где (a) модификация нуклеотидов в четном положении является 2'-O-метильной модификацией и модификация нуклеотидов в нечетном положении является 2'-F-модификацией или (b) модификация нуклеотидов в нечетном положении является 2'-O-метильной модификацией и модификация нуклеотидов в четном положении является 2'-F-модификацией.
55. Молекула нуклеиновой кислоты по п.44 или 45, где один или несколько нуклеотидов являются модифицированными в зависимости от положения в цепи.
56. Молекула нуклеиновой кислоты по п.55, где по всей длине первой и/или второй цепи или ее части нуклеотид в четном положении цепи является модифицированным.
57. Молекула нуклеиновой кислоты по п.55, где по всей длине первой и/или второй цепи или ее части нуклеотид в нечетном положении цепи является модифицированным.
58. Молекула нуклеиновой кислоты по п.55, где по всей длине первой и/или второй цепи или ее части нуклеотид в четном положении цепи является модифицированным и где по всей длине первой и/или второй цепи или ее части нуклеотид в четном положении цепи является модифицированным, где модификация нуклеотидов в четном положении отличается от модификации нуклеотидов в нечетном положении цепи.
59. Молекула нуклеиновой кислоты по п.55, где (a) модификация нуклеотидов в четном положении является 2'-O-метильной модификацией и модификация нуклеотидов в нечетном положении является 2'-F-модификацией или (b) модификация нуклеотидов в нечетном положении является 2'-O-метильной модификацией и модификация нуклеотидов в четном положении является 2'-F-модификацией.
60. Молекула нуклеиновой кислоты по п.41 или 42, где первый фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным.
61. Молекула нуклеиновой кислоты по п.60, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-O-метил-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
62. Молекула нуклеиновой кислоты по п.60, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
63. Молекула нуклеиновой кислоты по п.41 или 42, где второй фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-O-метил-модифицированным.
64. Молекула нуклеиновой кислоты по п.63, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине второго фрагмента или его части.
65. Молекула нуклеиновой кислоты по п.63, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-O-метил-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
66. Молекула нуклеиновой кислоты по п.60, где первый фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первого фрагмента или его части, где второй фрагмент содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где
по меньшей мере один нуклеотид является 2'-O-метил-модифицированным, и где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-O-метил-модифицированным нуклеотидом по всей длине первого фрагмента или его части.
67. Молекула нуклеиновой кислоты по п.60, где первый фрагмент содержит на своем 3'-конце два dT нуклеотида и второй фрагмент содержит на своем 3'-конце два dT нуклеотида, где два dT нуклеотида ковалентно связаны посредством фосфотиоатной связи.
68. Молекула нуклеиновой кислоты по п.41 или 42, где первая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным.
69. Молекула нуклеиновой кислоты по п.68, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-O-метил-модифицированным нуклеотидом по всей длине первой цепи или ее части.
70. Молекула нуклеиновой кислоты по п.68, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первой цепи или ее части.
71. Молекула нуклеиновой кислоты по п.41 или 42, где вторая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-O-метил-модифицированным.
72. Молекула нуклеиновой кислоты по п.71, где после по меньшей мере одного нуклеотида непосредственно следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине второй цепи или ее части.
73. Молекула нуклеиновой кислоты по п.71, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-O-метил-модифицированным нуклеотидом по всей длине первой цепи или ее части.
74. Молекула нуклеиновой кислоты по п.68, где первая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-F-модифицированным, где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-F-модифицированным нуклеотидом по всей длине первой цепи или ее части, где вторая цепь содержит на 5'-конце по меньшей мере один, предпочтительно два нуклеотида, где по меньшей мере один нуклеотид является 2'-O-метил-модифицированным, и где, начиная после по меньшей мере одного нуклеотида, второй следующий (в 5'->3' направлении) нуклеотид и каждый последующий второй нуклеотид является 2'-O-метил-модифицированным нуклеотидом по всей длине первой цепи или ее части.
75. Молекула нуклеиновой кислоты по п.68, где первая цепь содержит на своем 3'-конце два dT нуклеотида и вторая цепь содержит на своем 3'-конце два dT нуклеотида, где два dT нуклеотида ковалентно связаны посредством фосфотиоатной связи.
76. Молекула нуклеиновой кислоты по п.1, где
нуклеотидную последовательность 5'-ACGAGCUGGACCACUGGUC-3' (SEQ ID NO: 1) модифицируют следующим образом:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6) и
нуклеотидную последовательность 5'-CGAGCUGGACCACUGGU-3' (SEQ ID NO: 8) модифицируют следующим образом:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
77. Молекула нуклеиновой кислоты по п.1, где
нуклеотидную последовательность 5'-GACCAGUGGUCCAGCUCGU-3' (SEQ ID NO: 3) модифицируют следующим образом:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7) и
нуклеотидную последовательность 5'-ACCAGUGGUCCAGCUCG-3' (SEQ ID NO: 9) модифицируют следующим образом:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
78. Молекула нуклеиновой кислоты по п.1, где первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6) или
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
79. Молекула нуклеиновой кислоты по п.1, где второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7) или
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
80. Молекула нуклеиновой кислоты по п.1, где
a) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6) и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
b) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13) и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
c) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6) и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14), или
d) первый фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13) и
второй фрагмент смежных нуклеотидов содержит следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
81. Молекула нуклеиновой кислоты по п.1, где молекула нуклеиновой кислоты состоит из
a) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
b) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
c) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14), или
d) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
82. Молекула нуклеиновой кислоты по п.1, где молекула нуклеиновой кислоты состоит из
a) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
b) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGu-3' (SEQ ID NO: 7), или
c) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuC-3' (SEQ ID NO: 6), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14), или
d) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgU-3' (SEQ ID NO: 13), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCg-3' (SEQ ID NO: 14),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является 2'-O-метил-модифицированным.
83. Молекула нуклеиновой кислоты по п.1, где молекула нуклеиновой кислоты состоит из
a) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuCdTsdT-3' (SEQ ID NO: 69), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGudTsdT-3' (SEQ ID NO: 70), или
b) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgUdTsdT-3' (SEQ ID NO: 71), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-GAcCaGuGgUcCaGcUcGudTsdT-3' (SEQ ID NO: 70), или
c) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-acGaGcUgGaCcAcUgGuCdTsdT-3' (SEQ ID NO: 69), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCgdTsdT-3' (SEQ ID NO: 72), или
d) первого фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-cgAgCuGgAcCaCuGgUdTsdT-3' (SEQ ID NO: 71), и
второго фрагмента смежных нуклеотидов, содержащего следующую нуклеотидную последовательность:
5'-ACcAgUgGuCcAgCuCgdTsdT-3' (SEQ ID NO: 72),
где то, что нуклеотид указан строчной буквой, указывает на то, что нуклеотид является 2'-F-модифицированным, и подчеркивание нуклеотида указывает на то, что нуклеотид является
2'-O-метил-модифицированным и
где dTsdT указывает на то, что на 3'-конце присоединен динуклеотид, состоящих из двух dT, где указанные два dT ковалентно связаны посредством фосфотиоатной связи.
84. Молекула нуклеиновой кислоты по п.1 для применения в способе лечения и/или профилактики заболевания.
85. Молекула нуклеиновой кислоты по п.84, где заболевание является заболеванием, которое можно лечить, снижая экспрессию гена Notch 1 и, более конкретно, снижая трансляцию мРНК, кодирующей Notch 1.
86. Молекула нуклеиновой кислоты по п.84, где заболевание выбрано из группы, содержащей рак пищевода, плоскоклеточный рак полости рта, рак головы и шеи, рак языка, лейкоз, почечноклеточную карциному, рак желудка, аденокарциному толстого кишечника, рак эндометрия/тела матки, рак шейки матки, внутрипеченочную холангиокарциному, печеночноклеточную карциному, остеосаркому, карциному мочевого пузыря, злокачественную меланому, рак щитовидной железы, аденокарциному легких, рак предстательной железы, рак молочной железы, рак яичников, рак поджелудочной железы и глиому.
87. Молекула нуклеиновой кислоты по п.84, где способ включает дополнительное введение фармацевтически активного средства.
88. Молекула нуклеиновой кислоты по п.87, где фармацевтически активное средство является цитостатическим средством.
89. Молекула нуклеиновой кислоты по п.88, где фармацевтически активное средство выбрано из группы, содержащей гемцитабин, доцетаксел, цисплатин, оксалиплатин, 5-фторурацил, иринотекан, паклитаксел, дексаметазон и темозоломид.
90. Молекула нуклеиновой кислоты по п.1 для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
91. Молекула нуклеиновой кислоты по п.90, где чувствительность к лекарственному средству является чувствительностью к лекарственному средству, опосредуемой и/или включающей каскад NF-kappaB.
92. Применение молекулы нуклеиновой кислоты по любому из пп. 1-83 для получения лекарственного средства для лечения и/или профилактики заболевания.
93. Применение по п.92, где заболевание является заболеванием, которое можно лечить, снижая экспрессию гена Notch 1 и, более конкретно, снижая трансляцию мРНК, кодирующей Notch 1.
94. Применение по п.92, где заболевание выбрано из группы, включающей рак пищевода, плоскоклеточный рак полости рта, рак головы и шеи, рак языка, лейкоз, почечноклеточную карциному, рак желудка, аденокарциному толстого кишечника, рак эндометрия/тела матки, рак шейки матки, внутрипеченочную холангиокарциному, печеночноклеточную карциному, остеосаркому, карциному мочевого пузыря, злокачественную меланому, рак щитовидной железы, аденокарциному легких, рак предстательной железы, рак молочной железы, рак яичников, рак поджелудочной железы и глиому.
95. Применение по п.92, где лекарственное средство предназначено для введения вместе с дополнительным фармацевтически активным средством.
96. Применение по п.95, где фармацевтически активное средство является цитостатическим средством.
97. Применение по п.96, где фармацевтически активное средство выбрано из группы, содержащей гемцитабин, доцетаксел, цисплатин, оксалиплатин, 5-фторурацил, иринотекан, паклитаксел, дексаметазон и темозоломид.
98. Применение молекулы нуклеиновой кислоты по любому из пп. 1-83 в получении средства для восстановления чувствительности злокачественных клеток к лекарственному средству.
99. Применение по п.98, где чувствительность к лекарственному средству является чувствительностью к лекарственному средству, опосредуемой и/или включающей каскад NF-kappaB.
100. Наноэмульсия, содержащая дискретную фазу, непрерывную водную фазу и молекулу нуклеиновой кислоты по любому из пп. 1-83.
101. Наноэмульсия по п.100, где дискретная фаза содержит перфторуглеродную фазу.
102. Наноэмульсия по п.100, где наноэмульсия содержит усиливающую эндоцитоз поверхность, предпочтительно, усиливающая эндоцитоз поверхность содержит усиливающий эндоцитоз компонент, где усиливающий эндоцитоз компонент выбран из группы, содержащей по меньшей мере одно соединение, индуцирующее клеточный захват наноэмульсии или частиц наноэмульсии посредством эндоцитоза.
103. Наноэмульсия по п.100 для применения в лечении и/или профилактике заболевания.
104. Наноэмульсия по п.100 для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
105. Применение наноэмульсии по любому из пп. 100-102 для получения лекарственного средства для лечения и/или профилактики заболевания.
106. Применение наноэмульсии по любому из пп. 100-102 в получении средства для восстановления чувствительности злокачественных клеток к лекарственному средству.
107. Фармацевтическая композиция, содержащая молекулу нуклеиновой кислоты по любому из пп. 1-83 и/или наноэмульсию по любому из пп. 100-102 и фармацевтически приемлемый эксципиент.
108. Фармацевтическая композиция по п.107 для применения в лечении и/или профилактике заболевания.
109. Фармацевтическая композиция по п.107 для применения в способе восстановления чувствительности злокачественных клеток к лекарственному средству.
110. Способ лечения и/или профилактики заболевания, где способ включает введение индивидууму нуклеиновой кислоты по любому из пп. 1-83, наноэмульсии по любому из пп. 100-102 и/или фармацевтической композиции по п.107.
111. Способ восстановления чувствительности злокачественных клеток к лекарственному средству, где способ включает введение индивидууму нуклеиновой кислоты по любому из пп. 1-83, наноэмульсии по любому из пп. 100-102 и/или фармацевтической композиции по п.107, где индивидуум страдает злокачественным новообразованием и клетки злокачественного новообразования являются резистентными к лекарственному средству.
| RU 2010136040 A, 10.03.2012 | |||
| WO 2009114726 A1, 17.09.2009. |
Авторы
Даты
2018-04-19—Публикация
2014-09-30—Подача