1. Область техники
Предложенный способ относится к области медицины, биологии и биотехнологии и может быть использован при составлении индивидуального «генетического паспорта», реализации концепции индивидуальной медицины, для формирования персональных рекомендаций при назначении и корректировке химиотерапии с применением тамоксифена с учетом индивидуальных генетических особенностей пациента. Тамоксифен - селективный модулятор эстрогеновых рецепторов, является «золотым стандартом» в лечении эстроген-позитивного рака молочной железы начальных стадий. Продолжительные исследования показали, что его применение снижает риск рецидива и смерти на 30-50%. Ингибиторы ароматазы (анастрозол и летрозол) результативнее тамоксифена, но из-за значительного числа побочных эффектов подходят гораздо меньшему числу пациентов (Lash T.L. et al., 2009; Goetz M.P. et al., 2007; Ingelman-Sundberg M. et al., 2005). Метаболическая активность тамоксифена в организме определяется активностью одного из ферментов семейства цитохрома Р450, кодируемого геном CYP2D6: под действием фермента тамоксифен переходит в метаболически активную форму - эндоксифен. Было обнаружено, что различные аллельные варианты гена CYP2D6 по-разному влияют на активность фермента и, в конечном счете, на метаболическую активность тамоксифена. Ген CYP2D6 крайне полиморфичен - для него описано более 100 аллелей. Аллели CYP2D6*3, CYP2D6*4, CYP2D6*6 являются неактивными (нефункциональными) аллелями, ассоциированными с низким уровень метаболизма тамоксифена (poor metabolizer group). Для пациентов с двумя неактивными (нефункциональными) аллелями CYP2D6 характерен низкий уровень метаболизма тамоксифена (poor metabolizer group), для пациентов с одним или двумя малоактивными аллелями или с одним неактивным/малоактивным и одним активным аллелями - сниженный уровень метаболизма (intermediate metabolizer group), для пациентов с двумя активными аллелями - нормальный уровень метаболизма (ultrarapid metabolizer group). Для первых двух групп пациентов терапевтический эффект от применения тамоксифена снижен или даже отсутствует (Goetz M.P. et al., 2005; Schroth W. et al., 2007; Bradford L.D. et al., 2002; Ingelman-Sundberg M. et al., 2007).
2. Уровень техники
Широко распространен способ определения типа нуклеотида, находящегося в определенном месте ДНК, основанный на использовании аллель-специфичных праймеров с регистрацией результатов ПЦР по окончании реакции с помощью электрофореза. При использовании ПЦР с регистрацией результатов в ходе реакции известны различные способы определения генотипа исследуемого образца. Существуют различные способы, позволяющие определить тип нуклеотида, находящегося в определенном месте ДНК, основанные на использовании аллель-специфичных праймеров с регистрацией результатов ПЦР непосредственно в ходе реакции с помощью использования флуоресцентно-меченных проб (олигонуклеотидов) (Andreas R. Tobler at all, "THE SNPlex Genotiping System: A Flexible and Scalable Platform for SNP Genotyping", Journal of Biomolecular Techniques, V. 16, issue 4, Desember 2005). Например, в наборах производства Applied Biosystems используют одну пару праймеров для каждого аллеля и два зонда с различными флуорецентными метками, в зависимости от генотипа аллеля фиксируют разгорание различных меток ("TaqMan SNP Genotyping Assays", Applied Biosistems, Prodakt Bulletin, USA, 06/2006). Недостатком способа, используемого в данных наборах, является сравнительно невысокая достоверность результатов исследования из-за небольшой разницы между получаемыми кривыми флуоресценции для разных аллелей. Предлагаемым подходом к детекции генетического полиморфизма является использование двух аллель-специфичных и меченных разными флуоресцентными метками олигонуклеотидов, а также олигонуклеотида, несущего гаситель флуоресценции и гибридизирующегося на матрицу рядом с аллель-специфичным олигонуклеотидом. Гибридизация аллель-специфичного олигонуклеотида на матрицу ведет к переносу энергии с находящегося на нем флуорофора-донора на гаситель флуоресценции расположенного рядом «гасящего» олигонуклеотида. Регистрацию результатов амплификации ведут по окончании ПЦР путем снятия спектра флуоресценции при изменении температуры реакционной смеси в диапазоне от 25 до 80 градусов по Цельсию (так называемые «кривые плавления»). При получении графиков флуоресценции возможен как нагрев, так и охлаждение реакционной смеси в указанном интервале температур. Предлагаемое изобретение делает определение вариабельных позиций в ДНК более надежными, удешевляет подобные исследования благодаря использованию стандартного оборудования.
3. Раскрытие изобретения
Техническим результатом, на достижение которого направлено предлагаемое изобретение, является повышение доступности подобных исследований, поскольку способ может быть осуществлен на стандартном известном оборудовании. Также он обеспечивает возможность проводить исследование в одной пробирке, что снижает затраты на исследование. Использованный нами способ генотипирования является вариантом классического метода «примыкающих проб». При определении замен одиночных нуклеотидов вначале проводили ПЦР с праймерами, общими для обоих вариантов последовательности, затем температуру реакционной смеси снижали для гибридизации полученной матрицы с олигонуклеотидными пробами. Для определения варианта последовательности использовали два типа олигонуклеотидов, гибридизирующихся на матрицу рядом. Один из олигонуклеотидов метили флуорофором, другой - гасителем флуоресценции. В реакции использовали один общий олигонуклеотид с гасителем флуоресценции и пару аллель-специфичных (сиквенс-специфичных) олигонуклеотидов, несущих флуорофор. Олигонуклеотидные пробы, соответствующие тому или иному варианту последовательности, метили различными флуорофорами, что позволило определять оба варианта в одной пробирке. Определение генотипа проводили после ПЦР и гибридизации путем измерения уровня флуоресценции в ходе температурной денатурации дуплексов олигонуклеотидов и полученных матриц (или, наоборот, - гибридизации). Данное измерение проводили в режиме реального времени, его результатом являлись кривые плавления. Условия реакции подбирали так, чтобы максимизировать разницу в температурах плавления совершенного и несовершенного дуплексов. Таким образом, если анализируемый образец содержал только один вариант последовательности, т.е. был гомозиготен по данному полиморфизму, температура плавления для пробы, образующей совершенный дуплекс, была существенно выше, нежели для пробы образующей несовершенный дуплекс. Если же анализировали гетерозиготный образец, температуры плавления были практически одинаковы. Указанный результат достигается путем использования при постановке ПЦР флуоресцентно-меченных аллель-специфичных олигонуклеотидных проб и праймеров:

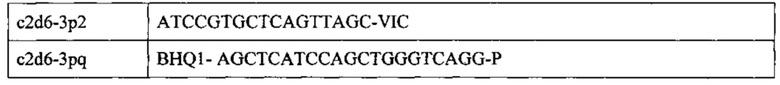
FAM - означает флуоресцентный краситель FAM, VIC - означает флуоресцентный краситель VIC, BHQ1 - означает присоединенный к 5'-концевому нуклеотиду темновой гаситель флуоресценции.

4. Осуществление изобретения
В качестве материала для исследования рекомендуется использовать периферическую кровь. Выделение ДНК из биоматериала производится с использованием комплекта реагентов для выделения ДНК (не является предметом данного патента). Полимеразную цепную реакцию и определение температуры плавления олигонуклеотидных проб проводили с помощью детектирующего амплификатора «ДТпрайм» (ООО «НПО ДНК-Технология», Россия). Использовали следующий температурный режим амплификации: 94°С - 10 с, 60°С - 30 с в течение 50 циклов. По завершении реакции амплификации реакционную смесь остужали до 25°С со скоростью 2°С/сек. Кривые плавления получали следующим образом: температуру реакционной смеси повышали с 25 до 75°С с шагом 1°С, измеряя уровень флуоресценции на каждом шаге. Результаты, т.е. отнесение образца к гомозиготе или гетерозиготе по данному аллелю, оцениваются по форме кривых плавления ДНК (рис. 1).
Список литературы
1. Lash TL, Lien EA, Sorensen HT, Hamilton-Dutoit S Genotype-guided tamoxifen therapy: time to pause for reflection?// Lancet Oncol. 2009 Aug;10(8):825-33.
2. Goetz MP, Rae JM, Suman VJ, Safgren SL, Ames MM, Visscher DW, Reynolds C, Couch FJ, Lingle WL, Flockhart DA, Desta Z, Perez EA, Ingle JN. Pharmacogenetics of tamoxifen biotransformation is associated with clinical outcomes of efficacy and hot flashes.// J Clin Oncol. 2005 Dec 20; 23(36):9312-8.
3. Goetz MP, Ingle J. Early discontinuation of tamoxifen: a lesson for oncologists.// Cancer. 2007 Dec 1; 110(11):2595-6.
4. Schroth W, Antoniadou L, Fritz P, Schwab M, Muerdter T, Zanger UM, Simon W, Eichelbaum M, Brauch H. Breast cancer treatment outcome with adjuvant tamoxifen relative to patient CYP2D6 and CYP2C19 genotypes.// J Clin Oncol. 2007 Nov 20; 25(33):5187-93.
5. Bradford L.D. CYP2D6 allele frequency in European Caucasians, Asians, Africans and their descendants. // Pharmacogenomics. 2002 Mar; 3(2):229-43.
6. Ingelman-Sundberg M, Sim SC, Gomez A, Rodriguez-Antona C. Influence of cytochrome P450 polymorphisms on drug therapies: pharmacogenetic, pharmacoepigenetic and clinical aspects. // Pharmacol Ther. 2007 Dec; 116(3):496-526. Epub 2007 Oct 9.
7. Ingelman-Sundberg M, Rodriguez-Antona C. Pharmacogenetics of drug-metabolizing enzymes: implications for a safer and more effective drug therapy.//. Philos Trans R Soc Lond В Biol Sci. 2005 Aug 29; 360 (1460):1563-70.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФИЗМУ В ГЕНЕ ЦИТОХРОМА Р450 CYP2D6*6 (1707delT) rs5030655 | 2016 |
|
RU2653492C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФИЗМУ В ГЕНЕ ЦИТОХРОМА P450 CYP2D6*9 (2615-2617delAAG) rs5030656 | 2016 |
|
RU2651773C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФИЗМУ В ГЕНЕ ЦИТОХРОМА P450 CYP2D6*4 (1846G>A), RS3892097 | 2016 |
|
RU2651774C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ В ГЕНЕ ГАЛАКТОЗО-1-ФОСФАТУРИДИЛТРАНСФЕРАЗЫ ЧЕЛОВЕКА МУТАЦИИ Q188R, RS75391579 | 2017 |
|
RU2675324C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФИЗМУ В ГЕНЕ МАТРИКСНОЙ МЕТАЛЛОПРОТЕИНАЗЫ 3 (ММР3) -11715А/6А | 2018 |
|
RU2699053C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФИЗМУ В ГЕНЕ МАТРИКСНОЙ МЕТАЛЛОПРОТЕИНАЗЫ ММР9-1562 С>Т (rs3918242) | 2012 |
|
RU2548811C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФИЗМУ В ГЕНЕ КОЛЛАГЕНА II ТИПА COL2A1 C>A (RS1635529) | 2012 |
|
RU2518301C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕНОТИПА ЧЕЛОВЕКА ПО ПОЛИМОРФНОЙ ПОЗИЦИИ rs1613662 В ГЕНЕ GP6, КОДИРУЮЩЕМ ГЛИКОПРОТЕИН VI | 2013 |
|
RU2556808C2 |
| Способ генотипирования крупного рогатого скота по аллелям А и В бета-лактоглобулина (полиморфизм rs109625649) на основе ПЦР с аллель-специфичными зондами | 2021 |
|
RU2767996C1 |
| Способ проведения ПЦР с аллель-специфичными зондами для генотипирования крупного рогатого скота по аллелям А и В гена каппа-казеина | 2021 |
|
RU2791519C1 |
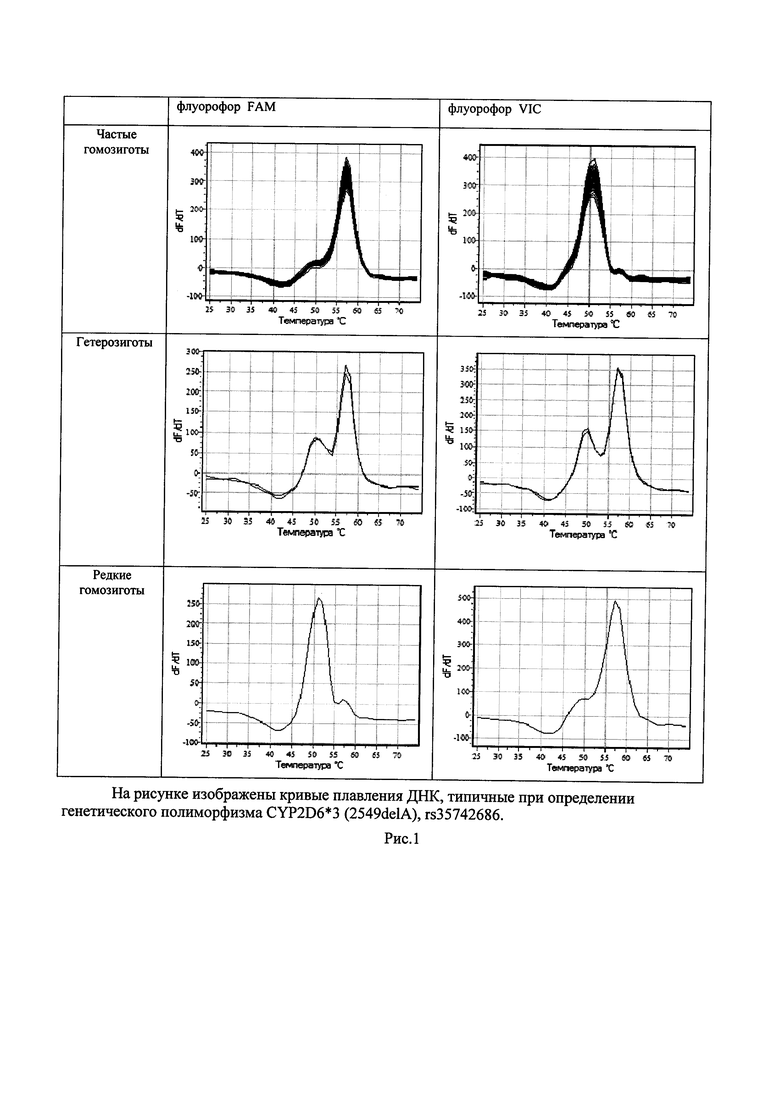
Изобретение относится к области медицины, биологии и биотехнологии и предназначено для определения генотипа человека по полиморфизму в гене цитохрома Р450 CYP2D6*3 (2549delA) rs35742686. Используют пару праймеров, флуоресцентно-меченые аллель-специфичные олигонуклеотидные пробы и универсальный олигонуклеотид, меченный гасителем флуоресценции. Отнесение образца к гомозиготе или гетерозиготе по данному аллелю оценивается по форме кривых плавления ДНК, а именно по максимуму первой производной графиков флуоресценции. Изобретение обеспечивает возможность проводить исследование в одной пробирке, что снижает затраты на исследование. 1 ил., 2 табл.
Способ определения генотипа человека по полиморфизму в гене цитохрома Р450 CYP2D6*3 (2549delA) rs35742686, основанный на снятии кривых плавления с флуоресцентно-мечеными аллель-специфичными олигонуклеотидными пробами, отличающийся тем, что используют общую для всех аллелей пару праймеров, отличающиеся для каждого аллеля флуоресцентно-меченые аллель-специфичные олигонуклеотидные пробы и универсальный олигонуклеотид, меченный гасителем флуоресценции, следующего нуклеотидного состава:

FAM - означает флуоресцентный краситель FAM, VIC - означает флуоресцентный краситель VIC, BHQ1 - означает присоединенный к 5'-концевому нуклеотиду темновой гаситель флуоресценции;
отнесение образца к гомозиготе или гетерозиготе по данному аллелю оценивается по форме кривых плавления ДНК, по максимуму первой производной графиков флуоресценции.
| LIM J.S | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Br J Clin Pharmacol | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| AZAD A.K | |||
| et al | |||
| Genetic sequence variants and the development of secondary primary cancers in patients with head and neck cancers | |||
| Cancer | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| BRADFORD L.D | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Pharmacogenomics | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| ОПРЕДЕЛЕНИЕ ПРЕДРАСПОЛОЖЕННОСТИ К РАКУ ПУТЕМ ИДЕНТИФИКАЦИИ ГЕНОТИПИЧЕСКИХ КОМБИНАЦИЙ СПЕЦИФИЧНЫХ ВАРИАНТОВ ГЕНОВ CYP1B1, BRCA2 И СНЕК2 | 2006 |
|
RU2470998C2 |
Авторы
Даты
2018-04-23—Публикация
2016-09-06—Подача