Предпосылки создания изобретения
Применение одноразовых тестовых элементов стало общепринятым для определения присутствия и/или измерения концентрации аналитов в тестируемых образцах. Например, пациентам, страдающим диабетом и подобными медицинскими состояниями, часто требуется осуществлять самомониторинг уровня глюкозы крови, это означает, что пациент сам осуществляет мониторинг уровней глюкозы крови. Целью мониторинга уровней глюкозы крови является определение уровня концентраций и при необходимости, если уровень является слишком высоким или слишком низким, осуществление корректирующих действий для возвращения уровня назад в приемлемый диапазон. Невозможность провести корректирующее действие может приводить к серьезным медицинским последствиям. Мониторинг глюкозы является фактом ежедневной жизни диабетиков и от точности такого мониторинга может зависеть буквально вопрос жизни и смерти. Невозможность поддерживать глюкозу крови на приемлемых уровнях может приводить к серьезным осложнениям, связанным с диабетом, включая сердечно-сосудистое заболевание, болезнь почек, повреждение нервной системы и слепоту.
Страдающие диабетом люди, которые осуществляют усиленный контроль сахара крови, достигают долговременной пользы. Национальным институтом диабета, болезней пищеварительной системы и почек (National Institute of Diabetes and Digestive and Kidney Diseases, NIDDK) в период с 1983 по 1993 г.г. было проведено клиническое исследование по контролю диабета и его осложнений (The Diabetes Control and Complications Trial - DCCT). При осуществлении DCCT сравнивали интенсивное лечение с общепринятым лечением. Пациенты, находящиеся на интенсивном лечении, поддерживали уровни глюкозы на уровне, максимально близком к нормальному, с помощью по меньшей мере трех инъекций инсулина в день или инсулинового насоса и осуществляли частый самомониторинг уровней глюкозы крови. Целью интенсивного лечения было поддержание уровня гликированного гемоглобина Alc (HbAlc), отражающего средний уровень глюкозы крови в течение периода времени, составлявшего 2-3 месяца, на уровне, максимально близком к нормальному. Общепринятое лечение состоит из одной или двух инъекций инсулина в день с тестированием один раз в день глюкозы мочи или крови. Результаты DCCT-исследования продемонстрировали, что поддержание уровней глюкозы крови на максимально близких к нормальным уровнях, замедляет возникновение и развитие заболеваний глаз, почек и нервов, вызываемых диабетом. Фактически, было продемонстрировано, что любое стабильное снижение уровней глюкозы крови оказывает благоприятное воздействие, даже в том случае, если пациент имеет историю плохого контроля.
В настоящее время доступен ряд аналитических инструментов или биосенсоров, таких как глюкометры, которые позволяют индивидууму тестировать уровень глюкозы в небольшом образце крови. Конструкции многих современных измерительных приборов основаны на применении одноразового тестового элемента, который в сочетании с измерительным прибором позволяет измерять количество глюкозы в образце крови электрохимически или оптически. В современных глюкометрах информация, отображаемая в качестве результата успешных измерений глюкозы крови, представляет собой соответствующую величину уровня глюкозы крови, как правило, в мг/дл или молярных единицах, и необязательно время и дату осуществления измерения. В большинстве случаев этой информации в сочетании с расчетом планируемого или известного потребления углеводов или планируемых или известных активностей и сведениями о других ситуационных или индивидуальных факторах достаточно для того, чтобы диабетики могли регулировать или устанавливать прием пищи и/или требуемую для немедленной инъекции дозу инсулина для краткосрочного контроля уровня глюкозы крови. Кроме того, в случае низких величин уровней глюкозы диабетики могут получать информацию о необходимости приема внутрь сахара для избегания гипогликемии.
Отсутствие или недостаточное количество инсулина не позволяет организму использовать глюкозу в качестве «источника топлива» для получения энергии. Когда это имеет место, организм продуцирует энергию путем расщепления жирных кислот, что приводит к образованию побочных продуктов в виде кетонов и повышению уровней кетонов. Повышенные уровни кетонов у диабетиков могут вызываться также сердечным приступом, «ударом», приемом рекреационных лекарственных средств или интеркуррентным заболеванием, таким как пневмония, грипп, гастроэнтерит или урологическая инфекция. Избыточные уровни кетонов у диабетиков приводят к диабетическому кетоацидозу (DKA), медицинскому критическому состоянию, которое без лечения может приводить к смерти. Симптомы DKA включают среди прочего тошноту, рвоту, избыточные жажду и образование мочи, боли в брюшной области, затрудненное дыхание, сонливость и кому. С учетом серьезности DKA требуется начинать лечение, направленное на снижение уровней кетонов, до начала полного приступа DKA. Кроме того, поскольку симптомы, связанные с приступом DKA, могут не иметь место до начала приступа DKA или уровни кетонов могут быть нежелательно высокими по другим причинам, как правило, предпочтительно не начинают лечение, направленное на снижение уровня кетонов, в ответ на эти симптомы.
Предупреждение эпизодов DKA можно достигать путем измерения уровней кетонов и уделять внимание медицинской помощи, если они превышают определенную концентрацию. Для определения уровней кетонов можно использовать анализы мочи. На веб-сайте ADA (Американская ассоциация по профилактике и лечению сахарного диабета) даны рекомендации о том, что уровни кетонов следует определять каждые 4-6 ч, если диабетик заболел (например, простудой или гриппом), или если у него(нее) уровень глюкозы крови превышает 240 мг/дл (см. http://www.diabetes.org/living-with-diabetes/complications/ketoacidosis-dka.html). Однако для диабетиков, которые в течение дня осуществляют несколько определений уровня глюкозы крови, проведение отдельных анализов мочи в дополнение к определениям ими уровня глюкозы крови требует затрат времени и является обременительным.
При наличии двойного теста, позволяющего измерять уровни глюкозы и кетонов на одной и той же тест-полоске, диабетику проще соблюдать рекомендации по тестированию и осуществлять более безопасную терапию путем более раннего обнаружения высоких уровней кетонов. Например, рекомендовано избегать физической нагрузки при высоких уровнях кетонов и глюкозы крови, поскольку повышенные уровни этих аналитов могут являться признаком того, что лечение диабета является неудовлетворительным. Однако большинство диабетиков не имеет возможность использовать легкодоступные тесты на кетоны и часто они не имеют легко доступной информации о том, как поступать в указанных ситуациях.
Применение отдельных анализов мочи для определения уровней кетонов требует также дополнительных диагностических средств и затрат на их обслуживания и затрудняет установление корреляции между уровнями глюкозы крови и кетонов. Можно также определять уровни кетонов в образцах крови. Когда применяют образцы крови, то уровни кетонов, как правило, определяют путем измерения концентрации гидроксибутирата, который является основным кетоном в крови. Концентрации гидроксибутирата в крови ниже 0,6 мМ считаются нормой, концентрации гидроксибутирата, находящиеся между 0,6 и 1,5 мМ, свидетельствуют о том, что проблема может возникнуть, а свыше 1,5 мМ свидетельствует о риске развития DKA. Концентрации гидроксибутирата в крови, превышающие 3 мМ, свидетельствуют о наличии DKA и требуют неотложного медицинского вмешательства.
Современные методики определения уровней кетонов крови включают однофункциональные тестовые элементы, которые пригодны, например, для определения концентраций гидроксибутирата. Однако, в значительной степени аналогично описанному выше анализу мочи, диабетики, которые осуществляют относительно многократно тесты на глюкозу крови в день могут считать, что для них является затратным по времени и обременительным осуществлять отдельные тесты на уровни кетонов крови в дополнение к тестам на глюкозу крови, прежде всего потому, что современные тесты на кетоны крови являются более медленными, чем существующие в данной области техники тесты на глюкозу крови. Тесты на уровни кетонов крови, которые осуществляют независимо от тестов на глюкозу крови, требуют также дополнительных диагностических средств и должны включать дополнительные затраты, связанные с их обслуживанием. Кроме того, осуществление отдельных тестов для определения уровней глюкозы крови и кетонов крови затрудняет установление корреляции между измеренными величинами глюкозы крови и кетонов крови.
Другие методики определения уровней кетонов крови включают тестовые элементы, пригодные для определения уровней глюкозы крови и кетонов крови. Однако в указанных существующих в настоящее время тестовых элементах уровни глюкозы крови измеряются быстрее, чем уровни кетонов крови, поэтому получение результатов теста на кетоны крови требует большего времени и они становятся известными после получения результатов теста на глюкозу крови. Альтернативно этому, результаты тестов как на глюкозу крови, так и на кетоны крови, не выдаются до окончательного завершения теста на кетоны крови. В любом случае, ожидание результатов одного или обоих тестов вплоть до завершения теста на кетоны крови может быть очень обременительным и затратным по времени для диабетика, который осуществляет относительно многократно тесты на глюкозу крови каждый день, прежде всего с учетом того, что в некоторых случаях на тест на кетоны крови может требоваться почти в два раза больше времени, чем на осуществление теста на глюкозу крови. Кроме того, когда результаты теста на глюкозу крови являются доступными до и отдельно от результатов теста на кетоны крови, то возрастает вероятность того, что пользователь прервет тестирование до завершения теста на кетоны крови и/или его внимание еще каким-то образом будет отвлечено после получения результатов теста на глюкозу, но до требуемого учета результатов теста на кетоны крови.
С учетом важности результатов точного определения, регистрации и анализа измерений кетонов крови в дополнение к измерениям глюкозы крови, требуются усовершенствование методик, процедур и оборудования для тестирования уровней кетонов крови и/или уровней кетонов крови и уровней глюкозы крови.
Краткое изложение сущности изобретения
В настоящем изобретении предложены реагентные материалы и соответствующие тестовые элементы. В одном из вариантов осуществления изобретения тестовый элемент, обладающий двойной функцией, включает первый коферментзависимый фермент или субстрат для первого фермента, второй коферментзависимый фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I) (описанного ниже). В одном из объектов изобретения первый аналит представляет собой гидроксибутират и первый фермент представляет собой гидроксибутиратдегидрогеназу, а второй аналит представляет собой глюкозу и второй фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу. Другими объектами настоящего изобретения являются уникальные реагентные материалы.
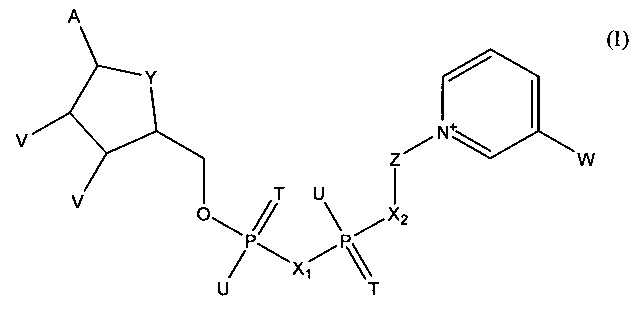
В одном из вариантов осуществления изобретения тестовый элемент, созданный для определения первого и второго аналитов, включает первый коферментзависимый фермент или субстрат для первого фермента и второй коферментзависимый фермент или субстрат для второго фермента. Тестовый элемент включает также кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I):
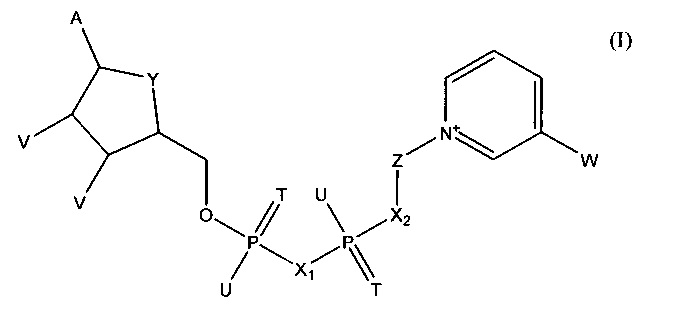
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или C1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы.
В одном из вариантов указанного варианта осуществления изобретения первый аналит представляет собой гидроксибутират и первый фермент представляет собой гидроксибутиратдегидрогеназу. В одном из аспектов этого варианта гидроксибутиратдегидрогеназа представляет собой 3-гидроксибутиратдегидрогеназу. В другом аспекте этого варианта второй фермент представляет собой дегидрогеназу, выбранную из группы, состоящей из глюкозодегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, глицериндегидрогеназы, алкогольдегидрогеназы, сорбитдегидрогеназы и дегидрогеназы аминокислоты, включая дегидрогеназу L-аминокислоты. В следующем аспекте этого варианта второй аналит представляет собой глюкозу и второй фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу. В следующем объекте изобретения кофермент представляет собой соединение формулы (I)
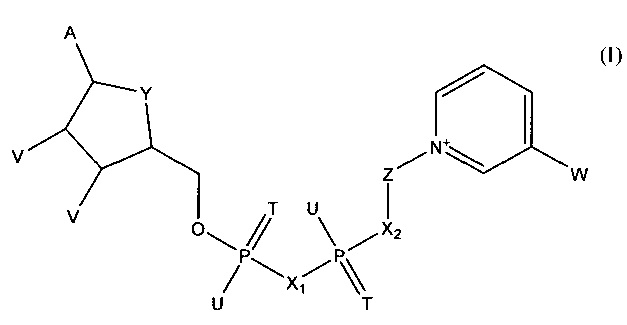
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
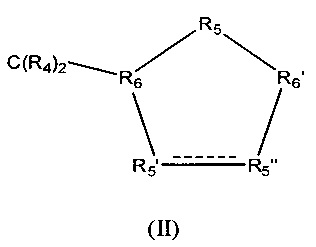
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
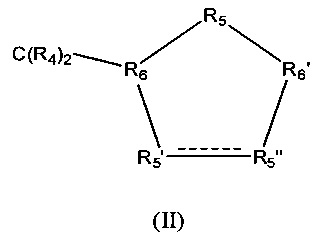
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
В другом объекте изобретения кофермент представляет собой соединение формулы (I)
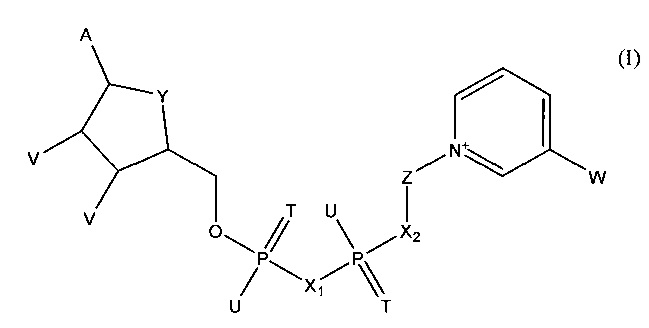
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
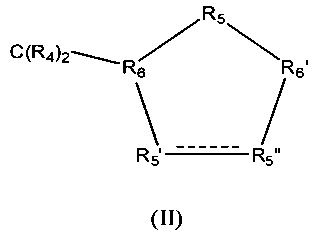
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
В следующем объекте изобретения кофермент представляет собой тио-NAD. В другом объекте изобретения кофермент представляет собой тио-NADP.
В следующем варианте этого варианта осуществления изобретения тестовый элемент включает первый реагентный материал, который включает первый фермент или субстрат для первого фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы. В одном из аспектов этого варианта тестовый элемент включает также второй реагентный материал, который включает второй фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из FAD, NAD, NADP и соединения формулы (I) или его соли или необязательно восстановленной формы. В другом объекте изобретения тестовый элемент включает тест-полоску, созданную так, чтобы она содержала первый и второй реагентные материалы. В следующем объекте изобретения тест-полоска включает первую электродную систему, ассоциированную с первым реагентным материалом, и вторую электродную систему, ассоциированную со вторым реагентным материалом. В другом аспекте этого варианта первый реагентный материал дополнительно включает один из таких ингредиентов как нитрозоанилин, ферроцианид калия и комбинацию феназинового производного и хлорида гексааминорутения.
В другом варианте осуществления изобретения реагентный материал включает 3-гидроксибутиратдегидрогеназу и кофермент формулы (I):
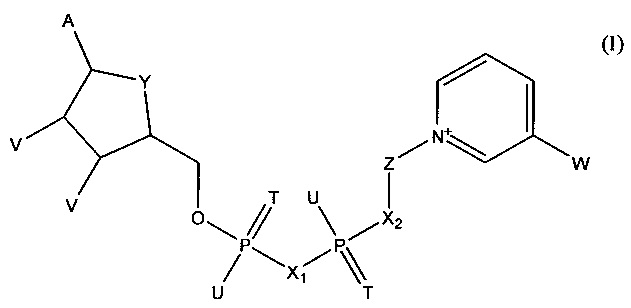
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соль или необязательно восстановленную форму.
В одном из вариантов указанного варианта осуществления изобретения кофермент представляет собой соединение формулы (I)
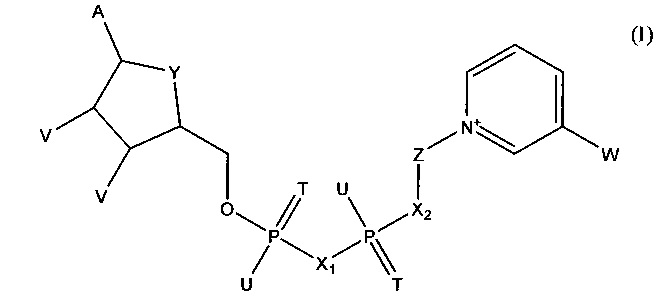
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
Y в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает насыщенное карбоциклическое 5-членное кольцо общей формулы (II)
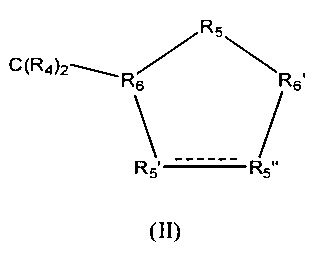
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
В другом варианте указанного варианта осуществления изобретения кофермент представляет собой соединение формулы (I)
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает насыщенное карбоциклическое 5-членное кольцо общей формулы (II)
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
В другом варианте реагентный материал включает также один из таких ингредиентов как нитрозоанилин, ферроцианид калия и комбинацию феназинового производного и хлорида гексааминорутения.
В другом варианте указанного варианта осуществления изобретения тестовый элемент включает тест-полоску, содержащую реагентный материал для определения первого аналита. В другом аспекте этого варианта тест-полоска содержит также второй реагентный материал для определения второго аналита. В следующем объекте изобретения реагентный материал включает фермент дегидрогеназу, выбранную из группы, состоящей из глюкозодегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, глицерин-дегидрогеназы, алкогольдегидрогеназы, сорбитдегидрогеназы и дегидрогеназы аминокислоты, включая дегидрогеназу L-аминокислоты. В следующем объекте изобретения второй реагентный материал включает кофермент, выбранный из группы, состоящей из FAD, NAD, NADP и соединения формулы (I):
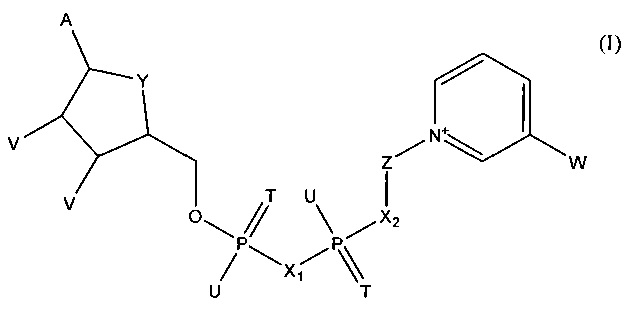
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Cl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы.
В следующем объекте изобретения тест-полоска предназначена для электрохимического определения первого и второго аналитов.
В следующем варианте осуществления изобретения предлагается способ определения первого и второго аналитов в образце, который заключается в создании тестового элемента, пригодного для определения первого и второго аналитов, и который включает первый коферментзависимый фермент или субстрат для первого фермента, второй коферментзависимый фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I):
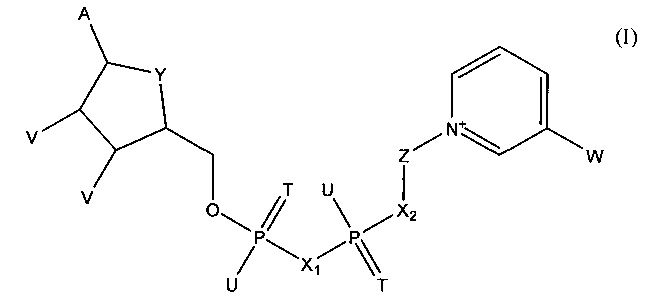
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы;
контактирования этого тестового элемента с образцом; определения первого аналита и определение второго аналита.
В одном из вариантов указанного варианта осуществления изобретения первый аналит представляет собой гидроксибутират, а второй аналит представляет собой глюкозу. В одном из аспектов этого варианта осуществления изобретения стадии определения первого аналита и определения второго аналита осуществляют одновременно. В другом аспекте этого варианта осуществления изобретения стадии определения первого аналита и определения второго аналита завершаются в пределах пяти секунд после контактирования тестового элемента с образцом.
В следующем варианте осуществления изобретения способ включает стадии получения тестового элемента, созданного для определения содержания глюкозы и кетонов в образце; контактирования этого тестового элемента с образцом; и определения содержания глюкозы и кетонов в образце в пределах 7,5 секунд после контактирования тестового элемента с образцом. В одном из вариантов осуществления изобретения тестовый элемент включает первый реагентный материал для определения содержания глюкозы и второй реагентный материал для определения содержания кетонов. В одном из аспектов этого варианта осуществления изобретения второй реагентный материал включает гидроксибутиратдегидрогеназу. В другом варианте стадия определения содержания глюкозы и кетонов завершается в пределах 5 секунд после контактирования тестового элемента с образцом. В следующем варианте осуществления изобретения разница в продолжительности стадий определения содержания глюкозы и кетонов находится в пределах 2 секунд. В следующем варианте образец содержит кровь.
В одном из вариантов осуществления указанного способа, тестовый элемент включает первый коферментзависимый фермент или субстрат для первого фермента и второй коферментзависимый фермент или субстрат для второго фермента. Тестовый элемент включает также кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I):
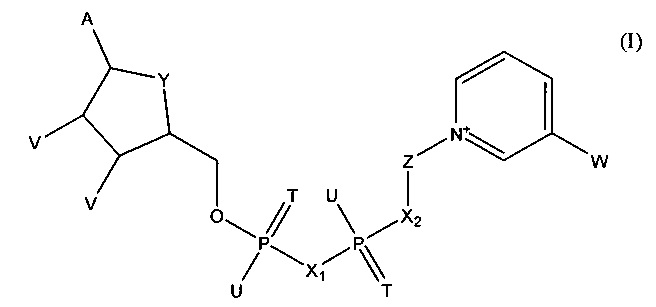
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
Х1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы.
В одном из объектов изобретения первый аналит представляет собой гидроксибутират и первый фермент представляет собой гидроксибутиратдегидрогеназу. В другом объекте изобретения гидроксибутиратдегидрогеназа представляет собой 3-гидроксибутиратдегидрогеназу. В следующем объекте изобретения второй фермент представляет собой дегидрогеназу, выбранную из группы, состоящей из глюкозодегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, глицерин-дегидрогеназы, алкогольдегидрогеназы, сорбитдегидрогеназы и дегидрогеназы аминокислоты, включая дегидрогеназу L-аминокислоты. В другом объекте изобретения второй фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу. В следующем объекте изобретения кофермент представляет собой соединение формулы (I)
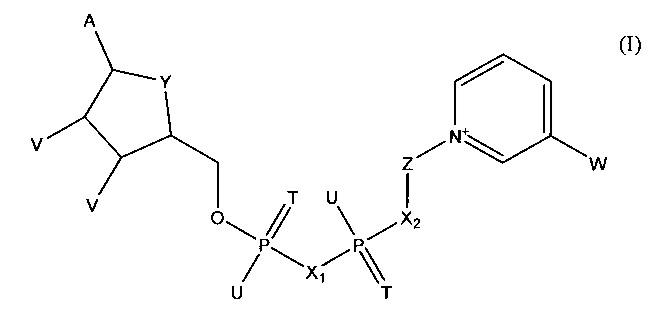
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
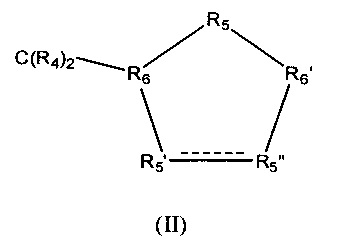
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
В следующем объекте изобретения кофермент представляет собой соединение формулы (I)
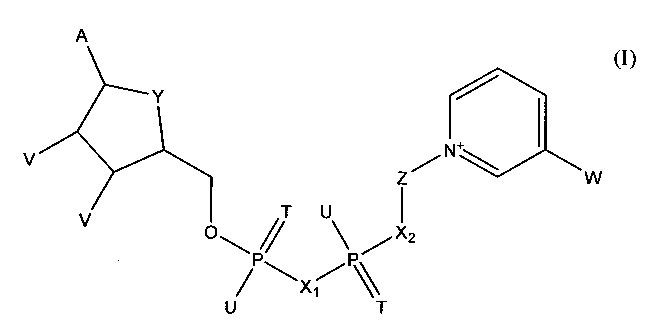
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
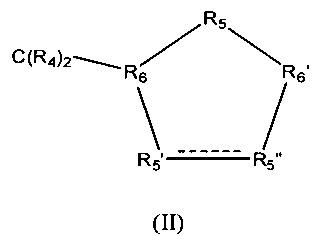
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
В еще одном объекте изобретения кофермент представляет собой тио-NAD. Еще в одном объекте изобретения кофермент представляет собой тио-NADP. В следующем объекте изобретения тестовый элемент включает первый реагентный материал, который включает первый фермент или субстрат для первого фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I) или его соли или восстановленной формы. В следующем объекте изобретения тестовый элемент включает также второй реагентный материал, который включает второй фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I) или его соли или восстановленной формы. В следующем объекте изобретения тестовый элемент включает тест-полоску, созданную таким образом, чтобы она содержала первый и второй реагентный материалы. Еще в одном объекте изобретения тест-полоска включает первую электродную систему, ассоциированную с первым реагентым материалом, и вторую электродную систему, ассоциированную со вторым реагентным материалом. В другом объекте изобретения первый реагентный материал дополнительно включает один из таких ингредиентов как нитрозоанилин, ферроцианид калия, и комбинацию феназинового производного и хлорида гексааминорутения.
Другим объектом настоящего изобретения является уникальная технология определения присутствия и/или измерения концентрации нескольких аналитов в тестируемых образцах. Другие объекты изобретения включают уникальные способы, системы, приборы, наборы, агрегаты, оборудование и/или устройства, пригодные для обнаружения аналита в образце.
Другие объекты, варианты осуществления изобретения, формы, отличительные признаки, полезные свойства, объекты и преимущества изобретения должны стать очевидными после ознакомления с подробным описанием изобретения и прилагаемыми чертежами.
Краткое описание чертежей
На Фиг. 1 представлено перспективное изображение первого варианта тестового элемента.
На Фиг. 2 представлено перспективное изображение с пространственным разделением различных деталей тестового элемента, показанного на Фиг. 1.
На Фиг. 3 представлено перспективное изображение с пространственным разделением различных деталей второго варианта тестового элемента.
На Фиг. 4 представлено изображение сечения фрагмента тестового элемента, показанного на Фиг. 3.
На Фиг. 5 представлена схематическая иллюстрация аналитического инструмента со структурой, пригодной для применения с тестовым элементом, показанным на Фиг. 1.
На Фиг. 6-18 представлены графические иллюстрации ответов на гидроксибутират, определенных с использованием различных реагентных материалов.
Подробное описание предпочтительных вариантов осуществления изобретения
Для целей лучшего понимания принципов настоящего изобретения ниже представлена ссылка на варианты осуществления изобретения, проиллюстрированные с помощью чертежей, и конкретные понятия, которые можно применять для их описания. Тем не менее, как должно быть очевидно, под объем изобретения подпадают изменения и другие модификации приведенного с целью иллюстрации устройства, и такие дополнительные применения проиллюстрированных принципов изобретения, которые, как правило, осуществляет специалист в области, к которой относится изобретение.
В настоящем изобретении предложены реагентные материалы и ассоциированные тестовые элементы. В одном из вариантов осуществления изобретения тестовый элемент, обладающий двойной функцией, включает первый коферментзависимый фермент или субстрат для первого фермента, второй коферментзависимый фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I). В одном из объектов изобретения первый аналит представляет собой гидроксибутират и первый фермент представляет собой гидроксибутиратдегидрогеназу, и второй аналит представляет собой глюкозу и второй фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу. В другом варианте осуществления изобретения тестовый элемент представляет собой часть системы и включает также измерительный прибор, пригодный для взаимодействия с тестовым элементом, для оценки первого и второго аналитов в образце. Указанная оценка может варьироваться от определения присутствия первого и второго аналитов до определения концентрации первого и второго аналитов. Первый и второй аналиты и образец жидкости могут являться любыми, для которых пригодна тестовая система, хотя в одном конкретном варианте, который не ограничивает объем изобретения, первый аналит представляет собой гидроксибутират, второй аналит представляет собой глюкозу, а образец жидкости представляет собой кровь или тканевую (интерстициальную) жидкость. Другими объектами настоящего изобретения являются уникальные реагентные материалы. Другие объекты и отличительные признаки настоящего изобретения описаны со ссылкой на представленные ниже приведенные в качестве иллюстрации варианты осуществления изобретения.
Ниже со ссылкой на Фиг. 1 и 2 представлено более подробное описание первого варианта тестового элемента 10, предназначенного для оценки первого и второго аналитов в образце. Предложен тестовый элемент 10, представляющий собой электрохимический сенсор, включающий камеру для приема образца, предназначенную для образца жидкости, и первый и второй реагентные материалы для получения электрохимических сигналов в присутствии первого и второго аналитов. В приведенном в качестве иллюстрации варианте тестовый элемент 10 расположен между концом 12, предназначенным для ввода измерителя, и концом 14 дозирующего устройства. В одном из не проиллюстрированных вариантов форма конца 14 дозирующего устройства может отличаться от формы конца 12, предназначенного для ввода измерителя, что позволяет пользователю правильно обращаться и использовать тестовый элемент 10. Тестовый элемент 10 может включать также одно или несколько графических изображений (не показаны), обеспечивающих руководство для пользователя по правильному обращению и применению.
Тестовый элемент 10 представлен в виде одноразовой тест-полоски, имеющей пластинчатую конструкцию, которая включает субстратную основу 16, разделяющий слой 18, крышку корпуса 20 и крышку камеры 22. Дополнительные детали тестового элемента, включающего сходную пластинчатую конструкцию, представлены в патенте US 7727467, полное содержание которого включено в настоящее описание в качестве ссылки. Разделяющий слой 18 включает пустотную область 24, что позволяет камере 26 для приема образца располагаться между субстратной основой 16 и крышкой корпуса 20 и крышкой камеры 22. При такой конфигурации камера 26 для приема образца открывается на конце 14 дозирующего устройства тестового элемента 10 отверстием 28, которое предназначено для облегчения прохождения образца жидкости в камеру 26 для приема образца. Под объем изобретения подпадают также формы, в которых камера 26 для приема образца открывается отверстием, расположенным вдоль бортика тестового элемента 10. Под объем изобретения подпадают также формы, в которых камера 26 для приема образца открывается отверстием, расположенным вдоль всей длины конца 14 дозирующего устройства, и включает часть бортиков.
Крышка корпуса 20 и крышка камеры 22 покрывают разделяющий слой 18 и между ними образуется желобок 30, который представляет вентилирующее отверстие, сообщающееся с камерой 26 для приема образца, позволяющее воздуху покидать камеру 26 для приема образца по мере поступления образца жидкости в камеру 26 для приема образца через отверстие 28. Желобок 30 локализован в положении относительно камеры 26 для приема образца, которое является внутренним относительно локализации электродных систем (описаны ниже), расположенных в камере 26 для приема образца 26. Образец жидкости, входящий в камеру 26 для приема образца, должен продвигаться до вентилирующего отверстия, но не дальше. При виде сверху желобок является визуальным индикатором «наливной линии», для подтверждения того, что электродные системы в камере 26 для приема образца соответствующим образом смочены или покрыты для обеспечения правильного функционирования. В дополнительном или альтернативном варианте электроды, определяющие достаточность дозы, можно располагать также рядом с желобком 30 для определения, когда образец жидкости достигает желобка 30, для гарантии того, что имеет место смачивание измерительных электродов.
Помимо электродных систем и реагентных материалов камера 26 для приема образца может быть пустой или альтернативно может включать сорбционный материал. Приемлемые сорбционные материалы включают сложный полиэфир, нейлон, целлюлозу и производные целлюлозы, такие как нитроцеллюлоза. Сорбционные материалы, если они включены, способствуют облегчению проникновения образца жидкости путем (капиллярного) затекания жидкости в камеру 26 для приема образца. Применение сорбционного материала может служить также дополнительному уменьшению пустого объема камеры 26 для приема образца, в которую поступает образец жидкости. В одном из вариантов заполнение камеры 26 для приема образца происходит в результате капиллярного действия. Заполнение камеры 26 для приема образца можно увеличивать с помощью других средств, таких как приложение давления к образцу жидкости для проталкивания его в камеру 26 для приема образца, и/или создание вакуума в камере 26 для приема образца для втягивания образца жидкости в камеру 26 для приема образца. Кроме того, одна или несколько поверхностей в камере 26 для приема образца может быть образована из гидрофильного материала, иметь покрытие из гидрофильного материала или подвергаться способствующей увеличению гидрофильности обработке для облегчения заполнения камеры 26 для приема образца тестируемым образцом.
Тестовый элемент 10 предназначен для определения присутствия и/или измерения концентрации первого и второго аналитов путем реакций электрохимического окисления и восстановления. Эти реакции преобразовываются в электрический сигнал, который может быть коррелирован с количеством или концентрацией аналита. Как продемонстрировано на Фиг. 2, на которой проиллюстрированы лишь некоторые особенности тестового элемента 10, субстрат 16 несет первую электродную систему 32, которая включает множество электродов 34 и электродные трассы 36, которые заканчиваются в контактных подушках 38. Электроды 34 представляют собой участки электродных трасс 36, которые расположены в камере 26 для приема образца. Субстрат 16 несет также вторую электродную систему 46, которая включает множество электродов 48 и электродные трассы 50, которые заканчиваются в контактных подушках 52. Электроды 48 представляют собой участки электродных трасс 50, которые расположены в камере 26 для приема образца. Как должно быть очевидно, проиллюстрированные конфигурации электродных систем 32, 46 не ограничивают объем изобретения, и под его объем подпадают альтернативные конфигурации.
Тестовый элемент 10 включает также первый реагентный материал 60, который покрывает по меньшей мере часть электродов 34 первой электродной системы 32 в камере 26 для приема образца, и второй реагентный материал 62, который покрывает по меньшей мере часть электродов 48 второй электродной системы 46 в камере 26 для приема образца. Первый и второй реагентные материалы 60, 62 пригодны для генерирования электрохимических сигналов в присутствии соответственно первого и второго аналитов, и они находятся в камере 26 для приема образца в положении, которое обеспечивает передачу электрохимического сигнала к электродам 34, 48 в камере 26 для приема образца. В приведенном в качестве иллюстрации варианте зазор 64 находится между первым и вторым реагентными материалами 60, 62, хотя варианты, в которых зазор 64 отсутствует и первый и второй реагентные материалы образуют непрерывный слой NAD электродами 34, 48, также подпадают под объем изобретения. Дополнительные детали, касающиеся первого и второго реагентных материалов 60, 62, представлены ниже в настоящем описании.
Электроды 34 первой электродной системы 32 включают набор измерительных электродов в форме рабочего электрода 40 и противоэлектрода 42, который включает участки 44а и 44b, расположенные на противоположных сторонах рабочего электрода 40. В контексте настоящего описания «рабочий электрод» представляет собой электрод, на котором аналит электроокисляется или электровосстанавливается с помощью окислительно-восстановительного медиатора или без него, а понятие «противоэлектрод» относится к электроду, который спарен с рабочим электродом и через который проходит электрохимический ток, равный по величине и противоположный по знаку току, протекающему через рабочий электрод. Подразумевается, что понятие «противоэлектрод» включает противоэлектроды, которые функционируют также в качестве контрольных электродов (т.е. представляют собой противоэлектроды/контрольные электроды). Электроды 48 второй электродной системы 46 включают набор измерительных электродов в форме рабочего электрода 54 и противоэлектрода 56, который включает участки 58а и 58b, расположенные на противоположных сторонах рабочего электрода 54. При такой организации камера 26 для приема образца имеет такую конфигурацию, что жидкий образец, входящий в камеру 26 для приема образца приходит в электролитический контакт с рабочими электродами 40 и 54 и противоэлектродами 42 и 56. Такое устройство позволяет также электрическому току протекать между измерительными электродами для воздействия на электроокисление или электровосстановление первого и второго аналитов. Однако, как должно быть очевидно, выше представлена лишь одна из нескольких конфигураций измерительных электродов.
Альтернативный вариант тестового элемента 110 для оценки первого и второго аналитов в образце проиллюстрирован на Фиг. 3 и 4. Тестовый элемент 110 действует на основе техники получения по типу «голова-к-голове». Дополнительные детали этой техники и тестовый элемент 110 в целом представлены в международной заявке на патент WO 2012/003306, полное содержание которой включено в настоящее описание в качестве ссылки. Как проиллюстрировано на Фиг. 3, электродные схемы 112 размещают в виде двух колонок (один набор электродных схем в колонке А и один набор электродных схем в колонке В) на удлиненном слое (лента) субстрата 114. Тестовый элемент 110 включает также электродные схемы 116 камеры для образца, расположенные вблизи друг друга и вблизи центра субстрата 114 и контактных подушек 118, расположенных друг против друга, и локализованных вблизи противоположных кромок субстрата 114. В приведенном в качестве иллюстрации варианте электродные схемы являются сходными; однако в альтернативных вариантах по меньшей мере некоторые из электродных схем могут отличаться от других электродных схем. Первый реагентный материал 120 наносят на электроды 116 камеры для образца в колонке А, а второй реагентный материал 122 наносят на электроды 116 камеры для образца в колонке В.
Разделяющий слой 124 присоединяют к верхней части субстрата 114 с помощью адгезивного слоя 126. В приведенном в качестве иллюстрации варианте одна удлиненная полоса или лента образует разделительный слой 124, предназначенный для покрытия электродных схем в обеих колонках А и В, хотя возможны также формы, в которых две различные полоски разделительного слоя 124 по отдельности присоединены к субстрату 114 в колонке А и в колонке В и выровнены вдоль центральной линии 128. Разделительный слой 124 включает множество вырезанных участков 130, расположенных вдоль центральной линии 128. Когда разделительный слой 124 объединен с субстратом 114, то вырезанные участки 130 могут образовывать периметры камер для образцов 132 (Фиг. 4). Один непрерывный верхний субстратный слой 134 присоединен к верхнему разделительному слою 124 с помощью адгезивного слоя 136, и он включает множество вентиляционных отверстий 142, 144 для облегчения вентиляции камер для образцов 132 по мере их заполнения образцом жидкости. Хотя это ранее не обсуждалось, но должно быть очевидно, что адгезивные слои 126, 136 включают множество вырезанных участков 138, 140 соответственно, расположенных вдоль центральной линии 128 и соответствующих вырезанным участкам 130 разделительного слоя 124. Альтернативно этому, подразумевается, что адгезивный слой 136 может представлять собой твердый слой без каких-либо отверстий или вырезов.
После того, как субстрат 114, реагентные материалы 120, 122, разделительный слой 124 и верхний субстрат 134 объединяют и ламинируют вместе, лист или рулон разделяют так, чтобы электродные схемы 116 в колонках А и В оставались присоединенными друг к другу, в то время как тест-полоски в соседних рядах (ориентированные бок о бок тест-полоски) были отделены. Другими словами, тест-полоски в колонке А не полностью отделены от тест-полосок в колонке В, и пары тест-полосок, образованные с использованием каждой пары тест-полосок, размещены по типу «голова-к-голове». Каждую пару тест-полосок можно сгибать для размещения контактных подушек 118 тест-полоски из колонки А вблизи контактных подушек 118 тест-полоски из колонки В, и для размещения предназначенного для нанесения образца конца тест-полоски из колонки А вблизи в ориентированную в том же направлении, что и предназначенный для нанесения образца конец тест-полоски из колонки В. Используя такое размещение пар тест-полосок по типу «голова-к-голове», получают биосенсор двойного назначения, в который пользователь может вносить тканевые жидкости на обе тест-полоски одновременно для того, чтобы тестировать первый и второй различные аналиты с использованием одного образца. В одном из вариантов осуществления изобретения в камерах 132 для двух образцов могут быть добавлены среды для фильтрации крови перед объединением пары для того, чтобы предупреждать смешение крови и реагентов между камерами 132.
Должно быть очевидно, что в каждой из камер 132 пара ориентированных по типу «голова-к-голове» тест-полосок должна экспонироваться, когда эту пару тест-полосок сгибают вдоль центральной линии 128. Можно применять альтернативные технологии изготовления для гарантии того, чтобы экспонировать обе камеры для образцов 132. Например, в одном из вариантов осуществления изобретения один из слоев субстрата, например, верхний слой 134, полностью отделяют вдоль центральной линии 128 в процессе изготовления, а субстрат 114 либо оставляют немодифицированным, либо модифицируют для запланированного сгиба вокруг центральной линии 128. В альтернативном варианте осуществления изобретения один из слоев субстрата модифицируют, так, чтобы через перфорации или частичные надрезы пользователь мог его легко отделять вдоль центральной линии 128, в другой субстрат модифицируют путем создания насечек, надрезов или обжатия для того, чтобы предсказуемо сгибать или производить отделение по прямой линии, например, центральной линии 128. В следующем варианте осуществления изобретения как верхний слой 134, так и нижний субстрат 114 модифицируют, чтобы позволять расположенным «голова-к-голове» тест-полоскам складываться в любом направлении, т.е. так чтобы пользователь мог выбирать сложенную «голова-к-голове» пару тест-полосок с получением верхних слоев 134 двух тест-полосок, расположенных рядом друг с другом, или с получением субстратов 114 двух тест-полосок, расположенных рядом друг с другом.
Субстраты 16, 114 могут образовывать изоляционный материал, на котором расположены каждая из электродных систем 32, 46 и электродная схема 112. Как правило пластики, такие как виниловые полимеры, полиимиды, сложные полиэфиры и стиролы, обеспечивают требуемые электрические и структурные свойства. Кроме того, поскольку тестовые элементы можно производить в массовых количествах из рулонов материала, то является желательным, чтобы материал обладал пригодными свойствами, в том числе обладал достаточной гибкостью для обработки рулона, при этом также обеспечивая приемлемую жесткость полученному в итоге элементу. Материал для субстратов 16, 114 можно выбирать из гибкого полимерного материала, такого сложный полиэфир, включая высокотемпературный сложный полиэфир; полиэтиленнафталин (PEN) и полиимид, или смеси двух или более этих веществ. Полиимиды поступают в продажу, например, под товарным знаком Kapton® от фирмы E.I. duPont de Nemours and Company of Wilmington, Del. (duPont). Одним из конкретных пригодных для субстратов 16, 114 материалов является MELINEX® 329 фирмы duPont.
Рабочий электрод и противоэлектрод и остальные компоненты электродных систем 32, 46 и электродных схем 112, можно изготавливать из различных материалов. В одном из объектов изобретения электроды должны иметь относительно низкое электрическое сопротивление и должны быть электрохимически инертными в рабочем диапазоне тестовых элементов. Приемлемые проводники для рабочего электрода включают среди прочего золото, палладий, платину, углерод, титан, диоксид рутения и оксид индия-олова, и иридий. Противоэлектрод можно изготавливать из таких же или других материалов, например, серебра/хлорида серебра. В одном из конкретных вариантов осуществления изобретения рабочий электрод и противоэлектрод оба представляют собой золотые электроды.
Электродные системы 32, 46 и электродные схемы 112 можно накладывать на субстраты 16, 114 соответственно любым образом, который позволяет получать электроды требуемой проводимости и целостности. Приведенные в качестве примеров процессы, включающие напыление и печать, должны обеспечивать несколько новых неограниченных возможностей. В одном конкретном варианте получают золотые электроды путем нанесения материалов субстратов 16, 114 и последующего удаления выбранных участков покрытия с получением электродных систем 32, 46 и электродных схем 112. Один из конкретных методов удаления участков покрытия включает лазерную абляцию и более конкретно широкопольную лазерную абляцию, описанную в патенте US 7073246, полное содержание которого включено в настоящее описание в качестве ссылки.
Техники лазерной абляции, как правило, включают абляцию одного слоя металла или многослойной композиции, которая включает изоляционный материал и проводящий материал, например, металлический ламинат слоя металла, покрытого или ламинированного изоляционным материалом. Металлический слой может содержать чистые металлы, сплавы или другие материалы, которые представляют собой металлические проводники. Примеры металлов или металлоподобных проводников включают: алюминий, углерод (такой как графит), кобальт, медь, галлий, золото, индий, никель, палладий, платину, серебро, титан, их смеси и сплавы или твердые растворы этих материалов. В одном из объектов изобретения выбирают материалы, практически не вступающие в реакцию с биологическими системами, примерами которых являются (но не ограничиваясь только ими) золото, платина, палладий, углерод и оксид иридия и олова. Металлический слой может иметь любую требуемую толщину, которая в одном из вариантов составляет примерно 500 нм.
Должно быть очевидно, что приведенная в качестве иллюстрации форма тестовых элементов 10, 110 не ограничивает объем изобретения, и что изобретение относится также к альтернативным конфигурациям тестовых элементов с двойной функцией, предлагаемых в настоящем описании, включая элементы, пригодные для оптических методов определения. В этой связи в одном дополнительном и не ограничивающем объем изобретения варианте тестовый элемент с двойной функцией может иметь конфигурацию сэндвич-типа, в которой первый субстрат, который несет первую электродную систему, расположен над вторым субстратом, который несет вторую электродную систему. Первый и второй субстраты отделены друг от друга с помощью промежуточного слоя, который включает капиллярный канал, или капиллярный канал иным образом сформирован между первым и вторым субстратами. В такой конфигурации образец жидкости, который поступает в капиллярный канал, движется к первой и второй электродным системам так, что покрытие первой и второй электродных систем происходит одновременно или практически одновременно. Хотя это ранее не обсуждалось, но также должно быть очевидно, что первый субстрат содержит первый реагентный материал, пригодный для определения первого аналита, а второй субстрат содержит второй реагентный материал, пригодный для определения второго аналита. В приведенном в качестве примера варианте, который не ограничивает объем изобретения, одна из технологий получения тестового элемента, имеющего указанную конфигурацию, включает раздельное получение первого субстрата, несущего первый реагентный материал и первую электродную систему, и второго субстрата, несущего второй реагентный материал и вторую электродную систему, и последующее объединение первого и второго субстратов.
В другом не ограничивающем объем изобретения варианте тестовый элемент с двойной функцией может включать несколько иную конфигурацию сэндвич-типа. В такой конфигурации первый субстрат, который несет первую электродную систему, расположен над вторым субстратом, который несет вторую электродную систему. Однако первый и второй субстраты соединены адгезивным слоем и каждый включает отдельную камеру для образца, расположенную над соответствующей ему электродной системой вместо одного капиллярного канала. В указанной форме тестовый элемент включает конфигурацию, которая облегчает одновременное или практически одновременное заполнение индивидуальных камер для образцов, в результате также имеет место одновременное или практически одновременное покрытие первой и второй электродных систем. Хотя это ранее не обсуждалось, но также должно быть очевидно, что первый субстрат содержит первый реагентный материал, пригодный для определения первого аналита, а второй субстрат содержит второй реагентный материал, пригодный для определения второго аналита. Указанный тестовый элемент можно получать также путем применения описанной выше технологии в сочетании с другой конфигурацией сэндвич-типа, представленной в настоящем описании. Дополнительные детали одного не ограничивающего объем изобретения тестового элемента, имеющего указанную форму, представлены в публикации международной заявки на патент WO 2012/003306 (указана выше в настоящем описании).
Другие не ограничивающие объем изобретения примеры устройств, которые можно использовать для тестового элемента, предлагаемого в настоящем описании, приведены в патентах US 6984307 и US 4397956, полное содержание которых включено в настоящее описание в качестве ссылки.
Предусматривается, что тестовые элементы 10, 110 можно применять для определения широкого разнообразия первых и вторых аналитов в биологической жидкости. Например, тестовые элементы 10, 110 легко можно адаптировать для применения в сочетании с реагентными материалами 60, 62 и 120, 122, которые имеют любой приемлемый химический состав, который можно применять для оценки присутствия и/или концентрации первого и второго аналитов. Реагентные материалы 60, 62 и 120, 122 пригодны для взаимодействия с первым и вторым аналитом с генерированием электрохимических сигналов, которые отражают присутствие и/или концентрацию первого и второго аналитов в образце жидкости. Как это будет описано более подробно ниже, реагентные материалы 60, 62 и 120, 122 могут включать широкое разнообразие активных компонентов, отобранных для определения присутствия и/или концентрации различных первых и вторых аналитов. Таким образом, предназначенные для тестирования химические соединения, входящие в реагентные материалы 60, 62 и 120, 122, отбирают в зависимости от подлежащих оценке первых и вторых аналитов. Указанные аналиты могут включать, например, глюкозу, холестерин, холестерин ЛПВП, триглицериды, глицерин, лактаты, лактатдегидрогеназу, малаты, спирты, мочевую кислоту, сорбит, аминокислоты, 1,5-ангидроглюцитол и аналиты, характерные для кетоновых тел, такие как гидроксибутират. В одном из конкретных вариантов осуществления изобретения тестовые элементы 10, 110 включают реагентные материалы 60, 62 и 120, 122 соответственно, которые отобраны для определения присутствия и/или концентрации гидроксибутирата и глюкозы в крови.
Примеры биологических жидкостей, в которых можно оценивать первый и второй аналиты, являются (но не ограничиваясь только ими) любые жидкости организма, в которых можно измерять аналиты, такие как тканевая (интерстициальная) жидкость, слезы, моча и кровь. Понятие «кровь» в контексте данного документа включает цельную кровь и ее бесклеточные компоненты, такие как плазма и сыворотка. Когда тестовые элементы предназначены для тестирования гидроксибутирата и глюкозы, то образец жидкости конкретно может включать, например свежую капиллярную кровь, полученную из кончика пальца или принятых альтернативных областей (например, предплечья, ладони, мочки уха, плеча, икры и бедра), свежую венозную кровь или мочу. Кроме того, тестовые элементы можно применять также в сочетании с контрольными жидкостями, которые используют общепринятым образом для подтверждения целостности системы, предназначенной для тестирования.
Жидкость организма, содержащую подлежащий оценке аналит, можно получать и вводить в тестовые элементы любым образом. Например, образец крови можно получать общепринятым путем посредством разрезания кожи, например, ланцетом, а затем приводить в контакт тестовый элемент с жидкостью, появившейся на поверхности кожи. В одном из объектов изобретения тестовые элементы функционируют в качестве средства оценки требуемого аналита при использовании лишь очень небольших образцов жидкости. Аналогично этому, согласно одному из объектов изобретения лишь небольшой разрез кожи является достаточным для получения объема жидкости, требуемого для осуществления теста, и с помощью такого метода боль и другие неприятные ощущения можно минимизировать или устранять.
Реагентные материалы 60, 120 включают первый коферментзависимый фермент или субстрат для первого фермента и приемлемый кофермент. Эти компоненты, как правило, растворяют или суспендируют в матриксе. Жидкий тестируемый образец гидратируют или растворяют в матриксе, и первый аналит диффундирует через матрикс для взаимодействия с одним или несколькими активными компонентами. Приемлемыми ферментами, которые можно включать в реагентные материалы 60, 120, являются например, дегидрогеназы, выбранные из глюкозодегидрогеназы (Е.С.1.1.1.47), лактатдегидрогеназы (Е.С.1.1.1.27, 1.1.1.28), малатдегидрогеназы (Е.С.1.1.1.37), глицериндегидрогеназы (Е.С.1.1,1.6), алкогольдегидрогеназы (Е.С.1.1.1.1), гидроксибутиратдегидрогеназы (HBDH), такой как 3-гидроксибутиратдегидрогеназа или бета-гидроксибутиратдегидро-геназа, альфа-гидроксибутиратдегидрогеназа и гамма-гидроксибутиратдегидро-геназа, сорбитдегидрогеназы и дегидрогеназы аминокислоты, например дегидрогеназы L-аминокислоты (Е.С.1.4.1.5). Другими приемлемыми ферментами являются оксидазы, такие как глюкозооксидаза (Е.С.1.1.3.4) или холестериноксидаза (Е.С.1.1.3.6), или аминотрансферазы, такие как аспартат- или аланинаминотрансфераза, 5'-нуклеотидаза или креатинкиназа. В зависимости от выбранного фермента потенциальные коферменты, пригодные для применения в реагентных материалах 60, 120, включают FAD, NAD, NADP, тио-NAD, тио-NADP и соединение формулы (I)
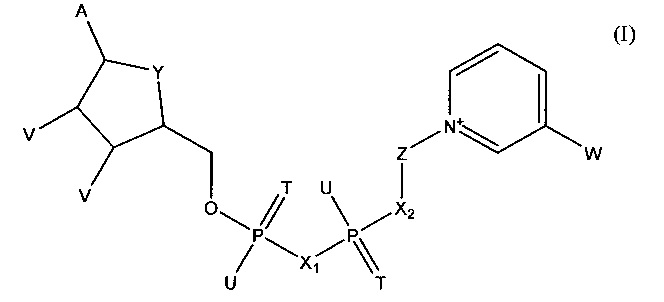
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
Х1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соль или необязательно восстановленная форма.
В одном из вариантов осуществления изобретения W обозначает CONH2 или СОСН3.
Приведенные в качестве примера заместители Z выбирают из группы, состоящей из ОН, F, Сl и С1-С2-алкила, который необязательно фторирован или хлорирован и/или замещен ОН, O-C1-С2-алкилом.
В другом варианте осуществления изобретения первый остаток V обозначает ОН, а второй остаток V обозначает фосфатную группу. Необязательно одна ОН-группа и одна фосфатная группа могут образовывать кольцо в сочетании с атомами углерода, с которыми они связаны.
Примеры аналогов аденина включают (но не ограничиваясь только ими) С8-замещенный и N6-замещенный аденин, деазапроизводные, такие как 7-деазапроизводные, азапроизводные, такие как 8-азапроизводные, или комбинации 7-деаза- или 8-азапроизвододных, или карбоциклические аналоги, такие как формицин, в которых 7-деазапроизводные могут быть замещены в 7-ом положении галогеном, С1-С6-алкинилом, C1-С6-алкенилом или C1-С6-алкилом. В другом варианте осуществления изобретения соединения содержат аналоги аденозина, которые содержат, например 2-метоксидезоксирибозу, 2'-фтордезоксирибозу, гексит, алтрит или полициклические аналоги, такие как бициклические, LNA (закрытая нуклеиновая кислота) и трициклические сахара, вместо рибозы. В одном из вариантов атомы кислорода (ди)фосфата можно также изоэлектронно замещать, например О- на S- и/или на ВН3-, О на NH, NCH3 и/или на СН2, и =O на =S. В одном из вариантов осуществления изобретения по меньшей мере один остаток U в соединении формулы (I) отличается от ОН, а в другом варианте осуществления изобретения по меньшей мере один остаток U обозначает ВН3-.
Другим более конкретным, но не ограничивающим объем изобретения соединением формулы (I), в котором:
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
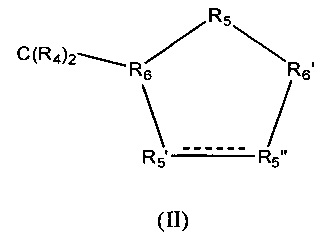
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН,
является карба-NAD или cNAD.
Карба-NAD имеет следующую структуру:
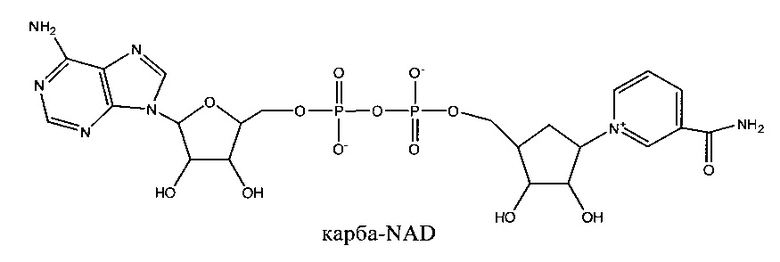
Другим более конкретным, но не ограничивающим объем изобретения соединением формулы (I), в котором:
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
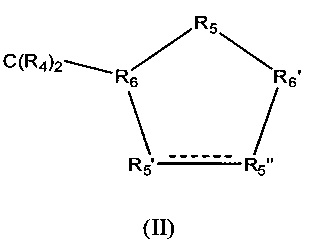
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН,
является карба-NADP или cNADP.
Карба-NADP имеет следующую структуру:
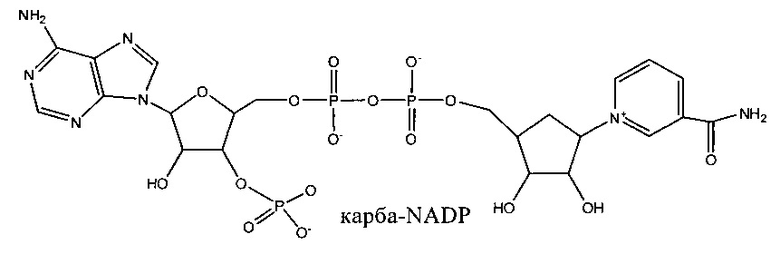
Другие конкретные, но не ограничивающие объем изобретения соединения формулы (I) включают боранокарбо-NAD, циклопентил-NAD и циклофосфат карбо-NAD. Эти соединения имеют следующие структуры:
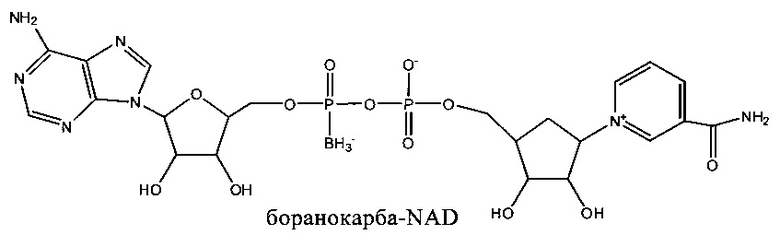
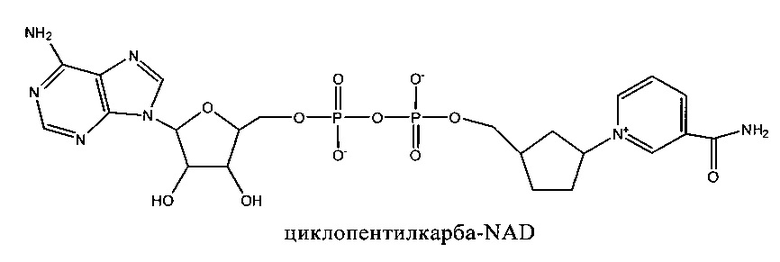
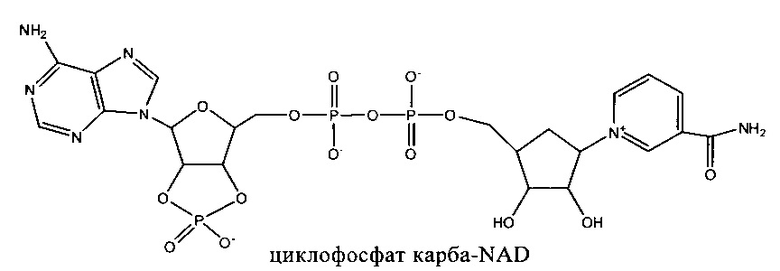
Дополнительные детали, касающиеся соединений формулы (I) их синтез описаны в публикации заявки на патент US 2008/0231809, полное содержание которой включено в настоящее описание в качестве ссылки.
В одном из вариантов осуществления изобретения функцией реагентных материалов 60, 120 является облегчение определение присутствия и/или концентрации гидроксибутирата, и они включают гидроксибутиратдегидрогеназу. Примеры гидроксибутиратдегидрогеназ включают (но не ограничиваясь только ими) альфа-гидроксибутиратдегидрогеназу, бета- или 3-гидроксибутиратдегидрогеназу и гамма-гидроксибутиратдегидрогеназу. В одном из конкретных вариантов гидроксибутиратдегидрогеназа представляет собой 3-гидроксибутиратдегидрогеназу. В этом варианте осуществления изобретения реагентные материалы 60, 120 включают также кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы. В одном из конкретных вариантов реагентные материалы 60, 120 включают 3-гидроксибутиратдегидрогеназу и одно из таких соединений как карба-NAD и карба-NADP. При создании изобретения неожиданно было установлено, что при использовании вариантов, в которых первый реагентный материал включает гидроксибутиратдегидрогеназу и кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы, обнаружение присутствия и/или концентрации гидроксибутирата может быть завершено в течение или примерно в течение пяти секунд после контактирования тестового элемента с образцом, что в целом соответствует известному в данной области тестированию глюкозы, которое занимает примерно пять секунд. Дополнительные касающиеся указанного детали описаны ниже в разделе «Примеры». Должно быть очевидно, что применение реагентных материалов, при использовании которых требуется более пяти секунд для завершения определения присутствия и/или концентрации гидроксибутирата, также пригодно для тестовых элементов, представленных в настоящем описании.
Кроме того, хотя применение реагентного материала, который включает гидроксибутиратдегидрогеназу и кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы, представлено в настоящем описании применительно к тестовым элементам, обладающим двойной функцией, должно быть очевидно, что возможно также применение указанного реагентного материала в сочетании с однофункциональными тестовыми элементами. Примерами дополнительных форм тестовых элементов, для которых можно применять указанный реагентный материал, являются (но не ограничиваясь только ими) тестовые элементы, описанные в публикации заявки на патент US 2005/0016844 и патенте US 7008799, полное содержание которых включено в настоящее описание в качестве ссылки. Должно быть очевидно, что реагентный материал не нуждается в каких-либо дополнительных ферментах, таких как диафораза, для того чтобы выполнять функцию определения присутствия и/или концентрации гидроксибутирата в варианте, в котором он включает гидроксибутиратдегидрогеназу и кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы. Однако возможно также включение дополнительных ферментов в первый реагентный материал.
Первый реагентный материал может включать также медиатор. Медиатор можно выбирать из любой химической субстанции (как правило, электроактивной), которая может принимать участие в реакционной схеме, включающей фермент, первый аналит и кофермент, и ее продукты реакции с получением поддающегося обнаружению электроактивного реакционного продукта. Как правило, участие медиатора в реакции включает изменение его окислительного состояния (например, восстановление) после взаимодействия с любым одним из компонентов, таких как первый аналит, фермент или кофермент, или субстанцией, представляющей собой реакционный продукт одного из них (например, кофермент, взаимодействующий с другим окислительным состоянием). Целый ряд медиаторов обладают пригодным электрохимическим поведением. Медиатор предпочтительно может также быть стабильным в его окисленной форме, может необязательно отличаться обратимой окислительно-восстановительной электрохимией, может предпочтительно отличаться высокой стабильностью в водных растворах и предпочтительно быстро вступает в реакцию с образованием электроактивного реакционного продукта. Примеры медиаторов включают бензохинон, синь Мелдола, комплексы переходных металлов, такие как феррицианид калия и производные осмия (см. публикацию международной заявки на патент WO 98/35225), и комбинацию феназинового производного и хлорида гексааминорутения (см. патент US 8008037). Первый реагентный материал может включать также соединение на основе нитрозоаналина, которое действует в качестве предшественника медиатора (например, см. патент US 5286362). При этом предшественник медиатора на основе нитрозоаналина расщепляется на обратимые компоненты медиатора, когда он контактирует с содержащим аналит образцом, таким как кровь.
Дополнительные примеры медиаторов и предшественников медиаторов на основе нитрозоаналина включают N-(2-гидроксиэтил)-N'-пара-нитрозофенилпиперазин, N,N-бис(2-гидроксиэтил)-пара-нитрозоанилин, орто-метокси-[N,N-бис(2-гидроксиэтил)]-пара-нитрозоанилин, пара-гидроксинитробензол, N-метил-N'-(4-нитрозофенил)пиперазин, пара-хинондиоким, N,N-диметил-пара-нитрозоанилин, N,N-диэтил-пара-нитрозоанилин, N-(4-нитрозофенил)морфолин, N-бензил-N-(5'-карбоксипентил)-пара-нитрозоанилин, N,N-диметил-4-нитрозо-1-нафтиламин, N,N,3-триметил-4-нитрозоанилин, N-(2-гидроксиэтил)-5-нитрозоиндолин, N,N-бис(2-гидроксиэтил)-3-хлор-4-нитрозоанилин, 2,4-диметоксинитрозобензол, N,N-бис(2-метоксиэтил)-4-нитрозоанилин, 3-метокси-4-нитрозофенол, N-(2-гидроксиэтил)-6-нитрозо-1,2,3,4-тетрагидрохинолин, N,N-диметил-3-хлор-4-нитрозоанилин, N,N-бис(2-гидроксиэтил)-3-фтор-4-нитрозоанилин, N,N-бис(2-гидроксиэтил)-3-метилтио-4-нитрозоанилин, N-(2-гидроксиэтил)-N-(2-(2-метоксиэтокси)этил)-4-нитрозоанилин, N-(2-гидроксиэтил)-N-(3-метокси-2-гидрокси-1 -пропил)-4-нитрозоанилин, N-(2-гидроксиэтил)-N-(3-(2-гидроксиэтокси)-2-гидрокси-1-пропил)-4-нитрозоанилин и N-(2-гидроксиэтил)-N-(2-(2-гидроксиэтокси)этил)-4-нитрозоанилин.
Реагентные материалы 62, 122 включают второй коферментзависимый фермент или субстрат для второго фермента и приемлемый кофермент.Эти компоненты, как правило, растворяют или суспендируют в матриксе. Жидкий тестируемый образец гидратируют или растворяют в матриксе, и аналит диффундирует через матрикс для взаимодействия с одним или несколькими активными компонентами. Приемлемыми ферментами, которые можно включать в реагентные материалы 62, 122, являются например, дегидрогеназы, выбранные из глюкозодегидрогеназы (Е.С.1.1.1.47), лактатдегидрогеназы (Е.С.1.1.1.27, 1.1.1.28), малатдегидрогеназы (Е.С.1.1.1.37), глицериндегидрогеназы (Е.С.1.1,1.6), алкогольдегидрогеназы (Е.С.1.1.1.1), гидроксибутиратдегидрогеназы (HBDH), такой как 3-гидроксибутиратдегидрогеназа или бета-гидроксибутиратдегидро-геназа, альфа-гидроксибутиратдегидрогеназа и гамма-гидроксибутиратдегидро-геназа, сорбитдегидрогеназы и дегидрогеназы аминокислоты, например дегидрогеназы L-аминокислоты (Е.С.1.4.1.5). Другими приемлемыми ферментами являются оксидазы, такие как глюкозооксидаза (Е.С.1.1.3.4) или холестериноксидаза (Е.С.1.1.3.6), или аминотрансферазы, такие как аспартат- или аланинаминотрансфераза, 5'-нуклеотидаза или креатинкиназа. В зависимости от выбранного фермента потенциальные коферменты, пригодные для применения в реагентных материалах 62, 122, включают FAD, NAD, NADP, тио-NAD, тио-NADP и соединение формулы (I) или его соль или необязательно восстановленную форму.
В одном из вариантов осуществления изобретения, в котором функция реагентных материалов 60, 120 заключается в облегчении определения присутствия и/или концентрации гидроксибутирата, функцией реагентных материалов 62, 122 является облегчение определения присутствия и/или концентрации глюкозы, и они включают фермент для обнаружения глюкозы. В конкретном варианте фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу. В этом варианте осуществления изобретения реагентные материалы 62, 122 дополнительно включают кофермент, выбранный из FAD, NAD, NADP и соединения формулы (I) или его соли или необязательно восстановленной формы. Хотя это не обсуждалось ранее, рассматриваются также варианты, в которых реагентные материалы 60 и 62 имеют общий кофермент, например, соединение формулы (I) или его соль или необязательно восстановленную форму, и объединяются с образованием одного слоя реагентов, в результате чего устраняется зазор (пространство) 64. Должно быть очевидно, что представленные в настоящем описании реагентные материалы, предназначенные для определения присутствия и/или концентрации глюкозы, не ограничивают объем изобретения, и что другие формы, предназначенные для этой цели, известны в данной области. Дополнительные примеры реагентых материалов, функцией которых является определение присутствия и/или концентрации глюкозы, включают (но не ограничиваясь только ими) описанные в патенте US 7727467 (указанный выше в настоящем описании) и патенте US 8008037, содержание которого полностью включено в настоящее описание в качестве ссылки. Второй реагентный материал может включать также медиатор. Медиатор можно выбирать из любой химической субстанции (как правило, электроактивной), которая может принимать участие в реакционной схеме, включающей второй фермент, второй аналит и кофермент, и ее продукты реакции с получением подающегося обнаружению электроактивного реакционного продукта. Как правило, участие медиатора в реакции включает изменение его окислительного состояния (например, восстановление) после взаимодействия с любым одним из компонентов, таких как второй аналит, второй фермент или кофермент, или субстанцией, представляющей собой реакционный продукт одного из них (например, кофермент, взаимодействующий с другим окислительным состоянием). Целый ряд медиаторов обладает пригодным электрохимическим поведением. Медиатор предпочтительно может также быть стабильным в его окисленной форме, может необязательно отличаться обратимой окислительно-восстановительной электрохимией, может предпочтительно отличаться высокой растворимостью в водных растворах и предпочтительно быстро вступает в реакцию с образованием электроактивного реакционного продукта. Примеры медиаторов включают бензохинон, синь Мелдола, комплексы переходных металлов, такие как феррицианид калия и производные осмия (см. публикацию международной заявки на патент WO 98/35225), и комбинацию феназинового производного хлорида гексааминорутения (см. патент US 8008037). Второй реагентный материал может включать также соединения на основе нитрозоаналина, которое действует в качестве предшественника медиатора (например, см. патент US 5286362). При этом предшественник медиатора на основе нитрозоаналина расщепляется на обратимые компоненты медиатора, когда он контактирует с содержащим аналит образцом, таким как кровь.
Дополнительные примеры медиаторов и предшественников медиаторов на основе нитрозоаналина включают N-(2-гидроксиэтил)-N'-пара-нитрозофенилпиперазин, N,N-бис(2-гидроксиэтил)-пара-нитрозоанилин, орто-метокси-[N,N-бис(2-гидроксиэтил)]-пара-нитрозоанилин, пара-гидроксинитробензол, N-метил-N'-(4-нитрозофенил)пиперазин, пара-хинондиоким, N,N-диметил-пара-нитрозоанилин, N,N-диэтил-пара-нитрозоанилин, N-(4-нитрозофенил)морфолин, N-бензил-N-(5'-карбоксипентил)-пара-нитрозоанилин, N,N-диметил-4-нитрозо-1-нафтиламин, N,N,3-триметил-4-нитрозоанилин, N-(2-гидроксиэтил)-5-нитрозоиндолин, N,N-бис(2-гидроксиэтил)-3-хлор-4-нитрозоанилин, 2,4-диметоксинитрозобензол, N,N-бис(2-метоксиэтил)-4-нитрозоанилин, 3-метокси-4-нитрозофенол, N-(2-гидроксиэтил)-6-нитрозо-1,2,3,4-тетрагидрохинолин, N,N-диметил-3-хлор-4-нитрозоанилин, N,N-бис(2-гидроксиэтил)-3-фтор-4-нитрозоанилин, N,N-бис(2-гидроксиэтил)-3-метилтио-4-нитрозоанилин, N-(2-гидроксиэтил)-N-(2-(2-метоксиэтокси)этил)-4-нитрозоанилин, N-(2-гидроксиэтил)-N-(3-метокси-2-гидрокси-1-пропил)-4-нитрозоанилин, N-(2-гидроксиэтил)-N-(3-(2-гидроксиэтокси)-2-гидрокси-1-пропил)-4-нитрозоанилин и N-(2-гидроксиэтил)-N-(2-(2-гидроксиэтокси)этил)-4-нитрозоанилин.
Реагентные материалы могут включать также широкое разнообразие адъювантов для улучшения их различных свойств или характеристик (например, см. патент US 7749437, указанный выше). Например, реагентные материалы 60, 62 и 120, 122 могут включать материалы, облегчающие их нанесение на соответствующие субстраты 16, 114, и улучшающие их адгезию к ним или повышающие скорость гидратации реагентных материалов образцом жидкости. Кроме того, реагентные материалы могут включать компоненты, выбранные для улучшения физических свойств образовавшегося высушенного реагентного слоя и поглощения жидкого тестируемого образца, предназначенного для анализа. Примеры адъювантов, которые можно применять в сочетании с реагентными материалами, включают загустители, модуляторы вязкости, пленкообразователи, стабилизаторы, буферы, детергенты, гелеобразователи, наполнители, распрямители для пленок, красители и агенты, обеспечивающие тиксотропию.
Примерами загустителей, которые можно включать в реагентные материалы, являются (но не ограничиваясь только ими) (1) крахмалы, камеди (например, пектин, гуаровая камедь, камедь рожкового дерева (семена кэроба), коньячная камедь, ксантановая камедь, альгинаты и агар), казеин, желатин и фикоколлоиды; (2) целлюлоза и полусинтетические производные целлюлозы (карбоксиметилцеллюлоза, метилцеллюлоза, гидроксиметилцеллюлоза, гидроксиэтилцеллюлоза, метилгидроксиэтилцеллюлоза); (3) поливиниловый спирт и карбоксивинилаты; и (4) бентонит, силикаты и коллоидный кремнезем. Более конкретные варианты загустителей включают комбинацию ксантановой камеди, поступающей в продажу под товарным знаком Keltrol F фирмы CP Kelco US, Inc., и карбоксиметилцеллюлозы, поступающей в продажу под товарным знаком AQUALON® CMC 7F РН фирмы Hercules Inc., Aqualon Division.
Пленкообразователи и тиксотропные агенты, которые можно включать в реагентные материалы, включают полимеры и кремнезем. Один из более конкретных тиксотропных агентов включает кремнезем, поступающий в продажу под товарным знаком Kieselsaure Sipemate FK 320 DS фирмы Degussa AG, а более конкретный пленкообразователь включает поливинилпирролидон, поступающий в продажу под товарным знаком поливинилпирролидон Kollidon 25, фирмы BASF, и дисперсию поливинилпропионата.
Стабилизаторы для ферментов в реагентных материалах можно выбирать из сахаридов и одно или двухосновных жирных кислот.Более специфические стабилизаторы включают трегалозу, поступающую в продажу под товарным знаком дигидрат D-(+)-трегалозы фирмы Sigma Chemical Co., и сукцинат натрия.
Примерами детергентов, которые можно включать в реагентные материалы, являются (но не ограничиваясь только ими) водорастворимые мыла, а также водорастворимые синтетические поверхностно-активные вещества, такие как соли щелочных, щелочноземельных металлов или необязательно замещенные аммониевые соли высших жирных кислот, например олеиновой или стеариновой кислоты, смеси встречающихся в естественных условиях жирных кислот, например, из кокосового или талового масла, жирные сульфаты, эфиры сульфоновых кислот, соли алкилсульфоновых кислот, тауриновые соли жирных кислот, амиды жирных кислот и сложные эфиры амидов. Более специфические виды детергентов включают сложный эфир амида, н-октаноил-N-метилглюкамид, поступающий в продажу под товарным знаком Mega-8 фирмы Dojindo Molecular Technologies, Inc., и соль жирной кислоты, натриевую соль N-метилолеилтаурата, поступающую в продажу под товарным знаком Geropon Т77 фирмы Rhodia НРСII (Home, Personal Care and Industrial Ingredients).
В одном из вариантов реагентные материалы приготавливают в форме в виде вязкого раствора, который включает загустители и тиксотропные агенты для улучшения физических свойств. Выбирают такие загустители, чтобы они создавали густой жидкий матрикс, в котором гомогенно диспергированы остальные компоненты. Кроме того, загустители и тиксотропные агенты ингибируют жидкий материал или материал в виде полупасты от растекания или распространения по поверхности субстратов 16, 114 после нанесения и до высушивания. После отложения реагентных материалов они быстро высыхают с образованием легко гидратируемого матрикса.
Как указано выше, при создании изобретения неожиданно было установлено, что определение присутствия и/или концентрации гидроксибутирата можно завершать в течение или примерно в течение пяти секунд после контактирования тестового элемента с образцом в формах, в которых первый реагентный материал включает гидроксибутиратдегидрогеназу и кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы. Согласно существующему уровню техники устройства для тестирования глюкозы должны завершать определение присутствия и/или концентрации глюкозы в течение или примерно в течение 5 секунд после приведения в контакт тестового элемента с образцом. В патенте US 8008037 описана одна (но не ограничиваясь только ею) форма для тестирования глюкозы, которая обеспечивает определение присутствия и/или концентрации глюкозы в указанных временных рамках. Другие формы (но не ограничиваясь только ими) для тестирования глюкозы, которые обеспечивают определение присутствия и/или концентрации глюкозы в указанных временных рамках, описаны в патентах US 7276146 и US 7276147, полное содержание которых включено в настоящее описание в качестве ссылки. Однако должно быть очевидно, что известны и могут применяться в тестовых элементах, представленных в настоящем описании, и другие реагентные материалы, которые обеспечивают определение присутствия и/или концентрации глюкозы в указанных или других временных рамках.
В свете вышеизложенного должно быть очевидно, что определение присутствия и/или концентрации гидроксибутирата и глюкозы может быть завершено в течение пяти секунд после приведения в контакт тестового элемента с образцом, когда тестовый элемент включает первый реагентный материал, который содержит гидроксибутиратдегидрогеназу и кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы, и второй реагентный материал, пригодный для определения глюкозы и имеющий соответствующий состав. Однако должно быть очевидно, что возможны также варианты периода времени, необходимого для завершения определения гидроксибутирата и глюкозы с помощью тестовых элементов, и они зависят среди прочего, например, от конкретного состава реагентных материалов. В одном из вариантов, например, определение гидроксибутирата и глюкозы завершается в пределах 10 секунд после контактирования тестового элемента с образцом. В другом варианте определение гидроксибутирата и глюкозы завершается в пределах 7,5 секунд после контактирования тестового элемента с образцом. Должно быть очевидно также, что период времени, необходимый для завершения определения гидроксибутирата и определения глюкозы, может быть различным. Например, в одном или нескольких из указанных выше или других вариантов определение гидроксибутирата завершается в пределах 4 секунд до или после завершения определения глюкозы. В другом варианте определение гидроксибутирата завершается в пределах 2 секунд до или после завершения определения глюкозы. В следующем варианте определение гидроксибутирата завершается одновременно или примерно одновременно с завершением определения глюкозы. Однако должно быть очевидно, что под объем изобретения подпадают другие вариации временных рамок завершения определения гидроксибутирата и глюкозы.
Примеры
Приведенные ниже примеры приведены с целью иллюстрации и не предусматривается, что описанное в данном документе изобретение ограничено только вариантами осуществления изобретения, которые описаны в этих примерах.
Приготовление реагентных материалов
Реагентный материал, указанный на Фиг. 6
Получали маточный буферный раствор путем добавления 7,344 г натриевой соли MOPS, 0,125 г Triton™ Х-100 (неионный детергент фирмы Sigma-Aldrich Corporation, Сент-Луис, шт. Миссури), 2,400 г трегалозы и 2,026 г гексагидрата сукцината натрия в 400 мл дважды дистиллированной воды и доводили значение рН раствора до 8,14. Этот раствор вносили в 500-миллилитровую мерную колбу и разводили дважды дистиллированной водой с получением 500 мл раствора.
Получение полимерного раствора буфер/ Natrosol®/ПЭО (полиэтиленоксид) завершали путем объединения 396 г начального буферного раствора с 2 г полиэтиленоксида (300К) и 2 г Natrosol® 250М (неионный водорастворимый полимер гидроксиэтилцеллюлозы фирмы Ashland, Inc., Ковингтион, шт. Кентукки). Смесь перемешивали в течение ночи перед использованием.
Реагентный материал нитрозоанилин/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 5,0595 г маточного раствора буфера/полимера: а) в контейнер добавляли 0,0415 г замещенного нитрозоанилинового производного (NA 1144 фирмы Roche Diagnostics, Inc.), матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,7; b) добавляли 0,0692 г свободной кислоты карба-NAD в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора нитрозоанилина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и с) добавляли в стакан 0,2134 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 7
Получали маточный буферный раствор путем добавления 9,086 г Трис-основания, 0,125 г Triton™ Х-100, 0,625 г Tergitol® 15-S-9 (неионное поверхностно-активное вещество фирмы The Dow Chemical Company, Минлэнд, шт. Мичиган), 2,400 г трегалозы и 2,026 г гексагидрата сукцината натрия в 400 мл дважды дистиллированной воды и доводили значение рН раствора до 7,95. Этот раствор вносили в 500-миллилитровую мерную колбу и разводили дважды дистиллированной водой с получением 500 мл раствора.
Получение полимерного раствора буфер/Natrosol®/ПЭО завершали путем объединения 396 г начального буферного раствора с 2 г полиэтиленоксида (300К) и 2 г Natrosol® 250М. Смесь перемешивали в течение ночи перед использованием. Реагентный материал гексааминорутений/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 4,048 г маточного раствора буфера/полимера: а) 0,0619 г хлорида гексааминорутения и b) 0,0034 г 1-(3-карбоксипропилокси)-5-этилфеназина добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,9; и с) добавляли 0,0791 г свободной кислоты карба-NAD в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора гексааминорутения/феназина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,24. Добавляли в стакан 0,0862 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 8 и 9
Реагентный материал гексааминорутений/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 4,048 г маточного полимерного раствора Трис-буфер/ПЭО/Natrosol®, описанного выше, в сочетании с реагентным материалом, указанным на Фиг. 7: а) 0,062 г хлорида гексааминорутения и b) 0,003 г 1-(3-карбоксипропилокси)-5-этилфеназина добавляли в стакан и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,9; и с) добавляли 0,079 г свободной кислоты карба-NAD в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора гексааминорутения/феназина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,24. Затем в контейнер добавляли 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 10
Получали маточный буферный раствор путем добавления 9,086 г Трис-основания, 0,125 г Triton™ Х-100, 0,625 г Tergitol® 15-S-9, 2,40 г трегалозы и 2,026 г гексагидрата сукцината натрия в 400 мл дважды дистиллированной воды и доводили значение рН раствора до 7,95. Этот раствор вносили в 500-миллилитровую мерную колбу и разводили дважды дистиллированной водой с получением 500 мл раствора.
Получение полимерного раствора буфер/Kollidon® VA 64 завершали путем объединения 392 г начального буферного раствора с 8 г Kollidon® VA 64 (сополимер винилпирролидона-винилацетата фирмы BASF Corporation, Флорхам Парк, шт. Нью-Джерси). Смесь перемешивали в течение ночи перед использованием.
Реагентный материал нитрозоанилин/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 6,071 г маточного раствора буфер/полимер: а) 0,0600 г необработанного дымящего кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс) и b) 0,050 г замещенного нитрозоанилинового производного (NA 1144 фирмы Roche Diagnostics, Inc., Индиаполис, шт. Индиана) добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,9; с) 0,069 г свободной кислоты карба-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора нитрозоанилина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и d) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 11
Реагентный материал гексааминорутений/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 4,049 г маточного раствора буфера и полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0.040 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс), b) 0,062 г хлорида гексааминорутения и с) 0,003 г 1-(3-карбоксипропилокси)-5-этилфеназина добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,9; d) 0,079 г свободной кислоты карба-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора гексааминорутения/феназина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и е) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 12
Реагентный материал нитрозоанилин/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 6,074 г маточного раствора буфера/полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,060 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс) и b) 0,050 г замещенного нитрозоанилинового производного (NA 1144 фирмы Roche Diagnostics, Inc., Индиаполис, шт. Индиана) добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,8; с) 0,069 г свободной кислоты карба-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора нитрозоанилина и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и е) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 13
Реагентный материал гексааминорутений/тио-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 6,074 г маточного раствора буфера и полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,060 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс), b) 0,093 г хлорида гексааминорутения и с) 0,005 г 1-(3-карбоксипропилокси)-5-этилфеназина добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,9; d) 0,079 г свободной кислоты тио-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора гексааминорутения/феназина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и е) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 14
Реагентный материал нитрозоанилин/тио-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый скоростной смесительный стакан, содержащий 6,074 г маточного раствора буфера/полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,060 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс) и b) 0,050 г замещенного нитрозоанилинового производного (NA 1144 фирмы Roche Diagnostics, Inc., Индиаполис, шт. Индиана) добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,8; с) 0,079 г свободной кислоты тио-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора нитрозоанилина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и d) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин. Реагентный материал, указанный на Фиг. 15
Реагентный материал гексааминорутений/карба-NADP получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 6,074 г маточного раствора буфера/полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,060 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс), b) 0,093 г хлорида гексааминорутения и с) 0,005 г 1-(3-карбоксипропилокси)-5-этилфеназина добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,9; с) 0,076 г свободной кислоты карба-NADP добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора гексааминорутения/феназина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и d) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 16
Реагентный материал нитрозоанилин/тио-NADP получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 6,074 г маточного раствора буфера/полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,060 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс) и b) 0,050 г замещенного нитрозоанилинового производного (NA 1144 фирмы Roche Diagnostics, Inc., Индиаполис, шт. Индиана) добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,8; с) 0,076 г свободной кислоты тио-NADP добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора нитрозоанилина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и d) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 17
Реагентный материал феррицианид/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 4,049 г маточного раствора буфера/полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,040 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс) и b) 0,026 г феррицианида калия добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,8; с) 0,076 г свободной кислоты карба-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора феррицианида, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и d) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Реагентный материал, указанный на Фиг. 18
Реагентный материал нитрозоанилин/карба-NAD получали путем последовательного добавления следующих ингредиентов в 20-миллилитровый центрифужный смесительный стакан, содержащий 6,074 г маточного раствора буфера/полимера Трис/Kollidon®, описанного выше, в сочетании с реагентным материалом, описанным на Фиг. 10: а) 0,060 г необработанного пирогенного кремнезема (Cabosil®, фирма Cabot Corporation, Бостон, шт. Массачуссетс) и b) 0,050 г замещенного нитрозоанилинового производного (NA 1144 фирмы Roche Diagnostics, Inc., Индиаполис, шт. Индиана) добавляли в стакан, матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,8; с) 0,079 г свободной кислоты карба-NAD добавляли в 10-миллилитровый центрифужный смесительный стакан, содержащий 3 мл раствора нитрозоанилина, и матрикс перемешивали в течение 1 мин при 24000 об/мин и значение рН доводили до 7,2; и d) 0,259 г бета-гидроксибутиратдегидрогеназы из Alcaligenes faecalis добавляли в стакан и осуществляли скоростное перемешивание в течение 2 мин при 24000 об/мин.
Получение тест-полосок
Для получения тест-полосок использовали платы для глюкометра марки ACCU-CHECK®Aviva с электродами, оснащенными спейсером и капиллярами. По 1,5 мкл описанных выше реагентных материалов вносили в каждый канал капиллярного электрода, используя распределительную систему серий PixSys™ SQ (фирма Cartesian Technologies Irvine California), и сушили в течение 1,5 мин при 45°С. Высушенные платы хранили в сухой атмосфере в течение ночи, и полоски гидрофильной наносимой на поверхность фольги вручную наслаивали на разделительный слой поверх капилляра. Затем платы разрезали на индивидуальные сенсоры и хранили в сушильных шкафах до использования.
Приготовление тестируемых растворов
Маточный раствор фосфатного буфера приготавливали путем добавления 0,1829 г первичного кислого фосфата калия, 0,2007 г вторичного кислого фосфата калия и 2,7956 г хлорида калия в 200 мл дважды дистиллированной воды и доводили значение рН раствора до 7,00. Этот раствор вносили в 250-миллилировую мерную колбу и разводили дважды дистиллированной водой с получением 250 мл раствора.21-кратный маточный раствор гидроксибутирата приготавливали путем добавления 1,3372 г натриевой соли гидроксибутирата в 40 мл раствора фосфатного буфера. Раствор вносили в 50-миллилировую мерную колбу и разводили раствором фосфатного буфера до 50 мл. Полученный маточный раствор серийно разводили фосфатным буфером с получением 11-кратных маточных растворов гидроксибутирата.
Конечные тестируемые растворы получали путем добавления в 1 мл либо фосфатного буфера, либо крови 0,05 мл тестируемых маточных растворов.
Кинетика зависимости ответа от дозы
Образцы цельной крови или физиологического раствора, содержащие гидроксибутират в различных концентрациях (мМ), оценивали с помощью тест-полосок, приготовленных согласно описанному выше методу. Требуемый потенциал (222 мВ для полосок с гексааминорутением и 450 мВ для полосок с нитрозоанилином) прилагали после контактирования образца с полоской. Общее время анализа составляло 6 секунд. В качестве конечной точки анализа принимали 0,5 секунд (Фиг. 7) и 5 секунд (Фиг. 9 и 10) после контактирования тест-полоски с образцом.
Конечная точка зависимости ответа от дозы
Образцы цельной крови или физиологического раствора, содержащие гидроксибутират в различных концентрациях (от 0 до 10мМ), оценивали с помощью тест-полосок, приготовленных согласно описанному выше методу. Анализ состоял из 4,5-секундного запаздывания после контактирования образца с тест-полоской с последующим наложением потенциала 450 мВ для полосок с нитрозоанилином и 222 мВ для полосок с гексааминорутением в течение 6 секунд после периода запаздывания. В качестве конечной точки анализа принимали момент времени 5 секунд после контактирования тест-полоски с образцом.
Хотя это не обсуждалось ранее, должно быть очевидно, что взаимосвязь между концентрацией гидроксибутирата и измеренным током позволяет использовать приведенные в качестве примера реагентные материалы для анализа гидроксибутирата.
Хотя изобретение было подробно проиллюстрировано и описано с помощью чертежей и представленного выше описания, их следует рассматривать как иллюстративные и не имеющие ограничительного характера, следует иметь в виду, что представлены и описаны лишь некоторые варианты осуществления изобретения, и что все изменения и модификации, не отклоняющиеся от сущности изобретения, следует рассматривать как подпадающие под его объем. Следует понимать, что хотя использование таких слов, как предпочтительный, предпочтительно, предпочитаемый или более предпочтительный в представленном выше описании указывает на то, что охарактеризованный таким путем признак может быть более желательным, тем не менее, он может не являться необходимым, и варианты осуществления изобретения, в которых он отсутствует, следует рассматривать как подпадающие под объем изобретения, где объем определяется представленной ниже формулой изобретения. При изучении формулы изобретения следует понимать, что когда используется упоминание понятие в неопределенной форме касательно единственного и множественного числа, и такие слова как «по меньшей мере один» или «по меньшей мере одна часть», то это не означает намерения ограничить пункт формулы изобретения только одним элементом, если в пункте специально не указано иное. Когда используется выражение «по меньшей мере часть» и/или «часть», то элемент может включать часть и/или весь элемент, если специально не указано иное.
Ниже представлены различные варианты осуществления настоящего изобретения.
1. Тестовый элемент, созданный для определения первого и второго аналитов, содержащий:
- первый коферментзависимый фермент или субстрат для первого фермента;
- второй коферментзависимый фермент или субстрат для второго фермента; и
- кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I):
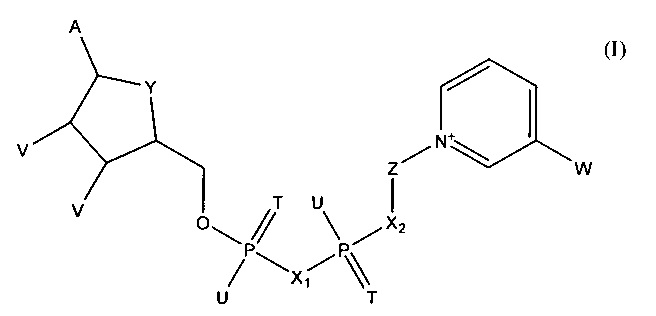
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, О или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы.
2. Тестовый элемент согласно 1-ому варианту осуществления изобретения в котором первый аналит представляет собой гидроксибутират и первый фермент представляет собой гидроксибутиратдегидрогеназу.
3. Тестовый элемент согласно 2-ому варианту осуществления изобретения в котором гидроксибутиратдегидрогеназа представляет собой 3-гидроксибутиратдегидрогеназу.
4. Тестовый элемент согласно 2-ому варианту осуществления изобретения в котором второй фермент представляет собой дегидрогеназу, выбранную из группы, состоящей из глюкозодегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, глицериндегидрогеназы, алкогольдегидрогеназы, сорбитдегидрогеназы и дегидрогеназы аминокислоты, включая дегидрогеназу L-аминокислоты.
5. Тестовый элемент согласно 2-ому варианту осуществления изобретения, в котором второй аналит представляет собой глюкозу и второй фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу.
6. Тестовый элемент согласно 5-ому варианту осуществления изобретения, в котором кофермент представляет собой соединение формулы (I)
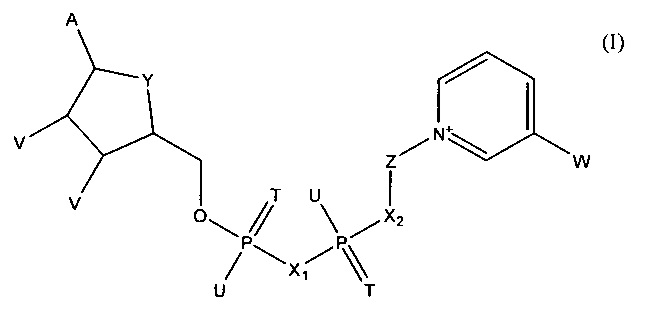
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
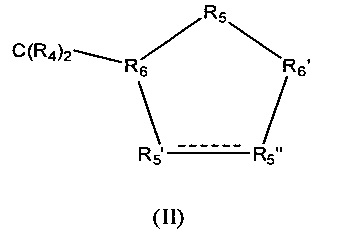
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
7. Тестовый элемент согласно 5-ому варианту осуществления изобретения, в котором кофермент представляет собой соединение формулы (I)
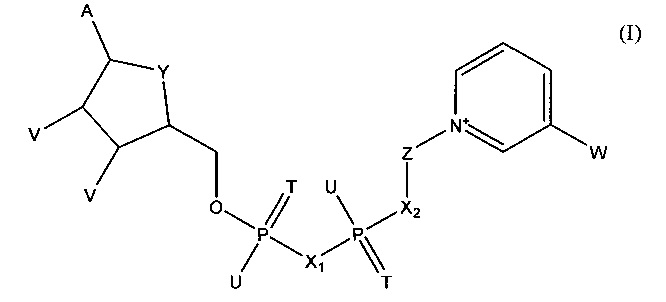
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
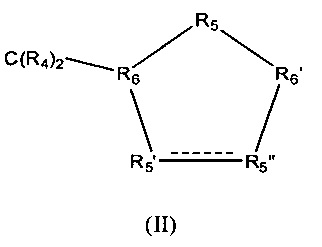
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
8. Тестовый элемент согласно 5-ому варианту осуществления изобретения, в котором кофермент представляет собой тио-NAD.
9. Тестовый элемент согласно 5-ому варианту осуществления изобретения, в котором кофермент представляет собой тио-NADP.
10. Тестовый элемент согласно 1-ому варианту осуществления изобретения, дополнительно содержащий первый реагентный материал, где первый реагентный материал включает первый фермент или субстрат для первого фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы.
11. Тестовый элемент согласно 10-ому варианту осуществления изобретения, дополнительно содержащий второй реагентный материал, где второй реагентный материал включает второй фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из FAD, NAD, NADP и соединения формулы (I) или его соли или необязательно восстановленной формы.
12. Тестовый элемент согласно 11-ому варианту осуществления изобретения, дополнительно содержащий тест-полоску, созданную таким образом, чтобы она содержала первый и второй реагентные материалы.
13. Тестовый элемент согласно 12-ому варианту осуществления изобретения, в котором тест-полоска включает первую электродную систему, ассоциированную с первым реагентным материалом, и вторую электродную систему, ассоциированную со вторым реагентным материалом.
14. Тестовый элемент согласно 10-ому варианту осуществления изобретения, в котором первый реагентный материал дополнительно содержит один из таких ингредиентов как нитрозоанилин, феррицианид калия и комбинацию феназинового производного и хлорида гексааминорутения.
15. Реагентный материал, содержащий:
- 3-гидроксибутиратдегидрогеназу; и
- кофермент, представляющий собой соединение формулы (I):
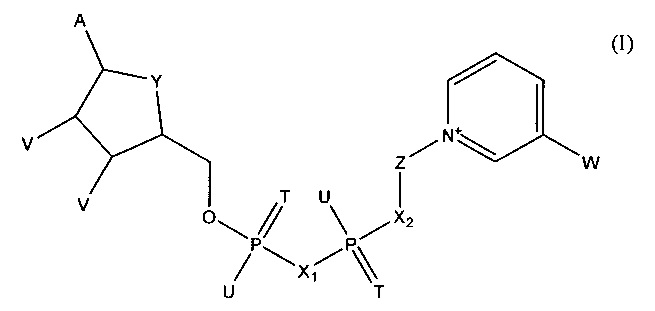
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
Х1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соль или необязательно восстановленную форму.
16. Реагентный материал согласно 15-ому варианту осуществления изобретения, в котором кофермент представляет собой соединение формулы (I)
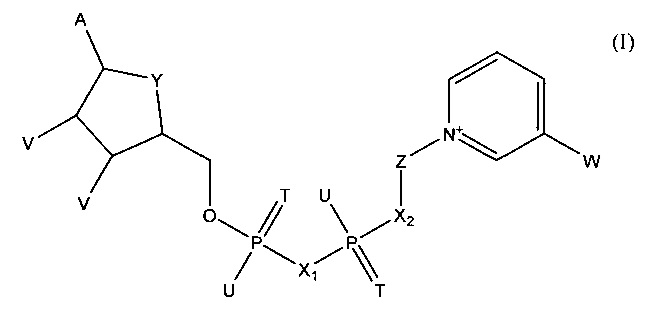
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает насыщенное карбоциклическое 5-членное кольцо общей формулы (II)
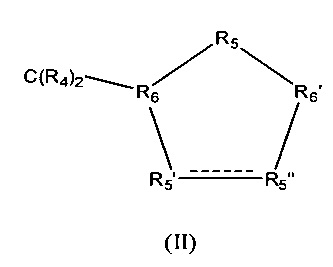
в которой простая связь присутствует между R5' и R5" и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
17. Реагентный материал согласно 15-ому варианту осуществления изобретения, в котором кофермент представляет собой соединение формулы (I)
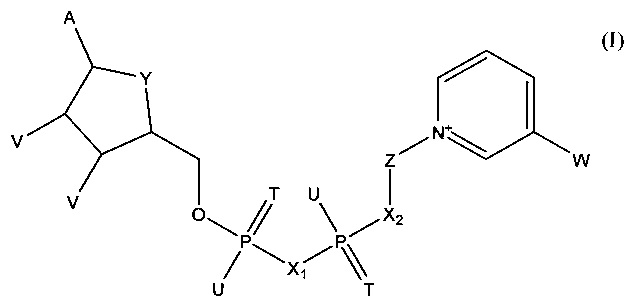
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает насыщенное карбоциклическое 5-членное кольцо общей формулы (II)
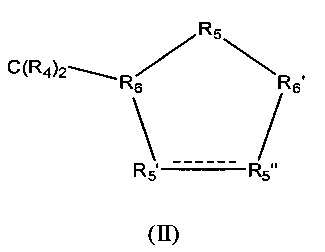
в которой между R5' и R5" присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5" обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
18. Реагентный материал согласно 15-ому варианту осуществления изобретения, дополнительно содержащий один из таких ингредиентов как нитрозоанилин, феррицианид калия и комбинацию феназинового производного и хлорида гексааминорутения.
19. Тестовый элемент, включающий тест-полоску, содержащую первый реагентный материал согласно 15-ому варианту осуществления изобретения, предназначенный для определения первого аналита.
20. Тестовый элемент согласно 19-ому варианту осуществления изобретения, в котором тест-полоска дополнительно содержит второй реагентный материал для определения второго аналита.
21. Тестовый элемент согласно 20-ому варианту осуществления изобретения, в котором второй реагентный материал включает фермент дегидрогеназу, выбранный из группы, состоящей из глюкозодегидрогеназы, лактатдегидрогеназы, малатдегидрогеназы, глицериндегидрогеназы, алкогольдегидрогеназы, сорбитдегидрогеназы и дегидрогеназы аминокислоты, включая дегидрогеназу L-аминокислоты.
22. Тестовый элемент согласно 21-ому варианту осуществления изобретения, в котором второй реагентный материал дополнительно содержит кофермент, выбранный из группы, состоящей из FAD, NAD, NADP и соединения формулы (I):
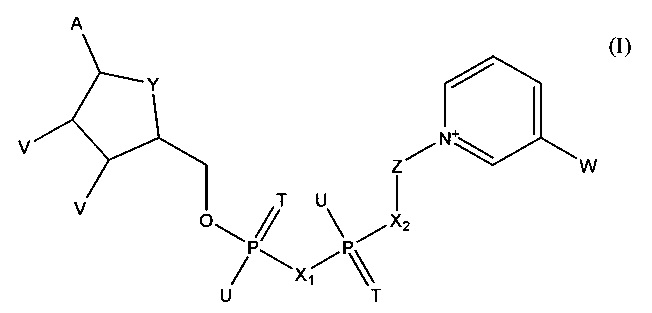
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Сl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы.
23. Тестовый элемент согласно 20-ому варианту осуществления изобретения, в котором тест-полоску создают для электрохимического определения первого и второго аналитов.
24. Способ определения первого и второго аналитов в образце, включающий стадии:
- получения тестового элемента согласно 1-ому варианту осуществления изобретения;
- контактирования тестового элемента с образцом;
- определения первого аналита; и
- определения второго аналита.
25. Способ согласно 24-ому варианту осуществления изобретения, в котором первый аналит представляет собой гидроксибутират, а второй аналит представляет собой глюкозу.
26. Способ согласно 25-ому варианту осуществления изобретения, в котором стадии определения первого аналита и определения второго аналита осуществляют одновременно.
27. Способ согласно 25-ому варианту осуществления изобретения, в котором стадии обнаружения первого аналита и определения второго аналита завершают в пределах пяти секунд после контактирования тестового элемента с образцом.
28. Способ, включающий:
- получение тестового элемента, созданного для определения уровней глюкозы и кетонов в образце;
- контактирование тестового элемента с образцом; и
- определение уровней глюкозы и кетонов в образце в пределах 7,5 секунд после контактирования тестового элемента с образцом.
29. Способ согласно 28-ому варианту осуществления изобретения, в котором тестовый элемент включает первый реагентный материал, предназначенный для определения уровня глюкозы, и второй реагентный материал, предназначенный для определения уровня кетонов.
30. Способ согласно 29-ому варианту осуществления изобретения, в котором второй реагентный материал включает гидроксибутиратдегидрогеназу.
31. Способ согласно 28-ому варианту осуществления изобретения, в котором стадию определения уровней глюкозы и кетонов в образце завершают в пределах 5 секунд после контактирования тестового элемента с образцом.
32. Способ согласно 28-ому варианту осуществления изобретения, в котором различие в продолжительности стадий определения уровней глюкозы и кетонов находится в пределах 2 секунд.
33. Способ согласно 28-ому варианту осуществления изобретения, в котором образец содержит кровь.
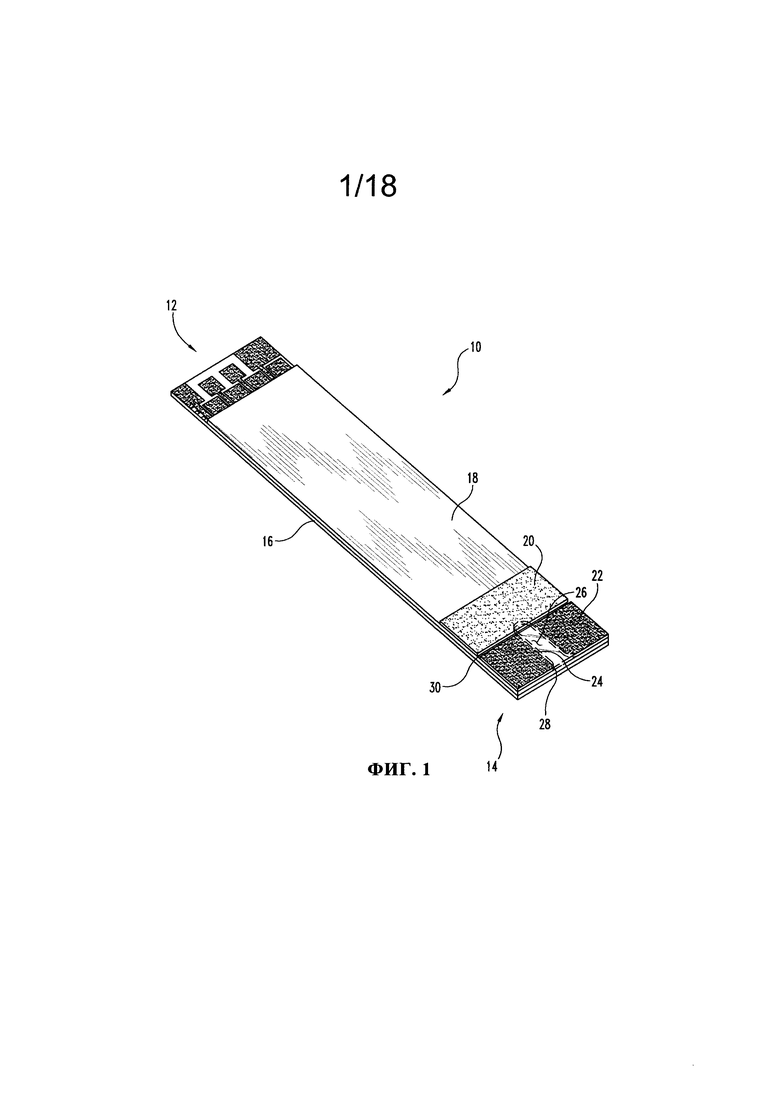
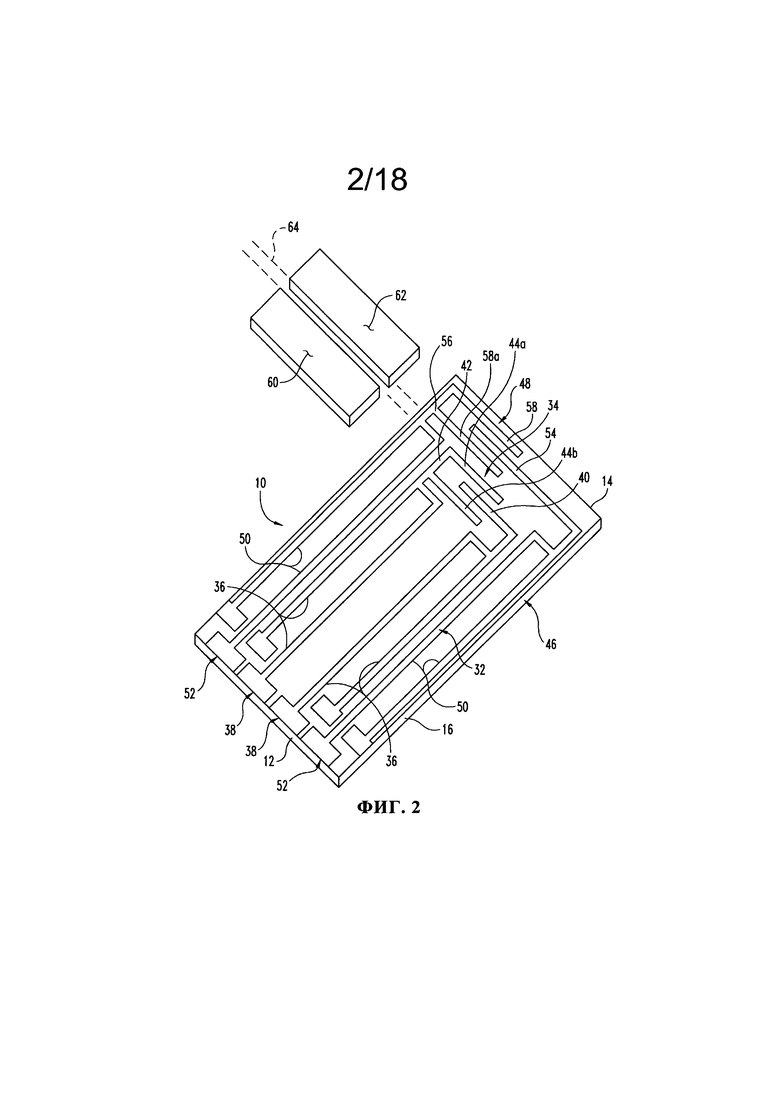
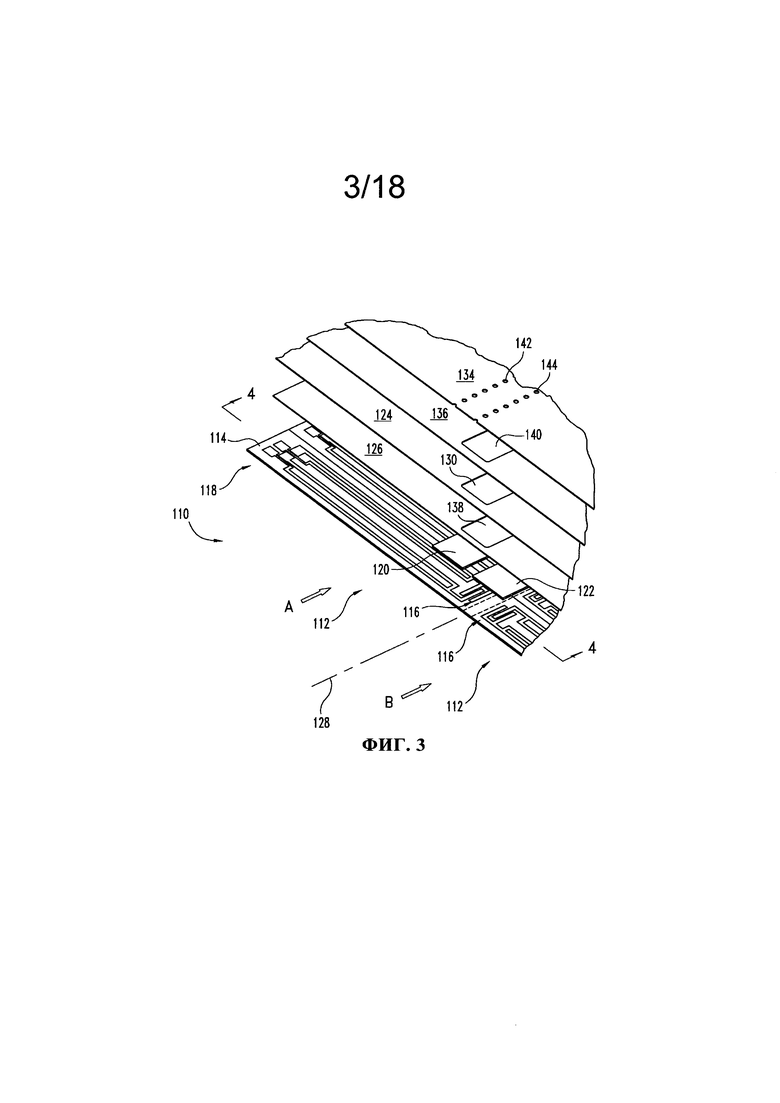
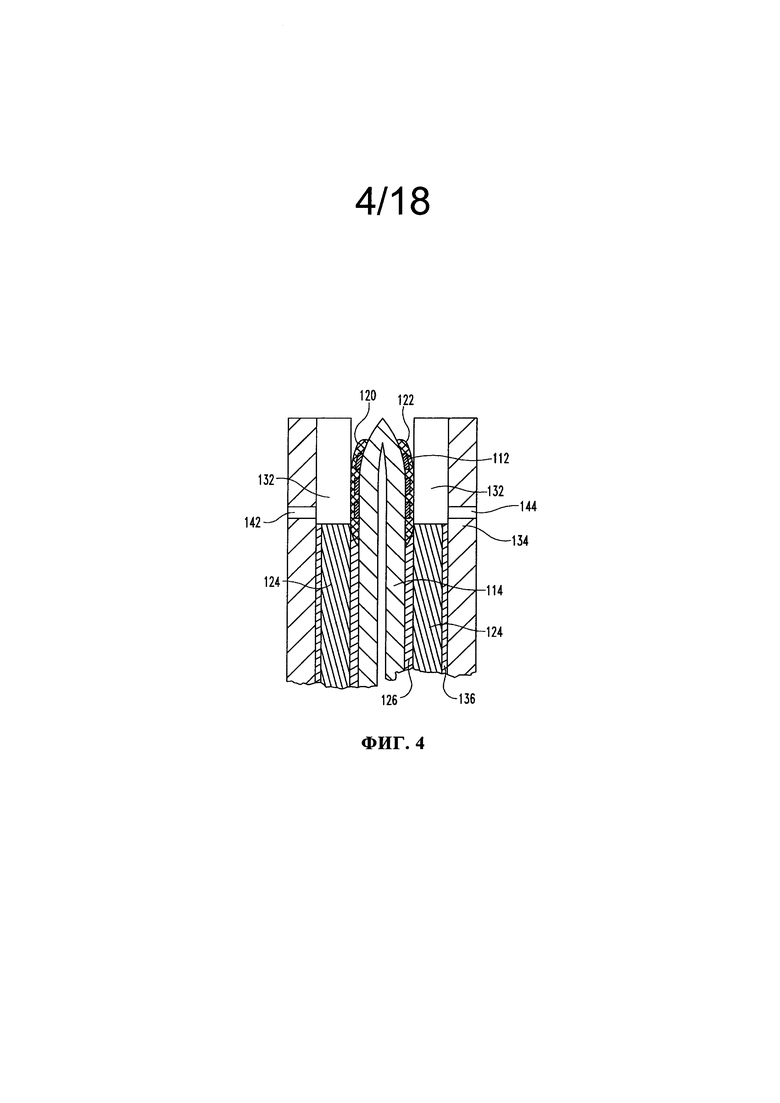
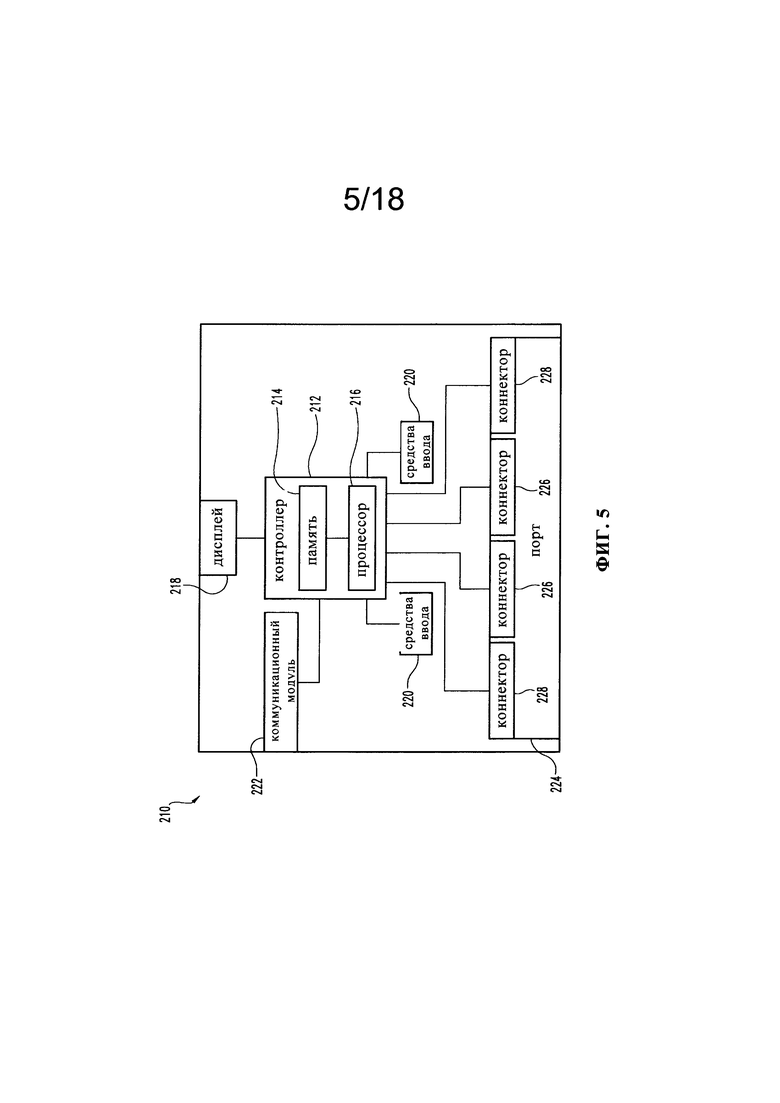




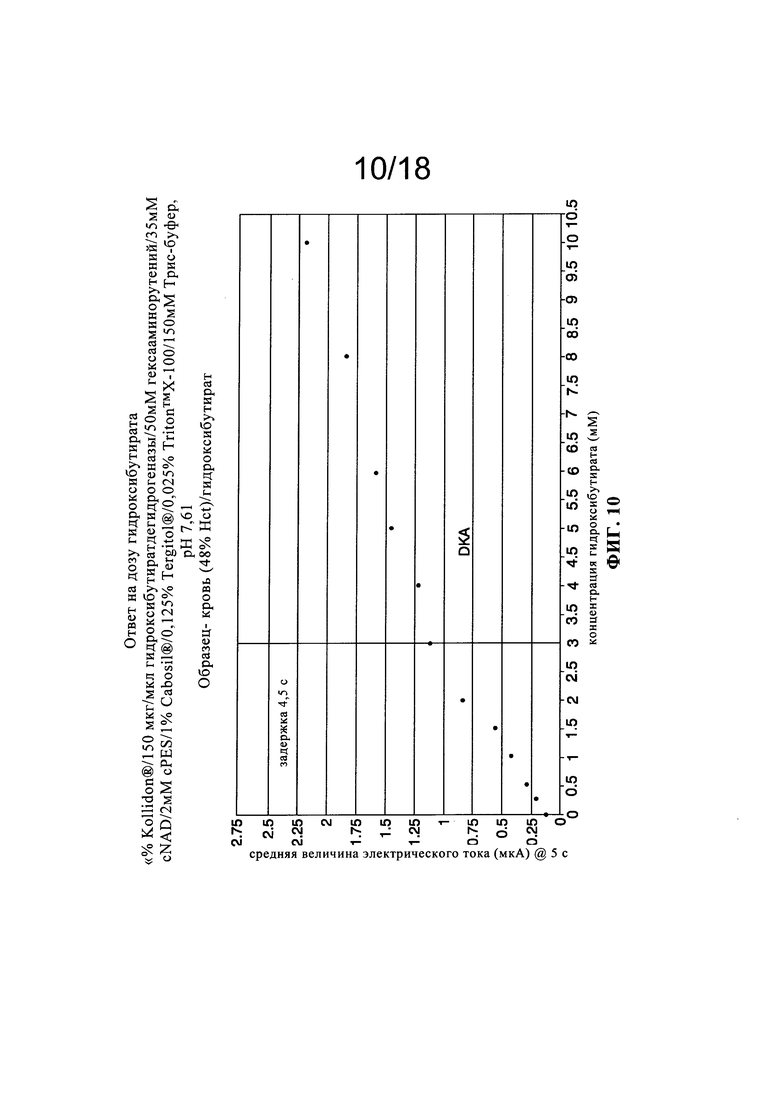


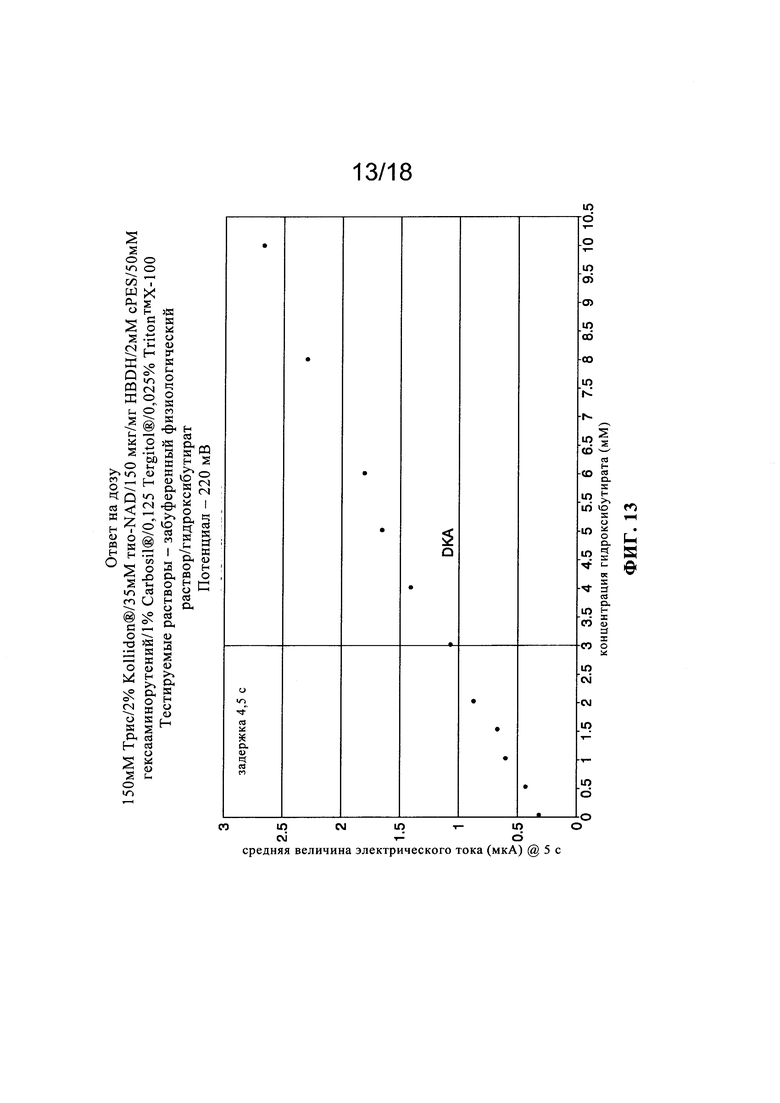





Группа изобретений относится к области биохимии. Предложен тестовый элемент для определения гидроксибутирата и глюкозы, содержащий первый коферментзависимый фермент или субстрат для первого фермента (гидроксибутиратдегидрогеназу), второй коферментзависимый фермент или субстрат для второго фермента (глюкозодегидрогеназу или глюкозооксидазу), кофермент, выбранный из тио-NAD, тио-NADP и соединения формулы (I). Предложен реагентный материал для определения гидроксибутирата, содержащий 3-гидроксибутиратдегидрогеназу и кофермент, представляющий собой тио-NAD, тио-NADP, карба-NAD, карба-NADP. Предложен тестовый элемент, содержащий тест-полоску для электрохимического определения первого и второго аналитов, содержащую указанный первый реагентный материал для определения гидроксибутирата и второй реагентный материал для определения глюкозы. Предложен способ определения уровней глюкозы и кетонов в образце биологической жидкости организма с использованием вышеуказанных тестовых элементов. Группа изобретений обеспечивает быстрое (до 10 секунд) и одновременное определение аналитов – глюкозы и гидроксибутирата в образце, что повышает удобства и улучшает безопасность для пользователя при, например, анализе на глюкозу и кетоны крови. 4 н. и 20 з.п. ф-лы, 18 ил., 16 пр.
1. Тестовый элемент, созданный для определения первого аналита, который представляет собой гидроксибутират, и второго аналита, который представляет собой глюкозу, содержащий:
- первый коферментзависимый фермент или субстрат для первого фермента, где первый фермент представляет собой гидроксибутиратдегидрогеназу;
- второй коферментзависимый фермент или субстрат для второго фермента, где второй фермент представляет собой глюкозодегидрогеназу или глюкозооксидазу; и
- кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I)
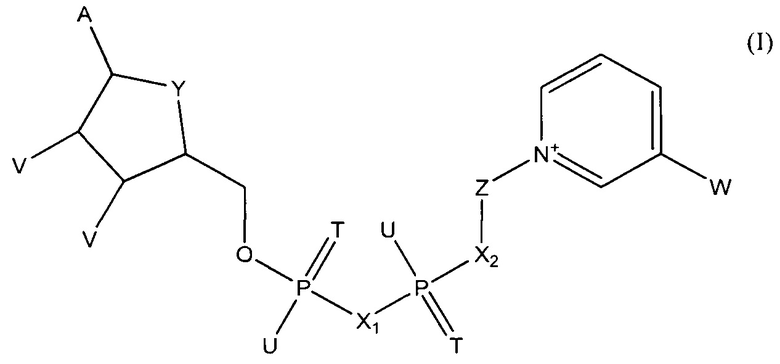
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
X1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Cl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли или необязательно восстановленной формы.
2. Тестовый элемент по п.1, в котором гидроксибутиратдегидрогеназа представляет собой 3-гидроксибутиратдегидрогеназу.
3. Тестовый элемент по п.1, в котором кофермент представляет собой соединение формулы (I)
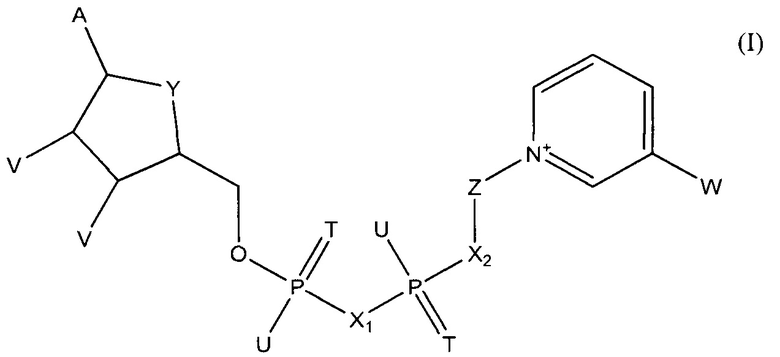
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в каждом случае обозначает ОН,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
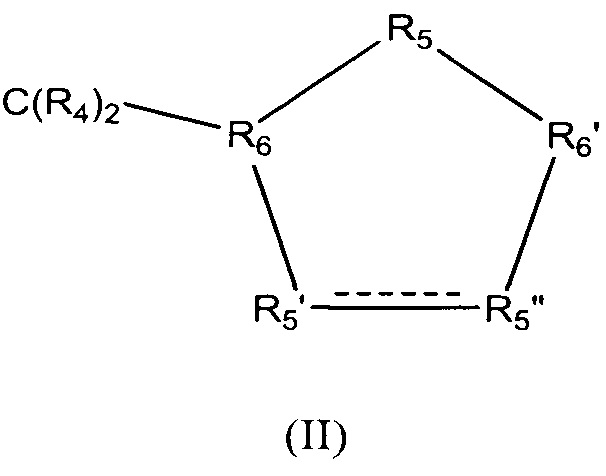
в которой между R5' и R5'' присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5'' обозначает СНОН,
R5 обозначает CR42.
R6 обозначает СН и
R6' обозначает СН.
4. Тестовый элемент по п.1, в котором кофермент представляет собой соединение формулы (I)
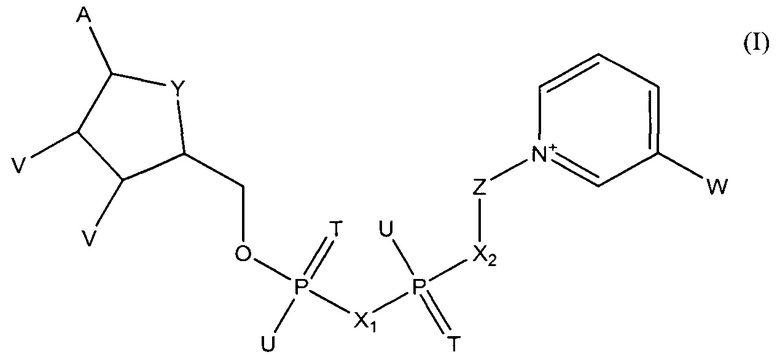
в которой
А обозначает аденин,
Т в каждом случае обозначает О,
U в каждом случае обозначает ОН,
V в первом случае обозначает ОН, а во втором случае обозначает фосфатную группу,
W обозначает CON(R)2, где R обозначает Н,
X1 обозначает О,
Х2 обозначает О,
Y обозначает О и
Z обозначает карбоциклическое 5-членное кольцо общей формулы (II)
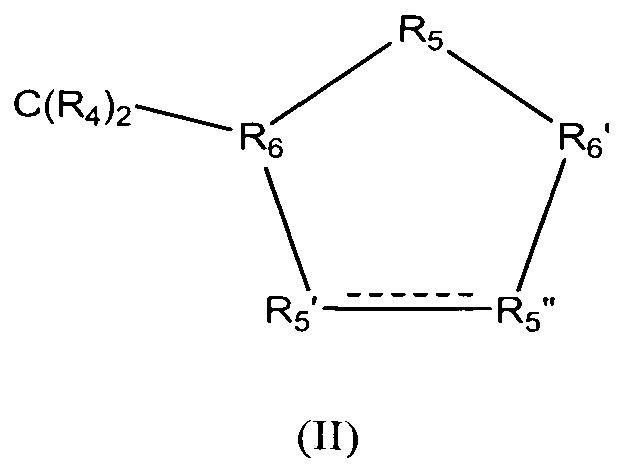
в которой между R5' и R5'' присутствует простая связь и в которой
R4 обозначает Н,
R5' обозначает СНОН,
R5'' обозначает СНОН,
R5 обозначает CR42,
R6 обозначает СН и
R6' обозначает СН.
5. Тестовый элемент по п.1, в котором кофермент представляет собой тио-NAD.
6. Тестовый элемент по п.1, в котором кофермент представляет собой тио-NADP.
7. Тестовый элемент по п.1, дополнительно содержащий первый реагентный материал, где этот первый реагентный материал включает первый фермент или субстрат для первого фермента и кофермент, выбранный из группы, состоящей из тио-NAD, тио-NADP и соединения формулы (I) или его соли или необязательно восстановленной формы.
8. Тестовый элемент по п.1, дополнительно содержащий второй реагентный материал, где этот второй реагентный материал включает второй фермент или субстрат для второго фермента и кофермент, выбранный из группы, состоящей из FAD, NAD, NADP и соединения формулы (I) или его соли или необязательно восстановленной формы.
9. Тестовый элемент по пп.7-8, дополнительно содержащий тест-полоску, созданную таким образом, чтобы она содержала первый и второй реагентные материалы.
10. Тестовый элемент по п.9, в котором тест-полоска включает первую электродную систему, ассоциированную с первым реагентным материалом, и вторую электродную систему, ассоциированную со вторым реагентным материалом.
11. Тестовый элемент по п.7, в котором первый реагентный материал дополнительно содержит один из таких ингредиентов как нитрозоанилин, феррицианид калия и комбинацию соединения феназина и хлорида гексааминорутения.
12. Реагентный материал для определения первого аналита, который используется в тестовом элементе по п.1, содержащий:
- 3-гидроксибутиратдегидрогеназу; и
- кофермент, представляющий собой тио-NAD, тио-NADP, карба-NAD и карба-NADP.
13. Реагентный материал по п.12, в котором кофермент представляет собой карба-NAD
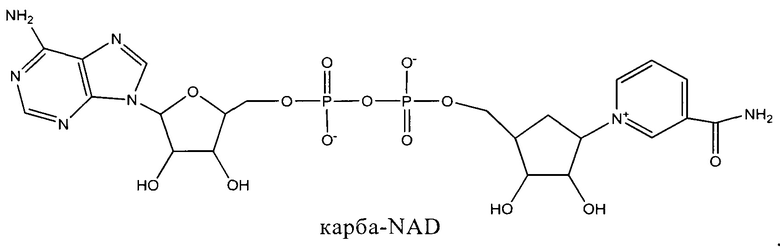
14. Реагентный материал по п.12, в котором кофермент представляет собой карба-NADP
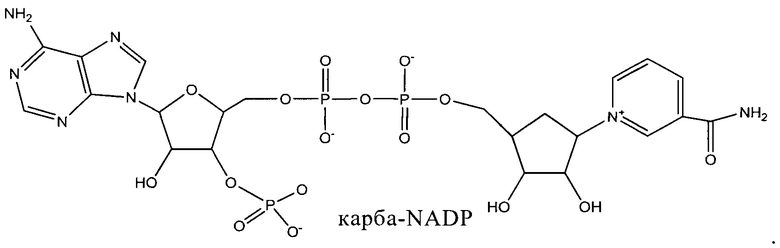
15. Реагентный материал по одному из пп.12-14, дополнительно содержащий один из таких ингредиентов как нитрозоанилин, феррицианид калия и комбинацию соединения феназина и хлорида гексааминорутения.
16. Тестовый элемент, включающий тест-полоску, содержащую первый реагентный материал по одному из пп.12-15, предназначенный для определения первого аналита, который представляет собой гидроксибутират, и второй реагентный материал для определения второго аналита, который представляет собой глюкозу, в котором тест-полоску создают для электрохимического определения первого и второго аналитов.
17. Тестовый элемент по п.16, в котором второй реагентный материал включает фермент глюкозодегидрогеназу.
18. Тестовый элемент по п.17, в котором второй реагентный материал дополнительно содержит кофермент, выбранный из группы, состоящей из FAD, NAD, NADP и соединения формулы (I)
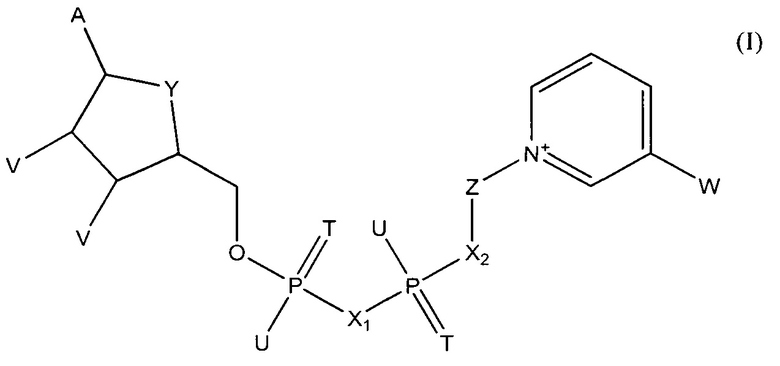
в которой
А обозначает аденин или его аналог,
Т в каждом случае независимо обозначает О или S,
U в каждом случае независимо обозначает ОН, SH, ВН3- или BCNH2-,
V в каждом случае независимо обозначает ОН или фосфатную группу,
W обозначает COOR, CON(R)2, COR или CSN(R)2, где R в каждом случае независимо обозначает Н или С1-С2-алкил,
Х1, Х2 в каждом случае независимо обозначают О, СН2, СНСН3, С(СН3)2, NH или NCH3,
Y обозначает NH, S, О или СН2,
Z обозначает остаток, содержащий циклическую группу с 5 атомами С, которая необязательно содержит гетероатом, выбранный из О, S и N, и необязательно один или несколько заместителей, и остаток CR42, где CR42 связан с циклической группой и с Х2, и
где R4 в каждом случае независимо обозначает Н, F, Cl или СН3, при условии, что Z и остаток пиридина не связаны гликозидной связью,
или его соли, или необязательно восстановленной формы.
19. Способ для определения уровней глюкозы и кетонов в образце биологической жидкости организма, включающий:
- получение тестового элемента по одному из пп.1-11 или 16-18, созданного для определения уровней глюкозы и кетонов в образце, где тестовые элементы создают для электрохимического определения уровней глюкозы и кетонов;
- контактирование тестового элемента с образцом; и
- определение уровней глюкозы и кетонов в образце в пределах 7,5 секунд или менее после контактирования тестового элемента с образцом.
20. Способ по п.19, в котором тестовый элемент включает первый реагентный материал, предназначенный для определения уровня глюкозы, и второй реагентный материал, предназначенный для определения уровня кетонов.
21. Способ по п.20, в котором второй реагентный материал включает гидроксибутиратдегидрогеназу.
22. Способ по одному из пп.19-21, в котором стадия определения уровней глюкозы и кетонов в образце завершается в пределах 5 секунд после контактирования тестового элемента с образцом.
23. Способ по п.19, в котором различие в продолжительности стадий определения уровней глюкозы и кетонов находится в пределах 2 секунд.
24. Способ по п.19, в котором образец содержит кровь.
| WO 2001049247 А2, 12.07.2001 | |||
| Мельница вибрационная | 2016 |
|
RU2614792C1 |
| US 20110048972 А1, 03.03.2011 | |||
| US 6380380 В1, 30.04.2002 | |||
| US 0005633143 А, 27.05.1997 | |||
| RU 2010138610 А, 27.03.2012. | |||
Авторы
Даты
2018-05-03—Публикация
2013-10-31—Подача