Изобретение относится к способу автоматической оценки ЭЭГ абсанса (кратковременной потери сознания) согласно пункту 1 формулы изобретения. Изобретение также относится к компьютерной программе для выполнения способа согласно пункту 11 формулы изобретения и устройству оценки для оценки ЭЭГ абсанса согласно пункту 12 формулы изобретения.
В общем, настоящее изобретение относится к области автоматической оценки ЭЭГ абсанса, как уже описано в WO 97/15013 A2, WO 2010/034305 А1 или WO 2010/034270 А1. При этом ЭЭГ является краткой формой термина ʺэлектроэнцефалограммаʺ. Здесь, из кривых ЭЭГ, т.е. из записанных последовательно во времени значений сигналов ЭЭГ пациента, посредством вычислительных способов, например, на основе статистических методов, выполняется классификация ЭЭГ, при которой определяется текущая глубина состояния абсанса пациента и определяется и выдается текущая стадия состояния абсанса на основе классификации. При этом под состоянием абсанса понимается любое состояние пациента, при котором он не реагирует или лишь реагирует ограниченно в соответствии с возрастом на речь/контакт, когда пациент не находится в состоянии бодрствования.
Типичные состояния абсанса имеют место, например, при наркозе, например, во время операции, или при любой другой седации пациента. При этом пациент находится под наркозом или под действием седативного эффекта вследствие подачи средств для наркоза. Вообще говоря, наркоз или седация являются состояниями, которые вызваны введением индуцирующих сон препаратов. Если пациенты отделения интенсивной терапии получают индуцирующие сон препараты, то говорят в общем случае о седации. Однако понятие седации не ограничивается пациентами отделения интенсивной терапии.
Если, например, при диагностических вмешательствах пациенты получают индуцирующие сон препараты в низких дозах, то также говорят о седации. Сюда относятся, например, вводимые внутривенно индуцирующие сон вещества. В качестве альтернативы, при наркозе и седации могут использоваться летучие анестетики на основе флурана, такие как севофлуран. Они могут вызвать при увеличении дозировки потенциалы спазма, которые могут быть распознаны в записанных кривых ЭЭГ при соответствующей оценке и, при необходимости, отфильтрованы, как уже объяснялось в вышеупомянутом известном уровне техники.
Дополнительные типичные состояния абсанса имеют место, например, при коме или при многих других состояниях при интенсивной терапии, т.е. в отделении интенсивной терапии (интенсивной ЭЭГ). Пациенты интенсивной терапии могут иметь различные заболевания, которые могут оказывать влияние на функцию мозга. Обычно это приводит на ЭЭГ с увеличением ослабления функции головного мозга к прогрессивному замедлению. По степени замедления роста можно различать различные стадии, например, от А до F. Замедления до стадии F могут быть вызваны, например, нарушениями метаболизма, переохлаждением, недостатком кислорода.
В общем, понятие ЭЭГ абсанса или состояния абсанса поэтому включает в себя случаи, в которых функция мозга пациента изменяется от нормального состояния в смысле ослабления. Помимо описанной выше схемы замедления, на ЭЭГ могут появляться особые паттерны, такие как типичная для эпилепсии активность.
Зарегистрированные кривые ЭЭГ также подвергаются некоторым изменениям ввиду прогрессивного развития человека. Особенно заметные изменения могут устанавливаться в развитии молодых людей, то есть от детского возраста до перехода во взрослый возраст. В частности, в течение первого года жизни, кривые ЭЭГ развиваются очень заметно.
Из WO 97/15013 A2 уже известно, что ЭЭГ человека имеет возрастные характеристики. Для улучшения разделения на стадии, там было предложено выбирать из сохраненных различных функций классификации, зависимых от возраста, функции классификации, специфические для возраста испытуемого. Это позволяет более надежным образом установить корректное разделение на стадии.
Известный способ должен быть дополнительно улучшен, чтобы обеспечить возможность, в частности для очень юных пациентов в течение первого года жизни, надежного определения текущей стадии состояния абсанса.
Эта задача решается в соответствии с пунктом 1 формулы изобретения способом автоматической оценки ЭЭГ абсанса, при котором кривые ЭЭГ записывают устройством оценки и посредством компьютера устройства оценки оценивают, причем при оценке из кривых ЭЭГ посредством компьютера на основе разделения на стадии ЭЭГ абсанса определяют по меньшей мере текущую стадию состояния абсанса пациента, причем в разделении на стадии различают стадии глубины состояния абсанса, и причем выдают текущую стадию, причем компьютером выбирается определенная схема разделения на стадии из нескольких предоставленных для выбора схем разделений на стадии, которые различаются количеством различимых стадий состояния абсанса, и применяется для автоматического выполнения разделения на стадии для определения текущей стадии. Изобретение имеет то преимущество, что может выполняться согласованное с развитием или возрастом разделение на стадии ЭЭГ абсанса, и соответствующим образом согласованная информация может отображаться пользователю. Последние могут быть определены с высокой степенью надежности. В частности, может осуществляться гибкое согласование для очень юных пациентов. У новорожденных и детей раннего возраста, как показывают новые данные исследований, различимы лишь небольшое количество стадий ЭЭГ абсанса. В зависимости от зрелости мозга, количество различимых стадий увеличивается.
Устройство оценки может быть выполнено, например, в виде компактного устройства, которое располагается вблизи от пациента. Устройство оценки может также быть выполнено как состоящее из нескольких компонентов устройство, причем эти компоненты также могут быть разделены, например, располагаться в различных помещениях здания. Так, например, устройство оценки может иметь станцию записи данных для записи кривых ЭЭГ и расположенный удаленно от нее компьютер, например, центральный компьютер в отделении интенсивной терапии для онлайн-оценки кривых ЭЭГ или компьютер для офлайн-оценки кривых ЭЭГ.
В соответствии с предпочтительным вариантом осуществления изобретения предусмотрено, что после начала состояния абсанса проверяется, имеют ли кривые ЭЭГ определенные признаки, на основе которых можно принять решение, какую схему разделения на стадии использовать далее. Таким образом, выбор определённой схемы из нескольких предоставленных для выбора схем разделения на стадии может осуществляться однократно сразу же после начала состояния абсанса. Также можно продолжать анализировать кривые ЭЭГ во время состояния абсанса на наличие признаков, на основании которых можно выбирать схему разделения на стадии, и при необходимости при дальнейшей работе перейти от ранее выбранной схемы на другую выбранную схему.
При этом определенная на основе выбранной схемы разделения на стадии текущая стадия состояния абсанса выводится, например, путем передачи к другому устройству через интерфейс устройства оценки или визуально отображается непосредственно на устройстве оценки, например, на дисплее. Согласно предпочтительному варианту осуществления изобретения, дополнительно выводится информация о текущей выбранной схеме разделения на стадии, например, путем вывода на упомянутый интерфейс или визуального отображения на устройстве оценки. Это позволяет пользователю устройства оценки быстро и интуитивно оценивать выводимые данные.
Для оценки кривых ЭЭГ посредством компьютера и разделения на стадии ЭЭГ абсанса принимаются в расчет различные методы и алгоритмы, из которых в качестве примера ниже поясняются некоторые.
Электроэнцефалография представляет собой метод отображения электрической активности, генерируемой головным мозгом. Традиционно, регистрация ЭЭГ осуществляется многоканальным записывающим устройством на рулонной бумаге. Все чаще запись выполняется с помощью компьютеров.
Состав форм волн в электроэнцефалограмме (ЭЭГ) зависит от функционального состояния головного мозга. Изображения ЭЭГ, которые встречаются у пациентов в хирургической области и области интенсивной терапии, разнообразны и могут испытывать влияние большого количества эндогенных и экзогенных факторов. Помимо нормального ЭЭГ состояния бодрствования, можно ожидать, например, элементов ЭЭГ сна, эффектов от лекарственных препаратов и других экзогенно водимых химических веществ, обусловленных вентиляцией и метаболическими влияниями, температурными эффектами, последствиями травматических повреждений головного мозга, а также воспалительными, сосудистыми, дегенеративными и вызванными новообразованиями изменений ЭЭГ.
Следующие частотные диапазоны соотносят с появляющимися на ЭЭГ волнами: альфа (7,5-12,5 Гц), бета (> 12,5 Гц), тета (3,5-7,5 Гц) и дельта (0,5-3,5 Гц). Кроме того, можно выделить суб-дельта (<0,5 Гц) и гамма-диапазон (> 30 Гц). При обследовании волны в частотных диапазонах описываются в отношении их амплитуд, частотности, регулярности, временной сегментации, пространственного распределения и изменений в ответ на раздражители. Амплитуды ЭЭГ измеряются в мкВ. Более высокочастотные волны обычно имеют меньшие амплитуды, в то время как с замедлением чаще всего связано увеличение амплитуды.
Для классификации стадий сна, наркоза или комы на ЭЭГ, Kugler предлагает разделение ЭЭГ, в котором состояние бодрствования обозначается как А, а изображения ЭЭГ при прогрессирующем ослаблении функции мозга обозначаются буквами от B до F. Для оценки кривых ЭЭГ применяются частотность и амплитуда волн в определенных частотных диапазонах и типичные паттерны.
ЭЭГ бодрствования, стадия А, характеризуется для большинства взрослых волнами в частотном диапазоне альфа. Стадия B характеризуется волнами с более короткой частотой и меньшей амплитудой. На стадиях C и D появляются тета- и дельта-волны. На стадии Е изображение кривой определяет высокоамплитудная дельта-активность. Стадия F характеризуется переходами от плоских до изоэлектрических участков кривой и группами более высоких волн, паттерном ʺвспышка-подавлениеʺ или непрерывной очень плоской активностью.
Вывод обычной ЭЭГ является относительно трудоемким. Интерпретация требует специальных знаний и опыта. Лучшая оценка динамически происходящих изменений ЭЭГ обеспечивается посредством записи исходного сигнала и спектрального анализа ЭЭГ. Для вычисления спектра мощности ЭЭГ сигналы ЭЭГ для определенного временного интервала после аналого-цифрового преобразования подвергаются, например, быстрому преобразованию Фурье (FFT). С помощью преобразования Фурье волновая картина ЭЭГ разлагается на основные компоненты колебаний, осуществляется преобразование из временной области в частотную область. Квадратичные амплитуды компонентов колебаний образуют спектр мощности. В спектре мощности ЭЭГ могут считываться частоты, возникающие во временном сигнале. Однако эти показания также требуют интерпретации, чтобы получить анализ стадии ЭЭГ и, таким образом, церебрального функционального состояния.
Дальнейшая обработка результатов преобразования Фурье включает в себя извлечение так называемых спектральных параметров, а также дальнейшие статистические вычисления. К параметрам, которые могут быть выведены из спектра, относятся, например, общая мощность, а также абсолютные и относительные мощности в различных частотных диапазонах. Другими часто применяемыми параметрами являются медиана, частота края спектра и доминирующая частота. Медиана является частотой, на которой площадь спектра делится на две равные части. Частота края спектра обычно определяется как 95%-квантиль, т.е. 95% от общей мощности спектра лежат ниже этой частоты. Доминирующая частота является частотой с наибольшей мощностью.
С помощью спектра мощности частотное распределение участков ЭЭГ может быть наглядно отображено. О специальных паттернах, таких как фазы вспышки-подавления или потенциалы приступа, из спектра, напротив, чаще всего невозможно сделать вывод.
Способом быстрого вычисления спектра мощности является быстрое преобразование Фурье (FFT).
Одной возможностью для анализа сигналов ЭЭГ во временной области является определение авторегрессионных параметров. Авторегрессионные (AR) параметры являются величинами из временной области. Измеренное значение в определенный момент времени отображается как взвешенная сумма его прошлых значений плюс случайная компонента. Весами являются AR-параметры. Общая формула для AR-процесса имеет вид:
Yt=a1*Yt-1+…+ap*Yt-p+et
При этом Yt обозначает измеренное значение в момент времени t; ai, i=1,… р - AR-параметры и et - независимые случайные составляющие со средним значением 0 и постоянной дисперсией для всех моментов времени t. Буква р обозначает порядок процесса, то есть, количество прошлых значений, которые учитываются. Параметры модели могут оцениваться с помощью уравнения Yule-Walker. Для определения порядка модели и проверки качества модели, как правило, применяется подход Box и Jenkins. Обзор других способов оценки и классов моделей дают Kay и Marple.
Часто используемым методом для характеристики измерений ЭЭГ является вычисление специальных параметров ЭЭГ, которые были предложены Hjorth и названы в его честь. При этом речь идет о трех параметрах, а именно активности, мобильности и сложности. Hjorth-параметры вычисляются из распределения сигнала ЭЭГ, а также его первой и второй производной. В качестве альтернативы, вычисление Hjorth-параметров также может выполняться в частотной области, т.е. с помощью спектрального анализа.
Активность соответствует общей мощности сигнала и, следовательно, является мерой величины амплитуды измерения ЭЭГ. Мобильность может быть интерпретирована как мера средней частоты, и сложность - как мера изменчивости сигнала.
Помимо чисто спектральных параметров или чисто AR- параметров, возможно комбинированное определение, например, спектральных параметров, AR-параметров, Hjorth-параметров или параметров хаоса и/или других параметров.
Для классификации данных ЭЭГ посредством многомерных функций классификации на основе спектральных параметров и/или AR-параметров и/или Hjorth-параметров и/или параметров хаоса и/или также дополнительных параметров пригодны, например, способы дискриминантного анализа или нейронные сети.
Способы классификации на основе дискриминантного анализа пригодны для того, чтобы на основе ряда выдвинутых признаков соотносить объекты с одной из нескольких определенных групп. При разделении на стадии ЭЭГ абсанса, участки ЭЭГ образуют классифицируемые объекты, которые характеризуются спектральными параметрами и/или AR-параметрами и/или Hjorth-параметрами и/или параметрами хаоса. Для вычисления соответствующих функций классификации существует ряд методов, которые можно разделить на параметрические и непараметрические подходы. Посредством выборки объектов, для которых известна принадлежность к группе, можно вывести функции классификации на основе наблюдаемых значений признаков.
В параметрических способах предполагается, что рассматриваемый вектор признаков в различных группах следует многомерному нормальному распределению. Линейный дискриминантный анализ предполагает равенство матриц ковариации в отдельных группах, квадратичный дискриминантный анализ позволяет учитывать различные матрицы ковариации групп. В качестве меры расстояния применяется Mahalanobis-расстояние, которое отображает взвешенное расстояние вектора наблюдения до средних значений групп. Объект тогда соотносится с той группой, для которой зависимая от выбранного способа функция Mahalanobis-расстояния является наименьшей.
Если распределение вектора признаков неизвестно или отличается от нормального распределения, могут быть использованы непараметрические способы для выведения правил классификации. Наглядным способом является метод k-ближайших соседей. При этом образуют расстояния классифицируемого вектора признаков до всех других векторов признаков имеющейся выборки, сортируют по величине, и определяют векторы наблюдений с k наименьшими расстояниями, причем количество k учитываемых значений должно устанавливаться заранее. Затем определяют, к каким группам принадлежат эти k значения, и определяет их долю от общего числа измерений в отдельных группах. Затем осуществляют соотнесение с группой, для которой эта доля наибольшая.
Этот непараметрический способ требует повышенных вычислительных затрат по отношению к параметрическим методам, так как для классификации объекта нужно обращаться ко всему исходному набору данных, в то время как при параметрических методах используются значения признаков объекта в функциях классификации.
Для оценки качества способа классификации может быть вовлечена соответствующая частота ошибок, причем под частотой ошибок понимается доля неправильных классификаций. Возможность оценки частоты ошибок состоит в повторной классификации данных. Однако определенная частота ошибок дает слишком положительную оценку реальной частоты ошибок. Более реалистичная оценка частоты ошибок достигается в том случае, когда классификации проверяются на независимом наборе данных. Это может быть сделано с помощью разбиения данного набора данных на обучающий набор данных для введения правила классификации и тестовый набор данных для валидации правильности классификации. Крайняя форма разбиения данных состоит в так называемой перекрестной валидации или способа с исключением по одному образцу (leave-one-out) . При этом соответствующее наблюдение удаляется из набора данных, и проводится классификация на основе дискриминантной функции, вычисленной из оставшихся данных.
Если существует большое количество потенциальных признаков для вывода дискриминантных функций, то можно с помощью соответствующего ступенчатого способа определять те параметры, которые обеспечивают максимально возможное разделение групп. С этой целью в литературе предлагается ряд способов, например, поэтапно в оценку включаются параметры, которые на основе Wilks Lambda обеспечивают, соответственно, наибольший вклад в разделение групп.
Разделение на стадии ЭЭГ наркоза или интенсивной терапии может быть выполнено на основе подхода Kugler, согласно которому, как упоминалось выше, состояние бодрствования обозначено как стадия A, а очень глубокое ослабление функции мозга - как стадия F. Промежуточные стадии В-Е, таким образом, могут быть дополнительно разделены, как показано в таблице 1 в WO 97/15013 A2. Также можно вместо обозначений классов А-F, например, применять шкалу с цифрами, например, от 100 до 0.
Дальнейшее улучшение разделения на стадии достигается в том случае, если из сохраненных различных зависимых от возраста функций классификации для испытуемого выбираются специфические для возраста функции классификации. Было обнаружено, что ЭЭГ человека имеют зависимые от возраста характеристики. Проще говоря, например, спектр у взрослых с увеличением возраста сдвигается в состоянии бодрствования к более низким частотам, в то время как при наркозе, например, дельта-мощность уменьшается. С учетом специфических для возраста функций классификации можно надежно выполнить надлежащее разделение на стадии.
В соответствии с предпочтительным вариантом осуществления изобретения показания о возрасте пациента, кривые ЭЭГ которого записываются, вводятся в устройство оценки. Автоматический выбор схемы разделения на стадии выполняется компьютером с учетом введенных показаний о возрасте. Это имеет то преимущество, что посредством ручного ввода возраста пациента, диапазон вероятных для выбора схем разделения на стадии может быть ограничен. Однако было показано, что однозначное установление выбираемой схемы разделения на стадии только на основе указаний возраста чаще всего не приводит к удовлетворительным результатам, потому что люди и их мозг развиваются с возрастом по-разному, и поэтому не может быть определена никакая конкретная возрастная граница, при которой в кривых ЭЭГ, например, у взрослых может быть предпринято обычное подразделение на стадии от А до F. Исследования показывают, что такое разделение на стадии возможно примерно с возраста полгода, однако рассеяние для возраста относительно велико. Для очень маленьких детей поэтому предпочтительно брать за основу менее дифференцированное разделение на стадии.
В соответствии с предпочтительным вариантом осуществления изобретения, автоматический выбор схемы разделения на стадии выполняется компьютером с учетом записанных кривых ЭЭГ и/или полученных из них данных. Это имеет то преимущество, что надежный выбор подходящей схемы разделения на стадии может выполняться автоматически, а именно, на основе и без того уже записанных кривых, так что использование устройства оценки дополнительно упрощается. Учет записанных кривых ЭЭГ может, например, осуществляться в том отношении, что кривые ЭЭГ исследуются на наличие некоторого характерного паттерна кривой или определенных статистических данных, которые могут быть определены из кривых и которые характерны для определенных стадий развития ЭЭГ. Таким образом, выбор схемы разделения на стадии может выполняться, например, на основе данных амплитуды, данных частоты и/или средних значений или временных характеристик амплитуд и/или частот кривых ЭЭГ.
В соответствии с предпочтительным вариантом осуществления изобретения при распознавании определенной минимальной доли низкочастотных сигнальных составляющих и нераспознавании определенной минимальной доли высокочастотных сигнальных составляющих в кривых ЭЭГ выбирается схема с меньшим количеством различимых стадий состояния абсанса, чем при распознавании минимальной доли высокочастотных сигнальных составляющих, которые могут комбинироваться с определенной минимальной долей низкочастотных сигнальных составляющих. Таким образом, можно, например, для пациентов в детском возрасте, которые преимущественно показывают медленную волновую картину с соответственно низкочастотными сигнальными составляющими в ЭЭГ, выбирать подходящую схему разделения на стадии с меньшим количеством различимых стадий. В случае пациентов старшего возраста, которые характеризуются более высокочастотными сигнальными составляющими в кривых ЭЭГ, могут выбираться схемы с согласованными, более тонко дифференцированными разделениями на стадии.
Под влиянием наркотических/седативных средств, в качестве низкочастотных сигнальных составляющих могут возникать дельта-волны. Если на эти низкочастотные волны накладывается минимальная доля высокочастотных волн - как проявление влияния наркотических средств - то может быть принято решение, что речь идет о дифференцированной ЭЭГ. Соответственно, тогда может быть выбрана схема с большим количеством различимых стадий состояния абсанса. Если ЭЭГ состоит только из низкочастотных волн, то должна выбираться схема с меньшим количеством различимых стадий.
Если у детей младшего возраста в процессе измерения проявляется высокочастотная активность с низкой или отсутствующей долей низкочастотных сигнальных составляющих, как она, например, является типичной на стадиях В и С у детей старшего возраста или взрослых, то выбирается схема с бóльшим количеством различимых стадий состояния абсанса.
В соответствии с предпочтительным вариантом осуществления изобретения, при распознавании определенной доли высокочастотных сигнальных составляющих в кривых ЭЭГ может выбираться схема с бóльшим количеством различимых стадий состояния абсанса. Однако в случае, когда имеет место ʺнераспознавание минимальной доли низкочастотных составляющихʺ и отсутствует ʺраспознавание определенной доли высокочастотных сигнальных составляющихʺ, не должна выбираться схема с бóльшим количеством различимых стадий состояния абсанса, потому что могла бы идти речь о почти полностью или полностью подавленной (ниже нормы) ЭЭГ (ʺстадия Fʺ с нулевыми линиями).
В соответствии с предпочтительным вариантом осуществления изобретения компьютер первоначально исходит из первой схемы с определенным количеством различимых стадий состояния абсанса и выбирает к моменту времени принятия решения, к которому имеется достаточное количество данных ЭЭГ, при распознавании определенных характеристик в кривых ЭЭГ, вторую схему разделения на стадии, которая имеет меньшее или большее количество различимых стадий состояния абсанса, чем первая схема. Таким образом, например, при распознавании минимальной доли низкочастотных сигнальных составляющих в кривых ЭЭГ может выбираться вторая схема разделения на стадии. Если условие выбора, т.е. распознавание определенных характеристик, не наступает, то компьютер может, например, продолжать применять первую схему или выбирать первую схему в качестве схемы, применяемой для автоматического выполнения разделения на стадии. Таким образом, в качестве первой схемы может применяться, например, схема разделения на стадии для взрослых, например, с разделением на стадии от А до F или более тонкое разделение со стадиями А0, А1, А2, B0, В1, В2, С0, С1, C2, D0, D1, D2, E и F, как описано в таблице 1 в WO 97/15013 А2. Вторая схема разделения на стадии может, например, иметь разделение на стадии А, Е и F. Вышеуказанное соотнесение разделений на стадии с первой и второй схемами также может осуществляться в обратном порядке.
Для установления первой схемы, из которой сначала исходит компьютер, можно также применять введенные данные возраста пациента. Для очень маленьких детей, в частности новорожденных или недоношенных, следует исходить из того, что сначала может применяться разделение на стадии с пониженным количеством стадий. Это могло бы иметь место для всех детей в течение первых двух-трех месяцев жизни, как показывают текущие собственные анализы ЭЭГ. При соответствующем вводе возраста устройство оценки исходит не из стандартной классификации на стадии A, B, …, F или от 100 до 0, а из схемы с сокращенным разделением на стадии. Для детей старшего возраста устройство оценки может первоначально исходить из схемы с бóльшим количеством различимых стадий, а затем при измерении, при необходимости, переходить к схеме с меньшим количеством различимых стадий.
В соответствии с предпочтительным вариантом осуществления изобретения по меньшей мере частотные составляющие в дельта-диапазоне оцениваются как низкочастотные сигнальные составляющие кривых ЭЭГ. Дополнительно частотные составляющие с частотами ниже дельта-диапазона также могут оцениваться как низкочастотные сигнальные составляющие. В одном варианте осуществления изобретения частотные составляющие с частотами выше дельта-диапазона могут оцениваться в качестве высокочастотных сигнальных составляющих.
В качестве дополнительного критерия для автоматического выбора схемы разделения на стадии могут оцениваться кривые ЭЭГ с точки зрения так называемых участков подавления в паттернах вспышки-подавления или в ЭЭГ подавлении. В качестве вспышки при этом понимается последовательность волн сигнала в кривой ЭЭГ. Участки подавления в кривых ЭЭГ являются участками кривых, на которых не возникает вспышек, и сигнал имеет плоский, по сравнению с сигнальными волнами вспышки, профиль. Участки между соседними вспышками обозначаются как участки подавления. В соответствии с предпочтительным вариантом осуществления изобретения при оценке кривых ЭЭГ выполняется распознавание паттернов вспышки-подавления, и при появлении предварительно определенных характеристик паттернов вспышки-подавления в кривых ЭЭГ выбирается схема разделения на стадии, которая имеет уменьшенное количество различимых стадий в состоянии абсанса, по сравнению с иной выбранной схемой разделения на стадии. В качестве характеристик паттернов вспышки-подавления могут привлекаться, например, длина участков подавления или коэффициент вспышки-подавления (BSR). Коэффициент вспышки-подавления указывает, какой процент участка кривой ЭЭГ состоит из участков подавления. Кроме того, интервал между вспышками (IBI), который является мерой расстояния между вспышками, может привлекаться в качестве характеристики.
В соответствии с предпочтительным вариантом осуществления изобретения, кроме стандартной схемы разделения на стадии, компьютером может выбираться дополнительная схема или в зависимости от ступени развития пациента несколько других схем разделения на стадии, особенно разделения на стадии с меньшим количеством различимых стадий состояния абсанса, чем в стандартной схеме. Это обеспечивает возможность разделения на стадии, особенно хорошо согласованного со степенью развития ЭЭГ.
Предпочтительной, в частности, является запись данных ЭЭГ до момента оценки после наступления состояния абсанса. Тем самым можно избежать возможных искажений при выборе подходящей схемы разделения на стадии из-за данных ЭЭГ, записанных еще в состоянии бодрствования. Исследования показывают, что практически невозможно на основе ЭЭГ в состоянии бодрствования оценить относящееся к развитию разделение на стадии ЭЭГ абсанса.
В соответствии с предпочтительным вариантом осуществления изобретения на основе выбранной схемы разделения на стадии определяется показание степени развития ЭЭГ. Это показание о степени развития ЭЭГ может в устройстве оценки дополнительно применяться внутренним образом, чтобы в зависимости от этого оказывать влияние на определенные дополнительные оценки или функции классификации анализа сигналов ЭЭГ. Показание о степени развития ЭЭГ может также выдаваться, например, через интерфейс устройства оценки на другое устройство или визуально отображаться, например, на дисплее устройства оценки.
В соответствии с предпочтительным вариантом осуществления изобретения кривые ЭЭГ анализируются на наличие паттернов кривых, генерируемых дополнительными биосигналами, и, если по меньшей мере один такой паттерн кривой распознается, то проверяется, следует ли выбрать схему для разделения на стадии иную, чем при нераспознавании такого паттерна кривой. Таким образом, могут, например, обнаруживаться сигнальные паразитные связи извне, артефакты, в частности артефакты движения и типичные для эпилепсии потенциалы и учитываться как при выборе схемы разделения на стадии, так и для собственно разделения на стадии, т.е. функции классификации.
Согласно предпочтительному варианту осуществления изобретения посредством датчиков артефактов, которые могут быть подключены к устройству оценки, определяются артефакты движения в записанных кривых ЭЭГ, и на основе определенных артефактов движения кривые ЭЭГ корректируются, и/или разделение на стадии корректируется и/или подавляется, и/или выбирается другая схема разделения на стадии. Такие датчики артефактов могут быть выполнены, например, как датчики деформации ЭЭГ-электродов. Такие датчики деформации могут включать в себя емкости, которые изменяются из-за деформации, и их изменение емкости коррелирует с деформацией ЭЭГ-электродов.
Для определения текущей стадии состояния абсанса и/или для выбора применяемой схемы разделения на стадии могут либо непосредственно применяться кривые ЭЭГ, либо данные, производные из них. Так, например, можно определять частотные составляющие с помощью анализа Фурье или подобного анализа. Могут статистически оцениваться значения амплитуды. Также может определяться амплитудно-интегрированная ЭЭГ. Амплитудно-интегрированная ЭЭГ является сжатым во времени отображением амплитуд участка ЭЭГ. При вычислении амплитудно-интегрированной ЭЭГ сигнал ЭЭГ может, например, сильно фильтроваться, выпрямляться и сглаживаться.
Вышеуказанная задача также решается в соответствии с пунктом 11 формулы изобретения компьютерной программой со средствами программного кода, приспособленной для выполнения способа вышеописанного типа, когда компьютерная программа выполняется на компьютере. Компьютерная программа может выполняться, в частности, на компьютере вышеописанного устройства оценки. Компьютерная программа может храниться на машиночитаемом носителе, например, на CD или DVD, флэш-памяти, на Интернет-сервере или на носителе хранения данных устройства оценки.
Вышеуказанная задача также решается в соответствии с пунктом 12 формулы изобретения посредством устройства оценки для оценки ЭЭГ абсанса, причем устройство оценки имеет по меньшей мере один компьютер, средство регистрации сигналов ЭЭГ и средство вывода, причем устройство оценки выполнено с возможностью выполнения способа вышеописанного типа. Таким образом, устройство оценки может быть приспособлено для выполнения способа с помощью компьютера, выполняющего компьютерную программу вышеописанного типа. Средство вывода может быть, например, интерфейсом устройства оценки или средством для визуального отображения, например, дисплеем.
Далее изобретение будет описано более подробно на примерах выполнения со ссылками на чертежи, на которых показано следующее:
Фиг. 1 - устройство оценки при записи ЭЭГ, и
Фиг. 2 - отображение записанных устройством оценки кривых ЭЭГ и полученных из них данных, и
Фиг. 3 - отображение процедуры при оценке ЭЭГ абсанса в устройстве оценки.
На фигурах используются одни и те же ссылочные позиции для обозначения соответствующих друг другу элементов.
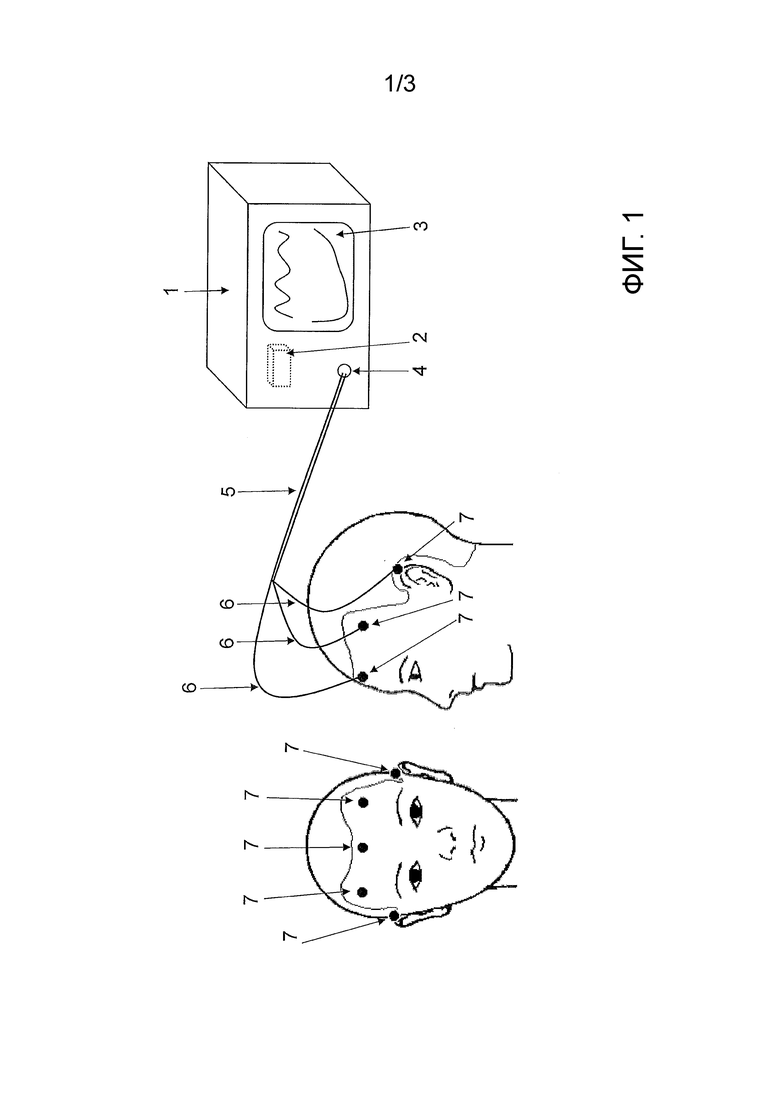
Фиг. 1 показывает устройство 1 оценки для оценки ЭЭГ абсанса. Устройство 1 оценки имеет размещенный в устройстве 1 оценки, например, на центральной плате компьютер 2, который может быть выполнен, например, в виде микропроцессора или микроконтроллера. Устройство 1 оценки также имеет средство 3 индикации, например, дисплей. На средстве 3 индикации могут графически отображаться профили кривой или воспроизводиться иные зарегистрированные и определенные из них данные. Устройство 1 оценки дополнительно имеет электрический разъем 4, который служит для подключения ЭЭГ-электродов 7, например, через штекерный разъем.
На фиг. 1 отображено, как несколько ЭЭГ-электродов 7 расположены на голове пациента. ЭЭГ-электроды 7 соединены через кабель 6, который вблизи устройства оценки объединены в общий кабельный жгут 5, с электрическим разъемом 4 устройства 1 оценки. Общий кабельный жгут 5 может, например, путем оценки существующих между кабелями значений емкости применяться в качестве одного или нескольких датчиков артефактов для распознавания артефактов движения. Для этой цели в устройстве 1 оценки предусмотрено средство регистрации для регистрации емкостей между проводниками 6 кабельного жгута 5.
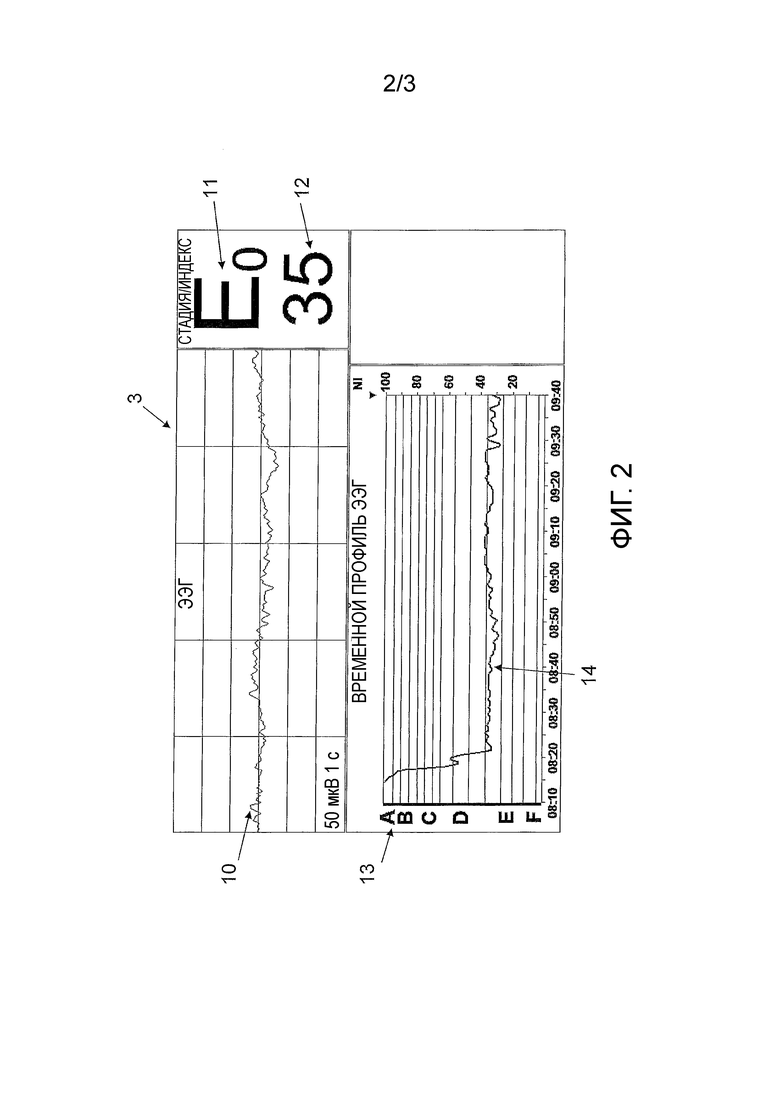
Фиг. 2 показывает в качестве примера типовые данные, выведенные на средство 3 индикации устройства 1 оценки. В верхнем окне могут отображаться, например, одна или более кривых ЭЭГ 10, как они записываются ЭЭГ-датчиками 7, как профиль кривой во времени. В области 11 индикации может отображаться текущая стадия состояния абсанса, как это определяется компьютером 2 путем оценки кривых ЭЭГ. В области 12 индикации может дополнительно выводиться глубина наркоза или седации как безразмерное число в диапазоне от 0 до 100. На отображении временной диаграммы внизу справа, временной профиль определенных стадий, как отображено в области 11, выводится как профиль 14 кривой. На вертикальной оси диаграммы в области 13 воспроизведены различимые стадии от А до F выбранной схемы разделения на стадии. Показание от А до F указывает разделение на стадии взрослого пациента. В случае менее развитой ЭЭГ, например, для очень маленького ребенка, в области 13, на основе другой схемы разделения на стадии, выбранной компьютером, осуществляется другой вывод, например, только буквы A, E и F. Также возможно вместо обозначений классов от А до F применять, например, шкалу с цифрами, например, от 100 до 0.
В следующей таблице показано примерное соответствие между стадиями с обозначениями классов от А до F и шкалами с числами (значениями индекса).
Как уже пояснено, в случае детей с незрелой ЭЭГ, следует применять разделение на стадии с меньшим количеством стадий (здесь, например, A, E, F). Значения индекса 100-0 могли бы согласовываться либо с сокращенным разделением на стадии (использовался бы весь диапазон индекса 100-0), или могла бы использоваться только часть диапазона индекса 100-0, например, только область 100-95 и область 36-0.
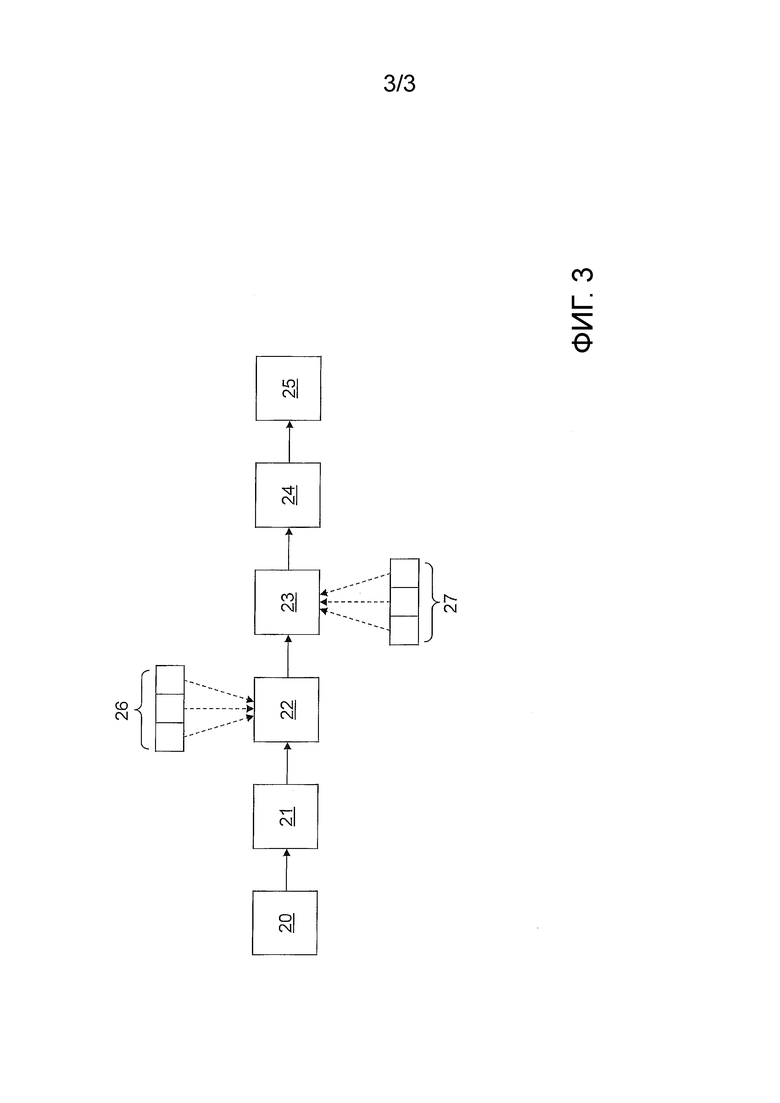
Фиг. 3 показывает процедуру при автоматической оценке кривых ЭЭГ с помощью компьютера 2. Воспроизведенные на фиг. 3 блоки 20, 21, 22, 23, 24, 25 указывают при этом определенные функции оценки или алгоритмы, которые выполняются на компьютере 2. Таким образом, блоки 20, 21, 22, 23, 24, 25 могут, например, быть выполнены как участки программы, программные модули или подпрограммы компьютерной программы, которая выполняется на компьютере 2.
В блоке 20 осуществляется считывание кривых ЭЭГ. В последующем блоке 21 осуществляется анализ сигналов кривых ЭЭГ, например, преобразованием Фурье, определение спектра мощности и/или амплитудно-интегрированной ЭЭГ. В последующем блоке 22 на основе одного или более из нижеописанных критериев осуществляется выбор подлежащей применению схемы разделения на стадии из нескольких предоставленных для выбора схем 26. В качестве примера тремя блоками 26 отображены три схемы для выбора, из которых компьютер 2 в блоке 22а осуществляет выбор.
В последующем блоке 23 осуществляется выбор функции классификации для выполняемой затем классификации кривых ЭЭГ и для определения текущей стадии на основе разделения на стадии ЭЭГ абсанса. В качестве примера отображается, что компьютер в блоке 23 может выбрать одну из трех предоставленных для выбора функций 27 классификации. В последующем блоке 24 осуществляется оценка кривых ЭЭГ или определенных из них данных на основании выбранной функции классификации таким образом, что выполняется разделение на стадии ЭЭГ абсанса с применением выбранной в блоке 22 схемы разделения на стадии. В последующем блоке 25 затем, при необходимости, помимо других данных выдается определенная текущая стадия состояния абсанса.
В блоке 22 может выполняться выбор подлежащей применению схемы разделения на стадии из доступных схем 26 на основе заранее введенного возраста пациента, для которого регистрируются кривые ЭЭГ, на основе записанных кривых ЭЭГ и/или выведенных из них данных и/или на основе ранее выбранных схем для разделения на стадии, как подробно обсуждено выше. В частности, для этого могут применяться кривые ЭЭГ после ввода состояния абсанса. Таким образом, может осуществляться согласованное с развитием ЭЭГ или развитием пациента и его возрастом разделение на стадии. Аналогичным образом в блоке 23 может осуществляться соответственно согласованный выбор функции классификации из доступных функций 27 классификации. Критериями при выборе в блоке 23 могут быть один или более из указанных выше критериев.
Соответственно, в блоке 24 осуществляется согласованное в двух аспектах к возрасту и степени развития пациента разделение на стадии ЭЭГ абсанса. Путем выбора соответствующих функций классификации в блоке 23 разделение на стадии оптимизируется в отношении дальнейшей оценки кривых ЭЭГ. При этом полученные из них данные классифицируются не так, как в известных устройствах оценки, всегда с одной и той же схемой разделения на стадии, а классифицируются варьируемым образом на основе выбранной в блоке 22 и оптимизированной для соответствующего возраста или степени развития пациента схемы разделения на стадии. Так, например, для взрослого пациента для функции классификации выбирается ʺвзрослый алгоритмʺ. Полученные таким образом результаты, затем классифицируются на основе выбранной схемы разделения на стадии на одну из шести стадий от А до F. В случае очень маленького ребенка в качестве функции классификации применялся бы ʺдетский алгоритмʺ. Для разделения на стадии применялась бы тогда менее детализированная схема, например, только с тремя различимыми стадиями.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ АВТОМАТИЗИРОВАННОГО ОПРЕДЕЛЕНИЯ АРХИТЕКТУРЫ СНА У ПАЦИЕНТОВ С ХРОНИЧЕСКИМИ НАРУШЕНИЯМИ СОЗНАНИЯ | 2022 |
|
RU2803957C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ЭПИЛЕПТИФОРМНОЙ АКТИВНОСТИ | 2009 |
|
RU2409315C1 |
| СПОСОБ РЕАБИЛИТАЦИИ БОЛЬНЫХ ПОСЛЕ ИНСУЛЬТА ИЛИ ТРАВМЫ С ИСПОЛЬЗОВАНИЕМ РОБОТИЗИРОВАННОГО КОМПЛЕКСА, ВКЛЮЧАЮЩЕГО ЭКЗОСКЕЛЕТ КОНЕЧНОСТИ ЧЕЛОВЕКА, УПРАВЛЯЕМЫЙ ЧЕРЕЗ ИНТЕРФЕЙС МОЗГ-КОМПЬЮТЕР ПОСРЕДСТВОМ ВООБРАЖЕНИЯ ДВИЖЕНИЙ | 2015 |
|
RU2622206C2 |
| СИСТЕМА ДЛЯ КОММУНИКАЦИИ ПОЛЬЗОВАТЕЛЕЙ БЕЗ ИСПОЛЬЗОВАНИЯ МЫШЕЧНЫХ ДВИЖЕНИЙ И РЕЧИ | 2018 |
|
RU2725782C2 |
| СПОСОБ ФОРМИРОВАНИЯ СИСТЕМЫ УПРАВЛЕНИЯ МОЗГ-КОМПЬЮТЕР | 2019 |
|
RU2704497C1 |
| СПОСОБ КЛАССИФИКАЦИИ ЭЛЕКТРОЭНЦЕФАЛОГРАФИЧЕСКИХ СИГНАЛОВ В ИНТЕРФЕЙСЕ МОЗГ - КОМПЬЮТЕР | 2009 |
|
RU2415642C1 |
| Способ реабилитации когнитивных функций у пациентов с очаговыми поражениями головного мозга | 2020 |
|
RU2749408C1 |
| СПОСОБ ВЫБОРА ПАЦИЕНТОВ С ХРОНИЧЕСКИМИ ТИКОЗНЫМИ РАССТРОЙСТВАМИ ДЛЯ НАЗНАЧЕНИЯ ЛЕЧЕНИЯ ВАЛЬПРОАТАМИ | 2014 |
|
RU2562894C1 |
| Способ оценки знаний учащегося при компьютерном тестировании | 2016 |
|
RU2640709C1 |
| СПОСОБ ДЕТЕКТИРОВАНИЯ ЭПИЛЕПТИФОРМНЫХ РАЗРЯДОВ В ДЛИТЕЛЬНОЙ ЗАПИСИ ЭЭГ | 2020 |
|
RU2747712C1 |
Группа изобретений относится к медицине и может быть использована для автоматической оценки ЭЭГ абсанса. Группа изобретений представлена способом, машиночитаемым носителем и устройством для автоматической оценки ЭЭГ абсанса. Кривые ЭЭГ записывают устройством оценки. Посредством компьютера устройства проводят их оценку. Определяют по меньшей мере текущую стадию состояния абсанса. Причем в разделении на стадии различают глубины состояния абсанса. Выбирают определенную схему разделения на стадии из нескольких предоставленных для выбора схем разделения на стадии, которые различаются количеством различимых стадий состояния абсанса. Осуществляют автоматическое разделение на стадии для определения текущей стадии. Группа изобретений позволяет проводить автоматическую оценку ЭЭГ абсанса за счет возможности выбора определенной схемы разделения на стадии из нескольких предоставленных для выбора схем разделения на стадии. 3 н. и 9 з.п. ф-лы, 3 ил., 1 табл.
1. Способ автоматической оценки ЭЭГ абсанса, при котором кривые ЭЭГ записывают устройством (1) оценки и посредством компьютера (2) устройства (1) оценки оценивают, причем при оценке из кривых ЭЭГ посредством компьютера (2) на основе разделения на стадии ЭЭГ абсанса определяют по меньшей мере текущую стадию состояния абсанса пациента, причем в разделении на стадии различают стадии глубины состояния абсанса и причем выдают текущую стадию, отличающийся тем, что с помощью компьютера (2) выбирают определенную схему разделения на стадии из нескольких предоставленных для выбора схем разделения на стадии, которые различаются количеством различимых стадий состояния абсанса, и применяют автоматическое выполнение разделения на стадии для определения текущей стадии.
2. Способ по п. 1, отличающийся тем, что показания о возрасте пациента, кривые ЭЭГ которого записывают, вводят в устройство (1) оценки, и выполняют компьютером (2) автоматический выбор схемы разделения на стадии с учетом введенных показаний о возрасте.
3. Способ по любому из предыдущих пунктов, отличающийся тем, что автоматический выбор схемы разделения на стадии выполняют компьютером (2) с учетом записанных кривых ЭЭГ и/или производных из них данных.
4. Способ по любому из предыдущих пунктов, отличающийся тем, что при распознавании определенной минимальной доли низкочастотных сигнальных составляющих и нераспознавании определенной минимальной доли высокочастотных сигнальных составляющих в кривых ЭЭГ выбирают схему с меньшим количеством различимых стадий состояния абсанса, чем при распознавании определенной минимальной доли высокочастотных сигнальных составляющих, которые могут комбинироваться с определенной минимальной долей низкочастотных сигнальных составляющих.
5. Способ по любому из предыдущих пунктов, отличающийся тем, что компьютер (2) первоначально исходит из первой схемы с определенным количеством различимых стадий состояния абсанса и выбирает к моменту времени принятия решения, к которому имеется достаточное количество данных ЭЭГ, при распознавании определенных характеристик в кривых ЭЭГ, вторую схему разделения на стадии, которая имеет меньшее или большее количество различимых стадий состояния абсанса, чем первая схема.
6. Способ по любому из предыдущих пунктов, отличающийся тем, что по меньшей мере частотные составляющие в дельта-полосе оценивают как низкочастотные сигнальные составляющие кривых ЭЭГ.
7. Способ по любому из предыдущих пунктов, отличающийся тем, что кроме стандартной схемы разделения на стадии компьютером (2) могут выбираться дополнительная схема или в зависимости от степени развития пациента несколько дополнительных схем разделения на стадии, в частности разделения на стадии с меньшим количеством различимых стадий состояния абсанса, чем в стандартной схеме.
8. Способ по любому из предыдущих пунктов, отличающийся тем, что на основе выбранной схемы разделения на стадии определяют степень развития ЭЭГ.
9. Способ по любому из предыдущих пунктов, отличающийся тем, что кривые ЭЭГ анализируют на паттерны кривых, генерируемых дополнительными биосигналами, и, если распознают по меньшей мере один такой паттерн кривой, то проверяют, следует ли выбрать схему для разделения на стадии, иную, чем при нераспознавании таких паттернов кривых.
10. Способ по любому из предыдущих пунктов, отличающийся тем, что посредством датчиков (5) артефактов определяют артефакты движения в записанных кривых ЭЭГ и на основе определенных артефактов движения корректируют кривые ЭЭГ, и/или корректируют разделение на стадии, и/или подавляют, и/или выбирают другую схему разделения на стадии.
11. Машиночитаемый носитель, содержащий компьютерную программу со средствами программного кода, выполненную с возможностью выполнения способа по любому из предыдущих пунктов, причем компьютерная программа выполняется на компьютере (2).
12. Устройство (1) оценки для оценки ЭЭГ абсанса, причем устройство (1) оценки содержит по меньшей мере один компьютер (2), средство (7) регистрации сигналов ЭЭГ и средство (3) вывода, отличающееся тем, что устройство (1) оценки выполнено с возможностью осуществления способа по любому из пп. 1-10.
| WO 9715013 A2, 24.04.1997 | |||
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 1991 |
|
RU2039524C1 |
| СПОСОБ ИССЛЕДОВАНИЯ ЭЛЕКТРОЭНЦЕФАЛОГРАММЫ ЧЕЛОВЕКА И ЖИВОТНЫХ | 2007 |
|
RU2332160C1 |
| US 6117074 A, 12.09.2000 | |||
| ГНЕЗДИЦКИЙ В.В | |||
| Современные технологии длительного мониторинга ЭЭГ и полиграфических показателей в неврологической практике | |||
| Журнал международной медицины, N 2 (3) 2013, стр | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| SCHULTZ A | |||
| Age-related effects in the EEG during propofol anaesthesia | |||
| Acta Anaesthesiol Scand | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2018-05-23—Публикация
2015-01-27—Подача