Изобретение относится к способам обработки воды и может быть использовано преимущественно в области хозяйственно-питьевого водоснабжения, в частности при получении питьевых вод.
Из уровня техники известны способы обработки воды коагулированием, включающие добавление к воде минеральных солей с гидролизующимися катионами, анодное растворение металлов или простое изменение рН среды, если в обрабатываемой воде уже содержатся в достаточном количестве катионы, способные образовывать при гидролизе малорастворимые соединения. В практике очистки питьевых вод в качестве коагулянтов обычно используются соли алюминия, соли железа или их смеси в разных пропорциях. В редких случаях находят применение соли магния, цинка и титана (Бабенков Е.В. Очистка воды коагулянтами. - М.: Наука, 1977, с. 72).
Известен способ очистки питьевой воды, включающий ее обработку сульфатом алюминия с пропусканием через фильтр (Бабенков Е.В. Очистка воды коагулянтами. - М.: Наука, 1977, с. 7). Недостатком известного способа является недостаточно высокая степень осветления воды, а также высокая коррозионная агрессивность воды, приводящая к вторичному загрязнению водопроводной воды соединениями железа при ее транспортировке по стальным трубопроводам и, как следствие, превышению показателя «железо общее» над нормативным значением (0,3 мг/дм3) и повышению аварийности трубопроводной системы из-за коррозионных повреждений.
Известен наиболее близкий по совокупности существенных признаков, выбранный в качестве прототипа способ очистки питьевой воды, включающий проведение контактной коагуляции сульфатом алюминия с фильтрацией на загрузке зернистых контактных осветлителей. На второй стадии очистки в воду вводят оксихлорид алюминия в количестве 1:(4-5) по Al2O3 по отношению к количеству ранее введенного сульфата алюминия. Суммарное количество введенных алюминийсодержащих коагулянтов определяется из соотношения  где Dк - суммарное количество коагулянта, мг/л; Ц - цветность очищаемой воды, град. В качестве загрузки зернистых контактных осветлителей использована колонка, загруженная гранитной крошкой (патент РФ №2218310 на изобретение «Способ очистки маломутных цветных вод», МПК C02F 1/52, C02F 103:04, опубл. 02.10.2002). Контактная коагуляция улучшает показатели процесса очистки воды. Термин «контактная коагуляция» характеризует сумму явлений, происходящих при пропускании коагулированной воды через слой зернистых материалов. Коагуляция в контакте с посторонней твердой поверхностью в отличие от коагуляции в объеме воды: 1) протекает быстрее; 2) требует меньших доз коагулянта; 3) менее чувствительна к температуре воды; 4) удовлетворительно протекает даже при малой мутности и низком щелочном резерве исходной воды (Бабенков Е.В. Очистка воды коагулянтами. - М.: Наука, 1977, с. 200). Вместе с тем, известный способ также характеризуется высокой коррозионной агрессивностью воды, что приводит к ее вторичному загрязнению соединениями железа при транспортировке по стальным трубопроводам и, как следствие, превышению показателя «железо общее» над нормативным значением (0,3 мг/дм3) и повышению аварийности трубопроводной системы из-за коррозионных повреждений. В результате образования на стенках водопроводных труб отложений снижается их пропускная способность.
где Dк - суммарное количество коагулянта, мг/л; Ц - цветность очищаемой воды, град. В качестве загрузки зернистых контактных осветлителей использована колонка, загруженная гранитной крошкой (патент РФ №2218310 на изобретение «Способ очистки маломутных цветных вод», МПК C02F 1/52, C02F 103:04, опубл. 02.10.2002). Контактная коагуляция улучшает показатели процесса очистки воды. Термин «контактная коагуляция» характеризует сумму явлений, происходящих при пропускании коагулированной воды через слой зернистых материалов. Коагуляция в контакте с посторонней твердой поверхностью в отличие от коагуляции в объеме воды: 1) протекает быстрее; 2) требует меньших доз коагулянта; 3) менее чувствительна к температуре воды; 4) удовлетворительно протекает даже при малой мутности и низком щелочном резерве исходной воды (Бабенков Е.В. Очистка воды коагулянтами. - М.: Наука, 1977, с. 200). Вместе с тем, известный способ также характеризуется высокой коррозионной агрессивностью воды, что приводит к ее вторичному загрязнению соединениями железа при транспортировке по стальным трубопроводам и, как следствие, превышению показателя «железо общее» над нормативным значением (0,3 мг/дм3) и повышению аварийности трубопроводной системы из-за коррозионных повреждений. В результате образования на стенках водопроводных труб отложений снижается их пропускная способность.
Задачей, на решение которой направлено заявляемое техническое решение, является разработка высокоэффективного способа обработки питьевой воды.
Техническими результатами, достигаемыми в результате решения поставленной задачи, являются снижение коррозионной агрессивности питьевой воды и минимизация негативного влияния агрессивной жидкой среды на материал стальных трубопроводов, что в целом обеспечивает повышение срока службы трубопроводов, снижение аварийности трубопроводной системы из-за коррозионных повреждений, снижение концентрации общего железа у потребителя до нормативных требований, увеличение пропускной способности трубопровода.
Указанные технические результаты достигаются тем, что способ очистки питьевой воды включает проведение контактной коагуляции сульфатом алюминия с фильтрацией на зернистой загрузке контактных осветлителей и последовательное введение хлористого кальция и соды технической. При этом введение хлористого кальция осуществляют до обработки коагулянтом, а введение соды технической осуществляют после фильтровальных сооружений перед резервуарами чистой воды.
Контактную коагуляцию осуществляют сульфатом алюминия с дозой 0,75÷0,8 мг/дм3 по Al2O3.
Доза по активному веществу соды составляет 7÷9 мг/ дм3, а доза по активному веществу хлористого кальция составляет 15÷20 мг/ дм3.
Предпочтительно, чтобы фильтрование осуществляли на песчаной загрузке контактных осветлителей.
Предпочтительно, чтобы способ очистки питьевой воды включал дохлорирование гипохлоритом натрия.
Сопоставительный анализ заявляемого технического решения с прототипом показал, что во всех случаях выполнения оно отличается от известного, наиболее близкого технического решения:
- последовательным введением хлористого кальция и соды технической;
- введением хлористого кальция до обработки коагулянтом;
- введением соды технической перед резервуарами чистой воды.
В предпочтительном случае выполнения заявляемое техническое решение отличается от известного, наиболее близкого технического решения:
- проведением контактной коагуляции сульфатом алюминия с дозой 0,75÷0,8 мг/дм3 по Al2O3;
- выполнением дозы по активному веществу соды, составляющей 7÷9 мг/дм3;
- выполнением дозы по активному веществу хлористого кальция, составляющей 15÷20 мг/дм3;
- фильтрованием на песчаной загрузке контактных осветлителей;
- дохлорированием гипохлоритом натрия.
Раздельный ввод реагентов позволяет предотвратить преждевременное осаждение карбоната кальция в водоочистных сооружениях вследствие возможного создания местных пересыщений по ионам кальция и карбонат-ионам ввиду неравномерного дозирования и перемешивания. При движении воды, перенасыщенной карбонатом кальция (с положительным индексом насыщения), в трубах образуются сплошные отложения, которые располагаются эксцентрично с утолщением в донной части трубы. В связи с коррозионным действием воды в стальных и чугунных трубах образуются бугристые отложения, отличающиеся прочностью и сильным сцеплением со стенками трубы. Коррозия (от лат. corrosio - «разъедание») представляет собой самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Коррозия труб может вызываться разнообразными агрессивными средами, к которым относятся воздух, реагенты, употребляемые для обработки воды и пр. Усиление агрессивного воздействия воды при очистке объясняется нарушением в ней карбонатного равновесия, поскольку при добавлении в воду 1 мг AL2(SO4)3 выделяется около 0,8 мг CO2 вследствие разложения гидрокарбонатов. Вода при этом становится нестабильной, т.е. способной растворять защитные пленки на внутренней поверхности трубопроводов в результате появления в ней агрессивной угольной кислоты. При оголении поверхности трубопроводов усиливается электрохимическая коррозия, которой благоприятствует присутствие растворенного в воде O2. Вода обогащается продуктами коррозии, ухудшающими ее вкусовые качества. Кислородная коррозия железа в воде (Кульский Л.А., Строкам П.П. Технология очистки природных вод. - Киев: Вища школа, 1986, с.29):
4Fe+3O2+2H2O=2Fe2O3⋅H2O.
Предусмотренный заявляемым способом порядок ввода реагентов обеспечивает сохранение условий коагуляции загрязняющих веществ сульфатом алюминия (химизм действия сернокислого алюминия значительно зависит от рН воды). Стабилизация предполагает повышение индекса Ланжелье до положительных значений, что приводит к образованию защитной пленки на внутренней поверхности трубопроводов. Индекс Ланжелье (LSI) - это разница между текущим водородным показателем воды (рН) и показателем (pHs), при котором происходит выделение из воды твердой фазы карбоната кальция CaCO3
LSI=pH-pHs.
Снижение агрессивности воды обеспечивает снижение скорости коррозии, что, в свою очередь, приводит к увеличению срока службы трубопроводов и снижению концентрация общего железа у потребителя в пределах предельно допустимого количества. Снижение агрессивности воды обуславливает значительное снижение необходимых доз реагентов по отношению к стабилизации.
Обработка воды хлоридом кальция и содой в целом оказывает положительное влияние на коррозионную стойкость стали. Проведенные испытания показали, что практически на всем протяжении водопроводных сетей скорость коррозии стали в результате обработки воды снижается в 1,4-1,7 раза, что позволяет устойчиво обеспечивать требуемое качество воды по такому показателю, как содержание железа в воде.
Фильтрование на песчаной загрузке контактных осветлителей обеспечивает высокую степень очистки от механических примесей, а дохлорирование гипохлоритом натрия обеспечивает пролонгирование эффекта предотвращения ухудшения свойств воды по микробиологическим показателям.
Заявляемое изобретение иллюстрируется материалами, представленными на Фиг. 1-6.
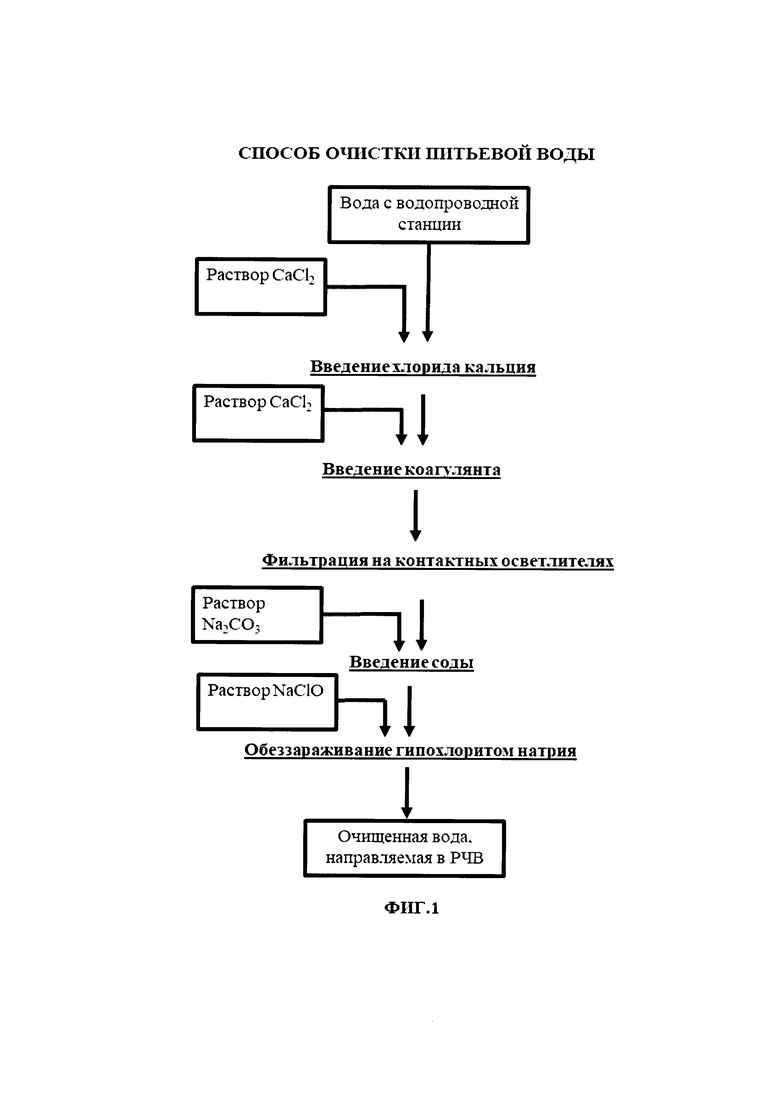
На Фиг. 1 представлена схема способа очистки питьевой воды.
На Фиг. 2 представлена диаграмма зависимости содержания железа в воде от индекса Ланжелье для воды в точке «пос. Солнечное» при очистке воды с использованием заявляемого способа и без него.
На Фиг. 3 представлена диаграмма зависимости содержания железа в воде от индекса Ланжелье в отдельных точках (Сестрорецк, ул. Токарева, 15; Санкт-Петербург, Приморское шоссе, 294, пос. Солнечное).
На Фиг. 4 представлен график взаимосвязи величины равновесного электрохимического потенциала с величиной скорости коррозии углеродистой стали в воде.
На Фиг. 5: в таблице 1 представлены сведения о скорости коррозии стали Ст20 в водных растворах различного состава; в таблице 2 представлены сведения об элементном составе пленок образцов-свидетелей.
На Фиг. 6 в таблице представлены сведения о коррозионных характеристиках образцов-свидетелей, установленных в различных точках Сестрорецкой водопроводной системы.
Способ очистки питьевой воды осуществляется следующим образом.
Заявляемый способ применяется для доочистки водопроводной воды, поступающей по распределительной трубопроводной системе от водопроводной станции. Поступающая на станцию вода, вследствие вторичного загрязнения за счет коррозии стальных труб, содержит до 0,4-0,5 мг/дм3 железа. Технологический процесс очистки состоит в проведении контактной коагуляции сульфатом алюминия, предпочтительно с дозами 0,75÷0,8 мг/дм3, совмещенной с фильтрацией на песчаной загрузке контактных осветлителей. С целью обеспечения пролонгированного эффекта предотвращения ухудшения свойств воды по микробиологическим показателям предусмотрено дохлорирование питьевой воды. В питьевую воду последовательно вводятся два реагента: хлористый кальций и сода техническая. Хлористый кальций вводится до контактных осветлителей, сода техническая вводится перед резервуарами чистой воды. Раздельный ввод реагентов позволяет предотвратить преждевременной осаждение карбоната кальция в водоочистных сооружениях вследствие возможного создания местных пересыщений по ионам кальция и карбонат-ионам ввиду неравомерного дозирования и перемешивания. Указанный порядок ввода реагентов необходим также для сохранения условий коагуляции загрязняющих веществ сульфатом алюминия (химизм действия сернокислого алюминия значительно зависит от рН воды). В итоге образуется карбонат кальция, рН воды увеличивается до 7,3-7,5, жесткость питьевой воды увеличивается с 0,9 до 1,3 ммоль/дм3. Технология снижения агрессивности питьевой воды основана на применении водных растворов карбоната натрия (10%-ный раствор) и хлористого кальция (32%-ный раствор).
В результате химических реакций взаимодействия активных веществ - применяемых химических реагентов с водой, и продуктов реакции гидролиза обоих реагентов образуется карбонат кальция, наличие которого в питьевой воде создает условия снижения скорости коррозии трубопроводов при транспортировке воды:
Na2CO3+H2O=NaHCO3+NaOH,
CaCl2+NaOH=CaOHCl+NaCl,
CaOHCl+NaHCO3=CaCO3+NaCl+H2O.
Дозы применяемых реагентов выбираются с учетом обеспечения рН питьевой воды на уровне 7,3-7,5, мольного соотношения участвующих в реакции веществ (соды-хлористого кальция). Выявлена сезонная зависимость от температуры обрабатываемой воды. При снижении температуры воды до 0,1°С дозы реагентов увеличиваются. Дозы по активному веществу соды: 7-9 мг/дм3, хлористого кальция - 15-20 мг/дм3.
Снижение коррозионной активности питьевой воды достигается за счет повышения рН обрабатываемой воды (предпочтительно до 8,5-8,9) и увеличения индекса Ланжелье (предпочтительно до значений -0,2 - +0,1). По результатам проведенных испытаний, фактическое значение индекса Ланжелье было достигнуто на уровне -0,15, что обеспечило сохранение качества воды в распределительной сети г. Сестрорецка. Диаграмма, представленная на фиг. 2, иллюстрирует зависимость содержания железа в воде от индекса Ланжелье для воды в точке «пос. Солнечное» при очистке воды с использованием заявляемого способа и без него (при отсутствии дозирования реагентов). Диаграмма, представленная на фиг. 3, иллюстрирует зависимость содержания железа в воде от индекса Ланжелье в отдельных точках: Сестрорецк, ул. Токарева, 15; Санкт-Петербург, Приморское шоссе, 294, пос. Солнечное.
Были апробированы режимы дозирования обоих реагентов хлористого кальция и соды с целью обеспечения благоприятных характеристик питьевой воды и сохранения эффекта снижения агрессивности питьевой воды. Апробированные режимы и изменение скорости коррозии приведены в таблице 1 (фиг.5).
Для контроля скорости коррозии были использованы:
- гравиметрический метод (определение потери массы образца за определенное время испытаний) - по ГОСТ 9502-82 «Единая система защиты от коррозии и старения. Ингибиторы коррозии металла для водных систем. Методы коррозионных испытаний». Взвешивание образцов-свидетелей осуществляли с точностью ±.0001 мг;
- метод контроля скорости коррозии путем измерения равновесного электрохимического потенциала (РЭХП) металла, из которого выполнен образец-свидетель при помещении последнего в воду, отобранную в точке нахождения образца-свидетеля или в стандартный буферный водный раствор.
В качестве электрода сравнения использовался хлор-серебряный электрод. Стандартный буферный раствор представлял собой раствор бората калия с концентрацией соли 0,1 моль/л и величиной рН 7,1-7,2. Метод основан на наличии корреляции между величиной РЭХП и скоростью коррозии металла в воде. Калибровочный график РЭХП=f(Vкоррозии) позволяет по определяемой экспериментально величине потенциала находить скорость коррозии металла. Метод отличается высокой оперативностью и простотой конструктивного исполнения. Для построения калибровочного графика используются данные гравиметрического определения скорости коррозии и данные, полученные при измерении соответствующих значений РЭХП. Такой калибровочный график, связывающий скорость коррозии, выраженную в г/м2⋅ч, с величиной равновесного электрохимического потенциала, выраженного в мВ, представлен на фиг. 4.
Было проведено изучение состава поверхностных отложений продуктов коррозии, сформировавшихся на образцах-свидетелях, установленных в различных частях исследуемых водопроводных систем. После удаления отложений механическим методом они подвергались растворению в соляной кислоте, после чего проводили анализ полученных растворов на содержание железа и кальция трилонометрическим методом. В результате проведенных исследований установлено, что основу отложений составляют железооксидные продукты коррозии. Содержание кальция в данных продуктах коррозии не превышает 1-5 масс. %.
Элементный состав образцов-свидетелей (данные приведены в таблице на фиг.5) свидетельствуют о том, что основу защитных поверхностных пленок составляют соединения железа с относительно небольшим включением в них соединений кальция. Соединения железа представлены в основном, гематитом (Fe2O3) и лепидокрокитом (FeOOH). Проведение коррекционной обработки воды приводит к изменению состава поверхностных пленок - помимо гематита и лепидокрокита отмечается появление магнетита (Fe3O4) и соединений кальция.
Таким образом, обработка воды хлоридом кальция и содой оказывает положительное влияние на коррозионную стойкость стали. Так, на Сестрорецкой ВС, практически на всем протяжении водопроводных сетей скорость коррозии стали в результате обработки воды снижается в 1,4-1,7 раза, что позволяет устойчиво обеспечивать требуемое качество воды по такому показателю, как содержание железа в воде. Исходный состав воды оказывает существенное влияние на эффективность ее коррекционной обработки, проводимой с целью защиты металла от коррозии. Так, при практически одинаковом регламенте обработки воды на Сестрорецкой и Петродворцовой водопроводных системах, эффект защиты металла от коррозии для двух указанных систем отличается - для Сестрорецкой ВС он значительно выше. Очевидно, что технологический регламент должен настраиваться на конкретную систему и должен учитывать ее особенности, в частности, необходимо принимать во внимание особенности химического состава исходной воды, формирование потоков исходной воды и другие факторы. Образующиеся на стали защитные пленки образованы, в основном, железооксидными продуктами коррозии. Коррекционная обработка воды приводит к изменению состава защитных пленок. В частности, отмечается появление включений магнетита и небольших количеств кальция. Эффективность защиты металла от коррозии при формировании таких пленок возрастает. Величина рН воды оказывает существенное влияние на скорость протекания коррозионных процессов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ ПИТЬЕВОЙ ВОДЫ | 2024 |
|
RU2836367C1 |
| Способ стабилизационной обработки питьевой воды | 2023 |
|
RU2836717C1 |
| КОАГУЛЯНТ ТИТАНОВЫЙ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ОЧИСТКИ НЕФТЕСОДЕРЖАЩИХ ПЛАСТОВЫХ СОЛЕНЫХ ВОД ДО ВОДЫ ПИТЬЕВОГО КАЧЕСТВА, СПОСОБ ОЧИСТКИ НЕФТЕСОДЕРЖАЩИХ ПЛАСТОВЫХ СОЛЕНЫХ ВОД ДО ВОДЫ ПИТЬЕВОГО КАЧЕСТВА (ВАРИАНТЫ) И КОМПЛЕКСНАЯ СИСТЕМА ДЛЯ ОЧИСТКИ НЕФТЕСОДЕРЖАЩИХ ПЛАСТОВЫХ СОЛЕНЫХ ВОД ДО ВОДЫ ПИТЬЕВОГО КАЧЕСТВА | 2007 |
|
RU2367618C2 |
| ЭКСПРЕСС-МЕТОД ПРИГОТОВЛЕНИЯ ПИТЬЕВОЙ ВОДЫ ИЗ ПРИРОДНЫХ ИСТОЧНИКОВ | 2016 |
|
RU2633898C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТЬЕВОЙ ВОДЫ | 2002 |
|
RU2220115C1 |
| СПОСОБ ОЧИСТКИ ПРИРОДНЫХ И СТОЧНЫХ ВОД | 2004 |
|
RU2250877C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТЬЕВОЙ ВОДЫ | 1997 |
|
RU2122982C1 |
| КОАГУЛЯНТ ДЛЯ ОЧИСТКИ ПРИРОДНЫХ И СТОЧНЫХ ВОД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 2000 |
|
RU2195434C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАПИТКА "ИСЦЕЛЕНИЕ" | 2004 |
|
RU2281003C2 |
| Коагулянт титановый для очистки природных и сточных вод, способ его получения и использование в подтоварных водах и потокоотклоняющих технологиях | 2021 |
|
RU2772365C1 |





Изобретение может быть использовано в области хозяйственно-питьевого водоснабжения при получении питьевых вод. Для осуществления способа проводят контактную коагуляцию сульфатом алюминия с фильтрацией на загрузке зернистых контактных осветлителей и последовательное введение хлористого кальция и соды технической. При этом введение хлористого кальция осуществляют до обработки коагулянтом, а введение соды технической осуществляют после фильтровальных сооружений перед резервуарами чистой воды. Контактную коагуляцию сульфатом алюминия проводят дозой 0,75÷0,8 мг/дм3 по Al2O3. Хлористый кальций вводят дозой по активному веществу 15÷20 мг/дм3, а доза по активному веществу соды составляет 7÷9 мг/дм3. Фильтрование осуществляют в контактных осветлителях на песчаной загрузке. В предпочтительном варианте проводят дохлорирование очищенной воды гипохлоритом натрия. Способ представляет высокоэффективную технологию очистки питьевой воды, при этом обеспечиваются снижение коррозионной агрессивности обработанной воды, что приводит к повышению срока службы трубопроводов, снижению аварийности трубопроводной системы из-за коррозионных повреждений, снижение концентрации общего железа у потребителя до нормативных требований, увеличение пропускной способности трубопровода. 2 з.п. ф-лы, 6 ил.
1. Способ очистки питьевой воды, включающий проведение контактной коагуляции сульфатом алюминия с фильтрацией на зернистой загрузке контактных осветлителей, отличающийся тем, что включает последовательное введение хлористого кальция дозой по активному веществу 15÷20 мг/дм3, сульфата алюминия дозой 0,75÷0,8 мг/дм3 по Al2O3, соды технической дозой по активному веществу 7÷9 мг/дм3, при этом введение хлористого кальция осуществляют до обработки коагулянтом, а введение соды технической осуществляют после фильтровальных сооружений, перед резервуарами чистой воды.
2. Способ очистки питьевой воды по п. 1, отличающийся тем, что фильтрование осуществляют на зернистой песчаной загрузке контактных осветлителей.
3. Способ очистки питьевой воды по любому из пп. 1-4, отличающийся тем, что включает дохлорирование гипохлоритом натрия.
| СПОСОБ ОЧИСТКИ МАЛОМУТНЫХ ЦВЕТНЫХ ВОД | 2002 |
|
RU2218310C1 |
| СПОСОБ ОЧИСТКИ СТОЧНЫХ ВОД (ВАРИАНТЫ) | 1992 |
|
RU2106312C1 |
| RU 2015114037 А, 10.11.2016 | |||
| СПОСОБ РЕГУЛИРОВАНИЯ ПРОЦЕССОВ ОЧИСТКИ ВОДЫ В КОНТАКТНЫХ ОСВЕТЛИТЕЛЯХ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2011 |
|
RU2471719C1 |
| US 5246686 A, 21.09.1993 | |||
| Способ определения кадмия | 1990 |
|
SU1778688A1 |
| CN 102020345 A, 20.04.2011. | |||
Авторы
Даты
2018-06-19—Публикация
2017-02-26—Подача