Изобретение относится к области медицины, конкретно к новому химическому соединению - L-энантиомеру 2-этил-6-метил-3-гидроксипиридиния L-гидроксибутандиоату, обладающему церебропротекторной активностью.
Цель изобретения - новое химическое соединение, обладающее церебропротекторными и другими видами активности.
Поставленная цель достигается новым соединением, а именно, энантиомером - 2-этил-6-метил-3-гидроксипиридиния L-гидроксибутандиоатом.
Уровень техники
Одним из перспективных направлений, развиваемых отечетсенными фармакологами, является изыскание и создание инновационных отечественных лекарственных препаратов в ряду производных гидроксипиридина.
Среди производных 2-этил-6-метил-3-гидроксипиридина известен ряд препаратов, обладающих широким спектром биологической активности.
В начале 1980-х гг. в ГУ НИИ Фармакологии РАМН Смирнов Л.Д. и Кузьмин В.И. синтезировали Мексидол - сукцинат 2-этил-6-метил-3-оксипиридина. Мексидол - препарат с поликомпонентным спектром фармакологических эффектов и многофакторным механизмом действия. Наиболее важными компонентами механизма действия Мексидола являются его антиоксидантные, мембранотропные эффекты, способность модулировать функционирование рецепторов и мембрано-связанных ферментов и восстанавливать нейромедиаторный баланс. (Мексидол: основные нейропсихотропные эффекты и механизм действия. Т.А. Воронина. ГУ "НИИ Фармакологии им. В.В. Закусова". М., РАН).
Мексидол широко применяется в медицине, а также ветеринарии в качестве антиоксидантного и антигипоксического средства, характеризующегося широким спектром фармакологического действия и высокой эффективностью (ноотропное и транквилизирующее действие - пат. RU 2065299, противоишемическое и антиатеросклеротическое действие - пат. RU 2144822, антиангинальное - пат. RU 2168993, гепатопротекторное - пат. RU 2189817, антибактериальное - пат. RU 2157686 и др.).
Известны композиции на основе 2-этил-6-метил-3-гидроксипиридина сукцината в виде различных лекарственных форм: раствора для парентерального введения (Приказ МЗ РФ от 31.12.1996 №432 «Раствор Мексидола® 5% для инъекций», пат. RU 2205640, 2380089, 2398583), таблеток (Приказ МЗ РФ от 26.01.1998 №21 «Мексидол® таблетки, покрытые оболочкой, 0,125 г»), капсул (пат. RU 2144822, 2145855), перевязочного материала (пат. RU 2149648) и др.
Предложена фармацевтическая композиция в виде таблеток для перорального применения на основе 2-этил-6-метил-3-гидроксипиридина сукцинат (RU 2444359).
Известно также лекарственное средство Этоксидол - 2-этил-6-метил-3-гидроксипиридиний гидроксибутандиоат (рацемат), обладающий противоишемической, церебропротекторной, нейротропной и липидрегулируемой активностями (RU 2377237), формулы:
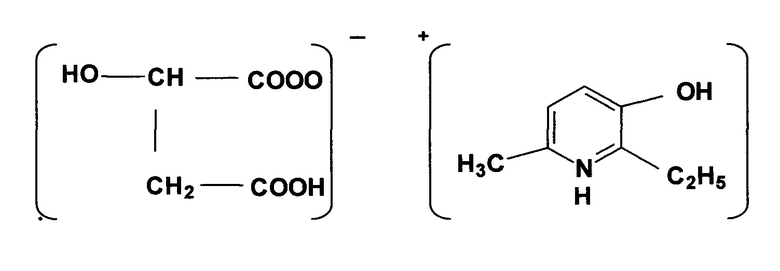
а также фармацевтические композиции, содержащие Этоксидол: таблетки, растворы для инъекций.
Показано, что Этоксидол в дозе 10 мг/кг устраняет фибрилляцию желудочков при окклюзии коронарных артерий и снижает количество животных, у которых возникает фибрилляция желудочков до 2 из 8 опытных в дозе 10 мг/кг и 2 из 9 - в дозе 23 мг/кг.
Этоксидол достоверно увеличивает порог фибрилляции желудочков миокарда кошек в дозе 23,0 мг/кг в период с 5 до 60 мин после окклюзии коронарных артерий, в то время как Анаприлин обладает таким эффектом в изотоксической дозе в период с 30 по 60 мин.
В условиях острой ишемии миокарда в дозе 15 мг/кг оказывает отчетливое кардиопротективное действие на кардиогемодинамику, приближая значения сократимости (dP/dt), АД и др. до уровня интактного контроля.
Этоксидол в дозе 1 мг/кг обладает способностью снижать интенсивность проявления процессов перекисного окисления липидов, вызванных иммобилизацией кроликов в течение 30 дней, о чем свидетельствует снижение уровня малонового диальдегида (МДА) в плазме крови на 46% и в ткани почек. При этом уровень общего холестерина снижается на 41,7%, а индекс атерогенности снижается на 82,9%.
Успехи стереофармакологии, достигнутые за последние десятилетия, обогатили науку пониманием универсальных закономерностей: структура - активность и структура - токсичность, которым подчиняются вещества, являющихся рацемическими смесями лево- и правовращающих изомеров, были получены D- и L-энантиомеры, обладающие различными фармакологическими свойствами. Исследования показали, что левовращающие изомеры, как правило, более токсичны, но и более активны, тогда как правовращающие и рацематы уступают левовращающим по силе фармакологического эффекта.
Классический пример - L-адреналин: его внутрисердечная концентрация в 11 раз выше, чем правовращающего изомера. Высокой стереоспецифичностью характеризуются рецепторные взаимодействия, в том числе процессы печеночного метаболизма, которые также определяются характером взаимосвязи лекарство-рецептор.
Клинические исследования S-амлодипина. Антигипертензивный и антиангинальный эффекты S-амлодипина подтверждаются результатами клинических исследований. Показано, что для достижения оптимального терапевтического действия S-амлодипина требуются вдвое меньшие дозы препарата.
В настоящее время только 15% лекарственных средств - это хирально чистые вещества, то есть состоящие из энантиомеров одного типа. Использование оптических изомеров известных сердечно-сосудистых средств - путь к повышению их эффективности и переносимости (М.И. Лутай, А.Ф. Лысенко, О.И. Моисеенко. Национальный научный центр "Институт кардиологии им. акад. Н.Д. Стражеско" АМН Украины, г. Киев).
Раскрытие изобретения
Целью изобретения является новое химическое соединение -L-энантиомер 2-этил-6-метил-3-гидроксипиридиния L-гидроксибутандиоата (соединение 1), а также изучение его антигипоксической активности с учетом требований, предъявляемых к доклиническому исследованию лекарственных средств:
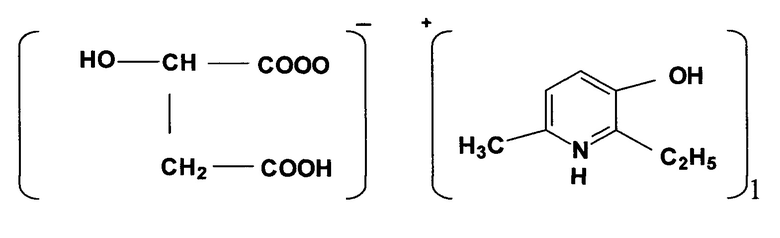 .
.
1. Синтез L-энантиомера 2-этил-6-метил-3-гидроксипиридиния L-гидроксибутандиоата.
Пример 1.
К 13,7 г (0,1 м) 2-этил-6-метил-3-гидроксипиридина присыпают 13,41 г (0,1 м) L-гидроксибутандиовой кислоты, массу тщательно перемешивают и нагревают до плавления при 100-110°С. К полученному плаву постепенно при перемешивании приливают 120 мл воды, полученный раствор фильтруют, отгоняют 60-70% воды в вакууме, к полученному остатку приливают 80 мл ацетона, массу кристаллизуют, полученный осадок отфильтровывают и сушат в вакууме. Получают 23,8 г белого кристаллического вещества, обладающего высокой гигроскопичностью, расплывается на воздухе.
C12H17NO6
Найдено, %: С 53,07; Н 6,38; N 5,11.
Вычислено, %: С 53,14; Н 6,27; N 5,17.
ИК-спектр, ν см-1: 3510, 3230, 1660, 1610, 1560, 1292, 1161.
УФ-спектр, нм: 228,291 (вода)
Угол вращения [α]D20 -13,6 (4,5% ацетонитрил).
2. Биологические исследования
Общая характеристика лабораторных животных
Исследования проведены на 69 белых SHK мышах самцах, 69 белых SHK мышах самках весом 20-22 г, полученных из питомника Филиала «Андреевка» ФГБНУ НЦБМТ ФМБА, Россия.
Количество животных
Формирование групп животных по 6 мышей каждого пола для проведения эксперимента по изучению острой токсичности и антигипоксической активности является репрезентативной выборкой и позволяет по многолетнему опыту токсикологических исследований получить статистически достоверные данные. Во время эксперимента животные содержались в контролируемых условиях: температура окружающего воздуха 20-24°C, относительная влажность 50-60%.
2.1. Определение острой токсичности соединения 1
В настоящем исследовании острую токсичность оценивали на мышах обоего пола при однократном внутривенном введении соединения 1 и препарата сравнения.
Белым аутбредным мышам (по 6 голов каждого пола в группе) вводили соединение 1 или препарат сравнения в нарастающих дозах 300, 400, 500, 600, 700 мг/кг веса животного в виде раствора в воде для инъекций общим объемом 0,5 мл, допустимого для данного вида животных.
Наблюдение за животными проводили в течение не менее 14 дней после введения. О токсичности препаратов судили по гибели животных и общей картине интоксикации.
Фиксировали общее состояние животных: особенности их поведения, интенсивность и характер двигательной активности, наличие и характер судорог, координацию движений, тонус скелетных мышц, реакцию на тактильные, болевые раздражители, частоту и глубину дыхательных движений, состояние волосяного и кожного покрова. Производили подсчет количества погибших животных в ходе эксперимента.
Полученные данные обрабатывались общепринятым методом вариационной статистики с вычислением среднего значения (М) и стандартной ошибки среднего значения (m). В качестве критерия оценки достоверности различия средних величин использовали парный критерий t Стьюдента с поправкой Бонферрони при уровне значимости Р<0,05, для определения достоверности различий абсолютных величин использовали непараметрический критерий «хи-квадрат», при объеме выборки менее 10 - точный критерий Фишера, для определения достоверности различий до и после введения фармакологического агента использовали критерий Уилкоксона.
На основании полученных результатов определяли характеристики «острой» токсичности с помощью пробит-анализа по Миллеру и Тейнтеру [10] (Табл. 1-4).
Клиническая картина интоксикации у мышей при введении обоих сравниваемых фармакологических агентов была идентичной. При введении токсических доз соединения 1 и препарата сравнения «Этоксидол», Россия отмечалось снижение двигательной активности животных. При увеличении дозы наблюдался кратковременный (2-3 мин) период гиперкинезии с явлениями беспокойства. Координация движений нарушалась, тонус скелетных мышц был повышен, наблюдались тонические и клонические судороги. В этот период наблюдались непроизвольные акты дефекации и мочеиспускания. Часть животных погибала на фоне судорог. Выжившие животные находились в «заторможенном» состоянии, что выражалось в сниженной реакции на световые, звуковые, тактильные и болевые раздражители (раздражение корня хвоста), при этом наблюдались судорожные подергивания мышц, снижение аппетита, диарея или обстипация на фоне возрастающего водопотребления. Дыхание было учащенным и поверхностным, регистрировали гипертермию. В указанном выше состоянии животные находились в течение первых двух суток, после чего постепенно принимали исходное физиологическое положение.
В течение последующих 14 суток явления интоксикации у животных проявлялись в сниженной реакции на раздражители. Волосяной покров терял блеск, характерный для здоровых животных, кожные покровы оставались без изменений. В дальнейшем состояние животных постепенно возвращалось к норме.
При динамическом наблюдении за животными в течение 14 суток гибели среди выживших животных не отмечали.
Результаты исследования летальности мышей после введения соединения 1 и препарата сравнения «Этоксидол» представлены в таблицах 1-4.
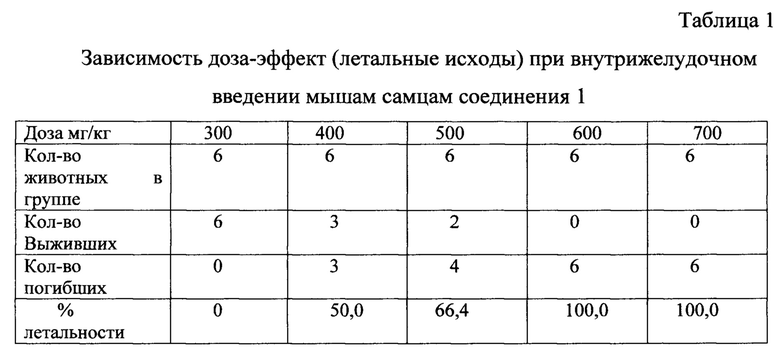
Расчет параметров острой токсичности дал следующие результаты:
DL50=419,74 (364,2÷474,3) мг/кг, DL16=304,3 мг/кг, DL84=523,8 мг/кг.
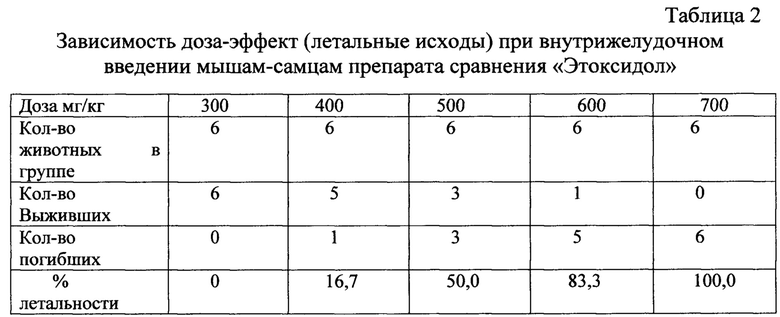
Расчет параметров острой токсичности дал следующие результаты:
DL50=498,93 (414,4÷643,9) мг/кг, DL16=391,2 мг/кг, DL84=622,3 мг/кг.


Расчет параметров острой токсичности дал следующие результаты:
DL50=428,81 (291,8÷554,4) мг/кг, DL16=313,4 мг/кг, DL84=574,7 мг/кг.
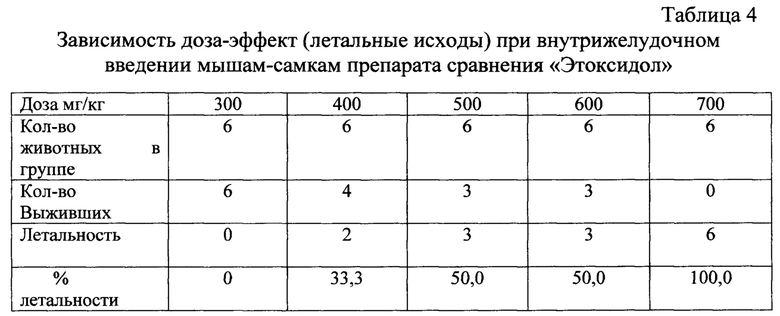
Расчет параметров острой токсичности дал следующие результаты:
DL50=499,36 (350,1÷628,3) мг/кг, DL16=367,3 мг/кг, DL84=628,0 мг/кг.
Динамика веса выживших мышей, получавших токсические дозы ФС и препарата сравнения «Этоксидол», значимо не отличалась от таковых контрольных групп. При анализе динамики водо- и пищепотребления внутривенного введения токсических доз соединения 1 и препарата сравнения в последующем существенной разницы по сравнению с контрольными группами мышей также не обнаружено (табл. 5-10).
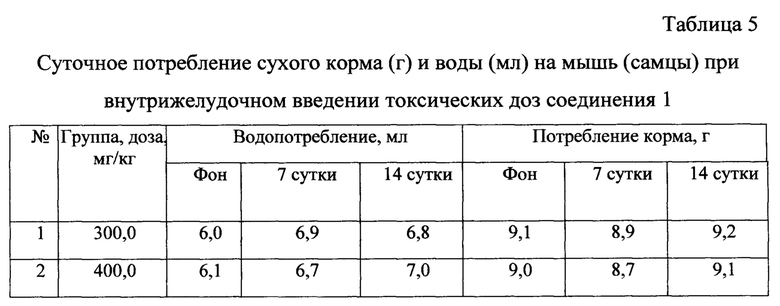

* Различия при сравнении с контролем достоверны при р<0,05 (критерий «хи-квадрат»).
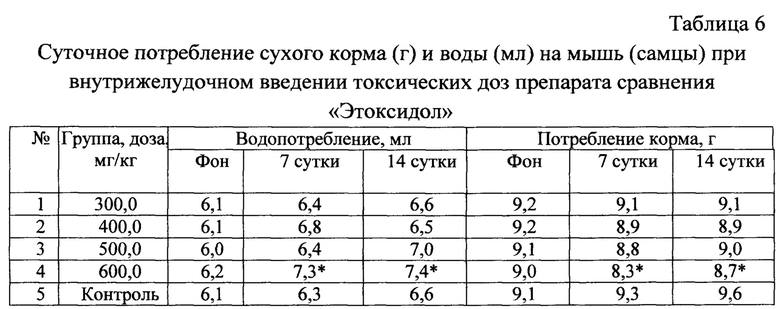
* Различия при сравнении с контролем достоверны при р<0,05 (критерий «хи-квадрат»).
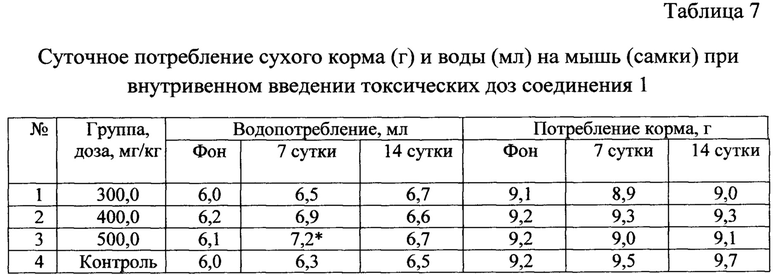
* Различия при сравнении с контролем достоверны при р<0,05 (критерий «хи-квадрат»).
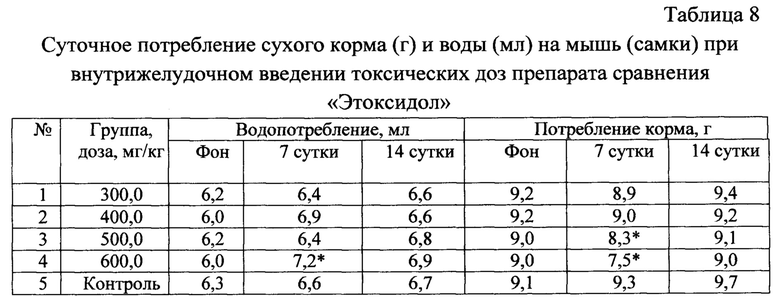
* Различия при сравнении с контролем достоверны при р<0,05 (критерий «хи-квадрат»).
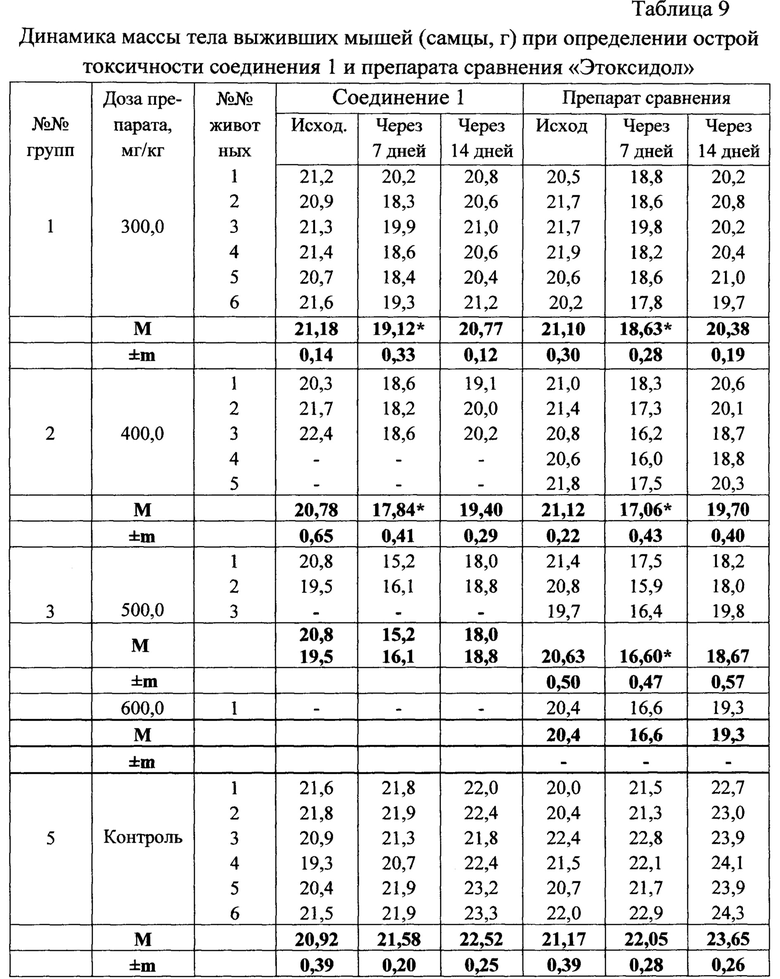
* Различия при сравнении с исходом (критерий Уилкоксона) и соответствующими значениями в контроле (t критерий Стьюдента) достоверны при р<0,05.
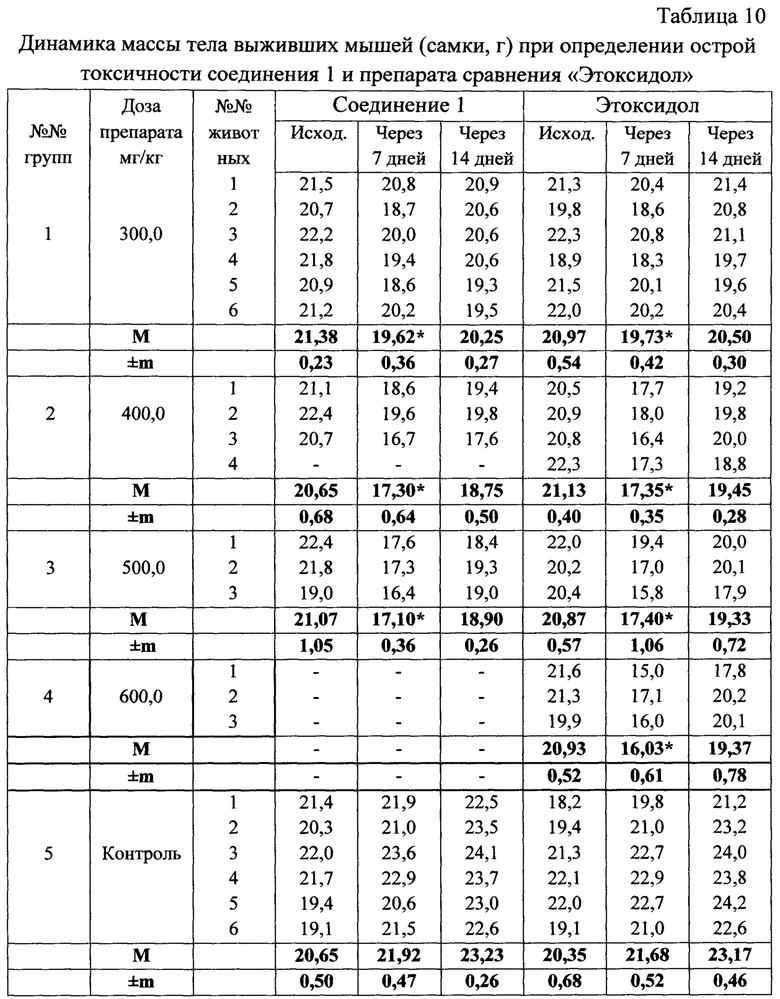
* Различия при сравнении с исходом (критерий Уилкоксона) и соответствующими значениями в контроле (t критерий Стьюдента) достоверны при р<0,05.
Таким образом, проведенный анализ полученных результатов позволяет сделать вывод о том, что соединение 1 по показателю «острой» токсичности относится к 3 классу токсичности (умеренно токсичные) [11] по ГОСТ 12.1.007-76.
2.1. Определение антигипоксической активности
Эксперименты по определению антигипоксической активности веществ поставлены на белых мышах массой 20-22 г, наркотизированных тиопента-натрием (50 мг/кг внутрибрюшинно).
Соединение 1 и препарат сравнения вводились внутривенно (в вену хвоста) в дозе, составляющей 5% от показателя LD50 в течение 3 минут с помощью электронного дозатора («Kent Scientific», США) за 5 минут до перевязки трахеи. Результаты исследования представлены в таблице 11.
Как показали результаты опытов, препарат сравнения «Этоксидол», применяемый в высшей терапевтической дозе, приводил к увеличению времени жизни подопытных животных - наименьшее время сохранения биоэлектрической активности составило 592 с, а наибольшее - 610 с, что значимо отличалось от аналогичных показателей у мышей контрольной группы. Кроме того, под влиянием вещества не наблюдалось заметного уменьшения частоты сердечных сокращений (табл. 11).
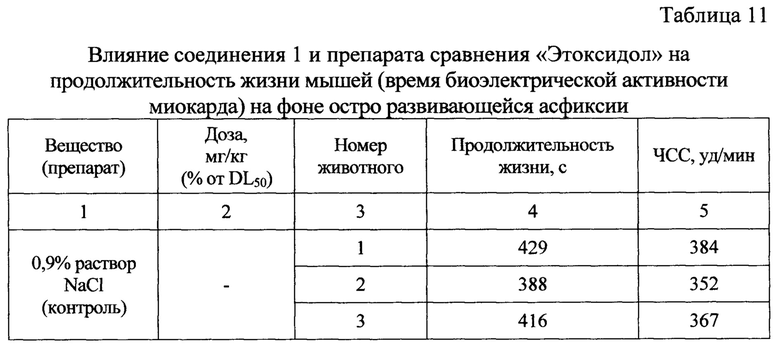
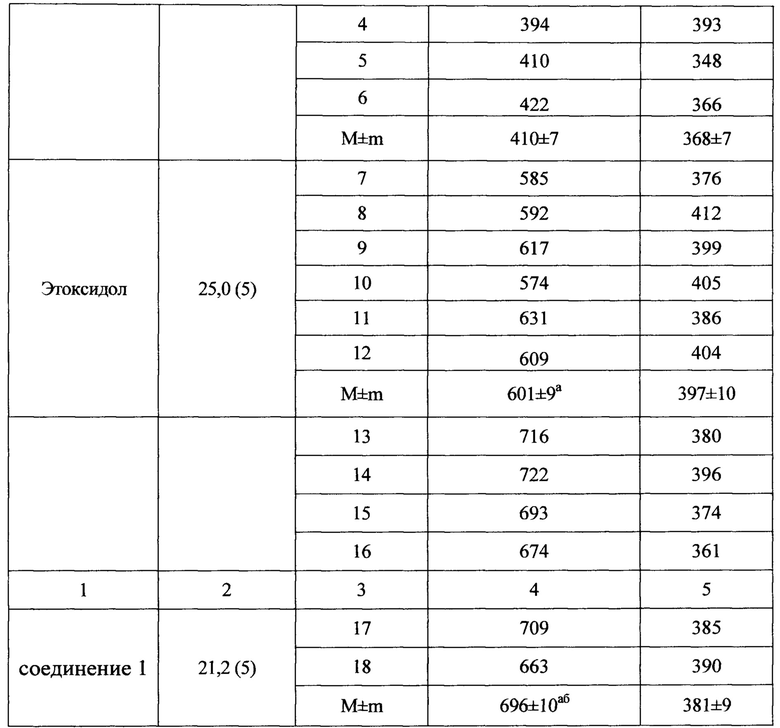
а Отличие от группы контроля достоверны, (критерий выживаемости Гехана с поправкой Йейтса); б Отличие от группы «Этоксидол» статистически достоверно при р<0,05 (одномерный дисперсионный анализ, критерий Ньюмена-Кейлса); * Отличие от контроля статистически достоверно при р<0,05 (одномерный дисперсионный анализ, критерий Ньюмена-Кейлса).
Соединение 1 пролонгировало период биоэлектрической активности миокарда, будучи вводимой мышам в дозе, составляющей 5% значения показателя LD50 до 696±10 с, что статистически значимо больше, чем в контроле и в группе препарата сравнения. Кроме того, под влиянием исследуемого вещества поддерживалась сократительная способность миокарда до 381±9 уд./мин.
Проведенное исследование острой токсичности энантиомера 2-этил-6-метил-3-гидроксипиридиния L-гидроксибутандиоата (соединение 1) в сравнении с препаратом «Этоксидол» показало, что при внутривенном однократном введении SHK мышам показатель DL50 соединения 1 для мышей самцов составил 419,7 мг/кг, для мышей самок - 428,8 мг/кг; показатель DL50 препарата сравнения «Этоксидол» для мышей самцов составил 498,9 мг/кг, для мышей самок - 499,4 мг/кг. Соединение 1 относится к 3 классу токсичности при парентеральных путях введения согласно ГОСТ 12.1.007-76.
При изучении антигипоксической активности соединения 1 в сравнении с готовой лекарственной формой препарата «Этоксидол» установлено, что левовращающий изомер при однократном профилактическом введении мышам в вену хвоста за 5 мин до воспроизведения гипоксии в дозе, составляющей 5% от показателя DL50, обладает антигипоксической активностью. При этом соединение 1 статистически значимо превосходит препарат сравнения по данном виду действия, о чем судили по продолжительности биоэлектрической активности сердца. Ни препарат сравнения, ни соединение 1 не обладают брадикардическим эффектом.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, проявляющее гепатопротекторную, липидрегулирующую, противоишемическую и нейротропную активность | 2018 |
|
RU2705575C1 |
| Комплексные соли ацексамовой кислоты, стимулирующие регенерацию костной ткани, ускоряющие процессы репаративного остеогенеза, стимулирующие минерализацию костной ткани при остеопорозе | 2018 |
|
RU2668966C1 |
| Новое производное 3-гидроксипиридина, обладающее липидрегулирующей активностью | 2020 |
|
RU2743923C1 |
| АНТИОКСИДАНТНОЕ И АНТИГИПОКСАНТНОЕ СРЕДСТВО НА ОСНОВЕ 6-МЕТИЛ-2-ЭТИЛ-3-ГИДРОКСИПИРИДИНА СУКЦИНАТА | 2008 |
|
RU2398583C2 |
| НЕЙРОТРОПНОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГИПОКСИЧЕСКОЙ, НЕЙРОПРОТЕКТОРНОЙ, АНТИАМНЕСТИЧЕСКОЙ И ВЕСТИБУЛОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2547728C1 |
| КОМПЛЕКС АЦЕТАТА ЦИНКА С 3-ГИДРОКСИПИРИДИНОМ, ОБЛАДАЮЩИЙ АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ В УСЛОВИЯХ ОСТРОЙ ЭКЗОГЕННОЙ ГИПОКСИИ | 2016 |
|
RU2631496C1 |
| 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЙГИДРОКСИБУТАНДИОАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ, НЕЙРОТРОПНОЙ И ЛИПИДРЕГУЛИРУЕМОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2377237C1 |
| ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ, ОБЛАДАЮЩЕЙ АНТИОКСИДАНТНЫМ, ВИРУЛИЦИДНЫМ, ИММУНОСТИМУЛИРУЮЩИМ, ПРОТИВОГИПОКСИЧЕСКИМ И АНТИАГРЕГАНТНЫМ ДЕЙСТВИЕМ | 2023 |
|
RU2808445C1 |
| ТЕТРАПЕПТИД И СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦЕРЕБРОПРОТЕКТОРНОЙ И АНТИАМНЕСТИЧЕСКОЙ АКТИВНОСТЯМИ (ВАРИАНТЫ) | 2013 |
|
RU2537560C2 |
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ 6-МЕТИЛУРАЦИЛА С ЯНТАРНОЙ КИСЛОТОЙ, ПРОЯВЛЯЮЩЕЕ АНТИГИПОКСИЧЕСКУЮ АКТИВНОСТЬ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2003 |
|
RU2259357C2 |
Изобретение относится к левовращающемуся энантиомеру 2-этил-6-метил-3-гидроксипиридиния L-гидроксиэтанбутандионата, который обладает церебропротекторной активностью и пролонгирует период биоэлектрической активности миокарда. Технический результат: получение нового соединения, которое может найти применение в медицине в качестве церебропротекторного средства. 11 табл.
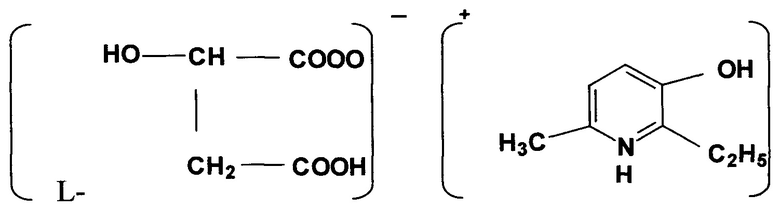
L-Энантиомер 2-этил-6-метил-3-гидроксипиридиния гидроксибутандиоата формулы:
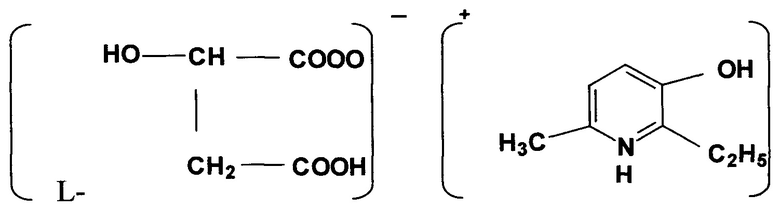
обладающий церебропротекторной активностью и пролонгирующий период биоэлектрической активности миокарда, по сравнению с рацематом.
| 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНИЙГИДРОКСИБУТАНДИОАТ, ОБЛАДАЮЩИЙ ПРОТИВОИШЕМИЧЕСКОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ, НЕЙРОТРОПНОЙ И ЛИПИДРЕГУЛИРУЕМОЙ АКТИВНОСТЯМИ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2008 |
|
RU2377237C1 |
| СОЛИ 2-ЭТИЛ-6-МЕТИЛ-3-ОКСИПИРИДИНА С ОРГАНИЧЕСКИМИ КАРБОНОВЫМИ КИСЛОТАМИ, ОБЛАДАЮЩИЕ АНКСИОЛИТИЧЕСКОЙ, АНТИДЕПРЕССИВНОЙ, ПРОТИВОГИПОКСИЧЕСКОЙ, АНТИАМНЕСТИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2002 |
|
RU2284993C2 |
| СОЛЬ 2-ЭТИЛ-6-МЕТИЛ-3-ГИДРОКСИПИРИДИНА С НИКОТИНОВОЙ КИСЛОТОЙ, ОБЛАДАЮЩАЯ ГИПОГЛИКЕМИЧЕСКОЙ, ГИПОЛИПИДЕМИЧЕСКОЙ И НЕЙРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2010 |
|
RU2454406C2 |
| US 4486440 A1, 04.12.1984. | |||
Авторы
Даты
2018-08-10—Публикация
2017-12-14—Подача