Изобретение относится к медицине и экологии, а именно к методу обоснования с помощью маркерных лабораторных и функциональных показателей негативных медико-биологических эффектов (нарушение здоровья, развитие заболевания) детей при воздействии алюминия и его соединений для диагностических целей, а также для расширения доказательной базы наличия связи дополнительной заболеваемости и/или связанных с ней функциональных нарушений со стороны центральной (ЦНС) или вегетативной нервной системы (ВНС) у наиболее чувствительных групп населения в зоне влияния алюминиевого производства.
В рамках настоящего изобретения используются следующие термины:
Негативное воздействие на человека - воздействие факторов среды обитания, создающее угрозу жизни или здоровью человека либо угрозу для жизни и здоровья будущих поколений.
«Негативный эффект» - изменения в морфологии, физиологии, росте, развитии или продолжительности жизни организма, популяции или потомства, проявляющиеся в ухудшении функциональной способности или способности компенсировать дополнительный стресс, или в повышении чувствительности к воздействиям других факторов среды обитания.
«Экспозиция» - контакт организма (рецептора) с химическим, физическим или биологическим агентом.
Зависимость «экспозиция-ответ» - связь между воздействующей экспозицией (алюминием и его соединениями), режимом, продолжительностью воздействия и степенью выраженности, распространенности (ответ) негативного эффекта в экспонируемой популяции.
Зависимость «экспозиция-негативный эффект» - связь между экспозицией и степенью выраженности негативного эффекта в экспонируемой популяции.
«Маркерные лабораторные и функциональные показатели негативного эффекта» - показатели, количественно или качественно характеризующий биохимическое, физиологическое или иное изменение в организме, в зависимости от степени которого определяется фактическое или потенциальное нарушение здоровья или развитие болезни.
«Медико-биологические исследования» - система наблюдений, оценки и прогноза любых изменений у идивидума, группы людей или популяции, вызванных воздействием факторов среды обитания антропогенного или природного происхождения.
«Лабораторный показатель» - биохимический показатель, определение которого осуществляется методами, направленными на анализ исследуемого материала с помощью различного специализированного лабораторного оборудования;
«Функциональный показатель» - показатель, отражающий состояние конкретной функции жизнеобеспечения организма, определение которого осуществляется методами, направленными на оценку этой функции с помощью специализированного функционального и инструментального оборудования;
«Оценка риска»: 1) процесс, который включает следующие элементы: идентификацию опасности, оценку воздействия, оценку зависимости «доза-ответ» и характеристику риска; 2) научная оценка свойств вредного фактора (алюминия) и условий его воздействия на человека, направленная на установление вероятности того, что экспонированные люди окажутся пораженными, а также на характеристику природы тех эффектов, которые у них могут возникнуть; 3) оценка вида и степени выраженности опасности, создаваемой агентом в результате существующего или возможного воздействия на определенную группу людей, а также существующий или потенциальный риск для здоровья, связанный с данным агентом;
«Моделирование зависимостей» - установление зависимостей одних величин от других с помощью методов статистического моделирования.
В соответствии с современными проблемно ориентированными направлениями научных исследований, как в мире, так и в России, важным направлением в задачах сохранения здоровья нации и защиты прав граждан на благоприятную среду обитания является формирование доказательства причинения вреда здоровью человека при воздействии опасных факторов. Согласно существующему определению, под причинением вреда здоровью понимается нарушение физиологической функции органов и тканей человека, связанное с действием физических, химических факторов (Об утверждении Медицинских критериев определения степени тяжести вреда, причиненного здоровью человека: Приказ Министерства здравоохранения РФ от 24.04.2008 №194н. Available at: http:/base.garant.ru/12162210/ (доступно 10.06.2016)).
Актуальность данных исследований подчеркивается экспертами ВОЗ, по мнению которых для выявления устойчивых причинно-следственных связей нарушений состояния здоровья с воздействием факторов опасности, в частности, воздействие токсикантов окружающей среды, основным диагностическим и прогностическим инструментом является обоснование и использование маркеров экспозиции и ответа (эффекта) на воздействие (WHO. Biomarkers and human biomonitoring. Children's Health and the Environment. Training Package for the Health Sector World Health Organization. 2011. Available at: who.int.ceh/capacity/biomarkers.pdf (accessed 19 August 2016); WHO. Principles for evaluating health risks in children associated with exposure to chemicals (Environmental Health Criteria 237). 2006. Available at: http:www.inchem.org (accessed 19 August 2016); CDC. National Report on Human Exposure to Environmental Chemicals. Centers for Disease Control and Prevention. 2015. Available at: http:www.cdc.gov/biomonitoring/ (accessed 19 August 2016).
Из уровня техники известны способы использования маркерных показателей при оценке риска возникновения различных заболеваний у населения от воздействия токсикантов.
Из патента РФ №2599973 известен способ оценки риска возникновения психических и поведенческих расстройств, вызванных внутривенным употреблением психоактивных веществ, которые можно рассматривать как токсиканты для организма. Согласно этому способу определяют уровень клинических признаков иммунологической недостаточности, нижний порог болевой чувствительности, индекс враждебности, уровень ситуативной тревожности, оценку отношения к изопропанолу с использованием визуально-аналоговой шкалы. Вычисляют риск возникновения расстройств с внутривенным употреблением психоактивных веществ по математической формуле. В зависимости от полученного значения результата расчета определяют высокий уровень риска расстройств или низкий уровень риска расстройств. Способ позволяет оценивать уровень риска возникновения психических и поведенческих расстройств, вызванных внутривенным употреблением психоактивных веществ, и своевременно проводить профилактические мероприятия за счет определения прогностических показателей.
Его недостатком является то, что риск возникновения психических и поведенческих расстройств изучался у лиц возрастом от 16 до 29 лет, которые не относятся к детской возрастной категории. Кроме этого, изопрапонол, который рассматривается в качестве токсиканта, не является фактором среды обитания и не формирует внешнесредовую аэрогенную экспозицию. Механизм его действия на ЦНС отличается от воздействия алюминия, а, следовательно, и ответные реакции организма также отличны.
Также известен способ оценки риска развития йоддефицитного состояния у населения административной территории в условиях антропотехногенного химического загрязнения окружающей среды (Патент РФ №2316260), заключающийся в том, что определяют показатель загрязнения окружающей среды для каждого химического элемента: Sn, Pb, Zn, Cu, Ag, V, Cr, Ni, Mn, Co, Mo, W, As, Bi, Li, Ba, Be, Sr, P, Sb, представляющего опасность для каждой из возрастной группы здоровья (рх). Определяют для каждого района исследуемой территории заболеваемость щитовидной железы (ЩЖ), ассоциируемой с йоддефицитным состоянием (ЙДС). Заболеваемость определяют для различных возрастных групп, и на основании выявленной заболеваемости определяют вероятность развития ЙДС (dx). на основании полученной заболеваемости ЩЖ, ассоциируемой с ЙДС, определяют нозологические формы заболеваний, определяют риск развития различных нозологических форм заболеваний ЩЖ, ассоциируемых с ЙДС, по формуле RX=PXDX, где х - какой-либо химический экотоксикант. Наносят полученные риски на карту района, отражающую заболеваемость в районе. На основании полученного осуществляют прогноз риска развития йоддефицитного состояния. Способ позволяет с большой степенью вероятности количественно оценить реальный и потенциальный риски развития НДС и возникновение заболеваний ЩЖ, ассоциированных с йоддефицитом в условиях антропотехногенного химического загрязнения окружающей среды.
Однако указанный известный способ не предназначен для оценки степени вероятности возникновения заболеваний со стороны центральной нервной системы и соподчиненной ей ВНС у наиболее чувствительной группы населения (дети) при аэрогенном воздействии алюминия с учетом выделения комплекса маркеров негативных эффектов.
Из патента РФ №2480755 известен способ оценки риска воздействия пестицидов на работающих, заключающийся в установлении параметров фактического содержания вредного вещества в воздухе рабочей зоны (мг/м3) и на кожных покровах (мг/см2), выведении коэффициента безопасности (КБ), причем рассчитывают поглощенную дозу вещества (Дп, мг/кг) при ингаляционном и дермальном поступлении (мг/кг массы тела) по формуле, также рассчитывают допустимый суточный уровень экспозиции для операторов по установленной недействующей дозе в хроническом токсикологическом эксперименте (ДСУЭО, мг/кг), затем определяют лимитирующий критерий - коэффициент безопасности (КБп) по формуле: КБп=Дп: ДСУЭО, и при значении КБп≤1 констатируют допустимый риск, при значении КБп>1 - недопустимый. Способ позволяет повысить точность и надежность оценки реального риска пестицида для работающих и внести коррективы по условиям применения пестицида в сельском хозяйстве и других отраслях.
Недостатком указанного способа является то, что предложенная оценка риска воздействия пестицидов применима только к работающим, что вносит значительные ограничения по использованию метода.
При этом из уровня техники не были выявлены известные способы обоснования возникновения у детей негативного эффекта в виде заболевания, связанного с центральной или вегетативной нервной системой, ассоциированного с аэрогенной экспозицией алюминия, поэтому сделать выбор ближайшего аналога к заявляемому объекту не представляется возможным.
Технический результат, достигаемый предлагаемым изобретением, заключается в создании информативного и доказательного способа обоснования возникновения у детей негативного эффекта в виде заболевания, связанного с центральной или вегетативной нервной системой, ассоциированного с аэрогенной экспозицией алюминия.
Поставленный технический результат достигается предлагаемым Способом обоснования возникновения у детей негативного эффекта в виде заболевания, связанного с центральной или вегетативной нервной системой, ассоциированного с аэрогенной экспозицией алюминия, заключающийся в том, что выделяют территорию с постоянным присутствием алюминия и/или с его повышенной, по сравнению с предельно-допустимой концентрацией в атмосферном воздухе, формирующей длительную хроническую экспозицию алюминия, устанавливают перечень наиболее вероятных негативных эффектов - нарушений здоровья у детей, ассоциированных с повышенной аэрогенной экспозицией алюминия, в качестве которых принимают заболевания, связанные с центральной (ЦНС) и вегетативной нервной системой (ВНС), из указанного перечня вероятных негативных эффектов выделяют ведущие конкретные заболевания, характерные для ЦНС и ВНС, путем формирования группы наблюдения, состоящей из детей, постоянно проживающих на территории и подвергающихся хронической экспозиции алюминия, и группы сравнения из детей с территории экологического благополучия, и установления ведущих конкретных заболеваний ЦНС и ВНС в каждой группе; причем при выборе указанных ведущих конкретных заболеваний учитывают два критерия: уровень конкретной заболеваемости в группе наблюдения должен достоверно отличаться от уровня конкретной заболеваемости в группе сравнения и иметь достоверную связь этого конкретного заболевания с аэрогенным воздействием соединений алюминия; далее, исходя из установленного ведущего конкретного заболевания, связанного с системой ЦНС и ВНС, - ведущего негативного эффекта, формируют перечень лабораторных и функциональных показателей, которые этиопатогенетически связаны с этим ведущим негативным эффектом, а именно: в качестве лабораторных и функциональных показателей принимают следующие: уровень гидроперекиси липидов в сыворотке крови; малонового диальдегида в плазме крови; 8-гидрокси-2-деоксигуанозина в моче; глутаминовой кислоты в сыворотке крови; γ-аминомасляной кислоты в сыворотке крови; ионизированного кальция в цельной крови; фосфора в сыворотке крови; нейронспецифической енолазы в сыворотке крови; абсолютный фагоцитоз в крови; фагоцитарное число в крови; исходный вегетативный тонус; тип вегетативной реактивности; отбирают пробы мочи и крови у детей из групп наблюдения и сравнения; определяют в моче содержание алюминия, а в крови - уровни лабораторных показателей, инструментальными методами определяют функциональные показатели; затем для детей обеих групп проводят количественную оценку связи изменения показателей относительно физиологической нормы с аэрогенным воздействием алюминия на основании расчета отношения шансов (OR) и его доверительного интервала (DI), и при OR>1 и величине нижней границы DI>1 связь считается достоверно установленной; затем рассчитывают вероятность Р'k отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче на основе оценки зависимости «маркер экспозиции, т.е. содержание алюминия в моче, - ответ, т.е. показатель ведущего негативного эффекта», которая выполняется отдельно для каждого k-ro показателя по формуле:
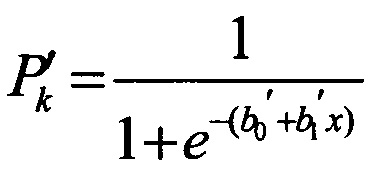 ,
,
где х - концентрация алюминия в моче, мг/дм3;
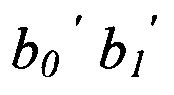 - параметры математической модели, представленные в таблице 1, содержащейся в описании;
- параметры математической модели, представленные в таблице 1, содержащейся в описании;
из ранее определенных лабораторных и функциональных показателей устанавливают уточненные лабораторные и функциональные показатели, характеризующие ответ в виде отклонения показателя ведущего негативного эффекта от физиологической нормы только на повышенный, относительно референтного уровня, уровень алюминия в моче; далее рассчитывают вероятность Р''k развития ведущего негативного эффекта при установленном уровне k-го уточненного показателя на основе оценки зависимости «уточненный показатель негативного эффекта - ведущий негативный эффект», которая выполняется отдельно для каждого k-го уточненного показателя по формуле:
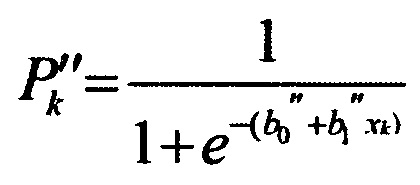 ,
,
где P''k - вероятность развития ведущего негативного эффекта при отклонении k-го уточненного показателя эффекта от физиологической нормы;
xk - уровень k-го уточненного показателя в единицах измерения соответственно конкретному установленному показателю;
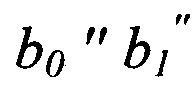 - параметры математической модели, представленные в таблице 2, содержащейся в описании;
- параметры математической модели, представленные в таблице 2, содержащейся в описании;
и те показатели, которые при этом будут достоверно присущи ведущему негативному эффекту, относят к комплексу маркерных лабораторных и функциональных показателей; затем проводят расчет общей вероятности развития ведущего негативного эффекта при повышенном относительно референтного уровня содержании алюминия в моче по формуле:
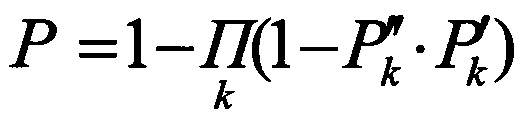 ,
,
где Р - общая вероятность возникновения ведущего негативного эффекта при повышенном содержании алюминия в моче;
P'k - вероятность отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче;
Р''k - вероятность развития ведущего негативного эффекта при отклонении k-го уточненного показателя эффекта от физиологической нормы;
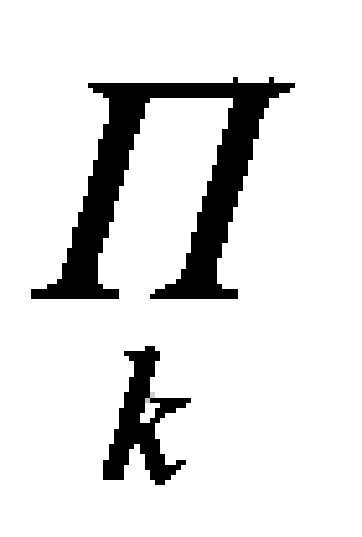 - произведение значений, полученных при выполнении действия
- произведение значений, полученных при выполнении действия 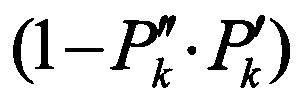 ;
;
при этом по полученной величине общей вероятности Р определяют степень ассоциированности ведущего негативного эффекта с аэрогенным воздействием соединений алюминия: при Р менее 0,05 - пренебрежительно малая, при Р 0,05 - 0,35 - средняя, при Р от более 0,35 до 0,6 включительно - высокая, при Р более 0,6 - очень высокая; а связь ведущего негативного эффекта в виде заболевания центральной или вегетативной нервной системой, ассоциированного с длительной аэрогенной экспозицией алюминием, считают обоснованной при одновременном содержании в моче алюминия более 0,0065 мг/дм3, наличии отклонений от физиологической нормы всех маркерных лабораторных и функциональных показателей, достоверно присущих ведущему негативному эффекту, и количественному значению общей вероятности Р>0,05.
Указанный технический результат достигается за счет следующего.
Для понимания существа вопроса необходимо пояснение.
Существенный вклад в загрязнение атмосферного воздуха селитебных территорий вносит цветная металлургия, в том числе алюминиевая промышленность. Производство алюминия, базирующееся на технологии Сордерберга (использование самообжигающихся непрерывных анодов верхнего токоподвода), сопровождается выделением в атмосферный воздух значительного количества токсичных веществ, в том числе неорганической пыли, обогащенной соединениями алюминия, фторсодержащих соединений, смолистых соединений, содержащих полициклические ароматические углеводороды. Алюминий, как специфический компонент технологического процесса, поступает в атмосферу в составе неорганической пыли в виде диАлюминия триоксида, относящегося ко второму классу опасности (высокоопасное соединение) в соответствии с Гигиеническим нормативом 2.1.6.1338-03 «Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населенных мест». Население селитебных территорий, находящихся в зоне влияния алюминиевого производства, подвергается аэрогенной экспозиции химических факторов, в том числе алюминия и его соединений, которая может обуславливать развитие негативных эффектов (заболеваний) со стороны критических органов и систем (центральной и вегетативной нервной системы, органов дыхания и др.). Следствием этого является формирование дополнительной заболеваемости населения, ассоциированной с экспозицией химических факторов опасности алюминиевого производства. Внешнесредовая экспозиция соединений алюминия оказывает модифицирующее влияние на механизм развития негативных эффектов в виде формирования дополнительных патогенетических звеньев функциональных нарушений.
Наиболее чувствительным контингентом к аэрогенной экспозиции химических факторов, в том числе алюминия и его соединений, является детское население, что обусловлено:
- продолжающейся морфо-функциональной дифференцировкой органов и регуляторных систем;
- несовершенством нейро-эндокринной регуляции в силу роста и развития центральной нервной и эндокринной систем;
- возрастными особенностями вентиляции легких, процессов всасывания в желудочно-кишечном тракте, проницаемости барьерных структур.
Вот почему актуальным является обоснование и применение маркерных показателей негативных эффектов у детей при аэрогенном воздействии соединений алюминия, практическое использование которых повышает эффективность формирования доказательной базы наличия связи дополнительной заболеваемости и/или связанных с ней функциональных нарушений со стороны ЦНС и ВНС у наиболее чувствительных групп населения в зоне влияния алюминиевого производства.
Повышение точности и достоверности предлагаемого способа обеспечивается за счет ряда дополнительных операций по проведению количественной оценки связи изменения лабораторных и функциональных показателей относительно физиологической нормы с аэрогенным воздействием алюминия на основании расчета отношения шансов (OR) и его доверительного интервала (DI), а также за счет последовательного установления вероятности отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном, относительно референтного уровня, содержании алюминия в моче; вероятности развития ведущего негативного эффекта при установленном уровне k-го уточненного показателя на основе оценки зависимости «уточненный показатель негативного эффекта - ведущий негативный эффект», которая выполняется отдельно для каждого k-го уточненного показателя.
Благодаря тому, что выделяют маркерные лабораторные и функциональные показатели, которые при этом будут достоверно присущи ведущему негативному эффекту, характеризующему заболевание ЦНС и ВНС, обеспечивается точность и достоверность отнесения влияния алюминия именно на конкретное заболевание, в результате чего можно не только поставить диагноз, но и обосновать, что этот диагноз ассоциирован именно с воздействием алюминия.
При последующем расчете общей вероятности Р развития ведущего негативного эффекта при повышенном содержании алюминия в моче определяют не только степень ассоциированности ведущего негативного эффекта с аэрогенным воздействием соединений алюминия по определенной шкале: при Р менее 0,05 - пренебрежительно малая, при Р 0,05-0,35 - средняя, при Р от более 0,35 до 0,6 включительно - высокая, при Р более 0,6 - очень высокая, но и достоверно устанавливают обоснованную связь ведущего негативного эффекта в виде заболевания центральной или вегетативной нервной системой, ассоциированного с длительной аэрогенной экспозицией алюминием, в том случае, если одновременно будут присутствовать три фактора: содержание в моче алюминия более 0,0065 мг/дм3, наличие отклонений от физиологической нормы всех маркерных лабораторных и функциональных показателей, достоверно присущих ведущему негативному эффекту, и количественное значение общей вероятности Р>0,05.
Использование в качестве биологического материала для исследования мочи ребенка позволяет не только упростить способ, но и сделать его количественно более точным и информативным, т.к. именно концентрация данного металла в моче и является индикаторным показателем экзогенного ингаляционного поступления алюминия в организм ( В., Buchta М.,
В., Buchta М.,  G.A., Filser J.G. eds. Biological monitoring of welders exposed to aluminium. Toxicology Letters. - 2006. Vol. 162. - P. 239-245).
G.A., Filser J.G. eds. Biological monitoring of welders exposed to aluminium. Toxicology Letters. - 2006. Vol. 162. - P. 239-245).
Исходя из вышеизложенного можно сделать вывод, что поставленный технический результат обеспечивается за счет совокупности всех операций предлагаемого способа, их последовательности и режимов реализации.
Предлагаемый способ осуществляют следующим образом, реализуя его на конкретном примере.
1. Выделяют территорию с постоянным присутствием алюминия и/или с его повышенной, по сравнению с предельно-допустимой концентрацией в атмосферном воздухе, формирующей длительную хроническую экспозицию алюминия.
Гигиеническая оценка качества атмосферного воздуха по содержанию алюминия в селитебной застройке, расположенной в зоне влияния алюминиевого производства, проводилась в точках расположения постов наблюдения управления по гидрометеорологии и мониторингу окружающей среды и/или в точках социально-гигиенического мониторинга. В качестве источников данных для установления количественных показателей содержания алюминия в атмосферном воздухе использованы результаты инструментальных наблюдений, проводимых в рамках социально-гигиенического мониторинга и/или в системе Росгидромета.
Количественная оценка содержания алюминия в атмосферном воздухе проводилась по уровню фактора в каждой точке и его сравнению с гигиеническими нормативами (ПДКм.р., ПДКс.с).
Количественная оценка индивидуальной экспозиции алюминием при ингаляционном поступлении проводилась стандартными методами расчета суммарной средней суточной дозы в соответствии с руководством по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду, на основе полученных расчетным путем значений 95-% персентиля концентраций по результатам оценки качества атмосферного воздуха в соответствии с РД 52.04.186-89 «Руководство по контролю загрязнения атмосферы»; проводилось сравнение фактической величины хронической экспозиции с ее референтным значением за тот же период усреднения.
2. Устанавливают перечень наиболее вероятных негативных эффектов - нарушений здоровья у детей, ассоциированных с повышенной аэрогенной экспозицией алюминия, в качестве которых принимают заболевания, связанные с центральной (ЦНС) и вегетативной нервной системой (ВНС).
Качественная характеристика индивидуальной экспозиции алюминия дана на основании оценки его тропности к органам и системам (вероятные негативные эффекты в виде нарушения функции и/или заболевания) при ингаляционном поступлении. И к таким вероятным заболеваниям относятся заболевания ЦНС или ВНС.
В качестве источников информации о тропности алюминия использованы следующие нормативно-методические документы и справочные материалы:
Руководство по оценке риска здоровью населения при воздействии химических веществ // Руководство 2.1.10.1920-04. - М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. - 143 с.
Воздействие на организм человека опасных и вредных экологических факторов. Метрологические аспекты. В 2-х томах. // Под ред. Исаева Л.К. Том I. - М.: ПАИМС, 1997. - 512 с.
Воздействие на организм человека опасных и вредных экологических факторов. Метрологические аспекты. В 2-х томах. // Под ред. Исаева Л.К. Том II. - М.: ПАИМС, 1997. - 496 с.
Справочник «Вредные вещества в окружающей среде и их соединения» [Вредные вещества в окружающей среде. Элементы I-IV групп периодической системы и их неорганические соединения: Справ.-энц. изд. / Пол ред. В.А. Филова и др. - СПб.: НПО «Профессионал», 2012. - 464 с.
Токсикологические профайлы по алюминию Агентства по токсичным веществам и регистру заболеваний (ATSDR) (Toxicological profile for aluminum. Agency for Toxic Substances and Disease Registry (ATSDR). U.S. Public Health Service, U.S. Department of Health and Human Services -2008. - Altanta, GA. - 357 p).
3. Из указанного перечня вероятных негативных эффектов выделяют ведущие конкретные заболевания, характерные для ЦНС и ВНС, путем формирования группы наблюдения, состоящей из детей, постоянно проживающих на территории и подвергающихся хронической экспозиции алюминия, и группы сравнения из детей с территории экологического благополучия, и установления ведущих конкретных заболеваний ЦНС и ВНС в каждой группе.
Количественная оценка детского населения, подвергающегося экспозиции алюминием, проводилась на основании результатов расчета уровня экспозиции и выделения территории в селитебной застройке, находящейся в зоне экспозиции (группа наблюдения).
Для проведения сравнительных оценок по частоте встречаемости и уровню изучаемого показателя выбиралась группа сравнения (дети селитебных территорий, не подвергающиеся экспозиции алюминием).
Выборки по половозрастному составу, социально-бытовым условиям проживания, среднему уровню материального обеспечения, по частоте и характеру вредных привычек и профессиональных вредностей у родителей, были сопоставимыми. На момент обследования дети не имели острых инфекционных заболеваний не менее, чем в течение 4 недель до начала исследования, не должны принимать лекарственных препаратов, оказывающих выраженное влияние на изучаемые функции/заболевания со стороны критических органов и систем, менее чем за 30 дней до начала исследования.
Характеристика риска развития неканцерогенных эффектов со стороны критически органов и систем осуществлялась на основе расчета коэффициента опасности (HQ) алюминия в соответствии с Руководством по оценке риска для здоровья населения при воздействии химических веществ, загрязняющих окружающую среду (Руководство по оценке риска здоровью населения при воздействии химических веществ // Руководство 2.1.10.1920-04. - М.: Федеральный центр Госсанэпиднадзора Минздрава России, 2004. - 143 с.). Если HQ>1, то вероятность развития у детей негативных эффектов при ежедневном поступлении алюминия в течение жизни являлось существенной и такое воздействие характеризовалось как недопустимое.
Для выделения ведущего негативного эффекта со стороны критических систем проводился анализ информации о заболеваемости детей (количество случаев и виды заболеваний).
Источником информации о заболеваниях детей (количество случаев и виды заболеваний) являлись результаты комплексного объективного врачебного осмотра, удовлетворяющие критериям Международной статистической классификации болезней и проблем, связанных со здоровьем, десятого пересмотра (МКБ-10).
4. При выборе указанных ведущих конкретных заболеваний учитывают два критерия: уровень конкретной заболеваемости в группе наблюдения должен достоверно отличаться от уровня конкретной заболеваемости в группе сравнения (р≤0,05) и иметь достоверную связь этого конкретного заболевания с аэрогенным воздействием соединений алюминия.
Количественная оценка связи развития негативных эффектов (заболеваний) у детского населения с аэрогенным воздействием изучаемого фактора опасности (соединения алюминия) проводится (по результатам эпидемиологических исследований) на основании расчета отношения шансов (OR) и его доверительного интервала (DI). Если величина OR>1, то предполагаемый фактор воздействия являлся весомым. Для оценки достоверности наличия связи «воздействие-негативный эффект» рассчитывался 95% доверительный интервал (DI). Критерием наличия достоверно установленной связи являлась величина OR>1 и величина нижней границы DI>1 (Флетчер Р., Флетчер С, Вагнер Э. Клиническая эпидемиология: Основы доказательной медицины. М.: Медиа Сфера; 1998).
5. Далее, исходя из установленного ведущего конкретного заболевания, связанного с системой ЦНС и ВНС, - ведущего негативного эффекта, формируют перечень лабораторных и функциональных показателей, которые этиопатогенетически связаны с этим ведущим негативным эффектом.
Формирование перечня лабораторных и функциональных показателей ответа организма на повышенное содержание алюминия в моче для исследования проводилось, исходя из установленного у детей ведущего заболевания (по критическим системам), ассоциированного с аэрогенным воздействием алюминия, и патогенетически связанных с этим заболеванием ответных реакций организма.
При длительной аэрогенной экспозиции алюминием одной из критических систем является ЦНС с подчиненной ей ВНС. Ведущим негативным эффектом со стороны ЦНС и ВНС является астено-вегетативный синдром (МКБ-10: G90.8), как предиктор синдрома дефицита внимания с гиперреактивностью (МКБ-10: F90.0), и патогенетически связанное с ними нарушение синаптической передачи нервного импульса между нейронами центральной и периферической нервной систем.
Учитывались элементы дополнительного этиопатогенетического влияния алюминия, которые включают:
- прямое цитотоксическое повреждение ядра нейронов ЦНС в результате окислительной модификации белков, что приводит к росту амилоидогенных фибрилл в нейронах, метаболическому дисбалансу, уменьшению плотности синапсов, их гибели;
- нарушение эффективности функции фосфора в результате антагонизма с алюминием, что приводит к нарушению синтеза нейронов, обеспечивающих передачу нервных импульсов.
Следствием этих процессов является нарушение синаптической передачи нервных импульсов от нервных рецепторов к клеткам тканей внутренних органов, либо между нейронами центральной и периферической нервными системами с обязательным участием вегетативного ствола.
Лабораторными и функциональными показателями, которые этиопатогенетически связаны с ведущим негативным эффектом: астено-вегетативный синдром, как предиктор синдрома дефицита внимания с гиперреактивностью, были следующие: уровень гидроперекиси липидов в сыворотке крови; малонового диальдегида в плазме крови; 8-гидрокси-2-деоксигуанозина в моче; глутаминовой кислоты в сыворотке крови; γ-аминомасляной кислоты в сыворотке крови; ионизированного кальция в цельной крови; фосфора в сыворотке крови; нейронспецифической енолазы в сыворотке крови; абсолютный фагоцитоз в крови; фагоцитарное число в крови; исходный вегетативный тонус (гиперсимпатикотонический); тип вегетативной реактивности (асимпатикотонический).
6. Отбирают пробы мочи и крови у детей из групп наблюдения и сравнения, определяют в моче содержание алюминия (методом масс-спектрометрии с индуктивно связанной плазмой СТО М25-2016. Оценка установленного содержания алюминия в моче проводилась относительно референтных уровней (Тиц Н.У. Клиническое руководство по лабораторным тестам. М.: ЮНИМЕД-пресс; 2003), и показателей в группе сравнения. В крови определяют уровни лабораторных показателей, а инструментальными методами (методом кардиоинтервалографии) определяют функциональные показатели.
Статистическая обработка полученных результатов выполнялась с учетом описания количественных признаков с использованием значения среднего (М) и ошибки репрезентативности (m), так как случайные величины анализируемых показателей соответствовали закону нормального распределения.
7. Затем для каждого установленного лабораторного и функционального показателя ответа проводят количественную оценку связи изменения показателей относительно физиологической нормы с аэрогенным воздействием алюминия на основании расчета отношения шансов (OR) и его доверительного интервала (DI), и при OR>1 и величине нижней границы DI>1 связь считается достоверно установленной.
Выявление и оценка зависимости концентрация алюминия в моче от концентрации алюминия в атмосферном воздухе выполнялась с помощью парных моделей регрессии с оценкой достоверности параметров и адекватности модели на основании однофакторного дисперсионного анализа по критерию Фишера (F≥3,96), коэффициенту детерминации (R2) и t-критерию Стьюдента (t≥2) при заданном уровне значимости р≤0,05 (Гланц С. Медико-биологическая статистика. М.: Практика, 1998). При построении математической модели определялись 95%-ные доверительные границы. В качестве адекватных моделей выбирались модели, соответствующие статистическому критерию и отвечающие требованию биологического правдоподобия. При установлении достоверной и адекватной модели, отражающей исследуемую зависимость, повышенное содержание алюминия в моче принималось в качестве маркера аэрогенной экспозиции алюминием.
8. Затем рассчитывалась вероятность Р'k отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче на основе оценки зависимости «маркер экспозиции, т.е. содержание алюминия в моче, - ответ, т.е. показатель ведущего негативного эффекта», которая выполняется отдельно для каждого k-го показателя по формуле:
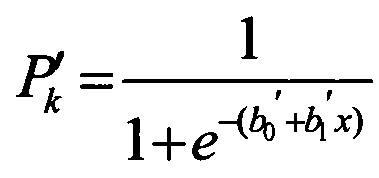 ,
,
где х - концентрация алюминия в моче, мг/дм3;
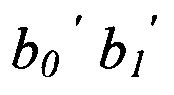 - параметры математической модели, представленные в таблице 1, содержащейся в описании.
- параметры математической модели, представленные в таблице 1, содержащейся в описании.
Моделирование зависимости (P') «маркер экспозиции - лабораторный и функциональный показатель ответа» проводилось отдельно для каждого показателя ответа. Построение модели выполнялось методом нелинейного регрессионного анализа, что позволило определить параметры модели, описываемой вышепредставленной формулой, 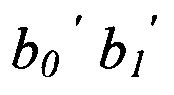 - параметры математической модели, определение которых произведено методом наименьших квадратов с применением пакетов программ по статистическому анализу данных (Statistica, SPSS, SAS и др.).
- параметры математической модели, определение которых произведено методом наименьших квадратов с применением пакетов программ по статистическому анализу данных (Statistica, SPSS, SAS и др.).
Параметры для расчета Р'k представлены в таблице 1.
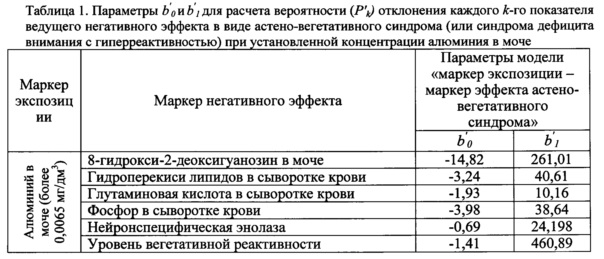
Оценка достоверности параметров и адекватности модели проводилась на основании однофакторного дисперсионного анализа по критерию Фишера при заданном уровне значимости р≤0,05. При построении математических моделей определялись 95%-ные доверительные границы. В качестве адекватных моделей выбирались модели, соответствующие статистическому критерию и отвечающие требованию биологического правдоподобия.
9. На основании этой расчетной вероятность P'k устанавливают уточненные лабораторные и функциональные показатели, способные образовывать внутренние связи и характеризующие ответ в виде отклонения показателя ведущего негативного эффекта (в виде астено-вегетативного синдрома или синдрома дефицита внимания с гиперреактивностью) от физиологической нормы только на повышенный уровень алюминия в моче.
Это уточнение производилось на основании количественной оценки и сравнительного анализа внутренних связей между лабораторными и функциональными показателями ответа, для которых установлена достоверная зависимость «маркер экспозиции - лабораторный и функциональный показатель ответа», выполненного отдельно для группы наблюдения и группы сравнения, в результате выделялись уточненные показатели ответа, образующие внутренние (патогенетически оправданные) связи, характеризующие ответ только на повышенный уровень алюминия в моче.
Указанные уточненные показатели были следующие: 8-гидрокси-2-деоксигуанозин в моче, гидроперекиси липидов, глутаминовая кислота, фосфор, нейронспецифическая энолаза в сыворотке крови, уровень вегетативной реактивности.
10. Далее рассчитывают вероятность Р''k развития ведущего негативного эффекта при установленном уровне k-го уточненного показателя на основе оценки зависимости «уточненный показатель негативного эффекта - ведущий негативный эффект», которая выполняется отдельно для каждого k-го уточненного показателя по формуле:
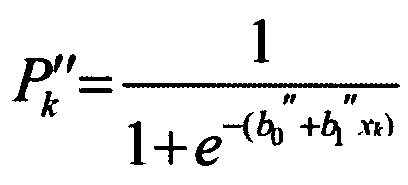 ,
,
где Р''k - вероятность развития ведущего негативного эффекта при отклонении k-го уточненного показателя эффекта от физиологической нормы;
xk - уровень k-го уточненного показателя в единицах измерения соответственно конкретному установленному показателю;
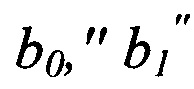 - параметры математической модели, представленные в таблице 2, содержащейся в описании.
- параметры математической модели, представленные в таблице 2, содержащейся в описании.
При установлении ведущего негативного эффекта в виде астено-вегетативного синдрома или синдрома дефицита внимания с гиперреактивностью и те показатели, которые при этом будут достоверно присущи этому ведущему негативному эффекту, относят к комплексу маркерных лабораторных и функциональных показателей.
Параметры для расчета Р''k представлены в таблице 2.
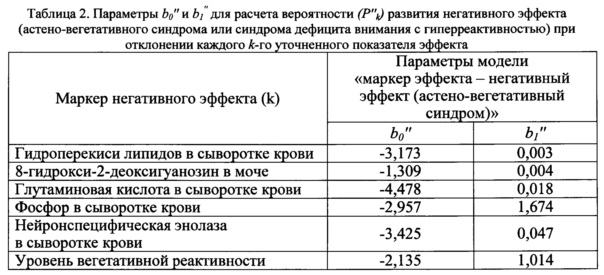
11. Проводят расчет общей вероятности развития ведущего негативного эффекта при повышенном содержании алюминия в моче по формуле:
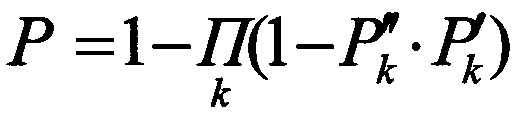 ,
,
где Р - общая вероятность возникновения ведущего негативного эффекта при повышенном содержании алюминия в моче;
Р'k - вероятность отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче;
Р''k - вероятность развития ведущего негативного эффекта при отклонении k-го уточненного показателя эффекта от физиологической нормы;
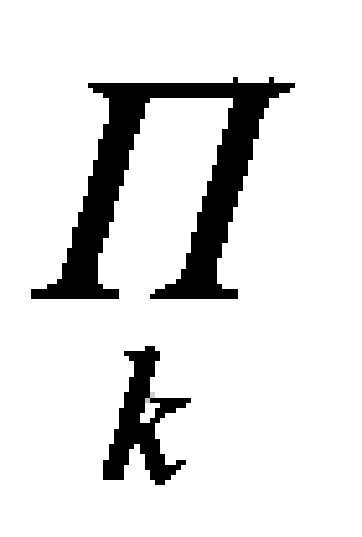 - произведение значений, полученных при выполнении действия
- произведение значений, полученных при выполнении действия 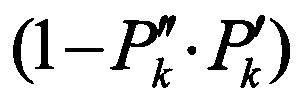 .
.
Полученная величина общей вероятности (Р) количественно характеризует общую вероятность развития у детей астено-вегетативного синдрома (или синдрома дефицита внимания с гиперреактивностью), ассоциированного с аэрогенным воздействием соединений алюминия.
Количественная оценка степени ассоциированности астено-вегетативного синдрома (или синдрома дефицита внимания с гиперреактивностью) с аэрогенным воздействием алюминия, установленного на индивидуальном (или групповом) уровне, определяется по шкале, приведенной в таблице 3.
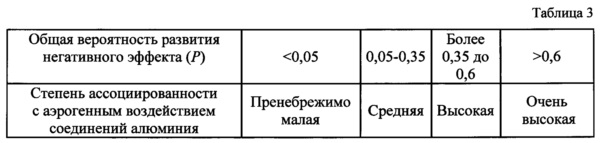
12. А связь ведущего негативного эффекта в виде заболевания центральной или вегетативной нервной системой, ассоциированного с длительной аэрогенной экспозицией алюминием, считают обоснованной при одновременном содержании в моче алюминия более 0,0065 мг/дм3, наличии отклонений от физиологической нормы всех маркерных лабораторных и функциональных показателей, достоверно присущих ведущему негативному эффекту, и количественному значению общей вероятности Р>0,05.
То есть негативный эффект в виде астено-вегетативного синдрома (или синдрома дефицита внимания с гиперреактивностью) является ассоциированным с длительной аэрогенной экспозицией алюминием при условии, что в моче содержится алюминий более 0,0065 мг/дм3, при наличии отклонений от физиологической нормы всех маркерных лабораторных и функциональных показателей, достоверно присущих астено-вегетативного синдрому (или синдрому дефицита внимания с гиперреактивностью) и полученная расчетная величина общей вероятности будет больше 0,05.
Иными словами связь будет обоснованной при обязательном выполнении комплекса условий:
- наличие статистически доказанной и параметризованной системы зависимостей:
- вероятности отклонения от физиологического уровня лабораторных и функциональных показателей нарушения проводимости нервного импульса от концентрации алюминия в моче;
- между уточненными лабораторными и функциональными показателями ответа, характеризующие связи, присущие только повышенному по сравнению с реферативным уровню алюминия в моче более 0,0065 мг/дм3 (реферативный уровень алюминия составляет 0,0065 мг/дм3);
- вероятности развития негативного эффекта со стороны ЦНС (в отношении которой установлена тропность и связь с аэрогенной экспозицией алюминием) в виде астено-вегетативного синдрома (или синдрому дефицита внимания с гиперреактивностью) при отклонении уточненных лабораторных и функциональных показателей нарушения проводимости нервного импульса от физиологической нормы;
- наличие биологической правдоподобности установленных зависимостей, отражающих патогенетическую обусловленность развития нарушения синаптической передачи нервного импульса в ЦНС и проявляющуюся в виде заболевания «астено-вегетативный синдром» при повышенной концентрации алюминия в моче.
На основании использованного методического подхода в качестве маркерных лабораторных и функциональных показателей ведущего негативного эффекта в виде астено-вегетативного синдрома (или синдрома дефицита внимания с гиперреактивностью) у детей при хронической аэрогенной экспозиции алюминием обоснован комплекс из 6 показателей: уровень глутаминовой кислоты, гидроперекиси липидов, нейронспецифической енолазы, фосфора в сыворотке крови, 8-гидрокси-2-деоксигуанозина в моче, наличие асимпатикотонического типа вегетативной реактивности.
Пример конкретной реализации предлагаемого способа:
1 этап.
Качество атмосферного воздуха селитебной застройки, расположенной в зоне влияния алюминиевого производства, характеризуется постоянным присутствием алюминия на уровне 0,1-0,5 ПДКс.с.
Формирует хроническую экспозицию при ингаляционном поступлении алюминия от 0,0014 до 0,0084 мг/(кг х сут).
Количество экспонированного детского населения порядка 24,9 тыс. детей от 0 до 18 лет.
Критическими органами и системами при хронической ингаляционной экспозиции алюминия являются: ЦНС.
Группа наблюдения из зоны экспозиции: 189 детей в возрасте 3-10 лет (100 девочек и 89 мальчиков).
Группа сравнения из зоны вне экспозиции: 45 детей аналогичного возраста (20 мальчиков и 25 девочек).
Выборка для группы сравнения абсолютно сопоставима с выборкой для группы наблюдения по половозрастному составу; по характеру и частоте встречаемости патологии в перинатальном, младенческом периоде и периоде раннего детства (в группе наблюдения 10%, в группе сравнения - 11%); по социально-бытовым условиям жизни (благоустроенное жилье в группе наблюдения имели 81%, в группе сравнения - 80%), имели средний уровень материальной обеспеченности относительно среднедушевого прожиточного минимума; по частоте и характеру отягощенного наследственного анамнеза у родственников 1 и 2 линии (в группе наблюдения 14%, в группе сравнения - 15%); по частоте и характеру вредных привычек и профессиональных вредностей у родителей (в группе наблюдения 17,6%, в группе сравнения - 18,2%). На момент обследования дети не имели острых инфекционных заболеваний не менее, чем в течение 4 недель до начала исследования, индекс инфекционности - 0,2-0,5; не принимали лекарственных препаратов, оказывающих выраженное влияние на центральную нервную систему (лекарственные средства общего обезболивания, снотворные, нейролептические, седативные, противосудорожные, жаропонижающие и анальгетические вещества из производных анилина, пиразолона и салициловой кислоты и т.д.), менее чем за 30 дней до начала исследования.
При выделении ведущих негативных эффектов (приоритетных заболеваний со стороны критической системы на примере ЦНС и соподчиненной ей ВНС) на основании сравнительного анализа структуры заболеваемости детей группы наблюдения и группы сравнения установлены достоверные различия:
- в распространенности заболеваемости детей болезнями центральной и вегетативной нервной систем (р≤0,001),
- в структуре заболеваемости по нозологическим формам заболеваний со стороны ЦНС и ВНС: астено-вегетативный синдром (G90.8) (р≤0,01), астено-невротический синдром (F48.0) (р≤0,02), синдром гиперактивности с дефицитом внимания (F89.0) (р≤0,03);
Связь с аэрогенными воздействием алюминия установлена для болезней ЦНС и ВНС, в том числе для астено-вегетативного синдрома (G90.8) и синдрома дефицита внимания с гиперактивностью (F90.0).
Дальнейшие исследования проведены на примере ведущего негативного эффекта у детей в виде астено-вегетативного синдрома (G90.8) и синдрома гиперактивности с дефицитом внимания (F89.0).
2 этап.
В условиях существующей хронической экспозиции при аэрогенном поступлении алюминия среднее содержание алюминия в моче детей группы наблюдения в 4,5 раза выше относительно аналогичных показателей у детей группы сравнения (р=0,0001) и в 5,5 раза выше референтного уровня (0,0065 мг/дм3) алюминия (р=0,0001).
Моделирование зависимости «концентрация алюминия в атмосферном воздухе - содержание алюминия в моче» позволило получить адекватную модель зависимости содержание алюминия в моче от концентрации алюминия в атмосферном воздухе (R2=0,26; F=69,46; р=0,0001), что позволило обосновать концентрацию алюминия в качестве маркера ингаляционной экспозиции, а его величина более 0,0065 мг/дм3 в моче может свидетельствовать о повышенной опасности нейротоксического воздействия.
3 этап.
У детей при аэрогенном воздействии алюминия ведущим негативным эффектом является астено-вегетативный синдром (G90.8) и синдром дефицита внимания с гиперактивностью (F90.0), с которыми патогенетически связанным является нарушение синаптической передачи нервного импульса. Сформирован перечень лабораторных и функциональных показателей для исследования ответных реакций организма исходя из ведущего негативного эффекта (астено-вегетативного синдрома и синдрома дефицита внимания с гиперактивностью), сведения о которых приведены в таблице 4.

Выделены показатели у детей группы наблюдения, уровень которых достоверно отличался от уровня сравнения и направленность отклонения от физиологической нормы биологически правдоподобна. Это:
- биохимические и иммунологические показатели: повышенный уровень гидроперекиси липидов, малонового диальдегида, глутаминовой кислоты, 8-гидрокси-2-деоксигуанозина, ионизированного кальция, нейронспецифической энолазы, сниженный уровень γ-аминомасляной кислоты, фосфора, абсолютного фагоцитоза и фагоцитарного числа;
- функциональные показатели вегетативной нервной системы: исходный вегетативный тонус, тип вегетативной реактивности;
Связь с экспозицией (по расчету отношения шансов) установлена для показателей: повышенный уровень гидроперекиси липидов, глутаминовой кислоты, 8-OH-2-dG, ионизированного кальция, нейронспецифической энолазы, сниженный уровень фосфора, абсолютного фагоцитоза и фагоцитарного числа, вегетативной реактивности;
Установлены достоверные зависимости вероятности отклонения от физиологической нормы лабораторного и функционального показателя нарушения проводимости нервного импульса при повышенной концентрации алюминия в моче (Р') для гидроперекиси липидов, глутаминовой кислоты, 8-OH-2-dG, ионизированного кальция, фосфора, нейронспецифической энолазы, абсолютного фагоцитиоза, фагоцитарного числа и типа вегетативной реактивности.
На основании оценки и сравнительного анализа внутренних связей между показателями нарушения проводимости нервного импульса в группе наблюдения и в группе сравнения выделены уточненные лабораторные и функциональные показатели, образующие внутренние связи, характеризующие ответ только на повышенный уровень алюминия в моче (Р''): 8-гидрокси-2-деоксигуанозин в моче, гидроперекиси липидов, глутаминовая кислота, фосфор, нейронспецифическая енолаза в сыворотке крови, уровень вегетативной реактивности (таблица 5).
В результате моделирования зависимости «маркерный показатель ответа - ведущий негативный эффект (астено-вегетативный синдром или синдром дефицита внимания с гиперактивностью) установлены достоверные вероятности развития негативного эффекта, имеющие зависимость от уровня маркерных показателей нарушения проводимости нервного импульса: повышение глутаминовой кислоты, гидроперекиси липидов и нейронспецифической энолазы в сыворотке крови, 8-OH-2dG в моче, снижение уровня фосфора в сыворотке крови, уровня вегетативной реактивности.
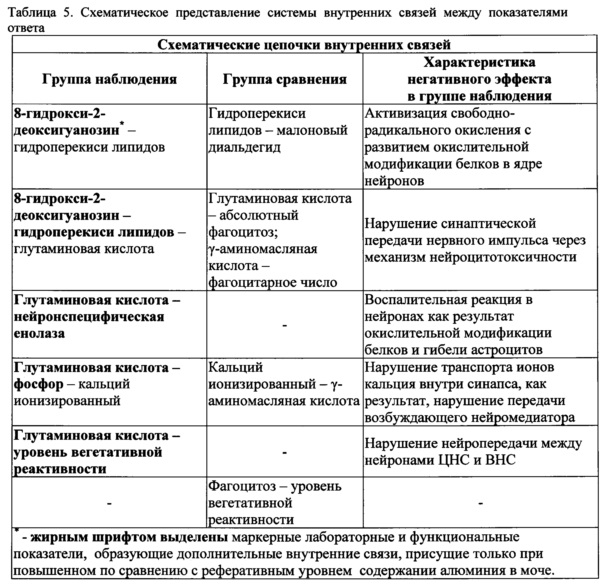
Условия, выполнение которых является обязательным при обосновании маркеров лабораторных и функциональных показателей ведущих негативных эффектов, выполнены, а именно:
1) установлена статистически доказанная и параметризованная система зависимостей:
- вероятности отклонения от физиологического уровня лабораторного и функционального показателя нарушения синаптической передачи нервного импульса от концентрации алюминия в моче;
- между маркерными показателями ответа, характеризующими связи, присущие только повышенному уровню алюминия в моче;
- вероятности развития ведущего негативного эффекта со стороны ЦНС и ВНС в виде астено-вегетативного синдрома или синдрома дефицита внимания с гиперактивностью, в отношении которых установлена тропность алюминия при аэрогенной экспозиции, а также связь с экспозицией;
2) установленные зависимости, отражающие патогенетическую обусловленность развития ведущего негативного эффекта в виде астено-вегетативного синдрома, с которым патогенетически связано нарушение синаптической передачи нервного импульса в ЦНС и ВНС, при установленной концентрации алюминия в моче, являются биологически правдоподобными.
Следовательно, комплекс маркерных лабораторных и функциональных показателей (при обязательном участии каждого без исключении), а именно: уровень глутаминовой кислоты, гидроперекиси липидов, 8-гидрокси-2-деоксигуанозина, фосфора, нейронспецифической энолазы, уровень вегетативной реактивности, обоснованы в качестве маркеров ведущего негативного эффекта - астено-вегетативного синдрома или синдрома дефицита внимания с гиперактивностью, у детей при аэрогенном воздействии алюминия.
Пример расчета общей вероятности развития астено-вегетативного синдрома при аэрогенном воздействии алюминия:
Условие задачи:
- содержание алюминия в атмосферном воздухе 0,0013 мг/м3 (0,13 ПДКс.с.)
- экспозиция при ингаляционном поступлении алюминия 0,002 мг/(кг⋅сут),
- содержание алюминия в моче ребенка 0,036 мг/дм3
- установлен диагноз - астено-вегетативный синдром (G90.8).
- уровень маркерных лабораторных и функциональных показателей:
- 8-гидрокси-2-деоксигуанозин в моче - 205,85 нг/см3,
- гидроперикиси липидов в сыворотке крови - 215,08 мкмоль/дм3,
- глутаминовая кислота в сыворотке крови - 101,48 мкмоль/дм3,
- нейронспецифическая енолаза в сыворотке крови - 5,04 мкг/дм3,
- фосфор в сыворотке крови - 1,52 моль/дм3,
- вегетативная реактивность - 0,5 у.е. (асимпатикотонический тип)
Вопрос: какова общая вероятность развития астено-вегетативного синдрома, ассоциированного с аэрогенной экспозицией алюминия?
Данные расчета приведены в таблице 6.
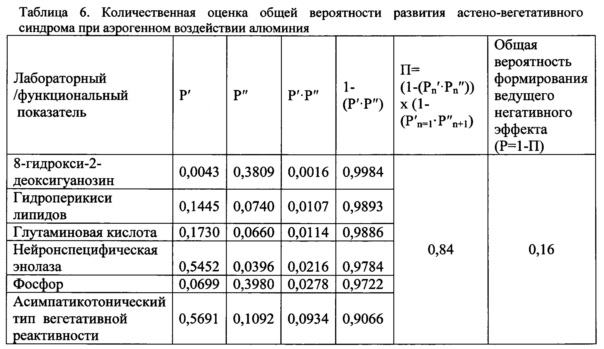
Ответ: общая вероятность развития астено-вегетативного синдрома, ассоциированного с аэрогенной экспозицией алюминия составляет 0,16, что оценивается как средняя степень (в соответствии со шкалой количественной оценки Р (0,05-0,35) таблица 3). При этом связь с аэрогенными воздействием алюминия обоснована для астено-вегетативного синдрома (G90.8) и синдрома дефицита внимания с гиперактивностью (F90.0) (OR=1,7-4,3; DI=1,45-43,65).
Изобретение относится к медицине. Выделяют территорию с постоянным присутствием алюминия и устанавливают перечень наиболее вероятных негативных эффектов - нарушений здоровья у детей, ассоциированных с повышенной аэрогенной экспозицией алюминия. В качестве негативных эффектов принимают заболевания, связанные с ЦНС и ВНС. Формируют группу наблюдения из детей с территории экспозиции и группу сравнения из детей с территории экологического благополучия. Устанавливают ведущие заболевания ЦНС и ВНС в каждой группе. Формируют перечень лабораторных и функциональных показателей, связанных с ведущим негативным эффектом. Отбирают пробы мочи и крови у детей из обеих групп. Определяют в моче содержание алюминия, а в крови - уровни лабораторных показателей. Инструментальными методами определяют функциональные показатели. По математической формуле рассчитывают вероятность Р'k отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче, устанавливая уточненные лабораторные и функциональные показатели. Далее по математической формуле рассчитывают вероятность Р''k развития ведущего негативного эффекта при установленном уровне k-го уточненного показателя. Показатели, которые при этом будут достоверно присущи ведущему негативному эффекту, относят к комплексу маркерных лабораторных и функциональных показателей. Проводят расчет общей вероятности Р развития ведущего негативного эффекта при повышенном относительно референтного уровня содержании алюминия в моче. Определяют степень ассоциированности ведущего негативного эффекта с аэрогенным воздействием соединений алюминия: при Р менее 0,05 – пренебрежительно малая, при Р 0,05-0,35 – средняя, при Р от более 0,35 до 0,6 включительно – высокая, при Р более 0,6 – очень высокая. Связь ведущего негативного эффекта в виде заболевания ЦНС или ВНС, ассоциированного с длительной аэрогенной экспозицией алюминием, считают обоснованной при одновременном содержании в моче алюминия более 0,0065 мг/дм3, наличии отклонений от физиологической нормы всех маркерных лабораторных и функциональных показателей, достоверно присущих ведущему негативному эффекту и количественному значению общей вероятности Р>0,05. Способ позволяет информативно и доказательно обосновать возникновение у детей негативного эффекта в виде заболевания, связанного с ЦНС) или ВНС, ассоциированного с аэрогенной экспозицией алюминия за счет оценки комплекса наиболее значимых показателей. 6 табл., 1 пр.
Способ обоснования возникновения у детей негативного эффекта в виде заболевания, связанного с центральной или вегетативной нервной системой, ассоциированного с аэрогенной экспозицией алюминия, заключающийся в том, что выделяют территорию с постоянным присутствием алюминия и/или с его повышенной по сравнению с предельно-допустимой концентрацией в атмосферном воздухе, формирующей длительную хроническую экспозицию алюминия, устанавливают перечень наиболее вероятных негативных эффектов - нарушений здоровья у детей, ассоциированных с повышенной аэрогенной экспозицией алюминия, в качестве которых принимают заболевания, связанные с центральной (ЦНС) и вегетативной нервной системой (ВНС), из указанного перечня вероятных негативных эффектов выделяют ведущие конкретные заболевания, характерные для ЦНС и ВНС, путем формирования группы наблюдения, состоящей из детей, постоянно проживающих на территории и подвергающихся хронической экспозиции алюминия, и группы сравнения из детей с территории экологического благополучия, и установления ведущих конкретных заболеваний ЦНС и ВНС в каждой группе; причем при выборе указанных ведущих конкретных заболеваний учитывают два критерия: уровень конкретной заболеваемости в группе наблюдения должен достоверно отличаться от уровня конкретной заболеваемости в группе сравнения и иметь достоверную связь этого конкретного заболевания с аэрогенным воздействием соединений алюминия; далее, исходя из установленного ведущего конкретного заболевания, связанного с системой ЦНС и ВНС, - ведущего негативного эффекта, формируют перечень лабораторных и функциональных показателей, которые этиопатогенетически связаны с этим ведущим негативным эффектом, а именно: в качестве лабораторных и функциональных показателей принимают следующие: уровень гидроперекиси липидов в сыворотке крови; малонового диальдегида в плазме крови; 8-гидрокси-2-деоксигуанозина в моче; глутаминовой кислоты в сыворотке крови; γ-аминомасляной кислоты в сыворотке крови; ионизированного кальция в цельной крови; фосфора в сыворотке крови; нейронспецифической енолазы в сыворотке крови; абсолютный фагоцитоз в крови; фагоцитарное число в крови; исходный вегетативный тонус; тип вегетативной реактивности; отбирают пробы мочи и крови у детей из групп наблюдения и сравнения; определяют в моче содержание алюминия, а в крови - уровни лабораторных показателей, инструментальными методами определяют функциональные показатели; затем для детей обеих групп проводят количественную оценку связи изменения показателей относительно физиологической нормы с аэрогенным воздействием алюминия на основании расчета отношения шансов (OR) и его доверительного интервала (DI), и при OR>1 и величине нижней границы DI>1 связь считается достоверно установленной; затем рассчитывают вероятность P'k отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче на основе оценки зависимости «маркер экспозиции, т.е. содержание алюминия в моче, - ответ, т.е. показатель ведущего негативного эффекта», которая выполняется отдельно для каждого k-го показателя по формуле:
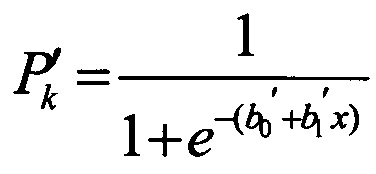 ,
,
где х - концентрация алюминия в моче, мг/дм3;
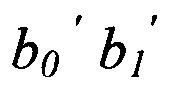 - параметры математической модели, представленные в таблице 1, содержащейся в описании;
- параметры математической модели, представленные в таблице 1, содержащейся в описании;
из ранее определенных лабораторных и функциональных показателей устанавливают уточненные лабораторные и функциональные показатели, характеризующие ответ в виде отклонения показателя ведущего негативного эффекта от физиологической нормы только на повышенный, относительно референтного уровня, уровень алюминия в моче; далее рассчитывают вероятность Р''k развития ведущего негативного эффекта при установленном уровне k-го уточненного показателя на основе оценки зависимости «уточненный показатель негативного эффекта - ведущий негативный эффект», которая выполняется отдельно для каждого k-го уточненного показателя по формуле:
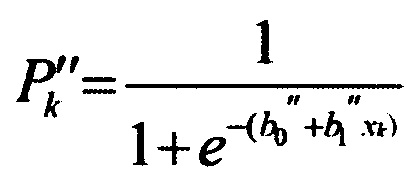 ,
,
где Р''k - вероятность развития ведущего негативного эффекта при отклонении k-го уточненного показателя эффекта от физиологической нормы;
xk - уровень k-го уточненного показателя в единицах измерения соответственно конкретному установленному показателю;
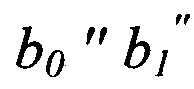 - параметры математической модели, представленные в таблице 2, содержащейся в описании;
- параметры математической модели, представленные в таблице 2, содержащейся в описании;
и те показатели, которые при этом будут достоверно присущи ведущему негативному эффекту, относят к комплексу маркерных лабораторных и функциональных показателей; затем проводят расчет общей вероятности развития ведущего негативного эффекта при повышенном относительно референтного уровня содержании алюминия в моче по формуле:
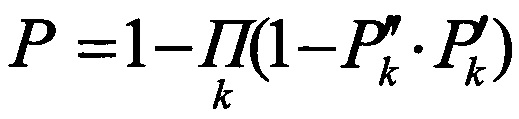 ,
,
где Р - общая вероятность возникновения ведущего негативного эффекта при повышенном содержании алюминия в моче;
P'k - вероятность отклонения k-го показателя ведущего негативного эффекта от физиологической нормы при повышенном относительно референтного уровня содержании алюминия в моче;
Р''k - вероятность развития ведущего негативного эффекта при отклонении k-го уточненного показателя эффекта от физиологической нормы;
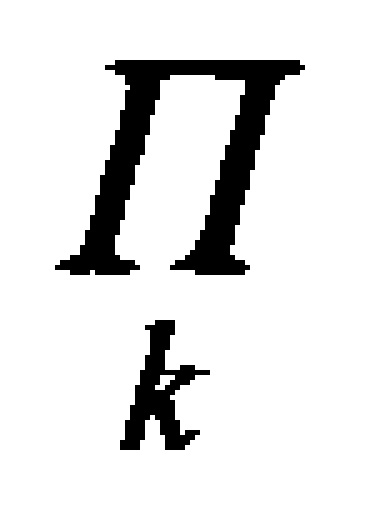 - произведение значений, полученных при выполнении действия
- произведение значений, полученных при выполнении действия 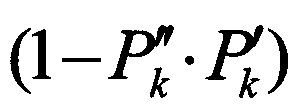 ;
;
при этом по полученной величине общей вероятности Р определяют степень ассоциированности ведущего негативного эффекта с аэрогенным воздействием соединений алюминия: при Р менее 0,05 - пренебрежительно малая, при Р 0,05-0,35 - средняя, при Р от более 0,35 до 0,6 включительно - высокая, при Р более 0,6 - очень высокая; а связь ведущего негативного эффекта в виде заболевания центральной или вегетативной нервной системой, ассоциированного с длительной аэрогенной экспозицией алюминием, считают обоснованной при одновременном содержании в моче алюминия более 0,0065 мг/дм3, наличии отклонений от физиологической нормы всех маркерных лабораторных и функциональных показателей, достоверно присущих ведущему негативному эффекту, и количественному значению общей вероятности Р>0,05.
| ШУГАЛЕЙ И.В | |||
| Некоторые аспекты влияния алюминия и его соединений на живые организмы | |||
| Экологическая химия, 21 (3), 2012, 172-186 | |||
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ЗАБОЛЕВАНИЙ НЕРВНОЙ СИСТЕМЫ У ДЕТЕЙ, ПОТРЕБЛЯЮЩИХ ВОДУ С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ МАРГАНЦА | 2014 |
|
RU2569763C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ДЕЙСТВИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ НА ОРГАНИЗМ | 1997 |
|
RU2138816C1 |
| СПОСОБ ВЫЯВЛЕНИЯ НАРУШЕНИЙ ВЕГЕТАТИВНОЙ РЕГУЛЯЦИИ И СТАДИЙ РАЗВИТИЯ НЕЙРОЦИРКУЛЯТОРНОЙ ДИСТОНИИ У ДЕТЕЙ И ПОДРОСТКОВ | 2000 |
|
RU2197174C2 |
| SHAW C.A | |||
| Aluminum in the central nervous system (CNS): toxicity in humans and animals, vaccine adjuvants, and autoimmunity | |||
| Immunol Res | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2018-09-13—Публикация
2017-09-19—Подача