Ссылка на родственные заявки
Настоящая заявка испрашивает приоритет предварительной заявки на патент США 61/739,026, поданной 19 декабря 2012 года, все описание которой настоящим прямо включено посредством ссылки.
Область техники, к которой относится изобретение
Изобретение, раскрытое в настоящем документе, связано с областью способов получения молекул, которые могут применяться в качестве пестицидов (например, акарицидов, инсектицидов, моллюскоцидов и нематоцидов), с такими молекулами и способами применения таких молекул для борьбы с вредителями.
Уровень техники
Ежегодно насекомые-вредители вызывают миллионы человеческих смертей во всем мире. Кроме того, существует более десяти тысяч видов вредителей, которые вызывают потери в сельском хозяйстве. Общемировые сельскохозяйственные потери составляют миллиарды долларов США ежегодно.
Термиты повреждают все виды частных и общественных сооружений. Общемировые потери от повреждений, связанных с термитами, ежегодно составляют миллиарды долларов США.
Насекомые-вредители пищевых запасов поедают и загрязняют запасы пищи. Общемировые потери запасов пищи составляют миллиарды долларов США ежегодно, но, что еще более важно, лишают людей необходимой пищи.
Существует острая потребность в новых пестицидах. У некоторых насекомых-вредителей развивается устойчивость к пестицидам, используемым в настоящее время. Сотни видов насекомых-вредителей устойчивы к одному или более пестицидам. Известно о развитии устойчивости к некоторым более старым пестицидам, таким как ДДТ, карбаматы и органофосфаты. Но устойчивость развилась даже к некоторым более новым пестицидам, например, имидаклоприду.
Поэтому, по многим причинам, включая вышеуказанные причины, существует потребность в новых пестицидах.
ОПРЕДЕЛЕНИЯ
Примеры, данные в определениях, в целом не являются исчерпывающими и не должны рассматриваться в качестве ограничения изобретения, раскрытого в настоящем документе. Подразумевается, что заместитель должен соответствовать правилам образования химических связей и пространственным ограничениям в отношении конкретной молекулы, к которой он присоединен.
ʺАлкенилʺ означает алифатический, ненасыщенный (по меньшей мере с одной двойной углерод-углеродной связью), разветвленный или неразветвленный заместитель, состоящий из углерода и водорода, например, винил, аллил, бутенил, пентенил и гексенил.
ʺАлкенилоксиʺ означает алкенил, дополнительно состоящий из одинарной углерод-кислородной связи, например, аллилокси, бутенилокси, пентенилокси, гексенилокси.
ʺАлкоксиʺ означает алкил, дополнительно состоящий из одинарной углерод-кислородной связи, например, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси и трет-бутокси.
ʺАлкилʺ означает алифатический, насыщенный, разветвленный или неразветвленный заместитель, состоящий из углерода и водорода, например, метил, этил, (C3)алкил, который представляет собой н-пропил и изопропил, (C4)алкил, который представляет собой н-бутил, втор-бутил, изобутил и трет-бутил.
ʺАлкинилʺ означает алифатический, ненасыщенный (по меньшей мере с одной тройной углерод-углеродной связью), разветвленный или неразветвленный заместитель, состоящий из углерода и водорода, например, этинил, пропаргил, бутинил и пентинил.
ʺАлкинилоксиʺ означает алкинил, дополнительно состоящий из одинарной углерод-кислородной связи, например, пентинилокси, гексинилокси, гептинилокси и октинилокси.
ʺАрилʺ означает циклический, ароматический заместитель, состоящий из водорода и углерода, например, фенил, нафтил и бифенил.
ʺ(Cx-Cy)ʺ, где индексы ʺxʺ и ʺyʺ являются целыми числами, такими как 1, 2 или 3, означает диапазон атомов углерода для заместителя, например, (C1-C4)алкил означает метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил и трет-бутил, каждый индивидуально.
ʺЦиклоалкенилʺ означает моноциклический или полициклический, ненасыщенный (по меньшей мере с одной двойной углерод-углеродной связью) заместитель, состоящий из углерода и водорода, например, циклобутенил, циклопентенил, циклогексенил, норборненил, бицикло[2.2.2]октенил, тетрагидронафтил, гексагидронафтил и октагидронафтил.
ʺЦиклоалкенилоксиʺ означает циклоалкенил, дополнительно состоящий из одинарной углерод-кислородной связи, например, циклобутенилокси, циклопентенилокси, норборненилокси и бицикло[2.2.2]октенилокси.
ʺЦиклоалкилʺ означает моноциклический или полициклический, насыщенный заместитель, состоящий из углерода и водорода, например, циклопропил, циклобутил, циклопентил, норборнил, бицикло[2.2.2]октил и декагидронафтил.
ʺЦиклоалкоксиʺ означает циклоалкил, дополнительно состоящий из одинарной углерод-кислородной связи, например, циклопропилокси, циклобутилокси, циклопентилокси, норборнилокси, и бицикло[2.2.2]октилокси.
ʺГалоʺ означает фтор, хлор, бром и иод.
ʺГалоалкоксиʺ означает алкокси, дополнительно состоящий из, от одного до максимального возможного количества идентичных или различных, галогенов, например, фторметокси, трифторметокси, 2,2-дифторпропокси, хлорметокси, трихлорметокси, 1,1,2,2-тетрафторэтокси и пентафторэтокси.
ʺГалоалкилʺ означает алкил, дополнительно состоящий из от одного до максимального возможного количества идентичных или различных галогенов, например, фторметил, трифторметил, 2,2-дифторпропил, хлорметил, трихлорметил, и 1,1,2,2-тетрафторэтил.
ʺГетероциклилʺ означает циклический заместитель, который может быть полностью насыщенным, частично ненасыщенным или полностью ненасыщенным, где циклическое структура содержит по меньшей мере один атом углерода и по меньшей мере один гетероатом, где указанный гетероатом является атомом азота, серы или кислорода. В случае серы этот атом может находиться в других степенях окисления, таких как сульфоксид и сульфон. Примеры ароматических гетероциклилов включают, без ограничения перечисленными, бензофуранил, бензоизотиазолил, бензоизоксазолил, бензоксазолил, бензотиенил, бензотиазолил, циннолинил, фуранил, имидазолил, индазолил, индолил, изоиндолил, изохинолинил, изотиазолил, изоксазолил, оксадиазолил, оксазолинил, оксазолил, фталазинил, пиразинил, пиразолинил, пиразолил, пиридазинил, пиридил, пиримидинил, пирролил, хиназолинил, хинолинил, хиноксалинил, тетразолил, тиазолинил, тиазолил, тиенил, триазинил и триазолил. Примеры полностью насыщенных гетероциклилов включают, без ограничения перечисленными, пиперазинил, пиперидинил, морфолинил, пирролидинил, оксетанил, тетрагидрофуранил, тетрагидротиенил и тетрагидропиранил. Примеры частично ненасыщенных гетероциклилов включают, без ограничения перечисленными, 1,2,3,4-тетрагидрохинолинил, 4,5-дигидро-оксазолил, 4,5-дигидро-1H-пиразолил, 4,5-дигидро-изоксазолил и 2,3-дигидро-[1,3,4]-оксадиазолил.
Дополнительные примеры включают следующие:
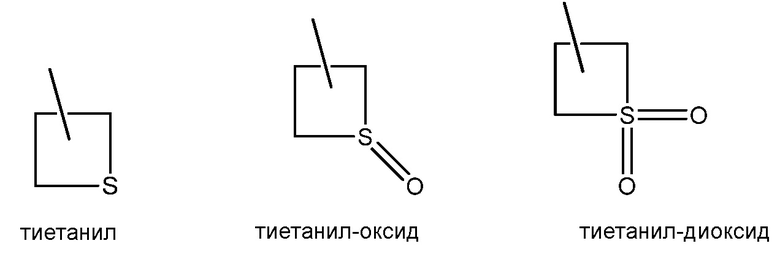
ПОДРОБНОЕ ОПИСАНИЕ
В настоящем документе раскрыты молекулы, имеющие следующую формулу (ʺФормула одинʺ):
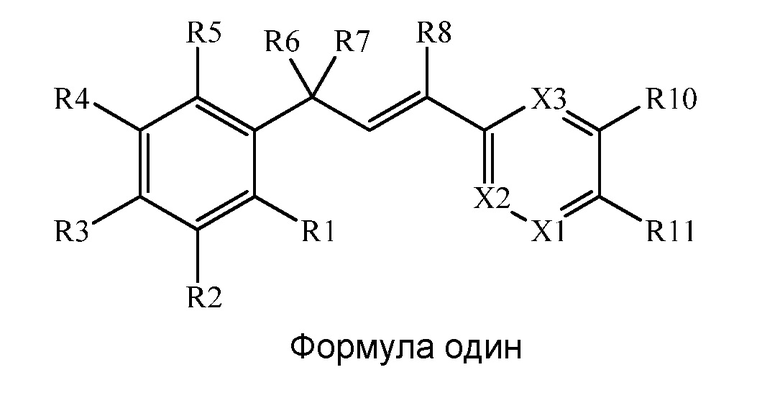
в которой:
(a) R1 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(b) R2 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(c) R3 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(d) R4 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(e) R5 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(f) R6 является (C1-C8)галоалкилом;
(g) R7 выбран из H, F, Cl, Br, I, OH, (C1-C8)алкокси и гало(C1-C8)алкокси;
(h) R8 выбран из H, (C1-C8)алкила, гало(C1-C8)алкила, OR14 и N(R14)(R15);
(i) R9 выбран из H, F, Cl, Br, I, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, OR14 и N(R14)(R15);
(j) R10 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, цикло(C3-C6)алкила, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), NR14R15, C(=O)H, C(=O)N(R14)(R15), CN(R14)(R15)(=NOH), (C=O)O(C1-C8)алкил, (C=O)О, гетероциклила, (C2-C8)алкенила, гало(C2-C8)алкенила, (C2-C8)алкинила,
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из OH, (C1-C8)алкокси, S(C1-C8)алкила, S(O)(C1-C8)алкила, S(O)2(C1-C8)алкила, NR14R15, и
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из (C1-C8)алкокси, S(C1-C8)алкила, S(O)(C1-C8)алкила, S(O)2(C1-C8)алкила и N(R14)(R15);
(k) R11 является C(=X5)N(X6)(R14), где:
X5 выбран из O, С или NH, и
X6 выбран из галоцикло(C3-C6)алкила, замещенного цикло(C3-C6)алкила и замещенного галоцикло(C3-C6)алкила,
где указанный замещенный цикло(C3-C6)алкил замещен одним или более заместителями, выбранными из CN, NO2, (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R15)(R16), C(=X5)N(R15)(R16), (C1-C8)алкил-C(=X5)N(R15)(R16), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила и C(=O)H, и
где указанный замещенный галоцикло(C3-C6)алкил замещен одним или более заместителями, выбранными из CN, NO2, (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R15)(R16), C(=X5)N(R15)(R16), (C1-C8)алкил-C(=X5)N(R15)(R16), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила и C(=O)H,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо), C(=O)(C1-C8)алкила, C(=O)(C3-C6)циклоалкила, S(=O)2(C1-C8)алкила, NR14R15 и оксо;
(l) R12 выбран из: (v), H, F, Cl, Br, I, CN, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси и цикло(C3-C6)алкила;
(m) R13 выбран из: (v), H, F, Cl, Br, I, CN, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси и гало(C1-C8)алкокси;
(n) каждый R14 независимо выбран из H, (C1-C8)алкила, (C2-C8)алкенила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R16)(R17), (C1-C8)алкил-C(=O)N(R16)(R17), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила, C(=O)H,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, (C3-C6)циклоалкил S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо), гетероциклила, C(=O)(C1-C8)алкила, C(=O)O(C1-C8)алкила и оксо, (где указанный алкил, алкокси и гетероциклил могут быть дополнительно замещены одним или более F, Cl, Br, I, CN и NO2);
(o) каждый R15 независимо выбран из H, (C1-C8)алкила, (C2-C8)алкенила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероцикли-ла), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R16)(R17), (C1-C8)алкил-C(=O)N(R16)(R17), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила, C(=O)H,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, (C3-C6)циклоалкил S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо), гетероциклила, C(=O)(C1-C8)алкила, C(=O)O(C1-C8)алкила и оксо, (где указанный алкил, алкокси и гетероциклил могут быть дополнительно замещены одним или более F, Cl, Br, I, CN и NO2);
(p) каждый R16 независимо выбран из H, (C1-C8)алкила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкила,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо;
(q) каждый R17 независимо выбран из H, (C1-C8)алкила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкила,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо;
(r) X1 выбран из N и CR12;
(s) X2 выбран из N, CR9 и CR13;
(t) X3 выбран из N и CR9; и
(v) R12 и R13 вместе образуют связь, содержащую 3-4 атома, выбранных из C, N, O и S, где указанная связь соединяется обратно с кольцом, образуя 5-6-членное насыщенное или ненасыщенное циклическое кольцо, где указанная связь имеет по меньшей мере один заместитель X4, где X4 выбран из R14, N(R14)(R15), N(R14)(C(=O)R14), N(R14)(C(=S)R14), N(R14)(C(=O)N(R14)(R14)), N(R14)(C(=S)N(R14)(R14)), N(R14)(C(=O)N(R14)((C2-C8)алкенил)), N(R14)(C(=S)N(R14)((C2-C8)алкенил)), где каждый R14 выбран независимо.
В другом варианте осуществления настоящего изобретения R1 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, CN, NO2, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R2 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, CN, NO2, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R3 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, CN, NO2, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R4 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, CN, NO2, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R5 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, CN, NO2, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R2 и R4 выбраны из F, Cl, Br, I, CN и NO2, а R1, R3 и R5 являются H.
В другом варианте осуществления настоящего изобретения R2, R3 и R4 выбраны из F, Cl, Br, I, CN и NO2, а R1 и R5 являются H.
В другом варианте осуществления настоящего изобретения R2, R3 и R4 независимо выбраны из F и Cl, а R1 и R5 являются H.
В другом варианте осуществления настоящего изобретения R1 выбран из Cl и H.
В другом варианте осуществления настоящего изобретения R2 выбран из CF3, CH3, Cl, F и H.
В другом варианте осуществления настоящего изобретения R3 выбран из OCH3, CH3, F, Cl или H.
В другом варианте осуществления настоящего изобретения R4 выбран из CF3, CH3, Cl, F и H.
В другом варианте осуществления настоящего изобретения R5 выбран из F, Cl и H.
В другом варианте осуществления настоящего изобретения R6 может быть выбран из любой комбинации одного или более следующего: галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил и гало(C8)алкил.
В другом варианте осуществления настоящего изобретения R6 является трифторметилом.
В другом варианте осуществления настоящего изобретения R7 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br и I.
В другом варианте осуществления настоящего изобретения R7 выбран из H, OCH3 и OH.
В другом варианте осуществления настоящего изобретения R8 может быть выбран из любой комбинации одного или более следующего: H, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил и гало(C8)алкил.
В другом варианте осуществления настоящего изобретения R8 выбран из CH3 и H.
В другом варианте осуществления настоящего изобретения R9 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R10 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, CN, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси, гало(C8)алкокси, циклопропил, циклобутил, циклопентил и циклогексил.
В другом варианте осуществления настоящего изобретения R10 может быть выбран из любой комбинации одного или более следующего: H, Cl, Br, CH3 и CF3.
В другом варианте осуществления настоящего изобретения R10 выбран из Br, C(=NOH)NH2, C(=O)H, C(=O)NH2, C(=O)OCH2CH3, C(=O)OH, CF3, CH2CH3, CH2OH, CH3, Cl, CN, F, H, NH2, NHC(=O)H, NHCH3, NO2, OCH3, OCHF2 и пиридила.
В другом варианте осуществления настоящего изобретения R11 является C(=O)N(H)(циклопропил-(C(=O)N(H)(CH2CF3)), C(=O)N(H)(циклопропил-(C(=S)N(H)(CH2CF3)), C(=O)N(H)(циклобутил-C(=O)N(H)(CH2CF3)) и C(=O)N(H)(циклопропил-CN).
В другом варианте осуществления настоящего изобретения R11 является C(=(O или S))N(H)(циклопропил-(C(=(O или S))N(H)(гало(C1-C6)алкилом)) или C(=(O или S)N(H)(циклобутил-(C=(O или S))N(H)(гало(C1-C6)алкилом)). Этот вариант осуществления может быть объединен с любым вариантом осуществления R1-R10 и любым вариантом осуществления X1-X3.
В другом варианте осуществления настоящего изобретения R12 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R12 выбран из CH3 и H.
В другом варианте осуществления настоящего изобретения R13 может быть выбран из любой комбинации одного или более следующего: H, F, Cl, Br, I, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
В другом варианте осуществления настоящего изобретения R13 выбран из CH3, Cl и H.
В другом варианте осуществления настоящего изобретения R12-R13 являются гидрокарбильной связью, содержащей CH=CHCH=CH.
В другом варианте осуществления настоящего изобретения R14 может быть выбран из любой комбинации одного или более следующего: H, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метил-арил, этил-арил, (C3)алкил-арил, (C4)алкил-арил, (C5)алкил-арил, (C6)алкил-арил, (C7)алкил-арил, (C8)алкил-арил, метил-(замещенный арил), этил-(замещенный арил), (C3)алкил-(замещенный арил), (C4)алкил-(замещенный арил), (C5)алкил-(замещенный арил), (C6)алкил-(замещенный арил), (C7)алкил-(замещенный арил), (C8)алкил-(замещенный арил), O-метил-арил, O-этил-арил, O-(C3)алкил-арил, O-(C4)алкил-арил, O-(C5)алкил-арил, O-(C6)алкил-арил, O-(C7)алкил-арил, O-(C8)алкил-арил, O-метил-(замещенный арил), O-этил-(замещенный арил), O-(C3)алкил-(замещенный арил), O-(C4)алкил-(замещенный арил), O-(C5)алкил-(замещенный арил), O-(C6)алкил-(замещенный арил), O-(C7)алкил-(замещенный арил), O-(C8)алкил-(замещенный арил), метил-гетероциклил, этил-гетероциклил, (C3)алкил-гетероциклил, (C4)алкил-гетероциклил, (C5)алкил-гетероциклил, (C6)алкил-гетероциклил, (C7)алкил-гетероциклил, (C8)алкил-гетероциклил, метил-(замещенный гетероциклил), этил-(замещенный гетероциклил), (C3)алкил-(замещенный гетероциклил), (C4)алкил-(замещенный гетероциклил), (C5)алкил-(замещенный гетероциклил), (C6)алкил-(замещенный гетероциклил), (C7)алкил-(замещенный гетероциклил), (C8)алкил-(замещенный гетероциклил), O-метил-гетероциклил, O-этил-гетероциклил, O-(C3)алкил-гетероциклил, O-(C4)алкил-гетероциклил, O-(C5)алкил-гетероциклил, O-(C6)алкил-гетероциклил, O-(C7)алкил-гетероциклил, O-(C8)алкил-гетероциклил, O-метил-(замещенный гетероциклил), O-этил-(замещенный гетероциклил), O-(C3)алкил-(замещенный гетероциклил), O-(C4)алкил-(замещенный гетероциклил), O-(C5)алкил-(замещенный гетероциклил), O-(C6)алкил-(замещенный гетероциклил), O-(C7)алкил-(замещенный гетероциклил), O-(C8)алкил-(замещенный гетероциклил), метил-C(=O)N(R16)(R17), этил-C(=O)N(R16)(R17), (C3)алкил-C(=O)N(R16)(R17), (C4)алкил-C(=O)N(R16)(R17), (C5)алкил-C(=O)N(R16)(R17), (C6)алкил-C(=O)N(R16)(R17), (C7)алкил-C(=O)N(R16)(R17) и (C8)алкил-C(=O)N(R16)(R17).
В другом варианте осуществления настоящего изобретения R14 может быть выбран из любой комбинации одного или более следующего: H, CH3, CH2CF3, CH2-галопиридил, оксо-пирролидинил, галофенил, тиетанил, CH2-фенил, CH2-пиридил, тиетанил-диоксид, CH2-галотиазолил, C((CH3)2)-пиридил, N(H)(галофенил), CH2-пиримидинил, CH2-тетрагидрофуранил, CH2-фуранил, O-CH2-галопиридил и CH2C(=O)N(H)(CH2CF3).
В другом варианте осуществления настоящего изобретения R15 может быть выбран из любой комбинации одного или более следующего: H, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метил-арил, этил-арил, (C3)алкил-арил, (C4)алкил-арил, (C5)алкил-арил, (C6)алкил-арил, (C7)алкил-арил, (C8)алкил-арил, метил-(замещенный арил), этил-(замещенный арил), (C3)алкил-(замещенный арил), (C4)алкил-(замещенный арил), (C5)алкил-(замещенный арил), (C6)алкил-(замещенный арил), (C7)алкил-(замещенный арил), (C8)алкил-(замещенный арил), O-метил-арил, O-этил-арил, O-(C3)алкил-арил, O-(C4)алкил-арил, O-(C5)алкил-арил, O-(C6)алкил-арил, O-(C7)алкил-арил, O-(C8)алкил-арил, O-метил-(замещенный арил), O-этил-(замещенный арил), O- (C3)алкил-(замещенный арил), O-(C4)алкил-(замещенный арил), O-(C5)алкил-(замещенный арил), O-(C6)алкил-(замещенный арил), O-(C7)алкил-(замещенный арил), O-(C8)алкил-(замещенный арил), метил-гетероциклил, этил-гетероциклил, (C3)алкил-гетероциклил, (C4)алкил-гетероциклил, (C5)алкил-гетероциклил, (C6)алкил-гетероциклил, (C7)алкил-гетероциклил, (C8)алкил-гетероциклил, метил-(замещенный гетероциклил), этил-(замещенный гетероциклил), (C3)алкил-(замещенный гетероциклил), (C4)алкил-(замещенный гетероциклил), (C5)алкил-(замещенный гетероциклил), (C6)алкил-(замещенный гетероциклил), (C7)алкил-(замещенный гетероциклил), (C8)алкил-(замещенный гетероциклил), O-метил-гетероциклил, O-этил-гетероциклил, O-(C3)алкил-гетероциклил, O-(C4)алкил-гетероциклил, O-(C5)алкил-гетероциклил, O-(C6)алкил-гетероциклил, O-(C7)алкил-гетероциклил, O-(C8)алкил-гетероциклил, O-метил-(замещенный гетероциклил), O-этил-(замещенный гетероциклил), O-(C3)алкил-(замещенный гетероциклил), O-(C4)алкил-(замещенный гетероциклил), O-(C5)алкил-(замещенный гетероциклил), O-(C6)алкил-(замещенный гетероциклил), O-(C7)алкил-(замещенный гетероциклил), O-(C8)алкил-(замещенный гетероциклил), метил-C(=O)N(R16)(R17), этил-C(=O)N(R16)(R17), (C3)алкил-C(=O)N(R16)(R17), (C4)алкил-C(=O)N(R16)(R17), (C5)алкил-C(=O)N(R16)(R17), (C6)алкил-C(=O)N(R16)(R17), (C7)алкил-C(=O)N(R16)(R17) и (C8)алкил-C(=O)N(R16)(R17).
В другом варианте осуществления настоящего изобретения R15 может быть выбран из любой комбинации одного или более следующего: H, CH3, CH2CF3, CH2-галопиридил, оксо-пирролидинил, галофенил, тиетанил, CH2-фенил, CH2-пиридил, тиетанил-диоксид, CH2-галотиазолил, C((CH3)2)-пиридил, N(H)(галофенил), CH2-пиримидинил, CH2-тетрагидрофуранил, CH2-фуранил, O-CH2-галопиридил и CH2C(=O)N(H)(CH2CF3).
В другом варианте осуществления настоящего изобретения R16 может быть выбран из любой комбинации одного или более следующего: H, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метил-арил, этил-арил, (C3)алкил- арил, (C4)алкил-арил, (C5)алкил-арил, (C6)алкил-арил, (C7)алкил-арил, (C8)алкил-арил, метил-(замещенный арил), этил-(замещенный арил), (C3)алкил-(замещенный арил), (C4)алкил-(замещенный арил), (C5)алкил-(замещенный арил), (C6)алкил-(замещенный арил), (C7)алкил-(замещенный арил), (C8)алкил-(замещенный арил), O-метил-арил, O-этил-арил, O-(C3)алкил-арил, O-(C4)алкил-арил, O-(C5)алкил-арил, O-(C6)алкил-арил, O-(C7)алкил-арил, O-(C8)алкил-арил, O-метил-(замещенный арил), O-этил-(замещенный арил), O-(C3)алкил-(замещенный арил), O-(C4)алкил-(замещенный арил), O-(C5)алкил-(замещенный арил), O-(C6)алкил-(замещенный арил), O-(C7)алкил-(замещенный арил), O-(C8)алкил-(замещенный арил), метил-гетероциклил, этил-гетероциклил, (C3)алкил-гетероциклил, (C4)алкил-гетероциклил, (C5)алкил-гетероциклил, (C6)алкил-гетероциклил, (C7)алкил-гетероциклил, (C8)алкил-гетероциклил, метил-(замещенный гетероциклил), этил-(замещенный гетероциклил), (C3)алкил-(замещенный гетероциклил), (C4)алкил-(замещенный гетероциклил), (C5)алкил-(замещенный гетероциклил), (C6)алкил-(замещенный гетероциклил), (C7)алкил-(замещенный гетероциклил), (C8)алкил-(замещенный гетероциклил), O-метил-гетероциклил, O-этил-гетероциклил, O-(C3)алкил-гетероциклил, O-(C4)алкил-гетероциклил, O-(C5)алкил-гетероциклил, O-(C6)алкил-гетероциклил, O-(C7)алкил-гетероциклил, O-(C8)алкил-гетероциклил, O-метил-(замещенный гетероциклил), O-этил-(замещенный гетероциклил), O-(C3)алкил-(замещенный гетероциклил), O-(C4)алкил-(замещенный гетероциклил), O-(C5)алкил-(замещенный гетероциклил), O-(C6)алкил-(замещенный гетероциклил), O-(C7)алкил-(замещенный гетероциклил) и O-(C8)алкил-(замещенный гетероциклил).
В другом варианте осуществления настоящего изобретения R16 может быть выбран из любой комбинации одного или более следующего: H, CH2CF3, циклопропил, тиетанил, тиетанил диоксид и галофенил.
В другом варианте осуществления настоящего изобретения R17 может быть выбран из любой комбинации одного или более следующего: H, метил, этил, (C3)алкил, (C4)алкил, (C5)алкил, (C6)алкил, (C7)алкил, (C8)алкил, галометил, галоэтил, гало(C3)алкил, гало(C4)алкил, гало(C5)алкил, гало(C6)алкил, гало(C7)алкил, гало(C8)алкил, метил-арил, этил-арил, (C3)алкил-арил, (C4)алкил-арил, (C5)алкил-арил, (C6)алкил-арил, (C7)алкил-арил, (C8)алкил-арил, метил-(замещенный арил), этил-(замещенный арил), (C3)алкил-(замещенный арил), (C4)алкил-(замещенный арил), (C5)алкил-(замещенный арил), (C6)алкил-(замещенный арил), (C7)алкил-(замещенный арил), (C8)алкил-(замещенный арил), O-метил-арил, O-этил-арил, O-(C3)алкил-арил, O-(C4)алкил-арил, O-(C5)алкил-арил, O-(C6)алкил-арил, O-(C7)алкил-арил, O-(C8)алкил-арил, O-метил-(замещенный арил), O-этил-(замещенный арил), O-(C3)алкил-(замещенный арил), O-(C4)алкил-(замещенный арил), O-(C5)алкил-(замещенный арил), O-(C6)алкил-(замещенный арил), O-(C7)алкил-(замещенный арил), O-(C8)алкил-(замещенный арил), метил-гетероциклил, этил-гетероциклил, (C3)алкил-гетероциклил, (C4)алкил-гетероциклил, (C5)алкил-гетероциклил, (C6)алкил-гетероциклил, (C7)алкил-гетероциклил, (C8)алкил-гетероциклил, метил-(замещенный гетероциклил), этил-(замещенный гетероциклил), (C3)алкил-(замещенный гетероциклил), (C4)алкил-(замещенный гетероциклил), (C5)алкил-(замещенный гетероциклил), (C6)алкил-(замещенный гетероциклил), (C7)алкил-(замещенный гетероциклил), (C8)алкил-(замещенный гетероциклил), O-метил-гетероциклил, O-этил-гетероциклил, O-(C3)алкил-гетероциклил, O-(C4)алкил-гетероциклил, O-(C5)алкил-гетероциклил, O-(C6)алкил-гетероциклил, O-(C7)алкил-гетероциклил, O-(C8)алкил-гетероциклил, O-метил-(замещенный гетероциклил), O-этил-(замещенный гетероциклил), O-(C3)алкил-(замещенный гетероциклил), O-(C4)алкил-(замещенный гетероциклил), O-(C5)алкил-(замещенный гетероциклил), O-(C6)алкил-(замещенный гетероциклил), O-(C7)алкил-(замещенный гетероциклил) и O-(C8)алкил-(замещенный гетероциклил).
В другом варианте осуществления настоящего изобретения R17 может быть выбран из любой комбинации одного или более следующего: H, CH2CF3, циклопропил, тиетанил, тиетанил диоксид и галофенил.
В другом варианте осуществления настоящего изобретения X1 представляет собой CR12, X2 представляет собой CR13, и X3 представляет собой CR9.
В другом варианте осуществления настоящего изобретения гетероциклил содержит предпочтительно приблизительно 6-10 атомов в кольцевой структуре, более предпочтительно - 6-8 атомов.
Молекула Формулы один обычно будет иметь молекулярную массу от приблизительно 100 Дальтонов до приблизительно 1200 Дальтонов. Однако обычно предпочтительно, если молекулярная масса составляет от приблизительно 120 Дальтонов до приблизительно 900 Дальтонов, и еще более предпочтительно, если молекулярная масса составляет от приблизительно 140 Дальтонов до приблизительно 600 Дальтонов.
Бензиловый спирт Формулы IV, где R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, может быть синтезирован двумя способами. Один способ, раскрытый в стадии a Схемы I, осуществляется путем обработки кетона Формулы II, где R1, R2, R3, R4, R5 и R6 являются такими, как раскрыто ранее, восстановителем, таким как борогидрид натрия (NaBH4), в основных условиях, таких как водный гидроксид натрия (NaOH), в полярном протонном растворителе, таком как метиловый спирт (CH3OH), при 0°C. В альтернативном варианте альдегид Формулы III, где R1, R2, R3, R4, R5 и R7 являются такими, как раскрыто ранее, реагирует с трифтортриметилсиланом в присутствии каталитического количества тетрабутиламмонийфторида в полярном апротонном растворителе, таком как тетрагидрофуран (ТГФ), как в стадии b Схемы I. Соединение Формулы IV может быть превращено в соединение Формулы V, где Y выбран из Br, Cl или I, и R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, в реакции с галогенирующим реагентом, таким как N-бромсукцинимид и триэтилфосфит в инертном растворителе, таком как дихлорметан (CH2Cl2), при температуре кипения с обратным холодильником, с получением Y=Br, или таким как тионилхлорид и пиридин в углеводородном растворителе, таком как толуол, при температуре кипения с обратным холодильником, с получением Y=Cl, как в стадии c Схемы I.
Схема I
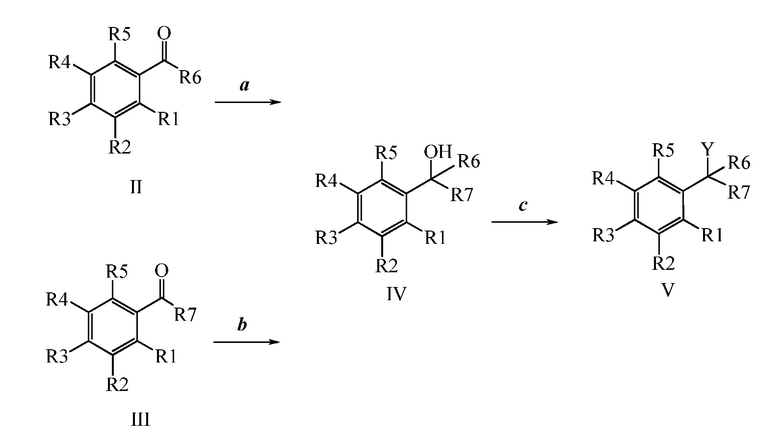
Получение стиролов, участвующих в реакции конденсации, может быть выполнено как на Схемах II, III, IV и V.
На Схеме II, винилбензойная кислота Формулы VI, где R11 представляет собой (C=O)OH, и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, может быть превращена в двух стадиях в винилбензамид Формулы VIIa, где R11 представляет собой (C=O)N(R14)(R15), и R8, R9, R10, R12, R13, R14, R15 и X являются такими, как раскрыто ранее. Как в стадии d Схемы II, бензойную кислоту Формулы VI обрабатывают оксалилхлоридом в присутствии каталитического количества N,N-диметилформамида (ДМФА) в инертном растворителе, таком как CH2Cl2, с получением хлорангидрида, который затем реагирует с амином (HN(R14)(R15)), где R14 и R15 являются такими, как раскрыто ранее, в присутствии основания, такого как триэтиламин, в полярном апротонном растворителе, таком как ТГФ, с получением винилбензамида Формулы VIIa, где R11 представляет собой (C=O)N(R14)(R15), и R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее, как в стадии e Схемы II.
Схема II
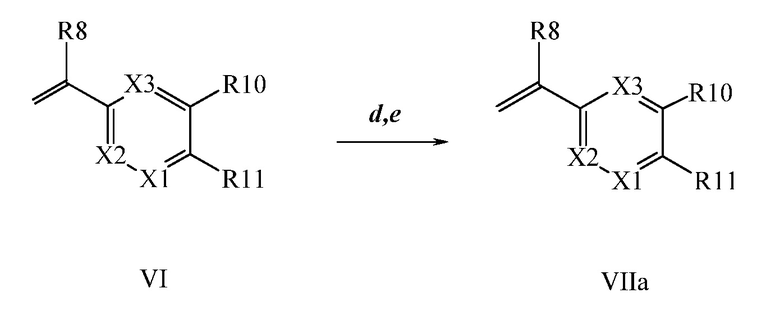
На Схемах III и IV галобензойная кислота Формулы VIII, где R18 представляет собой Br или I, R11 представляет собой (C=O)OH, и R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, может быть превращена в сложный эфир винилбензойной кислоты Формулы VIIb1 или Формулы VIIb2, где R18 представляет собой Br или I, R11 представляет собой (C=O)O(C1-C6 алкил), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. В стадии f Схемы III, галобензойную кислоту Формулы VIII, где R18 представляет собой Br, обрабатывают основанием, таким как н-бутиллитий (н-BuLi) и ДМФА, в полярном апротонном растворителе, таком как ТГФ, при температуре приблизительно -78°C. Полученная формилбензойная кислота реагирует с кислотой, такой как серная кислота (H2SO4), в присутствии спирта, такого как этиловый спирт (EtOH), как в стадии g, с получением этилового эфира формилбензойной кислоты Формулы IX, где R11 представляет собой (C=O)O(C1-C6 алкил), и R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Виниловый эфир бензойной кислоты Формулы VIIb1 получают через реакцию соединений Формулы IX, с основанием, таким как карбонат калия (K2CO3) и метилтрифенилфосфонийбромид, в полярном апротонном растворителе, таком как 1,4-диоксан, при температуре окружающей среды, как в стадии h Схемы III.
Схема III
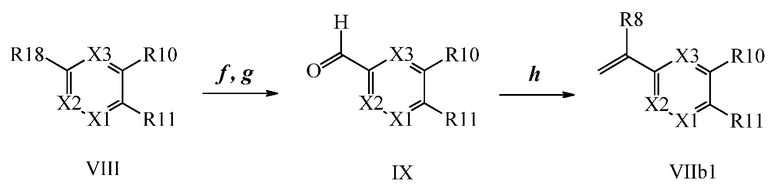
В стадии i Схемы IV, галобензойную кислоту Формулы VIII, где R18 представляет собой Br, R11 представляет собой (C=O)OH, и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, обрабытывают ди-трет-бутил-дикарбонатом в присутствии основания, такого как триэтиламин (Et3N) и каталитического количества 4-(диметиламино)пиридина (DMAP), в полярном апротонном растворителе, таком как ТГФ, при температуре окружающей среды. Полученному трет-бутиловому эфиру бензойной кислоты позволяют реагировать с пиридиновым комплексом винилборонового ангидрида в присутствии палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий (0) (Pd(PPh3)4), и основания, такого как K2CO3, в инертном растворителе, таком как толуол, при температуре кипения с обратным холодильником, как в стадии j, с получением винилового эфира бензойной кислоты Формулы VIIb2, где R11 представляет собой (C=O)O(C1-C6 алкил), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема IV
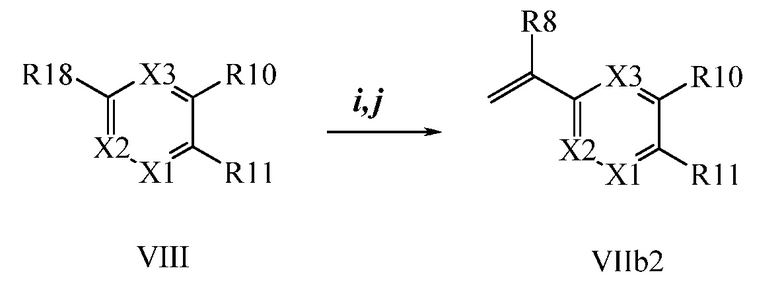
В стадии k Схемы V, виниловый эфир бензойной кислоты Формулы VIIb2, где R10 представляет собой Br, R11 представляет собой (C=O)O(C1-C6 алкил), и R8, R9, R12, R13, X1, X2 и X3 являются такими, как определено ранее, может быть далее превращен в соответствующий виниловый эфир бензойной кислоты Формулы VIIb3, где R10 представляет собой CN, R11 представляет собой (C=O)O(C1-C6 алкил), и R8, R9, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с цианидом меди (I) (CuCN) в полярном апротонном растворителе, таком как ДМФА, при 140°C.
Схема V
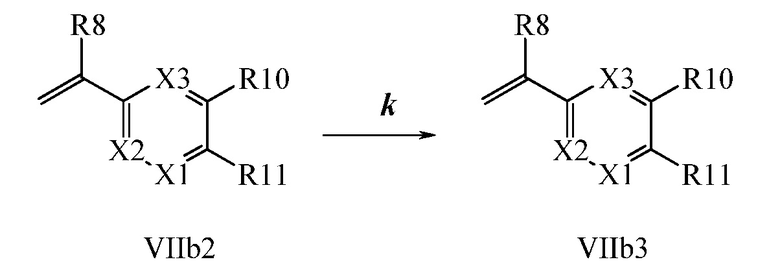
Конденсация соединений Формулы V с соединениями Формулы VIIa, VIIb1, VIIb2 и VIIb3 может быть проведена, как на Схемах VI, VII и VIII. В стадии l Схемы VI, соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и винилбензамиду Формулы VIIa, где R11 представляет собой (C=O)N(R14)(R15), и R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии хлорида меди (I) (CuCl) и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением молекулы Формулы один, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема VI
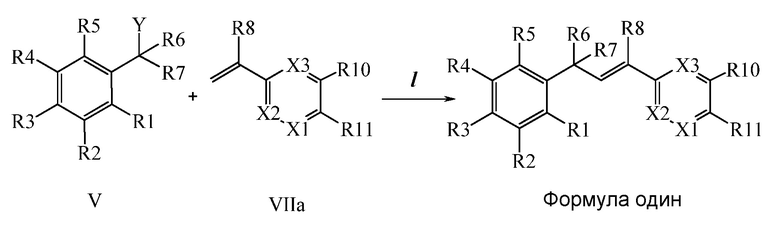
В стадии l Схемы VII, соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и сложному эфиру винилбензойной кислоты Формулы VIIb1, где R11 представляет собой (C=O)O(C1-C6 алкил), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридил в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соединений Формулы Xa, где R11 представляет собой (C=O)O(C1-C6 алкил), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы Xa затем превращают в молекулы Формулы один, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее, либо двухстадийным способом, как раскрыто в стадиях m и n, либо в одну стадию, как раскрыто в стадии o. В стадии m Схемы VII сложный эфир Формулы Xa омыляют до соответствующей кислоты в кислотных условиях, таких как приблизительно 11 нормальная (Н) хлороводородная кислота (HCl), в полярном апротонном растворителе, таком как 1,4-диоксан, приблизительно при 100°C. Кислота может быть затем сконденсирована с амином (HN(R14)(R15)), где R14 и R15 являются такими, как раскрыто ранее, при использовании реагентов для пептидного синтеза, таких как 1-гидроксибензотриазол (HOBt), гидрохлорид N-(3-диметиламинопропил)-N'-этил-карбодиимида (EDC·HCl), гексафторфосфат бензотриазол-1-ил-окситрипирролидино-фосфония (PyBOP), гексафторфосфат 2-хлор-1,3-диметилимидазоли-диния (CIP), 1-гидрокси-7-азабензотриазол (HOAt) или гексафторфосфат O-бензотриазол-N,N,N',N'-тетраметил-урония (HBTU), в присутствии основания, такого как N,N-диизопропилэтиламин (DIEA) или 4-(диметиламино)пиридин (DMAP), с получением молекулы Формулы один, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее. В альтернативном варианте сложному эфиру Формулы Xa позволяют реагировать с амином (HN(R14)(R15)) в присутствии раствора триметилалюминия в толуоле, в инертном растворителе, таком как CH2Cl2, при температуре окружающей среды, как в стадии o Схемы VII, с получением молекул Формулы один, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема VII
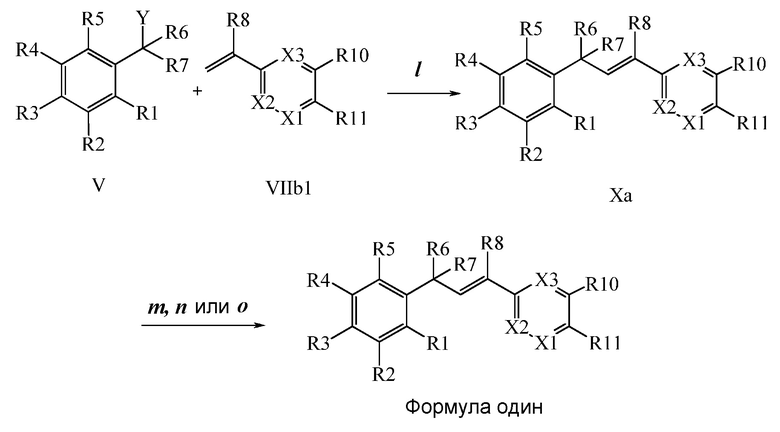
В стадии l Схемы VIII, соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и сложному эфиру винилбензойной кислоты Формулы VIIb2 или VIIb3, где R11 представляет собой (C=O)O(C1-C6 алкил), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соединений Формулы Xb, где R11 представляет собой (C=O)OH, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы Xb затем превращают в молекулы Формулы один, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее, в одну стадию, как раскрыто в стадии n. В стадии n Схемы VIII кислота Формулы Xb может быть сконденсирована с амином (HN(R14)(R15)), где R14 и R15 являются такими, как раскрыто ранее, при использовании реагентов для пептидного синтеза, таких как 1-гидроксибензотриазол (HOBt), гидрохлорид N-(3-диметиламинопропил)-N'-этил-карбодиимид (EDC·HCl), гексафтор-фосфат бензотриазол-1-ил-окситрипирролидинофосфония (PyBOP), гексафторфосфат 2-хлор-1,3-диметилимидазолидиния (CIP), 1-гидрокси-7-азабензотриазол (HOAt) или гексафторфосфат O- бензотриазол-N,N,N',N'-тетраметил-урония (HBTU), в присутствии основания, такого как N,N-диизопропилэтиламин (DIEA) или 4-(диметиламино)пиридин (DMAP), с получением молекул Формулы один, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, R14, R15, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема VIII
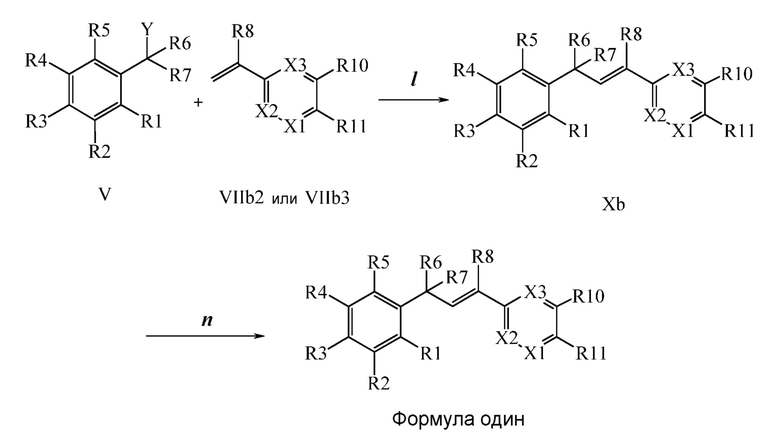
В стадии t Схемы XIII винилбензилхлорид Формулы XIa, где R11 представляет собой CH2Cl2, и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как определено ранее, может быть превращен в соответствующий фталимид-защищенный бензиламин Формулы XIIa, где R11 представляет собой CH2N (фталимид), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с фталимидом калия в полярном апротонном растворителе, таком как ДМФА, при 70°C.
Схема XIII
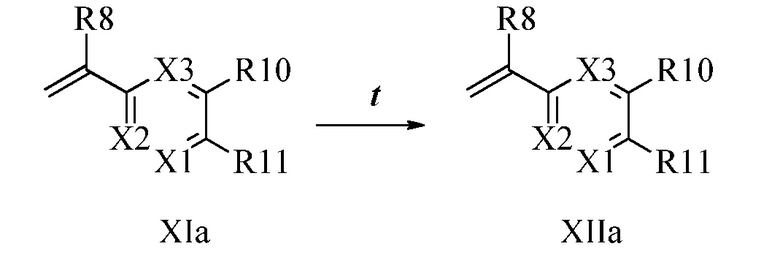
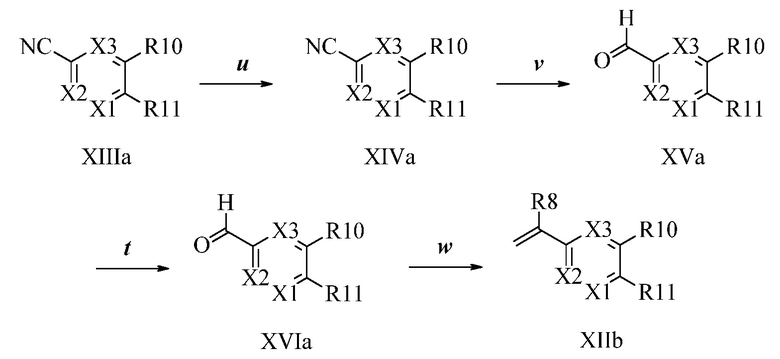
В стадии u Схемы XIV 4-метилбензонитрил Формулы XIIIa, где R11 представляет собой CH3, и R9, R10, R12, R13, X1, X2 и X3 являются такими, как определено ранее, может быть превращен в соответствующий бензилбромид Формулы XIVa, где R11 представляет собой CH2Br, и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с N-бромсукцинимидом (NBS) и азо-бисизобутиронитрилом (AIBN) в инертном растворителе, таком как тетрахлорметан, при 77°C. Нитрильная группа (CN) Формулы, XIVa может быть восстановлена до соответствующего альдегида Формулы XVa, где R11 представляет собой CH2Br, и R9, R10, R12, R13, X1, X2 и X3 являются такими, как определено ранее, в реакции с диизобутилалюминийгидридом (DIBAL-H) в апротонном растворителе, таком как толуол, при 0°C, с последующей остановкой реакции вливанием 1,0М соляной кислоты (HCl), как в стадии v Схемы XIV. Соединение Формулы XVa может быть далее превращено в соответствующий фталимид-защищенный бензиламин Формулы XVIa, где R11 представляет собой CH2N(фталимид), и R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с фталимидом калия в полярном апротонном растворителе, таком как ДМФА, при 60°C, как в стадии t Схемы XIV. В стадии w Схемы XIV альдегид Формулы XVIa может быть превращен в олефин Формулы XIIb, где R11 представляет собой CH2N(фталимид), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с метилтрифенилфосфонийбромидом в полярном апротонном растворителе, таком как 1,4-диоксан, в присутствии основания, такого как K2CO3, при температуре окружающей среды.
Схема XIV
Альдегид Формулы XVa, где R11 представляет собой CH2Br, и R9, R10, R12, R13, X1, X2 и X3 являются такими, как определено ранее, может реагировать с нуклеофилом, таким как 2-аминопиридин, в полярном апротонном растворителе, таком как N,N-диметилацетамид (DMA), в присутствии основания, такого как K2CO3, при температуре окружающей среды, с получением соединения Формулы XVII, где R11 представляет собой CH2NH(2-пиридин), и R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, как в стадии x Схемы XV. В стадии w Схемы XV соединение Формулы XVII может быть превращено в олефин Формулы XVIII, где R11 представляет собой CH2NH(2-пиридин), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема XV

В двухстадийной реакции, проводимой в одном сосуде, как в стадиях y и z Схемы XVI, соединение Формулы XIX может реагировать с соединениями Формулы XX, где R10 и R11 представляют собой Cl, X1 представляет собой N, и R9, R13, X2 и X3 являются такими, как раскрыто ранее, в присутствии основания, такого как гидрид натрия (NaH), и полярного апротонного растворителя, такого как ДМФА, при температуре окружающей среды, с получением соединения Формулы XXI, где R10 представляет собой Cl, R11 представляет собой (CH)NH2CO2CH2CH3, X1 представляет собой N, и R9, R13, X2 и X3 являются такими, как определено ранее. Гидролиз и декарбоксилирование соединений Формулы XXI могут быть проведены в реакции в кислых условиях, таких как в присутствии 3Н HCl, при температуре кипения с обратным холодильником, с получением соединения Формулы XXII, где R10 представляет собой Cl, R11 представляет собой CH2NH2·HCl, X1 представляет собой N, и R9, R13, X2 и X3 являются такими, как раскрыто ранее, как в стадии aa в Схеме XVI. Соединения Формулы XXII могут быть далее превращены в соответствующие фталимид-защищенные бензиламины Формулы XXIIIa, где R10 представляет собой Cl, R11 представляет собой CH2N(фталимид), X1 представляет собой N, и R9, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с фталевым ангидридом в присутствии основания, такого как Et3N, и апротонного растворителя, такого как толуол, при температуре дефлегмации, как в стадии ab Схемы XVI. Бромид Формулы XXIIIa может быть превращен в олефин Формулы XIIc, где R10 представляет собой Cl, R11 представляет собой CH2N(фталимид), X1 представляет собой N, и R8, R9, R13, X2 и X3 являются такими, как раскрыто ранее, в реакции с пиридиновым комплексом винилборонового ангидрида в присутствии палладиевого катализатора, такого как Pd(PPh3)4, и основания, такого как K2CO3, в инертном растворителе, таком как толуол, при температуре дефлегмации, как в стадии ac Схемы XVI.
Схема XVI

В стадии u Схемы XVII 4-метилнафтонитрил Формулы XIIIb, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH3, и R12, R13, X1 и X2 являются такими, как определено ранее, может быть превращен в соответствующий нафтилбромид Формулы XIVb, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2Br, и R12, R13, X1 и X2 являются такими, как раскрыто ранее, в реакции с N-бромсукцинимидом (NBS) и азо-бисизобутиронитрилом (AIBN) в инертном растворителе, таком как тетрахлорметан, при 77°C. Нитрильная группа (CN) Формулы XIVb может быть восстановлена до соответствующего альдегида Формулы XVb, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо (или, в случае необходимости, неароматическое кольцо), R11 представляет собой CH2Br, и R12, R13, X1 и X2 являются такими, как определено ранее в реакции с диизобутилалюминийгидридом (DIBAL-H) в апротонном растворителе, таком как толуол, при 0°C, с последующей остановкой реакции вливанием 1,0М HCl, как в стадии v Схемы XVII. Соединение Формулы XVb может быть далее превращено в соответствующий фталимид-защищенный бензиламин Формулы XVIb, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2N(фталимид), и R12, R13, X1 и X2 являются такими, как раскрыто ранее, в реакции с фталимидом калия в полярном апротонном растворителе, таком как ДМФА, при 60°C, как в стадии t Схемы XVII. В стадии w Схемы XVII альдегид Формулы XVIb может быть превращен в олефин Формулы XIId, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2N(фталимид), и R8, R12, R13, X1 и X2 являются такими, как раскрыто ранее, в реакции с метилтрифенилфосфонийбромидом в полярном апротонном растворителе, таком как 1,4-диоксан, в присутствии основания, такого как K2CO3, при температуре окружающей среды.
Схема XVII
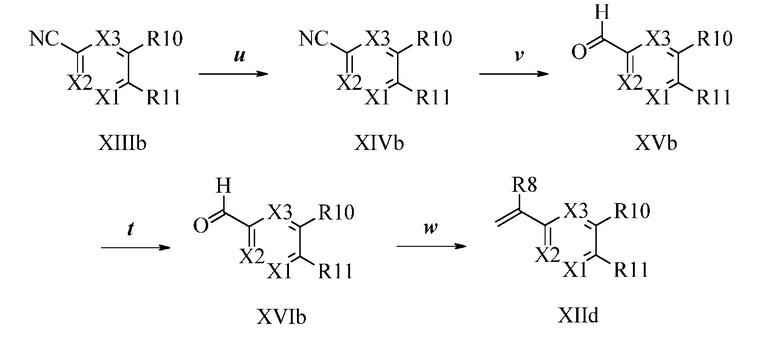
Соединение Формулы XXIV, где R11 представляет собой NHNH2·HCl, и R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, может быть превращено в соответствующий фталимид-защищенный гидразин Формулы XXV, где R11 представляет собой NHN(фталимид), и R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с фталевым ангидридом в ледяной уксусной кислоте при температуре кипения с обратным холодильником, как в стадии ad Схемы XVIII. Бромид Формулы XXV может быть превращен в олефин Формулы XIIe, где R11 представляет собой NHN(фталимид), и R8, R9, R10, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с пиридиновым комплексом винилборонового ангидрида в присутствии палладиевого катализатора, такого как Pd(PPh3)4, и основания, такого как K2CO3, в полярном апротонном растворителе, таком как 1,2-диметоксиэтан, при 150°C под воздействием СВЧ-излучения, как в стадии ae Схемы XVIII.
Схема XVIII
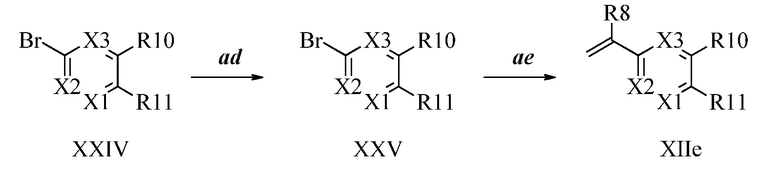
В стадии af Схемы XIX соединению Формулы XXVI, где R11 представляет собой B(OH)2, и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать с 2-гидроксиизоиндолин-1,3-дионом в присутствии CuCl и пиридина в растворителе, таком как 1,2-дихлорбензол, при температуре окружающей среды, с получением соединения Формулы XIIf, где R11 представляет собой ON(фталимид), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема XIX
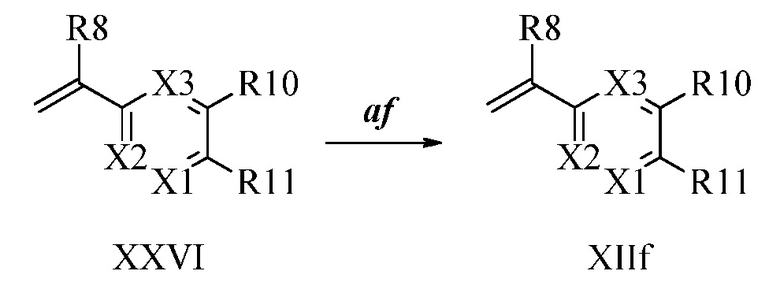
В стадии l Схемы XX соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XIIa, где R11 представляет собой CH2N(фталимид), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы XXVIIa, где R11 представляет собой CH2N(фталимид), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Защитную фталимидную группу в соединениях Формулы XXVIIa удаляют, как в стадии ag Схемы XX, в реакции с гидратом гидразина в полярном протонном растворителе, таком как EtOH, при 90°C, с получением соединений Формулы XXVIIIa, где R11 представляет собой CH2NH2, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы XXVIIIa могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=O)(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, путем ацилирования ангидридом, таким как уксусный ангидрид, и основанием, таким как Et3N, в инертном растворителе, таком как CH2Cl2, при 0°C, как в стадии ah1 Схемы XX.
Схема XX
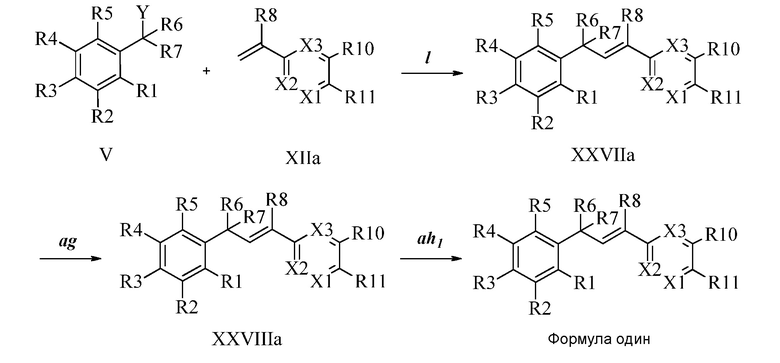
В стадии l Схемы XXI соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XIIb, где R11 представляет собой CH2N(фталимид), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы XXVIIb, где R11 представляет собой CH2N(фталимид), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Защитную фталимидную группу в соединениях Формулы XXVIIb удаляют, как в стадии ag Схемы XXI, в реакции с гидратом гидразина в полярном протонном растворителе, таком как EtOH, при 90°C, с получением соединения Формулы XXVIIIb, где R11 представляет собой CH2NH2, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=O)(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с кислотой в присутствии HOBt·H2O, EDC·HCl и основания, такого как DIEA, в полярном апротонном растворителе, таком как ДМФА, как в стадии ah2a Схемы XXI.
В другом варианте осуществления соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=S)(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с тиокислотой в присутствии HOBt·H2O, EDC·HCl и основания, такого как DIEA, в полярном апротонном растворителе, таком как ДМФА, как в стадии ah2 Схемы XXI.
В другом варианте осуществления соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в две стадии. Первая стадия (стадия ah3a Схемы XXI) включает реакцию с альдегидом в полярном протонном растворителе, таком как метиловый спирт, с последующей реакцией с борогидридом натрия. Вторая стадия (стадия ah3b Схемы XXI) включает ацилирование хлорангидридом, таким как циклопропилкарбонилхлорид, и основанием, таким как Et3N, в инертном растворителе, таком как CH2Cl2, при температуре окружающей среды, Схемы XXI.
В другом варианте осуществления соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с изоцианатом (стадия ai1 Схемы XXI) или карбамоилхлоридом (стадия ai2 Схемы XXI) в присутствии основания, такого как Et3N, и в инертном растворителе, таком как CH2Cl2, при 0°C.
В другом варианте осуществления соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=S)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с изотиоцианатом в присутствии основания, такого как Et3N, и в инертном растворителе, таком как CH2Cl2, при 0°C, как в стадиях aj Схемы XXI.
В другом варианте осуществления соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=O)O(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с дикарбонатом, таким как ди-трет-бутил-дикарбонат, в присутствии основания, такого как Et3N, и в инертном растворителе, таком как CH2Cl2, при температуре окружающей среды, как в стадиях ak Схемы XXI.
В еще одном варианте осуществления соединения Формулы XXVIIIb могут быть превращены в соединения Формулы один, где R11 представляет собой CH2N(C=O)(C=O)O(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции со сложным эфиром хлорщавелевой кислоты, таким как 2-хлор-2-оксоацетат, в присутствии основания, такого как Et3N, и в инертном растворителе, таком как CH2Cl2, при 0°C, как в стадиях al Схемы XXI.
Схема XXI
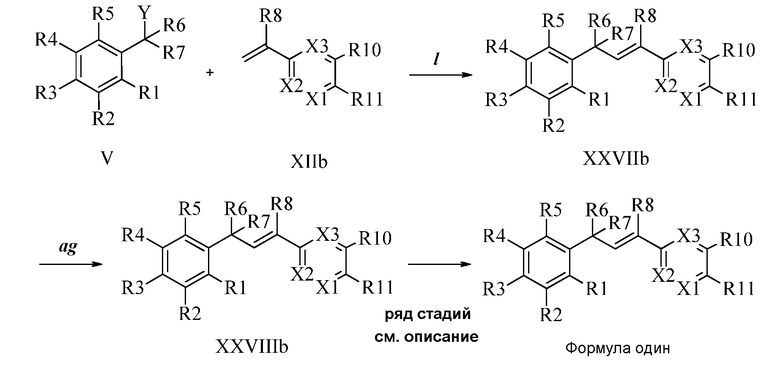
В стадии l Схемы XXII соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XIIc, где R10 представляет собой Cl, R11 представляет собой CH2N(фталимид), X1 представляет собой N, и R8, R9, R12, R13, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы XXVIIc, где R10 представляет собой Cl, R11 представляет собой CH2N(фталимид), X1 представляет собой N, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X2 и X3 являются такими, как раскрыто ранее. Защитную фталимидную группу в соединениях Формулы XXVIIc удаляют, как в стадии ag Схемы XXII, в реакции с гидратом гидразина в полярном протонном растворителе, таком как EtOH, при 90°C, с получением соединений Формулы XXVIIIc, где R10 представляет собой Cl, R11 представляет собой CH2NH2, X1 представляет собой N, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы XXVIIIc могут быть превращены в соединения Формулы один, где R10 представляет собой Cl, R11 представляет собой CH2N(C=O)(R14), X1 представляет собой N, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X2 и X3 являются такими, как раскрыто ранее, в реакции с кислотой в присутствии HOBt·H2O, EDC·HCl и основания, такого как DIEA, в полярном апротонном растворителе, таком как CH2Cl2, как в стадии ah2b Схемы XXII.
Схема XXII
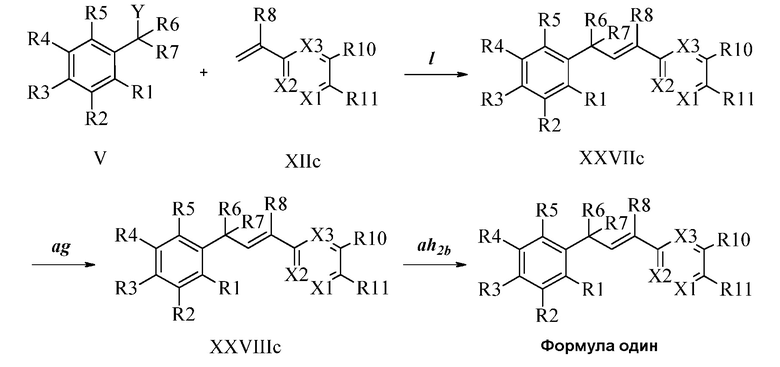
В стадии l Схемы XXIII соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XIId, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо (или, в случае необходимости, неароматическое кольцо), R11 представляет собой CH2N(фталимид), и R8, R9, R12, R13, X1 и X2 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы XXVIId, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2N(фталимид), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X1 и X2 являются такими, как раскрыто ранее. Защитную фталимидную группу в соединениях Формулы XXVIId удаляют, как в стадии ag Схемы XXIII, в реакции с гидратом гидразина в полярном протонном растворителе, таком как EtOH, при 90°C, с получением соединения Формулы XXVIIId, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2NH2, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X1 и X2 являются такими, как раскрыто ранее. Соединения Формулы XXVIIId могут быть превращены в соединения Формулы один, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2N(C=O)(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X1 и X2 являются такими, как раскрыто ранее, в реакции с кислотой в присутствии HOBt·H2O, EDC·HCl и основания, такого как DIEA, в полярном апротонном растворителе, таком как CH2Cl2, как в стадии ah2b Схемы XXIII.
В другом варианте осуществления соединения Формулы XXVIIId могут быть превращены в соединения Формулы один, где X3 представляет собой CR9, R10 и X3 вместе образуют связь, содержащую 4 атома углерода, и с атомами углерода в кольце образуют 6-членное ароматическое кольцо, R11 представляет собой CH2N(C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1 и X2 являются такими, как раскрыто ранее, в реакции с изоцианатом в присутствии основания, такого как Et3N, и в инертном растворителе, таком как CH2Cl2, при 0°C, как в стадии ai1 Схемы XXIII.
Схема XXIII
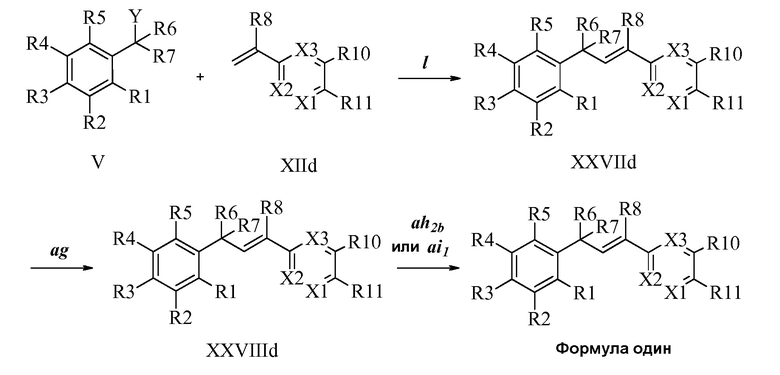
В стадии l Схемы XXIV соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XIIe, где R11 представляет собой NHN(фталимид), и R8, R9, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы XXVIIe, где R11 представляет собой NHN(фталимид), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Защитную фталимидную группу в соединениях Формулы XXVIIe удаляют, как в стадии ag Схемы XXIV, в реакции с гидратом гидразина в полярном протонном растворителе, таком как EtOH, при 90°C, с получением соединения Формулы XXVIIIe, где R11 представляет собой NHNH2, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы XXVIIIe могут быть превращены в соединения Формулы один, где R11 представляет собой NHN(C=O)(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с кислотой в присутствии HOBt·H2O, EDC·HCl и основания, такого как DIEA, в полярном апротонном растворителе, таком как CH2Cl2, как в стадии ah2b Схемы XXIV.
Схема XXIV
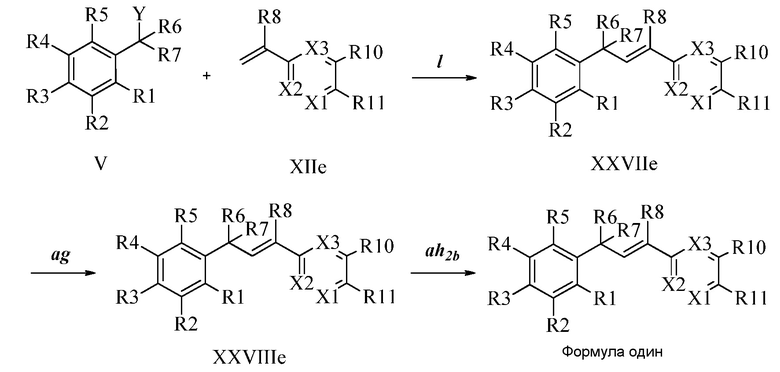
В стадии l Схемы XXV соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XIIf, где R11 представляет собой ON(фталимид), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы XXVIIf, где R11 представляет собой ON(фталимид), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Защитную фталимидную группу в соединениях Формулы XXVIIf удаляют, как в стадии ag Схемы XXV, в реакции с гидратом гидразина в полярном протонном растворителе, таком как EtOH, при 90°C, с получением соединения Формулы XXVIIIf, где R11 представляет собой ONH2, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы XXVIIIf могут быть превращены в соединения Формулы один, где R11 представляет собой ON(C=O)(R14), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с кислотой в присутствии HOBt·H2O, EDC·HCl и основания, такого как DIEA, в полярном апротонном растворителе, таком как CH2Cl2, как в стадии ah2b Схемы XXV.
Схема XXV
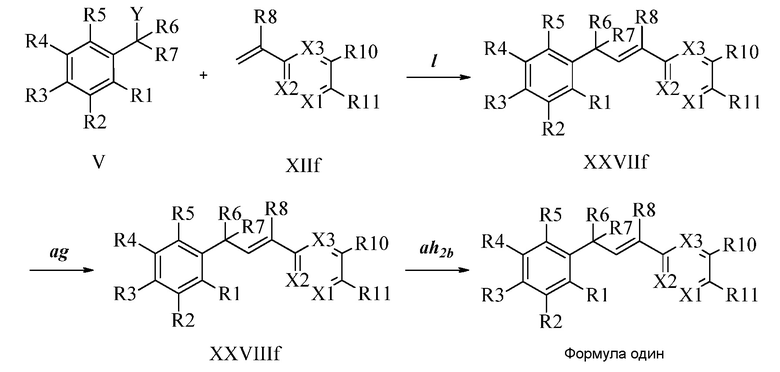
В стадии l Схемы XXVI соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XVIII, где R11 представляет собой CH2NH(2-пиридин), и R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующих соединений Формулы один, где R11 представляет собой CH2NH(2-пиридин), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R12, R13, X1, X2 и X3 являются такими, как раскрыто ранее.
Соединения Формулы один могут быть также получены стандартными методами. Например, когда R11 содержит тиоэфир, тиоэфир может быть окислен до сульфона при обработки оксоном в присутствии смеси ацетон:вода при температуре окружающей среды. Когда R11 содержит сложноэфирный оксалат, соединение Формулы один может быть превращено в соответствующий оксамид в реакции с гидрохлоридом амина и раствором триметилалюминия в толуоле в инертном растворителе, таком как CH2Cl2.
Схема XXVI
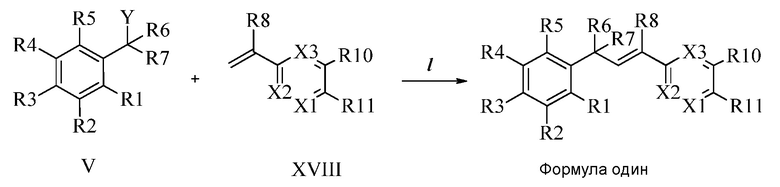
На Схеме XXVII фторбензальдегид Формулы XXIX, где R10, X1, X2 и X3 являются такими, как раскрыто ранее, может быть превращен в (1,2,4-триазол-1-ил)бензальдегид Формулы XXX, где R11 представляет собой замещенную или незамещенную 1,2,4-триазол-1-ильную группу, и R10, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с замещенным или незамещенным с 1,2,4 триазолом в присутствии основания, такого как карбонат калия, в растворителе, таком как ДМФА, как в стадии aj. В стадии ak (1,2,4-триазол-1-ил)бензальдегид Формулы XXX превращают в (1,2,4-триазол-1-ил)стирол Формулы XXXIa, где R11 представляет собой замещенную или незамещенную 1,2,4-триазол-1-ильную группу, и R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с трифенилфосфонийбромидом в присутствии основания, такого как карбонат калия, в апротонном растворителе, таком как 1,4-диоксан.
Схема XXVII
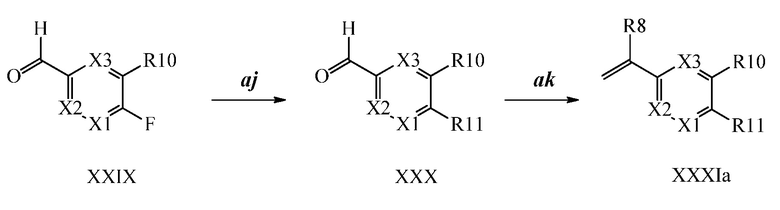
На Схеме XXVIII бромфторбензол Формулы XXXII, где R10, X1, X2 и X3 являются такими, как раскрыто ранее, может быть превращен в (1,2,4-триазол-1-ил)винилбензол Формулы XXXIb, где R11 представляет собой замещенную или незамещенную 1,2,4-триазол-1-ильную группу, и R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее, в две стадии. В стадии al бромфторбензол реагирует с замещенным или незамещенным 1,2,4-триазолом в присутствии основания, такого как карбонат калия, в растворителе, таком как ДМФА, с получением (1,2,4-триазол-1-ил)монобромбензола. В стадии cl (1,2,4-триазол-1-ил)монобромбензол реагирует с пиридиновым комплексом винилборонового ангидрида в присутствии катализатора, такого как Pd(PPh3)4, и основания, такого как карбонат калия, в растворителе, таком как толуол.
Схема XXVIII
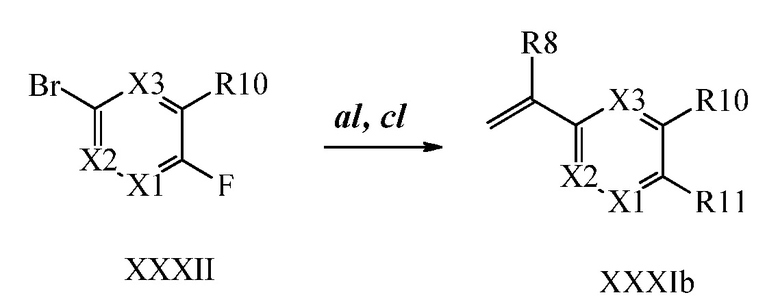
Конденсация соединений Формулы V с соединениями Формулы XXXIa и XXXIb может быть выполнена, как на Схемах XXIX. В стадии l соединению Формулы V, где Y представляет собой Br, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и винилбензолу Формулы XXXIa или XXXIb, где R11 представляет собой замещенную или незамещенную 1,2,4-триазол-1-ильную группу, и R8, R9, R10, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением молекул Формулы один, где R11 представляет собой замещенную или незамещенную 1,2,4-триазол-1-ильную группу, и R1, R2, R3, R4, R5, R6, R7, R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема XXIX
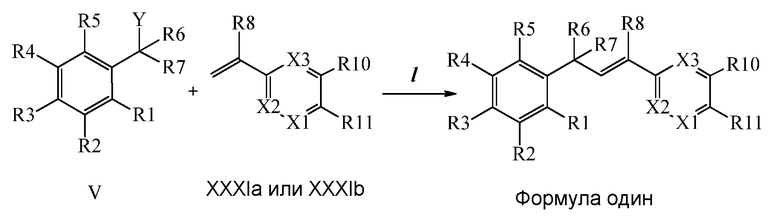
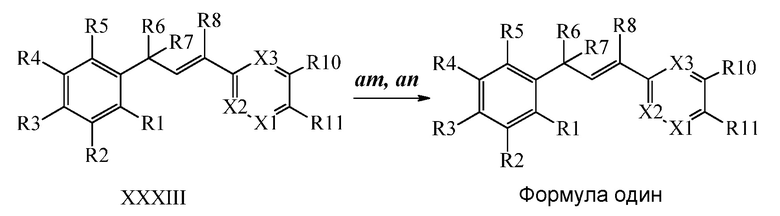
На Схеме XXX соединения Формулы XXXIII, где R11 представляет собой 3-нитро-1,2,4-триазол-1-ильную группу, и R1, R2, R3, R4, R5, R6, R7, R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее, могут быть превращены в соединения Формулы один, где R11 представляет собой 3-амидо-1,2,4-триазол-1-ильную группу, и R1, R2, R3, R4, R5, R6, R7, R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее, в двухстадийном процессе. В стадии am 3-нитро-1,2,4-триазол-1-ильную группу восстанавливают до 3-амино-1,2,4-триазол-1-ильной группы в присутствии цинковой пыли и хлорида аммония в протонном растворителе, таком как метанол. В стадии an 3-амино-1,2,4-триазол-1-ильную группу ацилируют хлорангидридом, таким как циклопропилкарбонилхлорид или ацетилхлорид, в присутствии основания, такого как триэтиламин, в растворителе, таком как дихлорметан.
Схема XXX
В стадии ao Схемы XXXI бромфенилметилкетон Формулы XXXIV, где R10, X1, X2 и X3 являются такими, как раскрыто ранее, превращают в ацетофенон Формулы XXXV, где R11 представляет собой 1,2,4-триазол-1-ильную группу, и R10, X1, X2 и X3 являются такими, как раскрыто ранее, при обработке 1,2,4-триазолом в присутствии основания, такого как карбонат цезия, и катализатора, такого как иодид меди, в растворителе, таком как ДМФА. В стадии ap 1,2,4-триазолилацетофенон Формулы XXXV превращают в триметилсилиленольный эфир Формулы XXXVI обработкой триметилсилил-трифторметансульфонатом в присутствии основания, такого как триэтиламин, в апротонном растворителе, таком как дихлорметан. В стадии aq силиленольный эфир реагирует с соединением Формулы V, где Y представляет собой Br, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением кетона Формулы XXXVII, где R11 представляет собой 1,2,4-триазол-1-ильную группу, и R1, R2, R3, R4, R5, R6, R7, R10, X1, X2 и X3 являются такими, как раскрыто ранее. В стадии ar кетон Формулы XXXVII обрабатывают метилмагнийбромидом в апротонном растворителе, таком как ТГФ, с получением третичного спирта. Третичный спирт затем подвергают реакции элиминирования при обработке каталитическим количеством п-толуолсульфоновой кислоты в растворителе, таком как толуол, при нагревании до температуры, позволяющей азеотропно удалить воду с получением соединения Формулы один, где R11 представляет собой 1,2,4-триазол-1-ильную группу, R8 представляет собой метил, и R1, R2, R3, R4, R5, R6, R7, R10, X1, X2 и X3 являются такими, как раскрыто ранее, как в стадии as.
Схема XXXI

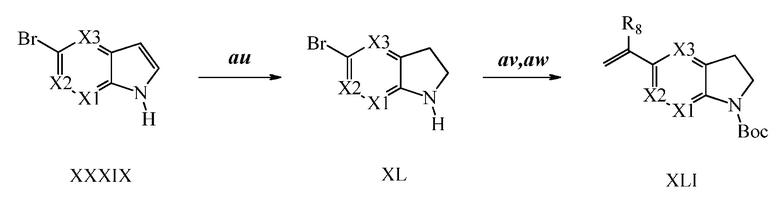
На Схеме XXXIII соединение Формулы XXXIX, где X1, X2 и X3 являются такими, как раскрыто ранее, превращают в молекулу Формулы XL, где X1, X2 и X3 являются такими, как раскрыто ранее, путем обработки восстановителем, таким как цианоборогидрид натрия, в растворителе, таком как уксусная кислота, как в стадии au. В стадии av атом азота защищают трет-бутилоксикарбонильной (BOC) группой в реакции с ди-трет-бутил-дикарбонатом в присутствии катализатора, такого как DMAP, в растворителе, таком как ацетонитрил. Бромид Формулы XL может быть превращен в олефин Формулы XLI, где R8, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с винилтрифторборатом калия в присутствии палладиевого катализатора, такого как PdCl2(dppf), и основания, такого как K2CO3, в полярном апротонном растворителе, таком как ДМСО, при 100°C, как в стадии aw.
Схема XXXIII
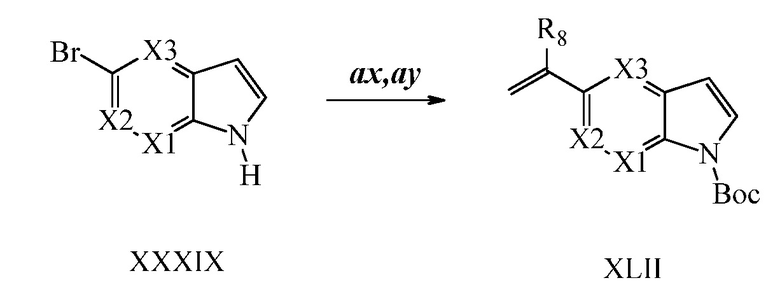
На Схеме XXXIV соединение Формулы XXXIX, где X1, X2 и X3 являются такими, как раскрыто ранее, превращают в молекулу Формулы XLII, где X1, X2 и X3 являются такими, как раскрыто ранее, в две стадии. В стадии ax олефин образуется при обработке бромида винилтрифторборатом калия в присутствии палладиевого катализатора, такого как PdCl2, и лиганда, такого как трифенилфосфин, и основания, такого как Cs2CO3, в смеси растворителей, такой как ТГФ/H2O. В стадии ay атом азота защищают трет-бутилоксикарбонильной (BOC) группой в реакции с ди-трет-бутил-дикарбонатом в присутствии катализатора, такого как DMAP, в растворителе, таком как ацетонитрил.
Схема XXXIV
В стадии l Схемы XXXV соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы XLI или XLII, где R8, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 150°C, с получением соответствующих соединений Формулы XLIIIa или XLIIIb, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее.
Схема XXXV
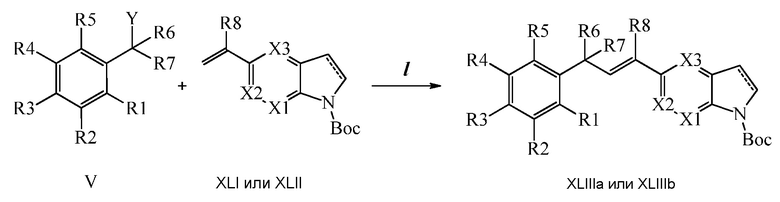
На Схеме XXXVI соединение Формулы XLIIIa, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, превращают в молекулу Формулы XLIV, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, при обработке трифторуксусной кислотой, в растворителе, таком как дихлорметан, как в стадии az. Соединения Формулы XLIV могут быть затем превращены в соединения Формулы XLV, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, в две стадии. В стадии ba индолин обрабатывают нитритом натрия (NaNO2) в кислоте, такой как концентрированная HCl, при температуре приблизительно 5°C, с получением нитрозоиндола. В стадии bb нитрозоиндол реагирует с хлоридом аммония в присутствии порошка цинка в протонном растворителе, таком как метанол. В стадии bc соединения Формулы XLV превращают в соединения Формулы XLVI, где X4 представляет собой N(R14)(C(=O)R14), и R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, при обработке кислотой, такой как 3,3,3-трифторпропановая кислота, PyBOP и основанием, таким как DIEA, в полярном апротонном растворителе, таком как дихлорметан.
Схема XXXVI
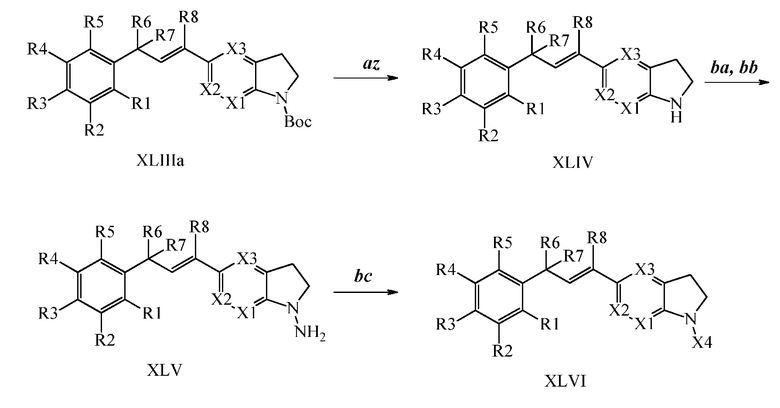
На Схеме XXXVII соединение Формулы XLIIIb, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, превращают в индол Формулы XLVII, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, при обработке трифторуксусной кислотой, в растворителе, таком как дихлорметан, как в стадии bd. Соединения Формулы XLVII могут быть превращены в соединения Формулы XLVIII, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с 4-нитрофенил-2-((трет-бутоксикарбонил)амино)ацетатом в присутствии фторида калия и краун-эфира, такого как 18-краун-6-эфир, в растворителе, таком как ацетонитрил, как в стадии be. Соединения Формулы XLVIII могут быть превращены в соединения Формулы XLIX, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, в две стадии. В стадии bf группу Boc удаляют обработкой трифторуксусной кислотой в растворителе, таком как дихлорметан. В стадии bg амин обрабатывают 3,3,3-трифторпропановой кислотой, PyBOP и основанием, таким как DIEA, в полярном апротонном растворителе, таком как дихлорметан.
Схема XXXVII
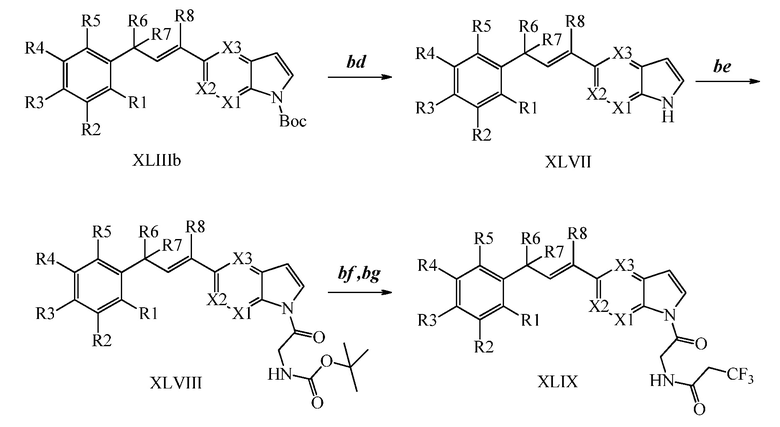
На Схеме XXXVIII соединение Формулы L, где X1, X2 и X3 являются такими, как раскрыто ранее, превращают в соединение Формулы LI, где X1, X2 и X3 являются такими, как раскрыто ранее, при обработке пентагидратом сульфата меди (II) и порошком Zn в основании, таком как гидроксид натрия, как в стадии bh. Соединения Формулы LI могут быть превращены в соединения Формулы LII, где X1, X2 и X3 являются такими, как раскрыто ранее, в реакции с гидразином в растворителе, таком как вода, при температуре приблизительно 95°C, как в стадии bi. В стадии bj олефин Формулы LIII, где X1, X2 и X3 являются такими, как раскрыто ранее, образуется при обработке бромида винилтрифторборатом калия в присутствии палладиевого катализатора, такого как PdCl2(dppf), и основания, такого как K2CO3, в смеси растворителей, таких как ДМСО. Соединения Формулы LIV, где X1, X2 и X3 являются такими, как раскрыто ранее, могут быть получены из соединений Формулы LIII в реакции с этилбромацетатом в присутствии основания, такого как Cs2CO3, в растворителе, таком как ДМФА.
Схема XXXVIII
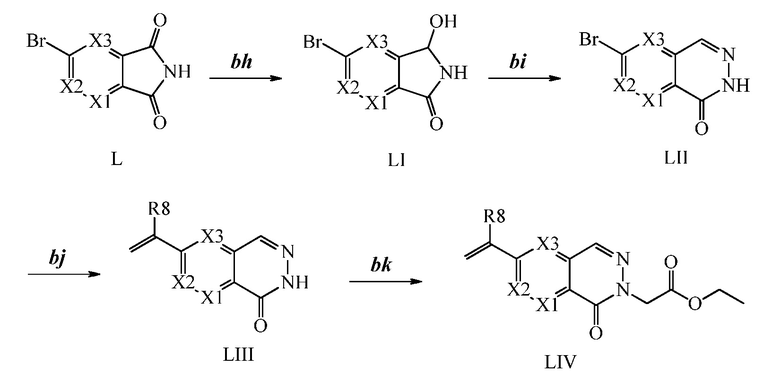
В стадии l Схемы XXXIX соединению Формулы V, где Y, R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, и соединению Формулы LIV, где R8, X1, X2 и X3 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как 1,2-дихлорбензол, при температуре приблизительно 180°C, с получением соответствующего соединения Формулы LV, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее. Соединение Формулы LV может быть далее превращено в соединение Формулы LVI, где R1, R2, R3, R4, R5, R6, R7, R8, X1, X2 и X3 являются такими, как раскрыто ранее, в две стадии. В стадии bl сложный эфир гидролизуется до кислоты в присутствии HCl и уксусной кислоты при температуре приблизительно 100°C. В стадии bm кислоту обрабатывают амином, таким как 2,2,2-трифторэтиламин, PyBOP и основанием, таким как DIEA, в полярном апротонном растворителе, таком как дихлорметан.
Схема XXXIX
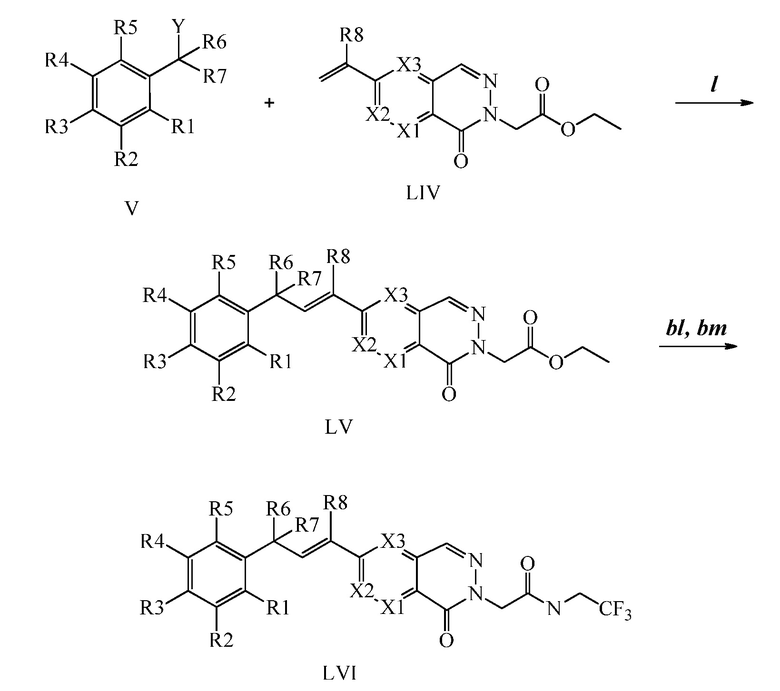
В стадии bn Схемы XL карбоновым кислотам Формулы LVII, где R11 представляет собой C(=O)OH, и R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее, и соединениям Формулы V, где Y представляет собой Br, и R1, R2, R3, R4, R5, R6 и R7 являются такими, как раскрыто ранее, позволяют реагировать в присутствии CuCl и 2,2-бипиридила в растворителе, таком как N-метил-пирролидин, при температуре приблизительно 150°C, с получением соединений Формулы LVIII, где R11 представляет собой (C=O)OH, и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X1, X2 и X3 являются такими, как раскрыто ранее. Соединения Формулы LVIII могут быть далее превращены в соответствующие бензамиды Формулы LIX, где R11 представляет собой (C=O)N(R14)(R15), и R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, X1, X2 и X3 являются такими, как раскрыто ранее, при обработке амином, таким как 2-амино-N-(2,2,2-трифторэтил)ацетамид, PyBOP и основанием, таким как DIEA, в полярном апротонном растворителе, таком как дихлорметан, как в стадии bo.
Схема XL
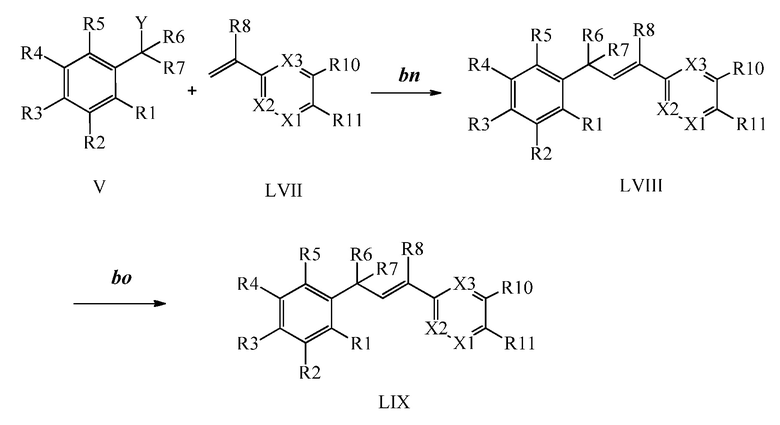
В стадии bp Схемы XLI карбоновые кислоты Формулы LX, где R1, R2, R3, R4, R5, R6, R7, R8, R10, X1, X2 и X3 являются такими, как раскрыто ранее, можно обработать галогенирующими реагентами, такими как тионилхлорид, при температурах от приблизительно 50ºC до приблизительно 80ºC, с получением соответствующего галогенида карбоновой кислоты. Промежуточные галогенагидриды можно обработать аминокислотами Формулы LXI, где X6 является таким, как раскрыто ранее, в присутствии основания, такого как Na2CO3, в растворителе, таком как ТГФ, при температурах от приблизительно 40°C до приблизительно 65°C, с получением соединений Формулы LXII. В стадии bq соединения Формулы LXII можно обработать активирующими агентами, такими как трифторуксусный ангидрид (TFAA) или EDC·HCl в растворителе, таком как CH2Cl2, при температурах от приблизительно 0ºC до приблизительно 25ºC, с образованием промежуточных азлактонов Формулы LXIII. Промежуточные азлактоны Формулы LXIII можно обработать аминами Формулы HN(R15)(R16), где R15 и R16 являются такими, как раскрыто ранее, в растворителе, таком как CH2Cl2 или EtOAc, при температурах от приблизительно 22ºC до приблизительно 70ºC, с получением соединений Формулы LXIV, как в стадии br. В альтернативном варианте промежуточные азлактоны Формулы LXIII можно обработать кислыми солями аминов Формулы HN(R15)(R16), где R15 и R16 являются такими, как раскрыто ранее, в присутствии основания, такого как триэтиламин (ТЭА), в растворителе, таком как ТГФ, при температурах от приблизительно 25ºC до приблизительно 70ºC, с получением соединений Формулы LXIV. Промежуточные азлактоны Формулы LXIII можно также обработать аминами Формулы HN(R15)(R16), где R15 и R16 являются такими, как раскрыто ранее, в присутствии каталитического количества кислоты, такой как AcOH, в растворителе, таком как толуол или EtOAc, при температурах от приблизительно 50ºC до приблизительно 110ºC, с получением соединений Формулы LXIV.
Схема XLI
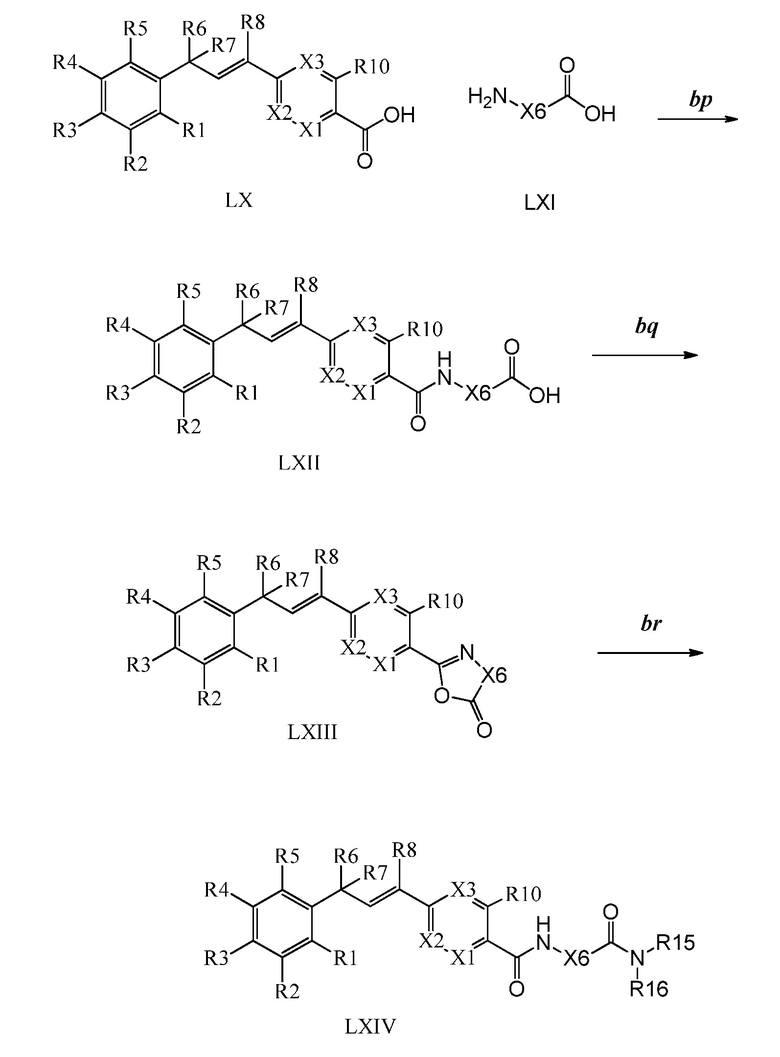
ПРИМЕРЫ
Примеры представлены в целях иллюстрации и не должны рассматриваться как ограничивающие изобретение, раскрытое в настоящем документе, только вариантами осуществления, раскрытыми в данных примерах.
Исходные соединения, реактивы и растворители, которые были получены из коммерческих источников, использовали без дополнительной очистки. Безводные растворители были приобретены как Sure/Seal™ у Aldrich и использовались в том виде, в каком они были получены. Температуры плавления были получены на приборе Thomas Hoover Unimelt для определения температур плавления в капилляре или с помощью системы OptiMelt Automated Melting Point System (Stanford Research Systems) и указаны без поправок. Молекулам давали их известные названия, которые были получены согласно программам присвоения называний в ISIS Draw, ChemDraw или ACD Name Pro. Если такие программы не были способны дать название молекулы, молекулу называли, используя стандартные правила номенклатуры. Данные спектров 1H-ЯМР представлены в м.д. (δ) и регистрировались при 300, 400 или 600 МГц, и данные спектров 13C-ЯМР представлены в м.д. (δ) и регистрировались при 75, 100 или 150 МГц, если не указано иное.
Пример 1: Получение 1-(1-бром-2,2,2-трифторэтил)-3,5-дихлорбензола (AI1)
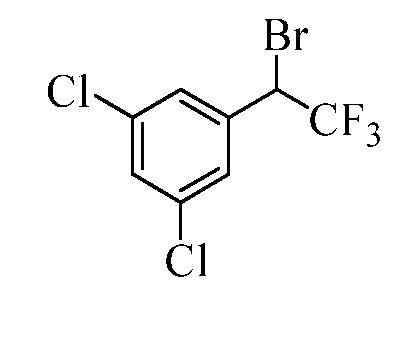
Стадия 1 Метод A. 1-(3,5-Дихлорфенил)-2,2,2-трифторэтанол (AI2). К перемешиваемому раствору 1-(3,5-дихлорфенил)-2,2,2-трифторэтанона (заказанного в Rieke Metals, UK; 5,0 граммов (г), 20,5 ммоль (ммоль)) в метиловом спирте (CH3OH; 100 миллилитров (мл)) при 0°C добавляли борогидрид натрия (NaBH4; 3,33 г, 92,5 мл) и 1 нормальный (N) водный раствор гидроксида натрия (NaOH; 10 мл). Реакционную смесь нагревали до 25°C и перемешивали в течение 2 часов (ч). После того, как реакцию сочли завершившейся согласно результатам тонкослойной хроматографии (ТСХ), насыщенный (нас.) водный (водн.) раствор хлорида аммония (NH4Cl) добавляли к реакционной смеси и выпаривали смесь при пониженном давлении. Остаток разбавляли диэтиловым эфиром (Et2O) и промывали водой (H2O; 3×50 мл). Органический слой сушили над сульфатом натрия (Na2SO4) и выпаривали при пониженном давлении с получением соединения, указанного в заголовке, в виде жидкости (4,0 г, 79%): 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (м, 3H), 5,00 (м, 2H), 2,74 (с, 1H); ЭРИ-МС m/z 242,97 ([M-H]-).
Стадия 1 Метод B. 1-(3,5-Дихлорфенил)-2,2,2-трифторэтанол (AI2). К перемешиваемому раствору 3,5-дихлорбензальдегида (10 г, 57 ммоль) в тетрагидрофуране (ТГФ; 250 мл), добавляли трифторметилтриметилсилан (9,79 г, 69,2 ммоль) и каталитическое количество фторида тетрабутиламмония (TBAF). Реакционную смесь перемешивали при 25°C в течение 8 ч. После того, как реакцию посчитали завершившейся согласно ТСХ, реакционную смесь разбавляли 3Н соляной кислотой (HCl) и затем перемешивали в течение 16 ч. Реакционную смесь разбавляли H2O и экстрагировали этилацетатом (EtOAc; 3×). Объединенные органические экстракты промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде жидкости (8,41 г, 60%).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Стадии 1 Методе A Примера 1 выше.
2,6-Дифтор-4-(2,2,2-трифтор-1-гидроксиэтил)бензонитрил
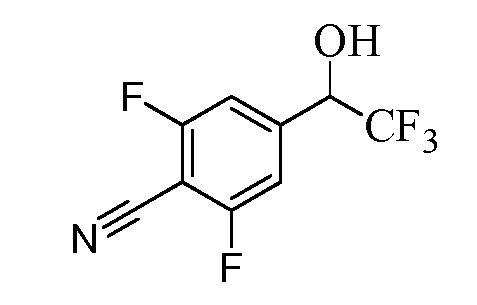
Продукт выделяли в виде коричневого твердого вещества: Т.пл. 83-87ºC; 1H-ЯМР (300 МГц, CDCl3) δ 7,26 (д, J=9,0 Гц, 2H), 5,12 (д, J=6,0 Гц, 1H), 3,06 (с, 1H); ЭРИ-МС m/z 237,1 ([M+H]+).
1-(3,5-Дифтор-4-метоксифенил)-2,2,2-трифторэтанол
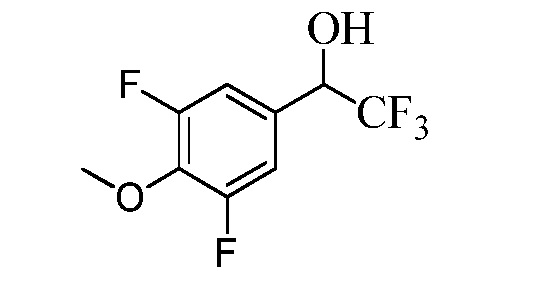
Продукт выделяли в виде светло-желтой жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,06 (д, J=8,4 Гц, 2H), 4,97-4,94 (м, 1H), 4,03 (с, 3H), 2,64 (с, 1H); ЭИ-МС m/z 242,1 ([М]+); ИК (тонкая пленка) 3459, 1135 см-1.
1-(3,4-Дихлорфенил)-2,2-дифторпропан-1-ол
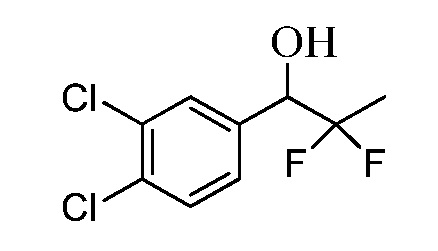
Продукт выделяли в виде бесцветной жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,65-7,62 (м, 2H), 7,41 (д, J=8,4 Гц, 1H), 6,49 (д, J=5,1 Гц, 1H), 4,87-4,78 (м, 1H), 1,53 (т, J=18,9 Гц, 3H); ЭИ-МС m/z 240,0 ([М]+); ИК (тонкая пленка) 3434, 1131, 801, 512 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Стадии 1 Методе B Примера 1 выше.
2,2,2-Трифтор-1-(3,4,5-трихлорфенил)этанол (AI3)
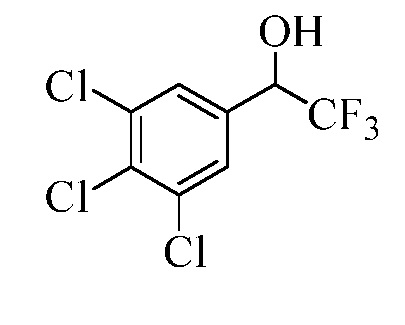
Продукт выделяли в виде светло-желтой жидкости (500 мг, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 7,45 (с, 2H), 5,00 (м, 1H), 2,80 (с, 1H); ЭРИ-МС m/z 278 ([M+H]+); ИК (тонкая пленка) 3420, 1133, 718 см-1.
1-(3,5-Дихлор-4-фторфенил)-2,2,2-трифторэтанол (AI4)
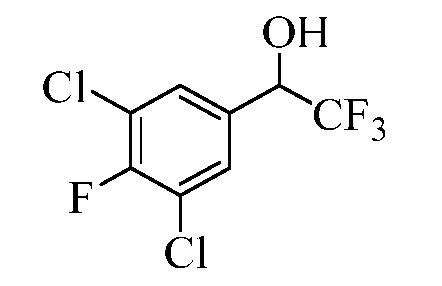
Продукт выделяли в виде светло-желтой жидкости (500 мг, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (с, 2H), 5,00 (м, 1H), 2,80 (с, 1H); ЭРИ-МС m/z 262 ([M+H]+); ИК (тонкая пленка) 3420, 1133, 718 см-1.
1-(3,4-Дихлорфенил)-2,2,2-трифторэтанол (AI5)
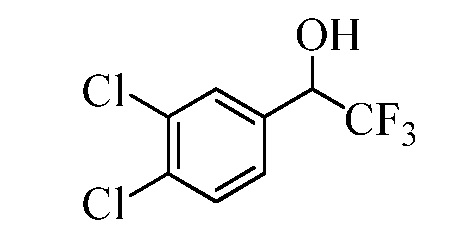
Продукт выделяли в виде светло-желтой жидкости (500 мг, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 7,60 (с, 1H), 7,51 (м, 1H), 7,35 (м, 1H), 5,01 (м, 1H), 2,60 (с, 1H); ЭИ-МС m/z 244 ([М]+).
1-(3,5-Дибромфенил)-2,2,2-трифторэтанол
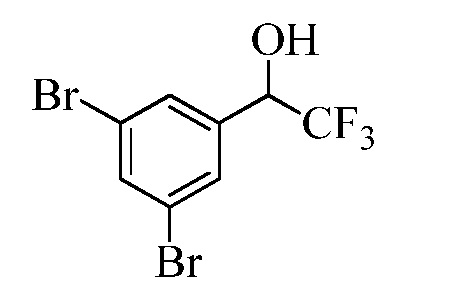
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,67 (с, 1H), 7,58 (с, 2H), 5,08-5,02 (м, 1H), 4,42 (шир.с, 1H); ЭИ-МС m/z 333,7 ([М]+); ИК (тонкая пленка) 3417, 2966, 1128, 531 см-1.
2,2,2-Трифтор-1-(3-фтор-5-(трифторметил)фенил)этанол
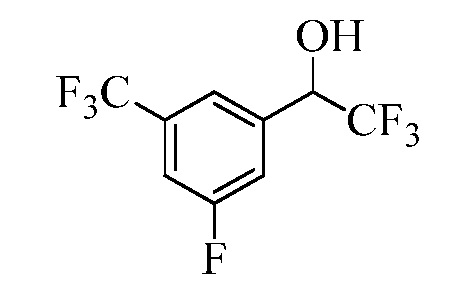
Молекула, указанная в заголовке, была выделена в виде прозрачного, бесцветного масла: 1H-ЯМР (400 МГц, CDCl3) δ 7,56 (с, 1H), 7,45-7,37 (м, 2H), 5,11 (кв., J=6,4 Гц, 1H), 3,22 (шир.с, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 162,42 (д, J=249,5 Гц), 137,46 (д, J=7,8 Гц), 132,89 (кв.д, J=33,5, 7,9 Гц), 123,67 (кв., J=283,8 Гц), 122,92 (кв., J=270,68 Гц), 120,10 (т, J=4,1 Гц), 118,13 (д, J=23,0 Гц), 113,94 (дк, J=24,2, 3,9 Гц), 71,57 (кв., J=32,4 Гц); ЭИ-МС m/z 262 ([М]+).
1-(3-Хлор-5-(трифторметил)фенил)-2,2,2-трифторэтанол
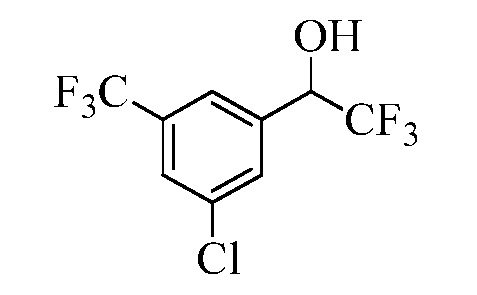
Продукт выделяли в виде белого твердого вещества (4,98 г, 77%): Т.пл. 42-46ºC; 1H-ЯМР (400 МГц, CDCl3) δ 7,83-7,50 (м, 3H), 5,10 (п, J=6,2 Гц, 1H), 2,88 (д, J=4,3 Гц, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 137,12, 135,84, 131,4, 133,03 (кв., J=33,3 Гц), 127,15 (кв., J=3,8 Гц), 124,50 (кв., J=308,0 Гц), 123,45 (кв., J=301,8 Гц), 123,04, 72,06 (кв., J=32,5 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -62,93, -78,43; ЭИ-МС m/z 278 ([М]+).
2,2,2-Трифтор-1-(4-фтор-3-(трифторметил)фенил)этанол
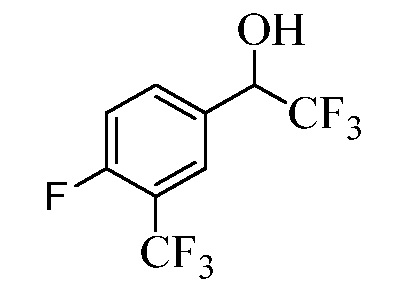
Продукт выделяли в виде коричневой жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=6,8 Гц, 1H), 7,69-7,67 (м, 1H), 7,28-7,23 (м, 1H), 5,05-5,02 (м, 1H); ЭРИ-МС m/z 261,1 ([M-H]-); ИК (тонкая пленка) 3418, 1131 см-1.
2,2,2-Трифтор-1-(3,4,5-трифторфенил)этанол
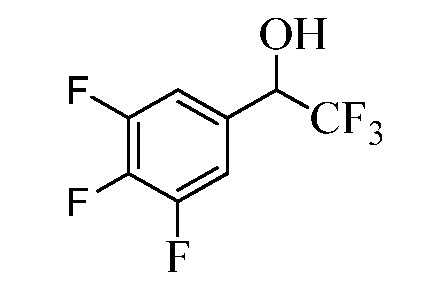
Продукт выделяли в виде бесцветной жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,19-7,10 (м, 2H), 5,03-4,96 (м, 1H), 2,85 (шир.с, 1H); ЭИ-МС m/z 230,1 ([М]+).
2,2,2-Трифтор-1-(2,3,4-трифторфенил)этанол
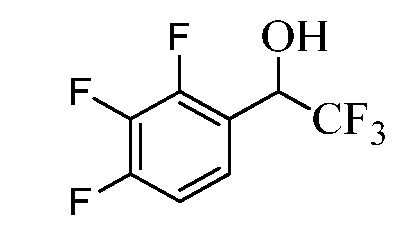
Продукт выделяли в виде прозрачной бесцветной жидкости (4,61 г, 66%): 1H-ЯМР (400 МГц, CDCl3) δ 7,23 (кв.д, J=7,4, 6,1, 4,2 Гц, 1H), 6,93 (тдд, J=9,2, 6,9, 2,2 Гц, 1H), 5,25 (кв., J=6,3 Гц, 1H), 3,02-2,74 (м, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 151,79 (ддд, J=254,5, 9,8, 3,4 Гц), 149,52 (ддд, J=253,5, 11,0, 3,5 Гц), 139,67 (дт, J=252,5, 15,3 Гц), 123,68 (кв., J=282,2 Гц), 122,48 (дт, J=8,2, 4,1 Гц), 118,95 (дд, J=10,6, 3,6 Гц), 112,73 (дд, J=17,7, 3,9 Гц), 66,58-64,42 (м); 19F-ЯМР (376 МГц, CDCl3) δ -78,95 (д, J=6,2 Гц), -132,02 (дд, J=20,0, 8,2 Гц), -137,89 (м), 159,84 (т, J=20,3 Гц); ЭИ-МС m/z 230 ([М]+).
2,2,2-Трифтор-1-(2,4,5-трихлорфенил)этанол
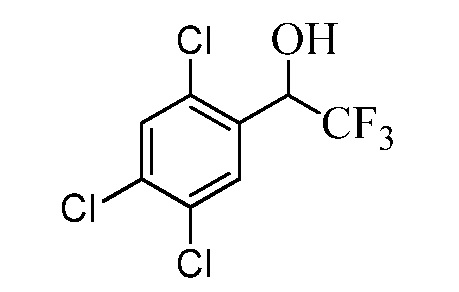
Продукт выделяли в виде белого твердого вещества (3,37 г, 73%): Т.пл. 70-73ºC; 1H-ЯМР (400 МГц, CDCl3) δ 7,63 (д, J=2,5 Гц, 1H), 7,54 (д, J=2,5 Гц, 1H), 5,72-5,57 (м, 1H), 2,85 (д, J=4,8 Гц, 1H); 19F-ЯМР (376 МГц, CDCl3) δ-77,84.
1-(4-Хлор-3-нитрофенил)-2,2,2-трифторэтанол
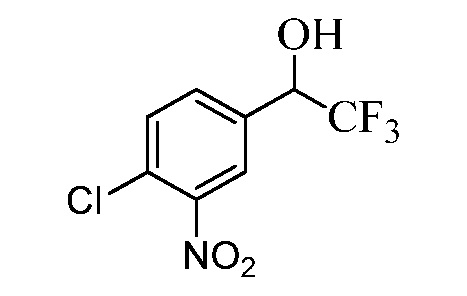
Продукт выделяли в виде желтого масла (6,52 г, 73%): 1H-ЯМР (400 МГц, CDCl3) δ 8,04 (д, J=2,0 Гц, 1H), 7,75-7,51 (м, 2H), 5,16 (м, 1H), 3,41 (д, J=4,3 Гц, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 147,65, 134,44, 132,23, 132,17, 128,11, 124,66, 123,60 (кв., J=283,8), 70,99 (кв., J=32,6 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -78,47; ЭИ-МС m/z 230 ([М]+).
2,2,2-Трифтор-1-(4-фтор-3,5-диметилфенил)этанол
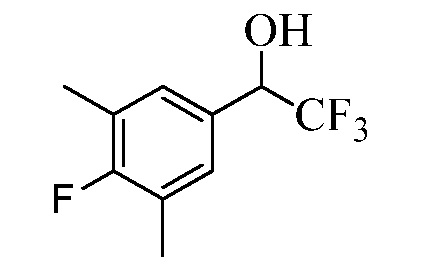
Продукт выделяли в виде белого твердого вещества (6,49 г, 84%): Т.пл. 45-49ºC; 1H-ЯМР (400 МГц, CDCl3) δ 7,10 (д, J=6,8 Гц, 2H), 4,89 (м, 1H), 2,63 (д, J=4,3 Гц, 1H), 2,27 (д, J=2,2 Гц, 6H); 13C-ЯМР (101 МГц, CDCl3) δ 160,45 (д, J=246,0 Гц), 128,73, 127,97, 124,92 (д, J=18,6 Гц), 124,19 (кв., J=279,1 Гц), 72,36 (кв., J=32,0 Гц), 14,61 (д, J=4,1 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -78,48, -120,14; ЭИ-МС m/z 222 ([М]+).
2,2,2-Трифтор-1-(4-фтор-3-метилфенил)этанол
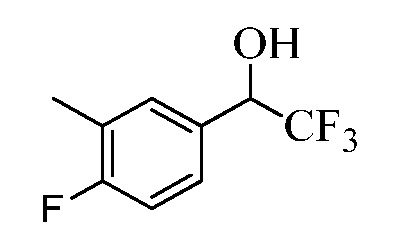
Продукт выделяли в виде белого твердого вещества (2,12 г, 33%): Т.пл. 40-46ºC; 1H-ЯМР (400 МГц, CDCl3) δ 7,28 (д, J=7,4 Гц, 1H), 7,25-7,14 (м, 1H), 7,01 (т, J=8,9 Гц, 1H), 5,05-4,63 (м, 1H), 3,03 (д, J=4,2 Гц, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 161,91 (д, J=247,0 Гц), 130,62 (д, J=5,6 Гц), 129,41 (д, J=3,5 Гц), 126,55 (д, J=8,5 Гц), 115,19 (д, J=22,9 Гц), 72,23 (кв., J=32,1 Гц), 14,44 (д, J=3,6 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -78,57, -116,15; ЭИ-МС m/z 208 ([М]+).
1-(3-Хлор-4-метилфенил)-2,2,2-трифторэтанол
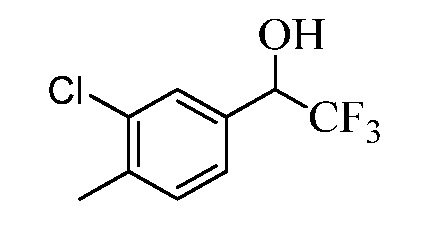
Продукт выделяли в виде прозрачного бесцветного масла (4,99 г, 75%): 1H-ЯМР (400 МГц, CDCl3) δ 7,31 (с, 1H), 7,10 (м, 2H), 4,79 (кв., J=6,1 Гц, 1H), 2,89 (шир.с, 1H), 2,25 (с, 3H); 13C-ЯМР (101 МГц, CDCl3) δ 137,64, 134,67, 132,99, 131,09, 128,01, 125,58, 124,02 (кв., J=284,8 Гц), 72,08 (кв., J=32,3 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -78,39; ЭИ-МС m/z 224,5 ([М]+).
1-(3,4-Дибромфенил)-2,2,2-трифторэтанол

Продукт выделяли в виде прозрачного бесцветного масла (5,92 г, 88%): 1H-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=2,0 Гц, 1H), 7,66 (д, J=8,3 Гц, 1H), 7,29 (дд, J=8,3, 2,0 Гц, 1H), 4,99 (кв.д, J=6,4, 4,2 Гц, 1H), 2,75 (д, J=4,3 Гц, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 134,52, 133,81, 132,60, 127,45, 126,19, 125,16, 123,71 (кв., J=283,8 Гц), 71,57 (кв., J=32,5 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -78,44; ЭИ-МС m/z 334 ([М]+).
2,2,2-Трифтор-1-(3-(трифторметокси)фенил)этанол
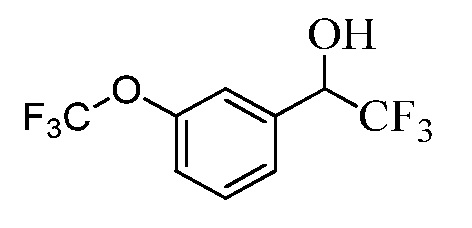
Продукт выделяли в виде прозрачного бесцветного масла (20,9 г, 79%): 1H-ЯМР (400 МГц, CDCl3) δ 7,55-7,36 (м, 3H), 7,33-7,14 (м, 1H), 5,06 (м, 1H), 2,80 (шир.м, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 149,36 (кв., J=2,0 Гц), 136,04, 129,99 125,78, 123,91 (кв., J=282,8 Гц), 121,90, 120,31 (кв., J=258,6 Гц), 120,12, 72,04 (кв., J=32,3 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -57,92, -78,49; ЭИ-МС m/z 260 ([М]+).
2-Фтор-5-(2,2,2-трифтор-1-гидроксиэтил)бензонитрил
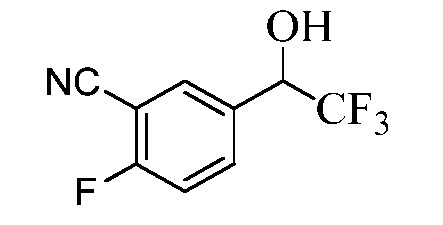
Продукт выделяли в виде прозрачного бесцветного масла (5,47 г, 58%): 1H-ЯМР (400 МГц, CDCl3) δ 7,80 (дд, J=5,9, 2,2 Гц, 1H), 7,76 (ддд, J=7,8, 5,0, 2,3 Гц, 1H), 7,30 (д, J=8,6 Гц, 1H), δ 5,09 (кв.д, J=6,3, 4,2 Гц, 1H), 3,12 (шир.м, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 163,49 (д, J=261,7 Гц), 134,23 (д, J=8,6 Гц), 132,67, 131,17, 123,66 (кв., J=282,4 Гц), 116,79 (д, J=20,1 Гц), 113,39, 100,96 (д, J=194,9), 71,07 (кв., J=32,5 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -78,70, -105,22; ЭИ-МС m/z 219 ([М]+).
1-(3-Бром-5-хлорфенил)-2,2,2-трифторэтанол
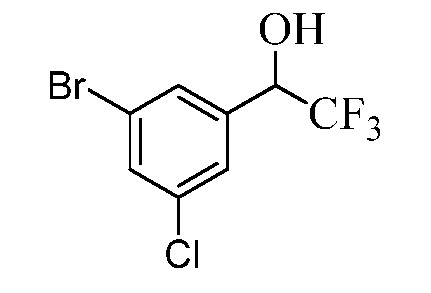
Продукт выделяли в виде желтой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,78 (с, 1H), 7,67 (с, 1H), 7,57 (с, 1H), 7,15 (д, J=5,7 Гц, 1H); ЭИ-МС m/z 288 ([М]+); ИК (тонкая пленка) 3435, 1175, 750 см-1.
1-(3-Бром-5-фторфенил)-2,2,2-трифторэтанол
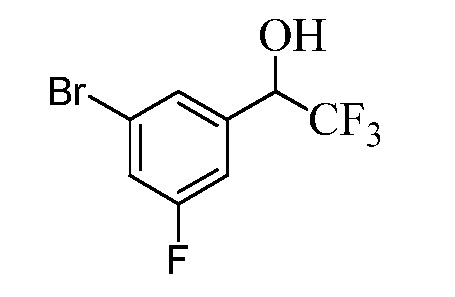
Продукт выделяли в виде светло-желтой жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,43 (с, 1H), 7,29-7,26 (м, 1H), 7,18 (д, J=8,8 Гц, 1H), 5,03-4,98 (м, 1H), 3,60 (шир.с, 1H); ЭИ-МС m/z 272,0 ([М]+); ИК (тонкая пленка) 3400, 1176, 520 см-1.
1-(3,5-Дихлорфенил)-2,2,3,3,3-пентафторпропан-1-ол
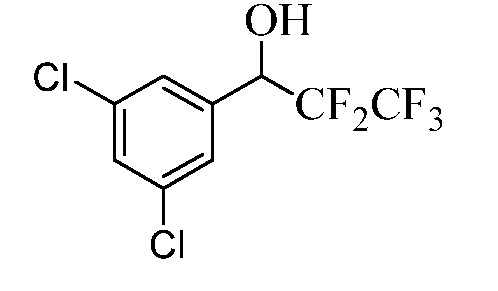
Используя пентафторэтилтриметилсилан, продукт выделяли в виде белого твердого вещества (6,22 г, 88%): Т.пл. 71-73ºC; 1H-ЯМР (400 МГц, CDCl3) δ 7,42 (т, J=1,9 Гц, 1H), 7,37 (д, J=1,8 Гц, 2H), 5,11 (дт, J=16,2, 5,7 Гц, 1H), 2,62 (д, J=4,9 Гц, 1H); 13C-ЯМР (101 МГц, CDCl3) δ 136,90, 135,31, 129,84, 126,38, 70,94 (дд, J=28,2, 23,1 Гц); 19F-ЯМР (376 МГц, CDCl3) δ -81,06, -120,94 (д, J=277,5 Гц), -129,18 (д, J=277,5 Гц); ЭИ-МС m/z 295 ([М]+).
2,2,3,3,3-Пентафтор-1-(3,4,5-трихлорфенил)пропан-1-ол
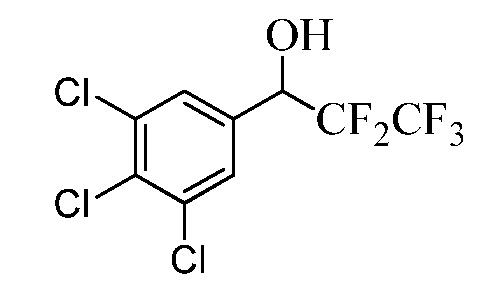
Используя пентафторэтилтриметилсилан, продукт выделяли в виде грязно-белого полутвердого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,78 (с, 2H), 7,29 (д, J=5,4 Гц,), 5,50-5,40 (м, 1H); ЭИ-МС m/z 328,0 ([М]+); ИК (тонкая пленка) 3459, 1188, 797 см-1.
2,2,2-Трифтор-1-(3-(трифторметил)фенил)этанол
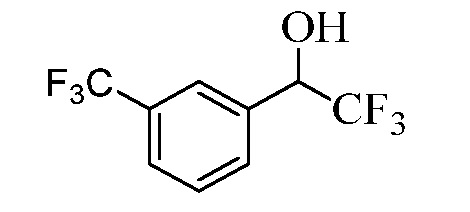
Продукт выделяли в виде светло-желтого вещества (13,8 г, 89%): 1H-ЯМР (400 МГц, CDCl3) δ 7,77 (с, 1H), 7,70-7,67 (м, 2H), 7,55 (т, J=7,8 Гц, 1H), 5,12 (кв., J=6,6 Гц, 1H), 2,76 (с, 1H); 19F-ЯМР (376 МГц, CDCl3) δ -62,8, -78,5; ЭИ-МС m/z 244 ([М]+).
1-(3,4-Дихлор-5-метилфенил)-2,2,2-трифторэтанол
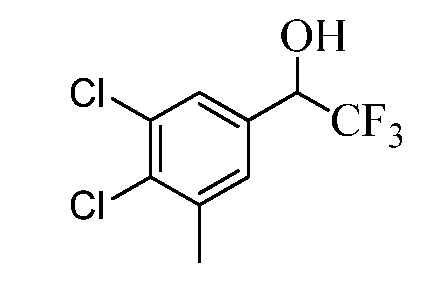
Продукт выделяли в виде бледно-желтого твердого вещества: 1H-ЯМР (400 МГц, CDCl3) δ 7,44 (с, 1H), 7,26 (с, 1H), 4,98-4,95 (м, 1H), 2,61 (д, J=4,4 Гц, 1H), 2,44 (с, 3H); ЭИ-МС m/z 258,1 ([М]+); ИК (тонкая пленка) 3421, 2926, 1129, 748 см-1.
1-(3-Хлор-5-этилфенил)-2,2,2-трифторэтанол
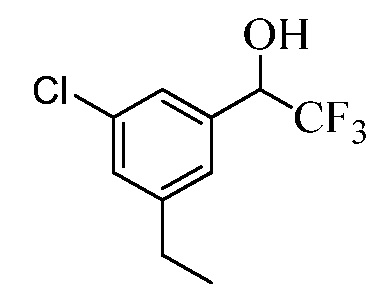
Продукт выделяли в виде коричневатой жидкости (0,43 г, 85%): 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,34 (с, 1H), 7,31-7,30 (м, 2H), 6,99 (д, J=5,7 Гц, 1H), 5,23-5,16 (м, 1H), 2,67 (м, 2H), 1,19 (т, J=7,8 Гц, 3H); ЭИ-МС m/z 238,0 ([М]+); ИК (тонкая пленка) 3361, 1172, 749 см-1.
1-(4-Бром-3,5-дихлорфенил)-2,2,2-трифторэтанол
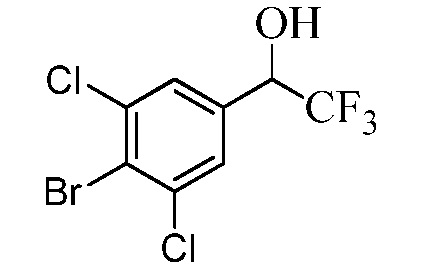
Продукт выделяли в виде бесцветной жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,75 (с, 2H), 7,24 (д, J=6,0 Гц, 1H), 5,34-5,29 (м, 1H); ЭИ-МС m/z 321,88 ([М]+); ИК (тонкая пленка) 3420, 1706, 1267, 804, 679 см-1.
1-(3,5-Дибром-4-хлорфенил)-2,2,2-трифторэтанол
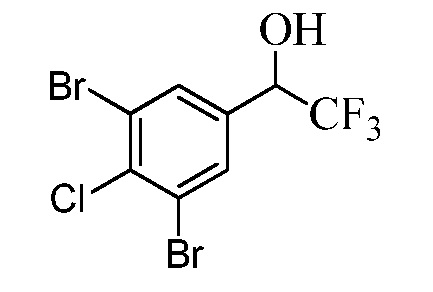
Продукт выделяли в виде светло-желтой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,89 (с, 2H), 7,20 (д, J=6,0 Гц, 1H) 5,34-5,30 (м, 1H); ЭИ-МС m/z 366,0 ([М]+).
Стадия 2. 1-(1-Бром-2,2,2-трифторэтил)-3,5-дихлорбензол (AI1). К перемешиваемому раствору 1-(3,5-дихлорфенил)-2,2,2-трифторэтанола (4,0 г, 16,3 ммоль) в дихлорметане (CH2Cl2; 50 мл), добавляли N-бромсукцинимид (NBS; 2,9 г, 16,3 ммоль) и трифенилфосфит (5,06 г, 16,3 ммоль), и полученную реакционную смесь нагревали до кипения с обратным холодильникомв течение 18 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до 25°C и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 100% пентаном) дала указанное в заголовке соединение в виде жидкости (2,0 г, 40%): 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (с, 3H), 5,00 (м, 1H); ЭИ-МС m/z 306 ([М]+).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Стадии 2 Примера 1.
5-(1-Бром-2,2,2-трифторэтил)-1,2,3-трихлорбензол (AI6)
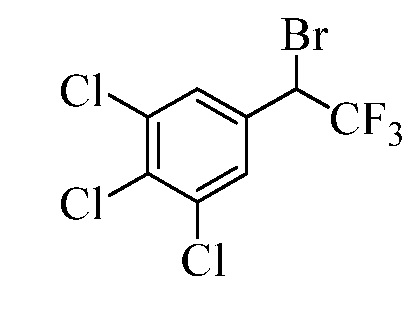
Продукт выделяли в виде бесцветного масла (300 мг, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,59 (с, 2H), 5,00 (м, 1H); ЭИ-МС m/z 340,00 ([М]+).
5-(1-Бром-2,2,2-трифторэтил)-1,3-дихлор-2-фторбензол (AI7)
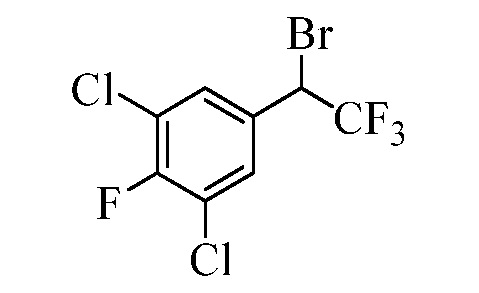
Продукт выделяли в виде бесцветного масла (320 мг, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,45 (с, 2H), 5,00 (м, 2H); ЭИ-МС m/z 324,00 ([М]+).
4-(1-бром-2,2,2-трифторэтил)-1,2-дихлорбензол (AI8)
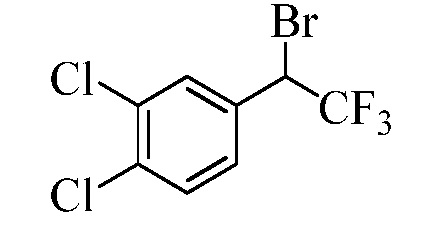
Продукт выделяли в виде бесцветного масла (300 мг, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,63 (с, 1H), 7,51 (м, 1H), 7,35 (м, 1H), 5,01 (м, 1H); ЭИ-МС m/z 306,00 ([М]+).
1,3-Дибром-5-(1-бром-2,2,2-трифторэтил)бензол
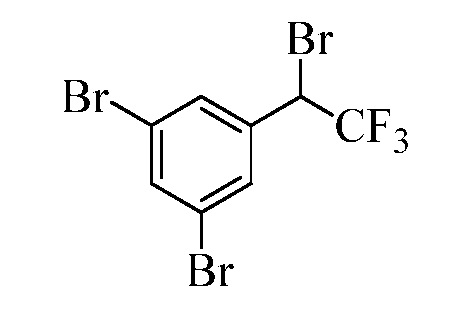
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,71 (с, 1H), 7,59 (с, 2H), 5,04-4,97 (м, 1H); ЭИ-МС m/z 394,6 ([М]+); ИК (тонкая пленка) 1114, 535 см-1.
1-(1-Бром-2,2,2-трифторэтил)-3-фтор-5-(трифторметил)бензол
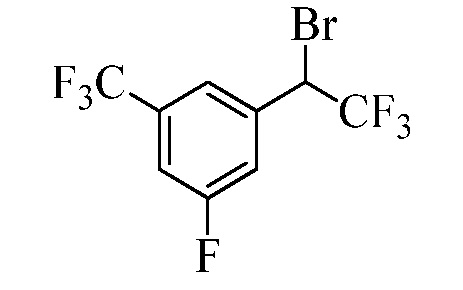
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,90 (д, J=8,4 Гц, 1H), 7,79-7,77 (м, 2H), 6,40-6,34 (м, 1H); ЭИ-МС m/z 324,00 ([М]+); ИК (тонкая пленка) 1175, 525 см-1.
1-(1-Бром-2,2,2-трифторэтил)-3-хлор-5-(трифторметил)бензол
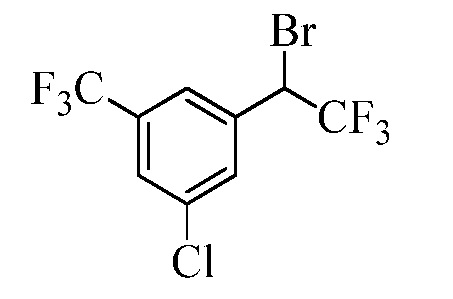
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,71 (с, 1H), 7,67 (с, 1H), 7,64 (с, 1H), 5,15-5,09 (м, 1H); ЭИ-МС m/z 340,00 ([М]+); ИК (тонкая пленка) 1178, 750, 540 см-1.
4-(1-Бром-2,2,2-трифторэтил)-1-фтор-2-(трифторметил)бензол
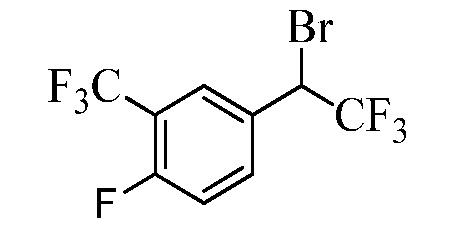
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,75-7,72 (м, 2H), 7,28-7,24 (м, 1H), 5,19-5,16 (м, 1H); ЭИ-МС m/z 326,0 ([М]+); ИК (тонкая пленка) 1114, 571 см-1.
5-(1-Бром-2,2,2-трифторэтил)-1,2,3-трифторбензол
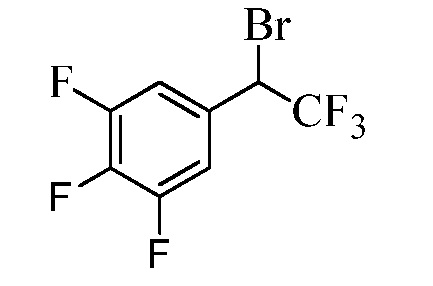
Молекула, указанная в заголовке, была выделена в виде коричневой жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,23-7,12 (м, 2H), 5,05-4,98 (м, 1H); ЭИ-МС m/z 292,0 ([М]+); ИК (тонкая пленка) 1116, 505 см-1.
1-(1-Бром-2,2,2-трифторэтил)-2,3,4-трифторбензол
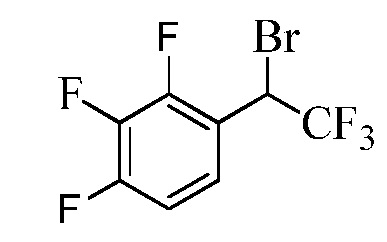
Молекула, указанная в заголовке, была выделена в виде бесцветного масла: 1H-ЯМР (300 МГц, CDCl3) δ 7,44 (кв.д, J=м, 1H), 7,11-7,03 (м, 1H), 5,53-5,45 (м, 1H).
1-(1-Бром-2,2,2-трифторэтил)-2,4,5-трихлорбензол
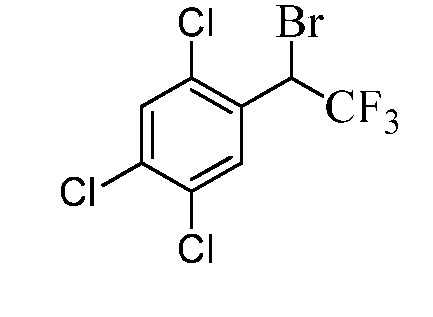
Молекула, указанная в заголовке, была выделена в виде грязно-белого твердого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,06 (д, J=2,1 Гц, 1H), 7,71 (с, 1H), 6,45-6,37 (м, 1H); ЭИ-МС m/z 340,0 ([М]+); ИК (тонкая пленка) 1186, 764, 576 см-1.
4-(1-Бром-2,2,2-трифторэтил)-1-хлор-2-нитробензол
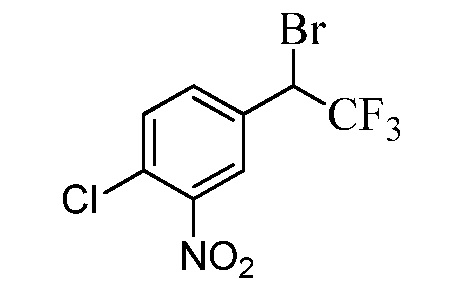
Молекула, указанная в заголовке, была выделена в виде грязно-белого твердого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,30 (с, 1H), 7,92 (д, J=9,0 Гц, 1H), 6,43-6,35 (м, 1H); ЭИ-МС m/z 317,0 ([М]+); ИК (тонкая пленка) 2927, 1540, 1353, 1177, 766, 530 см-1.
5-(1-Бром-2,2,2-трифторэтил)-2-фтор-1,3-диметилбензол
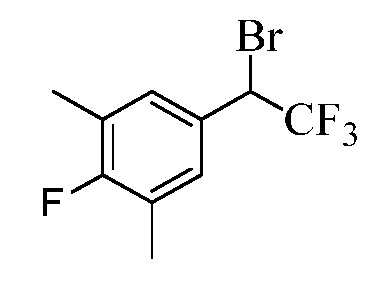
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,32 (д, J=7,2 Гц, 2H), 6,15-6,07 (м, 1H), 3,23 (с, 6H); ЭРИ-МС m/z 284,1 ([M+H]+); ИК (тонкая пленка) 2962, 1112, 500 см-1.
4-(1-Бром-2,2,2-трифторэтил)-1-фтор-2-метилбензол
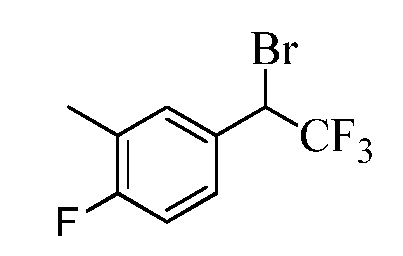
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,34-7,28 (м, 2H), 7,04-6,98 (м, 1H), 5,10-5,03 (м, 1H), 2,29 (с, 3H); ЭИ-МС m/z 270,1 ([М]+); ИК (тонкая пленка) 2989, 1163 см-1.
1-(1-Бром-2,2,3,3,3-пентафторпропил)-3,5-дихлорбензол
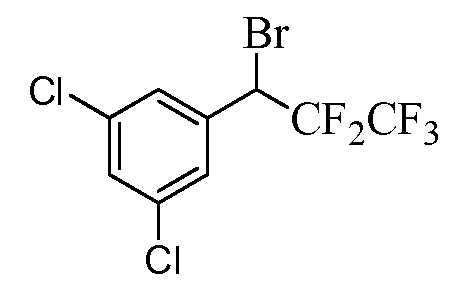
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,79 (т, J=2,0 Гц, 1H), 7,63 (С, 2H), 6,37-6,29 (м, 1H); ЭИ-МС m/z 356 ([М]+); ИК (тонкая пленка) 1673, 1130, 715, 518 см-1.
4-(1-Бром-2,2,2-трифторэтил)-2-хлор-1-метилбензол
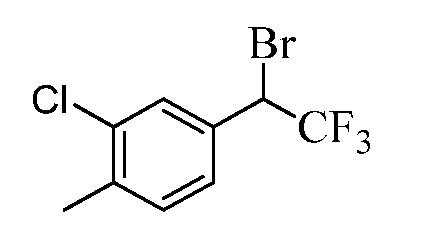
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,55-7,50 (м, 2H), 7,44 (д, J=8,4 Гц, 1H), 6,24-6,16 (м, 1H); ИК (тонкая пленка) 2983, 1112, 749, 564 см-1.
1,2-Дибром-4-(1-бром-2,2,2-трифторэтил)бензол

Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,75 (с, 1H), 7,67 (д, J=8,4 Гц, 1H), 7,33-7,30 (м, 1H), 5,07-5,00 (м, 1H); ЭИ-МС m/z 393,8 ([М]+); ИК (тонкая пленка) 2981, 1644, 1165 см-1.
1-(1-Бром-2,2,2-трифторэтил)-3-(трифторметокси)бензол
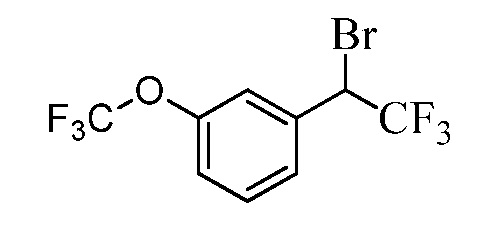
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,65-7,60 (м, 2H), 7,56-7,50 (м, 2H), 6,35-6,27 (м, 1H); ЭИ-МС m/z 322 ([М]+); ИК (тонкая пленка) 3413, 1161, 564 см-1.
5-(1-Бром-2,2,2-трифторэтил)-2-фторбензонитрил
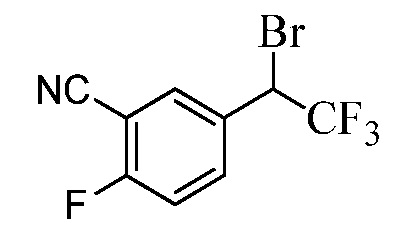
Молекула, указанная в заголовке, была выделена в виде светло-желтой жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 8,15-8,12 (м, 1H), 8,00-7,98 (м, 1H), 7,69-7,63 (м, 1H), 6,31-6,26 (м, 1H); ЭИ-МС m/z 280,9 ([М]+).
1-Бром-3-(1-бром-2,2,2-трифторэтил)-5-хлорбензол
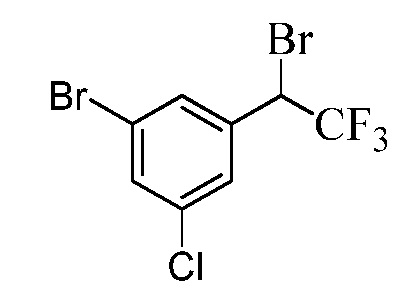
Молекула, указанная в заголовке, была выделена в виде светло-желтой жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,90 (с, 1H), 7,74 (с, 1H), 7,65 (с, 1H), 6,26-6,20 (м, 1H); ЭИ-МС m/z 349,9 ([М]+); ИК (тонкая пленка) 1114, 764 см-1.
1-Бром-3-(1-бром-2,2,2-трифторэтил)-5-фторбензол
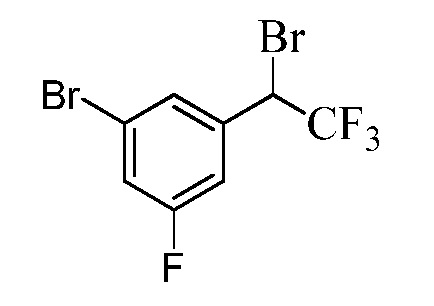
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,43 (с, 1H), 7,32-7,29 (м, 1H), 7,22 (д, J=8,8 Гц, 1H), 1,06 (кв., 1H); ЭИ-МС m/z 334,0 ([М]+); ИК (тонкая пленка) 3087, 1168, 533 см-1.
5-(1-Бром-2,2,3,3,3-пентафторпропил)-1,2,3-трихлорбензол
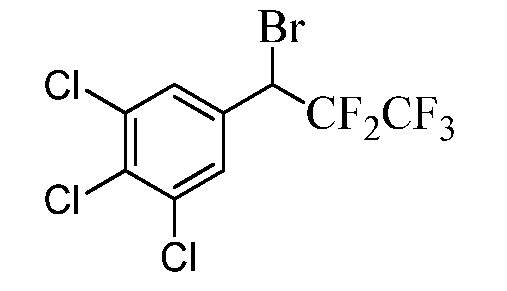
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,85 (с, 2H), 6,38-6,29 (м, 1H); ЭИ-МС m/z 389,9 ([М]+); ИК (тонкая пленка) 1208, 798, 560 см-1.
4-(1-Бром-2,2,2-трифторэтил)-2,6-дифторбензонитрил
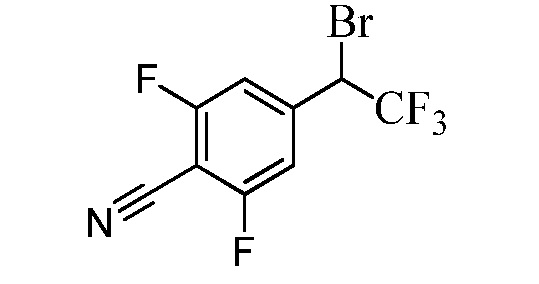
Молекула, указанная в заголовке, была выделена в виде фиолетового твердого вещества: Т.пл. 59-63ºC; 1H-ЯМР (400 МГц, CDCl3) δ 7,25 (с, 2H), 5,11-5,07 (м, 1H); ЭРИ-МС m/z 299,0 ([M+H]+).
1-(1-Бром-2,2,2-трифторэтил)-3-(трифторметил)бензол
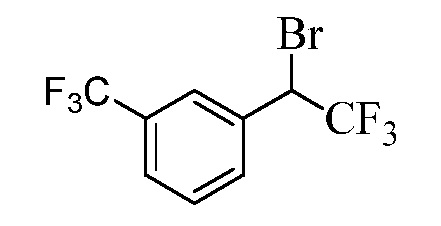
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: Т.пл. 59-63ºC; 1H-ЯМР (300 МГц, CDCl3) δ 7,75-7,67 (м, 3H), 7,57-7,52 (м, 1H), 5,20-5,13 (м, 1H); ЭРИ-МС m/z 306,0 ([М]+); ИК (тонкая пленка) 3436, 2925, 1265, 749 см-1.
5-(1-Бром-2,2,2-трифторэтил)-1,3-дифтор-2-метоксибензол
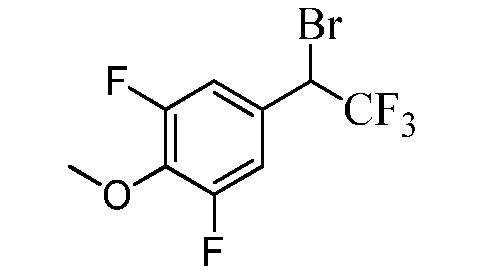
Молекула, указанная в заголовке, была выделена в виде светло-желтой жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,08 (д, J=8,4 Гц, 2H), 5,03-4,98 (м, 1H), 4,04 (с, 3H); ЭРИ-МС m/z 304,1 ([M+H]+); ИК (тонкая пленка) 1114, 613 см-1.
5-(1-Бром-2,2,2-трифторэтил)-1,2-дихлор-3-метилбензол
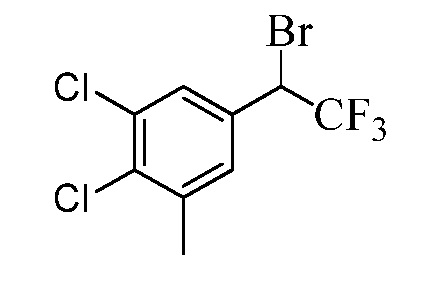
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,46 (с, 1H), 7,27 (с, 1H), 5,04-4,99 (м, 1H), 2,44 (с, 3H); ЭИ-МС m/z 320,0 ([М]+); ИК (тонкая пленка) 2925, 1112, 752, 580 см-1.
4-(1-Бром-2,2-дифторпропил)-1,2-дихлорбензол
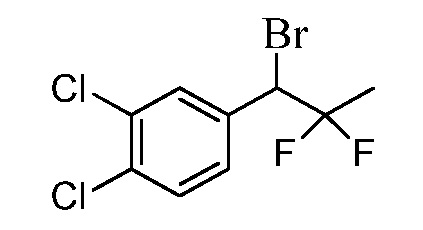
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,76-7,70 (м, 2H), 7,54 (дд, J=8,4 1,8 Гц, 1H), 5,81-5,73 (м, 1H), 1,67 (д, J=18,9 Гц, 3H); ЭИ-МС m/z 304,0 ([М]+); ИК (тонкая пленка) 1118, 800, 499 см-1.
1-(1-Бром-2,2,2-трифторэтил)-3-хлор-5-этилбензол
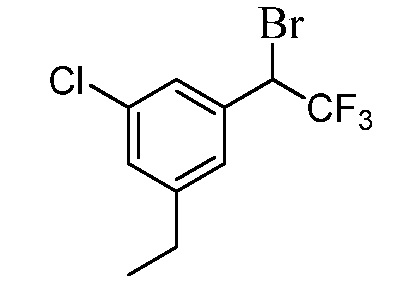
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,43 (д, J=5,6 Гц, 2H), 7,39 (с, 1H), 6,20-6,16 (м, 1H), 2,68-2,62 (м, 2H), 1,19 (т, J=7,6 Гц, 3H); ЭИ-МС m/z 300,0 ([М]+); ИК (тонкая пленка) 2970, 1167, 716, 539 см-1.
2-Бром-5-(1-бром-2,2,2-трифторэтил)-1,3-дихлорбензол
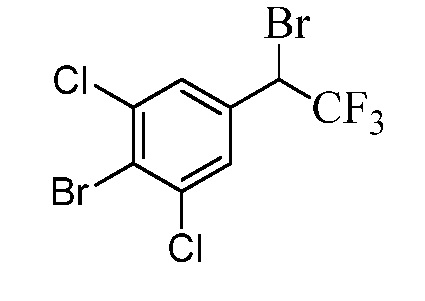
Молекула, указанная в заголовке, была выделена в виде бесцветной жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,79 (с, 2H), 6,27-6,21 (м, 1H); ЭИ-МС m/z 383,9 ([М]+); ИК (тонкая пленка) 2924, 1114, 749, 534 см-1.
1,3-Дибром-5-(1-бром-2,2,2-трифторэтил)-2-хлорбензол
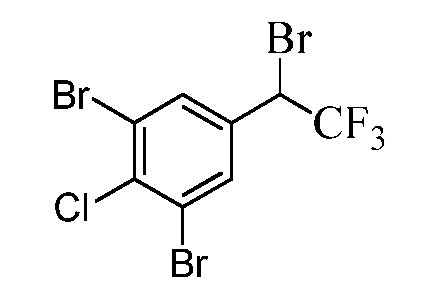
Молекула, указанная в заголовке, была выделена в виде светло-желтой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,97 (с, 2H), 6,27-6,19 (м, 1H); ЭИ-МС m/z 428,0 ([М]+).
Пример 2: Получение N-метил-4-винилбензамида (AI9)
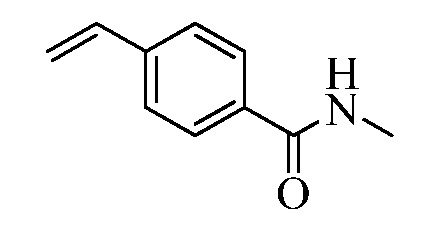
Стадия 1. 4-Винилбензоилхлорид (AI10). К перемешиваемому раствору 4-винилбензойной кислоты (1 г, 6,75 ммоль) в CH2Cl2 (20 мл) при 0°C по каплям добавляли каталитическое количество N,N-диметилформамида (ДМФА) и оксалилхлорида (1,27 г, 10,12 ммоль) в течение 15 минут (мин). Реакционную смесь перемешивали при 25°C в течение 6 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь выпаривали при пониженном давлении, получив неочищенный хлорангидрид.
Стадия 2. N-Метил-4-винилбензамид (AI9). К 1М N-метиламина в ТГФ (13,5 мл, 13,5 ммоль) при 0°C добавляли триэтиламин (Et3N; 1,34 мл, 10,12 ммоль) и хлорангидрид из Стадии 1 выше в ТГФ (10 мл), и реакционную смесь перемешивали при 25°C в течение 3 ч. После того, как реакцию посчитали завершенной согласно ТСХ, в реакционную смесь вливали воду и затем экстрагировали EtOAc (3×). Объединенный слой EtOAc промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (650 мг, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=8,0 Гц, 2H), 7,45 (д, J=8,0 Гц, 2H), 6,79 (м, 1H), 6,20 (шир. с, 1H), 5,82 (д, J=17,6 Гц, 1H), 5,39 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 161,95 ([M+H]+).
Следующие соединения были получены в соответствии с методиками, раскрытыми в соответствии с Примером 2.
N,N-диметил-4-винилбензамид (AI11)

Продукт выделяли в виде грязно-белого твердого вещества (650 мг, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,42 (м, 4H), 6,71 (м, 1H), 5,80 (д, J=17,6 Гц, 1H), 5,31 (д, J=10,8 Гц, 1H), 3,05 (с, 3H), 3,00 (с, 3H); ЭРИ-МС m/z 176,01 ([M+H]+).
N-(2,2,3-трифторметил)-4-винилбензамид (AI12)
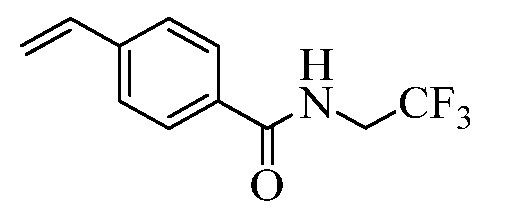
Продукт выделяли в виде грязно-белого твердого вещества (900 мг, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=8,0 Гц, 2H), 7,45 (д, J=8,0 Гц, 2H), 6,79 (м, 1H), 6,20 (шир. с, 1H), 5,82 (д, J=17,6 Гц, 1H), 5,39 (д, J=10,8 Гц, 1H), 4,19 (м, 2H); ЭРИ-МС m/z 230,06 ([M+H]+).
Морфолино(4-винилфенил)метанон (AI13)

Продукт выделяли в виде белого твердого вещества (850 мг, 60%): ЭРИ-МС m/z 218,12 ([M+H]+).
Пример 3: Получение этил-2-метил-4-винилбензоата (AI14)
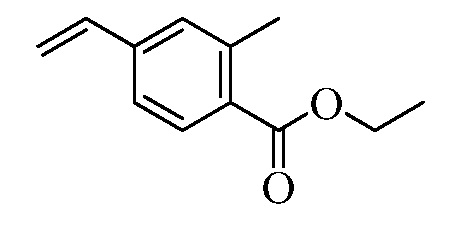
Стадия 1. 4-Формил-2-метилбензойная кислота (AI15). К перемешиваемому раствору 4-бром-2-метилбензойной кислоты (10 г, 46,4 ммоль) в сухом ТГФ (360 мл) при -78°C добавляли н-бутиллитий (н-BuLi, 1,6М раствор в гексане; 58,17 мл, 93,0 ммоль) и ДМФА (8 мл). Реакционную смесь перемешивали при -78°C в течение 1 ч, затем нагревали до 25°C и перемешивали в течение 1 ч. В реакционную смесь вливали 1Н раствор HCl и экстрагировали EtOAc. Объединенные экстракты EtOAc промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Остаток промывали н-гексаном с получением указанного в заголовке соединения в виде твердого вещества (3,0 г, 40%): Т.пл. 196-198°C; 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,32 (шир., с, 1H), 10,05 (с, 1H), 7,98 (м, 1H), 7,84 (м, 2H), 2,61 (с, 3H); ЭРИ-МС m/z 163,00 ([M-H]-).
Стадия 2. Этил-4-формил-2-метилбензоат (AI16). К перемешиваемому раствору 4-формил-2-метилбензойной кислоты (3 г, 18,2 ммоль) в этиловом спирте (EtOH; 30 мл) добавляли серную кислоту (H2SO4, × М; 2 мл) и реакционную смесь нагревали при 80°C в течение 18 ч. Реакционную смесь охлаждали до 25°C и выпаривали при пониженном давлении. Остаток разбавляли EtOAc и промывали H2O. Объединенные экстракты EtOAc промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении с получением указанного в заголовке соединения в виде твердого вещества (2,8 г, 80%): 1H-ЯМР (400 МГц, CDCl3) δ 10,05 (с, 1H), 8,04 (м, 1H), 7,75 (м, 2H), 4,43 (м, 2H), 2,65 (с, 3H), 1,42 (м, 3H).
Стадия 3. Этил-2-метил-4-винилбензоат (AI14). К перемешиваемому раствору этил-4-формил-2-метилбензоата (2,8 г, 4 ммоль) в 1,4-диоксане (20 мл) добавляли карбонат калия (K2CO3; 3,01 г, 21,87 ммоль) и метилтрифенилфосфонийбромид (7,8 г, 21,87 ммоль) при 25°C. Затем реакционную смесь нагревали при 100°C в течение 18 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до 25°C и фильтровали, и фильтрат выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; элюирование 25-30% EtOAc в н-гексане), получив указанное в заголовке соединение в виде твердого вещества (2,0 г, 72%): 1H-ЯМР (400 МГц, CDCl3) δ 7,86 (м, 1H), 7,27 (м, 2H), 6,68 (дд, J=17,6, 10,8 Гц, 1H), 5,84 (д, J=17,6 Гц, 1H), 5,39 (д, J=10,8 Гц, 1H), 4,39 (м, 2H), 2,60 (с, 3H), 1,40 (м, 3H); ЭРИ-МС m/z 191,10 ([M-H]-); ИК (тонкая пленка) 2980, 1716, 1257 см-1.
Пример 4: Получение трет-бутил-2-хлор-4-винилбензоата (AI17)
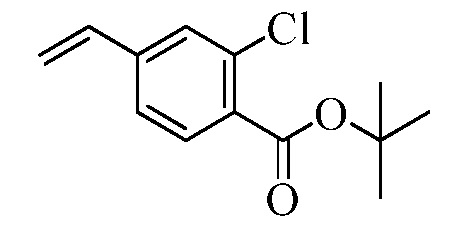
Стадия 1. трет-Бутил-4-бром-2-хлорбензоат (AI18). К перемешиваемому раствору 4-бром-2-хлорбензойной кислоты (5 г, 21,37 ммоль) в ТГФ (30 мл) добавляли ди-трет-бутил-дикарбонат (25,5 г, 25,58 ммоль), Et3N (3,2 г, 31,98 ммоль) и 4-(диметиламино)пиридин (DMAP; 0,78 г, 6,398 ммоль), и реакционную смесь перемешивали при 25°C в течение 18 ч. Реакционную смесь разбавляли EtOAc и промывали H2O. Объединенный органический слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Остаток очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; элюирование 2-3% EtOAc в н-гексане), получив указанное в заголовке соединение в виде жидкости (3,2 г, 51%): 1H-ЯМР (400 МГц, CDCl3) δ 7,62 (м, 2H), 7,44 (д, J=8,4 Гц, 1H), 1,59 (с, 9H); ЭРИ-МС m/z 290,10 ([M+H]+); ИК (тонкая пленка) 1728 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Стадии 1 Примера 4.
трет-Бутил-2-бром-4-иодбензоат (AI19)
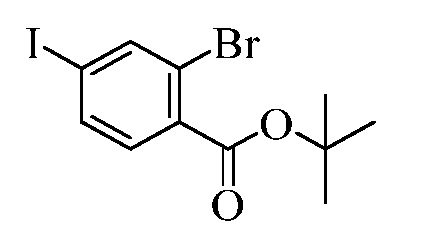
Продукт выделяли в виде бесцветного масла (1,2 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 8,01 (с, 1H), 7,68 (д, J=8,4 Гц, 1H), 7,41 (д, J=8,0 Гц, 1H), 1,59 (с, 9H); ЭРИ-МС m/z 382,10 ([M+H]+); ИК (тонкая пленка) 1727 см-1.
трет-Бутил-4-бром-2-(трифторметил)бензоат (AI20)
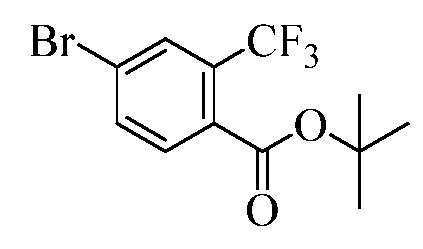
Продукт выделяли в виде бесцветного масла (1 г, 52%): 1H-ЯМР (400 МГц, CDCl3) δ 7,85 (с, 1H), 7,73 (д, J=8,4 Гц, 1H), 7,62 (д, J=8,4 Гц, 1H), 1,57 (с, 9H); ЭРИ-МС m/z 324,10 ([M+H]+); ИК (тонкая пленка) 1725 см-1.
Стадия 2. трет-Бутил-2-хлор-4-винилбензоат (AI17). К перемешиваемому раствору трет-бутил-4-бром-2-хлорбензоат (1,6 г, 5,50 ммоль) в толуоле (20 мл) добавляли тетракис(трифенилфосфин)палладий (0) (Pd(PPh3)4; (0,31 мг, 0,27 ммоль), K2CO3 (2,27 г, 16,5 ммоль) и пиридиновый комплекс винилборонового ангидрида (2,0 г, 8,3 ммоль) и реакционную смесь нагревали с обратным холодильником до кипения в течение 16 ч. Реакционную смесь фильтровали и фильтрат промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 5-6% EtOAc в н-гексане) дала указанное в заголовке соединение в виде жидкости (0,6 г, 46%): 1H-ЯМР (400 МГц, CDCl3) δ 7,72 (д, J=8,1 Гц, 1H), 7,44 (м, 1H), 7,31 (д, J=8,0 Гц, 1H), 6,69 (дд, J=17,6, 10,8 Гц, 1H), 5,85 (д, J=17,6 Гц, 1H), 5,40 (д, J=10,8 Гц, 1H), 1,60 (с, 9H); ЭРИ-МС m/z 238,95 ([M+H]+); ИК (тонкая пленка) 2931, 1725, 1134 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Стадии 2 Примера 4.
трет-Бутил-2-бром-4-винилбензоат (AI21)
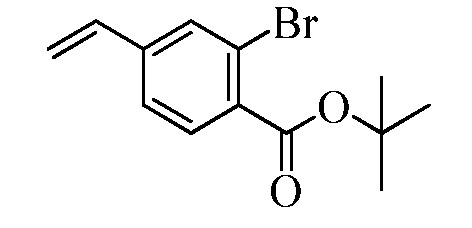
Продукт выделяли в виде бесцветного масла (1 г, 52%): 1H-ЯМР (400 МГц, CDCl3) δ 7,68 (м, 2H), 7,36 (д, J=8,0 Гц, 1H), 6,68 (дд, J=17,6, 10,8 Гц, 1H), 5,84 (д, J=17,6 Гц, 1H), 5,39 (д, J=10,8 Гц, 1H), 1,60 (с, 9H); ЭРИ-МС m/z 282,10 ([M+H]+); ИК (тонкая пленка) 2978, 1724, 1130 см-1.
трет-Бутил-2-(трифторметил)-4-винилбензоат (AI22)
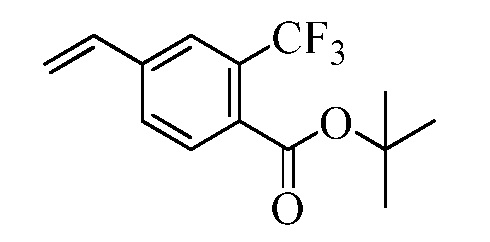
Продукт выделяли в виде бесцветного масла (1,2 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 7,71 (д, J=6,4 Гц, 2H), 7,59 (д, J=7,6 Гц, 1H), 6,77 (дд, J=17,6, 10,8 Гц, 1H), 5,89 (д, J=17,6 Гц, 1H), 5,44 (д, J=10,8 Гц, 1H), 1,58 (с, 9H); ЭРИ-МС m/z 272,20 ([M+H]+); ИК (тонкая пленка) 2982, 1727, 1159 см-1.
Пример 5: Получение трет-бутил-2-циано-4-винилбензоата (AI23)
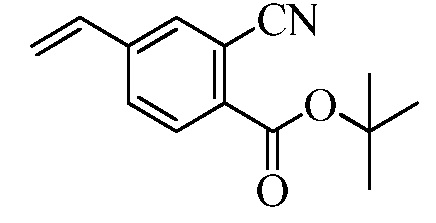
К перемешиваемому раствору трет-бутил-2-бром-4-винилбензоата (0,5 г, 1,77 ммоль) в ДМФА (20 мл) добавляли цианид меди (I) (CuCN; 0,23 г, 2,65 ммоль) и реакционную смесь нагревали при 140°C в течение 3 ч. Реакционную смесь охлаждали до 25°C, разбавляли H2O и экстрагировали EtOAc. Объединенный органический слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Остаток очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; элюирование 15% EtOAc в н-гексане), получив указанное в заголовке соединение в виде белого твердого вещества (0,3 г, 72%): Т.пл. 51-53°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,03 (с, 1H), 7,77 (с, 1H), 7,64 (д, J=8,4 Гц, 1H), 6,75 (дд, J=17,6, 10,8 Гц, 1H), 5,93 (д, J=17,6 Гц, 1H), 5,51 (д, J=10,8 Гц, 1H), 1,65 (с, 9H); ЭРИ-МС m/z 229,84 ([M+H]+); ИК (тонкая пленка) 2370, 1709, 1142 см-1.
Пример 6: Получение этил-2-бром-4-иодбензоата (AI46)

К перемешиваемому раствору 4-иод-2-бромбензойной кислоты (5 г, 15,29 ммоль) в этиловом спирте (EtOH; 100 мл) добавляли серную кислоту (H2SO4; 5 мл) и нагревали реакционную смесь при 80°C в течение 18 ч. Реакционную смесь охлаждали до 25°C и выпаривали при пониженном давлении. Остаток разбавляли EtOAc (2×100 мл) и промывали H2O (100 мл). Объединенные экстракты EtOAc промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении с получением соединения в виде светло-желтого твердого вещества (5 г, 92%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 8,04 (д, J=1,2 Гц, 1H), 7,71 (д, J=7,6 Гц, 1H), 7,51 (д, J=8,4 Гц, 1H), 4,41 (кв., J=7,2 Гц, 2H), 1,41 (т, J=7,2 Гц, 3H).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 6.
Этил-4-бром-2-хлорбензоат (AI47)
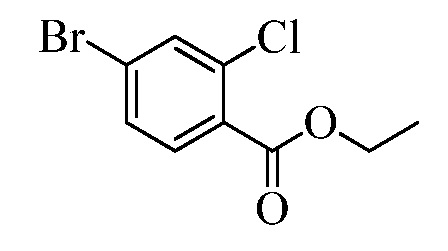
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (2,0 г, 80%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 8,25 (д, J=1,2 Гц, 1H), 7,79 (д, J=7,6 Гц, 1H), 7,65 (д, J=8,4 Гц, 1H), 4,65 (кв., J=7,2 Гц, 2H), 1,56 (т, J=7,2 Гц, 3H).
Этил-4-бром-2-метилбензоат (AI48)
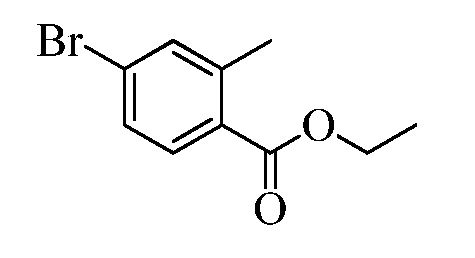
Указанное в заголовке соединение выделяли в виде светло-желтой жидкости (3,0 г, 83%): 1H-ЯМР (400 МГц, CDCl3) δ 7,79 (д, J=8,4 Гц, 1H), 7,41 (с, 1H), 7,39 (д, J=8,4 Гц, 1H), 4,42 (кв., J=7,2 Гц, 2H), 2,60 (с, 3H), 1,40 (т, J=7,2 Гц, 3H) ЭРИ-МС m/z 229,11 ([M+H]+); ИК (тонкая пленка) 1725 см-1.
Этил-4-бром-2-фторбензоат (AI49)
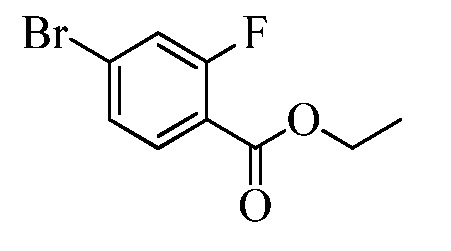
Указанное в заголовке соединение выделяли в виде бесцветной жидкости (9,0 г, 79%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,84 (т, J=8,4 Гц, 1H), 7,76 (д, J=2,0 Гц, 1H), 7,58 (д, J=1,6 Гц, 1H), 4,34 (кв., J=7,2 Гц, 2H), 1,32 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 246,99 ([M+H]+), ИК (тонкая пленка) 1734 см-1.
Пример 7: Получение этил-4-бром-2-этилбензоата (AI50)
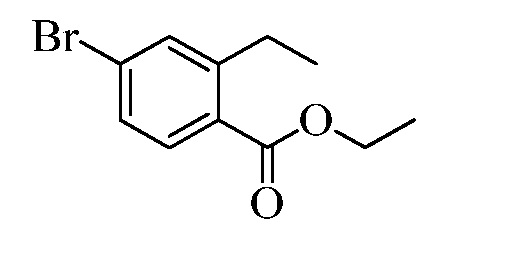
К перемешиваемому раствору 4-бром-2-фторбензойной кислоты (2,0 г, 9,17 ммоль) в ТГФ (16 мл) по каплям добавляли 1,0М этилмагнийбромид в ТГФ (32 мл, 32,0 ммоль) при 0°C и полученную реакционную смесь перемешивали при КТ в течение 18 ч. В реакционную смесь вливали 2Н HCl и экстрагировали этилацетатом. Объединенный этилацетатный слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении с получением неочищенной 4-бром-2-этилбензойной кислоты в виде бесцветной жидкости, которую использовали в следующей стадии без очистки (0,4 г): 1H-ЯМР (400 МГц, CDCl3) δ 7,64 (д, J=8,4 Гц, 1H), 7,47 (м, 1H), 7,43 (м, 1H), 2,95 (кв., J=4,0 Гц, 2H), 1,32 (т, J=4,0 Гц, 3H); ЭРИ-МС m/z 228,97 ([M+H]+).
Указанное в заголовке соединение синтезировали из 4-бром-2-этилбензойной кислоты в соответствии с методикой в Примере 6 и выделяли в виде бесцветной жидкости (0,15 г, 68%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,90 (д, J=8,4 Гц, 1H), 7,47 (м, 2H), 4,40 (кв., J=7,2 Гц, 2H), 3,06 (кв., J=7,6 Гц, 2H), 1,42 (т, J=7,2 Гц, 3H), 1,26 (т, J=7,6 Гц, 3H); ЭРИ-МС m/z 226,96 ([M-H]-); ИК (тонкая пленка) 3443, 1686, 568 см-1.
Пример 8: Получение этил-2-бром-4-винилбензоата (AI51)
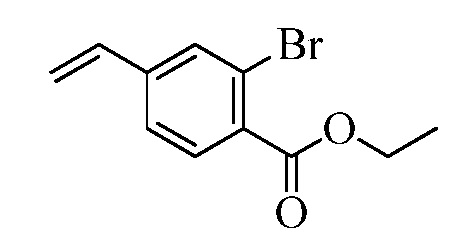
К перемешиваемому раствору этил-2-бром-4-иодбензоата (5 г, 14,3 ммоль) в ТГФ/воде (100 мл, 9:1) добавляли калий винилтрифторборат (1,89 г, 14,3 ммоль), Cs2CO3 (18,27 г, 56,07 ммоль) и трифенилфосфин (0,22 г, 0,85 ммоль), и реакционную смесь дегазировали аргоном в течение 20 минут, затем вводили PdCl2 (0,05 г, 0,28 ммоль). Реакционную смесь нагревали с обратным холодильником до кипения в течение 16 ч. Реакционная смесь охлаждали до КТ, фильтровали через слой целита и промывали этилацетатом. Фильтрат снова экстрагировали этилацетатом и промывали объединенные органические слои водой и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; элюирование 2% этилацетатом/петролейным эфиром), получив указанное в заголовке соединение в виде светло-коричневого смолистого материала (2 г, 56%): 1H-ЯМР (400 МГц, CDCl3) δ 7,78 (д, J=8,4 Гц, 1H), 7,71 (д, J=1,2 Гц, 1H), 7,51 (д, J=8,4 Гц, 1H), 6,69 (дд, J=17,6, 10,8 Гц, 1H), 5,86 (д, J=17,6 Гц, 1H), 5,42 (д, J=11,2 Гц, 1H), 4,42 (кв., J=7,2 Гц, 2H), 1,43 (т, J=3,6 Гц, 3H); ЭРИ-МС m/z 255,18 ([M+H]+); ИК (тонкая пленка) 1729 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 8.
Этил-2-метил-4-винилбензоат (AI52)
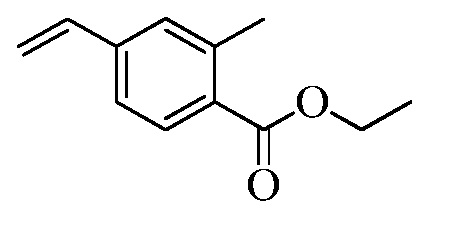
Указанное в заголовке соединение выделяли в виде бесцветной жидкости (0,8 г, 80%): 1H-ЯМР (400 МГц, CDCl3) δ 7,89 (д, J=8,4 Гц, 1H), 7,27 (м, 2H), 6,79 (дд, J=17,6, 10,8 Гц, 1H), 5,86 (д, J=17,6 Гц, 1H), 5,42 (д, J=11,2 Гц, 1H), 4,42 (кв., J=7,2 Гц, 2H), 2,60 (с, 3H), 1,43 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 191,10 ([M+H]+); ИК (тонкая пленка) 1717, 1257 см-1.
Этил-2-фтор-4-винилбензоат (AI53)
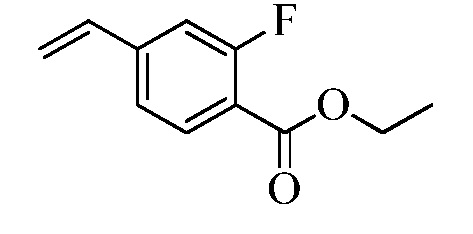
Указанное в заголовке соединение выделяли в виде светло-желтой жидкости (2,0 г, 50%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,87 (т, J=8,0 Гц, 1H), 7,51 (д, J=16,0 Гц, 1H), 7,48 (д, J=16,0 Гц, 1H), 6,82 (дд, J=17,6, 10,8 Гц, 1H), 6,09 (д, J=17,6 Гц, 1H), 5,50 (д, J=10,8 Гц, 1H), 4,35 (кв., J=7,2 Гц, 2H), 1,35 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 195,19 ([M+H]+); ИК (тонкая пленка) 1728 см-1.
Пример 9: Получение этил-2-хлор-4-винилбензоата (AI54)
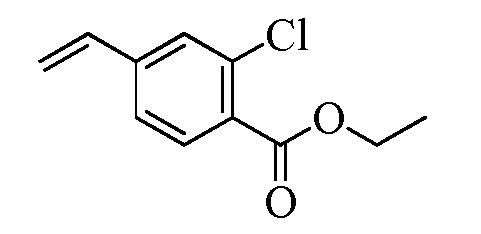
К перемешиваемому раствору этил-2-хлор-4-бромбензоата (2 г, 7,63 ммоль) в диметилсульфоксиде (20 мл) добавляли винилтрифторборат калия (3,06 г, 22,9 ммоль) и карбонат калия (3,16 г, 22,9 ммоль). Реакционную смесь дегазировали аргоном в течение 30 мин. Добавляли дихлорид бистрифенилфосфин(дифенил-фосфиноферроцен)палладия (0,27 г, 0,38 ммоль) и нагревали реакционную смесь до 80°C в течение 1 ч. Реакционную смесь разбавляли водой (100 мл), экстрагировали этилацетатом (2×50 мл), промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении с получением соединения в виде коричневого смолистого материала (1,1 г, 69%): 1H-ЯМР (400 МГц, CDCl3) δ 7,81 (д, J=8,4 Гц, 1H), 7,46 (с, 1H), 7,33 (д, J=8,4 Гц, 1H), 6,70 (дд, J=17,6, 11,2 Гц, 1H), 5,87 (д, J=17,6 Гц, 1H), 5,42 (д, J=10,8 Гц, 1H), 4,41 (кв., J=7,2 Гц, 2H), 1,43 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 211,22 ([M+H]+); ИК (тонкая пленка) 1729, 886 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 9.
Этил-2-этил-4-винилбензоат (AI55)
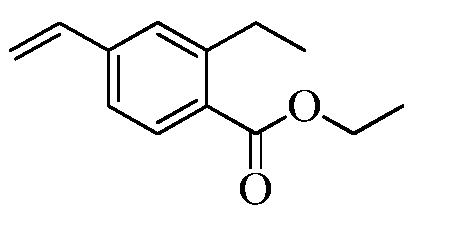
Указанное в заголовке соединение выделяли в виде бесцветной жидкости (1,0 г, 66%): 1H-ЯМР (300 МГц, CDCl3) δ 7,85 (м, 1H), 7,29 (м, 2H), 6,76 (д, J=10,8 Гц, 1H), 5,86 (д, J=17,6 Гц, 1H), 5,36 (д, J=10,5 Гц, 1H), 4,41 (кв., J=7,2 Гц, 2H), 3,10 (кв., J=7,2 Гц, 2H), 1,40 (т, J=7,2 Гц, 3H), 1,30 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 205,26 ([M+H]+); ИК (тонкая пленка) 1720, 1607, 1263 см-1.
Метил-2-метокси-4-винилбензоат (AI56)
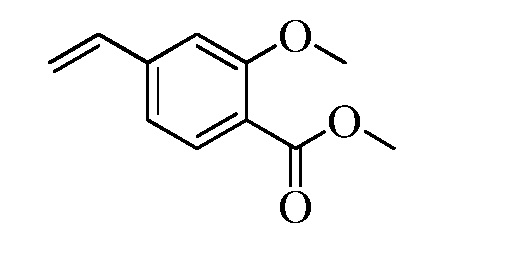
Указанное в заголовке соединение выделяли в виде светло-желтой жидкости (1,2 г, 75%): 1H-ЯМР (400 МГц, CDCl3) δ 7,79 (д, J=8,0 Гц, 1H), 7,04 (д, J=1,2 Гц, 1H), 6,97 (с, 1H), 6,74 (дд, J=11,2, 11,2 Гц, 1H), 5,86 (д, J=17,6 Гц, 1H), 5,39 (д, J=17,6 Гц, 1H) 3,93 (с, 3H), 3,91 (с, 3H), ЭРИ-МС m/z 193,18 ([M+H]+); ИК (тонкая пленка) 1732 см-1.
Этил-2-(метилтио)-4-винилбензоат
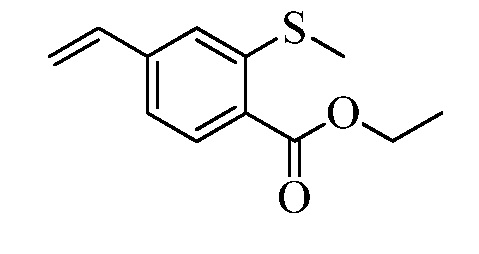
Указанное в заголовке соединение выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 7,98 (д, J=8,4 Гц, 1H), 7,23-7,18 (м, 2H), 6,78 (дд, J=17,7, 10,8, Гц, 1H), 5,89 (д, J=17,4 Гц, 1H), 5,42 (д, J=10,8 Гц, 1H), 4,39-4,36 (м, 2H), 2,48 (с, 3H), 1,39 (т, J=6,9 Гц, 3H); ЭРИ-МС m/z 221,9 ([M+H]+); ИК (тонкая пленка) 1708 см-1.
Пример 10: Получение (E)-этил-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензоата (AI24)
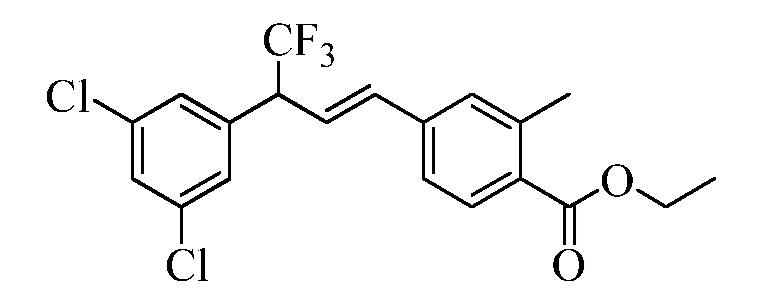
К перемешиваемому раствору этил-2-метил-4-винилбензоата (2,0 г, 10,5 ммоль) в 1,2-дихлорбензоле (25 мл) добавляли 1-(1-бром-2,2,2-трифторэтил)-3,5-дихлорбензол (6,44 г, 21,0 ммоль), хлорид меди (I) (CuCl; 208 мг, 21 ммоль) и 2,2-бипиридил (0,65 г, 4,1 ммоль). Реакционную смесь дегазировали аргоном в течение 30 мин и затем перемешивали при 180°C в течение 24 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до 25°C и фильтровали, и фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; элюирование 25-30% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (1,7 г, 40%): 1H-ЯМР (400 МГц, CDCl3) δ 7,91 (д, J=8,0 Гц, 1H), 7,37 (м, 1H), 7,27-7,24 (м, 4H), 6,59 (д, J=16,0 Гц, 1H), 6,59 (дд, J=16,0, 8,0 Гц, 1H), 4,38 (кв., J=7,2 Гц, 2H), 4,08 (м, 1H), 2,62 (с, 3H), 1,42 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 415,06 ([M-H]-); ИК (тонкая пленка) 1717, 1255, 1114 см-1.
Соединения AI25, AI57-AI68 и AC1-AC5 (Таблица 1) были получены в соответствии с методиками, раскрытыми в Примере 10.
(E)-Этил-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2-(трифторметил)-бензойная кислота (AI25)
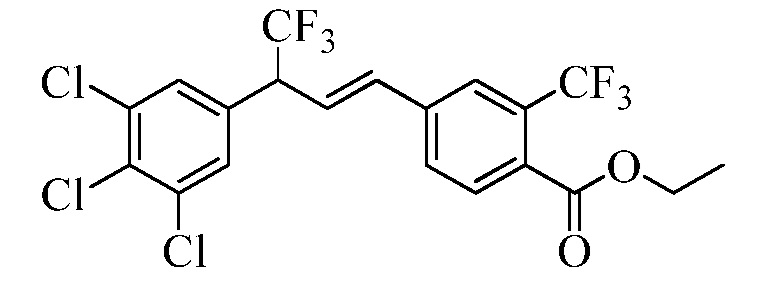
Продукт выделяли в виде светло-коричневой смолистой жидкости (500 мг, 40%): 1H-ЯМР (400 МГц, CDCl3) δ 7,79 (д, J=8,0 Гц, 1H), 7,71 (м, 1H), 7,61 (д, J=7,6 Гц, 1H), 7,42 (с, 2H), 6,70 (д, J=16,0 Гц, 1H), 6,57 (дд, J=16,0, 8,0 Гц, 1H), 4,42 (кв., J=7,2 Гц, 2H), 4,19 (м, 1H), 1,40 (т, J=7,6 Гц, 3H); ЭРИ-МС m/z 502,99 ([M-H]-); ИК (тонкая пленка) 1730, 1201, 1120, 749 см-1.
(E)-Этил-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-фторбензоат (AI57)
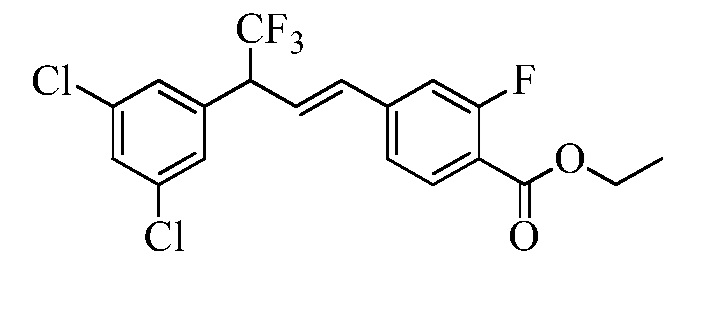
1H-ЯМР (400 МГц, CDCl3) δ 7,38 (с, 1H), 7,26 (с, 3H), 7,21 (д, J=8,4 Гц, 1H), 7,16 (д, J=11,6 Гц, 1H), 6,59 (д, J=16,0 Гц, 1H), 6,47 (дд, J=, 16,0, 8,0 Гц, 1H), 4,41 (кв., J=6,8 Гц, 2H), 4,18 (м, 1H), 1,41 (т, J=6,8 Гц, 3H); ЭРИ-МС m/z 419,33 ([M-H]-); ИК (тонкая пленка) 1723, 1115, 802 см-1.
(E)-Этил-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-бромбензоат (AI58)
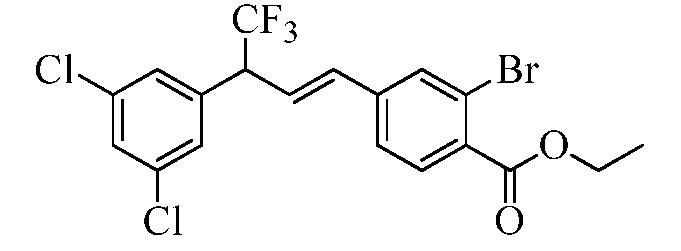
1H-ЯМР (400 МГц, CDCl3) δ 7,79 (д, J=8,0 Гц, 1H), 7,67 (с, 1H), 7,38 (м, 2H), 7,26 (м, 2H), 6,56 (д, J=16,0 Гц, 1H), 6,45 (дд, J=16,0, 7,6 Гц, 1H), 4,42 (кв., J=7,2 Гц, 2H), 4,39 (м, 1H), 1,42 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 481,22 ([M-H]-); ИК (тонкая пленка) 1727, 1114, 801, 685 см-1.
(E)-Этил-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензоат (AI59)
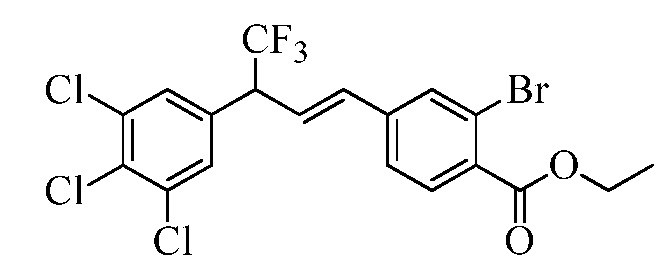
1H-ЯМР (400 МГц, CDCl3) δ 7,79 (д, J=8,0 Гц, 1H), 7,67 (д, J=1,6 Гц, 1H), 7,40 (с, 2H), 7,36 (д, J=1,6 Гц, 1H), 6,56 (д, J=16,0 Гц, 1H), 6,44 (дд, J=16,0, 7,6 Гц, 1H), 4,42 (кв., J=6,8 Гц, 2H), 4,15 (м, 1H), 1,42 (т, J=6,8 Гц, 3H); ЭРИ-МС m/z 514,74 ([M-H]-); ИК (тонкая пленка) 1726, 1115, 808, 620 см-1.
(E)-Этил-2-метил-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензоат (AI60)
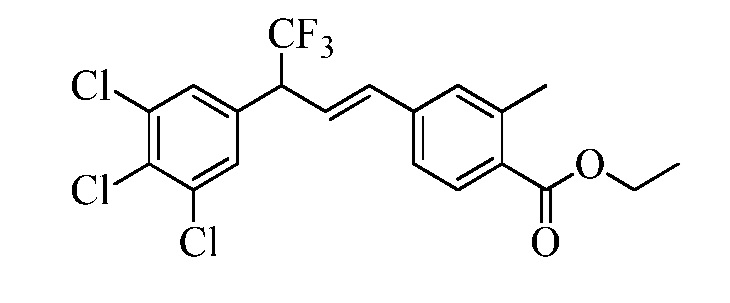
Указанное в заголовке соединение выделяли в виде светло-коричневого смолистого материала: 1H-ЯМР (400 МГц, CDCl3) δ 7,90 (д, J=8,8 Гц, 1H), 7,34 (д, J=6,0 Гц, 2H), 7,25 (д, J=7,2 Гц, 2H), 6,59 (д, J=16,0 Гц, 1H), 6,42 (дд, J=16,0, 8,0 Гц, 1H), 4,38 (кв., J=7,2 Гц, 2H), 4,19 (м, 1H), 2,63 (с, 3H), 1,41 (т, J=7,2 Гц, 3H).
(E)-Этил-2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензоат (AI61)
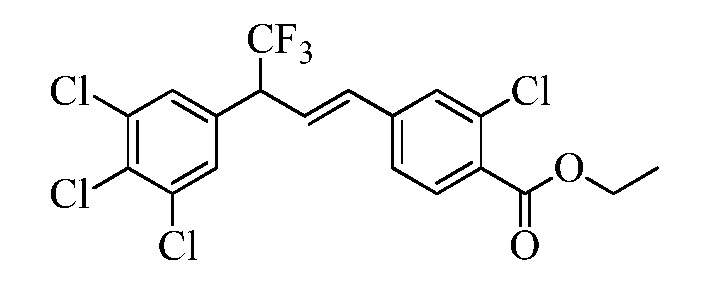
1H-ЯМР (400 МГц, CDCl3) δ 7,87 (д, J=8,0 Гц, 1H), 7,46 (д, J=1,6 Гц, 1H), 7,40 (с, 2H), 7,31 (д, J=1,6 Гц, 1H), 6,57 (д, J=16,0 Гц, 1H), 6,44 (дд, J=16,0 Гц, 8,0 Гц, 1H), 4,42 (кв., J=6,8 Гц, 2H), 4,15 (м, 1H), 1,42 (т, J=6,8 Гц, 3H); ЭРИ-МС m/z 470,73 ([M-H]-); ИК (тонкая пленка) 1726, 1115, 809, 3072 см-1.
(E)-Этил-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2-(трифторметил)бензоат (AI62)
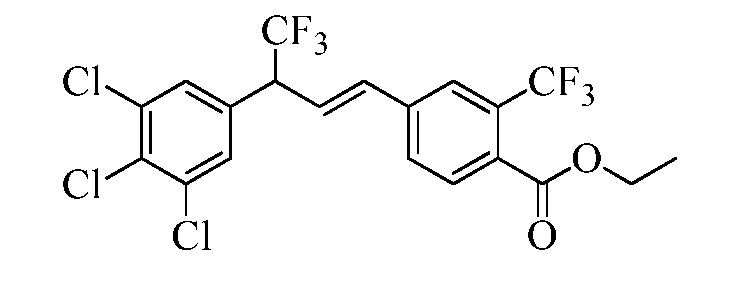
Указанное в заголовке соединение выделяли в виде бледно-коричневой жидкости (1,0 г, 46,3%): 1H-ЯМР (400 МГц, CDCl3) δ 7,79 (д, J=8,0 Гц, 1H), 7,71 (с, 1H), 7,61 (д, J=7,6 Гц, 1H), 7,41 (с, 2H) 6,65 (д, J=16,0 Гц, 1H), 6,49 (дд, J=16,0, 8,0 Гц, 1H), 4,42 (кв., J=7,6 Гц, 2H), 4,15 (м, 1H), 1,42 (т, J=7,6 Гц, 3H); ЭРИ-МС m/z 502,99 ([M-H]-); ИК (тонкая пленка) 1730, 1202, 1120, 750 см-1.
(E)-Этил-2-хлор-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензоат (AI63)
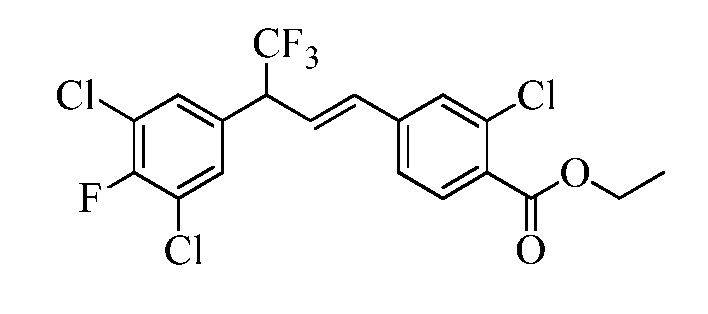
1H-ЯМР (400 МГц, CDCl3) δ 7,85 (д, J=6,0 Гц, 1H), 7,46 (д, J=1,8 Гц, 2H), 7,34 (м, 1H), 7,24 (м, 1H), 6,57 (д, J=16,2 Гц, 1H), 6,45 (дд, J=16,2, 7,2 Гц, 1H), 4,43 (кв., J=7,2 Гц, 2H), 4,13 (м, 1H), 1,41 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 455,0 ([M+H]+); ИК (тонкая пленка) 1728, 1115, 817 см-1.
(E)-Этил-2-фтор-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензоат (AI64)

1H-ЯМР (400 МГц, CDCl3) δ 7,93 (т, J=7,6 Гц, 1H), 7,34 (д, J=5,6 Гц, 2H), 7,21 (д, J=8,0 Гц, 1H), 7,16 (д, J=11,6 Гц, 1H), 6,59 (д, J=16,0 Гц, 1H), 6,49 (дд, J=16,0, 7,6 Гц, 1H), 4,42 (кв., J=7,6 Гц, 2H), 4,13 (м, 1H), 1,41 (т, J=7,6 Гц, 3H); ЭРИ-МС m/z 436,81 ([M-H]-); ИК (тонкая пленка) 1725 см-1.
(E)-Этил-2-бром-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензоат (AI65)
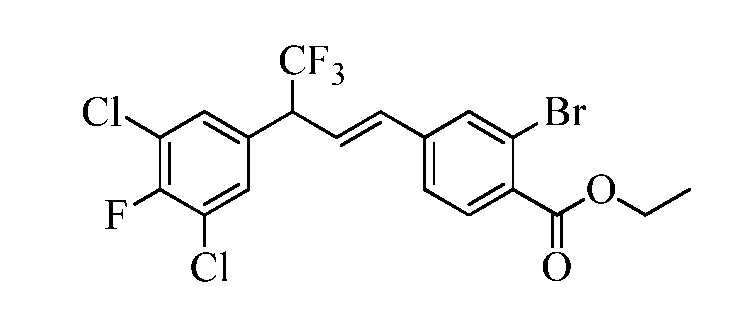
1H-ЯМР (400 МГц, CDCl3) δ 7,94 (д, J=8,0 Гц, 1H), 7,67 (с, 1H), 7,36 (м, 3H), 6,56 (д, J=15,6 Гц, 1H), 6,44 (дд, J=15,6, 8,0 Гц, 1H), 4,42 (кв., J=6,8 Гц, 2H), 4,10 (м, 1H), 1,42 (т, J=6,8 Гц, 3H); ЭРИ-МС m/z 498,74 ([M-H]-); ИК (тонкая пленка) 1726, 1114, 820, 623 см-1.
(E)-Этил-2-метил-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензоат (AI66)

Указанное в заголовке соединение выделяли в виде полутвердого коричневого вещества: 1H-ЯМР (400 МГц, CDCl3) δ 7,90 (д, J=8,8 Гц, 1H), 7,34 (д, J=6,0 Гц, 2H), 7,25 (д, J=7,2 Гц, 2H), 6,59 (д, J=16,0 Гц, 1H), 6,42 (дд, J=16,0 Гц, 8,0 Гц, 1H), 4,38 (кв., J=7,2 Гц, 2H), 4,19 (м, 1H), 2,63 (с, 3H), 1,41 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 432,90 ([M-H]-); ИК (тонкая пленка) 1715 см-1.
(E)-Метил-2-метокси-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензоат (AI67)

1H-ЯМР (400 МГц, CDCl3) δ 7,80 (д, J=8,4 Гц, 1H), 7,35 (д, J=6,0 Гц, 2H), 7,03 (д, J=1,2 Гц, 1H), 6,92 (с, 1H), 6,59 (д, J=15,6 Гц, 1H), 6,42 (дд, J=15,6, 8,0 Гц, 1H), 4,13 (м, 1H), 3,93 (с, 3H), 3,88 (с, 3H); ЭРИ-МС m/z 437,29 ([M+H]+); ИК (тонкая пленка) 1724 см-1.
(E)-Этил-2-этил-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензоат (AI68)
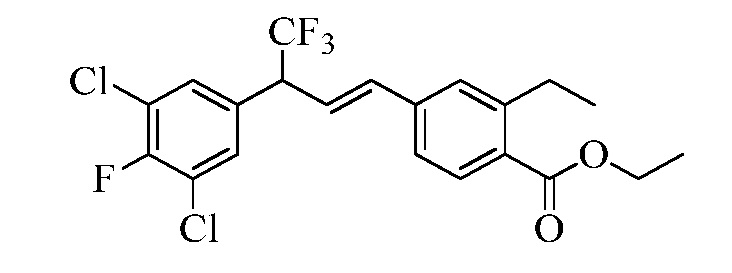
1H-ЯМР (400 МГц, CDCl3) δ 7,85 (д, J=8,0 Гц, 1H), 7,35 (д, J=9,6 Гц, 2H), 7,26 (м, 1H), 7,24 (м, 1H), 6,60 (д, J=15,6 Гц, 1H), 6,42 (дд, J=15,6, 8,0 Гц, 1H), 4,38 (кв., J=7,2 Гц, 2H), 4,14 (м, 1H), 3,01 (кв., J=7,6 Гц 2H), 1,41 (т, J=7,2 Гц, 3H), 1,26 (т, J=7,6 Гц, 3H); ЭРИ-МС m/z 447,05 ([M-H]-); ИК (тонкая пленка) 1715, 1115, 817 см-1.
(E)-Этил-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(метилтио)бензоат
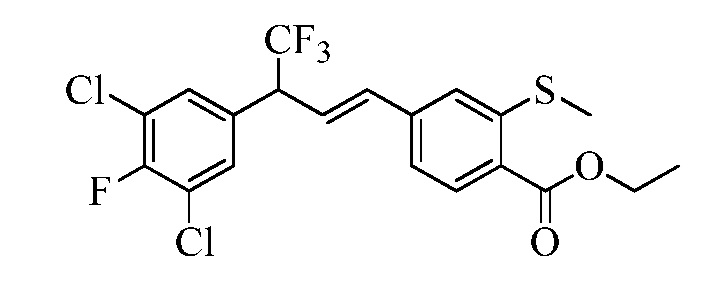
Выделен в виде коричневой жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,99 (д, J=8,1 Гц, 2H), 7,35-7,32 (м, 2H), 7,21-7,16 (м, 2H), 6,63 (д, J=15,8 Гц, 1H), 6,45 (дд, J=15,9, 7,8 Гц, 1H), 4,41-4,31 (м, 2H), 4,30-4,10 (м, 1H), 2,47 (с, 3H), 1,40 (т, J=7,5 Гц, 3H); ЭРИ-МС m/z 466,88 ([M+H]+); ИК (тонкая пленка) 1705, 1114 см-1.
(E)-Этил-2-бром-4-(3-(3,5-дифтор-4-метоксифенил)-4,4,4-трифтор-бут-1-ен-1-ил)бензоат
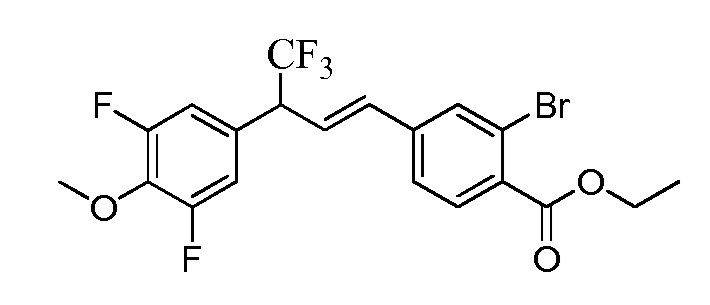
Продукт выделяли в виде светло-желтой жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,78 (д, J=8,0 Гц, 1H), 7,66 (д, J=1,6 Гц, 1H), 7,35-7,33 (м, 1H), 6,96-6,90 (м, 2H), 6,54 (д, J=15,6 Гц, 1H), 6,43 (дд, J=15,6, 8,0 Гц, 1H), 4,39 (кв., J=6,8 Гц, 2H), 4,09-4,05 (м, 1H), 4,02 (с, 3H), 1,40 (т, J=7,2 Гц, 3H); ЭИ-МС m/z 478,2 ([М]+); ИК (тонкая пленка) 1727, 1113 см-1.
Пример 11: Получение (E)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензойной кислоты (AI32)

К перемешиваемому раствору (E)-этил-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензоата (1,7 г, 4,0 ммоль) в 1,4-диоксане (10 мл) добавляли 11Н HCl (30 мл) и нагревали реакционную смесь при 100°C в течение 48 ч. Реакционную смесь охлаждали до 25°C и выпаривали при пониженном давлении. Остаток разбавляли H2O и экстрагировали хлороформом (CHCl3). Объединенный органический слой сушили над Na2SO4 и выпаривали при пониженном давлении, и неочищенное соединение промывали н-гексаном, получив указанное в заголовке соединение в виде белого твердого вещества (0,7 г, 50%): Т.пл. 142-143°C; 1H-ЯМР (400 МГц, ДМСО-d6) δ 12,62 (шир. с, 1H), 7,81 (д, J=8,0 Гц, 1H), 7,66 (с, 3H), 7,52-7,44 (м, 2H), 6,89 (дд, J=16,0, 8,0 Гц, 1H), 6,78-6,74 (д, J=16,0 Гц, 1H), 4,84 (м, 1H), 2,50 (с, 3H); ЭРИ-МС m/z 387,05 ([M-H]-); ИК (тонкая пленка) 3448, 1701, 1109, 777 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 11.
(E)-2-Метил-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойная кислота (AI26)
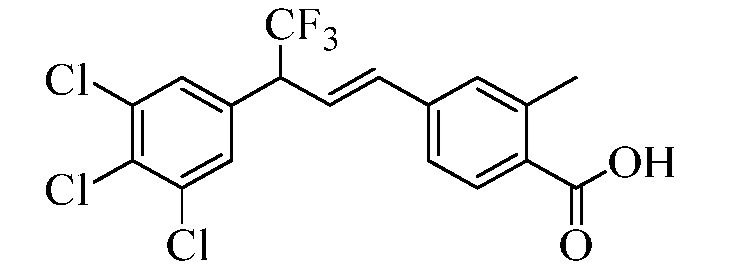
Продукт выделяли в виде светло-коричневой смолистой жидкости (1 г, 46%): 1H-ЯМР (400 МГц, CDCl3) δ 7,97 (д, J=8,0 Гц, 1H), 7,77 (с, 1H), 7,65 (м, 1H), 7,41 (с, 2H), 6,68 (д, J=16,0 Гц, 1H), 6,53 (дд, J=16,0, 8,0 Гц, 1H), 4,16 (м, 1H), 2,50 (с, 3H); ЭРИ-МС m/z 422,67 ([M-H]-).
(E)-2-Хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойная кислота (AI27)
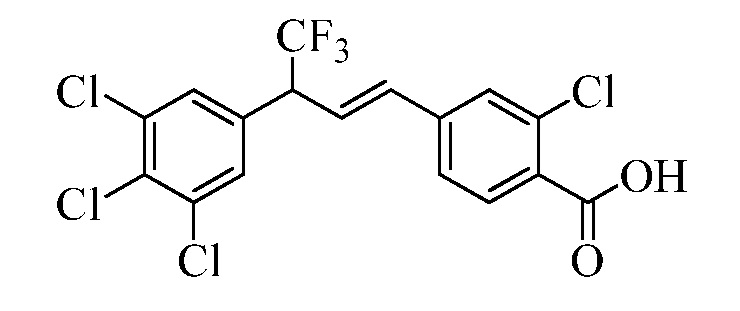
Продукт выделяли в виде грязно-белого полутвердого вещества (1 г, 45%): 1H-ЯМР (400 МГц, CDCl3) δ 7,99 (д, J=8,4 Гц, 1H), 7,50 (м, 1H), 7,40 (с, 1H), 7,36 (м, 2H), 6,59 (д, J=15,6 Гц, 1H), 6,48 (дд, J=15,6, 7,6 Гц, 1H), 4,14 (м, 1H); ЭРИ-МС m/z 442,72 ([M-H]-); ИК (тонкая пленка) 3472, 1704, 1113, 808 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойная кислота (AI28)
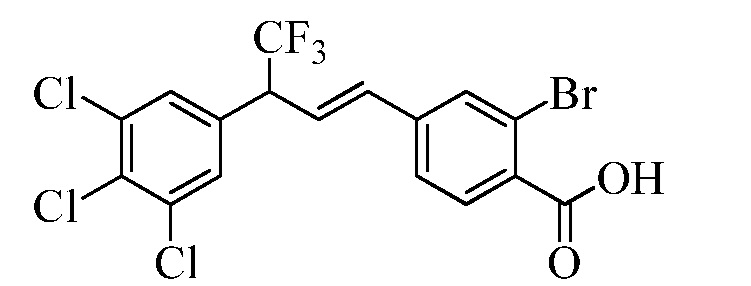
Продукт выделяли в виде коричневого твердого вещества (1 г, 45%): Т.пл. 70-71°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,99 (д, J=8,0 Гц, 1H), 7,72 (с, 1H), 7,40 (м, 3H), 6,58 (д, J=16,0 Гц, 1H), 6,48 (дд, J=16,0, 8,0 Гц, 1H), 4,14 (м, 1H); ЭРИ-МС m/z 484,75 ([M-H]-); ИК (тонкая пленка) 3468, 1700 см-1.
(E)-2-Циано-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойная кислота (AI29)
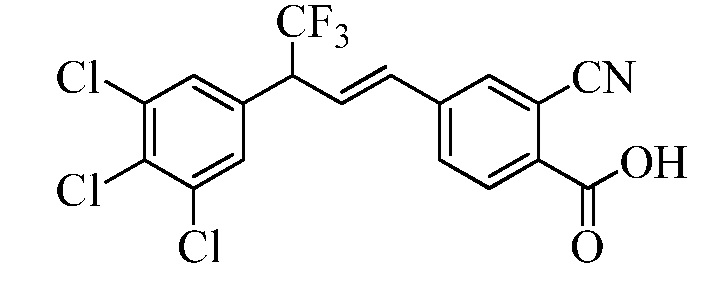
Продукт выделяли в виде грязно-белого твердого вещества (500 мг, 45%): Т.пл. 100-101°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,90 (с, 1H), 7,85 (д, J=7,6 Гц, 1H), 7,72 (д, J=8,0 Гц, 1H), 7,65 (шир. с, 1H), 7,42 (с, 2H), 6,73 (д, J=16,0 Гц, 1H), 6,58 (дд, J=16,0, 8,0 Гц, 1H), 4,19 (м, 1H); ЭРИ-МС m/z 431,93 ([M-H]-).
(E)-4-(3-(3,4-Дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензойная кислота (AI30)
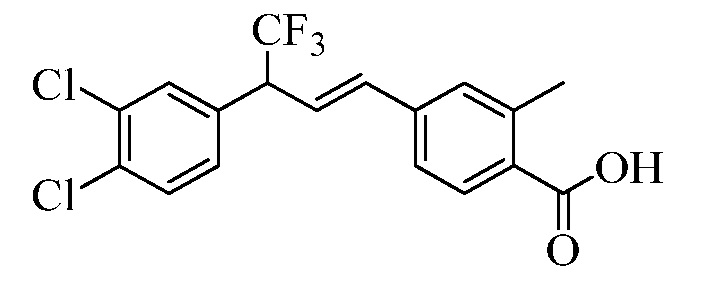
Продукт выделяли в виде светло-коричневой жидкости (500 мг, 46%): 1H-ЯМР (400 МГц, CDCl3) δ 8,03 (м, 1H), 7,49 (м, 2H), 7,29 (м, 1H), 7,22 (м, 2H), 6,73 (д, J=16,0 Гц, 1H), 6,58 (дд, J=16,0, 7,8 Гц, 1H), 4,16 (м, 1H), 2,64 (с, 3H); ЭРИ-МС m/z 386,84 ([M-H]-); ИК (тонкая пленка) 3428, 1690, 1113, 780 см-1.
(E)-4-(3-(3,5-Дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-2-метилбензойная кислота (AI31)
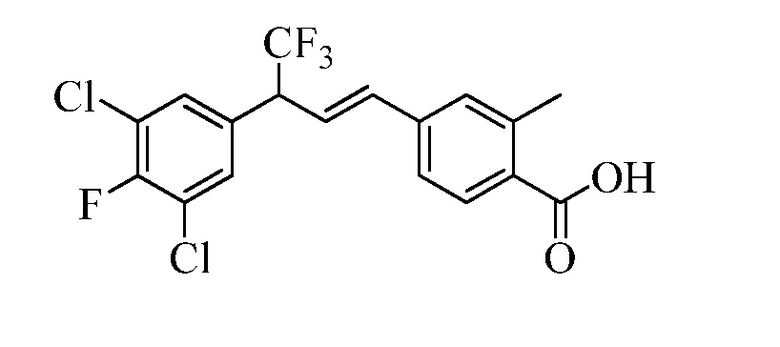
Продукт выделяли в виде белого твердого вещества (500 мг, 50%): 91-93°C Т.пл.; 1H-ЯМР (400 МГц, CDCl3) δ 8,02 (д, J=8,0 Гц, 1H), 7,35 (д, J=5,6 Гц, 1H), 7,30 (м, 3H), 6,61 (д, J=16,0 Гц, 1H), 6,48 (дд, J=16,0, 8,0 Гц, 1H), 4,13 (м, 1H), 2,65 (с, 3H); ЭРИ-МС m/z 406,87 ([M-H]-).
(E)-4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2-(трифторметил)бензойная кислота (AI33)
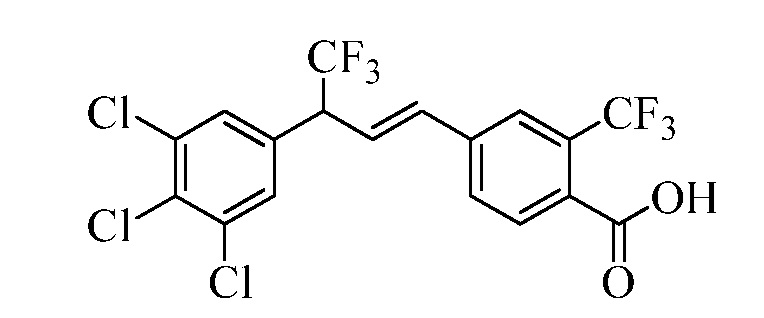
Продукт выделяли в виде белого твердого вещества (500 мг, 45%): Т.пл. 142-143°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,97 (д, J=8,0 Гц, 1H), 7,77 (с, 1H), 7,65 (м, 1H), 7,41 (с, 2H), 6,68 (д, J=16,0 Гц, 1H), 6,53 (дд, J=16,0, 8,0 Гц, 1H), 4,16 (м, 1H); ЭРИ-МС m/z 474,87 ([M-H]-).
(E)-2-Бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойная кислота (AI69)
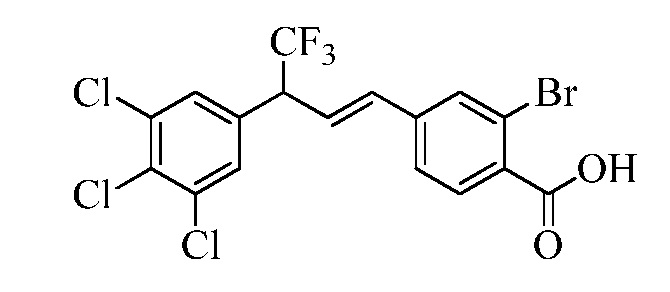
Указанное в заголовке соединение выделяли в виде коричневого твердого вещества (0,8 г, 28%): 1H-ЯМР (400 МГц, CDCl3) δ 13,42 (шир., 1H), 7,98 (д, J=1,5 Гц, 1H), 7,94 (м, 2H), 7,75 (д, J=8,1 Гц, 1H), 7,65 (м, 1H), 7,06 (дд, J=15,9, 9,0 Гц, 1H), 6,80 (д, J=15,9 Гц, 1H), 4,91 (м, 1H); ЭРИ-МС m/z 484,75 ([M-H]-); ИК (тонкая пленка) 3469, 1700 см-1.
(E)-2-Бром-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензойная кислота (AI70)
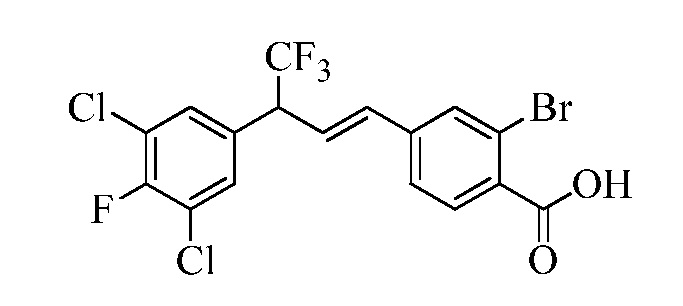
Указанное в заголовке соединение выделяли в виде желтой жидкости (0,3 г, неочищенная): 1H-ЯМР (300 МГц, CDCl3) δ 7,79 (д, J=8,1 Гц, 1H), 7,67 (с, 1H), 7,34 (м, 3H), 6,56 (д, J=15,9 Гц, 1H), 6,45 (дд, J=15,9, 7,6 Гц, 1H), 4,43 (м, 1H); ЭРИ-МС m/z 471,0 ([M-H]-).
(E)-4-(3-(3,5-Дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-2-этилбензойная кислота (AI71)
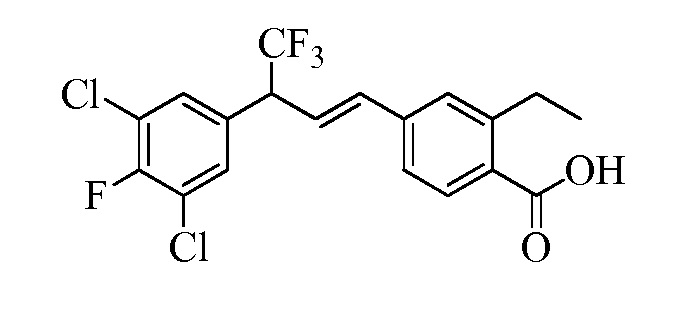
Указанное в заголовке соединение выделяли в виде коричневого смолистого материала (0,2 г, неочищенный): 1H-ЯМР (300 МГц, ДМСО-d6) δ 12,5 (шир., 1H), 7,85 (д, J=6,3 Гц, 2H), 7,75 (д, J=8,1 Гц, 1H), 7,52 (м, 2H), 6,96 (дд, J=8,7, 8,7 Гц, 1H), 6,78 (д, J=15,6 Гц, 1H), 4,80 (м, 1H), 4,06 (кв., J=7,2 Гц, 2H), 1,33 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 419,06 ([M-H]-).
(E)-2-Хлор-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензойная кислота (AI72)
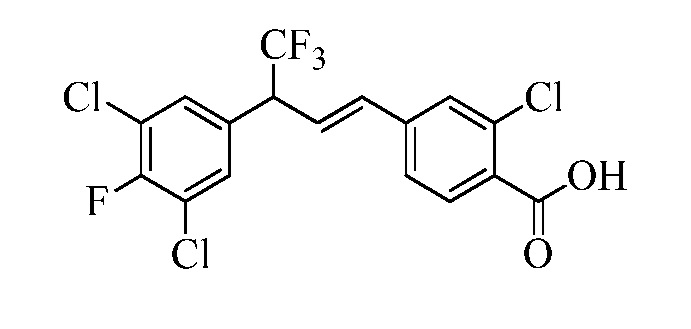
Указанное в заголовке соединение выделяли в виде желтой жидкости (0,7 г, 95%): 1H-ЯМР (300 МГц, CDCl3) δ 7,85 (д, J=6,0 Гц, 1H), 7,46 (д, J=1,8 Гц, 1H), 7,41 (с, 3H), 6,57 (д, J=16,0 Гц, 1H), 6,45 (дд, J=16,0, 8,0 Гц, 1H), 4,16 (м, 1H); ЭРИ-МС m/z 455,0 ([M+H]+); ИК (тонкая пленка) 1728, 1115, 817 см-1.
(E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-2-метилбензойная кислота (AI73)
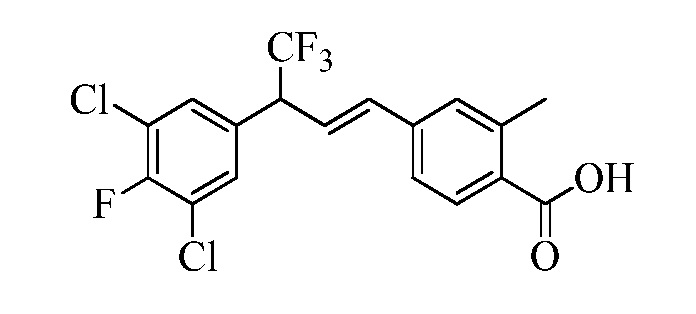
Указанное в заголовке соединение выделяли в виде светло-коричневого смолистого материала (0,7 г, 38%): Т.пл. 91-93°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,02 (д, J=8,0 Гц, 1H), 7,35 (д, J=5,6 Гц, 1H), 7,30 (м, 3H), 6,10 (д, J=16,0 Гц, 1H), 6,46 (дд, J=16,0, 8,0 Гц, 1H), 4,03 (м, 1H), 2,65 (с, 3H); ЭРИ-МС m/z 406,87 ([M-H]-).
(E)-4-(3-(3,5-Дихлорфенил)-4,4,4-трифторбут-1-енил)-2-фторбензойная кислота (AI74)
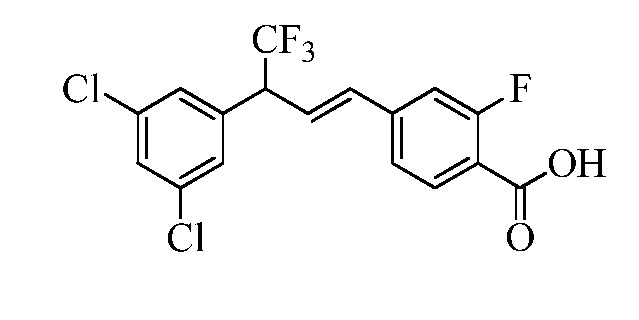
Указанное в заголовке соединение выделяли в виде светло-коричневой жидкости (0,3 г, неочищенная): ЭРИ-МС m/z 393,15 ([M-H]-).
(E)-2-Бром-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)бензойная кислота (AI75)
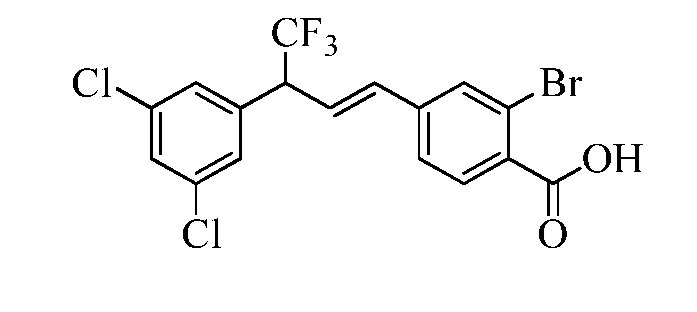
Указанное в заголовке соединение выделяли в виде светло-коричневой жидкости (0,35 г, неочищенная): ЭРИ-МС m/z 451,91 ([M-H]-).
(E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(метилтио)бензойная кислота

1H-ЯМР (400 МГц, CDCl3) δ 7,88-7,85 (м, 3H), 7,46 (д, J=6,8 Гц, 1H), 7,37 (с, 1H), 6,99 (дд, J=15,6, 8,8 Гц, 1H), 6,85 (д, J=16,0 Гц, 1H), 4,85-4,81 (м, 2H), 2,45 (с, 3H); ЭРИ-МС m/z 436,89 [(M-H)-]; ИК (тонкая пленка) 3469, 1686, 1259, 714 см-1.
(E)-2-Бром-4-(3-(3,5-дифтор-4-метоксифенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
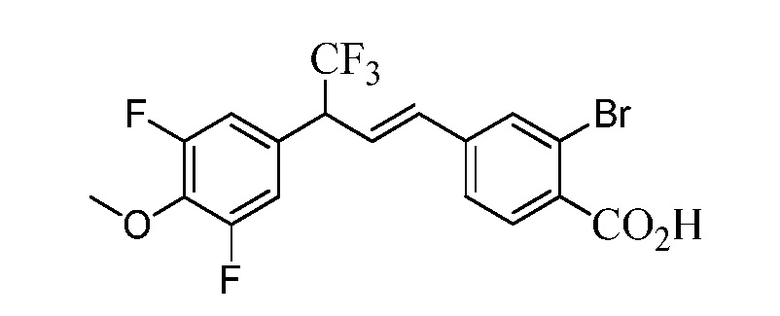
Молекула, указанная в заголовке, была выделена в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,48 (шир.с, 1H), 8,03 (с, 1H), 7,81 (д, J=7,8 Гц, 1H), 7,69 (д, J=8,1 Гц, 1H), 7,48 (д, J=9,3 Гц, 2H), 7,05 (дд, J=15,6, 9,0 Гц, 1H), 6,83 (д, J=15,9 Гц, 1H), 4,86-4,74 (м, 1H), 4,00 (с, 3H); ЭИ-МС m/z 451,18 ([М]+); ИК (тонкая пленка) 3431, 1132 см-1.
Предположительно, соединения AI34, AI36-AI41, AI44-AI45 (Таблица 1) могут быть получены в соответствии с методиками, раскрытыми в Примере 10 или Примерах 10 и 11.
Пример 12: Получение (E)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метил-N-(2,2,2-трифторэтил)бензамида (AC6)
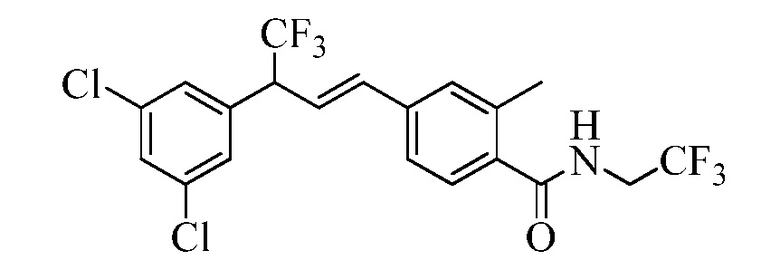
К перемешиваемому раствору (E)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензойной кислоты в ДМФА добавляли 2,2,2-трифторэтиламин, гидрат 1-гидроксибензотриазола (HOBt·H2O), гидрохлорид N-(3-диметиламинопропил)-N'-этилкарбодиимида (EDC·HCl) и N,N-диизопропилэтиламин (DIEA), и реакционную смесь перемешивали при 25°C в течение 18 ч. Реакционную смесь разбавляли H2O и экстрагировали EtOAc. Объединенный органический слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование гексаном:EtOAc) дала полутвердое белое вещество (110 мг, 50%): 1H-ЯМР (400 МГц, CDCl3) 7,40 (м, 2H), 7,26 (м, 3H), 6,56 (д, J=16,0 Гц, 1H), 6,48 (дд, J=16,0, 8,0 Гц, 1H), 5,82 (шир. с, 1H), 4,08 (м, 3H), 2,52 (с, 3H); ЭРИ-МС m/z 468,40 ([M-H]-); ИК (тонкая пленка) 1657, 1113, 804 см-1.
Соединения AC7-AC38, AC40-AC58, AC110-AC112, AC117 и AC118 (Таблица 1) были получены в соответствии с методиками, раскрытыми в Примере 12.
Пример 13: Получение 4-((E)-3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метил-N-((пиримидин-5-ил)метил)бензамида (AC39)
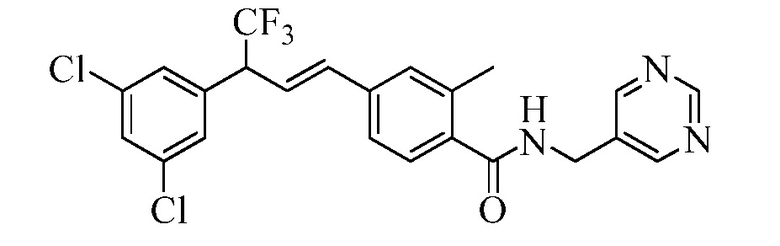
К перемешиваемому раствору (пиримидин-5-ил)метанамина (0,15 г, 1,43 ммоль) в CH2Cl2 (10 мл) по каплям добавляли триметилалюминий (2М раствор в толуоле; 0,71 мл, 1,43 ммоль) и реакционную смесь перемешивали при 25°C в течение 30 мин. К реакционной смеси по каплям при 25°C добавляли раствор этил-4-((E)-3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензо-ата (0,3 г, 0,71 ммоль) в CH2Cl2. Реакционную смесь перемешивали при кипении с обратным холодильником в течение 18 ч, охлаждали до 25°C, вливали 0,5Н раствор HCl (50 мл) и экстрагировали EtOAc (2×50 мл). Объединенные органические экстракты промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; элюция 40% EtOAc в н-гексане), получив указанное в заголовке соединение (0,18 г, 55%): Т.пл. 141-144°C; 1H (400 МГц, CDCl3) δ 9,19 (с, 1H), 8,79 (с, 2H), 7,37 (м, 2H), 7,23 (м, 2H), 7,21 (м, 1H), 6,57 (д, J=16,0 Гц, 1H), 6,40 (дд, J=16,0, 7,6 Гц 1H), 6,21 (м, 1H), 4,65 (с, 2H), 4,11 (м, 1H), 2,46 (с, 3H); ЭРИ-МС m/z 477,83 ([M-H]-).
Пример 14: Получение (E)-2-хлор-N-(2-оксо-2-((2,2,2-трифтор-этил)амино)этил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (AC64)
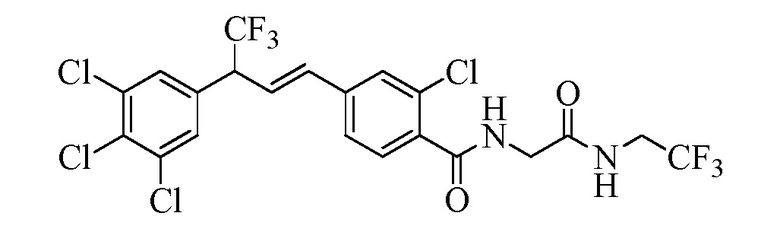
К перемешиваемому раствору глицинамида (0,15 г, 0,58 ммоль) в CH2Cl2 (5 мл) по каплям добавляли триметилалюминий (2М раствор в толуоле; 1,45 мл, 2,91 ммоль) и реакционную смесь перемешивали при 28°C в течение 30 мин. К реакционной смеси при 28°C по каплям добавляли раствор (E)-этил-2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензоата (0,3 г, 0,58 ммоль) в CH2Cl2 (5 мл). Реакционную смесь перемешивали при дефлегмации в течение 18 ч, охлаждали до 25°C, вливали 1Н раствор HCl (50 мл) и экстрагировали CH2Cl2 (2×50 мл). Объединенные органические экстракты промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; элюирование 40% EtOAc в н-гексане), получив указанное в заголовке соединение в виде желтого твердого вещества (0,15 г, 50%): Т.пл. 83-85°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,72 (д, J=8,0 Гц, 1H), 7,44 (с, 1H), 7,40 (с, 2H), 7,36 (д, J=6,8 Гц, 1H), 7,05 (т, J=5,2 Гц, 1H), 6,70 (т, J=5,2 Гц, 1H), 6,57 (д, J=15,6 Гц, 1H), 6,44 (дд, J=15,6, 8,0 Гц, 1H), 4,23 (д, J=5,6 Гц, 2H), 4,15 (м, 1H), 4,01 (м, 2H); ЭРИ-МС m/z 580,72 ([M-H]-).
Соединения AC59-AC75 (Таблица 1) были получены в соответствии с методиками, раскрытыми в Примере 14.
Пример 15: Получение (E)-2-бром-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-N-(2-оксо-2-((2,2,2-трифторэтил)амино)этил)бензамида (AC79)
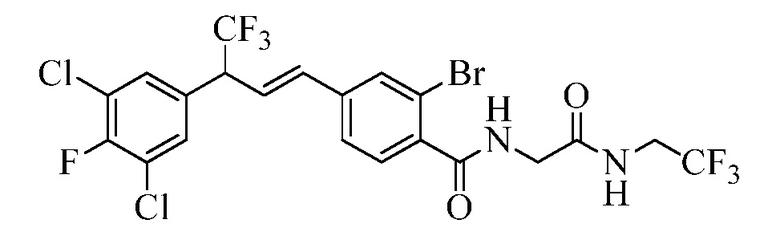
К перемешиваемому раствору (E)-2-бром-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)бензойной кислоты (300 мг, 0,638 ммоль) в ДХМ (5,0 мл) добавляли 2-амино-N-(2,2,2-трифторэтил)ацетамид (172 мг, 0,638 ммоль), затем гексафторфосфат бензотриазол-1-ил-окситрипирролидинофосфония (PyBOP) (364,5 мг, 0,701 ммоль) и DIPEA (0,32 мл, 1,914 ммоль), и перемешивали полученную реакционную смесь при КТ в течение 18 ч. Реакционную смесь разбавляли водой и экстрагировали ДХМ. Объединенный слой ДХМ промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 40% этилацетатом/петролейным эфиром) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (121 мг, 31%): 1H-ЯМР (400 МГц, CDCl3) δ 8,69 (т, J=6,0 Гц, 1H), 8,58 (т, J=6,0 Гц, 1H), 7,92 (с, 1H), 7,87 (д, J=6,4 Гц, 2H), 7,62 (д, J=8,4 Гц, 1H), 7,45 (д, J=8,4 Гц, 1H), 7,0 (м, 1H), 6,76 (д, J=15,6 Гц, 1H), 4,83 (т, J=8,0 Гц, 1H), 3,98 (м, 4H); ЭРИ-МС m/z 610,97 ([M+H]+); ИК (тонкая пленка) 3303, 1658, 1166, 817 см-1.
Соединения AC76-AC80, AC96-AC102 и AC113 (Таблица 1) были получены в соответствии с методиками, раскрытыми в Примере 15.
Пример 16: Получение (E)-4-(3-(3,5-дихлорфенил)-4,4,4-трифтор-бут-1-ен-1-ил)-N-(1,1-диоксидотиетан-3-ил)-2-фторбензамида (AC83)
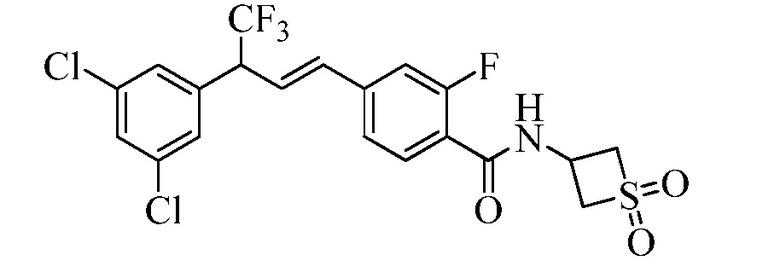
К перемешиваемому раствору (E)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-фтор-N-(тиетан-3-ил)бензамида (100 мг, 0,2159 ммоль) в ацетоне/воде (1:1, 5,0 мл) добавляли оксон (266 мг, 0,4319 ммоль) и перемешивали полученную реакционную смесь при КТ в течение 4 ч. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Объединенный этилацетатный слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 30% этилацетатом/петр. эфиром) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (70,0 мг, 66%): 1H-ЯМР (400 МГц, CDCl3) δ 8,07 (т, J=8,4 Гц, 1H), 7,39 (т, J=1,6 Гц, 1H), 7,31 (д, J=1,2 Гц, 1H), 7,26 (м, 2H), 7,23 (м, 2H), 7,19 (д, J=1,6 Гц, 1H), 6,60 (д, J=16,8 Гц, 1H), 6,49 (дд, J=16,8, 7,6 Гц, 1H), 4,90 (м, 1H), 4,64 (м, 2H), 4,14 (м, 2H); ЭРИ-МС m/z 493,83 ([M-H]-); ИК (тонкая пленка) 1527, 1113, 801, 1167, 1321 см-1.
Соединения AC81-AC87 (Таблица 1) были получены в соответствии с методиками, раскрытыми в Примере 16.
Пример 17: Получение (E)-N-((5-циклопропил-1,3,4-оксадиазол-2-ил)метил)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-метилбензамида (AC89)
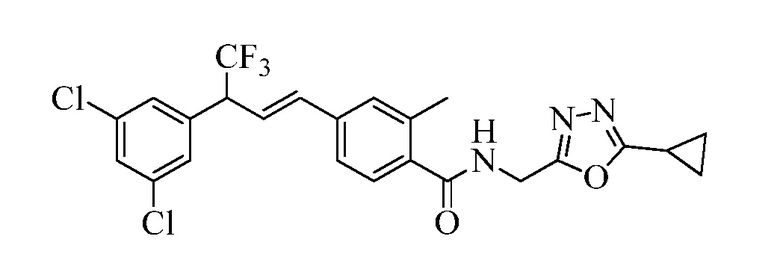
Раствор (E)-N-(2-(2-(циклопропанкарбонил)гидразинил)-2-оксоэтил)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензамида (200 мг, 0,379 ммоль) в POCl3 (2,0 мл) перемешивали при КТ в течение 10 минут, затем полученную реакционную смесь нагревали до 50°C в течение 1 ч. В реакционную смесь вливали воду со льдом при 0°C и экстрагировали этилацетатом. Объединенный этилацетатный слой промывали насыщенным раствором NaHCO3 и солевым раствором, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 50% этилацетатом/петр. эфиром) дала указанное в заголовке соединение в виде светло-коричневого смолистого материала (70,0 мг, 36%): 1H-ЯМР (400 МГц, CDCl3) δ 7,43 (м, 2H), 7,27 (м, 2H), 7,23 (м, 2H), 6,58 (д, J=16,0 Гц, 1H), 6,41 (дд, J=16,0, 7,6 Гц, 1H), 4,79 (д, J=5,6 Гц, 2H), 4,14 (м, 1H), 2,48 (с, 3H), 2,18 (м, 1H), 1,16 (м, 4H); ЭРИ-МС m/z 509,89 ([M+H]+); ИК (тонкая пленка) 1666, 1166, 1112, 800 см-1.
Пример 18: Получение (E)-2-бром-N-(2-тиоксо-2-((2,2,2-трифтор-этил)амино)этил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензотиоамида (AC90)
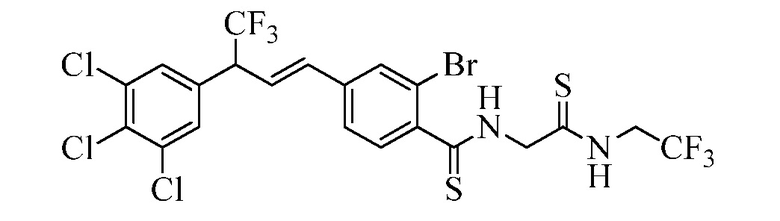
К перемешиваемому раствору (E)-2-бром-N-(2-оксо-2-((2,2,2-трифторэтил)амино)этил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфе-нил)бут-1-ен-1-ил)бензамида (400 мг, 0,638 ммоль) в 5 мл ТГФ при КТ добавляли 2,4-бис(4-метоксифенил)-1,3,2,4-дитиадифосфетан-2,4-дисульфид (реагент Лавессона) (336 мг, 0,830 ммоль) одной порцией. Полученную реакционную смесь перемешивали в течение 18 ч. ТСХ показала, что реакция прошла неполностью, поэтому добавляли дополнительное количество реагента Лавессона (168 мг, 0,415 ммоль) и перемешивали реакцию в течение 48 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 230-400 меш; элюирование 20% EtOAc в смеси гексанов) дала указанное в заголовке соединение в виде желтого стеклообразного масла (188 мг, 44,7%): 1H-ЯМР (400 МГц, CDCl3) δ 8,34 (м, 1H), 8,27 (м, 1H), 7,60 (д, J=1,6 Гц, 1H), 7,49 (д, J=8,0 Гц, 2H), 7,40 (с, 2H), 7,36 (дд, J=8,2, 1,7 Гц, 1H), 6,53 (д, J=16,0 Гц, 1H), 6,38 (дд, J=15,9, 7,9 Гц, 1H), 4,89 (д, J=8,4, 5,5 Гц, 2H), 4,48 (кв.д, J=9,0, 6,0 Гц, 2H), 4,11 (м, 1H); ЭРИ-МС m/z 656,9 ([M-H]-).
Пример 19: Получение (E)-2-(2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенилтиоамидо)-N-(2,2,2-трифтор-этил)ацетамида (AC91)
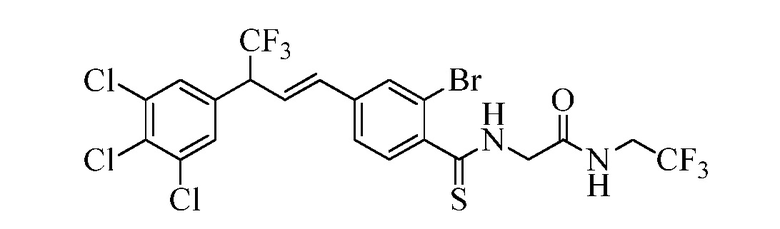
К перемешиваемому раствору (E)-2-бром-N-(2-оксо-2-((2,2,2-трифторэтил)амино)этил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфе-нил)бут-1-ен-1-ил)бензамида (400 мг, 0,638ммоль) в 5 мл ТГФ при КТ добавляли реагент Лавессона (64,5 мг, 0,160 ммоль) одной порцией. Полученную реакционную смесь перемешивали в течение 18 ч, после чего реакционную смесь выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 230-400 меш; элюирование 20% EtOAc в смеси гексанов) дала указанные в заголовке соединения в виде желтого масла (18,5 мг, 4,51%): 1H-ЯМР (400 МГц, CDCl3) δ 8,18 (т, J=5,0 Гц, 1H), 7,58 (д, J=1,6 Гц, 1H), 7,47 (д, J=8,0 Гц, 1H), 7,40 (с, 2H), 7,34 (дд, J=8,1, 1,6 Гц, 1H), 6,52 (м, 2H), 6,37 (дд, J=15,9, 7,9 Гц, 1H), 4,54 (д, J=4,9 Гц, 2H), 4,12 (м, 1H), 3,99 (кв.д, J=8,9, 6,5 Гц, 2H); ЭРИ-МС m/z 640,9 ([M-H]-).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 19.
(E)-2-Бром-N-(2-тиоксо-2-((2,2,2-трифторэтил)амино)этил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамид (AC92)
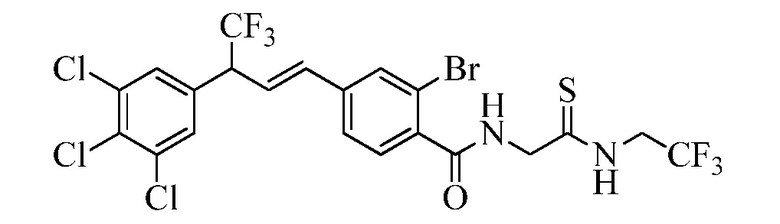
Продукт выделяли в виде бесцветного масла (17,9 мг, 4,36%): 1H-ЯМР (400 МГц, CDCl3) δ 9,16 (д, J=6,1 Гц, 1H), 7,65 (д, J=1,6 Гц, 1H), 7,57 (д, J=8,0 Гц, 1H), 7,41 (м, 3H), 7,21 (т, J=5,6 Гц, 1H), 6,55 (д, J=15,9 Гц, 1H), 6,41 (дд, J=15,9, 7,8 Гц, 1H), 4,59 (д, J=5,6 Гц, 2H), 4,45 (кв.д, J=9,0, 6,0 Гц, 2H), 4,12 (кв., J=7,2 Гц, 1H); ЭРИ-МС m/z 640,9 ([M-H]-).
Пример 106: Получение этил-(Z)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензоата (AI76)

Указанное в заголовке соединение получали в соответствии с методикой, раскрытой в Примере 88, и выделяли в виде вязкого желтого масла (416 мг, 23%): 1H-ЯМР (400 МГц, CDCl3) δ 7,80 (д, J=8,0 Гц, 1H), 7,40 (д, J=1,7 Гц, 1H), 7,35 (с, 2H), 7,12 (дд, J=8,0, 1,7 Гц, 1H), 6,86 (д, J=11,4 Гц, 1H), 6,23-5,91 (м, 1H), 4,42 (кв., J=7,1 Гц, 2H), 4,33-4,10 (м, 1H), 1,42 (т, J=7,2 Гц, 3H); 19F-ЯМР (376 МГц, CDCl3) δ-69,34 (д, J=8,3 Гц); ЭИ-МС m/z 514,10 ([М,]-); ИК (тонкая пленка) 2983, 1727, 1247, 1204, 1116 см-1.
Пример 107: Получение (Z)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензойной кислоты (AI77)
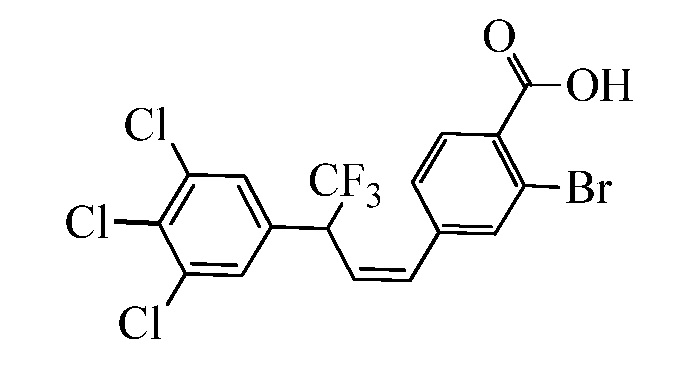
К перемешиваемому раствору (Z)-этил-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензоата (360 мг, 0,70 ммоль) в CH3CN (1,0 мл) добавляли иодтриметилсилан (0,28 мл, 2,8 ммоль). Реакционную смесь нагревали с обратным холодильником до кипения в течение 20 ч, позволяли охладиться до температуры окружающей среды и делили между CH2Cl2 и 10% водн. раствором Na2S2O3. Органическую фазу один раз промывали 10% водн. раствором Na2S2O3, сушили над MgSO4 и выпаривали в вакууме. Пропускание материала через слой силикагеля с использованием 10% EtOAc в смеси гексанов и затем 20% MeOH в CH2Cl2 в качестве элюирующих растворителей дало указанное в заголовке соединение в виде желтой пены (143 мг, 42%): 54-64°C Т.пл.; 1H-ЯМР (400 МГц, CDCl3) δ 11,36 (с, 1H), 7,99 (д, J=8,0 Гц, 1H), 7,43 (с, 1H), 7,30 (с, 2H), 7,14 (д, J=7,9 Гц, 1H), 6,85 (д, J=11,4 Гц, 1H), 6,15 (т, J=10,9 Гц, 1H), 4,36-4,09 (м, 1H); 19F-ЯМР (376 МГц, CDCl3) δ -69,30.
Пример 108: Получение (Z)-2-бром-N-(2-оксо-2-((2,2,2-трифторэтил)амино)этил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфе-нил)бут-1-ен-1-ил)бензамида (AC95)
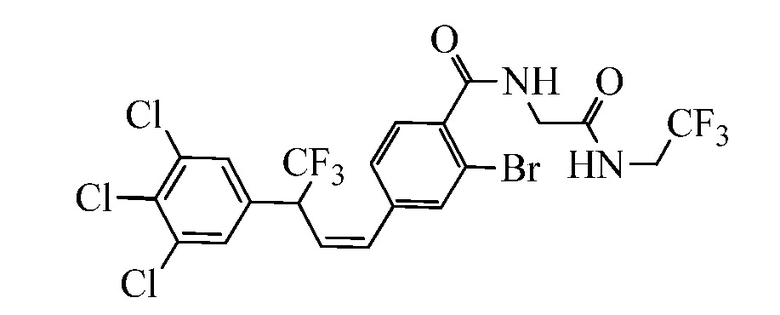
К перемешиваемому раствору (Z)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензойной кислоты (200 мг, 0,41 ммоль) в безводном ТГФ (5,0 мл) добавляли карбонилдиимида-зол (82 мг, 0,51 ммоль). Смесь нагревали при 50°C в масляной бане в течение 1,5 ч, обрабатывали гидрохлоридом 2-амино-н-(2,2,2-трифторэтил)ацетамида (109 мг, 0,57 ммоль) и нагревали полученную смесь с обратным холодильником до кипения в течение 8 ч. После охлаждения до температуры окружающей среды смесь собирали в Et2O и дважды промывали 5% водн. раствором NaHSO4 (2×) и один раз нас. NaCl (1×). После сушки над MgSO4, выпаривания в вакууме и очистки с помощью хроматографии среднего давления на силикагеле с использованием EtOAc/смеси гексанов в качестве растворителей для элюирования, указанное в заголовке соединение получали в виде белой пены (160 мг, 41%) 48-61°C Т.пл.: 1H-ЯМР (400 МГц, CDCl3) δ 7,58 (д, J=7,9 Гц, 1H), 7,44-7,29 (м, 3H), 7,14 (дд, J=7,9, 1,6 Гц, 1H), 6,86 (д, J=11,4 Гц, 1H), 6,76 (т, J=5,9 Гц, 1H), 6,59 (шир. с, 1H), 6,21-6,04 (м, 1H), 4,23 (д, J=5,5 Гц, 1H), 3,98 (кв.д, J=9,0, 6,5 Гц, 2H); 19F-ЯМР (376 МГц, CDCl3) δ -69,31,-72,3; ЭИ-МС m/z 626,9 ([M+1] +).
Пример 109a: Получение (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (AC114)
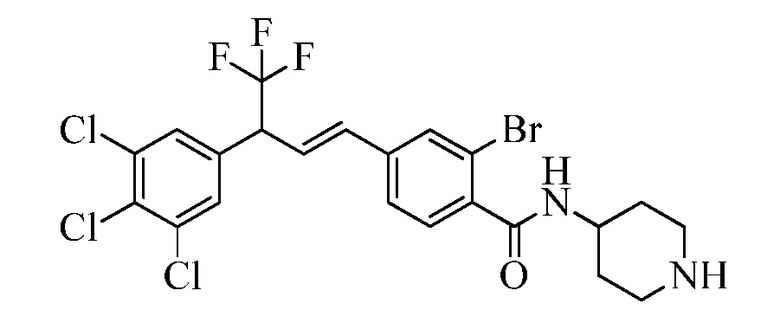
(E)-трет-бутил-4-(2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-енил)бензамидо)пиперидин-1-карбоксилат (0,75 г, 1,11 ммоль) добавляли к HCl в диоксане (10 мл) при 0°C и перемешивали в течение 18 ч. Реакционную смесь выпаривали при пониженном давлении и растирали с диэтиловым эфиром, получив соединение в виде светло-коричневого твердого вещества (0,6 г, 88%).
Пример 109b: Получение (E)-N-(1-ацетилпиперидин-4-ил)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (AC103)
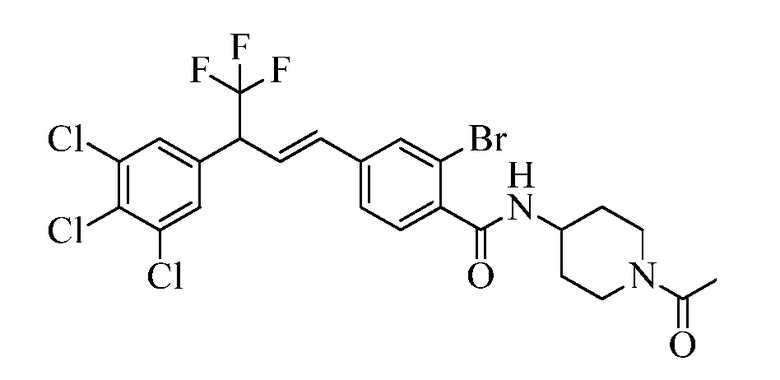
К перемешиваемому раствору (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамида (0,1 г, 0,16 ммоль) в ДХМ (10,0 мл) добавляли триэтиламин (0,046 мл, 0,35 ммоль) и перемешивали в течение 10 мин. Затем добавляли ацетилхлорид (0,014, 0,18 ммоль) и перемешивали в течение 16 ч при КТ. Реакционную смесь разбавляли ДХМ и промывали насыщенным раствором NaHCO3 и солевым раствором. Объединенный слой ДХМ сушили над Na2SO4 и выпаривали при пониженном давлении с получением неочищенного соединения. Неочищенное соединение промывали 5% диэтиловым эфиром/н-пентаном, получив указанное в заголовке соединение в виде белого твердого вещества (0,054 г, 50%).
Пример 110: Получение (E)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-N-(1-(3,3,3-трифторпропано-ил)пиперидин-4-ил)бензамида (AC104)
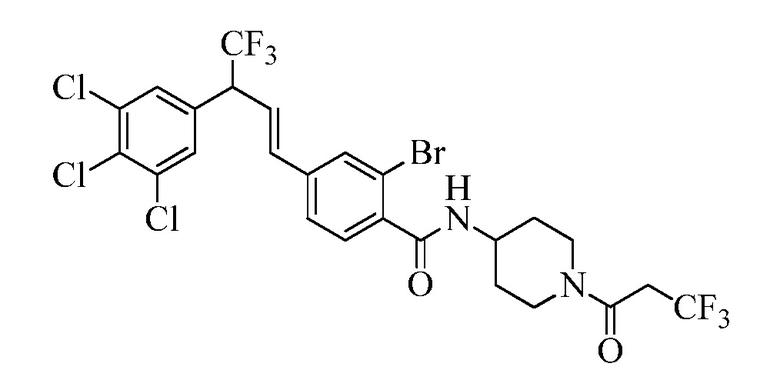
К перемешиваемому раствору 3,3,3-трифторпропановой кислоты (0,02 г, 0,16 ммоль) в ДХМ (10,0 мл) при КТ добавляли (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфе-нил)бут-1-енил)бензамид (0,1 г, 0,16 ммоль), PYBOP (0,09 г, 0,17 ммоль) и DIPEA (0,06 г, 0,48 ммоль). Реакционную смесь перемешивали при КТ в течение 5 ч. Реакционную смесь разбавляли ДХМ. Объединенный слой ДХМ промывали 3Н HCl и насыщенным раствором NaHCO3, отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении с получением неочищенного соединения. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; элюирование 2% метанолом в ДХМ), получив указанное в заголовке соединение в виде грязно-белого смолистого материала (0,035 г, 29%).
Пример 111: Получение (E)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-N-(1-(2,2,2-трифторэтил)пиперидин-4-ил)бензамида (AC105)
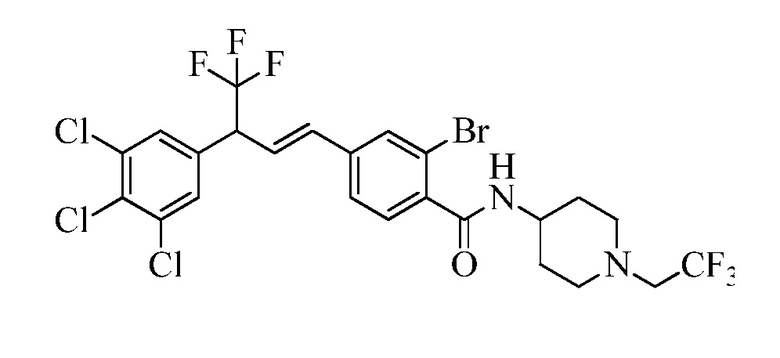
К перемешиваемому раствору (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамида (0,1 г, 0,16 ммоль) в ТГФ (5,0 мл) добавляли триэтиламин (0,06 мл, 0,64 ммоль) и перемешивали в течение 10 мин. Затем добавляли 2,2,2-трифторэтил-трифторметансульфонат (0,03, 0,16 ммоль) и перемешивали в течение 16 ч при КТ. Реакционную смесь разбавляли этилацетатом и промывали насыщенным раствором NaHCO3 и солевым раствором. Объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении с получением указанного в заголовке соединения в виде коричневого твердого вещества (0,05 г, 44%).
Пример 112: Получение (E)-2-бром-N-(1-метилпиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (AC106)
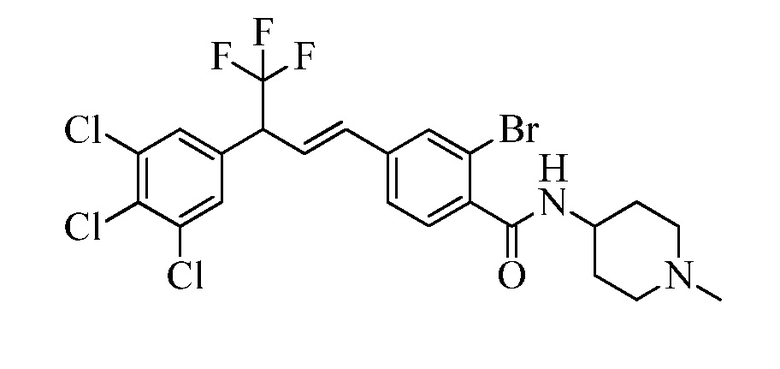
Раствор (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамида (0,1 г, 0,16 ммоль), формальдегида (30% в воде) (0,1 мл, 0,16 ммоль) и уксусной кислоты (0,01 мл) в метаноле (5,0 мл) перемешивали при КТ в течение 30 мин. После добавления NaBH3CN (0,01 г, 0,16 ммоль) при 0°C реакцию перемешивали в течение 8 ч при КТ. Растворитель удаляли при пониженном давлении, получив остаток, который разбавляли этилацетатом и промывали насыщенным водн. раствором NaHCO3 и солевым раствором. Объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении, получив остаток, который растирали с диэтиловым эфиром/пентаном, получив указанное в заголовке соединение в виде светло-желтого смолистого материала (0,06 г, 59%).
Пример 113: Получение ((E)-2-бром-N-(1-(цианометил)пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (AC107)
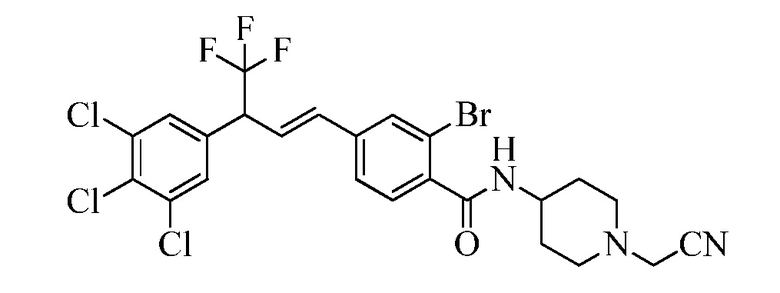
К перемешиваемому раствору (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамида (0,25 г, 0,43 ммоль) в ТГФ (10,0 мл) добавляли триэтиламин (0,16 мл, 1,29 ммоль) и реакцию перемешивали в течение 10 мин. Затем добавляли 2-бромацетонитрил (0,07, 0,65 ммоль) и перемешивали реакцию в течение 8 ч при КТ. Реакционную смесь разбавляли этилацетатом и промывали насыщенным солевым раствором. Объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (0,125 г, 46,8%).
Пример 114: Получение (E)-2-бром-N-(1-(оксетан-3-ил) пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамид (AC108)
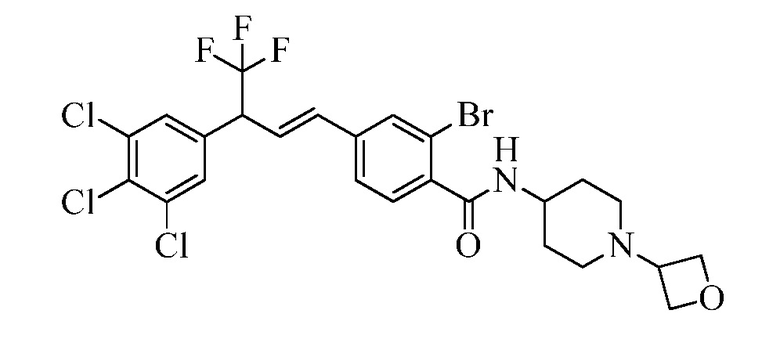
Раствор (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамида (0,2 г, 0,35 ммоль), оксетан-3-она (0,027 г, 0,38 ммоль) и уксусной кислоты (0,01 мл) в метаноле (5,0 мл) перемешивали при КТ в течение 30 мин. После этого при 0°C медленно, в течение 10 минут, порциями добавляли NaBH3CN (0,022 г, 0,35 ммоль) и реакцию перемешивали в течение 8 ч при КТ. Растворитель удаляли при пониженном давлении, получив остаток, который разбавляли этилацетатом и промывали насыщенным раствором NaHCO3 и солевым раствором. Объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении с получением остатка, который растирали с диэтиловым эфиром/пентаном, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (0,05 г, 23%).
Пример 115: Получение (E)-2-бром-N-(1-пиперидин-4-ил (с 2 оксиэтилами))-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (AC109)
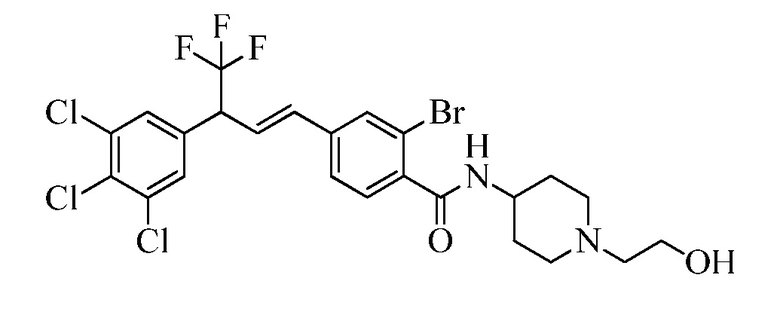
К перемешиваемому раствору (E)-2-бром-N-(пиперидин-4-ил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамида (0,25 г, 0,43 ммоль) в ТГФ (10,0 мл) добавляли триэтиламин (0,16 мл, 1,29 ммоль) и реакцию перемешивали в течение 10 мин. Затем добавляли 2-хлорэтанол (0,05, 0,65 ммоль) и реакцию перемешивали в течение 8 ч при КТ. Реакционную смесь разбавляли этилацетатом и промывали насыщенным солевым раствором. Объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (0,09 г, 34%).
Пример 116: Получение (E)-2-(2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамидо)уксусной кислоты (AI78)
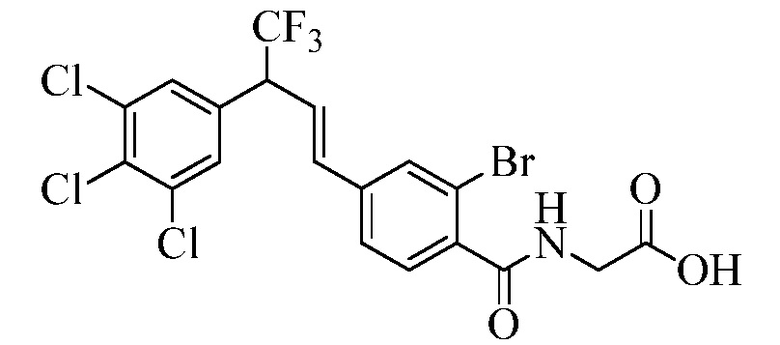
К перемешиваемому раствору (E)-трет-бутил-2-(2-бром-4- (4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензамидо)ацета-та (440 мг, 0,734 ммоль) в ДХМ (36,0 мл) добавляли ТФУ (4,0 мл) и перемешивали реакционную смесь при КТ в течение 1 ч. Реакционную смесь выпаривали при пониженном давлении с получением остатка, который промывали н-пентаном, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (310 мг, 78%): 1H-ЯМР (400 МГц, CDCl3) δ 13,0 (с, 1H), 8,75 (т, J=5,7 Гц, 1H), 7,93 (м, 2H), 7,62 (д, J=7,5 Гц, 1H), 7,40 (д, J=8,1 Гц, 1H), 6,96 (дд, J=15,3, 9,3 Гц, 1H), 6,78 (д, J=15,3 Гц, 1H), 4,83 (м, 1H), 3,90 (д, J=5,7 Гц, 2H); ЭРИ-МС m/z 543,61 ([M+H]+); ИК (тонкая пленка) 3429, 1635, 1114, 772 см-1.
Пример 117: Получение (E)-N-((6-хлорпиридин-3-ил)метил)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-метилбензотио-амида (AC115)
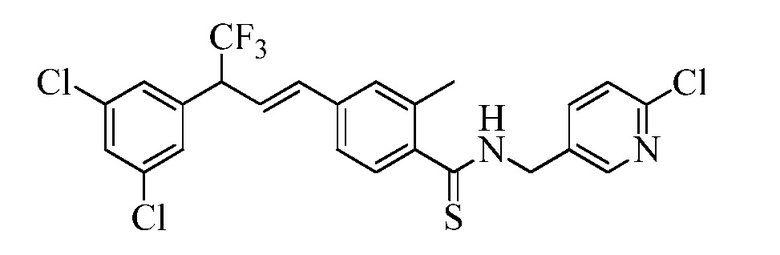
К перемешиваемому раствору (E)-N-((6-хлорпиридин-3-ил)метил)-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)-2-метилбензамида (0,06 г, 0,117 ммоль) в толуоле (3 мл) добавляли реагент Лавессона (0,14 г, 0,351 ммоль) и реакцию облучали при 100°C в течение 1 ч, затем охлаждали до КТ и выпаривали при пониженном давлении с получением неочищенного соединения. Неочищенный продукт очищали с помощью препаративной ВЭЖХ, получив продукт в виде желтого твердого вещества (0,03 г, 49%).
Пример 118: Получение (E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-N-(2-оксо-2-((2,2,2-трифторэтил)ами-но)этил)-2-(трифторметокси)бензамида (AC116)
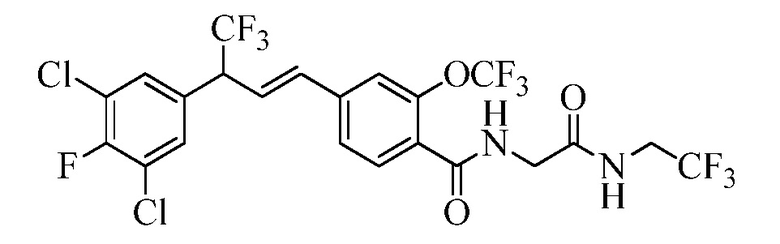
Стадия 1. 2-(Трифторметокси)-4-винилбензойная кислота (AI79): К перемешиваемому раствору 4-бром-2-(трифторметокси)бензойной кислоты (1 г, 3,67 ммоль) в ДМСО (20 мл) добавляли винилтрифторборат калия (1,47 г, 11,02 ммоль) и карбонат калия (1,52 г, 11,02 ммоль). Реакционную смесь дегазировали аргоном в течение 30 мин. добавляли дихлорид бистрифенилфосфин(дифенил-фосфиноферроцен)палладия (0,13 г, 0,18 ммоль) и реакционную смесь нагревали до 80ºC в течение 1 ч. Реакционную смесь разбавляли водой (100 мл), экстрагировали этилацетатом (2×50 мл), промывали рассолом и сушили над Na2SO4. После выпаривания при пониженном давлении получали неочищенное соединение, которое очищали с помощью колоночной флеш-хроматографии, получив продукт в виде бледно-желтого смолистого материала (0,4 г, 47%): 1H-ЯМР (400 МГц, CDCl3) δ 8,05 (д, J=8,1 Гц, 1H), 7,44 (д, J=1,8 Гц, 1H), 7,35 (с, 1H), 6,78 (дд, J=17,4,1, 11,1 Гц, 1H), 5,92 (д, J=17,4 Гц, 1H), 5,51 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 232,97 ([M+H]+).
Стадия 2. (E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифтор-бут-1-енил)-2-(трифторметокси)бензойная кислота (AI80): К перемешиваемому раствору 2-(трифторметокси)-4-винилбензойной кислоты (0,356 г, 1,53 ммоль) в 1Н метилпирролидине (5,0 мл) добавляли 1-(1-бром-2,2,2-трифторэтил)-3,5-дихлор-4-фторбензол (1,0 г, 3,07 ммоль), хлорид меди (I) (CuCl; 0,03 г, 0,307 ммоль) и 2,2-бипиридил (0,095 г, 0,614 ммоль). Реакционную смесь перемешивали при 150°C в течение 1 ч. После того, как реакция завершилась согласно ТСХ, реакционную смесь разбавляли водой (100 мл) и экстрагировали этилацетатом (2×50 мл). Объединенные органические слои промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении с получением неочищенного соединения, которое очищали с помощью колоночной флеш-хроматографии, получив продукт в виде бледно-желтого смолистого материала (0,3 г, 21%): 1H-ЯМР (400 МГц, CDCl3) δ 8,08 (д, J=8,0 Гц, 1H), 7,45 (д, J=1,6 Гц, 1H), 7,35 (с, 3H), 6,63 (д, J=16,0 Гц, 1H), 6,50 (дд, J=16,0, 8,0 Гц, 1H), 4,15 (м, 1H); ЭРИ-МС m/z 474,81 ([M-H]-).
Стадия 3. (E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифтор-бут-1-енил)-N-(2-оксо-2-(2,2,2-трифторэтиламино)этил)-2- (трифторметокси)бензамид (AC116): Смесь (E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-2-(трифторметокси)бензойной кислоты (0,25 г, 0,52 ммоль), 2-амино-N-(2,2,2-трифторэтил)ацет-амида (0,158 г, 0,62 ммоль), PyBOP (0,40 г, 0,78 ммоль) и DIPEA (0,134 г, 1,04 ммоль) в ДХМ (10,0 мл) перемешивали при КТ в течение 16 ч. Реакционную смесь разбавляли водой и экстрагировали ДХМ. Объединенный слой ДХМ промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 20% этилацетатом/петр. эфиром) дала указанное в заголовке соединение в виде бледно-желтого смолистого материала (0,15 г, 47%).
Следующие молекулы были получены в соответствии с методиками, раскрытыми в Примере 118, Стадия 2:
(E)-4-(3-(3,5-Дибромфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-метил-бензойная кислота
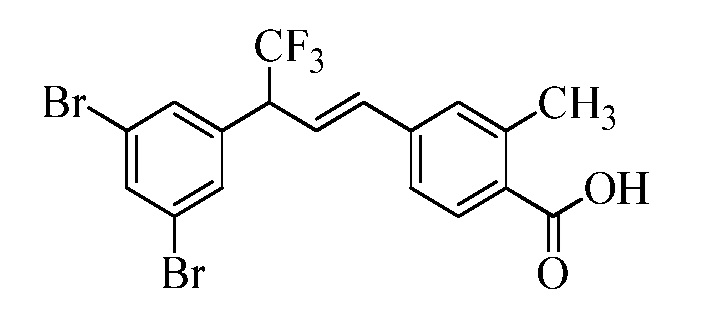
Молекула, указанная в заголовке, была выделена в виде твердого коричневого вещества: 1H-ЯМР (400 МГц, ДМСО-d6) δ 12,90 (шир.с, 1H), 7,85 (с, 1H), 7,78-7,75 (м, 3H), 7,47-7,41 (м, 2H), 6,89 (дд, J=15,6, 9,2 Гц, 1H), 6,72 (д, J=15,6 Гц, 1H), 4,80-4,75 (м, 1H), 2,33 (с, 3H); ЭРИ-МС m/z 474,90 ([M-H]-); ИК (тонкая пленка) 3437, 1689, 1165, 579 см-1.
(E)-4-(3-(3,5-Дибромфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
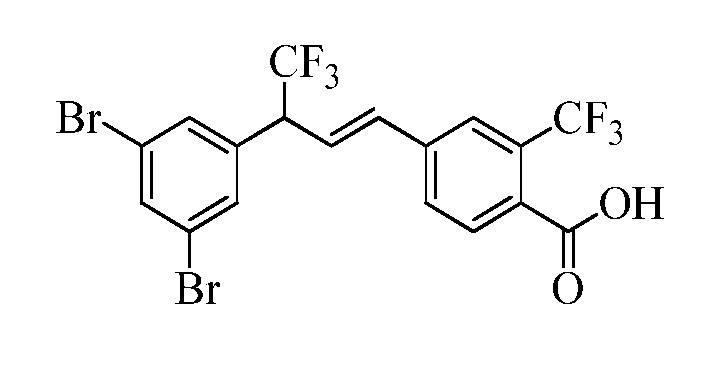
Молекула, указанная в заголовке, была выделена в виде твердого коричневого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,5 (шир.с, 1H), 8,03 (с, 1H), 7,95-7,85 (м, 4H), 7,81 (д, J=7,8 Гц, 1H), 7,14 (дд, J=15,6, 9,6 Гц, 1H), 6,90 (д, J=15,9 Гц, 1H), 4,86-4,79 (м, 1H); ЭРИ-МС m/z 528,82 ([M-H]+); ИК (тонкая пленка) 3437, 1707, 1153, 555 см-1.
(E)-2-Бром-4-(3-(3,5-дибромфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
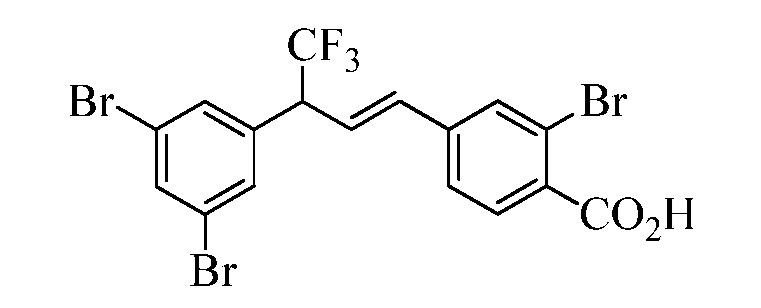
Молекула, указанная в заголовке, была выделена в виде коричневой жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,90 (шир.с, 1H), 7,98 (с, 1H), 7,88 (с, 1H), 7,84 (с, 2H), 7,74 (д, J=7,6 Гц, 1H), 7,64 (д, J=8,8 Гц, 1H), 7,04 (дд, J=15,6, 8,8 Гц, 1H), 6,78 (д, J=15,6 Гц, 1H), 4,80-4,78 (м, 1H); ЭРИ-МС m/z 538,74 ([M-H]-); ИК (тонкая пленка) 3424, 1695, 1168, 578 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(3-фтор-5-(трифторметил)фенил)бут-1-ен-1-ил)бензойная кислота
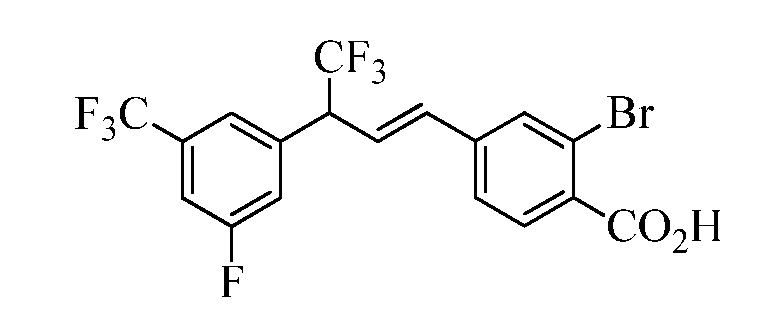
Молекула, указанная в заголовке, была выделена в виде коричневой жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,3 (шир.с, 1H), 7,93 (с, 1H), 7,82-7,77 (м, 2H), 7,72-7,66 (м, 2H), 7,59 (д, J=8,0 Гц, 1H), 7,03 (дд, J=15,6, 9,2 Гц, 1H), 6,76 (д, J=15,6 Гц, 1H), 4,94-4,90 (м, 1H); ЭРИ-МС m/z 469,02 ([M-H]-); ИК (тонкая пленка) 3444, 1704, 1172, 513 см-1.
(E)-4-(3-(3,5-Бис(трифторметил)фенил)-4,4,4-трифторбут-1-ен-1-ил)-2-бромбензойная кислота
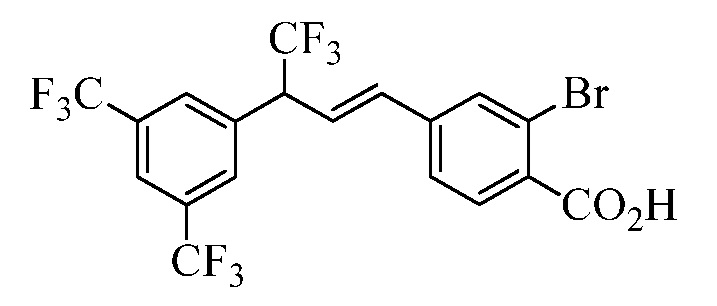
Молекула, указанная в заголовке, была выделена в виде твердого коричневого вещества: 1H-ЯМР (400 МГц, CDCl3) δ 7,98 (д, J=7,6 Гц, 1H), 7,92 (с, 1H), 7,83 (с, 2H), 7,73 (д, J=1,6 Гц, 1H), 7,42-7,40 (м, 1H), 6,62 (д, J=16,4 Гц, 1H), 6,55 (дд, J=16,0, 8,0 Гц, 1H), 4,40-4,30 (м, 1H); ЭРИ-МС m/z 518,94 ([M-H]-); ИК (тонкая пленка) 3447, 1705, 1171, 526 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(3-(трифторметил)фенил)бут-1-ен-1-ил)бензойная кислота
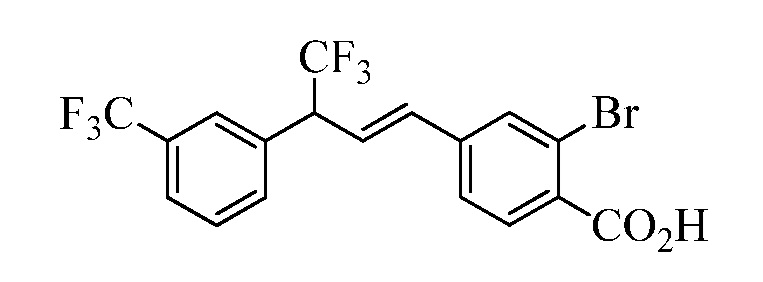
Молекула, указанная в заголовке, была выделена в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,50 (шир.с, 1H), 7,97-7,87 (м, 3H), 7,78-7,61 (м, 4H), 7,08 (дд, J=15,9, 9,3 Гц, 1H), 6,81 (д, J=15,9 Гц, 1H), 4,97-4,84 (м, 1H); ЭРИ-МС m/z 518,94 ([M-H]-); ИК (тонкая пленка) 3447, 1705, 1171, 526 см-1.
(E)-2-Бром-4-(3-(3-хлор-5-(трифторметил)фенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
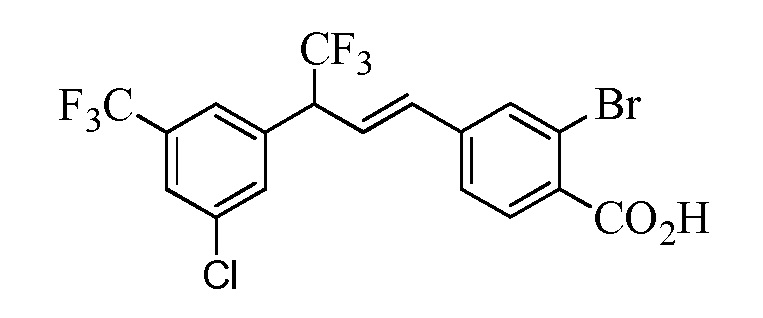
Молекула, указанная в заголовке, была выделена в виде бледно-желтой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,9 (с, 1H), 8,03 (с, 1H), 7,96-7,91 (м, 3H), 7,72 (д, J=8,1 Гц, 1H), 7,63-7,60 (м, 1H), 7,11 (дд, J=15,9, 9,6 Гц, 1H), 6,79 (д, J=15,9 Гц, 1H), 4,98-4,91 (м, 1H); ЭРИ-МС m/z 484,94 ([M-H]-); ИК (тонкая пленка) 3444, 1705, 1171, 764 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(4-фтор-3-(трифторметил)фенил)бут-1-ен-1-ил)бензойная кислота
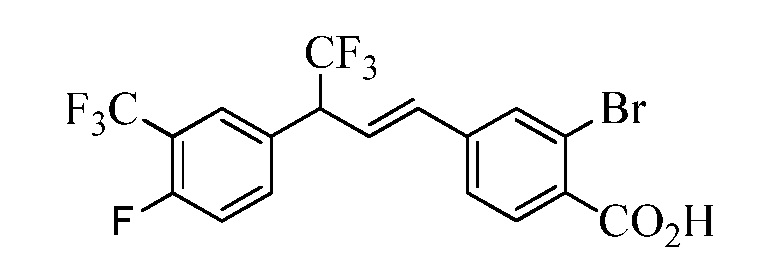
Молекула, указанная в заголовке, была выделена в виде коричневой жидкости: 1H-ЯМР (300 МГц, CDCl3) δ 8,00 (д, J=8,1 Гц, 1H), 7,71 (с, 1H), 7,61-7,59 (м, 2H), 7,41 (д, J=8,1 Гц, 1H), 7,30-7,24 (м, 1H), 6,59 (дд, J=16,2, 6,0 Гц, 1H), 6,48 (д, J=16,5 Гц, 1H), 4,26-4,21 (м, 1H); ЭРИ-МС m/z 469,0 ([M-H]-); ИК (тонкая пленка) 3444, 1699, 1327 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(3,4,5-трифторфенил)бут-1-ен-1-ил)бензойная кислота
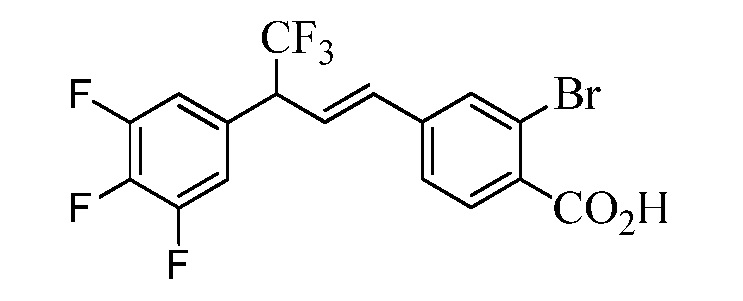
Молекула, указанная в заголовке, была выделена в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,60 (шир.с, 1H), 7,97 (с, 2H), 7,72 (д, J=7,2 Гц, 1H), 7,41-7,31 (м, 2H), 7,04 (дд, J=15,6, 9,0 Гц, 1H), 6,71 (д, J=15,9 Гц, 1H), 4,15-4,11 (м, 1H); ЭРИ-МС m/z 438,8 ([M+H]+).
(E)-4-(4,4,4-Трифтор-3-(2,3,4-трифторфенил)бут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
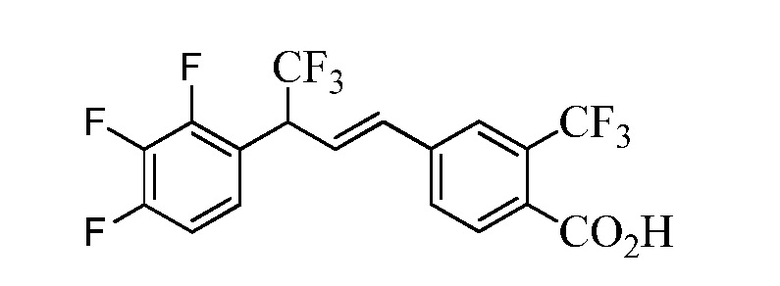
Молекула, указанная в заголовке, была выделена в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,00 (с, 1H), 7,93 (д, J=8,4 Гц, 1H), 7,81 (д, J=8,1 Гц, 1H), 7,63-7,60 (м, 1H), 7,47-7,44 (м, 1H), 7,02-7,01 (м, 1H), 5,10-4,90 (м, 1H).
(E)-2-Бром-4-(4,4,4-трифтор-3-(2,3,4-трифторфенил)бут-1-ен-1-ил)бензойная кислота
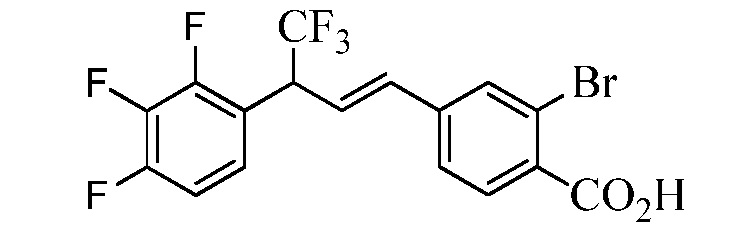
Молекула, указанная в заголовке, была выделена в виде коричневой смолы и неочищенную кислоту использовали непосредственно в следующей стадии: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,65 (шир.с, 1H), 7,95 (с, 1H), 7,75 (д, J=7,8 Гц, 1H), 7,62-7,59 (м, 2H), 7,50 (дд, J=15,6, 9,0 Гц, 1H), 6,95 (д, J=15,9 Гц, 1H), 4,86-4,74 (м, 1H); ЭРИ-МС m/z 436,92 ([M-H]-); ИК (тонкая пленка) 3445, 1641, 1116 см-1.
(E)-4-(4,4,4-Трифтор-3-(2,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
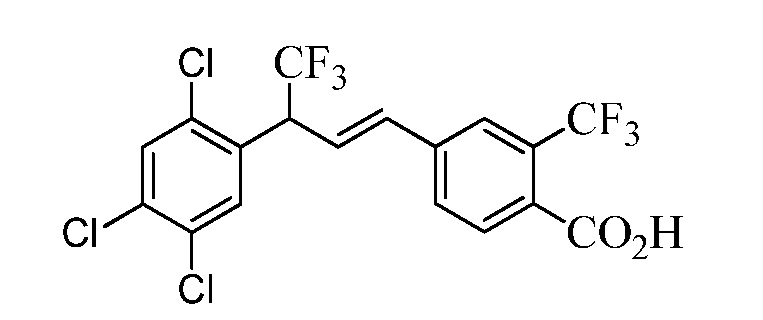
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,6 (с, 1H), 8,04 (с, 1H), 7,96 (д, J=8,4 Гц, 3H), 7,83 (д, J=8,1 Гц, 1H), 7,17-7,03 (м, 2H), 5,16-5,05 (м, 1H); ЭРИ-МС m/z 476,9 ([M-H]-); ИК (тонкая пленка) 3436, 1651, 1116, 661 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(2,4,5-трихлорфенил)бут-1-ен-1-ил)бензойная кислота
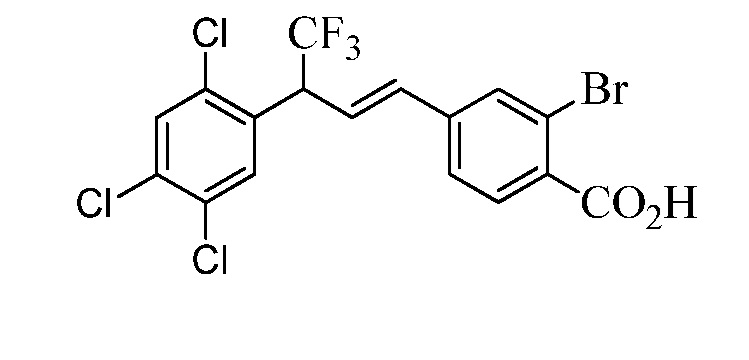
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ (300 МГц, ДМСО-d6) δ 13,4 (с, 1H), 7,99 (д, J=10,2 Гц, 3H), 7,76 (д, J=8,1 Гц, 1H), 7,65 (д, J=7,8 Гц, 1H), 7,09-6,91 (м, 2H), 5,11-5,05 (м, 1H); ЭРИ-МС m/z 486,8 ([M-H]-); ИК (тонкая пленка) 3436, 1651, 1115, 737 см-1.
(E)-4-(3-(4-Хлор-3-нитрофенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
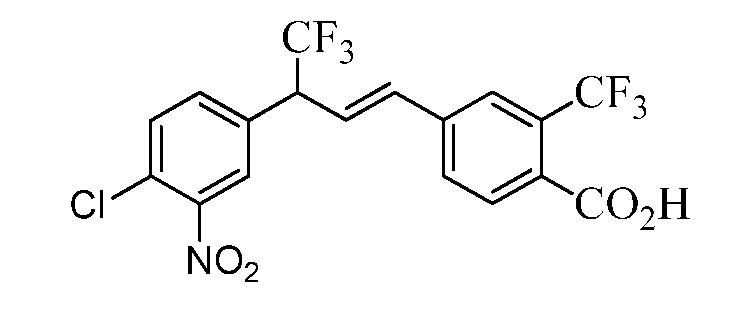
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы и неочищенную кислоту использовали непосредственно в следующей стадии: 1H-ЯМР (300 МГц, ДМСО-d6) 13,80 (шир.с, 1H), 8,33 (с, 1H), 7,94-7,81 (м, 5H), 7,75-7,72 (м, 1H), 7,06 (дд, J=15,9, 8,7 Гц, 1H), 6,90 (д, J=15,9 Гц, 1H), 5,02-4,81 (м, 1H).
(E)-2-Бром-4-(3-(4-хлор-3-нитрофенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
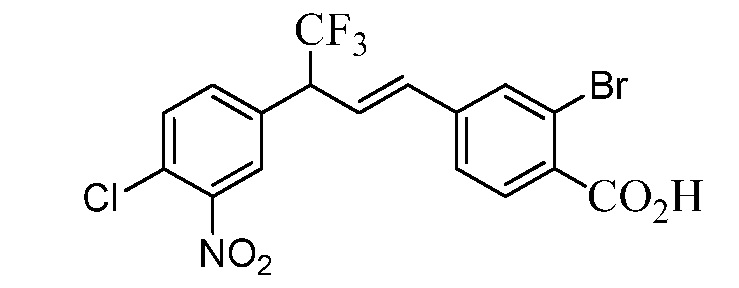
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) 13,50 (шир.с, 1H), 8,31 (с, 1H), 8,00-7,77 (м, 3H), 7,75-7,72 (м, 1H), 7,63-7,55 (м, 1H), 7,03 (дд, J=15,9, 9,0 Гц, 1H), 6,81 (д, J=15,9 Гц, 1H), 5,04-4,91 (м, 1H); ЭРИ-МС m/z 462,16 ([M-H]-); ИК (тонкая пленка) 3428, 1697, 1113, 749 см-1.
(E)-4-(4,4,4-Трифтор-3-(4-фтор-3,5-диметилфенил)бут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
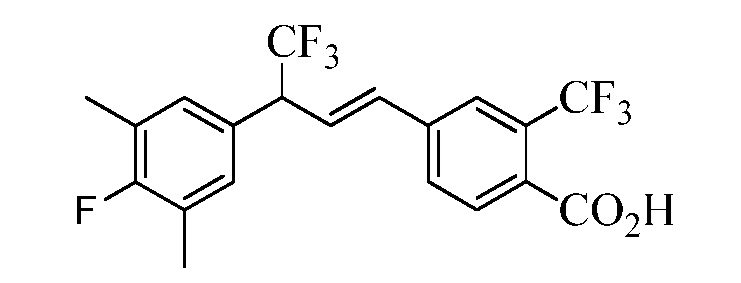
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,96 (с, 1H), 7,92 (д, J=8,4 Гц, 1H), 7,80-7,75 (м, 1H), 7,27 (д, J=6,9 Гц, 2H), 6,96 (дд, J=15,6, 8,7 Гц, 1H), 6,87 (д, J=15,6 Гц, 1H), 4,68-4,56 (м, 1H), 2,23 (с, 6H); ЭРИ-МС m/z 419,03 ([M-H]-); ИК (тонкая пленка) 3445, 2928, 1713, 1146 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(4-фтор-3,5-диметилфенил)бут-1-ен-1-ил)бензойная кислота

Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,91 (с, 1H), 7,74 (д, J=7,8 Гц, 1H), 7,61-7,58 (м, 1H), 7,26 (д, J=6,6 Гц, 2H), 6,93 (дд, J=15,9, 8,7 Гц, 1H), 6,87 (д, J=15,9 Гц, 1H), 4,59-4,53 (м, 1H), 2,23 (с, 6H); ЭРИ-МС m/z 428,97 ([M-H]-); ИК (тонкая пленка) 3473, 1701, 1111, 581 см-1.
(E)-4-(4,4,4-Трифтор-3-(4-фтор-3-метилфенил)бут-1-ен-1-ил)-2-(трифторметил)бензойная кислота

Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,58 (шир.с, 1H), 7,98 (с, 1H), 7,92-7,90 (м, 1H), 7,80 (д, J=8,1 Гц, 1H), 7,48-7,45 (м, 1H), 7,42-7,37 (м, 1H), 7,22-7,16 (м, 1H), 7,04 (дд, J=15,9, 8,7 Гц, 1H), 6,88 (д, J=15,9 Гц, 1H), 4,70-4,60 (м, 1H), 4,04-3,99 (м, 1H), 2,26 (с, 3H); ЭРИ-МС m/z 405,05 ([M-H]-); ИК (тонкая пленка) 3437, 1710, 1145 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(4-фтор-3-метилфенил)бут-1-ен-1-ил)бензойная кислота
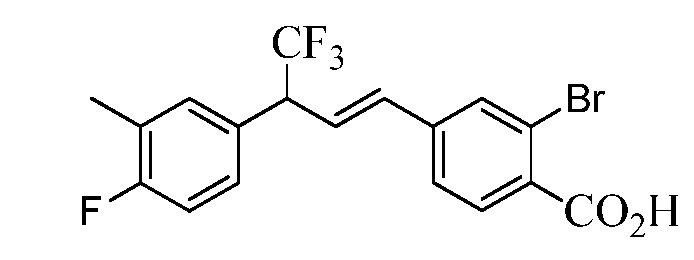
Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,39 (шир.с, 1H), 7,91 (с, 1H), 7,72 (д, J=8,1 Гц, 1H), 7,61-7,58 (м, 1H), 7,47-7,44 (м, 1H), 7,38-7,36 (м, 1H), 7,18 (т, J=9,6 Гц, 1H), 6,95 (дд, J=15,6, 8,7 Гц, 1H), 6,76 (д, J=15,9 Гц, 1H), 4,67-4,61 (м, 1H), 2,25 (с, 3H); ЭРИ-МС m/z 415,0 ([M-H]-); ИК (тонкая пленка) 3435, 2989, 1700, 1260 см-1.
(E)-4-(3-(3,5-Дихлорфенил)-4,4,5,5,5-пентафторпент-1-ен-1-ил)-2-(трифторметил)бензойная кислота
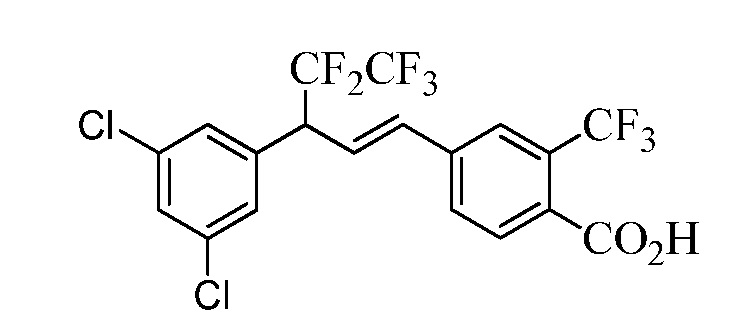
Молекулу, указанную в заголовке, выделяли в виде коричневого полутвердого вещества: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,70 (шир.с, 1H), 8,01 (с, 1H), 7,91 (с, 1H), 7,80 (д, J=8,4 Гц, 1H), 7,72 (J=1,6 Гц, 2H), 7,66 (т, J=3,2 Гц, 1H), 7,15 (дд, J=15,6, 9,6 Гц, 1H), 6,91 (д, J=15,6 Гц, 1H), 4,86-4,78 (м, 1H); ЭРИ-МС m/z 491,0 ([M-H]-); ИК (тонкая пленка) 3446, 1712 1141 749 см-1.
(E)-2-Бром-4-(3-(3,5-дихлорфенил)-4,4,5,5,5-пентафторпент-1-ен-1-ил)бензойная кислота
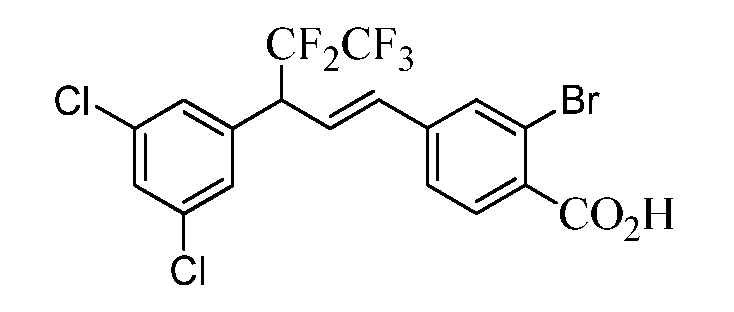
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,85 (с, 1H), 7,70 (с, 2H), 7,65-7,64 (м, 1H), 7,56-7,52 (м, 2H), 6,94 (д, J=9,2 Гц, 1H), 6,76 (д, J=16 Гц, 1H), 4,82-4,80 (м, 1H); ЭРИ-МС m/z 500,8 ([M-H]-); ИК (тонкая пленка) 3422, 1683, 1184, 750, 575 см-1.
(E)-4-(3-(3,4-Дибромфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
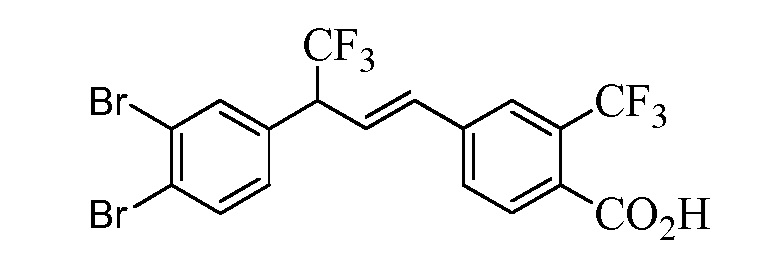
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,5 (шир.с, 1H), 8,01-7,99 (м, 2H), 7,94-7,91 (м, 1H), 7,85-7,78 (м, 2H), 7,53-7,50 (м, 1H), 7,09 (дд, J=15,6, 8,7 Гц, 1H), 6,89 (д, J=15,9 Гц, 1H), 4,85-4,78 (м, 1H); ЭРИ-МС m/z 528,8 ([M-H]-); ИК (тонкая пленка) 3437, 1722, 1168 см-1.
(E)-2-Бром-4-(3-(3,4-дибромфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
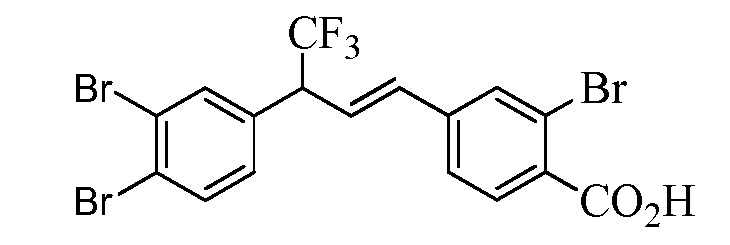
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,38 (шир.с, 1H), 7,98-7,96 (м, 2H), 7,84 (д, J=8,4 Гц, 1H), 7,74 (д, J=8,1 Гц, 1H), 7,63-7,61 (м, 1H), 7,51-7,49 (м, 1H), 7,01 (дд, J=15,9, 9,0 Гц, 1H), 6,78 (д, J=15,6 Гц, 1H), 4,82-4,76 (м, 1H); ЭРИ-МС m/z 538,8 ([(M-H]-); ИК (тонкая пленка) 3446, 1699, 1166, 581 см-1.
(E)-4-(4,4,4-Трифтор-3-(3-(трифторметокси)фенил)бут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
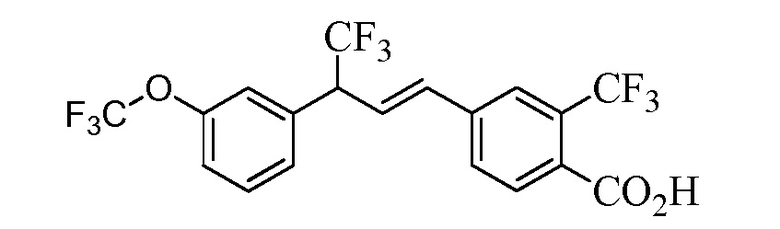
Молекулу, указанную в заголовке, выделяли в виде коричневого полутвердого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,01 (с, 1H), 7,94 (д, J=8,7 Гц, 1H), 7,80 (д, J=8,1 Гц, 1H), 7,63-7,55 (м, 3H), 7,41 (д, J=7,5 Гц, 1H), 7,11 (дд, J=15,6, 9,0 Гц, 1H), 6,92 (д, J=15,9 Гц, 1H), 4,89-4,82 (м, 1H); ЭРИ-МС m/z 456,98 ([M-H]-); ИК (тонкая пленка) 3413, 1668, 1161 см-1.
(E)-2-Бром-4-(4,4,4-трифтор-3-(3-(трифторметокси)фенил)бут-1-ен-1-ил)бензойная кислота
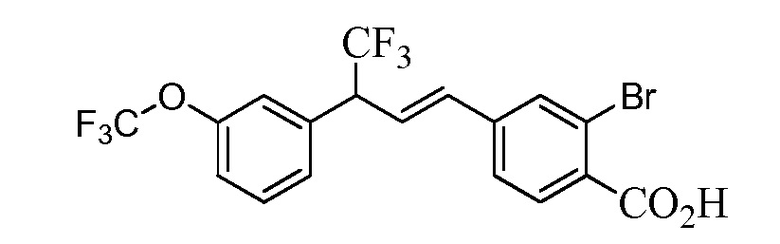
Молекулу, указанную в заголовке, выделяли в виде твердого коричневого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,73 (с, 1H), 7,59 (м, 3H), 7,44 (с, 1H), 7,40 (д, J=7,6 Гц, 2H), 6,88 (дд, J=15,6, 9,0 Гц, 1H), 6,73 (д, J=15,9 Гц, 1H), 4,85-4,82 (м, 1H); ЭРИ-МС m/z 466,93 ([M-H]-); ИК (тонкая пленка) 3437, 1703, 1111 см-1.
(E)-4-(3-(3-циано-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
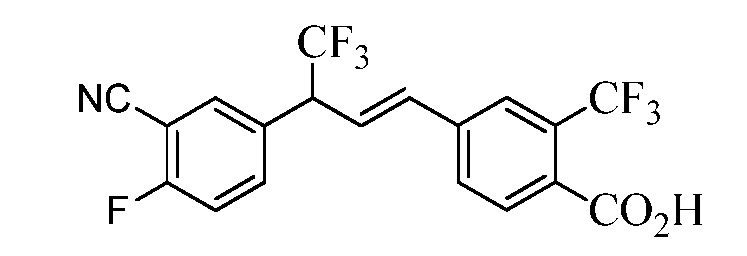
Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,60 (шир.с, 1H), 8,21-8,19 (м, 1H), 8,01-7,91 (м, 3H), 7,81 (д, J=8,4 Гц, 1H), 7,12 (дд, J=15,9 8,1 Гц, 1H), 6,91 (д, J=15,6 Гц, 1H), 4,92-4,86 (м, 1H); ЭРИ-МС m/z 416,27 ([M-H]-); ИК (тонкая пленка) 3429, 2238, 1713, 1116 см-1.
(E)-2-Бром-4-(3-(3-циано-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
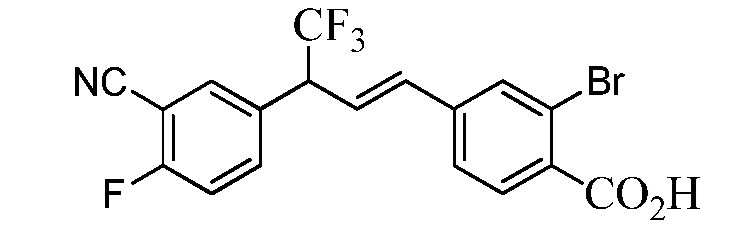
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,56 (шир.с, 1H), 8,21-8,18 (м, 1H), 8,00-7,95 (м, 2H), 7,73-7,59 (м, 3H), 7,03 (дд, J=15,9, 9,3 Гц, 1H), 6,79 (д, J=15,3 Гц, 1H), 4,87-4,84 (м, 1H); ЭРИ-МС m/z 426,0 ([M-H]-).
(E)-2-Бром-4-(3-(3,4-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
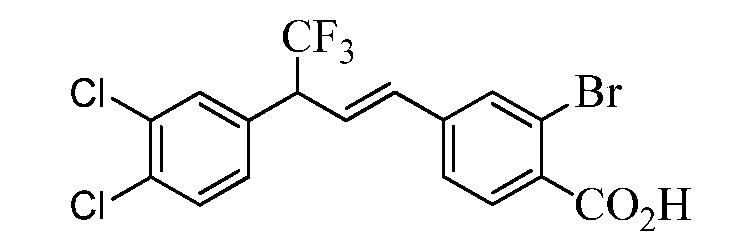
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,4 (с, 1H), 7,96 (д, J=1,2 Гц, 1H), 7,88 (д, J=1,8 Гц, 1H), 7,74-7,68 (м, 2H), 7,63 (дд, J=8,1, 1,2 Гц, 1H), 7,57 (дд, J=8,4, 1,8 Гц, 1H), 7,02 (дд, J=15,9, 9,3 Гц, 1H), 6,78 (дд, J=5,9 Гц, 1H), 4,84-4,78 (м, 1H); ЭРИ-МС m/z 451,0 ([M-H]-); ИК (тонкая пленка) 3445, 1704, 1113, 740 см-1.
(E)-4-(3-(3-бром-5-хлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
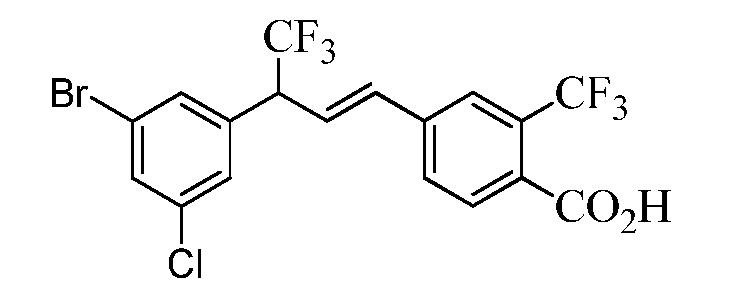
Молекулу, указанную в заголовке, выделяли в виде твердого коричневого вещества: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,50 (шир.с, 1H), 7,91 (с, 1H), 7,86-7,64 (м, 5H), 7,06 (дд, J=15,9, 9,0 Гц, 1H), 6,87 (д, J=15,9 Гц, 1H), 4,85-4,78 (м, 1H); ЭРИ-МС m/z 485,17 ([M-H]-); ИК (тонкая пленка) 3438, 1708, 1114, 774, 516 см-1.
(E)-2-Бром-4-(3-(3-бром-5-хлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
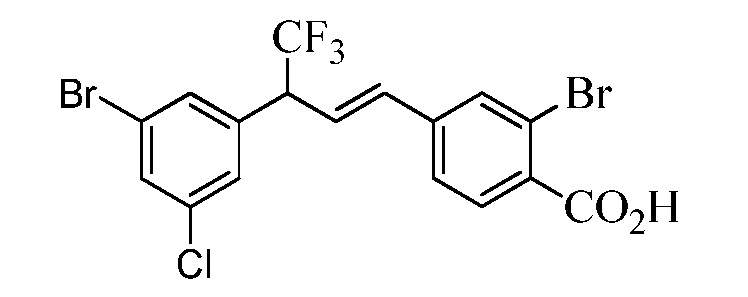
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,38 (шир.с, 1H), 7,98 (с, 1H), 7,80-7,72 (м, 4H), 7,64-7,61 (м, 1H), 7,06 (дд, J=15,9, 9,3 Гц, 1H), 6,79 (д, J=15,6 Гц, 1H), 4,88-4,80 (м, 1H); ЭРИ-МС m/z 495,05 ([M-H]-); ИК (тонкая пленка) 3436, 1699, 1116, 750, 531 см-1.
(E)-4-(3-(3-бром-5-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота

Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,6 (шир.с, 1H), 8,02 (с, 1H), 7,91-7,89 (м, 1H), 7,81 (д, J=8,0 Гц, 1H), 7,69 (с, 1H), 7,63-7,59 (м, 1H), 7,55 (д, J=9,3 Гц, 1H), 7,11 (дд, J=15,9, 9,0 Гц, 1H), 6,91 (д, J=15,9 Гц, 1H), 4,87-4,80 (м, 1H); ЭРИ-МС m/z 469,07 ([M-H]-); ИК (тонкая пленка) 3428, 1712, 1171, 523 см-1.
(E)-4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензойная кислота
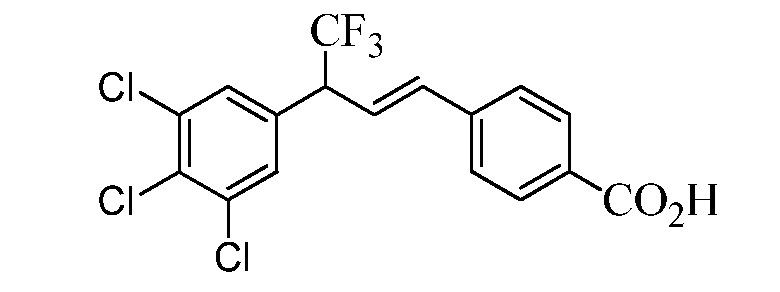
Молекулу, указанную в заголовке, выделяли в виде желтого твердого вещества: 1H-ЯМР (400 МГц, CDCl3) δ 8,18-8,03 (м, 2H), 7,49 (д, J=8,3 Гц, 2H), 7,42 (с, 2H), 6,66 (д, J=15,9 Гц, 1H), 6,47 (дд, J=15,9, 8,0 Гц, 1H), 4,13 (п, J=8,6 Гц, 1H); 19F-ЯМР (376 МГц, CDCl3) δ -68,65; ЭРИ-МС m/z 409,1 ([M-H]-).
(E)-2-Бром-4-(3-(3-хлор-4-метилфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
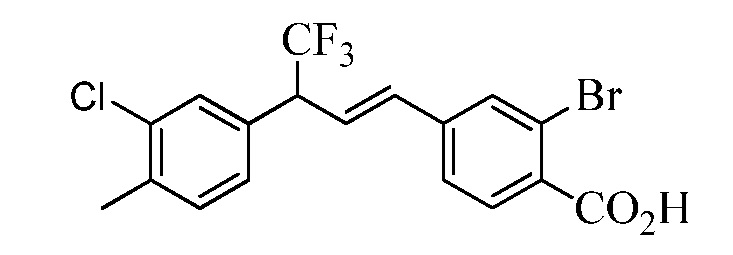
Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,30 (шир.с, 1H), 7,93 (д, J=1,2 Гц, 1H), 7,42 (д, J=8,1 Гц, 1H), 7,62 (дд, J=1,5, 8,1 Гц, 1H), 7,53 (с, 1H), 7,48 (д, J=7,8 Гц, 1H), 7,39 (д, J=7,8 Гц, 1H), 6,96 (дд, J=15,6, 8,7 Гц, 1H), 6,77 (д, J=15,6 Гц, 1H), 4,73-4,61 (м, 1H), 2,35 (с, 3H); ЭРИ-МС m/z 431,77 ([M-H]-); ИК (тонкая пленка) 3435, 1701, 1111, 750 см-1.
(E)-4-(3-(3-Хлор-4-метилфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
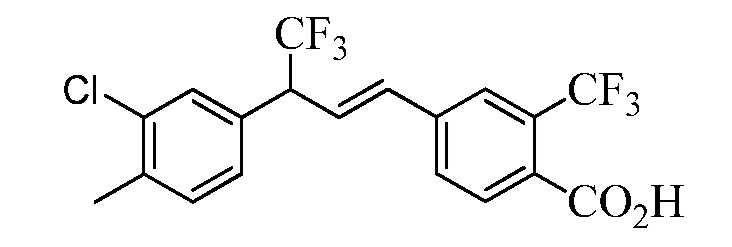
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,50 (шир.с, 1H), 7,98 (с, 1H), 7,92 (д, J=8,1 Гц, 1H), 7,80 (д, J=8,1 Гц, 1H), 7,53 (с, 1H), 7,48 (д, J=8,1 Гц, 1H), 7,40 (д, J=8,4 Гц, 1H), 7,04 (дд, J=15,6, 8,4 Гц, 1H), 6,88 (д, J=15,6 Гц, 1H), 4,72-4,66 (м, 1H), 2,35 (с, 3H); ЭРИ-МС m/z 421,82 ([M-H]-); ИК (тонкая пленка) 3460, 2926, 1712, 1170, 750 см-1.
(E)-4-(4,4,5,5,5-Пентафтор-3-(3,4,5-трихлорфенил)пент-1-ен-1-ил)-2-(трифторметил)бензойная кислота
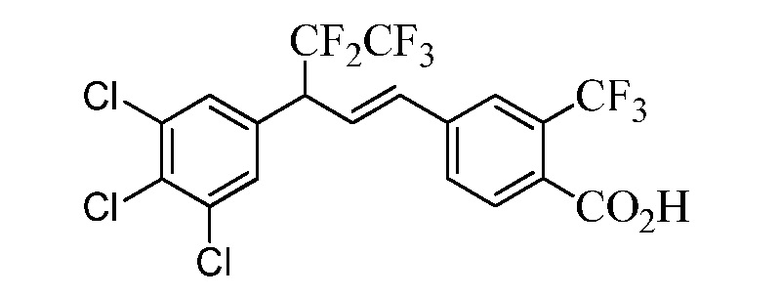
Молекулу, указанную в заголовке, выделяли в виде темно-коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,6 (шир.с, 1H), 8,03 (с, 1H), 7,95-7,86 (м, 3H), 7,81 (д, J=8,1 Гц, 1H), 7,16 (дд, J=15,3, 9,3 Гц, 1H), 6,92 (д, J=15,6 Гц, 1H), 4,95-4,88 (м, 1H); 19F-ЯМР (300 МГц, ДМСО-d6) δ -80,35,-58,02; ЭРИ-МС m/z 526,8 ([M+H]+).
(E)-2-Бром-4-(4,4,5,5,5-пентафтор-3-(3,4,5-трихлорфенил)пент-1-ен-1-ил)бензойная кислота
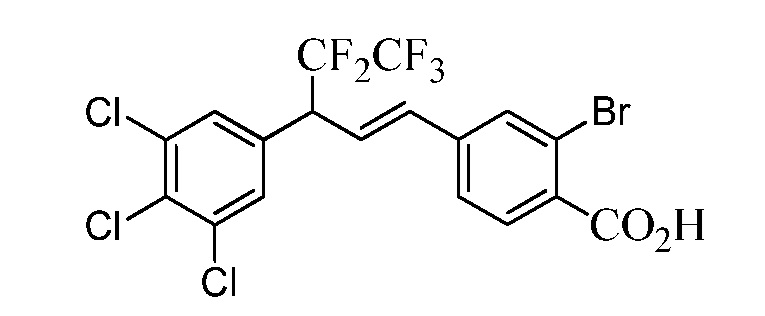
Молекулу, указанную в заголовке, выделяли в виде темно-коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,6 (шир.с, 1H), 7,94 (с, 2H), 7,78 (д, J=7,8 Гц, 1H), 7,71 (д, J=7,8 Гц, 1H), 7,60 (д, J=7,5 Гц 1H), 7,07 (дд, J=15,0, 8,7 Гц, 1H), 6,79 (д, J=15,6 Гц, 1H), 4,93-4,78 (м, 1H); ЭРИ-МС m/z 538,9 ([M+H]+); ИК (тонкая пленка) 3420, 1602, 1123, 746 см-1.
(E)-2-Бром-4-(3-(4-циано-3,5-дифторфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
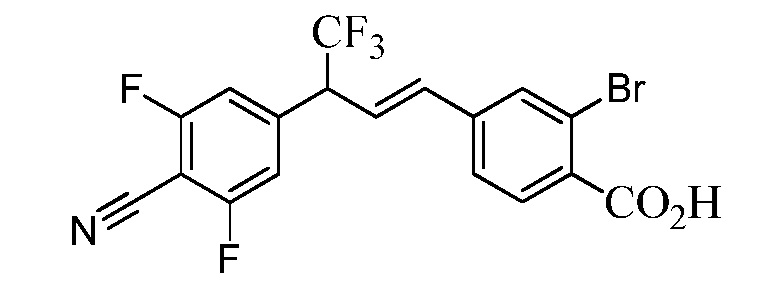
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: ЭРИ-МС m/z 443,91 ([M-H]-); ИК (тонкая пленка) 3447, 2244, 1703, 1114 см-1.
(E)-2-Хлор-4-(3-(3,5-дибромфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
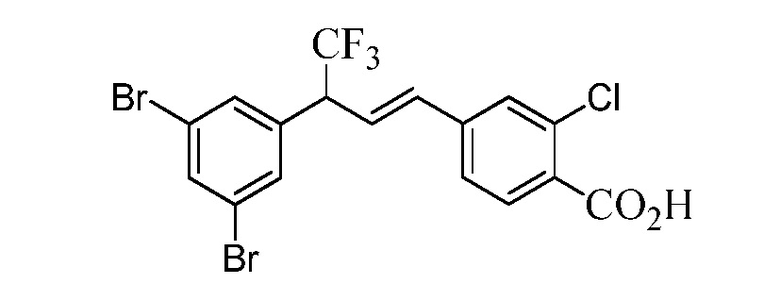
Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,39 (шир.с, 1H), 7,95-7,70 (м, 5H), 7,61 (д, J=8,1 Гц, 1H), 7,07 (дд, J=15,6, 9,3 Гц, 1H), 6,80 (д, J=15,6 Гц, 1H), 4,84-4,78 (м, 1H); ЭРИ-МС m/z 496,77 ([M-H]-); ИК (тонкая пленка) 3439, 2920, 1707, 1165 см-1.
(E)-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
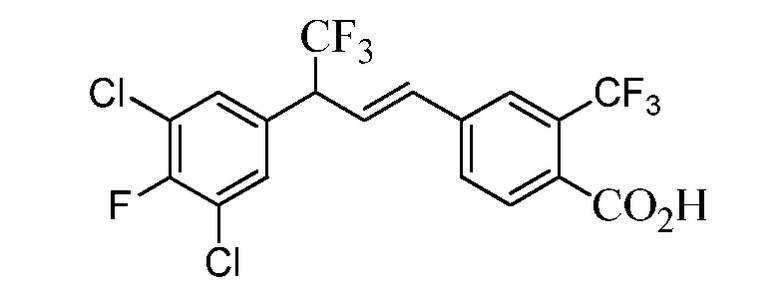
Молекулу, указанную в заголовке, выделяли в виде грязно-белого твердого вещества: Т.пл. 140-143ºC; 1H-ЯМР (400 МГц, ДМСО) δ 13,60 (шир.с, 1H), 8,02 (с, 1H), 7,94-7,90 (м, 1H), 7,88-7,86 (м, 2H), 7,81-7,79 (м, 1H), 7,12 (дд, J=15,6, 8,8 Гц, 1H), 6,89 (д, J=15,6 Гц, 1H), 4,86-4,81 (м, 2H); ЭРИ-МС m/z 458,88 ([M-H]-).
(E)-4-(3-(3,4-Дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
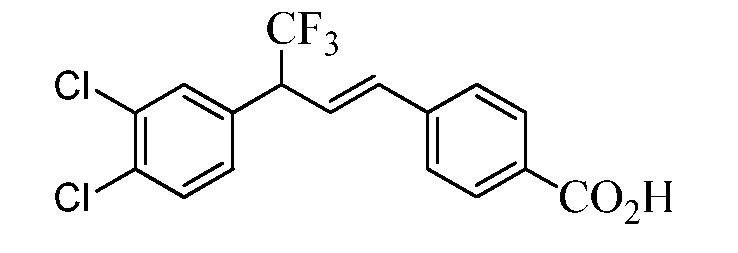
Молекулу, указанную в заголовке, выделяли в виде светло-оранжевого кристаллического вещества (875 мг, 88%): 1H-ЯМР (400 МГц, CDCl3) δ 12,35 (с, 1H), 8,08 (д, J=8,4 Гц, 2H), 7,55-7,41 (м, 4H), 7,24 (дд, J=8,3, 2,1 Гц, 1H), 6,64 (д, J=15,8 Гц, 1H), 6,51 (дд, J=15,9, 7,7 Гц, 1H), 4,15 (п, J=8,7 Гц, 1H); 19F-ЯМР 376 МГц, CDCl3) δ -68,75; ЭРИ-МС m/z 375 ([M+H]+).
(E)-4-(3-(3,4-Дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
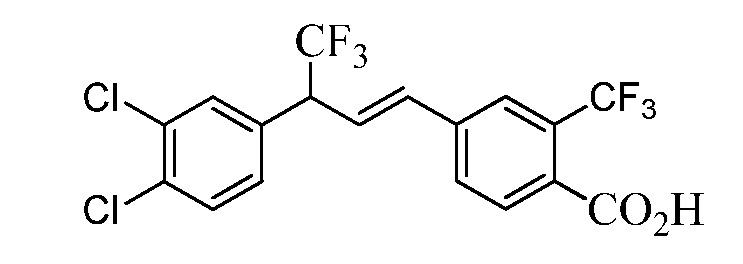
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,6 (с, 1H), 8,02 (с, 1H), 7,93-7,89 (м, 2H), 7,80 (д, J=7,6 Гц, 1H), 7,73 (д, J=8,4, Гц, 1H), 7,58 (дд, J=8,4, 2,0 Гц, 1H), 7,09 (дд, J=15,6, 8,8, Гц, 1H), 6,89 (д, J=15,6, Гц, 1H), 4,86-4,81 (м, 1H); ЭРИ-МС m/z 441,0 ([M-H]-); ИК (тонкая пленка) 3447, 1710, 1169, 749 см-1.
(E)-4-(3-(3,5-Дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
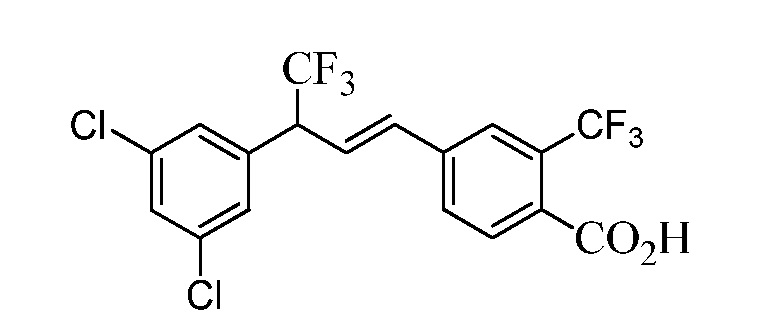
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,6 (шир.с, 1H), 7,98 (с, 1H), 7,91 (д, J=7,8 Гц 1H), 7,75-7,66 (м, 1H), 7,10 (дд, J=15,6, 9,0 Гц, 1H), 6,89 (д, J=15,9 Гц 1H), 4,86-4,80 (м, 1H); ЭРИ-МС m/z 441,1 ([M-H]-); ИК (тонкая пленка) 3460, 2928, 1721, 1170, 764 см-1.
(E)-4-(3-(3,4-дихлор-5-метилфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
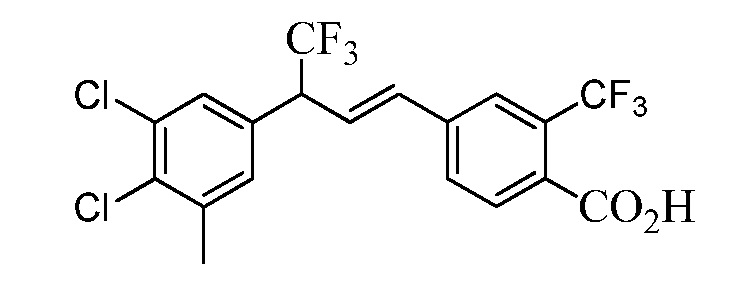
Молекулу, указанную в заголовке, выделяли в виде бледно-желтого полутвердого вещества: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,58 (шир.с, 1H), 8,00 (с, 1H), 7,93 (д, J=8,4 Гц, 1H), 7,80 (д, J=8,4 Гц, 1H), 7,72 (с, 1H), 7,55 (с, 1H), 7,07 (дд, J=16,4, 9,6 Гц, 1H), 6,89 (д, J=15,6 Гц, 1H), 4,78-4,73 (м, 1H), 2,42 (с, 3H); ЭРИ-МС m/z 455,0 ([M-H]-); ИК (тонкая пленка) 1713, 1170, 750 см-1.
(E)-2-Бром-4-(3-(3,4-дихлорфенил)-4,4-дифторпент-1-ен-1-ил)бензойная кислота
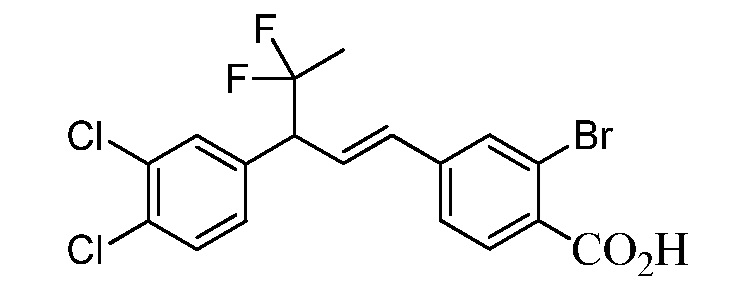
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,3 (с, 1H), 7,92 (с, 1H), 7,77-7,71 (м, 2H), 7,68-7,63 (м, 1H), 7,61-7,60 (м, 1H), 7,60-7,58 (м, 1H), 6,98 (дд, J=15,6, 9,2 Гц, 1H), 6,65 (д, J=15,6 Гц, 1H), 4,83-4,80 (м, 1H), 1,59-1,54 (м, 3H); ЭРИ-МС m/z 448,8 ([M-H]-).
(E)-2-Бром-4-(3-(3-хлор-5-этилфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
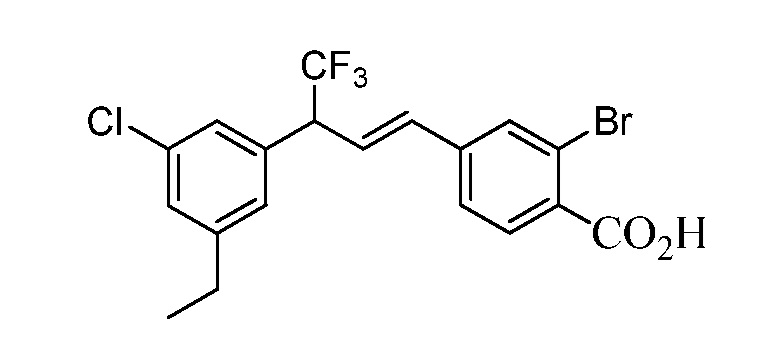
Молекулу, указанную в заголовке, выделяли в виде коричневой жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,4 (шир.с, 1H), 7,97 (с, 2H), 7,91 (с, 1H), 7,74 (д, J=8,4 Гц, 2H), 7,66-7,61 (м, 1H), 7,03 (дд, J=16,0, 8,4 Гц, 1H), 6,8 (д, J=15,6 Гц, 1H), 4,89-4,84 (м, 1H), 2,66-2,65 (м, 2H), 1,25 (т, J=9,2 Гц, 3H); ЭРИ-МС m/z 446,8 ([M+H]+).
(E)-2,6-Диметил-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойная кислота.
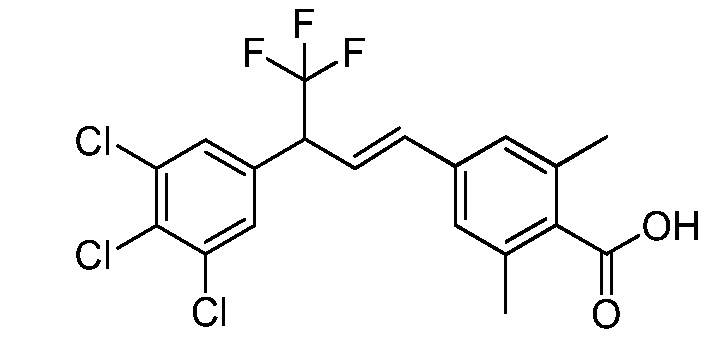
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,1 (с, 1H), 7,87 (с, 2H), 7,27 (с, 2H), 6,81 (дд, J=15,6, 8,7 Гц, 1H), 6,69 (д, J=15,3 Гц, 1H), 4,85-4,79 (м, 1H), 2,27 (с, 6H); ЭРИ-МС m/z 437,01 ([M-H]-); ИК (тонкая пленка) 3285, 1621, 1162, 954 см-1.
(E)-2-Бром-4-(3-(3,5-дибром-4-хлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота
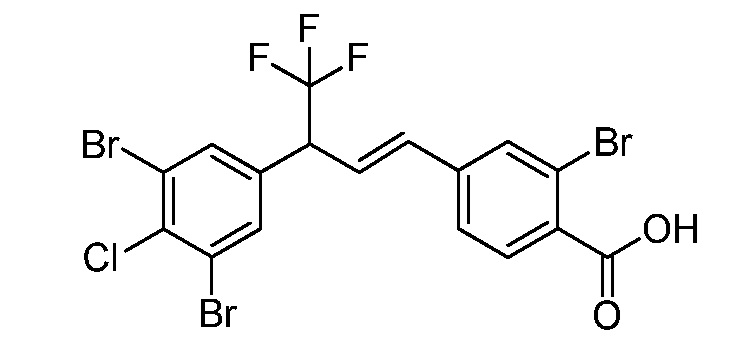
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,40 (шир.с, 1H), 8,07 (д, J=7,5 Гц, 1H), 7,94-7,89 (м, 2H), 7,66-7,60 (м, 2H), 7,10 (дд, J=8,7, 16,0 Гц, 1H), 6,96 (д, J=15,6 Гц, 1H), 4,82-4,80 (м, 1H); ЭРИ-МС m/z 574,7 ([M+H]+).
(E)-4-(3-(3,5-дибром-4-хлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
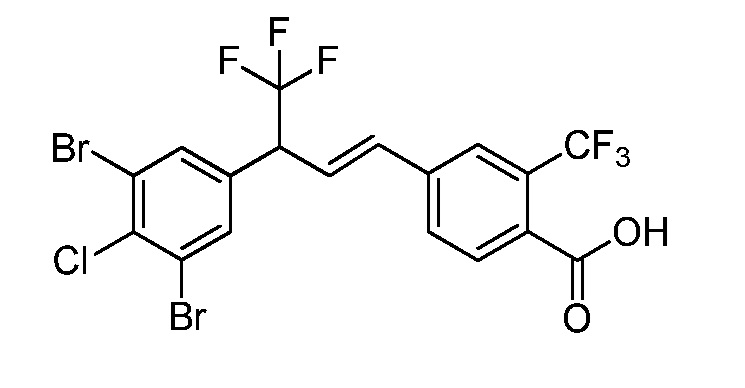
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,36 (шир.с, 1H) 8,05 (с, 2H), 7,95 (д, J=8,1 Гц, 1H), 7,87-7,67 (м, 2H), 7,14 (дд, J=9,0, 15,6 Гц, 1H), 6,96 (д, J=15,6 Гц, 1H), 4,88-4,82 (м, 1H); ЭРИ-МС m/z 564,58 ([M+H]+).
(E)-2-Бром-4-(3-(4-бром-3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензойная кислота

Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,40 (шир.с, 1H), 7,98 (с, 1H), 7,87 (с, 2H), 7,75 (д, J=8,1 Гц, 1H), 7,65-7,62 (м, 1H), 7,06 (дд, J=15,9, 9,3 Гц, 1H), 6,80 (д, J=15,9 Гц, 1H), 4,87-4,80 (м, 1H); ЭРИ-МС m/z 518,9 ([M-H]-).
(E)-4-(3-(4-бром-3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)бензойная кислота
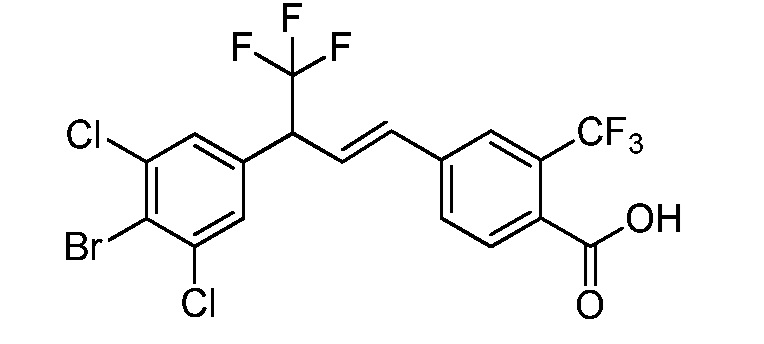
Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (300 МГц, ДМСО-d6) δ 13,6 (шир.с, 1H) 8,03 (с, 1H), 7,95 (д, J=8,4 Гц, 1H), 7,88 (с, 2H), 7,81 (д, J=8,1 Гц, 1H), 7,13 (дд, J=16,2, 7,5 Гц, 1H), 6,91 (д, J=15,9 Гц, 1H), 4,89-4,83 (м, 1H); ЭРИ-МС m/z 532,0 ([M+H]+).
(E)-2-Бром-4-(3-(3-хлор-4-(трифторметокси)фенил)-4,4,4-трифтор-бут-1-ен-1-ил)бензойная кислота

Молекулу, указанную в заголовке, выделяли в виде коричневой смолы: 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,36 (шир.с, 1H) 7,95 (с, 1H), 7,73 (д, J=7,6 Гц, 1H), 7,63 (д, J=8,1 Гц, 1H), 7,46 (с, 1H) 7,35-7,31 (м, 2H), 7,04 (дд, J=16,0, 8,8 Гц, 1H), 6,78 (д, J=16,4 Гц, 1H), 4,71-4,68 (м, 1H); ЭРИ-МС m/z 500,8 ([M-H]-).
Пример 20: Получение 5-винил-2,3-дигидро-1H-инден-1-она (BI1)
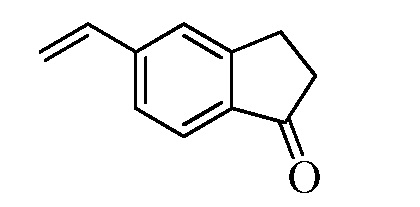
К перемешиваемому раствору 5-бром-2,3-дигидро-1H-инден-1-она (5 г, 23,7 ммоль) в толуоле добавляли пиридиновый комплекс винилборонового ангидрида (8,55 г, 35,54 ммоль), Pd(PPh3)4 (0,1 г, 0,094 ммоль), K2CO3 (22,88 г, 165,83 ммоль). Полученную реакционную смесь нагревали при кипячении с обратным холодильником в течение 16 ч. Реакционную смесь охлаждали до 25°C и фильтровали, и фильтрат выпаривали при пониженном давлении. Остаток разбавляли EtOAc и промывали H2O и рассолом. Объединенные органические экстракты сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Полученный остаток очищали с помощью колоночной флеш-хроматографии (SiO2, 5% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде твердого вещества (1,8 г, 48%): 1H-ЯМР (400 МГц, CDCl3) δ 7,74 (д, J=7,2 Гц, 1H), 7,49 (шир. с, 1H), 7,44 (д, J=7,2 Гц, 1H), 6,82 (м, 1H), 5,90 (д, J=7,4 Гц, 1H), 5,42 (д, J=6,4 Гц, 1H), 3,20 (м, 2H), 2,70 (м, 2H); ЭРИ-МС m/z 159,06 ([M+H]-).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 20.
6-Винил-3,4-дигидронафталин-1(2H)-он (BI2)
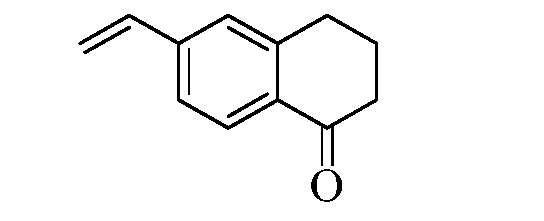
Продукт выделяли в виде грязно-белого твердого вещества (5 г, 48%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,85 (д, J=8,4 Гц, 1H), 7,48 (м, 2H), 6,82 (м, 1H), 6,02 (д, J=7,4 Гц, 1H), 5,44 (д, J=6,4 Гц, 1H), 2,95 (м, 2H), 2,60 (м, 2H), 2,00 (м, 2H); ЭРИ-МС m/z 173,14 ([M-H]-); ИК (тонкая пленка) 1681 см-1.
Пример 21: Получение (E)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфе-нил)бут-1-енил)-2,3-дигидро-1H-инден-1-она (BI3)
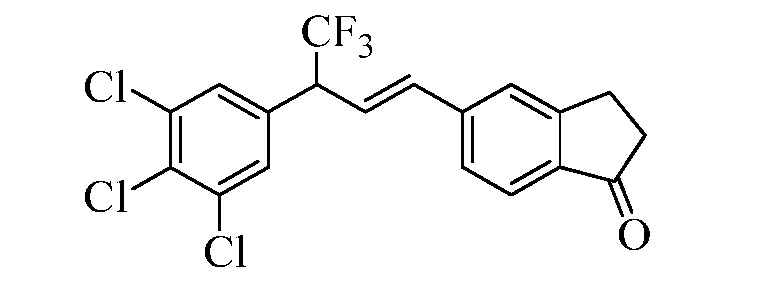
5-(1-Бром-2,2,2-трифторэтил)-1,2,3-трихлорбензол (4 г, 11,7 ммоль), 5-винил-2,3-дигидро-1H-инден-1-он (0,92 г, 5,8 ммоль), CuCl (0,115 г, 1,171 ммоль) и 2,2-бипиридил (0,053 г, 0,34 ммоль) в 1,2-дихлорбензоле (25 мл) нагревали при 180°C в течение 16 ч. Реакционную смесь охлаждали до 25°C и выпаривали при пониженном давлении. Остаток очищали с помощью колоночной флеш-хроматографии (SiO2, 5% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде жидкости (1,28 г, 25%): 1H-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=7,4 Гц, 1H), 7,52 (м, 3H), 6,68 (д, J=7,4 Гц, 1H), 6,52 (м, 1H), 4,18 (м, 1H), 3,18 (м, 2H), 2,75 (м, 2H); ЭРИ-МС m/z 419,14 ([M+H]-); ИК (тонкая пленка) 1708,94, 1113,60, 807,77 см-1.
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 21.
(E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2,3-дигидро-1H-инден-1-он (BI4)
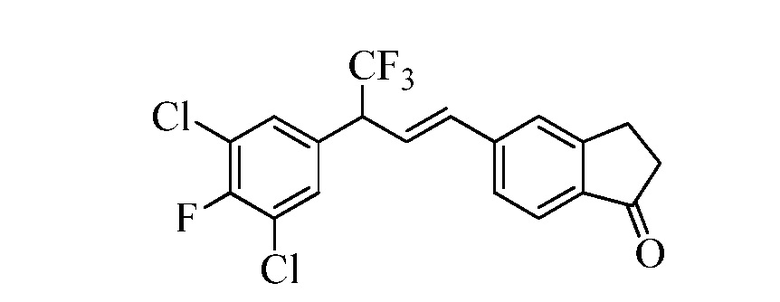
Продукт выделяли в виде полутвердого коричневого вещества (1,2 г, 16%): 1H-ЯМР (400 МГц, CDCl3) δ 7,76 (д, J=7,4 Гц, 1H), 7,54 (м, 3H), 7,30 (с, 1H), 6,68 (д, J=7,4 Гц, 1H), 6,52 (м, 1H), 4,18 (м, 1H), 3,18 (м, 2H), 2,75 (м, 2H); ЭРИ-МС m/z 400,84 ([M-H]-); ИК (тонкая пленка) 815, 1113, 1709 см-1.
(E)-6-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-3,4-дигидронафталин-1(2H)-он (BI5)
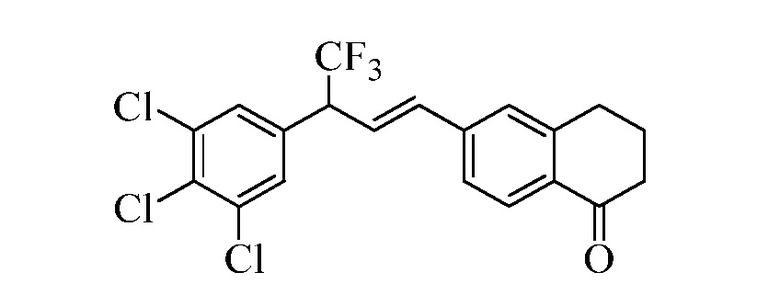
Продукт выделяли в виде бледно-желтого полутвердого вещества (1,2 г, 30%): 1H-ЯМР (400 МГц, CDCl3) δ 8,20 (д, J=8,0 Гц, 1H), 7,42 (с, 2H), 7,35 (м, 1H), 7,24 (м, 2H), 6,62 (д, J=16 Гц, 1H), 6,46 (м, 1H), 4,18 (м, 1H), 2,95 (м, 2H), 2,65 (м, 2H), 2,19 (м, 2H); ЭРИ-МС m/z 432,94 ([M-H]-); ИК (тонкая пленка) 1680, 1113, 808 см-1.
Пример 22: Получение (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-фтор-2,3-дигидро-1H-инден-1-она (BI6)
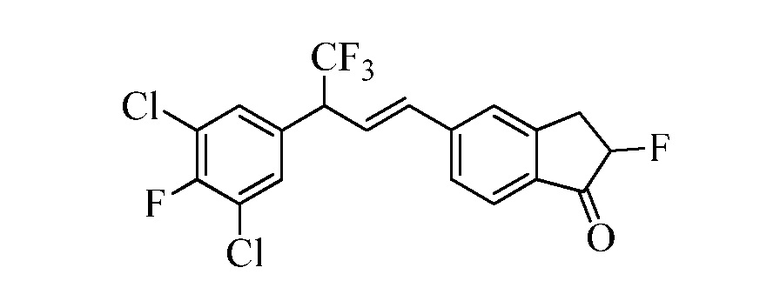
К перемешиваемому раствору (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-2,3-дигидро-1H-инден-1-она (0,5 г, 1,24 ммоль) в ацетонитриле (20 мл) добавляли Selectfluor® (0,52 г, 1,48 ммоль) и нагревали реакцию с обратным холодильником до температуры кипения в течение 16 ч. Реакционную смесь охлаждали до комнатной температуры, выпаривали при пониженном давлении и разбавляли ДХМ. Раствор промывали водой и рассолом, сушили над безводным сульфатом натрия и выпаривали при пониженном давлении с получением неочищенного продукта, который очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 15% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде бледно-желтого полутвердого вещества (0,1 г, 24%): 1H-ЯМР (400 МГц, CDCl3) δ 7,80 (м, 1H), 7,48 (м, 2H), 7,32 (м, 2H), 6,65 (д, J=16,0 Гц, 1H), 6,54 (дд, J=16,0, 8,0 Гц, 1H), 5,38 (м, 1H), 4,18 (м, 1H), 3,62 (м, 1H), 3,32 (м, 1H); ЭРИ-МС m/z 419,06 ([M-H]-); ИК (тонкая пленка) 1728, 1114, 817 см-1.
Пример 23: Получение (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-N-(3,3,3-трифторпропил)-2,3-дигидро-1H-инден-1-амина (BC10)
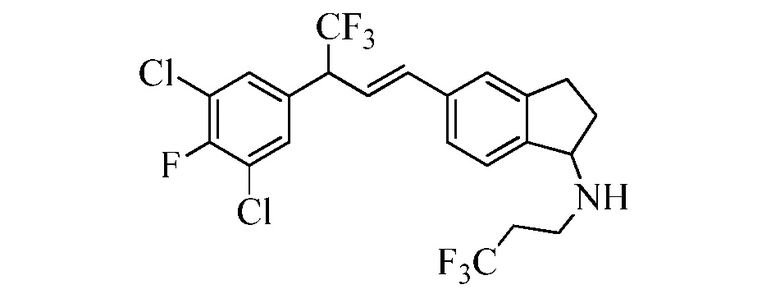
К перемешиваемому раствору (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-2,3-дигидро-1H-инден-1-она (0,15 г, 0,35 ммоль) в ДХЭ (10 мл) добавляли трифторпропиламин (0,048 г, 0,42 ммоль) и цианоборогидрид натрия (0,055 г, 0,875 ммоль) при охлаждении и перемешивали реакционную смесь при комнатной температуре в течение 16 ч. Реакционную смесь разбавляли ДХЭ, промывали водой и рассолом и сушили над безводным сульфатом натрия. Выпаривание при пониженном давлении дало неочищенное соединение, которое очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 10-15% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде бесцветного смолистого материала (0,042 г, 24%): 1H-ЯМР (400 МГц, CDCl3) δ 7,38-7,20 (м, 5H), 6,62 (д, J=16,0 Гц, 1H), 6,34 (дд, J=16,0, 8,0 Гц, 1H), 5,83 (шир., 1H), 5,52 (м, 1H), 4,12 (м, 1H), 3,02 (м, 3H), 2,82 (м, 1H), 2,50 (м, 2H), 1,82 (м, 1H), 1,42 (м, 1H); ЭРИ-МС m/z 497,98 ([M-H]-); ИК (тонкая пленка) 3027, 1654, 815 см-1.
Пример 24: Получение оксима 6-((E)-4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-3,4-дигидронафталин-1(2H)-она (BI5a)
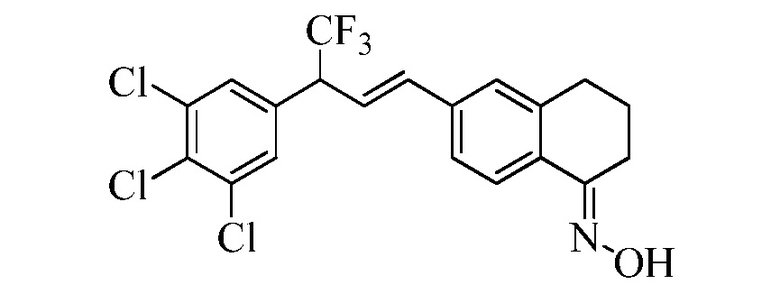
К перемешиваемому раствору ((E)-6-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-3,4-дигидронафталин-1(2H)-она (0,4 г, 0,92 ммоль) в EtOH (50 мл) добавляли гидрохлорид гидроксиламина (0,128 г, 1,85 ммоль) и ацетат натрия (0,23 г, 2,77 ммоль), и реакционную смесь нагревали при дефлегмации в течение 3 ч. Реакционную смесь выпаривали при пониженном давлении, остаток разбавляли H2O и экстрагировали EtOAc. Объединенные органические экстракты промывали рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение, которое очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 10-15% EtOAc в петролейном эфире). Указанное в заголовке соединение выделяли в виде твердого вещества (0,3 г, 73%): Т.пл. 155-158°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,89 (д, J=8,4 Гц, 1H), 7,41 (с, 2H), 7,24 (м, 1H), 7,17 (м, 1H), 6,57 (д, J=16 Гц, 1H), 6,46 (дд, J=16,0, 8,0 Гц, 1H), 4,13 (м, 1H), 2,82 (м, 4H), 2,04 (м, 2H); ЭРИ-МС m/z 445,95 ([M-H]-).
Пример 25: Получение (E)-5-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-енил)-2,3-дигидро-1H-инден-1-амина (BI5b)
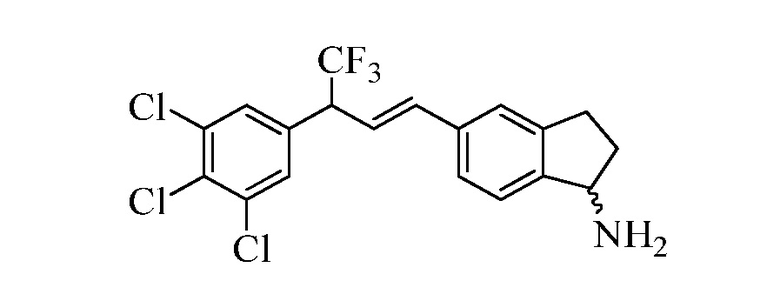
К перемешиваемому раствору (E)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2,3-дигидро-1H-инден-1-он (1 г, 2,39 ммоль) в CH3OH (10 мл) добавляли ацетат аммония (1,84 г, 23,9 ммоль) и цианоборогидрид натрия (NaCNBH3; 0,44 г, 7,17 ммоль), и реакционную смесь нагревали при дефлегмации в течение 16 ч. Реакционную смесь выпаривали при пониженном давлении, остаток разбавляли H2O и экстрагировали EtOAc. Объединенные органические экстракты промывали H2O и насыщенным водным раствором гидрокарбоната натрия (нас. водн. NaHCO3), сушили над безводным Na2SO4 и выпаривали при пониженном давлении с получением указанного в заголовке соединения в виде жидкости (500 мг, неочищенный): 1H-ЯМР (400 МГц, ДМСО-d6) δ 7,85 (с, 2H), 7,40 (с, 1H), 7,30 (с, 2H), 6,71 (с, 2H), 4,78 (м, 1H), 4,2 (м, 1H), 2,80 (м, 1H), 2,73 (м, 1H), 1,60 (м, 2H); ЭРИ-МС m/z 419,02 ([M+H]+); ИК (тонкая пленка) 2924, 1552, 1112, 807 см-1.
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 25.
(E)-5-(3-(3,5-Дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2,3-дигидро-1H-инден-1-амин (BI7)
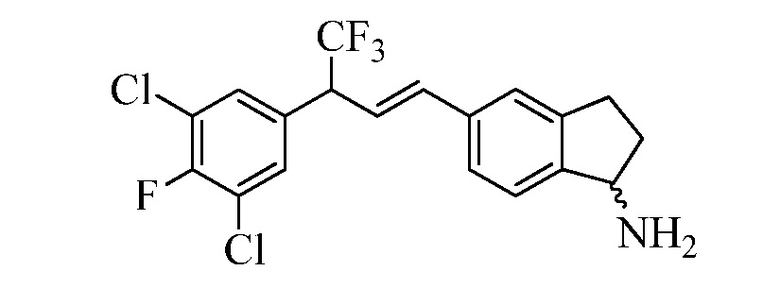
Продукт выделяли в виде светло-коричневого смолистого материала, который использовали без очистки в следующей стадии (0,15 г, неочищенное соединение): ЭРИ-МС m/z 401,97 ([M-H]-).
(E)-5-(3-(3,5-Дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-фтор-2,3-дигидро-1H-инден-1-амин (BI8)
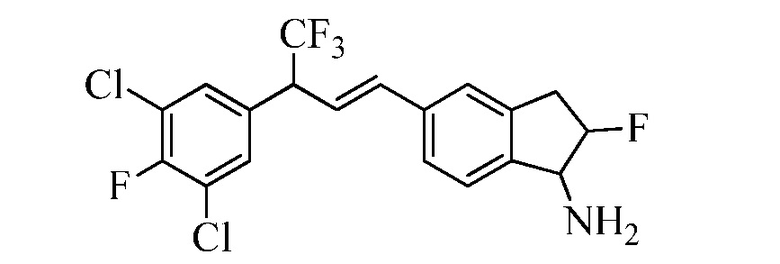
Продукт выделяли в виде светло-коричневого смолистого материала, который использовали без очистки в следующей стадии (0,15 г, неочищенное соединение): ЭРИ-МС m/z 420,15 ([M-H]-).
(E)-6-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-1,2,3,4-тетрагидронафталин-1-амин (BI9)
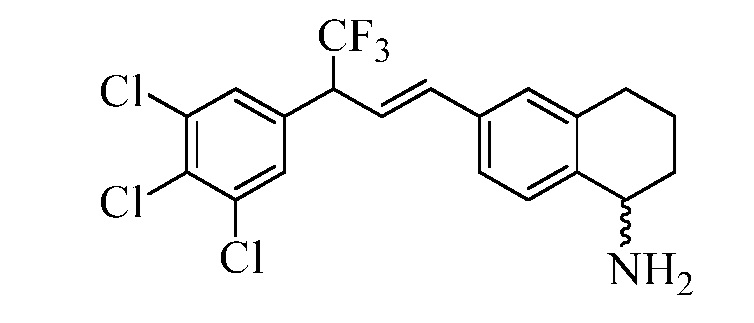
Продукт выделяли в виде светло-желтой жидкости (500 мг, неочищенный).
Пример 26: Получение (E)-1-метил-3-(5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)-бут-1-енил)-2,3-дигидро-1H-инден-1-ил)тиомочевины (BC1)

К перемешиваемому раствору (E)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2,3-дигидро-1H-инден-1-амина (0,1 г, 0,23 ммоль) в Et2O (5 мл) добавляли метилизотиоцианат (0,026 г, 0,35 ммоль) и перемешивали смесь в течение 2 ч при 25°C. Реакционную смесь выпаривали при пониженном давлении и остаток очищали с помощью колоночной флеш-хроматографии (SiO2, 20% EtOAc в петролейном эфире). Указанное в заголовке соединение выделяли в виде жидкости (65 мг, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 7,39 (с, 2H), 7,25-7,18 (м, 3H), 6,58 (д, J=16,0 Гц, 1H), 6,30 (дд, J=16,0, 8,4 Гц, 1H), 5,91-5,70 (шир., 2H), 4,05 (м, 1H), 3,05-2,80 (м, 6H), 2,70 (м, 1H), 1,81 (м, 1H); ЭРИ-МС m/z 492,17 ([M+H]+); ИК (тонкая пленка) 3211, 1569, 1113, 806 см-1.
Соединения BC2-BC3 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 26.
Пример 27: Получение (E)-3,3,3-трифтор-N-(5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2,3-дигидро-1H-инден-1-ил)пропанамида (BC4)
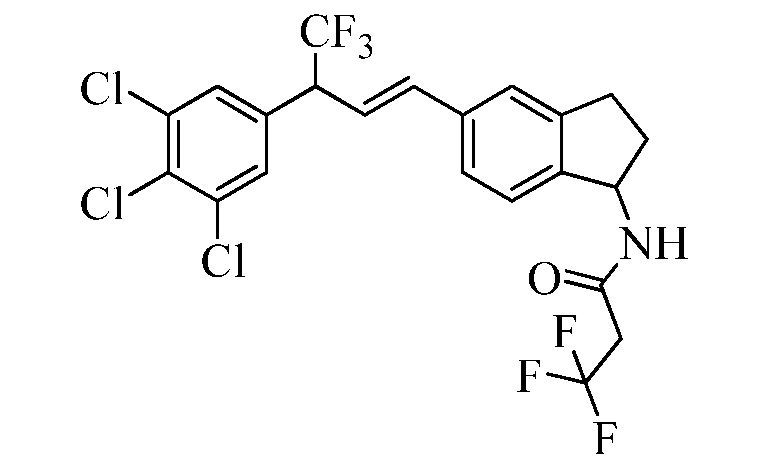
К перемешиваемому раствору (E)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2,3-дигидро-1H-инден-1-амина (0,1 г, 0,23 ммоль) в CH2Cl2 (10 мл) добавляли трифторпропионовую кислоту (0,044 г, 0,34 ммоль), EDC·HCl (0,038 г, 0,35 ммоль), HOBt·H2O (0,07 г, 0,46 ммоль) и DIEA (0,074 г, 0,57 ммоль), и реакционную смесь перемешивали в течение 16 ч при 25°C. Реакционную смесь разбавляли CH2Cl2 и промывали H2O. Объединенный органический слой промывали рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Неочищенный материал очищали с помощью колоночной флеш-хроматографии (SiO2, 15% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде жидкости (65 мг, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 7,39 (с, 2H), 7,25-7,20 (м, 3H), 6,34 (д, J=16,0 Гц, 1H), 6,30 (дд, J=16,0, 8,0 Гц, 1H), 5,81 (шир., 1H), 5,48 (м, 1H), 4,10 (м, 1H), 3,10 (м, 2H), 2,86-3,07 (м, 2H), 2,86 (м, 1H), 1,81 (м, 1H); ЭРИ-МС m/z 529,02 ([M+H]+); ИК (тонкая пленка) 3283, 1652, 1241, 811 см-1.
Соединения BC5-BC9, BC11 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 27.
Пример 28: Получение трет-бутил-5-винилиндолин-1-карбоксилата (BI10)
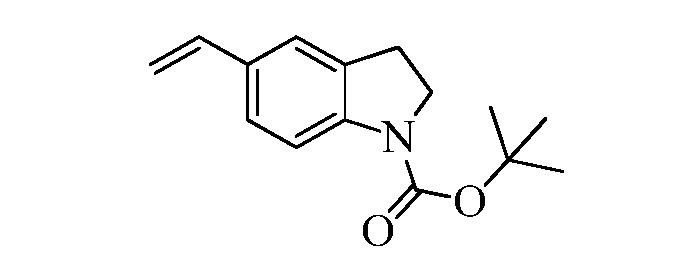
Стадия 1. 5-Бром-индолин (BI11): К 5-бром-1H-индолу (2,5 г, 12,82 ммоль) в уксусной кислоте (10,0 мл), порциями добавляли NaCNBH3 (2,38 г, 38,46 ммоль) при 10°C в течение 20 мин. После этого реакционную смесь перемешивали при КТ в течение 3 ч. Реакционную смесь разбавляли водой и экстрагировали диэтиловым эфиром. Органический слой промывали насыщенным NaHCO3, водой и солевым раствором. Объединенный эфирный слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде бледно-желтого полутвердого вещества (1,8 г, 71%).
Стадия 2. трет-Бутил-5-броминдолин-1-карбоксилат (BI12): К перемешиваемому раствору 5-бром-индолина (3,0 г, 15ммоль) в ацетонитриле (100 мл) добавляли DMAP (0,185 г, 1,522 ммоль) и ди-трет-бутил-дикарбонат (3,98 г, 18,3 ммоль) и реакцию перемешивали при КТ в течение 16 ч. Реакционную смесь выпаривали при пониженном давлении с получением остатка, который разбавляли диэтиловым эфиром и промывали солевым раствором (2×) и водой. Объединенный эфирный слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенный продукт в виде грязно-белого твердого вещества, который использовали в следующей стадии без дополнительной очистки (3,0 г).
Стадия 3. трет-Бутил-5-винилиндолин-1-карбоксилат (BI10): Перемешиваемый раствор трет-бутил-5-броминдолин-1-карбоксилата (2,0 г, 6,73 ммоль), винилтрифторбората калия (2,6 г, 20,20 ммоль) и K2CO3 (2,78 г, 20,2 ммоль) в ДМСО (50,0 мл) дегазировали аргоном в течение 20 минут при КТ. Добавляли PdCl2(dppf) (0,49 г, 0,67 ммоль) при КТ, после чего реакционную смесь нагревали до 100°C в течение 3 ч. Реакционную смесь охлаждали до КТ и фильтровали через слой целита под вакуумом и промывали диэтиловым эфиром. Реакционную смесь экстрагировали диэтиловым эфиром. Объединенный слой диэтилового эфира сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенный продукт. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; элюирование 2% этилацетатом/петролейным эфиром), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (1,2 г, 73%): Т.пл. 85,5-88,6°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,23 (м, 3H), 6,69 (дд, J=17,4, 10,8 Гц, 1H), 5,64 (д, J=10,5 Гц, 1H), 5,13 (д, J=10,5 Гц, 1H), 4,00 (т, J=9,0 Гц, 2H), 3,10 (т, J=9,0 Гц, 2H), 1,55 (шир.с, 9H).
Пример 29: Получение (E)-трет-бутил-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)индолин-1-карбоксилата (BI13)
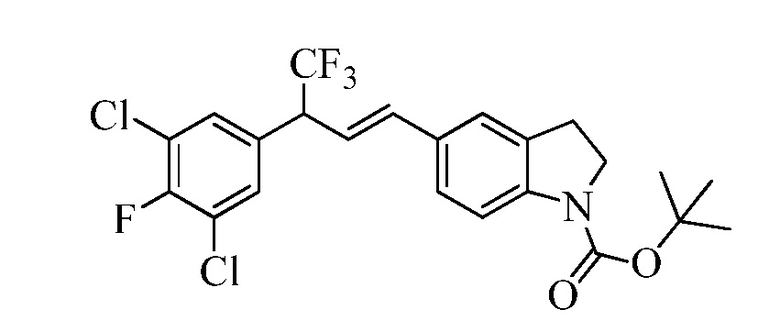
К перемешиваемому раствору трет-бутил-5-винилиндолин-1-карбоксилата (1,28 г, 5,23 ммоль) в 1,2-дихлорбензоле (10,0 мл), добавляли 5-(1-бром-2,2,2-трифторэтил)-1,3-дихлор-2-фторбензол (3,4 г, 10 ммоль), CuCl (103 мг, 1,05 ммоль) и 2,2-бипиридил (0,326 г, 2,092 ммоль) и дегазировали полученную реакционную смесь аргоном в течение 30 мин и нагревали до 150°C в течение 1 ч. Реакционную смесь охлаждали до КТ и фильтровали, и фильтрат выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 2% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде бледно-желтого смолистого вещества (0,3 г, 61%): 1H-ЯМР (400 МГц, CDCl3) δ 7,34 (д, J=6,0 Гц, 2H), 7,22 (с, 2H), 7,16 (д, J=8,4 Гц, 1H), 6,52 (д, J=16,0 Гц, 1H), 6,21 (дд, J=16,0, 7,6 Гц, 1H), 4,07 (м, 3H), 3,10 (т, J=8,4 Гц, 2H), 1,55 (с, 9H); ЭРИ-МС m/z 433,79 ([M-H]-); ИК (тонкая пленка) 1168, 858 см-1.
Пример 30: Получение (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)индолин-1-амин (BI14)
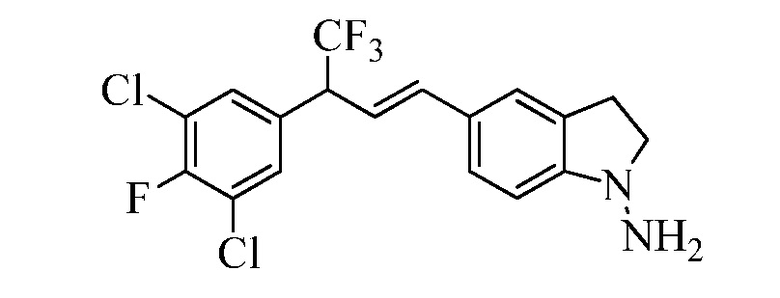
Стадия 1. (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифтор-бут-1-енил)индолин (BI15). К перемешиваемому раствору (E)-трет-бутил-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)индолин-1-карбоксилата (0,2 г, 0,4 ммоль) в ДХМ (10,0 мл) добавляли ТФУ (0,6 мл) и перемешивали реакцию при КТ в течение 2 ч. Реакционную смесь разбавляли ДХМ, промывали насыщенным водн. раствором NaHCO3, водой и солевым раствором. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенный продукт в виде светло-коричневого смолистого материала, который использовали в следующей стадии без дополнительной очистки (0,12 г): 1H-ЯМР (400 МГц, CDCl3) δ 7,33 (д, J=6,4 Гц, 2H), 7,21 (с, 1H), 7,02 (д, J=8,0 Гц, 1H), 6,57 (д, J=8,4 Гц, 1H), 6,49 (д, J=15,6 Гц, 1H), 6,21 (дд, J=15,6, 8,4 Гц, 1H), 4,07 (м, 1H), 3,61 (т, J=8,4 Гц, 2H), 3,05 (т, J=8,4 Гц, 2H); ЭРИ-МС m/z 389,89 ([M+H]+); ИК (тонкая пленка) 3385, 1112, 816 см-1.
Стадия 2. 5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1-нитрозоиндолин (BI16): К (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)индолину (0,2 г, 0,5 ммоль) в концентрированной HCl (5,0 мл) при 5°C медленно добавляли NaNO2 в воде и оставляли реакцию с перемешиванием при КТ в течение 2 ч. Реакционную смесь разбавляли ДХМ, и промывали слой ДХМ солевым раствором и водой. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенный продукт в виде светло-желтого твердого вещества, которое использовали в следующей стадии без дополнительной очистки (0,2 г): 1H-ЯМР (400 МГц, CDCl3) δ 7,33 (д, J=8,4 Гц, 1H), 7,39 (м, 4H), 6,61 (д, J=16,0 Гц, 1H), 6,35 (дд, J=16,0, 8,4 Гц, 1H), 4,07 (м, 3H), 3,23 (т, J=8,4 Гц, 2H); ЭРИ-МС m/z 418,82 ([M+H]+); ИК (тонкая пленка) 1488, 1112, 860 см-1.
Стадия 3. (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифтор-бут-1-ен-1-ил)индолин-1-амин (BI14): К (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1-нитрозоиндолину (0,1 г, 0,2 ммоль) в метаноле (10,0 мл) добавляли порошок цинка (77,5 мг) и NH4Cl (36,9 мг, 0,69 ммоль) в воде (2,0 мл). Реакционную смесь перемешивали при КТ в течение 3 ч. Реакционную смесь разбавляли ДХМ, и промывали слой ДХМ солевым раствором и водой. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение, которое очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; элюирование 2% этилацетатом/петролейным эфиром), получив указанное в заголовке соединение в виде светло-коричневого смолистого материала (0,08 г): ЭРИ-МС m/z 404,86 ([M+H]+).
Пример 31: Получение (E)-N-(5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)индолин-1-ил)-3,3,3-трифторпропанамида (BC12)
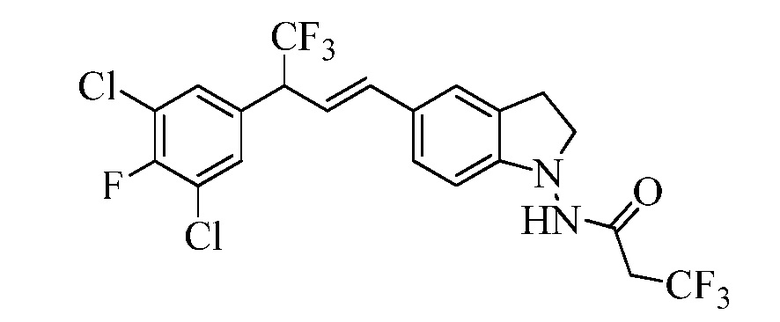
К перемешиваемому раствору (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)индолин-1-амина (0,1 г, 0,247 ммоль) в ДХМ (10,0 мл) добавляли 3,3,3-трифторпропановую кислоту (0,038 г, 0,297 ммоль), PyBOP (0,192 г, 0,370 ммоль) и DIEA (0,047 г, 0,370 ммоль) и реакцию перемешивали при КТ в течение 18 ч. Реакционную смесь разбавляли ДХМ, отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; этилацетат 20-25%/петролейный эфир), получив указанное в заголовке соединение в виде светло-коричневого смолистого материала (0,12 г, 33%): 1H-ЯМР (400 МГц, CDCl3) δ 7,32, (д, J=6,0 Гц, 2H) 7,28 (м, 1H), 7,20 (д, J=8,0, 1H), 7,14 (д, J=8,8, 1H), 6,70 (д, J=8,0 Гц, 1H), 6,60 (м, 2H), 4,15 (м, 1H), 3,85 (м, 1H), 3,65 (м, 1H), 3,46 (м, 2H), 3,19 (м, 2H); ЭРИ-МС m/z 514,86 ([M+H]+); ИК (тонкая пленка) 3428, 1112, 857 см-1.
Пример 32: Получение трет-бутил-5-винил-1H-индол-1-карбоксилата (BI17)
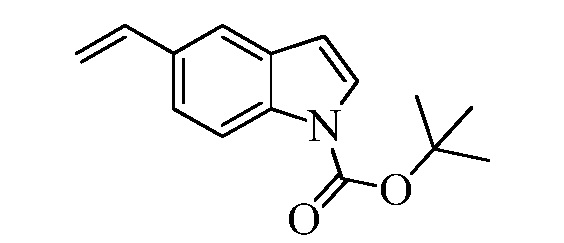
Стадия 1. 5-Винил-1H-индол (BI18): Смесь 5-бром-1H-индола (2,5 г, 12,82 ммоль), винилтрифторборат калия (2,57 г, 19,2 ммоль), Cs2CO3 (12,53 г, 38,46 ммоль) и трифенилфосфин (201 мг, 0,769 ммоль) в ТГФ/воде (9:1, 75 мл) дегазировали аргоном в течение 20 минут, затем вводили PdCl2 (45,3 мг, 0,256 ммоль). Реакционную смесь нагревали с обратным холодильником до кипения в течение 16 ч, затем охлаждали до КТ, фильтровали через слой целита и промывали этилацетатом. Фильтрат снова экстрагировали этилацетатом и объединенный органический слой промывали водой и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 2% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде светло-коричневого смолистого материала (1,5 г, 83%): 1H-ЯМР (400 МГц, CDCl3) δ 8,20 (шир., 1H), 7,68 (с, 1H), 7,45 (с, 2H), 7,21 (м, 1H), 6,90 (дд, J=16,0, 10,8 Гц, 1H), 6,55 (м, 1H), 5,75 (д, J=10,5 Гц, 1H), 5,21 (д, J=10,5 Гц, 1H); ЭРИ- МС m/z 142,05 ([M-H]-).
Стадия 2. трет-Бутил-5-винил-1H-индол-1-карбоксилат (BI17): К перемешиваемому раствору 5-винил-1H-индола (0,7 г, 4,89 ммоль) в ацетонитриле (20 мл) добавляли DMAP (59,65 мг, 0,489 ммоль) и ди-трет-бутил-дикарбонат (1,38 г, 6,36 ммоль) и перемешивали реакцию при КТ в течение 3 ч. Реакционную смесь выпаривали при пониженном давлении с получением остатка, который разбавляли ДХМ и промывали солевым раствором и водой. Объединенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 2% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде грязно-белого полутвердого вещества (0,7 г, 59%): 1H-ЯМР (400 МГц, CDCl3) δ 8,15 (д, J=8,0 Гц, 1H), 7,60 (с, 2H), 7,30 (д, J=8,4 Гц, 1H), 7,21 (м, 1H), 6,90 (дд, J=16,0, 10,8 Гц, 1H), 6,59 (с, 1H), 5,75 (д, J=10,5 Гц, 1H), 5,21 (д, J=10,5 Гц, 1H), 1,65 (с, 9H); ЭРИ-МС m/z 242,10 ([M-H]-); ИК (тонкая пленка) 1630 см-1.
Пример 33: Получение (E)-трет-бутил-5-(3-(3,5-дихлор-4-фторфе-нил)-4,4,4-трифторбут-1-ен-1-ил)-1H-индол-1-карбоксилата (BI19)
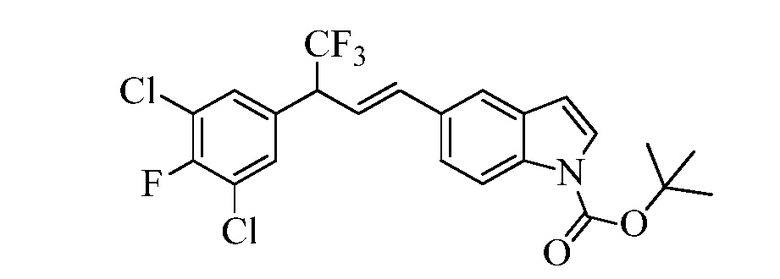
К перемешиваемому раствору трет-бутил-5-винил-1H-индол-1-карбоксилата (0,65 г, 2,67 ммоль) в 1,2-дихлорбензоле (10,0 мл) добавляли 5-(1-бром-2,2,2-трифторэтил)-1,3-дихлор-2-фторбензол (1,74 г, 5,37 ммоль), CuCl (53 мг, 0,537 ммоль) и 2,2-бипиридил (167 мг, 1,07 ммоль). Полученную реакционную смесь дегазировали аргоном в течение 30 мин и нагревали до 150°C в течение 2 ч. Реакционную смесь охлаждали до КТ и фильтровали, и фильтрат выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 2% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде светло-коричневого смолистого материала (0,25 г, 10%): 1H-ЯМР (400 МГц, CDCl3) δ 8,20 (д, J=8,0 Гц, 1H), 7,60 (м, 2H), 7,39 (м, 3H), 6,69 (д, J=16,0 Гц, 1H), 6,55 (д, J=10,5 Гц, 1H), 6,36 (дд, J=16,0, 8,0 Гц, 1H), 4,10 (м, 1H), 1,65 (с, 9H); ЭРИ-МС m/z 485,91 ([M-H]-); ИК (тонкая пленка) 1165, 854 см-1.
Пример 34: Получение (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1-индола (BI20)
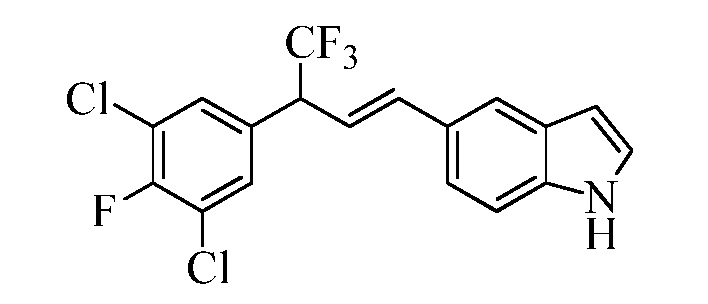
К перемешиваемому раствору (E)-трет-бутил-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1H-индол-1-карбоксилата (0,2 г, 0,40 ммоль) в ДХМ (10,0 мл) добавляли ТФУ (70 мг, 0,61 ммоль) и перемешивали реакцию при КТ в течение 2 ч. Реакционную смесь разбавляли ДХМ и промывали насыщенным раствором NaHCO3, водой и солевым раствором. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде светло-коричневого твердого вещества (0,2 г, 97%): Т.пл. 132,9-138,8°C; 1H-ЯМР (400 МГц, CDCl3) δ 11,19 (шир., 1H), 8,20 (д, J=8,0 Гц, 1H), 7,60 (м, 2H), 7,39 (м, 3H), 6,69 (д, J=16,0 Гц, 1H), 6,55 (д, J=10,5 Гц, 1H), 6,36 (дд, J=16,0, 8,0 Гц, 1H), 4,82 (м, 1H); ЭРИ-МС m/z 387,98 ([M+H]+).
Пример 35: Получение 4-нитрофенил-2-((трет-бутоксикарбонил)ами-но)ацетата (BI21)
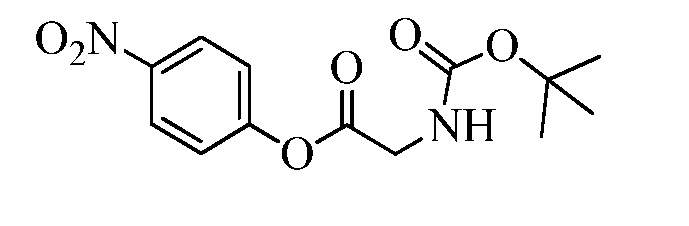
К перемешиваемому раствору 4-нитрофенола (1,0 г, 7,19 ммоль) в ДХМ (20,0 мл) добавляли N-Boc-глицин (1,38 г, 7,91 ммоль) и EDC·HCl (2,05 г, 10,785 ммоль) и перемешивали реакцию при КТ в течение 24 ч. Реакционную смесь разбавляли ДХМ и промывали водой и насыщенным солевым раствором. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде светло-коричневого смолистого материала, который использовали в следующей стадии без дополнительной очистки (1,1 г): 1H-ЯМР (400 МГц, CDCl3) δ 8,29 (д, J=9,2 Гц, 2H), 7,33 (д, J=8,8 Гц, 2H), 5,07 (шир., 1H), 4,20 (с, 2H), 1,47 (с, 9H); ЭРИ-МС m/z 296,27 ([M+H]+).
Пример 36: Получение (E)-трет-бутил-(2-(5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1H-индол-1-ил)-2-оксоэтил)карбамата (BI22)
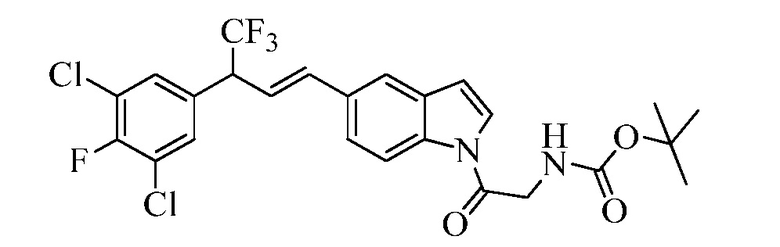
К перемешиваемому раствору (E)-5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1H-индола (0,1 г, 0,258 ммоль) в ацетонитриле (5,0 мл) добавляли 4-нитрофенил-2-(трет-бутоксикарбониламино)ацетат (0,114 г, 0,387 ммоль), фторид калия (0,03 г, 0,516 ммоль), 18-краун-6-эфир (0,075 г, 0,283 ммоль) и DIEA (0,0332 г, 0,258 ммоль) и реакцию перемешивали при КТ в течение 16 ч. Реакционную смесь выпаривали с получением остатка, который разбавляли ДХМ и промывали солевым раствором и водой. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке неочищенное соединение в виде светло-коричневого смолистого материала, который использовали в следующей стадии без дополнительной очистки (0,1 г): ЭРИ-МС m/z 545,23 ([M+H]+).
Пример 37: Получение (E)-N-(2-(5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1H-индол-1-ил)-2-оксоэтил)-3,3,3-трифторпропанамида (BC13)
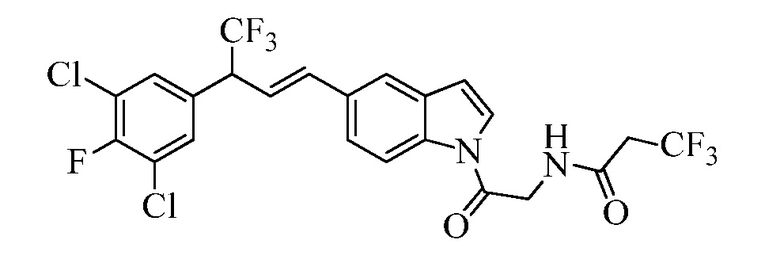
Стадия 1. (E)-2-Амино-1-(5-(3-(3,5-дихлор-4-фторфенил)- 4,4,4-трифторбут-1-енил)-1H-индол-1-ил)этанон (BI23): К перемешиваемому раствору (E)-трет-бутил-2-(5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1H-индол-1-ил)-2-оксоэтилкарбамата (0,05 г, 0,09 ммоль) в ДХМ (5,0 мл) добавляли ТФУ (0,01 мл) и перемешивали реакцию при КТ в течение 16 ч. Реакционную смесь разбавляли ДХМ и промывали насыщенным раствором NaHCO3, водой и солевым раствором. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке неочищенное соединение, которое использовали в следующей стадии без дополнительной очистки (50 мг).
Стадия 2. (E)-N-(2-(5-(3-(3,5-Дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1H-индол-1-ил)-2-оксоэтил)-3,3,3-трифторпропанамид (BC13): К перемешиваемому раствору (E)-2-амино-1-(5-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1H-индол-1-ил)этанона (0,04 г, 0,09 ммоль) в ДХМ (5,0 мл) добавляли 3,3,3-трифторпропановую кислоту (17,5 мг, 0,136 ммоль), PyBOP (70 мг, 0,135 ммоль) и DIEA (29 мг, 0,225 ммоль) и перемешивали реакцию при КТ в течение 16 ч. Реакционную смесь разбавляли ДХМ, и слой ДХМ промывали водой и насыщенный солевым раствором. Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение, которое очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 10% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (30 мг, 60%): Т.пл. 121-126°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,33 (шир., 1H), 7,59 (с, 1H), 7,45 (м, 4H), 6,72 (д, J=3,6 Гц, 3H), 6,39 (м, 1H), 4,71 (т, J=7,2 Гц, 2H), 4,15 (м, 1H), 3,51 (м, 1H), 3,28 (м, 1H); ЭРИ-МС m/z 553,06 ([M-H]-).
Пример 38: Получение этил-2-(1-оксо-6-винилфталазин-2(1H)-ил)ацетата (BI24)
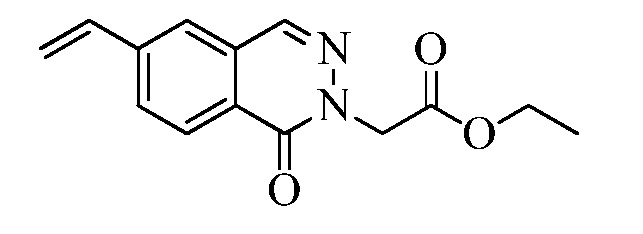
Стадия 1. 5-Бром-3-гидроксиизоиндолин-1-он (BI25): Смесь порошка Zn (1,73 г, 26,154 ммоль), пентагидрата сульфата меди (II) (0,02 г, 0,08 ммоль) и 2M водн. NaOH (27 мл) охлаждали до 0°C. При этой же температуре добавляли 5-бромизоиндолин-1,3-дион (5 г, 22 ммоль) в течение 30 мин, реакционную смесь перемешивали при 0°C в течение 30 мин и 3 ч при КТ. Реакционную смесь фильтровали и фильтрат нейтрализовывали концентрированной HCl. Реакционную смесь разбавляли этанолом и экстрагировали этилацетатом. Объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке неочищенное соединение в виде коричневого твердого вещества, которое использовали в следующей стадии без дополнительной очистки (1,3 г): 258-261°C Т.пл.; 1H-ЯМР (400 МГц, ДМСО-d6) δ 9,03 (шир., 1H), 7,81 (м, 2H), 7,69 (м, 1H), 6,44 (м, 1H), 5,88 (д, J=9,3 Гц, 1H); ЭРИ-МС m/z 225,83 ([M-H]-); ИК (тонкая пленка) 1684, 3246, 606 см-1.
Стадия 2. 6-Бромфталазин-1(2H)-он (BI26): К перемешиваемому раствору 5-бром-3-гидроксиизоиндолин-1-она (1,0 г, 4,40 ммоль) в воде добавляли гидрат гидразина (0,45 г, 8,80 ммоль) и нагревали до 95°C в течение 5 ч. Реакционную смесь охлаждали до КТ, фильтровали и промывали диэтиловым эфиром и пентаном (1:1), получив указанное в заголовке соединение в виде белого твердого вещества, которое использовали в следующей стадии без дополнительной очистки (0,5 г): ЭРИ-МС m/z 225,15 ([M+H]+).
Стадия 3. 6-Винилфталазин-1(2H)-он (BI27): Раствор 6-бромфталазин-1(2H)-она (0,25 г, 1,11 ммоль), винилтрифторбората калия (0,446 г, 3,33 ммоль) и K2CO3 (0,46 г, 3,33 ммоль) в ДМСО (2 мл) дегазировали аргоном в течение 20 мин при КТ. Добавляли PdCl2(dppf) (0,04 г, 0,055 ммоль) при КТ и реакционную смесь нагревали до 80°C в течение 2 ч. Реакционную смесь охлаждали до КТ, фильтровали через слой целита под вакуумом и промывали этилацетатом. Реакционную смесь экстрагировали этилацетатом, объединенный этилацетатный слой сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенный продукт. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 50% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде коричневого твердого вещества (0,12 г, 63%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,61 (шир., 1H), 8,33 (м, 1H), 8,19 (м, 1H), 8,01 (м, 2H), 6,97 (м, 1H), 6,15 (м, 1H), 5,56 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 172,93 ([M+H]+); ИК (тонкая пленка) 1748, 1655, 3241 см-1.
Стадия 4. Этил-2-(1-оксо-6-винилфталазин-2(1H)-илацетат (BI24): К перемешиваемому раствору 6-винилфталазин-1(2H)-она (0,5 г, 2,90 ммоль) в ДМФА (5,0 мл) добавляли Cs2CO3 (0,94 г, 2,90 ммоль) и реакцию перемешивали 10 мин. К реакционной смеси добавляли этилбромацетат (0,48 г, 2,90 ммоль) при КТ и реакцию перемешивали в течение 8 ч при КТ. Реакционную смесь разбавляли и экстрагировали этилацетатом и этилацетатный слой промывали солевым раствором (2×) и водой. Отделенный этилацетатный слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенный продукт. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 25% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде коричневого твердого вещества (0,34 г, 45%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 8,45 (м, 1H), 8,24 (м, 1H), 8,04 (м, 2H), 7,01 (м, 1H), 6,17 (д, J=2,1 Гц, 1H), 5,56 (д, J=10,8 Гц, 1H), 4,92 (с, 2H), 4,19 (м, 2H), 1,23 (м, 3H). ЭРИ-МС m/z 259,10 ([M+H]+); ИК (тонкая пленка) 1750, 1660 см-1.
Пример 39: Получение (E)-этил-2-(6-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1-оксофталазин-2(1H)-ил)ацетата (BI28)
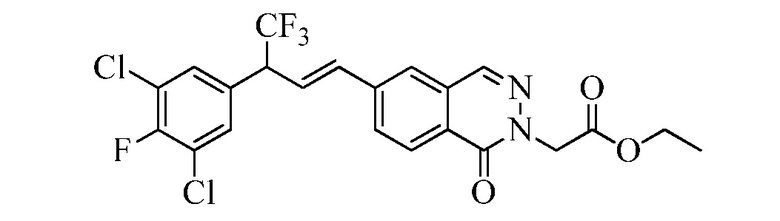
К перемешиваемому раствору этил-2-(1-оксо-6-винилфталазин-2 (1H)-илацетата (0,07 г, 0,27 ммоль) в 1,2-дихлорбензоле (1,0 мл) добавляли 5-(1-бром-2,2,2-трифторэтил)-1,3-дихлор-2фторбензол (0,17 г, 0,54 ммоль), CuCl (0,005 г, 0,05 ммоль) и 2,2-бипиридил (0,016 г, 0,10 ммоль) и полученную реакционную смесь дегазировали аргоном в течение 30 мин и нагревали до 180°C в течение 12 ч. Реакционную смесь охлаждали до КТ и фильтровали, и фильтрат выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 10-15% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде коричневого твердого вещества (40 мг, 29%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 8,40 (д, J=8,4 Гц, 1H), 7,84 (д, J=1,5 Гц, 1H), 7,65 (с, 1H), 7,37 (д, J=6,3 Гц, 2H), 6,76 (д, J=16,0 Гц, 1H), 6,59 (дд, J=16,0, 8,0 Гц, 1H), 4,96 (с, 2H), 4,29 (м, 3H), 1,31 (т, J=7,2 Гц, 3H); ЭРИ-МС m/z 503,0 ([M+H]+); ИК (тонкая пленка) 1660, 1114, 817 см-1.
Пример 40: Получение (E)-2-(6-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1-оксофталазин-2(1H)-ил)уксусной кислоты (BI29)
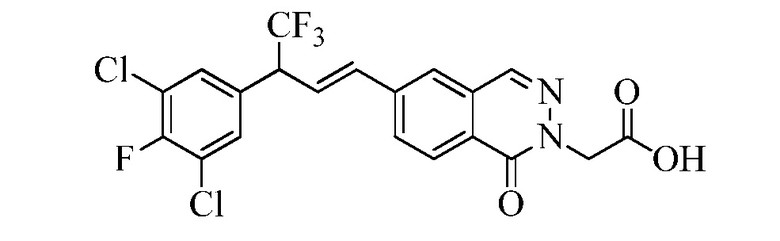
Раствор (E)-этил-2-(6-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1-оксофталазин-2(1H)-ил)ацетата (0,04 г, 0,07 ммоль) в HCl (0,5 мл) и уксусной кислоте (0,5 мл) нагревали до 100°C в течение 3 ч. Растворитель удаляли при пониженном давлении и остаток разбавляли водой. Водный слой экстрагировали этилацетатом, отделенный этилацетатный слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение. Неочищенное соединение растирали в смеси диэтилового эфира и пентана, получив указанное в заголовке соединение в виде коричневого твердого вещества (0,03 г): 1H-ЯМР (400 МГц, ДМСО-d6) δ 13,0 (шир. с, 1H), 8,43 (м, 1H), 8,23 (д, J=8,1 Гц, 1H), 8,14 (м, 2H), 7,91 (м, 2H), 7,16 (дд, J=16,0, 8,0 Гц, 1H), 6,99 (д, J=16,0 Гц, 1H), 4,96 (м, 3H); ЭРИ-МС m/z 473,0 ([M-H]-); ИК (тонкая пленка) 1629, 1168, 817 см-1.
Пример 41: Получение (E)-2-(6-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)-1-оксофталазин-2(1H)-ил)-N-(2,2,2-трифтор-этил)ацетамида (BC14)
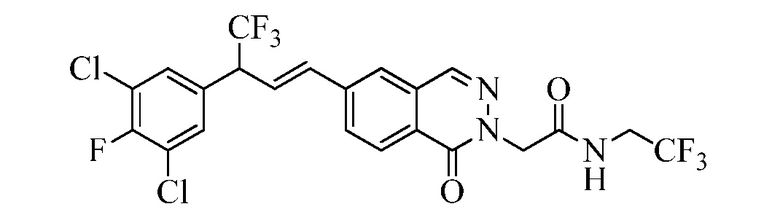
К перемешиваемому раствору (E)-2-(6-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-енил)-1-оксофталазин-2(1H)-ил)уксусной кислоты (0,15 г, 0,31 ммоль) в ДХМ (20,0 мл) добавляли 2,2,2,-трифторэтанамин (0,03 г, 0,31 ммоль), PyBOP (0,17 г, 0,34 ммоль) и DIEA (0,15 мл, 0,93 ммоль) при КТ и реакцию перемешивали в течение 18 ч. Реакционную смесь разбавляли ДХМ и промывали 3Н HCl (2×20 мл), NaHCO3 (2×20 мл) и солевым раствором (2×). Отделенный слой ДХМ сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение. Неочищенное соединение очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 20-25% этилацетат/петролейный эфир), получив указанное в заголовке соединение в виде коричневого твердого вещества (0,11 г): Т.пл. 172-175°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,83 (т, J=6,6 Гц, 1H), 8,42 (т, J=14,7 Гц, 1H), 8,22 (д, J=8,1 Гц, 1H), 8,13 (т, J=6,3 Гц, 1H), 7,98-7,86 (м, 2H), 7,16-7,07 (м, 1H), 7,01-6,93 (м, 1H), 4,96-4,81 (м, 3H), 4,00-3,88 (м, 2H); ЭРИ-МС m/z 554,0 ([M-H]-).
Пример 42: Получение 2-(4-Винилбензил)изоиндолин-1,3-диона (CI1)
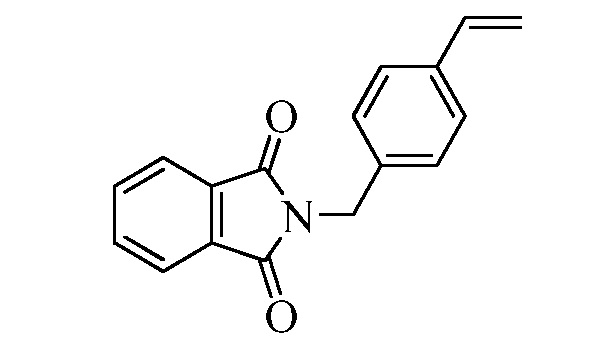
К перемешиваемому раствору 1-(хлорметил)-4-винилбензола (10 г, 66 ммоль) в ДМФА (100 мл) добавляли фталимид калия (13,3 г, 72,1 ммоль) и полученную реакционную смесь нагревали при 70°C в течение 16 ч. Реакционную смесь разбавляли H2O и экстрагировали CHCl3. Объединенный слой CHCl3 промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Перекристаллизация из CH3OH дала указанное в заголовке соединение в виде грязно- белого твердого вещества (8 г, 46%): 1H-ЯМР (400 МГц, CDCl3) δ 7,83 (м, 2H), 7,71 (м, 2H), 7,39 (м, 4H), 6,65 (дд, J=17,6, 10,8 Гц, 1H), 5,72 (д, J=17,6 Гц, 1H), 5,21 (д, J=10,8 Гц, 1H), 4,82 (с, 2H); GCMS m/z 263,2 ([М]+); ИК (тонкая пленка) 3420, 1133, 718 см-1.
Пример 43: Получение (E)-2-(4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)изоиндолин-1,3-диона (CI2)
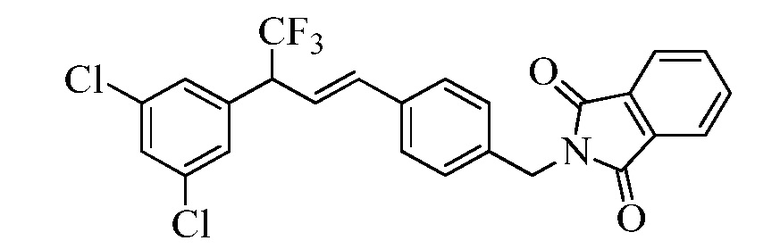
При использовании методики Примера 10 с 2-(4-винилбензил)изоиндолин-1,3-дионом и 1-(1-бромэтил)-3,5-дихлорбензолом в качестве исходных соединений, указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,3 г, 40-50%): Т.пл. 142-145°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,86 (м, 2H), 7,74 (м, 2H), 7,42 (м, 2H), 7,36 (м, 3H), 7,27 (м, 2H), 6,58 (д, J=16,0 Гц, 1H), 6,32 (дд, J=16,0, 8,0 Гц, 1H), 4,82 (с, 2H), 4,05 (м, 1H); ЭРИ-МС m/z 488,17 ([M-H]-).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 43.
(E)-2-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)изоиндолин-1,3-дион (CI3)
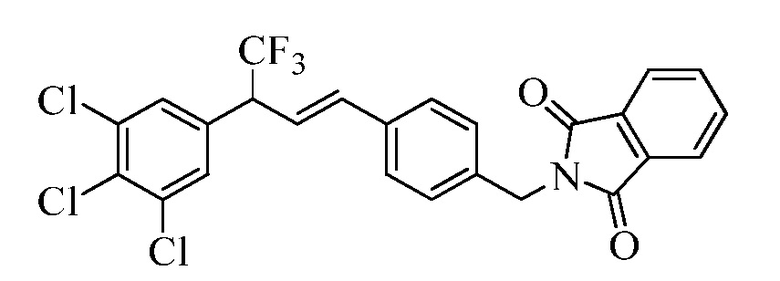
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,3 г, 56%): Т.пл. 145-146°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,86 (м, 2H), 7,74 (м, 2H), 7,42-7,31 (м, 6H), 6,58 (д, J=16,0 Гц, 1H), 6,53 (дд, J=16,0, 8,0 Гц, 1H), 4,82 (с, 2H), 4,05 (м, 1H); ЭРИ-МС m/z 522,2 ([M-H]-); ИК (тонкая пленка) 1716, 1110, 712 см-1.
Предположительно соединения CI4-CI5 (Таблица 1) могут быть получены в соответствии с методиками, раскрытыми в Примере 43.
Пример 44: Получение (E)-(4-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (CI6)
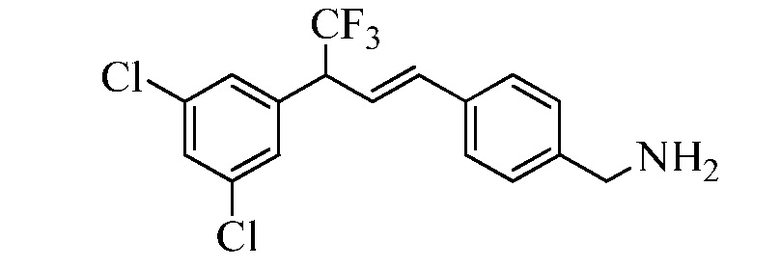
К перемешиваемому раствору (E)-2-(4-(3-(3,5-дихлорфенил)бут-1-ен-1-ил)бензил)-изоиндолин-1,3-диона (1,2 г, 2,45 ммоль) в EtOH добавляли гидрат гидразина (0,61 г, 12 ммоль) и нагревали полученную реакционную смесь при 90°C в течение 1 ч. Реакционную смесь фильтровали и выпаривали фильтрат. Остаток растворяли в CH2Cl2, промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке неочищенное соединение в виде смолистой жидкости (0,9 г), которую использовали без дополнительной очистки.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 44.
(E)-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)метанамин (CI7)
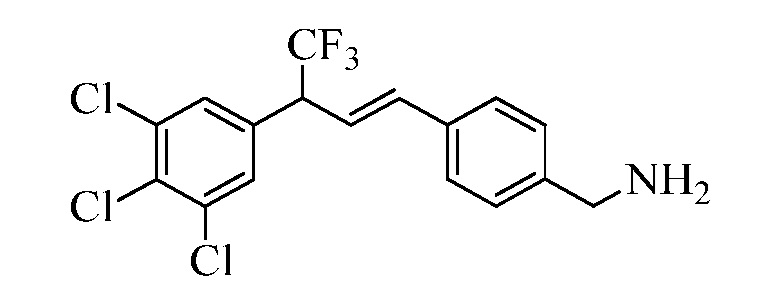
Указанное в заголовке соединение выделяли и использовали без дополнительной очистки.
Предположительно соединения CI8-CI9 (Таблица 1) могут быть получены в соответствии с методиками, раскрытыми в Примере 44.
Пример 45: Получение 4-(бромметил)-3-хлорбензонитрила (CI10)
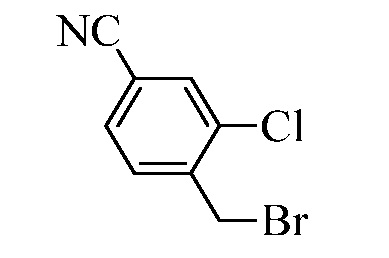
К перемешиваемому раствору 3-хлор-4-метилбензонитрила (5 г, 25,4 ммоль) в тетрахлорметане (CCl4; 50 мл) под атмосферой аргона добавляли NBS (5,16 г, 29 ммоль) и дегазировали смесь в течение 30 мин. К смеси добавляли азобисизобутиронитрил (AIBN; 0,3 г, 1,8 ммоль) и нагревали полученную реакционную смесь при дефлегмации в течение 4 ч. Реакционную смесь охлаждали до температуры окружающей среды, промывали H2O и экстрагировали CH2Cl2. Объединенный слой CH2Cl2 промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 5% EtOAc в н-гексане), получив указанное в заголовке соединение в виде белого твердого вещества (4,8 г, 68%): Т.пл. 87-88°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,71 (с, 1H), 7,59 (с, 2H), 4,60 (с, 2H); ЭРИ-МС m/z 229,77 ([M+H]+); ИК (тонкая пленка) 2235, 752, 621 см-1.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 45.
4-(Бромметил)-3-(трифторметил)бензонитрил (CI11)
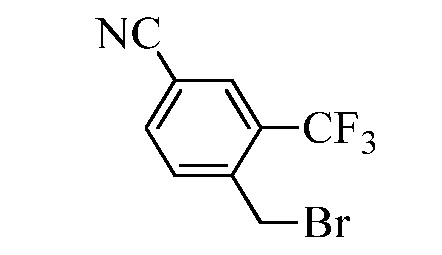
Указанное в заголовке соединение выделяли в виде грязно-белого смолистого материала (5 г, 66%): 1H-ЯМР (400 МГц, CDCl3) δ 7,96 (с, 1H), 7,86 (д, J=8,0 Гц, 1H), 7,76 (д, J=8,0 Гц, 1H), 4,62 (с, 2H); ЭРИ-МС m/z 262,11 ([M-H]-); ИК (тонкая пленка) 2236, 1132, 617 см-1.
3-Бром-4-(бромметил)бензонитрил (CI12)
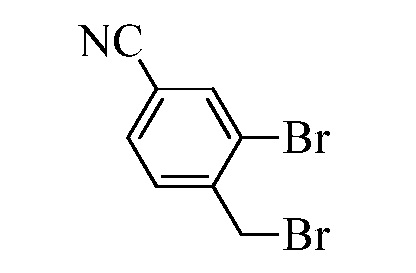
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (5 г, 67%): Т.пл. 82-83°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,90 (с, 1H), 7,61 (м, 2H), 4,62 (с, 2H); ЭИ-МС m/z 272,90; ИК (тонкая пленка) 2229, 618 см-1.
4-(Бромметил)-3-фторбензонитрил (CI13)
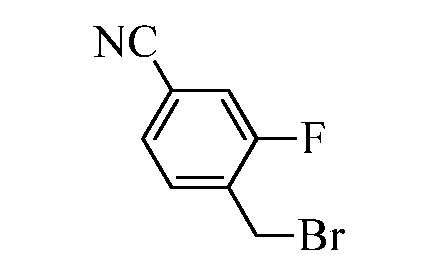
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (2 г, 60%): Т.пл. 79-81°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,54 (т, J=8,0 Гц, 1H), 7,48 (дд, J=8,0 Гц, 8,0, 1H), 7,38 (дд, J=5 Гц, 1H), 4,5 (с, 2H); ЭИ-МС m/z 215.
Пример 46: Получение 4-(бромметил)-3-хлорбензальдегида (CI14)
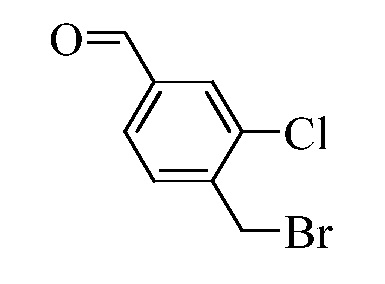
К перемешиваемому раствору 4-(бромметил)-3-хлорбензонитрила (4,8 г, 17 ммоль) в толуоле (50 мл) при 0°C по каплям добавляли диизобутилалюминийгидрид (DIBAL-H, 1,0М раствор в толуоле; 23,9 мл) и реакционную смесь перемешивали при 0°C в течение 1 ч. Добавляли 10М HCl в H2O (5 мл) до превращения реакционной смеси в белую суспензию, и затем добавляли дополнительное количество 1Н HCl (20 мл). Органический слой собирали и водный слой экстрагировали CHCl3. Объединенный органический слой сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 5% EtOAc в н-гексане), получив указанное в заголовке соединение в виде белого твердого вещества (3,8 г, 80%): Т.пл. 64-66°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,00 (с, 1H), 7,92 (с, 1H), 7,78 (д, J=8,0 Гц, 1H), 7,64 (д, J=8,0 Гц, 1H), 4,60 (с, 2H); ЭРИ-МС m/z 232,78 ([M+H]+).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 46.
4-(Бромметил)-3-(трифторметил)бензальдегид (CI15)
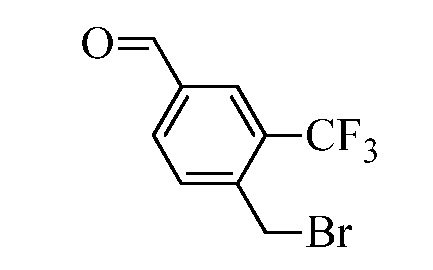
Указанное в заголовке соединение выделяли в виде бледно-желтого легкоплавкого твердого вещества (5 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 10,09 (с, 1H), 8,19 (с, 1H), 8,09 (м, 1H), 7,81 (м, 1H), 4,61 (с, 2H); ЭРИ-МС m/z 265,04 ([M-H]-); ИК (тонкая пленка) 1709, 1126, 649 см-1.
3-Бром-4-(бромметил)бензальдегид (CI16)
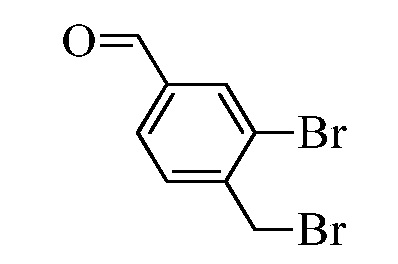
Указанное в заголовке соединение выделяли в виде светло-желтого твердого вещества (5 г, 62%): Т.пл. 94-95°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,96 (с, 1H), 8,05 (с, 1H), 7,81 (д, J=8,0 Гц, 1H), 7,62 (д, J=8,0 Гц, 1H), 4,60 (с, 2H); ЭИ-МС m/z 275,90.
4-(Бромметил)-3-фторбензальдегид (CI17)
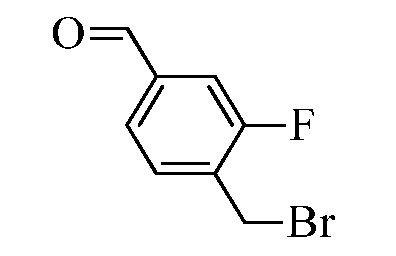
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (5 г, 61%): Т.пл. 43-45°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,1 (с, 1H), 7,54 (т, J=8 Гц, 1H), 7,48 (д, J=8 Гц, 1H), 7,38 (д, J=5 Гц, 1H), 4,5 (с, 2H); ЭИ-МС m/z 216.
Пример 47: Получение 3-хлор-4-((1,3-диоксоизоиндолин-2-ил)ме-тил)бензальдегида (CI18)
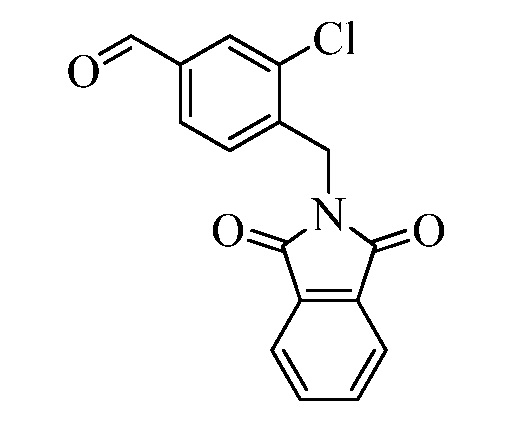
К перемешиваемому раствору 4-(бромметил)-3-хлорбензальдегида (3,8 г, 14 ммоль) в ДМФА (40 мл) добавляли фталимид калия (3,54 г, 19,14 ммоль) и смесь нагревали при 60°C в течение 6 ч. Реакционную смесь охлаждали до температуры окружающей среды и разбавляли H2O (100 мл). Полученное твердое вещество отделяли фильтрацией и сушили в вакууме, получив указанное в заголовке соединение в виде белого твердого вещества (2,8 г, 60%): Т.пл. 123-126°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,95 (с, 1H), 8,21 (с, 1H), 7,91 (м, 3H), 7,80 (м, 2H), 7,20 (м, 1H), 5,05 (с, 2H); ЭРИ-МС m/z 298,03 ([M-H]-).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 47.
4-((1,3-Диоксоизоиндолин-2-ил)-3-(трифторметил)бензальдегид (CI19)
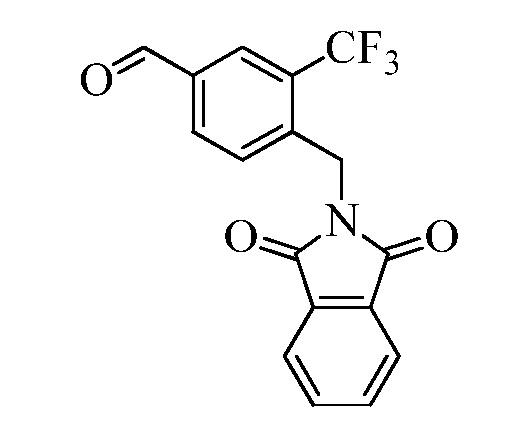
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (1 г, 62%): Т.пл. 142-143°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,05 (с, 1H), 8,15 (с, 1H), 7,91 (м, 2H), 7,80 (м, 3H), 7,27 (м, 1H), 5,19 (с, 2H); ЭРИ-МС m/z 332,03 ([M-H]-).
3-Бром-4-((1,3-диоксоизоиндолин-2-ил)метил)бензальдегид (CI20)
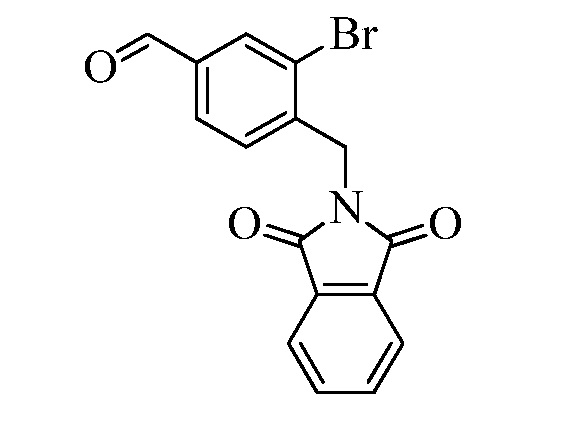
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,5 г, 64%): Т.пл. 159-161°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,95 (с, 1H), 8,21 (с, 1H), 7,91 (м, 3H), 7,80 (м, 2H), 7,20 (м, 1H), 5,05 (с, 2H); ЭРИ-МС m/z 314,00 ([М-CHO]-).
4-((1,3-Диоксоизоиндолин-2-ил)-3-фторбензальдегид (CI21)
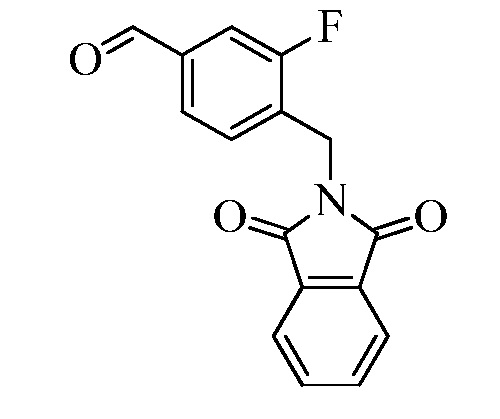
Указанное в заголовке соединение выделяли в виде белого твердого вещества (2 г, 60%): Т.пл. 154-156°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,95 (с, 1H), 7,9 (м, 2H), 7,75 (м, 2H), 7,6 (м, 2H), 7,5 (т, J=7,6 Гц, 1H), 5,05 (с, 2H); ЭИ-МС m/z 283,1.
Пример 48: Получение 2-(2-хлор-4-винилбензил)изоиндолин-1,3-диона (CI22)
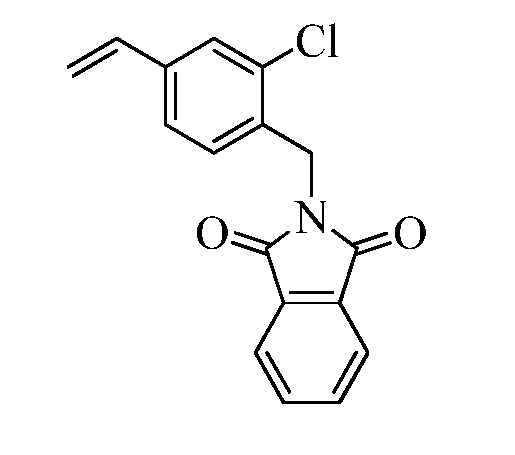
К перемешиваемому раствору 3-хлор-4-((1,3-диоксоизоиндолин-2-ил)метил)бензальдегида (2,8 г, 8,2 ммоль) в 1,4-диоксане (30 мл) добавляли K2CO3 (1,68 г, 12,24 ммоль) и метилтрифенилфос-фонийбромид (4,37 г, 12,24 ммоль) при температуре окружающей среды. Затем полученную реакционную смесь нагревали при 100°C в течение 18 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и полученный фильтрат выпаривали при пониженном давлении. Остаток очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; 20% EtOAc в н-гексане), получив указанное в заголовке соединение в виде белого твердого вещества (1,94 г, 70%): Т.пл. 141-143°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,85 (м, 2H), 7,70 (м, 2H), 7,41 (м, 1H), 7,21 (м, 2H), 6,71 (дд, J=17,6, 10,8 Гц, 1H), 5,72 (д, J=17,6 Гц, 1H), 5,23 (д, J=10,8 Гц, 1H), 4,92 (с, 2H); ЭРИ-МС m/z 298,10 ([M-H]-).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 48.
2-(2-(Трифторметил)-4-винилбензил)изоиндолин-1,3-дион (CI23)
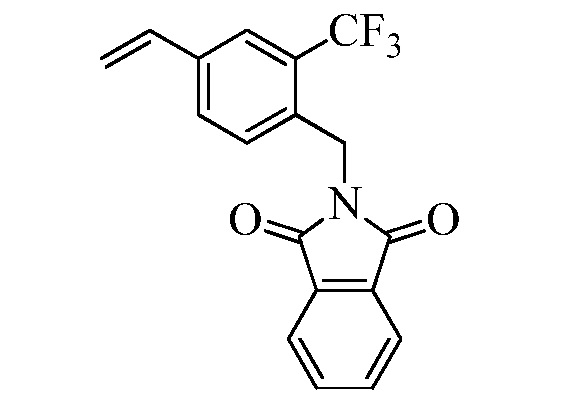
Указанное в заголовке соединение выделяли в виде светло-коричневого твердого вещества (0,5 г, 60%): Т.пл. 134-135°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,92 (м, 2H), 7,80 (м, 2H), 7,71 (с, 1H), 7,46 (д, J=8,0 Гц, 1H), 7,16 (д, J=8,0 Гц, 1H), 6,65 (м, 1H), 5,80 (д, J=17,8 Гц, 1H), 5,19 (д, J=10,8 Гц, 1H), 5,09 (с, 2H); ЭРИ-МС m/z 332,10 ([M+H]+).
2-(2-Бром-4-винилбензил)изоиндолин-1,3-дион (CI24)
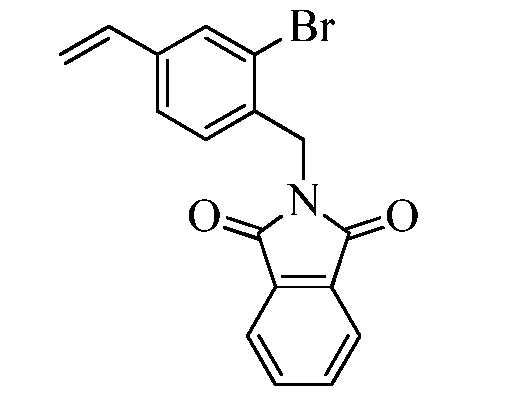
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,5 г, 62%): Т.пл. 126-128°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,92 (м, 2H), 7,79 (м, 2H), 7,62 (с, 1H), 7,21 (м, 1H), 7,16 (д, J=8,0 Гц, 1H), 6,62 (м, 1H), 5,72 (д, J=17,8 Гц, 1H), 5,15 (д, J=10,8 Гц, 1H), 4,95 (с, 2H); ЭИ-МС m/z 341,10.
2-(2-Фтор-4-винилбензил)изоиндолин-1,3-дион (CI25)
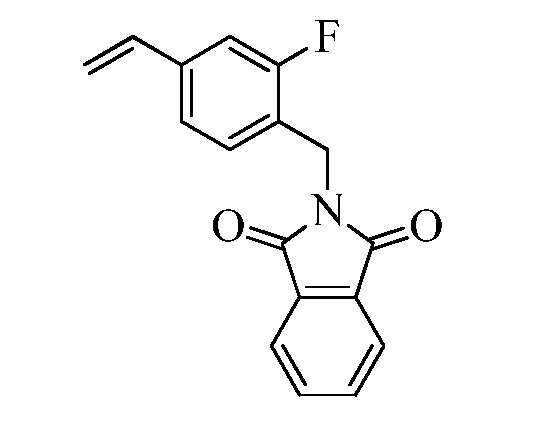
Указанное в заголовке соединение выделяли в виде белого твердого вещества (0,5 г, 61%): Т.пл. 140-142°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,85 (м, 2H), 7,72 (м, 2H), 7,25 (м, 1H), 7,11 (м, 2H), 6,63 (м, 1H), 5,80 (д, J=17,6 Гц, 1H), 5,28 (д, J=10,8 Гц, 1H), 4,92 (с, 2H); ЭИ-МС m/z 282,08.
Пример 49: Получение (E)-2-(2-хлор-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)изоиндолин-1,3-диона (CI26)
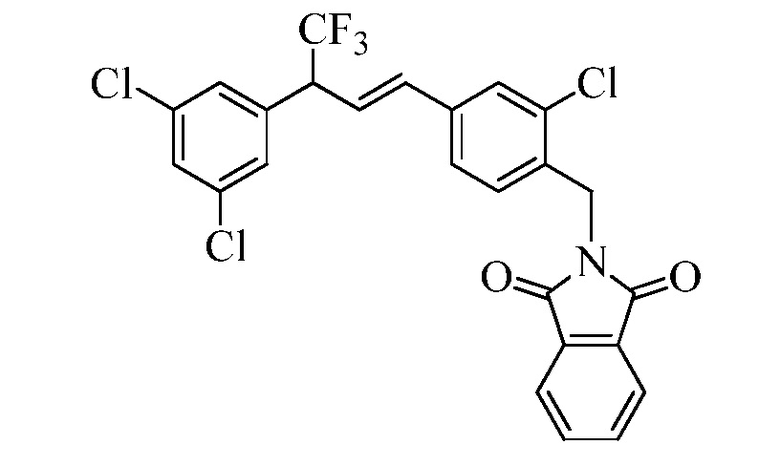
К перемешиваемому раствору 2-(2-хлор-4-винилбензил)изоиндо-лин-1,3-диона (2,0 г, 6,51 ммоль) в 1,2-дихлорбензоле (25 мл) добавляли 1-(1-бром-2,2,2-трифторэтил)-3,5-дихлорбензол (3,48 г, 11,36 ммоль), CuCl (112 мг, 1,13 ммоль) и 2,2-бипиридил (0,35 г). Полученную реакционную смесь дегазировали аргоном в течение 30 мин и затем перемешивали при 180°C в течение 24 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и фильтрат выпаривали при пониженном давлении. Остаток очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; 25-30% EtOAc в н-гексане), получив указанное в заголовке соединение в виде твердого вещества (1,3 г, 50%): Т.пл. 141-143°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,92 (м, 2H), 7,79 (м, 2H), 7,42 (м, 2H), 7,24 (м, 2H), 7,20 (м, 2H), 6,54 (д, J=16,0 Гц, 1H), 6,34 (дд, J=16,0, 8,0 Гц, 1H), 5,00 (с, 2H), 4,10 (м, 1H); ЭРИ-МС m/z 524,07 ([M+H]+).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 49.
(E)-2-(2-Хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)изоиндолин-1,3-дион (CI27)

Указанное в заголовке соединение выделяли в виде беловатого твердого вещества (0,2 г, 55%): Т.пл. 128-129°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,92 (м, 2H), 7,79 (м, 2H), 7,42 (м, 3H), 7,22 (м, 2H), 6,52 (д, J=16,0 Гц, 1H), 6,32 (дд, J=16,0, 8,0 Гц, 1H), 5,00 (с, 2H), 4,05 (м, 1H); ЭРИ-МС m/z 557,99 ([M+H]+).
(E)-2-(2-Хлор-4-(3-(3,5-дихлор-4-фторфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)изоиндолин-1,3-дион (CI28)
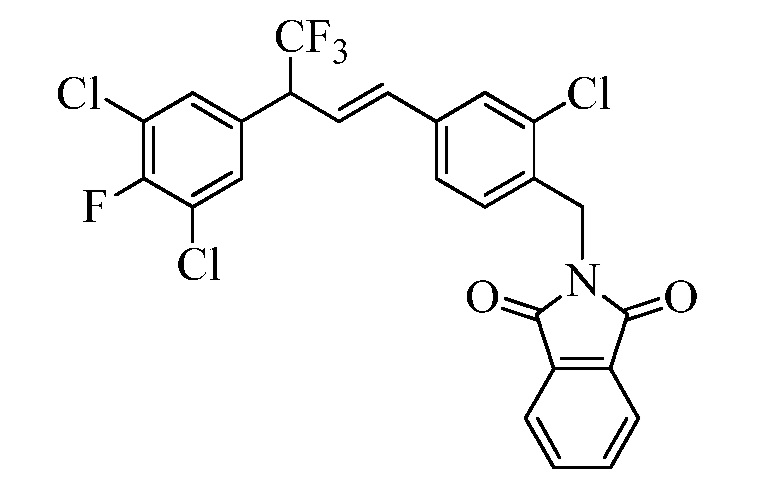
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,2 г, 54%): Т.пл. 177-180°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,90 (м, 2H), 7,77 (м, 2H), 7,42 (с, 1H), 7,32 (д, J=8,0 Гц, 2H), 7,21 (м, 2H), 6,52 (д, J=16,0 Гц, 1H), 6,32 (дд, J=16,0, 8,0 Гц, 1H), 5,00 (с, 2H), 4,05 (м, 1H); ЭРИ-МС m/z 540,08 ([M-H]-); ИК (тонкая пленка) 1716 см-1.
(E)-2-(2-Хлор-4-(3-(3,4-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)изоиндолин-1,3-дион (CI29)
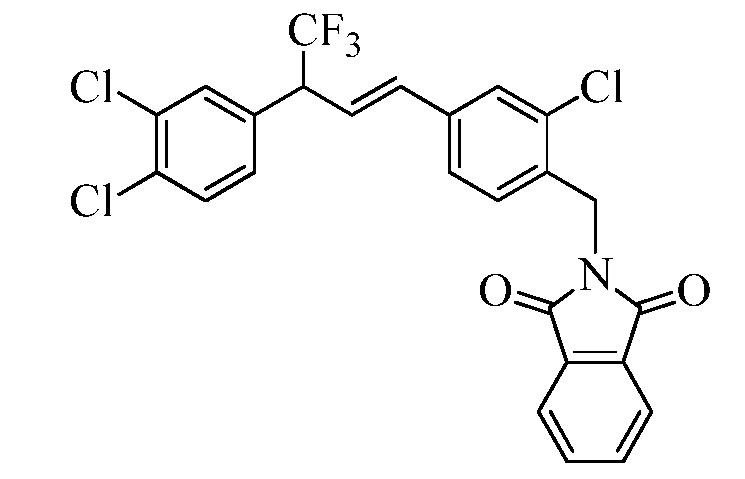
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,2 г, 59%): 1H-ЯМР (400 МГц, CDCl3) δ 7,89 (м, 2H), 7,76 (м, 2H), 7,47 (м, 3H), 7,21 (м, 3H), 6,50 (д, J=16,0 Гц, 1H), 6,32 (дд, J=16,0, 7,6 Гц, 1H), 4,97 (с, 2H), 4,11 (м, 1H); ЭРИ-МС m/z 522,27 ([M-H]-); ИК (тонкая пленка) 3064, 1717, 1111, 715 см-1.
(E)-2-(4-(3-(3,5-Дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(трифторметил)-бензил)изоиндолин-1,3-дион (CI30)
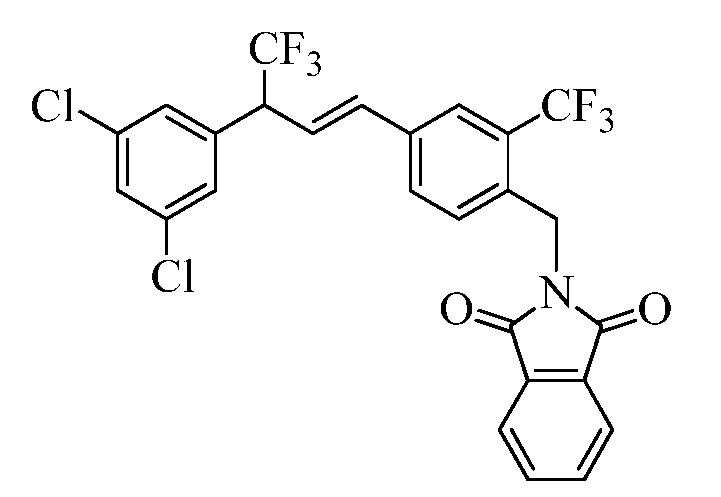
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,2 г, 54%): Т.пл. 141-142°C; 1H-ЯМР (400 МГц, CDCl3) 7,94 (м, 2H), 7,80 (м, 2H), 7,69 (с, 1H), 7,44 (м, 1H), 7,38 (м, 1H), 7,24 (м, 2H), 7,19 (м, 1H), 6,60 (д, J=16,0 Гц, 1H), 6,39 (дд, J=16,0, 7,6 Гц, 1H), 5,10 (с, 2H), 4,11 (м, 1H); ЭРИ-МС m/z 556,00 ([M-H]-).
(E)-2-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)-бензил)изоиндолин-1,3-дион (CI31)
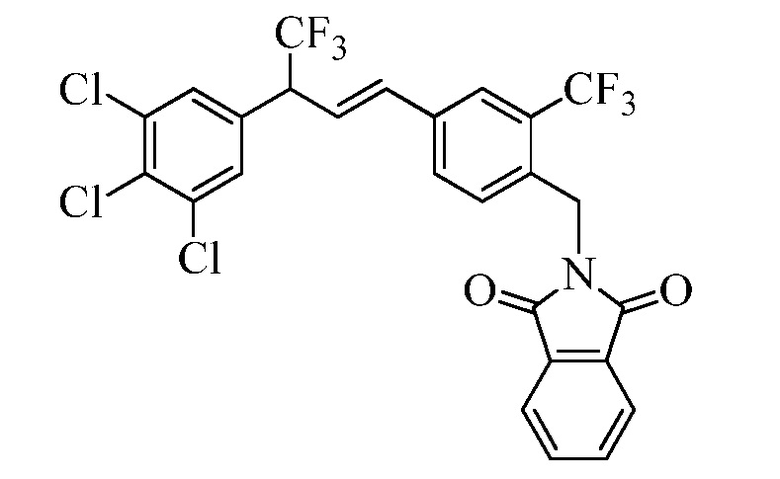
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,2 г, 56%): Т.пл. 130-132°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,94 (м, 2H), 7,80 (м, 2H), 7,69 (с, 1H), 7,44 (м, 3H), 7,19 (м, 1H), 6,61 (д, J=16,0 Гц, 1H), 6,38 (дд, J=16,0, 7,6 Гц, 1H), 5,10 (с, 2H), 4,12 (м, 1H); ЭРИ-МС m/z 589,57 ([М-2H]-).
(E)-2-(2-Бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-изоиндолин-1,3-дион (CI32)
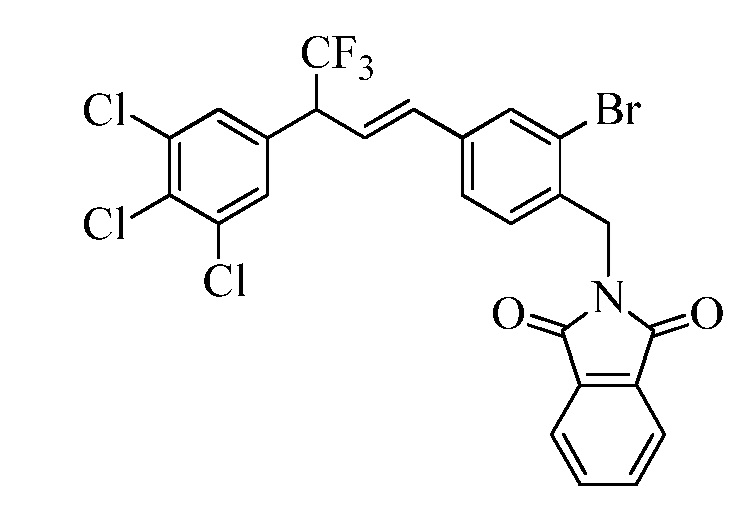
Указанное в заголовке соединение выделяли в виде бледно-желтого твердого вещества (0,2 г, 55%): Т.пл. 160-162°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,92 (м, 2H), 7,80 (м, 2H), 7,62 (с, 1H), 7,39 (с, 2H), 7,24 (м, 1H), 7,16 (м, 1H), 6,52 (д, J=16,0 Гц, 1H), 6,32 (дд, J=16,0, 8,0 Гц, 1H), 4,98 (с, 2H), 4,12 (м, 1H); ЭРИ-МС m/z 599,78 ([M-H]-).
(E)-2-(2-Фтор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-изоиндолин-1,3-дион (CI33)
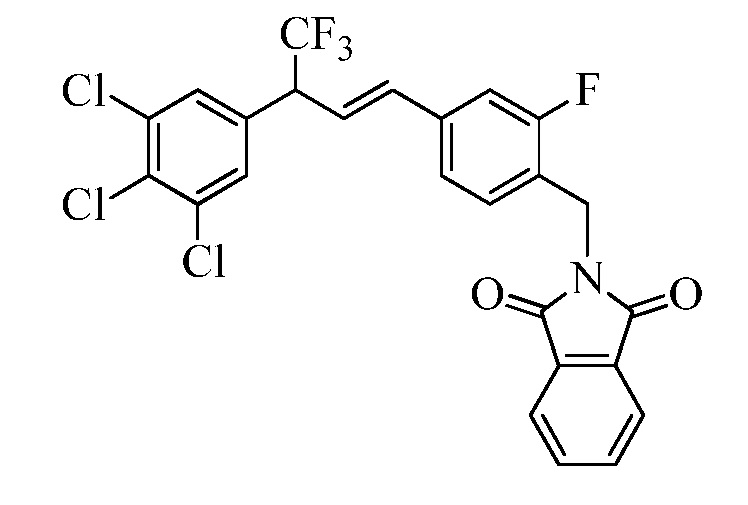
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,2 г, 55%): Т.пл. 72-74°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,88 (м, 2H), 7,74 (м, 2H), 7,38 (с, 2H), 7,34 (м, 1H), 7,18 (м, 2H), 6,54 (д, J=16,0 Гц, 1H), 6,32 (дд, J=16,0, 8,0 Гц, 1H), 4,91 (с, 2H), 4,08 (м, 1H); ЭРИ-МС m/z 539,89 ([M-H]-); ИК (тонкая пленка) 1773 см-1.
Предположительно соединения CI34-CI41 (Таблица 1) могут быть получены в соответствии с методиками, раскрытыми в Примере 49.
Пример 50: Получение (E)-(2-хлор-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (CI42)
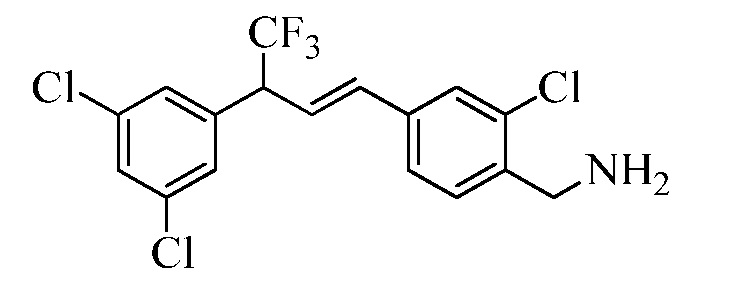
К перемешиваемому раствору (E)-2-(2-хлор-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)изоиндолин-1,3-диона (0,4 г, 0,76 ммоль) в EtOH добавляли гидрат гидразина (0,38 г, 7,6 ммоль) и полученную реакционную смесь нагревали при 80°C в течение 2 ч. Реакционную смесь фильтровали и выпаривали фильтрат. Остаток растворяли в CH2Cl2, промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде смолистой жидкости (0,3 г), которую использовали в следующей стадии без дополнительной очистки.
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 50.
(E)-(2-Хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)-метанамин (CI43)
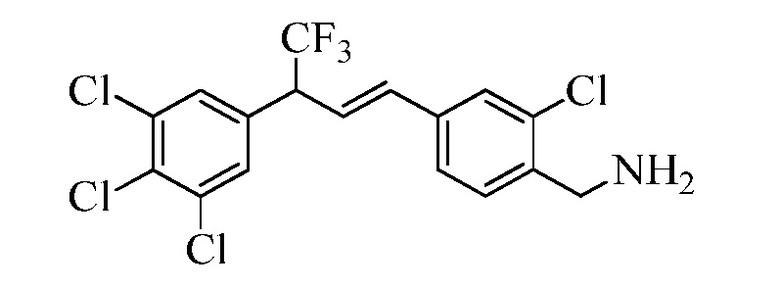
Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки.
(E)-(2-Хлор-4-(3-(3,4-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамин (CI44)
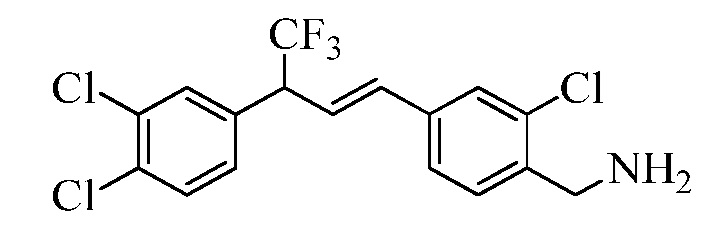
Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки: 1H-ЯМР (400 МГц, CDCl3) δ 7,48 (д, J=8,4 Гц, 2H), 7,39 (м, 2H), 7,23 (м, 2H), 6,52 (д, J=16,0 Гц, 1H), 6,38 (дд, J=16,0, 7,6 Гц, 1H), 4,12 (м, 1H), 3,90 (с, 2H); ЭРИ-МС m/z 391,90 ([M-H]-); ИК (тонкая пленка) 3370, 3280, 1111, 817 см-1.
(E)-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)фенил)метанамин (CI45)
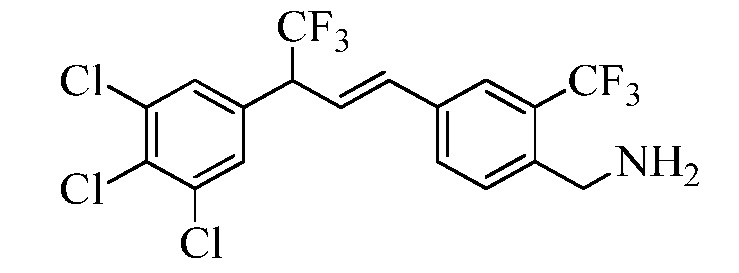
Указанное в заголовке соединение выделяли в виде смолистого материала. Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки.
(E)-(2-Бром-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамин (CI46)
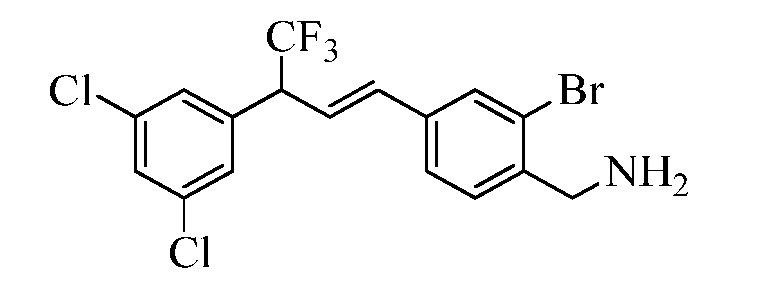
Указанное в заголовке соединение выделяли в виде смолистого материала. Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки.
(E)-(2-Бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)метанамин (CI47)
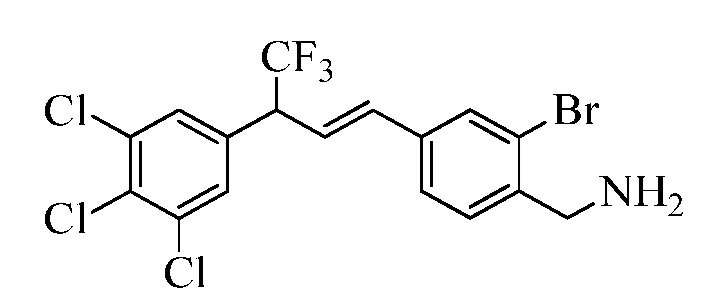
Указанное в заголовке соединение выделяли в виде смолистого материала. Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки.
(E)-(2-Фтор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)метанамин (CI48)
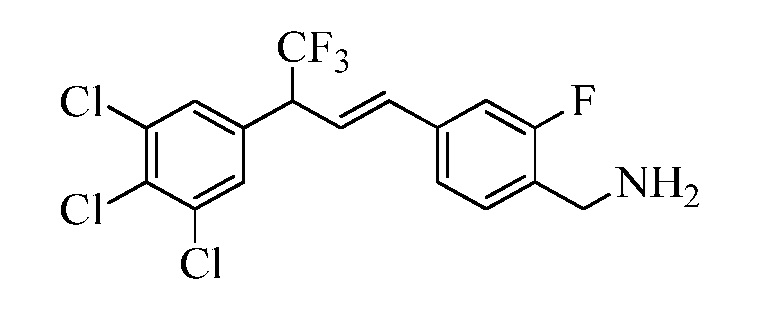
Указанное в заголовке соединение выделяли в виде смолистого материала: 1H-ЯМР (400 МГц, CDCl3) δ 7,40 (с, 2H), 7,33 (т, J=7,6 Гц, 1H), 7,13 (м, 2H), 6,56 (д, J=16,0 Гц, 1H), 6,33 (дд, J=16,0, 7,6 Гц, 1H), 4,08 (м, 1H), 3,90 (с, 2H); ЭРИ-МС m/z 413,84 ([M+H]+); ИК (тонкая пленка) 3368, 3274, 1114, 808 см-1.
Предположительно соединения CI49-CI57 (Таблица 1) могут быть получены в соответствии с методиками, раскрытыми в Примере 50.
Пример 51: Получение 3-хлор-4-((пиридин-2-иламино)метил)бенз-альдегида (CI58)
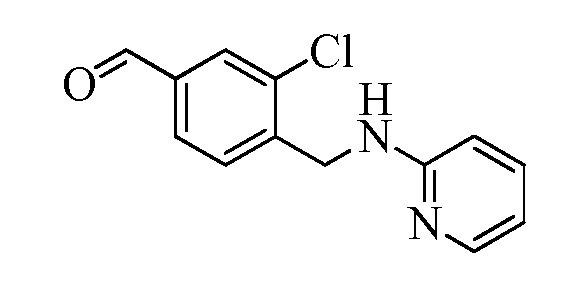
К перемешиваемому раствору 4-(бромметил)-3-хлорбензальдегида (2 г, 9 ммоль) в N,N-диметилацетамиде (DMA; 20 мл) добавляли K2CO3 (2,36 г, 17,16 ммоль) и 2-аминопиридин (0,84 г, 8,58 ммоль), и реакционную смесь перемешивали при температуре окружающей среды в течение 4 ч. Реакционную смесь разбавляли H2O и экстрагировали EtOAc. Объединенный органический слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Остаток очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 20% EtOAc в н-гексане), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (1,05 г, 50%): Т.пл. 122-123°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,94 (с, 1H), 8,11 (с, 1H), 7,88 (с, 1H), 7,72 (д, J=4,8 Гц, 1H), 7,62 (д, J=5,7 Гц, 1H), 7,4 (м, 1H), 6,64 (д, J=3,9 Гц, 1H), 6,38 (д, J=6,3 Гц, 1H), 5,04 (шир. с, 1H), 4,71 (с, 2H); ЭРИ-МС m/z 246,97 ([M+H]+).
Пример 52: Получение N-(2-хлор-4-винилбензил)пиридин-2-амина (CI59)
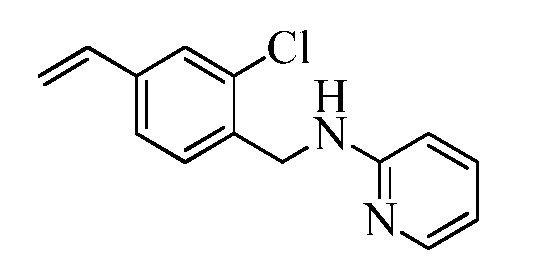
К перемешиваемому раствору 3-хлор-4-((пиридин-2-иламино)ме-тил)бензальдегида (1 г, 4 ммоль) в 1,4-диоксане (20 мл) добавляли K2CO3 (0,84 г, 6,09 ммоль) и метилтрифенилфосфоний-бромид (2,17 г, 6,09 ммоль) при температуре окружающей среды. Затем полученную реакционную смесь нагревали при 100°C в течение 18 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и полученный фильтрат выпаривали при пониженном давлении. Остаток очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; 10% EtOAc в н-гексане), получив указанное в заголовке соединение в виде белого твердого вещества (0,5 г, 50%): Т.пл. 119-121°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,12 (с, 1H), 7,42-7,40 (м, 3H), 7,26 (с, 1H), 6,66 (м, 2H), 6,36 (д, J=6,3 Гц, 1H), 5,75 (д, J=13,2 Гц, 1H), 4,92 (шир. с, 1H), 4,60 (с, 2H); ЭРИ-МС m/z 245,05 ([M+H]+).
Пример 53: Получение этил-2-амино-2-(5-бром-3-хлорпиридин-2-ил)ацетата (CI60)
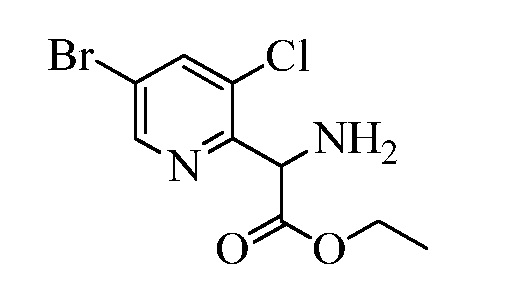
Этил-2-(дифенилметиленамино)ацетат (10,2 г, 38,2 ммоль) добавляли к гидриду натрия (NaH; 3,18 г, 133,52 ммоль) в ДМФА (50 мл) при 0°C и перемешивали смесь в течение 30 мин. К смеси добавляли 5-бром-2,3-дихлорпиридин (12,9 г, 57,23 ммоль) и перемешивали реакционную смесь в течение 3 ч при температуре окружающей среды. В реакционную смесь вливали 2Н раствор HCl и затем перемешивали в течение 4 ч при температуре окружающей среды. Смесь экстрагировали EtOAc. Объединенный слой EtOAc промывали рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (20-30% EtOAc в гексане) дала указанное в заголовке соединение в виде жидкости (1,3 г, 20%): 1H-ЯМР (400 МГц, CDCl3) δ 8,52 (с, 1H), 7,89 (с, 1H), 5,09 (с 1H), 4,23 (м, 2H), 2,27 (шир. с, 2H), 1,26 (м, 3H); ЭРИ-МС m/z 293,05 ([M+H]+); ИК (тонкая пленка) 3381, 3306, 1742, 759, 523 см-1.
Пример 54: Получение гидрохлорида (5-бром-3-хлорпиридин-2-ил)метанамина (CI61)
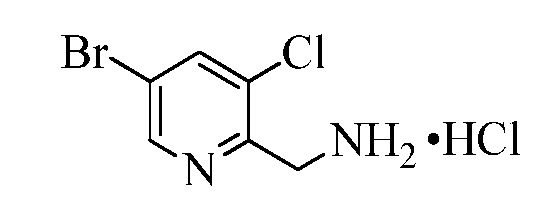
Перемешиваемый раствор этил 2-амино-2-(5-бром-3-хлор-пиридин-2-ил)ацетата (0,5 г, 1,7 ммоль) в 3Н HCl (25 мл) нагревали при дефлегмации в течение 4 ч. Реакционную смесь промывали диэтиловым эфиром и H2O. Объединенный эфирный слой выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (400 мг, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 8,78 (с, 1H), 8,70 (шир. с, 2H), 8,45 (с, 1H), 4,56 (м, 2H); ЭРИ-МС m/z 221,15 ([M+H]+).
Пример 55: Получение 2-((5-бром-3-хлорпиридин-2-ил)метил)изоин-долин-1,3-диона (CI62)
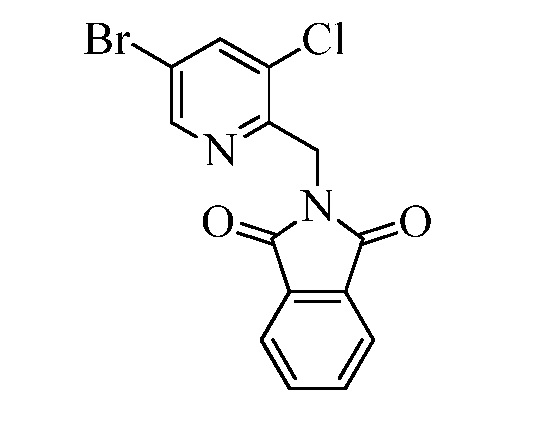
К перемешиваемому раствору гидрохлорида (5-бром-3-хлорпиридин-2-ил)метанамина (0,3 г, 1,4 ммоль) в толуоле (40 мл) добавляли Et3N (0,41 г, 4,08 ммоль) и фталевый ангидрид (0,24 г, 1,63 ммоль) и реакционную смесь нагревали при дефлегмации в течение 2 ч. Реакционную смесь выпаривали при пониженном давлении и остаток разбавляли H2O и экстрагировали EtOAc. Объединенный слой EtOAc промывали рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии (20-30% EtOAc в гексане), получив указанное в заголовке соединение в виде белого твердого вещества (0,25 г, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 8,78 (с, 1H), 8,45 (с, 1H), 7,88 (м, 2H), 7,74 (м, 2H), 4,56 (м, 2H); ЭРИ-МС m/z 349 ([M-H]-); ИК (тонкая пленка) 3307, 1665, 1114, 813 см-1.
Пример 56: Получение 2-((3-хлор-5-винилпиридин-2-ил)метил)изоин-долин-1,3-диона (CI63)

К перемешиваемому раствору 2-((5-бром-3-хлорпиридин-2-ил)метил)изоиндолин-1,3-диона (0,23 г, 0,65 ммоль) в толуоле (10 мл) добавляли Pd(PPh3)4 (3,7 мг, 0,003 ммоль), K2CO3 (0,269 г, 1,95 ммоль) и пиридиновый комплекс винилборонового ангидрида (0,78 г, 3,28 ммоль) и реакционную смесь нагревали при дефлегмации в течение 16 ч. Реакционную смесь фильтровали и фильтрат промывали H2O и рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (20-30% EtOAc в гексане) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (0,2 г, 65%): 1H-ЯМР (400 МГц, CDCl3) δ 8,30 (с, 1H), 7,91 (м, 2H), 7,77 (м, 3H), 7,72 (м, 1H), 6,63 (м, 1H), 5,79 (д, J=16,0 Гц, 1H), 5,39 (д, J=16,0 Гц, 1H), 5,12 (с, 2H); ЭРИ-МС m/z 299,20 ([M+H]+).
Пример 57: Получение (E)-2-((3-хлор-5-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)пиридин-2-ил)метил)изоиндолин-1,3-диона (CI64)
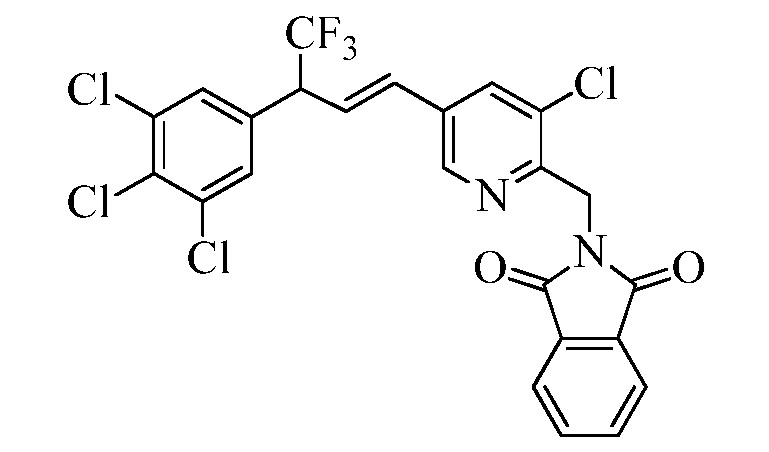
К перемешиваемому раствору 2-((3-хлор-5-винилпиридин-2-ил)метил)изоиндолин-1,3-диона (0,35 г, 1,17 ммоль) в 1,2-дихлорбензоле (10 мл) добавляли 5-(1-бром-2,2,2-трифторэтил)-1,2,3-трихлорбензол (0,8 г, 2,3 ммоль), CuCl (23 мг, 0,12 ммоль), 2,2-бипиридил (0,073 г, 0,234 ммоль) и реакционную смесь нагревали при 180°C в течение 16 ч. Реакционную смесь выпаривали при пониженном давлении и очищали с помощью колоночной хроматографии (20-30% EtOAc в гексане), получив указанное в заголовке соединение в виде жидкости (0,4 г, 50%): Т.пл. 79-82°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,27 (с, 1H), 7,91 (м, 2H), 7,77 (м, 3H), 7,36 (с, 2H), 6,51 (д, J=15,6 Гц, 1H), 6,32 (дд, J=15,6, 8,0 Гц, 1H), 5,30 (с, 2H), 4,13 (м, 1H); ЭРИ-МС m/z 559 ([M+H]+).
Пример 58: Получение (E)-(3-хлор-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)пиридин-2-ил)метанамина (CI65)
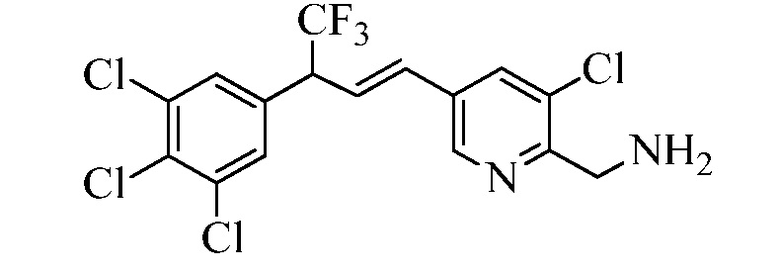
К перемешиваемому раствору (E)-2-((3-хлор-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)пиридин-2-ил)метил)изоиндо-лин-1,3-диона (200 мг, 0,358 ммоль) в EtOH (5 мл) добавляли гидрат гидразина (89,6 мг, 1,79 ммоль) и реакционную смесь нагревали при дефлегмации в течение 2 ч. Реакционную смесь выпаривали при пониженном давлении и остаток растворяли в CH2Cl2. Органический слой промывали H2O и рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде твердого вещества (100 мг). Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки.
Пример 59: Получение 4-(бромметил)-1-нафтонитрила (CI66)
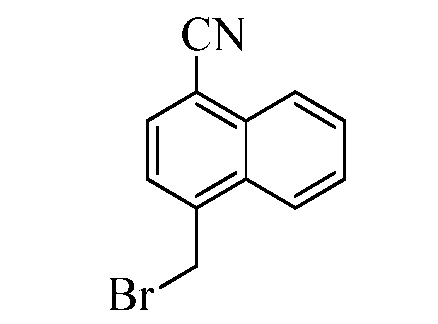
К перемешиваемому раствору 4-метил-1-нафтонитрила (5 г, 30 ммоль) в CCl4 (50 мл) под атмосферой аргона добавляли NBS (6,06 г, 34,09 ммоль) и дегазировали реакционную смесь в течение 30 мин. Добавляли AIBN (0,3 г, 2,1 ммоль) и нагревали полученную реакционную смесь при дефлегмации в течение 4 ч. Реакционную смесь охлаждали до температуры окружающей среды, разбавляли H2O и экстрагировали CH2Cl2 (3×100 мл). Объединенный слой CH2Cl2 промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Остаток очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 5% EtOAc в н-гексане), получив указанное в заголовке соединение в виде белого твердого вещества (3,8 г, 52%): Т.пл. 131-133°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,33 (м, 1H), 8,24 (м, 1H), 7,88 (д, J=8,0 Гц, 1H), 7,78 (м, 2H), 7,62 (д, J=8,0 Гц, 1H), 4,95 (с, 2H); ЭРИ-МС m/z 245,92 ([M+H]+); ИК (тонкая пленка) 2217 см-1.
Пример 60: Получение 4-(бромметил)-1-нафтальдегида (CI67)
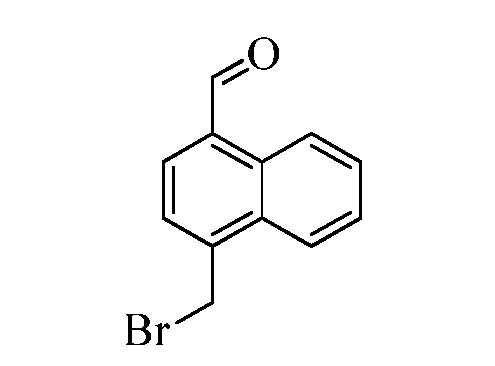
К перемешиваемому раствору 4-(бромметил)-1-нафтонитрила (8 г, 33 ммоль) в толуоле (100 мл) при 0°C по каплям добавляли DIBAL-H (1,0М раствор в толуоле; 43 мл) и реакционную смесь перемешивали при 0°C в течение 1 ч. К смеси добавляли 3Н HCl в H2O (50 мл), пока она не превращалась в белую суспензию, после чего добавляли дополнительное количество 1Н HCl (20 мл). Органический слой собирали и водный слой экстрагировали EtOAc (3×100 мл). Объединенный органический слой сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 5% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде белого твердого вещества (7 г, 88%): Т.пл. 115-116°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,41 (с, 1H), 9,35 (м, 1H), 8,22 (м, 1H), 7,90 (д, J=8,0 Гц, 1H), 7,75 (м, 3H), 4,95 (с, 2H); ЭРИ-МС m/z 248,88 ([M+H]+).
Пример 61: Получение 4-((1,3-диоксоизоиндолин-2-ил)метил)-1-нафтальдегида (CI68)
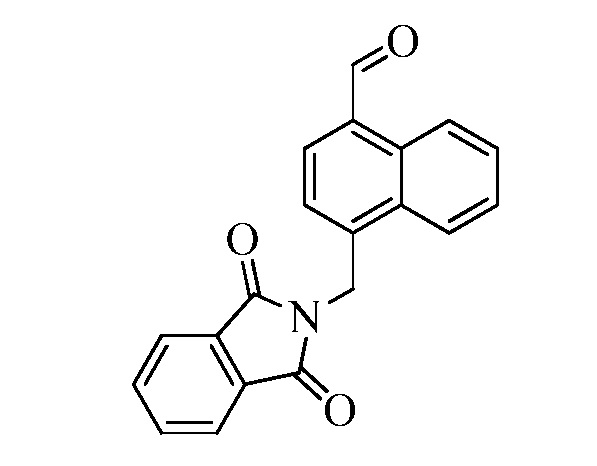
К перемешиваемому раствору 4-(бромметил)-1-нафтальдегида (7 г, 28 ммоль) в ДМФА (100 мл) добавляли фталимид калия (7,3 г, 39,5 ммоль) и смесь нагревали при 85°C в течение 2 ч. Реакционную смесь охлаждали до температуры окружающей среды и разбавляли H2O (100 мл). Полученное твердое вещество отделяли фильтрацией и сушили в вакууме, получив указанное в заголовке соединение в виде белого твердого вещества (8,8 г, 98%): Т.пл. 190-192°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,39 (с, 1H), 9,25 (м, 1H), 8,41 (м, 1H), 8,10 (д, J=8,0 Гц, 1H), 7,95 (м, 4H), 7,80 (м, 4H), 7,61 (м, 4H), 5,39 (с, 2H); ЭРИ-МС m/z 316,09 ([M+H]+); ИК (тонкая пленка) 1708 см-1.
Пример 62: Получение 2-((4-винилнафталин-1-ил)метил)изоиндолин-1,3-диона (CI69)
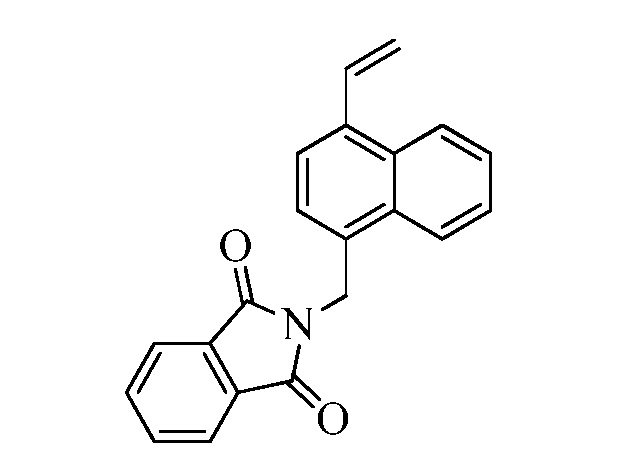
К перемешиваемому раствору 4-((1,3-диоксоизоиндолин-2-ил)метил)-1-нафтальдегида (9 г, 28,5 ммоль) в 1,4-диоксане (100 мл) добавляли K2CO3 (6 г, 42,8 ммоль) и метилтрифенилфосфоний-бромид (15,3 г, 35,7 ммоль) при температуре окружающей среды. Реакционную смесь нагревали при 100°C в течение 14 ч и затем охлаждали до температуры окружающей среды. Реакционную смесь фильтровали и полученный фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; 20% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде белого твердого вещества (6 г, 67%): Т.пл. 146-147°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,35 (м, 2H), 7,95 (м, 4H), 7,65 (м, 4H), 7,39 (м, 1H), 5,81 (м, 1H), 5,45 (м, 1H), 5,21 (с, 2H); ЭРИ-МС m/z 314,13 ([M+H]+).
Пример 63: Получение (E)-2-((4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)нафталин-1-ил)метил)изоиндолин-1,3-диона (CI70)
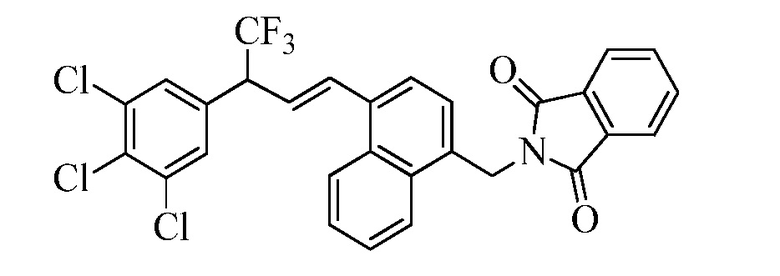
К перемешиваемому раствору 2-((4-винилнафталин-1-ил)метил)изоиндолин-1,3-диона (1,5 г, 4,79 ммоль) в 1,2-дихлорбензоле (15 мл) добавляли 1-(1-бром-2,2,2-трифторэтил)-3,4,5-трихлорбензол (3,2 г, 9,5 ммоль), CuCl (24 мг, 0,24 ммоль) и 2,2-бипиридил (0,149 г, 0,95 ммоль) и полученную реакционную смесь дегазировали аргоном в течение 30 мин и затем перемешивали при 180°C в течение 14 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; 25-30% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (1,5 г, 56%): Т.пл. 158-160°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,40 (м, 1H), 7,89 (м, 2H), 7,74 (м, 2H), 7,64 (м, 2H), 7,58 (м, 2H), 7,46 (с, 2H), 7,36 (м, 2H), 6,31 (м, 1H), 5,30 (с, 2H), 4,21 (м, 1H); ЭРИ-МС m/z 572,08 ([M-H]-).
Пример 64: Получение (E)-(4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)нафталин-1-ил)метанамина (CI71)

К перемешиваемому раствору (E)-2-((4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)нафталин-1-ил)метил)изоиндо-лин-1,3-диона (0,4 г, 0,7 ммоль) в EtOH добавляли гидрат гидразина (0,18 г, 3,5 ммоль) и полученную реакционную смесь нагревали при 80°C в течение 2 ч. Реакционную смесь фильтровали и выпаривали фильтрат. Остаток растворяли в CH2Cl2, раствор промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Указанное в заголовке соединение выделяли в виде смолистой жидкости (150 мг, 50%). Продукт, полученный в этой реакции, использовали в следующей стадии без дополнительной очистки.
Пример 65: Получение 2-((4-бромфенил)амино)изоиндолин-1,3-диона (CI72)
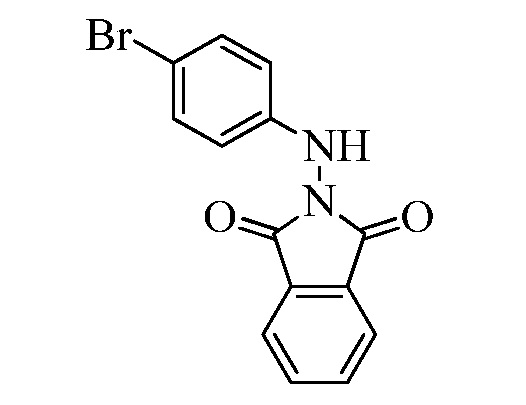
К перемешиваемому раствору гидрохлорида (4-бромфенил)гидра-зина (0,5 г, 2,2 ммоль) в ледяной уксусной кислоте (8 мл) добавляли фталевый ангидрид (0,398 г, 2,690 ммоль) и реакционную смесь перемешивали при 130°C в течение 1 ч под атмосферой азота. В реакционную смесь вливали нас. водн. раствор NaHCO3 и фильтровали с получением твердого вещества. Очистка с помощью колоночной хроматографии (SiO2, 0-10% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (60 мг, 84%): Т.пл. 205-206°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,71 (с, 1H), 7,99 (м, 4H), 7,32 (д, J=8,8 Гц, 2H), 6,79 (д, J=8,8 Гц, 2H); ЭРИ-МС m/z 314,95 ([M-H]-).
Пример 66: Получение 2-((4-Винилфенил)амино)изоиндолин-1,3-диона (CI73)
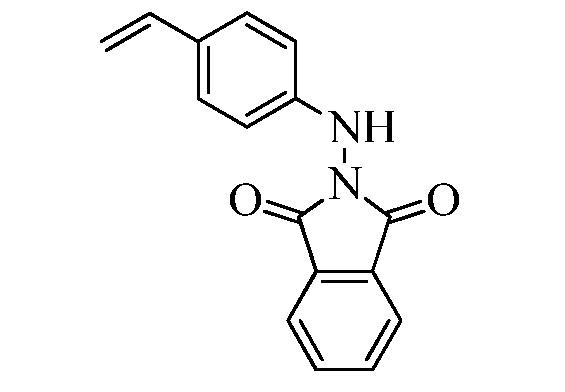
К раствору 2-(4-бромфениламино)изоиндолин-1,3-диона (2 г, 6 ммоль) в 1,2-диметоксиэтане (20 мл) и H2O (4 мл) добавляли пиридиновый комплекс винилборонового ангидрида (4,57 г, 18,98 ммоль) и K2CO3 (1,3 г, 9,5 ммоль), а затем Pd(PPh3)4 (0,219 г, 0,189 ммоль). Полученную реакционную смесь нагревали при 150°C в микроволновом реакторе в течение 30 мин и затем выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 15% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (200 мг, 13%): Т.пл. 174-176°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,65 (с, 1H), 7,94 (м, 4H), 7,29 (д, J=8,4 Гц, 2H), 6,72 (д, J=8,4 Гц, 2H), 6,61 (м, 1H), 5,61 (д, J=17,6 Гц, 1H), 5,05 (д, J=11,2 Гц, 1H); ЭРИ-МС m/z 263,18 ([M-H]-).
Пример 67: Получение (E)-2-((4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)фенил)амино)изоиндолин-1,3-диона (CI74)
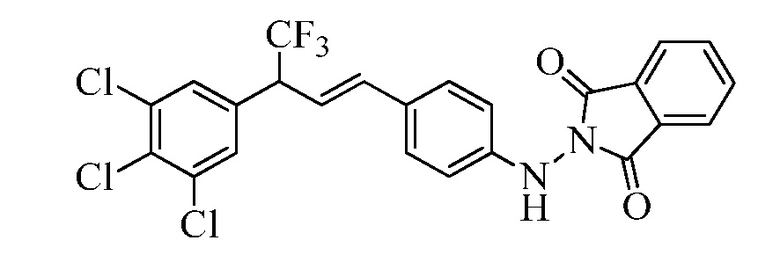
К перемешиваемому раствору 2-(4-винилфениламино)изоиндолин- 1,3-диона (0,3 г, 1,1 ммоль) в 1,2-дихлорбензоле (5 мл) добавляли CuCl (0,022 г, 0,273 ммоль), 2,2-бипиридил (0,07 г, 0,46 ммоль) и 5-(1-бром-2,2,2-трифторэтил)-1,2,3-трихлорбензол (0,77 г, 2,27 ммоль). Реакционную смесь дегазировали аргоном в течение 30 мин и нагревали при 180°C в течение 2 ч. Затем реакционную смесь выпаривали при пониженном давлении, а остаток очищали с помощью колоночной хроматографии (SiO2, 0-30% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде твердого вещества (450 мг, 75%): Т.пл. 187-189°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,75 (с, 1H), 7,96 (м, 4H), 7,82 (с, 2H), 7,37 (д, J=8,8 Гц, 1H), 6,73 (д, J=8,4 Гц, 2H), 6,61 (м, 2H), 6,58 (м, 1H), 4,59 (м, 1H); ЭРИ-МС m/z 523,05 ([M-H]-).
Пример 68: Получение (E)-(4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)фенил)гидразина (CI75)
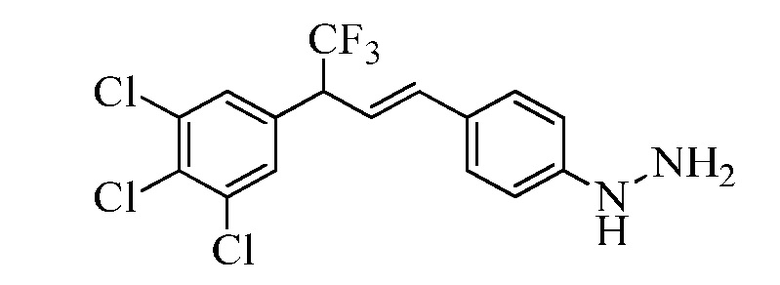
К перемешиваемому раствору (E)-2-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)фениламино)изоиндолин-1,3-диона (0,16 г, 0,31 ммоль) в EtOH (5 мл) добавляли гидрат гидразина (0,076 г, 1,52 ммоль) и реакционную смесь нагревали при 85°C в течение 1 ч. Реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и фильтрат выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде твердого вещества (0,08 г, 66%), которое использовали в следующей стадии без дополнительной очистки.
Пример 69: Получение 2-(4-винилфенокси)изоиндолин-1,3-диона (CI76)
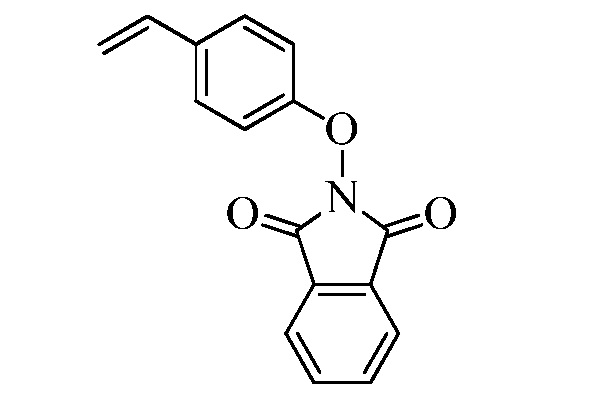
К перемешиваемому раствору 4-винилфенилбороновой кислоты (2 г, 13 ммоль), 2-гидроксиизоиндолин-1,3-диона (3,63 г, 24,53 ммоль) и CuCl (1,214 г 12,26 ммоль) в 1,2-дихлорэтане (50 мл) добавляли пиридин (1,065 г, 13,48 ммоль) и полученную реакционную смесь перемешивали при температуре окружающей среды в течение 48 ч. Реакционную смесь разбавляли H2O и экстрагировали CHCl3. Объединенный слой CHCl3 промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2; 20% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде белого твердого вещества (2 г, 63%): Т.пл. 129-131°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,93 (д, J=2,0 Гц, 2H), 7,82 (д, J=3,2 Гц, 2H), 7,38 (д, J=2,0 Гц, 2H), 7,14 (д, J=2,0 Гц, 2H), 6,70 (м, 1H), 5,83 (д, J=16,0 Гц, 1H), 5,22 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 266,12 ([M+H]+).
Пример 70: Получение (E)-2-(4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)фенокси)изоиндолин-1,3-диона (CI77)
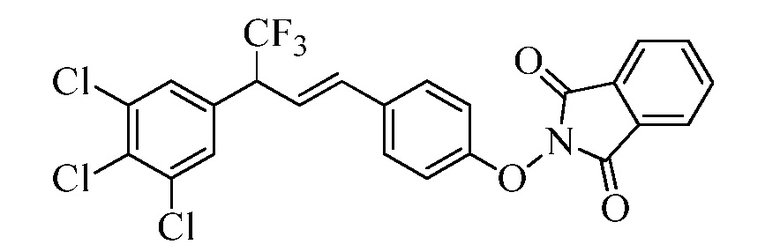
К перемешиваемому раствору 2-(4-винилфенокси)изоиндолин-1,3-диона (0,3 г, 1,1 ммоль) в 1,2-дихлорбензоле (10 мл) добавляли 1-(1-бромэтил)-3,4,5-трихлорбензол (769 мг, 2,26 ммоль), CuCl (22 мг, 0,22 ммоль) и 2,2-бипиридил (35 мг, 0,44 ммоль), и полученную реакционную смесь дегазировали аргоном в течение 30 мин и нагревали до 180°C в течение 24 ч. Реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и фильтрат выпаривали при пониженном давлении. Неочищенный материал очищали с помощью колоночной хроматографии (SiO2, 100-200 меш; 20% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде твердого вещества (0,29 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 7,90 (м, 1H), 7,62 (м, 2H), 7,50 (м, 1H), 7,40 (с, 2H), 7,12 (с, 1H), 6,90 (м, 2H), 6,60 (м, 2H), 6,20 (м, 1H), 4,08 (м, 1H); ЭРИ-МС m/z 524,09 ([M-H]-).
Пример 71: Получение (E)-O-(4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)фенил)гидроксиламина (CI78)
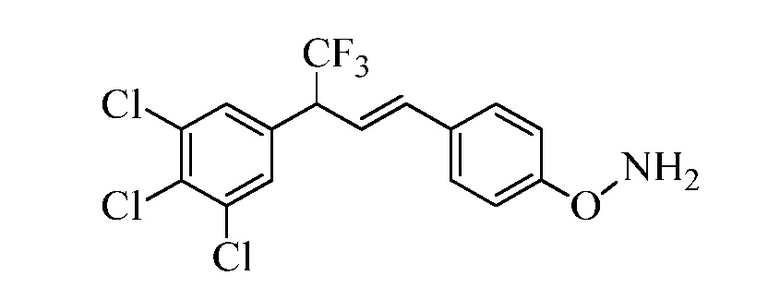
К перемешиваемому раствору (E)-2-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)фенокси)изоиндолин-1,3-диона (0,2 г, 0,4 ммоль) в EtOH добавляли гидрат гидразина (0,1 г, 1,9 ммоль) и полученную реакционную смесь нагревали при 90°C в течение 1 ч. Реакционную смесь фильтровали и выпаривали фильтрат. Остаток растворяли в CH2Cl2, промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке неочищенное соединение в виде смолистой жидкости (0,08 г, 53%): 1H-ЯМР (400 МГц, CDCl3) δ 7,40 (с, 2H), 6,98 (с, 1H), 6,82 (с, 2H), 6,48 (м, 1H), 6,20 (м, 1H), 5,02 (с, 1H), 4,08 (м, 1H); ЭРИ-МС m/z 394,94 ([M-H]-).
Пример 72: Получение (E)-N-(4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-енил)бензил)ацетамида (CC1)
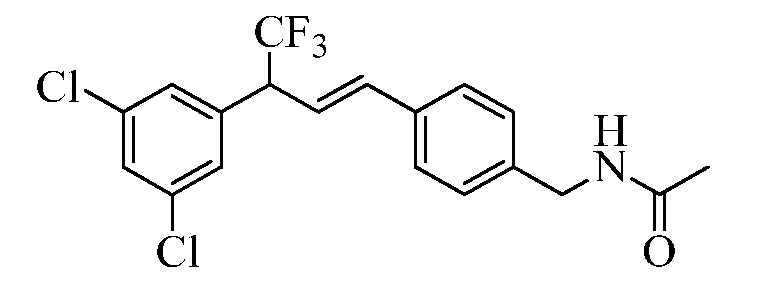
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,5-дихлор-фенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,3 г, 0,8 ммоль) в ДХМ (10 мл) добавляли уксусный ангидрид (0,12 мл, 1,14 ммоль) и ТЭА (0,217 мл, 1,52 ммоль), и полученную реакционную смесь перемешивали при температуре окружающей среды в течение 6 ч. Реакционную смесь разбавляли H2O и экстрагировали ДХМ. Объединенный слой ДХМ промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 30-50% этилацетата в гексане) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (0,2 г, 60%) Т.пл. 107-109°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,37 (м, 3H), 7,28 (м, 4H), 6,60 (д, J=16,0 Гц, 1H), 6,36 (дд, J=16,0, 8,0 Гц, 1H), 5,75 (шир. с, 1H), 4,46 (д, J=6 Гц, 2H), 4,01 (м, 1H), 2,11 (с, 3H); ЭРИ-МС m/z 402,00 ([M+H]+).
Соединения CC2-CC6 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 72. Кроме того, соединение DC56 в Таблице 1 было получено из соединения DC55 в соответствии с методиками, раскрытыми в Примере 72.
Пример 73: Получение (E)-N-(2-хлор-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)ацетамида (CC7)
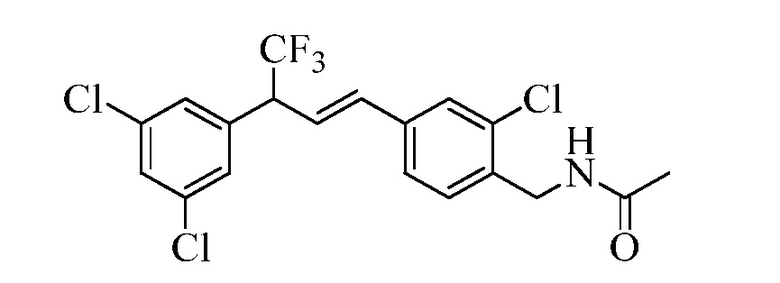
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,5-дихлор-фенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,3 г, 0,8 ммоль) в ДМФА (5 мл) добавляли 2,2,2-трифторпропановую кислоту (97 мг, 0,76 ммоль), HOBt·H2O (174 мг, 1,14 ммоль) и EDC·HCl (217 мг, 1,14 ммоль) и DIEA (196 мг, 1,52 ммоль) и полученную реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Реакционную смесь разбавляли H2O и экстрагировали EtOAc. Объединенный слой EtOAc промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 30-50% этилацетата в гексане) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (0,2 г, 60%): Т.пл. 127-128°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,42 (м, 4H), 7,24 (м, 2H), 6,53 (д, J=16,0 Гц, 1H), 6,36 (дд, J=16,0, 8,0 Гц, 1H), 5,86 (шир. с, 1H), 4,51 (д, J=6,0 Гц, 2H), 4,05 (м, 1H), 2,02 (с, 3H); ЭРИ-МС m/z 436,03 ([M+H]+).
Соединения CC8-CC28 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 73.
Пример 74: Получение (E)-N-(пиридин-2-илметил)-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2-(трифторметил)бен-зил)циклопропанкарбоксамида (CC29)
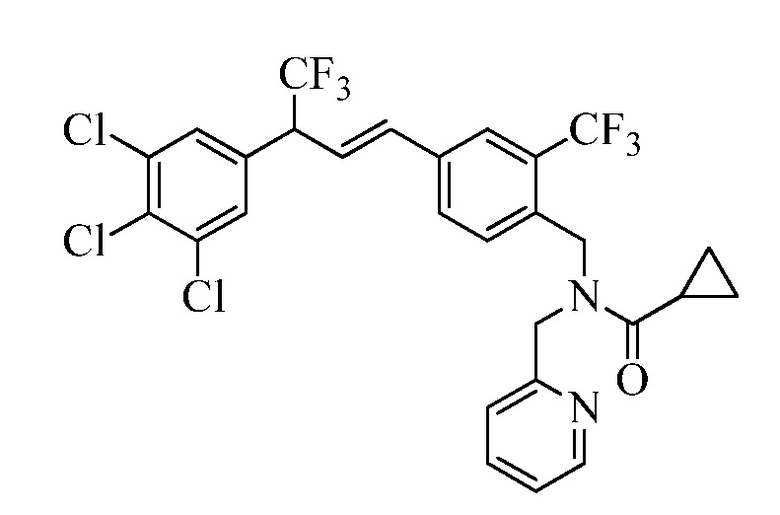
Стадия 1: (E)-1-(Пиридин-2-ил)-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2-(трифторметил)бензил)метанамин. (E)-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)фенил)метанамин (0,46 г, 1 ммоль) растворяли в CH3OH (3 мл). К смеси добавляли пиридин-2-карбальдегид (0,107 г, 1 ммоль). Реакционную смесь перемешивали в течение 1 ч. Через 1 ч добавляли NaBH4 (0,076 г, 2 ммоль) и оставляли при температуре окружающей среды на 3 ч. Реакционную смесь выпаривали с получением маслянистого остатка. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 30-50% EtOAc в гексане) дала указанное в заголовке соединение в виде бледно-желтой жидкости (0,22 г, 40%): 1H-ЯМР (400 МГц, CDCl3) δ 8,58 (д, J=4,8 Гц, 1H), 7,74 (м, 1H), 7,62 (м, 2H), 7,52 (м, 1H), 7,4 (с, 2H), 7,3 (м, 1H), 7,2 (м, 2H), 6,60 (д, J=16,0 Гц, 1H), 6,38 (дд, J=16,0, 8,0 Гц, 1H), 4,10 (м, 1H), 4,02 (с, 2H), 3,96 (с, 2H); ЭРИ-МС m/z 552,95 ([M+H]+); ИК (тонкая пленка) 3338, 1114, 808 см-1.
Стадия 2: (E)-N-(Пиридин-2-илметил)-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-2-(трифторметил)бензил)цикло-пропанкарбоксамид. (E)-1-(Пиридин-2-ил)-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензил)метан-амин (0,27 г, 0,05 ммоль) собирали в CH2Cl2 (3 мл). К смеси добавляли Et3N (0,14 мл, 0,1 ммоль). Реакционную смесь перемешивали в течение 10 мин. Через 10 мин реакционную смесь охлаждали до 0°C и добавляли циклопропилкарбонилхлорид (0,08 мл, 0,075 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 1 ч и затем промывали H2O и нас водн. раствором NaHCO3. Органический слой сушили над безводным Na2SO4 и выпаривали, получив бледно-желтый смолистый материал (0,15 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 8,58 (д, J=4,6 Гц, 1H), 7,74 (м, 1H), 7,62 (м, 2H), 7,52 (м, 1H), 7,4 (с, 2H), 7,3 (м, 1H), 7,2 (м, 2H), 6,60 (д, J=16,0 Гц, 1H), 6,38 (дд, J=16,0, 8,0 Гц, 1H), 5,02 (с, 1H), 4,8 (с, 1H), 4,8 (д, J=10 Гц, 2H), 4,10 (м, 1H), 1,8 (м, 1H), 1,2 (м, 2H), 0,6 (м, 2H); ЭРИ-МС m/z 620,86 ([M-H]-); ИК (тонкая пленка) 1645, 1115, 808 см-1.
Пример 75: Получение (E)-N-(2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-3-(метилсульфонил)пропанамида (CC30)
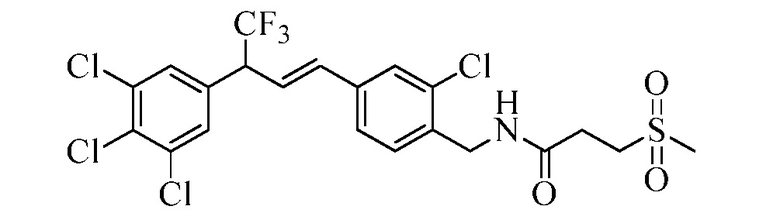
(E)-N-(2-Хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-3-(метилтио)пропанамид (0,15 г, 0,28 ммоль) обрабатывали оксоном (0,175 г, 0,569 ммоль) в смеси 1:1 ацетона:воды (20 мл) в течение 4 ч при температуре окружающей среды. Ацетон выпаривали с получением белого твердого вещества (0,095 г, 60%): Т.пл. 101-104°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (м, 4H), 7,24 (м, 1H), 6,53 (д, J=16,0 Гц, 1H), 6,35 (дд, J=16,0, 8,0 Гц, 1H), 6,12 (шир. с, 1H), 4,53 (м, 2H), 4,10 (м, 1H), 3,42 (м, 2H), 2,91 (с, 3H), 2,78 (м, 2H); ЭРИ-МС m/z 559,75 ([M-H]-).
Пример 76: Получение (E)-1-(2-хлор-4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)-3-этилмочевины (CC31)
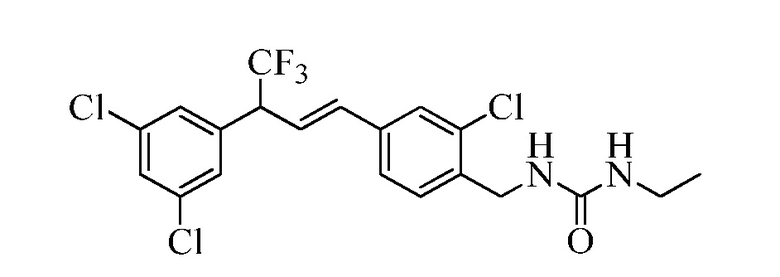
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,5-дихлор-фенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,2 г, 0,5 ммоль) в CH2Cl2 (5 мл) при 0°C добавляли Et3N (0,141 мл, 1 ммоль) и этилизоцианат (0,053 г, 0,75 ммоль), и реакционную смесь перемешивали в течение 1 ч при 0°C. Реакционную смесь разбавляли CH2Cl2. Органический слой промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 30-50% EtOAc в гексане) дала указанное в заголовке соединение в виде твердого вещества (0,141 г, 60%): Т.пл. 177-178°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,58 (м, 2H), 7,41 (м, 3H), 7,24 (м, 1H), 6,53 (д, J=16,0 Гц, 1H), 6,35 (дд, J=16,0, 8,0 Гц, 1H), 4,70 (шир. с, 1H), 4,43 (с, 2H), 4,08 (м, 1H), 3,21 (м, 2H), 1,25 (м, 3H); ЭРИ-МС m/z 463 ([M-H]-).
Соединения CC32-CC35 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 76.
Пример 77: Получение (E)-3-(2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-1,1-диметилмочевины (CC36)
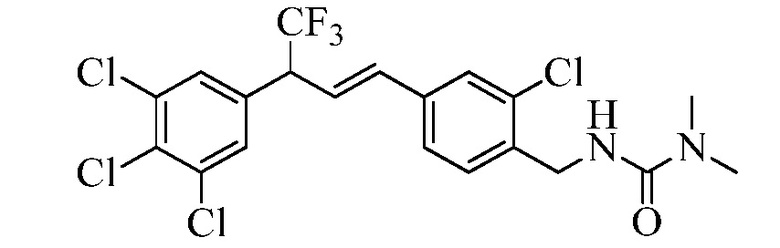
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,4,5-трихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,2 г, 0,5 ммоль) в CH2Cl2 (5 мл) при 0°C добавляли Et3N (0,141 мл, 1 ммоль) и N,N-диметилкарбамоилхлорид (0,08 г, 0,075 ммоль), и реакционную смесь перемешивали в течение 1 ч при 0°C. Реакционную смесь разбавляли CH2Cl2. Органический слой промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 30-50% EtOAc в гексане) дала указанное в заголовке соединение в виде твердого вещества (0,15 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,39 (м, 4H), 7,28 (м, 1H), 6,54 (д, J=16,0 Гц, 1H), 6,34 (дд, J=16,0, 8,0 Гц, 1H), 4,97 (шир. с, 1H), 4,38 (д, J=6,0 Гц, 2H), 4,10 (м, 1H), 2,9 (с, 3H), 2,7 (с, 3H); ЭРИ-МС m/z 497 ([M-H]-); ИК (тонкая пленка) 3350, 1705, 1114, 808 см-1.
Пример 78: Получение (E)-1-(2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-3-этилтиомочевины (CC37)
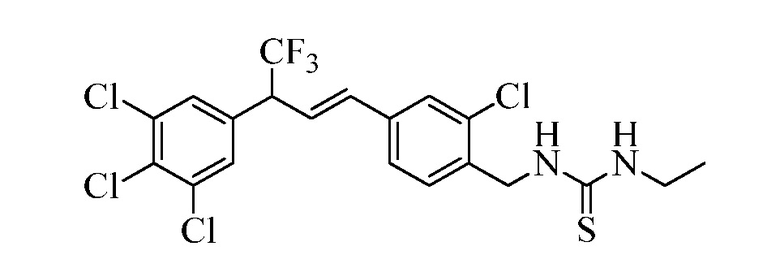
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,4,5-трихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,2 г, 0,5 ммоль) в CH2Cl2 (5 мл) при 0°C добавляли Et3N (0,141 мл, 1 ммоль) и этилизотиоцианат (0,053 г, 0,75 ммоль), и реакционную смесь перемешивали в течение 1 ч при 0°C. Реакционную смесь разбавляли CH2Cl2. Органический слой промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 30-50% EtOAc в гексане) дала указанное в заголовке соединение в виде твердого вещества (0,14 г, 60%): Т.пл. 88-91°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,49 (д, J=8 Гц, 1H), 7,41 (д, J=7,2 Гц, 2H), 7,26 (м, 2H), 6,50 (д, J=16 Гц, 1H), 6,35 (дд, J=16,0, 8,0 Гц, 1H), 6,0 (шир. с, 1H), 5,73 (шир. с, 1H), 4,80 (шир. с, 2H), 4,09 (м, 1H), 1,23 (м, 3H); ЭРИ-МС m/z 515,01 ([M+H]+).
Соединение CC38 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 78.
Пример 79: Получение (E)-трет-бутил-(2-хлор-4-(3-(3,5-дихлор-фенил)-4,4,4-трифторбут-1-ен-1-ил)бензил)-3-этилмочевины (CC39)
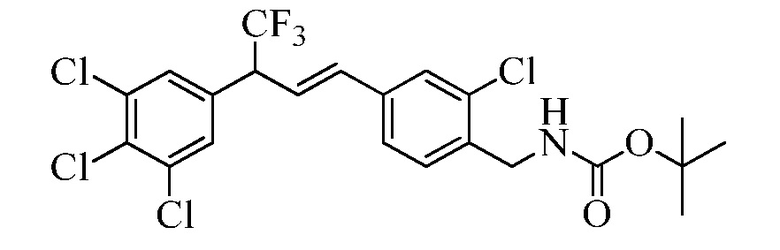
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,4,5-трихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,2 г, 0,5 ммоль в CH2Cl2 (5 мл) при 0°C добавляли Et3N (0,141 мл, 1 ммоль) и ди-трет-бутил-дикарбонат (0,163 мл, 0,75 ммоль) и реакционную смесь перемешивали в течение 4 ч при температуре окружающей среды. Реакционную смесь разбавляли CH2Cl2. Органический слой промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 10-20% EtOAc в гексане) дала указанное в заголовке соединение в виде белого твердого вещества (0,147 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,39 (м, 4H), 7,28 (м, 1H), 6,54 (д, J=16,0 Гц, 1H), 6,34 (дд, J=16,0, 8,0 Гц, 1H), 4,97 (шир. с, 1H), 4,38 (д, J=6,0 Гц, 2H), 4,10 (м, 1H), 1,53 (с, 9H); ЭРИ-МС m/z 526,09 ([M-H]-); ИК (тонкая пленка) 3350, 1705, 1114, 808 см-1.
Соединение CC40 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 79.
Пример 80: Получение (E)-метил-2-((2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)амино)-2-оксоацетата (CC41)
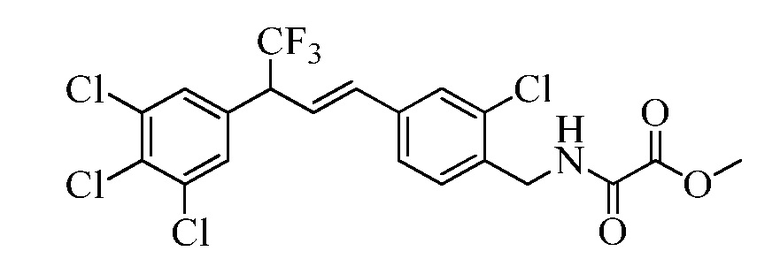
К перемешиваемому раствору (E)-(2-хлор-4-(3-(3,4,5-трихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)метанамина (0,2 г, 0,5 ммоль) в CH2Cl2 (5 мл) при 0°C добавляли Et3N (0,141 мл, 1 ммоль) и метил-2-хлор-2-оксоацетат (0,09 г, 0,75 ммоль), и реакционную смесь перемешивали в течение 1 ч при 0°C. Реакционную смесь разбавляли CH2Cl2. Органический слой промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 20% EtOAc в гексане) дала указанное в заголовке соединение в виде твердого вещества (0,12 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 7,48 (м, 1H), 7,43 (м, 3H), 7,38 (м, 1H), 7,23 (с, 1H), 6,55 (д, J=16,0 Гц, 1H), 6,36 (дд, J=16,0, 8,0 Гц, 1H), 4,60 (д, J=4,4 Гц, 2H), 4,18 (м, 1H), 3,85 (с, 3H); ЭРИ-МС m/z 512,22 ([M-H]-); ИК (тонкая пленка) 1740, 1701, 1114, 808 см-1.
Пример 81: Получение (E)-N1-(2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-N2-(2,2,2-трифторэтил)оксамида (CC42)
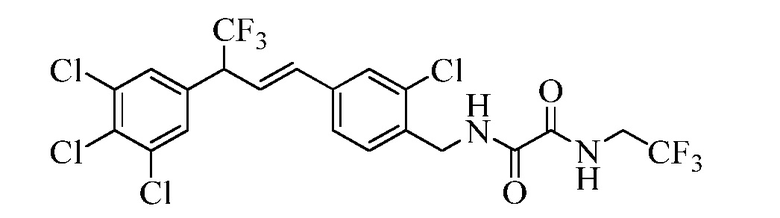
К перемешиваемому раствору гидрохлорида 2,2,2-трифторэтиламина (0,1 г, 0,77 ммоль) в CH2Cl2 (10 мл) по каплям добавляли триметилалюминий (2М раствор в толуоле; 0,39 мл, 0,77 ммоль) и реакционную смесь перемешивали при 25°C в течение 30 мин. К реакционной смеси по каплям добавляли раствор (E)-метил-2-((2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)-2-оксоацетата (0,2 г, 0,38 ммоль) в CH2Cl2 (5 мл) при 25°C. Реакционную смесь перемешивали при дефлегмации в течение 18 ч, охлаждали до 25°C, приливали 0,5Н раствор HCl (50 мл) и экстрагировали EtOAc (2×50 мл). Объединенные органические экстракты промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш; 20-40% EtOAc в н-гексане), получив указанное в заголовке соединение (0,13 г, 60%): Т.пл. 161-163°C; 1H-ЯМР (400 МГц, ДМСО-d6) δ 9,45 (шир. с, 2H), 7,90 (с, 2H), 7,75 (с, 1H), 7,46 (с, 1H), 7,28 (с, 1H), 6,93 (м, 1H), 6,75 (м, 1H), 4,80 (м, 1H), 4,40 (с, 2H), 3,90 (с, 2H); ЭРИ-МС m/z 578,96 ([M-H]-).
Пример 82: Получение (E)-N-(2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)пиридин-2-амина (CC43)
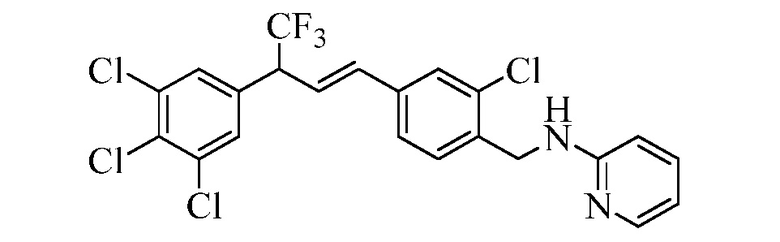
К перемешиваемому раствору N-(2-хлор-4-винилбензил)пиридин-2-амина (0,3 г, 1,22 ммоль) в 1,2-дихлорбензоле (5 мл) добавляли 5-(1-бром-2,2,2-трифторэтил)-1,2,3-трихлорбензол (0,83 г, 2,44 ммоль), CuCl (24 мг, 0,24 ммоль) и 2,2-бипиридил (76 мг, 0,48 ммоль). Полученную реакционную смесь дегазировали аргоном в течение 30 мин и затем перемешивали при 180°C в течение 24 ч. После того, как реакцию посчитали завершенной согласно ТСХ, реакционную смесь охлаждали до температуры окружающей среды и фильтровали, и фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; 15% EtOAc в н-гексане) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (0,2 г, 35%): Т.пл. 140-142°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,11 (д, J=4,0 Гц, 1H), 7,40 (м, 5H), 7,22 (м, 1H), 6,61 (м, 2H), 6,35 (м, 2H), 4,94 (шир. с, 1H), 4,61 (д, J=6,4 Гц, 2H), 4,11 (м, 1H); ЭРИ-МС m/z 505,39 ([M+H]+).
Пример 83: Получение (E)-N-((3-хлор-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)-бут-1-ен-1-ил)пиридин-2-ил)метил)-3,3,3-трифтор-пропанамида (CC44)
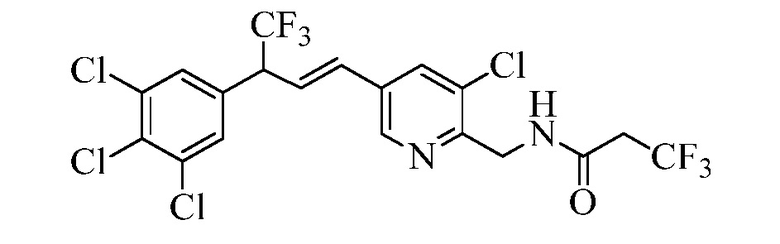
К перемешиваемому раствору (E)-(3-хлор-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)пиридин-2-ил)метанамина (0,1 г, 0,2 ммоль) в CH2Cl2 (5 мл) добавляли 3,3,3-трифторпропановую кислоту (45 мг, 0,350 ммоль), EDC·HCl (67 мг, 0,350 ммоль), HOBt·H2O (71 мг, 0,467 ммоль) и DIEA (60,2 мг, 0,467 ммоль), и реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Реакционную смесь разбавляли CH2Cl2 и промывали H2O. Объединенный слой CH2Cl2 промывали рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 15% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде бледно-желтой жидкости (30 мг, 35%): 1H-ЯМР (400 МГц, CDCl3) δ 8,41 (с, 1H), 7,77 (с, 1H), 7,47 (шир. с, 1H), 7,40 (с, 2H), 6,58 (д, J=16,0 Гц, 1H), 6,45 (дд, J=16,0, 8,0 Гц, 1H), 4,68 (д, J=4,0 Гц, 2H), 4,14 (м, 1H), 3,24 (кв., J=10,8 Гц, 2H); ЭРИ-МС m/z 536,88 ([M-H]-); ИК (тонкая пленка) 3320, 1674, 1114, 808.
Соединение CC45 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 83.
Пример 84: Получение (E)-3,3,3-трифтор-N-((4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)нафталин-1-ил)метил)пропан-амида (CC46)
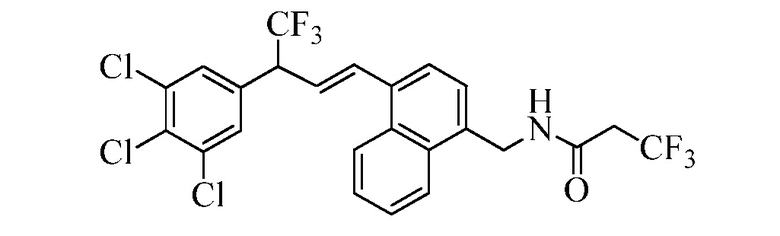
К перемешиваемому раствору (E)-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)нафталин-1-ил)метанамина (0,1 г, 0,22 ммоль) в CH2Cl2 (8 мл) добавляли 3,3,3-трифторпропановую кислоту (0,032 г, 0,24 ммоль), HOBt·H2O (52 мг, 0,33 ммоль), EDC·HCl (0,065 г, 0,33 ммоль) и DIEA (0,044 г, 0,45 ммоль), и полученную реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Реакционную смесь разбавляли H2O и экстрагировали EtOAc (3×30 мл). Объединенный слой EtOAc промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; 15% EtOAc в н-гексане) дала указанное в заголовке соединение в виде смолистого материала (60 мг, 50%): Т.пл. 151-153°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,06 (м, 1H), 7,61 (м, 4H), 7,48 (с, 2H), 7,44 (д, J=8,0 Гц, 1H), 7,38 (м, 1H), 6,42 (м, 1H), 5,92 (шир. с, 1H), 4,92 (м, 2H), 4,24 (м, 1H), 3,12 (м, 2H); ЭРИ-МС m/z 554,04 ([M-H]-).
Соединения CC47-CC48 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 84.
Пример 85: Получение (E)-1-этил-3-((4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)нафталин-1-ил)метил)мочевины (CC49)
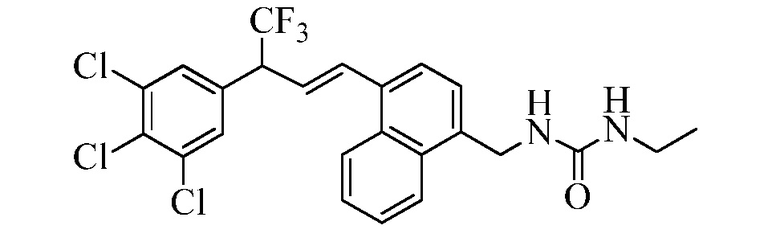
К перемешиваемому раствору (E)-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)нафталин-1-ил)метанамина (0,1 г, 0,22 ммоль) в CH2Cl2 при 0°C добавляли Et3N (0,064 мл, 0,44 ммоль) и этилизоцианат (0,023 мл, 0,33 ммоль), и реакционную смесь перемешивали в течение 1 ч при 0°C. Реакционную смесь разбавляли CH2Cl2. Органический слой промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 30% EtOAc в гексане) дала указанное в заголовке соединение в виде твердого вещества (0,07 г, 60%): Т.пл. 84-87°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,06 (м, 1H), 7,98 (м, 1H), 7,61 (м, 3H), 7,48 (с, 2H), 7,44 (д, J=8,0 Гц, 1H), 7,38 (м, 2H), 6,42 (м, 1H), 4,92 (с, 2H), 4,6 (шир. с, 1H), 4,24 (м, 1H), 3,21 (м, 2H), 1,2 (т, J=4,6 Гц, 3H); ЭРИ-МС m/z 515,33 ([M+H]+).
Пример 86: Получение (E)-N'-(4-(4,4,4-Трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)фенил)циклопропанкарбогидразида (CC50)
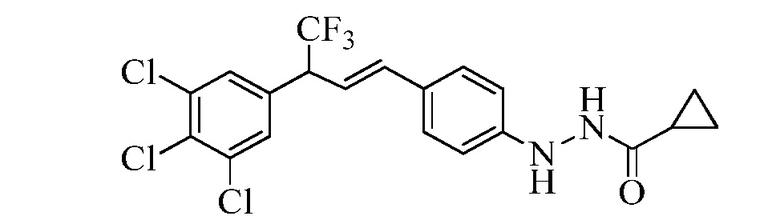
К перемешиваемому раствору (E)-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)гидразина (0,1 г, 0,3 ммоль) в CH2Cl2 (10 мл) добавляли DIEA (65 мг, 0,51 ммоль), HOBt·H2O (59 мг, 0,38 ммоль), EDC·HCl (73 мг, 0,38 ммоль) и циклопропанкарбонилхлорид (0,024 г, 0,28 ммоль), и реакционную смесь перемешивали при температуре окружающей среды в течение 1 ч. Реакционную смесь разбавляли нас водн. раствором NaHCO3 и экстрагировали CH2Cl2. Объединенный слой CH2Cl2 промывали рассолом, сушили над безводным Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2; 5-25% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (65 мг, 55%): Т.пл. 138-140°C; 1H-ЯМР (400 МГц, CDCl3) δ 9,81 (с, 1H), 7,90 (с, 1H), 7,84 (с, 2H), 7,34 (д, J=8,4 Гц, 2H), 6,65 (д, J=15,6 Гц, 1H), 6,61 (м, 1H), 6,57 (с, 1H), 6,48 (дд, J=15,6, 8,8 Гц, 1H), 4,74 (м, 1H), 1,64 (м, 1H), 0,75 (м, 4H); ЭРИ-МС m/z 461,32 ([M-H]-).
Соединение CC51 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 86.
Пример 87: Получение (E)-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)фенокси)циклопропанкарбоксамида (CC52)
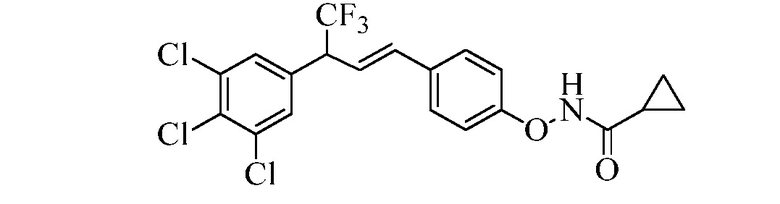
К перемешиваемому раствору (E)-O-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)гидроксиламина (0,15 г, 0,38 ммоль) в CH2Cl2 (5 мл) добавляли EDC·HCl (0,109 г, 0,569 ммоль), HOBt·H2O (0,087 г, 0,569 ммоль), DIEA (0,097 г, 0,758 ммоль) и циклопропанкарбоновую кислоту (0,049 г, 0,569 ммоль). Полученную реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч. Реакционную смесь разбавляли H2O и экстрагировали CHCl3 (35 мл), объединенный слой CHCl3 промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной флеш-хроматографии (SiO2; 20% EtOAc в гексане) дала указанное в заголовке соединение в виде коричневой жидкости (0,06 г, 34%): 1H-ЯМР (400 МГц, CDCl3) δ 7,40 (с, 2H), 7,18 (с, 1H), 7,08 (с, 1H), 6,85 (м, 1H), 6,45 (м, 1H), 6,65 (м, 1H), 6,20 (м, 1H), 5,55 (с, 1H), 4,08 (м, 1H), 1,90 (м, 1H), 1,30-1,10 (м, 4H); ЭРИ-МС m/z 464,87 ([M-H]-).
Соединение CC53 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 87.
Пример 88: Получение (Z)-3,3,3-трифтор-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)пропанамида (CC54)
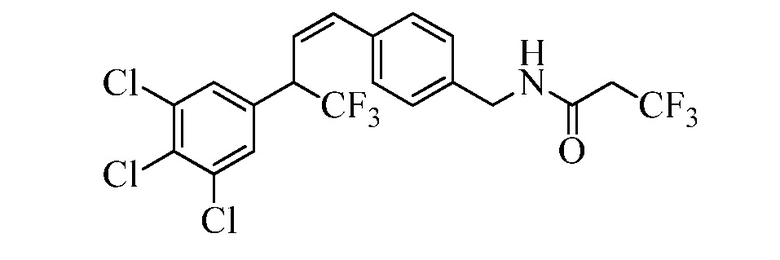
Во флакон из боросиликатного стекла вносили (E)-3,3,3-трифтор-N-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензил)пропанамид (133 мг, 0,269 ммоль) и диметилсульфоксид (ДМСО; 10 мл). Смесь помещали на расстоянии 0,6-1 метр (м) от батареи из восьми 115 Вт флуоресцентных УФ-ламп Sylvania FR48T12/350BL/VHO/180 и четырех 115 Вт флуоресцентных ламп (дневного света) Sylvania F48T12/D/VHO Straight T12 на 72 ч. Смесь выпаривали в вакууме и очищали с помощью обращено-фазовой хроматографии, получив указанное в заголовке соединение в виде бесцветного масла (11 мг, 8%): 1H-ЯМР (300 МГц, CDCl3) δ 7,28 (с, 2H), 7,25 (м, 2H), 7,10 (д, J=8,0 Гц, 2H), 6,89 (д, J=11,4 Гц, 1H), 6,07 (шир. с, 1H), 6,01 (м, 1H), 4,51 (д, J=5,8 Гц, 2H), 4,34 (м, 1H), 3,12 (кв., J=7,5 Гц, 2H); 13C-ЯМР (101 МГц, CDCl3) δ 162,44, 137,20, 135,38, 135,23, 134,82, 134,68, 131,71, 129,00, 128,80, 128,69, 128,10, 127,96, 122,63,76,70, 47,33 (кв., J=28 Гц), 43,59, 42,12 (кв., J=30 Гц); ЭРИ-МС m/z 504 ([M+H]+).
Соединения DC46, AC93, AC94 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 88.
Пример 89: Получение 1-(1-бром-2,2,2-трифторэтил)-3-хлорбензола (DI2)
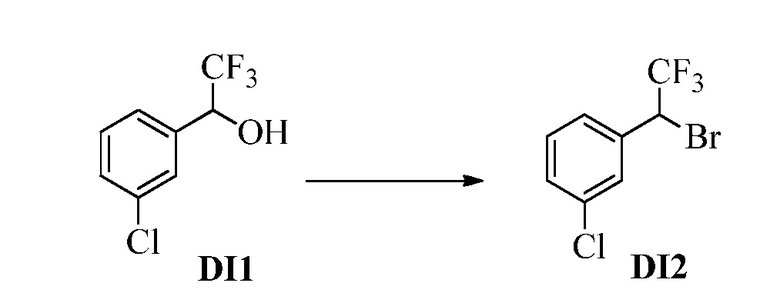
Указанное в заголовке соединение синтезировали в две стадии через 1-(3-хлорфенил)-2,2,2-трифторэтанол (DI1, полученный, как в Стадии 1, Метод B в Примере 1); выделенный в виде бесцветного вязкого масла (1,5 г, 75%): 1H-ЯМР (400 МГц, CDCl3) δ 7,50 (с, 1H), 7,42-7,35 (м, 3H), 5,02 (м, 1H), 2,65 (шир. с, 1H) и Стадию 2 в Примере 1 и выделяли (0,14 г, 22%): 1H-ЯМР (400 МГц, CDCl3) δ 7,50 (шир. с, 1H), 7,42-7,35 (м, 3H), 5,07 (м, 1H).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 89.
(1-Бром-2,2,2-трифторэтил)бензол (DI4)
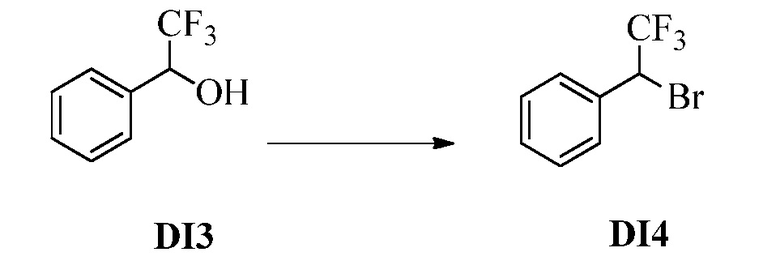
Выделяли 2,2,2-трифтор-1-фенилэтанол (DI3) (10 г, 80%): 1H-ЯМР (300 МГц, CDCl3) δ 7,48 (м, 2H), 7,40 (м, 3H), 5,02 (м, 1H), 2,65 (д, J=7,1 Гц, 1H). Указанное в заголовке соединение (DI4) выделяли в виде жидкости (8,0 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,50 (м, 2H), 7,40 (м, 3H), 5,00 (кв., J=7,5 Гц, 1H).
1-(1-Бром-2,2,2-трифторэтил)-3,5-диметилбензол (DI20)
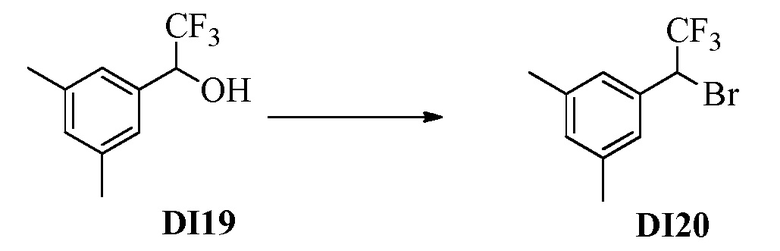
1-(3,5-Диметилфенил)-2,2,2-трифторэтанол (DI19) выделяли в виде белого твердого вещества: 1H-ЯМР (400 МГц, CDCl3) δ 7,05 (с, 2H), 7,02 (с, 1H), 4,95 (м, 1H), 2,32 (с, 6H); ЭРИ-МС m/z 204 ([М]-). Выделяли указанное в заголовке соединение (DI20) (3,0 г, 51%).
1-(1-Бром-2,2,2-трифторэтил)-2,4-дихлорбензол (DI22)
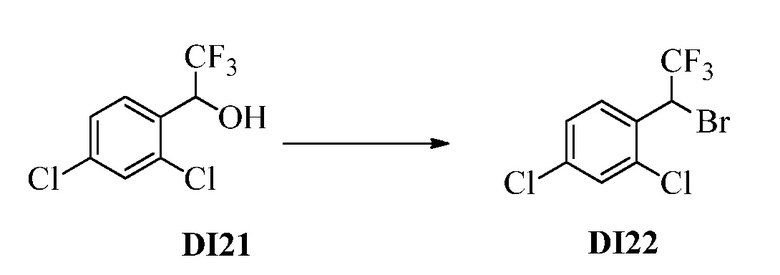
1-(2,4-Дихлорфенил)-2,2,2-трифторэтанол (DI21) выделяли в виде грязно-белого порошка (5,3 г, 61%): Т.пл. 49-51°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,62-7,66 (д, 1H), 7,42-7,44 (д, 1H), 7,32-7,36 (д, 1H), 5,6 (м, 1H), 2,7 (с, 1H); ЭРИ-МС m/z 244 ([М]+). Выделяли указанное в заголовке соединение (DI22) (3,2 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 7,62-7,72 (м, 1H), 7,4-7,42 (м, 1H), 7,3-7,38 (м, 1H), 5,7-5,8 (м, 1H).
1-(1-Бром-2,2,2-трифторэтил)-2,3-дихлорбензол (DI24)
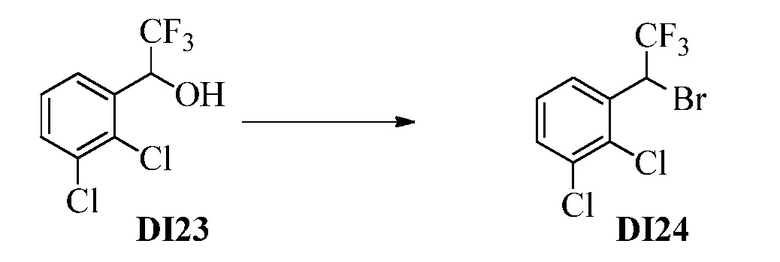
1-(2,3-Дихлорфенил)-2,2,2-трифторэтанол (DI23) выделяли в виде бледно-желтого масла (5,2 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,62-7,64 (д, 1H), 7,52-7,54 (м, 1H), 7,29-7,33 (т, 1H), 5,6-5,76 (м, 1H), 2,7 (с, 1H); ЭРИ-МС m/z 243,9 ([М]+). Указанное в заголовке соединение (DI24) выделяли в виде масла (8,7 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,62-7,71 (м, 1H), 7,44-7,52 (м, 1H), 7,27-7,3 (с, 1H), 5,81-5,91 (м, 1H).
2-(1-Бром-2,2,2-трифторэтил)-1,4-дихлорбензол (DI26)
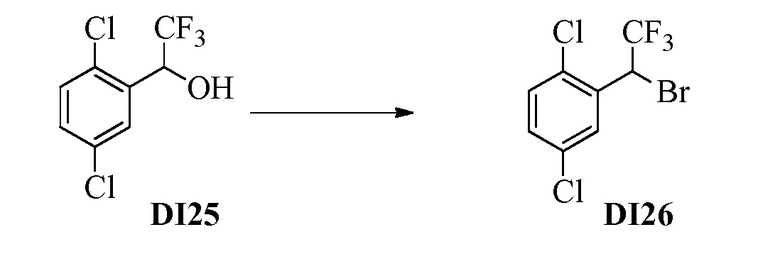
1-(2,5-Дихлорфенил)-2,2,2-трифторэтанол (DI25) выделяли в виде желтого масла (4,1 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,68-7,7 (с, 1H), 7,3-7,37 (м, 2H), 5,51-5,6 (м, 1H), 2,7 (с, 1H); ЭРИ-МС m/z 244 ([М]+)). Выделяли указанное в заголовке соединение (DI26) (3,0 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,7-7,78 (м, 1H), 7,3-7,4 (м, 2H), 5,7-5,8 (м, 1H).
1-(1-Бром-2,2,2-трифторэтил)-3,5-бис(трифторметил)бензол (DI28)
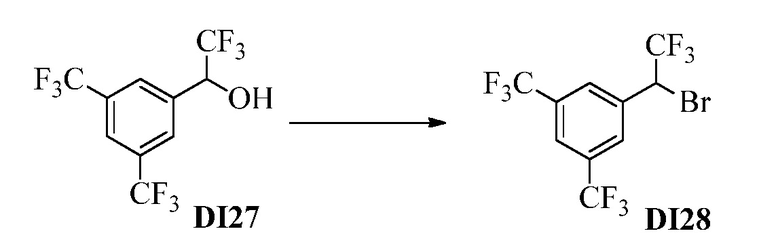
Выделяли 1-(3,5-бис(трифторметил)фенил)-2,2,2-трифторэтанол (DI27) (3,8 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,98 (м, 3H), 5,25 (м, 1H), 3,2 (шир., 1H); ЭРИ-МС m/z 312,2 ([М]+). Указанное в заголовке соединение (DI28) получали и использовали без очистки.
1-(1-Бром-2,2,2-трифторэтил)-2,3,5-трихлорбензол (DI30)
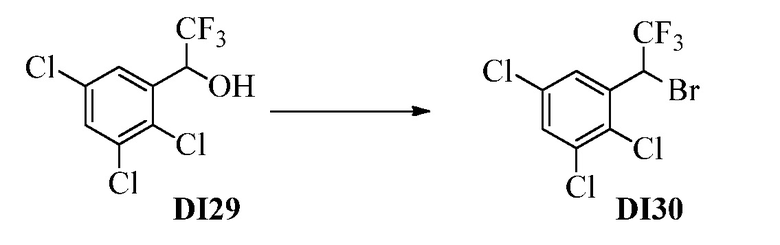
2,2,2-Трифтор-1-(2,3,5-трихлорфенил)этанол (DI29) выделяли в виде белого твердого вещества (4,0 г, 60%): Т.пл. 113-115°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,62 (д, 1H), 7,50 (д, 1H), 5,60-5,70 (м, 1H), 2,75 (с, 1H); ЭРИ-МС m/z 278,0 ([М+]). Выделяли указанное в заголовке соединение (DI30) (2,9 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 7,70 (д, 1H), 7,50 (д, 1H), 5,72-5,82 (м, 1H).
1-(1-Бром-2,2,2-трифторэтил)-3-хлор-5-(трифторметил)бензол (DI32)
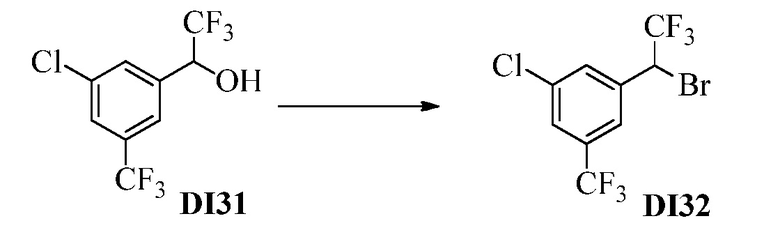
1-(3-Хлор-5-(трифторметил)фенил)-2,2,2-трифторэтанол (DI31) выделяли в виде бледно-желтого масла (2,0 г, 50%): 1H-ЯМР (400 МГц, CDCl3) δ 7,51 (м, 3H), 5,08 (м, 1H), 2,81 (с, 1H); ЭРИ-МС m/z 278,1 ([М]+). Указанное в заголовке соединение (DI32) выделяли в виде масла (2,0 г, 40%): ЭРИ-МС m/z 342 ([М]+).
5-(1-Бром-2,2,2-трифторэтил)-1,3-дихлор-2-метоксибензол (DI34)
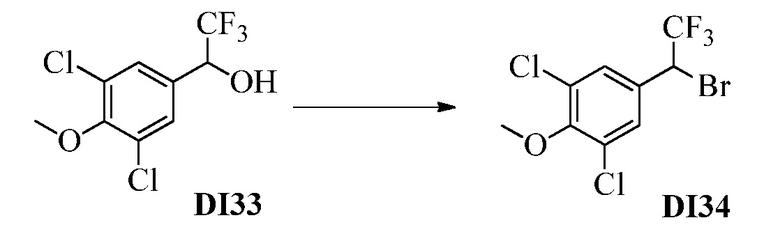
1-(3,5-Дихлор-4-метоксифенил)-2,2,2-трифторэтанол (DI33) выделяли в виде грязно-белого твердого вещества (0,8 г, 60%); Т.пл. 92-95°C: 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (с, 2H), 5,00 (м, 1H), 3,89 (с, 3H), 2,64 (м, 1H); ЭРИ-МС m/z 274 ([М]+). Указанное в заголовке соединение (DI34) выделяли в виде бесцветной жидкости (0,6 г, 57%).
Пример 90: Получение 1-(1-бром-2,2,2-трифторэтил)-3,5-дифтор-бензола (DI36)
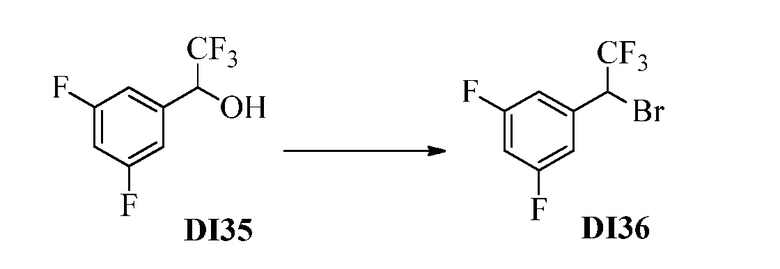
Указанное в заголовке соединение синтезировали в две стадии через 1-(3,5-дифторфенил)-2,2,2-трифторэтанол (DI35, полученный как в Стадии 1, Метод A в Примере 1; выделенный в виде бесцветного масла (0,2 г, 75%): 1H-ЯМР (400 МГц, CDCl3) δ 7,05 (м, 2H), 6,88 (м, 1H), 5,06 (м, 1H), 2,66 (с, 1H); ЭРИ-МС m/z 212 ([М]+) и Стадию 2 в Примере 1, и выделяли (3,2 г, 50%); 1H-ЯМР (400 МГц, CDCl3) δ 7,05 (м, 2H), 6,86 (м, 1H), 5,03 (кв., J=7,4 Гц, 1H).
Следующие соединения были получены в соответствии с методиками, раскрытыми в Примере 90.
1-(1-Бром-2,2,2-трифторэтил)-4-хлорбензол (DI38)
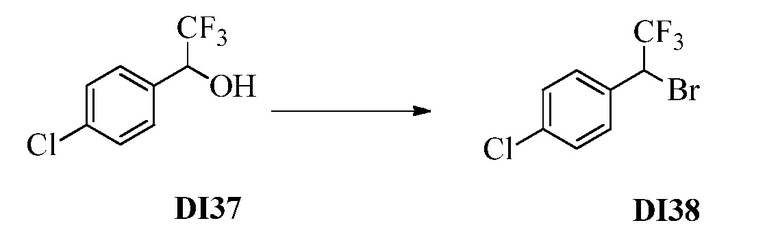
1-(4-Хлорфенил)-2,2,2-трифторэтанол (DI37) выделяли в виде бесцветного масла (5,0 г, 99%): 1H-ЯМР (400 МГц, CDCl3) δ 7,44-7,38 (м, 4H), 5,05 (м, 1H), 2,55 (с, 1H); ЭРИ-МС m/z 210 ([М]+). Выделяли указанное в заголовке соединение (DI38) (3,0 г, 46%): 1H-ЯМР (400 МГц, CDCl3) δ 7,45 (д, J=8,2 Гц, 2H), 7,37 (д, J=8,2 Гц, 2H), 5,10 (кв., J=7,2 Гц, 1H).
1-(1-Бром-2,2,2-трифторэтил)-4-анизол (DI40)
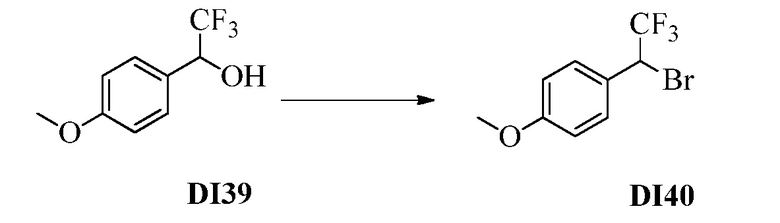
2,2,2-Трифтор-1-(4-метоксифенил)этанол (DI39) выделяли в виде светло-желтой жидкости: 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (д, J=8,8 Гц, 2H), 6,95 (м, J=8,8 Гц, 2H), 5,00 (м, 1H), 3,82 (с, 3H), 2,44 (с, 1H); ЭРИ-МС m/z 206,1 ([М]+). Выделяли указанное в заголовке соединение (DI40) (3,8 г, 62%).
1-(1-Бром-2,2,2-трифторэтил)-4-фторбензол (DI42)
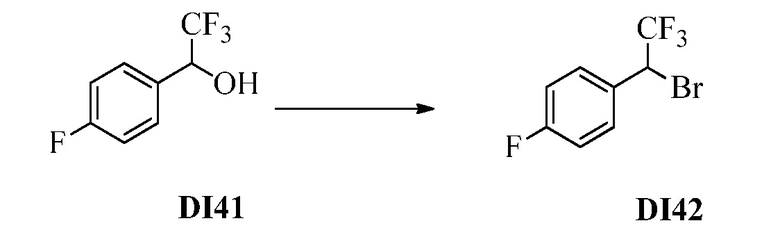
2,2,2-Трифтор-1-(4-фторфенил)этанол (DI41) выделяли в виде бесцветного масла (5 г, 99%): 1H-ЯМР (400 МГц, CDCl3) δ 7,48-7,45 (м, 2H), 7,13-7,07 (м, 2H), 5,06 (м, 1H), 2,53 (с, 1H); ЭРИ-МС m/z 194 ([М]+). Указанное в заголовке соединение (DI42) получали и использовали в качестве промежуточного соединения без очистки.
1-(1-Бром-2,2,2-трифторэтил)-4-метилбензол (DI44)
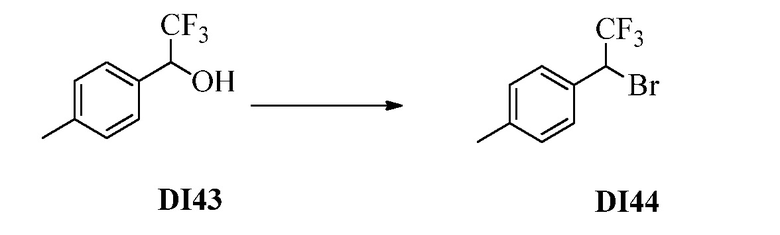
2,2,2-Трифтор-1-(п-толил)этанол (DI43) выделяли в виде бесцветного масла (5,0 г, 99%): 1H-ЯМР (400 МГц, CDCl3) δ 7,37 (д, J=8,0 Гц, 2H), 7,23 (д, J=8,0 Гц, 2H), 5,02 (м, 1H), 2,46 (м, 1H), 2,37 (с, 3H); ЭРИ-МС m/z 190 ([М]+). Выделяли указанное в заголовке соединение (DI44) (3,0 г, 45%).
1-(1-Бром-2,2,2-трифторэтил)-3-фторбензол (DI46)
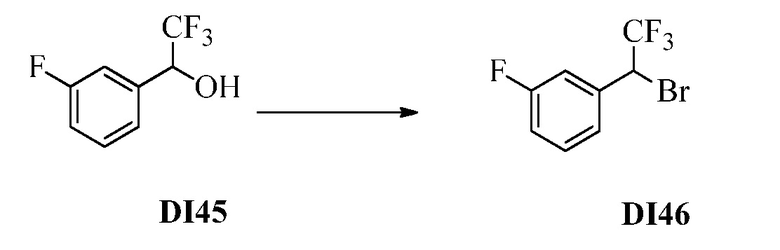
2,2,2-Трифтор-1-(3-фторфенил)этанол (DI45) выделяли в виде бесцветного вязкого масла (2,8 г, 93%): 1H-ЯМР (400 МГц, CDCl3) δ 7,41 (м, 1H), 7,25 (м, 2H), 7,14 (м, 1H), 5,06 (м, 1H), 2,60 (с, 1H); ЭРИ-МС m/z 194 ([М]+). Выделяли указанное в заголовке соединение (DI46) (2,0 г, 61%).
1-(1-Бром-2,2,2-трифторэтил)-2-фторбензол (DI48)
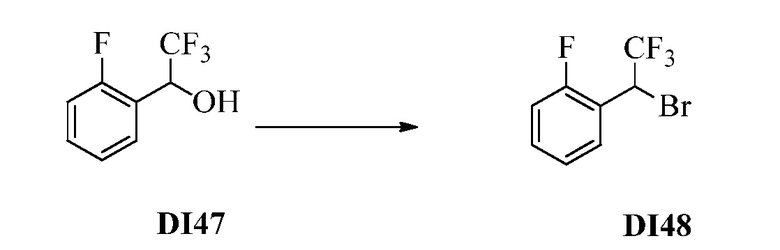
2,2,2-Трифтор-1-(2-фторфенил)этанол (DI47) выделяли в виде бесцветного масла (2,5 г, 99%): 1H-ЯМР (400 МГц, CDCl3) δ 7,40 (м, 1H), 7,43 (м, 1H), 7,24 (м, 1H), 7,13 (м, 1H), 5,42 (м, 1H), 2,65 (с, 1H); ЭРИ-МС m/z 194 ([М]+). Выделяли указанное в заголовке соединение (DI48) (2,0 г, 61%): 1H-ЯМР (400 МГц, CDCl3) δ 7,61 (м, 1H), 7,40 (м, 1H), 7,23 (м, 1H), 7,10 (м, 1H), 5,40 (м, 1H); ГХ-МС m/z 255 ([M-H]-).
Пример 91: Получение 4-(1H-1,2,4-триазол-1-ил)бензальдегида (DI5)
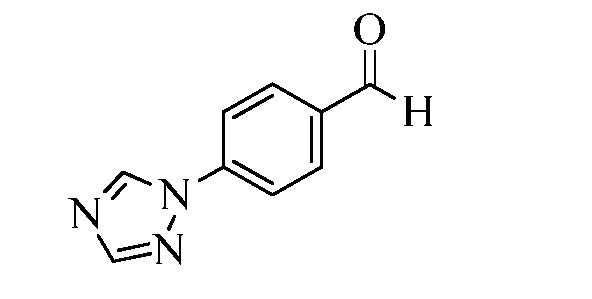
К перемешиваемому раствору 4-фторбензальдегида (10,0 г, 80,6 ммоль) в ДМФА (150 мл) добавляли K2CO3 (13,3 г, 96,7 ммоль) и 1,2,4-триазол (6,67 г, 96,7 ммоль) и полученную реакционную смесь перемешивали при 120°C в течение 6 ч. После завершения реакции (ТСХ) реакционную смесь разбавляли H2O и экстрагировали EtOAc (3×100 мл). Объединенный слой EtOAc промывали H2O и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде твердого вещества (9,0 г, 65%): Т.пл. 145-149°C: 1H-ЯМР (400 МГц, CDCl3) δ 10,08 (с, 1H), 8,70 (с, 1H), 8,16 (с, 1H), 8,06 (д, J=8,0 Гц, 2H), 7,92 (д, J=8,0 Гц, 2H); ЭРИ-МС m/z 173,9 ([M+H]+).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 91.
5-Формил-2-(1H-1,2,4-триазол-1-ил)бензонитрил (DI49)
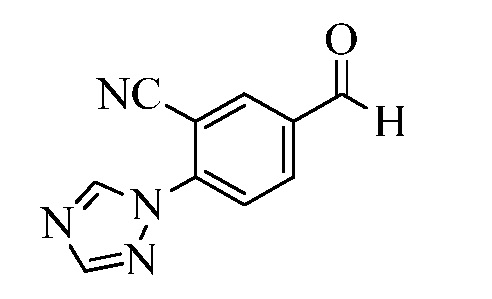
Выделяли указанное в заголовке соединение (2,8 г, 60%); 1H-ЯМР (400 МГц, CDCl3) δ 10,10 (с, 1H), 8,98 (с, 1H), 8,35 (с, 1H), 8,30 (д, 1H), 8,22 (с, 1H), 8,07 (д, 1H); ИК (тонкая пленка) 3433, 3120, 1702, 1599, 1510 см-1.
2-Хлор-4-(1H-1,2,4-триазол-1-ил)бензальдегид (DI50)

Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (3,0 г, 40%): Т.пл. 149-151°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,05 (с, 1H), 8,74 (с, 1H), 8,17 (с, 1H), 8,10 (с, 1H), 7,90 (м, 2H); ЭРИ-МС m/z 208,10 ([M+H]+).
5-Метил-4-(1H-1,2,4-триазол-1-ил)бензальдегид (DI51)
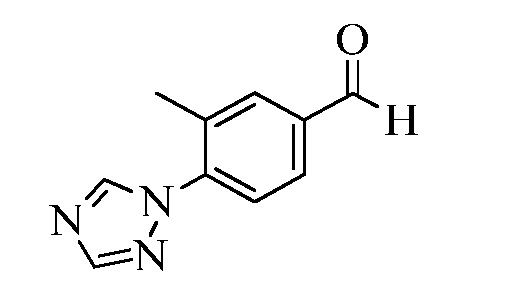
Указанное в заголовке соединение выделяли в виде белого твердого вещества (0,5 г, 74%): Т.пл. 109-111°C; 1H-ЯМР (400 МГц, D6-ДМСО) δ 10,06 (с, 1H), 9,00 (с, 1H), 8,30 (с, 1H), 7,99 (с, 1H), 7,92 (д, J=9,2 Гц, 1H), 7,69 (д, J=9,2 Гц, 1H), 2,30 (с, 3H); ЭРИ-МС m/z 188,13 ([M+H]+).
Пример 92: Получение 5-формил-2-(3-нитро-1H-1,2,4-триазол-1-ил)бензонитрила (DI52)
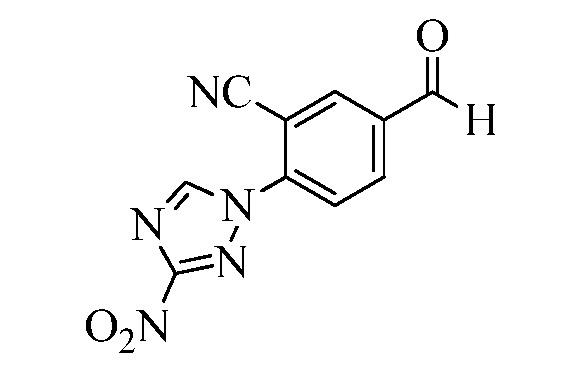
К перемешиваемому раствору 2-фтор-5-формилбензонитрила (0,5 г, 3,3 ммоль) в ДМФА (25 мл) добавляли K2CO3 (0,68 г, 4,95 ммоль) и 3-нитро-1,2,4-триазол (0,45 г, 4,2 ммоль) и полученную реакционную смесь перемешивали при КТ в течение 14 ч. После завершения реакции (ТСХ) реакционную смесь разбавляли водой и экстрагировали EtOAc. Объединенный слой EtOAc промывали водой и рассолом, затем сушили над Na2SO4 и выпаривали при пониженном давлении с получением указанного в заголовке соединения в виде светло-желтого твердого вещества (0,36 г, 45%): Т.пл. 170-172°C; 1H-ЯМР (300 МГц, ДМСО-d6) δ 10,12 (с, 1H), 9,61 (с, 1H), 8,69 (с, 1H), 8,45 (д, J=9,3 Гц, 1H), 8,23 (д, J=9,3 Гц, 1H); ЭРИ-МС m/z 242,3 ([M-H]-); ИК (тонкая пленка) 2238, 1705, 1551, 1314 см-1.
Пример 93: Получение 4-(3-метил-1H-1,2,4-триазол-1-ил)бензальде-гида (DI53)
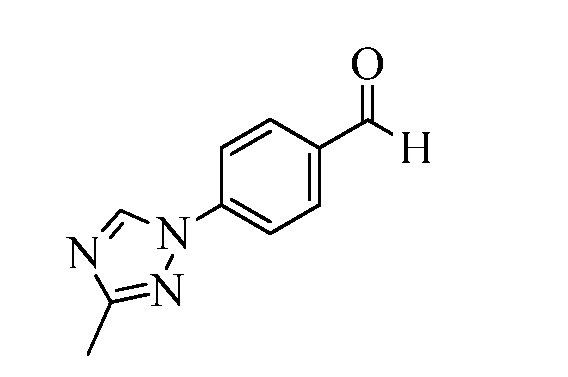
К перемешиваемому раствору 4-фторбензальдегида (5,0 г, 40,32 ммоль) в ДМФА (50 мл) добавляли K2CO3 (3,34 г, 40,32 ммоль) и 3-метил-1,2,4-триазол (3,34 г, 40,32 ммоль) и полученную реакционную смесь перемешивали при КТ в течение 4 ч. После завершения реакции (ТСХ) реакционную смесь разбавляли водой и экстрагировали EtOAc (3×). Объединенный слой EtOAc промывали водой и рассолом, затем сушили над Na2SO4 и выпаривали при пониженном давлении с получением указанного в заголовке соединения в виде белого твердого вещества (4,1 г, 60%): 125-128°C Т.пл.; 1H-ЯМР (400 МГц, CDCl3) δ 10,05 (с, 1H), 8,76 (с, 1H), 8,02 (д, 2H), 7,85 (д, 2H), 2,50 (с, 3H); ЭРИ-МС m/z 188,04 ([M+H]+).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 93.
4-(1H-1,2,4-Триазол-1-ил)-3-(трифторметил)бензальдегид (DI54)
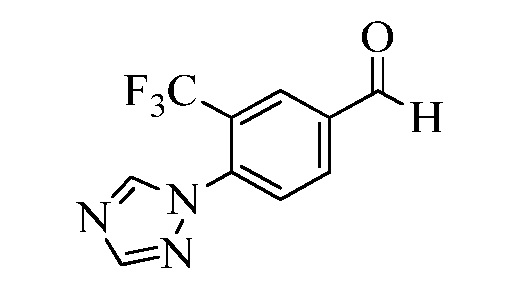
Указанное в заголовке соединение выделяли в виде белого твердого вещества (1,05 г, 60%): Т.пл. 81-83°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,15 (с, 1H), 8,43 (с, 1H), 8,37 (с, 1H), 8,25 (д, J=7,2 Гц, 1H), 8,18 (с, 1H), 7,79 (д, J=7,2 Гц, 1H); ЭРИ-МС m/z 241,0 ([М]+).
4-(3-Нитро-1H-1,2,4-триазол-1-ил)бензальдегид (DI55)

Указанное в заголовке соединение выделяли в виде бледно-желтого твердого вещества (0,10 г, 23%): Т.пл. 159-161°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,10 (с, 1H), 8,89 (с, 1H), 8,15 (м, 2H), 8,00 (м, 2H); ЭРИ-МС m/z 217,11 ([M-H]-).
3-Бром-4-(1H-1,2,4-триазол-1-ил)бензальдегид (DI56)
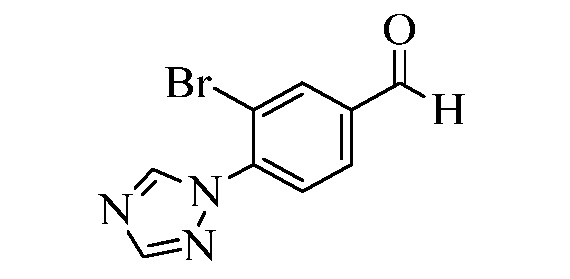
Указанное в заголовке соединение выделяли в виде белого твердого вещества (3,2 г, 51%): Т.пл. 126-128°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,04 (с, 1H), 8,69 (с, 1H), 8,27 (м, 1H, 8,18 (с, 1H) 7,99 (д, J=9,2 Гц, 1H), 7,76 (д, J=9,2 Гц, 1H); ЭРИ-МС m/z 250,9 ([М]+).
5-Формил-2-(3-метил-1H-1,2,4-триазол-1-ил)бензонитрил (DI57)
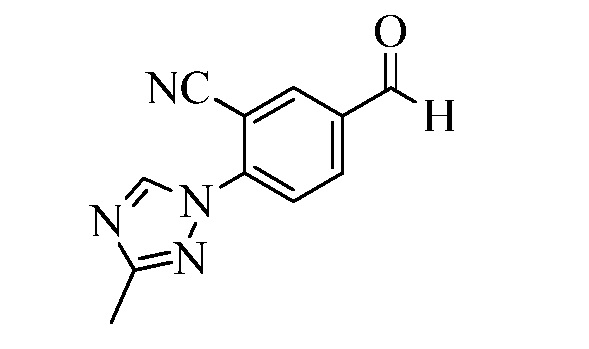
Указанное в заголовке соединение выделяли в виде белого твердого вещества (0,13 г, 30%): Т.пл. 147-149°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,07 (с, 1H), 8,89 (с, 1H), 8,32 (д, J=1,8 Гц, 1H), 8,24 (дд, J=8,6, 1,3 Гц, 1H), 8,06 (д, J=8,6 Гц, 1H), 2,54 (с, 3H); ЭРИ-МС m/z 213,09 ([M+H]+); ИК (тонкая пленка) 2239, 1697 см-1.
3-Нитро-4-(1H-1,2,4-триазол-1-ил)бензальдегид (DI58)
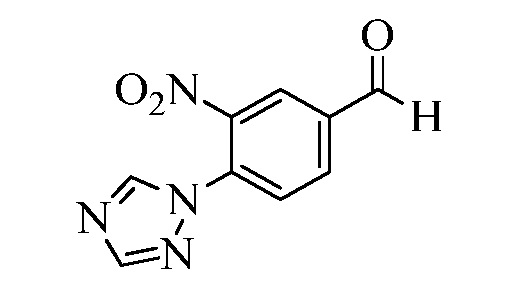
Указанное в заголовке соединение выделяли в виде светло-желтого твердого вещества (3,0 г, 60%): Т.пл. 116-118°C; 1H-ЯМР (400 МГц, CDCl3) δ 10,15 (с, 1H), 8,48 (с, 1H), 8,46 (с, 1H), 8,26 (д, J=6,9 Гц, 1H), 8,16 (с, 1H), 7,83 (д, J=6,9 Гц, 1H); ЭРИ-МС m/z 219,00 ([M+H]+).
Пример 94: Получение 1-(4-винилфенил)-1H-1,2,4-триазола (DI59)
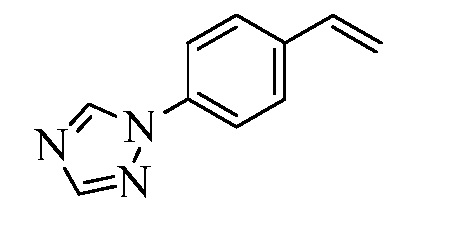
К перемешиваемому раствору 4-[1,2,4]триазол-1-ил-бензальдегида (9,0 г, 52 ммоль) в 1,4-диоксане (100 мл) добавляли K2CO3 (10,76 г, 78 ммоль) и метилтрифенилфосфонийбромид (22,2 г, 62,4 ммоль) при комнатной температуре. Полученную реакционную смесь нагревали до 70ºC в течение 18 ч. После завершения реакции (ТСХ) реакционную смесь охлаждали до комнатной температуры и фильтровали, и полученный фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; 25-30% EtOAc в петролейном эфире) с получением указанного в заголовке соединения в виде белого твердого вещества (5,6 г, 63%): ЭРИ-МС m/z 172,09 ([M+H]+).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 94.
1-(2-Метил-4-винилфенил)-1H-1,2,4-триазол (DI60)
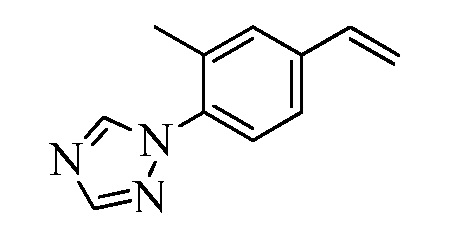
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (1,5 г, 76%): 1H-ЯМР (400 МГц, CDCl3) δ 8,25 (с, 1H), 8,11 (с, 1H), 7,35 (м, 2H), 7,27 (д, J=8,7 Гц, 1H), 6,74 (м, 1H), 5,82 (д, J=17,3 Гц, 1H), 5,36 (д, J=10,0 Гц, 1H), 2,25 (с, 3H); ЭРИ-МС m/z 186,14 ([M+H]+).
2-(1H-1,2,4-Триазол-1-ил)-5-винилбензонитрил (DI61)
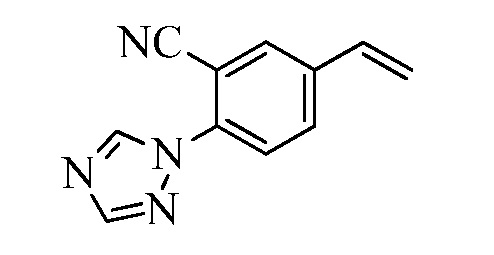
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (1,40 г, 71%): Т.пл. 126-129ºC; 1H-ЯМР (400 МГц, CDCl3) δ 8,76 (с, 1H), 8,18 (с, 1H), 7,82-7,84 (м, 1H), 7,72-7,80 (м, 2H), 6,70-6,80 (дд, J=17,6, 10,8 Гц, 1H), 5,90-5,95 (д, J=17,6 Гц, 1H), 5,50-5,70 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 197,03 ([M+H]+).
Пример 95: Получение 2-(3-Нитро-1H-1,2,4-триазол-1-ил)-5-винил-бензонитрил (DI62)
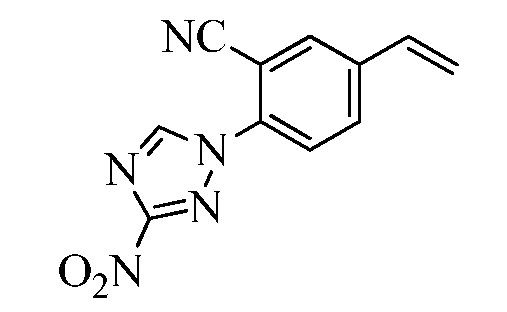
К перемешиваемому раствору 5-формил-2-(3-нитро-1H-1,2,4-триазол-1-ил)бензонитрила (0,36 г, 1,49 ммоль) в 1,4-диоксане (25 мл) добавляли K2CO3 (0,3 г, 2,2 ммоль) и метилтрифенил-фосфонийбромид (0,63 г, 1,79 ммоль). Полученную реакционную смесь нагревали до 100°C в течение 18 ч. После завершения реакции (ТСХ) реакционную смесь охлаждали до комнатной температуры и фильтровали, и полученный фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; 25-30% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (0,25 г, 70%): Т.пл. 103-105°C; 1H-ЯМР (400 МГц, ДМСО-d6) δ 9,50 (с, 1H), 8,34 (м, 1H), 7,98 (д, J=7,8 Гц, 1H), 7,68 (д, J=7,8 Гц, 1H), 6,87 (м, 1H), 6,20 (д, J=15,7 Гц, 1H), 5,56 (д, J=11,8 Гц, 1H); ЭРИ-МС m/z 240,27 ([M-H]-); ИК (тонкая пленка) 2240, 1514, 1312 см-1.
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 95.
1-(3-Хлор-4-винилфенил)-1H-1,2,4-триазол (DI63)
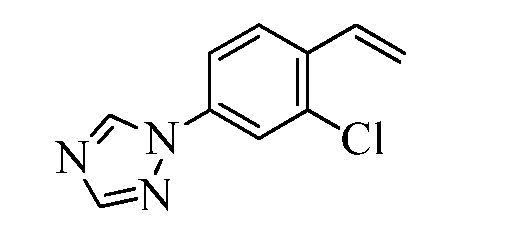
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (2,3 г, 80%): Т.пл. 134-137°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,56 (с, 1H), 8,11 (с, 1H), 7,76 (с, 1H), 7,70 (д, J=9,0 Гц, 1H), 7,57 (д, J=9,0 Гц, 1H), 7,10 (м, 1H), 5,80 (д, J=17,2 Гц, 1H), 5,47 (д, J=12,4 Гц, 1H); ЭРИ-МС m/z 206,04 ([M+H]+.
3-Метил-1-(4-винилфенил)-1H-1,2,4-триазол (DI64)
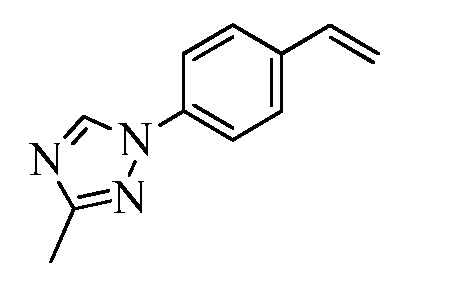
Указанное в заголовке соединение выделяли в виде белого твердого вещества (0,6 г, 60%): Т.пл. 109-111°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,42 (с, 1H), 7,40-7,60 (м, 4H), 6,70-7,00 (дд, J=17,6, 10,8 Гц, 1H), 5,80 (д, J=17,6 Гц, 1H), 5,30 (д, J=17,6 Гц, 1H), 2,50 (с, 3H); ЭРИ-МС m/z 186,20 ([M+H]+).
1-(2-(Трифторметил)-4-винилфенил)-1H-1,2,4-триазол (DI65)
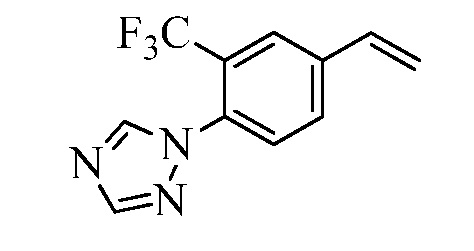
Указанное в заголовке соединение выделяли в виде бесцветного масла (0,6 г, 60%): 1H-ЯМР (400 МГц, CDCl3) δ 8,32 (с, 1H), 8,14 (с, 1H), 7,84 (с, 1H), 7,72 (д, J=8,0 Гц, 1H), 7,50 (д, J=7,6 Гц, 1H), 6,70-6,90 (дд, J=17,6, 10,8 Гц, 1H), 5,90-6,00 (д, J=17,6 Гц, 1H), 5,50-5,80 (д, J=10,8 Гц 1H); ЭРИ-МС m/z 240,16 ([M+H]+).
3-Нитро-1-(4-винилфенил)-1H-1,2,4-триазол (DI66)
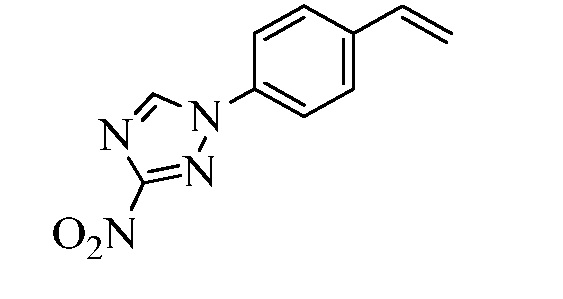
Указанное в заголовке соединение выделяли в виде светло- желтого твердого вещества (61 мг, 20%): Т.пл. 137-139°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,60 (с, 1H), 7,68 (д, J=7,7 Гц, 2H), 7,60 (д, J=8,3 Гц, 2H), 6,77 (дд, J=17,7, 10,8, 1H), 5,87 (д, J=17,7 Гц, 1H), 5,42 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 217,28 ([M+H]+).
1-(2-Бром-4-винилфенил)-1H-1,2,4-триазол (DI67)
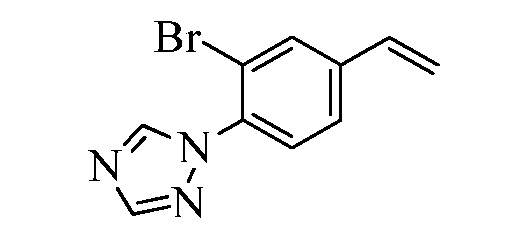
Указанное в заголовке соединение выделяли в виде белого твердого вещества (1,2 г, 40%): Т.пл. 75-77°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,48 (с, 1H), 8,12 (с, 1H), 7,75 (с, 1H) 7,42 (с, 2H), 6,70 (м, 1H), 5,83 (д, J=18 Гц, 1H), 5,42 (д, J=12 Гц, 1H); ЭРИ-МС m/z 249,1 ([М]+).
2-(3-Метил-1H-1,2,4-триазол-1-ил)-5-винилбензонитрил (DI68)
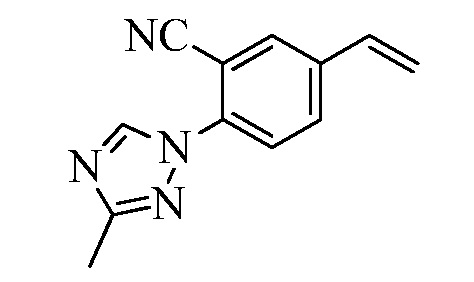
Указанное в заголовке соединение выделяли в виде грязно-белого твердого вещества (0,6 г, 60%): Т.пл. 96-97°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,66 (с, 1H), 7,80 (с, 1H), 7,74 (м, 2H), 6,73 (дд, J=17,6 Гц, 10,8 Гц, 1H), 5,88 (д, J=17,6 Гц, 1H), 5,49 (д, J=10,8 Гц, 1H), 2,52 (с, 3H); ЭРИ-МС m/z 211,10 ([M+H]+); ИК (тонкая пленка) 2229 см-1.
1-(2-Нитро-4-винилфенил)-1H-1,2,4-триазол (DI69)

Указанное в заголовке соединение выделяли в виде желтого твердого вещества (1,78 г, 60%): Т.пл. 102-104°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,40 (с, 1H), 8,12 (с, 1H), 8,02 (с, 1H), 7,72-7,76 (д, J=8,0 Гц, 1H), 7,52-7,56 (д, J=17,6 Гц, 1H), 6,70-6,82 (дд, J=17,6, 10,8 Гц, 1H), 5,85-6,00 (д, J=17,6 Гц, 1H), 5,50-5,60 (д, J=10,8, Гц 1H); ЭРИ-МС m/z 217,0 ([M+H]+).
Пример 96: Получение 3-метил-2-(1H-1,2,4-триазол-1-ил)-5-винил-бензонитрил (DI70)
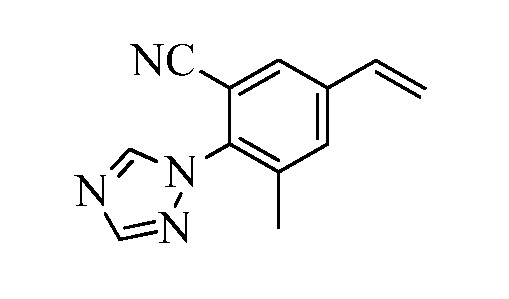
Стадия 1. 5-Бром-2-фтор-3-метилбензальдегид: К перемешиваемому раствору диизопропиламина (4,01 г, 39,88 ммоль) в ТГФ (20 мл) при -78°C медленно, по каплям, в течение 10 минут добавляли н-бутиллитий (1,6М в гексане) (19,9 мл, 31,91 ммоль), реакционную смесь перемешивали при -78°C в течение 30 мин. Добавляли раствор 4-бром-1-фтор-2-метилбензола (5,0 г, 26,6 ммоль) в ТГФ (30,0 мл) при -78°C, и реакционную смесь перемешивали в течение 1 ч при той же температуре. Добавляли ДМФА (5,0 мл) и перемешивали при -78°C еще 30 мин. Реакцию контролировали с помощью ТСХ; затем в реакционную смесь вливали 1Н раствор HCl (водн.) при 0°C. Водный слой экстрагировали диэтиловым эфиром, промывали водой и насыщенным солевым раствором. Объединенный органический слой сушили над безводным Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение, которое очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 5% этилацетатом/петр. эфиром), получив указанное в заголовке соединение в виде белого твердого вещества (3,6 г, 64%); 48-50°C Т.пл.: 1H-ЯМР (400 МГц, CDCl3) δ 8,33 (с, 1H), 8,22 (с, 1H), 7,67 (с, 1H), 7,60 (с, 1H), 6,75 (дд, J=17,6, 10,8 Гц, 1H), 5,92 (дд, J=17,6, 10,8 Гц, 1H), 5,52 (д, J=17,6 Гц, 1H), 2,21 (с, 3H); ЭРИ-МС m/z 211,35 ([M-H]-).
Стадия 2. Оксим (E)-5-бром-2-фтор-3-метилбензальдегида: К перемешиваемому раствору 5-бром-2-фтор-3-метилбензальдегида (3,5 г, 16,2 ммоль) в этаноле (50,0 мл) добавляли ацетат натрия (2,0 г, 24,3 ммоль) и гидрохлорид гидроксиламина (1,69 г, 24,3 ммоль) при КТ. Реакционную смесь перемешивали при КТ в течение 3 ч. Реакционную смесь выпаривали на роторном испарителе, получив неочищенное соединение, которое промывали водой, отфильтровывали и сушили под вакуумом с получением указанного в заголовке соединения в виде белого твердого вещества: Т.пл. 126-127°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,32 (с, 1H), 7,73 (д, J=2,4 Гц, 1H), 7,51 (с, 1H), 7,34 (д, J=2,4 Гц, 1H), 2,25 (с, 3H); ЭРИ-МС m/z 232,10 ([M+H]+).
Стадия 3. 5-Бром-2-фтор-3-метилбензонитрил: Перемешиваемый раствор оксима (E)-5-бром-2-фтор-3-метилбензальдегида (0,5 г, 2,2 ммоль) в уксусном ангидриде (5,0 мл) нагревали с обратным холодильником до дефлегмации в течение 18 ч. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Объединенный этилацетатный слой промывали рассолом и сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение в виде светло-коричневого смолистого материала (0,4 г, неочищенный): ЭРИ-МС m/z 213,82 ([M+H]+).
Стадия 4. 5-Бром-3-метил-2-(1H-1,2,4-триазол-1-ил)бензо-нитрил (DI71): К перемешиваемому раствору 5-бром-2-фтор-3-метилбензонитрила (1,0 г, 47,716 ммоль) в ДМФА (10,0 мл) добавляли карбонат калия (1,95 г, 14,14 ммоль) с последующим добавлением 1H-1,2,4-триазола (0,811 г, 9,433 ммоль) при КТ. Реакционную смесь нагревали до 140°C в течение 18 ч. Реакционную смесь охлаждали до КТ, разбавляли водой и экстрагировали этилацетатом (2×100 мл). Объединенный этилацетатный слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение, которое очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 30% этилацетатом/петр. эфиром), получив указанное в заголовке соединение в виде розового твердого вещества (0,6 г, 49%): 1H-ЯМР (400 МГц, CDCl3) δ 8,39 (с, 1H), 8,23 (с, 1H), 7,91 (д, J=2,4 Гц, 2H), 2,21 (с, 3H), ЭРИ-МС m/z 262,57 ([M+H]+); ИК (тонкая пленка) 2231, 554 см-1.
Стадия 5. 3-Метил-2-(1H-1,2,4-триазол-1-ил)-5-винилбензо-нитрил (DI70): Смесь 5-бром-3-метил-2-(1H-1,2,4-триазол-1-ил)бензонитрила (0,6 г, 2,3 ммоль), карбоната калия (0,95 г, 6,87 ммоль), винилборонового ангидрида (0,82 г, 3,43 ммоль) и трифенилфосфина (0,13 г, 0,114 ммоль) в толуоле (20,0 мл) перемешивали и дегазировали аргоном в течение 30 мин. Реакционную смесь нагревали с обратным холодильником до дефлегмации в течение 18 ч. Реакционную смесь охлаждали до КТ, разбавляли водой и экстрагировали этилацетатом (2×100 мл). Объединенный этилацетатный слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив неочищенное соединение, которое очищали с помощью колоночной флеш-хроматографии (SiO2, 100-200 меш; элюирование 30% этилацетатом/петр. эфиром), получив указанное в заголовке соединение в виде розового твердого вещества (0,25 г, 52%): 1H-ЯМР (400 МГц, CDCl3) δ 8,33 (с, 1H), 8,22 (с, 1H), 7,67 (с, 1H), 7,60 (с, 1H), 6,75 (дд, J=17,6, 10,8 Гц, 1H), 5,92 (д, J=17,6, 1H), 5,52 (д, J=10,8 Гц, 1H), 2,21 (с, 3H), ЭРИ-МС m/z 211,35 ([M+H]+); ИК (тонкая пленка) 2236, 1511 см-1.
Следующее соединение было получено в соответствии с методиками, раскрытыми на стадиях 4 и 5 из Примера 96.
1-(2-Фтор-4-винилфенил)-1H-1,2,4-триазол (DI72)
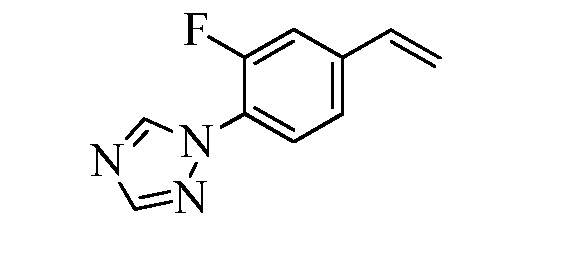
1-(4-Бром-2-фторфенил)-1H-1,2,4-триазол (DI73) выделяли в виде бледно-желтого твердого вещества (3,0 г, 75%): Т.пл. 113-116°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,69 (с, 1H), 8,13 (м, 2H), 7,50 (м, 1H), 7,21 (м, 1H); ЭРИ-МС m/z 241,93 ([М]+). Указанное в заголовке соединение (DI72) выделяли в виде желтого твердого вещества (1,0 г, 71%): Т.пл. 67-70°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,67 (с, 1H), 8,13 (с, 1H), 7,94 (м, 1H), 7,41 (м, 1H), 7,24 (с, 1H), 6,75 (дд, J=17,6, 10,8 Гц, 1H), 5,81 (д, J=17,6 Гц, 1H), 5,37 (д, J=10,8 Гц, 1H); ЭРИ-МС m/z 190,00 ([M+H]+).
Пример 119: Получение 1-(1-(4-винилфенил)-1H-1,2,4-триазол-5-ил)этанона (DI78)
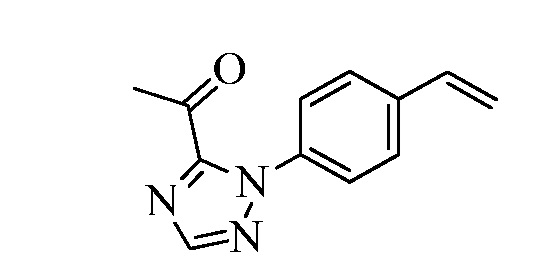
К перемешиваемому раствору 1-(4-винилфенил)-1H-[1,2,4]триазола (1 г, 5,8 ммоль) в 25 мл ТГФ при -78°C добавляли н-BuLi (0,37 г, 5,8 ммоль) и перемешивали в течение 30 мин. К смеси добавляли N-метокси-N-метилацетамид в ТГФ (0,66 г, 6,4 ммоль), и полученную реакционную смесь перемешивали при КТ в течение 16 ч. В реакционную смесь вливали насыщенный водный раствор NH4Cl и экстрагировали EtOAc (3×50 мл). Объединенный слой EtOAc промывали рассолом, сушили над сульфатом натрия и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш, 40% EtOAc в петр. эфире), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (280 мг, 23%): Т.пл. 97-98°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,10 (с, 1H), 7,50 (д, 2H), 7,38 (д, 2H), 6,68 (дд, 1H), 5,85 (д, 1H), 5,38 (д, 1H), 2,75 (с, 3H); ЭРИ-МС m/z 214,14 ([M+H]+).
Пример 120: Получение циклопропил(1-(4-винилфенил)-1H-1,2,4-триазол-5-ил)метанона (DI79)
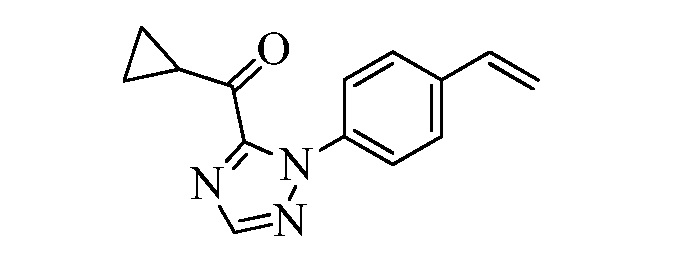
К перемешиваемому раствору 1-(4-винилфенил)-1H-[1,2,4]триазола (1 г, 5,8 ммоль) в 25 мл ТГФ при -78°C добавляли н-BuLi (0,37 г, 5,8 ммоль) и перемешивали в течение 30 мин. К смеси добавляли N-метокси-N-метилциклопропоксид в ТГФ (0,82 г, 6,4 ммоль) и полученную реакционную смесь перемешивали при КТ в течение 16 ч. В реакционную смесь вливали насыщенный водный раствор NH4Cl и экстрагировали EtOAc (3×25 мл). Объединенный слой EtOAc промывали рассолом и сушили над сульфатом натрия и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш, 40% EtOAc в петр. эфире), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (420 мг, 30%): Т.пл. 90-91°C; 1H-ЯМР (400 МГц, CDCl3) δ 8,12 (с, 1H), 7,50 (д, J=7,8 Гц, 2H), 7,38 (д, J=7,8 Гц, 2H), 6,75 (дд, J=16,3, 10,7 Гц, 1H), 5,81 (д, J=16,3 Гц, 1H), 5,35 (д, J=10,7 Гц, 1H), 3,22 (м, 1H), 1,27 (м, 2H), 1,18 (м, 2H); ЭРИ-МС m/z 240,18 ([M+H]+); ИК (тонкая пленка) 2922, 1630 см-1.
Пример 121: Получение 5-(метилтио)-1-(4-винилфенил)-1H-1,2,4-триазола (DI80)
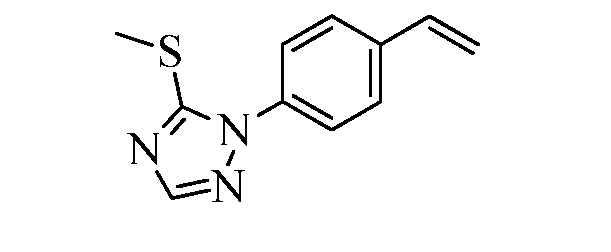
К перемешиваемому раствору 1-(4-винилфенил)-1H-[1,2,4]триазола (1 г, 5,8 ммоль) в 50 мл ТГФ при -78°C добавляли н-BuLi (0,41 г, 6,4 ммоль) и перемешивали в течение 30 мин. К смеси добавляли диметилдисульфид в ТГФ (0,6 г, 6,43 ммоль) и полученную реакционную смесь перемешивали при КТ в течение 16 ч. В реакционную смесь вливали насыщенный водный раствор NH4Cl и экстрагировали EtOAc (3×25 мл). Объединенный слой EtOAc промывали рассолом и сушили над сульфатом натрия и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш, 40% EtOAc в петр. эфире), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (0,6 г, 48%): Т.пл. 68-70°C; 1H-ЯМР (400 МГц, CDCl3) δ 7,96 (с, 1H), 7,05 (м, 4H), 6,75 (дд, J=16,4, 10,7 Гц, 1H), 5,81 (д, J=16,4 Гц, 1H), 5,35 (д, J=10,7 Гц, 1H), 2,73 (с, 3H); ЭРИ-МС m/z 218,09 ([M+H]+).
Пример 122: Получение 5-метил-1-(4-винилфенил)-1H-1,2,4-триазола (DI81)

К перемешиваемому раствору 1-(4-винилфенил)-1H-[1,2,4]триазола (0,5 г, 2,9 ммоль) в 10 мл ТГФ при -78°C добавляли н-BuLi (0,22 г, 3,5 ммоль) и перемешивали в течение 30 мин. К смеси добавляли метилиодид в ТГФ (0,50 г, 3,5 ммоль) и полученную реакционную смесь перемешивали при КТ в течение 16 ч. В реакционную смесь вливали насыщенный водный раствор NH4Cl и экстрагировали EtOAc (3×25 мл). Объединенный слой EtOAc промывали рассолом, сушили над сульфатом натрия и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью флеш-хроматографии (SiO2, 100-200 меш, 40% EtOAc в петр. эфире), получив указанное в заголовке соединение в виде бледно-коричневой жидкости (250 мг, 46%): 1H-ЯМР (400 МГц, CDCl3) δ 7,93 (с, 1H), 7,55 (д, J=9 Гц, 2H), 7,42 (д, J=9 Гц, 2H), 6,76 (дд, J=18, 11 Гц, 1H), 5,83 (д, J=18 Гц, 1H), 5,38 (д, J=11 Гц, 1H), 2,55 (с, 3H); ЭРИ-МС m/z 186,13 ([M+H]+); ИК (тонкая пленка) 1517, 1386, 1182, 847 см-1.
Пример 97: Получение (E)-1-(4-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)фенил)-1H-1,2,4-триазола (DC1)
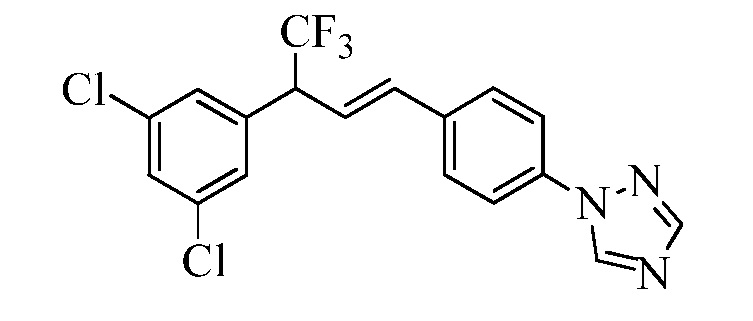
К перемешиваемому раствору 1-(1-бром-2,2,2-трифтор-этил)-3,5-дихлорбензола (2,0 г, 6,51 ммоль) в 1,2-дихлорбензоле (25 мл) добавляли 1-(4-винилфенил)-1H-[1,2,4]триазол (2,22 г, 13,0 ммоль), CuCl (64 мг, 0,65 ммоль) и 2,2-бипиридил (0,2 г, 1,3 ммоль). Полученную реакционную смесь дегазировали аргоном в течение 30 мин, затем перемешивали при 180°C в течение 24 ч. После завершения реакции (ТСХ) реакционную смесь охлаждали до КТ и фильтровали, и фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш; 25-30% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (0,8 г, 32%): Т.пл. 93-97°C; 1H-ЯМР (300 МГц, CDCl3) δ 8,56 (с, 1H), 8,11 (с, 1H), 7,68 (д, J=8,4 Гц, 2H), 7,54 (д, J=8,4 Гц, 2H), 7,38 (т, J=1,8 Гц, 1H), 7,29 (с, 2H), 6,62 (д, J=15,6 Гц, 1H), 6,42 (дд, J=15,6, 8,2 Гц, 1H), 4,15 (м, 1H); ЭРИ-МС m/z 398,05 ([M+H]+).
Соединения DC2-DC37, DC44, DC45, DC47-49, DC50, DC51, DC54, DC58, DC60, DC62 и DC63-DC67 в Таблице 1 были получены в соответствии с методиками, раскрытыми в Примере 97.
Пример 98: Получение (E)-2-(3-нитро-1H-1,2,4-триазол-1-ил)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензонитрила (DC40)
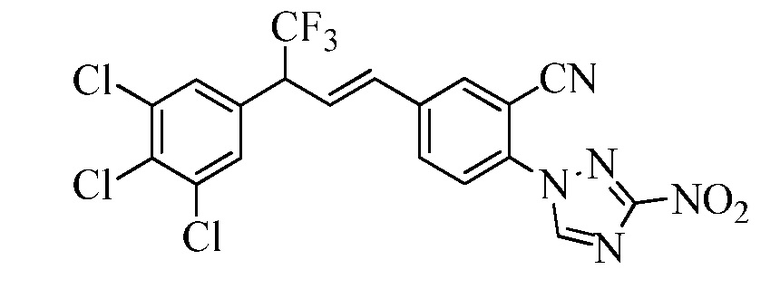
К перемешиваемому раствору 2-(3-нитро-1H-1,2,4-триазол-1-ил)-5-винилбензонитрила (0,9 г, 3,7 ммоль) в 1,2-дихлорбензоле (10 мл) добавляли 5-(1-бром-2,2,2-трифторэтил)-1,2,3-трихлорбензол (2,5 г, 7,5 ммоль), CuCl (73 мг, 0,74 ммоль) и 2,2-бипиридил (0,23 г, 1,49 ммоль) и полученную реакционную смесь дегазировали аргоном в течение 30 мин, а затем перемешивали при 180°C в течение 14 ч. После завершения реакции (ТСХ) реакционную смесь охлаждали до КТ и фильтровали, и фильтрат выпаривали при пониженном давлении. Очистка с помощью флеш-хроматографии (SiO2, 100-200 меш, 25-30% EtOAc в петр. эфире) дала указанное в заголовке соединение в виде грязно-белого твердого вещества (0,9 г, 50%): Т.пл. 70-73°C; 1H-ЯМР (300 МГц, CDCl3) δ 8,86 (с, 1H), 7,88 (м, 3H), 7,44 (с, 2H), 6,67 (д, J=16,0 Гц, 1H), 6,56 (дд, J=16,0, 7,6 Гц, 1H), 4,19 (м, 1H); ЭРИ-МС m/z 436,11 ([М-2H]-).
Пример 99: Получение (E)-2-(3-амино-1H-1,2,4-триазол-1-ил)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензонитрила (DC41)
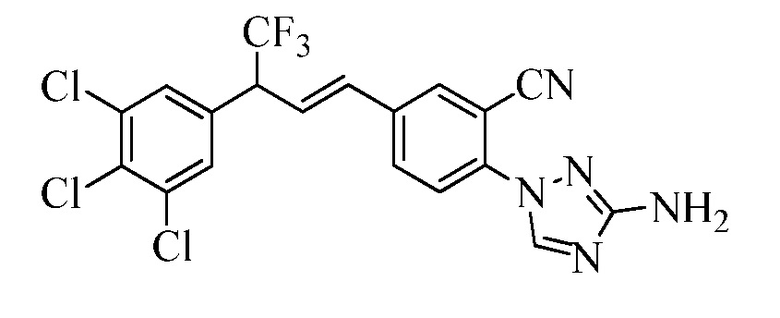
К перемешиваемому раствору (E)-2-(3-нитро-1H-1,2,4-триазол-1-ил)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензо-нитрила (0,6 г, 1,2 ммоль) в MeOH (10 мл) добавляли Zn пыль (0,39 г, 5,98 ммоль) и нас. водн. раствор NH4Cl (5 мл) и полученную реакционную смесь перемешивали при КТ в течение 2 ч. После завершения реакции (ТСХ) реакционную массу выпаривали при пониженном давлении. Реакционную массу разбавляли ДХМ, фильтровали через слой целита и полученный фильтрат выпаривали при пониженном давлении с получением указанного в заголовке соединения в виде твердого вещества (0,5 г, 89%): Т.пл. 72-75°C; 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,72 (с, 1H), 8,26 (с, 1H), 8,01 (д, J=8,4 Гц, 1H), 7,91 (с, 2H), 7,77 (д, J=8,4 Гц, 1H), 6,42 (дд, J=15,6, 9,2 Гц, 1H), 6,83 (д, J=15,6 Гц, 1H), 5,87 (с, 2H), 4,89 (м, 1H); ЭРИ-МС m/z 469,95 ([M-H]-).
Соединение DC38 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 99. Кроме того, соединение DC55 в Таблице 1 было получено из соединения DC54 в соответствии с методиками, раскрытыми в Примере 99, за исключением использования формиата аммония вместо хлорида аммония.
Пример 100: Получение (E)-N-(1-(2-циано-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)-1H-1,2,4-триазол-3-ил)-N-(циклопропанкарбонил)циклопропанкарбоксамида (DC42)
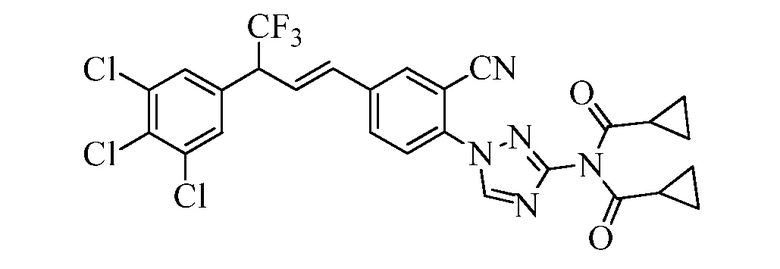
К перемешиваемому раствору (E)-2-(3-амино-1H-1,2,4-триазол-1-ил)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензо-нитрила (0,1 г, 0,21 ммоль) в ДХМ при КТ добавляли циклопропилкарбонилхлорид (0,045 г, 0,42 ммоль) и реакционную смесь перемешивали в течение 2 ч при КТ. Реакционную смесь разбавляли ДХМ, промывали водой и рассолом и сушили над Na2SO4. После выпаривания при пониженном давлении и очистки с помощью препаративной ВЭЖХ получали указанное в заголовке соединение в виде твердого вещества (0,09 г, 79%): Т.пл. 104-107°C; 1H-ЯМР (300 МГц, CDCl3) δ 8,78 (с, 2H), 7,83 (с, 1H), 7,80 (м, 2H), 7,42 (с, 2H), 6,65 (д, J=16,4 Гц, 1H), 6,51 (дд, J=7,6, 8,0 Гц, 1H), 4,17 (м, 1H), 2,16 (м, 2H), 1,25 (м, 4H), 1,00 (м, 4H); ЭРИ-МС m/z 609,98 ([M+H]+); ИК (тонкая пленка) 2234, 1714, 1114, 807 см-1.
Пример 101: Получение (E)-N-(1-(2-циано-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)-1H-1,2,4-триазол-3-ил)циклопропанкарбоксамида (DC43)
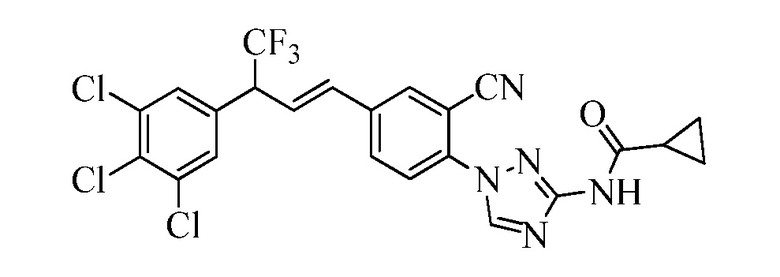
К перемешиваемому раствору (E)-2-(3-амино-1H-1,2,4-триазол-1-ил)-5-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензо-нитрила (0,15 г, 0,31 ммоль) в ДХМ при 0°C добавляли триэтиламин (0,1 г, 1 ммоль) и циклопропилкарбонилхлорид (0,04 г, 0,38 ммоль) и реакционную смесь перемешивали в течение 1 ч при 0°C. Реакционную смесь разбавляли ДХМ, промывали водой и рассолом и сушили над Na2SO4. После выпаривания при пониженном давлении и очистки с помощью колоночной хроматографии (SiO2, 100-200 меш) указанное в заголовке соединение получали в виде твердого вещества (66 мг, 34%): Т.пл. 109-112°C; 1H-ЯМР (300 МГц, ДМСО-d6) δ 10,94 (шир. с, 1H), 8,36 (с, 1H), 8,08 (м, J=8,4 Гц, 1H), 7,91 (с, 2H), 7,84 (д, J=8,4 Гц, 1H), 7,13 (дд, J=15,6, 9,2 Гц, 1H), 6,87 (д, J=15,6 Гц, 1H), 4,92 (м, 1H), 1,99 (шир. с, 1H), 0,82 (с, 4H); ЭРИ-МС m/z 540,04 ([M+H]+); ИК (тонкая пленка) 3233, 2233, 1699, 1114, 807 см-1.
Соединение DC39 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 101.
Пример 102: Получение 1-(4-(1H-1,2,4-триазол-1-ил)фенил)этанона (DI74)
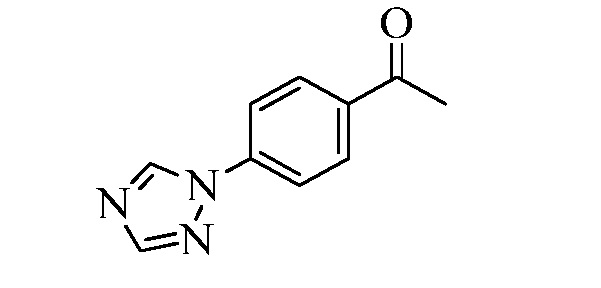
К перемешиваемому раствору 4-бромацетофенона (10 г, 50 ммоль) в ДМФА (100 мл) добавляли 1,2,4-триазол (5 г, 75 ммоль), Cs2CO3 (32,6 г, 100,5 ммоль) и CuI (1,4 г, 10,1 ммоль) и полученную реакционную смесь нагревали с обратным холодильником в течение 48 ч. После завершения реакции (ТСХ) реакционную смесь охлаждали до КТ, разбавляли водой (200 мл) и экстрагировали EtOAc. Объединенный органический слой промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка путем промывки диэтиловым эфиром дала указанное в заголовке соединение в виде твердого вещества (5 г, 96%): 1H-ЯМР (400 МГц, CDCl3) δ 8,71 (с, 1H), 8,16, (с, 1H), 8,13 (д, J=8,6 Гц, 2H), 7,83 (д, J=8,6 Гц, 2H), 2,66 (с, 3H); ЭРИ-МС m/z 186,02 ([M-H]-).
Пример 103: Получение 1-(4-(1H-1,2,4-триазол-1-ил)фенил)-3-(3,5-дихлорфенил)-4,4,4-трифторбутан-1-она (DI75)
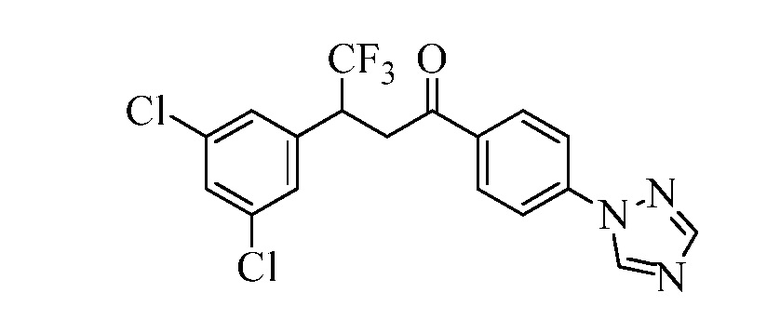
Стадия 1. 1-(4-(1-(Триметилсилилокси)винил)фенил)-1H-1,2,4-триазол (DI76). К перемешиваемому раствору 1-(4-(1H-1,2,4-триазол-1-ил)фенил)этанона (4,5 г, 24,0 ммоль) в ДХМ при 0°C добавляли ТЭА (3,7 г, 36,1 ммоль) и триметилсилил-трифторметансульфонат (8 г, 36 ммоль) и перемешивали полученную реакционную смесь в течение 1 ч. В реакционную смесь вливали смесь нас. водн. раствора гидрокарбоната натрия и эфира. Эфирный слой отделяли, промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение (5,5 г), которое непосредственно использовали в следующей стадии.
Стадия 2. 1-(4-(1H-1,2,4-триазол-1-ил)фенил)-3-(3,5-дихлор-фенил)-4,4,4-трифторбутан-1-он (DI75): Перемешиваемый раствор 1-(4-(1-(триметилсилилокси)винил)фенил)-1H-1,2,4-триазола (6 г, 23 ммоль) и 1-(1-бром-2,2,2-трифтор-этил)-3,5-дихлорбензола (7,1 г, 34,7 ммоль) в 1,2-дихлорбензоле (30 мл) дегазировали аргоном. К этой реакционной смеси добавляли CuCl (0,23 г, 2,31 ммоль) и 2,2-бипиридил (0,73 г, 4,63 ммоль) и полученную реакционную смесь нагревали до 180°C в течение 18 ч. После завершения реакции (ТСХ) реакционную смесь абсорбировали на силикагеле и очищали с помощью колоночной хроматографии (SiO2; 10% EtOAc в петролейном эфире), получив указанное в заголовке соединение в виде твердого вещества (3 г, 31%): 1H-ЯМР (400 МГц, CDCl3) δ 8,67 (с, 1H), 8,15 (с, 1H), 8,10 (д, J=8,3 Гц, 2H), 7,82 (д, J=8,3 Гц, 2H), 7,33 (м, 1H), 7,30 (м, 2H), 4,20 (м, 1H), 3,63 (м, 2H); ЭРИ-МС m/z 412,14 ([M-H]-).
Пример 104: Получение 2-(4-(1H-1,2,4-триазол-1-ил)фенил)-4-(3,5-дихлорфенил)-5,5,5-трифторпентан-2-ола (DI77)
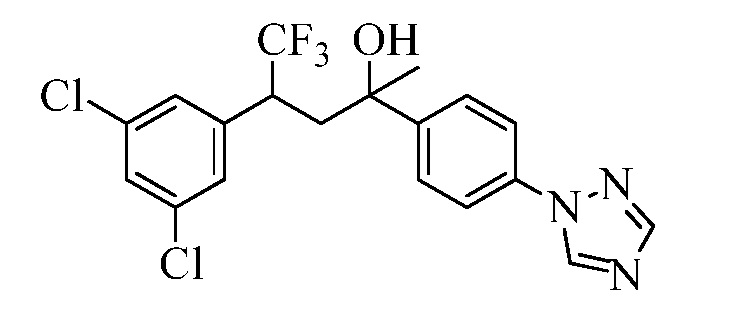
К раствору 1-(4-(1H-1,2,4-триазол-1-ил)фенил)-3-(3,5-дихлорфенил)-4,4,4-трифторбутан-1-она (300 мг, 0,726 ммоль) в ТГФ, охлажденном до 0°C, по каплям добавляли метилмагнийбромид (450 мг, 5 ммоль). Реакцию перемешивали в течение 3 ч при 0°C, затем в реакционную смесь вливали нас. водн. раствор NH4Cl и экстрагировали этилацетатом. Объединенный слой EtOAc промывали водой и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 20-25% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (100 мг, 32%): 1H-ЯМР (400 МГц, CDCl3) δ два диастереоизомера 8,58 (с, 1H, минорный), 8,48 (с, 1H, мажорный), 8,13 (с, 1H, минорный), 8,09 (с, 1H, мажорный), 7,70 (д, J=9,0 Гц, 2H, минорный), 7,53 (д, J=9,0 Гц, 2H, минорный), 7,40 (д, J=9,0 Гц, 2H, мажорный), 7,31 (м, 1H, минорный), 7,27 (д, J=9,0 Гц, 2H, мажорный), 7,20 (м, 2H, минорный), 7,01 (м, 1H, мажорный), 6,75 (м, 2H, мажорный), 350 (м, 1H), 2,50 (м, 2H), 1,56 (с, 3H, мажорный), 1,54 (с, 3H, минорный); ЭРИ-МС m/z 430,05 ([M+H]+).
Пример 105: Получение (E)-1-(4-(4-(3,5-дихлорфенил)-5,5,5-трифторпент-2-ен-2-ил)фенил)-1H-1,2,4-триазола (DC68)

К раствору 2-(4-(1H-1,2,4-триазол-1-ил)фенил)-4-(3,5-дихлорфенил)-5,5,5-трифторпентан-2-ола (100 мг, 0,233 ммоль) в толуоле добавляли каталитическое количество п-толуолсульфоновой кислоты (PTSA) и удаляли воду с помощью азеотропной перегонки в течение 12 ч. Реакционную смесь охлаждали до комнатной температуры и растворяли в этилацетате. Раствор промывали нас. водн. раствором NaHCO3 и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Очистка с помощью колоночной хроматографии (SiO2, 100-200 меш; 20-25% EtOAc в петролейном эфире) дала указанное в заголовке соединение в виде твердого вещества (30 мг, 31%).
Пример 123: Получение (E)-5-(3-(3,5-дихлорфенил)-4,4,4-трифтор-бут-1-ен-1-ил)-2-(1H-1,2,4-триазол-1-ил)бензальдегида (DC52)
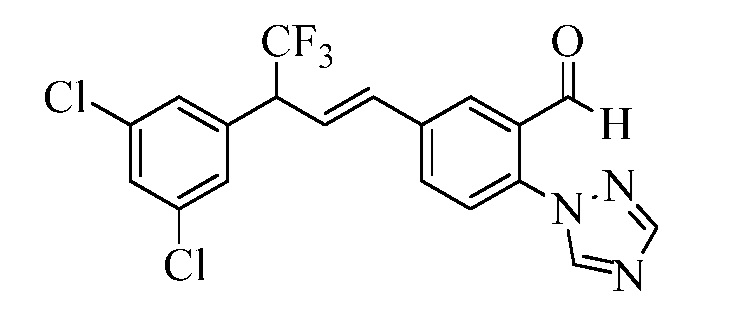
К перемешиваемому раствору (E)-5-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(1H-1,2,4-триазол-1-ил)бензонитрила (0,3 г, 0,71 ммоль) в толуоле (10 мл) при -78°C по каплям добавляли диизобутилалюминийгидрид (DIBAL-H, 1,0М раствор в толуоле; 0,85 мл) и реакционную смесь перемешивали при -78°C в течение 20 мин. В реакционную смесь вливали 1Н раствор HCl, затем водный слой экстрагировали EtOAc (2×). Объединенные органические слои промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной флеш-хроматографии (SiO2; 50% EtOAc/петр. эфир), получив указанное в заголовке соединение в виде желтого масла.
Соединение DC53 в Таблице 1 было получено в соответствии с методиками, раскрытыми в Примере 123.
Пример 124: Получение (E)-5-(3-(3,5-дихлорфенил)-4,4,4-трифтор-бут-1-ен-1-ил)-N-метил-2-(1H-1,2,4-триазол-1-ил)анилин (DC57)
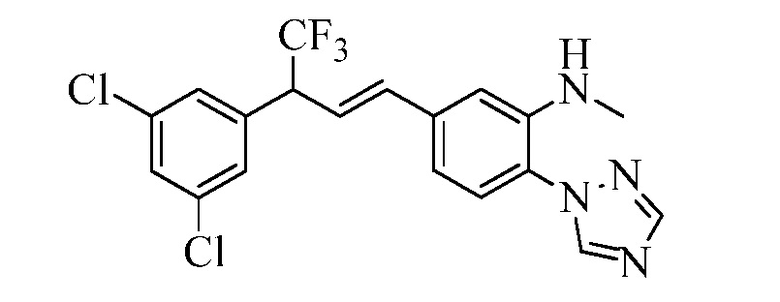
К перемешиваемому раствору (E)-5-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(1H-1,2,4-триазол-1-ил)анилина (0,3 г, 0,7 ммоль) в ДХМ (10 мл) добавляли триэтиламин (0,155 мл, 1,09 ммоль) и метилиодид (0,124 г, 0,873 ммоль). Реакцию перемешивали при КТ в течение 18 ч. Слой ДХМ промывали водой и рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной флеш-хроматографии (SiO2; 50% EtOAc/петр. эфир), получив указанное в заголовке соединение в виде желтого полутвердого вещества (0,07 г, 70%).
Пример 125: Получение (E)-5-(3-(3,5-дихлорфенил)-4,4,4-трифтор-бут-1-ен-1-ил)-2-(1H-1,2,4-триазол-1-ил)бензойной кислоты (DC61)

Раствор (E)-этил-5-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(1H-1,2,4-триазол-1-ил)бензоата (0,2 г, 0,4 ммоль) в 6Н HCl (10 мл) перемешивали при 100°C в течение 18 ч. Реакцию охлаждали до КТ с получением осадка белого твердого вещества. Осадок отфильтровывали с получением указанного в заголовке соединения в виде белого твердого вещества (0,12 г, 60%).
Пример 126: Получение (Z)-5-((E)-3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-N'-гидрокси-2-(1H-1,2,4-триазол-1-ил)бензимидамида (DC59)
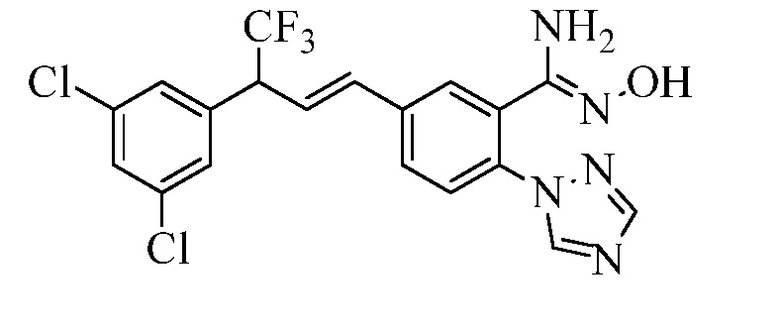
Раствор (E)-5-(3-(3,5-дихлорфенил)-4,4,4-трифторбут-1-ен-1-ил)-2-(1H-1,2,4-триазол-1-ил)бензонитрила (0,3 г, 0,71 ммоль), ацетата натрия (0,087 г, 1,065 ммоль) и хлорида гидроксиламмония (0,072 г, 1,065 ммоль) в смеси 9:1 этанола/воды (10 мл) перемешивали при 70°C в течение 8 ч. Реакцию охлаждали до КТ и отгоняли этанол. Остаток растворяли в воде и экстрагировали EtOAc (2×). Объединенные органические слои промывали рассолом, сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде грязно-белого твердого вещества.
Пример 127: Получение (E)-1-(4-(3-(3,5-дихлорфенил)-4,4,4-трифтор-3-метоксибут-1-ен-1-ил)фенил)-1H-1,2,4-триазола (DC70)
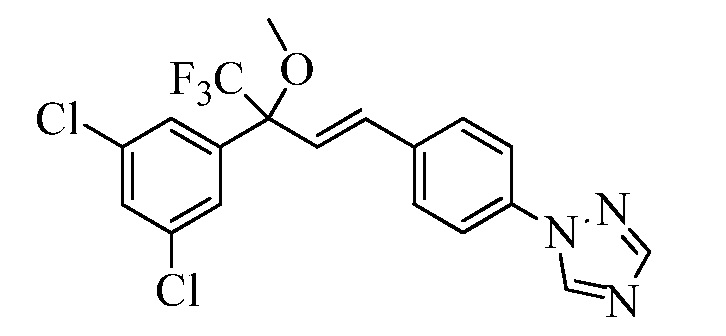
Стадия 1. (E)-3-(4-(1H-1,2,4-Триазол-1-ил)фенил)-1-(3,5-дихлорфенил)проп-2-ен-1-он: К раствору 1-(3,5-дихлорфенил)этано-на (0,5 г, 2,6 ммоль) в этаноле (20 мл) добавляли 4-(1H-1,2,4-триазол-1-ил)бензальдегид (0,46 г, 2,65 ммоль) и реакцию охлаждали до 0°C. Затем добавляли гидроксид натрия (0,22 г, 5,29 ммоль) в воде (10 мл) и реакцию оставляли с перемешиванием на 2 ч при 0°C. Реакцию экстрагировали EtOAc и объединенные органические слои сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение (0,149 г, 17%); ЭРИ-МС m/z 430,05 ([M+H]+) 344,08.
Стадия 2. (E)-4-(4-(1H-1,2,4-Триазол-1-ил)фенил)-2-(3,5-дихлорфенил)-1,1,1-трифторбут-3-ен-2-ол (DC69): К раствору (E)-3-(4-(1H-1,2,4-триазол-1-ил)фенил)-1-(3,5-дихлорфенил)проп-2-ен-1-она (1 г, 3 ммоль) в ТГФ (150 мл) добавляли трифторметил-триметилсилан (0,517 г, 3,644 ммоль) и фторид тетра-н-бутиламмония (TBAF) (1,0 М, 1 мл) при 0°C. Реакцию медленно нагревали до КТ и оставляли с перемешиванием на 2 ч. Затем реакцию охлаждали до 0°C, добавляли 5М раствор HCl и перемешивали реакцию еще 4 ч при КТ. Реакцию экстрагировали ДХМ, объединенные органические слои сушили над Na2SO4 и выпаривали при пониженном давлении. Неочищенное соединение очищали с помощью колоночной флеш-хроматографии (SiO2; 25% EtOAc/смесь гексанов), получив указанное в заголовке соединение в виде грязно-белого твердого вещества (0,3 г, 25%).
Стадия 3. (E)-1-(4-(3-(3,5-Дихлорфенил)-4,4,4-трифтор-3-метоксибут-1-ен-1-ил)фенил)-1H-1,2,4-триазол (DC70): К раствору (E)-4-(4-(1H-1,2,4-триазол-1-ил)фенил)-2-(3,5-дихлорфенил)-1,1,1-трифторбут-3-ен-2-ола (0,15 г, 0,36 ммоль) в ТГФ (5 мл) добавляли NaH (60%, 10 мг, 0,44 ммоль) при 0°C. Реакцию оставляли с перемешиванием при 0°C на 30 минут, затем медленно добавляли метилиодид (61 мг, 0,44 ммоль), нагревали реакцию до КТ и оставляли с перемешиванием на 4 ч. К реакции приливали водн. раствор NH4Cl и экстрагировали ДХМ. Объединенные органические слои сушили над Na2SO4 и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (55 мг, 35%).
Пример 128: Получение (E)-2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-N-(1-(2,2,2-трифторэтилкарбамоил)цикло-пропил)бензамида (F1)

К перемешиваемому раствору (E)-2-хлор-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)бензойной кислоты (300 мг, 0,67 ммоль) и 1-амино-N-(2,2,2-трифторэтил)циклопропанкарбоксамида (148 мг, 0,81 ммоль) в ДХМ/ДМФА (5 мл, 1:1) добавляли гексафторфосфат 2-хлор-1,3-диметилимидазолидиния (CIP) (92 мг, 0,33 ммоль), 1-гидрокси-7-азабензотриазол (HOAt) (48 мг, 0,33 ммоль) и DMAP (5 мол.%) и перемешивали полученную смесь при комнатной температуре (КТ) в течение 4 ч. Реакционную смесь вливали в воду со льдом и экстрагировали EtOAc. Органическую фазу сушили (Na2SO4), фильтровали, выпаривали и остаток очищали с помощью колоночной хроматографии на силикагеле (100-200 меш), используя в качестве элюента 30% EtOAc в петролейном эфире, с получением указанного в заголовке соединения в виде бледно-желтой смолы (300 мг, 75%). Характеристики этой молекулы перечислены в Таблице 2.
Пример 129: Получение (E)-2-бром-N-(1-цианоциклопропил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензамида (F7)
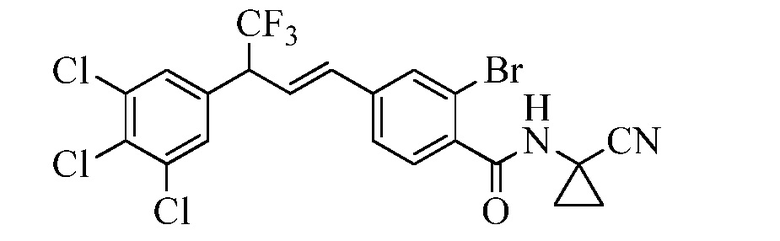
К перемешиваемому раствору (E)-2-бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)бензойной кислоты (100 мг, 0,205 ммоль) в ДХЭ (10,0 мл) при КТ добавляли гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (EDC гидрохлорид) (58,9 мг, 0,307 ммоль), гидрохлорид 1-амино-1-циклопропанкарбо-нитрила (24,3 мг, 0,296 ммоль), DMAP (каталитическое кол-во) и ТЭА (22,79 мг, 0,225 ммоль). Полученную реакционную смесь перемешивали при КТ в течение 18 ч. К реакционной смеси добавляли EtOAc (50 мл) и 0,1Н HCl (10 мл) и разделяли слои. Водный слой экстрагировали EtOAc (1×). Объединенные органические слои промывали водн. раствором NaHCO3 (1×), сушили (MgSO4), фильтровали и выпаривали при пониженном давлении с получением масла. Очистка с помощью флеш-хроматографии (SiO2, 230-400 меш; элюирование 35% EtOAc в смеси гексанов) дала указанное в заголовке соединение в виде белого твердого вещества (13 мг, 11,5%). Характеристики этой молекулы перечислены в Таблице 2.
Пример 130: Получение трет-бутил-(1-((2,2,2-трифторэтил)карбамо-ил)циклопропил)карбамата
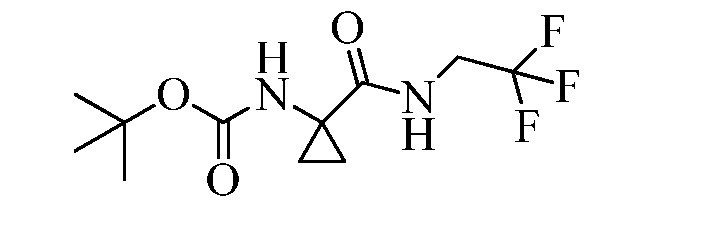
К перемешиваемому раствору 1-((трет-бутоксикарбонил)ами-но)циклопропанкарбоновой кислоты (10,0 г, 49,7 ммоль) в CH2Cl2 (80 мл) добавляли EDC·HCl (13,8 г, 71,8 ммоль) с последующим добавлением 2,2,2-трифторэтиламина (8,21 г, 82,8 ммоль) и 4-(диметиламино)пиридина (7,31 г, 59,8 ммоль). Реакционную смесь перемешивали при температуре окружающей среды в течение 18 ч, собирали в 300 мл EtOAC, затем промывали 10% водн. раствором HCl (3×), 10% водн. K2CO3 (2×) и нас. водн. NaCl (1×). Органическую фазу сушили (MgSO4) и выпаривали в вакууме с получением указанного в заголовке соединения в виде белого твердого вещества (11,8 г, 84%): Т.пл. 166-167°C; 1H-ЯМР (400 МГц, ДМСО-d6) ротамеры δ 8,43 (с, 0,3H), 8,20 (с, 0,7H), 7,41 (с, 0,7H), 7,11 (с, 0,3H), 3,84 (дт, J=9,9, 4,9 Гц, 2H), 1,38 (д, J=11,4 Гц, 9H), 1,24 (кв., J=4,3 Гц, 2H), 0,92 (кв., J=4,3 Гц, 2H); 19F-ЯМР (376 МГц, ДМСО-d6) δ-70,57; 13C-ЯМР (101 МГц, ДМСО-d6) ротамеры δ 172,82, 155,37, 124,64 (кв., J=281 Гц), 78,29, 40,18 (кв., J=34 Гц), 35,43, 34,70, 28,05, 27,84, 17,28, 16,62.
Следующие молекулы были получены в соответствии с методикой, раскрытой в Примере 130:
трет-Бутил-(1-((2,2,2-трифторэтил)карбамоил)циклобутил)карбамат
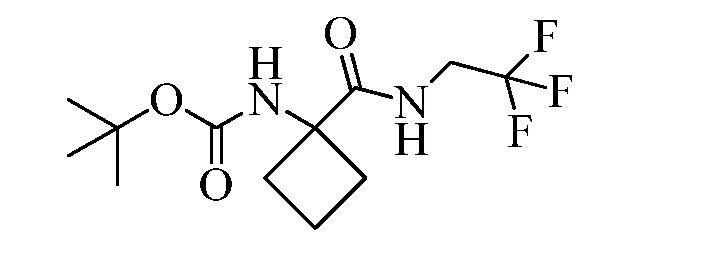
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (1,94, 28%): Т.пл.=185-188°C; 1H-ЯМР (400 МГц, ДМСО-d6) ротамеры δ 8,06 (с, 0,3H), 7,96 (д, J=7,0 Гц, 0,7H), 7,44 (с, 0,7H), 7,11 (с, 0,3H), 3,83 (кв.д, J=9,7, 6,4 Гц, 2H), 2,40 (дтд, J=12,1, 5,9, 2,5 Гц, 2H), 2,03 (ддд, J=12,1, 9,4, 7,1 Гц, 2H), 1,81 (ддд, J=26,1, 14,0, 7,0 Гц, 2H), 1,33 (д, J=34,8 Гц, 9H); 19F-ЯМР (376 МГц, ДМСО-d6) ротамеры δ -70,35, -70,75; ЭРИ-МС m/z 295 ([M-H]-).
трет-Бутил-(1-(этилкарбамоил)циклопропил)карбамат
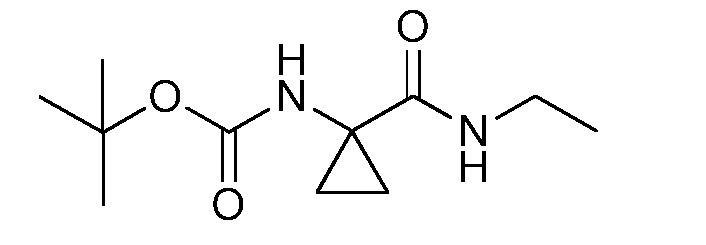
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (3,54 г, 68%): Т.пл.=113-116ºC; 1H-ЯМР (400 МГц, CDCl3) δ 6,44 (шир.с, 1H), 5,09 (шир.с, 1H), 3,43-3,17 (м, 2H), 1,63-1,51 (м, 2H), 1,46 (с, 9H), 1,15 (т, J=7,3 Гц, 3H), 1,00-0,97 (м, 2H); (101 МГц, CDCl3) δ 172,03, 155,89, 80,37, 35,53, 34,65, 28,23, 17,17, 14,85.
трет-Бутил-(1-((2,2-дифторэтил)карбамоил)циклопропил)карбамат
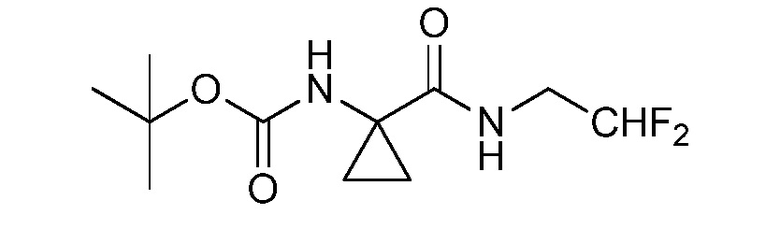
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (290 мг, 70%): Т.пл.=131-135ºC; 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,93 (шир.с, 1H), 7,39 (шир.с, 1H), 6,15-5,74 (м, 1H), 3,52-3,31 (м, 2H), 1,38 (с, 9H), 1,23-1,17 (м, 2H), 0,97-0,87 (м, 2H); ЭРИ-МС m/z 165,1 ([М-Boc]+).
трет-Бутил-(1-((2-фторэтил)карбамоил)циклопропил)карбамат
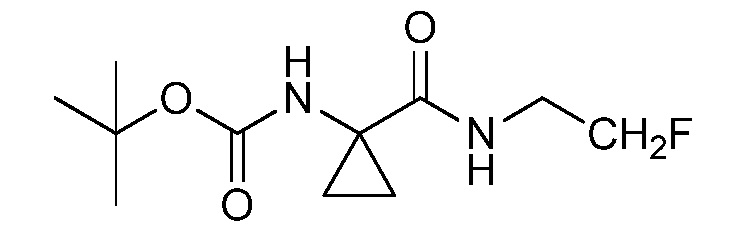
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (250 мг, 62%): Т.пл.=121-125ºC; 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,80 (шир.с, 1H), 7,41 (шир.с, 1H), 4,47 (т, J=5,7 Гц, 1H), 4,34 (т, J=5,4 Гц, 1H), 3,43-3,31 (м, 2H), 1,38 (с, 9H), 1,22-1,18 (м, 2H), 0,87-0,84 (м, 2H); ЭРИ-МС m/z 146,2 ([М-Boc]+).
трет-Бутил-(1-((3,3,3-трифторпропил)карбамоил)циклопропил)карба-мат
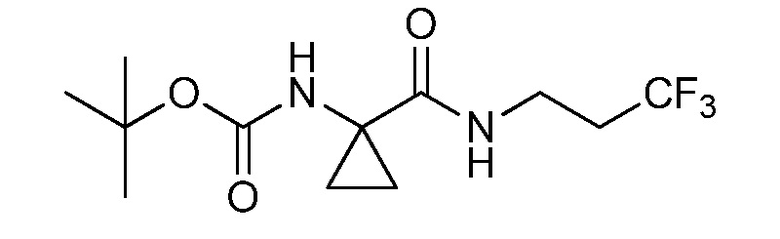
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (550 мг, 58%): Т.пл.=146-148ºC; 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,80 (шир.с, 1H), 7,40 (шир.с, 1H), 3,34-3,27 (м, 2H), 2,43-2,32 (м, 2H), 1,38 (с, 9H), 1,22-1,18 (м, 2H), 0,87-0,83 (м, 2H); ЭРИ-МС m/z 197,1 ([M-Boc+H]+).
Пример 131: Получение гидрохлорида трет-бутил-1-амино-N-(2,2,2-трифторэтил)циклопропанкарбоксамида
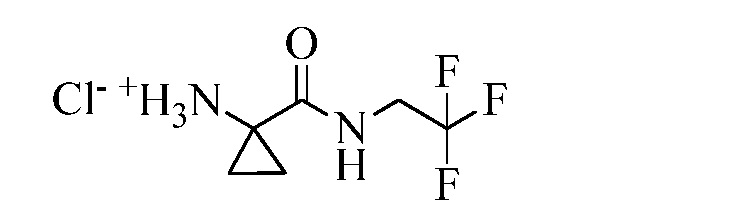
К трет-бутил-(1-((2,2,2-трифторэтил)карбамоил)цикло-пропил)карбамату (3,2 г, 11 ммоль) в CH2Cl2 (20 мл) добавляли 4М HCl в диоксане (20 мл). Раствор перемешивали в течение 18 ч при температуре окружающей среды. Реакционную смесь выпаривали в вакууме и остаток помещали в вакуумный сушильный шкаф на 60°C (24 ч) с получением указанного в заголовке соединения в виде грязно-белого твердого вещества (2,3 г, 93%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 8,77 (шир.с, 3H), 8,50 (т, J=6,3 Гц, 1H), 3,90 (кв.д, J=9,7, 6,1 Гц, 2H), 1,52-1,15 (м, 4H); 19F-ЯМР (376 МГц, ДМСО-d6) δ-70,54; 13C-ЯМР (101 МГц, ДМСО-d6) δ 175,33, 132,46 (кв., J=280,8 Гц), 45,13 (кв., J=34,34 Гц), 40,06, 17,57.
Следующие молекулы были получены в соответствии с методикой, раскрытой в Примере 131:
Хлорид 1-(этилкарбамоил)циклопропанаминия
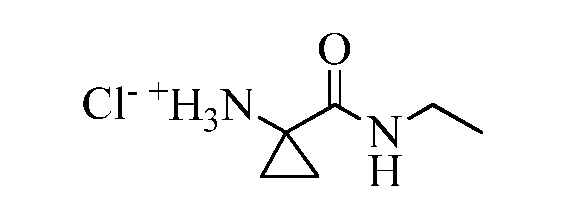
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (2,27 г, 98%): Т.пл.=165-196ºC; 1H-ЯМР (400 МГц, CDCl3) δ 8,69 (с, 3H), 7,89 (т, J=5,4 Гц, 1H), 3,10 (дд, J=7,4, 5,6 Гц, 2H), 1,43-1,32 (м, 2H), 1,31-1,23 (м, 2H), 1,01 (т, J=7,2 Гц, 3H); (101 МГц, ДМСО-d6) δ 168,41, 34,71, 33,93, 14,47, 11,89; ИК (тонкая пленка) 3313, 2983, 1678, 1537, 1251, 1159 см-1.
Хлорид 1-((2,2-дифторэтил)карбамоил)циклопропанаминия

Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (200 мг, 99%): Т.пл.=221-225ºC; 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,40 (шир.с, 3H), 8,12 (шир.с, 1H), 6,20-5,81 (м, 1H), 3,55-3,45 (м, 2H), 1,44-1,36 (м, 2H), 1,31-1,23 (м, 2H); ЭРИ-МС m/z 165,1 ([M+H]+).
Хлорид 1-((2-фторэтил)карбамоил)циклопропанаминия
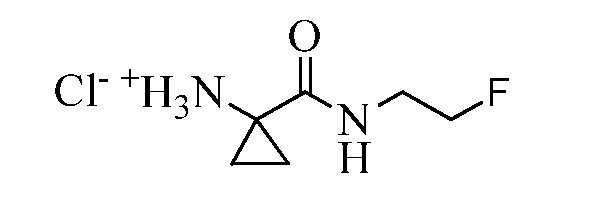
Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (180 мг, 89%): Т.пл.=157-161ºC; 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,62 (шир.с, 3H), 8,00 (шир.с, 1H), 4,51 (т, J=5,1 Гц, 1H), 4,35 (т, J=4,5 Гц, 1H), 3,35-3,32 (м, 2H), 1,41-1,37 (м, 2H), 1,29-1,25 (м, 2H); ЭРИ-МС m/z 147,1 ([M+H]+).
Хлорид 1-((3,3,3-трифторпропил)карбамоил)циклопропанаминия

Молекулу, указанную в заголовке, выделяли в виде белого твердого вещества (250 мг, 80%): Т.пл.=156-158ºC; 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,58 (шир.с, 3H), 7,99 (шир.с, 1H), 3,36-3,29 (м, 2H), 2,51-2,38 (м, 2H), 1,39-1,35 (м, 2H), 1,31-1,26 (м, 2H); ЭРИ-МС m/z 197,2 ([M+H]+).
Пример 132: Получение 2,2,2-трифторацетата 1-((2,2,2-трифтор-этил)карбамоил)циклобутанаминия
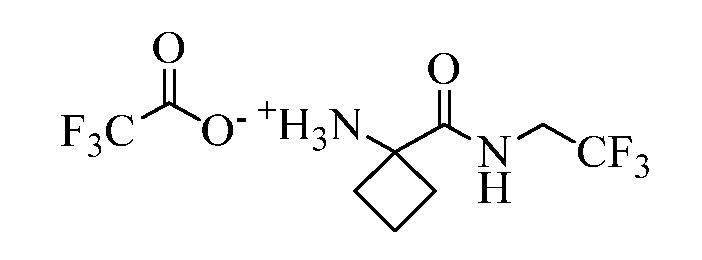
К перемешиваемому раствору трет-бутил-1-(2,2,2-трифторэтилкарбамоил)циклобутилкарбамата (500 мг, 1,68 ммоль) в CH2Cl2 (10 мл) по каплям добавляли трифторуксусную кислоту (ТФУ, 1,0 мл) и перемешивали реакционную смесь в течение ночи. Летучие вещества отгоняли, а остаток растирали с пентаном, получив указанное в заголовке соединение в виде бесцветной смолы, которую использовали в следующей стадии без дополнительной очистки (400 мг, 77%): 1H-ЯМР (300 МГц, ДМСО-d6) δ 9,14 (т, J=6,0 Гц, 1H), 8,52 (шир.с, 2H), 4,08-3,96 (м, 2H), 2,63-2,55 (м, 2H), 2,27-2,14 (м, 2H), 2,08-2,00 (м, 2H); ЭРИ-МС m/z 196,9 ([M+H]+); ИК (тонкая пленка) 3364, 2949, 1680, 1033 см-1.
Пример 133: Получение (E)-4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-енил)-N-(1-(2,2,2- трифторэтилкарбамотиоил)цикло-пропил)-2-(трифторметил)бензамида (F6)
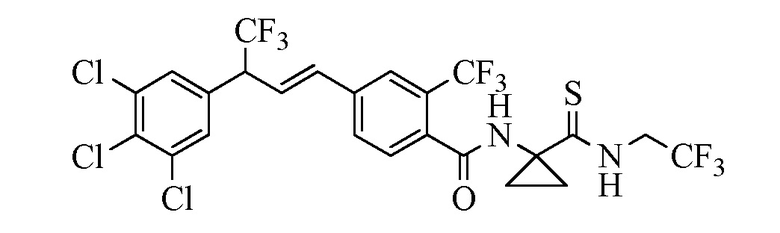
К перемешиваемому раствору (E)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-енил)-N-(1-(2,2,2-трифторэтилкарбамоил)цикло-пропил)-2-(трифторметил)бензамида (200 мг, 0,31 ммоль) в CH2Cl2 (20 мл) добавляли P4S10 (34 мг, 0,155 ммоль) и гексаметилдисилоксан (HMDO, 0,1 мл, 0,517 ммоль) и реакционную смесь нагревали с обратным холодильником в течение 4 ч. Реакционную смесь охлаждали до комнатной температуры и добавляли еще одну порцию P4S10 (34 мг, 0,155 ммоль) и HMDO (0,1 мл, 0,517 ммоль), и нагревали реакционную смесь с обратным холодильником в течение 16 ч. Реакционную смесь выпаривали при пониженном давлении, а остаток очищали с помощью флеш-хроматографии на силикагеле (100-200 меш), используя в качестве элюента 10% EtOAc в гексане, с получением указанных в заголовке соединений в виде желтой смолы (37 мг, 18%). Характеристики этой молекулы перечислены в Таблице 2.
Пример 134: Выделение (R,E)-4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)-N-(1-((2,2,2-трифторэтил)карбамоил)цикло-пропил)-2-(трифторметил)бензамида (F8A)
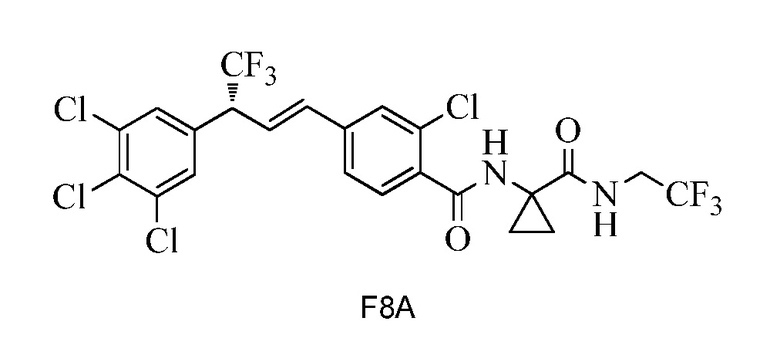
и (S,E)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-N-(1-((2,2,2-трифторэтил)карбамоил)циклопропил)-2-(трифторме-тил)бензамида (F8B)
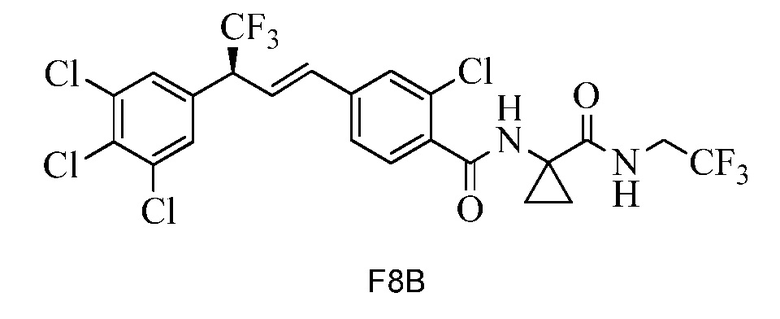
Энантиомерную пару F8, полученную как в Примере 28, разделяли с помощью хиральной ВЭЖХ, используя 5 μм колонку Chiralpak® IA (4,6×250 мм), при использовании 0,1% ТФУ в гексане и изопропаноле в качестве подвижной фазы (изократическая смесь 70:30) с объемной скоростью 1,0 мл/мин при температуре окружающей среды. Энантиомер F8A (изомер 1) собирали при времени удержания 10,62 мин. Энантиомер F8B (изомер 2) собирали при 12,28 мин. Характеристики этих молекул перечислены в Таблице 2A.
Пример 135: Получение (E)-5-(4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)-2-(трифторметил)фенил)-6-окса-4-азаспиро[2.4]гепт-4-ен-7-она
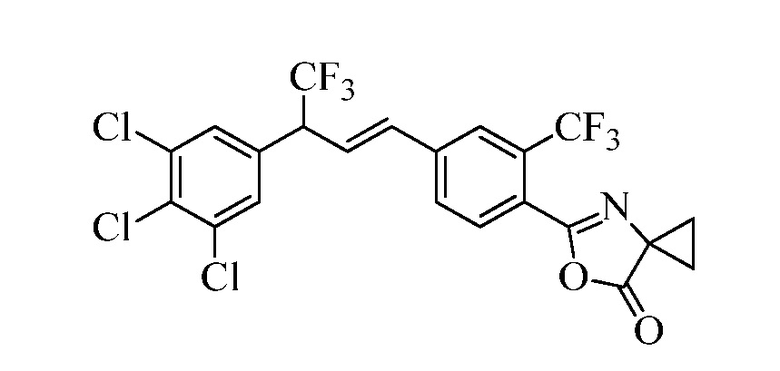
Стадия 1. (E)-1-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензамидо)циклопропанкарбоновая кислота: В круглодонную (rb) колбу объемом 250 мл, снабженную магнитной мешалкой, термодатчиком и обратным холодильником, вносили (E)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензойную кислоту (5,3 г, 11,10 ммоль) и дихлорэтан (ДХЭ) (40 мл). Добавляли чистый тионилхлорид (1,620 мл, 22,19 ммоль) одной порцией и полученную реакционную смесь нагревали при кипячении с обратным холодильником в течение 2,5 ч. После этого реакционной смеси позволяли охладиться и затем выпаривали с получением неочищенного хлорангидрида, который использовали без дополнительной очистки. Промежуточный хлорангидрид собирали в безводном ТГФ (56 мл) и переносили в колбу объемом 250 мл, снабженную магнитной мешалкой, термодатчиком и обратным холодильником. При перемешивании добавляли додецилтриметил-аммонийбромид (0,03 г, 0,111 ммоль), карбонат натрия (0,932 г, 11,10 ммоль) и 1-аминоциклопропанкарбоновую кислоту (1,6 г, 12,0 ммоль) в указанном порядке и оставляли с перемешиванием при дефлегмации на ночь. Реакции позволяли охладиться и белый твердый остаток отфильтровывали с помощью вакуумной фильтрации. Фильтрат выпаривали, получив указанное в заголовке соединение в виде светло-коричневого твердого вещества (4,8 г, 77%). Этот материал использовали без дополнительной очистки.
Стадия 2. (E)-5-(4-(4,4,4-Трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)фенил)-6-окса-4-азаспиро[2.4]гепт-4-ен-7-он: В rb колбу объемом 500 мл, снабженную магнитной мешалкой и термодатчиком, вносили (E)-1-(4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензами-до)циклопропанкарбоновую кислоту (9,2 г, 16,41 ммоль), дихлорметан (ДХМ) (30 мл) и охлаждали в ледяной бане. При перемешивании добавляли EDC·HCl (3,15 г, 16,4 ммоль) одной порцией. Через 5 минут ледяную баню убирали, позволяли реакционной смеси нагреться до комнатной температуры и перемешивали в течение 2 ч. Реакционную смесь разбавляли ДХМ (100 мл), промывали рассолом (1×100 мл), сушили над сульфатом натрия и выпаривали. Неочищенный материал очищали на установке ISCO Rf (хроматография среднего давления) при использовании колонки нормальной фазы с 330 г силикагеля и элюции в градиенте 0-30% EtOAc/гексан с получением указанного в заголовке соединения (6,5 г, 73%): 1H-ЯМР (400 МГц, CDCl3) δ 7,91 (д, J=8,1 Гц, 1H), 7,80 (дд, J=1,8, 0,8 Гц, 1H), 7,67 (дд, J=8,2, 1,8 Гц, 1H), 7,42 (с, 2H), 6,66 (д, J=15,9 Гц, 1H), 6,51 (дд, J=15,9, 7,8 Гц, 1H), 4,15 (п, J=8,7 Гц, 1H), 1,99-1,91 (м, 2H), 1,89-1,79 (м, 2H); 19F-ЯМР (376 МГц, CDCl3) δ-59,47,-68,51; ЭРИ-МС m/z 544,2 ([M+H]+).
Следующее соединение было получено в соответствии с методиками, раскрытыми в Примере 135.
(E)-5-(2-Бром-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)фенил)-6-окса-4-азаспиро[2.4]гепт-4-ен-7-он
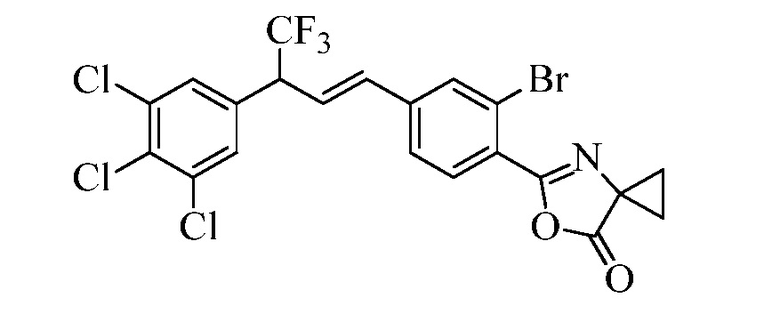
Выделенное количество (9 г, 45%): 1H-ЯМР (300 МГц, CDCl3) δ 7,82 (д, J=8,4 Гц, 1H), 7,73 (д, J=1,8 Гц, 1H), 7,46-7,40 (м, 3H), 6,56 (д, J=16,2 Гц, 1H), 6,44 (дд, J=16,2, 7,2 Гц, 1H), 4,20-4,05 (м, 1H), 2,00-1,94 (м, 2H), 1,87-1,80 (м, 2H); 19F-ЯМР (376 МГц, CDCl3) δ -68,56; ЭРИ-МС m/z 549,7 ([M-H]-).
Пример 136: Общие методики реакции азлактона с аминами
Метод A. Во флакон на 5 мл вносили азлактон, полученный в Примере 135 (0,145 ммоль), и ДХМ (2 мл). Добавляли амин (0,160-0,189 ммоль) и реакционную смесь перемешивали при КТ до окончания реакции. Реакционную смесь разбавляли ДХМ, промывали 0,1Н HCl (1×), водн. NaHCO3 (1×), сушили над Na2SO4 и выпаривали, получив продукт в виде желтой или белой пены. В случае необходимости неочищенный продукт очищали с помощью хроматографии на силикагеле.
Метод B. Во флакон на 5 мл вносили азлактон, полученный в Примере 135 (0,145 ммоль), и EtOAc (2 мл). Добавляли амин (0,160-0,189 ммоль) и реакционную смесь перемешивали при 60-75°C до окончания реакции. Реакционную смесь разбавляли EtOAc, промывали 0,1Н HCl (1×), водн. NaHCO3 (1×), сушили над Na2SO4 и выпаривали, получив продукт в виде желтой или белой пены. В случае необходимости неочищенный продукт очищали с помощью хроматографии на силикагеле.
Метод C. Во флакон на 5 мл вносили азлактон, полученный в Примере 135 (0,145 ммоль), HOAc (2 капли) и EtOAc (2 мл). Добавляли амин (0,160-0,189 ммоль) и реакционную смесь перемешивали при 65-75°C до окончания реакции. Реакционную смесь разбавляли EtOAc, промывали водн. раствором NaHCO3 (1×), сушили над Na2SO4 и выпаривали, получив продукт в виде желтой или белой пены. В случае необходимости неочищенный продукт очищали с помощью хроматографии на силикагеле.
Метод D. Во флакон на 5 мл вносили азлактон, полученный в Примере 135 (0,145 ммоль), HOAc (2 капли) и толуол (2 мл). Добавляли амин (0,160-0,189 ммоль) и реакционную смесь перемешивали при кипячении с обратным холодильником до окончания реакции. Реакционную смесь разбавляли EtOAc, промывали водн. раствором NaHCO3 (1×), сушили над Na2SO4 и выпаривали досуха. Неочищенный продукт очищали с помощью хроматографии на силикагеле.
Метод E. Во флакон на 5 мл вносили азлактон, полученный в Примере 135 (0,145 ммоль), и ТГФ (2 мл). Последовательно добавляли амин в виде HCl соли (0,218-0,290 ммоль) и ТЭА (0,232-0,305 ммоль). Полученную реакционную смесь перемешивали при 25-65°C до окончания реакции. Реакционную смесь разбавляли эфиром, промывали 0,1Н HCl (1×), водн. NaHCO3 (1×), сушили над Na2SO4 и выпаривали, получив продукт в виде желтой или белой пены. В случае необходимости неочищенный продукт очищали с помощью хроматографии на силикагеле.
Соединения FA15, FA16, FA17, FA18, FA19, FA20, FA21, FA22, FA23, FA24, FA25, FA26, FA27, FA28, FA29, FA30, FA31, FA32, FA33, FA34, FA35, FA36, FA37, FA38, FA39, FA40, FA41, FA42, FA43, FA44, FA45, FA46, FA47 и FA48 в Таблице 1C были получены в соответствии с методиками, раскрытыми в Примере 136.
Пример 137: Получение (E)-N-(1-(метокси(2,2,2-трифтор-этил)карбамоил)циклопропил)-4-(4,4,4-трифтор-3-(3,4,5-трихлор-фенил)бут-1-ен-1-ил)-2-(трифторметил)бензамида (FA49)

Стадия 1. трет-Бутил-(1-(метоксикарбамоил)циклопропил)карбамат: 1-((трет-Бутоксикарбонил)амино)циклопропанкарбоновую кислоту (2,00 г, 9,94 ммоль), гидрохлорид метоксиламина (1,09 г, 13,02 ммоль), EDC·HCl (2,50 г, 13,02 ммоль), HOBT (1,99 г, 13,02 ммоль) и N-метилморфолин (2,61 г, 25,8 ммоль) растворяли в безводном ДМФА (20,0 мл) и полученную реакционную смесь перемешивали при КТ в течение 5 дней. Реакционную смесь выпаривали досуха и остаток собирали в ДХМ и промывали насыщенным водным раствором NaHCO3. Органический слой сушили (MgSO4), фильтровали и выпаривали досуха. Остаток хроматографировали на колонке с силикагелем, используя в качестве элюента 70% EtOAc/смесь гексанов, с получением указанного в заголовке соединения (0,82 г, 36%): 1H-ЯМР (400 МГц, ДМСО-d6) δ 11,01 (с, 1H), 7,23 (с, 1H), 3,53 (с, 3H), 1,38 (с, 9H), 1,20 (кв., J=4,3 Гц, 2H), 0,85 (кв., J=4,3 Гц, 2H). Этот материал использовали без дополнительной очистки.
Стадия 2. Гидрохлорид 1-амино-N-метокси-N-(2,2,2-трифтор-этил)циклопропанкарбоксамида: В сухую трехгорлую круглодонную колбу объемом 50 мл вносили трет-бутил-(1-(метоксикарбамо-ил)циклопропил)карбамат (0,82 г, 3,56 ммоль) и 20 мл сухого ДМФА. Реакционную смесь охлаждали в ледяной бане и добавляли 60% NaH (0,16 г, 3,92 ммоль) одной порцией. Реакционную смесь перемешивали при КТ в течение 1,5 ч, после чего по каплям добавляли чистый 2,2,2-трифторэтил-трифторметансульфонат (0,87 г, 3,74 ммоль) и полученную реакционную смесь перемешивали при КТ в течение 18 ч. Реакционную смесь добавляли в H2O и экстрагировали 3× эфиром. Органический слой промывали рассолом, сушили над MgSO4, фильтровали и выпаривали, получив 0,92 г неочищенного продукта в виде белого твердого вещества. Этот материал собирали в 5 мл ДХМ и охлаждали в ледяной бане. Добавляли 2M HCl в эфире (4 мл) и реакционной смеси позволяли нагреться до КТ и перемешивали в течение 18 ч. Реакционную смесь выпаривали с получением твердого вещества. Этот материал несколько раз промывали 10% эфиром/гекс., получив 0,70 г указанного в заголовке соединения. Этот материал использовали далее без дополнительной очистки.
Стадия 3. (E)-N-(1-(Метокси(2,2,2-трифторэтил)карбамо-ил)циклопропил)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензамид: В rb колбу на 25 мл вносили (E)-4-(4,4,4-трифтор-3-(3,4,5-трихлорфенил)бут-1-ен-1-ил)-2-(трифторметил)бензойную кислоту (150 мг, 0,31 ммоль) и ДХЭ (5 мл). Добавляли чистый тионилхлорид (41,1 мг, 0,35 ммоль) одной порцией и полученную реакционную смесь нагревали при дефлегмации в течение 1,5 ч. После этого реакционной смеси позволяли охладиться и выпаривали с получением коричневого масла, которое использовали без дополнительной очистки. Неочищенный хлорангидрид собирали в безводном ДХМ (2 мл) и добавляли по каплям к холодному раствору, содержащему неочищенный гидрохлорид 1-амино-N-метокси-N-(2,2,2-трифторэтил)циклопропанкарбоксамида (78 мг, 0,31 ммоль), ТЭА (66,7 мг, 0,66 ммоль) и ДХМ (10 мл). Реакционную смесь перемешивали при КТ в течение 18 ч. Реакционную смесь разбавляли ДХМ и промывали 0,1Н HCl, водным раствором NaHCO3, сушили над MgSO4, фильтровали и выпаривали с получением масла. Остаток хроматографировали на колонке с силикагелем, используя в качестве элюента 10% EtOAc/гекс., получив указанное в заголовке соединение (17 мг, 8.%): 1H-ЯМР (400 МГц, CDCl3) δ 7,66 (дд, J=14,1, 1,6 Гц, 1H), 7,59 (дд, J=8,0, 1,8 Гц, 1H), 7,53 (д, J=8,0 Гц, 1H), 7,41 (с, 2H), 6,62 (д, J=15,9 Гц, 1H), 6,53 (с, 1H), 6,44 (м, 1H), 4,29 (кв., J=8,5 Гц, 2H), 4,12 (м, 1H), 3,78 (с, 3H), 1,62 (м, 2H), 1,29 (м, 2H); 19F-ЯМР (376 МГц, CDCl3) δ -58,81, -68,59, -69,22; ЭРИ-МС m/z 671,3 ([M-H]-).
Пример 138: Получение 1-(3,5-дифтор-4-метоксифенил)-2,2,2-трифторэтанона
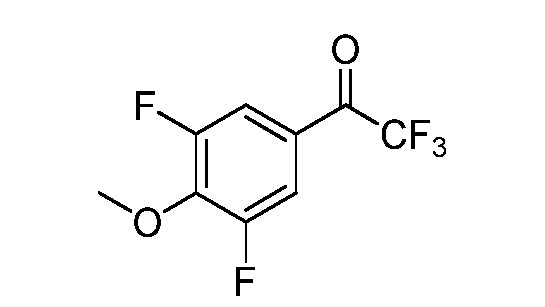
Комплекс изопропилмагнийхлорида и хлорида лития (22,0 мл, 28,02 ммоль) по каплям добавляли к перемешиваемому раствору 5-бром-1,3-дифтор-2-метоксибензола (5,0 г, 22,42 ммоль) при -5°C в ТГФ (100 мл) и реакционную смесь перемешивали при той же температуре в течение на 30 мин. По каплям добавляли метил-трифторацетат (3,67 г, 28,69 ммоль) и реакционную смесь перемешивали при температуре окружающей среды в течение 2 ч. Добавляли 2Н раствор HCl (200 мл) для остановки реакции, после чего смесь экстрагировали диэтиловым эфиром. Объединенные органические слои промывали рассолом, сушили (Na2SO4), фильтровали и выпаривали, получив указанное в заголовке соединение (5,4 г, неочищенное) в виде желтой жидкости. Материал использовали в следующей стадии без дополнительной очистки. 1H-ЯМР (400 МГц, CDCl3) δ 7,68-7,60 (м, 2H) 4,19 (с, 3H); ЭРИ-МС m/z 240,1 ([М]+).
Следующая молекула была получена в соответствии с методиками, раскрытыми в Примере 138:
2,6-Дифтор-4-(2,2,2-трифторацетил)бензонитрил
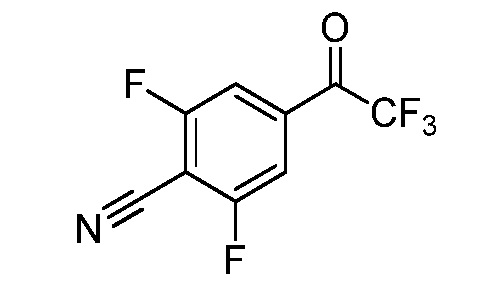
1H-ЯМР (400 МГц, CDCl3) δ 7,45 (д, J=8,4 Гц, 1H), 7,37 (д, J=8,4 Гц, 1H); ЭИ-МС m/z 235,1 ([М]+).
Пример 139: Получение 1-(3,4-дихлорфенил)-2,2-дифторпропан-1-она
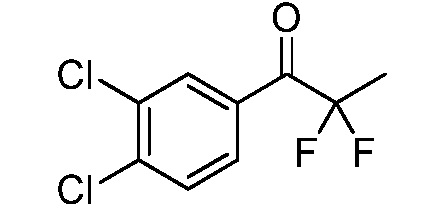
К перемешиваемому магнитной мешалкой раствору 4-бром-1,2-дихлорбензола (5,64 г, 24,98 ммоль) в сухом Et2O (109 мл) добавляли н-BuLi (10,86 мл, 24,98 ммоль) через капельную воронку под атмосферой азота. Реакционную смесь перемешивали при -78°C в течение 30 минут, по каплям добавляли раствор этил-2,2-дифторпропаноата (3,0 г, 21,7 ммоль) в Et2O (10 мл) в течение 15 мин и оставляли с перемешиванием в течение 1 ч. Затем реакцию осторожно останавливали 1Н HCl (4 мл) и позволяли нагреться до 23°C. Раствор разбавляли Et2O и промывали водой. Объединенные органические слои сушили над Na2SO4, выпаривали при пониженном давлении и полученный материал очищали с помощью колоночной флеш-хроматографии, используя в качестве элюента 100% смесь гексанов - 5% ацетон/95% смеси гексанов. Целевые фракции выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде бесцветного масла (3,89 г, 71%): 1H-ЯМР (400 МГц, CDCl3) δ 8,21-8,18 (м, 1H), 7,99-7,93 (м, 1H), 7,59 (дд, J=8,4, 4,2 Гц, 1H), 1,89 (т, J=19,6 Гц, 3H); 19F-ЯМР (376 МГц, CDCl3) δ -92,08, -93,21 (m); EISMS m/z 240 ([M-H]+).
Пример 140: Получение 3,5-дибром-4-хлорбензальдегида
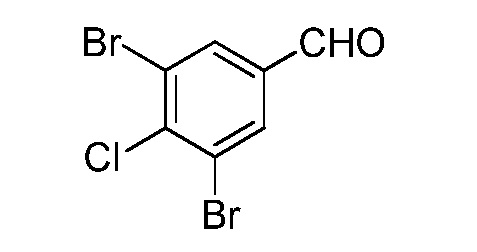
Стадия 1. Метил 4-амино-3,5-дибромбензоат: Конц. H2SO4 (1,35 мл, 25,48 ммоль) по каплям добавляли к перемешиваемому раствору 4-амино-3,5-дибромбензойной кислоты (5,0 г, 16,99 ммоль) в MeOH (50 мл) при температуре окружающей среды и затем реакционную смесь перемешивали при 80°C в течение 8 ч. Реакционную смесь доводили до температуры окружающей среды, летучие вещества выпаривали и к остатку добавляли воду со льдом, после чего смесь экстрагировали EtOAc. Органический слой промывали водным раствором NaHCO3, затем рассолом и водой. После этого раствор сушили (Na2SO4), фильтровали и выпаривали, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (5,0 г, 95%): 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,91 (с, 2H), 6,20 (шир.с, 2H), 3,78 (с, 3H); ЭРИ-МС m/z 307,0 ([М]+); ИК (тонкая пленка) 3312, 2953, 1726, 595 см-1.
Стадия 2. Метил-3,5-дибром-4-хлорбензоат: CuCl2 (2,82 г, 21,0 ммоль) в MeCN (30 мл) перемешивали при 80°C в течение 30 мин. К этой смеси по каплям добавляли трет-бутилнитрит (2,7 мл, 23 ммоль) при той же температуре и смесь перемешивали еще в течение 10 мин. К реакционной смеси по каплям добавляли метил-4-амино-3,5-дибромбензоат (5,0 г, 16 ммоль) в MeCN (30 мл) и затем перемешивали при 80°C в течение 30 мин. Реакционную смесь доводили до температуры окружающей среды, к реакционной смеси добавляли водный раствор аммиака (20 мл) и экстрагировали петролейным эфиром. Органический слой промывали рассолом, затем водой, сушили (Na2SO4), фильтровали и выпаривали, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (4,5 г, 84%). 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,21 (с, 2H), 3,94 (с, 3H); ЭРИ-МС m/z 326 ([М]+); ИК (тонкая пленка) 1732, 746 см-1.
Стадия 3. (3,5-Дибром-4-хлорфенил)метанол: NaBH4 (1,53 г, 40,65 ммоль) порциями добавляли к перемешиваемому раствору метил-3,5-дибром-4-хлорбензоата (4,45 г, 13,6 ммоль) в MeOH (50 мл) при 0°C. Реакционную смесь затем перемешивали при температуре окружающей среды в течение 8 ч. Летучие вещества выпаривали, остаток разбавляли CH2Cl2 и промывали рассолом, затем водой. Органический слой сушили (Na2SO4), фильтровали и выпаривали, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (3,3 г, 80%): 1H-ЯМР (300 МГц, ДМСО-d6) δ 7,71 (с, 2H), 5,49 (шир.с, 1H), 4,48 (д, J=4,5 Гц, 2H); ЭРИ-МС m/z 297,9 ([М]+); ИК (тонкая пленка) 3460, 747, 534 см-1.
Стадия 4. 3,5-Дибром-4-хлорбензальдегид: Хлорхромат пиридиния (PCC, 3,44 г, 15,9 ммоль) добавляли одной порцией к перемешиваемому раствору (3,5-дибром-4-хлорфенил)метанола (3,2 г, 11,0 ммоль) в CHCl3 (40 мл) при температуре окружающей среды и реакционную смесь оставляли с перемешиванием на ночь. Реакционную смесь фильтровали через Celite®, слой Celite® промывали CHCl3 и выпаривали фильтрат, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (2,0 г, 62%): Т.пл. 110-113°C; 1H-ЯМР (300 МГц, ДМСО-d6) δ 9,93 (с, 1H), 8,27 (с, 2H); ЭРИ-МС m/z 297,0 ([М]+).
Пример 141: Получение 4-бром-3,5-дихлорбензальдегида
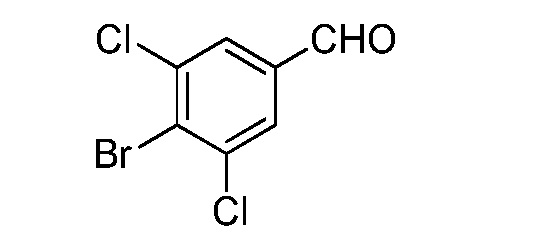
Стадия 1. Метил-4-амино-3,5-дихлорбензоат: Конц. H2SO4 (2,5 мл, 97,04 ммоль) добавляли по каплям к перемешиваемому раствору 4-амино-3,5-дихлорбензойной кислоты (10,0 г, 48,54 ммоль) в MeOH (150 мл) при 0°C и затем реакционную смесь перемешивали при 80°C в течение 8 ч. Летучие вещества выпаривали, к остатку добавляли воду со льдом и затем смесь экстрагировали EtOAc. Объединенные органические слои промывали рассолом, сушили (Na2SO4), фильтровали и выпаривали при пониженном давлении, получив указанное в заголовке соединение в виде белого твердого вещества (7,5 г, 70%): 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,05 (с, 2H), 3,96 (с, 3H); ЭРИ-МС m/z 282 ([М]+); ИК (KBr): 1733, 762, 514 см-1.
Стадия 2. Метил-4-бром-3,5-дихлорбензоат: CuBr2 (7,5 г, 34,08 ммоль) в MeCN (50 мл) перемешивали при 80°C в течение 30 мин. К этому раствору при той же температуре по каплям добавляли трет-бутилнитрит (6,5 мл, 54,55 ммоль) и смесь перемешивали еще в течение 10 мин. К реакционной смеси по каплям добавляли метил-4-амино-3,5-дихлорбензоат в MeCN (30 мл), затем смесь перемешивали при 80°C в течение 30 мин. Реакционную смесь доводили до температуры окружающей среды. Добавляли водный раствор аммиака (20 мл) и экстрагировали петролейным эфиром. Органический слой промывали рассолом, затем водой. Органический раствор сушили (Na2SO4), фильтровали и выпаривали, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (7,5 г, 77%): 1H-ЯМР (300 МГц, ДМСО-d6) δ 8,02 (с, 2H), 3,94 (с, 3H); ЭРИ-МС m/z 282 ([М]+); ИК (тонкая пленка) 1733, 762, 514 см-1.
Стадия 3. (4-Бром-3,5-дихлорфенил)метанол: DIBAL-H (1M в толуоле, 66 мл и 66,0 ммоль) по каплям добавляли к перемешиваемому раствору метил-4-бром-3,5-дихлорбензоата (7,5 г, 26,0 ммоль) в ТГФ (50 мл) при -78°C. Реакционную смесь доводили до температуры окружающей среды и перемешивали в течение 6 ч. Реакционную смесь вливали в воду со льдом и экстрагировали CH2Cl2. Органический слой промывали рассолом, затем водой, сушили (Na2SO4), фильтровали и выпаривали, получив смесь (4-бром-3,5-дихлорфенил)метанола и 4-бром-3,5-дихлорбензальдегида (6,0 г) в виде грязно-белого твердого вещества, которое использовали на следующей стадии без очистки.
Стадия 4. 4-Бром-3,5-дихлорбензальдегида: PCC (7,5 г, 35,16 ммоль) добавляли одной порцией к перемешиваемому раствору, содержащему смесь (4-бром-3,5-дихлорфенил)метанола и 4-бром-3,5-дихлорбензальдегида (6,0 г) в CHCl3 (40 мл) при температуре окружающей среды и реакционную смесь перемешивали в течение ночи. Реакционную смесь фильтровали через целит. Слой целита промывали CHCl3. Фильтрат выпаривали, получив указанное в заголовке соединение в виде грязно-белого твердого вещества (3,5 г, 67%): Т.пл. 125-128°C; 1H-ЯМР (300 МГц, ДМСО-d6) δ 9,96 (с, 1H), 8,10 (с, 2H); ЭРИ-МС m/z 252 ([М]+).
Пример 142: 3-Хлор-5-этилбензальдегид
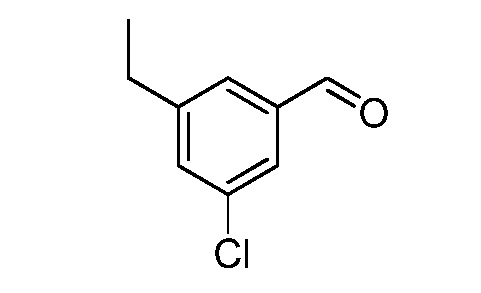
PdCl2(dppf) (37 мг, 0,046 ммоль), фосфат калия (1,93 г, 9,11 ммоль) и триэтилборан (1M в гексане, 0,45 г, 4,56 ммоль) добавляли к раствору 3-бром-5-хлор-бензальдегида (1,0 г, 4,56 ммоль) в ТГФ (20 мл) при температуре окружающей среды и смесь нагревали с обратным холодильником в течение 12 ч. Реакционную смесь доводили до температуры окружающей среды, разбавляли EtOAc и промывали водой. Органический слой сушили (Na2SO4), фильтровали, выпаривали и остаток очищали с помощью колоночной хроматографии на силикагеле (100-200 меш), используя в качестве элюента 2% EtOAc в петролейном эфире, получив указанное в заголовке соединение (330 мг, 41%) в виде светло-желтой жидкости: 1H-ЯМР (400 МГц, ДМСО-d6) δ 9,97 (с, 1H), 7,75 (д, J=1,6 Гц 1H), 7,73 (с, 1H), 7,65 (с, 1H), 2,74-2,68 (м, 2H), 1,23 (т, J=7,6 Гц, 3H); ЭРИ-МС m/z 168,0 ([М]+); ИК (тонкая пленка) 3071, 1699, 692 см-1.
Следующие предполагаемые молекулы могут быть получены в соответствии с методиками, раскрытыми в настоящей заявке:
Структуры предполагаемых соединений
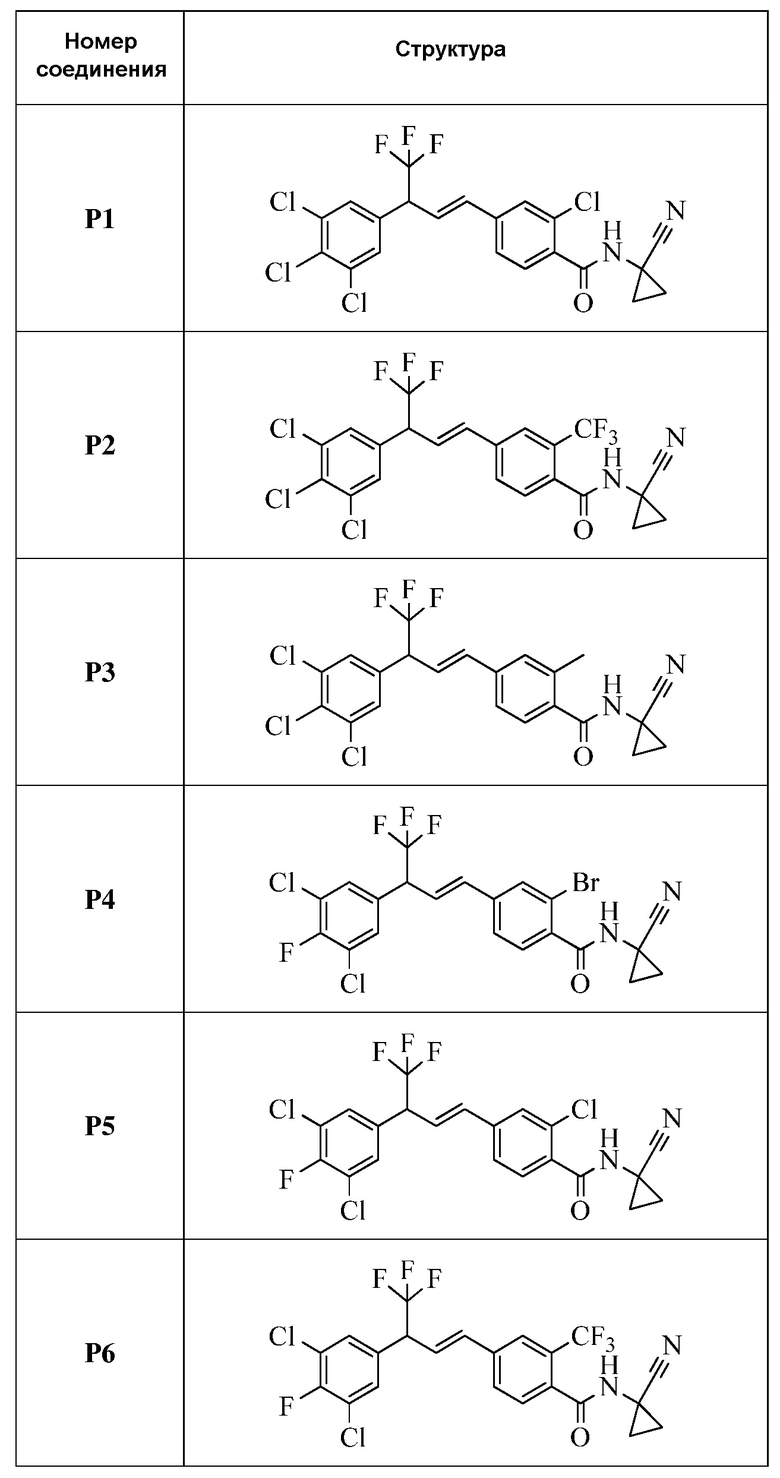
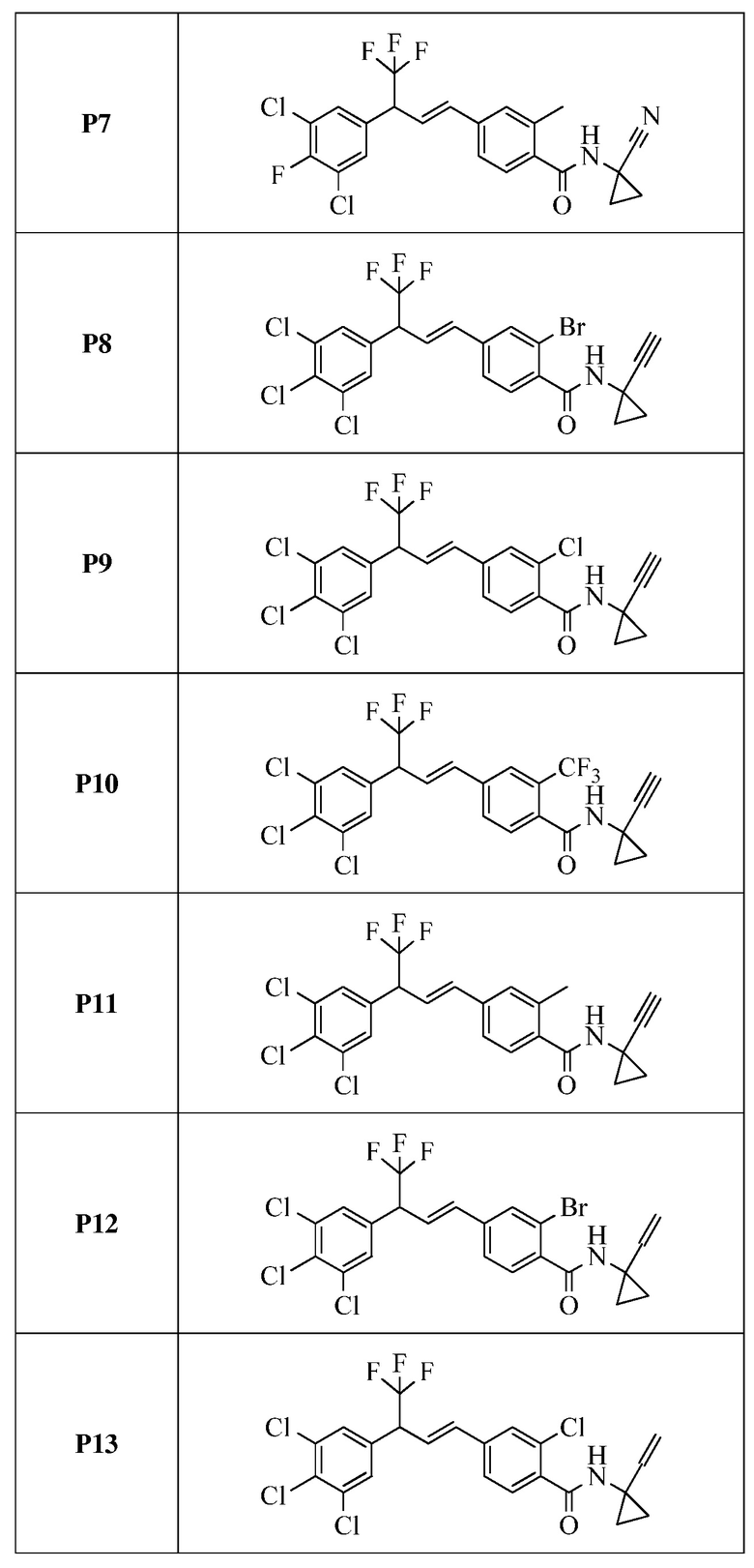
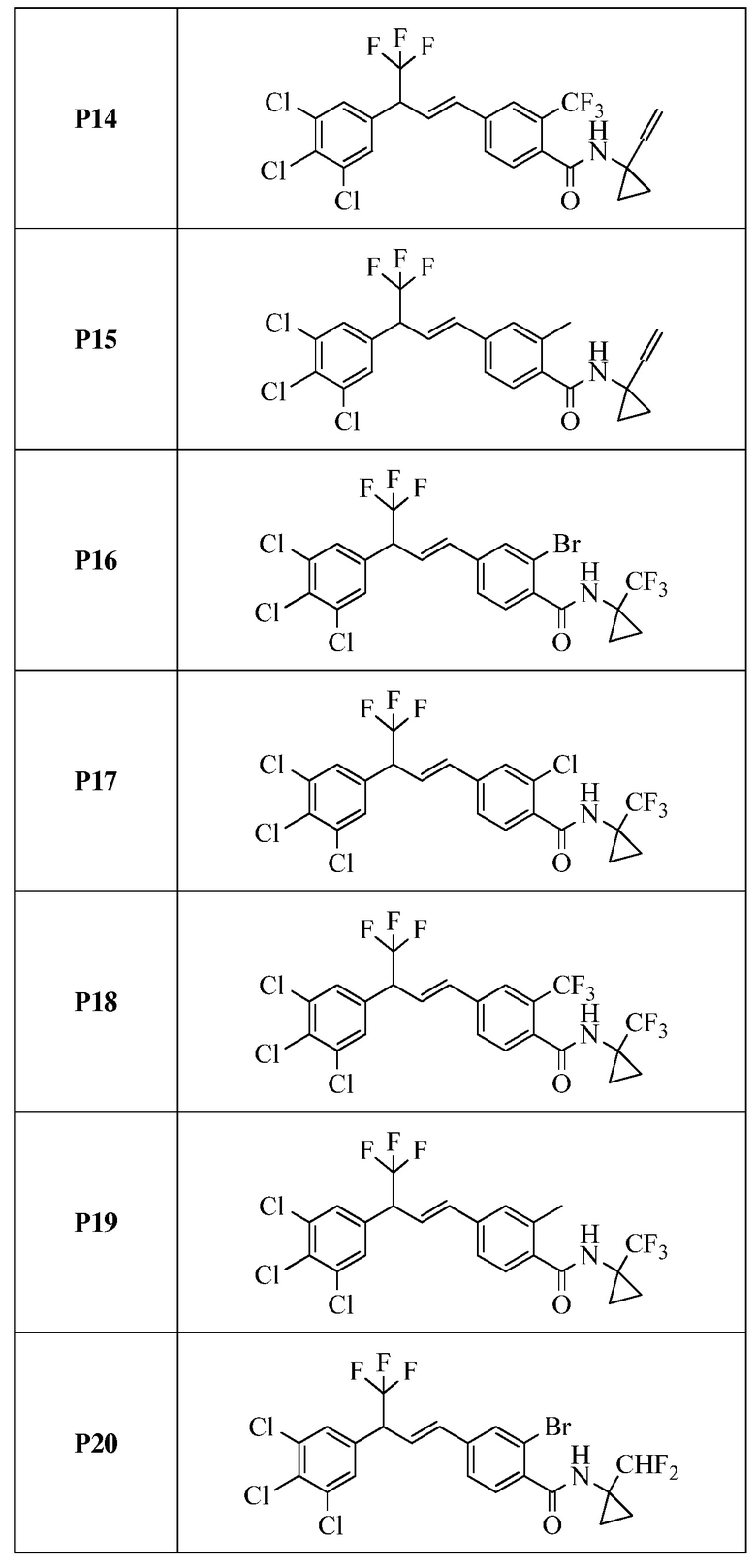
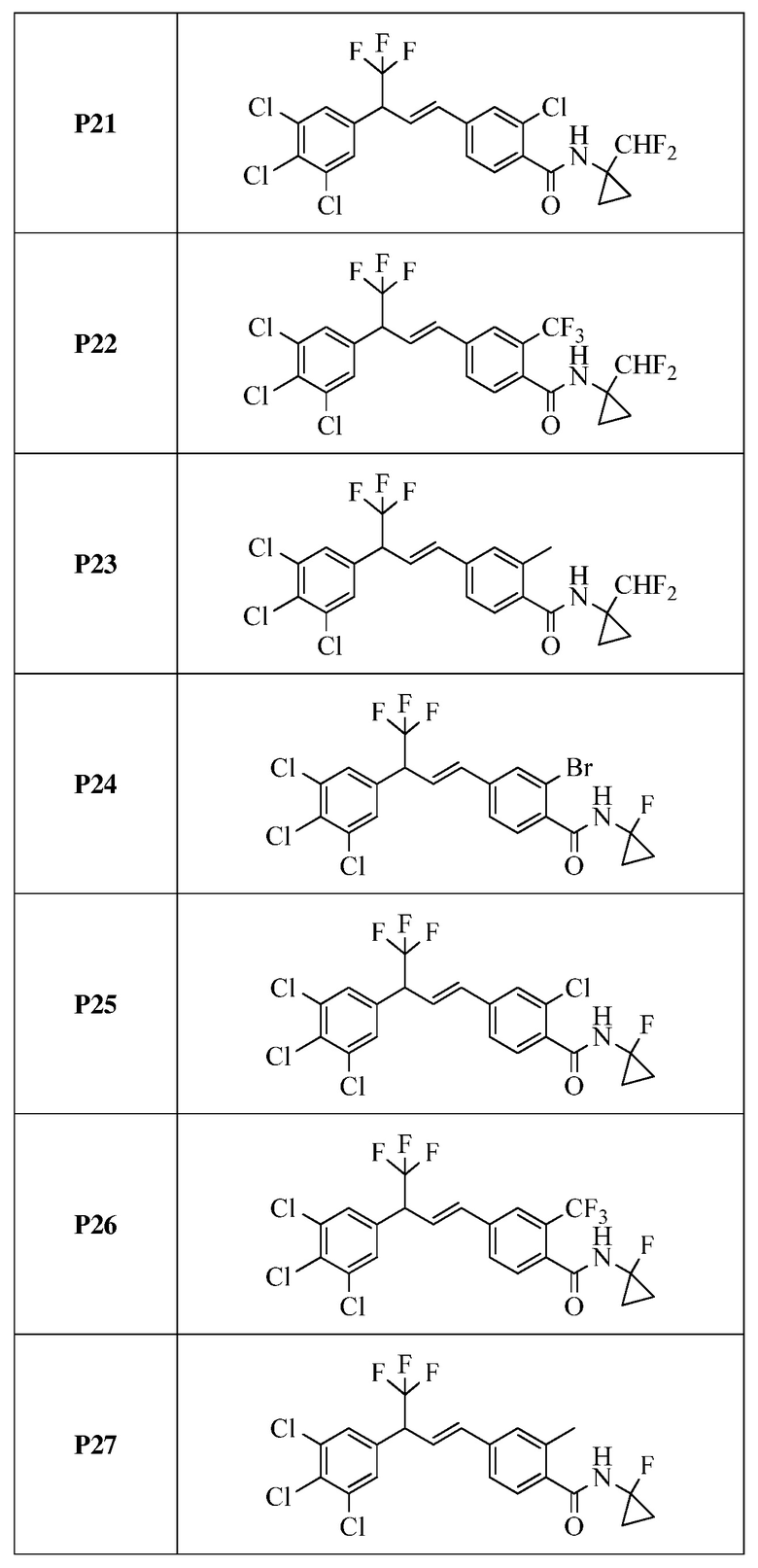
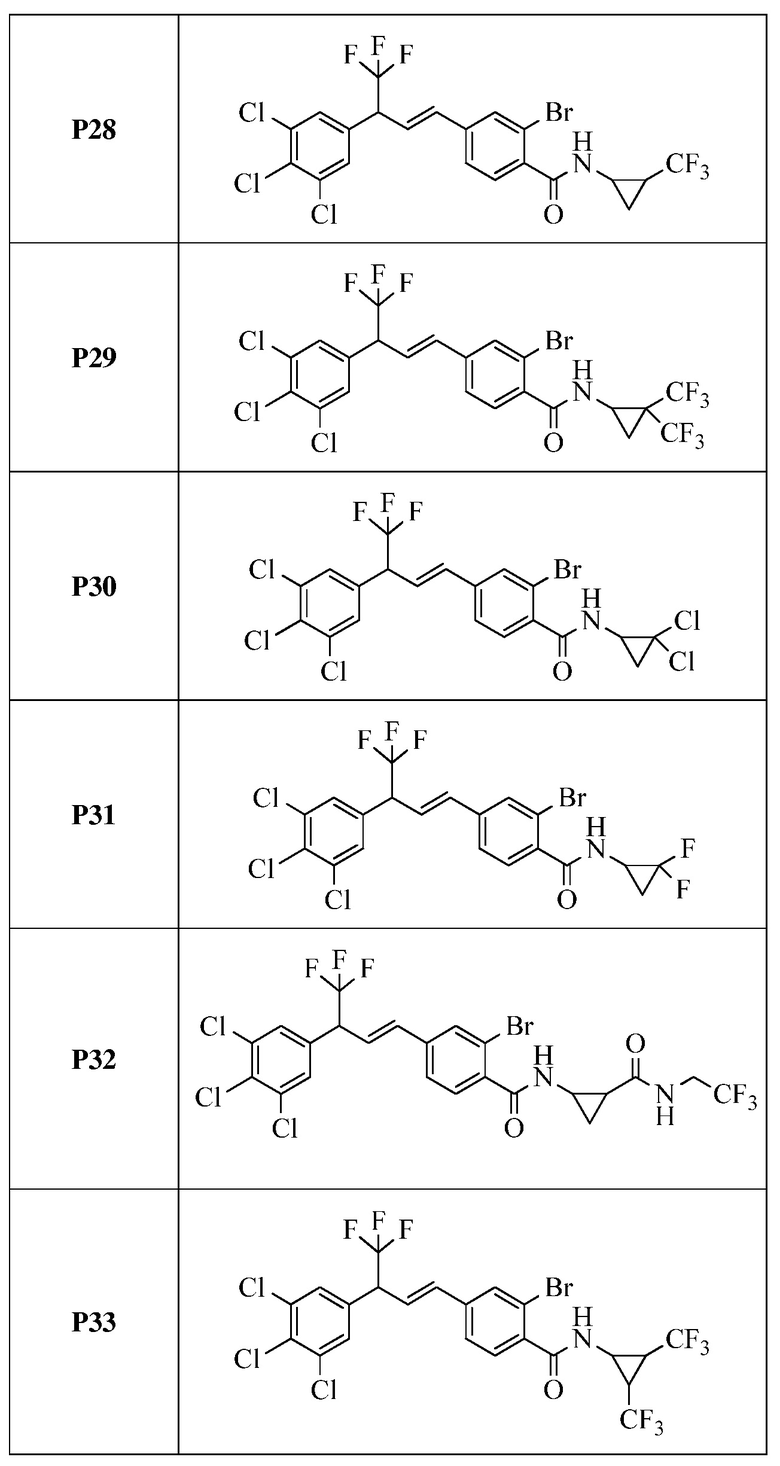
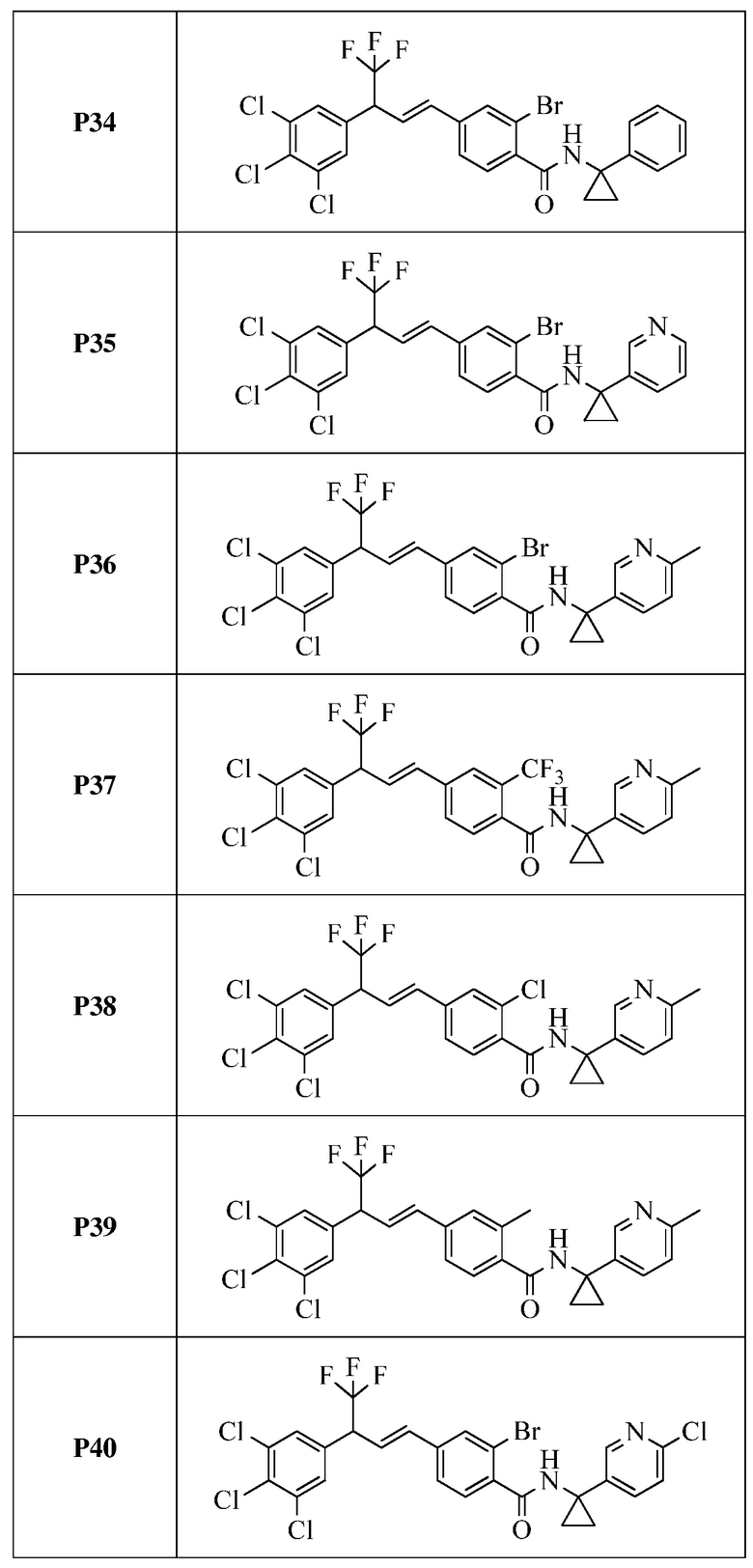
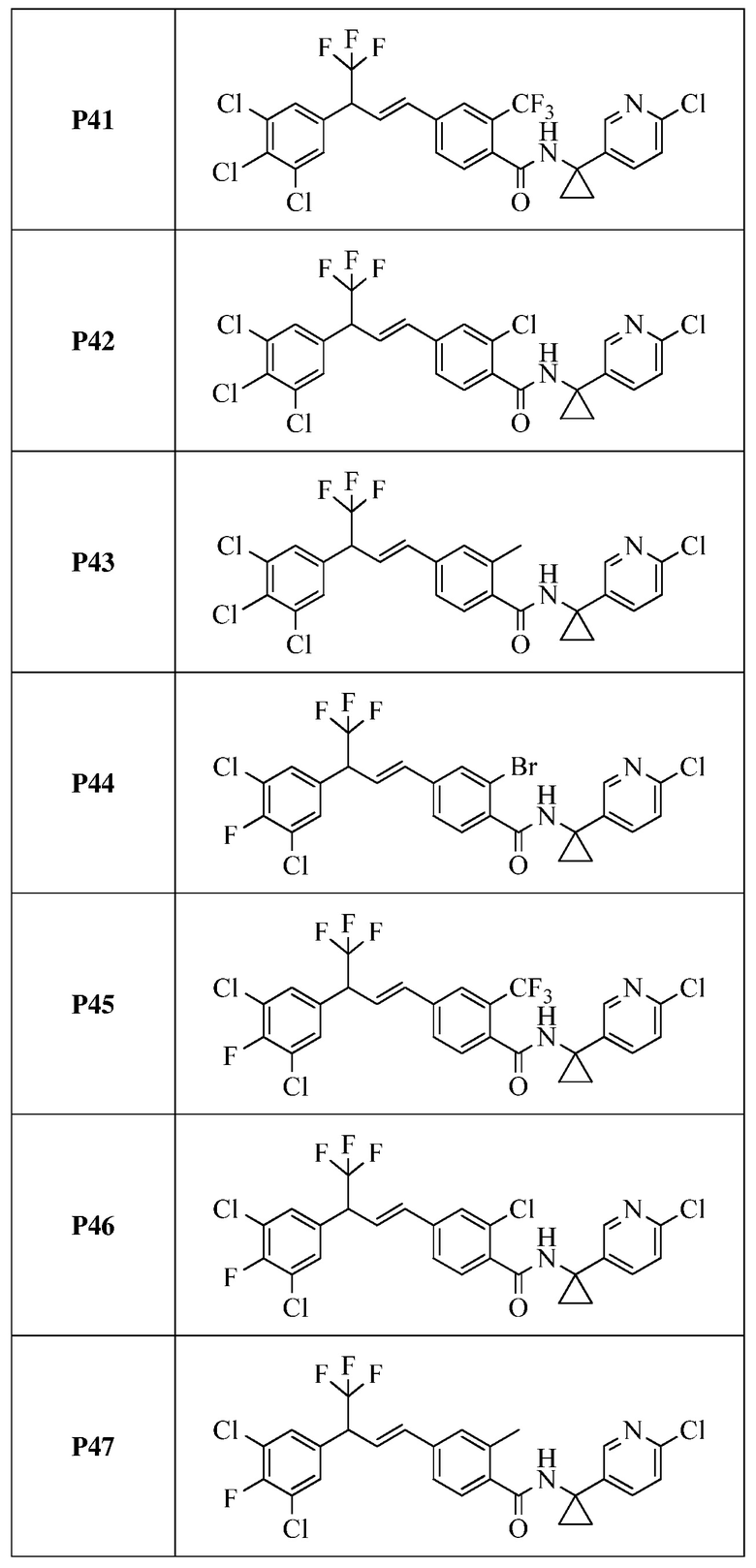
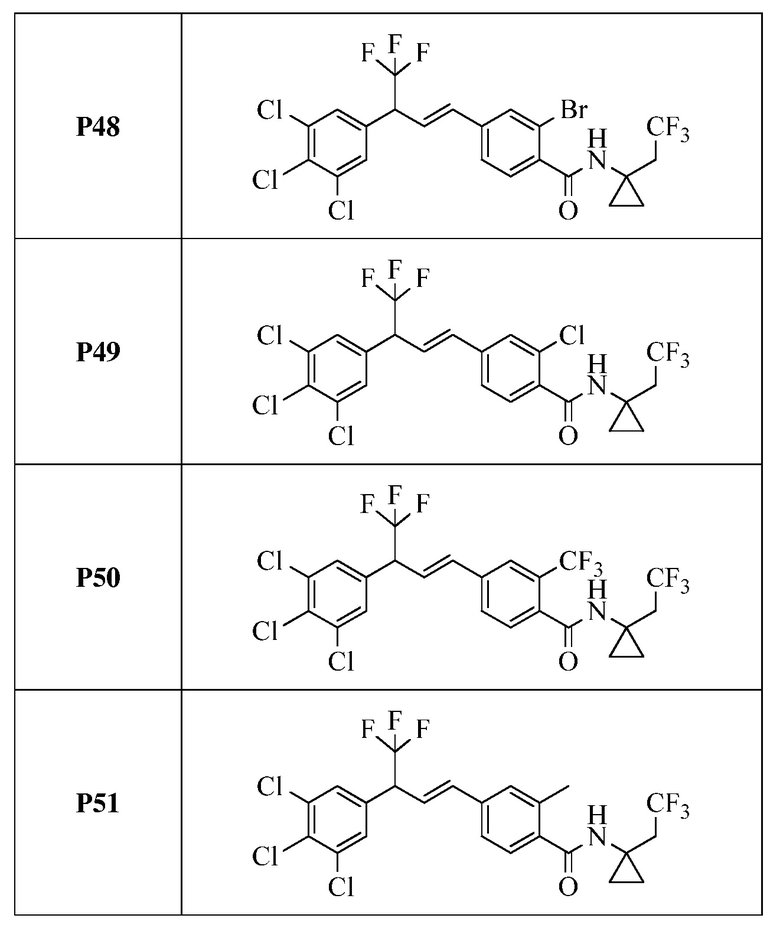
Следующие предполагаемые молекулы могут быть получены в соответствии с методиками, раскрытыми в настоящей заявке:
Структуры дополнительных предполагаемых соединений
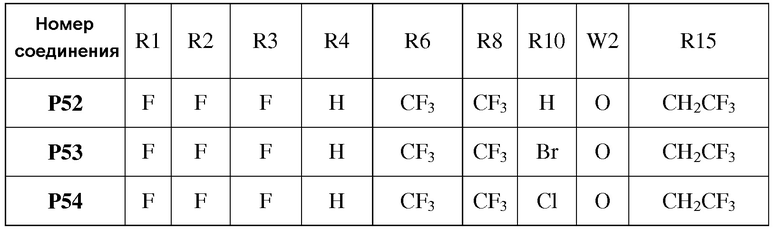

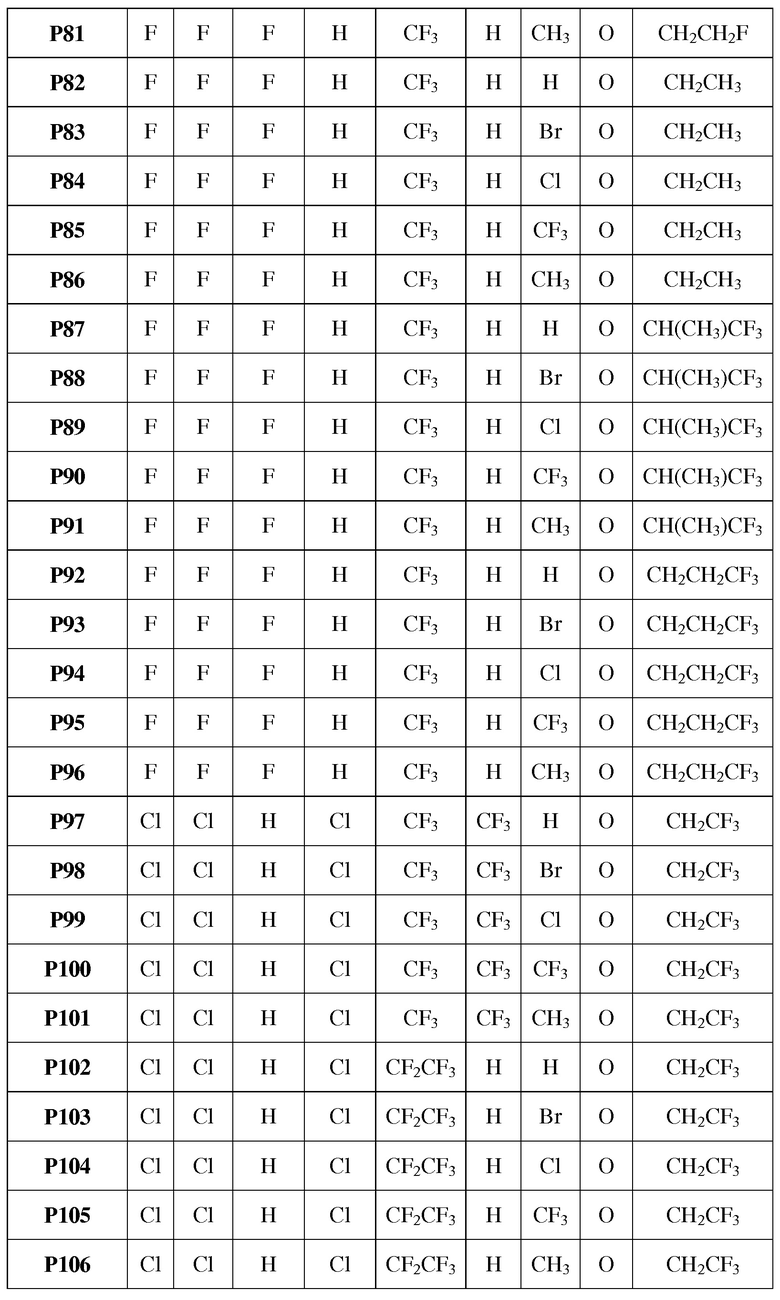

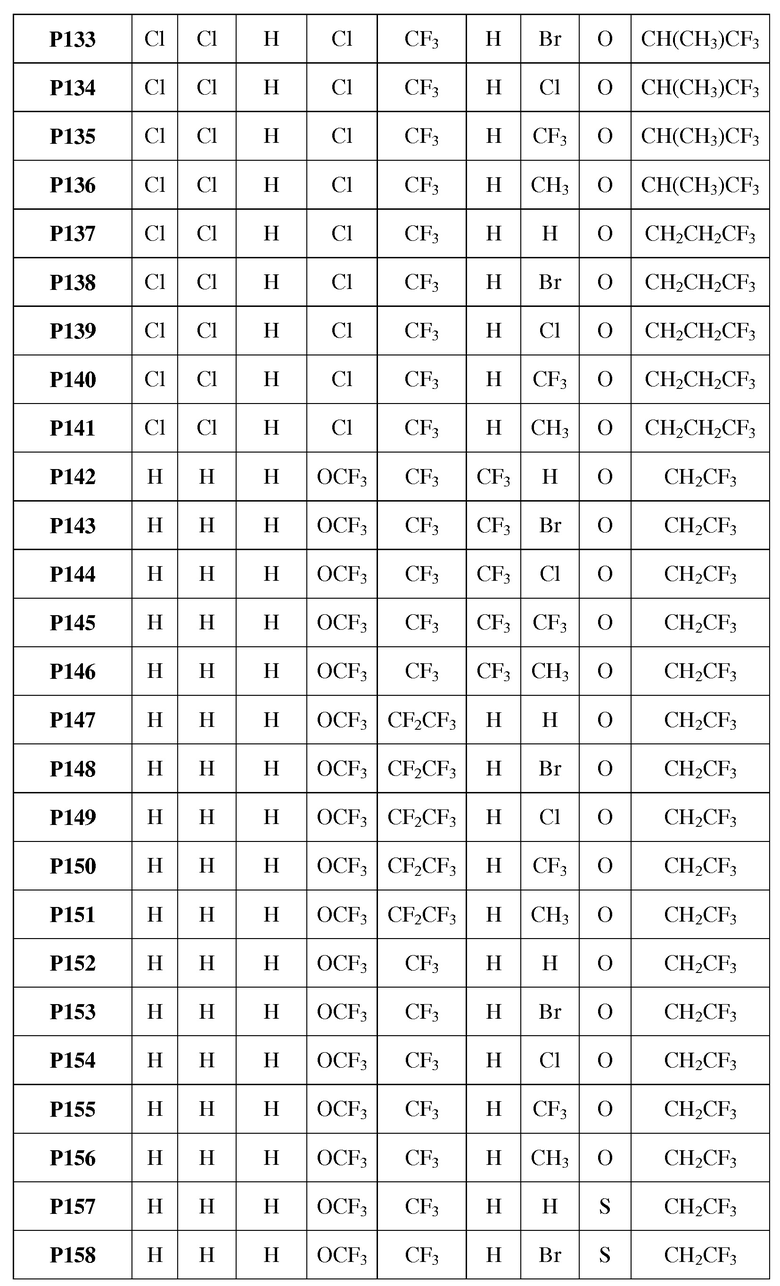
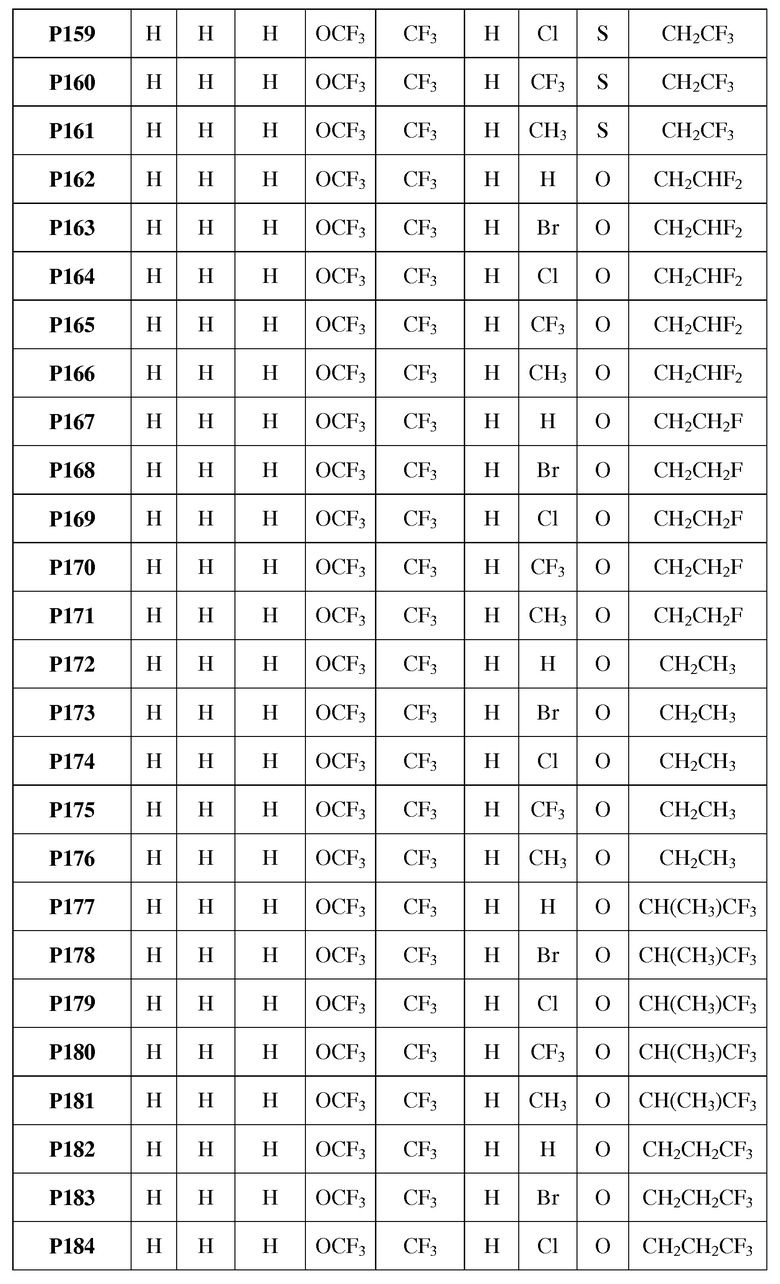
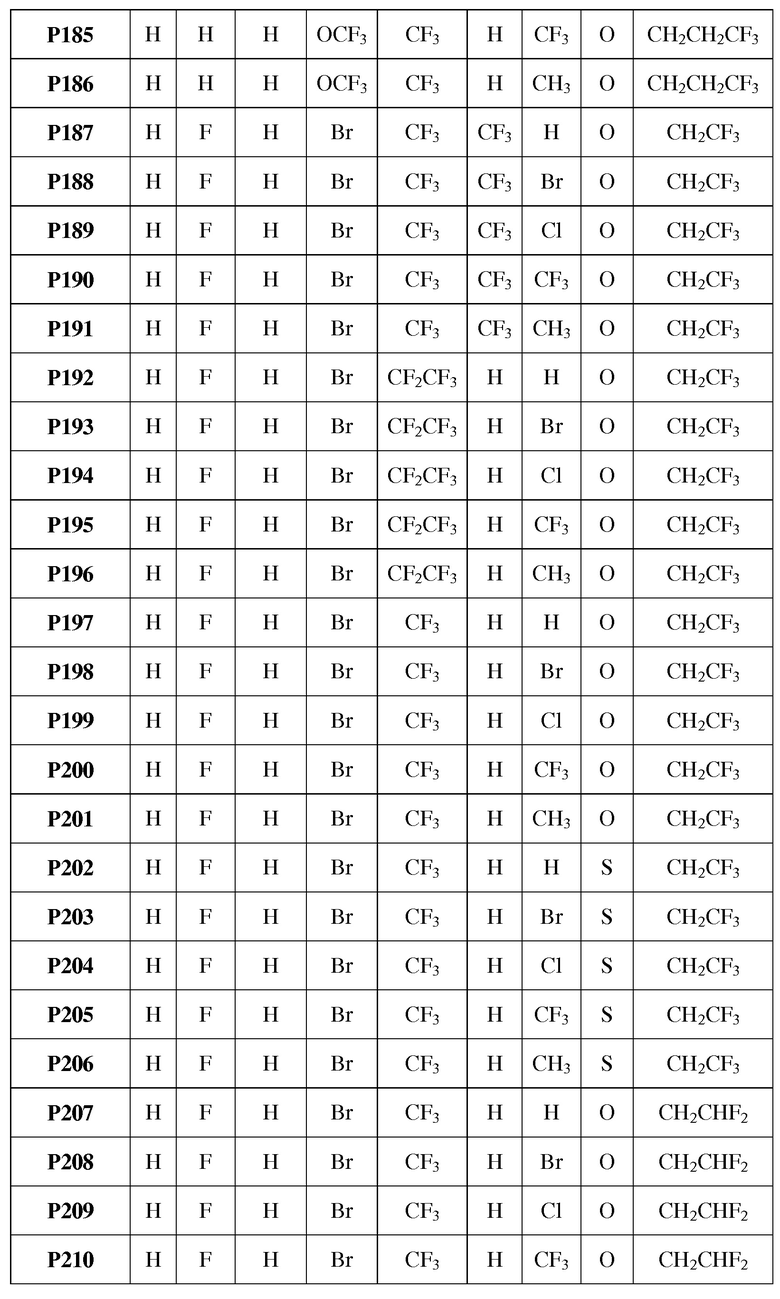
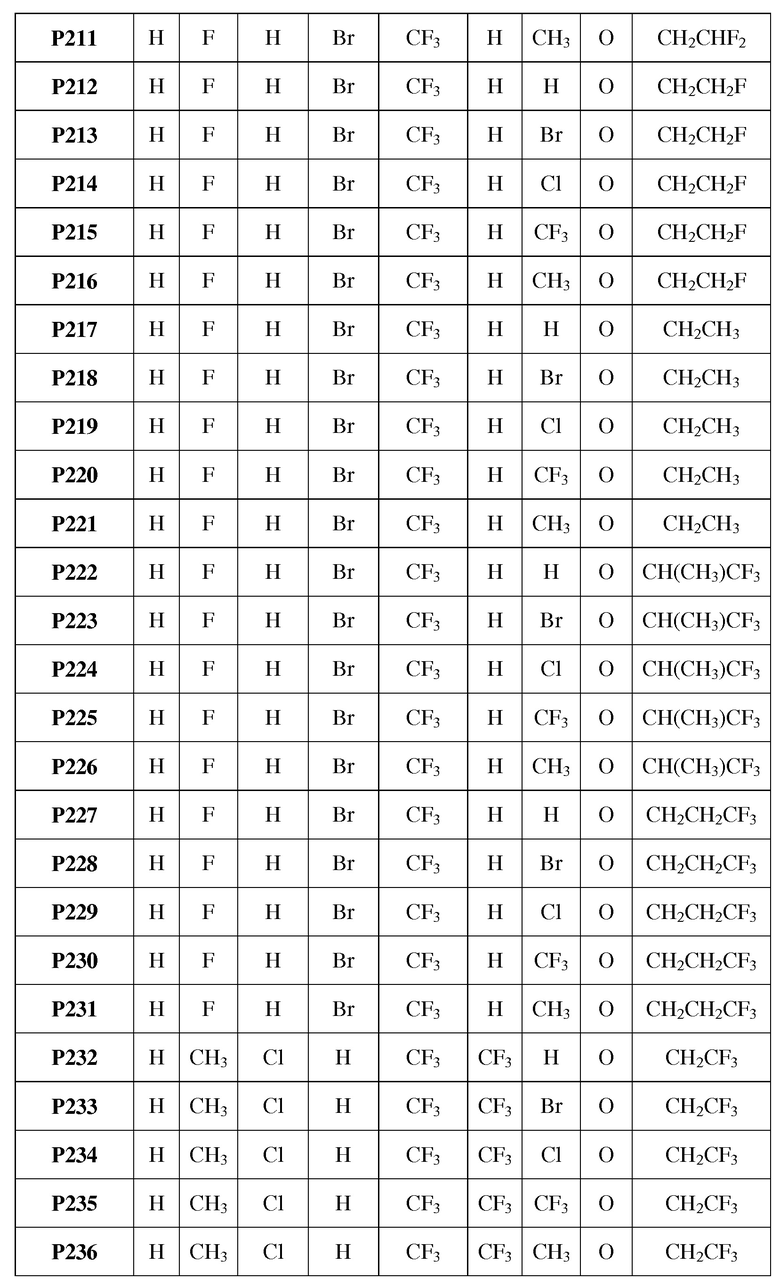
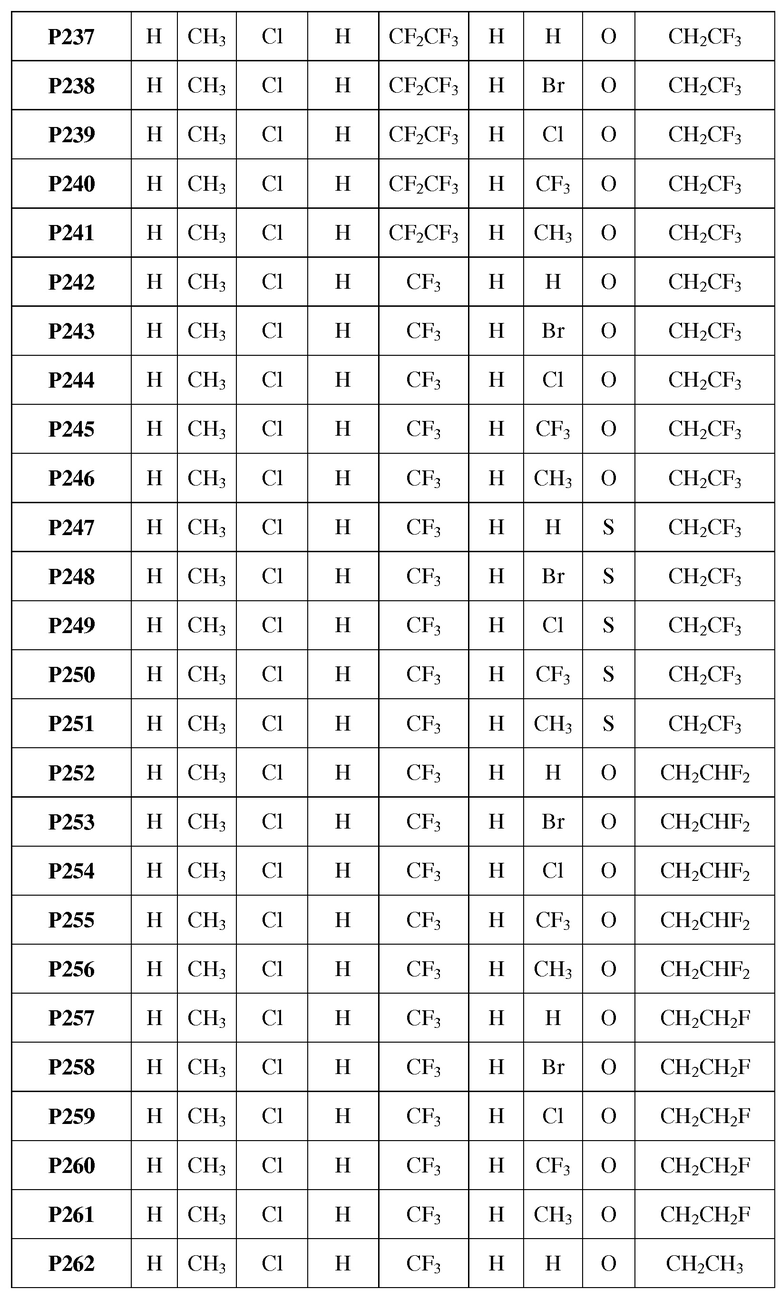
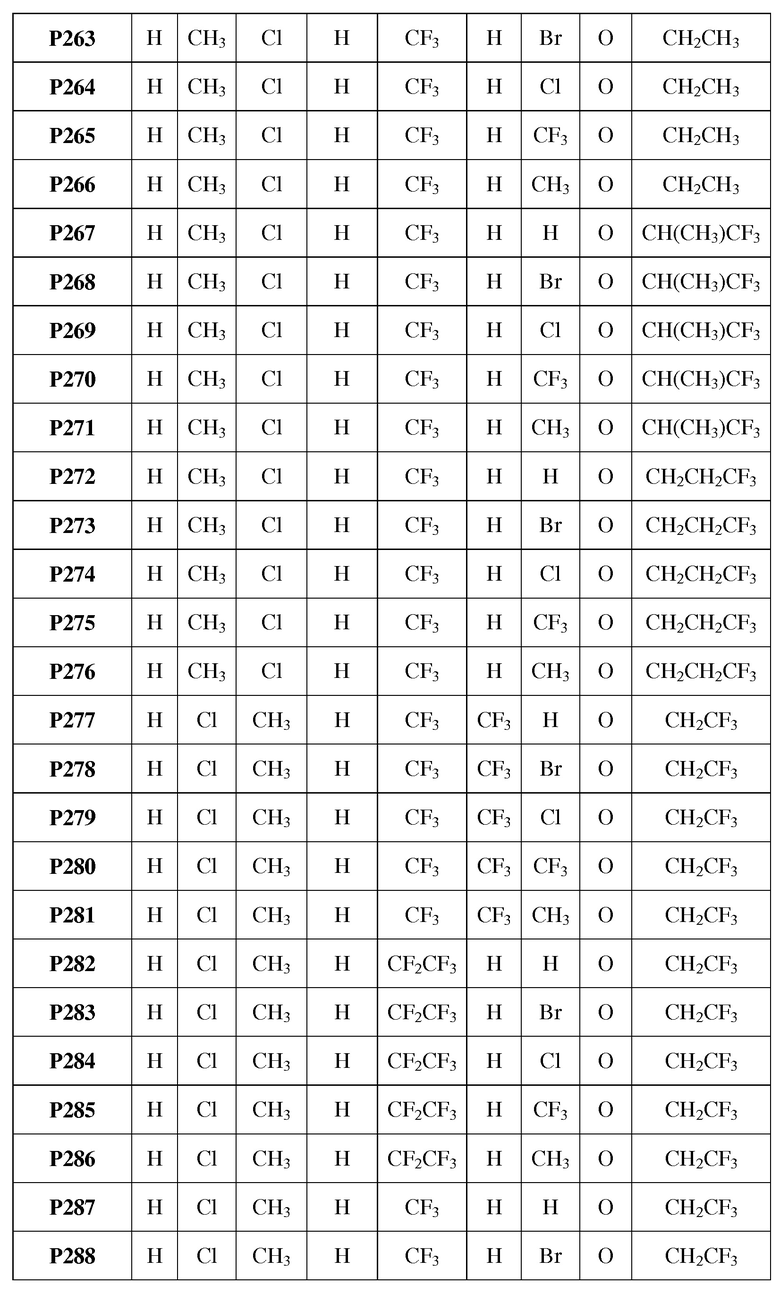
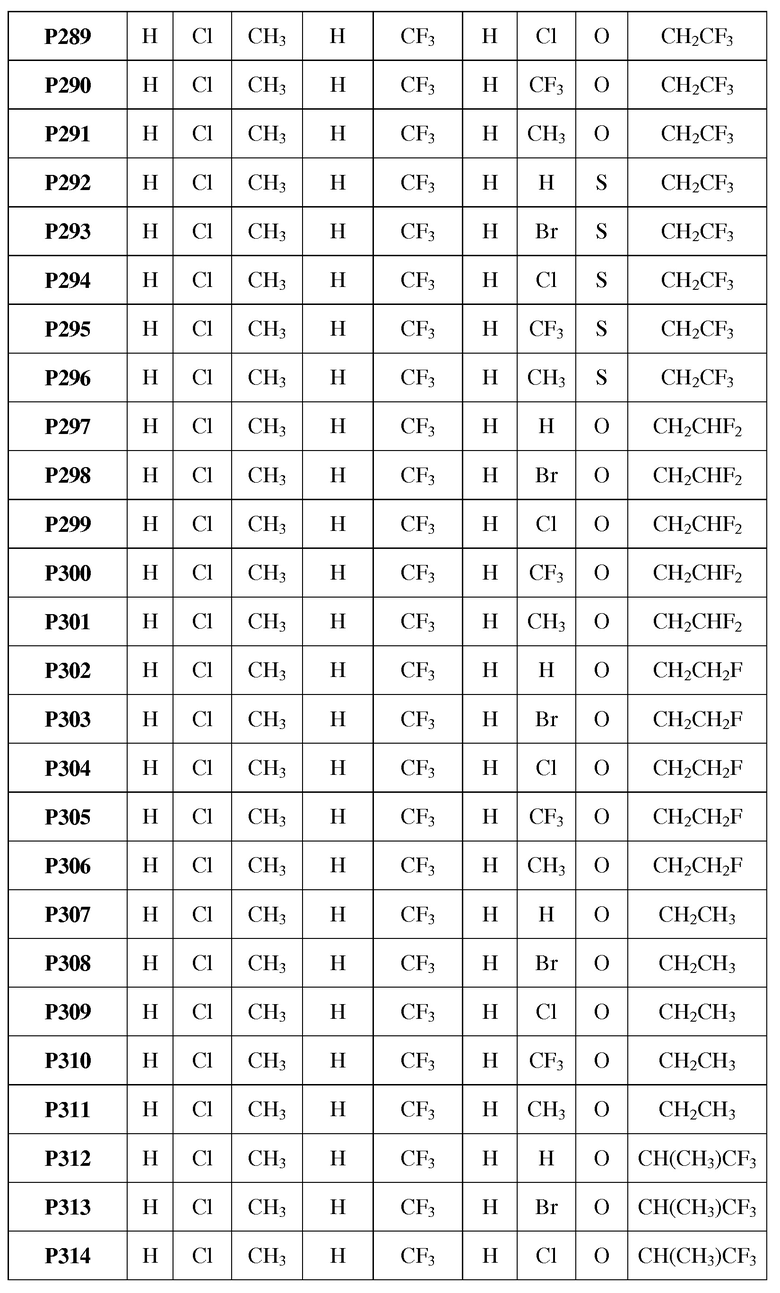
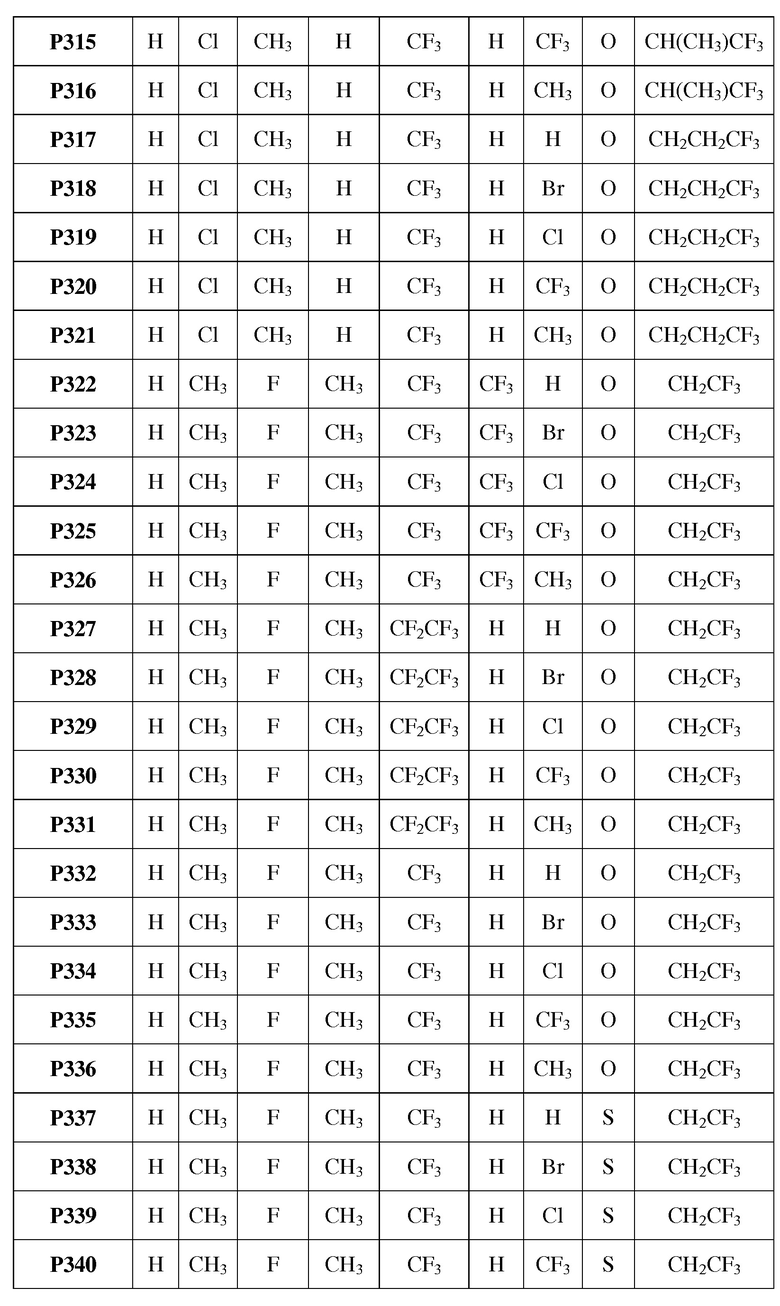
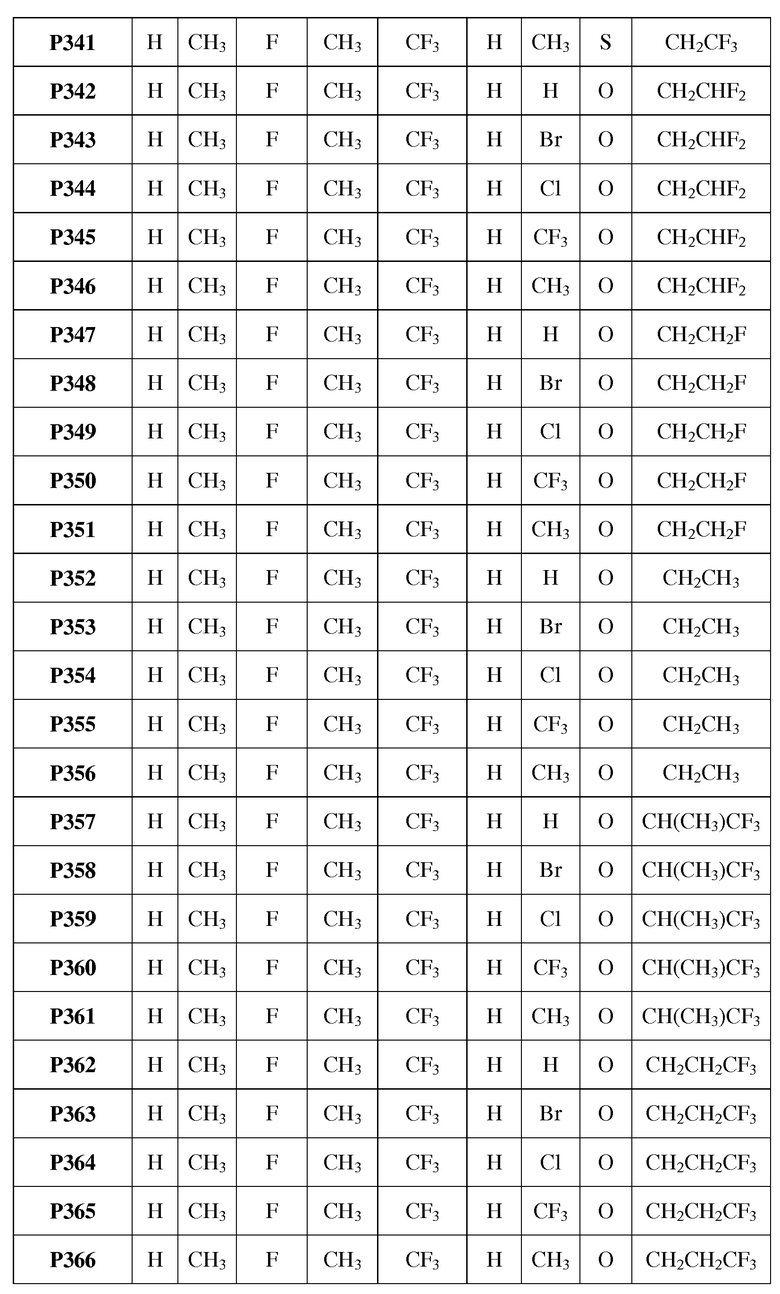
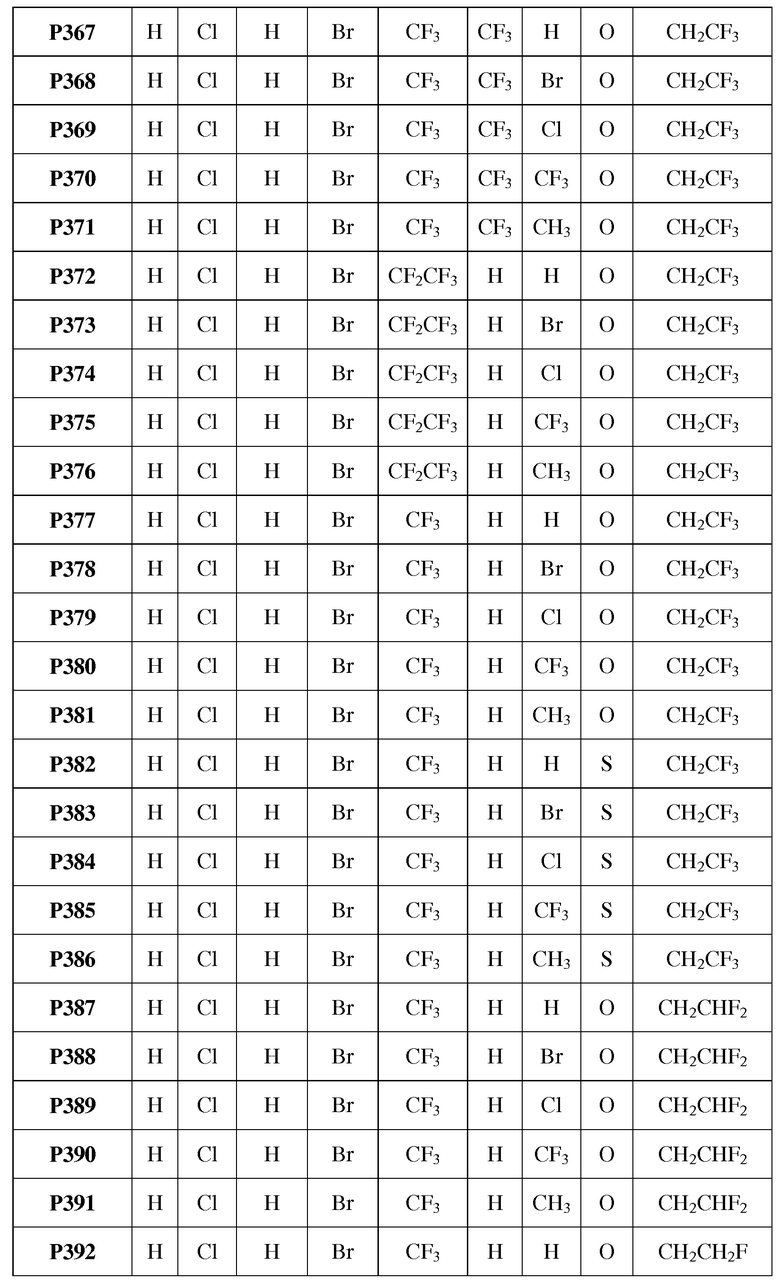
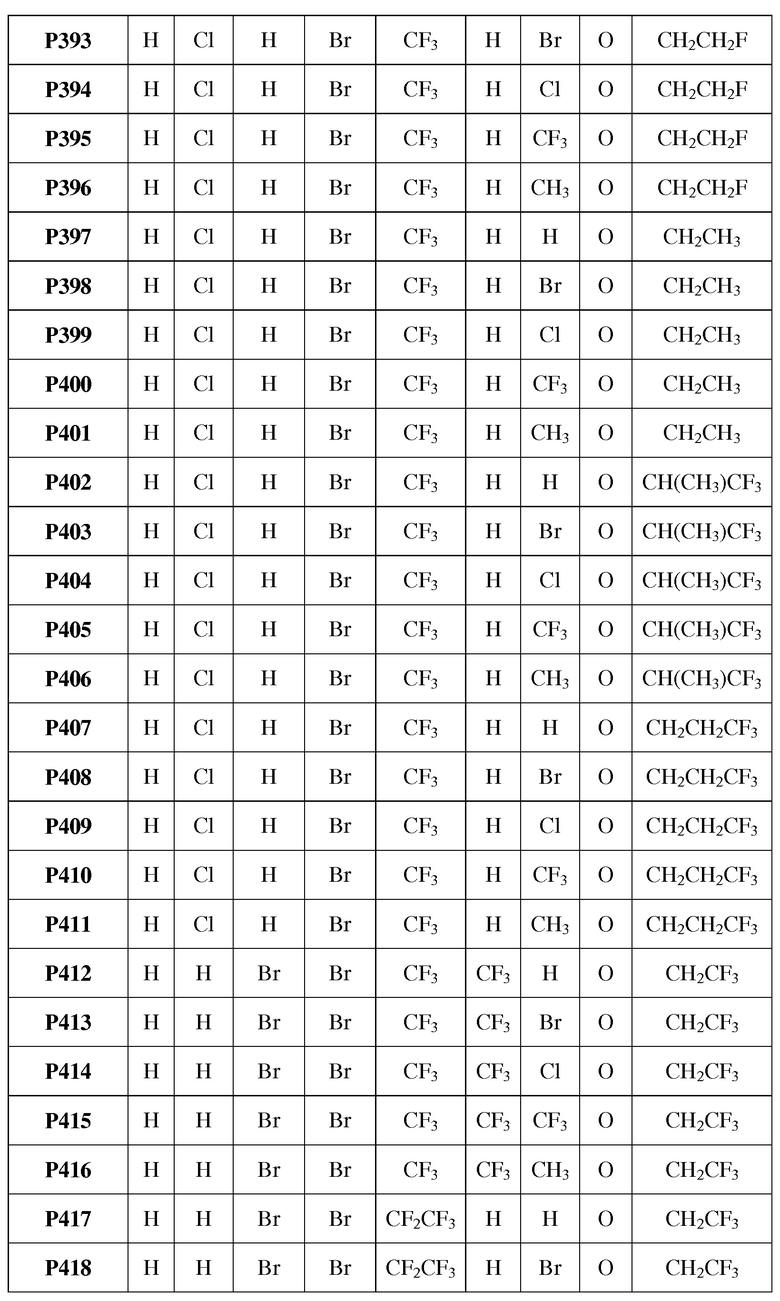
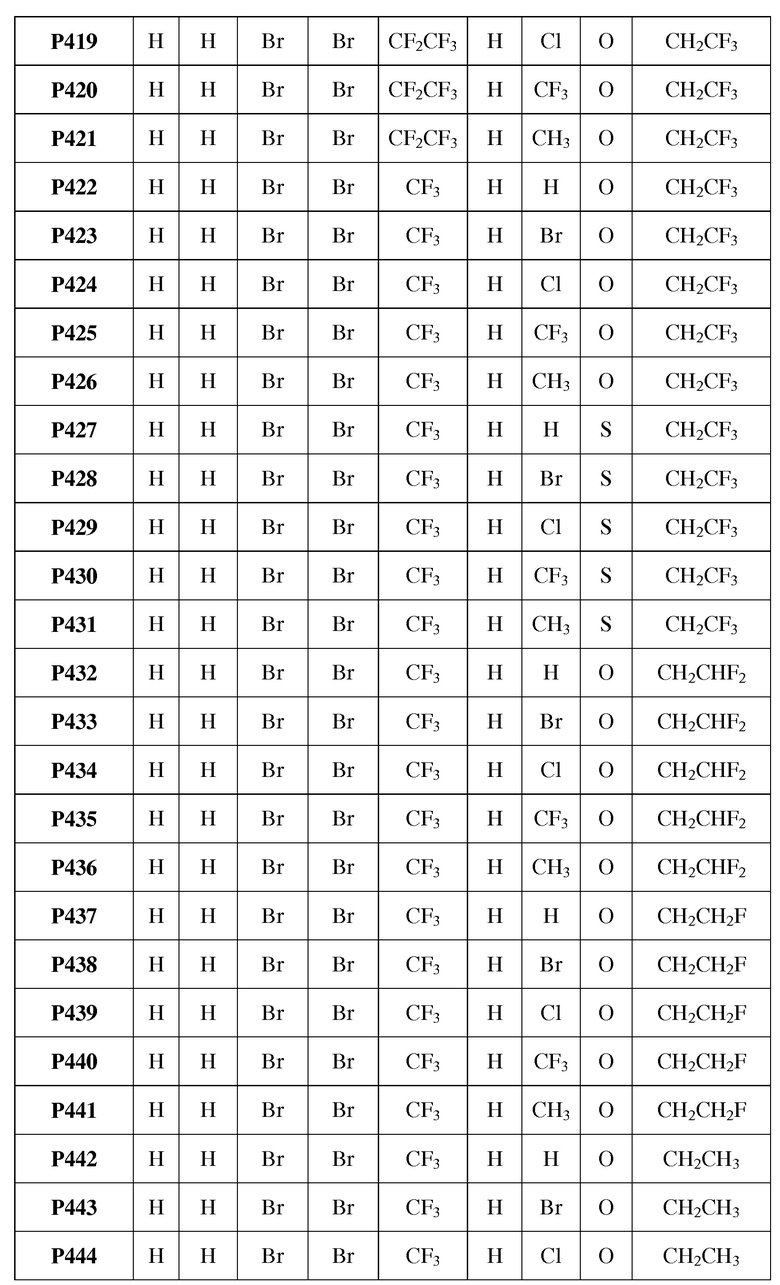
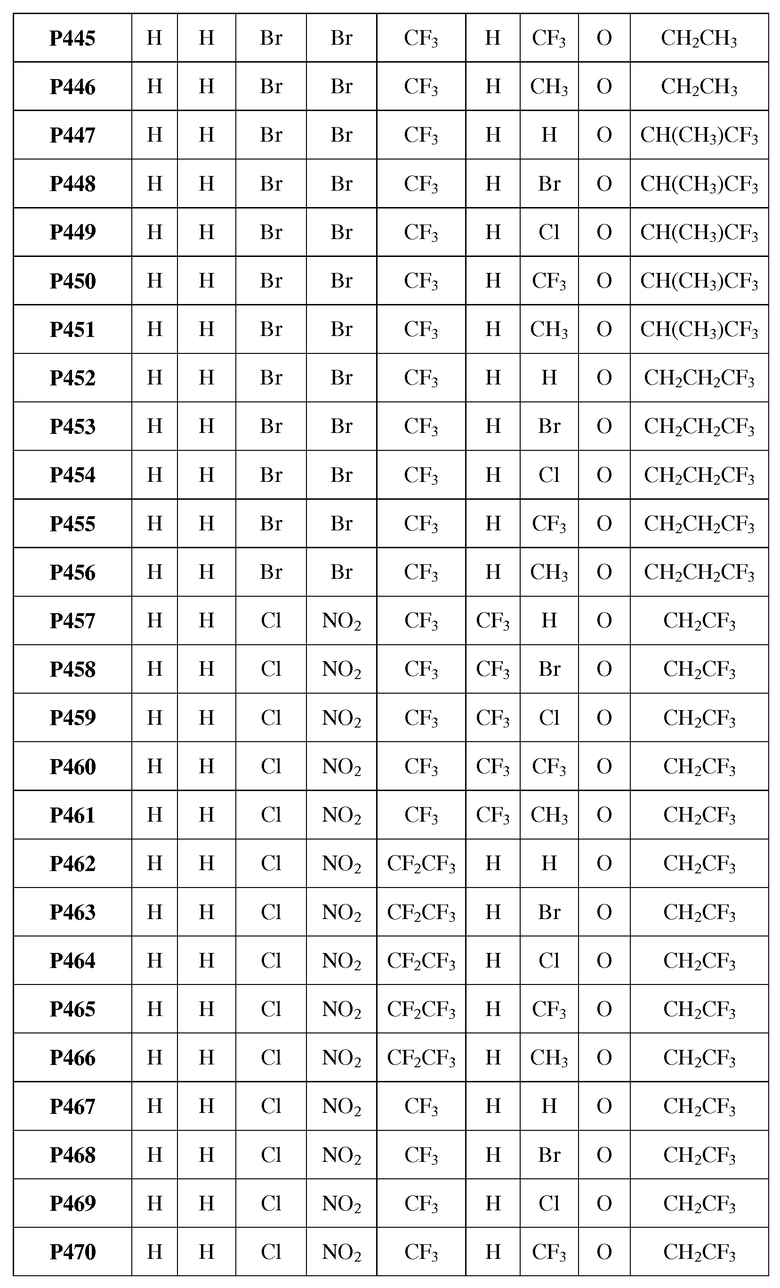
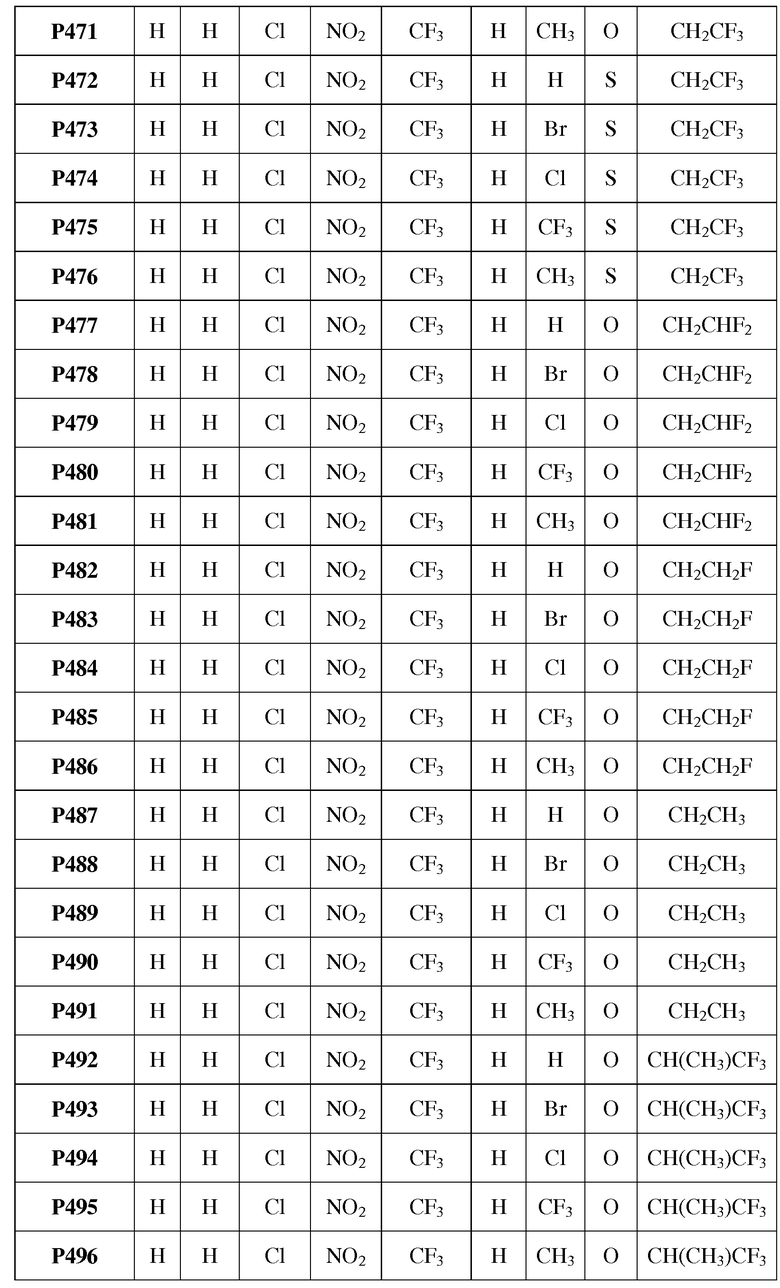
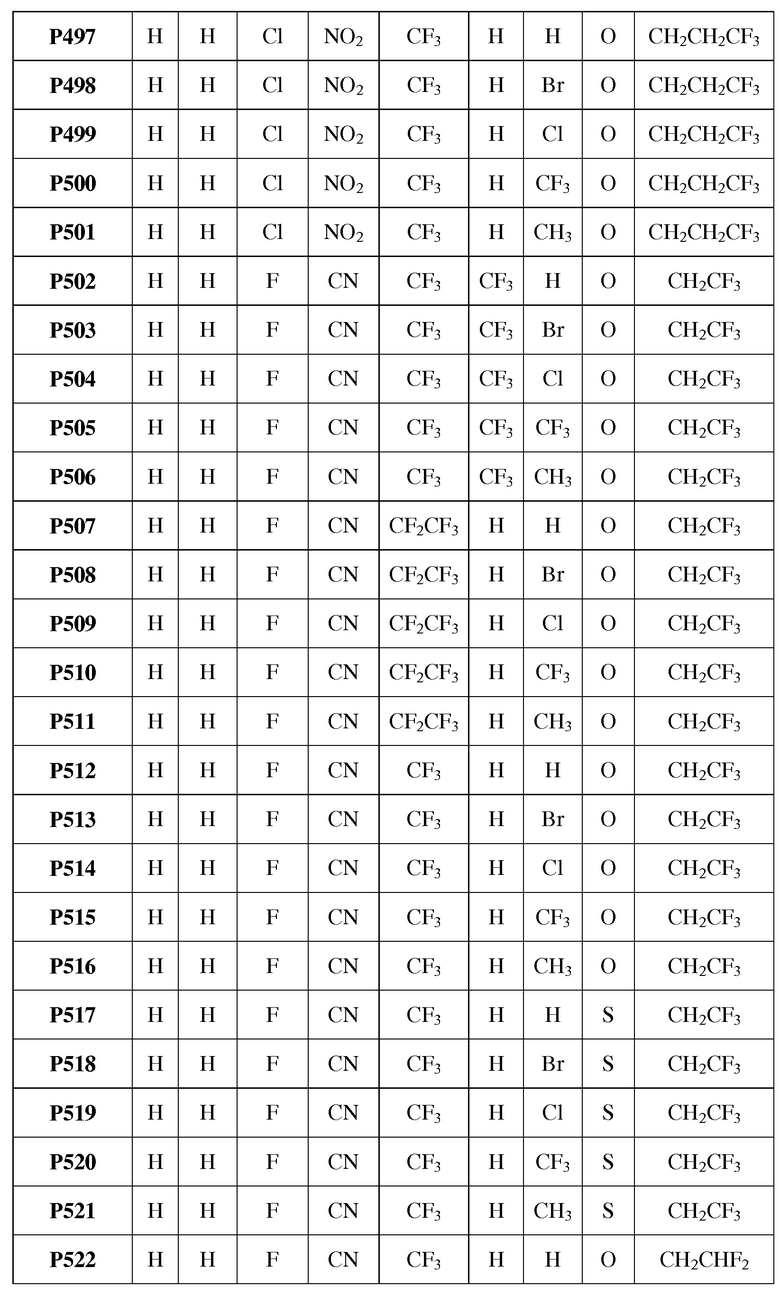
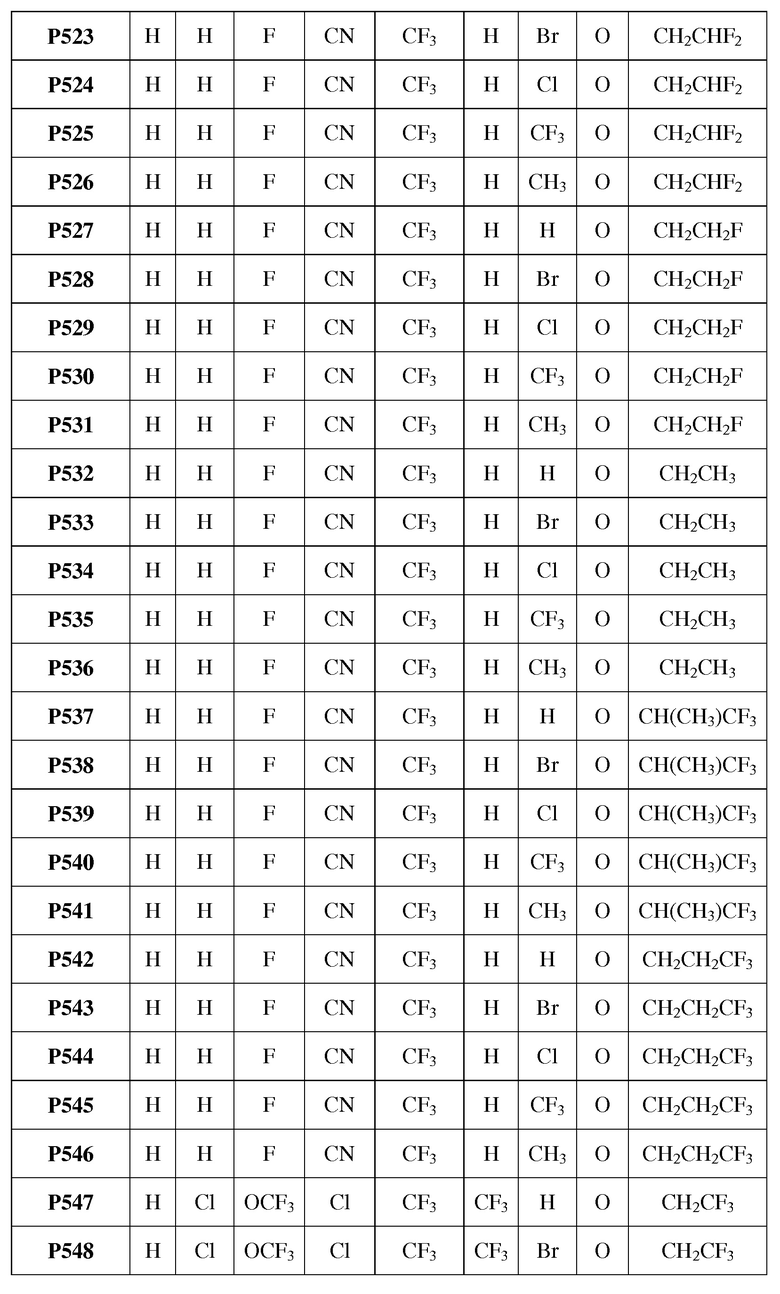
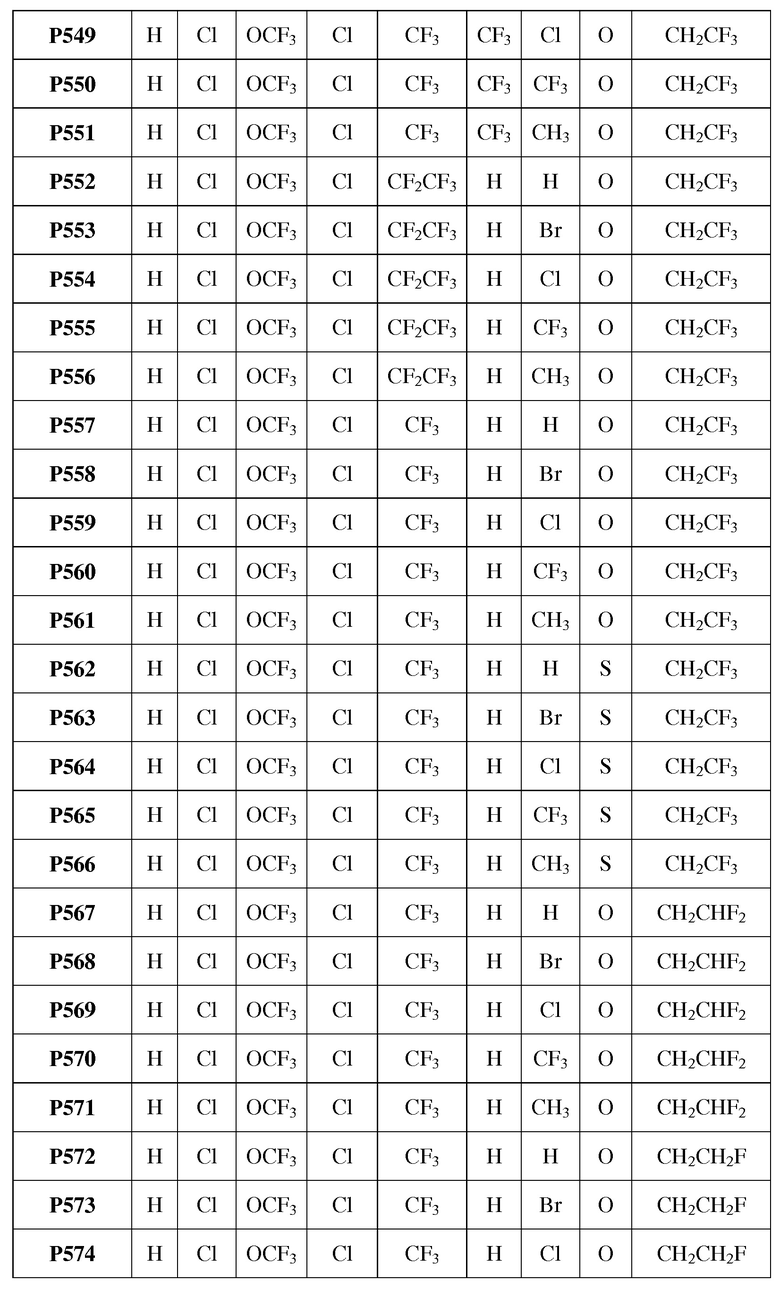
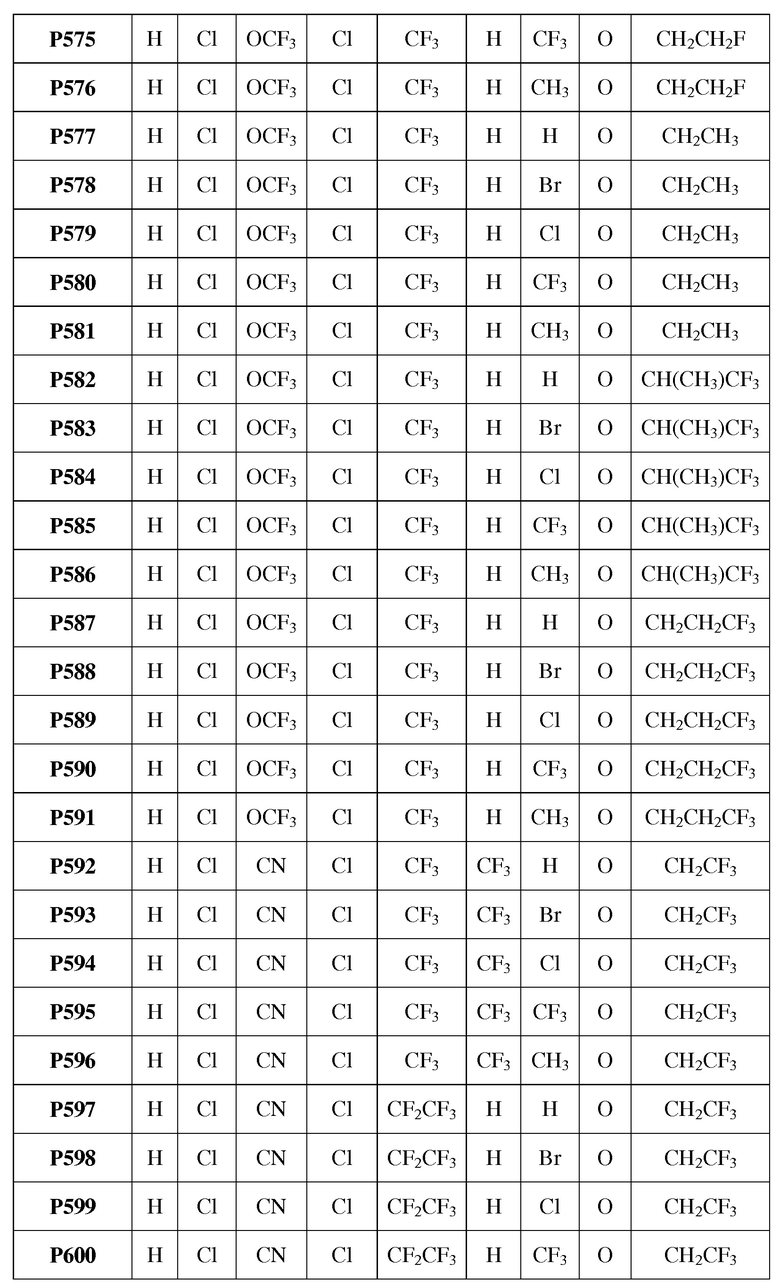
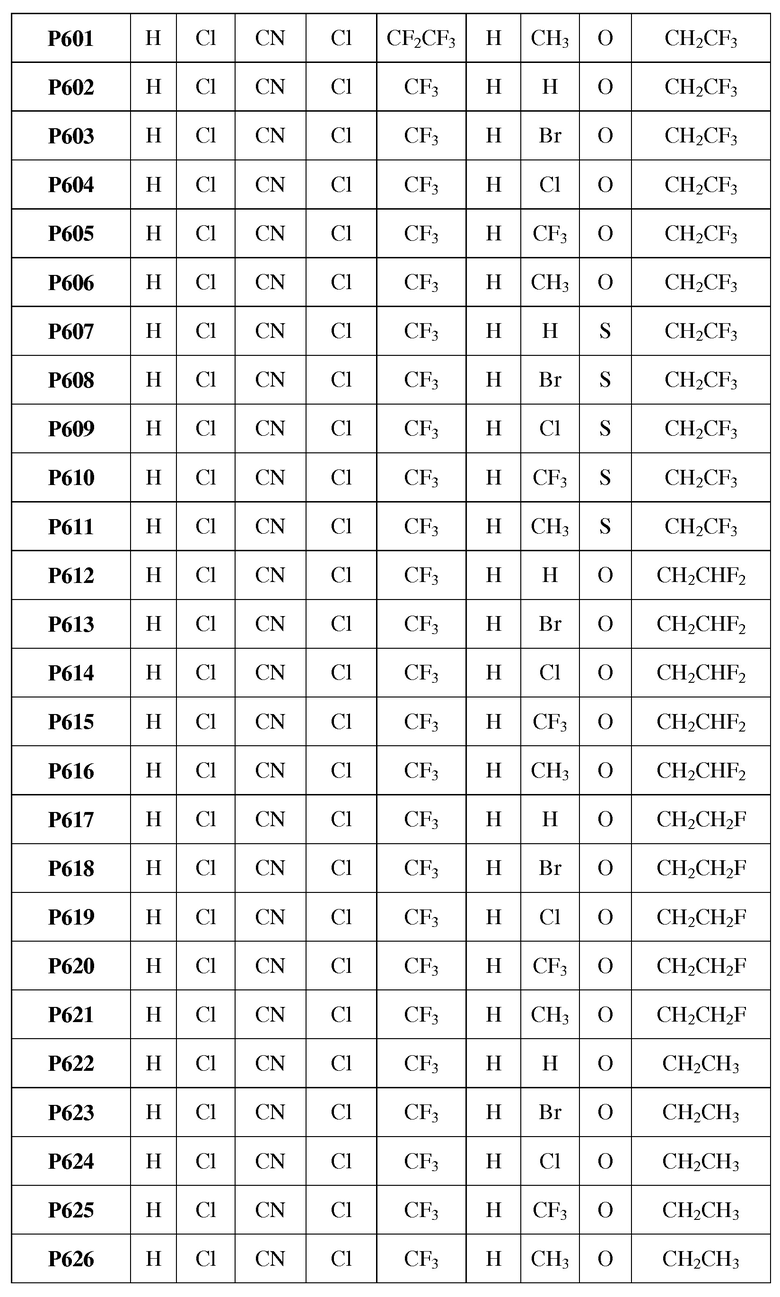
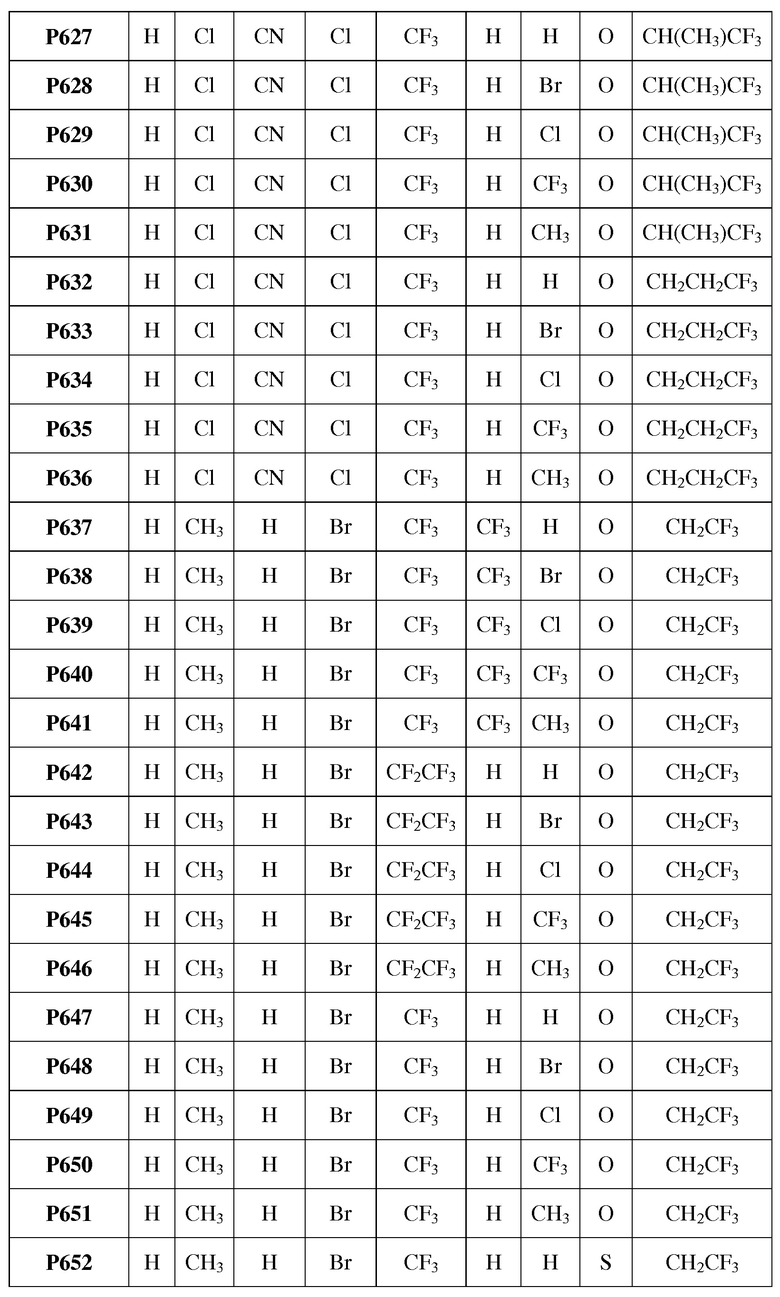


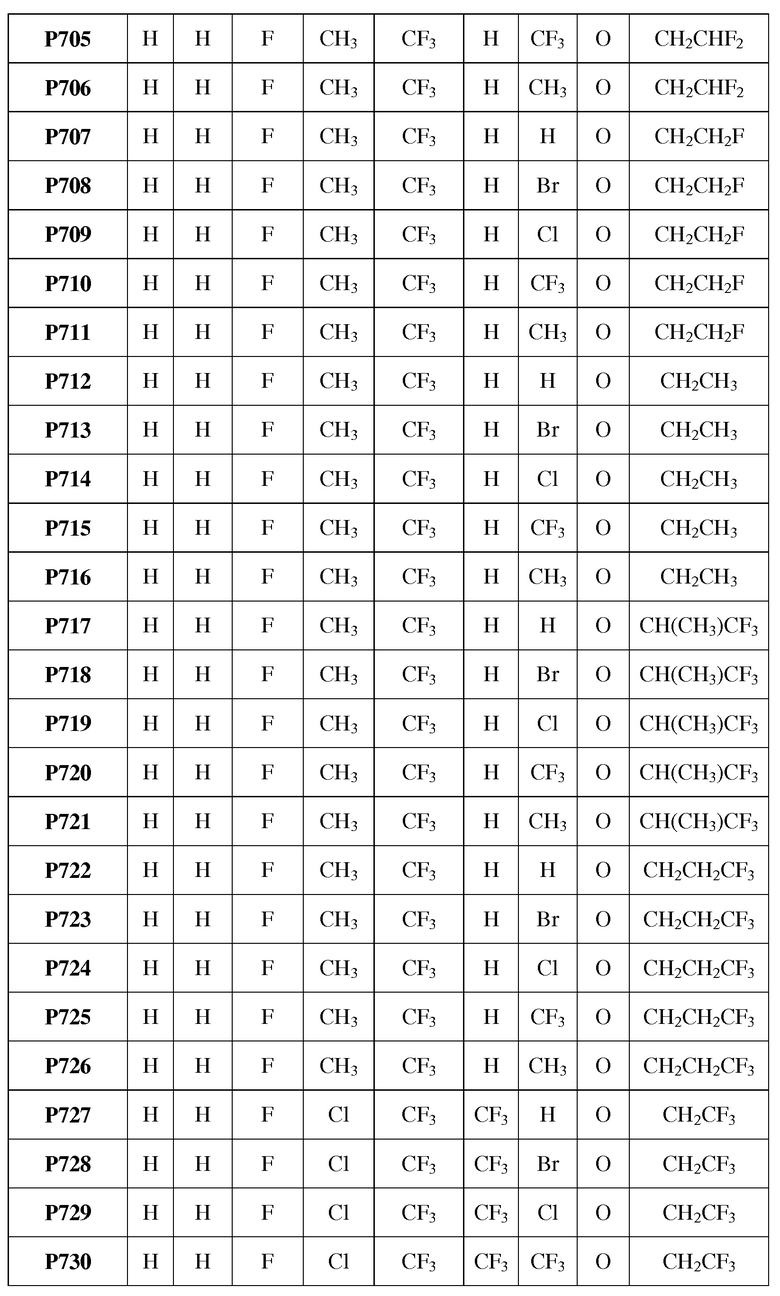
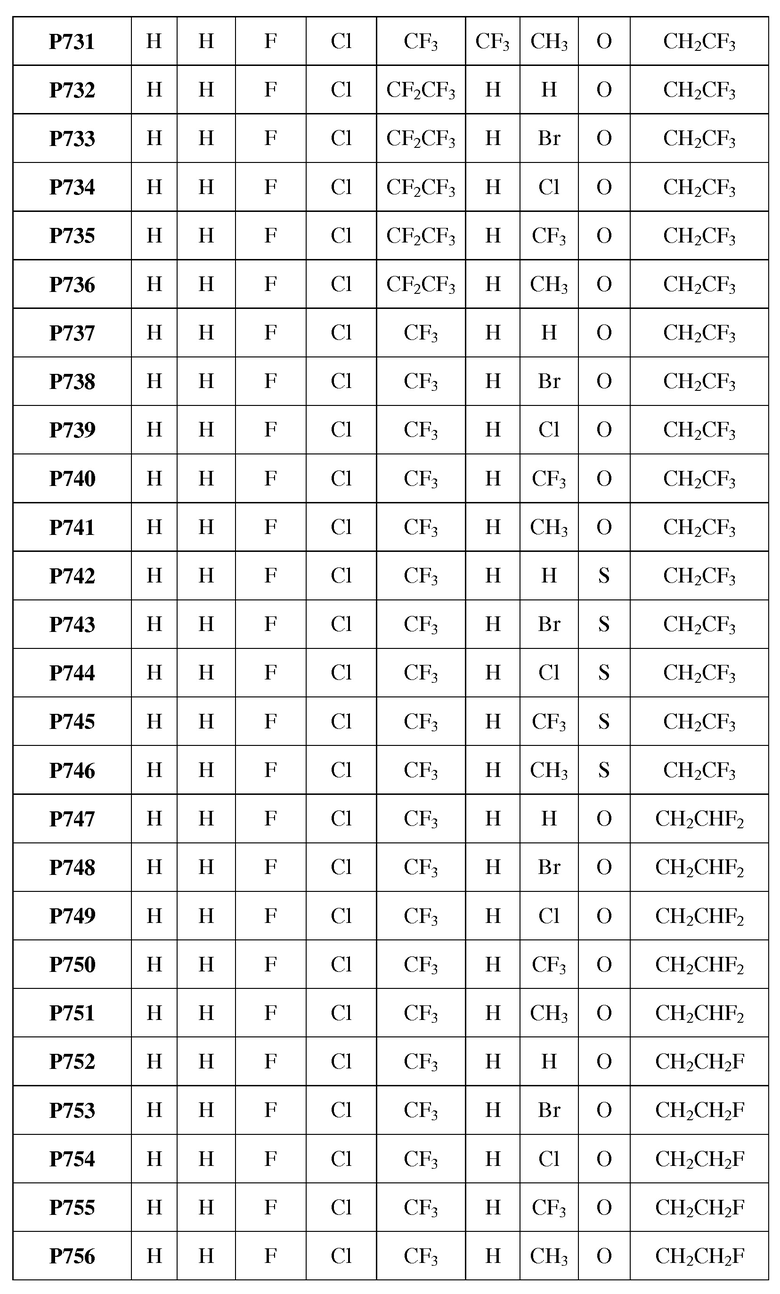
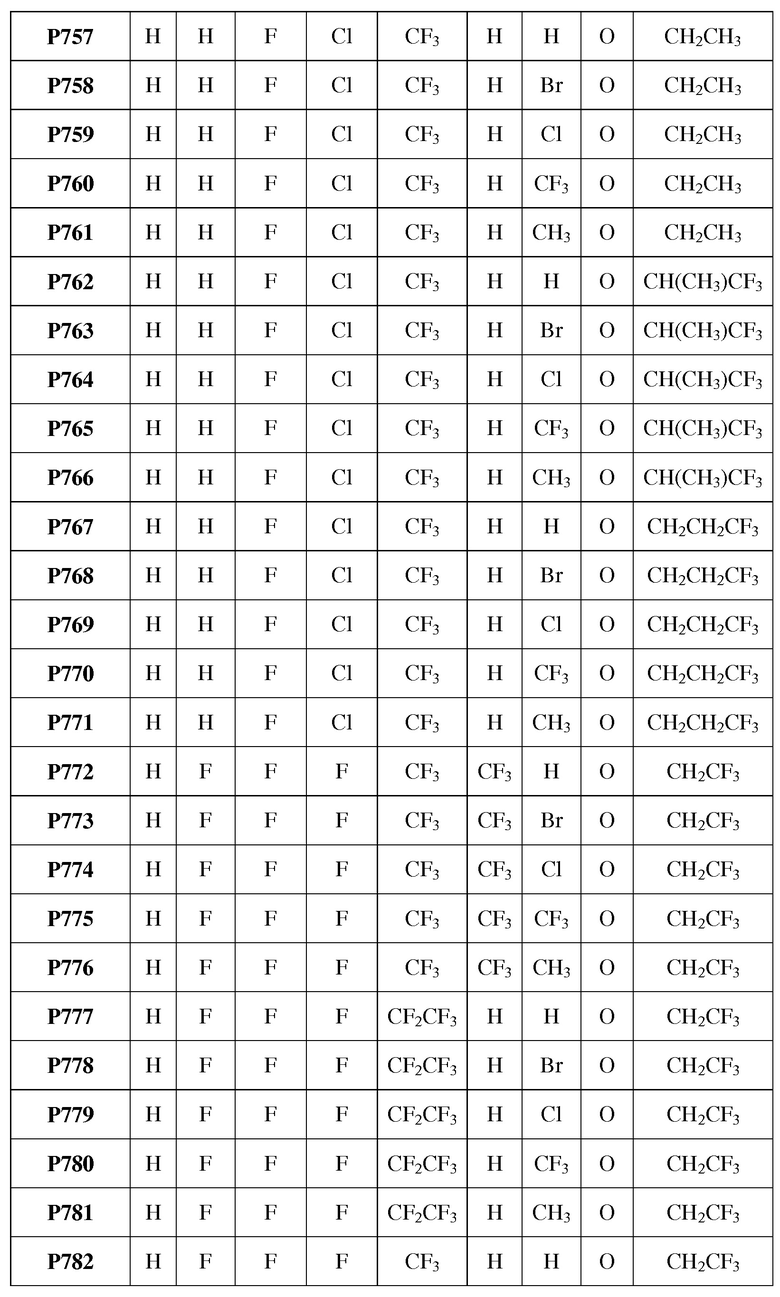
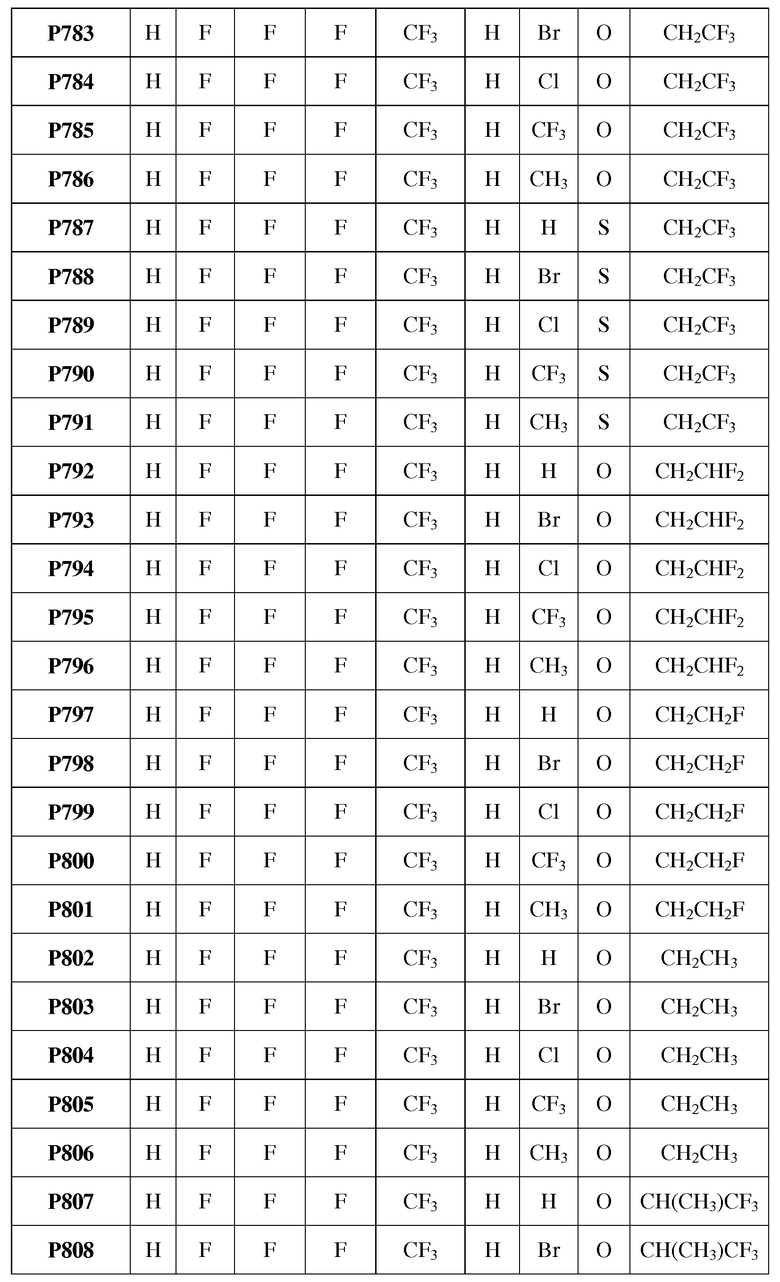
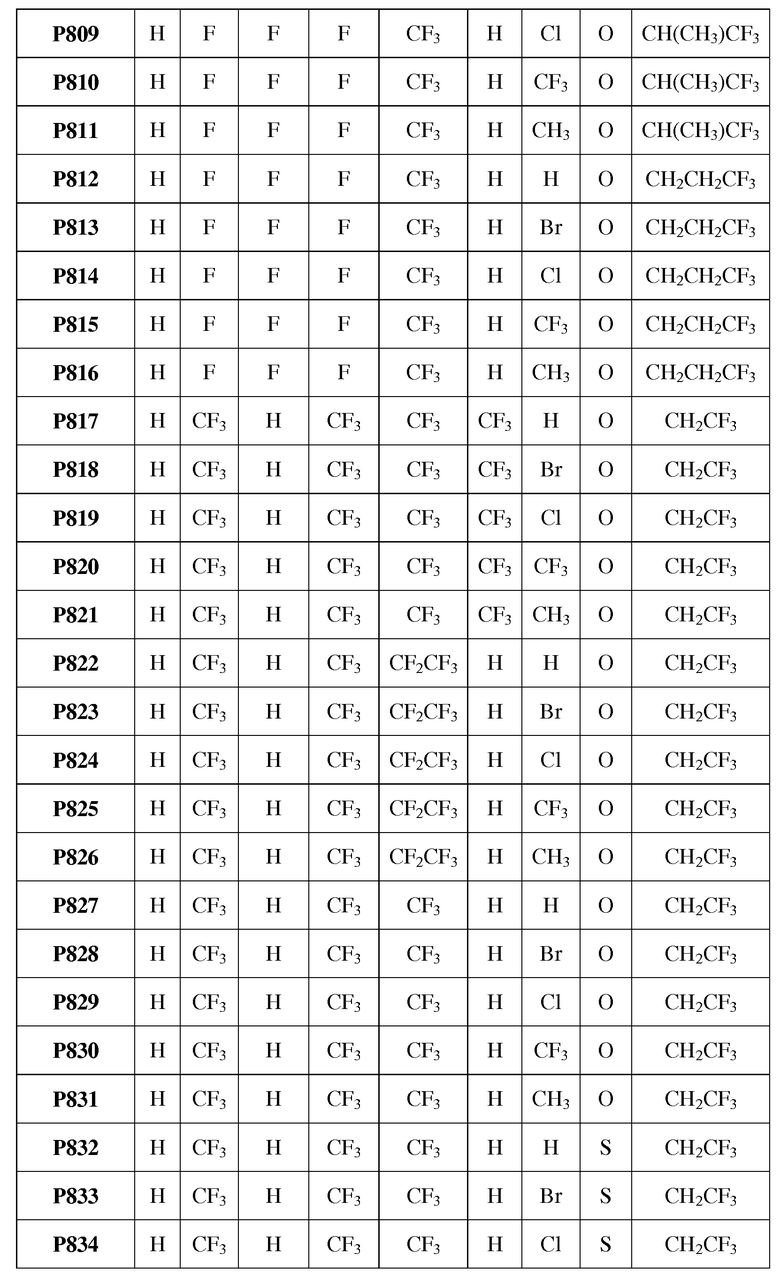
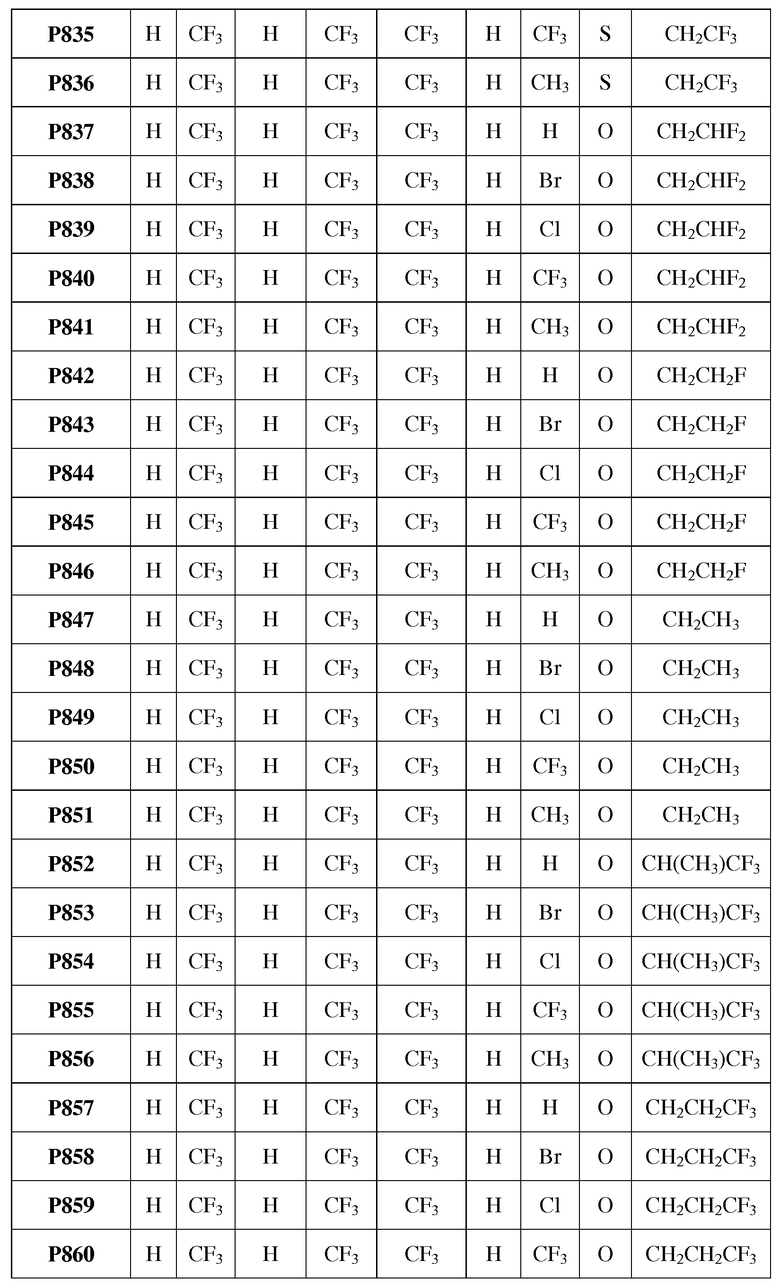
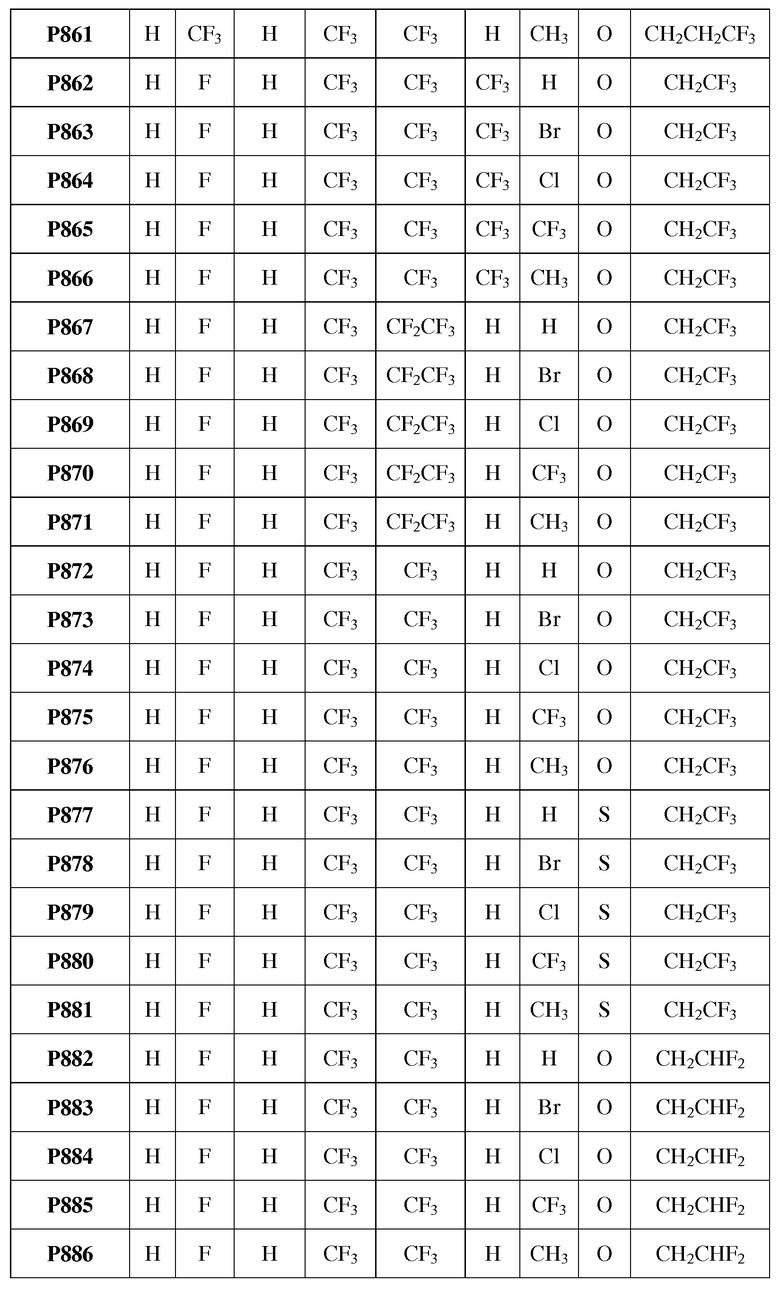
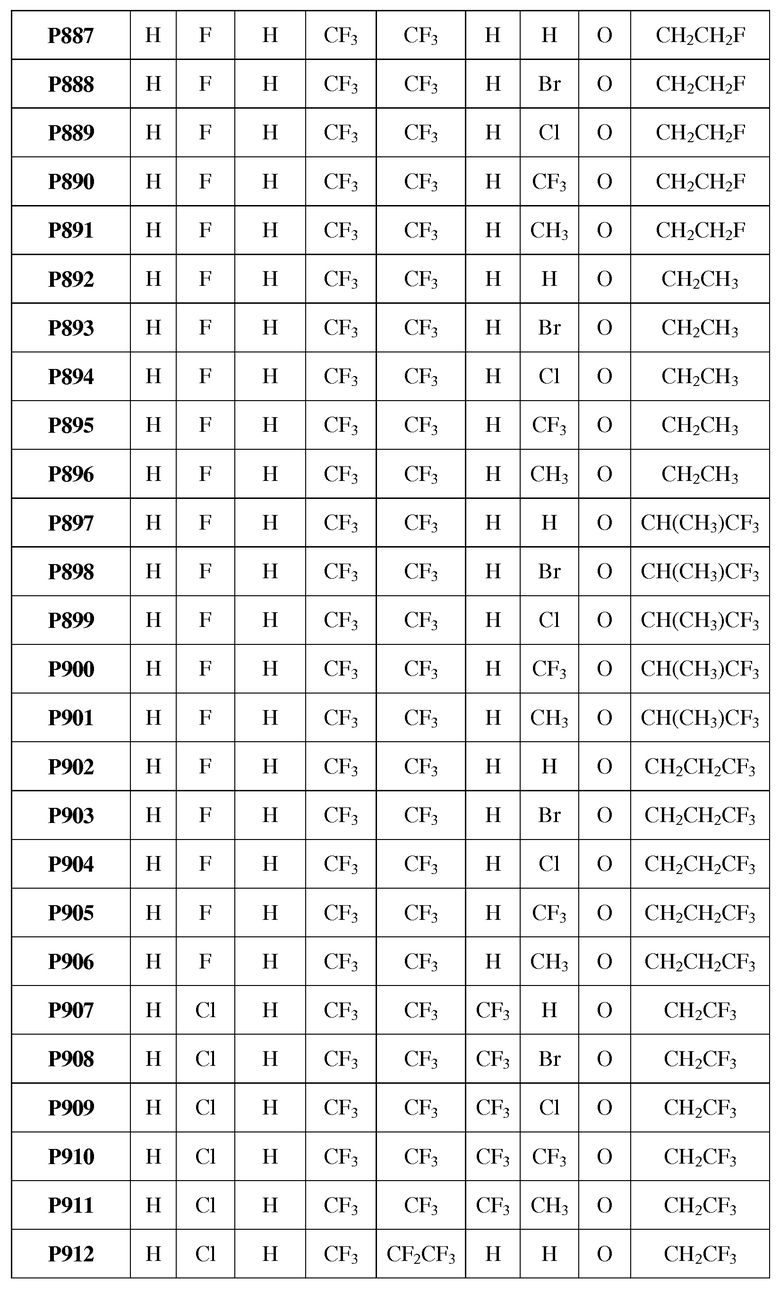
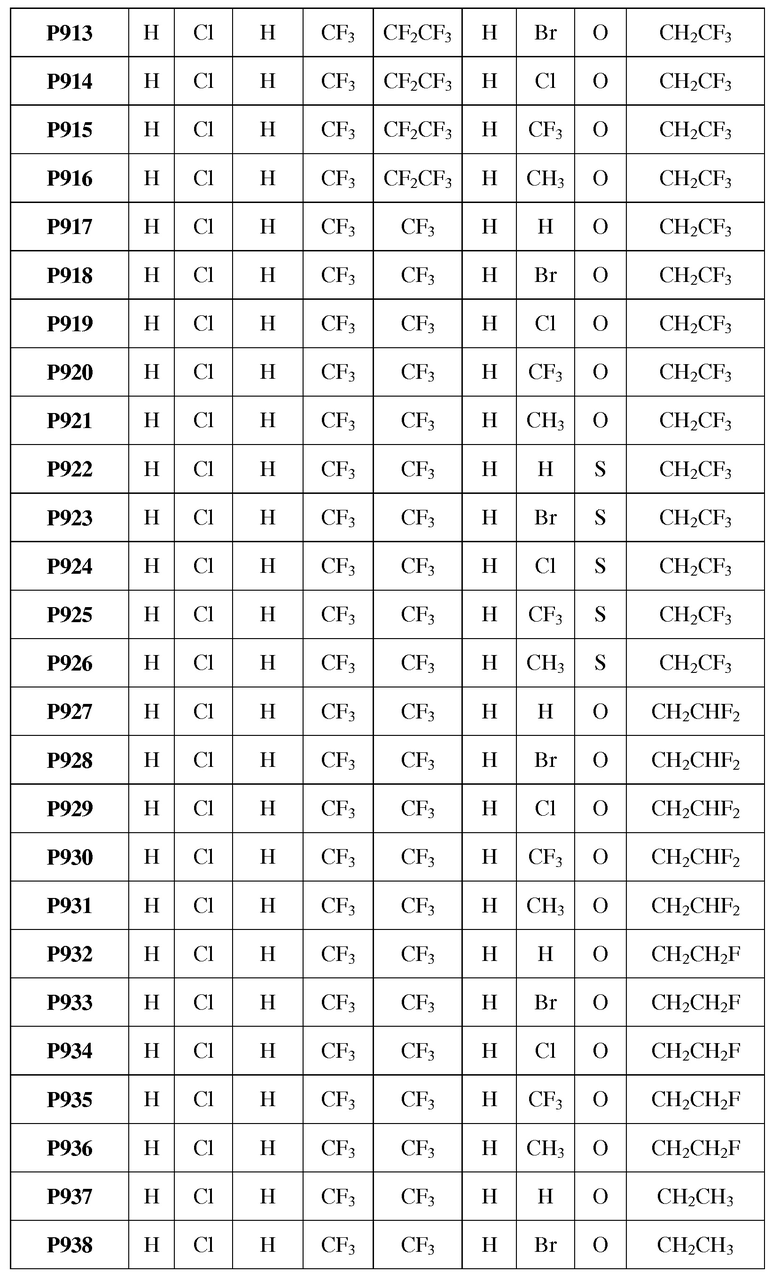
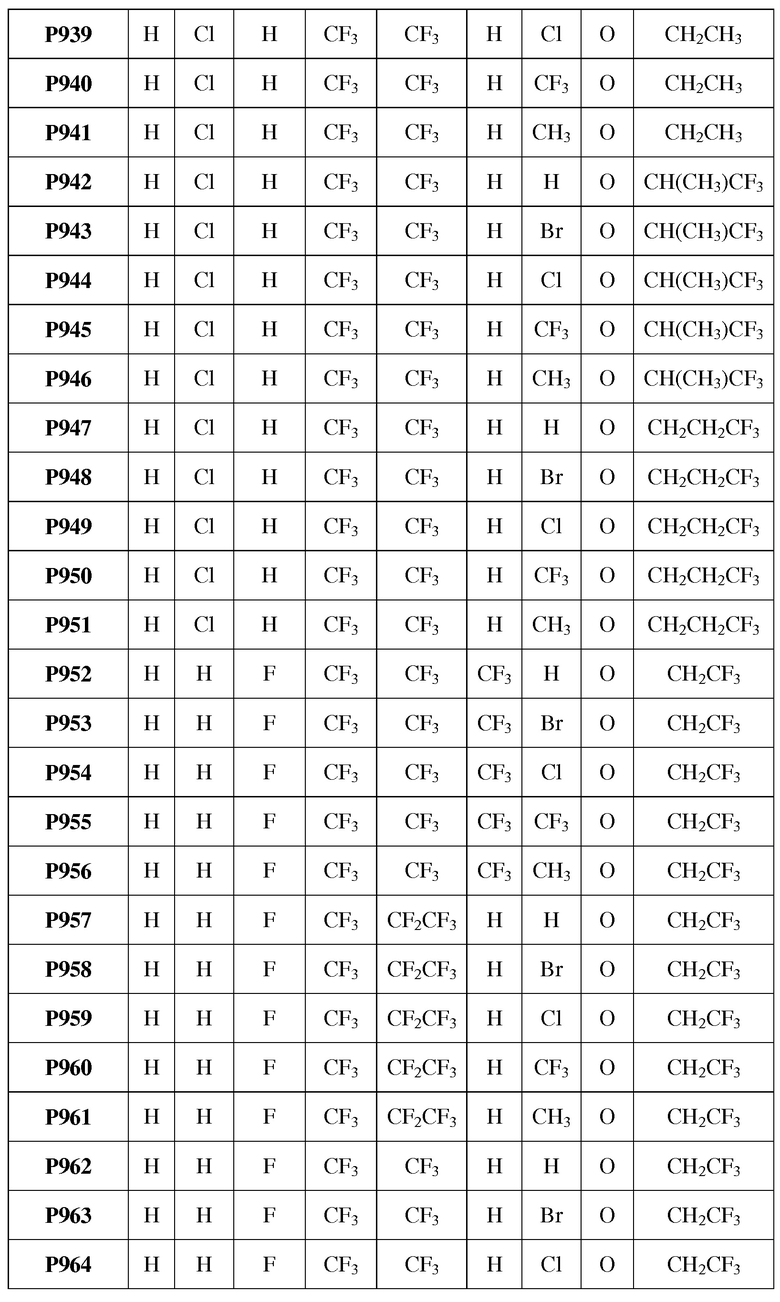
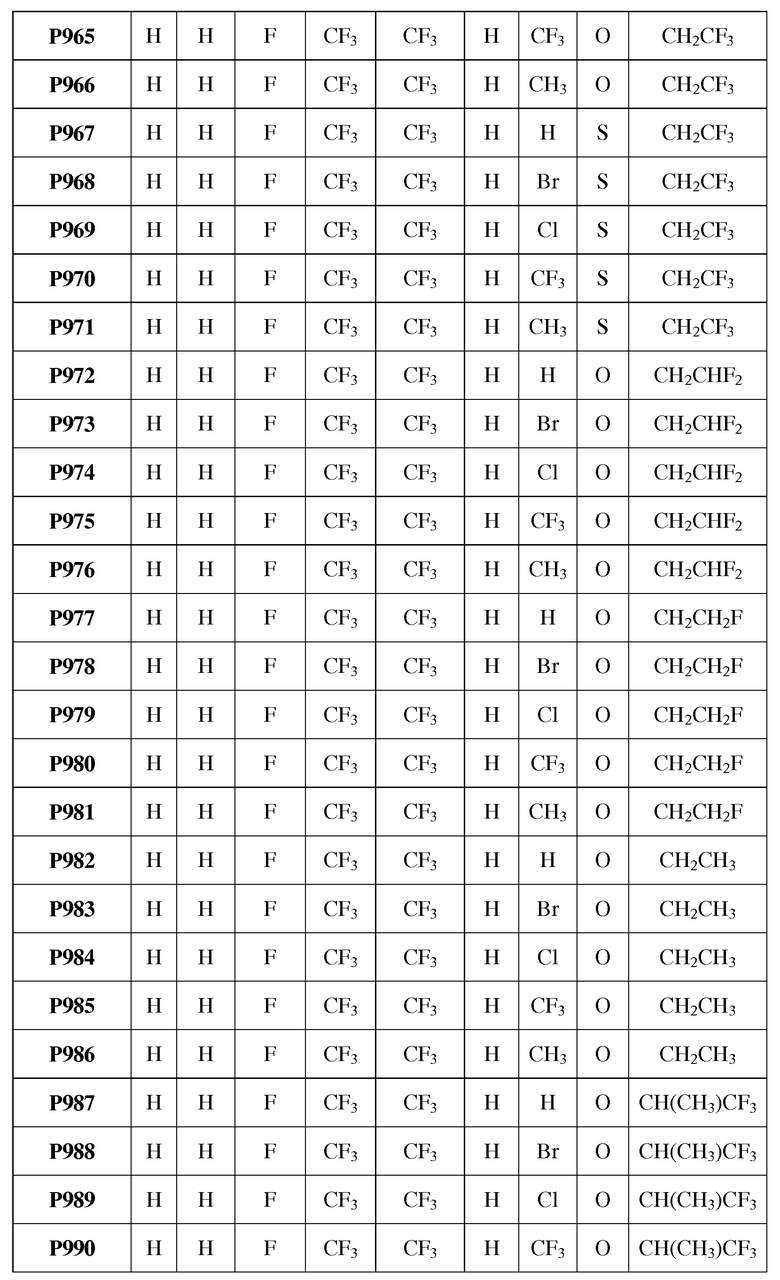
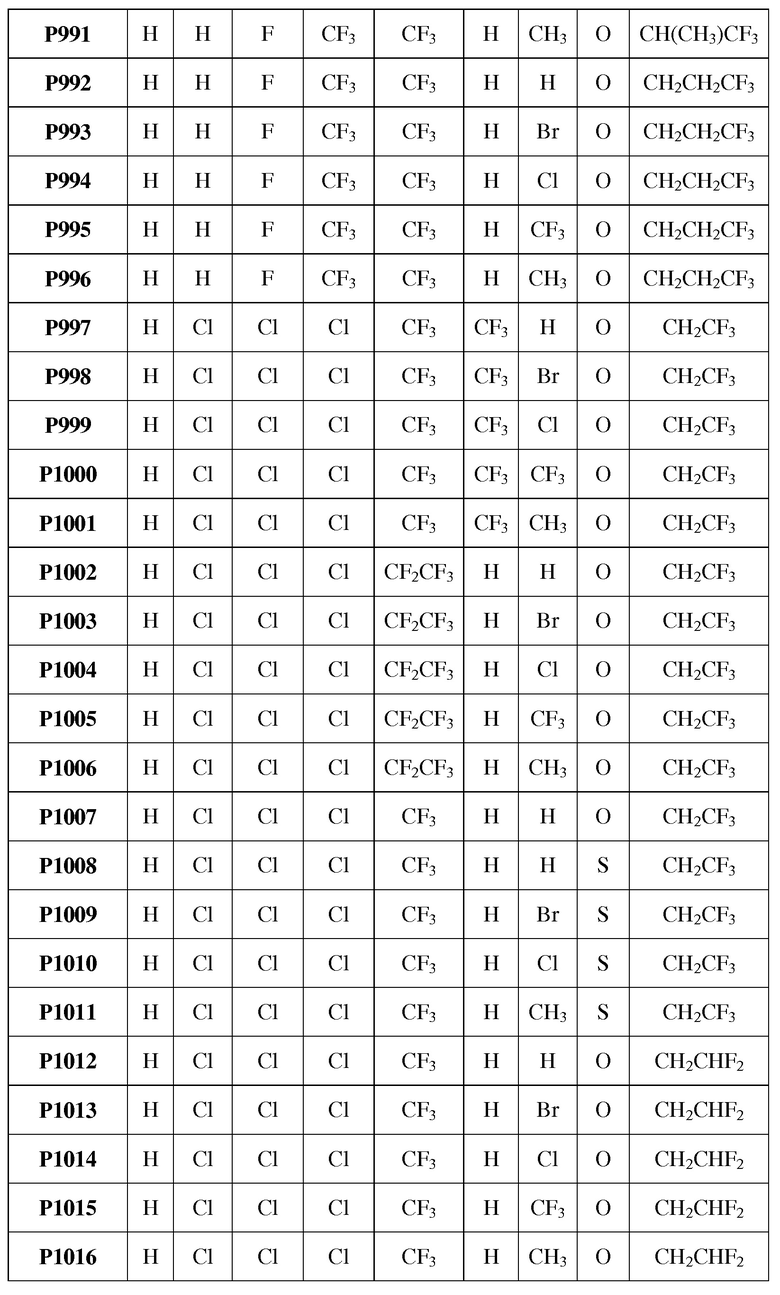
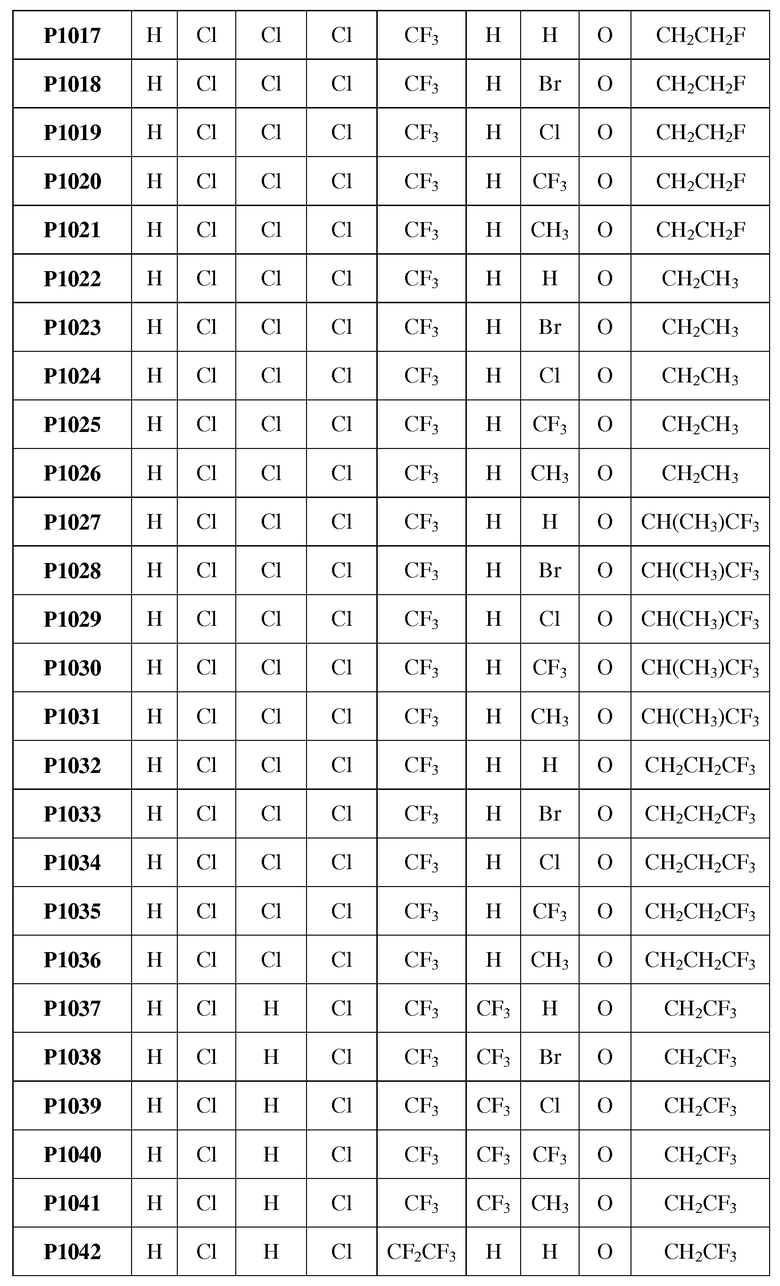
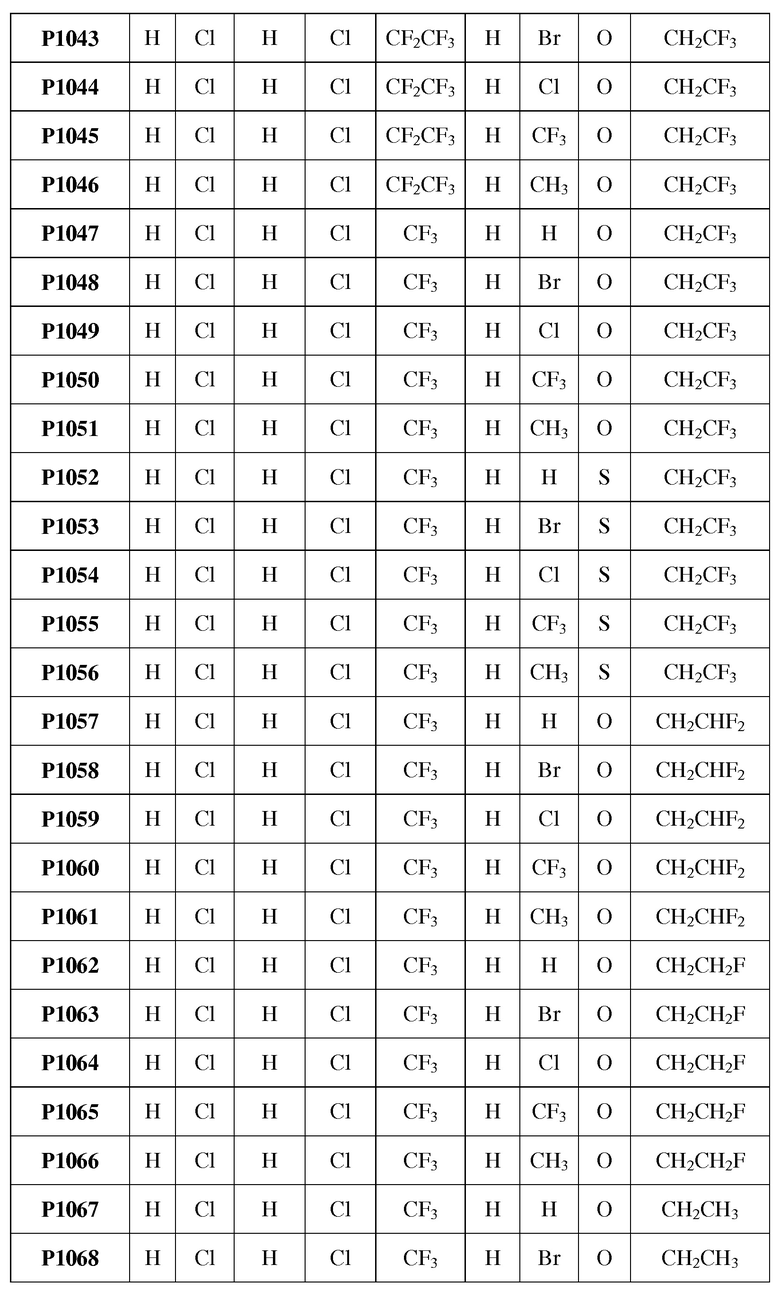
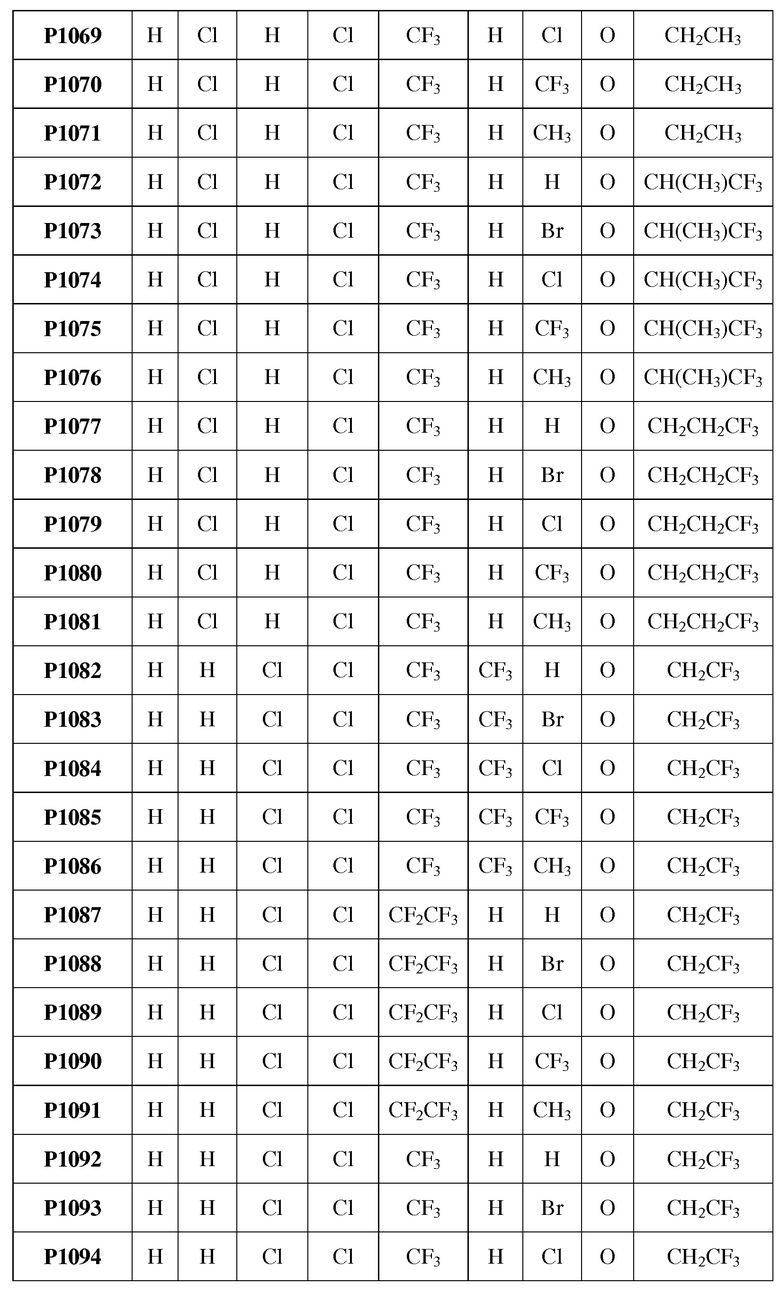
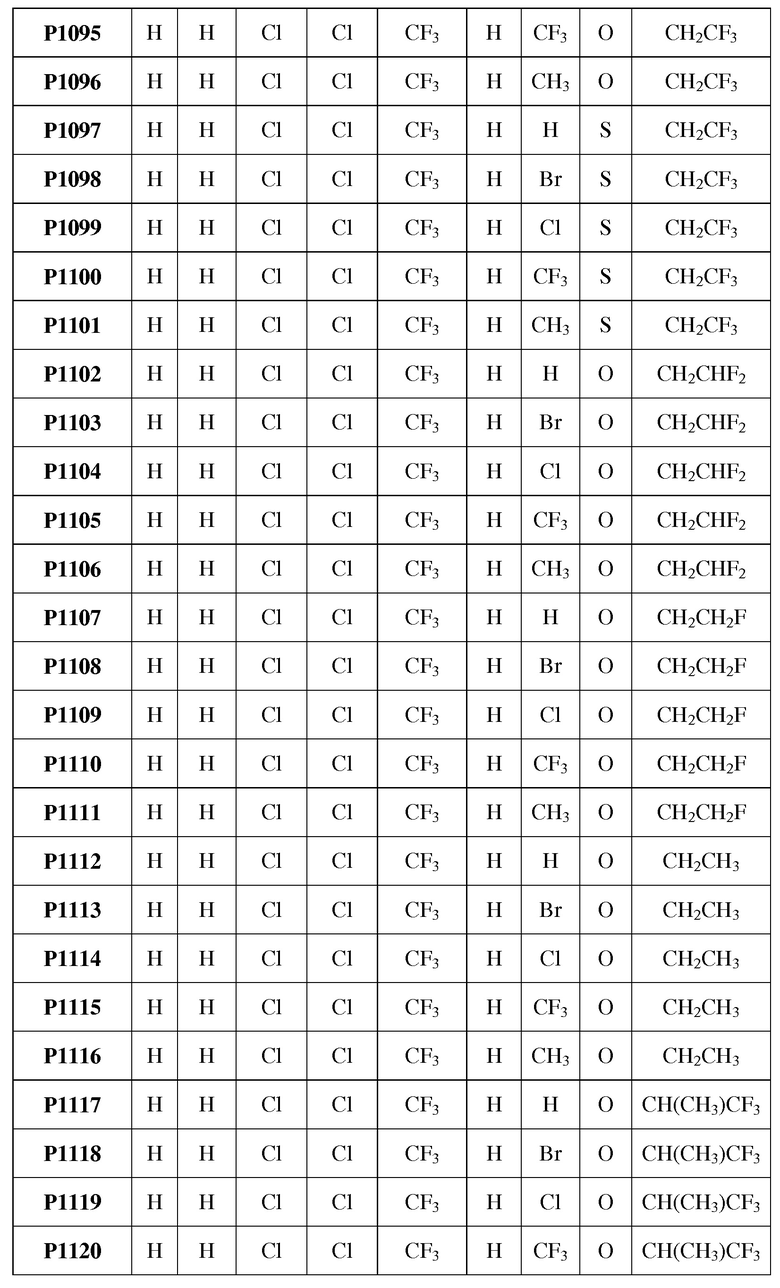

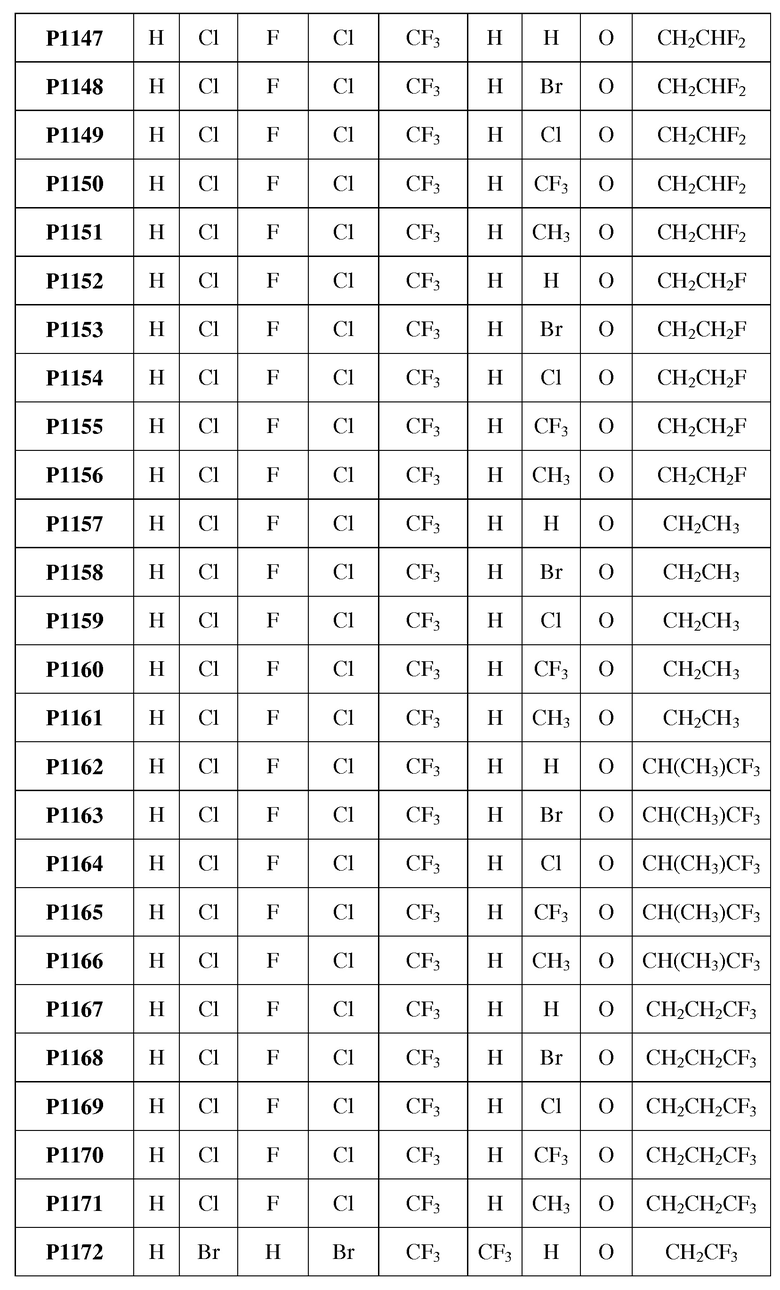
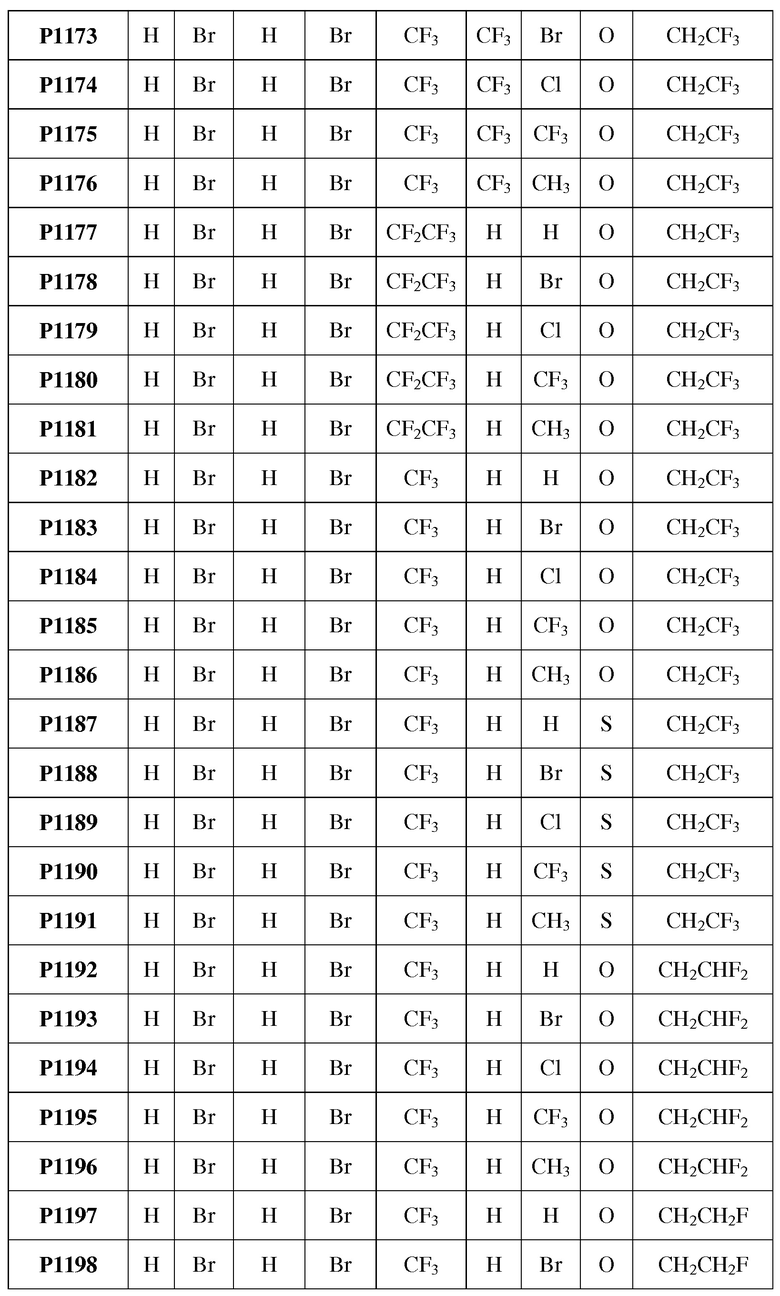
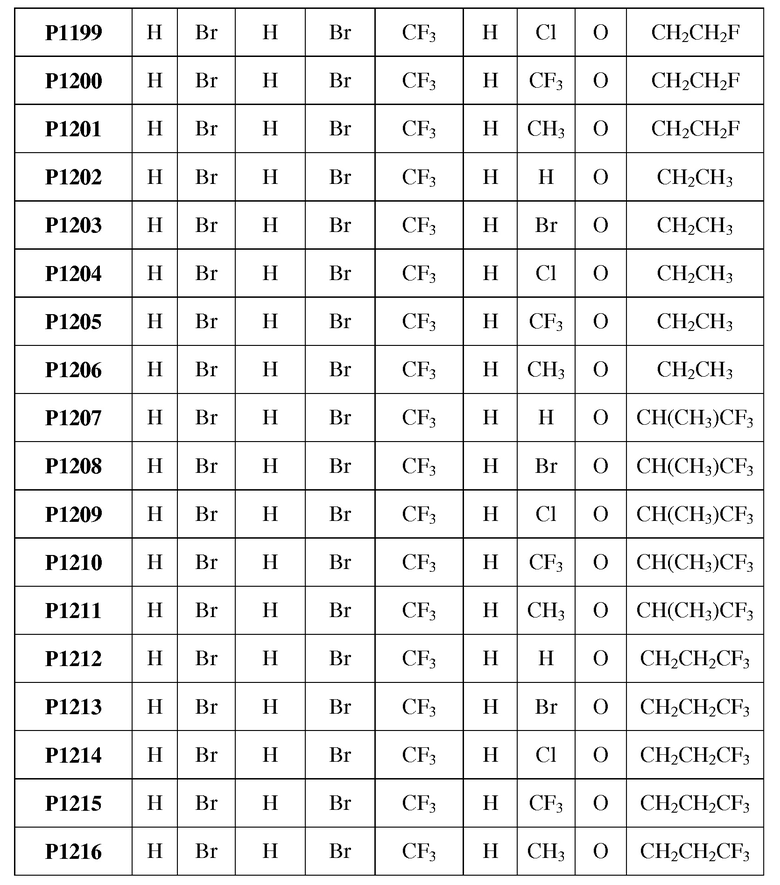
Пример A: Биотесты на совке малой (ʺСМʺ), хлопковой совке (ʺХСʺ) и металловидке серой (ʺМСʺ)
СМ имеет мало эффективных паразитов, болезней или хищников, которые снижают ее популяцию. СМ поражает многие сорняки, деревья, травы, бобовые и полевые культуры. В различных местах она вызывает экономические потери при выращивании спаржи, хлопка, кукурузы, сои, табака, люцерны, сахарной свеклы, перца, томатов, картофеля, лука, гороха, подсолнечника и цитрусовых, среди прочих растений. ХС, как известно, поражает кукурузу и томаты, но также она поражает артишок, спаржу, капусту, дыню канталупу, декоративную капусту, коровий горох, огурцы, баклажан, салат, фасоль луновидную, дыню, бамию, горох, перец, картофель, тыкву, зеленостручковую фасоль, шпинат, тыкву, батат и арбуз, среди прочих растений. ХС, как также известно, устойчива к некоторым инсектицидам. МС питается многими культурными растениями и сорняками. Она охотно питается на крестоцветных, при этом сообщали, что она поражает брокколи, капусту, цветную капусту, китайскую капусту, декоративную капусту, капусту кормовую, горчицу, редьку, брюкву, репу и кресс водяной. Другие поражаемые растительные культуры включают свеклу, канталупу, сельдерей, огурец, лимскую фасоль, салат, пастернак, горох, перец, картофель, зеленую фасоль, шпинат, тыкву, батат, томат и арбуз. МС, как также известно, устойчива к некоторым инсектицидам. Следовательно, с учетом вышеперечисленных факторов, важен контроль этих вредителей. Кроме того, молекулы, которые контролируют этих вредителей, могут применяться для борьбы с другими вредителями.
Некоторые молекулы, раскрытые в настоящем документе, тестировали против СМ, ХС и МС, используя методики, описанные в следующих примерах. При предоставлении результатов использовали Таблицу оценок СМ, ХС и МС (См. раздел Таблицы).
Биотесты на СМ (Spodoptera exigua)
Биотесты на СМ проводили, используя тест со 128-луночным кормовым лотком. Одну-пять личинок СМ второго возраста помещали в каждую лунку (3 мл) кормового лотка, который предварительно заполняли 1 мл искусственного корма, на который наносили 50 мкг/см2 тестируемого соединения (растворенного в 50 мкл смеси 90:10 ацетона-воды) (в каждую из восьми лунок), и затем оставляли для высыхания. Лотки накрывали прозрачной самоклеящейся мембраной и выдерживали при 25°C, в цикле 14:10 света-темноты, в течение пяти-семи дней. Процент летальности регистрировали для личинок в каждой лунке, затем активность в этих восьми лунках усредняли. Результаты представлены в таблицах, озаглавленных ʺТаблица 3: Результаты тестов Часть 1ʺ и ʺТаблица 4: Результаты тестов Часть 2ʺ (См. раздел Таблицы).
Биотесты на ХС (Helicoverpa zea)
Биотесты на ХС проводили, используя тест со 128-луночным кормовым лотком. Одну-пять личинок ХС второго возраста помещали в каждую лунку (3 мл) кормового лотка, который предварительно заполняли 1 мл искусственного корма, на который наносили 50 мкг/см2 тестируемого соединения (растворенного в 50 мкл смеси 90:10 ацетона-воды) (в каждую из восьми лунок) и затем оставляли для высыхания. Лотки накрывали прозрачной самоклеящейся мембраной и выдерживали при 25°C, в цикле 14:10 света-темноты, в течение пяти-семи дней. Процент летальности регистрировали для личинок в каждой лунке, активность в этих восьми лунках затем усредняли. Результаты представлены в таблице, озаглавленной ʺТаблица 3: Результаты тестов Часть 1ʺ (См. раздел Таблицы).
Биотесты на МС (Trichoplusia ni)
Биотесты на МС проводили, используя тест со 128-луночным кормовым лотком. Одну-пять личинок МС второго возраста помещали в каждую лунку (3 мл) кормового лотка, который предварительно заполняли 1 мл искусственного корма, на который наносили 50 мкг/см2 тестируемого соединения (растворенного в 50 мкл смеси 90:10 ацетона-воды) (в каждую из восьми лунок) и затем оставляли для высыхания. Лотки накрывали прозрачной самоклеящейся мембраной и выдерживали при 25°C, в цикле 14:10 света-темноты, в течение пяти-семи дней. Процент летальности регистрировали для личинок в каждой лунке, активность в этих восьми лунках затем усредняли. Результаты представлены в таблице, озаглавленной ʺТаблица 4: Результаты тестов Часть 2ʺ (См. раздел Таблицы).
Пример B: Биотесты на персиковой тле (ПТ) (Myzus persicae).
ПТ является наиболее значительным вредителем персика, вызывающим уменьшение роста, сморщивание листьев и гибель различных тканей. Она также опасна, поскольку она является переносчиком вирусов растений, таких как Y-вирус картофеля и вирус скручивания листьев картофеля, для представителей семейства паслена/картофеля Solanaceae, а также различных вирусов мозаики на многие другие пищевые культуры. ПТ поражает такие растения как брокколи, лопух, капусту, морковь, цветную капусту, дайкон, баклажан, зеленую фасоль, салат, макадамию, папайю, перец, батат, томат, кресс водяной и кабачок, среди прочих растений. ПТ также поражает многие декоративные культуры, такие как гвоздику, хризантему, декоративную капусту, пуансеттию и розы. У ПТ развилась устойчивость ко многим пестицидам.
Некоторые молекулы, раскрытые в настоящем документе, тестировали против ПТ, используя методики, описанные в следующем примере. При предоставлении результатов использовали Таблицу оценок ПТ (См. раздел Таблицы).
Рассаду капусты, выращенную в 3-дюймовых горшках, с 2-3 небольшими настоящими листьями (3-5 см) использовали в качестве субстрата для тестирования. Рассаду заражали 20-50 особями ПТ (бескрылые имаго и нимфы) за день до применения химиката. Четыре горшка с отдельной рассадой использовали для каждой обработки. Тестируемые соединения (2 мг) растворяли в 2 мл ацетона/метанола (1:1), получив стоковые растворы, содержащие 1000 м.д. тестируемых соединений. Стоковые растворы разбавляли 5× в 0,025% Tween 20 в H2O с получением раствора, содержащие 200 м.д. тестируемого соединения. Ручной разбрызгиватель аспираторного типа использовали для напыления раствора на обе стороны листьев капусты до стекания. На контрольные растения (проверка растворителем) распыляли только разбавитель, содержащий 20% по объему растворителя ацетона/метанола (1:1). Обработанные растения выдерживали в камере хранения в течение трех дней при температуре приблизительно 25°C и относительной влажности (RH) окружающего воздуха до сортировки. Оценку проводили путем подсчета количества живых тлей на растении под микроскопом. Процент контроля измеряли при использовании следующей поправочной формулы Аббота (W.S. Abbott, ʺA Method of Computing the Effectiveness of an Insecticideʺ, J. Econ. Entomol. 18 (1925), pp.265-267).
Скорректированный % контроля=100*(X-Y)/X
где
X=количество живых тлей на контрольных растениях и
Y=количество живых тлей на обработанных растениях
Результаты показаны в таблицах, озаглавленных ʺТаблица 3: Результаты тестовʺ и ʺТаблица 4: Результаты тестов Часть 2ʺ (См. раздел Таблицы).
ПЕСТИЦИДНО ПРИЕМЛЕМЫЕ СОЛИ ПРИСОЕДИНЕНИЯ КИСЛОТЫ, ПРОИЗВОДНЫЕ СОЛИ, СОЛЬВАТЫ, СЛОЖНОЭФИРНЫЕ ПРОИЗВОДНЫЕ, ПОЛИМОРФЫ, ИЗОТОПЫ И РАДИОНУКЛИДЫ
Молекулы Формулы один могут быть произведены в форме пестицидно приемлемых солей присоединения кислоты. В качестве неограничивающего примера, функциональная аминогруппа может образовывать соли с хлороводородной, бромоводородной, серной, фосфорной, уксусной, бензойной, лимонной, малоновой, салициловой, яблочной, фумаровой, щавелевой, янтарной, винной, молочной, глюконовой, аскорбиновой, малеиновой, аспарагиновой, бензолсульфоновой, метансульфоновой, этансульфоновой, гидрокси-метансульфоновой и гидроксиэтансульфоновой кислотами. Дополнительно, в качестве неограничивающего примера, кислотная функциональная группа может образовывать соли, включающие соли, полученные из щелочных или щелочноземельных металлов и полученные из аммиака и аминов. Примеры предпочтительных катионов включают натрий, калий и магний.
Молекулы Формулы один могут быть произведены в форме производных солей. В качестве неограничивающего примера, производная соль может быть получена при взаимодействии свободного основания и достаточного количества требуемой кислоты с получением соли. Свободное основание может быть регенерировано при обработке соли подходящим разбавленным водным раствором основания, таким как разбавленный водный раствор гидроксида натрия (NaOH), карбоната калия, аммиака и гидрокарбоната натрия. Например, во многих случаях пестициду, такому как 2,4-D, придают более высокую растворимость в воде, превращая его в соль диметиламина.
Молекулы Формулы один могут быть произведены в форме стабильных комплексов с растворителем, таких, что комплекс остается интактным после удаления растворителя, не включенного в комплекс. Такие комплексы часто называются ʺсольватамиʺ. Впрочем, особенно предпочтительно образование стабильных гидратов с водой в качестве растворителя.
Молекулы Формулы один могут быть превращены в сложноэфирные производные. Такие сложноэфирные производные могут затем применяться так же, как применяется изобретение, раскрытое в настоящем документе.
Молекулы Формулы один могут быть получены в виде различных кристаллических полиморфных форм. Полиморфизм важен при разработке агрохимикатов, поскольку различные кристаллические полиморфные формы или структуры одной и той же молекулы могут обладать совершенно разными физическими свойствами и биологической эффективностью.
Молекулы Формулы один могут быть получены с различными изотопами. Особое значение имеют молекулы, содержащие 2H (также известный как дейтерий) вместо 1H.
Молекулы Формулы один могут быть получены с различными радионуклидами. Особое значение имеют молекулы, содержащие 14C.
СТЕРЕОИЗОМЕРЫ
Молекулы Формулы один могут существовать в виде одного или более стереоизомеров. Таким образом, некоторые молекулы могут быть получены в виде рацемических смесей. Специалистам в данной области будет очевидно, что один стереоизомер может обладать более высокой активностью, чем другие стереоизомеры. Отдельные стереоизомеры могут быть получены при помощи известных методик селективного синтеза, при помощи стандартных методик синтеза с использованием разделенных исходных соединений или при помощи стандартных методик разделения. Некоторые молекулы, раскрытые в настоящем документе, могут существовать в виде двух или более изомеров. Различные изомеры включают геометрические изомеры, диастереомеры и энантиомеры. Таким образом, молекулы, раскрытые в настоящем документе, включают геометрические изомеры, рацемические смеси, отдельные стереоизомеры и оптически активные смеси. Специалистам в данной области будет очевидно, что один изомер может обладать более высокой активностью, чем другие. Структуры, раскрытые в настоящем описании, изображены в одной геометрической форме исключительно для ясности, но при этом предполагается, что они представляют все геометрические формы молекулы.
КОМБИНАЦИИ
Молекулы Формулы один могут также применяться в комбинации (например, в композиционной смеси или в одновременном или последовательном применении) с одним или более соединениями, обладающими акарицидной, альгицидной, авицидной, бактерицидной, фунгицидной, гербицидной, инсектицидной, моллюскоцидной, нематоцидной, родентицидной или вироцидной активностью. Кроме того, молекулы Формулы один также могут применяться в комбинации (например, в композиционной смеси или в одновременном или последовательном применении) с соединениями, которые являются антифидантами, репеллентами против птиц, хемостерилизаторами, гербицидными антидотами, аттрактантами для насекомых, репеллентами против насекомых, репеллентами против млекопитающих, соединениями, нарушающими спаривание, активаторами растений, регуляторами роста растений или синергическими соединениями. Примерами таких соединений в вышеуказанных группах, которые могут применяться совместно с молекулами Формулы один, являются: бромид (3-этоксипропил)ртути, 1,2-дихлорпропан, 1,3-дихлорпропен, 1-метилциклопропен, 1-нафтол, 2-(октилтио)этанол, 2,3,5-трийодбензойная кислота, 2,3,6-TBA, 2,3,6-TBA-диметиламмоний, 2,3,6-TBA-литий, 2,3,6-TBA-калий, 2,3,6-TBA-натрий, 2,4,5-T, 2,4,5-T-2-бутоксипропил, 2,4,5-T-2-этилгексил, 2,4,5-T-3-бутоксипропил, 2,4,5-TB, 2,4,5-T-бутометил, 2,4,5-T-бутотил, 2,4,5-T-бутил, 2,4,5-T-изобутил, 2,4,5-T-изоктил, 2,4,5-T-изопропил, 2,4,5-T-метил, 2,4,5-T-пентил, 2,4,5-T-натрий, 2,4,5-T-триэтиламмоний, 2,4,5-T-троламин, 2,4-D, 2,4-D-2-бутоксипропил, 2,4-D-2-этилгексил, 2,4-D-3-бутоксипропил, 2,4-D-аммоний, 2,4-DB, 2,4-DB-бутил, 2,4-DB-диметиламмоний, 2,4-DB-изоктил, 2,4-DB-калий, 2,4-DB-натрий, 2,4-DB-бутотил, 2,4-DB-бутил, 2,4-D-диэтиламмоний, 2,4-D-диметиламмоний, 2,4-D-диоламин, 2,4-D-додециламмоний, 2,4-DEB, 2,4-DEP, 2,4-D-этил, 2,4-D-гептиламмоний, 2,4-D-изобутил, 2,4-D-изоктил, 2,4-D-изопропил, 2,4-D-изопропиламмоний, 2,4-D-литий, 2,4-D-мептил, 2,4-D-метил, 2,4-D-октил, 2,4-D-пентил, 2,4-D-калий, 2,4-D-пропил, 2,4-D-натрий, 2,4-D-тефурил, 2,4-D-тетрадециламмоний, 2,4-D-триэтиламмоний, 2,4-D-трис(2-гидроксипропил)аммоний, 2,4-D-троламин, 2iP, хлорид 2-метоксиэтилртути, 2-фенилфенол, 3,4-DA, 3,4-DB, 3,4-DP, 4-аминопиридин, 4-CPA, 4-CPA-калий, 4-CPA-натрий, 4-CPB, 4-CPP, 4-гидроксифенэтиловый спирт, сульфат 8-гидроксихинолина, 8-фенилртутьоксихинолин, абамектин, абсцизовая кислота, ACC, ацефат, ацеквиноцил, ацетамиприд, ацетион, ацетохлор, ацетофос, ацетопрол, ацибензолар, ацибензолар-S-метил, ацифлуорфен, ацифлуорфен-метил, ацифлуорфен-натрий, аклонифен, акреп, акринатрин, акролеин, акрилонитрил, аципетакс, аципетакс-медь, аципетакс-цинк, алахлор, аланикарб, альбендазол, алдикарб, алдиморф, альдоксикарб, альдрин, аллетрин, аллицин, аллидохлор, аллосамидин, аллоксидим, аллоксидим-натрий, аллиловый спирт, алликсикарб, алорак, альфа-циперметрин, альфа-эндосульфан, аметокрадин, аметридион, аметрин, амибузин, амикарбазон, амикартиазол, амидитион, амидофлумет, амидосульфурон, аминокарб, аминоциклопирахлор, аминоциклопирахлор-метил, аминоцикло-пирахлор-калий, аминопиралид, аминопиралид-калий, аминопиралид-трис(2-гидроксипропил)аммоний, амипрофос-метил, амипрофос, амисульбром, амитон, амитон-оксалат, амитраз, амитрол, сульфамат аммония, альфа-нафталинацетат аммония, амобам, ампропилфос, анабазин, анцимидол, анилазин, анилофос, анисурон, антрахинон, анту, афолат, арамит, оксид мышьяка, асомат, аспирин, асулам, асулам-калий, асулам-натрий, атидатион, атратон, атразин, ауреофунгин, авиглицин, авиглицин-гидрохлорид, азаконазол, азадирахтин, азафенидин, азаметифос, азимсульфурон, азинфос-этил, азинфос-метил, азипротрин, азитирам, азобензол, азоциклотин, азотоат, азоксистробин, бахмедеш, барбан, гексафторсиликат бария, полисульфид бария, бартрин, BCPC, бефлубутамид, беналаксил, беналаксил-M, беназолин, беназолин- диметиламмоний, беназолин-этил, беназолин-калий, бенкарбазон, бенклотиаз, бендиокарб, бенфлуралин, бенфуракарб, бенфуресат, беноданил, беномил, беноксакор, беноксафос, бенквинокс, бенсульфурон, бенсульфурон-метил, бенсулид, бенсултап, бенталурон, бентазон, бентазон-натрий, бентиаваликарб, бентиаваликарб-изопропил, бентиазол, бентранил, бензадокс, бензадокс-аммоний, хлорид бензалкония, бензамакрил, бензамакрил-изобутил, бензаморф, бензфендизон, бензипрам, бензобициклон, бензофенап, бензофлуор, бензогидроксамовая кислота, бензоксимат, бензоилпроп, бензоилпроп-этил, бензтиазурон, бензилбензоат, бензиладенин, берберин, берберин-хлорид, бета-цифлутрин, бета-циперметрин, бетоксазин, бициклопирон, бифеназат, бифенокс, бифентрин, бифуцзиньши, биланафос, биланафос-натрий, бинапакрил, бинсингсиао, биоаллетрин, биоэтанометрин, биоперметрин, биоресметрин, бифенил, бисазир, бисмертиазол, биспирибак, биспирибак-натрий, бистрифлурон, битертанол, битионол, биксафен, бластицидин-S, бура, бордоская смесь, борная кислота, боскалид, брассинолид, брассинолид-этил, бревикомин, бродифакоум, брофенвалерат, брофлутринат, бромацил, бромацил-литий, бромацил-натрий, бромадиолон, брометалин, брометрин, брофенвинфос, бромацетамид, бромобонил, бромобутид, бромоциклен, бром-ДДТ, бромофеноксим, бромофос, бромофос-этил, бромпропилат, бромоталонил, бромоксинил, бромоксинил-бутират, бромоксинил-гептаноат, бромоксинил-октаноат, бромоксинил-калий, бромпиразон, бромуконазол, бронопол, букарполат, буфенкарб, буминафос, бупиримат, бупрофезин, бургундская смесь, бусульфан, бутакарб, бутахлор, бутафенацил, бутамифос, бутатиофос, бутенахлор, бутетрин, бутидазол, бутиобат, бутиурон, бутокарбоксим, бутонат, бутопироноксил, бутоксикарбоксим, бутралин, бутроксидим, бутурон, бутиламин, бутилат, какодиловая кислота, кадусафос, кафенстрол, арсенат кальция, хлорат кальция, цианамид кальция, полисульфид кальция, калвинфос, камбендихлор, камфехлор, камфора, каптафол, каптан, карбаморф, карбанолат, карбарил, карбасулам, карбендазим, карбендазим-бензолсульфонат, карбендазим-сульфит, карбетамид, карбофуран, сероуглерод, четыреххлористый углерод, карбофенотион, карбосульфан, карбоксазол, карбоксид, карбоксин, карфентразон, карфентразон-этил, карпропамид, картап, картап-гидрохлорид, карвакрол, карвон, CDEA, целлоцидин, CEPC, кералур, чешунтская смесь, хинометионат, хитозан, хлобентиазон, хлометоксифен, хлоралоз, хлорамбен, хлорамбен-аммоний, хлорабен-диоламин, хлорабен-метил, хлорабен-метиламмоний, хлорабен-натрий, хлорамин-фосфор, хлорамфеникол, хлораниформетан, хлоранил, хлоранокрил, хлорантранилипрол, хлоразифоп, хлоразифоп-пропаргил, хлоразин, хлорбенсид, хлорбензурон, хлорбициклен, хлорбромурон, хлорбуфам, хлордан, хлордекон, хлордимеформ, хлордимеформ-гидрохлорид, хлор-эмпентрин, хлоретоксифос, хлоретурон, хлорфенак, хлорфенак-аммоний, хлорфенак-натрий, хлорфенапир, хлорфеназол, хлорфенетол, хлорфенпроп, хлорфенсон, хлорфенсульфид, хлорфенвинфос, хлорфлуазурон, хлорфлуразол, хлорфлурен, хлорфлурен-метил, хлорфлуренол, хлорфлуренол-метил, хлоридазон, хлоримурон, хлоримурон-этил, хлормефос, хлормекват, хлормекват-хлорид, хлорнидин, хлорнитрофен, хлорбензилат, хлординитронафталины, хлороформ, хлоромебуформ, хлорметиурон, хлоронеб, хлорофацинон, хлорофацинон-натрий, хлорпикрин, хлоропон, хлорпропилат, хлороталонил, хлоротолурон, хлороксурон, хлороксинил, хлорфоний, хлорфоний-хлорид, хлорфоксим, хлорпразофос, хлорпрокарб, хлорпрофам, хлорпирифос, хлорпирифос-метил, хлорквинокс, хлорсульфурон, хлортал, хлортал-диметил, хлортал-монометил, хлортиамид, хлортиофос, хлозолинат, холин-хлорид, хромафенозид, цинерин I, цинерин II, цинерины, цинидон-этил, цинметилин, циносульфурон, циобутид, цисанилид, цисметрин, клетодим, климбазол, клиодинат, клодинафоп, клодинафоп-пропаргил, клоэтокарб, клофенцет, клофенцет-калий, клофентезин, клофибриновая кислота, клофоп, клофоп-изобутил, кломазон, кломепроп, клопроп, клопроксидим, клопиралид, клопиралид-метил, клопиралид-оламин, клопиралид-калий, клопиралид-трис(2-гидроксипропил)аммоний, клоквинтоцет, клоквинтоцет-мексил, клорансулам, клорансулам-метил, клозантел, клотианидин, клотримазол, клоксифонак, клоксифонак-натрий, CMA, кодлелур, колофонат, ацетат меди, ацетоарсенит меди, арсенат меди, карбонат меди основной, гидроксид меди, нафтенат меди, олеат меди, оксихлорид меди, силикат меди, сульфат меди, хромат меди-цинка, кумахлор, кумафурил, кумафос, куматетралил, кумитоат, кумоксистробин, CPMC, CPMF, CPPC, кредазин, крезол, кримидин, кротамитон, кротоксифос, круфомат, криолит, куелур, куфранеб, кумилурон, купробам, оксид меди, куркуменол, цианамид, цианатрин, цианазин, цианофенфос, цианофос, циантоат, циантранилипрол, циазофамид, цибутрин, циклафурамид, цикланилид, циклетрин, циклоат, циклогексимид, циклопрат, циклопротрин, циклосульфамурон, циклоксаприд, циклоксидим, циклурон, циенопирафен, цифлуфенамид, цифлуметофен, цифлутрин, цигалофоп, цигалофоп-бутил, цигалотрин, цигексатин, цимиазол, цимиазол-гидрохлорид, цимоксанил, циометринил, ципендазол, циперметрин, циперкват, циперкват-хлорид, цифенотрин, ципразин, ципразол, ципроконазол, ципродинил, ципрофурам, ципромид, ципросульфамид, циромазин, цитиоат, даимурон, далапон, далапон-кальций, далапон-магний, далапон-натрий, даминозид, даютонг, дазомет, дазомет-натрий, DBCP, d-камфора, DCIP, DCPTA, ДДТ, дебакарб, декафентин, декарбофуран, дегидроацетовая кислота, делахлор, дельтаметрин, демефион, демефион-O, демефион-S, деметон, деметон-метил, деметон-O, деметон-O-метил, деметон-S, деметон-S-метил, деметон-S-метилсульфон, десмедифам, десметрин, d-фаншилукуебинзуши, диафентиурон, диалифос, ди-аллат, диамидафос, диатомовая земля, диазинон, дибутилфталат, дибутилсукцинат, дикамба, дикамба-дигликольамин, дикамба-диметиламмоний, дикамба-диоламин, дикамба-изопропиламмоний, дикамба-метил, дикамба-оламин, дикамба-калий, дикамба-натрий, дикамба-троламин, дикаптон, дихлобенил, дихлофентион, дихлофлуанид, дихлон, дихлоральмочевина, дихлорбензурон, дихлорфлуренол, дихлорфлуренол-метил, дихлормат, дихлормид, дихлорфен, дихлорпроп, дихлорпроп-2-этилгексил, дихлорпроп-бутотил, дихлорпроп-диметиламмоний, дихлорпроп-этиламмоний, дихлорпроп-изоктил, дихлорпроп-метил, дихлорпроп-P, дихлорпроп-P-2-этилгексил, дихлорпроп-P-диметиламмоний, дихлорпроп-калий, дихлорпроп-натрий, дихлорвос, дихлозолин, дихлобутразол, диклоцимет, диклофоп, диклофоп-метил, дикломезин, дикломезин-натрий, диклоран, диклосулам, дикофол, дикумарол, дикрезил, дикротофос, дицикланил, дициклонон, дильдрин, диенохлор, диэтамкват, диэтамкват-дихлорид, диэтатил, диэтатил-этил, диэтофенкарб, диэтолат, диэтилпирокарбонат, диэтилтолуамид, дифенакум, дифеноконазол, дифенопентен, дифенопентен-этил, дифеноксурон, дифензокват, дифензокват-метилсульфат, дифетиалон, дифловидазин, дифлубензурон, дифлуфеникан, дифлуфензопир, дифлуфензопир-натрий, дифлуметорим, дикегулак, дикегулак-натрий, дилор, диматиф, димефлутрин, димефокс, димефурон, димепиперат, диметахлон, диметан, диметакарб, диметахлор, диметаметрин, диметенамид, диметенамид-P, диметипин, диметиримол, диметоат, диметоморф, диметрин, диметилкарбат, диметилфталат, диметилвинфос, диметилан, димексано, димидазон, димоксистробин, динекс, динекс-диклексин, динджунезуо, диниконазол, диниконазол-M, динитрамин, динобутан, динокап, динокап-4, динокап-6, диноктон, динофенат, динопентон, динопроп, диносам, диносеб, диносеб-ацетат, диносеб-аммоний, диносеб-диоламин, диносеб-натрий, диносеб-троламин, диносульфон, динотефуран, динотерб, динотерб-ацетат, динотербон, диофенолан, диоксабензофос, диоксакарб, диоксатион, дифацинон, дифацинон-натрий, дифенамид, бифенилсульфон, дифениламин, дипропалин, дипропетрин, дипиритион, дикват, дикват-дибромид, диспарлур, дисул, дисульфирам, дисульфотон, дисул-натрий, диталимфос, дитианон, дитикрофос, дитиоэфир, дитиопир, диурон, d-лимонен, DMPA, DNOC, DNOC-аммоний, DNOC-калий, DNOC-натрий, додеморф, додеморф-ацетат, додеморф-бензоат, додицин, додицин-гидрохлорид, додицин-натрий, додин, дофенапин, доминикалур, дорамектин, дразоксолон, DSMA, дуфулин, EBEP, EBP, экдистерон, эдифенфос, эглиназин, эглиназин-этил, эмамектин, эмамектин-бензоат, EMPC, эмпентрин, эндосульфан, эндотал, эндотал-диаммоний, эндотал-дикалий, эндотал-динатрий, эндотион, эндрин, энестробурин, EPN, эпохолеон, эпофенонан, эпоксиконазол, эприномектин, эпроназ, ЕРТС, эрбон, эргокальциферол, эрлуцзисианкаоан, эсдепаллетрин, эсфенвалерат, эспрокарб, этацеласил, этаконазол, этафос, этем, этабоксам, этахлор, эталфлуралин, этаметсульфурон, этаметсульфурон-метил, этапрохлор, этефон, этидимурон, этиофенкарб, этиолат, этион, этиозин, этипрол, этиримол, этоат-метил, этофумесат, этогексадиол, этопрофос, этоксифен, этоксифен-этил, этоксиквин, этоксисульфурон, этихлозат, этилформиат, этил-α-нафталинацетат, этил-DDD, этилен, дибромэтан, дихлорэтан, этиленоксид, этилицин, 2,3-дигидроксипропилмеркаптид этилртути, ацетат этилртути, бромид этилртути, хлорид этилртути, фосфат этилртути, этинофен, этнипромид, этобензанид, этофенпрокс, этоксазол, этридиазол, этримфос, эвгенол, EXD, фамоксадон, фамфур, фенамидон, фенаминосульф, фенамифос, фенапанил, фенаримол, фенасулам, феназафлор, феназаквин, фенбуконазол, фенбутатин-оксид, фенхлоразол, фенхлоразол-этил, фенхлорфос, фенклорим, фенетакарб, фенфлутрин, фенфурам, фенгексамид, фенитропан, фенитротион, фенджунтонг, фенобукарб, фенопроп, фенопроп-3-бутоксипропил, фенопроп-бутометил, фенопроп-бутотил, фенопроп-бутил, фенопроп-изоктил, фенопроп-метил, фенопроп-калий, фенотиокарб, феноксакрим, феноксанил, феноксапроп, феноксапроп-этил, феноксапроп-P, феноксапроп-Р-этил, феноксасульфон, феноксикарб, фенпиклонил, фенпиритрин, фенпропатрин, фенпропидин, фенпропиморф, фенпиразамин, фенпироксимат, фенридазон, фенридазон-калий, фенридазон-пропил, фенсон, фенсульфотион, фентеракол, фентиапроп, фентиапроп-этил, фентион, фентион-этил, фентин, фентин-ацетат, фентин-хлорид, фентин-гидроксид, фентразамид, фентрифанил, фенурон, фенурон-TCA, фенвалерат, фербам, феримзон, сульфат железа, фипронил, флампроп, флампроп-изопропил, флампроп-M, флампроп-метил, флампроп-M-изопропил, флампроп-М-метил, флазасульфурон, флокумафен, флометоквин, флоникамид, флорасулам, флуакрипирим, флуазифоп, флуазифоп-бутил, флуазифоп-метил, флуазифоп-P, флуазифоп-P-бутил, флуазинам, флуазолат, флуазурон, флубендиамид, флубензимин, флукарбазон, флукарбазон-натрий, флуцетосульфурон, флухлоралин, флукофурон, фуциклоксурон, флуцитринат, флудиоксонил, флуенетил, флуенсульфон, флуфенацет, флуфенерим, флуфеникан, флуфеноксурон, флуфенпрокс, флуфенпир, флуфенпир-этил, флуфипрол, флуметрин, флуметовер, флуметралин, флуметсулам, флумезин, флумиклорак, флумиклорак-пентил, флумиоксазин, флумипропин, флуморф, флуометурон, флуопиколид, флуопирам, флуорбенсид, флуоридамид, флуороацетамид, флуородифен, флуорогликофен, флуорогликофен-этил, флуороимид, флуоромидин, флуоронитрофен, флуотиурон, флуотримазол, флуоксастробин, флупоксам, флупропацил, флупропадин, флупропанат, флупропанат-натрий, флупирадифурон, флупирсульфурон, флупирсульфурон-метил, флупирсульфурон-метил-натрий, флуквинконазол, флуразол, флуренол, флуренол-бутил, флуренол-метил, флуридон, флурохлоридон, флуроксипир, флуроксипир-бутометил, флуроксипир-мептил, флурпримидол, флурсуламид, флуртамон, флусилазол, флусульфамид, флутиацет, флутиацет-метил, флутианил, флутоланил, флутриафол, флувалинат, флуксапироксад, флуксофеним, фолпет, фомезафен, фомезафен-натрий, фонофос, форамсульфурон, форхлорфенурон, формальдегид, форметанат, форметанат-гидрохлорид, формотион, формпаранат, формпаранат-гидрохлорид, фосамин, фосамин-аммоний, фосетил, фосетил-алюминий, фосметилан, фоспират, фостиазат, фостиетан, фронталин, фуберидазол, фукаоджинг, фукаоми, фунаигекаолинг, фуфентиомочевина, фуралан, фуралаксил, фураметрин, фураметпир, фуратиокарб, фуркарбанил, фурконазол, фурконазол-цис, фуретрин, фурфурол, фурилазол, фурмециклокс, фурофанат, фурилоксифен, гамма-цигалотрин, гамма-HCH, генит, гибберелиновая кислота, гиббереллины, глифтор, глуфосинат, глуфосинат-аммоний, глуфосинат-P, глуфосинат-P-аммоний, глуфосинат-P-натрий, глиодин, глиоксим, глифосат, глифосат-диаммоний, глифосат-диметиламмоний, глифосат-изопропиламмоний, глифосат-моноаммоний, глифосат-калий, глифосат-сесквинатрий, глифосат-тримезиум, глифосин, госсиплур, грандлур, гризеофульвин, гуазатин, гуазатин-ацетаты, галакринат, галфенпрокс, галофенозид, галосафен, галосульфурон, галосульфурон-метил, галоксидин, галоксифоп, галоксифоп-этотил, галоксифоп-метил, галоксифоп-P, галоксифоп-P-этотил, галоксифоп-P-метил, галоксифоп-натрий, НСН, гемел, гемпа, HEOD, гептахлор, гептенофос, гептопаргил, гетерофос, гексахлорацетон, гексахлорбензол, гексахлорбутадиен, гексахлорофен, гексаконазол, гексафлумурон, гексафлурат, гексалур, гексамид, гексазинон, гексилтиофос, гекситиазокс, HHDN, голосульф, хуанкайво, хуангкаолинг, хуанцзунзуо, гидраметилнон, гидраргафен, гашеная известь, синильная кислота, гидропрен, гимексазол, гиквинкарб, IAA, IBA, икаридин, имазалил, имазалил-нитрат, имазалил-сульфат, имазаметабенз, имазаметабенз-метил, имазамокс, имазамокс-аммоний, имазапик, имазапик-аммоний, имазапир, имазапир-изопропиламмоний, имазаквин, имазаквин-аммоний, имазаквин-метил, имазаквин-натрий, имазетапир, имазетапир-аммоний, имазосульфурон, имибенконазол, имициафос, имидаклоприд, имидаклотиз, иминоктадин, иминоктадин-триацетат, иминоктадин-триалбезилат, имипротрин, инабенфид, инданофан, индазифлам, индоксакарб, инезин, иодобонил, иодокарб, иодметан, иодосульфурон, иодосульфурон-метил, иодосульфурон-метил-натрий, йофенсульфурон, йофенсульфурон-натрий, иоксинил, иоксинил-октаноат, иоксинил-литий, иоксинил-натрий, ипазин, ипконазол, ипфенкарбазон, ипробенфос, ипродион, ипроваликарб, ипримидам, ипсдиенол, ипсенол, IPSP, изамидофос, исазофос, изобензан, изокарбамид, изокарбофос, изоцил, изодрин, изофенфос, изофенфос-метил, исолан, изометиозин, изонорурон, изополинат, изопрокарб, изопропалин, изопротиолан, изопротурон, изопиразам, изопиримол, изотиоат, изотианил, изоурон, изоваледион, изоксабен, изоксахлортол, изоксадифен, изоксадифен-этил, изоксафлутол, изоксапирифоп, изоксатион, ивермектин, изопамфос, японилур, япотринс, жасмолин I, жасмолин II, жасмоновая кислота, жиахуангчонгзонг, чжациценгсиаолинг, чжасиангчинжи, чжиекаован, чжиекаоси, жодфенфос, ювенильный гормон I, ювенильный гормон II, ювенильный гормон III, кадетрин, карбутилат, каретазан, каретазан-калий, касугамицин, касугамицин-гидрохлорид, кеджунлин, кевелан, кетоспирадокс, кетоспирадок-калий, кинетин, кинопрен, крезоксим-метил, куикаоси, лактофен, лямбда-цигалотрин, латилур, арсенат свинца, ленацил, лепимектин, лептофос, линдан, линеатин, линурон, лиримфос, литлур, луплур, луфенурон, людинджинши, люсинкаолин, литидатион, MAA, малатион, малеиновый гидразид, малонобен, мальтодекстрин, МАМА, манкоппер, манкозеб, мандипропамид, манеб, матрин, мазидокс, MCPA , MCPA-2-этилгексил, MCPA-бутотил, MCPA-бутил, MCPA-диметиламмоний, MCPA-диоламин, MCPA-этил, MCPA-изобутил, MCPA-изоктил, MCPA-изопропил, MCPA-метил, MCPA-оламин, MCPA-калий, MCPA-натрий, MCPA-тиоэтил, MCPA-троламин, MCPB, MCPB-этил, MCPB-метил, MCPB-натрий, мебенил, мекарбам, мекарбинзид, мекарфон, мекопроп, мекопроп-2-этилгексил, мекопроп-диметиламмоний, мекопроп-диоламин, мекопроп-этадил, мекопроп-изоктил, мекопроп-метил, мекопроп-P, мекопроп-P-2-этилгексил, мекопроп-P-диметиламмоний, мекопроп-P-изобутил, мекопроп-калий, мекопроп-P-калий, мекопроп-натрий, мекопроп-троламин, медимеформ, мединотерб, мединотерб-ацетат, медлур, мефенацет, мефенпир, мефенпир-диэтил, мефлуидид, мефлуидид-диоламин, мефлуидид-калий, мегатомовая кислота, меназон, мепанипирим, меперфлутрин, мефенат, мефосфолан, мепикват, мепикват-хлорид, мепикват-пентаборат, мепронил, мептилдинокап, дихлорид ртути, оксид ртути, хлорид ртути, мерфос, мезопразин, мезосульфурон, мезосульфурон-метил, мезотрион, месульфен, месульфенфос, метафлумизон, металаксил, металаксил-M, метальдегид, метам, метам-аммоний, метамифоп, метамитрон, метам-калий, метам-натрий, метазахлор, метазосульфурон, метазоксолон, метконазол, метепа, метфлуразон, метабензтиазурон, метакрифос, металпропалин, метамидофос, метасульфокарб, метазол, метфуроксам, метидатион, метиобенкарб, метиокарб, метиопирисульфурон, метиотепа, метиозолин, метиурон, метокротофос, метометон, метомил, метопрен, метопротрин, метоквин-бутил, метотрин, метоксихлор, метоксифенозид, метоксифенон, метил-афолат, метилбромид, метил-эвгенол, метилиодид, метилизотиоцианат, метилацетофос, метилхлороформ, метилдимрон, метиленхлорид, бензоат метилртути, дициандиамид метилртути, пентахлорфеноксид метилртути, метилнеодеканамид, метирам, метобензурон, метобромурон, метофлутрин, метолахлор, метолкарб, метоминостробин, метосулам, метоксадиазон, метоксурон, метрафенон, метрибузин, метсульфовакс, метсульфурон, метсульфурон-метил, мевинфос, мексакарбат, миешуан, милбемектин, милбемицин-оксим, милнеб, мипафокс, мирекс, MNAF, могучун, молинат, молосультап, моналид, монисоурон, монохлоруксусная кислота, монокротофос, монолинурон, моносульфурон, моносульфурон-эфир, монурон, монурон-TCA, морфамкват, морфамкват-дихлорид, мороксидин, мороксидин-гидрохлорид, морфотион, морзид, моксидектин, MSMA, мускалур, миклобутанил, миклозолин, N-(этилртуть)-п-толуолсульфонанилид, набам, нафталофос, налед, нафталин, нафталинацетамид, нафталевый ангидрид, нафтоксиуксусные кислоты, напроанилид, напропамид, напталам, напталам-натрий, натамицин, небурон, никлозамид, никлозамид-оламин, никосульфурон, никотин, нифлуридид, нипираклофен, нитенпирам, нитиазин, нитралин, нитрапирин, нитрилакарб, нитрофен, нитрофлуорфен, нитростирол, нитротал-изопропил, норбормид, норфлуразон, норникотин, норурон, новалурон, новифлумурон, нуаримол, OCH, октахлородипропиловый эфир, октилинон, офурас, ометоат, орбенкарб, орфралур, орто-дихлорбензол, ортосульфамурон, орикталур, орисастробин, оризалин, остол, острамон, оксабетринил, оксадиаргил, оксадиазон, оксадиксил, оксамат, оксамил, оксапиразон, оксапиразон-димоламин, оксапиразон-натрий, оксасульфурон, оксазикломефон, оксин-медь, оксолиновая кислота, окспоконазол, окспоконазол-фумарат, оксикарбоксин, оксидеметон-метил, оксидепрофос, оксидисульфотон, оксифлуорфен, оксиматрин, окситетрациклин, окситетрациклин-гидрохлорид, паклобутразол, пайхонгдинг, пара-дихлорбензол, парафлурон, паракват, паракват-дихлорид, паракват-диметилсульфат, паратион, паратион-метил, паринол, пебулат, пефуразоат, пеларгоновая кислота, пенконазол, пенцикурон, пендиметалин, пенфлуфен, пенфлурон, пенокссулам, пентахлорфенол, пентахлор, пентиопирад, пентметрин, пентоксазон, перфлуидон, перметрин, петоксамид, фенамакрил, феназин-оксид, фенисофам, фенкаптон, фенмедифам, фенмедифам-этил, фенобензурон, фенотрин, фенпроксид, фентоат, фенилртуть-мочевина, ацетат фенилртути, хлорид фенилртути, фенилртутное производное пирокатехина, нитрат фенилртути, салицилат фенилртути, форат, фосацетим, фозалон, фосдифен, фосфолан, фосфолан-метил, фосглицин, фосмет, фоснихлор, фосфамидон, фосфин, фосфокарб, фосфор, фостин, фоксим, фоксим-метил, фталид, пиклорам, пиклорам-2-этилгексил, пиклорам-изоктил, пиклорам-метил, пиклорам-оламин, пиклорам-калий, пиклорам-триэтиламмоний, пиклорам-трис(2-гидроксипропил)аммоний, пиколинафен, пикоксистробин, пиндон, пиндон-натрий, пиноксаден, пипералин, пиперонилбутоксид, пиперонил-циклонен, пиперофос, пипроктанил, пипроктанил-бромид, пипротал, пириметафос, пиримикарб, пиримиоксифос, пиримифос-этил, пиримифос-метил, плифенат, поликарбамат, полиоксины, полиоксорим, полиоксорим-цинк, политиалан, арсенит калия, азид калия, цианат калия, гиббереллат калия, нафтенат калия, полисульфид калия, тиоцианат калия, альфа-нафталинацетат калия, пп'-ДДТ, праллетрин, прекоцен I, прекоцен II, прекоцен III, претилахлор, примидофос, примисульфурон, примисульфурон-метил, пробеназол, прохлораз, прохлораз-марганец, проклонол, проциазин, процимидон, продиамин, профенофос, профлуазол, профлуралин, профлутрин, профоксидим, проглиназин, проглиназин-этил, прогексадион, прогексадион-кальций, прогидрожасмон, промацил, промекарб, прометон, прометрин, промурит, пропахлор, пропамидин, пропамидин-дигидрохлорид, пропамокарб, пропамокарб-гидрохлорид, пропанил, пропафос, пропаквизафоп, пропаргит, пропартрин, пропазин, пропетамфос, профам, пропиконазол, пропинеб, прописохлор, пропоксур, пропоксикарбазон, пропоксикарбазон-натрий, пропил-исом, пропирисульфурон, пропизамид, проквиназид, просулер, просульфалин, просульфокарб, просульфурон, протидатион, протиокарб, протиокарб-гидрохлорид, протиоконазол, протиофос, протоат, протрифенбут, проксан, проксан-натрий, принахлор, пиданон, пиметрозин, пиракарболид, пираклофос, пираклонил, пираклостробин, пирафлуфен, пирафлуфен-этил, пирафлупрол, пирамат, пираметостробин, пираоксистробин, пирасульфотол, пиразолинат, пиразофос, пиразосульфурон, пиразосульфурон-этил, пиразотион, пиразоксифен, пиресметрин, пиретрин I, пиретрин II, пиретрины, пирибамбенз-изопропил, пирибамбенз-пропил, пирибенкарб, пирибензоксим, пирибутикарб, пириклор, пиридабен, пирадафол, пиридалил, пиридафентион, пиридат, пиридинитрил, пирифенокс, пирифлуквиназон, пирифталид, пириметанил, пиримидифен, пириминобак, пириминобак-метил, пиримисульфан, пиримитат, пиринурон, пириофенон, пирипрол, пирипропанол, пирипроксифен, пиритиобак, пиритиобак-натрий, пиролан, пироквилон, пироксасульфон, пироксулам, пироксихлор, пироксифур, кассия, квинацетол, квинацетол-сульфат, квиналфос, квиналфос-метил, квиназамид, квинклорак, квинконазол, квинмерак, квинокламин, квинонамид, квинотион, квиноксифен, квинтиофос, квинтозен, хизалофоп, хизалофоп-этил, хизалофоп-P , хизалофоп-Р-этил, хизалофоп-P-тефурил, чивенжи, куингдинг, рабензазол, рафоксанид, ребемид, ресметрин, родетанил, родояпонин-III, рибавирин, римсульфурон, ротенон, рианиа, сафлуфенацил, саижунмао, саисентонг, салициланилид, сангвинарин, сантонин, шрадан, сциллиросид, себутилазин, секбуметон, седаксан, селамектин, семиамитраз, семиамитраз-хлорид, сесамекс, сезамолин, сетоксидим, шуангжиаанкаолин, сидурон, сиглур, силафлуофен, силатран, силикагель, силтиофам, симазин, симеконазол, семетон, симетрин, синтофен, SMA, S-метолахлор, арсенит натрия, азид натрия, хлорат натрия, фторид натрия, фторацетат натрия, гексафторсиликат натрия, нафтенат натрия, ортофенилфеноксид натрия, пентахлорфеноксид натрия, полисульфид натрия, тиоцианат натрия, α-нафталинацетат натрия, софамид, спинеторам, спиносад, спиродиклофен, спиромесифен, спиротетрамат, спироксамин, стрептомицин, стрептомицин-сесквисульфат, стрихнин, сулькатол, сулькофурон, сулькофурон-натрий, сулькотрион, сульфаллат, сульфентразон, сульфирам, сульфурамид, сульфометурон, сульфометурон-метил, сульфосульфурон, сульфотеп, сульфоксафлор, сульфоксид, сульфоксим, сера, серная кислота, сульфурилфторид, сульгликапин, сульпрофос, сультропен, свеп, тау-флувалинат, таврон, тазимкарб, TCA, TCA-аммоний, ТСА-кальций, TCA-этадил, ТСА-магний, TCA-натрий, TDE, тебуконазол, тебуфенозид, тебуфенпирад, тебуфлоквин, тебупиримфос, тебутам, тебутиурон, теклофталам, текназен, текорам, тефлубензурон, тефлутрин, тефурилтрион, темботрион, темефос, тепа, ТЕРР, тепралоксидим, тераллетрин, тербацил, тербукарб, тербухлор, тербуфос, тербуметон, тербутилазин, тербутрин, тетциклацис, тетрахлорэтан, тетрахлорвинфос, тетраконазол, тетрадифон, тетрафлурон, тетраметрин, тетраметилфлутрин, тетрамин, тетранактин, тетрасул, сульфат таллия, тенилхлор, тета-циперметрин, тиабендазол, тиаклоприд, тиадифтор, тиаметоксам, тиапронил, тиазафлурон, тиазопир, тикрофос, тициофен, тидиазимин, тидиазурон, тиенкарбазон, тиенкарбазон-метил, тифенсульфурон, тифенсульфурон-метил, тифлузамид, тиобенкарб, тиокарбоксим, тиохлорфенфим, тиоциклам, тиоциклам-гидрохлорид, тиоциклам-оксалат, тиадиазол-медь, тиодикарб, тиофанокс, тиофлуоксимат, тиогемпа, тиомерсал, тиометон, тионазин, тиофанат, тиофанат-метил, тиоквинокс, тиосемикарбазид, тиосультап, тиосультап-диаммоний, тиосультап-динатрий, тиосультап-натрий, тиотепа, тирам, турингиенсин, тиадинил, тиаоджиеан, тиокарбазил, тиоклорим, тиоксимид, тирпат, толклофос-метил, толфенпирад, толилфлуанид, ацетат толилртути, топрамезон, тралкоксидим, тралоцитрин, тралометрин, тралопирил, трансфлутрин, трансперметрин, третамин, триаконтанол, триадимефон, триадименол, триафамон, три-аллат, триамифос, триапентенол, триаратен, триаримол, триасульфурон, триазамат, триазбутил, триазифлам, триазофос, триазоксид, трибенурон, трибенурон-метил, трибуфос, оксид трибутилолова, трикамба, трихламид, трихлорфон, трихлорметафос-3, трихлоронат, триклопир, триклопир-бутотил, триклопир-этил, триклопир-триэтиламмоний, трициклазол, тридеморф, тридифан, триэтазин, трифенморф, трифенофос, трифлоксистробин, трифлоксисульфурон, трифлоксисульфурон-натрий, трифлумизол, трифлумурон, трифлуралин, трифлусульфурон, трифлусульфурон-метил, трифоп, трифоп-метил, трифопсим, трифорин, тригидрокситриазин, тримедлур, триметакарб, триметурон, тринексапак, тринексапак-этил, трипрен, трипропиндан, триптолид, тритак, тритиконазол, тритосульфурон, транк-колл, униконазол, униконазол-P, урбацид, уредепа, валерат, валидамицин, валифеналат, валон, вамидотион, вангард, ванилипрол, вернолат, винклозолин, варфарин, варфарин-калий, варфарин-натрий, сиаочонглиулин, синчжунан, сивочжунан, XMC, ксилахлор, ксиленолы, ксилилкарб, йишичжинг, зариламид, зеатин, зенгсиаоан, зета-циперметрин, нафтенат цинка, фосфид цинка, тиазол-цинк, цинеб, цирам, золапрофос, зоксамид, зомиханглонг, α-хлоргидрин, α-экдизон, α-мултистриатин и α-нафталинуксусная кислота. Для получения дополнительной информации см. ʺCompendium of Pesticide Common Namesʺ по адресу в интернете http://www.alanwood.net/pesticides/index.html. Также см. руководство ʺThe Pesticide Manualʺ 14th Edition, edited by C D S Tomlin, copyright 2006 by British Crop Production Council, или его более ранние или более поздние издания.
БИОПЕСТИЦИДЫ
Молекулы Формулы Один могут также применяться в комбинации (например, в композиционной смеси или в одновременном или последовательном применении) с одним или более биопестицидами. Термин ʺбиопестицидʺ используется в отношении средств для борьбы с вредителями, которые применяют тем же способом, что и химические пестициды. Обычно они являются бактериальными, но имеются также примеры грибковых средств для борьбы с вредителями, включающих Trichoderma spp. и Ampelomyces quisqualis (средство для борьбы с виноградной мучнистой росой). Bacillus subtilis используют для борьбы с патогенами растений. Сорняки и грызуны также уничтожают с помощью микробиологических средств. Одним хорошо известным примером инсектицида является Bacillus thuringiensis, вызывающая бактериальное заболевание у Lepidoptera, Coleoptera и Diptera. Из-за своего слабого действия на другие организмы, ее считают более экологически безопасной, чем синтетические пестициды. Биологические инсектициды включают продукты на основе:
1. энтомопатогенных грибов (например, Metarhizium anisopliae);
2. энтомопатогенных нематод (например, Steinernema feltiae); и
3. энтомопатогенных вирусов (например, грануловируса Cydia pomonella).
Другие примеры энтомопатогенных организмов включают, без ограничения перечисленными, бакуловирусы, бактерии и другие прокариотические организмы, грибы, простейшие и микроспроридии. Инсектициды биологического происхождения включают, без ограничения перечисленными, ротенон, вератридин, а также микробиологические токсины; толерантные или устойчивые к насекомым-вредителям сорта растений; и организмы, модифицированные с помощью генной инженерии либо для получения инсектицидов, либо придания генетически модифицированному организму свойства устойчивости к насекомому-вредителю. В одном варианте осуществления молекулы Формулы один могут применяться с одним или несколькими биопестицидами в области обработки семян и улучшения почв. The Manual of Biocontrol Agents дает обзор доступных биологических инсектицидов (и других продуктов для контроля вредителей на биологической основе). Copping L.G. (ed.) (2004). The Manual of Biocontrol Agents (formerly the Biopesticide Manual) 3rd Edition. British Crop Production Council (BCPC), Farnham, Surrey UK.
ДРУГИЕ АКТИВНЫЕ СОЕДИНЕНИЯ
Молекулы Формулы Один также могут применяться в комбинации (например, в композиционной смеси или в одновременном или последовательном применении) с одним или более следующими соединениями:
1. 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-окса-1-азаспи-ро[4,5]дец-3-ен-2-он;
2. 3-(4'-хлор-2,4-диметил[1,1'-дифенил]-3-ил)-4-гидрокси-8-окса-1-азаспиро[4.5]дец-3-ен-2-он;
3. 4-[[(6-хлор-3-пиридинил)метил]метиламино]-2(5H)-фуранон;
4. 4-[[(6-хлор-3-пиридинил)метил]циклопропиламино]-2(5H)-фуранон;
5. 3-хлор-N2-[(1S)-1-метил-2-(метилсульфонил)этил]-N1-[2-метил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]фенил]-1,2-бензолдикарбоксамид;
6. 2-циано-N-этил-4-фтор-3-метокси-бензолсульфонамид;
7. 2-циано-N-этил-3-метокси-бензолсульфонамид;
8. 2-циано-3-дифторметокси-N-этил-4-фтор-бензолсульфонамид;
9. 2-циано-3-фторметокси-N-этил-бензолсульфонамид;
10. 2-циано-6-фтор-3-метокси-N,N-диметил-бензолсульфонамид;
11. 2-циано-N-этил-6-фтор-3-метокси-N-метил-бензолсульфон-амид;
12. 2-циано-3-дифторметокси-N,N-диметилбензолсульфонамид;
13. 3-(дифторметил)-N-[2-(3,3-диметилбутил)фенил]-1-метил-1H-пиразол-4-карбоксамид;
14. N-этил-2,2-диметилпропионамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон;
15. N-этил-2,2-дихлор-1-метилциклопропан-карбоксамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон никотин;
16. O-{(E)-[2-(4-хлор-фенил)-2-циано-1-(2-трифторметил-фенил)-винил]}метил-тиокарбонат;
17. (E)-N1-[2-хлор-1,3-тиазол-5-илметил]-N2-циано-N1-метил-ацетамидин;
18. 1-(6-хлорпиридин-3-илметил)-7-метил-8-нитро-1,2,3,5,6,7-гексагидро-имидазо[1,2-a]пиридин-5-ол;
19. 4-[4-хлорфенил-(2-бутилидин-гидразоно)метил)]фенил-мезилат; и
20. N-этил-2,2-дихлор-1-метилциклопропанкарбоксамид-2-(2,6-дихлор-альфа,альфа,альфа-трифтор-п-толил)гидразон.
СИНЕРГИЧЕСКИЕ СМЕСИ
Молекулы Формулы Один могут применяться с некоторыми активными соединениями, с образованием синергических смесей, где механизм действия таких соединений в сравнении с механизмом действия соединений Формулы один является таким же, подобным или другим. Примеры механизмов действия включают, без ограничения перечисленными, следующие: ингибитор ацетилхолинэстеразы; модулятор натриевых каналов; ингибитор биосинтеза хитина; антагонист ГАМК- и глютамат-зависимых хлоридных каналов; агонист ГАМК- и глютамат-зависимых хлоридных каналов; агонист ацетилхолиновых рецепторов; антагонист ацетилхолиновых рецепторов; ингибитор МЕТ I; ингибитор Mg-стимулируемой АТФазы; никотиновый ацетилхолиновый рецептор; фактор, нарушающий целостность мембраны средней кишки; фактор, нарушающий окислительное фосфорилирование, и рецептор рианодина (RyRs). Как правило, весовые отношения молекул Формулы один в синергической смеси с другим соединением составляют от приблизительно 10:1 до приблизительно 1:10, в другом варианте осуществления от приблизительно 5:1 до приблизительно 1:5, и в другом варианте осуществления от приблизительно 3:1, и в другом варианте осуществления приблизительно 1:1.
КОМПОЗИЦИИ
Пестициды редко подходят для применения в чистом виде. Обычно требуется добавлять другие вещества, чтобы пестицид можно было использовать при требуемой концентрации и в подходящей форме, обеспечивающей легкость в применении, обращении, транспортировке, хранении, а также дающей максимальную пестицидную активность. Таким образом, пестициды могут быть включены в состав, например, приманок, концентрированных эмульсий, дустов, эмульгируемых концентратов, фумигантов, гелей, гранул, микрокапсул, протрав для семян, концентратов суспензий, суспоэмульсий, таблеток, водорастворимых жидкостей, диспергируемых в воде гранул или сухих текучих сред, смачиваемых порошков и растворов сверхмалых объемов. Для получения более подробных сведений о типах препаратов см. ʺCatalogue of Pesticide Formulation Types and International Coding Systemʺ Technical Monograph n°2, 5th Edition by CropLife International (2002).
Чаще всего пестициды применяются в виде водных суспензий или эмульсий, приготовленных из концентрированных форм таких пестицидов. Такие водорастворимые, суспендируемые в воде или эмульгируемые композиции являются либо твердыми, обычно известными как смачиваемые порошки или диспергируемые в воде гранулы, либо жидкими, обычно известными как эмульгируемые концентраты или водные суспензии. Смачиваемые порошки, которые могут быть спрессованы с получением диспергируемых в воде гранул, содержат гомогенную смесь пестицида, носителя и поверхностно-активных веществ. Концентрация пестицида обычно составляет от приблизительно 10% до приблизительно 90% по весу. Носитель обычно выбран из аттапульгитовых глин, монтмориллонитовых глин, диатомитов или очищенных силикатов. Эффективные поверхностно-активные вещества, содержащие от около 0,5% до около 10% смачиваемого порошка, выбирают из сульфонированных лигнинов, конденсированных нафталинсульфонатов, нафталинсульфонатов, алкилбензолсульфонатов, алкилсульфатов и неионогенных поверхностно-активных веществ, таких как аддукты этиленоксида и алкилфенолов.
Эмульгируемые концентраты пестицидов содержат подходящую концентрацию пестицида, такую как от приблизительно 50 до приблизительно 500 граммов на литр жидкости, растворенной в носителе, которым является либо смешивающийся с водой растворитель, либо смесь смешивающегося с водой органического растворителя и эмульгаторов. Подходящие органические растворители включают ароматические, в особенности ксилолы и нефтяные фракции, особенно высококипящие и олефиновые части нефти, такие как тяжелая ароматическая нафта. Также могут использоваться другие органические растворители, такие как терпеновые растворители, включая производные канифоли, алифатические кетоны, такие как циклогексанон, и сложные спирты, такие как 2-этоксиэтанол. Подходящие эмульгаторы для эмульгируемых концентратов выбирают из подходящих анионных и неионогенных поверхностно-активных веществ.
Водные суспензии содержат суспензии нерастворимых в воде пестицидов, диспергированных в водном носителе при концентрации в интервале от приблизительно 5% до приблизительно 50% по весу. Суспензии получают тонким измельчением пестицида и энергичным смешиванием с носителем, содержащим воду и поверхностно-активные вещества. Также могут быть добавлены такие ингредиенты, как неорганические соли и синтетические или природные смолы, служащие для повышения плотности и вязкости водного носителя. Часто более эффективным является одновременное измельчение и смешивание пестицида с получением водной смеси и ее гомогенизацией в аппарате, таком как песочная мельница, шаровая мельница или гомогенизатор поршневого типа.
Пестициды также могут применяться в виде гранулированных композиций, которые, в частности, используются для нанесения на почву. Гранулированные композиции обычно содержат от приблизительно 0,5% до приблизительно 10% по весу пестицида, диспергированного в носителе, который содержит глину или подобное вещество. Такие композиции обычно получают при растворении пестицида в подходящем растворителе и его нанесении на гранулированный носитель, который получен предварительно с требуемым размером частиц в пределах от приблизительно 0,5 до приблизительно 3 мм. Такие композиции также могут быть получены путем приготовления теста или пасты носителя и соединения и измельчения и сушки с получением гранулированных частиц нужного размера.
Дусты, содержащие пестицид, получают при тщательном смешивании пестицида в форме порошка с подходящим порошковым сельскохозяйственным носителем, таким как каолиновая глина, измельченная вулканическая порода и т.п. Дусты могут соответственно содержать от приблизительно 1% до приблизительно 10% пестицида. Они могут быть применяться для покрытия семян или внекорневого нанесения с помощью опыливателя.
В то же время на практике используется применение пестицида в виде раствора в подходящем органическом растворителе, обычно в минеральном масле, таком как распыляемые масла, которые широко используются в сельскохозяйственной химии.
Пестициды также могут применяться в форме аэрозольной композиции. В таких композициях пестицид растворяют или диспергируют в носителе, который представляет собой сжатую под давлением пропеллентную смесь. Аэрозольную композицию помещают в контейнер, из которого смесь распыляется через распылительный клапан.
Пестицидные приманки получают при смешивании пестицида с пищей и/или аттрактантом. Когда насекомые-вредители съедают приманку, они также поглощают пестицид. Приманки могут иметь форму гранул, гелей, текучих порошков, жидкостей или твердых веществ. Они могут использоваться в местах скопления насекомых-вредителей.
Фумиганты представляют собой пестициды, которые имеют относительно высокое давление пара и, следовательно, могут существовать в виде газа в достаточных концентрациях для уничтожения насекомых-вредителей на почве или в замкнутых пространствах. Токсичность фумиганта пропорциональна его концентрации и продолжительности воздействия. Они характеризуются хорошей способностью к диффузии и действию при проникновении в дыхательную систему насекомого-вредителя или через кутикулу насекомого-вредителя. Фумиганты применяются для борьбы с насекомыми-вредителями складированных продуктов под газонепроницаемыми покрытиями, в газоизолированных комнатах или строениях или в специальных камерах.
Пестициды могут быть микроинкапсулированы суспендированием частиц или капель пестицида в полимерах различных типов. При изменении химии полимера или изменении параметров обработки могут быть получены микрокапсулы различных размеров, растворимости, толщины стенок и степени проницаемости. Эти факторы влияют на скорость, с которой высвобождается активный ингредиент, что в свою очередь оказывает влияние на остаточную эффективность, скорость действия и запах продукта.
Маслорастворенные концентраты получают при растворении пестицида в растворителе, который будет удерживать пестицид в растворе. Масляные растворы пестицида обычно обеспечивают более быстрый нокдаун-эффект и уничтожение вредителей, чем другие композиции, благодаря тому, что растворители сами обладают пестицидным действием, а растворение воскового покрытия увеличивает скорость абсорбции пестицида. Другие преимущества масляных растворов включают более высокую стабильность при хранении, лучшее проникновение в мелкие щели и лучшую адгезию к жирным поверхностям.
Другим вариантом осуществления является эмульсия ʺмасло-в-водеʺ, где эмульсия содержит масляные капли, каждая из которых имеет ламеллярное жидкокристаллическое покрытие и диспергирована в водной фазе, где каждая масляная капля содержит по меньшей мере одно соединение, которое является сельскохозяйственно активным, и отдельно покрыта моноламеллярным или олиголамеллярным слоем, включающим: (1) по меньшей мере одно неионогенное липофильное поверхностно-активное вещество, (2) по меньшей мере одно неионогенное гидрофильное поверхностно-активное вещество и (3) по меньшей мере одно ионное поверхностно-активное вещество, где капли имеют средний диаметр частицы меньше 800 нм. Дополнительная информация о варианте осуществления раскрыта в публикации патента США 20070027034, опубликованной 1 февраля 2007 года под регистрационным номером заявки на патент 11/495228. Для простоты применения данный вариант осуществления будет именоваться как ʺOIWEʺ.
Для дополнительной информации см. ʺInsect Pest Managementʺ 2nd Edition by D. Dent, copyright CAB International (2000). Кроме того, для получения более подробной информации см. ʺHandbook of Pest Control - The Behavior, Life History, and Control of Household Pestsʺ, Arnold Mallis, 9th Edition, copyright 2004 by GIE Media Inc.
ДРУГИЕ КОМПОНЕНТЫ КОМПОЗИЦИИ
Как правило, когда молекулы, раскрытые в Формуле один, применяются в композиции, такая композиция может также содержать другие компоненты. Эти компоненты включают, без ограничения перечисленными (это неполный и невзаимоисключающий список), смачивающие вещества, распределительные вещества, адгезивные вещества, пенетранты, буферы, разделяющие вещества, вещества, снижающие снос, вещества, повышающие совместимость, пеногасители, чистящие вещества и эмульгаторы. Некоторые компоненты описаны непосредственно ниже.
Смачивающее вещество представляет собой вещество, которое при добавлении к жидкости увеличивает распространение или силу проникновения жидкости, уменьшая поверхностное натяжение между жидкостью и поверхностью, по которой она распространяется. Смачивающие вещества используют для двух основных функций в агрохимических композициях: в процессе обработки и получения, для увеличения скорости смачивания порошков водой для получения концентратов в случае растворимых жидкостей или концентратов суспензий; и процессе смешивания продукта с водой в баке распылителя для уменьшения времени смачивания смачиваемых порошков и улучшения проникновения воды в вододиспергируемые гранулы. Примерами смачивающих веществ, используемых в смачиваемом порошке, концентрате суспензии и вододиспергируемых гранулированных композициях, являются: лаурилсульфат натрия; диоктилсульфосукцинат натрия; этоксилаты алкилфенолов; и этоксилаты алифатических спиртов.
Диспергирующее вещество представляет собой вещество, которое адсорбируется на поверхности частиц и помогает сохранять состояние дисперсии частиц и препятствует их повторной агрегации. Диспергирующие вещества добавляют к агрохимическим композициям для облегчения образования дисперсии и суспензии в процессе производства и для гарантии того, что частицы повторно диспергируются в воде в баке распылителя. Они широко используются в смачиваемых порошках, концентратах суспензий и вододиспергируемых гранулах. Поверхностно-активные вещества, которые используются в качестве диспергирующих веществ, обладают способностью адсорбироваться с высокой силой на поверхности частицы и обеспечивать электростатический или стерический барьер для повторной агрегации частиц. Наиболее часто используемые поверхностно-активные вещества являются анионными, неионогенными или смесями двух типов. В случае композиций смачиваемых порошков, наиболее распространенными диспергирующими веществами являются лигносульфонаты натрия. В случае концентратов суспензий, очень хорошую адсорбцию и стабилизацию получают при использовании полиэлектролитов, таких как продукты конденсации нафталинсульфоната натрия и формальдегида. Применяются также тристирилфенолэтоксилатфосфатные эфиры. Иногда для получения концентратов суспензий неионогенные поверхностно-активные вещества, такие как продукты конденсации алкиларилэтиленоксида и ЭО-ПО блок-сополимеры, объединяют с анинонными соединениями в качестве диспергирующих веществ. В последние годы для применения в качестве диспергирующих веществ были разработаны полимерные поверхностно-активные вещества с очень высокой молекулярной массой. Они содержат очень длинные гидрофобные ʺскелетыʺ и большое количество этиленоксидных цепей, образующих ʺзубьяʺ ʺгребняʺ поверхностно-активного вещества. Такие высокомолекулярные полимеры могут обеспечивать длительную стабильность концентратов суспензий, поскольку гидрофобные скелеты содержат множество точек присоединения к поверхностям частиц. Примерами диспергирующих веществ, используемых в сельскохозяйственных композициях, являются лигносульфонаты натрия; продукты конденсации нафталинсульфонатов натрия с формальдегидом; тристирилфенолэтоксилатфосфатные эфиры; этоксилаты алифатических спиртов; алкилэтоксилаты; блок-сополимеры ЭО-ПО; и графт-сополимеры.
Эмульгатор представляет собой вещество, которое стабилизирует суспензию капель одной жидкой фазы в другой жидкой фазе. Без эмульгатора эти две жидкости разделились бы на две несмешивающиеся жидкие фазы. Обычно используемые смеси эмульгаторов содержат алкилфенол или алифатический спирт с двенадцатью или более звеньями этиленоксида и маслорастворимую кальциевую соль додецилбензолсульфоновой кислоты. Диапазон значений гидрофильно-липофильного баланса (ГЛБ) от 8 до 18 обычно будет обеспечивать хорошие стабильные эмульсии. Стабильность эмульсии иногда можно повышать добавлением небольшого количества поверхностно-активного блок-сополимера EO-ПО.
Солюбилизатор представляет собой поверхностно-активное вещество, которое будет образовывать мицеллы в воде при концентрациях выше критической концентрации мицеллообразования. Затем мицеллы способны растворять или солюбилизировать нерастворимые в воде вещества в гидрофобной части мицеллы. Типами поверхностно-активных веществ, обычно используемых для солюбилизации, являются неионогенные ПАВ, сорбитанмоноолеаты, этоксилаты сорбитанмоноолеатов и метилолеатные эфиры.
Иногда поверхностно-активные вещества используют либо в чистом виде, либо с другими добавками, такими как минеральные или растительные масла в качестве вспомогательных веществ к распыляемым смесям для улучшения биологической эффективности пестицида в отношении его мишени. Типы поверхностно-активных веществ, используемых для усиления биологического действия, обычно зависят от природы и механизма действия пестицида. Впрочем, они часто являются неионогенными ПАВ, такими как алкилэтоксилаты; этоксилаты линейных алифатических спиртов; этоксилаты алифатических аминов.
Носитель или разбавитель в сельскохозяйственной композиции представляет собой материал, добавляемый к пестициду для получения продукта с необходимой эффективностью. Носителями обычно являются материалы с высокими абсорбирующими способностями, тогда как разбавителями обычно являются материалы с низкими абсорбирующими способностями. Носители и разбавители используются в производстве дустов, смачиваемых порошков, гранул и вододиспергируемых гранул.
Органические растворители используются, главным образом, в производстве эмульгируемых концентратов, эмульсий типа ʺмасло в водеʺ, суспоэмульсий и композиций сверхмалого объема и, в меньшей степени, гранулированных композиций. Иногда используют смеси растворителей. В первую основную группу растворителей входят алифатические парафиновые масла, такие как керосин или очищенные парафины. Вторая основная группа (и наиболее распространенная) включает ароматические растворители, такие как ксилол и высокомолекулярные фракции C9 и C10 ароматических растворителей. Хлорпроизводные углеводородов используются в качестве сорастворителей для предотвращения кристаллизации пестицидов, в том случае, когда композиция эмульгирована в воде. Спирты иногда используются в качестве сорастворителей для повышения растворяющей способности. Другие растворители могут включать растительные масла, масла из семян и сложные эфиры растительных масел и масел из семян.
Загустители или желирующие вещества используются, главным образом, в концентратах суспензий, эмульсиях и суспоэмульсиях для изменения реологических свойств или текучести жидкости и предотвращения разделения и оседания диспергированных частиц или капель. Загустители, желирующие вещества и вещества, препятствующие оседанию, обычно подразделяются на две категории, а именно, водонерастворимые макрочастицы и растворимые в воде полимеры. Можно получать композиции концентратов суспензий при использовании глин и кварцев. Примеры этих типов веществ включают, без ограничения перечисленными, монтмориллонит, бентонит, силикат алюминия магния и аттапульгит. Растворимые в воде полисахариды использовали в качестве загустителей-желирующих веществ в течение многих лет. Типами обычно используемых полисахаридов являются натуральные экстракты семян и морских водорослей или синтетические производные целлюлозы. Примеры этих типов материалов включают, без ограничения перечисленными, гуаровую камедь; камедь рожкового дерева; каррагенан; альгинаты; метилцеллюлозу; натрий-карбоксиметилцеллюлозу (НКМЦ); гидроксиэтилцеллюлозу (ГЭЦ). Другие виды веществ, препятствующих оседанию, основаны на модифицированном крахмале, полиакрилатах, поливиниловом спирте и полиэтиленоксиде. Другим эффективным веществом, препятствующим оседанию, является ксантановая камедь.
Микроорганизмы могут вызывать порчу готовых продуктов. Поэтому, чтобы устранить или уменьшить действие этих микроорганизмов, используют консерванты. Примеры таких веществ включают, без ограничения перечисленными: пропионовую кислоту и ее натриевую соль; сорбиновую кислоту и ее натриевую или калиевую соли; бензойную кислоту и ее натриевую соль; натриевую соль п-оксибензойной кислоты; метил-п-гидроксибензоат; и 1,2-бензизотиазолин-3-он (БИТ).
Присутствие поверхностно-активных веществ часто вызывает вспенивание композиций на водной основе во время операций смешивания при производстве и нанесении с помощью распылителя. Для уменьшения тенденции к вспениванию, часто в процессе производства или перед заполнением в емкости добавляют пеногасители. Обычно существует два типа пеногасителей, а именно, силиконы и несиликоны. Силиконами обычно являются водные эмульсии диметилполисилоксана, тогда как несиликоновые пеногасители представляют собой нерастворимые в воде масла, такие как октанол и нонанол, или диоксид кремния. В обоих случаях функцией пеногасителя является вытеснение поверхностно-активного вещества с границы раздела фаз воздух-вода.
ʺЗеленыеʺ вещества (например, вспомогательные вещества, поверхностно-активные вещества, растворители) могут уменьшать общий экологический ʺследʺ композиций для защиты сельскохозяйственных культур. Зеленые вещества являются биоразлагаемыми и обычно их получают из природных и/или восполняемых источников, таких как растения и животные. Конкретные примеры включают: растительные масла, масла из семян и их сложные эфиры, а также алкоксилированные алкилполиглюкозиды.
Для получения дополнительной информации см. ʺChemistry and Technology of Agrochemical Formulationsʺ edited by D.A. Knowles, copyright 1998 by Kluwer Academic Publishers. Также см. ʺInsecticides in Agriculture and Environment - Retrospects and Prospectsʺ by A.S. Perry, I. Yamamoto, I. Ishaaya, and R. Perry, copyright 1998 by Springer-Verlag.
НАСЕКОМЫЕ-ВРЕДИТЕЛИ
Обычно молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями, например, жуками, уховертками, тараканами, мухами, тлями, щитовками, белокрылками, цикадками, муравьями, осами, термитами, молью, бабочками, вшами, кузнечиками, саранчой, сверчками, блохами, трипсами, щетинохвостками, зуднями, клещами, нематодами и симфилами.
В другом варианте осуществления соединения Формулы один могут применяться для борьбы с насекомыми-вредителями Phyla Nematoda и/или Arthropoda.
В другом варианте осуществления соединения Формулы один могут применяться для борьбы с насекомыми-вредителями Subphyla Chelicerata, Myriapoda и/или Hexapoda.
В другом варианте осуществления соединения Формулы один могут применяться для борьбы с насекомыми-вредителями классов Arachnida, Symphyla и/или Insecta.
В другом варианте осуществления соединения Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Anoplura. Неполный список конкретного рода включает, без ограничения перечисленными, Haematopinus spp., Hoplopleura spp., Linognathus spp., Pediculus spp. и Polyplax spp. Неполный список конкретных видов включает, без ограничения перечисленными, Haematopinus asini, Haematopinus suis, Linognathus setosus, Linognathus ovillus, Pediculus humanus capitis, Pediculus humanus humanus и Pthirus pubis.
В другом варианте осуществления молекулы Формулы Один могут применяться для борьбы с насекомыми-вредителями отряда Coleoptera. Неполный список конкретных родов включает, без ограничения перечисленными, Acanthoscelides spp., Agriotes spp., Anthonomus spp., Apion spp., Apogonia spp., Aulacophora spp., Bruchus spp., Cerosterna spp., Cerotoma spp., Ceutorhynchus spp., Chaetocnema spp., Colaspis spp., Ctenicera spp., Curculio spp., Cyclocephala spp., Diabrotica spp., Hypera spp., Ips spp., Lyctus spp., Megascelis spp., Meligethes spp., Otiorhynchus spp., Pantomorus spp., Phyllophaga spp., Phyllotreta spp., Rhizotrogus spp., Rhynchites spp., Rhynchophorus spp., Scolytus spp., Sphenophorus spp., Sitophilus spp. и Tribolium spp. Неполный список конкретных видов включает, без ограничения перечисленными, Acanthoscelides obtectus, Agrilus planipennis, Anoplophora glabripennis, Anthonomus grandis, Ataenius spretulus, Atomaria linearis, Bothynoderes punctiventris, Bruchus pisorum, Callosobruchus maculatus, Carpophilus hemipterus, Cassida vittata, Cerotoma trifurcata, Ceutorhynchus assimilis, Ceutorhynchus napi, Conoderus scalaris, Conoderus stigmosus, Conotrachelus nenuphar, Cotinis nitida, Crioceris asparagi, Cryptolestes ferrugineus, Cryptolestes pusillus, Cryptolestes turcicus, Cylindrocopturus adspersus, Deporaus marginatus, Dermestes lardarius, Dermestes maculatus, Epilachna varivestis, Faustinus cubae, Hylobius pales, Hypera postica, Hypothenemus hampei, Lasioderma serricorne, Leptinotarsa decemlineata, Liogenys fuscus, Liogenys suturalis, Lissorhoptrus oryzophilus, Maecolaspis joliveti, Melanotus communis, Meligethes aeneus, Melolontha melolontha, Oberea brevis, Oberea linearis, Oryctes rhinoceros, Oryzaephilus mercator, Oryzaephilus surinamensis, Oulema melanopus, Oulema oryzae, Phyllophaga cuyabana, Popillia japonica, Prostephanus truncatus, Rhyzopertha dominica, Sitona lineatus, Sitophilus granarius, Sitophilus oryzae, Sitophilus zeamais, Stegobium paniceum, Tribolium castaneum, Tribolium confusum, Trogoderma variabile и Zabrus tenebrioides.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Dermaptera.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Blattaria. Неполный список конкретных видов включает, без ограничения перечисленными, Blattella germanica, Blatta orientalis, Parcoblatta pennsylvanica, Periplaneta americana, Periplaneta australasiae, Periplaneta brunnea, Periplaneta fuliginosa, Pycnoscelus surinamensis и Supella longipalpa.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Diptera. Неполный список конкретных родов включает, без ограничения перечисленными, Aedes spp., Agromyza spp., Anastrepha spp., Anopheles spp., Bactrocera spp., Ceratitis spp., Chrysops spp., Cochliomyia spp., Contarinia spp., Culex spp., Dasineura spp., Delia spp., Drosophila spp., Fannia spp., Hylemyia spp., Liriomyza spp., Musca spp., Phorbia spp., Tabanus spp. и Tipula spp. Неполный список конкретных видов включает, без ограничения перечисленными, Agromyza frontella, Anastrepha suspensa, Anastrepha ludens, Anastrepha obliqa, Bactrocera cucurbitae, Bactrocera dorsalis, Bactrocera invadens, Bactrocera zonata, Ceratitis capitata, Dasineura brassicae, Delia platura, Fannia canicularis, Fannia scalaris, Gasterophilus intestinalis, Gracillia perseae, Haematobia irritans, Hypoderma lineatum, Liriomyza brassicae, Melophagus ovinus, Musca autumnalis, Musca domestica, Oestrus ovis, Oscinella frit, Pegomya betae, Psila rosae, Rhagoletis cerasi, Rhagoletis pomonella, Rhagoletis mendax, Sitodiplosis mosellana и Stomoxys calcitrans.
В другом варианте осуществления молекулы Формулы Один могут применяться для борьбы с насекомыми-вредителями отряда Hemiptera. Неполный список конкретных родов включает, без ограничения перечисленными, Adelges spp., Aulacaspis spp., Aphrophora spp., Aphis spp., Bemisia spp., Ceroplastes spp., Chionaspis spp., Chrysomphalus spp., Coccus spp., Empoasca spp., Lepidosaphes spp., Lagynotomus spp., Lygus spp., Macrosiphum spp., Nephotettix spp., Nezara spp., Philaenus spp., Phytocoris spp., Piezodorus spp., Planococcus spp., Pseudococcus spp., Rhopalosiphum spp., Saissetia spp., Therioaphis spp., Toumeyella spp., Toxoptera spp., Trialeurodes spp., Triatoma spp. и Unaspis spp. Неполный список конкретных видов включает, без ограничения перечисленными, Acrosternum hilare, Acyrthosiphon pisum, Aleyrodes proletella, Aleurodicus dispersus, Aleurothrixus floccosus, Amrasca biguttula biguttula, Aonidiella aurantii, Aphis gossypii, Aphis glycines, Aphis pomi, Aulacorthum solani, Bemisia argentifolii, Bemisia tabaci, Blissus leucopterus, Brachycorynella asparagi, Brevennia rehi, Brevicoryne brassicae, Calocoris norvegicus, Ceroplastes rubens, Cimex hemipterus, Cimex lectularius, Dagbertus fasciatus, Dichelops furcatus, Diuraphis noxia, Diaphorina citri, Dysaphis plantaginea, Dysdercus suturellus, Edessa meditabunda, Eriosoma lanigerum, Eurygaster maura, Euschistus heros, Euschistus servus, Helopeltis antonii, Helopeltis theivora, Icerya purchasi, Idioscopus nitidulus, Laodelphax striatellus, Leptocorisa oratorius, Leptocorisa varicornis, Lygus hesperus, Maconellicoccus hirsutus, Macrosiphum euphorbiae, Macrosiphum granarium, Macrosiphum rosae, Macrosteles quadrilineatus, Mahanarva frimbiolata, Metopolophium dirhodum, Mictis longicornis, Myzus persicae, Nephotettix cinctipes, Neurocolpus longirostris, Nezara viridula, Nilaparvata lugens, Parlatoria pergandii, Parlatoria ziziphi, Peregrinus maidis, Phylloxera vitifoliae, Physokermes piceae, Phytocoris californicus, Phytocoris relativus, Piezodorus guildinii, Poecilocapsus lineatus, Psallus vaccinicola, Pseudacysta perseae, Pseudococcus brevipes, Quadraspidiotus perniciosus, Rhopalosiphum maidis, Rhopalosiphum padi, Saissetia oleae, Scaptocoris castanea, Schizaphis graminum, Sitobion avenae, Sogatella furcifera, Trialeurodes vaporariorum, Trialeurodes abutiloneus, Unaspis yanonensis и Zulia entrerriana.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Hymenoptera. Неполный список конкретных родов включает, без ограничения перечисленными, Acromyrmex spp., Atta spp., Camponotus spp., Diprion spp., Formica spp., Monomorium spp., Neodiprion spp., Pogonomyrmex spp., Polistes spp., Solenopsis spp., Vespula spp. и Xylocopa spp. Неполный список конкретных видов включает, без ограничения перечисленными, Athalia rosae, Atta texana, Iridomyrmex humilis, Monomorium minimum, Monomorium pharaonis, Solenopsis invicta, Solenopsis geminata, Solenopsis molesta, Solenopsis richtery, Solenopsis xyloni и Tapinoma sessile.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Isoptera. Неполный список конкретных родов включает, без ограничения перечисленными, Coptotermes spp., Cornitermes spp., Cryptotermes spp., Heterotermes spp., Kalotermes spp., Incisitermes spp., Macrotermes spp., Marginitermes spp., Microcerotermes spp., Procornitermes spp., Reticulitermes spp., Schedorhinotermes spp., and Zootermopsis spp. Неполный список конкретных видов включает, без ограничения перечисленными, Coptotermes curvignathus, Coptotermes frenchi, Coptotermes formosanus, Heterotermes aureus, Microtermes obesi, Reticulitermes banyulensis, Reticulitermes grassei, Reticulitermes flavipes, Reticulitermes hageni, Reticulitermes hesperus, Reticulitermes santonensis, Reticulitermes speratus, Reticulitermes tibialis и Reticulitermes virginicus.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Lepidoptera. Неполный список конкретных родов включает, без ограничения перечисленными, Adoxophyes spp., Agrotis spp., Argyrotaenia spp., Cacoecia spp., Caloptilia spp., Chilo spp., Chrysodeixis spp., Colias spp., Crambus spp., Diaphania spp., Diatraea spp., Earias spp., Ephestia spp., Epimecis spp., Feltia spp., Gortyna spp., Helicoverpa spp., Heliothis spp., Indarbela spp., Lithocolletis spp., Loxagrotis spp., Malacosoma spp., Peridroma spp., Phyllonorycter spp., Pseudaletia spp., Sesamia spp., Spodoptera spp., Synanthedon spp. и Yponomeuta spp. Неполный список конкретных видов включает, без ограничения перечисленными, Achaea janata, Adoxophyes orana, Agrotis ipsilon, Alabama argillacea, Amorbia cuneana, Amyelois transitella, Anacamptodes defectaria, Anarsia lineatella, Anomis sabulifera, Anticarsia gemmatalis, Archips argyrospila, Archips rosana, Argyrotaenia citrana, Autographa gamma, Bonagota cranaodes, Borbo cinnara, Bucculatrix thurberiella, Capua reticulana, Carposina niponensis, Chlumetia transversa, Choristoneura rosaceana, Cnaphalocrocis medinalis, Conopomorpha cramerella, Cossus cossus, Cydia caryana, Cydia funebrana, Cydia molesta, Cydia nigricana, Cydia pomonella, Darna diducta, Diatraea saccharalis, Diatraea grandiosella, Earias insulana, Earias vittella, Ecdytolopha aurantianum, Elasmopalpus lignosellus, Ephestia cautella, Ephestia elutella, Ephestia kuehniella, Epinotia aporema, Epiphyas postvittana, Erionota thrax, Eupoecilia ambiguella, Euxoa auxiliaris, Grapholita molesta, Hedylepta indicata, Helicoverpa armigera, Helicoverpa zea, Heliothis virescens, Hellula undalis, Keiferia lycopersicella, Leucinodes orbonalis, Leucoptera coffeella, Leucoptera malifoliella, Lobesia botrana, Loxagrotis albicosta, Lymantria dispar, Lyonetia clerkella, Mahasena corbetti, Mamestra brassicae, Maruca testulalis, Metisa plana, Mythimna unipuncta, Neoleucinodes elegantalis, Nymphula depunctalis, Operophtera brumata, Ostrinia nubilalis, Oxydia vesulia, Pandemis cerasana, Pandemis heparana, Papilio demodocus, Pectinophora gossypiella, Peridroma saucia, Perileucoptera coffeella, Phthorimaea operculella, Phyllocnistis citrella, Pieris rapae, Plathypena scabra, Plodia interpunctella, Plutella xylostella, Polychrosis viteana, Prays endocarpa, Prays oleae, Pseudaletia unipuncta, Pseudoplusia includens, Rachiplusia nu, Scirpophaga incertulas, Sesamia inferens, Sesamia nonagrioides, Setora nitens, Sitotroga cerealella, Sparganothis pilleriana, Spodoptera exigua, Spodoptera frugiperda, Spodoptera eridania, Thecla basilides, Tineola bisselliella, Trichoplusia ni, Tuta absoluta, Zeuzera coffeae и Zeuzera pyrina.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Mallophaga. Неполный список конкретных родов включает, без ограничения перечисленными, Anaticola spp., Bovicola spp., Chelopistes spp., Goniodes spp., Menacanthus spp. и Trichodectes spp. Неполный список конкретных видов включает, без ограничения перечисленными, Bovicola bovis, Bovicola caprae, Bovicola ovis, Chelopistes meleagridis, Goniodes dissimilis, Goniodes gigas, Menacanthus stramineus, Menopon gallinae и Trichodectes canis.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Orthoptera. Неполный список конкретных родов включает, без ограничения перечисленными, Melanoplus spp. и Pterophylla spp. Неполный список конкретных видов включает, без ограничения перечисленными, Anabrus simplex, Gryllotalpa africana, Gryllotalpa australis, Gryllotalpa brachyptera, Gryllotalpa hexadactyla, Locusta migratoria, Microcentrum retinerve, Schistocerca gregaria и Scudderia furcata.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Siphonaptera. Неполный список конкретных видов включает, без ограничения перечисленными, Ceratophyllus gallinae, Ceratophyllus niger, Ctenocephalides canis, Ctenocephalides felis и Pulex irritans.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Thysanoptera. Неполный список конкретных родов включает, без ограничения перечисленными, Caliothrips spp., Frankliniella spp., Scirtothrips spp. и Thrips spp. Неполный список конкретных видов включает, без ограничения перечисленными, Frankliniella fusca, Frankliniella occidentalis, Frankliniella schultzei, Frankliniella williamsi, Heliothrips haemorrhoidalis, Rhipiphorothrips cruentatus, Scirtothrips citri, Scirtothrips dorsalis и Taeniothrips rhopalantennalis, Thrips hawaiiensis, Thrips nigropilosus, Thrips orientalis, Thrips tabaci.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Thysanura. Неполный список конкретных родов включает, без ограничения перечисленными, Lepisma spp. и Thermobia spp.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями отряда Acarina. Неполный список конкретных родов включает, без ограничения перечисленными, Acarus spp., Aculops spp., Boophilus spp., Demodex spp., Dermacentor spp., Epitrimerus spp., Eriophyes spp., Ixodes spp., Oligonychus spp., Panonychus spp., Rhizoglyphus spp. и Tetranychus spp. Неполный список конкретных видов включает, без ограничения перечисленными, Acarapis woodi, Acarus siro, Aceria mangiferae, Aculops lycopersici, Aculus pelekassi, Aculus schlechtendali, Amblyomma americanum, Brevipalpus obovatus, Brevipalpus phoenicis, Dermacentor variabilis, Dermatophagoides pteronyssinus, Eotetranychus carpini, Notoedres cati, Oligonychus coffeae, Oligonychus ilicis, Panonychus citri, Panonychus ulmi, Phyllocoptruta oleivora, Polyphagotarsonemus latus, Rhipicephalus sanguineus, Sarcoptes scabiei, Tegolophus perseaflorae, Tetranychus urticae и Varroa destructor.
В другом варианте осуществления молекулы Формулы один могут использоваться для борьбы с насекомым-вредителем отряда Symphyla. Неполный список конкретных видов включает, без ограничения перечисленными, Scutigerella immaculata.
В другом варианте осуществления молекулы Формулы один могут применяться для борьбы с насекомыми-вредителями типа Nematoda. Неполный список конкретных родов включает, без ограничения перечисленными, Aphelenchoides spp., Belonolaimus spp., Criconemella spp., Ditylenchus spp., Heterodera spp., Hirschmanniella spp., Hoplolaimus spp., Meloidogyne spp., Pratylenchus spp. и Radopholus spp. Неполный список конкретных видов включает, без ограничения перечисленными, Dirofilaria immitis, Heterodera zeae, Meloidogyne incognita, Meloidogyne javanica, Onchocerca volvulus, Radopholus similis и Rotylenchulus reniformis.
Для получения дополнительной информации см. ʺHandbook of Pest Control - The Behavior, Life History, and Control of Household Pestsʺ by Arnold Mallis, 9th Edition, copyright 2004 by GIE Media Inc.
ПРИМЕНЕНИЯ
Молекулы Формулы один обычно применяются в количествах от приблизительно 0,01 грамма на гектар до приблизительно 5000 граммов на гектар для уничтожения насекомых-вредителей. Количества от приблизительно 0,1 грамма на гектар до приблизительно 500 граммов на гектар обычно являются предпочтительными, и количества от приблизительно 1 грамма на гектар до приблизительно 50 граммов на гектар обычно являются более предпочтительными.
Площадь, на которой применяют соединения Формулы один, может быть любой площадью обитания (или вероятного обитания или перемещения) насекомых-вредителей, например: где произрастают сельскохозяйственные культуры, деревья, фрукты, злаки, кормовые культуры, виноград, травяной покров и декоративные растения; где находятся домашние животные; внешние или внутренние поверхности зданий (например, места, где хранится зерно), материалы конструкций, используемые при строении (такие как пропитанное дерево) и почва вокруг строений. Конкретные площади выращивания сельскохозяйственных культур, где используются соединения Формулы один, включают площади, где выращивают яблони, кукурузу, подсолнечник, хлопок, сою, канолу, пшеницу, рис, сорго, ячмень, овес, картофель, апельсины, люцерну, латук, клубнику, помидоры, перец, крестоцветы, груши, табак, миндаль, сахарную свеклу, фасоль и другие ценные растения, или их семена, используемые для посадки. При выращивании различных растений также успешным является применение сульфата алюминия с соединениями Формулы один.
Борьба с насекомыми-вредителями обычно означает, что популяции насекомых-вредителей, активность насекомых-вредителей или и то, и другое уменьшаются на площади. Это может происходить в тех случаях, когда: популяции насекомых-вредителей покидают площадь; когда насекомые-вредители нейтрализуются на или вокруг площади; или насекомые-вредители полностью или частично уничтожаются на или вокруг площади. Безусловно, может иметь место комбинация указанных результатов. Как правило, популяции насекомых-вредителей и/или их активность желательно уменьшить более чем на пятьдесят процентов, предпочтительно более чем на 90 процентов. Обычно, площадь не находится в или на человеке; следовательно, участок обычно является площадью, не относящейся к человеку.
Молекулы Формулы один могут применяться в смесях, применяться одновременно или последовательно, отдельно или вместе с другими соединениями для повышения силы растений (например, для лучшего роста корневой системы, для лучшего противостояния стрессовым условиям роста). Такими другими соединениями являются, например, соединения, которые модулируют этиленовые рецепторы растения, наиболее известным является 1-метилциклопропен (также известный как 1-MCP). Кроме того, такие молекулы могут применяться в течение времени, когда активность вредителя понижена, например, до того, как растения, которые растут, начинают производить ценные сельскохозяйственные продукты. Такое время включает сезон подготовки к посеву, когда давление насекомых-вредителей обычно низкое.
Молекулы Формулы один могут быть нанесены на лиственную и плодовую части растений для борьбы с насекомыми-вредителями. Молекулы либо попадают в непосредственный контакт с насекомыми-вредителями, либо насекомые-вредители поглощают пестицид при поедании листьев, плодовой массы или извлекают сок, который содержит пестицид. Молекулы Формулы один могут быть также нанесены на почву, и при таком нанесении можно бороться с насекомыми-вредителями, питающимися корнями и стеблем. Корни могут абсорбировать молекулу, перенося ее в лиственные части растения, для борьбы с насекомыми-вредителями, поедающими наземные части и потребляющими сок растений.
Как правило, в случае приманок, приманки помещают в землю, где, например, термиты могут контактировать с приманкой и/или привлекаться к приманке. Приманки могут также применяться на поверхности строения (на горизонтальной, вертикальной или наклонной поверхности), где, например, муравьи, термиты, тараканы и мухи могут контактировать с приманкой и/или привлекаться к приманке. Приманки могут содержать молекулу Формулы один.
Молекулы Формулы один могут быть инкапсулированы или нанесены на поверхность капсул. Размер капсул может изменяться от нанометрового размера (около 100-900 нанометров в диаметре) до микрометрового размера (около 10-900 микронов в диаметре).
Из-за уникальной способности яиц некоторых вредителей сопротивляться определенным пестицидам, может потребоваться повторное применение молекулы Формулы один для борьбы с недавно появившимися личинками.
Системное перемещение пестицидов в растениях может быть использовано для борьбы с насекомыми-вредителями в одной части растения при нанесении (например, распылении на участок) молекул Формулы один на другую часть растения. Например, уничтожение питающихся листьями насекомых может быть достигнуто капельным орошением или нанесением в борозды, при обработке почвы, например, при орошении до или после посадки, или при обработке семян растения перед посадкой.
Обработка семян может быть применена ко всем типам семян, в том числе к тем семенам, из которых будут произрастать генетически модифицированные растения, экспрессирующие специализированные признаки. Типичные примеры включают семена, которые экспрессируют белки, токсичные для беспозвоночных вредителей, такие как белки Bacillus thuringiensis, или другие инсектицидные токсины, факторы, которые демонстрируют устойчивость к гербицидам, например, семена ʺRoundup Readyʺ или семена с ʺпакетированнымиʺ чужеродными генами, экспрессирующими инсектицидные токсины, устойчивость к гербицидам, усиленное усвоение питательных веществ, засухоустойчивость или любые другие полезные свойства. Кроме того, такая обработка семян молекулами Формулы один может дополнительно увеличивать способность растения лучше переносить стрессовые условия роста. Это обеспечивает получение более здорового, более сильного растения, которое может давать более высокий урожай. Обычно, от приблизительно 1 грамма молекул Формулы один до приблизительно 500 граммов на 100000 семян, как ожидают, будет обеспечивать хорошие результаты, количество от приблизительно 10 граммов до приблизительно 100 граммов на 100000 семян, как ожидают, будет обеспечивать еще большее высокие результаты, и количество от приблизительно 25 граммов до приблизительно 75 граммов на 100000 семян, как ожидают, будет обеспечивать наиболее высокие результаты.
Должно быть вполне очевидно, что молекулы Формулы один могут применяться на, в или около растений, генетически модифицированных с целью экспрессии специализированных признаков, таких как Bacillus thuringiensis или другие инсектицидные токсины, или признаков, которые экспрессируют устойчивость к гербициду, или признаков с ʺпакетированнымиʺ чужеродными генами, экспрессирующими инсектицидные токсины, устойчивость к гербициду, усиленное усвоение питательных веществ, засухоустойчивость или любые другие полезные признаки.
Молекулы Формулы один могут применяться для борьбы с эндопаразитами и эктопаразитами в области ветеринарии или в области охраны животных, не относящихся к человеку. Соединения Формулы один могут применяться, например, путем перорального введения в форме, например, таблеток, капсул, напитков, гранул, путем нанесения на кожу в форме, например, пропитки, распыления, обливания, нанесения каплями и обсыпкой, и парентерального введения в форме, например, инъекции.
Молекулы Формулы один также могут эффективно применяться для охраны домашнего скота, например, рогатого скота, овец, свиней, кур и гусей. Они могут также эффективно применяться к домашним животным, таким как, лошади, собаки и кошки. Конкретными потенциальными насекомыми-вредителями, с которыми необходимо бороться, являются блохи и клещи, которые досаждают таким животным. Подходящие композиции вводят животным перорально с питьевой водой или кормом. Дозировки и композиции, которые являются подходящими, зависят от вида животного.
Молекулы Формулы один могут также применяться для борьбы с паразитирующими червями, в особенности в кишечнике, у указанных выше животных.
Молекулы Формулы один могут также применяться в терапевтических способах охраны здоровья человека. Такие способы включают, без ограничения, пероральное введение соединения в виде, например, таблеток, капсул, напитков, гранул, и наружное применение.
Вредители по всему миру мигрировали в новую окружающую среду (для такого вредителя) и после этого становились новым агрессивным видом в такой новой окружающей среде. Молекулы Формулы Один также могут применяться к таким новым агрессивным видам для борьбы с ними в такой новой окружающей среде.
Молекулы Формулы Один могут также применяться в области, где растут (например, перед посадкой, при посадке, до сбора урожая) растения, такие как сельскохозяйственные культуры, и где имеются низкие уровни (или даже нет фактического присутствия) вредителей, которые могут повреждать такие растения, принося экономический ущерб. Использование таких молекул в такой области должно приносить пользу растениям, выращиваемым в области. Такая польза может включать, без ограничения перечисленным, улучшение здоровья растения, повышение урожая растения (например, увеличение биомассы и/или увеличение содержания ценных компонентов), повышение мощности растения (например, улучшенный рост растения и/или более зеленые листья), повышение качества растения (например, повышение содержания или улучшение состава некоторых компонентов) и повышение устойчивости к абиотическому и/или биотическому стрессу растения.
Прежде, чем пестицид может применяться или выпускаться на рынок, такой пестицид подвергают длительным процессам оценки различными правительственными органами (местными, региональными, государственными, национальными и международными). Обширные требования к данным определяются контролирующими органами и должны рассматриваться посредством формирования данных и подачи заявки регистратором продукта или третьим лицом, действующим от имени регистратора продукта, обычно при использовании компьютера с выходом в Интернет. Затем эти правительственные органы рассматривают такие данные и, если исследование безопасности завершено, предоставляют потенциальному пользователю или продавцу регистрационные документы, разрешающие использовать продукт. После этого, в том регионе, где предоставляют и поддерживают регистрацию продукта, такой пользователь или продавец может использовать или продавать такой пестицид.
Заголовки в настоящем документе представлены исключительно для удобства и не должны использоваться для интерпретации какой-либо его части.
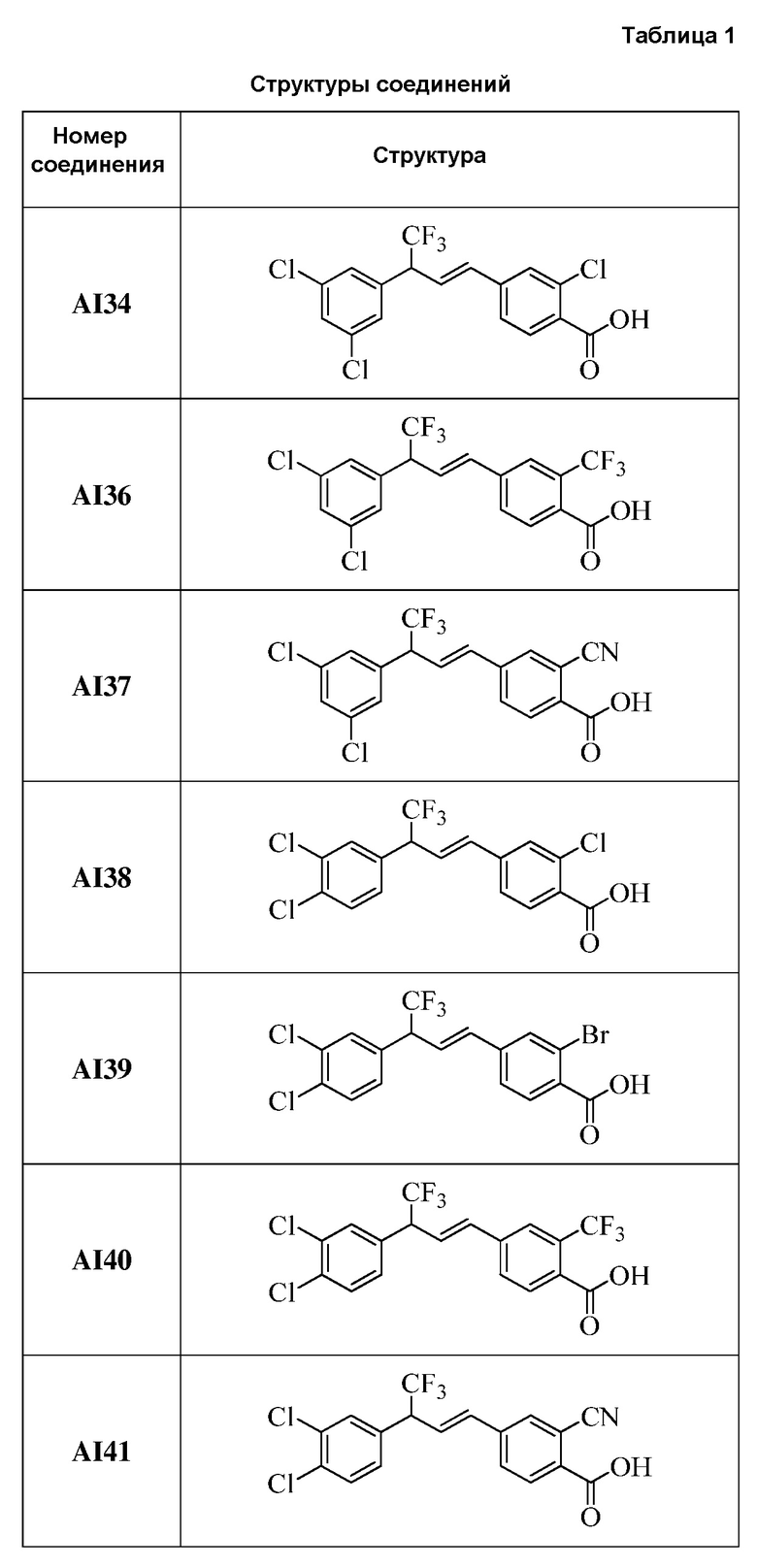
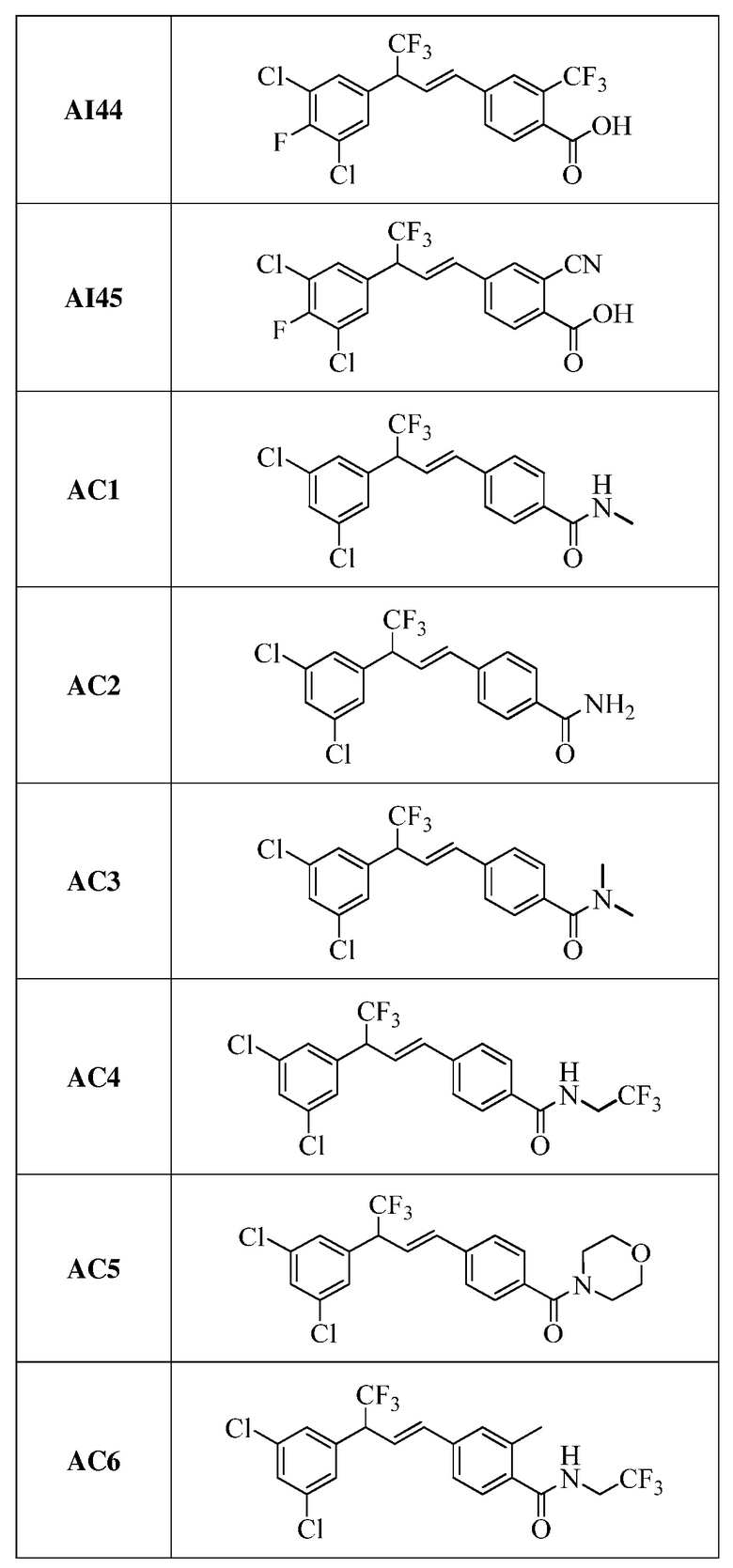
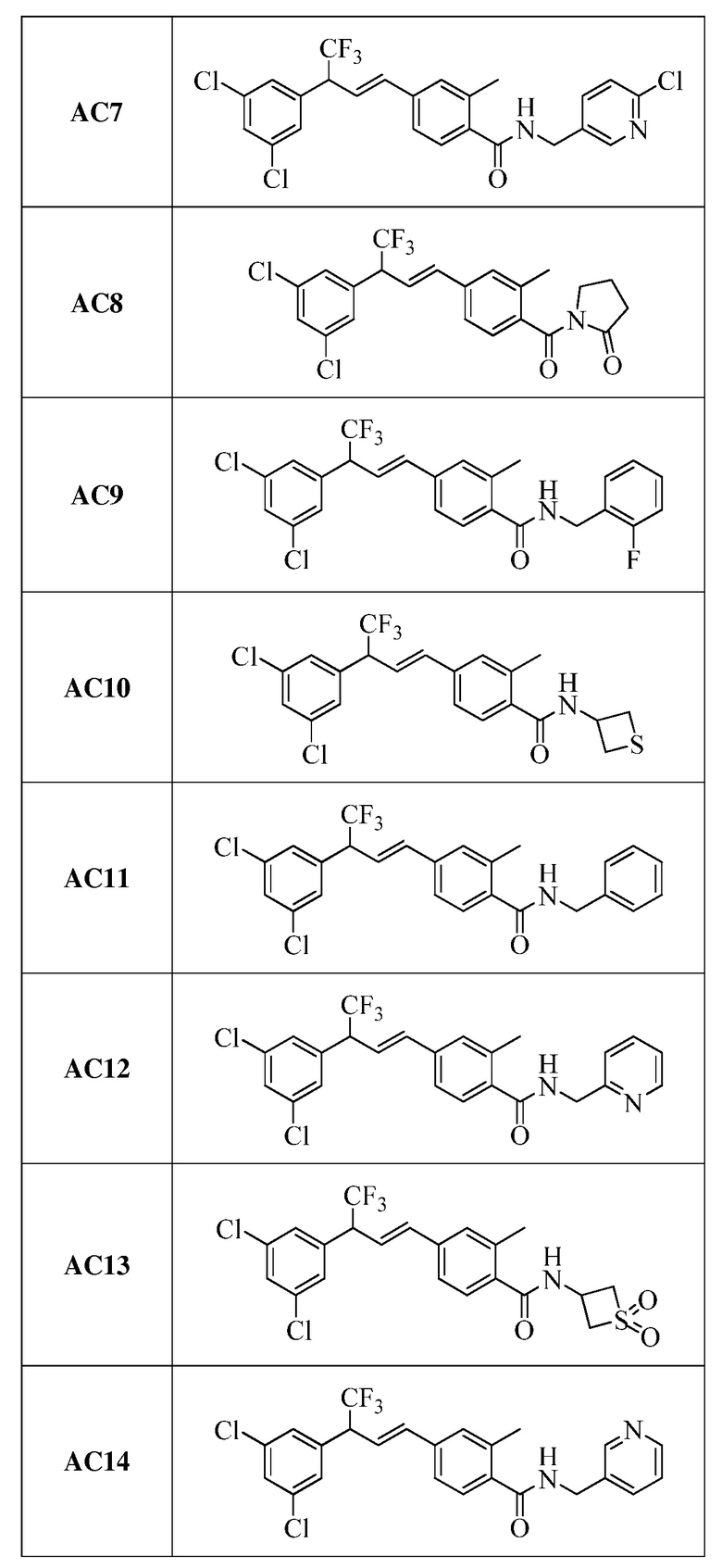
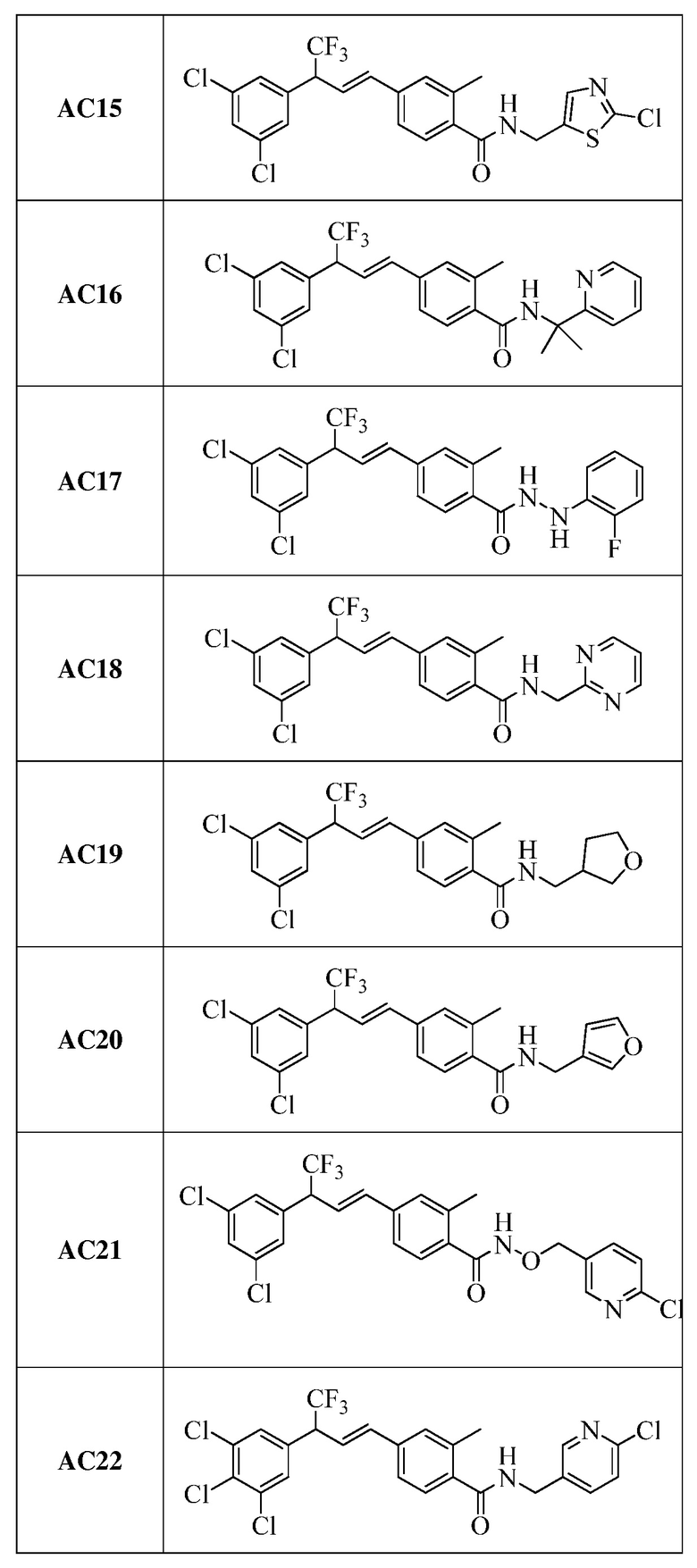
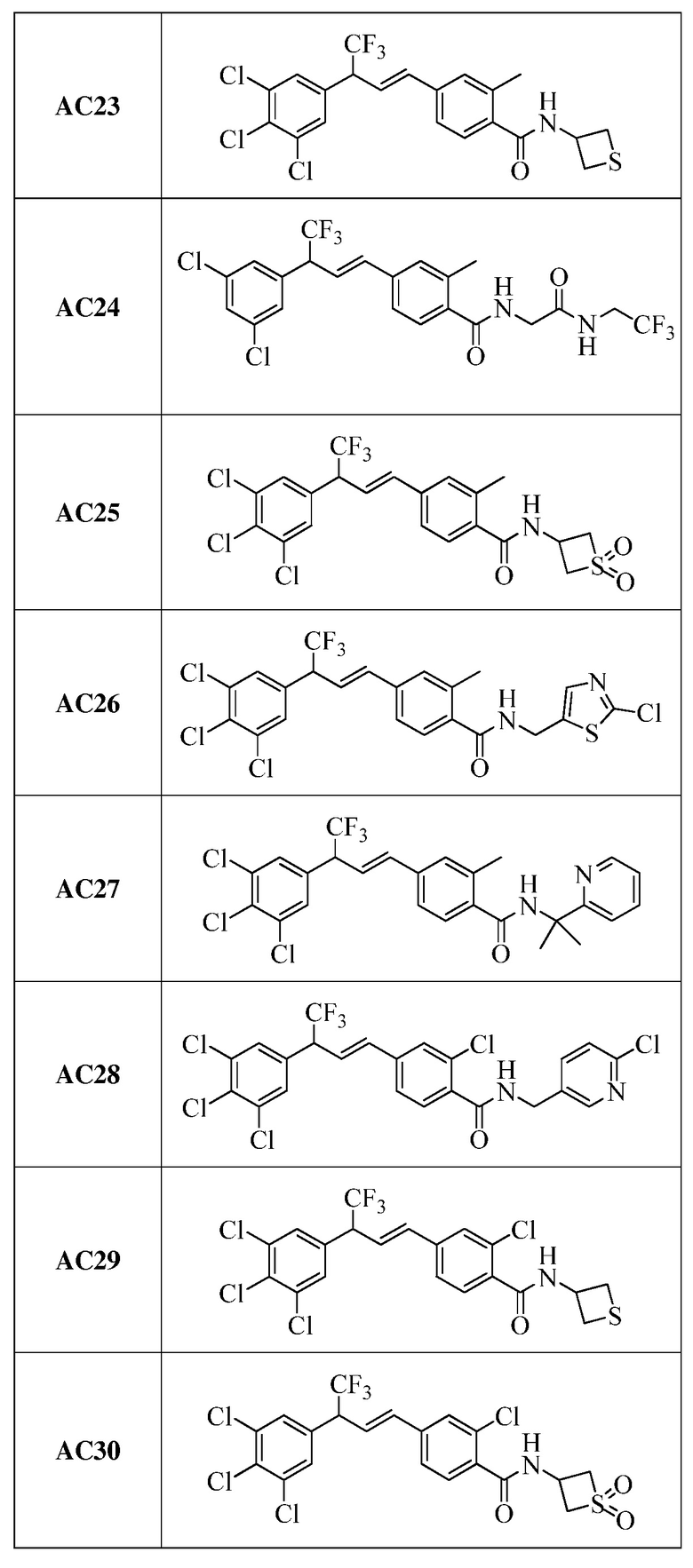
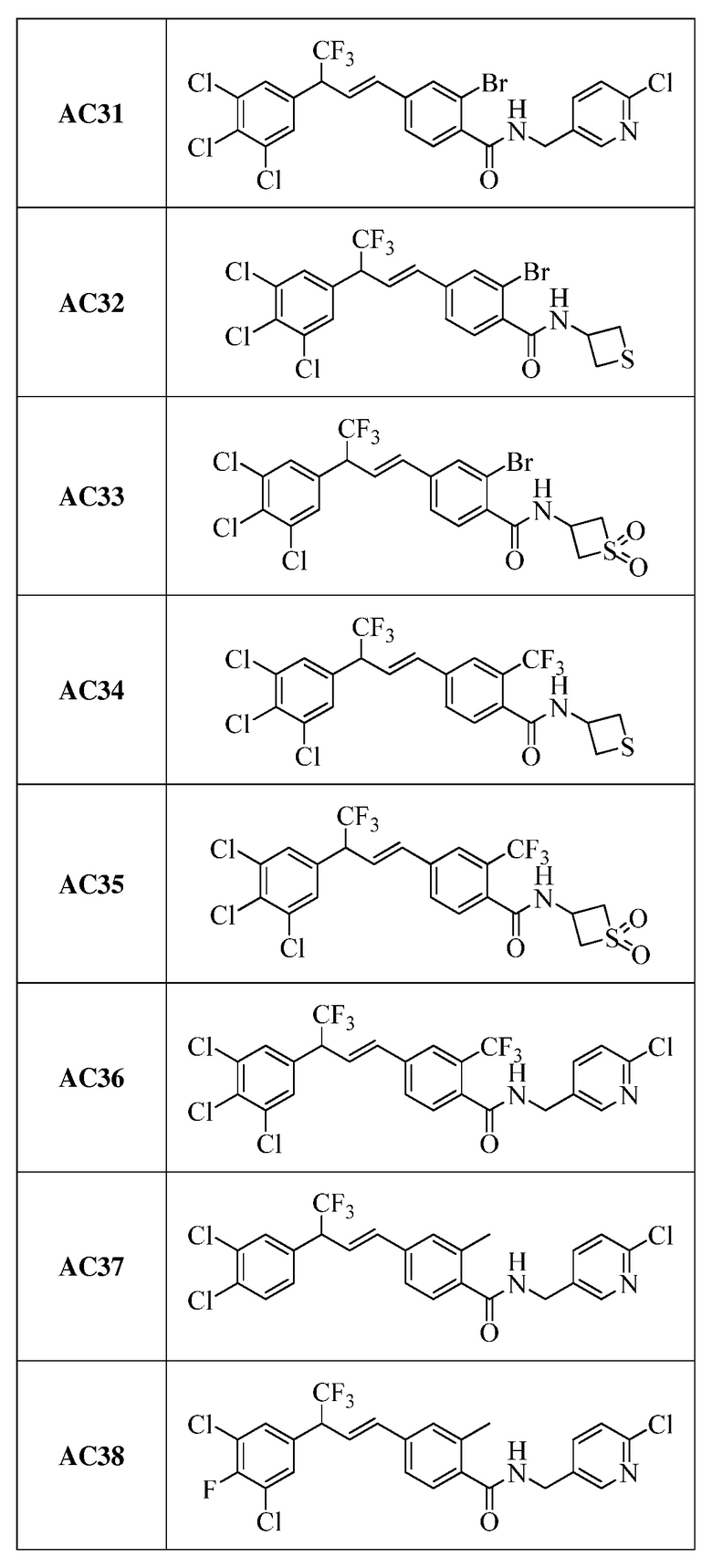
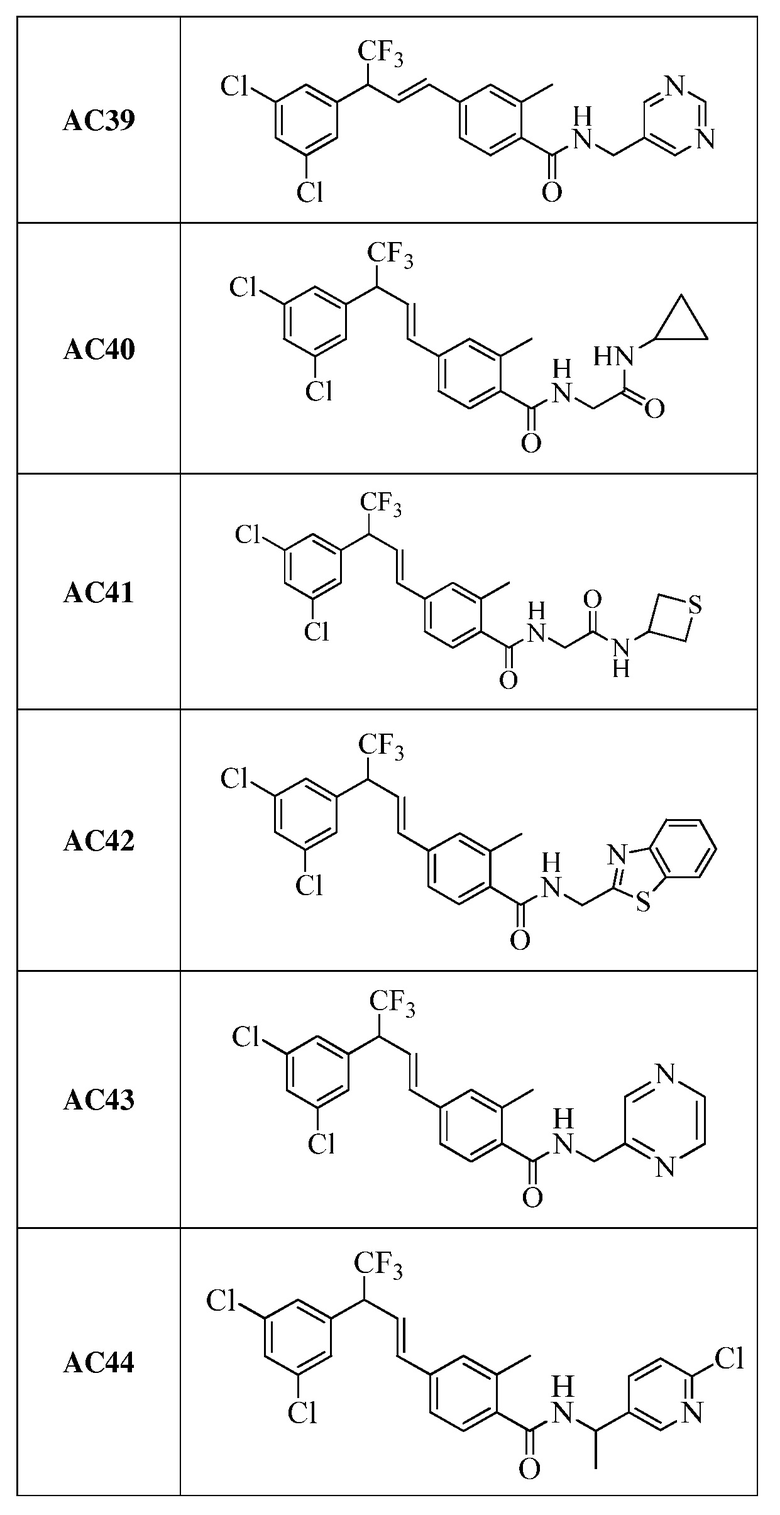
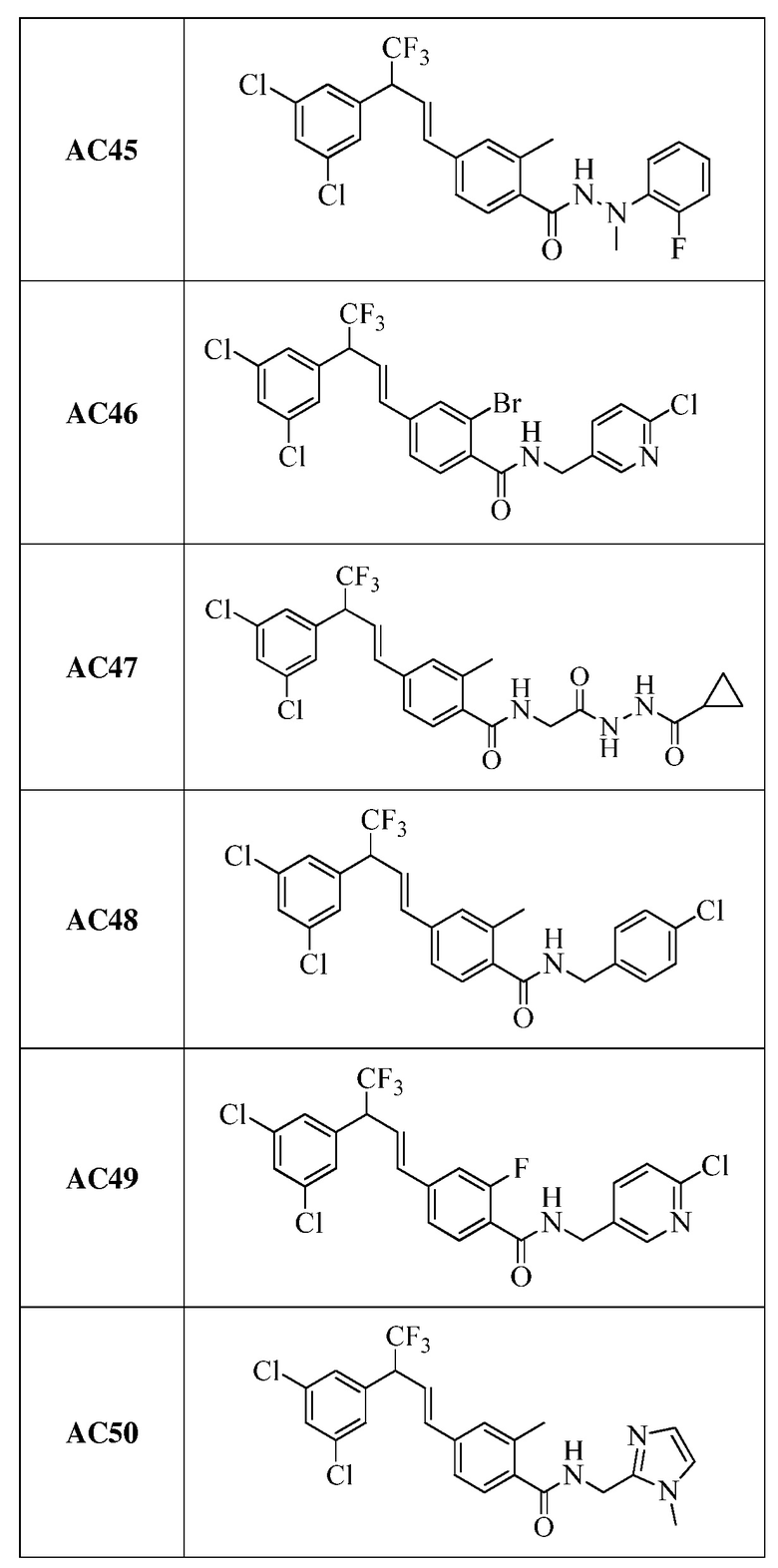
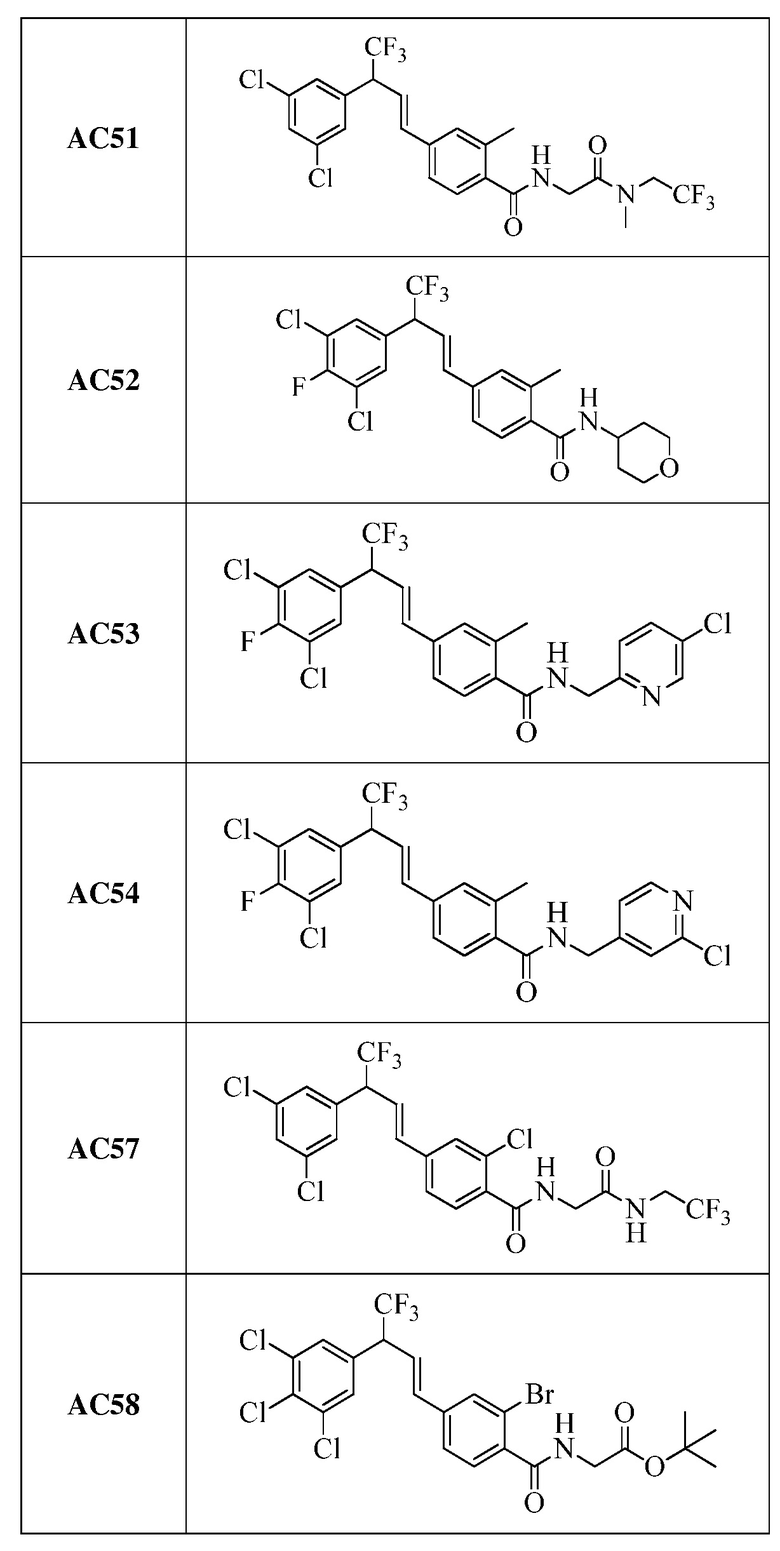
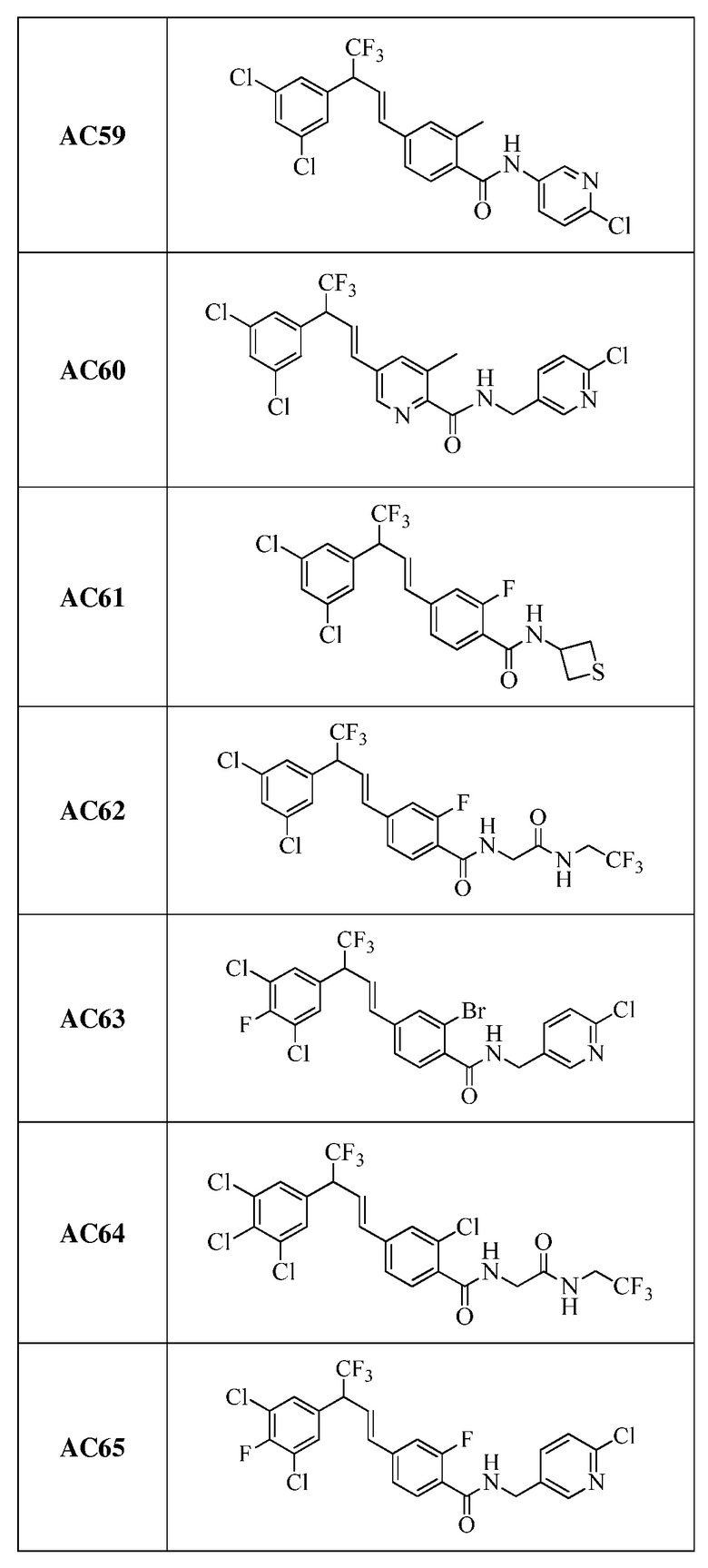
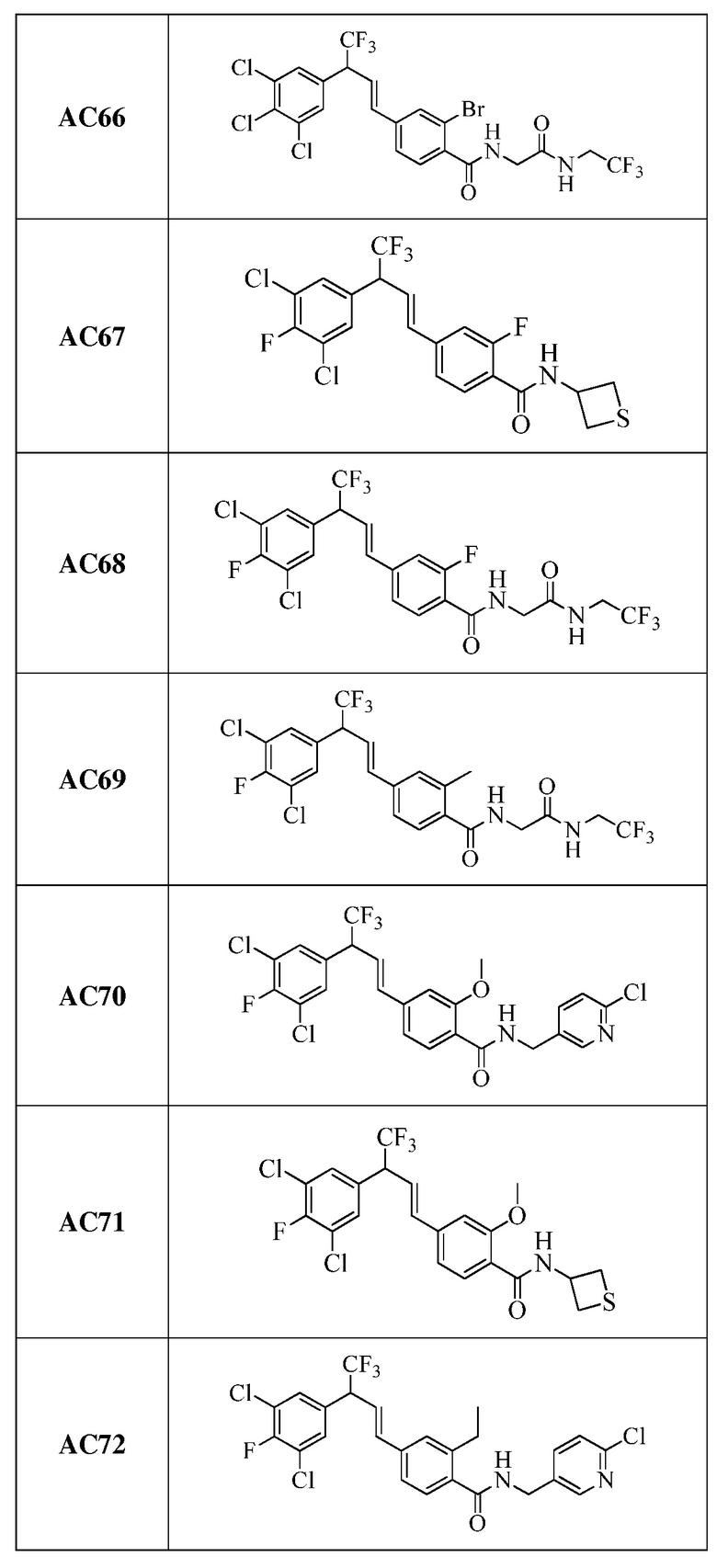
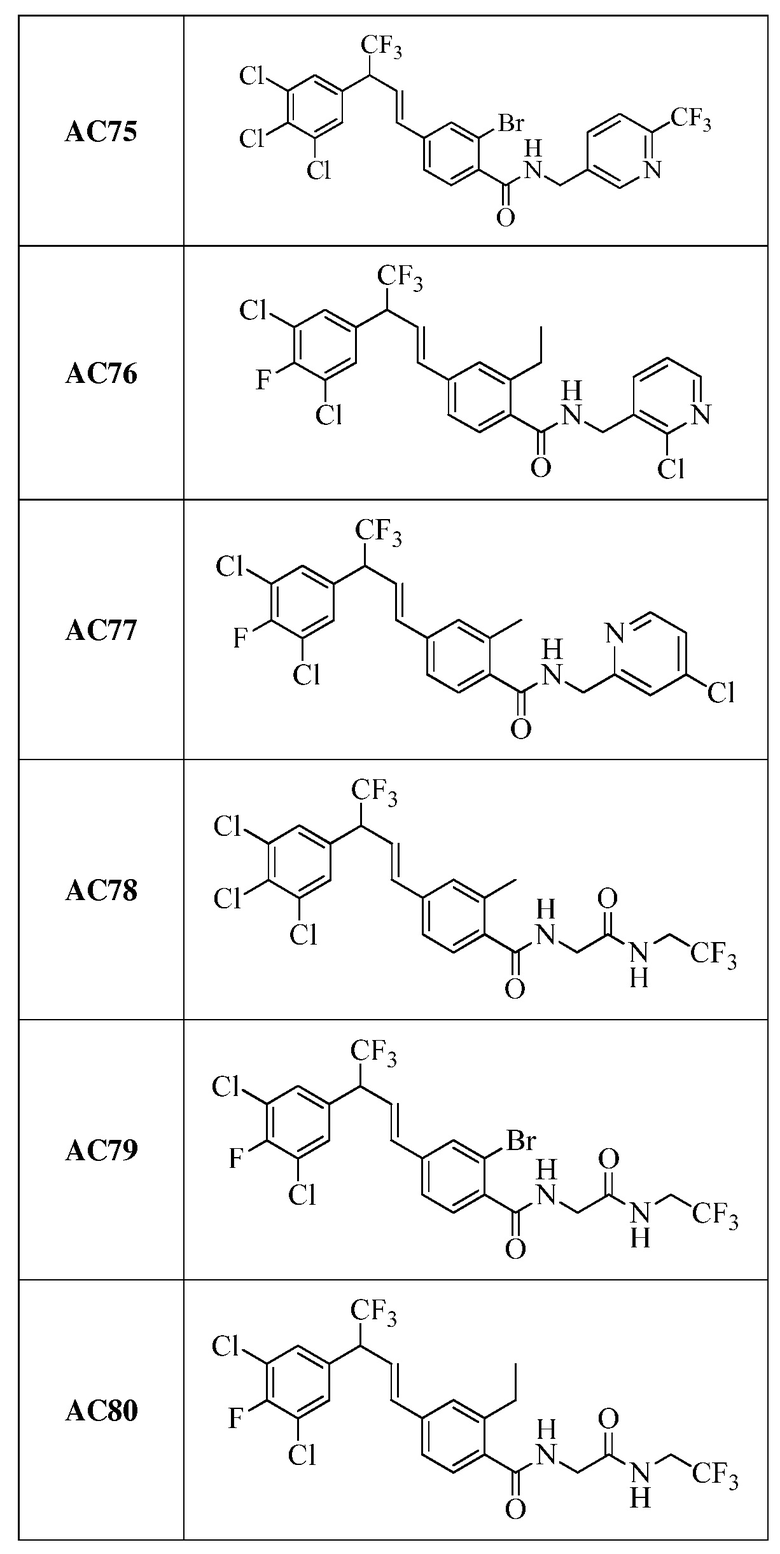
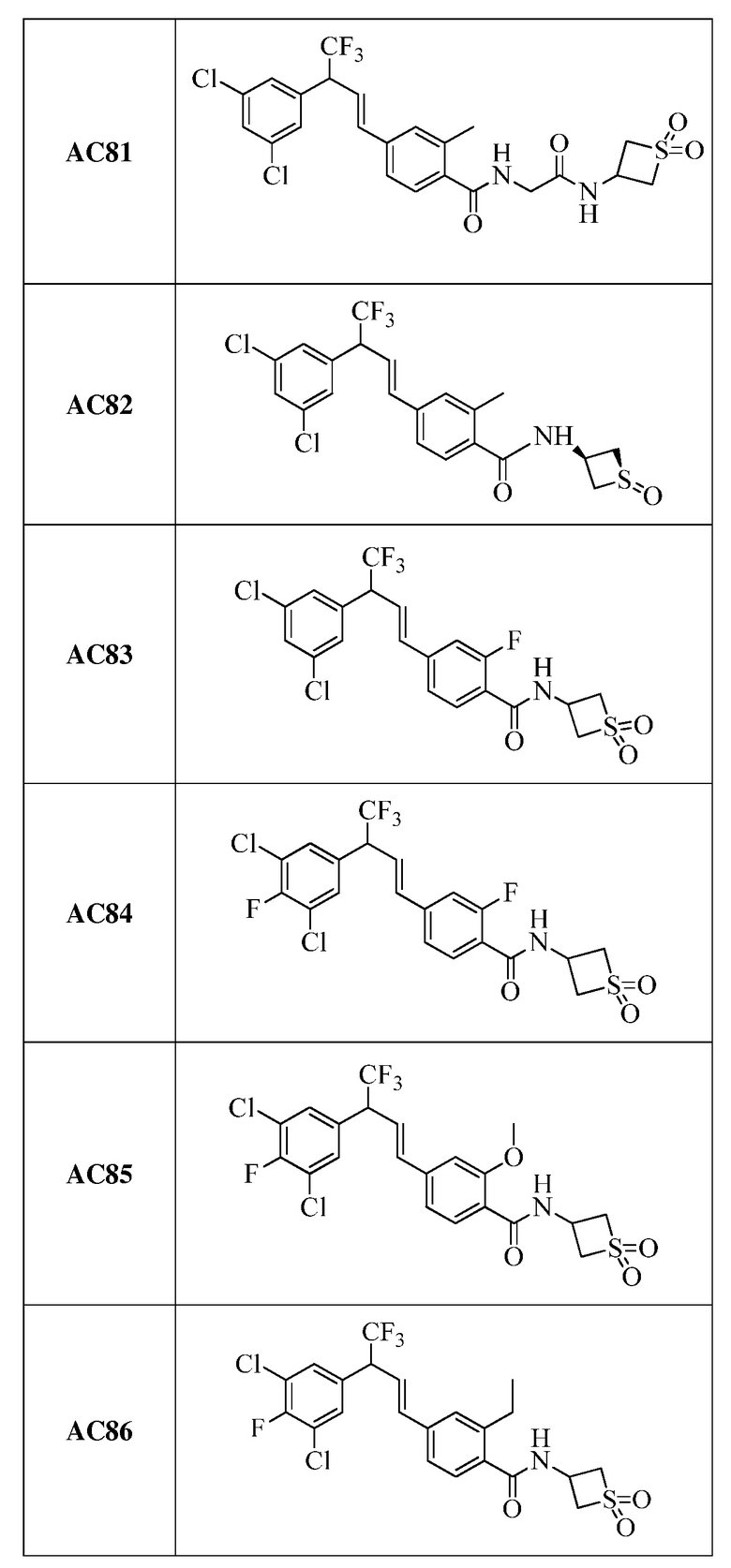
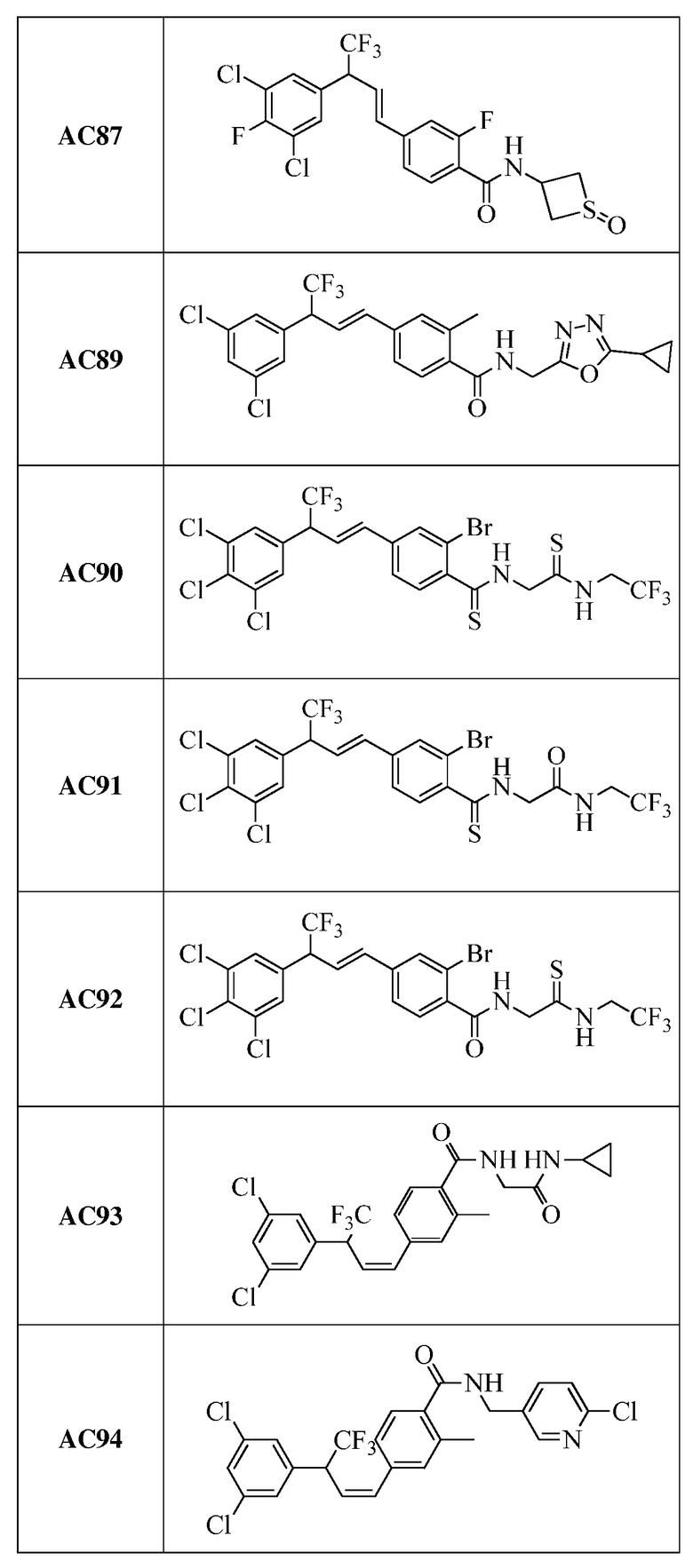
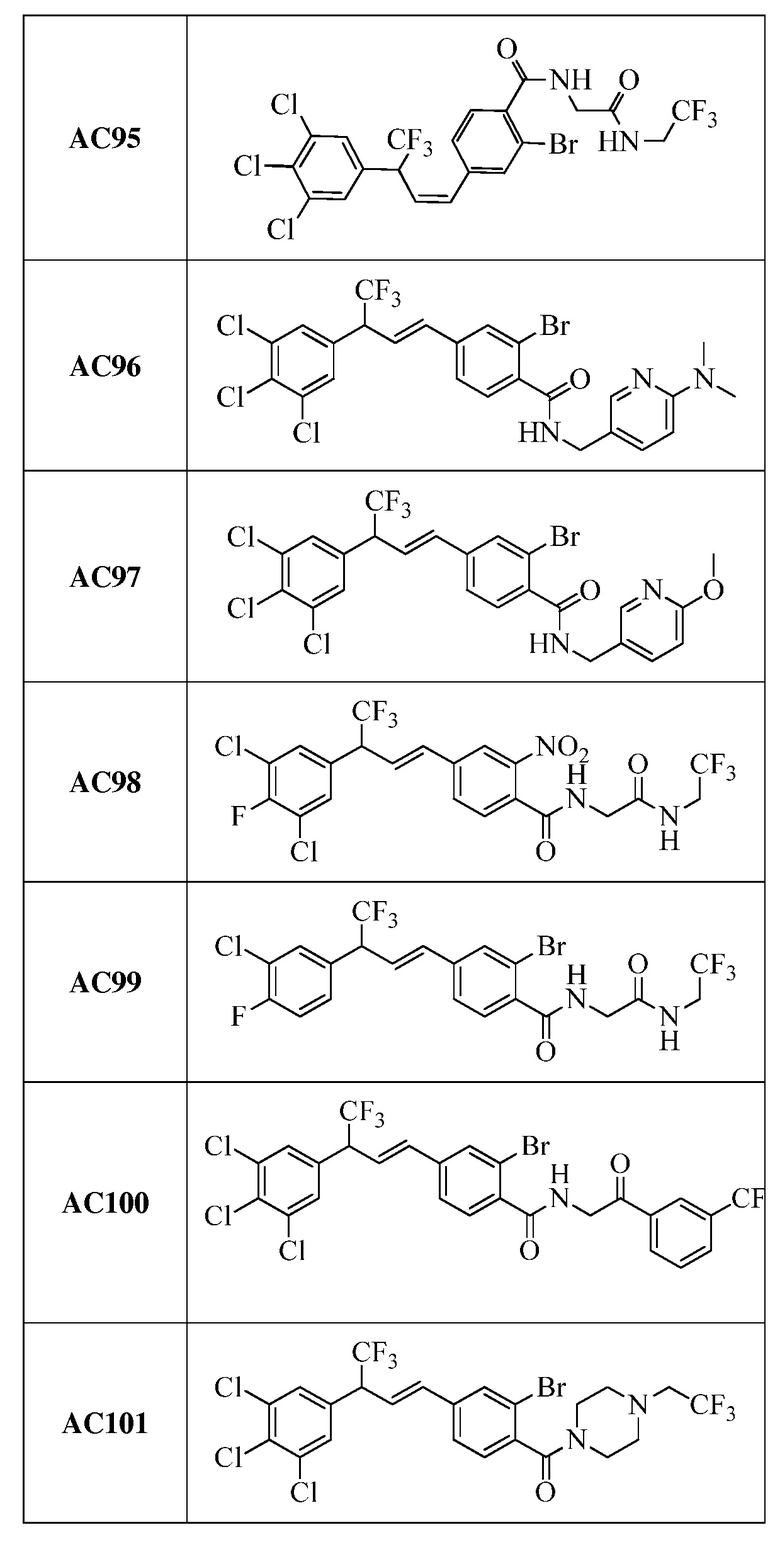
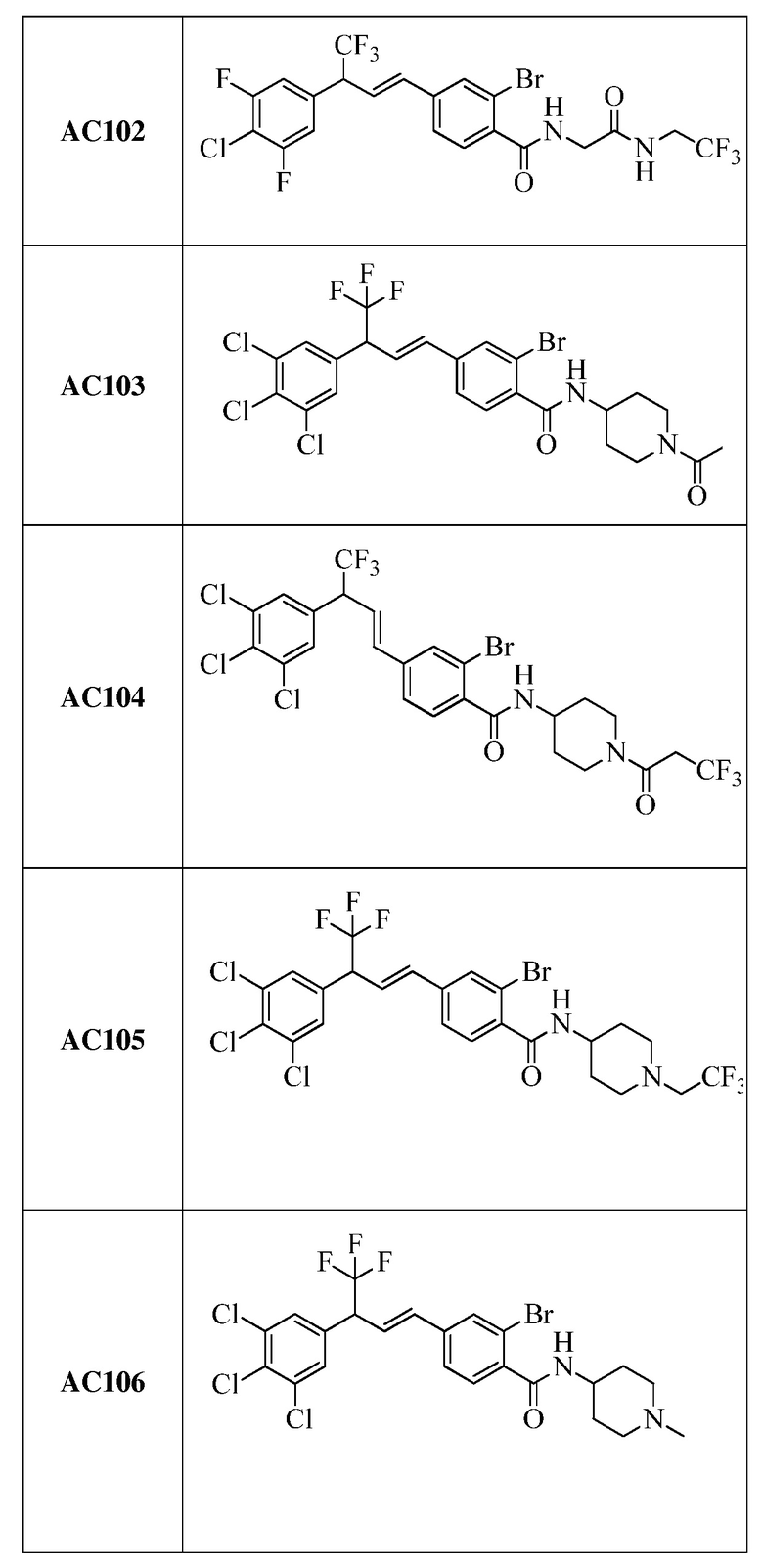
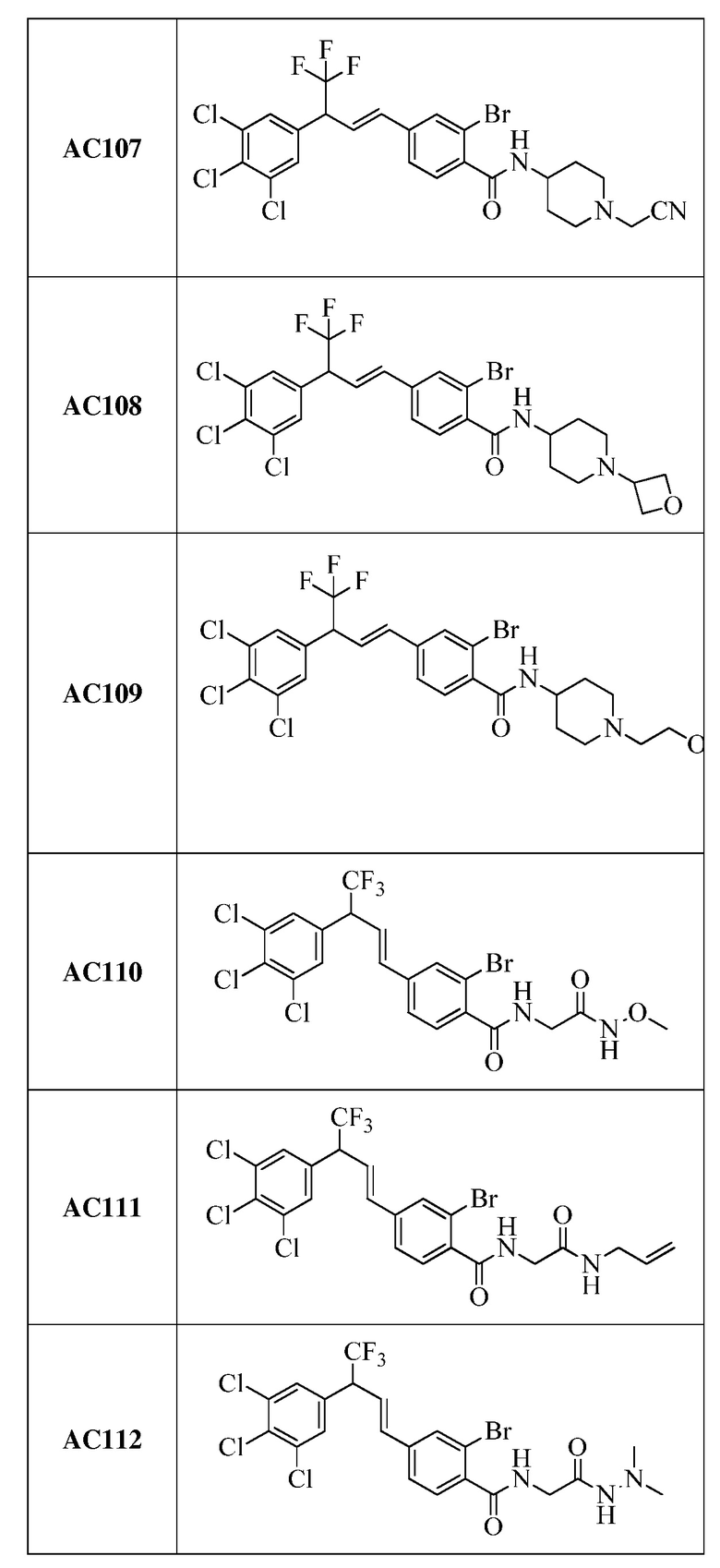
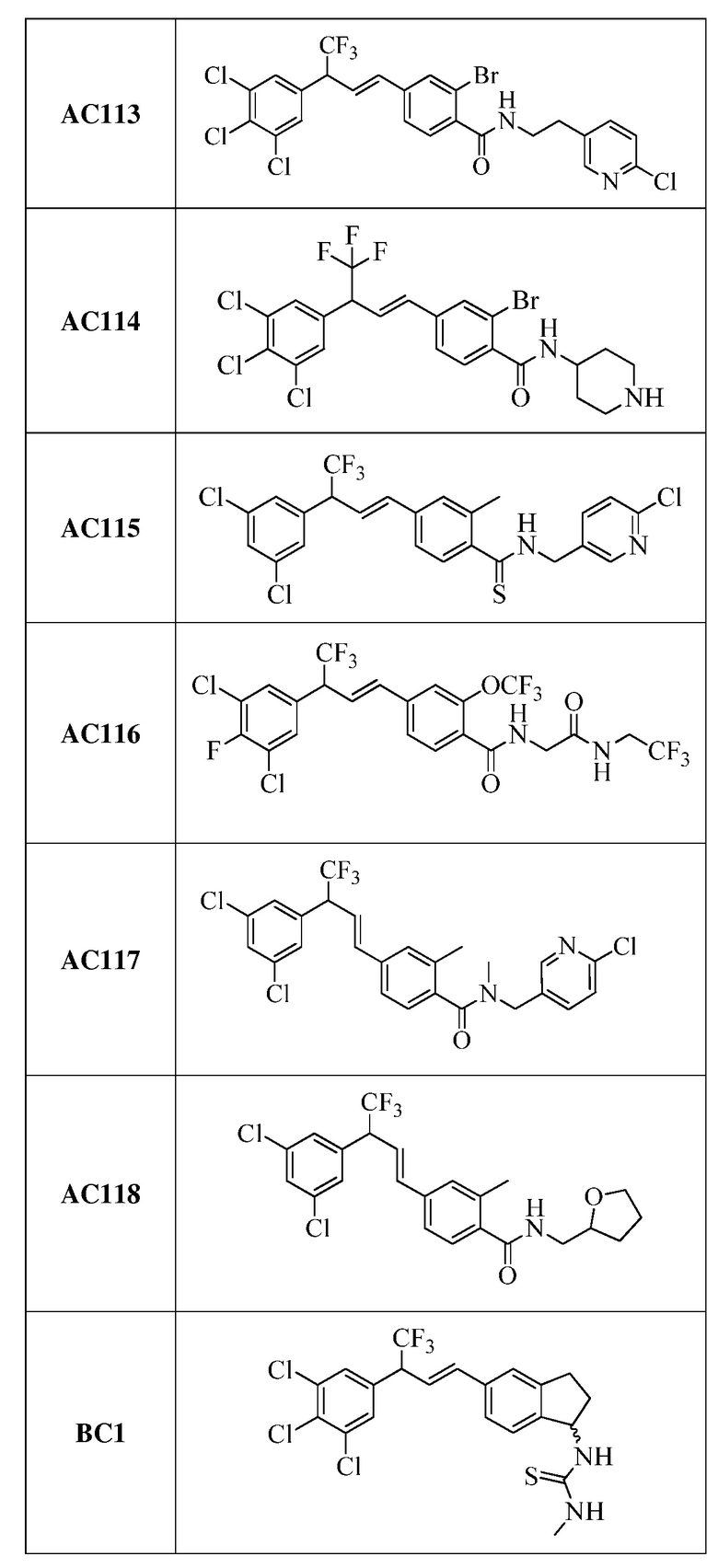
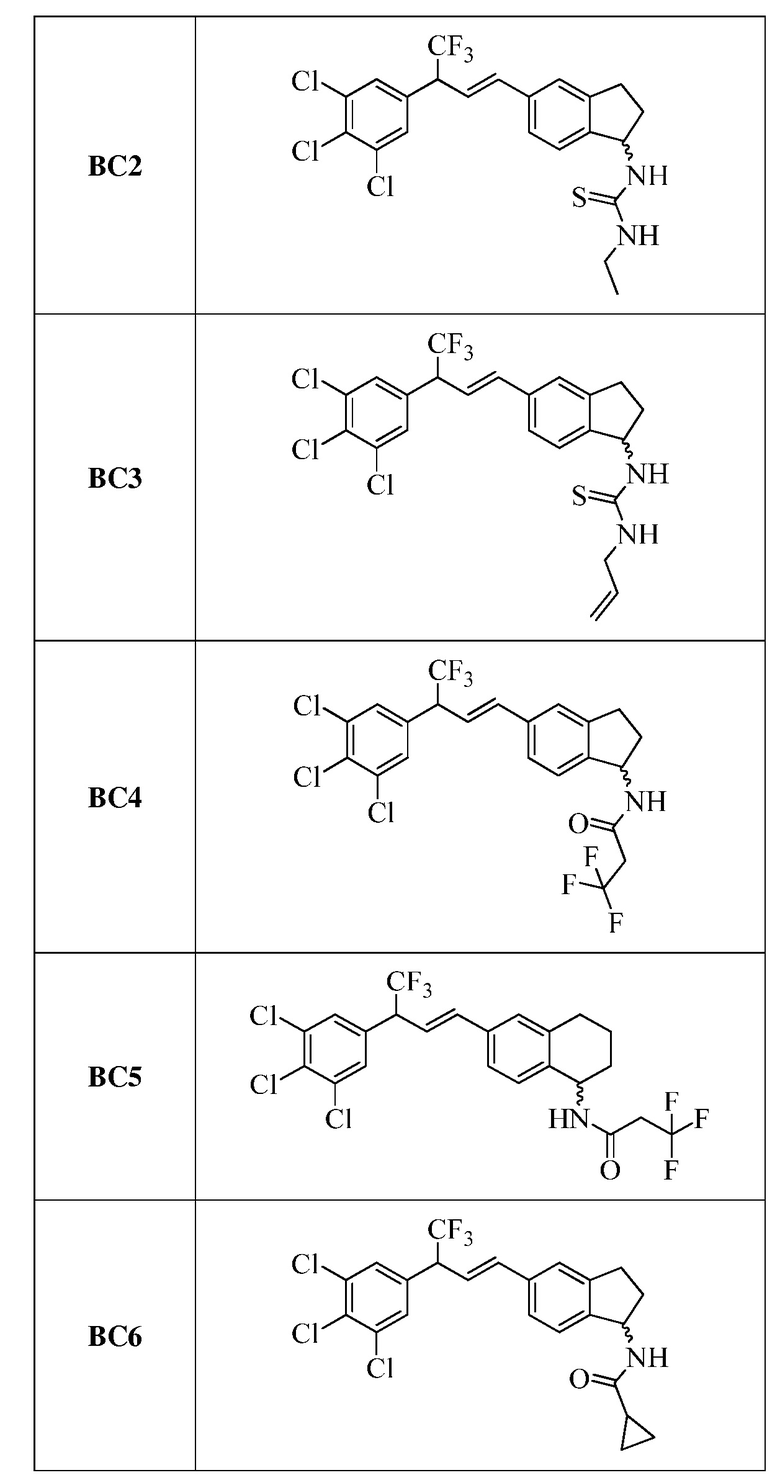
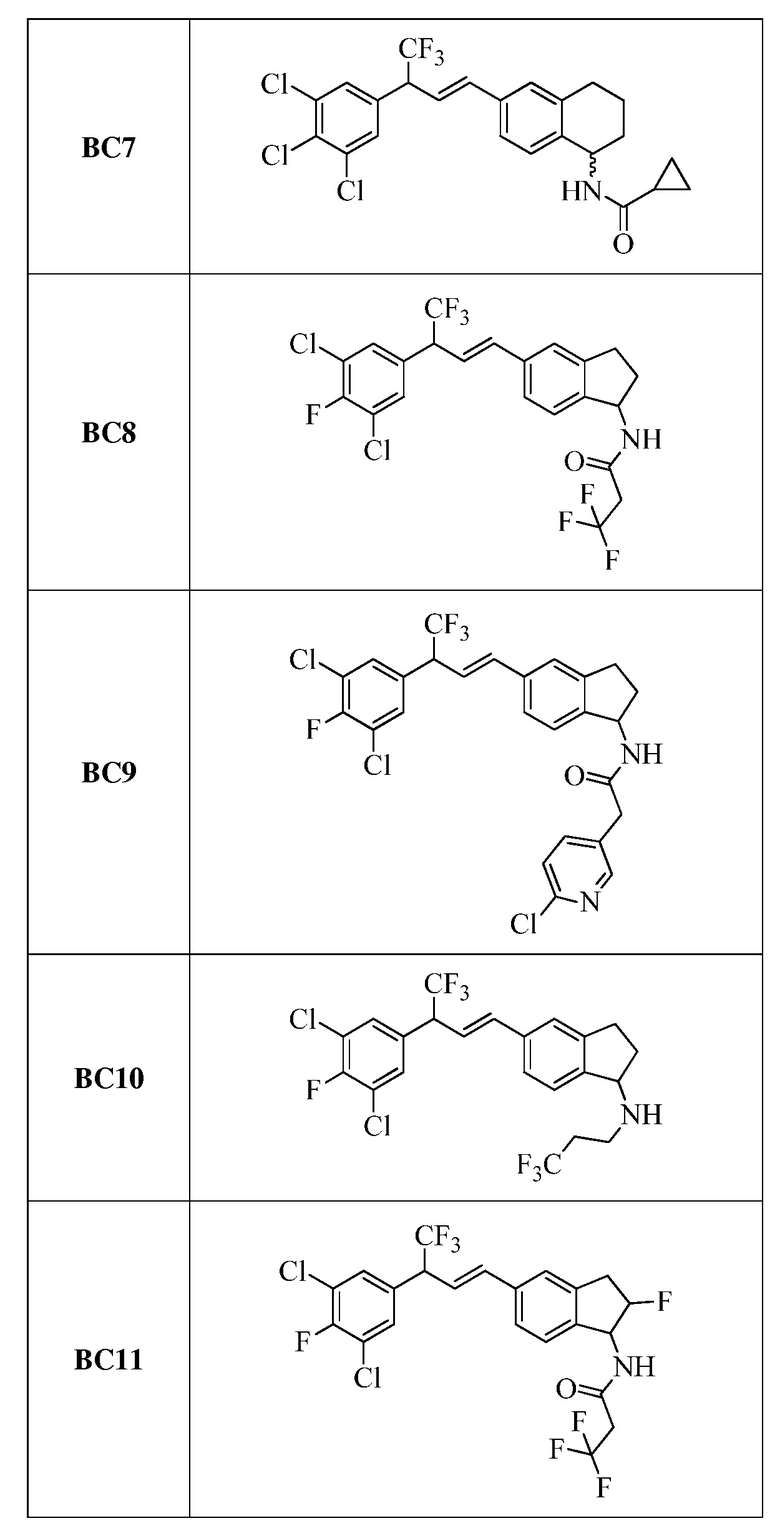
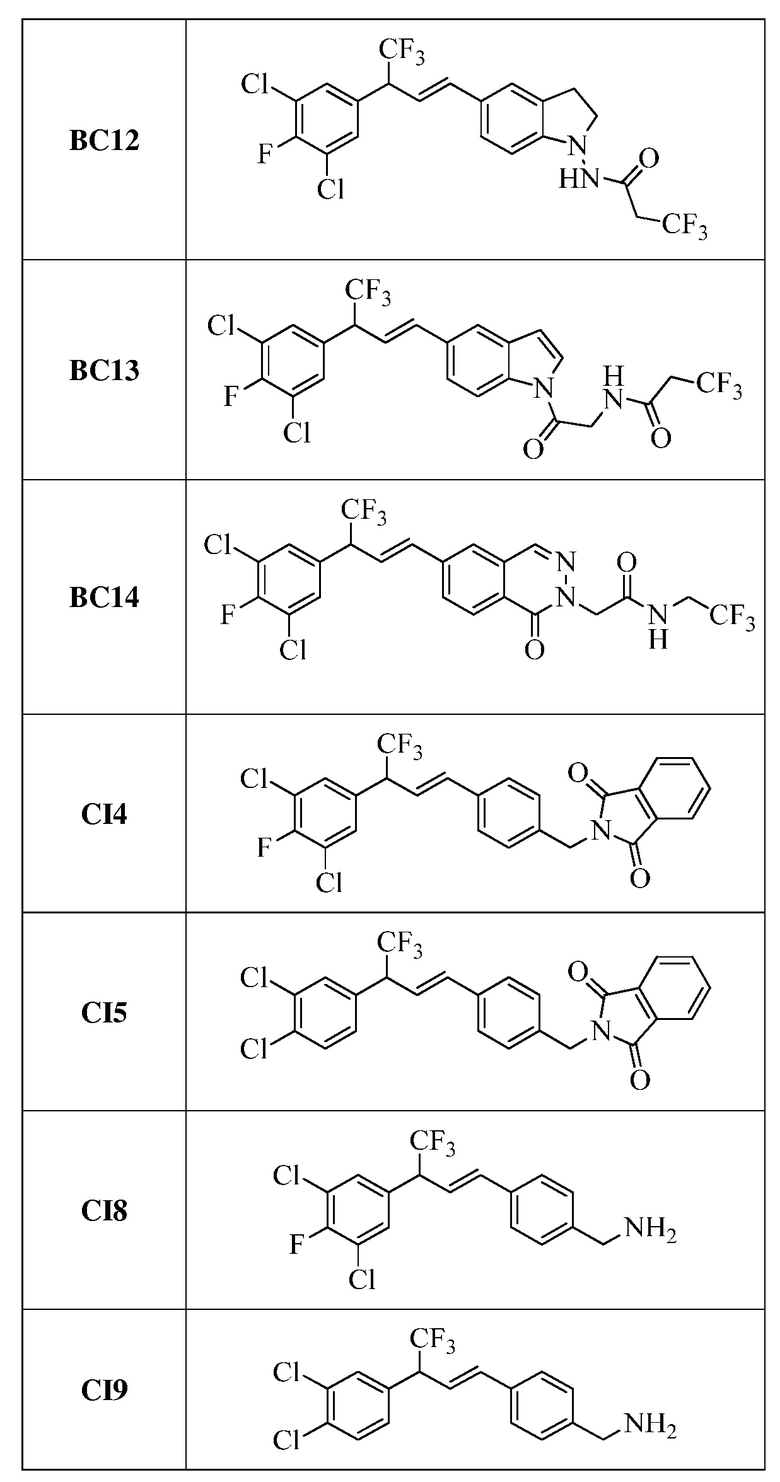
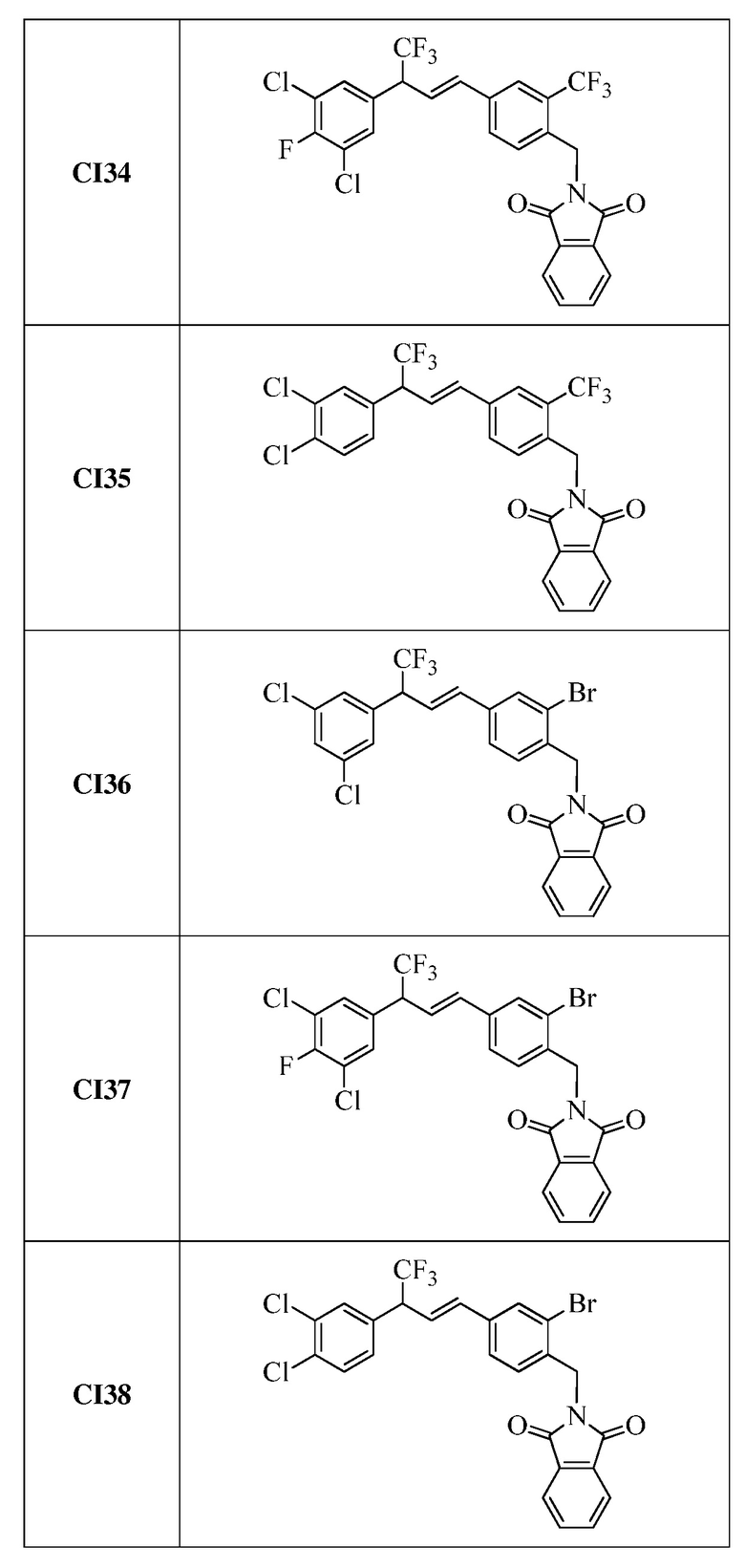
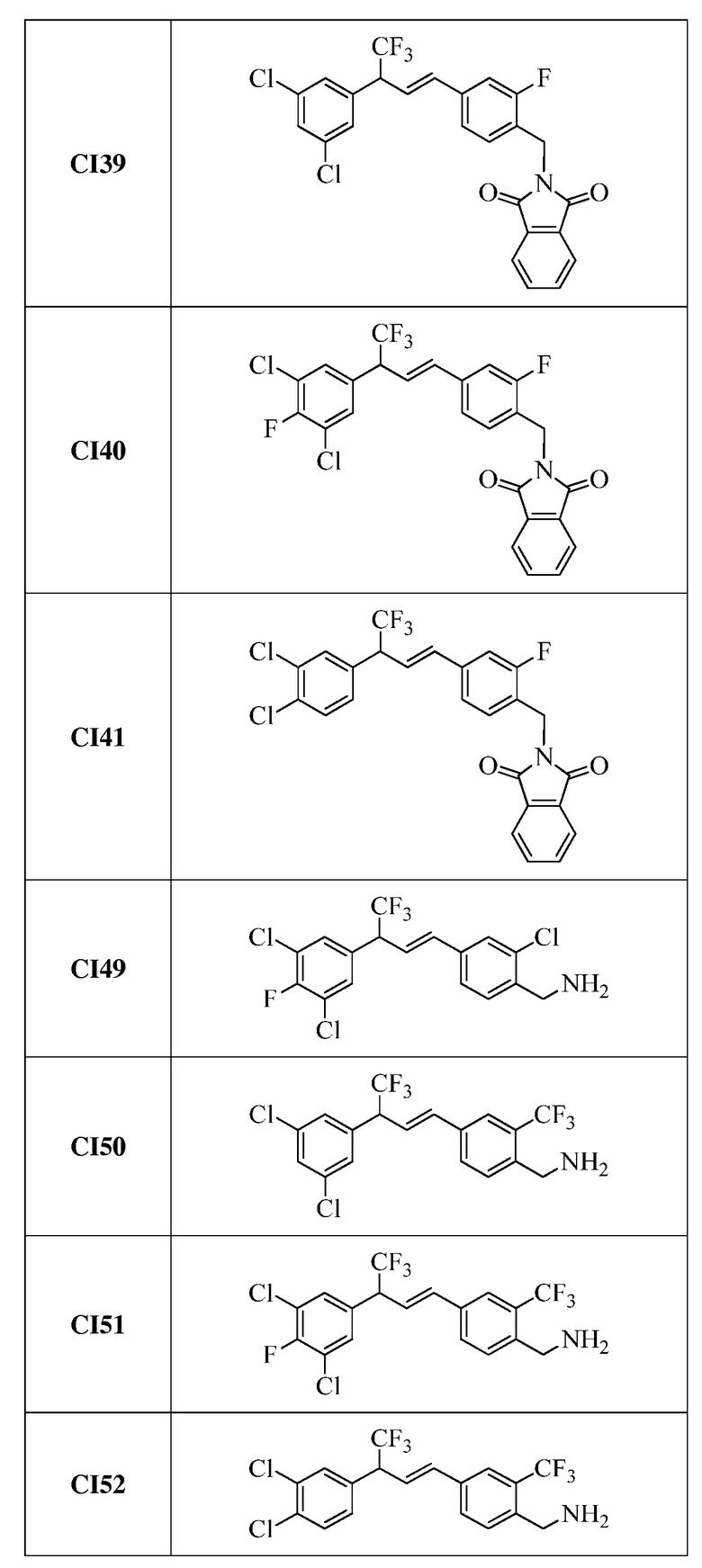
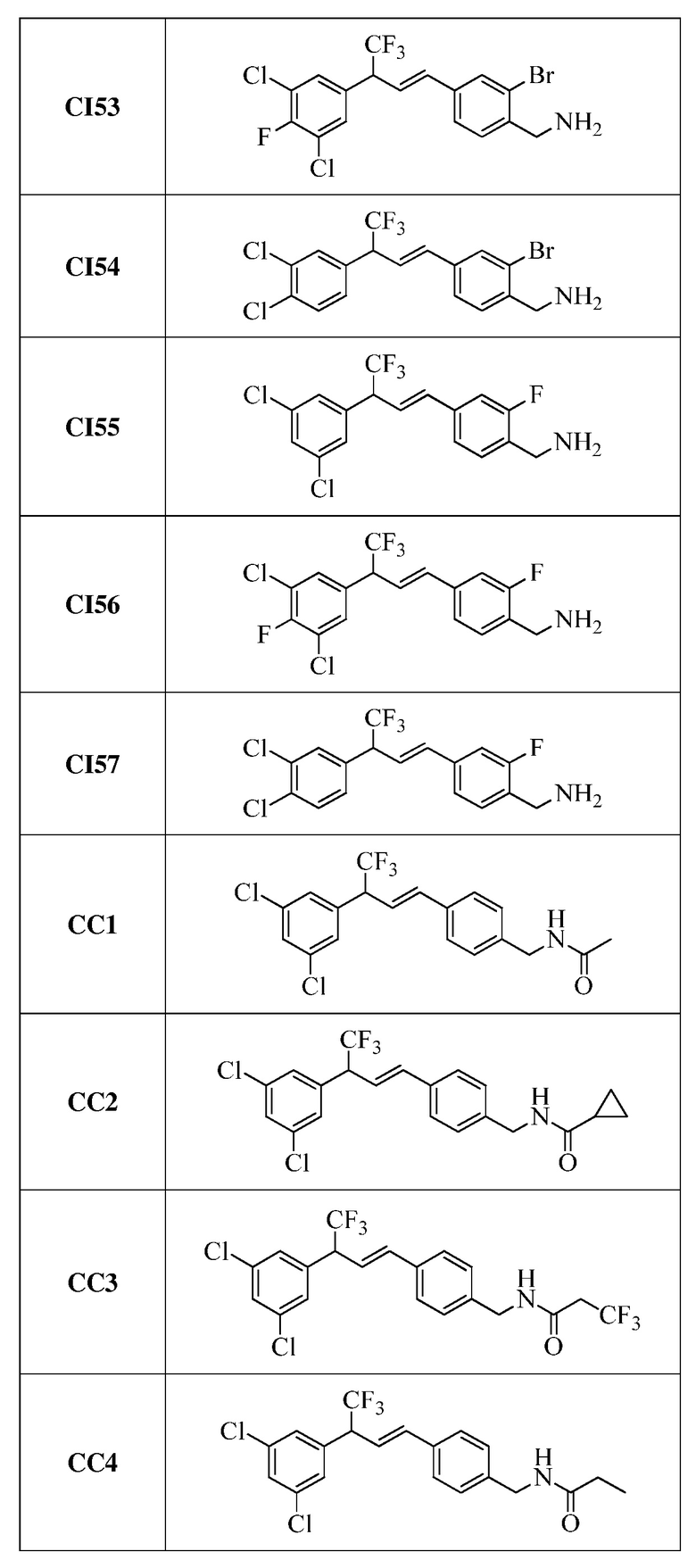
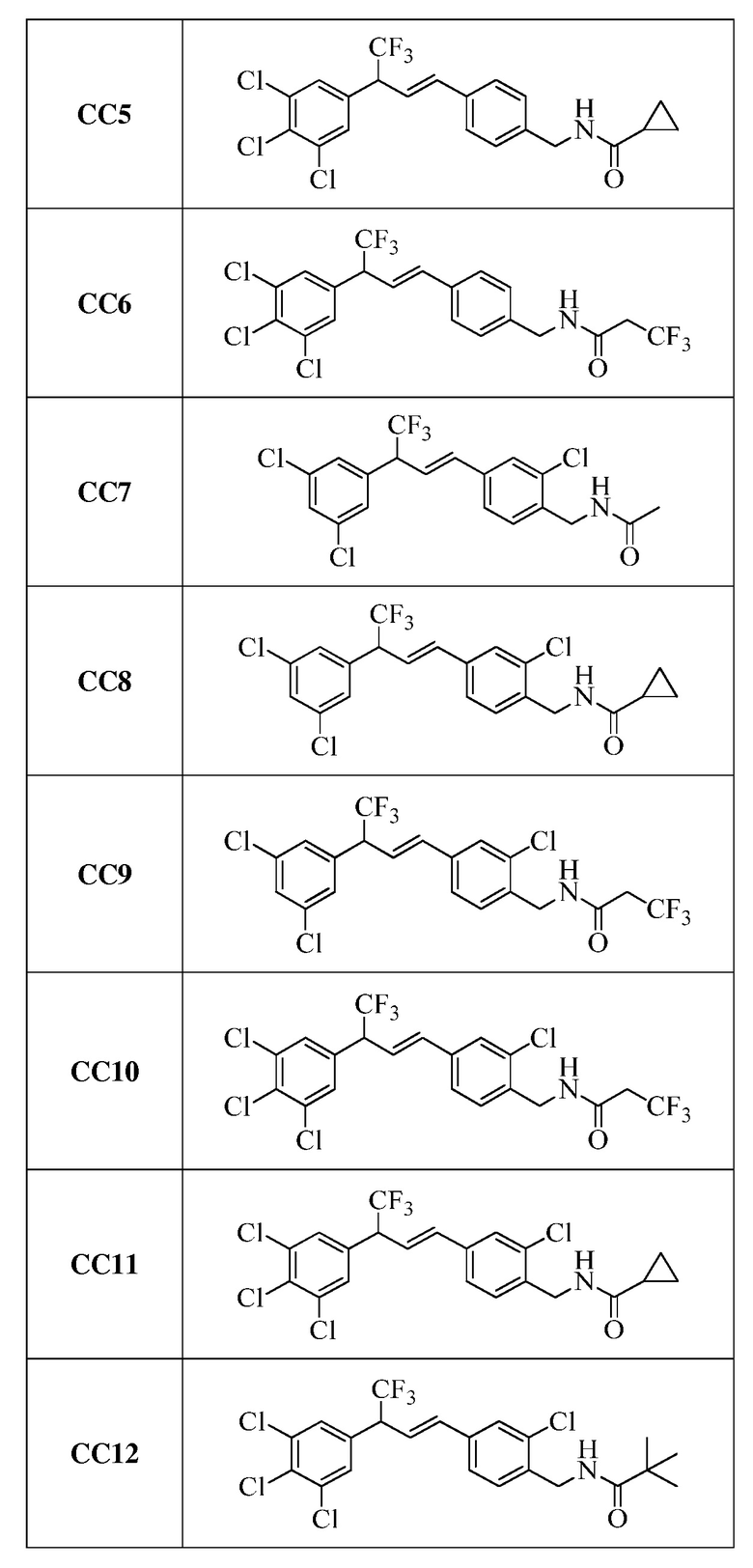
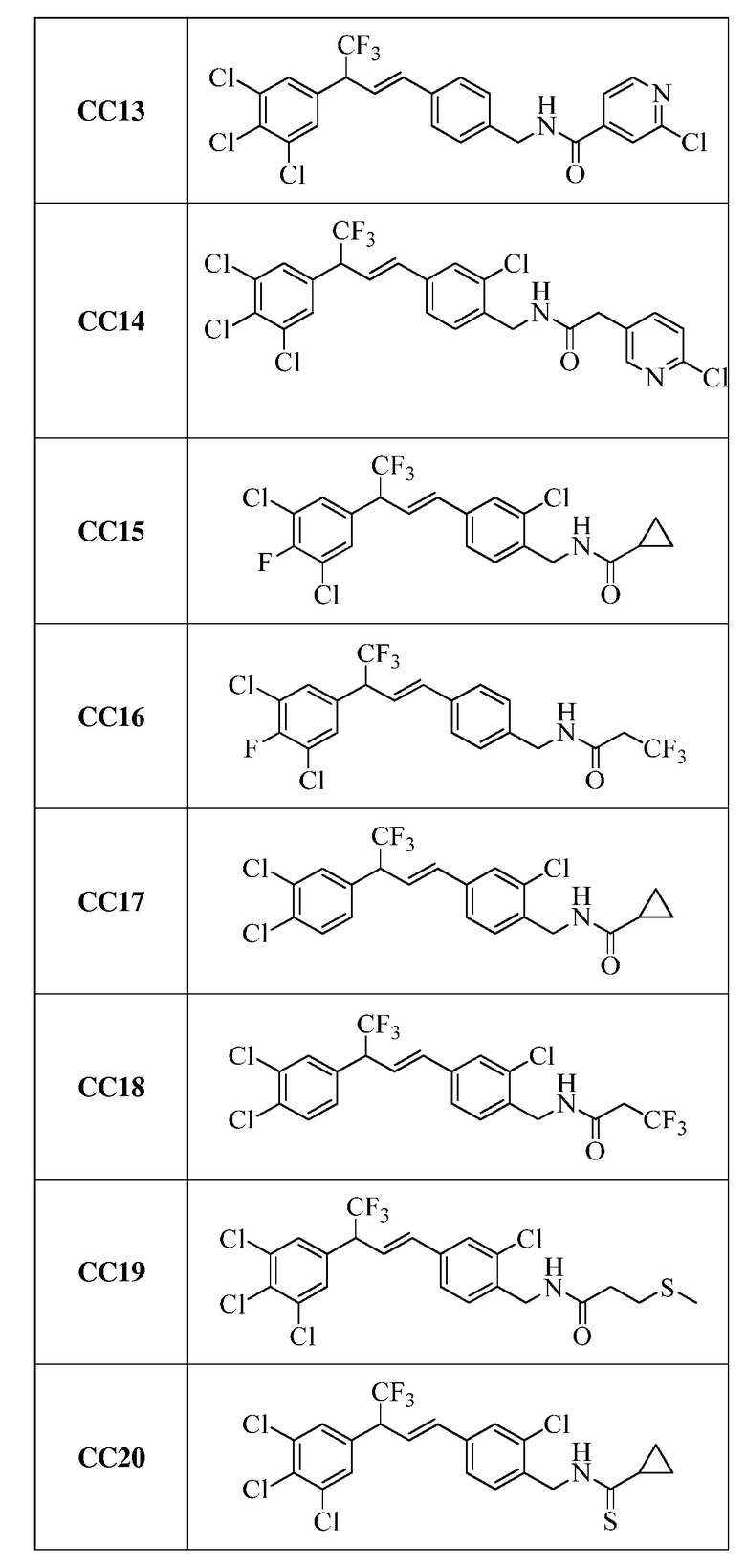
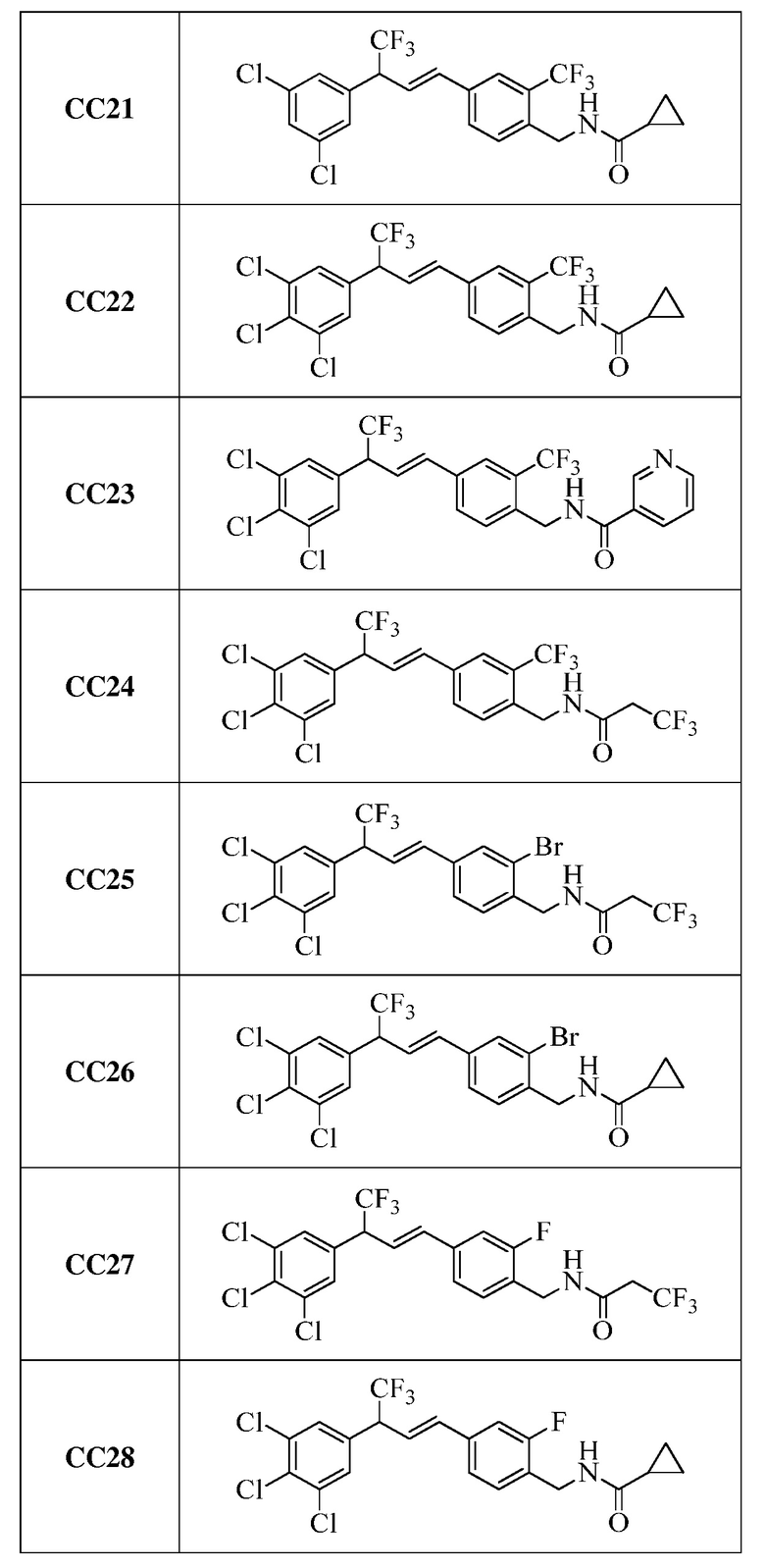
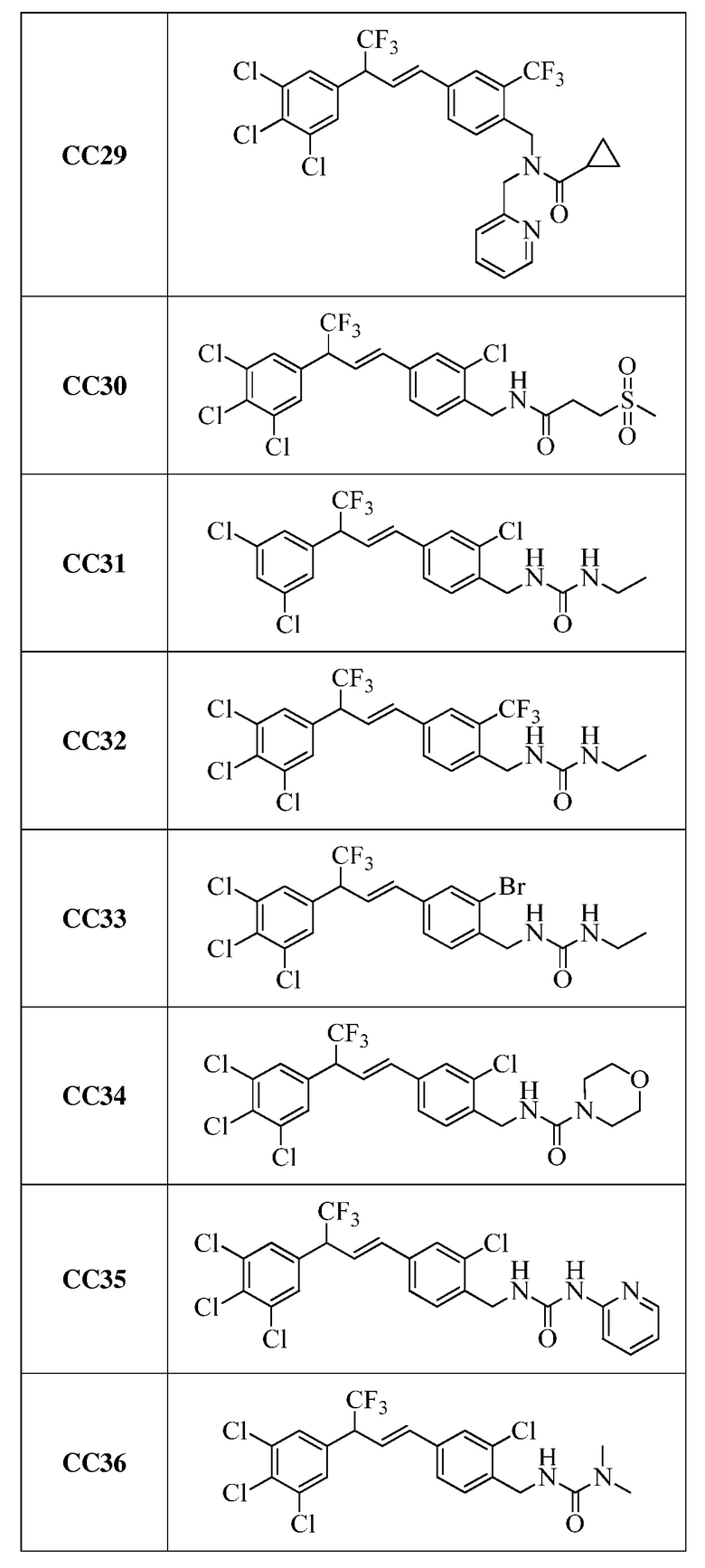
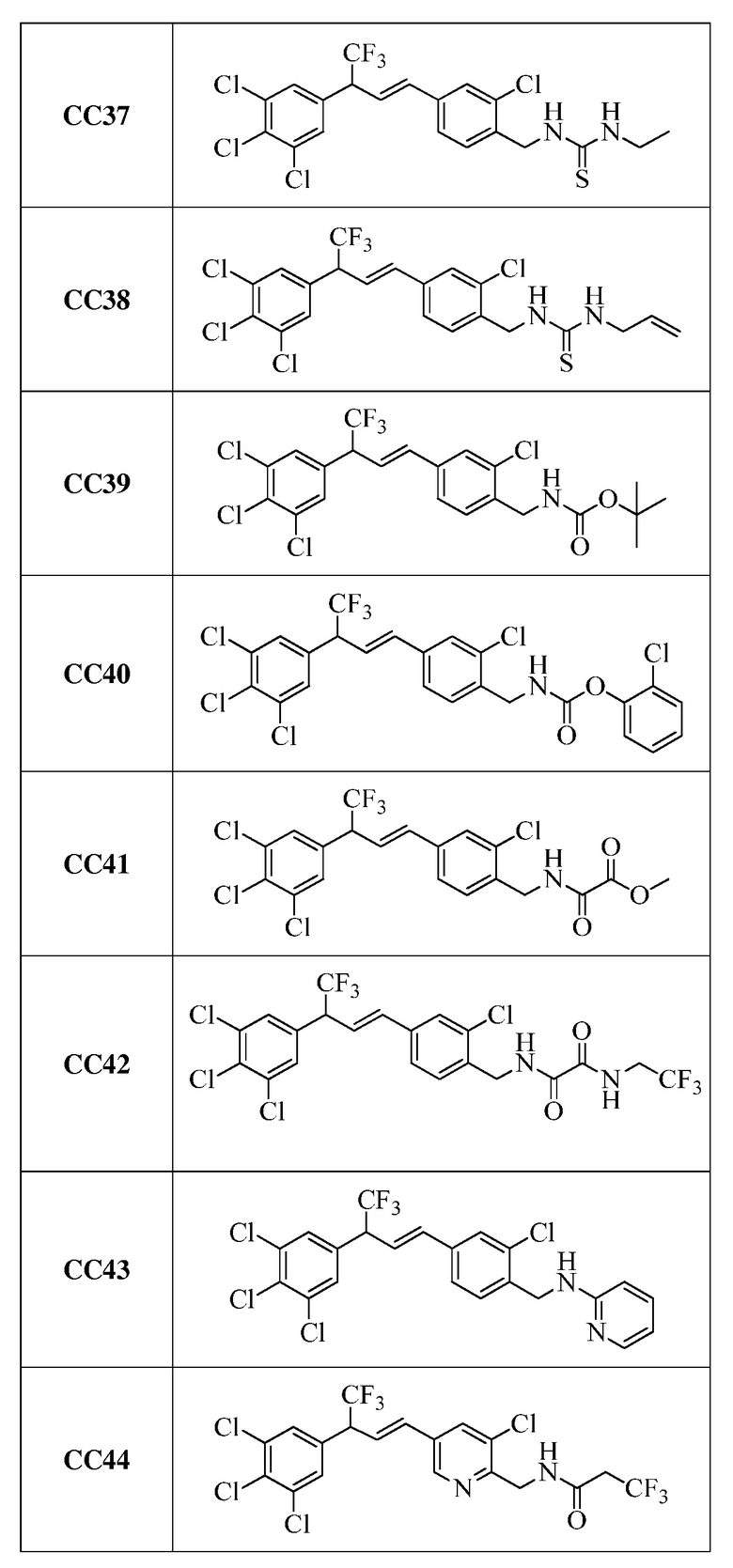
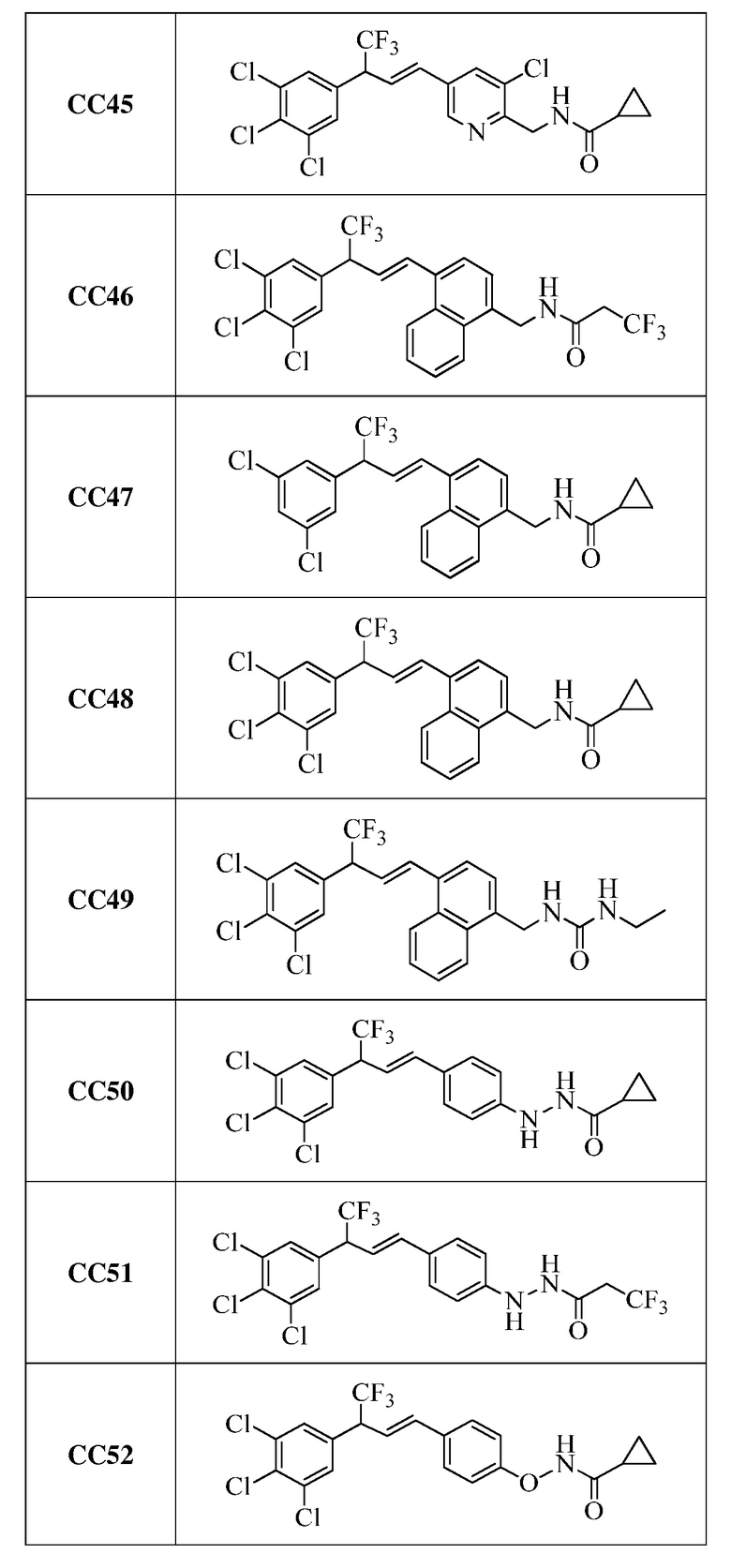
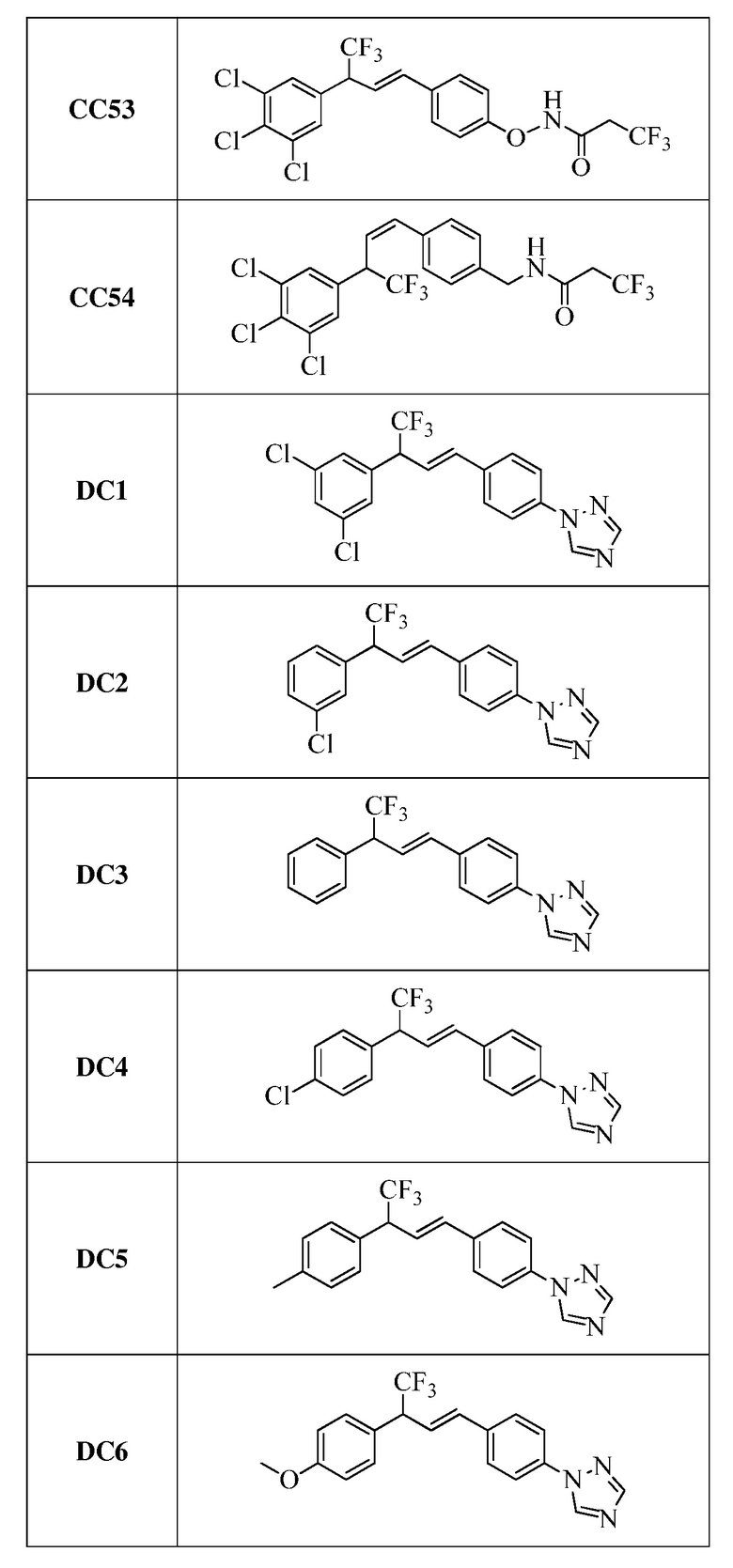
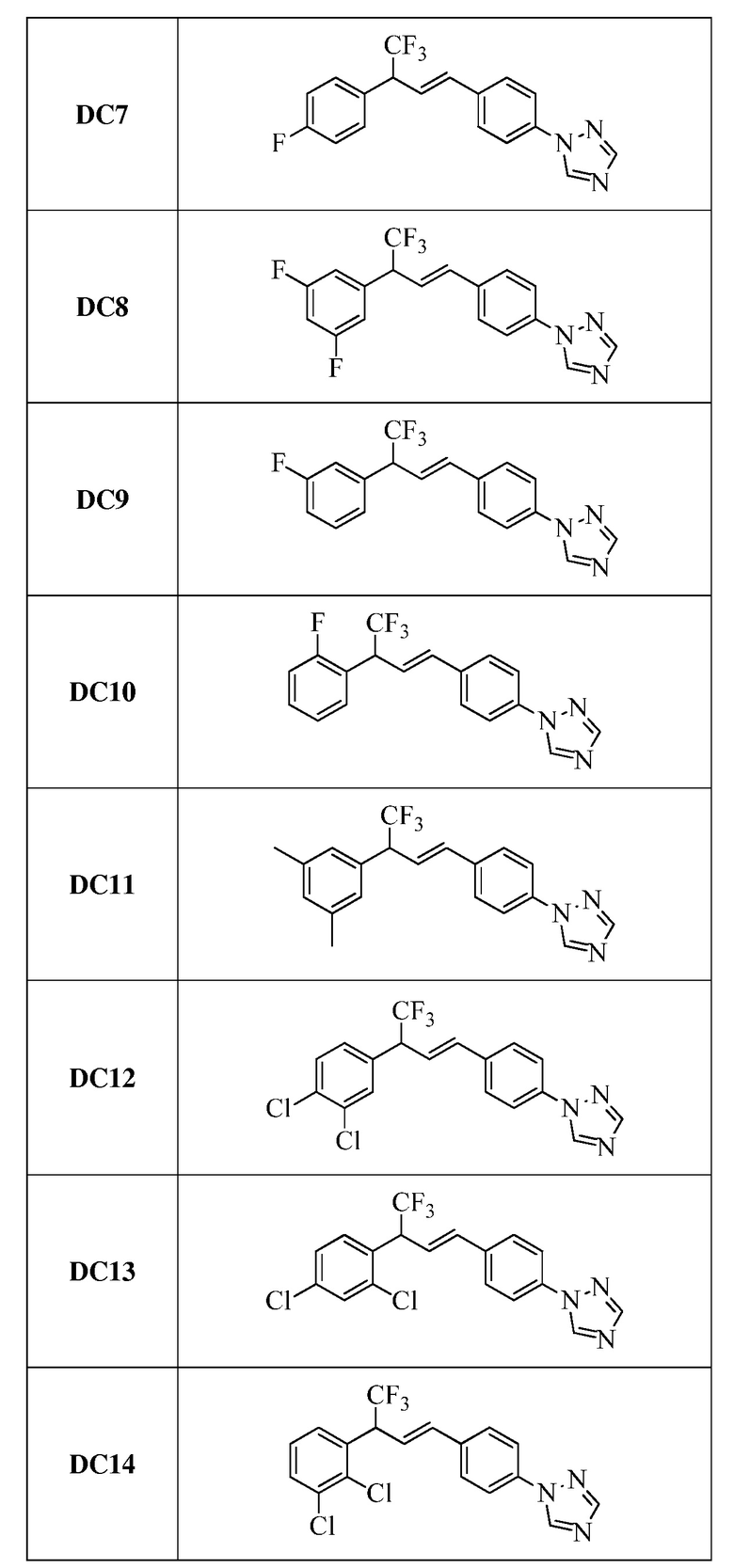
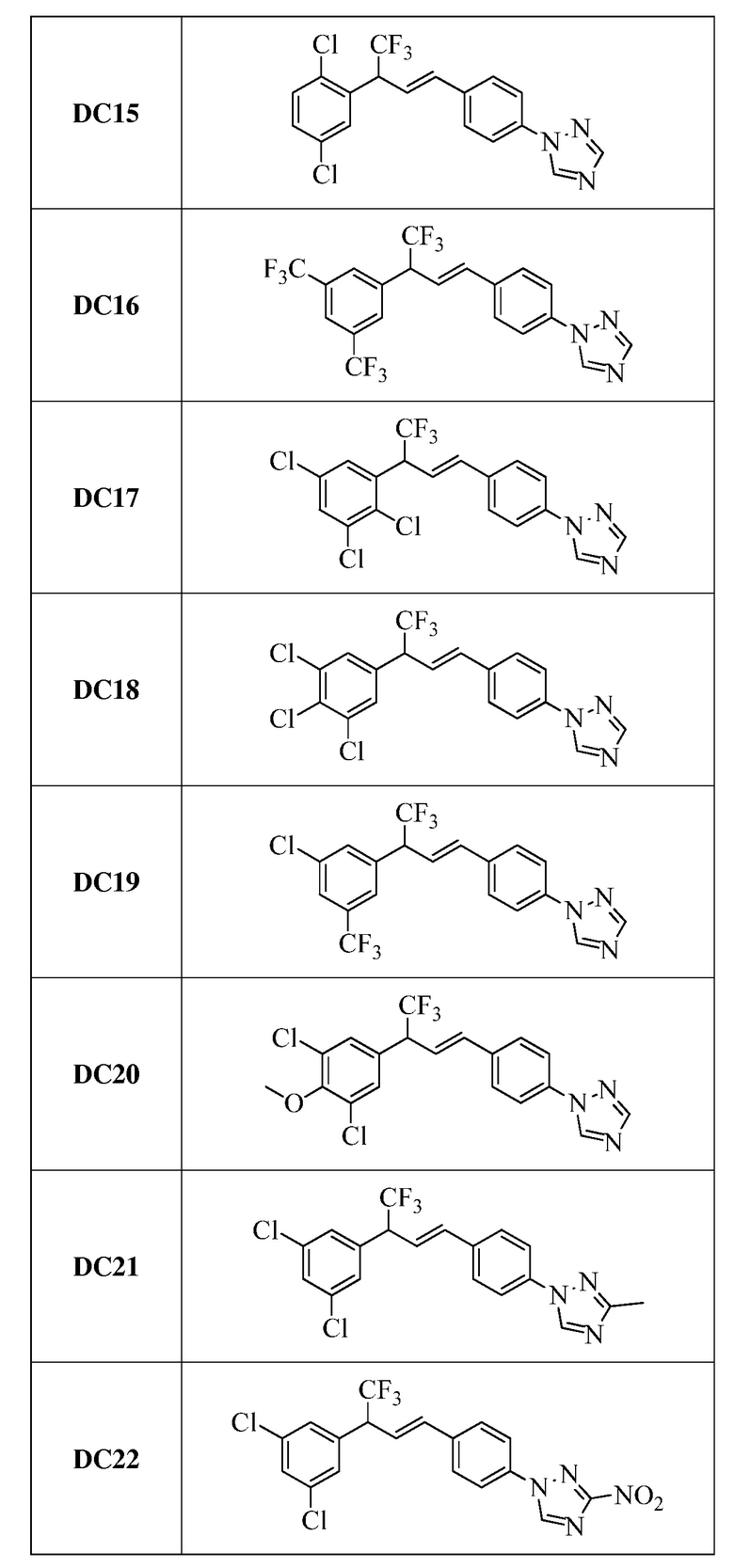
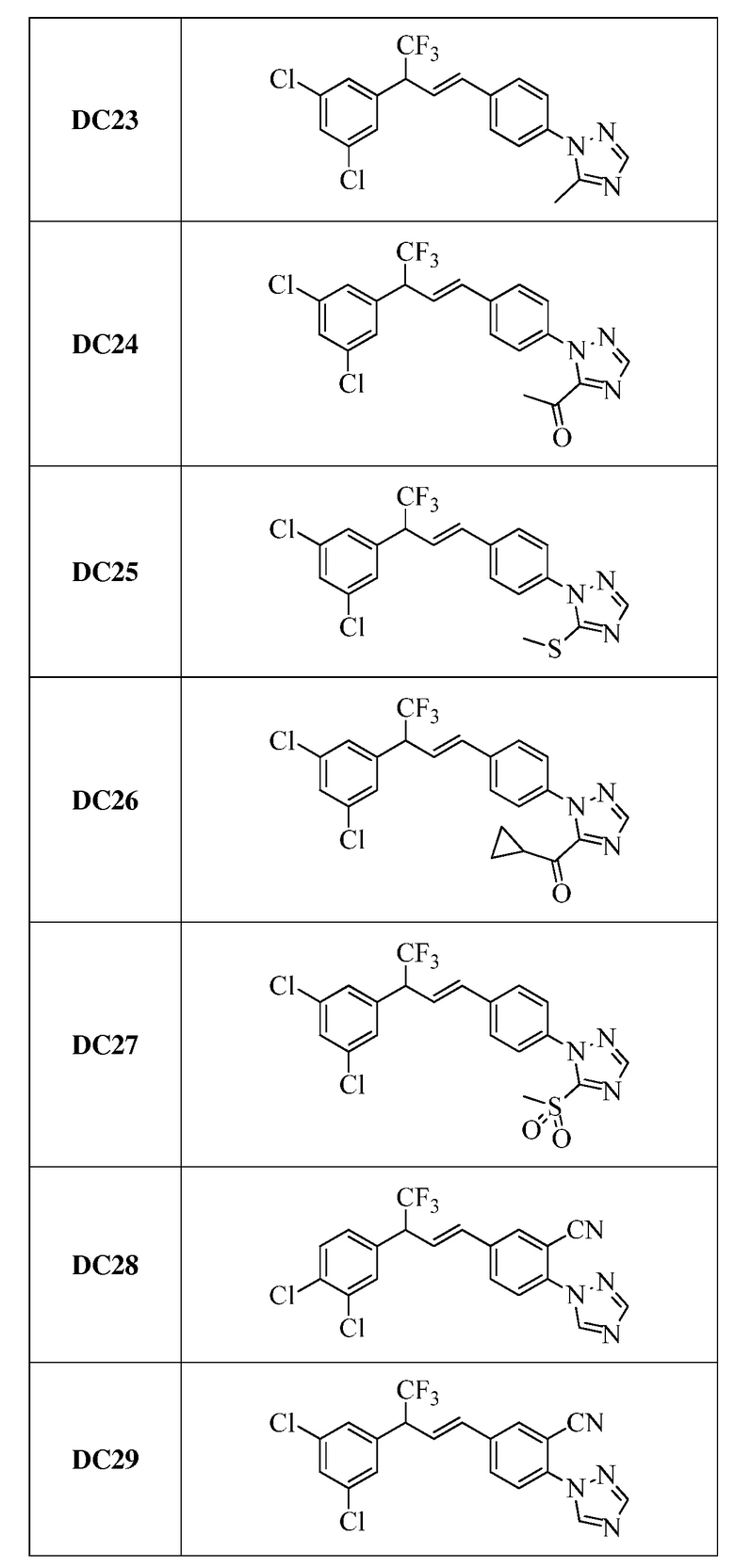
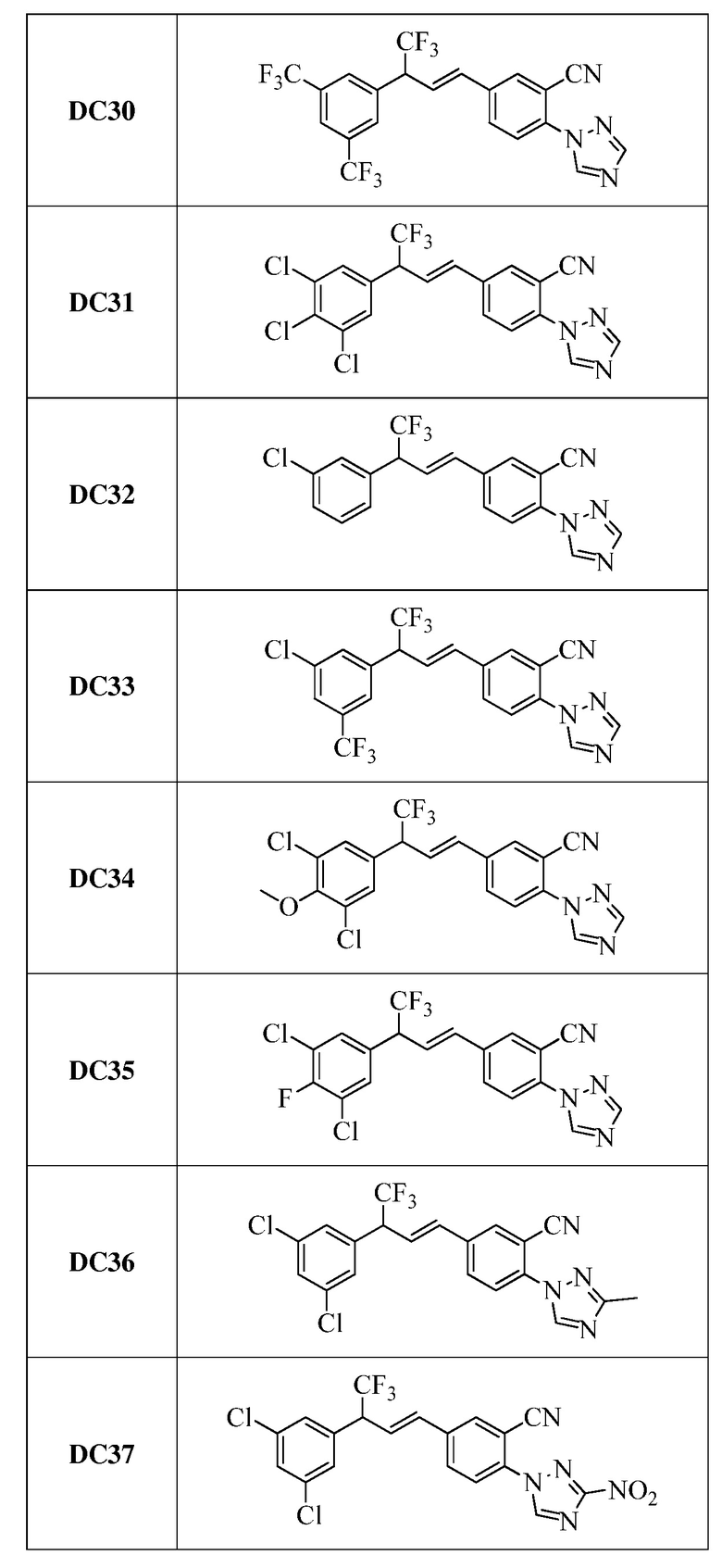
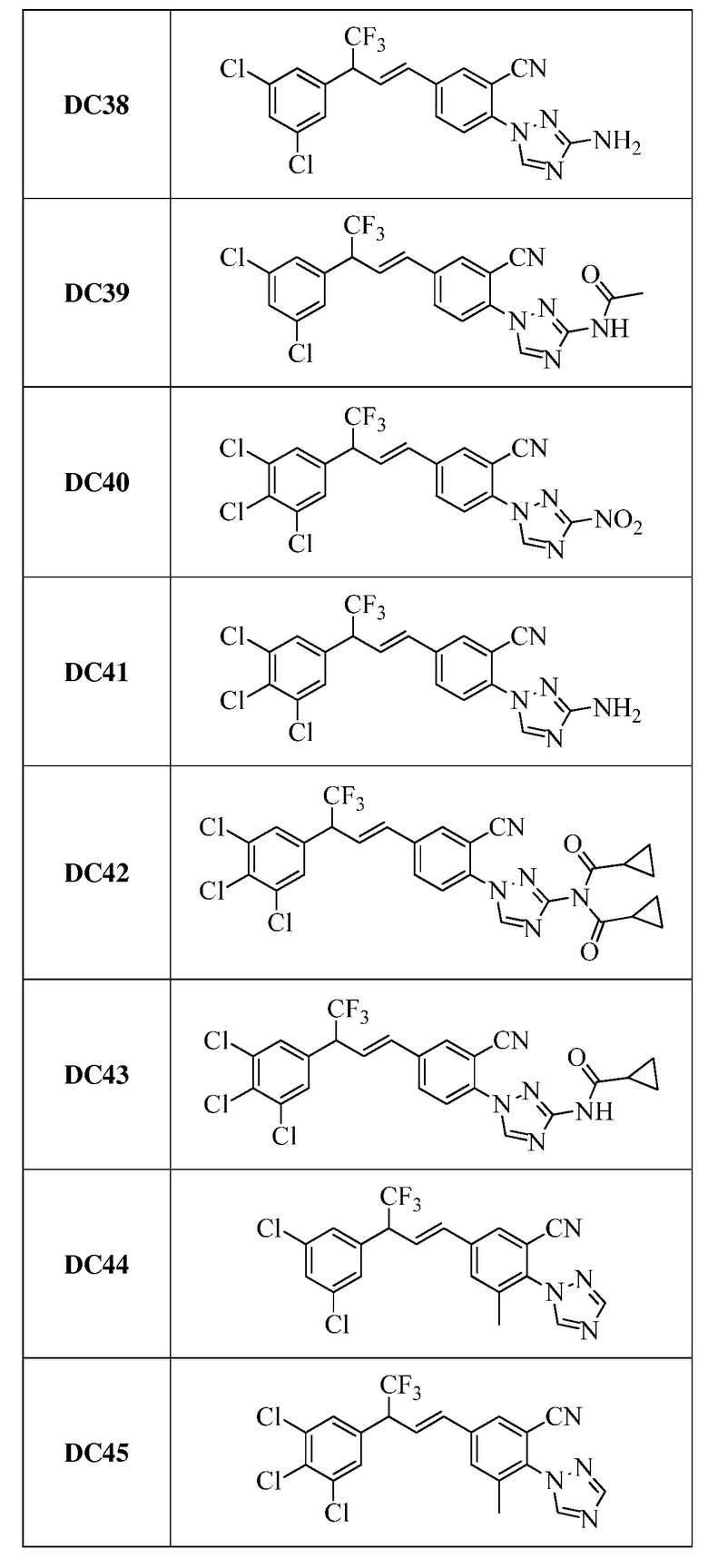
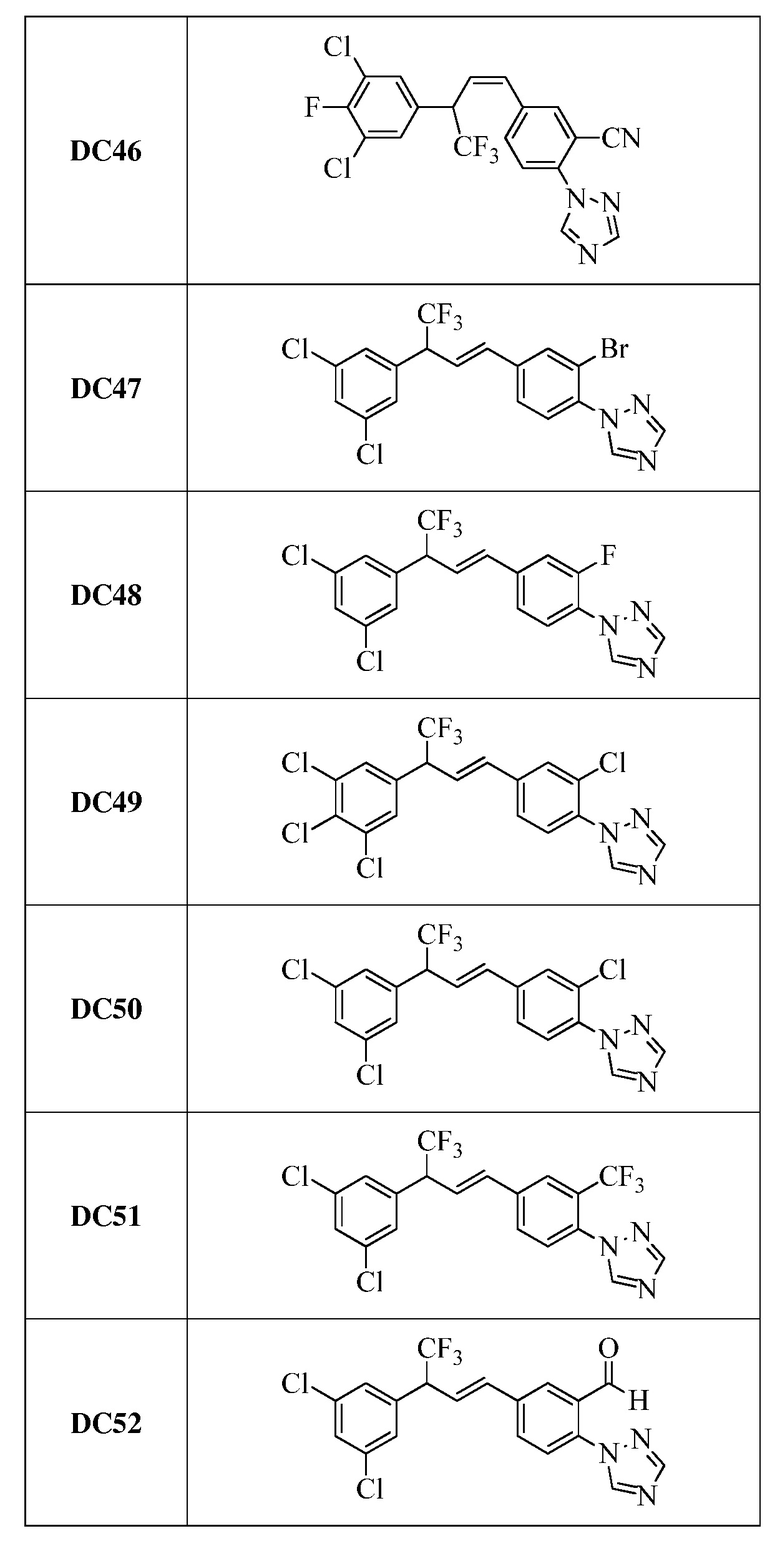
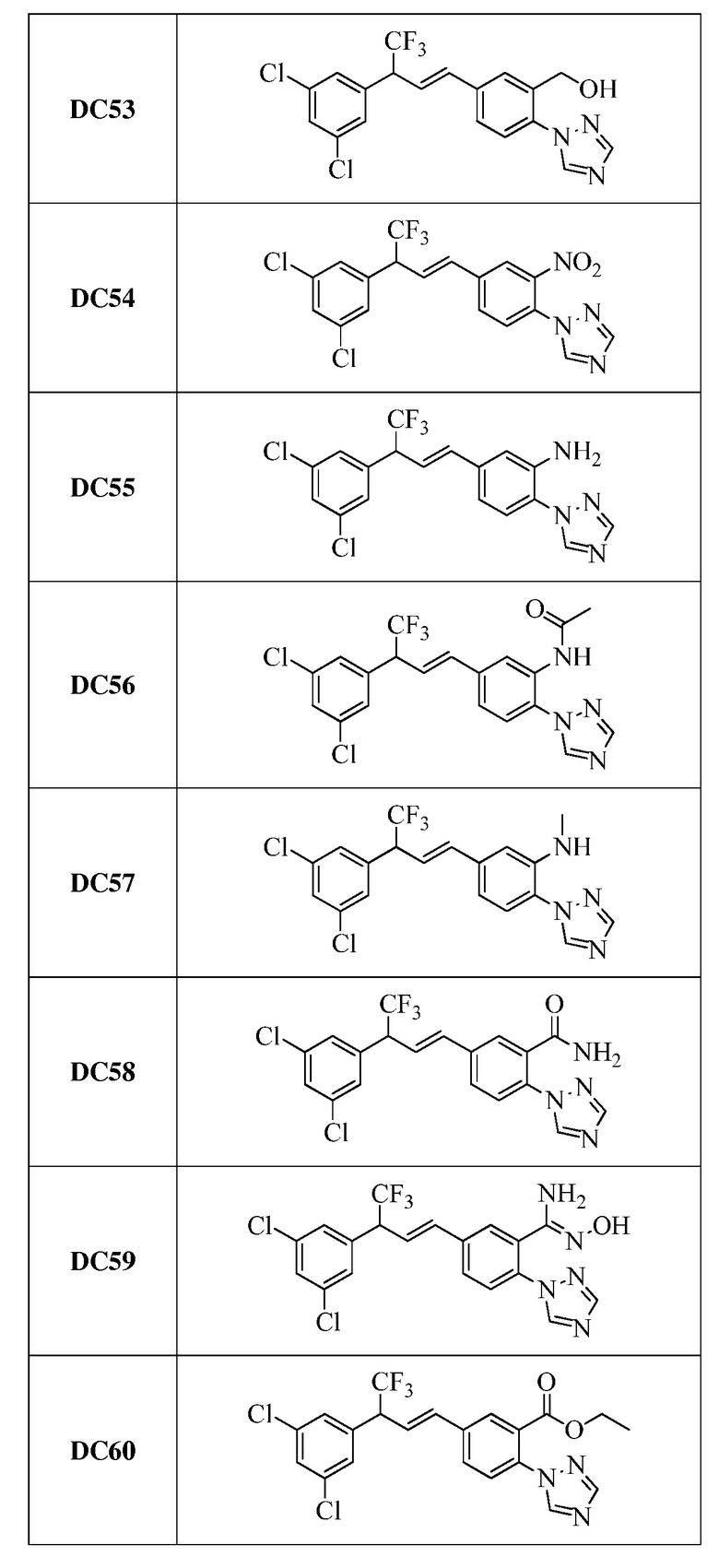
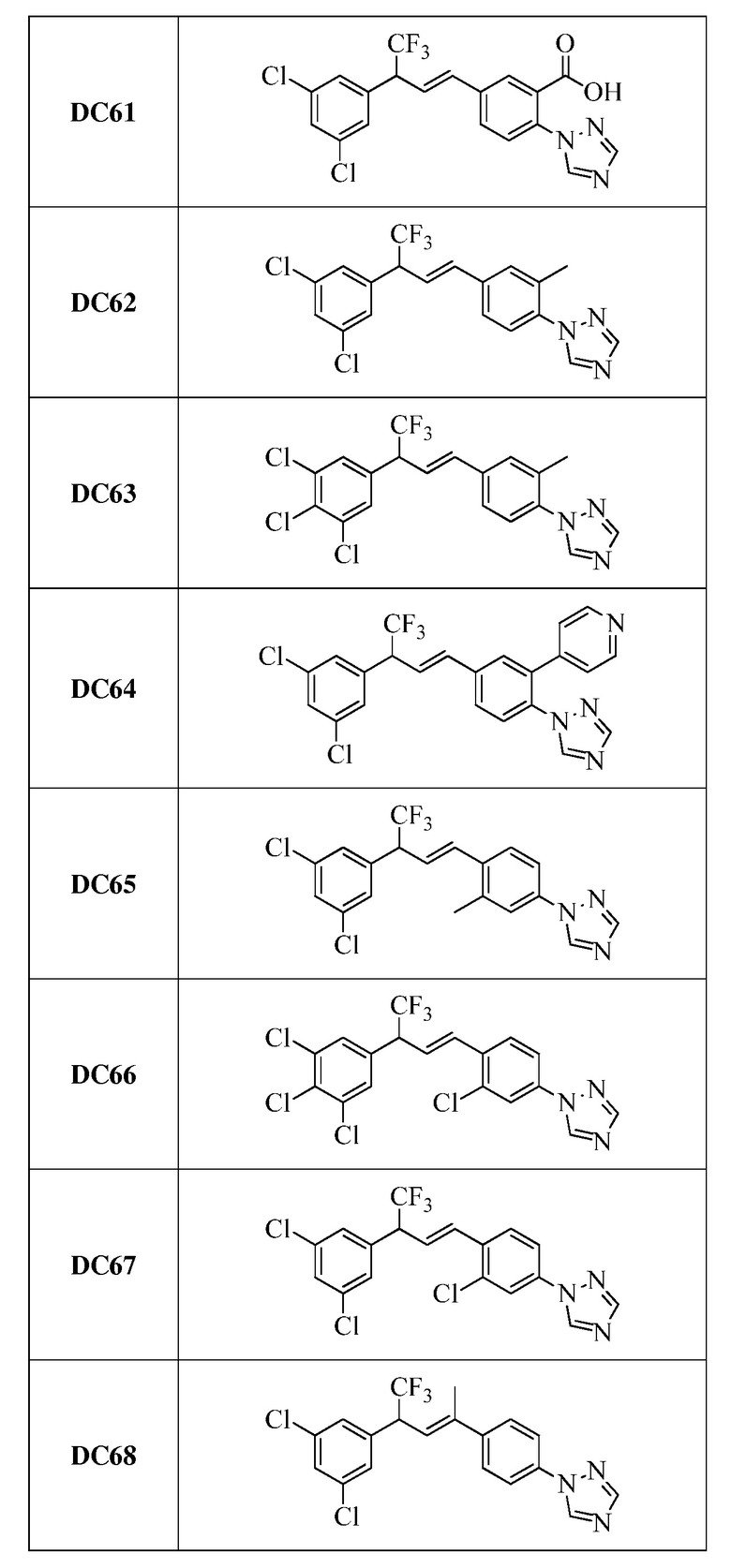
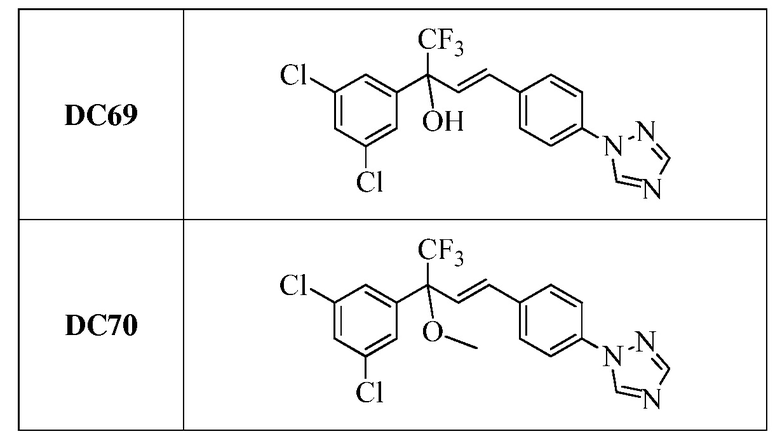
Структуры соединений F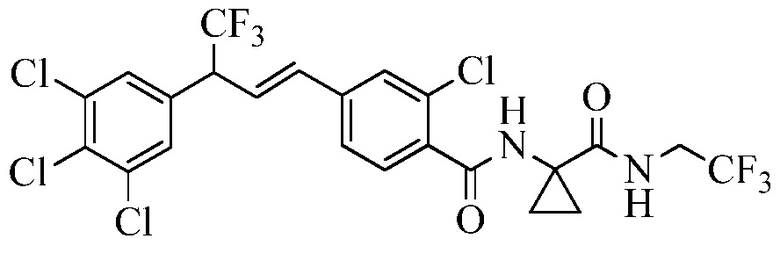
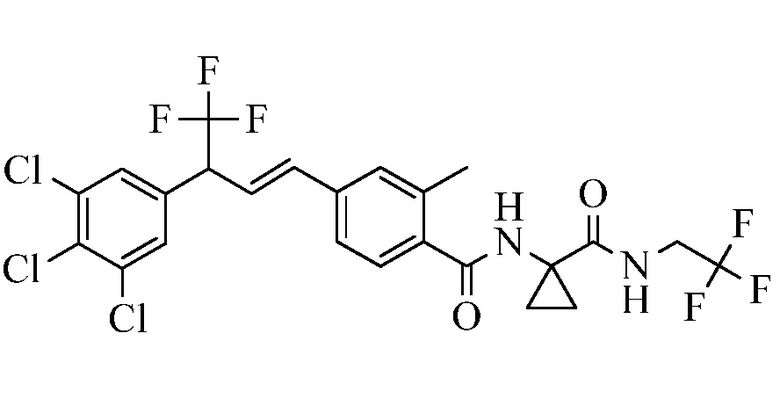
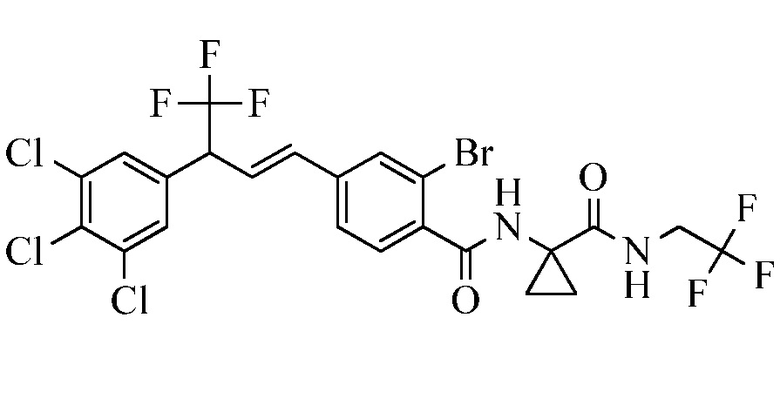
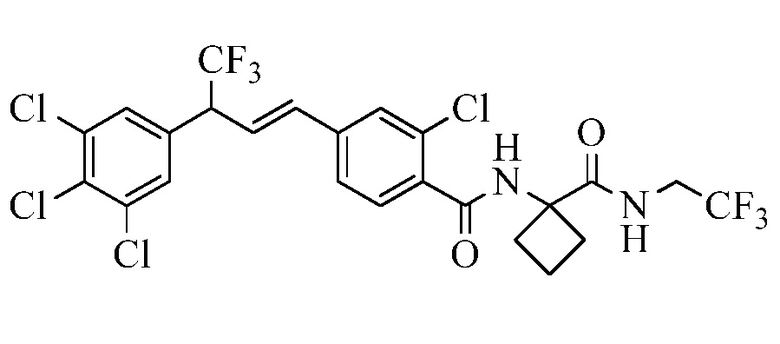

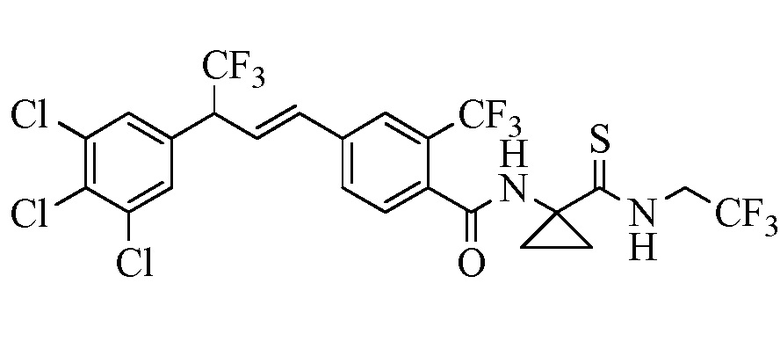
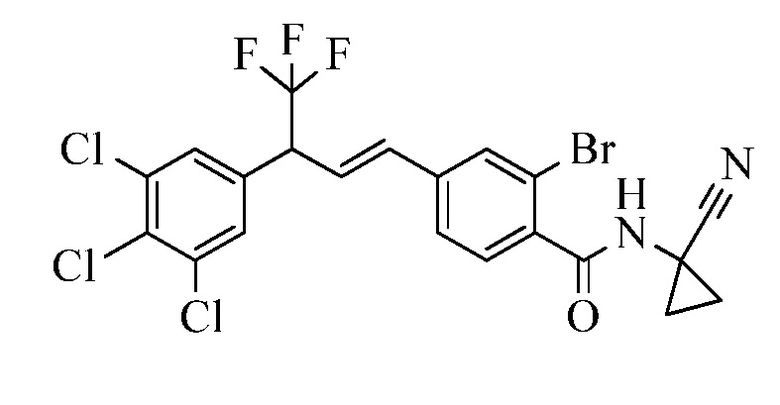
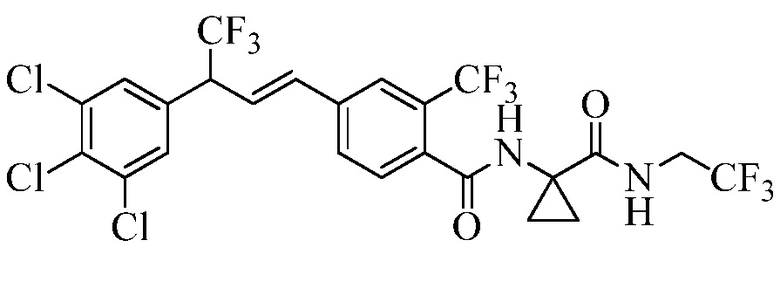

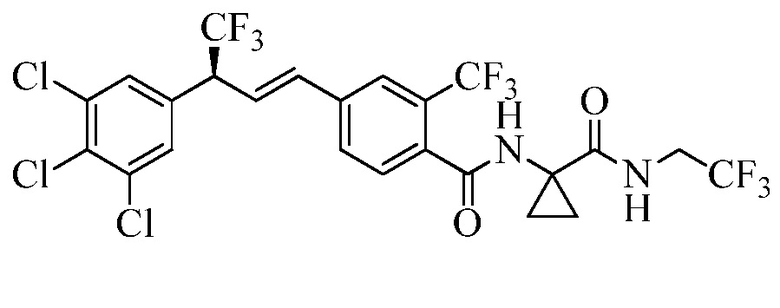
Структуры предполагаемых соединений, представленных впоследствии
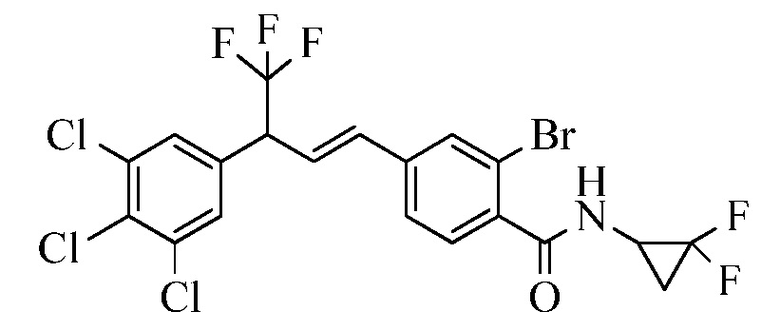
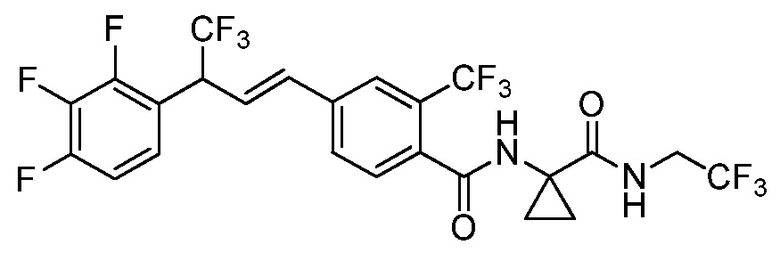
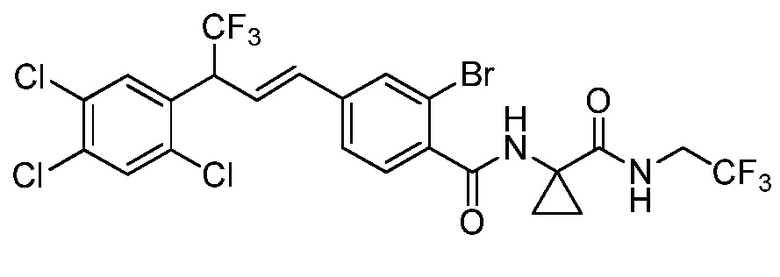
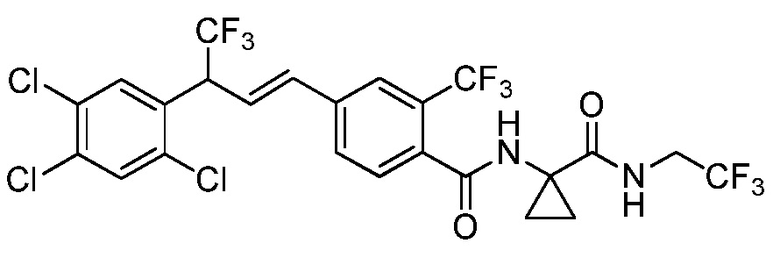
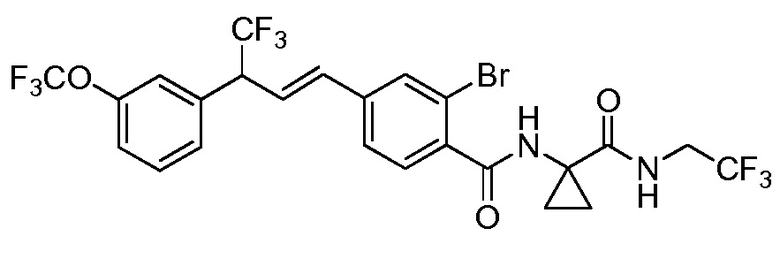
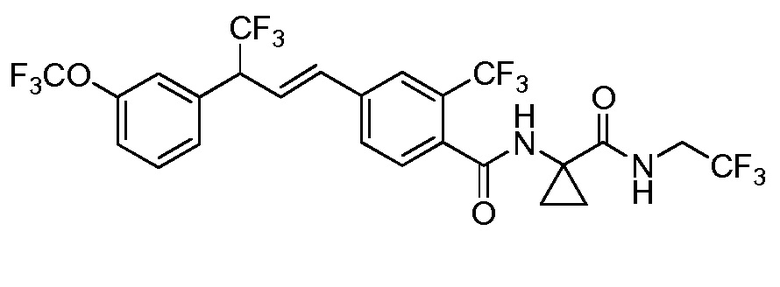
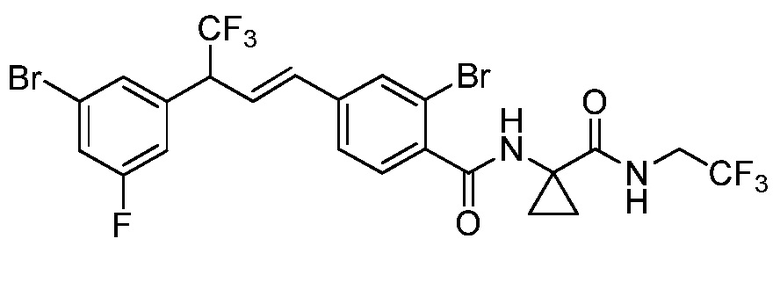
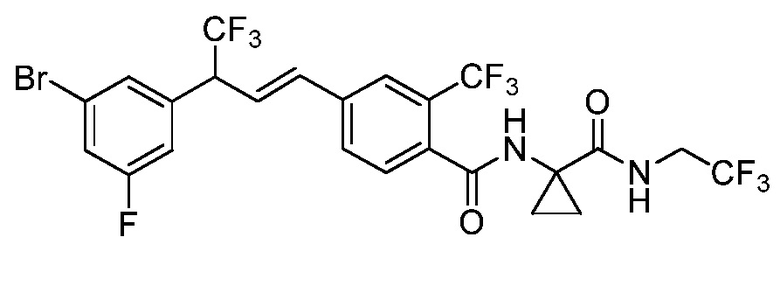
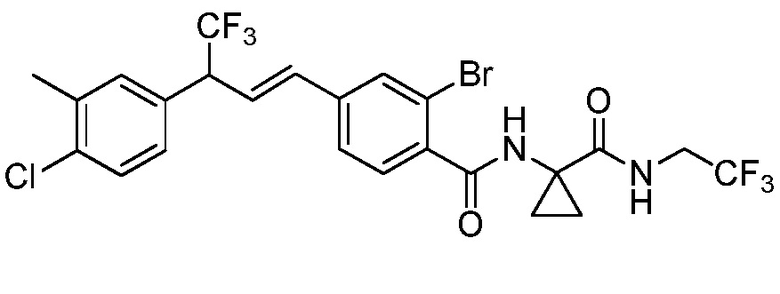
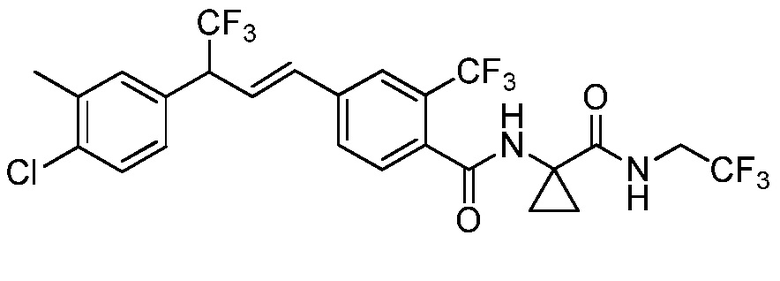
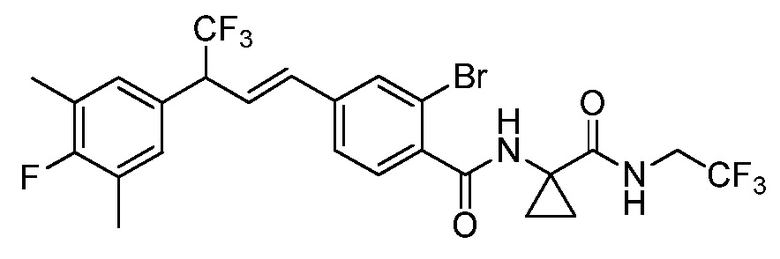
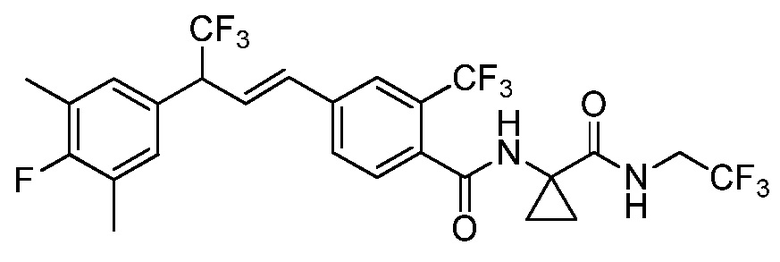
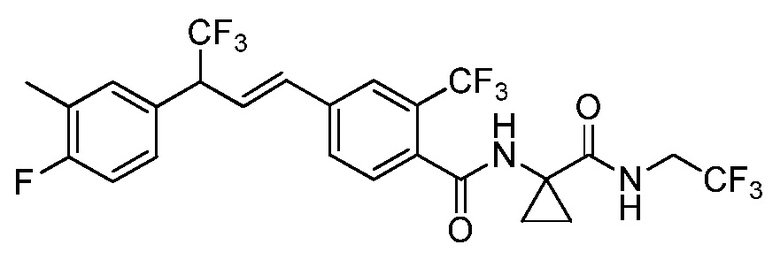
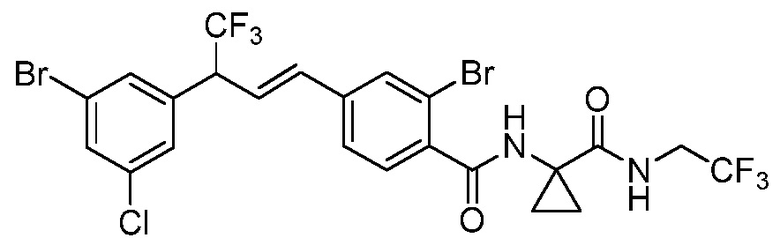


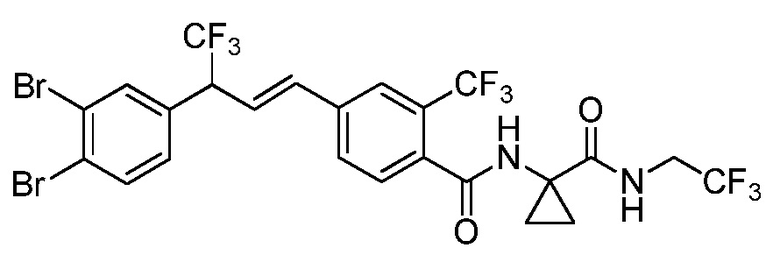

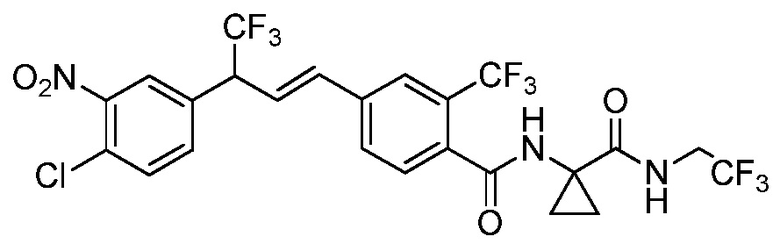
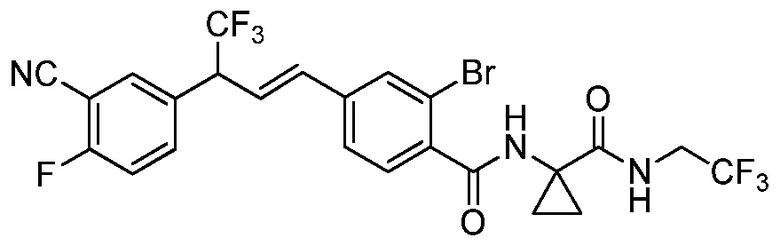
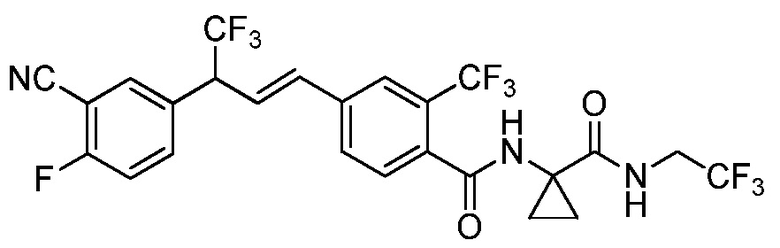
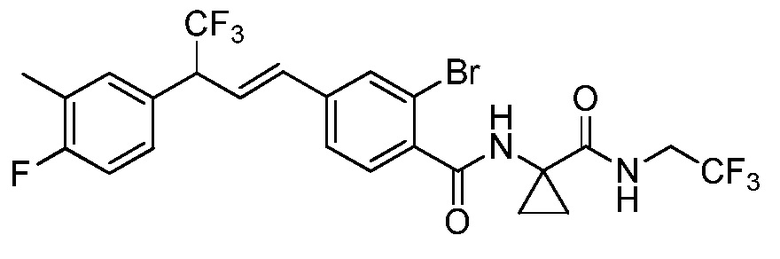
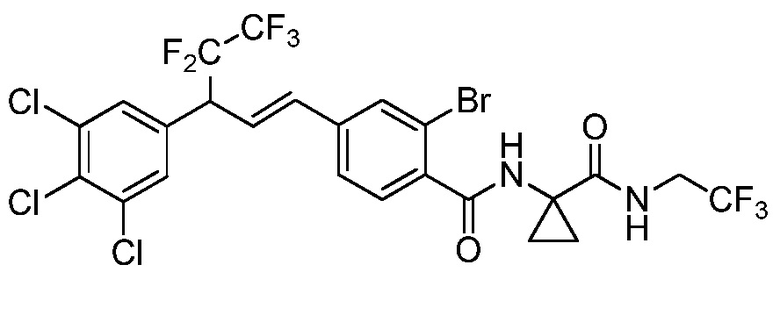
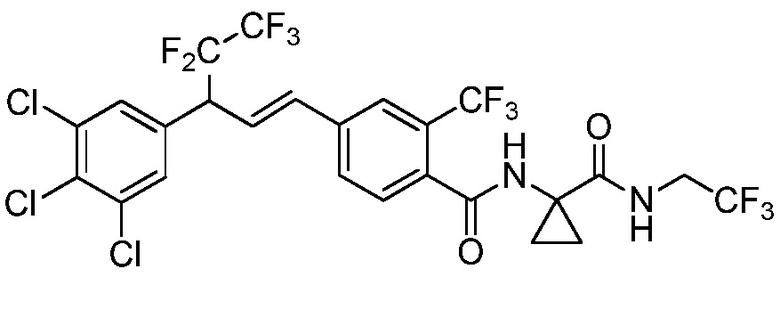
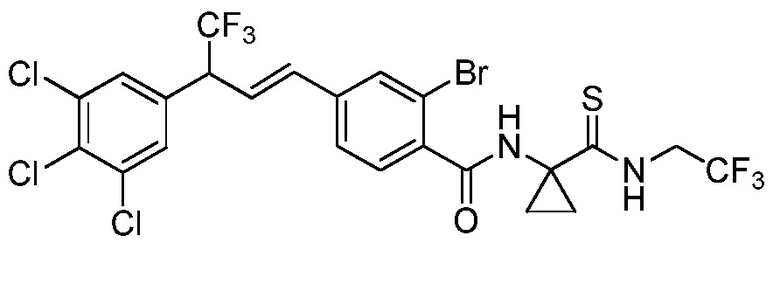
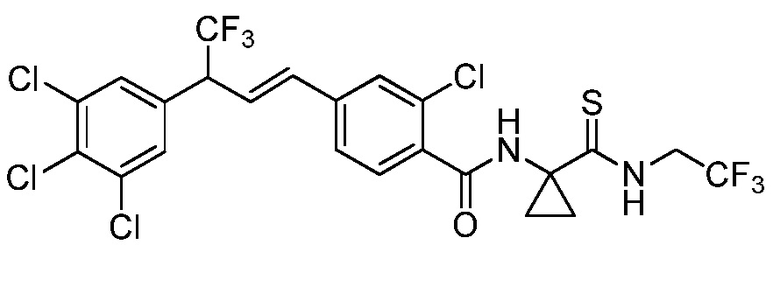
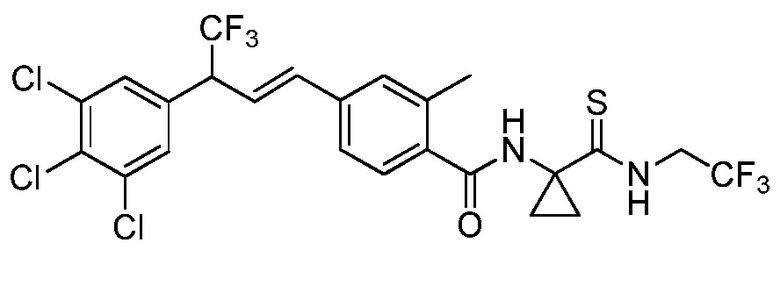
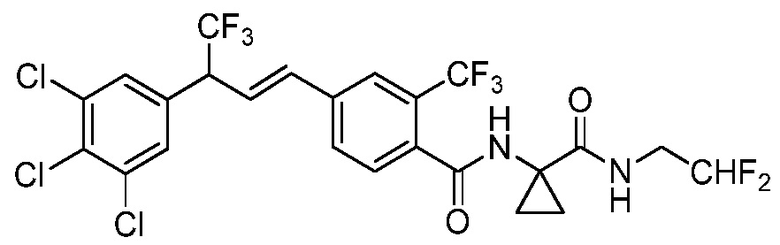
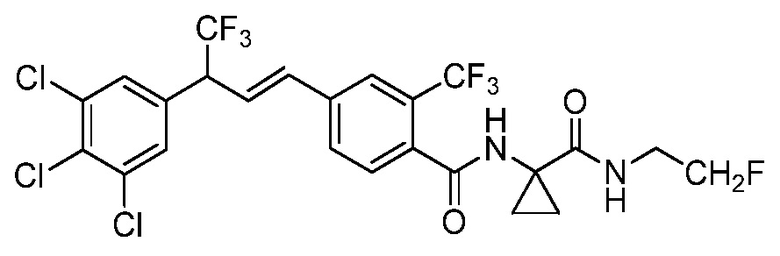
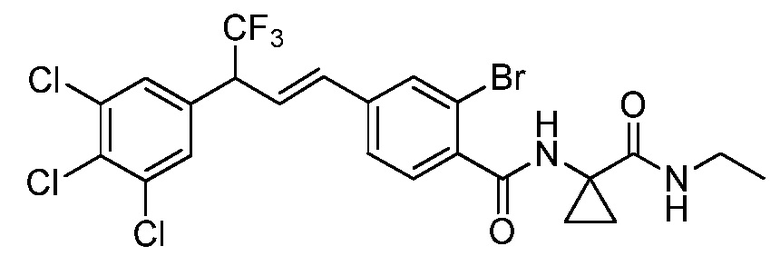
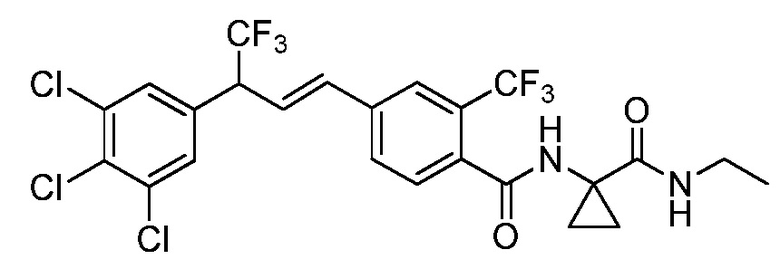
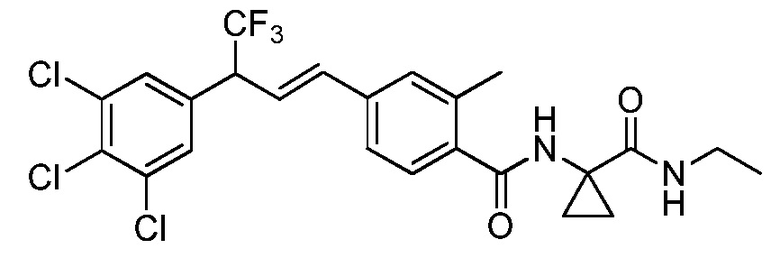
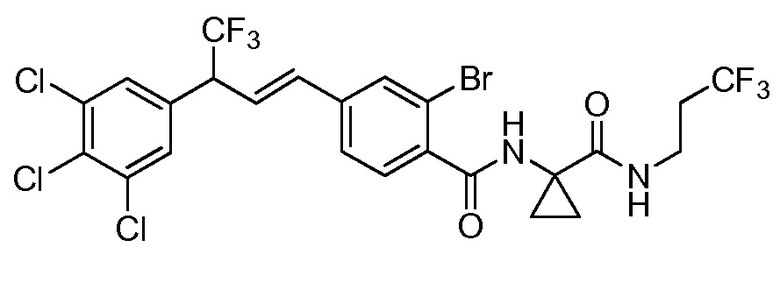
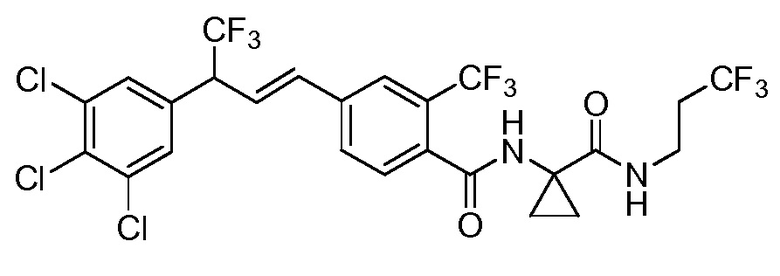
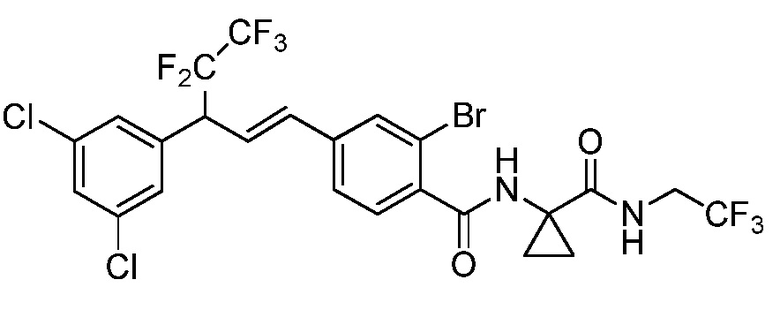
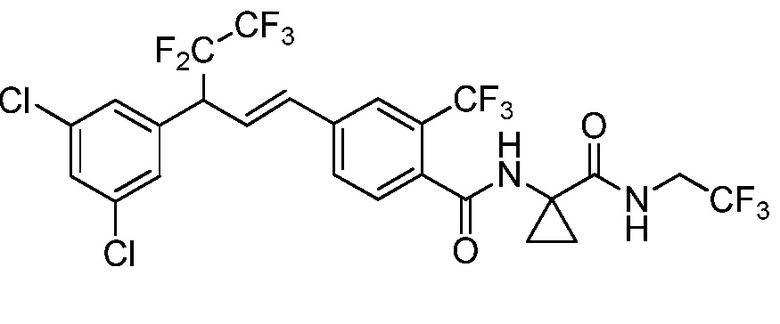
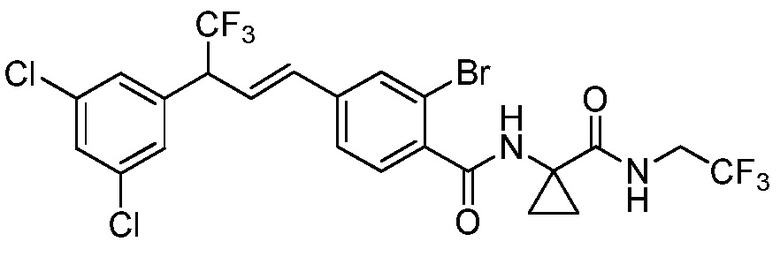
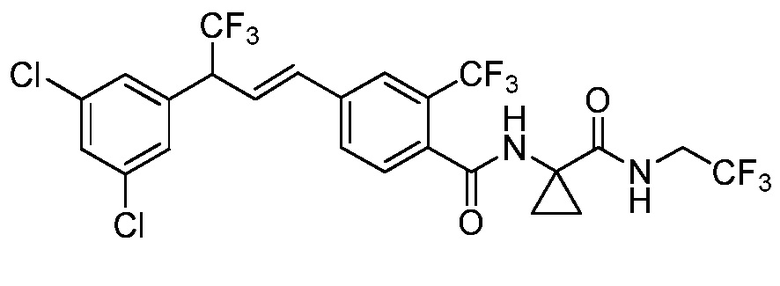
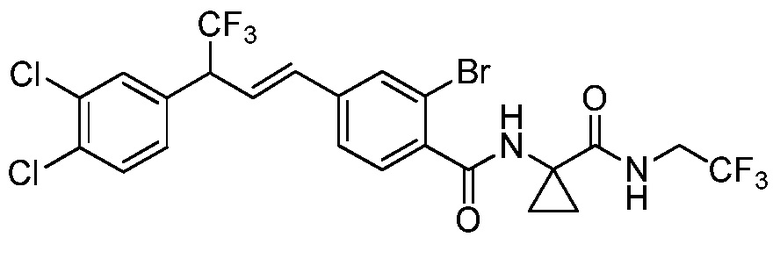
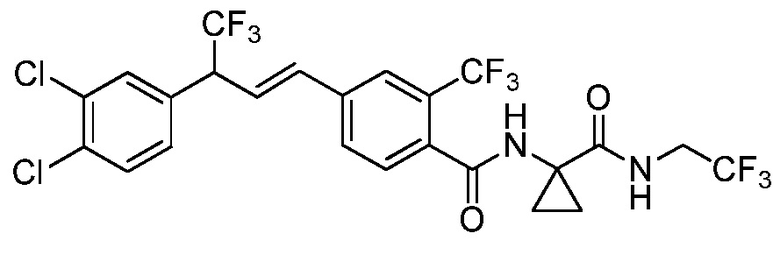
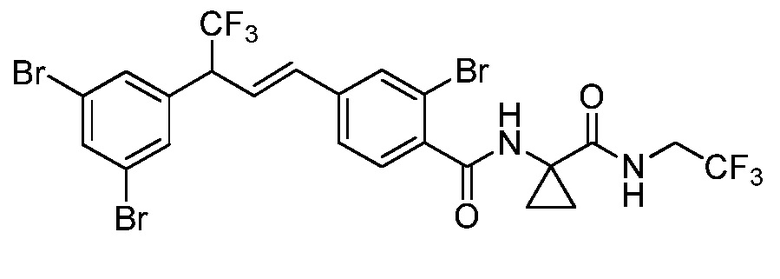

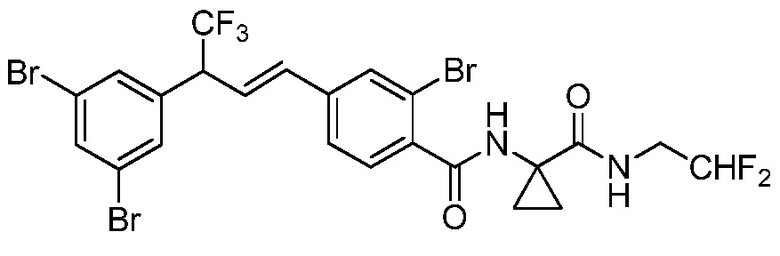
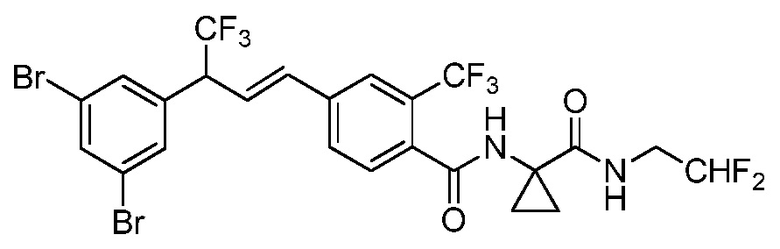
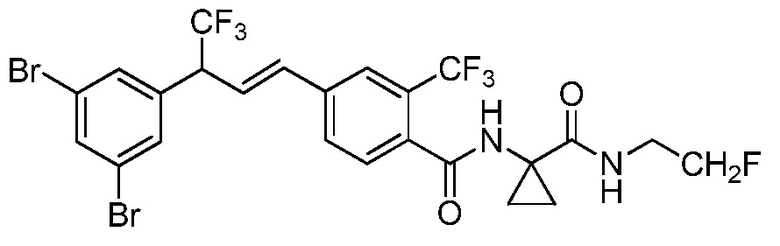
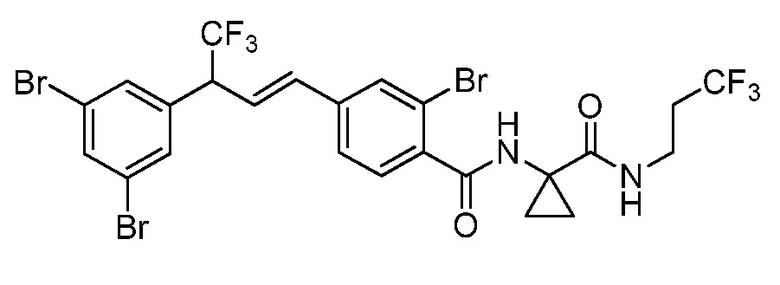
Структуры соединений FA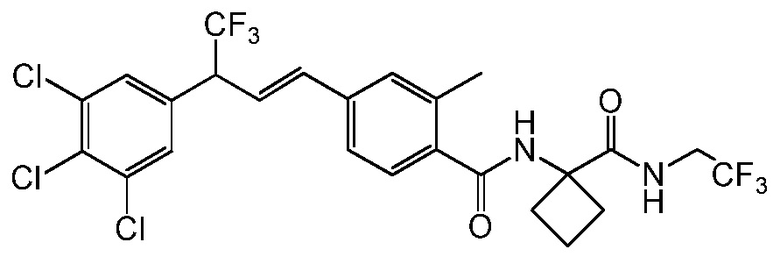

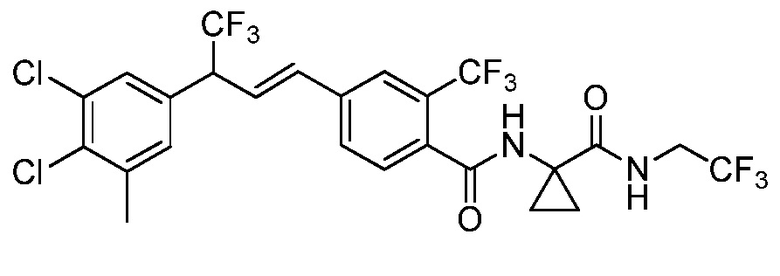
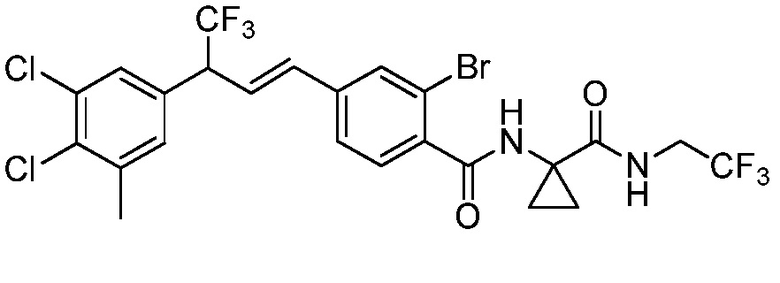
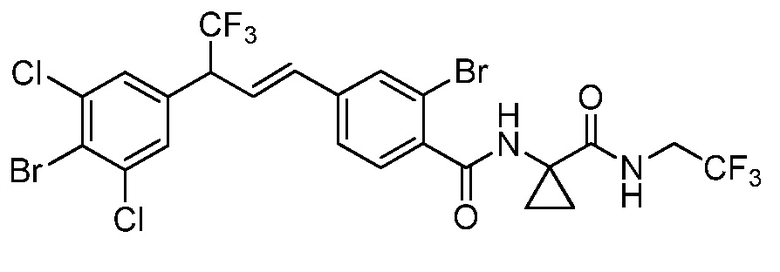
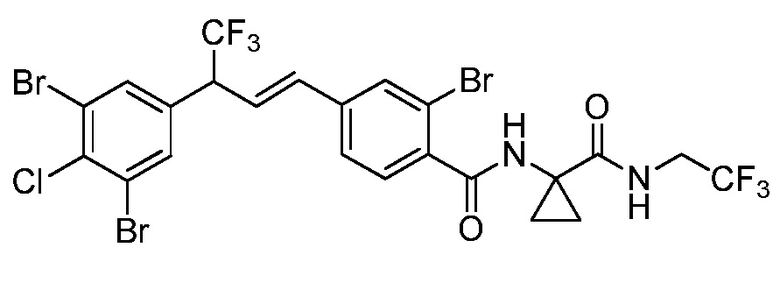

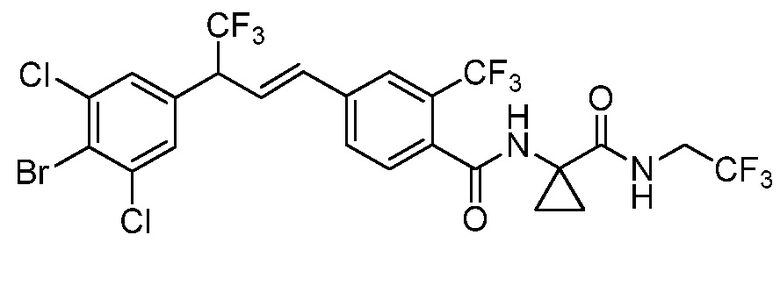
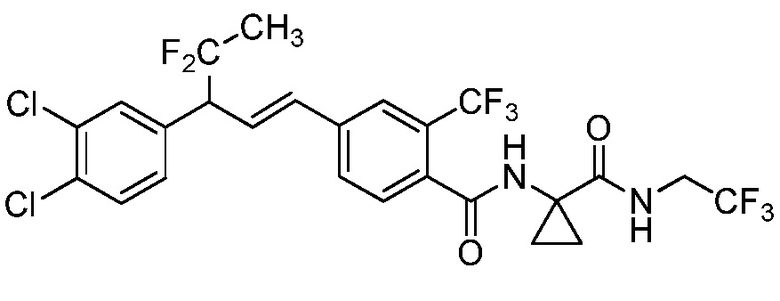
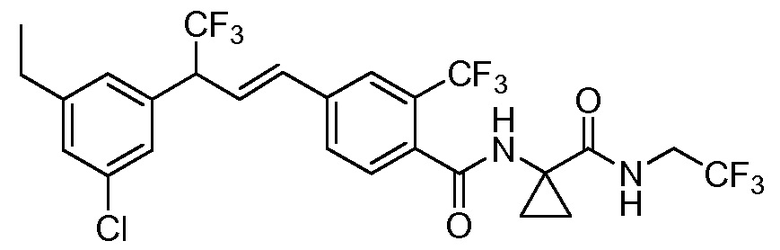
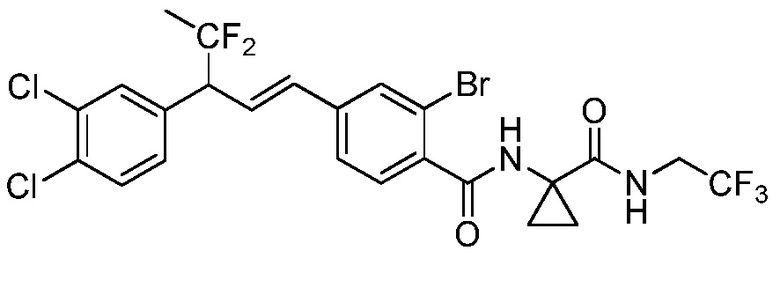
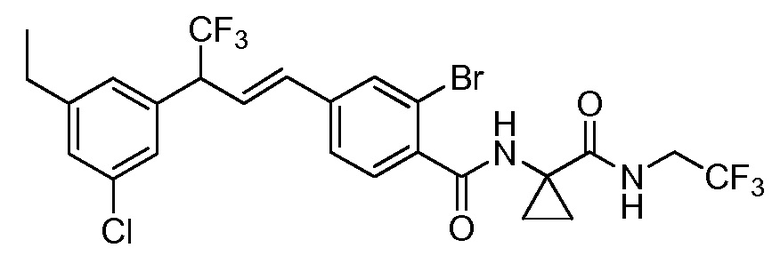
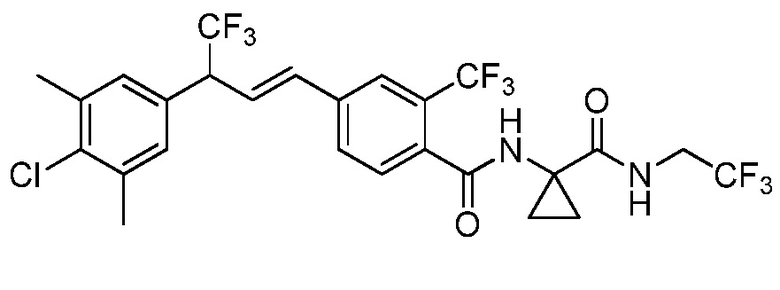
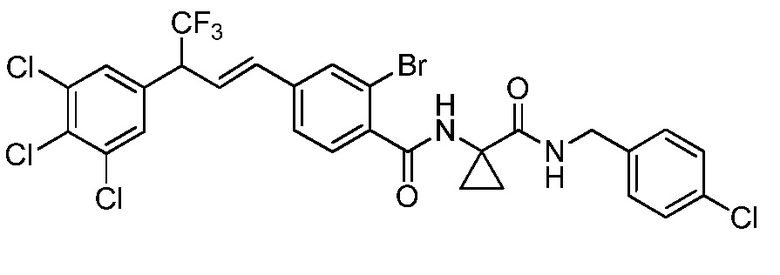
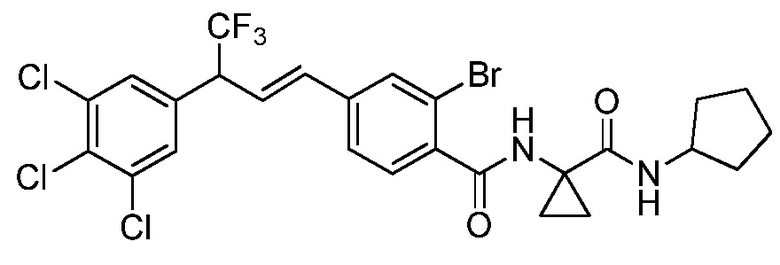
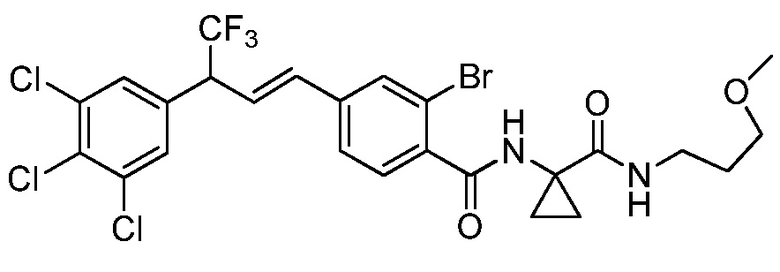
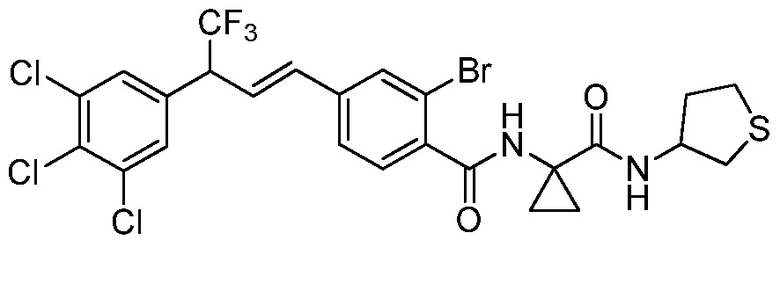
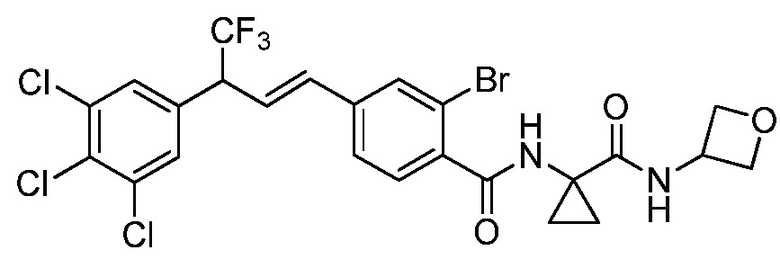
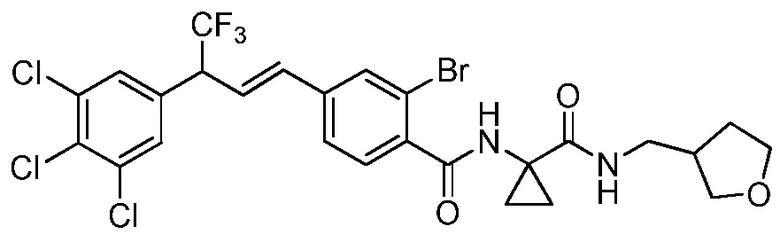
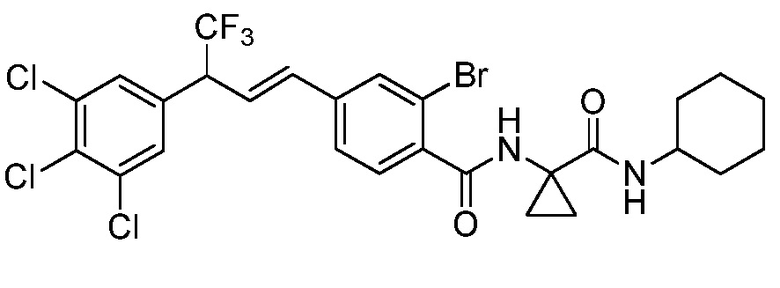
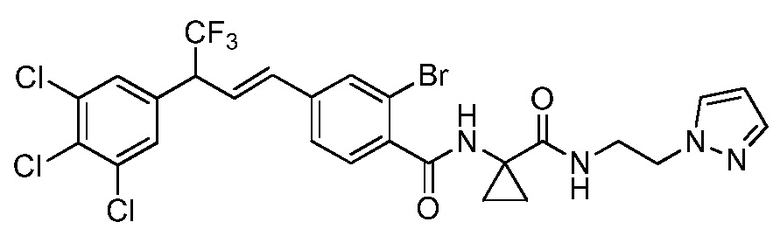

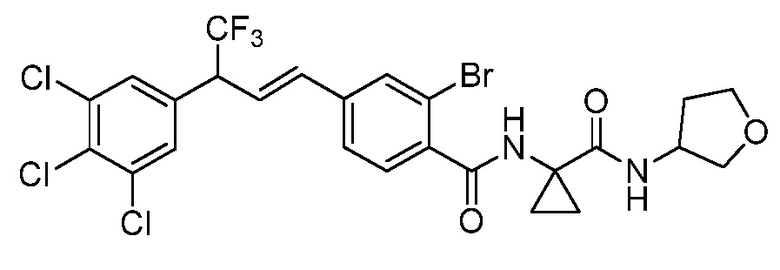
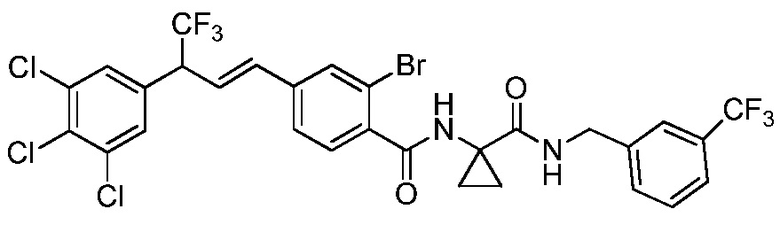
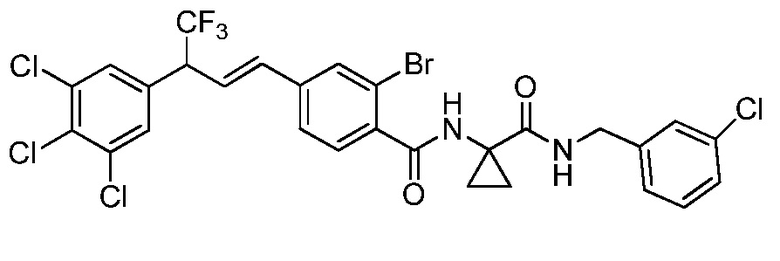
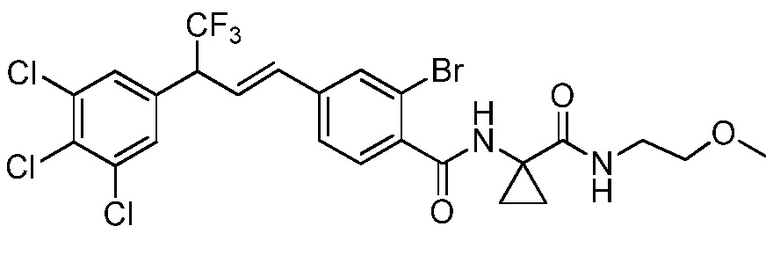
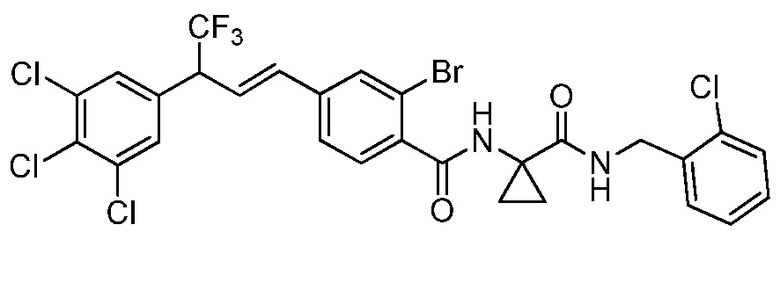
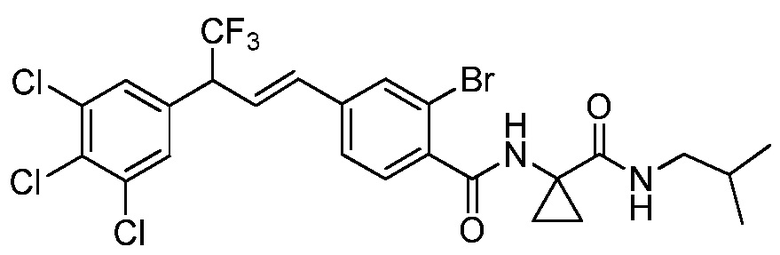
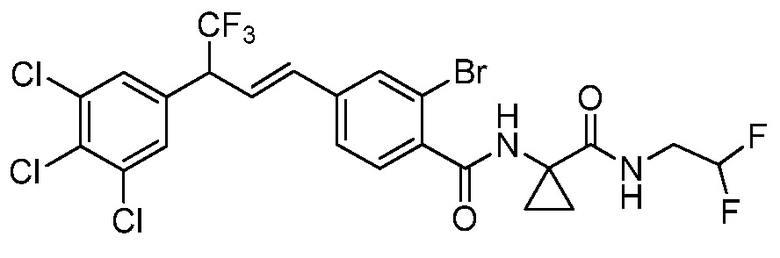
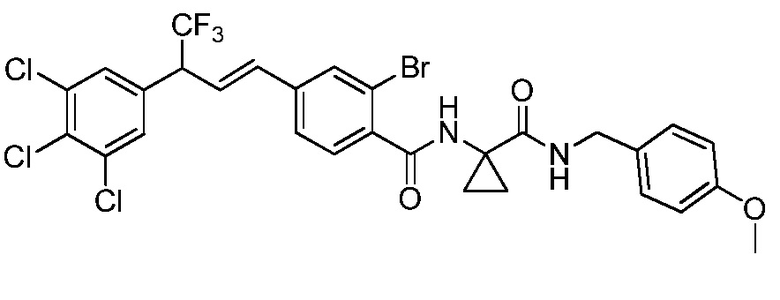
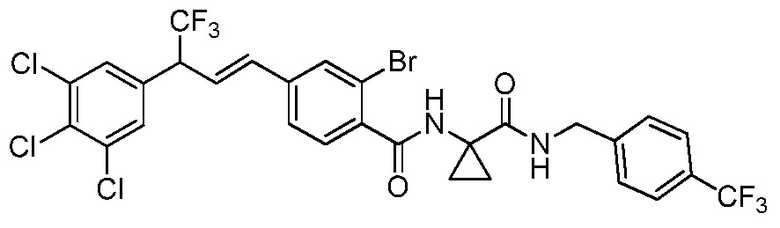
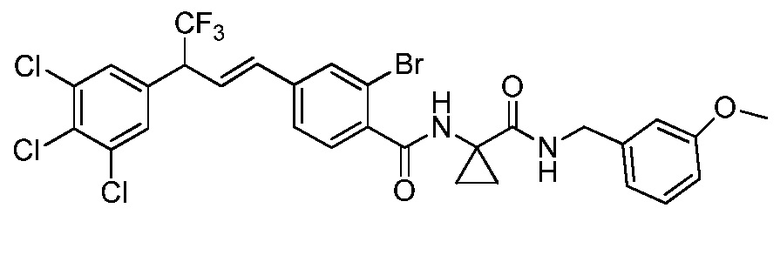
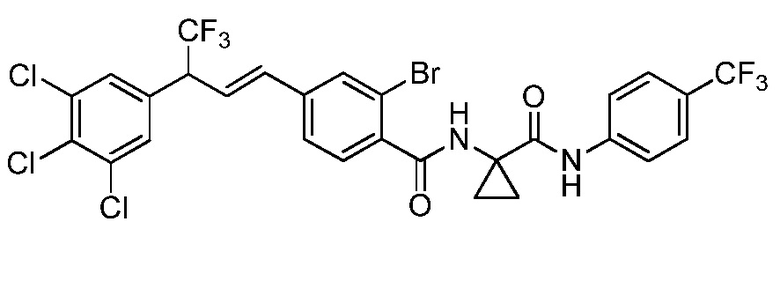
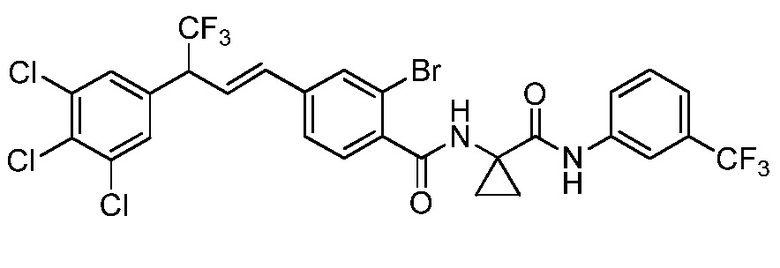
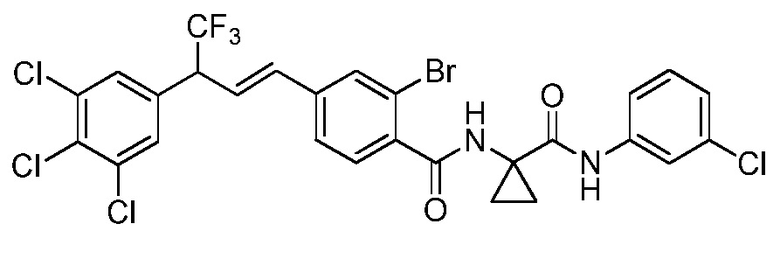
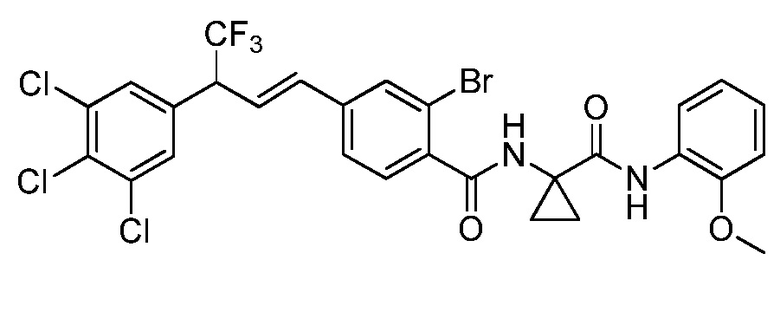
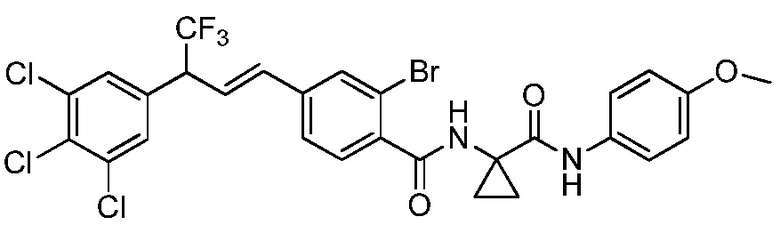
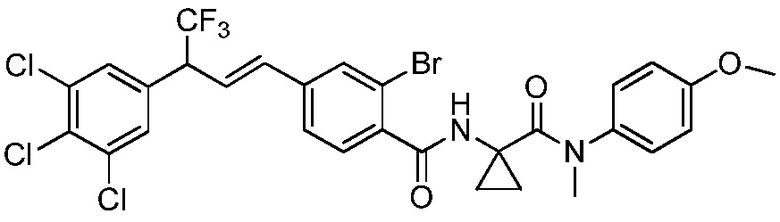
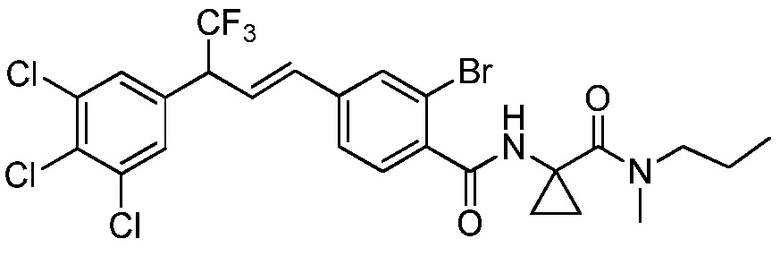
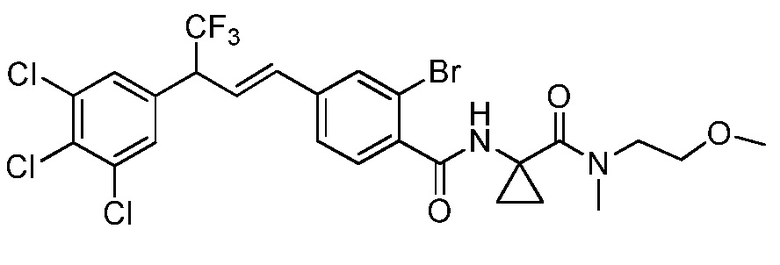
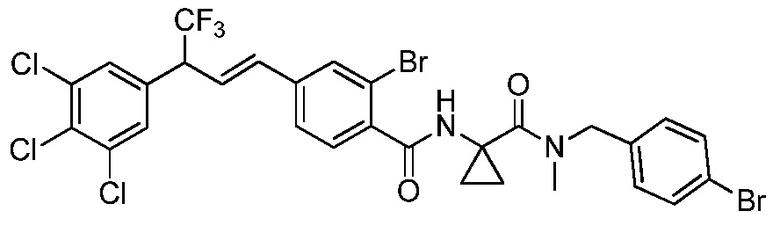
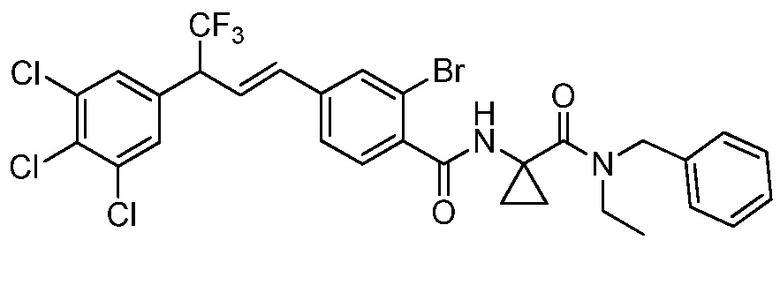
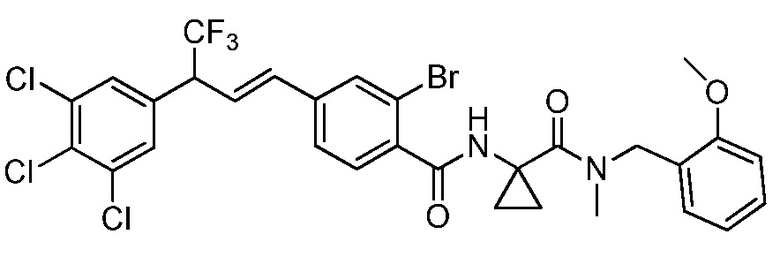
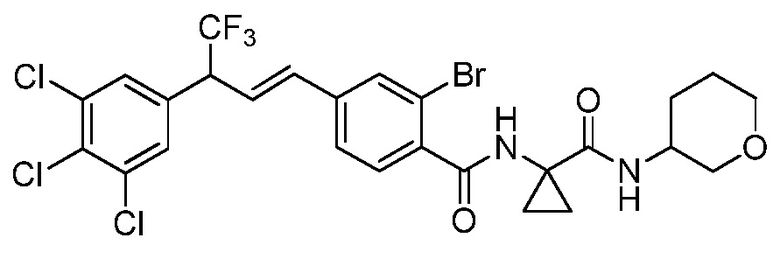
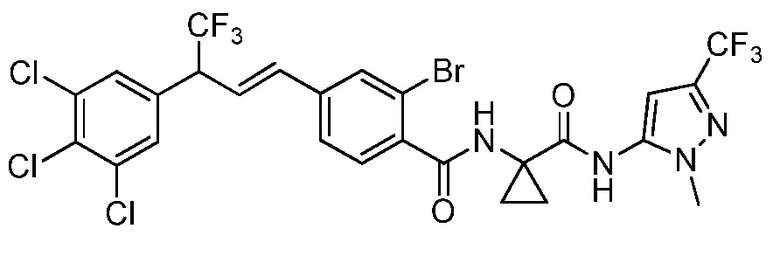
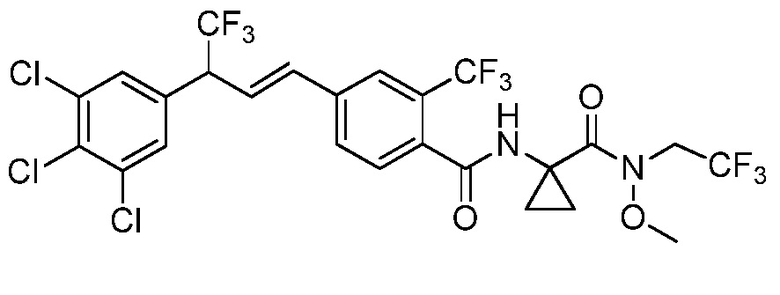
Аналитические данные соединений в Таблице 1.
(см-1)
([М-H]-)
1650, 1112,
809
820
([М+H]+)
([М-H]-)
([М+H]+)
([М+H]+)
1168, 1114,
801
([М+H]+)
800
([М+H]+)
([М+H]+)
([М-H]-)
([М-H]-)
([М+H]+)
([М+H]+)
([М+H]+)
([М-H]-)
([М+H]+)
([М-H]-)
([М+H]+)
([М+H]+)
([М-H]-)
([М+H]-)
([М-H]-)
([М-H]-)
([М+H]+)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М+H]+)
([М+H]+)
([М+H]+)
([М+H]+)
([М+H]+)
([М+H]+)
([М-H]-)
([М+H]+)
([М-H]-)
([М-H]-)
([М-H]-)
([М+H]+)
([М-H]-)
([М+H]+)
([М-H]-)
([М-H]-)
([М-H]-)
([М+H]+)
([М]-)
([М+H]+)
([М+H]+)
1644,
1113,
807,
511
([М+H]+)
1648,
1112,
805, 555
([М+H]+)
1645,
1115,
2243,
810,
507
1649,
1113,
809,
554
([М+H]+)
([М+H]+)
([М+H]+)
([М+H]+)
([М+H]+)
([М+H]+)
([М-H]-)
([М+H]+)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-H]-)
([М-1H]-)
([М-H]-)
0703)
0419)
[М-H]-
[М-H]-
([М]+)
155,63, 153,27, 153,12, 143,01, 137,89, 136,25, 134,03, 133,88, 132,23, 131,23, 131,18, 129,20, 126,17, 125,04, 124,99
[М-H]-
[М-H]-
[М-H]-)
([М-H]-)
0626)
0419)
0572)
([М+H]+)
([М+H]+)
Аналитические данные соединений в Таблице 1A.
(c, 0,5% в CH2Cl2)
36,4 (c, 0,5% в CH2Cl2)
Аналитические данные соединений в Таблице 1B.
(см-1);
19F-ЯМР (δ)
([М-H]-)
([М-H]-)
Аналитические данные соединений в Таблице 1C.
(см-1);
19F-ЯМР (δ)
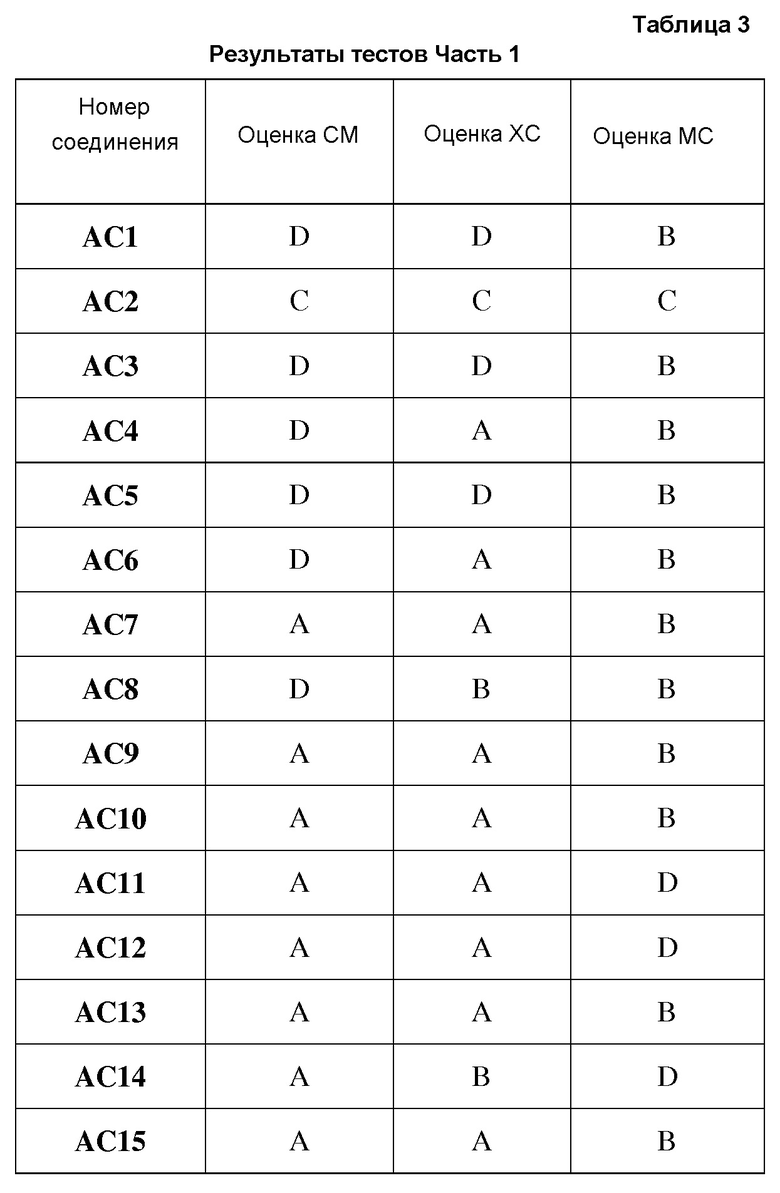
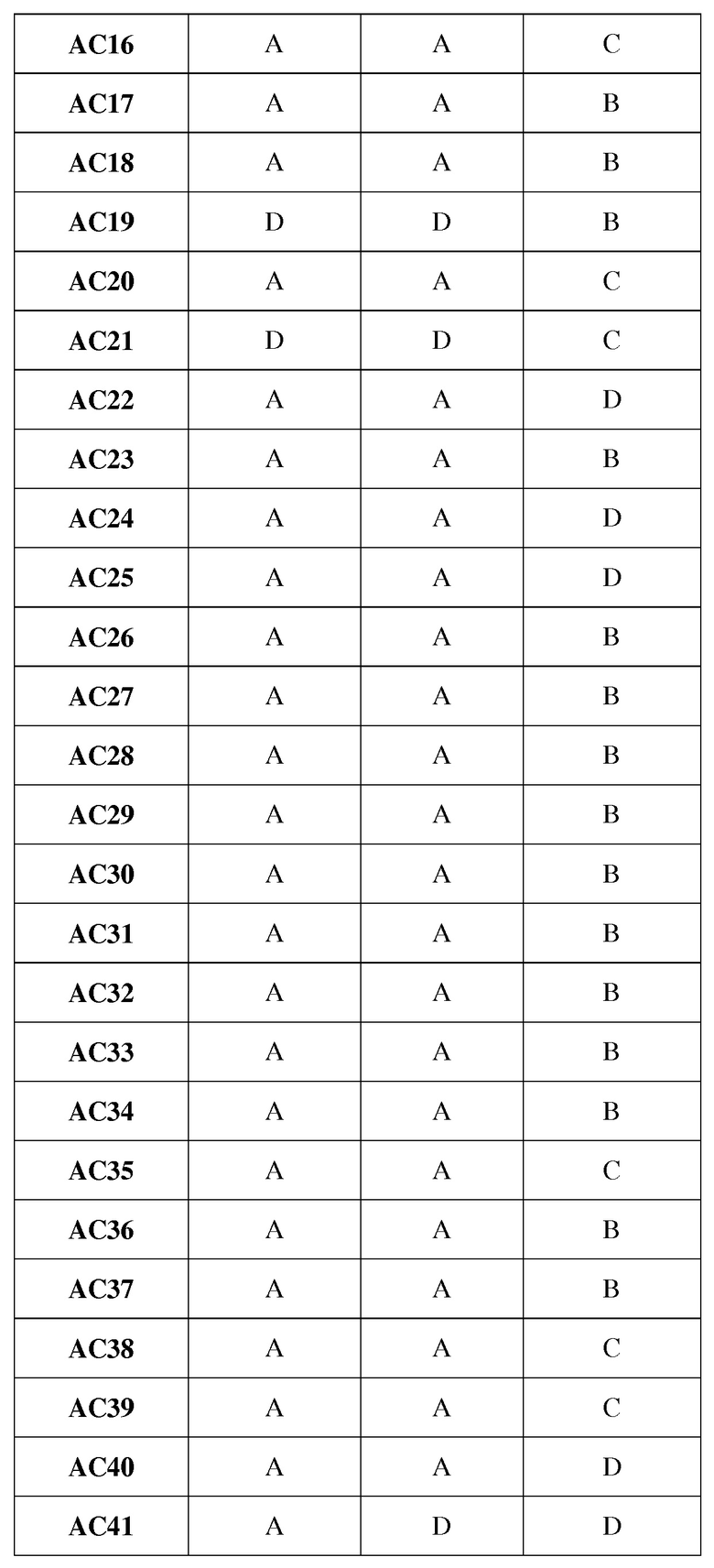
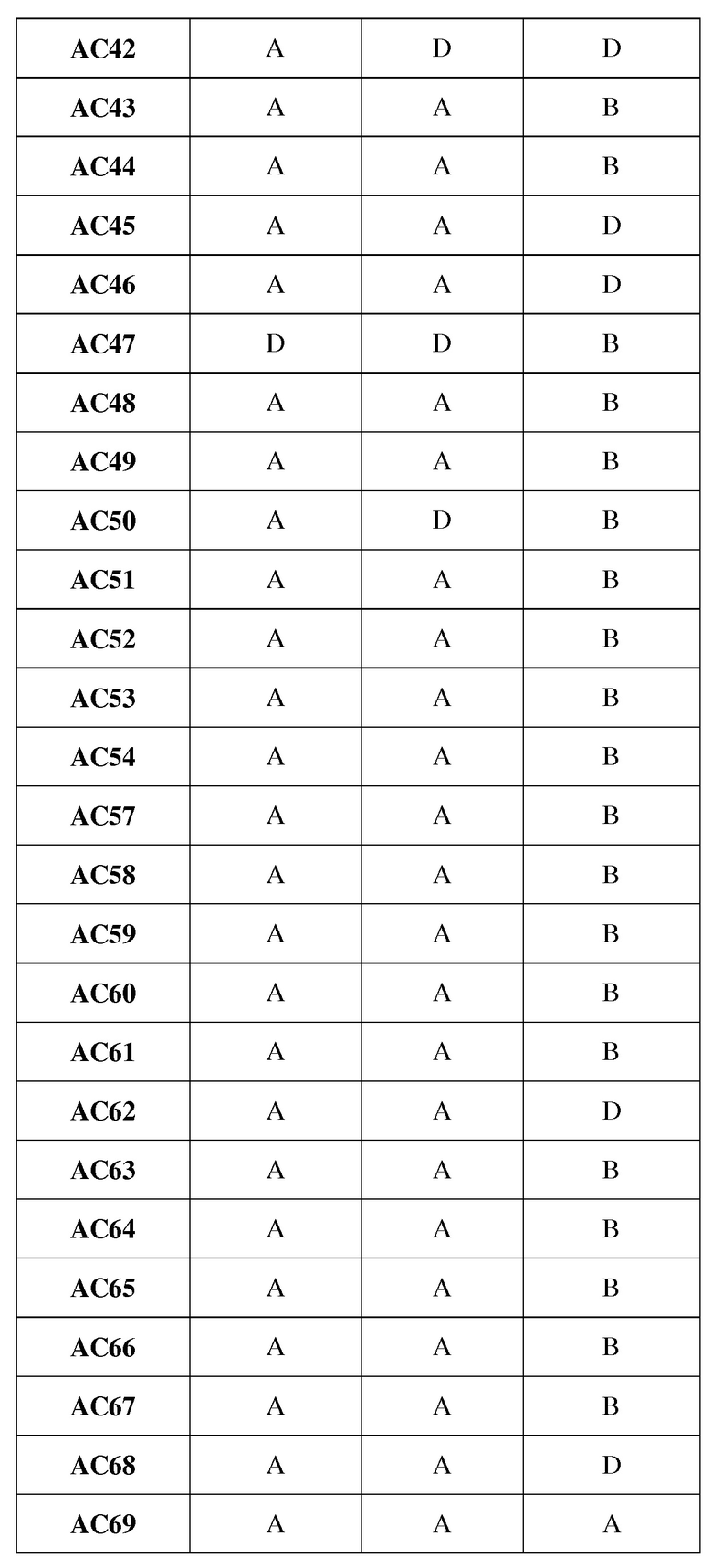
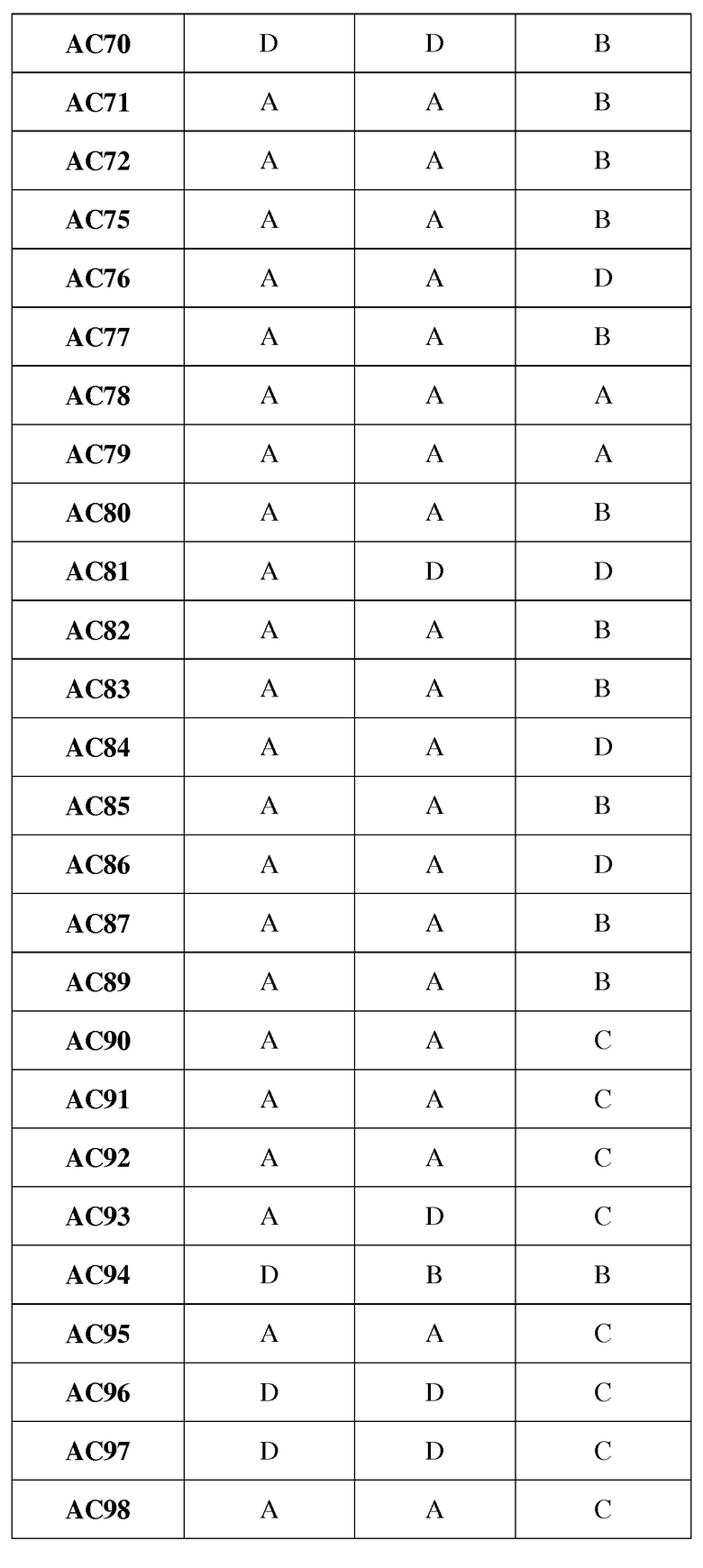
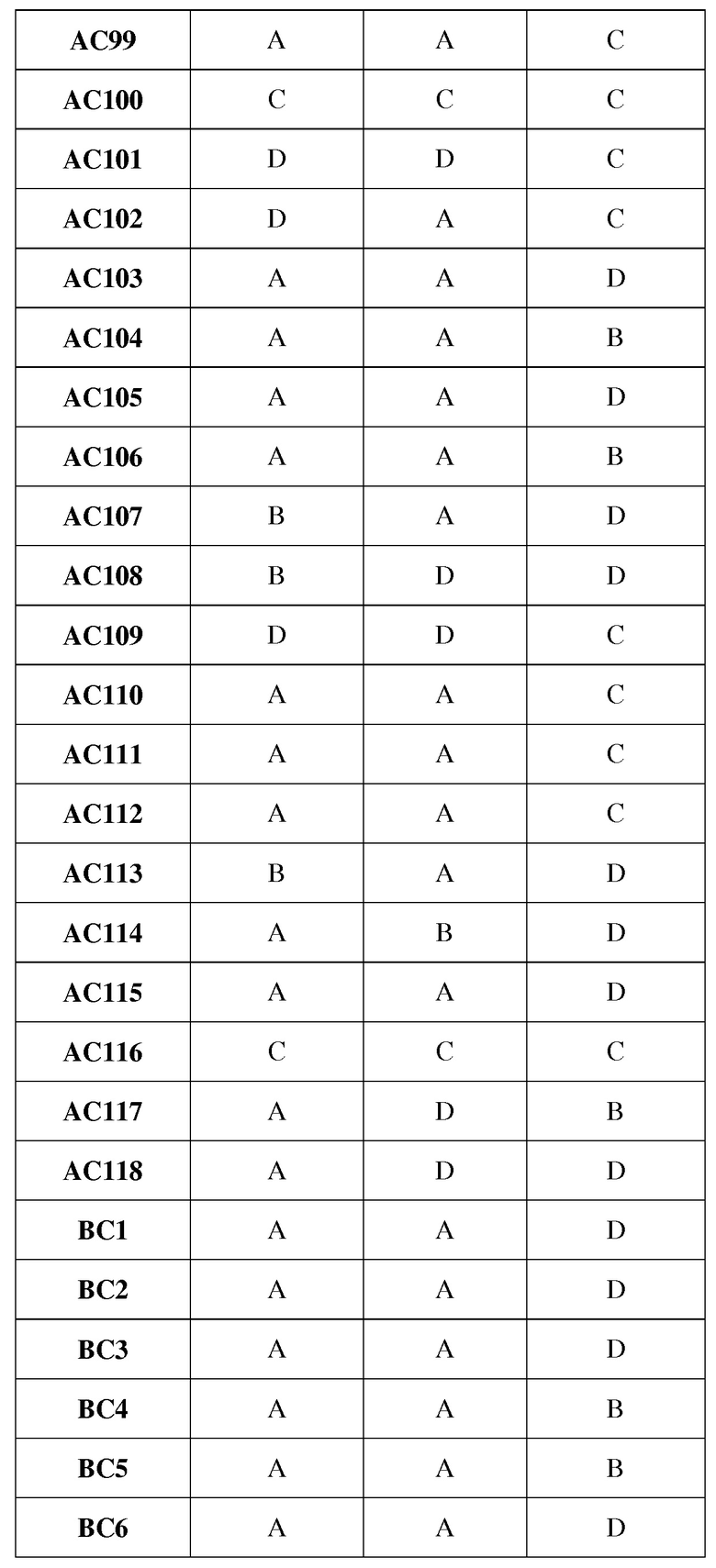
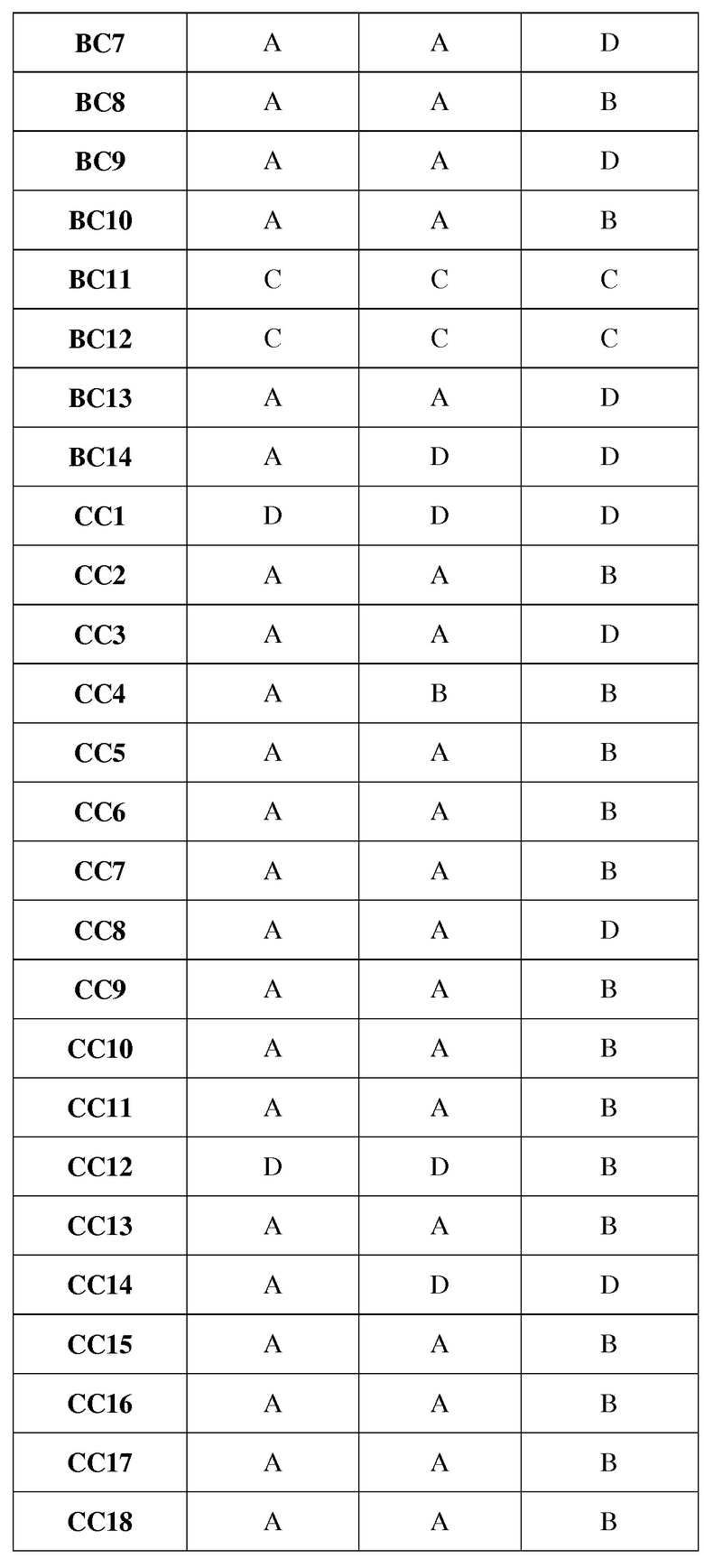
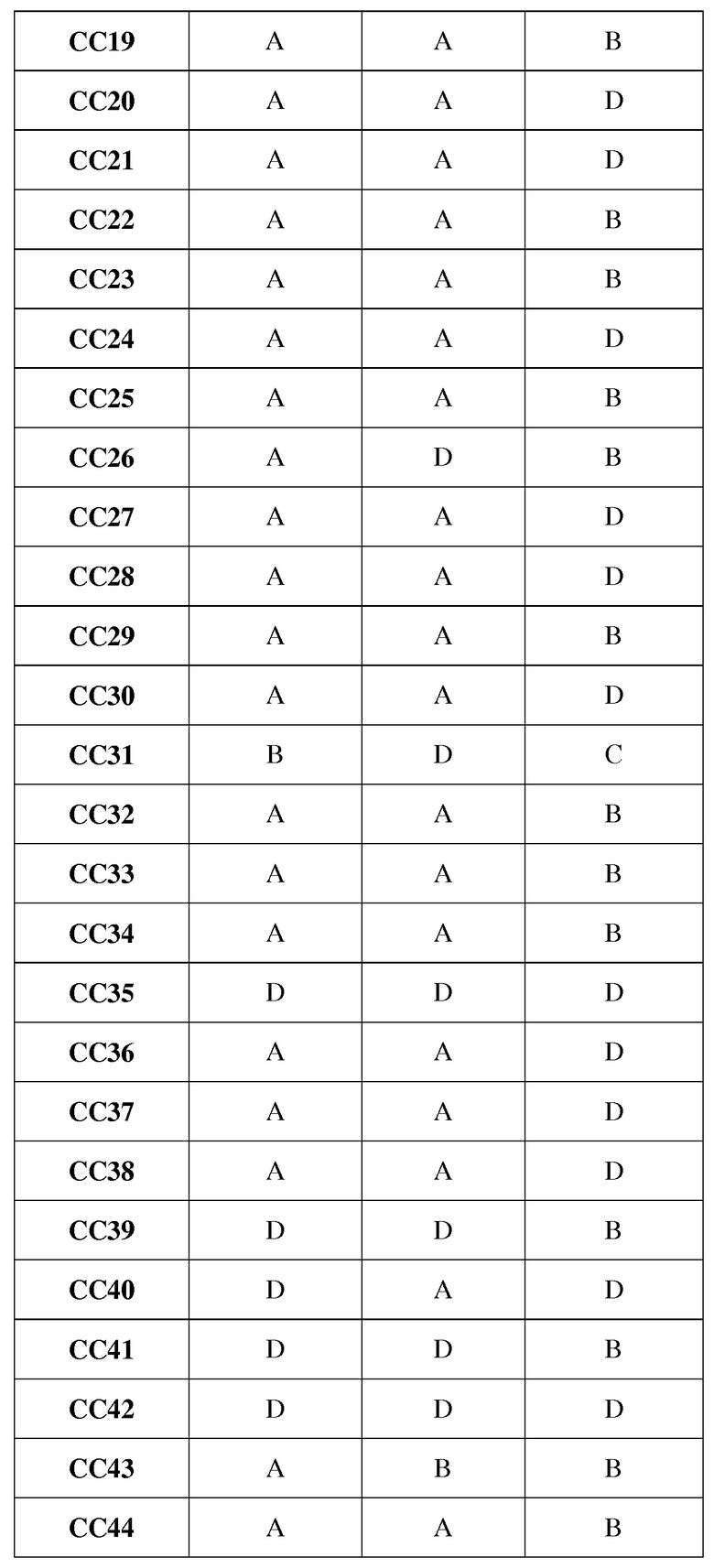
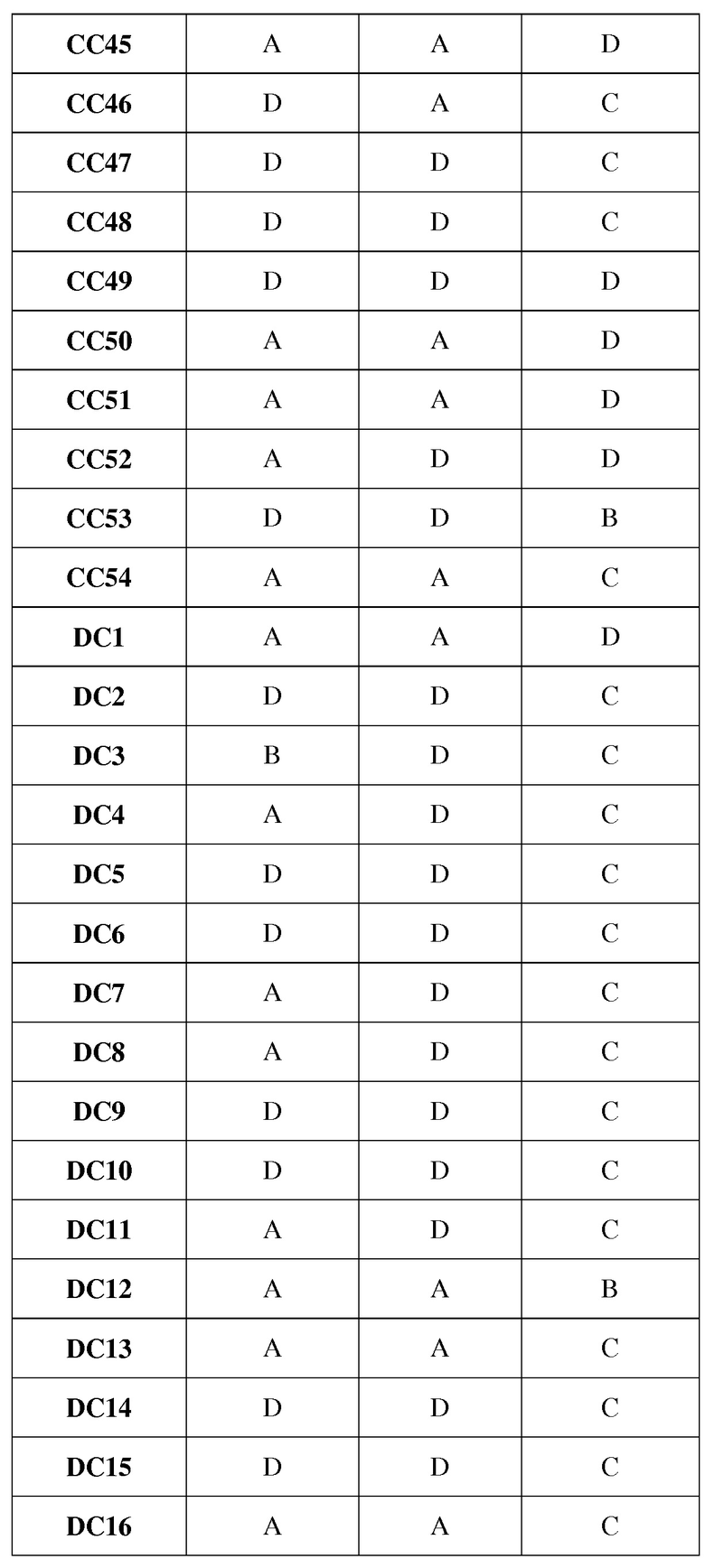
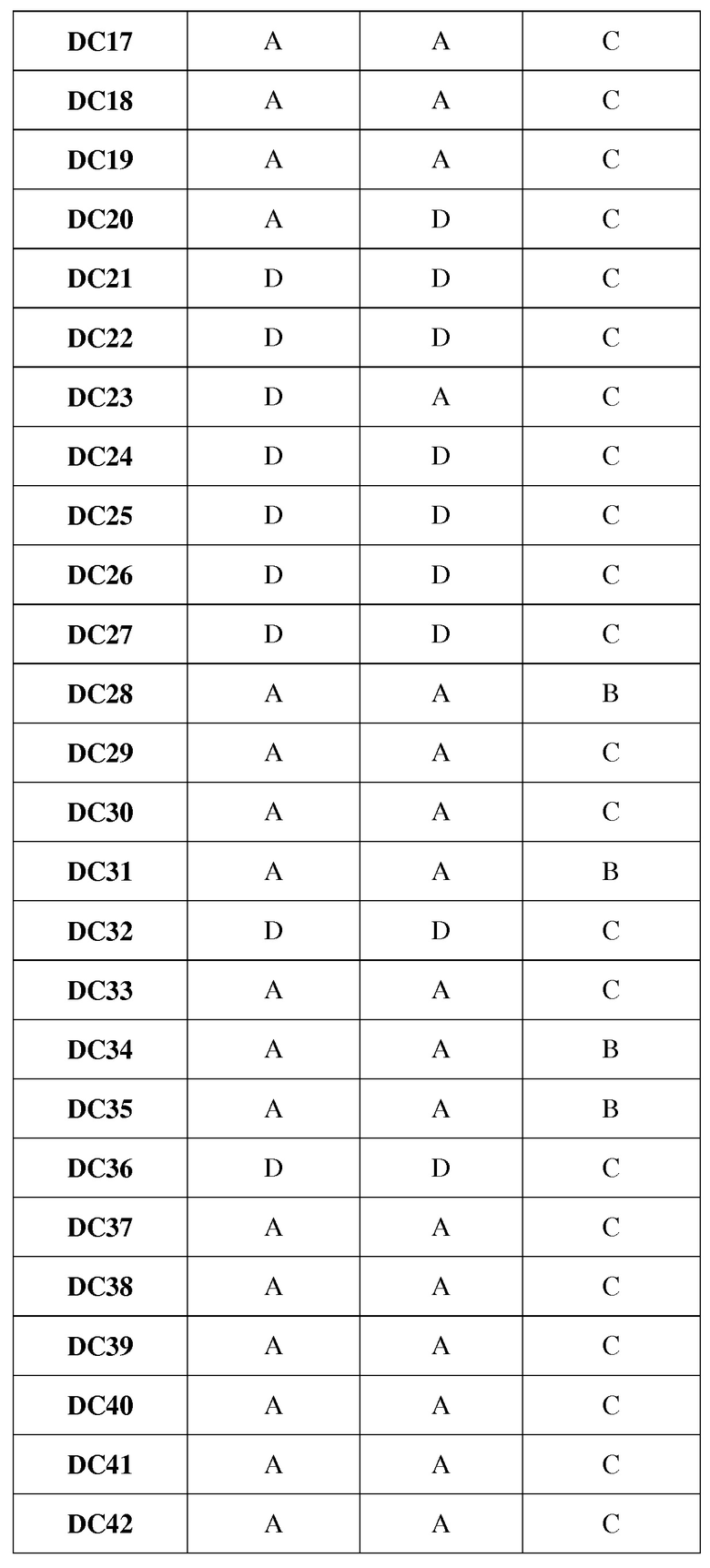
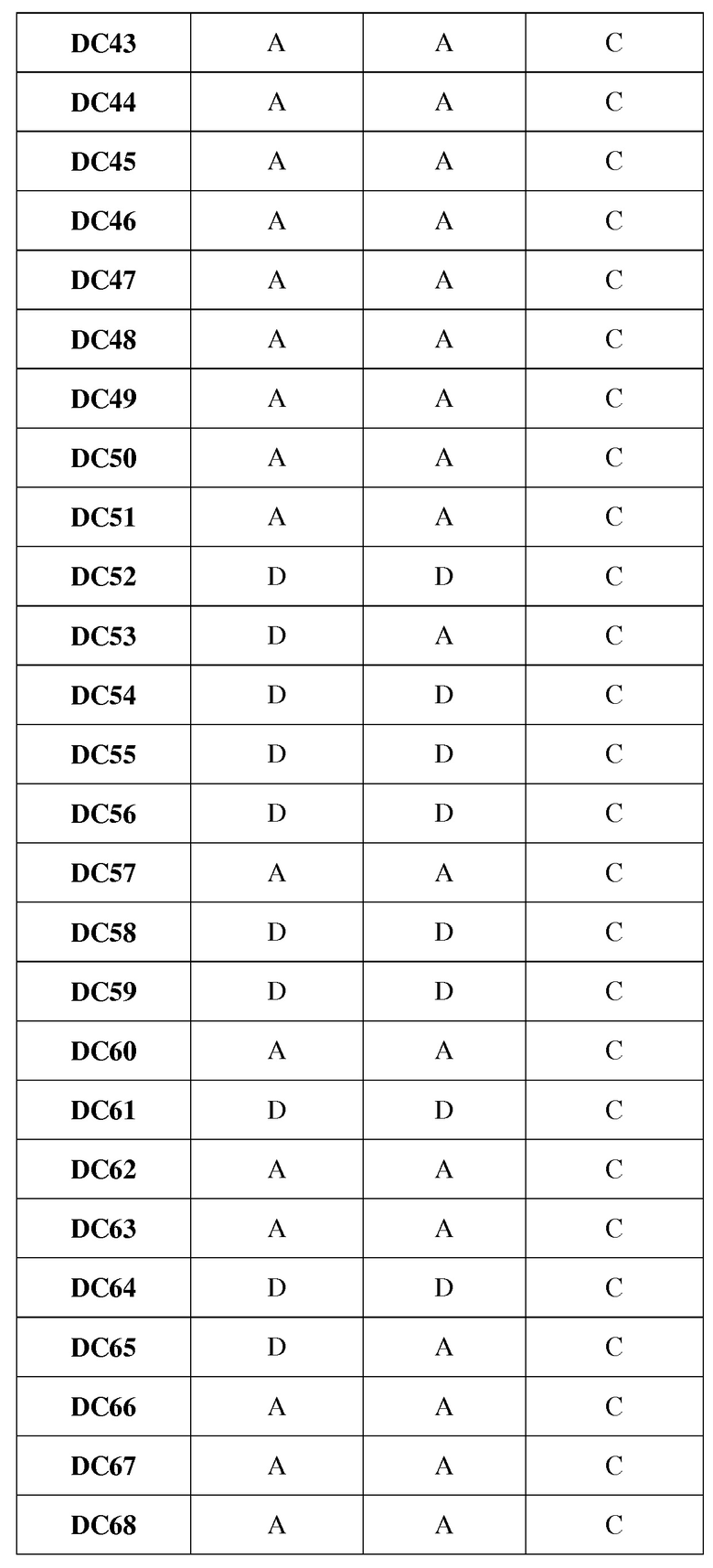
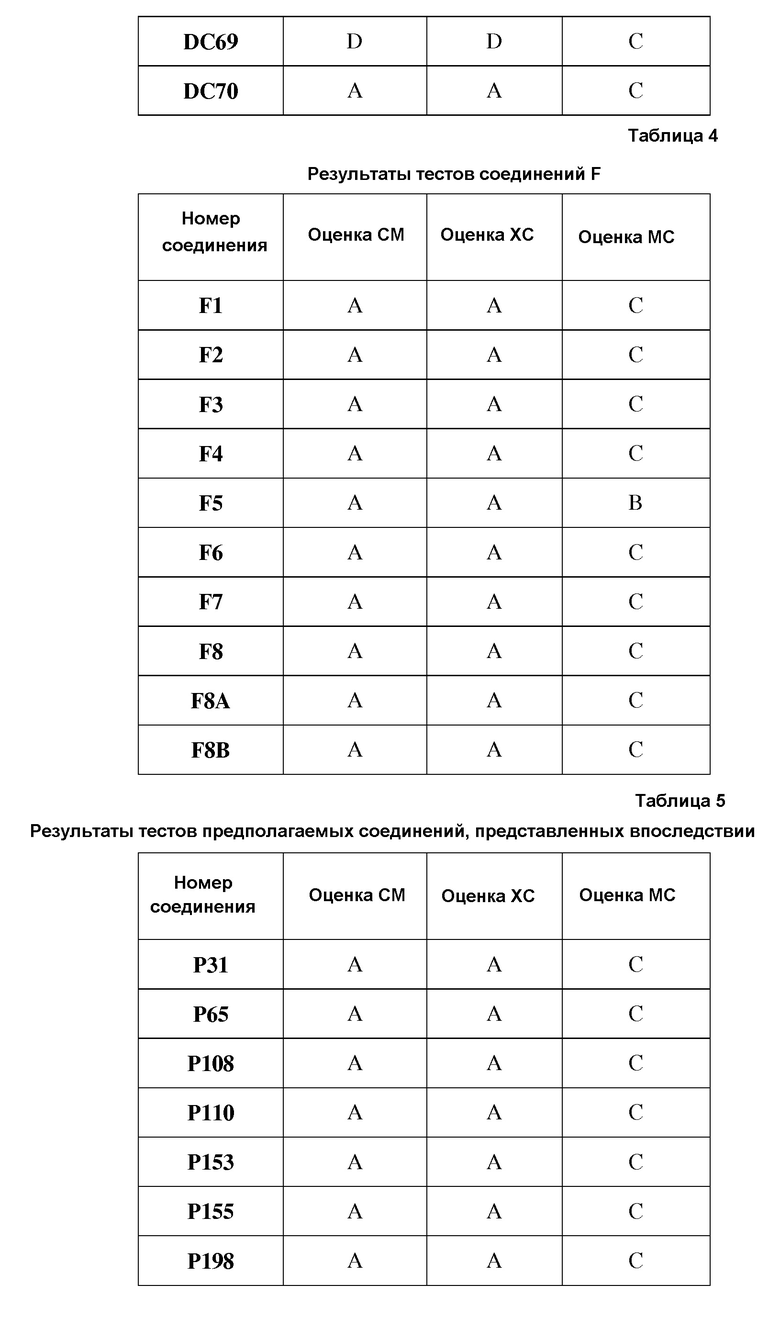
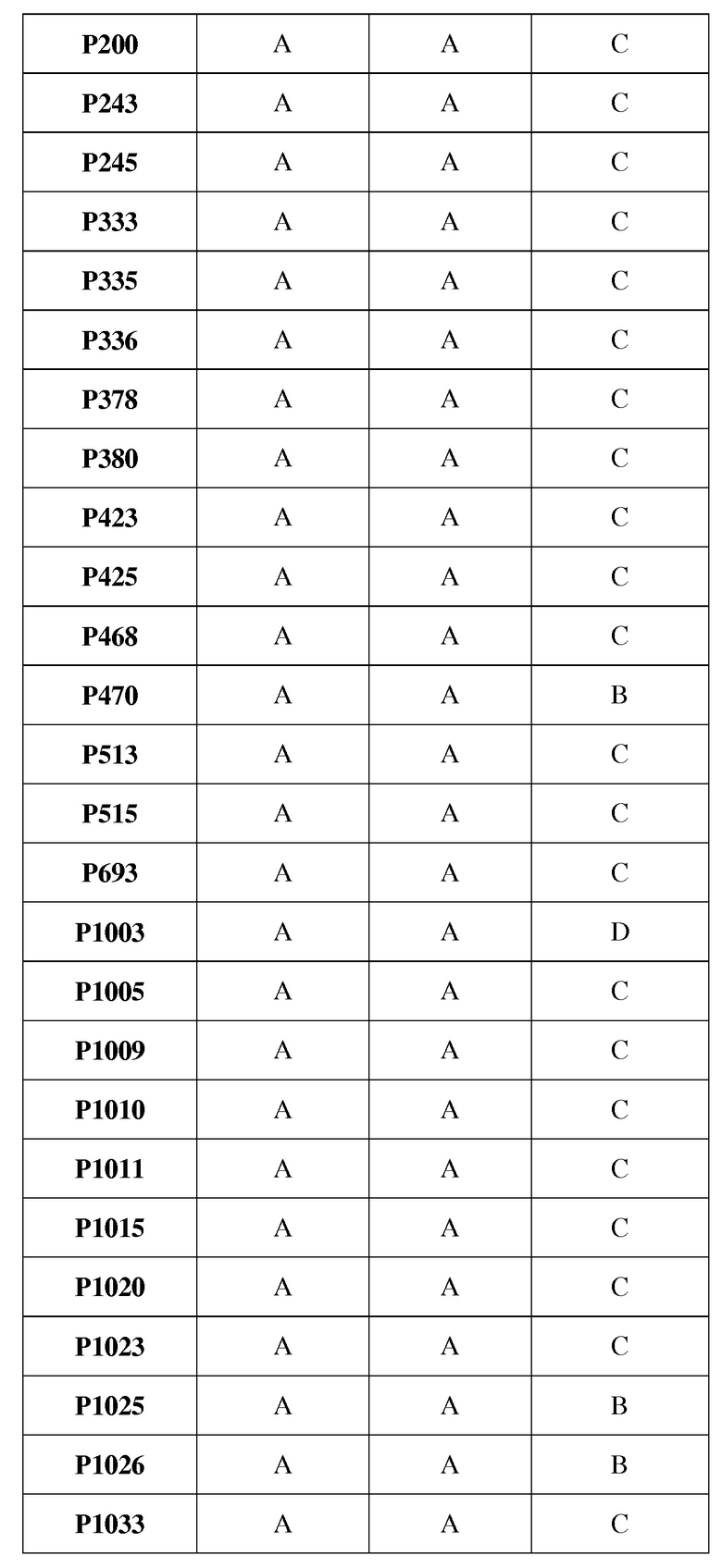
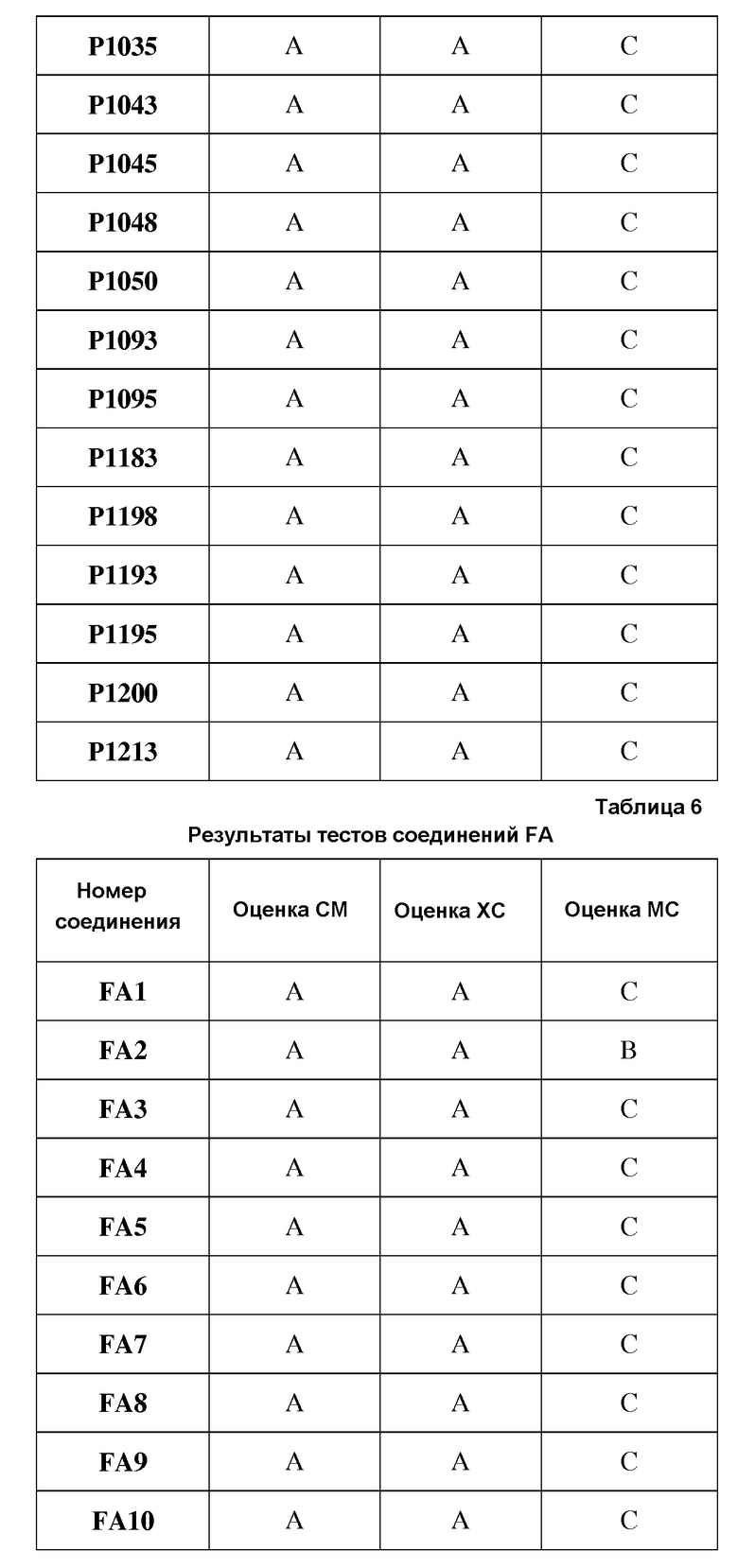
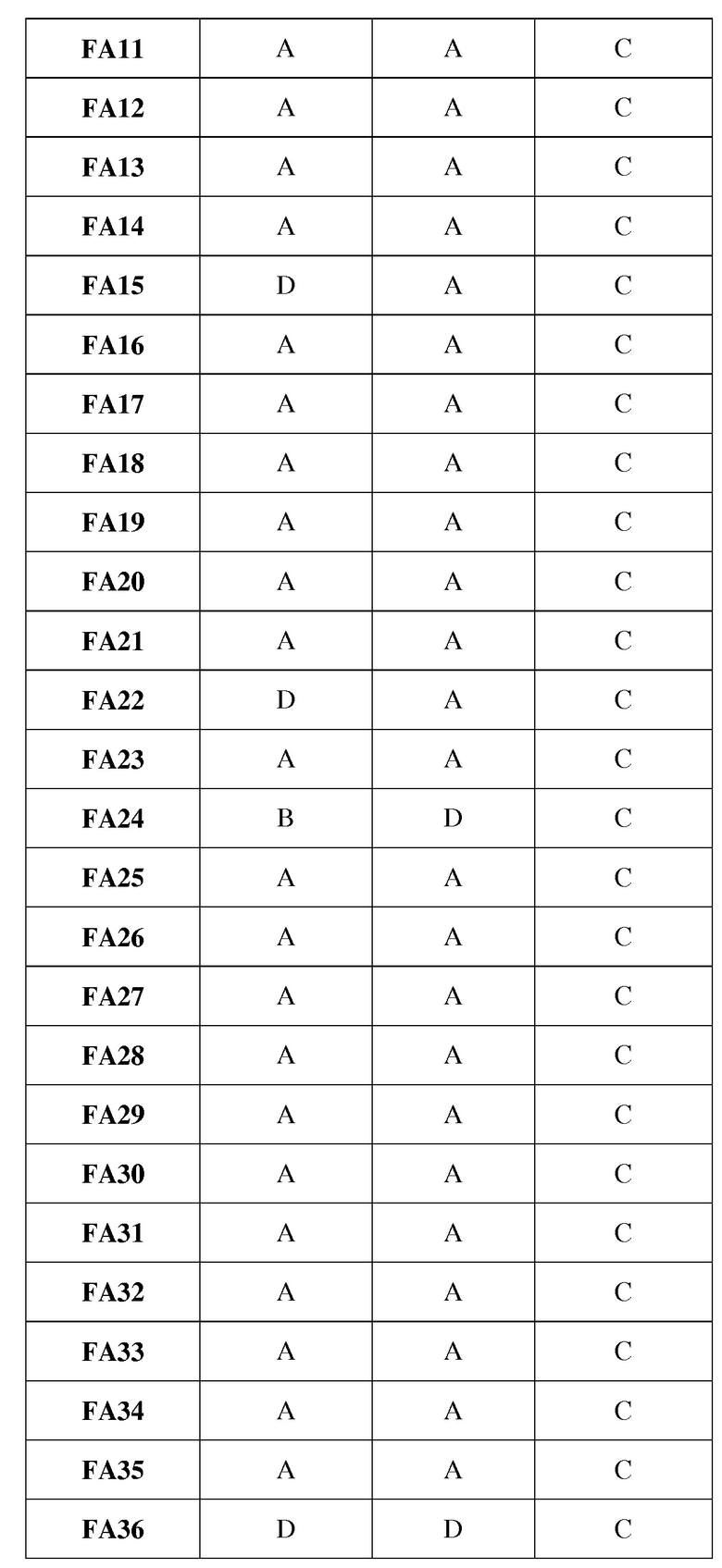
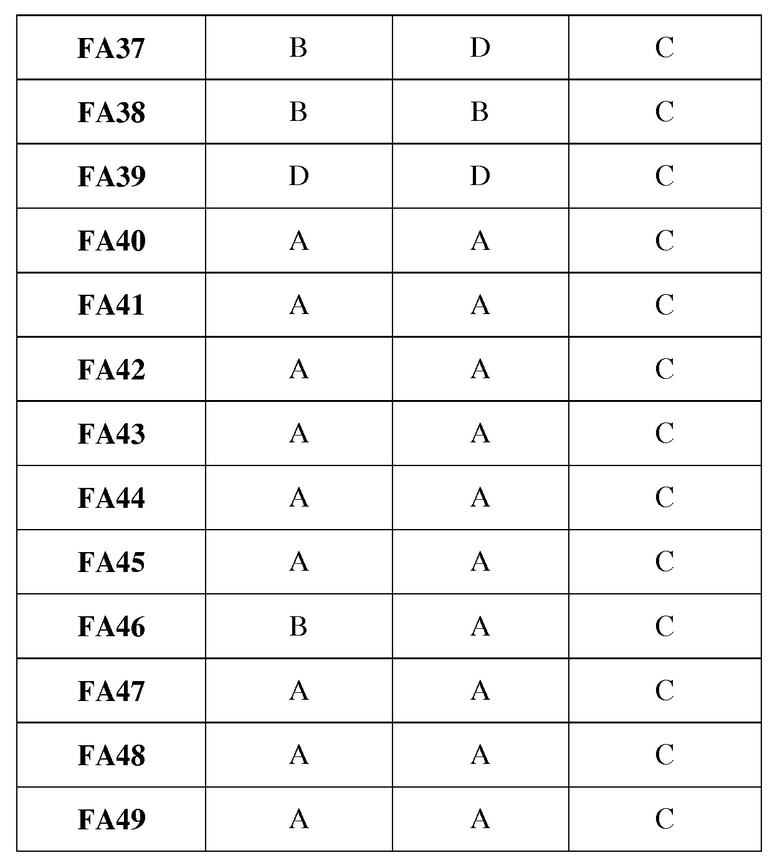
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2638043C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2654336C2 |
| СОЕДИНЕНИЕ, СОДЕРЖАЩЕЕ ОКСАДИАЗОЛ, И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2019 |
|
RU2789456C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2013 |
|
RU2654327C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2013 |
|
RU2623233C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СВЯЗАННЫЕ С НИМИ СПОСОБЫ | 2012 |
|
RU2614976C2 |
| 4-АМИНО-6-(ГЕТЕРОЦИКЛИЧЕСКИЕ)ПИКОЛИНАТЫ И 6-АМИНО-2-(ГЕТЕРОЦИКЛИЧЕСКИЕ)ПИРИМИДИН-4-КАРБОКСИЛАТЫ И ИХ ИСПОЛЬЗОВАНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2014 |
|
RU2672587C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ НЕКОТОРЫХ ЛЕЙКОЗОВ | 2019 |
|
RU2804709C2 |
| АКТИВИРУЮЩИЙ АГЕНТ ДЛЯ РЕЦЕПТОРА, АКТИВИРУЕМОГО СТИМУЛИРУЮЩИМИ РОСТ ПЕРОКСИСОМ АГЕНТАМИ | 2009 |
|
RU2501794C2 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И СПОСОБЫ, ОТНОСЯЩИЕСЯ К НИМ | 2012 |
|
RU2605537C2 |
Изобретение относится к сельскому хозяйству. Молекула имеет следующую формулу: 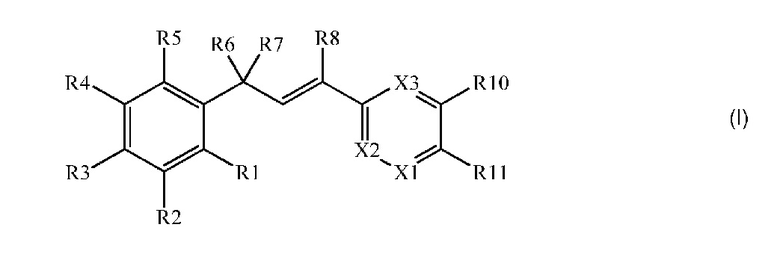
Применяют для борьбы с вредителями и паразитами. Изобретение позволяет повысить эффективность борьбы. 4 н. и 64 з.п. ф-лы, 6 табл., 142 пр.
1. Пестицидная композиция, включающая носитель и молекулу согласно Формуле Один
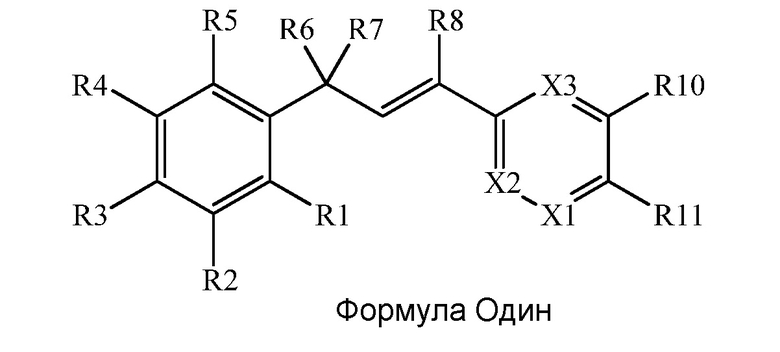
где (a) R1 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(b) R2 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(c) R3 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(d) R4 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(e) R5 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), N(R14)(R15),
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
(4) замещенного (C1-C8)алкокси, где указанный замещенный (C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2, и
(5) замещенного гало(C1-C8)алкокси, где указанный замещенный гало(C1-C8)алкокси имеет один или более заместителей, выбранных из CN и NO2;
(f) R6 представляет собой (C1-C8)галоалкил;
(g) R7 выбран из H, F, Cl, Br, I, OH, (C1-C8)алкокси и гало(C1-C8)алкокси;
(h) R8 выбран из H, (C1-C8)алкила, гало(C1-C8)алкила, OR14 и N(R14)(R15);
(i) R9 выбран из H, F, Cl, Br, I, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, OR14 и N(R14)(R15);
(j) R10 выбран из:
(1) H, F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, цикло(C3-C6)алкила, S(C1-C8)алкила, S(гало(C1-C8)алкила), S(O)(C1-C8)алкила, S(O)(гало(C1-C8)алкила), S(O)2(C1-C8)алкила, S(O)2(гало(C1-C8)алкила), NR14R15, C(=O)H, C(=O)N(R14)(R15), CN(R14)(R15)(=NOH), (C=O)O(C1-C8)алкила, (C=O)OH, гетероциклила, (C2-C8)алкенила, гало(C2-C8)алкенила, (C2-C8)алкинила,
(2) замещенного (C1-C8)алкила, где указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из OH, (C1-C8)алкокси, S(C1-C8)алкила, S(O)(C1-C8)алкила, S(O)2(C1-C8)алкила, NR14R15, и
(3) замещенного гало(C1-C8)алкила, где указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из (C1-C8)алкокси, S(C1-C8)алкила, S(O)(C1-C8)алкила, S(O)2(C1-C8)алкила и N(R14)(R15);
(k) R11 представляет собой C(=X5)N(X6)(R14), где
X5 выбран из O, S или NH и
X6 выбран из галоцикло(C3-C6)алкила, замещенного цикло(C3-C6)алкила и замещенного галоцикло(C3-C6)алкила,
где указанный замещенный цикло(C3-C6)алкил замещен одним или более заместителями, выбранными из CN, NO2, (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R15)(R16), C(=X5)N(R15)(R16), (C1-C8)алкил-C(=X5)N(R15)(R16), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила и C(=O)H, и
где указанный замещенный галоцикло(C3-C6)алкил замещен одним или более заместителями, выбранными из CN, NO2, (C1-C8)алкила, (C2-C8)алкенила, (C2-C8)алкинила, гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R15)(R16), C(=X5)N(R15)(R16), (C1-C8)алкил-C(=X5)N(R15)(R16), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила и C(=O)H,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо), C(=O)(C1-C8)алкила, C(=O)(C3-C6) циклоалкила, S(=O)2(C1-C8)алкила, NR14R15 и оксо;
(l) R12 выбран из H, F, Cl, Br, I, CN, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси и цикло(C3-C6)алкила;
(m) R13 выбран из H, F, Cl, Br, I, CN, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси и гало(C1-C8)алкокси;
(n) каждый R14 независимо выбран из H, (C1-C8)алкила, (C2-C8)алкенила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R16)(R17), (C1-C8)алкил-C(=O)N(R16)(R17), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила, C(=O)H,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, (C3-C6)циклоалкила, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо), гетероциклила, C(=O)(C1-C8)алкила, C(=O)O(C1-C8)алкила и оксо, (где указанный алкил, алкокси и гетероциклил могут быть дополнительно замещены одним или более F, Cl, Br, I, CN и NO2);
(o) каждый R15 независимо выбран из H, (C1-C8)алкила, (C2-C8)алкенила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, (C1-C8)алкокси, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), N(R16)(R17), (C1-C8)алкил-C(=O)N(R16)(R17), C(=O)(C1-C8)алкила, C(=O)(гало(C1-C8)алкила), C(=O)(C3-C6)циклоалкила, (C1-C8)алкил-C(=O)O(C1-C8)алкила, C(=O)H,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, (C3-C6)циклоалкила, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо), гетероциклила, C(=O)(C1-C8)алкила, C(=O)O(C1-C8)алкила и оксо (где указанный алкил, алкокси и гетероциклил могут быть дополнительно замещены одним или более F, Cl, Br, I, CN и NO2);
(p) каждый R16 независимо выбран из H, (C1-C8)алкила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкила,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо;
(q) каждый R17 независимо выбран из H, (C1-C8)алкила, замещенного (C1-C8)алкила, гало(C1-C8)алкила, замещенного гало(C1-C8)алкила, цикло(C3-C6)алкила, арила, замещенного арила, (C1-C8)алкил-арила, (C1-C8)алкил-(замещенного арила), O-(C1-C8)алкил-арила, O-(C1-C8)алкил-(замещенного арила), гетероциклила, замещенного гетероциклила, (C1-C8)алкил-гетероциклила, (C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкил-гетероциклила, O-(C1-C8)алкил-(замещенного гетероциклила), O-(C1-C8)алкила,
где каждый указанный замещенный (C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный гало(C1-C8)алкил имеет один или более заместителей, выбранных из CN и NO2,
где каждый указанный замещенный арил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо, и
где каждый указанный замещенный гетероциклил имеет один или более заместителей, выбранных из F, Cl, Br, I, CN, NO2, (C1-C8)алкила, гало(C1-C8)алкила, (C1-C8)алкокси, гало(C1-C8)алкокси, S(C1-C8)алкила, S(гало(C1-C8)алкила), N((C1-C8)алкил)2 (где каждый (C1-C8)алкил выбран независимо) и оксо;
(r) X1 выбран из N и CR12;
(s) X2 выбран из N, CR9 и CR13;
(t) X3 выбран из N и CR9; и
(v) R12 и R13 вместе образуют связь, содержащую 3-4 атома, выбранные из C, N, O и S, где указанная связь соединяется обратно с кольцом, образуя 5-6-членное насыщенное или ненасыщенное циклическое кольцо, где указанная связь имеет по меньшей мере один заместитель X4, где X4 выбран из R14, N(R14)(R15), N(R14)(C(=O)R14), N(R14)(C(=S)R14), N(R14)(C(=O)N(R14)(R14)), N(R14)(C(=S)N(R14)(R14)), N(R14)(C(=O)N(R14)((C2-C8)алкенила), N(R14)(C(=S)N(R14)((C2-C8)алкенила), где каждый R14 выбран независимо.
2. Композиция по п.1, где R1 выбран из H, F, Cl, Br, I, CN, NO2, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
3. Композиция по п.1, где R2 выбран из H, F, Cl, Br, I, CN, NO2, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
4. Композиция по п.1, где R3 выбран из H, F, Cl, Br, I, CN, NO2, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
5. Композиция по п.1, где R4 выбран из H, F, Cl, Br, I, CN, NO2, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
6. Композиция по п.1, где R5 выбран из H, F, Cl, Br, I, CN, NO2, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
7. Композиция по п.1, где R2 и R4 выбраны из F, Cl, Br, I, CN и NO2 и R1, R3 и R5 представляют собой H.
8. Композиция по п.1, где R2, R3 и R4 выбраны из F, Cl, Br, I, CN и NO2 и R1 и R5 представляют собой H.
9. Композиция по п.1, где R2, R3 и R4 независимо выбраны из F и Cl и R1 и R5 представляют собой H.
10. Композиция по п.1, где R1 выбран из Cl и H.
11. Композиция по п.1, где R2 выбран из CF3, CH3, Cl, F и H.
12. Композиция по п.1, где R3 выбран из OCH3, CH3, F, Cl или H.
13. Композиция по п.1, где R4 выбран из CF3, CH3, Cl, F и H.
14. Композиция по п.1, где R5 выбран из F, Cl и H.
15. Композиция по п.1, где R6 выбран из галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила и гало(C8)алкила.
16. Композиция по п.1, где R6 является трифторметилом.
17. Композиция по п.1, где R7 выбран из H, F, Cl, Br и I.
18. Композиция по п.1, где R7 выбрана из H, OCH3 и ОН.
19. Композиция по п.1, где R8 выбран из H, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила и гало(C8)алкила.
20. Композиция по п.1, где R8 выбран из CH3 и H.
21. Композиция по п.1, где R9 выбран из H, F, Cl, Br, I, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
22. Композиция по п.1, где R10 выбран из H, F, Cl, Br, I, CN, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метокси, этокси, (C3)алкокси, (C4)алкокси, (C5)алкокси, (C6)алкокси, (C7)алкокси, (C8)алкокси, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси, гало(C8)алкокси, циклопропила, циклобутила, циклопентила и циклогексила.
23. Композиция по п.1, где R10 выбран из H, Cl, Br, CH3 и CF3.
24. Композиция по п.1, где R10 выбран из Br, C(=NOH)NH2, C(=O)H, C(=O)NH2, C(=O)OCH2CH3, C(=O)OH, CF3, CH2CH3, CH2OH, CH3, Cl, CN, F, H, NH2, NHC(=O)H, NHCH3, NO2, OCH3, OCHF2 и пиридила.
25. Композиция по п.1, где R11 выбран из -C(=O)N(H)(циклопропил-(C(=O)N(H)(CH2CF3)), C(=O)N(H)(циклопропил-(C(=S)N(H)(CH2CF3)), C(=O)N(H)(циклобутил-C(=O)N(H)(CH2CF3)) и C(=O)N(H)(циклопропил-CN).
26. Композиция по п.1, где R11 представляет собой C(=(O или S))N(H)(циклопропил-(C(=(O или S))N(H)(гало(C1-C6)алкил)) или C(=(O или S)N(H)(циклобутил-(C=(O или S))N(H)(гало(C1-C6)алкил)).
27. Композиция по п.1, где R11 представляет собой C(=(O или S))N(H)(циклопропил-(C(=(O или S))N(H)(гало(C1-C6)алкил)).
28. Композиция по п.1, где R11 представляет собой C(=(O или S))N(H)(циклобутил-(C(=(O или S))N(H)(гало(C1-C6)алкил)).
29. Композиция по п.1, где R12 выбран из H, F, Cl, Br, I, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
30. Композиция по п.1, где R12 выбран из CH3 и H.
31. Композиция по п.1, где R13 выбран из H, F, Cl, Br, I, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, галометокси, галоэтокси, гало(C3)алкокси, гало(C4)алкокси, гало(C5)алкокси, гало(C6)алкокси, гало(C7)алкокси и гало(C8)алкокси.
32. Композиция по п.1, где R13 выбран из CH3, Cl и H.
33. Композиция по п.1, где R12-R13 является гидрокарбильной связью CH=CHCH=CH.
34. Композиция по п.1, где R14 и R15 независимо выбраны из H, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метил-арила, этил-арила, (C3)алкил-арила, (C4)алкил-арила, (C5)алкил-арила, (C6)алкил-арила, (C7)алкил-арила, (C8)алкил-арила, метил-(замещенного арила), этил-(замещенного арила), (C3)алкил-(замещенного арила), (C4)алкил-(замещенного арила), (C5)алкил-(замещенного арила), (C6)алкил-(замещенного арила), (C7)алкил-(замещенного арила), (C8)алкил-(замещенного арила), O-метил-арила, O-этил-арила, O-(C3)алкил-арила, O-(C4)алкил-арила, O-(C5)алкил-арила, O-(C6)алкил-арила, O-(C7)алкил-арила, O-(C8)алкил-арила, O-метил-(замещенного арила), O-этил-(замещенного арила), O-(C3)алкил-(замещенного арила), O-(C4)алкил-(замещенного арила), O-(C5)алкил-(замещенного арила), O-(C6)алкил-(замещенного арила), O-(C7)алкил-(замещенного арила), O-(C8)алкил-(замещенного арила), метил-гетероциклила, этил-гетероциклила, (C3)алкил-гетероциклила, (C4)алкил-гетероциклила, (C5)алкил-гетероциклила, (C6)алкил-гетероциклила, (C7)алкил-гетероциклила, (C8)алкил-гетероциклила, метил-(замещенного гетероциклила), этил-(замещенного гетероциклила), (C3)алкил-(замещенного гетероциклила), (C4)алкил-(замещенного гетероциклила), (C5)алкил-(замещенного гетероциклила), (C6)алкил-(замещенного гетероциклила), (C7)алкил-(замещенного гетероциклила), (C8)алкил-(замещенного гетероциклила), O-метил-гетероциклила, O-этил-гетероциклила, O-(C3)алкил-гетероциклила, O-(C4)алкил-гетероциклила, O-(C5)алкил-гетероциклила, O-(C6)алкил-гетероциклила, O-(C7)алкил-гетероциклила, O-(C8)алкил-гетероциклила, O-метил-(замещенного гетероциклила), O-этил-(замещенного гетероциклила), O-(C3)алкил-(замещенного гетероциклила), O-(C4)алкил-(замещенного гетероциклила), O-(C5)алкил-(замещенного гетероциклила), O-(C6)алкил-(замещенного гетероциклила), O-(C7)алкил-(замещенного гетероциклила), O-(C8)алкил-(замещенного гетероциклила), метил-C(=O)N(R16)(R17), этил-C(=O)N(R16)(R17), (C3)алкил-C(=O)N(R16)(R17), (C4)алкил-C(=O)N(R16)(R17), (C5)алкил-C(=O)N(R16)(R17), (C6)алкил-C(=O)N(R16)(R17), (C7)алкил-C(=O)N(R16)(R17) и (C8)алкил-C(=O)N(R16)(R17).
35. Композиция по п.1, где R14 и R15 независимо выбраны из H, CH3, CH2CF3, CH2-галопиридила, оксо-пирролидинила, галофенила, тиетанила, CH2-фенила, CH2-пиридила, тиетанил-диоксида, CH2-галотиазолила, C((CH3)2)-пиридила, N(H)(галофенила), CH2-пиримидинила, CH2-тетрагидрофуранила, CH2-фуранила, O-CH2-галопиридила и CH2C(=O)N(H)(CH2CF3).
36. Композиция по п.1, где R16 и R17 независимо выбраны из H, метила, этила, (C3)алкила, (C4)алкила, (C5)алкила, (C6)алкила, (C7)алкила, (C8)алкила, галометила, галоэтила, гало(C3)алкила, гало(C4)алкила, гало(C5)алкила, гало(C6)алкила, гало(C7)алкила, гало(C8)алкила, метил-арила, этил-арила, (C3)алкил-арила, (C4)алкил-арила, (C5)алкил-арила, (C6)алкил-арила, (C7)алкил-арила, (C8)алкил-арила, метил-(замещенного арила), этил-(замещенного арила), (C3)алкил-(замещенного арила), (C4)алкил-(замещенного арила), (C5)алкил-(замещенного арила), (C6)алкил-(замещенного арила), (C7)алкил-(замещенного арила), (C8)алкил-(замещенного арила), O-метил-арила, O-этил-арила, O-(C3)алкил-арила, O-(C4)алкил-арила, O-(C5)алкил-арила, O-(C6)алкил-арила, O-(C7)алкил-арила, O-(C8)алкил-арила, O-метил-(замещенного арила), O-этил-(замещенного арила), O-(C3)алкил-(замещенного арила), O-(C4)алкил-(замещенного арила), O-(C5)алкил-(замещенного арила), O-(C6)алкил-(замещенного арила), O-(C7)алкил-(замещенного арила), O-(C8)алкил-(замещенного арила), метил-гетероциклила, этил-гетероциклила, (C3)алкил-гетероциклила, (C4)алкил-гетероциклила, (C5)алкил-гетероциклила, (C6)алкил-гетероциклила, (C7)алкил-гетероциклила, (C8)алкил-гетероциклила, метил-(замещенного гетероциклила), этил-(замещенного гетероциклила), (C3)алкил-(замещенного гетероциклила), (C4)алкил-(замещенного гетероциклила), (C5)алкил-(замещенного гетероциклила), (C6)алкил-(замещенного гетероциклила), (C7)алкил-(замещенного гетероциклила), (C8)алкил-(замещенного гетероциклила), O-метил-гетероциклила, O-этил-гетероциклила, O-(C3)алкил-гетероциклила, O-(C4)алкил-гетероциклила, O-(C5)алкил-гетероциклила, O-(C6)алкил-гетероциклила, O-(C7)алкил-гетероциклила, O-(C8)алкил-гетероциклила, O-метил-(замещенного гетероциклила), O-этил-(замещенного гетероциклила), O-(C3)алкил-(замещенного гетероциклила), O-(C4)алкил-(замещенного гетероциклила), O-(C5)алкил-(замещенного гетероциклила), O-(C6)алкил-(замещенного гетероциклила), O-(C7)алкил-(замещенного гетероциклила) и O-(C8)алкил-(замещенного гетероциклила).
37. Композиция по п.1, где R16 и R17 независимо выбраны из H, CH2CF3, циклопропила, тиетанила, тиетанил диоксида и галофенила.
38. Композиция по п.1, где X1 представляет собой CR12, X2 представляет собой CR13 и X3 представляет собой CR9.
39. Композиция по п.1, в которой молекула согласно Формуле Один имеет одну из следующих структур:

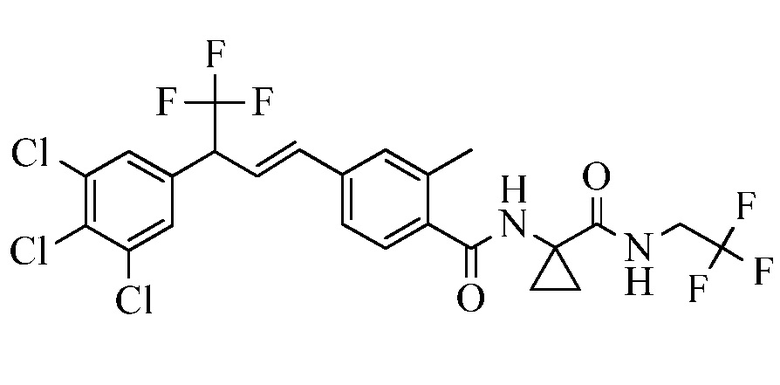
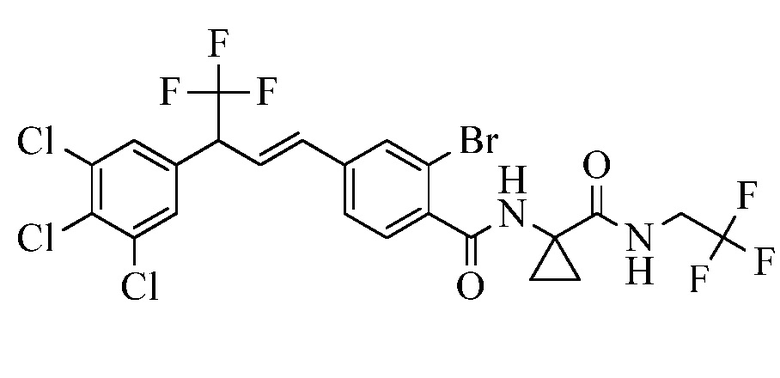
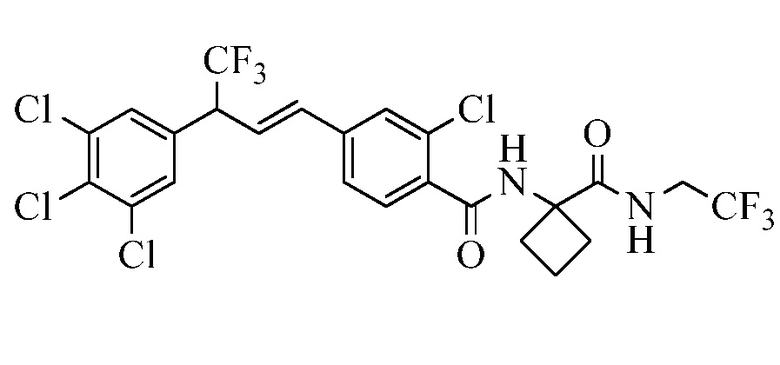
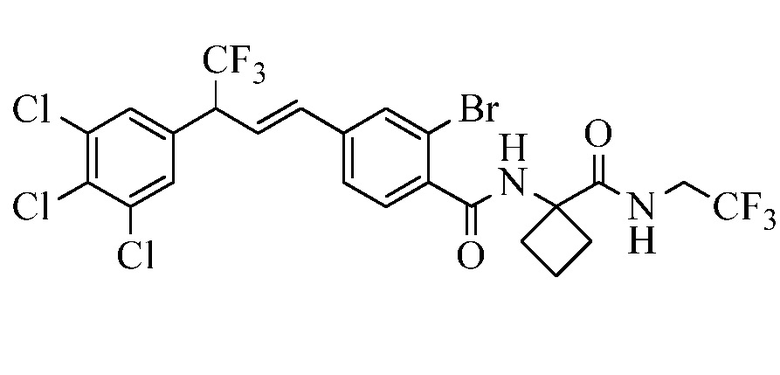
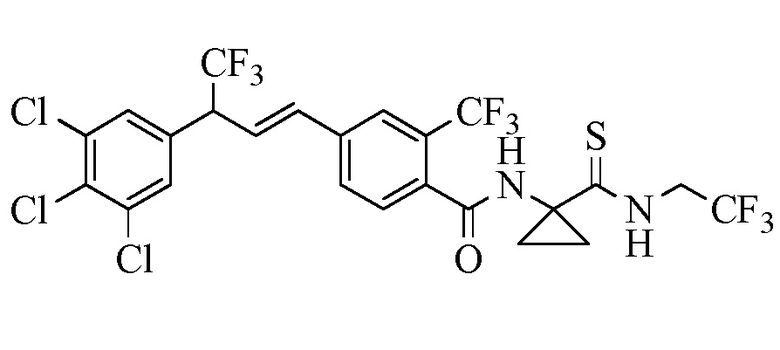
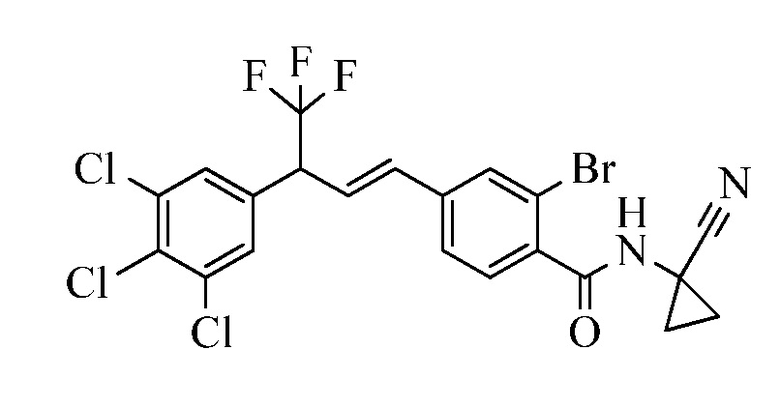
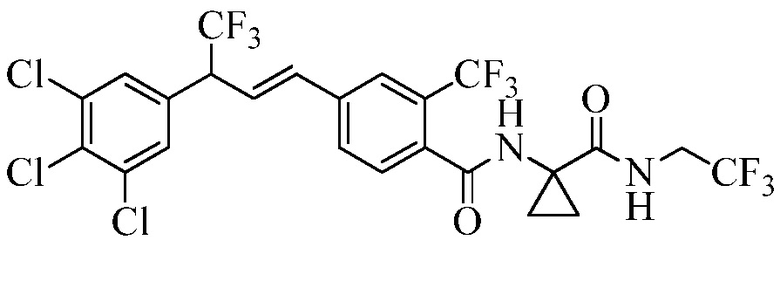

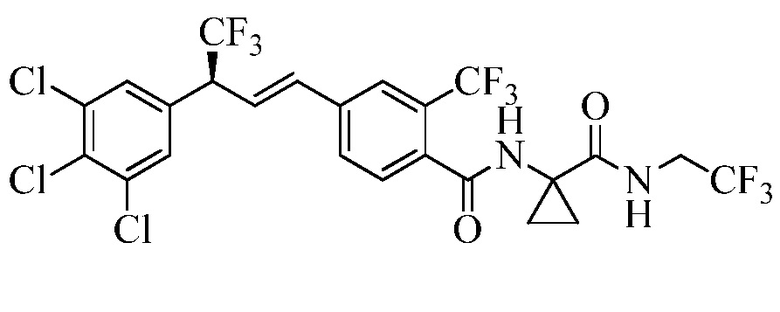

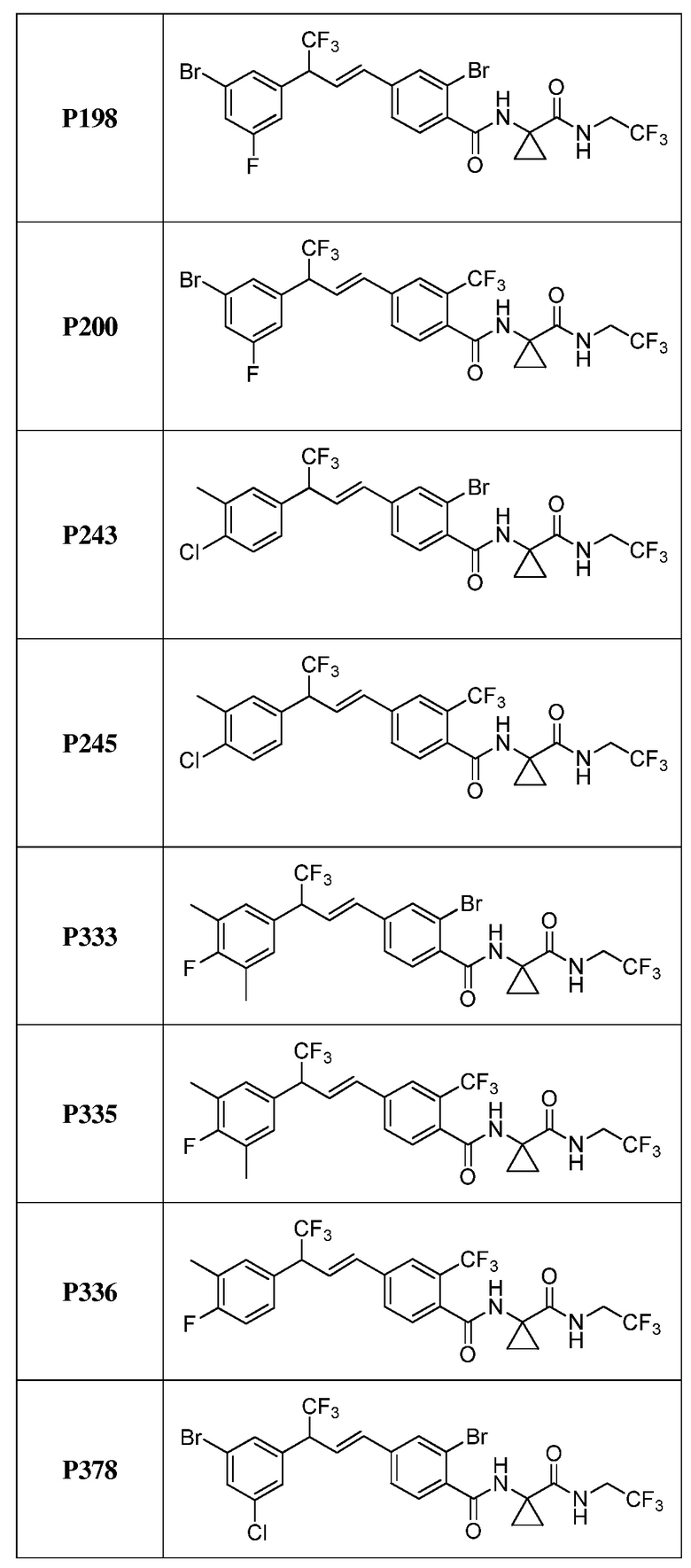
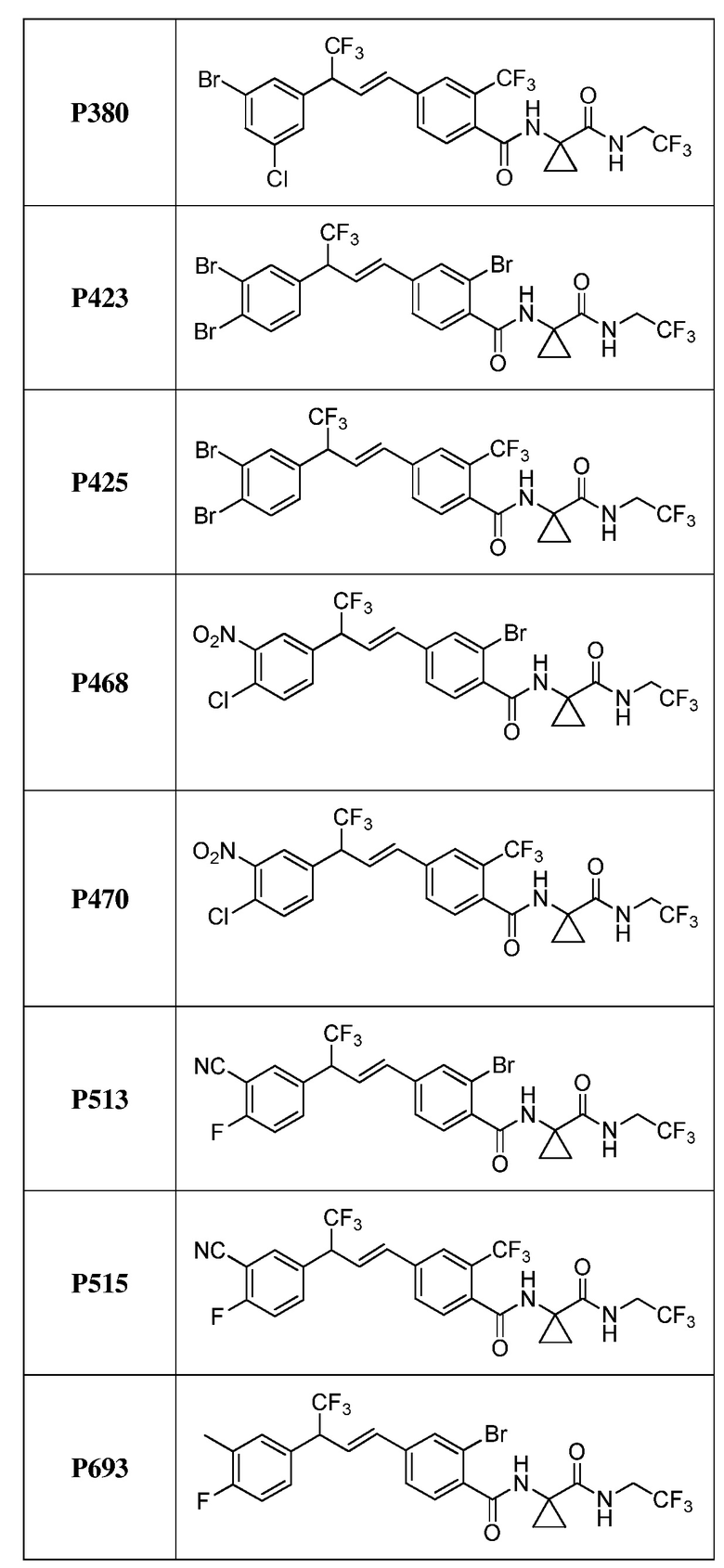
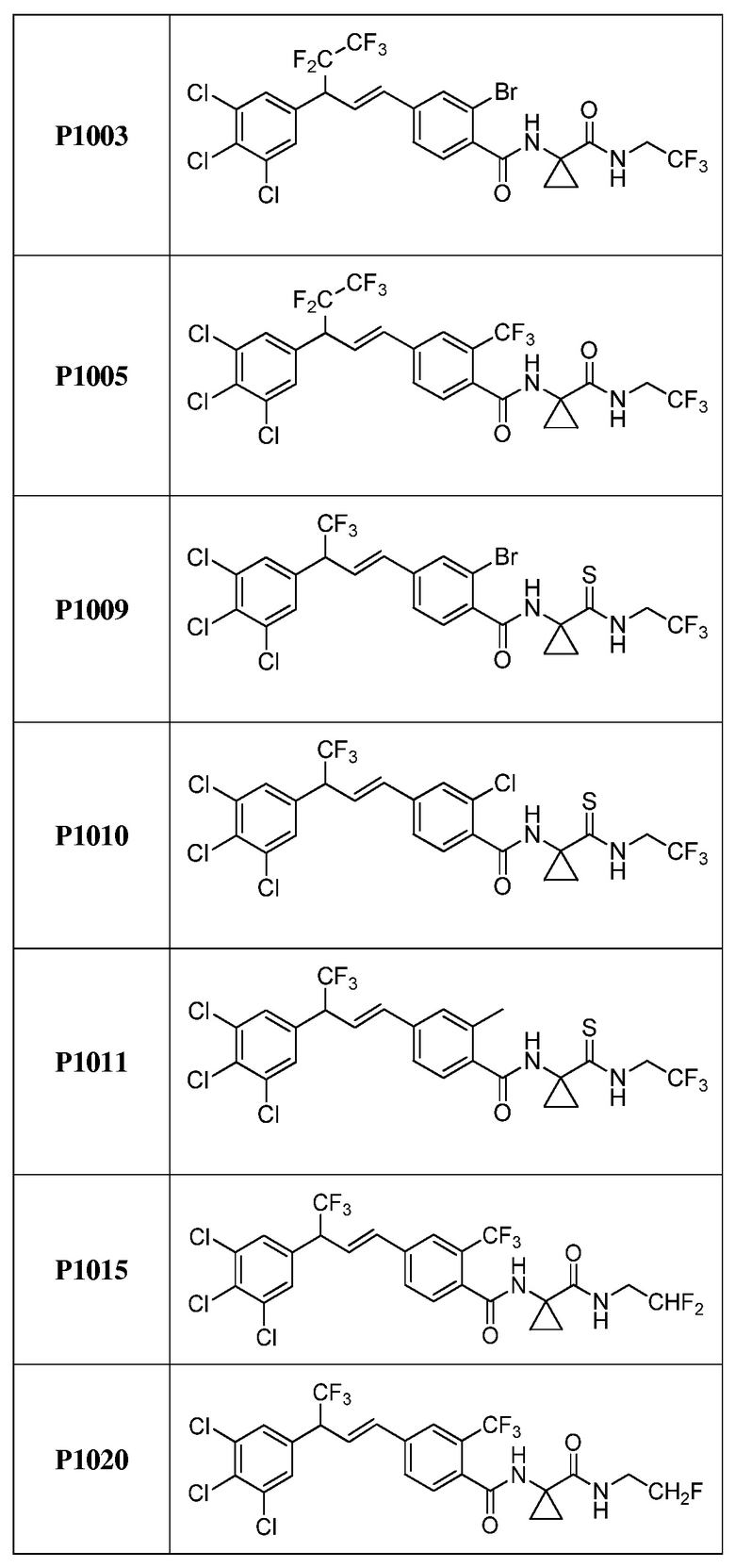
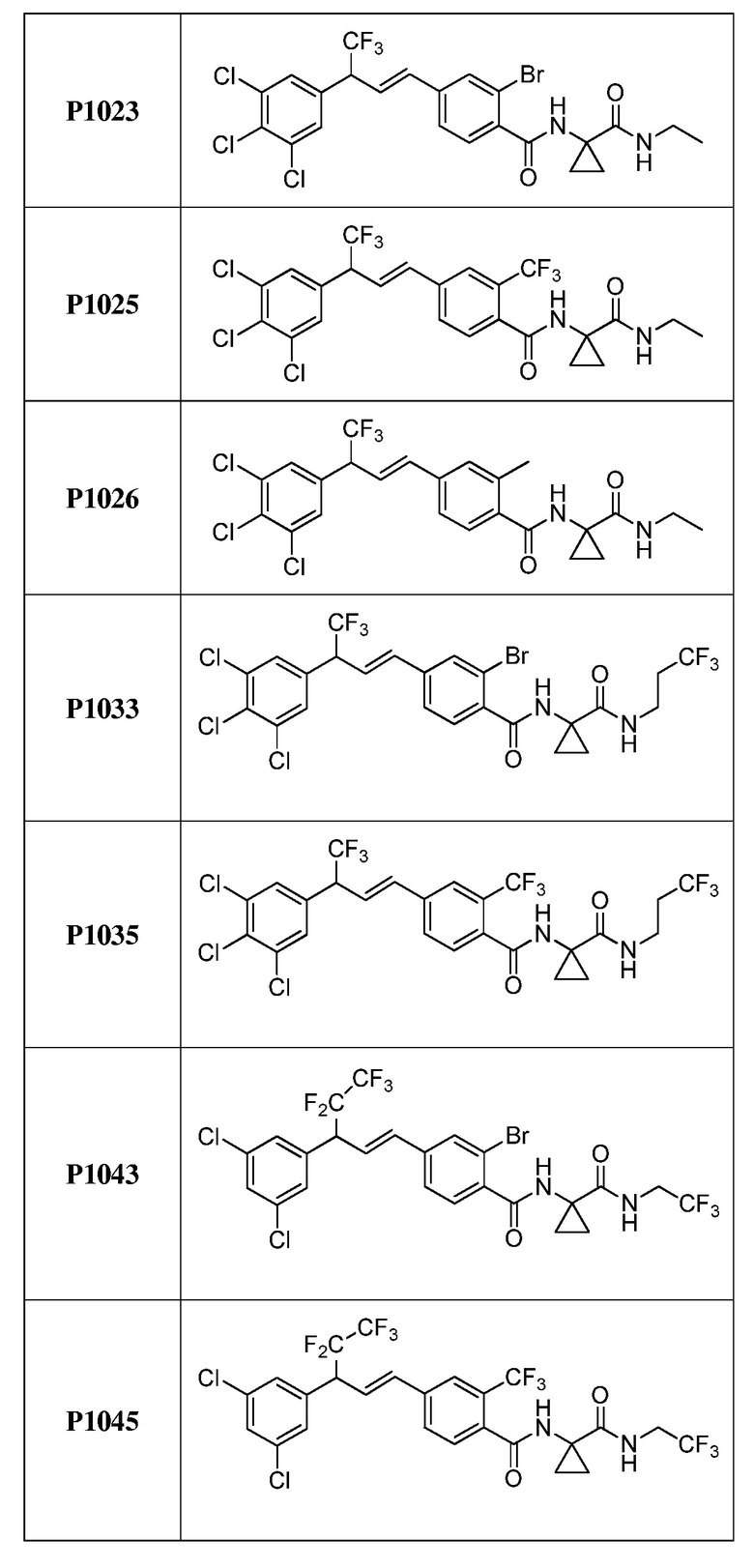
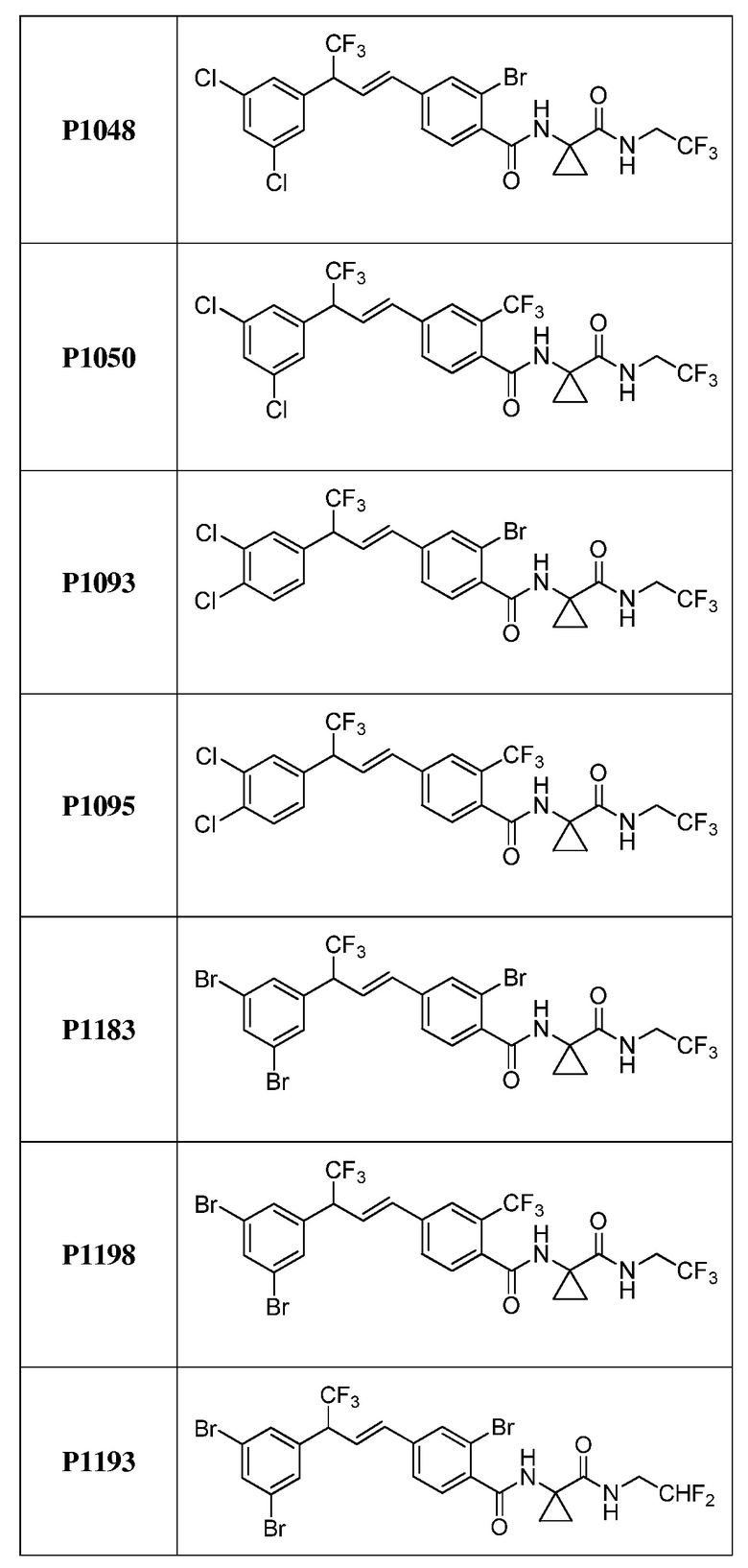
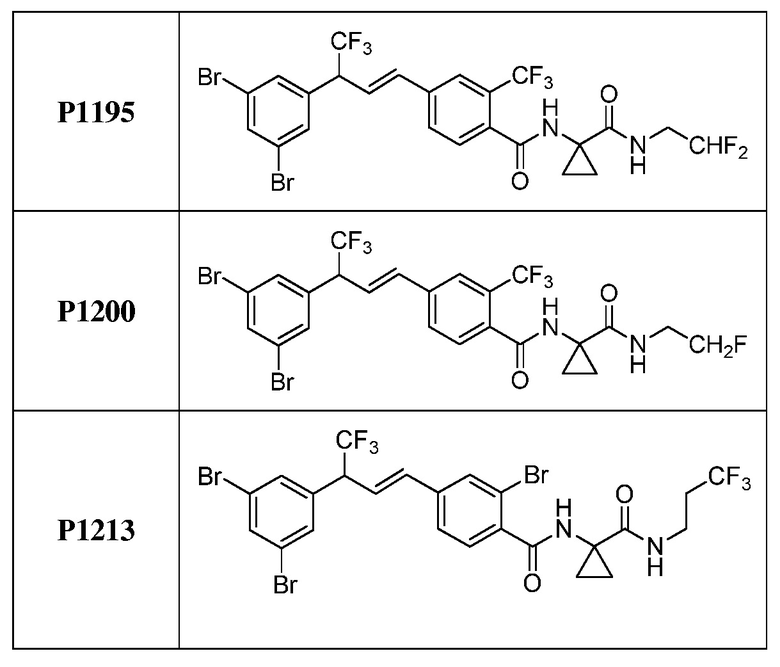
40. Композиция по п.1, в которой молекула согласно Формуле Один имеет одну из следующих структур:
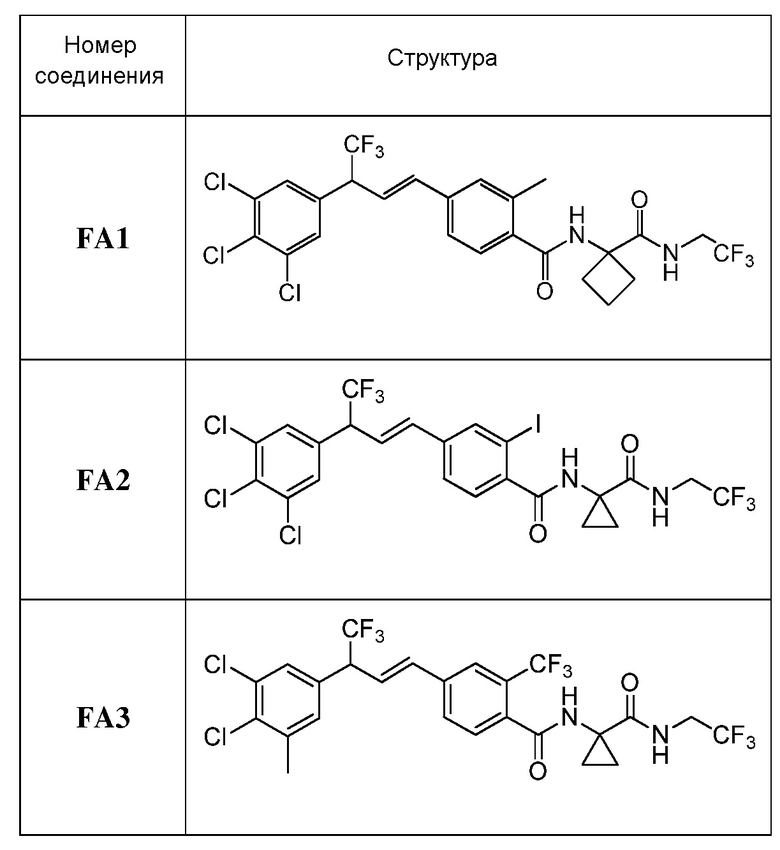
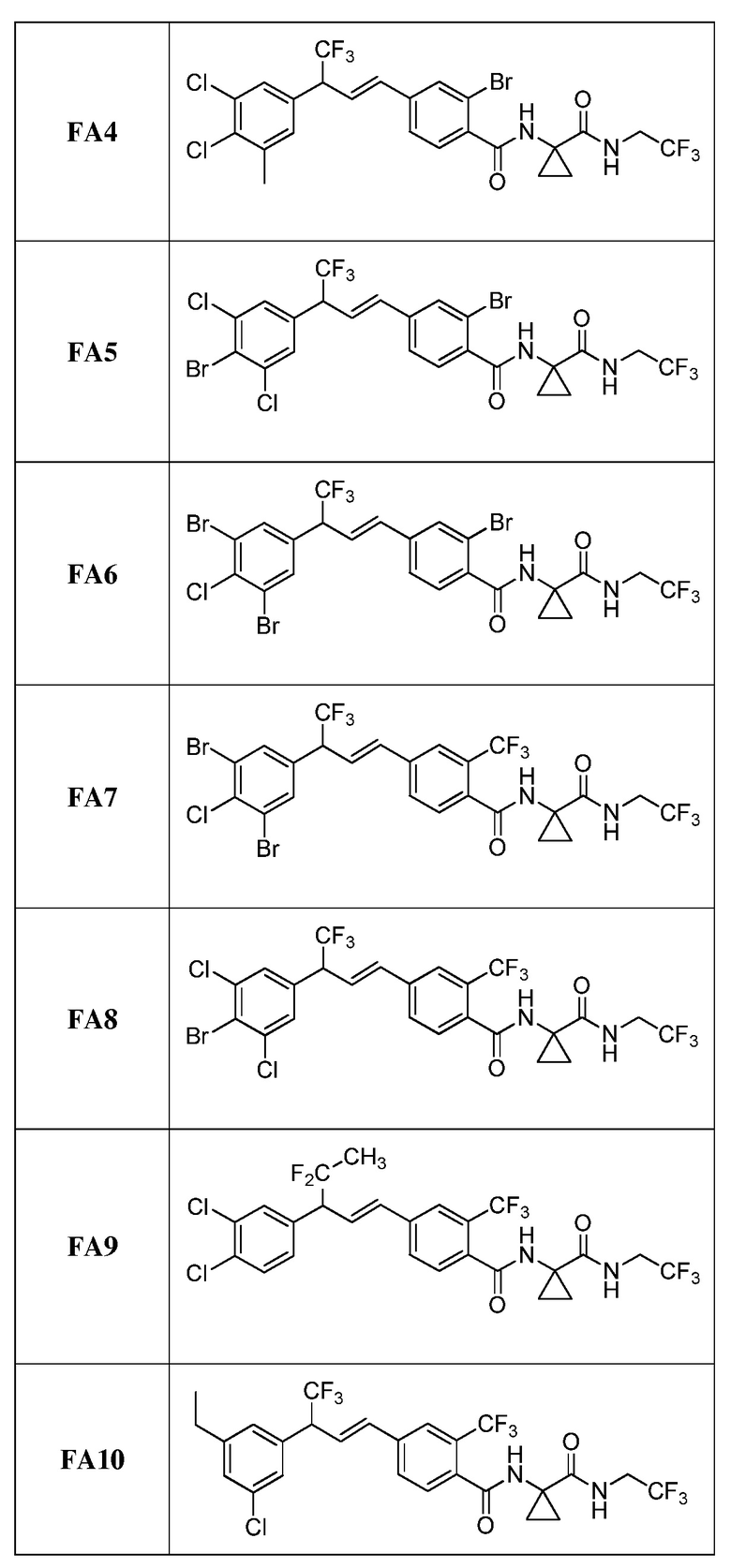
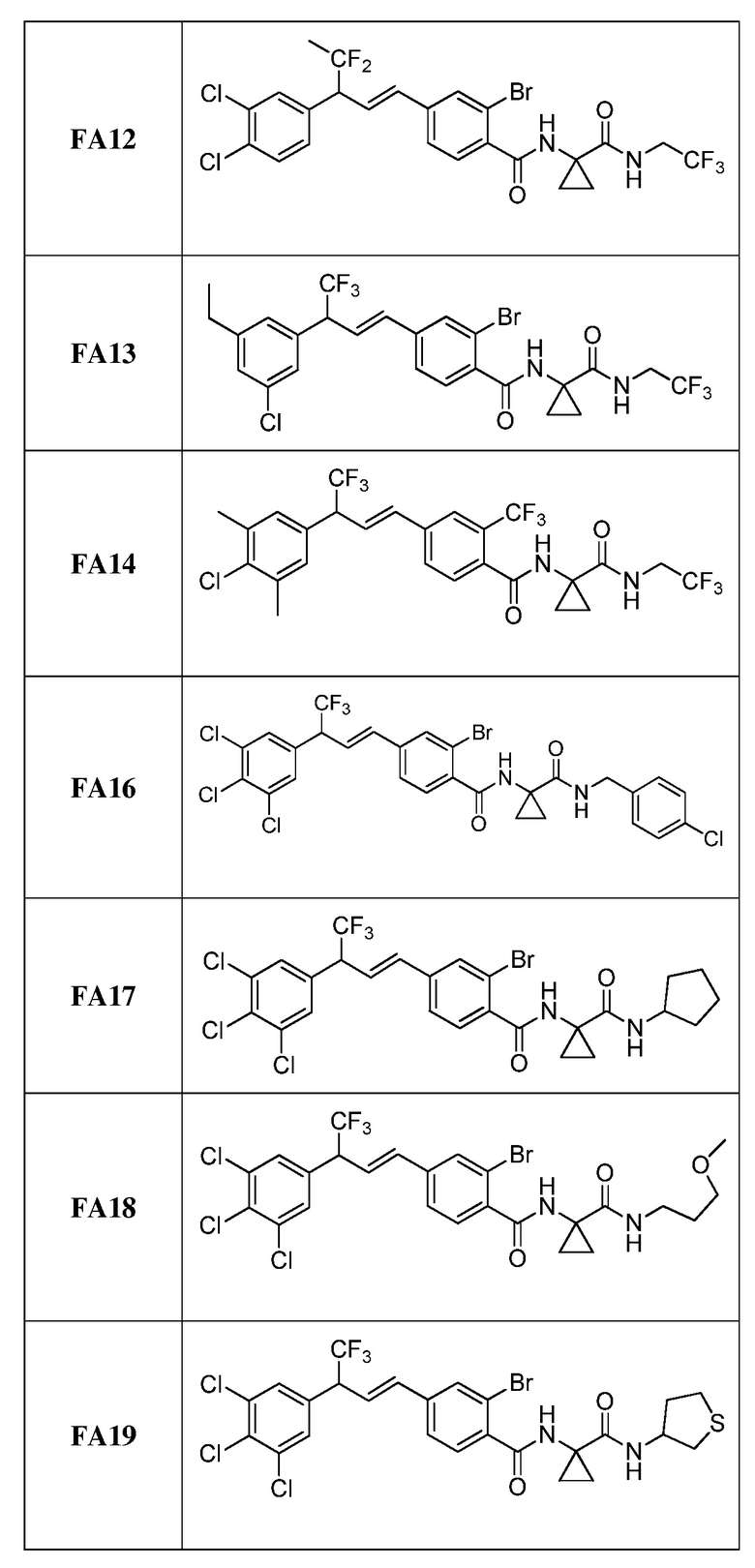
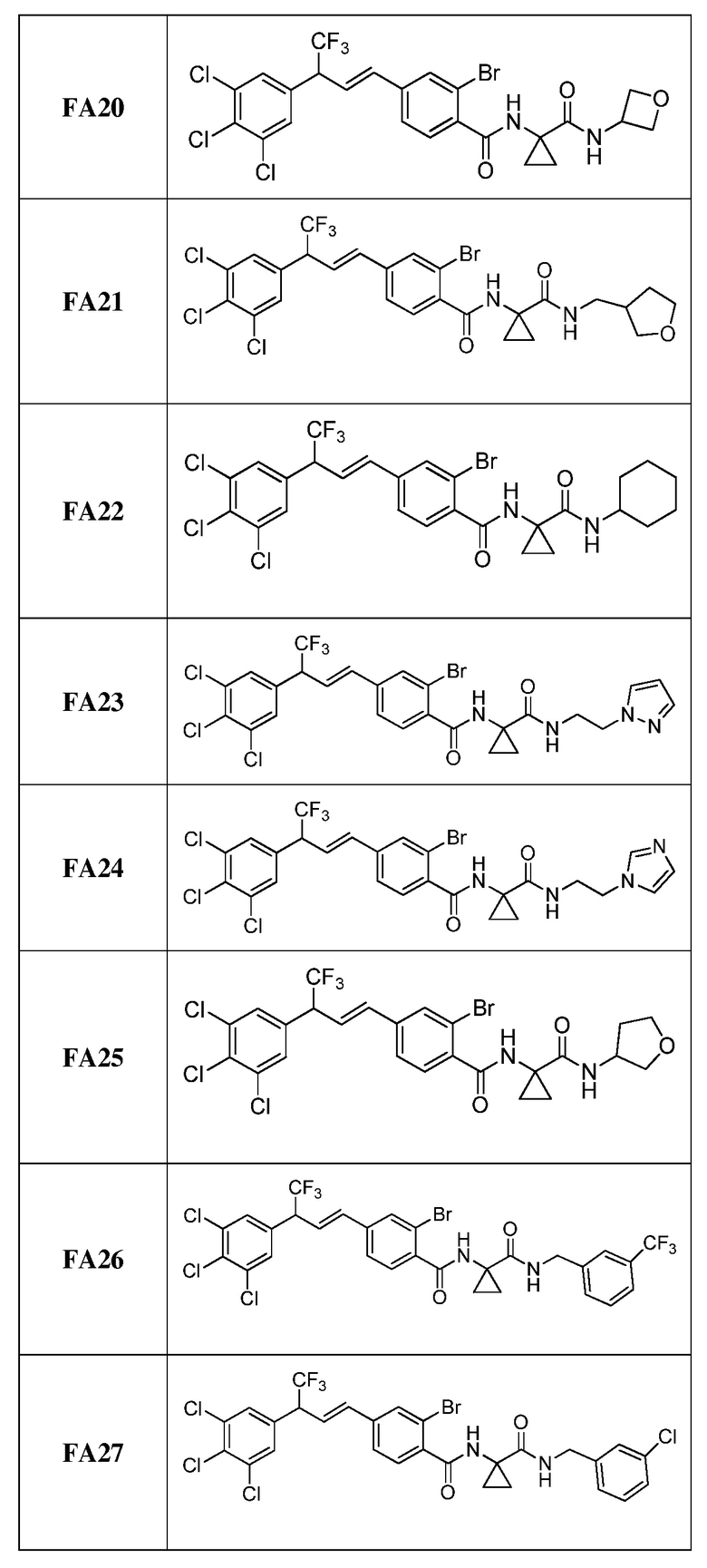
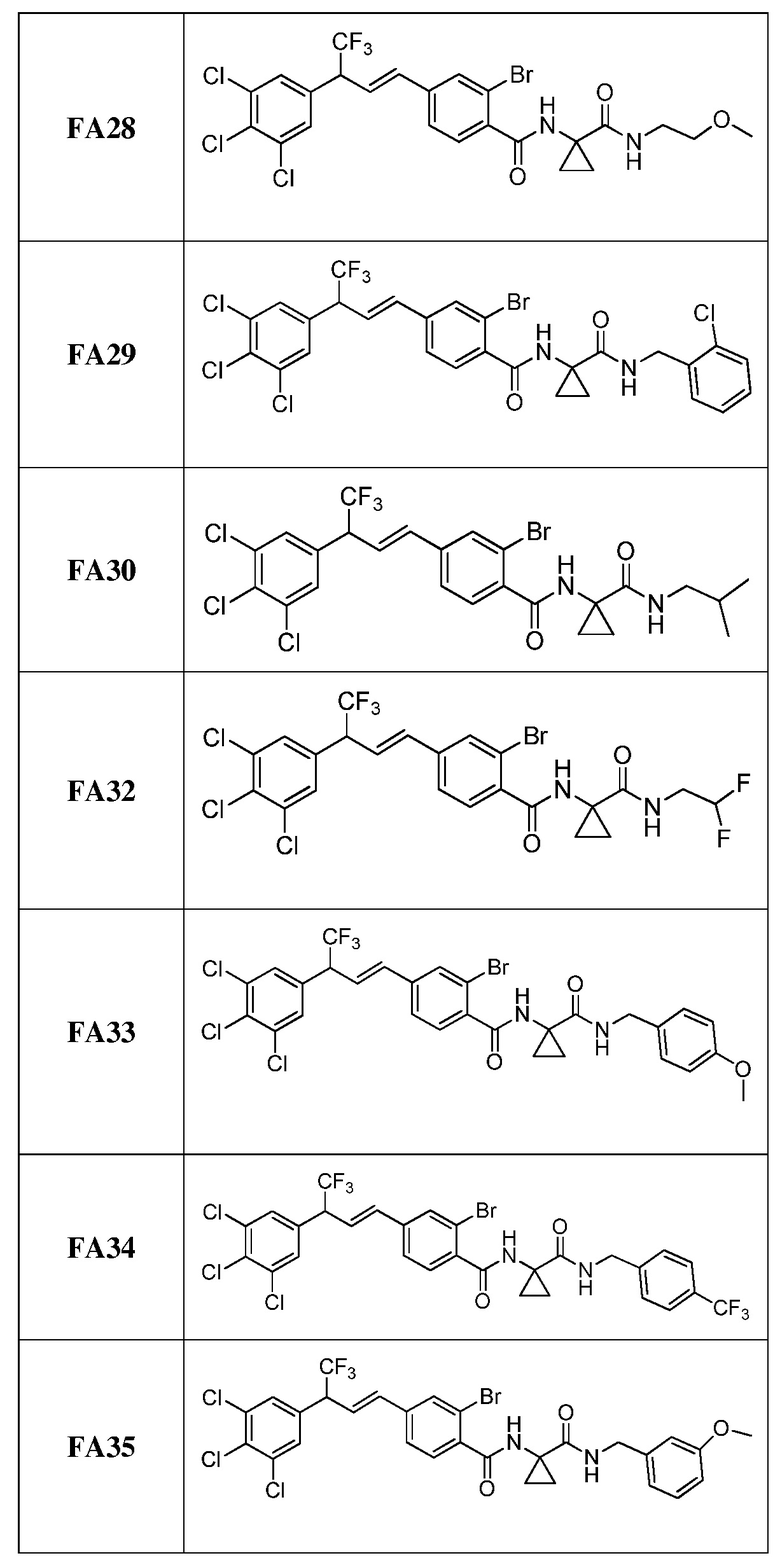
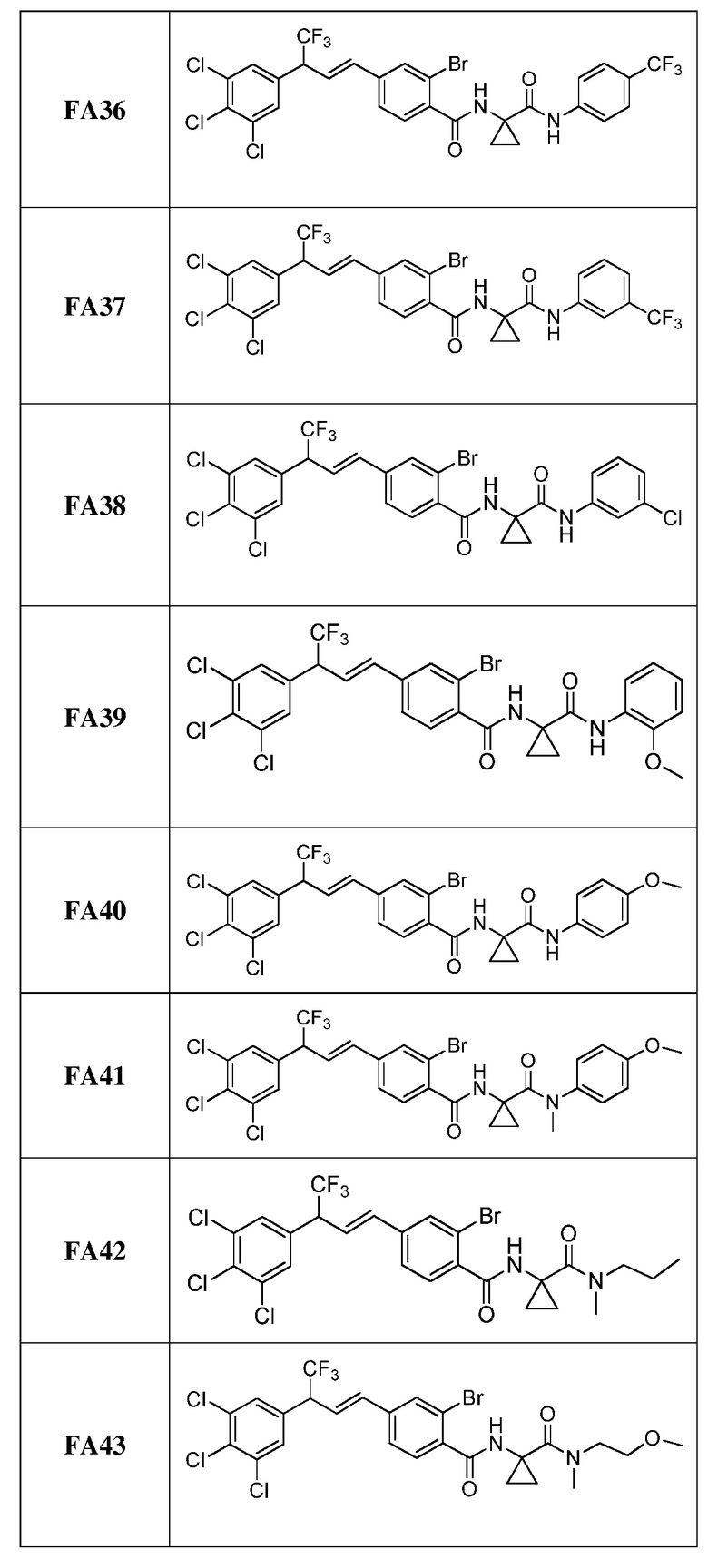
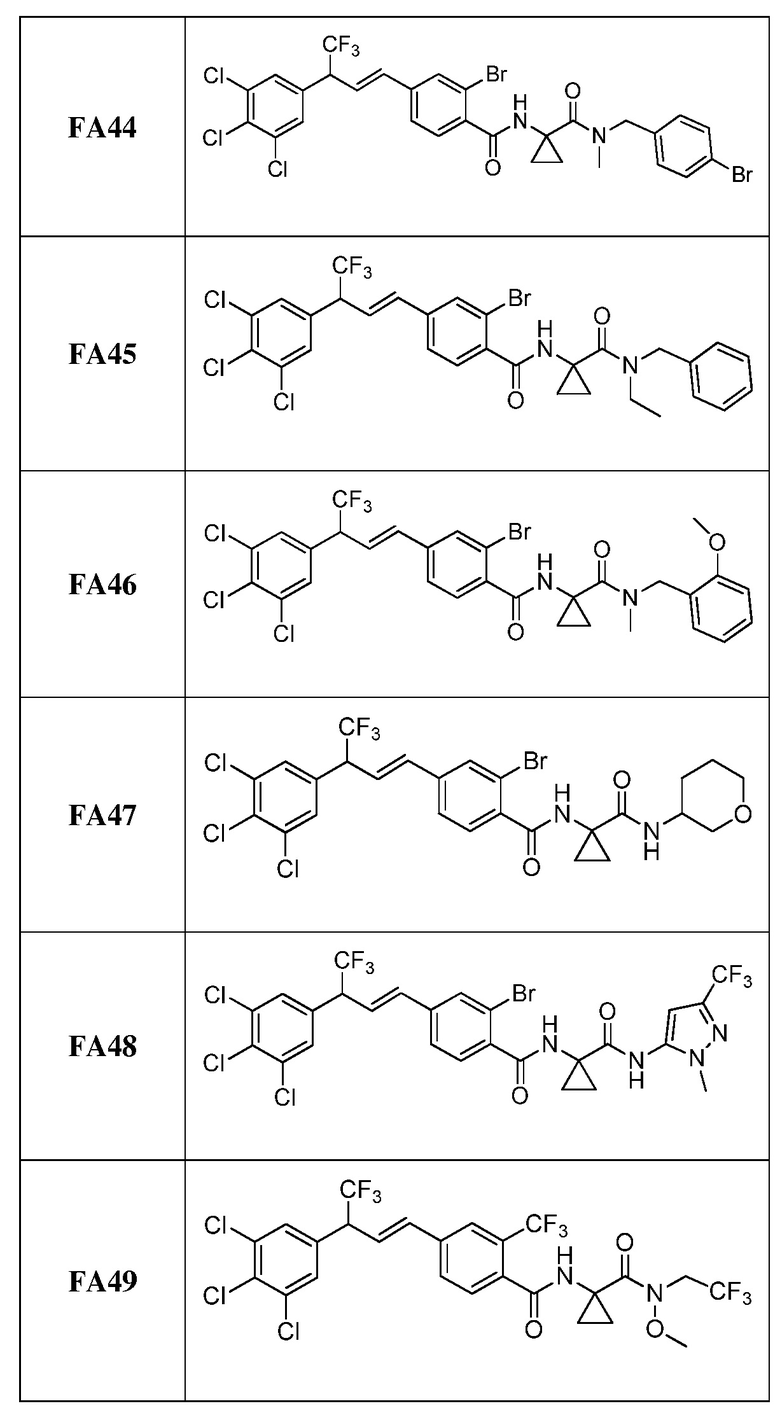
41. Композиция по п.1, дополнительно включающая:
(a) одно или более соединений, обладающих акарицидными, альгицидными, авицидными, бактерицидными, фунгицидными, гербицидными, инсектицидными, моллюскоцидными, нематоцидными, родентицидными или вироцидными свойствами; или
(b) одно или более соединений, которые являются антифидантами, репеллентами против птиц, хемостерилизаторами, гербицидными антидотами, аттрактантами для насекомых, репеллентами против насекомых, репеллентами против млекопитающих, соединениями, нарушающими спаривание, активаторами растений, регуляторами роста растений или синергическими соединениями; или
(c) (a) и (b).
42. Композиция по п.1, дополнительно включающая одно или более соединений, выбранных из следующих: бромид (3-этоксипропил)ртути, 1,2-дихлорпропан, 1,3-дихлорпропен, 1-метилциклопропен, 1-нафтол, 2-(октилтио)этанол, 2,3,5-трийодбензойная кислота, 2,3,6-TBA, 2,3,6-TBA-диметиламмоний, 2,3,6-TBA-литий, 2,3,6-TBA-калий, 2,3,6-TBA-натрий, 2,4,5-T, 2,4,5-T-2-бутоксипропил, 2,4,5-T-2-этилгексил, 2,4,5-T-3-бутоксипропил, 2,4,5-TB, 2,4,5-T-бутометил, 2,4,5-T-бутотил, 2,4,5-T-бутил, 2,4,5-T-изобутил, 2,4,5-T-изоктил, 2,4,5-T-изопропил, 2,4,5-T-метил, 2,4,5-T-пентил, 2,4,5-T-натрий, 2,4,5-T-триэтиламмоний, 2,4,5-T-троламин, 2,4-D, 2,4-D-2-бутоксипропил, 2,4-D-2-этилгексил, 2,4-D-3-бутоксипропил, 2,4-D-аммоний, 2,4-DB, 2,4-DB-бутил, 2,4-DB-диметиламмоний, 2,4-DB-изоктил, 2,4-DB-калий, 2,4-DB-натрий, 2,4-D-бутотил, 2,4-D-бутил, 2,4-D-диэтиламмоний, 2,4-D-диметиламмоний, 2,4-D-диоламин, 2,4-D-додециламмоний, 2,4-DEB, 2,4-DEP, 2,4-D-этил, 2,4-D-гептиламмоний, 2,4-D-изобутил, 2,4-D-изоктил, 2,4-D-изопропил, 2,4-D-изопропиламмоний, 2,4-D-литий, 2,4-D-мептил, 2,4-D-метил, 2,4-D-октил, 2,4-D-пентил, 2,4-D-калий, 2,4-D-пропил, 2,4-D-натрий, 2,4-D-тефурил, 2,4-D-тетрадециламмоний, 2,4-D-триэтиламмоний, 2,4-D-трис(2-гидроксипропил)аммоний, 2,4-D-троламин, 2iP, хлорид 2-метоксиэтилртути, 2-фенилфенол, 3,4-DA, 3,4-DB, 3,4-DP, 4-аминопиридин, 4-CPA, 4-CPA-калий, 4-CPA-натрий, 4-CPB, 4-CPP, 4-гидроксифенэтиловый спирт, сульфат 8-гидроксихинолина, 8-фенилртутьоксихинолин, абамектин, абсцизовая кислота, ACC, ацефат, ацеквиноцил, ацетамиприд, ацетион, ацетохлор, ацетофос, ацетопрол, ацибензолар, ацибензолар-S-метил, ацифлуорфен, ацифлуорфен-метил, ацифлуорфен-натрий, аклонифен, акреп, акринатрин, акролеин, акрилонитрил, аципетакс, аципетакс-медь, аципетакс-цинк, алахлор, аланикарб, альбендазол, алдикарб, алдиморф, альдоксикарб, альдрин, аллетрин, аллицин, аллидохлор, аллосамидин, аллоксидим, аллоксидим-натрий, аллиловый спирт, алликсикарб, алорак, альфа-циперметрин, альфа-эндосульфан, аметоктрадин, аметридион, аметрин, амибузин, амикарбазон, амикартиазол, амидитион, амидофлумет, амидосульфурон, аминокарб, аминоциклопирахлор, аминоциклопирахлор-метил, аминоцикло-пирахлор-калий, аминопиралид, аминопиралид-калий, аминопиралид-трис(2-гидроксипропил)аммоний, амипрофос-метил, амипрофос, амисульбром, амитон, амитон-оксалат, амитраз, амитрол, сульфамат аммония, альфа-нафталинацетат аммония, амобам, ампропилфос, анабазин, анцимидол, анилазин, анилофос, анисурон, антрахинон, анту, афолат, арамит, оксид мышьяка, асомат, аспирин, асулам, асулам-калий, асулам-натрий, атидатион, атратон, атразин, ауреофунгин, авиглицин, авиглицин-гидрохлорид, азаконазол, азадирахтин, азафенидин, азаметифос, азимсульфурон, азинфос-этил, азинфос-метил, азипротрин, азитирам, азобензол, азоциклотин, азотоат, азоксистробин, бахмедеш, барбан, гексафторсиликат бария, полисульфид бария, бартрин, BCPC, бефлубутамид, беналаксил, беналаксил-M, беназолин, беназолин-диметиламмоний, беназолин-этил, беназолин-калий, бенкарбазон, бенклотиаз, бендиокарб, бенфлуралин, бенфуракарб, бенфуресат, беноданил, беномил, беноксакор, беноксафос, бенквинокс, бенсульфурон, бенсульфурон-метил, бенсулид, бенсултап, бенталурон, бентазон, бентазон-натрий, бентиаваликарб, бентиаваликарб-изопропил, бентиазол, бентранил, бензадокс, бензадокс-аммоний, хлорид бензалкония, бензамакрил, бензамакрил-изобутил, бензаморф, бензфендизон, бензипрам, бензобициклон, бензофенап, бензофлуор, бензогидроксамовая кислота, бензоксимат, бензоилпроп, бензоилпроп-этил, бензтиазурон, бензилбензоат, бензиладенин, берберин, берберин-хлорид, бета-цифлутрин, бета-циперметрин, бетоксазин, бициклопирон, бифеназат, бифенокс, бифентрин, бифуцзиньши, биланафос, биланафос-натрий, бинапакрил, бинсингсиао, биоаллетрин, биоэтанометрин, биоперметрин, биоресметрин, бифенил, бисазир, бисмертиазол, биспирибак, биспирибак-натрий, бистрифлурон, битертанол, битионол, биксафен, бластицидин-S, бура, бордоская смесь, борная кислота, боскалид, брассинолид, брассинолид-этил, бревикомин, бродифакоум, брофенвалерат, брофлутринат, бромацил, бромацил-литий, бромацил-натрий, бромадиолон, брометалин, брометрин, брофенвинфос, бромацетамид, бромобонил, бромобутид, бромоциклен, бром-ДДТ, бромофеноксим, бромофос, бромофос-этил, бромпропилат, бромоталонил, бромоксинил, бромоксинил-бутират, бромоксинил-гептаноат, бромоксинил-октаноат, бромоксинил-калий, бромпиразон, бромуконазол, бронопол, букарполат, буфенкарб, буминафос, бупиримат, бупрофезин, бургундская смесь, бусульфан, бутакарб, бутахлор, бутафенацил, бутамифос, бутатиофос, бутенахлор, бутетрин, бутидазол, бутиобат, бутиурон, бутокарбоксим, бутонат, бутопироноксил, бутоксикарбоксим, бутралин, бутроксидим, бутурон, бутиламин, бутилат, какодиловая кислота, кадусафос, кафенстрол, арсенат кальция, хлорат кальция, цианамид кальция, полисульфид кальция, калвинфос, камбендихлор, камфехлор, камфора, каптафол, каптан, карбаморф, карбанолат, карбарил, карбасулам, карбендазим, карбендазим-бензолсульфонат, карбендазим-сульфит, карбетамид, карбофуран, сероуглерод, четыреххлористый углерод, карбофенотион, карбосульфан, карбоксазол, карбоксид, карбоксин, карфентразон, карфентразон-этил, карпропамид, картап, картап-гидрохлорид, карвакрол, карвон, CDEA, целлоцидин, CEPC, кералур, чешунтская смесь, хинометионат, хитозан, хлобентиазон, хлометоксифен, хлоралоз, хлорамбен, хлорамбен-аммоний, хлорабен-диоламин, хлорабен-метил, хлорабен-метиламмоний, хлорабен-натрий, хлорамин-фосфор, хлорамфеникол, хлораниформетан, хлоранил, хлоранокрил, хлорантранилипрол, хлоразифоп, хлоразифоп-пропаргил, хлоразин, хлорбенсид, хлорбензурон, хлорбициклен, хлорбромурон, хлорбуфам, хлордан, хлордекон, хлордимеформ, хлордимеформ-гидрохлорид, хлор-эмпентрин, хлоретоксифос, хлоретурон, хлорфенак, хлорфенак-аммоний, хлорфенак-натрий, хлорфенапир, хлорфеназол, хлорфенетол, хлорфенпроп, хлорфенсон, хлорфенсульфид, хлорфенвинфос, хлорфлуазурон, хлорфлуразол, хлорфлурен, хлорфлурен-метил, хлорфлуренол, хлорфлуренол-метил, хлоридазон, хлоримурон, хлоримурон-этил, хлормефос, хлормекват, хлормекват-хлорид, хлорнидин, хлорнитрофен, хлорбензилат, хлординитронафталины, хлороформ, хлоромебуформ, хлорметиурон, хлоронеб, хлорофацинон, хлорофацинон-натрий, хлорпикрин, хлоропон, хлорпропилат, хлороталонил, хлоротолурон, хлороксурон, хлороксинил, хлорфоний, хлорфоний-хлорид, хлорфоксим, хлорпразофос, хлорпрокарб, хлорпрофам, хлорпирифос, хлорпирифос-метил, хлорквинокс, хлорсульфурон, хлортал, хлортал-диметил, хлортал-монометил, хлортиамид, хлортиофос, хлозолинат, холин-хлорид, хромафенозид, цинерин I, цинерин II, цинерины, цинидон-этил, цинметилин, циносульфурон, циобутид, цисанилид, цисметрин, клетодим, климбазол, клиодинат, клодинафоп, клодинафоп-пропаргил, клоэтокарб, клофенцет, клофенцет-калий, клофентезин, клофибриновая кислота, клофоп, клофоп-изобутил, кломазон, кломепроп, клопроп, клопроксидим, клопиралид, клопиралид-метил, клопиралид-оламин, клопиралид-калий, клопиралид-трис(2-гидроксипропил)аммоний, клоквинтоцет, клоквинтоцет-мексил, клорансулам, клорансулам-метил, клозантел, клотианидин, клотримазол, клоксифонак, клоксифонак-натрий, CMA, кодлелур, колофонат, ацетат меди, ацетоарсенит меди, арсенат меди, карбонат меди основной, гидроксид меди, нафтенат меди, олеат меди, оксихлорид меди, силикат меди, сульфат меди, хромат меди-цинка, кумахлор, кумафурил, кумафос, куматетралил, кумитоат, кумоксистробин, CPMC, CPMF, CPPC, кредазин, крезол, кримидин, кротамитон, кротоксифос, круфомат, криолит, куелур, куфранеб, кумилурон, купробам, оксид меди, куркуменол, цианамид, цианатрин, цианазин, цианофенфос, цианофос, циантоат, циантранилипрол, циазофамид, цибутрин, циклафурамид, цикланилид, циклетрин, циклоат, циклогексимид, циклопрат, циклопротрин, циклосульфамурон, циклоксаприд, циклоксидим, циклурон, циенопирафен, цифлуфенамид, цифлуметофен, цифлутрин, цигалофоп, цигалофоп-бутил, цигалотрин, цигексатин, цимиазол, цимиазол-гидрохлорид, цимоксанил, циометринил, ципендазол, циперметрин, циперкват, циперкват-хлорид, цифенотрин, ципразин, ципразол, ципроконазол, ципродинил, ципрофурам, ципромид, ципросульфамид, циромазин, цитиоат, даимурон, далапон, далапон-кальций, далапон-магний, далапон-натрий, даминозид, даютонг, дазомет, дазомет-натрий, DBCP, d-камфора, DCIP, DCPTA, ДДТ, дебакарб, декафентин, декарбофуран, дегидроацетовая кислота, делахлор, дельтаметрин, демефион, демефион-O, демефион-S, деметон, деметон-метил, деметон-O, деметон-O-метил, деметон-S, деметон-S-метил, деметон-S-метилсульфон, десмедифам, десметрин, d-фаншилукуебинзуши, диафентиурон, диалифос, ди-аллат, диамидафос, диатомовая земля, диазинон, дибутилфталат, дибутилсукцинат, дикамба, дикамба-дигликольамин, дикамба-диметиламмоний, дикамба-диоламин, дикамба-изопропиламмоний, дикамба-метил, дикамба-оламин, дикамба-калий, дикамба-натрий, дикамба-троламин, дикаптон, дихлобенил, дихлофентион, дихлофлуанид, дихлон, дихлоральмочевина, дихлорбензурон, дихлорфлуренол, дихлорфлуренол-метил, дихлормат, дихлормид, дихлорфен, дихлорпроп, дихлорпроп-2-этилгексил, дихлорпроп-бутотил, дихлорпроп-диметиламмоний, дихлорпроп-этиламмоний, дихлорпроп-изоктил, дихлорпроп-метил, дихлорпроп-P, дихлорпроп-P-2-этилгексил, дихлорпроп-P-диметиламмоний, дихлорпроп-калий, дихлорпроп-натрий, дихлорвос, дихлозолин, дихлобутразол, диклоцимет, диклофоп, диклофоп-метил, дикломезин, дикломезин-натрий, диклоран, диклосулам, дикофол, дикумарол, дикрезил, дикротофос, дицикланил, дициклонон, дильдрин, диенохлор, диэтамкват, диэтамкват-дихлорид, диэтатил, диэтатил-этил, диэтофенкарб, диэтолат, диэтилпирокарбонат, диэтилтолуамид, дифенакум, дифеноконазол, дифенопентен, дифенопентен-этил, дифеноксурон, дифензокват, дифензокват-метилсульфат, дифетиалон, дифловидазин, дифлубензурон, дифлуфеникан, дифлуфензопир, дифлуфензопир-натрий, дифлуметорим, дикегулак, дикегулак-натрий, дилор, диматиф, димефлутрин, димефокс, димефурон, димепиперат, диметахлон, диметан, диметакарб, диметахлор, диметаметрин, диметенамид, диметенамид-P, диметипин, диметиримол, диметоат, диметоморф, диметрин, диметилкарбат, диметилфталат, диметилвинфос, диметилан, димексано, димидазон, димоксистробин, динекс, динекс-диклексин, динджунезуо, диниконазол, диниконазол-M, динитрамин, динобутан, динокап, динокап-4, динокап-6, диноктон, динофенат, динопентон, динопроп, диносам, диносеб, диносеб-ацетат, диносеб-аммоний, диносеб-диоламин, диносеб-натрий, диносеб-троламин, диносульфон, динотефуран, динотерб, динотерб-ацетат, динотербон, диофенолан, диоксабензофос, диоксакарб, диоксатион, дифацинон, дифацинон-натрий, дифенамид, бифенилсульфон, дифениламин, дипропалин, дипропетрин, дипиритион, дикват, дикват-дибромид, диспарлур, дисул, дисульфирам, дисульфотон, дисул-натрий, диталимфос, дитианон, дитикрофос, дитиоэфир, дитиопир, диурон, d-лимонен, DMPA, DNOC, DNOC-аммоний, DNOC-калий, DNOC-натрий, додеморф, додеморф-ацетат, додеморф-бензоат, додицин, додицин-гидрохлорид, додицин-натрий, додин, дофенапин, доминикалур, дорамектин, дразоксолон, DSMA, дуфулин, EBEP, EBP, экдистерон, эдифенфос, эглиназин, эглиназин-этил, эмамектин, эмамектин-бензоат, EMPC, эмпентрин, эндосульфан, эндотал, эндотал-диаммоний, эндотал-дикалий, эндотал-динатрий, эндотион, эндрин, энестробурин, EPN, эпохолеон, эпофенонан, эпоксиконазол, эприномектин, эпроназ, ЕРТС, эрбон, эргокальциферол, эрлуцзисианкаоан, эсдепаллетрин, эсфенвалерат, эспрокарб, этацеласил, этаконазол, этафос, этем, этабоксам, этахлор, эталфлуралин, этаметсульфурон, этаметсульфурон-метил, этапрохлор, этефон, этидимурон, этиофенкарб, этиолат, этион, этиозин, этипрол, этиримол, этоат-метил, этофумесат, этогексадиол, этопрофос, этоксифен, этоксифен-этил, этоксиквин, этоксисульфурон, этихлозат, этилформиат, этил-α-нафталинацетат, этил-DDD, этилен, дибромэтан, дихлорэтан, этиленоксид, этилицин, 2,3-дигидроксипропилмеркаптид этилртути, ацетат этилртути, бромид этилртути, хлорид этилртути, фосфат этилртути, этинофен, этнипромид, этобензанид, этофенпрокс, этоксазол, этридиазол, этримфос, эвгенол, EXD, фамоксадон, фамфур, фенамидон, фенаминосульф, фенамифос, фенапанил, фенаримол, фенасулам, феназафлор, феназаквин, фенбуконазол, фенбутатин-оксид, фенхлоразол, фенхлоразол-этил, фенхлорфос, фенклорим, фенетакарб, фенфлутрин, фенфурам, фенгексамид, фенитропан, фенитротион, фенджунтонг, фенобукарб, фенопроп, фенопроп-3-бутоксипропил, фенопроп-бутометил, фенопроп-бутотил, фенопроп-бутил, фенопроп-изоктил, фенопроп-метил, фенопроп-калий, фенотиокарб, феноксакрим, феноксанил, феноксапроп, феноксапроп-этил, феноксапроп-P, феноксапроп-Р-этил, феноксасульфон, феноксикарб, фенпиклонил, фенпиритрин, фенпропатрин, фенпропидин, фенпропиморф, фенпиразамин, фенпироксимат, фенридазон, фенридазон-калий, фенридазон-пропил, фенсон, фенсульфотион, фентеракол, фентиапроп, фентиапроп-этил, фентион, фентион-этил, фентин, фентин-ацетат, фентин-хлорид, фентин-гидроксид, фентразамид, фентрифанил, фенурон, фенурон-TCA, фенвалерат, фербам, феримзон, сульфат железа, фипронил, флампроп, флампроп-изопропил, флампроп-M, флампроп-метил, флампроп-M-изопропил, флампроп-М-метил, флазасульфурон, флокумафен, флометоквин, флоникамид, флорасулам, флуакрипирим, флуазифоп, флуазифоп-бутил, флуазифоп-метил, флуазифоп-P, флуазифоп-P-бутил, флуазинам, флуазолат, флуазурон, флубендиамид, флубензимин, флукарбазон, флукарбазон-натрий, флуцетосульфурон, флухлоралин, флукофурон, фуциклоксурон, флуцитринат, флудиоксонил, флуенетил, флуенсульфон, флуфенацет, флуфенерим, флуфеникан, флуфеноксурон, флуфенпрокс, флуфенпир, флуфенпир-этил, флуфипрол, флуметрин, флуметовер, флуметралин, флуметсулам, флумезин, флумиклорак, флумиклорак-пентил, флумиоксазин, флумипропин, флуморф, флуометурон, флуопиколид, флуопирам, флуорбенсид, флуоридамид, флуороацетамид, флуородифен, флуорогликофен, флуорогликофен-этил, флуороимид, флуоромидин, флуоронитрофен, флуотиурон, флуотримазол, флуоксастробин, флупоксам, флупропацил, флупропадин, флупропанат, флупропанат-натрий, флупирадифурон, флупирсульфурон, флупирсульфурон-метил, флупирсульфурон-метил-натрий, флуквинконазол, флуразол, флуренол, флуренол-бутил, флуренол-метил, флуридон, флурохлоридон, флуроксипир, флуроксипир-бутометил, флуроксипир-мептил, флурпримидол, флурсуламид, флуртамон, флусилазол, флусульфамид, флутиацет, флутиацет-метил, флутианил, флутоланил, флутриафол, флувалинат, флуксапироксад, флуксофеним, фолпет, фомезафен, фомезафен-натрий, фонофос, форамсульфурон, форхлорфенурон, формальдегид, форметанат, форметанат-гидрохлорид, формотион, формпаранат, формпаранат-гидрохлорид, фосамин, фосамин-аммоний, фосетил, фосетил-алюминий, фосметилан, фоспират, фостиазат, фостиетан, фронталин, фуберидазол, фукаоджинг, фукаоми, фунаигекаолинг, фуфентиомочевина, фуралан, фуралаксил, фураметрин, фураметпир, фуратиокарб, фуркарбанил, фурконазол, фурконазол-цис, фуретрин, фурфурол, фурилазол, фурмециклокс, фурофанат, фурилоксифен, гамма-цигалотрин, гамма-HCH, генит, гибберелиновая кислота, гиббереллины, глифтор, глуфосинат, глуфосинат-аммоний, глуфосинат-P, глуфосинат-P-аммоний, глуфосинат-P-натрий, глиодин, глиоксим, глифосат, глифосат-диаммоний, глифосат-диметиламмоний, глифосат-изопропиламмоний, глифосат-моноаммоний, глифосат-калий, глифосат-сесквинатрий, глифосат-тримезиум, глифосин, госсиплур, грандлур, гризеофульвин, гуазатин, гуазатин-ацетаты, галакринат, галфенпрокс, галофенозид, галосафен, галосульфурон, галосульфурон-метил, галоксидин, галоксифоп, галоксифоп-этотил, галоксифоп-метил, галоксифоп-P, галоксифоп-P-этотил, галоксифоп-P-метил, галоксифоп-натрий, НСН, гемел, гемпа, HEOD, гептахлор, гептенофос, гептопаргил, гетерофос, гексахлорацетон, гексахлорбензол, гексахлорбутадиен, гексахлорофен, гексаконазол, гексафлумурон, гексафлурат, гексалур, гексамид, гексазинон, гексилтиофос, гекситиазокс, HHDN, голосульф, хуанкайво, хуангкаолинг, хуанцзунзуо, гидраметилнон, гидраргафен, гашеная известь, синильная кислота, гидропрен, гимексазол, гиквинкарб, IAA, IBA, икаридин, имазалил, имазалил-нитрат, имазалил-сульфат, имазаметабенз, имазаметабенз-метил, имазамокс, имазамокс-аммоний, имазапик, имазапик-аммоний, имазапир, имазапир-изопропиламмоний, имазаквин, имазаквин-аммоний, имазаквин-метил, имазаквин-натрий, имазетапир, имазетапир-аммоний, имазосульфурон, имибенконазол, имициафос, имидаклоприд, имидаклотиз, иминоктадин, иминоктадин-триацетат, иминоктадин-триалбезилат, имипротрин, инабенфид, инданофан, индазифлам, индоксакарб, инезин, иодобонил, иодокарб, иодметан, иодосульфурон, иодосульфурон-метил, иодосульфурон-метил-натрий, йофенсульфурон, йофенсульфурон-натрий, иоксинил, иоксинил-октаноат, иоксинил-литий, иоксинил-натрий, ипазин, ипконазол, ипфенкарбазон, ипробенфос, ипродион, ипроваликарб, ипримидам, ипсдиенол, ипсенол, IPSP, изамидофос, исазофос, изобензан, изокарбамид, изокарбофос, изоцил, изодрин, изофенфос, изофенфос-метил, исолан, изометиозин, изонорурон, изополинат, изопрокарб, изопропалин, изопротиолан, изопротурон, изопиразам, изопиримол, изотиоат, изотианил, изоурон, изоваледион, изоксабен, изоксахлортол, изоксадифен, изоксадифен-этил, изоксафлутол, изоксапирифоп, изоксатион, ивермектин, изопамфос, японилур, япотринс, жасмолин I, жасмолин II, жасмоновая кислота, жиахуангчонгзонг, чжациценгсиаолинг, чжасиангчинжи, чжиекаован, чжиекаоси, жодфенфос, ювенильный гормон I, ювенильный гормон II, ювенильный гормон III, кадетрин, карбутилат, каретазан, каретазан-калий, касугамицин, касугамицин-гидрохлорид, кеджунлин, кевелан, кетоспирадокс, кетоспирадокс-калий, кинетин, кинопрен, крезоксим-метил, куикаоси, лактофен, лямбда-цигалотрин, латилур, арсенат свинца, ленацил, лепимектин, лептофос, линдан, линеатин, линурон, лиримфос, литлур, луплур, луфенурон, людинджинши, люсинкаолин, литидатион, MAA, малатион, малеиновый гидразид, малонобен, мальтодекстрин, МАМА, манкоппер, манкозеб, мандипропамид, манеб, матрин, мазидокс, MCPA, MCPA-2-этилгексил, MCPA-бутотил, MCPA-бутил, MCPA-диметиламмоний, MCPA-диоламин, MCPA-этил, MCPA-изобутил, MCPA-изоктил, MCPA-изопропил, MCPA-метил, MCPA-оламин, MCPA-калий, MCPA-натрий, MCPA-тиоэтил, MCPA-троламин, MCPB, MCPB-этил, MCPB-метил, MCPB-натрий, мебенил, мекарбам, мекарбинзид, мекарфон, мекопроп, мекопроп-2-этилгексил, мекопроп-диметиламмоний, мекопроп-диоламин, мекопроп-этадил, мекопроп-изоктил, мекопроп-метил, мекопроп-P, мекопроп-P-2-этилгексил, мекопроп-P-диметиламмоний, мекопроп-P-изобутил, мекопроп-калий, мекопроп-P-калий, мекопроп-натрий, мекопроп-троламин, медимеформ, мединотерб, мединотерб-ацетат, медлур, мефенацет, мефенпир, мефенпир-диэтил, мефлуидид, мефлуидид-диоламин, мефлуидид-калий, мегатомовая кислота, меназон, мепанипирим, меперфлутрин, мефенат, мефосфолан, мепикват, мепикват-хлорид, мепикват-пентаборат, мепронил, мептилдинокап, дихлорид ртути, оксид ртути, хлорид ртути, мерфос, мезопразин, мезосульфурон, мезосульфурон-метил, мезотрион, месульфен, месульфенфос, метафлумизон, металаксил, металаксил-M, метальдегид, метам, метам-аммоний, метамифоп, метамитрон, метам-калий, метам-натрий, метазахлор, метазосульфурон, метазоксолон, метконазол, метепа, метфлуразон, метабензтиазурон, метакрифос, металпропалин, метамидофос, метасульфокарб, метазол, метфуроксам, метидатион, метиобенкарб, метиокарб, метиопирисульфурон, метиотепа, метиозолин, метиурон, метокротофос, метометон, метомил, метопрен, метопротрин, метоквин-бутил, метотрин, метоксихлор, метоксифенозид, метоксифенон, метил-афолат, метилбромид, метил-эвгенол, метилиодид, метилизотиоцианат, метилацетофос, метилхлороформ, метилдимрон, метиленхлорид, бензоат метилртути, дициандиамид метилртути, пентахлорфеноксид метилртути, метилнеодеканамид, метирам, метобензурон, метобромурон, метофлутрин, метолахлор, метолкарб, метоминостробин, метосулам, метоксадиазон, метоксурон, метрафенон, метрибузин, метсульфовакс, метсульфурон, метсульфурон-метил, мевинфос, мексакарбат, миешуан, милбемектин, милбемицин-оксим, милнеб, мипафокс, мирекс, MNAF, могучун, молинат, молосультап, моналид, монисоурон, монохлоруксусная кислота, монокротофос, монолинурон, моносульфурон, моносульфурон-эфир, монурон, монурон-TCA, морфамкват, морфамкват-дихлорид, мороксидин, мороксидин-гидрохлорид, морфотион, морзид, моксидектин, MSMA, мускалур, миклобутанил, миклозолин, N-(этилртуть)-п-толуолсульфонанилид, набам, нафталофос, налед, нафталин, нафталинацетамид, нафталевый ангидрид, нафтоксиуксусные кислоты, напроанилид, напропамид, напталам, напталам-натрий, натамицин, небурон, никлозамид, никлозамид-оламин, никосульфурон, никотин, нифлуридид, нипираклофен, нитенпирам, нитиазин, нитралин, нитрапирин, нитрилакарб, нитрофен, нитрофлуорфен, нитростирол, нитротал-изопропил, норбормид, норфлуразон, норникотин, норурон, новалурон, новифлумурон, нуаримол, OCH, октахлородипропиловый эфир, октилинон, офурас, ометоат, орбенкарб, орфралур, орто-дихлорбензол, ортосульфамурон, орикталур, орисастробин, оризалин, остол, острамон, оксабетринил, оксадиаргил, оксадиазон, оксадиксил, оксамат, оксамил, оксапиразон, оксапиразон-димоламин, оксапиразон-натрий, оксасульфурон, оксазикломефон, оксин-медь, оксолиновая кислота, окспоконазол, окспоконазол-фумарат, оксикарбоксин, оксидеметон-метил, оксидепрофос, оксидисульфотон, оксифлуорфен, оксиматрин, окситетрациклин, окситетрациклин-гидрохлорид, паклобутразол, пайхонгдинг, пара-дихлорбензол, парафлурон, паракват, паракват-дихлорид, паракват-диметилсульфат, паратион, паратион-метил, паринол, пебулат, пефуразоат, пеларгоновая кислота, пенконазол, пенцикурон, пендиметалин, пенфлуфен, пенфлурон, пенокссулам, пентахлорфенол, пентахлор, пентиопирад, пентметрин, пентоксазон, перфлуидон, перметрин, петоксамид, фенамакрил, феназин-оксид, фенисофам, фенкаптон, фенмедифам, фенмедифам-этил, фенобензурон, фенотрин, фенпроксид, фентоат, фенилртуть-мочевина, ацетат фенилртути, хлорид фенилртути, фенилртутное производное пирокатехина, нитрат фенилртути, салицилат фенилртути, форат, фосацетим, фозалон, фосдифен, фосфолан, фосфолан-метил, фосглицин, фосмет, фоснихлор, фосфамидон, фосфин, фосфокарб, фосфор, фостин, фоксим, фоксим-метил, фталид, пиклорам, пиклорам-2-этилгексил, пиклорам-изоктил, пиклорам-метил, пиклорам-оламин, пиклорам-калий, пиклорам-триэтиламмоний, пиклорам-трис(2-гидроксипропил)аммоний, пиколинафен, пикоксистробин, пиндон, пиндон-натрий, пиноксаден, пипералин, пиперонилбутоксид, пиперонил-циклонен, пиперофос, пипроктанил, пипроктанил-бромид, пипротал, пириметафос, пиримикарб, пиримиоксифос, пиримифос-этил, пиримифос-метил, плифенат, поликарбамат, полиоксины, полиоксорим, полиоксорим-цинк, политиалан, арсенит калия, азид калия, цианат калия, гиббереллат калия, нафтенат калия, полисульфид калия, тиоцианат калия, альфа-нафталинацетат калия, пп'-ДДТ, праллетрин, прекоцен I, прекоцен II, прекоцен III, претилахлор, примидофос, примисульфурон, примисульфурон-метил, пробеназол, прохлораз, прохлораз-марганец, проклонол, проциазин, процимидон, продиамин, профенофос, профлуазол, профлуралин, профлутрин, профоксидим, проглиназин, проглиназин-этил, прогексадион, прогексадион-кальций, прогидрожасмон, промацил, промекарб, прометон, прометрин, промурит, пропахлор, пропамидин, пропамидин-дигидрохлорид, пропамокарб, пропамокарб-гидрохлорид, пропанил, пропафос, пропаквизафоп, пропаргит, пропартрин, пропазин, пропетамфос, профам, пропиконазол, пропинеб, прописохлор, пропоксур, пропоксикарбазон, пропоксикарбазон-натрий, пропил-исом, пропирисульфурон, пропизамид, проквиназид, просулер, просульфалин, просульфокарб, просульфурон, протидатион, протиокарб, протиокарб-гидрохлорид, протиоконазол, протиофос, протоат, протрифенбут, проксан, проксан-натрий, принахлор, пиданон, пиметрозин, пиракарболид, пираклофос, пираклонил, пираклостробин, пирафлуфен, пирафлуфен-этил, пирафлупрол, пирамат, пираметостробин, пираоксистробин, пирасульфотол, пиразолинат, пиразофос, пиразосульфурон, пиразосульфурон-этил, пиразотион, пиразоксифен, пиресметрин, пиретрин I, пиретрин II, пиретрины, пирибамбенз-изопропил, пирибамбенз-пропил, пирибенкарб, пирибензоксим, пирибутикарб, пириклор, пиридабен, пирадафол, пиридалил, пиридафентион, пиридат, пиридинитрил, пирифенокс, пирифлуквиназон, пирифталид, пириметанил, пиримидифен, пириминобак, пириминобак-метил, пиримисульфан, пиримитат, пиринурон, пириофенон, пирипрол, пирипропанол, пирипроксифен, пиритиобак, пиритиобак-натрий, пиролан, пироквилон, пироксасульфон, пироксулам, пироксихлор, пироксифур, кассия, квинацетол, квинацетол-сульфат, квиналфос, квиналфос-метил, квиназамид, квинклорак, квинконазол, квинмерак, квинокламин, квинонамид, квинотион, квиноксифен, квинтиофос, квинтозен, хизалофоп, хизалофоп-этил, хизалофоп-P , хизалофоп-Р-этил, хизалофоп-P-тефурил, чивенжи, куингдинг, рабензазол, рафоксанид, ребемид, ресметрин, родетанил, родояпонин-III, рибавирин, римсульфурон, ротенон, рианиа, сафлуфенацил, саижунмао, саисентонг, салициланилид, сангвинарин, сантонин, шрадан, сциллиросид, себутилазин, секбуметон, седаксан, селамектин, семиамитраз, семиамитраз-хлорид, сесамекс, сезамолин, сетоксидим, шуангжиаанкаолин, сидурон, сиглур, силафлуофен, силатран, силикагель, силтиофам, симазин, симеконазол, семетон, симетрин, синтофен, SMA, S-метолахлор, арсенит натрия, азид натрия, хлорат натрия, фторид натрия, фторацетат натрия, гексафторсиликат натрия, нафтенат натрия, ортофенилфеноксид натрия, пентахлорфеноксид натрия, полисульфид натрия, тиоцианат натрия, α-нафталинацетат натрия, софамид, спинеторам, спиносад, спиродиклофен, спиромесифен, спиротетрамат, спироксамин, стрептомицин, стрептомицин-сесквисульфат, стрихнин, сулькатол, сулькофурон, сулькофурон-натрий, сулькотрион, сульфаллат, сульфентразон, сульфирам, сульфурамид, сульфометурон, сульфометурон-метил, сульфосульфурон, сульфотеп, сульфоксафлор, сульфоксид, сульфоксим, сера, серная кислота, сульфурилфторид, сульгликапин, сульпрофос, сультропен, свеп, тау-флувалинат, таврон, тазимкарб, TCA, TCA-аммоний, ТСА-кальций, TCA-этадил, ТСА-магний, TCA-натрий, TDE, тебуконазол, тебуфенозид, тебуфенпирад, тебуфлоквин, тебупиримфос, тебутам, тебутиурон, теклофталам, текназен, текорам, тефлубензурон, тефлутрин, тефурилтрион, темботрион, темефос, тепа, ТЕРР, тепралоксидим, тераллетрин, тербацил, тербукарб, тербухлор, тербуфос, тербуметон, тербутилазин, тербутрин, тетциклацис, тетрахлорэтан, тетрахлорвинфос, тетраконазол, тетрадифон, тетрафлурон, тетраметрин, тетраметилфлутрин, тетрамин, тетранактин, тетрасул, сульфат таллия, тенилхлор, тета-циперметрин, тиабендазол, тиаклоприд, тиадифтор, тиаметоксам, тиапронил, тиазафлурон, тиазопир, тикрофос, тициофен, тидиазимин, тидиазурон, тиенкарбазон, тиенкарбазон-метил, тифенсульфурон, тифенсульфурон-метил, тифлузамид, тиобенкарб, тиокарбоксим, тиохлорфенфим, тиоциклам, тиоциклам-гидрохлорид, тиоциклам-оксалат, тиадиазол-медь, тиодикарб, тиофанокс, тиофлуоксимат, тиогемпа, тиомерсал, тиометон, тионазин, тиофанат, тиофанат-метил, тиоквинокс, тиосемикарбазид, тиосультап, тиосультап-диаммоний, тиосультап-динатрий, тиосультап-натрий, тиотепа, тирам, турингиенсин, тиадинил, тиаоджиеан, тиокарбазил, тиоклорим, тиоксимид, тирпат, толклофос-метил, толфенпирад, толилфлуанид, ацетат толилртути, топрамезон, тралкоксидим, тралоцитрин, тралометрин, тралопирил, трансфлутрин, трансперметрин, третамин, триаконтанол, триадимефон, триадименол, триафамон, три-аллат, триамифос, триапентенол, триаратен, триаримол, триасульфурон, триазамат, триазбутил, триазифлам, триазофос, триазоксид, трибенурон, трибенурон-метил, трибуфос, оксид трибутилолова, трикамба, трихламид, трихлорфон, трихлорметафос-3, трихлоронат, триклопир, триклопир-бутотил, триклопир-этил, триклопир-триэтиламмоний, трициклазол, тридеморф, тридифан, триэтазин, трифенморф, трифенофос, трифлоксистробин, трифлоксисульфурон, трифлоксисульфурон-натрий, трифлумизол, трифлумурон, трифлуралин, трифлусульфурон, трифлусульфурон-метил, трифоп, трифоп-метил, трифопсим, трифорин, тригидрокситриазин, тримедлур, триметакарб, триметурон, тринексапак, тринексапак-этил, трипрен, трипропиндан, триптолид, тритак, тритиконазол, тритосульфурон, транк-колл, униконазол, униконазол-P, урбацид, уредепа, валерат, валидамицин, валифеналат, валон, вамидотион, вангард, ванилипрол, вернолат, винклозолин, варфарин, варфарин-калий, варфарин-натрий, сиаочонглиулин, синчжунан, сивочжунан, XMC, ксилахлор, ксиленолы, ксилилкарб, йишичжинг, зариламид, зеатин, зенгсиаоан, зета-циперметрин, нафтенат цинка, фосфид цинка, тиазол-цинк, цинеб, цирам, золапрофос, зоксамид, зомиханглонг, α-хлоргидрин, α-экдизон, α-мултистриатин и α-нафталинуксусная кислота.
43. Композиция по п.1, дополнительно включающая сельскохозяйственно приемлемый носитель.
44. Композиция по п.1, где указанная молекула находится в форме пестицидно приемлемой соли присоединения кислоты.
45. Композиция по п.1, где указанная молекула находится в форме солевого производного.
46. Композиция по п.1, где указанная молекула находится в форме гидрата.
47. Композиция по п.1, где указанная молекула находится в форме сложноэфирного производного.
48. Композиция по п.1, где указанная молекула находится в форме кристаллического полиморфа.
49. Композиция по п.1, где указанная молекула содержит 2H вместо 1H.
50. Композиция по п.1, где указанная молекула содержит 14C вместо 12C.
51. Композиция по п.1, дополнительно включающая биопестицид.
52. Композиция по п.1, дополнительно включающая одно или более следующих соединений:
(a) 3-(4-хлор-2,6-диметилфенил)-4-гидрокси-8-окса-1-азаспиро[4.5]дец-3-ен-2-он;
(b) 3-(4'-хлор-2,4-диметил[1,1'-дифенил]-3-ил)-4-гидрокси-8-окса-1-азаспиро[4.5]дец-3-ен-2-он;
(c) 4-[[(6-хлор-3-пиридинил)метил]метиламино]-2(5H)-фуранон;
(d) 4-[[(6-хлор-3-пиридинил)метил]циклопропиламино]-2(5H)-фуранон;
(e) 3-хлор-N2-[(1S)-1-метил-2-(метилсульфонил)этил]-N1-[2-метил-4-[1,2,2,2-тетрафтор-1-(трифторметил)этил]фенил]-1,2-бензолдикарбоксамид;
(f) 2-циано-N-этил-4-фтор-3-метокси-бензолсульфонамид;
(g) 2-циано-N-этил-3-метокси-бензолсульфонамид;
(h) 2-циано-3-дифторметокси-N-этил-4-фтор-бензолсульфонамид;
(i) 2-циано-3-фторметокси-N-этил-бензолсульфонамид;
(j) 2-циано-6-фтор-3-метокси-N,N-диметил-бензолсульфонамид;
(k) 2-циано-N-этил-6-фтор-3-метокси-N-метил-бензолсульфон-амид;
(l) 2-циано-3-дифторметокси-N,N-диметилбензолсульфонамид;
(m) 3-(дифторметил)-N-[2-(3,3-диметилбутил)фенил]-1-метил-1H-пиразол-4-карбоксамид;
(n) N-этил-2,2-диметилпропионамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон;
(o) N-этил-2,2-дихлор-1-метилциклопропан-карбоксамид-2-(2,6-дихлор-α,α,α-трифтор-п-толил)гидразон никотин;
(p) O-{(E)-[2-(4-хлор-фенил)-2-циано-1-(2-трифторметил-фенил)-винил]}метил-тиокарбонат;
(q) (E)-N1-[2-хлор-1,3-тиазол-5-илметил]-N2-циано-N1-метилацетамидин;
(r) 1-(6-хлорпиридин-3-илметил)-7-метил-8-нитро-1,2,3,5,6,7-гексагидро-имидазо[1,2-a]пиридин-5-ол;
(s) 4-[4-хлорфенил-(2-бутилидин-гидразоно)метил)]фенил-мезилат; и
(t) N-этил-2,2-дихлор-1-метилциклопропанкарбоксамид-2-(2,6-дихлор-альфа,альфа,альфа-трифтор-п-толил)гидразин.
53. Композиция по п.1, дополнительно включающая соединение, имеющее один или более следующих механизмов действия: ингибитор ацетилхолинэстеразы; модулятор натриевых каналов; ингибитор биосинтеза хитина; антагонист ГАМК- и глютаматзависимых хлоридных каналов; агонист ГАМК- и глютаматзависимых хлоридных каналов; агонист ацетилхолиновых рецепторов; антагонист ацетилхолиновых рецепторов; ингибитор МЕТ I; ингибитор Mg-стимулируемой АТФазы; никотиновый ацетилхолиновый рецептор; фактор, нарушающий целостность мембраны средней кишки; фактор, нарушающий окислительное фосфорилирование и рецептор рианодина (RyRs).
54. Композиция по п.1, дополнительно включающая семя.
55. Композиция по п.1, дополнительно включающая семя, которое было генетически модифицировано для экспрессии одного или более специализированных признаков.
56. Композиция по п.1, где указанная композиция инкапсулирована в капсуле или нанесена на поверхность капсулы.
57. Композиция по п.1, где указанная композиция инкапсулирована в капсуле или нанесена на поверхность капсулы, где указанная капсула имеет диаметр приблизительно 100-900 нм или приблизительно 10-900 мкм.
58. Способ, включающий применение композиции по п.1 на площади для борьбы с насекомым-вредителем в количестве, достаточном для борьбы с таким насекомым-вредителем.
59. Способ по п.58, где указанное насекомое-вредитель выбрано из жуков, уховерток, тараканов, мух, тлей, щитовок, белокрылок, цикадок, муравьев, ос, термитов, моли, бабочек, вшей, кузнечиков, саранчи, сверчков, блох, трипсов, щетинохвостов, зудней, клещей, нематод и симфил.
60. Способ по п.58, где указанное насекомое-вредитель относится к типу Nematoda или Arthropoda.
61. Способ по п.58, где указанное насекомое-вредитель относится к подтипу Chelicerata, Myriapoda или Hexapoda.
62. Способ по п.58, где указанное насекомое-вредитель относится к классу Arachnida, Symphyla или Insecta.
63. Способ по п.58, где указанное насекомое-вредитель относится к отряду Anoplura, отряду Coleoptera, отряду Dermaptera, отряду Blattaria, отряду Diptera, отряду Hemiptera, отряду Hymenoptera, отряду Isoptera, отряду Lepidoptera, отряду Mallophaga, отряду Orthoptera, отряду Siphonaptera, отряду Thysanoptera, отряду Thysanura, отряду Acarina или отряду Symphyla.
64. Способ по п.58, где указанная площадь является площадью, на которой выращивают яблони, кукурузу, хлопок, сою, канолу, пшеницу, рис, сорго, ячмень, овес, картофель, апельсины, люцерну, латук, клубнику, помидоры, перец, крестоцветы, груши, табак, миндаль, сахарную свеклу или бобы или их семена, используемые для посадки.
65. Способ по п.58, дополнительно включающий применение указанной композиции на генетически модифицированном растении, которое было генетически модифицировано для экспрессии одного или более специализированных признаков.
66. Композиция по п.1, где указанная композиция дополнительно включает сульфат аммония.
67. Способ, включающий пероральное введение или наружное применение композиции по п.1 животному за исключением человека, для борьбы с эндопаразитами и/или эктопаразитами.
68. Способ, включающий применение композиции по п.1 к растению, для усиления здоровья растения, урожая, мощности, качества или устойчивости тогда, когда активность насекомого-вредителя является низкой.
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
| RU 2009136631 A, 20.04.2011. | |||
Авторы
Даты
2018-09-24—Публикация
2013-12-18—Подача